Documentos de Académico
Documentos de Profesional
Documentos de Cultura
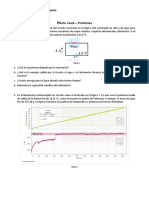
EfectoJoule
Cargado por
Jose GuzmanTítulo original
Derechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
EfectoJoule
Cargado por
Jose GuzmanCopyright:
Formatos disponibles
Universidad Autónoma de Occidente
Facultad de Ciencias Básicas
Departamento de Física
Efecto Joule
Objetivos
• Estudiar
la
disipación
de
calor
en
un
conductor
debido
al
paso
de
la
corriente
eléctrica.
• Determinar
la
capacidad
calorífica
de
un
calorímetro.
Motivación
La
temperatura
de
un
sistema
puede
elevarse
transfiriendo
calor,
pero
también
puede
conseguirse
realizando
trabajo
sobre
él.
Este
es
el
caso
del
famoso
experimento
desarrollado
por
el
físico
inglés
James
Prescott
Joule.
La
figura
1
es
un
diagrama
del
aparato
utilizado
por
Joule
en
su
famoso
experimento
para
determinar
el
trabajo
necesario
para
elevar
la
temperatura
de
1
g
de
agua
en
1°C.
En
este
caso
el
sistema
consiste
en
un
recipiente
aislado
térmicamente
que
contiene
1
g
de
agua.
El
aparato
de
Joule
convierte
la
energía
potencial
de
las
pesas
que
caen
en
trabajo
realizado
sobre
el
agua
por
medio
de
unas
paletas
adosadas,
como
se
muestra
en
la
figura.
Figura
1
Existen
otras
formas
de
realizar
trabajo
sobre
este
sistema.
Por
ejemplo,
podríamos
simplemente
dejar
caer
el
recipiente
de
agua
aislado
desde
cierta
altura
h,
de
forma
que
se
produzca
un
choque
inelástico
contra
el
suelo,
o
bien
podríamos
aprovechar
el
trabajo
mecánico
para
generar
electricidad
y
utilizar
luego
la
electricidad
para
calentar
el
agua.
En
estos
experimentos
se
necesita
la
misma
cantidad
de
trabajo
para
producir
un
determinado
cambio
de
temperatura
en
un
sistema
dado.
Según
la
conservación
de
la
energía,
el
trabajo
realizado
debe
traducirse
en
un
incremento
de
la
energía
interna
del
sistema.
Muchos
electrodomésticos
como
las
teteras,
secadoras,
tostadores
y
cobijas
eléctricas
son
ejemplos
que
contienen
elementos
calentadores.
Estos
elementos
producen
un
aumento
en
la
temperatura
debido
a
la
corriente
eléctrica
que
circula
a
través
de
él.
Cuando
se
establece
un
campo
eléctrico
en
un
conductor,
el
gas
de
electrones
incrementa
su
energía
cinética
debido
al
trabajo
que
el
campo
realiza
sobre
los
electrones
libres.
Sin
embargo,
pronto
se
va
alcanzando
el
estado
estacionario,
ya
que
esta
energía
adicional
se
convierte
rápidamente
en
energía
térmica
del
conductor
por
las
colisiones
entre
los
electrones
y
los
iones
reticulares
del
material.
La
disipación
de
calor
en
el
conductor
debido
a
la
corriente
eléctrica
se
denomina
efecto
Joule.
Práctica Efecto Joule
Elaborada por Alexánder Osorio y Mónica Rico
Revisada por Mónica Rico – 2014-03
Universidad Autónoma de Occidente
Facultad de Ciencias Básicas
Departamento de Física
Equipo Requerido
• Interfaz
Universal
850
• Fuente
de
voltaje
variable
• Calorímetro
• Beaker
plástico
de
500
mL
• Sensor
de
corriente
alta
• Balanza
• Sensor
de
voltaje
• Cables
de
conexión
eléctrica
• Sensor
de
temperatura
(acero
inoxidable)
Procedimiento
Parte I. Configuración de la interfaz y sensores
1. Conecte la interfaz Universal 850 al computador y enciéndala.
2. Conecte los sensores de voltaje, de corriente alta y el de temperatura-‐acero inoxidable a los canales
analógicos de la interfaz.
3. Ejecute el programa Capstone e instale virtualmente los sensores en los mismos canales donde
fueron conectados físicamente. Verifique que efectivamente sean estos los sensores configurados
(sensores de voltaje, de corriente alta y el de temperatura-‐acero inoxidable) de lo contrario los
datos obtenidos serán incorrectos y deberá repetir sus medidas.
4. En la barra de menú inferior haga click en el botón Condiciones de grabación, seleccione Condición
de detención. Elija el Tipo de condición como basada en tiempo y establezca un tiempo de 10
minutos (600 s).
5. Cree un gráfico Temperatura vs. tiempo. Recuerde que es conveniente reemplazar los nombres de
las gráficas y ensayos por unos que hagan referencia a los datos registrados.
Parte III. Toma de datos
1. Agregue
200
g
de
agua
(ma)
al
vaso
de
aluminio
del
calorímetro.
Sea
cuidadoso
con
la
precisión
en
esta
medida
y
recuerde
que
la
balanza
registra
hasta
centésimas
de
gramo.
Anote
este
valor
en
la
tabla
junto
con
su
incertidumbre
(Δm).
2. Ponga
el
vaso
en
el
cuerpo
del
calorímetro
y
tápelo.
Introduzca
el
sensor
de
temperatura
teniendo
cuidado
de
que
no
haga
contacto
con
la
resistencia
que
se
encuentra
en
el
interior
(Figura
2).
Sensor de
Temperatura
Sensor de Voltaje
Figura
2
Figura
3
Práctica Efecto Joule
Elaborada por Alexánder Osorio y Mónica Rico
Revisada por Mónica Rico – 2014-03
Universidad Autónoma de Occidente
Facultad de Ciencias Básicas
Departamento de Física
3. Conecte
los
bornes
de
la
resistencia
del
calorímetro
a
la
salida
de
voltaje
DC
de
la
fuente
(Figura
3).
4. Disponga
el
sensor
de
corriente
en
este
circuito.
5. Conecte
el
sensor
de
voltaje
a
los
extremos
de
la
resistencia
(Figura
2).
6. El
circuito
y
los
sensores
ya
conectados
se
observan
en
la
figura
4.a.
El
mismo
circuito
se
encuentra
esquematizado
en
la
figura
4.b.
Figura
4.a
Figura
4.b
7. Antes
de
encender
la
fuente
de
voltaje
verifique
que
las
perillas
de
corriente
DC
y
voltaje
DC
se
encuentren
en
el
mínimo
de
salida.
Posteriormente
gire
la
perilla
de
corriente
por
lo
menos
media
escala
y
luego
la
de
voltaje
hasta
alcanzar
un
valor
de
corriente
de
4
A.
PRECAUCIÓN:
Solo
puede
encender
la
fuente
si
la
resistencia
está
sumergida
en
agua.
8. Haga
clic
en
el
botón
Grabar.
Mueva
el
agua
esporádicamente
en
el
calorímetro
con
ayuda
del
mezclador
para
homogenizar
su
temperatura.
Tenga
cuidado
de
no
hacer
contacto
con
la
resistencia.
9. La
medida
se
detendrá
automáticamente
al
cabo
de
los
10
minutos.
10. Reduzca
a
cero
la
corriente
de
salida
de
la
fuente
(llevando
a
cero
la
perilla
de
voltaje)
y
apáguela.
11. Repita
el
procedimiento
anterior
con
otros
200
g
de
agua
y
con
un
valor
de
corriente
menor.
12. Una
vez
se
detenga
la
medida,
reduzca
a
cero
la
corriente
de
salida
de
la
fuente
(llevando
a
cero
la
perilla
de
voltaje)
y
apáguela.
13. Desmonte
el
circuito
y
seque
los
componentes
del
calorímetro.
Análisis
1. Use
la
Calculadora
(barra
de
menú
izquierda)
y
determine
con
ella
la
potencia
entregada
por
la
fuente
(P).
Cree
un
gráfico
de
potencia
vs.
tiempo.
2. Seleccione
de
la
barra
de
menú
del
gráfico
de
Temperatura
vs.
t
el
icono
.
Este
menú
aparece
cuando
el
mouse
está
sobre
un
gráfico.
Así
obtendrá
una
gráfica
donde
podrá
observar
simultáneamente
el
comportamiento
de
la
temperatura
y
la
potencia
respecto
al
tiempo
(Figura
5).
Práctica Efecto Joule
Elaborada por Alexánder Osorio y Mónica Rico
Revisada por Mónica Rico – 2014-03
Universidad Autónoma de Occidente
Facultad de Ciencias Básicas
Departamento de Física
Figura
5
3. Analice
el
comportamiento
de
la
curva
de
potencia,
determine
si
es
estable
a
lo
largo
de
la
medición.
4. Identifique
la
región
donde
la
potencia
se
mantiene
más
o
menos
estable
y
use
la
herramienta
estadística
(
)
para
determinar
el
valor
promedio,
así
como
su
incertidumbre
absoluta
(desviación
estándar).
5. Si
existen
fluctuaciones
notorias
de
la
potencia,
verifique
si
éstas
se
reflejan
en
el
comportamiento
de
la
gráfica
de
Temperatura
vs.
Tiempo.
6. Verifique
si
el
comportamiento
obtenido
en
la
gráfica
Temperatura
vs.
tiempo
es
el
esperado.
7. En
esta
gráfica
seleccione
la
misma
región
contemplada
en
la
gráfica
potencia
vs
tiempo
y
realice
un
ajuste
lineal.
De
un
significado
físico
a
la
pendiente
de
la
curva.
8. Con
ayuda
de
la
pendiente
calcule
la
capacidad
calorífica
del
calorímetro
(C=mc;
donde
m=masa
del
calorímetro
y
c=calor
específico
del
calorímetro).
9. Calcule
la
incertidumbre
absoluta
y
relativa
en
cada
caso.
Tabla 1
Masa agua, ma ( ): ___________
Incertidumbre en la medida de las masas, Δm ( ): ______________
Potencia promedio, P ( ): ____________
Incertidumbre absoluta, ΔP ( ): ____________
Incertidumbre relativa, ΔP/P ( ): ____________
Tabla 2
Pendiente de la gráfica T vs. t, ( ): ____________
Capacidad calorífica del calorímetro C ( ): ____________
Incertidumbre absoluta en C, ( ): ____________
Incertidumbre relativa en C, ( ): ____________
Práctica Efecto Joule
Elaborada por Alexánder Osorio y Mónica Rico
Revisada por Mónica Rico – 2014-03
Universidad Autónoma de Occidente
Facultad de Ciencias Básicas
Departamento de Física
Bibliografía
SEARS, Francis W.; ZEMANSKY, Mark W.; YOUNG, Hugh D.; FREEDMAN, Roger A. Física Universitaria con Física Moderna,
volumen 2. Undécima edición, Pearson Educación, México, 2005.
TIPLER, Paul A. Physics for scientists and engineers. 4th ed. W.H. Freeman, New York NY, 1999.
http://www.whfreeman.com/tipler
GIL, Salvador, RODRÍGUEZ, Eduardo; Física re-creativa, Experimentos de Física usando nuevas tecnologías, Pearson
Educación, Perú, 2001.
Práctica Efecto Joule
Elaborada por Alexánder Osorio y Mónica Rico
Revisada por Mónica Rico – 2014-03
También podría gustarte
- Experiencias sobre circuitos eléctricos en serie operados por corriente directaDe EverandExperiencias sobre circuitos eléctricos en serie operados por corriente directaAún no hay calificaciones
- Efecto JouleDocumento5 páginasEfecto JouleSEBASTIAN POSSO MUNOZAún no hay calificaciones
- Montaje de elementos y equipos de instalaciones eléctricas de baja tensión en edificios. ELES0208De EverandMontaje de elementos y equipos de instalaciones eléctricas de baja tensión en edificios. ELES0208Aún no hay calificaciones
- Potencia y Maxima Transferencia de PotenciaDocumento10 páginasPotencia y Maxima Transferencia de PotenciaPedro AguilarAún no hay calificaciones
- UntitledDocumento26 páginasUntitledValentin MontilvaAún no hay calificaciones
- Informe de Laboratorio (Medidas de Tension)Documento6 páginasInforme de Laboratorio (Medidas de Tension)Kevin DiazAún no hay calificaciones
- Informe 2 Laboratorio de Fisica 2.Documento8 páginasInforme 2 Laboratorio de Fisica 2.Juan David Gallego VaronAún no hay calificaciones
- Laboratorio Fisica 3Documento17 páginasLaboratorio Fisica 3william abel taboada gambiniAún no hay calificaciones
- Principio de ArquimidesDocumento5 páginasPrincipio de ArquimidesYoni VLAún no hay calificaciones
- Informe 3 Fisica 2Documento7 páginasInforme 3 Fisica 2Killa BayonaAún no hay calificaciones
- Efecto JouleDocumento8 páginasEfecto JouleBENJAMIN ED CAVERO YABARAún no hay calificaciones
- Fisica TerminadoooDocumento13 páginasFisica TerminadoooCarlos Alberto Leyva GiraldoAún no hay calificaciones
- Laboratorio EquivalenteDocumento3 páginasLaboratorio EquivalenteSharick GarzonAún no hay calificaciones
- Manejos de Instrumentos Electricos (Dfe Aqldair)Documento7 páginasManejos de Instrumentos Electricos (Dfe Aqldair)ydavid_1990Aún no hay calificaciones
- Guía de Práctica de Laboratorio #1Documento6 páginasGuía de Práctica de Laboratorio #1DIEGO MAURICIO SUAZO AMADOAún no hay calificaciones
- Laboratorio Fisica ElectricaDocumento6 páginasLaboratorio Fisica ElectricaJosé Manuel AnguloAún no hay calificaciones
- Laboratorio Fisica ElectricaDocumento6 páginasLaboratorio Fisica ElectricaJosé Manuel AnguloAún no hay calificaciones
- Módulo 2-2 Practica de Medicion e InstrumentaciónDocumento17 páginasMódulo 2-2 Practica de Medicion e Instrumentación1 ECA Diego Josué Hernández LópezAún no hay calificaciones
- EQUIPO 3 P5 - Instalacion Electrica de Los Interruptores TermomagneticosDocumento11 páginasEQUIPO 3 P5 - Instalacion Electrica de Los Interruptores Termomagneticosandrik TomatzinAún no hay calificaciones
- Practica Analisis Ley de OhmDocumento16 páginasPractica Analisis Ley de OhmEric Dueñas TrujilloAún no hay calificaciones
- Guia de Efecto JouleDocumento7 páginasGuia de Efecto JouleJhonatan ArenasAún no hay calificaciones
- Laboratorio 2 UFPSDocumento10 páginasLaboratorio 2 UFPSRicardo Colmenares100% (1)
- Potencia Eléctrica Lab f3Documento12 páginasPotencia Eléctrica Lab f3NOE LUNA VENTUROAún no hay calificaciones
- Preinforme 2Documento2 páginasPreinforme 2Jesús Alfonso Castro ParraAún no hay calificaciones
- LAB 3 - Ley de OhmDocumento10 páginasLAB 3 - Ley de Ohmjhonatancerna982Aún no hay calificaciones
- Practica 3 - Equipo 1Documento21 páginasPractica 3 - Equipo 1Cesar DoriaAún no hay calificaciones
- Labo 3Documento6 páginasLabo 3Anonymous 5vyOP5HMAún no hay calificaciones
- Guia para Uso Del MultimetroDocumento7 páginasGuia para Uso Del MultimetroMarco Antonio CarbajalAún no hay calificaciones
- INFORME DE LABORATORIO (Medidas de Tension)Documento6 páginasINFORME DE LABORATORIO (Medidas de Tension)Kevin DiazAún no hay calificaciones
- Practica 3 Lab Fisica 3Documento10 páginasPractica 3 Lab Fisica 3sofia covarrubias castilloAún no hay calificaciones
- Lab #02 - LEY OHMDocumento3 páginasLab #02 - LEY OHMJoaquin AlvarezAún no hay calificaciones
- Tension ElectricaDocumento4 páginasTension ElectricaMoisés CastrillonAún no hay calificaciones
- 12312321321314124122141232414Documento4 páginas12312321321314124122141232414Erick LagosAún no hay calificaciones
- Pre-Informe - Resistencia Interna de Una PilaDocumento10 páginasPre-Informe - Resistencia Interna de Una PilaAndres Felipe Salazar RamirezAún no hay calificaciones
- Cuestionario Maquinas Electricas IDocumento10 páginasCuestionario Maquinas Electricas ICARLOS NERI VENTURA PARAVECINOAún no hay calificaciones
- Informe Lab 7 - MergedDocumento7 páginasInforme Lab 7 - MergedNikolai Oscar Lopez JordanAún no hay calificaciones
- Práctica 3 Fis III Equipo 3Documento16 páginasPráctica 3 Fis III Equipo 3Rogelio AlejandroAún no hay calificaciones
- Informe de Laboratorio Mediciones Eléctricas Parte 2 Física ElectromagnéticaDocumento14 páginasInforme de Laboratorio Mediciones Eléctricas Parte 2 Física ElectromagnéticaJarlin Andres Fonseca BermonAún no hay calificaciones
- Informe1 CircuitosDocumento5 páginasInforme1 Circuitosmiguel antonio martinez moremoAún no hay calificaciones
- Práctica 2 y 3. Conocimiento Del Equipo BásicoDocumento19 páginasPráctica 2 y 3. Conocimiento Del Equipo BásicoFernando RodriguezAún no hay calificaciones
- AutomatizaciónDocumento8 páginasAutomatizaciónTamy ScastanedaAún no hay calificaciones
- Laboratorio 5 (Efecto Joule)Documento8 páginasLaboratorio 5 (Efecto Joule)Oskar Noa SanaAún no hay calificaciones
- Practica 1 ElectroDocumento13 páginasPractica 1 Electrostephany ramosAún no hay calificaciones
- Manejo de InstrumentosDocumento12 páginasManejo de InstrumentosJulian Camilo Beltran BustosAún no hay calificaciones
- Magnitudes EléctricasDocumento6 páginasMagnitudes EléctricasJHON MICHAEL PACHECO SUAREZ50% (2)
- Electrónica - Tarea 3Documento7 páginasElectrónica - Tarea 3Luis Mora100% (2)
- Metrologia y Normalizacion Tema 2Documento13 páginasMetrologia y Normalizacion Tema 2Adrian EsparzaAún no hay calificaciones
- Laboratorio Elec-002Documento12 páginasLaboratorio Elec-002Edgar Santiago Gomez AguirreAún no hay calificaciones
- MEDIDA de La IntensidadDocumento5 páginasMEDIDA de La IntensidadJuan NegretteAún no hay calificaciones
- Medidas Con Voltimetro, Amperimetro y OsciloscopioDocumento8 páginasMedidas Con Voltimetro, Amperimetro y OsciloscopioJenderson Tovar PiñeroAún no hay calificaciones
- Practica 04 - Divisor de Voltaje y CorrienteDocumento5 páginasPractica 04 - Divisor de Voltaje y CorrienteAdrian NavaAún no hay calificaciones
- PDF Informe 3 Divisores de Tension y de Corriente Utp - CompressDocumento6 páginasPDF Informe 3 Divisores de Tension y de Corriente Utp - Compressgiancarlo morilloAún no hay calificaciones
- Experiencia Final N°7Documento15 páginasExperiencia Final N°7CHRISTIAN SILVA CENTURIONAún no hay calificaciones
- (551888069) Lab 1 Generación de Electricidad (2013)Documento20 páginas(551888069) Lab 1 Generación de Electricidad (2013)ManuelJoseAcostaPongoAún no hay calificaciones
- Actividad3 ElectronicaDocumento7 páginasActividad3 ElectronicalauraAún no hay calificaciones
- Informe: Efecto JouleDocumento4 páginasInforme: Efecto JouleSteven EspinalAún no hay calificaciones
- 3 Informe Del Puente WheatstoneDocumento10 páginas3 Informe Del Puente WheatstoneElizabethArizacaSamaniegoAún no hay calificaciones
- Lab #7 - Ley de OhmDocumento8 páginasLab #7 - Ley de OhmYoni VLAún no hay calificaciones
- Leyes de Kirchhoff y de JouleDocumento5 páginasLeyes de Kirchhoff y de JouleGustavo SaenzAún no hay calificaciones
- Informe 8 TallerDocumento9 páginasInforme 8 TallerMarceloAún no hay calificaciones
- Sensor de Temperatura de Estado SolidoDocumento6 páginasSensor de Temperatura de Estado SolidoJose GuzmanAún no hay calificaciones
- Trabajo de Consulta 1 EXPDocumento1 páginaTrabajo de Consulta 1 EXPJose GuzmanAún no hay calificaciones
- Lab AskDocumento8 páginasLab AskJose GuzmanAún no hay calificaciones
- Lab Fisica EquipotencialDocumento4 páginasLab Fisica EquipotencialJose GuzmanAún no hay calificaciones
- 3a. Preinforme Efecto JouleDocumento2 páginas3a. Preinforme Efecto JouleJose GuzmanAún no hay calificaciones
- Clase CDocumento5 páginasClase CJose GuzmanAún no hay calificaciones
- Fallo MazdaDocumento1 páginaFallo MazdaJose GuzmanAún no hay calificaciones
- Final Lab3Documento5 páginasFinal Lab3Jose GuzmanAún no hay calificaciones
- Coseno Rectificada y Un Tren de PulsosDocumento6 páginasCoseno Rectificada y Un Tren de PulsosJose GuzmanAún no hay calificaciones
- Ask Lab 2Documento8 páginasAsk Lab 2Jose GuzmanAún no hay calificaciones
- Reporte RCDocumento5 páginasReporte RCJose GuzmanAún no hay calificaciones
- Lineas Equipotenciales B1 (Jose Robinson Guzman Cordoba)Documento11 páginasLineas Equipotenciales B1 (Jose Robinson Guzman Cordoba)Jose GuzmanAún no hay calificaciones
- Informe de ElectronicaDocumento4 páginasInforme de ElectronicaJose GuzmanAún no hay calificaciones
- Sensor de Temperatura de Estado SolidoDocumento5 páginasSensor de Temperatura de Estado SolidoJose GuzmanAún no hay calificaciones
- BernoulliDocumento11 páginasBernoulliCristian LaragomezAún no hay calificaciones
- ESTATICA CompletoDocumento13 páginasESTATICA CompletoJuan Carlos Mamani GomezAún no hay calificaciones
- Espectroscopia de MasasDocumento7 páginasEspectroscopia de MasasRodrigo OrnelasAún no hay calificaciones
- s5 - HT Ok - Práctica de Aula - 2020-2Documento2 páginass5 - HT Ok - Práctica de Aula - 2020-2Francisco Morales CuevasAún no hay calificaciones
- Turbinas de VaporDocumento5 páginasTurbinas de VapordiegoAún no hay calificaciones
- Transporte HidráulicoDocumento73 páginasTransporte Hidráulicominerosoy92% (12)
- Guia Aplicación Espejos CurvosDocumento1 páginaGuia Aplicación Espejos CurvosFrancoAún no hay calificaciones
- Ejercicio MulticomponenteDocumento6 páginasEjercicio MulticomponenteRenzo MuñozAún no hay calificaciones
- Propiedades de La MateriaDocumento4 páginasPropiedades de La MateriaSalas Castro J MAún no hay calificaciones
- Practica 1Documento4 páginasPractica 1Aldo ArgudinAún no hay calificaciones
- Avance Proyecto 1 PDFDocumento7 páginasAvance Proyecto 1 PDFLuis TapiaAún no hay calificaciones
- Cuadro PatologiasDocumento28 páginasCuadro PatologiasLeslie LópezAún no hay calificaciones
- AtmosfericaDocumento11 páginasAtmosfericaYaneth Patarroyp100% (1)
- Analisis PVTDocumento23 páginasAnalisis PVTAmhed Torrico VacaAún no hay calificaciones
- Fibras de Acero WirandDocumento25 páginasFibras de Acero WirandAlonso PolarAún no hay calificaciones
- ProbMolgases PDFDocumento2 páginasProbMolgases PDFEliut GomezAún no hay calificaciones
- Curado Del Curado Del Concreto Concreto PDFDocumento138 páginasCurado Del Curado Del Concreto Concreto PDFlaloAún no hay calificaciones
- CRISTALIZACIONESDocumento2 páginasCRISTALIZACIONESNata BarbieriAún no hay calificaciones
- Proyecto: '"Cierre de Mina en La U.M ANAMA 2022 - Cierre Progresivo Y Cierre Final"Documento21 páginasProyecto: '"Cierre de Mina en La U.M ANAMA 2022 - Cierre Progresivo Y Cierre Final"Triana Angulo RamosAún no hay calificaciones
- Capitulo 7 SecadoDocumento25 páginasCapitulo 7 SecadoSantiago GonzálezAún no hay calificaciones
- Problemas AplicacionDocumento12 páginasProblemas AplicacionEduardo Daniel Flores CarpioAún no hay calificaciones
- Membrana CelularDocumento42 páginasMembrana CelularJorge Alexander Clavijo SandobalAún no hay calificaciones
- Tema 4 - Hidraulica de La CementacionDocumento4 páginasTema 4 - Hidraulica de La CementacionYesely Pradel0% (1)
- Reporte 6 FIV 1917839Documento7 páginasReporte 6 FIV 1917839Maryo RamosAún no hay calificaciones
- #5 Troubleshooting SpanishDocumento320 páginas#5 Troubleshooting SpanishMiguel RomoAún no hay calificaciones
- Balances de MateriaDocumento27 páginasBalances de MateriaClari EsquivelAún no hay calificaciones
- Memoria Ejemplo Ejercicio Cálculo Instalación ACSDocumento28 páginasMemoria Ejemplo Ejercicio Cálculo Instalación ACSAleksDePasseyAún no hay calificaciones
- 05 Ajustes y Tolerancias de RodamientosDocumento37 páginas05 Ajustes y Tolerancias de RodamientosEduardo EstradaAún no hay calificaciones
- INTRODUCCION Practica 2 Materiales (Ensayo de Impacto)Documento2 páginasINTRODUCCION Practica 2 Materiales (Ensayo de Impacto)Samuel CastroAún no hay calificaciones
- Natación Principio de BernoulliDocumento3 páginasNatación Principio de BernoulliJuan Carlos Caviedes SanabriaAún no hay calificaciones
- La metamedicina. Cada síntoma es un mensaje: La curación a tu alcanceDe EverandLa metamedicina. Cada síntoma es un mensaje: La curación a tu alcanceCalificación: 5 de 5 estrellas5/5 (8)
- Batidos Verdes Depurativos y Antioxidantes: Aumenta tu Vitalidad con Smoothie Detox Durante 10 Días Para Adelgazar y Bajar de Peso: Aumenta tu vitalidad con smoothie detox durante 10 días para adelgazar y bajar de pesoDe EverandBatidos Verdes Depurativos y Antioxidantes: Aumenta tu Vitalidad con Smoothie Detox Durante 10 Días Para Adelgazar y Bajar de Peso: Aumenta tu vitalidad con smoothie detox durante 10 días para adelgazar y bajar de pesoCalificación: 5 de 5 estrellas5/5 (2)
- La revolución de la glucosa: Equilibra tus niveles de glucosa y cambiarás tu salud y tu vidaDe EverandLa revolución de la glucosa: Equilibra tus niveles de glucosa y cambiarás tu salud y tu vidaCalificación: 5 de 5 estrellas5/5 (203)
- Liberación del trauma: Perdón y temblor es el caminoDe EverandLiberación del trauma: Perdón y temblor es el caminoCalificación: 4 de 5 estrellas4/5 (4)
- 50 técnicas de mindfulness para la ansiedad, la depresión, el estrés y el dolor: Mindfulness como terapiaDe Everand50 técnicas de mindfulness para la ansiedad, la depresión, el estrés y el dolor: Mindfulness como terapiaCalificación: 4 de 5 estrellas4/5 (37)
- Homo antecessor: El nacimiento de una especieDe EverandHomo antecessor: El nacimiento de una especieCalificación: 5 de 5 estrellas5/5 (1)
- Cerebro y silencio: Las claves de la creatividad y la serenidadDe EverandCerebro y silencio: Las claves de la creatividad y la serenidadCalificación: 5 de 5 estrellas5/5 (2)
- Sistema nervioso y osteopatía: Nervios periféricos, meninges craneales y espinales, y sistema nervioso vegetativo (Color)De EverandSistema nervioso y osteopatía: Nervios periféricos, meninges craneales y espinales, y sistema nervioso vegetativo (Color)Calificación: 5 de 5 estrellas5/5 (9)
- Dieta Para El Reflujo Biliar y Gastritis Alcalina - Incluye 20 Deliciosas Recetas Libres de Gluten y de Lácteos Para Tratar y Aliviar el Reflujo Biliar y Sus Molestos SíntomasDe EverandDieta Para El Reflujo Biliar y Gastritis Alcalina - Incluye 20 Deliciosas Recetas Libres de Gluten y de Lácteos Para Tratar y Aliviar el Reflujo Biliar y Sus Molestos SíntomasCalificación: 4 de 5 estrellas4/5 (9)
- Ondas de choque extracorpóreas radiales: Aplicación en patologías músculo esqueléticasDe EverandOndas de choque extracorpóreas radiales: Aplicación en patologías músculo esqueléticasCalificación: 5 de 5 estrellas5/5 (3)
- Ciencia de datos: La serie de conocimientos esenciales de MIT PressDe EverandCiencia de datos: La serie de conocimientos esenciales de MIT PressCalificación: 5 de 5 estrellas5/5 (1)
- El psoas: Músculo vital (Color)De EverandEl psoas: Músculo vital (Color)Calificación: 3.5 de 5 estrellas3.5/5 (9)
- Guía práctica para la refracción ocularDe EverandGuía práctica para la refracción ocularCalificación: 5 de 5 estrellas5/5 (2)
- Zensorialmente : Dejá que tu cuerpo sea tu cerebroDe EverandZensorialmente : Dejá que tu cuerpo sea tu cerebroAún no hay calificaciones
- Cerebros rotos: Pacientes asombrosos que me enseñaron a vivirDe EverandCerebros rotos: Pacientes asombrosos que me enseñaron a vivirCalificación: 5 de 5 estrellas5/5 (3)
- Había una vez el átomo: O cómo los científicos imaginan lo invisibleDe EverandHabía una vez el átomo: O cómo los científicos imaginan lo invisibleCalificación: 5 de 5 estrellas5/5 (3)
- Guía para la aplicación de ISO 9001 2015De EverandGuía para la aplicación de ISO 9001 2015Calificación: 4 de 5 estrellas4/5 (1)
- Sesgos Cognitivos: Una Fascinante Mirada dentro de la Psicología Humana y los Métodos para Evitar la Disonancia Cognitiva, Mejorar sus Habilidades para Resolver Problemas y Tomar Mejores DecisionesDe EverandSesgos Cognitivos: Una Fascinante Mirada dentro de la Psicología Humana y los Métodos para Evitar la Disonancia Cognitiva, Mejorar sus Habilidades para Resolver Problemas y Tomar Mejores DecisionesCalificación: 4.5 de 5 estrellas4.5/5 (13)
- Historia del cuerpo humano: Evolución, salud y enfermedadDe EverandHistoria del cuerpo humano: Evolución, salud y enfermedadAún no hay calificaciones
- Anatomía & 100 estiramientos Esenciales (Color): Técnicas, beneficios, precauciones, consejos, tablas de series, dolenciasDe EverandAnatomía & 100 estiramientos Esenciales (Color): Técnicas, beneficios, precauciones, consejos, tablas de series, dolenciasCalificación: 4.5 de 5 estrellas4.5/5 (21)
- Las Cinco Leyes Biológicas De La Naturaleza: La Nueva Medicina (Color Edition) SpanishDe EverandLas Cinco Leyes Biológicas De La Naturaleza: La Nueva Medicina (Color Edition) SpanishCalificación: 4.5 de 5 estrellas4.5/5 (3)
- SNC - Soporte neurocrítico: De la urgencia a la terapia intensivaDe EverandSNC - Soporte neurocrítico: De la urgencia a la terapia intensivaAún no hay calificaciones