Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Materiales
Cargado por
Alvaro Jesus Matamoros Segovia0 calificaciones0% encontró este documento útil (0 votos)
4 vistas8 páginasEl hierro puro presenta tres estados alotrópicos (hierro α, γ y δ) a medida que aumenta la temperatura, cristalizando en diferentes sistemas. Entre 911 y 1400 °C cristaliza como hierro γ en sistema cúbico centrado en las caras, siendo más dúctil. Al añadir carbono al hierro, los átomos de carbono pueden situarse en los intersticios de la red de hierro o formar cementita (Fe3C), un compuesto químico definido.
Descripción original:
Derechos de autor
© © All Rights Reserved
Formatos disponibles
PDF, TXT o lea en línea desde Scribd
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoEl hierro puro presenta tres estados alotrópicos (hierro α, γ y δ) a medida que aumenta la temperatura, cristalizando en diferentes sistemas. Entre 911 y 1400 °C cristaliza como hierro γ en sistema cúbico centrado en las caras, siendo más dúctil. Al añadir carbono al hierro, los átomos de carbono pueden situarse en los intersticios de la red de hierro o formar cementita (Fe3C), un compuesto químico definido.
Copyright:
© All Rights Reserved
Formatos disponibles
Descargue como PDF, TXT o lea en línea desde Scribd
0 calificaciones0% encontró este documento útil (0 votos)
4 vistas8 páginasMateriales
Cargado por
Alvaro Jesus Matamoros SegoviaEl hierro puro presenta tres estados alotrópicos (hierro α, γ y δ) a medida que aumenta la temperatura, cristalizando en diferentes sistemas. Entre 911 y 1400 °C cristaliza como hierro γ en sistema cúbico centrado en las caras, siendo más dúctil. Al añadir carbono al hierro, los átomos de carbono pueden situarse en los intersticios de la red de hierro o formar cementita (Fe3C), un compuesto químico definido.
Copyright:
© All Rights Reserved
Formatos disponibles
Descargue como PDF, TXT o lea en línea desde Scribd
Está en la página 1de 8
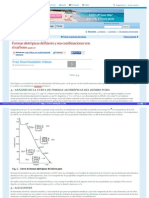
El hierro puro presenta tres estados alotrópicos a medida que se incrementa la
temperatura desde la temperatura ambiente:
• Hasta los 911 °C, el hierro ordinario, cristaliza en el sistema cúbico
centrado en el cuerpo (BCC) y recibe la denominación de hierro α.
Es un material dúctil y maleable responsable de la buena forjabilidad
de las aleaciones con bajo contenido en carbono y es ferromagnético
hasta los 768 °C La ferrita puede disolver muy pequeñas cantidades
de carbono.
• Entre 911 y 1400 °C cristaliza en el sistema cúbico centrado en las
caras (FCC) y recibe la denominación de hierro γ. La austenita se
deforma con mayor facilidad y es paramagnética.
• Entre 1400 y 1538 °C cristaliza de nuevo en el sistema cúbico
centrado en el cuerpo y recibe la denominación de hierro δ que es en
esencia el mismo hierro alfa pero con parámetro de red mayor por
efecto de la temperatura.
A mayor temperatura el hierro se encuentra en estado líquido.
Si se añade carbono al hierro, sus átomos podrían situarse simplemente en los
intersticios de la red cristalina de éste último; sin embargo en los aceros
aparece combinado formando carburo de hierro (Fe3C), es decir, un
compuesto químico definido y que recibe la denominación de cementita.
También podría gustarte
- Metalurgia de La SoldaduraDocumento73 páginasMetalurgia de La SoldaduraWilly Franco Correa Bautista100% (1)
- Diagrama Hierro CarbonoDocumento4 páginasDiagrama Hierro CarbonogcalitoAún no hay calificaciones
- Diagrama Hierro CarbonoDocumento14 páginasDiagrama Hierro CarbonoAnibal Vp100% (1)
- Introducción a la química de los metales de transiciónDe EverandIntroducción a la química de los metales de transiciónAún no hay calificaciones
- Metalurgia de La SoldaduraDocumento43 páginasMetalurgia de La SoldaduraCarlos German Mamani PizarroAún no hay calificaciones
- Diagrama Fe CDocumento3 páginasDiagrama Fe CCarlos Enrique Vina Miranda100% (2)
- Bladesmithing: Secretos del tratamiento térmico de la forja de cuchillosDe EverandBladesmithing: Secretos del tratamiento térmico de la forja de cuchillosAún no hay calificaciones
- Diagrama Hierro CarbonoDocumento20 páginasDiagrama Hierro CarbonoJhon AcevedoAún no hay calificaciones
- ACEROSDocumento30 páginasACEROSSuair DiazAún no hay calificaciones
- Diagrama HierroDocumento2 páginasDiagrama HierroDiego SalazarAún no hay calificaciones
- Tarea 7Documento5 páginasTarea 7JOSE RAMON HERNANDEZ BUSTOSAún no hay calificaciones
- Diagrama HierroDocumento8 páginasDiagrama Hierropineda1505Aún no hay calificaciones
- Diagrama Hierro CarbonoDocumento19 páginasDiagrama Hierro CarbonoCHRISTOPHER JAVIER HUAMANTANO CHUCTAYAAún no hay calificaciones
- Edwin Almanzar - Diagrama Hierro - CarbonoDocumento4 páginasEdwin Almanzar - Diagrama Hierro - Carbonocarolina perezAún no hay calificaciones
- Forma Alotropica HierroDocumento7 páginasForma Alotropica Hierroms_libroAún no hay calificaciones
- Aesthetic Charcoal Managing Brand Tips InfographicDocumento1 páginaAesthetic Charcoal Managing Brand Tips Infographicbrayan martinezAún no hay calificaciones
- DIAGRAMADocumento22 páginasDIAGRAMAMaría Jose Aranza Morales PalafoxAún no hay calificaciones
- TEMA 5 - Transf - Perliticasy MatertensiticasDocumento170 páginasTEMA 5 - Transf - Perliticasy MatertensiticasArien Nacilë ManzanoAún no hay calificaciones
- Presentación DIAGRAMA HIERRO CARBONODocumento17 páginasPresentación DIAGRAMA HIERRO CARBONOAndrea SuarezAún no hay calificaciones
- Tir 215 Aleacion Hierro - Carbono Ciclo 01 2019Documento8 páginasTir 215 Aleacion Hierro - Carbono Ciclo 01 2019Iveth DonoAún no hay calificaciones
- 04 Formas Alotrópicas Fe y CDocumento14 páginas04 Formas Alotrópicas Fe y Cabuelo36Aún no hay calificaciones
- Aleaciones HierroDocumento25 páginasAleaciones HierroMiguel pereyra nuñezAún no hay calificaciones
- Tarea 2.1 5C JFGGDocumento13 páginasTarea 2.1 5C JFGGFernando García Jr.Aún no hay calificaciones
- Polimorfismo y AlotropiaDocumento9 páginasPolimorfismo y Alotropiahector19999Aún no hay calificaciones
- 1 - Estructuras Cristalinas Del HierroDocumento6 páginas1 - Estructuras Cristalinas Del HierroValeria EsserAún no hay calificaciones
- Diagrama de Equilíbrio Fe-CDocumento5 páginasDiagrama de Equilíbrio Fe-CDaniel Ojeda PizarroAún no hay calificaciones
- Practica 7 de Tecnologia.Documento8 páginasPractica 7 de Tecnologia.Alberto CañongoAún no hay calificaciones
- Acerotratamientoscorrosion PDFDocumento19 páginasAcerotratamientoscorrosion PDFpudetoAún no hay calificaciones
- Que Es El Diagrama FeDocumento2 páginasQue Es El Diagrama FeEnrique RamirezAún no hay calificaciones
- Alotropia AceroDocumento6 páginasAlotropia AceroMaribel Bonifaz CcotoAún no hay calificaciones
- Polimorfismo y AlotropiaDocumento11 páginasPolimorfismo y AlotropiaYahaira Ruiz Ortega33% (3)
- Teoria AcerosDocumento31 páginasTeoria Aceroskikin312012Aún no hay calificaciones
- MEC 248 JajaDocumento4 páginasMEC 248 JajaIsmael Arequipa MirandaAún no hay calificaciones
- 10 Aceros Apunte GeneralDocumento28 páginas10 Aceros Apunte GeneralLuis BadoffAún no hay calificaciones
- Aceros Por Publio Galeano PeñaDocumento68 páginasAceros Por Publio Galeano Peñabebonga0% (1)
- Alotropía Del HierroDocumento2 páginasAlotropía Del HierroJorge QUAún no hay calificaciones
- Fases Del AceroDocumento4 páginasFases Del AceroAdrián LH100% (3)
- El Hierro y Sus Aleacione1Documento7 páginasEl Hierro y Sus Aleacione1EduardoVillaAún no hay calificaciones
- Diagrama Hierro - CarbonoDocumento5 páginasDiagrama Hierro - CarbonoSuampy MondragonAún no hay calificaciones
- Diagrama Hierro-CarbonoDocumento7 páginasDiagrama Hierro-CarbonoAlison MedinaAún no hay calificaciones
- Fases Comunes en Aceros y HierrosDocumento7 páginasFases Comunes en Aceros y Hierroseluisito xdAún no hay calificaciones
- Normalización de Las Diferentes Clases de AceroDocumento3 páginasNormalización de Las Diferentes Clases de AceroHenrry TangaAún no hay calificaciones
- Alotropia Del HierroDocumento12 páginasAlotropia Del HierroJhosep Ronald PMAún no hay calificaciones
- Diagrama FCDocumento23 páginasDiagrama FCAndersson Monago MoralesAún no hay calificaciones
- AUSTENITADocumento2 páginasAUSTENITAWalter Capuñay SiesquenAún no hay calificaciones
- Tema 6 - Fundiciones de Hierro-20-2022Documento20 páginasTema 6 - Fundiciones de Hierro-20-2022Victor JuarezAún no hay calificaciones
- Microestructura Fe CDocumento4 páginasMicroestructura Fe CAntonio Almenara LópezAún no hay calificaciones
- En ElDocumento3 páginasEn Elken kanekiAún no hay calificaciones
- Microconstituyentes de Los AcerosDocumento6 páginasMicroconstituyentes de Los AcerosLudmila VasquezAún no hay calificaciones
- Practica 3 Diagrama Fe-CDocumento11 páginasPractica 3 Diagrama Fe-CEmiliano Lozano BuenrrostroAún no hay calificaciones
- Actividad 4 - Tipos de AceroDocumento10 páginasActividad 4 - Tipos de AceroJosé Frank GonzalezAún no hay calificaciones
- Ud 2Documento41 páginasUd 2joseAún no hay calificaciones
- Diagrama HierrocarbonoDocumento2 páginasDiagrama HierrocarbonoCovers JLAún no hay calificaciones
- Leccion 5 Trat TermDocumento55 páginasLeccion 5 Trat TermJorge Andres Aravena OpazoAún no hay calificaciones
- Equipo 5Documento48 páginasEquipo 5nbeyrutAún no hay calificaciones
- El Diagrama de Aleación Hierro-CarbonoDocumento4 páginasEl Diagrama de Aleación Hierro-CarbonoMarianyer RomeroAún no hay calificaciones
- 3 Constituyentes Microscópicos Del Acero ...Documento23 páginas3 Constituyentes Microscópicos Del Acero ...Angelo Bustamante CuadrosAún no hay calificaciones
- Curvas TTTDocumento5 páginasCurvas TTTFranco Salinas VargasAún no hay calificaciones
- Ingeniería de procesos siderúrgicos: La experiencia de AHMSADe EverandIngeniería de procesos siderúrgicos: La experiencia de AHMSAAún no hay calificaciones
- Propiedades MaterialesDocumento12 páginasPropiedades MaterialesAlvaro Jesus Matamoros SegoviaAún no hay calificaciones
- Tema 2 Plan de MantenimientoDocumento22 páginasTema 2 Plan de MantenimientoAlvaro Jesus Matamoros SegoviaAún no hay calificaciones
- Neumatica 141023Documento73 páginasNeumatica 141023Alvaro Jesus Matamoros SegoviaAún no hay calificaciones
- Aleaciones Fe-CDocumento4 páginasAleaciones Fe-CAlvaro Jesus Matamoros SegoviaAún no hay calificaciones