Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Informe - SINTESIS ORGÁNICA
Informe - SINTESIS ORGÁNICA
Cargado por
Alejandra Velasquez Buitrago0 calificaciones0% encontró este documento útil (0 votos)
47 vistas2 páginasEste documento resume los resultados de varias síntesis orgánicas realizadas por estudiantes de ingeniería química. Reporta la recristalización de acetanilida con un 61.03% de rendimiento, la extracción de aceite de maní usando soxhlet, y las síntesis y espectros de absorción de la fenolftaleína y la fluoresceína. También describe la preparación de jabón a partir de lípidos y sus propiedades al mezclarse con agua, cloruro de calcio, ácido clorhíd
Descripción original:
Título original
Informe _ SINTESIS ORGÁNICA
Derechos de autor
© © All Rights Reserved
Formatos disponibles
DOC, PDF, TXT o lea en línea desde Scribd
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoEste documento resume los resultados de varias síntesis orgánicas realizadas por estudiantes de ingeniería química. Reporta la recristalización de acetanilida con un 61.03% de rendimiento, la extracción de aceite de maní usando soxhlet, y las síntesis y espectros de absorción de la fenolftaleína y la fluoresceína. También describe la preparación de jabón a partir de lípidos y sus propiedades al mezclarse con agua, cloruro de calcio, ácido clorhíd
Copyright:
© All Rights Reserved
Formatos disponibles
Descargue como DOC, PDF, TXT o lea en línea desde Scribd
0 calificaciones0% encontró este documento útil (0 votos)
47 vistas2 páginasInforme - SINTESIS ORGÁNICA
Informe - SINTESIS ORGÁNICA
Cargado por
Alejandra Velasquez BuitragoEste documento resume los resultados de varias síntesis orgánicas realizadas por estudiantes de ingeniería química. Reporta la recristalización de acetanilida con un 61.03% de rendimiento, la extracción de aceite de maní usando soxhlet, y las síntesis y espectros de absorción de la fenolftaleína y la fluoresceína. También describe la preparación de jabón a partir de lípidos y sus propiedades al mezclarse con agua, cloruro de calcio, ácido clorhíd
Copyright:
© All Rights Reserved
Formatos disponibles
Descargue como DOC, PDF, TXT o lea en línea desde Scribd
Está en la página 1de 2
LABORATORIOS DE QUÍMICA ORGÁ NICA
Peso de cristales con humedad: 1.296 g
Peso de cristales secos: 0.791 g
SINTESIS ORGÁNICA % recuperación: (0.791/1.296)*100= 61.033
Alejandra Velásquez, David Andrés Mena Marín 1.2) Extracción de soxhlet:
Ingeniería química (Segundo semestre), Ingeniería Maní empleado: 27.715 g
química (Séptimo semestre) Aceite obtenido:
alvelasquezbu@unal.edu.co, damenam@unal.edu.co
2) Síntesis de ftaleínas
RESULTADOS:
2.1) Síntesis de Fenolftaleína:
1) Recristalización de acetanilida y Extracción con
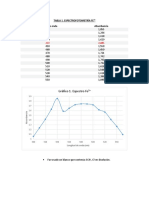
Al correr el espectro de la fenolftaleína en pH acido se observa
soxhlet
su mayor absorbancia a una longitud de onda de 558 nm:
Fenolftaleína acida (500 -
1.1) Síntesis de acetanilida:
600nm)
Longitud de onda (nm) Absorbancia
500 0.168
510 0.200
520 0.250
530 0.296
540 0.380
550 0.470
558 0.515
560 0.510
570 0.381
580 0.236
590 0.102
Cant/ Anili Anhíd Acetan Acetanili rendimi 600 0.059
compuest na rido ilida da ento
o acétic (teóric (experim
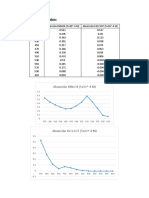
En medio básico el pico se observa en los 442 nm; con una
o a) ental
(masa 93.1 102.09 135.17 absorbancia de 0.900
molar 3
g/mol) Fenolftaleína básica (430 -
Densidad( 1.02 1.08 X X 55.23% 530nm)
g/ml) Longitud de onda (nm) Absorbancia
(ml) 1 1 X X % 430 0.681
recuper 440 0.888
ación
442 0.900
(moles) 0.01 0.0106 0.0106
09 61.03% 450 0.725
(g) 1.02 1.08 1.4328 0.791 460 0.346
470 0.089
Acetanilida experimental: 480 0.042
490 0.027
Peso total: 36.078 g 500 0.021
Peso vidrio de reloj: 34.962 g 510 0.019
Peso papel de filtro: 0.325 g 520 0.016
Peso acetanilida: 0.791 g 524 0.016
530 0.015
% de recuperación:
Reactividad de compuestos orgá nicos, Universidad Nacional de Colombia Sede Medellín
Profesor responsable: Samuel Vizcaíno Pá ez, svizcainop@unal.edu.co
LABORATORIOS DE QUÍMICA ORGÁ NICA
2.2) Síntesis de Fluoresceína:
La fluoresceína en medio básica muestra una mayor
absorbancia (1.339) en 494nm
Fluoresceína básica (430-
530 nm)
430 0.084
440 0.136
450 0.238
460 0.388
470 0.566
480 0.766
490 1.243
494 1.339
500 1.213
510 0.606
520 0.132
530 0.038
3) Lípidos: preparación de jabón
Propiedades del jabón:
Al mezclar el jabón con agua se observa la aparición de
espuma que prevalece después de la agitación.
Al mezclar el jabón con Cloruro de calcio (CaCl 2) se
forma un precipitado blanco.
Al mezclar el jabón con HCl no se observa la aparición
de espuma; la solución se torna de un color blanco turbio
sin presencia de precipitado
Al mezclar el jabón con CuSO 4 se forma una espuma
que no prevalece después de la agitación.
Reactividad de compuestos orgá nicos, Universidad Nacional de Colombia Sede Medellín
Profesor responsable: Samuel Vizcaíno Pá ez, svizcainop@unal.edu.co
También podría gustarte
- Determinación de Azul de TimolDocumento11 páginasDeterminación de Azul de TimolMiguel Jesus Antonio BobadillaAún no hay calificaciones
- Informe Práctica Analisis Cuantitativo de Colorante en Un Baño Textil Por Uv-VisDocumento10 páginasInforme Práctica Analisis Cuantitativo de Colorante en Un Baño Textil Por Uv-VisYubely MartinezAún no hay calificaciones
- Reporte 9 Cinetica de Adsorción de AntocianinasDocumento9 páginasReporte 9 Cinetica de Adsorción de AntocianinasRodrigo Colin HerreraAún no hay calificaciones
- Reporte 9Documento10 páginasReporte 9Dante FlowersAún no hay calificaciones
- Lab 4 Determinación de FeDocumento8 páginasLab 4 Determinación de FeJuan Varg ReAún no hay calificaciones
- Determinación Espectrofotométrica de Azul de Timol Mediante Curva de Calibración de Estándar ExternoDocumento12 páginasDeterminación Espectrofotométrica de Azul de Timol Mediante Curva de Calibración de Estándar ExternoBrenda KarenAún no hay calificaciones
- Antocianinas - Julio 2021Documento6 páginasAntocianinas - Julio 2021Rosa Carbajal telloAún no hay calificaciones
- AntocianinasDocumento6 páginasAntocianinasOrley Aldemar Vera PerezAún no hay calificaciones
- Laboratorio EspectrofotometríaDocumento11 páginasLaboratorio EspectrofotometríaLucho MarulandaAún no hay calificaciones
- Actividad de La Formiato Deshidrogenasa y Nitrato ReductasaDocumento9 páginasActividad de La Formiato Deshidrogenasa y Nitrato ReductasaSandra Shields0% (1)
- Actividad de La Formiato Deshidrogenasa y Nitrato ReductasaDocumento9 páginasActividad de La Formiato Deshidrogenasa y Nitrato ReductasaAlexis Temix ZarateAún no hay calificaciones
- Práctica 1 Bioquímica Estructual 2022BDocumento14 páginasPráctica 1 Bioquímica Estructual 2022BLuz CasteleyroAún no hay calificaciones
- Verificación Del Funcionamiento de Un EspectrofotómetroDocumento6 páginasVerificación Del Funcionamiento de Un EspectrofotómetroNaim GCAún no hay calificaciones
- 1er Repaso QA3LDocumento39 páginas1er Repaso QA3Lanaivonne1912agAún no hay calificaciones
- Informe Instrumental (1) 2020Documento17 páginasInforme Instrumental (1) 2020Luis Espinoza PortuguezAún no hay calificaciones
- Ingeniero de La ReacciónDocumento8 páginasIngeniero de La ReacciónBryan HurtadoAún no hay calificaciones
- PRÁCTICA 1 Bioquímica EstructuralDocumento10 páginasPRÁCTICA 1 Bioquímica EstructuralAlejaandra RoodriguezAún no hay calificaciones
- Balance de FermentacionDocumento7 páginasBalance de FermentacionKevinVerdiDiLanterneAún no hay calificaciones
- Informe #4 AnalisisDocumento6 páginasInforme #4 AnalisisSAYRA SCHMITT SÁNCHEZ PEÑAAún no hay calificaciones
- Informe 11Documento12 páginasInforme 11Dennis Ñaupari SalinasAún no hay calificaciones
- Practica #4 TerminadoDocumento6 páginasPractica #4 Terminadomarco antonioAún no hay calificaciones
- Laboratorio EspectofotometriaDocumento9 páginasLaboratorio EspectofotometriaLucho MarulandaAún no hay calificaciones
- Analisis Instrumental - Absorción MolecularDocumento12 páginasAnalisis Instrumental - Absorción MolecularFabian Alexis Klener YañezAún no hay calificaciones
- Aplicaciones EspectrofotometricasDocumento11 páginasAplicaciones EspectrofotometricasSofia Leon CastanedaAún no hay calificaciones
- Lab Espectrofotometria FeDocumento4 páginasLab Espectrofotometria FelarguedasAún no hay calificaciones
- 3 Determinacion de Hierro Por EspectrofDocumento7 páginas3 Determinacion de Hierro Por EspectrofElizabeth RomeroAún no hay calificaciones
- Práctica 14 - Determinación Espectrofotométrica de La Constante de Acidez Del Indicador Químico Verde de BromocresolDocumento16 páginasPráctica 14 - Determinación Espectrofotométrica de La Constante de Acidez Del Indicador Químico Verde de BromocresolDiego Legaspi0% (1)
- Cinetica 9Documento9 páginasCinetica 9GiovanniAún no hay calificaciones
- Parte Experimental-ResultadosDocumento7 páginasParte Experimental-ResultadosYoselin Medina FonsecaAún no hay calificaciones
- Practica 4. ABTDocumento10 páginasPractica 4. ABTIsa Fernández BedoyaAún no hay calificaciones
- Informe Practica Analisis Cuantitativo de Colorante en Un Bano Textil Por Uv Vis PDFDocumento10 páginasInforme Practica Analisis Cuantitativo de Colorante en Un Bano Textil Por Uv Vis PDFmanuela Guzmán ochoaAún no hay calificaciones
- Determinacion de FosforoDocumento10 páginasDeterminacion de FosforoCamila Jackelyne ApazaAún no hay calificaciones
- Reporte de Practica No.5Documento4 páginasReporte de Practica No.5Oz HdzAún no hay calificaciones
- Guia de Ejercicios 2-2018Documento2 páginasGuia de Ejercicios 2-2018Konsuelo RamírezAún no hay calificaciones
- Labo 6 Ino IIIDocumento9 páginasLabo 6 Ino IIIelmerAún no hay calificaciones
- Curva EspectralDocumento1 páginaCurva EspectralgpalaciosmAún no hay calificaciones
- Cálculos y ResultadosDocumento3 páginasCálculos y ResultadosWilbert RuedaAún no hay calificaciones
- DETERMINACION DE HIERRO EN MEDICAMENTOS Final PDFDocumento6 páginasDETERMINACION DE HIERRO EN MEDICAMENTOS Final PDFAndrea Arboleda MonsalveAún no hay calificaciones
- AbsorbanciaDocumento6 páginasAbsorbanciaRosmeryAún no hay calificaciones
- Informe N6 Estabilidad Térmica de EnzimasDocumento7 páginasInforme N6 Estabilidad Térmica de EnzimasVanessa PerezAún no hay calificaciones
- Espectro de Abs y T Del Azul de MetilenoDocumento7 páginasEspectro de Abs y T Del Azul de Metilenomedinakate763Aún no hay calificaciones
- Práctica 1 - Lab. Instrumental FotometriaDocumento7 páginasPráctica 1 - Lab. Instrumental FotometriaAnny Hieraldyn Guapacha CastroAún no hay calificaciones
- Test de BiodegradabilidadDocumento6 páginasTest de BiodegradabilidadHenry GambaAún no hay calificaciones
- Presentación Sistema Múltiple Métodos de Análisis ENCBDocumento14 páginasPresentación Sistema Múltiple Métodos de Análisis ENCBCDL LAún no hay calificaciones
- Práctica No. 3Documento7 páginasPráctica No. 3MICHELLE DANIELA JAIMES POVEDAAún no hay calificaciones
- Determinación de Hierro en Un MedicamentoDocumento6 páginasDeterminación de Hierro en Un MedicamentoMelissa OchoaAún no hay calificaciones
- Práctica Espectroscopia Uv VisibleDocumento6 páginasPráctica Espectroscopia Uv VisibleAmairani JiménezAún no hay calificaciones
- Lab FotosintesisDocumento3 páginasLab FotosintesisDIANA ESTEFANIA ROJAS TORRESAún no hay calificaciones
- GRAFICASDocumento18 páginasGRAFICASDayanaAún no hay calificaciones
- Azul de TimolDocumento10 páginasAzul de TimolArmando Chávez RojasAún no hay calificaciones
- 3MM2 Equipo4 Pract4Documento21 páginas3MM2 Equipo4 Pract4Gilberto BaltazarAún no hay calificaciones
- CALCULOS Y RESULTADOS - Informe 5Documento4 páginasCALCULOS Y RESULTADOS - Informe 5Almendra Herrera ChirreAún no hay calificaciones
- Practica N ° 9Documento10 páginasPractica N ° 9Gedion Gonzales MuchaAún no hay calificaciones
- Cinetica 9Documento9 páginasCinetica 9jonathan H.Aún no hay calificaciones
- Consolidación 2Documento1 páginaConsolidación 2William Andres Avila LopezAún no hay calificaciones
- AbsorbanceDocumento2 páginasAbsorbanceShuvro KunduAún no hay calificaciones
- Sistema MultipleDocumento10 páginasSistema MultipleGuerrillaScribdAún no hay calificaciones
- Informe SiderperuDocumento4 páginasInforme SiderperuMilagrosAún no hay calificaciones
- 04 - Lubrax-Grans-TAC4 SAE 50Documento12 páginas04 - Lubrax-Grans-TAC4 SAE 50prevencion cooperachileAún no hay calificaciones
- Integrador - Tubo y CorazaDocumento14 páginasIntegrador - Tubo y CorazaPablo CabreraAún no hay calificaciones
- Problema 16Documento4 páginasProblema 16Lisseth RoweAún no hay calificaciones
- Modulo Ees38 Iaq 5to 1raDocumento12 páginasModulo Ees38 Iaq 5to 1raErnestina TORRESAún no hay calificaciones
- Proyecto 2 Ciencia de Los MaterialesDocumento4 páginasProyecto 2 Ciencia de Los MaterialesloloAún no hay calificaciones
- Qué Es El MercaptanoDocumento4 páginasQué Es El MercaptanoWilian Merma PumaAún no hay calificaciones
- Fdocuments - Ec - Fisicoquimica 3conceptos TeoricosDocumento74 páginasFdocuments - Ec - Fisicoquimica 3conceptos TeoricosLoresole RissoAún no hay calificaciones
- Riesgos Higienicos Trabajo MonograficoDocumento26 páginasRiesgos Higienicos Trabajo MonograficomasterscannAún no hay calificaciones
- TERMOQUIMICADocumento5 páginasTERMOQUIMICAdjlAún no hay calificaciones
- Contenido Limpieza y Esterilizacion SterisDocumento5 páginasContenido Limpieza y Esterilizacion SterisEster Calle CalleAún no hay calificaciones
- Marco TeoricoDocumento6 páginasMarco TeoricoFranz Gustavo Eca PazosAún no hay calificaciones
- Tarea - 2 - Colaborativo (3) Procesos QuimicosDocumento12 páginasTarea - 2 - Colaborativo (3) Procesos Quimicossoluciones inmediatasAún no hay calificaciones
- Clase I, Aspectos Basicos, Calor I PDFDocumento34 páginasClase I, Aspectos Basicos, Calor I PDFMaria Camila De la RosaAún no hay calificaciones
- RCC Catalogo Momplet 2017 05 Componentes MaquinariaDocumento46 páginasRCC Catalogo Momplet 2017 05 Componentes MaquinariajswampAún no hay calificaciones
- UNIDAD IV. Alquinos y Aromaticos.Documento15 páginasUNIDAD IV. Alquinos y Aromaticos.OrianaAún no hay calificaciones
- Formula Empirica y MolecularDocumento10 páginasFormula Empirica y MolecularYASSER ALDRIC VENECIA CASTILLO ESTUDIANTE ACTIVOAún no hay calificaciones
- Calculo de Espesores y PesosDocumento24 páginasCalculo de Espesores y PesosjlvillaaAún no hay calificaciones
- Aplicaciones Del Tubo de PitotDocumento2 páginasAplicaciones Del Tubo de PitotGonzalo Martinez QuiqueAún no hay calificaciones
- Tabla Equivalencias de Aceros BiltraDocumento4 páginasTabla Equivalencias de Aceros BiltraLUIS BISIERAún no hay calificaciones
- Q AUNI Sem9 DiriDocumento3 páginasQ AUNI Sem9 DiriEdward WhiteAún no hay calificaciones
- Ejercicio Modulo 2Documento4 páginasEjercicio Modulo 2serviciosgenerales.hen2023Aún no hay calificaciones
- PRÁCTICA N 4 SO2Documento4 páginasPRÁCTICA N 4 SO2Marce Rafael AtapomaAún no hay calificaciones
- Muñoz San EmeterioDocumento441 páginasMuñoz San EmeterioCAMILA CHAVEZ PEREDOAún no hay calificaciones
- Eutéctico, Peritéctico y MonotécticoDocumento2 páginasEutéctico, Peritéctico y MonotécticoMiguel Angel López NavarreteAún no hay calificaciones
- Prueba - Diagnóstico - Ciencias - Naturales - Primer Año BachilleratoDocumento17 páginasPrueba - Diagnóstico - Ciencias - Naturales - Primer Año BachilleratoartomasterAún no hay calificaciones
- Contenidos de Lo Libros de BachilleratoDocumento12 páginasContenidos de Lo Libros de BachilleratoLaura MasseAún no hay calificaciones
- Ecoenergía TrípticoDocumento2 páginasEcoenergía TrípticoVidal BarbozaAún no hay calificaciones
- Diapositivas Formulación OrgánicaDocumento12 páginasDiapositivas Formulación OrgánicaAlexBerCondoriCarrilloAún no hay calificaciones