Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Purificación de ácido acetilsalicílico (Aspirina) mediante recristalización
Cargado por
Nicole Azcui0 calificaciones0% encontró este documento útil (0 votos)
10 vistas5 páginasINFORME PH
LABORATORIO QMC 100
FACULTAD DE INGENIERIA UMSA
Título original
INFORME 7 PH
Derechos de autor
© © All Rights Reserved
Formatos disponibles
DOCX, PDF, TXT o lea en línea desde Scribd
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoINFORME PH
LABORATORIO QMC 100
FACULTAD DE INGENIERIA UMSA
Copyright:
© All Rights Reserved
Formatos disponibles
Descargue como DOCX, PDF, TXT o lea en línea desde Scribd
0 calificaciones0% encontró este documento útil (0 votos)
10 vistas5 páginasPurificación de ácido acetilsalicílico (Aspirina) mediante recristalización
Cargado por
Nicole AzcuiINFORME PH
LABORATORIO QMC 100
FACULTAD DE INGENIERIA UMSA
Copyright:
© All Rights Reserved
Formatos disponibles
Descargue como DOCX, PDF, TXT o lea en línea desde Scribd
Está en la página 1de 5
UMSA QUIMICA 200L
GRUPO: D
FACULTAD DE INGENIERIA
GESTION: 2/2021
INGENIERIA QUIMICA
Apellidos y Nombres Azcui Bustillos Nicole Fabiana
Fecha de realización de la practica Miércoles, 18 de Agosto de 2021
Fecha de entrega Lunes, 23 de Agosto de 2021
CUESTIONARIO #1
1. En la purificación de un sólido por re cristalización en un
disolvente, ¿Qué es más aconsejable, enfriar la solución rápida o
lentamente? Explique.
Se debe hacer enfriar lentamente para formar cristales grandes y lograr
mayor pureza sin que intervengan otras partículas en la re cristalización.
2. ¿Sería adecuado la succión a través de un buchner para filtrar un a
disolución en que se haya utilizado el éter como disolvente?
No es adecuado ya que se perdería muchos cristales en el filtro
3. ¿Qué ventajas presenta el agua como disolvente de re
cristalización? ¿Qué ventajas tendrá el tetracloruro de carbono
sobre el éter y el benceno?
El agua es polar, no es volátil, no es inflamable y disuelve fácilmente las
sustancias polares mientras que el tetracloruro es una sustancia no polar
que disuelve sustancias no polares, mientras que el éter es volátil y el
benceno toxico.
4. Porque es importante reducir al mínimo la evaporación del
disolvente durante la filtración de una solución caliente?
Porque el disolvente el disolvente al evaporarse necesita una cantidad de
calor para cambiar de estado líquido a gaseoso, por lo tanto al reducir la
evaporación, se evita la perdida de calor del sistema, el mismo que es
necesario para que la muestra no se enfrié tan rápidamente, de ese modo
los cristales no taparan el filtro.
5. Cuando se filtra un sólido por succión en buchner ¿Por qué se debe
interrumpir la succión antes de cerrar la trompa de agua?
Para evitar la inundación del sistema provocada por el vacío.
6. Prediga razonablemente que compuesto de cada pareja será más
soluble en agua y éter
Acido oxálico: polar, disuelve en agua
Glioxal: polar, disuelve en agua
Etilendiamina: polar, disuelve en agua
Tetra metil etilendiamina: no polar, disuelve en éter
Acido malonico: polar disuelve en agua
Malonato de etilo: no polar disuelve en éter
Glicerina: polar disuelve en agua
Trimetileter: no polar disuelve en éter
7. ¿Por qué debe cerrarse ambos extremos del tubo capilar cuando se
determina el punto de fusión de un compuesto que sublima?
Para que no exista perdida de sustancia debido a la sublimación
8. Se determina experimental mente el punto de fusión de un
compuesto puroconocido x resultando este comprendido en el
intervalo 158-159 °c. a continuación se determinan los puntos de
fusión en cada caso.
-Punto de fusión de una mezcla de x con el acido salicilico (Punto de fusión
1589c)130-135 c.
- Punto de fusión de x con benzamilida (Punto de fusión 160% )158-159%
-Punto de fusión de una mezcla de x con p-metilbenzalamina (Punto de
fusión 160 c) 158-159⁹c.
Con benzamilida es el mismo de allí q es este compuesto
Mientras que con p-metilbenzalamina x esta en mayor cantidad.
9. ¿Qué comprimidos analgésicos traen acido metil salicílico?
Principalmente la aspirina y el paracetamol.
10. Si el compuesto a recristalizar es el ácido acetilsalicilico en un
compuesto analgésico cuáles serán las impurezas?
La impureza más común será, sin embargo, el propio ácido salicílico que
provendrá de una acetilación incompleta o de la hidrólisis del producto
durante su aislamiento. La presencia de producto hidrolizado se detecta
fácilmente por el olor a ácido acético y se puede analizar mediante ensayo
con FeCl3, ensayo de fenoles. El producto hidrolizado se eliminará a lo
largo del proceso de purificación y en la recristalización final del producto.
11. ¿Cuál es la estructura del ácido acetil salicilico?
12. Señale las funciones orgánicas que se pueden identificar en la
formula molecular de este compuesto
Presenta un anillo benzenico y dos grupos carboxilo
13. Consulte las propiedades físicas del ácido acetilsalicilico
Su punto de fusión es de 138°c y el de ebullición de 140°c su solubilidad en
agua es de 1mg/ml a 20°c densidad de 1.4 g/ml..
14. ¿Qué es una hidrolisis?
Es un proceso en el cual el agua actua para formar nuevos iones o nuevos
compuestos.
15. Consulte las propiedades fisicas del ácido salicilico
Su punto de fusión es de 158.5%c, punto de ebullición 211e, es incoloro.
16. Explique el fenómeno de coprecipitación
Es la formación de compuestas insolubles, paralelos al compuesto que se
desea purificar
17. en donde se pueden encontrar las tablas de solubilidad de
compuestos?
Las tablas de solubilidad se pueden encontrar en libros que traten de la
materia y se la expresa como la cantidad máxima de soluto, que se puede
disolver en cierta cantidad de disolvente a cierta temperatura.
18. es mejor obtener cristales pequeños o grandes? ¿Qué
procedimiento se utiliza para obtener cristales pequeños o grandes?
Es lo mejor obtener cristales grandes, para los cual necesitamos un
enfriamiento lento
19. Explique porque para evitar las reacciones de hidrolisis se puede
purificar con un sistema de purificación en alcohol y precipitando en
agua o bien utilizando una mezcla de solventes con ácido acético y
agua. Explique como lo haría experimentalmente.
El alcohol no reaccionara con el compuestos purificar, el ácido acético no
reaccionara en hidrolisis y si sucede seria muy pequeña, pues el ácido
interviene en la reacciones de hidrolisis
20. Se le ha encomendado purificar la sustancia A, para lo cual
dispones de los solventes x, y, vz,con las siguientes propiedades
¿Cuál de todos ellos consideras el más adecuado?
El más adecuado es 2 pues su solubilidad en frio es mínima y la solubilidad
en caliente es máxima.
21. ¿Por qué se debe filtrar en caliente y el embodo de vidrio al igual
que el matraz donde recibe el filtrado debe estar previamente
calentados?
Para evitar precipitaciones en el filtrado con el descenso de la temperatura.
MATERIALES Y REACTIVOS
-0,1-0,2 g de cristales secos -15 ml de agua destilada
-Una espátula -Un calefactor
-Tubo de ensayo -Un filtro de pliegues
-Un mortero -Un embudo de gravitación
de vástago corto
-Dos tubos capilares
(precaución: los tubos -Un vaso de precipitados de
capilares son muy frágiles) 100 ml
-Tubo de thiele -Varilla de vidrio
-Ácido acetilsalicilico -Acetona
(aspirina)
-Aspirina
-10 ml de etanol.
-Termo regulado
-Un filtro de pliegues -Un vaso precipitado de 500
ml con agua y hielo.
-Un embudo de gravitación
de vástago corto que -Un buchner
anteriormente debe ser
-Una balanza analítica
calentado.
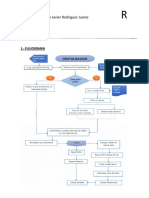
DIAGRAMA DE FLUJO.
También podría gustarte
- Mi Primer Pecera Todo lo que Necesitas Saber para Iniciarte en el Cuidado de los PecesDe EverandMi Primer Pecera Todo lo que Necesitas Saber para Iniciarte en el Cuidado de los PecesAún no hay calificaciones
- Pre Informe RecristalizacionDocumento6 páginasPre Informe RecristalizacionPAOLA ANDREA QUENALLATA CHIPANAAún no hay calificaciones
- Solucionario de Cuestionario de RecristalizacionDocumento3 páginasSolucionario de Cuestionario de RecristalizacionCz Ar81% (16)
- Cuestionario 1 QMC-200Documento5 páginasCuestionario 1 QMC-200marco asturizagaAún no hay calificaciones
- Recristalización y puntos de fusiónDocumento4 páginasRecristalización y puntos de fusiónRocio Andrea CasillaAún no hay calificaciones
- Practica 05 Determinacion de AldehidosDocumento3 páginasPractica 05 Determinacion de AldehidosGabriela Elisa Inca Martinez100% (1)
- Puntos de fusión y recristalización del ácido acetilsalicílicoDocumento5 páginasPuntos de fusión y recristalización del ácido acetilsalicílicoLuis Angel Chura100% (1)
- Práctica Química Orgánica 2018Documento9 páginasPráctica Química Orgánica 2018Ingrid PuertoAún no hay calificaciones
- Pre Informe Lab Cristalizacion y P.F.Documento10 páginasPre Informe Lab Cristalizacion y P.F.Sonia CastilloAún no hay calificaciones
- Recristalizacion y Puntos e FusionDocumento12 páginasRecristalizacion y Puntos e FusionAlvaro SierraAún no hay calificaciones
- Practica No.3 RecristalizaciónDocumento6 páginasPractica No.3 RecristalizaciónMontiel Luna AxelAún no hay calificaciones
- Pinf Recristalizacion Punto de FusionDocumento13 páginasPinf Recristalizacion Punto de FusionOscar Gabriel Miranda CallisayaAún no hay calificaciones
- Practica 7 y 8Documento6 páginasPractica 7 y 8DinaAún no hay calificaciones
- Cristalización de sustancias orgánicasDocumento15 páginasCristalización de sustancias orgánicasMery HuamanAún no hay calificaciones
- Cuestionario #1Documento4 páginasCuestionario #1Rocio Andrea CasillaAún no hay calificaciones
- Obtención y purificación del ácido acetilsalicílico mediante cristalizaciónDocumento8 páginasObtención y purificación del ácido acetilsalicílico mediante cristalizaciónMatias HernandezAún no hay calificaciones
- Informe 02 de Quimica OrganicaDocumento12 páginasInforme 02 de Quimica OrganicaDenisseAún no hay calificaciones
- Informe 02 de Quimica OrganicaDocumento12 páginasInforme 02 de Quimica OrganicaDenisse0% (2)
- Practica #4 Recristalización de Compuestos OrgánicosDocumento4 páginasPractica #4 Recristalización de Compuestos OrgánicosFelipe PinzonAún no hay calificaciones
- Laboratorio de Química Orgánica 3-UNMSMDocumento11 páginasLaboratorio de Química Orgánica 3-UNMSMSARA CHACPI ALFAROAún no hay calificaciones
- Practica 2 Cristalización SimpleDocumento7 páginasPractica 2 Cristalización SimpleGiovanny Tapia Carlos0% (1)
- Lab. Quimica 100Documento19 páginasLab. Quimica 100yariAún no hay calificaciones
- RESUMENDocumento20 páginasRESUMENAlejandro CortezAún no hay calificaciones
- Práctica 18:: Aislamiento Y Purificación Del Principio Activo de Un Fármaco ComercialDocumento20 páginasPráctica 18:: Aislamiento Y Purificación Del Principio Activo de Un Fármaco Comercial874089 874089Aún no hay calificaciones
- Aislamiento aceites esencialesDocumento8 páginasAislamiento aceites esencialesSamuel Callejas ConcepcionAún no hay calificaciones
- Sintesis de AcetanilidaDocumento9 páginasSintesis de AcetanilidaRivera Pabletz100% (1)
- Informe de Orgánica 2Documento14 páginasInforme de Orgánica 2edmundoAún no hay calificaciones
- Informe Nº01Documento6 páginasInforme Nº01Anonymous ZyVgMCraeAún no hay calificaciones
- Estereoisomería CisDocumento4 páginasEstereoisomería CisMaria JaraAún no hay calificaciones
- Informe de Laboratorio de Química Orgánica II: Síntesis de La AcetanilidaDocumento8 páginasInforme de Laboratorio de Química Orgánica II: Síntesis de La AcetanilidaCarolina Sánchez75% (20)
- Prac-Quimica Orgii-Nuevo 1Documento28 páginasPrac-Quimica Orgii-Nuevo 1Jesus Manuel DiazAún no hay calificaciones
- DAV AguaDocumento9 páginasDAV AguaAimee GutiérrezAún no hay calificaciones
- Practica Nº2 Operaciones BasicasDocumento5 páginasPractica Nº2 Operaciones BasicasQUÍMICA0% (1)
- P4 Sintesis y Recristalizacion de La Acetanilida - 23-24Documento10 páginasP4 Sintesis y Recristalizacion de La Acetanilida - 23-24Noelia GuayasAún no hay calificaciones
- Destilacion TPDocumento9 páginasDestilacion TPEster BritoAún no hay calificaciones
- Síntesis y análisis de acetilenoDocumento3 páginasSíntesis y análisis de acetilenoSulmy Olivera zeladaAún no hay calificaciones
- Determinacion de CristalizacionDocumento9 páginasDeterminacion de CristalizacionCristian Orozco ChavezAún no hay calificaciones
- Informe Practica IVDocumento4 páginasInforme Practica IVDiego Alejandro Muñoz LizcanoAún no hay calificaciones
- 3.practica 3Documento14 páginas3.practica 3Nitgma Dc0% (1)
- Practica Laboratorio 02Documento7 páginasPractica Laboratorio 02Alejandro León100% (1)
- CRISTacetanilidaDocumento3 páginasCRISTacetanilidaAlex EscobarAún no hay calificaciones
- Manual Organica Iii Con CuestionarioDocumento20 páginasManual Organica Iii Con CuestionarioMaryfer M. BeltranAún no hay calificaciones
- CRISTALIZACIONDocumento9 páginasCRISTALIZACIONLemon TeaAún no hay calificaciones
- Reporte de Resultados Laboratorio 2023-1 Semana5Documento5 páginasReporte de Resultados Laboratorio 2023-1 Semana5Ana BelenAún no hay calificaciones
- Extracción y purificación de ácido acetil salicílico a partir de aspirinaDocumento10 páginasExtracción y purificación de ácido acetil salicílico a partir de aspirinaOmar Martinez CastroAún no hay calificaciones
- Purificacion de Los Solidos Por CristalizacionDocumento9 páginasPurificacion de Los Solidos Por CristalizacionSantiago CuellarAún no hay calificaciones
- Informe 5 - Recristalizacion de Productos OrganicosDocumento10 páginasInforme 5 - Recristalizacion de Productos OrganicosCarlos MenesesAún no hay calificaciones
- Laboratorio Recristalizacion UnmsmDocumento8 páginasLaboratorio Recristalizacion UnmsmElizabethVargasAún no hay calificaciones
- Espejo de PlataDocumento2 páginasEspejo de PlataMaria Pilar Campos EscobarAún no hay calificaciones
- CristalizaciónDocumento12 páginasCristalizaciónLisbeth Alvarez SantillànAún no hay calificaciones
- Informe 2Documento14 páginasInforme 2Ortega Vilca Tabita RebecaAún no hay calificaciones
- Informe de Laboratorio #2 NuevoDocumento4 páginasInforme de Laboratorio #2 NuevoSARA MANUELA ANGEL CAROAún no hay calificaciones
- Re 10 Lab 021 001 Quimica Organica II 1Documento41 páginasRe 10 Lab 021 001 Quimica Organica II 1JhennyAún no hay calificaciones
- Síntesis de ÉsteresDocumento7 páginasSíntesis de ÉsteresIsbell Dayana Quispe CárdenasAún no hay calificaciones
- P.1. Obtencion de Halogenuros de Alquilo (Cloruro de Terbutilo)Documento4 páginasP.1. Obtencion de Halogenuros de Alquilo (Cloruro de Terbutilo)jennychoqueurey100% (2)
- Hidrodestilación extracta aceite esencialDocumento2 páginasHidrodestilación extracta aceite esencialLuis Enrique Muñoz OrtegaAún no hay calificaciones
- Practica 4 Métodos de SeparaciónDocumento7 páginasPractica 4 Métodos de SeparaciónNicolleAún no hay calificaciones
- La pintura sobre tela II: Alteraciones, materiales y tratamientos de restauraciónDe EverandLa pintura sobre tela II: Alteraciones, materiales y tratamientos de restauraciónCalificación: 5 de 5 estrellas5/5 (4)
- Acuarios para dummies (guía de iniciación a la acuariofilia)De EverandAcuarios para dummies (guía de iniciación a la acuariofilia)Aún no hay calificaciones
- RadarDocumento5 páginasRadarNicole AzcuiAún no hay calificaciones
- Teoria de La Energia MecanicaDocumento5 páginasTeoria de La Energia MecanicaNicole AzcuiAún no hay calificaciones
- Preinforme Hidrocarburos AromaticosDocumento2 páginasPreinforme Hidrocarburos AromaticosNicole AzcuiAún no hay calificaciones
- Ley de HookeDocumento5 páginasLey de HookeNicole AzcuiAún no hay calificaciones
- Preinforme Hidrocarburos AlifaticoDocumento2 páginasPreinforme Hidrocarburos AlifaticoNicole AzcuiAún no hay calificaciones
- Movimiento en Una Dimensión Azcui Bustillos Nicole FabianaDocumento15 páginasMovimiento en Una Dimensión Azcui Bustillos Nicole FabianaNicole AzcuiAún no hay calificaciones
- RECRISTALIZACION Y PUNTOS DE FUSION FinalDocumento9 páginasRECRISTALIZACION Y PUNTOS DE FUSION FinalNicole AzcuiAún no hay calificaciones
- Preinforme 2 QMC104LDocumento10 páginasPreinforme 2 QMC104LNicole AzcuiAún no hay calificaciones
- Colisiones BidimensionalesDocumento10 páginasColisiones BidimensionalesNicole AzcuiAún no hay calificaciones
- Cromatografia PreinformeDocumento5 páginasCromatografia PreinformeNicole AzcuiAún no hay calificaciones
- Informe Tabla PeriodicaDocumento21 páginasInforme Tabla PeriodicaNicole Azcui100% (1)
- Generación de TrayectoriaDocumento16 páginasGeneración de TrayectoriaKevin Daniel Espinoza MoralesAún no hay calificaciones
- Labo5 - MáquinasDocumento5 páginasLabo5 - MáquinasCarlos HernándezAún no hay calificaciones
- Conservación de la cantidad de movimientoDocumento14 páginasConservación de la cantidad de movimientoPool MauricioAún no hay calificaciones
- 2019 Spanish Uni-Line Catalog SMDocumento311 páginas2019 Spanish Uni-Line Catalog SMAlexis TenaAún no hay calificaciones
- Aletas TallerDocumento16 páginasAletas TallerJOSE LEONARDO SANTANA PACHECOAún no hay calificaciones
- Universidad NacionalDocumento3 páginasUniversidad NacionalPercy Torres Avalos KeplerAún no hay calificaciones
- Formato de Informe IluminaciónDocumento8 páginasFormato de Informe IluminaciónLUIS DANIEL ESCAMILLA ROJASAún no hay calificaciones
- Manual Cinta CaminadoraDocumento25 páginasManual Cinta CaminadoraCarlos Alfredo Llanos RamirezAún no hay calificaciones
- GRUPO 5 - Actividades Colaborativas - Semana 1Documento7 páginasGRUPO 5 - Actividades Colaborativas - Semana 1ericka sanchez aguirreAún no hay calificaciones
- Modelo Ieee PararrayoDocumento17 páginasModelo Ieee PararrayoDiego Alejandro Vera SuarezAún no hay calificaciones
- Guia 3 Movimiento SemiparabolicoDocumento2 páginasGuia 3 Movimiento SemiparabolicoAnyuli Salgado RomeroAún no hay calificaciones
- Ruta de Distribución ExponencialDocumento8 páginasRuta de Distribución Exponenciallisbeth yurmila Lolo RomanAún no hay calificaciones
- Fenix PDFDocumento47 páginasFenix PDFGonzalo Alejandro QHAún no hay calificaciones
- Sea Psiquico FinalDocumento241 páginasSea Psiquico FinalFernando Javier LeivaAún no hay calificaciones
- Problemas Oxidación y CorrosiónDocumento8 páginasProblemas Oxidación y CorrosiónPablo Merino DeniaAún no hay calificaciones
- Ejercicio 2 FisicaDocumento13 páginasEjercicio 2 FisicaKenny MárquezAún no hay calificaciones
- Unidad 5-1Documento14 páginasUnidad 5-1Luis Jose Senton CanaveriAún no hay calificaciones
- Induccion MagneticaDocumento8 páginasInduccion MagneticaTANIA ALVARADO -1202013100% (1)
- 4 Balanza Electronico Mezcladora de Sangre Modero CM735Documento1 página4 Balanza Electronico Mezcladora de Sangre Modero CM735E Alejandro G GarciaAún no hay calificaciones
- Ciencia-Mostra-Primera-edicion-SoberaniaDocumento53 páginasCiencia-Mostra-Primera-edicion-SoberaniamagfvaldezAún no hay calificaciones
- Crucigrama 2020Documento8 páginasCrucigrama 2020Roger Rea MincholaAún no hay calificaciones
- Test Terreno Respuestas 17 PreguntasDocumento4 páginasTest Terreno Respuestas 17 PreguntasJimenez PJAún no hay calificaciones
- 2017 Maestría FV Unidad IV Sistemas AisladosDocumento166 páginas2017 Maestría FV Unidad IV Sistemas AisladosDanyJimenez100% (1)
- Ejercicios-Integracion Por Partes-Tania Barcenas PDFDocumento3 páginasEjercicios-Integracion Por Partes-Tania Barcenas PDFtania barcenasAún no hay calificaciones
- TEO1 ProgramDocumento1 páginaTEO1 ProgramEdwien FtsAún no hay calificaciones
- Trayectorias Ortogonales y OblicuasDocumento4 páginasTrayectorias Ortogonales y OblicuasRonal Molina VergaraAún no hay calificaciones
- Teoremas integrales de Cauchy y Cauchy-GoursatDocumento3 páginasTeoremas integrales de Cauchy y Cauchy-GoursatJosephAún no hay calificaciones
- GP1 Sol HGU1Documento8 páginasGP1 Sol HGU1Renato Calderon AlarconAún no hay calificaciones
- S01.s1 - TIPOS Y OPERACIONES CON MATRICESDocumento20 páginasS01.s1 - TIPOS Y OPERACIONES CON MATRICESJason RodriguezAún no hay calificaciones
- Foro VeDocumento2 páginasForo VestevenAún no hay calificaciones