Documentos de Académico
Documentos de Profesional
Documentos de Cultura
2021 IT1 V1 Manzur Recalde
Cargado por
Tomas RecaldeDescripción original:
Título original
Derechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
2021 IT1 V1 Manzur Recalde
Cargado por
Tomas RecaldeCopyright:
Formatos disponibles
Informe Técnico Nro 1
Determinación
experimental de las
Aeronáutica General propiedades atmosféricas
del aire
Determinación experimental de las propiedades
atmosféricas del aire
Manzur Mayuli, Juan Sebastián – Recalde, Tomás1
Martes 30 de marzo de 2021
Resumen
El presente trabajo de laboratorio se basó en la determinación experimental de la densidad del aire mediante la
utilización de un barómetro para mediciones de presión y haciendo uso de la ecuación de estado de los gases
perfectos. Los datos utilizados en el mismo fueron proporcionados por la cátedra de Aeronáutica General de la
Facultad de Ciencias Exactas, Físicas y Naturales de la Universidad Nacional de Córdoba.
Palabras claves: Densidad, barómetro, ecuación de Estado.
Abstract
The following laboratory report aimed to experimentally determine the air density by the use of a barometer to
measure pressure and using the ideal gas law. The data was given by the Cathedra “Aeronáutica General” of the
“Facultad de Ciencias Exactas, Físicas y Naturales de la Universidad Nacional de Córdoba”.
Keywords: density, Barometer, Ideal gas law.
1 jmanzur65@mi.unc.edu.ar
tomasrecalde@mi.unc.edu.ar
Manzur Mayuli, Juan Sebastián – Recalde, Tomás Página 1 de 5
Informe Técnico Nro 1
Determinación
experimental de las
Aeronáutica General propiedades atmosféricas
del aire
Lista de unidades
• °C unidad de temperatura Celsius
• J unidad de energía
• K unidad de temperatura absoluta
• kg unidad de masa
• kg/m3 unidad de densidad
• mmHg unidad de presión
• Pa unidad de presión
1. Introducción
Utilizamos la ecuación de estado de los gases perfectos:
P
= (1)
RT
Si bien el aire no es un gas ideal, aquí suponemos que se comporta como tal, y que está compuesto
solamente por Oxígeno (21%) y Nitrógeno (78%). Esto es así ya que los valores brindados de presión y
temperatura se encuentran alejados de los puntos críticos, por lo tanto, es válido afirmar que los choques
de las moléculas son elásticos y sin pérdida de energía. Consideramos, además, aire sin humedad .
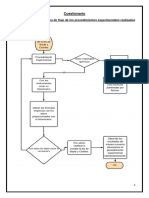
2. Descripción y esquema de la instalación experimental utilizada
El equipo utilizado para la realización del primer trabajo de laboratorio fue un barómetro, instrumento cuyo
objetivo tiene la medición de la presión atmosférica. Dicho instrumento fue inventado por Evangelista
Torricelli en el siglo XVII, y en la actualidad son muchas las variantes que se pueden encontrar.
El utilizado en el práctico fue un barómetro de mercurio. Este está formado por un tubo de vidrio, cerrado
en la parte superior y abierto en la inferior. Su funcionamiento radica en el hecho de llenar el tubo de vidrio
con un líquido, en este caso de mercurio, invertirlo, y acto seguido colocarlo por el extremo que se
encuentra abierto en un recipiente que contiene el mismo líquido. Gracias a la diferencia de presiones, se
puede observar como el mercurio que se encuentra en el tubo comienza a descender, dejando un espacio
vacío en su extremo superior. De esta manera, se puede obtener un valor de la presión atmosférica leyendo
la altura de columna de mercurio encerrada en el tubo de vidrio.
Manzur Mayuli, Juan Sebastián – Recalde, Tomás Página 2 de 5
Informe Técnico Nro 1
Determinación
experimental de las
Aeronáutica General propiedades atmosféricas
del aire
Figura 1: Experimento y Barómetro de mercurio de Torricelli
3. Metodología
Teniendo en cuenta el funcionamiento del barómetro, procedemos como sigue:
I. Llevamos la corredera inferior al cero de nuestra escala graduada y lo fijamos.
II. Enrasamos el menisco inferior, subiendo o bajando el nivel de la cuba de forma que quede
tangente al filo, una vez que el mercurio se estabilizó.
III. Ajustamos la corredera del visor con el menisco superior.
IV. La altura barométrica es tomada como la diferencia de alturas entre los meniscos con la ayuda del
tornillo micrométrico de la corredera del visor superior.
V. Con las tablas provistas por el fabricante se corrige la medición. (Ver “4. Resultados”).
VI. La temperatura es medida directamente del termómetro.
VII. La medición final se expresa en unidades del SIMELA con la incertidumbre correspondiente. (Ver
“4. Resultados”).
4. Resultados
I.Datos Experimentales
• Temperatura = 37.5 ± 0.5 [°C]
• Presión = 726.55 ± 0.05 [mmHg]
Manzur Mayuli, Juan Sebastián – Recalde, Tomás Página 3 de 5
Informe Técnico Nro 1
Determinación
experimental de las
Aeronáutica General propiedades atmosféricas
del aire
II.Corrección de la presión
Usando las tabulaciones de R. Fuess Berlin-Steglitz2 y los datos de la Ciudad de Córdoba:
Figura 2: Planilla de cálculo con correcciones de Presión
III. Pasaje de unidades
𝑇 = 273.15 + 𝑡[𝐾]
𝑇 = 273.15 + (37.5 ± 0.5) = 310.7 ± 0.5[𝐾]
760[mmHg] = 101324.71[𝑃𝑎]
731.26[mmHg] = 𝑃
731.26[mmHg] × 101324.71[𝑃𝑎]
⇒𝑃= = 97479.03[𝑃𝑎]
760[mmHg]
𝑃𝑒: = Apreciación del barómetro
𝑃𝑒 = 0.05[𝑚𝑚𝐻𝑔]
0.05[𝑚𝑚𝐻𝑔] × 101324.71[𝑃𝑎]
𝑃𝑒′[𝑃𝑎] = = 6.66[𝑃𝑎]
760[𝑚𝑚𝐻𝑔]
IV. Cálculo para la determinación de la densidad del aire
97479.70[𝑃𝑎] 𝐾𝑔
𝜌= = 1.093 [ 3 ]
286.9[𝐽/𝑘𝑔𝐾] × 310.65[𝐾] 𝑚
Figura 3: Planilla de cálculo con conversiones y cálculos
V. Cálculo de incertidumbre
𝑃 ∆𝜌 ∆𝑃 ∆𝑇 ∆𝑅
𝜌= ( )= ( )+( )+( ) (2)
𝑅𝑇 𝜌 𝑃 𝑇 𝑅
2
Para la elaboración de la corrección se extrapolan linealmente los datos proporcionados. Se omite la corrección
por menisco.
Manzur Mayuli, Juan Sebastián – Recalde, Tomás Página 4 de 5
Informe Técnico Nro 1
Determinación
experimental de las
Aeronáutica General propiedades atmosféricas
del aire
∆𝑃 ∆𝑇 ∆𝑅
∆𝜌 = 𝜌 [( ) + ( ) + ( )]
𝑃 𝑇 𝑅
Siendo:
∆𝑃 = 𝑃𝑒′ = 𝑎𝑝𝑟𝑒𝑐𝑖𝑎𝑐𝑖𝑜𝑛 𝑑𝑒𝑙 𝑏𝑎𝑟ó𝑚𝑒𝑡𝑟𝑜 = 6.66[𝑃𝑎]
𝑎𝑝𝑟𝑒𝑐𝑖𝑎𝑐𝑖ó𝑛 𝑑𝑒𝑙 𝑡𝑒𝑟𝑚ó𝑚𝑒𝑡𝑟𝑜 1
∆𝑇 = = = 0.5 [𝐾]
2 2
𝐽
∆𝑅 = 0.01 [ ]
𝐾𝑔. 𝐾
Entonces:
6.66 0.5 0.1
∆𝜌 = 1.093 [( )+( )+( )]
97493.03 310.7 286.9
𝐾𝑔
∆𝜌 = 0.0018[ 3 ]
𝑚
Figura 4: Planilla de cálculo de incertidumbre
VI.Resultado final
𝐾𝑔
𝜌 = 1.087 ± 0.002 [ 3 ]
𝑚
5. Conclusión
Luego de combinar conceptos teóricos termodinámicos como ser la ecuación de los gases ideales y
basándonos en la experiencia de Torricelli, obtuvimos satisfactoriamente un valor de densidad del aire,
haciendo uso de los datos experimentales de presión y temperatura. Dicho valor se expresa con las
correcciones pertinentes debidas a la propagación de incertidumbre.
Si bien la situación actual mundial nos privó de realizar la experiencia de forma presencial en el laboratorio,
a través del presente trabajo pudimos comprender el funcionamiento de un elemento tan importante como
lo es el barómetro.
6. Referencias
• Garcia, J. & Galeasso, A. (2021), Guía de Trabajos Prácticos de Aeronáutica General, Córdoba,
Argentina.
• Çengel, Y. & Boules M. (2014), Thermodynamics-An Engineering Approach, Nueva York, USA,
McGraw-Hill.
• Krause, G. (2021), Aeronautica General-Apuntes de la cátedra, Córdoba Argentina
• R. Fuess Berlin Steglitz (1958), Anweisung zur Benutzung der Nomalbarometer 2k, 4k, 20k.
Manzur Mayuli, Juan Sebastián – Recalde, Tomás Página 5 de 5
También podría gustarte
- Equilibrios de Fases y Transiciones de Fases: Parte IDe EverandEquilibrios de Fases y Transiciones de Fases: Parte IAún no hay calificaciones
- Informe Laboratorio #5 PDFDocumento5 páginasInforme Laboratorio #5 PDFEsteban MogollónAún no hay calificaciones
- UF1811 - Manejo de equipos de medida de contaminantes atmosféricosDe EverandUF1811 - Manejo de equipos de medida de contaminantes atmosféricosAún no hay calificaciones
- Práctica Número 6Documento5 páginasPráctica Número 6Camacho Villan ErikAún no hay calificaciones
- Grupo 9 - Práctica 4Documento27 páginasGrupo 9 - Práctica 4Emily IturraldeAún no hay calificaciones
- Guias de Laboratorios Hidraulica I Final 2019Documento92 páginasGuias de Laboratorios Hidraulica I Final 2019Ruiz XpresAún no hay calificaciones
- Laboratorio 4 MOTORES Cuya GersonDocumento17 páginasLaboratorio 4 MOTORES Cuya GersonGerson cuyaAún no hay calificaciones
- Práctica de Laboratorio NDocumento8 páginasPráctica de Laboratorio Nvictor huayhua choqueticoAún no hay calificaciones
- Guias de Laboratorios Hidraulica I 2018Documento91 páginasGuias de Laboratorios Hidraulica I 2018Francella GarcíaAún no hay calificaciones
- Informe Determinacion Del Coeficiente Adiabatico de GasesDocumento20 páginasInforme Determinacion Del Coeficiente Adiabatico de GasesJuan Pablo Moran CaballeroAún no hay calificaciones
- Laboratorio 1 de Fisicoquímica 1 Densidad y Peso Molecular Aparente Del AireDocumento17 páginasLaboratorio 1 de Fisicoquímica 1 Densidad y Peso Molecular Aparente Del AireOscar Gonzales100% (1)
- PresentacionEfectodecarga-rCS FULLSIZEDocumento25 páginasPresentacionEfectodecarga-rCS FULLSIZEJavier SerranoAún no hay calificaciones
- 2023-IT6-V1-Quintanilla y TubelloDocumento12 páginas2023-IT6-V1-Quintanilla y TubelloGera Tubello IribasAún no hay calificaciones
- 214 Guia 1Documento4 páginas214 Guia 1AlbaroMamaniVenizAún no hay calificaciones
- Finura Del CementoDocumento5 páginasFinura Del CementoAndres MedinaAún no hay calificaciones
- Laboratorio 1 Termodinámica USMDocumento3 páginasLaboratorio 1 Termodinámica USMVictor Reyes VidalAún no hay calificaciones
- Determinación de La Constante Del AireDocumento4 páginasDeterminación de La Constante Del AireCarlos Alfredo Martinez OrtegaAún no hay calificaciones
- Presion ManometricaDocumento5 páginasPresion ManometricaLiseth ZartoAún no hay calificaciones
- Inf. 1 de FisicoquimicaDocumento10 páginasInf. 1 de FisicoquimicaLucía Molina RamírezAún no hay calificaciones
- Informe de Practicas de Hidráulica 1Documento56 páginasInforme de Practicas de Hidráulica 1Bismarck Duarte Centeno100% (1)
- Aforo Mina Venti UsachDocumento8 páginasAforo Mina Venti UsachJaviera ArlineAún no hay calificaciones
- Informe de Laboratorio N 1Documento7 páginasInforme de Laboratorio N 1Nicolas LozadaAún no hay calificaciones
- Lab 1termoDocumento14 páginasLab 1termoRina Licet Socompi AguilarAún no hay calificaciones
- Guia de Laboratorio P2 - PresiónDocumento6 páginasGuia de Laboratorio P2 - PresiónCristofer AlomotoAún no hay calificaciones
- Practica 4Documento10 páginasPractica 4ad_jg25587Aún no hay calificaciones
- Calibracion Del Tunel de ImpactoDocumento7 páginasCalibracion Del Tunel de ImpactoAlan RiveraAún no hay calificaciones
- Experiencia N1 Aforo de Ventilacion en Mina El PimientoDocumento3 páginasExperiencia N1 Aforo de Ventilacion en Mina El PimientoYercco Antonio HurtadoAún no hay calificaciones
- Determinación Experimental de La VelocidadDocumento11 páginasDeterminación Experimental de La VelocidadESTEBAN TOMÁS SANABRIAAún no hay calificaciones
- Glab-02-Espinoza Vasquez Jhonatan HenryDocumento9 páginasGlab-02-Espinoza Vasquez Jhonatan HenryJhonatan Henry Espinoza VasquezAún no hay calificaciones
- Aplicación de Manometros en La Industria GaseraDocumento5 páginasAplicación de Manometros en La Industria GaseraLuis Angel AguilarAún no hay calificaciones
- Ley de Charles y BoylesDocumento5 páginasLey de Charles y BoylesAdrian Cabezas SolaresAún no hay calificaciones
- Ley de Charles y BoylesDocumento5 páginasLey de Charles y BoylesAdrian Cabezas SolaresAún no hay calificaciones
- Material de Lectura 6º 1 ElectronicaDocumento39 páginasMaterial de Lectura 6º 1 ElectronicaEliana JuarezAún no hay calificaciones
- Immo I - U2 - 2018Documento52 páginasImmo I - U2 - 2018Daniel Alejandro SanchezAún no hay calificaciones
- Semana02 1 Guía Practica 4 - Concentración de Gases ContaminantesDocumento3 páginasSemana02 1 Guía Practica 4 - Concentración de Gases ContaminantesJose GutierrezAún no hay calificaciones
- Calibracion de ManometroDocumento7 páginasCalibracion de ManometroClever HVAún no hay calificaciones
- Práctica #5 - Determinación de La Constante IdealDocumento6 páginasPráctica #5 - Determinación de La Constante IdealJose LeónAún no hay calificaciones
- Practica 4Documento8 páginasPractica 4Ray Cruz100% (1)
- Material de Lectura 7º 1 ElectronicaDocumento40 páginasMaterial de Lectura 7º 1 ElectronicaEliana JuarezAún no hay calificaciones
- Informe Calidad de Aire PM 10Documento11 páginasInforme Calidad de Aire PM 10DayanaPadillaRuizAún no hay calificaciones
- PRÁCTICA DE MEDICIÓN DE PRESIÓN ALVARO Y JEAN v2Documento42 páginasPRÁCTICA DE MEDICIÓN DE PRESIÓN ALVARO Y JEAN v2Jose RojasAún no hay calificaciones
- Informe Manometro FisicoDocumento5 páginasInforme Manometro FisicoLuisa Fernanda DíazAún no hay calificaciones
- Ventilación de Minas Laboratorio Nº5 - Nº7, Trabajo GrupalDocumento17 páginasVentilación de Minas Laboratorio Nº5 - Nº7, Trabajo GrupalEsgar Eduardo Espinoza CastilloAún no hay calificaciones
- Practica No 4Documento14 páginasPractica No 4Jose Ivan CarrilloAún no hay calificaciones
- LT P1 Presion+ManómetroDocumento14 páginasLT P1 Presion+ManómetroMelissa ChávezAún no hay calificaciones
- Tareaunidad1 OpiDocumento11 páginasTareaunidad1 OpiMayra Salome Lenes Condori100% (1)
- Aporte Portafolio Termodinámica Lab 3Documento21 páginasAporte Portafolio Termodinámica Lab 3RolexAún no hay calificaciones
- Informe Laboratorio ManometriaDocumento14 páginasInforme Laboratorio ManometriaJENNIFER YULIANA DELGADO BOLAÑOSAún no hay calificaciones
- Practica No 5Documento19 páginasPractica No 5Jose Ivan CarrilloAún no hay calificaciones
- Practica 4 DINAMICADocumento11 páginasPractica 4 DINAMICAjimmy0821Aún no hay calificaciones
- Guía de Laboratorio 1Documento5 páginasGuía de Laboratorio 1renato ferrel ariasAún no hay calificaciones
- Laboratorio 3 - TermodinámicaDocumento5 páginasLaboratorio 3 - TermodinámicaRolexAún no hay calificaciones
- Activiadad Nro. 2 MeteorologiaDocumento9 páginasActiviadad Nro. 2 Meteorologiajose joseAún no hay calificaciones
- Laboratorio 4Documento7 páginasLaboratorio 4Julian BurbanoAún no hay calificaciones
- Informe 2 Manometro BourdonDocumento16 páginasInforme 2 Manometro BourdonHenry CardozoAún no hay calificaciones
- Practica 7Documento10 páginasPractica 7Suker RodríguezAún no hay calificaciones
- Balance Termico de Un EquipoDocumento17 páginasBalance Termico de Un EquipoFreddy Andrés Irribarra VilAún no hay calificaciones
- Lim - Informe 2Documento22 páginasLim - Informe 2JUAN DANIEL TELLO CHUNGAAún no hay calificaciones
- Informe 5Documento18 páginasInforme 5ANTHONY ALEXANDER HUAMAN VIVANCOAún no hay calificaciones
- 04 Manual Práctico de Ventilación S&PDocumento47 páginas04 Manual Práctico de Ventilación S&PJLBR23100% (4)
- 2018 Seminario Aeronautica FormatoDocumento6 páginas2018 Seminario Aeronautica FormatoTomas RecaldeAún no hay calificaciones
- 20 Energia - Interna - de - Deformacion y PTV 040419Documento14 páginas20 Energia - Interna - de - Deformacion y PTV 040419Tomas RecaldeAún no hay calificaciones
- ElasticidadDocumento2 páginasElasticidadTomas RecaldeAún no hay calificaciones
- Jhon Maxwell Las 21 Cualidades Indispensables de Un LiderDocumento78 páginasJhon Maxwell Las 21 Cualidades Indispensables de Un LiderTomas Recalde67% (3)
- El Secreto de Mi Exito Cualidades Necesarias de Un Gerente Konosuke Matsushita (HACIA ARRIBA) PDFDocumento104 páginasEl Secreto de Mi Exito Cualidades Necesarias de Un Gerente Konosuke Matsushita (HACIA ARRIBA) PDFTomas Recalde83% (6)
- Tecnica - Scout 2 MetereologiaDocumento51 páginasTecnica - Scout 2 MetereologiaDaniel Martin AndresAún no hay calificaciones
- Capitulo I. Fundamentos de Meteorología - 2018 - IIDocumento31 páginasCapitulo I. Fundamentos de Meteorología - 2018 - IIEDINSON J. ACUÑA FERNANDEZ.Aún no hay calificaciones
- Presión AtmósfericaDocumento14 páginasPresión AtmósfericaLaddy AraujoAún no hay calificaciones
- 1 Fundamentos Presion y TemperaturaDocumento24 páginas1 Fundamentos Presion y TemperaturaLizzy DLAún no hay calificaciones
- Resolver Grupo N 2Documento7 páginasResolver Grupo N 2Anonymous WMNVv02ENkAún no hay calificaciones
- Emisiones Guias Corte 2Documento13 páginasEmisiones Guias Corte 2Alejandro RamirezAún no hay calificaciones
- TemperaturaDocumento39 páginasTemperaturaJuan Manuel Cortes PinedaAún no hay calificaciones
- Mano, Baro, VacuometroDocumento9 páginasMano, Baro, Vacuometroricardo767Aún no hay calificaciones
- Para Qué Sirven Los Instrumentos MeteorológicosDocumento16 páginasPara Qué Sirven Los Instrumentos MeteorológicosJose RodriguezAún no hay calificaciones
- Apuntes Basicos de Termodinamica IDocumento130 páginasApuntes Basicos de Termodinamica IJuan Juarez Ramos100% (1)
- Hidrostática Parte 2Documento35 páginasHidrostática Parte 2Guillermo TellAún no hay calificaciones
- Quimica Grado 11 GasesDocumento9 páginasQuimica Grado 11 GasesAndres AyalaAún no hay calificaciones
- Guia FisicoquimicaDocumento32 páginasGuia FisicoquimicaMartinez C. Jesus AAún no hay calificaciones
- Estatica de FluidosDocumento10 páginasEstatica de FluidosCesar HidalgoAún no hay calificaciones
- NivelacionDocumento13 páginasNivelacionAnonymous 9xbcntjsAún no hay calificaciones
- Experimento de TermodinámicaDocumento2 páginasExperimento de TermodinámicaPlanetGames ZacapaAún no hay calificaciones
- Estática de Fluidos - Física General II-optaciano VazquezDocumento140 páginasEstática de Fluidos - Física General II-optaciano VazquezJoe Anderson100% (1)
- Ejercicios DinamicaDocumento5 páginasEjercicios DinamicaDiego Del CastilloAún no hay calificaciones
- Actividad 2-Ejercicios Mecánica de Fluidos, Temperatura y Calor (Entregable)Documento17 páginasActividad 2-Ejercicios Mecánica de Fluidos, Temperatura y Calor (Entregable)Juan David MartinezAún no hay calificaciones
- Presion AtmosfericaDocumento13 páginasPresion AtmosfericayesseniaAún no hay calificaciones
- Hidrostática - ContenidosDocumento20 páginasHidrostática - ContenidosJean-Pierre Giusto CovarrubiasAún no hay calificaciones
- Apuntes de PresionDocumento18 páginasApuntes de PresionMIGUEL ANGEL ZUÑIGAAún no hay calificaciones
- Notas de Clase 4 V4Documento47 páginasNotas de Clase 4 V4Juan ErausquinAún no hay calificaciones
- Fisica IiDocumento196 páginasFisica IiJoel Almaraz MtzAún no hay calificaciones
- Procedimiento de Calibracion de Sensores de HR Tipo Capacitivo PDFDocumento823 páginasProcedimiento de Calibracion de Sensores de HR Tipo Capacitivo PDFgilbertolopezAún no hay calificaciones
- JULIODocumento23 páginasJULIOesbin mayder inga fernandezAún no hay calificaciones
- Separata N°7Documento5 páginasSeparata N°7Richard Payano YaleAún no hay calificaciones
- Cap - Iv. Requerimientos de Caudal en Una Mina - Instrumentos Usados en Mensuras de VentilacionDocumento76 páginasCap - Iv. Requerimientos de Caudal en Una Mina - Instrumentos Usados en Mensuras de VentilacionCristel Figueroa T100% (2)
- Informe Calibración de Un ManómetroDocumento10 páginasInforme Calibración de Un ManómetroVictor Pugliese50% (2)
- Apuntes Hidráulica BásicaDocumento91 páginasApuntes Hidráulica BásicaMiguel Ángel Jaime ParraAún no hay calificaciones
- La metamedicina. Cada síntoma es un mensaje: La curación a tu alcanceDe EverandLa metamedicina. Cada síntoma es un mensaje: La curación a tu alcanceCalificación: 5 de 5 estrellas5/5 (8)
- La revolución de la glucosa: Equilibra tus niveles de glucosa y cambiarás tu salud y tu vidaDe EverandLa revolución de la glucosa: Equilibra tus niveles de glucosa y cambiarás tu salud y tu vidaCalificación: 5 de 5 estrellas5/5 (206)
- Cómo Aprender por tu Cuenta: Los Secretos de los Mejores Autodidáctas para Acelerar tu Aprendizaje sin Depender de los DemásDe EverandCómo Aprender por tu Cuenta: Los Secretos de los Mejores Autodidáctas para Acelerar tu Aprendizaje sin Depender de los DemásCalificación: 4 de 5 estrellas4/5 (10)
- Manual de ortopedia maxilar: Modelo diagnóstico de maloclusiones para pacientes en crecimientoDe EverandManual de ortopedia maxilar: Modelo diagnóstico de maloclusiones para pacientes en crecimientoCalificación: 4.5 de 5 estrellas4.5/5 (14)
- Interpretación del ECG: Una Guía Práctica e Intuitiva para Aprender a Leer el ECG y Diagnosticar y Tratar ArritmiasDe EverandInterpretación del ECG: Una Guía Práctica e Intuitiva para Aprender a Leer el ECG y Diagnosticar y Tratar ArritmiasAún no hay calificaciones
- Homo antecessor: El nacimiento de una especieDe EverandHomo antecessor: El nacimiento de una especieCalificación: 5 de 5 estrellas5/5 (1)
- Tu futuro: Consejos de una Premio Nobel a los jóvenesDe EverandTu futuro: Consejos de una Premio Nobel a los jóvenesCalificación: 3.5 de 5 estrellas3.5/5 (5)
- 50 técnicas de mindfulness para la ansiedad, la depresión, el estrés y el dolor: Mindfulness como terapiaDe Everand50 técnicas de mindfulness para la ansiedad, la depresión, el estrés y el dolor: Mindfulness como terapiaCalificación: 4 de 5 estrellas4/5 (37)
- El concepto Mulligan de terapia manual (Color)De EverandEl concepto Mulligan de terapia manual (Color)Calificación: 5 de 5 estrellas5/5 (3)
- Disciplina Mental: Técnicas infalibles para lograr todo lo que te propones y eliminar la pereza y la procrastinación de tu vida para siempreDe EverandDisciplina Mental: Técnicas infalibles para lograr todo lo que te propones y eliminar la pereza y la procrastinación de tu vida para siempreCalificación: 5 de 5 estrellas5/5 (3)
- Liberación del trauma: Perdón y temblor es el caminoDe EverandLiberación del trauma: Perdón y temblor es el caminoCalificación: 4 de 5 estrellas4/5 (4)
- Resumen de Pensar rápido pensar despacio de Daniel KahnemanDe EverandResumen de Pensar rápido pensar despacio de Daniel KahnemanCalificación: 4.5 de 5 estrellas4.5/5 (11)
- Confección de cojines y ropa de hogar. TCPF0309De EverandConfección de cojines y ropa de hogar. TCPF0309Aún no hay calificaciones
- PREM de Pediatría: capacitación para el ENARMDe EverandPREM de Pediatría: capacitación para el ENARMCalificación: 1 de 5 estrellas1/5 (1)
- Batidos Verdes Depurativos y Antioxidantes: Aumenta tu Vitalidad con Smoothie Detox Durante 10 Días Para Adelgazar y Bajar de Peso: Aumenta tu vitalidad con smoothie detox durante 10 días para adelgazar y bajar de pesoDe EverandBatidos Verdes Depurativos y Antioxidantes: Aumenta tu Vitalidad con Smoothie Detox Durante 10 Días Para Adelgazar y Bajar de Peso: Aumenta tu vitalidad con smoothie detox durante 10 días para adelgazar y bajar de pesoCalificación: 5 de 5 estrellas5/5 (2)
- Mini granja para principiantes: La guía definitiva para convertir su jardín en una mini granja y crear un jardín orgánico autosuficienteDe EverandMini granja para principiantes: La guía definitiva para convertir su jardín en una mini granja y crear un jardín orgánico autosuficienteCalificación: 2 de 5 estrellas2/5 (1)
- Limpiar, Nutrir, Reparar: Adiós a Las Enfermedades, En Tres Pasos NaturalesDe EverandLimpiar, Nutrir, Reparar: Adiós a Las Enfermedades, En Tres Pasos NaturalesCalificación: 4 de 5 estrellas4/5 (6)
- Electricidad: Fundamentos y problemas de electrostática, corriente continua, electromagnetiDe EverandElectricidad: Fundamentos y problemas de electrostática, corriente continua, electromagnetiCalificación: 3.5 de 5 estrellas3.5/5 (5)