Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Cuadernillo #3 Ciencias 2015
Cargado por
Maurismer ArenasDescripción original:
Título original
Derechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
Cuadernillo #3 Ciencias 2015
Cargado por
Maurismer ArenasCopyright:
Formatos disponibles
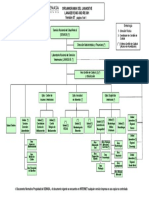
PREUNIVERSITARIO PREUCV 2015
DEPARTAMENTO DE CIENCIAS
ORGANIZACIÓN, ESTRUCTURA Y ACTIVIDAD CELULAR
PROCESOS Y FUNCIONES VITALES EN LOS SERES VIVOS
Curso Biología
Parto y lactancia 3
Guía de destrezas B – 13 4
Genética I: Variabilidad y Herencia 7
Guía de destrezas B – 14 8
Genética II. Variabilidad y Herencia 13
Guía de destrezas B – 15 14
Ecología I 17
Guía de destrezas B – 16 18
Ecología de poblaciones 23
Guía de destrezas B – 17 24
Ecosistemas 29
Guía de destrezas B – 18 30
BIOLOGIA PLAN COMÚN 1
PREUNIVERSITARIO PREUCV 2015
DEPARTAMENTO DE CIENCIAS
ORGANIZACIÓN, ESTRUCTURA Y ACTIVIDAD CELULAR
PROCESOS Y FUNCIONES VITALES EN LOS SERES VIVOS
2 BIOLOGÍA PLAN COMÚN
PREUNIVERSITARIO PREUCV 2015
DEPARTAMENTO DE CIENCIAS
BIOLOGIA PLAN COMÚN
PARTO Y LACTANCIA
Eje Temático: Procesos y funciones vitales en los seres vivos.
Sub – Eje: Biología Humana y Salud.
Tareas: Identificar – Comprender – Distinguir – Interpretar – Reconocer.
El parto humano, también llamado nacimiento, es
la culminación del embarazo humano, hasta el
periodo de salida del bebé del útero materno.
Se considera que una mujer inicia el parto con la
aparición de contracciones uterinas regulares, que
aumentan en intensidad y frecuencia,
acompañadas de cambios fisiológicos en el cuello
uterino.
El proceso del parto humano natural se categoriza
en tres fases: el borramiento y dilatación del cuello
uterino, el descenso y nacimiento del bebé y el
alumbramiento de la placenta. El parto puede
verse asistido con medicamentos como ciertos
anestésicos o la oxitocina, utilizada ante
complicaciones de retraso grave de
alumbramiento.
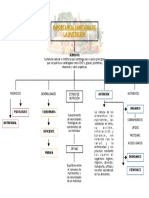
La lactancia materna es la
alimentación con leche del
seno materno. La OMS y
el UNICEF señalan
asimismo que la lactancia
"es una forma inigualable
de facilitar el alimento
ideal para el crecimiento y
desarrollo correcto de los
niños".
Nutrición óptima
Entrega defensas
Favorece el desarrollo
intelectual
Favorece la
calcificación de los
dientes y estimula un
buen desarrollo facial.
–BIOLOGÍA MODULO COMÚN – CLASE 13 3
PREUNIVERSITARIO PREUCV 2015
DEPARTAMENTO DE CIENCIAS
ESTRUCTURA Y FUNCION DE LOS SERES VIVOS
SUB - EJE: PROCESOS Y FUNCIONES VITALES.
Guía de Destrezas B – 13: Parto y Lactancia.
1. ¿Cuál es la hormona encargada de ampliar las 5. Lee la siguiente definición: “Una vez que ha nacido el
contracciones uterinas para iniciar el proceso de bebé, comienzan nuevamente las contracciones, que
dilatación? permitirán que la placenta se desprenda y sea expulsada
al exterior”.
A) Prolactina. ¿A qué fenómeno se está haciendo referencia en el
B) Estrógeno placentario. fragmento anterior?
C) Lactógeno placentario.
D) Oxitocina.
A) Contracciones.
E) Somatostatina.
B) Ruptura de bolsa.
C) Dilatación.
2. ¿Cuál es la hormona encargada de provocar las D) Expulsión.
contracciones de los alveolos mamarios para la expulsión E) Alumbramiento
de leche?
6. El orden correcto para las etapas del parto es:
A) Prolactina.
B) Cortisol
A) alumbramiento, nacimiento y dilatación.
C) Progesterona
B) dilatación, alumbramiento y nacimiento.
D) Estrógenos
C) dilatación, nacimiento y alumbramiento.
E) Oxitocina
D) nacimiento, dilatación y alumbramiento.
E) alumbramiento, dilatación y nacimiento.
3. La lactancia materna requiere de la(s) siguiente(s)
hormona(s): 7. La(s) fase(s) del parto es(son):
A) Prolactina que estimula la secreción de leche. I. Contracciones involuntarias y periódicas del útero.
B) Oxitocina que estimula la eyección de la leche. II. Desplazamiento del feto hasta el cuello del útero.
C) Prolactina que estimula la secreción y oxitocina que III. Rotura de la bolsa amniótica.
estimula la eyección de la leche.
D) Oxitocina que estimula la secreción y prolactina que A) Solo I.
estimula la eyección de la leche. B) Solo III.
E) Prolactina que estimula la secreción y la eyección de C) Solo I y II.
leche. D) Solo II y III.
E) I, II y III.
4. ¿Qué hormona realiza la función de la producción de 8. ¿Cuál de las siguientes hormonas no participa en el
la leche materna a nivel de los alvéolos mamarios? parto?
A) Prolactina. A) Estrógenos.
B) Progesterona. B) Relaxina.
C) Cortisol. C) Oxitocina.
D) Oxitocina. D) Prostaglandinas.
E) Somatostatina. E) Folículo estimulante.
4 BIOLOGÍA MÓDULO COMÚN – CLASE 13
PREUNIVERSITARIO PREUCV 2015
DEPARTAMENTO DE CIENCIAS
ESTRUCTURA Y FUNCION DE LOS SERES VIVOS
SUB - EJE: PROCESOS Y FUNCIONES VITALES.
Guía de Destrezas B – 13: Parto y Lactancia.
9. ¿Qué efectos tienen los estrógenos en la etapa previa 12. ¿Cuál de las siguientes opciones corresponden a
al parto? riesgos de una alimentación complementaria demasiado
temprana?
I. Capacitan a las células musculares para que
respondan a la oxitocina. I. Generación de alergias por absorción de moléculas
II. Favorecen la formación de conexiones íntimas entre proteicas enteras.
las células musculares del útero. II. Riesgo de caries del biberón por incorporación de
III. Estimulan la maduración final de los pulmones para azúcar en la leche.
que se puedan inflar luego del parto. III. Dificultad en la digestión de almidones por falta de
amilasa pancreática.
A) Sólo I
B) Sólo II A) Sólo I
C) Sólo III B) Sólo II
D) Sólo I y II C) Sólo III
E) I, II y III D) Sólo I y II
E) I, II y III
10. ¿Cuál(es) de las siguientes afirmaciones sobre la
lactancia es (son) correcta(s)?
13. ¿Qué sucedería si ante una enfermedad se deja de
I. Es un proceso regulado por retroalimentación secretar la oxitocina a una mujer embarazada?
positiva.
II. La eyección de la leche está regulada por la A) Se inhibe la formación de la leche.
prolactina. B) Se produce la leche materna.
III. Mientras un bebé succione el pezón, se seguirá C) No se provocan contracciones uterinas.
produciendo leche. D) Inhibe la función de las glándulas mamarias
E) La adenohipófisis secreta testosterona.
A) Sólo I.
B) Sólo II. 14. ¿Qué evento se desencadenaría si las
C) I y III. concentraciones de cortisol son escasas en el proceso de
D) II y III. parto?
E) I, II y III.
A) Aumenta la producción de la progesterona
placentaria
11. El traspaso de los anticuerpos de la madre al hijo a B) Fin de las inhibiciones de contracciones uterinas
través de la leche es importante porque: C) Se presenta una dilatación del cérvix o cuello uterino
D) No se desencadenaría la cadena de regulación
A) Permanecen para toda la vida. hormonal para efectuar el parto
B) Son la parte más abundante e importante de la E) Se estimula a la hipófisis para secretar oxitocina
leche materna.
C) Los anticuerpos son transformados en energía
rápidamente. 15. ¿Cuáles serían las consecuencias en el proceso de
D) Estos elementos forman la primera barrera lactancia si a pesar de que se produzca la succión del
inmunológica del neonato pezón por parte del bebe, el mensaje nervioso no se
E) Estos elementos son los precursores de la formación integra en la neuronas de la adenohipófisis?
de los propios anticuerpos para el neonato.
A) Se inhibe la secreción de la oxitocina.
B) Se inhibe la producción de leche por acción de la
somatostatina
C) Se deja de secretar la prolactina.
D) El alvéolo mamario genera una respuesta de tipo
positiva.
E) El calostro se secreta sin proteínas de la leche.
BIOLOGÍA MÓDULO COMÚN – CLASE 13 5
PREUNIVERSITARIO PREUCV 2015
DEPARTAMENTO DE CIENCIAS
ESTRUCTURA Y FUNCION DE LOS SERES VIVOS
SUB - EJE: PROCESOS Y FUNCIONES VITALES.
Guía de Destrezas B – 13: Parto y Lactancia.
16. Una mujer padeció una extraña enfermedad que le
provocó daños en el funcionamiento de la musculatura 18. Una madre ha notado que su producción de leche ha
lisa que compone órganos internos, incluido el disminuido desde que entró a trabajar y no puede
miometrio. Actualmente está a punto de dar a luz. Dada amamantar a su bebé. ¿Cómo puede explicarse esta
su condición, ¿qué es esperable que le suceda al disminución en la producción de leche?
momento del parto?
A) El bebé ha disminuido la succión del pezón.
A) Experimentará un peligroso aumento de su frecuencia B) La madre ya no está produciendo estrógenos.
cardiaca. C) La madre ya no está produciendo progesterona.
B) El miometrio se desprenderá de manera repentina y D) El bebé y la madre han perdido el vínculo afectivo.
facilitará el parto. E) El bebé ya ha creado todos sus anticuerpos.
C) Deberá someterse a una cesárea debido a la ausencia
de contracciones. 19. Se sabe que la lactancia materna exclusiva debería
D) Seguirá con normalidad el proceso, pues esta durar hasta los 6 meses. ¿Qué beneficios trae para el
musculatura no participa en el parto. bebé alimentarse de leche materna de manera exclusiva
E) Experimentará una peligrosa disminución de su hasta esa edad?
frecuencia cardiaca.
A) Aumenta la probabilidad de padecer obesidad en
17. Para una madre que no secreta leche durante la edad adulta.
lactancia, ¿cuál de las siguientes combinaciones de B) Disminuye el apego, favoreciendo la independencia en
hormonas resultaría más efectiva para su tratamiento? edad adulta.
C) Disminuye la probabilidad de que reciba anticuerpos a
A) Prolactina y estradiol. través de la leche.
B) Prolactina y oxitocina. D) Aumenta la protección inmune contra algunas
C) Vasopresina y oxitocina. enfermedades.
D) Progesterona y oxitocina. E) Disminuye la probabilidad de padecer obesidad en
E) Hormona luteinizante y prolactina. edad adulta.
20. A continuación se presenta un gráfico que muestra el comportamiento de distintas hormonas durante el embarazo.
A partir del gráfico, es posible deducir
que:
I. la progesterona mantiene un nivel
constante durante todo el embarazo.
II. la prolactina aumenta para estimular la
maduración de la glándula mamaria.
III. la progesterona disminuye al final del
embarazo para permitir el parto.
A) Sólo I
B) Sólo II
C) Sólo III
D) Sólo I y II
E) Sólo II y III
6 BIOLOGÍA MÓDULO COMÚN – CLASE 13
PREUNIVERSITARIO PREUCV 2015
DEPARTAMENTO DE CIENCIAS
BIOLOGIA PLAN COMÚN
GENÉTICA I: VARIABILIDAD Y HERENCIA
Eje Temático: Organismos, ambientes y sus interacciones
Sub – Eje: Herencia y Evolución
Tareas: Identificar – Comprender – Distinguir – Interpretar – Reconocer.
Se denomina Genética al estudio científico de cómo se trasmiten los caracteres físicos,
bioquímicos y de comportamiento de padres a hijos. Este término fue acuñado en 1906
por el biólogo británico William Bateson.
Los genetistas estudian los mecanismos hereditarios en organismos que se
reproducen de forma sexual, y determinan semejanzas, diferencias y similitudes entre
padres e hijos que se reproducen de generación en generación según determinados
patrones. La investigación de estos últimos ha dado lugar a algunos de los
descubrimientos más importantes de la biología moderna.
La ciencia de la genética nació en 1900, cuando varios investigadores de la
reproducción de las plantas descubrieron el trabajo del monje austriaco Gregor
Mendel, que aunque fue publicado en 1866 había sido ignorado en la práctica.
Mendel, que trabajó con la planta del guisante (chícharo o arveja), describió los patrones de la herencia en función
de siete pares de rasgos contrastantes que aparecían en siete variedades diferentes de esta planta. Observó que los
caracteres se heredaban como unidades separadas, y cada una de ellas lo hacía de forma independiente con respecto
a las otras. Señaló que cada progenitor tiene pares de unidades, pero que sólo aporta una unidad de cada pareja a
su descendiente. Más tarde, las unidades descritas por Mendel recibieron el nombre de genes.
Términos claves de Genética:
TÉRMINOS DEFINICIONES
Gen Factor genético (una región de ADN) que ayuda a determinar una
característica.
Alelos Una de las formas alternativas de un gen.
Locus Lugar específico ocupado por un alelo en un cromosoma.
Genotipo Conjunto de alelos que posee un organismo individual.
Fenotipo Manifestación o aparición de una característica, la cual puede ser física,
fisiológica, bioquímica o conductual.
Características Se refiere a un concepto general; ej. Color de ojos. En tanto que el término
rasgo o carácter se refiere a una manifestación específica de esa
característica; ej. ojos azules, verdes o negros.
Homocigoto o Se refiere a una característica, en la cual los genes alelos que ocupan igual
puro locus en un par de cromosomas homólogos son iguales; AA o aa.
Heterocigoto Se refiere a una característica, en la cual los genes alelos que ocupan igual
o Híbrido locus en un par de cromosomas homólogos son distintos; Aa
–BIOLOGÍA MODULO COMÚN – CLASE 14 7
PREUNIVERSITARIO PREUCV 2015
DEPARTAMENTO DE CIENCIAS
ORGANISMOS, AMBIENTES Y SUS INTERACCIONES
SUB - EJE: HERENCIA Y EVOLUCIÓN
Guía de Destrezas B – 14: Variabilidad y Herencia.
Leyes de Mendel
1ª Ley de Mendel: Ley de la 2ª Ley de Mendel: Ley de la 3ª Ley de Mendel: Ley de la
uniformidad de los híbridos segregación de los caracteres en la independencia de los
de la primera generación segunda generación filial. caracteres hereditarios.
filial.
1. ¿Cuál(es) de los siguientes aspectos corresponde(n) 3. ¿Cuál es la mejor definición para referirnos al
a características heredadas? fenotipo?
I. Desarrollo de la musculatura. A) El conjunto de caracteres observables que son
II. Tonalidad de la piel. determinados solamente por el genotipo
III. Intolerancia a la lactosa. B) El conjunto de caracteres observables que son
determinados solamente por el ambiente
A) Solo I. C) El producto de la interacción entre cromosomas
B) Solo II. durante la división celular
C) Solo III. D) El conjunto de alelos que dan origen a los caracteres
D) I y II. observables en un organismo
E) II y III. E) El conjunto de caracteres observables
determinados por el ambiente y el genotipo
2. ¿Cuál(es) de las siguientes afirmaciones con
respecto al experimento de Mendel es(son) 4. La ley de segregación (primera ley de Mendel) es la
correcta(s)? conclusión directa de la relación 3:1 de:
I. Un individuo homocigoto producirá dos gametos A) dominantes a recesivos en el cruce dihíbrido.
con distintos alelos. B) recesivos a dominantes en el cruce dihíbrido.
II. Un individuo homocigoto recesivo posee un gameto C) recesivos a dominantes en el cruce de prueba.
con el alelo recesivo y otro gameto con el alelo D) dominantes a recesivos en el cruce monohíbrido.
dominante. E) recesivos a dominantes en el cruce monohíbrido.
III. Si se cruzan dos organismos con fenotipo
dominante, el carácter recesivo no podrá
expresarse.
A) Solo I.
B) Solo III.
C) I y II.
D) II y III.
E) Ninguna de las anteriores.
8 BIOLOGÍA MÓDULO COMÚN – CLASE 14
PREUNIVERSITARIO PREUCV 2015
DEPARTAMENTO DE CIENCIAS
ORGANISMOS, AMBIENTES Y SUS INTERACCIONES
SUB - EJE: HERENCIA Y EVOLUCIÓN
Guía de Destrezas B – 14: Variabilidad y Herencia.
Observa el siguiente esquema de dos cromosomas 8. En las plantas de arvejas, semillas lisas (S) son
homólogos. dominantes sobre semillas rugosas (s). En un cruce
genético de dos plantas que son heterocigotos para
el carácter "forma de la semilla", ¿qué genotipos
resultan de este cruce monohíbrido?
I) 25% homocigotos dominantes.
II) 50% heterocigotos.
III) 25% homocigotos recesivos.
IV) 50% homocigotos dominantes.
A) II y III.
5. ¿Cuál de las siguientes afirmaciones es correcta con B) I, II y IV.
respecto a los genes en el esquema? C) II, III y IV.
D) I, II y III.
A) Existen tres genes homocigotos recesivos. E) II y IV.
B) No se observan genes heterocigotos.
C) Al expresarse el gen F, el fenotipo será dominante. 9. ¿Cuál(es) de las siguientes afirmaciones sobre la
D) Al formarse los gametos, solo habrá alelos “D” segunda ley de Mendel es(son) correcta(s)?
dominantes.
E) Si cualquiera de los dos cromosomas se expresan,
todos los fenotipos serán dominantes. I. Cada gameto recibe un miembro del par de copias
del gen.
6. Dos ratones homocigotos, uno blanco y uno negro, II. En la cruza dihíbrida, los alelos de genes distintos se
producen solo crías negras en la F1. Cuando las F1 distribuyen juntos en la formación de gametos.
se cruzan entre sí nuevamente resulta una F2 con III. Siempre es posible formar todas las combinaciones
75% de la progenie negros y el 25 % restante posibles de los caracteres en la formación gametos.
blancos. Además, en esta F2 hay un 25 % de ratones
negros homocigotos. De este resultado es posible A) Solo I.
deducir correctamente que: B) Solo II.
I. el alelo blanco es recesivo. C) Solo III.
II. el alelo negro es dominante. D) II y III.
III. la cruza entre ratones negros de la F1 siempre dará E) I, II y III.
como resultado fenotipos en proporción 3:1.
10. Al contabilizar el total de la descendencia en un
A) Solo I. cruzamiento de Pisum sativum (ambos parentales
B) Solo II heterocigotos para el color de semilla), ¿cuál(es) de
C) Solo III. estos resultados es (son) posible(s)?
D) Solo I y II.
E) I, II y III. I. 400 amarillos y 130 verdes.
II. 30 amarillos y 10 verdes.
7. Si las cejas gruesas son dominantes sobre las cejas III. 2 amarillos y 2 verdes.
delgadas, ¿qué probabilidad tendrá una pareja de
tener un hijo de cejas gruesas si el hombre es de A) Solo I.
cejas delgadas y la mujer es heterocigota para las B) Solo II.
cejas gruesas? C) Solo I y II.
A) 0%. D) Solo II y III.
B) 25%. E) I, II y III.
C) 50%.
D) 75%.
E) 100%.
BIOLOGÍA MÓDULO COMÚN – CLASE 14 9
PREUNIVERSITARIO PREUCV 2015
DEPARTAMENTO DE CIENCIAS
ORGANISMOS, AMBIENTES Y SUS INTERACCIONES
SUB - EJE: HERENCIA Y EVOLUCIÓN
Guía de Destrezas B – 14: Variabilidad y Herencia.
La siguiente información debe ser usada para responder 15. Según el modelo de herencia mendeliana con
las preguntas 11 y 12. dominancia completa, si el tener pétalos grandes es
un carácter recesivo respecto de tener pétalos
En los pulgones, el color verde oscuro (V) es dominante pequeños, en la descendencia de una planta
sobre el color verde claro (v). Además, las patas con dos homocigota de pétalos pequeños no habrá:
espolones (E) son dominantes sobre las patas con un
espolón (e). I. pétalos grandes.
II. pétalos pequeños.
11. ¿Cómo será el fenotipo de la descendencia al cruzar III. pétalos de tamaño intermedio.
un pulgón verde oscuro (heterocigoto) y patas con
un espolón con otro pulgón verde oscuro A) Solo III.
(homocigoto) y patas con dos espolones B) Solo I y III.
(homocigoto)? C) Solo I y II.
D) Solo II y III.
A) 100% verde oscuro, dos espolones.
E) I, II y III.
B) 50% verde oscuro, dos espolones; 50% verde
oscuro, un espolón.
16. ¿Cuál(es) de los siguientes enunciados
C) 100% verde oscuro, un espolón.
corresponde(n) a una situación de codominancia?
D) 50% verde oscuro, dos espolones; 50% verde claro,
dos espolones. I. Cruce de flores puras azules con flores puras blancas
E) 75% verde oscuro, dos espolones; 25% verde claro, produce descendencia celeste.
dos espolones. II. Roedor blanco con negro que es descendiente de
padre blanco y madre negra, ambos puros.
12. ¿Cómo será el genotipo de la descendencia si se
III. Perro con pelo largo se cruza con una perra de pelo
cruza un pulgón verde claro y dos espolones
corto. La mitad de la descendencia nace con pelo
(heterocigoto) con un pulgón verde oscuro
corto y la otra mitad con pelo largo.
(homocigoto) con dos espolones (heterocigoto)?
A) Solo I.
A) 25% VvEE, 50% VvEe, 25% Vvee.
B) Solo II.
B) 100% VvEe.
C) Solo I y III.
C) 50% VvEE, 50% vvEe.
D) II y III.
D) 25% VVEe, 50% VvEe, 25% vvEe.
E) I, II y III.
E) 50% Vvee, 50% VVEe.
13. En una cruza dihíbrida, AaBb x AaBb, ¿qué fracción 17. Un joven está realizando cruzamientos en una
de la descendencia será homocigota para ambos nueva especie de plantas que, en sus líneas puras,
caracteres recesivos? presentan hojas amarillas o verdes. Si la herencia de
este carácter es de tipo dominancia incompleta,
A) 1/16. ¿cómo será la F1?
B) 1/8.
C) 3/16. A) El total de las hojas será verde amarillento.
D) 1/4. B) La mitad inferior de las hojas será amarilla, la mitad
E) 3/4. superior será verde.
C) Cada hoja presentará tanto el color verde como
14. En un cruzamiento de prueba se obtuvo como amarillo.
descendencia un individuo de fenotipo recesivo. Se D) El 50% de las hojas será verde y el otro 50% será
puede inferir que el individuo puesto a prueba es: amarillo, sin importar su ubicación.
E) Cada hoja tendrá el 50% verde y el 50% amarillo.
A) indeterminable con esta información.
B) fenotipo recesivo, genotipo homocigoto.
C) fenotipo recesivo, genotipo heterocigoto.
D) fenotipo dominante, genotipo homocigoto.
E) fenotipo dominante, genotipo heterocigoto.
10 BIOLOGÍA MÓDULO COMÚN – CLASE 14
PREUNIVERSITARIO PREUCV 2015
DEPARTAMENTO DE CIENCIAS
ORGANISMOS, AMBIENTES Y SUS INTERACCIONES
SUB - EJE: HERENCIA Y EVOLUCIÓN
Guía de Destrezas B – 14: Variabilidad y Herencia.
18. El color de las escamas de un pez del Caribe está 19. Entre una madre del grupo A RH+ (heterocigota
determinado por un gen que posee tres alternativas para ambos caracteres) y un padre B RH+
de alelo: E+, Em, Ea. Estos alelos presentan una (homocigoto para ambos caracteres), ¿cuál de los
gradación respecto a su dominancia: E+> Em > Ea. Si siguientes grupos sanguíneos no es posible
la presencia del alelo E+ indica escamas rojas, el encontrar en su descendencia?
alelo Em indica escamas moradas y el alelo Ea indica
escamas azules, ¿cuál(es) de las siguientes I. AB RH-.
afirmaciones es(son) correcta(s)? II. AB RH+.
III. B RH+.
I. Un pez E+Ea es de color azul.
II. El genotipo EmEa corresponde al fenotipo morado. A) Solo I.
III. Un pez rojo solo puede tener el genotipo E+E+. B) Solo II.
C) Sólo III.
A) Solo I. D) Solo I y II
B) Solo II. E) I, II y III.
C) Solo III.
D) I y II.
E) II y III.
20. Se realiza un experimento con plantas en el que dos individuos parentales se cruzan en tres condiciones distintas
para obtener la siguiente descendencia:
Condición Homocigotos Heterocigotos Homocigotos
dominantes recesivos
1 0 0 34
2 0 0 56
3 0 0 71
Total 0 0 161
La deducción lógica acerca del genotipo de los parentales es que:
A) ambos son homocigotos dominantes.
B) ambos son homocigotos recesivos.
C) uno es dominante y el otro es recesivo.
D) uno es homocigoto recesivo y el otro es heterocigoto.
E) ambos son heterocigotos.
BIOLOGÍA MÓDULO COMÚN – CLASE 14 11
PREUNIVERSITARIO PREUCV 2015
DEPARTAMENTO DE CIENCIAS
ORGANISMOS, AMBIENTES Y SUS INTERACCIONES
SUB - EJE: HERENCIA Y EVOLUCIÓN
Guía de Destrezas B – 14: Variabilidad y Herencia.
12 BIOLOGÍA MÓDULO COMÚN – CLASE 14
PREUNIVERSITARIO PREUCV 2015
DEPARTAMENTO DE CIENCIAS
BIOLOGIA PLAN COMÚN
GENÉTICA II: VARIABILIDAD Y HERENCIA
Eje Temático: Organismos, ambientes y sus interacciones
Sub – Eje: Herencia y Evolución
Tareas: Identificar – Comprender – Distinguir – Interpretar – Reconocer.
HERENCIA LIGADA AL SEXO
Hay algunos caracteres que están determinados por genes que
se encuentran en los cromosomas sexuales y, por tanto, se
heredan a la vez que el sexo. El tipo de herencia de estos
caracteres se denomina herencia ligada al sexo.
Algunas enfermedades que padece la especie humana se
deben a la presencia de algún gen defectuoso en algún
cromosoma. Si el gen defectuoso se localiza en un cromosoma
sexual, las enfermedades a que dé lugar se heredan ligadas el
sexo.
El hombre solo tiene un cromosoma X. Por ello, todos los
genes situados en él se manifestarán, sean dominantes o
recesivos. En cambio, en la mujer, un gen recesivo no se
manifestará si en el otro cromosoma X se encuentra su alelo
dominante. En ese caso se dice que la mujer es portadora, y la
probabilidad de que sus hijos varones exhiban dicho carácter
es del 50%.
Herencia ligada al sexo en seres humanos:
En la especie humana los cromosomas X e Y presentan diferencias
morfológicas (el Y es más pequeño que el X) y tienen distinto
contenido génico. Están compuestos por un segmento homólogo
donde se localizan genes que regulan los mismos caracteres y otro
segmento diferencial.
Cromosoma X: genes ginándricos .
Cromosoma y: genes holándricos
Los caracteres cuyos genes se localizan en el segmento diferencial
del cromosoma X, como daltonismo, hemofilia, ictiosis están
ligados al sexo.
Enfermedades ligadas al sexo:
Por ejemplo, el daltonismo, un tipo de distrofia muscular y la hemofilia son enfermedades determinadas por
genes en el cromosoma X y, por tanto, se heredan ligadas al sexo.
Ambas anomalías se producen por sendos genes recesivos localizados en el cromosoma X.
Daltonismo: Consiste en la incapacidad de distinguir determinados
colores, especialmente el rojo y el verde. Es un carácter regulado por un
gen recesivo localizado en el segmento diferencial del cromosoma X. Los
genotipos y fenotipos posibles son:
–BIOLOGÍA MODULO COMÚN – CLASE 15 13
PREUNIVERSITARIO PREUCV 2015
DEPARTAMENTO DE CIENCIAS
ORGANISMOS, AMBIENTES Y SUS INTERACCIONES
SUB - EJE: HERENCIA Y EVOLUCIÓN
Guía de Destrezas B – 15: Variabilidad y Herencia.
1. Los genes ligados al sexo: 5. En una cruza entre una mosca de la fruta de ojos
blancos (w) y un macho de ojos rojos (w+), ¿qué
I. Se ubican en la porción no homóloga del cromosoma porcentaje de descendientes hembras tendrán ojos
X. blancos? (ojos blancos están ligados al X, recesivo)
II. Se expresan en condición homocigota en los hombres.
III. Incluyen alelos como los que determinan el A) 100%
daltonismo. B) 25%
C) 50%
A) Sólo I D) 75%
B) Sólo III E) 0%.
C) Sólo III
D) Sólo I y III 6. El albinismo es la falta de pigmentación en la piel y es
E) I, II y III ocasionada por un alelo recesivo “a “. La pigmentación
normal se debe a un alelo dominante “A“. Dos
2. En el caso de un gen dominante que se encuentre en progenitores normales tienen un hijo albino. ¿Cuál es la
la porción no homóloga del cromosoma X, es correcto probabilidad de que el siguiente hijo resulte albino?
que:
A) 1/4
I. Se expresa siempre en el varón. B) 1/2
II. Siempre se expresará en las mujeres. C) 3/8
III. Las mujeres presentan una copia del gen. D) 3/4
E) 3/16
A) Sólo I.
B) Sólo II. 7. Si se estudia una enfermedad controlada por un alelo
C) Sólo I y II. dominante ligado al cromosoma X. ¿Qué fenotipos se
D) Sólo II y III. esperan entre los hijos e hijas de un matrimonio donde
E) I, II y III. el hombre está afectado y la mujer es normal?
3. ¿Cuál es la probabilidad de encontrar un hijo sano para A) Hijos e hijas sanos
la Hipercolesterolemia familiar (rasgo autosómico B) Hijos e hijas afectados
dominante) si se cruza un hombre normal con una mujer C) Hombres afectados y mujeres normales
enferma de línea pura? D) Mujeres afectadas y hombres normales.
E) Mujeres portadoras y hombres afectados.
A) 100%
B) 25% 8. Si una mujer normal (no portadora de enfermedad) se
C) 50% casa con un hombre hemofílico, entonces en su
D) 75% descendencia encontraremos:
E) 0%.
I. mujeres que expresan la enfermedad.
4. Los genes Holándricos son transmitidos en un: II. hombres que tienen la enfermedad.
III. mujeres sanas portadoras.
A) 100% a las hembras.
B) 100% a los varones A) Solo I.
C) 50% a los varones y 50% a las hembras. B) Solo II.
D) 75% a los varones y 25% a las hembras. C) Solo III.
E) 75% a las hembras y 25% a los varones. D) Solo II y III.
E) I, II y III
14 BIOLOGÍA MÓDULO COMÚN – CLASE 15
PREUNIVERSITARIO PREUCV 2015
DEPARTAMENTO DE CIENCIAS
ORGANISMOS, AMBIENTES Y SUS INTERACCIONES
SUB - EJE: HERENCIA Y EVOLUCIÓN
Guía de Destrezas B – 15: Variabilidad y Herencia.
9. Una mujer normal y un hombre daltónico tuvieron una 13. En la especie humana un rasgo determinado por un
hija daltónica y un hijo normal. Los genotipos de los gen recesivo ligado al sexo:
padres son:
I) se encuentra con más frecuencia en el varón que en
A) XdXd y XDY. la mujer.
B) XDXD y XdY. II) no se manifiesta en la descendencia femenina a
C) XdXd y XdY. menos que también esté presente en el progenitor
D) XDXd y XdY. paterno.
E) XDXd y XdYd III) el padre afectado no transmite la característica a
sus hijos varones y éstos la presentan si la madre
10. ¿Cómo serán los hijos de un matrimonio en el que el por lo menos es portadora.
varón es de vista normal y la mujer es daltónica?
Es (son) correcta(s)
A) 100% de los hijos daltónicos y 100% de las hijas
portadoras. A) sólo I.
B) 50% mujeres daltónicas y 50% varones portadores. B) sólo II.
C) 50% mujeres daltónicas y 50% varones normales. C) sólo I y II.
D) Los varones normales y las mujeres portadoras. D) sólo II y III.
E) 100% de los hijos e hijas daltónicos. E) I, II y III.
11. De la hemofilia tipo A, es correcto afirmar que: 14. Los portadores de una enfermedad:
I) el gen se ubica en el cromosoma X. A) Se indican con un símbolo lleno en el pedigrí familiar.
II) la persona presenta incapacidad para coagular la B) Producirán solo hijos enfermos.
sangre. C) Son heterocigotos para el gen causante de la
III) los varones afectados transmiten el carácter a sus enfermedad.
hijos y no a sus hijas. D) Son fenotípicamente enfermos.
E) Son genotípicamente homocigotos recesivos.
Es (son) correcta(s)
15. Si se estudia una enfermedad controlada por un alelo
A) sólo I. dominante ligado al cromosoma X. ¿Qué fenotipos se
B) sólo III. esperan entre los hijos e hijas de un matrimonio donde
C) sólo I y II. el hombre está afectado y la mujer es normal?
D) sólo II y III.
E) I, II y III. A) Hijos e hijas sanos.
B) Hijos e hijas afectados.
12. Antonio (del grupo sanguíneo A) y María (del grupo C) Hombres afectados y mujeres normales.
sanguíneo AB) tienen cinco hijos. El padre de Antonio era D) Mujeres afectadas y hombres normales.
grupo A y la madre grupo B. ¿Cuáles son los posibles E) Mujeres portadoras y hombres afectados.
grupos sanguíneos de sus hijos?
16. ¿Qué es una genealogía?
I. A.
II. B. A) Un estudio de sólo las características recesivas de
III. AB. transmisión entre individuos.
B) Un diagrama en donde se identifican los sexos.
Es (son) correcta(s)
C) Un análisis genético de estudio de transferencia de
A) sólo I. características entre familiares y conocidos.
B) sólo II. D) Un análisis de características autosómicas
C) sólo III. dominantes.
D) sólo I y II. E) La representación gráfica de características ligadas al
E) I, II y III. sexo.
BIOLOGÍA MÓDULO COMÚN – CLASE 15 15
PREUNIVERSITARIO PREUCV 2015
DEPARTAMENTO DE CIENCIAS
ORGANISMOS, AMBIENTES Y SUS INTERACCIONES
SUB - EJE: HERENCIA Y EVOLUCIÓN
Guía de Destrezas B – 15: Variabilidad y Herencia.
17. Los árboles genealógicos muestran que cuando el
padre presenta una característica se transmite siempre a
las hijas, en cambio, cuando la madre presenta el rasgo,
lo transmite por igual a hijas e hijos. En base a esto se
puede afirmar que se trata de herencia:
A) Ligada a Y.
B) Recesiva ligada a Y.
C) Autosómica recesiva.
D) Dominante ligada a X.
E) Autosómica dominante.
18. Del árbol genealógico adjunto se desprende que el
rasgo marcado de negro puede representar un caso de A) 4 y 5 son portadores heterocigotos sanos.
herencia: B) 3 expresa la enfermedad.
C) 3 y 4 expresan la enfermedad.
D) 4 y 5 expresan la enfermedad.
E) 6 expresa la enfermedad.
20. En el siguiente árbol genealógico se muestra la
transmisión de una enfermedad autosómica recesiva:
I. ligada al sexo.
II. autosómica recesiva.
III. autosómica dominante.
A) Solo I.
B) Solo II.
C) Solo III.
Si la pareja formada por los individuos 3 y 4 en la
D) Solo I y III.
generación II decide tener un hijo, siendo la madre
E) Solo II y III.
heterocigota, ¿cuál es la probabilidad de que este tenga
la enfermedad?
19. La siguiente genealogía muestra la transmisión de
una enfermedad recesiva ligada al sexo. De acuerdo a
A) Cero.
esta información es correcto inferir que:
B) ¼.
C) ½.
D) ¾.
E) 1.
16 BIOLOGÍA MÓDULO COMÚN – CLASE 15
PREUNIVERSITARIO PREUCV 2014
DEPARTAMENTO DE CIENCIAS
BIOLOGÍA COMÚN
PREUNIVERSITARIO PREUCV 2014
DEPARTAMENTO DE CIENCIAS
BIOLOGIA PLAN COMÚN
Ecología I
Eje Temático: Organismos, ambientes y sus interacciones.
Sub – Eje: Organismos y ambientes
Tareas: Comprender – Interpretar – Resolver.
ECOLOGÍA: FLUJO Y PROCESAMIENTO DE ENERGÍA Y MATERIA EN LOS SISTEMAS BIOLÓGICOS.
La FOTOSÍNTESIS puede definirse como un proceso anabólico que se produce en los cloroplastos y en el que la
energía luminosa es transformada en energía química que posteriormente será empleada para la fabricación de
sustancias orgánicas a partir de sustancias inorgánicas.
FACTORES QUE INFLUYEN EN LA FOTOSÍNTESIS
El rendimiento de la fotosíntesis puede ser medido
fácilmente por la cantidad de CO2 absorbido por la
planta. En él influyen:
A. La intensidad y longitud de onda de la luz.
B. Temperatura.
C. Concentración de CO2
D. Concentración de O2
CADENAS TRÓFICAS
La cadena trófica describe el proceso de
transferencia de sustancias nutritivas a través
de las diferentes especies de una comunidad
biológica, en el que cada uno se alimenta del
precedente y es alimento del siguiente.
–BIOLOGÍA MODULO COMÚN – CLASE 16 17
PREUNIVERSITARIO PREUCV 2014
DEPARTAMENTO DE CIENCIAS
ORGANISMOS, AMBIENTES Y SUS INTERACCIONES.
SUB - EJE: ORGANISMOS Y AMBIENTES.
Guía de Destrezas B – 16: Ecología.
PIRAMIDE ECOLÓGICA: Una pirámide ecológica es una representación gráfica que permite conocer el número de
organismos, relaciones de la energía y la biomasa de un ecosistema.
Se distinguen tres pirámides ecológicas:
1. Pirámide de Biomasa.
2. Pirámide de Energía.
Pirámide de Números
1. ¿Qué es la fotosíntesis? 3. Los factores que influyen en la tasa fotosintética son:
A) Proceso que permite a las plantas utilizar los I. la temperatura.
nutrientes que ha fabricado solo a partir de agua y II. la intensidad de la luz.
sales disueltas en el medio. III. la concentración de CO2.
B) Proceso que utiliza sustancias orgánicas complejas
presentes en medio para sintetizar sustancias más A) Solo I
simples. B) Solo I y II
C) Proceso que utiliza la luz solar para sintetizar C) Solo I y III
compuestos complejos a partir de sustancias D) Solo II y III
sencillas disponibles en el medio. E) I, II y III
D) Proceso realizado por algas, plantas y bacterias que
utiliza CO2 y luz solar para fabricar glucosa como 4. ¿Qué secuencia refleja con precisión el flujo de
alimento. electrones en la fotosíntesis?
E) Proceso de transforma la materia orgánica en
inorgánica a través de la fuente energética de la luz. A) H2O → fotosistema II → fotosistema I → NADP
B) H2O → fotosistema I → fotosistema II → NADP
2. En la ecuación de la fotosíntesis, los productos y C) Fotosistema I → fotosistema II → NADP → H2O
reactantes corresponden respectivamente a: D) Fotosistema II →fotosistema I → NADP → H2O
E) Fotosistema I → fotosistema II → H2O → NADP
A + B + energía solar→ C+D
5. ¿Cuál es la relación correcta entre función y etapa de
En donde A, B, C y D corresponden respectivamente a: la fotosíntesis?
A) CO2- H2O-O2- C6H12O6 A) Ciclo de Calvin – Fase clara.
B) H2O-O2- C6H12O6- CO2 B) Fotólisis del agua – Fase oscura.
C) O2- C6H12O6- CO2- H2O C) Fijación del carbono – Fase oscura.
D) C6H12O6- CO2- H2O - O2 D) Catálisis de la rubisco – Fase clara.
E) C6H12O6- H2O- CO2 - O2 E) Formación de oxígeno – Fase oscura.
18 BIOLOGÍA MÓDULO COMÚN – CLASE 16
PREUNIVERSITARIO PREUCV 2014
DEPARTAMENTO DE CIENCIAS
ORGANISMOS, AMBIENTES Y SUS INTERACCIONES.
SUB - EJE: ORGANISMOS Y AMBIENTES.
Guía de Destrezas B – 16: Ecología.
6. Si tuviésemos dos placas de Petri, ambas con una 9. Acerca de las tramas alimentarias, es correcto
gran cantidad de bacterias quimiosintetizadoras, pero a afirmar que:
la placa A la colocamos a la luz solar y a la placa B se le
pone una gran cantidad de minerales, entonces al cabo I. la energía fluye de manera cíclica por ella.
de 48 horas se espera que: II. la energía siempre fluye de productores a
consumidores.
I. las bacterias en la placa A mueran paulatinamente por III. están formadas por varias cadenas alimentarias
falta de nutrientes. independientes.
II. las bacterias en la placa B se reproduzcan y
aumenten su número. A) Solo I
III. las bacterias de la placa A y B mueran por falta de B) Solo II
nutrientes. C) Solo III
D) Solo I y III
A) Solo I E) I, II y III
B) Solo II
C) Solo III 10. ¿Cuál de las siguientes afirmaciones sobre las
D) Solo I y II tramas tróficas es correcta?
E) Solo I y III
A) La punta de la flecha indica el organismo que se
está consumiendo.
7. ¿Cuál es el orden en que ocurren los siguientes pasos B) El origen de la energía de las tramas tróficas
de la fotosíntesis? proviene de los herbívoros.
I. Captación de luz por la clorofila. C) Muestra la relación que existe entre un productor,
II. Formación de NADPH. un consumidor primario y uno secundario.
III. Fijación del carbono. D) Puede mostrar que un organismo puede ser
IV. Fotólisis del agua. consumido por más de un animal.
E) Siempre tiene que mostrar consumidores
A) II – I – III – IV. terciarios.
B) I – II – III – IV.
C) I – II – IV – III. 11. El siguiente esquema representa una cadena
D) I – IV – II – III. trófica:
E) II – IV – III – I.
8. Se marcan radiactivamente los carbonos del dióxido Considerando que estos organismos se alimentan
de carbono (CO2) consumido por una planta durante el exclusivamente el uno del otro, ¿cuál sería el efecto si
día. El (los) compuesto(s) formado(s) por la planta en eliminamos a X de esta cadena?
que pueden aparecer las marcas radiactivas es(son):
I. No afectará al aguilucho.
I. la glucosa. II. Se observará un aumento del pasto.
II. el almidón. III. Generará una disminución de la población de
III. otras moléculas orgánicas como proteínas y zorzales.
vitaminas.
A) Solo I
A) Solo I B) Solo I y II
B) Solo II C) Solo I y III
C) Solo I y II D) Solo II y III
D) Solo II y III E) I, II y III
E) I, II y III
BIOLOGÍA MÓDULO COMÚN – CLASE 16 19
PREUNIVERSITARIO PREUCV 2014
DEPARTAMENTO DE CIENCIAS
ORGANISMOS, AMBIENTES Y SUS INTERACCIONES.
SUB - EJE: ORGANISMOS Y AMBIENTES.
Guía de Destrezas B – 16: Ecología.
12. En el siguiente esquema se presentan las 15. Con respecto a las pirámides de número, de
relaciones tróficas de tres especies (A, B y C). El biomasa y de energía es correcto afirmar que:
signo + indica una relación benéfica y el signo –
I. La pirámide de número y de biomasa puede
indica relación perjudicial.
invertirse, si los organismos productores son más
grandes en promedio que los consumidores.
II. La pirámide de energía siempre presenta forma de
pirámide bajo la condición que se consideran
todas las fuentes de energía alimenticia.
III. La pirámide de número siempre presenta forma de
pirámide real, ya que los productores siempre son
¿Cuál(es) de las siguientes afirmaciones es (son)
más pequeños que los consumidores.
correcta(s) en relación con el esquema?
A) Sólo I
I. La especie B se ve perjudicada por A y por C. B) Sólo II
II. La especie A beneficia a la especie C, pues depreda a C) Sólo III
B. D) Sólo I y II
III. La especie C se ve perjudicada por B y beneficiada E) Sólo II y III
por A.
16. El flujo de energía de los seres vivos responde a las
A) Solo I. leyes de la termodinámica, dentro de las cuales la
B) Solo II. segunda ley es la llamada ley de la entropía, que
C) Solo III. postula que cada vez que la energía se transforma,
D) Solo II y III. parte de ella se degrada a una forma no
E) I, II y III. aprovechable, como el calor. Al aplicar este
enunciado en los fenómenos biológicos, podemos
13. Dado que los organismos descomponedores deducir que:
actúan sobre el último nivel de la cadena trófica I. las cadenas tróficas ven limitados sus niveles por la
(que posee la menor energía), se podría entender pérdida de energía en cada traspaso de nivel.
que su aporte al ecosistema es irrelevante, pues la II. los productores, al ser el primer nivel trófico, no
cantidad de energía que pueden reincorporar a la pierden energía en forma de calor.
cadena es marginal. Sin embargo, estos organismos III. en las tramas tróficas pueden existir cadenas con
son fundamentales, dado que: siete niveles, dado que se compensa la baja energía
con la proveniente de otras cadenas más cortas.
A) La pérdida de energía es insignificante.
B) Son capaces de inyectar energía al ecosistema. A) Solo I
C) Lo importante no es la cantidad de energía, sino el B) Solo I y II
tipo. C) Solo I y III
D) La energía del último nivel aún es útil para los D) Solo II y III
productores. E) I, II y III
E) Su función en el ecosistema es el reciclaje de
materia, no de energía. 17. ¿De qué manera el carbono ingresa a los
organismos presentes en un ecosistema?
14. Si en una cadena trófica el consumidor terciario
recibe 5 kcal, ¿cuánta energía contiene el I. Mediante la fotosíntesis.
productor? II. Gracias a la presencia de plantas.
III. Gracias a la presencia de hongos.
A) 500.000 A) Solo I.
B) 50.000 B) Solo II.
C) 5.000 C) Solo III.
D) 500 D) I y II.
E) 50 E) I, II y III.
20 BIOLOGÍA MÓDULO COMÚN – CLASE 16
PREUNIVERSITARIO PREUCV 2014
DEPARTAMENTO DE CIENCIAS
ORGANISMOS, AMBIENTES Y SUS INTERACCIONES.
SUB - EJE: ORGANISMOS Y AMBIENTES.
Guía de Destrezas B – 16: Ecología.
18. El rol de los productores dentro del ciclo del 20. En un predio agrícola se realizó una prueba con
nitrógeno es: distintas mezclas que contenían fósforo y
nitrógeno, y que podrían actuar como fertilizantes.
Las mezclas tenían las siguientes formulaciones:
A) Fijar el nitrógeno atmosférico.
B) Devolver el nitrógeno a la atmósfera.
Mezcla Sustancia con Sustancia con
C) Transformar N2 en formas asimilables.
fósforo nitrógeno
D) Degradar proteínas hasta formas inorgánicas del
1 Nitrato Fosfato
nitrógeno.
2 Nitrito Fosfato
E) Transformar nitrógeno inorgánico en formas
orgánicas para la cadena trófica. 3 Amonio Fosfina
4 Nitrato Fosfina
19. El siguiente gráfico muestra la evolución de la 5 Amonio Fosfato
concentración atmosférica de CO2 a lo largo de los
últimos siglos: ¿Cuál de las mezclas resultaría un mejor fertilizante?
A) 1.
B) 2.
C) 3.
D) 4.
E) 5.
¿Qué se puede inferir acerca de las variaciones que
ha experimentado el ciclo del carbono desde la
revolución industrial?
A) Un desbalance entre la fijación de carbono y la
emisión a la atmósfera.
B) Los heterótrofos han aumentado su población y su
tasa de respiración.
C) Ha disminuido la transferencia de carbono dentro
de la cadena trófica.
D) Ha disminuido la fotosíntesis en ecosistemas
marinos.
E) Se ha incrementado la formación de petróleo.
BIOLOGÍA MÓDULO COMÚN – CLASE 16 21
PREUNIVERSITARIO PREUCV 2014
DEPARTAMENTO DE CIENCIAS
ORGANISMOS, AMBIENTES Y SUS INTERACCIONES.
SUB - EJE: ORGANISMOS Y AMBIENTES.
Guía de Destrezas B – 16: Ecología.
22 BIOLOGÍA MÓDULO COMÚN – CLASE 16
PREUNIVERSITARIO PREUCV 2015
DEPARTAMENTO DE CIENCIAS
BIOLOGIA PLAN COMÚN
Ecología de poblaciones.
Eje Temático: Organismo, ambientes y sus interacciones.
Sub – Eje: Organismos y ambientes.
Tareas: Identificar – Comprender – Distinguir – Interpretar – Reconocer.
POBLACIÓN Y COMUNIDAD
POBLACIÓN
La población es un conjunto de organismos de la misma especie que ocupan
un área más o menos definida y que comparten determinado tipo de
alimentos.
Aunque cada especie suele tener una o más poblaciones distribuidas cada
una en un área predeterminada, no existe ningún impedimento para que
dos poblaciones de una misma especie se fusionen ni tampoco para que una
población se divida en dos.
PROPIEDADES DE LAS POBLACIONES:
1. DENSIDAD:
Corresponde al número de individuos de la misma especie que habitan en una unidad de superficie.
DEPENDE DE 4 FACTORES:
1) Natalidad.
2) Inmigración
3) Mortalidad
4) Emigración
2. DISTRIBUCIÓN: Es la forma en que los individuos están dispersos dentro del área habitada por la población:
(a) Azar o Aleatorio.
(b) Agrupado o Conglomerado.
(c) Regular o Uniforme
3. CRECIMIENTO POBLACIONAL
- crecimiento exponencial
- crecimiento logístico
4. ESTRATEGIA DE VIDA: r y K
5. ESTRUCTURA DE EDADES DE POBLACIONES: Predice su crecimiento
COMUNIDAD:
Término biológico que hace referencia a los seres
vivos presentes en un ecosistema. Podría definirse como el
conjunto
de poblaciones biológicas
que comparten un área
determinada y difieren en
el tiempo. Una comunidad
puede ser definida a
cualquier
nivel taxonómico o
funcional y escala geográfica.
–BIOLOGÍA MODULO COMÚN – CLASE 17 23
PREUNIVERSITARIO PREUCV 2015
DEPARTAMENTO DE CIENCIAS
ORGANISMOS, AMBIENTES Y SUS INTERACCIONES
SUB - EJE: ORGANISMOS Y AMBIENTES
Guía de Destrezas B – 17: Ecología de Poblaciones
Se llama SUCESIÓN ECOLÓGICA a la evolución que se da
de manera natural, produciendo que un ecosistema por su
propia dinámica interna sustituya a los organismos que lo
integran. El término alude a que su aspecto esencial en la
sustitución a lo largo del tiempo de unas especies por
otras.
1. ¿Cuál(es) de las siguientes afirmaciones sobre las 4. ¿Cuál sería el efecto en una población cuya tasa de
poblaciones es(son) correcta(s)? emigración es mayor que la tasa de inmigración?
I. Puede estar formada por dos especies que habitan A) La población se reduciría a la mitad
el mismo lugar. inmediatamente.
II. Los individuos habitan en el mismo sitio y período B) La población aumentaría dada la llegada de nuevos
de tiempo. individuos
III. La población puede interactuar con poblaciones de C) La población aumentaría dada la salida de nuevos
otras especies. individuos.
A) Solo I. D) Si la tasa de natalidad es baja, no se vería un efecto
B) Solo II. perjudicial.
C) Solo III. E) Si la tasa de natalidad es baja y la de mortalidad alta,
D) I y III. la población disminuiría.
E) II y III.
5. El siguiente gráfico presenta el resultado del
2. Los organismos habitan en lugares determinados muestreo del número de peumos a distintas
interactúan con otros individuos, pero estos altitudes en un cerro.
también se relacionan con componentes físicos del En relación con este gráfico, el patrón de
ambiente, los llamados factores abióticos. De las distribución espacial que presenta esta población
alternativas que se mencionan a continuación, la es:
que no corresponde a un factor abiótico es:
A) el pH.
B) las aves.
C) el oxígeno.
D) la temperatura.
E) la luz.
3. ¿Cuál(es) de los siguientes factores puede(n) llevar
a un crecimiento poblacional?
I. Disminución del espacio que habita una población.
II. Aumento del alimento que consume la población. A) azaroso.
III. Disminución de las especies que compiten por el B) aleatorio.
espacio con la población. C) uniforme.
D) agregado.
A) Solo I.
E) conglomerado.
B) Solo II.
C) Solo III.
D) Solo I y II.
E) Solo II y III.
24 BIOLOGÍA MÓDULO COMÚN – CLASE 17
PREUNIVERSITARIO PREUCV 2015
DEPARTAMENTO DE CIENCIAS
ORGANISMOS, AMBIENTES Y SUS INTERACCIONES
SUB - EJE: ORGANISMOS Y AMBIENTES
Guía de Destrezas B – 17: Ecología de poblaciones.
6. El siguiente gráfico muestra un crecimiento 8. Lo que se observa en el gráfico de pirámide de
exponencial de una cepa bacteriana en una placa de edades, corresponde a una población:
Petri, hasta una hora después de haberse iniciado el
cultivo. Este tipo de crecimiento exponencial se tiene
que realizar correctamente sí:
I) Estable. II) En retroceso. III) En expansión.
A) La tasa de mortalidad es cero.
B) La tasa de natalidad es constante. A) Sólo I.
C) Aún no se ocupa todo el espacio físico. B) Sólo II.
D) La capacidad de carga es infinita. C) Sólo III.
E) Aún es baja la resistencia ambiental. D) I y II.
E) I y III.
7. Un grupo de estudiantes ha realizado un pequeño
ecosistema en un terrario con chanchitos de tierra. Al 9. Las poblaciones tienen estrategias de crecimiento. De
cabo de un tiempo se dan cuenta de que la población ello surgen dos tipos de estrategias, R y K, de las
de chanchitos de tierra no aumenta ni disminuye, tal cuales se puede afirmar correctamente que:
como se presenta en el siguiente gráfico.
I. los estrategas R y K tienen muchas crías para asegurar
su descendencia.
II. los estrategas R son de tamaño pequeño y los K son de
tamaño mayor.
III. los estrategas K presentan curva de sobrevivencia tipo
I y los R del tipo II o III.
A) Solo I.
B) Solo II.
C) Solo III.
D) Solo I y III.
De este experimento se puede concluir que: E) I, II y III.
I. la población de chanchitos de tierra ha llegado a la
10. La población de toninas del canal de Chacao se
capacidad de carga.
determinó que durante el año 2012 estuvo
II. si se añaden más alimentos al terrario,
constituida por 1.007 individuos. Durante el año
probablemente aumentará la población hasta
2013 nacieron 154 crías y murieron 72 individuos.
alcanzar la capacidad de carga.
Se detectó la emigración de 40 individuos y la
III. si los estudiantes agregaran nuevos chanchitos de
inmigración de 56 individuos. Con los datos
tierra, sobrepasarían la capacidad de carga y
presentados, ¿cuál es el valor de la tasa de
comenzarían a morir los individuos.
crecimiento poblacional de estas toninas?
A) Solo I.
A) 15.
B) Solo II.
B) 30.
C) Solo III.
C) 71.
D) Solo I y III.
D) 138.
E) I, II y III.
E) 152.
BIOLOGÍA MÓDULO COMÚN – CLASE 17 25
PREUNIVERSITARIO PREUCV 2015
DEPARTAMENTO DE CIENCIAS
ORGANISMOS, AMBIENTES Y SUS INTERACCIONES
SUB - EJE: ORGANISMOS Y AMBIENTES
Guía de Destrezas B – 17: Ecología de Poblaciones
11. ¿Cómo puede definirse una comunidad? 14. ¿Cuál de los siguientes casos corresponde a un
ejemplo de competencia?
A) Es una relación entre los factores bióticos y
abióticos presentes en un lugar determinado. A) Jirafa que se alimenta de hojas de un árbol.
B) Interacción entre los individuos de una misma B) Cebras y ñu ocupan el mismo hábitat.
especie que habitan en un determinado lugar y C) Pez payaso que habita en las anémonas.
tiempo. D) Pez rémora que nada junto a tiburón.
C) Interacción entre organismos de distintas especies E) Lombriz solitaria que habita en el intestino humano.
que habitan en un tiempo y lugar determinado.
D) Formación de pequeños grupos dentro de una 15. La siguiente ilustración corresponde a un diagrama
población determinada que interactúan con otros hipotético de parte del nicho espacial de dos
grupos de dicha población. especies S1 y S2.
E) Relación entre los individuos de una población con
los factores ambientales del hábitat que utilizan.
12. Dentro de las comunidades existen las llamadas
sucesiones ecológicas, las cuales presentan un
criterio de sucesos. Ordena correctamente las fases
de las sucesiones ecológicas que permitan visualizar
el asentamiento de las comunidades.
A) Fase exploratoria – clímax ecológico – fase gradual
de cambio.
B) Fase gradual de cambio – clímax ecológico – fase
exploratoria.
C) Clímax ecológicos – fase exploratoria – fase gradual De este diagrama es correcto afirmar que:
de cambio.
D) Fase exploratoria – fase gradual de cambios – clímax I. S2 vive en ambientes más cálidos y con menor
ecológico. humedad.
E) Fase gradual de cambio – fase exploratoria – clímax II. ambas especies compiten en una humedad cercana al
ecológico. 100 %.
III. ambas especies compiten entre los 0º y 10º C de
13. La sucesión ecológica es un evento fundamental en temperatura.
los ecosistemas dado que: A) Solo I.
B) Solo II
I. permite que nuevos ecosistemas se creen en C) Solo III.
ambientes modificados. D) Solo I y III.
II. permite la eliminación de los ecosistemas en caso E) I, II y III.
de que sea alterado el hábitat.
III. impide que nuevas comunidades de organismos se 16. ¿Qué factor(es) puede(n) llevar a la competencia
establezcan en sitios destruidos por el hombre o intraespecífica?
naturalmente.
I. La disponibilidad de alimento.
A) Solo I. II. El espacio disponible.
B) Solo II III. Presencia de hembras en período reproductivo.
C) Solo I y II.
A) Solo I.
D) Solo I y III.
B) Solo III.
E) I, II y III.
C) I y II.
D) II y III.
E) I, II y III.
26 BIOLOGÍA MÓDULO COMÚN – CLASE 17
PREUNIVERSITARIO PREUCV 2015
DEPARTAMENTO DE CIENCIAS
ORGANISMOS, AMBIENTES Y SUS INTERACCIONES
SUB - EJE: ORGANISMOS Y AMBIENTES
Guía de Destrezas B – 17: Ecología de poblaciones.
17. ¿Qué tipo de relación se establece entre dos 20. Esta imagen corresponde a la relación trófica
individuos en el amensalismo? denominada mutualismo, de la cual es correcto
afirmar que:
A) +/+
B) +/–
C) –/–
D) –/0
E) +/0
18. Son ejemplos de depredación las siguientes
situaciones:
I. una vaca pastando en una pradera.
II. un león alimentándose de una gacela. I. ambas mejoran su capacidad de sobrevivir y
III. una pulga consumiendo sangre de un perro. reproducirse.
II. la flor se beneficia al ser polinizada y el picaflor se
A) Solo I. beneficia con la alimentación.
B) Solo II. III. para que este mutualismo sea efectivo, ambas
C) Solo III. deben vivir en hábitats diferentes.
D) Solo II y III.
E) I, II y III. A) Solo I.
B) Solo I y II.
19. En una comunidad biológica, la eliminación de C) Solo I y III.
depredadores carnívoros traería como D) Solo II y III.
consecuencias: E) I, II y III.
I. La disminución de la densidad de la población
productora.
II. La muerte por inanición al cabo de un tiempo de
muchos herbívoros.
III. El aumento de la densidad de la población productora.
IV. El aumento de la densidad de la población herbívora,
inmediatamente después de la eliminación de los
depredadores.
A) Solo I.
B) Solo I y II.
C) Solo III.
D) Solo II y IV
E) Solo I, II y IV.
BIOLOGÍA MÓDULO COMÚN – CLASE 17 27
PREUNIVERSITARIO PREUCV 2015
DEPARTAMENTO DE CIENCIAS
ORGANISMOS, AMBIENTES Y SUS INTERACCIONES
SUB - EJE: ORGANISMOS Y AMBIENTES
Guía de Destrezas B – 17: Ecología de Poblaciones
28 BIOLOGÍA MÓDULO COMÚN – CLASE 17
PREUNIVERSITARIO PREUCV 2015
DEPARTAMENTO DE CIENCIAS
BIOLOGIA PLAN COMÚN
Ecosistemas.
Eje Temático: Organismos, ambientes y sus interacciones.
Sub – Eje: Organismos y ambientes
Tareas: Identificar – Comprender – Distinguir – Interpretar – Reconocer.
ECOSISTEMA:
El ecosistema es el conjunto de especies de un área determinada
que interactúan entre ellas y con su ambiente abiótico; mediante
procesos como la depredación, el parasitismo, la competencia y la
simbiosis, y con su ambiente al desintegrarse y volver a ser parte del
ciclo de energía y de nutrientes. Las especies del ecosistema,
incluyendo bacterias, hongos, plantas y animales dependen unas de
otras. Las relaciones entre las especies y su medio, resultan en el
flujo de materia y energía del ecosistema.
CICLOS BIOGEOQUIMICOS
Además de la energía, los organismos requieren para vivir el
suministro de elementos químicos que se pueden encontrar
en la biósfera, pero que deben ser reciclados constantemente,
a fin de asegurar su disponibilidad. Este proceso se
denomina ciclos de la materia o ciclos biogeoquímicos.
Los seres vivos toman carbono, nitrógeno y oxígeno y los usan para
vivir y crecer. Si están sustancias solo se usaran una vez, se habrían
agotado. Todos los animales y plantas respiran, crecen y, finalmente
mueren y se descomponen. La descomposición libera las sustancias
de su cuerpo a la biósfera para que se utilicen de nuevo
Efectos de la intervención humana en el planeta.
–BIOLOGÍA MODULO COMÚN – CLASE 18 29
PREUNIVERSITARIO PREUCV 2015
DEPARTAMENTO DE CIENCIAS
ORGANISMOS, AMBIENTES Y SUS INTERACCIONES
SUB - EJE: ORGANISMOS Y AMBIENTES
Guía de Destrezas B – 18: Ecosistemas
1. ¿Cuál(es) de las siguientes afirmaciones 5. ¿Cuál(es) de las siguientes opciones
corresponde(n) a ecosistema? corresponde(n) a problemas ambientales
ocasionados por el hombre?
I. Corresponde a una interacción entre biocenosis y
biotopo. I. Tala indiscriminada de árboles.
II. Se puede observar flujo de materia. II. Agotamiento de los océanos.
III. Existe flujo de energía. III. Desertificación.
A) Solo II. A) Solo I.
B) Solo III. B) Solo II.
C) I y II. C) I y II.
D) I y III. D) II y III.
E) I, II y III. E) I, II y III.
2. ¿Qué factor abiótico puede influir en un 6. El crecimiento de la población humana supone un
ecosistema? fuerte impacto en el ecosistema, ya que una
población biológica muy grande:
I. Las precipitaciones.
II. La presencia de depredadores. I. Requiere más recursos de los que están
III. La temperatura ambiental. disponibles.
A) Solo I. II. Requiere más espacio y desplaza a otras
B) Solo III. poblaciones.
C) I y III. III. Elimina gran cantidad de desechos, muchos de
D) II y III. ellos tóxicos.
E) I, II y III.
A) Solo I.
3. ¿Qué se entiende por “huella ecológica”? B) Solo I y II.
C) Solo I y III.
A) Uso de recursos para satisfacer las necesidades D) Solo II y III.
humanas. E) I, II y III.
B) Espacio que requiere cualquier animal para
satisfacer sus necesidades. 7. Este contaminante proviene mayormente de la
C) Impacto que generan los animales sobre el quema de combustibles fósiles es el principal
ambiente en el que habitan. causante del efecto invernadero y debido a él la
D) Utilización de recursos y generación de desechos temperatura del planeta aumentó durante el siglo
por parte de los animales. XX entre 0,4 y 0,8 ºC en promedio. ¿A qué
E) Ubicación de zonas más afectadas por los contaminante se hace referencia?
asentamientos humanos.
A) CH4.
4. ¿Qué consecuencia(s) trae el hecho de haber
B) NH3.
convertido diversos ambientes en ciudades?
C) NO2.
I. Disminución de los árboles.
D) CO2.
II. Aumento de los gases invernadero.
E) SO2.
III. Extinción de diversas especies de flora y fauna.
A) Solo I.
B) Solo II.
C) I y II.
D) II y III.
E) I, II y III.
30 BIOLOGÍA MÓDULO COMÚN – CLASE 18
PREUNIVERSITARIO PREUCV 2015
DEPARTAMENTO DE CIENCIAS
ORGANISMOS, AMBIENTES Y SUS INTERACCIONES
SUB - EJE: ORGANISMOS Y AMBIENTES
Guía de Destrezas B – 18: Ecosistemas.
8. ¿Cuál(es) de las siguientes sustancia(s) es (son) 11. El siguiente gráfico presenta el efecto de los
causante(s) de la contaminación del aire? pesticidas sobre un grupo de sujetos expuestos a
tales sustancias. A partir del análisis del gráficos
A) Sedimentos. es(son) correcta(s):
B) Uso de CFC.
C) Uso de pesticidas.
D) Desechos nucleares.
E) Uso excesivo de nutrientes
9. ¿Qué medida(s) ayuda(n) de manera efectiva a
disminuir los residuos sólidos de nuestro país?
I. Separar la basura y dejarla para que la recoja el
camión recolector.
II. Clasificar la basura y llevarla separada a depósitos
especializados.
III. Limitar la cantidad de residuos que pueden ser
eliminados por cada hogar.
Fuente: M. Sanborn (2007) Non-cancer health effects of
A) Solo I. pesticides: systematic review and implications for family
B) Solo II. doctors.
C) Solo III.
D) I y II. I. La exposición a pesticidas aumenta el riesgo de
E) II y III. presentar aberraciones cromosómicas.
II. Los sujetos expuestos a pesticidas duplicaron la
10. Dentro de las estrategias para la conservación de la frecuencia de aberraciones cromosómicas.
biodiversidad podemos mencionar: III. A una menor exposición a pesticidas, menor es
la probabilidad de presentar aberraciones
I. Crear áreas de protección de ecosistemas. cromosómicas.
II. Controlar el traslado de especies invasoras.
III. Crear corredores biológicos para conectar A) Solo I
ecosistemas. B) Solo II
C) Solo I y II
A) Solo I D) Solo II y III
B) Solo I y II. E) I, II y III
C) Solo I y III.
D) Solo II y III. 12. Dentro del impacto del ser humano sobre el
E) I, II y III. ecosistema está la deforestación. Al respecto se
estima que a nivel mundial se pierden diariamente
20.000 hectáreas de bosques. ¿Qué consecuencias
puede tener esta acción?
I. Elimina productores de la cadena trófica.
II. Aumenta la cantidad de CO2 en la atmósfera.
III. Pone en peligro de extinción a especies vegetales y
animales.
A) Solo II.
B) Solo I y II.
C) Solo I y III.
D) Solo II y III.
E) I, II y III.
BIOLOGÍA MÓDULO COMÚN – CLASE 18 31
PREUNIVERSITARIO PREUCV 2015
DEPARTAMENTO DE CIENCIAS
ORGANISMOS, AMBIENTES Y SUS INTERACCIONES
SUB - EJE: ORGANISMOS Y AMBIENTES
Guía de Destrezas B – 18: Ecosistemas
13. Hace algunos años, un grupo de científicos trajo 16.La tabla que se presenta a continuación contiene
ejemplares de ranas de la especie Xenopus laevis. información acerca de las causas del deterioro
Al ser liberada, atacó a una rana autóctona de ambiental y su contribución relativa. Comisión
Chile, Caudiverbera caudiverbera, y utilizó su Nacional del Medio Ambiente (CONAMA).
hábitat. ¿A qué tipo de problema ambiental
corresponde el anterior?
A) Consecuencias de la desertificación.
B) Introducción de especies foráneas.
C) Sobreexplotación de los océanos.
D) Contaminación del suelo.
E) Control de plagas.
14.Una industria agrícola, de manera ilícita, comienza a
liberar residuos de fertilizantes a un lago cercano a De los datos contenidos en la tabla es posible afirmar
la fábrica. ¿Qué se desencadenará en este lago si la que:
empresa continúa con esta práctica?
I. la principal causa de deterioro de suelos es la
A) El aumento de nutrientes en el lago. erosión por agua.
B) La disminución de nutrientes y, con ello, la pérdida II. la acción humana contribuye con un 22,8% de
del lago. los problemas de pérdida de suelo.
C) El aumento de animales en el lago y, con ello, un III. el aumento de áreas urbanas e industriales
mejoramiento en el ecosistema. ocupa el tercer lugar de las causas de deterioro.
D) La eutrofización del lago y, con ello, la destrucción
de todo el ecosistema presente. A) Solo I
E) No se alteraría el equilibrio natural, pues los B) Solo I y II.
fertilizantes ayudan a que los productores del lago C) Solo I y III.
sean más eficientes. D) Solo II y III.
E) I, II y III.
15. ¿Qué acciones humanas causa(n) un efecto
indirecto sobre las especies de flora y fauna? 17. Si el Servicio Agrícola y Ganadero detecta un tráfico
ilegal de animales extranjeros que no se encuentra
I. Aumento de la temperatura del planeta, derritiendo naturalmente en Chile, ¿qué acción es más
el hielo de los polos. adecuada respecto al animal, pensando en
II. La creación de nuevas ciudades en lugares prevenir impactos ambientales perjudiciales?
previamente ocupados por bosques.
III. Deforestación para crear nuevos campos de cultivos. A) Devolverlo a su lugar de procedencia.
B) Confiscarlo y encerrarlo hasta que muera
A) Solo I. naturalmente.
B) Solo II. C) Permitir su ingreso bajo pago de multa, pues no
C) I y II. debe morir.
D) II y III. D) Confiscarlo y liberarlo en bosques autóctonos para
E) I y III. que sobreviva por su cuenta.
E) Hacer firmar al propietario un documento que lo
comprometa a tenerlo bajo resguardo
32 BIOLOGÍA MÓDULO COMÚN – CLASE 18
PREUNIVERSITARIO PREUCV 2015
DEPARTAMENTO DE CIENCIAS
ORGANISMOS, AMBIENTES Y SUS INTERACCIONES
SUB - EJE: ORGANISMOS Y AMBIENTES
Guía de Destrezas B – 18: Ecosistemas.
18. ¿Qué consecuencia(s) se ha(n) podido observar por
efecto del calentamiento global? 20. Algunos ejemplos de reglamentos nacionales para
la conservación de nuestra biodiversidad es son:
I. Cambios en la distribución de vegetales.
II. Disminución de las temperaturas máximas. I. Protección de algunas especies animales en parques
III. Disminución de las reservas de agua dulce por y reservas.
derretimiento de los glaciares. II. Creación de los libros rojos de la flora y fauna sobre
las especies amenazadas.
A) Solo I. III. Prohibición de la explotación de árboles amenazados
B) Solo II. de extinción, como la araucaria, el alerce y el raulí.
C) Solo III.
D) I y III. A) Solo I
E) I, II y III. B) Solo I y II.
C) Solo I y III.
19. ¿Cuál(es) de las siguientes acciones genera(n) un D) Solo II y III.
gran impacto negativo sobre la fauna mundial? E) I, II y III.
I. Caza de elefantes para obtener el marfil para venta
internacional.
II. Caza de ballenas con fines científicos y
comerciales.
III. Cría de pollos en una parcela para consumo
personal.
A) Solo I.
B) Solo III.
C) I y II.
D) II y III.
E) I, II y III.
BIOLOGÍA MÓDULO COMÚN – CLASE 18 33
PREUNIVERSITARIO PREUCV 2015
DEPARTAMENTO DE CIENCIAS
ORGANISMOS, AMBIENTES Y SUS INTERACCIONES
SUB - EJE: ORGANISMOS Y AMBIENTES
Guía de Destrezas B – 18: Ecosistemas
34 BIOLOGÍA MÓDULO COMÚN – CLASE 18
PREUNIVERSITARIO PREUCV 2015
DEPARTAMENTO DE CIENCIAS
FUERZA Y MOVIMIENTO
MATERIA Y SU TRANSFORMACIÓN
Curso Física
Materia y su transformación: Calor y Equilibrio Térmico 37
Guía de Destrezas F-13 39
Tierra y Universo: Modelos Del Universo 43
Guía de Destrezas F-14 45
Tierra y Universo: La Tierra, El Sistema Solar Y Universo. 49
Guía de Destrezas F-15 51
FÍSICA PLAN COMÚN 35
PREUNIVERSITARIO PREUCV 2015
DEPARTAMENTO DE CIENCIAS
FUERZA Y MOVIMIENTO
MATERIA Y SU TRANSFORMACIÓN
36 FÍSICA PLAN COMÚN
PREUNIVERSITARIO PREUCV 2015
DEPARTAMENTO DE CIENCIAS
FÍSICA PLAN COMÚN
CALOR Y EQUILIBRIO TERMICO.
Eje Temático: Materia y su Transformación.
Sub – Eje: Calor y Equilibrio térmico.
Tareas: Reconocer -Distinguir-Comprender.
EQUILIBRIO TERMICO
¿Qué es el Calor? El equilibrio térmico no es más ni
El calor es la variación de la energía térmica de un cuerpo. Cuando un menos que una forma de expresar la
cuerpo aumenta su energía térmica se está calentando, es decir conservación de la energía térmica en
recibiendo calor. Cuando un cuerpo disminuye su energía térmica se un sistema aislado, esto significa que el
está enfriando, es decir, perdiendo calor. De esta forma, el calor no es sistema siempre tiende a buscar una
más que una forma de denominar a los aumentos y pérdidas de energía temperatura en común.
térmica.
El flujo de energía térmica siempre
tiene el mismo sentido y este es desde
los cuerpos de mayor temperatura
hacia los de menor temperatura
llamado “flujo natural del calor”
¿Qué es el frio?
La sensación de frio es la ausencia de esta energía térmica en los
cuerpos, cuando pierde o cede esta energía térmica un cuerpo se dice
que esta “frío”.
Entendiendo esto se deben conocer las formas en que se puede
transferir el calor, las cuales son 3.
Conducción: Esta forma se procede por el contacto
entre cuerpos a distinta temperatura, de ello
depende si los cuerpos son buenos conductores o
aislantes.
Convección: Esta forma se produce en fluidos,
donde el flujo de esta sustancia a mayor
temperatura sube y el de menor temperatura baja.
Radiación: Por último, esta forma de transferencia
se produce a distancia en forma de ondas
electromagnéticas las que son invisibles a simple
vista.
–FÍSICA MODULO COMÚN – CLASE 13 37
PREUNIVERSITARIO PREUCV 2015
DEPARTAMENTO DE CIENCIAS
MATERIA Y SU TRANSFORMACION
SUB - EJE: CALOR Y EQUILIBRIO TERMICO.
Guía de Destrezas F – 13: Calor y equilibrio térmico.
: Calor
La cantidad de calor entregada o absorbida por uny cuerpo
Equilibrio
está Térmico.
determinada por:
SUPER AISLANTES TERMICOS
𝑄 = 𝑚 ∙ 𝑐 ∙ ∆𝑇
Donde:
𝑄 = Cantidad de Calor Los aerogeles son, en el momento
actual, los materiales más
𝑚 = Masa prometedores para el desarrollo de
nuevos componentes super-aislantes
𝑐 = Calor especifico en el sector de la construcción.
∆𝑇 =Variacion de temperatura Los aerogeles de sílice son materiales
sólidos amorfos extremadamente
ligeros que presentan una porosidad
Calor específico (c) mayor del 90% de su volumen total y
El calor específico es la cantidad de calor necesaria para aumentar en tamaños de poros entre 4 y 20
un grado Celsius un gramo de maso de una sustancia. nanómetros de diámetro.
𝑄 𝐶𝑎𝑙 Estos materiales presentan un
𝑐= [ ] conjunto de propiedades químico-
𝑚∆𝑇 𝑔℃
Calor de transformación físicas que los convierten en los
El calor de cambio de estado es la cantidad de calor necesaria para mejores candidatos a la hora de
producir el cambio de estado. En donde todo cambio de estado se utilizarlos como aislantes térmicos,
produce a temperatura constante. acústicos y eléctricos.
En el caso de utilizarlos para aislar
térmicamente un edificio, se necesita
menos de la mitad de espesor para
conseguir el mismo efecto que
utilizando materiales aislantes
convencionales.
38 FÍISCA MÓDULO COMÚN – CLASE 13
PREUNIVERSITARIO PREUCV 2015
DEPARTAMENTO DE CIENCIAS
MATERIA Y SU TRANSFORMACION
SUB - EJE: CALOR Y EQUILIBRIO TERMICO.
Guía de Destrezas F – 13: Calor y Equilibrio Térmico.
1. La cantidad de calor que cede una sustancia al 4. Un recipiente de aluminio se encuentra a una
pasar de gas a liquido se denomina: temperatura de 20 [°C]. Se vierte 1 litro de agua
a 70 [°C], entonces se verifica que:
A) Calor de condensación.
B) Calor de sublimación. I. La temperatura del recipiente baja.
C) Calor de fusión. II. La temperatura del agua baja.
D) Calor de solidificación. III. El recipiente y el agua llegan a temperatura
E) Calor de vaporización. común.
IV. Hay transferencia de calor desde el recipiente al
2. El calor especifico del agua es 1 𝑐𝑎𝑙 ⁄𝑔 ∙ ℃ y del agua.
cobre es de 0,09 𝑐𝑎𝑙 ⁄𝑔 ∙ ℃. De lo anterior se
deduce que si tenemos 1 [Kg.] de agua y 1 [Kg.] Es verdadera:
de cobre resulta:
A) I y II.
A) Más fácil elevar o disminuir la temperatura del B) I y III.
agua que el del cobre. C) II y III.
B) Más fácil elevar o disminuir la temperatura del D) I, III y IV.
cobre que la del agua. E) II, III y IV.
C) Son masas iguales, se necesita la misma cantidad
de calor para cambiar la temperatura. 5. El calor especifico de algunos materiales son:
D) Más fácil elevar la temperatura del agua, pero Alcohol c = 0,58 [cal/g °C]
más fácil bajarla que el cobre. Diamante c = 0,12 [cal/g °C]
E) Ninguna de las anteriores. Parafina c = 0,2 [cal/g °C]
Agua c = 1,0 [cal/g °C]
3. Se tienen dos tazas de agua caliente. La taza M Cobre c = 0,09 [cal/g °C]
contiene 200 gramos de agua a 30 [°C] y la tasa
N contiene 50 gramos de agua a la 60 [°C]. Si se ¿Cuál material tiene mayor capacidad de aceptar
vierte el contenido de N en M de modo que no el calor?
exista perdida de calor, la temperatura a la que
llegará la mezcla es: A) Alcohol.
B) Agua.
C) Diamante.
D) Parafina.
E) Cobre.
6. De las siguientes afirmaciones:
I. El cambio de estado de una sustancia ocurre a
A) Mayor a 60 [°C] temperatura constante.
B) Igual a 60 [°C] II. En los líquidos el calor se propaga por
C) Un valor entre 30 [°C] y 60 [°C] convección.
D) Menor a 30 [°C] III. Al pasar el estado gaseoso al estado líquido se
E) Ninguna de las anteriores. agrega calor.
Es (son) falsa(s):
A) I.
B) I y III.
C) III.
D) II y III.
E) I, II y III.
FÍSICA MÓDULO COMÚN – CLASE 13 39
PREUNIVERSITARIO PREUCV 2015
DEPARTAMENTO DE CIENCIAS
MATERIA Y SU TRANSFORMACION
SUB - EJE: CALOR Y EQUILIBRIO TERMICO.
Guía de Destrezas F – 13: Calor y equilibrio térmico.
7. Si tomamos con una mano un tubo : Calor y Equilibrio
de cobre y 11.Térmico.
Identificar la aseveración falsa:
con la otra uno de cartón que se encuentran en
equilibrio térmico con la habitación en donde se A) El calor se produce por una diferencia de
encuentran, cuya temperatura es menor a la de temperatura entre dos cuerpos.
nosotros, notamos que el cobre se siente más B) El calor se transfiere por conducción.
frío que el cartón. ¿A qué se debe esta C) El equilibrio térmico se logra cuando se llega a una
sensación? temperatura común.
D) Para pasar del estado sólido a liquido se debe
A) La temperatura del tubo de cobre es mayor a la proporcionar calor.
del cartón. E) No hay aseveraciones falsas.
B) La temperatura del tubo de cartón es mayor a la
del cobre. 12. ¿De qué modo la energía del Sol se transmite a la
C) La mano que sostiene al cobre cede calor con Tierra?
mayor rapidez.
D) La mano que sostiene al cartón cede calor con A) Por conducción y radiación.
mayor rapidez. B) Por convección y radiación.
E) El cobre es mejor aislante que el cartón. C) Por conducción.
D) Por radiación.
8. Un objeto A posee el triple de calor específico E) Por convección.
que otro objeto B, con esta información, ¿cuál de
las siguientes alternativas es correcta si ambos 13. El calor se transfiere más fácilmente por
objetos son puestos dentro de un refrigerador? conducción a través de:
A) Metales.
A) A se “enfría” más rápido que B. B) Líquidos.
B) B se “enfría” más rápido que A. C) Gases.
C) A y B tardan lo mismo en “enfriarse”. D) Vacío.
D) A no se “enfría”. E) Madera.
E) Ninguna de las anteriores.
14. Al entrar a una pieza que ha estado cerrada por
9. Una masa de hierro de 200 𝑔 y calor específico una o más noches, se observan en ella objetos de
0,115 𝑐𝑎𝑙 ⁄𝑔 ∙ ℃, al colocarla al sol un cierto metal, de madera y alfombras. Al tocar estos
tiempo, absorbe 1610 𝑐𝑎𝑙. ¿Cuál es la variación elementos nos parecen que están a distinta
de temperatura que experimentará? temperatura, esto se debe a que estos objetos
A) Tienen distintas capacidad calórica.
A) 20 °C
B) Poseen distinto calor específico.
B) 40 °C
C) Tienen distinta conductividad térmica.
C) 60 °C
D) Están a distintas temperaturas.
D) 70 °C
E) Tienen distinta porosidad en su superficie, por
E) 100 °C
esto se sienten distinto al tacto de la mano.
10. El concepto de calor especifico se refiere a: 15. Una sustancia de 200 𝑔 que se encuentra en el
interior de un calorímetro de calor específico
A) Cantidad de calor que posee un gramo de masa. despreciable al recibir 200 𝑐𝑎𝑙 aumenta su
B) Cantidad de calor necesaria para que un cuerpo temperatura en 40 ℃, entonces su calor
cambie de estado. especifico es:
C) Cantidad de calor necesaria para que un cuerpo
de 1 [gr] eleve su temperatura en 1 [°C]. A) 2 𝑐𝑎𝑙 ⁄𝑔 ∙ ℃
D) Cantidad de calor que se transfiere a un cuerpo B) 0,125 𝑐𝑎𝑙 ⁄𝑔 ∙ ℃
hasta que alcance el equilibrio. C) 0,25 𝑐𝑎𝑙 ⁄𝑔 ∙ ℃
E) Ninguna de las anteriores. D) 0,0125 𝑐𝑎𝑙 ⁄𝑔 ∙ ℃
E) 0,025 𝑐𝑎𝑙 ⁄𝑔 ∙ ℃
40 FÍISCA MÓDULO COMÚN – CLASE 13
PREUNIVERSITARIO PREUCV 2015
DEPARTAMENTO DE CIENCIAS
MATERIA Y SU TRANSFORMACION
SUB - EJE: CALOR Y EQUILIBRIO TERMICO.
Guía de Destrezas F – 13: Calor y Equilibrio Térmico.
16. Cuando una sustancia está cambiando de 19. En relación a las distintas formas en que se
estado, debido a esto en este proceso debe: propaga el calor es correcto decir que:
A) Disminuir su densidad. I. Si en una habitación se saca el aire el calor igual se
B) Aumentar su masa. puede transmitir de un punto a otro.
C) Mantener su volumen. II. Al interior de una olla con agua y puesta a hervir,
D) Mantener su temperatura. el calor se propaga gracias a la convección.
E) Disminuir su volumen. III. Un cuchillo metálico al tocar con uno de sus
extremos un cuerpo que está a una elevada
17. La unidad de calor llamada caloria sirve para temperatura, el resto del cuchillo se calentará
cuantificar la energia gracias a la conducción del calor.
A) Calórica. A) I.
B) Química. B) II.
C) Eléctrica. C) III.
D) Mecánica. D) I y III.
E) Cualquiera de las anteriores. E) I, II y III.
18. Suele ocurrir que las regiones de la Tierra que 20 Dos cuerpos varían en igual cantidad su
están próximas al mar o a los lagos, tienen temperatura al recibir la misma cantidad de calor.
mayor estabilidad térmica que las regiones Si A es uno de los cuerpos cuyo calor específico es
que están al interior, donde se producen 0,8 cal/g·°C y B el otro cuerpo de calor específico
grandes variaciones de temperatura entre el 0,4 cal/g·°C, entonces la razón entre las masas de A
día y la noche. Esto se debe a que el agua tiene y B es
A) Una alta densidad. A) 1:1
B) Un gran calor especifico. B) 1:2
C) Gran cantidad térmica. C) 1:3
D) Un calor especifico parecido al de la tierra que D) 1:4
la rodea. E) 1:5
E) Ninguna de ellas.
FÍSICA MÓDULO COMÚN – CLASE 13 41
PREUNIVERSITARIO PREUCV 2015
DEPARTAMENTO DE CIENCIAS
MATERIA Y SU TRANSFORMACION
SUB - EJE: CALOR Y EQUILIBRIO TERMICO.
Guía de Destrezas F – 13: Calor y equilibrio térmico.
: Calor y Equilibrio Térmico.
42 FÍISCA MÓDULO COMÚN – CLASE 13
PREUNIVERSITARIO PREUCV 2015
DEPARTAMENTO DE CIENCIAS
FÍSICA PLAN COMÚN
MODELOS DEL UNIVERSO
Eje Temático: Tierra y Universo
Sub – Eje: Modelos Del Universo
Tareas: Conocer – Reconocer – Distinguir.
¡VENCISTE, GALILEO!
Desde los comienzo de la humanidad el hombre comenzó a preguntarse qué
forma tenía el universo. Siglos pasaron para llegar a la visión original.
En 1979, el papa Juan Pablo II reconoció
Modelo Geocéntrico que la Iglesia católica romana se había
equivocado al condenar a Galileo, y
El primer modelo del sistema planetario es nombro una comisión interdisciplinaria
planteado en la antigua Grecia y apoyado por para reabrir el caso:
Aristóteles (Sistema basado en el sentido común), “Espero que teólogos, eruditos e
historiadores, animados de un espíritu
el cual determina una tierra fija en su centro y su
colaborador, estudien el caso Galileo
alrededor girando los planetas conocidos a la época más profundamente y, en leal
. reconocimiento de las culpas de
cualquier lado que venga, disipen la
El único problema de este sistema es el
desconfianza que todavía se opone, en
movimiento errático de Marte, el que realiza una muchas mentes, a una fructífera
especie de lazo en el cielo donde en épocas concordancia entre la ciencia y la fe”
avanza y luego retrocede.
La comisión estudio el caso Galileo
En el siglo II Claudio Ptolomeo resolvió algunas durante diez años y concluyo que los
de las dificultades que planteaba el sistema jueces de la época cayeron en un error
geocéntrico de esferas concéntricas. subjetivo de juicio, incapaces de
disociar la fe de una cosmología
anticuada. Pensaron que si se adoptaba
Modelo Heliocéntrico el sistema copernicano no demostrado,
la tradición católica sufriría un daño
Hacia 1512, Nicolás Copérnico, postuló en su
manuscrito “Comentariolus” que la Tierra giraba La rehabilitación de Galileo es el
alrededor de su eje y que esta y los planetas se verdadero “triunfo romano”, pero
queda claro que Galileo no necesitaba
movían alrededor del Sol.
de tal gesto; era la Iglesia la que se
En el mismo año de su muerte (1543) vio la luz de rehabilitaba al reconocer su error de
365 años atrás.
su obra principal, “De revolutionibus”. Basándose en la rotación terrestre
descubrió que las complejas órbitas de los planetas descritas por Ptolomeo
podían simplificarse si se elegía el Sol, y no la Tierra, como centro del sistema
planetario.
El modelo de Copérnico fue apoyado después por los padres de la física
moderna, Galileo Galilei y Johannes Kepler.
–FÍSICA MODULO COMÚN – CLASE 14 43
PREUNIVERSITARIO PREUCV 2015
DEPARTAMENTO DE CIENCIAS
FUERZA Y MOVIMIENTO
SUB - EJE: ENERGIA MECANICA
Guía de Destrezas F – 14: Modelos Del Universo
Leyes de Kepler
Desde muy joven demostró gran habilidad en las matemáticas hasta cuando demuestra todo su talento en 1609 al
publicar su obra Astronomia Nova en la que plasma las tres leyes para el movimiento planetario.
Los planetas tienen movimientos elípticos alrededor del Sol, estando éste situado en uno de los 2 focos que
contiene la elipse.
Las áreas barridas por los radios de los planetas son proporcionales al tiempo empleado por estos en recorrer
el perímetro de dichas áreas.
El cuadrado de los períodos de la órbita de los planetas es proporcional al cubo de la distancia promedio al
Sol.
Ley Universal de Gravitación
Considerado uno de los genios más grandes de su época por su aporte a la física, en especial a la dinámica y además
por su descripción de la fuerza que atrae los cuerpos hacia la tierra, la Fuerza de Gravedad.
𝑚1 𝑚2
𝐹=𝐺
𝑟2
44 FÍSICA MÓDULO COMÚN – CLASE 14
PREUNIVERSITARIO PREUCV 2015
DEPARTAMENTO DE CIENCIAS
FUERZA Y MOVIMIENTO
SUB - EJE: ENERGIA MECANICA
Guía de Destrezas F – 14: Modelos Del Universo
1. La ley de Gravitación universal fue formulada por: 5. Las siguientes proposiciones son verdaderas
EXCEPTO:
A) Nicolás Copérnico.
B) Galileo Galilei. A) la órbita del sol en torno a la tierra es una elipse.
C) Isaac Newton. B) en el afelio la energía cinética de la tierra es
D) Johannes Kepler. mínima.
E) Tycho Brahe. C) la tierra es más rápida cuando está más cerca
del sol.
2. El primero en determinar que las órbitas de los D) la órbita de la tierra está contenida en un plano
planetas eran elípticas fue: que pasa por el sol.
E) el radio vector de la tierra barre áreas iguales en
A) Galileo Galilei. tiempos iguales.
B) Nicolás Copérnico.
C) Tycho Brahe. 6. Con respecto al Sol, un cometa describe una
D) Johanes Kepler. trayectoria elíptica con el sol en uno de sus
E) Isaac Newton. focos. La rapidez del cometa es máxima en el
punto:
3. La Primera Ley de Kepler propone que:
A) A
A) El sol se mueve en órbita circular en torno a la B) B
Tierra. C) C
B) La Tierra se mueve en círculos en torno al sol. D) D
C) Los planetas siguen trayectorias elípticas en E) Cualquiera, ya que es constante.
torno al sol.
D) El Sol sigue una trayectoria elíptica en torno a 7. Cuándo la distancia entre un cometa y el sol
la Tierra. disminuye a la mitad, la fuerza de atracción
E) La Tierra se ubica n el foco de una trayectoria entre el cometa y el sol:
elíptica.
A) disminuye a la mitad.
4. Los científicos nombrados a continuación B) se cuadruplica.
hicieron importantes contribuciones al C) permanece constante.
conocimiento actual de los movimientos D) disminuye a la cuarta parte.
planetarios: E) se duplica.
I. Copérnico. 8. Considere una estrella en torno de la cual
II. Tolomeo. gravitan un conjunto de planetas. De acuerdo
III. Kepler. con la primera Ley de Kepler:
Si estos nombres fueran ordenados A) todos los planetas gravitan en órbitas elípticas
cronológicamente, el orden correcto sería: en que la estrella ocupa uno de sus focos.
B) las órbitas de los planetas son trayectorias
A) III, I y II cerradas.
B) I, II y III C) las órbitas de los planetas son espirales.
C) II, III y I D) todos los planetas gravitan en órbitas circulares.
D) I, III y II E) todos los planetas gravitan en órbitas elípticas
E) II,I y III en cuyo centro está la estrella.
FÍSICA MÓDULO COMÚN – CLASE 14 45
PREUNIVERSITARIO PREUCV 2015
DEPARTAMENTO DE CIENCIAS
FUERZA Y MOVIMIENTO
SUB - EJE: ENERGIA MECANICA
Guía de Destrezas F – 14: Modelos Del Universo
9. En una órbita elíptica seguida por un planeta en 13. Señale la alternativa que contenga las palabras
torno al sol el PERIHELIO corresponde: que completan correctamente el siguiente
enunciado:
A) a la separación entre los focos de la elipse. “En el universo todo sucede como si los cuerpos
B) al punto de la órbita más cercana al sol. se ……… en razón ……… del producto de sus masas
C) al punto medio de la elipse. y en razón ………. del cuadrado de la distancia que
D) al punto de la órbita más alejado del sol. los separa”.
E) al foco de la elipse.
A) repelen - directa – inversa.
10. La fuerza gravitacional con que el Sol atrae a la B) atraen - directa – directa.
tierra: C) atraen - inversa – inversa.
D) atraen - directa – inversa.
A) es menor que la fuerza que la tierra atrae al sol. E) atraen - inversa – directa.
B) es mayor que la fuerza que la tierra atrae al sol.
C) es la misma para todos los planetas. 14. Suponga que la tierra hubiese sido originada
D) es la misma fuerza con que la tierra atrae a la luna. con el doble de su masa y que su volumen fuese
E) ninguna de las anteriores. el mismo que presenta hoy.
Entonces:
11. Señale la alternativa CORRECTA:
I. Los árboles serían más bajos y con el tronco más
A) A través de su Ley de Gravitación universal robusto.
Newton mostró que las Leyes de Kepler estaban II. Las patas de los animales serían más musculosas
erradas. y los huesos más robustos.
B) Kepler corrigió a Tolomeo que era partidario de III. La atmósfera sería más densa o pesada.
un sistema planetario heliocéntrico.
C) Kepler estableció sus Leyes basándose en la Ley Las afirmaciones anteriores son respectivamente:
de gravitación universal. A) VVV
D) por medio de la Ley de gravitación Universal se B) VFV
pueden deducir las Leyes de Kepler sobre el C) FVF
Sistema planetario. D) FFF
E) Kepler corrigió a Copérnico en cuanto a la E) VVF
trayectoria del planeta en un sistema
heliocéntrico 15. Si la tierra tuviese su masa reducida a la mitad y
permaneciera en su órbita actual, su período o
12 En la figura adjunta está representada la órbita tiempo en que recorre su órbita sería:
de un planeta en torno al sol. Los arcos AB y A’B’
fueron recorridos en tiempos iguales. A) la octava parte.
B) la mitad.
¿Cuál es la relación entre las áreas S y S’? C) la cuarta parte.
D) el mismo.
A) S = 4S E) el doble.
B) S = S’
C) S’ = 2S 16. ¿Cuál es el modelo planetario que postula que
D) S = 2S’ los planetas giran en torno al sol?
E) S’ = 3S
A) Modelo de los asteroides.
B) Modelo Big-Bang.
C) Modelo egocéntricos.
D) Modelo heliocéntrico.
E) Modelo de planetas internos.
46 FÍSICA MÓDULO COMÚN – CLASE 14
PREUNIVERSITARIO PREUCV 2015
DEPARTAMENTO DE CIENCIAS
FUERZA Y MOVIMIENTO
SUB - EJE: ENERGIA MECANICA
Guía de Destrezas F – 14: Modelos Del Universo
17. Considere un planeta en órbita elíptica en torno Es (son) verdadera(s):
de una estrella E.
A) Solo I
I. Si 𝑡12 = 𝑡34 = 𝑡56 entonces las áreas B) Solo II
achuradas son iguales. C) Solo III
II. La rapidez del planeta es máxima en el punto D) I y II
A. E) I y III
III. La rapidez del planeta es mínima en el punto
C. 20 Sean 𝐹1 y 𝐹2 los focos de la elipse que describe la
Tierra en torno al Sol. En el recorrido que hace el
planeta se han marcado 4 puntos. Al comparar la
rapidez de la Tierra en los puntos A, B, C y D es
correcto que en
A) A es más rápido.
B) B es más rápido.
C) C es más rápido.
D) D es más rápido.
E) A, B, C y D la rapidez es la misma.
Entonces es (son) verdadera (s):
A) ninguna es verdadera.
B) todas son verdaderas.
C) I y II.
D) II y III.
E) I y III.
18. Considerando la Ley de Gravitación Universal, la
fuerza de atracción depende de:
A) La masa de los cuerpos, si es mayor es más intensa.
B) La distancia entre los cuerpos, si es mayor es más
intensa.
C) La velocidad de los cuerpos, si es mayor es más
intensa.
D) La velocidad de los cuerpos, si es menor es más
intensa.
E) La masa de los cuerpos, si es menor es más intensa.
19 Respecto a las leyes de Kepler aplicable a los
planetas del Sistema solar se afirma que:
I. Los planetas describen orbitas elípticas en torno
al Sol, el cual se ubica al centro de la Elipse.
II. El radio vector de un planeta “barre” áreas
iguales en tiempos iguales, esto corresponde a
la segunda ley de Kepler.
III. La tercera ley de Kepler dice que la razón entre
el período y la rapidez de un planeta es
constante.
FÍSICA MÓDULO COMÚN – CLASE 14 47
PREUNIVERSITARIO PREUCV 2015
DEPARTAMENTO DE CIENCIAS
FUERZA Y MOVIMIENTO
SUB - EJE: ENERGIA MECANICA
Guía de Destrezas F – 14: Modelos Del Universo
48 FÍSICA MÓDULO COMÚN – CLASE 14
PREUNIVERSITARIO PREUCV 2015
DEPARTAMENTO DE CIENCIAS
FÍSICA PLAN COMÚN
LA TIERRA, EL SISTEMA SOLAR Y UNIVERSO.
Eje Temático: Tierra y el Universo.
Sub – Eje: La Tierra, El Sistema Solar Y Universo.
Tareas: Conocer-Reconocer-Distinguir.
La Tierra
Nuestro planeta es una agrupación de factores que propician la vida, MATERIA OSCURA
hasta ahora es el único planeta conocido con vida.
Algunas de sus características son:
A pesar de todos los adelantos
científicos, herramientas y radio
Radio:6.371 𝐾𝑚
telescopios es completamente
Edad:4,74 mil millones de años desconocido la procedencia de la
totalidad de la masa del universo, este
Masa: 5,74 × 1024 𝐾𝑔 trozo restante recibe el nombre de
“materia oscura”, en la actualidad se
Distancia al Sol:149.600.000 𝐾𝑚
conoce solo el 10 % de la masa del
Satélite Natural:Luna universo.
Como dijo Bruce H. Margon, un
Periodo de Rotación:23 Hr y 56 min astrónomo de la Universidad de
Washington, en el periódico New York
Periodo de Traslación: 365 𝐷𝑖𝑎𝑠, 6 𝐻𝑟𝑠 y 9 𝑚𝑖𝑛
Times en 2001:“Es una situación
Nuestro planeta contiene una atmosfera que nos protege del exceso sumamente embarazosa admitir que
de radiación proveniente del sol, además genera un campo no logramos hallar el 90% del
magnético que nos protege de los vientos solares. universo”
La estructura de interna de
nuestro planeta está constituida
por tres secciones, la primera
llamada Cortezaque es rígida,
mide hasta 100 Km, la segunda
llamada mantola cual contiene
una parte plástica y otra rígida,
mide hasta 2900 Km y la parte
central llamada núcleola cual
está dividida en una parte liquida y otra solida
En la parte superior del manto se encuentran fragmentada
en piezas llamadas placas tectónicas, estas placas son
elementos rígidos que se mueven en relación uno con otro,
el choque de ellas genera toda la actividad sísmica y
volcánica del planeta.
–FÍSICA MODULO COMÚN – CLASE 15 49
PREUNIVERSITARIO PREUCV 2015
DEPARTAMENTO DE CIENCIAS
TIERRA Y EL UNIVERSO
SUB - EJE: SISTEMA SOLAR Y UNIVERSO
Guía de Destrezas F – 15: La Tierra, El Sistema Solar Y Universo.
Nuestro astro acompañante es la luna, cuya cercanía produce una seria
de fenómenos sobre nuestro planeta.
Radio:1738 𝐾𝑚
Edad:4,52 mil millones de años En la actualidad, dos equipos de
científicos han dado nuevas luces
Masa:7,35 × 1022 𝐾𝑔 sobre este aspecto. Al observar la
radiación x provenientes de la galaxia
Periodo de traslación:27 𝐷𝑖𝑎𝑠, 7 ℎ𝑟𝑠 y 43,7 𝑚𝑖𝑛 de Andrómeda y del cumulo de
Perseo. Según estos equipos, no se
corresponde con ninguna energía de
rayos x conocida y, por tanto, podría
provenir de partículas de materia
oscura se habla de posibles signos de
partículas de materia oscura.
La misión Astro-H, cuyo lanzamiento
está previsto 2015, estará equipada
con aparatos mucho más potentes que
arrojarán luz sobre si se trata
finalmente de una señal inequívoca de
materia oscura.
Al igual que nuestro planeta, el astro predominante de nuestro sistema
solar tiene un ciclo de vida el cual se describe a continuación.
50 FÍSICA MÓDULO COMÚN – CLASE 15
PREUNIVERSITARIO PREUCV 2015
DEPARTAMENTO DE CIENCIAS
TIERRA Y EL UNIVERSO
SUB - EJE: SISTEMA SOLAR Y UNIVERSO.
Guía de Destrezas F – 15: La Tierra, El Sistema Solar Y Universo.
1. Lugar donde se libera la energía que produce un 6. Respecto a la Luna es equivocado decir:
sismo. Descripción hace referencia a:
A) Es un satélite natural de la Tierra.
A) Placa. B) Gira respecto a su eje.
B) Manto. C) El valor de la aceleración de gravedad en la Luna
C) Epicentro. es mayor que la de la Tierra.
D) Hipocentro. D) El plano de su órbita no coincide con el plano de
E) Foco. la órbita terrestre.
E) El periodo de rotación alrededor de la Tierra es
2. Lugar de la superficie que se encuentra justo aproximadamente de 27 días.
sobre el origen de un sismo. Descripción hace
referencia a: 7. ¿En qué galaxia se encuentra la tierra?
A) Placa. A) Nebulosa de Magallanes.
B) Manto. B) Vía láctea.
C) Epicentro. C) Galaxia de Antares.
D) Hipocentro. D) 𝛼 centauro.
E) Foco. E) Cromosfera.
3. Los terremotos en Chile se deben, 8. La Tierra no es precisamente esférica, una
preponderadamente al choque de las placas consecuencia de esto sería:
A) Sudamericana con la Antártica. A) La gravedad es más intensa en el Ecuador.
B) De Nazca con la Australiana. B) La gravedad es más intensa en los polos.
C) De Cocos con la de Nazca. C) La gravedad no depende de las distancias, es
D) Sudamericana con la de Nazca. siempre constante.
E) De Nazca con la Antártida. D) Si hay variación, es variación de la masa.
E) No existe ninguna consecuencia comprobada.
4. Con respecto a la intensidad de un sismo:
9. Una de las teorías más aceptadas respecto al
I. La intensidad se relaciona con la cantidad de achatamiento de los polos de la Tierra es:
energía liberada.
II. Escala Mercalli se usa para medir la magnitud. A) Porque en los polos existe mayor gravedad.
III. La intensidad se relaciona con los efectos y B) Porque las bajas temperaturas hacen que la
daños en un lugar. materia sea más densa y ocupe menos espacio.
C) Por la rotación del planeta en torno a su eje fijo.
Cual (es) es (son) falsa (s) D) Por la misma razón que existen polos
A) Solo I. magnéticos.
B) I y II. E) No se sabe con certeza.
C) I y III. 10. Los planetas con orbita más cercanas a la Tierra
D) II y III. son:
E) I, II y III.
A) Sol y Luna.
5. ¿Cómo se denomina el fenómeno, cuando la Luna B) Júpiter y Saturno.
se interpone entre el Sol y la Tierra? C) Marte y Venus.
D) Luna y Marte.
A) Eclipse solar. E) Mercurio y Venus.
B) Eclipse lunar.
C) Umbral de oscuridad.
D) Luna nueva.
E) Ninguna de las anteriores.
FÍSICA MÓDULO COMÚN – CLASE 15 51
PREUNIVERSITARIO PREUCV 2015
DEPARTAMENTO DE CIENCIAS
TIERRA Y EL UNIVERSO
SUB - EJE: SISTEMA SOLAR Y UNIVERSO
Guía de Destrezas F – 15: La Tierra, El Sistema Solar Y Universo.
11. Respecto a la hipótesis de la formación de la 16. La Luna tiene un periodo de rotación de:
Luna:
A) 24 días.
A) Un trozo de la Tierra se separó y se transformó B) 24 horas.
en la Luna. C) 365 días.
B) Era un asteroide que en su trayectoria fue D) 27,3 horas.
atrapado por el Campo Gravitacional de la Tierra. E) 27,3 días.
C) Se formó por acreción.
D) Todas las anteriores. 17. Las constelaciones son:
E) Ninguna de las anteriores.
12. Los cambios de estaciones son producidos A) polvo o gas en el espacio.
principalmente por: B) grupos de planetas.
C) grupos de estrellas de igual brillo.
A) La existencia de zonas climáticas. D) grupos de estrellas que semejan figuras.
B) La posición de la órbita en la traslación. E) grupos de rocas orbitando alrededor de una
C) La rotación en torno a su eje. estrella.
D) El grado de inclinación del eje terrestre.
E) Ninguna de las anteriores. 18 El planeta de mayor masa del Sistema solar es:
13. El fenómeno de las mareas depende de:
A) Tierra.
A) La posición relativa entre la Luna y el Sol. B) Júpiter.
B) El Sol. C) Saturno.
C) La Luna. D) Urano.
D) Las Corrientes. E) Neptuno.
E) Todas las anteriores.
19 Al nombrar un planeta rocoso y uno gaseoso,
14. Respecto a las capas que determinan la respectivamente, será correcto decir
estructura del planeta Tierra se afirma que:
A) Júpiter y Urano.
I. La corteza terrestre es la capa sobre la que B) Venus y Tierra.
construimos nuestras ciudades. C) Neptuno y Marte.
II. El manto es la capa más grande de la Tierra. D) Marte y Urano.
III. Es núcleo externo es líquido. E) Júpiter y Neptuno.
Es (son) correcta(s): 20 Una estrella como el Sol evoluciona hasta
convertirse en una gigante roja, aquella que en su
A) I.
etapa final ya no tiene temperatura suficiente para
B) II.
fusionar el carbono y el oxígeno, entonces la región
C) III.
central de la estrella se contrae y arroja al espacio
D) I y II.
las capas externas. En su interior queda un tipo de
E) I, II y III.
estrella llamada
15. El plano donde la mayoría de los planetas del A) enana marrón.
Sistema Solar está orbitando se le conoce como: B) enana blanca.
C) estrella de neutrones.
A) Elipse. D) agujero negro.
B) Geosfera. E) pulsar.
C) Exosfera.
D) Eclíptica.
E) Heliosfera.
52 FÍSICA MÓDULO COMÚN – CLASE 15
PREUNIVERSITARIO PREUCV 2015
DEPARTAMENTO DE CIENCIAS
QUÍMICA DE MATERIALES Y MEDIO AMBIENTE
Curso Química
Disolución y Concentraciones II 55
Guía de destrezas Q – 13 56
Estequiometría I 59
Guía de destrezas Q – 14 61
Estequiometría II 65
Guía de destrezas Q – 15 66
QUÍMICA PLAN COMÚN 53
PREUNIVERSITARIO PREUCV 2015
DEPARTAMENTO DE CIENCIAS
QUÍMICA DE MATERIALES Y MEDIO AMBIENTE
54 QUÍMICA PLAN COMÚN
PREUNIVERSITARIO PREUCV 2015
DEPARTAMENTO DE CIENCIAS
QUÍMICA PLAN COMÚN
DISOLUCIÓN Y CONCENTRACIONES II.
Eje Temático: Reactividad Química.
Sub – Eje: Disoluciones y concentraciones.
Tareas: Comprender - Distinguir- Aplicar.
CONCENTRACIONES QUÍMICAS
Mol (n)
Fracción Molar (X)
Molaridad (M)
Molalidad (m)
Dilución
DILUCIÓN: Procedimiento que se sigue para prerarar una disolución menos concentrada a partir de una más
concentrada. Para esto se toma una alícuota de la disolución original y se le agregan volúmenes crecientes de
solvente. Por lo tanto se mantienen constantes los moles pero varía la concentración.
–QUÍMICA MODULO COMÚN – CLASE 13 55
PREUNIVERSITARIO PREUCV 2015
DEPARTAMENTO DE CIENCIAS
QUIMICA ORGANICA
SUB - EJE: DISOLUCIONES Y CONCENTRACIONES.
Guía de Destrezas Q – 13: Disoluciones y Concentraciones II.
1. ¿Cuál es la fracción molar de 15 moles de azúcar 6. La cantidad de CaCl2 necesaria para preparar 50
en 10 moles de agua? ml de una solución 2M es de: (masa molar:
111g/mol)
a) 10/15
b) 10/25 a) 22,2 gramos
c) 15/10 b) 11,1 gramos
d) 15/25 c) 111 gramos
e) 15/(15 x10) d) 222 gramos
2. ¿Cuántos gramos de soluto se encuentran e) 2,2 gramos
disueltos en una disolución 0.1 M de glucosa
(Masa Molar: 180 g/mol) por cada litro de 7. ¿Cuál es la fracción molar de 58 gramos de NaCl en
solución? 18 gramos de agua? ( H2O: 18 g/mol NaCl: 58
g/mol)
a) 1,8 gramos
b) 18 gramos a) 2
c) 180 gramos b) 1
d) 0,18 gramos c) ½
e) 0,0018 gramos d) ¼
e) 4
3. ¿Cuál es la molaridad de la solución que contiene
6,3 gramos de HNO3 en 100 ml de solución? (H: 1 8. ¿Cuál es la molaridad de una solución que
g/mol N: 14 g/mol O: 16 g/mol) contiene 148 gr de Ca(OH)2 (PA: Ca = 40 gr/mol; O
= 16 gr/mol ; H = 1 gr/mol) en 2 litros de agua?
a) 1M a) 0,5 M
b) 10M b) 1,0 M
c) 63 M c) 1,5 M
d) 6,3 M d) 2,0 M
e) 5M e) 2,5 M
4. El número de moles de soluto que hay en 100 ml 9. ¿Cuántos moles de soluto son necesarios para
de una solución de KOH 0,5 M es de: preparar 2 litros de una solución 0,5 M?
a) 0,5
a) 0,5 moles b) 1,0
b) 0,05 moles c) 1,5
c) 0,005 moles d) 2,0
d) 5 moles e) 2,5
e) 0,15 moles
10. ¿Cuántos moles hay presentes en 2 litros de una
5. A 600 ml de una solución 0,6 M se le agrego
solución de ácido láctico (C3H6O3) 3,5 M?
solvente hasta completar 900 ml. La molaridad de
a) 0,6 M
la solución final es:
b) 1,7 M
c) 4,5 M
a) 0,4 M
d) 5,5 M
b) 0,9 M
e) 7,0 M
c) 0,5 M
d) 0,8 M
e) 0,2 M
QUÍMICA MÓDULO COMÚN – CLASE 13 56
PREUNIVERSITARIO PREUCV 2015
DEPARTAMENTO DE CIENCIAS
QUIMICA ORGANICA
SUB - EJE: DISOLUCIONES Y CONCENTRACIONES.
Guía de Destrezas Q – 13: Disoluciones y Concentraciones II.
11. ¿Cuál es la molalidad de una disolución si se 15. ¿Cuántos ml de agua se deben agregar para
disuelven 196 gr de ácido sulfúrico (H2SO4) en 500 preparar una solución de NH3 6 M, a partir de 120
ml de agua? (d H2O = 1 gr/ml) ml de una solución de NH3 15 M?
a) 0,5 m a) 180
b) 1,0 m b) 200
c) 2,5 m c) 250
d) 3,0 m d) 300
e) 4,0 m e) 400
12. ¿Qué alternativa representa una solución 0,1 M? 16. ¿Cuántos moles de cloruro (Cl-) hay en una mezcla
a) 1 mol de soluto disueltos en 1 litro de solución compuesta por 500 ml de NaCl 0,1 M y 500 ml de
b) 0,2 moles de solutos disueltos en 1 litro de MgCl2 0,1 M?
solución a) 0,15
c) 1 mol de soluto disueltos en 0,1 litros de solución b) 0,20
d) 0,3 moles de soluto disueltos en 3 litros de c) 0,30
solución d) 1,50
e) 5 moles de soluto disueltos en 5 litros de solución e) 2,00
13. Una solución que tiene una concentración 1, 5 17. A 4 litros de una solución acuosa 0,01 M, se le
molal, fue formada agregando cierta cantidad de adiciona agua hasta obtener el doble de volumen.
un soluto X (PM = 30 gr/mol) a 2 litros de agua (d ¿Cuál será la concentración final de la solución?
H2O = 1 gr/ml). ¿Cuál es la masa del soluto? a) 1x10-3 M
a) 20 gr b) 2x10-4 M
b) 40 gr c) 5x10-3 M
c) 60 gr d) 2x10-3 M
d) 90 gr e) 6x10-2 M
e) 100 gr
Con el siguiente encabezado responda las preguntas 18,
14. Se tienen dos soluciones: 19 y 20
A: 15 gr de sal (NaCl) en 3 litros de solución “Se mezclan 200 gr de una disolución de sulfato de sodio
B: 5 gr de sal (NaCl) en 1 litro de solución (Na2SO4) 10 % m/m y d = 1,00 g/ml con 100 ml de una
Si el PM del soluto es 40 gr/mol, solución con igual soluto pero al 30 % m/m y d = 1,5
¿Cuál o cuáles de las siguientes afirmaciones es o g/ml”
son correcta (s) si se mezcla A + B?
I. La concentración molar de la solución final es de 18. ¿Cuál es el % m/m de la solución final?
0,125 M a) 0,55
II. La concentración molar de la solución final es de b) 1,80
5,00 M c) 2,66
III. La solución final tiene 0,5 moles d) 3,84
a) Solo I e) 26,00
b) Solo II
c) Solo III
d) I y III
e) II y III
QUÍMICA MÓDULO COMÚN – CLASE 13 57
PREUNIVERSITARIO PREUCV 2015
DEPARTAMENTO DE CIENCIAS
QUIMICA ORGANICA
SUB - EJE: DISOLUCIONES Y CONCENTRACIONES.
Guía de Destrezas Q – 13: Disoluciones y Concentraciones II.
19. ¿Cuál es el % m/v de la solución final?
a) 0,86
b) 1,16
c) 4,60
d) 11,38
e) 21,6
20. ¿Cuál es la densidad de la solución final?
a) 0,21
b) 0,52
c) 0,83
d) 1,16
e) 1,50
QUÍMICA MÓDULO COMÚN – CLASE 13 58
PREUNIVERSITARIO PREUCV 2015
DEPARTAMENTO DE CIENCIAS
QUÍMICA PLAN COMÚN
ESTEQUIOMETRÍA I
Eje Temático: Reactividad Química.
Sub – Eje: Estequiometría.
Tareas: Relacionar - Calcular - Aplicar – Reconocer.
La estequiometria es la ciencia que mide las proporciones cuantitativas o relaciones de masa en la que los
elementos químicos que están implicados.
Ley
conservación de la
materia
Composición
porcentual
–QUÍMICA MODULO COMÚN – CLASE 14 59
PREUNIVERSITARIO PREUCV 2015
DEPARTAMENTO DE CIENCIAS
REACTIVIDAD QUÍMICA
SUB – EJE : ESTEQUIOMETRÍA
Guía de Destrezas Q – 14: Estequiometría.
Ley conservación de las masas Ley de las proporciones definidas
“En una reacción química ordinaria la “Cuando se combinan dos o más
elementos para dar un compuesto
masa permanece constante, es decir, la
determinado, siempre lo hacen en
masa consumida de los reactivos es igual a
la misma proporción fija”
la masa obtenida de los productos”
Ley de las proporciones múltiples
“Dos elementos se pueden combinar entre sí en más de
una proporción para dar diferentes compuestos. Una
cantidad fija determinada de un reactivo se combina con
otras cantidades variables de otros elementos, de manera
que las cantidades variables del segundo elemento
guardan entre sí una relación de números enteros
sencillos”
QUÍMICA MÓDULO COMÚN – CLASE 14 60
PREUNIVERSITARIO PREUCV 2015
DEPARTAMENTO DE CIENCIAS
REACTIVIDAD QUÍMICA
SUB – EJE : ESTEQUIOMETRÍA
Guía de Destrezas Q – 14: Estequiometría.
5. En las siguientes figuras se muestran los estados
1. La ley de conservación de la materia plantea que: iniciales uy finales de una reacción química
a) La materia no se crea ni se transforma solo se
destruye
b) La materia no se crea ni se destruye solo se
transforma
c) La masa no se crea ni se destruye solo se
transforma
Al respecto, es correcto afirmar que corresponde
d) La energía no se crea ni se destruye solo se
a una representación de la ley de
transforma
e) La energía no se crea ni se transforma solo se
a) Proporciones definidas
destruye
b) Proporciones múltiples
c) Conservación de las masas
2. Los factores estequiométrico de la siguiente
d) Combinación química
reacción Fe(OH)3 Fe + O2 + H2O son:
e) Estequiometría
a) 4-4-2-6
6. Al equilibrar la siguiente ecuación:
b) 4-4-3-6
c) 6-5-3-4
X H2 + Y O2 Z H2O
d) 3-4-2-5
e) 6-1-4-3
¿Cuáles son los valores de los coeficientes X, Y y Z?
3. Los factores estequiométrico de la siguiente
reacción CO2 + H2O C7H8O2 + O2 son:
a) 6-4-1-8
b) 4-6-1-8
c) 7-4-1-8
d) 7-5-8-2
e) 7-6-1-5
4. Si los compuestos de NO y N2O3 siguen la ley de las
proporciones múltiples, y se mantiene constante
la masa del nitrógeno. ¿En qué proporción se 7. 25 gramos de un compuesto contiene 0,17 mol de
encuentran los oxígenos respectivamente? átomos de potasio, 0,17 mol de átomos de cromo
a) 3:2 (masa molas = 52 g/mol) y 0,60 mol de átomos de
b) 1:3 oxígeno. Según estos datos, la fórmula empírica de
c) 3:1 este compuesto es
d) 2:3 a) KCrO4
e) 1:2 b) KCrO7
c) K2Cr2O4
d) K2Cr2O7
e) K3Cr3O14
QUÍMICA MÓDULO COMÚN – CLASE 14 61
PREUNIVERSITARIO PREUCV 2015
DEPARTAMENTO DE CIENCIAS
REACTIVIDAD QUÍMICA
SUB – EJE : ESTEQUIOMETRÍA
Guía de Destrezas Q – 14: Estequiometría.
8. La ecuación 11. ¿Cuál es la fórmula molecular del compuesto?
a) C2H2O2
b) C4H2O4
Queda equilibrada con los coeficientes:
c) C6H12O6
d) C2H4O6
e) C3H6O3
12. Se calientan 1,256 g de cloruro de platino y queda
un residuo de 0,7275 g de Pt. ¿Cuál es la fórmula
empírica del cloruro de platino?
a) PtCl4
b) Pt3Cl4
9. Para la siguiente reacción: c) Pt5Cl2
d) PtCl3
e) PtCl2
Se afirma que
13. La fórmula química del sulfato de aluminio es
I. La masa de los reactantes es igual a la masa de Al2(SO4)3. ¿Cuál es la composición porcentual del
los productor aluminio?
II. La cantidad de moléculas de los reactantes es a) 15,8
igual a la de los productor b) 19
III. Los enlaces de los reactivos son iguales a los c) 28
enlaces de los productos d) 44
e) 56,1
Es (son) correcta (s)
a) Solo I 14. La transformación de ozono a oxígeno, se
b) Solo II representa por:
c) Solo III 2O3 3O2
d) I y II Si inicialmente hay 72 g de O3. ¿Cuántos gramos de
e) I, II y III oxígeno se producen?
a) 36
Utilice los siguientes datos para contestar las preguntas b) 14
10 y 11 c) 72
d) 2,25
“El análisis de cierto compuesto, cuya masa molar es de e) 54
180 g/mol, revela que su composición porcentual es de
40% de C, 6,67 % de H y 53,33% de O”
10. ¿Cuál es la fórmula empírica del compuesto?
a) CH2O
b) C2HO
c) CHO2
d) C3H2O
e) CH2O3
QUÍMICA MÓDULO COMÚN – CLASE 14 62
PREUNIVERSITARIO PREUCV 2015
DEPARTAMENTO DE CIENCIAS
REACTIVIDAD QUÍMICA
SUB – EJE : ESTEQUIOMETRÍA
Guía de Destrezas Q – 14: Estequiometría.
15. El metano arde con oxígeno produciendo dióxido
de carbono y agua, como lo muestra la siguiente 19. A partir de la ecuación C + O2 CO2
reacción ¿Cuántos gramos de oxígeno son necesarios para
CH4 + O2 CO2 + H2O reaccionar con 10 g de carbono?
Si se queman 2 Kg de metano, ¿Cuántos Kg dióxido a) 0,83
de carbono se producen? b) 1,66
a) 2,0 c) 10,00
b) 2,2 d) 13,30
c) 5,0 e) 26,60
d) 5,5
e) 6,0 20. Los factores estequiométricos de la siguiente
reacción BCl3 + P4 + H2 BP + HCl son
16. Se tiene la siguiente reacción química a) 4 – 1 – 6 – 4 – 12
Cr2O3 + Si Cr + SiO2 b) 4 – 4 – 12 – 1 – 6
¿Cuántos moles de Si reaccionan con 5 moles de c) 2–1–3–2–6
Cr2O3? (Mm Cr = 52 g/mol ; Mn Si = 28 g/mol) d) 3–1–2–2–6
a) 0,0048 e) 4 – 2 – 6 – 4 – 12
b) 1,350
c) 3,300
d) 5,000
e) 7,500
17. En un horno se produce la siguiente reacción
Bi2S3 + O2 Bi2O3 + SO2
¿Cuál es la masa de dióxido de azufre que se
obtiene al hacer reaccionar 1Kg de Bi2S3? (Mm
Bi = 209 g/mol ; Mm S = 32 g/mol)
a) 0,002
b) 0,006
c) 0,370
d) 3,000
e) 2,200
18. El amoniaco se descompone de la siguiente forma
NH3 N2 + H2
¿Cuántos moles de hidrógeno se desprenden en la
descomposición de 68 g de amoniaco? (Mm N
= 14 g/mol)
a) 2,7
b) 4,0
c) 6,0
d) 68,0
e) 102,0
QUÍMICA MÓDULO COMÚN – CLASE 14 63
PREUNIVERSITARIO PREUCV 2015
DEPARTAMENTO DE CIENCIAS
REACTIVIDAD QUÍMICA
SUB – EJE : ESTEQUIOMETRÍA
Guía de Destrezas Q – 14: Estequiometría.
QUÍMICA MÓDULO COMÚN – CLASE 14 64
PREUNIVERSITARIO PREUCV 2015
DEPARTAMENTO DE CIENCIAS
QUÍMICA PLAN COMÚN
ESTEQUIOMETRÍA II
Eje Temático: Reactividad Química.
Sub – Eje: Estequiometría.
Tareas: Relacionar - Calcular - Aplicar – Reconocer.
Reactivo Limitante: Reactivo que se
consume primero en una reacción
química. La cantidad máxima de
producto que se forma depende de la
cantidad de este reactivo.
Reactivo en Exceso: Son los reactivos
presentes en mayor cantidad que la
necesaria para reaccionar con la
cantidad de reactivo limitante.
El % de rendimiento de una reacción
se utiliza para determinar la
eficiencia de una reacción. Describe
la proporción del rendimiento real
con respecto al rendimiento teórico.
–QUÍMICA MODULO COMÚN – CLASE 15 65
PREUNIVERSITARIO PREUCV 2015
DEPARTAMENTO DE CIENCIAS
REACTIVIDAD QUÍMICA
SUB – EJE : ESTEQUIOMETRÍA
Guía de Destrezas Q – 15: Estequiometría.
1. ¿Cuáles son los coeficientes estequiométricos para
la siguiente reacción?
KIO3 KI + 02 5. Si se posee 40 moles de SiO2 ¿Cuántos moles de H2O
a) 1 -1 -1 se necesitan para que ambos sean reactivos
b) 2–2–2 limitantes?
c) 3–3–3
d) 2–2–3 a) 6
e) 3–2–3 b) 6,7
c) 40
2. ¿Cuáles son los coeficientes estequiométricos para
d) 220
la siguiente reacción hace reaccionar?
Ag + HNO3 AgNO3 + H2 e) 240
a) 2- 2 – 2 – 2 Contesta las preguntas desde la 6 a la 10
b) 1–2–1–2 considerando la siguiente reacción
c) 2–1–2–1
d) 2–2–2–1 Si7H8S2 + 8 S2 7 SiS2 + 4 H2S
e) 1–1–1-2
6. ¿Cuál es el reactivo limitante de la reacción si
Contesta las preguntas desde la 3 a la 5 inicialmente se posee 268 gramos de Si7H8S2 y 576
considerando la siguiente reacción de S2?
6SiO2 + 6H2O Si6H12O6 + 6O2: a) Si7H8S2
b) S2
3. Si se posee 120 gramos de SiO2 y 120 gramos de H2O c) SiO2
cuál es el reactivo limitante(MM Si: 28 g/mol, O: 16 d) H2S
g/mol, H: 1g/mol): e) H2O
a) O2
b) Si6H12O6 7. ¿Cuál es el reactivo limitante si se posee 1,5 moles
c) H2O de Si7H8S2 y 12 moles de S2?
d) SiO2 a) Si7H8S2
e) O2 y Si6H12O6 b) S2
c) SiO2
4. Si se posee 48 moles de H2O y 6 moles de SiO2. d) Ninguno de los reactivos es limitante
¿Cuántos moles de H2O quedan al finalizar la e) Ambos reactivos son limitantes
reacción :
a) 54 8. ¿Cuántos moles de SiS2 se generan al tener
b) 42 inicialmente 3 moles de Si7H8S2 y 30 moles de S2?
c) 6
d) 47 a) 7 moles
e) 14 b) 14 moles
c) 21 moles
d) 26,25 moles
e) 12,15 moles
QUÍMICA MÓDULO COMÚN – CLASE 15 66
PREUNIVERSITARIO PREUCV 2015
DEPARTAMENTO DE CIENCIAS
REACTIVIDAD QUÍMICA
SUB – EJE : ESTEQUIOMETRÍA
Guía de Destrezas Q – 15: Estequiometría.
9. ¿Cuántos moles de H2S se generan al tener 14. ¿Cuál es el % de rendimiento de la reacción si
inicialmente 1 moles de Si7H8S2 y 8 moles de S2? realmente se obtienen 1,8 g de HCl?
a) 1 mol a) 6,08
b) 8 moles b) 12,16
c) 7 moles c) 24,32
d) 4 moles d) 36,48
e) 12 moles e) 48,68
10. ¿Cuántos moles de H2S se generan al tener 15. Se hacen reaccionar 100 g de Br2 con 200 g de H2.
inicialmente 536 gramos de Si7H8S2 y 1024 gramos Si la reacción tiene un 80% de rendimiento,
de S2? ¿cuánto producto de forma?
a) 12 moles Br2 + H2 HBr
b) 4 moles
c) 1 mol a) 40,5
d) 8 moles b) 81,0
e) 7 moles c) 101,2
d) 125,0
Con la información dada a continuación contesta las e) 160,0
preguntas 11 a la 14.
Se hacen reaccionar 20 g de aluminio con 100 ml
Se hacen reaccionar 100 ml de una solución 2 M de de HCl 4 M.
NaCl con 150 ml de una solución 1M de H2SO4 Al + HCl AlCl3 + H2
H2SO4 + NaCl Na2SO4 + HCl
16. ¿Cuántos moles del reactivo en exceso sobran?
11. ¿Cuál es el reactivo en exceso, y cuántos moles a) 0,27
sobran? b) 0,34
a) NaCl Quedan sin reaccionar 0,3 mol c) 0,50
b) H2SO4 Quedan sin reaccionar 0,3 mol d) 0,61
c) NaCl Quedan sin reaccionar 0,05 mol e) 0,80
d) H2SO4 Quedan sin reaccionar 0,05 mol
e) H2SO4 Quedan sin reaccionar 0,15 mol 17. ¿Cuántos moles de hidrógeno se producen?
a) 0,20
12. ¿Cuántos gramos de Na2SO4 se producen? b) 0,60
a) 0,1 c) 0,37
b) 0,2 d) 1,10
c) 14,2 e) 1,50
d) 28,8
e) 56,8 18. Si la reacción tiene un 70 % de rendimiento,
¿cuántos gramos de ALCl3 se producen?
13. ¿Cuántos gramos de HCl se producen? a) 12,28
a) 0,1 b) 17,55
b) 0,2 c) 24,56
c) 14,2 d) 37,8
d) 28,8 e) 54,00
e) 56,8
QUÍMICA MÓDULO COMÚN – CLASE 15 66
67
PREUNIVERSITARIO PREUCV 2015
DEPARTAMENTO DE CIENCIAS
REACTIVIDAD QUÍMICA
SUB – EJE : ESTEQUIOMETRÍA
Guía de Destrezas Q – 15: Estequiometría.
19. ¿Cuál es el reactivo limitante en la siguiente
reacción si se hacen reaccionar 3 moles de SnO2 y 7
moles de carbono?
SnO2 + C Sn + CO
a) SnO2
b) C
c) Sn
d) CO
e) No hay reactivo limitante
20. Se hace reaccionar 100 g de cinc con 7 g de Ag+
Zn + 2 Ag+ 2 Ag + Zn+2
¿Cuál es el reactivo en exceso y cuántos moles
quedan sin reaccionar? (Mm Zn = 65 g/mol ; Mm Ag
= 108 g/mol)
a) Ag+ Quedan sin reaccionar 0,03 moles
b) Zn. Quedan sin reaccionar 1,52 moles
c) Ag Quedan sin reaccionar 0,03 moles
d) Zn+2 Quedan sin reaccionar 1,52 moles
e) Zn Quedan sin reaccionar 0,03 moles
QUÍMICA MÓDULO COMÚN – CLASE 15 66
68
También podría gustarte
- Niños sanos, adultos sanos: La salud empieza a programarse en el embarazoDe EverandNiños sanos, adultos sanos: La salud empieza a programarse en el embarazoCalificación: 4 de 5 estrellas4/5 (5)
- Familia y LiderazgoDocumento62 páginasFamilia y LiderazgoElmAún no hay calificaciones
- Desarrollo PrenatalDocumento54 páginasDesarrollo PrenatalMaría Paola González Hernández100% (1)
- Presentacion Origenes Celulas Madre FEBRERO 2012Documento36 páginasPresentacion Origenes Celulas Madre FEBRERO 2012Miguel Cervantes100% (1)
- Baveno VDocumento42 páginasBaveno VFrank Valera0% (1)
- El Parto Desde La Perspectiva EcológicaDocumento6 páginasEl Parto Desde La Perspectiva EcológicaLuis VallesAún no hay calificaciones
- E y F 2 - Guía de Práctica Semana 15Documento9 páginasE y F 2 - Guía de Práctica Semana 15Liz Salcedo MamaniAún no hay calificaciones
- La Importancia de La Microbiota Intestinal y de La Nutricion para El Desarrollo y La Salud FuturaDocumento82 páginasLa Importancia de La Microbiota Intestinal y de La Nutricion para El Desarrollo y La Salud FuturaReme Esteban RuescasAún no hay calificaciones
- Tercer MóduloDocumento26 páginasTercer MóduloGabriela BlasAún no hay calificaciones
- Informe 07 DesarrolloDocumento7 páginasInforme 07 DesarrolloAbigail ParedesAún no hay calificaciones
- Presentación de Marca Personal Acuarela Elegante y Minimalista Azul y RosaDocumento59 páginasPresentación de Marca Personal Acuarela Elegante y Minimalista Azul y RosaDulce Danelly SánchezAún no hay calificaciones
- Modulo 5 - NicDocumento51 páginasModulo 5 - NicLuis Hernández TellezAún no hay calificaciones
- 1S Manual Biologia DesarrolloDocumento49 páginas1S Manual Biologia DesarrolloGilbert Adrian perez vazquezAún no hay calificaciones
- La Etapa Prenatal y NeonatalDocumento24 páginasLa Etapa Prenatal y NeonatalPaulina SotoAún no hay calificaciones
- Etapa Prenatal Del Desarrollo HumanoDocumento3 páginasEtapa Prenatal Del Desarrollo HumanoAMPUERO100% (1)
- Examen BioeticaDocumento5 páginasExamen Bioeticaesmerlin herediaAún no hay calificaciones
- Clase 05 AIP 2022-2Documento25 páginasClase 05 AIP 2022-2Lenia Lisbeth RiveraAún no hay calificaciones
- Embarazo - Clase 1Documento14 páginasEmbarazo - Clase 1renzo sepulvedaAún no hay calificaciones
- Concepcion de Una Nueva VidaDocumento8 páginasConcepcion de Una Nueva Vidamaria lulu gamboa parraAún no hay calificaciones
- Silabo Atencion MaternaDocumento13 páginasSilabo Atencion MaternaLenin Roberth Tacuri MateoAún no hay calificaciones
- Unidad 1 - Desarrollo Prenatal y Neonatal PDFDocumento12 páginasUnidad 1 - Desarrollo Prenatal y Neonatal PDFCasa Flor de lotoAún no hay calificaciones
- Normas ApaDocumento3 páginasNormas ApaKevin RomeroAún no hay calificaciones
- Guia Alimentaria Menores PDFDocumento36 páginasGuia Alimentaria Menores PDFDany RodriguezAún no hay calificaciones
- EmbriologíaDocumento39 páginasEmbriologíatooony7Aún no hay calificaciones
- Bioética 3Documento7 páginasBioética 3John Carlos Rojas UrdánigoAún no hay calificaciones
- Tarea Grupal 1Documento14 páginasTarea Grupal 1MARIA ISABEL CIANCA GONZALEZAún no hay calificaciones
- ART1234Documento10 páginasART1234Ararath EstrellaAún no hay calificaciones
- Maduracion CervicalDocumento24 páginasMaduracion CervicalClauMcClauAún no hay calificaciones
- Prueba de Tolerancia A Las Contracciones - PresentaciónDocumento28 páginasPrueba de Tolerancia A Las Contracciones - PresentaciónHomeolisticaAún no hay calificaciones
- Ud2 - Embarazo Nutricion en Ciclos - BarceloDocumento53 páginasUd2 - Embarazo Nutricion en Ciclos - BarceloTiniHryshchenkoAún no hay calificaciones
- Medicina, Embriología, Presentación de La PlacentaDocumento51 páginasMedicina, Embriología, Presentación de La PlacentaMaria Libertad AnnetteAún no hay calificaciones
- 4° SEC. EDA 5 SEMANA 3 CYT Explica 2023 La Gestación en Los Humanos y MétodosDocumento10 páginas4° SEC. EDA 5 SEMANA 3 CYT Explica 2023 La Gestación en Los Humanos y MétodosAlan CalderonAún no hay calificaciones
- 2° SEC. EDA 5 SEMANA 2 Explica CYT 2023 El Proceso ReproductivoDocumento14 páginas2° SEC. EDA 5 SEMANA 2 Explica CYT 2023 El Proceso ReproductivoEysa LujerioAún no hay calificaciones
- Trabajo de Biologia 5to D Cristian AngaritaDocumento6 páginasTrabajo de Biologia 5to D Cristian AngaritaCristian AngariitaAún no hay calificaciones
- Trabajo de PartoDocumento7 páginasTrabajo de Partojhonmonzon343Aún no hay calificaciones
- 2° SEC. EDA 5 SEMANA 2 Explica CYT 2023 El Proceso ReproductivoDocumento14 páginas2° SEC. EDA 5 SEMANA 2 Explica CYT 2023 El Proceso ReproductivoANGELICA CARRILLO VALENCIAAún no hay calificaciones
- Modulo 3.2Documento29 páginasModulo 3.2T7V3N JA7M3SAún no hay calificaciones
- Práctica 7. Comprensión de Conceptos Básicos de La LactanciaDocumento11 páginasPráctica 7. Comprensión de Conceptos Básicos de La LactanciaDannyWolf 016Aún no hay calificaciones
- AAVV - Aspectos Médicos y Quirúrgicos Del AbortoDocumento24 páginasAAVV - Aspectos Médicos y Quirúrgicos Del AbortoRuben RomanAún no hay calificaciones
- Enfermeria en La Cosmovision MayaDocumento60 páginasEnfermeria en La Cosmovision Mayaml1374051Aún no hay calificaciones
- Trabajo Colaborativo Repro Definitivo.Documento19 páginasTrabajo Colaborativo Repro Definitivo.rafaelAún no hay calificaciones
- Embriologia MonografiaDocumento13 páginasEmbriologia MonografiaMaria Elizabeth M. AlbercaAún no hay calificaciones
- 2c2b0 Manual de Autocuidado Del Puerperio1Documento101 páginas2c2b0 Manual de Autocuidado Del Puerperio1Felipe AlvarezAún no hay calificaciones
- Expo 5 - Fisiología y Farmacología Del Inicio Del PartoDocumento38 páginasExpo 5 - Fisiología y Farmacología Del Inicio Del PartoJimena CarrionAún no hay calificaciones
- Ficha - Explica Reproduccion HumanaDocumento14 páginasFicha - Explica Reproduccion HumanaNayely Jazmín Chambilla ChoqueAún no hay calificaciones
- La Lactancia Materna. Elizabeth Garcia y Marie ChirinoDocumento32 páginasLa Lactancia Materna. Elizabeth Garcia y Marie Chirinoelizabeth garciaAún no hay calificaciones
- Unidad 3 Atencion Al Niño Sano Su Crecimiento y DesarrolloDocumento26 páginasUnidad 3 Atencion Al Niño Sano Su Crecimiento y Desarrollojessica0% (1)
- Proyecto MaquetaDocumento27 páginasProyecto MaquetaSantiago Ortega HernandezAún no hay calificaciones
- Guia Laboratorio 1 Embriologia Nancy Emilsen Daza GonzalezDocumento3 páginasGuia Laboratorio 1 Embriologia Nancy Emilsen Daza GonzalezJhonAún no hay calificaciones
- 1000 Dias Microbioma EpigeneticaDocumento40 páginas1000 Dias Microbioma Epigeneticaorlandom61100% (1)
- Placenta y Líquido AmnióticoDocumento49 páginasPlacenta y Líquido AmnióticoCarlos RaizAún no hay calificaciones
- Fisiologia Del Trabajo de PartoDocumento8 páginasFisiologia Del Trabajo de PartoNicolas TamayoAún no hay calificaciones
- Cap 33 at Enf Proc PartoDocumento29 páginasCap 33 at Enf Proc PartocaroAún no hay calificaciones
- Examen Desarrollo HumanoDocumento5 páginasExamen Desarrollo HumanoElizabeth UzgAún no hay calificaciones
- U2 T3 CC DocbasDocumento32 páginasU2 T3 CC DocbasMaria belen Solis hazAún no hay calificaciones
- Clase 9 Determinismo Del PartoDocumento38 páginasClase 9 Determinismo Del PartoNOEMI MASCO LAURAAún no hay calificaciones
- Análisis de Un Artículo CientificoDocumento3 páginasAnálisis de Un Artículo CientificoJorge CordobaAún no hay calificaciones
- GUIA 05 Cambios Fisiológicos en El EmbarazoDocumento7 páginasGUIA 05 Cambios Fisiológicos en El EmbarazoLeydiLemaAún no hay calificaciones
- Guia Desarrollo Humano - Ii Pac 2023Documento14 páginasGuia Desarrollo Humano - Ii Pac 2023Julissa MontesinosAún no hay calificaciones
- Etica y Valores 2º Tetra Unid 2Documento12 páginasEtica y Valores 2º Tetra Unid 2MARCELO GUTIERREZ GARCÍAAún no hay calificaciones
- Ciclo MenstrualDocumento17 páginasCiclo MenstrualVidal BarbozaAún no hay calificaciones
- Mi Amor Te Amo Bipolar de MierdDocumento25 páginasMi Amor Te Amo Bipolar de Mierddarkblazer GAún no hay calificaciones
- Guia 1ro Medio Biologia Desarrollo SustentableDocumento2 páginasGuia 1ro Medio Biologia Desarrollo SustentableMaurismer ArenasAún no hay calificaciones
- Cuadernillo #1 Ciencias 2016Documento98 páginasCuadernillo #1 Ciencias 2016Maurismer ArenasAún no hay calificaciones
- Cuadernillo #2 Ciencias Plan Anual CHDocumento105 páginasCuadernillo #2 Ciencias Plan Anual CHMaurismer ArenasAún no hay calificaciones
- Biología Molecular y Celular - Final (RESUMEN)Documento265 páginasBiología Molecular y Celular - Final (RESUMEN)Maurismer ArenasAún no hay calificaciones
- Guardian de Mi CorazonDocumento1 páginaGuardian de Mi CorazonMaurismer ArenasAún no hay calificaciones
- Cuadro Comparativo Los EvangeliosDocumento5 páginasCuadro Comparativo Los EvangeliosMaurismer ArenasAún no hay calificaciones
- Guardian de Mi CorazonDocumento1 páginaGuardian de Mi CorazonMaurismer ArenasAún no hay calificaciones
- TermorregulacionDocumento23 páginasTermorregulacionMaurismer ArenasAún no hay calificaciones
- Seminario 3 PDFDocumento14 páginasSeminario 3 PDFJoselyNoemiSánchezMedinaAún no hay calificaciones
- Clase 9 - El Sistema Inmunitario en La Salud y EnfermedadDocumento33 páginasClase 9 - El Sistema Inmunitario en La Salud y EnfermedadAngiee ReyesAún no hay calificaciones
- Conceptosaludenfermedad Claudia Olivieri TV JUE Nuevos EscenariosDocumento25 páginasConceptosaludenfermedad Claudia Olivieri TV JUE Nuevos Escenariosc2014Aún no hay calificaciones
- Principios de Ventilación MecanicaDocumento63 páginasPrincipios de Ventilación Mecanicaangelito1985Aún no hay calificaciones
- Quimilab 02Documento1 páginaQuimilab 02MendozaMonicaAún no hay calificaciones
- Nietzsche y Su EnfermedadDocumento9 páginasNietzsche y Su Enfermedadmimjha100% (2)
- Sistema de Producción y Ventas de Ovinos Camilo AdsiDocumento19 páginasSistema de Producción y Ventas de Ovinos Camilo AdsicamiloAún no hay calificaciones
- Problemas de La Alimentación - SolucionesDocumento31 páginasProblemas de La Alimentación - SolucionesTuBienestarSanLuis CRISTIAN ESCUDEROAún no hay calificaciones
- 4-Curso de Tecnicas de Diagnostico Molecular 2020-8-12 - FinalDocumento62 páginas4-Curso de Tecnicas de Diagnostico Molecular 2020-8-12 - FinalMarcela FerrariAún no hay calificaciones
- Genética - Biología - DP2021Documento5 páginasGenética - Biología - DP2021Alvaro Bandenay CanalesAún no hay calificaciones
- Anatomía Radiológica: Dra. Ana Gema Blanco CabañeroDocumento171 páginasAnatomía Radiológica: Dra. Ana Gema Blanco CabañeroMaria MiguensAún no hay calificaciones
- Temario Proceso Selectivo de Enfermero Sacyl 2015Documento6 páginasTemario Proceso Selectivo de Enfermero Sacyl 2015ester9dAún no hay calificaciones
- Bacterias PatogenasDocumento63 páginasBacterias PatogenasMaricarmenAún no hay calificaciones
- Tsa2 5497 29-05-2021Documento10 páginasTsa2 5497 29-05-2021ATILIO ALEJANDRO ALVAREZ RAMOSAún no hay calificaciones
- Evolución Orgánica I MEDIODocumento34 páginasEvolución Orgánica I MEDIOThe Dark KnightAún no hay calificaciones
- Trabajo Oooooooooo OooooooDocumento19 páginasTrabajo Oooooooooo OooooooMar GaretAún no hay calificaciones
- Prevención de Riesgos en Los AncianosDocumento3 páginasPrevención de Riesgos en Los AncianosEdu Alvines Román DjEduAún no hay calificaciones
- El Tejido EpitelialDocumento14 páginasEl Tejido EpitelialAlex FernandezAún no hay calificaciones
- Limpia Tu Colon de Forma Natural Con Estos 5 Remedios CaserosDocumento5 páginasLimpia Tu Colon de Forma Natural Con Estos 5 Remedios Caserosradamantis67Aún no hay calificaciones
- Estudios de CohorteDocumento17 páginasEstudios de CohorteSebastian BuitragoAún no hay calificaciones
- Uso Predictivo de ProcaDocumento54 páginasUso Predictivo de ProcaelbartooriginalAún no hay calificaciones
- Nuevas Aportaciones TdahDocumento12 páginasNuevas Aportaciones TdahmlmleAún no hay calificaciones
- Actividad #3 (Còdigo Genètico)Documento2 páginasActividad #3 (Còdigo Genètico)Ambar Garcés AlvaradoAún no hay calificaciones
- Fuentes de Información 2Documento10 páginasFuentes de Información 2Melisa Martínez HernándezAún no hay calificaciones
- 3ro B Act 5 Meiosis 1ra ParteDocumento3 páginas3ro B Act 5 Meiosis 1ra ParteMaría moraAún no hay calificaciones
- Mapaconceptual Adrian CotaDocumento1 páginaMapaconceptual Adrian CotaAdrian Cota Gallegos100% (1)
- Muestreo de Manos en Área de Empaquetamiento en La Fábrica Quesos El PotreroDocumento8 páginasMuestreo de Manos en Área de Empaquetamiento en La Fábrica Quesos El PotreroIrvin Pech GarciaAún no hay calificaciones
- TeratógenosDocumento8 páginasTeratógenoscarmenmh2001100% (1)