Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Determinación de Grupo Sanguíneo y Subgrupos
Cargado por
ANGEL HUMBERTO ZELAYA OLIVERADescripción original:
Título original
Derechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
Determinación de Grupo Sanguíneo y Subgrupos
Cargado por
ANGEL HUMBERTO ZELAYA OLIVERACopyright:
Formatos disponibles
FACULTAD DE BIOANALISIS
LIC. QUIMICA CLINICA.
NOMBRE: MIGUEL ANGEL ORTIZ GIL.
CATEDRATICA: Q.C. RUTH ESTRADA MARQUEZ
DIVULGACION CIENTIFICA DE LA QUIMICA CLINICA
www.quimicaclinicauv.blogsp
ot.com
OBTENIDO DE: www.quimicaclinicauv.blogspot.com 1
CONTENIDO:
1. ―DETERMINACIÓN DE GRUPO SANGUÍNEO ABO Y RH‖
2. DETERMUNACION DE SUBGRUPOS
3. DETERMINACION DE RH
4. DETERMINACION DE GRUPO SANGUINEO POR TECNICA DE GEL
5. PRUEBA DE COMPATIBILIDAD
6. PRUEBA DE COMPATIBILIDAD SANGÍNEA (TÉCNICA SALINA)
7. PRUEBA DE COMPATIBILIDAD SANGUÍNEA (TÉCNICA ALBUMINA)
8. PRUEBA DE COMPATIBILIDAD SANGUINEA PRUEBA DE LISS.
9. DETERMINACION DE COOMBS DIRECTO
10. IDENTIFICACION DE ANTICUERPOS IRREGULARES
OBTENIDO DE: www.quimicaclinicauv.blogspot.com 2
Practica No. 1
“Determinación de grupo sanguíneo ABO y Rh”
Introducción:
Un grupo sanguíneo es una forma de agrupar ciertas características de la sangre que
dependen de los antígenos presentes en la superficie de los glóbulos rojos y en el suero de la
sangre.
Esta ha sido la base para que se pueda clasificar a la sangre en cuatro grupos en cuanto al
sistema ABO: grupo A, grupo AB, grupo B y grupo O; y en dos con respecto al sistema Rh: Rh
negativo o Rh positivo. Lo que a la postre trae ocho grupos posibles por las combinaciones
posibles entre ambos sistemas.
Las transfusiones de sangre entre grupos incompatibles pueden provocar una reacción
inmunológica que puede desembocar en muerte.
Las personas con sangre del tipo A tienen glóbulos rojos que expresan antígenos de tipo A en
su superficie y anticuerpos contra los antígenos B en el suero de su sangre.
Las personas con sangre del tipo B tiene la combinación contraria, glóbulos rojos con
antígenos de tipo B en su superficie y anticuerpos contra los antígenos A en el suero de su
sangre.
Los individuos con sangre del tipo O no expresan ninguna de los dos antígenos (A o B) en la
superficie de sus glóbulos rojos pero pueden fabricar anticuerpos contra ambos tipos, mientras
que las personas con tipo AB expresan ambos antígenos en su superficie y no fabrican ninguno
de los dos anticuerpos.
A causa de estas combinaciones, el tipo O puede ser transfundido sin ningún problema a
cualquier persona con cualquier tipo ABO y el tipo AB puede recibir de cualquier tipo ABO.
Los donantes de sangre y los receptores deben tener grupos compatibles. El grupo O- es
compatible con todos, por lo que quien tiene dicho grupo se dice que es un donante universal.
Por otro lado, una persona cuyo grupo sea AB+ podrá recibir sangre de cualquier grupo, y se
dice que es un receptor universal.
Material y equipo:
40 tubos de ensayo de 12 x 75
4 pipetas Pasteur
1 gradilla de unicel
3 tubos Vacutiner con muestra sanguínea anticoagulada con EDTA
1 tubo Vacutainer con muestra sanguínea sin anticoagulante
Antisuero Anti-A, Anti-AB, Anti-B y Anti-D *
Eritrocitos con antígenos conocidos A1, A2, B y O
OBTENIDO DE: www.quimicaclinicauv.blogspot.com 3
1 centrifuga
*Reactivos:
Antisuero A monoclonal Lafon Antisuero AB monoclonal Lafon
Lote:9662 Lote: 8764
Cad: 09NOV08 Cad: 31OCT08
Aspecto: transparente Aspecto:transparente
Color: azul Color: incoloro
Antisuero B monoclonal Lafon Antisuero D monoclonal NOVACLONE
Lote: 9762A Lote: NDMG04305
Cad:09NOV08 Cad: 29MAR08
Aspecto: transperente Aspecto: transperente
Color: amarillo Color: incoloro
Técnica:
Método directo
1. Centrifugar los 3 tubos Vacutiner con muestra sanguínea anticoagulada con EDTA y el
tubo Vacutainer con muestra sanguínea sin anticoagulante, a una velocidad de 2500
r.p.m. por 10 minutos, pues se utilizaran plasma y eritrocitos por separado.
2. Rotular los tubos de ensayo de la siguiente manera: en cada tubo rotular dos números
en la muestra, uno correspondiente del 1 al 4, el otro numero corresponde al que ya
traía la muestra, y con el tipo de antisuero: Anti-A, Anti-AB, Anti-B ó Anti-D. Ejemplo: 1,
13, Anti-A; 1,13, Anti-AB, etc. El procedimiento se repite para las tres muestras
restantes.
3. En cuatro tubos limpios hacer una dilución de 2-5 % de eritrocitos con agua destilada,
de cada muestra. La dilución tomara un color rojo tenue, similar a la sangría.
4. Colocar en cada tubo rotulado una gota de la dilución de eritrocitos preparada y una
gota de antisuero, según corresponda.
5. Al concluir lo anterior, llevar los tubos a la centrifuga y centrifugar por solo 15 segundos
a una velocidad de 1000 r.p.m. para observar mejor la reacción antigeno-anticuerpo
(formación de un botón).
6. Por ultimo leer los tubos, observando si hubo reacción o no, y correlacionando los
datos obtenidos con el método inverso para determinar el grupo sanguíneo.
Metodo inverso
1. Centrifugar los 3 tubos Vacutiner con muestra sanguínea anticoagulada con EDTA y el
tubo Vacutainer con muestra sanguínea sin anticoagulante, a una velocidad de 2500
r.p.m. por 10 minutos, pues se utilizaran plasma y eritrocitos por separado.
2. Rotular los tubos de ensayo de la siguiente manera: en cada tubo rotular dos números
en la muestra, uno correspondiente del 1 al 4, el otro numero corresponde al que ya
traía la muestra, y con el tipo de eritrocitos con antigeno conocido: A1, A2, B y O.
Ejemplo: 1,13, A1; 1,13, A2; etc. El procedimiento se repite para las tres muestras
restantes.
3. Colocar en cada tubo rotulado dos gotas ya sea de plasma o suero según corresponda
y una gota de los eritrocitos con antigeno conocido.
4. Al concluir lo anterior, llevar los tubos a la centrifuga y centrifugar por solo 15 segundos
a una velocidad de 1000 r.p.m. para observar mejor la reacción antigeno-anticuerpo
(formación de un botón).
OBTENIDO DE: www.quimicaclinicauv.blogspot.com 4
5. Por ultimo leer los tubos, observando si hubo reacción o no, y correlacionando los
datos obtenidos con el método inverso para determinar el grupo sanguíneo.
Resultados:
Muestra Método directo Método inverso Grupo y
Anti-A Anti-AB Anti-B Anti-D A1 A2 B O Rh
1 - - - + + + + - O+
2 - + + + + + - - B+
3 + + - + - - + - A+
4 + + + + + - - - AB +
Interpretación:
Para el método directo la lógica fue: si en un tubo hay formación de botón (reacción antigeno-
anticuerpo) quiere decir que los eritrocitos ensayados tienen el antigeno que reacciona con los
anticuerpos presentes en el antisuero para ese tubo; y si no presentan aglutinación querrá
decir que no corresponde el antigeno del eritrocito con el anticuerpo del antisuero, o que el
antigeno esta ausente en esos eritrocitos. De ahí que pueda observarse que una muestra
sanguínea muestre un solo tipo de antígenos del sistema ABO sobre su membrana (A o B),
ambos antígenos (AB), o ninguno de ellos (O). lo mismo sucede para el sistema Rh ; al
presentarlo (Rh +) o no (Rh -).
Para el método inverso el razonamiento fue: si en un tubo hay formación del botón (reacción
antigeno-anticuerpo) quiere decir que el plasma del paciente ensayado tiene los anticuerpos
que reaccionan con los eritrocitos con antigeno conocido, los cuales sirven de reactivo para
esta prueba. Por lo tanto una reacción positiva en este método definitivamente indica que el
paciente no tiene eritrocitos con antígenos que reaccionarían con los anticuerpos de su plasma.
De ahí que el método se le nombre inverso.
Conclusión:
Concluyo que Para realizar una transfusión sanguínea se debe tomar en cuenta la sangre del
donante y la del receptor. Los individuos pertenecientes al grupo O pueden donar sangre a
cualquier otro grupo sanguíneo, porque sus eritrocitos carecen de antigeno que puedan ser
reconocidos por la sangre del receptor. Las personas del grupo AB pueden recibir sangre de
cualquier grupo, ya que carecen de anticuerpos
OBTENIDO DE: www.quimicaclinicauv.blogspot.com 5
PRACTICA Nº 2
DETERMUNACION DE SUBGRUPOS
Anti- A1Lectina
(Dolichos biflorus)
Lectina de grupo sanguíneo
INTRODUCCION:
El sistema de grupos sanguíneos ABO sigue siendo el primero
a tener en cuenta en el momento de realizar una transfusión
de sangre. Los antígenos A y B son productos génicos
fácilmente detectables y constituyen marcadores
genéticos de gran valor. Entre los individuos A, se
distinguen 2 categorías: A1y A2.
La diferenciación entre ambas se realiza mediante la
utilización de anticuerpos monoclonales y lectinas
específicas de grupo sanguíneo Dolichos biflorus (anti A1)
y Ulex europaeus (anti H).
Uso: Inmucor anti-A1 Lectin se utiliza para diferenciar células rojas A1 de otros
subgrupos A en pruebas en tubo o en placa.
MATERIAL Y EQUIPO:
Tubos de ensaye de 10/75 mm.
Cronometro
Marcador
Centrifuga serológica
MUESTRA BIOLOGICA:
Células rojas de donador o paciente
REACTIVO:
Inmucor anti-A1 Lectin en gotero
MARCA: INMUCOR. INC
LOTE: SN2132
CADUCIDAD: 2007-12-14
TECNICA:
1. Adicione una gota de anti-A1 a tubos adecuadamente marcados.
2. Adicione una gota de una suspensión de eritrocitos bajo prueba del 3-5% en
salina. Mezcle completamente el contenido del tubo.
OBTENIDO DE: www.quimicaclinicauv.blogspot.com 6
3. Centrifugar de 15-30 minutos de 900-1000 rpm.
4. Agite suavemente el tubo y resuspenda el botón celular. Examine las reacciones
resultantes macroscópicamente. Registre resultados.
RESULTADOS ESPERADOS DE TIPIFICACION
GRUPO Anti-A Anti-A1 Porciento
SANGUINEO
A1 + + 80% DE TODOS
LOS GRUPOS A
A1b + + 80% DE TODOS
LOS GRUPOS AB
A2 + 0 20% DE TODOS
LOS GRUPOS A
A2B + 0 20% DE TODOS
LOS GRUPOS AB
A1NT + +DEBIL NO COMUN
A3AM1AX1 + DEBIL 0 NO CUMUN
ANTI-H (LECTINA)
Ulex europeaus
Para la determinación de del estado secretor y tipificación de las células rojas
INTRODUCCION:
La mayoría de los grupos sanguíneos ABO que se determinan
en el banco de sangre cumplen con las leyes establecidas de
antígenos y anticuerpos recíprocos para ese sistema.
Los anticuerpos del sistema ABO existen en el individuo
desde el momento en que son capaces de tener una respuesta
inmunológica y se producen contra los antígenos A y B.
Los subgrupos son fenotipos ABO que difieren en la cantidad
de antígeno presente en los eritrocitos y en la saliva de
los secretores. Se hallan con mayor frecuencia y tienen más
relevancia clínica los de A, que los de B. Al utilizar
lectinas se definen los subgrupos: A1 y A2: con el extracto
de Dolichos biflorus se aglutinan los eritrocitos A1, pero
no los de A2; y el anti H, semilla Ulex europeus, aglutina
eritrocitos que tienen antígeno H.
OBTENIDO DE: www.quimicaclinicauv.blogspot.com 7
MATERIAL Y EQUIPO:
Tubos de ensaye de 10/75mm.
Cronometro
Marcador
Centrifuga serológica
MUESTRA BIOLOGICA:
Células rojas de donador o paciente
REACTIVO:
Inmucor anti-H (Lectina) en gotero
MARCA: GANMA.
LOTE: ML1581
CADUCIDAD: 2007-11-14
TECNICA:
1. Adicione una gota de una suspensión de eritrocitos bajo prueba del 3-5% en
salina en tubos adecuadamente marcados.
2. Adicione dos gotas de anti-H Lectina y mezcle completamente el contenido del
tubo.
3. incube durante 5 minutos a temperatura ambiente.
4. Centrifugar de 15-30 minutos a 1000 rpm.
5. Agite suavemente el tubo y resuspenda el botón celular. Examine las reacciones
resultantes macroscópicamente. Registre resultados.
INTERPRETACIÓN:
PROBLEMA: ANTI A1 ANTI H RESULTADO
(ANTI A2) SUBGRUPO:
PACIENTE 1 + - ANTI A1
PACIENTE 2 - + ANTI A2
Prueba positiva: Aglutinación de las células rojas.
Nota: La hemólisis no debe interpretarse como un resultado positivo ya que esto
puede indetificarse como contaminación del reactivo.
Prueba negativa: Ausencia de aglutinación de las células rojas.
CONCLUSIONES:
Concluyo que para realizar una
transfusión sanguínea se debe tomar en
cuenta los subgrupos del donante y del
receptor. Los subgrupo con mayor
frecuencia y tienen más relevancia
clínica los de A, que los de B. Y se
identifican por medio de utilizar
lectinas. Los subgrupos A más
importantes son: A1 y A2.
OBTENIDO DE: www.quimicaclinicauv.blogspot.com 8
PRACTICA # 3
DETERMINACION DE Rh
INTRODUCCIÓN:
El factor Rh es una clase de proteína que se encuentra en
los glóbulos rojos de la sangre, cuando alguien tiene esa
proteína se le considera ―Rh Positivo‖. Cuando no la tiene
es ―Rh Negativo‖. El factor Rh es hereditario y se
transmite en dos genes. El Factor Rh positivo es dominante,
es decir si una persona tiene un gen positivo y otro
negativo, su factor Rh será positivo.
Esta prueba es importante en el diagnostico y estudio
de la eritroblastosis fetal, en la que los glóbulos
rojos del niño se encuentran sensibilizados con
anticuerpo materno. Es útil también en el diagnostico
de la anemia hemolítica adquirida (anticuerpos sobre
los glóbulo rojos del mismo paciente), así como la
determinación de eritrocitos sensibilizados en sangre
usados para transfusión.
Las dos clasificaciones más importantes para describir
grupos sanguíneos en humanos son los antígenos y el factor
Rh. Las transfusiones de sangre entre grupos incompatibles
pueden provocar una reacción inmunológica que puede
desembocar en hemólisis, anemia, fallo renal, shock, o
muerte.
MATERIAL:
Tubos de ensayo de 12 x 75
Pipetas Pasteur
Gradilla
EQUIPO:
Centrifuga
MUESTRA BIOLÓGICA:
Eritrocitos lavados 3-5% del paciente
REACTIVOS:
Antisuero Anti-D
Suero anti globulina humana.
Suero reactivo control
Antisuero D monoclonal NOVACLONE
Lote: NDMG04305
CAD: 29MAR08
Aspecto: transparente
Color: incoloro
OBTENIDO DE: www.quimicaclinicauv.blogspot.com 9
Suero anti globulina Humana
Lote: 405
CAD: 06-NOV-08
Aspecto: transparente
Color: verde
Reactivo control GAMMA-CLONE
Lote: GCM115-3
CAD: 2008-12-08
Aspecto: transparente
Color: incoloro
TÉCNICA:
Determinación de Rh
Prepare una suspensión de glóbulos rojos al 3-
5 % en solución salina. Los glóbulos deben ser
lavados previamente 5 veces con el objeto de
eliminar las proteínas del plasma.
Rotular 3 tubos, para la previa identificación
de Rh.
Ponga 1 gota de la suspensión lavada en cada
tubo.
Añada una gota de anti suero D monoclonal.
Mezcle y centrifugue 15 seg. Y observe si hay
aglutinación.
Preparación del control negativo
Ponga una gota de eritrocitos lavados al 3-5 %
Añada una gota de reactivo control.
Centrifugue 15 seg. y observe si hay aglutinación
Detección de sangre Du
Nota: esta técnica se le realizo a los tubos problemas
que no aglutinaron .
Los tubos que no tuvieron aglutinación en la
determinación de Rh se incuban 15 min, y
posteriormente se lavan 3 veces con sol. Salina
Previamente lavados se le agregan 2 gotas de suero de
COOMBS.
Centrifugar 15 seg y observar, desprender boton
OBTENIDO DE: www.quimicaclinicauv.blogspot.com 10
ESQUEMAS:
RESULTADOS:
problemas Aglutinación resultado
2 positiva Rh +
10 negativa Rh -
11 negativa Rh -
Paciente 2 código 021612 plata Lugo Javier
Paciente 10 código 021620 Hernández López Guillermo
Paciente 11 código 021621 camarillo Sonia rebeca
INTERPRETACIÓN:
Para el primer método:
Aglutinacion: Rh positivo
No aglutinación: realizar prueba de detección de
sangre Du.
Detección de sangre Du
Aglutinación. D débil (Du positivo)
No aglutinación: Rh negativo
CONCLUSIONES:
Con el descubrimiento del sistema Rh, se denominan Rh
positivos los hematíes que son aglutinados por este
anticuerpo y tienen, por tanto, el antígeno Rh en la
superficie. Se denominan Rh negativos los que no son
aglutinados y que, por tanto, no poseen el antígeno Rh en
su superficie.
De la misma manera que en el sistema ABO, en el sistema Rh
no se puede transfundir el antígeno Rh a las personas que
no lo tienen, ya que podría originar la producción de
anticuerpos Rh en el receptor. Los sujetos Rh negativos
sólo podrán recibir sangre de donantes Rh negativos.
OBTENIDO DE: www.quimicaclinicauv.blogspot.com 11
PRACTICA 4
INMUNOHEMATOLOGIA
DETERMINACION DE GRUPO SANGUINEO POR TECNICA DE GEL
INTRODUCCION:
El sistema utilizado en inmunohematología para investigar e identificar antígenos y
anticuerpos antieritrocitarios. Es de tecnología de microtipificación en gel se basa en la
separación por tamaño de los eritrocitos aglutinados, durante un proceso de
centrifugación en un gel poroso.
Los eritrocitos van perdiendo elasticidad en sus membranas de forma que los
aglutinados grandes quedan atrapados en la zona superior y los pequeños quedan
distribuidos a lo largo de la columna.
Esta técnica nos permite que estandaricemos la lectura de la reacción antígeno-
anticuerpo con facilidad y repetitividad. Así como la estandariza del uso de reactivos,
tiempos y lecturas disminuyendo sustancialmente la influencia de la mano de operador.
OBJETIVO: determinación de los antigenos del sistema ABO,Rh (D) y determinacion
del grupo serico , en tecnica de gel.
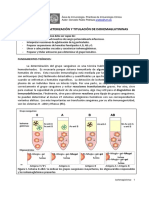
FUNDAMENTOS:
El principio del metdo se basa en la tecnica de gel descrita por Y. Lapierre para la
deteccion de las reacciones de aglutinacion de los hematies. La aglutinacion se produce
al entar en contacto los eritrocitos con los anticuerpos correspondientes.
La tarjeta DG gel es un soporte de plastico constituidos por 8 microtubulos. Cada
microtubulo esta formado por una columna y una camara de dispersion/incubacion.
La tecnología de microtipificación en gel se basa en la separación por tamaño de los
eritrocitos aglutinados, durante un proceso de centrifugación en un gel poroso.
Los eritrocitos van perdiendo elasticidad en sus membranas de forma que los
aglutinados grandes quedan atrapados en la zona superior y los pequeños quedan
distribuidos a lo largo de la columna.
OBTENIDO DE: www.quimicaclinicauv.blogspot.com 12
MATERIAL
Pipeta automática 10 ul, 50ul, 1 ml.
Puntas de pipeta desechable
Tubos de vidrios
DEG sol
Centrifugas para tarjetas DG gel
Hematies de reactivos para grupo inverso.
MUESTRA BIOLOGICA:
Células rojas de donador o paciente
REACTIVO:
Placa de gel
Reactivo de gel sol
TECNICA
1.- determinacion de los antigenos del sistema ABO/Rh.
-preparar una suspension de hematies al 5 % de DG sol. Asegurar la resuspencion de lso
hematies antes de utilizar.
Anadir en cada microtubulos indicados 10 ul de una suspension de hematies al 5%.
2.- determinacion de l grupo serico.
-homogenizar los hematies recativos A1/B
- dispersar el microtubulo N /a1 50 ul de hematies reactivos A1 en un microtubulo N/b
50 ul de hematies reactivos B.
-añadir suero o plasma.
3.- centrigugar en centrifuga para DG sol.
Leer los resultados.
RESULTADOS
NEGATIVO - Banda de hematies al fondo de la columna, resto de la columna sin
aglutinados
+/- Escasoa glutinados de pequeño tamaña d ela columna.
1+ Algunos aglutinados pequeñso en la columna
POSITIVO 2+ aglutinados pequeñso en la columna o mediano a lo largo de la columna
3+ Banda superior de aglutinado
4+ Banda de aglutinados en la parte superior de la columna.
DP Doble poblacion (doble banda de hematies , en el fondo y en la parte
superior.
INTERPRETACION DE RESULTADOS.
GRUPO HEMATICO GRUPO SERICO
microtubo microtubo microtubo microtubo MICROTUBUBO MICROTUBUBO ABO
N+ a1 N+ B GRUPO
A B AB CTL
0 0 0 0 + + 0
+ 0 + 0 0 + A
OBTENIDO DE: www.quimicaclinicauv.blogspot.com 13
0 + + 0 + 0 B
+ + + 0 0 0 AB
SISTEMA Rh
Micrutubo D Micrutubo Micrutubo INTERPRETACION
D” CTL
+ + 0 D positivo
0 0 0 D negativo
0 + 0 D débil parcial
+ 0 0
RESULTADO E INTERPRETACION DE LA PRACTICA
Resultado; A+
CONCLUSION
Concluyo que esta técnica, es una forma de estabilizar las reacciones de aglutinación y
reducir los resultados falsamente negativos a consecuencia de una técnica inapropiada,
asi como crear un método de interpretaciones sencillas y constantes.
OBTENIDO DE: www.quimicaclinicauv.blogspot.com 14
Practica No. 5
“Prueba de compatibilidad”
Introducción:
Para requerir una óptima transfusión actualmente se
requiere de aceptaciones inmunológicas receptor - donante,
ya que la transfusión de sangre o la de sus componentes
celulares de un donante a un receptor es una forma de
transplante.
La prueba de Coombs se usa para determinar la presencia de
anticuerpos no aglutinantes en el suero de sujetos
sensibilizados a uno o mas antígenos sanguíneos. Es útil en
el estudio del suero de mujeres con isoinmunización
materno-fetal y se emplea también en otro tipo de pruebas
como identificación de anticuerpos autoinmunes, detección
de algunos sistemas sanguíneos y pruebas de compatibilidad
sanguínea.
La prueba indirecta se realiza con eritrocitos normales
incubados in Vitro con el suero de estudio. Durante este
periodo, si existe un anticuerpo, este se fija sobre su
respectivo determinante antigénico. Una vez fijados, los
eritrocitos son igualmente lavados y se agrega el reactivo
de Coombs, produciendo aglutinación.
Una prueba de Coombs indirecta positiva significa que
existen anticuerpos libres en el suero de la persona, los
cuales puedan ser igualmente auto-anticuerpos o
isoanticuerpos.
Material y equipo:
Pipetas automáticas de 10 µl, 25 µl, 50 µl y 1 ml.
Puntas de pipetas desechables
Tubos de vidrio.
Incubador para tarjetas DG Gel.
Centrifuga para tarjetas DG Gel.
Material biológico:
Hematíes reactivo para investigación e identificación de anticuerpos irregulares de
Diagnostic Grifols, S.A.
Suero de hemoclasificación.
Muestras de sangre de extracción reciente, recogida con anticoagulante o sin
anticoagulante.
Reactivos:
OBTENIDO DE: www.quimicaclinicauv.blogspot.com 15
Tarjetas DG Gel.
DG Gel Sol.
*Reactivos:
Tarjetas DG Gel Coombs DG Gel Sol
Rango de temperatura: entre 2 y 25 ºC Rango de temperatura: entre 2 y 8ºC
Lote: 7049.01 Lote: 7003.701
Cad: 2008-03 Cad: 2008-06
Aspecto: transparente Aspecto: transparente
Color: verde Color: incoloro
Técnica:
Método manual:
1. Dejar atemperar (18-25ºC) muestras y reactivo.
2. Inspeccionar el estado de las tarjetas antes de utilizar.
3. Identificar las tarjetas y muestras a utilizar.
4. Despegar con precaución la lamina de metal que cubre los microtubos para prevenir
contaminaciones cruzadas entre ellos.
5. Preparar una suspensión con hematíes al 1% en DG Gel Sol (10 µl de sedimento o
concentrado de hematíes en 1 ml de DG Gel Sol). Utilizar los hematíes del donante
para la PC mayor y hematíes del receptor para la PC menor. Asegurar la suspensión
de los hematíes antes de utilizar.
6. Dispensar en el tubo correspondiente, 50 µl de suspensión de los hematíes al 1% del
donante (PC mayor) o 50 µl de suspensión de los hematíes al 1% del receptor (PC
menor).
7. Añadir 25 µl de suero o plasma del receptor (PC mayor) o 25 µl de suero o plasma del
donante (PC menor).
8. Preparar auto control con 50 µl de suspensión de los hematíes al 1% del receptor y 25
µl de suero o plasma del receptor.
9. Incubar 15 minutos a 37 ºC.
10. Centrifugar en la centrifuga para tarjetas DG Gel.
11. Leer los resultados.
Interpretación:
Negativo: - Banda de hematíes en el fondo de la columna, resto de la columna sin aglutinados visibles.
Positivo: +/- Escasos aglutinados de pequeño tamaño en la mitad inferior de la columna.
1+ Algunos aglutinados de pequeño tamaño en la columna.
2+ Aglutinados de tamaño pequeño o mediano a lo largo de la columna.
3+ Banda superior de aglutinados, de tamaño mediano en la mitad superior de la columna.
4+ Banda de hematíes aglutinados en la parte superior de la columna.
DP: Doble población (doble banda de hematíes, en el fondo y en la parte superior de la columna.
Resultados:
Paciente: Lira Cabrera Carlos Alberto (AB+)
OBTENIDO DE: www.quimicaclinicauv.blogspot.com 16
Donador 1: Orea Valero Erasmo. (A+)
Donador 2: Moreno Adolfo. (O+)
M1 m1 M2 m2 Autocontrol
GR de donador 1 + GR del paciente + GR de donador 2 + GR del paciente + GR del paciente +
suero del paciente suero de donador 1 suero del paciente suero de donador 2 suero del paciente
- + - + -
Por lo antes expuesto se puede deducir que el donador 1 (A+) puede donar eritrocitos al
paciente (AB+), lo mismo que el donador 2 (O+) puede donarle eritrocitos; no así plasma por
parte de ambos donadores pues la prueba muestra que hubo reacción en ambas pruebas
menores.
Conclusión:
Concluyo que es esencial que toda la sangre sea estudiada
antes de la transfusión para: Asegurar que todos los
glóbulos rojos transfundidos son compatibles con los
anticuerpos en el plasma del paciente. Evitar estimular la
producción de nuevos anticuerpos contra los glóbulos rojos
en el receptor, especialmente anti-Rh D.
OBTENIDO DE: www.quimicaclinicauv.blogspot.com 17
PRÁCTICA No. 6
PRUEBA DE COMPATIBILIDAD SANGÍNEA
(Técnica salina)
INTRODUCCIÓN
Landsteiner constató que cuando un aglutinógeno se pone
en contacto con la aglutinina homóloga se produce una
aglutinación.
La compatibilidad sanguínea es la posibilidad de mezcla
de sangre sin que se produzcan trastornos, tales como los
fenómenos de la lisis o de la aglutinación.
A causa de este fenómeno biológico en las transfusiones
de sangre no es suficiente con conocer que la sangre del
donante y la del receptor son del mismo grupo, o bien que
la del donante pertenezca al grupo O (cero), sino que es
necesario conocer si la compatibilidad es perfecta, porque
ningún otro fenómeno de inmunización interfiera. Es en
este sentido por lo que son empleadas las pruebas
cruzadas.
Además de los 6 antígenos del sistema ABO en los
eritrocitos humanos, existen numerosos sistemas de
aglutinógenos que contienen muchos antígenos individuales
en los eritrocitos (más de 500.000 millones posibles de
fenotipos de grupos sanguíneos conocidos). Para evitar
accidentes transfusionales es indispensable tener en
cuenta el sistema Rh además del ABO.
Del sistema de antígenos Rh es el D el más antigénico, y
el término Rh positivo indica que el individuo presenta
aglutinógeno D. El individuo Rh negativo no tiene antígeno
D y forma la aglutinina anti-D en contacto con éste.
Las reacciones antígeno-anticuerpo pueden observarse in
vitro por:
— Hemólisis: la unión antígeno-anticuerpo se traduce en
lisis de los eritrocitos en presencia
del complemento (siempre que el anticoagulante empleado no
capture los
iones Ca y Mg necesarios para la activación del
complemento).
— Aglutinación: los anticuerpos que reaccionan en medio
salino se conocen como
anticuerpos completos o aglutinantes (comúnmente tipo
IgM).
OBTENIDO DE: www.quimicaclinicauv.blogspot.com 18
OBJETIVO: Determinación de los antigenos del sistema ABO,
Rh (D) y su compatibilidad entre un paciente Donador y un
Paciente Receptor.
MATERIAL EQUIPO
*5 Tubos de ensaye. Microcentrífuga.
*6 Pipetas Pasteur. Baño María ó Estufa.
*1Gradilla.
*1 Bulbo.
*Papel Parafilm.
MUESTRA
Muestra de sangre con Anticoagulante EDTA.
REACTIVOS
Antisuero RO-Antiglobulina humana (Poliespecífico Anti IgG
C-d)
Para prueba de Coombs.
LABORATORIOS LAFON S.A de C. V.
Fecha de Caducidad: 31-Ene-09
Lote: 406
Hecho en México
Aspecto: Transparente:
Color: Verde
TÉCNICA
Lavar los eritrocitos con solución salina (3 veces).
SALINA RÁPIDA:
1. Agregar una gota de Eritrocitos Lavados.
2. Diluirlo al 3-5% con solución salina 0.9%.
3. Agregar 2 gotas de suero.
4. Centrifugar y observar, anotar desprendimiento del botón.
PRUEBA MAYOR PRUEBA MENOR AUTOTESTIGO
G. Rojos del DONADOR G. Rojos del RECEPTOR G. Rojos del RECEPTOR
+ (paciente) (paciente)
Suero del RECEPTOR + +
(paciente) Suero del DONADOR Suero del RECEPTOR
(paciente)
SALINA 37° BAÑO MARÍA:
1. Incubar tubos a Baño maría a 37°C durante 1
hora (o 20 min).
OBTENIDO DE: www.quimicaclinicauv.blogspot.com 19
2. Centirfugar después de haber pasado el
tiempo.
3. Desprender el botón de eritrocitos y
observar.
AGLUTINACIÓN– No es compatible.
NO AGLUTINACIÓN - Lavar 3 veces.
SALINA COOMBS:
1. Con solución salina 0.9% lavar los
eritrocitos de los tubos q no tuvieron
aglutinación 3 veces.
2. Decantar y agregar 2 gotas de reactivo
de Coombs
AGLUTINACIÓN – No es compatible.
NO AGLUTINACIÓN - Lavar 3 veces.
RESULTADOS
Paciente: Madrigal Méndez Luis Eduardo (B+)
Folio: 009164
Fecha:30/10/07
Donador 1: Torres Avilés José Ramón (O+)
Folio: 022604
Fecha:31/10/07
Donador 2: Rodríguez Núñez José Angel (A+)
Folio: 022605
Fecha:31/10/07
SALINA RÁPIDA:
M1 m1 M2 m2 Autotestigo
GR de donador 1 GR del paciente GR de donador 2 GR del paciente GR del paciente
+ suero del + suero de + suero del + suero de + suero del
paciente donador 1 paciente donador 2 paciente
- 4+ 4+ 4+ -
SALINA 37° BAÑO MARÍA:
M1 m1 M2 m2 Autotestigo
- 4+ 4+ 4+ -
Compatible No No No Compatible
compatible compatible compatible
SALINA COOMBS:
M1 Autotestigo
- - -
Compatible Compatible
OBTENIDO DE: www.quimicaclinicauv.blogspot.com 20
Por lo tanto se puede decir que el donador 1 (O+) puede
donar suero al paciente (B+), debido a que en el suero no
hay anticuerpos de ningún tipo que reaccionen con los
antígenos de los eritrocios del Donador 1. Mientras tanto
el Donador 2 no puede donar al Paciente ni suero ni
eritrocitos.
INTERPRETACIÓN
PRUEBA POSITIVA: Existe una aglutinación de las
células sanguíneas que indica la presencia del
antígeno A o B. En el suero de Coombs notamos si esta
la precencia de Antígeno D en los eritrocitos. La
hemólisis no se debe interpretar como resultado
positivo ya que puede indicar contaminación del
reactivo.
PRUEBA NEGATIVA: La no aglutinación indica un
resultado negativo e indica que las células son
negativas para Antígenos del sisitema ABO y D
CONCLUSIÓN
He concluido que en las transfusiones de sangre no es
suficiente con conocer que la sangre del donante y la del
receptor son del mismo grupo, o bien que la del donante
pertenezca al grupo O (cero), sino que es necesario
conocer si la compatibilidad es perfecta, porque ningún
otro fenómeno de inmunización interfiera. Es en este
sentido por lo que son empleadas las pruebas cruzadas.
OBTENIDO DE: www.quimicaclinicauv.blogspot.com 21
Práctica No. 7
“Prueba de compatibilidad sanguínea (técnica albumina)”
Introducción:
La tipificación de sangre identifica el tipo sanguíneo determinando
antígenos presentes en los eritrocitos, detecta aloanticuerpos en
contra esos antígenos. Así los aloanticuerpos pueden aparecer
naturalmente o ser inducidos y pueden ser dirigidos contra del grupo
conocido o a los antígenos de superficie de los eritrocitos. La prueba
de compatibilidad sanguínea o cross matching esta formada por la
prueba mayor y menor.La prueba de cruzamiento mayor para los
aloanticuerpos, consiste en probar el plasma del receptor contra los
glóbulos rojos del donante. Es incompatible cuando se genera una
reacción hemolítica, los eritrocitos del donante se destruyen por los
aloanticuerpos del plasma del receptor. La prueba menor es una prueba
para los aloanticuerpos del plasma del donante en contra los glóbulos
rojos del receptor. Una incompatibilidad menor es una causa menos
frecuente para causar una reacción en contra una transfusión, porque
el volumen de plasma del donante es menor y es diluido marcadamente en
el receptor. Para llevar a cabo dicho procedimiento se utilizan
diversos reactivos como potencializadores que mejoran la unión de
eritrocitos con algún tipo de anticuerpo. Uno de esos
potencializadores es la albúmina. La albumina bovina polimerizada es
un reactivo muy utilizado en el laboratorio de inmunohematologia y en
centros de bancos de sangre, funciona como un potencializador que
facilita la reaccion de aglutinación de eritrocitos sensibilizados. Al
final de la prueba se prueban los eritrocitos con el reactivo de
Coombs. El principio de la prueba de Coombs fue descrito por Moreschi
en 1908, pero Coombs, Mourant y Race, en 1946, la introdujeron en el
estudio de los grupos sanguíneos y anticuerpos, cuando una parte de
sangre (suero) fue usada para la inoculación de animales para
inmunizarlos con proteína humana, utilizando el anticuerpo obtenido en
la detección de los llamados anticuerpos incompletos. Esta prueba se
usa para determinar la presencia de anticuerpos no aglutinantes en el
suero de sujetos sensibilizados a uno o mas antígenos sanguíneos. Es
útil en el estudio del suero de mujeres con isoinmunización materno-
fetal y se emplea también en otro tipo de pruebas como identificación
de anticuerpos autoinmunes, detección de algunos sistemas sanguíneos y
pruebas de compatibilidad sanguínea. La prueba indirecta se realiza
con eritrocitos normales incubados in Vitro con el suero de estudio.
Durante este periodo, si existe un anticuerpo, este se fija sobre su
respectivo determinante antigénico. Una vez fijados, los eritrocitos
son igualmente lavados y se agrega el reactivo de Coombs, produciendo
aglutinación. Una prueba de Coombs indirecta positiva significa que
existen anticuerpos libres en el suero de la persona, los cuales
puedan ser igualmente auto-anticuerpos o isoanticuerpos.
Objetivo: Determinación de los antígenos del sistema ABO, Rh (D) y su
compatibilidad entre un paciente Donador y un Paciente Receptor.
Material y equipo:
5 Tubos de ensaye.
6 Pipetas Pasteur.
1Gradilla.
1 Bulbo.
Papel Parafilm.
Microcentrífuga.
Baño María ó Estufa.
OBTENIDO DE: www.quimicaclinicauv.blogspot.com 22
Material biológico:
Muestras de sangre de extracción reciente, recogida con
anticoagulante o sin anticoagulante.
Reactivos:
Suero de Coombs*
Albúmina bovina °
*Suero anti-globulina humana Lafon. Lote 406. Cad: 31/01/09. Color: verde. Aspecto:
transparente.
°Albumina de bovino polimerizada Interbiol. Lote APO107. Cad: 15/01/09. Color: incoloro.
Aspecto: transparente.
Técnica:
1. Montar prueba mayor 1 y 2, prueba menor 1 y 2, y autotestigo,
con el procedimiento ya anteriormente conocido.
2. Agregar 2 gotas de albúmina al 22%.
3. Centrifugar 20 segundos.
4. observar aglutinación o hemolisis, o no aglutinación.
5. A los tubos con lecturas negativas, incubar 20 minutos en baño
María a 37 °C.
6. Centrifugar y observar:
Aglutinación o hemólisis: reportar incompatible.
No aglutinación: llevar a Coombs.
7. Lavar tres veces, decantar, y quitar el exceso de salina con
gasa y agregar 2 gotas de reactivo de Coombs y centrifugar 20
segundos y observar:
Aglutinación o hemólisis: reportar incompatible.
No aglutinación: reportar compatible.
Resultados:
1 PRUEBA MAYOR 1: 2 Gotas de suero del paciente + 1 gota de G.R. al 3-5% del
donador 1.
2 PRUEBA MENOR 1: 2 Gotas de suero del donador 1 + 1 gota de G.R. al 3-5% del
paciente.
3 PRUEBA MAYOR 2: 2 Gotas de suero del paciente + 1 gota de G.R. al 3-5% del
donador 2.
4 PRUEBA MENOR 2: 2 Gotas de suero del donador 2 + 1 gota de G.R. al 3-5% del
paciente.
5 AUTOTESTIGO: 2 Gotas de suero del paciente + 1 gota de G.R. al 3-5% del paciente.
M1 m1 M2 m2 Autotestigo
Con albúmina. - - - - -
Después de incubación a 37 °C. - - - - -
Después de Coombs. - - - - -
Después de validación con glóbulos + + + + +
positivos.
Interpretación:
Prueba positiva: Alutinación o hemolisis. Indica no compatibilidad.
Prueba negativa:No aglutinación. Indica compatibilidad.
OBTENIDO DE: www.quimicaclinicauv.blogspot.com 23
Esquemas:
Conclusión:
Concluyo que la prueba de compatibilidad sanguínea en su modalidad con
albúmina bovina ofrece mucha ventaja al ser, al igual que otros
reactivos, un potencializador de la reacción antígeno-anticuerpo. Esto
permite que el operador o realizador de la prueba tenga mayor
confianza y certeza en los resultados que obtenga.
OBTENIDO DE: www.quimicaclinicauv.blogspot.com 24
PRACTICA No. 8
PRUEBA DE COMPATIBILIDAD SANGUINEA PRUEBA DE LISS.
FUNDAMENTO:
LISS es utilizado para reducir la fuerza iónica del medio
de reacción en los procedimientos de detección e
identificación de anticuerpos y en las pruebas de
compatibilidad. La presencia de este reactivo refuerza la
interacción antígeno - anticuerpo durante la incubación.
GENERALIDADES:
El uso de solución salina de baja fuerza iónica fue
descrito inicialmente en 1964 por Hughes-Jones y col. y
Elliot y col., pero en ese tiempo su uso era limitado ya
que la concentración molar obtenida provocaba la hemólisis
de los eritrocitos suspendidos.
En 1974, Low y Messeter describieron el uso rutinario de la
solución Liss de 0,03 M que lograba reducir el tiempo de
incubación y no presentaba tendencia a la hemólisis al ser
suspendidos en salina a baja fuerza iónica, restableciendo
la presión osmótica de la solución mediante la adición de
glicina.
Las soluciones de baja fuerza iónica son actualmente las
más utilizadas en inmunohematología, provocando un aumento
en la velocidad de asociación entre antígenos y anticuerpos
permitiendo así acortar el tiempo de incubación de 60
minutos a 10-15 minutos, sin sacrificar la sensibilidad de
las mismas y sin costos elevados.Se ha observado que las
reacciones antígeno-anticuerpo se ven potenciadas al
reducir la fuerza iónica del medio de reacción.
La fuerza iónica es uno de los factores más importantes que
determinan la tasa y la cantidad de captación de
anticuerpos por parte de los eritrocitos. El uso de medios
de reacción de baja fuerza iónica permite disminuir el
tiempo de incubación y potenciar las reacciones de los
anticuerpos sin incrementar las reacciones inespecíficas.
Los iones Na+ y Cl-, presentes en la solución salina
fisiológica, se agrupan alrededor de las moléculas de
antígeno y anticuerpo neutralizando sus cargas opuestas, lo
cual dificulta la unión entre ellos. Este efecto se reduce
utilizando soluciones de baja fuerza iónica y disminuyendo
de esta manera la incubación de las pruebas.
OBTENIDO DE: www.quimicaclinicauv.blogspot.com 25
En esta etapa de sensibilización, las posibilidades de
asociación pueden incrementarse mediante agitación,
centrifugación y/o variación de la concentración del
anticuerpo.
Después de que el anticuerpo se ha fijado al antígeno, los
eritrocitos sensibilizados deben unirse para dar lugar a la
aglutinación visible; esta red también solidifica y
estabiliza la reacción.
En esta etapa la reacción depende de factores como las
características del anticuerpo, localización en la membrana
y número de sitios antigénicos, fuerzas que mantienen la
distancia entre los eritrocitos.
Las características del anticuerpo que deben considerarse
son el tamaño del anticuerpo involucrado y el número de
sitios de combinación con el antígeno. Los anticuerpos IgM
pueden establecer puentes entre los eritrocitos y
aglutinarlos espontáneamente en solución salina, mientras
que los IgG no, ya que las IgM, pentaméricas poseen 10
sitios de combinación con el antígeno y las IgG dímeros
sólo dos sitios.
Los eritrocitos tienen una carga neta negativa en su
superficie, su interacción con los iones del medio altera
esta carga y producen una carga neta crítica denominada
potencial zeta, y la reducción de dicha carga permite que
los eritrocitos se aproximen lo suficiente para que sean
aglutinados por medio de los IgG que los sensibilizaron.
Las soluciones de baja fuerza ionica empleadas en banco de
sangre tienen un pH entre 6.5 – 7.0, se recomienda una
osmolalidad de 270 – 305 mosm/kg y una conductividad de 3.7
mm/cm. El control diario implica el examen de su apariencia
física: ausencia de turbidez, particulas o sedimento, así
como, corroborar la capacidad para generar hemólisis,
crenacion o prueba de coombs positiva en eritrocitos
normales. Cada lote nuevo se valora mediante el rastreo de
un anticuerpo ya sea un anti- D, un anti- jk, anti- fy o
anti- kell diluido; se compara su capacidad de detección
contra un medio salino normal incubando 10min a 37ºC, en
LISS debe poder rastrearse un anticuerpo, en tanto que en
medio salino no.
MATERIAL Y EQUIPO:
Material Cantidad
10 Tubos de ensayo de 12 x 75
1 Gradilla
10 Pipetas pasteur
OBTENIDO DE: www.quimicaclinicauv.blogspot.com 26
1 Bulbo
1 Marcador
1 Microcentrífuga
1 Baño María
MATERIAL BIOLOGICO:
Glóbulos rojos lavados al 3 - 5%
Suero
REACTIVOS:
Reactivo de LISS
Reactivo de Coombs
TECNICA:
1.- Lavar los eritrocitos:
Separar el suero del paquete de glóbulos rojos.
Agregar cierta cantidad de eritrocitos a un tubo de
ensayo y agregarle solución salina
Centrifugar y decantar
Repetir este proceso 3 veces
2.- Realizar la Prueba de LISS:
Enumerar los tubos
Poner dos gotas de LISS en cada tubo, agregar una gota
de eritrocitos lavados y al 3 - 5%, según el número de
tubo correspondiente,
Mezclar y centrifugar un minuto, decantar el
sobrenadante y con la ayuda de una gasa limpiar el
exceso del reactivo.
Poner nuevamente 2 gota de LISS, resuspender por
agitación, agregar 2 gotas de suero problema, mezclar,
incubar 15 minutos a 37º C. centrifugar 30 seg. A 1000
R.P.M.
Anotar los resultados.
3.- A las pruebas negativas realizar Coombs:
Lavar 3 veces las células, agregar suero de Coombs,
centrifugar 30 seg.
Leer aglutinaciones y anotar resultados.
REACTIVOS UTILIZADOS:
REACTIVO MARCA FECHA DE ASPECTO COLOR LOTE
CADUCIDAD
Suero Lafon 31/ 01/ Transparente Verde 406
OBTENIDO DE: www.quimicaclinicauv.blogspot.com 27
Antiglobuina 2009
humana
LISS Casero 1 año Transparente Transp
realiza arente
do en ------
CMN ----
SIGLO
XXI
PACIENTE: ASCANIO MENDEZ JOSUE O (+)
DONADOR 1: GARCIA CARBAJAL OSCAR O (+)
DONADOR 2: GARCIA SUAREZ ORLANDO A (+)
RESULTADOS:
Tubo Resultado
M1 NEGATIVO
m1 NEGATIVO
M2 POSITIVO
M2 NEGATIVO
AUTOTES. NEGATIVO
INTERPRETACIÓN DE LOS RESULTADOS
La hemólisis o la aglutinación representan un resultado positivo e indican la
presencia de una reacción antígeno-anticuerpo. Los resultados negativos no se
vera aglutinación o hemolisis.
ESQUEMAS:
CONCLUSIONES:
Concluyo que la prueba de compatibilidad sanguínea en su modalidad con
liss ofrece mucha ventaja al ser, al igual que otros reactivos, un
potencializador de la reacción antígeno-anticuerpo. Esto permite que
el operador o realizador de la prueba tenga mayor confianza y certeza
en los resultados que obtenga.
OBTENIDO DE: www.quimicaclinicauv.blogspot.com 28
PRACTICA 9
INMUNOHEMATOLOGIA
DETERMINACION DE COOMBS DIRECTO
INTRODUCCION:
PRUEBA DE COOMBS DIRECTA
El examen de Coombs directo se utiliza para detectar autoanticuerpos contra
los propios glóbulos rojos (GR) de un individuo. Es una prueba que sirve para
demostrar el revestimiento de los eritrocitos in vivo, (mientras los eritrocitos
están circulando en el individuo). La prueba se realiza agregando directamente
el reactivo de Coombs a los eritrocitos, previamente lavados para eliminar
otras proteínas no fijadas a el; una prueba directa positiva significa que la
relación antígeno-anticuerpo ocurrió in vivo, es decir que la fijación del
anticuerpo sobre el antígeno se realizo en el organismo del individuo en
estudio.
Las indicaciones principales de esta prueba son: diagnostico de enfermedades
hemolíticas, ictericia o anomalías en la apariencia de los glóbulos rojos bajo el
microscopio, ya que estos anticuerpos algunas veces destruyen los glóbulos
rojos y causan anemia; para investigar reacciones en transfusiones. Para
investigar la inducción de drogas en células rojas sensibilizadas, medicamentos
(por ejemplo, quinidina, metildopa, procainamida y otros) que pueden llevar a la
producción de estos anticuerpos.
OBJETIVO: Determinar la presencia de anticuerpos en la superficie de los
glóbulos rojos del individuo.
MATERIAL
10 Tubos de 12/75
10 Pipetas Pasteur
1
Gradilla.
1
Bulbo.
P
apel Parafilm.
M
icrocentrífuga.
B
año María a 37°C.
MUESTRA BIOLOGICA:
Eritrocitos lavados de (3-5%) del donador o paciente.
REACTIVO:
Suero de Coombs*
OBTENIDO DE: www.quimicaclinicauv.blogspot.com 29
*Suero anti-globulina humana Lafon. Lote 406 Cad: 31/01/09. Color: verde. Aspecto: transparente.
TECNICA:
Colocar en un tubo de ensaye dos gotas de suero de Coombs mas una gota de
globulos rojos (3-5%).
Centrifugar a 1000 rpm durante 20 seg.
Desprender el boton suavemente y buscar la presencia de aglutinacion.
Rotular y enumerar 8 tubos de ensayes con las diferentes diluciones
(½,¼,1/8...)
Enumerar 8 tubos mas del 1 al 8.
Agregar a cada tubo de las diluciones 10 gotas de solucion salina mas 10 gotas
de suero de Coombs.
Colocar Al primer tubo de la dilucion 1 gota de globulos rojos (3-5%), mezclar
completamente y agregar al tubo #1
Centrifugar todos los tubos a 1000 rpm durante 20 seg.
LECTURA:
Aglutina.- Prueba de Coombs directa es positiva.
No aglutina.- Prueba de Coombs directa es negativa.
ESQUEMAS y RESULTADOS:
DILUCIONES
½ positiva
¼ positiva
1/8 positiva
1/16 negativa
1/32 negativa
1/64 negativa
1/128 negativa
1/256 negativa
CONCLUCION:
He concluido que la prueba de Coombs directa es una prueba que se utiliza para medir
la presencia de anticuerpos en la superficie de los glóbulos rojos que se encuentran
circulando en el paciente y se realiza para investigar reacciones en transfusiones además
sirve para la determinación de anemia hemolítica autoinmune entre otras afecciones.
OBTENIDO DE: www.quimicaclinicauv.blogspot.com 30
Practica 10
IDENTIFICACION DE ANTICUERPOS IRREGULARES
Fundamento:
Los anticuerpos del sistema ABO aparecen una vez que el
individuo entra en contacto con el medio ambiente y en el
cual se encuentran microorganismos como algunas bacterias
coliformes que contienen sustancias químicas en su
estructura parecidas a las de este sistema. Por anticuerpos
regulares debemos identificar a los que existen en todos
los individuos y que éstos tendrán durante toda su vida.
Los anticuerpos irregulares son los que no están de esa
manera, aunque en el caso de los naturales no se conoce a
ciencia cierta qué o cómo se induce su producción. Los
adquiridos se conocen también como inmunes y son el
resultado de la exposición a antígenos desconocidos por el
individuo al momento de la transfusión o en las mujeres
por el embarazo; estos anticuerpos son dirigidos contra
antígenos de sistemas diferentes al ABO.
Los anticuerpos naturales regulares son preferentemente
inmunoglobulinas M, las cuales fijan de manera tan
eficiente el complemento que pueden provocar lisis
intravascular y ocasionar insuficiencia renal o incluso la
muerte del paciente. Los anticuerpos adquiridos o inmunes
son generalmente inmunoglobulinas G, las cuales producen
hemólisis extravascular en el bazo o en el hígado mediante
fagocitosis del complejo eritrocito más anticuerpo.
Los aloanticuerpos irregulares (adquiridos) más comunes en
nuestra población son los que involucran a los sistemas
MNSs, P1, Kidd (Jka, Jkb), Duffy (Fya, Fyb), Kell, Lewis y
Diego.
OBJETIVO: identificación del anticuerpo irregular a través
de las diferentes técnicas.
MATERIAL EQUIPO
10 Tubos de ensaye. 1. Microcentrífuga.
2. Baño María ó Estufa.
10 Pipetas Pasteur.
1Gradilla.
1 Bulbo.
Papel Parafim.
MATERIAL BIOLOGICO:
Glóbulos rojos lavados al 3 - 5%
Suero
OBTENIDO DE: www.quimicaclinicauv.blogspot.com 31
REACTIVOS
Reactivos:
1. Suero de Coombs*
2. Albúmina bovina
3. SOLUCION SALINA
4. SOLUCION DE LISS
TÉCNICA SOLUCION SALINA
Lavar los eritrocitos con solución salina (3
veces).
SALINA RÁPIDA:
Agregar una gota de Eritrocitos Lavados.
Diluírlo al 3-5% con solución salina 0.9%.
Agregar 2 gotas de suero.
Centrifugar y observar, anotar desprendimiento
del botón.
SALINA 37° BAÑO MARÍA:
1) Incubar tubos a Baño maría a 37°C durante 1
hora (o 20 min).
2) Centirfugar después de haber pasado el
tiempo.
3) Desprender el botón de eritrocitos y
observar.
AGLUTINACIÓN– No es compatible.
NO AGLUTINACIÓN - Lavar 3 veces.
SALINA COOMBS:
1) Con solución salina 0.9% lavar los
eritrocitos de los tubos q no tuvieron
aglutinación 3 veces.
2) Decantar y agregar 2 gotas de reactivo
de Coombs
AGLUTINACIÓN – No es compatible.
NO AGLUTINACIÓN - Lavar 3 veces.
TECNICA LISS
1. Poner dos gotas de LISS en cada tubo, agregar una gota
de eritrocitos lavados y al 3 - 5%, según el número de
tubo correspondiente,
2. Mezclar y centrifugar un minuto, decantar el
sobrenadante y con la ayuda de una gasa limpiar el
exceso del reactivo.
3. Poner nuevamente 2 gota de LISS, resuspender por
agitación, agregar 2 gotas de suero problema, mezclar,
incubar 15 minutos a 37º C. centrifugar 30 seg. A 1000
R.P.M.
4. Anotar los resultados.
A las pruebas negativas realizar Coombs:
OBTENIDO DE: www.quimicaclinicauv.blogspot.com 32
1. Lavar 3 veces las células, agregar suero de Coombs,
centrifugar 30 seg.
2. Leer aglutinaciones y anotar resultados.
TECNICA ALBUMINA BOVINA
8. Agregar 2 gotas de albúmina al 22%.
9. Centrifugar 20 segundos.
10. o
bservar aglutinación o hemolisis, o no aglutinación.
11. A
los tubos con lecturas negativas, incubar 20 minutos
en baño María a 37 °C.
12. C
entrifugar y observar:
Aglutinación o hemólisis: reportar incompatible.
No aglutinación: llevar a Coombs.
13. L
avar tres veces, decantar, y quitar el exceso de
salina con gasa y agregar 2 gotas de reactivo de
Coombs y centrifugar 20 segundos y observar:
Aglutinación o hemólisis: reportar incompatible.
No aglutinación: reportar compatible.
Resultados
ANTICUERPO IRREGULAR: Anticuerpo c.
Interpretación
Estos anticuerpos son generalmente inmunoglobulinas tipo M
y ocasionalmente tipo G, y debido a esa temperatura de
reacción carecen de importancia clínica salvo que su
reacción ocurra también a 37 °C, su importancia radica en
pacientes que serán intervenido a 22 ºc como es el caso de
operación de corazón.
Los llamados anticuerpos calientes tienen una temperatura óptima de
reacción a 37 °C, a Estos anticuerpos tienen una relevante
importancia clínica ya que se les asocia con reacciones
transfusionales de intensidad moderada a severa, que pueden
ocasionar la muerte.
Esquemas:
CONCLUSION:
OBTENIDO DE: www.quimicaclinicauv.blogspot.com 33
He concluido que es importante determinar los anticuerpos
irregulares ya que estos anticuerpos tienen una relevante
importancia clínica ya que se les asocia con reacciones
transfusionales de intensidad moderada a severa.
OBTENIDO DE: www.quimicaclinicauv.blogspot.com 34
También podría gustarte
- Manual Completo de InmunohematologiaDocumento34 páginasManual Completo de Inmunohematologiamiguel angel98% (95)
- Manual Completo de InmunohematologiaDocumento54 páginasManual Completo de InmunohematologiaYurith PadillaAún no hay calificaciones
- Prct. GRUPO SANG. para Banco de SangreDocumento5 páginasPrct. GRUPO SANG. para Banco de SangreOrtiz GrettelAún no hay calificaciones
- Manual Completo de InmunohematologiaDocumento33 páginasManual Completo de InmunohematologiaGreeceGreeCeAún no hay calificaciones
- Básico de Banco de Sangre. Guaditoca Chaves AguiónDocumento26 páginasBásico de Banco de Sangre. Guaditoca Chaves Aguiónguaditoca chaves aguión100% (1)
- Trabajo SuperDocumento6 páginasTrabajo SuperAbel Condori GarciaAún no hay calificaciones
- Laboratorio de Inmunología GeneralDocumento10 páginasLaboratorio de Inmunología GeneralRoman EsquivelAún no hay calificaciones
- Guia Banco de Sangre VirginioDocumento22 páginasGuia Banco de Sangre VirginioCamila MedinaAún no hay calificaciones
- Banco de Sangre Tipo SanguineoDocumento35 páginasBanco de Sangre Tipo SanguineoCarlos Roberto Flores CruzAún no hay calificaciones
- GUIA #6 REACCION Ag-Ac NUEVA VERSIONDocumento5 páginasGUIA #6 REACCION Ag-Ac NUEVA VERSIONAura RamirezAún no hay calificaciones
- Agentes Transmisibles Infecciosos Por Transfusion SanguineaDocumento14 páginasAgentes Transmisibles Infecciosos Por Transfusion SanguineagalmichehernandezdulcemarielAún no hay calificaciones
- Eq - No.4 & 11 OctDocumento12 páginasEq - No.4 & 11 Octcinthya cristell castellanos hernandezAún no hay calificaciones
- Práctica 5 InmunoaglutinaciónDocumento5 páginasPráctica 5 InmunoaglutinaciónJeniffert CutipaAún no hay calificaciones
- Reportes Practica BsDocumento8 páginasReportes Practica Bsdracumara234Aún no hay calificaciones
- Práctica 1 InmunologíaDocumento11 páginasPráctica 1 InmunologíaAlex VillarrealAún no hay calificaciones
- INFORME #9 Grupo y Factor SanguineoDocumento5 páginasINFORME #9 Grupo y Factor SanguineoDAMARIS BALTAZAR FLORESAún no hay calificaciones
- Funciones Banco SangreDocumento36 páginasFunciones Banco SangreBrenda VenancioAún no hay calificaciones
- LAB INMUNOLOGIA 2019Documento6 páginasLAB INMUNOLOGIA 2019Juan Fernando Ocampo GarciaAún no hay calificaciones
- Guia Practica 8 AglutinacionDocumento5 páginasGuia Practica 8 AglutinacionKevin Andre Cusi CahuataAún no hay calificaciones
- Reacciones de Hemaglutinación Directa e IndirectaDocumento8 páginasReacciones de Hemaglutinación Directa e IndirectaLivia Nina100% (1)
- Determinación de Grupos Sanguíneos Y Factor RHDocumento3 páginasDeterminación de Grupos Sanguíneos Y Factor RHHugo Hernandez CruzAún no hay calificaciones
- Determinación de Grupos Sanguíneos Y Factor RHDocumento3 páginasDeterminación de Grupos Sanguíneos Y Factor RHHugo Hernandez CruzAún no hay calificaciones
- Practica de Banco de Sangre 6aDocumento10 páginasPractica de Banco de Sangre 6avicenteledezma2020Aún no hay calificaciones
- Informe 1Documento8 páginasInforme 1Maximiliano AguaguiñaAún no hay calificaciones
- Determinación de grupos sanguíneos ABO y Rh mediante aglutinación (40Documento17 páginasDeterminación de grupos sanguíneos ABO y Rh mediante aglutinación (40Deyvi VillanuevaAún no hay calificaciones
- GUIA #6 REACCION Ag-AcDocumento5 páginasGUIA #6 REACCION Ag-AcKatia MartínezAún no hay calificaciones
- Práctica 3. - Tipificación Sanguíneo Formato 22Documento6 páginasPráctica 3. - Tipificación Sanguíneo Formato 22Gabriel Alexander TaimalAún no hay calificaciones
- Grupos sanguíneos ABO y antígenos en salivaDocumento6 páginasGrupos sanguíneos ABO y antígenos en salivaJosé Francisco Valenzuela SánchezAún no hay calificaciones
- Pruebas de CompatibilidadDocumento16 páginasPruebas de CompatibilidadDanitxa CifuenTes PadillaAún no hay calificaciones
- Determinacion Del Grupo Sanguíneo y Factor RHDocumento30 páginasDeterminacion Del Grupo Sanguíneo y Factor RHAnonymous 8z9XAvAún no hay calificaciones
- Grupos sanguíneos y factor Rh (40/40Documento11 páginasGrupos sanguíneos y factor Rh (40/40José Alejandro LEAún no hay calificaciones
- Vázquez_Alejandra_P8Documento8 páginasVázquez_Alejandra_P8aaleev1924234Aún no hay calificaciones
- Grupo y FactorDocumento4 páginasGrupo y FactorEdgard CubasAún no hay calificaciones
- Informe de Practica Fisiologia I #3Documento16 páginasInforme de Practica Fisiologia I #3Cesar Del Aguila MattaAún no hay calificaciones
- Determinación grupos sanguíneos (hemoclasificaciónDocumento21 páginasDeterminación grupos sanguíneos (hemoclasificaciónjoheinys redondoAún no hay calificaciones
- Practica 8 Prueba Inversa2Documento11 páginasPractica 8 Prueba Inversa2Valeria Guerrero50% (2)
- Determiancion de Grupo SanguineoDocumento9 páginasDetermiancion de Grupo SanguineoK'anchaq RamArAún no hay calificaciones
- Tecnicas para Bancos de SangreDocumento25 páginasTecnicas para Bancos de SangreJhon Leyva100% (2)
- Reacciones de aglutinacioìn17XI20Documento12 páginasReacciones de aglutinacioìn17XI20Karen DiazAún no hay calificaciones
- AglutinacionDocumento11 páginasAglutinacionFaNi Saucedo C100% (1)
- Fecha: 18/09/2019 Titulo Objetivo: Practica 2.determinación Del Grupo ABODocumento5 páginasFecha: 18/09/2019 Titulo Objetivo: Practica 2.determinación Del Grupo ABOana hervellaAún no hay calificaciones
- Practica de Laboratorio Nº3Documento12 páginasPractica de Laboratorio Nº3sindy tapiasAún no hay calificaciones
- Semana 6 PracticaDocumento14 páginasSemana 6 PracticaLeonardo Marrufo100% (1)
- Determinación Del Grupo SanguineoDocumento5 páginasDeterminación Del Grupo SanguineoVALERY RUBY RODRIGUEZ FRONTANILLAAún no hay calificaciones
- Practica 4 Grupo Sanguineo y Prueba de Compatibilidad Cruzada MayorDocumento8 páginasPractica 4 Grupo Sanguineo y Prueba de Compatibilidad Cruzada MayorMishiel Nicole Gomez CentellasAún no hay calificaciones
- Poe de HematologiaDocumento4 páginasPoe de HematologiaÁlvaro José Villamizar JimenezAún no hay calificaciones
- PRACTICA No 1 Grupos SanguineosDocumento6 páginasPRACTICA No 1 Grupos SanguineosmariceladiazbeltranAún no hay calificaciones
- P4 Grupo Sanguíneo y Pruebas de Compatibilidad 2017Documento5 páginasP4 Grupo Sanguíneo y Pruebas de Compatibilidad 2017Juan Carlos CazaresAún no hay calificaciones
- Protocolo para Pruebas de Compatibilidad PDFDocumento4 páginasProtocolo para Pruebas de Compatibilidad PDFCarolina García GutiérrezAún no hay calificaciones
- Practica 3 Tipificacion SanguineaDocumento6 páginasPractica 3 Tipificacion SanguineaANGELO MOISES ABAD MACIASAún no hay calificaciones
- Detección y Titulación de IsohemaglutininasDocumento6 páginasDetección y Titulación de IsohemaglutininasALEXANDRA ANTONIETA URRUTIA ZEGARRAAún no hay calificaciones
- GuíaBurros Análisis clínicos: Todo lo que necesitas saber para entender tus análisisDe EverandGuíaBurros Análisis clínicos: Todo lo que necesitas saber para entender tus análisisCalificación: 4 de 5 estrellas4/5 (9)
- Interpretación Rápida De La Gasometría Arterial: Gasometría Arterial En 4 PasosDe EverandInterpretación Rápida De La Gasometría Arterial: Gasometría Arterial En 4 PasosAún no hay calificaciones
- Fundamentos y técnicas básicas en biología molecularDe EverandFundamentos y técnicas básicas en biología molecularAún no hay calificaciones
- Guía práctica para técnico superior de laboratorio de diagnóstico clínico y biomédicoDe EverandGuía práctica para técnico superior de laboratorio de diagnóstico clínico y biomédicoCalificación: 4.5 de 5 estrellas4.5/5 (10)
- Manual práctico de ensayos de toxicidad en medio acuático con organismos del género DaphniaDe EverandManual práctico de ensayos de toxicidad en medio acuático con organismos del género DaphniaCalificación: 1 de 5 estrellas1/5 (1)
- GUÍA DE TINCIONES MICROBIOLOGÍCAS: HERRAMIENTAS PARA EL ÉXITO EN El LABORATORIODe EverandGUÍA DE TINCIONES MICROBIOLOGÍCAS: HERRAMIENTAS PARA EL ÉXITO EN El LABORATORIOAún no hay calificaciones
- Introducción a la antropología biológica: Origen, variabilidad y adaptación de las poblaciones humanasDe EverandIntroducción a la antropología biológica: Origen, variabilidad y adaptación de las poblaciones humanasAún no hay calificaciones
- Ideas Fundamentales - Segunda Edicion PDFDocumento305 páginasIdeas Fundamentales - Segunda Edicion PDFFrancisco Guevara100% (1)
- Aprende BillingsDocumento10 páginasAprende BillingsSiri SoriaAún no hay calificaciones
- Diapositivas Medicina Forense Arma BlancaDocumento22 páginasDiapositivas Medicina Forense Arma BlancaANGEL HUMBERTO ZELAYA OLIVERAAún no hay calificaciones
- 06 Sanchez e 101 112Documento12 páginas06 Sanchez e 101 112Ivan ArangoAún no hay calificaciones
- De La Dictadura A La Democracia V - 2 PDFDocumento288 páginasDe La Dictadura A La Democracia V - 2 PDFOscar CastroAún no hay calificaciones
- Adenovirus Antigeno Fecal ElisaDocumento2 páginasAdenovirus Antigeno Fecal ElisaMathias Serpa ArceAún no hay calificaciones
- Etiopatogenia de Las NeoplasiasDocumento79 páginasEtiopatogenia de Las NeoplasiasCristopherJairEstupiñanVirúAún no hay calificaciones
- Punto 11 de Acuerdo Con Los Niveles de Exposición A Los Riesgos Físicos y QuímicosDocumento6 páginasPunto 11 de Acuerdo Con Los Niveles de Exposición A Los Riesgos Físicos y QuímicosANGIE DANIELA AMADOR RIVERAAún no hay calificaciones
- Sesion Educativa Enfermedades No TransmisiblesDocumento9 páginasSesion Educativa Enfermedades No TransmisiblesMaría Milagros Piscoya Chapoñán100% (1)
- Cuartilla de Psiquiatria de EnlaceDocumento3 páginasCuartilla de Psiquiatria de EnlaceADRIAN JOSE AGUILAR CAMARGOAún no hay calificaciones
- Seminario de Casos Farmacologia en OdontopediatriaDocumento51 páginasSeminario de Casos Farmacologia en OdontopediatriaDra. Iray mbAún no hay calificaciones
- Virus y EnfermedadesDocumento24 páginasVirus y EnfermedadesMartha lucia García CifuentesAún no hay calificaciones
- Diagnóstico y opciones de tratamiento para la ureterolitiasis felinaDocumento2 páginasDiagnóstico y opciones de tratamiento para la ureterolitiasis felinaMelissa AyalaAún no hay calificaciones
- Esavi VacunasDocumento32 páginasEsavi Vacunasfish goldenAún no hay calificaciones
- Taller Oftalmoscopia Directa para Futuros PediatrasDocumento45 páginasTaller Oftalmoscopia Directa para Futuros PediatrasArgenis Bautista SánchezAún no hay calificaciones
- Ejemplo de Una NOTA DE PRENSADocumento1 páginaEjemplo de Una NOTA DE PRENSAreidickAún no hay calificaciones
- Triptico Que Es La TBC EspañolDocumento2 páginasTriptico Que Es La TBC EspañolYorkanys Cb100% (1)
- Examen Final RalcDocumento9 páginasExamen Final RalcLorena CastroAún no hay calificaciones
- Evaluar TDAH escuela familiaDocumento3 páginasEvaluar TDAH escuela familiaDaniela Carolina Feljoo JorgeAún no hay calificaciones
- Protocolo de Prevención y Tratamiento COVID 19 (Dudoso)Documento43 páginasProtocolo de Prevención y Tratamiento COVID 19 (Dudoso)Philippus Von Hohenheim100% (1)
- EpistaxisDocumento11 páginasEpistaxisPedro PedrazaAún no hay calificaciones
- Equilibrio Liq Parte 3Documento8 páginasEquilibrio Liq Parte 3ADRIANA CRESPO MARTÍNEZAún no hay calificaciones
- Quemaduras Art 2.en - EsDocumento12 páginasQuemaduras Art 2.en - EsMaria BolañosAún no hay calificaciones
- Enfermedad de Von GierkeDocumento5 páginasEnfermedad de Von GierkeMauricio Rojo LorcaAún no hay calificaciones
- Dosis PediatricasDocumento8 páginasDosis Pediatricashanzel EcheverriaAún no hay calificaciones
- Guía Clínica de Urticaria Aguda y AngioedemaDocumento14 páginasGuía Clínica de Urticaria Aguda y AngioedemaFedericoAún no hay calificaciones
- Tubo Endotraqueal Adulto - GCL 1.2 - v.4 PDFDocumento21 páginasTubo Endotraqueal Adulto - GCL 1.2 - v.4 PDFmyriamsepulvedaAún no hay calificaciones
- CIE 10 Volumen 3Documento9 páginasCIE 10 Volumen 3Ogallo JerlAún no hay calificaciones
- Publication 05Documento93 páginasPublication 05Milo Fernandez100% (1)
- Pulposis AtróficaDocumento1 páginaPulposis AtróficaBernny Danilo0% (1)
- PRIMEROS AUXILIOS Modulo IIDocumento9 páginasPRIMEROS AUXILIOS Modulo IIAlan TisnadoAún no hay calificaciones
- Dra Gladis Trombotto - Estudio Epidemiol Gico de Las Malformaciones Cong NitasDocumento6 páginasDra Gladis Trombotto - Estudio Epidemiol Gico de Las Malformaciones Cong NitasAnonymous QzMpdciOAAún no hay calificaciones
- Informe Fenilcetonuria Albarran TorresDocumento10 páginasInforme Fenilcetonuria Albarran Torreschat gptAún no hay calificaciones
- El SidaDocumento3 páginasEl SidaJonathan CaselliAún no hay calificaciones
- Enfermedad de Membrana HialinaDocumento11 páginasEnfermedad de Membrana HialinaBoris Hernandez AlejoAún no hay calificaciones