Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Cuestionario Previo Propiedades Coligativas P6 ARH PDF
Cargado por
Abraham Rodriguez HernandezTítulo original
Derechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
Cuestionario Previo Propiedades Coligativas P6 ARH PDF
Cargado por
Abraham Rodriguez HernandezCopyright:
Formatos disponibles
Grupo: 22
Abraham Rodríguez Hernández
Previo práctica propiedades coligativas
Fecha de entrega: 24 de noviembre del 2020
Cuestionario Previo:
1. Investigar los conceptos de soluto, disolvente y disolución.
Soluto: Se llama soluto a la sustancia minoritaria en una disolución, esta sustancia se
encuentra disuelta en un determinado disolvente. También se le conoce como la
sustancia que se disuelve, por lo que se puede encontrar en un estado de agregación
diferente al comienzo del proceso de disolución.
Disolvente: Es una sustancia liquida que se disuelve o disocia a otra sustancia en una
forma más elemental, y que normalmente está presente en mayor cantidad que esa
otra sustancia.
Disolución: Es la mezcla homogénea resultante tras disolver cualquier sustancia en un
líquido.
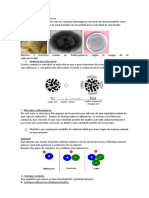
2. Explicar que es una disolución ideal de noelectrolito.
Una disolución ideal es aquella que obedece la Ley de Raoult, la cual establece que
la presión de vapor del disolvente es igual a la presión de vapor del disolvente puro
multiplicada por la fracción mol del disolvente. La presión parcial de un disolvente
sobre una disolución P1 está dada por la presión de vapor del disolvente puro P°1,
multiplicada por la fracción molar del disolvente en la disolución X1.
P1= X1P°1
Es decir que la presión de vapor del soluto crece linealmente con su fracción molar. En
una solución que solo contenga un soluto, se tiene que X1= 1-X2 , donde X2 es la
fracción molar del soluto, pudiendo escribir la formulación de la ley como:
P1= (1-X2)P°1
P°1 – P1 = ∆P =X2P°1
Se puede ver de esta forma que una disminución en la presión de vapor,
∆P es directamente proporcional a la concentración del soluto presente. Una
disolución de no electrolitos es aquella que no conduce la electricidad, ya que no
genera iones.
3. Definir el término molalidad e indicar que unidades tiene.
La molalidad (m) es el numero de moles de soluto disueltos en 1kg (1000
g) de un disolvente.
moles de soluto
molalidad = masa de disolvente(kg)
Por lo tanto, las unidades de la molalidad son: mol/kg
4. ¿De qué factores dependen las propiedades coligativas de disoluciones de no
electrolitos?
Dependen de la concentración total de partículas de soluto, sin importar si las
partículas son iones o moléculas.
5. Explicar que es una curva de enfriamiento y cuál es su utilidad.
Son una representación gráfica de la temperatura de un material frente al tiempo
conforme este se enfría.
Por ejemplo: Cuando se elimina calor de una masa de agua a velocidad
constante, su temperatura desciende hasta alcanzar los 0°C, momento en que
empieza a separarse el hielo. La temperatura permanece constante hasta que
toda el agua es transformada en hielo por que el calor elimina de la masa del
agua formada de calor latente de cambio de estado, Después de la formación
total de hielo, la temperatura desciende de nuevo. La presencia de solutos
disueltos cambia la curva de enfriamiento del agua como consecuencia del
descenso crioscópico.
6. Investigar qué diferencia existe entre las propiedades coligativas de
disoluciones de no electrolitos y de electrolitos.
No Electrolitos: Se caracterizan por que sus disoluciones conducen la electricidad.
Se disuelven como moléculas neutras que no pueden moverse en presencia de un
campo eléctrico. (Metanol)
Electrolitos: Las disoluciones acuosas de estas sustancias conducen la electricidad,
En disolución estos solutos se disocian en iones. (NaCl)
Los solutos no electrolitos en general son poco solubles, a excepción de los que
pueden formar puentes de hidrógeno (metanol, glucosa, FH, NH3). Por su lado los
electrolitos son muy solubles debido a las atracciones ión-dipolo.
En la solubilidad influyen la presión y la temperatura. En general, la solubilidad de
un sólido en un líquido aumenta con la temperatura. Esto se puede explicar
recurriendo a factores entrópicos.
∆G = ∆H - T∆S
Un equilibrio dinámico tiende a oponerse a cualquier cambio en sus condiciones. Si
el proceso de la disolución es endotérmico, en este caso ∆H >0 , entonces un
aumento de la temperatura implicará un aumento de la solubilidad. La mayoría de
las
disoluciones de un sólido en un líquido son endotérmicas, porque es necesario
romper la energía de red del sólido para que este se disuelva.
Si el proceso es exotérmico entonces ∆H <0, y aumento de la temperatura
conllevará una disminución de la solubilidad. La mayoría de las disoluciones de
gases en líquidos son exotérmicas. En general un aumento de la presión implica
una mayor solubilidad de un gas en un líquido. La Ley de Henry nos dice que la
solubilidad es directamente proporcional a la presión parcial.
p =(K )(c)
7. Definir el factor de van´t Hof
Una medida del grado en que los electrolitos se disocian es el factor de Van´t Hof.
Este factor es la relación entre el valor real de una propiedad coligativa y el valor
calculado (considerando que la sustancia es un no electrolito).
El valor ideal de factor Van´t Hof para una sal puede calcularse observando la
fórmula del compuesto.
Al factor ideal de Van´t Hof se le simboliza por la letra v(nu), debemos
considerar este factor como un valor limitante, es decir, el factor Van´t Hof para el
NaCl tiene como máximo valor v=2.
8. Rellena la tabla 1
m(mol/kg) Gramos de Gramos de Gramos de Gramos de
urea dextrosa NaCl CaCl2
0.15 0.45 1.35 0.43 0.73
0.30 0.90 2.70 0.87 1.66
0.45 1.35 4.05 1.31 2.49
0.60 1.80 5.40 1.75 3.32
Bibliografía:
Cristóbal Valenzuela Calahorro, 1995, Química General:
Introducción a la química teórica, 2da edición,pp.25
Raymod Chang, 2010, Química, Ed. Mc Graw Hill. 5ta edición, pp.514
También podría gustarte
- Cuestionario Previo Propiedades Coligativas P6 ARHDocumento5 páginasCuestionario Previo Propiedades Coligativas P6 ARHAbraham Rodriguez HernandezAún no hay calificaciones
- Rio Previo No.4Documento3 páginasRio Previo No.4emiliogankaku67% (3)
- Investigar Los Conceptos de SolutoDocumento2 páginasInvestigar Los Conceptos de Solutonayelii TrejoAún no hay calificaciones
- Solís Steve - GR4 - Propiedades ColigativasDocumento7 páginasSolís Steve - GR4 - Propiedades ColigativasSteve SolisAún no hay calificaciones
- Propiedades ColigativasDocumento6 páginasPropiedades ColigativasKarla VillegasAún no hay calificaciones
- Propiedades Coligativas de Las Soluciones.Documento6 páginasPropiedades Coligativas de Las Soluciones.fernandoAún no hay calificaciones
- Práctica 6 Propiedades Coligativas. Soluciones de Noe y Electrolitos Cuestionario PrevioDocumento9 páginasPráctica 6 Propiedades Coligativas. Soluciones de Noe y Electrolitos Cuestionario PrevioKazuyaUedaTatsuyaAún no hay calificaciones
- ElectroquímicaDocumento4 páginasElectroquímicaFlores Aranda Aracely MarianaAún no hay calificaciones
- 3 - ColigativasDocumento6 páginas3 - Coligativasdarkwolf1003Aún no hay calificaciones
- Previo PROPIEDADES COLIGATIVASDocumento6 páginasPrevio PROPIEDADES COLIGATIVASIván Gerardo López VenturaAún no hay calificaciones
- Propiedades ColigativasDocumento11 páginasPropiedades ColigativasAbath Vlandimir100% (1)
- Aplicaciones de Las Leyes de Roult y Henry y MasDocumento12 páginasAplicaciones de Las Leyes de Roult y Henry y MasJuan Pablo Galindo Beltran100% (1)
- QuimicaDocumento20 páginasQuimicaMaría Pía Lupérdiga CavaAún no hay calificaciones
- Lab. 3 Propiedades ColigativasDocumento16 páginasLab. 3 Propiedades ColigativasMarlon GamarraAún no hay calificaciones
- Cuestionario Previo Practica 6 EycDocumento2 páginasCuestionario Previo Practica 6 EycXIMENA RUIZ LOPEZAún no hay calificaciones
- ColigativasDocumento26 páginasColigativasverushkitaAún no hay calificaciones
- Practica TermoquimicaDocumento9 páginasPractica TermoquimicaDiana MejíaAún no hay calificaciones
- Previo 6 P7 Propiedades ColigativasDocumento7 páginasPrevio 6 P7 Propiedades ColigativasLucia CeballosAún no hay calificaciones
- DisolucionesDocumento22 páginasDisolucionesChristopher Harris100% (1)
- DisolucionesDocumento33 páginasDisolucionesNicolas EHAún no hay calificaciones
- CP5 Propiedades Coligativas de No-Electrolitos (Urea, Dextrosa) PelaezCrucesEdwinDocumento4 páginasCP5 Propiedades Coligativas de No-Electrolitos (Urea, Dextrosa) PelaezCrucesEdwinedwin pelaezAún no hay calificaciones
- 5 - Propiedades de Las DisolucionesDocumento56 páginas5 - Propiedades de Las DisolucionesSantiago PellejeroAún no hay calificaciones
- Ultimo de Quimica Kike.Documento8 páginasUltimo de Quimica Kike.Luis Yoani Berrio CardonaAún no hay calificaciones
- Propiedades Coligativas de Las SolucioneDocumento8 páginasPropiedades Coligativas de Las SolucioneFernando José RiveiroAún no hay calificaciones
- Propiedades Coligativas de Las SolucionesDocumento5 páginasPropiedades Coligativas de Las SolucionesJaner Urango AnayaAún no hay calificaciones
- Actividad Propiedades ColigativasDocumento11 páginasActividad Propiedades ColigativasMemo GranadosAún no hay calificaciones
- Ultimo Taller de Quimica Yoani.Documento10 páginasUltimo Taller de Quimica Yoani.Luis Yoani Berrio CardonaAún no hay calificaciones
- Fundamento TeoricoDocumento6 páginasFundamento TeoricoLUIS JAIME RAMOS POMPAAún no hay calificaciones
- I - SolucionesDocumento31 páginasI - SolucionesCesitar Calcina100% (1)
- Investigación PROPIEDADES COLIGATIVAS Marlin Stefany CaicedoDocumento5 páginasInvestigación PROPIEDADES COLIGATIVAS Marlin Stefany CaicedoMarlyn CaicedoAún no hay calificaciones
- Disoluciones TeoriaDocumento9 páginasDisoluciones TeoriaCamila ContrerasAún no hay calificaciones
- Propiedades ColigativasDocumento2 páginasPropiedades ColigativasEmma Moreno ZavalaAún no hay calificaciones
- Ley de HenryDocumento33 páginasLey de HenryQkriiz ArriolaAún no hay calificaciones
- Propiedades ColigativasDocumento20 páginasPropiedades ColigativasPatricia BusteloAún no hay calificaciones
- Se Llaman Propiedades Coligativas A Aquellas Propiedades de Una Disolución Que Dependen Únicamente de La ConcentraciónDocumento4 páginasSe Llaman Propiedades Coligativas A Aquellas Propiedades de Una Disolución Que Dependen Únicamente de La ConcentraciónRoss Castiliansk MoralskeAún no hay calificaciones
- Quiz 5 QuimicaDocumento8 páginasQuiz 5 QuimicaAldo D'AndreaAún no hay calificaciones
- Propiedades Coligativas Wagner Nicolas Ramirez PaezDocumento3 páginasPropiedades Coligativas Wagner Nicolas Ramirez PaezWagner Nicolas Ramirez PaezAún no hay calificaciones
- Química General e InorgánicaDocumento8 páginasQuímica General e InorgánicaMagicCriticalAún no hay calificaciones
- Tema 1 Propiedades ColigativasDocumento31 páginasTema 1 Propiedades ColigativasLieska LopezAún no hay calificaciones
- Informe de Lectura Capítulo 12Documento4 páginasInforme de Lectura Capítulo 12Raylin Ismael MordanAún no hay calificaciones
- Propiedades ColigativasDocumento29 páginasPropiedades ColigativasjorgeAún no hay calificaciones
- Ley de Henry Ejercicio 3Documento10 páginasLey de Henry Ejercicio 3willignton100% (2)
- Efecto de La Temperatura Sobre Entalpías de ReacciónDocumento13 páginasEfecto de La Temperatura Sobre Entalpías de ReacciónFelipe SotoAún no hay calificaciones
- Unidad 5Documento28 páginasUnidad 5Geozac Gamboa HoyosAún no hay calificaciones
- Taller Corte 3 - QuimicaDocumento8 páginasTaller Corte 3 - QuimicaSantiago MartinezAún no hay calificaciones
- Propiedades Coligativas de Las SolucionesDocumento11 páginasPropiedades Coligativas de Las SolucionesRoberto GonzálezAún no hay calificaciones
- Soluciones ElectroliticasDocumento2 páginasSoluciones ElectroliticasEsliDavidMolerosIngunzaAún no hay calificaciones
- DisolucionesDocumento9 páginasDisolucionesHéctor DomínguezAún no hay calificaciones
- INVESTIGACIÓNDocumento10 páginasINVESTIGACIÓNCamila BravoAún no hay calificaciones
- Informe Practica 10Documento6 páginasInforme Practica 10Nicolás Osorio RamírezAún no hay calificaciones
- Practica 3 Propiedades ColigativasDocumento12 páginasPractica 3 Propiedades ColigativasRocio Carrillo FloresAún no hay calificaciones
- Propiedades ColigativasDocumento10 páginasPropiedades ColigativasIvan ViteAún no hay calificaciones
- Teoría Del Gas Real: La Relación Exacta Para Gases RealesDe EverandTeoría Del Gas Real: La Relación Exacta Para Gases RealesAún no hay calificaciones
- Psicometría. Principios básicos y protocolos experimentales diversosDe EverandPsicometría. Principios básicos y protocolos experimentales diversosAún no hay calificaciones
- Ingeniería química. Soluciones a los problemas del tomo IDe EverandIngeniería química. Soluciones a los problemas del tomo IAún no hay calificaciones
- El ambiente acuoso para el tratamiento de obras polìcromasDe EverandEl ambiente acuoso para el tratamiento de obras polìcromasAún no hay calificaciones
- P6 Propiedades Coligativas PDFDocumento9 páginasP6 Propiedades Coligativas PDFAbraham Rodriguez HernandezAún no hay calificaciones
- Previo #6 Propiedades Coligativas LLDocumento6 páginasPrevio #6 Propiedades Coligativas LLcachorra11860100% (2)
- Síntomas Estrategias FarmacológicasDocumento1 páginaSíntomas Estrategias FarmacológicasAbraham Rodriguez HernandezAún no hay calificaciones
- Crucigrama PsicoDocumento1 páginaCrucigrama PsicoAbraham Rodriguez HernandezAún no hay calificaciones
- Previo Practica 9 Calor CombustionDocumento7 páginasPrevio Practica 9 Calor CombustionAbraham Rodriguez Hernandez100% (1)
- Las Vacas de QuiviquintaDocumento1 páginaLas Vacas de QuiviquintaAbraham Rodriguez HernandezAún no hay calificaciones
- Sexta Declaración de La Selva LacandonaDocumento9 páginasSexta Declaración de La Selva LacandonaAbraham Rodriguez HernandezAún no hay calificaciones
- 1712 Estadistica y Probabilidad UcaDocumento5 páginas1712 Estadistica y Probabilidad UcaAbraham Rodriguez HernandezAún no hay calificaciones
- EVAGLOabr 21Documento2 páginasEVAGLOabr 21Abraham Rodriguez HernandezAún no hay calificaciones
- Trabajo de InvestigaciónDocumento21 páginasTrabajo de InvestigaciónAbraham Rodriguez HernandezAún no hay calificaciones
- Previo 6 Capacidad TérmicaDocumento4 páginasPrevio 6 Capacidad TérmicaAbraham Rodriguez HernandezAún no hay calificaciones
- Formula MinimaDocumento3 páginasFormula MinimaAbraham Rodriguez HernandezAún no hay calificaciones
- Calificaciones Ordinario ADocumento1 páginaCalificaciones Ordinario AAbraham Rodriguez HernandezAún no hay calificaciones
- Lab. 9. Separacion y Espectro Pigmentos VGDocumento5 páginasLab. 9. Separacion y Espectro Pigmentos VGJannCarlosVargasAún no hay calificaciones
- 6Documento3 páginas6KanaAún no hay calificaciones
- Sánchez MiguelDocumento13 páginasSánchez MiguelMiguelSánchezAún no hay calificaciones
- Biosfera y Sus ComponentesDocumento15 páginasBiosfera y Sus ComponentesFranciscoAún no hay calificaciones
- Rep - Lab S01 Esarmiento 2022 02Documento5 páginasRep - Lab S01 Esarmiento 2022 02fainiTraxAún no hay calificaciones
- Termometria y Sensores de TemperaturaDocumento11 páginasTermometria y Sensores de TemperaturaenmaAún no hay calificaciones
- GUIA DE APRENDIZAJE No 1 QUIMICADocumento2 páginasGUIA DE APRENDIZAJE No 1 QUIMICAMilton BuendiaAún no hay calificaciones
- Proyección CartográficaDocumento2 páginasProyección CartográficaGonzalez YeralAún no hay calificaciones
- Paralelo Organica 15Documento15 páginasParalelo Organica 15Raul Leon EspinozaAún no hay calificaciones
- Guia de Completacion y Reacondicionamiento de PozosDocumento11 páginasGuia de Completacion y Reacondicionamiento de PozoscskpettaAún no hay calificaciones
- Ejercicio 3 Proceso 1Documento3 páginasEjercicio 3 Proceso 1Cristhyan Willy Raa TorresAún no hay calificaciones
- Gruas TorreDocumento113 páginasGruas TorreJeiler VelasquezAún no hay calificaciones
- Practica 1 - Destilacion Simple Del AguaDocumento2 páginasPractica 1 - Destilacion Simple Del AguaAntonioAún no hay calificaciones
- Concentracion de MineralesDocumento27 páginasConcentracion de MineralesAnamar NoriegaAún no hay calificaciones
- EXPERIMENTO 49 y 50Documento11 páginasEXPERIMENTO 49 y 50Martinelis JaenAún no hay calificaciones
- Metabolismo de Hidratos de Carbono Parte 1Documento61 páginasMetabolismo de Hidratos de Carbono Parte 1Mundo VacioAún no hay calificaciones
- Ada02 Cetina FarqDocumento1 páginaAda02 Cetina FarqDiana CetinaAún no hay calificaciones
- Ensayo de ModeladoDocumento2 páginasEnsayo de Modeladojuan diego pertuzAún no hay calificaciones
- Documento Sin TítuloDocumento2 páginasDocumento Sin TítuloProyecto Solar TrackerAún no hay calificaciones
- Sismo Yauca Acari 2013Documento23 páginasSismo Yauca Acari 2013Richard W Machaca HAún no hay calificaciones
- La LunaDocumento3 páginasLa LunaPau CentenoAún no hay calificaciones
- PREGUNTAS - Tabla PeriodicaDocumento9 páginasPREGUNTAS - Tabla PeriodicaDanielaHernandezAún no hay calificaciones
- Reconocimiento de Carbono e Hidrogeno-Nº Lab 1Documento11 páginasReconocimiento de Carbono e Hidrogeno-Nº Lab 1YaninaReyes75% (4)
- Clase 3 EAP Enfermeria JOliveraDocumento86 páginasClase 3 EAP Enfermeria JOliveraRonald Freddy Rimac SalcedoAún no hay calificaciones
- Problemas Propuestos QuimicaDocumento4 páginasProblemas Propuestos QuimicaemanuelAún no hay calificaciones
- 9Documento8 páginas9Galac TicosAún no hay calificaciones
- Nitro Bence NoDocumento12 páginasNitro Bence NomishelAún no hay calificaciones
- DIFRACCIONDocumento7 páginasDIFRACCIONjuan esteban pachon henaoAún no hay calificaciones
- Cap 8 Vol Redox Aplicaciones 2015Documento17 páginasCap 8 Vol Redox Aplicaciones 2015RosalynNeciosupRamosAún no hay calificaciones
- Problemas de Química Del Suelo-2019Documento8 páginasProblemas de Química Del Suelo-2019AniAún no hay calificaciones