Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Potenciales Termodinámicos y Criterios de Espontaneidad y Equilibrio
Cargado por
Daniel MeloDescripción original:
Título original
Derechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
Potenciales Termodinámicos y Criterios de Espontaneidad y Equilibrio
Cargado por
Daniel MeloCopyright:
Formatos disponibles
FACULTAD DE QUÍMICA, UNAM DEPARTAMENTO DE FISICOQUÍMICA 21/SEPT/2020
UNIDAD 0. POTENCIALES TERMODINÁMICOS Y CRITERIOS DE
ESPONTANEIDAD Y EQUILIBRIO
𝑑𝑆𝑢𝑛𝑖𝑣 ≥ 0 𝑑𝑆𝑢𝑛𝑖𝑣 = 𝑑𝑆𝑠𝑖𝑠𝑡 + 𝑑𝑆𝑎𝑙𝑟
𝑑𝑄𝑎𝑙𝑟
𝑑𝑆𝑠𝑖𝑠𝑡 + 𝑑𝑆𝑎𝑙𝑟 ≥ 0 𝑝𝑒𝑟𝑜 𝑑𝑆𝑎𝑙𝑟 =
𝑇
𝑑𝑄𝑎𝑙𝑟
𝑑𝑆𝑠𝑖𝑠𝑡 + ≥0 𝑑𝑄𝑎𝑙𝑟 = −𝑑𝑄𝑠𝑖𝑠
𝑇
𝑑𝑄𝑠𝑖𝑠
𝑑𝑆𝑠𝑖𝑠 − ≥0 𝑠𝑖 𝑃 = 𝑐𝑡𝑒 (𝑑𝑄𝑠𝑖𝑠 )𝑃 = 𝑑𝐻𝑠𝑖𝑠
𝑇
𝑑𝐻𝑠𝑖𝑠
𝑑𝑆𝑠𝑖𝑠 − ≥0 𝑚𝑢𝑙𝑡𝑖𝑝𝑙𝑖𝑐𝑎𝑛𝑑𝑜 𝑝𝑜𝑟 − 1
𝑇
𝑑𝐻𝑠𝑖𝑠
− 𝑑𝑆𝑠𝑖𝑠 ≤ 0 𝑚𝑢𝑙𝑡𝑖𝑝𝑙𝑖𝑐𝑎𝑛𝑑𝑜 𝑝𝑜𝑟 𝑇
𝑇
𝑑𝐻𝑠𝑖𝑠 − 𝑇𝑑𝑆𝑠𝑖𝑠 ≤ 0
𝑑𝐺𝑠𝑖𝑠 ≤ 0 𝑇, 𝑃 = 𝑐𝑡𝑒𝑠
∆𝐺𝑠𝑖𝑠 ≤ 0
Se define:
𝐺 = 𝐻 − 𝑇𝑆 𝐸𝑛𝑒𝑟𝑔í𝑎 𝑑𝑒 𝐺𝑖𝑏𝑏𝑠 (𝑒𝑐𝑢𝑎𝑐𝑖ó𝑛 𝑑𝑒 𝑒𝑠𝑡𝑎𝑑𝑜), , 𝑑𝑖𝑓𝑒𝑟𝑒𝑛𝑐𝑖𝑎𝑛𝑑𝑜
𝑑𝐺 = 𝑑(𝐻 − 𝑇𝑆) = 𝑑𝐻 − 𝑑(𝑇𝑆)
𝑑𝐺 = 𝑑𝐻 − 𝑇𝑑𝑆 − 𝑆𝑑𝑇 𝑠𝑖 𝑇 = 𝑐𝑡𝑒 𝑑𝑇 = 0
𝑑𝐺 = 𝑑𝐻 − 𝑇𝑑𝑆 , 𝑖𝑛𝑡𝑒𝑛𝑔𝑟𝑎𝑛𝑑𝑜
𝐺2 𝐻2 𝑆2
∫ 𝑑𝐺 = ∫ 𝑑𝐻 − 𝑇 ∫ 𝑑𝑆
𝐺1 𝐻1 𝑆1
∆𝐺 = ∆𝐻 − 𝑇∆𝑆 𝑐𝑢𝑎𝑛𝑑𝑜 𝑇 𝑦 𝑃 = 𝑐𝑡𝑒𝑠
Criterio de espontaneidad y equilibrio T y P = ctes.
∆𝐺𝑠𝑖𝑠 ≤ 0
Tiene ventaja sobre la entropía, pues ahora se enfoca en el sistema.
𝑆𝑖 ∆𝐺𝑠𝑖𝑠 < 0 𝑃𝑟𝑜𝑐𝑒𝑠𝑜 𝑒𝑠𝑝𝑜𝑛𝑡á𝑛𝑒𝑜
𝑆𝑖 ∆𝐺𝑠𝑖𝑠 > 0 𝑃𝑟𝑜𝑐𝑒𝑠𝑜 𝑛𝑜 𝑒𝑠𝑝𝑜𝑛𝑡á𝑛𝑒𝑜
𝑆𝑖 ∆𝐺𝑠𝑖𝑠 = 0 𝐸𝑞𝑢𝑖𝑙𝑖𝑏𝑟𝑖𝑜 𝑡𝑒𝑟𝑚𝑜𝑑𝑖𝑛á𝑚𝑖𝑐𝑜
ELABORÓ: GERARDO OMAR HERNÁNDEZ SEGURA EQUILIBRIO Y CINÉTICA (CLAVE: 1308)
FACULTAD DE QUÍMICA, UNAM DEPARTAMENTO DE FISICOQUÍMICA 21/SEPT/2020
Evolución de un proceso a T y P = ctes.
G es una función de estado llamada energía de Gibbs y es una propiedad extensiva.
Unidades:
S.I. (J)
S. Inglés (Btu)
Otras unidades (cal)
Se define:
𝐴 = 𝑈 − 𝑇𝑆 𝐸𝑛𝑒𝑟𝑔í𝑎 𝑑𝑒 𝐻𝑒𝑙𝑚ℎ𝑜𝑙𝑡𝑧
Se procede con la misma diferenciación que para ΔG.
𝑑𝐴 = 𝑑𝑈 − 𝑇𝑑𝑆
𝐴2 𝑈2 𝑆2
∫ 𝑑𝐴 = ∫ 𝑑𝑈 − 𝑇 ∫ 𝑑𝑆
𝐴1 𝑈1 𝑆1
∆𝐴 = ∆𝑈 − 𝑇∆𝑆 𝑐𝑢𝑎𝑛𝑑𝑜 𝑇 𝑦 𝑉 = 𝑐𝑡𝑒𝑠
Criterio de espontaneidad y equilibrio T y V = ctes.
∆𝐴𝑠𝑖𝑠 ≤ 0
𝑆𝑖 ∆𝐴𝑠𝑖𝑠 < 0 𝑃𝑟𝑜𝑐𝑒𝑠𝑜 𝑒𝑠𝑝𝑜𝑛𝑡á𝑛𝑒𝑜
𝑆𝑖 ∆𝐴𝑠𝑖𝑠 > 0 𝑃𝑟𝑜𝑐𝑒𝑠𝑜 𝑛𝑜 𝑒𝑠𝑝𝑜𝑛𝑡á𝑛𝑒𝑜
𝑆𝑖 ∆𝐴 = 0 𝐸𝑞𝑢𝑖𝑙𝑖𝑏𝑟𝑖𝑜 𝑡𝑒𝑟𝑚𝑜𝑑𝑖𝑛á𝑚𝑖𝑐𝑜
ELABORÓ: GERARDO OMAR HERNÁNDEZ SEGURA EQUILIBRIO Y CINÉTICA (CLAVE: 1308)
FACULTAD DE QUÍMICA, UNAM DEPARTAMENTO DE FISICOQUÍMICA 21/SEPT/2020
Evolución de un proceso a T y V = ctes.
✓ A es una función de estado llamada energía de Helmholtz y es una propiedad
extensiva.
✓ Sus unidades son igual que las de G
✓ Tanto la energía de Helmholtz y Gibbs predicen la espontaneidad de un proceso.
✓ Su comportamiento en la gráfica es igual que G.
Ecuaciones fundamentales de la Termodinámica.
✓ 1ª Ley de la Termodinámica
𝑑𝑈 = 𝛿𝑄 + 𝛿𝑊
✓ Para proceso reversible
𝛿𝑄 = 𝛿𝑄𝑟𝑒𝑣
𝑑𝑈 = 𝛿𝑄𝑟𝑒𝑣 + 𝛿𝑊
𝛿𝑊 = −𝑃𝑜𝑝 𝑑𝑉
✓ Para proceso cuasiestático Pop ≈ Psistema
𝛿𝑊 = −𝑃𝑑𝑉
𝑑𝑈 = 𝛿𝑄𝑟𝑒𝑣 − 𝑃𝑑𝑉
De la 2ª Ley de la Termodinámica:
𝛿𝑄𝑟𝑒𝑣
𝑑𝑆 =
𝑇
𝛿𝑄𝑟𝑒𝑣 = 𝑇𝑑𝑆
ELABORÓ: GERARDO OMAR HERNÁNDEZ SEGURA EQUILIBRIO Y CINÉTICA (CLAVE: 1308)
FACULTAD DE QUÍMICA, UNAM DEPARTAMENTO DE FISICOQUÍMICA 21/SEPT/2020
𝑑𝑈 = 𝑇𝑑𝑆 − 𝑃𝑑𝑉 𝑃𝑟𝑖𝑚𝑒𝑟𝑎 𝐸𝑐𝑢𝑎𝑐𝑖ó𝑛 𝐹𝑢𝑛𝑑𝑎𝑚𝑒𝑛𝑡𝑎𝑙 𝑑𝑒 𝑙𝑎 𝑇𝑒𝑟𝑚𝑜𝑑𝑖𝑛á𝑚𝑖𝑐𝑎
Criterio de Euler.
𝑠𝑒𝑎 𝑓 = 𝑓(𝑥,𝑦) 𝑑𝑖𝑓𝑒𝑟𝑒𝑛𝑐𝑖𝑎𝑛𝑑𝑜
𝜕𝑓 𝜕𝑓
𝑑𝑓 = ( ) 𝑑𝑥 + ( ) 𝑑𝑦
𝜕𝑥 𝑦 𝜕𝑦 𝑥
𝜕𝑓 𝜕𝑓
𝑆𝑒 ℎ𝑎𝑐𝑒: Μ = ( ) Ν=( )
𝜕𝑥 𝑦 𝜕𝑦 𝑥
𝑑𝑓 = Μ𝑑𝑥 + Ν𝑑𝑦
𝜕Μ 𝜕Ν
( ) =( ) 𝑝𝑎𝑟𝑎 𝑒𝑐𝑢𝑎𝑐𝑖𝑜𝑛𝑒𝑠 𝑑𝑖𝑓𝑒𝑟𝑒𝑛𝑐𝑖𝑎𝑙𝑒𝑠 𝑒𝑥𝑎𝑐𝑡𝑎𝑠
𝜕𝑦 𝑥 𝜕𝑥 𝑦
Aplicando el criterio de Euler a la primera ecuación fundamental.
𝑑𝑈 = 𝑇𝑑𝑆 − 𝑃𝑑𝑉
𝜕T 𝜕𝑃
( ) = ( ) 𝑃𝑟𝑖𝑚𝑒𝑟𝑎 𝑟𝑒𝑙𝑎𝑐𝑖ó𝑛 𝑑𝑒 𝑀𝑎𝑥𝑤𝑒𝑙𝑙
𝜕𝑉 𝑆 𝜕𝑆 𝑉
𝑑𝑈 = 𝑇𝑑𝑆 − 𝑃𝑑𝑉
𝑈 = 𝑈(𝑆, 𝑉) 𝑑𝑖𝑓𝑒𝑟𝑒𝑛𝑐𝑖𝑎𝑛𝑑𝑜
𝜕𝑈 𝜕𝑈
𝑑𝑈 = ( ) 𝑑𝑆 + ( ) 𝑑𝑉
𝜕𝑆 𝑉 𝜕𝑉 𝑆
𝜕𝑈 𝜕𝑈
( ) =𝑇 ( ) = −𝑃
𝜕𝑆 𝑉 𝜕𝑉 𝑆
Empleando la primera ecuación fundamental:
𝑑𝑈 = 𝑇𝑑𝑆 − 𝑃𝑑𝑉 , 𝑠𝑢𝑚𝑎𝑛𝑑𝑜 𝑑(𝑃𝑉)
𝑑𝑈 + 𝑑(𝑃𝑉) = 𝑇𝑑𝑆 − 𝑃𝑑𝑉 + 𝑑(𝑃𝑉)
𝑑(𝑈 + 𝑃𝑉) = 𝑇𝑑𝑆 − 𝑃𝑑𝑉 + 𝑃𝑑𝑉 + 𝑉𝑑𝑃
𝑑𝐻 = 𝑇𝑑𝑆 + 𝑉𝑑𝑃 𝑆𝑒𝑔𝑢𝑛𝑑𝑎 𝐸𝑐𝑢𝑎𝑐𝑖ó𝑛 𝐹𝑢𝑛𝑑𝑎𝑚𝑒𝑛𝑡𝑎𝑙
Aplicando el criterio de Euler a la 2ª ecuación fundamental.
𝑑𝐻 = 𝑇𝑑𝑆 + 𝑉𝑑𝑃
𝜕T 𝜕𝑉
( ) =( ) 𝑆𝑒𝑔𝑢𝑛𝑑𝑎 𝑟𝑒𝑙𝑎𝑐𝑖ó𝑛 𝑑𝑒 𝑀𝑎𝑥𝑤𝑒𝑙𝑙
𝜕𝑃 𝑆 𝜕𝑆 𝑃
ELABORÓ: GERARDO OMAR HERNÁNDEZ SEGURA EQUILIBRIO Y CINÉTICA (CLAVE: 1308)
FACULTAD DE QUÍMICA, UNAM DEPARTAMENTO DE FISICOQUÍMICA 21/SEPT/2020
𝑑𝐻 = 𝑇𝑑𝑆 + 𝑉𝑑𝑃
𝐻 = 𝐻(𝑆, 𝑃) , 𝑑𝑖𝑓𝑒𝑟𝑒𝑛𝑐𝑖𝑎𝑛𝑑𝑜:
𝜕𝐻 𝜕𝐻
𝑑𝐻 = ( ) 𝑑𝑆 + ( ) 𝑑𝑃
𝜕𝑆 𝑃 𝜕𝑃 𝑆
𝜕𝐻 𝜕𝐻
( ) =𝑇 ( ) =𝑉
𝜕𝑆 𝑃 𝜕𝑃 𝑆
Retomando la 2ª ecuación fundamental
𝑑𝐻 = 𝑇𝑑𝑆 + 𝑉𝑑𝑃 , 𝑟𝑒𝑠𝑡𝑎𝑛𝑑𝑜 𝑑(𝑇𝑆)
𝑑𝐻 − 𝑑(𝑇𝑆) = 𝑇𝑑𝑆 + 𝑉𝑑𝑃 − 𝑑(𝑇𝑆)
𝑑(𝐻 − 𝑇𝑆) = 𝑇𝑑𝑆 + 𝑉𝑑𝑃 − 𝑇𝑑𝑆 − 𝑆𝑑𝑇
𝑑𝐺 = −𝑆𝑑𝑇 + 𝑉𝑑𝑃 𝑇𝑒𝑟𝑐𝑒𝑟𝑎 𝑒𝑐𝑢𝑎𝑐𝑖ó𝑛 𝑓𝑢𝑛𝑑𝑎𝑚𝑒𝑛𝑡𝑎𝑙
Aplicando el criterio de Euler.
𝑑𝐺 = −𝑆𝑑𝑇 + 𝑉𝑑𝑃
𝜕S 𝜕𝑉
−( ) =( ) 𝑇𝑒𝑟𝑐𝑒𝑟𝑎 𝑟𝑒𝑙𝑎𝑐𝑖ó𝑛 𝑑𝑒 𝑀𝑎𝑥𝑤𝑒𝑙𝑙
𝜕𝑃 𝑇 𝜕𝑇 𝑃
𝑑𝐺 = −𝑆𝑑𝑇 + 𝑉𝑑𝑃
𝐺 = 𝐺(𝑇, 𝑃) 𝑑𝑖𝑓𝑒𝑟𝑒𝑛𝑐𝑖𝑎𝑛𝑑𝑜:
𝜕𝐺 𝜕𝐺
𝑑𝐺 = ( ) 𝑑𝑇 + ( ) 𝑑𝑃
𝜕𝑇 𝑃 𝜕𝑃 𝑇
𝜕𝐺 𝜕𝐺
( ) = −𝑆 ( ) =𝑉
𝜕𝑇 𝑃 𝜕𝑃 𝑇
Retomando la primera ecuación fundamental.
𝑑𝑈 = 𝑇𝑑𝑆 − 𝑃𝑑𝑉 , 𝑟𝑒𝑠𝑡𝑎𝑛𝑑𝑜 𝑑(𝑇𝑆)
𝑑𝑈 − 𝑑(𝑇𝑆) = 𝑇𝑑𝑆 − 𝑃𝑑𝑉 − 𝑑(𝑇𝑆)
𝑑(𝑈 − 𝑇𝑆) = 𝑇𝑑𝑆 − 𝑃𝑑𝑉 − 𝑆𝑑𝑇 − 𝑇𝑑𝑆
𝑑𝐴 = −𝑆𝑑𝑇 − 𝑃𝑑𝑉 𝐶𝑢𝑎𝑟𝑡𝑎 𝑒𝑐𝑢𝑎𝑐𝑖ó𝑛 𝑓𝑢𝑛𝑑𝑎𝑚𝑒𝑛𝑡𝑎𝑙
Aplicando el criterio de Euler.
𝜕S 𝜕𝑃
−( ) = −( )
𝜕𝑉 𝑇 𝜕𝑇 𝑉
𝜕S 𝜕𝑃
( ) = ( ) 𝐶𝑢𝑎𝑟𝑡𝑎 𝑟𝑒𝑙𝑎𝑐𝑖ó𝑛 𝑑𝑒 𝑀𝑎𝑥𝑤𝑒𝑙𝑙
𝜕𝑉 𝑇 𝜕𝑇 𝑉
ELABORÓ: GERARDO OMAR HERNÁNDEZ SEGURA EQUILIBRIO Y CINÉTICA (CLAVE: 1308)
FACULTAD DE QUÍMICA, UNAM DEPARTAMENTO DE FISICOQUÍMICA 21/SEPT/2020
𝑑𝐴 = −𝑆𝑑𝑇 − 𝑃𝑑𝑉
𝐴 = 𝐴(𝑇, 𝑉) 𝑑𝑖𝑓𝑒𝑟𝑒𝑛𝑐𝑖𝑎𝑛𝑑𝑜
𝜕𝐴 𝜕𝐴
𝑑𝐴 = ( ) 𝑑𝑇 + ( ) 𝑑𝑉
𝜕𝑇 𝑉 𝜕𝑉 𝑇
𝜕𝐴 𝜕𝐴
( ) = −𝑆 ( ) = −𝑃
𝜕𝑇 𝑉 𝜕𝑉 𝑇
Otras identidades Termodinámicas.
𝐺 = 𝐻 − 𝑇𝑆 𝐺 = 𝐺(𝑇, 𝑃)
𝜕𝐺 𝜕 𝜕𝐻 𝜕𝑆 𝜕𝑇
( ) = (𝐻 − 𝑇𝑆)𝑃 = ( ) − 𝑇 ( ) − 𝑆 ( )
𝜕𝑇 𝑃 𝜕𝑇 𝜕𝑇 𝑃 𝜕𝑇 𝑃 𝜕𝑇 𝑃
𝜕𝐺 𝜕𝐻 𝜕𝑆
( ) = ( ) −𝑇( ) −𝑆
𝜕𝑇 𝑃 𝜕𝑇 𝑃 𝜕𝑇 𝑃
𝜕𝐻
𝑝𝑒𝑟𝑜: ( ) = 𝐶𝑝
𝜕𝑇 𝑃
𝜕𝐺 𝜕𝑆
( ) = 𝐶𝑝 − 𝑇 ( ) − 𝑆
𝜕𝑇 𝑃 𝜕𝑇 𝑃
𝜕𝐺
𝑝𝑒𝑟𝑜: ( ) = −𝑆
𝜕𝑇 𝑃
𝜕𝑆
−𝑆 = 𝐶𝑝 − 𝑇 ( ) 𝑜 𝑏𝑖𝑒𝑛, 𝑠𝑖𝑚𝑝𝑙𝑖𝑓𝑖𝑐𝑎𝑛𝑑𝑜:
𝜕𝑇 𝑃
𝜕𝑆
𝑇( ) = 𝐶𝑃
𝜕𝑇 𝑃
𝜕𝑆 𝐶𝑃
( ) =
𝜕𝑇 𝑃 𝑇
𝜕𝐺 𝜕 𝜕𝐻 𝜕𝑇 𝜕𝑆
( ) = (𝐻 − 𝑇𝑆) 𝑇 = ( ) − 𝑆 ( ) − 𝑇 ( )
𝜕𝑃 𝑇 𝜕𝑃 𝜕𝑃 𝑇 𝜕𝑃 𝑇 𝜕𝑃 𝑇
𝜕𝐺 𝜕𝐻 𝜕𝑆 𝜕𝐺
( ) = ( ) −𝑇( ) 𝑃𝑒𝑟𝑜 ( ) =𝑉
𝜕𝑃 𝑇 𝜕𝑃 𝑇 𝜕𝑃 𝑇 𝜕𝑃 𝑇
𝜕𝑆 𝜕𝑉
( ) = −( )
𝜕𝑃 𝑇 𝜕𝑇 𝑃
𝜕𝐻 𝜕𝑉
𝑉=( ) +𝑇( )
𝜕𝑃 𝑇 𝜕𝑇 𝑃
𝜕𝐻 𝜕𝑉
( ) = 𝑉 −𝑇( )
𝜕𝑃 𝑇 𝜕𝑇 𝑃
ELABORÓ: GERARDO OMAR HERNÁNDEZ SEGURA EQUILIBRIO Y CINÉTICA (CLAVE: 1308)
FACULTAD DE QUÍMICA, UNAM DEPARTAMENTO DE FISICOQUÍMICA 21/SEPT/2020
Otras identidades termodinámicas.
𝐴 = 𝑈 − 𝑇𝑆 𝐴 = 𝐴(𝑇, 𝑉)
𝜕𝐴 𝜕 𝜕𝑈 𝜕𝑆 𝜕𝑇
( ) = (𝑈 − 𝑇𝑆 )𝑉 = ( ) − 𝑇 ( ) − 𝑆 ( )
𝜕𝑇 𝑉 𝜕𝑇 𝜕𝑇 𝑉 𝜕𝑇 𝑉 𝜕𝑇 𝑉
𝜕𝐴 𝜕𝑈 𝜕𝑆 𝜕𝐴 𝜕𝑈
( ) = ( ) −𝑇( ) −𝑆 𝑃𝑒𝑟𝑜 ( ) = −𝑆 ( ) = 𝐶𝑉
𝜕𝑇 𝑉 𝜕𝑇 𝑉 𝜕𝑇 𝑉 𝜕𝑇 𝑉 𝜕𝑇 𝑉
𝜕𝑆
−𝑆 = 𝐶𝑉 − 𝑇 ( ) −𝑆
𝜕𝑇 𝑉
𝜕𝑆
0 = 𝐶𝑉 − 𝑇 ( )
𝜕𝑇 𝑉
𝜕𝑆
𝑇( ) = 𝐶𝑉
𝜕𝑇 𝑉
𝜕𝑆 𝐶𝑉
( ) =
𝜕𝑇 𝑉 𝑇
𝜕𝐴 𝜕 𝜕𝑈 𝜕𝑆 𝜕𝑇
( ) = (𝑈 − 𝑇𝑆 ) 𝑇 = ( ) − 𝑇 ( ) − 𝑆 ( )
𝜕𝑉 𝑇 𝜕𝑉 𝜕𝑉 𝑇 𝜕𝑉 𝑇 𝜕𝑉 𝑇
𝜕𝐴 𝜕𝑈 𝜕𝑆 𝜕𝐴 𝜕𝑆 𝜕𝑃
( ) = ( ) −𝑇( ) 𝑃𝑒𝑟𝑜 ( ) = −𝑃 ( ) =( )
𝜕𝑉 𝑇 𝜕𝑉 𝑇 𝜕𝑉 𝑇 𝜕𝑉 𝑇 𝜕𝑉 𝑇 𝜕𝑇 𝑉
𝜕𝑈 𝜕𝑃
−𝑃 = ( ) −𝑇( )
𝜕𝑉 𝑇 𝜕𝑇 𝑉
𝜕𝑈 𝜕𝑃
( ) = 𝑇( ) −𝑃
𝜕𝑉 𝑇 𝜕𝑇 𝑉
¿Cuál es el significado físico de ΔG y ΔA aparte de ser los criterios de espontaneidad y
equilibrio?
1ª Ley de la Termodinámica: 𝑑𝑈 = 𝑑𝑄 + ∑𝑖 𝑑𝑊𝑖
Para proceso reversible dQ=𝛿Qrev
𝑑𝑈 = 𝛿𝑄𝑟𝑒𝑣 + ∑ 𝛿𝑊𝑖 = 𝛿𝑄𝑟𝑒𝑣 + 𝛿𝑊𝑃𝑉 + 𝛿𝑊
𝑖
𝛿𝑊𝑃𝑉 = −𝑃𝑜𝑝 𝑑𝑉 𝑠𝑖 𝑒𝑙 𝑝𝑟𝑜𝑐𝑒𝑠𝑜 𝑒𝑠 𝑐𝑢𝑎𝑠𝑖𝑒𝑠𝑡á𝑡𝑖𝑐𝑜 𝑃𝑜𝑝 ≈ 𝑃𝑠𝑖𝑠𝑡𝑒𝑚𝑎
𝑑𝑈 = 𝛿𝑄𝑟𝑒𝑣 − 𝑃𝑑𝑉 + 𝛿𝑊
𝛿𝑄𝑟𝑒𝑣
2ª Ley de la Termodinámica 𝑑𝑆 = 𝑇
𝛿𝑄𝑟𝑒𝑣 = 𝑇𝑑𝑆
𝑑𝑈 = 𝑇𝑑𝑆 − 𝑃𝑑𝑉 + 𝛿𝑊 𝑠𝑢𝑚𝑎𝑛𝑑𝑜 𝑑(𝑃𝑉)
𝑑𝑈 + 𝑑(𝑃𝑉) = 𝑇𝑑𝑆 − 𝑃𝑑𝑉 + 𝛿𝑊 + 𝑑(𝑃𝑉)
ELABORÓ: GERARDO OMAR HERNÁNDEZ SEGURA EQUILIBRIO Y CINÉTICA (CLAVE: 1308)
FACULTAD DE QUÍMICA, UNAM DEPARTAMENTO DE FISICOQUÍMICA 21/SEPT/2020
𝑑(𝑈 + 𝑃𝑉) = 𝑇𝑑𝑆 − 𝑃𝑑𝑉 + 𝑃𝑑𝑉 + 𝑉𝑑𝑃 + 𝛿𝑊
𝑑𝐻 = 𝑇𝑑𝑆 + 𝑉𝑑𝑃 + 𝛿𝑊 𝑟𝑒𝑠𝑡𝑎𝑛𝑑𝑜 𝑑(𝑇𝑆)
𝑑𝐻 − 𝑑(𝑇𝑆) = 𝑇𝑑𝑆 + 𝑉𝑑𝑃 − 𝑑(𝑇𝑆) + 𝛿𝑊
𝑑(𝐻 − 𝑇𝑆) = 𝑇𝑑𝑆 + 𝑉𝑑𝑃 − 𝑆𝑑𝑇 − 𝑇𝑑𝑆 + 𝛿𝑊
𝑑𝐺 = −𝑆𝑑𝑇 + 𝑉𝑑𝑃 + 𝛿𝑊
𝑠𝑖 𝑇 𝑦 𝑃 𝑐𝑡𝑒𝑠 𝑇 = 0 𝑑𝑃 = 0
𝑑𝐺 = 𝛿𝑊 𝑠𝑖 𝑇 𝑦 𝑃 𝑐𝑡𝑒𝑠
Donde:
𝑊𝑠𝑢𝑝 = 𝛾∆𝐴
𝑊𝑒𝑙𝑒𝑐 = −𝑛𝐹𝐸°
𝑊𝑒𝑥𝑡 = 𝑓∆𝑙
∆𝐺 = 𝑊 𝑠𝑖 𝑇, 𝑃 𝑐𝑡𝑒𝑠
Para el gas ideal: ∆𝐺 = 𝑊𝑃𝑉
“ΔG es igual al trabajo de expansión y compresión”
Retomando la ecuación
𝑑𝑈 = 𝑇𝑑𝑆 − 𝑃𝑑𝑉 + 𝛿𝑊 𝑟𝑒𝑠𝑡𝑎𝑛𝑑𝑜 𝑑(𝑇𝑆)
𝑑𝑈 − 𝑑(𝑇𝑆) = 𝑇𝑑𝑆 − 𝑃𝑑𝑉 − 𝑑(𝑇𝑆) + 𝛿𝑊
𝑑(𝑈 − 𝑇𝑆) = 𝑇𝑑𝑆 − 𝑃𝑑𝑉 − 𝑇𝑑𝑆 − 𝑆𝑑𝑇 + 𝛿𝑊
𝑑𝐴 = −𝑆𝑑𝑇 − 𝑃𝑑𝑉 + 𝛿𝑊
𝑆𝑖 𝑇, 𝑉 𝑐𝑡𝑒𝑠 𝑑𝑇 = 0 𝑑𝑉 = 0
𝑑𝐴 = 𝛿𝑊 𝑠𝑖 𝑇, 𝑉 𝑐𝑡𝑒𝑠
∆𝐴 = 𝑊 𝑠𝑖 𝑇, 𝑉 𝑐𝑡𝑒𝑠
Para el gas ideal: ∆𝐴 = 𝑊𝑃𝑉
✓ Proceso natural o espontáneo libera energía en forma de trabajo. ΔG < 0 T,P=ctes.
ΔA <0 T,V ctes. Proceso exergónico.
✓ El proceso no espontáneo o no natural consume energía en forma de trabajo.
ΔG>0 T,P ctes. ΔA > 0 T,V ctes. Proceso endergónico.
Si T y P ctes:
dWsup=σdA dG=σdA → ΔG=σΔA
dWelec=-nFE dG=δW dG=Edq → ΔG=-nFE
ELABORÓ: GERARDO OMAR HERNÁNDEZ SEGURA EQUILIBRIO Y CINÉTICA (CLAVE: 1308)
FACULTAD DE QUÍMICA, UNAM DEPARTAMENTO DE FISICOQUÍMICA 21/SEPT/2020
dWext=fdL dG = fdL → ΔG=fΔL
El que más se utiliza es ΔG.
Propiedades intensivas de G y A.
Energía de Gibbs molar (potencial químico).
Sustancia pura
𝐺 𝐽 𝐵𝑡𝑢 𝑐𝑎𝑙
𝐺𝑚 = 𝜇 = ( )( )( )
𝑛 𝑚𝑜𝑙 𝑙𝑏 𝑚𝑜𝑙 𝑚𝑜𝑙
Mezcla de sustancias reaccionantes
𝜕𝐺
𝜇𝑖 = ( )
𝜕𝑛𝑖 𝑇,𝑃,𝑛𝑗 ≠𝑖
Energía de Helmholtz molar (potencial químico).
Sustancia pura a T,V ctes
𝐴 𝐽 𝐵𝑡𝑢 𝑐𝑎𝑙
𝐴𝑚 = 𝜇 = ( )( )( )
𝑛 𝑚𝑜𝑙 𝑙𝑏 𝑚𝑜𝑙 𝑚𝑜𝑙
Mezcla de sustancias reaccionantes
𝜕𝐴
𝜇𝑖 = ( )
𝜕𝑛𝑖 𝑇,𝑃,𝑛𝑗 ≠𝑖
Interpretación física de los potenciales Termodinámicos.
ΔG, ΔH y ΔS: predicción del comportamiento del sistema y el proceso.
∆𝐺 = ∆𝐻 − 𝑇∆𝑆
∆𝐻 = 𝑡é𝑟𝑚𝑖𝑛𝑜 𝑒𝑛𝑡á𝑙𝑝𝑖𝑐𝑜 𝑇∆𝑆 = 𝑡é𝑟𝑚𝑖𝑛𝑜 𝑒𝑛𝑡𝑟ó𝑝𝑖𝑐𝑜
Criterio de espontaneidad y equilibrio a T,P = ctes.
𝑆𝑖 ∆𝐺 < 0 , 𝑝𝑟𝑜𝑐𝑒𝑠𝑜 𝑒𝑠𝑝𝑜𝑛𝑡á𝑛𝑒𝑜, (𝑝𝑟𝑜𝑐𝑒𝑠𝑜 𝑒𝑥𝑒𝑟𝑔ó𝑛𝑖𝑐𝑜).
𝑆𝑖 ∆𝐺 > 0 , 𝑝𝑟𝑜𝑐𝑒𝑠𝑜 𝑛𝑜 𝑒𝑠𝑝𝑜𝑛𝑡á𝑛𝑒𝑜, (𝑝𝑟𝑜𝑐𝑒𝑠𝑜 𝑒𝑛𝑑𝑒𝑟𝑔ó𝑛𝑖𝑐𝑜).
𝑆𝑖 ∆𝐺 = 0 , 𝑠𝑖𝑠𝑡𝑒𝑚𝑎 𝑒𝑛 𝑒𝑞𝑢𝑖𝑙𝑖𝑏𝑟𝑖𝑜 𝑡𝑒𝑟𝑚𝑜𝑑𝑖á𝑚𝑖𝑐𝑜.
A T y P cotes, ΔG=W (pero no de PV).
Calor transferido a P = cte.
𝑆𝑖 ∆𝐻 = 𝑄𝑝
𝑆𝑖 ∆𝐻 < 0 , 𝑝𝑟𝑜𝑐𝑒𝑠𝑜 𝑒𝑥𝑜𝑡é𝑟𝑚𝑖𝑐𝑜
𝑆𝑖 ∆𝐻 > 0 , 𝑝𝑟𝑜𝑐𝑒𝑠𝑜 𝑒𝑛𝑑𝑜𝑡é𝑟𝑚𝑖𝑐𝑜
ELABORÓ: GERARDO OMAR HERNÁNDEZ SEGURA EQUILIBRIO Y CINÉTICA (CLAVE: 1308)
FACULTAD DE QUÍMICA, UNAM DEPARTAMENTO DE FISICOQUÍMICA 21/SEPT/2020
Cambio en el número de microestados.
𝑆𝑖 ∆𝑆 > 0 , 𝑎𝑢𝑚𝑒𝑛𝑡𝑎 𝑒𝑙 𝑛ú𝑚𝑒𝑟𝑜 𝑑𝑒 𝑚𝑖𝑐𝑟𝑜𝑒𝑠𝑡𝑎𝑑𝑜𝑠
𝑆𝑖 ∆𝑆 < 0 , 𝑑𝑖𝑠𝑚𝑖𝑛𝑢𝑦𝑒 𝑒𝑙 𝑛𝑢𝑚𝑒𝑟𝑜 𝑑𝑒 𝑚𝑖𝑐𝑟𝑜𝑒𝑠𝑡𝑎𝑑𝑜𝑠
ΔG = ΔH – TΔS T,P = ctes asumiendo ΔH y ΔS independientes de T.
✓ Caso 1: ΔH<0 , ΔS>0 → Proceso favorecido entálpicamente y entrópicamente;
proceso favorable a cualquier temperatura.
✓ Caso 2: ΔH>0 , ΔS<0 → Proceso desfavorecido entálpicamente y entrópicamente;
proceso desfavorecido a cualquier temperatura.
✓ Caso 3: ΔH>0 , ΔS>0 → Proceso desfavorable entálpicamente, pero favorable
entrópicamente; proceso favorable a altas temperaturas.
✓ Caso 4: ΔH<0 , ΔS<0 → Proceso favorecido entálpicamente, desfavorable
entrópicamente; proceso favorable a bajas temperaturas.
Dependencia de ∆𝑺𝟎𝒓 con la temperatura.
∆𝑆𝑟0 = ∑ 𝑛𝑖 𝑆𝑖0 𝑝𝑟𝑜𝑑 − ∑ 𝑛𝑗 𝑆𝑗0 𝑟𝑒𝑎𝑐𝑡 , 𝑑𝑒𝑟𝑖𝑣𝑎𝑛𝑑𝑜 𝑟𝑒𝑠𝑝𝑒𝑐𝑡𝑜 𝑎 𝑇 𝑎 𝑃 = 𝑐𝑡𝑒
𝑖 𝑗
𝑑𝑆𝑟0 𝑑
( ) = [∑ 𝑛𝑖 𝑆𝑖0 𝑝𝑟𝑜𝑑 − ∑ 𝑛𝑗 𝑆𝑗0 𝑟𝑒𝑎𝑐𝑡]
𝑑𝑇 𝑃 𝑑𝑇
𝑖 𝑗
𝑑𝑆𝑟0 𝑑𝑆𝑖 𝑝𝑟𝑜𝑑 𝑑𝑆𝑗 𝑟𝑒𝑎𝑐𝑡 𝑑𝑆 𝐶𝑃
( ) = ∑ 𝑛𝑖 ( ) − ∑ 𝑛𝑗 ( ) , 𝑝𝑒𝑟𝑜 ( ) =
𝑑𝑇 𝑃 𝑑𝑇 𝑃
𝑑𝑇 𝑃
𝑑𝑇 𝑃 𝑇
𝑖 𝑗
∆𝑆𝑟0 𝐶𝑃,𝑚 𝑝𝑟𝑜𝑑 𝐶𝑃,𝑚 𝑟𝑒𝑎𝑐𝑡
= ∑ 𝑛𝑖 − ∑ 𝑛𝑗
𝑑𝑇 𝑇 𝑇
𝑖 𝑗
𝑆𝑒 𝑑𝑒𝑓𝑖𝑛𝑒 ∆𝐶𝑝 = ∑ 𝑛𝑖 𝐶𝑃,𝑚 𝑝𝑟𝑜𝑑 − ∑ 𝑛𝑗 𝐶𝑃,𝑚 𝑟𝑒𝑎𝑐𝑡
𝑖 𝑗
∆𝑆𝑟0 ∆𝐶𝑃
=
𝑑𝑇 𝑇
∆𝐶𝑃
𝑑∆𝑆𝑟0 = 𝑑𝑇 , 𝑖𝑛𝑡𝑒𝑔𝑟𝑎𝑛𝑑𝑜
𝑇
∆𝑆𝑟0 𝑇 𝑇
∆𝐶𝑃
∫ ∆𝑆𝑟0 = ∫ 𝑑𝑇
𝑇
∆𝑆𝑟0 𝑇0 𝑇0
𝑇
∆𝐶𝑃
∆𝑆𝑟0 𝑇 − ∆𝑆𝑟0 𝑇0 = ∫ 𝑑𝑇
𝑇
𝑇0
ELABORÓ: GERARDO OMAR HERNÁNDEZ SEGURA EQUILIBRIO Y CINÉTICA (CLAVE: 1308)
FACULTAD DE QUÍMICA, UNAM DEPARTAMENTO DE FISICOQUÍMICA 21/SEPT/2020
𝐼) 𝑆𝑖 ∆𝐶𝑝 = 𝑐𝑡𝑒
𝑇
∆𝐶𝑃
∆𝑆𝑟0 𝑇 = ∆𝑆𝑟0 𝑇0 + ∫ 𝑑𝑇
𝑇
𝑇0
𝑇
∆𝑆𝑟0 𝑇 = ∆𝑆𝑟0 𝑇0 + ∆𝐶𝑝 𝑙𝑛 ( )
𝑇𝑜
𝐼𝐼) 𝑆𝑖 ∆𝐶𝑝 = 𝑓(𝑇)
𝑇
∆𝐶𝑃 (𝑇)
∆𝑆𝑟0 𝑇 = ∆𝑆𝑟0 𝑇0 + ∫ 𝑑𝑇
𝑇
𝑇0
To = 298.15 K ∆𝑆𝑟0 𝑇0 = ∆𝑆𝑟0 298.15 𝐾
Cálculo de ΔGr y ΔAr para procesos químicos a condiciones estándar.
0 0
∆𝐺𝑟0 = ∑ 𝑛𝑖 ∆𝐺𝑓𝑖 𝑝𝑟𝑜𝑑 − ∑ 𝑛𝑗 ∆𝐺𝑓𝑗 𝑟𝑒𝑎𝑐𝑡
𝑖 𝑗
A condiciones estándar ∆𝐺𝑓0=0 para los elementos.
∆𝐺𝑟0 = ∆𝐻𝑟0 − 𝑇∆𝑆𝑟0 𝑇, 𝑃 𝑐𝑡𝑒𝑠
∆𝑈𝑟0 = ∆𝐻𝑟0 − ∆𝑛(𝑔𝑎𝑠𝑒𝑠) 𝑅𝑇
∆𝐴0𝑟 = ∆𝑈𝑟0 − 𝑇∆𝑆𝑟0 𝑇, 𝑃 𝑐𝑡𝑒𝑠
Cálculo de ΔG y ΔA para gas ideal.
𝑆𝑖 𝑑𝐺 = −𝑆𝑑𝑇 + 𝑉𝑑𝑃 𝑠𝑖 𝑇 = 𝑐𝑡𝑒 𝑦 𝑑𝑇 = 0
𝑛𝑅𝑇
𝑑𝐺 = 𝑉𝑑𝑃 𝑝𝑎𝑟𝑎 𝑔𝑎𝑠 𝑖𝑑𝑒𝑎𝑙. 𝑃𝑉 = 𝑛𝑅𝑇 → 𝑉 =
𝑃
𝑛𝑅𝑇
𝑑𝐺 = 𝑑𝑃 , 𝑖𝑛𝑡𝑒𝑔𝑟𝑎𝑛𝑑𝑜
𝑃
𝐺2 𝑃2
𝑑𝑃
∫ 𝑑𝐺 = 𝑛𝑅𝑇 ∫
𝑃
𝐺1 𝑃1
𝑃2
∆𝐺 = 𝑛𝑅𝑇 𝑙𝑛 ( ) 𝑝𝑎𝑟𝑎 𝑔𝑎𝑠 𝑖𝑑𝑒𝑎𝑙 𝑝𝑟𝑜𝑐𝑒𝑠𝑜 𝑖𝑠𝑜𝑡é𝑟𝑚𝑖𝑐𝑜 𝑐𝑢𝑎𝑠𝑖𝑒𝑠𝑡á𝑡𝑖𝑐𝑜 − 𝑟𝑒𝑣𝑒𝑟𝑠𝑖𝑏𝑙𝑒
𝑃1
𝑑𝐴 = −𝑆𝑑𝑇 − 𝑃𝑑𝑉 𝑠𝑖 𝑇 = 𝑐𝑡𝑒, 𝑑𝑇 = 0
𝑛𝑅𝑇
𝑑𝐴 = −𝑃𝑑𝑉 𝑝𝑎𝑟𝑎 𝑔𝑎𝑠 𝑖𝑑𝑒𝑎𝑙 𝑃 =
𝑉
𝑛𝑅𝑇
𝑑𝐴 = − 𝑑𝑉 𝑖𝑛𝑡𝑒𝑔𝑟𝑎𝑛𝑑𝑜
𝑉
ELABORÓ: GERARDO OMAR HERNÁNDEZ SEGURA EQUILIBRIO Y CINÉTICA (CLAVE: 1308)
FACULTAD DE QUÍMICA, UNAM DEPARTAMENTO DE FISICOQUÍMICA 21/SEPT/2020
𝐴2 𝑉2
𝑑𝑉
∫ 𝑑𝐴 = −𝑛𝑅𝑇 ∫
𝑉
𝐴1 𝑉1
𝑉2
∆𝐴 = −𝑛𝑅𝑇 𝑙𝑛 ( ) 𝑝𝑎𝑟𝑎 𝑔𝑎𝑠 𝑖𝑑𝑒𝑎𝑙 𝑝𝑟𝑜𝑐𝑒𝑠𝑜 𝑖𝑠𝑜𝑡é𝑟𝑚𝑖𝑐𝑜 𝑟𝑒𝑣𝑒𝑟𝑠𝑖𝑏𝑙𝑒 − 𝑐𝑢𝑎𝑠𝑖𝑒𝑠𝑡á𝑡𝑖𝑐𝑜
𝑉1
Cálculo de ΔG para fases condensadas.
𝑑𝐺 = −𝑆𝑑𝑇 + 𝑉𝑑𝑃 𝑠𝑖 𝑇 = 𝑐𝑡𝑒 , 𝑑𝑇 = 0
𝑑𝐺 = 𝑉𝑑𝑃 𝑝𝑎𝑟𝑎 𝑓𝑎𝑠𝑒𝑠 𝑐𝑜𝑛𝑑𝑒𝑛𝑠𝑎𝑑𝑎𝑠 𝑉 ≈ 𝑐𝑡𝑒 𝑒 𝑖𝑛𝑡𝑒𝑔𝑟𝑎𝑛𝑑𝑜
𝐺2 𝑃2
∫ 𝑑𝐺 = 𝑉 ∫ 𝑑𝑃
𝐺1 𝑃1
∆𝐺 = 𝑉(𝑃2 − 𝑃1 )
𝑉
𝑝𝑒𝑟𝑜 𝑉𝑚 = → 𝑉 = 𝑛𝑉𝑚
𝑛
∆𝐺 = 𝑛𝑉𝑚 (𝑃2 − 𝑃1 )
Cálculo de ΔG para un cambio de fase reversible a T,P ctes.
∆𝐻𝑡𝑟𝑎𝑛𝑠
∆𝐺𝑡𝑟𝑎𝑛𝑠 = ∆𝐻𝑡𝑟𝑎𝑛𝑠 − 𝑇∆𝑆𝑡𝑟𝑎𝑛𝑠 , 𝑝𝑒𝑟𝑜 ∆𝑆𝑡𝑟𝑎𝑛𝑠 =
𝑇
∆𝐻𝑡𝑟𝑎𝑛𝑠
∆𝐺𝑡𝑟𝑎𝑛𝑠 = ∆𝐻𝑡𝑟𝑎𝑛𝑠 − 𝑇 ( )=0
𝑇
∆𝐺𝑡𝑟𝑎𝑛𝑠 = 0 𝑇, 𝑃 = 𝑐𝑡𝑒𝑠 𝑒𝑥𝑖𝑠𝑡𝑒 𝑒𝑞𝑢𝑖𝑙𝑖𝑏𝑟𝑖𝑜 𝑡𝑒𝑟𝑚𝑜𝑑𝑖𝑛á𝑚𝑖𝑐𝑜 (𝑓𝑎𝑠𝑒𝑠 𝑒𝑛 𝑒𝑞𝑢𝑖𝑙𝑖𝑏𝑟𝑖𝑜)
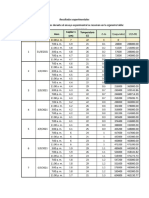
I) La oxidación del SO2 ocurre en el interior de los motores de combustión interna
para producir SO3 a una T= 500 K y una P= 1 bar. Se presentan los datos a
condiciones estándar:
SO2 (g) + ½ O2 (g) → SO3 (g)
Sustancia 𝑲𝑱 𝑱 𝑪𝑷,𝒎 (𝑻)
∆𝑯𝟎𝒇 ( ) 𝑺𝟎 ( ) 𝑱
𝒎𝒐𝒍 𝒎𝒐𝒍 𝑲
= 𝑨 + 𝑩𝑻 ( )
𝒎𝒐𝒍 𝑲
-3
SO2 (g) -296.83 248.22 47.38 + 6.65x10 T
O2 (g) 0 205.13 30.25 + 4.20x10-3 T
SO3 (g) -395.72 256.76 67.01 + 8.77x10-3 T
Calcular: ∆𝐻𝑟0 , ∆𝑆𝑟0, ∆𝑈𝑟0 y ∆𝐴0𝑟 a 500 K, 1 bar dando la interpretación física para cada
potencial termodinámico.
ELABORÓ: GERARDO OMAR HERNÁNDEZ SEGURA EQUILIBRIO Y CINÉTICA (CLAVE: 1308)
FACULTAD DE QUÍMICA, UNAM DEPARTAMENTO DE FISICOQUÍMICA 21/SEPT/2020
To= 298.15 K T= 500 K
𝐾𝐽 𝐾𝐽 𝐾𝐽
∆𝐻𝑟0 𝑇0 = (1) (−395.72 ) − (1) (−296.83 ) = −98.89
𝑚𝑜𝑙 𝑚𝑜𝑙 𝑚𝑜𝑙
𝐽 𝐽 1 𝐽 𝐽
∆𝑆𝑟0 𝑇0 = (1) (256.76 ) − (1) (248.22 ) + ( ) (205.13 ) = −94.03
𝑚𝑜𝑙 𝐾 𝑚𝑜𝑙 𝐾 2 𝑚𝑜𝑙 𝐾 𝑚𝑜𝑙 𝐾
1
∆𝐶𝑝 = 𝐶𝑝,𝑚 𝑆𝑂3 − [𝐶𝑝,𝑚 𝑆𝑂2 + 𝐶𝑝,𝑚 𝑂2 ]
2
1
∆𝐶𝑝 = (67.01 + 8.77x10−3 T) − (47.38 + 6.65x10−3 T) − (30.25 + 4.20x110−3 T)
2
∆𝐶𝑝 = 4.505 + 2.5𝑥10−5 𝑇
𝑇
∆𝐻𝑟0 𝑇 = ∆𝐻𝑟0 𝑇0 + ∫ ∆𝐶𝑃 (𝑇) 𝑑𝑇
𝑇𝑜
∆𝐻𝑟0 𝑇 = ∆𝐻𝑟0 𝑇0 + 4.505 + 2.5𝑥10−5 𝑇 + 1.5𝑥10−5 (500 𝐾 2 − 298.15 𝐾 2 )
𝐽 𝐽
∆𝐻𝑟0 𝑇 = −98890 + 898.76
𝑚𝑜𝑙 𝑚𝑜𝑙
𝐽
∆𝐻𝑟0 𝑇 = −97979.23 𝑝𝑟𝑜𝑐𝑒𝑠𝑜 𝑎 𝑇 = 500 𝐾 𝑦 1 𝑏𝑎𝑟
𝑚𝑜𝑙
Se libera más calor a 298.15 K.
𝑇
∆𝐶𝑃 (𝑇)
∆𝑆𝑟0 𝑇 = ∆𝑆𝑟0 𝑇0 + ∫ 𝑑𝑇
𝑇
𝑇𝑜
𝑇
∆𝑆𝑟0 𝑇 = ∆𝑆𝑟0 𝑇0 + ∫(4.505 + 2𝑥10−5 𝑇) 𝑑𝑇
𝑇𝑜
𝑇
∆𝑆𝑟0 𝑇 = ∆𝑆𝑟0 𝑇0 + 4.505 𝑙𝑛 + 2.5𝑥10−5 (𝑇 − 𝑇𝑜 )
𝑇0
𝐽 500 𝐾
∆𝑆𝑟0 500 𝐾 = −94.03 + 4.505 𝑙𝑛 + 2.5𝑥10−5 (500 𝐾 − 298.15 𝐾)
𝑚𝑜𝑙 𝐾 298.15 𝐾
𝐽
∆𝑆𝑟0 500 𝐾 = −91.69 𝑒𝑙 𝑛ú𝑚𝑒𝑟𝑜 𝑑𝑒 𝑚𝑖𝑐𝑟𝑜𝑒𝑠𝑡𝑎𝑑𝑜𝑠 𝑑𝑖𝑠𝑚𝑖𝑛𝑢𝑦𝑒.
𝑚𝑜𝑙 𝐾
∆𝐺𝑟0 𝑇 = ∆𝐻𝑟0 𝑇 − 𝑇∆𝑆𝑟0 𝑇
𝑗 𝐽 𝐽
∆𝐺𝑟0 𝑇 = −97979 − (500 𝐾) (−91.69 ) = −52134
𝑚𝑜𝑙 𝑚𝑜𝑙 𝐾 𝑚𝑜𝑙
El proceso es espontáneo a T= 500 K y 1 bar (proceso exergónico).
El proceso es favorable a temperaturas bajas (∆𝐻𝑟0 𝑇 < 0 ; ∆𝑆𝑟0 𝑇 < 0)
ELABORÓ: GERARDO OMAR HERNÁNDEZ SEGURA EQUILIBRIO Y CINÉTICA (CLAVE: 1308)
FACULTAD DE QUÍMICA, UNAM DEPARTAMENTO DE FISICOQUÍMICA 21/SEPT/2020
∆𝑈𝑟0 𝑇 = ∆𝐻𝑟0 𝑇 − ∆𝑛(𝑔𝑎𝑠𝑒𝑠) 𝑅𝑇
3 1
∆𝑛(𝑔𝑎𝑠𝑒𝑠) = 1 − =−
2 2
𝐽 1 𝐽 𝐽
∆𝑈𝑟0 𝑇 500 𝐾 = −97979 − (− ) (8.314 ) (500 𝐾) = −95900.5
𝑚𝑜𝑙 2 𝑚𝑜𝑙 𝐾 𝑚𝑜𝑙
El proceso es exotérmico a T= 500K y V=cte.
A presión constante se libera más calor que a volumen constante.
∆𝐻𝑟0 𝑇 < ∆𝑈𝑟0 𝑇
𝐽 𝐽 𝐽
∆𝐴0𝑟 = ∆𝑈𝑟0 𝑇 − 𝑇∆𝑆𝑟0 𝑇 = −95900.5 − (500 𝐾) (−91.69 ) = −50054.5
𝑚𝑜𝑙 𝑚𝑜𝑙 𝐾 𝑚𝑜𝑙
El proceso es espontáneo a 500 K y V=cte.
A presión constante se libera más calor que a volumen constante
II) 5 moles de propano a 500 K se expanden isotérmicamente y
cuasiestáticamente desde 2 L a 100 L. Con esta información, calcular: ΔH, ΔU
y W, Q, ΔS, ΔA y ΔG.
𝑉2 𝑐𝑎𝑙 100 𝐿
𝑊 = −𝑛𝑅𝑇 𝑙𝑛 = (5 𝑚𝑜𝑙) (1.987 ) (500 𝐾) ln ( )
𝑉1 𝑚𝑜𝑙 𝐾 2𝐿
𝑊 = −19433.3 𝑐𝑎𝑙
𝑄 = 19433.3 𝑐𝑎𝑙
𝑄𝑟𝑒𝑣 19433.3 𝑐𝑎𝑙
∆𝑆 = = = 38.86 𝑢. 𝑒.
𝑇 500 𝐾
∆𝐺 = ∆𝐻 − 𝑇∆𝑆 = −𝑇∆𝑆 = −(500 𝐾)(38.86 𝑢. 𝑒. ) = −19433.3 𝑐𝑎𝑙
∆𝐴 = ∆𝑈 − 𝑇∆𝑆 = −19433.3 𝑐𝑎𝑙
Coinciden con el trabajo de expansión y compresión para gas ideal.
ELABORÓ: GERARDO OMAR HERNÁNDEZ SEGURA EQUILIBRIO Y CINÉTICA (CLAVE: 1308)
FACULTAD DE QUÍMICA, UNAM DEPARTAMENTO DE FISICOQUÍMICA 21/SEPT/2020
III) Para la celda electroquímica:
2 Ag+(ac) + Cu (s) → 2 Ag (s) + Cu2+(ac)
Se presentan a continuación los datos. Calcular el Welec desarrollado por la celda, el
potencial electroquímico producido, ΔH y ΔS a condiciones estándar indicando si la
reacción es espontánea: exotérmica o endotérmica y si aumenta el número de
microestados y si es favorable a bajas o altas temperaturas.
Sustancia 𝑲𝑱 𝑱
∆𝑮𝟎𝒇 ( ) 𝑺𝟎 ( )
𝒎𝒐𝒍 𝒎𝒐𝒍 𝑲
Ag+(ac) 77.11 72.68
Cu(s) 0 33.15
Cu2+(ac) 65.49 -99.6
Ag(s) 0 42.55
𝐾𝐽 𝐾𝐽 𝐾𝐽
∆𝐺𝑟0 = (1) (65.49 ) + (0) − (2) (77.11 ) + (−0) = 8 − 88.73
𝑚𝑜𝑙 𝑚𝑜𝑙 𝑚𝑜𝑙
Proceso espontáneo a T, P = ctes
𝐽 𝐽 𝐽 𝐽
∆𝑆𝑟0 = (2) (42.55 ) + (1) (−99.6 ) + (2) (72.68 ) + (1) (33.15 )
𝑚𝑜𝑙 𝐾 𝑚𝑜𝑙 𝐾 𝑚𝑜𝑙 𝐾 𝑚𝑜𝑙 𝐾
𝐽
= −193.01
𝑚𝑜𝑙 𝐾
Disminuye el número de microestados.
∆𝐺𝑟0 = ∆𝐻𝑟0 − 𝑇∆𝑆𝑟0
𝐽 𝐽
∆𝐻𝑟0 = ∆𝐺𝑟0 + 𝑇∆𝑆𝑟0 = −88730 + 298.15 𝐾 (−193.01 )
𝑚𝑜𝑙 𝑚𝑜𝑙 𝐾
𝐽
∆𝐻𝑟0 = −146276 = 𝑄𝑝 𝑒𝑙 𝑝𝑟𝑜𝑐𝑒𝑠𝑜 𝑒𝑠 𝑒𝑥𝑜𝑡é𝑟𝑚𝑖𝑐𝑜
𝑚𝑜𝑙
Si T y P = ctes
∆𝐺 = 𝑊𝑒𝑙𝑒𝑐 = −88730 𝐽
𝑊𝑒𝑙𝑒𝑐 = ∆𝐺𝑟0 = −𝑛𝐹𝐸°
∆𝐺𝑟0
𝐸° = −
𝑛𝐹
𝐽
− (−88730 )
𝐸° = 𝑚𝑜𝑙 = 0.46 𝑉
(2)(96500 𝐶)
ELABORÓ: GERARDO OMAR HERNÁNDEZ SEGURA EQUILIBRIO Y CINÉTICA (CLAVE: 1308)
También podría gustarte
- Equilibrio Químico en Sistemas Ideales PDFDocumento34 páginasEquilibrio Químico en Sistemas Ideales PDFDaniel MeloAún no hay calificaciones
- Examen Fisicoquimica I.Q. E-J 2021 U.4-Aniceto HJDocumento4 páginasExamen Fisicoquimica I.Q. E-J 2021 U.4-Aniceto HJMexico CampeonAún no hay calificaciones
- Regla de Las Fases y ClapeyronDocumento7 páginasRegla de Las Fases y Clapeyronmauricio.d.posAún no hay calificaciones
- Reporte Q.A 1.2Documento10 páginasReporte Q.A 1.2MisaelAún no hay calificaciones
- Equilibrio de Fases en Sistemas de Dos Componentes 2015-2Documento3 páginasEquilibrio de Fases en Sistemas de Dos Componentes 2015-2JuanQueteImportaAún no hay calificaciones
- Caso de Estudio FisicoquímicaDocumento14 páginasCaso de Estudio FisicoquímicaAxel Velazquez MoralesAún no hay calificaciones
- IQI 313. Serie 6 Ejercicios I 2016Documento2 páginasIQI 313. Serie 6 Ejercicios I 2016alexofigurinAún no hay calificaciones
- TD13 - Equilibrio Liquido - LiquidoDocumento20 páginasTD13 - Equilibrio Liquido - LiquidoAngelly SalazarAún no hay calificaciones
- FISICOQUIMICA2Documento14 páginasFISICOQUIMICA2Jesus Alexis Cervantes RamirezAún no hay calificaciones
- Problemario fq2Documento6 páginasProblemario fq2JorgeAún no hay calificaciones
- Análisis Instrumental Curvas EspectralesDocumento6 páginasAnálisis Instrumental Curvas EspectralesIsrael VegaAún no hay calificaciones
- Notas Del Curso de Equilibrio y CinéticaDocumento77 páginasNotas Del Curso de Equilibrio y CinéticaEmilioMadaraAún no hay calificaciones
- Apuntes 2 05 MarzoDocumento14 páginasApuntes 2 05 MarzoFernanda Nieto UriosteguiAún no hay calificaciones
- Presión de Vapor y Ecuaciones de EstadoDocumento8 páginasPresión de Vapor y Ecuaciones de EstadoVALENTINA RUIZ GARCIAAún no hay calificaciones
- Calor Diferencial de SolucionDocumento14 páginasCalor Diferencial de Solucionapi-380235780% (5)
- Serie 5 - Resolución. Parte IDocumento22 páginasSerie 5 - Resolución. Parte Ieliana vegaAún no hay calificaciones
- Equilibrio en Sistemas Con Reacciones QuímicasDocumento35 páginasEquilibrio en Sistemas Con Reacciones QuímicasAngel EuanAún no hay calificaciones
- Práctica 3 - Equilibrio Líquido Vapor - FINALDocumento7 páginasPráctica 3 - Equilibrio Líquido Vapor - FINALAlejandra Rosero BastidasAún no hay calificaciones
- Practica 2 Termo FinalDocumento12 páginasPractica 2 Termo FinalAnonymous jU0TwwIAún no hay calificaciones
- Mecanismos de Reacción en Catálisis HeterogéneaDocumento2 páginasMecanismos de Reacción en Catálisis HeterogéneaYevMaltabarAún no hay calificaciones
- Metodo Grafico de WinkelmannDocumento4 páginasMetodo Grafico de WinkelmannCarmen HernandezAún no hay calificaciones
- Calor de Combustion13Documento19 páginasCalor de Combustion13Jorge TrejoAún no hay calificaciones
- Masa Molar de Un LíquidoDocumento12 páginasMasa Molar de Un LíquidoAlfonso RodríguezAún no hay calificaciones
- Universidad VeracruzanaDocumento18 páginasUniversidad VeracruzanaEnrique Hernandez LiraAún no hay calificaciones
- Clase 3a. Clase Magnitudes Molares ParcialesDocumento39 páginasClase 3a. Clase Magnitudes Molares ParcialesJhon Ardila BariosAún no hay calificaciones
- 5 Ingridh. Elkinv PDFDocumento73 páginas5 Ingridh. Elkinv PDFOscar Fernando Portilla GómezAún no hay calificaciones
- EQUILIBRIO-QUÍMICO Practica 2Documento6 páginasEQUILIBRIO-QUÍMICO Practica 2MoOnse MoOnseAún no hay calificaciones
- Clase Solidos PDFDocumento56 páginasClase Solidos PDFJosue Hernandez MrkzAún no hay calificaciones
- Reporte 3 de Equilibrio QuímicoDocumento7 páginasReporte 3 de Equilibrio QuímicoJose Antonio VazquezAún no hay calificaciones
- Practica Calor de NeutralizacionDocumento3 páginasPractica Calor de NeutralizacionAldair LugoAún no hay calificaciones
- Calculo Del Perfil de Concentraciones para Un Reactor Tubular y Del Volumen Del Reactorcon Solución Numérica Con El Método de RungeDocumento3 páginasCalculo Del Perfil de Concentraciones para Un Reactor Tubular y Del Volumen Del Reactorcon Solución Numérica Con El Método de RungeLemuelMoralesAún no hay calificaciones
- Ejercicios Energía Libre de GibbsDocumento6 páginasEjercicios Energía Libre de GibbsCindy MuñozAún no hay calificaciones
- Bird. Capitulo Cero y PrologoDocumento2 páginasBird. Capitulo Cero y PrologoLu GutierrezAún no hay calificaciones
- HCL Informe FinalDocumento16 páginasHCL Informe FinalWilly Alexander López AlvaAún no hay calificaciones
- Determinación de La Constante de Velocidad Mediante La Cinética de La Hidrólisis de Un Ester Por Conductividad EléctricaDocumento3 páginasDeterminación de La Constante de Velocidad Mediante La Cinética de La Hidrólisis de Un Ester Por Conductividad EléctricaSebas Soto0% (1)
- Entalpía de Vaporización de Un Líquido PuroDocumento4 páginasEntalpía de Vaporización de Un Líquido PuromagicianchemistAún no hay calificaciones
- Previo CiclohexanoDocumento3 páginasPrevio CiclohexanoWilliams D Hernández GAún no hay calificaciones
- Concentración y Temperatura en El Desplazamiento Del Equilibrio Químico de Una Sustancia Poco Soluble.Documento19 páginasConcentración y Temperatura en El Desplazamiento Del Equilibrio Químico de Una Sustancia Poco Soluble.Stephanie MeloAún no hay calificaciones
- Ejercicio de Entropía-5.38 de Smith Van NessDocumento4 páginasEjercicio de Entropía-5.38 de Smith Van NesskenyacornejoAún no hay calificaciones
- Determinacion de La Razón CP-CV Practica 2Documento4 páginasDeterminacion de La Razón CP-CV Practica 2hellmasterAún no hay calificaciones
- Tarea 2. Sistemas BinariosDocumento4 páginasTarea 2. Sistemas BinariosMontsZs G-oAún no hay calificaciones
- Relación CP/CVDocumento6 páginasRelación CP/CVhanscortesAún no hay calificaciones
- Clase 11 Problemas Termoquímica Termodinámica y Cinética 1Documento10 páginasClase 11 Problemas Termoquímica Termodinámica y Cinética 1Camila AndradeAún no hay calificaciones
- FUGACIDADDocumento26 páginasFUGACIDADAidee Lopez SantiagoAún no hay calificaciones
- Ecuación Soave-Redlich-KwongDocumento16 páginasEcuación Soave-Redlich-KwongMajo GuevaraAún no hay calificaciones
- SolucionesNoElectrolitos 14274 PDFDocumento22 páginasSolucionesNoElectrolitos 14274 PDFCindyDArttigasAún no hay calificaciones
- Reducción de Ácidos CarboxílicosDocumento17 páginasReducción de Ácidos CarboxílicosJorge Mario Fernandez PeñaAún no hay calificaciones
- Tarea U-I-A-1Documento1 páginaTarea U-I-A-1astroboyatlas0% (1)
- PresentacionDocumento61 páginasPresentacionJhoan Andre'Aún no hay calificaciones
- Practica 6-E&CDocumento9 páginasPractica 6-E&CRicardo CruzAún no hay calificaciones
- Sesión 01 Termodinámica SolucionesDocumento39 páginasSesión 01 Termodinámica SolucionesAdolfo GuerreroAún no hay calificaciones
- P4 - Reacción de ÓxidoReducción (Síntesis de Yodoformo) - Martinez - GR1ADocumento5 páginasP4 - Reacción de ÓxidoReducción (Síntesis de Yodoformo) - Martinez - GR1AKarla ArceAún no hay calificaciones
- Practica Num 4Documento5 páginasPractica Num 4victacito100% (1)
- Notas Termodinamica Del EquilibrioDocumento94 páginasNotas Termodinamica Del EquilibrioIsseiAún no hay calificaciones
- Practica3 Equilibrio-QuimicoDocumento7 páginasPractica3 Equilibrio-QuimicoJocelynAún no hay calificaciones
- Reporte Fuerzas Intermoleculares2Documento14 páginasReporte Fuerzas Intermoleculares2Juana CruzAún no hay calificaciones
- Volumenes Molares ParcialesDocumento9 páginasVolumenes Molares ParcialesFranzMichaelSanchezAlbaAún no hay calificaciones
- Taller Leyes Newton-KirchhoffDocumento2 páginasTaller Leyes Newton-KirchhoffCristian Cabrera ValenciaAún no hay calificaciones
- Taller-Leyes NewtonDocumento2 páginasTaller-Leyes NewtonCristian Cabrera ValenciaAún no hay calificaciones
- Serie 1 2021-1Documento3 páginasSerie 1 2021-1Daniel MeloAún no hay calificaciones
- Notas Eq2Documento10 páginasNotas Eq2Daniel MeloAún no hay calificaciones
- Problema 3Documento1 páginaProblema 3Daniel MeloAún no hay calificaciones
- Notas Ef2Documento8 páginasNotas Ef2Daniel MeloAún no hay calificaciones
- Problema 2Documento1 páginaProblema 2Daniel Melo100% (1)
- Nomenclatura Asesoria 24 10 2020 Anotaciones PDFDocumento11 páginasNomenclatura Asesoria 24 10 2020 Anotaciones PDFDaniel MeloAún no hay calificaciones
- Equilibrios Redox PDFDocumento1 páginaEquilibrios Redox PDFDaniel MeloAún no hay calificaciones
- Práctica 7. SDocumento10 páginasPráctica 7. SDaniel MeloAún no hay calificaciones
- Equilibrios Redox.s PDFDocumento1 páginaEquilibrios Redox.s PDFDaniel MeloAún no hay calificaciones
- Práctica 8.SDocumento7 páginasPráctica 8.SDaniel MeloAún no hay calificaciones
- Práctica 7 PDFDocumento8 páginasPráctica 7 PDFDaniel MeloAún no hay calificaciones
- Práctica 12 QG2Documento9 páginasPráctica 12 QG2Daniel MeloAún no hay calificaciones
- Equilibrios RedoxDocumento1 páginaEquilibrios RedoxDaniel MeloAún no hay calificaciones
- Clase Casos de La Entropia Parte 2Documento8 páginasClase Casos de La Entropia Parte 2Daniel MeloAún no hay calificaciones
- Clase 1era Ley de La TermodinámicaDocumento8 páginasClase 1era Ley de La TermodinámicaDaniel MeloAún no hay calificaciones
- Dependencia de H Con La TDocumento7 páginasDependencia de H Con La TDaniel MeloAún no hay calificaciones
- Predicción RedoxDocumento2 páginasPredicción RedoxDaniel MeloAún no hay calificaciones
- Práctica 10 QG2Documento5 páginasPráctica 10 QG2Daniel MeloAún no hay calificaciones
- Práctica 10 QG2Documento5 páginasPráctica 10 QG2Daniel MeloAún no hay calificaciones
- Producto Académico - 3 - SMRYDocumento5 páginasProducto Académico - 3 - SMRYJosue Luis100% (3)
- Términos QuímicosDocumento8 páginasTérminos QuímicosCyber ShalomAún no hay calificaciones
- Leyes de Las Combinaciones QuimicasDocumento17 páginasLeyes de Las Combinaciones Quimicasconstansa opazoAún no hay calificaciones
- Sesión 1 Eda 3 - Cyt 4°Documento7 páginasSesión 1 Eda 3 - Cyt 4°Fabrizio SilvaAún no hay calificaciones
- Macias Escamilla Cesar - Tema 2 - Analisis de Casos 1Documento6 páginasMacias Escamilla Cesar - Tema 2 - Analisis de Casos 1Cesar MaciasAún no hay calificaciones
- Vaso Topformado 10 Onz PP PlanosDocumento1 páginaVaso Topformado 10 Onz PP PlanosWESLEY FABIAN ANGULO ARIZAAún no hay calificaciones
- Celula AnimalDocumento1 páginaCelula AnimalBryan dennis villa100% (1)
- Quincena 7Documento29 páginasQuincena 7william BarreraAún no hay calificaciones
- AparatologiaDocumento9 páginasAparatologiaMarlin TavarezAún no hay calificaciones
- BIOLOGÍA Tema 1-2Documento6 páginasBIOLOGÍA Tema 1-2Marcos José Leiva OcañaAún no hay calificaciones
- 01 Evaluación Cuantitativa Contaminantes Químicos UEES DIANA TRELLESDocumento7 páginas01 Evaluación Cuantitativa Contaminantes Químicos UEES DIANA TRELLESDIANA CAROLINA TRELLES PILAY33% (3)
- Informe 1 QADocumento21 páginasInforme 1 QANicol QuinteroAún no hay calificaciones
- Amerlock 400 SdsDocumento18 páginasAmerlock 400 SdsAna Elizabeth Luna MtzAún no hay calificaciones
- HEMPADUR AvantGuard 550 1734U19830 Es-EsDocumento12 páginasHEMPADUR AvantGuard 550 1734U19830 Es-EsFredii LopezAún no hay calificaciones
- 1 A 9. PRAC TOXDocumento19 páginas1 A 9. PRAC TOXAnonymous GNiOkl3nsl100% (1)
- Comparto 'LMT - EA3 - Formato' Con UstedDocumento3 páginasComparto 'LMT - EA3 - Formato' Con UstedPerfecto Samuel Rodriguez BaezAún no hay calificaciones
- Descripcion de Items QuimicosDocumento4 páginasDescripcion de Items Quimicosayde.alconzAún no hay calificaciones
- Resistencia de MaterialesDocumento34 páginasResistencia de MaterialesLeidy JohanaAún no hay calificaciones
- Trabajo Toxico Metales PesadosDocumento26 páginasTrabajo Toxico Metales PesadosJunior BardalezAún no hay calificaciones
- Hds Kit Ez Fix Max Rev - 1 - MsdsDocumento65 páginasHds Kit Ez Fix Max Rev - 1 - MsdsAngelito Henry HPAún no hay calificaciones
- Sikaguard 62 - Recubrimiento Epóxico Xa AcabadoDocumento3 páginasSikaguard 62 - Recubrimiento Epóxico Xa AcabadoLoperacoAún no hay calificaciones
- Métodos de Separación de Mezclas.1Documento7 páginasMétodos de Separación de Mezclas.1Shirley BustamanteAún no hay calificaciones
- Hoja de Seguridad PolywaterDocumento6 páginasHoja de Seguridad PolywaterMaria MozoAún no hay calificaciones
- LAS ENZIMASfDocumento21 páginasLAS ENZIMASfAnshel MJAún no hay calificaciones
- Tabla Periodica Ejemplos y EjerciciosDocumento9 páginasTabla Periodica Ejemplos y EjerciciosMargarita Flores Torrejón0% (1)
- BARNIZ ElaboraciónDocumento3 páginasBARNIZ ElaboraciónAlix HernándezAún no hay calificaciones
- Ud Enf Iv AamDocumento24 páginasUd Enf Iv AamBRYAN CALDERON YARANGAAún no hay calificaciones
- Presentación TaninosDocumento9 páginasPresentación TaninosTamara Michelle Naula100% (1)
- SolucionesDocumento6 páginasSolucionesJose ricardo Mejia HernandezAún no hay calificaciones
- Tema 14. Proceso de Obtención de AceitesDocumento37 páginasTema 14. Proceso de Obtención de AceitesFdxExsfAún no hay calificaciones