0% encontró este documento útil (0 votos)
626 vistas5 páginasSolubilidad de Sales en Agua
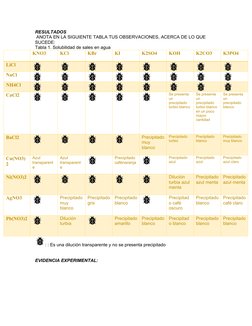
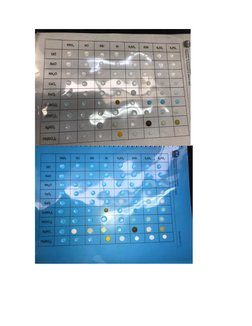
La estudiante realizó un experimento para determinar la solubilidad de varias sales en agua. Observó si había precipitados al mezclar sales de diferentes cationes con aniones comunes como nitratos, cloruros y sulfatos. Sus resultados mostraron que los nitratos son solubles mientras que los cloruros, bromuros y yoduros de plata, plomo y níquel no lo son. Determinó que los hidróxidos son poco solubles excepto los de bario y calcio.
Cargado por
Gab OCDerechos de autor
© © All Rights Reserved
Nos tomamos en serio los derechos de los contenidos. Si sospechas que se trata de tu contenido, reclámalo aquí.
Formatos disponibles
Descarga como DOCX, PDF, TXT o lee en línea desde Scribd
0% encontró este documento útil (0 votos)
626 vistas5 páginasSolubilidad de Sales en Agua
La estudiante realizó un experimento para determinar la solubilidad de varias sales en agua. Observó si había precipitados al mezclar sales de diferentes cationes con aniones comunes como nitratos, cloruros y sulfatos. Sus resultados mostraron que los nitratos son solubles mientras que los cloruros, bromuros y yoduros de plata, plomo y níquel no lo son. Determinó que los hidróxidos son poco solubles excepto los de bario y calcio.
Cargado por
Gab OCDerechos de autor
© © All Rights Reserved
Nos tomamos en serio los derechos de los contenidos. Si sospechas que se trata de tu contenido, reclámalo aquí.
Formatos disponibles
Descarga como DOCX, PDF, TXT o lee en línea desde Scribd