Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Calor Especifico2
Calor Especifico2
Cargado por
Jean Pool BenavidesCopyright:
Formatos disponibles
También podría gustarte
- Cadenas de Markov Parte 02 Utec 2013 - 2Documento45 páginasCadenas de Markov Parte 02 Utec 2013 - 2Connie GV100% (1)
- Equivalente en Agua de Un Calorímetro y Calor Específico de Un SólidoDocumento8 páginasEquivalente en Agua de Un Calorímetro y Calor Específico de Un SólidoTazann24Aún no hay calificaciones
- Equivalente en Agua de Un CalorimetroDocumento6 páginasEquivalente en Agua de Un CalorimetroMaria Gary100% (1)
- Informe de Calor EspecíficoDocumento8 páginasInforme de Calor EspecíficoOmar CaamañoAún no hay calificaciones
- Calor Especifico de Un SolidoDocumento7 páginasCalor Especifico de Un SolidoAlejandro Trujillo AcostaAún no hay calificaciones
- CALORIMETRIADocumento15 páginasCALORIMETRIADylan Vargas AguilarAún no hay calificaciones
- Informe Determinación de La Capacidad CaloríficaDocumento13 páginasInforme Determinación de La Capacidad CaloríficakaylaniariannequispecuizaAún no hay calificaciones
- Determinacion Del Calor Especifico de Un SolidoDocumento7 páginasDeterminacion Del Calor Especifico de Un SolidoAjimenez35Aún no hay calificaciones
- CALORIMETRIA LabDocumento15 páginasCALORIMETRIA LabRenancho BelAún no hay calificaciones
- CALORIMETRÍADocumento7 páginasCALORIMETRÍAlicanoxdAún no hay calificaciones
- Calor Específico de Los Sólidos 22Documento7 páginasCalor Específico de Los Sólidos 22Roger PrzAún no hay calificaciones
- Informe 8 Calor Específico UTPDocumento14 páginasInforme 8 Calor Específico UTPE. R. Reinoso NúñezAún no hay calificaciones
- Capacidad Calorífica Del CalorímetroDocumento16 páginasCapacidad Calorífica Del CalorímetroMary Cruz Meza CahuanaAún no hay calificaciones
- LABORATORIODocumento9 páginasLABORATORIOCELINA MALU FLORES ROMEROAún no hay calificaciones
- Equivalente Del Agua en El CalorimetroDocumento6 páginasEquivalente Del Agua en El Calorimetrodayimar01Aún no hay calificaciones
- Practica Calor Especifico de SolidosDocumento8 páginasPractica Calor Especifico de Solidosfer piñaAún no hay calificaciones
- Laboratorio 9 - DETERMINACION DEL CALOR ESPECÍFICO DE SÓLIDOSDocumento11 páginasLaboratorio 9 - DETERMINACION DEL CALOR ESPECÍFICO DE SÓLIDOSHarold Choque CanquiAún no hay calificaciones
- CALORIMETRÍADocumento10 páginasCALORIMETRÍAXimenaAún no hay calificaciones
- MARCO TEORICO CalorimetriaDocumento18 páginasMARCO TEORICO CalorimetriaKeithy CgAún no hay calificaciones
- Lab QMC 11Documento16 páginasLab QMC 11Stefany Michelle Huanca ChoqueAún no hay calificaciones
- Informe Equilibrio TermicoDocumento7 páginasInforme Equilibrio TermicoMaicol Hernández MárquezAún no hay calificaciones
- Informe - Equivalente en Agua CalorimetroDocumento6 páginasInforme - Equivalente en Agua CalorimetroLuis Eduardo100% (5)
- CalorímetroDocumento11 páginasCalorímetroEMERITA OJEDA CHOCLOTEAún no hay calificaciones
- USAT GUÍA N°05 - Calor Específico en Los Cuerpos SólidosDocumento20 páginasUSAT GUÍA N°05 - Calor Específico en Los Cuerpos SólidosAraceli PurihuamanAún no hay calificaciones
- CalorimetríaDocumento3 páginasCalorimetríaNas LizcanoAún no hay calificaciones
- Trabajo Final de CalorimetriaDocumento16 páginasTrabajo Final de CalorimetriaJeydi TelloAún no hay calificaciones
- CalorimetriaDocumento6 páginasCalorimetriaCarlos VarelaAún no hay calificaciones
- Equivalente en Agua de Un CalorimetroDocumento4 páginasEquivalente en Agua de Un CalorimetroJuan Fernando Arenas MercadoAún no hay calificaciones
- Calor Específico de Los SólidosDocumento7 páginasCalor Específico de Los SólidosDaniel ZhunioAún no hay calificaciones
- Capacidad Calorifica de Un SolidoDocumento8 páginasCapacidad Calorifica de Un SolidoEliiana ColónAún no hay calificaciones
- CalorimetriaDocumento22 páginasCalorimetriaXiomara Pinares CáceresAún no hay calificaciones
- Laboratorio!Documento19 páginasLaboratorio!Suyapa PonceAún no hay calificaciones
- Calor Especifico InformeDocumento5 páginasCalor Especifico InformeEsther MoreiraAún no hay calificaciones
- LABORATORIO EXPERIMENTAL #05. Calor Específico de Los Cuerpos SolidosDocumento17 páginasLABORATORIO EXPERIMENTAL #05. Calor Específico de Los Cuerpos SolidosCarlos Becerra salazarAún no hay calificaciones
- Practica de Laboratorio #06 CalorimetriaDocumento13 páginasPractica de Laboratorio #06 CalorimetriaSergio HoyosAún no hay calificaciones
- Citation 318311489Documento22 páginasCitation 318311489Carolei Capcha BedoyaAún no hay calificaciones
- Laboratorio de Termodinamica de Materiales N FinalDocumento14 páginasLaboratorio de Termodinamica de Materiales N FinalGianellaAponteAún no hay calificaciones
- Calor Especifico y Calor LatenteDocumento14 páginasCalor Especifico y Calor LatenteNadiaAún no hay calificaciones
- Temperatura y DilataciónDocumento9 páginasTemperatura y DilataciónPaulinaAún no hay calificaciones
- Practica 3Documento14 páginasPractica 3VICTOR IVAN ROCHA GONZALEZAún no hay calificaciones
- Clase 05-3 FisicaDocumento8 páginasClase 05-3 FisicaManuel ParreñoAún no hay calificaciones
- Laboratorio Fisica Ii CalorimetriaDocumento7 páginasLaboratorio Fisica Ii CalorimetriaCristian JuarezAún no hay calificaciones
- Laboratorio N°05 - Calor Específico en Los Cuerpos Sólidos - Docx - CompressedDocumento17 páginasLaboratorio N°05 - Calor Específico en Los Cuerpos Sólidos - Docx - CompressedAnderson Flores diasAún no hay calificaciones
- P2 - Eq 1 - QI-2IV23Documento12 páginasP2 - Eq 1 - QI-2IV23Andres Zayas AguilarAún no hay calificaciones
- Calor EspecificoDocumento15 páginasCalor Especificoluis antpnyAún no hay calificaciones
- Reporte CalorimetroDocumento9 páginasReporte CalorimetroEmmanuel SanchezAún no hay calificaciones
- Fisica II CalorimetriaDocumento9 páginasFisica II CalorimetriaManuel RuizAún no hay calificaciones
- Informe - Calor EspecíficoDocumento23 páginasInforme - Calor EspecíficoLili CastroAún no hay calificaciones
- Practica # 2. Determinación Del Calor Específico de Un SólidoDocumento5 páginasPractica # 2. Determinación Del Calor Específico de Un SólidoSantiago CazorlaAún no hay calificaciones
- Calorimetria TeoriaDocumento3 páginasCalorimetria TeoriaANDRES FELILPEAún no hay calificaciones
- Pre Informe 5.2Documento7 páginasPre Informe 5.2linda mendozaAún no hay calificaciones
- Estudio A) Del Equivalente en Agua y Del Calor Específico de SólidosDocumento10 páginasEstudio A) Del Equivalente en Agua y Del Calor Específico de SólidosAlfonsoJimenezAún no hay calificaciones
- INFORME-N10FISICA UnmsmDocumento16 páginasINFORME-N10FISICA UnmsmhollyAún no hay calificaciones
- CalorimetriaDocumento7 páginasCalorimetriaJose Enrique Briceño HurtadoAún no hay calificaciones
- Informe de Calor EspecificoDocumento8 páginasInforme de Calor EspecificoFredyson QuesadaAún no hay calificaciones
- Segura Cuvi - Laboratorio de Termodinámica - LAS CALORÍASDocumento24 páginasSegura Cuvi - Laboratorio de Termodinámica - LAS CALORÍASEdison GuarangoAún no hay calificaciones
- Experiencias sobre la propiedad temperaturaDe EverandExperiencias sobre la propiedad temperaturaAún no hay calificaciones
- Preparar y acondicionar elementos y máquinas de la planta química. QUIE0108: Operaciones básicas en planta químicaDe EverandPreparar y acondicionar elementos y máquinas de la planta química. QUIE0108: Operaciones básicas en planta químicaCalificación: 3 de 5 estrellas3/5 (2)
- UF1026 - Caracterización de procesos e instalaciones frigoríficasDe EverandUF1026 - Caracterización de procesos e instalaciones frigoríficasCalificación: 4 de 5 estrellas4/5 (1)
- IntroToControl PIDControllerVfDocumento43 páginasIntroToControl PIDControllerVfConnie GVAún no hay calificaciones
- Read A Plant - Fast - Español Corregido RevisadoDocumento17 páginasRead A Plant - Fast - Español Corregido RevisadoConnie GV0% (2)
- Read A Plant - Fast - Español Corregido RevisadoDocumento17 páginasRead A Plant - Fast - Español Corregido RevisadoConnie GV0% (2)
Calor Especifico2
Calor Especifico2
Cargado por
Jean Pool BenavidesTítulo original
Derechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
Calor Especifico2
Calor Especifico2
Cargado por
Jean Pool BenavidesCopyright:
Formatos disponibles
ESCUELA SUPERIOR POLITECNICA DEL LITORAL
Instituto de Ciencias FISICAS
RESUMEN:
En la práctica que se relata en este informe, se determinó el calor específico de un cuerpo
desconocido mediante el método de las mezclas.
El método de las mezclas consiste en el equilibrio y conservación de la energía, puesto que si se
mezclan dos cuerpos de distinta temperatura, se tendrá que el calor que cede un cuerpo es igual al
calor que gana el otro cuerpo.
Para llevar a cabo esto se usó las definiciones:
𝑄 = 𝑚𝑐 𝑇
Donde Q es la transferencia de energía en forma calorífica en el entre el sistema y su entorno u otro
sistema, m es la masa del sistema, c el calor especifico del material y T es el cambio de
temperatura.
La ley de la conservación de la energía para el calor:
N n º de cuerpos
i 1
Qi Q1 Q2 ......... Qn 0
Como en nuestro caso, 3 fueron los materiales en contacto, el calorímetro, el agua y el material
desconocido, aplicando ambas definiciones tenemos:
𝑄1 + 𝑄2 + 𝑄3 = 0
𝑚𝐻2 𝑂 𝑐𝐻2 𝑂 (𝑇𝐸 − 𝑇𝐴𝑚𝑏. ) + 𝑚𝐶𝑎𝑙 𝑐𝐴𝑙. (𝑇𝐸 − 𝑇𝐴𝑚𝑏. ) + 𝑐𝑠𝑢𝑠𝑡. 𝑚𝑠𝑢𝑠𝑡. (𝑇𝐸 − 𝑇𝑠𝑢𝑠𝑡. ) = 0
Despejando la ecuación hallamos el Calor específico del cuerpo desconocido.
(𝑚𝐻2 𝑂 𝑐𝐻2 𝑂 + 𝑚𝐶𝑎𝑙 𝑐𝐴𝑙. )(𝑇𝐸 − 𝑇𝐴𝑚𝑏. )
𝑐𝑠𝑢𝑠𝑡. =
𝑚𝑠𝑢𝑠𝑡. (𝑇𝑠𝑢𝑠𝑡. − 𝑇𝐸 )
Con esta ecuación, procedimos a calcular TE, TSUB, TAMB, y las debidas masas.
Para este experimento se utilizo una maquina que generaba vapor de agua, el cual se conducía hacia
el material (50gr), provocando su cambio de temperatura a una mucho mayor a la inicial.
Poco después se inserto en el calorímetro, 200gr de agua, se midió dicha temperatura la cual
corresponde al ambiente.
Luego se inserto rápidamente el material caliente en el calorímetro y se lo tapo, se espero a que
llegue al equilibrio térmico y se tomo dicha temperatura de equilibrio.
Con ya todos los valores calculados en el experimento, se procedió a usar la definición obtenida
anteriormente y se calculo el valor de calor específico del material desconocido, dando como
resultado: (0.102 ± 0.015) cal/g °C.
Como el valor es muy aproximado al calor especifico del HIERRO porque el teórico del mismo es
de 0.110 cal/g °C, decimos que el material desconocido es Hierro.
El porcentaje de error de la practica fue de 7.22%, dando a entender que la practica fue muy exacta.
DANIEL MARX PETROCHE SANCHEZ – LABORATORIO DE FISICA B Página 1
ESCUELA SUPERIOR POLITECNICA DEL LITORAL
Instituto de Ciencias FISICAS
INTRODUCCIÓN
El calor es la transferencia de energía térmica desde un sistema a otro de menor temperatura. La
energía térmica puede ser generada por reacciones químicas (como en la combustión), reacciones
nucleares (como en la fusión nuclear de los átomos de hidrógeno que tienen lugar en el interior
del Sol), disipación electromagnética (como en los hornos de microondas) o por disipación
mecánica (fricción). Su concepto está ligado al Principio Cero de la Termodinámica, según el cual
dos cuerpos en contacto intercambian energía hasta que su temperatura se equilibre.
La temperatura es una propiedad que tienen los cuerpos, para determinar si están o no en equilibrio
térmico con otros. Los instrumentos diseñados para medir la temperatura se los conoce con el
nombre de "termómetros*. Para elevar la temperatura de un cuerpo se le debe añadir calor y la
cantidad de calor (𝑄) requerida es proporcional a la masa m del cuerpo y a la elevación de la
temperatura ∆𝑇.
𝑄 𝑚
𝑄 (𝑇2 – 𝑇1 ) ó 𝑇
Para convertir ésta expresión en una ecuación, introducimos el valor de la constante c.
𝑄 = 𝑚𝑐 𝑇
Esta constante c, es una constante de proporcionalidad y se la denomina "CALOR ESPECÍFICO".
Se define como calor específico de una sustancia a la cantidad de calor necesaria para aumentar en
un grado Celsius la temperatura de 1 g de dicha sustancia.
Puesto que el calor es una forma de energía, se podría expresar esta energía en el sistema de
unidades métrico, y también en el sistema de unidades británico.
𝑐𝑎𝑙𝑜𝑟í𝑎𝑠
𝑆𝑖𝑠𝑡𝑒𝑚𝑎 𝑚é𝑡𝑟𝑖𝑐𝑜
𝑔. °𝐶
𝐵𝑡𝑢
𝑆𝑖𝑠𝑡𝑒𝑚𝑎 𝑏𝑟𝑖𝑡á𝑛𝑖𝑐𝑜
𝑙𝑖𝑏. ° 𝐹
Medición del calor específico de un sólido (Procedimiento Guía de Laboratorio de Física B)
Cuando dos o más cuerpos que tienen distintas temperaturas se ponen en contacto térmico se
observa que, al cabo de cierto tiempo, todos ellos tienen la misma temperatura.
Uno de los métodos para determinar el calor específico de un cuerpo, es el método de las mezclas.
Para ello pondremos dos cuerpos A y B en contacto térmico en el interior de un calorímetro aislado
térmicamente del medio exterior.
A B
DANIEL MARX PETROCHE SANCHEZ – LABORATORIO DE FISICA B Página 2
ESCUELA SUPERIOR POLITECNICA DEL LITORAL
Instituto de Ciencias FISICAS
Al no existir, o ser muy pequeño el intercambio de calor con el medio exterior a través de las
paredes del calorímetro, la cantidad de calor cedida por el cuerpo más caliente será igual a la
absorbida por el cuerpo de menor temperatura.
La ecuación correspondiente será:
Q1 Q2
O también:
Q1 Q2 0.
En donde se han tenido en cuenta el signo de las cantidades de calor, positivas cuando son
absorbidas y negativas cuando son cedidas por un cuerpo.
Cuando se ponen en contacto térmico varios cuerpos y solo puede intercambiar calor entre ellos y
no con el medio exterior, la ecuación correspondiente seria:
Generalizando, se tiene la ley de conservación de la energía para el calor:
En un sistema cerrado, la suma algebraica de las cantidades de calor intercambiadas entre los
cuerpos que forman un sistema es igual a cero.
N n º de cuerpos
i 1
Qi Q1 Q2 ......... Qn 0
Donde, el subíndice 1 hace referencia al cuerpo frío y el subíndice 2 al caliente. La temperatura en
el equilibrio será superior a e inferior a .
La anterior ecuación indica que si se conocen los valores del calor específico, midiendo
temperaturas y masas, es posible determinar cantidades de calor.
Para nuestro caso, como tenemos al calorímetro, al agua y a nuestro solido desconocido, planteamos
la ecuación de la ley de conservación de la energía para el calor.
𝑄1 + 𝑄2 + 𝑄3 = 0
𝑚𝐻2 𝑂 𝑐𝐻2 𝑂 (𝑇𝐸 − 𝑇𝐴𝑚𝑏. ) + 𝑚𝐶𝑎𝑙 𝑐𝐴𝑙. (𝑇𝐸 − 𝑇𝐴𝑚𝑏. ) + 𝑐𝑠𝑢𝑠𝑡. 𝑚𝑠𝑢𝑠𝑡. (𝑇𝐸 − 𝑇𝑠𝑢𝑠𝑡. ) = 0
Despejando la ecuación hallamos el Calor específico del cuerpo desconocido.
(𝑚𝐻2𝑂 𝑐𝐻2 𝑂 +𝑚𝐶𝑎𝑙 𝑐𝐴𝑙. )(𝑇𝐸 −𝑇𝐴𝑚𝑏. )
𝑐𝑠𝑢𝑠𝑡. = 𝑚𝑠𝑢𝑠𝑡. (𝑇𝑠𝑢𝑠𝑡. −𝑇𝐸 )
(ECUACIÓN 1)
DANIEL MARX PETROCHE SANCHEZ – LABORATORIO DE FISICA B Página 3
ESCUELA SUPERIOR POLITECNICA DEL LITORAL
Instituto de Ciencias FISICAS
El aparato que se utiliza para ello se denomina Calorímetro. Un
calorímetro es un sistema formado por dos vasos de paredes
plateadas, separados por una capa de aire. El vaso mayor lleva una
tapa de madera con dos perforaciones: una para insertar un
termómetro y otra para dejar pasar un agitador. El aire y la madera
son malos conductores del calor (buenos aislantes), mientras que la
radiación es reflejada por las paredes especulares de los dos
recipientes. Así queda térmicamente aislado el vaso interior y aquello
que en él se coloque. Este aparato es muy utilizado en el cálculo de
calores específicos de algunos materiales. El material a cierta
temperatura es introducido al calorímetro el cual contiene un líquido
calorimétrico, que es generalmente agua. Cuando un cuerpo a
diferente temperatura que la del agua se sumerge en ella y se cierra el
calorímetro, se produce una cesión de calor entre ambos hasta que se alcanza el equilibrio térmico.
El termómetro permite leer las temperaturas inicial y final del agua y con un ligero movimiento del
agitador se consigue una temperatura uniforme. Conociendo el calor específico y la masa del agua
utilizada, mediante la ecuación calorimétrica se puede determinar la cantidad de calor cedida o
absorbida por el agua.
Se utilizó un termómetro de mercurio para medir las diferentes temperaturas, fabricaron
aprovechando el fenómeno de la dilatación, por lo que se prefería el uso de materiales con elevado
coeficiente de dilatación, de modo que, al aumentar la temperatura, su estiramiento era fácilmente
visible. El metal base que se utilizaba en este tipo de termómetros ha sido el mercurio, encerrado en
un tubo de vidrio que incorporaba una escala graduada.
También un generador de vapor, el cual mediante un calentador, procede a elevar la temperatura
del liquido que en este caso fue agua, y al momento de llegar al punto de ebullición del mismo, pasa
el vapor por un conducto que va hasta donde está el cuerpo desconocido, elevando la temperatura
del mismo.
Para realizar la práctica correctamente colocamos todos los materiales de la manera en que la
expresa el grafico siguiente:
DANIEL MARX PETROCHE SANCHEZ – LABORATORIO DE FISICA B Página 4
ESCUELA SUPERIOR POLITECNICA DEL LITORAL
Instituto de Ciencias FISICAS
PROCEDIMIENTO EXPERIMENTAL
Una vez explicada las indicaciones de la profesora, se procedió a colocar los aparatos en la forma
indicada en la explicación anteriormente dada por la Catedrática.
Se midió 60 g de muestra del cuerpo desconocido, el cual se lo colocó en el receptor metálico de la
estructura usada.
Con el termómetro se midió la temperatura inicial para el agua y el calorímetro, T1.
Se calentó agua en el generador de vapor, haciendo que el vapor de agua pase a través de una
manguera, hacia el receptor metálico, esperamos a que alcance una temperatura cercana a 100℃.
Para realizar una buena práctica esperamos a una temperatura mayor a 85℃.
Mientras se calienta el generador de vapor, en el calorímetro se vertió 200𝑐𝑐 de agua medidos con
una probeta, lo cual equivale a 200𝑔.
Cuando la muestra ya está caliente, con ayuda del embudo se depositó la muestra en el calorímetro,
agitamos un poco el calorímetro y esperamos hasta que haya un equilibrio térmico.
Con ayuda del termómetro se midió la temperatura de equilibrio 𝑇𝐸 .
Con aquellos datos, se procedió a llenar la tabla a1).
Con dicha tabla llena y teniendo todo los valores necesarios, aplicamos la Ecuación 1 despejada
anteriormente y calculamos experimentalmente el calor latente de dicho solido desconocido.
Aplicamos los cálculos y con los resultados obtenidos calculamos el porcentaje de error de la
práctica.
RESULTADOS
a1) Complete la tabla de datos mostrada.
𝑨𝒈𝒖𝒂 𝑪𝒂𝒍𝒐𝒓í𝒎𝒆𝒕𝒓𝒐 𝑺𝒖𝒔𝒕𝒂𝒏𝒄𝒊𝒂
𝑴𝒂𝒔𝒂 [gr] 200.0 ± 0.1 200.0 ± 0.1 50.0 ± 0.1
𝒄𝒂𝒍 1.00 ± 0.01 0.20 ± 0.01 0.10 ± 0.01
𝑪𝒂𝒍𝒐𝒓 𝒆𝒔𝒑𝒆𝒄í𝒇𝒊𝒄𝒐 [ ]
𝒈𝒓 ∗ °𝑪
𝑻𝒆𝒎𝒑𝒆𝒓𝒂𝒕𝒖𝒓𝒂 𝒊𝒏𝒊𝒄𝒊𝒂𝒍 [°C] 24.0 ± 0.1 24.0 ± 0.1 96.0 ± 0.1
𝑻𝒆𝒎𝒑𝒆𝒓𝒂𝒕𝒖𝒓𝒂 𝒇𝒊𝒏𝒂𝒍 [°C] 27.5 ± 0.1 27.5 ± 0.1 27.5 ± 0.1
DANIEL MARX PETROCHE SANCHEZ – LABORATORIO DE FISICA B Página 5
ESCUELA SUPERIOR POLITECNICA DEL LITORAL
Instituto de Ciencias FISICAS
a2) Obtenga el calor específico de la muestra utilizada en esta práctica.
𝑄1 +𝑄2 + 𝑄3 = 0
𝑚𝑐 𝑐𝑐 (𝑇𝐸 −𝑇0 ) + 𝑚𝑠 𝑐𝑠 (𝑇𝐸 −𝑇0 ) + 𝑚𝐻2 𝑂 𝑐𝐻2 𝑂 (𝑇𝐸 −𝑇0 ) = 0
(𝑚𝑐 𝑐𝑐 + 𝑚𝐻2 𝑂 𝑐𝐻2 𝑂 )(𝑇𝐸 −𝑇0 )
𝑐𝑠 =
𝑚𝑠 (𝑇0 −𝑇𝐸 )
((200)(0.20) + (200)(1))(25.5 − 24.0)
𝑐𝑠 =
(50)(96 − 25.5)
𝑐𝑎𝑙𝑜𝑟𝑖𝑎𝑠
𝑐𝑠 = 0.102
𝑔℃
𝑎 = (𝑚1 𝑐1 + 𝑚2 𝑐2 )
∆𝑎 = 𝛿(𝑚1 𝑐1 ) + 𝛿(𝑚2 𝑐2 )
∆𝑎 = 𝑚1 𝛿𝑐1 + 𝑐1 𝛿𝑚1 + 𝑚2 𝛿𝑐2 + 𝑐2 𝛿𝑚2
∆𝑎 = 200(0.01) + 1(0.1) + 200(0.01) + 0.20(0.1)
∆𝑎 = 4.12
𝑏 = (𝑇𝐸 − 𝑇1 )
∆𝑏 = 0.2
𝑐 = 𝑚3 (𝑇3 − 𝑇𝐸 )
∆𝑐 = 𝑚3 𝛿(𝑇3 − 𝑇𝐸 ) + (𝑇3 − 𝑇𝐸 )𝛿𝑚3
∆𝑐 = 50(0.2) + 70.5(0.1)
∆𝑐 = 17.05
𝑑 = 𝑎𝑏
𝑎 = (𝑚1 𝑐1 + 𝑚2 𝑐2 ) = ((200)(0.20) + (200)(1)) = 240
𝑏 = (𝑇𝐸 − 𝑇1 ) = (25.5 − 24.0) = 1.5
∆𝑑 = 𝑎∆𝑏 + 𝑏∆𝑎 = 240(0.2) + 1.5(4.12)
DANIEL MARX PETROCHE SANCHEZ – LABORATORIO DE FISICA B Página 6
ESCUELA SUPERIOR POLITECNICA DEL LITORAL
Instituto de Ciencias FISICAS
∆𝑑 = 54.18
𝑑
𝑐3 =
𝑐
𝑐 = 𝑚3 (𝑇3 − 𝑇𝐸 ) = (50)(96 − 25.5) = 3525
𝑑 = 𝑎𝑏 = 240 ∗ 1.5 = 360
1 𝑑
𝛿𝑐3 = 𝛿𝑑 + 2 𝛿𝑐
𝑐 𝑐
3525(54.18) + 360(17.05)
𝛿𝑐𝑠 =
35252
𝛿𝑐𝑠 = 0.015
𝑐𝑎𝑙𝑜𝑟𝑖𝑎𝑠
𝑐𝑠 = (0.102 ± 0.015)
𝑔℃
b) Encuentre la diferencia relativa entre el valor teórico y el valor experimental del calor
específico de la muestra. Utilice la diferencia % = (𝐓𝐞𝐨 − 𝐄𝐱𝐩)(𝟏𝟎𝟎%)/𝐓𝐞𝐨
𝑉𝑇 − 𝑉𝐸
%=| | × 100%
𝑉𝑇
0.110 − 0.102
%=| | × 100%
0.110
% = 7.22%
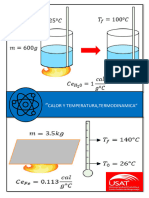
GRÁFICOS:
Ilustración 1.-Paso de la sustancia hacia el calorímetro. Ilustración 2.- Medición de temperatura
de equilibrio.
DANIEL MARX PETROCHE SANCHEZ – LABORATORIO DE FISICA B Página 7
ESCUELA SUPERIOR POLITECNICA DEL LITORAL
Instituto de Ciencias FISICAS
DISCUSIÓN
Tabla de datos: cada uno de los datos son indispensables para obtener un buen resultados, al
momento de tomar los datos tuvimos que hacer nuestro mejor esfuerzo para coger un dato confiable
es decir con un margen de error muy pequeño.
Cálculos: Aplicamos la formula que nos dan para calcular el calor específico y comprobamos que
verdaderamente se obtiene un valor aproximado al que nos pedían encontrar lo que nos da a
entender que todos los cálculos hechos fueron los correctos.
Tabla de resultados: Una vez con todos los cálculos realizados junto con el cálculo de sus errores
procedimos a completar la tabla. Con el valor obtenido del calor específico de la muestra podemos
concluir de que el material con el que estábamos experimentando era el hierro, puesto que este valor
experimental se acerca mucho al valor teórico de hierro (0,110 𝑐𝑎𝑙/ 𝑔 °𝑐)
Errores: Cada uno de los errores obtenidos es el correcto, la aplicación de la fórmula para calcular
el error fue indispensable. Como siempre debemos recordar que una medición por nunca puede
anotarse, si que lleve su respectivo error ya sea que la medición sea directa o indirecta.
ANÁLISIS
a) De acuerdo a los resultados obtenidos, ¿de qué material está hecha la muestra?
Explique.
De HIERRO porque el teórico es de 0.110 𝑐𝑎𝑙/𝑔 °𝑐 y experimentalmente obtuvimos
0.102𝑐𝑎𝑙/𝑔 °𝑐.
c) Tomando en cuenta el aparato que utilizó, señale ¿por qué no se obtuvo una
concordancia exacta en la pregunta anterior?
Mala observación al momento de medir los cambios de temperatura, o cambios de
temperatura que se pudieron dar durante la práctica. También el cambio del receptor
metálico al calorímetro puede afectar mucho haciendo dispar un poco de calor en el
ambiente.
d) ¿Por qué el agua y el hielo tienen diferentes calores específicos?
Es debido a las diferencias de estado en que se encuentran, es decir diferente composición
molecular, debido a la presencia de puentes de H, las densidades de los mismos cambian,
haciendo que el hielo necesite menos energía para elevar la temperatura en 1 grado Celsius
que la que se necesita para el agua, por lo tanto tienen diferentes calores específicos.
e) ¿Por qué se utilizan vasos de poliestireno para servir café? Explique.
Porque el poliestireno tiene un alto calor específico, y esto hace que se necesite más calor
para la transferencia de calor, por lo tanto este material mantiene la mayor parte del calor
dentro del vaso.
DANIEL MARX PETROCHE SANCHEZ – LABORATORIO DE FISICA B Página 8
ESCUELA SUPERIOR POLITECNICA DEL LITORAL
Instituto de Ciencias FISICAS
CONCLUSIÓN
En base al desarrollo de la práctica y al resultado de la misma. podemos concluir lo
siguiente:
Se determinó el calor específico de un cuerpo desconocido mediante el método de
las mezclas.
Se aplicó la Ley de equilibrio Térmico a sistemas termodinámicos.
Se comprobó el principio de la conservación de la energía, el cual establece que la
energía total inicial de un sistema es igual a la energía final total del mismo sistema.
Se definió al calor como energía, que es transferida de un sistema a otro, debido a
que se encuentran a diferentes niveles de temperatura.
Mediante el cálculo, se dedujo que el calor específico sirve como una constante para
obtener una igualación entre la cantidad de calor, la masa y la variación de
temperatura.
Se observó que al poner los dos cuerpos en contacto, el que se encuentra a mayor
temperatura transfiere calor al otro hasta que se logra el equilibrio térmico.
Mediante el cálculo, se concluyó que el valor experimental obtenido en la presente
práctica es de (0.102 ± 0.015) cal/g °C.
Se reconoció al material desconocido como HIERRO porque el teórico del mismo
es de 0.110 cal/g °C y experimentalmente obtuvimos 0.102cal/g °C.
El porcentaje de error de la practica fue de 7.22%, con esto concluimos que la
practica fue un éxito, ya que logramos porcentajes muy bajos, no exactos pero muy
aproximados
REFERENCIAS BIBLIOGRAFICAS
Guía de Laboratorio de Física B. ICF - ESPOL. Revisión II
http://es.wikipedia.org/wiki/Calor_específico
http://es.wikipedia.org/wiki/Aluminio
http://es.wikipedia.org/wiki/Hierro
http://es.wikipedia.org/wiki/Agua
http://es.wikipedia.org/wiki/Poliestireno
http://es.wikipedia.org/wiki/Calor%C3%ADmetro
http://es.wikipedia.org/wiki/Term%C3%B3metro
http://es.wikipedia.org/wiki/Generador_de_vapor
DANIEL MARX PETROCHE SANCHEZ – LABORATORIO DE FISICA B Página 9
También podría gustarte
- Cadenas de Markov Parte 02 Utec 2013 - 2Documento45 páginasCadenas de Markov Parte 02 Utec 2013 - 2Connie GV100% (1)
- Equivalente en Agua de Un Calorímetro y Calor Específico de Un SólidoDocumento8 páginasEquivalente en Agua de Un Calorímetro y Calor Específico de Un SólidoTazann24Aún no hay calificaciones
- Equivalente en Agua de Un CalorimetroDocumento6 páginasEquivalente en Agua de Un CalorimetroMaria Gary100% (1)
- Informe de Calor EspecíficoDocumento8 páginasInforme de Calor EspecíficoOmar CaamañoAún no hay calificaciones
- Calor Especifico de Un SolidoDocumento7 páginasCalor Especifico de Un SolidoAlejandro Trujillo AcostaAún no hay calificaciones
- CALORIMETRIADocumento15 páginasCALORIMETRIADylan Vargas AguilarAún no hay calificaciones
- Informe Determinación de La Capacidad CaloríficaDocumento13 páginasInforme Determinación de La Capacidad CaloríficakaylaniariannequispecuizaAún no hay calificaciones
- Determinacion Del Calor Especifico de Un SolidoDocumento7 páginasDeterminacion Del Calor Especifico de Un SolidoAjimenez35Aún no hay calificaciones
- CALORIMETRIA LabDocumento15 páginasCALORIMETRIA LabRenancho BelAún no hay calificaciones
- CALORIMETRÍADocumento7 páginasCALORIMETRÍAlicanoxdAún no hay calificaciones
- Calor Específico de Los Sólidos 22Documento7 páginasCalor Específico de Los Sólidos 22Roger PrzAún no hay calificaciones
- Informe 8 Calor Específico UTPDocumento14 páginasInforme 8 Calor Específico UTPE. R. Reinoso NúñezAún no hay calificaciones
- Capacidad Calorífica Del CalorímetroDocumento16 páginasCapacidad Calorífica Del CalorímetroMary Cruz Meza CahuanaAún no hay calificaciones
- LABORATORIODocumento9 páginasLABORATORIOCELINA MALU FLORES ROMEROAún no hay calificaciones
- Equivalente Del Agua en El CalorimetroDocumento6 páginasEquivalente Del Agua en El Calorimetrodayimar01Aún no hay calificaciones
- Practica Calor Especifico de SolidosDocumento8 páginasPractica Calor Especifico de Solidosfer piñaAún no hay calificaciones
- Laboratorio 9 - DETERMINACION DEL CALOR ESPECÍFICO DE SÓLIDOSDocumento11 páginasLaboratorio 9 - DETERMINACION DEL CALOR ESPECÍFICO DE SÓLIDOSHarold Choque CanquiAún no hay calificaciones
- CALORIMETRÍADocumento10 páginasCALORIMETRÍAXimenaAún no hay calificaciones
- MARCO TEORICO CalorimetriaDocumento18 páginasMARCO TEORICO CalorimetriaKeithy CgAún no hay calificaciones
- Lab QMC 11Documento16 páginasLab QMC 11Stefany Michelle Huanca ChoqueAún no hay calificaciones
- Informe Equilibrio TermicoDocumento7 páginasInforme Equilibrio TermicoMaicol Hernández MárquezAún no hay calificaciones
- Informe - Equivalente en Agua CalorimetroDocumento6 páginasInforme - Equivalente en Agua CalorimetroLuis Eduardo100% (5)
- CalorímetroDocumento11 páginasCalorímetroEMERITA OJEDA CHOCLOTEAún no hay calificaciones
- USAT GUÍA N°05 - Calor Específico en Los Cuerpos SólidosDocumento20 páginasUSAT GUÍA N°05 - Calor Específico en Los Cuerpos SólidosAraceli PurihuamanAún no hay calificaciones
- CalorimetríaDocumento3 páginasCalorimetríaNas LizcanoAún no hay calificaciones
- Trabajo Final de CalorimetriaDocumento16 páginasTrabajo Final de CalorimetriaJeydi TelloAún no hay calificaciones
- CalorimetriaDocumento6 páginasCalorimetriaCarlos VarelaAún no hay calificaciones
- Equivalente en Agua de Un CalorimetroDocumento4 páginasEquivalente en Agua de Un CalorimetroJuan Fernando Arenas MercadoAún no hay calificaciones
- Calor Específico de Los SólidosDocumento7 páginasCalor Específico de Los SólidosDaniel ZhunioAún no hay calificaciones
- Capacidad Calorifica de Un SolidoDocumento8 páginasCapacidad Calorifica de Un SolidoEliiana ColónAún no hay calificaciones
- CalorimetriaDocumento22 páginasCalorimetriaXiomara Pinares CáceresAún no hay calificaciones
- Laboratorio!Documento19 páginasLaboratorio!Suyapa PonceAún no hay calificaciones
- Calor Especifico InformeDocumento5 páginasCalor Especifico InformeEsther MoreiraAún no hay calificaciones
- LABORATORIO EXPERIMENTAL #05. Calor Específico de Los Cuerpos SolidosDocumento17 páginasLABORATORIO EXPERIMENTAL #05. Calor Específico de Los Cuerpos SolidosCarlos Becerra salazarAún no hay calificaciones
- Practica de Laboratorio #06 CalorimetriaDocumento13 páginasPractica de Laboratorio #06 CalorimetriaSergio HoyosAún no hay calificaciones
- Citation 318311489Documento22 páginasCitation 318311489Carolei Capcha BedoyaAún no hay calificaciones
- Laboratorio de Termodinamica de Materiales N FinalDocumento14 páginasLaboratorio de Termodinamica de Materiales N FinalGianellaAponteAún no hay calificaciones
- Calor Especifico y Calor LatenteDocumento14 páginasCalor Especifico y Calor LatenteNadiaAún no hay calificaciones
- Temperatura y DilataciónDocumento9 páginasTemperatura y DilataciónPaulinaAún no hay calificaciones
- Practica 3Documento14 páginasPractica 3VICTOR IVAN ROCHA GONZALEZAún no hay calificaciones
- Clase 05-3 FisicaDocumento8 páginasClase 05-3 FisicaManuel ParreñoAún no hay calificaciones
- Laboratorio Fisica Ii CalorimetriaDocumento7 páginasLaboratorio Fisica Ii CalorimetriaCristian JuarezAún no hay calificaciones
- Laboratorio N°05 - Calor Específico en Los Cuerpos Sólidos - Docx - CompressedDocumento17 páginasLaboratorio N°05 - Calor Específico en Los Cuerpos Sólidos - Docx - CompressedAnderson Flores diasAún no hay calificaciones
- P2 - Eq 1 - QI-2IV23Documento12 páginasP2 - Eq 1 - QI-2IV23Andres Zayas AguilarAún no hay calificaciones
- Calor EspecificoDocumento15 páginasCalor Especificoluis antpnyAún no hay calificaciones
- Reporte CalorimetroDocumento9 páginasReporte CalorimetroEmmanuel SanchezAún no hay calificaciones
- Fisica II CalorimetriaDocumento9 páginasFisica II CalorimetriaManuel RuizAún no hay calificaciones
- Informe - Calor EspecíficoDocumento23 páginasInforme - Calor EspecíficoLili CastroAún no hay calificaciones
- Practica # 2. Determinación Del Calor Específico de Un SólidoDocumento5 páginasPractica # 2. Determinación Del Calor Específico de Un SólidoSantiago CazorlaAún no hay calificaciones
- Calorimetria TeoriaDocumento3 páginasCalorimetria TeoriaANDRES FELILPEAún no hay calificaciones
- Pre Informe 5.2Documento7 páginasPre Informe 5.2linda mendozaAún no hay calificaciones
- Estudio A) Del Equivalente en Agua y Del Calor Específico de SólidosDocumento10 páginasEstudio A) Del Equivalente en Agua y Del Calor Específico de SólidosAlfonsoJimenezAún no hay calificaciones
- INFORME-N10FISICA UnmsmDocumento16 páginasINFORME-N10FISICA UnmsmhollyAún no hay calificaciones
- CalorimetriaDocumento7 páginasCalorimetriaJose Enrique Briceño HurtadoAún no hay calificaciones
- Informe de Calor EspecificoDocumento8 páginasInforme de Calor EspecificoFredyson QuesadaAún no hay calificaciones
- Segura Cuvi - Laboratorio de Termodinámica - LAS CALORÍASDocumento24 páginasSegura Cuvi - Laboratorio de Termodinámica - LAS CALORÍASEdison GuarangoAún no hay calificaciones
- Experiencias sobre la propiedad temperaturaDe EverandExperiencias sobre la propiedad temperaturaAún no hay calificaciones
- Preparar y acondicionar elementos y máquinas de la planta química. QUIE0108: Operaciones básicas en planta químicaDe EverandPreparar y acondicionar elementos y máquinas de la planta química. QUIE0108: Operaciones básicas en planta químicaCalificación: 3 de 5 estrellas3/5 (2)
- UF1026 - Caracterización de procesos e instalaciones frigoríficasDe EverandUF1026 - Caracterización de procesos e instalaciones frigoríficasCalificación: 4 de 5 estrellas4/5 (1)
- IntroToControl PIDControllerVfDocumento43 páginasIntroToControl PIDControllerVfConnie GVAún no hay calificaciones
- Read A Plant - Fast - Español Corregido RevisadoDocumento17 páginasRead A Plant - Fast - Español Corregido RevisadoConnie GV0% (2)
- Read A Plant - Fast - Español Corregido RevisadoDocumento17 páginasRead A Plant - Fast - Español Corregido RevisadoConnie GV0% (2)