Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Lab 7 PDF
Cargado por
MargaritaSegoviaTítulo original
Derechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
Lab 7 PDF
Cargado por
MargaritaSegoviaCopyright:
Formatos disponibles
CINTICA DE LAS REACCIONES
LABORATORIO 7
CINTICA DE LAS REACCIONES
I.
OBJETIVOS
Determinar el orden de la reaccin del ion yoduro (I-) con el ion
peroxodisulfato (S2O82-) con respecto a cada reactivo.
Determinar la ley de velocidad para la reaccin estudiada.
Determinar el efecto de la temperatura y catalizadores en la reaccin
estudiada.
II. FUNDAMENTO TERICO
La velocidad y los mecanismos de las reacciones qumicas constituyen el
campo de estudio de la cintica qumica o cintica de las reacciones.
Realizar un estudio cintico es determinar el orden de la reaccin, la ecuacin
cintica y la energa de activacin; adems implica establecer el mecanismo
molecular de la transformacin de reactivos en productos.
Experimentalmente se ha encontrado que la velocidad de una reaccin
depende de la temperatura, naturaleza y concentracin de las especies
implicadas. La presencia de un catalizador puede aumentar la velocidad
considerablemente.
Mediante el anlisis de la velocidad de una reaccin y de su dependencia
respecto a los factores enunciados, se puede aprender mucho sobre las etapas
por las que los reaccionantes se transforman en productos.
Reacciones con Yodo
El yodo es soluble en agua en la proporcin de 0,001 moles por litro a la
temperatura ambiente. Sin embargo en presencia de yoduros solubles como el
yoduro potsico, aumenta la solubilidad por formacin del complejo triyoduro:
I2 + I I3
(1)
El ion triyoduro es el ion principal en las disoluciones de yodo pero por
conveniencia en la representacin de las ecuaciones se escribir normalmente
I2 en lugar del complejo I3-.
El yodo se puede usar como valorante en dos tcnicas llamadas:
a. Yodimetra: es un mtodo directo en el que se utiliza una disolucin
patrn de yodo para valorar reductores fuertes, normalmente en disolucin
neutra o dbilmente cida.
MANUAL DE LABORATORIO 2014
QUMICA II
CINTICA DE LAS REACCIONES
LABORATORIO 7
b. Yodometra es un mtodo indirecto en que los oxidantes se determinan
hacindolos reaccionar con un exceso de yoduro; el yodo liberado se valora
en disolucin dbilmente cida con un reductor patrn, como tiosulfato
sdico.
Estos mtodos son posibles dado que el potencial normal del sistema:
I3 + 2e-
3I
es E
Entonces, los oxidantes fuertes oxidan el I
= + 0,536 V
a I3 y los reductores fuertes
reducen el I3 a I .
Los mtodos en los que interviene el yodo tienen facilidad y sensibilidad para
detectar el punto final.
En el mtodo directo, el yodo es autoindicador; una gotita de yodo 0,1 N le da
un color amarillo a 200 mL de agua.
En los mtodos indirectos se usa el almidn como indicador; cuando se
calientan en agua grnulos de almidn, estos se rompen y originan productos
de descomposicin, entre ellos -amilosa que da lugar a un color azul intenso
con yodo en presencia de yoduro. El material coloreado es un complejo de
adsorcin de yodo, -amilosa y yoduro. El almidn debe prepararse el mismo
da de uso porque se descompone y ya no es sensible al yodo.
Una reaccin reloj es aquella en la que ocurre un cambio de color dramtico
a un tiempo, determinado por la concentracin y la temperatura. La ms
famosa es la reaccin reloj del yodo que se produce entre el ion yoduro y el
oxidante fuerte peroxodisulfato. La reaccin completa en estudio es:
2I
( ac )
+ S2O8
> I2
( ac )
( ac )
+ 2 SO 4
2
( ac )
(2)
Cuando se forma el I2, se consume con una cantidad fija de tiosulfato, S2O32-,
adicionado:
I2 ( ac ) + 2 S 2 O 3 2 ( ac ) > 2 I ( ac ) + S 4 O 6 2 ( ac )
Una vez que se consume el S 2 O 3
(3)
, el exceso de I2 forma un producto azul-
negro con el almidn preparado y presente en la solucin. Debe notar que la
velocidad de aparicin de I2 , en la ecuacin (2), es igual a la mitad de la
velocidad de desaparicin del S 2 O 3
, en la ecuacin (3).
En el estudio cintico se tomar como tiempo cero el momento de la mezcla, y
como punto final la aparicin de color azul.
MANUAL DE LABORATORIO 2014
QUMICA II
CINTICA DE LAS REACCIONES
LABORATORIO 7
III. PROCEDIMIENTO EXPERIMENTAL
Experimento No 1: Determinacin el orden de la reaccin de
oxidacin del ion yoduro cuando interacta con el in
peroxodisulfato (temperatura constante)
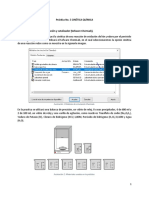
1. En cada uno de cinco tubos coloque la cantidad de peroxodisulfato
potsico 0,1 M que indica la tabla 1.
2. En otro tubo, coloque yoduro potsico 0,1 M, la cantidad que se indica en
la tabla 1; previamente adicione 5 mL del indicador (almidn 2 %) +
tiosulfato de sodio 0,0001 M que los sacar de un frasco donde ya se
encuentran mezclados y adems agregue H2O. Proceda en las cantidades
segn la tabla 1.
3. Antes de mezclar el tubo de peroxodisulfato y el tubo del yoduro (con el
almidn, el tiosulfato y el H2O) coloque ambos tubos en agua a
temperatura ambiente por 5 minutos para lograr homogenizar la
temperatura.
4. En el tiempo de inicio (tiempo cero) mezcle rpidamente ambas soluciones
y homogenice la mezcla. Tome el tiempo cronomtricamente hasta la
aparicin del color azul.
Tabla 1
N de
Tubo
01
02
03
04
05
K2S2O8
0,1 M (mL)
2,5
2,5
1,5
2,5
2,5
KI 0,1 M
(mL)
2,5
2,0
2,0
1,0
0,5
Almidn +
tiosulfato (mL)
5
5
5
5
5
H2O
(mL)
0,0
0,5
1,5
1,5
2,0
Tiempo
Experimento No 2: Efecto de la temperatura sobre la velocidad de
reaccin
1. Del experimento anterior escoja la mezcla que haya reportado menor valor
de velocidad de reaccin.
2. Seguir el procedimiento anterior. Pero antes de proceder a mezclar el
contenido de los dos tubos, calentarlos en bao mara por espacio de 5
minutos.
Experimento No 3: Efecto de los catalizadores sobre la velocidad de
reaccin
1. Del experimento N 1 escoja la mezcla que haya reportado menor valor de
velocidad de reaccin y prepare dos muestras de peroxodisulfato potsico
de la misma concentracin en dos tubos a los que marcar como: A, B.
2. En el tubo A agregue, una gota de nitrato de cobre 1M.
3. En el tubo B agregue una gota de nitrato de plata 1M.
4. Proceda a mezclar con KI + almidn + tiosulfato y agua igual que en el
experimento 1.
5. Tomar tiempos de reaccin y observe si alguna muestra ha sido catalizada.
MANUAL DE LABORATORIO 2014
QUMICA II
CINTICA DE LAS REACCIONES
LABORATORIO 7
IV. CLCULO
1. Para la Ley de Velocidad considerar la expresin general como:
Velocidad = k [ I ] [S 2 O 8
2. Calcule la concentracin inicial de los reaccionantes considerando los
mililitros tomados de cada reactivo y el volumen total de la mezcla que es
10 mL.
3. Calcule la concentracin del tiosulfato, S 2 O 3
4. Calcule la velocidad de desaparicin del tiosulfato considerando que es el
doble de la velocidad de aparicin del yodo.
MANUAL DE LABORATORIO 2014
QUMICA II
También podría gustarte
- 13-Cinética de La Reacción Persulfato-YoduroDocumento10 páginas13-Cinética de La Reacción Persulfato-YoduroBrayanPinchaoRevelo100% (1)
- Fico Informe 8Documento20 páginasFico Informe 8Dalton Einsten Darwin100% (1)
- Previo 2. Fico VDocumento8 páginasPrevio 2. Fico VEdwin TapiaAún no hay calificaciones
- Experimento Del Reloj de Yodo para Aplicar Los Conocimientos de Equilibrio QuímicoDocumento13 páginasExperimento Del Reloj de Yodo para Aplicar Los Conocimientos de Equilibrio Químicoteresa sanabria0% (2)
- Presentacion 2: Cinetica QuimicaDocumento13 páginasPresentacion 2: Cinetica Quimicaquimica100% (1)
- Laboratorio 02Documento3 páginasLaboratorio 02Jhon Alex Gonzales QuispeAún no hay calificaciones
- Práctica de Laboratorio #3Documento4 páginasPráctica de Laboratorio #3miguel EncarnacionAún no hay calificaciones
- Trabajo Práctico #08, Velocidad de ReacciónDocumento9 páginasTrabajo Práctico #08, Velocidad de ReacciónMauro GardinettiAún no hay calificaciones
- UntitledDocumento10 páginasUntitledCarlos BrandaoAún no hay calificaciones
- Subtema 2.3 Practica de Metodos de Velocidad de Reaccion 2Documento9 páginasSubtema 2.3 Practica de Metodos de Velocidad de Reaccion 2Adán Fonseca HernandezAún no hay calificaciones
- Cine TicaDocumento4 páginasCine TicaGina MLAún no hay calificaciones
- Estudio cinético de la reacción de oxidación de yoduro con persulfatoDocumento12 páginasEstudio cinético de la reacción de oxidación de yoduro con persulfatoMartin Nanga0% (1)
- Informe#2Documento10 páginasInforme#2JamesAún no hay calificaciones
- Experimento RelojDocumento15 páginasExperimento RelojLizz Frizz RockAún no hay calificaciones
- Química General Practica 7Documento16 páginasQuímica General Practica 7mildrey gonzalezAún no hay calificaciones
- Laboratorio 4 QiiDocumento4 páginasLaboratorio 4 QiiStephania OcampoAún no hay calificaciones
- Laboratorio 10Documento5 páginasLaboratorio 10Piero RojasAún no hay calificaciones
- Oxidacion de I Con PeroxidoDocumento10 páginasOxidacion de I Con PeroxidoInés BeltránAún no hay calificaciones
- Practica 1- Reloj Oscilante- Cobix LópezDocumento2 páginasPractica 1- Reloj Oscilante- Cobix Lópezrosapolito879Aún no hay calificaciones
- Informe de PrácticasDocumento12 páginasInforme de PrácticasMedalyth RamirezAún no hay calificaciones
- Reacciones de Oxido - ReduccionDocumento12 páginasReacciones de Oxido - ReduccionLina Torres0% (1)
- PRACTICA #CineticaDocumento4 páginasPRACTICA #CineticaCarmely Maronn0% (1)
- Oxidacion Del Yoduro Con Peroxido de HidrogenoDocumento8 páginasOxidacion Del Yoduro Con Peroxido de HidrogenoAna Claudia Caballero Fiorilo50% (2)
- 06 Cinetica RecreativaDocumento14 páginas06 Cinetica RecreativasleydermpAún no hay calificaciones
- Pre Informe 2Documento10 páginasPre Informe 2DanielAún no hay calificaciones
- Ejercicios Quimica UndécimoDocumento8 páginasEjercicios Quimica Undécimonaomy juanita vanegas garzonAún no hay calificaciones
- INFORME 4 - Práctica 4 CORREGIDODocumento16 páginasINFORME 4 - Práctica 4 CORREGIDOsofia santamaria medinaAún no hay calificaciones
- Ion Yoduro PersulfatoDocumento3 páginasIon Yoduro PersulfatoAlexa BedoyaAún no hay calificaciones
- Determinación Del Contenido de Hipoclorito Sódico en Un Producto Comercial y El Contenido de Yodo en Un Antiséptico BucalDocumento10 páginasDeterminación Del Contenido de Hipoclorito Sódico en Un Producto Comercial y El Contenido de Yodo en Un Antiséptico BucalLuna Violeta Chamorro PortillaAún no hay calificaciones
- Practica N°2 Evaluación de La Cinética de Una Reacción Química (Oxidación de Una Solución Neutra de Yoduro Por Persulfato)Documento11 páginasPractica N°2 Evaluación de La Cinética de Una Reacción Química (Oxidación de Una Solución Neutra de Yoduro Por Persulfato)-Dz' ‼ Antequera-Aún no hay calificaciones
- Laboratorio 6Documento5 páginasLaboratorio 6Gustavo ChoqueAún no hay calificaciones
- Informe-2-Oxidación Del Yoduro Con PersulfatoDocumento14 páginasInforme-2-Oxidación Del Yoduro Con PersulfatoPameCMAún no hay calificaciones
- 03 - Tablas Termodinamica - Van WylenDocumento12 páginas03 - Tablas Termodinamica - Van WylenDiego Medrano Hidalgo100% (1)
- Estandarización de Una Solución de Tiosulfato de Sodio y Análisis de Hipoclorito de Sodio en Blanqueador Comercial Por Método Yodométrico.Documento10 páginasEstandarización de Una Solución de Tiosulfato de Sodio y Análisis de Hipoclorito de Sodio en Blanqueador Comercial Por Método Yodométrico.Ivana Llinás Morales50% (2)
- Index 5Documento11 páginasIndex 5Claudia GonzalesAún no hay calificaciones
- Reaccion de Yoduro de PotasioDocumento13 páginasReaccion de Yoduro de Potasiojorge11daAún no hay calificaciones
- CINÉTICADocumento10 páginasCINÉTICACarlos Sebas Rea CallisayaAún no hay calificaciones
- EJERCICIOS y Laboratorio DE CINÉTICA QUÍMICADocumento2 páginasEJERCICIOS y Laboratorio DE CINÉTICA QUÍMICAdianacaro2889100% (2)
- Cinética química: Efecto concentración y catalizadorDocumento18 páginasCinética química: Efecto concentración y catalizadorAlejandro TorresAún no hay calificaciones
- Informe de Laboratorio N.3Documento8 páginasInforme de Laboratorio N.3melanie NaranjoAún no hay calificaciones
- Informe Lab 7 8 9Documento17 páginasInforme Lab 7 8 9Daniel Alejandro Gutierrez Gonzalez75% (4)
- Práctica 5Documento9 páginasPráctica 5MARIO GARCÍA MARTÍNEZAún no hay calificaciones
- Informe Quimica Practica 7Documento7 páginasInforme Quimica Practica 7Henry Jom GueAún no hay calificaciones
- Practica No 6 Cinetica QuimicaDocumento6 páginasPractica No 6 Cinetica QuimicaDaniel GarciaAún no hay calificaciones
- Informe Reloj de YODODocumento5 páginasInforme Reloj de YODOpaula maldonado0% (2)
- Reacciones químicas laboratorioDocumento20 páginasReacciones químicas laboratorioJhon Maicol Chavez Alaya0% (1)
- Trabajo de Laboratoria 7 y 8Documento20 páginasTrabajo de Laboratoria 7 y 8Correa Asencios WilliamsAún no hay calificaciones
- Informe 9Documento9 páginasInforme 9Marcela QuijanoAún no hay calificaciones
- Partes Del Informe Con EjemploDocumento18 páginasPartes Del Informe Con EjemploRosa SayanAún no hay calificaciones
- Determinación de la cinética de reacción y energía de activación mediante el estudio de la velocidad de reacciónDocumento2 páginasDeterminación de la cinética de reacción y energía de activación mediante el estudio de la velocidad de reacciónmorrantiaoAún no hay calificaciones
- Cinetica P2Documento10 páginasCinetica P2Natalia De la RosaAún no hay calificaciones
- Práctica 4. Velocidad de Una Reacción QuímicaDocumento6 páginasPráctica 4. Velocidad de Una Reacción QuímicaBrayan GuttierrezAún no hay calificaciones
- Informe Práctico II Yodo IntroDocumento4 páginasInforme Práctico II Yodo IntroPamee MancillaAún no hay calificaciones
- Valoración Del Tiosulfato de Sodio 0,1N...Documento4 páginasValoración Del Tiosulfato de Sodio 0,1N...Diego ArmandoAún no hay calificaciones
- Oxidación del ion yoduro con persulfato de amonioDocumento8 páginasOxidación del ion yoduro con persulfato de amonioKAREN ANDIA GUZMAN100% (1)
- Calidad del agua para estudiantes de ciencias ambientalesDe EverandCalidad del agua para estudiantes de ciencias ambientalesAún no hay calificaciones