Documentos de Académico
Documentos de Profesional
Documentos de Cultura
27-9-13 Manual - de - Quimica - General
27-9-13 Manual - de - Quimica - General
Cargado por
Pedro Cerna VelasquezTítulo original
Derechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
27-9-13 Manual - de - Quimica - General
27-9-13 Manual - de - Quimica - General
Cargado por
Pedro Cerna VelasquezCopyright:
Formatos disponibles
Manual de prcticas de Laboratorio de Qumica General
NDICE
Prctica
Prctica
Prctica
Prctica
Prctica
#
#
#
#
#
1
2
3
4
5
Realizado por
Luisa Villanueva Hinojos
Reglas bsicas ..................................................................
Tcnicas comunes de laboratorio ....................................
Reacciones qumicas .........................................................
Identificacin de metales a la flama .................................
Preparacin de soluciones y determinacin de pH .........
1
8
12
17
19
ndice
Manual de prcticas de Laboratorio de Qumica General
PRCTICA No. 1
REGLAS BSICAS A OBSERVAR EN EL LABORATORIO
I. Normas generales de seguridad.
Con la finalidad de evitar accidentes:
a) Los alumnos debern utilizar bata de laboratorio, toalla o lienzo para limpieza y en caso
de requerirse, guantes y anteojos de proteccin, durante el tiempo de permanencia en el
laboratorio.
b)
El botiqun de primeros auxilios se localizar en una lugar accesible y deber contar con
material de curacin y sustancias medicinales, tales como: gasa, algodn, alcohol, curitas,
aspirina, merthiolate, cinta adhesiva o microporo, picrato, agua oxigenada, etc.
c)
Verificar el funcionamiento adecuado de la campana extractora de gases y que exista una
ventilacin adecuada en el laboratorio.
d)
Localizar los extintores de incendio y verificar que se encuentren siempre con la carga
adecuada y en buen estado de funcionamiento.
e)
Que la regadera de seguridad funcione adecuadamente con la presin y flujo de agua
suficientes.
f)
Nunca fume o ingiera alimentos en el laboratorio, porque es frecuente trabajar con
sustancias inflamables o txicas; adems, cualquier distraccin produce errores o
accidentes.
g)
Durante la realizacin de las prcticas, la puerta del laboratorio deber mantener abierta
la cerradura.
h)
Cuando se realicen las prcticas, se prohibir el ingreso de personas ajenas y la salida de
alumnos.
II. Medidas de seguridad durante el desarrollo de la prctica.
a) Informe inmediatamente al profesor de laboratorio de cualquier accidente y memorice la
ubicacin en el laboratorio de los dispositivos de seguridad, como regaderas, botiqun,
frazadas y extinguidores, para una rpida intervencin.
b)
c)
d)
e)
Nunca pruebe ni huela las sustancias qumicas, a menos que el proceso lo seale.
La manipulacin de cidos concentrados debe efectuarse dentro de la campana de
extraccin, para evitar salpicaduras que puedan afectar a uno mismo o a sus compaeros;
cuando trabaje con sustancias orgnicas, evite el uso de cido perclrico. Para medir
volmenes de cidos o bases concentrados, use probetas o buretas, nunca pipetas.
Nunca mezcle las sustancias qumicas a menos que el procedimiento lo seale.
Cuando prepare soluciones de sustancias qumicas, no altere la tcnica establecida para
ello. Una vez preparada la solucin, etiqutela indicando composicin, concentracin,
fecha, nombres y nmero de equipo.
1
Realizado por
Luisa Villanueva Hinojos
Manual de prcticas de Laboratorio de Qumica General
f)
Antes de usar un reactivo qumico o una solucin lea cuidadosamente la etiqueta para
identificar el contenido y tome exactamente la cantidad necesaria y tape el recipiente.
g)
En caso de salpicadura de un cido o una base en la piel o en la bata, enjuguelo
inmediatamente, Excepto en el caso de cido sulfrico, deber enjuagarse con una solucin
de bicarbonato de sodio.
h)
Al dejar de usar los reactivos o soluciones, regrselos a su lugar de almacenamiento;
esto facilitar su trabajo experimental y el de sus compaeros; tenga siempre su mesa de
trabajo con el mnimo de riesgos potenciales; en caso de ensuciarse la mesa, lmpiela
inmediatamente con la toalla hmeda.
i)
Cuando utilice materiales y aparatos especiales y de uso general, entrguelos limpios al
instructor; la balanza, por ningn motivo, se debe mover de posicin o lugar.
j)
k)
Deseche todas las sustancias siguiendo las indicaciones del instructor
Cuando se calientan soluciones o sustancias que desprenden gases corrosivos o txicos,
debe usarse la campana de extraccin; el calentamiento de tubos de ensaye se efecta
inclinando el tubo 45 , en direccin opuesta a la que se encuentren los compaeros de
trabajo.
l)
Use las pinzas para manejar objetos y recipientes que hayan sido calentados.
m) No se debe cambiar por iniciativa propia el sistema que se indica en los experimentos
para el calentamiento.
n)
o)
Al encender la flama de un mechero, encienda primero el cerillo y acrquelo a la parte
superior del mechero y abra lentamente la vlvula del gas. Al iniciar el calentamiento de
una sustancia, principie con el mnimo de calor y aumntelo lentamente hasta obtener la
temperatura adecuada.
Al terminar la prctica, lvese las manos.
III. Recomendaciones para la realizacin de las prcticas.
a) El alumno deber estudiar previamente el experimento a efectuar, con el propsito de
comprender su objetivo, los principios en que se fundamenta y el procedimiento a seguir.
b) Observar con atencin la demostracin del experimento que efecte el profesor, as
como las instrucciones especiales que le sean dadas.
c) En caso de daar material y/o equipo, deber ser reemplazado en un plazo mximo de una
semana.
IV. Registro de los datos del experimento.
a) Registre inmediatamente despus de efectuar la medida, los resultados o datos obtenidos;
nunca trate de memorizarlos; use tinta para anotarlos.
2
Realizado por
Luisa Villanueva Hinojos
Manual de prcticas de Laboratorio de Qumica General
b) Realice los clculos en los espacios destinados para ello en el folleto de prcticas; en
caso de cometer errores en el registro de datos, clculos o resultados, nunca borre, sino
tache, y al lado escriba los valores correctos.
c) En caso de que se le soliciten grficas, figuras o dibujos, hgalos correctamente en el
mismo texto de experimentos, usando las escalas apropiadas.
d) Para evitar errores en las medidas de peso y volumen de las sustancias, procure efectuar
esas operaciones siempre a temperatura ambiente.
V. Evaluacin de la prctica.
a) Los alumnos debern realizar un reporte con las observaciones y resultados de la
prctica, segn sea solicitado por el profesor.
b) Segn sea el tipo de prctica realizada, el reporte en cuestin ser presentado en forma
individual o por equipo, en el formato que le sea indicado.
VI. Limpieza del material.
a) Si el material se encuentra aparentemente limpio, lvelo primero con agua de la llave,
luego con agua destilada y colquelo sobre un papel absorbente o en el escurridor.
b) Si el material no queda perfectamente limpio, use un escobilln y detergente, tallando
varias veces sobre las superficies externa e interna del material, lave luego con agua de
la llave y posteriormente con agua destilada.
c) Cuando la suciedad persista, utilice soluciones diluidas de cido clorhdrico, hidrxido de
sodio o de un solvente orgnico como la acetona o el etanol, luego proceda como se
indic antes.
Cuestionario sobre reglas de seguridad en el laboratorio
1. - Escriba su propia definicin de accidente y consecuencias.
- Es el resultado de un acto inseguro, provoca daos.
- Cualquier suceso que, provocado por una accin violenta y repentina ocasionada
por un agente externo involuntario, da lugar a una lesin corporal.
______________________________________________________________________________________________
______________________________________________________________________________________________
______________________________________________________________________________________________
______________________________________________________________________________________________
2 . De acuerdo con los 3 tipos de accidentes ms comunes, d un ejemplo de cada uno de ellos.
a) Transporte: __________________________________________________________
b) Laborales: ____________________________________________________________
c) Domsticos: __________________________________________________________
3. De acuerdo con las preguntas anteriores, mencione 5 formas de prevenir riesgos y accidentes
3
Realizado por
Luisa Villanueva Hinojos
Manual de prcticas de Laboratorio de Qumica General
a) ___________________________________________________________________
b) ___________________________________________________________________
c) ___________________________________________________________________
d) ___________________________________________________________________
e) ___________________________________________________________________
4. Qu tipos de fuego existen, segn el agente que lo provoca,
ejemplos?
cul es este agente y d
a)______ _________________
____________________________________________
b)______ _________________
____________________________________________
c) ______ ________________
_____________________________________________
d) ______ ________________
_____________________________________________
5. Mencione 4 formas de extinguir un incendio.
a) ____________________________________________________________________
b) ____________________________________________________________________
c) ____________________________________________________________________
d) ____________________________________________________________________
6. Que instrucciones deben seguirse en caso de incendio?
a) ____________________________________________________________________
b) ____________________________________________________________________
c) ____________________________________________________________________
d) ____________________________________________________________________
e) ____________________________________________________________________
7. De acuerdo con sus caractersticas de peligrosidad (CRETIB), mencione dos ejemplos de cada
una:
4
Realizado por
Luisa Villanueva Hinojos
Manual de prcticas de Laboratorio de Qumica General
Corrosivas:_________________________________________________________________________
____________________________________________________________________________________
____________________________________________________________________________________
Reactivas: _________________________________________________________________________
____________________________________________________________________________________
____________________________________________________________________________________
Explosivas: ________________________________________________________________________
____________________________________________________________________________________
____________________________________________________________________________________
Txicas: ___________________________________________________________________________
____________________________________________________________________________________
____________________________________________________________________________________
Inflamables: ________________________________________________________________________
____________________________________________________________________________________
____________________________________________________________________________________
Biolgico-infecciosas: ______________________________________________________________
____________________________________________________________________________________
____________________________________________________________________________________
8. - Cules son los organismos responsables de la vigilancia y control de la contaminacin
ambiental, a niveles federal , estatal y municipal si lo hay:
a) ______________________
_____________________ ________________________
b) _______________________
_____________________
________________________
c)________________________
_____________________
________________________
d) _______________________
_____________________
________________________
9. - Indique el equipo de proteccin personal que debe usarse en el laboratorio.
a) ____________________________________________________________________________________
b) ____________________________________________________________________________________
c) ____________________________________________________________________________________
d) ____________________________________________________________________________________
10. - Con qu equipo de reduccin de riesgos de trabajo cuenta el laboratorio? Mencione al
menos 4?
a)____________________________________
5
Realizado por
Luisa Villanueva Hinojos
Manual de prcticas de Laboratorio de Qumica General
b)_____________________________________
c)_____________________________________
d)_____________________________________
11. - Cules son las normas de conducta al interior del laboratorio?
a)
b)
c)
d)
e)
f)
12. - Mencione las medidas de seguridad que deben observarse durante el trabajo en el
laboratorio.
a)
b)
c)
d)
e)
13. Antes y durante la realizacin de una prctica, qu debe hacer el alumno?
a)
b)
c)
6
Realizado por
Luisa Villanueva Hinojos
Manual de prcticas de Laboratorio de Qumica General
d)
14. Por qu es necesario realizar un registro de los datos manejados y obtenidos de un
experimento?
_____________________________________________________________________________________________
_____________________________________________________________________________________________
_____________________________________________________________________________________________
_____________________________________________________________________________________________
15. Sugerencias para el mejoramiento de la realizacin de las prcticas de laboratorio.
_____________________________________________________________________________________________
_____________________________________________________________________________________________
_____________________________________________________________________________________________
_____________________________________________________________________________________________
_____________________________________________________________________________________________
_____________________________________________________________________________________________
_____________________________________________________________________________________________
_____________________________________________________________________________________________
_____________________________________________________________________________________________
_____________________________________________________________________________________________
_____________________________________________________________________________________________
_____________________________________________________________________________________________
7
Realizado por
Luisa Villanueva Hinojos
Manual de prcticas de Laboratorio de Qumica General
PRCTICA No. 2
TCNICAS COMUNES DE LABORATORIO
OBJETIVO:
El alumno se adiestrar en algunas tcnicas usuales en el laboratorio de qumica,. Tales como la
filtracin, destilacin, sublimacin y preparacin de soluciones.
CONSIDERACIONES TERICAS:
En el estudio experimental de las propiedades qumicas de las sustancias y de sus reacciones se
usan diferentes tcnicas, entre las cuales destacan la filtracin, evaporacin, destilacin, y
sublimacin.
La filtracin es una tcnica que consiste en separar slidos de lquidos por medio de una
membrana semipermeable.
La sublimacin es una tcnica de separacin de slidos, uno de los cuales no se funde sino pasa
del estado slido al gaseoso.
La destilacin es una tcnica de separacin de lquidos de diferente punto de ebullicin.
La evaporacin nos permite separar un lquido de un slido al aplicar calor.
Materiales y equipo:
Balanza
2 vasos de precipitados. De 100 mL
1 vaso de precipitados. De 250 mL
Embudo de vidrio
Soporte con anillo
Tela de asbesto
Varilla de vidrio
2 cpsulas de porcelana de 90 mL
Mechero de Bunsen
Tubo de ensaye de 29 x 200 mm
Papel filtro
Piseta
Perlas de vidrio
Refrigerante recto de 600 mm
Manguera de hule
Matraz de destilacin
Tapn de hule con termmetro
2 matraces volumtricos de 100 mL
Probeta de 25 mL
Esptula
Sustancias
Permanganato de Potasio (KMnO4)
Arena comercial
Yodo (I2)
Cloruro de Sodio (NaCl)
cido Clorhdrico Concentrado (HCl)
8
Realizado por
Luisa Villanueva Hinojos
Manual de prcticas de Laboratorio de Qumica General
PROCEDIMIENTOS:
I. FILTRACIN:
1. Pese exactamente 5 g. de arena comercial en un vaso de precipitado seco de 100 mL y
agregar 30 mL de agua destilada.
2. Coloque un embudo de vidrio en un soporte con anillo, y un vaso de precipitados de 100 mL
en su parte inferior.
3. Prepare un papel filtro de acuerdo a las siguientes indicaciones:
Doble el crculo de papel filtro por la mitad
Vulvalo a doblar por la mitad
bralo y colquelo en el embudo
4. Humedezca el papel filtro con agua destilada utilizando una piseta y presinelo contra las
paredes del embudo.
5. El papel debe quedar completamente adherido a la superficie interior del embudo sin que se
observen burbujas de aire.
6. Pese una cpsula de porcelana de 90 mL seca y limpia y colquela en la parte inferior del
embudo.
7. Agite el vaso de precipitados que contiene arena, utilizando una varilla de vidrio. Vierta el
contenido en el embudo, teniendo cuidado de colocar la varilla en el pico del vaso. Vea la
figura.
8. Con una piseta, lave cuidadosamente el vaso de precipitados con agua destilada hasta que no
quede residuo.
9. Con la piseta lave varias veces el residuo que se encuentra en el papel filtro.
9
Realizado por
Luisa Villanueva Hinojos
Manual de prcticas de Laboratorio de Qumica General
II. EVAPORACIN
1. Coloque la cpsula de porcelana en un soporte con tela de asbesto y caliente
suavemente con un mechero de Bunsen hasta que se evapore toda el agua.
2. Enfre la cpsula y psela.
3. Repita la operacin anterior hasta que obtenga peso constante.
REGISTRO DE DATOS:
Peso del vaso de precipitados, P1,
___________ gramos
Peso del vaso de precipitados con arena, P2,
___________ gramos
Peso de la arena = P2 - P1
___________ gramos
Peso de la cpsula, P3
___________ gramos
Peso de la cpsula ms el residuo, P4
___________ gramos
Peso del residuo, = P4 - P3
___________ gramos
CUESTIONARIO :
1. Basndose en sus observaciones y resultados, explique si la arena contena sustancias
solubles en agua.
COLOR?
TURBIDEZ?
RESIDUO?
CALCULARLO EN FORMA DE SLIDOS DISUELTOS
2. Calcule el porcentaje de slidos solubles en agua.
PESO ARENA
5 gr. de arena100 gr. de arena
% SLIDOS SOLUBLES
_______________________
X
10
Realizado por
Luisa Villanueva Hinojos
Manual de prcticas de Laboratorio de Qumica General
III. DESTILACIN :
1. En un matraz de destilacin agregue 50 mL de agua de la llave, unos cuantos cristales de
permanganato de potasio y algunas perlas de vidrio.
2. Monte el aparato de destilacin como se muestra en la figura.
3. Caliente el matraz hasta obtener una ebullicin moderada del agua coloreada por el
permanganato de potasio y colecte en un tubo de ensaye aproximadamente 10 mL de agua
destilada. Suspenda el calentamiento. Anote y explique sus observaciones.
11
Realizado por
Luisa Villanueva Hinojos
Manual de prcticas de Laboratorio de Qumica General
PRCTICA No. 3
REACCIONES QUMICAS
OBJETIVO:
El alumno efectuar diferentes tipos de reacciones qumicas.
CONSIDERACIONES TERICAS:
Las reacciones qumicas se pueden clasificar en los siguientes tipos:
Reacciones
Reacciones
Reacciones
Reacciones
Reacciones
de
de
de
de
de
Combinacin;
Descomposicin;
Desplazamiento;
Doble Descomposicin (mettesis);
Oxidacin - Reduccin.
Las reacciones de combinacin son aqullas en las cuales se forma una sustancia a partir de dos o
ms sustancias.
Reaccin General:
A+B=C
Las reacciones de descomposicin son aqullas en que se forman dos o ms sustancias a partir de
una. Muchos compuestos se comportan de sta manera cuando se calientan.
Reaccin General:
C=A+B
Las reacciones de desplazamiento son aqullas en que un elemento sustituye a otro en un
compuesto.
Reaccin General:
A + BX = AX + B
Las reacciones de doble descomposicin o mettesis son aqullas en las cuales hay un
intercambio de elementos o de radicales entre los compuestos reaccionantes.
Reaccin General:
AX + BY = AY + BX
Las reacciones de oxidacin - reduccin son aqullas en las cuales las sustancias que intervienen
en la reaccin aumentan (oxidacin) o disminuyen (reduccin) su valencia o nmero de oxidacin,
por el intercambio de electrones entre dichas sustancias.
12
Realizado por
Luisa Villanueva Hinojos
Manual de prcticas de Laboratorio de Qumica General
Materiales y equipo:
Mechero de Bunsen
Pinzas
Placa de asbesto
5 tubos de ensaye de 13 x 100 mm
2 vasos de precipitados de 100 mL
Salero
Probeta de 25 Ml
2 goteros
Sustancias:
Cinta de Magnesio (Mg)
Granalla de Hierro (Fe)
Dicromato de Amonio ((NH4)2Cr2O7)
Oxido de Mercurio (II) (HgO)
Solucin de Nitrato de Plata al 4 %
(AgNO3)
Solucin concentrada de Nitrito de
Sodio (NaNO2)
Lmina o alambre de Cobre (Cu)
Solucin de cido Sulfrico 1 :10 (V/V)
(H2SO4)
Solucin de cido Clorhdrico 1 :4 (V/V)
(HCl)
Solucin de Permanganato de Potasio al
4%
(KMnO4)
Solucin de Sulfato de Hierro (II) al 4 %
(FeSO4)
Solucin de Nitrato de Mercurio (I) al 4
% (Hg2(NO3)2)
PROCEDIMIENTOS:
1. REACCIONES DE COMBINACIN
a)
Con unas pinzas, tome un pedazo pequeo de una cinta de magnesio (Mg) y
qumela usando un mechero.
b)
Coloque en un salero granalla de Hierro (Fe); agitando el salero, deje caer el
hierro en la flama de un mechero.
Anote sus observaciones:
a) ___________________________________________________________________________________
___________________________________________________________________________________
___________________________________________________________________________________
___________________________________________________________________________________
b) ___________________________________________________________________________________
___________________________________________________________________________________
___________________________________________________________________________________
___________________________________________________________________________________
13
Realizado por
Luisa Villanueva Hinojos
Manual de prcticas de Laboratorio de Qumica General
Escriba las ecuaciones de las reacciones de combinacin efectuadas:
a)
b)
2. REACCIONES DE DESCOMPOSICIN
a)
En una placa de asbesto coloque una pequea cantidad de Dicromato de Amonio
((NH4)2Cr2O7), en forma de cono invertido. Queme el slido con un cerillo hasta
que inicie la reaccin. Para iniciar ms fcilmente la reaccin aada al slido unas
gotas de alcohol y acerque un cerillo encendido.
b)
En un tubo de ensaye limpio y seco, vierta una pequea cantidad de xido de
mercurio (II) (HgO); caliente el tubo con la llama de un mechero, usando pinzas y
coloque una astilla de madera con un punto de ignicin en la boca del tubo.
Anote sus observaciones:
a) ___________________________________________________________________________________
___________________________________________________________________________________
___________________________________________________________________________________
___________________________________________________________________________________
b) ___________________________________________________________________________________
___________________________________________________________________________________
___________________________________________________________________________________
___________________________________________________________________________________
Escriba las ecuaciones de las reacciones de descomposicin efectuadas:
a)
b)
3. REACCIONES DE DESPLAZAMIENTO
a)
b)
En un vaso de 50 mL. Vierta 5 mL de una solucin de Nitrato de Plata al 4 %
(AgNO3) e introduzca una pieza de cobre limpia.
En un vaso de precipitados de 100 mL vierta 10 mL de solucin de Nitrato de
Mercurio (I) al 4 % (Hg2(NO3)2) e introduzca una pieza de cobre.
Anote sus observaciones:
a) ___________________________________________________________________________________
___________________________________________________________________________________
___________________________________________________________________________________
___________________________________________________________________________________
b) ___________________________________________________________________________________
___________________________________________________________________________________
14
Realizado por
Luisa Villanueva Hinojos
Manual de prcticas de Laboratorio de Qumica General
___________________________________________________________________________________
___________________________________________________________________________________
Escriba las ecuaciones de las reacciones de desplazamiento efectuadas:
a)
b)
4.
REACCIONES DE DOBLE DESCOMPOSICIN O METTESIS
a)
Llene las dos terceras partes de un tubo de ensaye con agua destilada, agregue
agitando dos o tres gotas de solucin de Nitrato de Plata al 4 % (AgNO3), ms dos o
tres gotas de cido clorhdrico diluido 1:4 en volumen.
b)
Repita la misma operacin y reemplace el agua destilada por agua de la llave.
Anote sus observaciones:
a) ___________________________________________________________________________________
___________________________________________________________________________________
___________________________________________________________________________________
___________________________________________________________________________________
___________________________________________________________________________________
b) ___________________________________________________________________________________
___________________________________________________________________________________
___________________________________________________________________________________
___________________________________________________________________________________
___________________________________________________________________________________
Escriba las ecuaciones de las reacciones de doble descomposicin efectuadas:
a)
b)
5.
REACCIONES DE OXIDACIN REDUCCIN
a)
Coloque en un tubo de ensaye 4 gotas de Solucin de Permanganato de Potasio al 4
% (KMnO4); aada dos gotas de cido Sulfrico 1 :10 (V/V) (H2SO4). Caliente y
agregue gota a gota una solucin concentrada de Nitrito de Sodio (NaNO2)
recientemente preparada, hasta observar cambios en la coloracin.
b)
En un tubo de ensaye coloque dos gotas de cido Sulfrico 1 :10 (V/V) (H2SO4) y
agregue cuatro gotas de solucin de Permanganato de Potasio al 4 % (KMnO4) ;
agite y aada 5 mL de solucin de Solucin de Sulfato de Hierro (II) al 4 %
(FeSO4).
Anote sus observaciones:
a) ___________________________________________________________________________________
___________________________________________________________________________________
___________________________________________________________________________________
15
Realizado por
Luisa Villanueva Hinojos
Manual de prcticas de Laboratorio de Qumica General
___________________________________________________________________________________
___________________________________________________________________________________
b) ___________________________________________________________________________________
___________________________________________________________________________________
___________________________________________________________________________________
___________________________________________________________________________________
___________________________________________________________________________________
Escriba las ecuaciones de las reacciones Redox efectuadas:
a)
b)
16
Realizado por
Luisa Villanueva Hinojos
Manual de prcticas de Laboratorio de Qumica General
PRCTICA No. 4
IDENTIFICACIN DE METALES A LA FLAMA
OBJETIVO :
El alumno someter diferentes sales a la prueba de la Flama y conocer la caracterstica de
algunos metales.
CONSIDERACIONES TERICAS:
Los metales son sustancias cuyos tomos por lo general contienen uno o dos electrones en su
configuracin electrnica externa (capa de valencia). Al reaccionar tienden a formar compuestos
inicos (sales) por transferencia de electrones. Son muy activos por ceder fcilmente electrones
y emiten luz al excitarse, produciendo llamas de diferentes colores. Esta propiedad se utiliza para
identificarlos.
Materiales y equipo :
Mechero de Bunsen
Alambre de platino o nicromio
Vidrio de Cobalto
7 vidrios de reloj
1 cpsula de porcelana
Sustancias :
Sales de metales (nitratos o cloruros) :
sodio, potasio, calcio, bario, litio, cobre,
estroncio
cido Clorhdrico
Procedimiento :
1. Se limpia el alambre de platino humedecindolo en cido clorhdrico, que debe estar en la
cpsula de porcelana, y se introduce en la llama del mechero.
2. Si en la llama se observa alguna coloracin, se humedece en el HCl y se calienta varias veces
el alambre de platino, hasta que la llama no se coloree.
3. Cuando el alambre est limpio, se humedece en HCl y se toca la primera sustancia colocada en
los vidrios de reloj, se introduce el alambre en la llama y se anota la coloracin que adquiere.
4. Se limpia nuevamente el alambre y se repite el experimento anterior con cada una de las
sustancias restantes.
Anote en el cuadro de observaciones los siguientes datos :
Nombre de la sustancia
Frmula
Color de la
llama
Metal que la
produce
Longitud de
onda ()
17
Realizado por
Luisa Villanueva Hinojos
Manual de prcticas de Laboratorio de Qumica General
18
Realizado por
Luisa Villanueva Hinojos
Manual de prcticas de Laboratorio de Qumica General
PRCTICA No. 5
PREPARACIN DE SOLUCIONES Y DETERMINACIN DE SU POTENCIAL DE HIDRGENO (pH)
OBJETIVO:
El alumno aprender a preparar soluciones, a realizar diluciones y determinar su potencial de
hidrgeno.
CONSIDERACIONES TERICAS:
La preparacin de soluciones es una tcnica que permite obtener concentraciones conocidas de
solutos en determinados solventes, entendiendo por solvente aquella sustancia que se encuentra
en mayor proporcin en la solucin preparada.
1. Porcentaje en peso. Una de las formas que ms se usan para expresar la concentracin de
una solucin, es el porcentaje en peso, lo cual es el peso en gramos de la sustancia disuelta en
100 mL de solucin. De acuerdo con el porcentaje deseado, se pesa exactamente la cantidad
en gramos del slido, se pone en un matraz volumtrico adecuado y se agrega el solvente
hasta la marca de aforo.
2.
Porcentaje en volumen. El porcentaje en volumen de una solucin es el volumen en mL de la
sustancia disuelta en 100 mL de solucin. Segn el porcentaje deseado, se mide el volumen
del lquido con una pipeta o en una probeta, se vierte en un matraz volumtrico apropiado y
se agrega el solvente hasta la marca de aforo.
El Potencial Hidrgeno (pH) es una medida de la concentracin de iones H+. Se define como el
logaritmo negativo de la concentracin de iones hidrgeno expresada en moles/Litro.
Algunas sustancias cuando estn en solucin tienen la capacidad de formar iones1 . A estas
sustancias se les llaman electrlitos. Dependiendo del grado de ionizacin, pueden ser fuertes o
dbiles. En el caso del agua, por s misma es capaz de formar iones, aunque lo hace de manera
muy dbil, pudindose representar de la siguiente forma:
H2O = H+ + OH-
La Ley del Equilibrio Qumico establece lo siguiente: El producto de las concentraciones de los
productos de una reaccin qumica, dividido por el producto de las concentraciones de los
reactivos es igual a una constante.
A su vez, lo anterior se puede representar como sigue:
Ion : tomo o grupo de tomos con carga elctrica positiva (catin) o negativa (anin).
19
Realizado por
Luisa Villanueva Hinojos
Manual de prcticas de Laboratorio de Qumica General
[ H+ ] [ OH-]
------------------------ = K
[ H2O]
Como se indic anteriormente, la capacidad de ionizacin del agua es extremadamente limitada,
de tal forma que el trmino correspondiente a [H2O] puede considerarse que permanece
constante. Arreglando la expresin de acuerdo a esto:
[ H+ ] [ OH-] = K [ H2O] = Kw = 1 x 10
-14
Kw se conoce como Constante de ionizacin del agua. De la expresin anterior se desprende que
para el agua pura a 25 C
[ H+ ] = [ OH-] = 1 x 10
-7
moles/Litro.
Dependiendo de la concentracin de iones Hidrgeno, las soluciones y sustancias en general
tendrn un comportamiento especfico. Pero manejar cifras con exponenciales de 10 puede ser
complicado y prestarse a confusin, por lo que se maneja el valor logartmico de su
concentracin y esto se conoce como potencial de hidrgeno (pH):
pH = - log [ H+ ]
Material y equipo
8
4
1
2
2
1
vasos de precipitado de 250 ml
pipetas
potencimetro
frascos de reactivos
probetas
piseta de 500 mL
Reactivos
HCl Concentrado 12 M
NaOH concentrado a 10M
Solucin amortiguadora
Agua destilada
PROCEDIMIENTO:
I. Preparacin de una solucin acuosa de cido Clorhdrico al 10 % en volumen, o sea, 1:10 (V/V)
1. Mida 5 mL de HCl con una probeta o con una bureta (equipo # 1).
2. Vierta el cido en un matraz volumtrico de 100 mL.
3. Con una piseta llene la probeta con agua destilada y virta la cantidad necesaria en el matraz
volumtrico.
4. Repita esta operacin con 20 ml de cido y agregue el agua destilada al matraz volumtrico
hasta la marca de aforo. Tape el matraz y agite vigorosamente para obtener una solucin
homognea o uniforme.
5. Tome la mitad exacta de cada matraz y colquela en 2 matraces aforados marcados a la mitad
del valor tal y como se indica en el siguiente nmero ( II )
6. El equipo # 2 siga las mismas instrucciones utilizando 60 mL en un matraz y 80 mL en otro
matraz volumtrico de 100 mL
7. Equipos # 3 y #4 repetir los pasos anteriores, pero ahora con la solucin de NaOH.
20
Realizado por
Luisa Villanueva Hinojos
Manual de prcticas de Laboratorio de Qumica General
II. Preparacin de soluciones diluidas.
1. De las soluciones anteriores, tome 50 mL con una probeta o bureta y pselos a un segundo
matraz aforado de 100 mL marcado con la mitad del valor correspondiente .
2. Agregue agua destilada hasta la marca o lnea de aforo. Tape el matraz y agtelo
vigorosamente hasta mezclar completamente.
3. Vaciar a un vaso de precipitados de 250 mL marcado adecuadamente.
4. Proceder a leer el pH en orden creciente de concentracin : 2.5, 5, 10, 20, 30, 40, 50, 60, 80
y directamente de la botella de reactivos (100)
III. Medicin del Potencial de Hidrgeno (pH).
1. Encienda el potencimetro y deje que se estabilice por espacio de 10 minutos en la posicin
standby.
2. Enjuague los electrodos del potencimetro con suficiente agua destilada.
3. Vierta una porcin de cada una de las soluciones diluidas en vasos de precipitados. Las
muestras que se van a analizar, deben estar a una temperatura prxima a los 25 C.
4. Sumerja los electrodos en la muestra, y mida el valor del pH girando la perilla del
potencimetro a esa posicin.
5. Una vez obtenida la lectura, regstrela.
6. Regrese la perilla a la posicin standby, saque los electrodos de la muestra y enjuguelos con
abundante agua destilada.
7. Coloque los electrodos en la solucin amortiguadora.
CUESTIONARIO:
1. Segn El volumen de HCl y /o de NaOH medido, indique la concentracin de las soluciones
en porcentaje en volumen (%V).
a)
b)
2. Indique la concentracin resultante de las soluciones diluidas.
a)
b)
21
Realizado por
Luisa Villanueva Hinojos
Manual de prcticas de Laboratorio de Qumica General
3. Con los datos obtenidos, haga una tabla de resultados.
Concentracin
pH HCl
pH NaOH
2.5
5.0
10.0
20.0
30.0
40.0
50.0
60.0
80.0
100
4. Con los datos de la tabla de resultados, construya una grfica de pH vs. Concentracin en
moles/litro y haga una interpretacin.
pH
NaOH
PH
HCl
Concentracin
Concentracin %
5. Se tiene una solucin de HCl y se desconoce su pH. Se sabe que la concentracin de iones
hidrgeno (H+) es 4.29 x 10-6 moles/L. Calcule el pH de la solucin ( con la frmula de la
pgina 21).
6. Investigue las aplicaciones de la medicin del pH, indicando la bibliografa consultada.
22
Realizado por
Luisa Villanueva Hinojos
Universidad Autnoma de Chihuahua.
FACULTAD DE INGENIERA
Manual de Prcticas de Laboratorio de Qumica.
También podría gustarte
- Método de Los Tres MomentosDocumento55 páginasMétodo de Los Tres MomentosLR Raul86% (63)
- Tema 5 - Función de DisipaciónDocumento10 páginasTema 5 - Función de DisipaciónLuis SuarezAún no hay calificaciones
- Producto de MateDocumento42 páginasProducto de MateJV Jhonny100% (1)
- CR (Acac) 3Documento2 páginasCR (Acac) 3Davis Bernardo0% (2)
- CusiDocumento119 páginasCusiluzvid alejo ochoaAún no hay calificaciones
- Control e Instrumentación de Procesos QuímicosDocumento9 páginasControl e Instrumentación de Procesos QuímicosNorberto Soto10% (20)
- Diapositivas de Notacion Cientifica - 2021Documento23 páginasDiapositivas de Notacion Cientifica - 2021Richard BuitronAún no hay calificaciones
- Bvco U1 Ea-1 MagpDocumento3 páginasBvco U1 Ea-1 MagpAngeles GrajalesAún no hay calificaciones
- Ejercicios de Limites de Funciones Vectoriales1Documento5 páginasEjercicios de Limites de Funciones Vectoriales1Alexis ManuelAún no hay calificaciones
- Integrales de Tan, Cot, Sec y CSC Calculo Integral CooperativaDocumento4 páginasIntegrales de Tan, Cot, Sec y CSC Calculo Integral CooperativaEyvin Stiven PinedaAún no hay calificaciones
- Funciones ImplícitasDocumento10 páginasFunciones ImplícitasAMYNNXXXXAún no hay calificaciones
- Guía de Trabajos Prácticos Cálculo IIDocumento28 páginasGuía de Trabajos Prácticos Cálculo IIDamian ZabalaAún no hay calificaciones
- ActividadAprendizaje S5Documento5 páginasActividadAprendizaje S5Nicolas ArboledaAún no hay calificaciones
- Presión HidrostáticaDocumento10 páginasPresión HidrostáticaSOFIA RAMOS CASTILLOAún no hay calificaciones
- Ejerciciosde Reactivos LimitantesDocumento3 páginasEjerciciosde Reactivos LimitantesKaren TaypeAún no hay calificaciones
- Integracion Metodo Del Rectangulo TrapecDocumento4 páginasIntegracion Metodo Del Rectangulo TrapecRamiro O CFAún no hay calificaciones
- Integral Indefinida 2 - Ing Civil y AmbientalDocumento19 páginasIntegral Indefinida 2 - Ing Civil y AmbientalRodolfo Jesus Calle FloresAún no hay calificaciones
- Libro Integrales Resueltas PDFDocumento242 páginasLibro Integrales Resueltas PDFJordan Hernandez Vidal100% (2)
- Reglamento Lgeepa TerminadaDocumento34 páginasReglamento Lgeepa TerminadaMaría José VegaAún no hay calificaciones
- Reglamento POETDocumento4 páginasReglamento POETGraciela GuintoAún no hay calificaciones
- Sesion 8 Modelamiento Calidad Aire - Informacion MeteorologicaDocumento30 páginasSesion 8 Modelamiento Calidad Aire - Informacion MeteorologicaNayib EdwinAún no hay calificaciones
- Calc1 Mod1 Unidad 1 2Documento14 páginasCalc1 Mod1 Unidad 1 2Roberto SantamariaAún no hay calificaciones
- La Integral IndefinidaDocumento14 páginasLa Integral Indefinidaxavega72Aún no hay calificaciones
- AP Limites y ContinuidadDocumento7 páginasAP Limites y ContinuidadJiancarlo O. HidalgoAún no hay calificaciones
- 2da Práctica EMODocumento20 páginas2da Práctica EMOFátima IxchelAún no hay calificaciones
- Planeaciones - Cálculo Integral. Unidad 3Documento18 páginasPlaneaciones - Cálculo Integral. Unidad 3yolomanAún no hay calificaciones
- LímitesDocumento6 páginasLímitesfrancozamora0100Aún no hay calificaciones
- Datos Interesantes MATLABDocumento15 páginasDatos Interesantes MATLABCarlos M. ArizaAún no hay calificaciones
- La Ecologia GeneralDocumento3 páginasLa Ecologia GeneralRobert SmithAún no hay calificaciones
- AlgoritmosDocumento74 páginasAlgoritmosJuan Andres PabonAún no hay calificaciones
- HidrodinámicaDocumento5 páginasHidrodinámicaJhon NaquicheAún no hay calificaciones
- PRÁCTICA No. 1 DESCARGAR UNA IMAGEN SATELITAL.Documento14 páginasPRÁCTICA No. 1 DESCARGAR UNA IMAGEN SATELITAL.berserk815Aún no hay calificaciones
- Temperatura y Dilatacion 2Documento37 páginasTemperatura y Dilatacion 2Jean Carlos TupAún no hay calificaciones
- 3 Limites y ContinuidadDocumento7 páginas3 Limites y Continuidadofi700% (1)
- Etapas Del Trabajo para Una Biorremediación Más EficazDocumento2 páginasEtapas Del Trabajo para Una Biorremediación Más EficazAlex CristhianAún no hay calificaciones
- Clase 2-2019-2 PDFDocumento56 páginasClase 2-2019-2 PDFSelene 3800Aún no hay calificaciones
- S04 - Estabilidad de LyapunovDocumento20 páginasS04 - Estabilidad de LyapunovFernando Choque PumaAún no hay calificaciones
- TermofluenciaDocumento2 páginasTermofluenciaJhnPadillaAún no hay calificaciones
- Formacion de Imagenes Por Refraccion - Lentes CyDDocumento23 páginasFormacion de Imagenes Por Refraccion - Lentes CyDManuel Morales VazquezAún no hay calificaciones
- Deberías Contárselo Todo A Tu ParejaDocumento1 páginaDeberías Contárselo Todo A Tu ParejaAlfredo JimenezAún no hay calificaciones
- Aprendiendo A Medir. Reporte de Laboratorio Fisica 1Documento8 páginasAprendiendo A Medir. Reporte de Laboratorio Fisica 1Diego TorresAún no hay calificaciones
- Unidad 2 Fase 3 CALCULO INTEGRALDocumento21 páginasUnidad 2 Fase 3 CALCULO INTEGRALnelsy.profe1012Aún no hay calificaciones
- TRABAJO N°2 Integrales DoblesDocumento21 páginasTRABAJO N°2 Integrales DoblesBLANCA MOLINAAún no hay calificaciones
- Monitoreo de Emisiones Contaminantes en Fuentes Fijas y MóvilesDocumento13 páginasMonitoreo de Emisiones Contaminantes en Fuentes Fijas y MóvilesIris Thayli Lopez SanchezAún no hay calificaciones
- Calc1 Mod1 Unidad 1 1Documento10 páginasCalc1 Mod1 Unidad 1 1Roberto SantamariaAún no hay calificaciones
- FUNCIONESDocumento32 páginasFUNCIONESLuis David Espinoza CadenasAún no hay calificaciones
- Biologia Compuestos OrganicosDocumento16 páginasBiologia Compuestos OrganicosFerMorales100% (1)
- Inducción Al Pensamiento MatemáticoDocumento55 páginasInducción Al Pensamiento MatemáticoMelisa SanvcnteAún no hay calificaciones
- MA263 - 2013 - 2 - S15.2 - Teorema - de - La - DivergenciaDocumento8 páginasMA263 - 2013 - 2 - S15.2 - Teorema - de - La - DivergenciaGustavo NavarroAún no hay calificaciones
- Introducción Al Tensor EsfuerzoDocumento7 páginasIntroducción Al Tensor EsfuerzoJoselyn Ramirez EspejoAún no hay calificaciones
- Informe IDocumento25 páginasInforme IricardoAún no hay calificaciones
- Descripción de La Selva de La YungasDocumento17 páginasDescripción de La Selva de La YungasAracelli ReinagaAún no hay calificaciones
- Ecuaciones No Lineales Newton-RaphsonDocumento11 páginasEcuaciones No Lineales Newton-RaphsonAlejandro Trejo FriasAún no hay calificaciones
- Taller 2Documento3 páginasTaller 2Diego Morán0% (1)
- Diagramas de CorrelaciónDocumento26 páginasDiagramas de CorrelaciónHumbertoAdrianRodriguezHernandezAún no hay calificaciones
- MÓDULO 1 QG-Materia y ReactividadDocumento39 páginasMÓDULO 1 QG-Materia y ReactividadAndrés Cárdenas100% (1)
- Vectores Tangente Unitario y Normal UnitarioDocumento5 páginasVectores Tangente Unitario y Normal UnitarioAlexisGuillendelaCruzAún no hay calificaciones
- 12 Integral Definida Aplicaciones PDFDocumento3 páginas12 Integral Definida Aplicaciones PDFjesusgarciasanchezAún no hay calificaciones
- Laboratorio de Quimica 2022 - 2Documento46 páginasLaboratorio de Quimica 2022 - 2FRANCO BOCANEGRAAún no hay calificaciones
- Manual de Laboratorio Química General PDFDocumento56 páginasManual de Laboratorio Química General PDFDerly Isabel Martínez BaronAún no hay calificaciones
- Guía de Laboratorio 2022Documento90 páginasGuía de Laboratorio 2022YERAL FRANCO LLICA TAIPEAún no hay calificaciones
- Manulab 1 QDocumento117 páginasManulab 1 QAlejandroAún no hay calificaciones
- Guia de Lab Quimica 2016-I PDFDocumento88 páginasGuia de Lab Quimica 2016-I PDFDaniel DanielAún no hay calificaciones
- Guiones Cinética Quà Mica Aplicada 22-23 2Documento28 páginasGuiones Cinética Quà Mica Aplicada 22-23 2Adri PRAún no hay calificaciones
- Actividad 1 La ComunicacionDocumento2 páginasActividad 1 La ComunicacionDavis BernardoAún no hay calificaciones
- Practica No 2 Extraccion de AdnDocumento8 páginasPractica No 2 Extraccion de AdnDavis BernardoAún no hay calificaciones
- Grin GardDocumento9 páginasGrin GardDavis Bernardo100% (1)
- Inuyasha El Castillo de Sueños en El Interior Del Espejo (Español)Documento1 páginaInuyasha El Castillo de Sueños en El Interior Del Espejo (Español)Davis BernardoAún no hay calificaciones
- CanizzaroDocumento4 páginasCanizzaroDavis BernardoAún no hay calificaciones
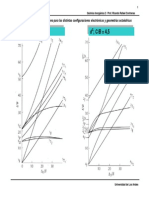
- Diagramas de Tanabe-Sugano y OrgelDocumento10 páginasDiagramas de Tanabe-Sugano y OrgelDavis BernardoAún no hay calificaciones
- Sulfato Sulfito y TiosulfatoDocumento12 páginasSulfato Sulfito y TiosulfatoDavis BernardoAún no hay calificaciones
- Practica 1 PeroxiboratoDocumento3 páginasPractica 1 PeroxiboratoDavis BernardoAún no hay calificaciones
- Examen Final de QuímicaDocumento11 páginasExamen Final de QuímicaValeria HuarezAún no hay calificaciones
- Procesos de InyeccionDocumento28 páginasProcesos de InyeccionCèsar TobarAún no hay calificaciones
- 417 - Modelos de RegresiónDocumento16 páginas417 - Modelos de RegresiónpuanAún no hay calificaciones
- Primer Ejercicio PortafolioDocumento14 páginasPrimer Ejercicio Portafolioae_oliveraAún no hay calificaciones
- El Sistema Solar y El UniversoDocumento5 páginasEl Sistema Solar y El UniversoCristina Micaela CasimiroAún no hay calificaciones
- Materiales de Diafragmas ParlantesDocumento9 páginasMateriales de Diafragmas ParlantesJose MustafhaAún no hay calificaciones
- Taller FotogametriaDocumento15 páginasTaller FotogametriaJaime Oviedo GumisAún no hay calificaciones
- Rm2 01 Metodo de Area de MomentosDocumento20 páginasRm2 01 Metodo de Area de MomentoskettyAún no hay calificaciones
- Creación de La Carrera de Psicología en La U.N.T.Documento4 páginasCreación de La Carrera de Psicología en La U.N.T.Flavio GarlatiAún no hay calificaciones
- Acero Sae 40xx y 46xxDocumento2 páginasAcero Sae 40xx y 46xxRonald Gomez Orellana100% (2)
- Catalogo Ventilacion Industrial Curiel PDFDocumento31 páginasCatalogo Ventilacion Industrial Curiel PDFAndres MArtinex21Aún no hay calificaciones
- Análisis de Un Ciclo y Su Rendimiento TérmicoDocumento10 páginasAnálisis de Un Ciclo y Su Rendimiento TérmicoEnmanuel MonteroAún no hay calificaciones
- Treybal 6.3Documento7 páginasTreybal 6.3Daniel MoralesAún no hay calificaciones
- Campos MagneticosDocumento2 páginasCampos MagneticosFredy Jose Villarreal YepezAún no hay calificaciones
- Medidas de CorrelacionDocumento22 páginasMedidas de CorrelacionRoosevelt Gonzalez100% (3)
- Conductividad y Difusividad TérmicaDocumento17 páginasConductividad y Difusividad TérmicaJocelynAún no hay calificaciones
- RP4 Con SolucionesDocumento22 páginasRP4 Con SolucionesNirbas99Aún no hay calificaciones
- Métodos para Evaluar Riesgos de IncendiosDocumento3 páginasMétodos para Evaluar Riesgos de IncendiosSergio CedeñoAún no hay calificaciones
- Materiales VitrocerámicosDocumento5 páginasMateriales VitrocerámicosYoanela VargasAún no hay calificaciones
- Taller #4 PDFDocumento2 páginasTaller #4 PDFKatherine RodriguezAún no hay calificaciones
- Que Es Un Sistema de AudioDocumento3 páginasQue Es Un Sistema de AudioNataliaAún no hay calificaciones
- Quinto de Secundaria Fisica 2do Examen BimestarlDocumento2 páginasQuinto de Secundaria Fisica 2do Examen BimestarlMine Rayan ShAún no hay calificaciones
- Guía de V..Documento43 páginasGuía de V..Cesar Sp100% (5)
- Medidores de Velocidad y Caudal en TuberiasDocumento4 páginasMedidores de Velocidad y Caudal en TuberiasCastillo Luis100% (1)
- Ecuación de Estado de Los Gases RealesDocumento13 páginasEcuación de Estado de Los Gases RealesDaana TaianaAún no hay calificaciones
- Magnetismo e InductoresDocumento5 páginasMagnetismo e Inductoresviento0921Aún no hay calificaciones