0% encontró este documento útil (0 votos)
278 vistas12 páginasPropiedades Intensivas y Extensivas en Química
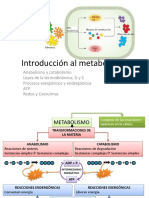
Este documento describe las diferencias entre propiedades intensivas y extensivas. Las propiedades intensivas no dependen de la cantidad de materia y mantienen el mismo valor cuando se divide un sistema, mientras que las propiedades extensivas sí dependen de la cantidad de materia y su valor cambia cuando se divide un sistema. Se proporcionan ejemplos como la temperatura y densidad para propiedades intensivas, y el volumen y la masa para propiedades extensivas.
Cargado por
KeniaDerechos de autor
© © All Rights Reserved
Nos tomamos en serio los derechos de los contenidos. Si sospechas que se trata de tu contenido, reclámalo aquí.
Formatos disponibles
Descarga como PPTX, PDF, TXT o lee en línea desde Scribd
0% encontró este documento útil (0 votos)
278 vistas12 páginasPropiedades Intensivas y Extensivas en Química
Este documento describe las diferencias entre propiedades intensivas y extensivas. Las propiedades intensivas no dependen de la cantidad de materia y mantienen el mismo valor cuando se divide un sistema, mientras que las propiedades extensivas sí dependen de la cantidad de materia y su valor cambia cuando se divide un sistema. Se proporcionan ejemplos como la temperatura y densidad para propiedades intensivas, y el volumen y la masa para propiedades extensivas.
Cargado por
KeniaDerechos de autor
© © All Rights Reserved
Nos tomamos en serio los derechos de los contenidos. Si sospechas que se trata de tu contenido, reclámalo aquí.
Formatos disponibles
Descarga como PPTX, PDF, TXT o lee en línea desde Scribd