Documentos de Académico
Documentos de Profesional
Documentos de Cultura
5ta Semana Quimica General Ucs
Cargado por
Rebeca Teresa Guevara Huaman0 calificaciones0% encontró este documento útil (0 votos)
28 vistas13 páginasquinta semana química general UCSUR
Derechos de autor
© © All Rights Reserved
Formatos disponibles
PPTX, PDF, TXT o lea en línea desde Scribd
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoquinta semana química general UCSUR
Copyright:
© All Rights Reserved
Formatos disponibles
Descargue como PPTX, PDF, TXT o lea en línea desde Scribd
0 calificaciones0% encontró este documento útil (0 votos)
28 vistas13 páginas5ta Semana Quimica General Ucs
Cargado por
Rebeca Teresa Guevara Huamanquinta semana química general UCSUR
Copyright:
© All Rights Reserved
Formatos disponibles
Descargue como PPTX, PDF, TXT o lea en línea desde Scribd
Está en la página 1de 13
QUIMICA GENERAL
TEORIA
Quinta sesión
DOCENTE Mg. Domingo Javier Nieto Freire
Características de la estructura Lewis
Enceles químicos según Lewis
Estructura Lewis para el oxigeno
Propanol
Enlace covalente Polar o Apolar
1.Si la diferencia de electronegatividades es menor que
0,4 tenemos moléculas no polares
2.- Si la diferencia de electronegatividades esta entre 0,4
y 1,7 la molécula es polar.
3.- Si la diferencia es mayor a 1,7 la molécula es iónica.
Moléculas Apolares
Son moléculas apolares las no
simétricas
• Dióxido de azufre SO2 .- molécula polar
Moléculas polares
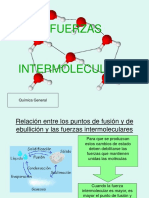
Fuerzas intermoleculares
• Dipolo-Dipolo.-La interacción dipolo-dipolo
consiste en la atracción electrostática entre el
extremo positivo de una molécula polar y el
negativo de otra. El enlace de hidrógeno es un
tipo especial de interacción dipolo-dipolo.
• Ejemplo.-
Fuerzas Intermoleculares
• London.- Surgen entre moléculas no polares,
en las que pueden aparecer dipolos
instantáneos.
Fuerzas intermoleculares
• Puente Hidrogeno.- Resulta de la formación
de una fuerza carga-dipolo con un átomo de
hidrógeno unido a un átomo de nitrógeno,
oxígeno o flúor ,de ahí el nombre de enlace de
hidrógeno.
También podría gustarte
- CLASE 1 Fuerzas IntermolecularesDocumento20 páginasCLASE 1 Fuerzas IntermolecularesAlisont Mella OlaveAún no hay calificaciones
- CTM Clase 9Documento62 páginasCTM Clase 9SEBASTIAN ALEJANDRO ARCE VILLARAún no hay calificaciones
- Fuerzas Intermoleculares Liquidos y Solidos DiaposotivasDocumento138 páginasFuerzas Intermoleculares Liquidos y Solidos DiaposotivaslouaveraAún no hay calificaciones
- Enlace QuimicoDocumento10 páginasEnlace QuimicoAngélica Sixtos100% (1)
- Quimica CamDocumento6 páginasQuimica CamNicolas LedesmaAún no hay calificaciones
- BrayanDocumento12 páginasBrayanBrayan Ayna RamosAún no hay calificaciones
- Tabla Periódica, Enlaces, Interacciones, Estructura de Lewis y Geometría MolecularDocumento40 páginasTabla Periódica, Enlaces, Interacciones, Estructura de Lewis y Geometría MolecularLina ManriquezAún no hay calificaciones
- Fuerzas Intermoleculares.Documento22 páginasFuerzas Intermoleculares.EfraínAún no hay calificaciones
- Clases de Elace y Caso - UPCDocumento23 páginasClases de Elace y Caso - UPCAlonzAún no hay calificaciones
- Tema 6Documento10 páginasTema 6elcapiteniarazonAún no hay calificaciones
- Fuerzas IntermolecularesDocumento12 páginasFuerzas IntermolecularesRenzoAún no hay calificaciones
- Guia PSU Enlace Ionico, Covalente GeometriaDocumento2 páginasGuia PSU Enlace Ionico, Covalente GeometriayzavelitaAún no hay calificaciones
- Seminario N°5 - Fuerzas Intermoleculares - Problemas ResueltosDocumento9 páginasSeminario N°5 - Fuerzas Intermoleculares - Problemas ResueltosPatricio AlmadaAún no hay calificaciones
- Enlace QuimicoDocumento3 páginasEnlace QuimicoPaula Fernandez LomanaAún no hay calificaciones
- Monografia de QuimicaDocumento8 páginasMonografia de QuimicaJoa King Chaupis AdrianoAún no hay calificaciones
- Objetivo 1.5 Fuerzas Intermoleculares.Documento10 páginasObjetivo 1.5 Fuerzas Intermoleculares.Mario Alberto Juarez VillaAún no hay calificaciones
- Semana 5 Fuerzas Intermoleculares 2024-1Documento28 páginasSemana 5 Fuerzas Intermoleculares 2024-1PRINS JEREMY VILLEGAS JULCAAún no hay calificaciones
- Clase 7. Fuerzas IntermolecularesDocumento18 páginasClase 7. Fuerzas IntermolecularesDavid AlexAún no hay calificaciones
- Tema 3. Enlace QuímicoDocumento22 páginasTema 3. Enlace Químicor494y99bdkAún no hay calificaciones
- 5 ClaseDocumento41 páginas5 ClaseWILSON PABLO VALENCIA LLAJARUNAAún no hay calificaciones
- Tipos de Enlaces Cuadro Comparativo Edilson PDFDocumento12 páginasTipos de Enlaces Cuadro Comparativo Edilson PDFDaniel FierroAún no hay calificaciones
- Enlace MetálicoDocumento3 páginasEnlace MetálicoCarlos Valentino Ruiz DiazAún no hay calificaciones
- EXPOSICION QuimicaDocumento24 páginasEXPOSICION QuimicaDanna Paulina Gutierrez RosasAún no hay calificaciones
- Tabla Periódica, Enlaces, Interacciones, Estructura de Lewis y Geometría MolecularDocumento41 páginasTabla Periódica, Enlaces, Interacciones, Estructura de Lewis y Geometría MolecularfranciscoAún no hay calificaciones
- Quimica Dif Presentacion Fuerzas IntermolecularesDocumento15 páginasQuimica Dif Presentacion Fuerzas IntermolecularesTony LedesmaAún no hay calificaciones
- Fundamentos P-Fisicas F IntermolecDocumento22 páginasFundamentos P-Fisicas F IntermolecAndres RomeroAún no hay calificaciones
- Tópico 4.4 Fuerzas IntermolecularesDocumento80 páginasTópico 4.4 Fuerzas Intermolecularesdlati1Aún no hay calificaciones
- Química General II ExamenDocumento6 páginasQuímica General II ExamenAyrton SangabrielAún no hay calificaciones
- INVESTIGACIONDocumento12 páginasINVESTIGACIONAylin CantoAún no hay calificaciones
- Clase 3Documento27 páginasClase 3Leonel Andrés Mendoza MalagónAún no hay calificaciones
- Tema 8Documento2 páginasTema 8Sandra Sánchez GomezAún no hay calificaciones
- Laboratorio de Química OrgánicaDocumento23 páginasLaboratorio de Química Orgánicamarlene-stemkeAún no hay calificaciones
- Fuerzas Intermoleculares UeDocumento52 páginasFuerzas Intermoleculares Ueuser nameAún no hay calificaciones
- 8 Interacciones IntermolecularesDocumento9 páginas8 Interacciones IntermolecularesLucia GarzonAún no hay calificaciones
- Práctica Enlaces QuímicosDocumento11 páginasPráctica Enlaces QuímicosDaniel RFAún no hay calificaciones
- Clase 6 Enlaces QuimicosDocumento26 páginasClase 6 Enlaces QuimicosGustavo Fernando CumbajínAún no hay calificaciones
- Enlaces QuímicosDocumento12 páginasEnlaces QuímicosGabriel GarcíaAún no hay calificaciones
- FUERZAS IntermolecularesDocumento20 páginasFUERZAS IntermolecularesL O L U X OAún no hay calificaciones
- FUERZAS IntermolecularesDocumento20 páginasFUERZAS IntermolecularesmercedesAún no hay calificaciones
- FUERZAS IntermolecularesDocumento20 páginasFUERZAS Intermoleculareskike18mxAún no hay calificaciones
- Seminario #3Documento13 páginasSeminario #3Kristell QuezadaAún no hay calificaciones
- Fuerzas IntermolecularesDocumento20 páginasFuerzas Intermolecularesfabian ojedaAún no hay calificaciones
- Fuerzas Intermoleculares Quimica 1Documento45 páginasFuerzas Intermoleculares Quimica 1Esteban CastilloAún no hay calificaciones
- Clase 6 CB33 Polaridad de Las Moléculas y Fuerzas Intermoleculares 2017Documento34 páginasClase 6 CB33 Polaridad de Las Moléculas y Fuerzas Intermoleculares 2017luisAún no hay calificaciones
- Fuerzas IntermolecularesDocumento34 páginasFuerzas IntermolecularesJuan David Oliveros50% (4)
- Fuerzas IntermolecularesDocumento20 páginasFuerzas IntermolecularesjvvvAún no hay calificaciones
- Conceptos de Materia Parte IIDocumento22 páginasConceptos de Materia Parte IIAriadna SánchezAún no hay calificaciones
- Fuerzas IntermocularesDocumento2 páginasFuerzas Intermocularesedithzamora0524Aún no hay calificaciones
- Fuerzas de LondonDocumento7 páginasFuerzas de LondonCriiZtiian Morales0% (1)
- MCO - Fuerzas Intermoleculares UnicaDocumento31 páginasMCO - Fuerzas Intermoleculares UnicaAnthony EdgarAún no hay calificaciones
- Fuerzas IntermolecularesDocumento15 páginasFuerzas IntermolecularesWendy CedeñoAún no hay calificaciones
- FUERZAS IntermolecularesDocumento15 páginasFUERZAS Intermolecularesloquillo1Aún no hay calificaciones
- Fuerzas IntermolecularesDocumento29 páginasFuerzas IntermolecularesLeibniz FourierAún no hay calificaciones
- V-Fuerzas Intermoleculares - PPTMDocumento50 páginasV-Fuerzas Intermoleculares - PPTMBrayan Rivera ArgumedoAún no hay calificaciones
- Fuerzas IntermolecularesDocumento9 páginasFuerzas IntermolecularesMelisa A.Aún no hay calificaciones
- Tema 3 Enlace QuímicoDocumento20 páginasTema 3 Enlace Químicounai 007Aún no hay calificaciones
- Biofísica MolecularDocumento30 páginasBiofísica MolecularValeria GarciaAún no hay calificaciones
- Fuerzas Inter e IntramolecularesDocumento28 páginasFuerzas Inter e IntramolecularesGABRIELA ANDREA VALLE VARGASAún no hay calificaciones
- Práctica ALIMENTACDocumento2 páginasPráctica ALIMENTACRebeca Teresa Guevara HuamanAún no hay calificaciones
- Seminario 7Documento27 páginasSeminario 7Rebeca Teresa Guevara HuamanAún no hay calificaciones
- Ejercicios Propuestos: 1. Determinar, en Cada Caso El Tipo de Variable, de Acuerdo A Su NaturalezaDocumento1 páginaEjercicios Propuestos: 1. Determinar, en Cada Caso El Tipo de Variable, de Acuerdo A Su NaturalezaLeydi BravoAún no hay calificaciones
- Práctica ALIMENTACDocumento2 páginasPráctica ALIMENTACRebeca Teresa Guevara HuamanAún no hay calificaciones
- CALENDARIZACION DE LAS EVALUACIONES 2018-2-FinalDocumento1 páginaCALENDARIZACION DE LAS EVALUACIONES 2018-2-FinalRebeca Teresa Guevara HuamanAún no hay calificaciones
- 7-Ficha de Práctica 5 Genética Del Grupo SanguíneoDocumento3 páginas7-Ficha de Práctica 5 Genética Del Grupo SanguíneoRebeca Teresa Guevara HuamanAún no hay calificaciones
- Que Son y Donde Estan Las Uniones ComunDocumento2 páginasQue Son y Donde Estan Las Uniones ComunRebeca Teresa Guevara HuamanAún no hay calificaciones
- Examen 1Documento4 páginasExamen 1Rebeca Teresa Guevara HuamanAún no hay calificaciones
- Ejercicios Propuestos: 1. Determinar, en Cada Caso El Tipo de Variable, de Acuerdo A Su NaturalezaDocumento1 páginaEjercicios Propuestos: 1. Determinar, en Cada Caso El Tipo de Variable, de Acuerdo A Su NaturalezaLeydi BravoAún no hay calificaciones
- 02 - Ciclo SexualDocumento69 páginas02 - Ciclo Sexualandre carhuallanqui cioccaAún no hay calificaciones
- Practica No 4 Reconocimiento de ProteinasDocumento3 páginasPractica No 4 Reconocimiento de ProteinasRebeca Teresa Guevara HuamanAún no hay calificaciones
- Evaluacion VacacionalDocumento2 páginasEvaluacion VacacionalRebeca Teresa Guevara Huaman100% (2)
- Informe de DestilacionDocumento19 páginasInforme de Destilacionleonjeferson94% (17)
- Práctica ALIMENTACDocumento2 páginasPráctica ALIMENTACRebeca Teresa Guevara HuamanAún no hay calificaciones
- Art 8Documento9 páginasArt 8alexi_aldebaran2680Aún no hay calificaciones
- RolExamenesSustitutorios2014 1 MedicinaDocumento4 páginasRolExamenesSustitutorios2014 1 MedicinaRebeca Teresa Guevara HuamanAún no hay calificaciones
- Laminas ParcialDocumento77 páginasLaminas ParcialRebeca Teresa Guevara HuamanAún no hay calificaciones
- 4 Práctica de Muscular Estrido Esquelético - 2020Documento22 páginas4 Práctica de Muscular Estrido Esquelético - 2020Rebeca Teresa Guevara HuamanAún no hay calificaciones
- 5 Muscular Estriado Cardiaco y Liso - 2020Documento27 páginas5 Muscular Estriado Cardiaco y Liso - 2020Rebeca Teresa Guevara HuamanAún no hay calificaciones
- 7-San Juan de MirafloresDocumento34 páginas7-San Juan de MirafloresRebeca Teresa Guevara HuamanAún no hay calificaciones
- Informe IntroduccionDocumento13 páginasInforme IntroduccionRebeca Teresa Guevara HuamanAún no hay calificaciones
- 2b EspañolDocumento5 páginas2b EspañolRebeca Teresa Guevara HuamanAún no hay calificaciones
- El Siglo de Los CirujanosDocumento296 páginasEl Siglo de Los CirujanosGustavo Mardones Gagliano63% (8)
- 4TA SEM Situacion Comunidades Nativas 2020Documento1 página4TA SEM Situacion Comunidades Nativas 2020Rebeca Teresa Guevara HuamanAún no hay calificaciones
- 02 - Ciclo SexualDocumento69 páginas02 - Ciclo Sexualandre carhuallanqui cioccaAún no hay calificaciones
- Importancia Del Texto AcadémicoDocumento1 páginaImportancia Del Texto AcadémicoRebeca Teresa Guevara HuamanAún no hay calificaciones
- Biologia 4Documento7 páginasBiologia 4Rebeca Teresa Guevara HuamanAún no hay calificaciones
- MATERIAL de LaboratoriosDocumento5 páginasMATERIAL de LaboratoriosRebeca Teresa Guevara HuamanAún no hay calificaciones