Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Práctica No. 4 Lenguaje Químico II - Virtual
Cargado por
mofin.ponciano1Título original
Derechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
Práctica No. 4 Lenguaje Químico II - Virtual
Cargado por
mofin.ponciano1Copyright:
Formatos disponibles
ESCUELA DE QUÍMICA
DEPARTAMENTO DE QUÍMICA GENERAL
QUÍMICA GENERAL I
PRÁCTICA No. 4
LENGUAJE QUÍMICO II
1. INTRODUCCIÓN:
La introducción de la práctica Lenguaje Químico Parte I, es válida para esta práctica.
Consecuentemente, antes de dar inicio al desarrollo del Lenguaje Químico, Parte II,
conviene leer una vez más dicha introducción. Antes de realizar esta práctica, deberá
estudiar la Segunda Parte del Manual de Nomenclatura que se publicó en el grupo
2024 Información QG1 y Plataforma Moodle del curso y laboratorio, correspondiente
a los compuestos ternarios y cuaternarios.
Pág. 1
2. OBJETIVOS:
Proporcionar al estudiante los medios educacionales que alternativamente le permita:
2.1 Iniciar el estudio de la nominación de las sustancias correspondientes al mundo
material inorgánico.
2.2 Descubrir la importancia que tiene el Lenguaje Químico para el desarrollo de la
carrera electa.
2.3 Interiorizar las formas de clasificación de las sustancias químicas y las reglas del
lenguaje químico.
2.4 Interpretar los símbolos y fórmulas propias del Lenguaje Químico.
2.5 Reconocer el nombre implícito tanto en un símbolo químico como en una
fórmula química.
2.6 Escribir fórmulas químicas correspondientes a sustancias químicas inorgánicas.
2.7 Manejar con propiedad y adecuadamente la nomenclatura y la notación
química.
Práctica No. 4 Lenguaje Químico II
3. CONOCIMIENTOS PREVIOS:
Hoja de Trabajo
3.1 ¿Qué es un compuesto ternario?
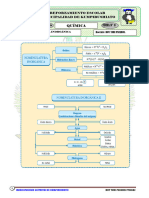
3.2 Elabore un mapa mental de los nombres genéricos de los compuestos ternarios.
3.3 ¿Qué es un compuesto cuaternario?
3.4 Elabore un mapa mental de los nombres genéricos de los compuestos
cuaternarios
3.5 ¿Qué es un ácido monoprotónico (monoprótico) y diprotónico (diprótico)?
3.6 Escribir 3 fórmulas y los respectivos nombres de cada uno de los compuestos
siguientes:
No. Compuestos Fórmula Nombre
1
2 Hidróxidos
3
1
2 Oxácidos
3 Pág. 2
1
2 Oxisales Neutras
3
1
2 Sales dobles
3
3.7 Resolver el siguiente crucigrama:
HORIZONTALES VERTICALES
2. Compuesto binario formado por oxígeno y un 1. Hidróxido cúprico
no metal 3. HMnO 4
5. Bicarbonato de Sodio 4. NH 3
7. H P O
4 2 7 6. Na O
2
8. HCl (ac) 8. Compuesto formado por
9. Molibdato doble de sodio y potasio mercurio y otro metal
10. Producto de la sustitución total de los 13. Elementos que
hidrógenos en un ácido o los hidróxidos en pertenecen al grupo VII
una base 14. Peryodato de Sodio
11. Yodato argéntico heptahidratado
12. Anhídrido hiposulfuroso 15. Teluricarbonato de litio
16. Compuesto formado por la unión de dos o 18. Ácido perclórico
más metales
Práctica No. 4 Lenguaje Químico II
17. BrO-
19. Compuesto que contiene moléculas de agua
estructuralmente unidas.
20. Compuesto binario formado por oxígeno y
un metal
Pág. 3
Cuadro de Toxicidades
3.8 No se consideran sustancias a investigar en esta práctica.
3.9 Material para práctica en casa, ver la tabla del inciso 4.1.
3.10 Diagrama de Flujo: Realizar en formato de diagrama de flujo, la secuencia de
pasos a seguir.
3.11 Citar cada uno de los conceptos investigados para dar respuesta a la hoja de
trabajo. Posteriormente en la sección de referencias debe incluir la fuente
correspondiente a cada cita en formato APA 7ma edición. Todas las citas deben
tener su respectiva referencia para tener derecho a ponderación de esta
sección.
Práctica No. 4 Lenguaje Químico II
4. MATERIALES
4.1 Práctica en casa
• Tabla periódica
• Manual de Nomenclatura de Compuestos
5. PROCEDIMIENTO
A. PRIMERA PARTE: PROCEDIMIENTO TEÓRICO:
5.1 Plataforma Moodle:
Revise las veces que considere oportuno los videos de Nomenclatura de
Compuestos Ternarios y Cuaternarios. Se tomará asistencia ÚNICAMENTE si
registra, que visualizó todos los videos correspondientes a esta práctica.
B. SEGUNDA PARTE: PROCEDIMIENTO EXPERIMENTAL (EN CASA):
Pág. 4
5.2 Resolución de la Hoja de Práctica:
Haciendo uso del manual de nomenclatura, el libro de texto del curso, la tabla
periódica y la asesoría del Instructor de laboratorio, cada grupo o equipo de
trabajo, el día de laboratorio, resolverá la siguiente HOJA DE PRÁCTICA.
5.2.1 Unir cada uno de los cationes numerados con las letras A, B, C, D, con
los aniones bajo cada número romano de manera que, en cada cuadrito
numerado en la esquina izquierda, quede escrita una fórmula química
que represente un compuesto químico. Recuerde hacer el intercambio
de valencias y simplificar cuando el caso lo requiera.
I II III IV V VI VII VIII IX
Orden Anión - -
OH CO3
2-
PO4
3-
IO3 Cr2 O7
2- 2-
CrO4 PO3
3-
Br- BO3
3-
Catión
A Li+ LiOH
B Au3+
C Ni2+
D Sb5+
Práctica No. 4 Lenguaje Químico II
5.2.2 Con base de lo expuesto en el CUADRO ANTERIOR, responder las
preguntas:
5.2.2.1 El nombre genérico de los compuestos ubicados en las columnas II, III, IV:
A) B) C)
5.2.2.2 Escribir el nombre de tres hidróxidos o bases diferentes:
A) B) C)
5.2.2.3 Escribir el nombre de tres sales haloideas:
A) B) C)
5.2.2.4 Escribir el nombre que corresponde a las fórmulas de las casillas: IVA, VIB,
IXC:
A) B) C)
5.2.2.5 Escribir el nombre genérico de las columnas V, VII y VIII:
A) B) C)
Pág. 5
5.2.2.6 Los aniones de las columnas: II, IV y V se derivan respectivamente de las
sustancias que se llaman:
A) B) C)
5.2.2.7 Usando el Sistema Stock, escribir el nombre de los compuestos que
corresponden a las casillas IIB, IIIC, IVD:
A) B) C)
5.2.2.8 El símbolo y el número de oxidación que corresponde al NO METAL de los
aniones: III, V y VI respectivamente son:
A) B) C)
5.2.2.9 Son sales neutras derivadas de oxácido monoprotónico las siguientes:
A) B) C)
5.2.2.10 Son sales neutras derivadas de ácidos diprotónicos las fórmulas:
A) B) C)
5.2.2.11 El nombre genérico de los compuestos representados por las fórmulas de
las columnas IX, I y VI respectivamente es:
A) B) C)
Práctica No. 4 Lenguaje Químico II
5.2.2.12 En el sistema estequiométrico los respectivos nombres de los compuestos
de las fórmulas VIIA, VIIB, VIIC:
A) B) C)
5.2.2.13 ¿Qué fórmulas de las del cuadro corresponden a sales de ácidos
triprotónicos?
A) B) C)
5.2.2.14 ¿Cuál es el nombre de las sustancias que representa cada una de las
fórmulas de la pregunta anterior?
A) B) C)
5.2.2.15 Corresponden a SALES NEUTRAS derivadas de un oxácido las siguientes:
A) B) C)
5.2.2.16 ¿Qué nombre tiene el compuesto que presenta cada fórmula del inciso 5.2.
2.9?
A) B) C)
Pág. 6
5.2.2.17 ¿Qué nombre tiene el compuesto que representa las fórmulas VIB, VIID,
VIIIC? Usar Sistema Stock.
A) B) C)
5.2.2.18 ¿Qué número de oxidación tiene el no metal en los iones I, II y IV?
A) B) C)
5.2.2.19 ¿Qué nombre tienen los ácidos en 5.2.2.10?
A) B) C)
6. CUESTIONARIO:
Incluir en el reporte de laboratorio.
6.1 ¿Cómo se forman los hidróxidos?
6.2 ¿Cómo se producen los oxácidos?
6.3 ¿Qué oxácidos pueden formar el bromo?
6.4 ¿En qué consiste una sal ácida?
6.5 ¿En qué consiste una sal doble?
6.6 ¿En qué consiste una aleación triple?
6.7 ¿Qué elementos forman aniones con oxígeno?
6.8 Llene los espacios en blanco del siguiente cuadro: en la columna de colocar si
pertenece a: oxisales neutras, hidratos, oxisales ácidas, oxisales dobles y
Práctica No. 4 Lenguaje Químico II
oxisales básicas y en la casilla de nombre indique el nombre correcto en el
sistema clásico o funcional de la fórmula propuesta.
Fórmula Clasificación Nombre (sistema funcional)
LiSrPO4
Na2HPO4
CuSO4.4H2O
CaSO4
Cu2SO4
CaSiO3
NH4NO2
Fe2O3.3H2O
LiFrCO3
Li3PO3
Bi(OH)2NO3
CsNO3
MgCO3
NaNO3
Al(HSO4)3
KMnO4 Pág. 7
NaHCO3
Bi(OH)CO3
Fe(NO3)3
K2SO4
CaSO3
AlPO4
ZnSO4
KClO4
NaIO3
Revisado: enero 2024
Práctica No. 4 Lenguaje Químico II
También podría gustarte
- Práctica No. 4 Química General PDFDocumento6 páginasPráctica No. 4 Química General PDF18. Katherin Magdalí Mata ChinchillaAún no hay calificaciones
- Prc3a1ctica No. 4 2019 Lenguaje Quc3admico IIDocumento5 páginasPrc3a1ctica No. 4 2019 Lenguaje Quc3admico IIHanztGomezAún no hay calificaciones
- Práctica No. 4 Lenguaje Químico II QG1 2021Documento7 páginasPráctica No. 4 Lenguaje Químico II QG1 2021Jimin MinAún no hay calificaciones
- Práctica No. 3 de LaboratorioDocumento5 páginasPráctica No. 3 de Laboratorio18. Katherin Magdalí Mata ChinchillaAún no hay calificaciones
- Práctica No. 3 Lenguaje Químico I - VirtualDocumento6 páginasPráctica No. 3 Lenguaje Químico I - Virtualmofin.ponciano1Aún no hay calificaciones
- Evaluación Quimica 10Documento3 páginasEvaluación Quimica 10Linita Nezumi Kawai100% (1)
- Química Actividades 2do. ParcialDocumento19 páginasQuímica Actividades 2do. Parcialcharo berlangaAún no hay calificaciones
- Guia 2 2o ParcialDocumento5 páginasGuia 2 2o Parcialmarifer bonillaAún no hay calificaciones
- Taller de Nomenclatura Quimica InorganicaDocumento5 páginasTaller de Nomenclatura Quimica InorganicaDalmaAún no hay calificaciones
- Taller Nomenclatura InorganicaDocumento1 páginaTaller Nomenclatura InorganicaLaura Sofia Soler CortesAún no hay calificaciones
- Listo DESEMPEÑO QUIMICA OCTAVODocumento3 páginasListo DESEMPEÑO QUIMICA OCTAVOjoseAún no hay calificaciones
- Taller-Nomenclatura-Inorganica RecuperacionDocumento2 páginasTaller-Nomenclatura-Inorganica RecuperacionPATRICIA ARIZAAún no hay calificaciones
- Actividad # 1 - QuímicaDocumento5 páginasActividad # 1 - QuímicaDaniel Peñaloza Mendinueta100% (2)
- Taller Nomenclatura InorganicaDocumento1 páginaTaller Nomenclatura InorganicaEdwin SánchezAún no hay calificaciones
- Examen Quimica para 6to Ano Diciembre 2023Documento2 páginasExamen Quimica para 6to Ano Diciembre 2023anime235fAún no hay calificaciones
- Taller Nomenclatura Inorganica 2023 1Documento1 páginaTaller Nomenclatura Inorganica 2023 1DANIEL ELIAS VELASQUEZ GARCIAAún no hay calificaciones
- Nomenclatura Inorgánica OkDocumento16 páginasNomenclatura Inorgánica OkJorge Luis Valdez Condeña100% (1)
- Quimica Kumpirushiato 8Documento2 páginasQuimica Kumpirushiato 8Roy PecerosAún no hay calificaciones
- Maritza CuestionarioDocumento5 páginasMaritza CuestionarioKristel CedeñoAún no hay calificaciones
- Guias para Imprimir QuimicaDocumento7 páginasGuias para Imprimir QuimicaJose MoraAún no hay calificaciones
- Química Semana 5 P Evidencia de AprendizajeDocumento6 páginasQuímica Semana 5 P Evidencia de AprendizajeLuis Angel Gárate ChambillaAún no hay calificaciones
- Qui MicaDocumento2 páginasQui MicaJorge GonzalesAún no hay calificaciones
- Word-Ultimo Cuestionario NomenclaturaDocumento2 páginasWord-Ultimo Cuestionario NomenclaturaLaura Paulina Yepes BarbaranAún no hay calificaciones
- Taller de Nivelacion Segundo Periodo: Indicador de Desempeño #1 NotaDocumento3 páginasTaller de Nivelacion Segundo Periodo: Indicador de Desempeño #1 NotaJesús MedinaAún no hay calificaciones
- Química 05Documento3 páginasQuímica 05sullonjoselinAún no hay calificaciones
- Plan de Mejoramiento III Peri 8 PDFDocumento5 páginasPlan de Mejoramiento III Peri 8 PDFmariamaAún no hay calificaciones
- Semana 05 Regular Banco Set - DicDocumento3 páginasSemana 05 Regular Banco Set - DicJeffer RomeroAún no hay calificaciones
- Taller Nomenclatura InorganicaDocumento3 páginasTaller Nomenclatura InorganicaOrlando Rafael Payares GuzmanAún no hay calificaciones
- Ejercicios Plan de Mejoramiento DecimoDocumento3 páginasEjercicios Plan de Mejoramiento DecimoTsukiHikariAnjeraAún no hay calificaciones
- Cuestionario EII Química InorgánicaDocumento9 páginasCuestionario EII Química InorgánicaSKYFIRE 999Aún no hay calificaciones
- IUPAC2005 ActividadesDocumento8 páginasIUPAC2005 ActividadesQuine07Aún no hay calificaciones
- TALLER DE RECUPERACION GRADO 10 III PeríodoDocumento1 páginaTALLER DE RECUPERACION GRADO 10 III Períodoandres ortizAún no hay calificaciones
- GUIA 4 NomenclaturaDocumento4 páginasGUIA 4 NomenclaturaYULIANA SOFIA LOPEZ ORTIZAún no hay calificaciones
- Química 06 CN RptaDocumento4 páginasQuímica 06 CN RptaAdrián ChancoAún no hay calificaciones
- Guia Repaso Prueba Compuestos Binarios I MediosDocumento2 páginasGuia Repaso Prueba Compuestos Binarios I MediosJuan Eduardo Herrera SeguraAún no hay calificaciones
- Prueba de NomenclaturaDocumento2 páginasPrueba de NomenclaturaRoqueAún no hay calificaciones
- Taller de QuimicaDocumento2 páginasTaller de QuimicaMayerlis Gomez100% (1)
- Laboratorio 5 JhoanaDocumento12 páginasLaboratorio 5 JhoanaOSCAR MARIO ROLANDO HERRERA GIRONAún no hay calificaciones
- Taller Nomenclatura InorganicaDocumento1 páginaTaller Nomenclatura InorganicaDiana HerreraAún no hay calificaciones
- Cuadernillo-20211218 1414239lorDocumento3 páginasCuadernillo-20211218 1414239lorYuliana yanelaAún no hay calificaciones
- TALLER NIVELATORIO, 8, Quimi 4 PeriDocumento2 páginasTALLER NIVELATORIO, 8, Quimi 4 Periandres poloAún no hay calificaciones
- IUPAC2005 ActividadesDocumento10 páginasIUPAC2005 ActividadesNicolás Ruiz GarcíaAún no hay calificaciones
- Taller Nomenclatura InorganicaDocumento2 páginasTaller Nomenclatura Inorganicafabian_granobles100% (1)
- Quimica Ades Inv21 05 Nomenclatura InorganicaDocumento2 páginasQuimica Ades Inv21 05 Nomenclatura Inorganicaveronica salazarAún no hay calificaciones
- Química 1 Práctica Semestral Semana-06Documento3 páginasQuímica 1 Práctica Semestral Semana-06KENNEDY PAUL MIRANDA MEZAAún no hay calificaciones
- Actividad de Laboratorio B Nomenclatura (Cont..)Documento2 páginasActividad de Laboratorio B Nomenclatura (Cont..)Xela ScAún no hay calificaciones
- Examen de Quimica Blo3Documento3 páginasExamen de Quimica Blo3Amado Santos AltamiranoAún no hay calificaciones
- Ejercicios de Nomenclatura InorganicaDocumento2 páginasEjercicios de Nomenclatura InorganicaMarcelo PasacaAún no hay calificaciones
- Únicamente El Estado de Oxidación +3 en SusDocumento2 páginasÚnicamente El Estado de Oxidación +3 en SusEdson Luis Egusquiza CordovaAún no hay calificaciones
- Quimica 3Documento9 páginasQuimica 3ivcscribdAún no hay calificaciones
- Trabajo Práctico 3 RevDocumento3 páginasTrabajo Práctico 3 RevYaki AlancayAún no hay calificaciones
- Taller de NomenclaturaDocumento1 páginaTaller de NomenclaturayanethAún no hay calificaciones
- Taller Nomenclatura InorganicaDocumento1 páginaTaller Nomenclatura Inorganicaアレハンド ロカバジェロ アコスタAún no hay calificaciones
- Cuadernillo Semana 06Documento2 páginasCuadernillo Semana 06MISHELL JULISA MAMANI FLORESAún no hay calificaciones
- Control de Compuestos BinariosDocumento11 páginasControl de Compuestos Binariosjonathan becerraAún no hay calificaciones
- Guia Problemas Unidad #4Documento3 páginasGuia Problemas Unidad #4lidbetAún no hay calificaciones
- Practica Com 18Documento47 páginasPractica Com 18kaesar66Aún no hay calificaciones
- Química de los compuestos de coordinaciónDe EverandQuímica de los compuestos de coordinaciónAún no hay calificaciones
- Operaciones básicas del proceso, mezclas y disoluciones. QUIE0108De EverandOperaciones básicas del proceso, mezclas y disoluciones. QUIE0108Aún no hay calificaciones
- Cambios Químicos + Experimento en El Que Se Dan Cambíos QuímicosDocumento2 páginasCambios Químicos + Experimento en El Que Se Dan Cambíos QuímicosBella OsorioAún no hay calificaciones
- Simbolos y Valencias - PDF - Conjuntos de Elementos Químicos - Tabla PeriódicaDocumento1 páginaSimbolos y Valencias - PDF - Conjuntos de Elementos Químicos - Tabla PeriódicaJermy SalazarAún no hay calificaciones
- Biomateriales Libres de Metal V2Documento22 páginasBiomateriales Libres de Metal V2José Nathan Hernández Pangan100% (1)
- Actividad 1.3Documento3 páginasActividad 1.3Gael Rodriguez Animas50% (2)
- Minerologia y PetrologiaDocumento35 páginasMinerologia y PetrologiaAlex SabinoAún no hay calificaciones
- LABORATORIO de Registro FosilDocumento2 páginasLABORATORIO de Registro FosilJuan DavidAún no hay calificaciones
- GUIA5 FINAL La Fotosintesis Respiración Decimo 2021Documento23 páginasGUIA5 FINAL La Fotosintesis Respiración Decimo 2021cristian javier medina yance100% (3)
- Enlaces Químicos2Documento6 páginasEnlaces Químicos2Sofia Rincón LondoñoAún no hay calificaciones
- Problema #1 20 Puntos: PRQ-3212 Electroquímica Industrial EXAMEN DE MESA - (4 de Agosto de 2021)Documento1 páginaProblema #1 20 Puntos: PRQ-3212 Electroquímica Industrial EXAMEN DE MESA - (4 de Agosto de 2021)ROXANAAún no hay calificaciones
- Agro Quimica 6.1Documento13 páginasAgro Quimica 6.1Dolores de Jesús Marvin YahirAún no hay calificaciones
- BIOLOGIA RESUMEN FINAL 200 Pag..Documento206 páginasBIOLOGIA RESUMEN FINAL 200 Pag..Mario SantayAún no hay calificaciones
- Tesis 100612080727 Phpapp02Documento78 páginasTesis 100612080727 Phpapp02Jose Manuel Martinez RiveraAún no hay calificaciones
- Interacciones MolecularesDocumento33 páginasInteracciones MolecularesQfb Sergio Jaime Paz GonzálezAún no hay calificaciones
- E-2do PPT Historia y Ramas de La QuimicaDocumento17 páginasE-2do PPT Historia y Ramas de La Quimicasoledad leon100% (1)
- Taller 1 Nivelatorio 2021-1Documento3 páginasTaller 1 Nivelatorio 2021-1Pablo ZapataAún no hay calificaciones
- CosmeticosDocumento28 páginasCosmeticosRichard TorresAún no hay calificaciones
- Tema 7 - Formulacion OrganicaDocumento161 páginasTema 7 - Formulacion OrganicaLaura Esosa Osazuwa MathewAún no hay calificaciones
- Correcciones Quimica Derlys UDocumento38 páginasCorrecciones Quimica Derlys UAndres Suarez Gonzalez100% (2)
- Estudio de Las Enzimas Amilasas-Efecto de La Temperatura y PH en La Actividad EnzimáticaDocumento6 páginasEstudio de Las Enzimas Amilasas-Efecto de La Temperatura y PH en La Actividad EnzimáticaJulia EsquivelAún no hay calificaciones
- Pia BorradorDocumento7 páginasPia BorradorChaires Trejo Héctor YahirAún no hay calificaciones
- Previo 11 Sintesis Rojo paraDocumento8 páginasPrevio 11 Sintesis Rojo paraDaniel RomeroAún no hay calificaciones
- Bitacora No.11Documento6 páginasBitacora No.11Sponja75Aún no hay calificaciones
- UNIDAD XIII - HidrocarburosDocumento152 páginasUNIDAD XIII - HidrocarburosMariel QuinteroAún no hay calificaciones
- Apuntes Tema 3Documento8 páginasApuntes Tema 3Ricard CrzAún no hay calificaciones
- Infografia Linea Del Tiempo Original Azul PDFDocumento2 páginasInfografia Linea Del Tiempo Original Azul PDFLaury FrancoAún no hay calificaciones
- Aldehidos y CetonasDocumento4 páginasAldehidos y CetonasWilson ChoqueAún no hay calificaciones
- Fósforo en ColasDocumento15 páginasFósforo en ColasAaronAún no hay calificaciones
- Efectos de La Administración de Una Dosis Creciente Aguda de Dióxido de Cloro, Clorato y Clorito A Voluntarios Varones Adultos Sanos NormalesDocumento1 páginaEfectos de La Administración de Una Dosis Creciente Aguda de Dióxido de Cloro, Clorato y Clorito A Voluntarios Varones Adultos Sanos Normalesjuan gomezAún no hay calificaciones
- Normas NMXDocumento19 páginasNormas NMXROBERTO MIRANDAAún no hay calificaciones
- Estabilizacion de Suelos Quimica (Presentacion) - 1Documento12 páginasEstabilizacion de Suelos Quimica (Presentacion) - 1Angel MVAún no hay calificaciones