Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Práctica Gases Ideales 4
Práctica Gases Ideales 4
Cargado por
yara0 calificaciones0% encontró este documento útil (0 votos)
9 vistas1 páginaLos estudiantes realizaron un experimento sobre gases ideales midiendo la presión y temperatura. Calcularon la masa de gas en el volumen dado y luego usaron la ecuación de los gases ideales para calcular las presiones reales correspondientes a diferentes temperaturas medidas. Concluyeron que hubo un error significativo en las mediciones de presión y temperatura reales debido a problemas en el procedimiento experimental.
Descripción original:
Termodinámica.
Derechos de autor
© © All Rights Reserved
Formatos disponibles
PDF, TXT o lea en línea desde Scribd
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoLos estudiantes realizaron un experimento sobre gases ideales midiendo la presión y temperatura. Calcularon la masa de gas en el volumen dado y luego usaron la ecuación de los gases ideales para calcular las presiones reales correspondientes a diferentes temperaturas medidas. Concluyeron que hubo un error significativo en las mediciones de presión y temperatura reales debido a problemas en el procedimiento experimental.
Copyright:
© All Rights Reserved
Formatos disponibles
Descargue como PDF, TXT o lea en línea desde Scribd
0 calificaciones0% encontró este documento útil (0 votos)
9 vistas1 páginaPráctica Gases Ideales 4
Práctica Gases Ideales 4
Cargado por
yaraLos estudiantes realizaron un experimento sobre gases ideales midiendo la presión y temperatura. Calcularon la masa de gas en el volumen dado y luego usaron la ecuación de los gases ideales para calcular las presiones reales correspondientes a diferentes temperaturas medidas. Concluyeron que hubo un error significativo en las mediciones de presión y temperatura reales debido a problemas en el procedimiento experimental.
Copyright:
© All Rights Reserved
Formatos disponibles
Descargue como PDF, TXT o lea en línea desde Scribd
Está en la página 1de 1
UNIVERSIDAD DE GUADALAJARA
CENTRO UNIVERSITARIO DEL NORTE
INGENIERÍA MECÁNICA-ELÉCTRICA
GASES IDEALES
ALUMNOS: JOSÉ VÉLEZ SOLÓRZANO
DANIEL FLORES MARTÍNEZ
JUAN JOSÉ LÓPEZ MUÑOZ
YARA GAUADALUPE GABRIEL SÁNCHEZ
PRÁCTICA
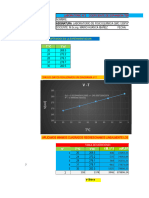
TABLA PRESIÓN TEMPERATURA CÁLCULO DE LA MASA CONCLUSIÓN
𝑚 Conforme las diferentes presentaciones de la
T (C°) P (Pa) 𝑑= evaluación de presión y temperatura el cambio
𝑉
27 107.586 fue totalmente diferente en cuanto a la presión
𝑚 =𝑑∗𝑉 y temperaturas reales ya que fue un
28.7 978.057 procedimiento en el experimento fue prueba y
𝑘𝑔
30 1515.988 𝑚 = 997 ∗ 0.000529𝑚 3 error en la cual comparando y en esta tomando
𝑚3
en cuenta las distancias obtenidas. No se
31.2 2484.264 𝑚 = 0.527 𝑘𝑔 espera un cambio tan excesivo de la presión a
32.9 3217.807 temperatura real.
CÁLCULO PRESIÓN Y
FOTO
GRÁFICA PRESIÓN TEMPERATURA TEMPERATURAS REALES
𝑇1 = 19°𝐶
𝑇2 = 20.7°𝐶 𝑃𝑉 = 𝑚𝑅𝑇 𝑚𝑅𝑇
PRESIÓN VS 𝑇3 = 22°𝐶 𝑃=
P 𝑉
3500 TEMPERATURA 3217.807
𝑇4 = 23.2°𝐶
𝑇5 = 24.9°𝐶
Series1 Series2 Lineal (Series2) 𝑘𝑗
3000 (0.527 𝑘𝑔) (0.2870 𝑘) (292𝑘) 1000𝑃𝑎
𝑘𝑔
2484.264 𝑃= = 83487160.68 𝑃𝑎
0.000529𝑚 3 1𝑘𝑃𝑎
2500
y = 772.66x - 657.25 𝑘𝑗
(0.527 𝑘𝑔) (0.2870 𝑘) (293.7𝑘) 1000𝑃𝑎
𝑘𝑔
2000 𝑃= 3
= 83973216.07 𝑃𝑎
1515.988 0.000529𝑚 1𝑘𝑃𝑎
1500 𝑘𝑗
(0.527 𝑘𝑔) (0.2870 𝑘) (295𝑘) 1000𝑃𝑎
978.057 𝑘𝑔
𝑃= 3
= 84344905.48 𝑃𝑎
1000 0.000529𝑚 1𝑘𝑃𝑎
𝑘𝑗
500 (0.527 𝑘𝑔) (0.2870 𝑘) (296.2𝑘) 1000𝑃𝑎
107.586 𝑘𝑔
27 28.7 30 31.2 32.9 𝑃= 3
= 84688003.4 𝑃𝑎
0.000529𝑚 1𝑘𝑃𝑎
0
1 2 3 4 5
T 𝑘𝑗
(0.527 𝑘𝑔) (0.2870 𝑘) (297.9𝑘) 1000𝑃𝑎
𝑘𝑔
𝑃= = 85174058.79 𝑃𝑎
0.000529𝑚 3 1𝑘𝑃𝑎
También podría gustarte
- P.8.determinación Del Coeficiente de Difusión de Gases Del Sistema Aire-AcetonaDocumento4 páginasP.8.determinación Del Coeficiente de Difusión de Gases Del Sistema Aire-AcetonaElizabeth Huerta100% (1)
- Practico de Hidrologia 2Documento17 páginasPractico de Hidrologia 2roger50% (2)
- Práctica Nro 11Documento11 páginasPráctica Nro 11Alex FernandoAún no hay calificaciones
- Practica 3 Determinacion de La Capacidad Calorifica de Los LiquidosDocumento3 páginasPractica 3 Determinacion de La Capacidad Calorifica de Los LiquidosMariana Buritica NaranjoAún no hay calificaciones
- Camisa y SerpentinDocumento23 páginasCamisa y Serpentinkdra0715Aún no hay calificaciones
- Lab 2 QMC 1206 A R - 094722Documento9 páginasLab 2 QMC 1206 A R - 094722alejandroflorestolaAún no hay calificaciones
- Laboratorio Fenomenos 1 y 2Documento15 páginasLaboratorio Fenomenos 1 y 2Daniel CarlosAún no hay calificaciones
- Laboratorio 1 y 2 FenomenosDocumento15 páginasLaboratorio 1 y 2 FenomenosDaniel CarlosAún no hay calificaciones
- Equivalente ElectricoDocumento5 páginasEquivalente ElectricoAbigail Ancasi LauraAún no hay calificaciones
- Laboratorio 1 - Calor de Disolucion y NeutralizacionDocumento5 páginasLaboratorio 1 - Calor de Disolucion y NeutralizacionSebastian ArangoAún no hay calificaciones
- Equivalente Electrico RevisarDocumento2 páginasEquivalente Electrico RevisarGuillermo LarreaAún no hay calificaciones
- Informe Calor EnergiaDocumento4 páginasInforme Calor EnergiaIsabella MartinezAún no hay calificaciones
- Presentación Presion de Vapor-LAB2-Agosto 2021-Enero 2022Documento9 páginasPresentación Presion de Vapor-LAB2-Agosto 2021-Enero 2022José Luis González ZárateAún no hay calificaciones
- Escala Absoluta de TemperaturaDocumento5 páginasEscala Absoluta de TemperaturaEver Donaldo Pinzon JimenezAún no hay calificaciones
- TP5 Equilibrio HeterogeneoDocumento9 páginasTP5 Equilibrio Heterogeneosanandrea2002Aún no hay calificaciones
- TermoDocumento9 páginasTermoalejandro villa pradoAún no hay calificaciones
- 1er. Rec. 1er. Parcial Con Resolucion 8-11-21Documento4 páginas1er. Rec. 1er. Parcial Con Resolucion 8-11-21Facundo BellaeraAún no hay calificaciones
- Fase 3 Aplicación de La Primera Ley de La Termodinámica en Situaciones IndustrialesDocumento11 páginasFase 3 Aplicación de La Primera Ley de La Termodinámica en Situaciones IndustrialesAle ZapataAún no hay calificaciones
- PRÁCTICA EntropiaDocumento11 páginasPRÁCTICA EntropiaAndrea GuangasigAún no hay calificaciones
- Practica 2 Medición de Presión Total, Presión Dinámica y Presión EstáticaDocumento6 páginasPractica 2 Medición de Presión Total, Presión Dinámica y Presión EstáticaNathalyTorresAún no hay calificaciones
- Informe Lab. FisicoquimicaDocumento5 páginasInforme Lab. FisicoquimicaAmanda ArizaAún no hay calificaciones
- Inf 2.0 Equivalente Electrico Calsina Mallcu Jhuliana - 030954Documento7 páginasInf 2.0 Equivalente Electrico Calsina Mallcu Jhuliana - 030954Jhuliana CalsinaAún no hay calificaciones
- Vmlvst°C: Los Volumenes Sugeridos A Intervalos de Temperatura SonDocumento7 páginasVmlvst°C: Los Volumenes Sugeridos A Intervalos de Temperatura SonAlison GonzalesAún no hay calificaciones
- 2iv51-3-Intercambiador Vertical-Mata Ruiz Hannia ClaredDocumento24 páginas2iv51-3-Intercambiador Vertical-Mata Ruiz Hannia ClaredHannia Mata RuizAún no hay calificaciones
- Apendice Lab 2 FisqmcDocumento9 páginasApendice Lab 2 FisqmcalejandroflorestolaAún no hay calificaciones
- Tareas 4 de TermodinamicaDocumento8 páginasTareas 4 de TermodinamicavitorioAún no hay calificaciones
- Presión de Vapor de Un Líquido PuroDocumento15 páginasPresión de Vapor de Un Líquido PuroVanessa CastroAún no hay calificaciones
- Lab. #02 Desplzamiento de Flujo Calorifico A Travez de Un Solido MetalicoDocumento5 páginasLab. #02 Desplzamiento de Flujo Calorifico A Travez de Un Solido Metalicoruel yanio sierra mezaAún no hay calificaciones
- Practica 9 SiDocumento9 páginasPractica 9 SiJazmín SaldivarAún no hay calificaciones
- Ilovepdf MergedDocumento6 páginasIlovepdf MergedPierre LlerenaAún no hay calificaciones
- Practica No 3 Calorimetría A Presión ConstanteDocumento4 páginasPractica No 3 Calorimetría A Presión ConstanteSebastian GuerreroAún no hay calificaciones
- Informe de Laboratorio Nro3Documento14 páginasInforme de Laboratorio Nro3NELLY YOHANA TARAZONA GONZALESAún no hay calificaciones
- Huarita Adrian LAB2Documento6 páginasHuarita Adrian LAB2VANESSA ARELIS HUARITA ADRIANAún no hay calificaciones
- Reporte 2, CalorDocumento2 páginasReporte 2, CalorGabriell CotaAún no hay calificaciones
- Lopezvargas Oscaralfonso M12S3 UnaleydelosgasesDocumento4 páginasLopezvargas Oscaralfonso M12S3 UnaleydelosgasesLovo Vargas100% (19)
- Variacion de Temperatura y CalorimetriaDocumento13 páginasVariacion de Temperatura y CalorimetriaOmar LopezAún no hay calificaciones
- Practica 5 Lab TermiodinamicaDocumento9 páginasPractica 5 Lab TermiodinamicadoomAún no hay calificaciones
- Práctica de Evaporador de Simple EfectoDocumento10 páginasPráctica de Evaporador de Simple EfectoJazbeth JimenezAún no hay calificaciones
- Taller de Termodinamica Química No 1Documento25 páginasTaller de Termodinamica Química No 1LUZ ANDREA RAMOS VITOLAAún no hay calificaciones
- Balance de CompresorDocumento11 páginasBalance de CompresorFabianFloresAAún no hay calificaciones
- Practica 3 Tuvo Venturi IPNDocumento5 páginasPractica 3 Tuvo Venturi IPNEdgar DomínguezAún no hay calificaciones
- Laboratorio 7 FinalDocumento2 páginasLaboratorio 7 FinalSamuel TorresAún no hay calificaciones
- Memorias de Calculo Grupo 2Documento19 páginasMemorias de Calculo Grupo 2omar fonsecaAún no hay calificaciones
- PRÁCTICA 1 Termo DE SUSTANCIAS PURASDocumento7 páginasPRÁCTICA 1 Termo DE SUSTANCIAS PURASEstrella VillegasAún no hay calificaciones
- Proceso Adiabático: Caso 0Documento7 páginasProceso Adiabático: Caso 0ALEXIS GAEL REBOLLEDO VALENCIAAún no hay calificaciones
- Equivalente Electrico Humerez Aliaga KevinDocumento15 páginasEquivalente Electrico Humerez Aliaga KevinKevin Humerez AliagaAún no hay calificaciones
- Tarea en Clase 2 Grupo 1Documento27 páginasTarea en Clase 2 Grupo 1Patricio Toaquiza ChiguanoAún no hay calificaciones
- EntropiaDocumento14 páginasEntropiaVeronica izquierdo gomezAún no hay calificaciones
- DiscusionDocumento13 páginasDiscusionAstrid SantibañezAún no hay calificaciones
- Taller Primer Corte TermodinamicaDocumento5 páginasTaller Primer Corte TermodinamicaAnggie Gabriela Palacios LizarazoAún no hay calificaciones
- Balance Térmico y EntropíaDocumento11 páginasBalance Térmico y EntropíaEva RhenalsAún no hay calificaciones
- Termo Uni 4 ExPDocumento8 páginasTermo Uni 4 ExPAlberto AdrianoAún no hay calificaciones
- Equivalencia Caloria-Joule WCDocumento4 páginasEquivalencia Caloria-Joule WCWilson CárdenasAún no hay calificaciones
- Fase 3 Aplicación de La Primera Ley de La Termodinámica en Situaciones IndustrialesDocumento11 páginasFase 3 Aplicación de La Primera Ley de La Termodinámica en Situaciones IndustrialesYeisson FonsecaAún no hay calificaciones
- Torre Enfriamiento EmpacadoDocumento14 páginasTorre Enfriamiento EmpacadoNathanael RiveraAún no hay calificaciones
- Clase 2Documento7 páginasClase 2Oscar AsistiriAún no hay calificaciones
- EXPOTERMODocumento2 páginasEXPOTERMOTonatiuhAún no hay calificaciones
- Proy. TermoDocumento18 páginasProy. Termoandy villar lobatoAún no hay calificaciones
- Cálculo de La ViscosidadDocumento5 páginasCálculo de La ViscosidadLópez Ascención JesúsAún no hay calificaciones
- Lab Ciclo de RefrigeraciónDocumento7 páginasLab Ciclo de Refrigeraciónmaria gonzalezAún no hay calificaciones
- Ingeniería química. Soluciones a los problemas del tomo IDe EverandIngeniería química. Soluciones a los problemas del tomo IAún no hay calificaciones
- Mapa Mental y ConceptualDocumento2 páginasMapa Mental y ConceptualyessiAún no hay calificaciones
- Muro de Concreto CiclopeoDocumento4 páginasMuro de Concreto CiclopeoAldair Lope RamosAún no hay calificaciones
- Manual de Medicion de FluidosDocumento169 páginasManual de Medicion de FluidosLuisa RodríguezAún no hay calificaciones
- Quimica de La Madera-1Documento36 páginasQuimica de La Madera-1Marco SoLedAún no hay calificaciones
- Ejercicio de RuidoDocumento1 páginaEjercicio de RuidoMaribel PeláezAún no hay calificaciones
- Ing Civl Adscripcion Sanitaria 2 221 443 PDFDocumento223 páginasIng Civl Adscripcion Sanitaria 2 221 443 PDFAlvaro Alejandro Guzman GarciaAún no hay calificaciones
- ChatGPT - Que Es Un MegaparsecDocumento5 páginasChatGPT - Que Es Un MegaparsecsgousseAún no hay calificaciones
- Intento 2Documento9 páginasIntento 2LAURA ESTER ROMERO NUÑEZAún no hay calificaciones
- CTM-Ejemplo ExamenDocumento7 páginasCTM-Ejemplo ExamenterterAún no hay calificaciones
- Practicas de Mecanica de Fluidos 56912 DownloableDocumento120 páginasPracticas de Mecanica de Fluidos 56912 DownloableMilton JaraAún no hay calificaciones
- Práctica 3. Determinación de La Constante Universal de Los Gases Ideales - Equipo1Documento8 páginasPráctica 3. Determinación de La Constante Universal de Los Gases Ideales - Equipo1Luis LaraAún no hay calificaciones
- Descargadores de Sobretension 1Documento5 páginasDescargadores de Sobretension 1jairo mahechaAún no hay calificaciones
- Final ApuntesDocumento54 páginasFinal Apuntesp4mdh4mwg5Aún no hay calificaciones
- Proyecto IPM458 1 19Documento3 páginasProyecto IPM458 1 19Sergio Urzua GajardoAún no hay calificaciones
- Procesos de Manufactura No ConvencionalesDocumento6 páginasProcesos de Manufactura No ConvencionalesJorge Enrique0% (2)
- T 08 Motores TérmicosDocumento17 páginasT 08 Motores TérmicosClaudia C .MuñozAún no hay calificaciones
- 25-26 Enrique Escobedo Hernandez - Luis Alberto Zamora CamposDocumento191 páginas25-26 Enrique Escobedo Hernandez - Luis Alberto Zamora CamposFidel RamonAún no hay calificaciones
- 2015 LMFFL Pra8 Eq1 6B RevLUTDocumento21 páginas2015 LMFFL Pra8 Eq1 6B RevLUTMayren RománAún no hay calificaciones
- FQ2 Tarea 3Documento27 páginasFQ2 Tarea 3Brenda GallegosAún no hay calificaciones
- 2° Parcial Recuperatorio Tema 2 ClaveDocumento4 páginas2° Parcial Recuperatorio Tema 2 ClaveLeandro Valentin SilveroAún no hay calificaciones
- Analisis de Velocidades y Aceleraciones PDFDocumento11 páginasAnalisis de Velocidades y Aceleraciones PDFJosé M. SánchezAún no hay calificaciones
- Practica 4 Fuerzas de Arrastre y SustentacionDocumento12 páginasPractica 4 Fuerzas de Arrastre y SustentacionJorgeGarciaAún no hay calificaciones
- Fisica 3ero 2020 11 Hidrostatica PDFDocumento2 páginasFisica 3ero 2020 11 Hidrostatica PDFJavierFernandoSandovalDiosesAún no hay calificaciones
- Viscosidad, Capilaridad CuestionarioDocumento4 páginasViscosidad, Capilaridad CuestionarioJhanfranAún no hay calificaciones
- Tema 11a PresentDocumento16 páginasTema 11a Presentwilfredoroman16Aún no hay calificaciones
- 3.climatología & MeteorologíaDocumento25 páginas3.climatología & MeteorologíaEdAún no hay calificaciones
- Taller Unad Campos MagnéticosDocumento4 páginasTaller Unad Campos MagnéticosOSCAR CORREAAún no hay calificaciones
- Deber Acústica Musical 1Documento3 páginasDeber Acústica Musical 1José A. MedinaAún no hay calificaciones
- Electrocardiogram ADocumento22 páginasElectrocardiogram Asurahima mendezAún no hay calificaciones