Documentos de Académico
Documentos de Profesional
Documentos de Cultura
5.1. - Apuntes Enlace Quimico
Cargado por
Yuyunis De la cruzTítulo original
Derechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
5.1. - Apuntes Enlace Quimico
Cargado por
Yuyunis De la cruzCopyright:
Formatos disponibles
UNIDAD 3: ENLACE QUIMICO E INTERACCIONES
MOLECULARES.
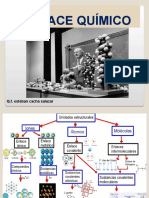
ENLACE QUIMICO
Átomos Aislados Átomos No aislados
Átomos de la tabla Átomos en la naturaleza.
En conjunto
Actividad Química
Reside en los electrones, es decir que los electrones de valencia dan o generan la
actividad química.
ELECTRONES DE VALENCIA: Electrones localizados en la última capa o nivel de
energía de un átomo.
Los átomos se unen entre sí por medio de fuerzas de atracción, las cuales los atraen y
los mantienen unidos a nivel de los electrones de valencia; así, un ENLACE
QUÍMICO es la unión entre átomos y entre moléculas por medio de fuerzas de
atracción.
Átomos no aislados: Agrupaciones de átomos implican uniones y por lo tanto ACTIVIDAD
QUÍMICA
Es un tipo de enlace
Enlace Químico
Es un conjunto de fuerzas que mantiene unido a los átomos, iones o moléculas.
Se produce porque los átomos en conjunto son MÁS ESTABLES que los átomos aislados,
y UNIDOS OCUPAN UNA MÍNIMA ENERGÍA.
Los átomos se combinan para estar más estables.
Los responsables de formar los enlaces químicos son los ELECTRONES DE
VALENCIA (electrones ubicados en la última capa electrónica).
Los enlaces químicos pueden ser de tres tipos:
1. Enlace Metálico.
2. Enlace Iónico.
3. Enlace Covalente.
1. Enlace Metálico
Se establecen entre átomos metálicos. Estos átomos dejan ē libres en orbitales s y
d, formando así, un conjunto de Iones positivos que se ordenan en forma de redes.
En general ceden los electrones para poder parecerse al gas noble más cercano y
se ubican en el grupo 1 (todos liberan un electrón) y 2 (todos liberan 2 electrones) y
desde el 3 al 12 (elementos metales).
Siempre forman iones positivos.
Recordar: los metales siempre se quieren parecer al gas noble más cercano.
Los ē liberados se deslocalizan, moviéndose libremente por una extensa región
entre los iones positivos, formando la nube electrónica.
Este tipo de enlace se produce cuando se combinan entre sí los elementos metálicos,
es decir, elementos de electronegatividad baja y que se diferencian poco.
Habitualmente estas sustancias metálicas están formadas por átomos de un solo
elemento aunque también se obtienen por combinación de elementos (aleaciones).
Ejem: bronce (cobre + estaño), Hierro (cobre + carbono + hierro), Imanes, etc.
Propiedades Físicas: -Alta conductividad térmica y eléctrica, esta propiedad
está asociada con el libre movimiento de los electrones entre
las capas de la red.
-Maleables (capacidad de ser moldeados con herramientas)
se debe a que las capas de los cationes metálicos se deslizan
una sobre otras..
-Dúctiles (factibles de hilar), su deformación no implica una
rotura de enlaces.
Aplicación de Aleaciones en Ortopedia: La aplicación principal de estas
aleaciones, son remplazar sistemas de unión como la cadera y la rodilla, se
utilizan también para realizar placas para huesos, tornillos, clavos, etc.
2. Enlace Iónico
Se forma por atracción electrostática entre los iones de distintas cargas (Las
interacciones que se presentan entre iones de carga opuestas.)
Metal (catión, pierde e) + No metal (anión, gana e).
Ejem: sodio + cloro, litio + flúor
Generalmente forman redes cristalinas.
Clasificación de los Iones:
ANIÓN carga eléctrica negativa exceso de electrones
- Formados por no metales.
CATIÓN carga eléctrica positiva déficit de electrones
Formados a partir de metales
Propiedades Físicas: -En general son sólidos quebradizos.
-Tienen puntos de ebullición muy altos.
-Las fuerzas electrostáticas organizan los iones en un arreglo
rígido tridimensional bien ordenado.
-Son solubles en agua y líquidos polares.
-Son enlaces resultantes de la interacción entre los metales de
los grupos 1 ó IA y 2 ó IIA y los no metales de los grupos 14 ó
IVA 15 ó VA ,16 Ó VIA y 17 ó VIIA. (ejem:
3. Enlace Covalente
Se forma entre dos átomos no metálicos (11), por compartición de ē de valencia.
No metal + No metal.
El par de ē compartidos giran alrededor de ambos átomos de un orbital perteneciente a
la molécula.
Hay un compartir de electrones (no hay un electrón que le ceda con mayor intensidad
al otro)
Ejem: H2, O2, N2, S2, H2O, CO2, HCL, etc, cosas cotidianas.
Tipos de enlaces: Dependiendo de electrones compartidos:
Simple átomos enlazados comparten un par de electrones de su última
capa (un electrón cada uno). Separar los átomos es mucho más facíl.
Doble átomos enlazados comparten dos pares de electrones de su última
capa (un electrón cada uno)
Triple átomos enlazados aportan tres pares de electrones, es decir, seis en
total. Tienes mucha más fuerza por ende es más difícil separarlo.
Dependiendo de la polaridad de los compuestos formados:
La diferencia de electronegatividad entre los átomos de un enlace determina que átomo
adquiere la mayor parte de la densidad electrónica del enlace, y por lo tanto determina
el carácter del enlace.
Para lograr saber si algún átomo es apolar o polar se debe saber la electronegatividad.
La distancia entre dos átomos enlazados decrece al aumentar el número de pares
electrones compartidos.
Mientras más enlaces tenga el enlace, más difícil va a ser de separarlo.
Covalente Polar:
- Los átomos son diferentes, la unión de ellos tienden a atraer los ē con
más fuerza hacia si (un átomo más electronegativo).
- Se observa una nube asimétrica.
- Según su electronegatividad se puede determinar en el rango de 0 a 0,4.
- Se simboliza mediante una flecha dirigida hacia el átomo que más atrae el
par de electrones.
Nube electrónica
La nube se encuentras “más
gordita” hacia el flúor ya que es
más electronegativo
Covalente Apolar (No polar):
- Los átomos son iguales o con la misma electronegatividad, forma
moléculas homoatómicas.
- Se observa una nube simétrica.
- Según su electronegatividad se puede determinar en un rango de 0,41 a 1,7.
Generalmente los átomos diatónicos son apolares. Nube electrónica
PROPIEDADES FÍSICAS
Prácticamente están presentes en cualquier estado de agregación de la
materia: sólido- líquido y gases.
Estos compuestos se disuelven fácilmente en solventes polares o no polares
(apolares), esto depende si el compuestos tiene enlace covalente polar o no
polar.
Estos compuestos presentan variados puntos de ebullición y generalmente
son bajos.
Al momento de disolverse no forman iones y por esto no se comportan como
electrolitos (no conducen electricidad).
La mayoría de las moléculas están en estado gaseoso. (H2, O2, etc)
Ejem: yodo, bromo, cloro, etc.
También podría gustarte
- Ejercicios TeóricosDocumento22 páginasEjercicios TeóricosMar Carrasco CarrascoAún no hay calificaciones
- Trabajo Fisica y Quimica IntermolecularDocumento27 páginasTrabajo Fisica y Quimica IntermolecularFernando M. TorresAún no hay calificaciones
- Guía para El Examen de La Unidad IIIDocumento22 páginasGuía para El Examen de La Unidad IIIRene Israel Ibarra100% (1)
- Química - Enlaces químicosDocumento5 páginasQuímica - Enlaces químicosAgnesAún no hay calificaciones
- 1.7 Enlaces QuímicosDocumento57 páginas1.7 Enlaces QuímicosEmi ZárateAún no hay calificaciones
- Tema 2 B Enlace QuímicoDocumento15 páginasTema 2 B Enlace QuímicoAselaAún no hay calificaciones
- Uniones QuìmicasDocumento28 páginasUniones QuìmicasAlu AbadieAún no hay calificaciones
- Enlaces PrimariosDocumento7 páginasEnlaces PrimariosEnrique Diaz RubioAún no hay calificaciones
- 9 Enlace QuímicoDocumento9 páginas9 Enlace Químicojosé felicianoAún no hay calificaciones
- UD2 - Enlace Químico-2Documento22 páginasUD2 - Enlace Químico-2Libertad Sanchez GonzalezAún no hay calificaciones
- Unidad 4-ENLACES QUIMICOS-Parte 1Documento55 páginasUnidad 4-ENLACES QUIMICOS-Parte 1Sintia RedAún no hay calificaciones
- CLASE 7-Enlace QuímicoDocumento59 páginasCLASE 7-Enlace Químicojhonnatan loyolaAún no hay calificaciones
- Enlaces QuimicoDocumento22 páginasEnlaces Quimicomandrake1233Aún no hay calificaciones
- Enlaces Atomicos y Estructturas CristalinasDocumento13 páginasEnlaces Atomicos y Estructturas CristalinasMarcial GonzalezAún no hay calificaciones
- Enlace QuímicoDocumento9 páginasEnlace QuímicoCamilaAún no hay calificaciones
- Diapositivas Enlace AtomicoDocumento29 páginasDiapositivas Enlace Atomicoyonatan yovaniAún no hay calificaciones
- Apuntes de Quimica Inorgánica Unidad 2Documento33 páginasApuntes de Quimica Inorgánica Unidad 2Isidoro Valente Torres DiazAún no hay calificaciones
- Cristalografia Estructural (2021)Documento8 páginasCristalografia Estructural (2021)Fernando Velasquez DiazAún no hay calificaciones
- Material 2022B1 IND201 01 151291Documento26 páginasMaterial 2022B1 IND201 01 151291ALEXANDER PAUL LIQUINCHANA MARTINEZAún no hay calificaciones
- Enlaces Químicos en MedicinaDocumento30 páginasEnlaces Químicos en MedicinaChristian Raul Rojas Tarrillo25% (4)
- Estructura Atomica y Enlace en MaterialesDocumento22 páginasEstructura Atomica y Enlace en Materialesmoises moralesAún no hay calificaciones
- Enlace QuimicoDocumento19 páginasEnlace QuimicoDiego Hanan HerreraAún no hay calificaciones
- Enlaces químicos octavo gradoDocumento9 páginasEnlaces químicos octavo gradoFreddy Santiago MartinezAún no hay calificaciones
- Enlaces químicos y fuerzas intermolecularesDocumento3 páginasEnlaces químicos y fuerzas intermolecularesAriadnaAún no hay calificaciones
- Química PC 2do E 26abr30Documento8 páginasQuímica PC 2do E 26abr30Lore SilveraAún no hay calificaciones
- Tipos de enlaces químicos: metálico, iónico, covalente polar y no polarDocumento4 páginasTipos de enlaces químicos: metálico, iónico, covalente polar y no polarDesInc Colectivo de DiseñoAún no hay calificaciones
- ACFrOgB0FfLHVzxBqcTDmNHmwn5 FV8Il HWKah2YE3CGdVcGvjLaUwKYk 1Iqz1vxvalI Za7Tf9uL3WM0BRkuKD7izobB DuvRzSYiRGfCGg0MHxUDruDQ5Ej DYN2i0s8deopNW5s Ez95JsDocumento9 páginasACFrOgB0FfLHVzxBqcTDmNHmwn5 FV8Il HWKah2YE3CGdVcGvjLaUwKYk 1Iqz1vxvalI Za7Tf9uL3WM0BRkuKD7izobB DuvRzSYiRGfCGg0MHxUDruDQ5Ej DYN2i0s8deopNW5s Ez95Jsangela moyaAún no hay calificaciones
- Trabajo de Quimica.Documento5 páginasTrabajo de Quimica.Anthony LomasAún no hay calificaciones
- Informe 3Documento14 páginasInforme 3Miguel Angel Chavez GuillenAún no hay calificaciones
- Practica 4Documento9 páginasPractica 4ingdaniel.biomedAún no hay calificaciones
- Enlaces Quimicos Primarios y SecundariosDocumento12 páginasEnlaces Quimicos Primarios y SecundariosAgustin Flores AscencionAún no hay calificaciones
- Química InorgánicaDocumento7 páginasQuímica InorgánicaRoxana100% (1)
- Enlaces QuimicosDocumento40 páginasEnlaces QuimicosMike FonsecaAún no hay calificaciones
- Uniones - Quimicas Pawer Point (Clase2) - 2016Documento27 páginasUniones - Quimicas Pawer Point (Clase2) - 2016MiLulu lunaAún no hay calificaciones
- Qué Es Un Enlace IónicoDocumento5 páginasQué Es Un Enlace IónicoBrithani MeraAún no hay calificaciones
- Enlaces químicos: covalente, iónico y metálicoDocumento11 páginasEnlaces químicos: covalente, iónico y metálicoTalia Belén Cabral CabreraAún no hay calificaciones
- Enlaces QuímicosDocumento20 páginasEnlaces QuímicosheydyAún no hay calificaciones
- Enlaces QuimicosDocumento3 páginasEnlaces QuimicosJessica MendezAún no hay calificaciones
- .Nlace QuimicoDocumento25 páginas.Nlace Quimicolizbeth jimenezAún no hay calificaciones
- 804 U1 - Uniones QuimicasDocumento4 páginas804 U1 - Uniones QuimicaswinxtexAún no hay calificaciones
- Quimica 10° #33Documento7 páginasQuimica 10° #33abel hernandezAún no hay calificaciones
- Enlaces QuimicosDocumento5 páginasEnlaces QuimicosBárbara MHAún no hay calificaciones
- Semana 04 Enlaces QuímicosDocumento34 páginasSemana 04 Enlaces QuímicosKevin Eduardo Medina DiazAún no hay calificaciones
- Material de Estudio para Exponer QuimicaDocumento4 páginasMaterial de Estudio para Exponer QuimicaEduardo GueteAún no hay calificaciones
- 1AM1. Equipo 4 - EnlacesDocumento20 páginas1AM1. Equipo 4 - EnlacesGarcía Martínez VictorAún no hay calificaciones
- Unidad 2 QuimicaDocumento33 páginasUnidad 2 QuimicaJose ManuelAún no hay calificaciones
- Enlaces QuímicosDocumento12 páginasEnlaces Químicosregulo jose morontaAún no hay calificaciones
- Cuestionario 1 CementoDocumento3 páginasCuestionario 1 CementoMaria Cristina CuracachiAún no hay calificaciones
- Act#9 - ResumenDocumento7 páginasAct#9 - ResumenJoelEmiliano195Aún no hay calificaciones
- QuimicaDocumento3 páginasQuimicaShaAún no hay calificaciones
- Enlace QuimicaDocumento10 páginasEnlace QuimicaMarina BenvenutiAún no hay calificaciones
- 5to Repaso 48Documento9 páginas5to Repaso 48Celeste SalvatierraAún no hay calificaciones
- Clase 8 Cup Quimica 2021Documento23 páginasClase 8 Cup Quimica 2021Flores Alcocer Walter JhimmyAún no hay calificaciones
- Enlace MetálicoDocumento27 páginasEnlace MetálicoJazmin Garcia GarciaAún no hay calificaciones
- Enlaces Quimicos (13 Nov 13)Documento32 páginasEnlaces Quimicos (13 Nov 13)Juan Juan CamaneyAún no hay calificaciones
- Enlaces QuimicosDocumento40 páginasEnlaces QuimicosSalvador Hernandez AlpizarAún no hay calificaciones
- 2.7 Enlaces Quimicos 5Documento34 páginas2.7 Enlaces Quimicos 5Ismael IgnacioAún no hay calificaciones
- EXPOSICION_ENLACES_QUIMICOS[1]Documento34 páginasEXPOSICION_ENLACES_QUIMICOS[1]balaneli385Aún no hay calificaciones
- Teoría electromagnética para estudiantes de ingeniería: Notas de claseDe EverandTeoría electromagnética para estudiantes de ingeniería: Notas de claseCalificación: 4.5 de 5 estrellas4.5/5 (7)
- 5.1. - Apuntes Unidades de ConcentraciónDocumento5 páginas5.1. - Apuntes Unidades de ConcentraciónYuyunis De la cruzAún no hay calificaciones
- Disoluciones: Clasificación, Tipos y Factores que Afectan la SolubilidadDocumento3 páginasDisoluciones: Clasificación, Tipos y Factores que Afectan la SolubilidadYuyunis De la cruzAún no hay calificaciones
- 4.1. - Apuntes Reacciones RedoxDocumento3 páginas4.1. - Apuntes Reacciones RedoxYuyunis De la cruzAún no hay calificaciones
- 4.1. - Apuntes Propiedades PeriódicasDocumento4 páginas4.1. - Apuntes Propiedades PeriódicasYuyunis De la cruzAún no hay calificaciones
- 2.2. - Apuntes Equilibrio de EcuacionesDocumento4 páginas2.2. - Apuntes Equilibrio de EcuacionesYuyunis De la cruzAún no hay calificaciones
- 1.2. - Apuntes Fundamentos de La QuimicaDocumento4 páginas1.2. - Apuntes Fundamentos de La QuimicaYuyunis De la cruzAún no hay calificaciones
- 2.1 - Apuntes El AtómoDocumento3 páginas2.1 - Apuntes El AtómoYuyunis De la cruzAún no hay calificaciones
- 1.1. - Apuntes Reacciones Quimicas y EstequiometríaDocumento5 páginas1.1. - Apuntes Reacciones Quimicas y EstequiometríaYuyunis De la cruzAún no hay calificaciones
- 1.1 - Apuntes Metodo CientificoDocumento2 páginas1.1 - Apuntes Metodo CientificoYuyunis De la cruzAún no hay calificaciones
- Monografia Extraccion Con Fluidos - Quimica AnaliticaDocumento36 páginasMonografia Extraccion Con Fluidos - Quimica AnaliticaGiampierre VillenaAún no hay calificaciones
- Biología 01 Turno TarderepasoDocumento2 páginasBiología 01 Turno TarderepasoLis ChavezAún no hay calificaciones
- Curso Bombas Centrifugas Witter PerezDocumento140 páginasCurso Bombas Centrifugas Witter Perezgilmer perezAún no hay calificaciones
- Representación logarítmica de sistemas ácido-baseDocumento63 páginasRepresentación logarítmica de sistemas ácido-baseMNMAún no hay calificaciones
- pROCEDIEMIENTOS SOLDARDocumento9 páginaspROCEDIEMIENTOS SOLDAREdwar Fabian MengualAún no hay calificaciones
- Universidad Autónoma Juan Misael Saracho hormigónDocumento13 páginasUniversidad Autónoma Juan Misael Saracho hormigónAlex TorrejonAún no hay calificaciones
- Minería Volcan PerúDocumento15 páginasMinería Volcan PerúFrank RosalesAún no hay calificaciones
- Membrana transporte osmosisDocumento12 páginasMembrana transporte osmosisCarlos Alberto Bravo ReyesAún no hay calificaciones
- Tema 3. Transferencia de Energía Entre Los Seres VivosDocumento17 páginasTema 3. Transferencia de Energía Entre Los Seres VivosJesús González0% (2)
- Formas Alotropicas FeDocumento16 páginasFormas Alotropicas Fevictor howardAún no hay calificaciones
- Quimica LecitinaDocumento11 páginasQuimica LecitinaCecilia AlejandraAún no hay calificaciones
- Tareas Lípidos170131Documento9 páginasTareas Lípidos170131Xiadany MendozaAún no hay calificaciones
- Informe Energia GeotermicaDocumento3 páginasInforme Energia GeotermicaFabián IgnacioAún no hay calificaciones
- Cambio de entropía en gases idealesDocumento5 páginasCambio de entropía en gases idealesWilm Hosenfeld100% (1)
- Biosintesis TyrDocumento1 páginaBiosintesis TyrAndreziithoMgAún no hay calificaciones
- Universidad Tenologica de Izucar de MatamorosDocumento16 páginasUniversidad Tenologica de Izucar de Matamorosrosendogoku48Aún no hay calificaciones
- PolinDocumento1 páginaPolingeorgelennon68Aún no hay calificaciones
- Ramas de La QuímicaDocumento1 páginaRamas de La QuímicaValeAún no hay calificaciones
- Ley Cero de La TermodinamicaDocumento4 páginasLey Cero de La TermodinamicaJaguarAún no hay calificaciones
- Fotodiodos: Detección luz usando uniones PNDocumento5 páginasFotodiodos: Detección luz usando uniones PNMaariia SegoviaAún no hay calificaciones
- C 6 Agitacion y AireacionDocumento49 páginasC 6 Agitacion y AireacionAloha QtalcaAún no hay calificaciones
- Ensayo CientificoDocumento6 páginasEnsayo CientificoAndinoba NoriegaAún no hay calificaciones
- Lect - S2 - 3ro Sec - IvbimDocumento4 páginasLect - S2 - 3ro Sec - IvbimWillyrex1234Aún no hay calificaciones
- Diseño de Una Planta para Desorción de Carbón Activado Por El Método Zadra PDFDocumento41 páginasDiseño de Una Planta para Desorción de Carbón Activado Por El Método Zadra PDFEnrique Gerardo Antunez RuizAún no hay calificaciones
- Los EsteresDocumento14 páginasLos EsteresIbiza ToapantaAún no hay calificaciones
- NP-013-v 3 0 PDFDocumento15 páginasNP-013-v 3 0 PDFRafaelSitgesLehoucqAún no hay calificaciones
- A. Nuevo Formato Explosivos-Class-EteDocumento52 páginasA. Nuevo Formato Explosivos-Class-EteMayra GomezzAún no hay calificaciones
- Ejemplos AgendaDocumento17 páginasEjemplos AgendajmurquijoAún no hay calificaciones
- Lexico Hidrogeologico: Nilda González M Ario Alberto Hernández César Reinaldo VilelaDocumento217 páginasLexico Hidrogeologico: Nilda González M Ario Alberto Hernández César Reinaldo VilelaGabriela GuillenAún no hay calificaciones
- Proceso SelexolDocumento3 páginasProceso SelexolRodrigo RodrigoAún no hay calificaciones
























































![EXPOSICION_ENLACES_QUIMICOS[1]](https://imgv2-2-f.scribdassets.com/img/document/720420678/149x198/f368d41366/1712350565?v=1)








































