Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Termodinámica Química
Cargado por
Katherine AlarconTítulo original
Derechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
Termodinámica Química
Cargado por
Katherine AlarconCopyright:
Formatos disponibles
Termodinámica química
La termodinámica quí mica (o termoquímica) es la rama de la termodinámica que
estudia los efectos térmicos causados por reacciones químicas, llamados el calor de
reacción. Por lo tanto, la termodinámica química se refiere a las conversiones
de energía química en energí a térmica y viceversa, que ocurren durante una
reacción y estudia las variables conectadas a ellas, como la entalpía de enlace,
la entropía de formación estándar, etc. Todas estas conversiones se rea lizan dentro
de los límites de las leyes de la termodinámica.
La energía del uni verso es constante: primera ley de l a termodinámica.
En cualquier proceso espontáneo, siempre hay un aumento en la entropía del
uni verso: segunda ley de la termodinámica.
La entropía de un cristal perfecto (bien ordenado) a 0 Kelvin es cero: tercera ley
de la termodi námica.
Además de los pri ncipi os termodinámicos existen dos leyes rigen toda la disciplina
de la termoquímica:
Ley de Lavoisier y Laplace (formulada en 1780): la transferencia de calor que
acompaña a una reacci ón química dada es igual y contraria a la transferencia de
calor de la reacción opuesta;
Ley de Hess (formul ada en 1840): la variación de la entalpía de reacción es la
misma que la reacción se produce en una o más etapas sucesivas e independientes
(incl uso puramente hipotéticas).
Las dos leyes se dedujeron empíricamente y se enunciaron antes del primer principio
de la termodinámi ca: sin embargo, puede probar que son consecuencias directas de
la misma, así como el hecho de que l a entalpía H y la energía interna U son
funciones termodinámicas del estado.
La termodi námica química implica no solo mediciones de laboratorio de
varias propiedades termodinámicas , sino también la aplicación de métodos
matemáticos para el estudio de preguntas químicas y la espontaneidad de los
procesos.
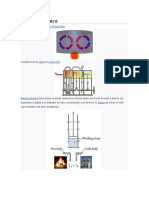
En la energía solar fotovoltaica la termodinámica química tiene especial relevancia
en la carga y l a descarga de baterías. Durante este proceso se experimenta un
intercambio entre energía quími ca y electricidad.
Descripción de la termodinámica
química
El objetivo pri ncipal de la termodinámica química es el establecimiento de un criterio
para determi nar la factibilidad o espontaneidad de una transformación dada. De esta
manera, la termodinámica química se usa típicamente para predecir los intercambios
de energía que ocurren en los siguientes procesos: reacciones químicas, cambios de
fase, formación de soluciones.
Las siguientes funciones de estado son de interés principal en termodinámica
química: energía i nterna (U), entalpía (H), entropía (S), energía libre de Gibbs (G).
La estructura de l a termodinámica química se basa en las dos primeras leyes de la
termodinámica. A parti r de l a primera ley de la termodinámica y la segunda ley de
la termodinámi ca, se pueden derivar cuatro ecuaciones denominadas "ecuaciones
fundamentales de Gibbs". A partir de estos cuatro, se pueden derivar una multitud
de ecuaciones, que relacionan las propiedades termodinámicas del sistema
termodinámico, usando matemáticas relativamente simples. Esto delinea el marco
matemático de la termodinámica química.
Sistemas termodinámicos
En termoquí mica exi sten vari as definiciones termodinámicas muy útiles. Un
sistema termodinámi co es la porción específica del universo que se está estudiando.
Todo lo que está fuera del sistema se considera entorno o entorno. Un sistema puede
ser:
Un sistema termodinámico (completamente) aislado que no puede intercambiar
energía ni materia con el entorno, como un calorímetro de bomba aislado.
Un sistema aislado térmicamente que puede intercambiar trabajo mecánico, pero
no calor o materia, como un pistón o globo cerrado aislado.
Un sistema ai slado mecánicamente que puede intercambiar calor, pero no trabajo
o materia mecánic a, como un calorímetro de bomba no aislado
Un sistema cerrado que puede intercambiar energía, pero no importa, como un
globo o pistón cerrado sin aislamiento
Un sistema abierto que puede intercambiar materia y energía con el entorno,
como una olla de agua hirviendo
Reacciones químicas
En la mayorí a de los casos de i nterés en l a termodinámica química, existen grados
internos de libertad y procesos, como las reacciones químicas y las transiciones de
fase. Estas reacciones químicas siempre crean entropía a menos que estén en
equilibrio o se mantengan en un equilibrio continuo.
Incluso para materiales homogéneos, las funciones de energía libre dependen de l a
composición, al igual que todos los potenciales termodinámicos extensos, incluida la
energía interna.
Historia de la termodinámica química
En 1865, el fí sico alemán Rudolf Clausius, en su Mechanical Theory of Heat, sugirió
que los pri ncipios de la termoquímica, por ejemplo, el calor generado en
las reacciones de combustión, podrían aplicarse a los principios de
la termodinámica. Sobre la base del trabajo de Clausius, entre los años 1873-76 el
físico matemático estadounidense Willard Gibbs publicó una serie de tres artículos,
el más famoso fue el documento Sobre el equilibrio de sustancias heterogéneas.
En estos artículos, Gibbs mostró cómo las dos primeras leyes de la termodinámica
podría medirse gráfi ca y matemáticamente para determinar tanto el equilibrio
termodinámico de las reacciones químicas como sus tendencias a ocurrir o
avanzar. La colección de documentos de Gibbs proporcionó el primer cuerpo
uni ficado de teoremas termodi námicos a partir de los principios desarrollados por
otros, como Cl ausius y Sadi Carnot.
A pri ncipios del siglo XX, dos publicaciones importantes aplicaron con éxito los
principios desarrollados por Gibbs a los procesos químicos, y así establecieron los
cimientos de la ciencia de la termodinámica química. El primero fue el libro de texto
de 1923 Termodinámi ca y la Energía Libre de Sustancias Químicas de Gilbert N.
Lewis y Merle Randall. Este libro fue responsable de suplantar l a afinidad
química con el término energí a libre en el mundo de habla inglesa.
El segundo fue el libro de 1933 Modern Thermodynamics por los métodos de Willard
Gibbs, escrito por EA Guggenheim.. De esta manera, Lewis, Randall y Guggenheim
son considerados los fundadores de la termodinámica química moderna debido a la
gran contribución de estos dos libros para unificar la aplicación de
la termodinámica a la química.
También podría gustarte
- La Termodinámica QuímicaDocumento3 páginasLa Termodinámica Químicajose chacaliazaAún no hay calificaciones
- Definición y leyes de la termodinámica químicaDocumento3 páginasDefinición y leyes de la termodinámica químicaIsabella TorresAún no hay calificaciones
- Sistemas TermodinámicosDocumento2 páginasSistemas TermodinámicosKatherine AlarconAún no hay calificaciones
- TermodinámicaDocumento12 páginasTermodinámicaDeryn Quispe MendozaAún no hay calificaciones
- Termodinámica: definición, leyes y aplicacionesDocumento17 páginasTermodinámica: definición, leyes y aplicacionesDayana CastroAún no hay calificaciones
- Termodinámica - Wikipedia, La Enciclopedia Libre PDFDocumento10 páginasTermodinámica - Wikipedia, La Enciclopedia Libre PDFkronam1Aún no hay calificaciones
- Termodinámica QuímicaDocumento7 páginasTermodinámica QuímicaJimmyRiveraAún no hay calificaciones
- Portafolio Termo PDFDocumento18 páginasPortafolio Termo PDFYomary QuezadaAún no hay calificaciones
- TermodinámicaDocumento19 páginasTermodinámicaJoseph López PasmiñoAún no hay calificaciones
- TermodinámicaDocumento5 páginasTermodinámicaReyes EsmeraldaAún no hay calificaciones
- Evolucion HumanaDocumento764 páginasEvolucion HumanaLobaton Flores JamilAún no hay calificaciones
- TermodDocumento18 páginasTermodPetra Banda RamirezAún no hay calificaciones
- Cuarto Principio de La TermodinámicaDocumento8 páginasCuarto Principio de La TermodinámicaAnonymous wH8gUfAFnAún no hay calificaciones
- 3introducción A La TermodináicaDocumento7 páginas3introducción A La TermodináicaRicardo CastroAún no hay calificaciones
- Termodinamica en FisicaDocumento19 páginasTermodinamica en FisicaJhimy AruquipaAún no hay calificaciones
- Conferencias Tema 1Documento41 páginasConferencias Tema 1Rubisel Bueno AldanaAún no hay calificaciones
- Termodinámica en El Cambio ClimáticoDocumento10 páginasTermodinámica en El Cambio Climáticobruce vegaAún no hay calificaciones
- Actividad 2 - TermodinámicaDocumento3 páginasActividad 2 - TermodinámicaDavid Ruiz LópezAún no hay calificaciones
- TERMODINAMICADocumento17 páginasTERMODINAMICAHéctor VillanuevaAún no hay calificaciones
- Proyecto Segunda Unidad FisicaDocumento26 páginasProyecto Segunda Unidad Fisicayirehblanco1601Aún no hay calificaciones
- TermodinámicaDocumento18 páginasTermodinámicaMily DanielaAún no hay calificaciones
- Termo DinamicaDocumento4 páginasTermo Dinamicavicuru12Aún no hay calificaciones
- La Termodinámica 1Documento12 páginasLa Termodinámica 1sachaa8hotmail.comAún no hay calificaciones
- TermodinDocumento13 páginasTermodinalejandroAún no hay calificaciones
- Fis Sem 5Documento14 páginasFis Sem 5Javier Medrano CiméAún no hay calificaciones
- 1deber - Consulta Leyes de La TermodinamicaDocumento7 páginas1deber - Consulta Leyes de La TermodinamicaLuis Soria TorresAún no hay calificaciones
- Termodinámica - Wikipedia, La Enciclopedia LibreDocumento19 páginasTermodinámica - Wikipedia, La Enciclopedia LibrealgarabrielaAún no hay calificaciones
- Fisicoquìmica Intro 1 PDFDocumento6 páginasFisicoquìmica Intro 1 PDFlauraAún no hay calificaciones
- Practica Fuera de AulaDocumento11 páginasPractica Fuera de AulaMoises CanaviriAún no hay calificaciones
- 4 - TermodinámicaDocumento13 páginas4 - TermodinámicaJulio C. Velasco XoloAún no hay calificaciones
- TermodinamicaDocumento3 páginasTermodinamicaPaolo Guarniz TufinioAún no hay calificaciones
- TermodinámicaDocumento6 páginasTermodinámicamigyendrichAún no hay calificaciones
- Historia de La TermodinámicaDocumento11 páginasHistoria de La TermodinámicaTatianaAún no hay calificaciones
- Termodinámica en Ingeniería QuímicaDocumento7 páginasTermodinámica en Ingeniería QuímicaEsther CanazaAún no hay calificaciones
- Termodinamica Unidad 5Documento7 páginasTermodinamica Unidad 5Marcos Galaz CampilloAún no hay calificaciones
- Introducción A La TermodinámicaDocumento5 páginasIntroducción A La TermodinámicaFlor TorresAún no hay calificaciones
- República Bolivariana de VenezuelaDocumento14 páginasRepública Bolivariana de VenezuelaNorwis GonzalezAún no hay calificaciones
- Fisicoquímica - Wikipedia, La Enciclopedia LibreDocumento10 páginasFisicoquímica - Wikipedia, La Enciclopedia LibreJuan Francisco Palomeque SackAún no hay calificaciones
- Gas Ideal y Leyes de La TermodinámicaDocumento47 páginasGas Ideal y Leyes de La TermodinámicaWalther MendozaAún no hay calificaciones
- Leyes Termodinámica ExperimentoDocumento7 páginasLeyes Termodinámica ExperimentoAndy Infantes Valenzuela100% (2)
- Apuntes TermodinamicaDocumento41 páginasApuntes TermodinamicaEfra ChAún no hay calificaciones
- 01 TemperaturaDocumento6 páginas01 TemperaturaSamuel PérezAún no hay calificaciones
- La Termodinamica EoyeDocumento9 páginasLa Termodinamica Eoyetenorioe322Aún no hay calificaciones
- Termoquímica: estudio cambios calor en reaccionesDocumento5 páginasTermoquímica: estudio cambios calor en reaccionesMario Alberto Montero SánchezAún no hay calificaciones
- Introduccion A TermodinamicaDocumento5 páginasIntroduccion A TermodinamicaCarlos Claros RiveraAún no hay calificaciones
- Termodinámica: Estudio energía transformacionesDocumento4 páginasTermodinámica: Estudio energía transformacionesAlejandroAriasAún no hay calificaciones
- Ecuaciones Fundamentales de La TermodinamicaDocumento5 páginasEcuaciones Fundamentales de La TermodinamicaDANIEL GUARDADO RUIZAún no hay calificaciones
- Quimica Termodinca 2 BachilleratoDocumento6 páginasQuimica Termodinca 2 BachilleratoEdgard Alonso Rebaza CarpioAún no hay calificaciones
- TermoquímicaDocumento6 páginasTermoquímicavaneAún no hay calificaciones
- Term Odin Á MicaDocumento48 páginasTerm Odin Á MicaJose HuapayaAún no hay calificaciones
- Los principios de la termodinámicaDocumento4 páginasLos principios de la termodinámicaJohan CantorAún no hay calificaciones
- Ensayo Sobre La Unidad de Termodinamica OBTADocumento7 páginasEnsayo Sobre La Unidad de Termodinamica OBTAAndrea FonsecaAún no hay calificaciones
- TERMODINAMICADocumento9 páginasTERMODINAMICAhectorAún no hay calificaciones
- Ley de La TermodinamicaDocumento12 páginasLey de La TermodinamicaJesus VenturaAún no hay calificaciones
- Term Odin A MicaDocumento3 páginasTerm Odin A MicaCésar PCAún no hay calificaciones
- Ley ZerothDocumento4 páginasLey ZerothDavid Cabrera MartinezAún no hay calificaciones
- TERMOQUIMICADocumento8 páginasTERMOQUIMICAabrahamAún no hay calificaciones
- Capitulo 5Documento19 páginasCapitulo 5Patricia BalcazarAún no hay calificaciones
- Estos ConocimientosDocumento4 páginasEstos ConocimientosKatherine AlarconAún no hay calificaciones
- Las Dos Leyes Se Dedujeron Empíricamente y Se Enunciaron Antes DelDocumento2 páginasLas Dos Leyes Se Dedujeron Empíricamente y Se Enunciaron Antes DelKatherine AlarconAún no hay calificaciones
- Descripción de La Termodinámica QuímicaDocumento2 páginasDescripción de La Termodinámica QuímicaKatherine AlarconAún no hay calificaciones
- Reacciones QuímicasDocumento1 páginaReacciones QuímicasKatherine AlarconAún no hay calificaciones
- Sin Realizar Algunos Rituales Establecidos Por Su ReligiónDocumento1 páginaSin Realizar Algunos Rituales Establecidos Por Su ReligiónKatherine AlarconAún no hay calificaciones
- Qué es la cienciaDocumento4 páginasQué es la cienciaKatherine AlarconAún no hay calificaciones
- Lo que debes saber sobre la ciencia, su origen y ramasDocumento5 páginasLo que debes saber sobre la ciencia, su origen y ramasKatherine AlarconAún no hay calificaciones
- Características de La CienciaDocumento4 páginasCaracterísticas de La CienciaKatherine AlarconAún no hay calificaciones
- La Molécula Como Caballo de TroyaDocumento2 páginasLa Molécula Como Caballo de TroyaKatherine AlarconAún no hay calificaciones
- La Filosofía y La Religión Están RelacionadasDocumento2 páginasLa Filosofía y La Religión Están RelacionadasKatherine AlarconAún no hay calificaciones
- La Filosofía y La ReligiónDocumento3 páginasLa Filosofía y La ReligiónKatherine AlarconAún no hay calificaciones
- Otra Diferencia Entre Las Dos Es La Fuerza de Las CreenciasDocumento1 páginaOtra Diferencia Entre Las Dos Es La Fuerza de Las CreenciasKatherine AlarconAún no hay calificaciones
- Así Que Un Individuo No Puede Ser Completamente ReligiosoDocumento2 páginasAsí Que Un Individuo No Puede Ser Completamente ReligiosoKatherine AlarconAún no hay calificaciones
- Junto Con La FísicaDocumento2 páginasJunto Con La FísicaKatherine AlarconAún no hay calificaciones
- Es Una Disciplina Con Una Esfera de Acción Mucho Más GrandeDocumento2 páginasEs Una Disciplina Con Una Esfera de Acción Mucho Más GrandeKatherine AlarconAún no hay calificaciones
- QuiimicaDocumento4 páginasQuiimicaميندوزا غوستافوAún no hay calificaciones
- Los Movimientos Del MecanizadoDocumento3 páginasLos Movimientos Del MecanizadoKatherine AlarconAún no hay calificaciones
- Planteamiento Examen de Conocimientos IIDocumento2 páginasPlanteamiento Examen de Conocimientos IIKatherine Alarcon0% (1)
- Los Movimientos Del MecanizadoDocumento3 páginasLos Movimientos Del MecanizadoKatherine AlarconAún no hay calificaciones
- Tipos de Mecanizado No ConvencionalDocumento2 páginasTipos de Mecanizado No ConvencionalKatherine AlarconAún no hay calificaciones
- En El Ámbito de La Biología Es Donde Más Sorprendente Resulta El Papel de Las Interacciones MolecularesDocumento2 páginasEn El Ámbito de La Biología Es Donde Más Sorprendente Resulta El Papel de Las Interacciones MolecularesKatherine AlarconAún no hay calificaciones
- Origen Del MecanizadoDocumento5 páginasOrigen Del MecanizadoKatherine AlarconAún no hay calificaciones
- Las Empresas de Mecanizado en EspañaDocumento1 páginaLas Empresas de Mecanizado en EspañaKatherine AlarconAún no hay calificaciones
- Origen y características del mecanizadoDocumento8 páginasOrigen y características del mecanizadoKatherine AlarconAún no hay calificaciones
- Origen y características del mecanizadoDocumento8 páginasOrigen y características del mecanizadoKatherine AlarconAún no hay calificaciones
- MecanizadoDocumento7 páginasMecanizadoKatherine AlarconAún no hay calificaciones
- Qué Es Materia Prima y El Producto ElaboradoDocumento4 páginasQué Es Materia Prima y El Producto ElaboradoKatherine AlarconAún no hay calificaciones
- Los Sectores de EconomíaDocumento4 páginasLos Sectores de EconomíaKatherine AlarconAún no hay calificaciones
- Normas ISO y Calidad en La Calibración de EquiposDocumento7 páginasNormas ISO y Calidad en La Calibración de EquiposgeorgenzAún no hay calificaciones
- Lab 4 FSC 2Documento8 páginasLab 4 FSC 2Rigel AlphardAún no hay calificaciones
- Cable N2xoh Libre HalogenoDocumento2 páginasCable N2xoh Libre HalogenoXinoko MosqueiraAún no hay calificaciones
- Actividad 3 - Unidad 3 Maquinas Asincronas Junio 2021Documento2 páginasActividad 3 - Unidad 3 Maquinas Asincronas Junio 2021Alexander Sam100% (1)
- CatalogoTecnicoSerieZ - FGZN25Documento1 páginaCatalogoTecnicoSerieZ - FGZN25Leonardo SosaAún no hay calificaciones
- Electricidad y Electrónica AutomotrizDocumento4 páginasElectricidad y Electrónica AutomotrizFABIANAún no hay calificaciones
- Fis T2 2022Documento20 páginasFis T2 2022antoniogarciaflores27Aún no hay calificaciones
- 06-12-2020 120703 PM 8. TemperaturaDocumento2 páginas06-12-2020 120703 PM 8. Temperaturalexmar chinchay bermeoAún no hay calificaciones
- Procedimiento de Diseño SPTDocumento6 páginasProcedimiento de Diseño SPTLuis MontañoAún no hay calificaciones
- HT No. 9 F.B. 2S2022 Newton 2Documento2 páginasHT No. 9 F.B. 2S2022 Newton 2Yazid VicenteAún no hay calificaciones
- Universidad Pedagógica y Tecnológica de ColombiaDocumento2 páginasUniversidad Pedagógica y Tecnológica de ColombiaestebanAún no hay calificaciones
- Presentacion Exposicion Motor DevanadoDocumento12 páginasPresentacion Exposicion Motor DevanadoGJ28Aún no hay calificaciones
- Que Es La EntropíaDocumento5 páginasQue Es La EntropíaBryan Castro.00Aún no hay calificaciones
- NOMBREDocumento6 páginasNOMBRENeymar FloresAún no hay calificaciones
- Práctica1 IPAC2023 PRESENCIALDocumento10 páginasPráctica1 IPAC2023 PRESENCIALOmar MelaraAún no hay calificaciones
- 000 PROTOC Pract 01 LABO A.T. 2018 v11Documento13 páginas000 PROTOC Pract 01 LABO A.T. 2018 v11Daniel JaraAún no hay calificaciones
- Fuerzas - Equilibrio EstáticoDocumento4 páginasFuerzas - Equilibrio EstáticoProf. Ignacio CaggianoAún no hay calificaciones
- Laboratorio 5 Versión AlumnoDocumento13 páginasLaboratorio 5 Versión AlumnoWilAún no hay calificaciones
- Certificado de Calibración - Laboratorio de Fuerza: Page / Pág 1 de 4Documento4 páginasCertificado de Calibración - Laboratorio de Fuerza: Page / Pág 1 de 4Iván Dario Bustos AriasAún no hay calificaciones
- 2016-1 DIN Prac09Documento4 páginas2016-1 DIN Prac09sebastianAún no hay calificaciones
- Los signos vitales en primeros auxiliosDocumento8 páginasLos signos vitales en primeros auxiliosSarah MezaAún no hay calificaciones
- 9º Practica - Hidrostatica - 6-8Documento2 páginas9º Practica - Hidrostatica - 6-8Blade XAún no hay calificaciones
- Lab 4 Transfe de Calor-5Documento20 páginasLab 4 Transfe de Calor-5Ignacio YacAún no hay calificaciones
- Glosario FisicaDocumento12 páginasGlosario FisicaNaileti100% (2)
- La electricidad en nuestras vidas: circuitos eléctricos y corriente continuaDocumento7 páginasLa electricidad en nuestras vidas: circuitos eléctricos y corriente continuaYeisson Bautista PoccoriAún no hay calificaciones
- ARITMÉTICADocumento5 páginasARITMÉTICA실비아SilviaAún no hay calificaciones
- Caída LibreDocumento2 páginasCaída LibreJULIOAún no hay calificaciones
- Localizacion de Faltas Tesis MaestriaDocumento120 páginasLocalizacion de Faltas Tesis MaestriaJuan CarlosAún no hay calificaciones
- Termodinámica aplicada a la medicinaDocumento23 páginasTermodinámica aplicada a la medicinaJikeyAún no hay calificaciones
- Electricidad Del BuqueDocumento54 páginasElectricidad Del Buquei lopezAún no hay calificaciones
- La metamedicina. Cada síntoma es un mensaje: La curación a tu alcanceDe EverandLa metamedicina. Cada síntoma es un mensaje: La curación a tu alcanceCalificación: 5 de 5 estrellas5/5 (8)
- La revolución de la glucosa: Equilibra tus niveles de glucosa y cambiarás tu salud y tu vidaDe EverandLa revolución de la glucosa: Equilibra tus niveles de glucosa y cambiarás tu salud y tu vidaCalificación: 5 de 5 estrellas5/5 (200)
- La invasión de la pseudociencia: Claves para orientarse en un mundo en donde casi todo es posibleDe EverandLa invasión de la pseudociencia: Claves para orientarse en un mundo en donde casi todo es posibleCalificación: 4.5 de 5 estrellas4.5/5 (15)
- Batidos Verdes Depurativos y Antioxidantes: Aumenta tu Vitalidad con Smoothie Detox Durante 10 Días Para Adelgazar y Bajar de Peso: Aumenta tu vitalidad con smoothie detox durante 10 días para adelgazar y bajar de pesoDe EverandBatidos Verdes Depurativos y Antioxidantes: Aumenta tu Vitalidad con Smoothie Detox Durante 10 Días Para Adelgazar y Bajar de Peso: Aumenta tu vitalidad con smoothie detox durante 10 días para adelgazar y bajar de pesoCalificación: 5 de 5 estrellas5/5 (2)
- Fisiopatología de las enfermedades cardiovascularesDe EverandFisiopatología de las enfermedades cardiovascularesCalificación: 5 de 5 estrellas5/5 (1)
- Disciplina Mental: Técnicas infalibles para lograr todo lo que te propones y eliminar la pereza y la procrastinación de tu vida para siempreDe EverandDisciplina Mental: Técnicas infalibles para lograr todo lo que te propones y eliminar la pereza y la procrastinación de tu vida para siempreCalificación: 5 de 5 estrellas5/5 (3)
- Psiconeuroinmunología para la práctica clínicaDe EverandPsiconeuroinmunología para la práctica clínicaCalificación: 5 de 5 estrellas5/5 (4)
- Resumen de Pensar rápido pensar despacio de Daniel KahnemanDe EverandResumen de Pensar rápido pensar despacio de Daniel KahnemanCalificación: 4.5 de 5 estrellas4.5/5 (11)
- Anatomía & 100 estiramientos Esenciales (Color): Técnicas, beneficios, precauciones, consejos, tablas de series, dolenciasDe EverandAnatomía & 100 estiramientos Esenciales (Color): Técnicas, beneficios, precauciones, consejos, tablas de series, dolenciasCalificación: 4.5 de 5 estrellas4.5/5 (21)
- Nunca fuimos modernos: Ensayos de antropología simétricaDe EverandNunca fuimos modernos: Ensayos de antropología simétricaAún no hay calificaciones
- Borges y la memoria: De "Funes el memorioso" a la neurona de Jennifer AnistonDe EverandBorges y la memoria: De "Funes el memorioso" a la neurona de Jennifer AnistonCalificación: 5 de 5 estrellas5/5 (4)
- Zensorialmente : Dejá que tu cuerpo sea tu cerebroDe EverandZensorialmente : Dejá que tu cuerpo sea tu cerebroAún no hay calificaciones
- En busca de la mente: El largo camino para comprender la vida mental (y lo que aún queda por descubrir)De EverandEn busca de la mente: El largo camino para comprender la vida mental (y lo que aún queda por descubrir)Calificación: 4.5 de 5 estrellas4.5/5 (3)
- Estoicismo y dureza mental: Descubre los secretos psicológicos de la filosofía estoica en la vida moderna. Construir una autodisciplina inquebrantable y hábitos diarios que garanticen el éxitoDe EverandEstoicismo y dureza mental: Descubre los secretos psicológicos de la filosofía estoica en la vida moderna. Construir una autodisciplina inquebrantable y hábitos diarios que garanticen el éxitoCalificación: 4 de 5 estrellas4/5 (23)
- Desastres y emergencias. Prevención, mitigación y preparaciónDe EverandDesastres y emergencias. Prevención, mitigación y preparaciónCalificación: 4 de 5 estrellas4/5 (5)
- Investigación de operaciones: Conceptos fundamentalesDe EverandInvestigación de operaciones: Conceptos fundamentalesCalificación: 4.5 de 5 estrellas4.5/5 (2)
- Cálculo infinitesimal: El lenguaje matemático de la naturalezaDe EverandCálculo infinitesimal: El lenguaje matemático de la naturalezaCalificación: 5 de 5 estrellas5/5 (3)
- Estadística básica: Introducción a la estadística con RDe EverandEstadística básica: Introducción a la estadística con RCalificación: 5 de 5 estrellas5/5 (8)
- Reconstrucción de dientes endodonciados: Pautas de actuación clínicaDe EverandReconstrucción de dientes endodonciados: Pautas de actuación clínicaCalificación: 5 de 5 estrellas5/5 (4)
- Interpretación del ECG: Una Guía Práctica e Intuitiva para Aprender a Leer el ECG y Diagnosticar y Tratar ArritmiasDe EverandInterpretación del ECG: Una Guía Práctica e Intuitiva para Aprender a Leer el ECG y Diagnosticar y Tratar ArritmiasAún no hay calificaciones