100% encontró este documento útil (1 voto)
246 vistas4 páginasRedes de Bravais en Cristales
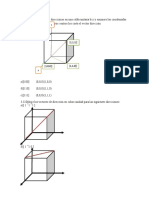
El documento resume las redes de Bravais, las cuales son las 14 celdas unitarias tridimensionales en las que pueden ubicarse los átomos de un cristal. Estas celdas se subdividen en 7 grupos según su geometría y cada grupo tiene parámetros propios como el tamaño de la celda y número de átomos. Las redes más comunes son las cúbicas, las cuales incluyen la red cúbica simple y las redes cúbicas centradas en las caras o en el cuerpo.
Cargado por
kimroo66Derechos de autor
© © All Rights Reserved
Nos tomamos en serio los derechos de los contenidos. Si sospechas que se trata de tu contenido, reclámalo aquí.
Formatos disponibles
Descarga como PDF, TXT o lee en línea desde Scribd
100% encontró este documento útil (1 voto)
246 vistas4 páginasRedes de Bravais en Cristales
El documento resume las redes de Bravais, las cuales son las 14 celdas unitarias tridimensionales en las que pueden ubicarse los átomos de un cristal. Estas celdas se subdividen en 7 grupos según su geometría y cada grupo tiene parámetros propios como el tamaño de la celda y número de átomos. Las redes más comunes son las cúbicas, las cuales incluyen la red cúbica simple y las redes cúbicas centradas en las caras o en el cuerpo.
Cargado por
kimroo66Derechos de autor
© © All Rights Reserved
Nos tomamos en serio los derechos de los contenidos. Si sospechas que se trata de tu contenido, reclámalo aquí.
Formatos disponibles
Descarga como PDF, TXT o lee en línea desde Scribd