Documentos de Académico
Documentos de Profesional
Documentos de Cultura
4
Cargado por
yojanaDerechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
4
Cargado por
yojanaCopyright:
Formatos disponibles
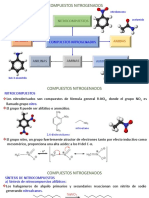
Ácido nítrico
Mezclas nitrantes, por ejemplo, ácido nítrico mezclado con un agente deshidratante
como el óleum, ácido sulfúrico, anhídrido acético, pentóxido de fósforo.
Nitratos alcalinos en presencia de ácido sulfúrico.
Nitratos orgánicos como nitratos de acetilo de benzoilo.
Nitratos metálicos con ácido acético.
Tetróxido de nitrógeno.
Anhídrido nítrico.
Dióxido de nitrógeno
Ácido nítrico.
El método industrial más importarte para producirlo es el proceso Ostwald.
Las materias primas son amoniaco y oxígeno molecular, y se calienta en presencia del
catalizador platino radio a 800º C.
El ácido nítrico necesario para la nitración puede preparase ahí mismo mezclando
nitratos alcalinos y ácido sulfúrico.
NaNO3 + NaHSO4 HNO3 + Na2SO4
El ácido nítrico es un agente de nitración débil puesto que su constitución se altera
durante el proceso por la presencia del agua producida. Para superar esto es necesario
recurrir a procedimientos de separación del agua resultante en la nitración, a fin de
mantener una concentración relativamente constante y satisfactoria de HNO3 o emplear
un exceso de ácido nítrico.
El ácido nítrico no existe como líquido puro por que en reposo se descompone en:
4HNO3 4NO2 + 2H2O + O2
La reacción generalizada de nitración con ácido nítrico es:
R - H + HNO3 R - NO2 + H2O
as mezclas nitrantes están formadas por la sustancia a nitrar, el agente nitrante y un
agente deshidratante para eliminar el agua. La mayor ventaja es que las mezclas
sulfonítricas atan sólo ligeramente los depósitos y aparatos de nitración.
La nitración se realiza con el anhídrido mixto HOSO2 - O - NO2 que se obtiene así:
HONO2 + H2SO4 HOSO2 - O - NO2 + H2O
La reacción generalizada de nitración con el ácido nitrosulfúrico es:
HOSO2 - O - NO2 + RH R - NO2 + H2SO4
Nitratos alcalinos y ácido sulfúrico.
El ácido nítrico necesario para la nitración se obtiene de mezclar un nitrato alcalino y ácido
sulfúrico como se vio en la obtención del HNO3 anteriormente. Se utiliza como agente la
sal alcalina siendo el puente el ácido sulfúrico que ataca la metal para regenerarse.
Nitratos orgánicos ( nitrato de acetilo de benzoilo ).
El anhídrido acético y el nítrico se combinan para forma nitrato de acetilo:
CH3 - CO NO2
O + O 2CH3COO - NO2
( nitrato de acetilo )
CH3 - CO NO2
Donde lo que se nitra es el anhídrido acético, que sirve de puente, siendo el CH3 - CO el
agente deshidratante y el agente nitrante el NO2
Para obtener el nitrato de benzoilo se descompone
La reacción generalizada :
Nitración con nitrato de acetilo:
R - H + CH3COO - NO2 R - NO2 + CH3COOH
Nitración de benzoilo:
R - H + C6H5COO - NO2 R - NO2 + C6H5COOH
Nitratos metálicos.
Sirven como agentes nitrantes algunos metálicos disueltos en anhídrido acético como los
nitratos cúprico, férrico y de aluminio.
Cuando se hacen reaccionar aminas se obtiene su acetilación y su nitración.
M - ( NO2 )3 + 3R - H 3R - NO2 + M3H
( nitrato metálico ) ( hidruro )
Se utilizan metales de las familias I, II y III.
Tetróxido de nitrógeno ( N2O4 ).
El tetróxido de nitrógeno muestra una pequeña reactividad con el benceno, clorobenceno y
el tolueno. Con éste agente se da la unión de dos grupos nitro.
La reacción generalizada es:
R - H + NO2 - NO2 R - NO2 + HNO2
También podría gustarte
- Acido Nitrico InformeDocumento22 páginasAcido Nitrico InformeNirza Sanchez MejiaAún no hay calificaciones
- Síntesis HNO3 proceso OstwaldDocumento11 páginasSíntesis HNO3 proceso OstwaldDaily Ch TAún no hay calificaciones
- Obtención de ácido nítrico por oxidación de amoniacoDocumento4 páginasObtención de ácido nítrico por oxidación de amoniacoGary Watson50% (2)
- Nitración Del FenolDocumento8 páginasNitración Del Fenolmarisa_boo5924Aún no hay calificaciones
- NitraciónDocumento14 páginasNitraciónGaby Lizana VásquezAún no hay calificaciones
- Ácido Pícrico y FenolftaleínaDocumento33 páginasÁcido Pícrico y FenolftaleínafernandaAún no hay calificaciones
- Acido Pícrico1Documento32 páginasAcido Pícrico1fernandaAún no hay calificaciones
- Nitracion LabDocumento5 páginasNitracion LabRene BenavidesAún no hay calificaciones
- Tema NitraciónDocumento14 páginasTema Nitraciónjvalencia_196986Aún no hay calificaciones
- Info 3Documento8 páginasInfo 3Giuliana Katia Morales FuertesAún no hay calificaciones
- NitracionDocumento15 páginasNitracionIvan BerlotAún no hay calificaciones
- Ac NitricoDocumento7 páginasAc NitricoMartha MendozaAún no hay calificaciones
- Informe N°5 Lab.q.inorganica - Grupo 1Documento12 páginasInforme N°5 Lab.q.inorganica - Grupo 1CAICAY OTOYA LUIS EDUARDOAún no hay calificaciones
- Compuestos de nitrógeno: amoniaco, nitritos y nitratosDocumento6 páginasCompuestos de nitrógeno: amoniaco, nitritos y nitratosKevin TandazoAún no hay calificaciones
- Reducción Del NitrobencenoDocumento6 páginasReducción Del NitrobencenoCrezpo YzAún no hay calificaciones
- Fulminado y NitrolatoDocumento3 páginasFulminado y NitrolatoMoises Valdivia BaldomeroAún no hay calificaciones
- Ac - Nitrico PresentacionDocumento31 páginasAc - Nitrico PresentacionNirza Sanchez MejiaAún no hay calificaciones
- MARCO TEORICO Grupo 5ADocumento5 páginasMARCO TEORICO Grupo 5Akarel caceres huaringaAún no hay calificaciones
- Configuración Electrónica y Propiedades QuímicasDocumento5 páginasConfiguración Electrónica y Propiedades QuímicasCarolina GomezAún no hay calificaciones
- Nitración de La AcetanilidaDocumento9 páginasNitración de La AcetanilidaGuisela Quispe Velez100% (1)
- 8.0 Elementos Grupo NitrogenoDocumento9 páginas8.0 Elementos Grupo NitrogenoEduardo Steven AmayoAún no hay calificaciones
- Temas 3 y 4 PRQ 142 Semestre Dos 2021Documento76 páginasTemas 3 y 4 PRQ 142 Semestre Dos 2021Esther VelasquezAún no hay calificaciones
- Procesos industriales de nitraciónDocumento54 páginasProcesos industriales de nitraciónDeyni Darline Bel0% (1)
- Preparación y propiedades oxidantes del ácido nítricoDocumento5 páginasPreparación y propiedades oxidantes del ácido nítricoedis diazAún no hay calificaciones
- Ácido NitrosoDocumento4 páginasÁcido NitrosoJorge Alberto Estrada TorresAún no hay calificaciones
- Proceso de Obtencion Del Acido NitricoDocumento3 páginasProceso de Obtencion Del Acido Nitriconemmisam100% (1)
- Procesos de OstwaldDocumento3 páginasProcesos de OstwaldJhonier Lopez Quintanilla100% (1)
- Nitracion de La AcetanilidaDocumento13 páginasNitracion de La AcetanilidazanniazorzaAún no hay calificaciones
- Ácido NítricoDocumento4 páginasÁcido NítricoChuchAún no hay calificaciones
- Producción y usos del ácido nítrico HNO3Documento31 páginasProducción y usos del ácido nítrico HNO3Maximiliano Nahuel Zapata OrueAún no hay calificaciones
- Producccion de AcidosDocumento7 páginasProducccion de AcidosJESUS FRANCISCO DUARTEAún no hay calificaciones
- El Ácido NítricoDocumento7 páginasEl Ácido NítricoAngel SantiagoAún no hay calificaciones
- Pia InorganicaDocumento11 páginasPia InorganicaEl VaqueroskyAún no hay calificaciones
- El NitrogenoDocumento27 páginasEl NitrogenoCarlos PiñeiroAún no hay calificaciones
- Nitración química: reacción, agentes, tipos y aplicaciones industrialesDocumento25 páginasNitración química: reacción, agentes, tipos y aplicaciones industrialesFederico GonzálezAún no hay calificaciones
- Q.Inorgánica NITROGENOIDESDocumento8 páginasQ.Inorgánica NITROGENOIDESBronco Wlady Corn-CarrAún no hay calificaciones
- COMPUESTOS NITROGENADOS - 2022-DepuradoDocumento29 páginasCOMPUESTOS NITROGENADOS - 2022-DepuradoEnriqueAún no hay calificaciones
- Química orgánica: nitroderivados y funciones nitrogenadasDocumento50 páginasQuímica orgánica: nitroderivados y funciones nitrogenadasHeber Daniel Andrade RiveraAún no hay calificaciones
- Diagrama de Flujo para Obtener Acido Nitrico Por Oxidacion Del AmoniacoDocumento4 páginasDiagrama de Flujo para Obtener Acido Nitrico Por Oxidacion Del AmoniacoElizabeth Canales RivasAún no hay calificaciones
- Nitración de La AcetanilidaDocumento9 páginasNitración de La AcetanilidaGilvert J Vasquez MendozaAún no hay calificaciones
- TrinitrotoluenoDocumento41 páginasTrinitrotoluenoTonyMoreno100% (1)
- Proceso Del Acido Nitrico para Convertir Un Explosivo Inv8Documento5 páginasProceso Del Acido Nitrico para Convertir Un Explosivo Inv8Juan Emiliano CastilloAún no hay calificaciones
- Acido Nitrico Complemento de Lamonografia IDocumento11 páginasAcido Nitrico Complemento de Lamonografia IMarleneCortezAún no hay calificaciones
- Química Inorgánica Grupo V NitrogenoDocumento9 páginasQuímica Inorgánica Grupo V NitrogenoRocco Del VecchioAún no hay calificaciones
- ALCALOIDESDocumento67 páginasALCALOIDESjefferson84Aún no hay calificaciones
- Preparación Del Ácido NítricoDocumento4 páginasPreparación Del Ácido NítricoWendy GarciaAún no hay calificaciones
- Preparación de ácido nítrico en laboratorioDocumento27 páginasPreparación de ácido nítrico en laboratorioAngiie DilAún no hay calificaciones
- NITRACION AlumnosDocumento54 páginasNITRACION AlumnosJamesMorenoBustamanteAún no hay calificaciones
- NitrllDocumento8 páginasNitrllBrayan HHAún no hay calificaciones
- Clase 10 Sem 7 - Acidos Oxiácidos Del NitrógenoDocumento13 páginasClase 10 Sem 7 - Acidos Oxiácidos Del NitrógenoDel1al9Aún no hay calificaciones
- TEMA IV-2020Documento37 páginasTEMA IV-2020cosasdelcelu37Aún no hay calificaciones
- Ingeniería de procesos siderúrgicos: La experiencia de AHMSADe EverandIngeniería de procesos siderúrgicos: La experiencia de AHMSAAún no hay calificaciones
- 2Documento2 páginas2yojanaAún no hay calificaciones
- 2Documento2 páginas2yojanaAún no hay calificaciones
- VVVVVDocumento8 páginasVVVVVyojanaAún no hay calificaciones
- Programa de Seguridad y Salud Ocupacional 2017Documento15 páginasPrograma de Seguridad y Salud Ocupacional 2017Axelito RbAún no hay calificaciones
- FTH 157Documento8 páginasFTH 157deybiAún no hay calificaciones
- Bases Del Concurso de Oratoria Fic 2018Documento2 páginasBases Del Concurso de Oratoria Fic 2018yojanaAún no hay calificaciones
- Anexo M. PROGRAMA DE INSPECCIONES PLANEADASDocumento16 páginasAnexo M. PROGRAMA DE INSPECCIONES PLANEADASManuel José Díaz BarreraAún no hay calificaciones
- 2Documento2 páginas2yojanaAún no hay calificaciones
- Clase 09 OctubreDocumento10 páginasClase 09 OctubreyojanaAún no hay calificaciones
- STFL01Documento6 páginasSTFL01yojanaAún no hay calificaciones
- Normas Apa Revisada y Actualizada Mayo 2019Documento26 páginasNormas Apa Revisada y Actualizada Mayo 2019JOHAN FERNANDO QUIROZ SERNAQUE80% (5)
- Preparación de Nitroparafinas en Fase Líquida Con Ácido NítricoDocumento5 páginasPreparación de Nitroparafinas en Fase Líquida Con Ácido NítricoyojanaAún no hay calificaciones
- Apa TutorialDocumento8 páginasApa TutorialYeison Orellano RAún no hay calificaciones
- 2 PetroperuDocumento1 página2 PetroperuyojanaAún no hay calificaciones
- Bases Concurso de OratoriaDocumento5 páginasBases Concurso de OratoriayojanaAún no hay calificaciones
- Informe (Gas 1)Documento22 páginasInforme (Gas 1)mariaquispemamaniAún no hay calificaciones
- Formato Apa GeneralDocumento18 páginasFormato Apa GeneralJonathan' Cuotto Dellán'Aún no hay calificaciones
- Preparación de Nitroparafinas en Fase Líquida Con Ácido NítricoDocumento18 páginasPreparación de Nitroparafinas en Fase Líquida Con Ácido NítricoyojanaAún no hay calificaciones
- 1Documento1 página1yojanaAún no hay calificaciones
- 2Documento1 página2yojanaAún no hay calificaciones
- Oxigeno Disuelto 3Documento3 páginasOxigeno Disuelto 3yojanaAún no hay calificaciones
- Anhídrido Nítrico.: NitroderivadosDocumento2 páginasAnhídrido Nítrico.: NitroderivadosyojanaAún no hay calificaciones
- ST Fo 25 Inspeccion EppDocumento3 páginasST Fo 25 Inspeccion EppAlberto Gamez GarciaAún no hay calificaciones
- 03 Clase RseDocumento4 páginas03 Clase RseyojanaAún no hay calificaciones
- Anhídrido NítricoDocumento1 páginaAnhídrido NítricoyojanaAún no hay calificaciones
- Oxigeno Disuelto 4Documento3 páginasOxigeno Disuelto 4yojanaAún no hay calificaciones
- Oxigeno Disuelto 3Documento3 páginasOxigeno Disuelto 3yojanaAún no hay calificaciones
- Oxigeno Disuelto 3Documento3 páginasOxigeno Disuelto 3yojanaAún no hay calificaciones
- 3Documento1 página3yojanaAún no hay calificaciones
- Semana 10 - QuimicaDocumento11 páginasSemana 10 - QuimicaVictor DefazAún no hay calificaciones
- AnhídridosDocumento5 páginasAnhídridosnorbertoAún no hay calificaciones
- Programas de Equilibrio Liquido Vapor ISOBÁRICOSDocumento7 páginasProgramas de Equilibrio Liquido Vapor ISOBÁRICOSRonaldo OrihuelaAún no hay calificaciones
- Ejercicios InorgánicaDocumento12 páginasEjercicios InorgánicaAcademicScientistsAún no hay calificaciones
- Ácidos y Bases Aplicados en CriminalísticaDocumento7 páginasÁcidos y Bases Aplicados en Criminalísticakiller0310 MaVaAún no hay calificaciones
- Lista de Productos Vitaminas y MineralesDocumento1 páginaLista de Productos Vitaminas y MineralesCésar Jesús Bautista HernándezAún no hay calificaciones
- Tarea NomenclaturaDocumento4 páginasTarea Nomenclaturaloqui lloAún no hay calificaciones
- Compuestos Organicos OxigenadosDocumento59 páginasCompuestos Organicos OxigenadosElvis CuevaAún no hay calificaciones
- Reacción de CannizzaroDocumento3 páginasReacción de Cannizzaromagykiss20100% (1)
- Taller Alcoholes y AldehidosDocumento9 páginasTaller Alcoholes y AldehidosVALENTINA VEGA MENDOZAAún no hay calificaciones
- Chicaiza Domenica - Deber4rDocumento5 páginasChicaiza Domenica - Deber4rDomenica Abigail Chicaiza EspinAún no hay calificaciones
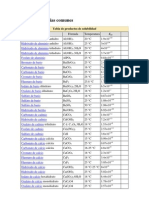
- Kps de Sustancias ComunesDocumento5 páginasKps de Sustancias ComunesLuiz Joaquim da SilvaAún no hay calificaciones
- QOI Clasificaci N y Nomenclatura JPODocumento86 páginasQOI Clasificaci N y Nomenclatura JPOMaximiliano TlatlitlúAún no hay calificaciones
- Tetróxido de plomo - propiedades, preparación y usos del pigmento rojo minioDocumento1 páginaTetróxido de plomo - propiedades, preparación y usos del pigmento rojo minioChristian VegegaAún no hay calificaciones
- OXISALDocumento2 páginasOXISALJavier AlonsoAún no hay calificaciones
- Óxidos, hidróxidos y salesDocumento3 páginasÓxidos, hidróxidos y salesJaco RAAún no hay calificaciones
- Tarea de QuimicaDocumento9 páginasTarea de QuimicaVíctor SupoAún no hay calificaciones
- Guía para nombrar óxidos e hidróxidosDocumento6 páginasGuía para nombrar óxidos e hidróxidosUriel Garcia SalazarAún no hay calificaciones
- Ejercicios nomenclatura inorgánica óxidos metales no metales salesDocumento1 páginaEjercicios nomenclatura inorgánica óxidos metales no metales salesAlexander Navarro SalazarAún no hay calificaciones
- Adrián Pastor Martín - Actividades Sobre Óxidos y PeróxidosDocumento7 páginasAdrián Pastor Martín - Actividades Sobre Óxidos y PeróxidosLola100% (1)
- QUIMICADocumento3 páginasQUIMICARaimy Rey Reyes NarvaezAún no hay calificaciones
- SoluciónDocumento10 páginasSoluciónMaria JaraAún no hay calificaciones
- Cuadro de SolucionesDocumento2 páginasCuadro de SolucionesAdriana Bravo JimenezAún no hay calificaciones
- Formulación y Nomenclatura de InorgánicaDocumento14 páginasFormulación y Nomenclatura de InorgánicamarianaAún no hay calificaciones
- Nomenclatura InorgánicaDocumento9 páginasNomenclatura InorgánicaISMAún no hay calificaciones
- Formación y Nomenclatura de Compuestos InorgánicosDocumento21 páginasFormación y Nomenclatura de Compuestos InorgánicosAgostina Orecchini AlemAún no hay calificaciones
- Nomenclatura PolifuncionalesDocumento27 páginasNomenclatura PolifuncionalesGUTIERREZ DAVILA NICOLLE STHEPHANIEAún no hay calificaciones
- Recuperación QUIMICA 11Documento3 páginasRecuperación QUIMICA 11Manuel Felipe Echeverry Gracés100% (1)
- Proceso AcetonaDocumento42 páginasProceso AcetonaAngel IsidoroAún no hay calificaciones
- Ésteres: formación, propiedades y aplicacionesDocumento4 páginasÉsteres: formación, propiedades y aplicacionesJuan José AgredaAún no hay calificaciones