Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Laboratorio #1 Mediciones Hidrológicas
Cargado por
Karla MagallonDerechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
Laboratorio #1 Mediciones Hidrológicas
Cargado por
Karla MagallonCopyright:
Formatos disponibles
MEDICIONES HIDROLÓGICAS Y AMBIENTALES
LABORATORIO NO. 1 PARÁMETROS FÍSICOS
GRUPO NO. 3
UNIVERSIDAD TECNOLÓGICA DE PANAMÁ
FACULTAD DE INGENIERÍA CIVIL
LICENCIATURA EN INGENIERÍA CIVIL
MEDICIONES HIDROLÓGICAS Y AMBIENTALES
LABORATORIO NO. 1 PARÁMETROS FÍSICOS
GRUPO NO. 3
ESTUDIANTES:
KARLA MAGALLÓN 2-741-474
LUISA MORENO 20-14-3365
ELISERÉ VIRUET 3-728-1073
PROFESOR:
CENOBIO CARDENAS
GRUPO: 1IC-154
FECHA DE ENTREGA:
MARTES 9 DE FEBRERO DE 2021
Laboratorio No. 1 Parámetros Físicos Pág. 2
ÍNDICE
INTRODUCCIÓN.......................................................................................................................4
MEDIDAS DE SEGURIDAD EN EL LABORATORIO..........................................................4
SUSTANCIAS QUÍMICAS PELIGROSAS.............................................................................5
PRIMEROS AUXILIOS EN CASO DE EMERGENCIA........................................................7
REGLAMENTO INTERNO DEL LABORATORIO.................................................................8
EXPERIENCIA DE LABORATORIO.....................................................................................10
POTENCIAL DE HIDRÓGENO (PH)................................................................................10
CONDUCTIVIDAD ELÉCTRICA.......................................................................................18
SALINIDAD...........................................................................................................................21
SÓLIDOS SUSPENDIDOS................................................................................................23
SOLIDOS DISUELTOS TOTALES...................................................................................26
TEMPERATURA..................................................................................................................29
SÓLIDOS SUSPENDIDOS................................................................................................32
TURBIEDAD.........................................................................................................................35
COLOR VERDADERO.......................................................................................................39
BIBLIOGRAFÍA........................................................................................................................44
Laboratorio No. 1 Parámetros Físicos Pág. 3
INTRODUCCIÓN
En este informe de laboratorio se describen las medidas de seguridad en el
laboratorio, sustancias químicas peligrosas, primeros auxilios en caso de
emergencias y el reglamento interno del laboratorio; además se desarrollan
actividades para determinar los parámetros físicos del agua, los cuales tienen
los resultados y las conclusiones al final de cada experiencia, los parámetros
desarrollados son: potencial de hidrógeno pH, conductividad eléctrica,
salinidad, sólidos suspendidos, sólidos disueltos totales, temperatura, sólidos
suspendidos, turbiedad y color verdadero.
MEDIDAS DE SEGURIDAD EN EL LABORATORIO
Para trabajar en el laboratorio es condición necesaria el uso de la bata protectora
debidamente abotonada ya que evita que las sustancias químicas lleguen a la piel.
En caso de cualquier accidente notifique inmediatamente a su profesor.
Cada grupo se responsabilizará de su zona de trabajo y de su material.
Es muy aconsejable, si se tiene el pelo largo, llevarlo recogido o metido en la ropa, así
como no llevar colgantes.
En el laboratorio no se podrá fumar, ni tomar bebidas ni comidas.
Evite todo contacto directo de los productos químicos con la boca, ojos, nariz o
cualquier área sensible del cuerpo.
Localice los equipos de seguridad y primeros auxilios y úselos correctamente (extintor,
ducha, lavador de ojos, guantes de asbesto, máscara contra gases, gafas de
seguridad, cámara de extracción, etc.).
Cuando vierta líquidos no acuosos y ácidos o bases fuertes por el desagüe, use una
fuerte corriente de agua.
Vierta los ácidos sobre el agua, nunca al revés.
Use la cámara de extracción siempre que se desprendan gases tóxicos o molestos en
una reacción.
Laboratorio No. 1 Parámetros Físicos Pág. 4
SUSTANCIAS QUÍMICAS PELIGROSAS
Las sustancias químicas se clasifican, en función de su peligrosidad, en:
Explosivos.
Sustancias y preparados que pueden explosionar bajo el efecto de una llama.
Comburentes.
Sustancias y preparados que, en contacto con otros, particularmente con los
inflamables, originan una reacción fuertemente exotérmica.
Extremadamente inflamables.
Sustancias y productos químicos cuyo punto de ignición sea inferior a 0°C, y su punto
de ebullición inferior o igual a 35°C.
Fácilmente inflamables.
Se definen como tales:
Sustancias y preparados que, a la temperatura ambiente, en el aire y sin aporte de
energía, puedan calentarse e incluso inflamarse.
Sustancias y preparados en estado líquido con un punto de ignición igual o superior a
0°C e inferior a 21°C.
Sustancias y preparados sólidos que puedan inflamarse fácilmente por la acción breve
de una fuente de ignición y que continúen quemándose o consumiéndose después del
alejamiento de la misma.
Sustancias y preparados gaseosos que sean inflamables en el aire a presión normal.
Sustancias y preparados que, en contacto con el agua y el aire húmedo, desprendan
gases inflamables en cantidades peligrosas.
Inflamables.
Sustancias y preparados cuyo punto de ignición sea igual o superior a 21°C e inferior a
55°C.
Muy tóxicos.
Sustancias y preparados que por inhalación, ingestión o penetración cutánea puedan
entrañar riesgos graves, agudos o crónicos, e incluso la muerte.
Nocivos.
Sustancias y preparados que por inhalación, ingestión o penetración cutánea puedan
entrañar riesgos de gravedad limitada.
Corrosivos.
Sustancias y preparados que en contacto con los tejidos vivos puedan ejercer sobre
ellos una acción destructiva.
Irritantes.
Laboratorio No. 1 Parámetros Físicos Pág. 5
Sustancias y preparados no corrosivos que por contacto inmediato, prolongado o
repetido con la piel o mucosas pueden provocar una reacción inflamatoria.
Peligrosos para el medio ambiente.
Sustancias y preparados cuya utilización presente o pueda presentar riesgos
inmediatos o diferidos para el medio ambiente.
Carcinógenos.
Sustancias y preparados que por inhalación, ingestión o penetración cutánea puedan
producir cáncer o aumento de su frecuencia.
Teratogénicos.
Sustancias y preparados que por inhalación, ingestión o penetración cutánea puedan
inducir lesiones en el feto durante su desarrollo intrauterino.
Mutagénicos.
Sustancias y preparados que por inhalación, ingestión o penetración cutánea puedan
producir alteraciones en el material genético de las células.
Algunas de estas sustancias se reflejan en el etiquetado de los productos químicos
mediante un símbolo o pictograma, de manera que se capte la atención de la persona
que va a utilizar la sustancia.
Laboratorio No. 1 Parámetros Físicos Pág. 6
PRIMEROS AUXILIOS EN CASO DE EMERGENCIA
TRATAMIENTO DE QUEMADURAS:
Quemaduras de ácido:
Lave la parte lesionada con un gran volumen de agua, aplique gasa empapada en
solución de bicarbonato de sodio y vende.
Quemadura de álcalis:
Lave la parte lesionada con un volumen de agua, aplique una gasa empapada en
solución de ácido bórico y vende.
Quemadura con llamas u objetos calientes:
No deben lavarse con agua. Aplique pomada y vende.
Quemadura de ácido o álcalis en los ojos:
Lave los ojos inmediatamente con un gran volumen de agua, después con solución de
bicarbonato de sodio si la lesión se debe a ácidos o con solución de ácido bórico en
caso de lesiones producidas por álcalis. Complete el tratamiento en ambos casos
agregando una gota de aceite de oliva, de semilla de algodón o de ricino.
Quemaduras de Bromo:
Lave completamente el área afectada y aplíquele glicerina o una solución diluida al 1
% de fenol.
Quemadura de fenol:
Lave completamente el área afectada y aplíquele una solución diluida al 1% de
bromo.
INCENDIO DE TEJIDOS:
Los fuegos pequeños pueden apagarse con una toalla o una bata de laboratorio. Si el
fuego prende en los vestidos de alguna persona, envuélvase a ésta en una manta
incombustible o colóquese a la persona bajo la ducha.
CORTE:
Es mejor dejar sangrar algo al principio, para prevenir la infección. Lave la herida
cuidadosamente y quite la suciedad y los trocitos de vidrio. Desinféctese con algún
antiséptico, como tintura de yodo, methiolato o metaphen. Aplique una venda estéril y
llévese al herido a un médico para un tratamiento completo.
ENVENENAMIENTO:
a. Llámese inmediatamente a un médico o envíese al paciente al hospital sin la
menor demora.
INCENDIO DE REACTIVOS:
Laboratorio No. 1 Parámetros Físicos Pág. 7
Apáguense todos los materiales combustibles de las proximidades del fuego. Los
fuegos pequeños pueden apagarse con un trozo de papel de asbesto o con una toalla.
Un líquido orgánico ardiendo en un vaso es menos peligroso que si se extiende
encima de la mesa. No soplar sobre la llama.
REGLAMENTO INTERNO DEL LABORATORIO
El laboratorio constituye el 15% de la nota final de Calidad y es requisito indispensable
para tener derecho a nota en el curso.
El trabajo de laboratorio se evaluará en forma individual, a pesar de que existan
informes que representan un trabajo de grupo.
Los estudiantes deberán asistir al laboratorio única y exclusivamente en el período que
les corresponda y, no podrán cambiarlo, permanente o temporalmente, si no es con
previa autorización del profesor de laboratorio.
En aquellas ocasiones en que el laboratorio no se pudiese realizar por motivo de días
feriados u otra causa, se harán los ajustes necesarios entre los estudiantes y el
instructor para reponer dicha práctica.
Las ausencias al laboratorio sólo podrán reponerse si el estudiante, a la mayor
brevedad posible, presenta al profesor de laboratorio excusa en forma escrita por
razones de enfermedad u otra causa justificada.
El estudiante que faltare a un experimento sin causa justificada o que al faltar no
presentase excusa escrita, perderá el derecho a reponer el experimento, y además no
podrá presentar el correspondiente informe.
El estudiante podrá reponer hasta un máximo de 1 práctica de laboratorio por lo que al
faltar a dos períodos no tendrá derecho a nota.
El estudiante debe leer y estudiar las indicaciones del experimento, antes de venir al
laboratorio.
El estudiante debe asistir puntualmente al laboratorio. Los alumnos que lleguen con
un retraso mayor de 5 minutos no podrán realizar la experiencia en ese período y
tendrán que reponerla en otro, con una evaluación inferior.
El estudiante realizará solamente los experimentos asignados o permitidos por su
profesor y esperará sus instrucciones para iniciar el trabajo.
Para trabajar en el laboratorio el estudiante deberá traer siempre bata.
El alumno estará obligado a reponer el material que rompa. El estudiante responsable
del deterioro o pérdida estará obligado a reponerlo en un plazo máximo de una
semana. En caso de no hacerlo en ese plazo no podrá continuar sus prácticas.
Todo estudiante comparte en la misma medida que su compañero de grupo la
responsabilidad del material entregado.
El estudiante es responsable por cualquier daño que, por su imprudencia o descuido
en su manejo, cause al material y equipo del laboratorio.
Laboratorio No. 1 Parámetros Físicos Pág. 8
Los papeles y residuos sólidos deberán botarse en el cesto de la basura, siendo cada
alumno responsable de la limpieza de su mesa, área de trabajo y del piso que le
corresponde. Si ocasionalmente, se derramase algún reactivo o agua, es
responsabilidad del alumno limpiarlo inmediatamente.
Los estudiantes están obligados a dejar limpio y ordenado la mesa de trabajo, el área
de reactivos, los implementos usados, el equipo y el piso de laboratorio antes de
retirarse previa notificación a su profesor.
Laboratorio No. 1 Parámetros Físicos Pág. 9
EXPERIENCIA DE LABORATORIO
POTENCIAL DE HIDRÓGENO (PH)
OBJETIVO GENERAL: Determinación cuantitativa de la concentración de iones
hidrógeno en aguas.
OBJETIVO ESPECÍFICO: Determinar la concentración del pH en muestras de aguas
en general, a través de potenciómetro o pHmetro.
METAS: Que el estudiante al finalizar la experiencia tenga la capacidad de determinar
el pH en muestra de aguas superficiales, subterráneas, potables, residuales e
industriales. Así como también de interpretar los resultados obtenidos de los mismos.
GRUPO DE TRABAJO Y EVALUACIÓN DEL APRENDIZAJE:
Los grupos de trabajo de laboratorio serán formados por tres (3) estudiantes y se
analizarán alrededor de tres (3) parámetros por cada sesión de laboratorio.
La evaluación de laboratorio sería un 20% del total de la nota; esta se divide en un
15% de informe de la experiencia, que se debe entregar una la siguiente sesión de
laboratorio y el 5% restante de asistencia y desempeño en el laboratorio.
CONTENIDO O RESUMEN TEÒRICO:
El término pH es utilizado universalmente para expresar la intensidad de las
condiciones ácidas o alcalinas de una solución y se define como el logaritmo negativo
de la concentración de iones de hidrógeno, o más precisamente, de la actividad de
iones de hidrógeno.
La escala de pH se extiende desde cero (muy ácido) hasta catorce (muy básico)
correspondiendo a pH=7 la neutralidad a 25°C.
En los procesos de potabilización (cloración, coagulación, ablandamiento y control de
la corrosión) el pH juega un papel importante. La prueba del valor del pH permite al
operador de una planta potabilizadora descubrir los cambios que se presenten entre la
calidad del agua cruda y del agua potabilizada para proceder de acuerdo con ello a
regular la adición apropiada de los reactivos para el mejor desarrollo de las reacciones
de clarificación y de ablandamiento. En algunas plantas, el agua terminada se ajusta,
con cal o carbonato de sodio, a valores ligeramente alcalinos del pH (mayores de 8)
con el propósito de reducir la corrosión en el sistema de distribución.
En el tratamiento de aguas negras por medio de procesos biológicos, el pH se debe
mantener en un ámbito que sea favorable para los organismos que están tomando
parte en el tratamiento.
Laboratorio No. 1 Parámetros Físicos Pág. 10
RECURSOS (REACTIVOS Y EQUIPOS)
1.- pHmetro
2.- Electrodo de vidrio
3.- Electrodo de calomel
4.- Agitador magnético
5.- Soluciones amortiguadoras para calibrar el pHmetro
PROCEDIMIENTO O METODOLOGÍA:
Debido a la amplia variedad de modelos de pHmetros disponibles comercialmente es
imposible proporcionar instrucciones detalladas para la operación de todos los
instrumentos. En cada caso, siga las instrucciones del fabricante.
En términos generales se recomienda lo siguiente:
1.- Mientras el pHmetro no está en uso mantenga la punta de los electrodos sumergida
en agua destilada o desmineralizada.
2.- Antes de utilizarlo saque el electrodo del agua y enjuáguelo con agua destilada.
3.- Seque los electrodos con papel absorbente y suave.
4.- Estandarice el instrumento, sumergiendo los electrodos en una solución
amortiguadora que tenga un pH aproximado al pH de la muestra.
5.- Remueva los electrodos de la solución amortiguadora, enjuáguelos muy bien y
séquelos.
6.- Sumerja los electrodos en una segunda solución amortiguadora, que sea
aproximadamente cuatro (4) unidades de pH diferente a la primera solución y anote la
lectura de pH. La lectura debe de estar dentro de las 0.1 unidades de pH para esta
segunda solución.
7.- Enjuague los electrodos, séquelos y sumérjalos en la muestra (200 mL
aproximadamente). Agite la muestra muy bien para proporcionar homogeneidad y
mantener los sólidos en suspensión. Corrija la temperatura del aparato si es posible.
Laboratorio No. 1 Parámetros Físicos Pág. 11
8.- Enjuague los electrodos y manténgalos en agua destilada o desmineralizada hasta
la próxima determinación.
Nota: En lugares donde las determinaciones de pH ocasionales estandaricen el
instrumento antes de cada determinación. Donde las determinaciones son muy
frecuentes estandarice cada una o dos horas. Sin embargo, si los valores de pH de las
muestras son muy variados estandarice con más frecuencia y con soluciones
amortiguadoras que tengan una o dos unidades de pH de diferencia con el pH de la
muestra. Cuando la respuesta del electrodo a dos soluciones amortiguadoras que
difieren en cuatro unidades de pH se aleja más allá de 0.1 unidades de pH, reemplace
el electrodo de vidrio.
Resultados:
pH
M-1: 5.05
M-2: 9.15
M-3: 7.05
M-4: 6.71
CÁLCULOS:
Reporte los resultados con una precisión de 0.1 unidades de pH. Calcule pOH; [H+]:
[OH-]
Grafique
Ecuaciones utilizadas:
Laboratorio No. 1 Parámetros Físicos Pág. 12
pOH = 14 – pH
pH = -log(H+)
pOH = -log (OH-)
pH medido: 5.05
pOH = 8.95
H+ = 8.9125093x10-6
OH- = 1.1220184-9
pH medido: 9.15
pOH = 4.85
H+ = 7.079457 x10-10
OH- =1.4125375 x10-5
pH medido: 7.05
pOH = 6.95
H+ = 8.9125093 x10-8
OH- = 1.1220184 x10-7
pH medido: 6.71
pOH = 7.29
H+ = 1.7782794 x10-7
OH- = 5.1286138 x10-8
Gráficos
Muestra pH pOH H+ OH-
M1 5.05 8.95 9.91E-06 1.12E-09
M2 9.15 4.85 7.07E-10 1.41E-05
M3 7.05 6.95 8.91E-08 1.12E-07
M34 6.71 7.29 1.78E-07 5.13E-08
Laboratorio No. 1 Parámetros Físicos Pág. 13
Ph
10 9.15
9
8
7.05 6.71
7
6
Parámetro
5.05
5
4
3
2
1
0
0 1 2 3 4 5
Muestras
pOH
10
8.95
9
8 7.29
6.95
7
6
Parámetro
4.85
5
4
3
2
1
0
0 1 2 3 4 5
Muestras
H+
1.20E-05
9.91E-06
1.00E-05
8.00E-06
Parámetro
6.00E-06
4.00E-06
2.00E-06
7.07E-10 8.91E-08 1.78E-07
0.00E+00
0 1 2 3 4 5
Muestras
Laboratorio No. 1 Parámetros Físicos Pág. 14
OH
1.60E-05
1.41E-05
1.40E-05
1.20E-05
1.00E-05
Parámetro
8.00E-06
6.00E-06
4.00E-06
2.00E-06
1.12E-09 1.12E-07 5.13E-08
0.00E+00
0 1 2 3 4 5
Muestras
pH, pOH, H+, OH
10
9
8
7
6
Parámetros
5
4
3
2
1
0
0 1 2 3 4 5
Muestras
pH pOH H+ OH
PREGUNTAS:
1.- Una muestra de agua tomada en el campo registró un valor de pH de 6.8 . Desde
ese momento hasta su llegada al laboratorio para ser analizada, el pH aumentó hasta
7.5. Dé una posible explicación para este cambio.
La muestra al ser tomada tenía mayor acidez y cuando fue transportada al laboratorio
al analizar esta acidez bajó, por lo tanto, aumento su pH, esto pude ser por un mal
manejo en la muestra, alguna contaminación mediante el muestreo, incluso el envase
podría haber estado contaminado.
Laboratorio No. 1 Parámetros Físicos Pág. 15
2.- Investigue los límites para el valor de pH aceptados por la Normas Panameñas
Actuales y la OMS.
Los limites o valores máximos permisibles de pH aceptados son
Normativa Panameña: 5.5 – 9.0 en unidades de pH.
OMS: 6.5 – 8.5 en unidades de pH.
Conclusión
La conversión utilizada de H+ es una manera oportuna de medir la relativa acidez o
basicidad de una solución. La pate logarítmica en la escala de pH significa que este
cambia 1 unidad por cada factor de 10 en el cambio de concentración de H+. El signo
negativo delante del log nos dice que hay una relación inversa entre el pH y el H+, de
manera que cuando aumenta el pH, H+ disminuye y viceversa.
Esta experiencia arroja que 3 de las muestras son ácidas, mientras que una es básica,
encontrándose en el límite, ya que esta de haber arrojado un valor de 7 (muestra No.
3) se consideraría agua pura. Según la normativa panameña todas las muestras con
excepción de la No. 1 serían aptas para el consumo humano.
Recolección de la muestra y almacenamiento
Para tomar la muestra utilice recipientes de vidrio. Determine el pH dentro de un
periodo de 24 horas y almacene la muestra en refrigeración.
Laboratorio No. 1 Parámetros Físicos Pág. 16
CONDUCTIVIDAD ELÉCTRICA
Introducción:
La conductividad es una variable que se controla en muchos sectores, desde la
industria química a la agricultura. Esta variable depende de la cantidad de sales
disueltas presentes en un líquido y es inversamente proporcional a la resistividad del
mismo.
Objetivo: Medir el valor de conductividad eléctrica, para determinar la calidad del agua
superficial.
Discusión: La conductividad se define como la capacidad de una sustancia de
conducir la corriente eléctrica y es lo contrario de la resistencia.
La unidad de medición utilizada comúnmente es el Siemens/cm (S/cm), con una
magnitud de 10 elevado a -6, es decir microSiemens/cm (µS/cm), o en 10 elevado a
-3, es decir, miliSiemens (mS/cm).
Conductividad del agua:
Agua pura: 0.055 µS/cm
Agua destilada: 0.5 µS/cm
Agua de montaña: 1.0 µS/cm
Agua para uso doméstico: 500 a 800 µS/cm
Máx. para agua potable: 10055 µS/cm
Agua de mar: 52 mS/cm
En el caso de medidas en soluciones acuosas, el valor de la conductividad es
directamente proporcional a la concentración de sólidos disueltos, por lo tanto, cuanto
mayor sea dicha concentración, mayor será la conductividad. La relación entre
conductividad y sólidos disueltos se expresa, dependiendo de las aplicaciones, con
una buena aproximación por la siguiente regla:
grados ingleses grados americanos
1.4 µS/cm = 1ppm o 2 µS/cm = 1 ppm (partes por millón de CaCO3)
donde 1 ppm = 1 mg/L es la unidad de medida para sólidos disueltos.
Además de los normales conductivímetros, existen instrumentos que convierten
automáticamente el valor de conductividad en ppm, ofreciendo directamente las
medidas de la concentración de sólidos disueltos.
La conductividad de una solución se determina por un movimiento molecular.
Reactivos y Equipos:
1. Multiparámetro
Laboratorio No. 1 Parámetros Físicos Pág. 17
2.Vaso químico
3.Muestra de agua superficial
4.Agua destilada
Procedimiento
1.Inicialmente se procede a encender y calibrar el conductivímetro, utilizando una
solución de conductividad eléctrica conocida a una temperatura de 25°C
aproximadamente; se introduce el sensor hasta la mitad y pasar a registrar en la
pantalla del mismo, la medida requerida para su calibración y se ajusta.
2.Para realizar las lecturas de conductividad eléctrica se introduce el sensor
directamente en el cuerpo de agua o en el vaso químico donde se encuentra la
muestra y se genera automáticamente la lectura por el instrumento.
3.Finalmente, se analiza los datos tomados y se genera también un informe detallado.
Resultados: Haga graficas de los resultados
Conductividad Eléctrica
(µS/cm)
M-1: 439.4
M-2: 272.2
M-2: 135.9
M-4: 176.3
Laboratorio No. 1 Parámetros Físicos Pág. 18
Conductividad Eléctrica (µS/cm)
500
450
400
350
300
µS/cm
250
200
150
100
50
0
0 1 2 3 4
Muestras
Conclusión:
De las muestras tomadas se puede deducir que, hasta la tercera de estas, se observó
una disminución en la medida de conductividad eléctrica, ya en la cuarta muestra
volvía a elevarse. El rango presentado en µS/cm por las muestras, indican que están
dentro de los valores observados en agua potable, por ejemplo, en los Estados Unidos
el agua potable tiene una conductividad eléctrica de 30-1500 µS/cm.
Otra conclusión es que la primera muestra va a tener mayor cantidad de sólidos
totales disueltos por tener mayor conductividad eléctrica debido a que estos dos
términos están relacionados y son directamente proporcionales. Actualmente existen
aparatos de medición que por medio de la conductividad eléctrica del agua (o
solución), calcula la cantidad de TDS en ppm (mg / L).
Laboratorio No. 1 Parámetros Físicos Pág. 19
SALINIDAD
Introducción:
La salinidad es la cantidad de sales disueltas en un kilogramo de agua. La mayor parte
del agua de la Tierra se puede considerar una solución de diversas sales. Un valor
medio para todos los océanos del mundo es de 35 gramos por kilogramo, o 35 ppm.
En esta práctica vamos a medir y comparar la salinidad de cuatro muestras de agua.
Objetivo: Determinar el contenido de salinidad en las diferentes muestras de agua en
estudio.
Discusión:
La salinidad es el contenido de sal disuelta en un cuerpo de agua, aunque el término
también es válido para referirse al contenido salino en suelos. Esta característica está
definida por el contenido de la sustancia de cloruro de sodio tanto en suelos como en
el agua.
La salinidad es la medida más comúnmente usada para referirse a la salobridad
del agua de mar y se define como el número total de gramos de sales inorgánicas
disueltas en 1 Kg de en este tipo de agua.
Equipo:
Vaso químico
Papel absorbente
Agua destilada
Muestra a utilizar
Multiparámetro
Procedimiento:
Se utiliza un equipo llamado multiparámetros, el cual mide parámetros como la
temperatura, conductividad eléctrica, los sólidos disueltos totales, pH, entre otros.
Tomamos la muestra (nuestro grupo tomo la #1), la agitamos antes de utilizarla para
así evitar la sedimentación.
Vertimos la muestra en un vaso químico.
Laboratorio No. 1 Parámetros Físicos Pág. 20
Procedimos a encender el Multiparámetros (botón verde), y con ayuda de agua
destilada, rociamos un poco en donde se encuentran los electrodos del equipo, y los
colocamos dentro de la probeta con la muestra de agua en estudio.
Esperamos a que los valores del Multiparámetros se estabilizaran, y obtenemos el
valor de salinidad en cada muestra.
Sacamos los electrodos y los enjuagamos con agua destilada.
Resultados: Grafique
Salinidad (%)
M-1: 0.21
M-2: 0.13
M-3: 0.06
M-4: 0.08
Salinidad (%)
0.25
0.21
0.2
0.15
Parámetro
0.13
0.1 0.08
0.06
0.05
0
0 1 2 3 4 5
Muestras
Laboratorio No. 1 Parámetros Físicos Pág. 21
Conclusión:
Partiendo del hecho de que la salinidad es una medida de la cantidad de sales
disueltas en agua. Ahora bien, la salinidad y la conductividad están relacionadas
porque la cantidad de iones disueltos aumentan los valores de ambas.
Por otra parte, el agua dulce se encuentra en rangos menores de 0.05% mientras que
el agua salobre está de 0.05% a 3%, que son los valores obtenidos en esta
experiencia, lo que quiere decir es que tiene más sales disueltas que el agua dulce,
pero menos que el agua de mar. La muestra más cercana a agua dulce es la No. 3 y
la de mayor concentración de salinidad es la muestra No. 1.
SÓLIDOS SUSPENDIDOS
Introducción:
Los Sólidos suspendidos son partículas que permanecen en suspensión en el agua
debido al movimiento del líquido o debido a que la densidad de la partícula es menor o
igual que la del agua. La concentración de sólidos en suspensión es un valor utilizado
como uno de los indicadores de la calidad del agua. Todos los sólidos en suspensión
se pueden eliminar del agua mediante filtrado.
Objetivo: Determinar el contenido de material sólido suspendido en muestras de agua
Discusión: Para la determinación de los sólidos suspendidos o no filtrables como
también se les llama, pueden usarse diferentes métodos como lo son el gravimétrico,
que consiste en el filtrado, secado y pesado de la muestra, proceso que es un poco
más largo que el método espectrofotométrico, el cual vamos a emplear en este
laboratorio. El método espectrofotométrico en una manera simple de determinar los
sólidos suspendidos en una muestra de agua y es aplicado generalmente para
comprobar los procesos en fábricas debido a su rapidez y practicidad.
Equipo:
Agitador mecánico de alta velocidad
Recipiente de 250-500 mL
Pipeta serológica de 25 mL
Un juego de celdas de 25 mL
Papel absorbente
Espectrofotómetro de longitud de onda nanométrica
Laboratorio No. 1 Parámetros Físicos Pág. 22
Procedimiento:
Vertimos 50 ml de la muestra de agua en un vaso químico, colocándolo en el agitador
de alta velocidad, introduciéndole un imán, procedimos a encenderlo y esperamos un
tiempo de 2 minutos; apagando así el agitador y sacando el imán de la muestra.
Vertimos 25 ml de la muestra de agua contenida en el vaso químico en un recipiente
de vidrio con tapa, y utilizamos el recipiente de agua destilada con 25 ml.
Encendimos el Espectrofotómetro, y metimos el programa 630 para los sólidos
suspendidos ajustando la frecuencia indicada por el equipo, e insertamos el recipiente
de agua destilada (25ml), y presionamos ENTER, arrojándonos así el valor de cero (0).
Introducimos el recipiente de la muestra (25ml), y presionamos READ, dándonos así el
valor de sólidos suspendidos en mg/L
Nota: Los recipientes de agua destilada y de la muestra (25ml), antes de introducirlos
al Espectrofotómetro, se limpiaban con papel toalla de arriba hacia abajo.
Preguntas:
¿Qué importancia tienen los sólidos suspendidos en una muestra de agua para
consumo humano?
Los Sólidos suspendidos son partículas que permanecen en suspensión en el agua
debido al movimiento del líquido o debido a que la densidad de la partícula es menor o
igual que la del agua. La concentración de los sólidos suspendidos es un valor que es
utilizado como indicador de la calidad del agua. Los sólidos suspendidos son
importantes ya que los contaminantes y patógenos que contiene se transportan en la
superficie de las partículas. Cuanto menor sea el tamaño de partícula, mayor será el
área de superficie total por unidad de masa de partícula en gramos, y por lo tanto,
mayor será la carga de contaminantes que es probable que se transporte. Por ello es
importante determinar qué cantidad de solidos suspendidos tienen las aguas que son
designadas para el consumo humano.
¿Cómo pueden ser removidos los sólidos suspendidos de una muestra de
agua?
La eliminación de sólidos en suspensión se logra generalmente mediante el uso de
sedimentación y/o filtros de agua. Al eliminar la mayoría de los sólidos suspendidos en
un suministro de agua, el agua significativa generalmente se convierte cerca de la
Laboratorio No. 1 Parámetros Físicos Pág. 23
calidad de la bebida. A esto le sigue la desinfección para asegurar que cualquier
patógeno libre flotante, o patógenos asociados con la pequeña cantidad restante de
sólidos en suspensión, se vuelvan ineficaces.
Resultados: Grafique
mg
Solidos Suspendidos ( )
L
M-1: 5
M-2: 20
M-3: 13
M-4: 7
Conclusión:
De acuerdo con la Norma Panameña COPANIT, establece que el valor máximo
permitido para los sólidos suspendidos es de 35 mg/L, y al ver nuestros resultados,
cada uno de los valores para las diferentes muestras están dentro del rango.
Laboratorio No. 1 Parámetros Físicos Pág. 24
SOLIDOS DISUELTOS TOTALES
Introducción:
Solidos Disueltos Totales son el número de miligramos del residuo que queda
después de evaporar una muestra de agua previamente filtrada a través de un filtro
de fibra de vidrio.
El contenido de SDT de un agua puede estimarse midiendo
la conductividad eléctrica (CE) de la misma, ya que aquellos sólidos que se ionizan,
aumentan la CE. El agua pura tiene una CE prácticamente de cero.
Objetivo: Determinar el contenido de material sólido disueltos totales en las diferentes
muestras de agua.
Discusión:
Estrictamente hablando todo lo que es materia excepto el agua contenida en las
sustancias líquidas se considera como materia sólida. Sin embargo, el termino de
sólidos comúnmente utilizado se refiere al material sólido que permanece como un
residuo una vez realizado el proceso de evaporación y secado.
El termino de solidos totales se refiere al material que queda en el recipiente después
de la evaporación de la muestra y su subsiguiente secado en un horno a una
temperatura definitiva. Estos incluyen los sólidos filtrables y no filtrables, es decir, la
porción de los sólidos totales que paran a través del filtro y la porción que es retenida,
respectivamente.
Equipo:
Vaso químico
Papel absorbente
Agua destilada
Muestra a utilizar
Multiparámetro
Procedimiento:
Se utiliza un equipo llamado multiparámetros, el cual mide parámetros como la
temperatura, conductividad eléctrica, los sólidos disueltos totales, pH, entre otros.
Tomamos la muestra (nuestro grupo tomo la #1), la agitamos antes de utilizarla para
así evitar la sedimentación.
Vertimos la muestra en un vaso químico.
Laboratorio No. 1 Parámetros Físicos Pág. 25
Procedimos a encender el Multiparámetros (botón verde), y con ayuda de agua
destilada, rociamos un poco en donde se encuentran los electrodos del equipo, y los
colocamos dentro de la probeta con la muestra de agua en estudio.
Esperamos a que los valores del Multiparámetros se estabilizaran, y captamos los
valores.
Sacamos los electrodos y los enjuagamos con agua destilada.
Preguntas:
¿Qué importancia tienen los datos de sólidos en la práctica de ingeniería
sanitaria?
La ingeniería sanitaria se dedica al saneamiento de ámbitos de actividades humanas,
esto con lleva a que los principales datos que se requieren sean de sólidos, puesto
que, dichas actividades humanas están conformadas por dichos sólidos.
¿Qué otros tipos de análisis de sólidos se realizan y que importancia desde el
punto de vista sanitarios esos poseen?
Solido sedimentable: causan problemas en plantas de tratamiento y también pueden
provocar la obstrucción en canales y tuberías.
Solidos coloidales suspendidos: la importancia del análisis de estos solidos es que
consisten en limo fino, bacterias, sustancias que ocasionan el color, entre otros; los
cuales en su mayoría no se sedimentan después de un largo periodo de tiempo.
Donde su efecto se da en el color y la turbidez de aguas sedimentadas sin
coagulación.
Resultados: Grafique
mg
Solidos Disueltos Totales ( )
L
M-1: 290
M-2: 150
M-3: 90
M-4: 110
Laboratorio No. 1 Parámetros Físicos Pág. 26
Conclusión:
Para los sólidos disueltos totales la norma panameña COPANIT, presenta un valor
máximo permisible de 500 mg/L y todas las muestras presentan un valor inferior al 500
mg/L, por ende estamos cumpliendo con lo establecido en la norma.
Laboratorio No. 1 Parámetros Físicos Pág. 27
TEMPERATURA
Introducción:
La temperatura es la propiedad física que se refiere a las nociones comunes de calor o
ausencia de calor. Es una de las magnitudes más utilizadas para describir el estado de
la Atmósfera.
Toda sustancia en determinado estado de agregación (sólido, líquido o gas), está
constituida por moléculas que se encuentran en continuo movimiento. La suma de las
energías de todas las moléculas del cuerpo se conoce como energía térmica; y la
temperatura es la medida de esa energía promedio.
Objetivos: Practicar el uso del equipo para determinar la temperatura del agua.
Discusión: La temperatura es un parámetro físico que permite medir las sensaciones
de calor y frío.
Desde el punto de vista microscópico, la temperatura se considera representación de
la energía cinética interna media de las moléculas que integran el cuerpo estudiado,
en este caso el agua. Esta energía cinética se manifiesta en forma de agitación
térmica, que resulta de la colisión entre las moléculas que forman el agua.
Los animales las plantas acuáticas son sensibles a los cambios de temperatura del
agua y requieren que esta se mantenga dentro de un intervalo determinado para poder
sobrevivir y reproducirse. Si la temperatura del agua permanece fuera de este intervalo
durante mucho tiempo, los organismos quedarán expuestos a condiciones
inadecuadas.
La temperatura afecta a la cantidad de oxígeno que puede transportar el agua. El agua
a menor temperatura transporta más oxígeno y todos los animales acuáticos necesitan
este para sobrevivir. También influye en la fotosíntesis de plantas y algas, y la
sensibilidad de los organismos frente a los residuos tóxicos.
El aumento de la temperatura en nuestros ríos se puede deber a vertidos de agua
caliente de plantas industriales, especialmente de agua de refrigeración. También se
puede deber a la escasez de árboles en la orilla del rio, provocando que no haya
mucha sombra.
La unidad de medida de la temperatura es el grado centígrado (ºC). Corresponde a la
centésima parte entre el punto de fusión del agua y el punto de su ebullición en la
escala que fija el valor de cero grados para la fusión y cien para la ebullición.
Reactivos y Equipos
1.pHmetro
2.Vaso químico
3.Muestra de agua superficial
4.Agua destilada
Procedimiento
Laboratorio No. 1 Parámetros Físicos Pág. 28
Debido a la amplia variedad de modelos de pHmetros disponibles comercialmente es
imposible proporcionar instrucciones detalladas para la operación de todos los
instrumentos. En cada caso, siga las instrucciones del fabricante.
En términos generales se recomienda lo siguiente:
Mientras el pHmetro no está en uso mantenga la punta de los electrodos sumergida en
agua destilada o desmineralizada.
Antes de utilizarlo saque el electrodo del agua y enjuáguelo con agua destilada.
Seque los electrodos con papel absorbente y suave.
Estandarice el instrumento, sumergiendo los electrodos en una solución amortiguadora
que tenga un pH aproximado al pH de la muestra.
Remueva los electrodos de la solución amortiguadora, enjuáguelos muy bien y
séquelos.
Sumerja los electrodos en una segunda solución amortiguadora, que sea
aproximadamente cuatro (4) unidades de pH diferente a la primera solución y anote la
lectura de pH. La lectura debe de estar dentro de las ± 0.1 unidades de pH para esta
segunda solución.
Enjuague los electrodos, séquelos y sumérjalos en la muestra (200 mL
aproximadamente). Agite la muestra muy bien para proporcionar homogeneidad y
mantener los sólidos en suspensión. Corrija la temperatura del aparato si es posible.
Enjuague los electrodos y manténgalos en agua destilada o desmineralizada hasta la
próxima determinación.
Resultados: Grafique
Temperatura (°C)
M-1: 21.6
Laboratorio No. 1 Parámetros Físicos Pág. 29
M-2: 21.3
M-3: 20.7
M-4 21.1
Temperatura
25
20
15
10
0
0 1 2 3 4 5
Temperatura
Conclusión:
Según la norma panameña COPANIT, dice que el valor máximo permisible es de ±
3°C de la Temperatura normal del sitio, pero la diferencia es que la temperatura
normal del sitio no nos la dan, pero si podemos hacer una suposición que sería de
20°C, podemos decir que nuestros datos están en el rango permitido.
SÓLIDOS SUSPENDIDOS
Introducción:
Laboratorio No. 1 Parámetros Físicos Pág. 30
Los Sólidos suspendidos son partículas que permanecen en suspensión en el
agua debido al movimiento del líquido o debido a que la densidad de la
partícula es menor o igual que la del agua. La concentración de sólidos en
suspensión es un valor utilizado como uno de los indicadores de la calidad del
agua. Todos los sólidos en suspensión se pueden eliminar del agua mediante
filtrado.
Objetivo: Determinar el contenido de material sólido suspendido en muestras
de agua
Discusión: Para la determinación de los sólidos suspendidos o no filtrables
como también se les llama, pueden usarse diferentes métodos como lo son el
gravimétrico, que consiste en el filtrado, secado y pesado de la muestra,
proceso que es un poco más largo que el método espectrofotométrico, el cual
vamos a emplear en este laboratorio. El método espectrofotométrico en una
manera simple de determinar los sólidos suspendidos en una muestra de agua
y es aplicado generalmente para comprobar los procesos en fábricas debido a
su rapidez y practicidad.
Equipo:
• Agitador mecánico de alta velocidad
• Recipiente de 250-500 mL
• Pipeta serológica de 25 mL
• Un juego de celdas de 25 mL
• Papel absorbente
• Espectrofotómetro de longitud de onda nanométrica
Procedimiento:
1. Vertimos 50 ml de la muestra de agua en un vaso químico, colocándolo
en el agitador de alta velocidad, introduciéndole un imán, procedimos a
encenderlo y esperamos un tiempo de 2 minutos; apagando así el
agitador y sacando el imán de la muestra.
2. Vertimos 25 ml de la muestra de agua contenida en el vaso químico en un
recipiente de vidrio con tapa, y utilizamos el recipiente de agua destilada con 25
ml.
Laboratorio No. 1 Parámetros Físicos Pág. 31
3. Encendimos el Espectrofotómetro, y metimos el programa 630 para los
sólidos suspendidos ajustando la frecuencia indicada por el equipo, e
insertamos el recipiente de agua destilada (25ml), y presionamos ENTER,
arrojándonos así el valor de cero (0).
4. Introducimos el recipiente de la muestra (25ml), y presionamos READ,
dándonos así el valor de sólidos suspendidos en mg/L
Nota: Los recipientes de agua destilada y de la muestra (25ml), antes de
introducirlos al Espectrofotómetro, se limpiaban con papel toalla de arriba hacia
abajo.
Resultados: Grafique
Solidos Suspendidos
25
SÓLIDOS SUSPENDIDOS mg/L (mg/L)
SÓLIDOS SUSPENDIDOS mg/L
20 SÓLIDOS
SUSPENDIDOS (mg/L)
M-1
15 5
M-2 20
10
M-3 13
M-4
5 7
0
0 1 2 3 4
MUESTRAS
Preguntas:
¿Qué importancia tienen los sólidos suspendidos en una muestra de agua
para consumo humano?
Los sólidos en suspensión son partículas que permanecen en suspensión en el
agua debido al movimiento del líquido o debido a que la densidad de la
partícula es menor o igual que la del agua. La concentración de sólidos en
suspensión es un valor utilizado como uno de los indicadores de la calidad del
agua. Los sólidos en suspensión pueden ser de origen orgánico o inorgánico.
Los materiales orgánicos tienen origen animal o vegetal. Las sustancias
Laboratorio No. 1 Parámetros Físicos Pág. 32
orgánicas siempre contienen carbono, oxígeno e hidrógeno. Las sustancias
inorgánicas tienen, por otro lado, origen mineral y no suelen contener carbono.
¿Cómo pueden ser removidos los sólidos suspendidos de una muestra
de agua?
Todos los sólidos en suspensión se pueden eliminar del agua mediante filtrado;
sin embargo, si los sólidos en suspensión tienen una densidad mayor que el
agua, estas partículas se pueden eliminar también por sedimentación, si la
turbulencia del agua es mínima.
Sedimentación: el agua que se va a tratar se manda al sedimentador y
después
de cierto tiempo los sólidos suspendidos en la misma se separan del
líquido por
acción de tratamiento de las aguas separándolas mediante
sedimentación por gravedad.
Coagulación y Floculación: la coagulación se lleva a cabo
agregándoles reactivos
necesarios en un recipiente para que una turbina agite a alta velocidad y
mezcle
bien los reactivos con el agua a tratar, luego de esto, la floculación se
lleva a cabo
en un tanque con paletas que giran y que provocaran el choque entre
partículas
logrando un floculo de gran tamaño que vence la resistencia del fluido,
provocando
una separación del solido del fluido.
Conclusión:
Según la Norma panameña COPANIT establece que el límite máximo permitido
de sólidos suspendidos en el agua es de 35 mg/L. observando todas las
muestras obtenidas podemos concluir que todas se encuentran dentro del
límite permitido. Donde podemos observar que el agua de dichas muestras en
bastante clara permitiendo el paso de la Luz por sus bajos niveles de partículas
en suspensión donde estas no obstruyen el paso de la luz y dando como
resultado un agua bastante clara sin color y una buena estética para el
consumo de agua potable, pero aun así esto no quiere decir que el agua este
lista para consumir ya que el agua potable tiene que pasar por características
químicas y también verificar los otras características físicas.
Laboratorio No. 1 Parámetros Físicos Pág. 33
TURBIEDAD
Introducción
Se entiende por turbidez o turbiedad a la medida del grado de transparencia
que pierde el agua o algún otro líquido incoloro por la presencia de partículas
en suspensión. Cuanto mayor sea la cantidad de sólidos suspendidos en el
líquido, mayor será el grado de turbidez. En potabilización del agua y
tratamiento de aguas residuales, la turbidez es considerada como un buen
parámetro para determinar la calidad del agua, a mayor turbidez menor calidad.
Objetivos generales: Determinación cuantitativa de la turbiedad (partículas
suspendidas) que se encuentran en el agua.
Objetivo específico: Determinar la cantidad material en suspensión por medio
de la turbiedad que se encuentran en las aguas, utilizando para ello método
espectrofotométrico.
Contenido o resumen teórico:
El término turbiedad es aplicado a aguas que contienen materiales en
suspensión que interfieren con el paso de la luz a través del agua. La turbiedad
puede ser causada por una amplia variedad de materiales en suspensión cuyo
tamaño va desde las dispersiones coloidales hasta las dispersiones
moleculares dependiendo del grado de turbulencia del cuerpo de agua.
La naturaleza de estos materiales en suspensión es muy amplia. La mayor
parte son de origen inorgánico (arrastre de partículas del suelo, etc.) pero
cantidades considerables son de origen orgánico (desechos industriales,
domésticos, etc.).
Los materiales de naturaleza orgánica que alcanzan los ríos sirven como
alimentos para las bacterias y otros microorganismos que también alimentan
las bacterias y este crecimiento bacterial contribuye aún más a la turbiedad
total.
Los nutrientes inorgánicos tales como nitrógeno y fósforo presentes en las
descargas de aguas negras y los procedentes de los desechos de las labores
de la agricultura estimulan el crecimiento de las algas que también contribuyen
a la turbiedad.
Recolección y almacenamiento de la muestra
Tome muestras representativas en un recipiente de vidrio o plástico que esté
limpio. Analice la muestra el mismo día o guárdela en lugar oscuro si va a ser
analizada en un periodo superior a 24 horas.
Recursos (reactivos y equipos):
Espectrofotómetro DR/ 2010
Laboratorio No. 1 Parámetros Físicos Pág. 34
Procedimiento o metodología:
1. Seleccione el programa de turbiedad introduciendo el número clave
(750) y oprima ENTER.
2. Coloque el dial en 860 nm.
3. Llene uno de los recipientes de 25 mL con agua destilada (blanco).
4. Limpie el recipiente con un papel absorbente, coloque el recipiente
dentro del aparato y oprima ZERO.
5. Llene el otro recipiente de 25 mL con el agua de muestra, límpielo con el
papel absorbente, colóquelo dentro del aparato oprima READ y anote el
resultado.
NOTA: Efectúe todas las operaciones tan rápidamente como sea posible,
especialmente cuando se analizan aguas con altas turbiedades, con el fin de
Laboratorio No. 1 Parámetros Físicos Pág. 35
mantener las partículas en suspensión. Para resultados más confiables Re
disperse agitando el recipiente con la muestra.
Muestras que tengan turbiedades mayores de 4400 UNT, deben ser analizadas
diluyendo la muestra con el agua que tenga cero turbiedades y multiplicar el
resultado por el factor de dilución. Ejemplo, si 10 ml de la muestra se diluyen a
50 ml el resultado debe multiplicarse por 5.
Dilución realizada: 10 ml de muestra
------------------------------------------------------
50 ml (total agua de muestra + agua dilución)
Factor de dilución: 50 ml /10 ml = 5.0
Resultados: Grafique
Turbiedad (FAN=UNT)
M-1: 1
M-2: 16
M-3 22
M-4: 15
TURBIEDAD
25
TURBIEDA
20 D
15
TURBIEDAD
10
0
1 1.5 2 2.5 3 3.5 4 4.5
MUESTRAS
PREGUNTAS:
1. Discuta la naturaleza de materiales que ocasionan turbiedad en:
• Aguas negras: la turbiedad es ocasionada por materiales orgánicos que
pueden provenir por descargas domésticas, industriales u otras, que no han
sido tratadas apropiadamente.
Laboratorio No. 1 Parámetros Físicos Pág. 36
• Aguas de río contaminadas: esta turbulencia se debe desechos orgánicos,
productos químicos, bacterias; resultado de la actividad humana.
• Aguas de río en tiempo de crecidas: es debido al transporte de material de
origen orgánico originado por el arrastre producido por la corriente de agua.
2. Cuáles son los límites para turbiedad en aguas utilizadas para consumo
humanos
establecidos por las normas panameñas. Mencione la razón por el cual han
sido fijados tales valores.
La Norma Panameña DGNTI-COPANIT 395 establece como valor máximo
permisible para la turbiedad es 1.0 UNT, pero preferiblemente menor a dicho
valor. La razón por la que fue establecido este valor es por la parte estética
debido a que una persona no tomaría agua estando sucia y lo importante es
eliminar esta turbidez para que el agua pueda ser consumible.
Conclusión.
La Norma Panameña DGNTI-COPANIT 395 establece como valor máximo
permisible para la turbiedad es 1.0 UNT, pero preferiblemente menor a dicho
valor. La razón por la que fue establecido este valor es por la parte estética
debido a que una persona no tomaría agua estando sucia y lo importante es
eliminar esta turbidez para que el agua pueda ser consumible.
De las 4 muestras utilizadas en laboratorio, solo la muestra (1) cumple con el
valor máximo permitido por la norma siendo el valor máximo de 1.0.
los resultados que se obtuvieron en las muestras dan niveles de turbidez
superiores a lo permitido en la norma panameña COPANIT por lo que no se
puede considerar apta para el consumo humano. Para hacer el agua apta para
el consumo humano hay que bajar los niveles de turbiedad y esto quiere decir
que las muestras tienes demasiado materiales en suspensión, estas
características son directamente proporcionales.
Laboratorio No. 1 Parámetros Físicos Pág. 37
COLOR VERDADERO
Introducción
El color del agua es importante tanto en aguas potables, en uso industrial,
como en ambientes acuáticos. El color aparente sería el color de la muestra, tal
y como ha sido obtenida, mientras que el color verdadero sería el color de la
muestra una vez ha sido filtrada o centrifugada, dejando solamente las
sustancias o especies disueltas.
Objetivo general: Determinación cuantitativa de los materiales que ocasionan
color verdadero en las aguas.
Objetivo específico: Determinar la cantidad de color verdadero que se
encuentra en muestras de aguas por el método espectrofotométrico.
Contenido o resumen teórico:
El color en el agua puede ser el resultado de la presencia de iones metálicos
presentes en la naturaleza (hierro y magnesio), humus, plancton, hiervas o
desechos industriales.
Para que un agua sea apropiada para consumo humano y para usos
industriales debe eliminarse el color.
Se habla de color verdadero y color aparente. El color verdadero es el color del
agua una vez eliminada la turbiedad. El término color aparente, incluye el color
debido a las sustancias en solución y el debido al material en suspensión. Este
color aparente se determina a partir de la muestra original que no ha sido
filtrada ni centrifugada.
El color de un agua puede determinarse por comparación de la muestra con
soluciones coloreadas de concentración conocida o por comparación con
discos de vidrio coloreados calibrados apropiadamente. También por método
espectrofotométrico y por el método del filtro triestímulos.
Recolección de la muestra: Tome muestras que sean representativas en un
recipiente de vidrio limpio. Realice la determinación lo más pronto posible
porque los cambios físicos o biológicos que ocurren mientras se almacena
pueden afectar el color.
Recursos (equipos y reactivos):
Espectrofotómetro DR/ 2010
Equipo de filtración.
Procedimiento o metodología:
1. Arme el equipo de filtración y proceda a filtrar 50 mL de agua destilada.
Laboratorio No. 1 Parámetros Físicos Pág. 38
2. Coloque el agua destilada filtrada en uno de los recipientes de 25 mL
(blanco).
3. Seleccione el programa de color introduciendo el número clave (120) y
oprima ENTER.
4. Coloque el dial en 455 nm.
5. Proceda a filtrar 50 mL del agua de muestra y colóquela en el otro
recipiente de 25 mL.
6. Limpie el recipiente que tiene agua destilada con un papel absorbente e
introdúzcalo dentro del aparato, oprima seguidamente ZERO.
7. Tome el recipiente con la muestra límpielo e introdúzcalo dentro del
aparato, luego oprima READ y anote el resultado.
Laboratorio No. 1 Parámetros Físicos Pág. 39
NOTA: Este método es útil para medir el color del agua potable y de aguas
cuyo color es debido a materiales que se encuentran en la naturaleza. No se
aplica para desechos industriales altamente coloreados.
Cálculos:
El resultado se obtiene directamente el aparato al hacer la comparación
de colores entre el patrón y la muestra.
Muestras que tengan color mayor de 500 unidades, deben ser
analizadas diluyendo la muestra con el agua que tenga cero colores y
multiplicar el resultado por el factor de dilución. Ejemplo, si 10 ml de la muestra
se diluyen a 50 ml el resultado debe multiplicarse por 5.
Dilución realizada: 10 ml de muestra
------------------------------------------------------
50 ml (total agua de muestra + agua dilución)
Factor de dilución: 50 ml /10 ml = 5.0
COLOR VERDADERO
12
COLOR
10 VERDADERO
COLOR VERDADERO
0
0.5 1 1.5 2 2.5 3 3.5 4 4.5
MUESTRAS
Resultados: Grafique
Color
Verdadero
(PtCo)
M-1:
4
M-2:
3
M-3:
10 Preguntas:
M-4: 1. ¿A qué se debe la presencia de color en el agua?
6
Laboratorio No. 1 Parámetros Físicos Pág. 40
La presencia de color en el agua se debe a sustancias que se encuentran
disueltas y a partículas suspendidas en el agua, como iones metálicos
presentes en la naturaleza, también plantón, algas y demás
2. ¿Qué importancia tiene el color en el agua desde el punto de vista de la
salud humana?
El agua es el líquido esencial para nuestra vida y la importancia del color en
ella desde el punto de vista de la salud humana tiene mucha relevancia,
puesto que, una persona no se tomaría un agua que tuviese color oscuro, es
decir que, como su color depende de las partículas que en ella se
encuentren, dichas partículas son importantes porque pueden contaminar el
agua y al consumirla puede provocar enfermedades.
3. ¿Cuál es el valor aceptable para el color, según normas panameñas y de la
OMS y por qué razón fue establecido?
El valor máximo permisible para el color según la OMS es de 15 en unidades
de color en la escala Platino-Cobalto. Y al igual que la turbidez, estos valores
fueron tomados como base debido a la estética, puesto que, nadie consume
un agua oscura, usando de referencia Platino-Cobalto.
Conclusión.
Todos los resultados obtenidos de las 4 muestras cumplen con lo requerido en
la norma COPANIT 395 la cual nos indica que el valor aceptado de color para
el agua potable de consumo debe ser menor a 15 Pt-Co. La muestra que más
se acerca al valor máximo permitido por la norma es la muestra 3, con un
resultado de 10 Pt-Co, pero aun así no excede el rango máximo permitido por
esta norma para el color del agua y así tener una estética agradable para el
usuario.
Tabla #1. resultados: color verdadero, turbiedad y solidos suspendidos
TABLA #1
COLOR SÓLIDOS
TURBIEDAD
MUESTRAS VERDADERO SUSPENDIDOS
(FAN=UNT)
(PtCo) (mg/L)
1 4 5 1
2 3 20 16
3 10 13 22
4 6 7 15
Laboratorio No. 1 Parámetros Físicos Pág. 41
Graficas.
COLOR VERDADERO, SOLIDOS SUSPENDIDOS, TURBIEDAD
25
COLOR VERDADERO, TURBIEDAD Y SOLIDOS SUSPENDIDOS
COLOR VERDADERO (PtCo)
20 SOLIDOS SUSPENDIDOS
(mg/L)
TURBIEDAD (FAN=UNT)
15
10
0
0.5 1 1.5 2 2.5 3 3.5 4 4.5
MUESTRAS
Gráfica. Resultados obtenidos para Turbidez, Sólidos Suspendidos y Color
Verdadero para las 4 muestras. En la gráfica podemos observar el
comportamiento que tiene las muestras con respecto a solidos suspendidos y
turbiedad donde ambas en la muestra 1 y 2 tienen un comportamiento similar
en forma creciente donde ambas se están comportando directamente
proporcional hasta ese punto, pero en la muestra 3 para lo contrario con
respecto a los sólidos, pero si con el color donde la turbiedad sigue aumentan y
el color también aumenta donde el color del agua así mismo aumenta por la
cantidad de partículas en suspensión que impiden el paso de la luz y dando un
color más oscuro a dichas agua.
Laboratorio No. 1 Parámetros Físicos Pág. 42
BIBLIOGRAFÍA
Composición de aguas residuales en:
https://cidta.usal.es/cursos/edar/modulos/edar/unidades/LIBROS/logo/pdf/Aguas_Resi
duales_composicion.pdf
Folleto informativo de turbidez en.
https://www.waterboards.ca.gov/water_issues/programs/swamp/docs/cwt/guidance/31
50sp.pdf
Standard Methods for the Examination of Water and Wastewater. 21'h Edition, 2005.
APHA, AWWA, WPCF.
Química para Ingeniería Ambiental. Cuarta Edición, 2001. Clair N. Sawyer; Perry L
McCarty; Gene F. Parkin. McGraw-Hill Book Company.
PROCEDIMIENTOS Simplificados para el Examen de Aguas, 1978, OMS.
Dirección general de normas y tecnología industrial. (1999, noviembre 12). Resolución
N° 597. Reglamento técnico DGNTI-COPANIT 23-395-99. Agua Potable. Panamá,
Panamá, Panamá: Ministerio de comercio e industrias.
Manual de Procedimientos del Espectrofotómetro DREL/2010-HACH. (2002).
OMS. (1978). PROCEDIMIENTOS Simplificados para el Examen de Aguas.
OMS. (2006). Guías para la calidad del agua potable. Primer apéndice a la tercera
edición. Volumen 1.
Guía de laboratorio., parámetros físicos.
Laboratorio No. 1 Parámetros Físicos Pág. 43
También podría gustarte
- Guias de Laboratorio de Mediciones Hidrológicas Y AmbientalesDocumento73 páginasGuias de Laboratorio de Mediciones Hidrológicas Y AmbientalesLisseth UrriolaAún no hay calificaciones
- Laboratorio 1. Parámetros-FísicosDocumento36 páginasLaboratorio 1. Parámetros-FísicosFrancisco FilosAún no hay calificaciones
- Practica 1 QuimicaDocumento12 páginasPractica 1 QuimicaKarla Marcela Tang VelaAún no hay calificaciones
- Informe Supervivencia en El Laboratorio - Grupo 4Documento13 páginasInforme Supervivencia en El Laboratorio - Grupo 4Raul GasparAún no hay calificaciones
- PRACTICA1 Reporte de Laboratorio PDFDocumento15 páginasPRACTICA1 Reporte de Laboratorio PDFNAHOMY GARDEAAún no hay calificaciones
- Lab FQ Unidad 1Documento20 páginasLab FQ Unidad 1emygutAún no hay calificaciones
- Normas de Seguridad para El Trabajo en El Laboratorio de Quimica Grupo5Documento17 páginasNormas de Seguridad para El Trabajo en El Laboratorio de Quimica Grupo5David Esteban GalvisAún no hay calificaciones
- PRÁCTICA 1 - Normas y Materiales de LaboratorioDocumento15 páginasPRÁCTICA 1 - Normas y Materiales de LaboratorioMiguel PomaAún no hay calificaciones
- Laboratorio 01Documento8 páginasLaboratorio 01EMANUEL YERCKOF SOTOMAYOR CHIREAún no hay calificaciones
- 03 Manual de Contingencia en LaboratorioDocumento8 páginas03 Manual de Contingencia en LaboratorioMarco RequenaAún no hay calificaciones
- Hipoclorito de CalcioDocumento8 páginasHipoclorito de CalciopablostAún no hay calificaciones
- Normas de Seguridad e Higiene en El Laboratorio de QuímicaDocumento7 páginasNormas de Seguridad e Higiene en El Laboratorio de QuímicaMonse T. MuñozAún no hay calificaciones
- Guia de Laboratorio de MicrobiologíaDocumento97 páginasGuia de Laboratorio de MicrobiologíafranmarcleAún no hay calificaciones
- Seguridad en El LaboratorioDocumento15 páginasSeguridad en El LaboratorioAndrés RieraAún no hay calificaciones
- Informe Organica 1Documento14 páginasInforme Organica 1jhon dareAún no hay calificaciones
- Práctica 1, Seguridad Equipo 3Documento7 páginasPráctica 1, Seguridad Equipo 3Paloma NizarindaniAún no hay calificaciones
- Ficha TecnicaDocumento11 páginasFicha TecnicaSandy Vanessa ARIAS JULIOAún no hay calificaciones
- Reglas de Seguridad e Higiene en El LaboratorioDocumento8 páginasReglas de Seguridad e Higiene en El LaboratorioJhonny IbañezAún no hay calificaciones
- Laboratorio 1 Seguridad en El LaboratorioDocumento8 páginasLaboratorio 1 Seguridad en El LaboratorioFABIANA ALEXANDRA ESCUDERO QUISPEAún no hay calificaciones
- Normas de BioseguridadDocumento4 páginasNormas de BioseguridadCinthya CoralAún no hay calificaciones
- Bioseguridad InformacionDocumento25 páginasBioseguridad InformacionjeffrefmAún no hay calificaciones
- p1 Gisi Acido - BaseDocumento18 páginasp1 Gisi Acido - BaseCésar AguirreAún no hay calificaciones
- Grupo1 Medidas de Seguridad Lab 91gDocumento25 páginasGrupo1 Medidas de Seguridad Lab 91gAdxell Carhuapoma QuispeAún no hay calificaciones
- Normas de Bioseguridad Laboratorio de Biociencias I VeterinariaDocumento4 páginasNormas de Bioseguridad Laboratorio de Biociencias I VeterinariaLourdesAún no hay calificaciones
- Informe Sobre Las Normas de Bioseguridad y Materiales Del LaboratorioDocumento16 páginasInforme Sobre Las Normas de Bioseguridad y Materiales Del LaboratorioMiguel PomaAún no hay calificaciones
- HistologiaDocumento11 páginasHistologiaMiguel SalcedoAún no hay calificaciones
- Guia Practica Bioquimica 2016-II - LaboratorioDocumento55 páginasGuia Practica Bioquimica 2016-II - LaboratorioAnonymous TgYJlA4uRRAún no hay calificaciones
- G3-Informe - Medidas de Seguridad en El LaboratorioDocumento12 páginasG3-Informe - Medidas de Seguridad en El LaboratorioRommy RuizAún no hay calificaciones
- Informe 01 - Grupo 09Documento11 páginasInforme 01 - Grupo 09EMANUEL YERCKOF SOTOMAYOR CHIREAún no hay calificaciones
- Guía de Práctica Presencial Escuela Profesional de EnfermeríaDocumento19 páginasGuía de Práctica Presencial Escuela Profesional de EnfermeríaDenzel RMAún no hay calificaciones
- Simbolo SDocumento13 páginasSimbolo SBryan Isnado ArceAún no hay calificaciones
- Seguridad en El LaboratorioDocumento19 páginasSeguridad en El LaboratorioAngel MartinezAún no hay calificaciones
- Equipo D Laboratorio-Práctica 1Documento20 páginasEquipo D Laboratorio-Práctica 1GIOVANI MAICOL BAQUERIZO REVOLLARAún no hay calificaciones
- Manual Laboratorio Quimica General-Enfermeria 2023 20Documento67 páginasManual Laboratorio Quimica General-Enfermeria 2023 20MariaAún no hay calificaciones
- Practica 1 - Introduccion A La QuimicaDocumento16 páginasPractica 1 - Introduccion A La QuimicaErnesto Andre Lobo HdzAún no hay calificaciones
- Informe de Laboratorio Introducción, Materiales y NormasDocumento19 páginasInforme de Laboratorio Introducción, Materiales y NormasEMELY ARAGON SILVAAún no hay calificaciones
- GUIA # 1 y 2 IRENE GIRALDODocumento58 páginasGUIA # 1 y 2 IRENE GIRALDOKimberly Juliana Castillo CastilloAún no hay calificaciones
- Práctica #1 Seguridad en El Laboratorio de QuimicaDocumento4 páginasPráctica #1 Seguridad en El Laboratorio de QuimicaJavier ZarateAún no hay calificaciones
- Topax 66 HDS Dic 2021Documento5 páginasTopax 66 HDS Dic 2021jrv.csalinas83Aún no hay calificaciones
- Manual Farmacognosia.Documento123 páginasManual Farmacognosia.Anonymous jfH5W1jAún no hay calificaciones
- Equilibrio Completa PDFDocumento20 páginasEquilibrio Completa PDFJuanesVascoAún no hay calificaciones
- Protocolo LaboratorioDocumento14 páginasProtocolo LaboratorioJennifer GonzálezAún no hay calificaciones
- Guia de PracticaDocumento39 páginasGuia de PracticaJhuvaly Laura LlamocuriAún no hay calificaciones
- HDS CP40 Lubricante - EcolabDocumento5 páginasHDS CP40 Lubricante - EcolabCandace ChaseAún no hay calificaciones
- Medidas de Seguridad, Primeros Auxilios y Materiales en El LaboratorioDocumento11 páginasMedidas de Seguridad, Primeros Auxilios y Materiales en El LaboratorioanchiO07Aún no hay calificaciones
- Quik Fill 540 HDS Enero 2019Documento5 páginasQuik Fill 540 HDS Enero 2019Glady0% (1)
- NORMAS DE SEGURIDAD EN EL LABORATORIO 2,,editDocumento9 páginasNORMAS DE SEGURIDAD EN EL LABORATORIO 2,,editLina KelseyAún no hay calificaciones
- Informe Laboratorio 2Documento21 páginasInforme Laboratorio 2EDIVER LealAún no hay calificaciones
- Practica N 1 BioseguridadDocumento12 páginasPractica N 1 BioseguridadireneAún no hay calificaciones
- T.P Normas de SeguridadDocumento6 páginasT.P Normas de SeguridadMiriam Graciela MaidanaAún no hay calificaciones
- BC Fist HDS 2018Documento5 páginasBC Fist HDS 2018Soporte InfraestructuraAún no hay calificaciones
- Práctica NDocumento6 páginasPráctica NJEAN PIERRE ROJAS BAEZAún no hay calificaciones
- Actividad Quimica Fisica Semana 7Documento5 páginasActividad Quimica Fisica Semana 7Raul ZuletaAún no hay calificaciones
- Nitro Plus HDS 2016Documento5 páginasNitro Plus HDS 2016Ignacio OneilAún no hay calificaciones
- GUION IEQI v3Documento74 páginasGUION IEQI v3Dionisio MayorgaAún no hay calificaciones
- CFQ Sanitizer HDS 2019Documento5 páginasCFQ Sanitizer HDS 2019Katherine Constanza Huerta CarrascoAún no hay calificaciones
- Manual Laboratorio de Analisis InstrumentalDocumento63 páginasManual Laboratorio de Analisis InstrumentalErick El Pinche ZurdoAún no hay calificaciones
- Limpieza y desinfección en laboratorios e industrias químicas. QUIE0308De EverandLimpieza y desinfección en laboratorios e industrias químicas. QUIE0308Calificación: 4 de 5 estrellas4/5 (4)
- Asignacion 7Documento30 páginasAsignacion 7Karla MagallonAún no hay calificaciones
- Clase No 1suministroDocumento22 páginasClase No 1suministroKarla MagallonAún no hay calificaciones
- Cálculo de Estructuras - Ramón Arguelles Álvarez (1ra Edición - Tomo I)Documento650 páginasCálculo de Estructuras - Ramón Arguelles Álvarez (1ra Edición - Tomo I)Karla MagallonAún no hay calificaciones
- Clase Redes SuministroDocumento68 páginasClase Redes SuministroKarla MagallonAún no hay calificaciones
- Clase Tanquede ReservaDocumento10 páginasClase Tanquede ReservaKarla MagallonAún no hay calificaciones
- T2 - Modulo 8 - JUNTAS EN PAVIMENTOS RIGIDOS-2020-8 PDFDocumento41 páginasT2 - Modulo 8 - JUNTAS EN PAVIMENTOS RIGIDOS-2020-8 PDFBerning GonzalezAún no hay calificaciones
- APUNTES Del Curso ING. TRANSPORTE II 2015 PDFDocumento195 páginasAPUNTES Del Curso ING. TRANSPORTE II 2015 PDFEdgarCoronadoAún no hay calificaciones
- Talud Con BanquetaDocumento103 páginasTalud Con BanquetaAnthony Michel Nunez100% (1)
- 12 - Modulo 1 Respuesta Acta de ConstitucionDocumento2 páginas12 - Modulo 1 Respuesta Acta de ConstitucionEvelin Hernandez Gonzalez100% (4)
- 12 - Modulo 1 Respuesta Acta de ConstitucionDocumento2 páginas12 - Modulo 1 Respuesta Acta de ConstitucionEvelin Hernandez Gonzalez100% (4)
- Librodeslizamientost2 Cap8Documento22 páginasLibrodeslizamientost2 Cap8Jerson Tonino Mundaca SosaAún no hay calificaciones
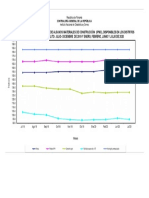
- Grafica Julio 2020 InecDocumento1 páginaGrafica Julio 2020 InecKarla MagallonAún no hay calificaciones
- Capítulos 9 y 10 PE Bravo - Modulo 1 - Movimiento de TierraDocumento37 páginasCapítulos 9 y 10 PE Bravo - Modulo 1 - Movimiento de TierraAstrid Carolina Urriola PradoAún no hay calificaciones
- Lab No.5 FISICADocumento13 páginasLab No.5 FISICAKarla MagallonAún no hay calificaciones
- Lab No.4 FISICADocumento9 páginasLab No.4 FISICAKarla MagallonAún no hay calificaciones
- Consumo de Energia Electrica en El HogarDocumento7 páginasConsumo de Energia Electrica en El HogarKarla MagallonAún no hay calificaciones
- Lab No.2 FISICADocumento12 páginasLab No.2 FISICAKarla MagallonAún no hay calificaciones
- Hidrologia - David CedeñoDocumento254 páginasHidrologia - David CedeñoKirara Nagakane100% (2)
- Lab No.3 FISICADocumento9 páginasLab No.3 FISICAKarla MagallonAún no hay calificaciones
- Lab No.1 FISICADocumento16 páginasLab No.1 FISICAKarla MagallonAún no hay calificaciones
- Consumo de Energia Electrica en El HogarDocumento7 páginasConsumo de Energia Electrica en El HogarKarla MagallonAún no hay calificaciones
- Lab. No. 2 FluidosDocumento14 páginasLab. No. 2 FluidosKarla MagallonAún no hay calificaciones
- Lab. No. 1 de Física.Documento10 páginasLab. No. 1 de Física.Karla MagallonAún no hay calificaciones
- Guías Envía Transportadora Colombia LogísticaDocumento5 páginasGuías Envía Transportadora Colombia LogísticaStevenson Rivera50% (2)
- Ficha Semana 11 BiologiaDocumento7 páginasFicha Semana 11 BiologiaElkin TumbacoAún no hay calificaciones
- Etica y DeontologiaDocumento10 páginasEtica y DeontologiaBeyker PrincipeAún no hay calificaciones
- Semana 14Documento14 páginasSemana 14Maria Elena Diaz GarayAún no hay calificaciones
- Guía para El Uso de Recursos Educativos - Pagina WixDocumento2 páginasGuía para El Uso de Recursos Educativos - Pagina Wixjavier cuadroAún no hay calificaciones
- Lectura GAO y GAFDocumento13 páginasLectura GAO y GAFARIANA SOFIAAún no hay calificaciones
- Presentacion FinalDocumento42 páginasPresentacion FinalLucas Palacios PedescollAún no hay calificaciones
- Introduccion A La BibliaDocumento25 páginasIntroduccion A La BibliaVictor Tirado100% (1)
- Misterio en Las Cuevas - Gregg DunnettDocumento295 páginasMisterio en Las Cuevas - Gregg DunnettMaxi RuizAún no hay calificaciones
- Limache WikipediaDocumento12 páginasLimache WikipediaDavid Patricio Fernandezz Navarrete100% (1)
- 1.3 y 1.4 Economia Internacional - Quezada Villanueva Marco AntonioDocumento5 páginas1.3 y 1.4 Economia Internacional - Quezada Villanueva Marco AntonioMARCO ANTONIO QUEZADA VILLANUEVAAún no hay calificaciones
- Informe #6 Estructura PoblacionalDocumento6 páginasInforme #6 Estructura PoblacionalAlejandra VallejoAún no hay calificaciones
- La Oracion de DavidDocumento11 páginasLa Oracion de DavidTimur Romero CherkezovaAún no hay calificaciones
- Tarea Practica 1Documento6 páginasTarea Practica 1Terry Bryan Jaime GranjaAún no hay calificaciones
- Tesis en Ing Industrial BY Castro - VCDocumento272 páginasTesis en Ing Industrial BY Castro - VCJohannes Aucaylle NietoAún no hay calificaciones
- EcologíaDocumento3 páginasEcologíaRafael VidesAún no hay calificaciones
- A. Varios Autores - Revista de Interpretación Latinoamericana Salmos PDFDocumento180 páginasA. Varios Autores - Revista de Interpretación Latinoamericana Salmos PDFJairo Andres Rodriguez Londoño100% (1)
- Pedido 212207 26062023Documento9 páginasPedido 212207 26062023Andrés FigueroaAún no hay calificaciones
- Examen Bimestral de Raz. Verbal Iii BimestreDocumento2 páginasExamen Bimestral de Raz. Verbal Iii BimestreDiana PereiraAún no hay calificaciones
- Contra La Democracia y La Igualdad - Tomislav Sunic PDFDocumento222 páginasContra La Democracia y La Igualdad - Tomislav Sunic PDFgonzalo1954Aún no hay calificaciones
- Modelo Informe Neuropsicologico - Adultos - Caso CompletoDocumento5 páginasModelo Informe Neuropsicologico - Adultos - Caso CompletoalavergaaaaAún no hay calificaciones
- Reglas de La Composición GraficaDocumento3 páginasReglas de La Composición GraficaGerald UlateAún no hay calificaciones
- Proceso de Selección Transferencia Transformación Digital para ExtensionistasDocumento23 páginasProceso de Selección Transferencia Transformación Digital para ExtensionistasLucy Angélica VásquezAún no hay calificaciones
- ComunicadoDocumento2 páginasComunicadoEdwin Ivan Cubas DiazAún no hay calificaciones
- Formulario SurDocumento2 páginasFormulario SurJaviera EastmanAún no hay calificaciones
- Reina Del Sur - Buscar Con GoogleDocumento2 páginasReina Del Sur - Buscar Con GoogleLenUshioAún no hay calificaciones
- Violeta Martínez - Trabajo Final Clase de Historia de Colombia IIDocumento7 páginasVioleta Martínez - Trabajo Final Clase de Historia de Colombia IIVioleta Martinez CalleAún no hay calificaciones
- María Luisa MendozaDocumento6 páginasMaría Luisa MendozaBryan DerryAún no hay calificaciones
- Sexo en PlantasDocumento10 páginasSexo en PlantasRubenFrancoAún no hay calificaciones
- Manual para Leer Rapida y EficazmenteDocumento34 páginasManual para Leer Rapida y EficazmenteLudin TulAún no hay calificaciones