Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Laboratorio N°7 - Proteínas
Cargado por
eleazarTítulo original
Derechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
Laboratorio N°7 - Proteínas
Cargado por
eleazarCopyright:
Formatos disponibles
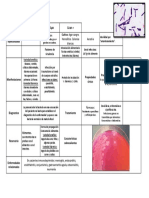
PARTE EXPERIMENTAL
Se separó la clara de
huevo en un vaso y
se enrazó con agua
hasta 75 ml
Se preparó HCl 0.25 M,
amoniaco 0.25M y también
NaOH en agua destialda
1) PRUEBA DE BIURET
Se preparó en un tubo solución de caseína + H20 + 2
gotas de sulfato de Cu y en otro tubo se preparó una
solución de albúmina + H2O + 2 gotas de sulfato de
Cu.
Ambas muestras colorean violeta por tener
mucho enlace peptídico
2) DESNATURALIZACIÓN
Se colocó albúmina en 4 tubos, al primer tubo se lo envió a baño de agua por 3 min, en
el segundo tubo se agregó alcohol etílico, en el tercer tubo se agregó 2 gotas de NaOH
al 20% y 2 gotas de acetato de plomo y al cuarto tubo con albúmina se le agregó 2 gotas
de acetato de plomo.
En el caso del primer tubo, la albúmina coaguló.
En el caso del segundo también coaguló.
En el tercer tubo, presentó turbidez y precipitación, más que en el cuarto tubo.
En el cuarto tubo se observó poco precipitado.
En el caso del tercer y caurto tubo se formó el PROTEINATO.
3) PUNTO ISOELÉCTRICO
Se preparó 17 ml de
amoniaco y se agregó a un
matraz con caseína hasta
disolver, luego se agregó 18
ml de HCl desde una bureta
Bajó el pH de la
solución de
amoniaco hasta
5 y precipitó
4)
Se agregó 1 gota de NaOH
3 4
1 2 0.1 M a los tubos 1 y 2, a los
tubos 3 y 4 se les agregó 1
gota de HCl 0.1 M
Bajó el pH de la
solución de
amoniaco hasta
5 y precipitó
+ 1gota de fenolftaleína + 1gota de anaranjado de metilo
A los tubos 2 y 3 se les agregó
unas gotas de albúmina, se 1 2 3 4
observó que el tubo tres actúó
como una base y colorea
naranja
En el caso del tubo 2 al agregar
unas gotas de albúmina se
observó una coloración violeta
leve, actúó como ácido.
DISCUSIONES Y CONCLUSIONES
Para el método del Biuret, en solución alcalina el Cu+2 reacciona con el enlace
peptídico de las proteínas dando un color purpúreo que se cuantifica
espectrofotométricamente (540nm). Como estándar se utiliza una solución de
albúmina. Las cadenas de proteínas presentes en la clara de huevo cuando fueron
sometidas al reactivo de Biuret, que en su composición tiene NaOH (el cual no participa
de la reacción pero es de fundamental importancia su presencia ya que proporciona el
medio básico necesario) junto con el CuSO4, se pudo apreciar que el sulfato cúprico
reaccionó con la proteína presente en la solución de albúmina de huevo, y esta se torna
de color violeta lo que nos indica que la reacción fue positiva.
Proteína + Cu+2 Complejo Cu-Proteína (púrpura)
La desnaturalización de proteínas, en la clara de huevo, se evidencia por acción del calor
formando una masa sólida intercomunicada. Esta misma desnaturalización puede
producirse a través de solventes orgánicos, por ejemplo por acción de alcohol etílico en
ambos casos, ocurre una desnaturalización irreversible, con formación de coágulos.
Las proteínas se mantienen en una forma natural debido a las interacciones de grupos
laterales en los aminoácidos de una región a otra de la molécula. Se conoce como
desnaturalización a la pérdida de las estructuras de orden superior de la proteína y por
tanto de su función. Estas interacciones pueden ser puentes de hidrógeno o puentes de
disulfuro. Se puede desnaturalizar una proteína alterando los enlaces por puentes de
hidrógeno que están en la estructura. La mayor parte de las proteinas experimentan
desnaturalizaciones cuando se calientan entre 50 y 60 ºC; otras se desnaturalizan
también cuando se enfrian por debajo de los 10 a 15 ºC.
El punto isoeléctrico se define como el pH en el cual el número de cargas
positivas se iguala al número de cargas negativas que aportan los grupos ionizables de
una molécula. En el punto isoeléctrico la carga neta de la molécula es cero (0). En el
experimento se observó que el punto isoeléctrico depende de cada proteína ya que
también se relaciona con el pH.
En la última prueba se observó que las proteinas tienen un comportamiento anfótero y
ésto las hace capaces de neutralizar las variaciones de pH del medio, ya que pueden
comportarse como un ácido o una base y por tanto liberar o retirar protones (H+) del
medio donde se encuentran.
También podría gustarte
- Metabolismo de Acido UricoDocumento2 páginasMetabolismo de Acido UricoAntonio PiñaAún no hay calificaciones
- EgoDocumento17 páginasEgoCynthiaAún no hay calificaciones
- Práctica 13Documento4 páginasPráctica 13Alondra FortunatAún no hay calificaciones
- PREGUNTASDocumento5 páginasPREGUNTASyeniAún no hay calificaciones
- VTK Urea SalicilatoDocumento2 páginasVTK Urea SalicilatoJuanCarlosHernándezAún no hay calificaciones
- Clase 4 Funcion RenalDocumento49 páginasClase 4 Funcion RenalJaz Ntvg100% (1)
- Aseguramineto de La Calidad en Hematologia y HemostasiaDocumento27 páginasAseguramineto de La Calidad en Hematologia y HemostasiaBernabéMaqueraQuispe0% (1)
- Informe CKDocumento4 páginasInforme CKKarla Orozco0% (1)
- Trabajo de FarmacoDocumento14 páginasTrabajo de FarmacoJonathan MurgaAún no hay calificaciones
- Anemia Por AlcoholDocumento11 páginasAnemia Por AlcoholJazitaRomero100% (1)
- Cuadro Características EnterobacteriasDocumento3 páginasCuadro Características EnterobacteriasCesar Nicolas SosaAún no hay calificaciones
- PlaquetasDocumento14 páginasPlaquetasJose AvilaAún no hay calificaciones
- Analisis Instrumental ZDocumento109 páginasAnalisis Instrumental ZOrlando MandujanoAún no hay calificaciones
- Caso Clinico Leucemia Linfocitica AgudaDocumento22 páginasCaso Clinico Leucemia Linfocitica AgudaLesly Del CarpioAún no hay calificaciones
- Antibiograma 2022Documento54 páginasAntibiograma 2022Ricardo DoroteoAún no hay calificaciones
- Aspirin ADocumento9 páginasAspirin ADiego VelásquezAún no hay calificaciones
- Bacterias de Importancia Medica PDFDocumento62 páginasBacterias de Importancia Medica PDFEmiliano MasseroniAún no hay calificaciones
- Hemoclasificación NCDocumento8 páginasHemoclasificación NCsergio quinteroAún no hay calificaciones
- 1 WidalDocumento2 páginas1 WidalHans YoveraAún no hay calificaciones
- Uremia ProspectoDocumento3 páginasUremia ProspectoYuMi BautistaAún no hay calificaciones
- Reporte # 5 - Determinación de Ácido ÚricoDocumento4 páginasReporte # 5 - Determinación de Ácido ÚricoKenlly TerranovaAún no hay calificaciones
- Caseina PaperDocumento6 páginasCaseina PaperRobin Guevara100% (1)
- Prueba de LowryDocumento4 páginasPrueba de LowryErick Amador GaytánAún no hay calificaciones
- Head SpaceDocumento52 páginasHead Spaceyesicaberth100% (1)
- Laboratorio OrinaDocumento27 páginasLaboratorio OrinaAngie Villar RuizAún no hay calificaciones
- Pract UreaDocumento2 páginasPract UreaLesli Lisbeth Molina SotoAún no hay calificaciones
- VDRL en Suero Serologia ABCDocumento6 páginasVDRL en Suero Serologia ABCgamalielAún no hay calificaciones
- Química Del Proceso de FijaciónDocumento52 páginasQuímica Del Proceso de FijaciónAdolfo Antonio Ríos AlcortaAún no hay calificaciones
- Amilasa CNPG Liquiform 142 EspDocumento6 páginasAmilasa CNPG Liquiform 142 Espelsa ramirezAún no hay calificaciones
- Mac Conkey AgarDocumento6 páginasMac Conkey Agareliz1415Aún no hay calificaciones
- Guia Paso Químico de OrinaDocumento6 páginasGuia Paso Químico de OrinaElizabeth100% (1)
- Quimica Clinica "Determinación de Pruebas de Funcionamiento Hepático: Proteínas Totales, Albumina, (Método de Verde Bromocresol), Bilirrubina Total, Directa e Indirecta"Documento12 páginasQuimica Clinica "Determinación de Pruebas de Funcionamiento Hepático: Proteínas Totales, Albumina, (Método de Verde Bromocresol), Bilirrubina Total, Directa e Indirecta"Jair Emmanuel Rendon RendonAún no hay calificaciones
- Informe de Hemato Serie RojaDocumento6 páginasInforme de Hemato Serie RojaAnonymous BvzMO9Aún no hay calificaciones
- Práctica #3 - Analisis Clinico IDocumento5 páginasPráctica #3 - Analisis Clinico IKety León MoyaAún no hay calificaciones
- Amilasa 15Documento3 páginasAmilasa 15Samiri SamiriAún no hay calificaciones
- Informe de Acidez BromatologiaDocumento9 páginasInforme de Acidez BromatologiaJohnAndresPinargoteAún no hay calificaciones
- Poe-4 Hemoglobina ClorimetricaDocumento8 páginasPoe-4 Hemoglobina ClorimetricaBrido ClarosAún no hay calificaciones
- Practica # 6 - Fosfatasa AlcalinaDocumento7 páginasPractica # 6 - Fosfatasa Alcalinarockakicha100% (1)
- Valoración Química de Drogas VegetalesDocumento6 páginasValoración Química de Drogas VegetalesSIRCARLOS MOLINA RETAMOZOAún no hay calificaciones
- Tarea Individual Resolucion de Casos ClinicosDocumento6 páginasTarea Individual Resolucion de Casos ClinicosDANIELA BEATRIZ JUMBO MAZAAún no hay calificaciones
- Practica EnterobacteriasDocumento7 páginasPractica EnterobacteriasSelene Ruiz MoriAún no hay calificaciones
- Pracctica # 5 Determinación Cuantitativa de Urea en SueroDocumento9 páginasPracctica # 5 Determinación Cuantitativa de Urea en SueroPaula Chavez ArellanoAún no hay calificaciones
- Reporte de Laboratorio, Práctica 1 PDFDocumento9 páginasReporte de Laboratorio, Práctica 1 PDFCésar CidAún no hay calificaciones
- Guía Práctica para Determinación de Calcio, Fósforo, Magnesio y Hierro 2023-IiDocumento18 páginasGuía Práctica para Determinación de Calcio, Fósforo, Magnesio y Hierro 2023-IiMARIA DEL PILAR SANCHEZ VALDEZAún no hay calificaciones
- PRACTICA #7 Acido UricoDocumento3 páginasPRACTICA #7 Acido UricoYasne Ospino100% (1)
- Proteinuria Rojo de PirogalolDocumento3 páginasProteinuria Rojo de PirogalolJuly QBAún no hay calificaciones
- Informe Práctica 9 Cinética EnzimáticaDocumento13 páginasInforme Práctica 9 Cinética EnzimáticaNomo lestarAún no hay calificaciones
- Estreptolisina Liofilizada SPDocumento3 páginasEstreptolisina Liofilizada SPJesus MartAún no hay calificaciones
- Caso Clinico VIHDocumento5 páginasCaso Clinico VIHmary2609Aún no hay calificaciones
- Bacillus CereusDocumento1 páginaBacillus CereusHector Adrian SalasAún no hay calificaciones
- Alfa Oxidacion y CetogeneDocumento19 páginasAlfa Oxidacion y Cetogenenico0% (1)
- MacrodantinaDocumento8 páginasMacrodantinaangelicaAún no hay calificaciones
- Prueba de La UreasaDocumento5 páginasPrueba de La UreasaJOSE ANTONIO PINTORAún no hay calificaciones
- Marco TeoricoDocumento7 páginasMarco TeoricoAmbar Peña MejiaAún no hay calificaciones
- Practica Fosfatasa y ProteinaDocumento11 páginasPractica Fosfatasa y ProteinaFernanda YañezAún no hay calificaciones
- Farmacologia RenalDocumento143 páginasFarmacologia RenalRosalía LozanoAún no hay calificaciones
- Informe No 7 - Identificacion de Los LipidosDocumento9 páginasInforme No 7 - Identificacion de Los LipidosJose Daniel LopezAún no hay calificaciones
- Salmonella y Shigella AgarDocumento24 páginasSalmonella y Shigella AgarAngie NumpaqueAún no hay calificaciones
- Informe #3 - GGT y ALPDocumento8 páginasInforme #3 - GGT y ALPKar BejaranoAún no hay calificaciones
- Marcha Analitica de Grupos OrganicosDocumento2 páginasMarcha Analitica de Grupos OrganicosedisonAún no hay calificaciones
- 5991-6593 Agilent Atomic Spectroscopy Hardware ESDocumento46 páginas5991-6593 Agilent Atomic Spectroscopy Hardware ESeleazarAún no hay calificaciones
- Quimica Del Estado Solido 22 C3 Enlace QuimicoDocumento19 páginasQuimica Del Estado Solido 22 C3 Enlace QuimicoeleazarAún no hay calificaciones
- Quimica Del Estado Solido. C4 - 22. Cristalografia 1Documento27 páginasQuimica Del Estado Solido. C4 - 22. Cristalografia 1eleazarAún no hay calificaciones
- Absorción de Agua para El MaízDocumento2 páginasAbsorción de Agua para El MaízeleazarAún no hay calificaciones
- Quimica Del Estado Solido. C5 - 22 Cristalografia 2Documento18 páginasQuimica Del Estado Solido. C5 - 22 Cristalografia 2eleazarAún no hay calificaciones
- Avance - ElectroquímicaDocumento7 páginasAvance - ElectroquímicaeleazarAún no hay calificaciones
- Abraham - Tesis - Borrador V5 FinalDocumento140 páginasAbraham - Tesis - Borrador V5 FinaleleazarAún no hay calificaciones
- Presentación PrecipitometríaDocumento22 páginasPresentación PrecipitometríaeleazarAún no hay calificaciones
- Problemas de PrecipitometriaDocumento1 páginaProblemas de PrecipitometriaeleazarAún no hay calificaciones
- 1 EjerciciosDocumento2 páginas1 EjercicioseleazarAún no hay calificaciones
- IntroducciónDocumento28 páginasIntroduccióneleazarAún no hay calificaciones
- Miscelania de EjerciciosDocumento2 páginasMiscelania de EjercicioseleazarAún no hay calificaciones
- Parte IDocumento28 páginasParte IeleazarAún no hay calificaciones
- ¿Qué Es Una Emulsión?Documento2 páginas¿Qué Es Una Emulsión?eleazarAún no hay calificaciones
- IRIDIODocumento10 páginasIRIDIOeleazarAún no hay calificaciones
- Problemas de PrecipitometriaDocumento1 páginaProblemas de PrecipitometriaeleazarAún no hay calificaciones
- Práctica 07 EmulsionesDocumento3 páginasPráctica 07 EmulsioneseleazarAún no hay calificaciones
- Laboratorio 6 - Coloides Liofílicos y Liofóbicos - ExperimentalDocumento3 páginasLaboratorio 6 - Coloides Liofílicos y Liofóbicos - ExperimentaleleazarAún no hay calificaciones
- Informe Semana 5Documento9 páginasInforme Semana 5eleazarAún no hay calificaciones
- QumioDocumento151 páginasQumioeleazarAún no hay calificaciones
- Laboratorio 5 - Propiedades Eléctricas de Sistemas DispersosDocumento4 páginasLaboratorio 5 - Propiedades Eléctricas de Sistemas DispersoseleazarAún no hay calificaciones
- Silabos Ingles Tecnico 2019 I Epq.Documento11 páginasSilabos Ingles Tecnico 2019 I Epq.eleazarAún no hay calificaciones
- InvestigacionDocumento14 páginasInvestigacionMiller Flores J. FloresAún no hay calificaciones
- Ejercicio - U1 - Calculos Matematicos - 01Documento6 páginasEjercicio - U1 - Calculos Matematicos - 01DARWIN GARAY ASTOCONDORAún no hay calificaciones
- Cultivo Orgánico de CacaoDocumento2 páginasCultivo Orgánico de CacaocpkakopeAún no hay calificaciones
- Aditivos AlimentariosDocumento22 páginasAditivos AlimentariosMarvin R. GómezAún no hay calificaciones
- Proceso AlmendrasDocumento28 páginasProceso AlmendrasFarissa Ch. LázaroAún no hay calificaciones
- TilapiaDocumento11 páginasTilapiaAbel de jesus Diaz MolinaAún no hay calificaciones
- 30 Caracteristicas de GuatemalaDocumento11 páginas30 Caracteristicas de Guatemala123kkAún no hay calificaciones
- 101 Usos Limón Menta Lavanda MÉXICODocumento19 páginas101 Usos Limón Menta Lavanda MÉXICOFernandoEspondaAún no hay calificaciones
- Cuadernillo de Vacaciones de Proyectos PDFDocumento17 páginasCuadernillo de Vacaciones de Proyectos PDFRosyLeyva83% (6)
- Control Usando Hongos EntomopatogenosDocumento14 páginasControl Usando Hongos EntomopatogenosJulio GamarraAún no hay calificaciones
- Determinacion de Los Indices de Madurez en FrutasDocumento16 páginasDeterminacion de Los Indices de Madurez en FrutassamanthaAún no hay calificaciones
- Listado Insumos Junio 2020 Gardenia Naturals Cosmética NaturalDocumento16 páginasListado Insumos Junio 2020 Gardenia Naturals Cosmética NaturalTalento FamsaAún no hay calificaciones
- Moleculas OrganicasDocumento25 páginasMoleculas OrganicasJuan Francisco Suárez SuárezAún no hay calificaciones
- Formato de Inspeccion Sanitaria IVC-InS-FM008Documento10 páginasFormato de Inspeccion Sanitaria IVC-InS-FM008Lorenzo FuentesAún no hay calificaciones
- Expresiones Guías y Scout Aplausos, Canciones y DanzasDocumento18 páginasExpresiones Guías y Scout Aplausos, Canciones y DanzassensanleeAún no hay calificaciones
- FisiologiaDocumento5 páginasFisiologiajhonelAún no hay calificaciones
- Karp - Biologia Celular y Molecular-277-306Documento30 páginasKarp - Biologia Celular y Molecular-277-306Marielt sunshineAún no hay calificaciones
- Danielle Joseph - Shrinking Violet PDFDocumento0 páginasDanielle Joseph - Shrinking Violet PDFmanalimandalde100% (1)
- Planta de AlimentoDocumento17 páginasPlanta de AlimentoLuis Alberto Santillan RuizAún no hay calificaciones
- Informe Mermeladas, Miel y Jarabe PDFDocumento30 páginasInforme Mermeladas, Miel y Jarabe PDFYenny EstradaAún no hay calificaciones
- Los Ojos Del Lobo by Care SantosDocumento117 páginasLos Ojos Del Lobo by Care SantosCarlota SantosAún no hay calificaciones
- Informe Mensual de Actividades MarzoDocumento2 páginasInforme Mensual de Actividades MarzoJulio TorresAún no hay calificaciones
- Presentacion PonenciaDocumento18 páginasPresentacion PonenciaLUIS EDUARDO REY HUERTASAún no hay calificaciones
- Tratado de ObbiDocumento12 páginasTratado de ObbiJohannes Hernandez ChaconAún no hay calificaciones
- Diaposituiva de LiquenesDocumento24 páginasDiaposituiva de LiquenesAdam VasquezAún no hay calificaciones
- Lipoproteínas GuíaDocumento23 páginasLipoproteínas GuíaYarara YararaAún no hay calificaciones
- La Carta de ZaragozaDocumento10 páginasLa Carta de Zaragozajuanchen2910Aún no hay calificaciones
- Gómez - Aplicación de Spirulina en El Desarrollo de Alimentación Humana y AnimalDocumento22 páginasGómez - Aplicación de Spirulina en El Desarrollo de Alimentación Humana y AnimalkellyAún no hay calificaciones
- ACTIVIDAD 22 - 4°-5º (Números Racionales e Irracionales)Documento3 páginasACTIVIDAD 22 - 4°-5º (Números Racionales e Irracionales)MONICA VARGAS NOLAZCOAún no hay calificaciones
- Concreto - EsnaiderDocumento99 páginasConcreto - EsnaiderEsnaider SanchezAún no hay calificaciones