Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Libro Sistema Nervioso
Cargado por
manggita18Título original
Derechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
Libro Sistema Nervioso
Cargado por
manggita18Copyright:
Formatos disponibles
1
________
Estructura y funcin Parte II _____
MIRIAN DIAZ B.
GABRIELA DIAZ S.
2002
______
Las autoras
_______
Profesora Gabriela Daz Silva
Su carrera acadmica se desarroll durante ms de 30 aos en la Facultad de Medicina de la Universidad de Chile, donde alcanz todos los grados de la jerarqua acadmica, hasta llegar a Profesor Titular de Fisiologa de la Universidad de Chile. Su trabajo de investigacin estuvo centrado especialmente en la fisiologa respiratoria, publicando ms de 40 trabajos en revistas nacionales e internacionales. Ha editado 11 textos de estudio tanto de su especialidad como de Drogadiccin y de Etimologa Griega. Actualmente se desempea como acadmico en Facultades de Medicina y Psicologa en Universidades Privadas.
Profesora Mirian Daz Barraza
Licenciada en Ciencias con mencin en Biologa, Master en Ciencias Biolgicas, Universidad de Chile. Se desempea como acadmica desde el ao 1993 a la fecha en diversas Escuelas de Psicologa, a cargo de las ctedras de Bases Biolgicas de la Conducta Humana, Neurobiologa, Fisiologa y Psicofisiologa, especializndose en reas relacionadas con las terapias biopsicolgicas, tales como Neurofeedback y Programacin Neurolingstica (PNL) y Salud.
PROLOGO.
Conocer el Sistema Nervioso humano puede parecer, en primera instancia, una meta a la vez lejana y pretenciosa. No obstante, muchos de los profesionales en cuya formacin colaboramos, necesitan conocer este sistema en mayor o menor grado. Es por ello que hemos confeccionado este texto que contiene los elementos esenciales relacionados con la estructura, la fisiologa y la psicofisiologa, de modo que el estudiante disponga de todos estos aspectos en forma compacta, moderna, estimulante, novedosa; as, el anlisis del Sistema Nervioso se coloca al alcance del estudiante ya desde los comienzos embriolgicos del sistema nervioso. El avance tecnolgico est facilitando enormemente el trabajo de quienes expresamos nuestras experiencias acadmicas tambin en lenguaje escrito. Este es el primer texto que presentamos a nuestros alumnos en disco compacto; esperamos que al estar visual y tecnolgicamente ms cerca de la juventud actual (naci en la era de la computacin), este disco compacto (CD) agregue una motivacin que les facilite el aprendizaje del sistema nervioso. Escribir un texto de estudio es un trabajo enriquecedor, donde el primer y principial beneficiario es el autor. Ordenar las materias implica desarrollar el orden mental, tan necesario para un docente; revisar bibliografa aumenta el bagaje de conocimientos; escribir ayuda a pulir el lenguaje, obligando a que las expresiones sean correctas y exactas, lo que esperamos haber logrado. Este CD va dedicado a nuestros alumnos, ya que a travs de nuestros aos de docencia, es mucho lo que hemos aprendido de ellos; el tratar de facilitarles el estudio del Sistema Nervioso, es una forma de agradecerles cuanto han enriquecido nuestra labor acadmica.
Al mismo tiempo, quisiramos agradecer a Universidades Privadas en que nos desempeamos, por inters constante de superacin, manifestado en este caso la presentacin de material docente acorde con metodologas modernas.
las su en las
Mirian Daz B. Magster en Biologa Fisiologa.
Gabriela Daz S. Profesor Titular de
INDICE.
I.- Embriologa. Neurulacin. Histognesis del sistema nervioso. Formacin de la mdula espinal. II.- Histologa del sistema nervioso. Tejido nervioso Estructura de la neurona. Neuroglia. Fibra nerviosa. III.- Anatoma del sistema nervioso. Planos de simetra. Mdula espinal. Metmera morfo-funcional. Vas medulares. Hemisferios cerebrales. Tronco cerebral Mdula oblongada o bulbo raqudeo. Puente o protuberancia. Mesencfalo. Ventrculos cerebrales, meninges y lquido cfaloraqudeo. Sistema nervioso perifrico. Nervios espinales o raqudeos. Nervios craneanos.
Diencfalo. Tlamo. Hipotlamo. Ncleos basales. Cerebelo. Corteza cerebral Paleocortex. Archicortex. Neopalio o isocortex. Sistema neurovegetativo. Sistema simptico. Sistema parasimptico. Plexos neurovegetativos. IV.- Neurofisiologa. Biopotenciales. Potencial de membrana o de reposo. Potencial de accin. Sinapsis y neurotransmisores. Neurotransmisores. Sensibilidad. Los receptores Sensopercepcin Codificacin sensorial Leyes psicofsicas. Algunas sensaciones en particular. Dolor. Visin. Audicin y funcin vestibular. Audicin. Sistema smatomotor. Estructura de la fibra muscular. Contraccin muscular.
Transmisin neuromuscular Acoplamiento excitacin-contraccin. Algunas caractersticas de la contraccin muscular. Reflejos medulares. Reflejo miottico. Principio de inervacin recproca. Regulacin neuromuscular. Regulacin de las funciones viscerales. V.- Sistemas de integracin global. Sistema reticular. Sueo y vigilia. Actividad cerebral elctrica: EEG. Sistema lmbico. Regulacin de las funciones endocrinas. Conductas instintivas. Conducta sexual. Motivaciones. Hambre y saciedad. Sed. Emociones. Stress. Ritmos biolgicos. Sistema tlamo-neocortical. Aprendizaje y memoria. Plasticidad cerebral. Neurognesis humana. Envejecimiento cerebral. Lenguaje. Dominancia hemisfrica. Elaboracin de pensamiento. Inteligencia. VI.- Bibliografa.
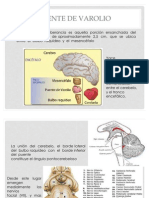
I.- EMBRIOLOGIA. La embriologa estudia el desarrollo de un organismo desde la formacin del huevo hasta el nacimiento. Parece necesario conocer a grandes rasgos sus diferentes etapas para comprender ms cabalmente la formacin del sistema nervioso. Como consecuencia de la fecundacin, por un proceso llamado clivaje o segmentacin, se obtiene el cigoto o huevo fecundado; esta clula se divide por mitosis, hasta formar la mrula, que es un embrin cuyas clulas se denominan blastmeros. Todo este proceso ocurre mientras el embrin va por la tuba uterina o trompa de Falopio y en el ser humano demora alrededor de 4 a 5 das; durante este trayecto el embrin contina rodeado por la zona pelcida, la cual evita que l se implante prematuramente en la trompa. Al llegar al tero, el embrin rompe esta cubierta y se implanta en el endometrio ya preparado. La mrula, por el proceso de blastulacin, se transforma en una blstula, que en los mamferos se denomina blastocisto. Estos procesos empiezan a producirse aproximadamente a los 21 das de vida intrauterina, es decir, en el embrin propiamente tal. Estas clulas migran como una masa cordonal hacia ceflico originando la notocorda, la cual al ser visualizada por transparencia a travs del neurectoblasto, se la v como una prolongacin que nace de la fosita primitiva; esto ha llevado a denominarla prolongacin ceflica. Una vez que ha terminado la migracin del cordoblasto y mesoblasto, se tiene un embrin denominado gstrula tridrmica o embrin trilaminar; en ste se pueden reconocer en un corte transversal las tres hojas embrionarias antes citadas (Fig 1).
El embrin trilaminar o gstrula tridrmica se origina como consecuencia de la gastrulacin, proceso por el cual las clulas migran desde los territorios presuntivos a su ubicacin definitiva, que en general es la siguiente: el ectoderma y el neurectoderma quedan ubicados en la superficie externa y el endoderma se ubica en la superficie interna; entre estas dos hojas quedan, al centro, la notocorda y lateralmente a sta, el mesoderma. Previo a la migracin definitiva de los territorios presuntivos, es posible ver que inicialmente las clulas del mesoblasto migran caudalmente y hacia el centro de la discoblstula, originando la lnea primitiva, la que se transforma en estra primitiva una vez que las clulas mesoblsticas se invaginan y empiezan a migrar lateral y ceflicamente por entre el epi y el hipoblasto. Las clulas del cordoblasto migran convergiendo y condensndose en un punto en donde ellas forman un solevantamiento llamado nudo de Hensen; en la parte central de este solevantamiento aparece una cavidad, la fosita primitiva, resultante de la invaginacin de las clulas cordoblsticas. En el blastocisto se puede observar una cavidad, que es la cavidad del blastocisto, en cuyas paredes se puede reconocer: a) el embrioblasto o nudo embrionario, del que se formarn el alantoides, y por cavitacin, el amnios y el saco vitelino; b) el trofoblasto, del cual se formarn el corion y la placenta. El piso del amnios y el techo del saco vitelino forman el embrin bilaminar o discoblstula, el cual por un proceso muy dinmico denominado gastrulacin, se transforma en gstrula. A las dos hojas de la discoblstula se les denomina epiblasto a la superior e hipoblasto a la inferior. En el epiblasto hay grupos de clulas llamadas territorios presuntivos; stos, como consecuencia de la gastrulacin, darn origen a las hojas embrionarias: ectoderma (neurectoderma), mesoderma, endoderma y notocorda.
10
Tabla N 1 Territorios presuntivos en el embrin bilaminar Ectoblasto (azul) Mesoblasto (rojo) Endoblasto (amarillo) Cordoblasto (verde) Estructuras embrionarias correspondientes Ectoderma Mesoderma Endoderma Notocorda o cuerda dorsal
Los territorios presuntivos se representan convencionalmente con los colores antes sealados. En la embriognesis es preciso que diferentes tejidos que primitivamente estaban ubicados en la superficie del embrin (blstula), tomen una ubicacin definitiva, de modo que ellos queden sobre o lateralmente en la vecindad de otros; esto permite que puedan llevarse a cabo importantes procesos de induccin embrionaria que determinarn que un tejido que funciona como inductor logre que el vecino (tejido inducido) se transforme en un rgano u otra estructura del embrin. Es as como la notocorda inducir a que el ectoderma ubicado sobre ella se diferencie en placa neural y el mesoderma que inicialmente aparece como una masa de clulas ubicado
11
lateralmente a ambos lados de la notocorda, se metamerice (segmente) y origine masas de tejido mesodrmico embrionario llamadas somitos. Como la accin inductora de la notocorda es local y no difusa, el mesoderma ubicado lateralmente ms all del somito no se segmenta ( nefrotomo) y slo experimenta una delaminacin (mesoderma lateral), transformndose en una estructura bilaminar cuyas hojas reciben los nombres de smatopleura y esplacnopleura, interponindose entre ambas una cavidad llamada celoma. Considerando lo antes mencionado, la notocorda es una estructura embrionaria de primera importancia y ella es la responsable de la aparicin de un eje cfalo - caudal en todos los cordados; adems, por su accin inductora aparecern el sistema nervioso y los somitos, que son claves en el ulterior desarrollo del embrin. La notocorda recibe el su capacidad inductora ya cordoblasto; por eso al embriolgicamente como el nombre de inductor primario , pero est presente desde el estado de nudo de Hensen se le conoce inductor primario de Spemann .
Del somito se van a diferenciar tres porciones: 1) el dermatomo, que va a formar la dermis; 2) el miotomo, que formar los msculos; 3) el esclerotomo, que dar origen a huesos y cartlagos; de esta estructura provendrn clulas que rodeando a la cuerda dorsal y al tubo neural, formarn las vrtebras; ulteriormente la cuerda dorsal queda en el espesor del cuerpo vertebral (ncleo pulposo). Una vez terminada la gastrulacin se inicia el proceso de neurulacin en que se forma una nurula; es decir, en la gstrula, por induccin de la notocorda, se formar la placa neural. Antes de analizar la formacin del sistema nervioso propiamente tal, se mencionarn las etapas del desarrollo en relacin con los tiempos de duracin de cada una de ellas. El desarrollo intrauterino del ser humano se puede dividir en tres perodos: pre-embrionario, embrionario y fetal.
12
Perodo pre-embrionario .Se inicia con la fecundacin y comprende los fenmenos de segmentacin, cavitacin y gastrulacin; tiene una duracin total de tres semanas y cada una de ellos dura aproximadamente una semana. Al finalizar la primera semana se ha formado el disco unilaminar, al final de la segunda semana se ha constitudo el disco bilaminar y a la tercera semana ya est el disco trilaminar, que est implantado en el tero. Perodo embrionario . Comprende desde la cuarta hasta la octava semana de desarrollo intrauterino. En esta etapa se producen los esbozos de rganos u organognesis, las diferenciaciones tisulares o histognesis, a la vez que se inicia la consolidacin de las formas o morfognesis. Se forman algunos inductores primarios como el nudo de Hensen y la notocorda, que va a inducir la formacin del sistema nervioso. Perodo fetal. Comienza en la novena semana del desarrollo y termina con el nacimiento; en esta etapa prevalece el crecimiento corporal. Se forma el tubo neural, la hipfisis y precursores del sistema nervioso perifrico. En el segundo mes, el tubo neural se diferencia dando lugar a las vesculas primitivas. Neurulacin. Se denomina as a todo el proceso por el cual en la gstrula tridrmica se forma el tubo neural. Por accin inductora del cordoblasto, el ectoderma superficial adyacente experimenta una serie de cambios que culminarn con la aparicin de un tubo. Las etapas de este estado se describen a continuacin. a) Estado de placa neural. Es aquel estado en el cual el epitelio plano del epiblasto se hace prismtico, traducindose en un aplastamiento cfalo - caudal en todo el dorso del embrin. b) Estado de canal neural. A medida que contina el desarrollo, la placa neural empieza a invaginarse, originando a nivel de todo el dorso del embrin un canal que lo recorre de cabeza a cola.
13
c) Estado de tubo neural. La invaginacin del canal es cada vez mayor, llegando finalmente a contactar los bordes de este canal. En este momento se produce una soldadura y separacin del tubo de las paredes de la epidermis, cubriendo sta ltima al tubo, el cual se internaliza. Las clulas que forman los bordes del canal y que reciben el nombre de clulas de la cresta neural, se separan del tubo como una barra nica ubicada a ambos lados del tubo y migran a diferentes lugares, ubicndose y originando las estructuras que a continuacin se sealan: a.- neuronas de ganglios espinales, craneales y neurovegetativos; melanoblastos drmicos; b.- clulas de Schwann; meninges aracnoides y piamadre (la duramadre deriva del mesoderma).
ETAPAS DE LA NEURULACION
14
Tambin derivan de la cresta neural los odontoblastos, las clulas cartilaginosas del crneo y las clulas cromafines de la mdula adrenal. El tubo neural crece mostrando en su porcin ceflica un aumento de volumen, el que posteriormente formar las tres vesculas enceflicas: a.- prosencfalo b.- mesencfalo c.- rombencfalo. En esta etapa trivesicular ya se pueden observar dos evaginaciones laterales que son los recesos pticos y que van a originar los bulbos de los ojos o globos oculares. Las vesculas pticas van a constituir el lmite en que el prosencfalo se divide en dos nuevas vesculas: telencfalo y diencfalo. A su vez, en el rombencfalo empieza a formarse el cerebelo, que va a delimitar en aqul otras dos vesculas, el metencfalo y el mielencfalo. El mesencfalo no se modifica, de modo que ahora en la porcin ceflica del tubo neural se pueden reconocer cinco vesculas:
VESICULAS PRIMITIVAS DE LA NEURULACION
15
PROSENCEFALO TELENCEFALO: DIENCEFALO: HEMISFERIOS CEREBRALES EPITALAMO EPIFISIS TALAMO HIPOTALAMO NEUROHIPOFISIS PEDUNCULOS CEREBRALES COLICULOS O TUBERCULOS CUADRIGEMINOS
MESENCEFALO
ROMBENCEFALO METENCEFALO PUENTE O PROTUBERANCIA CEREBELO BULBO RAQUDEO
MIELENCEFALO
A su vez, la mdula espinal deja en su interior el canal central medular o conducto ependimario. Los ventrculos cerebrales estn comunicados entre s; los laterales comunican con el tercer ventrculo a travs del foramen interventricular o de Monro; tercero y cuarto ventrculo se conectan por el acueducto cerebral o de Silvio.
16
Durante el desarrollo embrionario del sistema nervioso, en el tubo neural se observa la formacin de tres curvaturas : dos dorsales y una ventral. Curvaturas dorsales. a) Ceflica o dorsal propiamente tal, se forma como consecuencia del crecimiento del prosencfalo; est ubicada entre el prosencfalo y el mesencfalo. b) Cervical, que se produce entre el mielencfalo y la mdula espinal. Curvatura ventral. a) Pontina o ventral propiamente tal, se forma a nivel del ulterior puente o protuberancia. Como consecuencia de la curvatura pontina, el tubo neural se abre a nivel de la lmina del techo, las placas alares se alejan, ubicndose en posicin ms ventral y lateral, originando as el piso del cuarto ventrculo, con un techo revestido por epitelio ependimario. El cuarto ventrculo ser recubierto por el cerebelo, que se est desarrollando a partir del metencfalo.
17
18
DESARROLLO DE SISTEMA NERVIOSO
Mesencfalo Metencfalo
Mielencfalo
Diencfalo
17.0 mm S. N. Central a los 49 das Mdula Espinal Telencfalo
Hemisferios Cerebrales Mesencfalo Cerebelo Bulbo Regin Cervical de la Mdula Espinal Puente
Diencfalo
78.0 mm S. N. Central a los 3 meses
Regin Lumbosacra de la Mdula Espinal
Histognesis del sistema nervioso.
19
En la pared del tubo neural se pueden distinguir varias zonas. As, el interior va recubierto por el epitelio ependimario entre cuyos elementos hay clulas germinativas que van a originar las diferentes clulas presentes en el tejido nervioso. Una vez que se cierra el tubo neural, a partir de la capa ependimaria se origina un tipo particular de clulas, los neuroblastos o clulas nerviosas primitivas, las que rodeando a la capa ependimaria forman la llamada capa del manto, que es la futura sustancia gris de la mdula espinal. De los neuroblastos se originan las fibras nerviosas que quedan includas en la capa ms perifrica y que rodeando a la capa del manto se le conoce con el nombre de velo marginal; una vez ocurrida la mielinizacin, ste origina la sustancia blanca de la mdula espinal. Inicialmente los neuroblastos son clulas apolares; cuando pierden la capacidad de multiplicarse originan dos prolongaciones que las hacen ser bipolares; ms tarde, una de las prolongaciones desaparece y la otra contina creciendo con lo cual se forma el axn; luego se desarrollan las dendritas constituyendo el neuroblasto multipolar; en ste se forman elementos intracelulares como neurofibrillas y cuerpos de Nissl. Debido a que contina la adicin de neuroblastos en la capa del manto, a cada lado del tubo neural se originan dos engrosamientos, uno ventral o placas basales (rea motora) y otro dorsal o placas alares (rea sensitiva); un estrechamiento longitudinal, el surco limitante, indica el lmite entre ambas zonas. Las porciones dorsal y ventral de la lnea media del tubo neural, que carece de neuroblastos, reciben el nombre de placas del techo y del piso respectivamente. Algunas clulas ependimarias permanecen como epitelio y revisten todas las cavidades del sistema nervioso; otras evolucionan como espongioblastos, que en la capa del manto se diferencian para originar los astrocitos protoplasmticos y fibrosos. Las clulas de la oligodendroglia pueden provenir tanto de los espongioblastos como del mesnquima, y por ltimo la microglia se forma a partir del mesodermo que rodea al tubo neural. Histolgicamente, el tubo neural va a presentar una configuracin como la descrita slo hasta el mesencfalo, en
20
donde en un corte transversal se pueden encontrar las siguientes estructuras : a.- lmina del techo o tectum; b.- lmina del piso; c.- pared lateral con un surco limitante que la separa en una placa alar dorsal y otra placa basal o ventral; orificio central revestido de una capa ependimaria. Esta divisin morfo - embriolgica tiene una repercusin funcional ya que de la porcin alar derivan estructuras sensitivas y de la porcin basal, estructuras motoras. Tanto el diencfalo como el telencfalo slo contienen elementos provenientes del crecimiento de la placa alar, por lo cual de ellos no provienen nervios motores y slo constituyen origen de nervios sensitivos (nervios ptico y olfatorio). La placa alar da origen a neuronas smatosensitivas y vscerosensitivas; la placa basal origina neuronas smatomotoras y vsceromotoras. Formacin de la mdula espinal. Al continuar el desarrollo del tubo neural, su porcin caudal se organiza como mdula espinal, en la cual las clulas de la placa dorsal constituyen los cuernos o astas posteriores, que funcionalmente son sensitivas; las clulas de los cuernos o astas anteriores son motoras y tienen su origen en la placa basal. Las clulas vecinas al surco limitante dan origen a un cuerno o asta lateral, de participacin neurovegetativa, lo cual sucede en los segmentos espinales torcico y lumbar, donde van a constituir parte del sistema simptico; en la mdula sacra, las clulas precursoras en la placa basal van a formar centros parasimpticos. Las estructuras constitudas por somas neuronales conforman sustancia gris que se encuentra en el centro de la mdula. La zona perifrica del tubo est constituda por funculos o cordones medulares de fibras nerviosas que conforman la sustancia blanca de la mdula espinal. En el centro queda el canal central o conducto del epndimo. Rodeando al tubo neural y por tejido proveniente del esclerotomo, se forman las vrtebras, de modo que la parte del tubo neural correspondiente a la mdula espinal se ubica en un
21
verdadero canal denominado canal vertebral. Los cuerpos vertebrales crecen ms que los segmentos medulares, de modo que los nervios espinales que se originaron de la mdula y que salen por los agujeros intervertebrales, van perdiendo paulatinamente su perpendicularidad con respecto a la mdula y adoptan una conformacin en ngulo agudo hacia abajo. II.-HISTOLOGIA DEL SISTEMA NERVIOSO. Introduccin. La clula es la unidad biolgica de la materia viva, y es el elemento mnimo capaz de desarrollar existencia autnoma; se agrupa formando tejidos, que se pueden considerar como el conjunto organizado de clulas que poseen la misma especializacin, o especializaciones cercanamente complementarias. Las clulas de un tejido suelen tener el mismo origen. Por el fenmeno de la adaptabilidad, en los tejidos se producen reducciones en las funciones celulares, lo que determina la especializacin, en que se observa una optimizacin de las propiedades que persisten. Los elementos celulares tisulares se complementan entre s, contribuyendo cada grupo celular con sus propiedades especializadas al desarrollo armnico del sistema. Un rgano es un conjunto de tejidos que se pueden definir funcional y morfolgicamente, con funciones complementarias. Los aparatos son conjuntos de rganos con funciones complementarias. El sistema est constitudo estructuralmente por un conjunto de aparatos cuyos rganos poseen el mismo tejido funcional o parnquima. Funcionalmente un sistema es un conjunto de unidades o entidades coordinadas segn leyes que las relacionan entre s , en tal forma que el sistema cumple un determinado objetivo. Cuando las estructuras se organizan en sistema, ste presenta propiedades que no necesariamente
22
tienen los elementos componentes, y que derivan justamente de las interrelaciones entre ellos. En los rganos existen uno o ms tejidos que los definen funcionalmente y que constituyen el parnquima. Adems, en todos los rganos hay tejidos trofoconectivales que proveen de cohesin y nutricin a las clulas, a la vez que forman el armazn o estroma del tejido. Existen diferentes clases de tejidos, que bsicamente se pueden agrupar en epitelial, conectivo, muscular y nervioso. El tejido epitelial se caracteriza por una gran cohesin de sus clulas, con relativamente poca sustancia intercelular; los tejidos trofoconectivales poseen pocas clulas, las que producen diferentes sustancias intercelulares que junto con sus clulas van a caracterizar cada una de las variedades del tejido conjuntivo; el tejido muscular se caracteriza por la propiedad de contraerse y el tejido nervioso por su irritabilidad. Tejido nervioso. Constituye un tipo de epitelio especializado, que se caracteriza por poseer muy desarrollada la propiedad de la irritabilidad, que comprende la excitabilidad y la conduccin, que le permite comunicacin intercelular y con los efectores. Sus clulas son las neuronas y los gliocitos o clulas de la gla. Las neuronas constituyen las unidades morfo - funcionales del sistema nervioso y son las clulas que poseen un alto grado de irritabilidad, es decir, son extremadamente excitables y pueden conducir los impulsos que deriven de tal excitacin; presentan caractersticas estructurales con diversidad de formas y tamaos, as como prolongaciones que pueden alcanzar gran longitud. Son diez veces menos numerosas que los gliocitos. La excitabilidad neuronal es la capacidad de responder a agentes fsicos, qumicos, etc, que constituyen los estmulos, y que pueden desencadenar cambios en el potencial elctrico de la membrana celular; se debe a caractersticas de protenas especficas de la membrana neuronal que constituyen canales inicos y mecanismos de bomba. La conductibilidad es la
23
capacidad de trasmitir tales cambios en forma de impulsos nerviosos. Adems, la irritabilidad puede inducir cambios estructurales ms complejos y permanentes, por activacin de agentes metablicos. La neurona est formada por un cuerpo neuronal o soma y prolongaciones neuronales; posee un ncleo, citoplasma o pericarion y una o ms extensiones protoplasmticas que son: a.- axn, neurito o cilindroeje; b.- dendritas. A las neuronas se les puede clasificar considerando diversos puntos de vista, como ser el nmero y/o la longitud de los neuritos, las caractersticas de sus dendritas, la forma de sus somas, sus funciones, etc. Segn sea el nmero de sus prolongaciones axnicas, las neuronas pueden ser: a.- monoaxonales, con un neurito; b.- biaxonales, con dos neuritos; c.- anaxonales, sin neurito. Las neuronas anaxonales slo poseen dendritas. Las neuronas biaxonales tienen dos neuritos, uno receptor y otro efector, a la vez que carecen de dendritas; pueden ser bi o uni polares (pseudounipolares). La bipolar es alargada, fusiforme, con una prolongacin en cada extremo o polo; se les encuentra , por ejemplo, en la retina y en el epitelio olfatorio. Las neuronas pseudounipolares son las neuronas sensitivas clsicas; su soma neuronal est ubicado en los ganglios sensitivos, ya sean espinales o pertenecientes a los nervios craneanos; en un corto trecho desde el soma, el neurito es nico, para luego bifurcarse y prolongarse en direcciones opuestas. Su extremo perifrico o receptor est orientado hacia la periferia, proviniendo de estructuras receptoras; en cambio, su prolongacin efectora se dirige hacia el sistema nervioso central.
24
A las neuronas biaxonales se les denomina tambin neuronas receptoras, porque son las nicas que diferencian terminaciones receptoras en el extremo distal de su neurito perifrico. Estos receptores son importantes porque a nivel de ellos el sistema nervioso puede ser estimulado por cambios ambientales o internos del organismo. Las neuronas monoaxonales poseen un solo neurito y desarrollan dendritas. Son las neuronas ms numerosas y segn las caractersticas de sus dendritas se les puede clasificar en: A.- leptodendrticas, cuyas dendritas son lisas y poco ramificadas; B.- isodendrticas, con dendritas ramificadas y portadoras de espinas, que son estructuras especializadas en conecciones interneuronales (contactos sinpticos); C.- idiodendrticas, que poseen dendritas con muchas ramificaciones y que son caractersticas segn el grupo neuronal; poseen abundantes espinas y un ejemplo tpico lo constituyen las neuronas de Purkinje del cerebelo. Segn la longitud del axn, a las neuronas se les puede clasificar en: A.- neuronas Golgi tipo I, de axones largos; se encuentran en los nervios perifricos y en los fascculos del sistema nervioso central, donde por lo general sus prolongaciones axnicas constituyen sustancia blanca; B.- neuronas tipo Golgi II, de axn corto que se ramifica en las inmediaciones del pericarion; son por lo general neuronas de asociacin y son numerosas en los hemisferios cerebrales, cerebelo, retina, etc. Segn la forma del pericarion, las neuronas pueden ser: A.- globosas, de soma redondeado; se encuentran en los ganglios espinales sensitivos y neurovegetativos;
25
B.- piramidales, cuyo soma posee forma de pirmide; se les encuentra en la corteza cerebral; C.- estrelladas, con sus dendritas orientadas en todas direcciones; son ejemplo caracterstico las motoneuronas de las astas anteriores medulares; D.- piriformes, cuyo soma posee una porcin redondeada y otra alargada; es el caso de las neuronas de Purkinje del cerebelo. Por ltimo, atendiendo a una clasificacin funcional, las neuronas pueden ser: A.- sensitivas; B.- de asociacin, denominadas tambin intercalares o internunciales; C.- motoras. Tanto las neuronas sensitivas como las motoras son de tipo Golgi I. Estructura de la neurona . Soma o cuerpo celular. Es el centro metablico de la neurona, pues si una parte se separa del cuerpo neuronal, dicha parte degenera. Su pericarion tiene forma variable, es grande, con un dimetro que vara entre 4 y 150 micrones de dimetro. El soma contiene el ncleo y la maquinaria bioqumica encargada de la sntesis enzimtica y otras molculas vitales. El ncleo puede ser tambin voluminoso, de hasta 20 micrones de dimetro, y contiene uno o ms nuclolos. El citoplasma neuronal contiene organelos como las neurofibrillas,los grnulos de Nissl o sustancia cromfila, el aparato de Golgi, mitocondrias, centrosoma, lisosomas y algunas inclusiones, como melanina, lipocromo o lipofucsina, fierro, lpidos y glicgeno.
26
Neurofibrillas . Se observan como hebras entrelazadas que atraviesan el citoplasma, formando una verdadera malla en el cuerpo y en las prolongaciones (dendritas y axn). Se agrupan en haces que pueden ramificarse y que poseen neurotbulos y neurofilamentos; ambas estructuras intervienen en el transporte intracelular de iones y metabolitos, sirven de sostn a la clula y le ayudan a conservar su forma. Sustancia de Nissl o cromfila . Es el componente basfilo del citoplasma; su principal componente son las ribonucleoprotenas . A microscopa electrnica se observa que est constituda por acmulos de cisternas del retculo endoplsmico rugoso y est relacionada con la sntesis proteica. Forma grumos o masas que son los cuerpos de Nissl y se encuentra ampliamente distribuda en el citoplasma. Est en mayor concentracin en las neuronas motoras que en las sensitivas; existe en el soma y en las dendritas pero no en el axn. Aparato de Golgi . Generalmente es perinuclear. A microscopa electrnica se le reconoce como acmulos de cisternas aplanadas; puede estar conectado con el retculo endoplsmico liso y ste con el rugoso. Mitocondrias . Son similares a las de otras clulas del organismo. Se encuentran dispersas, entremezcladas con la sustancia de Nissl y las neurofibrillas; tiene diversas formas, como ovoides, filamentosas ,etc. y son ms pequeas y numerosas en las terminaciones nerviosas. Estn en constante movimiento, cambiando su forma, tamao y posicin, tendiendo a emigrar del pericarion para luego regresar. Su concentracin es ndice del intenso metabolismo neuronal.
27
Inclusiones citoplasmticas . Suelen observarse gotas de lpidos, glicgeno (slo en los neuroblastos) y pigmentos. Prolongaciones neuronales . Constituyen extensiones citoplasmticas del cuerpo neuronal y son estructuras de recepcin y de conduccin de impulsos, a la vez que aumentan el rea de contacto interneuronal. Las dendritas son las prolongaciones cortas y se ramifican por dicotoma irregular, con un patrn caracterstico segn los diversos tipos neuronianos. No poseen cubierta de mielina y en las neuronas multipolares se ramifican ampliamente. Se denomina campo dendrtico el espacio delimitado por las dendritas de una neurona. Es la regin dentro de la cual una neurona recibe contactos eficientes. De este modo se puede decir que las dendritas definen espacialmente a la neurona. El citoplasma dendrtico contiene sustancia de Nissl, mitocondrias, retculo endoplsmico liso,abundantes neurotbulos y pocos neurofilamentos. La mayor parte de las dendritas est cubierta de espinas dendrticas, que son sitios especializados de contactos sinpticos. En general, las dendritas conducen impulsos en forma centrpeta hacia el soma neuronal. El cilindro - eje o neurito o axn constituye la prolongacin de mayor longitud. A diferencia de las dendritas que son anisodiamtricas (dimetro diferente), el dimetro de los axones permanece constante a lo largo de su trayecto, es decir, los neuritos son isodiamtricos, con un dimetro que vara entre 1 y 21 micrones, y una longitud tambin variable, desde milmetros a metros. El axn no posee espinas y puede dar ramas colaterales que siempre emergen en ngulo recto;
28
termina en ramificaciones que constituyen el telodendron . Los telodendrones pueden ser: terminaciones efectoras, que son las que poseen las neuronas monoaxonales y el neurito central de las neuronas biaxonales; permiten que una neurona excitada pueda perturbar (estimular) a las clulas con que establece contacto; se caracterizan por la presencia de terminales sinpticos: terminaciones receptoras, que son siempre telodendrones de neuronas biaxonales. Se caracterizan por la diferenciacin de estructuras (terminaciones receptoras) que se excitan fcilmente con cambios ambientales ajenos al sistema nervioso. El neurito nace generalmente en una regin de la neurona llamada cono axnico, zona que no contiene cuerpos de Nissl y por el cual pasan las neurofibrillas hacia el axn. El cono de origen o el segmento inicial del axn puede constituir un sitio reactivo para seales inhibitorias. Los impulsos generalmente llevan en el axn una direccin centrfuga, es decir, se alejan del soma neuronal, salvo en el neurito receptor de las neuronas biaxonales y en el neurito perifrico de las neuronas pseudounipolares, en que los impulsos van desde el telodendron receptor al soma, es decir, llevan una direccin centrpeta. El axoplasma del neurito contiene retculo endoplsmico liso que va en forma longitudinal, as como mitocondrias largas y delgadas, neurotbulos y abundantes neurofilamentos. La neurona est formando citoplasma en forma continua, el cual fluye hacia las prolongaciones; en esta forma se repone el protoplasma catabolizado, especialmente las protenas que no pueden ser sintetizadas por el axoplasma y en cambio se pueden sintetizar en el retculo endoplsmico rugoso del soma neuronal. Este flujo axnico es lento ( 1 a 5 mm diarios) si las sustancias son de peso molecular alto (protenas) o rpido (10 cm por da) si las sustancias son pequeas y de mayor difusin. En este flujo los neurotbulos y los neurofilamentos desempean una funcin importante en la movilizacin de vesculas sinpticas, mitocondrias, etc. Con respecto al desplazamiento del impulso nervioso, el potencial de accin puede propagarse por el axn en ambos
29
sentidos, centrfugo y centrpeto; no obstante, en el funcionamiento normal del organismo, el impulso va desde las dendritas o desde el telodendron receptor hacia el soma y de aqu al telodendron efector. Desde este punto de vista funcional, en la neurona se reconocen tres zonas o campos: a.- receptor: dendritas, cuerpo, cono de origen en las neuronas monoaxonales y terminaciones receptoras en las neuronas biaxonales; b.- conductor: axn; c.- efector: telodendron de las neuronas monoaxonales y del neurito central en las neuronas biaxonales.
30
NEURONA
Sustancia de Nissl Dendritas
Soma
Organelos Ncleo
Vaina de Mielina Nodos de Ranvier
Botones Sinpticos
Axn
Telodendron
31
Neuroglia . Constituye el sostn mecnico y metablico de la neurona. Sus clulas se denominan gliocitos y forman el tejido intersticial del sistema nervioso central. En el sistema nervioso central de los vertebrados, son diez a cincuenta veces ms numerosas que las neuronas y sus mltiples prolongaciones constituyen una verdadera trama que sostiene y protege a los cuerpos neuronianos y a sus prolongaciones. Participan en la nutricin de las neuronas, en la reparacin de lesiones y en la conduccin nerviosa. En relacin con aspectos morfofuncionales, se pueden distinguir dos grupos de clulas gliales, que conforman una macrogla y una microgla. La microgla est constituda por clulas pequeas de origen mesodrmico y de cuerpo alargado. Son los macrfagos del sistema nervioso central y pertenecen al sistema retculo endotelial. Constituyen el 5% de las clulas gliales del sistema nervioso central y se encuentran tanto en la sustancia gris como en la sustancia blanca. La macrogla est constituda por los astrocitos, los oligodendrocitos y las clulas de Schwann. Los astrocitos son los elementos gliales de mayor tamao, se encuentran solamente en el sistema nervioso central, tanto en la sustancia blanca como en la gris, y hay una variedad fibrosa y otra protoplasmtica. Forman el epitelio de base del sistema nervioso central; entre sus clulas se disponen las neuronas y los capilares, los que son envueltos por las prolongaciones de los astrocitos; en esta forma, constituyen parte de la barrera hmato-enceflica. Esta es ms bien de tipo funcional y en ella intervienen diferentes estructuras; as, los
32
capilares del sistema nervioso central presentan menor intercambio que otros capilares porque su pared es continua, con pocas vesculas pinocitcicas de transporte; esto determina que difcilmente filtren sustancias de peso molecular alto, entre las que pueden existir algunas sustancias txicas.
ESQUEMA BARRERA HEMATOENCEFLICA
Capilar Sanguneo
Soma Neuronal
Astrocito
Los astrocitos que rodean las regiones sinpticas suelen presentar afinidad por algunos neurotransmisores y contribuyen a retirarlos de la hendidura sinptica. Por otra parte, la membrana de los astrocitos presenta una gran permeabilidad al K+ , el cual determina prcticamente su potencial de reposo. Esta facilidad de captar iones K+ les permite a los astrocitos tamponar el exceso de este ion liberado por las neuronas, con lo cual no se acumula en el espacio extracelular an cuando la actividad neuronal sea intensa. Con
33
este mecanismo buffer se protege a las neuronas vecinas de despolarizacin que podra producirse por la acumulacin de K+ extracelular. Adems, se sabe que los vasos cerebrales son muy sensibles a la accin de los iones K+, de modo que indirectamente los astrocitos participan en la autorregulacin del flujo cerebral. Los oligodendrocitos son clulas pequeas, poco ramificadas, que rodean ntimamente a las neuronas del sistema nervioso central y del sistema nervioso perifrico, formando la vaina oligodendrglica que aisla al tejido nervioso del tejido conectivo. En el sistema nervioso central se encuentran los oligodendrocitos propiamente tales y en el sistema nervioso perifrico estn las clulas de Schwann, los anficitos y la telogla. En conjunto, las clulas mencionadas constituyen aproximadamente un 75 % de las clulas gliales, y como todas ellas, se pueden multiplicar en la vida post natal. Los anficitos o clulas satlites se encuentran rodeando y protegiendo los somas de las neuronas en los ganglios, tanto espinales como neurovegetativos. Las clulas de la telogla rodean y cubren las terminaciones nerviosas perifricas, tanto receptoras como efectoras, dejando desnudos slo los sitios activos y constituyendo aislante elctrico de dichas terminaciones. Las clulas de Schwann se encuentran en el sistema nervioso perifrico rodeando a los axones formando parte de las fibras nerviosas que constituyen los nervios. En trminos generales, las funciones de las clulas de la gla se pueden resumir en las siguientes: a) constituyen elementos de soporte y pueden separar y an aislar grupos neuronales; b) desempean funciones trficas, interviniendo en la nutricin y metabolismo de neuronas, especialmente en el de las protenas y los cidos nucleicos;
34
c) tienen una funcin mielogentica; es as como los oligodendrocitos en el sistema nervioso central y las clulas de Schwann en el sistema nervioso perifrico forman la mielina, que es una sustancia aislante que recubre muchos axones; d) algunas clulas gliales desempean funciones de macrfagos; e) otros gliocitos ejercen funciones buffer o de tampn para la concentracin de iones K+ en el lquido extracelular , as como captacin y remocin de neurotransmisores liberados a nivel sinptico; f) a travs de la vaina de mielina, participan en la conduccin del impulso nervioso, puesto que los nodos de Ranvier que quedan entre las clulas de Schwann dan lugar a la conduccin saltatoria que se caracteriza por su rapidez para conducir los impulsos nerviosos; g) algunos gliocitos, como los oligodendrocitos, participan en el flujo axnico, realizando un verdadero masaje del axn, lo cual contribuye a propulsar el axoplasma; h) durante el desarrollo embrionario algunas clulas de la gla forman verdaderas guas biomecnicas que facilitan la migracin de neuronas; i) clulas gliales como los astrocitos constituyen parte de la barrera hmato-enceflica. Fibra nerviosa. Est constituda por el axn y sus vainas que lo recubren. As, en el sistema nervioso central, los axones poseen una vaina oligodendrglica, y en el sistema nervioso perifrico tienen adems una vaina conectiva ms externa. Los axones presentan dimetros que varan aproximadamente entre 0,5 a 21 micrones, siendo en general
35
ms gruesos los de las neuronas ms grandes. Segn su dimetro, los neuritos (no las fibras) se agrupan en cuatro categoras: I : 12 - 22 micrones II : 6 - 12 micrones III : 1 - 6 micrones IV : 0,3 - 1,4 micrones En los neuritos de ms de un micrn de dimetro, la vaina oligodendrglica o de clulas de Schwann se organiza como vaina de mielina. Como ya se explicit, todos los axones poseen una vaina oligodendrglica, pero en las fibras llamadas mielnicas, los oligodendrocitos en el sistema nervioso central y las clulas de Schwann en el sistema nervioso perifrico, forman una nueva envoltura que es la mielina. En las fibras amielnicas, un solo oligodendrocito puede envolver a varios axones, pero las clulas de Schwann rodean un solo axn. En el sistema nervioso tanto central como perifrico, se encuentran las fibras mielnicas y las amielnicas distribudas ms o menos homogneamente. Las fibras amielnicas del sistema nervioso central tienen vaina oligodendrglica y poseen axones cortos; en el sistema nervioso perifrico las fibras amielnicas van cubiertas por una vaina de Schwann (neurolema o neurilema) y constituyen fibras sensoriales delgadas y fibras post ganglionares del sistema neurovegetativo. La mielina constituye una envoltura que se desarrolla en los neuritos de un dimetro mayor de un micrn, y la forman los oligodendrocitos en el sistema nervioso central y las clulas de Schwann en el sistema nervioso perifrico. En el proceso de formacin de la mielina, los oligodendrocitos o las clulas de Schwann envuelven al axn y luego la clula glial se enrrolla repetidas veces como en espiral, su citoplasma se va expulsando, se modifica y se forma la mielina, constituda por capas bimoleculares de lpidos interpuestas por capas adyacentes de protenas. El anlisis bioqumico ha demostrado que la mielina tiene una composicin similar a la de las membranas plasmticas, con un 70 % de lpidos y un 30 % de protenas, con una alta concentracin de colesterol y fosfolpidos. La mielina misma presenta un aspecto blanco
36
brillante que le da su coloracin a la sustancia blanca del sistema nervioso. La zona en que limitan dos oligodendrocitos o dos clulas de Schwann vecinas en las fibras mielnicas, constituye un nodo de Ranvier, descubierto de mielina; estos nodos van a determinar un tipo especial de conduccin de los impulsos nerviosos, la conduccin saltatoria, que es ms rpida que la que presentan las fibras amielnicas. A modo de ejemplo, en las fibras sensitivas femorales, la distancia internodal es de 1 a 1,5 mm . La mielina del sistema nervioso central difiere de la del sistema nervioso perifrico no solamente por las clulas que la originan. En el caso de las clulas de Schwann, los genes que codifican la mielina se activan en presencia de los axones; en cambio en los oligodendrocitos, la expresin de los genes depende de la presencia de astrocitos. Tambin existen algunas diferencias en las protenas componentes de ambas mielinas, central y perifrica. No obstante, ambas contienen el mismo grupo de protenas bsicas similares constitudo por unas siete variedades que en algunos animales son inmunognicas, lo cual ha permitido producir experimentalmente una encefalitis alrgica que produce demielinizacin; este cuadro ha servido de modelo para explicar los efectos de la esclerosis mltiple, enfermedad que en los humanos se manifiesta por demielinizacin sensitiva y/o motora. La mielina contribuye al aislamiento elctrico de los neuritos y aumenta la velocidad de conduccin del impulso nervioso debido a las caractersticas de los nodos de Ranvier. Las clulas de Schwann son metablicamente muy activas y podran proveer la energa necesaria para la movilizacin de iones que determinan el potencial de accin. Tejido nervioso en los sistemas nerviosos central y perifrico. Una forma de clasificar al sistema nervioso es considerar una divisin central y otra perifrica.
37
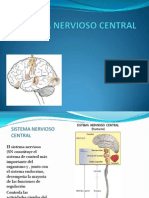
El sistema nervioso central est constitudo por la mayor parte del encfalo (se excluyen los nervios craneanos y sus ganglios correspondientes, todo lo cual pertenece al sistema nervioso perifrico) y la mdula espinal; salvo por la sustancia reticular, el tejido nervioso central presenta dos zonas bien definidas, que son la sustancia blanca y la sustancia gris. Funcionalmente est especializado en la integracin de funciones, en la regulacin de las actividades viscerales y somticas y en el desarrollo de las funciones psquicas propiamente tales. El sistema nervioso perifrico est constitudo esencialmente por los nervios y los ganglios. Los nervios se definen como conjuntos de fibras nerviosas ubicados fuera del sistema nervioso central; estn conformados por fibras mielnicas y amielnicas y funcionalmente pueden ser sensitivos, motores o mixtos. Se encuentran distribudos en todos los rganos . Los ganglios se definen como grupos de somas neuronales del sistema nervioso perifrico.
38
ESTRUCTURA DEL NERVIO
Ganglio
Epineurio
Perineurio
Endoneurio
Axn Fascculo Vaina de Mielina
Corte transversal de nervio Citico
La sustancia gris debe su coloracin a los cuerpos neuronales, a fibras amielnicas y a algunas clulas neurglicas de sostn. As, en ella se encuentran somas neuronianos, dendritas, axones amielnicos, astrocitos protoplasmticos, oligodendrocitos, microgla y pequeos vasos sanguneos. En la mdula espinal, la sustancia gris se encuentra en la parte
39
central, rodeando al conducto del epndimo y formando una especie de H al corte transversal. En cambio, en los hemisferios cerebrales y en el cerebelo, la sustancia gris se encuentra en la periferia, rodeando a la sustancia blanca, y en los ncleos, que son conjuntos de somas neuronianos ubicados en el sistema nervioso central.
CORTE CORONAL ENCFALO Regin Occipital Sustancia Gris y Blanca
Sustancia Blanca
Sustancia Gris
Cerebelo
La sustancia blanca est constituda fundamentalmente por fibras nerviosas mielnicas y tambin por clulas neurglicas, principalmente astrocitos fibrilares, oligodendrocitos, clulas de Schwann y microgla; prcticamente no contiene somas neuronianos ni dendritas. El color blanco se lo debe a la mielina que rodea a la mayor parte de las fibras nerviosas que conforman la sustancia blanca. La composicin descrita permite deducir que en la sustancia blanca existe un predominio de elementos neuronales
40
conductores , por lo cual ella constituye los fascculos, haces o tractos del sistema nervioso central y los nervios en el sistema nervioso perifrico. Con respecto al tejido nervioso que constituye el sistema nervioso perifrico, se analizar en esta oportunidad; en cambio, la composicin respectiva en el sistema nervioso central se considerar al describir la estructura anatmica de cada uno de sus elementos componentes. Los nervios estn constitudos por fibras nerviosas que a su vez se agrupan en fascculos, cuyo conjunto va a formar el nervio. Las fibras nerviosas mielnicas y amielnicas poseen una cubierta conectiva que es el endoneurio; est formado por fibroblastos, macrfagos fijos, fibras colgenas y reticulares. Estas fibras mielnicas y amielnicas con su endoneurio se agrupan formando los fascculos nerviosos, que a su vez poseen una envoltura externa conectiva que es el perineurio, constitudo por 4 a 12 capas de clulas aplanadas dispuestas en forma concntrica; entre los facsculos nerviosos existe tejido conectivo laxo y tejido adiposo. Los fascculos a su vez se renen rodendose de otra cubierta que es el epineurio, de tejido conectivo; est conformado por fibras colgenas,escasas fibras elsticas y vasos sanguneos. La irrigacin del nervio la suministran pequeas arteriolas nutricias que se anastomosan en el epineurio, formando redes arteriolares en el perineurio, de las que derivan los plexos capilares cuyos vasos penetran en el endoneurio. Los ganglios son estructuras del sistema nervioso perifrico constitudos esencialmente por somas neuronales. Existen dos tipos de ganglios, los sensitivos, llamados tambin cerebro-espinales, y los neurovegetativos. Los ganglios sensitivos son somas de neuronas sensitivas o aferentes; constituyen un conjunto que es la cadena de ganglios espinales o raqudeos y otro grupo ms bien disperso que corresponde a los ganglios de los nervios craneanos sensitivos o a la porcin sensitiva de los nervios mixtos.
41
Las fibras nerviosas sensitivas estn constitudas por neuronas pseudounipolares o en T, que poseen un neurito perifrico cuyo telodendron se diferencia en elementos receptores, y un neurito central que se dirige a la mdula espinal o al encfalo; ambos axones se originan de una corta estructura axonal que proviene del soma neuronal, el cual se encuentra ubicado en los ganglios sensitivos; en stos hay adems clulas satlites o anficitos que rodean aislando a cada soma, vasos sanguneos y una cubierta o cpsula de tejido conectivo, de la cual se origina una fina red de tejido conectivo distribudo dentro del ganglio y compuesta por prolongaciones de fibras reticulares y colgenas; en el interior estn los vasos sanguneos y entre el retculo van los elementos nerviosos. Los ganglios neuro-vegetativos presentan una organizacin similar a la de los sensitivos, pues estn constitudos por somas neuronales y poseen un estroma de tejido conectivo y oligodendrocitos. La mayor parte de las neuronas son multipolares y estrelladas. Las fibras estn conformadas por axones que pueden ser amielnicos y no muestran tendencia a agruparse en haces de fibras. Estos ganglios son los que pertenecen a los sistemas simptico y parasimptico y se encuentran en la unin o sinapsis de las fibras preganglionares con las postganglionares, es decir, en la rama motora del circuito neurovegetativo. Constituyen estos ganglios diferentes agrupaciones; as, los ganglios simpticos constituyen una cadena paravertebral y algunos ganglios colaterales; los ganglios parasimpticos en cambio no forman conjuntos definidos sino que se encuentran en las paredes de las vsceras que inerva el sistema o en sus cercanas. Algunas clulas de ganglios neurovegetativos son muy modificadas, como en la mdula suprarrenal, donde carecen de axn y dendritas y contienen grnulos secretorios de catecolaminas.
III .- ANATOMIA DEL SISTEMA NERVIOSO.
42
El tejido nervioso est constitudo por el conjunto organizado de neuronas y clulas gliales en estructuras bien definidas . El sistema nervioso constituye, como su nombre lo indica, un sistema, es decir, un conjunto de entidades que se rigen por leyes propias y que se orientan a un fin determinado; el sistema pasa a constituir una estructura funcional que posee propiedades que derivan precisamente de su organizacin sistmica y que trascienden las propiedades de sus componentes individuales. As considerado, se le puede clasificar en un sistema nervioso central, que comprende la mayor parte del encfalo y la mdula espinal, y otro sistema nervioso perifrico, formado por los nervios y los ganglios. Funcionalmente se puede distinguir un sistema nervioso somtico , relacionado con la actividad de la musculatura esqueltica, y uno neurovegetativo que regula las funciones viscerales. El encfalo es tal vez la estructura ms compleja del sistema nervioso y est conformado por las siguientes partes: A.- tronco cerebral, constitudo por la mdula oblongada o bulbo raqudeo, el puente de Varolio o protuberancia anular y el mesencfalo, que a su vez consta de dos estructuras, cuales son los pednculos cerebrales y el tectum o techo o lmina cuadrigmina; B.- cerebelo; C.- diencfalo, tambin denominado tlamo-encfalo, que comprende el tlamo, el hipotlamo, la hipfisis, el epitlamo y el subtlamo; D.- telencfalo o hemisferios cerebrales, que contienen la corteza cerebral y los ncleos de la base. La mdula espinal es la estructura ms antigua del neuroeje y la ms sencilla desde el punto de vista funcional.
43
En cuanto al sistema nervioso perifrico est constitudo por los nervios y ganglios nerviosos; desde el punto de vista funcional, los nervios pueden ser sensitivos, motores o mixtos, siendo estos ltimos los ms abundantes. Otra clasificacin los agrupa en nervios somticos y vegetativos. Planos de simetra . Como en toda descripcin anatmica, para efectuar la del sistema nervioso se supone al cuerpo en la posicin anatmica, que para el ser humano se la describe como estacin de pie, eje vertical, con la cabeza, los ojos, los dedos de los pies y las palmas de las manos dirigidos todos hacia adelante. En los animales cordados el sistema nervioso presenta simetra axial, en que las estructuras se repiten simtricamente a cada lado del plano medio (o meso) sagital. Este es un plano que pasa por una lnea media vertical ntero-posterior, dividiendo al cuerpo en dos mitades simtricas derecha e izquierda. Cualquier seccin paralela al plano medio sagital se dice que est en el plano sagital y se le denomina plano parasagital. En el sistema nervioso, el plano medio sagital permite describir una hemiseccin vertical de una estructura, y como existe simetra axial, la descripcin de una mitad puede extrapolarse a la estructura completa, a la vez que se facilita el anlisis de las vas de informacin directas y cruzadas.. En cambio los planos parasagitales permiten ms bien ubicar zonas o partes del elemento que se analiza. Los planos frontales o coronales son tambin verticales, perpendiculares al plano sagital, y dividen al cuerpo en una parte anterior o ventral y otra posterior o dorsal. Los planos horizontales o transversos son perpendiculares tanto al sagital como al frontal y dividen al cuerpo en una porcin superior o rostral o craneal y otra inferior o caudal. De los planos derivan posiciones con respecto a ellos, como ser: a.- rostral, hacia la parte superior del eje; b.- caudal, hacia la parte inferior del eje;
44
c.- ventral, anterior a un plano frontal; d.- dorsal, posterior a un plano frontal; e.- lateral, hacia los lados del plano sagital; f.- medial, en direccin a una lnea media.
UBICACIN ESPACIAL DE REAS EN EL SISTEMA NERVIOSO
Dorsal , Superior
Rostral o Anterior
Ventral, Inferior
Dorsal , Posterior Caudal
Ventral, Anterior
45
Mdula Espinal. Es una estructura larga y cilndrica que va ubicada dentro del canal vertebral o raqudeo y que se extiende desde la primera vrtebra cervical hasta la segunda lumbar. Est constituda por sustancia gris que ocupa la parte central, y sustancia blanca que rodea a la gris; en el centro de la mdula est el conducto del epndimo que, a nivel del bulbo raqudeo se abre en el cuarto ventrculo y en su porcin ms caudal presenta el ventrculo terminal. Al igual que el encfalo, la mdula espinal est revestida por las meninges. La columna vertebral est constituda por vrtebras que son el elemento protector de la mdula espinal. Tienen en su parte central un orificio que considerado en el conjunto de las vrtebras forma el canal raqudeo; entre dos vrtebras consecutivas estn los orificios intervertebrales por los cuales emergen los pares de nervios espinales o raqudeos que llevan fibras sensitivas y motoras desde y hacia las vsceras respectivamente; el primer par de nervios raqudeos emerge entre el crneo y la primera vrtebra cervical que es el atlas. Las vrtebras forman subconjuntos segn la regin en que se encuentran ubicadas; as, hay 7 vrtebras cervicales, 12 dorsales, 5 lumbares, 5 sacras que van unidas formando un solo hueso, el sacro, y 1 cocgea. Esta clasificacin da origen a segmentos medulares o metmeras, que consideran para cada uno su par de nervios espinales correspondientes; es por ello que se describen 8 segmentos cervicales (C) , 12 torcicos (T), 5 lumbares (L) , 5 sacros (S) y 1 coccgeo (c). Caudal al ensanchamiento lumbar est el cono medular, rodeado por los pares nerviosos lumbosacros de la cola de caballo o cauda equina. Una condensacin de la piamadre forma el filamento terminal o filum terminale, que a la altura de la segunda vrtebra sacra se recubre de duramadre, constituyendo el ligamento cocgeo. Durante el desarrollo fetal el crecimiento de la columna vertebral sobrepasa al de la mdula, de modo que los segmentos medulares no se corresponden estrictamente con los vertebrales y adems los nervios no emergen en ngulo recto por los agujeros intervertebrales sino en forma oblicua inferior.
46
Al corte transversal la mdula presenta una forma ms o menos cilndrica, ligeramente aplanada en el sentido nteroposterior y engrosada en los extremos; estos engrosamientos constituyen las intumescencias cervical y lumbar, zonas de emergencia de las races de los nervios raqudeos que inervan los miembros superiores e inferiores respectivamente.
47
MDULA ESPINAL
Metmera Morfofuncional
Haces de Fibras Nerviosas
Cisura Posterior Canal Ependimario o Central Sustancia Blanca
Sustancia Gris
Raz Nervio Sensitivo
Cisura Anterior
Ganglio Piamadre Aracnoides Duramadre Raz Nervio Motor
An cuando la mdula espinal presenta una configuracin bsica similar en sus diferentes segmentos, hay diferencias regionales entre las cantidades absolutas y relativas de sustancias gris y blanca, como tambin en la forma que presenta la sustancia gris. As, se puede observar que la sustancia blanca disminuye progresivamente desde los segmentos cervicales a los sacros, debido al menor nmero de fibras que van conteniendo los haces ascendentes y
48
descendentes a medida que dichas fibras van emergiendo hacia las diferentes partes del cuerpo que inervan, como ser los miembros superiores, los msculos torcicos y abdominales, los miembros inferiores, etc. Con fines analticos, se describir un corte transversal tpico de mdula espinal, tomando como ejemplo un segmento torcico. La sustancia gris, que est ubicada en la parte central y rodeando al canal central o conducto del epndimo, presenta una forma de H, que tiene dos cuernos o astas anteriores o ventrales y dos cuernos o astas posteriores o dorsales. Al cruzar el plano medio, alrededor del conducto del epndimo, la sustancia gris forma las comisuras anterior y posterior, segn se trate de las porciones ventral y dorsal respectivamente. El trmino comisura es aplicable no solamente a la mdula espinal, sino que se define como una estructura que conecta dos partes simtricas del sistema nervioso central. Como en la mdula espinal existe simetra axial, es vlido analizar una hemiseccin medular pues la misma configuracin se repite en ambas mitades. En cada mitad existe, entonces, un cuerno anterior y otro posterior; entre los segmentos C8 y L3 existe adems un cuerno lateral. Los cuernos o astas anteriores o ventrales tienen una funcin motora, pues contienen los somas de las motoneuronas cuyos axones forman parte de los nervios motores. Estos cuernos ventrales son gruesos, compactos y homogneos y poseen una base que va unida a la comisura gris anterior y a la regin intermedio-lateral, y una cabeza, que es ancha y algo irregular, de la cual emergen las fibras motoras. Tienen un mayor desarrollo a nivel de los engrosamientos medulares cervical y lumbo-sacro, debido probablemente al mayor nmero de somas de las motoneuronas que inervan las extremidades superiores e inferiores. Los cuernos posteriores o dorsales son funcionalmente sensitivos, puesto que reciben a los neuritos centrales o sus ramificaciones de las neuronas bipolares o pseudounipolares que traen los impulsos sensitivos. Estos cuernos poseen base, cuello y cabeza, la cual va cubierta, de adentro hacia afuera,
49
por la sustancia gelatinosa de Rolando, el estrato zonal de Waldeyer y la zona marginal de Lissauer. La regin intermedio-lateral de sustancia gris une los cuernos anterior y posterior de cada lado y en la regin torcica (en realidad entre C8 y L2 ) se expande formando el cuerno lateral que desempea una funcin vegetativa o visceral. La sustancia blanca rodea a la gris y est constituda fundamentalmente por haces de fibras mielnicas. En la parte ventral de la mdula hay una profunda fisura media, que no llega hasta la sustancia gris, por lo cual deja una comisura blanca anterior. En la zona medular dorsal hay un surco medio posterior o dorsal que llega hasta la sustancia gris. La emergencia de las races de los nervios espinales conforma los surcos laterales; hay un surco lateral ventral, demarcado por la salida de las races ventrales motoras, y un surco lateral dorsal, marcado por la entrada de las races dorsales sensitivas. Adems, en la regin medular cervical existe un surco intermedio posterior, situado entre los surcos medio posterior y lateral dorsal. La sustancia blanca de la mdula va quedando entonces dividida en funculos o cordones por los surcos y fisura media; as, hay un funculo anterior limitado por la fisura media y el surco lateral ventral; un funculo lateral, ubicado entre ambos surcos laterales, y un funculo posterior que limita con el surco medio posterior y el lateral dorsal; en la mdula cervical el funculo posterior va dividido, adems, por el surco intermedio posterior, en dos fascculos: uno interno o gracilis o de Goll y uno externo o cuneatus o cuneiforme o de Burdach. Metmera morfo-funcional . En el estudio segmentario de la mdula espinal, se considera como unidad estructural una porcin entre dos planos transversos que contiene los dos pares de nervios espinales sensitivos y motores; se le denomina metmera morfofuncional y es la base del reflejo espinal elemental.
50
Las fibras sensitivas se originan en receptores, que son telodendrones o bien clulas especializadas que establecen contacto con las terminaciones de los neuritos perifricos; stos llevan los impulsos hacia los somas neuronales que se encuentran en el ganglio espinal. Estas protoneuronas sensitivas son funcionalmente bipolares y sus neuritos centrales llevan los impulsos a la mdula espinal, a la cual penetran por la parte posterior, formando las races dorsales de los nervios espinales; pueden entrar directamente a los cuernos posteriores o bien a los funculos o cordones medulares posteriores. En dichos cuernos sinaptan generalmente con neuronas intercalares, internunciales o de asociacin; slo en pocos casos de reflejos monosinpticos se conectan directamente con las motoneuronas o neuronas eferentes cuyos cuerpos neuronales se encuentran en los cuernos anteriores; de aqu emergen las fibras que van a constituir la porcin motora de los nervios mixtos y que terminan en estructuras efectoras, que pueden ser msculos o glndulas. Por otra parte, la informacin que entra a la mdula por las fibras sensitivas, asciende hacia estructuras enceflicas; a su vez, desde zonas motoras y reguladoras del encfalo llegan impulsos a las neuronas motoras, ya sea directamente o a travs de neuronas intercalares. Otras conecciones de la metmera morfofuncional son intersegmentarias, regionales, intramedulares. Es as como el axn central de la protoneurona sensitiva, luego de penetrar a la mdula, se ramifica en porciones ascendentes, descendentes y colaterales para la sustancia gris homo y hterolateral; en esta forma se relacionan entre s las metmeras vecinas. Ncleos de la sustancia gris medular . Las neuronas intercalares de las vas sensitivo-motoras constituyen ncleos medulares en que la informacin recibida se puede modificar en cuanto a intensidad y a velocidad de transmisin. Se encuentran formando parte de la sustancia gris; los centros sensitivos estn en los cuernos posteriores, los motores en los cuernos anteriores y los vegetativos (vscerosensitivos y vscero-motores) estn agrupados alrededor del canal central y en los cuernos laterales.
51
De los ncleos sensitivos de los cuernos posteriores se pueden mencionar los siguientes: a.- sustancia gelatinosa (de Rolando); b.- ncleos de Bechterew, que son los centros propioceptivos para las extremidades, estn en las regiones cervical y sacra; c.- ncleo propio del cuerno posterior, ubicado en el cuello del cuerno y que da origen a los fascculos espinotalmicos y espino-tectales; d.- ncleo dorsal o columna de Clarke, ubicado en la base del cuerno y que da origen al tracto espino-cerebeloso dorsal. Los ncleos motores del cuerno anterior constituyen el origen de la inervacin motora del tronco, cuello, extremidades, diafragma. Entre estos ncleos cabe mencionar: 1.- ncleos nteromediales que proveen inervacin a los msculos perivertebrales; 2.- ncleos nterolaterales que envan fibras a los msculos parietales y de las extremidades. Los ncleos vegetativos controlan las funciones viscerales y se sitan en las astas laterales y en la sustancia gris periependimaria. Dermatomas. Se da esta denominacin a los territorios cutneos dependientes de los centros segmentarios sensitivos del cuerno posterior. Cada dermatoma est inervado por un nervio segmentario, que intercambia fibras que se anastomosan con nervios segmentarios supra y subyacentes para formar el nervio perifrico, de modo que ste recibe influjos de los segmentos vecinos. Por ello, los dermatomas no concuerdan con los territorios sensitivos de cada nervio. Relaciones medulares intersegmentarias.
52
Las metmeras medulares estn interconectadas entre s, pues los neuritos centrales de las neuronas sensitivas que han penetrado al cuerno posterior, dan ramas ascendentes y descendentes que a su vez emiten colaterales para la sustancia gris homo y hterolateral. Se constituyen as vas de asociacin intramedulares cuyos cuerpos celulares estn situados en la sustancia gris; los fascculos de asociacin son cortos, las clulas se denominan cordonales, preferentemente estn ubicadas en el cuerno posterior y conectan cuatro a cinco metmeras. Las races de los plexos (cervical, lumbosacro) y las vas de asociacin intersegmentaria dan origen a centros de la sustancia gris medular. En cortes longitudinales, los ncleos forman columnas. Las fibras de asociacin pueden cruzar a la mitad opuesta de la mdula (fibras hetermeras), pueden ser unilaterales (tautmeras) o bien mixtas (hecatmeras). Algunas forman fascculos bien definidos y otras establecen conecciones difusas. Entre los fascculos se pueden mencionar algunos. Ascendentes: - fascculo fundamental, que va por el cordn nterolateral; - zona cornucomisural, ubicada en el cordn posterior; Descendentes: - fascculo en vrgula, en las regiones medulares cervical y torcica rostral; - cintilla perifrica dorsal, en la zona torcica caudal; - centro oval, de la mdula lumbar; - fascculo triangular, de la mdula sacra y cono terminal. Existen tambin conecciones difusas, constitudas fundamentalmente por neuronas de tipo Golgi II, que le dan a la sustancia gris un aspecto granuloso, por lo cual se le denomina sustancia puntiforme molecular o neuropilema. Vas medulares.
53
Constituyen la sustancia blanca medular, que est organizada en cordones anteriores, laterales y posteriores. La informacin sensitiva penetra a la mdula espinal por la parte dorsal; la protoneurona sensitiva puede hacer contacto con neuronas intercalares y an a veces directamente con motoneuronas; esta informacin sensitiva asciende tambin hacia el encfalo, llegando a lugares precisos de destino. La informacin es procesada en centros enceflicos y enviada a los efectores somticos y viscerales por las vas medulares descendentes. Las vas ascendentes y descendentes se organizan en tractos, haces o fascculos; todos ellos son conjuntos de fibras, fundamentalmente mielnicas, pero los fascculos se caracterizan porque sus fibras tienen el mismo origen , curso y terminacin. Las vas nerviosas se denominan por lo general segn su origen y destino en este mismo orden. As, una va que va desde la corteza cerebral a la mdula espinal se denomina crtico-espinal; si lleva informacin desde la mdula espinal al bulbo raqudeo ser espino-bulbar. Otras veces se describe todo un circuito que comprende varias estructuras; as, una va cerebelo-rubro-talmica va desde el cerebelo al tlamo, haciendo estacin en el ncleo rojo; y una va crtico-cerebelocortical lleva informacin desde la corteza cerebral al cerebelo, el cual la devuelve procesada y en retroaccin, a la propia corteza cerebral. Vas ascendentes . Se describirn tres grupos que son los que llevan la mayor parte de la sensibilidad exteroceptiva o externa y propioceptiva, que se relaciona con la posicin del cuerpo. Se describen dos formas de sensibilidad; la sensibilidad protoptica, que se refiere a una sensibilidad burda o primitiva, como el dolor o las temperaturas extremas, y una sensibilidad epicrtica que es ms fina o discriminativa. Para cada va es conveniente conocer tanto su recorrido como la ubicacin de los diferentes haces o tractos en la mdula espinal. Estos tres grupos son los fascculos del cordn posterior medular, los espinocerebelosos y los espinotalmicos.
54
Fascculos grcil y cuneiforme. Se denominan tambin gracilis y cuneatus o de Goll y Burdach respectivamente. Llevan los impulsos de la propiocepcin consciente y del tacto discriminativo. La protoneurona sensitiva entra directamente a los cordones medulares posteriores homolaterales, da una rama descendente que abarca varias metmeras medulares y localmente da colaterales que sinaptan con motoneuronas del cuerno anterior. Una rama ascendente llega hasta los ncleos gracilis y cuneatus del bulbo raqudeo, donde la protoneurona propiamente tal hace la primera sinapsis; de estos ncleos se originan los lemniscos mediales cuyas fibras cruzan y se dirigen hacia el tlamo, especficamente al ncleo ventral psterolateral. Fibras tlamo-neocorticales llevan los impulsos hasta la corteza sensitiva primaria somtica general ubicada en el giro parietal ascendente. Las fibras bulbpetas no tienen otro relevo medular, pero en su trayecto van dando algunas colaterales. Vas espino-cerebelosas. Llevan los impulsos de la propiocepcin inconsciente; su protoneurona entra al cuerno posterior y va a establecer contacto con: - ncleo torcico (columna de Clarke); desde aqu la deuteroneurona (segunda neurona) alcanza el cordn lateral de su lado y asciende constituyendo el tracto espinocerebelar posterior o directo (de Flechsig), que entra al cerebelo por el pednculo cerebelar inferior; - ncleos de Bechterew, desde donde la deuteroneurona emite un axn que cruza por la comisura gris anterior y en el cordn lateral integra el tracto espinocerebelar anterior o ventral ( de Gowers), que desde el mesencfalo penetra al cerebelo por el pednculo cereberal superior. Tractos espinotalmicos. Constituyen dos vas sensitivas cruzadas, las del tacto burdo y presin y las del dolor y temperatura.
55
VAS ESPINOTALMICAS Tacto, presin, dolor y temperatura
Vas de tacto burdo y presin. El neurito central de la neurona pseudounipolar penetra a la zona de Lissauer del cuerno posterior, donde se divide en ramas ascendentes y descendentes intersegmentarias para cada dos o tres segmentos medulares, y va dando ramas que conectan con interneuronas cuyos axones pasan por la comisura blanca anterior hasta el funculo anterior hterolateral, de aqu ascienden formando el tracto espinotalmico anterior o ventral y llegan al ncleo ventral pstero-lateral del tlamo. Vas del dolor y la temperatura. La protoneurona se divide en la zona de Lissauer en cortas ramas ascendentes y descendentes que sinaptan con neuronas
56
del cuerno posterior, cuyos axones pasan al funculo lateral del lado opuesto. Estos conforman el tracto espinotalmico lateral que termina en el ncleo ventral pstero-lateral del tlamo. Slo no cruzan a nivel medular algunas fibras de la regin anogenital. Vas interoceptivas ascendentes. Adems de la informacin exteroceptiva y propioceptiva, por la mdula espinal asciende tambin informacin sensitiva relacionada con funciones vegetativas. La protoneurona proveniente de las vsceras termina en las astas laterales o en la sustancia gris periependimaria, en la cual las fibras de las neuronas simpticas pueden recorrer varios segmentos; las que ascienden al encfalo llegan hasta el tlamo. Los impulsos relacionados con dolores viscerales ascienden por los fascculos espino-talmicos laterales hasta el tlamo y de aqu se proyectan a la corteza cerebral sensitiva primaria; se produce por lo tanto una transferencia interoceptiva a las neuronas propioceptivas que ocurre en el ganglio espinal o en los cuernos posteriores, transferencia que determina que los dolores viscerales sean referidos a la piel.
57
CORTE TRANSVERSAL DE MEDULA Vas Ascendentes y Descendentes
Fascculo Gracilis Tracto Crticoespinal Lateral o cruzado
Fascculo Cuneiforme Tracto Espinocerebelar posterior o directo
Tracto Rubroespinal Tracto Espinotalmico lateral Tracto Retculoespinal lateral Tracto Vestbuloespinal medial Tracto Vestbuloespinal lateral Tracto Retculoespinal medial o anterior Tracto Tectoespinal
Tracto Espinocerebelar anterior o ventral Tracto Olivoespinal Tracto Espinotalmico anterior o ventral Tracto Crticoespinal ventral directo
Vas descendentes. Sus haces provienen de diversas regiones enceflicas y llevan impulsos motores. A nivel de la mdula espinal, sus axones pueden terminar en tres grupos funcionales; uno de ellos se relaciona con el control centrfugo de la sensibilidad del funcionamiento muscular (huso neuromuscular); otro controla el funcionamiento de las interneuronas y un tercero se conecta directamente con las motoneuronas del asta anterior medular. De todos ellos, realmente slo el ltimo, denominado la va final comn, se considera va motora propiamente tal.
58
Las vas motoras se han clasificado segn diversos aspectos, por lo general coincidentes entre s. Para su conformacin se puede considerar el lugar que las vas ocupan en la mdula espinal, la funcin que desempea cada va, los msculos esquelticos o estriados que inervan, su origen. Tomando en cuenta estos diferentes aspectos, la clasificacin ms moderna se centra en los lugares de terminacin de cada sistema de fibras; es as como en la topografa motora medular se describen fundamentalmente dos sistemas: un sistema lateral y un sistema medial. En trminos ms estrictos, las motoneuronas ubicadas ventromedialmente inervan los msculos axiales de cuello y espalda; a su vez, en el grupo lateral se distinguen motoneuronas ubicadas ms medialmente que inervan los msculos proximales de las extremidades, y motoneuronas de ubicacin ms lateral que inervan los msculos distales de las extremidades. La organizacin espacial de los ncleos motores a nivel medular tiene en cuenta dos reglas que conjugan aspectos anatmicos y funcionales. Ellas son una norma proximal - distal y otra que considera los sitemas de funcin muscular flexin extensin. La regla proximal - distal establece que las motoneuronas que inervan los msculos axiales del cuello y espalda, as como los centrales de las extremidades, a nivel de los hombros y pelvis, constituyen grupos ubicados en la zona ms medial de los cuernos medulares anteriores o ventrales; en cambio, las motoneuronas que inervan los msculos de las extremidades distales (manos y pies), tienen en la mdula espinal una ubicacin ms lateral dentro de las astas motoras. Segn la regla de flexin - extensin, las motoneuronas que inervan msculos extensores estn ubicadas en posicin ms ventral con respecto a las que inervan msculos flexores. Esta ubicacin tiene una repercusin funcional en el sentido que los msculos proximales, especialmente los extensores de las extremidades inferiores, participan fundamentalmente en la mantencin de postura y equilibrio del cuerpo; en cambio los msculos distales, especialmente los de las extremidades superiores, realizan ms bien los movimientos de manipulacin fina.
59
Las vas descendentes se pueden analizar segn su origen, que puede ser el tronco cerebral o las reas motoras de la corteza cerebral. El tronco cerebral modula la actividad de las motoneuronas e interneuronas a travs de tres sistemas: vas mediales, vas laterales y vas aminrgicas. Estas ltimas presentan una ramificacin difusa en la mdula espinal y modulan la excitabilidad de las neuronas espinales. De la corteza cerebral se originan los fascculos crtico-espinales, cuyas fibras directas y cruzadas pertenecen tanto al sistema medial como al lateral. Las principales vas se describirn segn su ubicacin topogrfica medular medial y lateral, pues al describir cada tracto se deduce claramente su origen.
VAS CORTICOESPINALES
MOTONEURONA
MDULA ESPINAL
Haz Crticoespinal Lateral
Funculo Lateral
Funculo Anterior
Haz Crticoespinal Ventral
Mdula Oblongada
Ncleo Oculo Motor (III)
Ncleo Trigeminal del puente (V)
Ncleo del Facial (VII)
Corteza Motora
Vas Crticoespinales
Ncleo Troclear (IV)
Ncleos del: Motor ocular externo (VI) Glosofarngeo (IX) Vago (X) Espinal (XI) Hipogloso (XII)
60
Vas del sistema lateral. En las motoneuronas medulares de ubicacin lateral terminan dos vas principales: el tracto rubroespinal y el tracto crtico - espinal lateral. El tracto rubro-espinal se origina en el ncleo rojo, ubicado en los pednculos cerebrales del mesencfalo; cruza a nivel del tegmento mesenceflico, atraviesa la protuberancia y la mdula oblongada para localizarse en la mdula espinal en el funculo lateral. El tracto crtico-espinal contiene aproximadamente un milln de axones; presenta dos divisiones, de las cuales la mayor, que es cruzada, pertenece al sistema lateral; sin embargo, su origen es comn, por lo cual se describir en conjunto. Un tercio de sus fibras se origina en la corteza motora primaria, ubicada en el giro frontal ascendente; otro tercio se origina en las reas premotoras, ubicadas en el lbulo frontal, por delante del rea motora primaria; el tercio restante se origina en la corteza sensitiva somtica, desde donde regula la transmisin de impulsos aferentes a las estructuras de control motor. Las fibras crtico-espinales descienden por la cpsula interna junto con fibras crtico-bulbares, pasando por el mesencfalo; a medida que descienden hacia el puente, se separan en manojos de fibras que pasan entre los ncleos pontinos, para luego reagruparse en el bulbo raqudeo. En la porcin ms rostral de la mdula oblongada, unos tres cuartos de las fibras cruzan, constituyendo la decusacin de las pirmides; las fibras cruzadas descienden por los cordones medulares laterales, constituyendo los tractos crtico-espinales laterales, que son los que pertenecen al sistema lateral. Las fibras directas, es decir, un cuarto de las que componan cada tracto crtico-espinal, descienden por los cordones anteriores conformando los haces crtico-espinales ventrales, que pertenecen al sistema medial.
61
El tracto crtico-espinal lateral se proyecta a los ncleos motores de la porcin lateral de las astas ventrales y a interneuronas de la zona intermedia. Hay algunas consideraciones que escapan a lo anteriormente explicitado. As, por ejemplo, el componente del tracto crtico-espinal que se origina en el rea sensitiva primaria, ubicada en el giro post-central, termina en las astas medulares dorsales y funciona modulando los impulsos aferentes que llegan a dichos cuernos. Otras fibras de las que se originan en el rea motora primaria del giro precentral, terminan en ncleos de nervios craneanos, con lo cual controlan la actividad motora de la cabeza y cara; entre ellas se pueden mencionar las que sinaptan con motoneuronas de los nervios trigmino, facial e hipogloso. Por otra parte, y a medida que descienden los componentes sensitivo y motor del tracto crtico-espinal, van dando colaterales a numerosos niveles del neuroeje, incluyendo los ncleos de la base, el tlamo y el tronco cerebral. Vas del sistema medial. Pertenecen a este sistema las vas que controlan los msculos axiales de cuello y espalda y de la musculatura proximal de las extremidades, es decir, las que participan en el movimiento de la extremidad como un todo. En trminos generales, la va medial se relaciona con el control de la posicin del cuerpo y extremidades, sobre la cual el sistema lateral puede organizar movimientos diferenciados ms finos, ms complejos. Los tractos que pertenecen a este sistema son fundamentalmente los siguientes: vestbulo-espinales medial y lateral, retculo-espinales medial y lateral, tecto-espinal y crtico-espinal anterior o ventral, ya descrito. Los tractos vestbulo-espinales se originan en los ncleos vestibulares del puente y transmiten informacin desde el aparato vestibular del odo interno, por lo cual estas vas se relacionan fundamentalmente con el equilibrio corporal. Ambos son directos y en la mdula espinal se ubican en los cordones anteriores.
62
Los tractos retculo-espinales se originan en la formacin reticular de estructuras del tronco cerebral y llevan impulsos que modulan movimientos tanto voluntarios como reflejos, o bien coordinan funciones vegetativas, como vasomotora,respiracin, sudoracin, etc. Ejercen su accin a nivel de motoneuronas o de interneuronas espinales. El haz retculo-espinal medial o anterior se origina en la formacin reticular pontina y ejerce una accin facilitadora sobre las motoneuronas del asta anterior medular, influyendo en parte sobre las motoneuronas gama. En la mdula se ubica en el cordn anterior. El haz retculo-espinal lateral se origina en la formacin reticular de la mdula oblongada y es de accin inhibidora sobre las motoneuronas espinales. En la mdula se ubica en los cordones laterales. El haz tecto-espinal se origina en los colculos superiores del tectum mesenceflico y cruza antes de descender por los cordones medulares anteriores. Llega hasta los segmentos cervicales rostrales e interviene en las acciones reflejas de los ojos, la cabeza y los miembros superiores en respuesta a estmulos luminosos; puede ser controlado desde la corteza cerebral mediante una va crtico-tecto-espinal. Vas vegetativas descendentes. A nivel del tronco cerebral existen vas descendentes que llevan impulsos vegetativos desde el hipotlamo hacia centros vegetativos del mesencfalo, protuberancia y mdula oblongada. En la mdula espinal continan como fibras dispersas en el fascculo fundamental que termina en los cuernos laterales, coordinando as los centros viscerales enceflicos con los medulares.; finalmente hacen sinapsis con clulas motoras de los cuernos anteriores. Hemisferios Cerebrales. El encfalo es la parte del sistema nervioso contenido en la cavidad craneana. Su peso es variable, se considera que es un 2 a 3 % del peso corporal; sin embargo, no es conveniente aventurar una cifra, puesto que adems el peso del encfalo es
63
funcin de la edad, aumentando hasta los 18-30 aos, tras los cuales hay una disminucin gradual. Se podra dar una cifra de 1400 gramos como promedio para adultos, y luego es necesario considerar variaciones que derivan de edad y sexo.
Modelo de la posicin del encfalo en la caja craneana Vista lateral
Sus funciones, as como sus estructuras, son diversas y complejas; en l tienen su base los mecanismos de regulaciones somticas y viscerales; otro grupo de funciones se relaciona con los estados de conciencia, sueo y vigilia, memoria, aprendizaje, emociones, motivaciones, es decir, con toda la gama de funciones psquicas. Por constituir la sede de dos funciones como inteligencia y voluntad, es tambin el origen de la conciencia y conducta morales del individuo, lo que podramos calificar como el aspecto espiritual de la integracin
64
cuerpo - mente - espritu que en conjunto constituye el ser humano; ste, adems, por estar ubicado en un ambiente social, desarrolla otras caractersticas que derivan de su vida de relacin. El encfalo se puede describir desde varios puntos de vista, que incluyen su aspecto exterior, las estructuras componentes, sus funciones, sus interrelaciones, etc. En trminos generales, se distinguen en el encfalo cuatro grandes grupos estructurales: A.- tronco cerebral B.- cerebelo C.- diencfalo D.- hemisferios cerebrales, que constituyen comnmente se denomina cerebro.
lo
que
El tronco cerebral est constitudo por la mdula oblongada, el puente o protuberancia anular y el mesencfalo. Algunos autores describen separadamente el istmo como la parte que atraviesa el foramen oval de Pacchioni y une el cerebelo con el tronco cerebral, es decir, conecta los pednculos cerebrales con los colculos o tubrculos cuadrigminos y los pednculos cerebelares superiores. El diencfalo consta de varias estructuras, como el tlamo, el hipotlamo, el epitlamo, el subtlamo y la hipfisis. Los hemisferios cerebrales contienen a la corteza cerebral y a los ncleos de la base. Aspecto exterior de los hemisferios cerebrales. En los hemisferios cerebrales, la sustancia gris est situada en la superficie, formando la corteza cerebral y rodeando a la sustancia blanca central. Un conjunto de masas grises localizadas profundamente constituyen los ncleos de la base. La corteza cerebral presenta en su superficie numerosos surcos y giros o circunvoluciones. Los surcos constituyen
65
hendiduras o depresiones que si son profundas se denominan cisuras; los giros son la parte ms prominente de los repliegues; ambos tipos de accidentes contribuyen a aumentar el rea de la corteza cerebral. Los hemisferios cerebrales son pareados y estn separados por la fisura longitudinal cerebral o gran cisura interhemisfrica, que es completa en las regiones frontal y occipital, pero en el centro llega slo hasta el cuerpo calloso, que es un conjunto de fibras que constituyen la comisura interhemisfrica o cuerpo calloso. Cada hemisferio est compuesto por lbulos, que son regiones cerebrales especficas y reciben su nombre del hueso del crneo que los protege; as, existen cuatro pares de lbulos que son los frontales, los parietales, los temporales y los occipitales.
66
HUESOS DEL CRNEO
PARIETAL
FRONTAL
TEMPORAL
OCCIPITAL
Existen adems dos estructuras que funcionalmente se consideran lbulos, son los lbulos insular y lmbico, el primero de los cuales est en la profundidad de la fosa insular y el lbulo lmbico comprende diversas estructuras ms bien dispersas.
67
En la descripcin externa de los hemisferios cerebrales se consideran tres caras: una superior-lateral, una basal o inferior y otra medial o interna. Cara superior - lateral. Presenta dos surcos profundos o cisuras que se denominan surco o cisura central (de Rolando) y surco o cisura lateral (de Silvio). El surco central constituye el lmite de los lbulos frontal y parietal; se extiende desde el borde superior del hemisferio hacia abajo y adelante por la cara externa, en direccin hacia el surco lateral; por arriba no se prolonga hacia la cara interna del hemisferio. El surco central se utiliza como referencia para describir estructuras vecinas, denominndolas pre o post centrales, segn estn por delante de l (en el lbulo frontal) o por detrs de dicho surco (en el lbulo parietal). El surco lateral separa a los lbulos frontal y temporal y parcialmente a los lbulos parietal y temporal. Como este surco no divide totalmente la cara lateral o externa del hemisferio, una zona llamada lobulillo del pliegue curvo une los tres lbulos, parietal, temporal y occipital. Las porciones de estos tres lbulos adyacentes al surco central y que estn sobre la porcin insular se denominan operculares.
68
CARA LATERAL IZQUIERDA Lbulos
Lbulo Frontal
Lbulo Parietal
Lbulo frontal.
Lbulo Occipital
Lbulo Temporal
Lbulo frontal. Es el mayor de los lbulos cerebrales y su rea constituye aproximadamente la tercera parte de la superficie del hemisferio. Sus lmites son los surcos central y lateral y en el se destacan cuatro giros principales: tres horizontales (superior, medio e inferior) y uno ascendente que es precentral.; ste ltimo constituye el rea motora primaria y por delante de ella est el rea premotora. El giro frontal inferior est dividido por dos surcos cortos en tres porciones: orbital, triangular y opercular o pie; estas dos ltimas, en el hemisferio dominante constituyen el rea del lenguaje de Broca. Lbulo parietal. Tiene como lmites al perpendicular externo que surco central constituye la y al surco prolongacin
69
imaginaria, en la cara lateral externa, del surco lateral interno o cisura parieto-occipital. El lbulo parietal tiene tres giros principales: uno ascendente post central y dos giros transversos, uno superior y otro inferior; estos dos ltimos van separados por el surco intraparietal. El giro parietal ascendente y el margen posterior y superior del surco central constituyen el rea somestsica primaria. El giro parietal inferior es un rea de asociacin sensorial y contiene a su vez dos giros, el supramarginal y el angular. Lbulo temporal. Su lmite superior es el surco lateral y a partir de l se pueden describir tres giros temporales en la cara lateral del hemisferio: son los giros superior, medio e inferior. En el borde inferior interno del surco lateral estn los giros temporales transversos, de los cuales el anterior es el giro de Heschl que en el ser humano constituye la corteza auditiva primaria. Parte de los giros temporales se contina en la cara inferior de los hemisferios cerebrales. Lbulo occipital. Es pequeo y est apoyado sobre la tienda del cerebelo; su lmite anterior es la cisura perpendicular externa ya descrita; en la cara externa se observan tres giros occipitales, primero, segundo y tercero. Lbulo de la nsula. Se encuentra en la profundidad del surco lateral y est cubierto por las regiones operculares frontal, parietal y temporal; posee cinco giros principales denominados insulares. Cara medial o interna.
70
Se observa al efectuar un corte mesosagital del encfalo. En el centro se observa el cuerpo calloso, hasta el cual llega la fisura longitudinal del cerebro. Uno de los surcos de la cara medial es el surco del cngulo, que separa la cara interna de cada hemisferio en dos pisos o zonas; en la parte superior est el giro frontal interno, y por debajo, el giro del cuerpo calloso. En esta cara, el lbulo occipital est dividido por el surco o cisura calcarina en la cua (sexto giro occipital) y el giro lingual. Por debajo del surco calcarino estn el cuarto y quinto giro occipital y parte del cuarto giro temporal. A ambos lados de la cisura calcarina est la corteza visual primaria, o estriada o calcarina. El cuerpo calloso es la gran comisura cerebral o interhemisfrica, compuesto por fibras mielnicas las cuales se despliegan como abanico hacia toda la corteza cerebral. Debido a que conecta ambos hemisferios cerebrales, desempea un papel importante en las asociaciones interhemisfricas de las discriminaciones adquiridas, la experiencia sensorial y la memoria. Los giros ascendentes frontal y parietal de la cara externa pasan a la cara medial formando el lobulillo paracentral, atravesado por el surco central.
71
CORTE SAGITAL DEL ENCFALO (Flujo del lquido cfalo raqudeo)
Lugar de Reabsorcin (granulaciones Menngeas) Lugar de produccin (Plexos Corodeos)
Crneo Duramadre Seno Venoso Cuerpo Calloso
Ventrculo Lateral
Tercer Ventrculo Acueducto de Silvio
Cerebelo
Cuarto Ventrculo
Lquido Cefalorraqudeo, su produccin y circulacin
Lbulo lmbico.
72
Est constitudo por los giros subcalloso, del cngulo, parahipocampal o quinto giro temporal y dentado, as como por la formacin del hipocampo. El giro parahipocampal se contina con el giro del cngulo, y hacia adelante forma el gancho o uncus del hipocampo.
CARA BASAL MODELO DEL ENCFALO
L. Frontal
Bulbo olfativo Cintilla olfativa L. Temporal Quiasma ptico
Puente
Origen Aparente de Nervios Craneanos
Cerebelo Hemisferio Izquierdo
Cara basal hemisferios cerebrales. En cada hemisferio se pueden observar dos partes, separadas por el surco lateral: - una porcin anterior o lobulillo orbitario, que es prolongacin del lbulo frontal; - una porcin posterior, de mayor tamao, que corresponde a parte de los lbulos temporal y occipital; la porcin anterior del lbulo temporal va en la fosa craneal media y la ms posterior descansa en la tienda del cerebelo.
73
En el lobulillo orbitario estn las estructuras olfatorias; sobre el surco olfatorio estn la cintilla y el bulbo olfatorio; por dentro del surco olfatorio est el giro orbital interno. En su extremo posterior, la cintilla olfatoria se divide en estras, luego se contina con el trgono y la sustancia perforada anterior.
CARA BASAL ENCFALO
(AMPLIACIN QUIASMA)
Quiasma ptico
Vasos Sanguneos (color gris)
74
En la regin occpito-temporal se puede observar: - el giro lingual, ubicado posteriormente; - un gran giro occpito-temporal, que comprende el tercer giro temporal y los giros cuarto y quinto tanto temporal como occipital. El quinto giro temporal es el parahipocampal, que se une al del cngulo formndose as el gran giro lmbico de Broca. Tronco Cerebral. Es la porcin que se extiende desde la parte ms rostral de la mdula espinal hasta el diencfalo, en la base del cerebro. Se distinguen en el tronco tres estructuras bien definidas: a.- mdula oblongada o bulbo raqudeo; b.- puente o protuberancia anular y c.- mesencfalo, que posee a su vez dos estructuras diferentes: por delante estn los pednculos cerebrales y en la regin dorsal se encuentra el tectum o lmina cuadrigmina. Para su estudio se puede considerar su aspecto exterior, as como cortes transversales a diferentes niveles que permiten observar ncleos y cordones de fibras. En cuanto al aspecto exterior del tronco cerebral, en la cara anterior o ventral se pueden reconocer fcilmente sus tres componentes; el puente (de Varolio) se reconoce por la direccin transversal de sus fibras y porque va claramente separado de la mdula oblongada por el surco bulbo-pontino y del mesencfalo por el surco ponto-peduncular. En esta cara se encuentra la emergencia u origen aparente de la mayor parte de los nervios craneanos.
75
TRONCO CEREBRAL CARA VENTRAL
Quiasma Optico
Cuerpos Mamilares Cerebelo
Cintillas pticas
Nervios craneanos Origen aparente
Puente Olivas Bulbares
Bulbo
La cara dorsal, in situ est cubierta parcialmente por el cerebelo, el cual debe retirarse para visualizar el tronco completo por su parte posterior; en esta forma se hacen visibles los pednculos cerebelares o cerebelosos, que unen al cerebelo con las tres porciones del tronco cerebral. A nivel de la mdula oblongada caudal se observa la continuacin de los funculos medulares posteriores y los surcos correspondientes; luego, la fisura media posterior se abre en el cuarto ventrculo, cuyo piso est constitudo por la cara dorsal del puente y parte de la mdula oblongada; a nivel del mesencfalo, el cuarto ventrculo confluye en el acueducto cerebral. Por otra parte, en
76
la cara dorsal del mesencfalo se encuentra el tectum o techo o lmina cuadrigmina, donde son visibles los dos pares de colculos o tubrculos cuadrigminos, dos superiores y dos inferiores.
TRONCO CEREBRAL CARA DORSAL
Tlamo Tercer ventrculo
Cerebelo
Colculos cuadrigminos
Pednculos cerebelosos
Cuarto ventrculo Bulbo
Mdula
En el tronco cerebral, pero considerando para el mesencfalo los pednculos cerebrales, la porcin anterior o ventral se denomina basilar o pie, en tanto que la porcin posterior o dorsal es el tegmento. En cuanto a su constitucin interna, presenta numerosos ncleos de sustancia gris, a la vez que lo atraviesan cordones de fibras nerviosas (sustancia blanca). La sustancia gris de la mdula espinal se dispersa paulatinamente en la mdula oblongada, especialmente debido a la decusacin de las pirmides y el entrecruzamiento de las
77
fibras arciformes internas. Van quedando, entonces, neuronas distribudas en una verdadera red de fibras, lo que constituye la sustancia o formacin reticular, que se extiende por todo el tronco cerebral y el tlamo; en algunas zonas, la sustancia reticular forma ncleos bien definidos. El tronco cerebral es lugar de trnsito de las grandes vas ascendentes (desde la mdula espinal) y descendentes (desde la corteza cerebral y el diencfalo), las cuales van enviando colaterales que conectan con estructuras del tronco cerebral. Pero adems ste posee vas longitudinales propias entre las cuales se pueden mencionar: - la cintilla longitudinal posterior, que va ubicada en la cara ventral del tronco cerebral y lleva diversas aferencias a los ncleos motores de los bulbos o globos oculares y a las neuronas espinales que participan en los movimientos culo-cefalgiros; conecta tambin los centros del equilibrio con los ncleos motores oculares y participa en los movimientos de la expresin facial; - el fascculo longitudinal dorsal, que conecta al hipotlamo con los ncleos vegetativos de pares craneanos, como glosofarngeo y vago; - el fascculo mamilo-tegmental, que participa en los reflejos olfatorios, conectando al hipotlamo con ncleos del tegmento mesenceflico; - el tracto central del tegmento, que lleva informacin ascendente y descendente; las fibras ascendentes llegan a la formacin reticular del tlamo, el cual a su vez establece sinapsis con vas activadoras del hipotlamo y corteza cerebral; las fibras descendentes se originan en el sistema reticular del tronco cerebral y ncleos basales caudado y lentiforme, para terminar en la oliva bulbar donde establecen sinapsis con fibras que van por el pednculo cerebelar inferior al hemisferio cerebeloso contralateral; de aqu sale informacin hacia el ncleo rojo y el tlamo por los pednculos cerebelares superiores. Mdula oblongada o bulbo raqudeo.
78
Es la estructura del tronco cerebral que se extiende desde la emergencia de las races del primer nervio raqudeo o espinal hasta el surco bulbo-pontino; tiene una longitud aproximada de 3 cm. En su exterior, y especialmente en el extremo caudal, presenta similitud con la mdula espinal, ensanchndose hacia el extremo rostral. En la cara ventral se observan los cordones anteriores, constitudos por los fascculos crtico-espinales; estos cordones son ms prominentes que los funculos de la mdula espinal, y reciben el nombre de pirmides. La mayor parte de las fibras de los fascculos crtico-espinales cruzan al lado opuesto lo que constituye la decusacin de las pirmides. En la cara dorsal est la fisura media posterior, cuyos bordes o labios se separan en la parte superior y conforman los bordes laterales inferiores del cuarto ventrculo; ulteriormente se orientan hacia el cerebelo formando el par de pednculos cerebelares inferiores. En las caras laterales hacen prominencia las olivas bulbares, que corresponden a la eminencia que a cada lado hace el ncleo olivar inferior. En el bulbo raqudeo emergen races de nervios craneanos; esta salida se denomina origen aparente del nervio craneal correspondiente. Estructura interna de la mdula oblongada. Los elementos que la componen pueden ser exclusivos de la mdula oblongada, o ser compartidos con las otras estructuras del tronco cerebral, o bien constituir vas de coneccin entre la mdula espinal y partes superiores del encfalo. Entre los haces de fibras que cruzan el tronco del encfalo, y por lo tanto la mdula oblongada, estn los que conforman las vas ascendentes y descendentes de la mdula espinal descritos en su oportunidad. Cabe recordar que entre las vas descendentes estn los tractos crtico-espinales; algunas de
79
sus fibras son crtico-bulbares, las que despus de cruzar terminan en ncleos de nervios craneanos. En cuanto a las vas ascendentes, hay algunos elementos relacionados especialmente con el bulbo raqudeo. As, por ejemplo, en l se encuentran los ncleos gracilis y cuneatus, ubicados en la parte medio-dorsal de la mdula oblongada, en los cuales terminan los fascculos gracilis y cuneatus y se originan los lemniscos mediales; stos estn conformados por fibras arciformes internas que cruzan al lado opuesto y llegan hasta los ncleos ventrales pstero-laterales del tlamo. El cruzamiento de los lemniscos mediales es la razn anatmica por la cual parte de la representacin sensorial de una mitad del cuerpo est en la corteza cerebral contralateral; otras vas cruzadas tambin relacionadas con este fenmeno son los fascculos espino-talmicos y el haz trigeminal, que lleva los impulsos relacionados con la sensibilidad facial. Otras neuronas de los ncleos cuneatus dan origen a las fibras arciformes externas dorsales que se dirigen al cerebelo por el pednculo cerebelar inferior ipsilateral (del mismo lado); se denominan fibras cneo-cerebelares directas y retransmiten impulsos de la propiocepcin desde los husos neuromusculares, los rganos tendinosos de Golgi y aferencias cutneas. Tambin algunas clulas de los ncleos gracilis y cuneatus envan fibras al ncleo olivar accesorio dorsal, constituyendo un enlace en las vas olivo-cerebelo-medulares en relacin con aferencias de reflejos flexores de las extremidades. Ncleos olivares. Existen dos grupos, uno en la mdula oblongada y otro en el puente. Por razones de ubicacin y de importancia, los de la mdula oblongada reciben los nombres de ncleos olivares inferiores principal y accesorios. Les llegan aferencias desde el ncleo rojo, formacin reticular, subtlamo, corteza cerebral, mdula espinal y sustancia gris periacueductal; las fibras aferentes van por el tracto tegmental central. A su vez, de los ncleos olivares van eferencias al cerebelo a travs de los pednculos cerebelares inferiores homolateral y del lado opuesto.
80
Formacin reticular. Recibe su nombre del hecho que las fibras que la conforman van entrecruzadas, presentando aspecto de red; entre ellas se encuentran somas neuronales que en algunos casos llegan a constituir ncleos definidos. Es filogenticamente la parte ms antigua del tronco cerebral. Entre las aferencias a la formacin reticular del bulbo cabe destacar: a.- tracto espinorreticular; algunas de sus fibras son colaterales de las fibras espino- talmicas; b.- fibras colaterales de vas sensoriales de los nervios craneanos, como auditivas, vestibulares,trigminas y viscerales; c.- fibras crtico-reticulares, provenientes de las reas sensorio-motoras de la corteza cerebral; d.- fibras cerebelosas. A su vez, la sustancia reticular se conecta por fibras eferentes con: a.- ncleos talmicos, mediante fibras del tracto central del tegmento; este sistema participa en el mecanismo del despertar; b.- mdula espinal, a travs del tracto retculo-espinal, que ejerce una influencia inhibitoria a nivel espinal. Entre los grupos nucleares de la formacin reticular se puede mencionar el ncleo arqueado, que es el relevo de una va crtico-cerebelar, y el rea postrema, que es un quimiorreceptor emtico (del vmito), sensible a la apomorfina y glucsidos digitlicos.
81
Pednculo cerebelar inferior. Es un fascculo de fibras que salen de la porcin psterolateral de la mdula oblongada y limita caudal y lateralmente al cuarto ventrculo. Conecta diversas estructuras con el cerebelo; las fibras que lleva corresponden a parte de los tractos cerebelares posteriores, a fibras arciformes que provienen de los ncleos cuneiforme y arqueado, a eferencias de los ncleos reticulares y a otras que conectan el complejo olivar con el cerebelo. Ncleos de nervios craneanos. En la mdula oblongada se encuentra el origen real de algunos de ellos. Ncleo del trigmino (V par craneano). Existen porciones nucleares de este nervio en las tres partes del tronco cerebral. Esta parte ms caudal corresponde a la raz descendente y ncleo de la raz descendente o espinal del V par que se extiende desde el nivel de la raz trigmina en el puente hasta C2. Las fibras aferentes provienen del ganglio semilunar, en el cual se origina el haz trigmino-espinal, cuyas fibras penetran en la parte rostral del puente y llegan en la mdula espinal hasta C2. Algunas fibras del haz terminan en el ncleo solitario, otras son fibras aferentes somticas generales descendentes de los nervios vago, glosofarngeo y facial. Ncleos del vago (X par craneano). En la mdula oblongada se encuentra el ncleo motor dorsal del vago, que da origen a las fibras preganglionares, las cuales en los ganglios parasimpticos sinaptan con las fibras que inervan la musculatura lisa y las glndulas que estn bajo control de este sistema neurovegetativo. Existe tambin otro ncleo bulbar, denominado ncleo ambiguo, que es origen de fibras motoras de los nervios vago (X par), glosofarngeo (IX par) y espinal (XI par); por su ubicacin y por participar en el origen de fibras vagales, se le
82
denomina tambin ncleo motor ventral del vago. Funcionalmente se relaciona con la fonacin y la deglucin. Ncleo del hipogloso (XII par craneano). Se extiende por toda la mdula oblongada y su funcin es motora para los msculos de la lengua. Ncleo salivatorio inferior. Se encuentra ubicado en la regin bulbo-pontina y sus clulas dan origen a ramas del glosofarngeo que inervan a las partidas y forman parte del plexo timpnico. Ncleo del tracto solitario. El tracto solitario est constitudo por fibras sensitivas de los nervios facial, glosofarngeo y vago, las cuales terminan en las neuronas del ncleo del tracto solitario. Su parte superior se denomina ncleo gustativo, pues recibe aferencias desde las papilas gustativas por fibras de los pares craneanos VII (facial) y IX (glosofarngeo). Puente. En l se distinguen con bastante precisin las porciones basilar y tegmental. La parte ventral o basilar est constituda por fibras de ubicacin longitudinal que corresponden a tractos ascendentes y descendentes, y fibras que van en sentido transversal, formando una especie de puente bajo el cual van las fibras longitudinales. Entre los haces de fibras se encuentran ncleos denominados pnticos. Las vas medulares ascendentes y descendentes atraviesan longitudinalmente el puente, pero algunas tienen un destino local, como es el caso de fibras crtico-pnticas, que vienen en los tractos crtico-espinales pero sinaptan en ncleos pnticos. En cuanto a las fibras transversas, que son las que forman la parte ventral del puente, se originan en los ncleos pnticos, la mayora son cruzadas y, constituyendo los pednculos cerebelares medios, unen al puente con el cerebelo. A su vez, a
83
los ncleos pnticos han llegado fibras corticales, con lo cual ellos forman parte de un circuito crtico-pntico-cerebelar, que participa en la regulacin motora. La porcin tegmental es en gran parte la continuacin rostral de la formacin reticular de la mdula oblongada. Posee un buen acmulo de masas nucleares y tambin haces de fibras. Entre stos cabe mencionar: el lemnisco medial, continuacin de los fascculos gracil y cuneiforme, y que sinapta en el tlamo; tambin lleva fibras cruzadas del fascculo trigmino-talmico; el fascculo longitudinal medio, que establece conecciones entre los ncleos motores oculares, los relacionados con la motilidad de la cabeza y los ncleos vestibulares; tractos espino-cerebelares anteriores y espino-talmicos, relacionados con la funcin motora los primeros y con la sensibilidad protoptica los segundos, van en la parte lateral del tegmento. En cuanto a los ncleos del tegmento pontino, hay algunos de la formacin reticular y otros relacionados con los nervios craneanos. La formacin reticular del puente est ubicada en la porcin tegmental central y posee dos ncleos grandes, el caudalis y el oralis, adems del ncleo caudal del tegmento y el ncleo central superior. Ncleos de nervios craneanos. Como se expres anteriormente, existen ncleos del nervio trigmino en las tres partes del tronco cerebral; en el tegmento pontino estn los ncleos motor y sensitivo principal del trigmino. Una zona prominente, el colculo facial, contiene al ncleo del motor ocular externo (VI par craneano), y en la zona ventrolateral inferior del tegmento est el ncleo motor del facial. Otra prominencia, el colculo acstico, contiene los ncleos cocleares.
84
Los ncleos vestibulares del tegmento pontino reciben aferencias del nervio vestibular, aunque muchas de sus fibras van directamente al cerebelo por el pednculo cerebelar inferior. Las eferencias de los ncleos vestibulares forman el tracto vestbulo-cerebelar y parte del fascculo longitudinal medial. Finalmente se puede mencionar el complejo olivar superior, a donde llegan aferencias de los ncleos cocleares y van eferencias al ncleo del motor ocular externo. Istmo del rombencfalo. Suele denominarse as a la porcin inmediatamente caudal al mesencfalo y donde se encuentran algunas estructuras como: - tracto y ncleo mesenceflico del trigmino; - locus coeruleus (lugar azul), de probable participacin en la regulacin respiratoria, en el sueo paradjico, en los estados de angustia y en los ataques de pnico; Por el istmo pasa el pednculo cerebelar superior, que es el sistema eferente ms importante del cerebelo. Mesencfalo. Es la porcin ms rostral del tronco cerebral y en l se pueden distinguir dos partes bien definidas: - tectum o lmina cuadrigmina, de ubicacin dorsal; - pednculos cerebrales o porcin ventral; en ellos hay una parte basilar o pie y un tegmentum, separados ambos por la sustancia nigra. A nivel de la cara dorsal del mesencfalo pasa el acueducto cerebral, que comunica a los ventrculos tercero y cuarto. Los pednculos cerebrales contienen fibras aferentes del lemnisco medial y de los tractos espino-talmicos, que pasan hacia el tlamo por el tegmento mesenceflico. En cambio la
85
mayora de las fibras descendentes van por el pie de los pednculos y son fundamentalmente eferencias de la corteza cerebral hacia la parte inferior del tronco cerebral y mdula espinal; ellos son los tractos fronto-pntico, tmporo-pntico, crtico-bulbares y crtico-espinales. El fascculo longitudinal dorsal, que lleva impulsos viscerales eferentes desde el hipotlamo hacia ncleos reticulares y vegetativos del tronco cerebral, pasa por el tegmento, cercano a la sustancia gris periacueductal. En el tegmento mesenceflico se encuentran algunas estructuras caractersticas de significacin funcional importante, como son la sustancia nigra y el ncleo rojo. La sustancia nigra est en el lmite con el pie de los pednculos cerebrales; debe su nombre al pigmento melanina que poseen sus neuronas. Tiene una porcin compacta, con mayor densidad celular, que contiene una concentracin alta de dopamina, que es el origen de la dopamina que utilizan como neurotransmisor los cuerpos estriados caudado y putamen. A la sustancia nigra se le asocian los trastornos metablicos y funcionales de la enfermedad de Parkinson. El principal sistema aferente est constitudo por las fibras estrio-nigras, que probablemente transportan GABA (cido gama-amino-butrico); existen tambin fibras crtico-nigras y otras provenientes de ncleos subtalmicos. En cuanto a las eferencias, algunas van a los cuerpos estriados, son las fibras nigro-estriadas y son las que transportan la dopamina; otras eferencias van al tlamo. El ncleo rojo es parte de la formacin reticular del tegmento. Recibe impulsos de los ncleos cerebelares a travs de los pednculos cerebelares superiores, de la corteza cerebral, del subtlamo y del globo plido. A su vez el ncleo rojo enva eferencias al cerebelo, tlamo, ncleo del facial, mdula oblongada y mdula espinal. Hay un sindrome denominado de Benedikt, que se produce por lesin del tegmento mesenceflico y del ncleo rojo; se producen trastornos oculares ipsilaterales y trastornos
86
motores contralaterales, como temblor muscular y ataxia, probablemente por lesin de las fibras cruzadas del pednculo cerebelar superior correspondiente. Los pednculos cerebelares superiores constituyen la coneccin entre el cerebelo y el mesencfalo, especficamente con el ncleo rojo. Las fibras son cruzadas y muchas de ellas pasan directamente, sin sinaptar, al tlamo y a diversos ncleos reticulares del tronco cerebral. Ncleos de nervios craneanos. En el mesencfalo se encuentran los siguientes: - ncleo del nervio troclear (IV par craneano), que inerva al msculo oblicuo superior del globo ocular; - ncleo del motor ocular comn (III par craneano); - ncleo de Edinger - Westphal, de donde salen las fibras que controlan al msculo ciliar y al msculo constrictor de la pupila; - ncleo del trigmino: la porcin mesenceflica de este ncleo recibe aferencias propioceptivas de los msculos masticatorios y de la articulacin tmporo-mandibular, y se conecta con el ncleo motor del V par, con lo cual se establece el arco reflejo de la masticacin. Por va del lemnisco trigeminal, este ncleo enva al tlamo los impulsos sensitivos del territorio ceflico que inerva el trigmino. Tectum o lmina cuadrigmina. Es la porcin dorsal del mesencfalo, se encuentra por detrs del acueducto cerebral y sus elementos ms caractersticos lo constituyen los colculos o tubrculos cuadrigminos. Entre el tectum y el diencfalo est la zona pre-tectal, que contiene al ncleo pre-tectal, el cual se relaciona con fibras del tracto ptico ipsilateral y con los ncleos de Edinger - Westphal.
87
Por el rea pre-tectal pasa el pednculo mamilar, que lleva fibras aferentes somticas y viscerales al hipotlamo; a su vez, el fascculo longitudinal dorsal lleva eferencias hipotalmicas al mesencfalo. Los colculos cuadrigminos son cuatro eminencias que se clasifican en un par superior y otro inferior. Los superiores forman la mitad rostral del tectum y son estaciones primarias de enlace con el sistema visual. Reciben aferencias desde: - retina, a travs de fibras de la cintilla ptica; - corteza cerebral; - colculos inferiores; - cuerpos geniculados laterales del tlamo; - otras regiones del tronco cerebral, por va de los lemniscos medio y trigeminal. A su vez, los colculos cuadrigminos superiores envan eferencias por los tractos: tecto-talmicos; tecto-reticulares; tecto-pontinos; tecto-bulbares; tecto-espinales.
Los colculos inferiores se encuentran en la porcin caudal del tectum mesenceflico y participan en la funcin auditiva. Se conectan con otras estructuras enceflicas, recibiendo fibras del lemnisco lateral, colculo del lado opuesto y cuerpo geniculado medial del tlamo. Las fibras eferentes van al colculo inferior del lado opuesto, al cuerpo geniculado medio, al colculo superior y a los ncleos de enlace inferiores del sistema auditivo. Comisura posterior.
88
Es un fascculo de fibras provenientes, a lo menos, de los ncleos pre-tectales, intersticial y de la comisura posterior. Este fascculo est en la zona de transicin entre el mesencfalo y el diencfalo, ah donde el acueducto cerebral se ensancha en el tercer ventrculo. La formacin reticular del tronco cerebral. Se ubica en el tegmento del tronco cerebral, y como se expres anteriormente, est constituda por fibras que, en lugar de formar haces definidos, van entrecruzadas, dispersas, lo que le da el aspecto de red; entre las fibras hay somas neuronales que pueden estar agrupadas en ncleos. Esta disposicin de las fibras y el gran nmero de sinapsis que se originan entre ellas, da a la formacin reticular su carcter de actividad difusa; en cambio, la disposicin de somas neuronales formando ncleos, le permite controlar tambin algunas actividades especficas. Existen algunas estructuras que estn en ntima asociacin con la formacin reticular, como es el caso del ncleo rojo, la sustancia nigra y la oliva bulbar. Cuando se considera a la formacin reticular con las estructuras asociadas, sus conecciones y la actividad funcional que desempean, este conjunto constituye el sistema reticular. Y cuando un ncleo o una parte de l desempea una funcin especfica, se le denomina centro. Esta definicin de centro trasciende al sistema reticular, pues es aplicable a cualquiera estructura nerviosa que cumple funciones determinadas. Los ncleos reticulares pueden describirse segn su ubicacin, la funcin que desempean, etc. Estos dos aspectos mencionados estn relacionados, lo cual facilita su estudio. La formacin reticular no es exclusiva del tronco cerebral, sino que comienza en la mdula espinal y se extiende hasta el diencfalo. En el tronco, los ncleos reticulares se han clasificado en centrales, medianos, laterales y paramedianos. Los ncleos reticulares centrales se denominan tambin del tegmento, debido a su ubicacin; entre ellos pasa el tracto central del tegmento. En este conjunto nuclear se distinguen dos partes, lateral y mediana. La porcin lateral es de funcin sensitiva, para lo cual est conectada con los tractos espino-
89
talmicos y solitario, el nervio trigmino y los ncleos cocleares y vestibulares. La porcin mediana es motora y recibe informacin sensorial. Est conectada con el tlamo, ya sea mediante sus ramificaciones polisinpticas o por va del tracto tegmentario central; a su vez, el tlamo establece conecciones con el hipotlamo y la corteza cerebral. La otra coneccin importante de estos ncleos reticulares de accin motora se establece con la mdula espinal; ellos envan impulsos a los ncleos del cuerno anterior espinal por dos vas: - tracto retculo-espinal medial, de accin inhibitoria; - tracto retculo-espinal lateral, de accin facilitadora. A su vez, esta porcin nuclear central recibe aferencias de la corteza cerebral por vas crtico-reticulares, y de los ncleos estriados por fibras estrio-reticulares. Los ncleos lateral y paramediano forman parte de un circuito retculo-cerebelo-reticular, y por lo tanto participan en las funciones propias del cerebelo. Los ncleos medianos participan en la regulacin vegetativa, reciben aferencias desde el hipotlamo y del rinencfalo (sistema lmbico); se conectan con ncleos vegetativos del tronco cerebral. Centros vegetativos del tronco cerebral. Si bien es cierto que el hipotlamo es considerado el cerebro visceral, a nivel del tronco cerebral existen varios centros que constituyen comandos respiratorio, circulatorio, de funciones digestivas y de miccin. Centros respiratorios. En la formacin reticular de la mdula oblongada estn los centros inspiratorio y espiratorio, y en la zona caudal del mesencfalo est el centro neumotxico, que podra corresponder al locus coeruleus. Estos tres centros mantienen el ritmo respiratorio con un mecanismo coordinado que comienza con la activacin de las neuronas inspiratorias, las cuales determinan la inspiracin por contraccin de la musculatura inspiratoria y tambin envan impulsos al centro neumotxico; ste estimula al centro espiratorio, el cual inhibe al inspiratorio y se produce la espiracin. En el puente habra un
90
centro apnustico, que ejerce una accin excitadora sobre las clulas inspiratorias. Centros cardiovasculares. Hay un centro depresor y dos centros presores. El centro depresor corresponde al ncleo motor dorsal del vago, ubicado en la mdula oblongada; el X par constituye la va eferente de un arco reflejo cuya activacin deprime la actividad cardaca. Los centros presores estn en la formacin reticular de la mdula oblongada y tienen una divisin vasomotora y otra cardioaceleradora; la estimulacin de la primera determina vasoconstriccin arteriolar y la activacin del centro cardioacelerador aumenta la actividad cardaca. Ambos efectos contribuyen a aumentar la presin arterial, de ah el nombre de centros presores; sus vas eferentes son simpticas. Centros vasodilatadores. Se ha demostrado que a nivel de la regin dorsal del mesencfalo existen grupos neuronales cuya estimulacin provoca vasodilatacin muscular y vasoconstriccin cutnea y visceral. Se puede considerar que estos centros forman parte de un circuito que comprende la corteza cerebral,el hipotlamo y el mesencfalo y su activacin es la responsable de la redistribucin del flujo sanguneo durante el ejercicio muscular. Centro emtico o del vmito. Se encuentra en la formacin reticular de la mdula oblongada y recibe aferencias desde la faringe, el estmago, las vas biliares, el peritoneo, as como impulsos del sistema vestibular y de naturaleza psquica, a la vez que coordina a las diversas estructuras participantes. Son vas aferentes el simptico, el vago y fibras venstibulares; en cambio, las vas eferentes son neurovegetativas para las contracciones gstricas y cierre del ploro, y somticas para el diafragma, msculos abdominales farngeos y suprahiodeos. Centros de miccin. Hay zonas facilitadoras de la miccin en la formacin reticular de la mdula oblongada y puente, y zonas inhibitorias en el mesencfalo.
91
Ventrculos Cerebrales, Meninges y Lquido CfaloRaqudeo. El encfalo y la mdula espinal estn protegidos por estructuras seas constitudas por el crneo y las vrtebras, que en conjunto conforman la columna vertebral, as como por las membranas denominadas meninges y el lquido cfaloraqudeo. Cada uno de los elementos mencionados ejerce su accin protectora de acuerdo con sus caractersticas fsicas o qumicas predominantes. El crneo es de tejido seo y externamente est constitudo por los huesos frontal, parietal, temporal y occipital. Son huesos planos y duros; en la zona temporal, la parte que protege al odo interno se denomina petrosa, precisamente por su consistencia tan dura semejante a piedra. Las meninges son tres membranas que recubren tanto el encfalo como la mdula espinal, y de afuera hacia adentro se denominan duramadre, aracnoides y piamadre. La duramadre es de tejido fibroso denso y posee dos capas; en las partes donde ambas capas van juntas, estn fusionadas con los huesos del crneo; tambin recubre la mdula espinal, donde va separada del hueso del canal vertebral por tejido adiposo, que acta especialmente como amortiguador. En algunas zonas intracraneanas, las dos capas de duramadre se separan, la externa permanece siempre adherida a los huesos del crneo, pero la capa interna forma invaginaciones que van a constituir algunas estructuras especiales, como ser: - a nivel de la lnea media, en direccin cfalo-caudal y en la zona de la cisura interhemisfrica, la capa interna de duramadre se introduce entre los hemisferios cerebrales, formando la hoz o false del cerebro, que separa a ambos hemisferios; - al llegar al cerebelo, la hoz del cerebro se bifurca nuevamente y forma la tienda del cerebelo, que va a separar a los hemisferios cerebrales del cerebelo;
92
- nuevamente, la capa interna de duramadre, a este nivel denominada tienda del cerebelo, se bifurca en la lnea media, constituyendo la hoz o false cerebelar. En la zona en que se separan originalmente ambas capas de duramadre, como la capa externa permanece adosada al crneo y la capa interna se invagina, quedan unas cmaras o senos venosos, que estn llenos de sangre y hacia donde drena el lquido cfalo-raqudeo. La aracnoides es la meninge media; sus clulas epiteliales poseen verdaderos pseudopodios que se entrelazan. Existe un espacio subdural, ubicado entre la duramadre y la aracnoides, que contiene un lquido linfoide, cuya funcin parece ser el permitir pequeos movimientos al encfalo. El espacio ms conocido por su significacin funcional es el que se encuentra por debajo de la aracnoides, por lo que se le denomina espacio sub-aracnodeo y por el cual circula el lquido cfalo-raqudeo. En la zona de los senos venosos, la aracnoides proyecta las vellosidades aracnodeas, que constituyen la principal va de drenaje del lquido cfalo-raqudeo hacia la sangre. La piamadre recubre directamente al encfalo y a la mdula espinal; unida a una capa de astrocitos sub-piales, sus clulas epiteliales constituyen una capa fusionada denominada pa-gla. Los vasos sanguneos se distribuyen sobre esta pagla, y las colaterales sanguneas penetran en la masa enceflica sin horadar la membrana sino recubiertas por ella; se forma as alrededor de los capilares sanguneos un espacio perivascular denominado espacio de Virchow-Robin, que es continuo con el espacio subaracnodeo, lo que determina que el lquido cfalo-raqudeo llegue a todas las neuronas, as como todas ellas reciben circulacin sangunea.
93
RIEGO SANGUNEO EN ENCFALO
ReginFrontal
ReginParietal
Regin Occipital Regin Temporal
En trminos generales, la duramadre y la aracnoides siguen estrechamente la forma del crneo, en cambio, la pa sigue ms bien la forma externa del encfalo; ambos hechos determinan que el espacio sub-aracnodeo presente diferentes dimensiones; cuando se ensancha constituye las cisternas, entre las cuales se pueden mencionar la cisterna cerebelomedular o magna y la cisterna pontina. En la mdula espinal se observa otro ensanchamiento del espacio sub-aracnodeo, cual es la cisterna lumbar, donde se realizan las punciones lumbares con fines anestsicos y diagnsticos. El lquido cfalo-raqudeo se forma en los plexos corodeos, que son invaginaciones vasculares de la pared ventricular. El capilar est rodeado por una capa de piamadre y otra de clulas ependimarias que presentan caractersticas secretorias, es decir, ncleos grandes, algunos nuclolos, numerosas mitocondrias, grandes cuerpos de Golgi, grnulos secretorios y vacuolas; las clulas adyacentes van interdigitadas, constituyendo una barrera intercelular. Debido a esta estructura tan particular, el lquido cfalo-raqudeo se forma tanto por un proceso activo de secrecin como por productos sanguneos que atraviesan selectivamente esta
94
barrera. Si bien es cierto que el lquido cfalo-raqudeo contiene elementos plasmticos, stos estn en proporcin diferente a la de la sangre. El lquido cfalo-raqudeo, una vez formado, circula por los ventrculos cerebrales y por el espacio sub-aracnodeo. Los ventrculos son cavidades que se formaron en el encfalo durante el desarrollo embrionario y fetal, y estn comunicados entre s. Los ventrculos laterales son dos y se encuentran en el interior de los hemisferios cerebrales; estn comunicados con el tercer ventrculo mediante los agujeros de Monro. El tercer ventrculo est ubicado entre los tlamos y se comunica con el cuarto ventrculo a travs del acueducto cerebral o de Silvio. El cuarto ventrculo se encuentra por detrs del tronco cerebral, a nivel del puente y de la porcin rostral de la mdula oblongada; esta parte dorsal del tronco cerebral constituye el piso del cuarto ventrculo, y conforma su techo el velo medular, sobre el cual se encuentra el cerebelo; aqu se encuentra tambin el agujero de Magendie, por el cual circula el lquido cfaloraqudeo hacia la cisterna cerebelo-medular o magna. Los bordes inferiores del cuarto ventrculo estn conformados por los tubrculos grcil y cuneiforme y los pednculos cerebelares inferiores; los bordes superiores son los pednculos cerebelares superiores. Los ngulos de unin de ambos bordes constituyen los recesos laterales, en cada uno de los cuales se encuentra una apertura lateral del cuarto ventrculo o agujero de Luschka hacia el espacio sub-aracnodeo, a nivel de la cisterna pontina En el piso del cuarto ventrculo existen varias estructuras caractersticas, como son el surco medio, la eminencia media que corresponde al ncleo del VI par y a la rodilla del facial, el locus coeruleus y las foveas superior e inferior.
95
VENTRCULOS CEREBRALES
Ventrculos Laterales
Cuarto ventrculo
Tercer Ventrculo
Acueducto de Sylvio
El lquido cfalo-raqudeo circula por todo el espacio subaracnodeo, tanto del encfalo como de la mdula espinal; llega hasta las vellosidades aracnodeas, desde donde drena hacia la sangre. Estas vellosidades estn constitudas por tbulos que comunican el espacio sub-aracnodeo con los senos venosos. La presin del lquido cfalo-raqudeo en el espacio sub-aracnodeo es de unos 15 cm. de H2O y en el seno venoso es de unos 9 cm. de H2O, por lo cual el lquido cfalo-raqudeo fluye hacia ste ltimo. Si la presin en el seno venoso se hace mayor que la del espacio subaracnodeo, los tubos que constituyen las vellosidades sub-aracnodeas se colapsan, funcionando as como vlvulas unidireccionales que impiden que pase sangre al espacio sub-aracnodeo. El lquido cfalo-raqudeo es un lquido cristalino que llena los ventrculos cerebrales y el espacio sub-aracnodeo, con un volumen de unos 150 mililitros; en condiciones normales, presenta un aspecto transparente, como de cristal de roca, y entre otros elementos contiene agua,glucosa, iones como Na+, K+, Ca++, Cl- y algunas clulas. Una caracterstica bioqumica
96
es que no posee sistemas amortiguadores de hidrogeniones. Diariamente se forman entre 600 - 700 ml, por lo cual su tasa de recambio es alta, se renueva 4 a 5 veces en las 24 horas, es decir, tiene un tiempo de recambio de unas 6 horas. Esta alta tasa de recambio permite una extraccin rpida de muchas sustancias, lo cual tambin depende de la mayor o menor facilidad con que los diversos elementos atraviesen la barrera hmato-enceflica. Esta se origina debido al transporte activo de sustancias en los plexos corodeos y a la permeabilidad selectiva de las membranas que rodean a las estructuras nerviosas; se produce entonces una verdadera regulacin de la transferencia de elementos entre la sangre, el lquido cfaloraqudeo y el tejido nervioso, producindose una homeostasis del lquido perineural que contribuye a mantener la excitabilidad neuronal. La barrera hmato-enceflica significa funcionalmente que no todos los elementos sanguneos pueden llegar a las neuronas, y est constituda esencialmente por la pared de los capilares enceflicos, la membrana pa-gla que los rodea y el propio lquido cfalo-raqudeo. En general, los componentes liposolubles como el alcohol etlico, pasan fcilmente desde la sangre al lquido cfalo-raqudeo. La penicilina atraviesa con cierta facilidad la barrera hmato-enceflica, pero la gran tasa de recambio del lquido cfalo-raqudeo impide que esta sustancia se acumule en los ventrculos cerebrales. El agua, el oxgeno, el CO2 atraviesan la barrera en forma irrestricta, como tambin los iones y la glucosa, pero no las protenas; tambin pasan aminocidos como la L-dopa y el 5-hidroxitriptofano, precursores de la dopamina y serotonina respectivamente. Sustancias de importancia funcional que no la atraviesan son la dopamina y las encefalinas, por lo cual estas sustancias no son de uso teraputico habitual. La barrera hmato-enceflica termina de desarrollarse totalmente en la edad adulta; sto es la causa por la cual algunas sustancias exgenas que son inocuas para el adulto pueden ser txicas para los nios. Otro hecho interesante es que existen algunas zonas del encfalo, como la neurohipfisis y el rea postrema, que se encuentran desprotegidas de la accin de la barrera hmato-enceflica; se supone que en estas zonas existen quimiorreceptores a hormonas en el caso de la
97
hipfisis posterior, y a alteraciones qumicas de la sangre en el rea postrema, pues esta estructura constituye un centro emtico. El lquido cfalo-raqudeo tiene tambin funciones de sostn y amortiguamiento de traumatismos; por contener al encfalo, hace que ste disminuya su peso por el principio de Arqumedes relativo a un cuerpo que flota. Otras funciones que se le atribuyen son las de nutricin y excrecin de catabolitos, en las cuales participa ms bien la circulacin cerebral. El lquido cfalo-raqudeo ejerce una presin en los compartimientos que ocupa, la cual vara de acuerdo a la posicin del cuerpo; habitualmente se mide por puncin a nivel de la cisterna lumbar. As, en el individuo normal en decbito horizontal es de 10 a 15 cm.de H2O y un poco menor en los ventrculos. En posicin vertical aumenta a 30 - 50 cm. de H2O en la regin lumbar y llega a ser negativa en los ventrculos, del orden de -3 cm.de H2O. Sistema Nervioso Perifrico. An cuando no se ha terminado de describir el sistema nervioso central, parece oportuno analizar, a este nivel de la descripcin anatmica, el sistema nervioso perifrico, puesto que l se relaciona fundamentalmente con dos estructuras ya conocidas, cuales son la mdula espinal y el tronco cerebral. El sistema nervioso perifrico est constitudo por el conjunto de ganglios y nervios craneanos, espinales y vegetativos. Segn sus funciones, los nervios pueden ser sensitivos, motores o mixtos; o bien se les puede clasificar en somticos, que inervan la musculatura esqueltica, y viscerales. Nervios espinales o raqudeos. El ser humano posee 31 pares de nervios espinales que emergen a travs de los agujeros intervertebrales, con lo cual determinan la segmentacin medular externa; los nervios reciben su nombre segn la regin medular de origen, existiendo 8 nervios cervicales, 12 torcicos, 5 lumbares, 5
98
sacros y 1 coccgeo. El primer nervio espinal emerge entre el occipital y el atlas (primera vrtebra cervical), de modo que la raz del octavo nervio cervical sale por el agujero intervertebral entre la sptima vrtebra cervical y la primera torcica.
99
NERVIOS ESPINALES
Regin Cervical (C1 a C8) Plexo Cervical (C1 a C4) Plexo Braquial (C5 a C8 y T1)
Regin Torcica (T1 a T12)
Regin Lumbar (L1 a L5) Plexo lumbar (L1 a L4) L4 y L5 se unen con los sacros S1 a S4.
Regin del Sacro (S1 a S5) Plexo Sacro (L5 a S3) Plexo Sacrococcgeo (S4, S5 y nervio coccgeo, Co1)
100
Los nervios espinales son mixtos, es decir, llevan fibras sensitivas y motoras, e inervan prcticamente toda la musculatura esqueltica del tronco y extremidades. En parte, fibras viscerales del sistema neurovegetativo pueden ir includas tambin en los nervios espinales, de modo que en un nervio espinal se podran distinguir cuatro componentes: 1.2.3.4.aferentes aferentes eferentes eferentes somticos generales (ASG); viscerales generales (AVG); somticos generales (ESG); viscerales generales (EVG).
Los componentes aferentes son sensitivos y los eferentes son motores. Nervios craneanos. Estn constitudos por 12 pares cuyos ncleos, ya sea sensitivos o motores, son de ubicacin enceflica, especficamente en el tronco cerebral. Se les designa por los nmeros de orden I al XII y pueden ser tambin sensitivos, motores o mixtos. Adems de los cuatro grupos de los nervios espinales, en los nervios craneanos se pueden encontrar otros tres componentes: 1.- aferentes somticos especiales (ASE); 2.- aferentes viscerales especiales (AVE); 3.- eferentes viscerales especiales (EVE). Los nervios craneanos motores, o su porcin motora en los mixtos, se originan en ncleos del tronco cerebral y emergen de alguna de sus partes (mdula oblongada, puente, mesencfalo), lo que constituye el origen aparente . Cabe recordar que en el tubo neural se desarrollaron las placas alar (dorsal) y basal (ventral); de la porcin alar derivaron estructuras sensitivas y de la porcin basal, estructuras motoras. El telencfalo y el diencfalo slo se originan de la placa alar, por lo cual estas estructuras no dan origen a nervios motores, el primero de los cuales que es el III par craneano o motor ocular comn, se origina en el mesencfalo.
101
Las fibras sensitivas de los nervios craneanos se originan en receptores; los cuerpos celulares de sus neuronas se ubican en algn ganglio anlogo al de la raz sensitiva de los nervios espinales y las fibras convergen finalmente hacia alguna porcin o ncleo sensitivo especfico del sistema nervioso central.
NERVIOS CRANEANOS
102
N. ptico ( I I )
N. olfatorio ( I )
N. culomotor ( III )
N. Trigmino ( V )
N. Troclear ( IV ) N. Abducens ( VI )
N. Vestibular ( VIII ) N. Facial ( VII )
N. Glosofarngeo ( IX )
N. Hipogloso ( XII ) N. Accesorio Espinal ( XI ) N. Vago ( X )
Par craneano I: nervio olfatorio. Es un nervio sensitivo que se origina en las clulas receptoras olfatorias de la mucosa nasal. Sus fibras son amielnicas y llegan a las clulas mitrales del bulbo olfatorio, donde hacen sinapsis; neuronas secundarias conectan con el bulbo olfatorio del lado opuesto a travs de la comisura
103
anterior, y con la corteza olfatoria primaria; neuronas terciarias conectan esta ltima con la corteza entorrinal, el rea preptica lateral y el cuerpo amigdaloide, de modo que relaciona a las estructuras olfatorias con elementos del sistema lmbico. Par craneano II: nervio ptico. Es solamente sensitivo y se origina en las clulas ganglionares de la retina, cuyos axones mielinizados constituyen las fibras del nervio ptico. Se considera que la retina de cada ojo est constituda por dos partes, una hemirretina nasal, que es la que queda ms cercana a la nariz, y una hemirretina temporal, que est ubicada hacia el hueso temporal. Las fibras de cada ojo, y por lo tanto, de cada retina completa, van a formar los nervios pticos, que llegan hasta el quiasma ptico, lugar en que las fibras de cada hemirretina nasal se cruzan; en cambio, las fibras de cada hemirretina temporal continan sin cruzar. Del quiasma ptico se originan las dos cintillas pticas, cada una de las cuales lleva fibras de ambos ojos; as, la cintilla izquierda lleva la continuacin de las fibras de la hemirretina temporal del ojo izquierdo y de las fibras de la hemirretina nasal del ojo derecho. Las cintillas pticas llegan hasta los cuerpos geniculados laterales del tlamo , donde se originan los tractos genculo-calcarinos que terminan en la corteza visual primaria o estriada o calcarina, ubicada en el lbulo occipital. Algunas fibras del nervio ptico pasan a los colculos cuadrigminos superiores, que participan en la orientacin de ojos y cabeza para ubicar en el campo visual algn objeto de inters atencional. Por otra parte, a la regin pretectal le llega informacin desde el nervio ptico y corteza visual; esta rea pretectal est involucrada en los reflejos pupilares a la luz y de acomodacin del cristalino. Par craneano III: nervio culo-motor o motor ocular comn. Como su nombre lo indica, es de funcin motora para los bulbos o globos oculares, es decir, inerva msculos externos o extrnsecos del ojo.
104
Se origina en el ncleo oculomotor o del III par y en el ncleo de Edinger-Westphal, ubicados en el mesencfalo, en el piso del acueducto cerebral. Las fibras, principalmente no cruzadas, pasan por el ncleo rojo y por el lado interno de la sustancia negra, para emerger a nivel del surco pontopeduncular. Su funcin es motora para los msculos oculares rectos interno, superior e inferior, oblicuo menor y elevador del prpado. Tambin lleva fibras parasimpticas al esfinter de la pupila y al msculo ciliar que controla el funcionamiento del cristalino. Par craneano IV: nervio troclear o pattico o motor ocular interno. Tiene su origen en el ncleo troclear, ubicado en el mesencfalo, en el piso del acueducto cerebral. Es el nico nervio que emerge por la cara dorsal del tronco cerebral, por debajo de los colculos inferiores. Llega a la rbita por la fisura orbital superior e inerva al msculo oblicuo superior o mayor, que rota al bulbo ocular hacia afuera y hacia abajo. Par craneano V: nervio trigmino. Es un nervio mixto, sensitivo y motor; sus fibras transmiten impulsos de la sensibilidad exteroceptiva y propioceptiva de la cabeza (cara y cuero cabelludo), y las fibras motoras inervan los msculos mandibulares. El ncleo motor se encuentra en el tercio superior del puente; sus fibras van a inervar los msculos mandibulares (mastero, temporal y pterigodeos), msculos tensores del tmpano (como el msculo del martillo) y el tensor del velo del paladar. El ncleo motor funciona en estrecha relacin con el ncleo mesenceflico del V par, que recibe la informacin sensitiva propioceptiva del aparato masticatorio, con lo cual ambos ncleos regulan el proceso automtico de la masticacin. Las fibras sensitivas trigeminales se originan en receptores de diversas estructuras de la cabeza y estn constitudas por neuronas pseudounipolares; las ramas perifricas conforman tres nervios, que son el oftlmico, el
105
maxilar y el mandibular. Los somas de estos nervios se ubican en el ganglio semilunar o trigeminal, de donde emerge el conjunto de neuritos centrales de las neuronas sensitivas pseudounipolares y que van a constituir la raz sensitiva trigeminal, que entra al tronco cerebral y termina en los ncleos sensitivos. El nervio oftlmico lleva los impulsos sensitivos desde la crnea, el cuerpo ciliar, el iris, las glndulas lagrimales, la conjuntiva ocular,la mucosa nasal, los prpados, las cejas, la frente y la nariz. Se junta con filamentos del plexo simptico carotdeo interno y se comunica con los pares craneanos III, IV y VI (motores oculares). El nervio maxilar transmite impulsos desde la piel de las mejillas, el labio inferior, las aletas de la nariz, el maxilar superior, los dientes, la mucosa de la boca, el seno maxilar y regiones esfenopalatinas y pterigodeas. Al igual que el nervio oftlmico, tambin sirve de vehculo para distribuir fibras simpticas y parasimpticas. La divisin mandibular inerva los msculos de la masticacin, la mucosa inferior de la boca, la piel del odo externo, el conducto auditivo externo, las partidas, la articulacin mandibular y la mandbula, las glndulas sublinguales y los dos tercios anteriores de la lengua. La porcin motora del V par se une a este nervio mandibular. Los ncleos sensitivos se encuentran ubicados en las estructuras que se indican a continuacin. En el mesencfalo est la raz mesenceflica del trigmino, a donde llegan los impulsos de la sensibilidad propioceptiva de los msculos masticatorios y de la articulacin tmporo-mandibular. Fibras del ncleo mesenceflico sinaptan con el ncleo motor del trigmino, estableciendo el arco reflejo de los msculos masticadores. Ramas centrales se unen a las del ncleo de la raz descendente y ncleo sensitivo principal, llevando las sensaciones musculares y articulares de la cabeza hasta el tlamo a travs del lemnisco trigeminal.
106
En la parte superior del puente se encuentra el ncleo sensitivo principal del trigmino. Las fibras que llevan los impulsos de dolor, temperatura y tacto de la cara y cuero cabelludo, llegan al puente, donde se dividen en ramas cortas que van a este ncleo sensitivo principal, y en ramas descendentes que terminan en el ncleo espinal del V par. En la mdula oblongada se encuentra el ncleo de la raz descendente o espinal del trigmino; sus fibras descienden en la parte dorsal del tronco cerebral y llegan a la mdula espinal hasta C2, formando el haz trigmino-espinal, que transmite impulsos de dolor y temperatura. El nervio trigmino emerge en las caras laterales del puente. Par craneano VI : nervio abducens o motor ocular externo. Su ncleo de origen est en el puente, a nivel del colculo facial, que es un engrosamiento de la eminencia media producido por el ncleo del VI par y la rodilla del nervio facial. Emerge por el surco bulbo-pontino y entra a la rbita por la fisura orbital superior. Inerva el msculo recto lateral, que rota el bulbo ocular hacia afuera. Par craneano VII : nervio facial. Tiene tambin una divisin sensitiva y otra motora. El ncleo motor del facial est en el tegmento inferior del puente; el nervio emerge por el surco bulbo-pontino y va a inervar los msculos faciales, que controlan la expresin facial, cuero cabelludo, odo (estapedio o msculo del estribo), orejas y otros. La divisin sensitiva del facial se relaciona con las sensaciones gustativas en los dos tercios anteriores de la lengua y la sensibilidad del paladar blando; tambin inerva las glndulas salivales. Las ramas sensitivas traen los impulsos perifricos por el nervio lingual y la cuerda del tmpano y hacen estacin en el ganglio geniculado; las ramas sensitivas centrales pasan por el nervio intermediario al ncleo del tracto solitario. En general, las ramas sensitivas de los nervios facial,
107
glosofarngeo y vago se unen en el tronco cerebral formando el tracto solitario que termina en el ncleo del tracto solitario de la mdula oblongada. La cuerda timpnica y el nervio intermedio llevan adems fibras viscerales motoras parasimpticas que inervan las glndulas salivales submaxilares y sublinguales; y en el nervio petroso van fibras que inervan las glndulas lagrimales. Todas ellas provienen del ncleo salival superior. Par craneano VIII: nervio vestbulo-coclear. Es un nervio sensitivo que tiene una divisin coclear o auditiva y una divisin vestibular relacionada con el equilibrio. La divisin coclear se origina en los receptores auditivos del rgano de Corti, ubicado en la cclea o caracol del odo interno; las ramas perifricas de las neuronas sensitivas pseudo-unipolares llegan hasta el ganglio espiral de la cclea y las fibras centrales llegan a los ncleos cocleares del puente; los axones de las clulas de estos ncleos forman el lemnisco lateral que termina en el colculo inferior homolateral (las fibras pueden o no haber cruzado antes de formar el lemnisco). De aqu las fibras van a la corteza cerebral auditiva, ubicada en el lbulo temporal. Las fibras vestibulares se originan en receptores del odo interno ubicados en los canales semicirculares, en el sculo y en el utrculo; los neuritos perifricos que se originan de estos receptores llegan al ganglio vestibular y los neuritos centrales van a hacer sinapsis en los ncleos vestibulares que estn en el rea acstica del piso del IV ventrculo. Algunas fibras eferentes de estos ncleos forman parte del fascculo longitudinal medial que se extiende por todo el tronco cerebral y mdula espinal rostral; relaciona los ncleos motores con los encargados de la motilidad de la cabeza y los vestibulares. Otras fibras del nervio vestibular no sinaptan en los ncleos vestibulares sino que, junto a fibras eferentes de estos ncleos, entran al cerebelo como tracto vestbulocerebelar por el pednculo cerebelar inferior. Su origen aparente se encuentra en el surco bulbo-pontino.
108
Par craneano IX: nervio glosofarngeo. Es un nervio mixto, sensitivo y motor; parte de sus fibras pertenecen a la divisin parasimptica del sistema neurovegetativo. Transmite las sensaciones gustativas del tercio posterior de la lengua y sensaciones de las fauces, tonsilas, faringe, paladar blando, trompa de Eustaquio y caja del tmpano. A travs del nervio sinusal conectan con los quimiorreceptores y tensoceptores del cuerpo y seno carotdeo que participan en la regulacin de la respiracin y la presin sangunea arterial. Las ramas sensitivas del glosofarngeo penetran al tronco cerebral y con las fibras sensitivas de los nervios facial y vago forman el tracto solitario de la mdula oblongada; estas fibras sinaptan con el ncleo del tracto solitario. Las fibras motoras se originan en el ncleo ambiguo de la mdula oblongada y se relacionan con los mecanismos de la deglucin y la actividad de las cuerdas vocales. Sus fibras emergen de la parte superior del surco retroolivar. Par craneano X: nervio vago. Es el principal componente del sistema parasimptico y tiene divisiones sensitiva y motora. Los receptores de origen y las estructuras efectoras son tantos y tan variados, que sobrepasan esta descripcin; aqu se considerarn los ncleos de origen y destino y parte de sus vas principales y su descripcin se complementar al analizar el sistema parasimptico. A nivel de la mdula oblongada se encuentra el ncleo motor dorsal del X par, de donde se originan las fibras motoras que inervan la musculatura lisa y el tejido glandular que controla este nervio. Otras fibras motoras se originan del ncleo ambiguo, por lo cual a ste se le llama tambin ncleo motor ventral del nervio vago.
109
Las ramas sensitivas provienen de receptores viscerales y en el tronco cerebral pasan a formar parte del tracto solitario ya descrito. Sus fibras emergen por el surco retro-olivar de la mdula oblongada. Dcimo primer (XI) par craneano: nervio espinal accesorio. El nervio espinal tiene una porcin craneal y otra espinal. La porcin craneal deriva de cuatro o cinco races en la porcin lateral de la mdula oblongada; luego se junta con la porcin espinal que nace de las clulas motoras en la columna gris anterior en C5 . Esta porcin craneal es de fibras motoras para la faringe, laringe, vula y paladar; enva fibras a los nervios larngeo recurrente y cardaco. Estas fibras motoras se originan en el ncleo ambiguo, situado en la formacin reticular de la mdula oblongada, ncleo relacionado con la deglucin y la fonacin. La porcin espinal de este nervio es motora para los msculos esternocleidomastodeo y trapecio, y enva ramas a los nervios espinales C2, C3 y C4. Dcimo segundo (XII) par craneano: nervio hipogloso. Es un nervio motor para msculos del cuello y lengua (estilohiodeo, milohiodeo, omohiodeo, esternotirodeo, estilogloso, geniogloso, geniohiodeo y msculos intrnsecos de la lengua). Su ncleo de origen est en la mdula oblongada y sus fibras emergen por el surco pre-olivar. Diencfalo. Est ubicado en el espacio supratentorial y lo constituyen esencialmente el tlamo, el hipotlamo, el epitlamo, el subtlamo y la neurohipfisis. Funcionalmente es apropiado considerarlo como parte del paleoencfalo (tlamo ms ncleos estriados) por sus conecciones tlamo-estriadas. El tercer ventrculo separa las estructuras dienceflicas pareadas. Del acueducto cerebral se origina el surco hipotalmico que separa al tlamo del hipotlamo. La cpsula interna conforma el lmite lateral del diencfalo.
110
Tlamo. Es un conjunto nuclear pareado de gran importancia funcional, lo que se refleja en la existencia de las amplias radiaciones tlamo-corticales, constitudas por conglomerados de fibras que atraviesan la cpsula interna y terminan en la corteza cerebral. El tlamo posee grupos nucleares susceptibles de clasificarse ya sea por su localizacin o por su implicancia funcional. Una estructura de sustancia blanca, la lmina medular externa, divide al tlamo en tres partes: anterior, lateral y medial. A. E. Walker ha descrito cinco grupos nucleares talmicos, que se detallan a continuacin. Ncleos anteriores. Forman el tubrculo anterior del tlamo; reciben aferencias desde los cuerpos mamilares del hipotlamo a travs del fascculo mamilo-talmico y envan eferencias al giro del cngulo. Ncleos de la lnea media. Estn ubicados debajo del tercer ventrculo y de la masa intermedia. Son de coneccin intratalmica y con el hipotlamo. Ncleos mediales. Se ubican por dentro de la lmina medular interna. En la especie humana est muy desarrollado el ncleo mediano ventral, que participa en los mecanismos de integracin y activacin difusa tlamo-cortical. Otro ncleo importante de este grupo es el dorsomediano, que recibe aferencias desde otros ncleos talmicos y enva eferencias al hipotlamo, complejo amigdalino y corteza frontal. Tambin pertenecen a este grupo los ncleos intralaminares, conectados con otros grupos del tlamo y con el tronco cerebral.
111
Ncleos laterales. Hay un grupo ventral y otro dorsal. Ncleos ventrales. A su vez hay ncleos ventrales anteriores, laterales y posteriores. Ncleo lteroventral anterior: se conecta con el globo plido por medio del fascculo talmico. Ncleo ltero-ventral lateral: constituye un nexo entre el cerebelo y la corteza motora, pues recibe fibras del pednculo cerebelar superior y del ncleo rojo, y enva eferencias a la corteza motora. Ncleo ltero-ventral posterior. Es el gran centro sensitivo del tlamo, debido a las aferencias que recibe a travs del lemnisco medial, de los tractos espinotalmicos, del lemnisco trigeminal y del tracto solitario (fibras gustativas). Las dos primeras hacen estacin en el ncleo ventral pstero-lateral propiamente tal, y las dos ltimas en la porcin pstero medial. De aqu las eferencias van a la corteza sensitiva. Ncleos dorsales. Son el dorsolateral y el pstero-lateral, de conecciones intratalmicas y con eferencias a las cortezas parietal y temporal. Ncleos posteriores. Se destacan fundamentalmente tres: el pulvinar y los cuerpos geniculados medial y lateral. El pulvinar se relaciona especialmente con mecanismos de asociacin auditiva y visual; recibe aferencias desde otros ncleos talmicos y enva eferencias a las cortezas parietal, temporal y occipital. El cuerpo geniculado medial o interno recibe aferencias desde los ncleos cocleares, olivar superior y colculos inferiores; sus eferencias las enva a la corteza auditiva (giro de Heschl del lbulo temporal).
112
El cuerpo geniculado lateral o externo recibe aferencias del tracto ptico; de este ncleo se origina el tracto genculocalcarino que conecta al cuerpo geniculado lateral con la corteza visual o calcarina.
NCLEOS TALMICOS
Lmina medular Interna Ncleo anterior
N. Medial Dorsal
Adhesin Intertalmica N. Dorsolateral N. Ventral anterior N. Ventral lateral N. Intralaminar N. Pulvinar
N. Ventral intermedio N. Ventral Posterolateral N. Posterolateral N. Ventral Posteromedial N. Centro medial Tracto ptico
Consideraciones funcionales de los ncleos talmicos. Si se tienen en cuenta las relaciones de los ncleos talmicos con otras estructuras, o bien su participacin en ciertas funciones especficas, se pueden distinguir los ncleos de asociacin y los de proyeccin o radiacin; estos ltimos pueden ser a su vez especficos e inespecficos. Los ncleos dorsomediano, dorsolateral, psterolateral y pulvinar, establecen conecciones intratalmicas y se proyectan
113
a las grandes reas de asociacin cortical, por lo cual pertenecen al grupo de los ncleos de asociacin. Considerando los grupos talmicos que constituyen estaciones de relevo, ya sea sensitivo o motor, se distinguen los de proyeccin especfica que se describen a continuacin. Ncleo ventral pstero-lateral: es el lugar de destino del lemnisco medial, que trae la informacin sobre las sensaciones de tacto discriminativo y propiocepcin consciente de la mitad contralateral del cuerpo y las proyecta a la corteza post-central; recibe tambin las aferencias del fascculo espinotalmico anterior, sobre tacto burdo y presin, y del espinotalmico lateral, sobre dolor y temperatura; ambos traen informacin de la mitad contralateral del cuerpo y la proyectan a la corteza sensitiva primaria somtica general. Ncleo ventral pstero-medial: constituye una estacin de relevo para el lemnisco trigeminal, que es va smato-sensitiva de la regin facial contralateral. Cuerpo geniculado lateral: a travs del tracto ptico recibe informacin visual y la proyecta a la corteza calcarina. Cuerpo geniculado medial: recibe los impulsos auditivos y los proyecta a la corteza auditiva. Ncleo ltero-ventral lateral: forma parte de un circuito motor que desde el cerebelo enva impulsoso a la corteza motora. Ncleo ltero-ventral anterior: recibe aferencias desde el globo plido y las proyecta hacia ncleos relacionados con funciones motoras y a las reas 4 y 6 de la corteza cerebral. Por ltimo, ncleos intralaminares y reticulares transmiten impulsos desde el sistema reticular ascendente y se proyectan como ncleos inespecficos a toda la neocorteza. Del anlisis de su estructura y sus conecciones se puede deducir la enorme importancia del tlamo en los fenmenos de sensibilidad; puede agregarse que an en el ser humano, participa en la sensopercepcin tactil, trmica y dolorosa, slo que con poco grado de discriminacin. En especies animales
114
inferiores puede constituir un centro superior de integracin sensorial. Hipotlamo. Como su nombre lo indica, est ubicado bajo el tlamo, en direccin ms bien ventral. Es indudable que su nombre no le hace justicia, puesto que sus funciones le permiten describirlo como un verdadero cerebro visceral, a la vez que como un centro de transduccin de fenmenos psquicos en manifestaciones fisiolgicas y an orgnicas. A este respecto, cabe sealar que se le considera formando parte del sistema lmbico, que es uno de los sistemas de integracin global, por lo cual se le denomina sistema lmbico-hipotalmico. Posee diversos grupos nucleares, que se pueden clasificar regionalmente en : - regin anterior o supraptica, que comprende a los ncleos preptico, supraptico y paraventricular; su activacin produce disminucin de las frecuencias cardaca y respiratoria y de la presin arterial sistmica, por lo cual se le denomina el sistema trofotropo; - zona intermedia o tuberal; - zona posterior o mamilar, cuya estimulacin aumenta la presin sangunea arterial y la frecuencia cardaca, por lo cual se le llama el sistema ergotropo; contiene ncleos como los cuerpos mamilares, con sus ncleos lateral y medial.
115
NCLEOS HIPOTALMICOS
Adhesin Intertalmica
N. Paraventricular rea hipotalmica Lateral rea hipotalmica Dorsal N. Dorsomedial rea Posterior
N. Preptico Lateral N. Intercalatus
N. Periventricular
N. Preptico Medial rea hipotalmica Anterior Ncleo Supraptico
Complejo Mamilar
Ncleo Rojo
Ncleo Ventromedial Hipfisis
Puente
116
El hipotlamo recibe conecciones aferentes entre las que se pueden mencionar las siguientes: - fascculo medial del cerebro anterior, que conecta con el rea paraolfatoria y los cuerpos estriados; - fibras tlamo-hipotalmicas; - fornix, que conecta al hipocampo y giro dentado con los cuerpos mamilares y otros ncleos; - fibras plido-hipotalmicas; - pednculo mamilar inferior, que trae aferencias desde el tegmento mesenceflico; - estra terminal, que proviene del cuerpo amigdaloide. Entre las eferencias del hipotlamo se encuentran los siguientes fascculos: - hipotlamo-hipofisiario; - mamilo-talmico; - mamilo-tegmental, que lleva impulsos al mesencfalo; - longitudinal dorsal, que conecta con porciones caudales del tronco cerebral, especialmente con ncleos viscerales motores y ncleos reticulares. Consideraciones funcionales del hipotlamo. El hipotlamo interviene en la regulacin de prcticamente todas las funciones vegetativas; participa en el comando central de los ritmos biolgicos y de gran parte del sistema endocrino. Ritmos biolgicos. Las funciones biolgicas presentan periodicidad circadiana, nictimeral o ultradiana. La circadiana se refiere a
117
variaciones alrededor del da, es decir, de las 24 horas; la nictimeral est indicando influencia de los ciclos luz-oscuridad, es decir, relativos al da y a la noche; y la ultradiana se refiere a perodos distintos, generalmente mayores, de las 24 horas. A nivel del hipotlamo existen dos grandes marcapasos centrales que regulan la ritmicidad de grupos de funciones. Hay un marcapasos X, ubicado en el hipotlamo ventromedial o lateral, que regula a lo menos el sueo REM o MOR o sueo activado o paradjico, la temperatura central o del ncleo homeotermo, la concentracin plasmtica de cortisol y la excrecin urinaria de K+. Otro marcapaso, denominado Y, parece estar ubicado a nivel de los ncleos supraquiasmticos y se relaciona con el sueo de ondas lentas, la temperatura cutnea, la concentracin plasmtica de hormona de crecimiento y la excrecin urinaria de Ca++. Regulacin del equilibrio hdrico. En los ncleos suprapticos y paraventriculares del hipotlamo se elabora la hormona antidiurtica, que se almacena en la hipfisis y cuya accin es controlar la reabsorcin facultativa de agua a nivel de los tbulos distal y colector del rin. Los osmorreceptores que informan de la concentracin extracelular de solutos osmticamente activos tambin se encuentran en el hipotlamo. Regulacin trmica, de la ingesta de alimentos y endocrina. En el hipotlamo se encuentran ubicados los termorreceptores centrales, que se informan de la temperatura del ncleo homeotermo por va sangunea; los centros termorreguladores estn a su vez ubicados en el hipotlamo, donde existe un centro de la termognesis (hipotlamo popsterior) y otro de la termolisis (hipotlamo anterior). Otro grupo de neuronas hipotalmicas controla la ingesta de alimentos.; al parecer, el centro de la saciedad estara en el ncleo ventromedial, y el centro del hambre, en el rea hipotalmica lateral. Tambin los cuerpos mamilares intervienen en los reflejos de alimentacin.
118
Un aspecto importante de la regulacin endocrina lo realizan las hormonas liberadoras e inhibidoras hipotalmicas, que regulan las secreciones de tropinas hipofisiarias y a travs de ellas, a las hormonas efectoras del eje hipotlamohipofisiario. En la regulacin neuro-endocrina participa fundamentalmente la hipfisis, que en realidad es una glndula de secrecin interna, pero que por sus estrechas relaciones funcionales con el hipotlamo se describir brevemente. La hipfisis se encuentra situada por debajo del hipotlamo, con el cual se encuentra unida por medio del tallo hipofisiario. Consta de dos partes, una hipfisis anterior o adenohipfisis y una hipfisis posterior o neurohipfisis; cada una se encuentra conectada con el hipotlamo en forma diferente. La hipfisis anterior o adenohipfisis recibe irrigacin a travs de la arteria hipofisiaria superior, que se ramifica en un plexo capilar primario que confluye en venas, para luego volverse a ramificar en un plexo secundario de capilares sinusoidales; esta doble capilarizacin constituye el sistema portal hipofisiario. El hipotlamo enva, mediante el plexo primario, hormonas liberadoras y hormonas inhibidoras hacia la adenohipfisis, donde se producen a su vez otras hormonas, la mayora de las cuales se denominan tropinas hipofisiarias; todas estas hormonas se liberan hacia el plexo capilar secundario, desde donde entran a la circulacin general y van a ejercer su efecto sobre otras glndulas endocrinas o bien sobre rganos efectores. La neurohipfisis o hipfisis posterior est tambin conectada con el hipotlamo, pero sus conecciones son esencialmente nerviosas. En los ncleos suprapticos y paraventriculares del hipotlamo se producen dos hormonas, la ocitocina y la hormona antidiurtica o vasopresina; por va axnica, estas hormonas llegan a la neurohipfisis, donde se almacenan y se van entregando a la circulacin general segn necesidades. Ncleos Basales.
119
Como su nombre lo indica, estn ubicados en la base del cerebro y comprenden los siguientes grupos : a.- ncleo caudado; b.- ncleo lentiforme o lenticular, con su porcin externa o putamen y sus dos porciones internas o globus pallidum; c.- ncleo amigdalino; d.- claustrum o antemuro. Existen otras estructuras que estn en estrecha correlacin funcional con los ncleos basales, por lo que se les puede considerar formando parte del sistema de ncleos de la base; estas estructuras son: ncleo subtalmico (de Luys); zona incerta, ubicada en la regin subtalmica; regin prerrbrica; ncleo rojo; sustancia nigra.
Desde un punto de vista filogentico, el globo plido constituye el paleoestriado y el caudado y el putamen el neoestriado; estos cuerpos estriados tienen una participacin destacada en las funciones smato-motoras. Como estaciones de relevo, los ncleos caudado, putamen y claustro son fundamentalmente receptores; en cambio el pallidum es el efector esencial del sistema. El complejo amigdalino est relacionado con el hipotlamo y se le considera parte integrante del sistema lmbico; este complejo est ubicado en el lbulo temporal y est vinculado con funciones viscerales, endocrinas y de conductas lmbicas. Aferencias a los ncleos estriados. Les llega informacin proveniente de: corteza cerebral, especialmente de las zonas motora y premotora, constituyendo las proyecciones crtico-estriadas; cerebelo, son las proyecciones cerebelo-estriadas: tegmento mesenceflico; al putamen y al caudado les llegan fibras desde la sustancia nigra y de la formacin reticular ventral del mesencfalo.
120
En cuanto a las eferencias que salen desde los cuerpos estriados, se pueden mencionar las que van a: - mdula espinal; - hipotlamo; - corteza cerebral. Cerebelo. Se encuentra situado en la zona occipital, por debajo de la tienda del cerebelo, que es un repliegue de la duramadre. Consta de dos porciones laterales o lbulos y una parte central, el vermis cerebelar. Est unido al tronco cerebral mediante los tres pares de pednculos cerebelares .
CEREBELO Y SUS NCLEOS
Tlamo Vermis
Fisura primaria
Pednculos cerbelosos Superior Medio N. Dentado Inferior
N. Emboliformes N. Globosos N. Fastigio
121
La cara anterior del cerebelo forma la parte culminante deel techo del IV ventrculo; la cara superior est en relacin con los hemisferios cerebrales a travs de la tienda del cerebelo, y la cara inferior descansa en las fosas cerebelares del occipital. En su parte externa presenta surcos concntricos, que si son profundos se denominan fisuras; entre los surcos estn las laminillas cerebelares; en cambio, las fisuras delimitan los lbulos cerebelares y an dividen al vermis . Del centro de la cara anterior y a cada lado de la lnea media salen desde una masa nica los pednculos cerebelares; primero salen unos cordones de sustancia blanca que luego se separan, constituyendo los tres pares de pednculos: - superiores, que llegan a los pednculos cerebrales; - medios, que se dirigen al puente; - inferiores, que conectan al cerebelo con la mdula oblongada. El cerebelo consta de una corteza gris externa y sustancia blanca en el interior; sin embargo, hay unas masas grises centrales que son los cuatro pares de ncleos cerebelares, a saber: ncleos dentados, emboliformes, globosos y del fastigio. Desde un punto de vista filogentico y morfo-funcional, el cerebelo se divide en tres partes que se describirn a continuacin. Arquicerebelo o cerebelo primitivo. Comprende el ndulo del vermis y los flculos de los hemisferios, constituyendo todo el conjunto el lbulo flculonodular; est asociado con los ncleos del fastigio y funcionalmente es el centro del control del equilibrio, regulando la posicin de la cabeza en el espacio. Las aferencias al arquicerebelo estn relacionadas con el sistema vestibular; se originan en el aparato vestibular del odo
122
interno y por va del nervio vestbulo-coclear (VIII par craneano), la protoneurona sensitiva llega hasta los ncleos vestibulares bulbo-pontino; una segunda neurona , por va del pednculo cerebelar inferior, lleva la informacin a la corteza flculo-nodular. La va eferente proviene de la corteza cerebelar, pasa por el flculo y por el pednculo cerebelar inferior llega a los ncleos vestibulares bulbo-pontinos; de aqu, por los tractos vestbulo-espinales directos y cruzados llega a la motoneurona del cuerno anterior espinal. Paleocerebelo. Es de desarrollo filogentico ms reciente que el arquicerebelo. Est constitudo por las zonas del vermis llamadas lngula, lobulillo central, culmen, declive, pirmide y vula, as como por las prolongaciones y lobulillos correspondientes, vale decir, el vnculo, el ala, los lobulillos semilunares anterior y posterior, el lobulillo digstrico y la amgdala. Al paleocerebelo le corresponden los ncleos cerebelares globosos y emboliformes. Est relacionado con los impulsos propioceptivos que rigen el tono postural, ejerciendo un control sobre los msculos antigravitacionales. Adems est involucrado en el control de funciones vegetativas. Las vas cerebelares aferentes del paleocerebelo estn constitudas por los tractos cerebelosos directo o posterior y cruzado o anterior, que provienen de la mdula espinal. Terminan en el lobulillo central para las fibras procedentes de los miembros inferiores y en el culmen para las de los miembros superiores. A estas vas se agregan: - fibras de los ncleos grcil y cuneiforme y de ncleos sensitivos bulbo-pontinos, como el trigmino; - fibras del sistema reticular y otros ncleos bulbares, como los laterales y paramedianos y la oliva bulbar. Las eferencias del paleocerebelo tienen un primer relevo en los ncleos globosos y emboliformes, se dirigen al ncleo rojo y forman luego el tracto rubro-espinal cruzado que llega a
123
la motoneurona perifrica. Una parte de las fibras eferentes van al tlamo, configurando la va cerebelo-rubro-talmica, conectada mediante radiaciones talmicas con la corteza motora, por lo cual el cerebelo participa en el control de la motilidad voluntaria.
Neocerebelo. Est formado por el folium y el tuber del vermis y por el lbulo ansiforme. De los ncleos cerebelares, est asociado con el dentado. El neocerebelo est conectado con la corteza cerebral, especialmente con el rea motora, y con los ncleos suprasegmentarios del sistema smato-motor en general; interviene en el control automtico de la motilidad voluntaria y semivoluntaria, a travs de una larga va crtico-cerebelocortical. En cuanto a las aferencias al neocerebelo, se describe una va cuya primera neurona es crtico-pntica y que puede formar fascculos tmporo-pnticos y fronto-pnticos, a los que se pueden agregar fibras parieto-pnticas y occpito-pnticas. Todas terminan en ncleos del puente donde sinaptan con una segunda neurona que es ponto-cerebelar y que cruza para llegar a la neocorteza cerebelar. Con respecto a las eferencias del neocerebelo, la primera neurona va desde la corteza cerebelar al ncleo dentado; la segunda neurona es cruzada y va al tlamo, desde cuyo ncleo ltero-ventral intermedio parte una tercera neurona que puede ir a: - corteza cerebral temporal o precentral; a este nivel el circuito cerebelar puede relacionarse con fibras del tracto crtico-espinal, que coordina los movimientos semiautomticos y semivoluntarios; - cuerpos estriados, de donde se conecta con el ncleo rojo y por ltimo a la mdula espinal, pasando por la
124
formacin reticular del tronco cerebral; esta va participa en la regulacin de los movimientos automticos involuntarios. Como se puede deducir por su participacin en la motilidad somtica, el cerebelo puede ser considerado un verdadero rgano terminal que controla toda la actividad motriz de la musculatura esqueltica o estriada.
Estructura microscpica de la corteza cerebelar. Se encuentran en ella neuronas muy caractersticas que se distribuyen en tres capas, que de afuera hacia adentro son la capa molecular, la central o de las clulas de Purkinje y la granular o interna. Capa profunda o granular. Posee unas neuronas pequeas llamadas grnulos cuyos axones llegan a la capa molecular superficial y all se ramifican en ngulo recto constituyendo las fibras paralelas. Las dendritas de los grnulos sinaptan con fibras musgosas, que son aferentes a la corteza cerebelosa; dichas sinapsis se denominan glomrulos y a ellos tambin confluyen los axones de neuronas Golgi tipo II, que son elementos de la capa granular. Las dendritas de estas clulas Golgi II reciben adems sinapsis de las fibras paralelas. Capa central de las clulas de Purkinje. Son neuronas de tipo idiodendrtico, ya que sus ramificaciones cortas presentan un aspecto profuso muy particular. Alrededor de su soma se ramifica el axn de las clulas en cesto de la capa ms externa, estableciendo mediante sinapsis axo-somticas una relacin estrecha entre estas neuronas de ambas capas de la corteza cerebelar. Las profusas ramificaciones dendrticas de las clulas de Purkinje llegan a la capa molecular y sinaptan tambin con ramificaciones de las fibras paralelas provenientes de los axones de los grnulos y con las fibras trepadoras que traen las aferencias desde el complejo olivar inferior.
125
Capa externa molecular. Sus neuronas propias son las clulas en cesto y algunas grandes clulas estrelladas. En esta capa se distribuyen tambin las fibras paralelas, las dendritas de las clulas de Purkinje y las fibras trepadoras. Como se puede observar, las informaciones aferentes llegan a las tres capas de la corteza cerebelar, constituyendo las clulas de Purkinje un enlace funcional importante. En cuanto a los mecanismos interneuronales de funcionamiento, los impulsos aferentes llegan al cerebelo por va de las fibras musgosas y las trepadoras; estos impulsos son excitatorios y activan a las clulas de Purkinje y a tres tipos de interneuronas que son inhibitorias, a saber: las clulas de Golgi, las clulas en cesto y las estrelladas. Los axones de las clulas de Purkinje constituyen la nica eferencia desde el cerebelo y su accin est regulada por un mecanismo de retroaccin o feed back negativo; es as como a travs de interneuronas, las fibras paralelas inhiben su propia excitacin, con lo cual frenan la actividad de las clulas de Purkinje. Corteza Cerebral. Es la capa de sustancia gris que recubre los hemisferios cerebrales y que posee un rea de unos 2200 cm2, con unos 14 x 1012 neuronas. La corteza de los hemisferios, junto con la sustancia blanca que envuelve, se puede clasificar desde un punto de vista filogentico y por su significacin sistemtica en dos grandes territorios: neopalio o isocortex y allocortex. El allocortex consta a su vez de dos partes: el paleopalio o corteza olfatoria y el arquipalio, constitudo fundamentalmente por las formaciones del hipocampo y algunos ncleos asociados. El trmino palio significa manto; en cambio paleo significa antiguo. Paleocortex.
126
Las formaciones olfatorias estn ubicadas en la cara inferior orbitaria del lbulo frontal; constituyen el pednculo olfatorio que tiene un bulbo, una cintilla y en el trgono olfatorio se divide en tres races o estras olfativas. Funcionalmente se distinguen: - un rea sensorial, formada por el lbulo piriforme (rea entorrinal), situada en el lbulo temporal; - un rea de asociacin y de centros reflejos, formada por el rea septal y la sustancia perforada anterior (lbulo frontal).
Archicortex. En las formaciones del hipocampo que constituyen gran parte del archicortex o arquipalio, se consideran varias estructuras, como ser: - hipocampo o asta de Amn, que se encuentra en la prolongacin temporal del ventrculo lateral, del cual forma su piso; - giro dentado; - giro supracalloso, que est situado entre el giro del cngulo y el cuerpo calloso; - giro subcalloso; - giro del cngulo. Entre los ncleos involucrados en el arquicortex se encuentran los siguientes: - ncleo amigdalino o archistriatum; - ncleos del septum, situados por delante de la comisura blanca anterior; constituyen un centro importante de empalme, pues reciben aferencias desde el bulbo
127
olfatorio, el hipocampo, el ncleo amigdalino y la corteza prefrontal; es un centro de asociacin entre el rinencfalo, la corteza visceral, el hipotlamo y el epitlamo. Neopalio o isocortex. Forma aproximadamente el 90 % de la superficie hemisfrica. Es un centro de integracin motora y sensitiva, as como el centro de la actividad consciente, voluntaria, intelectual, personal, propiamente psquica, de gran desarrollo en el ser humano. La corteza cerebral est constituda por somas de neuronas y fibras aferentes y eferentes. En general, las clulas van distribudas en seis capas, an cuando distintas reas corticales presentan marcadas diferencias en su constitucin; se describirn brevemente. Capa molecular: es la ms externa, contiene clulas horizontales de Cajal y Golgi tipo II, as como tambin prolongaciones terminales de clulas de capas inferiores, por ejemplo, dendritas apicales piramidales. Capa granular externa o de las pirmides pequeas: es una densa capa de clulas granulares y piramidales. Capa piramidal externa: tiene dos subcapas, segn el tamao de los somas piramidales. Sus dendritas apicales se proyectan a la capa molecular y los axones entran a la sustancia blanca como fibras comisurales o de asociacin. Capa granular interna: est compuesta por clulas estrelladas tipo II de Golgi, cuyos axones se proyectan dentro de la misma capa (cortos) o van a otras capas (largos). Capa piramidal interna o ganglionar o de las pirmides grandes: al igual que las otras capas, se encuentra en toda la neocorteza, pero en el rea motora estn las clulas piramidales gigantes o de Betz, cuyos axones forman parte de los tractos crtico-espinales. Capa de clulas fusiformes o polimorfas.
128
Von Economo clasific cinco tipos de corteza cerebral, segn el predominio celular: I : corteza agranular, que comprende las reas motoras y premotoras; II : corteza frontal, que posee las seis capas tpicas; III : corteza parietal, que tambin posee las seis capas, pero son amplias las capas granulares externa e interna; IV : corteza polar, que se encuentra en las regiones frontal y occipital, con especial desarrollo granular y poco espesor; V : koniocortex o corteza granular, en que predominan los grnulos en todas las capas; est en las reas de proyeccin visual y auditiva. Representaciones corticales. Las reas corticales pueden clasificarse de diversas formas, segn sean receptoras, efectoras o de asociacin, o simplemente mediante un mapeo topogrfico. Utilizando ambos enfoques, se describirn los territorios corticales . I. Centros receptores. Area de la sensibilidad general. Es post-central, ubicada en el giro parietal ascendente. Es el rea smato-sensitiva general primaria, y en ella se puede representar un homnculo sensitivo. La sensacin se completa con la percepcin, es decir, con la interpretacin discriminativa y la sntesis poliestsica; ellas determinan un fenmeno psicolgico complejo, la sensopercepcin, a cargo del rea smato-psquica o post-central intermediaria, que ocupa la mitad posterior del giro parietal ascendente. Y por sobre la sensopercepcin est el reconocimiento, a cargo del territorio tactognstico parietal (pie de los giros parietales superior e
129
inferior). Debe tenerse presente que la sensibilidad de dolor, temperatura y tacto indiscriminado se concreta ya a nivel del tlamo. En la corteza cerebral se produce la discriminacin de las sensaciones en cuanto a reconocer los objetos por el tacto, diferencias de grado e intensidad, localizacin de un punto, reconocimiento de distancia entre dos puntos, etc. Las aferencias sensitivas se analizaron al estudiar la sistematizacin medular (tractos provenientes de la mdula espinal ) y los nervios craneanos (ramas sensitivas). Las eferencias van, en general, hacia zonas motoras de la corteza cerebral. Area gustativa. Se ubica en la parte inferior del giro parietal ascendente. Recibe fundamentalmente impulsos desde la lengua, que van por diferentes vas como ser el glosofarngeo, el trigmino, el tracto solitario, etc. Area auditiva. Est situada en la porcin superior del primer giro temporal (rea supratemporal o giro transverso). Aqu terminan las vas cocleares centrales desde su ltima sinapsis en el cuerpo geniculado medial. Areas vestibulares. Las vas vestibulares terminan en el primer giro temporal. Tambin parecen existir centros vestibulares corticales en los giros frontales primero y segundo, de donde se originan fibras motoras. Area visual. La zona de proyeccin cortical visual es el rea striata, sensoriovisual o calcarina y se proyecta ligeramente sobre el polo occipital. En esta rea terminan las fibras de las radiaciones pticas; alrededor de esta zona sensoriovisual existe una de asociacin visuo-psquica que corresponde a las reas peri y para estriadas, ubicadas en las caras externa e
130
inferior del lbulo occipital; aqu se realiza la sntesis de las sensaciones visuales, percepcin y conocimiento de los objetos. Su alteracin determina la ceguera psquica o agnosia visual. II. Centros efectores. Corresponden a las zonas motoras de las cuales se originan las eferencias de la corteza cerebral, y que pueden dar lugar a actividades motrices voluntarias, automticas, subconscientes y vegetativas. Areas motora y premotora. En el giro frontal ascendente se encuentra el rea motora primaria, cuya capa V posee las clulas piramidales gigantes o de Betz; se le denomina rea smatomotriz y es de ubicacin precentral. Existe tambin una representacin motora somatotpica en forma de homnculo. Las eferencias forman dos grandes fascculos: - crtico-espinal, que llega a la mdula espinal; - crtico-nuclear, que llega a los ncleos motores de los nervios craneanos en el tronco cerebral. Debe tenerse presente que, debido principalmente a la decusacin de las vas crtico-espinales a nivel de las pirmides bulbares, la representacin motora de una mitad del cuerpo est en la corteza motora contralateral. Por delante del rea motora se encuentra el rea premotora, que funciona en estrecha relacin con el rea motora, an cuando precisa de estmulos ms intensos para ser activada. Areas corticales extrapiramidales. Estn en interrelacin regulatoria con centros subcorticales como los ncleos estriados, el ncleo rojo, la sustancia nigra, los ncleos vestibulares, el complejo olivar, la formacin reticular, el cerebelo, etc. Estas reas representan aproximadamente el 85 % de la corteza motora considerada en su totalidad. Se les clasifica en dos grandes grupos:
131
- reas supresoras, y - reas extrapiramidales propiamente tales. Las reas supresoras son capaces de inhibir el funcionamiento del rea motora principal. Se encuentran en los lbulos frontal y occipital y en la corteza cingular. Los impulsos inhibitorios van a los cuerpos estriados y al tlamo, para volver a la corteza cerebral; las fibras efectoras finales van al cuerno medular anterior, probablemente por fibras denominadas parapiramidales. Las reas extrapiramidales propiamente tales se relacionan tambin con estructuras subcorticales, dando origen a numerosas vas, entre las que cabe mencionar: - tracto fronto-pntico, que a su vez en ncleos pontinos sinapta con neuronas ponto-cerebelosas; - tracto parieto-pntico; - tracto tmporo-pntico; - vas crtico-estriadas; - vas crtico-rbricas; - vas crtico-nigras; - vas crtico-mesenceflicas. Las tres primeras, es decir, las vas crtico-pnticas, van al cerebelo y retornan a la corteza cerebral, formando un circuito de retroaccin o feed back de autorregulacin. Areas crtico-culo-cefalgiras. Los bulbos oculares se mueven sinrgicamente y asociados con movimientos de la cabeza. El centro funcional que los coordina se encuentra en la base del segundo giro frontal y enva eferencias a los ncleos de nervios craneanos relacionados con su accin. Areas neurovegetativas. Algunas se encuentran ubicadas alrededor de la cisura central; se relacionan con la salivacin, la masticacin y la deglucin. En el lbulo de la nsula se controlan algunas
132
funciones gastro-intestinales, como el peristaltismo, las nuseas, la defecacin, etc. El giro del cngulo participa en la apnea (detencin de la respiracin). Ciertas partes del rea premotora ejercen control sobre las actividades cardiovasculares y modificaciones del dimetro pupilar. Por ltimo, en la porcin basal de los lbulos frontales hay un rea importante de control sobre la presin arterial, la respiracin y la motricidad gastro-intestinal. III. Areas de asociacin. Son extensas en los seres humanos y se les ubica fundamentalmente en los cuatro lbulos cerebrales clsicos, a saber, frontal, parietal, temporal y occipital. Algunas de ellas, como las de asociacin sensorial, reciben la informacin de las reas primarias y elaboran un mayor nivel interpretativo. Otras tienen funciones especficas como el lenguaje, el control de las habilidades manuales, etc. La corteza frontal est involucrada en la coordinacin motora, en la elaboracin de pensamiento, en el lenguaje, en la memoria de corto plazo, en la respuesta emocional y en el sentido tico. La corteza temporal contiene estructuras lmbicas, reas de proyeccin auditiva, reas de lenguaje y grandes reas de asociacin. En la parte pstero-superior del lbulo temporal, donde entran en contacto los lbulos parietal, temporal y occipital, hay una zona denominada rea interpretativa general, a la que confluyen con su informacin las reas de asociacin somtica, visual y auditiva, constituyendo un rea de asociacin de orden superior. Funcionalmente se relaciona con niveles interpretativos abstractos y pensamientos complejos. En la corteza parietal, salvo el giro post central que es rea sensitiva primaria, todo el resto del lbulo es corteza de asociacin o interpretativa somtica. La corteza occipital contiene fundamentalmente reas visuales, tanto primarias como de asociacin de diferentes niveles de complejidad.
133
Las reas neocorticales tambin se pueden clasificar realizando una distribucin topogrfica o mapeo de la corteza teniendo en cuenta la citoarquitectura y sus caractersticas funcionales. Brodman distingui 47 reas corticales,de las cuales se pueden mencionar, por ser ms conocidas, las reas sensitivas 1 , 2 y 3 de Brodman, la motora 4, la visual primaria 17, la auditiva 41, etc.
PRINCIPALES REAS CORTICALES rea Premotora Movimientos oculares rea Motora rea Sensitiva reas Sensitivas de Asociacin
rea Prefrontal
rea Gustativa primaria
rea Visual primaria
rea del lenguaje de Broca rea Auditiva primaria rea interpretativa general rea Visual de Asociacin
134
Sistema Neurovegetativo. La regulacin de las funciones viscerales est a cargo de una divisin especial del sistema nervioso, denominado por muchos autores sistema nervioso autnomo. Este trmino no es exacto, pues el sistema en s no es independiente, est a lo menos bajo el control del sistema lmbico-hipotalmico. Por ello, parece ms apropiada la denominacin de sistema neurovegetativo o visceral. Realiza sus funciones tanto a nivel reflejo, como por activacin proveniente de sus propios centros o de estructuras nerviosas que los influencian. Las aferencias al sistema nervioso vegetativo provienen de receptores denominados interoceptores ubicados en las vsceras que inerva, constituyendo un arco reflejo visceral. Los efectores estn constitudos por las musculaturas lisa y cardaca, las glndulas exocrinas y la mdula suprarrenal. La accin del sistema neurovegetativo se realiza mediante la accin de neurotransmisores que actan sobre receptores viscerales, lo cual se analizar en el captulo correspondiente a sus funciones. Las vas neurovegetativas son complejas, dndose en ellas la caracterstica nica de poseer ganglios en la va efectora. Estas vas pueden ser exclusivas, o bien sus fibras pueden formar parte del sistema somtico, lo cual tambin ocurre con parte de sus vas aferentes. Las vas motoras neurovegetativas poseen dos neuronas que sinaptan a nivel de los ganglios, por lo cual a la primera neurona eferente se le denomina preganglionar y la segunda neurona, que es la que inerva directamente las vsceras, se le denomina neurona postganglionar. El sistema neurovegetativo est compuesto por dos grandes divisiones: el sistema simptico o traco-lumbar u ortosimptico y el sistema parasimptico o crneo-sacro.
135
SISTEMA NEUROVEGETATIVO
136
Simptico
Parasimptico
Mesencfalo Puente cervical
torcica
lumbar sacra
Preganglionar Postganglionar
Sistema simptico. Su nombre de traco-lumbar proviene del hecho que tiene centros de origen ubicados en la mdula torcica y lumbar. Las vas sensitivas se originan en interoceptores o receptores viscerales; sus fibras van distribudas en conjunto con las fibras eferentes en los nervios simpticos; en las cercanas de la mdula espinal, las fibras aferentes pasan a los nervios espinales somticos, directamente o formando manojos de fibras denominadas ramos comunicantes blancos. Los somas de estas neuronas sensitivas se ubican en los ganglios espinales sensitivos somticos y luego los neuritos centrales de las fibras sensitivas penetran a la mdula espinal por la raz posterior, alcanzando las astas posteriores medulares; las fibras neurovegetativas se distribuyen en el fascculo de Lissauer y van dando colaterales a los centros vegetativos medulares, ya
137
sea de la columna intermediolateral (cuernos laterales que se encuentran entre C8 y L3) o de la sustancia gris yuxtaependimaria. A estos centros espinales les pueden llegar influencias de ncleos o centros enceflicos, especialmente del tronco cerebral, del hipotlamo y an de la corteza cerebral.
VAS SIMPTICAS
Las fibras que se originan de las neuronas que conforman los centros simpticos espinales van a constituir las vas simpticas eferentes o motoras, que poseen dos neuronas, las cuales hacen sinapsis en los ganglios simpticos.
Los ganglios simpticos constituyen dos grandes grupos; uno de ellos es la cadena simptica paravertebral y el otro grupo lo constituyen los ganglios colaterales.
138
La cadena simptica ganglionar es un conjunto linear de 22 a 23 ganglios neurovegetativos de ubicacin paravertebral; a ellos les llegan las fibras pre-ganglionares que emergen de la mdula espinal por los cuernos ventrales, junto con las fibras motoras somticas, de las cuales se separan para formar parte de los ramos comunicantes blancos y llegan a los ganglios paravertebrales; las fibras pre-ganglionares pueden inervar ganglios simpticos al mismo nivel espinal de emergencia, o bien inervar ganglios ms rostrales o caudales formando parte del tronco ganglionar conectivo; cada fibra pre-ganglionar sinapta con muchas neuronas post-ganglionares que a menudo van distribudas entre diferentes ganglios paravertebrales. Las fibras post-ganglionares salen de los ganglios paravertebrales formando los ramos comunicantes grises. A nivel de los ganglios paravertebrales se producen dos situaciones que se describen a continuacin. Existen fibras que sinaptan en los ganglios de esta cadena, por lo cual de ellos se originan fibras postganglionares; las fibras preganglionares que salen de la mdula torcica pueden llegar a ganglios paravertebrales cervicales, que son tres: superior, medio e inferior, y que inervan estructuras viscerales de cabeza, cuello, corazn, pulmones y bronquios; o bien pueden sinaptar con ganglios paravertebrales de su nivel de emergencia espinal. En trminos generales, estas fibras postganglionares de la cadena paravertebral pueden seguir varias vas en su trayecto hacia las vsceras efectoras: - con los nervios espinales perifricos; - formando nervios especficos, como los cardacos y farngeos; - asociadas a vasos sanguneos formando plexos como los plexos articos y carotdeos. Otro gran grupo de fibras post-ganglionares simpticas pasan por la cadena de ganglios paravertebrales sin sinaptar, por lo cual cuando salen de ellos an son fibras preganglionares que constituyen tres grandes grupos:
139
- las fibras preganglionares que se originan entre T6 a T9 pasan a constituir el nervio esplcnico mayor y terminan haciendo sinapsis con las neuronas del ganglio celaco y clulas de la mdula suprarrenal; - fibras preganglionares que emergen de los segmentos T10 a T12 forman el nervio esplcnico menor y terminan en los ganglios celacos, mesentricos superiores y artico-renales; - fibras preganglionares del segmento T12 forman generalmente el nervio esplcnico inferior que termina en el ganglio articorenal. Las fibras post-ganglionares emergen de estos ganglios colaterales y van a inervar vsceras abdominales como vas biliares, bazo, estmago, intestinos, mdula suprarrenal, riones, y vsceras plvicas como colon, recto,vejiga urinaria y rganos genitales. En trminos generales, las fibras preganglionares simpticas son ms cortas que las fibras postganglionares. Sistema parasimptico. Su nombre de crneo-sacro deriva del hecho de tener ncleos de origen en el encfalo y centros espinales que derivan de la columna intermedio-lateral de S2 a S4. La informacin aferente proviene, al igual que la del simptico, de receptores ubicados en las vsceras que inerva; y tambin los ncleos del parasimptico pueden recibir influencias de diferentes estructuras del sistema nervioso. Los ganglios sensitivos son propios, ubicados segn sea el nervio craneano que contiene las vas aferentes. En cambio, los ganglios de las vas eferentes se encuentran ubicados en las mismas vsceras que inervan o en sus cercanas, lo cual determina que las fibras parasimpticas preganglionares sean largas comparadas con las fibras postganglionares que son cortsimas. Las aferencias del parasimptico craneal van en las fibras sensitivas de nervios craneanos.
140
El nervio facial conduce la informacin sensitiva visceral de la cara, el odo medio, la faringe y las glndulas salivales; los somas neuronales estn ubicados en el ganglio geniculado. El nervio glosofarngeo lleva impulsos sensitivos de la lengua, las tonsilas, la trompa de Eustaquio y los cuerpos carotdeos; los somas neuronales estn en el ganglio petroso y los neuritos centrales van al ncleo solitario junto con las fibras sensitivas del facial y del vago. El nervio vago lleva numerosas fibras sensitivas provenientes del aparato digestivo, el sistema respiratorio, el arco artico, el atrio derecho, etc.; los cuerpos neuronales estn en el ganglio nudoso del vago y los neuritos centrales forman parte del tracto solitario con el cual llegan al ncleo del mismo nombre. Las aferencias de la divisin sacra del parasimptico provienen de receptores de las vsceras plvicas y pasan por los respectivos ganglios sensitivos. Como se dijo, los centros espinales estn entre S2 y S4; las fibras eferentes de estos centros abandonan la mdula espinal constituyendo los nervios plvicos y junto con ramas de los ltimos nervios simpticos, forman el plexo hipogstrico que regula el funcionamiento de los rganos urinarios, genitales y colon. La porcin craneal del sistema parasimptico posee varios ncleos que dan origen a las eferencias de dicho sistema. Dichos ncleos y sus eferencias son: - ncleo de Edinger-Westphal, que est ubicado en la parte rostral del mesencfalo; sus fibras van con las del III par craneano hasta el ganglio ciliar; las fibras postganglionares inervan el msculo ciliar y el constrictor o esfnter pupilar; - ncleos salivales superior e inferior, que estn ubicados en la formacin reticular ponto-bulbar; el superior sinapta en el ganglio submaxilar y el inferior en el ganglio
141
tico; las fibras postganglionares inervan las glndulas salivales; - ncleo lacrimal, de ubicacin ponto-bulbar; sus fibras hacen estacin en el ganglio esfeno-palatino, de aqu las fibras postganglionares van en el trigmino, en el nervio esfeno-palatino, para inervar las glndulas lacrimales y de la mucosa nasal y palatina; - ncleo motor dorsal del vago, situado en la fosa romboidal; los ganglios estn en las vsceras que inerva o en sus cercanas, que son principalmente la musculatura atrial, el ndulo sinusal del automatismo cardaco, la musculatura lisa bronquial, el esfago, el estmago, el intestino y la vescula biliar. Plexos neurovegetativos. La distribucin de las fibras simpticas y parasimpticas hacia las vsceras se puede realizar por medio de conjuntos de redes nerviosas denominadas plexos, de los cuales se pueden describir los siguientes: - plexo cardaco, formado por nervios simpticos cardacos y ramas del vago; inerva el corazn y los grandes vasos; - plexos pulmonares, formados por el vago y nervios simpticos torcicos superiores; inervan bronquios y arteria pulmonar; - plexo celaco o solar, que posee fibras vagales y simpticas; est situado en el epigastrio e inerva las vsceras abdominales a travs de sub-plexos; - plexo hipogstrico, que recibe fibras simpticas del plexo artico y ganglios lumbares, as como fibras parasimpticas del nervio plvico.
142
IV.- NEUROFISIOLOGIA. El funcionamiento biolgico del sistema nervioso constituye su fisiologa; en cambio, las funciones que se relacionan con los fenmenos psicolgicos como memoria, emociones, lenguaje, etc. constituyen la psicofisiologa. El elemento ms bsico en el funcionamiento del sistema nervioso lo constituyen los biopotenciales, que se podran considerar como las unidades funcionales de este sistema, as como la neurona es su unidad morfo-funcional, es decir, la estructura en que se desarrollan las funciones primarias del sistema nervioso. Biopotenciales. Debido a la composicin diferente de los lquidos intra y extracelulares, resulta que a ambos lados de la membrana celular, las concentraciones inicas son diferentes, lo que va a determinar que a travs de dicha membrana se produzca una diferencia de potencial elctrico. Estas diferencias inicas son dinmicas, producidas ya sea por difusin, por transporte activo, por cambios en la permeabilidad de la membrana, etc. Los biopotenciales adquieren especial importancia en el funcionamiento de las neuronas, de las fibras musculares estriadas, lisas y cardacas y en las clulas de marcapasos. Se pueden distinguir: -un potencial de reposo o de membrana; -potenciales de actividad, entre los cuales se pueden mencionar el potencial de accin, cuya propagacin constituye el impulso nervioso, los potenciales sinpticos, los potenciales generadores o de receptores, los potenciales de marcapaso. Como estos potenciales se deben a diferencias inicas, es conveniente analizar brevemente sus concentraciones intra y extracelulares.
143
Potencial de membrana o de reposo. No es un nombre muy apropiado en el sentido que todos los biopotenciales se producen en las membranas celulares y en parte su mecanismo de produccin es en este caso un transporte activo. No obstante, se le denomina de reposo porque se produce en ausencia de estmulos especiales. Las clulas de un organismo vivo son excitables, es decir, modifican su permeabilidad inica frente a estmulos. Normalmente, la membrana celular es permeable al agua y solutos, pero prcticamente impermeable a las protenas por mecanismos de difusin. Las sustancias liposolubles atraviesan la membrana celular disolvindose en ella; en cambio el agua y los solutos pasan a travs de canales cuyas paredes desarrollan tambin cargas elctricas. Al pH de los lquidos tisulares, las protenas se comportan como aniones, por lo cual la diferencia de concentraciones proteicas en el interior celular con respecto al exterior, determina que aniones difusibles salgan al espacio extracelular movidos por gradiente electro-qumica; esta tendencia a mantener el equilibrio electro-qumico se denomina equilibrio de Gibbs-Donnan. En la parte interna de la membrana celular se acumula un exceso de iones negativos o aniones y por fuera de ella un nmero similar de iones positivos o cationes.
144
Los potenciales de difusin de cada in se pueden medir separadamente. Para el caso del potencial de reposo se han medido los potenciales de difusin del potasio y del sodio, por ser los principales cationes involucrados. Resulta que la membrana celular es muy permeable al potasio, pero slo ligeramente permeable al sodio, de modo que la difusin del potasio contribuye mayoritariamente a mantener una diferencia de potencial en reposo. De hecho, en una fibra nerviosa normal,por ejemplo , la membrana celular es unas 100 veces ms permeable al potasio que al sodio. En cuanto a los aniones , o no pueden difundir o lo hacen pobremente, por lo cual las cargas negativas tienden a permanecer en el interior celular. Pero adems en la membrana celular existe un mecanismo de transporte activo de iones cual es la bomba Na + - K+ . Este es un mecanismo de transporte activo que realiza un bombeo continuo de los iones involucrados, aunque no en la misma proporcin, es decir, por cada tres iones Na + que saca desde el interior al exterior, slo bombea dos iones K+ hacia el interior. Dicho en otras palabras, se est produciendo continuamente una prdida de cargas positivas en el interior de la membrana. Ambos mecanismos, de transporte activo por la bomba Na+ - K+ y de mayor difusin del potasio, determinan la diferencia de potencial conocida como potencial de reposo o de membrana, que en la membrana de la fibra nerviosa y en las grandes fibras musculares estriadas, puede alcanzar un valor de -90 milivolts; en cambio, en las fibras musculares lisas y en muchas neuronas del SNC puede ser de -40 a -60 milivolts. En otros trminos, la bomba mencionada tiene un efecto electrognico, puesto que saca ms cationes desde el interior celular que los que introduce. La bomba Na+ - K+ es quien mantiene las grandes gradientes de concentracin intra y extracelular para los iones involucrados, las que medidas en mEq/L son: Na+ extracelular 142
145
Na+ intracelular K+ extracelular K+ intracelular
14 4 140
La bomba Na+ - K+ est constituda por dos protenas globulares diferentes, llamadas subunidades alfa y beta. La subunidad alfa, de mayor tamao, posee tres caractersticas especficas: 1.- posee tres sitios receptores para el sodio en la parte interna (hacia el interior celular), 2.- posee dos sitios receptores para el potasio en la parte que da al exterior celular; 3.- su parte interna posee actividad ATPasa. Cuando entra el sodio, se activa la funcin ATPasa, la cual desdobla al ATP liberando un enlace fosfato de alta energa, la cual moviliza ambos iones, sodio hacia el exterior y potasio hacia el interior. El mecanismo de bomba se trata de un transporte activo que como tal: 1.- gasta energa, que la provee el ATP; 2.- transporta elementos contra gradiente de concentracin o electro-qumica 3.- utiliza transportadores; 4.- es susceptible de bloquearse. El potencial de reposo se puede medir y calcular. La medicin se realiza mediante un microelectrodo colocado en el interior celular y otro indiferente en el exterior de la membrana celular, ambos conectados a un voltmetro que mide la diferencia de potencial a ambos lados de la membrana celular. Se ha acordado que el signo del biopotencial va a ser el que exista en el interior celular, motivo por el cual el potencial de membrana es negativo. Tambin se puede calcular mediante ecuaciones, como la de Goldman-Hodgkin-Katz, que considera los iones sodio, potasio y cloruro. Una forma ms simple e igualmente efectiva es la ecuacin de Nernst, que considera lo siguiente:
146
RT C1 FEM (milivolts) = ---- ln ---ZF C2 en que: FEM es la fuerza electromotriz o diferencia de potencial R es la constante universal de los gases perfectos T es la temperatura absoluta Z es la valencia del ion F es la constante de Faraday C1 y C2 son las concentraciones inicas extra e intracelular Para el caso del potasio, de valencia 1,considerando temperatura de 20 C y cambiando ln por log10 , la ecuacin se simplifica a: 4 FEM = 58 mV log10 ---- = 58 x log 0,02857 = 58 x (-1,54407) 140 FEM = - 89,556 mV. Potencial de accin. Las informaciones, aludiendo especialmente al sistema nervioso, se transmiten por medio de impulsos nerviosos, que son potenciales de accin (PA) propagados. Los potenciales de accin son cambios del potencial de membrana, provocados porque algn estmulo modifica en forma rpida, la permeabilidad de la membrana a los iones sodio, primero, y luego a los iones potasio; estos estmulos pueden ser elctricos, mecnicos, qumicos, etc. En relacin a la produccin del potencial de accin, al potencial de reposo se le considera como una fase polarizada, con un potencial negativo interior. Cuando se aplica un estmulo a la membrana de la fibra nerviosa, aumenta su permeabilidad al sodio(se abren los canales de sodio) entre 500 a 5000 veces, por lo cual este catin penetra violentamente al interior celular, el cual se torna primero menos negativo y luego positivo, es decir,
147
de un estado polarizado de reposo, pasa a una fase de despolarizacin; puede alcanzar apenas el nivel cero (fibras pequeas y algunas neuronas del SNC) hasta unos +40 mV en fibras nerviosas grandes. La entrada del sodio al interior de la membrana se refuerza por mecanismos de feed back positivo. Unos diezmilsimos de segundo depus de la apertura de los canales de sodio, stos comienzan a cerrarse, se cierran y se abren los canales de potasio ms de lo habitual. Como en el interior existe un exceso de cargas positivas y los canales de sodio estn cerrados, ahora sale el potasio, con lo cual el potencial tiende de nuevo a volver a los valores de reposo, es decir, a hacerse negativo, pero ahora con los iones sodio en el interior y los iones potasio en el exterior. Esta vuelta a los valores del potencial de membrana se denomina fase de repolarizacin. Causas del potencial de accin. . En los movimientos inicos a travs de la membrana celular es preciso considerar : 1.- los canales de escape de sodio y potasio; 2.- la bomba de sodio-potasio; 3.- los canales de sodio con puertas de voltaje (potenciales de compuerta) 4.- los canales de potasio con puertas de voltaje. Los dos primeros participan fundamentalmente en el potencial de reposo, los dos ltimos son esenciales en la produccin del potencial de accin. El canal de sodio con puerta de voltaje posee dos puertas, una puerta de activacin ubicada cerca del exterior del canal, y otra prxima al interior, denominada puerta de inactivacin. El estmulo capaz de provocar un potencial de accin "abre" la puerta de activacin, con lo cual penetran violentamente los iones sodio al interior de la membrana. Algunas diezmilsimas de segundo despus, se cierra la puerta de inactivacin, con lo cual el ion sodio no puede entrar ms pero tampoco salir; esta puerta
148
de inactivacin no se volver a abrir hasta que el potencial se aproxime al valor del potencial de reposo. Pero en la medida que el potencial sobrepasa el valor cero y se hace positivo, cambia la conformacin de las puertas de potasio y dejan salir a este ion, el que difunde hacia el exterior por la gran gradiente electroqumica positiva en el interior con respecto al exterior. En otros trminos, mientras los canales de sodio se estn cerrando, los de potasio se estn abriendo. Las aperturas de los canales de sodio y potasio se refuerzan por mecanismos de feed back positivo. En la etapa final de la repolarizacin, la bomba sodio-potasio restaura las concentraciones inicas originales, es decir, el sodio sale y el potasio entra. En la fase de repolarizacin es posible distinguir, en la primera parte, una subfase llamada perodo refractario absoluto, pues ningn estmulo es capaz de provocar un nuevo potencial de accin; pero a medida que transcurre la fase de repolarizacin, los canales de sodio son susceptibles de reabrirse por estmulos supraumbrales, con lo cual se puede obtener una nueva respuesta. Debido a los mecanismos descritos, en la fase de repolarizacin se tiende a alcanzar los valores del potencial de reposo, pero los iones estn trastocados, es decir, el sodio est mayoritariamente en el interior de la membrana y el potasio en el exterior. Es la bomba Na - K quien restablece la condicin original del potencial de membrana. Por otra parte, en esta fase se producen pequeas variaciones del potencial, que oscila alrededor del potencial de reposo, produciendo breves estados an de hiperpolarizacin. Caractersticas del potencial de accin. 1.- Umbral de excitacin. Existe una intensidad mnima del estmulo para que ste sea capaz de excitar a la membrana, es decir, aumente su permeabilidad inica a tal punto que se desencadene el potencial de accin. Esta intensidad mnima constituye el umbral de excitacin de la fibra nerviosa.
149
La excitabilidad de la fibra puede variar, en cuyo caso tambin varan los umbrales de excitacin; por ejemplo, el ion calcio normalmente disminuye la permeabilidad al sodio, por lo cual se precisan estmulos umbrales mayores; si el calcio disminuye, la membrana se vuelve hiperexcitable. 2.- Ley del todo o nada. El potencial de accin, una vez producido, se desarrolla siempre con su mxima intensidad; dicho de otro modo, o se produce al mximo o no se produce. Ello significa que no es la intensidad del PA quien puede dar cuenta de cambios en la informacin a que da lugar. 3.- Propagacin. Los potenciales de accin se pueden propagar a lo largo de una fibra nerviosa, lo que constituye el impulso nervioso. Esta propagacin puede realizarse hacia ambos lados de la fibra , pero en el individuo vivo, la disposicin de las neuronas en las vas nerviosas (sucesin de neuronas que transmiten una informacin definida) le imprime un carcter unidireccional; a esto contribuye tambin la asimetra de la sinapsis o contacto entre dos neuronas (o neurona con fibra muscular). 4.- Los PA se propagan con una cierta frecuencia, que es importante porque es la caracterstica que va a modular la intensidad de la informacin que se transmite. Dicho de otro modo, en lo que se refiere a transmisin, se realiza en FM o modulacin de frecuencia, y no en AM o modulacin de amplitud, lo que s sucede en potenciales locales como los sinpticos o los de receptores. La propagacin de los impulsos nerviosos depende fundamentalmente de dos caractersticas de las fibras nerviosas: - su condicin de mielnica o amielnica, transmitiendo las primeras a mayor velocidad; - el grosor de la fibra misma, transmitiendo a mayor velocidad las ms gruesas . Esta velocidad transmite desde velocidades tan pequeas como 0,2 metros/segundo hasta 120 metros/segundo.
150
Los potenciales de accin se pueden producir tanto en las neuronas como en las fibras musculares. En las fibras musculares cardacas, la membrana no se repolariza inmediatamente despus de la despolarizacin, formando una "meseta" de algunos milisegundos antes que comience la repolarizacin. Al analizar las causas de este fenmeno, es necesario tener presente que existen dos tipos de canales inicos: a) los canales rpidos de sodio y b) canales de calcio que son lentos, y que permiten adems la difusin lenta del sodio; es esta difusin lenta del sodio la responsable de la meseta antes descrita. Tambin pueden contribuir a ella una apertura ms lenta de los canales de potasio responsables de la repolarizacin, que no se abren totalmente sino hasta el final de la meseta. 5.- Perodos refractarios. Estos perodos, ya descritos, constituyen tambin una caracterstica de los potenciales de accin. 6.- Relacin intensidad tiempo. Ya se estableci que los estmulos, para ser eficaces, deben tener cierta intensidad; se necesita tambin que dicho estmulo se aplique durante un cierto tiempo. Si se correlacionan ambas variables se obtiene una curva intensidad tiempo, en la cual se distinguen dos caractersticas: la reobase y la cronaxia. Se denomina reobase a la mnima intensidad de un estmulo capaz de excitar una fibra, cuando dicho estmulo tiene una duracin indefinida; en cambio, la cronaxia es el tiempo mnimo que debe durar un estmulo de intensidad igual al doble de la reobase para desencadenar una respuesta. Sinapsis y Neurotransmisores. Las sinapsis son zonas en que se transmiten las seales o informaciones entre dos neuronas o entre una neurona y un
151
efector, que puede ser un msculo, por ejemplo. Existen sinapsis qumicas y elctricas. Las sinapsis elctricas se comunican mediante canales por los cuales los impulsos elctricos se transmiten en forma directa. Por lo general contienen pequeas estructuras tubulares proteicas denominadas uniones intercelulares laxas, que algunos autores denominan gap junctions o uniones comunicantes; ellas permiten el paso de iones por el interior de las clulas que sinaptan. En estas uniones comunicantes la resistencia elctrica es baja, de modo que los potenciales elctricos pueden fluir a travs de ellas con facilidad. Este mecanismo se puede observar en el msculo liso y en el msculo cardaco. Existen unas pocas sinapsis elctricas en el sistema nervioso central, sin funcin conocida. Las sinapsis elctricas pueden transmitir los potenciales en ambas direcciones. Se denomina rectificacin al hecho que estas sinapsis transmiten ms rpido en un sentido que en el otro. Adems, en ella no existe retardo sinptico. Las partculas intramembrana son seis unidades que rodean un canal central accesible al agua; este conjunto hexagonal se denomina conexn y cada una de las unidades es una protena llamada conexina. Los conexones de clulas acopladas estn alineados formando canales de conexones; por estos canales se produce el flujo de corriente. Los canales pueden cerrarse por aumento del calcio intracelular o de iones hidrgeno o bien por despolarizacin de una de ambas clulas. En cambio, en el sistema nervioso, la gran mayora de las sinapsis son de tipo qumico; fundamentalmente en este captulo se describirn los contactos entre neuronas, y en el captulo correspondiente a msculo estriado se describir el funcionamiento de la placa motora o sinapsis neuromuscular. En las neuronas, cualquiera de sus partes puede contactar con otra neurona; as, en los mamferos existen sinapsis axosomticas y axodendrticas (90 % ), axoaxnicas ( 9 % ),
152
dendrosomticas, dendrodendrticas, dendroaxnicas, smatosomaticas, smatodendriticas y smatoaxonicas ( 1 % ). Estructura de la sinapsis qumica.
153
SINAPSIS
Axn
Microfilamentos
Microtbulos Ion sodio
Vesculas de neurotransmisor
Molculas de neurotransmisores
Canal abierto Lugares de recepcin del neurotransmisor Canal cerrado
154
En ella es posible distinguir tres partes fundamentales, cuales son la porcin presinptica, la hendidura sinptica y la porcin postsinptica. La porcin presinptica pertenece a la neurona presinptica y forma en esta regin un botn o pie terminal, que puede estar en nmero de 1 a 5500 por neurona postsinptica. El botn se caracteriza porque en l se encuentran las vesculas sinpticas, en que estn almacenados los neurotransmisores como verdaderos paquetes multimoleculares o quanta. Ms adelante se explicar que la porcin presinptica contiene un tipo especial de receptor denominado autorreceptor, y eventualmente hay heterorreceptores, que actan con los moduladores de la respuesta sinptica. En el pie terminal existen en el citoplasma abundantes mitocondrias, neurofilamentos, microtbulos y retculo endoplsmico liso. La hendidura sinptica es el espacio que existe entre las membranas pre y postsinpticas, y su tamao es por lo general pequeo, del orden de unos 200 ngstrom, pero tambin puede medir milmetros, como es el caso de las terminaciones neurovegetativas de la musculatura lisa del iris. Las sustancias neurotransmisoras que se liberan desde las vesculas sinpticas entran a la hendidura, donde pueden ser destrudas por enzimas degradadoras; no obstante, la mayor parte de las molculas de neurotransmisores logran llegar a los receptores postsinpticos. La porcin postsinptica pertenece a la neurona postsinptica y se caracteriza por poseer receptores especficos para cada neurotransmisor. Cuando ambos, receptor y neurotransmisor se unen, conforman la unin receptorneurotransmisor ( R NT ), que puede producir su efecto especfico en la segunda neurona. Es frecuente que las dendritas postsinpticas posean espinas dendrticas, que son sitios especializados para recibir los contactos sinpticos. Como se observa por la descripcin anterior, la sinapsis es asimtrica, por cuanto las porciones pre y post sinpticas son
155
diferentes; esta asimetra determina que en condiciones in vivo, la transmisin de la informacin sea unidireccional, desde la regin presinptica a la postsinptica. El concepto de receptor ( R ) se debe a Langley (1905), basado en la potencia y especificidad de algunos frmacos. Los receptores postsinpticos son macromolculas proteicas que reconocen al neurotransmisor en forma estereoespecfica, saturable y reversible. El trmino receptor se refiere a todo el complejo bioqumico asociado que se requiere para producir el efecto biolgico. Los receptores sinpticos tienen dos componentes importantes: 1) un complejo de fijacin, que asoma a la hendidura; 2) un componente ionforo que atraviesa la membrana hasta el interior de la neurona postsinptica. A su vez, el componente ionforo puede ser de dos clases: un canal, o bien un activador del segundo mensajero. El canal puede ser: - canal de cationes, generalmente sodio, a veces potasio y calcio; estos canales estn rodeados de cargas negativas que atraen cationes y repelen aniones; - canal de aniones, por el que pasa especialmente cloro y en parte otros aniones; estos canales actan ms bien por tamao; como el cloro es pequeo, el canal se abre y pasa el cloro, pero no los cationes hidratados. El activador del segundo mensajero, que no es un canal inico, activa dentro de la neurona una o ms sustancias. Dicho de otro modo, un receptor puede activar varias unidades bioqumicas de transduccin. Los receptores se podran clasificar en: -receptores unidos directamente a canales inicos, denominados tambin receptores ionotrpicos; al unirse al neurotransmisor o frmaco, abren el canal; por este mecanismo actan los receptores nicotnicos de acetilcolina, los de glicina y
156
de GABA; -receptores unidos a sistemas bioqumicos de segundos mensajeros (receptores metabotropos); en este caso el receptor est unido a una enzima amplificadora, a travs de una verdadera familia de protenas, que constituyen las protenas G. Para su activacin, las protenas G precisan unirse al GTP, al que una GTPasa convierte en GDP. Hay protenas G activadoras (Gs) e inhibidoras (Gi) de la adenilcilasa. A este nivel, parece conveniente describir brevemente los canales inicos en general. Estos canales se pueden concebir como macromolculas proteicas dentro del plano fludo lpido de la membrana, que pueden o no permitir el paso de iones a travs de ellos. Sus cambios conformacionales son sensibles a los cambios elctricos que operan en las membranas; al facilitar o retardar los cambios conformacionales, los canales inicos son gatillados. A este respecto, el calcio acta en la superficie de la membrana alterando su permeabilidad debido al efecto que ejerce su carga elctrica sobre el campo elctrico de cargas orgnicas negativas; sus potenciales despolarizantes pueden determinar que estas macromolculas prefieran la conformacin abierta a la cerrada al flujo inico. Los canales mejor descritos son los del sodio, potasio, calcio y cloruro. Segn Hille, los canales son verdaderos poros que se abren o cierran en forma todo o nada, en tiempos de 0,1 a 10 milisegundos para proporcionar canales acuosos a travs de la membrana plasmtica que pueden atravesar los iones. Existen diferentes clases de canales inicos: 1) canales pasivos a iones, denominados filtracin, que estn continuamente abiertos; canales de
2) canales dependientes de voltaje o sensibles a voltaje, cuyos cierres y aperturas son afectados por el potencial de membrana dentro de las clulas; 3) canales qumicamente gatillados cuyos cierres y aperturas estn determinados por receptores de la membrana
157
plasmtica externa, como aqullos afectados por drogas y otros transmisores; estos canales tambin pueden ser sensibles a segundos mensajeros celulares, como el AMP cclico; 4) canales gatillados por iones, cuyos cierres y aperturas son afectados por cambios en las concentraciones inicas intracelulares; generalmente son sensibles al potencial de membrana y a receptores reguladores externos. Los canales qumicamente gatillados son a menudo sensibles a voltaje. Los canales de calcio se gatillan por diferentes intensidades en las seales; se han descrito canales T, L y N, que se gatillan por diferentes drogas, iones y voltajes, y adems presentan diferentes tiempos de apertura. As por ejemplo, el canal L puede ser bloqueado por la nifedipina. En la accin R NR (neurorreguladores ) y los canales de calcio est involucrada la protena G y segundos mensajeros como el AMP cclico y el DAG o diacilglicerol. La entrada de calcio al botn terminal (ms bien su presencia en este terminal) es sumamente importante, puesto que puede participar en la degeneracin neuronal del envejecimiento o destruccin neuronal por txicos ambientales o por hipoxia isquemia. Hay protenas reguladoras que ligan calcio, como la calmodulina, que es una protena reguladora involucrada en la activacin de enzimas pre y post sinpticas; tambin la calcineurina, capaz de inactivar canales de calcio despus que ingresa el ion, es decir, desarrolla un mecanismo de retroaccin negativa que impide la saturacin del sistema. Otras protenas de este tipo son la calbindina (28 kDa) y la protena PEP 19 (7,6 k Da). Estas protenas estn distribudas en forma diferente en distintos grupos neuronales; por ejemplo, la calbindina se encuentra en las clulas de Purkinje, en las clulas
158
dopaminrgicas nigroestriadas, en las clulas piramidales del hipocampo; por ello se supone podran estar involucradas en las enfermedades de Parkinson y de Alzheimer. Funcionamiento de la sinapsis qumica. Los impulsos nerviosos de la neurona presinptica llegan a la porcin presinptica, donde van favoreciendo que las vesculas sinpticas se vayan ubicando, concentrando, hacia la membrana presinptica. Estos impulsos tambin aumentan la permeabilidad de dicha membrana a los iones calcio, que se movilizan por canales de calcio con barrera dependiente de voltaje. Las vesculas sinpticas se adosan a la membrana del botn terminal, se fusionan ambas y por un proceso de exocitosis dependiente de calcio, los neurotransmisores se liberan hacia la hendidura sinptica. Desde aqu, su funcin principal es unirse a los receptores postsinpticos en forma especfica, ambos se reconocen entre s como la cerradura a su llave, y van a producir el efecto correspondiente. No obstante, parte de las molculas neurotransmisoras son destrudas en la hendidura por enzimas degradadoras, otras pasan a la circulacin general, otras son recaptadas de nuevo hacia el interior de los botones presinpticos, otras se unen a los autorreceptores del botn o pie terminal. En este ltimo caso, la unin receptor neurotransmisor ( R - NT ) gatilla un mecanismo de feed back negativo con respecto a la exocitosis, es decir, mientras ms uniones se realicen, menos liberacin de neurotransmisor se produce. Cuando la unin R NT modifica la permeabilidad inica, pueden producirse fenmenos de excitacin o de inhibicin en la membrana postsinptica. La excitacin, consecuencia de una despolarizacin de la membrana postsinptica, se produce principalmente por un aumento de la permeabilidad al sodio, el cual penetra al interior de la membrana y desarrolla un PEPS o potencial excitatorio postsinptico; tambin participan en su produccin una disminucin del paso de los cloruros, del potasio o de ambos; y por cambios metablicos celulares que aumenten la actividad celular, como tambin por aumento del nmero de receptores
159
excitadores o disminucin del nmero de receptores inhibidores. Este PEPS es susceptible de sumarse espacial y temporalmente; cuando solo o sumado alcanza el umbral de excitacin de la neurona postsinptica, se producen en sta nuevos potenciales de accin que se propagan, y la informacin contina por la va nerviosa. El PEPS es un potencial local, aumenta la excitabilidad de la neurona postsinptica a otros estmulos, presenta sumacin espacial y temporal y no responde a la ley del todo o nada, es decir, su magnitud es proporcional a la intensidad del estmulo(magnitud de las uniones R NT ). Sumacin espacial. Un botn terminal libera neurotransmisor que produce un PEPS no mayor que 0,5 a 1,0 milivolt y se necesitan 10 a 20 milivolts (mV) para alcanzar el umbral habitual de excitacin. Si se activan varios terminales simultneamente, sus efectos pueden sumarse espacialmente. En la sumacin temporal, cuando se activa un terminal, los canales se abren por 1 milisegundo y un PEPS dura unos 15 milisegundos; un segundo potencial alcanza a aumentar ms el PEPS dentro de los 15 milisegundos, es decir , se suman los potenciales en el tiempo. Se pueden sumar PEPS sucesivos. Sin embargo, los PEPS pequeos dejan algo excitada a la neurona, se dice que est facilitada, su potencial de membrana est ms cerca del umbral de excitacin, por lo cual es ms fcil de estimular. Por otra parte, si el aumento de la permeabilidad inica de la membrana postsinptica, consecuencia de la unin R NT, es a los iones cloruro (entran) y /o potasio (salen), los primeros entran al interior de la membrana y los iones potasio salen del interior, con lo cual sta se hiperpolariza, se produce un PIPS o potencial inhibitorio postsinptico; en este caso, la informacin se detiene a este nivel, no continuando por la neurona postsinptica. A la produccin del PIPS tambin puede contribuir la activacin de enzimas del receptor que inhiban las funciones metablicas
160
celulares. El PIPS tiene caractersticas similares al PEPS en el sentido que se trata de un potencial local, presenta sumacin espacial y temporal, no responde a la ley del todo o nada y hace menos sensible a la neurona postsinptica frente a otros estmulos. Tambin pueden producirse procesos inhibitorios a este nivel por inhibicin de las funciones metablicas celulares. En todo caso, la respuesta resultante a nivel sinptico va a depender de un balance entre los PEPS y los PIPS producidos. El mecanismo de apertura y cierre de los canales es un mecanismo rpido; en algunas funciones del sistema nervioso, como la memoria por ejemplo, las funciones de transmisin se realizan por el sistema del segundo mensajero, que son capaces de provocar cambios prolongados. Entre estos mecanismos puede mencionarse el del grupo de la protena G que funciona de la siguiente forma. Cuando un neurotransmisor se une a un sitio del receptor, se activa la protena G, que posee tres subunidades, alfa, beta y gama. La subunidad alfa se desprende de la protena G y se desplaza hacia el citoplasma celular, donde puede producir una de diversas reacciones: 1.- abrir canales inicos especficos, pero estos canales, a diferencia de la apertura y cierre producidos directamente por los mecanismos previamente explicados, permanecen abiertos por tiempos prolongados, por lo cual sus efectos tambin lo son; 2.- activar al AMP cclico o al GMP cclico a travs de la activacin de las enzimas adenilciclasa o guanilciclasa respectivamente; estos nucletidos cclicos son capaces de controlar la actividad metablica especfica de la neurona y provocar cambios de largo plazo; 3.- activar otras enzimas intracelulares, lo que se traduce en cambios celulares especficos; 4.- activacin de la transcripcin de un gen, lo que puede producir la sntesis de nuevas protenas intraneuronales, modificando as los mecanismos metablicos y an la estructura celular; ste
161
puede ser uno de los procesos de la memoria de largo plazo. A nivel del sistema nervioso central, existe tambin un mecanismo inhibitorio presinptico. En este caso, un terminal nervioso secreta su neurotransmisor inhibitorio en otro terminal nervioso que es de naturaleza excitatoria, y al cual inhibe, es decir, le frena o disminuye la liberacin de quanta de neurotransmisor excitatorio. Este mecanismo de inhibicin presinptica implica la interrelacin de sinapsis axo axnicas y acta modulando las influencias excitatorias e inhibitorias sobre una misma neurona presinptica.. A nivel sinptico se pueden producir algunos fenmenos derivados de su funcionamiento. Entre ellos se puede mencionar la eficiencia sinptica, que es funcin especialmente de la superficie sinptica y del nmero de receptores postsinpticos; adems, aumenta con el uso eficaz de la sinapsis, es decir, con la actividad capaz de generar impulsos en las neuronas postsinpticas. Otra caracterstica ya mencionada es la transmisin unidireccional de la informacin, debido a la asimetra sinptica. Tambin, y a causa de los diferentes procesos sinpticos, a este nivel se produce un retardo sinptico. Por ltimo, se puede mencionar el hecho que a nivel de las sinapsis qumicas se producen fenmenos de transduccin elctrico qumico elctrica. (Se debe recordar que transduccin es el cambio de una forma de energa en otra). Neurotransmisores. Bajo la denominacin de neurorreguladores se incluyen las molculas que transducen las seales entre las neuronas o bien las modulan, o sea, incluyen a los neurotransmisores y a los neuromoduladores; los primeros se liberan en las sinapsis, en cambio los neuromoduladores no necesariamente se liberan en las sinapsis, pudiendo hacerlo en otras regiones de los botones terminales. La mayora de los pptidos neuroactivos son neuromoduladores.
162
Los neurotransmisores actan modificando el potencial de membrana de la clula que posee receptores especficos; en cambio, los neuromoduladores no modifican precisamente este potencial, pero s producen marcados cambios de conductancia que modifican la accin de otros neurorreguladores. El cambio de conductancia se produce en los canales dependientes de voltaje, cambio que tambin producen algunos neurotransmisores clsicos, como la noradrenalina actuando sobre los receptores beta del locus coeruleus (produce una facilitacin de las neuronas blanco cuando son estimuladas por otro neurotransmisor). Las acciones neuromodulatorias se producen por general con la participacin de nucletidos cclicos. Los efectos de neurorreguladores pueden ser tanto de habilitacin como de inhabilitacin. Los neurotransmisores (NT) son sustancias que se liberan a nivel de las terminaciones nerviosas y actan sobre receptores especficos de la membrana postsinptica, provocando una respuesta determinada. En el funcionamiento de los neurotransmisores es posible distinguir diversas etapas; a ttulo de ejemplo, se va a analizar este funcionamiento para la noradrenalina.
163
ESQUEMA SINAPSIS
164
Las etapas comienzan con la sntesis del neurotransmisor a partir de sustancias precursoras, en este caso la tirosina; sta penetra al botn terminal y mediante enzimas sintetizadoras se forma la dopa; nuevos mecanismos de sntesis la transforman en dopamina; hasta aqu, la neurona podra quedarse como dopaminrgica (de accin de dopamina), pero si existen enzimas que continen el proceso, se va a formar la noradrenalina (NA). Esta noradrenalina del citoplasma celular puede seguir varias vas: 1.- puede frenar la sntesis de ms noradrenalina, mediante un feed back negativo; 2.- puede ser destruda por enzimas degradadoras, como la MAO - A o monoamino-oxidasa A, presente en el citoplasma neuronal; se puede mencionar la existencia de MAO - A y MAO B; la primera destruye a la noradrenalina y la segunda acta sobre la dopamina; 3.- el neurotransmisor puede encerrarse en vesculas sinpticas en cantidades definidas o quanta; la MAO no penetra al interior de las vesculas; 4.- desde las vesculas, la noradrenalina se puede liberar a la hendidura sinptica por un proceso de exocitosis dependiente de calcio. El transporte de los neurotransmisores al interior de las vesculas de almacenamiento se realiza por un mecanismo de gradiente de protones que genera carga positiva al interior; en el caso de las catecolaminas, el transportador es un antiportador de protones que extrae dos protones por molcula de catecolamina; un ejemplo prctico es la unin del antiportador a la reserpina, que es una droga que depleta las vesculas catecolaminrgicas. Ya se explic anteriormente los caminos que puede seguir un neurotransmisor cuando es liberado a la hendidura sinptica. Una pregunta interesante sera, a propsito de estos mecanismos, deducir cmo se puede aumentar o disminuir la accin de un neurotransmisor. Los neurotransmisores son ms de 50 sustancias qumicas, se pueden clasificar segn su composicin qumica, su tamao
165
molecular, su accin rpida o lenta, su respuesta excitatoria o inhibitoria, etc. Esto ltimo no es tan claro, pues un mismo neurotransmisor puede ser excitatorio o inhibitorio, segn los receptores o el rgano efector sobre el cual acte. Un ejemplo claro es el de la noradrenalina, que a nivel del miocardio tiene accin excitatoria y a nivel del msculo liso digestivo es de accin inhibitoria. Los neurotransmisores clsicos, como la acetilcolina (Ach), las catecolaminas (noradrenalina, dopamina y adrenalina, sta ltima no siendo neurotransmisor pero s pertenece al grupo de las catecolaminas), la serotonina, la histamina, el cido gammaamino-butrico (conocido como GABA), la glicina, el cido glutmico, el cido asprtico, se sintetizan en el botn terminal, a diferencia de los pptidos neuroactivos que se sintetizan en el soma neuronal. A nivel de la sntesis se puede reforzar o bien inhibir la accin de un neurotransmisor. As, inbiben la sntesis de noradrenalina y de dopamina, la alfa metil DOPA, la cual acta as como hipotensor arterial; otros, como la L DOPA estimulan la sntesis de dopamina, actuando como anti-parkinsonianos. Otros frmacos psicotropos pueden actuar a nivel de las enzimas sintetizadoras o degradadoras, o bien ayudar a la persistencia del neurotransmisor en la hendidura, ya sea inhibiendo su recaptacin o actuando a nivel de los autorreceptores que controlan la exocitosis. Los mecanismos de inhibicin de la accin neurotransmisora se utilizan en muchas acciones teraputicas y tambin en algunos txicos empleados en forma gaseosa en las guerras qumicas. Algunas drogas antidepresivas son inhibidoras de la MAO (IMAO), inhiben las enzimas degradadoras de catecolaminas y de serotonina; otras inhiben la recaptacin, como son los antidepresivos tricclicos, con lo cual potencian la accin del neurotransmisor; la cocana acta en parte por este ltimo mecanismo. Algunas patologas producidas por dficit de neurotransmisores, como la miastenia gravis, se benefician inhibiendo las enzimas degradadoras, en este caso la acetilcolinoesterasa (Ach E).
166
Modulacin. En un sentido amplio, se puede denominar neuromodulacin a la regulacin de la transmisin sinptica. Ella determina la plasticidad funcional que permite explicar los cambios conductuales, el aprendizaje, etc. Esta modulacin puede ser pre o post sinptica; la primera produce un cambio en el neurotransmisor liberado y la postsinptica modifica el ritmo de descarga de la neurona o efector postsinptico. Con respecto a la modulacin presinptica, se debe recordar que a nivel presinptico existen los autorreceptores, que son activados por el neurotransmisor liberado en la misma neurona y autorregulan la exocitosis; en cambio, el heterorreceptor es tambin un receptor presinptico que es activado por un neuromodulador que se produce en otra clula o neurona. Los moduladores se diferencian de los neurotransmisores en que no tienen actividad intrnseca, sino que modulan (modifican) la actividad neuronal que se est realizando. La modulacin presinptica puede actuar por: 1.- la activacin del receptor presinptico, produciendo: - cambios en la frecuencia de los impulsos; es la forma ms comn; - cambios en el transporte o recaptacin del neurotransmisor o precursor , o en la sntesis, almacenamiento, liberacin o catabolismo del neurotransmisor; - efecto sobre la conductancia inica en el terminal, especialmente de los iones potasio, calcio y cloruro; 2.- efecto directo de frmacos u otras sustancias en el proceso de liberacin del neurotransmisor; ste podra ser un efecto del neuromodulador sobre la aposicin vesicular o interferencia con la exocitosis. La modulacin postsinptica produce un cambio en el pattern ( o modelo) de disparo de impulsos de la neurona
167
postsinptica. Se puede producir por: 1.- cambio a largo plazo en el nmero de receptores; no es un proceso fisiolgico sino ms bien farmacolgico; 2.- cambio en la afinidad del ligando por un receptor; suele suceder que un neuromodulador modifique la afinidad por otro receptor; 3.- efecto en la conductancia inica, que se traduce en una modulacin de frecuencia. El CO (monxido de carbono) y el NO (xido ntrico) son segundos mensajeros en la modulacin. Neurotransmisores especficos. Para que una sustancia pueda ser considerada neurotransmisor debe reunir las siguientes condiciones: 1.-estar presente en las neuronas presinpticas, las que deben poder sintetizarlo; 2.- estmulos apropiados provocarn su liberacin; 3.- administrado en dosis fisiolgicas a nivel sinptico debe reproducir los efectos naturales; 4.- los efectos de frmacos deben actuar de igual manera cuando la sustancia se libera normalmente que cuando se administra a nivel sinptico. Las tres catecolaminas ms prominentes son la noradrenalina, la dopamina y la adrenalina, siendo ms bien esta ltima una hormona que un neurotransmisor, puesto que se libera de la mdula suprarrenal y pasa a la sangre para llegar as a los rganos efectores; la noradrenalina se libera en las terminaciones presinpticas como neurotransmisor y tambin en la mdula suprarrenal, junto con la adrenalina, con la cual acta tambin como una hormona. En la formacin de la dopamina a partir de la tirosina intervienen una tirosina-hidroxilasa y una decarboxilasa especfica que transforma a la L-DOPA en dopamina; hasta aqu la neurona es dopaminrgica; pero si adems existe dopamina-betahidroxilasa, la dopamina se convierte en noradrenalina. Existen neuronas noradrenrgicas en las tres porciones del
168
tronco cerebral. Desde el bulbo raqudeo, las fibras de estas neuronas se proyectan hacia la mdula espinal, puente, cerebelo, hipotlamo y corteza cerebral. Las neuronas noradrenrgicas del puente van al hipotlamo, donde influyen sobre las secreciones hormonales. Otras se encuentran en el locus coeruleus y sus fibras inhiben a las neuronas de Purkinje del cerebelo; adems, se dirigen a la corteza cerebral y al hipocampo. La noradrenalina es neurotransmisor en la mayora de las fibras simpticas postganglionares, es decir, acta a nivel de la mayora de los efectores que inerva el simptico. Tanto la adrenalina como la noradrenalina (ambas se liberan durante la estimulacin simptica), actan unindose a receptores alfa 1, alfa 2, beta 1, beta 2 y beta 3, segn lo cual ser en parte la respuesta fisiolgica que se produzca. Este mecanismo no es tan sencillo, puesto que la respuesta depende adems del nmero de receptores capaces de activarse que posea el rgano efector y de la cantidad de neurotransmisor actuante. Este ltimo factor es el que determina que la accin farmacolgica de la noradrenalina (y tambin de la adrenalina) sean diferentes en condiciones fisiolgicas que farmacolgicas, en que las dosis son mayores que las naturales. Las neuronas noradrenrgicas intervienen en el ritmo sueovigilia; as, las neuronas del locus coeruleus participan en la regulacin del sueo paradjico o REM o MOR; la noradrenalina est relacionada con la formacin de memoria, funciones intelectuales, mecanismos de recompensa; a travs del sistema simptico, interviene en la reaccin de alarma del estrs y en la regulacin de prcticamente todas las funciones viscerales. Algunas drogas de abuso, como la cocana, ejercen parte de su efecto estimulando la liberacin de noradrenalina y dopamina, a la vez que inhibiendo su recaptacin presinptica, con lo cual estos neurotransmisores permanecen mayor tiempo en la hendidura sinptica y as se potencia su efecto, puesto que aumentan sus probabilidades de unirse a los receptores postsinpticos.
169
La dopamina se encuentra tambin ampliamente distribuda en el sistema nervioso central. As, por ejemplo, se la encuentra en la sustancia nigra y calota peduncular (mesencfalo); desde la sustancia nigra sus axones se extienden al neoestriado (caudado y putamen), a ncleos del sistema lmbico y a algunas zonas de la corteza prefrontal. Otro ncleo dopaminrgico est en el hipotlamo; en el sistema nervioso perifrico se la encuentra en los ganglios neurovegetativos. La dopamina es degradada por la enzima MAO-B, cuya actividad es un 40 % menor en los fumadores que en los no fumadores. El sistema dopaminrgico de la sustancia nigra participa en la regulacin motora; el dficit de dopamina, por alteracin de la sustancia nigra, da origen al mal de Parkinson. En relacin con lo anterior, al parecer los fumadores presentan una incidencia menor del mal de Parkinson que los no fumadores. El sistema dopaminrgico del hipotlamo interviene en la regulacin de las funciones hipofisiarias, como inhibicin de la prolactina y de la hormona de crecimiento (GH). Tambin la dopamina participa en las respuestas emocionales, en el estado de vigilia, en los mecanismos de placer y en funciones mentales. La serotonina o 5 hidroxitriptamina se encuentra en el sistema nervioso central en los ncleos de la base, hipotlamo, bulbo raqudeo, mesencfalo, hipocampo. Fuera del sistema nervioso se la encuentra en las plaquetas y en las clulas nterocromafines. Sus funciones no son del todo conocidas, pero se postula que participa en la regulacin de temperatura, en la percepcin sensorial, en la regulacin del sueo de onda lenta (neuronas de los ncleos del rafe), en reacciones motoras, emocionales y afectivas; en el intestino, a travs de su accin en el plexo de Auerbach, parece intervenir en el peristaltismo. La acetilcolina (Ach) se forma por la accin de la enzima colina-acetiltransferasa (CAT), la cual promueve la transferencia del grupo acetilo del acetil-coenzimo A (acetil-CoA) a la colina, de lo que resulta acetilcolina y coenzimo A. La CAT se sintetiza en el cuerpo neuronal y se traslada por flujo axnico a las
170
terminaciones nerviosas; la mayor parte de la sntesis de Ach se realiza en el axn y luego se almacena en las vesculas sinpticas. Es un neurotransmisor abundante en el sistema nervioso y participa en un sinnmero de funciones. Se le encuentra en la corteza cerebral, ncleos de la base, sistema reticular activador, vas visuales y auditivas, tlamo, neuronas de Renshaw, sistema neurovegetativo, placa motora o sinapsis neuromuscular, etc. Sus funciones son muy amplias, de modo que se enumerarn slo algunas, agrupndolas segn efectos afines. 1.- Funciones motoras. La acetilcolina es el neurotransmisor normal a nivel de la placa motora, donde ejerce un efecto excitador, es decir, puede desencadenar la contraccin muscular. Al igual que en las otras regiones donde acta,, es destruda in situ por la acetilcolinoesterasa. La importancia de estas enzimas degradadoras se pone de manifiesto a nivel de la sinapsis neuromuscular en la enfermedad denominada miastenia gravis, en la cual un exceso de acetilcolinoesterasa destruye gran cantidad de acetilcolina; esto determina que la excitacin muscular y an el tonus muscular se vean disminudos. Tambin las clulas de Betz de la corteza motora utilizan la acetilcolina como neurotransmisor. Por otra parte, ejerce un efecto excitador sobre los ncleos de la base, de los cuales los cuerpos estriados son inhibidores motrices. Las motoneuronas espinales emiten colaterales que van a sinaptar con interneuronas inhibitorias denominadas clulas de Renshaw; esta sinapsis es colinrgica. 2.- Funciones centrales. Las neuronas colinrgicas forman parte del sistema reticular activador, que se origina en el tronco cerebral y participa en la mantencin de la vigilia. Tambin se ha demostrado su accin en las vas visuales (colculos superiores y corteza occipital), en la percepcin dolorosa y en la memoria. 3.- Funciones neurovegetativas. La acetilcolina es el neurotransmisor de todas las fibras preganglionares tanto simpticas como parasimpticas, es decir, es un neurotransmisor
171
ganglionar del sistema neurovegetativo. Tambin es el neurotransmisor de todas las fibras postganglionares parasimpticas, o sea, a nivel de efectores, y de algunas fibras postganglionares simpticas, denominadas por ello fibras simptico-colinrgicas; stas son las fibras que inervan las glndulas sudorparas y algunas que inervan vasos sanguneos de las extremidades inferiores y que participan en la vasodilatacin del ejercicio muscular. 4.- La acetilcolina participa tambin en funciones neuroendocrinas; es as como neuronas colinrgicas del hipotlamo son capaces de estimular la secrecin de hormona antidiurtica (ADH) e inhibir la secrecin de prolactina por la hipfisis posterior. A nivel de los efectores, la acetilcolina acta mediante interaccin con receptores colinrgicos, que son de dos tipos, nicotnicos y muscarnicos; deben su nombre a que son estimulados selectivamente por la nicotina o por la muscarina; en cambio, la acetilcolina los activa a ambos. La muscarina es un principio activo extrado de un hongo denominado Amanita muscharia. Los diferentes efectores poseen receptores colinrgicos distintos, unos nicotnicos y otros muscarnicos. As, en la placa motora de la musculatura estriada o esqueltica se encuentran receptores nicotnicos; en cambio en las vsceras hay receptores muscarnicos. A este respecto es interesante hacer notar que algunos frmacos bloquean selectivamente la unin de la acetilcolina con sus receptores correspondientes. As, el curare impide la accin de la acetilcolina sobre los receptores nicotnicos, es decir, inhibe su accin en la placa motora provocando parlisis de la musculatura estriada. En cambio, la atropina interfiere con la accin a nivel de los receptores muscarnicos, con lo cual inhibe la contraccin de la musculatura lisa visceral, actuando como antiespasmdico. Neurotransmisores aminocidos. Entre ellos se nombrar la glicina, el GABA, el aspartato y el glutamato. pueden
La glicina es un neurotransmisor inhibitorio liberado por
172
interneuronas espinales, donde ejerce su efecto sobre las neuronas motoras. El GABA o cido gamma-amino-butrico se obtiene a partir del cido glutmico mediante la accin de una glutamatodecarboxilasa (GAD) especfica, presente nicamente en el sistema nervioso central; como la enzima mencionada slo es activa en presencia de vitamina B6 o piridoxina, su dficit provoca disminucin del GABA cerebral. El GABA mismo fue sintetizado en 1883, pero slo en 1950 se le encontr en el sistema nervioso central, tanto en el encfalo como en la mdula espinal; en pequesimas cantidades se le ha aislado del nervio citico, del bazo y del corazn. No atraviesa la barrera hmato-enceflica. El GABA es el neurotransmisor inhibitorio habitual del encfalo, donde se le encuentra en la sustancia nigra, los cuerpos estriados, la corteza cerebral, la retina, el bulbo olfatorio, las clulas de Purkinje y la mdula espinal. Los receptores postsinpticos para glicina y GABA poseen canales dependientes de cloruro, que al fluir al interior de la membrana postsinptica, la hiperpolarizan, produciendo un PIPS. Los anestsicos generales prolongan el tiempo de apertura de los canales de cloruro de los receptores de GABA, prolongando as la inhibicin de las neuronas postsinpticas en las sinapsis gabargicas.. Un efecto inhibitorio importante lo produce a nivel de las neuronas motoras de la mdula espinal, en el cerebelo, en los ncleos de la base, en la corteza cerebral. Existe una patologa especfica denominada corea de Huntington, que se manifiesta con movimientos incontrolados y que se produce por deterioro progresivo de los cuerpos estriados, con disminucin consiguiente del GABA cerebral. Al igual que la dopamina, este neurotransmisor no atraviesa la barrera hmato-enceflica, por lo cual no produce efecto administrado por las vas usuales (oral, parenteral). Existen receptores gabargicos A y B. Un receptor gabargico tiene a lo menos tres sitios receptores; uno es el receptor sedante-convulsivante, otro es el receptor a GABA
173
propiamente tal y un tercer sitio receptor es el lugar de unin con benzodiacepinas, que son frmacos ansiolticos. La unin de la benzodiacepina con su sitio receptor facilita la unin del receptor con el GABA, lo cual se puede expresar en dos formas: 1.- las benzodiacepinas son moduladores de la unin R GABA, o bien 2.- las benzodiacepinas actan facilitando la unin del GABA con su receptor (aumentan la afinidad entre GABA y el receptor). El GABA est implicado en el corea de Huntington, en la enfermedad de Parkinson, en la epilepsia, en la esquizofrenia, en la demencia senil. Un hecho curioso es que los niveles endgenos de GABA aumentan rpidamente post mortem, un 30 a 40 % en ratas dentro de los dos primeros minutos; se ignora su significado. El neurotransmisor excitatorio liberado en las neuronas primarias aferentes es el glutamato; tambin es el principal neurotransmisor excitatorio en el cerebro y en la mdula espinal. Sus receptores son de dos grandes categoras: ionotrpicos, que controlan directamente las barreras a canales inicos, y los receptores metabotrpicos, que tambin controlan canales inicos, pero a travs de segundos mensajeros. A su vez, los receptores ionotrpicos a glutamato son NMDA (activan) y no NMDA (inhiben); sus receptores regulan canales permeables a calcio, potasio y sodio. ( NMDA = N methyl D aspartate). Oxido ntrico (NO). Su descubrimiento es relativamente reciente. Los primeros estudios que condujeron a desentraar su accin datan de 1980, cuando se demostr casualmente la accin vasodilatadora de la acetilcolina en el endotelio de algunos vasos sanguneos. Por su descubrimiento y sus mecanismos de accin celular, los Drs. R. Furchgott, L. Ignaro y F. Murad recibieron el premio Nobel de Fisiologa y Medicina en 1998. El xido ntrico acta como neurotransmisor en las sinapsis inhibitorias del sistema nervioso entrico y en las clulas del msculo liso gastrointestinal. Tambin acta en sinapsis del sistema nervioso central y es mediador en los sistemas cardiovascular, renal, pulmonar, endocrino e inmune. No se
174
acumula en vesculas sinpticas ni se libera por exocitosis, sino que simplemente difunde desde el lugar en que se produce a las clulas vecinas. Adems de actuar como neurotransmisor, el NO puede actuar como una molcula de transduccin de seales celulares en neuronas y tambin en otras clulas, por ejemplo, las del msculo liso vascular. Una forma de su mecanismo ntimo de accin es activando a la guanilciclasa, que produce GMP cclico a partir del GTP. El GMP cclico puede influir sobre diferentes procesos celulares, de modo que el NO puede actuar como neurotransmisor, como segundo mensajero o como neuromodulador. El NO se sintetiza a partir de la arginina por accin de la enzima sintetasa de xido ntrico. En las neuronas y endotelios, su sntesis es activada por el calcio y la calmodulina. Entre sus aplicaciones se ha podido demostrar que la nitroglicerina que se utiliza en los cuadros anginosos, acta generando NO en la pared vascular, dilatando as los vasos coronarios. La accin del sildenafil, ms conocido por su nombre comercial de Viagra, est tambin relacionado con la accin del xido ntrico. Neuropptidos. Corresponden a una numerosa familia de sustancias que se liberan en diversos rganos, entre ellos estructuras enceflicas. Algunos de ellos son hormonas, pero otros constituyen verdaderos neurotransmisores y neuromoduladores. Se han identificado a lo menos 25 y poseen entre 2 y 40 aminocidos en su molcula. Los neurotransmisores no peptdicos se sintetizan en los botones terminales; en cambio, los neuropptidos se sintetizan en los ribosomas del soma neuronal; en el aparato de Golgi se liberan en vesculas, que por flujo axnico llegan al pie terminal donde funcionan como vesculas sinpticas. Pptidos opiceos. Los opiceos son sustancias que tienen una accin semejante a la morfina, que es un derivado del opio; provienen de la amapola doble o adormidera, la papaver
175
somniferum. Nuestro organismo posee tres grupos de pptidos opiceos endgenos, que son las encefalinas, las endorfinas y las dinorfinas. Los pptidos opiceos se encuentran distribudos ampliamente en el sistema nervioso; se les encuentra en el hipotlamo, hipfisis, mdula suprarrenal, ncleo del tracto solitario, sistema neurovegetativo. Se encuentran estrechamente asociados a las estructuras que regulan las respuestas del organismo al estrs. Su efecto ms conocido es la analgesia; se ha descrito una SIA (stress induced analgesia) o analgesia asociada al estrs. Este activa a la mdula suprarrenal va hipotlamo sistema simptico y se liberan sustancias encefalina smiles. Pero estos pptidos opioides se liberan adems en el complejo vagal solitario del bulbo raqudeo, todos los cuales contribuyen a moderar el aumento de presin arterial que acompaa a la reaccin de alarma del estrs. Existen diversos tipos de receptores opioides, que se designan con las letras griegas kapa, mu, sigma y delta. Todos ellos han demostrado tener acoplamiento con la protena G. Los receptores mu y kapa se relacionan con la analgesia; en cambio, sigma y delta estn ms bien involucrados con conductas lmbicas. De los neuropptidos no opiceos cabe mencionar la sustancia P, presente en neuronas sensoriales primarias, en la mdula espinal y en neuronas de los plexos gastrointestinales. Se supone que la sustancia P es el neurotransmisor de la primera neurona sensitiva de la va del dolor a nivel de los ganglios sensitivos de la raz dorsal. Las encefalinas actan reduciendo la liberacin de sustancia P en estas sinapsis, por lo cual inhiben la transmisin de la sensibilidad dolorosa a este nivel. El VIP o PIV (pptido intestinal vasoactivo) es tambin un neuropptido, descrito inicialmente como una hormona gastrointestinal, pero hoy se sabe que acta tambin en el
176
sistema nervioso central. El mbito de los neurotransmisores es amplio y su historia es tambin presente y futura. Un buen ejemplo de ello es que ya se ha determinado que tenemos receptores para la marihuana, puesto que el ser humano posee un endocanabinoide que es la anandamida (en snscrito significa felicidad, satisfaccin, bienestar). Existen a lo menos dos receptores para marihuana, los CB1 y los CB2 , que son activados tanto por la marihuana como por los canabinoides endgenos; estos receptores se encuentran en el sistema nervioso y en el sistema inmune. Los receptores CB1 forman parte de una red neuronal difusamente distribuda en el sistema nervioso y aparentemente se relacionan con la percepcin de diversas sensaciones, entre ellas el dolor. Los receptores CB2 se encuentran en clulas del sistema inmune. La anandamida tiene accin analgsica y participa en la hipotensin post hemorragia, curiosamente produciendo hipotensin arterial, que podra interpretarse ya sea como una forma de disminuir la hemorragia, o tambin como una forma de aumentar la seal hipotensora que desencadena los mecanismos reguladores de la presin arterial. Tal vez los canabinoides podran utilizarse en el tratamiento de la hipertensin arterial. Sensibilidad. La sensibilidad es el fenmeno fisiolgico que proporciona informacin al organismo, tanto sobre sus funciones viscerales (interocepcin), como en la actividad smato-motora (propiocepcin) y con respecto al mundo exterior (exterocepcin) . La informacin para cualquier organismo vivo es fundamental para la supervivencia, la homeostasis, la conservacin de la especie, su vida de relacin, etc. Cuando la sensibilidad adquiere carcter consciente se denomina sensopercepcin. Esta involucra un grado de subjetividad que se podra considerar como el aspecto psicolgico de las sensaciones. La mayora de las seales interoceptivas (viscerales) y muchas propioceptivas (postura y movimiento) son por lo general
177
inconscientes. Un problema importante en el fenmeno sensitivo lo constituye la forma como se percibe el mundo circundante. Cualquier variacin ambiental o estmulo es captada por detectores o receptores, transmitida por el sistema nervioso mediante vas especficas denominadas sensitivas o aferentes, por las cuales la informacin se transmite al sistema nervioso central, el cual no slo la recibe, sino que la interpreta y generalmente la modifica y diversifica espacialmente.Adems de analizar el funcionamiento de los receptores y las caractersticas fisiolgicas de las vas, se plantearn los mecanismos de la codificacin sensorial, es decir, aqullos que determinan que el sistema nervioso central reciba la informacin sensitiva con todas sus caractersticas , y en muchos casos le d una interpretacin psicolgica, lo cual ha sido investigado mediante las leyes psicofsicas. Los receptores. En este caso se trata de estructuras histolgicas, a diferencia de los receptores sinpticos, que son molculas qumicas, generalmente protenas. Los receptores actan como transductores, transformando la energa provocada por un estmulo, en un fenmeno elctrico o biopotencial. Se les puede clasificar atendiendo a diversos aspectos, como su localizacin, su estmulo preferencial, su funcin, etc. En trminos generales, se puede establecer que su localizacin es estratgica segn cual sea la variable fisiolgica cuyas caractersticas captan. Si se consideran los estmulos que actan sobre ellos, pueden ser mecanorreceptores, quimiceptores, termoceptores, nociceptores, receptores electromagnticos, etc. Segn sea la funcin en que participan, pueden ser exteroceptores, propioceptores e interoceptores. En la mayora de los casos, los receptores se caracterizan porque son excitados por un estmulo especfico que es ptimo, es decir, presentan sensibilidad diferencial. Estructuralmente son terminaciones nerviosas o telodendrones del axn perifrico de una neurona sensitiva que es
178
del tipo pseudounipolar. Estos telodendrones pueden constituir simples terminaciones libres, como es el caso de los algorreceptores, o estar asociadas con otro tipo de tejido constituyendo todo un rgano sensitivo o sensorial. Existen numerosas variedades de estos receptores compuestos, como por ejemplo los quimioreceptores carotdeos, en los cuales existen sinapsis entre las clulas del glomus carotdeo y la terminacin nerviosa. En sistemas an ms complejos como visin, audicin, equilibrio, etc., los receptores son clulas separadas y la relacin con las fibras nerviosas aferentes se realiza a travs de sinapsis. Es necesario tener presente los receptores multimodales, que se pueden estimular con varios tipos de estmulos, como es el caso de los receptores carotdeos, que pueden ser estimulados por la hipoxia, la hipercapnia o la disminucin del pH; en cualquiera de los casos, la informacin indica una alteracin respiratoria en el mismo sentido. Tambin se debe recordar que algunos receptores pueden ser excitados por estmulos no especficos, como es el caso de la presin que a nivel del globo ocular provoca fenmenos visuales. Y por ltimo, hay que tener presente que el estmulo elctrico, de uso ms bien restringido al laboratorio, es capaz de excitar cualquier estructura nerviosa. Los estmulos apropiados pueden desencadenar en el receptor un potencial generador o de receptor o sensorial, que se produce por un fenmeno de despolarizacin local., cuya intensidad es proporcional a la intensidad del estmulo. Se denomina estmulo especfico aqul para el cual el receptor posee el umbral ms bajo. No obstante, los receptores pueden ser activados tambin por varios estmulos, como es el caso de los quimiorreceptores carotdeos que responden bien a la hipoxia, a la hipercapnia, a los cambios de temperatura, de pH y de osmolaridad; se trata de receptores polimodales, pero la respuesta que desencadenan es especfica. Si la intensidad de un estmulo apropiado es umbral, el receptor se despolariza, lo que constituye el potencial generador o de receptor; y si este potencial sensorial es de magnitud adecuada, puede generar potenciales de accin en la fibra
179
sensorial, los cuales se propagan como impulso nervioso. En el corpsculo de Pacini, el potencial de accin se origina cuando el potencial de receptor alcanza 10 mV (milivolt). Al menos en este corpsculo de Pacini, las bases inicas del potencial generador corresponden a un aumento de la conductancia al Na+, el cual penetra al interior del receptor, involucrando a su vez a los iones K+ y Cl-. El potencial generador tiene caractersticas diferentes al potencial de accin, como ser: -no responde a la ley del todo o nada, sino que su magnitud es funcin creciente de la intensidad del estmulo; puede alcanzar intensidades del orden de 100 mV; -es un fenmeno local; -si su intensidad es umbral o supraumbral con respecto a la fibra sensitiva, puede desencadenar potenciales de accin, existiendo una relacin definida entre la magnitud del potencial generador y la frecuencia de descarga de los potenciales de accin; -es poco afectado por anestsicos locales; -se da en membranas sin perodo refractario. -presenta sumacin espacial y temporal; esto puede afectar tambin a las fibras sensitivas. En la sumacin espacial aumenta el nmero de receptores y fibras activadas; en la sumacin temporal aumenta el nmero de impulsos que se desplazan por cada fibra. Se denomina campo receptivo al rea alrededor del receptor en el cual los estmulos umbrales o supraumbrales desencadenan un potencial generador. Aludiendo a los exteroceptores, se podra definir como el rea de la piel dentro de la cual un estmulo evoca actividad en un receptor. Sus dimensiones exceden la zona inervada directamente por la fibra sensitiva correspondiente, ya que la energa del estmulo se puede transmitir a travs de los tejidos circundantes. Algunos receptores presentan la propiedad de la adaptacin, que se refiere a la disminucin de la respuesta, o sea, del potencial generador, ante un estmulo mantenido o frecuente. Segn ello, los receptores pueden ser de adaptacin lenta o nula (
180
husos neuromusculares, quimiorreceptores, algorreceptores), o bien de adaptacin rpida (tactiles por ejemplo). En los receptores que adaptan, la respuesta en trminos de potencial generador es mayor al comienzo de una estimulacin que al final de ella. Un buen ejemplo de adaptacin de los receptores tactiles es que habitualmente no percibimos la ropa que llevamos puesta si es cmoda. Cuando la amplitud del potencial generador disminuye por debajo del umbral de la fibra nerviosa, sta deja de transmitir informacin con respecto a la sensibilidad especfica a que pertenece el receptor. Este fenmeno de la adaptacin determina que generalmente no seamos conscientes de muchos estmulos exteroceptivos. Los receptores presentan descargas rtmicas del potencial generador, fenmeno aparentemente producido por una accin inhibitoria del potencial de accin originado, que se propaga hacia el sistema nervioso central y tambin invade al complejo en que se inici el potencial de receptor; finalizado este efecto del potencial de accin, vuelve a manifestarse el potencial generador, originando nuevos potenciales de accin. Clasificacin de los receptores sensoriales. Los receptores sensitivos se pueden clasificar considerando diversas caractersticas, como ser el tipo de receptor, la informacin que transmiten, su estmulo especfico, entre otras. Es frecuente clasificarlos teniendo en cuenta su estmulo eficaz y la funcin fisiolgica en que ellos participan. I.- Mecanorreceptores. 1.- Sensibilidades tactiles de la piel. - Terminaciones nerviosas libres - Terminaciones con extremo ensanchado Terminaciones de Ruffini Discos de Merkel - Terminaciones encapsuladas Corpsculos de Meissner, de Pacini y de Krause
181
- Terminaciones de folculo piloso. 2.- Sensibilidades de tejido profundo. - Terminaciones nerviosas libres - Terminaciones de extremo ensanchado Terminaciones de Ruffini - Terminaciones encapsuladas Corpsculos de Pacini - Terminaciones especializadas Husos neuromusculares Receptores tendinosos de Golgi. 3.- Audicin. - Receptores auditivos cocleares. 4.- Equilibrio. - Receptores vestibulares. 5.- Presin arterial. - Tensoceptores articos y carotdeos. 6.- Otras funciones. - Tensoceptores pulmonares. II.- Termorreceptores. 1.- Fro 2.- Calor nerviosas libres) III. Nociceptores. 1.- Dolor: terminaciones nerviosas libres. IV.- Receptores electromagnticos. 1.- Visin. (Probablemente ambos son terminaciones atriales, gstricos, vesicales,
182
- Bastones - Conos. V.- Quimiorreceptores. 1.- Gusto: receptores de los botones gustativos 2.- Olfato : receptores del epitelio olfatorio 3.- pO2 arterial: receptores articos y carotdeos 4.-Osmolaridad: neuronas de ncleos suprapticos; receptores del bulbo duodenal 5.- pCO2 arterial : bulbares, articos y carotdeos 6.- glucosa sangunea, aminocidos, cidos grasos: receptores hipotalmicos 7.- pH: receptores bulbares, duodenales, articos y carotdeos.
Propagacin de los impulsos sensitivos. Los impulsos sensitivos se propagan por los diferentes tipos de fibras hacia estructuras nerviosas centrales, como la mdula espinal y el tronco cerebral, donde se encuentran los ncleos sensitivos de los nervios craneanos; por lo tanto, esta propagacin se realiza a travs de nervios espinales y craneanos. Pueden dar origen a mecanismos reflejos y tambin enviar informacin a estructuras nerviosas superiores, dando lugar a sensopercepcin. Las fibras nerviosas transmiten los impulsos a diferentes velocidades, dependiendo del dimetro del neurito y de la condicin de mielnica o amielnica de la fibra nerviosa. En la tabla siguiente se encuentra su clasificacin atendiendo a diferentes caractersticas. Dimetro Velocidad Duracin Funcin de (micrones (Metros/seg. Espiga ) ) (miliseg.
Tipo fibra
183
A alfa I A beta II A gama III A delta III B III C IV
13 - 22 8 - 13 4-8 1.4 1-3 0.2 1.0
70 - 120 40 70 15 40 5 - 15 3 - 14 0.2
) 0.4 0.5 Motora, propiocepcin 0.4 0.6 Tacto,presin, Cenestesia 0.5 0.7 Tacto,excitacin de husos musc. 0.6 1.0 Dolor, prurito, Calor, fro. 1.2 Neurovegetativa s Preganglionares 2.0 Dolor, prurito, calor,fro,presin , neurovegetativa s postganglionare s, olfato.
La primera neurona de una va sensitiva es una neurona pseudounipolar cuyo soma queda en un ganglio sensitivo, ya sea espinal (raqudeo) o de nervio craneano. En el caso de las vas sensitivas que entran a la mdula espinal, penetran por su parte dorsal, ya sea a los cuernos o astas posteriores o directamente a los cordones medulares posteriores. Existen dos sistemas ascendentes principales que llevan informacin sensorial por la mdula espinal: I.- sistema de las columnas dorsales y lemnisco medial; II.- sistema ntero-lateral. El sistema de las columnas dorsales transmite impulsos relacionados con: tacto discriminativo, vibracin, informacin articular y posicin de las extremidades. Las fibras de la propiocepcin consciente y tacto
184
discriminativo penetran en la mdula dorsal directamente a los cordones posteriores; localmente dan ramas colaterales que sinaptan con interneuronas y motoneuronas del asta anterior, dando lugar a reflejos medulares, entre ellos forman el arco monosinptico del reflejo miottico. Ramas ascendentes llegan a los ncleos gracilis y cuneatus de la mdula oblongada donde, despus de hacer sinapsis, las fibras que emergen cruzan y forman el lemnisco medial, que llega al ncleo ventral pstero lateral del tlamo. El lemnisco medial recibe en su trayecto fibras del trigmino; desde la sinapsis talmica se originan fibras que constituyen radiaciones tlamo-corticales, por cuanto terminan en la corteza sensitiva . El sistema ntero lateral est constituido a su vez por dos grandes grupos de tractos, los espinocerebolosos y los espinotalmicos. Los fascculos espinocerebelosos llevan propioceptiva inconsciente por dos grandes vas: informacin
1.- los axones de la protoneurona sensitiva penetran a los cordones medulares laterales, cruzando en su mayora y ascienden formando el fascculo espinocerebeloso ventral o cruzado, el cual llega hasta el mesencfelo para dirigirse al cerebelo por el pednculo cerebeloso superior; 2.- otras fibras propioceptivas forman el fascculo espinocerebelar dorsal o directo, que en la mdula se ubica en el cordn homolateral, asciende hasta el bulbo raqudeo y penetra al cerebelo por el pednculo cerebelar inferior. Los fascculos espinocerebelares llevan informacin propioceptiva que, por ser inconsciente, no da lugar a sensopercepcin. La informacin sobre dolor, temperatura, tacto burdo y presin va tambin en el sistema ntero-lateral, constituyendo los dos fascculos espinotalmicos.
185
1.- El haz espinotalmico anterior o ventral, cruzado, lleva los impulsos de tacto y presin hasta el ncleo ventral pstero lateral del tlamo. 2.- El fascculo espinotalmico lateral, que tambin cruza a nivel medular, transmite informacin de dolor y temperatura hasta el ncleo ventral pstero lateral del tlamo. Radiaciones tlamo-corticales proyectan toda la informacin talmica hacia la corteza sensitiva. En cuanto a los impulsos sensitivos de la cabeza, van en gran parte por el nervio trigmino; desde los exteroceptores la informacin se transmite por fibras mielnicas gruesas a los ncleos trigeminales de la protuberancia; estas aferencias corresponden a informacin sobre tacto, presin, dolor y temperatura. Los impulsos que conciernen a la actividad muscular (tensin muscular, longitud del msculo, velocidad de acortamiento y/o extensin muscular) terminan en el ncleo sensitivo mesenceflico del V par. Todas las aferencias llegan al tlamo, el cual puede irradiarlas a la corteza sensitiva.
Sensopercepcin. Se le define como la apreciacin consciente de un cambio ambiental captado por los receptores; tiene un componente subjetivo importante, es un proceso aprendido que se adquiere por condicionamiento y consiste en asociar una respuesta con un estmulo. La sensopercepcin establece una relacin entre un patrn de actividad de neuronas y un patrn de estimulacin ambiental. Para que se produzca una sensopercepcin, son necesarias algunas condiciones biolgicas como:
186
- estimulacin de receptores; - sistemas de transmisin de los impulsos desde los receptores a la corteza cerebral; son los sistemas especficos aferentes corticales (SEAC), los que deben estar en buenas condiciones de funcionamiento; -reas corticales en estado funcional y en condicin de vigilia; -nivel suficiente de facilitacin de los centros implicados. Una cualidad de la sensopercepcin es su modalidad,quecorresponde a una clase claramente identificable de sensacin: fro, calor, dolor, tacto, visin, etc. Se denomina proyeccin de la sensopercepcin al fenmeno por el cual la sensacin se experimenta en el punto de aplicacin del estmulo. Los sistemas especficos aferentes corticales son generales y especiales. Son especiales el olfato, la visin, la audicin, el gusto; son generales las percepciones somticas como dolor, termocepcin, tacto, peso, presin, posicin, movimiento, vibracin. Estas ltimas forman parte de la propiocepcin, que se refiere a las sensaciones dependientes de la posicin y el desplazamiento del cuerpo. Existen tambin sensaciones viscerales, muchas de las cuales no son conscientes, como son la mayora de las que regulan la homeostasis; en cambio, constituyen sensopercepciones viscerales las de dolor y distensin, por ejemplo. Existen algunas alteraciones de la sensopercepcin, que sin llegar a ser patolgicas, deforman la percepcin real o inducen algunas inexistentes. En la apreciacin consciente normal, el organismo relaciona un determinado patrn de actividad neuronal con una estimulacin especfica. A este respecto, se dan las siguientes alteraciones: -en la alucinacin se presenta el patrn de actividad neuronal sin que exista el patrn de estimulacin, con el individuo
187
en estado consciente; - en la ensoacin tambin se presenta el patrn de actividad neuronal sin el patrn de estimulacin, pero en estado onrico; - en la sugesin hipntica se produce la apreciacin de situaciones ambientales que son inducidas en estado hipntico; el patrn de actividad es evocado por estimulacin externa proporcionada por el hipnotizador; - la ilusin es una percepcin real en que el juicio de la situacin es distorsionado porque los indicadores estn falseados. Codificacin sensorial. El sistema sensitivo recibe la informacin final sobre el fenmeno de sensibilidad utilizando diferentes cdigos. El ms elemental se refiere a la existencia o ausencia de informacin, es decir, si existe o no actividad en el sistema. Este dato lo proporciona la existencia de impulsos o potenciales de accin propagados. Un segundo aspecto se refiere a la modalidad de sensibilidad, o sea, a la clase o tipo de fenmeno sensitivo, que puede ser de calor, fro, presin, tacto, dolor, etc. Esta modalidad es codificada a diferentes niveles; comienza por la especificidad del estmulo, acoplada a la especificidad de receptores, para continuar con la especificidad de vas, que incluye la de los ncleos de relevo, para terminar con la especificidad de las estaciones terminales, que pueden ser una corteza sensitiva primaria o ncleos subcorticales en el caso de la sensibilidad no consciente. En relacin con la especificidad, es necesario considerar dos aspectos: la especificidad del estmulo y la especificidad del receptor; ambos informan con respecto a la modalidad de la sensacin. Ya se defini la especificidad del estmulo como la caracterstica para la cual el receptor posee el menor umbral. Ahora bien, lo habitual es que al activarse un receptor determinado, d origen a una sensacin de modalidad bien definida; por ejemplo, si por su estmulo especfico o por otro (estmulo elctrico por ejemplo) se activan receptores de fro, se
188
tendr la sensacin de fro y no de presin o de dolor (cuando el fro provoca dolor, se supone que se estn activando algorreceptores). Por otra parte, una fibra aferente est en contacto con receptores de un solo tipo y su velocidad de conduccin es funcin del dimetro de la fibra y de su condicin de mielnica o amielnica. Esta relacin biunvoca entre receptores y vas sensitivas determina que estas ltimas tambin codifiquen modalidad, en el sentido que las vas sensitivas son selectivas para transmitir su informacin. Ya en 1826, Johannes Mller propuso que los receptores y sus fibras aferentes exhiben especificidad de respuesta, ya sea que se estimulen por su estmulo natural especfico o uno artificial como el elctrico, dando siempre lugar a la misma sensacin. Esto explica el hecho que individuos amputados de una extremidad experimenten sensaciones en una estructura que no tienen, debido probablemente a que los procesos de cicatrizacin u otros pueden estimular las fibras nerviosas que habitualmente conducan la informacin fantasma que estn experimentando, y que trasmiten la informacin hasta la corteza sensitiva correspondiente. Se deduce entonces que el sistema sensitivo tambin es capaz de discriminar el sitio estimulado en forma bastante precisa; ello depende de la ubicacin de los receptores activados y de la trasmisin de la informacin por vas determinadas, las cuales a su vez llegan a estructuras enceflicas definidas; a cualquiera de estos niveles que se efecte una estimulacin, las estructuras enceflicas, ms precisamente la corteza sensitiva, van a proyectar la sensacin al sitio estimulado, o que habitualmente es estimulado. En cuanto a la extensin del rea estimulada, est regida por el cdigo de poblacin en cuanto a nmero de receptores estimulados, lo que determina el nmero de vas estimuladas y de estructuras enceflicas correspondientes. La intensidad del estmulo puede ser codificada o interpretada mediante dos sistemas de cdigos, el cdigo de
189
frecuencia y el cdigo de poblacin. En 1920, Lord Adrian demostr que la frecuencia de descarga de una fibra sensitiva aumenta con la intensidad del estmulo, lo que se denomina cdigo de frecuencia para la intensidad del estmulo; los estmulos de mayor intensidad evocan potenciales generadores mayores, los que a su vez producen potenciales de accin de mayor frecuencia; indirectamente, entonces, el aumento en la intensidad de estmulos supraumbrales, aumenta la frecuencia de descarga de los impulsos, con lo cual dicha frecuencia informa sobre la caracterstica mencionada del estmulo. Por otra parte, un estmulo de intensidad creciente activa a un mayor nmero de receptores, lo cual constituye el cdigo de poblacin para la intensidad del estmulo. Sin embargo, este no es el nico factor involucrado en el cdigo de poblacin; como los receptores pertenecen a porciones de neuritos perifricos de fibras sensitivas, si se activa mayor nmero de receptores, puede excitarse tambin un nmero mayor de fibras nerviosas, lo cual dar cuenta en ltima instancia de la intensidad del estmulo. La informacin sensitiva originada a nivel de los receptores es transmitida por las vas sensitivas aferentes hacia regiones centrales del sistema nervioso. Las fibras sensitivas van a constituir nervios sensitivos o partes sensitivas de un nervio mixto, las cuales llegan hasta la mdula espinal u otra estructura del sistema nervioso central en el caso de los nervios craneanos. Las fibras sensitivas transmiten a velocidades diferentes, determinadas por su dimetro y su condicin de mielnica o amielnica. A nivel de la mdula espinal, las vas sensitivas se organizan en haces o fascculos ascendentes, de ubicacin muy definida, que se analizaron en el captulo de anatoma correspondiente. As, los cordones posteriores medulares llevan por sus fascculos gracilis y cuneatus, los impulsos de tacto discriminativo y propiocepcin consciente; los fascculos espinotalmicos laterales llevan informacin sobre dolor y temperatura, etc. Las seales
190
interoceptivas son en su mayora inconscientes, puesto que su informacin no llega a la neocorteza cerebral. con excepcin de algunas como las de dolores viscerales, otras de distensin, etc. En cuanto a la informacin propioceptiva, puede tener tanto el carcter consciente (posicin de las extremidades) como inconsciente (informacin de los husos neuromusculares). A nivel de las estructuras enceflicas, las caractersticas sensitivas se codifican en forma compleja. Intervienen las estaciones de relevo en los ncleos, en los cuales el fenmeno sensitivo se puede magnificar, inhibir, suprimir, diversificar hacia otras reas, etc.Estudiando los mecanismos de accin de las drogas psicodlicas, se ha podido establecer que los ncleos del rafe y el locus coeruleus participaran en la discriminacin sensorial; de hecho, la estimulacin sensitiva produce aumento de la frecuencia de potenciales de accin en las neuronas del locus coeruleus, al parecer por va de los ncleos del rafe; aqul est siendo considerado un verdadero integrador de las funciones sensoriales; cuando se produce una estimulacin generalizada de las neuronas del locus coeruleus, se produce la sinestesia, en que las diferentes sensaciones pierden sus lmites. A nivel de la corteza cerebral sensitiva, se encuentran representadas las diferentes partes del cuerpo en relacin con los fenmenos sensitivos; ello da lugar al homnculo sensitivo, que es un hombrecito deforme, en el cual el tamao de sus estructuras corporales est en relacin directa con la extensin de las reas corporales sensitivas. En la corteza cerebral existe para cada sensacin un patrn de actividad neuronal, constitudo por grupos neuronales especficos que se activan en una forma determinada. Si dicho pattern de actividad neuronal se excita por medios no convencionales, tiene lugar el fenmeno sensitivo que este patrn comanda. En la corteza cerebral, las diferentes capas tienen diferentes funciones sensitivas.
191
La capa IV es excitada primero y en forma principal por los impulsos sensoriales; desde aqu los impulsos van a la superficie de la corteza y a capas profundas. Las capas I y II reciben impulsos aferentes difusos, poco especficos, desde centros ms caudales, que pueden facilitar a una regin cerebral completa al mismo tiempo; este mecanismo regula el nivel global de excitabilidad de la regin estimulada. Las neuronas de las capas II y III envan axones a las porciones cercanas de la corteza. Las neuronas de las capas V y VI envan eferencias a diferentes partes del sistema nervioso, por ejemplo, la capa VI enva sus impulsos principalmente al tlamo. La corteza cerebral funciona tambin en base a columnas verticales, que incluyen a las seis capas corticales. Cada columna tiene un dimetro de 0,3 a 0,5 micrones, con unas 10.000 neuronas cada una. Cada columna funciona para una modalidad sensorial especfica, como ser estiramiento, sensacin tactil, de presin, etc. Adems, las columnas de cada modalidad van interpuestas entre s. Los impulsos originados por accin del potencial generador se transmiten hacia la mdula espinal o hacia ncleos del tronco cerebral en el caso de los nervios craneanos por las fibras sensitivas correspondientes, llegando la informacin a diferentes estructuras enceflicas. En el caso de los impulsos espinales, llegan por los nervios espinales a la mdula espinal; en cambio, los impulsos exteroceptivos y propioceptivos de la cabeza llegan por los nervios craneanos.
Leyes psicofsicas.
192
Con respecto al mundo que nos rodea, cabe preguntarse si l es tal cual lo percibimos o si el sistema nervioso obtiene una informacin distorsionada de l, es decir , que puede tratarse de una ilusin perceptual aunque parcial. Pero si tal es el caso, se trata de una ilusin muy consistente, que tiene color, forma, materia, etc., que se repite, que se percibe aproximadamente igual en consenso; es as como de cada ente que posee existencia real, la mente se ha formado una idea concreta sobre sus atributos materiales, a la vez que por abstraccin de sus caractersticas se ha originado la idea conceptual de dicho ente u objeto. Indudablemente que el aspecto psicolgico le proporciona una connotacin individual. Vernon Mouncastle ha expresado que percibimos el mundo mediante un cerebro ligado a aquello que est afuera, a travs de receptores, vas sensitivas y centros de percepcin. Nuestras sensaciones se establecen por funciones de estimulacin, codificacin y procesamiento del fenmeno sensitivo, mediante la fisiologa integrada del sistema nervioso. Las relaciones psico-fsicas analizan los nexos existentes entre las dimensiones fsicas reales del estmulo sensorial y la percepcin o interpretacin dimensional de ellos. Su estudio puede proporcionar mayor informacin sobre los receptores y el procesamiento nervioso. Es un rea de la psicologa experimental relacionada con la cuantificacin de las experiencias sensoriales. Suministra una poderosa herramienta experimental para correlacionar la conducta con las propiedades fisiolgicas de las neuronas; desde un punto de vista subjetivo, el procesamiento sensorial relaciona los estmulos reales y nuestra experiencia sobre ellos. En el siglo XIX, E.H. Weber desarroll una descripcin cuantitativa de las relaciones entre la intensidad del estmulo y su discriminacin, estableciendo lo siguiente: S S = K S ( ------ ] x K So S es la mnima diferencia de intensidad que se puede percibir en relacin con un estmulo de referencia So ; K es la constante de
193
proporcionalidad. A medida que aumenta el estmulo de referencia, tambin aumenta la magnitud del incremento de intensidad necesaria para percibir el estmulo como diferente. En 1860, Gustav Fechner aplic la ley de Weber a la experiencia sensorial; encontr que la intensidad de la sensacin experimentada por un sujeto es proporcional al logaritmo de la intensidad del estmulo: S I = K log -----So I es la intensidad subjetiva percibida So es la intensidad umbral S es el estmulo supraumbral utilizado para estimar la diferencia K es una constante propia para cada sensacin Se define el umbral sensorial absoluto como la menor intensidad del estmulo que puede detectar un sujeto; la determinacin de este umbral es un fenmeno estadstico; en este contexto se le define como la intensidad del estmulo detectada en el 50 % de los casos experimentales. Stevens en 1953 propuso que la relacin entre estmulo real y percibido no era logartmica sino exponencial, y estableci la siguiente ley psico-fsica: I = K ( S So )
n
en que las letras involucradas tienen el mismo significado que para la ley logartmica de Weber-Fechner; n es un exponente de la relacin. Esta ley exponencial est actualmente aceptada por cuanto cuenta con una buena demostracin experimental. Si se homologa la intensidad juzgada del estmulo I con la frecuencia de descarga de los impulsos en las fibras nerviosas involucradas en la sensacin estudiada, y se le relaciona con la intensidad real del estmulo,se obtiene la ley de Stevens. Es decir, se puede sustituir
194
la experiencia subjetiva de la magnitud del estmulo por la frecuencia de descarga nerviosa. Esto significa que la intensidad del estmulo que se experimenta ( I ) es realmente la que indica la frecuencia de descarga de las fibras sensitivas y estaciones de relevo. Algunas sensaciones en particular. Sensaciones cenestsicas. Cenestesia es el reconocimiento de la orientacin del cuerpo en el espacio y de las partes del cuerpo entre ellas. Sus receptores son de diferentes tipos: -rganos terminales de Ruffini, que son estimulados por movimientos articulares bruscos; presentan una leve adaptacin inicial y luego descargan en forma constante; -receptores similares a los tendinosos existen tambin en los ligamentos periarticulares; -corpsculos de Pacini, ubicados en los tejidos periarticulares. Sensaciones tactiles, de presin y de vibracin. Son percibidas por los mismos tipos de receptores ubicados a distintos niveles de profundidad de la piel. Los tactiles son ms bien superficiales, los de presin van ubicados a mayor profundidad y los de vibracin se caracterizan por emitir seales repetitivas de alta frecuencia. Los receptores tactiles son abundantes en las puntas de los dedos, labios, lengua, y permiten no slo percibir el contacto, sino tambin la textura de los objetos, la zona precisa estimulada y la discriminacin espacial entre dos zonas excitadas. Por ejemplo, dos estimulaciones tactiles simultneas en la piel de la espalda permiten discriminar distancias del orden de 5 a 10 cms.; en cambio la lengua discrimina distancias menores de 1 mm. Los receptores de presin estn distribuidos ms
195
profundamente en toda la superficie de la piel; Dolor. En un concepto amplio, se consideran dos formas o clases de dolor, uno psquico y otro fisiolgico. El dolor psquico se refiere al pesar que se produce por la carencia de un bien deseado, y que se manifiesta como tristeza. En este captulo se analizar lo relativo al dolor fisiolgico, que es una sensacin aversiva, displacentera,que constituye un mecanismo protector del organismo y que se produce en respuesta a una agresin tisular como golpe, herida, escara, etc. Esta forma de dolor tiene un grado de subjetividad, que es el componente psicolgico del dolor fsico. El ser humano , y tambin los animales, presentan diferente reaccin segn si el dolor es interno (visceral) o responde a una agresin exterior, reaccin que deriva de la sensacin objetiva y subjetiva de dao orgnico. El dolor suele desviarse de su objetivo y al transformarse en crnico representa un problema de ms difcil tratamiento. Existe una Asociacin Internacional para el Estudio del Dolor, que lo ha definido as: Es una experiencia sensorial y emocional desagradable asociada con una lesin tisular real o potencial o descrita en trminos de tal lesin. La respuesta dolorosa presenta cinco parmetros bien definidos que son: 1.- umbral doloroso, que se relaciona con la magnitud del estmulo necesaria para provocar dolor; 2.- limen diferencial, que es la diferencia apenas perceptible de dolor; se relaciona con las leyes psicofsicas; 3.- tolerancia al dolor; es una especie de umbral mximo que el individuo puede soportar antes de alejarse del estmulo doloroso; tiene grandes variaciones individuales, as como por edad, sexo y raza; 4.- punto de solicitud de droga, que est entre el umbral y la
196
tolerancia; 5.- rango de sensibilidad dolorosa, que comprende la diferencia entre tolerancia y umbral, es decir, la zona en que el individuo es capaz de soportar estoicamente un dolor. Los receptores al dolor se denominan algorreceptores o nociceptores; son terminaciones libres ubicadas en la piel, periostio, paredes arteriales, superficies articulares, meninges, vsceras huecas, pleuras, peritoneo, msculos, etc. Algunos son mecanonociceptores y otros son polimodales. Los primeros son terminaciones de fibras mielnicas Adelta, y responden no slo a factores mecnicos, sino tambin a temperaturas menores de 10 C y mayores de 45 C; a esta temperatura comienzan las lesiones tisulares. Los receptores polimodales son terminaciones libres de fibras mielnicas C y responden a estmulos mecnicos, trmicos y qumicos. Hay nociceptores cutneos, viscerales, musculares y articulares. Los viscerales son mecanoceptores de fibras A delta, ubicados en las paredes de vsceras huecas, en las fascias, alrededor de los vasos sanguneos y en meninges. En el corazn hay receptores polimodales de fibras C. En las articulaciones, los mecanonociceptores se encuentran en el periostio, en la cpsula articular y en tendones, ligamentos y fascias; algunos se activan con la hiperflexin o la hiperextensin articular. En los msculos, los mecanonociceptores son terminaciones libres de fibras III (A delta) y IV (C). La mayora de estos receptores son silentes, slo se activan si son previamente sensibilizados. Son quimiorreceptores que al ser sensibilizados desarrollan sensibilidad mecnica; es por ello que las articulaciones, el peritoneo y otras estructuras slo producen dolor si estn inflamados o lesionados; tambin hay receptores silentes en los msculos y an en la piel.
197
Los algorreceptores no presentan adaptacin; a la inversa, en ciertas condiciones el umbral llega a disminuir provocando una hiperalgesia. Son estmulos qumicos la bradicinina, la serotonina, la histamina, los iones K+, sustancias cidas, acetilcolina y enzimas proteolticas; stas ltimas actan en las terminaciones nerviosas. Adems, las prostaglandinas y la sustancia P aumentan la sensibilidad de los algorreceptores. Si se inyecta extracto de tejido lesionado, se produce un dolor intenso, debido a las sustancias qumicas liberadas, siendo la bradicinina la ms potente. La isquemia produce dolor por acumulacin de cido lctico, debido al metabolismo anaerbico, y accin de las dems sustancias qumicas mencionadas; este dolor isqumico se alivia proporcionando oxgeno. El espasmo muscular produce dolor al menos por tres mecanismos: -estimulacin mecnica de algorreceptores -isquemia -aumento del metabolismo muscular, que produce ms metabolitos que la isquemia no permite eliminar. Se denomina sensibilizacin de un nociceptor al proceso por el cual la fibra sensitiva aumenta la intensidad de la respuesta, disminuye el umbral de activacin y algunas veces puede descargar espontneamente. La sensibilizacin se puede producir si cerca de un nociceptor se liberan o forman algunas sustancias por lesin o inflamacin tisular; las sustancias pueden ser potasio, bradicinina, histamina, serotonina, prostaglandina E, leucotrienos, etc. Si se liberan enzimas proteolticas que dan origen a la formacin de bradicinina, sta se une a receptores en la membrana del nociceptor, lo que da origen a la activacin de segundos mensajeros que intervienen en la sensibilizacin del receptor. Las sustancias sensibilizantes tambin pueden actuar abriendo canales inicos, como la serotonina. Se observa que algunas de las sustancias sensibilitantes son adems vasodilatadoras y aumentan la permeabilidad capilar.
198
Las sustancias qumicas liberadas en el tejido daado pueden producir reacciones de hiperalgesia y an alodinia, es decir, dolor provocado por estmulos habitualmente inocuos. El dolor presenta dos componentes: - dolor rpido, que se produce unos 0,1 segundos despus de aplicado el estmulo; se denomina dolor punzante; - dolor lento o urente, se produce 1 segundo despus de aplicar el estmulo. Por otra parte, en la percepcin dolorosa se describe un aspecto sensorial-discriminativo y otro emocional-afectivo. Estas diferentes modalidades se deben a varios mecanismos. En primer lugar, debido a que las fibras que transmiten el dolor son rpidas (A delta) y lentas (C ). Pero adems, los haces espinotalmicos tienen dos grandes grupos de fibras, que constituyen los sistemas: - neoespinotalmico, por el que se transmiten los impulsos que provocan el dolor rpido, y se relaciona con el aspecto sensorial-discriminativo del dolor, como ser cualidad, localizacin, intensidad, duracin; sus fibras llegan a la sustancia reticular del tronco cerebral y terminan en el ncleo ventral pstero lateral del tlamo; - paleoespinotalmico, que da cuenta del dolor lento y se relaciona con el componente emocional-afectivo del dolor, que incluye el estado de alerta y la atencin, as como reflejos somticos, neurovegetativos, endocrinos y cambios emocionales, que en conjunto le dan el carcter desagradable al dolor. Algunas manifestaciones conductuales de este sistema son las reacciones de defensa, huda, vocalizacin, excitacin, depresin, ansiedad, modificaciones viscerales incluyendo midriasis, piloereccin, miccin, defecacin, etc.; las
199
fibras paleoespinotalmicas terminan en los ncleos intralaminares del tlamo y en estructuras lmbicas como amgdala, cuerpos estriados e hipotlamo. Las fibras de la va paleoespinotalmica llegan en su mayora al tronco cerebral, tanto a los ncleos reticulares, como al tectum y a la sustancia gris periacueductal; slo entre un 10 a un 25 % llegan al tlamo. Adems, la proyeccin de la sensopercepcin informada por las fibras paleoespinotalmicas es difusa, no permite ubicar el dolor en un punto sino en una zona. Por ltimo, los neurotransmisores involucrados en cada tipo de dolor se liberan en tiempos diferentes. El dolor se percibe aunque no exista corteza sensitiva, debido a la informacin dolorosa que llega al tronco cerebral y al tlamo. En cuanto a las estaciones dolorosas terminales, los impulsos sensitivos llegan a la corteza sensitiva primaria somtica general, ubicada en el giro parietal ascendente contralateral, que posee neuronas nociceptivas especficas y otras de rango espandido; tambin se observa una distribucin somatotpica. Es decir, la corteza primaria est relacionada con el procesamiento de la informacin sensorial nociceptiva. Sus impulsos pasan a la corteza secundaria o de asociacin, que tiene una funcin integradora y se le asocia con el componente emocional-afectivo del dolor. En estas reaciones participa tambin la corteza del cngulo o callosomarginal, cuya ablacin suprime las respuestas emocionalafectivas del dolor; el paciente lo percibe pero no le molesta. Visin. El sistema ptico representa un modelo funcional y estructuralmente bien conocido de un sistema sensorial, por lo cual se analizar en particular. El estmulo visual es la luz, la cual
200
debe atravesar las estructuras oculares hasta llegar a la retina, donde se encuentran los fotorreceptores, que pueden dar origen a los potenciales generadores; stos, a su vez, pueden desencadenar potenciales de accin que constituirn los impulsos luminosos que llevarn su informacin hasta la corteza occipital visual o estriada o calcarina, la que en conjunto con las reas de asociacin visual, va a dar lugar a la sensopercepcin correspondiente. El funcionamiento del sistema visual incluye algunos mecanismos reflejos que permiten la acomodacin del cristalino, la variacin del dimetro pupilar y los movimientos oculares. Descripcin anatmica bsica. El globo ocular est constituido por membranas que dejan en su interior cmaras con lquido, separadas por el cristalino y sus estructuras adyacentes. Las membranas son, de afuera hacia adentro, la esclertica, la coroides y la retina. En la parte anterior, la esclertica forma la crnea transparente que va externamente recubierta por la conjuntiva. La esclertica es una membrana muy resistente; la coroides contiene vasos sanguneos, de funcin nutricia, y en su parte anterior forma el iris. Revistiendo los dos tercios posteriores de la coroides est la retina, que contiene los fotorreceptores. El cristalino es la lente del ojo; est mantenido en su lugar por un ligamento que es la znula ciliar de Zinn, adherida al cuerpo ciliar Estos ligamentos elsticos y las formaciones musculares se insertan en la cpsula del cristalino, de tal modo que su grado de contracin o de relajacin modifica la convexidad de la lente, y por lo tanto, su poder de refraccin. Enfrente del cristalino est el iris, estructura pigmentada que deja en el centro una abertura circular llamada pupila. El iris posee dos grupos de fibras musculares: 1.- circulares, bajo control parasimptico, y cuya contraccin provoca miosis o disminucin del dimetro pupilar, la cual es evocada por aumento de la luminosidad ambiente; 2.- radiales, que estn bajo control simptico, y cuya contraccin
201
produce midriasis o dilatacin pupilar; sta se observa en cualquier estado de estimulacin simptica general, como en los estados emocionales y en el estrs; no se trata de una reaccin a la luz. La cmara anterior del ojo est llena de humor acuoso; en cambio el interior del globo ocular contiene humor vtreo, de consistencia gelatinosa . El humor acuoso es secretado por los procesos ciliares (epitelio); consisten en pliegues lineales que se proyectan desde el cuerpo ciliar hacia el espacio cercano al iris. Su secrecin se produce por transporte activo de sodio hacia los espacios entre las clulas epiteliales; los iones sodio arrastran a su vez iones bicarbonatos y cloruros; tambin contiene aminocidos, cido ascrbico y glucosa; por osmosis, arrastran agua. El lquido entra a la cmara anterior del ojo; de aqu fluye hacia el ngulo entre la crnea y el iris, para llegar al canal de Schlemm y a las venas extraoculares. La presin intraocular es de 12 a 20 mm Hg, con un promedio de 15. Est determinada especialmente por la resistencia al flujo del humor acuoso desde la cmara anterior al canal de Schlemm; la mayor resistencia la ofrecen las trabculas, de dimetro 2 a 3 micrones. La retina es la estructura que contiene los fotorreceptores y sobre ella se forma la imagen visual. Posee 10 capas de clulas; en ellas, los componentes principales son los receptores conos y bastones, las clulas bipolares,las ganglionares, las horizontales y las amacrinas. Las fibras que contienen los receptores sinaptan con las clulas bipolares y stas con las ganglionares. La retina. contiene melanina, un pigmento oscuro que evita la reflexin de la luz. En cada ojo humano existen unos 6 millones de conos, unos 120 millones de bastones y 1.2 millones de fibras nerviosas en cada nervio ptico; por lo tanto, hay una convergencia global de los receptores sobre las clulas ganglionares cercana a 105 : 1. Los axones de las clulas ganglionares forman el nervio ptico, abandonando el ojo por la papila ptica, por la cual penetran tambin los vasos sanguneos. La papila no posee
202
fotorreceptores, por lo cual se le denomina mancha o punto ciego. En el polo posterior del ojo est tambin la fovea central de la retina, cuya localizacin est marcada por la mcula ltea. La fovea no posee bastones pero s muchos conos, es el sitio de mayor agudeza visual, de la visin detallada. Los bastones son muy sensibles a la luzson los receptores para la visin nocturna (visin escotpica). Los conos tienen un umbral ms elevado para la luz, siendo responsables de la visin en luz brillante (visin fotpica) y de colores. Los receptores poseen pigmentos fotosensible. As, los bastones contienen rodopsina, compuesto de escotopsina (protena) y el pigmento carotenoide retinal 11-cis-retinal. La rodopsina activada (pasa por batorrodopsina, lumirrodopsina, metarrodopsina I y metarrodopsina II, que es la rodopsina activada) excita los cambios elctricos en los bastones, de donde se origina la imagen visual que se transmite hacia la corteza visual. En la formacin de la rodopsina interviene la vitamina A. El potencial de receptor de los bastones es hiperpolarizante y no despolarizante, es decir, se produce una mayor negatividad interna, pues al descomponerse la rodopsina, disminuye la conductancia al Na+. Cuando la rodopsina del segmento externo del bastn se expone a la luz y comienza a descomponerse, disminuye la conductancia al sodio hacia el interior del bastn; los iones sodio continan siendo bombeados al exterior (salen ms de los que entran). Al mximo de luz, el potencial de membrana se aproxima a 70 -80 mV. La descomposicin de la rodopsina produce una cascada de eventos que desencadenan la hiperpolarizacin El potencial de receptor es proporcional al log de la intensidad luminosa. No se conocen con exactitud los neurotransmisores de la retina; se piensa que puede ser glutamato en los conos y
203
bastones; en cambio, las clulas amacrinas liberaran GABA, glicina, dopamina, acetilcolina e indolamina; todos son neurotransmisores inhibitorios. Las clulas ganglionares son las nicas neuronas retinianas que siempre transmiten los potenciales de accin. Todas las neuronas conducen en forma electrotnica, que es un flujo de corriente, no potenciales de accin, en el citoplasma neuronal. Permite una conduccin gradual de la potencia de la seal, no es todo o nada. Vas pticas.
IMAGEN VISUAL
VA Y PROCESAMIENTO
Ojo izquierdo
Ojo derecho Imagen Retinal
Nervio ptico Cuerpo Geniculado Lateral Quiasma ptico Cintilla ptica
Fascculo Genculo Calcarino
204
Las vas aferentes parten de la retina; las fibras de las neuronas ganglionares van a formar los nervios pticos. A este respecto, la retina de cada ojo se considera dividida en dos mitades, con lo cual se describe una hemirretina nasal y otra temporal; cada nervio ptico lleva todas las fibras nasales y temporales del ojo correspondiente. Estas fibras llegan a una zona denominada quiasma ptico, en que las fibras de cada nervio ptico se separan; las de ambas hemirretinas nasales se cruzan, en cambio las de cada hemirretina temporal continan sin cruzar. Del quiasma ptico se originan las cintillas pticas derecha e izquierda, cada una lleva ahora fibras de la hemirretina nasal de un ojo y de la hemirretina temporal del ojo contralateral. Desde Corteza de Corteza de las cintillas van fibras a los ncleos pretectales del mesencfalo y Asociacin Visual Asociacin Visual a los tubrculos cuadrigminos superiores, pero el grueso de las Corteza Visual fibras se dirigen a los ncleos o cuerpos geniculados laterales del Calcarina tlamo; de aqu se originan ambos fascculos genculo-calcarinos que llegan hasta la corteza visual primaria. Una vez procesada la informacin, sta parte por las vas eferentes, pasa por los ncleos de Edinger Westphal; un grupo de fibras acompaa al tercer par craneano y otro grupo va al ganglio ciliar cuyas fibras inervan al esfnter pupilar; es as como el III par contiene fibras parasimpticas que inervan al msculo circular del iris.
205
VA DE LA VISIN
La corteza visual se encuentra ubicada en el lbulo occipital; como en todo fenmeno sensitivo, hay un rea primaria y otras de asociacin. El rea visual primaria o rea 17 de Brodman, se encuentra situada principalmente a ambos lados de la cisura calcarina. En sentido horizontal estn representados, punto por punto, los campos receptivos de ambas retinas; tambin se puede observar otro tipo de localizaciones, como ser visin de formas, de movimiento, sentido de lugar, atencin ptica, reconocimiento ptico de objetos, de nmeros, de colores y memoria topogrfica. Las columnas verticales de la corteza visual contienen varios millones de columnas verticales de neuronas, con dimetros de 30-50 micrones. Al igual que en toda la corteza, cada columna es una unidad funcional; cada una tiene unas 1000 o ms neuronas.
206
En las reas primarias y secundarias hay reas columnares especiales llamadas manchas de color, que decodifican el color. Funcionamiento del cristalino. Los rayos luminosos deben atravesar diferentes estructuras en el ojo para luego converger en los fotorreceptores. Sobre la retina se forma una imagen ms pequea que la natural e invertida. El cristalino puede modificar su poder de refraccin y as determinar que la imagen se forme exactamente sobre la retina. Se denomina acomodacin del cristalino el mecanismo por el cual esta lente modifica su curvatura segn necesidades de foco. Sin embargo en el ojo, su poder refractario est determinado en su mayor parte por la superficie anterior de la crnea y no por el cristalino. Como adems hay lquido alrededor del cristalino, su poder refractario es de unas 20 dioptras. En cambio la acomodacin del cristalino es de unas 14 dioptras. La importancia, sin embargo, del cristalino en el proceso de acomodacin, es que ella puede variar de un instante a otro en respuesta a las necesidades de actualizar el foco. El msculo ciliar tiene fibras meridionales y circulares. Su contraccin relaja los ligamentos de la cpsula, sta se relaja y el cristalino se vuelve ms esfrico, tiene el mximo de dioptras. Cuando el msculo ciliar est relajado, la intensidad diptrica del cristalino es la ms dbil. Estas variaciones en la curvatura del cristalino, y por ende, en su poder de refraccin, se deben a que la cpsula del cristalino es ms delgada en el centro y el cristalino es elstico. El reflejo del msculo ciliar tiene vas aferentes que se originan en la retina, continan por las vas pticas para llegar a la corteza cerebral estriada o calcarina, de la cual parte la va eferente; sta va a los ncleos de Edingher Westphal y ganglios ciliares, para inervar al msculo ciliar. La regulacin del msculo ciliar es parasimptica, mediante
207
fibras del III par craneano. La estimulacin parasimptica contrae el msculo ciliar; se relajan los ligamentos y el cristalino aumenta su poder de refraccin. (Una dioptra es el poder de una lente para enfocar los rayos luminosos a un metro de distancia focal. 1 dioptra = 1 / f , en que f es la distancia focal medida en metros) Se denomina punto lejano de la visin a la menor distancia a la cual un objeto se puede focalizar sin acomodacin del cristalino; normalmente es del orden de 6 metros. El punto cercano es el punto ms prximo al ojo desde el cual se puede enfocar claramente un objeto; en este caso, el cristalino exhibe su mximo poder de refraccin, o sea su mayor grado de curvatura; puede llegar a tener 10 dioptras, es decir, se enfoca el objeto a una distancia de 10 cms., con lo cual 1 / 0.10 = 10 dioptras. Reflejo pupilar a la luz. Como se indica, es un reflejo a la luz, para diferenciarlo de lo que ocurre con la estimulacin simptica general, que es una respuesta a estados de emergencia. El reflejo pupilar es consensual, pues basta que la luz llegue a un ojo para que se contraigan ambas pupilas.El dimetro pupilar es de 1,5 a 8 mm. y su tamao grada la cantidad de luz que penetra al ojo, la cual es proporcional al cuadrado del dimetro pupilar. Desde las cintillas van fibras a: -ncleo supraquiasmtico del hipotlamo -ncleos pretectales ( movimientos oculares y reflejo pupilar) -cuerpos geniculados laterales del tlamo. El ncleo de Edinger Westphal , ubicado en la regin pretectal, es estimulado por la luz e inhibido en la oscuridad, lo que determina que el dimetro pupilar disminuya o aumente respectivamente.
208
CONTROL DEL DIAMETRO PUPILAR
Como se mencion anteriormente, en la estimulacin simptica general se produce una midriasis, por contraccin de la musculatura radial del iris; estas fibras iridodilatadoras simpticas se originan en neuronas de la mdula torcica (T1), de aqu entran fibras a la cadena simptica hasta el ganglio cervical superior y luego, fibras postganglionares terminan en las fibras radiales del iris. Movimientos oculares. Los movimientos oculares permiten dirigir y fijar la mirada en puntos u objetos que se desea ver. Una observacin somera establece que se producen en estrecha asociacin con movimientos asociados del cuello y cabeza, para lo cual, a nivel del tronco, existen conexiones estrechas entre los ncleos motores oculares y los que controlan los giros ceflicos. Por otra parte, el fascculo longitudinal medial interconecta los tres ncleo de los pares III, IV y VI. Seis pares de msculos oculares son responsables de los
209
movimientos de los globos oculares; estos msculos estn inervados por los pares craneanos motor ocular comn (III par) , pattico o troclear (IV par) y motor ocular externo (VI par). Cada msculo culomotor realiza uno o ms tipos diferentes de movimientos del globo ocular, a saber: el recto externo o lateral es abductor; el recto interno o medial es adductor; el recto superior y el oblicuo menor o inferior giran el ojo hacia arriba; en cambio, el recto inferior y el oblicuo mayor o superior lo giran hacia abajo. Cada uno de los tres grupos de msculos oculares est inervado de manera recproca, de modo que funcionan como agonistas y antagonistas; por ejemplo, para realizar un movimiento lateral, se contrae un grupo de msculos y el opuesto se relaja. Si se desea mirar hacia el lado derecho del cuerpo, se producen los siguientes fenmenos musculares: se contraen el recto externo del ojo derecho y se relaja el recto interno del mismo ojo. Pero como los movimientos de ambos ojos son sincrnicos, simultneamente se contrae el recto interno del ojo izquierdo y se relaja el recto externo del mismo ojo. Si se trata de movimientos oculares hacia arriba y hacia abajo, los rectos superiores e inferiores de ambos ojos se contraen y se relajan sinrgicamente, es decir, si el movimiento ocular es hacia arriba, se contraen los rectos superiores de ambos ojos y se relajan sus rectos inferiores. Los msculos oblicuos permiten girar los ojos y mantener as el campo visual en la posicin deseada. Los impulsos motores van desde las reas occipitales visuales por los haces occpitotectal y occpitocolicular hacia las zonas pretectales y de los tubrculos cuadrigminos superiores. Adems, un haz frontectal pasa de la corteza frontal al rea pretectal. Desde ambas zonas, pretectal y tubrculo cuadrigmino superior, van los impulsos a los ncleos de nervios culomotores y de aqu a las motoneuronas de los efectores, que son los msculos extrnsecos del ojo. Adems, el sistema vestibular les enva impulsos desde los ncleos vestibulares a travs del
210
fascculo longitudinal medial, con lo cual el sistema visual participa en le regulacin del equilibrio y posicin del cuerpo. Movimientos de fijacin: permiten centrarse en un objeto, primero voluntariamente (regin premotora frontal) y luego se mantiene la fijacin en forma involuntaria , lo que se denomina bloqueo (reas visuales secundarias de la corteza occipital). En la fijacin involuntaria intervienen los colculos superiores. Audicin y funcin vestibular. El rgano que se denomina odo desempea dos funciones bien diferentes: 1.- audicin; 2.- regulacin del equilibrio corporal. El fenmeno de la audicin consiste en la captacin de ondas sonoras, su transduccin en fenmenos elctricos (biopotenciales) y su interpretacin por la corteza cerebral, lo que permite que dichas ondas adquieran sentido, es decir, representen un mensaje para el individuo. En cuanto al equilibrio corporal, la funcin vestibular participa en su regulacin junto a otros sistemas, como la funcin cerebelosa, la visin, etc. Audicin. El odo externo tiene un pabelln u oreja, que en algunos animales puede moverse como antena; en todo caso, ayuda a ubicar el sitio de origen del sonido, pero su funcin principal es captar las ondas sonoras y trasladarlas hasta el tmpano; estas ondas penetran por el conducto auditivo externo y hacen vibrar la membrana timpnica, la cual separa al odo externo del odo medio. Este est constitudo por una cavidad llena de aire, ubicada en el hueso temporal y que se abre a la nasofaringe por la trompa de Eustaquio, que lo comunica con el exterior. La
211
trompa se abre con la masticacin, la deglucin y el bostezo. El odo medio posee los tres huesecillos martillo, yunque y estribo, ubicados en cadena. El manubrio o mango del martillo est adherido a la cara interna del tmpano, la cabeza a la pared del odo medio y su proceso corto al yunque; este articula con la cabeza del estribo, cuya base va unida a la pared de la ventana oval; desde sta, los sonidos se transmiten al caracol o cclea del odo interno. La unin tan especial por medio de ligamentos de los huesecillos, determina que si se mueve el martillo (por vibracin del tmpano), el yunque se mueve consecutivamente. Existen en el odo medio dos pequeos msculos esquelticos, el tensor del tmpano y el estapedio del estribo. La contraccin del tensor del tmpano tira el manubrio del martillo hacia adentro y disminuye las vibraciones del tmpano; la contraccin del estapedio tracciona la base del estribo desde la ventana oval. Cuando el mango del martillo se mueve hacia adentro, el estribo hace desplazar el lquido coclear hacia adentro o hacia fuera, segn el caso. Ligamentos y msculos atraen constantemente hacia adentro al mango del martillo, de modo que el tmpano est permanentemente tenso. El odo interno consta de dos partes pricipales: los canales o conductos semicirculares y la cclea o caracol. Los primeros participan en la funcin vestibular. La cclea es un tubo enrollado de unos 35 mm de longitud, que en el ser humano da aproximadamente 2.75 vueltas. Dos membranas lo dividen longitudinalmente en tres cmaras, que se pueden observar en un corte transversal del tubo: 1.- cmara o rampa vestibular, llena con perilinfa y separada de la cmara media por la membrana vestibular o de Reissner, la cual es muy fina y permite que desde un punto de vista funcional, las rampas vestibular y media formen una sola entidad; 2.- rampa o cmara media, que posee endolinfa y se separa de la rampa timpnica mediante la membrana basilar;
212
3.- rampa timpnica, que tambin contiene perilinfa y se comunica con la rampa vestibular mediante una abertura llamada helicotrema; esta rampa termina en la ventana redonda, que posee una membrana timpnica secundaria. Las vibraciones sonoras penetran a la rampa vestibular a travs de la ventana oval, donde est apoyado el estribo. Estas vibraciones hacen mover el lquido en las rampas vestibular y media, movimiento que se transmite a la rampa timpnica y repercute en la membrana de la ventana redonda, que hace protrusin hacia fuera. Segn la rapidez con que se muevan las ondas sonoras ser el camino que tomen para llegar a la ventana redonda; en el caso de movimientos lentos del estribo, las ondas se mueven hacia la rampa timpnica a travs del helicotrema; si las ondas sonoras que mueven al estribo son rpidas, la onda lquida toma un camino ms corto a travs de la membrana basilar. Cada frecuencia de sonido produce una vibracin diferente. Organo de Corti. Las clulas receptoras auditivas se encuentran organizadas en una estructura denominada rgano de Corti, situado sobre la membrana basilar. Los receptores son clulas ciliadas cubiertas por la membrana tectorial; estn rodeadas de endolinfa, lquido necesario para el funcionamiento normal de las clulas ciliadas. El potencial generador se origina por el desplazamiento de los cilios debido a las vibraciones de la membrana basilar que hace que aqullos se froten contra la membrana tectorial. Este potencial generador depende de la sonoridad que producen las ondas, la cual es funcin de: -intensidad del sonido, de la que depende la amplitud de la vibracin de la membrana basilar y por lo tanto de los cilios; a mayor intensidad sonora, mayor amplitud del potencial
213
generador; -amplitud de la vibracin sonora: aumenta el nmero de clulas ciliadas estimuladas, lo que da la sumacin espacial. Existen variaciones en el umbral de excitacin de los receptores; as, algunas clulas ciliadas slo se estimulan si la vibracin de la membrana basilar es de gran intensidad. Adems de la transmisin de ondas sonoras por la cadena de huesecillos, existe transmisin sea por los huesos del crneo, que a travs de la perilinfa pueden hacer vibrar a la membrana basilar y estimular as a los receptores auditivos o clulas ciliadas; este mecanismo no participa en la audicin normal, pero podra adquirir importancia en ciertos casos de hipoacucia. Los cuerpos celulares de las neuronas aferentes o sensitivas estn situados en el ganglio espiral o de Corti dentro del modiolo o eje seo sobre el cual est enrollada la cclea; el axn perifrico est en estrecho contacto con las clulas ciliares, los axones centrales forman la rama auditiva del nervio auditivo y terminan en los ncleos cocleares dorsal y ventral del puente. La segunda neurona va al ncleo olivar superior, de aqu la va auditiva contina por el lemnisco lateral a los colculos inferiores de la lmina cuadrigmina, luego a los ncleos geniculados mediales del tlamo para llegar finalmente a la corteza auditiva primaria, ubicada en el lbulo temporal. Fibras colaterales de las vas auditivas pasan directamente al sistema reticular activador del tronco cerebral, y otras vas llegan al cerebelo, activando al vermis cerebeloso en caso de ruidos bruscos.
214
VA AUDITIVA
La corteza cerebral auditiva primaria est ubicada en el giro temporal superior, en el fondo de la cisura lateral o de Silvio, y constituye las reas 41 y 42 de Brodman; adyacentes a ella existen reas auditivas de asociacin, distribudas en forma extensa y que llegan hasta la nsula. Funcin vestibular. Se relaciona con el equilibrio del cuerpo y su estructura ms caracterstica son los conductos o canales semicirculares. El odo interno est conformado por una porcin sea y por dentro un laberinto membranoso, constituido por los tres conductos semicirculares, el sculo, el utrculo y el caracol; ste ltimo participa en la audicin y no en la funcin vestibular. Por fuera del laberinto membranoso existe perilinfa y en su interior est la endolinfa, sin que exista comunicacin entre ambos lquidos.
215
Los tres conductos semicirculares nacen del utrculo y despus de su recorrido, vuelven a l; tienen forma de arco y estn orientados en los planos frontal, sagital y horizontal de la cabeza; segn eso, se les denomina anterior, posterior y lateral. En su llegada al utrculo forman una dilatacin o ampolla, en cuyo interior hay un tabique o cresta ampular, que es una estructura receptora, para lo cual posee clulas ciliares las que estn cubiertas por una cpula de material mucoide. En ntimo contacto con las clulas ciliares hay terminaciones aferentes de la rama vestibular del VIII par. Dentro del laberinto membranoso, en la base del sculo y del utrculo, estn las mculas u rganos otolticos; al igual que la cresta ampular, tienen clulas de sustentacin y clulas ciliares, que poseen una cubierta mucoide y sobre ella estn los otolitos, que son cristales de carbonato de calcio. Las clulas ciliares de las mculas reciben idntica inervacin que las clulas ciliares de las crestas ampulares. No se conoce a cabalidad la funcin que desempean los otolitos; indudablemente que facilitan el movimiento de la cpula mucoide; ha existido una curiosa teora que los vincula a la fijacin del calcio seo, accin que estara disminuda en los individuos que permanecen en decbito horizontal por perodos prolongados. Otro hecho curioso es que se ha demostrado que algunas aves migratorias poseen en sus canales semicirculares molculas de fierro, que al parecer les ayudaran a orientarse con el magnetismo terrestre. Los cuerpos celulares de estas neuronas estn en el ganglio stibular; los axones perifricos son los que hacen contacto con las clulas ciliares y las fibras centrales van al cerebelo y al ncleo vestibular ipsilateral; de aqu parten los haces vestbulo-espinales, que se dirigen a la mdula espinal llevando los impulsos de ajustes posturales, y por el fascculo longitudinal medial a los ncleos motores de los nervios craneanos culo-motores. A travs del tlamo, las vas llegan a la corteza cerebral.
216
VAS VESTIBULARES
La estimulacin de los receptores vestibulares se produce por el movimiento de los cilios ocasionado por la endolinfa. A nivel de los conductos semicirculares, la aceleracin del movimiento de la cabeza moviliza a la endolinfa, la que por su inercia se mueve relativamente en direccin opuesta a la rotacin de la cabeza. La cpula de la cresta ampular es empujada por el lquido, el que la hace girar doblando las prolongaciones de las clulas ciliares. Cuando la aceleracin es nula con velocidad constante del movimiento de la cabeza, la endolinfa gira a la misma velocidad del cuerpo y la cpula vuelve a su posicin normal. Si cesa la rotacin, la aceleracin negativa determina que la endolinfa se desplace en la direccin de la rotacin y la cpula
217
vuelve a la posicin media en 25-30 segundos. El nistagmus es un movimiento brusco espasmdico de los ojos que se observa al comienzo y al final de un perodo de rotacin. Tiene un componente lento en direccin opuesta a la rotacin, y otro rpido en que los ojos regresan a un nuevo punto de fijacin.; el lento se produce por impulsos desde el laberinto y el rpido por accin de un centro del tronco cerebral. El nistagmo es generalmente horizontal, pero tambin puede ser vertical y/o rotatorio, dependiendo del movimiento de la cabeza. Por convencin, la direccin del movimiento ocular se identifica por la direccin del componente rpido. Respuestas maculares. En los mamferos, las mculas del utrculo y del sculo responden tanto a la aceleracin angular como a la lineal. Los otolitos son ms densos que la endolinfa y la aceleracin los hace desplazarse en direccin opuesta, deformando las clulas ciliares y generando potenciales. Las mculas presentan actividad tnica, debido a la accin de la gravedad sobre los otolitos. La mayor parte de las respuestas a estimulacin macular son reflejas, pero los impulsos vestibulares tambin alcanzan la corteza cerebral; as se permite la percepcin consciente del movimiento y proveen informacin para la orientacin en el espacio. La estimulacin vestibular excesiva puede provocar nuseas, variacin de la presin arterial, sudoracin, palidez y vmitos. Se denomina vrtigo a la sensacin de rotacin sin que sta exista realmente. Se puede producir experimentalmente (con fines diagnstico) estimulando los canales semicirculares mediante instilacin de lquido en el conducto auditivo externo a temperaturas diferentes de 37 C, lo que moviliza a la endolinfa por conveccin. Por ltimo, la orientacin del cuerpo en el espacio depende de impulsos vestibulares, de propioceptores articulares, de exteroceptores cutneos de presin y de seales visuales.Cuando
218
las seales son contradictorias, las mujeres confan ms en la informacin visual y los varones en la vestibular. Sistema Somatomotor. El movimiento es una de las caractersticas ms sobresalientes del ser vivo; aunque no es exclusivo del sistema smatomotor, de l dependen funciones tan importantes como la locomocin, las reacciones de defensa, las manifestaciones conductuales derivadas de procesos psicolgicos y las conductas somticas en general. En la conducta smato-motora se incluye toda aquella actividad que deriva de la accin de la musculatura esqueltica o estriada, la cual en un adulto normal constituye alrededor de un 40 % de su masa corporal. Las actividades cardaca y visceral no corresponden a la designacin de smato-motoras, sino que tienen su denominacin propia, puesto que su musculatura tiene caractersticas peculiares que les hacen presentar un funcionamiento diferente al de la musculatura esqueltica. Estructura de la fibra muscular. El msculo estriado est constituido por clulas denominadas fibras musculares, cuyos dimetros son del orden de 10 a 80 micrones. A su vez, cada fibra muscular est inervada por una sola terminacin nerviosa, binomio que constituye la unidad neurmuscular; ambos elementos estn relacionados mediante una sinapsis llamada placa motora de Roget o placa neuromuscular. La membrana celular de la fibra muscular es el sarcolema y su citoplasma es el sarcoplasma. Por otra parte, una sola fibra nerviosa puede inervar mltiples fibras musculares, entre 2 y 1000, con un promedio de 180. Se denomina unidad motora al conjunto de fibras musculares inervadas por una misma fibra nerviosa. En msculos rpidos como los larngeos, una fibra nerviosa no inerva ms de 2 0 3 fibras musculares; en cambio, msculos encargados de mantener
219
la posicin del cuerpo pueden presentar una relacin de 1000 fibras musculares por cada fibra nerviosa. El sarcolema se fusiona en los extremos de la fibra muscular con fibras tendinosas, formando haces que constituyen los tendones, los que se insertan en los huesos; esta insercin constituye un punto fijo o punto de apoyo para el desarrollo de fuerza cuando el msculo se contrae. La fibra muscular contiene cientos a miles de miofibrillas, las que poseen las protenas contrctiles que son los filamentos de actina y miosina, as como el complejo troponina-tropomiosina. El filamento de miosina es ms grueso que el de actina y contiene unas 200 molculas de miosina; est formado por una meromiosina ligera que articula con una meromiosina pesada; sta ltima posee un brazo y una cabeza que tambin son articuladas y que constituyen un puente cruzado. El filamento de actina est conformado por dos bandas enrolladas en hlice, entre las cuales van polmeros de tropomiosina, unida a la cual hay una molcula de troponina que posee gran afinidad por el Ca++ . La actina posee sitios activos a los cuales puede adherirse la cabeza de la miosina. Los filamentos de actina y de miosina van dispuestos en forma paralela y parcialmente interdigitados, lo cual determina que las miofibrillas presenten bandas claras y oscuras que, sumadas transversalmente, le dan al msculo su aspecto estriado. Los filamentos de actina se originan desde los discos Z, y entre dos discos Z est la unidad funcional de la miofibrilla que es el sarcmero, de longitud aproximada de 2 micrones. A ambos lados de los discos Z slo hay filamentos de actina que dan origen a una banda clara I (istropa para la luz polarizada). En la parte central del sarcmero los filamentos de actina y de miosina se superponen parcialmente, constituyendo la banda A (anistropa para la luz polarizada); en el msculo
220
relajado, al centro del sarcmero slo hay filamentos de miosina que forman la banda H. Estas bandas claras y oscuras y los discos Z se repiten en cada miofibrilla muchas veces, y como se dijo, al repetirse en sentido transversal, le dan las estriaciones al msculo esqueltico. Las miofibrillas estn inmersas en sarcoplasma, rico en mitocondrias, y que posee dos sistemas tubulares: 1.- retculo sarcoplsmico, ms abundante en los msculos de accin rpida, cuyos tbulos van dispuestos en forma paralela con las miofibrillas y sus extremos terminan en cisternas; 2.- tbulos transversos o en T, dispuestos en sentido perpendicular a las miofibrillas. La zona en que un tbulo T se junta con dos cisternas se denomina trada; hay dos tradas por sarcmero. Los tbulos T estn en coneccin con el lquido extracelular y por su interior se transmiten los potenciales de accin.
221
ESTRUCTURA MUSCULAR MACRO Y MICROSCPICA
Msculo
Fascculo Capilares Miofibrilla
Fibras Musculares
Sarcmero
Miofilamento delgado
Miofilamento grueso
222
Contraccin muscular. Se produce por deslizamiento de los filamentos de actina y miosina, los cuales estn dispuestos en forma interdigitada; la banda H en el centro del sarcmero tiende a desaparecer porque los filamentos de actina se acercan. Se ha propuesto una teora de la cremallera para explicar el deslizamiento de los filamentos, y por lo tanto, la contraccin muscular. En reposo, los sitios activos de la actina se encuentran inhibidos por el complejo troponina-tropomiosina. En presencia de iones calcio, ste se une a la troponina, entonces se desinhiben los sitos activos de la actina y los puentes cruzados, ms bien la cabeza de la miosina, se unen a los lugares activos de la actina; entonces se alteran las fuerzas de enlace qumico entre cabeza y brazo, por lo cual la cabeza gira hacia el centro del filamento de miosina y tracciona al de actina; cada inclinacin de la cabeza se llama un golpe activo, despus del cual la cabeza vuelve a su posicin anterior y se repite el ciclo de golpes activos. La energa necesaria para la realizacin de este proceso proviene del adenosin-tri-fosfato o ATP. Transmisin neuromuscular. Los potenciales de accin llegan a las fibras musculares por las motoneuronas alfa, que son fibras mielnicas gruesas. Las terminaciones nerviosas se ramifican en un telodendron amplio y forman con la fibra muscular la sinapsis denominada placa motora; toda la estructura est cubierta por clulas de Schwann, que ejercen un efecto aislante. La terminacin nerviosa se aplica sobre un lecho muscular con repliegues; la parte nerviosa corresponde a la porcin presinptica y la muscular a la postsinptica; entre ambas queda la hendidura sinptica; la estructura tiene la forma de una gotera. Los repliegues contribuyen a aumentar el rea postsinptica donde se encuentran los receptores nicotnicos colinrgicos, puesto que el neurotransmisor en esta sinapsis es acetilcolina. En
223
la superficie de la gotera existe acetilcolinoesterasa, enzima que degrada a la acetilcolina. El proceso del funcionamiento sinptico es el de cualquier sinapsis, en que el neurotransmisor se libera por un proceso de exocitosis dependiente del ion calcio. De la interaccin entre la acetilcolina y los receptores nicotnicos postsinpticos resulta la excitacin de la membrana muscular o sarcolema, la cual aumenta su permeabilidad a los iones Na+; stos entran a la fibra muscular, aumentando el potencial local (PEPS) o de placa terminal, el cual desencadena potenciales de accin en la fibra muscular. El potencial de reposo de la fibra muscular es alrededor de 85 mV y el voltaje umbral al cual se estimula, es decir, al cual se produce el potencial de accin, es aproximadamente 50 mV; por lo tanto, con un potencial de placa terminal de 35 mV se puede desencadenar el potencial de accin en la fibra muscular. Al igual de lo que sucede en otras sinapsis del sistema nervioso central, la unin neuromuscular es susceptible de fatigarse si el nmero de vesculas de acetilcolina disminuye a valores crticos, pero esto rara vez sucede porque la frecuencia de estimulacin de fatiga es de 150 / seg.; y los nervios raqudeos prcticamente no alcanzan esta frecuencia de transmisin de impulsos. Acoplamiento excitacin-contraccin. Una vez que se producen los potenciales de accin en la fibra muscular, difunden por la membrana de la fibra y desencadenan mecanismos que promueven la liberacin de calcio desde las cisternas terminales hacia el sarcoplasma. Actualmente se plantea la existencia de un segundo mensajero, el inositoltrifosfato o IP3 , que acta en la liberacin de calcio desde el retculo sarcoplsmico. En este mecanismo intervendran receptores de localizaciones precisas en el retculo, en la zona de las cisternas terminales.
224
En el proceso de la contraccin muscular, el Ca++ liberado difunde a las miofibrillas vecinas, se une fuertemente a la troponina y desencadena la contraccin muscular. Esta persiste mientras haya abundante Ca++ presente en el sarcoplasma. En las paredes de los tbulos del retcuo sarcoplsmico hay una bomba de calcio que retira estos iones del sarcoplasma y los concentra hasta unas 2000 veces en el interior de los tbulos longitudinales; con este mecanismo, el calcio disminuye a valores nfimos su concentracin en el sarcoplasma; en esta condicin, el complejo troponina-tropomiosina se mantiene inhibido y el msculo est relajado. Existen verdaderos pulsos de Ca++ que se producen porque los potenciales de accin aumentan la concentracin sarcoplsmica de Ca++, lo cual dura aproximadamente 1/50 de segundo; luego, la bomba de Ca++ hace disminuir su concentracin hasta que nuevos potenciales de accin la hacen aumentar. En cuanto a los valores de la concentracin de Ca++, en el msculo en reposo es del orden de 10-9 molar y en el msculo en actividad mxima es de 10-6 molar. Algunas caractersticas de la contraccin muscular. El tonus muscular es un pequeo grado de contraccin que persiste en el msculo en reposo y probablemente se debe a impulsos de origen espinal. En la contraccin muscular estriada se observa el fenmeno de la tetanizacin, que consiste en la fusin de contracciones sucesivas obtenidas a lo menos a una frecuencia crtica. La fuerza de contraccin puede aumentar por fenmenos de sumacin espacial y temporal. En la sumacin espacial aumenta el nmero de unidades motoras que se contraen simultneamente. En cambio en la sumacin temporal aumenta la rapidez de contraccin de cada unidad motora. Una contraccin puede ser isomtrica si no vara la longitud
225
del msculo que se contrae, o bien puede ser isotnica, en la cual el msculo se acorta pero su tensin permanece constante. En cuanto a la velocidad de contraccin, existen msculos rpidos, como los oculares, que se contraen en 1/100 seg., y otros lentos, como los antigravitacionales, que se contraen en 1/30 seg. Contracciones enrgicas y prolongadas pueden llegar a provocar fatiga muscular, la cual se debe a incapacidad de los procesos contrctiles y metablicos de las fibras musculares, en las cuales se ha depletado el ATP, para responder a los impulsos nerviosos que llegan a la unin neuromuscular. Reflejos medulares. A nivel medular existe lo que se podra denominar un primer nivel de integracin de la funcin motora.Es as como los impulsos sensitivos llegan a las races dorsales y a los cordones medulares posteriores, desde donde pueden seguir dos rutas principales: 1.- hacer sinapsis directamente o por medio de interneuronas, con neuronas motoras que van a inervar msculos estriados; 2.- ascender por los cordones posteriores hasta el tronco del encfalo y an hasta la corteza cerebral. Las interneuronas (o neuronas intercalares o internunciales) existen en toda la sustancia gris medular y son las ms numerosas, unas 30 veces el nmero de motoneuronas. Si bien las neuronas internunciales son pequeas, pueden descargar hasta 1500/seg.; sus funciones son de conexin e integracin y presentan diversas caractersticas como convergencia, divergencia, descarga ulterior, sumacin espacial y temporal, etc. La convergencia se refiere al control de una sola neurona por dos o ms fibras nerviosas separadas, al contrario de la divergencia, en que la excitacin de una sola fibra nerviosa estimula a varias neuronas con las que hace contacto.
226
La mayora de los impulsos motores provenientes de la corteza cerebral, o los sensoriales provenientes de receptores, terminan en las neuronas internunciales, y muy pocos lo hacen en forma directa sobre las motoneuronas. Adems, la mayor parte de los reflejos medulares son bi o poli sinpticos, es decir, poseen dos o ms sinapsis, y slo muy pocos no poseen interneuronas, o sea, son monosinpticos, en que la relacin se establece directamente entre la neurona sensitiva y la motoneurona. Fibras musculares. El msculo estriado est conformado por haces de fibras musculares que en sus extremos y en conjunto con el sarcolema y fibras tendinosas, forman los tendones que unen el msculo al hueso y le proporcionan un punto fijo de insercin. Las fibras musculares estriadas son de extrafusales e intrafusales, ubicadas en paralelo. dos tipos,
Las fibras extrafusales son las que al contraerse desarrollan fuerza muscular; las intrafusales contienen los receptores que son los husos neuromusculares y aunque tambin son fibras musculares, su contraccin no contribuye realmente al desarrollo de fuerza sino que influye en la autorregulacin de la contraccin muscular. Las fibras musculares reciben inervacin de motoneuronas cuyos somas estn localizados en las astas medulares anteriores. Las motoneuronas alfa inervan las fibras extrafusales y las motoneuronas gama inervan las fibras intrafusales. Las motoneuronas alfa reciben directa o indirectamente (por neuronas intercalares) todas las influencias sensitivas y motoras perifricas y centrales que regulan la actividad muscular, y luego van a inervar directamente el msculo, por lo cual dichas motoneuronas constituyen la va final comn a la musculatura
227
esqueltica. Las motoneuronas gama constituyen aproximadamente el 31 % de todas las fibras de motoneuronas musculares, activan y contraen a las fibras intrafusales , con lo cual se excitan los husos neuromusculares. Esta estimulacin provoca impulsos sensitivos que van por vas aferentes hasta hacer contacto finalmente con las motoneuronas alfa, las cuales modifican el grado de contraccin muscular. Algunas estructuras centrales que controlan la actividad muscular ejercen su efecto excitando o inhibiendo a las motoneuronas gama. Los husos neuromusculares son terminaciones nerviosas nulo-espirales ubicadas en las fibras intrafusales. Cada huso est constitudo por 3 a 10 pequeas fibras musculares que estn unidas a las vainas de las fibras musculares extrafusales. Los extremos musculares de la fibra intrafusal son las que reciben la inervacin gama, cuyos impulsos provocan la contraccin en dichos extremos musculares; esto determina que la parte central del huso se elongue, lo que significa la excitacin de este receptor nuloespiral. Estos receptores intrafusales captan tanto los cambios de longitud del huso como el ritmo de dicho cambio. Otro mecanismo de elongacin del huso lo constituye la traccin de todo el msculo, que puede producir un estiramiento de las fibras extrafusales y por consiguiente tambin de las fibras intrafusales, por el hecho de estar ubicadas en paralelo. El huso acta comparando las longitudes de ambos tipos de fibras musculares y se estimula en caso que que la longitud de las fibras extrafusales sea mayor que la longitud de las intrafusales; en caso contrario, el huso se inhibe. En resumen, los husos neuromusculares captan modificaciones en el grado, direccin y velocidad de cambio de la tensin muscular. Organos tendinosos de Golgi. Se encuentran ubicados en las fibras tendinosas y poseen un
228
umbral de excitacin ms bien alto, puesto que las tensiones de reposo muscular no los activan; su estmulo selectivo es el cambio rpide de la tensin, ya sea de aumento por contraccin muscular, o de disminucin de la tensin por relajacin muscular. La respuesta ante la estimulacin de los rganos tendinosos de Golgi es la relajacin del propio msculo, es decir, se trata de un mecanismo reflejo protector contra los desgarros de los tendones. Con los impulsos originados en ambos sistemas aferentes, los provenientes de los husos neuromusculares y de los rganos tendinosos de Golgi, se transmite al sistema nervioso central una informacin bastante completa. As, por ejemplo, si un msculo presenta un grado moderado de tensin, los rganos tendinosos de Golgi envan impulsos de frecuencia baja y constante, al mismo tiempo que los husos descargan a una frecuencia mayor. Ante un aumento repentino y mantenido de la tensin, las fibras provenientes de los receptores tendinosos aumentan su descarga de impulsos para luego disminuirla y mantenerla baja; a su vez, los impulsos de las fibras del huso aumentan su frecuencia y la mantienen alta. Si, por otra parte, la tensin muscular disminuye, los receptores de Golgi determinan que sus fibras mantengan descargas a niveles bajos de frecuencia y las fibras del huso reduzcan el nmero de impulsos y se estabilicen a una frecuencia menor. Clulas de Renshaw. Ramas colaterales de los axones motores vuelven a establecer contacto con neuronas intercalares medulares, denominadas clulas de Renshaw, que transmiten seales inhibitorias a neuronas vecinas. Por ltimo, existen fibras nerviosas propioespinales cuya funcin es interconectar los segmentos medulares, por lo cual se ramifican en sentido rostral y caudal. Los reflejos medulares son reflejos no condicionados que se producen en un sistema morfo-funcional denominado arco reflejo,
229
el cual consta de receptores, vas aferentes, centro reflejo, vas eferentes y efectores. Sobre los receptores actan los estmulos selectivos y los efectores provocan una respuesta motora. No obstante su carcter medular, los reflejos pueden ser modulados por estructuras superiores del sistema nervioso central. Tiempo reflejo y tiempo de reaccin. La respuesta refleja demora un tiempo en producirse desde que se aplica el estmulo; este tiempo depende de diversos factores, como ser la velocidad de conduccin de los impulsos (depende del tipo y dimetro de la fibra nerviosa), la longitud de las vas aferente y eferente y el nmero de sinapsis involucradas, puesto que en cada sinapsis existe un retardo sinptico. A esto debe agregarse, en los reflejos que tienen participacin psicolgica (como evaluacin de situaciones y decisin), un tiempo de reaccin, cuya cuanta depende del entrenamiento y de factores personales. Reflejo miottico. Se le denomina tambin reflejo del huso muscular o de estiramiento o de traccin; relaciona el grado de estiramiento de las fibras intrafusales con la contraccin de las fibras extrafusales. La va aferente, que va desde la terminacin nulo-espiral a la mdula espinal, est constituda por fibras I a y la va eferente es la motoneurona alfa. Al ser traccionado, el huso muscular se excita, y como respuesta dinmica se produce la contraccin de las fibras extrafusales del mismo msculo. La estimulacin del huso neuromuscular por traccin, junto con excitar a las motoneuronas alfa, enva impulsos hacia las motoneuronas gama, eferencias que inervan a las fibras extrafusales y que permiten que stas readecen su propia longitud a la nueva longitud de la fibra extrafusal. Existe tambin un reflejo de traccin negativo, consistente
230
en que el acortamiento muscular brusco desencadena una inhibicin del mecanismo reflejo que se opone al acortamiento muscular. En lo que se refiere al control central del reflejo miottico, las seales del huso que ingresan a la mdula, van al cerebelo y a la formacin reticular bulbar; a su vez, el sistema eferente gama es excitado preferencialmente por la formacin reticular facilitadora del bulbo raqudeo y secundariamente por el cerebelo, ncleos de la base y corteza cerebral. Reflejo tendinoso. Es fundamentalmente un reflejo inhibitorio de la contraccin muscular, cuyos impulsos se originan en los receptores tendinosos de Golgi y van por vas aferentes del tipo I b; producen inhibicin de la motoneurona alfa excitando a interneuronas inhibitorias, a la vez que enviando impulsos al cerebelo por los fascculos espinocerebelosos. Principio de inervacin recproca. En la ejecucin de un movimiento, y por lo tanto, de un reflejo flexor o extensor, participan msculos agonistas y antagonistas, siendo agonistas los que se contraen y antagonistas los que se relajan, en una dualidad de accin que deriva del principio de inervacin recproca. El mecanismo puede ser segmentario y/o con participacin de ncleos supramedulares. En el primer caso, la estimulacin de los husos neuromusculares provoca, como ya se explic, la contraccin de las fibras extrafusales del mismo msculo, que en este caso se denomina agonista. Por otra parte, los mismos impulsos provenientes de los husos neuromusculares y que van por la neurona sensitiva I a , estimulan tambin a una neurona intercalar inhibitoria, que es la que enva impulsos inhibitorios al msculo antagonista, el cual se relaja. A las neuronas internunciales inhibitorias les llegan tambin impulsos desde ncleos supramedulars como el cerebelo,
231
formacin reticular y ncleos extrapiramidales, los cuales actuaran inhibiendo a las motoneuronas de los msculos antagonistas. Por otra parte, existen relaciones recprocas entre ambas porciones laterales de la mdula, pudiendo provocar un reflejo flexor en una extremidad y la extensin de la extremidad del lado contrario. El principio de inervacin recproca es de importancia fundamental en la marcha, pues al tiempo que permite mover una extremidad hacia delante, determina que la otra permanezca atrs. Rebote. Terminado un reflejo, un segundo reflejo del mismo tipo es ms difcil de provocar durante un cierto tiempo; pero por inervacin recproca, los reflejos antagonistas son ms fciles de desencadenar en el mismo perodo. Reflejo flexor. Consiste en una contraccin potente de los msculos flexores de una extremidad, con relajacin de los extensores antagonistas. Generalmente es la respuesta a un estmulo nociceptivo, en cuyo caso se puede acompaar de un movimiento de retraccin o alejamiento de todo el cuerpo. Reflejo extensor cruzado. Inmediatamente despus de desencadenarse el reflejo flexor en una extremidad, se extiende la extremidad contraletaral; puede impulsar a todo el cuerpo, alejndolo del estmulo nociceptivo. Reflejos posturales. Se describe una reaccin positiva de sostn del cuerpo, que
232
consiste en que la extremidad que lo sostiene se extiende contra la presin aplicada en la planta del pie; es un reflejo polisinptico. Se denomina reaccin magntica al hecho que la presin aplicada en un pie hace que ste se mueva en la misma direccin, es decir, si la presin se aplica hacia delante, el pie se mueve hacia adelante. Con este mecanismo se ayuda a la mantencin del equilibrio, por cuanto la extremidad se extiende hacia el lado de la mayor presin, impulsando el cuerpo en direccin opuesta. El reflejo de la marcha rtmica consiste en que la flexin de una extremidad hacia delante, va seguida de extensin hacia atrs, en ciclos repetitivos. Es el resultado de inhibicin recproca y rebote, en la siguiente secuencia: la flexin hacia delante provoca inhibicin recproca de los extensores; luego desaparece la flexin y entonces la inhibicin por rebote de los flexores y la excitacin de los extensores hace que la pierna se mueva hacia abajo y atrs. Es decir, cuando una pierna se mueve hacia delante, la opuesta se mueve hacia atrs, lo que resulta del principio de inervacin recproca entre ambas extremidades. Reflejo del rascado. Se inicia por la sensacin de prurito e incluye dos actuaciones: ubicacin del punto preciso de la picazn y el movimiento de rascado propiamente tal, en que participan circuitos oscilatorios de interneuronas. Regulacin neuromuscular. Uno de los aspectos fundamentales del movimiento lo constituyen los mecanismos de contraccin y de relajacin muscular; no obstante, ni los movimientos ms elementales se podran realizar de no existir una perfecta armona entre las acciones de los grupos musculares involucrados, as como una orientacin clara, definida, rpida, de los objetivos del movimiento. De aqu deriva la importancia de la regulacin neuromuscular, que comprende aspectos tales como:
233
1.- reflejo miottico, que regula los cambios de longitud y de tensin de la propia fibra muscular; 2.- reflejos tendinosos, que protegen a la musculatura de tracciones excesivas; 3.- principio de inervacin recproca; 4.- funcin inhibitoria de las clulas de Renshaw; 5.- impulsos activadores o inhibidores provenientes de estructuras enceflicas, como formacin reticular, ncleos de la base, aparato vestibular, cerebelo, corteza cerebral. Estos constituyen los mecanismos centrales de la regulacin neuromuscular, generalmente difciles de separar de los mecanismos ms propiamente espinales, puesto que ambos grupos funcionan muy interrelacionados y se complementan. Conviene recordar que en el ser humano est muy desarrollada la encefalizacin, es decir, el papel importante que desarrolla la corteza cerebral en la realizacin y coordinacin de diferentes funciones, entre ellas la motora. Formacin reticular. Se encuentra distribuda en el tronco cerebral y diencfalo, continundose con las neuronas internunciales espinales. En trminos generales, se ha establecido que las zonas centrales son motoras, en cambio las porciones laterales son sensitivas. Existen estructuras no reticulares que mantienen con la formacin reticular interrelaciones tan estrechas que se le considera formando parte funcional de ella, y con la cual pasan a constituir un sistema reticular. Entre estas estructuras cabe mencionar la capa VI de la neocorteza, el ncleo rojo, la sustancia nigra y el complejo olivar. La formacin reticular recibe mltiples aferencias, de las cuales, y en relacin con la regulacin neuromuscular, se pueden mencionar las de la mdula espinal (haces espinorreticulares y colaterales de los haces espinotalmicos), de los haces vestibulares, los impulsos cerebelosos, de los ncleos basales y
234
de la corteza cerebral motora. La mayor parte de la formacin reticular es excitadora (facilitadora o activadora); se le denomina sustancia reticular activadora ascendente (SRAA). Tanto ella como los ncleos vestibulares son intrnsecamente excitables, lo cual significa que si no son inhibidos, estn enviando continuamente impulsos a las zonas motoras espinales y cerebrales. Sin embargo, normalmente la SRAA est recibiendo impulsos inhibidores desde los ncleos de la base, cerebelo y corteza cerebral, lo que impide que la SRAA est hiperactivada; en este ltimo caso de hiperactivacin se produce rigidez de todos los msculos extensores antigravitatorios. Se ha descrito tambin un rea reticular inhibitoria (SRI), ubicada principalmente en la regin medial ventral de la parte caudal del bulbo raqudeo. Su estimulacin provoca disminucin del tonus de gran parte de la musculatura esqueltica. La SRI no es intrnsecamente excitable, pero recibe impulsos estimulantes desde los ncleos basales, cerebelo y corteza cerebral. Ambas sustancias reticulares, la activadora y la inhibidora, funcionan estrechamente interrelacionadas. En la posicin antigravitacional, hay impulsos continuos desde la sustancia reticular y ncleos asociados hacia la mdula y msculos extensores, con lo cual se mantienen rgidas las extremidades; los impulsos van principalmente por los fascculos retculoespinales y vestbuloespinales; el grado de actividad de los msculos extensores depende de los mecanismos de equilibrio. Ncleos de la base. De ellos, los ncleos caudado, putamen y globo plido participan en las funciones motoras, no as los ncleos amigdalino y clastrum o antemuro. Los de funcin motora se denominan cuerpos estriados. En relacin con ellos y la funcin motora, cabe mencionar las estrechas relaciones existentes entre:
235
1.- corteza motora y premotora con caudado y putamen y viceversa; 2.- corteza motora con protuberancia y cerebelo y viceversa, en cuyo caso los impulsos pasan por el tlamo y van a los ncleos de la base; 3.- ncleos de la base y porcin inferior del tronco del encfalo proyectndose a ncleos reticulares, ncleo rojo y oliva inferior; 4.- ncleos de la base entre s; 5.- conexiones directas entre corteza motora y ncleos reticulares del tronco. En relacin con la motricidad, los ncleos basales tienen algunas funciones especficas; es as como su activacin inhibe a la sustancia reticular activadora y excita a la sustancia reticular inhibidora, con lo cual disminuye el tono muscular. Los cuerpos estriados caudado y putamen parecen controlar y an iniciar los movimientos intencionales simples, para lo cual transmiten impulsos por las siguientes vas: 1.- al globo plido y corteza cerebral por el tlamo, y a la mdula espinal por vas piramidales y extrapiramidales; 2.- al globo plido y sustancia nigra por vas cortas o la formacin reticular, y hacia la mdula espinal por los haces retculoespinales. El globo plido mantiene un tonus basal movimientos voluntarios, actuando por dos circuitos: para los
1.- retroaccin al tlamo, corteza cerebral y mdula espinal por las vas de los sistemas lateral y medial; 2.- por vas cortas a la formacin reticular del tronco, para continuar a la mdula espinal por los haces retculoespinales. Las lesiones de los ncleos de la base ilustran en cierto modo su participacin en la funcin motora. Es as como las lesiones difusas del cuerpo estriado producen el corea, que se caracteriza por contracciones desordenadas, incontroladas, de varios grupos
236
musculares. En cambio, la enfermedad de Parkinson se debe a la destruccin de la sustancia negra, con dficit de los neurotransmisores involucrados. Sistema vestibular. Es la estructura sensorial que produce las sensaciones relacionadas con el equilibrio; se encuentra ubicada en el odo interno y se relaciona con el movimiento de la cabeza. Fibras nerviosas de origen vestibular terminan en los ncleo vestibulares, ubicados en la unin bulboprotuberancial del tronco y en el cerebelo (ncleos del fastigo, vula y lbulo flculonodular); por los fascculos vestbulo-espinales van los impulsos relacionados con los ajustes posturales. Por medio del fascculo longitudinal medial, el aparato vestibular se conecta con los ncleos de los nervios craneanos culomotores, pares III, IV y Vi , relacionndose as con los movimientos oculares. La orientacin en el espacio depende de impulsos provenientes del sistema vestibular, de los propioceptores articulares, de exteroceptores cutneos y del sistema visual. Cerebelo y funciones motoras. Su accin principal consiste en el comando de ajustes correctores de actividades motoras originadas en otras partes del encfalo. Esta funcin la realiza mediante mecanismos de comparacin entre la posicin del cuerpo que indica la informacin sensorial y el estado que intenta producirle el sistema motor, despus de lo cual desencadena las seales correctas correspondientes. Como es fcil de comprender, los ajustes deben ser muy rpidos, por lo cual la informacin aferente y eferente es amplia. Para ello, el cerebelo recibe aferencias desde la corteza cerebral motora o precentral, oliva inferior, sistema vestibular, formacin reticular, husos neuromusculares, rganos tendinosos de Golgi, receptores cutneos, etc.; las vas aferentes son los haces espinocerebelosos y los cordones medulares dorsales.
237
A su vez, el cerebelo enva eferencias desde sus ncleos profundos, siendo las principales las siguientes: - el ncleo dentado se conecta a trvs del tlamo con los cuerpos estriados y a travs del ncleo rojo con la sustancia reticular y la mdula espinal; - los cuatro ncleos cerebelosos se conectan con la formacin reticular; - los ncleos del fastigio estn en relacin con los ncleos vestibulares. En relacin con las funciones motoras, el cerebelo participa en los movimientos voluntarios e involuntarios y en el equilibrio. Cerebelo y movimientos voluntarios. Los impulsos que los producen se originan en la corteza cerebral motora, desde donde van a la musculatura estriada; desde los receptores musculares, tendinosos y articulares va informacin al cerebelo por los haces espinocerebelosos y espinoolivares; desde el cerebelo los impulsos continan por la siguiente va: ncleo dentado tlamo corteza motora. Este es un mecanismo frenador de tipo feed back y permite amortiguar los movimientos. En general, los movimientos del cuerpo tienden a ser pendulares, y de la funcin cerebelosa depende que el movimiento se detenga exactamente en el sitio requerido. La falla en este mecanismo produce el temblor intencional, en que la extremidad que se mueve oscila alrededor del punto espacial elegido. Adems, el cerebelo ejerce funciones de prediccin y de progresin en sucesin ordenada, de los movimientos.
238
Cerebelo y movimientos involuntarios. Los movimientos involuntarios se relacionan con seales extrapiramidales, que pueden originarse en los ncleos basales o en el sistema reticular, para llegar al cerebelo, especialmente al paleocerebelo. Otra informacin llega al cerebelo desde los msculos en actividad, ejerciendo un control de error con un mecanismo de feed back similar al de los movimientos voluntarios; la va de retorno es: Cerebelo corteza cerebral motora ncleos basales tlamo sustancia reticular Luego, las seales correctoras van por las fibras retculoespinales hacia el sistema eferente gama del huso neuromuscular, siendo el cerebelo uno de los activadores ms potentes de este sistema. En cuanto al control del equilibrio, el cerebelo participa en conjunto con los sistemas vestibular y culomotor. Corteza cerebral motora y premotora. El control cortical de la funcin motora es esencialmente, pero no solamente, voluntario; el control subconsciente lo realizan otras estructuras ya descritas. La corteza motora es precentral, contiene las neuronas piramidales gigantes o clulas de Betz; se le denomina corteza motora primaria porque es excitada por una estimulacin elctrica mnima. Hay tambin una zona motora suplementaria, en la pared media del hemisferio, a nivel de la fisura longitudinal; su estimulacin ayuda a alejarse de los peligros. Y por ltimo, las reas sensitivas I y II son en realidad sensitivomotrices, pues funcionan asociadas con las reas motoras. El 75 % de las fibras de los haces crticoespinales provienen
239
del rea motora y el 25 % del rea somestsica, la cual probablemente realiza un control de feed back de ingreso sensorial. El haz piramidal da colaterales hacia la propia corteza cerebral, inhibiendo regiones vecinas, a los cuerpos estriados (caudado y putamen), al ncleo rojo, a la sustancia reticular del tronco cerebral, a ncleos del puente y olivares inferiores; todas estas conexiones constituyen parte de las vas extrapiramidales que se conectan con la mdula espinal y el cerebelo. En un 85 %, los haces crticoespinales terminan en interneuronas de la base de las astas dorsales, y en un 15 % en las motoneuronas anteriores.
Otras vas extrapiramidales van directamente desde la corteza a algunos ncleos: Corteza cerebral caudado putamen globo plido ncleos subtalmicos ncleo rojo sustancia negra SR del tronco mdula espinal. A la corteza motora primaria le llegan aferencias desde zonas corticales vecinas, fibras subcorticales desde el hemisferio opuesto que cruzan por el cuerpo calloso, fibras desde el tlamo, etc. La representacin cortical es proporcional a la delicadeza de los movimientos y da lugar a un homnculo motor. La corteza premotora est ubicada 1 a 3 cms. delante del rea motora primaria. Tiene capacidad para controlar los movimientos coordinados, como vocalizacin, movimientos rtmicos, movimientos oculares, deglucin, masticacin. Se le podra llamar rea de asociacin motora, para lo cual posee
240
conecciones con zonas parietales, corteza motora primaria, tlamo y ncleos basales. Su lesin provoca prdida o alteracin de las siguientes funciones: vocalizacin de palabras complejas (rea de Broca), movimientos oculares, rotacin de la cabeza y destreza manual, producindose apraxia motora (movimientos incoordinados). Engrama sensorial para los movimientos. En las zonas sensoriales y de asociacin sensorial, la persona experimenta los efectos de los movimientos y registra los recuerdos motrices, lo que constituye los engramas sensoriales de los movimientos. Son como las experiencias o los entrenamientos que despus sirven para repetir los movimientos. La que aprende es la corteza sensorial y despus se utiliza el engrama para activar al sistema motor. Movimientos rpidos como escribir a mquina, no se pueden realizar por seales transmitidas por circuitos largos. Al parecer, estos movimientos coordinados rpidos se establecen en el propio sistema motor, incluyendo circuitos complejos de la corteza motora primaria, corteza premotora, ncleos basales, cerebelo. Durante las primeras experiencias los movimientos sern lentos, hasta que se establece el engrama y la actividad se realiza sin control de retroaccin. En cuanto al inicio de la actividad motora voluntaria, no parece estar solamente radicado en la corteza motora, ms bien son las regiones basales del cerebro las que se activan primero; a su vez, estas zonas estn bajo control de ingresos sensoriales, zonas de almacenamiento de memoria, etc. Regulacin de las Funciones Viscerales. Las funciones viscerales o vegetativas estn bajo el comando del sistema neurovegetativo, con sus dos divisiones, simptico y parasimptico. Ya se describi su estructura, por lo cual aqu slo corresponde especificar sus funciones reguladoras; estas se realizan mediante la accin de neurotransmisores sobre
241
receptores especficos; fundamentalmente los neurotransmisores son la noradrenalina y la acetilcolina, an cuando la adrenalina que produce la mdula suprarrenal estimula tambin receptores adrenrgicos simpticos. A nivel de los ganglios neurovegetativos, el neurotransmisor es la acetilcolina, tanto para el sistema simptico como para el parasimptico, o sea, el neurotransmisor preganglionar es comn. En cambio, a nivel de los efectores la situacin es diferente: - las terminaciones parasimpticas postganglionares son colinrgicas, vale decir que actan mediante la accin de la acetilcolina sobre sus receptores, que corresponden a la variedad muscarnica, puesto que responden eficaz y unvocamente a la droga muscarina; - las terminaciones postganglionares simpticas pueden ser noradrenrgicas si actan mediante el neurotransmisor noradrenalina; sin embargo, existen tambin terminaciones simptico colinrgicas, como las que inervan las glndulas sudorparas y vasculatura muscular esqueltica. Los receptores del sistema simptico noradrenrgicos y adrenrgicos pueden ser del tipo alfa uno, alfa dos, beta uno, beta dos y beta tres. Cada uno de ellos produce efectos diferentes, por lo cual las acciones de la adrenalina y noradrenalina van a depender del tipo de receptor que exista en el rgano afectado, de la densidad de los receptores y tambin de la dosis de neurotransmisor liberado y a veces administrado. Diversas reas y estructuras enceflicas controlan a su vez las acciones del sistema neurovegetativo; en el tronco cerebral se encuentran diversos ncleos de origen y de control de funciones viscerales como presin arterial, frecuencia cardaca, secreciones digestivas, peristaltismo, contracciones vesicales, etc. Zonas ms altas, especialmente del hipotlamo y an de la corteza cerebral, influyen sobre los centros de control vegetativo del tronco
242
cerebral. En el hipotlamo se encuentran numerosos centros de control vegetativo, ubicados en diferentes reas o ncleos que lo constituyen. Es as como se ha podido demostrar que el rea hipotalmica anterior est relacionada con el sistema parasimptico y que el rea hipotalmica posterior se relaciona con el sistema simptico. El hipotlamo ha recibido el apelativo de cerebro visceral, debido a la importancia que tiene en el control de las funciones viscerales. Especficamente, las zonas hipotalmicas que se enumeran influyen sobre las funciones que se indican. 1.- El rea hipotalmica posterior provoca efectos similares a las de una estimulacin simptica. 2.- El rea hipotalmica anterior provoca efectos similares a las de una estimulacin parasimptica. 3.- La estimulacin del ncleo dorsomedial determina estimulacin gastrointestinal. 4.- El ncleo ventromedial provoca sensacin de saciedad al ser activado. 5.- En los cuerpos mamilares se ubican los centros reflejos de alimentacin. 6.- Los ncleos suprapticos y paraventriculares se relacionan con la retencin de agua a travs de la accin de la hormona antidiurtica. 7.- El rea preptica medial es ms bien hipotensora, ya que su estimulacin disminuye la frecuencia cardaca y la presin arterial; adems produce contraccin vesical. 8.- Las reas prepticas posteriores (estn en el hipotlamo anterior) estn involucradas en la regulacin trmica, incluyendo la sudoracin, y tambin en la inhibicin de la tirotropina hipofisiaria. En cuanto a la accin de la corteza cerebral, se ha demostrado que al menos en una zona vecina a la cisura lateral existe un rea relacionada con el control visceral. Los sistemas simptico y parasimptico se encuentran en un cierto equilibrio homeosttico, en condiciones de reposo. No
243
obstante, en muchos individuos existe un predominio de alguno de ellos, lo que da origen a que la persona sea de tipo simpticotnico o bien vagotnico, presentando manifestaciones viscerales de una hiperactividad del sistema correspondiente. En la tabla siguiente se resumen algunos de los efectos resultantes de la estimulacin simptica y parasimptica.
ORGANO EFECTOR
SISTEMA SIMPATICO
244
Receptor Alfa Msculo Contraccin: radial del Midriasis. iris Msculo circular del iris Msculo ciliar del ojo Corazn: Fuerza Aumento contrctil Frecuencia Velocidadde conduccin Excitabilida d Vasos Vasoconstric. sanguneos cutnea y renal
Receptor Beta
SISTEMA PARASIMPATIC O Receptor Muscarnico
Contraccin: miosis Relajacin (visin lejana) Aumento Aumento Aumento Aumento Contraccin (visin cercana)
Disminucin Disminucin Disminucin
Dilatacin coronaria; vasos musculares: dilatacin colinrgica y vasoconstricci n adrenrgica
Bazo
Esplenocontracc . Bronquios Constriccin Dilatacin Constriccin Fuerzacontr. Aumento en Msculo msculos esqueltico rpidos y dism. en msculos lentos Msculo Contraccin Relajacin uterino Msculo Relajacin intestinal Secreciones Inhibicin digestivas GluconeoAumento gnesis Relajacin Inhibicin Contraccin Aumento
245
Glicgeno-
Lisis
Aumento hgado de
Consumo oxgeno Liplisis
en Aumento en corazn y msculo esqueltico Aumento Aumento Aumento Aumento Aumento Aumento Aumento
Calorignesis Secrecin de: glucagn insulina Disminucin hormona paratirodea renina acetilcolina Facilta en placa motora e inhibe en ganglio noradrenalin simptico a Inhibe Potasio Hiperkalemia Msculos Contraccin piloerectores Glndulas Secrecin salivales viscosa Vejiga urinaria Vescula biliar Esfnter anal Sudoracin Contraccin esfnter
Facilita
Secrecin fluida Relajaci Contraccin n detrusor detrusor Inhibe Contrae Aumenta (colinrgica) Estimula Relaja
246
V.-SISTEMAS DE INTEGRACION GLOBAL . Entre los sistemas neuronianos, es posible distinguir dos grandes grupos: I.- sistemas especficos, que a su vez pueden ser: 1.- aferentes, implicados en la transmisin desde los receptores a los centros y en la sensopercepcin; 2.- eferentes, que se relacionan con los impulsos que envan los centros o comandos a los efectores; determinan las conductas efectoras viscerales y somticas; II.-sistemas de integracin global, que determinan el funcionamiento del sistema nervioso y an del organismo como un todo integrado; se pueden distinguir tres grandes grupos: 1.- sistema reticular, cuya funcin ms relevante se relaciona con estados de activacin del sistema nervioso. 2.- sistema lmbico hipotalmico, ms relacionado con el manejo incondicionado de la vida, como conductas instintivas y emocionales, mecanismos de refuerzo (premio y castigo), conductas motivadas, control superior endocrino, ritmos biolgicos,etc.; 3.- sistema tlamo cortical, relacionado con los fenmenos conscientes y la actividad propiamente intelectual; participa en la percepcin sensorial, aprendizaje y memoria, control de las conductas, lenguaje, pensamiento, sentimientos, etc. Sin embargo, los tres sistemas mencionados no son independientes entre s, sino que coparticipan y se complementan en diversos fenmenos fisiolgicos y psicolgicos en que intervienen; as, por ejemplo, si se trata de una sensopercepcin o
247
del desarrollo de un pensamiento, el sistema tlamo-cortical tendr una participacin preponderante; pero a su vez, el sistema reticular proveer el estado de excitacin neuronal necesario para mantener la vigilia y el alerta difuso, sin los cuales no hay sensopercepcin ni actividad intelectual; y por ltimo, en el ejemplo sealado, el sistema lmbico hipotalmico participa orientando la atencin segn sean los estados anmicos y las motivaciones del individuo. Sistema Reticular. Est constituido por un conjunto de centros que se extienden desde el diencfalo a la mdula espinal. La sustancia reticular se caracteriza porque las fibras mielnicas no presentan una agrupacin definida, de modo tal que aparecen formando un retculo blanco sobre fondo gris; alcanza su mximo desarrollo en el tegmento del tronco cerebral. De rostral a caudal, constituyen el sistema reticular las siguientes estructuras: - ncleos inespecficos del tlamo - zona incierta del subtlamo - centros reticulares del tronco cerebral - sustancia gris periacueductual - neuronas intercalares de la mdula espinal. Adems estn las estructuras no reticulares pero que forman parte funcional del sistema reticular, como son la capa VI de la neocorteza, el ncleo rojo, la sustancia nigra y el complejo olivar. El tracto tegmental central tiene una participacin importante en la asociacin de los elementos que componen el sistema reticular. Desde un punto de vista funcional, la formacin reticular est asociada a la activacin y depresin difusa e incondicionada del sistema nervioso, para lo cual mantiene conexiones con todos los niveles del sistema nervioso. Algunas drogas como los barbitricos tienen un efecto depresor especfico sobre el sistema
248
reticular activador mesenceflico; en cambio, la cafena estimulante reticular.
es un
Una clasificacin funcional de los centros reticulares permite agruparlos segn sea su participacin neurofisiolgica. 1.- Sistema reticular activador ascendente (SRAA). Incluye a lo menos las siguientes estructuras: - capa VI de la neocorteza; - ncleos centrales del tegmento, algunos de los cuales se conectan con el tracto espinotalmico, por lo que estn implicados en la percepcin del dolor; - ncleos inespecficos del tlamo. Las fibras del sistema reticular activador ascienden desde los ncleos reticulares de la mdula oblongada hasta el diencfalo, formano parte del tracto tegmental central, conectando entre s los centros reticulares o bien con otras estructuras, como hipotlamo, cerebelo y ncleos del sistema extrapiramidal; muchas de estas conecciones son recprocas. 2.- Sistema reticular descendente. Tiene centros activadores e inhibidores, ubicados los primeros en el mesencfalo y puente; un centro inhibidor importante lo constituyen los ncleos gigantocelular y ventral del bulbo raqudeo. 3.- Centros relacionados con los mecanismos del sueo; entre ellos cabe mencionar los ncleos del rafe, del puente rostral, del mesencfalo caudal y el locus coeruleus. 4.- Centros relacionados con: - control de reflejos incondicionados de la circulacin, respiracin y digestin; - reflejos incondicionados segmentarios plurisinpticos ( neuronas intercalares) 5.- Centros relacionados con circuitos cerebelo-reticulares, de ubicacin preferente en la mdula oblongada. Formacin reticular y actividad motora.
249
En la formacin reticular se han delimitado zonas excitadores e inhibidoras de la actividad muscular, las que actuaran sincronizadamente coordinando la accin de los msculos agonistas y antagonistas (principio de inervacin recproca) La accin motora del sistema reticular se efecta sobre la motoneurona alfa, directamente o a travs de neuronas intercalares, y tambin sobre la motoneurona gama, con lo cual influye en el reflejo miottico. Mediante sus conecciones con el sistema visual, los ncleos vestibulares y los del sistema extrapiramidal, el sistema reticular ejerce una accin reguladora general sobre la actividad motora. Y recprocamente, uno de los estmulos ms poderosos para el sistema reticular activador procede de la actividad de la musculatura esqueltica. Formacin reticular y regulacin endocrina. La formacin reticular mantiene conecciones con el hipotlamo, a travs del cual influye sobre la regulacin de las hormonas que estn bajo el control del eje hipotlamohipofisiario. Esto se manifiesta, por ejemplo, en la secrecin de adrenocorticotropina (ACTH), especialmente en el sndrome de alarma; a su vez, la adrenalina puede activar, por va sangunea, a los ncleos reticulares mesenceflicos y stos estimular la liberacin del ACTH. Formacin reticular y regulacin neurovegetativa. Algunos centros de coordinacin visceral estn constituidos por neuronas de la formacin reticular del tronco cerebral, como es el caso de los centros respiratorio y vasomotor. Sueo y vigilia. El sistema reticular es un centro sensitivo y motor inespecfico y que en relacin con el resto del sistema nervioso
250
mantiene un estado de actividad bsica indiferenciada sobre la cual se implantan las actividades especficas. Sus conecciones con la corteza cerebral son la base para la mantencin normal de los ciclos de sueo y vigilia. El sistema reticular activador ejerce una accin sobre la corteza cerebral; este sistema posee una excitacin intrnseca que determinara una estimulacin permanente sobre la corteza; no obstante, existe un sistema reticular inhibitorio (SRI) que funciona en interrelacin con el sistema reticular activador. El sistema reticular inhibidor no es autoexcitable, sino que se activa por impulsos provenientes del cerebelo, los ncleos de la base y la corteza cerebral. Por ltimo, la formacin reticular ejerce una funcin de filtro o de control de los impulsos aferentes, de modo que stos disminuyen su efectividad como estimulantes de la actividad cortical. Por ejemplo, si un individuo despierto centra su atencin en un objeto, se inhibe la atencin sobre estmulos ajenos a dicho objeto, por seleccin segn experiencias previas, y anulando los estmulos distractores por accin sobre neuronas sensitivas de segundo orden (ncleos cocleares, trigeminales, gracilis, etc.) El trmino conciencia puede subentenderse con tres significados: - estar consciente, como sinnimo de vigilia; - ser consciente, en el sentido de poner atencin a algo en especial; - conciencia tica o moral, que se refiere al hecho de poder distinguir entre los conceptos de bien y mal. En relacin con los estados de conciencia, se pueden distinguir dos situaciones bsicas, cuales son el sueo y la vigilia; sta ltima puede presentar variantes, como ser el alerta difuso y la atencin localizada. El estado de vigilia o de conciencia se caracteriza por la accin volitiva con el ambiente, y en este estado se puede producir la percepcin, la atencin y la abstraccin.
251
El alerta difuso o inespecfico es una facilitacin no selectiva de la corteza cerebral, con aumento de la perceptividad, sin definicin de rea o clase de estmulo. La atencin o alerta localizado se produce por facilitacin de reas corticales determinadas; su ocurrencia en la neocorteza se asocia a la experiencia consciente de la fijacin de la atencin. Estn implicados el sistema reticular y la neocorteza, en que la localizacin del alerta est mediada por la corteza lmbica. Una persona despierta, entonces, puede dirigir su atencin hacia aspectos especficos en grados variables, como ser ausencia total de atencin, atencin amplia a lo que ocurre alrededor, o bien atencin puntual. Slo se conocen datos indirectos de los mecanismos de la atencin: -los cambios de grado en la atencin general parecen depender del sistema reticular mesenceflico; -el sistema reticular talmico estara involucrado en la atencin hacia aspectos especficos, puesto que reas talmicas bien determinadas activan a zonas precisas de la corteza cerebral; -regiones activadas de la corteza pueden controlar su propio ingreso sensorial, por lo cual el cerebro podra dirigir as su atencin hacia fases especficas de la actividad mental. La actividad reticular ascendente excesiva interfiere con la localizacin de la atencin, particularmente si sta es intencionada. Para el estado de vigilia se requieren dos condiciones esenciales: -cierto nivel de actividad del sistema reticular activador; -canalizacin adecuada de la actividad nerviosa del cerebro; en las crisis epilpticas est mucho ms activo que normalmente, pero el paciente est inconsciente. En relacin con el electroencefalograma (EEG), en la vigilia se observan ondas alfa y beta. Las ondas alfa son caractersticas del reposo despierto, ms notorias mientras menores sean las
252
estimulaciones sensoriales; las ondas beta se observan en los estados de alerta, atencin, actividad mental intensa, aunque tambin se encuentran en una etapa del sueo. El sueo es un estado fisiolgico de ritmo circadiano, aunque presenta algunas influencias nictimerales; se caracteriza por la prdida del estado de conciencia, por lo cual no hay sensopercepcin ni conducta intencionada. La motilidad somtica (esqueltica) es baja, y tambin es escasa la respuesta a los estmulos externos; es caracterstico del estado de sueo la posibilidad de despertar de l. El estado de sueo es inducido espontneamente en forma peridica y se alterna con el estado de vigilia. Se producen en el sueo modificaciones en el comportamiento visceral y en el metabolismo y su induccin puede ser condicionada. Considerando al individuo en estado de vigilia, se puede describir que la condicin de sueo progresa desde un estado despierto pero relajado, a cuatro etapas de sueo tranquilo o de onda lenta (algunos autores denominan as slo a las etapas 3 y 4), para pasar luego al sueo paradjico o activado, llamado tambin sueo MOR o de movimientos oculares rpidos que lo caracterizan. La primera etapa es una transicin entre vigilia y sueo, de duracin corta, uno a siete minutos. La persona mantiene cerrados los ojos, su musculatura est relajada, su respiracin tranquila; suele tener pensamientos momentneos; el EEG muestra actividad alfa . Si la persona despierta, no tiene conciencia clara de que ha dormido. Por supuesto, esta fase se presenta una sola vez en el ciclo completo de sueo, puesto que corresponde a su comienzo. La segunda etapa puede considerarse de sueo verdadero aunque superficial. En el EEG se observan los husos de sueo, como verdaderas salvas de ondas alfa muy marcadas. La tercera etapa comienza unos 20 minutos despus que el individuo se ha dormido; en ella se observa sueo
253
moderadamente profundo; el sistema smato-motor est muy relajado, la temperatura corporal y la presin arterial sistmica han disminudo ligeramente; el despertar en esta etapa es ms bien difcil. En el EEG se observan husos de sueo y actividad delta. La cuarta etapa es la del sueo profundo; la relajacin smato-motora es mxima y la persona difcilmente responde a estimulacin externa; es difcil el despertar en esta etapa, si sucede, la persona parece confusa. Cuando se llegan a producir, es en esta etapa que ocurren el sonambulismo y la enuresis. Contina la actividad electroencefalogrfica delta.Es habitual que de esta etapa se vuelva a la tres y a an a la dos, para pasar luego al sueo paradjico o activado o desincronizado o sueo MOR. Su gran caracterstica son las ensoaciones; cuando es tranquilo, hay disminucin del tonus muscular, pero algunas funciones viscerales aumentan , como la presin arterial, y las frecuencias cardaca y respiratoria pueden ser variables. Durante el sueo MOR la persona queda como paralizada, debido a que la mayora de las motoneuronas espinales y cerebrales se inhiben fuertemente, con excepcin de las respiratorias y las culomotoras. Sin embargo, el individuo est ms sensible a su entorno; si la persona despierta durante esta etapa, parece estar alerta y atenta; habitualmente da cuenta de ensoaciones. El EEG muestra actividad beta. Luego del sueo paradjico, se vuelve a la etapa de sueo de onda lenta. En cuanto a la duracin de cada una de las etapas , es variable. As, el sueo paradjico puede durar 5 a 10 minutos en el primer ciclo, para extenderse hasta unos 50 minutos en el ltimo ciclo; un perodo completo de sueo tiene en promedio una duracin de unos noventa minutos. En un estado de sueo de ocho horas de duracin total, se producen unos 4 a 5 perodos de sueo activado. Cada tipo de sueo es producido por estructuras nerviosas diferentes. As, el centro del sueo de onda lenta parece estar en los ncleos del rafe, que tienen como neurotransmisor la serotonina; cuando sta se agota, se produce insomnio.
254
Investigaciones ms recientes proponen que una zona de la regin basal del prosencfalo controlara el sueo de onda lenta. En cambio, el sueo paradjico sera controlado por neuronas colinrgicas pontinas, cuyo mecanismo sera inhibido por las neuronas serotoninrgicas de los ncleos del rafe. Tanto los agonistas serotoninrgicos como los noradrenrgicos tendran efectos inhibitorios sobre el sueo MOR, y las neuronas de los ncleos del rafe as como las del locus coeruleus estaran en sus niveles ms bajos durante esta etapa del sueo. o que est ms claramente establecido es que neuronas colinrgicas de la formacin reticular y neuronas noradrenrgicas del locus coeruleus son esenciales para la vigilia y mecanismos del despertar; el tronco cerebral tiene una energa despertadora intrnseca, a la que se pueden agregar impulsos sensoriales. La zona reticular despertadora estara en ncleos centrales del puente y mesencfalo, en la sustancia gris periacueductal, en la formacin reticular del hipotlamo, del tlamo y del bulbo raqudeo. Desde el tlamo, los impulsos iran a activar a la corteza cerebral. En cuanto a los impulsos sensitivos, los ms efectivos para estimular a las zonas despertadoras son los que provienen de la musculatura estriada, aunque tambin son eficaces estmulos auditivos, visuales , trmicos, dolorosos, etc. El despertar se produce por estimulacin del sistema reticular activador; ste enva impulsos a la corteza cerebral y al sistema nervioso perifrico, seales que vuelven al sistema reticular constituyendo as un mecanismo de feed back positivo que termina con la saturacin del sistema. Tambin se han descritos zonas hipnognicas ubicadas en el diencfalo, en el bulbo raqudeo, en la regin preptica lateral y banda diagonal de Broca adyacente. A estas reas les llegara la informacin sensitiva montona, que es productora de sueo, como lo es el mecer un beb para inducirle sueo. Se ha logrado producir sueo experimentalmente por estimulacin elctrica de diversas zonas, como ser la porcin pontina rostral de los haces solitarios, la cual es considerada como el centro del sueo; tambin son reas hipnognicas los
255
ncleos difusos del tlamo y la regin basal del cerebro anterior. Las etapas alternantes sueo-vigilia constituyen uno de los fenmenos rtmicos caractersticos en el individuo normal, lo cual implica la existencia de un regulador endgeno o reloj biolgico que controla dicha ritmicidad. Estos marcapasos se encuentran en el hipotlamo, de los cuales el marcapasos X controla el sueo activado y el marcapasos Y se relaciona con el sueo de onda lenta; como este marcapaso se encuentra en los ncleos supraquiasmticos, se supone que a este nivel influyen los ciclos de luz-oscuridad en la ritmicidad de dichos ciclos. Desde otro punto de vista, existen dos teoras que pretenden explicar la alternancia sueo-vigilia: -el sueo es un proceso pasivo que se produce por fatiga de los mecanismos de la vigilia; -centros activos del cerebro transmiten seales inhibitorias al sistema reticular activador y se produce sueo. Por otra parte, existe una influencia cortical descendente sobre el sueo y la vigilia, influencia que es responsable de la atencin voluntaria, la autoinduccin del sueo y la habituacin. Algunas evidencias experimentales permiten plantear una hiptesis humoral para la produccin de sueo. As, por ejemplo, si a un animal que ha dormido normalmente, se le inyecta sangre o lquido cfalo-raqudeo de otro animal que ha sido mantenido despierto durante varios das, el primero se duerme. No obstante, no ha sido posible asignar estos resultados a una sola sustancia; lo ms probable, a la luz de resultados no siempre consistentes, es que las sustancias productoras de sueo y viglia no acten por va sangunea sino que sean neurotransmisores de accin local los involucrados en las etapas de sueo, vigilia y despertar. Otro hecho bastante discutido se refiere a los objetivos del sueo. Parece indudable que el sueo es un proceso restaurador en que el individuo se repone del agotamiento y desgaste de la vigilia, no solamente en el aspecto smato-motor y visceral, sino especialmente en las funciones del sistema nervioso central. Psiclogos han propuesto para el sueo el objetivo de constituir
256
una conducta evasiva. Para el sueo paradjico se han planteado adems objetivos tales como: -cierto estado de vigilancia, especialmente importante en los animales, que estn as ms sensibles a su entorno y evitan que los sorprendan los depredadores; -aprendizaje: los recuerdos del da se consolidan e integran con los recuerdos pre-existentes; asimismo se puede desechar informacin intil; reprogramacin de conductas de la especie, puesto que ayuda a integrar las conductas aprendidas e instintivas. Entre los animales se pueden observar algunas caractersticas interesantes relacionadas con el sueo. As por ejemplo, los flamencos duermen parados sobre una de sus patas, por lo cual en esa extremidad no pierden el tono muscular antigravitacional; en este caso, la actividad propioceptiva no sera un estmulo importante para el sistema reticular activador despertador. En relacin con los objetivos del sueo, ste constituye una conducta que resguarda al animal del peligro cuando no existe otra actividad importante, puesto que en la oscuridad sera ms probable y peligroso toparse con depredadores difciles de identificar; tambin en la oscuridad es ms difcil encontrar alimentos. Los depredadores peligrosos como los leones y los animales que viven en cuevas duermen mucho, pues tienen menos probabilidades de ser atacados. En cambio, el ganado y los animales ms indefensos duermen poco. El delfn nariz de botella y la marsopa han desarrollado un curiossimo sistema de alerta: duermen alternando sus hemisferios cerebrales. Actividad cerebral elctrica: electroencefalograma (EEG). La superficie cortical cerebral presenta una vasta red de dendritas que provienen de neuronas de las capas inferiores de la corteza. Los impulsos que llegan a estas dendritas producen potenciales tipo PEPS (potencial excitador post sinptico). Este estado de descarga parcial vuelve muy excitables a las neuronas corticales, y esta gran excitabilidad cerebral da lugar a potenciales que pueden registrarse desde la superficie del crneo.
257
Una de las principales causas de la activacin de la corteza son impulsos provenientes del sistema reticular activador ascendente. La actividad elctrica proveniente de los millones de neuronas cerebrales puede ser detectada desde el cuero cabelludo como una secuencia de ondas de bajo voltaje en un registro que se conoce con el nombre de electroencefalograma (EEG). El EEG presenta ondas caractersticas cuyas intensidades varan entre 0 y 300 microvolts, y su frecuencia es de 1 a 50 por segundo. Ondas alfa. Tienen una frecuencia de 8 - 13 /segundo y una intensidad promedio de 50 microvolts. Estn presentes en los individuos normales despiertos con actividad cerebral moderada; desaparecen en el sueo, y con cualquier tipo especfico de actividad mental son reemplazadas por ondas asincrnicas de mayor frecuencia y menor voltaje. Las ondas alfa slo estn presentes si hay conecciones con el tlamo; se acepta que estas ondas resultan de la actividad espontnea del sistema tlamocortical difuso, ya que ellas aparecen al estimular los ncleos difusos del tlamo. Ondas beta. Presentan una frecuencia de 14 - 50 /segundo. Hay ondas beta I, que se parecen a las alfa, especialmente cuando existe actividad mental. Las ondas beta II aparecen en la activacin intensa del sistema nervioso central o en los estados de tensin. La clasificacin de Jasper define las ondas beta si su frecuencia es de 18 30 /seg. y las gama son las de frecuencia 30 50 /seg. Ondas theta. Son de frecuencia 4 7 /seg., se observan en los nios y en algunos estados de tensin emocional en los adultos, especialmente si se produce frustracin y decepcin. Ondas delta. Se denominan as a todas las ondas cuya frecuencia es menor de 3 5 /seg. Se presentan en el estado de sueo profundo, en la infancia, en enfermedades cerebrales
258
orgnicas graves, en la inconsciencia de la anestesia, durante convulsiones. Ondas kapa. Son de una frecuencia de 8 - 12 /seg.; se presentan en brotes fusiformes, asociados con procesos intelectuales. Las correlaciones entre los estados psico-fisiolgicos y los registros elctricos cerebrales se resumen en la siguiente Tabla.
Estado o Condicin Emocin, excitacin,mied o, ira, ansiedad. Alerta; atencin.
Electroencfalograma
Estado de conciencia Atencin difusa; confusin. Concentracin; anticipacin, determinacin anticipacin selectiva. Atencin difusa; asociacin libre. Vigilia parcial; alternancia con estados de sueo. Prdida de conciencia.
Desincronizado;ondas de amplitud baja o moderada; frecuencias mixtas. Parcialmente sincronizado; ondas de frecuencia alta y de amplitud baja Vigilia, relajado. Sincronizado; ritmo alfa. Somnolencia Sueo superficial Sueo profundo Ritmo alfa reducido; ocasionalmente ondas lentas de baja amplitud. Ondas amplias de baja frecuencia.
Ondas muy amplias de Inconsciencia de baja frecuencia; patrn sueo, con posibilidad
259
irregular. Estado de coma Perodos alternados amplias, irregulares
de despertar.
Muerte
isoelctricos Prdida completa de con ondas conciencia, sin lentas e posibilidad de despertar; sin respuesta aparente a estimulacin; amnesia. Isoelctrico; desaparicin Estado de muerte. gradual a permanente de toda actividad elctrica.
EEG
VIGILIA Y ETAPAS DEL SUEO
260
Sistema Lmbico. Se le denomina tambin sistema lmbico hipotalmico, debido a que las estructuras lmbicas propiamente tales y el hipotlamo se mantienen en una relacin tan estrecha que en
261
realidad constituyen una unidad funcional. De hecho, este sistema tiene una gran funcin general, que es la transduccin psico fisiolgica, y en esta funcin el hipotlamo desempea un papel preponderante. El sistema lmbico- hipotalmico est constituido por: 1.- reas corticales propias o exclusivas que en conjunto forman el lbulo lmbico y que comprende diversas estructuras como: - formacin del hipocampo, que incluye el hipocampo propiamente tal, el giro dentado, el giro supracalloso, el subcalloso y el giro del cngulo; - corteza parahipocampal o rea 28 de Brodman; - ncleo amigdaloide, constitudo por masas nucleares ubicadas en el lbulo temporal; 2.- componentes dienceflicos, como hipotlamo, epitlamo, ncleos anteriores del tlamo; tambin se incluyen entre estas estructuras el rea preptica, el septum pellucidum, el rea paraolfatoria, porciones de ncleos basales y amgdala.
SISTEMA LMBICO
Componentes
Cngulo
Trgono Cerebral Mesencfalo Puente Hipocampo
Circunvolucin del Parahipocampo
Bulbos Olfatorios Cuerpo Mamilar
Columna Del Trgono Cerebral
262
SeptumPellucidum
Amgdala
Limbus significa franja, y en el caso del lbulo lmbico se refiere a un verdadero anillo alrededor del tronco cerebral; por tener conecciones directas con estructuras olfatorias, se le ha llamado tambin rinencfalo. Se considera que las conductas humanas presentan componentes heredados, del desarrollo y aprendidos. Al comienzo de la vida, el desarrollo del organismo y por lo tanto, tambin del sistema nervioso, est en gran parte regido por aspectos genticos y programas del desarrollo, pero ya in tero, el ambiente exterior empieza a ejercer sus influencias. En un perodo crtico temprano, las influencias del ambiente social, fsico, hormonal, etc., pueden tener profundas consecuencias para la maduracin ulterior del cerebro, y por lo tanto, de la conducta. El sistema lmbico hipotalmico es la base de funciones relacionadas con la supervivencia del individuo y de la especie,
263
as como con la integracin emocional del comportamiento. En concreto, el sistema lmbico hipotalmico es el centro de la generacin de conductas lmbicas y comportamientos bsicos como: 1.- alimentacin y ciclos de hambre y saciedad; 2.- conductas instintivas, como la reproduccin; 3.- emociones y conductas emocionales, como la agresividad que tiende a expandir el dominio individual, y el temor, que busca preservar la integridad ante las amenazas; 4.- ritmos biolgicos; 5.- control superior endocrino; 6.- integracin de impulsos viscerales y origen de respuestas vscero-motoras; 7.- regulacin de temperatura. Al hipotlamo se le considera como un cerebro visceral, por su importancia en la regulacin de las funciones vegetativas y en la homeostasis, para lo cual se mantiene en estrecha relacin con el sistema neurovegetativo; especficamente, el rea hipotalmica anterior o trofotropa est en coneccin con el sistema parasimptico, y el rea hipotalmica posterior o ergotropa se relaciona con el sistema simptico. Algunas de las describirn en especial. funciones lmbicas mencionadas se
Regulacin de las funciones endocrinas. El sistema lmbico, a travs del hipotlamo, ejerce un control sobre las secreciones endocrinas mediante una relacin denominada hipotlamo hipofisiaria. Hasta hace unas cuatro dcadas, la hipfisis anterior o adenohipfisis era considerada una pieza maestra autnoma en los mecanismos de regulacin de varias glndulas endocrinas, como las gnadas, tiroides, corteza suprarrenal. Hoy se sabe que con el hipotlamo, la hipfisis forma una unidad funcional
264
integrada y ya no se considera a la adenohipfisis el director de orquesta endocrina. Entre el hipotlamo y la hipfisis existen dos formas de relaciones. Las conexiones con la hipfisis anterior consisten en una red portal hipotlamo hipofisiaria, de modo que hormonas hipotalmicas llegan a controlar las secreciones hipofisiarias por va sangunea. La hipfisis est ubicada por debajo del hipotlamo; un grupo de capilares hipotalmicos basales van a constituir pequeos vasos que pasan a travs del tallo hipofisiario y luego se ramifican, formando la mayor parte de los capilares de la hipfisis anterior; es decir, existe entre ambos rganos una relacin circulatoria en serie que se denomina sistema portal hipotlamo hipofisiario. Por otra parte, los axones de neuronas del hipotlamo terminan en la eminencia media alrededor de los orgenes de los capilares de los vasos portales; en esta forma, las secreciones de las neuronas hipotalmicas entran a la sangre portal y son distribudas en la adenohipfisis, donde controlan las secreciones de esta ltima. En cambio, la hipfisis posterior se relaciona con el hipotlamo mediante conecciones nerviosas. A lo menos dos grupos neuronales, los ncleos suprapticos y paraventriculares presentan claras relaciones con la hipfisis. En estos ncleos se sintetiza ocitocina y hormona antidiurtica, las que unidas a protenas transportadoras van por flujo axnico y se almacenan en la neurohipfisis; aqu las terminaciones nerviosas estn organizadas en un aparato secretor que descarga directamente a la sangre, en respuesta a potenciales de accin de los nervios correspondientes. En la adenohipfisis se han descrito varios grupos glandulares que secretan hormonas tales como: 1.- hormona tiroestimulante o TSH, que induce la secrecin de tiroxina y triyodotironina por la glndula tiroides; 2.- adrenocorticotropina o ACTH, que regula las secreciones de la corteza suprarrenal; 3.- gonadotropinas folculoestimulante o FSH y hormona
265
luteinizante o LH, que regulan la secrecin de hormonas sexuales, testosterona, estrgenos y progesterona; 4.- prolactina, cuyos rganos blanco son las glndulas mamarias; 5.- hormona de crecimiento o GH, de efectos metablicos mltiples sobre rganos y tejidos; 6.- intermedina u hormona melanocito estimulante (MSH). Hormonas hipotalmicas. En 1960, Guillemin, Schally y colaboradores, aislaron, identificaron y sintetizaron factores liberadores hipotalmicos que regulan las secreciones hipofisiarias. En 1969 se publicaron los primeros trabajos sobre el factor liberador de tirotropina o TRF, ms tarde hormona liberadora de tirotropina o TRH. Este descubrimiento abri una nueva era en neuroendocrinologa; ms tarde se aisl la hormona liberadora de gonadotropinas o GnRH, que estimula la liberacin de LH y FSH, otra que estimula la secrecin de ACTH; en 1973 se describi la somatostatina u hormona inhibidora de hormona de crecimiento (GHIH); tambin existe una GHRH u hormona liberadora de hormona de crecimiento , as como hormonas estimulante e inhibidora de prolactina (PRH y PIH). Al respecto, es preciso aclarar que la sigla RH se utiliza para indicar una hormona liberadora o Releasing Hormone, as como la sigla IH proviene de los vocablos en ingls Inhibiting Hormone. Por otra parte, se les denomin factores hormonales cuando las sustancias aisladas presentaban todas las caractersticas de una hormona, salvo que no se conoca su identificacin qumica precisa; cuando esto ltimo se consigui, el factor hormonal pas a la categora de hormona. De los descubrimientos sealados se dedujeron algunas interrogantes: 1.- Cul es el significado del control hipotalmico sobre las hormonas hipofisiarias? 2.- Cul es el mecanismo de accin de las hormonas hipotalmicas?
266
3.- Qu interrelaciones existen entre hipotalmicas, las hipofisiarias y las efectoras?.
las
hormonas
Con respecto al significado del control que el hipotlamo ejerce sobre algunas hormonas efectoras, es preciso tener presente que esta estructura nerviosa pertenece al sistema lmbico, por lo cual capta diversas situaciones de activacin del sistema nervioso y del organismo, como las emociones, diversos estados de tensin psicolgica, el estrs, etc. En estos casos se modifican algunas secreciones endocrinas que ayudan al organismo a enfrentar dichas situaciones; es decir, se tratara de un mecanismo de heterostasis en estados de emergencias fisiolgicas. Tambin ha sido posible demostrar que entre las hormonas hipotalmicas, las hipofisiarias y las secretadas por glndulas efectoras, existe una relacin de feed back negativo que permite una autorregulacin entre las secreciones hormonales especficas. As como la accin de las hormonas hipotalmicas e hipofisiarias es de tipo puntual, tambin lo es su autorregulacin. La accin puntual es posible debido a que para cada una de ellas existen receptores especficos que confieren caractersticas unvocas entre las hormonas del eje hipotlamo hipofisiario. A su vez, cada hormona hipotalmica, hipofisiaria y efectora es secretada por un grupo neuronal definido. Las hormonas hipotalmicas no slo controlan la secrecin de hormonas hipofisiarias sino tambin su sntesis; es ms, se postula que diversas patologas endocrinas se deberan a trastornos en las hormonas liberadoras (tambin inhibidoras?) hipotalmicas y no necesariamente a una disfuncin hipofisiaria o de la glndula efectora. Cada secrecin hormonal se controla a s misma, es decir, junto con ejercer su efecto especfico, inhibe su propia secrecin en forma graduada. Pero adems cada tropina hipofisiaria inhibe la secrecin de su correspondiente hormona liberadora hipotalmica. La hormona efectora produce un efecto inhibitorio a tres niveles: en su propia glndula, en la poblacin endocrina
267
hipofisiaria especfica y a nivel de su correspondiente hormona liberadora hipotalmica.
ESQUEMA DEL EJE HIPOTLAMO HIPOFISIARIO
SLHT
_ _
HIPOTLAMO
_ Hormonas Liberadoras + _
HIPFISIS
Tropinas +
GLNDULAS EFECTORAS _
Hormonas Efectoras +
RGANO EFECTOR
FUNCIN BIOLGICA
Un ejemplo digno de considerar es el que se produce cuando se administra una hormona efectora exgena, puesto que ella va a inhibir las secreciones hormonales a los tres niveles
268
mencionados; pero adems, si la administracin hormonal es prolongada, puede llegar a atrofiar las poblaciones endocrinas secretoras, con lo cual la secrecin hormonal se suprime en forma ms o menos definitiva. A continuacin se describen las hormonas hipotalmicas conocidas y que regulan la accin de las hormonas del eje hipotlamo hipofisiario. TRH es la hormona liberadora de tirotropina; es un tripptido que estimula la secrecin de TSH y de prolactina, diferente de la hormona liberadora de prolactina (PRH). TRH parece estimular la liberacin de GH (hormona de crecimiento) en los pacientes acromeglicos; a su vez, la somatostatina inhibe la secrecin de TSH y de GH. GnRH u hormona liberadora de gonadotropinas, es un decapptido, denominado tambin LH FSH RH, por cuanto acta sobre ambas tropinas, FSH y LH. Fue la segunda hormona liberadora identificada qumicamente y sintetizada. Un amplio espectro de trastornos funcionales de la secrecin de gonadotropinas, desde la amenorrea psicognica al pseudoembarazo, se concibe en trminos de las alteraciones de la secrecin de LHRH por influencias corticales o lmbicas. Somatostatina o GHIH o factor inhibidor de somatotropina. Es un pptido de 14 aminocidos, que adems de su accin sobre GH, inhibe las secreciones de glucagn, insulina y TSH. Suprime la secrecin de diversas hormonas y sustancias tales como: gastrina, secretina, pptido inhibidor gstrico o GIP, pptido intestinal vasoactivo o VIP, colecistoquinina o CCK, calcitonina, hormona paratirodea, inmunoglobulinas secretoras o IgS, renina. Adems, deprime la secrecin gstrica cida, la secrecin de bicarbonato y enzimas digestivas, as como la absorcin intestinal de glucosa; tambin inhibe la motricidad intestinal y el flujo sanguneo esplcnico. Tiene efectos notables en las funciones del sistema nervioso central, como cambios conductuales y elctricos, y alteraciones en la coordinacin motora; en los seres humanos produce sedacin. En el sistema nervioso se le encuentra en la
269
eminencia media, corteza cerebral, tronco cerebral, mdula espinal y ganglios sensitivos. GHRH u hormona liberadora de hormona de crecimiento; estimula la secrecin de GH u hormona de crecimiento CRH u hormona liberadora de corticotropina; estimula la secrecin de ACTH o adrenocorticotropina. PIH es la hormona inhibidora de prolactina y PRH es la hormona liberadora de prolactina. MIH o melanostatina es la hormona inhibidora de melanina y MRH es la hormona liberadora de melanina. Conductas instintivas. Una definicin elemental de instinto es considerarlo como la capacidad innata del ser vivo para actuar adecuadamente; se dice que el comportamiento innato es aqul que no ha sido modificado por el aprendizaje. Sin embargo, an las conductas innatas presentan componentes aprendidos, y en el ser humano existe un control de las conductas lmbicas, an de las instintivas, por el lbulo frontal. Conducta sexual. Se desarrolla en los seres vivos que presentan reproduccin sexuada, la que se observa en la mayora de los animales y an en vegetales. En el ser humano tiene algunas caractersticas peculiares que se describirn a travs del captulo. Su objetivo ms obvio es la reproducin, y por lo tanto, la conservacin de la especie; sin embargo, otro de sus objetivos especficos es el de provocar cambios evolutivos rpidos, ya que al producirse por la unin de gametos provenientes de individuos diferentes, se producen entre los genes permutaciones y combinaciones que determinan no solamente que el hijo no sea
270
idntico a sus padres, sino que sus caractersticas diferentes pueden permitirle otras adaptaciones al medio ambiente. El placer que acompaa a la relacin sexual o al apareamiento no es un objetivo en s, sino que constituye una forma de activar la procreacin y la continuidad de la especie, as como el placer que acompaa a la alimentacin asegura la conservacin de la vida individual. Analizada en forma amplia, la conducta sexual se relaciona con el comportamiento materno-paterno y la crianza de los hijos. Se sabe que la determinacin del sexo en los seres humanos depende de los cromosomas sexuales, especficamente del cromosoma Y. Sin embargo, se debe considerar que si bien este cromosoma es el determinante sexual, el desarrollo de los rganos sexuales depende tambin del resto del juego cromosomtico. El papel especfico del cromosoma Y es controlar el desarrollo de las gnadas masculinas. Es as como en las primeras semanas de desarrollo prenatal, los embriones masculinos y femeninos contienen gnadas indiferenciadas . Un gen nico del cromosoma Y, el gen SRY, determina la produccin de una enzima denominada factor determinante de los testculos, gracias a la cual las gnadas no diferenciadas se convierten en testculos; cuando este gen no est presente (por ausencia del cromosoma Y), las gnadas evolucionan como ovarios. Experimentalmente se ha injertado el gen SRY en un cromosoma X de un ratn hembra y se ha desarrollado un macho. Una vez que se diferencian y desarrollan las gnadas, comienzan a secretar sus hormonas; durante el desarrollo prenatal, las hormonas van a determinar el desarrollo de los rganos sexuales, a la vez que influirn en algunas estructuras enceflicas, cambios que sern permanentes. En las primeras etapas del desarrollo prenatal, el embrin es bisexual, pues posee simultneamente los esbozos de los rganos genitales internos masculinos (conductos de Wolff) y de los femeninos (conductos de Mller), los que van a constituir los sistemas precursores masculinos y femeninos respectivamente. Son las hormonas secretadas por los testculos las que permiten que se desarrolle el sistema precursor masculino de Wolff, el cual contiene receptores a los andrgenos testiculares (la testosterona es secretada en el feto por las clulas
271
de Leydig); de esta unin hormona-receptor se desencadenan los mecanismos celulares que van a dar origen a los rganos sexuales masculinos internos. Adems, los testculos (clulas de Sertoli) secretan una hormona peptdica que es la hormona inhibidora del sistema de Mller, el cual posee receptores para esta hormona, cuyo efecto impide que se desarrollen los rganos internos sexuales femeninos. El sistema de Mller o precursor femenino se desarrolla por ausencia de hormonas testiculares andrognicas, es decir, no se precisa de una accin hormonal directa para que se desarrolle una hembra. Dicho de otro modo, si faltan las hormonas testiculares, se van a desarrollar los rganos sexuales femeninos internos. Segn nomenclatura clsica, el perodo pre-embrionario va de 0 a 3 semanas de vida intrauterina, el embrionario se extiende desde la cuarta a la octava semana del desarrollo y el perodo fetal comienza en la novena semana y termina con el nacimiento. En la sptima semana, las gnadas de los embriones genticamente masculinos han comenzado a transformarse en testculos. Existe una anomala gentica denominada el sindrome de Turner, en que la persona posee un solo cromosoma sexual que es X (X0 -0); este trastorno es causado por un espermatozoide defectuoso. Al no existir cromosoma Y, no se desarrollan testculos; tampoco hay ovarios, pues para que se produzcan se precisan dos cromosomas XX. Sin embargo, la falta de hormonas testiculares va a determinar que se desarrolle un individuo con caractersticas femeninas, con rganos sexuales internos y externos femeninos; no obstante, son estriles por no poseer gnadas, ovarios en este caso. Esta anomala viene a confirmar, adems, otro hecho interesante: para que se desarrollen los genitales externos femeninos no se precisan las hormonas sexuales ovricas. En cambio para el desarrollo de los genitales externos masculinos s se precisa de la accin de las hormonas testiculares andrognicas.
272
En la poca de la pubertad, se desarrollan las caractersticas sexuales secundarias, como la distribucin caracterstica del tejido adiposo, crecimiento de las mamas, crecimiento de barba, modificaciones de la voz, segn sea el caso. El comienzo de la pubertad se debe fundamentalmente al hipotlamo, que secreta las hormonas liberadoras de gonadotropinas; stas estimulan la secrecin hipofisiaria, cuyas gonadotropinas FSH y LH van a provocar la madurez sexual. Los efectos de estas hormonas van a ser tanto la secrecin de las hormonas sexuales correspondientes como de los respectivos gametos, vulos y espermatozoides. A su vez, las hormonas sexuales van a ser las desencadenantes directas de la maduracin de los rganos sexuales y su preparacin para las funciones reproductoras. En la conducta sexual misma interviene principalmente el sistema nervioso, condicionada por las hormonas sexuales. El sistema nevioso y la conducta sexual. Su participacin es algo diferente en la conducta de los machos que en las hembras. Aqu, como en muchas otras funciones fisiolgicas, ha sido de gran utilidad la experimentacin en animales, la que ha permitido desarrollar observaciones y extrapolar consecuencias a la conducta sexual humana. Sistema nervioso y conducta sexual en los machos. La regin enceflica ms significativa es el rea preptica medial del prosencfalo, situada en posicin rostral con respecto al hipotlamo (las reas septales y prepticas del telencfalo a menudo se les agrupa con los ncleos hipotalmicos dienceflicos); a esta rea preptica medial pertenece el tercer ncleo intersticial del hipotlamo anterior o NIHA 3. Malsbury demostr en 1971 que la estimulacin elctrica de esta regin en ratas macho provoca conducta copulativa; a su vez, la cpula incrementa la actividad metablica del rea preptica medial e induce la produccin de protenas Fos. Si se destruye el rea preptica medial, la conducta sexual masculina se elimina en forma permanente. (La protena Fos es la ms importante de las protenas nucleares producidas durante la activacin nerviosa). Los andrgenos activan las neuronas del rea preptica medial.
273
Se sabe que los machos castrados en la edad adulta pierden su conducta sexual, pero sta se recupera si se implanta testosterona directamente en el rea preptica medial , la cual contiene unas cinco veces ms receptores a andrgenos que en las hembras. En esta rea preptica existe un ncleo perteneciente al ncleo preptico, denominado ncleo sexualmente dimrfico (tambin presente en los seres humanos), que es significamente de mayor tamao en los machos que en las hembras (tres a siete veces mayor); este mayor tamao se debe a la accin de los andrgenos en la vida fetal. Algunos datos interesantes se refieren a que el tamao de este ncleo est en relacin directa con el nivel de actividad sexual del macho; el estrs prenatal reduce el tamao del ncleo y su lesin reduce la conducta sexual masculina. Al rea preptica medial converge la informacin genital tactil (por va del mesencfalo) y la olfatoria (por va de la amgdala medial), que contribuyen a la excitacin sexual. Tambin en la amgdala medial existe una zona con una alta concentracin de receptores andrognicos y tiene casi el doble de tamao en los machos que en las hembras. La destruccin de la amgdala medial disminuye la conducta sexual de las ratas macho. Del rea preptica medial van fibras al tegmento lateral del mesencfalo; si se destruyen estas fibras, se interrumpe la actividad sexual del macho. Durante el apareamiento normal, aumenta la actividad de las neuronas del tegmento lateral mesenceflico. Se deduce que el rea preptica medial acta controlando los mecanismos motores del mesencfalo que intervienen en la cpula. En los seres humanos se han podido correlacionar trastornos del lbulo temporal (all se localiza la amgdala) con la reduccin de los impulsos sexuales. Por otra parte, el cerebro se puede masculinizar en el perodo prenatal crtico por efecto de drogas como los barbituratos, y pesticidas como el DDT (dicloro-difenil-
274
tricloroetano). Sistema nervioso y conducta sexual en las hembras. En este caso, la regin enceflica ms significativa es el ncleo ventromedial del hipotlamo; se puede estimular la conducta sexual de las hembras mediante inyecciones de estradiol (aumenta el nmero de receptores a la progesterona) y progesterona en este ncleo, an en ratas castradas. Las neuronas del ncleo ventromedial envan eferencias al mesencfalo (sustancia gris periacueductal), regin que tambin participa en la conducta sexual femenina; de aqu van fibras a la formacin reticular del bulbo raqudeo, que a su vez se conecta con la mdula espinal. Hormonas y conducta sexual. Ya se analiz el papel fundamental que desempean los andrgenos, por presencia o por ausencia, en el dimorfismo sexual, y por supuesto, la constitucin sexual orgnica constituye la estructura fundamental sobre la cual se desarrolla la conducta sexual. Pero adems, las hormonas sexuales son responsables de la produccin y maduracin de los gametos, as como de una interaccin con el sistema nervioso en los adultos en relacin con dicha conducta. Si en el perodo prenatal crtico, el encfalo de un roedor es expuesto a andrgenos, el animal va a presentar ulteriormente masculinizacin y defeminizacin de su conducta. En cambio, si en dicho perodo crtico no existen andrgenos, el animal adulto va a presentar una conducta sexual femenina., bajo la accin de estrgenos y progesterona. Se ha demostrado experimentalmente en ratas que la principal hormona activa que determina el pattern cerebral masculino normal es el estradiol, que es una hormona femenina. Ello se debe a que gran parte de la testosterona que llega al cerebro es convertida en estradiol por enzimas en las clulas blanco de la diferenciacin sexual.
275
La masculinizacin conductual se refiere al efecto organizacional de los andrgenos que determina la conducta sexual masculina del adulto. La defeminizacin, por su parte, impide que el animal adulto presente una conducta sexual femenina. En los roedores hembras, la conducta sexual depende en gran parte de la secuencia estrgenos-progesterona.; esta secuencia aumenta la proceptividad (deseo de copular), la receptividad ( deseo y capacidad de copular) y el atractivo (cambios fisiolgicos y conductuales que afectan al macho, especialmente olor y conducta). Estos efectos se acentan durante el perodo de estro; en cambio, el macho ignora a una hembra castrada. Andrgenos y conducta sexual. En el perodo crtico de desarrollo, la falta de exposicin del cerebro a los andrgenos, va a determinar que el animal adulto presente una conducta sexual femenina, ayudado por la administracin de estrgenos y progesterona. En cambio, si en este perodo crtico, el cerebro del roedor se expone a los andrgenos, se va a producir masculinizacin y defeminizacin de la conducta sexual. La defeminizacin se produce porque se inhibe el desarrollo de los circuitos neurales que controlan la conducta sexual femenina.; en cambio, en la masculinizacin se estimula el desarrollo de los circuitos nerviosos que controlan la conducta sexual de los machos. Feromonas. Se les denomina tambin hormonas sociales, por cuanto trascienden los mbitos individuales y ejercen su efecto sobre otros animales. Por lo general su existencia es captada por el sistema olfatorio, pero algunas son ingeridas o absorbidas por la piel. Es conocido el hecho que animales como el perro huelen las catecolaminas simpticas y suprarrenales, que para l son ndice que el sujeto tiene miedo. Las feromonas influyen sobre la conducta sexual en los animales y probablemente en el ser humano. Se ha comprobado que la convivencia prolongada de puras
276
ratas hembra, con ausencia de machos, reduce sus ciclos estrales, los cuales pueden llegar a detenerse, fenmeno que se conoce como el efecto Lee-Boot. Pero si esta hembras son expuestas al olor de un macho o de su orina, normalizan nuevamente sus ciclos estrales y an pueden sincronizarse, lo que constituye el efecto Whitten. Por otra parte, la pubertad puede adelantarse en roedores hembra por el olor de un macho (efecto Vandenbergh). Estos efectos se producen por la accin de una feromona presente en machos adultos normales. El efecto Bruce consiste en que si una rata recin preada se encuentra con otro macho adulto, puede tener un microaborto, originado tambin por feromonas urinarias provenientes del nuevo macho; esto tiene una interpretacin sobre la supervivencia del ms apto, ya que si el nuevo ratn se aparea con la hembra, puede darle una descendencia mejor dotada (el nuevo ratn invadi un territorio ajeno, lo que le supone ms fuerte); se deduce que este efecto se basa en aprendizaje, en el sentido que la rata aprende a reconocer al macho con que se aparea, el cual no la har abortar. Uno de los pocos datos que se tienen sobre la intervencin de neurotransmisores en la conducta sexual se refiere precisamente a que en este aprendizaje participan axones noradrenrgicos que son aferentes a los bulbos olfatorios. Experimentalmente se han destrudo estos axones (con 6 - hidroxidopamina), y el efecto Bruce se produce con el propio macho primariamente fecundante. Se supone que en la cpula se estimula el sistema noradrenrgico y deja en la rata el olor de la noradrenalina de un macho determinado. La estimulacin vaginal aumenta la actividad noradrenrgica de los bulbos olfatorios. En el mecanismo de accin de las feromonas interviene el sistema olfatorio, que consta de un sistema olfativo primario, el rgano vomeronasal y el bulbo olfatorio accesorio. Los bulbos olfatorios envan eferencias al ncleo medial de la amgdala, y sta al rea preptica, al hipotlamo anterior y al ncleo ventromedial del hipotlamo. Las feromonas influyen en los ratones machos, cuyos niveles de testosterona sangunea aumentan con la presencia de una hembra nueva, efecto que se suprime al eliminar el rgano
277
vomeronasal. Tambin se encuentran feromonas en las secreciones vaginales. Es importante el efecto del olor en la conducta sexual, ya que puede producir estados de excitacin, reconocimiento de las hembras de un clan, reconocimiento de los compaeros sexuales, etc. Adems, se ha demostrado en animales el efecto rejuvenecedor de una hembra nueva, que se conoce como el efecto Coolidge. El rgano vomeronasal existe tambin en los seres humanos, segn estudios en 1000 casos realizados por dos cirujanos plsticos, Garca Velasco y Mondragn , pero no se le conocen sus funciones fisiolgicas. Un ejemplo que podra fundamentar la accin de feromonas en humanos es la sincronizacin de los ciclos menstruales en mujeres que conviven normalmente juntas , as como el acortamiento de los ciclos en mujeres que estn habitualmente en presencia de hombres. Experimentos con el sudor femenino demostraron que la sincronizacin de los ciclos se puede producir por mecanismos olfatorios. Y por ltimo, la industria de los perfumes presupone estas acciones. Para la conducta sexual humana, se pueden afirmar algunos hechos. Las hormonas son factores decisivos en la determinacin normal del sexo en el perodo prenatal, pero la castracin en el adulto y la administracin de hormonas sexuales contrarias a su sexo, no le hacen cambiar su preferencia sexual. An, parece que la testosterona administrada a mujeres (y la proveniente de las suprarrenales en macacus rhesius) les aumenta su sexualidad normal.Se plantea que las hormonas desempean un papel activador y modulador de la conducta sexual. Por otra parte, la corteza frontal controla la conducta sexual, al igual que cualquier otra conducta lmbica, de modo que dicha conducta presenta variaciones normales en lugar de seguir un cierto estereotipo rgido. Un efecto que las mujeres comparten con los animales, especialmente con la coneja, es que estmulos provenientes de la regin genital pueden provocar ovulacin.
278
En la mujer, factores psquicos que acten a travs del sistema lmbico y su control sobre las hormonas del eje hipotlamo-hipofisiario, pueden tener efectos tanto ovulatorios como anovulatorios. Por ejemplo, en casos de violaciones(por una fuerte excitacin del sistema lmbico), se desencadena el peak de LH y en consecuencia la ovulacin; lo mismo puede suceder durante la relacin sexual si la mujer desea evitar el embarazo; o en casos de ansiedad por quedar embarazada, se puede frenar la secrecin de LH por va sistema lmbico-hipotalmico. De experimentos con monas, se puede extrapolar que tambin en las mujeres, las hormonas ovricas ejercen un efecto sobre su deseo sexual. En los seres humanos existe un factor incuestionable que gobierna la conducta sexual y es el afecto por la pareja, lo que determina que la mujer acepte las relaciones sexuales an en casos que no lo desee preferentemente, lo cual est indicando la importancia de los factores psicolgicos, (lmbicos y corticales). Un cuadro anormal interesante es el sindrome de insensibilidad a los andrgenos. Es una mutacin gentica que impide la formacin de receptores andrognicos (este gen se encuentra en el cromosoma X). Los testculos de un feto genticamente masculino, pero con este sindrome, secretan andrgenos y hormona inhibidora del sistema de Mller, pero slo sta influye en su desarrollo ulterior, formando una vagina estrecha e impidiendo el desarrollo uterino. Por la falta de respuesta a los andrgenos, se desarrollan genitales externos femeninos, lo cual hace que se desarrollen como nias, pero al no tener ovarios ni tero, sern infrtiles. Por lo general se les extirpan los testculos, que adems presentan una mayor incidencia de tumores malignos. A ttulo de curiosidad, se puede mencionar que de este sindrome han derivado complicaciones en los Juegos Olmpicos (1992), pues se decidi aceptar como mujeres a quienes poseen el genotipo XX; pero puede tratarse de una mujer con insensibilidad a los andrgenos, que posee el genotipo XY, y que adems no tendrn el desarrollo muscular masculino, pues no poseen receptores andrognicos (tampoco
279
tiene sentido que usen esteroides anablicos, que son andrgenos sintticos). Los varones presentan respuestas sexuales variadas a la testosterona. La falta de testosterona determina el cese de la espermatognesis y la disminucin gradual de la conducta sexual. Por otra parte, factores psquicos como ver pelculas erticas, aumenta los niveles de testosterona. Orientacin sexual. Normalmente los seres humanos son heterosexuales y lo mismo es vlido para los animales que presentan dimorfismo sexual. Se han analizado como factores causales o determinantes tanto los biolgicos (hereditarios, nerviosos, hormonales), como los psicolgicos y sociolgicos; an no existe una respuesta definida, tal vez precisamente por tratarse de un problema multicausal. El aspecto gentico se ha estudiado especialmente en relacin con la homosexualidad, y de estos estudios se ha podido derivar lo concerniente a la heterosexualidad. La homosexualidad exclusiva (o su equivalente en los animales) parece producirse slo en los seres humanos; la bisexualidad suele observarse tambin en animales; las estadsticas existentes indican que hay ms varones homosexuales que bisexuales, pero naturalmente los datos pueden estar falseados. Lo que distingue normalmente la actividad sexual de hombres y mujeres no es exactamente su conducta sexual en s, sino el gnero del compaero (a) que eligen. (Recordar que la conducta sexual del macho, por ejemplo, incluye la penetracin, el impulso plvico y la eyaculacin). Existe gran controversia sobre el origen de la homosexualidad, especialmente la masculina, considerando factores psicolgicos, sociolgicos, hormonales y nerviosos. El factor ms descartado es el hormonal post natal, basado en que en el adulto la castracin no lo transforma en un homosexual, ni
280
tampoco la administracin de testosterona a un homosexual lo vuelve heterosexual (ms bien acenta su conducta homosexual). Ms an, la mayora de los homosexuales tienen niveles normales de testosterona. En estudios sobre lesbianas, se encontr que un 30 % de ellas presenta niveles aumentados de testosterona, sin alcanzar al nivel masculino (esto puede deberse a ciertos estilos de vida). Hoy da se acepta como la causa ms plausible para la homosexualidad masculina una sutil diferencia en la estructura cerebral producida por modificaciones de grado en la androgenizacin prenatal. Segn esto, las posibilidades enceflicas del varn seran: -normal: encfalo masculinizado y defeminizado; -homosexual: encfalo no masculinizado ni defeminizado; -bisexuales: encfalo masculinizado pero no defeminizado. Los cambios enceflicos encontrados hasta hoy se refieren a tres estructuras: ncleo supraquiasmtico, ncleo sexualmente dimrfico y comisura anterior (haz de fibras que conecta ambos lbulos temporales entre s). El ncleo supraquiasmtico es ms grande en homosexuales y ms pequeo en hombre y mujeres heterosexuales. El ncleo sexualmente dimrfico es ms grande en hombres heterosexuales y ms pequeo en hombres homosexuales y mujeres heterosexuales. La comisura anterior es ms grande en hombres homosexuales y mujeres heterosexuales, y ms pequea en hombres heterosexuales. Con respecto a estas diferencias, se postulan algunas hiptesis. Una se refiere al hecho que no se ha demostrado que estas alteraciones constituyan una causa de homosexualidad, sino que podran constituir un fenmeno que acompae a la condicin homosexual. Otra incgnita se relaciona con el origen mismo de los cambios enceflicos; la teora ms aceptada se refiere a que los encfalos pueden haber experimentado exposiciones prenatales hormonales diferentes, es decir, la diferencia estara en algn
281
pequeo grado de alteracin en la androgenizacin prenatal, con lo cual las modificaciones de los ncleos mencionados pasaran a constituir ms una consecuencia que una causa. Un estudio realizado con animales de laboratorio, ha relacionado el estrs prenatal con la conducta sexual del animal adulto; se encontraron mayores probabilidades de conductas desviadas si las ratas eran sometidas a estrs prenatal (con liberacin hormonal propia del estrs); coincidentemente, este estrs provoca una disminucin del tamao del ncleo sexualmente dimrfico. Otro aspecto que se ha podido demostrar parcialmente es el efecto de la herencia en la orientacin sexual. Los estudios genticos presentan algunas limitantes, por el hecho que los homosexuales por lo general no se reproducen y provienen de padres heterosexuales (eventualmente bisexuales). A este respecto se han efectuado estudios de gemelos y sus familias. Para el caso de los varones, los datos obtenidos arrojan los siguientes resultados: el 57 % de los gemelos idnticos, el 24 % de los gemelos fraternos y el 13 % de los hermanos de varones homosexuales son tambin homosexuales. Para las mujeres, el 50 % de las gemelas idnticas, el 16 % de las gemelas fraternas y el 13 % de las hermanas de lesbianas, son tambin lesbianas; comparando con las tasas generales de homosexuales, resulta un agrupamiento familiar importante en la orientacin sexual. Otras conclusiones de los estudios genticos parecen indicar que los genes responsables son ms importantes en unas familias que en otras (en algunas se dan ms varones homosexuales que en otras), y que la herencia parece provenir a travs de la rama materna, a pesar que an no se ha demostrado un ligamiento al cromosoma X. Sin embargo de los estudios de Hamer y col. se puede deducir que existe un gen, ubicado en la regin cromosmica Xq28, que influye en la orientacin sexual de los varones. Planteada as la posibilidad de una transmisin gentica, cabe preguntarse de qu modo podra afectar a la orientacin sexual. Podra ser a travs de algn mecanismo relacionado con
282
hormonas, por lo cual se analiz el gen relacionado con los receptores andrognicos, que regula la sntesis de una protena esencial para la masculinizacin del cerebro humano, y que adems se encuentra en el cromosoma X. Esto se descart porque no se encontraron diferencias significativas entre los individuos que manifestaban orientaciones sexuales diferentes. Otra posibilidad es que el gen hipottico actuara sobre la personalidad, determinando que unos individuos muy seguros de s mismos no tengan problemas para elegir compaero de su mismo sexo, sin depender del qu dirn . Aqu cabe preguntarse si no podra existir, a la inversa, una personalidad muy segura de su identidad sexual, que incline al individuo por una u otra orientacin sexual. Y una tercera posibilidad es que el gen que influye en la orientacin sexual (regin cromosmica Xq28) altere directamente regiones enceflicas involucradas en el dimorfismo sexual, como es el tercer ncleo intersticial del hipotlamo anterior (NIHA3). No escapa al anlisis de la homosexualidad un aspecto sociodemogrfico, por cuanto la reproduccin humana precisa no solamente de un dimorfismo sexual, sino adems de una conducta heterosexual, que permita que se fusionen los gametos masculino y femenino. Como la homosexualidad no conlleva a la reproduccin, es fcil suponer que esta anormalidad atenta contra la conservacin de la especie humana. En cuanto a la influencia de factores sociales o ambientales puros, es prcticamente imposible analizarlos, dada la existencia de factores biolgicos (genticos, del desarrollo y enceflicos) que enmascaran la accin exclusiva del medio ambiente. Una teora bastante aceptada sobre el desarrollo homosexual relaciona un factor inicial constitudo por una ligera alteracin en la androgenizacin prenatal y luego, los factores ambientales potenciaran esta alteracin. A todo lo anterior, hay que agregar una teora no demostrada sobre la participacin de algunos contaminantes ambientales como el plomo. Del anlisis histrico de civilizaciones antiguas como la griega y la romana, se conoce una incidencia
283
alta de homosexualidad en dichos grupos tnicos; al pretender encontrar una explicacin, se ha aventurado la hiptesis de la influencia del plomo en las alteraciones de la orientacin sexual, elemento que fu muy utilizado como constituyente de la vajilla en que se preparaban y servan los alimentos. Y como consecuencia, se plantea la homosexualidad como una de las causas de la desaparicin de estas civilizaciones, lo que habra recibido una ayuda efectiva de los brbaros que los invadieron. Aspectos bio- psicolgicos de la conducta sexual. La reproduccin sexuada trae algunas consecuencias psicolgico-sociales que se pueden resumir en los siguientes puntos. La reproduccin sexuada es una forma de mantener jvenes a las especies. Es fcil deducir que en la reproduccin asexuada, los elementos constituyentes de las clulas hijas tienen la edad de la clula madre y en la medida que crecen, se hacen an ms viejas que su progenitora. En cambio, en la reproduccin sexuada, una vez que se unen ambos gametos, el nuevo ser comienza a formar sus propias clulas (obviamente, con material proveniente de la madre); es por ello que se considera como el comienzo de la vida el momento de la fusin de las membranas de los gametos. Biolgicamente, entonces, se descarta para la reproduccin sexuada aqullo de carne de mi carne y sangre de mi sangre. En la reproduccin sexuada, el cuerpo desarrolla un poder creador, que en los animales es manifiesto en el perodo de celo; por ejemplo, el plumaje de las aves se vuelve ms hermoso y brillante, la cresta se torna majestuosa. En las sociedades primitivas, las danzas rituales corresponden a este poder creador, el individuo manifiesta como una poesa de la vida, como si la naturaleza obligara al cuerpo a superarse, desarrollando al mximo su poder seductor. Para los animales, esto constituye un inconveniente en relacin con los depredadores. En el caso del ser humano, este efecto es especialmente notorio en las nias, que en la pubertad comienzan a preocuparse acentuadamente de su figura y arreglo personal, como ropa, maquillaje, etc.
284
Otra consecuencia de la reproduccin sexuada humana es que ella viene a abolir la soledad del ser humano, por el hecho que el individuo precisa de una pareja de su misma especie aunque diferente, agregando el sentimiento amoroso de alguien no familiar. Incluso en la antigedad constitua un medio de cultura, (tambin en la actualidad?) pues como ya se saba que no era conveniente el matrimonio entre parientes cercanos, especialmente los nmades o pertenecientes a pequeas comunidades, deban ir a lugares lejanos, con otras costumbres y an otras idiomas, a buscar esposa. Conducta materna. Se ha estudiado fundamentalmente en animales del tipo de los roedores, poco en los primates. Sin embargo, en el estudio de efectos de drogas, se ha demostrado que la marihuana administrada sistemticamente a monos machos y hembras, les disminuye el impulso sexual y en las hembras suprime totalmente el inters por las cras. Como se est demostrando que los seres humanos poseen una sustancia similar a la marihuana, la anandamida, se abre otro camino inexplorado en el estudio de la conducta sexual. Es indudable que en los animales , la conducta materna especialmente es instintiva; basta observar la construccin de nidos en las aves y roedores (facilitada por la progesterona y eliminada por el estradiol), as como el cuidado de cras y su preparacin para enfrentar los enemigos de la supervivencia, lo cual es facilitado por la presencia de las cras mismas. Existen algunas hiptesis anatmicas que fundamentan el desarrollo de la conducta materna, la cual parece depender de estmulos hormonales y olfatorios, segn se ha demostrado con lesiones de la amgdala medial y de la estra terminal (haz de fibras que conecta la amgdala medial con diversas regiones del prosencfalo, incluyendo el rea preptica medial). Algunas cras de roedores emiten dos tipos diferentes de mensajes ultrasnicos, uno relacionado con su temperatura corporal (fro) o con el manejo brusco, situaciones ambas que constituyen un alerta para
285
modificar la conducta materna. Las hormonas no parecen ser esenciales para el desarrollo de la conducta materna, aunque la condicionan. La secuencia progesterona-estradiol es especialmente eficaz; a su vez, la prolactina tiene tambin efectos estimulantes sobre la conducta maternal. En cuanto a las estructuras nerviosas que participan en la conducta materna,la ms importante parece ser el rea preptica medial del prosencfalo (aqu actuara el estradiol, pues contiene receptores de estrgenos); sus lesiones interrumpen la construccin de nidos y el cuidado de las cras; segn experimentos de Numan y Smith, los efectos se producen porque se interrumpe la va entre el rea preptica medial y el rea tegmental ventral del mesencfalo. Adems, si se coloca estradiol en el rea preptica medial, se facilita la conducta materna. Muy relacionada con la conducta olfatoria, se encuentra el contacto directo con las cras, cuyo olor potencia el instinto materno. Bases biolgicas de la constitucin de la familia. Por mecanismos evolutivos, en el ser humano se fueron desarrollando dos caractersticas que fueron determinantes biolgicos de la constitucin familiar: la posicin bpeda o estacin de pie y el tamao enceflico-craneano. La posicin bpeda produjo un estrechamiento del canal pelviano, y el desarrollo de los homnidos hacia homo sapiens determin un encfalo de mayor tamao; en estas condiciones, se haca difcil que en el parto se expulsara un feto de cabeza grande por un canal pelviano estrechado. La naturaleza opt por la solucin de provocar el nacimiento antes que se completara el desarrollo cerebral, una especie de neotenia o desceleracin del desarrollo embrionario y fetal. El resultado fu un recin nacido humano desvalido, a quien deban dedicrsele cuidados especiales, fundamentalmente relacionados con la alimentacin. Como la
286
madre posea naturalmente el alimento, se hizo cargo del recin nacido, mientras el hombre sala a procurar alimento, especialmente protenas animales. As, con la labores compartidas, el ncleo familiar se fortaleci y la especie humana ha podido subsistir desde sus ancestros, como el Australopitecus hasta nuestros das. Pero con el desarrollo de la civilizacin, an en los perodos incipientes de la raza humana, la mujer experiment necesidades socio-culturales que la empezaron a alejar de su habitat y otra persona se encargaba por momentos del cuidado de los recin nacidos; el resto de la historia es bien conocido. Efectos generales del dimorfismo sexual. Una amplia gama de conductas no necesariamente sexuales son caractersticas de machos o de hembras, incluyendo la especie humana. Es caractersticamente reconocido el mayor grado de agresividad que ocasiona la testosterona, siendo, por lo tanto, el macho ms agresivo que la hembra; en los animales, las conductas agresivas pueden ser ofensivas, defensivas, de depredacin, de connotacin sexual. Entre las estructuras nerviosas involucradas en la agresin, las de mayor implicancia son el hipotlamo y el complejo amigdalino. Dos grupos amigdalinos, el grupo crtico-medial y el basolateral se relacionan con las reas de agresividad del hipotlamo. El grupo basolateral, conectado con el hipotlamo lateral, desencadena conductas agresivas; si se le destruye o desconecta del hipotlamo, el efecto agresivo desaparece. A la inversa, la lesin del grupo crticomedial se traduce en aumento de la conducta agresiva, lo cual indicara que este grupo amigdalino tiene influencias inhibitorias sobres las reas de agresividad del hipotlamo. Adems, se ha logrado aumentar y disminuir la agresividad en primates machos y hembras administrndoles andrgenos y estrgenos respectivamente. En macaccus rhesius, el desarrollo de los lbulos frontales es
287
sexualmente dimrfico, lo que se traduce en mejores condiciones de aprendizaje de tareas sobre discriminacin espacial en los machos. En humanos, se pueden mencionar varias diferencias derivadas del dimorfismo sexual. Las asimetras cerebrales, presentes en ambos sexos, tienen algunas diferencias en varones y en mujeres; los estudios se han realizado especialmente en nios-as y muchos en condiciones patolgicas. Sin embargo, cada vez se estn obteniendo mayores evidencias sobre diferencias sexuales en estilos cognitivos no atribuibles simplemente a diferencias de aprendizaje o influencias del medio; dichas diferencias no se manifiestan en el C.I. (mide funciones intelectuales totales) sino que ms bien reflejan habilidades (destrezas) intelectuales especficas. Derivado de los estudios de Maccoby y Jacklin, las mujeres adultas reflejan mayor facilidad de palabra (habilidad verbal) que los varones, mejores resultados en los test de velocidad perceptual (como el tiempo necesario para reconocer una cara), de clculos aritmticos y en la precisin para realizar tareas manuales. Por otra parte, los varones realizan mejor los test que exploran relaciones espaciales, razonamiento matemtico y habilidad motora de precisin. Para la habilidad visuo-espacial se ha encontrado an en los seres humanos, un gen recesivo ligado al sexo; la mitad de los varones y un 25 % de las mujeres presentan el fenotipo correspondiente. Naturalmente que a esto se deben agregar factores de aprendizaje como entrenamiento y prctica.
Motivaciones. Los estados motivacionales o impulsos son las condiciones internas que controlan las conductas. O bien se puede considerar a la motivacin como la energa que desencadena el funcionamiento del organismo. Puede decirse que son las causas de las conductas. Hay autores que consideran que todas las conductas humanas son motivadas, incluyendo las regulaciones
288
viscerales. As, por ejemplo, un aumento de la presin arterial sera la motivacin que desencadene los mecanismos regulatorios de dicha presin. En este caso, las respuestas homeostticas se regularan por mecanismos innatos y aprendidos que modulen los efectos de las seales de feed back o retroaccin que son indicadores de necesidades tisulares. No obstante, desde el punto de vista psicofisiolgico, las motivaciones ms interesantes se refieren a las conductas voluntarias, o a lo menos lmbicas, es decir, conductas impulsivas pero que pueden ser controladas por la corteza frontal. Los impulsos o estados motivacionales son mecanismos cerebrales hipotticos que determinaran la direccin e intensidad de diversas conductas complejas, como son la alimentacin, el beber, etc. Las necesidades tisulares pueden inducir al sistema nervioso a iniciar conductas apropiadas y respuestas fisiolgicas que minimicen o supriman los deficit tisulares. Otras conductas motivadas no responden necesariamente a necesidades tisulares, como son las respuestas sexuales, la curiosidad, etc. Las conductas motivadas se describen generalmente como orientadas a una meta; no parecen producirse por azar, sino que orientadas por sus consecuencias y realizadas de tal manera que satisfagan las necesidades individuales o de la especie. En las motivaciones existen variaciones de sensibilidad frente a los estmulos; por ejemplo, no siempre se desea comer, o bien, lo que en ocasiones es motivante, en otras situaciones carece de inters. La respuesta a determinado estmulo externo depende no slo del estmulo sino tambin del estado interno del organismo. En algunas conductas complejas, el mecanismo motivante no es muy claro. Qu necesidades impulsan nuestras actividades profesionales, sociales, etc.? Tres factores regulan las conductas motivadas: -factores hedonsticos -requerimientos ecolgicos particulares del organismo -mecanismos anticipatorios. Los factores hedonsticos se basan en las sensaciones de
289
placer que acompaan a las conductas motivadas. Se podra postular que los factores hedonsticos constituyen una meta en muchas de las conductas humanas; es ms, conductas como la sexual y la alimentacin, entre otras, van acompaadas de placer a fin de asegurar la reproduccin y la conservacin de la integridad individual respectivamente. No obstante, el placer no puede ser considerado un objetivo, sino un elemento que asegura la realizacin de una conducta determinada. Los requerimientos ecolgicos se refieren a las necesidades que las motivaciones permiten satisfacer. As, la alimentacin es motivada por el hambre y su realizacin permite la nutricin. Adems, como el organismo funciona en base a un diseo ptimo, la alimentacin es naturalmente rtmica, lo que permite que en los perodos interdigestivos, el sistema digestivo se reponga y a su vez prepare los jugos digestivos necesarios para la prxima ingesta. Los mecanismos anticipatorios comienzan las respuestas fisiolgicas antes que se produzcan las necesidades tisulares. Es una de las bases para la existencia de los ritmos biolgicos. La recompensa o refuerzo es un factor importante en los mecanismos del impulso; acta evocando un estado impulsivo y activando circuitos de reforzamiento. Recompensa y castigo orientan la mayora de las conductas humanas, pues determinan las motivaciones. Las experiencias sensitivas neutras se olvidan fcilmente; en cambio, asociadas con recompensa o castigo, la respuesta cortical se acenta a medida que se repite el estmulo, es decir, la respuesta se refuerza positiva o negativamente. Algunos tranquilizantes como la clorpromazina, inhiben los centros de recompensa y castigo, es decir, disminuyen la reactividad afectiva. La estimulacin de los centros hipotalmicos de castigo (especialmente ncleos perifornicales del hipotlamo) produce en el animal reacciones de ataque, con todas sus concomitantes; en cambio, si se estimulan las reas de castigo ms internas, se produce miedo, ansiedad y tendencia a la huda. En cambio, la
290
estimulacin de las reas de premio vuelven al animal dcil, al punto de poderlo domesticar. Algunas reas enceflicas, especialmente hipotalmicas, que son efectivas en producir reacciones de recompensa, tambin estimulan modelos o patrones conductuales complejos, como alimentacin y bebida. Circuito de recompensa y placer. Los mecanismos de refuerzo o de recompensa funcionan en un circuito que incluye a varias estructuras mesolmbicas que incluyen como componentes esenciales el rea tegmental ventral (ATV) y el ncleo accumbens, con dopamina como neurotransmisor. El ATV es activada por situaciones placenteras como la alimentacin, el sexo, las drogas psicotrpicas, las interacciones sociales. Esta informacin es transmitida hacia tres estructuras enceflicas: - la amgdala, que evala el carcter agradable o repulsivo de la vivencia actual: - el hipocampo, que relaciona lo actual con el recuerdo de hechos similares; - la corteza frontal, que coordina y procesa la informacin, eterminando segn esto las estrategias de conducta. El rea tegmental ventral estimula a su vez al ncleo accumbens mediante el neurotransmisor dopamina y ste produce la sensacin placentera. A este nivel actan tambin los opiceos, de lo que se deduce que tambin sera un sitio de accin de las endorfinas. Por otra parte, el ATV recibe la influencia de algunas neuronas silenciadoras de las que producen la dopamina; ciertas drogas como la herona y otros opiceos desbloquean este freno, lo que aumenta la liberacin de dopamina y por lo tanto, se estimula con mayor intensidad el ncleo accumbens.
291
Las relaciones descritas se han representado en un circuito de cajas negras, que permiten visualizar con mayor facilidad y en forma global los mecanismos de recompensa y de placer que constituyen factor esencial en las motivaciones de las conductas lmbicas.
CIRCUITO DE RECOMPENSA
DROGAS
ALIMENTOS
SEXO
INTERACCIONES SOCIALES
AMIGDALA HIPOCAMPO CORTE ZA FRONTAL
GLUTAMATO
AREA TEGMENTAL VENTRAL DOPAMINA
NEURONAS SILENCIADORAS
OPIACEOS
NUCLEO ACCUMBENS
PLACER
Hambre y saciedad como conductas motivadas. La ingesta de alimentos tiene como objetivo bsico la nutricin del individuo, y por lo tanto, su conservacin como elemento de la especie. La naturaleza ha dotado de placer al acto de comer, con lo cual asegura que cumpla su objetivo. No obstante, en las culturas avanzadas, se tiende a comer ms por gusto que por razones nutritivas, es decir, aspecto, olor y gusto de los alimentos constituyen un factor esencial en la conducta
292
alimentaria, lo cual se emplea en la propaganda alimenticia y en la presentacin de los alimentos a la hora de ingerirlos. El organismo controla tanto la ingesta de alimentos como la de lquidos, para lo cual existen mecanismos reflejos en cuyo desarrollo inervienen motivaciones y factores voluntarios. Este control permite que el organismo mantenga un equilibrio energtico y regule el peso corporal. En el hipotlamo se encuentran centros que controlan el hambre, la saciedad y la sed. De las subdivisiones del hipotlamo, interesa su clasificacin en: -hipotlamo anterior -hipotlamo lateral -hipotlamo ventromedial. Existe un centro alimentario lateral o centro del hambre, ubicado en el ncleo del fascculo medio del cerebro anterior, cuya excitacin estimula la ingesta y su destruccin provoca anorexia mortal. En el hipotlamo ventromedial hay un centro de saciedad; al ser estimulado, el animal deja de comer; en cambio sus lesiones provocan hiperfagia. El centro de la saciedad funciona inhibiendo al centro alimentario; este centro del hambre est constantemente activo y su actividad es inhibida por el centro de la saciedad despus de la ingesta. Se postula la existencia de un ponderostato, que regula el funcionamiento de los centros de hambre y saciedad. En cuanto a las aferencias que ellos reciben, se ha demostrado que el centro de la saciedad est controlado por la utilizacin de glucosa de sus clulas, que son por lo tanto glucostticas. Si disminuye la diferencia arterio-venosa de glucosa, disminuye la actividad del centro, no se inhibe el centro del hambre y se experimenta el deseo de comer. Si la utilizacin
293
de glucosa aumenta, tambin aumenta la actividad de los glucostatos, se inhibe el centro del hambre y se experimenta saciedad. Los diabticos con concentraciones bajas de insulina tienen hambre porque las clulas de su centro de saciedad no utilizan glucosa. Algunas estructuras lmbicas como los ncleos amigdalinos, tambin intervienen en los mecanismos del hambre, ya que sus lesiones producen una hiperfagia moderada, an con ingesta de elementos no comestibles. Las amfetaminas inhiben el apetito; el hipotlamo capta estas aminas simpticomimticas, pero se desconoce su mecanismo de accin anorexgeno. Hay tambin una hiptesis liposttica, en que las aferencias provienen de los depsitos de grasa. Tambin influye la ingestin proteica, el fro (aumenta el hambre) y el calor (disminuye el hambre). La colecistoquinina y la calcitonina disminuyen el deseo de comer, as como la distensin del aparato digestivo; en cambio, las contracciones de hambre promueven la ingesta. La denervacin gstrica no afecta la cantidad de alimento que se ingiere. Tienen marcada influencia los factores culturales relacionados con aspecto, olor y sabor de loa alimentos. Consideradas como conductas motivadas, la ingesta de alimentos incluye mltiples factores causales, como las aferencias a los centros hipotalmicos, el tiempo de los perodos interdigestivos, la hora del da, la sensacin de hambre, el estado emocional, factores corticales como hablar de comidas, verlas (propaganda televisiva), etc. Dentro de ciertos mrgenes, comer y beber son conductas voluntarias, y al igual que las conductas lmbicas, pueden ser controladas por la corteza cerebral. El control de la ingesta de alimentos se relaciona con el metabolismo energtico y con el peso corporal, el cual es regulado por el organismo. En la iniciacin y trmino de la ingesta de alimentos participan tres grupos de factores: -oral -gstrico
294
-metablico. Los factores orales estn involucrados en el cese de la ingesta. Sin embargo, por el hecho que el placer es, aunque errneamente, determinante en la ingesta de alimentos, los elementos orales gustativos influyen en el inicio y especialmente en la mantencin del acto de comer, a la vez que dificultan su trmino. Los factores gstricos son ms importantes en el cese de la ingesta; las seales provienen de tensorreceptores gstricos y de la osmolaridad de los alimentos, seales que son enviadas a los centros de hambre y saciedad. En cuanto a los factores metablicos, se relacionan con las informaciones que la glicemia y la lipemia proporcionan a las neuronas de los centros de saciedad.
Sed. Su gran objetivo es la mantencin del equilibrio hdrico del organismo; tanto la sed como la conducta de beber estn controladas por centros del hipotlamo anterior. En trminos globales, el grado de hidratacin, y por lo tanto la osmolaridad tisular, se mantienen gracias a un balance entre la ingesta de lquido y su eliminacin por diversos medios (orina, sudoracin, heces, etc). La ingesta de lquido tiene como variable regulada la osmolaridad de los lquidos tisulares, lo que influye a su vez en el volumen del LEC (lquido extracelular). Se ha demostrado que el grado de deshidratacin normal del organismo tiene un ritmo circadiano, encontrndose su mximo en el ser humano entre las 17 y 19 horas, por lo cual alrededor de estas horas la ingesta de agua debe ser mayor. Los osmorreceptores del hipotlamo anterior captan la
295
osmolaridad del LEC, envan impulsos a los ncleos suprapticos y paraventriculares, que secretan la hormona antidiurtica; sta modifica la permeabilidad al agua de los tbulos distal y colector del rin, con lo cual puede modificar la reabsorcin facultativa de agua, que puede tener un mximo de 19 a 19,5 % del agua filtrada en los glomrulos. As, por ejemplo, si aumenta la presin osmtica de los lquidos tisulares (puede ser por una ingesta exagerada de NaCl), los osmorreceptores disminuyen de tamao, lo cual es una seal para que los ncleos suprapticos y paraventriculares secreten mayor cantidad de hormona antidiurtica y la neurohipfisis la libere en mayor cantidad; al llegar por va sangunea a los tbulos distales y colectores del rin, aumenta en ellos la permeabilidad al agua, la que se reabsorbe entonces en mayor cantidad, con lo cual disminuye la concentracin de solutos osmticamente activos y, por ende, la presin osmtica, hasta llevarla a sus valores normales; es decir, la osmolaridad tisular se regula por mecanismos de retroaccin o feed back negativos. Lo inverso sucede si la presin osmtica de los lquidos tisulares disminuye. Factores ajenos a este mecanismo pueden modificar la secrecin de hormona antidiurtica; as, aumentan esta secrecin el dolor, las emociones, el estrs, el ejercicio, la angiotensina II, y frmacos como la morfina, la nicotina, los barbitricos; en cambio el alcohol, al disminuir la secrecin de hormona antidiurtica, aumenta la diuresis. Otro mecanismo que participa es la sed, la cual aumenta si es mayor la osmolaridad tisular. Tambin el volumen del LEC desencadena otros mecanismos que, al mantener dicho volumen, mantienen en su rango normal a la variable regulada que es la osmolaridad. La disminucin del volumen del LEC aumenta la sed por el mecanismo de la interaccin renina-angiotensina; el producto final, la angiotensina II acta estimulando los centros hipotalmicos de la sed. Los cambios de volumen sanguneo producen distensin de los vasos sanguneos, estimulando tensorreceptores que se encuentran en las grandes venas, atrios, vasos pulmonares, arco artico y seno carotdeo.
296
Otros factores que regulan la ingesta de agua son psicolgicos y sociales, la sequedad de la mucosa oral, etc. Por otra parte, el aumento de la glicemia o una mayor ingesta proteica aumentan la diuresis, que provocar o no cambios en el grado de hidratacin segn sea compensada por un aumento concomitante de la ingestin de agua, lo que normalmente sucede provocada por la sed. Emociones. Se pueden definir como estados de excitacin, complejos, generalmente desorganizados, que presentan dos grandes componentes principales: vivencia o experiencia emocional; es la apreciacin consciente de un estado emocional particular; conducta emocional; en sta ltima, se consideran tanto las modificaciones viscerales y hormonales, como las smatomotoras (o esquelticas). Ambas conductas estn integradas y controladas por el sistema lmbico, del cual las estructuras ms involucradas en los estados emocionales son el hipotlamo y el complejo amigdalino. La conducta emocional, tanto la somtica (de la musculatura esqueltica) como la visceral, se pueden analizar objetivamente, por sus manifestaciones. En cambio la vivencia emocional slo se conoce por correlato del propio sujeto. De aqu derivan los mtodos de estudio, que pueden ser experimentales o bien estudiando los cambios producidos en el individuo a raz de emociones de ocurrencia espontnea. Estos mtodos se basan en el relato verbal, en la observacin de signos y en las correlaciones fisiolgicas o mediciones de los parmetros neurovegetativos y las expresiones corporales. En los cambios viscerales se fundamenta la tcnica del detector de mentiras, el cual fundamentalmente mide las frecuencias cardaca y respiratoria, registra el electrocardiograma, la resistencia elctrica de la piel y eventualmente la presin arterial.
297
Para cada emocin se puede identificar su modalidad y su intensidad. Las emociones pueden comprometer al mbito netamente individual o relacionarse con situaciones sociales. La respuesta emocional puede ser condicionada, cuando se asocia a un estmulo neutro. Tambin se clasifica a las emociones en positivas o negativas, segn produzcan deleite o disgusto en el individuo. Hoy se admite que la diferenciacin de las emociones es progresiva desde el nacimiento; en el recin nacido hay ms bien una excitacin generalizada, que con la maduracin y el aprendizaje se van a diferenciar en emociones positivas y negativas. En las situaciones emocionales pueden describirse algunos aspectos, separables pero a la vez relacionados entre s.; se describirn brevemente. 1) Estmulos antecedentes; se refiere a que existe una reactividad emocional innata, la cual puede modificarse por el aprendizaje; un ejemplo es el caso de los miedos innatos, que pueden presentar una reactividad innata, con o sin componentes aprendidos. 2) Condiciones fisiolgicas: aunque influyen en el estado emocional, no parece posible asignarle a cada emocin un patrn de reaccin fisiolgica. 3) Patrn de comportamiento , se refiere a la forma de reaccionar ante una causa emocional. 4) Metas de la conducta emocional: el comportamiento emocional puede llevar a evitar tensiones (huir por ejemplo), o bien a incrementar el estado emocional. 5) Experiencia consciente: se basa en lo que relata el sujeto, lo que permite clasificar la emocin y su intensidad. Existen numerosas teoras que tratan de explicar los mecanismos de produccin de las emociones y las estructuras involucradas. Entre ellas se puede mencionar la de James-Lange, que establece que primero se produce la respuesta emocional y despus la experiencia; aunque es objetable, parece indudable que es valedera en el incremento del estado emocional. La ms
298
actual es la teora cognoscitivo-fisiolgica de Stanley Schachter; este autor propuso en 1971 que la experiencia de una emocin no se puede explicar simplemente por las conductas emocionales (viscerales y somticas) ni por los cambios neurales que se producen en las estructuras enceflicas. Su teora postula que la emocin incluye lo anterior, pero que adems existe un componente cognitivo que seala los efectos de la interpretacin que el individuo realiza sobre la situacin emocional. Estructuras nerviosas involucradas en los estados emocionales. Son varias, y no siempre su participacin o sus mecanismos de accin aparecen muy claros. Hipotlamo. Es la estructura emocional ms bsica; es as como estimulando diferentes zonas hipotalmicas se puede producir temor, ansiedad, irritacin, ira, curiosidad, etc. Si bien no hay an un cuadro topogrfico claro, se ha demostrado que la estimulacin del hipotlamo lateral desencadena en el animal reacciones de ataque con ira verdadera. En cambio, si se estimula la porcin gris central, se produce una falsa ira, en que se manifiestan las conductas agresivas sin que exista la condicin de enojo. En relacin con el hipotlamo y las conductas viscerales, se ha demostrado que se pueden llegar a controlar algunas conductas viscerales como salivacin, frecuencia cardaca, motilidad intestinal, entre otras. En conejos y ratas, se ha logrado modificar el flujo sanguneo de una oreja; estos controles se obtienen por medio de mecanismos apropiados de recompensa, provocando la conducta y luego reforzndola, a veces aprovechando conductas que han variado normalmente. Tlamo. Directa o indirectamente se relaciona con la experiencia y la conducta emocionales. Hay algunas localizaciones en ncleos determinados, aunque no siempre son muy especficas; se puede
299
mencionar el resultado de algunas estimulaciones experimentales: a) ncleo ventral pstero-lateral; al estimularlo se puede provocar ansiedad, movimientos defensivos y ofensivos, vocalizacin y manifestaciones neurovegetativas; b) ncleo dorsomedial; cuando se lo estimula, se producen respuestas de temor, depresin o ansiedad, provocando sensaciones desagradables y aversivas; est asociado con el lbulo frontal; c) ncleo anterior; su estimulacin directa tambin produce temor y abatimiento, o a lo menos respuesta de alerta, tambin efectos de recompensa; su lesin produce una marcada disminucin en la emocionalidad. Amgdala. Es un complejo de ncleos de la base, ubicada en los lbulos temporales. Tiene una participacin amplia y compleja en los procesos emocionales, especialmente en las conductas agresivas y se supone que participa en los estados emocionales a travs del hipotlamo; su activacin general provoca las respuestas neurovegetativas, conductuales y hormonales debido a sus conecciones con el hipotlamo y con el tronco cerebral. No obstante, la amgdala no decide por s sola provocar tales respuestas emocionales, sino que en stas estn involucrados, adems de las estructuras sealadas, el tlamo y la corteza cerebral. Se pueden distinguir en ella diversos grupos o ncleos. As, hay un grupo anterior que se relaciona con aferencias olfatorias y participa en las conductas agresivas de los vertebrados inferiores; el olfato les permite distinguir, por ejemplo, entre cras y machos adultos, lo cual puede ser determinante en algunas conductas a seguir. El ncleo central recibe aferencias desde la corteza sensitiva primaria y de asociacin, as como desde el tlamo; esta informacin es transmitida por el grupo basolateral, quien le proporciona la informacin sensorial. Las eferencias del ncleo central van al hipotlamo, mesencfalo, puente y bulbo raqudeo; este ncleo responde principalmente a estmulos aversivos, amenazadores. Algunos ansiolticos parecen actuar a travs del ncleo central, el
300
cual posee una concentracin alta de receptores opiceos. El grupo basolateral se conecta con el hipotlamo lateral; al ser estimulado, se observan conductas agresivas, las que no se evidencian si se le desconecta del hipotlamo; de esto se deduce que la amgdala basolateral excita las estructuras hipotalmicas comprometidas en la agresin. El ncleo basolateral posee una concentracin alta de receptores a benzodiacepinas. El grupo crticomedial est conectado con el hipotlamo ventromedial y medial; la lesin de este grupo desencadena las conductas agresivas, al igual que su desconexin con el hipotlamo; de todo ello se deduce que este grupo ejerce influencias inhibitorias sobre el hipotlamo, actuando como zona de evasin. Tambin aumentan las reacciones de agresividad si se seccionan las conecciones entre los ncleos crticomediales y el hipotlamo ventromedial y medial. Experimentos interesantes se han realizado en animales que viven en clanes, como es el caso de los monos; en estos grupos, la extirpacin de la amgdala hace perder al lder su carcter dominante. Se ha descrito que la extirpacin de la amgdala produce indiferencia afectiva. Septum. Normalmente ejerce influencias inhibitorias sobre el hipotlamo Sus lesiones producen animales feroces, pero el fenmeno decae con el tiempo; es probable que el septum inhiba los centros agresivos del hipotlamo. En relacin con las conductas agresivas, John Flynn, de la Universidad de Yale, ha realizado importantes estudios que le han permitido describir en los animales dos formas de ataque: ataque efectivo, caracterizado por un despertamiento simptico acentuado y reacciones de ataque con ira; ataque tranquilo, aunque productivo, puesto que lo desarrolla el animal en la caza de alimento. Corteza cerebral.
301
La corteza frontal ejerce control sobre las conductas lmbicas, entre ellas sobre los estados emocionales. Este control es en su mayor parte un mecanismo aprendido, que llega hasta la madurez emocional, en la cual el individuo experimenta emociones pero las vivencias estn algo atenuadas y las conductas controladas apropiadamente; el sujeto mantiene en general una actitud que se podra describir como serena y estable; naturalmente que esta situacin ideal se altera en casos de emociones intensas. La corteza rbito-frontal, que es la zona cortical que forma la base de los lbulos frontales por encima de las rbitas, participa en emociones relacionadas con situaciones sociales, que a su vez involucran experiencias, recuerdos y juicios. Esta corteza recibe aferencias desde el tlamo, la corteza temporal, el rea tegmental, e indirectamente desde la amgdala y el sistema olfatorio. Enva sus eferencias a la corteza del cngulo, al hipocampo, a la corteza temporal, al hipotlamo, a la amgdala y a otras regiones frontales. Los estudios ms significativos del control de la corteza rbito-frontal sobre el sistema lmbico se han realizado al estudiar daos accidentales de dicha corteza y mediante las lobotomas prefrontales. El caso ms precoz estudiado y el ms espectacular fu el de Phineas Gage. Este fu un trabajador especializado que vivi a mediados del siglo XIX; era un individuo responsable, serio, enrgico; trabajaba con dinamita, la que colocaba en agujeros horadados en las rocas ayudado de una barra de acero; una explosin prematura determin que la barra de acero le atravesara la mejilla y parte del lbulo frontal, especficamente la corteza rbito-frontal. Si bien sobrevivi a su accidente, aparentemente sin lesiones ulteriores, su personalidad se transform, llegando a ser un sujeto irresponsable, irreflexivo, indiferente, incapaz de planificar sus acciones ni su futuro. Otro caso notable fu reportado en 1987 por Solyom, Turnbull y Wilensky; un estudiante universitario, con fines suicidas , se dispar en la boca con un rifle calibre 22; no perdi la vida, sino que se da los lbulos frontales. Curiosamente no se alter su cuociente intelectual ni su capacidad de ejecutar planes, pero
302
desapareci el desorden compulsivo obsesivo que lo llevaron a tomar la determinacin de autoeliminarse; o sea, se autoinfiri una ciruga prefrontal exitosa. En 1935 se dieron a conocer los resultados de lobotomas prefrontales con el fin de terminar con conductas agresivas en psicpatas; con esta intervencin se reducan la ansiedad, las obsesiones y las compulsiones, desaparecan los miedos irracionales; pero se produca un gran cambio de personalidad, el individuo se manifestaba indiferente a las consecuencias sociales de su conducta, a sus sentimientos por otras personas, observndose interferencia con la capacidad de tomar decisiones y ejecutar planes, de desarrollar conductas sociales apropiadas y responsabilidad laboral y familiar. Los cambios de personalidad fueron tan drsticos, que se suspendieron las lobotomas prefrontales por razones ticas. Stress o estrs o sindrome de alarma. Ambas denominaciones representan lo que el fenmeno es en s mismo. Es una forma de tensin o reaccin de alarma ante estmulos que eventualmente pueden ser nocivos para el organismo. Para su desarrollo se precisan, por una parte, los estmulos determinantes, pero tambin un organismo que reaccione frente a esos estmulos; dicho de otra forma, un mismo estmulo o estmulos pueden afectar seriamente a un organismo, y en cambio, los mismos pueden no provocar respuesta en otro individuo. Es por ello que se plantea que el estrs responde a una reaccin personal. Como en cualquier situacin de emergencia, en el stress tienen una participacin preponderante el sistema neurovegetativo y el sistema endocrino, los cuales por una parte pretenden adecuar al organismo para las respuestas estresantes, y por otra, dentro de lo posible, mantener una cierta homeostasis del medio interno. En condiciones de rgimen estacionario, el sistema de
303
regulacin visceral mantiene un cierto tono neurovegetativo, ms bajo durante el sueo tranquilo y ms alto en la vigilia. Pero en la reaccin de alarma, especialmente el sistema simptico, se activa fuertemente y produce sus conocidos efectos a travs de sus neurotransmisores noradrenalina y acetilcolina, y en los cuales tambin participa la adrenalina secretada por la mdula suprarrenal. El estado tensional que acompaa al stress puede ser agudo o crnico; se puede producir por un estmulo intenso, como un accidente con riesgo vital, o bien por estmulos estresantes reiterativos que acten durante semanas o meses. Hans Selye estudi la respuesta a la tensin crnica, respuesta que denomin sindrome general de adaptacin. Es una respuesta trifsica, en que se distingue: 1.- reaccin de alarma; 2.- resistencia a la tensin; 3.- agotamiento. Diversas estructuras nerviosas participan en la reaccin de alarma; ya se mencion el sistema neurovegetativo; tambin participa en forma preeminente el hipotlamo, ya que es quien transduce las reacciones psico-somticas, con consecuencias endocrinas y viscerales. Por otra parte, la corteza cerebral y el sistema reticular aumentan el estado de alerta. La reaccin de alarma se caracteriza por una actividad neurovegetativa exacervada, especialmente del sistema simptico, an cuando tambin participa el sistema parasimptico, con reacciones fundamentalmente digestivas. El sistema endocrino se activa en forma masiva, con las consecuencias que cada hormona produce en forma especfica. En La Fig.... se encuentran resumidas las principales alteraciones neuroendocrinas y sus efectos. Es posible considerar cualquier efecto psicosomtico y llegar hasta sus agentes causales; por ejemplo, si se considera que en el estado de stress se produce un aumento de la presin arterial, y uno se pregunta qu factores
304
inmediatos lo determinan, se pueden observar varios, como ser: - vasoconstriccin provocada por la noradrenalina - aumento de la actividad cardaca - aumento de la reabsorcin renal de sodio y agua producido por la aldosterona - aumento de la reabsorcin renal de agua provocada por el aumento de la secrecin de hormona antidiurtica. Otros efectos interesantes que se producen ya en la reaccin de alarma son los siguientes: - aumento metablico general, producido por la estimulacin simptica y el aumento de secrecin de las hormonas tirodeas; en relacin con este efecto, diversos sistemas determinan un aumento de la oferta energtica a los tejidos, como ser hiperglicemia, glicgenolisis y neoglucognesis; - estimulacin de las contracciones uterinas, debido a una mayor secrecin de ocitocina; esto puede ser causa de abortos o partos prematuros si existe embarazo; - midriasis por estimulacin simptica; puede ser de gran utilidad diagnstica, especialmente si es mantenida; - inmunodepresin, lo que determina que en condiciones de stress, el individuo est muy susceptible a las infecciones, especialmente virales como herpes, resfros, etc.; - trastornos de tipo sexual derivados de modificaciones en la secrecin de las hormonas sexuales; por lo general estos cambios se manifiestan como una disminucin del impulso sexual y alteraciones de los ciclos menstruales.
305
ESTRESORES Mdula Suprarrenal A y NA Actividad Cardiaca Volumen minuto cardaco Pas circulacin coronaria vasodilatacin (A) vasoconstriccin (NA) sudoracin broncodilatacin midriasis secreciones digestivas motricidad digestiva metabolismo energtico consumo de oxgeno hiperglicemia gluconeognesis gluclisis secrecin ACTH SNVS NA CRH HIPOTLAMO GnRH GHRH TRH NEUROHIPFISIS TSH Tiroides Occitocina tero ADH Rin
ADENOHIPFISIS
ACTH FSH LH Gnadas GH Hgado
Corteza Suprarrenal
Contracciones Gluconeognesis MC GC Estrgenos Progesterona Testosterona metabolismo consumo de O2 metabolismo de carbohidratos T3 T4
Reabsorcin De Agua
MINERALOCORTICOIDES (Aldosterona) Reabsocin Na+ Reabsorcin de H2O Excrecin K+ e H+ Volemia Pas
GLUCOCORTICOIDES (Cortisol) Gluconeognesis Anti-inflamacin Inmunodepresin Atrofia linfoide
Con respecto a la inmunodepresin,al parecer se producira
306
en parte por la superproduccin de un producto qumico, el pptido derivado del gen de la calcitonina o CGRP, en los terminales nerviosos de la piel. Como resultado, el CGRP recubre excesivamente la superficie de las clulas de Langerhans, que son clulas inmuno-relacionadas cuya funcin normal es capturar agentes infecciosos y entregarlos a los linfocitos para que el sistema inmune pueda contrarrestar su presencia. Cuando las clulas de Langerhans estn completamente revestidas de CGRP, quedan incapacitadas para desempear su funcin defensiva, con lo cual el organismo queda desprotegido en una va importante de acceso para los grmenes, con lo cual queda ms vulnerable a las infecciones. Por ltimo, se ha postulado que estados de angustia prolongados e intensos pueden hacer al individuo susceptible a desarrollar algunos tipos de cncer. En la etapa de resistencia a la tensin, el organismo pretende volver a su estado homeosttico, intentando llevar a las variables reguladas a sus valores normales; para ello, debe activar al mximo sus mecanismos de regulacin, y consiga o no establecer una pseudo-homeostasis, este esfuerzo fisiolgico le significa un enorme gasto energtico, que acenta la disminucin de peso corporal que suele acompaar a las situaciones de stress. En relacin con variaciones del peso corporal, la fuerte estimulacin simptica que acompaa al sndrome de alarma y que produce disminucin de las secreciones y de la motricidad digestivas, disminuyen las sensaciones de hambre, con lo cual el individuo disminuye su ingesta de alimentos. En cambio, en estados de ansiedad moderados, la persona suele aumentar su ingesta, con lo cual estimula sus centros hipotalmicos de placer, que se encuentran situados vecinos a los centros de saciedad, y as disminuye el grado de ansiedad; en estos casos, se producirn naturalmente aumentos del peso corporal. De la etapa de resistencia a la tensin, el organismo puede seguir una de las alternativas siguientes: - sobreponerse a la agresin; ello implica una aceptacin
307
psicolgica y orgnica de la situacin tensional, con lo cual el organismo regresa a su condicin homeosttica normal, se adapta al medio hostil; significa que el individuo ha ganado su batalla frente a la agresin; -pasar a una etapa de alteraciones crnicas o enfermedades psicosomticas; ello significa que en la reaccin de alarma se han producido daos crnicos como lesiones de la mucosa gastroduodenal (lceras), estados de vasoconstriccin coronaria (angina cardaca), alteraciones de la motricidad intestinal (disfuncin del colon), etc.; -entrar a una fase de agotamiento fisiolgico, en que el individuo puede morir. La multiplicidad de situaciones tensionales que enfrenta el individuo en nuestra civilizacin y poca actual, contribuye a desarrollar enfermedades como hipertensin arterial, artritis, alergias, lceras digestivas, jaquecas, etc. En experimentos realizados con monos, se demostr que slo los animales que deban tomar decisiones desarrollaron lceras del sistema digestivo. Existen tambin situaciones tensionales episdicas, como en los estados emocionales; as, en la ira, desencadenada en gran parte con participacin del hipotlamo, los impulsos del sistema lmbico van hacia la formacin reticular y la mdula espinal, determinando descarga simptica masiva y provocando reaccin de lucha o de fuga. Ritmos biolgicos. Una observacin superficial de las actividades biolgicas permite deducir la ritmicidad de las funciones fisiolgicas. Los perodos de sueo vigilia, ingestin de alimentos y de agua, ciclos reproductivos, son buenos ejemplos de conductas rtmicas. No obstante, los mecanismos que determinan cualquiera de estos ritmos son en gran parte desconocidos; de la investigacin de ellos se deduce una gran complejidad y estrechas relaciones de
308
integracin entre los mecanismos reguladores. Otras funciones peridicas las constituyen la temperatura corporal, las funciones endocrinas, renal, etc. Es posible plantear que los ritmos biolgicos tienen uno o ms centros reguladores endgenos o marcapasos que reciben influencias del propio organismo y del ambiente exterior; en relacin con las influencias ambientales, se definen los condicionadores o Zeitgeber, que son factores peridicos externos que entrenan o condicionan un ritmo biolgico; ejemplo de un condicionador (tal vez el ms influyente en las conductas rtmicas humanas) es el ciclo circadiano nictimeral luz oscuridad. Segn sea la duracin de su perodo, los ritmos biolgicos pueden ser circadianos, nictimerales o ultradianos. El trmino circadiano proviene etimolgicamente del latn; circa diem significa alrededor del da, y se utiliza para designar variaciones alrededor de las 24 horas. En cambio, el tmino nictimeral se refiere especficamente a las influencias de la luz y de la oscuridad; deriva del griego, y significa relativo al da y a la noche. A veces es importante destacar la diferencia, por ejemplo en el caso de trabajadores nocturnos que se desempean en un ambiente nocturno profusamente iluminado (hoteles, hospitales, etc), en que no hay exactamente ritmo nictimeral, pero s circadiano; algo similar sucede en las regiones cercanas a los polos, en que el da en verano y la noche en invierno, tienen una duracin prolongada; sin embargo, los ritmos biolgicos se mantienen especialmente en base a su condicin de circadianos. No obstante, cuando se modifican las situaciones ambientales, las funciones rtmicas tienden a alterarse. Se denominan ultradianos los ritmos que tienen una duracin mayor de 24 horas, como es el caso de los ciclos sexuales femeninos (menstruales, ovricos, hormonales). Los mecanismos rtmicos se originan en un marcapaso interno, que puede ser nico o bien ser el producto de osciladores mltiples, que eventualmente podran funcionar en forma independiente.; en este caso, existiran jerarquas entre los
309
osciladores, que determinan la primaca de unos sobre otros. Todo ello presupone interrelaciones entre los marcapasos que influyen sobre una funcin rtmica; y sta a su vez puede determinar la oscilacin de otras funciones. Los marcapasos pueden ser influenciados por los condicionadores ambientales; para ello deben existir transductores que proporcionen informacin al sistema circadiano, ya sea a un marcapaso jerrquicamente importante para la funcin rtmica, o bien varios osciladores por separado. Podra ser que cada funcin fisiolgica tuviera un marcapaso propio, aunque interrelacionado con los dems; o bien podran existir marcapasos para algunas funciones, de cuya oscilacin podran depender otras. Se han identificado dos grandes grupos rtmicos, ubicados en el hipotlamo: 1.- el marcapsos X ; 2.-el marcapasos Y; ste estara ubicado en los ncleos supraquiasmticos, por lo cual recibe ms directamente las influencias luminosas. Existen evidencias que ambos marcapasos estn acoplados, por mecanismos nerviosos u hormonales, y que el marcapasos X ejerce mayor influencia sobre el marcapasos Y que a la inversa. A su vez, los condicionadores ambientales influiran sobre estos marcapasos, modulando su ritmo propio; el principal condicionador humano es el ciclo luz oscuridad. Un aspecto que se debe considerar en relacin con el perodo y frecuencia de las oscilaciones es la duracin de la vida del animal y su intensidad metablica. El tiempo de vida de un ratn, por ejemplo, es equivalente al tiempo de vida de un elefante, en el sentido que ambos, durante su vida, realizan su ciclo vital en que nacen, crecen y se desarrollan, se reproducen, envejecen y mueren, slo que el ratn vive ms acelerado que el elefante, puesto que su perodo de vida es notoriamente menor. Ello determina tambin que el metabolismo de los animales pequeos es ms intenso, por unidad de peso, que el de los animales
310
grandes. Por ltimo, tambin las influencias sociales pueden actuar como condicionadores. De hecho, el ser humano, a travs de la cultura, de los avances cientficos y tecnolgicos, ha logrado prolongar la vida de su especie.
Ritmo sueo vigilia. Normalmente se correlaciona bien con el ciclo reposo actividad. El ser humano duerme alrededor de un tercio de las 24 horas; los extremos lo constituyen el burro, que slo duerme un 13 % y la zorra mochilera, que duerme un 80 %. Considerando al ser humano, la duracin del ritmo de sueo depende de la edad; as el recin nacido duerme gran parte de las 24 horas, en cambio el senescente suele dormir unas cinco horas. En el reino animal, hay animales diurnos y nocturnos, cuya actividad se relaciona, adems de los ciclos luz oscuridad, con la facilidad para obtener el alimento. Ciclos de alimentacin. La captacin y la ingestin del alimento requieren que el animal est activo y en muchos casos alerta; ello determina en parte que la alimentacin sea rtmica y acoplada al ciclo sueo vigilia. Indudablemente que la ritmicidad alimenticia permite que la actividad digestiva se realice en forma ptima. Tambin la ingesta de lquido presenta cierta ritmicidad, relacionada con el grado de hidratacin del organismo; se ha podido determinar que entre las 17 a 19 horas, el ser humano presenta su mayor grado de deshidratacin, por lo cual es conveniente hidratar al organismo alrededor de estas horas, idealmente previniendo el dpeficit acuoso.
311
Ritmos de temperatura corporal. La temperatura del ncleo homeotermo presenta un ritmo circadiano que es entrenado por la alternancia de los ciclos luz oscuridad; no obstante, el ritmo persiste en condiciones de luminosidad o de oscuridad constantes. Experimentalmente se han demostrado pequeos aumentos trmicos con slo prender la luz y disminuciones en oscuridad. Como un marcapasos, el X, controla la temperatura del ncleo homeotermo, se le asocia con oscilaciones de la termognesis; en cambio, el marcapasos Y se relaciona con la temperatura cutnea, y por ende, con la termolisis. Ritmos endocrinos. Se ha demostrado que la mayora de las concentraciones plasmticas de hormonas presentan ritmos circadianos, como es el caso del cortisol, hormona de crecimiento, aldosterona, prolactina, testosterona, trirotropina, renina, insulina, melatonina; an las hormonas sexuales femeninas, dentro de sus ritmos ultradianos de duracin mensual, presentan pequeas variaciones circadianas y tal vez nictimerales. La hormona de crecimiento alcanza su mximo en las horas de sueo, tiempo en que el cortisol plasmtico alcanza el mnimo. El ritmo de cortisol se establece a los 2 3 aos de edad, estando ausente en el recin nacido. Las hormonas del eje hipotlamo hipofisiario tienen regulacin nerviosa; cada etapa del eje presenta ritmo circadiano, adems de las influencias que puedan ejercer otros condicionadores. Su marcapaso central estara en el ncleo supraquiasmtico. Finalmente se puede concluir que los diferentes ritmos funcionan integrados, lo que lleva a plantear la existencia de un reloj biolgico que determina la ritmicidad de cada funcin en el concierto del funcionamiento del organismo.
312
Sistema Tlamo Neocortical. Es indudablemente el ms difcil de concretar, puesto que en l tienen su base las funciones intelectuales, las relacionadas con aspectos ticos, la voluntad, el control de conductas lmbicas, adems de otras ms concretas como el lenguaje, el control smatomotor, la integracin sensitiva, etc. Sus funciones se pueden agrupar, entre otras formas, de la manera siguiente: 1.- rea cognitiva, relacionada con la sensopercepcin, la que a su vez se asocia al lenguaje y al pensamiento; 2.- rea volitiva, relacionada con la intencionalidad y que se manifiesta en: - la capacidad de generar conductas con conciencia de finalidad o intencin, como la generacin voluntaria de conductas somticas; - el control intencionado de las conductas lmbicas, aprendizaje que se termina de adquirir aproximadamente a los 30 aos de edad; la madurez emocional es la que provee de estabilidad conductual; 3.- rea afectiva, que se refiere a los fenmenos conscientes relacionados con esta rea, inducidos por actividades lmbicas, como la experiencia emocional y los sentimientos. La corteza cerebral se puede analizar tambin considerando las diversas funciones que se originan en sus diferentes lbulos. Lbulo parietal. A l se le pueden asignar las funciones de recepcin de la informacin sensitiva somtica general, la distribucin topogrfica del cuerpo, su ubicacin en el espacio y en el tiempo y la mezcla de las sensaciones que originarn sensopercepciones complejas. La corteza somestsica recibe, analiza y combina las informaciones sensitivas exteroceptivas y propioceptivas. Otras regiones del lbulo parietal mezclan estas sensaciones con otras que pueden provenir de los lbulos occipital (visuales) o temporal
313
(sonoras), de modo que en este lbulo se integran las aferencias provenientes de varios sistemas, especialmente del smatosensorial, visual, auditivo y vestibular. El resultado es un esquema complejo, de mayor significacin, en el cual el yo empieza a tomar forma en su ambiente. Este entrelazamiento sensitivo, unido al recuerdo de experiencias, es necesario para interpretar las sensopercepciones visuales, los sonidos, la ubicacin espacial y temporal, etc. Este significado de los sucesos va a permitir la decisin de las conductas a realizar. La sntesis es rapidsima, de modo que el sujeto pueda tomar las decisiones de su actuar en un tiempo breve. Cuando se daa el lbulo parietal se produce una agnosia o prdida de la nocin del significado de las cosas o sucesos. Se puede producir incapacidad de localizar sensaciones o de reconocer el significado de objetos palpados, o bien prdida o falla para atender a acciones visuales o auditivas, aunque la visin y la audicin estn intactas, lo que constituye una ceguera y sordera psquicas. Existen casos extremos, en que se ha producido el dao de todo el lbulo parietal derecho, por ejemplo, que es necesario para apreciar las relaciones espaciales; en estos casos, se pierde la nocin y aceptacin de una mitad del espacio personal y extrapersonal. El individuo afectado puede fallar en vestir o desvestir el lado izquierdo del cuerpo, o atender a su cuidado cosmtico, y an quejarse respecto a una presencia extraa que parece estar en su cama. El lbulo parietal coordina las seales nerviosas en relacin con la naturaleza de los objetos que nos rodean y nuestros propios impulsos. El cuadro integrado as formado pasa desde el lbulo parietal hacia el lbulo frontal, donde se elaboran las estrategias globales de conducta. Lbulo frontal. Es la base del movimiento (reas motoras), lenguaje, pensamiento, capacidad de juzgar y de planificar, principios ticos, responsabilidad, control sobre conductas lmbicas.
314
Los lbulos frontales humanos estn extraordinariamente bien informados de lo que sucede en otras regiones del sistema nervioso central y ejercen una influencia poderosa y selectiva sobre los sucesos relacionados con dicha informacin. Las regiones prefrontales o anteriores mantienen conecciones recprocas con el sistema lmbico, lo que le proporciona al lbulo frontal la funcin nica de asociar la informacin cortical con las aferencias emocionales . La regin del polo frontal elabora los patrones de movimiento, pero tambin est involucrada en la regulacin del tono emocional, asignando prioridades a las demandas orgnicas y ambientales, a la vez que estabiliza programas para lograr metas de corto y largo plazo. Cuando se daa o se produce prdida del lbulo frontal, se observa un deterioro de la personalidad. Disminuyen la ansiedad y la inquietud, llevando a un estado de tranquilidad e indiferencia; se reducen los standards ticos, siendo especialmente notoria la irresponsabilidad. Disminuye la capacidad de juicio individual y la habilidad para planificar. Todo sto es sntoma que el sistema lmbico est operando sin su control superior. No se trastorna el intelecto, la memoria ni los estados de conciencia, pero s la habilidad para responder apropiadamente en las esferas emocionales y sociales. El lbulo frontal tiene conecciones masivas con el lbulo temporal, de modo que ambos trabajan en conjunto en muchas de las funciones corticales superiores. Lbulo temporal. A l se le pueden asignar funciones como el lenguaje, la audicin, las ensoaciones, la memoria. En l se encuentran reas de audicin, de elaboracin de sonidos, imgenes, olores , con que se elaboran experiencias en forma compleja mediante el registro, la percepcin y la evocacin de sucesos; tambin es importante en los matices emocionales de la expresin. Parte del
315
lbulo temporal est involucrado en el registro y almacenamiento de informacin, as como en la evaluacin de lo que es agradable o desagradable. Indudablemente que el almacenamiento de informacin no se produce solamente en el lbulo temporal, aunque hay algunas memorias, como las auditivas y olfatorias, que se registran en este lbulo. Si se lesiona o se destruye este lbulo, se producen trastornos emocionales, alucinatorios y mnmicos. Si el dao afecta al complejo amigdalino, se puede observar hiperfagia, hipersexualidad y placidez excesiva, fantasas de olores, as como un sentimiento temeroso de irrealidad del ambiente. Si se lesionan ambos lados, se pierde la memoria reciente. Durante ciruga cerebral se han podido estimular reas del lbulo temporal, obtenindose alucinaciones e ilusiones dramticas, como un cuadro en movimiento con sonido y color; se puede evocar todo tipo de recuerdos. Lbulo occipital. Est prcticamente todo involucrado en el proceso de la visin. En el polo posterior se encuentra el rea visual primaria, donde se recibe informacin con respecto a colores, formas, movimiento de objetos, etc. Otras regiones occipitales se relacionan con el sentido de lugar, atencin ptica, reconocimiento ptico de objetos, de colores, de nmeros, de escritura. Existe en la parte anterior del lbulo occipital un rea denominada visuo-psquica, que corresponde precisamente a la interpretacin psicolgica de los elementos observados visualmente. Si esta rea se daa, se produce la ceguera psquica. Aprendizaje y Memoria. Se considera que el aprendizaje es el factor ambiental ms importante que modula la conducta humana; es el proceso
316
mediante el cual los animales y los seres humanos modifican su sistema nervioso y su conducta. Este cambio adaptativo del comportamiento individual es resultado de la experiencia. Existen diversas formas de aprendizaje; entre ellas se puede mencionar: -aprendizaje perceptivo, que permite reconocer estmulos percibidos anteriormente y distinguirlos de otros similares; aqu estn involucrados los sistemas sensoriales; -aprendizaje estmulo-respuesta, que es la capacidad de aprender una conducta evocada por un estmulo determinado; incluye el condicionamiento clsico, que implica asociacin entre dos estmulos, y el condicionamiento instrumental, o de asociacin entre una respuesta y un estmulo. En el condicionamiento clsico, un estmulo neutro o condicionado (luz o sonido), es pareado con un estmulo no condicionado (alimento). Este tipo de aprendizaje sirve para preparar al organismo para un acontecimiento ulterior; ejemplo: aviso-dao; comida-secreciones digestivas. En el condicionamiento instrumental, el organismo adapta su conducta en funcin de las consecuencias de ella. Dicho de otro modo, si una conducta determina sucesos favorables, tiende a repetirse; y en cambio a evitarse si provoca sucesos desfavorables. En el primer caso, las consecuencias favorables constituyen un estmulo reforzante (positivo) y en el segundo, las consecuencias desfavorables constituyen un castigo. Memoria. Memoria es el proceso por el cual la informacin aprendida es almacenada y evocada. Es el producto final del proceso de aprendizaje; es como la consolidacn de lo aprendido. Existe una memoria de corto plazo, que dura minutos, y una de largo plazo, que dura horas hasta permanente. Segn Hebb, la memoria de corto plazo involucra cambios en el patern de potenciales; en cambio la memoria de largo plazo comprende cambios fsicos en el pattern de conecciones neuronales. Se denomina engrama al conjunto de procesos y cambios
317
fsicos que se operan en el cerebro y forman la base del aprendizaje. La consolidacin es el fundamento de la memoria permanente o de largo plazo; se le puede definir como el proceso de estabilizacin de una huella de memoria. Existen numerosas interrogantes con respecto a los engramas. Por ejemplo, en las reas corticales que aprenden, las memorias se almacenan difusamente o bien lo hacen en grupos neuronales discretos? Al respecto, Lashley formul dos principios: -principio de equipotencialidad, que establece que las neuronas de un rea sensorial dada son todas capaces de participar en la formacin de memoria respecto de una tarea que utiliza ese sistema sensorial; -principio de accin de masas: se puede utilizar informacin desde diferentes modalidades sensoriales, utilizando pistas visuales, smatosensoriales, cenestsicas, etc; todas pueden contribuir a la formacin de memoria en grandes reas corticales. Adems puede existir transferencia modal cruzada de informacin; las neuronas de un rea sensorial estn disponibles para otras reas sensoriales a travs de conecciones de fibras. El proceso de aprender considera tres etapas: -registro de la informacin, que realizan los sentidos y la corteza cerebral; -retencin, en que los mensajes se transforman y almacenan; -recuerdo o evocacin, en que el material almacenado reaparece. Las estructuras cerebrales especialmente involucradas en los procesos mnmicos son el hipocampo, la amgdala y la corteza cerebral. El hipocampo es determinante para la consolidacin de la memoria, para pasar de la memoria de corto plazo a la de largo plazo, formando redes de memoria en la corteza de asociacin. De hecho, las lesiones del lbulo temporal con el hipocampo incluido, no destruyen la memoria anterior, sino que interfieren con la adquisicin de nueva memoria de largo plazo; dicho de otro
318
modo, estas lesiones producen una amnesia antergrada. Pero adems, el hipocampo desempea un papel importante en la reactivacin de redes neurales por recuerdo o reconocimiento, por lo cual los pacientes con lesiones del hipocampo tambin pueden presentar dificultades para recordar eventos antiguos, es decir, tambin pueden presentar amnesia retrgrada. Como se plantear ms adelante, las redes de memorias nuevas son expansiones de las antiguas, por lo cual ambos procesos, formacin y recuperacin de la memoria estn estrechamente relacionados, participando en ambos el hipocampo. En relacin con el hipocampo y la memoria de largo plazo, se ha demostrado que la sntesis proteica aumenta en el hipocampo en las etapas precoces del aprendizaje, y a medida que el aprendizaje se va consolidando, este aumento se traslada desde el hipocampo al rea cortical que aprende. Adems, en animales criados en medio enriquecido ( ME ), se ha encontrado una mayor relacin RNA / DNA, lo que es un ndice de aumento de sntesis de RNA. En la formacin y consolidacin de la memoria interviene tambin la amgdala, que es una estructura necesaria para evaluar el significado afectivo y emocional de las percepciones. Se pensaba que cada memoria tena un lugar en el cerebro, pero al parecer, las diferentes clases de memoria estn constitudas por redes interneuronales que conectan reas corticales entre s. El sistema nervioso puede almacenar informacin sobre nuestro medio interno y sobre el ambiente exterior. La memoria se almacena en gran parte de la neocorteza, segn se ha podido demostrar en primates. La adquisicin de memoria consiste bsicamente en la modulacin de las sinapsis; las memorias estn formadas por la facilitacin de las uniones sinpticas entre las neuronas involucradas. Esto implica que las memorias son esencialmente asociativas.
319
Segn Donald O. Hebb, cuando una neurona excita a otra en forma repetida, se producen cambios metablicos en una neurona o en ambas, de modo que aumenta la eficacia de la transmisin entre ambas. Se acepta que en los mamferos, la potenciacin a largo plazo consiste en un fenmeno elctrico duradero de facilitacin sinptica que resulta de la transmisin de impulsos a travs de la sinapsis. Las neuronas simultneamente activas se asocian en el sentido que la actividad de una facilita la actividad de la otra. En la corteza cerebral, muchas neuronas reciben informacin convergente; sumando sus informaciones, las neuronas se van a asociar entre s y pueden llegar a sustituirse para activar a otras neuronas. En la potenciacin de largo plazo se observan fundamentalmente dos fenmenos: una activacin sinptica y despolarizacin de la neurona postsinptica. En el hipocampo a lo menos, interviene el receptor NMDA ( receptor a N-metil- Daspartato, que es un agonista del glutamato), que controla un canal inico de calcio. Este canal est normalmente bloqueado por iones magnesio; si la membrana postsinptica se despolariza (por sinapsis fuertes de la misma dendrita), el magnesio es expulsado del canal y el calcio puede entrar; para ello se requieren dos condiciones: la despolarizacin postsinptica, y unin de glutamato al receptor (se abre el canal de calcio). Esto significa que el canal de calcio controlado por NMDA es dependiente del neurotransmisor y del voltaje. En el proceso mismo de aprender se ha estudiado tambin la influencia de moduladores en la formacin de memoria; resultados consistentes se han encontrado con la adrenalina, de la cual mucha o poca inhiben la formacin de memoria; en cambio, cantidades moderadas aumentan la retencin de tareas. Se supone que la adrenalina podra actuar en las sinapsis noradrenrgicas, en las cuales tambin pueden actuar otros agentes amnsicos, como el shock elctrico y los inhibidores de la sntesis proteica.
320
El registro de la informacin comienza con la percepcin; luego de captados los fenmenos sensitivos por la corteza primaria, se produce un proceso de asociacin que permite la percepcin propiamente tal; aqu se activan redes asociativas que permiten clasificar los objetos y representarlos en la memoria, aadiendo nuevas conexiones a redes ya pre-existentes; por ello, neuronas o grupos de ellas pueden formar parte de muchas memorias. Estos fenmenos vienen a confirmar la idea que todos los sistemas neuronianos son capaces de formar memorias. Para constituir memoria, la experiencia actual se incorpora y activa a redes pre-establecidas; es decir, las experiencias nuevas se instalan sobre un sustrato de memoria antigua asociada a ella, la cual es evocada por su semejanza o bien por ocurrencia previa; as, lo nuevo evoca lo antiguo, con lo cual se ha asociado y ahora se consolida, formando parte del fenmeno. Se podra considerar que en las reas corticales primarias existe una memoria de la especie, que es innata , de ubicacin sinptica, y producto de la experiencia esencial que la especie ha adquirido en su interaccin con el medio; mediante esta memoria, la especie ha almacenado informacin que puede ser evocada tanto por estmulos sensitivos como por la necesidad de actuar. Para completar su eficacia, esta memoria precisa de experiencia personal, mediante la repeticin, al comienzo de la vida, y en la medida que el individuo crece, su memoria de especie se ampla y an modifica; sobre ella se va implantando la memoria personal. De estos planteamientos derivan una serie de interrogantes aseveraciones, que no son objeto de este texto. Por ejemplo, la existencia de la memoria de la especie es una base que se inclina ms bien por la teora del innatismo que del empirismo; por otra parte, constituye la base de la existencia de los instintos en los animales; y una gran interrogante sera la existencia de correlacin entre la memoria de la especie y la capacidad personal de aprendizaje ulterior. Se denomina memoria perceptiva a la que se adquiere a
321
travs de los sentidos. Abarca lo que consideramos memoria personal y conocimiento: representacin de eventos, objetos, personas, animales, hechos, nombres y conceptos. Existe una jerarqua de memorias perceptivas que va desde lo sensorialmente concreto a lo conceptualmente general. Las reas de asociacin sensorial almacenan en sus redes memoria sensorial. Su lesin provoca agnosia o dficit en el reconocimiento de la modalidad sensorial correspondiente. El hecho que las mismas reas corticales sirvan tanto para almacenar la memoria perceptiva como para el procesamiento de informacin sensorial, proporciona fundamento neural para la estecha relacin que existe entre la percepcin y la memoria. Recordamos lo que percibimos y percibimos lo que recordamos. Tambin es este un fundamento para reforzar la importancia de la estimulacin sensorial con medio enriquecido en la formacin de redes de memoria, con facilitacin de nuevas sensopercepciones, aprendizaje y elaboracin ulterior de pensamiento. El nivel superior en la jerarqua de la memoria perceptiva es el conocimiento intelectual. Poco se sabe sobre su topografa cortical, pero el hecho que requiera para su elaboracin de mltiples experiencias y asociaciones entre modalidades sensitivas, hace suponer que comprende una distribucin cortical extensa. Se pueden describir diversos tipos de memoria, segn el fenmeno que evoquen; as, est la memoria sensorial, que por va de los sentidos (gusto, olfato, visin, audicin) nos permite evocar un hecho simple; pero este fenmeno bsico se puede asociar con algn evento que lo relacione, lo que constituye la memoria episdica; o con el significado del fenmeno, que sera la memoria semntica y finalmente con el concepto de lo evocado, que constituye la memoria conceptual. Todas estas memorias, por constituir redes, estn en relaciones jerrquicas. As como existe una memoria propiamente perceptiva, tambin se describe una memoria motora, a cargo esencialmente de la mdula espinal, el tronco cerebral, el cerebelo y la corteza motora. Indudablemente que en su nivel ms bsico, existe una
322
memoria de especie, de localizacin cortical, puesto que el funcionamiento elemental del sistema motor es innato y est ntimamente relacionado con las conductas instintivas, como los reflejos, los mecanismos de defensa, la simple locomocin. Sobre esta memoria motora bsica se producen fenmenos de aprendizaje personal, modulacin, control neocortical, etc. Las redes neurales de la corteza premotora contienen las memorias de acciones definidas por su objetivo, secuencia y trayectoria. La corteza prefrontal de asociacin est muy bien relacionada con las estructuras que intervienen en las funciones motoras, y mantiene en sus redes los esquemas motores en una relacin accin objetivo. Al comienzo de un aprendizaje motor, las reas frontales estn muy activas, pero en la medida que se aprende la tarea, la mayor actividad se va a observar en los ncleos de la base y el cerebelo, con decremento de la actividad netamente cortical. En relacin con las memorias en general, ya sean perceptivas o motoras, se postula que no existiran sustratos corticales diferentes para las memorias de corto y largo plazo; tal vez ambas utilicen las mismas redes neuronales, aunque sus mecanismos ntimos puedan ser diferentes. Finalmente, se puede plantear que muchas de las asociaciones especficas que constituyen la memoria, se pueden debilitar y an perder por lesiones y por envejecimiento natural, a la vez que se pueden fortalecer por estimulacin sensorial y por ejercitacin consistente. Plasticidad Cerebral. Se ha establecido que al nacer, el individuo tiene un nmero determinado de neuronas que en la vida postnatal van disminuyendo en cantidad. No obstante, en cualquier edad pre y post natal se evidencian hechos que demuestran la plasticidad del sistema nervioso, es decir, su propiedad permanentemente
323
mutable. La corteza cerebral es fundamentalmente plstica. En la vida embrionaria se observan fenmenos de migracin y rotacin de los neuroblastos desde el tlamo a la corteza cerebral, fenmenos que son la causa de las conecciones tlamo-corticales. La corteza tiene posibilidades limitadas de crecer en grosor, pero no pierde posibilidades de coneciones sinpticas pues crece expansiva y horizontalmente. En la migracin de neuronas hacia la corteza intervienen diversos mecanismos, como guas biomecnicas, sustancias qumicas, etc. Las clulas gliales guan la migracin de neuronas hacia la corteza cerebral; en el proceso de migracin algunos neuroblastos rotan, con lo cual los axones se van disponiendo horizontales a la corteza. Tambin en este proceso de micracin se producen movimientos en columna, con lo cual las clulas que se movilizan entre las columnas entran en contacto con las neuronas vecinas, aunque este contacto se establezca slo en alguna etapa de la histognesis. En cuanto a las sustancias qumicas que intervienen en los fenmenos plsticos embrionarios, hay un plasmingeno activador, que es una sustancia ltica que permite que los conos de crecimiento se vayan abriendo paso en el sustrato. El cono de crecimiento es la porcin distal de axones y dendritas y va buscando contacto con alguna estructura, generalmente otra neurona, con la cual establece sinapsis. En la etapa prenatal, el sistema nervioso forma mayor nmero de neuronas, dendritas y espinas dendrticas que lo necesario; despus del nacimiento hay una reduccin natural de ellas, pero diversos factores pueden aumentar los contactos sinpticos. Las modificaciones plsticas continan en la vida postnatal. Aunque existen algunos datos que indican lo contrario, el concepto clsico establece que las neuronas no se multiplican despus del nacimiento, sino que su nmero va disminuyendo,
324
muy poco en las etapas de la vida joven, pero con ms intensidad en la vida adulta. Lo que s est bien demostrado es que las neuronas modifican el nmero y longitud de sus prolongaciones, fundamentalmente dendritas, como consecuencia de la nutricin, la estimulacin sensorial y el aprendizaje como los factores ms relevantes. Se denomina medio enriquecido (ME) a aqul que junto a una nutricin normal, provee una buena estimulacin sensorial, es decir, con estimulacin ambiental diversa (visual, auditiva, tctil, gustativa, del movimiento). Se ha demostrado en animales que el desarrollo postnatal en un medio enriquecido favorece el desarrollo dendrtico en nmero y longitud de las dendritas, lo que determina mayores posibilidades de contactos sinpticos. En los seres humanos se ha podido observar algo similar. La desnutricin, especialmente en relacin a carencia de protenas, produce campos dendrticos pobres, con escasos contactos sinpticos; esto se observa en animales jvenes y nios especialmente hasta unos tres aos de edad. Para obtener un buen desarrollo neuronal influenciado por el estado nutritivo, basta que la nutricin sea normal, es decir, una hiperalimentacin no determina un mejor desarrollo dendrtico. La estimulacin sensorial, por otra parte, promueve la formacin de campos dendrticos con mejores contactos sinpticos; si bien este efecto podra aducirse para todas las etapas de la vida, est demostrado ms bien en animales jvenes y nios pequeos. Tal vez en el adulto contribuya a la mantencin del desarrollo sinptico alcanzado previamente. Se plantea ahora una pregunta interesante. Podran evitarse los efectos de la desnutricin proveyendo de una buena estimulacin sensorial? Algunas observaciones permiten deducir que si a una desnutricin se le asocia una rica estimulacin ambiental, en edades tempranas de la vida, se pueden alcanzar niveles de coeficiente intelectual de un nio bien nutrido; pero despus de los tres aos de edad, la mejora del ambiente siempre deja un retraso con respecto a los individuos eutrficos.
325
Ciertas poblaciones celulares son ms susceptibles de modificarse cuando se mantiene a un animal en medio enriquecido; as, por ejemplo, a nivel de la corteza cerebral aumenta el desarrollo dendrtico y de espinas especialmente en las capas III y V y en las clulas estrelladas; aumenta el nmero y tamao de las sinapsis. La edad influye en estos cambios plsticos, siendo ms eficaces los estmulos en animales jvenes; ya se mencion que en el ser humano, los mejores resultados se obtienen antes de los tres aos de edad. En los animales viejos, crecen ms los extremos terminales de las dendritas, no tanto el nmero de ramificaciones Neurognesis humana. Hasta hace unos cuarenta aos, se consider que en el cerebro humano no exista reproduccin neuronal despus del nacimiento, y que en la vida postnatal slo se destruan neuronas, especialmente evidente despus de los cuarenta aos de edad. Los primeros indicios de proliferacin neuronal datan desde los experimentos de Joseph Altman, en la dcada de 1960, an cuando en sus experimentos no qued claro si la renovacin post traumtica observada abarcaba solamente gla o inclua neuronas. Luego se demostr que efectivamente inclua a las neuronas, con sinapsis, an cuando su nmero apareca como poco significativo. Hoy se ha descrito neurognesis en ratas, ratones, primates incluido el ser humano. Adems, al comienzo se la describi en zonas restringidas; en cambio hoy en da se ha encontrado renovacin de neuronas en bulbo olfatorio, hipocampo, giro dentado y an en reas corticales. Sin embargo, se confirma la idea primitiva en cuanto a que mayoritariamente las neuronas del adulto se han producido hasta la poca del nacimiento. En los estudios sobre neocortex en primates, se encuentra renovacin neuronal en la corteza de asociacin y no en el rea
326
primaria estudiada (corteza estriada). Sin embargo, no ha sido posible demostrar la funcionalidad de las nuevas neuronas, debido a que las tcnicas electrofisiolgicas no son concluyentes al respecto. Se han estudiado dos factores que controlan la neurognesis en el giro dentado y que a su vez participan en los procesos de aprendizaje y memoria. Estos factores son el estrs y la accin del glutamato. El estrs reduce la produccin de nuevas neuronas granulares debido a la alteracin en la concentracin de corticoides; la ablacin de las suprarrenales aumenta la produccin de nuevas neuronas. Estas hormonas presentan ritmo nictimeral, con un mnimo al despertar. Las neuronas granulares o granos son clulas presentes en el bulbo olfatorio, en el hipocampo y en el giro dentado; se les ha denominado as por su soma redondeado y pequeo. Son especiales para crecer en el cerebro adulto porque son de rbol dendrtico poco ramificado. El estrs crnico podra bloquear la neurognesis por semanas o meses. Las experiencias nuevas aumentan la concentracin de corticoides, produciendo un estrs ligero; esto hace ms lenta la neurognesis. Una interpretacin teleolgica (relativa a los fines) podra ser que el aprendizaje permite mejor supervivencia neuronal, y con el mecanismo descrito se evita la sobrepoblacin de neuronas. El segundo factor es la accin del glutamato, que participa en el hipocampo en los procesos de aprendizaje. El glutamato se enlaza con un receptor llamado NMDA ( N methyl D aspartate). Si este receptor se perturba, por bloqueo por ejemplo, el aprendizaje se deteriora. Con ello aumenta la produccin de neuronas granulares; si los receptores se activan, se reduce dicha produccin. ltimamente se ha demostrado que la serotonina y los
327
opiceos tambin intervienen en la proliferacin neuronal. En sntesis, las neuronas granulares activas inhiben la neurognesis; en cambio, las inactivas promueven la proliferacin neuronal. En el ser humano se han encontrado neuronas recin nacidas en el hipocampo hasta los 72 aos de edad, an cuando su ritmo de produccin va disminuyendo. En ratas, el proceso se revierte, hasta alcanzar los niveles jvenes, suprimiendo los corticoides suprarrenales. En las ratas viejas, la concentracin de corticoides es elevada, fenmeno que sera responsable de la disminucin de la neurognesis con la edad. An ms, hay correlacin entre el aumento de corticoides en seres humanos viejos y prdidas benignas de memoria. Se postula que estas prdidas de memoria se relacionan con la disminucin de la produccin de neuronas granulares en el hipocampo. Hoy se sabe que las neuronas involucradas en los procesos de aprendizaje se renuevan continuamente, pero no todas. Se postula que las neuronas que intervienen en la memoria de largo plazo, as como en funciones sensitivas y motoras, son poco plsticas y tienen una duracin de vida larga; en cambio, se regeneraran las que estn involucradas en los procesos de aprendizaje rpido y memoria de corto plazo. En la actualidad, no es posible estimular la renovacin de neuronas en el adulto, de modo que esto constituir un desafo para los especialistas en sistema nervioso, es de esperar que con solucin a corto plazo. Envejecimiento cerebral. Las modificaciones plsticas cerebrales adquieren ms importancia en la vejez. Sin embargo, estos cambios ya empiezan en el adulto, alrededor de los 45 50 aos, slo que no producen efectos notorios.
328
Con los aos, el nmero de neuronas disminuye pero no uniformemente. Por ejemplo, hay grupos neuronales del hipotlamo que son ms resistentes a la destruccin con la edad; en cambio, son ms lbiles en este sentido las neuronas de la sustancia nigra y el locus coeruleus, por lo cual no es extrao que despus de los 70 aos se manifiesten signos similares a un parkinsonismo moderado. En el hipocampo, desaparece aproximadamente un 5 % de las neuronas en cada dcada de la segunda mitad de la vida, es decir, en este perodo se pierde ms o menos un 20 % de sus neuronas. An cuando muchas neuronas sobrevivan, se pueden atrofiar sus prolongaciones, axones y dendritas.; esto puede suceder en reas cerebrales involucradas en el aprendizaje, memoria, planificacin, etc. Pero no todos los cambios neuronales son destructivos; algunos representan intentos de las neuronas sobrevivientes por compensar la prdida neuronal o atrofia de sus prolongaciones; mientras este mecanismo solidario sea capaz de asumir las funciones de las neuronas faltantes, no ser notorio un trastorno psicolgico ni fisiolgico. Este comportamiento compensatorio ha sido demostrado por Paul Coleman, quien describe un crecimiento neto de dendritas en algunas zonas del hipocampo y corteza cerebral entre los 40 a 70 aos de edad, seguido por una regresin de las dendritas en las edades 80 a 90 aos, etapa en que ya las neuronas no pueden mantener los mecanismos de apoyo. Tambin aqu cabe preguntarse si alguna clase de terapia podra estimular esta forma natural de plasticidad positiva; tambin sera necesario determinar la funcionalidad de las dendritas que se desarrollan en la vejez. Tambin en los senescentes se modifica la estructura neuronal interna; esto se ha estudiado especialmente en neuronas del hipocampo u otras reas involucradas en el proceso de aprendizaje y memoria. En etapas avanzadas de la vida, se ha encontrado que estas neuronas suelen llenarse con verdaderos
329
manojos de filamentos proteicos llamados ovillos neurifibrilares. Adems, en la enfermedad de Alzheimer, estos ovillos son muy abundantes y se cree que contribuyen a la demencia que acompaa a esta enfermedad; sin embargo, no est claro el significado de las pequeas cantidades que se han encontrado en el cerebro viejo sano. Otras veces, el citoplasma neuronal se llena de grnulos que contienen lipofucsina, que es un pigmento fluorescente. Se cree que este pigmento deriva de membranas intracelulares ricas en lpidos que han sido digeridos en forma incompleta. En la vejez tambin se alteran las clulas gliales; los astrocitos fibrosos aumentan en nmero y tamao despus de los 60 aos de edad. No se conocen las consecuencias de esta proliferacin celular, pero se postula que estas clulas gliales podran liberar factores que promuevan el crecimiento neuronal; as, su proliferacin significara otro intento del tejido nervioso por compensar la disminucin gradual en el nmero de neuronas y las modificaciones estructurales que limitan su funcionamiento. Otros cambios seniles se observan en los espacios interneuronales; se ha observado en animales y en el ser humano que, especialmente en el hipocampo y corteza cerebral, se acumulan en los espacios extraneuronales unos depsitos esfricos que se han denominado placas seniles. Presentan desarrollo lento y son acmulos de una protena amiloide beta. Tambin se deposita esta protena en los vasos sanguneos de las zonas enceflicas mencionadas, y en las meninges. An no est determinado el origen celular de estos depsitos proteicos y cmo afectan a las neuronas vecinas. Tambin en la enfermedad de Alzheimer se produce un aumento dramtico de depsitos de protena amiloide beta. Se han propuesto diversas teoras para explicar el envejecimiento; una de ellas se refiere a alteraciones que podra experimentar el ADN, especialmente el de los cromosomas del ncleo. En el caso de afectar al ADN mitocondrial, podran producirse protenas alteradas. Si bien el ADN nuclear es ms
330
susceptible de dao, el ADN mitocondrial est ms expuesto a la accin de los radicales libres. Estos son compuestos oxigenados reactivos, producto de las reacciones por las cuales las mitocondrias producen energa; tambin se producen en respuesta a radiaciones ionizantes. Los radicales libres oxidan a las molculas, alterndolas. Se ha demostrado que diversas protenas se alteran con la edad; por ejemplo, aumentan los niveles de protenas oxidadas en la piel y en el cerebro; en ratas muy viejas, hasta un 50 % de las protenas pueden alterarse por oxidacin. Tal vez sean las enzimas las protenas que ms repercuten en las funciones celulares al ser oxidadas; as, se ha demostrado que la edad determina una disminucin de la citocromo-oxidasa en el cerebro de ratas, enzima que participa en la cadena respiratoria celular. Tambin disminuyen otras enzimas (como la catalasa y la superxido-dismutasa) que normalmente inactivan radicales libres y defienden contra dao oxidativo a diversos tipos de molculas. Experimentos interesantes al respecto han desarrollado Carney y Floyd, que proporcionan cierta evidencia con respecto a que las oxidaciones de protenas ocasionaran prdida de algunas funciones cerebrales. Ellos administraron N tert butyl alfa phenilnitrona a gerbos viejos; esta sustancia disminuye los procesos oxidativos, con lo cual disminuy en estos roedores el nivel de protenas oxidadas; se encontr que las actividades enzimticas aumentaban a los niveles normales de animales jvenes; la detencin del tratamiento determin una vuelta de las protenas oxidadas a los niveles de animales senescentes. En todos los casos, los efectos conductuales se midieron controlando la habilidad de los animales para recorrer laberintos y sortear su camino con xito. La vejez provoca tambin modificaciones de molculas no proteicas, como los lpidos de las membranas celulares, debido a oxidacin destructiva por radicales libres. Se alteran, por ejemplo, las vesculas sinpticas y la mielina. Ello significa que se alteran negativamente las funciones que dependen de la indemnidad de estas estructuras, como el almacenamiento de neurotransmisores y la velocidad de transmisin de impulsos, respectivamente.
331
La multiplicidad de cambios que se producen en el sistema nervioso en la vejez permiten explicarse las limitaciones y trastornos psicolgicos y fisiolgicos que acompaan a la edad senescente, a la vez que el anlisis de sus causas puede constituir una base cientfica de la prevencin de muchas de las alteraciones. Lenguaje. Todos los animales se comunican entre s; las hormigas lo hacen mediante seales qumicas, algunos peces por seales elctricas, las aves mediante cantos, las abejas por danzas. El ser humano posee la caracterstica nica del lenguaje articulado y escrito; no obstante, comparte tambin con los animales el lenguaje corporal. El lenguaje corporal humano permite expresar los estados emocionales, as como enfatizar el lenguaje articulado; especial importancia tienen la expresin facial, la actitud corporal, el lenguaje de las manos y eventualmente de la mirada. El ser humano posee lenguaje articulado gracias a la existencia de dos tipos de estructura, a saber: un aparato fonador y centros cerebrales de lenguaje. El aparato fonador est constitudo por la laringe y las cuerdas vocales, el aparato bucal que incluye la lengua, los maxilares y los dientes, y el aparato respiratorio, que al movilizar el aire hace vibrar las cuerdas vocales. Papel importante lo desempea la saliva, que al lubricar la cavidad oral, permite que la lengua se deslice fcil y rpidamente para emitir slabas y palabras. A su vez, tanto la cavidad oral como los senos maxilares y frontal actan como resonadores que amplifican el sonido. Las reas cerebrales de lenguaje, localizadas en ambos hemisferios, tienen en la mayora de los individuos (95 %) predominio izquierdo; es este predominio el que determina la
332
dominancia hemisfrica. Para hablar, leer, escribir y entender el lenguaje, estas reas deben estar comunicadas con las cortezas visual y auditiva, as como con los sistemas motores que controlan el movimiento mandibular y de la lengua. Para determinar el rea dominante del lenguaje se ha utilizado el test de Wada; consiste en inyectar en una de ambas arterias cartidas, izquierda o derecha, un anestsico de accin fugaz,mientras se mantiene al individuo realizando un conteo verbal; si ste se detiene por efecto del anestsico, significa que se anestesi el rea dominante del lenguaje. Las dos reas cerebrales involucradas en el lenguaje son las de Broca y de Wernicke. El rea de Broca se encuentra localizada en el lbulo frontal y se le denomina el rea motora del lenguaje, por cuanto controla la articulacin de palabras. Cuando se lesiona el rea de Broca, el individuo emite los vocablos con dificultad, es decir, presenta disartria o dificultad para articular palabras; su lenguaje es pobre y emite las palabras con gran esfuerzo. Pero no tiene problemas para comprender el lenguaje hablado o el escrito; tampoco se afectan las habilidades musicales, ya que el individuo puede cantar canciones familiares fluidamente. Al trastorno por lesin del rea de Broca se le denomina afasia expresiva y la disartria puede llegar a la anartria. El rea de Wernicke est localizada en el lbulo temporal y se le denomina el rea de la comprensin del lenguaje, tanto hablado como escrito. Su lesin produce un lenguaje semnticamente aberrante, es decir, falto de contenido; el individuo no comprende lo que se le dice ni lo que lee, y sus frases carecen de significado. Esta afasia se denomina receptiva, debido a que presenta dificultad en la apreciacin del significado de las palabras habladas o escritas. Ambas reas se encuentran conectadas mediante el fascculo arqueado; si ste se destruye, se produce una afasia de
333
tipo Wernicke. En la corteza motora de ambos hemisferios se encuentran las reas respectivas que comandan la actividad motora de mandbula, labios y lengua; su lesin produce afasia transitoria, de recuperacin ms bien pronta. Tambin el tlamo est involucrado en el lenguaje; su lesin, en el pulvinar por ejemplo, produce efectos extraos y variados, como ser incoherencias o cambio de nombre a los objetos. Wernicke postul algunos fenmenos tericos con respecto a la elaboracin del lenguaje. Plante que el rea de Broca, por su proximidad con la corteza motora, desarrolla programas para la coordinacin de los movimientos de la diccin. En cambio, el rea de Wernicke, ubicada cerca del rea auditiva, tiene importancia en la comprensin del lenguaje articulado. El lenguaje escrito recibe su informacin sensorial en la corteza visual; de aqu pasa al rea de Wernicke por medio del giro angular. Es por ello que las lesiones del rea de Wernicke alteran tanto la comprensin del lenguaje articulado como del escrito. Y adems, como el lenguaje tiene predominio izquierdo, los mensajes visuales recibidos en el hemisferio visual derecho, pasan a travs del cuerpo calloso desde un giro angular al otro. Dominancia Hemisfrica. Se considera como hemisferio globalmente dominante a aqul en que el rea de lenguaje es dominante. Sin embargo, los hemisferios cerebrales tienen sus propias especializaciones; cada uno tiene sus propias ideas, pensamientos y habilidades, as como funciones parecidas pero separadas. Como ambos hemisferios se encuentran ampliamente intercomunicados, especialmente por el cuerpo calloso o gran comisura cerebral, habitualmente no hay indicios de lateralizacin cerebral, pues la informacin pasa rpidamente de un hemisferio al otro. En el ser humano, el cuerpo calloso tiene unos 200 millones de fibras que interconectan ambos hemisferios.
334
En relacin con las funciones sensitivas y motoras, cada hemisferio se relaciona con la mitad contralateral del cuerpo. En el caso de la sensibilidad, ello se debe al cruce de la mayora de las vas sensitivas como el lemnisco medial, el lemnisco trigeminal, ambos fascculos espinotalmicos y un fascculo espinocerebeloso. En relacin con la funcin motora, las principales vas son tambin cruzadas. A este respecto, se ha podido determinar por ejemplo, que los individuos zurdos (10 % de los seres humanos) tienen un predominio de su rea motora derecha, y en cambio los individuos diestros, presentan un predominio motor cerebral izquierdo. Se ha determinado que la dominancia hemisfrica tiene un origen gentico. Un gen determina cul va a ser el hemisferio dominante, siendo el alelo para el hemisferio no dominante. Un segundo gen determina si la dominancia motora ser contralateral o ipsilateral con el hemisferio del lenguaje, que es el dominante, siendo alelo recesivo el ipsilateral. Elaboracin de Pensamiento. Inteligencia. El pensamiento se elabora a partir del lenguaje y de elementos guardados como engrama, lo que permite aumentar la profundidad y el concepto abstracto de las ideas. An cuando no se conocen los mecanismos neurales ntimos del pensamiento, s se han determinado algunas reas corticales que participan en l, como son las reas frontales y prefrontales, zonas temporales y el rea interpretativa general. Como en el desarrollo de pensamiento tienen gran importancia los elementos mnmicos, en realidad toda zona cortical que mantiene engramas especialmente de sensopercepcin, participan en esta compleja funcin. Tal vez de ello deriva la importancia del rea interpretativa general (AIG), ubicada en la confluencia de los lbulos parietal, temporal y occipital. Por ltimo, cabe sealar que en el concepto de inteligencia se considera tanto la capacidad intelectual como el criterio. Si
335
bien de difcil definicin, podra decirse que la inteligencia es la capacidad para resolver dificultades utilizando la lgica y el pensamiento crtico. Por otra parte, el criterio es la capacidad de actuar adecuadamente a las circunstancias. Estos conceptos, especialmente el de inteligencia, estn siendo objeto de diversas modificaciones, cuyo anlisis sobrepasa los objetivos de este texto, y que se manifiestan en la teora de las inteligencias mltiples.
VI.- BIBLIOGRAFIA. Allen, L.S. y Gorsky, R.A. Sexual orientation and the size of the anterior commissure in the human brain. Documentos de la Academia Nacional de Ciencias 89: 7199-7202; 1992
336
Bustamante, Jairo Neuroanatoma funcional. Fondo Educativo Interamericano, S.A. 1978. Cameron, Heather: Nacimiento Cientfico 212, Mayo 2000. de las neuronas. Mundo
Carlson, Neil R. Fisiologa de la conducta. Editorial Ariel S.A. Barcelona, 1998. Davidson, J.M. Hormones and sexual behavior in the male. Neuroendocrinology, edit by D.T. Krieger and J.C. Hughes. Sunderland, Mass.:Sinauer Associates, 1980 Daz, Gabriela: Drogadiccin. Ediciones Universidad Las Condes, Santiago, Chile, 1996. Daz, Gabriela. Sistema nervioso: Estructura y funcin Ediciones Universidad Gabriela Mistral, Santiago, Chile, 1989. .
Florez, Jess: Farmacologa Humana. 3a edicin. Masson S.A. 1999. Garca-Velasco,J. y Mondragn,M.: The incidence of the vomeronasal organ in 1000 human subjects and its possible clinical significance. Journal of Steroid Biochemistry and Molecular Biology 39:561-563; 1991. Kandel, Eric R., Schwartz, James H. Y Jessell, Thomas M. Neurociencia y conducta. Prentice Hall, Espaa, 1998. Koopman, P., Gubbay, J., Vivian, N., Goodfellow, P.N. y LovellBadge, R.: Male development of chromosomally female mice transgenic for SRY. Nature 351: 117- 121; 1991. Knebelmann,B., Boussin, L., Guerrier,D., Legeai, L.,Kahn,A., Josso, N. y Picard, J.: Anti-Mllerian hormone Bruxlles: a non-sense mutation associated with the persistent Mellerian duct syndrome Documentos de la Academia Nacional de Ciencias, EUA, 88: 3767-3771; 1991.
337
LeVay, S.A.: A difference in hypothalamic structure between heterosexual and homosexual men Science 253: 1034-1037; 1991. Malsbury, C.W.: Facilitation of male rat copulatory behavior by electric stimulation of the medial preoptic area. Physiology and Behavior 7: 797-805; 1971. McClintock,M.K. Menstrual synchrony and suppression. Nature 229: 244-245; 1971 Morrell, M.J.: Sexual dysfunction in epilepsy. Epilepsia 32: S38S45; 1991 Nestler, Eric J. y Malenka, Robert C. : El cerebro adicto. Investigacin y Ciencia, Mayo 2004. Represa, Alfonso y Arsenijevic, Yvan: Los orgenes de las neuronas en el adulto. Mundo cientfico 212, Mayo 2000. Rosenzweig, Mark R. Y Leiman, Arnold L. Psicologa Fisiolgica. McGraw-Hill, Espaa, 1992. Rosser, A.E. y Keverne, E.B.: The importance of central noradrenergic neurons in the formation of an olfactory memory in the prevention of pregnancy block. Neuroscience 16: 1141-1147; 1985. Russell, M.J.,Switz, G.M. y Thompson, K.: Olfactory influences on the human menstrual cycle. Asociacin estadounidense para el estudio de la ciencia, San Francisco, Junio de 1977. Swaab, D.F. y Hofman, M.A.: An enlarged suprachiasmatic nucleus in homosexual men Brain Research 537: 141-148; 1990. Wysocki, C.J., Katz, Y. and Bernhard, R.: The male vomeronasal organ mediates female- induced testosterone surges. Biology of Reproduction 28: 917-922; 1983.
338
También podría gustarte
- DiencefaloDocumento15 páginasDiencefaloAddy GonzalezAún no hay calificaciones
- Tema 11 Derivados GerminativosDocumento11 páginasTema 11 Derivados GerminativosAle Pedraza Milos100% (1)
- Desarrollo Embrionario Del Sistema Nervioso 2014Documento5 páginasDesarrollo Embrionario Del Sistema Nervioso 2014Lily Del Valle Herrera100% (1)
- Guia Area de AsociacionDocumento2 páginasGuia Area de Asociacionalejandro gutierrez100% (2)
- MesencefaloDocumento6 páginasMesencefaloAlejandra HernándezAún no hay calificaciones
- ÁREAS DE BRODMAN - TerminarDocumento5 páginasÁREAS DE BRODMAN - TerminarCarola AilínAún no hay calificaciones
- Neurofisiologia de La VisionDocumento49 páginasNeurofisiologia de La VisionLina Marcela FierroAún no hay calificaciones
- Fisiologia SensorialDocumento12 páginasFisiologia SensorialJesus Vilchez100% (1)
- Puente de VarolioDocumento10 páginasPuente de VarolioAndi VinsmokeAún no hay calificaciones
- Áreas de BrodmannDocumento30 páginasÁreas de Brodmanngenprogeria100% (2)
- EVALUAR Recordar y Evaluar Los Pares Craneales FácilmenteDocumento4 páginasEVALUAR Recordar y Evaluar Los Pares Craneales FácilmenteMabel FreixesAún no hay calificaciones
- NEURODESARROLLO DE ETAPAS EDUCATIVAS - Pilar PDFDocumento85 páginasNEURODESARROLLO DE ETAPAS EDUCATIVAS - Pilar PDFKellytaTqm100% (2)
- Configuración Interna Del Bulbo RaquídeoDocumento4 páginasConfiguración Interna Del Bulbo RaquídeoCami GonzalezAún no hay calificaciones
- Apuntes de NeuroanatomiaDocumento157 páginasApuntes de NeuroanatomiaMauricio Escobar Castañeda100% (1)
- Pares Craneanos - NeuroanatomiaDocumento18 páginasPares Craneanos - NeuroanatomiaYasmidMayorgaAún no hay calificaciones
- Histologia SNCDocumento50 páginasHistologia SNCcarlos david gonzález troconisAún no hay calificaciones
- TEMA 15 - Corteza CerebralDocumento11 páginasTEMA 15 - Corteza Cerebraledu_alimania100% (24)
- Neuroanatomia Clínica de Nava SeguraDocumento212 páginasNeuroanatomia Clínica de Nava Seguraapi-3710666100% (15)
- Principios de Nueroanatomia FuncionalDocumento109 páginasPrincipios de Nueroanatomia Funcionalysa03048149100% (4)
- Reflejos PrimitivosDocumento12 páginasReflejos PrimitivosMaherbel100% (2)
- Sistema Vestibular PeriféricoDocumento30 páginasSistema Vestibular PeriféricoMili SanabríaAún no hay calificaciones
- Senos VenososDocumento34 páginasSenos VenososSebastian Salvador100% (1)
- Cerebro, Cognición y MatematicasDocumento34 páginasCerebro, Cognición y MatematicascocarinAún no hay calificaciones
- Unidad 2. Histología y OrganigrafíaDocumento20 páginasUnidad 2. Histología y OrganigrafíaAlex Rivera100% (1)
- El Tálamo y Sus ConexionesDocumento35 páginasEl Tálamo y Sus ConexionesJonathan Ovando67% (3)
- Pares CranealesDocumento45 páginasPares CranealesConstanza Paz González100% (1)
- Conceptos Basicos de Neurociencias 2016Documento17 páginasConceptos Basicos de Neurociencias 2016mariozappaAún no hay calificaciones
- 11 Via Piramidal y ExtrapiramidalDocumento46 páginas11 Via Piramidal y ExtrapiramidalGiancarlo MoyaAún no hay calificaciones
- Vía PiramidalDocumento4 páginasVía PiramidalGonzalo Medina100% (1)
- Ganglios AutónomosDocumento4 páginasGanglios AutónomosFlory DonisAún no hay calificaciones
- Arco ReflejoDocumento34 páginasArco ReflejoCarmen AndradeAún no hay calificaciones
- Desarrollo Del Sistema Nervioso CentralDocumento28 páginasDesarrollo Del Sistema Nervioso CentralKaterine BurbanoAún no hay calificaciones
- Exposicion de Lobulo ParietalDocumento12 páginasExposicion de Lobulo ParietalGabriela Santillan100% (1)
- Guia de Neuroanatomia URP - Dr. EnriquezDocumento67 páginasGuia de Neuroanatomia URP - Dr. EnriquezHinO - Arturo100% (2)
- HipotalamoDocumento4 páginasHipotalamoIrvin Mtz AristaAún no hay calificaciones
- Anatomía Tema 6Documento8 páginasAnatomía Tema 6gabiis1512Aún no hay calificaciones
- Neurorradiologia PediatricaDocumento123 páginasNeurorradiologia PediatricaTio Alf Eugenio100% (1)
- Esquema Funcionamiento Areas de Aprendizaje Del CerebroDocumento2 páginasEsquema Funcionamiento Areas de Aprendizaje Del CerebroEsttelitta100% (1)
- Sistema Nervioso CentralDocumento20 páginasSistema Nervioso CentralA̶g̶u̶s̶t̶i̶n̶ V̶a̶l̶d̶e̶z̶Aún no hay calificaciones
- Derivados Del EctodermoDocumento54 páginasDerivados Del EctodermoHinO - Arturo67% (3)
- Alteraciones de La Conciencia PDFDocumento5 páginasAlteraciones de La Conciencia PDFcesar100% (1)
- Anatomia Del Sistema NerviosoDocumento23 páginasAnatomia Del Sistema Nerviosoprofe999Aún no hay calificaciones
- Replicación Del ADNDocumento3 páginasReplicación Del ADNRuben QuispheAún no hay calificaciones
- 35 Estimulacion TempranaDocumento18 páginas35 Estimulacion Temprana13kakak13Aún no hay calificaciones
- Cavi Dad Oral y DientesDocumento37 páginasCavi Dad Oral y DientesAlan Ala AndresAún no hay calificaciones
- Embriologia Sistema NerviosoDocumento53 páginasEmbriologia Sistema NerviosoJaime QuimbayAún no hay calificaciones
- El Sistema Nervioso Desde La ConcepcionDocumento53 páginasEl Sistema Nervioso Desde La ConcepcionALEJANDRO OSTOIC ROZZI100% (1)
- Versión TAPQOLDocumento2 páginasVersión TAPQOLKatherine PucoAún no hay calificaciones
- Gnosias Final 1 EdadesDocumento31 páginasGnosias Final 1 EdadesDayana ErazoAún no hay calificaciones
- Bases Del Neurodesarrollo PDFDocumento182 páginasBases Del Neurodesarrollo PDFgemma galvezAún no hay calificaciones
- 8.conciencia y Atencion Psicologia MedicaDocumento69 páginas8.conciencia y Atencion Psicologia MedicaArmando CcosiAún no hay calificaciones
- Sistema Nervioso Neurona y Glias 9Documento19 páginasSistema Nervioso Neurona y Glias 9Hernán FernándezAún no hay calificaciones
- BertaIsabelEstradaReyes - Tarea Unidad III Semana 1 - HUEHUEDocumento11 páginasBertaIsabelEstradaReyes - Tarea Unidad III Semana 1 - HUEHUEAndrea VillatoroAún no hay calificaciones
- ZoologiaDocumento6 páginasZoologiagonzalo CHINOAún no hay calificaciones
- Informe Desarrollo de Las Capas Embrionarias y Tubo Neural - Semana2Documento12 páginasInforme Desarrollo de Las Capas Embrionarias y Tubo Neural - Semana2Laura MarAún no hay calificaciones
- Universidad para El Desarrollo Andino Facultad Humanidades Y Ciencias SocialesDocumento43 páginasUniversidad para El Desarrollo Andino Facultad Humanidades Y Ciencias SocialesJhakilin m Huacho JanampaAún no hay calificaciones
- Capítulo 1. Resumen. FinalDocumento9 páginasCapítulo 1. Resumen. FinalVera DelacroixAún no hay calificaciones
- Derivados de Las Capas EmbrionariasDocumento12 páginasDerivados de Las Capas EmbrionariasAbigail Anjeli Jaco Inga100% (1)
- Embriologia e Histologia Bucal EnaoDocumento239 páginasEmbriologia e Histologia Bucal EnaoGermanLoopezzAún no hay calificaciones
- Trabajo ShereDocumento11 páginasTrabajo ShereMini moto 46Aún no hay calificaciones
- Black Sabbath y El Cronotopo Del Carnaval. Bianca Natascha Pérez GonzálezDocumento9 páginasBlack Sabbath y El Cronotopo Del Carnaval. Bianca Natascha Pérez GonzálezMarijoAún no hay calificaciones
- Guia Del Docente de Lengua y Literatura de Segundo GradoDocumento208 páginasGuia Del Docente de Lengua y Literatura de Segundo GradoPaulo Sixto Huaraca Caisaguano70% (10)
- Comunidad Ética en HusserlDocumento12 páginasComunidad Ética en HusserlRodrigoVásquezAlarcónAún no hay calificaciones
- Uni 2013-2 - Solucionario Razonamiento Verbal AduniDocumento12 páginasUni 2013-2 - Solucionario Razonamiento Verbal AduniChristian T. HornaAún no hay calificaciones
- IDEA Inventario Espectro Autista Angel RiviereDocumento19 páginasIDEA Inventario Espectro Autista Angel RiviereMirta CuomoAún no hay calificaciones
- VYGOTSKY, Pensamiento y LenguajeDocumento9 páginasVYGOTSKY, Pensamiento y LenguajeEdzon MaldonadoAún no hay calificaciones
- Análisis de Texto - La AntigüedadDocumento4 páginasAnálisis de Texto - La AntigüedadFran Aguirre0% (1)
- Planifico Un Mapa MentalDocumento5 páginasPlanifico Un Mapa MentalMaritza Rodriguez100% (1)
- Sobre El HumanismoDocumento1 páginaSobre El HumanismoJuanAún no hay calificaciones
- Que Onda Con Los ChavosDocumento2 páginasQue Onda Con Los ChavosLau CorzoAún no hay calificaciones
- Enfoque Neuropsicológico de La MotivaciónDocumento17 páginasEnfoque Neuropsicológico de La Motivaciónsahid jordan100% (1)
- Carpeta de Recuperacion Ept 3ros 2022 - 2023 FaltaDocumento28 páginasCarpeta de Recuperacion Ept 3ros 2022 - 2023 FaltaJose Luis Santa CruzAún no hay calificaciones
- Exp. 00756-2018-0-0901-JR-LA-01 - Anexo - 22943-2019 PDFDocumento17 páginasExp. 00756-2018-0-0901-JR-LA-01 - Anexo - 22943-2019 PDFAnonymous 2TNnoU7Aún no hay calificaciones
- Guia Tematica de LenguajeDocumento107 páginasGuia Tematica de LenguajeAnonymous etW8Yv3S1Aún no hay calificaciones
- Guìa Verbal, No Verbal y para Verbal.Documento9 páginasGuìa Verbal, No Verbal y para Verbal.Araceli Nuñez ChaveraAún no hay calificaciones
- DessarrolloDocumento13 páginasDessarrollojose luis86% (7)
- Caso EllenDocumento13 páginasCaso EllenPepe Huatuco Camarena100% (1)
- Trabajo en EquipoDocumento13 páginasTrabajo en EquipoEduardo TomasAún no hay calificaciones
- Aristoteles 12Documento6 páginasAristoteles 12Diego PaniAún no hay calificaciones
- Tecnicas de La Entrevista PsicologicaDocumento19 páginasTecnicas de La Entrevista PsicologicaAnnytza Hernández De Abreu0% (2)
- 1.1 Plan Curricular Anual 5Documento7 páginas1.1 Plan Curricular Anual 5Arturo RosalesAún no hay calificaciones
- Crismely Espinal Diaz Practica Apa PDF Actividad 2 Unidad 2Documento8 páginasCrismely Espinal Diaz Practica Apa PDF Actividad 2 Unidad 2crismelyespinaldiaz1Aún no hay calificaciones
- Liderazgo y Pueblos Indígenas PDFDocumento8 páginasLiderazgo y Pueblos Indígenas PDFSoledad CarrascoAún no hay calificaciones
- Su Primera Reunion CodaDocumento2 páginasSu Primera Reunion CodaNat Rivera100% (1)
- Clase 8Documento3 páginasClase 8Nikol Paz Belen Castillo CaniulaoAún no hay calificaciones
- 4 - Guias de Aprendizaje Legislacion LaboralDocumento4 páginas4 - Guias de Aprendizaje Legislacion LaboralEuniceSoteloGuevaraAún no hay calificaciones
- Platón en La Caverna. Una Lectura Peirceana Del Mito PDFDocumento15 páginasPlatón en La Caverna. Una Lectura Peirceana Del Mito PDFElisabet SchlegelAún no hay calificaciones
- Miguel Ayllon-Auto EvaluacionDocumento1 páginaMiguel Ayllon-Auto EvaluacionAYLLON PARRAGA MIGUEL ANGELAún no hay calificaciones
- Cuadro Comparativo Clasico-OperanteDocumento3 páginasCuadro Comparativo Clasico-OperanteDayana Alfonso100% (1)
- Clases Ética 2023 - ConiDocumento161 páginasClases Ética 2023 - ConiGonzalo RivasAún no hay calificaciones