Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Aritmética Química
Cargado por
Santiago Ivan Pascual Panduro57%(7)57% encontró este documento útil (7 votos)
2K vistas33 páginasEste documento proporciona información sobre conceptos químicos fundamentales como masa atómica, masa molecular, mol y composición porcentual. Explica cómo calcular la masa molecular de compuestos usando las fórmulas químicas y pesos atómicos. También describe cómo determinar el número de moles, moléculas y átomos en una cantidad dada de una sustancia.
Descripción original:
Título original
ARITMÉTICA QUÍMICA
Derechos de autor
© © All Rights Reserved
Formatos disponibles
PDF, TXT o lea en línea desde Scribd
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoEste documento proporciona información sobre conceptos químicos fundamentales como masa atómica, masa molecular, mol y composición porcentual. Explica cómo calcular la masa molecular de compuestos usando las fórmulas químicas y pesos atómicos. También describe cómo determinar el número de moles, moléculas y átomos en una cantidad dada de una sustancia.
Copyright:
© All Rights Reserved
Formatos disponibles
Descargue como PDF, TXT o lea en línea desde Scribd
57%(7)57% encontró este documento útil (7 votos)
2K vistas33 páginasAritmética Química
Cargado por
Santiago Ivan Pascual PanduroEste documento proporciona información sobre conceptos químicos fundamentales como masa atómica, masa molecular, mol y composición porcentual. Explica cómo calcular la masa molecular de compuestos usando las fórmulas químicas y pesos atómicos. También describe cómo determinar el número de moles, moléculas y átomos en una cantidad dada de una sustancia.
Copyright:
© All Rights Reserved
Formatos disponibles
Descargue como PDF, TXT o lea en línea desde Scribd
Está en la página 1de 33
ARITMTICA QUMICA
Cmo determinamos la masa
molecular de un compuesto?
Qu es un peso-frmula?
Cmo determinamos el nmero
de moles de una sustancia?
QU PORCENTAJE DE CARBONO HAY EN UN MOL
DE GAS PROPANO (C
3
H
8
)?
LOGRO ESPECFICO:
Al finalizar la sesin, el estudiante resuelve ejercicios y
problemas relacionados a las unidades de masa
atmica, masa molecular , mol y composicin porcentual
haciendo uso de las frmulas qumicas y de los pesos
atmicos de los elementos qumicos, en base a la
interpretacin del problema, fundamentacin e
interpretacin de sus resultados.
UNIDADES QUMICAS DE MASA
Es la masa de un tomo,
expresada en unidad de masa
atmica (u.m.a.).
Es la suma de la masa de
protones y neutrones de un
solo tomo.
Masa Atmica
MASA ATMICA PROMEDIO
Se multiplica la masa de cada istopo por su abundancia y
se suman los productos.
Masa atmica promedio = mifi
mi : masa de los istopos
fi: fraccin porcentual de abundancia
Viene a ser la suma de las masas de los tomos
correspondientes a una frmula.
MASA MOLECULAR
Ejemplo:
La frmula del agua es H
2
O.
Su masa molar ser:
(2 x 1.008) + (1 x 15.99)= 18.006 g
EJEMPLOS
Acido Sulfrico : H
2
SO
4
Su masa molar :
(2x1,008) + (1x32,06) + (4x15,99)= 98,036 g.
Hidrxido de Calcio : Ca(OH)
2
Su masa molar:
(1 x 40,08) + 2(15,99 + 1,008) = 74,076 g
MOL
Es la cantidad de una sustancia que contiene tantas
entidades elementales como tomos hay en 12 g de
carbono.
Cuando se usa mol las entidades elementales deben ser
establecidas como: tomos, molculas, iones, electrones,
etc.
El nmero de Avogadro (6,022 X 10
23
) que seala el
nmero de entidades elementales que estn contenidas en
un mol.
EJEMPLOS:
Un mol de tomos de Carbono - 12 tiene una
masa de 12g.
Un mol de tomos de O tiene una masa de
16,00 g.
Un mol de molculas de O2 tiene 32,00g.
Un mol de iones Cloro tiene una masa atmica
de 35,45g.
es la cantidad de sustancia existente en un
mol de la misma.
NMERO DE MOLES
N de moles (n) = Masa total de sustancia (g)
Masa molar (g/mol)
MASA MOLAR
Es la masa en gramos de un mol de sustancia.
La masa molar de tomos de hidrgeno es la masa de 1
mol de tomos de Hidrgeno, la cual es 1,008 g/mol.
La masa molar de molculas de Hidrgeno, es la masa de
un mol de molculas de Hidrgeno, H2, es decir (2x 1,008)
= 2,016 g/mol.
NMERO DE AVOGADRO
Indica el nmero de partculas que hay en un mol de
cualquier entidad fundamental y es 6,022 x10
23
. Tambien
representa el nmero de tomos en x gramos de
cualquier sustancia, siendo x la masa molar de la
sustancia.
1 mol = 6,022 x10
23
partculas
Por lo tanto:
1 mol de tomos = 6,022 x10
23
tomos
1 mol de molculas = 6,022 x10
23
molculas
1 mol de ines = 6,022 x10
23
ines
CONCEPTO DE MOL APLICADO A ELEMENTOS
El nmero de tomos en 1 mol de cualquier elemento se
llama el Nmero de Avogadro y es igual a 6.022x10
23
.
1 mol de cualquier elemento es una muestra del
elemento con una masa en gramos igual a la masa
atmica de ese elemento.
Ejemplos
1 mol Na = 22.99 g Na = 6,022x10
23
tomos Na
1 mol Ca = 40.08 g Ca = 6,022x10
23
tomos Ca
1 mol S = 32.07 g S = 6,022x10
23
tomos S
CONCEPTO DE MOL APLICADO A
COMPUESTOS
El nmero de molculas en 1 mol de cualquier compuesto
se llama el nmero de Avogadro y es igual a 6.022x10
23
.
1 mol de cualquier compuesto es una muestra del
compuesto con una masa en gramos igual a la masa
molecular de ese compuesto.
Ejemplos
1 mol H
2
O = 18,02 g H
2
O = 6,022x10
23
molculas H
2
O
1 mol CO
2
= 44,01 g CO
2
= 6,022x10
23
molculas CO
2
1 mol NH
3
= 17,03 g NH
3
= 6,022x10
23
molculas NH
3
EL MOL Y LOS CLCULOS QUMICOS
El concepto de MOL se puede utilizar para obtener
factores de conversin tiles en clculos qumicos
que relacionan elementos y compuestos.
Para elementos: ejemplo calcio Ca
1 mol Ca = 40,08 g Ca = 6,022x10
23
atomos de Ca
23
1 mol Ca 40.08 g Ca
40.08 g Ca 6.022 10 Ca atoms
EL CONCEPTO DE MOL SE PUEDE APLICAR A LAS
MOLCULAS PARA CALCULAR LA MASA MOLECULAR.
Ejemplo : compuesto H
2
O
1 mol de una molcula de H
2
O = 2 moles de tomos
de H y 1 mol de tomos de O
Masa molar (g) H
2
O = 2 moles H (1,008g H / 1 mol H) + 1 mol
O (16 g O / 1 mol O)
= 18,00g H
2
O)
COMPOSICIN PORCENTUAL
Es el porcentaje en masa de cada elemento
contenido en una sustancia o compuesto.
La masa molar de la sustancia o compuesto es
el 100%.
% elemento = Masa total del elemento x 100
Masa Molar
EJEMPLO 1:
Hallar la composicin porcentual de hidrgeno y oxgeno en el agua.
Solucin: Masa molar de H
2
O : 18,006 g
% H = 2,016 x 100 = 11,2 %
18,006
% O = 15,99 x 100 = 88,8 %
18,006
EJEMPLO 2
Calcular la composicin porcentual del cloruro de potasio.
Solucin:
Masa molar de KCl: 39,0 + 35,5 = 74,5 g
% K = 39,00 x 100 = 52,35 %
74,5
% Cl = 35,5 x 100 = 47,65 %
74,5
DETERMINACIN DE FRMULAS QUMICAS
A.- FRMULA SIMPLE O EMPRICA
Es una expresin que representa la proporcin mas
simple en la que estn presentes los tomos que forman
un compuesto qumico. Se considera la representacin
ms sencilla de un compuesto.
Ejemplo 1: El anlisis de muestra de un compuesto indica
que contiene un 27,3% de carbono y un 72,7 % de
oxgeno en masa. Determinar la frmula emprica de
ese compuesto.
Solucin:
Tomamos como base 100 g de compuesto, entonces
tenemos 27,3 g de Carbono y 72,7 g de Oxgeno.
Ahora hallamos el nmero de moles de cada elemento.
Moles C = 27,3 g de C x 1 mol de C = 2,275 mol C
12,0 g de C
Moles O = 72,7 g de O x 1 mol de O = 4,544 mol O
16,0 g de O
Dividimos la cantidad de moles calculados entre el
menor valor de ellos, de modo que tengamos una
relacin de nmeros enteros sencillos.
C = 2,275 = 1,0
2,275
O = 4,544 = 2,0
2,275
La frmula ser: CO
2
correspondiente al dixido de
carbono.
Ejemplo 2: Determinar la frmula emprica de un
compuesto formado por 26,6% de potasio, 35,4%
de cromo y 38,0 % de oxgeno.
Solucin:
100 g de compuesto como base.
Mol K = 26,6 g de K x 1 mol de K = 0,682 mol K
39,0 g de K
Mol Cr = 35,4 g de Cr x 1 mol de Cr = 0,680 mol Cr
52,0 g de Cr
Mol O = 38,0 g de O x 1 mol de O = 2,375 mol O
16,0 g de O
Dividimos la cantidad de moles entre el menor valor de ellos:
K = 0,682 = 1.0 Cr = 0,680 = 1,0 O = 2,375 = 3,5
0,680 0,680 0,680
Como tenemos un coeficiente con decimal, se multiplica
por un factor de tal manera que dicho coeficiente nos
resulte un nmero entero.
De la siguiente manera:
K = 1,0 x 2,0 = 2,0
Cr = 1,0 x 2,0 = 2,0
O = 3,5 x 2,0 = 7,0
La frmula ser : K
2
Cr
2
O
7
correspondiente al dicromato
de Potasio.
B.- FRMULA MOLECULAR
Indica el nmero de tomos diferentes que hay
en cada molcula. En algunos casos puede ser
la misma que la frmula emprica o sino ser un
mltiplo entero de ella.
Ejemplo 1:
Un Hidrocarburo tiene una masa molar de 42,0 g
y contiene 14,3% de H y 85,7% de C . Hallar su
frmula molecular.
Solucin:
Hallamos su frmula emprica: Tomando 100 g de
compuesto como base y hallando el nmero de moles
obtenemos 14,3 mol de H y 7,14 mol de C.
Dividiendo por la menor cantidad queda:
H = 14,3 = 2,0 , C = 7,14 = 1,0
7,14 7,14
Luego tenemos que la frmula emprica es CH
2
Adems la masa molar de la sustancia es 42.0 g. Entonces:
(CH
2
)
x
= C
x
H
2x
12X + 2X = 42 X = 3
Finalmente la frmula molecular ser : (CH
2
)
x
= (CH
2
)
3
C
3
H
6
correspondiente al Propeno.
EVALUACIN
1. Calcular la masa molecular de los siguientes
compuestos:
a. CaSO4
b. Al2(SO4)3
2. Calcular el nmero de moles en:
a. 360 gramos de aluminio
b. 8,10 kg de carbonato de calcio
3. Analizando una solucin salina se hall: 5,85% y
14,9% en peso de NaCl y KCl respectivamente.
Calcular:
a. Relacin de moles de NaCl y KCl.
b. Gramos de Cl2 en 100 gramos de solucin.
4. Calcular la composicin porcentual en:
a. Cloroformo (CHCl
3
)
b. Sulfato Ferroso
5. Determinar la frmula emprica de de un compuesto que
est formado por 62,6 % de plomo; 8,5 % de nitrgeno y 28,9
% de oxgeno.
6.Determina la frmula molecular de un compuesto que est
formado por: 83,7 % de carbono y 16,3 % de hidrgeno; si tiene
un peso molecular de 86 g.
También podría gustarte
- Aritmética QuímicaDocumento25 páginasAritmética QuímicaLizbethAún no hay calificaciones
- PRÁCTICA #4 - TerminadaDocumento12 páginasPRÁCTICA #4 - TerminadaJuan Antonio Mujica CabreraAún no hay calificaciones
- Trabajo Campo 2Documento6 páginasTrabajo Campo 2Eduardo Rodriguez Javier100% (2)
- Unidades Quimicas de Masa (Clase)Documento3 páginasUnidades Quimicas de Masa (Clase)Samuel0% (1)
- SOLUCIONARIO DEL EXAMEN PARCIAL DE QUIMICA 20202 I (4) .Docx Ver 2Documento5 páginasSOLUCIONARIO DEL EXAMEN PARCIAL DE QUIMICA 20202 I (4) .Docx Ver 2Sandro Elías CurayAún no hay calificaciones
- S10 - Hoja Taller GrupalDocumento3 páginasS10 - Hoja Taller GrupalJulissa Marianella Roncal Barrientos100% (1)
- Lab 02. Quino.Documento14 páginasLab 02. Quino.hugoAún no hay calificaciones
- Cinética y Equilibrio Químico.-Test 02Documento3 páginasCinética y Equilibrio Químico.-Test 02Diego ParedesAún no hay calificaciones
- Grupo 1 Informe de Laboratorio N5Documento7 páginasGrupo 1 Informe de Laboratorio N5Arsemio CorreaAún no hay calificaciones
- Hoja Taller Grupal #7 Aritmética QuímicaDocumento7 páginasHoja Taller Grupal #7 Aritmética QuímicaJair Salinas VargasAún no hay calificaciones
- Práctica Calificada - Estado GaseosoDocumento1 páginaPráctica Calificada - Estado GaseosoAimezinha RBAún no hay calificaciones
- Ejercicios Quimica EstequiometriaDocumento6 páginasEjercicios Quimica EstequiometriaEnmanuel De la PazAún no hay calificaciones
- Reporte Principio PascalDocumento2 páginasReporte Principio PascalJulhs Jake Pro C100% (1)
- Taller Semanal 7Documento5 páginasTaller Semanal 7Lucia CaceresAún no hay calificaciones
- Guía Laboratorio Química Orgánica UPNDocumento5 páginasGuía Laboratorio Química Orgánica UPNJorgeAún no hay calificaciones
- Estequiometria - Ore Quispe-QuimicaDocumento8 páginasEstequiometria - Ore Quispe-QuimicaAron Ore QuispeAún no hay calificaciones
- Unidad 01 - Química OrgánicaDocumento29 páginasUnidad 01 - Química OrgánicaWilliam Alexander Flores Palomino0% (1)
- Noviembre - Quimica - 1roDocumento12 páginasNoviembre - Quimica - 1roDionne BeckAún no hay calificaciones
- Diapositivas - Trabajo de CampoDocumento17 páginasDiapositivas - Trabajo de CampoLUIS SANCHEZAún no hay calificaciones
- ESTEQUIOMETRIADocumento6 páginasESTEQUIOMETRIAEdwis Castañeda VelásquezAún no hay calificaciones
- Estequiometría 1Documento7 páginasEstequiometría 1MayhuascaCristhianAún no hay calificaciones
- Laboratorio #03Documento17 páginasLaboratorio #03Almilser Marin VasquezAún no hay calificaciones
- Solucionario Concentración de Soluciones 2014-2Documento6 páginasSolucionario Concentración de Soluciones 2014-2Angela Cerquin100% (2)
- Grupo 4 - Informe de Laboratorio - P - 3 - Química Inorgánica - Wa-Cod2141Documento12 páginasGrupo 4 - Informe de Laboratorio - P - 3 - Química Inorgánica - Wa-Cod2141Luz Chavez Ruiz75% (4)
- T1 Quimica InorganicaDocumento2 páginasT1 Quimica InorganicaJosselynAún no hay calificaciones
- 3 HT - 19 2Documento5 páginas3 HT - 19 2NILTON CONDORAún no hay calificaciones
- Trabajo Campo 3Documento4 páginasTrabajo Campo 3Javier Ruiz0% (1)
- Ejercicios Aritmetica QuimicaDocumento2 páginasEjercicios Aritmetica QuimicaAldo Gonzales Chavez100% (1)
- Trabajo Campo 3Documento9 páginasTrabajo Campo 3Javier Ruiz0% (1)
- Taller Grupal Semana 1Documento5 páginasTaller Grupal Semana 1Carla MedraniAún no hay calificaciones
- Práctica #9 - ÉsteresDocumento8 páginasPráctica #9 - ÉsteresRonaldo Nuñez Calua0% (1)
- S14 Taller GrupalDocumento5 páginasS14 Taller GrupalMarco Huaripata SolteroAún no hay calificaciones
- 3-HT - 19-2 - Hoja de Trabajo 3-GRUPO 8Documento6 páginas3-HT - 19-2 - Hoja de Trabajo 3-GRUPO 8Enrique QuispeAún no hay calificaciones
- Realiza Una Lista de 7 Hidruros No Metálicos ConDocumento4 páginasRealiza Una Lista de 7 Hidruros No Metálicos ConBernardoUrrutiaDiazAún no hay calificaciones
- Funcion Oxidos BasicosDocumento4 páginasFuncion Oxidos Basicospepito floresAún no hay calificaciones
- HOJA6 Enlace QuimicoDocumento2 páginasHOJA6 Enlace QuimicoMilena Velasco AlosillaAún no hay calificaciones
- S9 Hoja de TallerDocumento5 páginasS9 Hoja de TallerMilesca ECAún no hay calificaciones
- Ejercicios de EstequiometriaDocumento8 páginasEjercicios de Estequiometrianuñezgonzalo kevinAún no hay calificaciones
- Trabajo de Campo 2 - Quimica InorganicaDocumento2 páginasTrabajo de Campo 2 - Quimica InorganicaJavier Ruiz100% (2)
- Solucionario Func Hidruros, Ácido y SalesDocumento5 páginasSolucionario Func Hidruros, Ácido y Salestkevin100% (1)
- Laboratorio 3 Upn - Reacciones Quimicas - Quimica InorganicaDocumento10 páginasLaboratorio 3 Upn - Reacciones Quimicas - Quimica InorganicaCristinaLeiva100% (1)
- TALLER GRUPAL Semana 7Documento4 páginasTALLER GRUPAL Semana 7Ailthon SareAún no hay calificaciones
- s08 Taller GrupalDocumento3 páginass08 Taller Grupalwilfredo jesus iraulaAún no hay calificaciones
- S03 - Hoja Taller GrupalDocumento5 páginasS03 - Hoja Taller GrupalDiego Jhonatan Paredes RojasAún no hay calificaciones
- QUIIN - PRÁCTICA #2 - Reconocimiento de Funciones QuímicasDocumento11 páginasQUIIN - PRÁCTICA #2 - Reconocimiento de Funciones QuímicasJhoseph Ah100% (1)
- LABORATORIO N°1 QUIMICA ORGANICA-lucasDocumento7 páginasLABORATORIO N°1 QUIMICA ORGANICA-lucasAlcántara Rodríguez Percy JohnAún no hay calificaciones
- Hoja de Taller de PràcticaDocumento4 páginasHoja de Taller de PràcticaBelén EleutAún no hay calificaciones
- Hoja de TRAJO N°3 Ecuaciones - REACCIONES QUIMICASDocumento3 páginasHoja de TRAJO N°3 Ecuaciones - REACCIONES QUIMICASLiz Marcos Carbajal100% (1)
- Lab n5 Compuestos OxigenadosDocumento35 páginasLab n5 Compuestos OxigenadosDiegoFernandoCuadraAmez100% (6)
- Cerebro Termina A ADocumento12 páginasCerebro Termina A ALucas OchoaAún no hay calificaciones
- S - 3 Práctica de AulaDocumento3 páginasS - 3 Práctica de AulaAnonymous BMlkqknbjAún no hay calificaciones
- Ejercicios Propuestos 4Documento2 páginasEjercicios Propuestos 4Jonathan Murga100% (1)
- Problemas Propuestos-1Documento2 páginasProblemas Propuestos-1Joel Orellana LopezAún no hay calificaciones
- Trabajo de Campo 3Documento2 páginasTrabajo de Campo 3Joao Coaquira50% (2)
- 6 Diap Estequiometría PDFDocumento45 páginas6 Diap Estequiometría PDFAriel Dorian100% (1)
- Ejercicio1 NomenclaturaDocumento6 páginasEjercicio1 NomenclaturaalfpimAún no hay calificaciones
- Práctica #1 - Normas de Seguridad y Primeros Auxilios en LaboratorioDocumento12 páginasPráctica #1 - Normas de Seguridad y Primeros Auxilios en LaboratorioDiego Martin Castillo AlzaAún no hay calificaciones
- Química 5to Secundaria 15Documento21 páginasQuímica 5to Secundaria 15Metade Marvel A ChAún no hay calificaciones
- Aritmética QuímicaDocumento43 páginasAritmética QuímicaAngellina Quiroz PeraltaAún no hay calificaciones
- Aritmética QuímicaDocumento43 páginasAritmética QuímicaDeyman Becerra100% (2)
- Ht-10 - Balance de MateriaDocumento2 páginasHt-10 - Balance de MateriaSantiago Ivan Pascual Panduro100% (1)
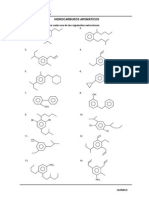
- Ht-Hidrocarburos AromáticosDocumento2 páginasHt-Hidrocarburos AromáticosSantiago Ivan Pascual Panduro50% (2)
- HT-11 Alcanos Alquenos y AlquinosDocumento4 páginasHT-11 Alcanos Alquenos y AlquinosSantiago Ivan Pascual PanduroAún no hay calificaciones
- Seminario Quimica T2Documento2 páginasSeminario Quimica T2Santiago Ivan Pascual PanduroAún no hay calificaciones
- Suelos Unidad 3. Subtema 3.1 Propiedades FísicasDocumento67 páginasSuelos Unidad 3. Subtema 3.1 Propiedades Físicaselizabeth quimisAún no hay calificaciones
- Practica 1. Microcompostaje en Botella PlásticaDocumento3 páginasPractica 1. Microcompostaje en Botella PlásticaWalter Velasquez OrjuelaAún no hay calificaciones
- Planificación 2° 2022Documento5 páginasPlanificación 2° 2022Paola Andrea Hernández PradenasAún no hay calificaciones
- Matriz de LeopoldDocumento6 páginasMatriz de LeopoldMARLENY ROCIO MIRANDA LAVADOAún no hay calificaciones
- Sergio RevahDocumento1 páginaSergio RevahJhan Carlos ZapataAún no hay calificaciones
- Flujo en Tuberías y DuctosDocumento2 páginasFlujo en Tuberías y DuctosDany Elith Chota Valera0% (1)
- Experiencia S 1Documento19 páginasExperiencia S 1Mac HargitayAún no hay calificaciones
- Leavin Groom AngelsDocumento281 páginasLeavin Groom AngelsNR100% (1)
- Práctica 3: Obtención de La Viscosidad Dinámica, Aplicando El Método de La Ley de StokesDocumento8 páginasPráctica 3: Obtención de La Viscosidad Dinámica, Aplicando El Método de La Ley de StokesAarón LeónAún no hay calificaciones
- La Contaminacion Del Aire Por Quema de MalezasDocumento39 páginasLa Contaminacion Del Aire Por Quema de MalezasAliyjhosy BarbozaAún no hay calificaciones
- Cambio de FaseDocumento7 páginasCambio de FaseEddison CalisayaAún no hay calificaciones
- Muestreo de MineralesDocumento79 páginasMuestreo de MineralesJorge Triveño HAún no hay calificaciones
- Práctica 8 Leyes de Newton XXXXDocumento5 páginasPráctica 8 Leyes de Newton XXXXBryan DarkAún no hay calificaciones
- Trabajo Monografico SismoDocumento16 páginasTrabajo Monografico Sismoraul_dekoAún no hay calificaciones
- La Verdad Sobre La Raza HumanaDocumento14 páginasLa Verdad Sobre La Raza HumanaLuis ArguelloAún no hay calificaciones
- Unidad 2 Energia Tradicional Alternativa y Fuentes en BoliviaDocumento31 páginasUnidad 2 Energia Tradicional Alternativa y Fuentes en BoliviaBeatriz Velásquez LeónAún no hay calificaciones
- Control Lectura Señor de Las MoscasDocumento2 páginasControl Lectura Señor de Las Moscasuzielx100% (2)
- Crianza Recíproca, Grimaldo Rengifo, CuestionarioDocumento15 páginasCrianza Recíproca, Grimaldo Rengifo, CuestionarioHilmar Q. SilvestreAún no hay calificaciones
- UPME-SENER - GNL Buenaventura - Entregable 2 - 1 - No Control Cambios PDFDocumento187 páginasUPME-SENER - GNL Buenaventura - Entregable 2 - 1 - No Control Cambios PDFhernanito8Aún no hay calificaciones
- Implementacion de Chimeneas Con El Metodo Vcr-HORIZONTEDocumento86 páginasImplementacion de Chimeneas Con El Metodo Vcr-HORIZONTEJorge Miguel GQ100% (2)
- Depuración de Aguas Residuales Modelización de Proceso de Lodos ActivosDocumento33 páginasDepuración de Aguas Residuales Modelización de Proceso de Lodos ActivosTatiana ArturiAún no hay calificaciones
- Taller Plataforma Grado NovenoDocumento5 páginasTaller Plataforma Grado NovenoPaula GuzmanAún no hay calificaciones
- Guia Elaborar Tesis GradoDocumento60 páginasGuia Elaborar Tesis GradoArturo OrlandoAún no hay calificaciones
- Informe CalicheDocumento21 páginasInforme CalicheMaria Yaupi100% (1)
- Seccion QuimicaDocumento16 páginasSeccion QuimicaLiam CruzAún no hay calificaciones
- Selecion de Blowers PDF FreeDocumento10 páginasSelecion de Blowers PDF Freejose RuizAún no hay calificaciones
- DIAPOSDocumento25 páginasDIAPOSjorge luisAún no hay calificaciones
- Trabajo de Titulacion CAYAPAS MATAJEDocumento136 páginasTrabajo de Titulacion CAYAPAS MATAJEMONICA PORTILLAAún no hay calificaciones
- QuímicaDocumento16 páginasQuímicasarafanola1Aún no hay calificaciones
- Ensayo Biodiversidad Jose EliasDocumento7 páginasEnsayo Biodiversidad Jose Eliaspenelope navajasAún no hay calificaciones