Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Presentación Trabajo de Química y Ciencia Ilustraciones Moléculas Verde Turquesa
Cargado por
pwnsionjwijssi0 calificaciones0% encontró este documento útil (0 votos)
8 vistas12 páginasLa tabla periódica contiene 118 elementos químicos ordenados por número atómico y agrupados en periodos según sus propiedades. El documento describe los grupos 13 y 14, conocidos como térreos y carbonoides respectivamente. Los térreos incluyen boro, aluminio, galio, indio y talio, y son metales opacos y conductores. Los carbonoides incluyen carbono, silicio, germanio, estaño, plomo y flevorio, siendo el silicio el más abundante en la corteza terrestre.
Descripción original:
Título original
Presentación trabajo de química y ciencia ilustraciones moléculas verde turquesa (1)
Derechos de autor
© © All Rights Reserved
Formatos disponibles
PPTX, PDF, TXT o lea en línea desde Scribd
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoLa tabla periódica contiene 118 elementos químicos ordenados por número atómico y agrupados en periodos según sus propiedades. El documento describe los grupos 13 y 14, conocidos como térreos y carbonoides respectivamente. Los térreos incluyen boro, aluminio, galio, indio y talio, y son metales opacos y conductores. Los carbonoides incluyen carbono, silicio, germanio, estaño, plomo y flevorio, siendo el silicio el más abundante en la corteza terrestre.
Copyright:
© All Rights Reserved
Formatos disponibles
Descargue como PPTX, PDF, TXT o lea en línea desde Scribd
0 calificaciones0% encontró este documento útil (0 votos)
8 vistas12 páginasPresentación Trabajo de Química y Ciencia Ilustraciones Moléculas Verde Turquesa
Cargado por
pwnsionjwijssiLa tabla periódica contiene 118 elementos químicos ordenados por número atómico y agrupados en periodos según sus propiedades. El documento describe los grupos 13 y 14, conocidos como térreos y carbonoides respectivamente. Los térreos incluyen boro, aluminio, galio, indio y talio, y son metales opacos y conductores. Los carbonoides incluyen carbono, silicio, germanio, estaño, plomo y flevorio, siendo el silicio el más abundante en la corteza terrestre.
Copyright:
© All Rights Reserved
Formatos disponibles
Descargue como PPTX, PDF, TXT o lea en línea desde Scribd
Está en la página 1de 12
TABLA PERIODICA
Trabajo de familias químicas
3roB
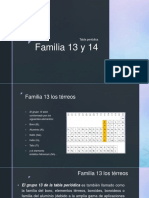
¿elementos En la actualidad se
químicos? conoce 118 elementos
químicos de la tabla
periódica. Están
ordenados por orden
creciente de números
atómicos y se agrupan en
periodos según sus
propiedades.
GRUPOS
TÉRREOS
GRUPO 13 O GRUPO IIIA
5 BORO (B) 2s²2p¹
13 ALUMINIO (Al) 3s²3p¹
31 GALIO (Ga) 3d10 4s2 4p1
49 INDIO (In) 4d10 5s2 5p1
81 TALIO (Tl) 4f14 5d10 6s2 6p1.
CARACTERÍSTICAS:
PROPIEDADES FÍSICAS PROPIEDADES QUÍMICAS
-Son opacos, de color blanco, plateado o grisáceo. -Bastante reactivos, suelen aparecer en la naturalea
-Son conductores del calor y de la electricidad. combinados con otros elementos.
-Tienen bajos puntos de fusión a excepción del -Reaccionan con los halogenos y forman haluros
boro. como tricoluro de boro o tricoluro de aluminio.
-El carácter metálico aumenta al descender en el -Tienen estado de oxidación +3 pero también +1 en
grupo. varios elementos.
-Son metales moldeables y blandos a excepción del -El boro reacciona con hidrógeno formando boranos
boro. siendo el más simple el diborano B2H6
Usos en la vida ALUMINIO
BORO Se extrae del mineral
BAUXITA, se aplica mucho
Se usa en la industria del en la industria, solo o con
GALIO
vidrio, la cerámica y para aleaciones con otros metales
fabricar semiconductores. como el cobre y el magnesio. El arseniuro de galio (Ga
As) se usa como
INDIO
TALIO semiconductor y para
Se emplea en la fabricación obtener LED (diodos
se emplea en la de aleaciones de bajo punto emisores de luz). Funde a
fabricación de artículos de fusión, su óxido se 30 grados y es junto con el
electrónicos emplea en paneles mercurio un metal líquido a
(interruptores) y en electroluminiscentes temperatura ambiente
pruebas médicas
Carbonoides
GRUPO IVA O GRUPO 14
s2 p2
(C) Carbono - 6
(Si) Silicio - 14
(Ge) Germanio - 32
(Sn) Estaño - 50
(Pb) Plomo - 82
(Fl) Flevorio - 114
Carbonoideos
Son menos reactivos que los térreos pero lo
suficientemente inestables como para no exitir en la
naturleza. El elemento químico SILICIO es uno de los
elementos mas abundantes en la corteza terrestre (28%),
con gran importancia para la sociedad a partir del siglo
XXI. Al bajar en el periodo, estos elementos van
teniendo características cada vez mas metálicas: el
carbono es un no metal, el silicio y el germanio son
semimetales, y el estaño, el plomo y el flevorio son
metales.
CARACTERÍSTICAS
GENERALES
Silicio y Germanio Carbono y derivados Carácter metálico
Se utilizan como semiconductores en
electrónica, mas en transistores para Se utilizan como combustibles y en Aumenta considerablemente
lo cual deben obtenerse muy puros. la síntesis de productos orgánicos. conforme se desciende en el
grupo, siendo el carbono no-
Silicio Plomo
Su óxido se emplea en
metal, el silicio y el germanio
fabricación de vidrios. Tradicionalmente usado en fabricación de semimetales y el estaño, el
Estaño tuberías de fontanería, está siendo plomo y el enunciativo típicos
reemplazado por el cobre y el PVC debido
Se usa para soldadura y en metales.
aleaciones con otros metales. a su toxicidad.
Método de obtención de los carbonoides
ESTAÑO
PLOMO Se obtiene del mineral
casiterita (óxido de estaño
CARBONO Se obtiene a partir de
(IV) ). Dicho mineral se
los sulfuros minerales;
En la naturaleza se muele y se enriquece en
el cual, tras un previo
encuentra como dióxido de estaño de estaño
enriquecimiento es
diamante y grafito. por flotación.
tostado y sinterizado en
un horno.
SILICIO
Obtiene como subproducto en
los procesos de obtención de
cobre, zinc y en las cenizas de
ciertos carbones.
¡Gracias por la
atención!
También podría gustarte
- ALCALINOSDocumento12 páginasALCALINOSgamiokiara011Aún no hay calificaciones
- Grupo IIIA y IVA - Equipo 3,204ADocumento9 páginasGrupo IIIA y IVA - Equipo 3,204ALux GalvezAún no hay calificaciones
- Monografia Tabla Periodica 1.2)Documento13 páginasMonografia Tabla Periodica 1.2)Olenka Salas MirandaAún no hay calificaciones
- Elementos Térreos o BoroideosDocumento5 páginasElementos Térreos o BoroideosAndrea PachecoAún no hay calificaciones
- Grupo 14 de La Tabla PeriódicaDocumento3 páginasGrupo 14 de La Tabla PeriódicaDaniel Rodriguez MuñozAún no hay calificaciones
- Informe Carbonoides Sem09Documento20 páginasInforme Carbonoides Sem09Jeampieero Gabriel Cuadros MenachoAún no hay calificaciones
- Vitreo Principales Materiales Utilizados en La Industria Materiales Cer Micos Usados en La IndustriaDocumento12 páginasVitreo Principales Materiales Utilizados en La Industria Materiales Cer Micos Usados en La IndustriaHiramRubiAún no hay calificaciones
- Familias de La Tabla PeriodicaDocumento2 páginasFamilias de La Tabla PeriodicaXDXD XDXDAún no hay calificaciones
- Metales Alcalinos-Terreos 20 - 21Documento49 páginasMetales Alcalinos-Terreos 20 - 21Juan Antonio Salazar AlarcónAún no hay calificaciones
- Informe Carbonoides Sem09Documento18 páginasInforme Carbonoides Sem09Lusbet Yaquelin NtAún no hay calificaciones
- Aleaciones No FerrosasDocumento64 páginasAleaciones No FerrosasK-nissi LuksAún no hay calificaciones
- Metalurgia Unidad 4 Metales No FerreosDocumento14 páginasMetalurgia Unidad 4 Metales No Ferreoslara240506Aún no hay calificaciones
- Alcalinos y Alcalino TerreosDocumento41 páginasAlcalinos y Alcalino TerreosAndrés Molina100% (1)
- Comercialización Del PlomoDocumento53 páginasComercialización Del PlomoJeffryCallupeReáteguiAún no hay calificaciones
- Obtención Del Plomo PBDocumento12 páginasObtención Del Plomo PBchrisriv0202Aún no hay calificaciones
- Actividad 3 Procesos PDFDocumento9 páginasActividad 3 Procesos PDFLuis Fabricio Miranda RodriguezAún no hay calificaciones
- Elementos Carbonoideos y NitrogenoideosDocumento5 páginasElementos Carbonoideos y NitrogenoideosAndrea PachecoAún no hay calificaciones
- Metales Alcalinos TerreosDocumento6 páginasMetales Alcalinos TerreosJavi OlmAún no hay calificaciones
- HIerro y Otros MetalesDocumento5 páginasHIerro y Otros Metaleslore y terryAún no hay calificaciones
- Metalurgia Del CobreDocumento32 páginasMetalurgia Del CobreSonia Chamorro ArmasAún no hay calificaciones
- Metales No FerrososDocumento15 páginasMetales No FerrososSilvanaAún no hay calificaciones
- Materiales No FerrososDocumento26 páginasMateriales No FerrososAlonso Saucedo100% (1)
- Materiales FundentesDocumento19 páginasMateriales Fundentesmadenicola10100% (3)
- Minero 2Documento19 páginasMinero 2Roy RomeroAún no hay calificaciones
- Boro Generalidades Grupo 3 ADocumento26 páginasBoro Generalidades Grupo 3 AUriel MoralexAún no hay calificaciones
- Grupo 13 Tabla PeriódicaDocumento4 páginasGrupo 13 Tabla PeriódicaMaria JaraAún no hay calificaciones
- Elementos TérreosDocumento3 páginasElementos TérreosAngel Elias Garcia CarreroAún no hay calificaciones
- TerreosDocumento41 páginasTerreosCamila SuárezAún no hay calificaciones
- Materiales No FerrososDocumento17 páginasMateriales No Ferrososalex120170Aún no hay calificaciones
- Carbonoides Por ElementosDocumento46 páginasCarbonoides Por ElementosMarlene Esther Huamani Quillas0% (1)
- La Importancia de Los Metales en Nuestra Vida y Sus Perjudicaciones de Un Uso ContinuoDocumento2 páginasLa Importancia de Los Metales en Nuestra Vida y Sus Perjudicaciones de Un Uso ContinuoDany Arrieta FloresAún no hay calificaciones
- Semana 7. Elementos de Transición DúctilesDocumento34 páginasSemana 7. Elementos de Transición DúctilesEvelin HPAún no hay calificaciones
- Familia 13 y 14 (Tabla Periodica)Documento24 páginasFamilia 13 y 14 (Tabla Periodica)Ivan Mtz HdezAún no hay calificaciones
- Elementos Del Grupo IvaDocumento11 páginasElementos Del Grupo Ivaivan1441Aún no hay calificaciones
- Exposicion Quimica InorganicaDocumento14 páginasExposicion Quimica InorganicaJose A Torres RiveraAún no hay calificaciones
- Z 39Documento32 páginasZ 39Fredy LópezAún no hay calificaciones
- Material ZirconioDocumento16 páginasMaterial ZirconioTony Garrido LiñanAún no hay calificaciones
- Presentación Conociendo La Tabla Periódica QuímicaDocumento27 páginasPresentación Conociendo La Tabla Periódica QuímicaJOHVANAAún no hay calificaciones
- Grupo de Los BoroidesDocumento17 páginasGrupo de Los BoroidesATIRO COBEÑAS ESTEBAN FELIPEAún no hay calificaciones
- Indicadores Actuales Del Estado SocioeconomicoDocumento3 páginasIndicadores Actuales Del Estado Socioeconomicomaria del rosario perezAún no hay calificaciones
- Caracteristicas de Los MineralesDocumento7 páginasCaracteristicas de Los MineralesJuan Guillermo Arrieta SenaAún no hay calificaciones
- Deber 31-08-2022Documento2 páginasDeber 31-08-2022mateo nicolas villalba pozoAún no hay calificaciones
- Elementos Del Grupo IV ADocumento72 páginasElementos Del Grupo IV AJhonny IbañezAún no hay calificaciones
- Aleaciones DanielaDocumento1 páginaAleaciones DanielaFernandaYanixelRiveraRosasAún no hay calificaciones
- 706 U7 Fundición PDFDocumento9 páginas706 U7 Fundición PDFwinxtexAún no hay calificaciones
- Grupo 2 de La Tabla PeriódicaDocumento3 páginasGrupo 2 de La Tabla PeriódicaPaola100% (3)
- Metales AlcalinosDocumento12 páginasMetales AlcalinosrecluisAún no hay calificaciones
- INFORME N°5 - Q.INORGÁNICA-alca-terreosDocumento13 páginasINFORME N°5 - Q.INORGÁNICA-alca-terreosDj GamerPlays YT0% (1)
- Metales AlcalinotérreosDocumento4 páginasMetales AlcalinotérreosINNI COHFIAún no hay calificaciones
- Quimica Juan CamiloDocumento15 páginasQuimica Juan CamiloNidia GuerreroAún no hay calificaciones
- 003 Materiales - No - FerrososDocumento64 páginas003 Materiales - No - FerrosossalvadorAún no hay calificaciones
- Tarea 2.3Documento5 páginasTarea 2.3carlos duarteAún no hay calificaciones
- Reacciones Quimicas 01-11Documento8 páginasReacciones Quimicas 01-11Rosita Tenorio CollazosAún no hay calificaciones
- INORGANICADocumento25 páginasINORGANICAirma rojas landeonAún no hay calificaciones
- Aleaciones No FerrosasDocumento14 páginasAleaciones No FerrosasDaniel Quiñones100% (1)
- Equipo N°5 - Caracteristicas Fisicas y Quimicas Del Zinc y PlomoDocumento10 páginasEquipo N°5 - Caracteristicas Fisicas y Quimicas Del Zinc y PlomoJESUS FRANCISCO DUARTEAún no hay calificaciones
- Tabla MineralesDocumento6 páginasTabla MineralesIssac GuillenAún no hay calificaciones
- Cap 21 - Descriptiva InorganicaDocumento135 páginasCap 21 - Descriptiva InorganicaAntonio Gustavo GonzálezAún no hay calificaciones
- Fmateriales 1aca PDF TerDocumento17 páginasFmateriales 1aca PDF Termiyer gonzalez castilloAún no hay calificaciones
- Ingeniería de procesos siderúrgicos: La experiencia de AHMSADe EverandIngeniería de procesos siderúrgicos: La experiencia de AHMSAAún no hay calificaciones
- Niveles de PrevencionDocumento17 páginasNiveles de PrevencionpwnsionjwijssiAún no hay calificaciones
- Presentación Historia Aesthetic Beige PastelDocumento10 páginasPresentación Historia Aesthetic Beige PastelpwnsionjwijssiAún no hay calificaciones
- Ficha 7 - 3ero - Eda8Documento2 páginasFicha 7 - 3ero - Eda8pwnsionjwijssiAún no hay calificaciones
- MoscasDocumento1 páginaMoscaspwnsionjwijssiAún no hay calificaciones
- Composición y Estructura de La Tierra: Presentado Por Sonia Aguilar y Camila Tangoa 05/12/2023Documento10 páginasComposición y Estructura de La Tierra: Presentado Por Sonia Aguilar y Camila Tangoa 05/12/2023pwnsionjwijssiAún no hay calificaciones
- Ficha 03 - Undad 07Documento3 páginasFicha 03 - Undad 07pwnsionjwijssiAún no hay calificaciones
- Tarea 03 - Equipo 03 - Mec FluidosDocumento26 páginasTarea 03 - Equipo 03 - Mec FluidosJOSE MIGUEL ARBILDO ZAPATAAún no hay calificaciones
- Trabajo Final - Cementos Balboa PDFDocumento46 páginasTrabajo Final - Cementos Balboa PDFXimena Alessandra Bonifacio MedinaAún no hay calificaciones
- Test Ciencia de Los MaterialesDocumento14 páginasTest Ciencia de Los MaterialesPablo JsjsbssAún no hay calificaciones
- Sector Forestal Medio Ambiente 2022Documento52 páginasSector Forestal Medio Ambiente 2022Eduardo Muñoz MolinaAún no hay calificaciones
- Adif-Pg - 22-Procedimiento General de Gestión y Coordinación de Actividades AmbientalesDocumento83 páginasAdif-Pg - 22-Procedimiento General de Gestión y Coordinación de Actividades AmbientalesAlberto Resino AlfonsoAún no hay calificaciones
- Informe de ProyectoDocumento11 páginasInforme de ProyectoISAAC LÓPEZ TOMASAún no hay calificaciones
- Toto Martínez 2C Diferentes FuerzasDocumento14 páginasToto Martínez 2C Diferentes FuerzasSzvalbAún no hay calificaciones
- 08-Lectura Previa Fuerzas ActivasDocumento4 páginas08-Lectura Previa Fuerzas ActivasMaxwell RodriguezAún no hay calificaciones
- Geologia Iberia 003Documento31 páginasGeologia Iberia 003dertekAún no hay calificaciones
- Geologia Del Area San Vicente de Tagua TDocumento123 páginasGeologia Del Area San Vicente de Tagua TAmanda Santis CAún no hay calificaciones
- Estudio de Suelos Villa Carlos PazDocumento25 páginasEstudio de Suelos Villa Carlos PazSanti WolfelAún no hay calificaciones
- Bhopal IndiaDocumento35 páginasBhopal IndiaFrancescaAún no hay calificaciones
- Primera Ley 2.20Documento2 páginasPrimera Ley 2.20Samantha Gamarra DominguezAún no hay calificaciones
- Condensación NubesDocumento5 páginasCondensación NubesGeraldyn SotoAún no hay calificaciones
- Termodinámica Clásica - Unidad 2Documento10 páginasTermodinámica Clásica - Unidad 2magalyAún no hay calificaciones
- Ecofisiologia Del Cacao PublicDocumento16 páginasEcofisiologia Del Cacao PublicHenry SolórzanoAún no hay calificaciones
- Reporte de Laboratorio 2 - Grupo 4Documento3 páginasReporte de Laboratorio 2 - Grupo 4Angel Fabricio Rodríguez SánchezAún no hay calificaciones
- Cadena de Suministro Del TelevisorDocumento1 páginaCadena de Suministro Del TelevisorOsvaldo J Flores GarciaAún no hay calificaciones
- Mezcla Rica y Mezcla PobreDocumento11 páginasMezcla Rica y Mezcla PobreEmmanuel Homem Christo Bautista50% (2)
- 01 Atlas Cuenca S 2010 ADocumento4 páginas01 Atlas Cuenca S 2010 AMateus AlvezAún no hay calificaciones
- Relaciones EstequiometricasDocumento11 páginasRelaciones EstequiometricasnelialkysAún no hay calificaciones
- Presentación Proyecto Trabajo Doodle Orgánico MulticolorDocumento18 páginasPresentación Proyecto Trabajo Doodle Orgánico MulticolorLuis Ivan Salazar EscobarAún no hay calificaciones
- Boletin de Arqueologia #11Documento407 páginasBoletin de Arqueologia #11Eduardo Eche VegaAún no hay calificaciones
- Ununquadio Elemento PuroDocumento1 páginaUnunquadio Elemento PuroEdson Isaac MamaniAún no hay calificaciones
- Proyecto Físicat3Documento9 páginasProyecto Físicat3Anguie BacaAún no hay calificaciones
- El Origen Del Universo de La Vida y Del Ser HumanoDocumento77 páginasEl Origen Del Universo de La Vida y Del Ser HumanoCarlos Milank'sAún no hay calificaciones
- Ingles-Paleo en EsDocumento9 páginasIngles-Paleo en EsAnonymous WOv31hAún no hay calificaciones
- SESIÓN 13 (1° y 2°) C y TDocumento4 páginasSESIÓN 13 (1° y 2°) C y TLedith Rivasplata RuizAún no hay calificaciones
- Actividad A Realiza4Documento2 páginasActividad A Realiza4Aneudy GermánAún no hay calificaciones
- h51 Catalogue 3eq Spanish PDFDocumento12 páginash51 Catalogue 3eq Spanish PDFnicklionsAún no hay calificaciones