Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Mapa Conceptual de Enlaces Quimicos 4
Cargado por
Micol Yakson0 calificaciones0% encontró este documento útil (0 votos)
98 vistas1 páginaMapa sobre enlace químico.
Título original
Mapa-conceptual-de-enlaces-quimicos-4
Derechos de autor
© © All Rights Reserved
Formatos disponibles
PPTX, PDF, TXT o lea en línea desde Scribd
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoMapa sobre enlace químico.
Copyright:
© All Rights Reserved
Formatos disponibles
Descargue como PPTX, PDF, TXT o lea en línea desde Scribd
0 calificaciones0% encontró este documento útil (0 votos)
98 vistas1 páginaMapa Conceptual de Enlaces Quimicos 4
Cargado por
Micol YaksonMapa sobre enlace químico.
Copyright:
© All Rights Reserved
Formatos disponibles
Descargue como PPTX, PDF, TXT o lea en línea desde Scribd
Está en la página 1de 1
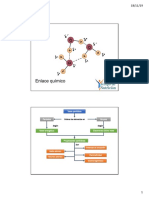
Enlace químico
Se clasifica en:
Enlace Enlaces por fuerzas
Enlace iónico Enlace covalente metálico intermoleculares
Se subdivide en:
Se clasifican en:
Explicación
Tiene una Electronegatividad
Este enlace se expresa muy
Puro o no Coordinado o bien por medio del “modelo de
Igual a 1.7 o mayor Polar dativo
polar burbujas”, propuesto por el
británico Sir. Lawrence Rragg.
Presentan las siguientes características Este autor representó cada uno
de los átomos de un metal por Enlace por Fuerzas de
medio de una burbuja de Atracción
puente de London
El átomo electropositivo jabón. Mediante esta dipolo-dipolo
Electronegatividad: Electronegatividad:
Se forma representación se ilustra la red
igual a cero o menor a Mayor a 0.5 y menor a tiene un par de electrones hidrógeno
0.5 1.7 libres en un orbital exterior y metálica, pues las burbujas se Ejemplos Ejemplos Ejemplos
comportan en muchos
Se forman el átomo electronegativo
aspectos como los átomos que
tiene capacidad para recibir constituyen los metales, este H2O, Enlaces
HF, HBr, HI He
Al combinarse dos no ese par de electrones en su tipo de enlace permite la presentes en el
Al combinarse un metales iguales o Se forma al última capa de valencia creación de aleaciones.
metal y un no metal ADN
entre átomos con muy combinarse dos no
poca diferencia de metales diferentes
electronegatividad
Ejemplos Ejemplos
Ejemplos
Ejemplos Ejemplos
Bronce (Unión entre cobre y
NH4 , H 2SO
+ estaño)
4
Peltre (Unión entre cobre,
NaCl, KBr, CaI2 N2, H2, CH4 SO3, NO2, CO2 estaño, antimonio y plomo)
También podría gustarte
- Mapa ConceptualDocumento1 páginaMapa ConceptualbdanailinAún no hay calificaciones
- QI ENLACES QUÍMICOS Lectura con cuestionario Sem. 21-1Documento9 páginasQI ENLACES QUÍMICOS Lectura con cuestionario Sem. 21-1Kaled Emiliano Viveros HernándezAún no hay calificaciones
- Evidencia de Aprendizaje Semana 4Documento5 páginasEvidencia de Aprendizaje Semana 4Martha CCAún no hay calificaciones
- Capítulo 4Documento2 páginasCapítulo 4Carlos Jiménez RomeroAún no hay calificaciones
- En LacesDocumento1 páginaEn LacesChelo ZRAún no hay calificaciones
- Cim Tareas1 GonzalezsolisjaimeDocumento3 páginasCim Tareas1 GonzalezsolisjaimepedroAún no hay calificaciones
- Act 9Documento2 páginasAct 9duranximena96Aún no hay calificaciones
- UC1 - 1. Enlace Iónico: Chang 11 Ed. Cap 9.1-9.3 Brown 12 Ed. Cap 8.1-8.2Documento33 páginasUC1 - 1. Enlace Iónico: Chang 11 Ed. Cap 9.1-9.3 Brown 12 Ed. Cap 8.1-8.2LUCIANA BETZABE ANCHATU�A MORALESAún no hay calificaciones
- Química Semana 4 P Evidencia de AprendizajeDocumento8 páginasQuímica Semana 4 P Evidencia de AprendizajeLuis Angel Gárate Chambilla100% (3)
- 18qu - Mica 3S - Ii-Enlaces QuimicosDocumento18 páginas18qu - Mica 3S - Ii-Enlaces Quimicosana maria salamanca chaconAún no hay calificaciones
- Enlaces Quimicos e Interacciones IntermolecularesDocumento5 páginasEnlaces Quimicos e Interacciones Intermolecularesfelipedejesus.2508Aún no hay calificaciones
- Marco TeóricoDocumento2 páginasMarco TeóricoANYELI LUCIANO FLORESAún no hay calificaciones
- Química - Semana 4 - TERMINADODocumento8 páginasQuímica - Semana 4 - TERMINADOJose Redentor Vargas LiconaAún no hay calificaciones
- Enlaces Químicos P II 2020Documento30 páginasEnlaces Químicos P II 2020LilithAún no hay calificaciones
- Tema 4Documento18 páginasTema 4alejasp1708Aún no hay calificaciones
- Tarea 11 - Enlaces QuímicosDocumento2 páginasTarea 11 - Enlaces QuímicosJimmy Robles HerreraAún no hay calificaciones
- Diferencias entre átomo, molécula y compuestoDocumento14 páginasDiferencias entre átomo, molécula y compuestolauren yulieth wilches ramirezAún no hay calificaciones
- ACFrOgB0FfLHVzxBqcTDmNHmwn5 FV8Il HWKah2YE3CGdVcGvjLaUwKYk 1Iqz1vxvalI Za7Tf9uL3WM0BRkuKD7izobB DuvRzSYiRGfCGg0MHxUDruDQ5Ej DYN2i0s8deopNW5s Ez95JsDocumento9 páginasACFrOgB0FfLHVzxBqcTDmNHmwn5 FV8Il HWKah2YE3CGdVcGvjLaUwKYk 1Iqz1vxvalI Za7Tf9uL3WM0BRkuKD7izobB DuvRzSYiRGfCGg0MHxUDruDQ5Ej DYN2i0s8deopNW5s Ez95Jsangela moyaAún no hay calificaciones
- Enlace químicoDocumento2 páginasEnlace químicoLuis Enrique MNAún no hay calificaciones
- Cuadro Comparativo Fuerzas Intramoleculares e Intermoleculares.Documento4 páginasCuadro Comparativo Fuerzas Intramoleculares e Intermoleculares.Krystel Dariana Valiente Hernández BAún no hay calificaciones
- Enlace QuimicoDocumento15 páginasEnlace QuimicobdcabezasAún no hay calificaciones
- S03 - Ahora Tú Solo - Enlace QuímicoDocumento2 páginasS03 - Ahora Tú Solo - Enlace Químicoalvaro santosAún no hay calificaciones
- Mapa SinopticoDocumento1 páginaMapa SinopticosofiaAún no hay calificaciones
- Guia Enlace QuimicoDocumento3 páginasGuia Enlace QuimicoIsidora arayaAún no hay calificaciones
- Enlace - Químico - Parte IDocumento24 páginasEnlace - Químico - Parte Idania muñozAún no hay calificaciones
- Enlaces químicos e interacción molecularDocumento3 páginasEnlaces químicos e interacción molecularEduardo Lara100% (1)
- Tipos de Enlace QuímicoDocumento4 páginasTipos de Enlace Químico5IM9- Corona Guzmán Ingrid AnahiAún no hay calificaciones
- Bloc de Notas Sin TítuloDocumento1 páginaBloc de Notas Sin TítulocatalinaAún no hay calificaciones
- Enlaces químicos y tipos de unionesDocumento3 páginasEnlaces químicos y tipos de unionesNahomi Martinez100% (2)
- Tipos de enlaces químicosDocumento36 páginasTipos de enlaces químicosPatryAún no hay calificaciones
- Practica 3Documento5 páginasPractica 3SergioArturoCervantesMedinaAún no hay calificaciones
- Quim. (03) 23 - 01 - 14Documento6 páginasQuim. (03) 23 - 01 - 14Percy TorresAún no hay calificaciones
- Clase 7 - U3 (Enlace Químico-Enlace Iónico-Covalente)Documento50 páginasClase 7 - U3 (Enlace Químico-Enlace Iónico-Covalente)BrunoAún no hay calificaciones
- Bloque VDocumento40 páginasBloque VMafer SolanoAún no hay calificaciones
- 5-Estructura MolecularDocumento35 páginas5-Estructura Molecularivan carvajalAún no hay calificaciones
- Enlaces Covalente Quimica IIDocumento2 páginasEnlaces Covalente Quimica IISamuel CruzAún no hay calificaciones
- Unidad 2 Enlaces Quimicos - Clasificacion de Enlaces QuimicosDocumento29 páginasUnidad 2 Enlaces Quimicos - Clasificacion de Enlaces QuimicosMarcos SolisAún no hay calificaciones
- 16°enlaces QuimicosDocumento2 páginas16°enlaces QuimicosMishell Cárdenas MaytaAún no hay calificaciones
- Enlaces Ionicos y Nomenclatura QuimicaDocumento9 páginasEnlaces Ionicos y Nomenclatura QuimicaIsabel Palacios NoleAún no hay calificaciones
- Quimica 2Documento12 páginasQuimica 2Wall RemAún no hay calificaciones
- Enlaces QuimicosDocumento4 páginasEnlaces QuimicosAngie JaimesAún no hay calificaciones
- Enlace QuimicoDocumento6 páginasEnlace QuimicoJeferson rodriguez lozanoAún no hay calificaciones
- Tipos de EnlacesDocumento2 páginasTipos de EnlacesLares EnriqueAún no hay calificaciones
- Taller Enlace QuimicoDocumento2 páginasTaller Enlace QuimicoMerlin Viviana Mogollon ChavezAún no hay calificaciones
- Enlaces químicos y fuerzas intermolecularesDocumento4 páginasEnlaces químicos y fuerzas intermolecularesHector MejíaAún no hay calificaciones
- 5 Enlaces QuímicosDocumento51 páginas5 Enlaces QuímicosMariel CervantesAún no hay calificaciones
- Enlace Químico e Interacción Molecular PDFDocumento8 páginasEnlace Químico e Interacción Molecular PDFCarlos Andres Valbuena LealAún no hay calificaciones
- Enlaces químicosDocumento9 páginasEnlaces químicosdavid vasquez valenciaAún no hay calificaciones
- PRESABERESDocumento9 páginasPRESABERESDiego UribeAún no hay calificaciones
- Cuadro Comparativo Enlaces QuimicosDocumento2 páginasCuadro Comparativo Enlaces QuimicosPedro Antonio RT100% (6)
- Enlace QuímicoAV de Microsoft PowerPointDocumento5 páginasEnlace QuímicoAV de Microsoft PowerPointmarcelo 7u7Aún no hay calificaciones
- Tarea 5. Enlaces QuímicosDocumento2 páginasTarea 5. Enlaces QuímicosjusellyAún no hay calificaciones
- Química Semana 4 PDocumento8 páginasQuímica Semana 4 PJuan Jose MasvalAún no hay calificaciones
- Trabajo de QuímicaDocumento8 páginasTrabajo de QuímicaNatalia Romero VillaAún no hay calificaciones
- 3ro Abl Enlace Quimico-Estructura de LewisDocumento3 páginas3ro Abl Enlace Quimico-Estructura de Lewisrokiquino5Aún no hay calificaciones
- Diapositivas de ENLACE QUIMICODocumento30 páginasDiapositivas de ENLACE QUIMICOMax Percy Carhuamaca RojasAún no hay calificaciones
- Regla del Octeto y Tipos de Enlaces QuímicosDocumento27 páginasRegla del Octeto y Tipos de Enlaces Químicosstigma subs ;;Aún no hay calificaciones
- Enlaces químicos y regla del octetoDocumento9 páginasEnlaces químicos y regla del octetoRichard LuqueAún no hay calificaciones
- Introducción a la química de los metales de transiciónDe EverandIntroducción a la química de los metales de transiciónAún no hay calificaciones
- Reseña Historica en Honor A La Santísima Virgen Del Rosario de CajabambaDocumento5 páginasReseña Historica en Honor A La Santísima Virgen Del Rosario de CajabambaMicol YaksonAún no hay calificaciones
- 13 Deliberamos Sobre El Impacto de La Problempatica Ambiental en La Salud de Nuestra Comunidad - .Documento14 páginas13 Deliberamos Sobre El Impacto de La Problempatica Ambiental en La Salud de Nuestra Comunidad - .Micol YaksonAún no hay calificaciones
- PDF 20221025 070540 0000Documento2 páginasPDF 20221025 070540 0000Micol YaksonAún no hay calificaciones
- Tutoría 1 Nos Empoderamos para EmprenderDocumento11 páginasTutoría 1 Nos Empoderamos para EmprenderMicol YaksonAún no hay calificaciones
- Taller de Estrategias de Comprensión Lectora 2Documento30 páginasTaller de Estrategias de Comprensión Lectora 2Micol YaksonAún no hay calificaciones
- 18 Difundimos Nuestros Atractivos Turísticos A Través de Un FanzineDocumento14 páginas18 Difundimos Nuestros Atractivos Turísticos A Través de Un FanzineMicol YaksonAún no hay calificaciones
- 10 Explicamos La Importancia de Los Sistemas Financieros en Un EmprendimientoDocumento14 páginas10 Explicamos La Importancia de Los Sistemas Financieros en Un EmprendimientoMicol YaksonAún no hay calificaciones
- Actividad12 3º y 4ºDocumento14 páginasActividad12 3º y 4ºMicol YaksonAún no hay calificaciones
- Lescano PLIDocumento82 páginasLescano PLIMicol YaksonAún no hay calificaciones
- Energía solar y térmicaDocumento12 páginasEnergía solar y térmicaMicol YaksonAún no hay calificaciones
- Práctica 4 ValoracionDocumento8 páginasPráctica 4 ValoracionUlises ParraAún no hay calificaciones
- Taller 1. Cargas ElectricasDocumento3 páginasTaller 1. Cargas ElectricasWILSON EMIDIO ORDONEZ GRUESOAún no hay calificaciones
- Recursos - SanitariasDocumento3 páginasRecursos - SanitariasJose Carlos Olano RestucciaAún no hay calificaciones
- TDS - Gadus S3 V220C 2 PDFDocumento2 páginasTDS - Gadus S3 V220C 2 PDFRoger ObregonAún no hay calificaciones
- Bioelementos y biomoléculas: niveles molecularesDocumento108 páginasBioelementos y biomoléculas: niveles molecularesIuliaAún no hay calificaciones
- 7.2 Estudio de SuelosDocumento77 páginas7.2 Estudio de SuelosCami BaskesAún no hay calificaciones
- Plasticidad de Las Vigas de AceroDocumento6 páginasPlasticidad de Las Vigas de AceroGuillermo RamírezAún no hay calificaciones
- Mejoramiento de La Resistencia Del Concreto Mediante El Uso de Ceniza en La Ciudad de Huancayo - 2019Documento7 páginasMejoramiento de La Resistencia Del Concreto Mediante El Uso de Ceniza en La Ciudad de Huancayo - 2019Gusstock Concha FloresAún no hay calificaciones
- Klaukol Rapibrick Ficha TecnicaDocumento2 páginasKlaukol Rapibrick Ficha TecnicaAnii Quiros0% (1)
- Esmerilado VSV80 P1 K135Documento4 páginasEsmerilado VSV80 P1 K135Brenda Ortiz SolizAún no hay calificaciones
- Analisis P.UDocumento23 páginasAnalisis P.UCristopher Triveños RamirezAún no hay calificaciones
- Riesgos para La Operacion de Soldadura OxiacetilenicaDocumento10 páginasRiesgos para La Operacion de Soldadura OxiacetilenicaRamiro Andres Lopez LealAún no hay calificaciones
- Clases CarbonizaciónDocumento103 páginasClases CarbonizaciónRM MirianAún no hay calificaciones
- CONCLUSIONESDocumento9 páginasCONCLUSIONESjose manuel muñoz veintemillaAún no hay calificaciones
- Elasticidad (Fisica)Documento13 páginasElasticidad (Fisica)Magno Cuba50% (6)
- Informe Gr.1Documento10 páginasInforme Gr.1Michael Johan Salgado MolinaAún no hay calificaciones
- YACIMIENTO MINERAL DE RENDIMIENTO ECONÓMICO IntroDocumento8 páginasYACIMIENTO MINERAL DE RENDIMIENTO ECONÓMICO Introkenner diazAún no hay calificaciones
- DISEÑO - DE - MEZCLA - T2S2 (1) Holcim El Salvador PDFDocumento21 páginasDISEÑO - DE - MEZCLA - T2S2 (1) Holcim El Salvador PDFHerman E Freund RuaAún no hay calificaciones
- CATALOGO DE MADERAS - EspañolDocumento50 páginasCATALOGO DE MADERAS - EspañolLek LvzAún no hay calificaciones
- Gestión ambiental en planta procesadora de lácteosDocumento3 páginasGestión ambiental en planta procesadora de lácteosCALLE VIZA GERSON CARLOSAún no hay calificaciones
- Reparación de La Culata y Sus ComponentesDocumento68 páginasReparación de La Culata y Sus ComponentesJose Juarez Avila67% (3)
- Abladamiento QuimicoDocumento47 páginasAbladamiento QuimicoJOE SANCHEZ SIGUENASAún no hay calificaciones
- 0.2 Simulación de Electrólisis en La MineríaDocumento10 páginas0.2 Simulación de Electrólisis en La MineríaPatricio Candia InostrozaAún no hay calificaciones
- PROCEDIMIENTO TRABAJOS EN CALIENTE OkDocumento8 páginasPROCEDIMIENTO TRABAJOS EN CALIENTE OkjhazAún no hay calificaciones
- Como Poner Un Taller de Hierro Forjado - Guía de NegocioDocumento5 páginasComo Poner Un Taller de Hierro Forjado - Guía de NegocioAlbertoAún no hay calificaciones
- Trabajo de ProcesosDocumento6 páginasTrabajo de ProcesosWilliam CruzAún no hay calificaciones
- Especificaciones Tec.Documento28 páginasEspecificaciones Tec.williams ramosAún no hay calificaciones
- Química 1Documento5 páginasQuímica 1raq1123Aún no hay calificaciones
- NTC 2206 EléctricoDocumento26 páginasNTC 2206 EléctricoantorvezadiazAún no hay calificaciones
- RA5-103 Nueva 001 PDFDocumento5 páginasRA5-103 Nueva 001 PDFjevmcuAún no hay calificaciones