Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Resume N
Cargado por
Dianella SepúlvedaTítulo original
Derechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
Resume N
Cargado por
Dianella SepúlvedaCopyright:
Formatos disponibles
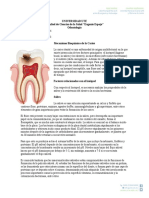
La caries dental es una enfermedad común que involucra la destrucción localizada
de los tejidos calcificados de los dientes. Su desarrollo se ve influenciado por
diversos factores. Los principales son la presencia de microorganismos
cariogénicos en la saliva y la placa dental, junto con un diente susceptible y la
presencia de azúcares y carbohidratos fermentables. Sin embargo, hay otros
factores que pueden frenar o aumentar la aparición de la caries, como la
composición y flujo de la saliva, la higiene bucal y la presencia de fluoruros.
La causa de la caries dental está asociada con ciertos microorganismos,
especialmente el grupo Mutans Streptococci, que incluye especies como
Streptococcus mutans, S. salivarius y S. mitis, así como diferentes tipos de
Lactobacillus, que se encuentran en la placa dental y la saliva. Estos
microorganismos tienen la capacidad de transportar carbohidratos rápidamente,
fermentarlos rápidamente y producir ácidos incluso en entornos con bajo pH. Esto
lleva a un descenso marcado del pH que contribuye a la desmineralización de los
tejidos duros de los dientes, como el esmalte, la dentina y el cemento,
favoreciendo así la formación de lesiones cariosas.
La caries dental, causada por ácidos producidos por bacterias en la placa dental,
está influenciada por el estilo de vida, la higiene bucal, la dieta y la presencia de
flúor. Para evaluar el riesgo de caries, se consideran factores inherentes al
individuo, la dieta y los microorganismos cariogénicos.
Se pueden realizar pruebas de susceptibilidad a la caries, como:
1. **Análisis cualitativo del pH de la placa dental antes y después de enjuagues
con glucosa o sacarosa al 10%:** La diferencia significativa en el pH indica mayor
susceptibilidad a la caries.
2. **Cuantificación de Streptococcus mutans:** Se diluye una muestra de placa
dental en solución y se cultiva en un medio selectivo. El crecimiento se confirma
con pruebas bioquímicas.
3. **Aislamiento de otros microorganismos como Lactobacillus spp. en la saliva:**
Estos microorganismos disminuyen el pH bucal, aumentando la susceptibilidad a
la caries.
4. **Evaluación de la capacidad buffer y la tasa de secreción salival:** La
capacidad buffer neutraliza los ácidos en la boca. Se analizan sistemas de
amortiguación como el fosfato y el ácido carbónico/carbonato.
5. **Determinación cuantitativa de colonias de levaduras:** Se investiga la
interacción entre Candida albicans y la formación de placa dental, considerándose
como un indicador de riesgo de caries.
Existen kits comerciales para realizar pruebas en la clínica dental, como
aislamiento de microorganismos y determinación de la capacidad buffer de la
saliva.
Anteriormente, el enfoque para controlar la caries era la eliminación quirúrgica y el
reemplazo del tejido cariado. Ahora, se busca diagnosticar y tratar la enfermedad
en etapas tempranas, cuando es reversible. Esto implica el diagnóstico del riesgo
cariogénico y el control de la enfermedad en sus inicios, cuando hay un
desequilibrio microbiológico o lesiones que pueden remineralizarse.
hay mucho en esa información. La cavidad oral es un ambiente donde coexisten
diversos microorganismos y estos desempeñan un papel clave en la salud bucal y
la aparición de caries. Los dientes, al no sufrir recambio, son propicios para la
formación de biopelícula, donde bacterias se adhieren y se unen entre sí.
La caries dental es una enfermedad multifactorial causada por microorganismos,
siendo Streptococcus mutans uno de los principales asociados. Se ha encontrado
una relación directa entre la cantidad de S. mutans en la boca y la prevalencia de
caries. Además, este microorganismo puede provocar infecciones sistémicas si
entra al torrente sanguíneo.
El laboratorio de microbiología juega un papel fundamental en identificar estas
bacterias y determinar su susceptibilidad a antimicrobianos. Esto permite diseñar
estrategias de tratamiento más efectivas.
El reconocimiento de la caries como una enfermedad en la que intervienen
microorganismos específicos ha llevado al uso de antimicrobianos locales, como
enjuagues bucales, para controlar la placa bacteriana y reducir el riesgo de caries.
La efectividad de estos enjuagues se evalúa en estudios clínicos controlados y se
busca demostrar su sensibilidad ante microorganismos como S. mutans, un
importante causante de caries.
En resumen, la relación entre microorganismos como Streptococcus mutans y la
caries dental ha impulsado el uso de enjuagues bucales y otras estrategias de
control de la placa bacteriana, con el objetivo de reducir el riesgo de padecer esta
enfermedad. Los estudios en laboratorio son fundamentales para entender la
interacción entre estos microorganismos y los tratamientos efectivos.
Los antimicrobianos son sustancias que inhiben o destruyen específicamente
ciertos microorganismos a bajas concentraciones sin ser tóxicos para el
organismo hospedero. Pueden ser producidos por seres vivos (antibióticos) o
sintetizados químicamente (quimioterapéuticos).
Cada antimicrobiano tiene un modo único de actuar, relacionado con la estructura
celular bacteriana y los blancos de ataque en la célula.
Características clave de un antimicrobiano:
1. **Especificidad:** Su capacidad para unirse a un sitio específico en la bacteria
determina su espectro de actividad.
2. **Eficacia "in vivo":** Debe mantener su capacidad de detener o matar
bacterias dentro del organismo.
3. **Toxicidad selectiva:** Debe ser tóxico para el microorganismo pero seguro
para el huésped, permitiendo su uso clínico.
Se clasifican por:
1. **Origen:** Producidos por hongos, bacterias, semisintéticos o sintéticos.
2. **Espectro de acción:** Efectivos contra bacterias Gram positivas, Gram
negativas o específicos para ciertos grupos.
3. **Forma de acción:** Bacteriostáticos, bactericidas o bacteriolíticos. Actúan
inhibiendo síntesis de proteínas, ácidos nucleicos, pared celular o afectando la
membrana plasmática.
4. **Estructura:** Con anillo beta-lactámico, tetraciclinas, polipéptidos,
aminoglicósidos, etc.
5. **Mecanismo de acción:** Cómo inhiben o eliminan bacterias, como la
interferencia en la síntesis de componentes vitales para la bacteria.
Estas clasificaciones permiten comprender la diversidad de los antimicrobianos y
cómo cada uno actúa específicamente contra las bacterias.
Claro, la clasificación de los antimicrobianos se divide en bactericidas, que causan
la muerte de las bacterias, y bacteriostáticos, que solo detienen temporalmente su
crecimiento.
Los antibióticos pueden comportarse de manera diferente según la concentración
en el objetivo o su afinidad por ciertos microorganismos. Generalmente, los
bactericidas interfieren en la síntesis de la pared celular, la membrana
citoplasmática o el metabolismo del ADN, mientras que los bacteriostáticos
inhiben la síntesis proteica, con excepción de los aminoglucósidos.
Los agentes bacteriostáticos, como las tetraciclinas, detienen el crecimiento
bacteriano y la división celular. Si se retira el agente, las células pueden volver a
multiplicarse. Por otro lado, los bactericidas, como las fluoroquinolonas, no solo
detienen el crecimiento, sino que también activan procesos celulares que llevan a
la muerte de las bacterias. La acción de los bactericidas es irreversible: una vez
expuestas al agente, las células susceptibles mueren.
Claro, los agentes antimicrobianos tienen distintos modos de acción contra las
células bacterianas, que se pueden clasificar de varias maneras:
1. **Interferencia con la Síntesis de la Pared Celular:**
- Agentes que bloquean la síntesis del péptidoglicano, siendo bactericidas.
- En bacterias Gram negativas, los antimicrobianos beta lactámicos ingresan a
través de canales porínicos de la membrana externa, unen a las proteínas de unión
de penicilina (PBPs), lo que debilita la pared y lleva a la lisis celular.
- En bacterias Gram positivas, los beta lactámicos difunden a través de la pared
celular, se unen a las PBPs y debilitan la pared.
2. **Interferencia con la Membrana Citoplásmica:**
- Las polimixinas se difunden hacia la membrana citoplásmica, la alteran y
desestabilizan, causando el derrame del citoplasma y la muerte celular. Son
bactericidas.
3. **Inhibición de la Síntesis de Proteínas (Subunidad Ribosómica 30S):**
- Tetraciclinas y aminoglucósidos se unen a la subunidad 30S del ribosoma. Las
tetraciclinas bloquean el tRNA y detienen la síntesis de proteínas
(bacteriostáticas), mientras que los aminoglucósidos pueden bloquear la unión del
mRNA al ribosoma o causar lecturas incorrectas, resultando en la muerte
bacteriana (bactericidas).
4. **Inhibición de la Síntesis de Proteínas (Subunidad Ribosómica 50S):**
- Macrólidos y lincosamidas se unen a la subunidad 50S del ribosoma,
deteniendo el crecimiento de la cadena proteica y la síntesis de proteínas
(principalmente bacteriostáticos).
- El cloranfenicol también se une a la subunidad 50S y evita la unión de
aminoácidos a la proteína en crecimiento, siendo bacteriostático.
5. **Interferencia con la Síntesis de Proteínas (Mecanismos en Investigación):**
- La linezolida, una oxazolidinona, es un nuevo inhibidor de la síntesis de
proteínas activo contra bacterias Gram positivas.
6. **Interferencia con la Síntesis de Ácido Nucleico:**
- Las fluoroquinolonas bloquean la enzima ADN girasa, necesaria para enrollar y
desenrollar el ADN durante su replicación, causando la muerte celular.
- La rifampicina se une a la ARN polimerasa ADN dependiente, bloqueando la
síntesis de ARN y provocando la muerte de la célula.
7. **Inhibición de la Ruta Metabólica de la Síntesis de Ácido Fólico:**
- Sulfonamidas y trimetoprima compiten con el ácido para-amino benzoico
(PABA) en la síntesis de ácido fólico. La trimetoprima bloquea la dihidrofolato
reductasa. Usadas juntas, producen un bloqueo en la ruta de síntesis del ácido
fólico, siendo bacteriostáticas.
¡Por supuesto! La resistencia antimicrobiana (ATM) engloba una serie de
mecanismos que las bacterias desarrollan para protegerse de los agentes
antimicrobianos. Aquí está el resumen:
### Mecanismos de Resistencia:
1. **Producción de Enzimas:**
- **Beta-lactamasas:** Destruyen los antimicrobianos beta-lactámicos,
volviendo la célula resistente a estos medicamentos.
- **Modificación de Aminoglucósidos:** Enzimas como adenilantes, fosforilantes
o acetilantes modifican los aminoglucósidos para inactivarlos.
- **Cloranfenicol acetil transferasa:** Las bacterias pueden producir esta enzima
para modificar el cloranfenicol y volverlo ineficaz.
2. **Impermeabilidad de la Membrana Bacteriana Externa:**
- **Alteración de Porinas:** En bacterias Gram negativas, las porinas alteradas
en la membrana externa impiden la entrada de antibióticos beta-lactámicos.
3. **Alteración de los Blancos:**
- Las Proteínas de Unión de Penicilina (PBPs) pueden ser mutadas en bacterias
Gram positivas y Gram negativas, evitando que los beta-lactámicos se unan a
ellas.
- **Ribosomas:** La metilación del ARN ribosómico confiere resistencia a los
macrólidos.
- **ADN Girasa y Topoisomerasa IV:** Mutaciones en estos genes confieren
resistencia a las quinolonas.
4. **Bombas de Eflujo:**
- Proteínas transmembrana expulsan activamente antimicrobianos fuera de la
célula, evitando que alcancen su objetivo.
5. **Alteración de Rutas Metabólicas:**
- Mutaciones que inactivan enzimas en rutas metabólicas clave eluden la acción
de los antimicrobianos.
### Determinación de la Concentración Inhibitoria Mínima (CIM):
- La CIM es la concentración más baja de un antimicrobiano que inhibe el
crecimiento bacteriano. Se utiliza para seleccionar el antimicrobiano más efectivo
para tratar una infección.
- Los resultados de CIM se interpretan como sensible, intermedia o resistente,
proporcionando información crucial para la elección del tratamiento.
### Pruebas de Sensibilidad a Antimicrobianos:
- Los antibiogramas son técnicas que muestran la sensibilidad o resistencia de un
microorganismo a varios antimicrobianos.
- Métodos como la difusión en agar (Kirby-Bauer), dilución en caldo y la técnica
del Epsilómetro (E-test) son utilizados para este propósito en aerobios y
anaerobios facultativos.
Estos métodos ayudan a identificar la sensibilidad o resistencia de las bacterias a
los antimicrobianos, crucial para determinar el tratamiento más efectivo.
¡Claro! Aquí tienes un resumen de los puntos clave sobre los microorganismos
asociados con la progresión de la lesión de caries dental y un análisis de las
técnicas de recuento de microorganismos:
### Microorganismos en la Progresión de la Caries Dental:
1. **Streptococcus mutans y S. sobrinus:**
- Tradicionalmente asociados con lesiones de caries, estos microorganismos son
acidogénicos, acidúricos y se mantienen constantes en lesiones cariosas.
- Su capacidad para producir ácido y adherirse a las superficies dentales
contribuye a la progresión de la caries.
2. **Especies de Lactobacillus:**
- Anaerobios facultativos, acidogénicos y acidúricos, favorecen su crecimiento
en pH ácido.
- Se asocian con la colonización en zonas retentivas, como fosas, fisuras o
lesiones cavitadas, contribuyendo a la progresión de la caries.
3. **Importancia de Lactobacillus spp.:**
- La alta infección por lactobacilos se relaciona con una mayor actividad de
caries y el consumo de carbohidratos fermentables.
- Diferentes especies de Lactobacillus tienen variaciones en su capacidad
acidogénica, siendo algunas más eficientes en disminuir el pH del medio.
4. **Aislamiento y Cultivo de Lactobacillus:**
- La identificación y cuantificación precisa de Lactobacillus en muestras
alimenticias permiten comprender las condiciones y medios de cultivo que
favorecen su crecimiento.
### Análisis de Técnicas de Recuento de Microorganismos:
1. **Recuento en Placa:**
- Método común para determinar el número de microorganismos viables en un
medio líquido.
- Se realizan diluciones seriadas de la muestra y se siembran en placas de agar,
donde las bacterias forman colonias.
2. **Recuento Microscópico:**
- Permite determinar el número total de células microbianas por observación
directa en el microscopio.
- No distingue entre células vivas o viables.
3. **Variantes del Recuento en Placa:**
- Siembra en profundidad: se añade medio fundido sobre la placa para permitir
el crecimiento dentro y en la superficie del agar.
- Siembra en superficie: se siembra sobre la superficie del medio de cultivo en
placa, útil para bacterias aerobias.
Estos métodos permiten determinar la cantidad y tipo de microorganismos
presentes en muestras, siendo esenciales en el estudio de la microbiología y su
relación con la caries dental.
También podría gustarte
- Técnicas ómicas aplicadas al estudio de la microbiotaDe EverandTécnicas ómicas aplicadas al estudio de la microbiotaAún no hay calificaciones
- Funcion de Microflora y Microor Asoci CarieDocumento4 páginasFuncion de Microflora y Microor Asoci CarieVictoria BarretoAún no hay calificaciones
- Pract3 Tercer AñoDocumento7 páginasPract3 Tercer AñoKarenina LeónAún no hay calificaciones
- Bioquimica de Caries DentalDocumento23 páginasBioquimica de Caries Dentalricardo reyes100% (1)
- Luque Practica3Documento18 páginasLuque Practica3luqueAún no hay calificaciones
- Texto de La Presentacion 1Documento9 páginasTexto de La Presentacion 1andrea espinelAún no hay calificaciones
- CariesDocumento20 páginasCariesLucia ManzanoAún no hay calificaciones
- Factores Bacterianos de Cariogenicidad... Infecciones Odontogénicas y Sus Etapas ClinicasDocumento4 páginasFactores Bacterianos de Cariogenicidad... Infecciones Odontogénicas y Sus Etapas ClinicasSamaniego Adame ElaineAún no hay calificaciones
- Trabajo de Caries Dental No y Vacunas para Su Control 1Documento5 páginasTrabajo de Caries Dental No y Vacunas para Su Control 1Carito Tamayo100% (2)
- Cuestionario de Caries Dental - Nadia LópezDocumento3 páginasCuestionario de Caries Dental - Nadia LópezNadia LopezAún no hay calificaciones
- Streptococo MutansDocumento9 páginasStreptococo MutansJaviqAún no hay calificaciones
- Microbacteriana Dental y Bucal Compañera FedraDocumento14 páginasMicrobacteriana Dental y Bucal Compañera FedraMilagrosAún no hay calificaciones
- Resumen Lindhe en Antibióticos y Terapia PeriodontalDocumento5 páginasResumen Lindhe en Antibióticos y Terapia Periodontaljorge alberto bravoAún no hay calificaciones
- Bacterias Patogenas y No PatogenasDocumento12 páginasBacterias Patogenas y No PatogenasGenesis Tacuri MAún no hay calificaciones
- Generalidades Sobre La Placa DentalDocumento7 páginasGeneralidades Sobre La Placa DentalRafael Andrés Hanssen HargitayAún no hay calificaciones
- PLACADocumento5 páginasPLACALupita RiveraAún no hay calificaciones
- Mecanismo de La Caries DentalDocumento8 páginasMecanismo de La Caries DentalRebeca RodríguezAún no hay calificaciones
- Bioquímica de La Caries Dental y Los Microorganismos CariogenicosDocumento31 páginasBioquímica de La Caries Dental y Los Microorganismos CariogenicosCarlos Armando Esqueche Angeles50% (2)
- Practica # 5 Microflora de La Placa DentalDocumento3 páginasPractica # 5 Microflora de La Placa DentalSelene GonzalezAún no hay calificaciones
- ANTIBIOTICOSDocumento22 páginasANTIBIOTICOSmilagros chocoAún no hay calificaciones
- Objetivos GeneralDocumento2 páginasObjetivos GeneralCHRISTIAN MORALESAún no hay calificaciones
- PDF Vargas Arriaga Ximenna Salud OralDocumento20 páginasPDF Vargas Arriaga Ximenna Salud Oralximenna nicold vargas arriagaAún no hay calificaciones
- Placa DentalDocumento16 páginasPlaca DentalVanessa Blanco100% (2)
- Microbiología Bucal Resumen 2019Documento6 páginasMicrobiología Bucal Resumen 2019Patricia MartinezAún no hay calificaciones
- Tema 3. Determinantes Ecologicos OralesDocumento10 páginasTema 3. Determinantes Ecologicos OralesrikyAún no hay calificaciones
- Cuestionario 07Documento5 páginasCuestionario 07MARIA MILAGROS BRIONES ESPINOZAAún no hay calificaciones
- Bacterias Cariogenicas y PeriodontogenicasDocumento27 páginasBacterias Cariogenicas y PeriodontogenicasLuis Antonio Navarro SanchezAún no hay calificaciones
- Microbiologia de La Placa DentalDocumento10 páginasMicrobiologia de La Placa DentalRaul RodriguezAún no hay calificaciones
- Cuestionario MicrobiologíaDocumento3 páginasCuestionario Microbiologíajael.hernandezAún no hay calificaciones
- UntitledDocumento3 páginasUntitledBri MeraAún no hay calificaciones
- Diapositivas Biofilm OralDocumento21 páginasDiapositivas Biofilm OralAldo Sibille GrentzAún no hay calificaciones
- LAB de Microbiologia Sobre Recuento de MicroorganismosDocumento9 páginasLAB de Microbiologia Sobre Recuento de Microorganismosorlando delgado100% (1)
- Antibioticos - MicrobiologiaDocumento11 páginasAntibioticos - MicrobiologiaStephanie Narumy Nuñez MocarroAún no hay calificaciones
- TRABAJO INVESTIGACION BucodentalDocumento52 páginasTRABAJO INVESTIGACION BucodentalFelix Bernabe M. SalazarAún no hay calificaciones
- MONOGRAFIA Biogaia ProdentisDocumento13 páginasMONOGRAFIA Biogaia ProdentisCatalina Guzman ReinaAún no hay calificaciones
- Cuestionario N°7Documento7 páginasCuestionario N°7Yina Saldaña GaribayAún no hay calificaciones
- Bioquimica de La Caries DentalDocumento22 páginasBioquimica de La Caries DentalKarla Chevez CercadoAún no hay calificaciones
- 2 Do Pacial MicroDocumento8 páginas2 Do Pacial Microaurorazapata563Aún no hay calificaciones
- Sem Biofilm Dep Sup 2013Documento35 páginasSem Biofilm Dep Sup 2013Cristina CbzAún no hay calificaciones
- Universitaria Aguilar Luis Wara YoselineDocumento6 páginasUniversitaria Aguilar Luis Wara YoselinePablo David EspinozaAún no hay calificaciones
- Etiología de Infecciones OdontogénicasDocumento16 páginasEtiología de Infecciones OdontogénicasLuis Antonio Navarro SanchezAún no hay calificaciones
- Microbiologia Caries DentalDocumento33 páginasMicrobiologia Caries DentalPinola cbmfAún no hay calificaciones
- Taller #2 MicrobiologiaDocumento4 páginasTaller #2 MicrobiologiaMaria Fda Parraga BAún no hay calificaciones
- Tincion de BacteriasDocumento5 páginasTincion de BacteriasJuan JácomeAún no hay calificaciones
- Microbiologia - Word - Composicion y Funcion-WbayasDocumento5 páginasMicrobiologia - Word - Composicion y Funcion-WbayasAnnerryBarriosAún no hay calificaciones
- Caries Dental. Guía 2Documento15 páginasCaries Dental. Guía 2Merys JiménezAún no hay calificaciones
- Caries DentalDocumento6 páginasCaries DentalAndreaAún no hay calificaciones
- Microbioma Ejemplos-Grupo 8Documento13 páginasMicrobioma Ejemplos-Grupo 8CHAHUA GÓMEZ YONELAún no hay calificaciones
- Quimioterapia Antimicrobiana 1Documento7 páginasQuimioterapia Antimicrobiana 1Dennise MolinaAún no hay calificaciones
- Metabolismo CariogenicoDocumento18 páginasMetabolismo Cariogenicoa371376Aún no hay calificaciones
- Análisis de La Microbiota Oral Cariogénica TesisDocumento8 páginasAnálisis de La Microbiota Oral Cariogénica TesisRoc RacAún no hay calificaciones
- Antisépticos en El Tratamiento de La Enfermedad PeriodontalDocumento14 páginasAntisépticos en El Tratamiento de La Enfermedad PeriodontalSergio Pacheco S.Aún no hay calificaciones
- UNIDAD VI. Composición y Ecología de La Microbiota Oral y Determinantes Ecológicos Orales PDFDocumento30 páginasUNIDAD VI. Composición y Ecología de La Microbiota Oral y Determinantes Ecológicos Orales PDFVerania GironAún no hay calificaciones
- Antibiotic OsDocumento13 páginasAntibiotic OsLucero Iza TorresAún no hay calificaciones
- Biofilm Sin BiblioDocumento5 páginasBiofilm Sin BiblioKarina PerezAún no hay calificaciones
- Placa DentobacterianaDocumento33 páginasPlaca DentobacterianaGustavo Cadena100% (1)
- Placa DentobacterianaDocumento5 páginasPlaca DentobacterianaEloy MoralesAún no hay calificaciones
- Dental Caries Capitulo 7 TraducidoDocumento30 páginasDental Caries Capitulo 7 TraducidoLuis Fernando LenzuéAún no hay calificaciones
- Mecanismos de Acción de AntimicrobianosDocumento8 páginasMecanismos de Acción de AntimicrobianosJDGCAún no hay calificaciones
- Enfermedad Periodontal y Microorganismos PeriodontopatogenosDocumento10 páginasEnfermedad Periodontal y Microorganismos PeriodontopatogenosSarita AnticonaAún no hay calificaciones
- Personajes de La BiotecnologíaDocumento2 páginasPersonajes de La BiotecnologíaMichel Alejandro PadrónAún no hay calificaciones
- TraduccionDocumento7 páginasTraduccionCamila cuiAún no hay calificaciones
- Biologia 1Documento100 páginasBiologia 1Jhoana PeñaAún no hay calificaciones
- Código GenéticoDocumento5 páginasCódigo GenéticojuanAún no hay calificaciones
- Los Cromosomas Guia 9Documento3 páginasLos Cromosomas Guia 9genovitaAún no hay calificaciones
- Charla ADNDocumento6 páginasCharla ADNAstrid RodríguezAún no hay calificaciones
- (B) Inmunodeficiencias Primarias - InmunomodulaciónDocumento17 páginas(B) Inmunodeficiencias Primarias - InmunomodulaciónAlexandra AndreaAún no hay calificaciones
- Las ProteinasDocumento40 páginasLas Proteinaseliasid buelvas jimenezAún no hay calificaciones
- OperonDocumento32 páginasOperonfrancisco lozano gomezAún no hay calificaciones
- Bioinformatica Aplicado A La Medicina VeterinariaDocumento18 páginasBioinformatica Aplicado A La Medicina VeterinariaJose Abelardo QuiñonesAún no hay calificaciones
- Lectura Membrana CelularDocumento1 páginaLectura Membrana CelularDiana Claros AlvarezAún no hay calificaciones
- Escherichia Coli: Una Comparación y Optimización de Métodos y Factores Que Afectan La Transformación deDocumento13 páginasEscherichia Coli: Una Comparación y Optimización de Métodos y Factores Que Afectan La Transformación deJamith VargasAún no hay calificaciones
- Agroecologia - IAP Desarrollo SustentableDocumento30 páginasAgroecologia - IAP Desarrollo SustentableestudiosubalternosAún no hay calificaciones
- Estructura y Morfologia BacterianaDocumento22 páginasEstructura y Morfologia BacterianaVictoria GonzalesAún no hay calificaciones
- Capitulo 10Documento9 páginasCapitulo 10Gabriela C.Aún no hay calificaciones
- Alimentos Cuerpo Humano Grado 8Documento25 páginasAlimentos Cuerpo Humano Grado 8alsaapa0% (2)
- Biotecnologia en ColombiaDocumento10 páginasBiotecnologia en ColombiaSebastián FloridoAún no hay calificaciones
- Tema 1. Introducción A La GeneticaDocumento9 páginasTema 1. Introducción A La GeneticaMari VegaAún no hay calificaciones
- Cebador: DifteriaDocumento18 páginasCebador: DifteriaMax ChafloqueAún no hay calificaciones
- Ensayo de Ribosoma - GENETICADocumento5 páginasEnsayo de Ribosoma - GENETICACapry De Leon RadaAún no hay calificaciones
- Práctica de Extracción de ADNDocumento2 páginasPráctica de Extracción de ADNJocelin CervantesAún no hay calificaciones
- Acidos NucleicosDocumento21 páginasAcidos NucleicosFranco Apaza AlaveAún no hay calificaciones
- UntitledDocumento38 páginasUntitledCarla OVAún no hay calificaciones
- TareaDocumento2 páginasTareajosvvvAún no hay calificaciones
- Biologia 100Documento15 páginasBiologia 100Elisa Cobeña JAún no hay calificaciones
- Biologia Celular Uba, MEMBRANA PLASMÁTICADocumento75 páginasBiologia Celular Uba, MEMBRANA PLASMÁTICALu GonzálezAún no hay calificaciones
- Ayuno Intermitente - Tupiza Jean PDFDocumento8 páginasAyuno Intermitente - Tupiza Jean PDFJeanAún no hay calificaciones
- Calidad - Buenas Practicas OCDE (1) Aurora ZuzuarreguiDocumento37 páginasCalidad - Buenas Practicas OCDE (1) Aurora Zuzuarreguijulieth cAún no hay calificaciones
- Lectura 7.pt - EsDocumento7 páginasLectura 7.pt - Esrolo v:Aún no hay calificaciones
- 10° Taller Superaciã N 1 PeriodoDocumento3 páginas10° Taller Superaciã N 1 PeriodoSimon ValenciaAún no hay calificaciones