Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Formulario Química
Cargado por
Karen0 calificaciones0% encontró este documento útil (0 votos)
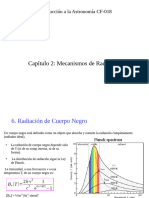
8 vistas1 páginaEste documento presenta información sobre celdas unitarias, incluidas sus fórmulas, radios atómicos y tipos (cúbica simple, centrada en el cuerpo y centrada en las caras). También cubre conceptos del estado gaseoso como presión, temperatura y las leyes de Boyle, Charles, Gay-Lussac y la ley combinada/universal de los gases.
Descripción original:
Estado Sólido
Derechos de autor
© © All Rights Reserved
Formatos disponibles
PDF, TXT o lea en línea desde Scribd
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoEste documento presenta información sobre celdas unitarias, incluidas sus fórmulas, radios atómicos y tipos (cúbica simple, centrada en el cuerpo y centrada en las caras). También cubre conceptos del estado gaseoso como presión, temperatura y las leyes de Boyle, Charles, Gay-Lussac y la ley combinada/universal de los gases.
Copyright:
© All Rights Reserved
Formatos disponibles
Descargue como PDF, TXT o lea en línea desde Scribd
0 calificaciones0% encontró este documento útil (0 votos)
8 vistas1 páginaFormulario Química
Cargado por
KarenEste documento presenta información sobre celdas unitarias, incluidas sus fórmulas, radios atómicos y tipos (cúbica simple, centrada en el cuerpo y centrada en las caras). También cubre conceptos del estado gaseoso como presión, temperatura y las leyes de Boyle, Charles, Gay-Lussac y la ley combinada/universal de los gases.
Copyright:
© All Rights Reserved
Formatos disponibles
Descargue como PDF, TXT o lea en línea desde Scribd
Está en la página 1de 1
Karen Angelica Samaniego Corona FORMULARIO 2FM2 Química Aplicada - Parcial 1
Celdas unitarias Radio atómico
NM Celda Fórmula
d=
NAa3 𝑎
Cúbica simple r=2
𝑔
d = densidad ( 𝑚𝑜𝑙 )
Cúbica centrada en el cuerpo 4r = a√3
N = no. de átomos por celda
Cúbica centrada en las caras 4r = a√2
𝑔
M = peso molecular ( 𝑚𝑜𝑙 )
Longitud equivalente
4{ r = radio atómico (pm)
NA = no. de Avogadro
á𝑡𝑜𝑚𝑜𝑠
(6.023x1023 𝑚𝑜𝑙 ) a 4 radios atómicos
a = arista (pm)
V = volumen de la celda (cm3) V = a3 (l*l*l)
Celda unitaria cúbica simple: 1 átomo
3
a = arista de la celda (cm) 𝑎 = √𝑉 𝑐𝑒𝑙𝑑𝑎
Celda unitaria centrada en el cuerpo (BCC): 2 átomos
−10
Å = 1x10 cm
a={ a = ax10−10 = 𝑎3 Celda unitaria centrada en las caras (FCC): 4 átomos
pm = 1x10−10 cm
Cristalografía Estado gaseoso (gases ideales y gases reales)
nλ = 2d sin θ Fuerza
Presión=FuerzaÁrea Presión = Área
n = número entero (1, 2, 3, 4 … ) Presión
λ = longitud de onda (nm, pm) 1 atm = 10, 132 Pa = 101.32 Kpa
d = distancia entre los planos (nm, pm) 1 atm = 760 torr
θ = ángulo de incidencia y reflexión de rayos X 1 atm = 760 mmHg
Volumen 1L = 1,000 mL , 1mL = 1 cm3
Ley de Boyle Ley de Charles Temperatura ℃ , ℉ , °K T. absoluta: 0℃ = 273°K
1 P
P∝𝑉 PV = K V∝T =K
T
Ley combinada/universal de los gases
K = constante T = temperatura
P1V1 P2V2
absoluta (1,2) =
Temperatura = constante T1 T2
P = presión
V = volumen (1,2) T = temperatura absoluta (1,2)
constante (1,2)
P = presión (1,2) V = volumen (1,2)
P = presión (1,2)
Ley de Gay - Lussac
P
P∝T =K
T
T = temperatura
absoluta (1,2)
V = volumen
constante (1,2)
También podría gustarte
- Materiales para ingeniería 1: Introducción a las propiedades, las aplicaciones y el diseñoDe EverandMateriales para ingeniería 1: Introducción a las propiedades, las aplicaciones y el diseñoCalificación: 5 de 5 estrellas5/5 (3)
- Ingeniería química. Soluciones a los problemas del tomo IDe EverandIngeniería química. Soluciones a los problemas del tomo IAún no hay calificaciones
- Examen Fisica Opcion BDocumento5 páginasExamen Fisica Opcion BJavaeAún no hay calificaciones
- Fisicoquimica - Formulario 1Documento10 páginasFisicoquimica - Formulario 1LeslieAsipuelaAún no hay calificaciones
- Todo Junto para FisicoDocumento50 páginasTodo Junto para FisicoEmily LopezAún no hay calificaciones
- Fenomenos de TrasporteDocumento10 páginasFenomenos de TrasporteRuth Gabriela Lozano HervacioAún no hay calificaciones
- Electroacústica - I. PolitécnicoDocumento236 páginasElectroacústica - I. PolitécnicoAsereperu100% (1)
- Ciencia de MaterialesDocumento15 páginasCiencia de MaterialesFaby Avilés NavarroAún no hay calificaciones
- Capi. 7 y 8 Fisica Estadistica 2017Documento66 páginasCapi. 7 y 8 Fisica Estadistica 2017dayannaAún no hay calificaciones
- Tarea 1 - Señales y SistemasDocumento6 páginasTarea 1 - Señales y SistemasJose Eduardo Garcia CamargoAún no hay calificaciones
- Formulario (Quimica Aplicada)Documento20 páginasFormulario (Quimica Aplicada)luisAún no hay calificaciones
- Tema 7: Radiometría de MicroondasDocumento20 páginasTema 7: Radiometría de MicroondasDinastíaAún no hay calificaciones
- Formulario QuimicaDocumento5 páginasFormulario QuimicadavidAún no hay calificaciones
- Formulario CineticaDocumento3 páginasFormulario CineticaALAN EMMANUEL CRUZ RUIZAún no hay calificaciones
- Propiedad de La Física CuanticaDocumento83 páginasPropiedad de La Física CuanticaArnold smith Machado camachoAún no hay calificaciones
- Problema 4Documento2 páginasProblema 4UlisesAún no hay calificaciones
- Taller de Fisica OndulatoriaDocumento3 páginasTaller de Fisica OndulatoriaHamilton MtzAún no hay calificaciones
- Formulario Quimica General I PDFDocumento14 páginasFormulario Quimica General I PDFNicole Ponce AguiñoAún no hay calificaciones
- Leyes de Los Gases y Ec. Del Gas IdealDocumento33 páginasLeyes de Los Gases y Ec. Del Gas IdealOctavio AmtzAún no hay calificaciones
- Formulas Carreteras IIDocumento5 páginasFormulas Carreteras IIDra Ana Robles De MorenoAún no hay calificaciones
- Formulario 2Documento2 páginasFormulario 2ALAN EMMANUEL CRUZ RUIZAún no hay calificaciones
- Fisica NuclearDocumento13 páginasFisica NuclearFaby AvilésAún no hay calificaciones
- Laguna de MaduraciónDocumento6 páginasLaguna de MaduraciónJuan AyalaAún no hay calificaciones
- Taller 1-SoluciónDocumento8 páginasTaller 1-SoluciónCarolina Solano CáceresAún no hay calificaciones
- Conceptos Teoricos Juan MontesDocumento1 páginaConceptos Teoricos Juan Montesale martinezAún no hay calificaciones
- Doble Rendija. Postulados de de BroglieDocumento20 páginasDoble Rendija. Postulados de de BroglieVirginia BertelloAún no hay calificaciones
- Fórmulas Matem. y CienciasDocumento3 páginasFórmulas Matem. y CienciasGodscar AlegreAún no hay calificaciones
- FisEst2006 2Documento5 páginasFisEst2006 2Cris TinaAún no hay calificaciones
- Tarea 1Documento2 páginasTarea 1octavioAún no hay calificaciones
- Conveccion Natural y Forzada Tema 6Documento16 páginasConveccion Natural y Forzada Tema 6Jake VazquezAún no hay calificaciones
- Termo FórmulasDocumento3 páginasTermo FórmulasCynthia Hernández'Aún no hay calificaciones
- Ejericios Latex PDFDocumento22 páginasEjericios Latex PDFFausto ArandaAún no hay calificaciones
- Fuerzas en El Espacio EstaticaDocumento16 páginasFuerzas en El Espacio EstaticaAlbertoAún no hay calificaciones
- Ondas y CuanticaDocumento4 páginasOndas y CuanticaGabriel LeónAún no hay calificaciones
- Lab 05 Oyc Ec JihouigyfycfDocumento10 páginasLab 05 Oyc Ec JihouigyfycfAnderson VelardeAún no hay calificaciones
- OPE1 formulasTransmisionCalorC PDFDocumento10 páginasOPE1 formulasTransmisionCalorC PDFLesly Judith Yaipen GonzalesAún no hay calificaciones
- Resumen de Fc3b3rmulas Fc3adsica 1Documento10 páginasResumen de Fc3b3rmulas Fc3adsica 1Laura GomezAún no hay calificaciones
- Formulario FiquiDocumento8 páginasFormulario FiquiJuan Carlos ChuzonAún no hay calificaciones
- Espectro de PotenciaDocumento5 páginasEspectro de PotenciaAlexander CasablancaAún no hay calificaciones
- Teoria Cinetica de GasesDocumento4 páginasTeoria Cinetica de GasesJesus Manuel Saldaña VasquezAún no hay calificaciones
- Anilloieee802000 70KGDocumento9 páginasAnilloieee802000 70KGErica Alexandra Blanquicet PalmaAún no hay calificaciones
- Propagación-Y-Radiación-Electromagnética II-1 PDFDocumento80 páginasPropagación-Y-Radiación-Electromagnética II-1 PDFDavid DraAún no hay calificaciones
- 2018 - ParteII - SolDocumento6 páginas2018 - ParteII - SolLAún no hay calificaciones
- Tarea 1 - Señales y Sistemas - Trabajo ColaborativoDocumento63 páginasTarea 1 - Señales y Sistemas - Trabajo ColaborativoJose Eduardo Garcia CamargoAún no hay calificaciones
- Tarea3 G30Documento44 páginasTarea3 G30cesar100% (1)
- Preparatorio6 EpDocumento9 páginasPreparatorio6 EpKevin CarpioAún no hay calificaciones
- Ce Examen 21 1Documento8 páginasCe Examen 21 1Benjamin Antonio Guzman CarocaAún no hay calificaciones
- FísicavirtualDocumento20 páginasFísicavirtualJuan David Collazos DelgadoAún no hay calificaciones
- Constante de Stefan-Boltzmann Laboratorio de Física Contemporánea IDocumento5 páginasConstante de Stefan-Boltzmann Laboratorio de Física Contemporánea IUnSimpleUsuarioAún no hay calificaciones
- Tema 3. Apuntes - Fundamentos - Cuanticos PDFDocumento23 páginasTema 3. Apuntes - Fundamentos - Cuanticos PDFRaúl López SánchezAún no hay calificaciones
- Formulas Resumen PDFDocumento2 páginasFormulas Resumen PDFjoAún no hay calificaciones
- Tabla Formulas PDFDocumento2 páginasTabla Formulas PDFFranciscoVicianaDelgadoAún no hay calificaciones
- Cap 2 CF 04622 IibDocumento10 páginasCap 2 CF 04622 IibRODRIGO ALONZO VELASQUEZ FLORESAún no hay calificaciones
- SolExamen 1 EDII MafaldaDocumento4 páginasSolExamen 1 EDII MafaldaAngie GarcíaAún no hay calificaciones
- Lab - 7 - Análisis Senoidal en Estado Estable RLCDocumento17 páginasLab - 7 - Análisis Senoidal en Estado Estable RLCKEVIN DANIEL ORTEGA FRANCOAún no hay calificaciones
- PRODUCTO ACADÉMICO N°1 - FÍsica IIDocumento10 páginasPRODUCTO ACADÉMICO N°1 - FÍsica IIJean Paul Castro BuendiaAún no hay calificaciones
- Entrega7 Guía7Documento2 páginasEntrega7 Guía7Raul PAún no hay calificaciones
- Formulario Eym 2 SinejerciciosDocumento1 páginaFormulario Eym 2 Sinejercicioseithants.protecoAún no hay calificaciones
- Ejemplos GasesDocumento9 páginasEjemplos GasesŘôjâš ĞřôvĕřAún no hay calificaciones
- ParcialOndas 2015-1solucionDocumento3 páginasParcialOndas 2015-1solucionAlfonso Escobar SilvaAún no hay calificaciones
- Semana 5 QuimicaDocumento6 páginasSemana 5 QuimicadoraAún no hay calificaciones
- Monografia Fisica Tension SuperficialDocumento11 páginasMonografia Fisica Tension SuperficialJhoncito R. Huaynalaya SolanoAún no hay calificaciones
- Guía Lab Nº1-SecadoDocumento5 páginasGuía Lab Nº1-SecadoÁlvaro Alcayaga CuadraAún no hay calificaciones
- 2023-10-02 - BGómezM - Interacción Partículas Materia PDFDocumento79 páginas2023-10-02 - BGómezM - Interacción Partículas Materia PDFjmmedranoh17Aún no hay calificaciones
- Cap 6Documento42 páginasCap 6Eugenio DerbesAún no hay calificaciones
- Informe de Presion AtmosfericaDocumento5 páginasInforme de Presion AtmosfericaHarold Isai Silvestre Gomez0% (1)
- Propiedades Del Agua CongenitaDocumento18 páginasPropiedades Del Agua CongenitaJoselyn TorcuatoAún no hay calificaciones
- Introducció1Documento17 páginasIntroducció1Pedro RamirezAún no hay calificaciones
- T Uce 0012 308Documento199 páginasT Uce 0012 308Maderas FinasAún no hay calificaciones
- Endress-Hauser Cerabar M PMP51 ESDocumento9 páginasEndress-Hauser Cerabar M PMP51 ESAndres Felipe Castellanos PulidoAún no hay calificaciones
- Solido Liquido GaseosoDocumento21 páginasSolido Liquido GaseosoKevin GonzalesAún no hay calificaciones
- Líquidos CristalinosDocumento5 páginasLíquidos CristalinosDaniel hernandoAún no hay calificaciones
- Investigacion de Maquinas Reciprocantes y Ciclo OttoDocumento6 páginasInvestigacion de Maquinas Reciprocantes y Ciclo OttoFernanda MorenoAún no hay calificaciones
- Apuntes de PresionDocumento18 páginasApuntes de PresionMIGUEL ANGEL ZUÑIGAAún no hay calificaciones
- Punto de EbullicionDocumento3 páginasPunto de EbullicionMäiidiiTä EspiinözäAún no hay calificaciones
- Enlace Covalente 2013 BreveDocumento57 páginasEnlace Covalente 2013 BreveLópez Vázquez Carlos YaelAún no hay calificaciones
- Clase 10 TermodinámicaDocumento18 páginasClase 10 TermodinámicaHiCarlAún no hay calificaciones
- ManometroDocumento4 páginasManometroVioleta PerezAún no hay calificaciones
- Fluidos2 PDFDocumento14 páginasFluidos2 PDFSarita ZambranoAún no hay calificaciones
- T2 TermodinamicaDocumento16 páginasT2 TermodinamicaJeremy RojasAún no hay calificaciones
- Bases TeóricasDocumento7 páginasBases TeóricasJuan VelásquezAún no hay calificaciones
- 08 Sifón Hidráulico - 20170911Documento9 páginas08 Sifón Hidráulico - 20170911Valen RamiirezAún no hay calificaciones
- Laboratorio Quimica Organica I 6Documento6 páginasLaboratorio Quimica Organica I 6karen jhakelin pajaro sotoAún no hay calificaciones
- Guia de Estudio ReynoldsDocumento12 páginasGuia de Estudio ReynoldsGary RiveraAún no hay calificaciones
- Práctica 2Documento9 páginasPráctica 2jezabel andradeAún no hay calificaciones
- Taller Gases 2 IdealsyRealesDocumento12 páginasTaller Gases 2 IdealsyRealesMari MelianAún no hay calificaciones
- Practica 5 Influencia de La Presion Sobre El Punto de EbullicionDocumento10 páginasPractica 5 Influencia de La Presion Sobre El Punto de EbullicionAbner MartinezAún no hay calificaciones
- Relación #4Documento8 páginasRelación #4Alejandro Tagalos MuñozAún no hay calificaciones
- Informe Punto Fusion y Ebullicio Sustancia OrganicaDocumento6 páginasInforme Punto Fusion y Ebullicio Sustancia Organicamercedes_benitez_8100% (3)
- Guia 2Documento3 páginasGuia 2Valeria EspíndolaAún no hay calificaciones