Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Mapa Conceptual-Electrólisis
Cargado por
José Andrés Sánchez Bagüi100%(1)100% encontró este documento útil (1 voto)
860 vistas1 páginaLas celdas electrolíticas se utilizan para producir y purificar metales como el aluminio y el cobre mediante la aplicación de una corriente eléctrica continua que descompone las sustancias inmersas en una disolución. También se emplean para generar halógenos como el flúor y el cloro, que son indispensables en la industria química, y para almacenar energía en baterías recargables como las de litio utilizadas en dispositivos móviles.
Descripción original:
la Electrolisis y sus debidos procesos mapa conceptual
Título original
MAPA CONCEPTUAL-ELECTRÓLISIS
Derechos de autor
© © All Rights Reserved
Formatos disponibles
DOCX, PDF, TXT o lea en línea desde Scribd
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoLas celdas electrolíticas se utilizan para producir y purificar metales como el aluminio y el cobre mediante la aplicación de una corriente eléctrica continua que descompone las sustancias inmersas en una disolución. También se emplean para generar halógenos como el flúor y el cloro, que son indispensables en la industria química, y para almacenar energía en baterías recargables como las de litio utilizadas en dispositivos móviles.
Copyright:
© All Rights Reserved
Formatos disponibles
Descargue como DOCX, PDF, TXT o lea en línea desde Scribd
100%(1)100% encontró este documento útil (1 voto)
860 vistas1 páginaMapa Conceptual-Electrólisis
Cargado por
José Andrés Sánchez BagüiLas celdas electrolíticas se utilizan para producir y purificar metales como el aluminio y el cobre mediante la aplicación de una corriente eléctrica continua que descompone las sustancias inmersas en una disolución. También se emplean para generar halógenos como el flúor y el cloro, que son indispensables en la industria química, y para almacenar energía en baterías recargables como las de litio utilizadas en dispositivos móviles.
Copyright:
© All Rights Reserved
Formatos disponibles
Descargue como DOCX, PDF, TXT o lea en línea desde Scribd
Está en la página 1de 1
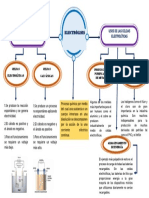
USOS DE LAS CELDAS
ELECTRÓLISIS
ELECTROLÍTICAS
DIFERENCIA
S
CELDAS CELDAS PRODUCCIÓN Y
PURIFICACIÓN DE PRODUCCIÓN DE
ELECTROLÍTICAS GALVÁNICAS HIDRÓGENO
METALES
Algunos de los metales Los halógenos como el flúor y el
1.Se produce la reacción Proceso químico por medio del
1.Se produce un proceso no más importantes para el cloro son de gran importancia en
espontánea y se genera cual una sustancia o un cuerpo la industria química. Son
espontáneo aplicando ser humano como el
electricidad. inmersos en una disolución se aluminio y el cobre se reactivos indispensables para la
electricidad.
descomponen por la acción de producen industrialmente producción de muchos derivados
2.El cátodo es positivo y el 2.El cátodo es negativo y el la una corriente eléctrica por medio de celdas del petróleo tal como el PVC y el
ánodo es negativo. ánodo es positivo continua. electrolíticas. teflón
3.Para el funcionamiento se 3.Para el funcionamiento se
requiere un voltaje más requiere un voltaje más ALMACENAMIENT
bajo. alto. O DE ENERGÍA
El ejemplo más palpable de esto es el
proceso de carga de todas las baterías
recargables. Sin las celdas electrolíticas,
las baterías de litio que proporcionan
energía a la gran mayoría de los
dispositivos móviles que utilizamos
diariamente no serían recargables.
También podría gustarte
- Mapa Conceptual TemperaturaDocumento2 páginasMapa Conceptual TemperaturaHUGO DE GONZALEZ OSPINOAún no hay calificaciones
- TRIPTICO MitosisDocumento3 páginasTRIPTICO MitosisMia Camila Carazas PerezAún no hay calificaciones
- Mapa ConceptualDocumento1 páginaMapa Conceptualmariluz martinez50% (2)
- Triptico Sistema de AlcantarilladoDocumento2 páginasTriptico Sistema de AlcantarilladoSalvadorMN100% (1)
- Mapa Conceptual Sobre CatalizadoresDocumento1 páginaMapa Conceptual Sobre CatalizadoresEduardo Osorio67% (3)
- Las TaxiasDocumento3 páginasLas Taxias0 0Aún no hay calificaciones
- Laguna de Las IlusionesDocumento10 páginasLaguna de Las IlusionesMarco Antonio Custodio LopezAún no hay calificaciones
- Mapa ConceptualDocumento1 páginaMapa ConceptualCarlosAún no hay calificaciones
- Molino de Agua InfoDocumento7 páginasMolino de Agua InfoHugo LopezAún no hay calificaciones
- Mapa Conceptual PDFDocumento1 páginaMapa Conceptual PDFMiansaon100% (1)
- Circuitos Electricos Actividad de Empalme Con ConclusionDocumento4 páginasCircuitos Electricos Actividad de Empalme Con ConclusionMaria CardenasAún no hay calificaciones
- Coliseo RomanoDocumento1 páginaColiseo RomanoJilMar SanchezAún no hay calificaciones
- InfografíaDocumento1 páginaInfografíaAlejandra CalderónAún no hay calificaciones
- Informe de InvestigacionDocumento12 páginasInforme de InvestigacionAldheir Anacleto IreneAún no hay calificaciones
- Mapa ConceptualDocumento1 páginaMapa ConceptualAlejandra Bermudez M0% (1)
- Triptico GiamDocumento3 páginasTriptico GiamPedro Villagaray Medina100% (2)
- Problemas de Trabajo y Potencia Electrica.Documento3 páginasProblemas de Trabajo y Potencia Electrica.Hairo Euan MooAún no hay calificaciones
- Infografía CT PDFDocumento1 páginaInfografía CT PDFBrian Alexander Remuzgo Palacios100% (2)
- Marco Teorico Osmosis y Presion OsmoticaDocumento2 páginasMarco Teorico Osmosis y Presion OsmoticaGuillermo67% (3)
- Mapa MentalDocumento1 páginaMapa Mentalazalia flor de frioAún no hay calificaciones
- CONSULTA Acido y BasesDocumento7 páginasCONSULTA Acido y BasesDaniela AlejandroAún no hay calificaciones
- Mapa Clasificacion de La FisicaDocumento1 páginaMapa Clasificacion de La FisicaDafne Marquez50% (2)
- Tutupaka LlaktaDocumento2 páginasTutupaka LlaktaCristhian Horna Pastor100% (2)
- Hoja de Trabajo 1 Conversión de UnidadesDocumento7 páginasHoja de Trabajo 1 Conversión de UnidadesARIANA BRISIP CHOZO LOPEZAún no hay calificaciones
- Proteinas TripticoDocumento2 páginasProteinas TripticoRober Johan Olivas Inocente0% (1)
- Genética Mendeliana Mapa Mental PDFDocumento1 páginaGenética Mendeliana Mapa Mental PDFGiancarlo Ciarrocchi SotoAún no hay calificaciones
- Informe Circuitos BasicosDocumento17 páginasInforme Circuitos BasicoswilliamshurtadoAún no hay calificaciones
- Evolucion Del AtomoDocumento1 páginaEvolucion Del AtomoWendy Guaman Mendoza0% (1)
- Proyecto 6 Semana 3 - BiologiaDocumento1 páginaProyecto 6 Semana 3 - BiologiaJahir Noles OrdoñezAún no hay calificaciones
- Qué Es La Savia BrutaDocumento1 páginaQué Es La Savia BrutaJheymel Romero100% (1)
- Genetica Ovejas AnconDocumento19 páginasGenetica Ovejas AnconsofiaignaciaAún no hay calificaciones
- Carga Eléctrica para Segundo Grado de Segundaria PDFDocumento2 páginasCarga Eléctrica para Segundo Grado de Segundaria PDFYann Pablo PachecoAún no hay calificaciones
- Aminas EditadoDocumento13 páginasAminas EditadoMaria Paulina Villa ContrerasAún no hay calificaciones
- Bio Qui MicaDocumento2 páginasBio Qui MicaMony Jimenez Fierro0% (1)
- Guia 3 Determinacion de La DensidadDocumento10 páginasGuia 3 Determinacion de La DensidadNayeli Abigail PerdomoAún no hay calificaciones
- INFOGRAFIADocumento1 páginaINFOGRAFIAGloria Santos100% (2)
- Metales AlcalinotérreosDocumento12 páginasMetales AlcalinotérreosDIEGO FERNANDO CRUZ PRIETOAún no hay calificaciones
- 25 Energía MecánicaDocumento7 páginas25 Energía MecánicaANDRES JIMENEZAún no hay calificaciones
- Act - Mapa Mental BencenoDocumento1 páginaAct - Mapa Mental BencenoAri AnzuresAún no hay calificaciones
- InfografíaDocumento2 páginasInfografíaDayanne Nathaly Valencia RomeroAún no hay calificaciones
- Cuadro Sinoptico MicroorganismosDocumento3 páginasCuadro Sinoptico MicroorganismosαlιzAún no hay calificaciones
- Observación Experimental de La Emisión de Espectros A La LlamaDocumento12 páginasObservación Experimental de La Emisión de Espectros A La LlamaLEIDY VANESSA ROMERO ORTIZAún no hay calificaciones
- Prevención en Situaciones de Riesgos y Cuidado SocioambientalDocumento4 páginasPrevención en Situaciones de Riesgos y Cuidado SocioambientalcristianAún no hay calificaciones
- Mapa Cifras SignificativasDocumento2 páginasMapa Cifras SignificativasLisbeth RomeroAún no hay calificaciones
- Fundamento 2 - Campo EléctricoDocumento1 páginaFundamento 2 - Campo EléctricoJoe Coloma AñazcoAún no hay calificaciones
- Mapa Mental de Las Magnitudes EléctricasDocumento1 páginaMapa Mental de Las Magnitudes EléctricasYugi Roses100% (1)
- Ciclo Del Nitrogeno Mapa ConceptualDocumento1 páginaCiclo Del Nitrogeno Mapa ConceptualJonathanAún no hay calificaciones
- Cambiado y Qué Ha Permanecido en La Actividad Laboral de Las Mujeres de Mi Comunidad?Documento3 páginasCambiado y Qué Ha Permanecido en La Actividad Laboral de Las Mujeres de Mi Comunidad?Franklin VilcaAún no hay calificaciones
- Fotosintesis Tema PDFDocumento5 páginasFotosintesis Tema PDFZenobio Gonzales CopAún no hay calificaciones
- Laboratorio 5. ElectromagnetismoDocumento6 páginasLaboratorio 5. ElectromagnetismoCesar Augusto Fernandez GarciaAún no hay calificaciones
- ¿Qué Es El Movimiento?Documento3 páginas¿Qué Es El Movimiento?Alexandra Ramos GarciaAún no hay calificaciones
- Infografia Celula VegetalDocumento1 páginaInfografia Celula VegetalJessica García López100% (1)
- Azul Claro Suave y Redondeado Infografía CronológicaDocumento2 páginasAzul Claro Suave y Redondeado Infografía CronológicaJosé Leonardo Flores RodríguezAún no hay calificaciones
- Carbohidratos Organizador GraficoDocumento1 páginaCarbohidratos Organizador GraficoQuebin Pichucho0% (1)
- Infografia de La SexualidadDocumento1 páginaInfografia de La SexualidadManuel González100% (2)
- EL ÁTOMO Mapa ConceptualDocumento1 páginaEL ÁTOMO Mapa ConceptualCarlos CastroAún no hay calificaciones
- Ecuacion Canonica de La ParabolaDocumento4 páginasEcuacion Canonica de La ParabolaPercy Adolfo Torres Avalos100% (1)
- Mapa Conceptual ElectrólisisDocumento1 páginaMapa Conceptual ElectrólisisJosé Andrés Sánchez BagüiAún no hay calificaciones
- ElectroquímicaDocumento9 páginasElectroquímicaInstrumentos RAún no hay calificaciones
- Informe Electroquimica ReDocumento7 páginasInforme Electroquimica RePaola AndreaAún no hay calificaciones
- Proyectos Pecuarios Exposición Aves Pollos ParrillerosDocumento15 páginasProyectos Pecuarios Exposición Aves Pollos ParrillerosJosé Andrés Sánchez BagüiAún no hay calificaciones
- Exposición Razas y Líneas Especies Avícolas Sánchez Bagüi José AndrésDocumento6 páginasExposición Razas y Líneas Especies Avícolas Sánchez Bagüi José AndrésJosé Andrés Sánchez BagüiAún no hay calificaciones
- Estudio Técnico en La Crianza de Pollos ParrillerosDocumento23 páginasEstudio Técnico en La Crianza de Pollos ParrillerosJosé Andrés Sánchez BagüiAún no hay calificaciones
- Manejo de Aves Ponedoras Expo GrupoDocumento17 páginasManejo de Aves Ponedoras Expo GrupoJosé Andrés Sánchez BagüiAún no hay calificaciones
- Ayuno y Faenamiento Expo GrupalDocumento19 páginasAyuno y Faenamiento Expo GrupalJosé Andrés Sánchez Bagüi100% (1)
- Caracterizacion Particular en Ciertas Razas de Especie Ovinos y Caprinos en El Ecuador Trabajo Grupal 7mo A P.O&C.Documento10 páginasCaracterizacion Particular en Ciertas Razas de Especie Ovinos y Caprinos en El Ecuador Trabajo Grupal 7mo A P.O&C.José Andrés Sánchez BagüiAún no hay calificaciones
- EXTENCIONISMO-INFO GRUPO #2 EXPO 9noDocumento9 páginasEXTENCIONISMO-INFO GRUPO #2 EXPO 9noJosé Andrés Sánchez BagüiAún no hay calificaciones
- Informe de Proceso de FaenamientoDocumento11 páginasInforme de Proceso de FaenamientoJosé Andrés Sánchez BagüiAún no hay calificaciones
- Mapa Conceptual ElectrólisisDocumento1 páginaMapa Conceptual ElectrólisisJosé Andrés Sánchez BagüiAún no hay calificaciones
- Desarrollo-Poblacional Bovinos de Leche Yinio Castro para Copiar.Documento1 páginaDesarrollo-Poblacional Bovinos de Leche Yinio Castro para Copiar.José Andrés Sánchez BagüiAún no hay calificaciones
- Titulacion Acido BaseDocumento75 páginasTitulacion Acido BaseBiblio ScribAún no hay calificaciones
- LABORATORIO No 2 - SUSTITUCIÓN NUCLEOFÍLICADocumento8 páginasLABORATORIO No 2 - SUSTITUCIÓN NUCLEOFÍLICACarlos ZambranoAún no hay calificaciones
- Anotomofisiología y PatologíaDocumento70 páginasAnotomofisiología y Patologíanuedus corporativoAún no hay calificaciones
- Prototipo Alarma CaseraDocumento19 páginasPrototipo Alarma Caserachicaespia-46100% (4)
- Cuestionario de QuímicaDocumento11 páginasCuestionario de QuímicaWilsom RomeroAún no hay calificaciones
- NTP 339.178 SulfatosDocumento21 páginasNTP 339.178 SulfatosVladimir Aquino Rivera100% (2)
- DIGESTIÓN IN VITRO DE ALMIDÓN Informe 7Documento11 páginasDIGESTIÓN IN VITRO DE ALMIDÓN Informe 7Juan Diego VelasquezAún no hay calificaciones
- 6 Calculos EstequiometricosDocumento3 páginas6 Calculos Estequiometricosaltar13Aún no hay calificaciones
- Evidencia Procedimiento "Prevención de Riesgos"Documento25 páginasEvidencia Procedimiento "Prevención de Riesgos"Alonso Niño Bueno100% (1)
- Cuento de QuímicaDocumento2 páginasCuento de Químicavalenthinarodriguez199878% (9)
- Informe 1 de Quimica OrganicaDocumento10 páginasInforme 1 de Quimica OrganicaANDERSSONAún no hay calificaciones
- Practica BiomaterialesDocumento3 páginasPractica BiomaterialesalissonAún no hay calificaciones
- PRÁCTICA 05, Marcos Isaias Chuquiruna Chunque.Documento21 páginasPRÁCTICA 05, Marcos Isaias Chuquiruna Chunque.MARCOS ISAIAS CHUQUIRUNA CHUNQUEAún no hay calificaciones
- Mapa Mental 8 Ideas de Marketing Minimalista Verde y LilaDocumento5 páginasMapa Mental 8 Ideas de Marketing Minimalista Verde y LilaJACK LENIN MERINO GARCIAAún no hay calificaciones
- Ajuste y Protocolo de Cementación en Restauraciones Estéticas y MetálicasDocumento47 páginasAjuste y Protocolo de Cementación en Restauraciones Estéticas y MetálicasMoctezuma Pavón CitlallyAún no hay calificaciones
- Grasas y AceitesDocumento29 páginasGrasas y Aceitesana huamanAún no hay calificaciones
- Obtención Del Nylon 6Documento7 páginasObtención Del Nylon 6Angie TatianaAún no hay calificaciones
- Experimento 6Documento2 páginasExperimento 6MarinaChavesAún no hay calificaciones
- Practica N 5 Alcoholes y FenolesDocumento5 páginasPractica N 5 Alcoholes y FenolesSaul LopezAún no hay calificaciones
- ORLANDO FARID REYES BAUTISTA - Reactivos y ProductosDocumento6 páginasORLANDO FARID REYES BAUTISTA - Reactivos y ProductosOscar I. Reyes BautistaAún no hay calificaciones
- Lab. Organica II Informe 5 - FenolftaleinaDocumento7 páginasLab. Organica II Informe 5 - FenolftaleinaAnonymous GdWMlV46bUAún no hay calificaciones
- Clase 9-Pirometalurgia-2020Documento35 páginasClase 9-Pirometalurgia-2020yairAún no hay calificaciones
- Baraja Loteria Tabla PeriodicaDocumento12 páginasBaraja Loteria Tabla PeriodicaSpriggan2010100% (2)
- Inor 2P 2022 2Documento2 páginasInor 2P 2022 2Fabritzio- KunAún no hay calificaciones
- Informe FarmacologiaDocumento23 páginasInforme FarmacologiajhonnyAún no hay calificaciones
- Problemario de Equilibrio QuímicoDocumento2 páginasProblemario de Equilibrio QuímicoLaloulisesAún no hay calificaciones
- Clase #19 Obtención de Metales A Patir de SulfurosDocumento20 páginasClase #19 Obtención de Metales A Patir de SulfurosBraulio ala andia100% (1)
- Biologia CompletaDocumento561 páginasBiologia CompletaKatrina YañezAún no hay calificaciones
- HDS Hipoclorito de CalcioDocumento3 páginasHDS Hipoclorito de Calcioviviana castilloAún no hay calificaciones
- Trabajo NomenclaturaDocumento4 páginasTrabajo NomenclaturaCarlos Andres CosuegraAún no hay calificaciones