Documentos de Académico
Documentos de Profesional
Documentos de Cultura
04 Adap Curricular
04 Adap Curricular
Cargado por
joseDerechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
04 Adap Curricular
04 Adap Curricular
Cargado por
joseCopyright:
Formatos disponibles
ADAPTACIÓN CURRICULAR
4 LA MATERIA
EN LA NATURALEZA
1. Los estados de la materia
2. Propiedades de los estados de la materia
3. La teoría cinético-molecular
4. Los cambios de estado
5. Clasificación de la materia
6. Mezclas homogéneas o disoluciones
7. ¿Qué es y cómo se calcula la concentración de la
disolución?
8. Los coloides
9. Métodos de separación de mezclas
© Oxford University Press España, S. A.
4 La materia en la naturaleza. Adaptación curricular
Física y Química 2º ESO
Adaptación curricular. La materia en la naturaleza 4
1. LOS ESTADOS DE LA MATERIA
La materia es todo aquello que tiene masa y ocupa un lugar en el espacio, ya sea
algo visible, como una piedra, o no visible para nuestros ojos, como el aire.
La materia ordinaria se puede encontrar en tres estados: sólido (como nuestra
mesa), líquido (como la tinta del bolígrafo con el que escribimos) y gaseoso
(como el aire que respiramos).
ACTIVIDADES
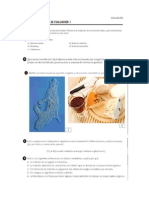
1.1. Observa los frascos de la imagen. ¿Crees que hay materia dentro de ellos?
Justifica tu respuesta.
1.2. Busca, a tu alrededor, algún ejemplo de materia en estado sólido.
1.3. ¿Qué ejemplos de materia en estado líquido conoces? Indica, al menos dos.
1.4. ¿Existe materia en estado gaseoso a nuestro alrededor? Pon algún ejemplo.
1.5. Busca en esta sopa de letras dos sustancias sólidas, dos líquidas y dos gaseo-
sas:
T R M A N S F O Sustancias sólidas:
© Oxford University Press España, S. A.
O Z R A U C R M
S E A R D C I B Sustancias líquidas:
A O T C N E D U
N E S I O L R T Sustancias gaseosas:
G I D L E O E A
R N L L I C Q N
E R I A D O A O
Física y Química 2º ESO
4 La materia en la naturaleza. Adaptación curricular
1.6. Completa los siguientes enunciados:
a) La materia se presenta en tres estados, que son: ,
y .
b) Algunos ejemplos de sustancias sólidas son: y
.
c) En nuestro cuerpo podemos encontrar como los
huesos y los músculos, como la sangre y la orina,
y como el aire que contiene nuestros pulmones.
© Oxford University Press España, S. A.
Física y Química 2º ESO
Adaptación curricular. La materia en la naturaleza 4
2. PROPIEDADES DE LOS ESTADOS
DE LA MATERIA
Los estados de la materia poseen propiedades diferentes entre sí, lo que les hace
tener comportamientos muy distintos.
Estado sólido Estado líquido Estado gaseoso
Los sólidos no cambian Los líquidos cambian de Los gases tienen
de forma ni de masa forma si cambiamos el masa y ocupan cierto
aunque los cambiemos recipiente en el que se volumen. Su volumen
de recipiente. Su encuentran. Su masa y su forma varían
volumen tampoco y su volumen no según el recipiente que
cambiará. cambian. los contenga.
No se pueden No se pueden Se pueden comprimir
comprimir. comprimir. con facilidad.
Los gases ocupan todo el volumen del recipiente en el que se encuentran: puedes
comprobarlo abriendo un frasco de colonia en un extremo de la clase: al cabo de
un tiempo el olor se percibirá en toda la habitación.
ACTIVIDADES
2.1. Propón algún experimento en el que se demuestre que los gases tienen masa.
2.2. Completa el siguiente cuadro con una de estas dos palabras:
❚❚ Constante
❚❚ Variable
Sólidos Líquidos Gases
Masa
Forma
© Oxford University Press España, S. A.
Volumen
Física y Química 2º ESO
4 La materia en la naturaleza. Adaptación curricular
2.3. Indica si las siguientes afirmaciones son verdaderas o falsas:
a) Los líquidos adquieren la forma del recipiente que los contiene.
b) Los sólidos pueden comprimirse.
c) Los gases ocupan siempre el mismo volumen aunque cambiemos su reci-
piente.
d) Los gases y los líquidos tienen siempre la misma forma.
© Oxford University Press España, S. A.
Física y Química 2º ESO
Adaptación curricular. La materia en la naturaleza 4
3. LA TEORÍA CINÉTICO-MOLECULAR
La Teoría cinético-molecular es un modelo que explica la naturaleza de la mate-
ria y permite justificar su comportamiento. Propone las siguientes ideas:
❚❚ La materia está compuesta por pequeñísimas partículas, invisibles.
❚❚ Entre las que existen fuerzas de atracción.
❚❚ Estas partículas están en continuo movimiento.
❚❚ A mayor temperatura, mayor velocidad tienen las partículas.
Sólidos Líquidos Gases
❚❚ Las partículas están muy próximas. ❚❚ Las partículas están bastante próximas. ❚❚ Las partículas están muy separadas.
❚❚ Las fuerzas de atracción son muy ❚❚ Las fuerzas de atracción son intensas ❚❚ Las fuerzas de atracción son muy
intensas. (menos que en los sólidos). débiles.
❚❚ Las partículas ocupan posiciones fijas ❚❚ Las partículas pueden desplazarse ❚❚ Las partículas pueden moverse
y solo pueden vibrar. y vibrar. libremente.
ACTIVIDADES
3.1. Visita el siguiente enlace web:
http://inicia.oupe.es/fq2s0408
En él podrás observar qué es lo que ocurre en el interior de la materia, según
cuál sea el estado de agregación en el que se encuentre. A continuación,
responde a las siguientes cuestiones:
a) ¿En qué estado se encuentran más libres las partículas?
b) ¿En qué estado están más juntas las partículas?
c) Las partículas de los sólidos, ¿pueden cambiar de posición unas con otras?
¿Cuál es el único tipo de movimiento que pueden hacer?
© Oxford University Press España, S. A.
d) ¿Pueden las partículas de los líquidos desplazarse y cambiar de posición?
Física y Química 2º ESO
4 La materia en la naturaleza. Adaptación curricular
3.2. Explica la siguiente afirmación: «El agua no se comprime al apretar el émbolo
de una jeringuilla, pero el aire sí».
© Oxford University Press España, S. A.
Física y Química 2º ESO
Adaptación curricular. La materia en la naturaleza 4
4. LOS CAMBIOS DE ESTADO
La materia puede pasar de un estado a otro. Por ejemplo, si sacamos un cubito
de hielo del congelador, éste se derrite y se transforma en agua líquida. Si después
calentamos el agua, ésta pasará a estado gaseoso. A estos cambios se les llama
cambios de estado.
En los cambios de estado la materia sigue siendo la misma, no cambia la sus-
tancia de partida, tan sólo varía su estado.
En el siguiente esquema se muestran los nombres de todos los cambios de estado:
Sublimación
Fusión Vaporización
SÓLIDO LÍQUIDO GAS
Solidificación Condensación
El hielo seco (CO2 sólido) pasa directa-
Sublimación mente de estado sólido a gaseoso sin
inversa o regresiva pasar por el estado líquido.
ACTIVIDADES
4.1. Piensa y explica: ¿Por qué aparecen algunas veces en invierno placas de hielo
sobre el asfalto de las carreteras?
4.2. Piensa y explica: ¿Por qué se empaña el espejo de nuestro baño cuando nos
duchamos?
4.3. Completa los espacios en blanco:
a) El paso de sólido a líquido recibe el nombre de .
b) La solidificación es el cambio de líquido a .
c) Cuando se derrite el hielo, decimos que se ha .
d) El paso de gas a líquido se denomina .
© Oxford University Press España, S. A.
e) Cuando una sustancia pasa de un estado a otro diferente se dice que ha
experimentado un .
Física y Química 2º ESO
4 La materia en la naturaleza. Adaptación curricular
4.1. Dos formas de vaporizar: evaporación y ebullición
El paso del estado líquido al gaseoso se llama vaporización. Puede producirse de
dos formas diferentes, conocidas como evaporación y ebullición:
Evaporación Ebullición
❚❚ Ocurre a cualquier temperatura. ❚❚ Ocurre a una temperatura fija para
cada sustancia (por ejemplo, el agua
❚❚ Se produce en la superficie del
líquida hierve a 100 oC).
líquido, capa a capa.
❚❚ Afecta a toda la masa del líquido.
Gracias a la evaporación la ropa que
lavamos puede secarse sea invierno o ❚❚ Ocurre de forma violenta.
verano.
Este fenómeno ocurre cuando ponemos
agua a hervir.
ACTIVIDADES
4.4. Piensa y completa los espacios en blanco:
La vaporización puede darse de dos formas: a una temperatura fija y en
toda la masa del líquido (llamada )
o a cualquier temperatura y en la superficie del líquido (llamada
).
4.5. ¿Qué ocurrirá si echas un poco de colonia en un vaso y lo dejas al aire?
4.6. ¿Es imprescindible que los líquidos hiervan para conseguir que pasen a estado
gaseoso? Justifica tu respuesta ayudándote de algún ejemplo.
© Oxford University Press España, S. A.
4.7. El agua hierve a 100 oC. ¿Podemos afirmar que el aceite que utilizamos en la
freidora o en la sartén también hervirá a esa temperatura?
Física y Química 2º ESO
Adaptación curricular. La materia en la naturaleza 4
5. CLASIFICACIÓN DE LA MATERIA
La materia se puede clasificar en dos grupos:
❚❚ Sustancias puras: no se pueden separar en otras sustancias más simples por
procedimientos físicos. Ejemplos: el hierro, el oxígeno, el dióxido de carbono, el
agua.
❚❚ Mezclas: combinación de dos o más sustancias que se pueden separar por pro-
cedimientos físicos. Ejemplos: el agua salada, el aceite con agua.
Los procedimientos físicos son aquellos que no alteran el tipo de partículas que
componen las sustancias originales.
Las mezclas, a su vez, pueden dividirse en:
Mezclas homogéneas o disoluciones Mezclas heterogéneas
Sus componentes no se pueden Sus componentes se distinguen a
distinguir, ni a simple vista ni con ni simple vista o con un microscopio
microscopio óptico. Ejemplos: el agua óptico. Ejemplos: el granito o el agua
azucarada o el aire. con aceite.
ACTIVIDADES
5.1. Pon dos ejemplos de sustancias puras, dos de mezclas homogéneas y otros
dos de mezclas heterogéneas frecuentes en la vida diaria.
5.2. Indica si son homogéneas o heterogéneas las mezclas siguientes:
a) arena con hierro
b) agua con sal
c) aire
d) azúcar glas (o glasé) con azúcar en grano © Oxford University Press España, S. A.
e) agua con vinagre
f) vinagre con aceite
g) agua con serrín
Física y Química 2º ESO
4 La materia en la naturaleza. Adaptación curricular
6. MEZCLAS HOMOGÉNEAS O DISOLUCIONES
En las mezclas homogéneas o disoluciones las partículas de todas las sustancias
se entremezclan tan bien, que resulta imposible distinguirlas.
Todas las disoluciones constan de dos componentes:
❚❚ Disolvente: sustancia que se encuentra en mayor cantidad en la disolución.
❚❚ Soluto: sustancia o sustancias que se encuentran en menor cantidad en la
disolución.
El soluto y el disolvente pueden estar en cualquier estado de agregación. Lo más
habitual es que el disolvente se encuentre en estado líquido.
Algunas de las disoluciones más frecuentes que podemos encontrar son:
❚❚ Disoluciones acuosas: el disolvente es el
agua.
❚❚ Aleaciones: disoluciones formadas por dos o
más elementos químicos, siendo al menos uno
de ellos un metal. Ejemplos: bronce, acero o
latón.
ACTIVIDADES
6.1. Pon algún ejemplo de disolución acuosa.
6.2. Busca dos ejemplos de disoluciones que no sean líquidas.
6.3. Busca información sobre la mezcla de gases que forman el gas natural.
6.4. La composición de un refresco es: 10 % de azúcar, 45 % de agua, 30 % de
zumo de naranja, 14,9 % de dióxido de carbono y 0,1 % de conservantes y
colorantes. Indica cuál es el disolvente, cuáles los solutos y en qué estado se
encuentra cada uno.
© Oxford University Press España, S. A.
Física y Química 2º ESO
Adaptación curricular. La materia en la naturaleza 4
7. ¿QUÉ ES Y CÓMO SE CALCULA LA
CONCENTRACIÓN DE UNA DISOLUCIÓN?
La concentración de una disolución nos indica la cantidad de soluto presente en
una cantidad dada de disolvente o de disolución.
Para medir la concentración de una disolución podemos usar distintas unidades:
7.1. Tanto por ciento en masa
masa de soluto (g)
% en masa (soluto) = ⋅100
masa de disolución (g)
EJERCICIO RESUELTO
1. Preparamos una disolución disolviendo 5 g de azúcar en 45 g de
agua. Calcula el tanto por ciento en masa de soluto de la disolución.
En primer lugar, debemos reconocer cuál es el soluto y cuál es el
disolvente en esta disolución:
❚❚ Soluto → azúcar (en menor proporción)
❚❚ Disolvente → agua (en mayor proporción)
A continuación, calculamos la masa de disolución a partir de los
datos del problema:
m (soluto) = 5 g
m (disolvente) = 45 g
m (disolución) = m (soluto) + m (disolvente) = 5 g + 45 g = 50 g
Sustituimos en la expresión del tanto por ciento en masa de soluto:
masa de soluto (g) 5g
% en masa (azúcar) = ⋅100 = ⋅100 = 10%
masa de disolución (g) 50 g
7.2. Concentración en masa (g/L)
masa de soluto (g)
g/L =
volumen de disolución (L)
EJERCICIO RESUELTO
2. Un estudiante prepara una disolución disolviendo 15 g de yodo en
alcohol hasta conseguir un volumen final de disolución de 250 mL.
Calcula la concentración en masa de la disolución resultante.
❚❚ Soluto → yodo (en menor proporción)
❚❚ Disolvente → alcohol (en mayor proporción)
© Oxford University Press España, S. A.
A continuación, puesto que ya conocemos los gramos de soluto
(15 g), debemos calcular el volumen de disolución en litros:
m (soluto) = 15 g
V (disolución) = 250 mL = 0,25 L
Sustituimos en la expresión de la concentración en masa:
masa de soluto (g) 15 g
g/L = = = 60 g/L
volumen de disolución (L) 0 ,25 L
Física y Química 2º ESO
4 La materia en la naturaleza. Adaptación curricular
ACTIVIDADES
7.1. Se disuelven 15 g de azúcar y 5 g de sal en 230 g de agua.
a) Indica cuál o cuáles son los solutos y cuál es el disolvente.
b) Calcula el tanto por ciento en masa de cada soluto en la disolución resul-
tante.
7.2. Calcula el tanto por ciento en masa de una disolución de azúcar en agua si
contiene 30 g de soluto en 600 g de agua.
7.3. ¿Qué concentración en masa tendrá una disolución preparada a partir de 12
g de cloruro de potasio y 300 cm3 de agua?
7.4. Calcula la concentración en g/L de una disolución que contiene 7 g de una
sustancia pura en medio litro de agua.
7.5. Tomamos un vaso de agua de mar (200 g) y dejamos que se evapore todo el
agua, quedando en el recipiente 4,5 g de sal común. Calcula el porcentaje en
© Oxford University Press España, S. A.
masa de sal común que contiene el agua de ese mar.
Física y Química 2º ESO
Adaptación curricular. La materia en la naturaleza 4
7.3. ¿Cómo se prepara una disolución?
El procedimiento consta de los siguientes pasos:
1. Calcular la masa de soluto que 2. Pesar la masa de soluto con una 3. Añadir un poco de agua destilada
necesitamos. balanza digital, empleando un vaso al vaso de precipitados, agitando
de precipitados. bien con una varilla de vidrio hasta
disolverlo por completo.
#
*
0 %
4. Con la ayuda de un embudo, echar la disolución que se 5. Añadir agua al matraz hasta acercarnos a la marca
acaba de obtener en un matraz aforado del volumen de enrase. El volumen que falte para llegar exactamente
que necesitamos, enjuagando al menos un par de veces el a esa marca, se añadirá con un cuentagotas para no
vaso de precipitados con un poco más de agua. pasarnos. Poner el tapón al matraz aforado y agitar bien
el contenido.
ACTIVIDADES
7.6. ¿Qué material de laboratorio se emplea en la preparación de una disolución?
Indica los nombres y haz un dibujo de cada uno de ellos en tu cuaderno.
7.7. Un estudiante quiere preparar 0,5 L de una disolución de nitrato de potasio
(KNO3), para lo cual debe pesar 6,5 g de dicha sustancia.
a) Describe, paso a paso, el procedimiento que debe seguir y el material que
debe utilizar.
b) Calcula la concentración en masa que tendrá la disolución preparada.
© Oxford University Press España, S. A.
Física y Química 2º ESO
4 La materia en la naturaleza. Adaptación curricular
8. LAS DISPERSIONES COLOIDALES
Algunos sistemas materiales parecen disoluciones pero realmente no lo son.
Las dispersiones o disoluciones coloidales son un tipo especial de mezclas
heterogéneas en las que las partículas de soluto (invisibles a simple vista) tienen un
tamaño intermedio entre el de las disoluciones y el de las mezclas heterogéneas.
Debido a su tamaño, las partículas de soluto son
capaces de dispersar la luz, algo que no ocurre
en las disoluciones. Este fenómeno se denomina
efecto Tyndall y puede observarse al circular en
coche con las luces dadas un día de niebla: la luz
de los faros será dispersada en muchas direccio-
nes por las gotitas de agua, pudiéndose observar
fácilmente el haz e incluso distinguir las pequeñas
gotas de agua en suspensión.
A nuestro alrededor encontramos muchos ejem-
plos de dispersiones coloidales: jabones, mante-
quillas, cremas, espumas, niebla, aerosoles, nu-
bes, gelatina…
ACTIVIDADES
8.1. Los días de niebla es frecuente apreciar la dispersión de la luz de los faros por
las finísimas gotas de agua que hay en suspensión en el aire.
a) ¿Cómo se denomina este efecto?
b) ¿Se te ocurre algún otro fenómeno cotidiano en el que se dé también
dicho efecto?
8.2. ¿Reconoces algún coloide entre las siguientes mezclas?
a) niebla
b) agua con sal
c) espuma de jabón
d) agua con arena
e) agua con alcohol
f) cremas cosméticas
g) gelatina
© Oxford University Press España, S. A.
8.3. Busca en internet ejemplos de coloides que podamos encontrar en alimentos.
Física y Química 2º ESO
Adaptación curricular. La materia en la naturaleza 4
9. MÉTODOS DE SEPARACIÓN DE MEZCLAS
Las sustancias puras presentan propiedades específicas que nos permiten separar-
las de otras.
Los métodos de separación más usados son:
9.1. Separación magnética
Solo puede emplearse si alguna de las sustancias a separar presenta propiedades
magnéticas (como el hierro) y el resto no.
Para ello se aproxima el imán a la mezcla, de manera que atraerá el material con Separación
propiedades magnéticas, separándolo del resto de componentes. magnética.
9.2. Decantación
Se emplea para separar líquidos con densidades diferentes y que no se mezclan
entre sí (inmiscibles), como ocurre con el agua y el aceite. Se utiliza un embudo
de decantación.
1. Se vierte la mezcla dentro del embudo de decantación y se deja reposar hasta
que las sustancias se separen, quedando una encima de otra.
2. Se abre la llave y pasa primero el líquido más denso (el agua).
3. Cuando el líquido más denso ha pasado, se cierra la llave para que el otro líqui-
do no pase.
4. El líquido más denso queda en un vaso que se sitúa debajo del embudo, mien-
tras que el menos denso permanece en el embudo de decantación; éste se
sacará por la parte superior del embudo.
Decantación.
9.3. Filtración
Se usa para separar un sólido de un líquido en el cual no se disuelve, como sería
el caso de agua con arena.
Para ello, se hace pasar la mezcla heterogénea a través de un filtro (generalmente
un papel de filtro acoplado a un embudo), de manera que el sólido queda retenido
en el filtro, y el líquido pasa a un vaso de precipitados o a un erlenmeyer.
ACTIVIDADES
9.1. ¿Cómo separarías los componentes de una mezcla de aceite y vinagre?
9.2. ¿Cómo separarías los componentes de una mezcla de serrín y agua?
Filtración.
9.3. ¿Podrías utilizar la separación magnética para separar una mezcla de aluminio
y sal?
© Oxford University Press España, S. A.
Física y Química 2º ESO
4 La materia en la naturaleza. Adaptación curricular
termómetro cabeza de destilación 9.4. Destilación
refrigerante Se utiliza para separar líquidos solubles entre sí que tienen
destilado temperaturas de ebullición muy diferentes, como es el
caso del agua y el alcohol. Para llevarla a cabo es necesario
colector
usar un montaje como el que aparece en la figura.
Se echa la mezcla en un matraz esférico y se calienta.
salida
de agua Cuando se alcanza la temperatura de ebullición más baja de
entrada los componentes, dicho líquido comienza a convertirse en
de agua vapor, pasando por el refrigerante, donde se enfriará y con-
densará.
Destilación. El líquido resultante (destilado) se recoge en un recipiente (un
vaso de precipitados, por ejemplo).
9.5. Evaporación y cristalización
Se emplea para separar un soluto sólido disuelto en un
cristalización
disolvente líquido, como por ejemplo la sal en agua.
El disolvente se evapora (de forma natural o forzada median-
te calefacción) y el sólido queda en el fondo del recipiente
concentración filtración
(generalmente un cristalizador) en forma de cristales. Cuan-
Evaporación y cristalización. to más lento sea el proceso, más grandes serán los cristales.
9.6. Cromatografía
Se usa para separar los componentes de una mezcla, según la mayor o menor
afinidad de cada uno de ellos por el disolvente empleado.
Una de las técnicas de cromatografía más sencillas es la cromatografía en papel,
que utiliza una tira de papel de filtro.
1. Se deposita en la tira de papel una pequeñísima porción de la mezcla (un punti-
to) y se introduce la parte inferior en un disolvente (por ejemplo, alcohol).
2. El disolvente ascenderá lentamente por el papel, arrastrando en su camino los
Cromatografía.
componentes de la mezcla.
3. Los componentes que alcancen mayor altura en la tira serán los que mayor afi-
nidad tenían por el disolvente y los que alcancen menor altura, los que menor
afinidad presentaban por el disolvente.
Este método se utiliza para separar los pigmentos fotosintéticos (clorofila, carote-
nos, etc.) de las espinacas y otros vegetales.
ACTIVIDADES
9.4. Tienes un recipiente con agua salada. ¿Cómo separarías los componentes de
esta mezcla?
© Oxford University Press España, S. A.
9.5. ¿Se te ocurre alguna técnica para separar los distintos colores que forman la
tinta negra de un rotulador?
9.6. ¿Para qué sirve el refrigerante en la destilación?
Física y Química 2º ESO
Adaptación curricular. La materia en la naturaleza 4
EVALUACIÓN. SOLUCIÓN
1. Coloca en la columna correspondiente según se trate de sólidos, líquidos o gases: agua, aire, papel, dióxido de carbono,
aceite, acero, zumo de naranja, oro, butano y mármol.
SÓLIDOS LÍQUIDOS GASES
2. Indica si son verdaderos o falsos estos enunciados y corrígelos:
a) Las partículas sólo se mueven en los gases.
b) Los líquidos y los sólidos no se pueden comprimir.
c) Las partículas de los sólidos tienen total libertad de movimiento.
d) Los líquidos tienden a ocupar todo el volumen del recipiente que los contiene.
e) Las fuerzas de atracción entre las partículas de los sólidos son muy intensas.
3. Completa los espacios en blanco con la palabra adecuada:
a) El paso de líquido a sólido recibe el nombre de .
b) La fusión es el cambio de sólido a .
c) Cuando la vaporización ocurre a una temperatura fija, en toda la masa del líquido y de forma violenta se denomina
.
d) El paso de gas a sólido se denomina .
4. ¿Qué proceso ocurre para que podamos percibir el olor de un perfume cuyo frasco está abierto?
© Oxford University Press España, S. A.
5. Clasifica según se trate de mezclas homogéneas o heterogéneas: arena fina con grava, agua con miel, chocolate con pi-
catostes, agua con hielo, café molido con café en grano, acero, agua salada, bronce, agua con cereales, arena con hierro,
agua con aceite, bebidas gaseosas.
Física y Química 2º ESO
4 La materia en la naturaleza. Adaptación curricular
6. ¿Cuál es la concentración en masa de una disolución de bromuro de potasio en agua, obtenida al disolver 5 g de dicha
sal en agua hasta conseguir un volumen final de disolución de medio litro?
7. Preparamos una disolución disolviendo 30 g de sal en 120 g de agua.
a) Justifica cuál es el soluto y cuál el disolvente.
b) Calcula la masa de la disolución.
c) Calcula el porcentaje en masa de soluto de esta disolución.
8. ¿Qué son las dispersiones coloidales? Indica al menos tres ejemplos.
9. Dado el siguiente montaje:
a) Indica, en los espacios en blanco, el nombre de cada una de estas partes: Refrigerante, termómetro, destilado, matraz
esférico, erlenmeyer.
b) ¿De qué método de separación se trata? ¿Qué condición deben cumplir los componentes de la mezcla para poder
separarlos con este método?
10. ¿Cómo separarías los componentes de estas mezclas? Explica qué propiedad se utiliza para su separación:
© Oxford University Press España, S. A.
a) Arena y trocitos de hierro.
b) Alcohol y agua.
c) Azúcar y arena.
Física y Química 2º ESO
También podría gustarte
- Ud6 - Las Fuerzas en La Naturaleza - Fyq2ºesoDocumento4 páginasUd6 - Las Fuerzas en La Naturaleza - Fyq2ºesoAllan IntriagoAún no hay calificaciones
- Examen TEMA 2 GEOGRAFÍA 2º Eso EDocumento6 páginasExamen TEMA 2 GEOGRAFÍA 2º Eso EDIEGO REINA ALMAGROAún no hay calificaciones
- Solucionario Fisica y Quimica 2 ESO Santillana TEMA 4 Cambios en La MateriaDocumento15 páginasSolucionario Fisica y Quimica 2 ESO Santillana TEMA 4 Cambios en La MateriaAnitaAún no hay calificaciones
- Que Es NujolDocumento6 páginasQue Es NujolCinthya MaciasAún no hay calificaciones
- Fyq 2º EsoDocumento9 páginasFyq 2º EsoBrianAB7Aún no hay calificaciones
- Docsity Tema 2 Fyq 3o Eso SolucionarioDocumento16 páginasDocsity Tema 2 Fyq 3o Eso Solucionariomarina saldaaAún no hay calificaciones
- Resumen Física y Química La Materia 2 Eso Tema 2 AnayaDocumento2 páginasResumen Física y Química La Materia 2 Eso Tema 2 AnayaNenupharum50% (2)
- Historia 2º ESO - T2 y 3 Anaya AlexandraDocumento1 páginaHistoria 2º ESO - T2 y 3 Anaya AlexandraSgonezeAún no hay calificaciones
- FyQ 2º ESO - Actividades Adaptación Cambio UnidadesDocumento3 páginasFyQ 2º ESO - Actividades Adaptación Cambio UnidadesElena100% (1)
- Ficha Ref Fís-Quí 2º ESO-tema 7 CAMBIOS QUÍMICOSDocumento3 páginasFicha Ref Fís-Quí 2º ESO-tema 7 CAMBIOS QUÍMICOSLpFernandez 26100% (1)
- Examen UD 3Documento2 páginasExamen UD 3JuliaAún no hay calificaciones
- ACEITEDocumento7 páginasACEITEDaniel CebraAún no hay calificaciones
- CS 2º EsoDocumento25 páginasCS 2º EsoVanessa Estefanía Cendagorta100% (1)
- SOL FyQ 2ESO AVANZA U1 PDFDocumento16 páginasSOL FyQ 2ESO AVANZA U1 PDFMiguel Muñoz Hernández50% (2)
- Cuaderno Refuerzo 2esoDocumento17 páginasCuaderno Refuerzo 2esoJosé CalvoAún no hay calificaciones
- Practica 8. Transposicion Bencilica-E8Documento20 páginasPractica 8. Transposicion Bencilica-E8Alexandra Marlene100% (1)
- 02 Adapt Curricular Materia Sus PropiedadesDocumento13 páginas02 Adapt Curricular Materia Sus Propiedadesjose100% (1)
- Cuadernillo 3 ESO Aplic Parte 1 (Pmar)Documento8 páginasCuadernillo 3 ESO Aplic Parte 1 (Pmar)Miriam Avila BenitezAún no hay calificaciones
- Physics and Chemistry 2eso Students PDFDocumento21 páginasPhysics and Chemistry 2eso Students PDFMARIAAún no hay calificaciones
- 05 Guia Didactica Reacciones QuimicasDocumento44 páginas05 Guia Didactica Reacciones QuimicasJesús GarcíaAún no hay calificaciones
- Física y Química 2ºESODocumento12 páginasFísica y Química 2ºESOJuan100% (1)
- Tema 4 - Guía Didáctica PDFDocumento32 páginasTema 4 - Guía Didáctica PDFJulio CasalloAún no hay calificaciones
- Fichafiskim 3Documento2 páginasFichafiskim 3Alma Stephanie GutierrezAún no hay calificaciones
- 3ºESO Soluciones FyQ Tema 1 PDFDocumento51 páginas3ºESO Soluciones FyQ Tema 1 PDFBárbara FernándezAún no hay calificaciones
- Cs. Naturales 7°básico Guía de Aprendizaje Los Gases.Documento6 páginasCs. Naturales 7°básico Guía de Aprendizaje Los Gases.Cuerpa Espinas Fran100% (1)
- 30251Documento79 páginas30251Adolfo Gonzalez VidalAún no hay calificaciones
- 03 Guia DidacticaDocumento28 páginas03 Guia DidacticaSara Morcillo García100% (1)
- 02 Guia Didactica Materia Sus Propiedades 2 EsoDocumento32 páginas02 Guia Didactica Materia Sus Propiedades 2 EsoAuxi BurgosAún no hay calificaciones
- 03 Guia Didactica Mundo Material Atomos 2 EsoDocumento28 páginas03 Guia Didactica Mundo Material Atomos 2 EsoAuxi BurgosAún no hay calificaciones
- Repaso T6. Lengua Algaida. 2°ESODocumento4 páginasRepaso T6. Lengua Algaida. 2°ESOMil Sal100% (1)
- Adaptacion CurricularDocumento20 páginasAdaptacion CurricularRocío González50% (2)
- Naturales 2 EsoDocumento23 páginasNaturales 2 EsoAna PerezAún no hay calificaciones
- Libro Anaya Fyq 3esoDocumento97 páginasLibro Anaya Fyq 3esoCarlos Alvarez Glez100% (1)
- Repaso Tema 2Documento2 páginasRepaso Tema 2Sonsoles EncinarAún no hay calificaciones
- Tema 1 FyQ 3 ESO AnayaDocumento8 páginasTema 1 FyQ 3 ESO AnayaDEAún no hay calificaciones
- TEMA2Documento24 páginasTEMA2emiAún no hay calificaciones
- Tema 5 Física y Química. 2 EsoDocumento5 páginasTema 5 Física y Química. 2 EsoSandra Sagrario Baos Rodrigo100% (1)
- 2ºESOT4.Cambios en La Materia ProfesorDocumento8 páginas2ºESOT4.Cambios en La Materia ProfesorMj Fdez100% (1)
- 02 El Movimiento - Ejercicios Ampliacion 2Documento3 páginas02 El Movimiento - Ejercicios Ampliacion 2colhonsAún no hay calificaciones
- Adaptaciones Curriculares Física y Química 3º ESO PDFDocumento2 páginasAdaptaciones Curriculares Física y Química 3º ESO PDFGonzalo Caso GarcíaAún no hay calificaciones
- Evaluacion de Las Competencias PDFDocumento18 páginasEvaluacion de Las Competencias PDFAnonymous Dd7j6KEBM100% (2)
- Refuerzo Fyq 2Documento84 páginasRefuerzo Fyq 2Jonathan Jurado BenitezAún no hay calificaciones
- IncondicionalDocumento3 páginasIncondicionalmanu_iribarrenAún no hay calificaciones
- 4 EsoDocumento17 páginas4 Esoapi-2404217590% (1)
- Actividades de La Lectura El Extraño Crimen de Mary RobertDocumento16 páginasActividades de La Lectura El Extraño Crimen de Mary Robertlucia100% (1)
- 4esolcen LP Es PDFDocumento25 páginas4esolcen LP Es PDFpepins poiulosAún no hay calificaciones
- Repaso 1 Evaluacion 2º EsoDocumento1 páginaRepaso 1 Evaluacion 2º EsoJosueAún no hay calificaciones
- Examen de F y Q 2 de EsoDocumento4 páginasExamen de F y Q 2 de EsoGemma MonteroAún no hay calificaciones
- Actividades de Biología y Geologia para 1º EsoDocumento14 páginasActividades de Biología y Geologia para 1º EsoMaría José Ocaña SantosAún no hay calificaciones
- 1º ESO Geografía .Tema 2 - GeosferaDocumento5 páginas1º ESO Geografía .Tema 2 - GeosferaAmpa San UrbanoAún no hay calificaciones
- E 01 01 Vocabulario Cientifico Bg1esoDocumento1 páginaE 01 01 Vocabulario Cientifico Bg1esoEncarni López HinojosaAún no hay calificaciones
- Richmond Fast 1eso Unit8Documento6 páginasRichmond Fast 1eso Unit8MariCarmen ZarcoAún no hay calificaciones
- 2º EsoDocumento64 páginas2º EsoMnbnbn LopezAún no hay calificaciones
- Los Estados de La Materia - Quimica Corte IIIDocumento12 páginasLos Estados de La Materia - Quimica Corte IIIAntonio cañizalesAún no hay calificaciones
- Guía Semana 28 y 29 Biología, Ed Física y ÉticaDocumento17 páginasGuía Semana 28 y 29 Biología, Ed Física y ÉticayeisongalvanAún no hay calificaciones
- Actividades de Ciencias (Parte 2)Documento11 páginasActividades de Ciencias (Parte 2)Ranulfo JimenezAún no hay calificaciones
- Apunte Ingles I - Ingenieria Quimica 2018 PDFDocumento44 páginasApunte Ingles I - Ingenieria Quimica 2018 PDFManu OzanAún no hay calificaciones
- Masa Molecular de Una Sustancia VolátilDocumento7 páginasMasa Molecular de Una Sustancia VolátilAmadeus MüllerAún no hay calificaciones
- Guia Gases y Leyes - 7° BásicoDocumento4 páginasGuia Gases y Leyes - 7° BásicoPablina Marisol Contreras GonzàlezAún no hay calificaciones
- Prueba Ciencias MateriaDocumento4 páginasPrueba Ciencias MateriaWaldo Ramirez OrdoñezAún no hay calificaciones
- Album de Los Grupos Funcionales Organicos 341522 Downloable 1520424Documento81 páginasAlbum de Los Grupos Funcionales Organicos 341522 Downloable 1520424ACOPA CRUZ NATIVIDADAún no hay calificaciones
- Propiedades Químicas Del SueloDocumento2 páginasPropiedades Químicas Del SueloKilvio DislaAún no hay calificaciones
- Elementos Quimicos Importantes en Mexico y Sus AplicacionesDocumento2 páginasElementos Quimicos Importantes en Mexico y Sus AplicacionesLuis Campos100% (1)
- Ficha Tecnica Bioincrust-50 - Desincrustante y AntisarroDocumento2 páginasFicha Tecnica Bioincrust-50 - Desincrustante y Antisarrojoelmy zaraAún no hay calificaciones
- Diclofenaco SodicoDocumento24 páginasDiclofenaco SodicoAnonymous SwqsnOtAún no hay calificaciones
- Resolucion de Problemas Acido Base Fuerte Debil 2023Documento2 páginasResolucion de Problemas Acido Base Fuerte Debil 2023Soraya FredesAún no hay calificaciones
- Capitulo 31 LigieDocumento2 páginasCapitulo 31 Ligie5421100112Aún no hay calificaciones
- Especificaciones AcerosDocumento5 páginasEspecificaciones AcerosSOLO PARA TUS OIDOSAún no hay calificaciones
- Tierras RarasDocumento5 páginasTierras RarasisabelAún no hay calificaciones
- WO2013040721A1Documento35 páginasWO2013040721A1Rider LuisitoAún no hay calificaciones
- Aplicaciones Piritionato de ZincDocumento2 páginasAplicaciones Piritionato de ZinckobeAún no hay calificaciones
- Solubilidad Acidez Complejos - EjercicioClaseDocumento1 páginaSolubilidad Acidez Complejos - EjercicioClaseScott Thomas WeilandAún no hay calificaciones
- Shell Ceramic Chuctaya-GarcíaDocumento16 páginasShell Ceramic Chuctaya-GarcíaHana Bts KookAún no hay calificaciones
- Certificado Calidad Inka3Documento1 páginaCertificado Calidad Inka3Jhonny YgredaAún no hay calificaciones
- 1er Prob MQADocumento2 páginas1er Prob MQASergioEspejelAún no hay calificaciones
- Jabon LiquidoDocumento19 páginasJabon Liquidoyudy silvaAún no hay calificaciones
- Aldehídos 2Documento3 páginasAldehídos 2Danna PaolaAún no hay calificaciones
- EnzimasDocumento15 páginasEnzimasW̵i̵l̵ ̵n̵e̵i̵r̵a̵ C̵h̵Aún no hay calificaciones
- Lección CuatroDocumento4 páginasLección Cuatrocarla sanchezAún no hay calificaciones
- Clasificacion de Los AceitesDocumento7 páginasClasificacion de Los Aceitesjonathan barrazaAún no hay calificaciones
- Taller Nomeclatura.Documento4 páginasTaller Nomeclatura.Mateo Gaviria RuizAún no hay calificaciones
- Introducción A La Química Orgánica PDFDocumento12 páginasIntroducción A La Química Orgánica PDFSebastian CuevasAún no hay calificaciones
- Matriz Elementos Proteccion PersonalDocumento2 páginasMatriz Elementos Proteccion PersonalMarcela TorresAún no hay calificaciones
- Respusta de La Unidad 2 Ciencias Naturales 11Documento4 páginasRespusta de La Unidad 2 Ciencias Naturales 11yaira pachecoAún no hay calificaciones
- Ficha Tecnica 110014354Documento2 páginasFicha Tecnica 110014354AB ToledoAún no hay calificaciones
- Volumetria Con Formacion de ComplejosDocumento4 páginasVolumetria Con Formacion de Complejosandres chamorro95% (20)
- Ev. Quimica 2°Documento5 páginasEv. Quimica 2°Fernanda Diaz de ArcayaAún no hay calificaciones