0% encontró este documento útil (0 votos)
1K vistas12 páginas1 Al 17
1) El documento proporciona datos sobre la combustión de glucosa y solicita calcular la entalpía estándar de combustión de la glucosa, el cambio de energía interna de la combustión y la entalpía estándar de formación de la glucosa a 25°C.
2) Solicita calcular la entalpía estándar de formación del N2O5 a temperatura estándar basándose en datos de reacciones químicas.
3) Pregunta por la entalpía estándar de combustión del propano líquido a 25
Cargado por
VICENTE ELIAS MAYTA MAMANIDerechos de autor
© © All Rights Reserved
Nos tomamos en serio los derechos de los contenidos. Si sospechas que se trata de tu contenido, reclámalo aquí.
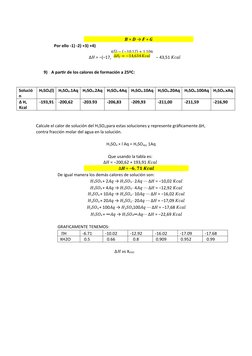
Formatos disponibles
Descarga como DOCX, PDF, TXT o lee en línea desde Scribd
0% encontró este documento útil (0 votos)
1K vistas12 páginas1 Al 17
1) El documento proporciona datos sobre la combustión de glucosa y solicita calcular la entalpía estándar de combustión de la glucosa, el cambio de energía interna de la combustión y la entalpía estándar de formación de la glucosa a 25°C.
2) Solicita calcular la entalpía estándar de formación del N2O5 a temperatura estándar basándose en datos de reacciones químicas.
3) Pregunta por la entalpía estándar de combustión del propano líquido a 25
Cargado por
VICENTE ELIAS MAYTA MAMANIDerechos de autor
© © All Rights Reserved
Nos tomamos en serio los derechos de los contenidos. Si sospechas que se trata de tu contenido, reclámalo aquí.
Formatos disponibles
Descarga como DOCX, PDF, TXT o lee en línea desde Scribd