0% encontró este documento útil (1 voto)
547 vistas23 páginasDifusión de Átomos e Iones: Mecanismos y Leyes
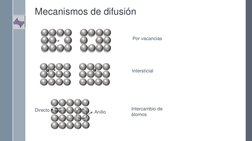
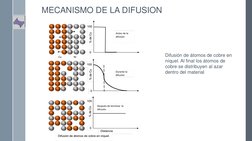
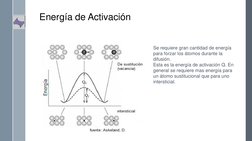
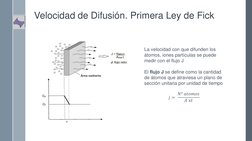
El documento describe los conceptos fundamentales de la difusión de átomos y iones. Explica que la difusión ocurre como resultado del movimiento aleatorio de las partículas para minimizar las diferencias de concentración. Describe los mecanismos de difusión por vacantes e intersticiales, y factores que afectan la difusión como la energía de activación y la temperatura. También presenta las leyes de Fick que relacionan la velocidad y perfil de difusión con el gradiente de concentración.
Cargado por
Rafael MolinaDerechos de autor
© © All Rights Reserved
Nos tomamos en serio los derechos de los contenidos. Si sospechas que se trata de tu contenido, reclámalo aquí.
Formatos disponibles
Descarga como PDF, TXT o lee en línea desde Scribd
0% encontró este documento útil (1 voto)
547 vistas23 páginasDifusión de Átomos e Iones: Mecanismos y Leyes
El documento describe los conceptos fundamentales de la difusión de átomos y iones. Explica que la difusión ocurre como resultado del movimiento aleatorio de las partículas para minimizar las diferencias de concentración. Describe los mecanismos de difusión por vacantes e intersticiales, y factores que afectan la difusión como la energía de activación y la temperatura. También presenta las leyes de Fick que relacionan la velocidad y perfil de difusión con el gradiente de concentración.
Cargado por
Rafael MolinaDerechos de autor
© © All Rights Reserved
Nos tomamos en serio los derechos de los contenidos. Si sospechas que se trata de tu contenido, reclámalo aquí.
Formatos disponibles
Descarga como PDF, TXT o lee en línea desde Scribd