Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Resumen Capítulo 3.2 de Lodish
Cargado por
Danii Alejandra0 calificaciones0% encontró este documento útil (0 votos)
85 vistas2 páginasDerechos de autor
© © All Rights Reserved
Formatos disponibles
PDF, TXT o lea en línea desde Scribd
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
© All Rights Reserved
Formatos disponibles
Descargue como PDF, TXT o lea en línea desde Scribd
0 calificaciones0% encontró este documento útil (0 votos)
85 vistas2 páginasResumen Capítulo 3.2 de Lodish
Cargado por
Danii AlejandraCopyright:
© All Rights Reserved
Formatos disponibles
Descargue como PDF, TXT o lea en línea desde Scribd
Está en la página 1de 2
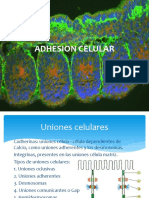
La secuencia de aminoácidos de una proteína determina su plegamiento en
una conformación tridimensional específica, el estado nativo.
El plegamiento de proteínas in vivo requiere la asistencia de chaperonas
moleculares (proteínas Hsp70), que se unen a los polipéptidos nacientes que
emergen de los ribosomas e impiden su plegamiento erróneo (figura. 3-11).
Figura 3-11. Plegamiento de proteínas mediado por chaperonas y chaperoninas.
Las chaperoninas, grandes complejos de proteínas similares a Hsp60, cubren
algunas proteínas parcialmente plegadas o mal plegadas en una cavidad
semejante a un barril, proporcionándoles tiempo adicional para que alcancen
un plegamiento correcto.
Después de la síntesis, la mayoría de las proteínas se modifican por la adición
de diversos grupos químicos a los residuos de aminoácidos. Estas
modificaciones, que alteran la estructura y función de las proteínas, incluyen
la acetilación, la hidroxilación, la glucosilación y la fosforilación.
La duración de la vida de una proteína intracelular es determinada en gran
parte por su susceptibilidad a la degradación proreolítica por diversas vías.
Las proteínas virales
que se producen dentro
de las células
infectadas, las proteínas
citosólicas normales y
las proteínas mal
plegadas se marcan
para la destrucción
mediante la adición
covalente de una
cadena de poliubicuirina
y luego se degradan
dentro de los
proteasomas, grandes
complejos cilíndricos
con múltiples proteasas
en su interior (figura. 3-
13). Figura. 3-13. Vía proteolítica mediada
por ubicuitina.
Algunas enfermedades neurodegenerarivas son causadas por agregados de
proteínas que están establemente plegadas en una conformación alternativa.
También podría gustarte
- El Proteosoma ResumenDocumento2 páginasEl Proteosoma ResumenKisakiaas Rodriguez JacoboAún no hay calificaciones
- Resumen Capítulo 3.5 de LodishDocumento1 páginaResumen Capítulo 3.5 de LodishDanii AlejandraAún no hay calificaciones
- Resumen Capitulo 3.6 de LodishDocumento2 páginasResumen Capitulo 3.6 de LodishDanii AlejandraAún no hay calificaciones
- Resumen Capítulo 3.1 de LodishDocumento2 páginasResumen Capítulo 3.1 de LodishDanii AlejandraAún no hay calificaciones
- Resumen Capitulo 4.4 de LodishDocumento2 páginasResumen Capitulo 4.4 de LodishDanii AlejandraAún no hay calificaciones
- Qué Es y Que Función Tiene Un Factor de TranscripciónDocumento3 páginasQué Es y Que Función Tiene Un Factor de TranscripciónMaria Elizabeth GaliciaAún no hay calificaciones
- Tema 7 Uniones CelularesDocumento6 páginasTema 7 Uniones CelularesDavid Molina LópezAún no hay calificaciones
- Biología-Sem-InformeDocumento10 páginasBiología-Sem-InformeXiomara Janne Linares SaldañaAún no hay calificaciones
- Tema 14.3 - Biosíntesis de AminoácidosDocumento15 páginasTema 14.3 - Biosíntesis de AminoácidosAntonio100% (1)
- Aparato de GolgiDocumento34 páginasAparato de GolgiMoisés J. Duran CanevaroAún no hay calificaciones
- Inhibidor EnzimáticoDocumento18 páginasInhibidor EnzimáticoAdri CruzAún no hay calificaciones
- Biosíntesis de InsulinaDocumento3 páginasBiosíntesis de InsulinaChristopher VargasAún no hay calificaciones
- Transporte de ProteinasDocumento9 páginasTransporte de ProteinasGise MathierAún no hay calificaciones
- Remodelación de La CromatinaDocumento2 páginasRemodelación de La CromatinaFidel José Castilla FrancoAún no hay calificaciones
- Operon LactosaDocumento52 páginasOperon LactosaAmbar GabrielaAún no hay calificaciones
- Envoltura NuclearDocumento2 páginasEnvoltura NuclearKatiuska SumozaAún no hay calificaciones
- CitoesqueletoDocumento45 páginasCitoesqueletoCarlos GiraldoAún no hay calificaciones
- Esquema Del Ciclo CelularDocumento5 páginasEsquema Del Ciclo CelularAntonio Servin GarciaAún no hay calificaciones
- La Fisión BinariaDocumento3 páginasLa Fisión BinariaRobert Mayta100% (1)
- ProteosomasDocumento14 páginasProteosomasSandra SolanoAún no hay calificaciones
- Guia de La Via de La PentosaDocumento3 páginasGuia de La Via de La PentosaOrfinaMarroquinAún no hay calificaciones
- Operón TriptófanoDocumento6 páginasOperón TriptófanoMelody PoloAún no hay calificaciones
- 13) Reticulo EndoplasmicoDocumento27 páginas13) Reticulo EndoplasmicoPerla Gutiérrez RogelAún no hay calificaciones
- Metabolismo de CarboidratosDocumento23 páginasMetabolismo de CarboidratosVerónica VelásquezAún no hay calificaciones
- Transporte de ProteinasDocumento4 páginasTransporte de ProteinasEsteban RuedaAún no hay calificaciones
- Aparato de Golgi Lisosomas y VacuolasDocumento43 páginasAparato de Golgi Lisosomas y VacuolasscribdenesimoAún no hay calificaciones
- Especialización de La MembranaDocumento2 páginasEspecialización de La MembranaMarisol100% (2)
- Adhesion CelularDocumento30 páginasAdhesion CelularBeto HdzAún no hay calificaciones
- Señalización Celular - Matriz ExtracelularDocumento7 páginasSeñalización Celular - Matriz ExtracelularEnzo Guillermo RamirezAún no hay calificaciones
- Inmunoprecipitación de CromatinaDocumento1 páginaInmunoprecipitación de CromatinaAlberto GallegoAún no hay calificaciones
- Sistema de EndomembranasDocumento27 páginasSistema de EndomembranasSofía TorresAún no hay calificaciones
- Replicación - KarpDocumento14 páginasReplicación - KarpCuarto Paralelo 1100% (1)
- Aparato de GolgiDocumento4 páginasAparato de Golgiapi-382665850% (2)
- 9 Teórica Tráfico de Proteínas PDFDocumento74 páginas9 Teórica Tráfico de Proteínas PDFIrene CarballoAún no hay calificaciones
- Notas Borrador Sobre AlzheimerDocumento4 páginasNotas Borrador Sobre AlzheimerSofíaAún no hay calificaciones
- Replicación Traduccion y Transcripcion Del AdnDocumento9 páginasReplicación Traduccion y Transcripcion Del AdnRobertoFabianCossioSalgadoAún no hay calificaciones
- 17 - Integración y Regulación Del Metabolismo Intermediario Clase 17Documento19 páginas17 - Integración y Regulación Del Metabolismo Intermediario Clase 17Fabrizzio Piffaretti RomeroAún no hay calificaciones
- Taller de Bioquimica ProteinaDocumento7 páginasTaller de Bioquimica ProteinaRosman Ramos MartinezAún no hay calificaciones
- Código GenéticoDocumento18 páginasCódigo Genéticopaz_saavedra_3Aún no hay calificaciones
- Transporte IntracelularDocumento1 páginaTransporte IntracelularAnonymous hkjp4qMVRsAún no hay calificaciones
- Dogma CentralDocumento6 páginasDogma CentralRaul Huayanay CarranzaAún no hay calificaciones
- Cuestionario 2° ParcialDocumento4 páginasCuestionario 2° ParcialMariela Angeles RodriguezAún no hay calificaciones
- Reticulo EndoplasmaticoDocumento5 páginasReticulo Endoplasmaticointer celAún no hay calificaciones
- Diapositiva de Reticulo Endoplasmatico LisoDocumento8 páginasDiapositiva de Reticulo Endoplasmatico LisoDaniela Monserrat Olarte SalazarAún no hay calificaciones
- AdipocinasDocumento2 páginasAdipocinasadriana gonzalez esparzaAún no hay calificaciones
- Actividad 11 TallerSeñalizacionCelular-InteracciónCélulaCélulaDocumento9 páginasActividad 11 TallerSeñalizacionCelular-InteracciónCélulaCélulaAndrés FelipeAún no hay calificaciones
- Diapos D.B.2 PDFDocumento53 páginasDiapos D.B.2 PDFJose Fernando Funes RomeroAún no hay calificaciones
- Estructura Terciaria y Cuaternaria Del AdnDocumento1 páginaEstructura Terciaria y Cuaternaria Del AdnAdrian Balon PereroAún no hay calificaciones
- Clonación Acelular PCRDocumento23 páginasClonación Acelular PCRVanessa Huirse LizanoAún no hay calificaciones
- Citoplasma LibrosDocumento2 páginasCitoplasma LibrosMayra VásquezAún no hay calificaciones
- Clase 6 Metabolismo de Ácidos NucleicosDocumento18 páginasClase 6 Metabolismo de Ácidos NucleicosAguss FernandezAún no hay calificaciones
- Maduracion de PlaquetasDocumento19 páginasMaduracion de PlaquetasIvanRodríguezInfante0% (1)
- Transcripcion Del AdnDocumento2 páginasTranscripcion Del Adnflorencia barrientosAún no hay calificaciones
- Guia de Seminario BCM 2023 - 1 PDFDocumento32 páginasGuia de Seminario BCM 2023 - 1 PDFBruno FernándezAún no hay calificaciones
- 4-6 Difusión y Transporte Pasivo PDFDocumento5 páginas4-6 Difusión y Transporte Pasivo PDFBrayan Andrės CerónAún no hay calificaciones
- Funciones Del AmpcDocumento3 páginasFunciones Del AmpcRaulAún no hay calificaciones
- Célula y MembranaDocumento21 páginasCélula y Membranazaini munirAún no hay calificaciones
- Síntesis de Proteínas.Documento45 páginasSíntesis de Proteínas.LucianoAún no hay calificaciones
- Chaperonas y ChaperoninasDocumento30 páginasChaperonas y ChaperoninasDokhurAún no hay calificaciones
- Articulo ChaperonasDocumento2 páginasArticulo ChaperonasMaría DelgadoAún no hay calificaciones
- Metabolism oDocumento5 páginasMetabolism oDanii AlejandraAún no hay calificaciones
- LEUCEMIADocumento6 páginasLEUCEMIADanii AlejandraAún no hay calificaciones
- PH, Complejos, CoprecipitacionDocumento14 páginasPH, Complejos, CoprecipitacionDanii AlejandraAún no hay calificaciones
- Resumen Capitulo 16.1 de LodishDocumento1 páginaResumen Capitulo 16.1 de LodishDanii Alejandra100% (1)
- Acuña, Cap16.2Documento1 páginaAcuña, Cap16.2Danii AlejandraAún no hay calificaciones
- Codex AlimentariusDocumento3 páginasCodex AlimentariusDanii AlejandraAún no hay calificaciones