Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Oxido de Etileno
Cargado por
Ety Viloria CastilloTítulo original
Derechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
Oxido de Etileno
Cargado por
Ety Viloria CastilloCopyright:
Formatos disponibles
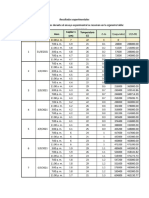
Considere la oxidación en fase gaseosa ideal del etileno a óxido de etileno a una presión de 1 bar y 25% de exceso de
aire. Si los reactivos entran a 25° C y los productos salen a 970 K, y si no hay reacciones laterales, determine: a) la
composición molar del producto del reactor; b) el flujo de calor por cada kmol/s de etileno alimentado. Considere Cp de
las especies químicas constante. Use la ecuación de Gibbs para la constante de equilibrio.
Ti (K) = 298 P (bar) = 1 Reacción: C2H4 + 0,5O2 <------> C2H4O
Tj (K) = 1103.5 B de C: 1 kmol/s de C2H4
Exceso (%) = 25% a= 0.500 kmol/s Tj (K) =
nki Dh°f298 Dg°f298
nk nkj (kmol) Cpk/R ykj
(kmol/s) (kJ/kmol) (kJ/kmol) KeqT = EXP[-Dg°/(RT)] =
C2H4 (g) 1.000 -1 0.500 5.325 52510 68460 0.1342 K
O2 (g) 0.625 -0.5 0.375 3.535 0 0 0.1006
N2 (g) 2.351 0 2.351 3.502 0 0 0.6310
C2H4O (g) 0.000 1 0.500 5.784 -52630 -13010 0.1342
Sumas ----> 3.976 -0.5 3.726 -1.309 -105140 -81470 1.0000
D
nk = -1 -0.5 0 1
nkj = 0.500 0.375 2.351 0.500
PROBLEMA ALTERNATIVO 1
Si la conversión fraccional de etileno es de 90%, determine la temperatura de equilibrio y el flujo de calor, en kW
Solución:
Se ingresa el valor del grado de conversión y se usa la herramienta "buscar objetivo" cambiando la temperatura.
Resultados: T = 913,9 K; Q = -19909,6 kW
PROBLEMA ALTERNATIVO 2
Si la conversión fraccional del etileno es de 50%, determine la temperatura de equilibrio y el flujo de calor, en kW
Solución:
Se ingresa el valor del exceso y el valor del grado de conversión y se usa la herramienta "buscar objetivo" cambiando la tem
Resultados: T = 1103,5 K; Q = 48560,4 kW
Si la reacción es adiabática, ¿cómo se determinan el grado de conversión y la temperatura?
Reacción estequiométrica:
r y 25% de exceso de Balance de materia:
, determine: a) la C2H4 (g) 1
entado. Considere Cp de
O2 (g) 0.5
C2H4O (g) 1
H4 + 0,5O2 <------> C2H4O
Función objetivo: F(a) = Kycalc - KeqT = 0
1103.5
Dg°/(RT) = -1.148
KeqT = EXP[-Dg°/(RT)] = 3.152
KyT = KeqT(P)-Dn = 3.152
Kycalc = P(yk)
n
= 3.152 Simulaciones:
F(a) = 0.00 Tj (K) a (kmol/s) Q (kW)
Balance de energìa: 970.0 0.81 -3020.9
913.9 0.90 -19909.6
835.0 0.97 -37250.7
S(nkjCpk) = 125.66 kW/K
Q (kW) = 48650.4
de calor, en kW
la temperatura.
o de calor, en kW
objetivo" cambiando la temperatura.
También podría gustarte
- Fisicoquimica PIADocumento22 páginasFisicoquimica PIAsierplopAún no hay calificaciones
- Presión de Vapor y Ecuaciones de EstadoDocumento8 páginasPresión de Vapor y Ecuaciones de EstadoVALENTINA RUIZ GARCIAAún no hay calificaciones
- Practica 5-2p - Metodo DiferencialDocumento4 páginasPractica 5-2p - Metodo DiferencialMelisa ParedesAún no hay calificaciones
- FINAL Fis Quim II 21 IDocumento2 páginasFINAL Fis Quim II 21 IVICTOR ENRIQUE QUISPE SAMANEZAún no hay calificaciones
- Problemas Capítulo 3 PolimerosDocumento5 páginasProblemas Capítulo 3 PolimerosNeydy Tellez Rivera0% (1)
- Deber 3 Kevin VasquezDocumento8 páginasDeber 3 Kevin VasquezKvn Vqz0% (1)
- Ley de RaoultDocumento3 páginasLey de RaoultMattheoGonzalezBalderas50% (2)
- Ejercicios Resueltos de CineticaDocumento6 páginasEjercicios Resueltos de CineticabryggyttAún no hay calificaciones
- Modelos de LHHW y Rideal 2021BDocumento42 páginasModelos de LHHW y Rideal 2021Baslkdjdas asdadaAún no hay calificaciones
- Tarea3 FTCM Equipo3Documento44 páginasTarea3 FTCM Equipo3Sergio GuzmánAún no hay calificaciones
- TerDocumento9 páginasTerAnonymous K75YmDxG61Aún no hay calificaciones
- Informe Final de SimuDocumento56 páginasInforme Final de Simuirving_mendoza_58Aún no hay calificaciones
- 3.8 LevenspielDocumento2 páginas3.8 LevenspielBrenda KarenAún no hay calificaciones
- Guía 4Documento9 páginasGuía 4Juan AparicioAún no hay calificaciones
- Deber FoglerDocumento7 páginasDeber FoglerDanny LemaAún no hay calificaciones
- 1.5 Ejercicio de CineticaDocumento3 páginas1.5 Ejercicio de CineticaJacqueline AmezcuaAún no hay calificaciones
- Determinacion Crioscopica Del Peso Molecular FinalDocumento13 páginasDeterminacion Crioscopica Del Peso Molecular FinalPier Navarro100% (1)
- Edoc - Pub - Auto Evaluacion de La Unidad 2docxDocumento10 páginasEdoc - Pub - Auto Evaluacion de La Unidad 2docxBryan Sait De León ReyesAún no hay calificaciones
- Sol Eda D1 TMA (25 02 13) PDFDocumento2 páginasSol Eda D1 TMA (25 02 13) PDFLeonardo GranadosAún no hay calificaciones
- Problemas CombustionDocumento27 páginasProblemas CombustionAndrea del AguilaAún no hay calificaciones
- Tarea Cinetica 23 10Documento8 páginasTarea Cinetica 23 10Gloria GarcíaAún no hay calificaciones
- Ejercicios Diagrama de FasesDocumento2 páginasEjercicios Diagrama de FasesBrayan Calalpa LopezAún no hay calificaciones
- 1 Parcial SolucionarioDocumento3 páginas1 Parcial SolucionarioRogher Uluri YanaAún no hay calificaciones
- Cap5 Tarea HimeblauDocumento17 páginasCap5 Tarea HimeblauMercury's VlogsAún no hay calificaciones
- F1 Etlihexanol A Partir de Propileno y de Gas de Si NtesisDocumento4 páginasF1 Etlihexanol A Partir de Propileno y de Gas de Si Ntesisdayana palmaAún no hay calificaciones
- Ejemplo de 5.1Documento6 páginasEjemplo de 5.1Kevin Jholsin Soto CalixtoAún no hay calificaciones
- Cer Vera AndreaDocumento21 páginasCer Vera AndreaAndrea CerveraAún no hay calificaciones
- Series Tema 2Documento3 páginasSeries Tema 2villalobosmilenaAún no hay calificaciones
- Problemas Reacciones Heterogeneas No CatalitiasDocumento3 páginasProblemas Reacciones Heterogeneas No CatalitiasIrene HinostrozaAún no hay calificaciones
- TALLER #3 Ajuste de Curva e Interpolación.Documento4 páginasTALLER #3 Ajuste de Curva e Interpolación.ronni bermudezAún no hay calificaciones
- Problemas UMD EMDDocumento1 páginaProblemas UMD EMDJuan Jose Tamayo Juarez0% (1)
- Tarea 3. Martínez Rodríguez DanielDocumento21 páginasTarea 3. Martínez Rodríguez DanielDANIEL MARTINEZ RODRIGUEZAún no hay calificaciones
- ADA 1 ReactoresDocumento6 páginasADA 1 ReactoresSilvanaEscobedoNoveloAún no hay calificaciones
- Guia de Aprendizaje 2UI - CP1Documento6 páginasGuia de Aprendizaje 2UI - CP1javier gagoAún no hay calificaciones
- Equilibrio-Químico. v2Documento23 páginasEquilibrio-Químico. v2Nadia NollyAún no hay calificaciones
- Cinética IntrínsecaDocumento2 páginasCinética IntrínsecacaabernalraAún no hay calificaciones
- P. Lab. 03 - Determinación de GammaDocumento11 páginasP. Lab. 03 - Determinación de GammaLUIS ALBERTO PEREZ GARCIA100% (1)
- Solucion Parcial IDocumento11 páginasSolucion Parcial ILeonardo ReyesAún no hay calificaciones
- Tarea 3Documento5 páginasTarea 3Uriel Fabián Del Río Félix100% (1)
- Dokumen - Tips Prob 39Documento3 páginasDokumen - Tips Prob 39Percy Axel Cholan RoqueAún no hay calificaciones
- Metodo Grafico de WinkelmannDocumento4 páginasMetodo Grafico de WinkelmannCarmen HernandezAún no hay calificaciones
- Informe de Produccion de EtilenglicolDocumento123 páginasInforme de Produccion de EtilenglicolDeysi Salazar BozaAún no hay calificaciones
- Calculo Del Perfil de Concentraciones para Un Reactor Tubular y Del Volumen Del Reactorcon Solución Numérica Con El Método de RungeDocumento3 páginasCalculo Del Perfil de Concentraciones para Un Reactor Tubular y Del Volumen Del Reactorcon Solución Numérica Con El Método de RungeLemuelMoralesAún no hay calificaciones
- YolandaDocumento15 páginasYolandaNoel Carballido MezaAún no hay calificaciones
- Obtencion de EstirenoDocumento2 páginasObtencion de EstirenoCitlali ReyesAún no hay calificaciones
- EJERCICIODocumento1 páginaEJERCICIOyessicaAún no hay calificaciones
- Pp1 - Mezcla Gaseosa IdealDocumento69 páginasPp1 - Mezcla Gaseosa IdealLUIS FERNANDO MARTINEZ PRICEAún no hay calificaciones
- 1er Examen Parcial de Ingeniería de Reactores Químicos II 26Documento2 páginas1er Examen Parcial de Ingeniería de Reactores Químicos II 26TobiI SempaiAún no hay calificaciones
- Reporte de Ejercicios Reactores (COCO)Documento4 páginasReporte de Ejercicios Reactores (COCO)Nats BenitezAún no hay calificaciones
- Taller FisicoquimicaDocumento5 páginasTaller FisicoquimicadavidAún no hay calificaciones
- Practico 1 Icp280Documento10 páginasPractico 1 Icp280marco antonioAún no hay calificaciones
- Fogler 4 6bDocumento22 páginasFogler 4 6bJacky V. HerbasAún no hay calificaciones
- Formulario de CineticaDocumento2 páginasFormulario de Cineticashina20% (1)
- Operaciones UnitariasDocumento5 páginasOperaciones UnitariasIngridAún no hay calificaciones
- Clase3 - Balance - 1P PDFDocumento1 páginaClase3 - Balance - 1P PDFRodrigo SurculentoAún no hay calificaciones
- Proyecto Ingeniería de ReaccionesDocumento5 páginasProyecto Ingeniería de ReaccionesManuel Fernando Carrillo HuertasAún no hay calificaciones
- Sistemas Con Reacciones QuimicasDocumento6 páginasSistemas Con Reacciones QuimicasNatali CondeñaAún no hay calificaciones
- Ef 72115 G1 - G2Documento6 páginasEf 72115 G1 - G2Moises RodriguezAún no hay calificaciones
- Calor de Combustion #2Documento7 páginasCalor de Combustion #2Jose Miguel MedinaAún no hay calificaciones
- Asignacion 2g1 Gomez DanielaDocumento6 páginasAsignacion 2g1 Gomez DanielaDANIELA ALEJANDRA GOMEZ ORTEGAAún no hay calificaciones
- Diapositiva Fundamentos y Usos Del PQS Tipo ABCDocumento14 páginasDiapositiva Fundamentos y Usos Del PQS Tipo ABCAndrea VillalobosAún no hay calificaciones
- Evaporación Al VacíoDocumento2 páginasEvaporación Al VacíoJuanma JaraAún no hay calificaciones
- Planteamiento Del ProblemaDocumento18 páginasPlanteamiento Del ProblemaAnonymous pSj2xjXwt100% (1)
- Clase 6. DisolucioneDocumento30 páginasClase 6. Disolucionecristian ortizAún no hay calificaciones
- Anexo 3 CromatografiaDocumento11 páginasAnexo 3 Cromatografialeidi murilloAún no hay calificaciones
- Aumento Del Punto de Ebullicion .Descenso Del Punto de Ebullicion - Presion OsmoticaDocumento18 páginasAumento Del Punto de Ebullicion .Descenso Del Punto de Ebullicion - Presion OsmoticaJesús NavarroAún no hay calificaciones
- Caucho, Vulcanizado o Termoplástico Determinación Del Efecto de Los LíquidosDocumento4 páginasCaucho, Vulcanizado o Termoplástico Determinación Del Efecto de Los LíquidosNorma PazAún no hay calificaciones
- Práctica 4Documento6 páginasPráctica 4America Campoy VelázquezAún no hay calificaciones
- Ciclo - HV - 23-I - Qui - Semana 1Documento8 páginasCiclo - HV - 23-I - Qui - Semana 1PROFESOR ADOLFO RAMÓNAún no hay calificaciones
- Condensado y Aislante TermicoDocumento45 páginasCondensado y Aislante TermicorenzoAún no hay calificaciones
- Tarea 3 EAtom SistPerDocumento1 páginaTarea 3 EAtom SistPerPaco MartínezAún no hay calificaciones
- Practica 6 - Disoluciones - Formas de Expresarla Concentración.Documento10 páginasPractica 6 - Disoluciones - Formas de Expresarla Concentración.brandon moralesAún no hay calificaciones
- Mecanizado ElectroquimicoDocumento13 páginasMecanizado ElectroquimicoandresAún no hay calificaciones
- Estados de La Materia Boson-EinsteinDocumento3 páginasEstados de La Materia Boson-EinsteinJocaro FilosofoAún no hay calificaciones
- Contenido S15 - C59Documento21 páginasContenido S15 - C59Karen MonarAún no hay calificaciones
- Cap 01 Materia 1Documento7 páginasCap 01 Materia 1Teofilo Donaires Flores0% (1)
- Primera Ecuacion de BerthelotDocumento8 páginasPrimera Ecuacion de BerthelotFernando Talavera100% (1)
- Conceptos Basicos de ElectroquimicaDocumento3 páginasConceptos Basicos de ElectroquimicaNatasha Ramirez LunaAún no hay calificaciones
- EspectroscopíaDocumento3 páginasEspectroscopíaJulio César Guzmán CortésAún no hay calificaciones
- Equilibrio QuimicoDocumento3 páginasEquilibrio QuimicoAngela CussiAún no hay calificaciones
- Informe Laboratorio QuímicaDocumento9 páginasInforme Laboratorio Químicajesu100% (1)
- Propiedades Acido-Base de Los AminoacidosDocumento11 páginasPropiedades Acido-Base de Los AminoacidosLidia MezaAún no hay calificaciones
- LIBbacarsDocumento274 páginasLIBbacarsMayte SalazarAún no hay calificaciones
- Laboratorio Nro 1 de Ope 1Documento15 páginasLaboratorio Nro 1 de Ope 1Darwin Aima CruzAún no hay calificaciones
- Introduccion Ciencia Ingenieria Materiales CallisterDocumento11 páginasIntroduccion Ciencia Ingenieria Materiales CallisterJulian DiazAún no hay calificaciones
- A La ChingadaDocumento8 páginasA La ChingadaDaniel LCAún no hay calificaciones
- Determinación Del DabDocumento29 páginasDeterminación Del DabcproyectAún no hay calificaciones
- Ejercicio RMN 2 PROBLEMASDocumento4 páginasEjercicio RMN 2 PROBLEMASlizbeth neriAún no hay calificaciones
- Cap 2 Refrigerantes y LubricantesDocumento77 páginasCap 2 Refrigerantes y LubricantesRodrigoAún no hay calificaciones
- Catalogo de Bombas de VacioDocumento8 páginasCatalogo de Bombas de VacioGuillermo BolívarAún no hay calificaciones