Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Primera Ley de La Termodinámica
Cargado por
Mishel Quispe Condori0 calificaciones0% encontró este documento útil (0 votos)
78 vistas2 páginasLa primera ley de la termodinámica establece que la energía no se crea ni se destruye, solo se transforma. La segunda ley establece que la entropía del universo tiende a incrementarse en el tiempo. La tercera ley afirma que no se puede alcanzar el cero absoluto en un número finito de procesos. El principio cero establece que dos sistemas conectados evolucionarán hasta igualar sus temperaturas y que sistemas en equilibrio térmico con un tercero estarán en equilibrio entre sí.
Descripción original:
Primera Ley de La Termodinámica
Derechos de autor
© © All Rights Reserved
Formatos disponibles
DOCX, PDF, TXT o lea en línea desde Scribd
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoLa primera ley de la termodinámica establece que la energía no se crea ni se destruye, solo se transforma. La segunda ley establece que la entropía del universo tiende a incrementarse en el tiempo. La tercera ley afirma que no se puede alcanzar el cero absoluto en un número finito de procesos. El principio cero establece que dos sistemas conectados evolucionarán hasta igualar sus temperaturas y que sistemas en equilibrio térmico con un tercero estarán en equilibrio entre sí.
Copyright:
© All Rights Reserved
Formatos disponibles
Descargue como DOCX, PDF, TXT o lea en línea desde Scribd
0 calificaciones0% encontró este documento útil (0 votos)
78 vistas2 páginasPrimera Ley de La Termodinámica
Cargado por
Mishel Quispe CondoriLa primera ley de la termodinámica establece que la energía no se crea ni se destruye, solo se transforma. La segunda ley establece que la entropía del universo tiende a incrementarse en el tiempo. La tercera ley afirma que no se puede alcanzar el cero absoluto en un número finito de procesos. El principio cero establece que dos sistemas conectados evolucionarán hasta igualar sus temperaturas y que sistemas en equilibrio térmico con un tercero estarán en equilibrio entre sí.
Copyright:
© All Rights Reserved
Formatos disponibles
Descargue como DOCX, PDF, TXT o lea en línea desde Scribd
Está en la página 1de 2
1.
Primera ley de la termodinámica:
El primer principio de la termodinámica, también conocido como primera
ley de la termodinámica, establece que “la energía no se crea ni se
destruye, solo se transforma“. Esto quiere decir que si se
realiza trabajo sobre un sistema o bien éste intercambia calor con otro,
la energía interna del sistema cambiará.
Más formalmente, este principio se descompone en dos partes:
El «principio de la accesibilidad adiabática»
(en termodinámica, adiabático quiere decir que no intercambia calor con su
entorno), que dice que “el conjunto de los estados de equilibrio a los que
puede acceder un sistema termodinámico cerrado es, adiabáticamente, un
conjunto simplemente conexo“.
El «principio de conservación de la energía», que establece que
“el trabajo de la conexión adiabática entre dos estados de equilibrio de
un sistema cerrado depende exclusivamente de ambos estados
conectados“.
2. Segunda ley de la termodinámica:
El segundo principio de la termodinámica, también conocido
como segunda ley de la termodinámica, establece que “la cantidad
de entropía del universo tiende a incrementarse en el tiempo“. Esta ley
marca la dirección en la que deben llevarse a cabo los
procesos termodinámicos y, por lo tanto, la imposibilidad de que ocurran en
el sentido contrario (por ejemplo, que una mancha de tinta dispersada en
el agua pueda volver a concentrarse en un pequeño volumen). También
establece, en algunos casos, la imposibilidad de convertir completamente
toda la energía de un tipo en otro sin pérdidas. De esta forma, la segunda
ley impone restricciones para las transferencias de energía que
hipotéticamente pudieran llevarse a cabo teniendo en cuenta sólo el primer
principio. Esta ley apoya todo su contenido aceptando la existencia de
una magnitud física llamada entropía, de tal manera que, para un sistema
aislado (que no intercambia materia ni energía con su entorno), la variación
de la entropía siempre debe ser mayor que cero.
3. Tercera ley de la termodinámica:
El tercer principio de la termodinámica, también conocido como tercera
ley de la termodinámicay, más adecuadamente como postulado de
Nernst, afirma que “no se puede alcanzar el cero absoluto en un número
finito de procesos físicos“, lo que, sucintamente, puede definirse como:
Al llegar al cero absoluto, 0 K, cualquier proceso de un sistema físico se
detiene.
Al llegar al cero absoluto la entropía alcanza un valor mínimo y constante.
Algunas fuentes se refieren incorrectamente al postulado
de Nernst (denominado así por ser propuesto por Walther Nernst) como
“la tercera de las leyes de la termodinámica“, pero es importante
reconocer que no es una noción exigida por la termodinámica clásica, por lo
que resulta inapropiado tratarlo de «ley», siendo incluso inconsistente con
la mecánica estadística clásica y necesitando el establecimiento previo de
la estadística cuántica para ser valorado adecuadamente.
La mayor parte de la termodinámica no requiere la utilización de este
postulado, que afirma (como ya se ha visto) que es imposible alcanzar
una temperatura igual al cero absoluto mediante un número finito de
procesos físicos, y que puede formularse también como que a medida que
un sistema dado se aproxima al cero absoluto, su entropía tiende a un valor
constante específico, siendo la entropía de los sólidos cristalinos
puros considerada como nula bajo temperaturas iguales al cero
absoluto. No obstante, debido a estas dos afirmaciones, la tercera
ley provee de un punto de referencia absoluto para la determinación de
la entropía
4. Principio cero de la termodinámica:
Este principio o ley cero establece que existe una determinada propiedad,
denominada temperatura empírica (θ), que es común para todos los
estados de equilibrio termodinámico que se encuentren en equilibrio mutuo
con uno dado. En palabras llanas: “dos sistemas a
distintas temperaturas conectados entre sí evolucionarán hasta que
sus temperaturas se igualen“. Además, establece que “si dos sistemas A y
B están en equilibrio térmico con un tercer sistema C, entonces
los sistemas A y B estarán en equilibrio térmico entre sí“. Este principio
tiene una gran importancia experimental, puesto que permite construir
instrumentos que midan la temperatura de un sistema, aunque no resulta
tan importante en el marco teórico de la termodinámica.
También podría gustarte
- ASME B31.4 Memoria Codigo Tubería Transporte de Hidrocarburos LíquidosDocumento168 páginasASME B31.4 Memoria Codigo Tubería Transporte de Hidrocarburos LíquidosFabian Barragán Ramírez100% (1)
- Leyes de La TermodinámicaDocumento13 páginasLeyes de La Termodinámicakaterine100% (1)
- Leyes de La TermodinámicaDocumento14 páginasLeyes de La TermodinámicaDayan MelvinAún no hay calificaciones
- Herramientas de Perforacion DireccionalDocumento27 páginasHerramientas de Perforacion DireccionalMishel Quispe Condori100% (1)
- Simulador PipesimDocumento7 páginasSimulador PipesimMishel Quispe Condori100% (2)
- MERCADO BarcelonetaDocumento3 páginasMERCADO BarcelonetaJairo Jair100% (1)
- Teoría Del Gas Real: La Relación Exacta Para Gases RealesDe EverandTeoría Del Gas Real: La Relación Exacta Para Gases RealesAún no hay calificaciones
- Leyes de La TermodinámicaDocumento12 páginasLeyes de La Termodinámicasebitas45100% (4)
- Tercera Ley de La Termodinámica CLASE30ABR020Documento13 páginasTercera Ley de La Termodinámica CLASE30ABR020Ivan Rivera ArgumedoAún no hay calificaciones
- SIMONDON, La IndividuaciónDocumento256 páginasSIMONDON, La Individuaciónalacrisviam100% (1)
- Leyes TermodinamicasDocumento2 páginasLeyes Termodinamicasbuscador77Aún no hay calificaciones
- Preguntas de RepasoDocumento1 páginaPreguntas de RepasopedroAún no hay calificaciones
- Las 4 Leyes de La Termodinámica-EstudiarDocumento6 páginasLas 4 Leyes de La Termodinámica-EstudiarMaryori E Guerrra RamirezAún no hay calificaciones
- Leyes de La TermodinamicaDocumento2 páginasLeyes de La TermodinamicaXimena DuranAún no hay calificaciones
- Principios de La TermodinámicaDocumento3 páginasPrincipios de La TermodinámicaLUIS SANTIAGO GOMEZ HERNANDEZAún no hay calificaciones
- Leyes de La TermodinámicaDocumento3 páginasLeyes de La TermodinámicadarioAún no hay calificaciones
- Principios de La TermodinámicaDocumento2 páginasPrincipios de La TermodinámicaFUTURE ENGINEERSAún no hay calificaciones
- Leyes de La TermodinámicaDocumento4 páginasLeyes de La TermodinámicaLa Toronja LokaAún no hay calificaciones
- Guía #2 - Grado 10 - Termodinamica - Leyes de La TermodinamicaDocumento3 páginasGuía #2 - Grado 10 - Termodinamica - Leyes de La Termodinamicaeimer mestraAún no hay calificaciones
- Leyes de La TermodinámicaDocumento3 páginasLeyes de La TermodinámicaAndrés LópezAún no hay calificaciones
- Cuáles Son Los Principios de La TermodinámicaDocumento4 páginasCuáles Son Los Principios de La TermodinámicaJohan CantorAún no hay calificaciones
- LEYES DE LA TERMODINÁMICA. Paula-Andrea - Gomez-Avirama 104718021359Documento2 páginasLEYES DE LA TERMODINÁMICA. Paula-Andrea - Gomez-Avirama 104718021359Paula Andrea Gomez AviramaAún no hay calificaciones
- Termodinamica y Sus LeyesDocumento2 páginasTermodinamica y Sus LeyesDulce Maria Vazquez DiazAún no hay calificaciones
- Principio Cero de La TermodinámicaDocumento41 páginasPrincipio Cero de La TermodinámicaleyterperezAún no hay calificaciones
- Definición de TermodinámicaDocumento2 páginasDefinición de TermodinámicaGunar MurilloAún no hay calificaciones
- Nociones de Termodinámica y Sus Leyes en Profesor en LineaDocumento4 páginasNociones de Termodinámica y Sus Leyes en Profesor en LineaCarlos Andrés Díaz ValderramaAún no hay calificaciones
- TermodinamicaDocumento4 páginasTermodinamicaAlejandroAriasAún no hay calificaciones
- Leyes de La TermodinmicaDocumento3 páginasLeyes de La TermodinmicaAndreita ContrerasAún no hay calificaciones
- Escrito Sobre Termodinamica 1611737Documento5 páginasEscrito Sobre Termodinamica 1611737GENNESIS CAMILA ORTEGA ROPEROAún no hay calificaciones
- Demostración de Las Leyes de La TermodinamicaDocumento2 páginasDemostración de Las Leyes de La TermodinamicaAlberto perez williamAún no hay calificaciones
- Primera LeyDocumento3 páginasPrimera LeyLuisFernandoAún no hay calificaciones
- La TermodinamicaDocumento5 páginasLa TermodinamicaMarco TatosAún no hay calificaciones
- 1 Leyes de La TermodinámicaDocumento5 páginas1 Leyes de La TermodinámicaAlberto Castillo LaraAún no hay calificaciones
- Leyes de La TermodinámicaDocumento8 páginasLeyes de La TermodinámicaJose Edison Campos VargasAún no hay calificaciones
- Leyes de La TermodinámicaDocumento3 páginasLeyes de La TermodinámicaBlack DiamondAún no hay calificaciones
- Leyes de La TermodinamicaDocumento4 páginasLeyes de La TermodinamicaJuan Ricardo Sandoval SalcedoAún no hay calificaciones
- Nociones de TermodinámicaDocumento4 páginasNociones de Termodinámicapablo salinasAún no hay calificaciones
- Parte 1.4 TermodinamicaDocumento9 páginasParte 1.4 TermodinamicaMoyse Alejandro VigilAún no hay calificaciones
- Qué Son Las Leyes de La TermodinámicaDocumento3 páginasQué Son Las Leyes de La TermodinámicaKevin Fernando Tadeo GonzálezAún no hay calificaciones
- Leyes de La TermodinámicaDocumento8 páginasLeyes de La TermodinámicavalenciabarriosmiguelangelAún no hay calificaciones
- Termodinamica, Maquinas Termicas. Olimpiadas ElectromecanicaDocumento14 páginasTermodinamica, Maquinas Termicas. Olimpiadas ElectromecanicaValeria SantuchoAún no hay calificaciones
- TermodinámicaDocumento5 páginasTermodinámicaEDUARDO JOSIMARK FARIAS TOMALAAún no hay calificaciones
- Leyes de La TermodinámicaDocumento5 páginasLeyes de La TermodinámicaEmilioCisternaLizaAún no hay calificaciones
- Principios de TermodinámicaDocumento8 páginasPrincipios de TermodinámicaIng. Gustavo Javier MANAAún no hay calificaciones
- TERMODINAMICADocumento26 páginasTERMODINAMICADavid AbreuAún no hay calificaciones
- Tarea Final de FisicaDocumento11 páginasTarea Final de FisicakenAún no hay calificaciones
- Leyes de La TermodinamicaDocumento6 páginasLeyes de La TermodinamicaJosué Aarón Carril Del ÁguilaAún no hay calificaciones
- Leyes de La TermodinamicaDocumento4 páginasLeyes de La TermodinamicaMalyAún no hay calificaciones
- Practica Fuera de AulaDocumento11 páginasPractica Fuera de AulaMoises CanaviriAún no hay calificaciones
- Segunda Ley de La TermodinamicaDocumento3 páginasSegunda Ley de La TermodinamicaJennifer Carolina Diaz ArrietaAún no hay calificaciones
- TERMODINAMICADocumento9 páginasTERMODINAMICAhectorAún no hay calificaciones
- TermodinamicasDocumento3 páginasTermodinamicasErick TorresAún no hay calificaciones
- Leyes de La TermodinámicaDocumento5 páginasLeyes de La TermodinámicaSaraiAún no hay calificaciones
- Conceptos Basicos de TermodinamicaDocumento13 páginasConceptos Basicos de TermodinamicaROnaldo' MgAún no hay calificaciones
- Trabajo Refrigeracion Leyes TermodinamicasDocumento7 páginasTrabajo Refrigeracion Leyes TermodinamicasMaría Rosa TomapascaAún no hay calificaciones
- Termodinámica InvestigacionDocumento13 páginasTermodinámica InvestigacionAngie ManzanaresAún no hay calificaciones
- La Termodinamica EoyeDocumento9 páginasLa Termodinamica Eoyetenorioe322Aún no hay calificaciones
- Termodinamica FisicaDocumento10 páginasTermodinamica Fisicadalex_tauro93100% (1)
- Las Leyes de La TermodinámicaDocumento8 páginasLas Leyes de La Termodinámicajose luisAún no hay calificaciones
- Conceptos Basicos de La TermodinamicaDocumento29 páginasConceptos Basicos de La TermodinamicaMayra Leal100% (2)
- TermodinamicaDocumento71 páginasTermodinamicaDavid Evaristo HernandezAún no hay calificaciones
- Ley Cero de La Termodinámic1Documento3 páginasLey Cero de La Termodinámic1Oxan Shyb Mori VAún no hay calificaciones
- Valvulas Parte 3Documento2 páginasValvulas Parte 3Mishel Quispe CondoriAún no hay calificaciones
- Valvulas Parte 2Documento3 páginasValvulas Parte 2Mishel Quispe CondoriAún no hay calificaciones
- Valvulas Parte 4Documento2 páginasValvulas Parte 4Mishel Quispe CondoriAún no hay calificaciones
- Valvulas Parte 1Documento5 páginasValvulas Parte 1Mishel Quispe CondoriAún no hay calificaciones
- Ecuacion de Caudal y DiametroDocumento1 páginaEcuacion de Caudal y DiametroMishel Quispe CondoriAún no hay calificaciones
- Informe Obtencion Del EtilenoDocumento12 páginasInforme Obtencion Del EtilenoMishel Quispe CondoriAún no hay calificaciones
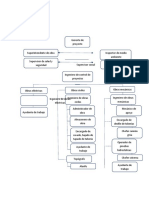
- OrganigramaDocumento2 páginasOrganigramaMishel Quispe CondoriAún no hay calificaciones
- Antecedentes Del Campo San AlbertoDocumento10 páginasAntecedentes Del Campo San AlbertoMishel Quispe Condori100% (1)
- Enmienda 2Documento4 páginasEnmienda 2Mishel Quispe CondoriAún no hay calificaciones
- Campo Montecristo-1Documento5 páginasCampo Montecristo-1Mishel Quispe CondoriAún no hay calificaciones
- Campo El DoradoDocumento2 páginasCampo El DoradoMishel Quispe CondoriAún no hay calificaciones
- Bloques Gasiferos de BoliviaDocumento2 páginasBloques Gasiferos de BoliviaMishel Quispe CondoriAún no hay calificaciones
- Bombeo MecanicoDocumento18 páginasBombeo MecanicoMishel Quispe CondoriAún no hay calificaciones
- Tapon Superior e Inferior de CementacionDocumento2 páginasTapon Superior e Inferior de CementacionMishel Quispe CondoriAún no hay calificaciones
- Trabajo Final Diseño de ProyectosDocumento47 páginasTrabajo Final Diseño de ProyectosNestor Cortina Viana0% (1)
- Capacitores y DieléctricoDocumento62 páginasCapacitores y DieléctricoarmandoAún no hay calificaciones
- Ejercicio 5. Velocidad Del Sonido de NitrogénoDocumento4 páginasEjercicio 5. Velocidad Del Sonido de NitrogénoIsaac Reyes BarrientosAún no hay calificaciones
- Registros de Producción en Pozo Petrolero: Registro de Presión, Temperatura y Gasto A Condiciones Del PozoDocumento19 páginasRegistros de Producción en Pozo Petrolero: Registro de Presión, Temperatura y Gasto A Condiciones Del Pozoalex armando mendez perezAún no hay calificaciones
- Aceite Exxon MobilDocumento2 páginasAceite Exxon MobilAle Samy VillaAún no hay calificaciones
- Practica #03 - Diagrama IshikawaDocumento3 páginasPractica #03 - Diagrama IshikawaA J V ZAún no hay calificaciones
- Feldespato 05Documento9 páginasFeldespato 05Orlando LeonAún no hay calificaciones
- Contacostos2ae Ud PDFDocumento66 páginasContacostos2ae Ud PDFAndres Estupiñan0% (1)
- Mantenimiento de Una Trituradora de MartillosDocumento4 páginasMantenimiento de Una Trituradora de MartillosPatricio CastilloAún no hay calificaciones
- Mecanizado Por LaserDocumento12 páginasMecanizado Por Laserantonio ibañezAún no hay calificaciones
- Presentación Agueera Acigra - v3Documento88 páginasPresentación Agueera Acigra - v3flywheel2006Aún no hay calificaciones
- Modelos de Producción SocialDocumento11 páginasModelos de Producción SocialUPTA OnlineAún no hay calificaciones
- La Selva Nuestra Vida: Sabiduría Ecológica Del Pueblo ShuarDocumento123 páginasLa Selva Nuestra Vida: Sabiduría Ecológica Del Pueblo Shuarluis angelAún no hay calificaciones
- Informe Practica ProfesionalDocumento39 páginasInforme Practica ProfesionalJulian PaezAún no hay calificaciones
- Energía RadianteDocumento18 páginasEnergía RadianteGonzalo Ccahuana Yanque100% (1)
- Hogares Sostenibles de Desarrollo Progresivo PDFDocumento15 páginasHogares Sostenibles de Desarrollo Progresivo PDFjohan jaimesAún no hay calificaciones
- McDonald Responsabilidad AmbientalDocumento3 páginasMcDonald Responsabilidad AmbientalValentina ChavezAún no hay calificaciones
- Tarea 2 Mate 6 1er Sem 2018Documento2 páginasTarea 2 Mate 6 1er Sem 2018Luis EduardoAún no hay calificaciones
- Tema 5 1 Gen IntroducciónDocumento32 páginasTema 5 1 Gen IntroducciónNuriaAún no hay calificaciones
- Tribología: Félix García Mora, MengDocumento552 páginasTribología: Félix García Mora, Mengfernando sangoquizaAún no hay calificaciones
- Ejemplo Casa BatDocumento2 páginasEjemplo Casa Batcristian garciaAún no hay calificaciones
- MX Manual IaDocumento40 páginasMX Manual IaHugo Mioses Garcia HernandezAún no hay calificaciones
- Havoline Premium SAE 25W50Documento2 páginasHavoline Premium SAE 25W50Juan IbaAún no hay calificaciones
- Plan de Prevencion y Reduccion Del Riesgo de Desastres para El Distrito de Tupac Amaru IncaDocumento52 páginasPlan de Prevencion y Reduccion Del Riesgo de Desastres para El Distrito de Tupac Amaru IncaIngrid Victoria VillalobosAún no hay calificaciones
- Revista Cuadrilla 174Documento40 páginasRevista Cuadrilla 174jcpacco3145100% (1)
- Analisis Procesos Unitarios Und 1 34306Documento53 páginasAnalisis Procesos Unitarios Und 1 34306francoAún no hay calificaciones
- Biomasa y Bioproductos PPT Prodero-1Documento14 páginasBiomasa y Bioproductos PPT Prodero-1EcoformanAlbertoAún no hay calificaciones