Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Manual 12 de Octubre (2016) PDF
Manual 12 de Octubre (2016) PDF
Cargado por
Camila GarceteCopyright:
Formatos disponibles
También podría gustarte
- Cuadro Historia Del DX FTDocumento1 páginaCuadro Historia Del DX FTStephany Rendón100% (1)
- Hoja de Salud Depilacion LaserDocumento1 páginaHoja de Salud Depilacion LaserCarlos HernándezAún no hay calificaciones
- Consentimiento Informado Cancer de PielDocumento2 páginasConsentimiento Informado Cancer de PielBaldur SernaAún no hay calificaciones
- Informe - Caso de Fobia Social Desde El Modelo Conigtivo ConductualDocumento11 páginasInforme - Caso de Fobia Social Desde El Modelo Conigtivo ConductualYulieth Paola Salas MachucaAún no hay calificaciones
- Examen - (ACDB1-15%) (SUP1) Actividad Suplementaria - Analice Los Criterios Diagnósticos de Los Trastornos Alimentarios y de La Ingestión de AlimentosDocumento4 páginasExamen - (ACDB1-15%) (SUP1) Actividad Suplementaria - Analice Los Criterios Diagnósticos de Los Trastornos Alimentarios y de La Ingestión de AlimentosBryan RuizAún no hay calificaciones
- Ejemplos de Trastornos de La Personalidad ExtrañaDocumento2 páginasEjemplos de Trastornos de La Personalidad ExtrañaEdwin Rodrigo Sulca Huaynate100% (1)
- TDH en Los NiñosDocumento7 páginasTDH en Los Niñosluisa reyesAún no hay calificaciones
- Enfoque de Riesgo CVDocumento11 páginasEnfoque de Riesgo CVRoberto Páez BravoAún no hay calificaciones
- 01 Diabetes Gestacional - ResDocumento8 páginas01 Diabetes Gestacional - ResYennyHerreraQuirozAún no hay calificaciones
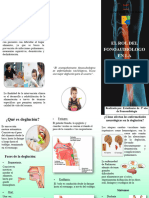
- El Rol Del Fonoaudiólogo en La DegluciónDocumento2 páginasEl Rol Del Fonoaudiólogo en La DegluciónMaría Eloísa García AbelloAún no hay calificaciones
- Ponencia Guadilla Marisa Jornada - OctubreDocumento15 páginasPonencia Guadilla Marisa Jornada - OctubreMia CuentaAún no hay calificaciones
- Maniobras de Reposición CanalicularDocumento5 páginasManiobras de Reposición Canalicularjuan jorqueraAún no hay calificaciones
- Anorexia NerviosaDocumento15 páginasAnorexia NerviosaMaría Yojaira Barrera RomeroAún no hay calificaciones
- Hoja de Triaje ActualDocumento2 páginasHoja de Triaje ActualXiomara TrujilloAún no hay calificaciones
- TriageDocumento21 páginasTriageAlexis ORhpositivoAún no hay calificaciones
- Enfermedades Priónicas PDFDocumento15 páginasEnfermedades Priónicas PDFEliana CamargoAún no hay calificaciones
- Epoc - 2023Documento34 páginasEpoc - 2023Luis VasquezAún no hay calificaciones
- Sindrome de Oht.Documento2 páginasSindrome de Oht.Aylin Revilla VargasAún no hay calificaciones
- El AbortoDocumento11 páginasEl AbortoAna GerreroAún no hay calificaciones
- Evaluacion Por Hipotesis Diagnostic A de Deficit AtencionalDocumento2 páginasEvaluacion Por Hipotesis Diagnostic A de Deficit AtencionalMiguel Angel FloresAún no hay calificaciones
- Neuro - Esquemas para ExamenDocumento6 páginasNeuro - Esquemas para Examennolas16100% (3)
- Sindrome Piramidal y Evento Cerebro VascularDocumento9 páginasSindrome Piramidal y Evento Cerebro VascularSara Lisbeth Mora LedesmaAún no hay calificaciones
- AcidosisDocumento10 páginasAcidosisAriangel Zurita BustamanteAún no hay calificaciones
- Tratamiento Post QuirúrgicoDocumento2 páginasTratamiento Post QuirúrgicoDiegoAún no hay calificaciones
- EGAN'S Fundamentals of Respiratory Care 12th Ed (1) (1) .En - EsDocumento21 páginasEGAN'S Fundamentals of Respiratory Care 12th Ed (1) (1) .En - EsHelí Ricardo Carmona0% (1)
- SRQ Cuestionario AutorreporteDocumento2 páginasSRQ Cuestionario AutorreporteLaly Huarca CcansayaAún no hay calificaciones
- Enfermedades Mentales HereditariasDocumento2 páginasEnfermedades Mentales HereditariasnicolasAún no hay calificaciones
- Enfermedad de AlzheimerDocumento6 páginasEnfermedad de AlzheimerDamián GalindoAún no hay calificaciones
- HEMORRAGIASDocumento11 páginasHEMORRAGIASYuli Esquivel RodrigezAún no hay calificaciones
- Lectura 1. RESUMEN DEPRESIÓNDocumento10 páginasLectura 1. RESUMEN DEPRESIÓNliongadoAún no hay calificaciones
Manual 12 de Octubre (2016) PDF
Manual 12 de Octubre (2016) PDF
Cargado por
Camila GarceteTítulo original
Derechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
Manual 12 de Octubre (2016) PDF
Manual 12 de Octubre (2016) PDF
Cargado por
Camila GarceteCopyright:
Formatos disponibles
ÍNDICE
1. Introducción a la práctica clínica ................................................................................................ 14
I. RELACIÓN MÉDICO/PACIENTE .............................................................................................................. 14
II. HISTORIA CLÍNICA ................................................................................................................................. 15
III. TRONCALIDAD Y SISTEMA MÉDICO INTERNO RESIDENTE .................................................................... 16
IV. ÉTICA Y MEDICINA ................................................................................................................................ 16
V. ECONOMÍA Y MEDICINA ....................................................................................................................... 18
2. Técnicas y procedimientos instrumentales ................................................................................. 19
I. VÍAS VENOSAS DE ACCESO PERIFÉRICO................................................................................................ 19
II. VÍAS VENOSAS CENTRALES ................................................................................................................... 19
III. INTUBACIÓN ENDOTRAQUEAL ............................................................................................................. 23
IV. CRICOTIROIDOTOMÍA ........................................................................................................................... 27
V. DRENAJE ENDOTORÁCICO .................................................................................................................... 27
VI. PERICARDIOCENTESIS ........................................................................................................................... 28
VII. TORACOCENTESIS ................................................................................................................................. 29
VIII. PARACENTESIS ...................................................................................................................................... 31
IX. SONDAJE GÁSTRICO .............................................................................................................................. 32
X. SONDA DE SENGSTAKEN-BLAKEMORE ................................................................................................. 33
XI. PUNCIÓN LUMBAR ............................................................................................................................... 34
XII. SONDAJE VESICAL ................................................................................................................................. 35
XIII. ARTROCENTESIS .................................................................................................................................... 36
3. Resucitación cardiopulmonar y valoración del paciente politraumatizado ................................... 38
I. INTRODUCCIÓN .................................................................................................................................... 38
II. SOPORTE VITAL BÁSICO ........................................................................................................................ 39
III. DESFIBRILADOR EXTERNO AUTOMÁTICO ............................................................................................. 41
IV. OBSTRUCCIÓN DE LA VÍA AÉREA POR CUERPO EXTRAÑO .................................................................... 41
V. RESUCITACIÓN CARDIOPULMONAR BÁSICA PEDIÁTRICA .................................................................... 42
VI. SOPORTE VITAL AVANZADO ................................................................................................................. 43
VII. CALIDAD DE LA RESUCITACIÓN CARDIOPULMONAR Y ECOGRAFÍA ..................................................... 48
VIII. CUIDADOS POSRESUCITACIÓN ............................................................................................................. 49
IX. PRONÓSTICO ........................................................................................................................................ 51
X. VALORACIÓN DEL PACIENTE POLITRAUMATIZADO .............................................................................. 52
4. Shock ........................................................................................................................................ 60
I. CONCEPTO ............................................................................................................................................ 60
II. FISIOPATOLOGÍA ................................................................................................................................... 60
III. CLASIFICACIÓN DEL SHOCK................................................................................................................... 61
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1]
IV. CLÍNICA Y APROXIMACIÓN DIAGNÓSTICA ............................................................................................ 62
V. ABORDAJE TERAPÉUTICO ..................................................................................................................... 63
5. Dolor y sedoanalgesia ................................................................................................................ 71
I. CONCEPTO ............................................................................................................................................ 71
II. CLASIFICACIÓN DEL DOLOR .................................................................................................................. 71
III. APROXIMACIÓN DIAGNÓSTICA ............................................................................................................ 73
IV. TRATAMIENTO ...................................................................................................................................... 74
V. SEDOANALGESIA ................................................................................................................................... 84
6. Principios básicos en cuidados paliativos .................................................................................... 91
I. CONCEPTOS .......................................................................................................................................... 91
II. CRITERIOS DE TERMINALIDAD .............................................................................................................. 92
III. COMUNICACIÓN ................................................................................................................................... 95
IV. EVALUACIÓN Y CONTROL DE LOS SÍNTOMAS....................................................................................... 95
V. VÍA SUBCUTÁNEA ............................................................................................................................... 103
VI. FASE TERMINAL .................................................................................................................................. 105
VII. SEDACIÓN PALIATIVA ......................................................................................................................... 106
VIII. DUELO ................................................................................................................................................. 109
7. Disnea e insuficiencia respiratoria ............................................................................................ 110
I. DISNEA ................................................................................................................................................ 110
II. INSUFICIENCIA RESPIRATORIA ............................................................................................................ 117
8. Síncope ................................................................................................................................... 126
I. CONCEPTO .......................................................................................................................................... 126
II. FISIOPATOLOGÍA ................................................................................................................................. 126
III. ETIOLOGÍA .......................................................................................................................................... 126
IV. ABORDAJE DIAGNÓSTICO ................................................................................................................... 128
V. DIAGNÓSTICO DIFERENCIAL ............................................................................................................... 132
VI. ESTRATIFICACIÓN DEL RIESGO ........................................................................................................... 133
VII. TRATAMIENTO .................................................................................................................................... 135
9. Dolor torácico .......................................................................................................................... 136
I. INTRODUCCIÓN .................................................................................................................................. 136
II. EVALUACIÓN INICIAL .......................................................................................................................... 136
III. PERFILES CLÍNICOS .............................................................................................................................. 139
IV. CAUSAS SEGÚN EL PERFIL CLÍNICO ..................................................................................................... 141
V. PRUEBAS COMPLEMENTARIAS ........................................................................................................... 141
VI. ALGORITMO ........................................................................................................................................ 142
10. Dolor abdominal agudo ........................................................................................................... 144
I. INTRODUCCIÓN .................................................................................................................................. 144
II. FISIOPATOLOGÍA ................................................................................................................................. 144
III. ETIOLOGÍA .......................................................................................................................................... 144
IV. DIAGNÓSTICO ..................................................................................................................................... 145
V. ENTIDADES CLÍNICAS MÁS RELEVANTES ............................................................................................ 151
VI. SITUACIONES ESPECIALES ................................................................................................................... 153
VII. MANEJO TERAPÉUTICO ...................................................................................................................... 154
11. Síndrome confusional agudo .................................................................................................... 157
I. CONCEPTO .......................................................................................................................................... 157
II. ETIOLOGÍA .......................................................................................................................................... 157
III. CLÍNICA ............................................................................................................................................... 158
IV. APROXIMACIÓN DIAGNÓSTICA .......................................................................................................... 158
V. PRONÓSTICO ...................................................................................................................................... 162
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [2]
VI. ABORDAJE TERAPÉUTICO ................................................................................................................... 162
12. Lumbalgia................................................................................................................................ 165
I. DEFINICIÓN ......................................................................................................................................... 165
II. ETIOLOGÍA .......................................................................................................................................... 165
III. CLÍNICA ............................................................................................................................................... 166
IV. DIAGNÓSTICO ..................................................................................................................................... 166
V. TRATAMIENTO Y MANEJO .................................................................................................................. 168
13. Monoartritis y poliartritis......................................................................................................... 171
I. MONOARTRITIS .................................................................................................................................. 171
II. POLIARTRITIS ...................................................................................................................................... 177
14. Fiebre de origen desconocido. Alteraciones de la termorregulación .......................................... 184
I. CONCEPTO .......................................................................................................................................... 184
II. EPIDEMIOLOGÍA ................................................................................................................................. 184
III. ETIOLOGÍA .......................................................................................................................................... 185
IV. DIAGNÓSTICO ..................................................................................................................................... 185
V. PRONÓSTICO ...................................................................................................................................... 188
VI. TRATAMIENTO .................................................................................................................................... 188
VII. ALTERACIONES DE LA TERMORREGULACIÓN ..................................................................................... 189
15. Patología urológica más frecuente ........................................................................................... 198
I. SÍNTOMAS DEL TRACTO URINARIO INFERIOR .................................................................................... 198
II. RETENCIÓN URINARIA ........................................................................................................................ 203
III. SÍNDROME DE ESCROTO AGUDO ....................................................................................................... 205
IV. HEMATURIA MACROSCÓPICA ............................................................................................................ 205
V. NEFROLITIASIS-CRISIS RENOURETERAL .............................................................................................. 209
16. Patología oftalmológica ........................................................................................................... 213
I. OJO ROJO ............................................................................................................................................ 213
II. ALTERACIONES DE LA AGUDEZA VISUAL ............................................................................................ 216
III. DIPLOPÍA ............................................................................................................................................. 217
17. Patología otorrinolaringológica. Manejo de traqueotomías ...................................................... 219
I. PATOLOGÍA INFLAMATORIA E INFECCIOSA (Tabla I) .......................................................................... 219
II. PARÁLISIS FACIAL PERIFÉRICA ............................................................................................................ 223
III. CUERPOS EXTRAÑOS EN EL CONDUCTO AUDITIVO EXTERNO ........................................................... 225
IV. PATOLOGÍA TRAUMÁTICA .................................................................................................................. 225
V. RINOSINUSITIS AGUDA ....................................................................................................................... 227
VI. EPISTAXIS ............................................................................................................................................ 230
VII. GLÁNDULAS SALIVALES ...................................................................................................................... 232
VIII. FARINGOAMIGDALITIS AGUDA INFECCIOSA ...................................................................................... 233
IX. PATOLOGÍA INFECCIOSA/INFLAMATORIA. LARINGITIS ...................................................................... 237
X. MANEJO DE TRAQUEOTOMÍAS .......................................................................................................... 238
18. Patologías dermatológicas: Exantemas. Urticaria y angiodemas ................................................ 244
I. EXANTEMAS ........................................................................................................................................ 244
II. URTICARIA Y ANGIOEDEMA ................................................................................................................ 252
III. ANGIOEDEMA HEREDITARIO Y ADQUIRIDO ....................................................................................... 257
19. Patología psiquiátrica importante para el médico general ......................................................... 261
I. ANSIEDAD ........................................................................................................................................... 261
II. DEPRESIÓN ......................................................................................................................................... 264
III. AGITACIÓN PSICOMOTRIZ .................................................................................................................. 267
20. Hipertensión arterial y riesgo cardiovascular ............................................................................ 272
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [3]
I. DEFINICIÓN Y CLASIFICACIÓN ............................................................................................................. 272
II. EVALUACIÓN DIAGNÓSTICA ............................................................................................................... 272
III. TRATAMIENTO .................................................................................................................................... 275
IV. HIPERTENSIÓN EN EL ANCIANO.......................................................................................................... 278
V. HIPERTENSIÓN EN EL EMBARAZO ...................................................................................................... 278
VI. HIPERTENSIÓN ARTERIAL RESISTENTE ................................................................................................ 278
VII. EMERGENCIA Y URGENCIA HIPERTENSIVA ......................................................................................... 279
VIII. RIESGO VASCULAR .............................................................................................................................. 282
21. Insuficiencia cardíaca ............................................................................................................... 286
I. DEFINICIÓN ......................................................................................................................................... 286
II. ETIOLOGÍA .......................................................................................................................................... 286
III. CLASIFICACIÓN ................................................................................................................................... 286
IV. CLÍNICA ............................................................................................................................................... 287
V. PRUEBAS COMPLEMENTARIAS ........................................................................................................... 287
VI. INSUFICIENCIA CARDIACA AGUDA...................................................................................................... 289
VII. INSUFICIENCIA CARDIACA CRÓNICA ................................................................................................... 295
22. Arritmias ................................................................................................................................. 304
I. TAQUIARRITMIAS ............................................................................................................................... 304
II. BRADIARRITMIAS ................................................................................................................................ 324
III. MARCAPASOS: CONCEPTO, INDICACIONES Y DISFUNCIÓN................................................................ 330
23. Cardiopatía isquémica ............................................................................................................. 332
I. CONCEPTO .......................................................................................................................................... 332
II. FISIOPATOLOGÍA ................................................................................................................................. 332
III. ETIOLOGÍA .......................................................................................................................................... 333
IV. CLÍNICA ............................................................................................................................................... 333
V. APROXIMACIÓN DIAGNÓSTICA .......................................................................................................... 334
VI. TRATAMIENTO .................................................................................................................................... 343
VII. OTRAS CONSIDERACIONES ................................................................................................................. 355
24. Valvulopatías........................................................................................................................... 359
I. VALVULOPATÍA MITRAL ...................................................................................................................... 359
II. VALVULOPATÍA AÓRTICA .................................................................................................................... 368
III. VALVULOPATÍA TRICUSPÍDEA ............................................................................................................. 377
IV. VALVULOPATÍA PULMONAR ............................................................................................................... 378
V. PRÓTESIS VALVULARES ....................................................................................................................... 379
25. Enfermedades del pericardio ................................................................................................... 384
I. INTRODUCCIÓN .................................................................................................................................. 384
II. PERICARDITIS AGUDA ......................................................................................................................... 384
III. DERRAME PERICÁRDICO ..................................................................................................................... 389
IV. TAPONAMIENTO CARDIACO ............................................................................................................... 390
V. CONSTRICCIÓN PERICÁRDICA ............................................................................................................. 391
26. Síndrome aórtico agudo. Enfermedad vascular periférica ......................................................... 396
I. SÍNDROME AÓRTICO AGUDO ............................................................................................................. 396
II. ENFERMEDAD VASCULAR PERIFÉRICA ................................................................................................ 403
27. Hipertensión pulmonar ............................................................................................................ 409
I. CONCEPTO Y CLASIFICACIÓN .............................................................................................................. 409
II. EPIDEMIOLOGÍA ................................................................................................................................. 410
III. MANIFESTACIONES CLÍNICAS DE LA HIPERTENSIÓN ARTERIAL PULMONAR ...................................... 411
IV. DIAGNÓSTICO DE LA HIPERTENSIÓN ARTERIAL PULMONAR ............................................................. 412
V. TRATAMIENTO DE LA HIPERTENSIÓN ARTERIAL PULMONAR ............................................................ 415
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [4]
VI. PRONÓSTICO DE LA HIPERTENSIÓN ARTERIAL PULMONAR ............................................................... 419
VII. CARACTERÍSTICAS DE LOS OTROS TIPOS DE HIPERTENSIÓN PULMONAR .......................................... 419
VIII. SITUACIONES ESPECIALES EN HIPERTENSIÓN ARTERIAL PULMONAR SEVERA EN URGENCIAS ......... 421
IX. UNIDADES ESPECIALIZADAS MULTIDISCIPLINARES Y CENTROS DE REFERENCIA ............................... 422
28. Tos crónica y hemoptisis .......................................................................................................... 424
I. TOS CRÓNICA ...................................................................................................................................... 424
II. HEMOPTISIS ........................................................................................................................................ 428
29. Asma y enfermedad pulmonar obstructiva crónica ................................................................... 435
I. ASMA .................................................................................................................................................. 435
II. ENFERMEDAD PULMONAR OBSTRUCTIVA CRÓNICA ......................................................................... 446
30. Bronquiectasias ....................................................................................................................... 461
I. INTRODUCCIÓN .................................................................................................................................. 461
II. ETIOLOGÍA .......................................................................................................................................... 461
III. CLÍNICA ............................................................................................................................................... 461
IV. DIAGNÓSTICO ..................................................................................................................................... 462
V. TRATAMIENTO .................................................................................................................................... 465
VI. COMPLICACIONES............................................................................................................................... 469
VII. INMUNOPROFILAXIS ........................................................................................................................... 470
31. Trastornos respiratorios durante el sueño: síndrome de apneas-hipopneas del sueño. Otros..... 471
I. SÍNDROME DE APNEAS-HIPOPNEAS DEL SUEÑO ............................................................................... 471
II. OTROS TRASTORNOS RESPIRATORIOS DURANTE EL SUEÑO .............................................................. 478
32. Enfermedad tromboembólica venosa ....................................................................................... 480
I. DEFINICIÓN Y ETIOPATOGENIA .......................................................................................................... 480
II. DIAGNÓSTICO ..................................................................................................................................... 481
III. EVALUACIÓN PRONÓSTICA Y GRAVEDAD DEL TROMBOEMBOLISMO PULMONAR ........................... 487
IV. TRATAMIENTO .................................................................................................................................... 488
V. SEGUIMIENTO Y DURACIÓN DE LA ANTICOAGULACIÓN .................................................................... 491
VI. SITUACIONES ESPECIALES ................................................................................................................... 493
VII. PREVENCIÓN DE LA ENFERMEDAD TROMBOEMBÓLICA VENOSA ..................................................... 494
VIII. HIPERTENSIÓN PULMONAR TROMBOEMBÓLICA CRÓNICA (HPTEC) ................................................. 498
33. Enfermedades pulmonares intersticiales difusas....................................................................... 501
I. CONCEPTO .......................................................................................................................................... 501
II. CLASIFICACIÓN Y ETIOLOGÍA .............................................................................................................. 502
III. CLÍNICA ............................................................................................................................................... 502
IV. DIAGNÓSTICO (Figura 1) ..................................................................................................................... 502
V. CRITERIOS DE INGRESO ...................................................................................................................... 507
VI. ABORDAJE TERAPÉUTICO ................................................................................................................... 507
VII. PRONÓSTICO Y SEGUIMIENTO ........................................................................................................... 508
34. Patología pleural ..................................................................................................................... 509
I. INTRODUCCIÓN. DEFINICIÓN Y FISIOPATOLOGÍA .............................................................................. 509
II. ETIOLOGÍA .......................................................................................................................................... 509
III. CLÍNICA Y APROXIMACIÓN DIAGNÓSTICA INICIAL ............................................................................. 510
IV. ABORDAJE DIAGNÓSTICO ................................................................................................................... 511
V. TIPOS MÁS FRECUENTES DE DERRAME PLEURAL Y SU ABORDAJE ESPECÍFICO ................................. 516
VI. NEUMOTÓRAX .................................................................................................................................... 524
35. Principios de ventilación mecánica. Síndrome de distrés respiratorio agudo. Trasplante pulmonar
............................................................................................................................................... 527
I. PRINCIPIOS DE VENTILACIÓN MECÁNICA ........................................................................................... 527
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [5]
II. SÍNDROME DE DISTRÉS RESPIRATORIO AGUDO ................................................................................. 532
III. TRASPLANTE PULMONAR ................................................................................................................... 536
36. Bacteriemia y sepsis ................................................................................................................ 538
I. INTRODUCCIÓN .................................................................................................................................. 538
II. DEFINICIONES ..................................................................................................................................... 538
III. FISIOPATOLOGÍA ................................................................................................................................. 540
IV. MANIFESTACIONES CLÍNICAS ............................................................................................................. 540
V. DIAGNÓSTICO ..................................................................................................................................... 542
VI. CRITERIOS DE AVISO AL SERVICIO DE MEDICINA INTENSIVA ............................................................. 544
VII. ABORDAJE TERAPÉUTICO DE LA SEPSIS .............................................................................................. 544
37. Endocarditis infecciosa. Infecciones endovasculares y fungemia ............................................... 553
I. ENDOCARDITIS.................................................................................................................................... 553
II. INFECCIONES ENDOVASCULARES ....................................................................................................... 565
III. CANDIDEMIA ...................................................................................................................................... 567
38. Infecciones de las vías respiratorias.......................................................................................... 571
I. BRONQUITIS AGUDA .......................................................................................................................... 571
II. NEUMONÍA ADQUIRIDA EN LA COMUNIDAD (NAC) Y NEUMONÍA ASOCIADA A ENTORNOS
SANITARIOS (NAES) ............................................................................................................................ 572
III. GRIPE .................................................................................................................................................. 583
39. Infecciones del tracto urinario.................................................................................................. 586
I. INTRODUCCIÓN .................................................................................................................................. 586
II. BACTERIURIA ASINTOMÁTICA ............................................................................................................ 587
III. CISTITIS AGUDA NO COMPLICADA ..................................................................................................... 588
IV. CISTITIS AGUDA COMPLICADA ........................................................................................................... 593
V. PIELONEFRITIS AGUDA ....................................................................................................................... 593
VI. PROSTATITIS AGUDA .......................................................................................................................... 597
VII. EPIDIDIMITIS Y ORQUITIS ................................................................................................................... 599
VIII. INFECCIONES URINARIAS ASOCIADAS A CATÉTERES URINARIOS ....................................................... 601
IX. INFECCIÓN DEL TRACTO URINARIO EN LA EMBARAZADA .................................................................. 603
X. INFECCIÓN URINARIA RECURRENTE ................................................................................................... 604
40. Infecciones de transmisión sexual ............................................................................................ 608
I. INTRODUCCIÓN .................................................................................................................................. 608
II. APROXIMACIÓN A LAS ÚLCERAS GENITALES ...................................................................................... 608
III. URETRITIS, EPIDIDIMITIS Y CERVICITIS ............................................................................................... 613
IV. VAGINITIS............................................................................................................................................ 615
V. PROCTITIS ........................................................................................................................................... 615
VI. ENFERMEDAD INFLAMATORIA PÉLVICA ............................................................................................. 616
VII. OTRAS INFECCIONES DE TRANSMISIÓN SEXUAL ................................................................................ 617
VIII. ABUSO O AGRESIÓN SEXUAL .............................................................................................................. 618
41. Infección de piel y partes blandas. Osteomielitis....................................................................... 620
I. INFECCIÓN DE PIEL Y PARTES BLANDAS ............................................................................................. 620
II. ÚLCERAS POR PRESIÓN ....................................................................................................................... 626
III. OSTEOMIELITIS ................................................................................................................................... 628
42. Infecciones del sistema nervioso central................................................................................... 639
I. INTRODUCCIÓN .................................................................................................................................. 639
II. ABORDAJE DEL PACIENTE CON SOSPECHA DE INFECCIÓN AGUDA DEL SISTEMA NERVIOSO CENTRAL
............................................................................................................................................................ 639
III. MENINGITIS BACTERIANA AGUDA ...................................................................................................... 643
IV. MENINGITIS SUBAGUDA O CRÓNICA ................................................................................................. 648
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [6]
V. MENINGITIS LINFOCITARIA O ASÉPTICA ............................................................................................. 652
VI. ENCEFALITIS VÍRICA ............................................................................................................................ 653
VII. INFECCIONES FOCALES DEL SISTEMA NERVIOSO CENTRAL ................................................................ 654
43. Infecciones intraabdominales. Diarrea por Clostridium difficile ................................................. 659
I. INTRODUCCIÓN .................................................................................................................................. 659
II. APENDICITIS AGUDA ........................................................................................................................... 660
III. DIVERTICULITIS AGUDA ...................................................................................................................... 661
IV. PERFORACIÓN DE VÍSCERA HUECA..................................................................................................... 664
V. COLECISTITIS AGUDA .......................................................................................................................... 666
VI. COLANGITIS AGUDA O COLANGITIS AGUDA ASCENDENTE ................................................................ 668
VII. ABSCESOS INTRAABDOMINALES ........................................................................................................ 671
VIII. TRATAMIENTO ANTIBIÓTICO EMPÍRICO DE LAS INFECCIONES INTRAABDOMINALES (IIA) ............... 674
IX. INFECCIÓN POR CLOSTRIDIUM DIFFICILE ........................................................................................... 677
44. Hepatitis virales ....................................................................................................................... 683
I. INTRODUCCIÓN .................................................................................................................................. 683
II. ETIOLOGÍA .......................................................................................................................................... 683
III. EPIDEMIOLOGÍA ................................................................................................................................. 683
IV. CLÍNICA ............................................................................................................................................... 684
V. DIAGNÓSTICO ..................................................................................................................................... 685
VI. EVOLUCIÓN Y TRATAMIENTO ............................................................................................................. 688
VII. PROFILAXIS ......................................................................................................................................... 693
45. Tuberculosis ............................................................................................................................ 696
I. DEFINICIÓN ......................................................................................................................................... 696
II. FISIOPATOLOGÍA ................................................................................................................................. 696
III. PRESENTACIONES CLÍNICAS ................................................................................................................ 697
IV. DIAGNÓSTICO ..................................................................................................................................... 699
V. TRATAMIENTO .................................................................................................................................... 704
46. Infección por VIH ..................................................................................................................... 717
I. EPIDEMIOLOGÍA ................................................................................................................................. 717
II. DIAGNÓSTICO Y VALORACIÓN INICIAL ............................................................................................... 717
III. SÍNDROMES Y PROBLEMAS CLÍNICOS ASOCIADOS AL VIH ................................................................. 719
IV. TRATAMIENTO ANTIRRETROVIRAL (TAR) ........................................................................................... 726
V. SIRI (SÍNDROME INFLAMATORIO DE RECONSTITUCIÓN INMUNE) .................................................... 733
VI. ABREVIATURAS UTILIZADAS EN EL TEXTO Y NOMBRES COMERCIALES DE LOS FÁRMACOS
ANTIRRETROVIRALES (®) MÁS USADOS (POR ORDEN ALFABÉTICO) ................................................... 735
47. Infecciones en el paciente inmunodeprimido. Neutropenia febril ............................................. 738
I. INTRODUCCIÓN .................................................................................................................................. 738
II. NEUTROPENIA FEBRIL ......................................................................................................................... 738
III. INFECCIONES EN EL PACIENTE TRASPLANTADO ................................................................................. 745
48. Infecciones nosocomiales ........................................................................................................ 751
I. INFECCIÓN DEL TRACTO URINARIO .................................................................................................... 751
II. INFECCIÓN ASOCIADA AL CATÉTER INTRAVASCULAR ........................................................................ 754
III. INFECCIÓN DEL SITIO QUIRÚRGICO .................................................................................................... 762
IV. NEUMONÍA NOSOCOMIAL ................................................................................................................. 766
49. Enfermedades importadas del viajero y del inmigrante............................................................. 774
I. INTRODUCCIÓN .................................................................................................................................. 774
II. CRIBADO EN EL INMIGRANTE ASINTOMÁTICO .................................................................................. 776
III. EOSINOFILIA........................................................................................................................................ 779
IV. FIEBRE ................................................................................................................................................. 782
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [7]
V. SÍNDROMES DIGESTIVOS .................................................................................................................... 792
VI. SÍNDROME RESPIRATORIO ................................................................................................................. 794
VII. SÍNDROME NEUROLÓGICO ................................................................................................................. 795
VIII. FILARIASIS (Tabla XI) ........................................................................................................................... 795
50. Exposición a material biológico ................................................................................................ 798
I. INTRODUCCIÓN .................................................................................................................................. 798
II. ACTUACIÓN ANTE UNA EXPOSICIÓN ACCIDENTAL............................................................................. 799
III. EXPOSICIÓN AL VIRUS DE LA HEPATITIS B .......................................................................................... 801
IV. EXPOSICIÓN AL VIRUS DE LA HEPATITIS C .......................................................................................... 802
V. EXPOSICIÓN AL VIRUS DE LA INMUNODEFICIENCIA HUMANA .......................................................... 802
51. Ictericia ................................................................................................................................... 806
I. DEFINICIONES Y FISIOPATOLOGÍA ...................................................................................................... 806
II. ETIOPATOGENIA ................................................................................................................................. 806
III. APROXIMACIÓN DIAGNÓSTICA .......................................................................................................... 809
IV. TRATAMIENTO .................................................................................................................................... 812
V. SITUACIONES ESPECIALES ................................................................................................................... 814
52. Ascitis ..................................................................................................................................... 816
I. CONCEPTO .......................................................................................................................................... 816
II. ETIOPATOGENIA ................................................................................................................................. 816
III. CLÍNICA ............................................................................................................................................... 817
IV. DIAGNÓSTICO ..................................................................................................................................... 818
V. ENTIDADES CLÍNICAS .......................................................................................................................... 820
VI. TRATAMIENTO .................................................................................................................................... 824
53. Hemorragia digestiva ............................................................................................................... 825
I. CONCEPTO .......................................................................................................................................... 825
II. MANEJO INICIAL ................................................................................................................................. 825
III. HEMORRAGIA DIGESTIVA ALTA .......................................................................................................... 829
IV. HEMORRAGIA DIGESTIVA BAJA .......................................................................................................... 841
V. HEMORRAGIA DE ORIGEN INCIERTO .................................................................................................. 845
VI. HEMORRAGIA DIGESTIVA OCULTA ..................................................................................................... 846
54. Diarrea aguda y crónica ........................................................................................................... 848
I. DIARREA .............................................................................................................................................. 848
II. DIARREA AGUDA ................................................................................................................................. 848
III. DIARREA CRÓNICA .............................................................................................................................. 854
55. Enfermedad inflamatoria intestinal .......................................................................................... 863
I. INTRODUCCIÓN .................................................................................................................................. 863
II. APROXIMACIÓN DIAGNÓSTICA .......................................................................................................... 863
III. DIAGNÓSTICO DIFERENCIAL ............................................................................................................... 868
IV. COLITIS ULCEROSA .............................................................................................................................. 868
V. ENFERMEDAD DE CROHN ................................................................................................................... 876
VI. SITUACIONES ESPECIALES ................................................................................................................... 881
VII. MANEJO DEL PACIENTE CON ENFERMEDAD INFLAMATORIA INTESTINAL EN EL SERVICIO DE
URGENCIAS ......................................................................................................................................... 882
56. Hepatitis aguda y fallo hepático fulminante.............................................................................. 884
I. HEPATITIS AGUDA .............................................................................................................................. 884
II. FALLO HEPÁTICO FULMINANTE (FHF) ................................................................................................ 901
57. Hepatopatía crónica. Cirrosis hepática y sus complicaciones ..................................................... 911
I. HEPATOPATÍA CRÓNICA Y CIRROSIS ................................................................................................... 911
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [8]
II. COMPLICACIONES DE LA CIRROSIS HEPÁTICA .................................................................................... 915
III. TRASPLANTE HEPÁTICO ...................................................................................................................... 928
58. Pancreatitis ............................................................................................................................. 931
I. PANCREATITIS AGUDA ........................................................................................................................ 931
II. PANCREATITIS CRÓNICA ..................................................................................................................... 941
59. Patología vascular intestinal .................................................................................................... 948
I. INTRODUCCIÓN .................................................................................................................................. 948
II. COLITIS ISQUÉMICA ............................................................................................................................ 948
III. ISQUEMIA MESENTÉRICA ARTERIAL AGUDA ...................................................................................... 953
IV. ISQUEMIA MESENTÉRICA CRÓNICA: ANGINA INTESTINAL ................................................................. 957
V. ISQUEMIA MESENTÉRICA VENOSA: TROMBOSIS VENOSA MESENTÉRICA ......................................... 960
60. Obstrucción intestinal y estreñimiento ..................................................................................... 964
I. INTRODUCCIÓN .................................................................................................................................. 964
II. EVALUACIÓN INICIAL Y APROXIMACIÓN DIAGNÓSTICA ..................................................................... 964
III. OBSTRUCCIÓN INTESTINAL ................................................................................................................. 966
IV. ESTREÑIMIENTO ................................................................................................................................. 968
V. ESTREÑIMIENTO EN EL ANCIANO E IMPACTACIÓN FECAL ................................................................. 972
61. Alteraciones del sistemático y sedimento de orina. Aproximación diagnóstica a la hematuria y la
proteinuria .............................................................................................................................. 974
I. ANÁLISIS DE ORINA ............................................................................................................................. 974
II. APROXIMACIÓN DIAGNÓSTICA DE LA HEMATURIA Y LA PROTEINURIA ............................................ 977
III. GRANDES SÍNDROMES GLOMERULARES ............................................................................................ 982
62. Fracaso renal agudo ................................................................................................................. 987
I. DEFINICIÓN ......................................................................................................................................... 987
II. APROXIMACIÓN DIAGNÓSTICA (Tabla II) ........................................................................................... 987
III. ETIOPATOGENIA ................................................................................................................................. 994
IV. TRATAMIENTO .................................................................................................................................... 996
V. SITUACIONES ESPECIALES ................................................................................................................... 998
63. Enfermedad renal crónica ...................................................................................................... 1002
I. CONCEPTO ........................................................................................................................................ 1002
II. APROXIMACIÓN DIAGNÓSTICA ........................................................................................................ 1005
III. PROGRESIÓN DE LA ENFERMEDAD RENAL CRÓNICA. CRITERIOS DE DERIVACIÓN A NEFROLOGÍA . 1008
IV. MANEJO DE LA ENFERMEDAD RENAL CRÓNICA ............................................................................... 1009
64. Trastornos del equilibrio ácido-base ....................................................................................... 1017
I. CONCEPTO ........................................................................................................................................ 1017
II. INTERPRETACIÓN GASOMÉTRICA ..................................................................................................... 1017
III. ACIDOSIS METABÓLICA .................................................................................................................... 1018
IV. ALCALOSIS METABÓLICA .................................................................................................................. 1022
V. ACIDOSIS RESPIRATORIA .................................................................................................................. 1025
VI. ALCALOSIS RESPIRATORIA ................................................................................................................ 1027
VII. TRASTORNOS MIXTOS ...................................................................................................................... 1028
65. Trastornos del equilibrio hidroelectrolítico. Síndrome de secreción inadecuada de hormona
antidiurética. Fluidoterapia .................................................................................................... 1030
I. ALTERACIONES EN EL EQUILIBRIO DEL SODIO Y DEL AGUA ............................................................. 1030
II. ALTERACIONES DEL POTASIO ........................................................................................................... 1038
III. FLUIDOTERAPIA ................................................................................................................................ 1045
66. Trastornos del metabolismo del calcio, fósforo y magnesio ..................................................... 1052
I. ALTERACIONES EN EL METABOLISMO DEL CALCIO .......................................................................... 1052
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [9]
II. ALTERACIONES EN EL METABOLISMO DEL FÓSFORO ....................................................................... 1060
III. ALTERACIONES EN EL METABOLISMO DEL MAGNESIO .................................................................... 1063
67. Fluidoterapia y principios de nutrición ................................................................................... 1067
I. FLUIDOTERAPIA ................................................................................................................................ 1067
II. PRINCIPIOS DE NUTRICIÓN ............................................................................................................... 1073
68. Enfermedades del tiroides ..................................................................................................... 1084
I. EVALUACIÓN DE LA MORFOLOGÍA Y FUNCIÓN TIROIDEA ................................................................ 1084
II. BOCIO ............................................................................................................................................... 1089
III. NÓDULO TIROIDEO ........................................................................................................................... 1091
IV. TIROIDITIS ......................................................................................................................................... 1093
V. HIPERTIROIDISMO ............................................................................................................................ 1094
VI. HIPOTIROIDISMO .............................................................................................................................. 1098
69. Patología suprarrenal ............................................................................................................ 1101
I. SÍNDROME DE CUSHING ................................................................................................................... 1101
II. INSUFICIENCIA SUPRARRENAL.......................................................................................................... 1106
III. HIPERALDOSTERONISMO ................................................................................................................. 1113
IV. HIPOALDOSTERONISMO ................................................................................................................... 1118
V. FEOCROMOCITOMA ......................................................................................................................... 1119
VI. INCIDENTALOMA ADRENAL .............................................................................................................. 1124
70. Diabetes mellitus. Manejo a largo plazo ................................................................................. 1128
I. DEFINICIÓN ....................................................................................................................................... 1128
II. TIPOS DE DIABETES MELLITUS .......................................................................................................... 1128
III. ETIOPATOGENIA ............................................................................................................................... 1128
IV. CLÍNICA ............................................................................................................................................. 1130
V. DIAGNÓSTICO ................................................................................................................................... 1130
VI. EVALUACIÓN INICIAL Y MANEJO DE LA DIABETES ............................................................................ 1131
VII. VALORACIÓN DE OTRAS COMORBILIDADES ASOCIADAS A LA DIABETES ......................................... 1138
VIII. OBJETIVOS Y ESTRATEGIAS DE CONTROL ......................................................................................... 1138
IX. TRATAMIENTO .................................................................................................................................. 1141
X. DIABETES GESTACIONAL ................................................................................................................... 1151
XI. DIABETES ESTEROIDEA ..................................................................................................................... 1152
XII. DIABETES EN EL ANCIANO ................................................................................................................ 1153
71. Complicaciones agudas de la diabetes .................................................................................... 1155
I. CETOACIDOSIS DIABÉTICA Y SÍNDROME HIPERGLUCÉMICO HIPEROSMOLAR ................................. 1155
II. TRATAMIENTO DE LA HIPERGLUCEMIA EN PACIENTE HOSPITALIZADO ........................................... 1165
III. HIPOGLUCEMIA ................................................................................................................................ 1168
72. Osteoporosis ......................................................................................................................... 1172
I. CONCEPTO Y CLÍNICA ....................................................................................................................... 1172
II. APROXIMACIÓN DIAGNÓSTICA ........................................................................................................ 1172
III. TRATAMIENTO Y PREVENCIÓN ......................................................................................................... 1174
73. Trastornos lipídicos................................................................................................................ 1179
I. INTRODUCCIÓN ................................................................................................................................ 1179
II. CONCEPTO Y CLASIFICACIÓN ............................................................................................................ 1180
III. APROXIMACIÓN DIAGNÓSTICA ........................................................................................................ 1180
IV. OBJETIVOS TERAPÉUTICOS ............................................................................................................... 1181
V. TRATAMIENTO .................................................................................................................................. 1183
74. Trastornos de la serie roja ...................................................................................................... 1192
I. ANEMIA ............................................................................................................................................ 1192
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [10]
II. PRINCIPALES TIPOS DE ANEMIA ....................................................................................................... 1197
III. ERITROCITOSIS (POLICITEMIA) ......................................................................................................... 1210
75. Trastornos de la serie blanca .................................................................................................. 1213
I. INTRODUCCIÓN ................................................................................................................................ 1213
II. LEUCOCITOSIS ................................................................................................................................... 1213
III. LEUCOPENIA ..................................................................................................................................... 1218
76. Trombocitopenia. Trombocitosis. Pancitopenia ...................................................................... 1223
I. TROMBOCITOPENIA ......................................................................................................................... 1223
II. TROMBOCITOSIS ............................................................................................................................... 1228
III. PANCITOPENIA ................................................................................................................................. 1230
77. Trastornos de la hemostasia. Anticoagulación ........................................................................ 1241
I. HEMOSTASIA .................................................................................................................................... 1241
II. TRASTORNOS DE LA HEMOSTASIA ................................................................................................... 1245
III. ANTICOAGULACIÓN .......................................................................................................................... 1255
IV. MANEJO PERIOPERATORIO EN PACIENTES QUE RECIBEN TRATAMIENTO ANTICOAGULANTE ....... 1262
78. Hemoterapia ......................................................................................................................... 1265
I. GRUPOS SANGUÍNEOS ...................................................................................................................... 1265
II. ASPECTOS GENERALES DE LA DONACIÓN ........................................................................................ 1265
III. ASPECTOS PRETRANSFUSIONALES ................................................................................................... 1266
IV. TRANSFUSIÓN DE CONCENTRADOS DE HEMATÍES .......................................................................... 1266
V. TRANSFUSIÓN DE PLAQUETAS ......................................................................................................... 1268
VI. TRANSFUSIÓN DE PLASMA FRESCO CONGELADO ............................................................................ 1269
VII. REACCIONES ADVERSAS A LA TRANSFUSIÓN ................................................................................... 1269
VIII. AFÉRESIS ........................................................................................................................................... 1271
79. Adenopatías. Esplenomegalia. Esplenectomía ........................................................................ 1273
I. ADENOPATÍAS ................................................................................................................................... 1273
II. ESPLENOMEGALIA ............................................................................................................................ 1277
III. ESPLENECTOMÍA. HIPOESPLENISMO ................................................................................................ 1280
80. Urgencias oncológicas ............................................................................................................ 1283
I. COMPRESIÓN MEDULAR .................................................................................................................. 1283
II. METÁSTASIS CEREBRALES ................................................................................................................. 1288
III. SÍNDROME DE VENA CAVA SUPERIOR .............................................................................................. 1291
IV. SÍNDROME DE LISIS TUMORAL ......................................................................................................... 1293
V. MUCOSITIS ........................................................................................................................................ 1296
VI. EMESIS INDUCIDA POR QUIMIOTERAPIA ......................................................................................... 1299
VII. NEUTROPENIA FEBRIL ....................................................................................................................... 1302
VIII. HIPERCALCEMIA ............................................................................................................................... 1302
81. Cefaleas y algias craneofaciales .............................................................................................. 1304
I. INTRODUCCIÓN ................................................................................................................................ 1304
II. APROXIMACIÓN DIAGNÓSTICA ........................................................................................................ 1304
III. CLASIFICACIÓN SEGÚN PERFIL TEMPORAL ....................................................................................... 1306
82. Alteración del nivel de consciencia. Coma .............................................................................. 1318
I. CONCEPTO ........................................................................................................................................ 1318
II. ETIOLOGÍA ........................................................................................................................................ 1318
III. CLÍNICA ............................................................................................................................................. 1320
IV. DIAGNÓSTICO ................................................................................................................................... 1326
V. PRONÓSTICO .................................................................................................................................... 1329
VI. ABORDAJE TERAPÉUTICO ................................................................................................................. 1330
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [11]
83. Demencia y otros trastornos neurodegenerativos. Enfermedad de Parkinson ......................... 1332
I. DEMENCIA ........................................................................................................................................ 1332
II. TRATAMIENTO FARMACOLÓGICO .................................................................................................... 1339
III. OTROS TRASTORNOS NEURODEGENERATIVOS: ENFERMEDAD DE PARKINSON .............................. 1341
IV. TRATAMIENTO .................................................................................................................................. 1344
V. CONSIDERACIONES PARA EL MANEJO DE LA ENFERMEDAD DE PARKINSON EN LA
URGENCIA/HOSPITALIZACIÓN .......................................................................................................... 1347
84. Mielopatías, neuropatías periféricas y miopatías .................................................................... 1349
I. CONCEPTO ........................................................................................................................................ 1349
II. APROXIMACIÓN DIAGNÓSTICA ........................................................................................................ 1349
III. ENTIDADES CLÍNICAS ........................................................................................................................ 1361
85. Enfermedad cerebrovascular ................................................................................................. 1367
I. ICTUS ISQUÉMICO ............................................................................................................................ 1367
II. HEMORRAGIA INTRAPARENQUIMATOSA ......................................................................................... 1382
III. HEMORRAGIA SUBARACNOIDEA ...................................................................................................... 1386
IV. TROMBOSIS VENOSA CEREBRAL ....................................................................................................... 1392
86. Crisis comiciales..................................................................................................................... 1395
I. CONCEPTO ........................................................................................................................................ 1395
II. CLASIFICACIÓN DE LAS CRISIS COMICIALES ...................................................................................... 1395
III. ETIOLOGÍA ........................................................................................................................................ 1396
IV. APROXIMACIÓN DIAGNÓSTICA ........................................................................................................ 1397
V. TRATAMIENTO .................................................................................................................................. 1400
VI. ESTATUS EPILÉPTICO ........................................................................................................................ 1404
VII. SITUACIONES ESPECIALES ................................................................................................................. 1406
87. Trastornos relacionados con el consumo de alcohol................................................................ 1408
I. INTRODUCCIÓN Y DEFINICIONES ...................................................................................................... 1408
II. DIAGNÓSTICO DE TRASTORNOS RELACIONADOS CON EL ALCOHOL ............................................... 1409
III. TRASTORNOS RELACIONADOS CON EL CONSUMO AGUDO DE ALCOHOL ....................................... 1410
IV. TRASTORNOS RELACIONADOS CON EL CONSUMO CRÓNICO DE ALCOHOL .................................... 1411
V. SÍNDROME DE ABSTINENCIA ALCOHÓLICA ...................................................................................... 1415
VI. DESHABITUACIÓN ALCOHÓLICA ....................................................................................................... 1418
88. Trastornos relacionados con el consumo de drogas ................................................................ 1420
I. INTRODUCCIÓN ................................................................................................................................ 1420
II. CANNABIS ......................................................................................................................................... 1420
III. COCAÍNA ........................................................................................................................................... 1421
IV. ANFETAMINAS Y DERIVADOS DE SÍNTESIS ....................................................................................... 1423
V. ALUCINÓGENOS ................................................................................................................................ 1425
VI. OPIOIDES .......................................................................................................................................... 1425
VII. SUSTANCIAS EMERGENTES ............................................................................................................... 1427
89. Intoxicaciones ....................................................................................................................... 1430
I. INTRODUCCIÓN ................................................................................................................................ 1430
II. MANEJO GENERAL DE LAS INTOXICACIONES ................................................................................... 1430
III. INTOXICACIONES MEDICAMENTOSAS .............................................................................................. 1438
IV. AGENTES CÁUSTICOS ........................................................................................................................ 1449
V. INTOXICACIÓN POR GASES ............................................................................................................... 1451
VI. INTOXICACIÓN POR HUMO .............................................................................................................. 1454
VII. INTOXICACIÓN POR SETAS................................................................................................................ 1454
VIII. MORDEDURAS Y PICADURAS DE ANIMALES .................................................................................... 1458
IX. INSECTICIDAS .................................................................................................................................... 1459
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [12]
X. RATICIDAS ......................................................................................................................................... 1460
XI. HERBICIDAS....................................................................................................................................... 1460
XII. METALES ........................................................................................................................................... 1461
XIII. INTOXICACIONES POR SUSTANCIAS INDUSTRIALES Y DERIVADOS ................................................... 1462
XIV. INTOXICACIÓN POR DISOLVENTES ORGÁNICOS Y SUS VAPORES ..................................................... 1464
90. Anexo I. Valores de referencia de laboratorio ......................................................................... 1465
I. INTRODUCCIÓN ................................................................................................................................ 1465
II. INFORMACIÓN AL PACIENTE PARA LA RECOGIDA DE MUESTRAS.................................................... 1476
91. Anexo II. Monitorización de fármacos .................................................................................... 1479
92. Anexo III. Fármacos y embarazo ............................................................................................. 1483
93. Anexo IV. Fármacos usados en perfusión continua intravenosa ............................................... 1488
94. Anexo V. Enfermedades de declaración obligatoria ................................................................ 1493
95. Anexo VI. Inmunosupresión y sus complicaciones ................................................................... 1496
I. GLUCOCORTICOIDES ......................................................................................................................... 1496
II. FÁRMACOS MODIFICADORES DE LA ENFERMEDAD NO BIOLÓGICOS .............................................. 1497
III. FÁRMACOS MODIFICADORES DE LA ENFERMEDAD BIOLÓGICOS .................................................... 1500
IV. INMUNOGLOBULINAS INTRAVENOSAS ............................................................................................ 1502
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [13]
[1] INTRODUCCIÓN A LA PRÁCTICA CLÍNICA
1. Introducción a la práctica clínica
Agustín Blanco Echevarría.
Médico Adjunto de Medicina Interna.
Tutor de residentes
Juan Manuel Guerra Vales.
Jefe de Sección de Medicina Interna y Vicepresidente de la Comisión de Docencia.
Tutor de residentes
La medicina es una profesión de servicio, que existe no por sí misma, sino por su utilidad para los
demás. El paciente (del latín: padecer, sufrir) es el principal motor de nuestra profesión. La práctica clínica
integra una serie de conocimientos científicos y técnicos junto con unas habilidades y aptitudes para su
aplicación en un paciente concreto.
Precisa de una interacción bidireccional entre el médico y el paciente a la que llamamos relación
médico/paciente. Esta entrevista o relación médico/paciente se lleva a cabo en un medio: consultorio,
hospital o despacho médico. El conjunto de documentos en que se refleja este encuentro es la historia
clínica. Como toda actividad clínica está basado en unas normas éticas.
I. RELACIÓN MÉDICO/PACIENTE
El paciente, cuando acude al médico, solicita ayuda técnica y profesional que le permita restablecer
la salud, mejorarla y conocer qué le sucede, así como cuál va a ser su pronóstico. Necesita sentirse
escuchado, comprendido y acompañado. Demanda del médico su interés como persona, esto es, solicita
atención y comprensión. Espera de la capacidad del profesional y de la tecnología médica una solución para
su problema. Desea ser informado en un grado razonable y, cuando no exista posibilidad de curación, no
sentirse abandonado. En la actualidad el paciente cada vez está más informado, aunque no siempre
correctamente, a través de medios de comunicación, internet, redes sociales, etc.
El médico, para dar una respuesta adecuada, precisa tener una base de conocimientos profunda,
no solo de medicina, sino también de otras ciencias como psicología, antropología, sociología y economía.
Sin embargo, a pesar de todo esto, el médico debe saber que la medicina como ciencia es incompleta (pero
no debemos olvidar que la ciencia es, en sí misma y por naturaleza, incompleta). Con frecuencia el médico
se siente insatisfecho por su falta de conocimientos. Esto debe ser siempre un estímulo y un acicate para la
búsqueda de respuestas. No obstante, debe buscar la excelencia, intentando aplicar una medicina lo más
apegada posible a la llamada medicina basada en la evidencia, pero también evitando caer en el
cientificismo radical. La práctica de la medicina es ciencia y arte: el médico, además de poseer sólidos y
amplios conocimientos médicos, debe de tener empatía, prudencia, tacto, buen juicio y sentido común,
además de capacidad de decisión. Cada paciente y sus circunstancias son distintas y únicas, aunque se trate
de la misma enfermedad.
Por lo tanto, aunque es bueno y necesario conocer las distintas guías clínicas, algoritmos y
protocolos, nunca debemos olvidar a quién y cómo las aplicamos, teniendo siempre presente el buen juicio
y razonamiento clínico.
El médico ha de ser íntegro, honrado y comprensivo, buscando lo mejor para cada paciente
concreto sin olvidar el sistema sanitario del que forma parte. No debe de olvidar que el médico es el rostro
humano de la medicina.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [14]
[1] INTRODUCCIÓN A LA PRÁCTICA CLÍNICA
La entrevista médico/paciente debe realizarse en un lugar cómodo que garantice la privacidad, y
esto debe formar parte del acto clínico/tratamiento del enfermo. No se tratan enfermos “a distancia” ni en
el “ordenador”: es necesario ver, escuchar, tocar y estar en contacto con el paciente.
II. HISTORIA CLÍNICA
La historia clínica es el elemento fundamental del historial clínico. Su obtención y la manera de
hacerlo dependen en gran medida de la habilidad del médico para obtener una anamnesis cuidadosa y una
buena exploración física. Es una técnica que se aprende y que se perfecciona. Siempre que sea posible es
necesario corroborar los hechos manifestados, ya que a veces el paciente tiene dificultad para recordar los
síntomas o no es consciente de los mismos. Los antecedentes personales, familiares y sociales aportan
mucha información, a veces esencial, sobre las enfermedades que deben tenerse en cuenta. Cuando se
escucha al paciente descubrimos no solo algo de su enfermedad, sino también algo acerca de sí mismo. Da
una oportunidad al clínico de establecer una buena relación médico/paciente. Nos permite conocer la
perspectiva del paciente, sus deseos e inquietudes personales (incluso acerca de la familia). La exploración
física debe realizarse de forma metódica y sistemática, teniendo en cuenta la comodidad y el pudor del
paciente. La habilidad se adquiere con la experiencia, pero es importante mantener una buena atención.
Sin duda los últimos avances científico-técnicos (genética, biología molecular, nuevas técnicas de imagen,
etc.) han supuesto un cambio en el ejercicio de la medicina. El conocimiento y manejo de la ecografía
clínica llegará a ser esencial en la exploración física, evitando traslados innecesarios del paciente y
ayudando a tomar decisiones clínicas “a pie de cama”. Ello no implica “desterrar” de nuestra práctica clínica
habitual el fonendoscopio, la palpación cuidadosa y el contacto con el enfermo. La ecografía ayuda y se
convertirá en imprescindible, pero no sustituye a otros elementos de la exploración física.
En los últimos años se ha producido una auténtica revolución al implantarse, en la mayoría de
hospitales y consultas, la historia clínica en formato digital. El Ministerio de Sanidad, Servicios Sociales e
Igualdad decidió abordar en el año 2006 el proyecto de una Historia Clínica Digital común para todo el
Sistema Nacional de Salud (HCDSNS). Son indudables las ventajas de una historia clínica digital. Entre ellas,
la accesibilidad a la información, el almacenamiento de datos de los pacientes, la fácil lectura de los
informes por parte de los profesionales y de los pacientes, la posibilidad de acceder a la historia clínica
desde cualquier centro del Sistema Nacional de Salud, etc. No obstante, la implantación de la HCDSNS lleva
mucho retraso, depende demasiado del entorno económico actual y de los diferentes sistemas de
información implantados, no ya en cada Comunidad Autónoma, sino que en ocasiones dentro de estas cada
centro hospitalario tiene su propia historia clínica digital.
A pesar de las indudables ventajas que hemos reseñado, no debemos olvidar varios problemas o
inconvenientes que genera el propio “concepto” de historia digital, y que se ha exacerbado en los últimos
tiempos:
Abuso del “corta y pega”. Debido a la presión asistencial y a la comodidad se abusa de dejar por
sentado unos determinados antecedentes clínicos que pasan de informe clínico a informe
clínico sin que se replanteen o se eliminen. Es decir, la historia clínica se despersonaliza, lo cual
puede crear problemas incluso legales.
Se está más pendiente de escribir en el ordenador que de ver y observar la manera en que el
paciente transmite sus síntomas, lo cual empeora la correcta interpretación de los mismos y del
proceso clínico en general.
Escasez de planes de contingencia en la mayoría de los hospitales y centros de salud, de tal
manera que cuando se “cae” el sistema informático, “no se puede hacer nada”.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [15]
[1] INTRODUCCIÓN A LA PRÁCTICA CLÍNICA
Obviados todos estos problemas, que con el tiempo se irán perfeccionando, son indudables las
enormes ventajas que proporcionaría una HCDSNS común, por lo que la actual coyuntura económica no
debiera retrasar su implantación más allá de lo razonable.
III. TRONCALIDAD Y SISTEMA MÉDICO INTERNO RESIDENTE
Son insoslayables los avances en la formación del médico en nuestro país que han ido de la mano
del sistema médico interno residente (MIR). La formación con contrato laboral, que incluye la asistencia y la
propia formación, ha contribuido enormemente al prestigio del Sistema Nacional de Salud gracias a la
competencia de sus profesionales. Sin embargo, el sistema MIR actual no está exento de problemas. La
“superespecialización” ha llevado a formar grandes especialistas en determinadas enfermedades o
procesos asistenciales, consiguiéndose una excelente formación en determinadas patologías, pero con una
visión reduccionista de la realidad, perdiendo el concepto holístico del enfermo, así como su visión
integradora y global. La superespecialización es buena, pero no en demasía. Se necesitan un mínimo de
conocimientos globales que permitan tener una visión más integradora de la enfermedad sin perder la
globalidad del paciente y la visión de conjunto. La famosa troncalidad, con unos años de formación
comunes, vendría a paliar en parte esta situación. Son ya demasiados años en los que se habla del tema sin
acabar de concretarse. Quizás por ello la Medicina Interna, tan denostada en los últimos tiempos, vuelve,
como siempre, a desempeñar un papel imprescindible en esta situación, pues precisamente se caracteriza
por aportar una visión global del paciente.
El residente “quemado” o burned-out es otro de los grandes problemas del sistema MIR. La enorme
presión asistencial de determinados centros, unido en ocasiones a una escasa o nula supervisión, con
jornadas laborales interminables, ha germinado en una creciente desmotivación por parte del residente,
que es necesario corregir y evitar, ya que el principal perjudicado es este último. A ello contribuye también
la mala formación pregrado en el ámbito práctico, que hace que muchos residentes no sepan nada acerca
de su especialidad hasta que la escogen. La inmigración hacia nuestro país también ha supuesto la
aceptación de residentes con otras culturas y distinta formación pregrado, obligándoles en muchas
ocasiones a un esfuerzo suplementario para una integración más completa en el sistema. Pero esto no
supone solo un problema, sino afortunadamente también una oportunidad de enriquecimiento e
integración cultural.
IV. ÉTICA Y MEDICINA
La responsabilidad de la medicina alcanza el punto de generar conocimientos científicos y
transmitirlos a los demás, usar de los conocimientos para mejorar la salud del paciente y de la comunidad y
juzgar la propiedad moral y ética de todo acto médico que afecta de forma directa a otro ser humano.
Como recoge el Código de Ética y Deontología de la Organización Médica Colegial, la sociedad actual exige,
además de calidad científica, “calidad humana” (art. 18.1), “trato correcto” (art. 8.2), “información
delicada” (art. 10.1), “respeto a la dignidad de la persona” (art. 4.11), “atención diligente” (art. 4.4),
“lealtad al paciente” (art. 4.3), “entorno acorde con el respeto debido al paciente” (art. 12) y “medios
técnicos para la debida garantía de calidad” (art. 20.1).
1. Consideraciones generales
Los problemas éticos de atención al paciente deben valorarse con tanta habilidad como los
mismos problemas de índole médica.
El paciente competente, es decir, capaz de extraer conclusiones de las informaciones, tiene
todo el derecho a que sean respetadas sus preferencias (por ejemplo, transfusiones sanguíneas
en testigos de Jehová). Solamente en caso de daños a terceros puede obligarse al paciente a
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [16]
[1] INTRODUCCIÓN A LA PRÁCTICA CLÍNICA
seguir un determinado tratamiento; este es el caso de pacientes con tuberculosis bacilífera que
no realizan correctamente la terapia, obligándose por ley al ingreso hospitalario.
Un paciente incompetente es aquel con incapacidad por alteración del nivel de consciencia o
demencia, que es valorada por el médico y por el psiquiatra. Para conocer las preferencias del
paciente nos guiaremos, si no existe “Documento de instrucciones previas”, por el familiar más
próximo y, en caso necesario, se tomará la decisión de forma conjunta.
2. Confidencialidad
Es preciso mantener el secreto profesional en todo momento. Actualmente se puede acceder a
todos los pacientes desde un ordenador, por lo que la confidencialidad debe ser máxima. Está
regulada por ley. La confidencialidad pasa a un segundo término solamente cuando existen
daños a terceros (en beneficio de estos) o por un imperativo legal (declaración obligatoria de
enfermedades, asistencia a procedimientos judiciales, malos tratos, violencia de género, etc.).
3. Alta voluntaria
Ocasionalmente el paciente no desea atención médica y opta, previo aviso o no, por abandonar
el hospital. Siempre habrá que valorar si es o no un paciente competente. En el primer caso se
le pedirá que firme el alta al hacerlo en contra del criterio del médico. En caso de marcharse sin
previo aviso se comunicará al jefe de hospital y al juzgado de guardia.
En otras ocasiones el alta sobreviene como consecuencia de la ruptura del contrato terapéutico
(por ejemplo, paciente usuario de drogas por vía parenteral y dependencia a las mismas que
padece una endocarditis y continúa administrándose e inyectándose dichas sustancias), hecho
que haremos constar en el expediente clínico.
4. Paciente terminal o gravemente enfermo
La muerte no es el fracaso de la medicina, sino algo inherente a la vida. Un paciente
competente y bien informado tiene derecho a rechazar un procedimiento determinado. Ni el
paciente ha de ser forzado a ser informado ni el médico debe informar de “todo”. Es
importante recordar que siempre hay algo que hacer por el paciente; incluso cuando este sufre
una enfermedad incurable y la muerte es inevitable, el médico debe proporcionar apoyo físico,
emocional y espiritual. Debe ser paciente, compasivo y sincero. Es importante el compromiso
con el enfermo, aliviar el miedo y la angustia al dolor y a la soledad.
Se ha de hablar con el paciente de sus preferencias religiosas y ofrecerle el apoyo adecuado en
este sentido. El alivio del dolor, el mantenimiento de la dignidad humana y evitar el aislamiento
son importantes para el paciente. El “Documento de instrucciones previas” o “Testamento
vital” es un documento médico legal en el que el paciente expresa su deseo sobre
determinadas actitudes y el médico debe preguntar acerca de su existencia.
Así como todos los códigos deontológicos rechazan el encarnizamiento terapéutico, también
reclaman al médico la atención al paciente, evitándole el dolor y haciendo todos los esfuerzos
para restablecer la salud. La eutanasia directa (que significa “una acción u omisión que por su
naturaleza y en su intención causa la muerte”) no le está permitida al médico ni al personal
sanitario según la actual legislación vigente. La eutanasia pasiva, es decir, la abstención de
tratamiento específico de un enfermo terminal, no significa detener el tratamiento paliativo.
A veces se produce como consecuencia del tratamiento de la agonía una aceleración de la
muerte (teoría del doble efecto) sin quererlo: esto es lo que se denomina eutanasia indirecta.
Es muy reconfortante para el paciente y su familia, conseguir que el enfermo que se enfrenta a
la muerte se encuentre tratado, acompañado y querido.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [17]
[1] INTRODUCCIÓN A LA PRÁCTICA CLÍNICA
Cuando en una orden de tratamiento se indica que el paciente no es subsidiario de reanimación
cardiopulmonar (RCP), es su médico el que asume esta responsabilidad justificando las razones
en la historia clínica. La orden de no RCP no conlleva la supresión de todo tratamiento.
V. ECONOMÍA Y MEDICINA
Los avances científicos y técnicos en las últimas décadas han sido notables, tanto en el aspecto
diagnóstico como terapéutico. Como consecuencia de todo ello se han elevado los costes en la atención
médica. A ello vienen unidos el aumento de la esperanza de vida de la población, la “cronificación” de
enfermedades antaño incurables y la aparición de la llamada “medicina del deseo”. Con este término nos
referimos a la aparición de nuevos problemas de salud, que anteriormente se consideraban “fisiológicos” o
inherentes a la edad (menopausia en la mujer, envejecimiento, estética…). Todo esto tiene un precio que la
sociedad debe conocer. El médico es el principal gestor del gasto y no debe ser insensible a esta realidad,
pero nunca en menoscabo de la correcta y adecuada actividad asistencial.
BIBLIOGRAFÍA
Aguilar Rodríguez F, Bisbal Pardo O, Gómez Cuervo C, et al. Manual de diagnóstico y terapéutica
médica. Hospital Universitario 12 de Octubre. 7ª edición. Madrid: MSD; 2012.
Consejo General de Colegios Oficiales de Médicos, Organización Médica Colegial de España. Código de
deontología médica. Guía de ética médica. [Internet]. [Consultado 6 de mayo de 2016]. Disponible en:
https://www.cgcom.es/sites/default/files/codigo_deontologia_medica.pdf
Etreros Huerta J, Alonso Villar C, Cabronero Fernández M, et al. Instituto de Información Sanitaria -
Sistema de historia clínica digital del SNS. [Internet]. [Consultado 6 de mayo de 2016]. Disponible en:
http://www.msssi.gob.es/organizacion/sns/planCalidadSNS/docs/HCDSNS_Castellano.pdf
González Quirós JL, Puerta JL. Tecnología, demanda social y “medicina del deseo”. Med Clin (Barc).
2009;133(17):671-5.
Longo DL, Kasper DL, Jameson JL, et al. La práctica de la medicina clínica. En: Longo DL, Kasper DL,
Jameson JL, et al, editores. Harrison. Principios de Medicina Interna. 18ª ed. México DF: McGraw-Hill
Interamericana Editores, S.A.; 2012. pp. 1-13.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [18]
[2] TÉCNICAS Y PROCEDIMIENTOS INSTRUMENTALES
2. Técnicas y procedimientos instrumentales
Helena Domínguez Aguado.
Medicina Intensiva
Mario Aramberri del Vigo.
Medicina Interna
Asesor: Luis Juan Terceros Almanza. Médico Adjunto de Medicina Intensiva
Realización de ilustraciones: José María Martínez Ávila
En la práctica clínica diaria se requiere el conocimiento de diversos procedimientos para un
adecuado diagnóstico y tratamiento de los pacientes, tanto de sus indicaciones y contraindicaciones como
de la técnica y sus complicaciones. Es fundamental valorar el riesgo-beneficio y obtener un consentimiento
informado firmado por el paciente, sus familiares o el tutor legal.
I. VÍAS VENOSAS DE ACCESO PERIFÉRICO
Canulación por punción de una vena periférica.
1. Indicaciones
Administración de fármacos, sueroterapia o reposición de fluidos (transfusión de hemoderivados),
extracción de muestras sanguíneas, acceso a la circulación venosa central empleando catéteres largos
(Drum).
2. Material
Guantes, gasas y apósitos estériles, compresor venoso, solución antiséptica y catéter. En general se
utilizan catéteres de aguja metálica (palomilla) o angiocatéteres (Abbocath®).
3. Técnica
Elegimos el punto de punción según la accesibilidad, siendo preferibles las venas del antebrazo
o el dorso de la mano.
Con el brazo del paciente en abducción, colocamos el compresor proximal al lugar elegido y
aplicamos solución antiséptica.
Una vez que la vena esté rellena, la fijamos traccionando la piel circundante con el pulgar e
introducimos el catéter con una inclinación de 10-30º y el bisel hacia arriba.
Al observar el reflujo de sangre avanzamos el catéter, retiramos la aguja y el compresor y
fijamos la vía.
4. Complicaciones
Extravasación de fluidos, hematoma local, rotura venosa, canalización arterial accidental, infección
(celulitis, flebitis o bacteriemia), trombosis y embolia por sección del catéter.
II. VÍAS VENOSAS CENTRALES
Las venas centrales son vasos de grueso calibre que proporcionan un acceso directo a la vena cava
superior o inferior, pudiendo acceder a ellas a través de la vena subclavia, yugular, femoral o de la
circulación venosa periférica (vena basílica o cefálica).
1. Indicaciones
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [19]
[2] TÉCNICAS Y PROCEDIMIENTOS INSTRUMENTALES
Falta de disponibilidad de accesos periféricos, administración de fármacos irritantes, soluciones
hiperosmolares (por ejemplo, nutrición parenteral), drogas vasoactivas, fluidoterapia y hemoderivados a
alta velocidad de infusión, monitorización hemodinámica, realización de técnicas de depuración extrarrenal
o plasmaféresis e implantación de marcapasos endocavitarios.
2. Material
Gorro, mascarilla, gafas protectoras, guantes, bata, gasas, paños y apósitos estériles. Solución
antiséptica. Anestésico local (mepivacaína 1-2% o lidocaína 1-2%), jeringa de 10 ml, aguja intramuscular, set
de vía central de una luz o multilumen (aguja, jeringa 5 ml, guía metálica, dilatador, vía central). Bisturí,
seda 2/0 con aguja recta, suero salino fisiológico al 0,9%, apósito estéril.
3. Técnica
A la hora de elegir la zona de inserción del catéter se debe tener en cuenta el tipo de paciente
(peso, movilidad, etc.), patología crónica, enfermedad actual, alteraciones analíticas, para qué y por cuánto
tiempo es necesaria la vía venosa central y la experiencia del operador.
Catéter venoso central de inserción periférica (Drum®)
Bajo técnica aséptica y con el brazo del paciente a unos 45º del cuerpo, se punciona la vena
periférica al nivel de la fosa antecubital (basílica o cefálica); tras ello, se avanza el catéter (girando la cabeza
del paciente hacia el mismo lado) y se retira la aguja. Para finalizar, aseguramos la permeabilidad de las
luces y fijamos el catéter.
Catéter venoso de acceso central
Se posiciona al paciente en decúbito supino y ligero Trendelenburg si es posible (para disminuir el
riesgo de embolia gaseosa). Bajo rigurosa asepsia, se canaliza la vía central mediante técnica de Seldinger
(Figura 1): una vez localizada la vena mediante punción con aguja (calibre 14-16 G) se desliza la guía
metálica a su través (siempre se debe tener bajo control la guía metálica).
A continuación, se retira la aguja y se introduce el dilatador a través de la guía. Tras la dilatación del
trayecto subcutáneo se retira el dilatador y se introduce la vía central a través de la guía metálica.
Aseguramos la permeabilidad de todas las luces (aspirando sangre y posteriormente lavando con suero
salino fisiológico), fijamos el catéter a la piel mediante puntos y cubrimos la zona de punción con un apósito
estéril.
En el caso de canalización subclavia o yugular, es preciso realizar un control radiológico para
asegurar la correcta posición del catéter y diagnosticar posibles complicaciones. No puncionar la vena
subclavia o yugular contralateral sin dicho control por riesgo de producir complicaciones bilaterales.
Canalización de la vena subclavia
Es la vía más cómoda para el paciente. La vena subclavia se localiza en el borde inferior de la
clavícula y asciende por la superficie externa del músculo escaleno anterior. Se coloca al paciente en
decúbito supino y ligero Trendelenburg, con los brazos extendidos y pegados a ambos lados del cuerpo y la
cabeza girada hacia el lado contralateral a la punción. Debemos introducir el catéter hasta 15-17 cm en el
lado derecho y 17-20 cm en el izquierdo.
Existen dos abordajes:
– Vía de abordaje infraclavicular: la más utilizada. La punción se realiza 1 cm por debajo del borde
inferior de la clavícula, en la unión del tercio externo con los dos tercios internos de la misma, dirigiendo el
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [20]
[2] TÉCNICAS Y PROCEDIMIENTOS INSTRUMENTALES
bisel hacia arriba en dirección a la escotadura supraesternal, con un ángulo máximo de la aguja respecto a
la piel de 10-20º.
– Vía de abordaje supraclavicular: mucho menos empleada por el mayor número de com-
plicaciones. La zona de punción se localiza en el ángulo formado por el borde externo del músculo
esternocleidomastoideo y la clavícula, dirigiendo la aguja bajo la clavícula hacia la mamila contralateral. Por
esta vía de abordaje la vena subclavia es más superficial.
Figura 1. Canalización de un catéter venoso central. Técnica de Seldinger.
Canalización de la vena yugular interna
La vena yugular interna discurre entre los dos haces del músculo esternocleidomastoideo y
posterolateral a la arteria carótida interna. El riesgo de neumotórax es menor que en el caso de la vía
subclavia y es una vena compresible en caso de sangrado o punción arterial. El paciente se coloca en
decúbito supino, en posición Trendelenburg, con la cabeza girada hacia el lado contralateral a la punción.
Los abordajes más empleados son:
- Vía media o abordaje central: la más utilizada.
Se identifica el triángulo formado por los dos haces del músculo esternocleidomastoideo y la
clavícula, se palpa la carótida y se inserta la aguja con el bisel hacia arriba en el vértice superior de ese
triángulo, lateral a la arteria carótida, con una angulación de 45º, en dirección a la mamila homolateral. Por
este abordaje la vena yugular es bastante superficial, no debemos introducir la aguja más de 2-3 cm.
- Vía posterior:
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [21]
[2] TÉCNICAS Y PROCEDIMIENTOS INSTRUMENTALES
El lugar de inserción se encuentra a 1 cm por encima de la unión de la vena yugular externa con el
haz anterior del músculo esternocleidomastoideo, dirigiendo la aguja en dirección a la escotadura
supraesternal con una angulación de 10-15º.
Canalización de la vena femoral
La vena femoral se localiza por debajo del ligamento inguinal, medial a la arteria femoral. Es una
vena compresible, la posición de Trendelenburg es prescindible y su canalización no interfiere con las
maniobras de reanimación cardiopulmonar (RCP), pero presenta mayor riesgo de infección.
El paciente se coloca en decúbito supino con ligera abducción de la cadera. Si se palpa pulso
arterial, se punciona 2 cm por debajo del ligamento femoral y 1-2 cm medial al pulso femoral, con el bisel
hacia arriba y una angulación de 45º. Si el pulso arterial no es palpable, se traza una línea imaginaria entre
la espina ilíaca anterosuperior y la sínfisis púbica, dividiendo dicha línea en tres segmentos. La unión del
tercio interno con el tercio medio marca el punto donde se encuentra la arteria, encontrándose la vena
femoral 1-2 cm medial a dicho punto.
4. Complicaciones
Inmediatas
Punción arterial, hematoma: se debe comprimir durante 5-10 min. Avisar a cirugía
vascular en caso de que no cese o se canalice de forma inadvertida la arteria.
Arritmias: al introducir la guía metálica o por posición avanzada del catéter. Se debe
retirar inmediatamente hasta el cese de las alteraciones del ritmo. Se recomienda la
monitorización electrocardiográfica durante el procedimiento.
Neumotórax: más frecuente en la canalización de la subclavia. Generalmente son de
escasa cuantía y evolucionan favorablemente con manejo conservador. En caso
contrario, precisa la colocación de un drenaje endotorácico.
Embolismo aéreo: se manifiesta por hipoxia, hipotensión y roce precordial.
Lesión del conducto torácico: en canalizaciones supradiafragmáticas izquierdas.
Perforación cardiaca, taponamiento.
Tardías
Trombosis: frecuente, especialmente en la vena femoral.
Infección del punto de punción, bacteriemia relacionada con el catéter.
Fístula arteriovenosa o pseudoaneurisma.
5. Canalización de catéter venoso central guiado por ecografía
En la actualidad, la ecografía como método para guiar la cateterización de vías venosas centrales
forma parte de la práctica clínica habitual. Ha demostrado reducir el número de complicaciones, aumentar
la tasa de éxito e incluso disminuir la duración de la técnica.
Material: ecógrafo con sonda lineal (5-10 mHz), gel estéril para ecografía y funda estéril para la
sonda. Se recomienda que la sonda del ecógrafo sea manipulada por la misma persona que
esté realizando la punción.
Técnica: para identificar el vaso a canalizar será preciso localizar el plexo vascular por las
referencias anatómicas y, posteriormente, colocaremos la sonda lineal de alta frecuencia
perpendicular al vaso, pudiendo diferenciar la arteria de la vena con los siguientes criterios: la
arteria presenta una forma más redondeada, una pared más gruesa, pulso más evidente y,
sobre todo, no se colapsa al ejercer presión sobre la piel con la sonda (Figura 2).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [22]
[2] TÉCNICAS Y PROCEDIMIENTOS INSTRUMENTALES
Figura 2. Canalización de un catéter venoso central ecoguiado.
Se introduce la aguja siguiendo la dirección habitual, e identificaremos la aguja en la imagen o tan
solo la distorsión que ocasiona su entrada en los tejidos. Si fuera preciso, se corregirá la posición de la aguja
a la vista de la imagen. Es fundamental, como en la técnica tradicional, no perder de vista la jeringa para
detectar el momento en el que se aspire sangre.
III. INTUBACIÓN ENDOTRAQUEAL
La laringoscopia directa con intubación orotraqueal es el principal método de intubación dada su
velocidad, tasa de éxito y disponibilidad del equipo. La indicación de la intubación es asegurar el
aislamiento y permeabilidad de la vía aérea.
1. Indicaciones
Las indicaciones de la intubación endotraqueal se resumen en la tabla I.
Tabla I.Indicaciones de intubación endotraqueal.
2. Grado de dificultad para la intubación
Antes de la intubación, se debe valorar la condición clínica del paciente, la situación hemodinámica
y la vía aérea:
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [23]
[2] TÉCNICAS Y PROCEDIMIENTOS INSTRUMENTALES
Movilidad del cuello: si está limitada, restringirá la capacidad para una colocación adecuada y
dificultará la intubación.
Boca: una apertura menor de 2-3 dedos (4 cm) está asociada con un aumento en el riesgo de
intubación difícil.
Mallampati: se basa en referencias anatómicas de la cavidad oral. La ausencia de visualización
de los pilares posteriores, así como de la úvula, indica una mayor probabilidad de dificultad
para la intubación.
Mandíbula: una distancia tiromentoniana menor de 6 cm indica que la laringe puede tener una
localización más anterior.
Cuando se prevean dificultades para la ventilación con mascarilla facial o en la intubación se debe
tener precaución antes de suprimir la ventilación espontánea, y preparar un plan de intubación difícil por si
fuese necesario.
3. Material
Guantes y mascarilla quirúrgica.
Monitor electrocardiográfico, presión arterial y pulsioxímetro.
Fuente de suministro de oxígeno.
Mascarilla facial y bolsa autohinchable (Ambú®) conectada a la fuente de oxígeno.
Cánula orofaríngea (Guedel): existen diferentes tamaños; el adecuado para cada paciente sería
aquel que tiene la misma longitud que la existente entre el ángulo de la mandíbula y la
comisura bucal.
Sistema de aspiración.
Pinzas de Magyll: permiten retirar cuerpos extraños y/o guiar la entrada del tubo endotraqueal.
Laringoscopio: tiene dos partes, el mango y la pala. La pala puede ser recta (Miller®, empleada
más en niños) o curva (Macintosh®, en adultos). En adultos una pala de tamaño 4-5 cm es
apropiada, a menos que el cuello del paciente sea muy largo.
Tubo orotraqueal: consta de un neumotaponamiento en el extremo distal; se debe comprobar
siempre su integridad antes del procedimiento. Debe emplearse el tubo de mayor diámetro
posible (varones: 8-9,5; mujeres: 7-8,5).
Fiador semirrígido: varilla maleable que se introduce en el interior del tubo para darle mayor
rigidez. Se emplea en situaciones de intubación difícil. Puede lesionar la vía aérea superior, por
lo que siempre se debe verificar que el fiador no sobrepasa la punta del tubo.
Fonendoscopio.
Jeringa de 10 ml.
Venda.
Medicación para la inducción. (Ver Apartado “Sedantes-hipnóticos”).
Sedantes-hipnóticos
En la tabla II se recogen algunos sedantes-hipnóticos.
Bloqueantes neuromusculares
Despolarizantes: succinilcolina 1-1,5 mg/kg (Anectine®) presenta un inicio de acción
ultracorta (un minuto) y duración corta (de seis a ocho minutos). Su empleo está
contraindicado en hiperpotasemia, quemados, lesión ocular, distrofias musculares,
hipertensión intracraneal, inmovilización prolongada y déficit conocido de
acetilcolinesterasa. Puede precipitar hipertermia maligna.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [24]
[2] TÉCNICAS Y PROCEDIMIENTOS INSTRUMENTALES
No despolarizantes: rocuronio 0,6-1 mg/kg (Esmerón®), vecuronio 0,1-0,3 mg/kg
(Norcuron®), cisatracurio 0,1-0,2 mg/kg (Nimbex®). Inicio de acción más lento (de dos a
cinco minutos) y mayor duración (30 minutos) que la succinilcolina. No producen
fasciculaciones.
Tabla II.Sedantes-hipnóticos en la inducción para la intubación.
4. Técnica
Comprobación del material.
Extraer prótesis dentales o cuerpos extraños.
Monitorización electrocardiográfica, presión arterial y pulsioximetría.
Canalización/comprobación del acceso venoso.
Preparación de la medicación.
Preoxigenación y premedicación: preoxigenación con una fracción inspiratoria de oxígeno del
100% durante tres a cuatro minutos mediante mascarilla facial y bolsa autohinchable, si la
situación lo permite. Administrar de forma simultánea el sedante y el bloqueante
neuromuscular (secuencia de inducción rápida).
Colocación del paciente: en decúbito supino, se extiende la cabeza y se flexiona ligeramente el
cuello; con esta maniobra se consigue la mejor visión de la glotis al alinear los ejes oral,
faríngeo y traqueal. En caso de sospecha de traumatismo cervical o subluxación atloaxoidea, se
debe realizar tracción cervical controlada.
Laringoscopia directa (Figura 3): sujetando el laringoscopio con la mano izquierda, se introduce
por la comisura bucal derecha, desplazando la lengua hacia la izquierda con la pala. Se avanza
identificando estructuras, hasta visualizar la epiglotis; en ese momento se coloca el extremo
distal de la pala en la vallécula (entre la base de la lengua y la epiglotis en caso de utilizar pala
curva, sobre la epiglotis si se usa la pala recta) y se tracciona hacia delante y arriba hasta la
visualización de la glotis y las cuerdas vocales. Nos podemos ayudar con la maniobra de
Backward, Upward, Rightward Pressure (BURP): consiste en la manipulación externa de la
laringe por otro operador, realizando un desplazamiento hacia atrás, arriba y hacia la derecha
del paciente. Tras la visualización de la glotis, deslizaremos el tubo endotraqueal con la mano
derecha, a través de las cuerdas, quedando el neumotaponamiento distal a la glotis (se infla
con 5-10 ml de aire posteriormente). A nivel de la comisura bucal el tubo debe quedar con la
marca 23-25 cm en hombres y 21-23 cm en mujeres.
Comprobación de la correcta posición del tubo: la mejor confirmación se tiene al ver pasar el
tubo a través de las cuerdas vocales. Además, debemos auscultar de forma bilateral los sonidos
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [25]
[2] TÉCNICAS Y PROCEDIMIENTOS INSTRUMENTALES
respiratorios y la ausencia de sonidos a nivel epigástrico, así como observar la expansión de
ambos hemitórax con la ventilación.
Una vez fijado el tubo, debe realizarse una radiografía de tórax para comprobar la correcta
posición del mismo (con su extremo distal > 2 cm de la carina para evitar la intubación
selectiva, generalmente de bronquio derecho por su disposición anatómica).
Figura 3. Laringoscopia directa.
5. Complicaciones
Durante la intubación: rotura dental, fracaso de la intubación (riesgo de hipoxia, hipercapnia y
asistolia), aspiración del contenido gástrico, laceración de la mucosa oral, laríngea o traqueal,
traumatismo o rotura de la vía aérea superior o el esófago, intubación bronquial selectiva o
esofágica, barotrauma, aumento de la presión intracraneal, lesión neurológica por movilización
cervical, hipertensión arterial, taquicardia y arritmias.
Durante la permanencia del tubo: extubación accidental, progresión del tubo con desarrollo de
atelectasia, obstrucción del tubo (secreciones, acodamientos, oclusión dentaria, etc.). La
excesiva presión del neumotaponamiento puede producir isquemia de la mucosa traqueal con
aumento del riesgo de granulomas, estenosis, traqueomalacia o fístula traqueoesofágica.
Postextubación: aspiración, odinofagia, disfonía, edema de glotis, laringoespasmo, parálisisde
cuerdas, úlceras laríngeas.
6. Vía aérea difícil
Es aquella en la que un operador experimentado encuentra dificultad en cualquiera o en todas
estas situaciones: ventilación con mascarilla facial, laringoscopia directa o indirecta, intubación traqueal.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [26]
[2] TÉCNICAS Y PROCEDIMIENTOS INSTRUMENTALES
Ante intentos fallidos para la intubación (no más de dos), disponemos de diferentes dispositivos
que nos podrían facilitar el rescate de la ventilación y/o aislamiento definitivo de la vía aérea: guías,
fiadores, dispositivos supraglóticos, videolaringoscopio, fibrobroncoscopio flexible, etc. En el caso de que
con estos dispositivos no logremos ventilar y/o intubar al paciente, debemos valorar la opción quirúrgica
(cricotiroidotomía o traqueostomía urgente).
IV. CRICOTIROIDOTOMÍA
Ver Capítulo 17. “Patología otorrinolaringológica”.
V. DRENAJE ENDOTORÁCICO
Es el procedimiento mediante el cual se puede evacuar aire o líquido del espacio pleural a través de
un tubo torácico, permitiendo la expansión pulmonar.
1. Indicaciones
Neumotórax, neumomediastino, derrame pleural, hemotórax, empiema, quilotórax.
2. Contraindicaciones
Trastornos de la coagulación, tratándose de una contraindicación relativa en caso de urgencia.
3. Material
Paños, gasas, bata, guantes y apósitos estériles, antiséptico, anestésico local, aguja intramuscular,
jeringa de 10 ml, bisturí, mosquito, tubo de tórax (18-24 F para neumotórax, 26-28 F para derrame pleural,
32-40 F en hemotórax/empiema), seda con aguja recta, sistema de drenaje con tres cámaras (Pleurevac®):
una conectada al paciente, otra conectada con la anterior mediante un sello de agua de 2 cm y una tercera
conectada a la segunda y a aspiración.
4. Técnica
El paciente debe colocarse en decúbito supino con el brazo homolateral elevado sobre el plano de
la cabeza.
Inserción lateral: 4º-5º espacio intercostal a nivel de la línea media o axilar anterior.
Inserción anterior: 2º espacio intercostal a nivel de la línea media clavicular.
Tras esterilizar el campo e infiltrar la zona con anestésico local, se realiza una incisión transversa en
la piel y tejido subcutáneo de unos 2 cm y se diseca, con el mosquito o mediante disección roma con el
dedo índice, el tejido subcutáneo y la musculatura intercostal hasta alcanzar la pleura, apoyándose sobre el
borde superior de la costilla inferior. Tras alcanzar el espacio pleural, se inserta el tubo de tórax (en
dirección apical en caso de neumotórax y posteroinferior en caso de derrame) y se conecta al sistema de
drenaje, confirmando la correcta colocación del tubo mediante la obtención de burbujeo o salida de líquido
(Figura 4). Para finalizar, se fija el tubo a la piel dando un punto en bolsa de tabaco y anudando los
extremos en forma de cadena. Se debe realizar una radiografía de tórax para comprobar la posición del
drenaje endotorácico y descartar complicaciones.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [27]
[2] TÉCNICAS Y PROCEDIMIENTOS INSTRUMENTALES
Figura 4. Drenaje endotorácico.
5. Complicaciones
Colocación extrapleural, laceración pulmonar, hemotórax por lesión de vasos intercostales o
mamarios, lesión del paquete vasculonervioso, neumotórax, edema pulmonar por reexpansión (no drenar
más de 1 L/h), laceración del diafragma o víscera intratorácica/intraabdominal, infecciones.
6. Consideraciones especiales
Válvula de Heimlich: se trata de un sistema de válvula unidireccional; solo se emplea en caso de
neumotórax. Está formado por dos tubos, uno rígido externo y otro flexible interno, permitiendo su colapso
en inspiración y la salida de aire en espiración.
VI. PERICARDIOCENTESIS
Procedimiento mediante el cual se extrae líquido del espacio pericárdico con finalidad diagnóstica
y/o terapéutica.
1. Indicaciones
Taponamiento cardiaco, evacuación terapéutica o diagnóstica de derrame agudo o crónico.
2. Contraindicaciones
Trastorno de coagulación, tratándose de una contraindicación relativa en situaciones de urgencia.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [28]
[2] TÉCNICAS Y PROCEDIMIENTOS INSTRUMENTALES
3. Material
Monitorización electrocardiográfica, pulsioximetría y presión arterial, bata, guantes, gasas, paños
estériles, gorro, mascarilla quirúrgica, solución antiséptica, anestésico local (mepivacaína 1-2% o lidocaína
1-2%), aguja, jeringa 10-20 ml, guía metálica, bisturí, material de sutura, catéter de drenaje. Se puede
conectar la aguja a un electrodo epicárdico para poder detectar alteraciones electrocardiográficas.
4. Técnica
Siempre que sea posible se realizará bajo control ecográfico o radioscópico.
Posicionar al paciente en decúbito supino y el cabecero elevado a 30º.
Si durante el procedimiento se visualizan alteraciones electrocardiográficas, indica que se ha tocado
el miocardio y es necesario retirar la aguja unos milímetros. En el caso de obtener sangre al aspirar,
debemos asegurarnos de que es pericárdica y no intracardiaca (la sangre pericárdica no coagula).
Tras asegurar la posición intrapericárdica, se avanza la guía metálica y, a través de ella, el catéter
conectado a un sistema de drenaje. Para finalizar, se debe realizar una radiografía de tórax para descartar
complicaciones y una ecocardiografía para valorar la eficacia del drenaje pericárdico. Existen varios
abordajes:
Subxifoideo: el más empleado y de elección; presenta menor riesgo de lesión pleural y de los
vasos coronarios. El punto de punción se localiza a 0,5 cm a la izquierda del apéndice xifoides y
0,5-1 cm por debajo del reborde costal. Introducimos la aguja con una angulación de 45º, en
dirección al hombro izquierdo. Tras pasar por debajo de la costilla, disminuir la angulación a
15º.
Paraesternal: a 1 cm del borde esternal izquierdo, a la altura del 5º-6º espacio intercostal.
Apical: a varios centímetros del borde esternal izquierdo, a la altura del 5º-7º espacio
intercostal.
Subcostal: 1 cm inferior al ángulo xifocostal.
5. Complicaciones
Arritmias, parada cardiaca, hemorragia por punción o desgarro de una arteria coronaria o del
miocardio, perforación de cavidades cardiacas, neumo/hemopericardio, neumo/hemotórax, lesión de
vísceras abdominales, infección.
VII. TORACOCENTESIS
Inserción de una aguja en el espacio pleural para extraer líquido o aire del mismo (Figura 5).
1. Indicaciones
Filiación de derrame pleural, evacuación de derrame pleural moderado que ocasiona dificultad
respiratoria o neumotórax a tensión.
2. Contraindicaciones
Absolutas
Evidencia clínica de fibrinólisis o de coagulación intravascular diseminada.
Relativas
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [29]
[2] TÉCNICAS Y PROCEDIMIENTOS INSTRUMENTALES
Tratamiento anticoagulante, tiempo de tromboplastina parcial activada el doble del valor normal,
plaquetopenia por debajo de 50.000/mm³, ventilación mecánica con presión positiva elevada, infección de
la pared torácica.
Figura 5. Toracocentesis.
3. Material
Guantes, gasas, apósitos y paños estériles, jeringa de 10 ml, aguja intramuscular, anestésico local,
llave de tres pasos, tubos de laboratorio, sistema de gotero, frascos de vacío.
4. Técnica
Colocamos al paciente sentado, con los brazos apoyados sobre una superficie e inclinado hacia
delante.
Localizamos el líquido/aire a drenar por medio de ecografía o auscultación pulmonar y
marcamos un punto de punción en la costilla inferior del espacio intercostal señalado, en el
reborde costal superior, a la altura de la línea media axilar posterior.
Aplicamos antiséptico en zona señalada e infiltramos la superficie cutánea con anestésico local.
Se introduce la aguja perpendicular al tórax, aspirando hasta perforar la pleura parietal, y se
extraen las muestras pertinentes.
Conectamos la aguja a una llave de tres pasos y esta a un sistema de vacío.
5. Complicaciones
Neumotórax, hemotórax, empiema, infección del punto de punción, punción esplénica o hepática,
cuadro vasovagal, diseminación tumoral (en casos de masas de pared torácica).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [30]
[2] TÉCNICAS Y PROCEDIMIENTOS INSTRUMENTALES
6. Consideraciones especiales
No se recomienda la evacuación de más de 1 L de líquido pleural por el riesgo de producir un
edema pulmonar ex vacuo.
En los pacientes con enfermedad pulmonar obstructiva crónica (EPOC) o tratados con ventilación
mecánica se aconseja realizar una radiografía postoracocentesis para descartar un neumotórax
yatrogénico.
VIII. PARACENTESIS
Punción percutánea abdominal destinada a extraer líquido de la cavidad abdominal (Figura 6).
1. Indicaciones
Despistaje de peritonitis bacteriana espontánea o secundaria, evacuación de ascitis refractaria a
tratamiento convencional.
Figura 6.Paracentesis.
2. Contraindicaciones
Absolutas
Evidencia clínica de fibrinólisis o de coagulación intravascular diseminada. Otras alteraciones de la
coagulación no contraindican la realización de una paracentesis.
Relativas
Obstrucción intestinal, bridas, globo vesical, embarazo o grandes visceromegalias. Se pueden
realizar guiadas por ecografía.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [31]
[2] TÉCNICAS Y PROCEDIMIENTOS INSTRUMENTALES
3. Material
Guantes, gasas, apósitos y paños estériles, antiséptico, aguja intramuscular (20-22 G), jeringa de 10
ml, tubos de laboratorio, sistema de gotero, frascos de hemocultivos, frascos de vacío.
4. Técnica
Colocamos al paciente con el cabecero ligeramente elevado e inclinado hacia el lado izquierdo.
Identificamos el punto de punción, preferiblemente en el cuadrante inferior izquierdo, en la
unión entre el tercio medio y el tercio externo de la línea imaginaria que une el ombligo con la
espina ilíaca anterosuperior izquierda. Evitar las zonas de la pared abdominal con circulación
colateral visible, hematoma, celulitis o cicatrices.
Se desinfecta la región y se introduce la aguja en sentido perpendicular al plano de la pared
abdominal aspirando simultáneamente hasta llegar a la cavidad peritoneal.
Si se realiza con fines evacuadores, es necesario fijar la cánula y conectarlo a un sistema de
drenaje. Al finalizar, la aguja ha de retirarse rápidamente.
5. Complicaciones
Hematoma de pared abdominal. Sangrado por laceración de vasos epigástricos, epiploicos o
mesentéricos. Absceso de la pared. Fuga de líquido ascítico. Perforación de asa intestinal, vejiga o útero.
IX. SONDAJE GÁSTRICO
Introducción de una sonda a través de la nariz o de la boca hasta el estómago.
1. Indicaciones
Descompresión gástrica (íleo paralítico u obstrucción intestinal), realización de lavado gástrico,
administración de nutrición enteral o medicamentos.
2. Contraindicaciones
Estenosis esofágica. Son contraindicaciones relativas la presencia de varices esofágicas o la diátesis
hemorrágica. La fractura de la base del cráneo obliga a usar una sonda orogástrica.
3. Material
Sonda gástrica o duodenal, lubricante, jeringa de 50 ml con punta adaptable a la sonda, bolsa de
recogida, fonendoscopio.
4. Técnica
Se coloca al paciente con el cabecero elevado a 90º y en flexión anterior de la cabeza.
Se calcula la porción de sonda que queremos introducir simulando el recorrido de la misma
sobre la superficie del paciente.
Se aplica gel lubricante a la punta de la sonda y se introduce a través de una narina en dirección
perpendicular al macizo facial. Nos ayudaremos de los movimientos deglutorios del paciente
para que la sonda progrese.
Comprobamos su colocación mediante la insuflación de aire mientras auscultamos en la región
epigástrica. También podemos comprobarlo aspirando secreciones gástricas o realizando una
radiografía de tórax.
5. Complicaciones
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [32]
[2] TÉCNICAS Y PROCEDIMIENTOS INSTRUMENTALES
Epistaxis, malposición de la sonda, ulceración del ala nasal, úlcera por presión en la mucosa
esofágica o gástrica, esofagitis por reflujo, rotura de varices esofágicas, neumonía, sinusitis u otitis media.
X. SONDA DE SENGSTAKEN-BLAKEMORE
Taponamiento de sangrado por varices esofágicas mediante la introducción de un balón. La sonda
de Sengstaken-Blakemore es la más utilizada. Presenta tres vías, una para el lavado gástrico y dos para el
llenado del balón gástrico y esofágico.
1. Indicaciones
Hemorragia digestiva alta por varices esofágicas en la que ha fracasado la escleroterapia.
2. Contraindicaciones
Suponen una contraindicación relativa la presencia de hernia de hiato, estenosis esofágica o cirugía
esofágica reciente.
3. Material
Sonda de Sengstaken-Blakemore, jeringas de 50 ml con punta adaptable a la sonda, manómetro,
pinzas, lubricante hidrosoluble con anestésico, llave de tres pasos, fonendoscopio.
4. Técnica
En pacientes hemodinámicamente inestables o con deterioro del nivel de consciencia es
necesario realizar una intubación orotraqueal para el control de la vía aérea.
Se coloca al paciente con el cabecero elevado a 90º y en flexión anterior de la cabeza.
Ha de vaciarse el contenido gástrico con una sonda nasogástrica convencional y comprobarse la
indemnidad de los balones gástrico y esofágico.
Se aplica el gel lubricante con anestésico al extremo distal y se introduce por vía oral hasta al
menos la marca de 50 cm.
Se confirma su correcta colocación mediante la aspiración de secreciones y la insuflación de
aire con auscultación del epigastrio.
Se infla progresivamente el balón gástrico hasta un volumen de 200-250 ml y se tracciona
suavemente hasta anclarse en la unión esofagogástrica. Se pinza para evitar su vaciado.
Si el sangrado continúa, se ha de inflar el balón esofágico con control manométrico a través de
una llave de tres pasos hasta alcanzar valores en torno a 35-45 mm Hg, sin superar jamás la
presión arterial media del paciente, y se pinza también.
5. Complicaciones
Neumonía por aspiración. Ulceración de la mucosa en la zona esófagogástrica. Perforación gástrica
o esofágica.
6. Consideraciones especiales
Ha de desinflarse el balón esofágico cinco minutos cada seis horas para disminuir el riesgo de
isquemia en la mucosa gastroesofágica. El dispositivo no debe ser utilizado menos de 24 horas ni más de
72. Se desinfla el balón esofágico a las 24 horas y, si no se observa resangrado en las próximas cuatro horas,
se puede desinflar el balón gástrico. La ausencia de sangrado en las cuatro horas posteriores permite la
retirada de la sonda.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [33]
[2] TÉCNICAS Y PROCEDIMIENTOS INSTRUMENTALES
XI. PUNCIÓN LUMBAR
Extracción de líquido cefalorraquídeo (LCR) mediante punción del espacio intradural (Figura 7).
Figura 7. Punción lumbar.
1. Indicaciones
Sospecha de meningitis o encefalitis, hemorragia subaracnoidea, esclerosis múltiple o diagnóstico
de neuropatías periféricas. Tratamiento de la hipertensión intracraneal idiopática (pseudotumor cerebri).
Administración de fármacos o anestésicos intratecales.
2. Contraindicaciones
Absolutas
Hipertensión intracraneal (se debe descartar antes de realizar el procedimiento, mediante TC
craneal y/o fondo de ojo). Coagulopatía (plaquetas < 80.000/mm³, International Normalized Ratio [INR] >
1,4). Tratamiento anticoagulante. Absceso en la zona de punción.
Relativas
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [34]
[2] TÉCNICAS Y PROCEDIMIENTOS INSTRUMENTALES
Tratamiento antiagregante distinto de ácido acetilsalicílico (AAS) (no se ha demostrado más riesgo
de sangrado en pacientes antiagregados con AAS).
3. Material
Guantes, gasas, apósitos y paños estériles, jeringa de 10 ml, aguja intramuscular, antiséptico y
anestésico local, trócar, manómetro y tubos estériles.
4. Técnica
El paciente ha de colocarse en decúbito lateral (izquierdo si el que realiza la técnica es diestro y
viceversa), lo más próximo al borde de la cama posible. Se recomienda que el paciente realice
una flexión genupectoral de modo que mantenga las rodillas lo más pegadas al pecho y flexione
anteriormente la cabeza y el cuello.
Se identifica el punto de punción. El espacio ideal para realizar la punción lumbar se encuentra
por debajo de la línea imaginaria que une el borde superior de ambas crestas ilíacas (línea de
Tuffier), a la altura aproximada de L3-L4. Han de palparse las apófisis espinosas a ese nivel y
elegir un punto intermedio. Es útil marcar con la uña el punto de punción que consideremos
oportuno.
Se aplica antiséptico y se infiltra el anestésico local.
Se inserta el trócar en dirección paralela a la cama y con una inclinación cefálica de unos 20º.
Tras unos 7 cm notaremos una ligera resistencia (duramadre) que hemos de atravesar para
alcanzar el espacio intradural.
Se retira el fiador y, si hemos alcanzado nuestro objetivo, observaremos cómo refluye el LCR. Si
no lo hemos logrado, se recomienda extraer unos centímetros el trócar y volver a intentarlo
con mayor inclinación cefálica y/o cambiar de espacio.
Se conecta el manómetro al trócar para medir la presión de apertura y, a continuación, se
extraen las muestras pertinentes.
5. Complicaciones
Cefalea pospunción (típicamente frontal u occipital, a las 24-48 horas del procedimiento),
meningitis o infección local, hematoma epidural o subdural, lesión radicular o discal, herniación cerebral,
siembra tumoral.
6. Consideraciones especiales
Importante para realizar la punción lumbar con éxito es la adecuada colocación del
Se recomienda reposo en cama durante las cuatro horas posteriores a la realización de la punción
para prevenir la aparición de cefalea pospunción, aunque su eficacia no está demostrada.
XII. SONDAJE VESICAL
Colocación de un catéter en la vejiga a través de la uretra.
1. Indicaciones
Control de diuresis, uropatía obstructiva infravesical, vejiga neurógena, medición del residuo
posmiccional, irrigación continua en casos de hematuria grave, instilación de fármacos o de contraste en
estudios radiológicos, obtención de muestras.
2. Contraindicaciones
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [35]
[2] TÉCNICAS Y PROCEDIMIENTOS INSTRUMENTALES
Sospecha de rotura uretral.
3. Material
Guantes, gasas y paños estériles, antiséptico, lubricante urológico y sonda vesical (las más
empleadas son las sondas Foley, calibres 14 a 20).
4. Técnica
Lavado de genitales con agua, jabón y posteriormente antiséptico.
Varones: con el pene en posición vertical y retrayendo el prepucio, se introduce la sonda
adecuadamente lubricada a través de la uretra con suavidad hasta que refluya orina.
Mujeres: se separan los labios mayores y menores con la mano izquierda y se introduce
cuidadosamente la sonda a través de la uretra hasta que refluya orina.
Se avanzan 3 cm más y se hincha el globo. Finalmente, se tracciona hasta que se ancle en la
unión vesicouretral.
5. Complicaciones
5.1. Inmediatas
Sondaje imposible, uretrorragia, falsa vía, hematuria ex vacuo.
5.2. Precoces
Infecciones, espasmo vesical, depósitos de sales minerales.
5.3. Tardías
Estenosis, cistitis polipoide, litiasis vesical, abscesos y fístulas periuretrales.
XIII. ARTROCENTESIS
Extracción de líquido sinovial de una cavidad articular mediante punción percutánea.
1. Indicaciones
Diagnóstico de monoartritis. Evacuación de derrames a tensión o hemartros secundarios a artritis
traumática.
2. Contraindicaciones
Infección local en la zona de punción, bacteriemia, actividad de protrombina menor del 50%,
plaquetopenia por debajo de 50.000/mm³ (no está contraindicada en pacientes que reciben tratamiento
antiagregante o anticoagulante).
3. Material
Guantes, gasas y paños estériles, antiséptico y anestésico local, jeringa de 10 ml, aguja
intramuscular, tubos de laboratorio.
4. Técnica
Se desinfecta la región y se punciona en perpendicular aspirando continuamente hasta obtener
líquido sinovial.
Rodilla
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [36]
[2] TÉCNICAS Y PROCEDIMIENTOS INSTRUMENTALES
Paciente en decúbito supino con la pierna extendida y el cuádriceps relajado. Se sitúa la rótula
entre los dedos pulgar e índice y se desplaza lateralmente, localizando el espacio entre esta y el fémur. Se
punciona en dicho espacio, en la unión del tercio medio rotuliano con el tercio superior.
Tobillo
Paciente en decúbito supino y con el pie apoyado sobre la camilla. Se localiza el tendón del flexor
largo del primer dedo pidiendo al paciente que realice flexión dorsal del dedo, y se punciona de forma
medial a dicho tendón a nivel del relieve superior del astrágalo.
Hombro
Paciente en sedestación, hombro en rotación externa. Se punciona de forma medial a la cabeza del
húmero e inferolateral a la apófisis coracoides.
Codo
Paciente en sedestación, codo flexionado a 90º y antebrazo en posición neutra. Se punciona en el
punto medio de la línea imaginaria que une la punta del olécranon con el epicóndilo, con una inclinación de
45º respecto al plano horizontal y perpendicular al eje longitudinal del antebrazo.
5. Complicaciones
Dolor local, infección, hemartros.
BIBLIOGRAFÍA
Christensen T, Christensen M. The implementation of a guideline of care for patients with a
Sengstaken- Blakemore tube in situ in a general intensive care unit using transitional change theory.
Intens Crit Care Nurs. 2007;23(6):234-42.
FCCS. Fundamentos de cuidados críticos en soporte inicial. 3ª ed. Society of Critical Care Medicine;
2013.
Firestein GS, Budd RC, Gabriel SE, et al. Kelley’s Textbook of Rheumatology. 9th ed. Philadelphia:
Saunders; 2013.
Frerk C, Mitchell VS, McNarry AF, et al. Difficult Airway Society 2015 guidelines for management of
unanticipated difficult intubation in adults. Br J Anaesthes. 2015;115(6):827-48.
Mariano PL. El libro de la UCI. 4ª ed. Lippincott Williams & Wilkins; 2014.
Montejo JC, García de Lorenzo A, Marco P, Ortiz C. Manual de Medicina Intensiva. Sección 2. Técnicas.
4ª ed. Barcelona, España: Elsevier; 2013.
Quesada A, Rabanal JM. Procedimientos técnicos en Urgencias, Medicina Crítica y Pacientes de riesgo.
Madrid: Ergón; 2009.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [37]
[3] RESUCITACIÓN CARDIOPULMONAR Y VALORACIÓN DEL PACIENTE POLITRAUMATIZADO
3. Resucitación cardiopulmonar y valoración del
paciente politraumatizado
Helena Domínguez Aguado.
Medicina Intensiva
Silvia Chacón Alves.
Medicina Intensiva
Asesora: Carolina Mudarra Reche. Médica Adjunta de Medicina Intensiva
I. INTRODUCCIÓN
La parada cardiorrespiratoria (PCR) es la interrupción brusca, inesperada y potencialmente
reversible de la respiración y la circulación espontánea. El diagnóstico es clínico, objetivándose
inconsciencia, apnea o respiración agónica (gasping) y ausencia de circulación espontánea.
La parada cardiaca súbita es una de las principales causas de muerte en el mundo. A nivel
extrahospitalario, la causa más frecuente de PCR es la cardiopatía isquémica, encontrando en el análisis
inicial del ritmo cardiaco fibrilación ventricular (FV) en el 25-50% de las víctimas, pero cuando el ritmo es
registrado poco después de la parada, la proporción de víctimas en FV puede alcanzar el 76% (con el paso
de los minutos degeneran a asistolia). A nivel intrahospitalario, con un perfil de mayor edad,
comorbilidades y procesos agudos graves, el ritmo inicial es asistolia (AS) o actividad eléctrica sin pulso
(AESP) en el 75% de los casos. El tratamiento recomendado de la PCR es la resucitación cardiopulmonar
(RCP) inmediata por testigos y la desfibrilación eléctrica precoz (en los ritmos desfibrilables, FV y
taquicardia ventricular sin pulso [TVSP]).
La RCP es el conjunto de maniobras necesarias para sustituir y restablecer la respiración y
circulación espontáneas, con el objetivo de recuperar las funciones cerebrales completas. Todo paciente en
PCR debe ser reanimado, a menos que la víctima tenga voluntades anticipadas de no serlo, presente signos
de muerte irreversible (rigor mortis, decapitación o livideces en zonas en declive) o no se espere un
beneficio fisiológico. Dentro de las maniobras de reanimación podemos distinguir entre:
RCP básica o soporte vital básico: soporte de vía aérea, respiración y circulación sin el uso de
otro equipo que no sea un dispositivo de barrera para evitar el contacto directo con la boca de
la víctima.
RCP instrumentalizada o soporte vital instrumentalizado: introduce al soporte vital básico
determinados dispositivos (cánula orofaríngea, mascarilla facial y bolsa auto- hinchable,
desfibrilador automático/semiautomático).
RCP avanzada o soporte vital avanzado: llevado a cabo por un equipo de profesionales
cualificados y equipados. Incluye el manejo de la vía aérea, fármacos y corrección de los
factores causales.
La cadena de supervivencia es la concatenación de eslabones vitales, que de realizarse en el orden
debido y en el menor tiempo posible, aumenta la supervivencia de las víctimas:
1. Reconocimiento de la situación y activación precoz del servicio de emergencias médicas.
2. RCP precoz.
3. Desfibrilación precoz.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [38]
[3] RESUCITACIÓN CARDIOPULMONAR Y VALORACIÓN DEL PACIENTE POLITRAUMATIZADO
4. Cuidados posresucitación.
II. SOPORTE VITAL BÁSICO
El objetivo es mantener, sin la ayuda de ningún tipo de material, la vía aérea permeable, la
ventilación y la circulación sanguínea, de forma que se consiga una oxigenación tisular suficiente hasta que
llegue ayuda especializada. El algoritmo de actuación es el siguiente (Figura 1).
Figura 1.Algoritmo de la resucitación cardiopulmonar básica.
1. Asegurar la seguridad del reanimador y de la víctima
2. Valorar el nivel de consciencia
Acercarse a la víctima y preguntar qué le ocurre, mientras se le sacude ligeramente por los
hombros. No movilizar en lo posible a los pacientes con sospecha de traumatismo craneal y/o cervical.
2.1. Si está consciente, responde verbalmente o con movimientos, intentar saber qué le ocurre y
prestarle ayuda. Solicitar ayuda especializada si fuese necesario.
2.2. Si está inconsciente y no responde a estímulos:
Pedir ayuda especializada.
Abrir la vía aérea mediante la maniobra frente-mentón: con la víctima en decúbito supino
apoyar una mano sobre la frente para hiperextender la cabeza, y con el dedo índice y medio de
la otra mano elevar el mentón. Si hay sospecha de lesión traumática se realizará la maniobra de
tracción mandibular (se colocan los dedos de ambas manos detrás de los ángulos mandibulares
y se tracciona la mandíbula hacia arriba).
Retirar aquellos objetos que puedan estar obstruyendo la vía aérea.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [39]
[3] RESUCITACIÓN CARDIOPULMONAR Y VALORACIÓN DEL PACIENTE POLITRAUMATIZADO
3. Valoración de la ventilación
Manteniendo abierta la vía aérea de la víctima, aproximar la mejilla a su boca para oír la salida del
aire, ver cómo se eleva el pecho y sentir el aire exhalado, sin emplear en ello más de 10 segundos. En los
primeros momentos de PCR la víctima con frecuencia puede realizar algún intento de respiración agónica o
gasping que no se deben confundir con una respiración normal.
3.1. Si respira
Tras comprobar que la víctima está inconsciente, pero que respira con normalidad, se debe colocar
en posición lateral de seguridad (evita la obstrucción de la vía aérea con la lengua y la broncoaspiración), y
se solicitará ayuda especializada (en pacientes con traumatismo se puede realizar movilización en bloque).
Mientras la ayuda especializada llega se vigilará continuamente que la víctima continúe respirando
espontáneamente.
Para colocar a la víctima en posición lateral de seguridad, el reanimador se pondrá de rodillas junto
a la víctima, situará el brazo más próximo de esta en ángulo recto hacia la cabeza, con la palma de la mano
hacia arriba, y cruzará el otro brazo sobre el pecho poniendo la mano sobre el hombro contralateral.
Luego flexionará la pierna más alejada, sujetando al paciente por el hombro más alejado y el hueco
poplíteo de la pierna flexionada se gira 90º. Si la víctima tuviera que estar en esta posición mucho tiempo
es conveniente cambiar de lado cada 30 minutos.
3.2. Si no respira (incluye gasping o respiración agónica)
La comprobación del pulso ha demostrado ser un método inexacto para confirmar la presencia o
ausencia de circulación. En caso de que no presente pulso o se tengan dudas, y el paciente esté
inconsciente y no respire, comenzar RCP:
Avisar a los servicios de emergencia y activar la alerta de parada. Si es posible envíe a alguien a
buscar un desfibrilador externo automático (DEA), si el reanimador está solo y tiene un DEA
localizado y cercano, puede abandonar momentáneamente a la víctima antes de iniciar RCP.
Compresiones torácicas: iniciar las maniobras de RCP básica con 30 compresiones torácicas.
Con la víctima en decúbito supino y sobre una superficie firme, el reanimador se arrodilla a su
lado, descubre el tórax y coloca la base de una mano en el centro del tórax y la otra mano
encima, entrelazando los dedos. El reanimador se sitúa verticalmente sobre el tórax de la
víctima, con los brazos extendidos, y presiona deprimiéndolo unos 5 cm (no más de 6 cm).
Después de cada compresión se libera toda la presión sin quitar las manos, para permitir la
reexpansión del tórax. El ritmo será de unas 100-120 compresiones por minuto con el menor
número de interrupciones posible.
Respiraciones de rescate: tras las 30 compresiones se realiza la apertura de la vía aérea con la
maniobra frente-mentón, y posteriormente, se pinza con los dedos índice y pulgar las fosas
nasales, se abre la boca y se colocan los labios alrededor de la misma, asegurando un buen
sellado. Se inspira profundamente y se insufla el aire en la boca de la víctima. Se realizarán dos
ventilaciones, y tras ello volverá a colocar las manos en el centro del tórax y se continuará con
otras 30 compresiones torácicas. La duración de cada insuflación debe ser de 1 segundo, con el
volumen suficiente para hacer que el tórax se eleve. Si las ventilaciones no fueron efectivas se
debe reevaluar la boca de la víctima y extraer cualquier cuerpo extraño, y confirmar una
apertura adecuada de la vía aérea; no se debe intentar más de 2 ventilaciones cada vez. Si no se
puede, o no se desea dar ventilaciones, se seguirá únicamente con las compresiones torácicas
con un ritmo de 100-120 por minuto.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [40]
[3] RESUCITACIÓN CARDIOPULMONAR Y VALORACIÓN DEL PACIENTE POLITRAUMATIZADO
La relación compresiones-ventilaciones recomendada es de 30:2.
Si hay más de un reanimador se relevarán cada 2 minutos para prevenir la fatiga, siempre
asegurando el mínimo retraso durante el cambio.
Si se dispone de un DEA, ponerlo en funcionamiento y seguir las instrucciones de los mensajes
de voz. Si hay más de un reanimador, las maniobras de RCP se deben continuar mientras se
colocan los parches.
Tras la desfibrilación, continuar con otros dos minutos de RCP y posteriormente volver a
evaluar ritmo cardiaco.
Continuar la RCP hasta que llegue ayuda especializada, la víctima empiece a despertar o
respirar con normalidad o el reanimador esté exhausto.
III. DESFIBRILADOR EXTERNO AUTOMÁTICO
El DEA es un desfibrilador externo que incorpora un sistema automático para analizar el ritmo
cardiaco y permite la desfibrilación en aquellos ritmos desfibrilables (FV y TVSP).
Se ha incluido en las últimas guías el empleo del DEA como parte de la RCP básica. El primer testigo,
sea trabajador sanitario o no, debería emplear el desfibrilador externo automático, puesto que la FV
revierte en hasta un 90% si se inicia la desfibrilación en el primer minuto, perdiendo un 10% de eficacia por
cada minuto de retraso.
El DE es automático si analiza, detecta y descarga cuando está indicado sin ayuda del operador; y es
semiautomático cuando analiza y detecta la arritmia desfibrilable, pero solo recomienda la descarga, la cual
debe ser accionada por el operador. Guía de actuación:
Encender el DEA; tras ello el aparato comienza a emitir indicaciones verbales. Primero solicita
que se conecten los electrodos autoadhesivos al tórax descubierto (uno al nivel paraesternal
derecho e infraclavicular y el otro en el ápex cardiaco).
La RCP debería continuarse con la mínima interrupción de las compresiones torácicas mientras
se coloca el DEA y durante su uso.
Asegurarse de que nadie toca a la víctima mientras el DEA realiza el análisis del ritmo. Si el
ritmo es desfibrilable, el DEA realiza la descarga o la recomienda y el reanimador la activa
(asegurar previamente que nadie esté tocando a la víctima).
Tras efectuar el choque no se deben buscar signos de circulación. Comenzar inmediatamente
después de la desfibrilación, RCP 30:2. El propio DEA cronometrará dos minutos tras los cuales
avisará de un nuevo análisis del ritmo.
Si el ritmo no es desfibrilable el DEA indica continuar la RCP durante dos minutos.
Los DEA estándar son adecuados para su uso en niños mayores de ocho años. Para niños entre uno
y ocho años se deben utilizar parches pediátricos con un atenuador o en modo pediátrico si está disponible.
IV. OBSTRUCCIÓN DE LA VÍA AÉREA POR CUERPO EXTRAÑO
La obstrucción de la vía aérea por cuerpo extraño es una causa poco frecuente, pero
potencialmente tratable, de muerte accidental. Habitualmente ocurre mientras la víctima está comiendo o
bebiendo. Puede producir una obstrucción leve/incompleta (capaz de hablar, toser y respirar) o
grave/completa (no puede hablar ni respirar, tos débil e ineficaz) (Figura 2).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [41]
[3] RESUCITACIÓN CARDIOPULMONAR Y VALORACIÓN DEL PACIENTE POLITRAUMATIZADO
Figura 2. Algoritmo obstrucción de vía aérea por cuerpo extraño.
En caso de obstrucción leve animar a toser enérgicamente (la tos genera presiones altas en vía
aérea y puede provocar la expulsión del cuerpo extraño). Si la obstrucción se hace completa y la víctima
está consciente:
Dar golpes interescapulares, apoyando una mano en el pecho de la víctima e inclinándole
ligeramente hacia delante, dar 5 golpes secos con la base de la otra mano en la espalda, a nivel
interescapular.
Si con ello no se ha resuelto la obstrucción realizar compresiones abdominales (maniobra de
Heimlich): situándose detrás de la víctima rodearla con los brazos e inclinarla hacia delante;
colocar el puño de una mano al nivel epigástrico y agarrar ese puño con la otra mano,
empujando fuerte y rápido hacia adentro y hacia arriba; repetir la maniobra hasta cinco veces.
Continuar alternando cinco golpes en la espalda y cinco compresiones abdominales hasta su
resolución o hasta que la víctima esté inconsciente. La probabilidad de éxito se incrementa al
realizar combinaciones de golpes en la espalda y compresiones abdominales.
Si la víctima está inconsciente con obstrucción completa de la vía aérea iniciar algoritmo de RCP.
Cuando el objeto sea accesible se puede proceder a su extracción manual. Si no se está seguro de poder
sacarlo no debe intentarse, por riesgo de introducirlo más.
V. RESUCITACIÓN CARDIOPULMONAR BÁSICA PEDIÁTRICA
Muchos niños no reciben resucitación por temor a causar daño. Es mejor usar la secuencia de
soporte vital básico para adultos en la resucitación de un niño que no hacer nada. Los siguientes puntos son
modificaciones de la RCP básica pediátrica con respecto a la del adulto:
Dar inicialmente cinco ventilaciones de rescate antes de las compresiones torácicas (la causa
más frecuente de PCR en la población pediátrica es la insuficiencia respiratoria).
Dar RCP durante un minuto antes de ir en busca de ayuda en el caso de que el reanimador esté
solo.
Comprimir el tórax por lo menos un tercio de su profundidad, utilizar dos dedos en menores de
un año y emplear una o dos manos en mayores de un año.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [42]
[3] RESUCITACIÓN CARDIOPULMONAR Y VALORACIÓN DEL PACIENTE POLITRAUMATIZADO
VI. SOPORTE VITAL AVANZADO
Requiere un tratamiento integrado, con un equipo de personas capacitadas y dotadas del material
necesario para realizar maniobras de aislamiento de la vía aérea, técnicas de ventilación y oxigenación,
masaje cardiaco, canalización de accesos vasculares, administración de fármacos y líquidos iv, etc.
El objetivo final del SVA es resolver definitivamente la causa de la parada cardiorrespiratoria,
sabiendo que solo la desfibrilación precoz y la RCP básica de calidad han demostrado mejorar la
supervivencia, de ahí que en las últimas guías se haga especial énfasis en las compresiones torácicas de
calidad y tener acceso a un desfibrilador de forma temprana.
1. Algoritmo de actuación
Cuando nos encontramos ante un paciente con sospecha de PCR, lo primero que se debe hacer es
llevar a cabo el diagnóstico, para lo que es fundamental la comprobación del nivel de consciencia, así como
el conocimiento del soporte vital básico. Una vez que se ha comprobado que el paciente está inconsciente,
se solicitará ayuda y se continuará las siguientes maniobras.
Se llevará a cabo la apertura de la vía aérea y una vez comprobada la ausencia de respiración (o la
presencia de gasping) se solicitará ayuda a los Servicios de Emergencia y se comenzará de forma rápida
masaje cardiaco, realizando 30 compresiones torácicas, seguidas de dos ventilaciones, de forma sucesiva.
Estas maniobras continuarán hasta que se disponga de un desfibrilador. Una vez que esté
disponible se debe proceder a su colocación para valorar el ritmo eléctrico del paciente con PCR. Es
preferible el empleo de las palas-pegatina, ya que permiten mantener las compresiones torácicas de forma
continua. De manera simultánea a la monitorización y realización de masaje cardiaco, se canalizará acceso
venoso periférico y se llevará a cabo el manejo de la vía aérea (se verá más adelante).
Este es el punto en que el algoritmo se va a dividir en dos posibles secuencias a seguir, en función
del tipo de ritmo encontrado en el monitor: aquellos con ritmo desfibrilable (FV o TVSP) y aquellos con
ritmo no desfibrilable (asistolia y disociación electromecánica [DEM]) (Figura 3).
Figura 3.Algoritmo de comienzo de soporte vital avanzado. En él se especifican los dos posibles ritmos encontrados tras la
monitorización.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [43]
[3] RESUCITACIÓN CARDIOPULMONAR Y VALORACIÓN DEL PACIENTE POLITRAUMATIZADO
2. Ritmos desfibrilables
Forman parte de este grupo la FV (se trata de actividad ventricular desorganizada e ineficaz sin
morfología precisa en el electrocardiograma) y la TVSP (se identifica como una taquiarritmia regular de QRS
ancho en el monitor, sin pulso a la palpación).
Cuando nos encontramos con uno de estos ritmos en el monitor se mantiene el masaje cardiaco
mientras otro operador carga el desfibrilador.
Una vez cargado se detiene el masaje cardiaco y se procede a administrar una única descarga con
360 julios si el desfibrilador es monofásico y con 150-200 julios si es bifásico. De forma inmediata,
reanudamos el masaje cardiaco, sin comprobar ritmo, durante dos minutos (manteniendo la secuencia de
30 compresiones y dos ventilaciones, excepto en pacientes con aislamiento de la vía aérea, que se
realizarán compresiones a 100 latidos por minuto aproximadamente y en torno a 10 ventilaciones por
minuto). Pasados los dos minutos se comprueba de nuevo el ritmo, si observamos ritmo desfibrilable
repetimos la maniobra y administramos un nuevo choque, para continuar con masaje durante otros dos
minutos, y así sucesivamente.
Se recomienda minimizar el tiempo entre la suspensión de las compresiones torácicas y la
administración de choque eléctrico. Además, mientras se realiza la RCP se debe revisar la monitorización,
esto es, verificar la correcta posición de los electrodos, el contacto de las palas, etc.
Si mantiene ritmo desfibrilable se debe administrar 1 mg de adrenalina en el tercer choque, que se
repetirá cada tres a cinco minutos si persiste la PCR. Además, antes del cuarto choque se pueden
administrar 300 mg de amiodarona.
Se mantendrá el mismo ciclo de forma continua en caso de que el ritmo siga siendo desfibrilable:
RCP dos minutos-comprobar ritmo-choque-RCP dos minutos, 1 mg de adrenalina cada tres a cinco minutos
a partir del segundo choque y 300 mg de amiodarona a partir del tercer choque, que se repetirá en el
cuarto choque, a dosis de 150 mg (Figura 4).
Mantendremos este algoritmo hasta que el paciente recupere signos vitales (pulso, respiración,
movimientos espontáneos…) o si al analizar el ritmo encontramos ritmo no desfibrilable, por lo que
pasaremos al algoritmo de ritmo no desfibrilable.
Figura 4.Algoritmo de ritmo desfibrilable.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [44]
[3] RESUCITACIÓN CARDIOPULMONAR Y VALORACIÓN DEL PACIENTE POLITRAUMATIZADO
3. Ritmos no desfibrilables
A este grupo pertenecen la asistolia (AS) y la actividad eléctrica sin pulso (AESP) o DEM.
Cuando nos encontramos un ritmo no desfibrilable el pronóstico es desfavorable. En el caso de
asistolia hay que comprobar que los electrodos están bien colocados, y en caso de ver actividad eléctrica en
el monitor habrá que asegurarse de la ausencia de pulso. Se administrará 1 mg de adrenalina tan pronto
como sea posible y se interrumpirán lo menos posible las compresiones. La secuencia será masaje cardiaco
durante dos minutos, comprobar ritmo y continuar con el masaje cardiaco durante otros dos minutos. Se
administrará adrenalina cada tres a cinco minutos. No se administra ni amiodarona ni atropina (quedando
relegada a pacientes con bradicardia extrema previa a PCR). En caso de duda acerca del ritmo encontrado
se tratará como ritmo no desfibrilable.
En estos ritmos hay que tener más presentes y descartar las causas potencialmente reversibles de
la RCP que se comentarán más adelante.
4. Manejo de la vía aérea en la resucitación cardiopulmonar avanzada
Los pacientes que requieren resucitación, a menudo tienen una obstrucción de la vía aérea.
Normalmente, esta obstrucción es debida al bajo nivel de consciencia, aunque en ocasiones puede ser la
causa primera de la PCR. Por ello, realizar una rápida evaluación y control de la vía aérea es esencial.
En el medio intrahospitalario se optimizará la ventilación con los distintos dispositivos. Inicialmente
se realiza apertura de la vía aérea mediante la maniobra frente-mentón y se colocará una cánula
orofaríngea para ayudarnos a vencer la obstrucción de la lengua y poder ventilar al paciente mediante una
mascarilla facial y bolsa autoinflable conectada a un flujo de oxígeno al 100%. Se mantendrá la secuencia
30:2.
Para asegurar el aislamiento definitivo de la vía aérea se debe proceder a la intubación orotraqueal
(IOT). Se deberá realizar únicamente por personal altamente cualificado y con la mínima interrupción sobre
las compresiones torácicas, de forma que no se debe emplear más de 10 segundos y no se detendrán las
compresiones mientras se realiza la laringoscopia directa.
En cuanto al momento óptimo para proceder al aislamiento de la vía aérea no está establecido. No
obstante, habrá que pensar en realizarlo de forma más precoz en aquello s ritmos no desfibrilables, donde
la causa de la parada podría deberse a la hipoxia.
Tras la IOT se confirma la correcta posición del tubo orotraqueal (TOT) mediante la auscultación de
ambos campos pulmonares, y se interrumpe la secuencia 30:2 para realizar compresiones a un ritmo de por
lo menos 100 al minuto y en torno a 10 ventilaciones por minuto, de forma independiente.
Existen otros métodos para confirmar la correcta colocación del TOT, como es el empleo de la
capnografía. Las últimas guías de la RCP hacen especial énfasis en el empleo de la misma, no solo por la
importancia de reconocer una correcta IOT, sino como determinante de la calidad de la RCP, así como
indicador temprano de recuperación de circulación espontánea.
En cuanto a los parámetros respiratorios recomendados, no existe evidencia suficiente en el
momento actual sobre cuáles son los más adecuados. Se debe mantener un volumen tidal que evite la
hiperventilación, ya que empeora el pronóstico neurológico. La concentración óptima de oxígeno inspirado
durante la RCP no está establecida, recomendándose mantener la saturación de O2 entre el 94% y el 98%.
En ausencia de personal no cualificado para la IOT, esta no se debe realizar, ya que se ha
demostrado una mayor tasa de complicaciones relacionadas con la técnica, así como mayor interrupción en
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [45]
[3] RESUCITACIÓN CARDIOPULMONAR Y VALORACIÓN DEL PACIENTE POLITRAUMATIZADO
las compresiones torácicas. Existen dispositivos alternativos, que se podrían emplear en esta circunstancia,
como son los dispositivos supraglóticos (mascarilla laríngea, etc.). En caso de emplearlos se debe continuar
con la secuencia 30:2, puesto que no aseguran un correcto aislamiento de la vía aérea.
5. Causas potencialmente reversibles en la resucitación cardiopulmonar
Siempre se deben tener en cuenta durante la RCP, especialmente ante ritmos no desfibrilables.
Para recordarlas se establece la regla de las “4H y 4T”.
Hipoxia: hay que minimizar el riesgo de hipoxia, asegurándose la correcta ventilación y
oxigenación del paciente, administrando oxígeno al 100% durante la PCR. Hay que comprobar
la correcta posición del TOT y la ventilación de ambos campos pulmonares mediante la
auscultación.
Hipovolemia: normalmente causada por hemorragia grave (en sangrado intestinal,
traumatismo, síndrome aórtico con rotura de aneurisma, etc.) hay que restaurar el volumen
intravascular mediante la administración de fluidos intravenosos, incluso valorar la intervención
quirúrgica urgente en función de la etiología.
Hiper/hipopotasemia: las alteraciones metabólicas también pueden ser causa de PCR, tanto
alteraciones en los niveles de potasio en sangre como hipocalcemia o acidosis severa. Se
sospecharán por la historia clínica del paciente (antecedentes de insuficiencia renal, toma de
fármacos…) y se confirmarán mediante análisis sanguíneo. Se llevará a cabo tratamiento
etiológico, al mismo tiempo que se continúa con la RCP, por ejemplo el cloruro cálcico estaría
indicado en la hiperpotasemia tóxica, la hipocalcemia y la intoxicación por antagonistas del
calcio.
Hipotermia: sobre todo en el caso de ahogamientos o accidentes se diagnostica mediante la
medición de la temperatura y se maneja mediante un protocolo específico. Es una indicación de
mantenimiento de la RCP de forma prolongada, hasta alcanzar una temperatura superior a 32
ºC.
Neumotórax a tensión: probablemente la causa más frecuente de actividad eléctrica sin pulso.
Su diagnóstico es clínico y su tratamiento es la colocación urgente de un drenaje torácico. Hay
que pensar en él cuando estamos ante un paciente con traumatismo o cuando han existido
intentos de canalización de catéter venoso central subclavio.
Taponamiento cardiaco: el diagnóstico es más complejo, sospechándolo en caso de
traumatismo torácico penetrante. Hay que realizar pericardiocentesis o toracotomía urgente.
Tóxicos y sobredosis de fármacos: el diagnóstico final lo da el laboratorio, sospechándose en
función de la historia clínica. Si se dispone de antídoto específico se debe emplear.
Tromboembolismo pulmonar: si se sospecha como posible causa de la PCR se debe considerar
la realización de fibrinólisis urgente.
6. Fármacos y vías de administración
Aunque la administración de fármacos durante la PCR esté incluida en las guías de RCP, lo cierto es
que falta evidencia suficiente para saber qué fármaco es mejor y en qué momento de la RCP administrarlo.
Por ello, las últimas guías hacen hincapié en que la administración de fármacos es menos importante que la
desfibrilación precoz y las compresiones torácicas de calidad.
A la hora de su administración la vía de elección será la vía intravenosa (iv) periférica, con el acceso
central las concentraciones pico del fármaco son mayores y el tiempo es más corto, pero su inserción
requiere de personal entrenado en la técnica y supone una mayor interrupción en las maniobras de RCP. Si
no se establece el acceso intravenoso en los dos primeros minutos de la reanimación, la vía alternativa será
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [46]
[3] RESUCITACIÓN CARDIOPULMONAR Y VALORACIÓN DEL PACIENTE POLITRAUMATIZADO
la intraósea (io) a nivel tibial o humeral, que es fácil, segura, eficaz y utiliza las mismas dosis que la vía
intravenosa.
Hay tres grandes grupos de fármacos empleados durante la RCP: vasopresores, antiarrítmicos y
otros.
6.1. Vasopresores
A pesar de la utilización generalizada de adrenalina y el aumento del uso de la vasopresina, no hay
ningún estudio controlado con placebo que muestre que el uso rutinario de los mismos durante la RCP
aumente la supervivencia al alta hospitalaria, aunque sí a corto plazo. En el momento actual el vasopresor
de elección en cualquier ritmo en la parada cardiaca es la adrenalina. Se trata de un estimulador de los
receptores alfa-adrenérgicos que produce una vasoconstricción sistémica y una acción beta-adrenérgica
con efecto inotrópico y cronotrópico, aumentando así la presión de perfusión coronaria y cerebral.
Indicaciones y dosis en la PCR: ritmos desfibrilables (FV/TVSP) se administrará 1 mg iv o io después del
tercer choque, y luego cada tres a cinco minutos (ciclos alternos). Ritmos no desfibrilables (asistolia/AESP)
se administrará 1 mg cada tres a cinco minutos lo antes posible, junto con las maniobras de RCP.
Precaución en las PCR asociadas a intoxicación por cocaína u otros simpaticomiméticos y cuando se
ha recuperado el pulso; pequeñas dosis como 50-100 μg pueden inducir un nuevo episodio de taquicardia
ventricular (TV), FV o isquemia coronaria.
6.2. Antiarrítmicos
Hay evidencia limitada sobre su beneficio en la PCR, ninguno de ellos utilizado durante el paro
cardiaco ha demostrado aumentar la supervivencia al alta hospitalaria, aunque la amiodarona ha
demostrado aumentar la supervivencia durante la estancia en el hospital. La amiodarona es un fármaco
estabilizador de la membrana que aumenta la duración del potencial de acción y periodo refractario en el
miocardio, enlentece la conducción auriculoventricular y de las vías accesorias, tiene una leve acción
inotrópica negativa y provoca vasodilatación periférica a través un efecto bloqueador alfa periférico.
Indicación y dosis en la RCP: en ritmos desfibrilables (FV/TVSP) que persistan después del tercer
choque fallido administraremos un bolo de 300 mg iv antes del cuarto choque; si no es eficaz se puede
administrar otra dosis de 150 mg. La amiodarona puede ser arritmogénica, especialmente si se administra
simultáneamente con fármacos que prolongan el intervalo QT.
La lidocaína se recomienda solo cuando la amiodarona no está disponible y nunca de forma
conjunta. Se trata de un estabilizador de la membrana que actúa aumentando el periodo refractario del
miocito, disminuye la automaticidad ventricular y la actividad de despolarización de los tejidos
arritmogénicos, mientras que interfiere mínimamente con la actividad eléctrica de los tejidos normales; por
tanto, es eficaz en la supresión de las arritmias asociadas a la despolarización (isquemia, toxicidad
digitálica), pero relativamente ineficaz contra arritmias que ocurren en células normalmente polarizadas (la
fibrilación o flutter auricular). Se recomienda una dosis de 1-1,5 mg/kg (bolo de 100 mg) en FV/TVSP
refractaria a tres choques, pudiendo dar otro bolo adicional de 50 mg si es necesario. La dosis total no debe
superar los 3 mg/kg durante la primera hora.
El magnesio no se recomienda de forma rutinaria. Es un componente de los sistemas de generación
de ATP en el músculo y de la transmisión neuroquímica. Niveles bajos se asocian con hipopotasemia y
pueden contribuir a la producción de arritmias y parada cardiaca. El sulfato de magnesio se indica en TV o
taquicardia supraventricular (TSV) asociadas a hipomagnesemia y en la torsade de pointes. La dosis es de 2
g iv y puede repetirse cada 10-15 minutos.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [47]
[3] RESUCITACIÓN CARDIOPULMONAR Y VALORACIÓN DEL PACIENTE POLITRAUMATIZADO
El calcio solo está indicado en la AESP causada por hiperpotasemia, hipocalcemia o sobredosis de
los bloqueadores de los canales del calcio. La dosis recomendada es de 2-4 mg/kg en solución al 10%.
6.3. Otros: agentes alcalinizantes
En la parada cardiaca el mejor indicador de la relación ácido-base de los tejidos es el análisis de la
sangre venosa central. La acidosis que se produce es fundamentalmente metabólica, secundaria al
metabolismo celular anaeróbico, ya que la circulación sistémica y la pulmonar están comprometidas y el
intercambio alveolar de gases y entrega de oxígeno a los tejidos cesa. Por tanto, el mejor tratamiento son
las compresiones torácicas que restablecen la circulación y el estado ácido-base.
El bicarbonato no está indicado de forma habitual porque genera dióxido de carbono que difunde
rápidamente a las células y produce un agravamiento de la acidosis intracelular, efecto inotrópico negativo
sobre el miocardio isquémico y desviación a la izquierda de la curva de disociación de la hemoglobina,
reduciendo la entrega de oxígeno a los tejidos. Solo se ha visto beneficio en PCR asociadas a
hiperpotasemia y a sobredosis de antidepresivos tricíclicos con gran toxicidad cardiovascular (hipotensión,
arritmias cardiacas). La dosis es 50 mmol de bicarbonato de sodio iv y guiar la terapia según la situación
clínica y gasométrica.
Fibrinólisis durante la RCP: se considera su administración cuando se sospeche que la causa de la
parada cardiaca es un tromboembolismo pulmonar agudo. El éxito de la fibrinólisis en reanimación
cardiopulmonar se asocia generalmente con buen pronóstico neurológico, por lo que en estos casos se
recomienda realizar la RCP durante al menos 60-90 minutos antes de la terminación de la misma.
Fluidos: la hipovolemia es una causa potencialmente reversible de PCR y cuando se sospeche habría
que infundir líquidos rápidamente. No se han demostrado ventajas en el uso de coloides o cristaloides. Hay
que evitar la dextrosa, que se redistribuye rápidamente en el espacio extravascular y causa hiperglucemia
que empeora el pronóstico neurológico.
En ausencia de hipovolemia, la infusión de un volumen excesivo de líquido es perjudicial.
VII. CALIDAD DE LA RESUCITACIÓN CARDIOPULMONAR Y ECOGRAFÍA
En los últimos años se ha desarrollado tecnología que sirve de ayuda a la hora de la realización del
masaje cardiaco. Si bien todavía faltan estudios donde se establezca de forma contundente su utilidad en la
RCP, existen dispositivos llamados de feedback que informan de cómo se está realizando la RCP, de forma
que se establece la calidad de la misma de forma objetiva. Con su empleo se ha demostrado que se lleva a
cabo una menor interrupción de las compresiones, mejoría del ritmo y aumento de la profundidad de las
mismas en 1 cm. Igualmente, se están empleando de forma satisfactoria en el entrenamiento de la RCP.
De la misma forma, en los últimos años se está aumentando el empleo de la ecografía en diferentes
ámbitos, habiéndose extendido su utilización en la parada cardiaca. Con su empleo (normalmente a través
de la ventana subxifoidea) se puede llevar a cabo la detección de causas reversibles de la parada, se
reconoce la “asistolia verdadera” y puede ser útil en la toma de decisiones y en el cese de la reanimación.
De hecho, para muchos autores el papel de la ecografía es fundamental, formando parte de la “resucitación
óptima”, que sigue el CABDE: C (compresión), A (vía aérea), B (ventilación), D (desfibrilación), E
(ecocardiograma dirigido).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [48]
[3] RESUCITACIÓN CARDIOPULMONAR Y VALORACIÓN DEL PACIENTE POLITRAUMATIZADO
VIII. CUIDADOS POSRESUCITACIÓN
En los últimos años se ha llevado a cabo una optimización de la respuesta a la parada cardiaca, a
nivel extrahospitalario, con la implementación de la “cadena de supervivencia”. No obstante, a pesar de
que muchos pacientes llegan al hospital habiendo recuperado circulación espontánea, la mayoría (hasta el
70%) fallecen en los primeros días de ingreso, normalmente por causas neurológicas.
Por ello, desde el año 2010 se incorporó a las guías Europeas de RCP los cuidados posresucitación.
Igualmente se han incorporado a la “cadena de la supervivencia” como otro de los eslabones
fundamentales en la RCP, adquiriendo un papel fundamental en la última revisión de las guías de 2015.
Dentro de estos cuidados destaca la presencia del síndrome posparada cardiaca. Se trata de una
entidad clínica que se produce como consecuencia de la aplicación de maniobras de RCP que consiguen la
recuperación de circulación espontánea tras la PCR. Los componentes clave de este síndrome son los
siguientes:
Persistencia de la enfermedad precipitante. En el caso de las paradas extrahospitalarias lo más
frecuente es la cardiopatía isquémica, por lo que habrá que valorar la realización de
revascularización coronaria urgente (mediante intervencionismo percutáneo o trombolisis).
Daño cerebral posparada: como consecuencia de la isquemia, con generación de radicales libes
de oxígeno y pérdida de la autorregulación cerebral. Es la principal causa de muerte.
Daño miocárdico posparada: aturdimiento miocárdico y disfunción diastólica y sistólica, por
depleción de depósitos de alta energía.
Síndrome de respuesta inflamatoria sistémica (SIRS): produce un cuadro hemodinámico similar
al de la sepsis.
Por lo tanto, los cuidados posparada cardiaca tienen como objetivo el tratamiento de la causa
precipitante, así como el manejo óptimo de los otros tres subsíndromes.
Para ello, se llevará a cabo un manejo estandarizado y escalonado, basado en la secuencia ABCDE.
Normalmente se lleva a cabo en una unidad de cuidados intensivos.
Pasos a seguir:
Recoger de forma breve los antecedentes y sintomatología del paciente para orientar la causa
de la PCR, así como los tiempos de la misma.
Realización de una coronariografía urgente: en aquellos pacientes en que se sospeche que la
causa de la parada cardiaca puede ser isquémica, se llevará a cabo una coronariografía urgente
para poder realizar angioplastia sobre la arteria responsable. Habrá que pensar en ello
especialmente en pacientes con ritmos desfibrilables. En caso de no tener clara la causa de la
parada cardiaca, el ecocardiograma será de ayuda para detectar alteraciones segmentarias de
la contractilidad.
Medidas de soporte
Soporte respiratorio
Se administrará oxigenoterapia a través de mascarilla (si el paciente se encuentra consciente, con
poco tiempo de PCR) o bien mediante IOT y ventilación mecánica invasiva (en pacientes con tiempos de
reanimación prolongados y bajo nivel de consciencia). Hay que evitar tanto la hiperoxia como la hipoxia, así
como mantener ni veles normales de pCO2.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [49]
[3] RESUCITACIÓN CARDIOPULMONAR Y VALORACIÓN DEL PACIENTE POLITRAUMATIZADO
Se recomienda la monitorización de la oxigenación y la ventilación mediante la realización de
gasometrías arteriales, pulsioximetría (para SatO2 del 94-98%) y utilización de capnografía. Hay que realizar
a todos los pacientes radiografía de tórax para comprobar la correcta posición de TOT y descartar
complicaciones.
Soporte hemodinámico
Como hemos comentado previamente, los pacientes pueden presentar un cuadro de shock mixto,
con disfunción miocárdica y vasoplejía por el SRIS.
Debido a ello se llevará a cabo la administración de fluidoterapia, así como soporte vasoactivo e
inotrópico, en función de las necesidades del paciente. La monitorización constará de electrocardiograma
continuo (tras la PCR existe un alto riesgo de desarrollo de arritmias cardiacas), tensión arterial (de elección
la medición invasiva continua) y de forma muy recomendable presión capilar pulmonar, gasto cardiaco,
presión venosa central y medición del ácido láctico. Se llevará a cabo una resucitación guiada por objetivos,
con una tensión arterial media en las primeras 24 horas que ha de ser superior a 70 mm Hg (en torno a 80-
90 mm Hg), para evitar hipoperfusión cerebral. Posteriormente, el objetivo será de 65-70 mm Hg.
Soporte neurológico
El tipo de sedación a emplear dependerá en gran medida de la situación hemodinámica del
paciente. No existe consenso sobre qué sedación es de elección, pero se recomienda sedación de corta
duración (como propofol) para poder valorar la situación neurológica de forma rápida tras su suspensión.
Hay que evitar las alteraciones en el control glucémico, buscando una glucemia inferior a 180 mg/dL, sin
episodios de hipoglucemia.
Debemos llevar a cabo un adecuado control de la temperatura, evitando la hipertermia. Pueden
aparecer crisis convulsivas, la mayoría de las veces son mioclonías, apareciendo en el 18-25%. Hay que
tratarlas de forma precoz, no estando recomendado su tratamiento profiláctico. Conllevan peor pronóstico
neurológico comparado con aquellos pacientes que no las presentan. Dentro del soporte neurológico, es
fundamental la valoración pupilar, explorando tanto el tamaño pupilar como el reflejo fotomotor, que
también tendrán valor pronóstico como se verá a continuación.
Hipotermia terapéutica
Se trata de un tema controvertido. Varios estudios demostraron mejoría neurológica al aplicar
hipotermia terapéutica en las primeras 12-24 horas, a 32-34 ºC. Se aplicaba a pacientes con bajo nivel de
consciencia tras la PCR, cuyo ritmo inicial era FV/TVSP. No obstante, luego se ha aplicado también a ritmos
no desfibrilables. Sin embargo, a raíz de un estudio publicado en la revista New England Journal of
Medicine, en el que no se objetivaban diferencias, esta práctica ha quedado en entredicho, no quedando
claro a qué temperatura mantener a los pacientes ni a quién aplicar esta hipotermia.
Las últimas guías tampoco aclaran la situación, pero independientemente de ello, lo que sí queda
claro es que se debe llevar a cabo un control estricto de la temperatura, evitando la hipotermia, pero sin
superar los 36 ºC.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [50]
[3] RESUCITACIÓN CARDIOPULMONAR Y VALORACIÓN DEL PACIENTE POLITRAUMATIZADO
Figura 5. Algoritmo de soporte vital avanzado.
IX. PRONÓSTICO
Las lesiones hipóxico-isquémicas cerebrales son muy frecuentes tras la resucitación después de una
parada cardiaca. Estas lesiones son muy importantes, porque de las personas que son dadas de alta de la
Unidad de Cuidados Intensivos (UCI) y fallecen en el hospital dos tercios lo hacen debido a causas
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [51]
[3] RESUCITACIÓN CARDIOPULMONAR Y VALORACIÓN DEL PACIENTE POLITRAUMATIZADO
neurológicas. Por ello, cuando hablamos de pronóstico tras la PCR recuperada, lo más importante es
conocer la situación neurológica de los pacientes.
Para poder llevar a cabo una correcta valoración neurológica se debe esperar al menos 72 horas,
que el paciente se encuentre en situación de estabilidad, sin sedación y con normotermia.
En los últimos años se intenta conseguir test diagnósticos que puedan predecir de forma fiable la
evolución a muerte encefálica o estado vegetativo persistente de forma precoz, para poder facilitar la
actuación y decisión médica. No obstante, en el momento actual no existe ninguno que de forma individual
tenga tanta fiabilidad, por lo que se debe llevar a cabo una valoración global del paciente, aplicando varias
herramientas e individualizando según los hallazgos encontrados.
Existen hallazgos que indican mal pronóstico: en cuanto a la exploración física, la ausencia de
reflejo pupilar fotomotor y corneal bilateral a las 72 horas son predictores aceptables de mal pronóstico
neurológico. La ausencia de potenciales evocados somatosensoriales, así como las alteraciones en el
electroencefalograma, son útiles pasadas las primeras 24 horas para predecir mal pronóstico. Igualmente,
la elevación de biomarcadores como la proteína S-100 y la enolasa específica neuronal, también podrían
predecir mal pronóstico, puesto que se cree que su elevación se correlaciona con el grado de lesión
hipóxico-isquémica cerebral. No obstante, todavía son necesarios más estudios, así como establecer el
momento de medición y valores de corte. En cuanto a las pruebas de imagen tampoco son buenas
predictoras de forma precoz.
Por lo tanto, como hemos dicho previamente, la valoración se debe hacer de forma global y
aplicando las herramientas disponibles que nos ayudarán en la toma de decisiones.
X. VALORACIÓN DEL PACIENTE POLITRAUMATIZADO
INTRODUCCIÓN
La enfermedad traumática sigue siendo en la actualidad un grave problema, constituyendo una de
las principales causas de muerte en las primeras cuatro décadas de la vida en los países occidentales. Causa
un enorme impacto social, puesto que afecta a personas jóvenes, produciendo una gran pérdida de años
potenciales de vida, así como un gran impacto económico. Además de la tragedia que supone el
fallecimiento de personas jóvenes, supone también importantes costes sanitarios.
Por todo ello, además de políticas de prevención, se debe establecer un sistema de emergencias
que garantice una atención sistematizada y precoz al traumatismo grave o potencialmente grave.
TRAUMATISMO POTENCIALMENTE GRAVE
La enfermedad traumática varía según determinados factores, dando lugar a diferentes niveles de
gravedad. Estos factores son el mecanismo lesional, la propia respuesta fisiológica al traumatismo (que es
individual e impredecible), la comorbilidad asociada y el tiempo transcurrido desde la lesión hasta recibir
los cuidados necesarios. Todo ello va a condicionar el resultado final, por lo que es importante realizar una
atención sistematizada, por orden de prioridades y en el tiempo correcto. Igualmente, hay que saber que
los recursos sanitarios son limitados, debiéndose utilizar en función de las necesidades. Esto determina y
justifica la existencia de un método de clasificación de los pacientes, basado en las necesidades
terapéuticas y los recursos disponibles. Es lo que se conoce como triage.
Estos sistemas se caracterizan por ser fáciles de aprender y aplicar. Se pueden basar en diferentes
parámetros y hay que saber que en los pacientes con traumatismo se debe realizar tanto un triage
extrahospitalario como otro intrahospitalario, para intentar disminuir los errores del triage. Estos errores
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [52]
[3] RESUCITACIÓN CARDIOPULMONAR Y VALORACIÓN DEL PACIENTE POLITRAUMATIZADO
son el sobretriage (cuando damos a un paciente más prioridad de la que tiene) y el infratriage (cuando no
identificamos como críticos a pacientes que sí lo son).
Entre los pacientes con enfermedad traumática existen sujetos con lesiones graves que
comprometen su vida y requieren reanimación urgente e ingreso en la UCI. Igualmente, existe otro grupo
de pacientes con lesiones leves, que no requieren ingreso hospitalario y son dados de alta con seguridad.
No obstante, existe otro tipo de pacientes que no pueden ser clasificados claramente como graves, pero
que por mecanismo lesional, lesión anatómica o comorbilidades asociadas pueden presentar lesiones que
comprometan su vida. Son los pacientes potencialmente graves.
Ya desde la década de los noventa, en los diferentes centros de traumatología se identifica un
grupo de pacientes traumáticos que presentan lesiones ocultas graves, que inicialmente pasaban
desapercibidas puesto que aparentemente el paciente se encontraba estable. No obstante, estas lesiones
ocultas fueron responsables de un porcentaje de casos de mortalidad evitable. De ahí que sea tan
importante identificar a este tipo de pacientes y llevar a cabo una valoración integral y sistemática.
Una vez atendidos, si se descarta cualquier lesión amenazante, el paciente pasará a cargo del
especialista oportuno. No obstante, si durante la asistencia del paciente se diagnostica alguna lesión oculta
con compromiso vital, el paciente deberá ser ingresado en una UCI y ser manejado como paciente con
enfermedad traumática grave.
1. Criterios de pacientes potencialmente graves (Figura 6)
Figura 6.Detección de pacientes potencialmente graves.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [53]
[3] RESUCITACIÓN CARDIOPULMONAR Y VALORACIÓN DEL PACIENTE POLITRAUMATIZADO
Según criterios fisiológicos: tensión arterial sistólica inferior a 90 mm Hg, taquipnea, escala de
coma Glasgow inferior a 14 (forman parte del Trauma score revisado).
Según mecanismo lesional: atropello, precipitación, accidente de automóvil a alta velocidad o
con tiempo de extricación prolongado, accidente de moto o bicicleta a más de 30 Km/h, alta
deformidad del vehículo, deformidad del techo más de 45 cm, algún otro pasajero fallecido,
etc.
Según lesión anatómica: fractura de más de dos huesos largos, fractura pélvica, tórax inestable,
traumatismo penetrante, parálisis de extremidades, amputación proximal a muñeca/tobillo,
etc.
Según comorbilidades asociadas: edad superior a 55 años, pacientes anticoagulados, pacientes
cirróticos, embarazadas, pacientes con cardiopatía, neumopatía, etc.
2. Pruebas complementarias en el despistaje de lesión oculta
Normalmente en este tipo de pacientes en el reconocimiento primario no se van a detectar
lesiones que comprometan la vida. No obstante, en el reconocimiento secundario se puede detectar algún
síntoma o signo sugerente de lesión oculta. Ante estos signos las pruebas complementarias nos ayudarán
en su despistaje.
2.1. Datos de laboratorio
Analítica completa, con hemograma, bioquímica, gasometría, coagulación y pruebas cruzadas. Será
útil para valorar anemización progresiva, así como presencia de coagulopatía o hiperlactacidemia.
2.2. Pruebas de imagen
Con la radiografía de tórax se descartan lesiones que puedan comprometer la vida, como
neumotórax o hemotórax, así como valorar fracturas costales, ensanchamiento mediastínico o contusión
pulmonar.
Para valorar una posible fractura pélvica se realizará radiografía de pelvis anteroposterior. Se
realizará en pacientes con alta sospecha o en aquellos que estén inestables. En pacientes en los que se
sospeche lesión raquídea se debe realizar tomografía axial computarizada (TAC) (presenta una alta
sensibilidad y especificidad).
La TAC craneal está indicada ante traumatismos craneoencefálicos moderados o graves, o en
traumatismos craneales leves con pérdida de conocimiento, amnesia del episodio, focalidad neurológica,
náuseas, vómitos, cefalea intensa, otorragia, crisis, datos de intoxicación, cirugía neurológica previa o
pacientes anticoagulados.
La TAC torácica: presenta mayor sensibilidad que la radiografía para descartar lesiones
intratorácicas. Se debe realizar con contraste intravenoso si existe ensanchamiento mediastínico, para
descartar patología vascular, o cuando el mecanismo lesional consista en desaceleración brusca.
La TAC abdominopélvica: indicada si existe irritación peritoneal o cuando el mecanismo lesional
implique un golpe en la región abdominal y se sospeche lesión de víscera hueca o de los pedículos
vasculares. Es necesaria la administración de contraste intravenoso para detectar fugas vasculares.
2.3. Lesiones cervicales
Si se sospecha que pueda existir lesión de columna cervical se deberá realizar TAC de cuello para
descartarlo, con la radiografía de columna cervical que se debería realizar en 3 proyecciones no se puede
descartar con seguridad, por lo que no se recomienda su uso.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [54]
[3] RESUCITACIÓN CARDIOPULMONAR Y VALORACIÓN DEL PACIENTE POLITRAUMATIZADO
En aquellos pacientes con traumatismo facial o hematoma cervical asociado, así como estigmas de
lesión de cinturón de seguridad, estaría indicada la realización de estudio vascular cervical.
En caso de pacientes que se encuentran conscientes y que cumplan los criterios NEXUS (Tabla I) o
los criterios de las guías canadienses Canadian Cervical Spine Rule (Tabla II), se puede retirar el collarín
cervical sin realización de prueba de imagen.
Hay que recordar que durante la valoración del paciente, así como durante la realización de las
pruebas complementarias, se mantendrá el collarín cervical, así como la movilización en bloque del
paciente, hasta que se hayan descartado lesiones ocultas.
Tabla I.Criterios NEXUS.
Tabla II.Guías Canadian Cervical Spine Rule.
Si no existen factores de alto riesgo, se cumplen los de bajo riesgo y el paciente puede girar la
cabeza sin dolor cervical, no sería necesario la realización de estudios radiológicos adicionales.
2.4. Exploración clínica
En todo paciente potencialmente grave se realizará valoración inicial y exploración secundaria al
igual que en pacientes con traumatismo grave.
ATENCIÓN INICIAL AL PACIENTE CON TRAUMATISMO GRAVE
Para guiar la valoración y el tratamiento del paciente politraumatizado existen varios métodos,
siendo el incluido en las guías Advanced Trauma Life Support (ATLS) el más extendido en el ámbito
intrahospitalario. Estas guías establecen una sistemática de prioridades, disminuyendo así el número de
lesiones potencialmente graves que pasarían inadvertidas; su objetivo principal es tratar aquello que pone
en peligro la vida de forma más inmediata, aunque se carezca de diagnóstico claro.
Se describen tres fases: valoración primaria, resucitación inmediata y valoración secundaria; con
ello se establecerá un plan de cuidados definitivos.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [55]
[3] RESUCITACIÓN CARDIOPULMONAR Y VALORACIÓN DEL PACIENTE POLITRAUMATIZADO
Cabe destacar la importancia de la presencia de un líder que dirija los cuidados y una adecuada
comunicación entre el personal durante la atención inicial.
La movilización de los pacientes debe realizarse en bloque, de forma coordinada y dirigida. Debe
emplearse collarín cervical, camilla cuchara y aquel material necesario para la inmovilización en función de
las lesiones.
1. Valoración primaria
Siguiendo las pautas establecidas por el ATLS, la valoración inicial de un paciente politraumatizado
se basa en la realización meticulosa y sistemática del clásico ABCDE; para su realización no hay que emplear
más de 15 segundos. De este modo, se establecen una serie de prioridades, siendo primordiales las que
comprometen la vía aérea, seguido de la ventilación, control de foco hemorrágico y soporte circulatorio, y
las neurológicas.
1.1. Vía aérea y control de la columna cervical
Lo primordial es asegurar la permeabilidad de la vía aérea, ya que la obstrucción de la misma es la
principal causa de muerte prevenible en el traumatismo; debe indicarse aislamiento de la vía aérea según
los siguientes criterios (Tabla III).
Para valorar la vía aérea se puede comenzar con la realización de preguntas al paciente, seguido de
una inspección de la cavidad orofaríngea y del macizo facial, y vigilar datos de alarma (taquipnea, estridor,
uso de musculatura accesoria, cianosis, etc.).
En todo paciente politraumatizado debe suponerse que tiene lesión de la columna cervical hasta
que se demuestre lo contrario, por ello se colocará un collarín cervical. En caso de que esté indicada la
intubación, debe retirarse el collarín cervical y realizar una inmovilización cervical manual.
Tabla III. Criterios de intubación endotraqueal.
1.2. Ventilación
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [56]
[3] RESUCITACIÓN CARDIOPULMONAR Y VALORACIÓN DEL PACIENTE POLITRAUMATIZADO
Busca asegurar una correcta oxigenación y ventilación. Para evaluar la ventilación expondremos la
cara, el cuello y el tórax del paciente, abriremos la vía aérea y comprobaremos la respiración espontánea; si
es adecuada continuaremos con la exploración en busca de signos de inestabilidad ventilatoria: taquipnea o
bradipnea extremas, movimiento torácico paradójico, disociación toracoabdominal, tiraje, enfisema
subcutáneo, desviación traqueal, alteración del murmullo vesicular, desaturación, cianosis e ingurgitación
yugular. Las patologías que pueden producir un compromiso tanto ventilatorio como hemodinámico son:
hemotórax masivo, neumotórax abierto o a tensión y el tórax inestable.
1.3. Circulación y control de hemorragias
Una vez asegurada la vía aérea y la oxigenación/ventilación se debe evaluar la situación
hemodinámica. El shock refractario es la primera causa de muerte en las primeras horas de atención al
paciente con traumatismo grave. El shock hemorrágico es el más frecuente, pero se debe tener en cuenta
la posible existencia de otros tipos de shock: obstructivo (neumotórax o hemotórax a tensión,
taponamiento cardiaco), medular, cardiogénico, hipotermia grave o en relación con el consumo de
fármacos o tóxicos.
Se deben valorar la presencia de signos de shock: nivel de consciencia, coloración de la piel (palidez,
frialdad, sudoración), taquicardia, pulso filiforme, relleno capilar enlentecido.
El tratamiento del shock hemorrágico tiene dos componentes principales:
Control de la hemorragia. Se debe identificar el foco de sangrado teniendo en cuenta cinco
focos principales: hemorragia externa, tórax, abdomen, pelvis y fractura de huesos largos.
Resucitación mediante control de daños. Consistente en una resucitación hemostática,
hipotensión permisiva (salvo traumatismo craneoencefálico, lesión medular o embarazo),
limitación del uso de cristaloides y coloides, uso precoz de hemoderivados, lucha contra la
acidosis e hipotermia, cirugía con control de daños (control de la hemorragia con métodos
temporales, realizándose la cirugía definitiva de las lesiones a las 12-48 h, tras la estabilización
del paciente). Se tiende a un uso precoz de fármacos vasoactivos en caso de incapacidad de
mantener cifras de tensión arterial objetivo a pesar de una adecuada resucitación inicial. Para
la resucitación será necesaria la colocación de dos catéteres venosos periféricos cortos de gran
calibre (nº 14 y 16) o acceso venoso central de grueso calibre en situación de shock refractario.
1.4. Valoración neurológica
Evaluar el estado de consciencia (escala Glasgow), situación pupilar (tamaño, asimetría, reactividad)
y focalidad neurológica.
1.5. Exposición del paciente y prevención de hipotermia
El paciente debe ser expuesto por completo y la valoración de la lesiones debe realizarse durante el
menor tiempo posible para prevenir la hipotermia.
Mantener al paciente caliente empleando una adecuada ambientación de la sala, fluidos calientes y
mantas térmicas.
2. Otras consideraciones
Extracción de analíticas: hemograma, bioquímica, coagulación, gasometría con lactato, pruebas
cruzadas, tóxicos, test de embarazo.
Monitorización continua del ritmo cardiaco, pulsioximetría y frecuencia respiratoria, así como
medición de las cifras tensionales en intervalos cortos de tiempo por métodos no invasivos.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [57]
[3] RESUCITACIÓN CARDIOPULMONAR Y VALORACIÓN DEL PACIENTE POLITRAUMATIZADO
Sondaje vesical: permite valorar el ritmo de diuresis y la presencia de hematuria (sugiere lesión
abdominopélvica). No se procederá al sondaje vesical en caso de sospecha de lesión uretral
(sangre en meato, equimosis perineal).
Sondaje gástrico: disminuye la distensión gástrica y el riesgo de broncoaspiración. Se realizará
sondaje orogástrico en paciente con traumatismo craneal o facial (por posible lesión al nivel de
la base del cráneo).
Estudios radiológicos: se realizará radiografía de tórax y pelvis de forma portátil (esta última en
caso de sospecha de traumatismo pélvico o inestabilidad hemodinámica). En caso de shock
refractario está indicado la realización de Extended Focussed Assessment with Sonography for
Trauma, valora la presencia de líquido libre a nivel peritoneal, pleural o pericárdico,
permitiendo un manejo precoz de los pacientes.
Sedación y analgesia: los analgésicos más apropiados son los opioides, se debe emplear con
cuidado los agentes sedantes para no interferir en la valoración del paciente. Se puede valorar
el empleo de ketamina para procedimientos cortos y dolorosos, siempre que el paciente no
presente traumatismo craneoencefálico.
Reconocimiento secundario
Tras la valoración primaria y el inicio de la resucitación, se realiza la exploración secundaria
reevaluando de forma frecuente el ABCDE.
3.1. Anamnesis
Debe interrogarse sobre alergias, antecedentes personales, tratamiento habitual, cuándo fue la
última ingesta de alimentos y cómo se produjo el accidente (interrogando tanto por el mecanismo lesional
como por los mecanismos de seguridad).
3.2. Exploración física
Cabeza y cara: examinar en busca de laceraciones, contusiones o fracturas, datos que sugieran
fractura al nivel de la base craneal (ojos de mapache, otorragia, otorrea, rinorrea), valorar la
cavidad oral y la posible pérdida de piezas dentarias.
Cuello y columna cervical: se debe retirar el collarín cervical para su exploración, pero
manteniendo una inmovilización manual del mismo. Se realizará palpación, auscultación
carotídea, valorar la presencia de ingurgitación yugular, hematomas, correcta alineación
cervical, desviación traqueal, enfisema subcutáneo.
Tórax: inspección, palpación, auscultación cardiaca y pulmonar. Búsqueda de asimetría
ventilatoria, crepitación, percusión (hiperresonancia y timpanismo que indiquen la presencia de
hemotórax o neumotórax, respectivamente).
Abdomen: inspección en busca de contusiones, deformidades, heridas, palpación para valorar
irritación peritoneal, auscultación de posibles soplos y ruidos hidroaéreos; aunque una
exploración abdominal anodina no descarta patología abdominal.
Pelvis y periné: no realizar más de una exploración del anillo pélvico mediante compresión
lateral o anteroposterior de la pelvis. Se debe realizar tacto rectal en caso de sospecha de
lesión medular o de lesiones abdominopélvicas, valorando la presencia de tono, sangrado o
integridad de las paredes. En caso de realización de tacto vaginal también se debe valorar la
integridad de la pared y la presencia de sangrado.
Musculoesquelético: inspeccionar contusiones y deformidades, palpación en busca de dolor o
crepitación, movilidad anormal, explorar la sensibilidad y los pulsos para descartar afectación
vasculonerviosa (principalmente ante la presencia de fracturas).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [58]
[3] RESUCITACIÓN CARDIOPULMONAR Y VALORACIÓN DEL PACIENTE POLITRAUMATIZADO
Neurológico: exploración neurológica en busca de focalidad lo más completa posible.
Espalda: se realizará mediante movilización en bloque del paciente. Se buscará la presencia de
lesiones, hematomas, contusiones, crepitación, deformidades y dolor a la palpación de las
apófisis espinosas.
3.3. Exploración radiológica
En los últimos años la TAC body ha tomado una gran importancia como prueba diagnóstica en
pacientes con traumatismo grave.
El estudio radiológico se realizará de modo individualizado dependiendo de los hallazgos de la
valoración inicial y del reconocimiento secundario, así como teniendo en cuenta el mecanismo lesional.
BIBLIOGRAFÍA
2015 American Heart Association Guidelines Update for Cardiopulmonary Resuscitation and
Emergency Cardiovascular Care. Circulation. 2015;18(132).
American College of Surgeons, Committee on Trauma. Advanced trauma life support. 9th ed. Chicago:
American College of Surgeons; 2012.
European Resuscitation Council Guidelines for Resuscitation 2015. Resuscitation. 2015;95:1-80.
García Gigorro R, Alted López E. Manejo del trauma potencialmente grave. En: Guía para la atención al
trauma grave. 1ª ed. Madrid: Ergo; 2009. pp. 49-59.Guidelines for de management of acute cervical
spine and spinal cord injuries. Neurosurgery. 2013;72:3-279.
Marino P. El libro de la UCI. 3ª ed. España: Wolters Kluwer Health España, S.A.; 2008.
Martín Hernández H, López Messa JB, Pérez Vela JL, Molina Latorr R, Cárdenas Cruz A, Lesmes Serrano
A, et al. Manejo del síndrome posparada cardiaca. Med Intensiva. 2010;34(2):107-26.
Perales Rodríguez N, López Messa J, Ruano Marco M. Manual de soporte vital avanzado. 4ª ed.
Madrid: Masson; 2007.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [59]
[4] SHOCK
4. Shock
Guillermo Morales Varas.
Medicina Intensiva
Ángel Torralba Morón.
Medicina Interna
Tutor de residentes
Asesora: Zaira Molina Collado. Médica Adjunta de Medicina Intensiva
I. CONCEPTO
El shock es la expresión clínica del colapso circulatorio, que ocasiona un deterioro de la perfusión
tisular como resultado de la disminución o mala utilización del oxígeno celular. Esto conlleva a que se
desarrolle una acidosis metabólica, una respuesta inflamatoria sistémica y una coagulopatía, con el
consecuente fallo multiorgánico. Esta situación constituye una emergencia médica que requiere un
reconocimiento y abordaje precoz. Tradicionalmente se diferencian tres fases de shock: compensado,
descompensado e irreversible.
II. FISIOPATOLOGÍA
Dentro de la fisiología del sistema cardiovascular se deben considerar tres aspectos importantes. El
primero se refiere a la precarga, que es la relación existente entre la capacitancia de sangre, es decir, la
capacidad de contener sangre (especialmente en el sistema venoso), y la cantidad de volumen sanguíneo.
El segundo se refiere a la bomba cardiaca, que es la capacidad contráctil del corazón que lo hace funcionar
como tal. El tercero es la poscarga, que alude a la resistencia que opone el sistema vascular al flujo
sanguíneo (especialmente referido al sistema arterial). Estos tres factores van a ser los responsables de
definir un estado de shock y de compensación del mismo a través de los diferentes mecanismos de
regulación, tales como el sistema simpático, que actúa liberando sustancias simpaticomiméticas frente a
determinados estímulos que actúan en la contracción de los vasos sanguíneos y en la estimulación de la
función cardiaca. La interacción de este y de otros mecanismos de regulación va a determinar la
fisiopatología del cuadro de shock. Cuando estos mecanismos no funcionan correctamente se produce un
inadecuado transporte de oxígeno o mala utilización del mismo por parte de la célula. Esta, para su
adecuado funcionamiento, necesita energía, obteniéndola en esta situación por vía anaeróbica, con la
producción final de ácido láctico y la consecuente acidosis metabólica y disfunción celular.
Existen tres fases que determinan la gravedad del cuadro. Una primera fase compensada, en la que
se ponen en marcha los mecanismos compensadores y en la que los síntomas y signos son mínimos, como
nerviosismo, agitación, cifras de tensión arterial normales, taquicardia, frialdad cutánea (en el shock
distributivo la piel está caliente), enlentecimiento del relleno capilar y disminución de la diuresis. En esta
fase es primordial un abordaje precoz de la causa desencadenante y el comienzo de la resucitación. Una
segunda fase descompensada, en la que se objetiva inestabilidad hemodinámica y deterioro de la función
cardiovascular. La tensión arterial sistólica es menor de 90 mm Hg y/o hay un descenso de la tensión
arterial sistólica de más de 30 mm Hg, taquicardia, frialdad cutánea, diaforesis, confusión y obnubilación, y
la diuresis es menor de 0,5 ml/kg/h; analíticamente se objetiva un estado de acidosis metabólica. Por
último, una tercera fase irreversible, en la que los órganos sufren importantes daños. La piel presenta
livideces y cianosis, la hipotensión es grave, existe anuria y finalmente el paciente entra en coma.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [60]
[4] SHOCK
III. CLASIFICACIÓN DEL SHOCK
El shock constituye alrededor de un 30% de los ingresos en la unidad de cuidados intensivos (UCI).
Existen cuatro tipos de shock (Tabla I), cada uno de los cuales presenta un patrón hemodinámico
predominante (Tabla II). Los diferentes tipos de shock pueden solaparse; por ejemplo, ante un trauma
grave con hemorragia puede desarrollarse un shock hipovolémico así como uno distributivo a consecuencia
de la respuesta inflamatoria sistémica durante la resucitación. El shock séptico es la forma más frecuente
de shock, seguido del cardiogénico y del hipovolémico.
Tabla I.Tipos de shock y sus causas.
Tabla II.Patrones hemodinámicos propios de cada tipo de shock.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [61]
[4] SHOCK
IV. CLÍNICA Y APROXIMACIÓN DIAGNÓSTICA
Ante la presencia de shock, la evaluación diagnóstica se fundamenta en la historia clínica, analítica,
perfil hemodinámico y pruebas complementarias, donde la ecocardiografía se ha convertido en una
herramienta fundamental en la evaluación y manejo del paciente en estado de shock. La evaluación
diagnóstica debe realizarse mientras se comienzan las medidas de resucitación.
Aunque la presentación clínica varía dependiendo del tipo de shock y su causa, existen
características comunes y esenciales que requieren una valoración cuidadosa e inmediata.
El perfil hemodinámico es importante para establecer la caracterización del shock; la hipotensión
arterial (tensión arterial sistólica inferior a 90 mm Hg, tensión arterial media inferior a 65 mm Hg o una
caída de más de 40 mm Hg sobre la tensión arterial sistólica basal) es un dato casi constante. Sin embargo,
en la fase de shock compensado, la hipotensión puede estar ausente gracias a la existencia de mecanismos
compensatorios que producen una redistribución del flujo sanguíneo en un intento de preservar la función
de órganos vitales. En la fase descompensada la monitorización hemodinámica es fundamental; para ello
existe una serie de herramientas: el catéter de arteria pulmonar (catéter de Swan-Ganz), la termodilución
transpulmonar (Volume View, PICCO, etc.) y la ecocardiografía.
La historia clínica debe encaminarse a confirmar o descartar la presencia de alguna o varias de las
entidades siguientes: cardiopatía, infección, tromboembolismo pulmonar (TEP), ingesta de fármacos,
alergias, hemorragia o deshidratación, así como enfermedades previas, inmunosupresión o estados de
hipercoagulabilidad.
La exploración física debe valorar de manera general los siguientes datos: cifras de tensión arterial
(TA), pulso (simetría), relleno capilar, frecuencia cardiaca (FC) y respiratoria (FR), temperatura (hipertermia,
hipotermia, escalofríos), presión venosa yugular (dato esencial para clasificar el shock), auscultación
cardiaca (soplos, ritmo de galope) y pulmonar (crepitantes, afonesis o hipofonesis unilateral), extremidades
(edemas), abdomen (peritonismo, peristaltismo), piel (frialdad, humedad, púrpura, ectima) y sistema
genitourinario (úlceras, lesiones). Especialmente importantes son las tres “ventanas del cuerpo”: piel,
función renal y estado neurológico:
Piel: manifestaciones clínicas como livideces, frialdad y sudoración cutánea son secundarias a la
vasoconstricción periférica reactiva a la hipotensión para mantener la perfusión de los órganos
vitales (salvo en la fase inicial del shock distributivo o en las fases terminales de cualquier tipo
de shock por fracaso de los mecanismos compensatorios).
Función renal: oliguria (diuresis < 0,5 ml/kg/h).
Estado neurológico: alteración del nivel de consciencia, agitación, confusión, delirio,
obnubilación y finalmente coma.
Las pruebas complementarias deben incluir: hemograma (incluyendo pruebas cruzadas para
eventuales transfusiones), bioquímica completa con perfil hepático, cardiaco, ácido láctico y amilasa,
proteína C reactiva (PCR), procalcitonina (PCT), péptido natriurético cerebral tipo B (NT pro-BNP),
coagulación (con productos de degradación del fibrinógeno y dímeros D), orina con iones, gasometría
arterial basal (GAB), hemocultivos y urocultivo, electrocardiograma (ECG) y radiografía de tórax. Según el
tipo de shock y la etiología más probable, se deben realizar otras pruebas dirigidas tales como: punción
lumbar, pruebas de imagen como ecografía, tomografía computarizada (TC), gammagrafía o angio-TC
pulmonar, estudios toxicológicos y estudios microbiológicos. Entre las diversas pruebas complementarias es
prioritario otorgar un papel fundamental en la actualidad a la ecocardiografía, ya que constituye una
herramienta accesible que se puede realizar “a pie de cama” y que puede orientar el diagnóstico (derrame
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [62]
[4] SHOCK
pericárdico, función sistólica, alteraciones de la contractilidad segmentaria, hipertensión pulmonar, fracaso
del ventrículo derecho, etc.), así como la respuesta al tratamiento. En cuanto a los valores analíticos, la
gasometría arterial inicial es fundamental, especialmente para estratificar la gravedad del cuadro y orientar
las medidas de resucitación, así como la respuesta a la misma, dando un especial protagonismo a la acidosis
metabólica, generalmente láctica (debida al metabolismo anaerobio por la hipoxia tisular y a la disminución
del aclaramiento hepático y renal del ácido láctico).
V. ABORDAJE TERAPÉUTICO
1. Medidas generales
El adecuado y precoz soporte hemodinámico es primordial para evitar la disfunción orgánica, por lo
que es imprescindible mantener una monitorización hemodinámica y metabólica estrecha. Las actitudes
diagnósticas y terapéuticas deben gestarse al unísono y estar en consonancia con la gravedad de la
situación. Es importante descartar, al inicio, condiciones que amenazan la vida de forma inminente y que
son potencialmente abordables (hipoglucemia, neumotórax, taponamiento cardiaco, arritmias, etc.).
Siempre se debe valorar como primera actitud el ingreso en la UCI, tanto por la gravedad inicial
como por la mala respuesta hemodinámica a las medidas de resucitación inicial. Si bien dentro del manejo
del shock existen medidas específicas para cada subtipo, hay medidas generales que son comunes y que
deben realizarse de manera escalonada valorando el riesgo, el beneficio y atendiendo a la gravedad y
respuesta al tratamiento:
Monitorizar cifras de TA, FC, ECG y saturación de oxígeno (SO2).
Sondaje vesical: estricto control de la diuresis y del balance hídrico horario.
Acceso vascular: canalización de dos vías venosas de calibre grueso. Inicialmente son
preferibles las periféricas ya que permiten mayor velocidad de infusión, aunque puede
requerirse la inserción de un catéter central para la perfusión de fármacos vasoactivos y/o la
medición de la presión venosa central (PVC).
En caso de mala respuesta al tratamiento y en aras de caracterizar de manera adecuada el tipo
de shock, pueden requerirse medidas más invasivas de monitorización como el catéter de
Swan-Ganz o sistemas de termodilución transpulmonar. Este tipo de dispositivos son necesarios
para realizar una adecuada resucitación guiada por objetivos.
El objetivo inicial primordial del manejo del shock es restaurar la perfusión tisular. La resucitación
debe estar orientada a problemas y objetivos. Es importante definir los objetivos que se deben valorar
como respuesta al tratamiento:
Objetivo hemodinámico: es fundamental mantener una tensión arterial media (TAM) superior a
65 mm Hg para asegurar una adecuada presión de perfusión a los diferentes órganos. La
saturación de oxígeno venosa mixta (SvmO2) o venosa central (ScvO2) es una herramienta útil
para orientar el tratamiento. El catéter de Swan-Ganz, la termodilución transpulmonar y el
análisis del contorno de la onda de pulso informan sobre el gasto cardiaco, las resistencias
vasculares y la respuesta al volumen.
Objetivos metabólicos: la obtención de energía por vía anaerobia como consecuencia de la
hipoxia celular origina hiperlactacidemia y acidosis metabólica, por lo que su monitorización es
primordial.
Objetivos regionales: la tonometría gástrica, la capnografía sublingual y la espectrometría
cercana al infrarrojo (NIRS) son herramientas útiles pero poco prácticas que traducen la
perfusión tisular en los diferentes tejidos donde son realizadas.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [63]
[4] SHOCK
Objetivo hemostático: la coagulopatía que se produce durante el shock, secundaria a la
patología de base o durante la resucitación, ha adquirido una atención especial en los últimos
años y es un objetivo principal que se ha de evaluar durante el tratamiento. Para ello existe el
estudio de coagulación habitual así como distintas herramientas que valoran la coagulación de
forma detallada (durante todas las fases que implican la formación y consolidación del
coágulo); un ejemplo de ellas son las técnicas viscoelásticas, como la tromboelastografía
rotacional (ROTEM).
La resucitación establece las diferentes medidas dedicadas a mantener una adecuada oxigenación
de los tejidos. Los tres pilares fundamentales son: 1) la ventilación, que es la administración de oxígeno de
manera no invasiva o invasiva; 2) la resucitación con fluidos, y 3) los vasopresores.
1.1. Administración de oxígeno
Se realiza mediante la aplicación de oxigenoterapia externa con la fracción inspirada de oxígeno
(FiO2) necesaria para mantener una SO2 arterial por encima de 60-65 mm Hg. Se realiza de forma no
invasiva con los diferentes dispositivos existentes, los cuales se deben usar de forma escalonada y
progresiva. En caso de que sea necesario, como en las situaciones de insuficiencia respiratoria refractaria,
taquipnea grave o una medición en la escala de coma de Glasgow (ECG) inferior a 8 puntos que requiera
aislamiento de la vía aérea, se procederá a la intubación orotraqueal y conexión a ventilación mecánica.
1.2. Resucitación con fluidos
Debe realizarse de forma equilibrada y enérgica (también en el shock cardiogénico). En situaciones
especiales (shock hemorrágico) se recomienda el uso precoz de hemoderivados. Hay que tener en cuenta
los problemas derivados de la reposición con fluidos que pueden acontecer: congestión pulmonar,
coagulopatía dilucional, hipotermia, etc. Para ello es importante vigilar la respuesta, de manera invasiva,
con la monitorización hemodinámica, o de forma no invasiva mediante una elevación pasiva de las piernas
(valorando su impacto sobre la TAM y el gasto cardiaco). Debe tenerse en cuenta la acidosis metabólica
intensa (pH < 7,15) y la administración de bicarbonato, que ha de realizarse en los casos indicados (la
cantidad de bicarbonato que se debe administrar se calcula según la fórmula: déficit de HCO3- = 0,6 × peso
corporal (kg) × [HCO3- deseado - HCO3- real]). La rapidez de la reposición depende de la gravedad del
cuadro; en casos de acidosis metabólica intensa se proponen pautas de reposición rápidas (por ejemplo,
100 ml de bicarbonato 1 M en 20-30 minutos iv) con control gasométrico tras al menos 30 minutos desde el
fin de la perfusión.
1.3. Fármacos vasoactivos
Su uso requiere monitorizar la tensión arterial y cardiaca. Es conveniente que el pH esté corregido
ya que su acción no es plenamente efectiva con un valor de pH < 7,20-7,25.
Noradrenalina (NA). Es un precursor de la adrenalina. Agonista directo sobre receptores α1 y
α2 y β1, de forma que a dosis bajas producirá fundamentalmente estimulación cardiaca (β1) y a
dosis mayores producirá vasoconstricción periférica por efecto α. Rango de dosis: 0,03-5
μg/kg/min. Aumenta la contractilidad, el trabajo cardiaco y el volumen-minuto, así como la TA.
Es un potente vasoconstrictor que aumenta las resistencias vasculares sistémicas (RVS) en casi
todos los lechos vasculares, con disminución del flujo sanguíneo en riñón, hígado y músculo
esquelético, lo que la hace especialmente indicada en el shock distributivo, siendo, junto con la
dopamina, el fármaco vasopresor de primera elección en el shock séptico. Hay suficientes datos
que sugieren su uso de manera precoz en el shock cardiogénico. Sus principales efectos
secundarios son el aumento de la demanda miocárdica de oxígeno, el dolor anginoso por
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [64]
[4] SHOCK
isquemia, la hipertensión y la vasoconstricción excesiva. Su extravasación puede producir
necrosis tisular, por lo que se recomienda su administración a través de un acceso vascular
central.
Dopamina (DA). Amina precursora de la NA. Actúa de forma directa sobre los receptores
adrenérgicos y dopaminérgicos, o de forma indirecta favoreciendo la liberación de NA. En los
últimos años su uso se ha limitado dada la capacidad arritmogénica y su no superioridad a la
noradrenalina. Los efectos son dependientes de dosis:
2-5 μg/kg/min: acción sobre receptores dopaminérgicos (efecto dopa): aumento del
flujo renal (acción vasodilatadora renal) y esplácnico, aumento del filtrado glomerular,
estimulación de la diuresis y natriuresis. Puede aumentar la contractilidad cardiaca.
5-10 μg/kg/min: predomina el efecto β1 por lo que aumenta la contractilidad y el gasto
cardiaco (GC). Tiene el inconveniente de que la relación dosis-respuesta varía
notablemente según los individuos y es poco previsible.
10-20 μg/kg/min: efecto mixto.
20-40 μg/kg/min: predomina la acción vasoconstrictora (aumento de las RVS) por
estimulación de los receptores α1 y, por tanto, eleva la TA. Aumenta el riesgo de
arritmias. Se utiliza fundamentalmente como fármaco vasopresor en el shock séptico y
en el shock cardiogénico. Se puede emplear también en la insuficiencia cardiaca
congestiva en oligoanuria. Sus principales efectos secundarios son la aparición de
taquiarritmias, fundamentalmente de origen auricular, náuseas, vómitos y los
relacionados con la utilización de fármacos vasopresores (aumento de la demanda
miocárdica de oxígeno, dolor anginoso, isquemia miocárdica, hipertensión arterial,
vasoconstricción excesiva y necrosis tisular).
Dobutamina (DB). Es un análogo sintético del isoproterenol. Tiene selectividad sobre
receptores β, con efecto dominante sobre el corazón aumentando la contractilidad cardiaca. Su
efecto principal es el aumento del gasto cardiaco (GC), dependiente de dosis, permaneciendo la
TA generalmente invariable (ya que el descenso de la poscarga que origina, por estímulo
vasodilatador β2, se compensa con el aumento del GC). Se utiliza a dosis habituales de 2-20
μg/kg/min, aunque en pacientes que reciben tratamiento previo con β-bloqueantes pueden ser
necesarias dosis más altas. Es el fármaco de elección en el shock cardiogénico. Como efectos
secundarios puede producir un aumento o descenso excesivo de la TA, arritmias cardiacas,
reacciones por hipersensibilidad, dolor anginoso, dolor torácico inespecífico, palpitaciones,
ansiedad, temblores, náuseas y cefalea. Está contraindicada en la miocardiopatía hipertrófica.
Adrenalina (A). Es una catecolamina endógena derivada de la NA. Tiene efecto agonista sobre
receptores β1, β2 y α, produciendo tres efectos fundamentales: aumento del inotropismo,
aumento de las RVS y broncodilatación. Efecto β: 0,005-0,02 μg/kg/min; efecto α: > 0,03
μg/kg/min. Es el fármaco de primera elección en la resucitación cardiopulmonar (paro cardiaco
por taquicardia ventricular sin pulso, fibrilación ventricular, disociación electromecánica y
asistolia), en el shock anafiláctico (ver más adelante) y en las crisis asmáticas graves junto al
tratamiento con β2-agonistas. También está indicada en el shock séptico y cardiogénico
refractarios a DA, NA y DB. Entre sus efectos secundarios incluye el aumento del consumo
miocárdico de oxígeno, arritmias auriculares y ventriculares y acidosis láctica (por
vasoconstricción e isquemia regional)
Vasopresina (VA). La vasopresina es un potente vasoconstrictor que actúa mediante
mecanismos diferentes a los fármacos adrenérgicos, uniéndose a los receptores V1 y V2
situados a nivel vascular y renal respectivamente. El déficit de vasopresina puede existir en
pacientes con formas muy hiperdinámicas de shock distributivo, y la administración de una
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [65]
[4] SHOCK
dosis baja de la misma puede dar lugar a aumentos sustanciales de la TA. El estudio VASST
afirma que el uso de vasopresina a dosis bajas añadido a la noradrenalina en pacientes con
shock séptico produce un aumento en la supervivencia. La dosis utilizada no puede ser superior
a 0,04 UI/min
Inhibidores de la fosfodiesterasa III (milrinona, amrinona, enoximona). Son un grupo de
inodilatadores (inotropos positivos y vasodilatadores periféricos) que actúan inhibiendo una de
las isoenzimas de la fosfodiesterasa cardiaca (la F-III), lo que se traduce en un aumento del
AMPc (adenosina 3′,5′-monofosfato cíclico) intracelular. Este aumento del AMPc favorece la
entrada de calcio en la célula y la movilización del calcio intracelular, facilitando la contracción
muscular. Estos efectos conllevan un aumento del gasto cardiaco y una reducción de las
resistencias vasculares pulmonares y sistémicas sin aumento de la FC. Pueden ser útiles en
pacientes tratados recientemente con β-bloqueantes. Producen hipotensión y tienen una vida
media larga (4-6 horas), lo que dificulta enormemente su manejo en el shock.
Levosimendán. Es un fármaco de reciente introducción, con efecto inodilatador (inotropo
positivo y vasodilatador periférico). Se une a la troponina C cardiaca aumentando la
sensibilidad de los canales de calcio; también actúa como un vasodilatador por apertura de los
canales de potasio dependiente de trifosfato de adenosina (ATP) en el músculo liso vascular. Sin
embargo, este agente tiene una vida media de varios días, lo que limita su uso en la etapa
aguda del shock.
2. Medidas terapéuticas específicas para cada subtipo de shock
Además del tratamiento del estado de colapso circulatorio, es necesario iniciar un tratamiento
dirigido a la causa del shock.
2.1. Shock hipovolémico
Se produce por un descenso de la precarga provocado por una pérdida de volumen circulante
efectivo. Si esta pérdida es superior a un 40% del volumen intravascular total, el pronóstico suele ser fatal a
pesar de los esfuerzos terapéuticos de resucitación. La disminución de la precarga provoca una reducción
del GC, con un aumento de las RVS en un intento de mantener la perfusión de los órganos vitales.
Se debe sospechar ante la presencia de: a) signos de sangrado agudo, como hematemesis, melenas,
herida penetrante, hematoma retroperitoneal, etc.; b) situaciones que causen deshidratación, como
vómitos, diarrea, quemaduras extensas, poliuria, etc.; c) formación de un tercer espacio en pacientes
posquirúrgicos, cirróticos, obstrucciones intestinales, pancreatitis, etc. Se objetivará taquicardia,
hipotensión ortostática y disminución de la PVC, datos que permiten clasificar la gravedad del shock
hipovolémico y la estabilidad clínica (Tablas III y IV).
Tabla III.Clasificación del shock hipovolémico según la gravedad.
La mortalidad se relaciona con la duración de la hipoperfusión tisular, por lo que es fundamental
una rápida reposición de volumen. Para la reanimación volumétrica se canalizarán dos vías venosas
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [66]
[4] SHOCK
periféricas de gran calibre (lo que es más rápido que canalizar una vía venosa central) y se iniciará la
infusión de líquidos cristaloides y/o coloides, bien en bolo intravenoso o en perfusión a un ritmo de 0,6
ml/kg/min. Se continuará la reposición volumétrica con cristaloides si se consiguen los objetivos de
resucitación (Tabla V). Si no se consiguen, se añadirán coloides, productos sanguíneos si existe hemorragia
(no conviene superar un hematocrito del 35%) y/o fármacos vasoactivos. El ritmo de infusión de volumen,
hemoderivados y fármacos vasoactivos lo determinará la situación clínica y hemodinámica del paciente.
Tabla IV.Puntuación de estabilidad del shock hemorrágico.
Tabla V.Objetivos de la reposición en el shock hipovolémico.
Resulta imprescindible diagnosticar y tratar la causa de la hipovolemia, al mismo tiempo que se
mantienen las maniobras de resucitación.
2.2. Shock distributivo
Se produce como consecuencia de un descenso en las RVS, lo que genera un aumento de GC para
intentar compensar esta situación. La presión capilar pulmonar (PCP) puede estar normal o disminuida.
Dos tipos de shock distributivo son el shock séptico y el shock anafiláctico.
Shock séptico. (Ver Capítulo 34. “Bacteriemia y sepsis”).
Shock anafiláctico. Se inicia de forma aguda (minutos u horas) tras la exposición a un alérgeno,
posible o conocido, por parte del paciente. Frecuentemente cursa con afectación cutánea o de mucosas
(urticaria, prurito, eritema, edema de labios, lengua o úvula), junto con uno de los siguientes: compromiso
respiratorio (disnea, broncoespasmo, hipoxemia), hipotensión y/o síntomas gastrointestinales (dolor
abdominal, vómitos, diarrea). Hasta un 20% de los casos tienen presentación bifásica, con reaparición de
los síntomas, a pesar de un correcto tratamiento, durante las primeras 8-72 horas. Por ello se recomienda
un periodo de observación de al menos 8-10 horas.
El tratamiento consiste en las siguientes medidas:
Oxigenoterapia y monitorización.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [67]
[4] SHOCK
Valorar la necesidad de intubación orotraqueal si existe broncoespasmo grave o edema de
laringe que precisen aislamiento de la vía aérea o si la situación hemodinámica es
comprometida.
Aporte rápido de volumen intravenoso, 1.000-2.000 cc de suero salino fisiológico (SSF) al 0,9%.
Si no remonta la TA, administrar adrenalina intramuscular (ampollas de 1 mg/1 ml al 1:1.000; se
administra una dosis de 0,3-0,5 ml, preferiblemente en la cara anterolateral del muslo. Puede
repetirse la dosis cada 10-20 minutos hasta un máximo de 1,5 mg). Si no existe respuesta, debe
administrarse adrenalina intravenosa: diluir una ampolla de 1 mg en 10 ml de SSF, e infundir ml
a ml hasta un máximo de 5 ml (0,5 mg). Si continúa sin haber respuesta, iniciar una perfusión
continua: diluir tres ampollas de 1 mg en 250 cc de suero glucosado (SG) al 5%, e infundir a 5-50
ml/h (ajustar según la respuesta de la TA y la FC).
Pueden ser útiles los antihistamínicos (dexclorfeniramina 5 mg iv cada 6 horas), β2-agonistas
(salbutamol nebulizado) y corticoides (metilprednisolona 2 mg/kg/día iv).
Suspender la exposición a todo fármaco o sustancia sospechosa de ser causante de la reacción
anafiláctica.
2.3. Shock cardiogénico
Situación provocada por una disfunción cardiaca primaria. Cursa con las manifestaciones clínicas
del shock de cualquier etiología y con signos y síntomas de insuficiencia cardiaca izquierda (disnea,
crepitantes pulmonares, congestión pulmonar radiológica) y/o derecha (aumento de la presión venosa
yugular, reflujo hepatoyugular, edemas en miembros inferiores).
Su causa más frecuente es el infarto agudo de miocardio (IAM), habitualmente con fracaso
ventricular izquierdo, o las complicaciones mecánicas de este: insuficiencia mitral (IM) aguda, rotura del
tabique interventricular o rotura de la pared ventricular libre. Otras causas son la miocarditis, la
insuficiencia valvular aguda o la miocardiopatía hipertrófica.
Entre las pruebas complementarias diagnósticas fundamentales, debe considerarse la
ecocardiografía urgente, que permite estimar los dos únicos factores ecocardiográficos predictores
individuales de mortalidad: la fracción de eyección del ventrículo izquierdo (FEVI) y la gravedad de la IM, así
como valorar la presencia de complicaciones mecánicas. La vía transesofágica es más sensible para valorar
la IM y la rotura del septo interventricular. La coronariografía debe realizarse de manera urgente si se
sospecha un IAM como causa del shock y el paciente es candidato a revascularización percutánea o
quirúrgica. La monitorización hemodinámica a través de un catéter de Swan-Ganz puede aportar datos
valiosos para establecer el diagnóstico de shock cardiogénico.
El tratamiento de soporte hemodinámico no consigue disminuir la mortalidad del shock
cardiogénico si no se trata la causa desencadenante.
El tratamiento adecuado debe incluir:
Oxigenoterapia: con el objetivo de mantener una SO2 > 90%. Si esto no se logra, el siguiente
paso es iniciar la ventilación mecánica no invasiva, teniendo en cuenta que, por sus efectos
hemodinámicos, puede favorecer la hipotensión arterial. En caso de insuficiencia respiratoria
refractaria o agotamiento de los músculos respiratorios, está indicada la intubación orotraqueal
y la ventilación mecánica invasiva. Los bolos de morfina 2-5 mg por vía iv (puede causar
hipotensión y la absorción subcutánea estará disminuida por la hipoperfusión tisular) alivian la
disnea, mejoran la dinámica respiratoria y ayudan a disminuir la precarga ventricular.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [68]
[4] SHOCK
Volumen y diuréticos: debe administrarse volumen iv en casos de hipotensión sin datos de
congestión pulmonar (IAM del ventrículo derecho, taponamiento cardiaco), monitorizando la
PVC. Los diuréticos están indicados ante la presencia de congestión pulmonar, con el objetivo
de mantener una precarga óptima del ventrículo izquierdo (VI) y mantener una PCP entre 15 y
20 mm Hg (medida con un catéter arterial pulmonar).
Fármacos vasoactivos: la DB es el fármaco de elección en situaciones de bajo gasto cardiaco y
congestión pulmonar (shock cardiogénico) debido a su efecto inotrópico positivo. Por sus otros
mecanismos de acción puede generar taquicardia y vasodilatación y, por tanto, hipotensión
arterial. En estos casos, debe combinarse con fluidoterapia o fármacos vasopresores, que están
indicados cuando la combinación de inotrópicos y fluidoterapia no logra restablecer la
perfusión tisular. Frente a la NA, la dopamina ha demostrado mayor riesgo de complicaciones
(arritmias) y mortalidad, por lo que su uso deber evitarse y considerar la NA como fármaco
vasopresor de primera elección. El levosimendán actúa aumentado la sensibilidad de los
canales de calcio del miocito y, de este modo, aumentando el gasto cardiaco y reduciendo las
necesidades de NA para el mantenimiento de la perfusión periférica. Aunque los datos son
contradictorios, el estudio SURVIVE, que compara el levosimendán con la DA en el tratamiento
de la insuficiencia cardiaca aguda, no mostró diferencias en la mortalidad a 6 meses por todas
las causas. Podría plantearse el uso de levosimendán, añadido a la DA, cuando el tratamiento
con esta no logre remontar por sí mismo la situación de shock cardiogénico, y antes de pasar a
otras medidas terapéuticas.
Vasodilatadores: en el shock cardiogénico, su indicación principal es la IM aguda. Pueden
presentar utilidad cuando se ha logrado estabilizar la TA sistólica por encima de 90 mm Hg, y
siempre con precaución si no puede asegurarse una adecuada precarga del ventrículo derecho
(hipovolemia, IAM del ventrículo derecho, taponamiento cardiaco, pericarditis constrictiva,
etc.).
Balón de contrapulsación intraaórtico (BCIAo): se inserta por vía arterial femoral y se implanta
en la arteria aorta, distal a la arteria subclavia izquierda, inflándose y desinflándose
sincrónicamente con el ciclo cardiaco. Está indicado ante un shock cardiogénico secundario a
IAM que no revierte con medidas farmacológicas y como puente a la coronariografía, cirugía de
revascularización o reparación de complicaciones mecánicas. Produce una rápida estabilización
hemodinámica, aunque temporal, y no disminuye la mortalidad si no se trata rápidamente la
causa desencadenante. Está contraindicado en la insuficiencia aórtica.
Reperfusión coronaria: en situaciones de IAM, lograr la reperfusión de la arteria coronaria
responsable, independientemente del modo de conseguirlo, se asocia a menor mortalidad
intrahospitalaria. En los pacientes con shock cardiogénico secundario a IAM está indicada la
revascularización sin límite de tiempo tras iniciarse el cuadro clínico.
Dispositivos de asistencia circulatoria: su utilización ha aumentado en los últimos años y la
indicación se restringe a los casos de shock cardiogénico refractario a la terapia convencional
en los que se plantea la posibilidad de puente a trasplante, recuperación o decisión. El
dispositivo que por antonomasia constituye este grupo de asistencia es la membrana de
oxigenación extracorpórea venoarterial (ECMO v-a). Sin embargo, existe un sinnúmero de
asistencias ventriculares y dispositivos para soporte mecánico como el Impella®.
2.4. Shock obstructivo
Se debe a una obstrucción mecánica al flujo cardiaco, por lo que podría considerarse un tipo de
shock cardiogénico, pero con un patrón hemodinámico propio y cuyo manejo, además de las medidas de
soporte hemodinámico, debe dirigirse al tratamiento de la causa que lo produce. Entre las principales
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [69]
[4] SHOCK
causas destacan: tromboembolismo pulmonar agudo masivo, neumotórax a tensión y taponamiento
cardiaco.
Las medidas terapéuticas incluyen:
Mantener una adecuada perfusión periférica mediante el aporte de volumen iv y fármacos
vasoactivos y vasopresores.
Confirmar el origen obstructivo del cuadro mediante las pruebas complementarias necesarias,
según la sospecha clínica, generalmente radiografía o TC de tórax. La ecocardiografía urgente
está indicada ante sospecha de taponamiento cardiaco, imposibilidad para la realización de
otras pruebas de imagen, o cuando estas no sean concluyentes y persista la sospecha clínica de
shock obstructivo. Sin embargo, un ecocardiograma normal sí debe poner en duda la causa
obstructiva del shock, ya que es la técnica de elección para valorar la situación de
funcionamiento cardiaco.
Tratar la causa del shock: iniciar terapia anticoagulante ante un TEP. Debe considerarse el
tratamiento fibrinolítico ante situaciones de TEP con inestabilidad hemodinámica, pero
también ante pacientes hemodinámicamente estables con datos ecocardiográficos o analíticos
(elevación de BNP o troponina T) de sufrimiento de ventrículo derecho. Ante el taponamiento
cardiaco, deberá realizarse una pericardiocentesis urgente. Ante un neumotórax, debe
considerarse un drenaje torácico.
BIBLIOGRAFÍA
Cohn SM, Nathens AB, Moore FA, Rhee P, Puyana JC, Moore EE, et al., the StO2 in Trauma Patients
Trial Investigators. Tissue oxygen saturation predicts the development of organ dysfunction during
traumatic shock resuscitation. J Trauma. 2007;62:44-54.
Connelly CR, Schreiber MA. Endpoints in resuscitation. Curr Opin Crit Care. 2015;21(6):512-9.
Dellinger RP, Levy MM, Rhodes A, Annane D, Gerlach H, Opal SM, et al. Surviving sepsis campaign:
international guidelines for management of severe sepsis and septic shock: 2012. Crit Care Med.
2013;41(2):580-637.
Finfer SR, Vincent JL. Circulatory Shock. NEJM. 369;18:1726-34.
González E, Sáez I. En: Aguilar F, Bisbal O, Gómez C, de Lagarde M, Maestro G, Pérez-Jacoíste MA, et
al.; editores. Manual de diagnóstico y terapéutica médica. 7ª ed. Madrid: MSD; 2012. p. 43-51.
Hall JB, Schmidt GA, editores. Principles of Critical Care. 4ª ed. Chicago: McGraw Hill; 2015.
Marino PL. The ICU book. 4ª ed. Baltimore: William and Wilkins; 2013.
Moore FA, Davis J, Moore E, Cocanour C, West M, McIntyre R. Western Trauma Association (WTA)
critical decisions in trauma: management of adult blunt splenic trauma. J Trauma. 2008; 65:1007-11.
Moskovitz J, Levy Z, Slesinger T. Cardiogenic shock. Emerg Med Clin N Am. 2015;33:645-52.
Richards J, Wilcox S. Diagnosis and management of shock in the emergency department. Emerg Med
Pract. 2014;16:1-24.
Rippe JM, Irwin RS, editores. Intensive care medicine. 7ª ed. Boston: Little Brown and Company; 2011.
Task Force on Myocardial Revascularization of the European Society of Cardiology (ESC) and the
European Association for Cardio-Thoracic Surgery (EACTS); European Association for Percutaneous
Cardiovascular Interventions (EAPCI). ESC/EACTS guidelines on myocardial revascularization. Eur Heart
J. 2014;35:2541- 619.
The Task Force for the Diagnosis and Management of Acute Pulmonary Embolism of the European
Society of Cardiology (ESC) endorsed by the European Respiratory Society (ERS). Guidelines on the
diagnosis and management of acute pulmonary embolism. Eur Heart J. 2014;35:3033-80.
The Task Force for the Diagnosis and Treatment of Acute and Chronic Heart Failure 2012 of the
European Society of Cardiology. Developed in collaboration with the Heart Failure Association (HFA) of
the ESC. ESC guidelines for the diagnosis and treatment of acute and chronic heart failure 2012. Eur
Heart J. 2012;33:1787- 847.
Tisherman SA, Barie P, Bokhari F, Bonadies J, Daley B, Diebel L, et al. Clinical practice guideline:
endpoints of resuscitation. J Trauma. 2004;57(4):898-912.
Zilberstein J, McCurdy M, Winters M. Anaphylaxis. J Emerg Med. 2014;47:182-7.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [70]
[5] DOLOR Y SEDOANALGESIA
5. Dolor y sedoanalgesia
Inés Almagro Vidal.
Anestesiología, Reanimación y Terapéutica del Dolor
Jaime Laureiro Gonzalo.
Medicina Interna
Asesores:
Antonio J. Carrascosa Fernández.
Jefe de Sección de Anestesiología, Reanimación y Terapéutica del Dolor
Raquel Saldaña Casado.
Médica Adjunta de Anestesiología, Reanimación y Terapéutica del Dolor
I. CONCEPTO
El dolor es la causa más frecuente de consulta médica. Se define como una experiencia sensorial y
emocional desagradable asociada a un daño tisular real o potencial, o que el paciente describe en términos
de tal daño. Es siempre subjetivo, siendo una evaluación cognitiva, no cuantificable, que se produce en el
cerebro, estando influenciada por factores culturales, por el entorno, las creencias y las actitudes de cada
individuo. Cumple una función biológica que es la de informar y proteger del daño, pero también es una
emoción, siempre desagradable, abarcando en la definición a aquel dolor sin causa fisiopatológica, pero
que el paciente lo vive como tal.
II. CLASIFICACIÓN DEL DOLOR
1. SEGÚN LA DURACIÓN
1.1. Agudo
Es una respuesta fisiológica ocasionada por un daño, lesión o disfunción, destinada a evitar el
empeoramiento de la lesión y a poner en marcha la reparación de la misma. Los mecanismos subyacentes
son mejor conocidos, es de diagnóstico sencillo y suele tener un tratamiento médico o quirúrgico. No suele
prolongarse más de días o semanas.
1.2. Crónico
Se define por consenso como aquel dolor presente durante más de tres meses, de forma continua o
intermitente, más de cinco días por semana. No siempre responde a una causa fisiopatológica subyacente,
y no se asocia a una respuesta de alarma biológica como en el dolor agudo, siendo así considerado una
enfermedad en sí misma. Dentro del mismo diferenciamos entre dolor crónico oncológico (DCO) y dolor
crónico no oncológico (DCNO).
2. SEGÚN LA ETIOPATOGENIA
2.1. Nociceptivo
Es aquel que se produce por transducción fisiológica de un estímulo mecánico, térmico o químico a
través de un sistema nervioso intacto y sin lesiones. Puede ser de dos tipos:
Somático (piel, músculos y huesos): es sordo, fijo, continuo, se exacerba con el movimiento y
mejora con el reposo; suele estar bien localizado y ser congruente con la causa subyacente. Ejemplos son el
dolor óseo metastásico o el dolor articular por artrosis.
Visceral (órganos y vísceras profundas): en presencia de inflamación, la pleura, el pericardio y el
peritoneo dan lugar a un dolor importante, que varía de intensidad con el movimiento, y que se describe
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [71]
[5] DOLOR Y SEDOANALGESIA
como una puñalada, lancinante, cortante u opresivo. Suele estar mal localizado en el comienzo
(habitualmente referido) y puede asociar síntomas vegetativos. Cuando hay distensión de vísceras huecas
puede añadirse un componente cólico. Son ejemplos el dolor de la apendicitis, del cáncer de páncreas o el
cólico renoureteral.
2.2. Neuropático
Derivado de una actividad anormal neuronal producida por una lesión o enfermedad del propio
sistema somatosensorial, a nivel central o periférico.
Es difícil de describir (tirante, tipo “corriente eléctrica”, urente, etc.) y puede acompañarse de
síntomas negativos (hipoalgesia, hipoestesia) o síntomas positivos (parestesias, disestesias). También
puede aparecer en forma de dolor evocado, con signos como la alodinia (percepción dolorosa frente a un
estímulo no doloroso) o hiperalgesia (respuesta exagerada a un estímulo doloroso). Son ejemplos de dolor
neuropático la polineuropatía diabética, la neuralgia posherpética y el dolor de miembro fantasma. Dentro
de este tipo de dolor podemos distinguir:
Dolor del sistema nervioso periférico (SNP): en relación con lesiones o enfermedades de los nervios
periféricos, como compresión, irritación, enfermedades metabólicas o infecciosas. Se mezclan trastornos
sensitivos y motores diversos, y está caracterizado por tener una distribución neuroanatómica probable y
lógica que permite localizar el nervio, plexo o raíces afectados.
Dolor de origen central: por lesiones o enfermedades del sistema nervioso central (SNC), a nivel
medular o cerebral, afectando a regiones más extensas del cuerpo.
Dolor por desaferentización: puede aparecer tras una lesión del SNP o SNC, ocasionado por un
daño que puede originar en un espacio de tiempo variable un dolor persistente y rebelde a las terapias
convencionales.
2.3. Dolor psicógeno
No es posible identificar la naturaleza orgánica del mismo, posee características psicosomá- ticas y
asocia síntomas psiquiátricos que se pueden encuadrar dentro de la depresión, el dolor somatomorfo u
otros cuadros. Suele ser resistente a cualquier tratamiento farmacológico o quirúrgico que no tenga en
cuenta su naturaleza psiquiátrica, siendo un diagnóstico por exclusión.
2.4. Mixto
Es aquel que combina características de más de uno de los anteriores.
3. SEGÚN SU CURSO
3.1. Continuo
Persiste a lo largo de todo el día, aunque pueden existir variaciones en su intensidad.
3.2. Episódico
Es transitorio y aparece sobre un dolor basal controlado. Se considera dolor irruptivo si es
espontáneo, y dolor incidental si hay un estímulo que lo desencadene (toser, cambios posturales). Se
tratará de dolor de final de dosis si aparece antes de la siguiente toma de analgesia.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [72]
[5] DOLOR Y SEDOANALGESIA
III. APROXIMACIÓN DIAGNÓSTICA
La correcta identificación de las características y del tipo de dolor es el primer paso imprescindible
para el diseño de una estrategia de tratamiento que resulte eficaz. La valoración inicial del paciente cobra
una vital importancia, teniendo como pilares fundamentales:
Una anamnesis exhaustiva sobre la historia y evolución del dolor (Tabla I).
Una exploración física sistematizada.
Una adecuada utilización e interpretación de las pruebas complementarias necesarias.
Tabla I.Anamnesis del dolor.
Partiendo de la premisa de que el dolor es un síntoma subjetivo, y dada la importante influencia de
los factores sociales, culturales, religiosos, etc., debemos realizar una aproximación psicobiosocial a dicho
síntoma o enfermedad, con un abordaje integral y una entrevista centrada en el paciente. En los casos de
dolor crónico, el tratamiento no irá dirigido muchas veces a la erradicación del mismo, sino a mejorar la
calidad de vida del paciente, disminuir los síntomas, el estrés y la ansiedad, y a favorecer cambios cognitivo-
conductuales que permitan mecanismos de adaptación a la nueva situación.
1. MÉTODOS DE EVALUACIÓN DEL DOLOR
1.1. Escalas de valoración del dolor
Las más utilizadas son:
Escala categórica verbal: destaca por su sencillez y fácil comprensión. El paciente describe el
dolor desde su subjetividad como ausente, leve, moderado, intenso o insoportable.
Escala numérica verbal: igual de sencilla, valora el dolor según su intensidad en una escala del 0
(ausencia de dolor) al 10 (el dolor más terrible imaginable).
Escala visual analógica (EVA o VAS): el paciente señala sobre una regleta con los extremos 0
(ausencia de dolor) y 10 (dolor de máxima intensidad) cómo percibe su dolor.
1.2. Cuestionarios de valoración del dolor
Los más conocidos son McGill Pain Questionnaire (MPQ) y el cuestionario DN4 para la detección del
dolor neuropático.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [73]
[5] DOLOR Y SEDOANALGESIA
IV. TRATAMIENTO
1. PRINCIPIOS BÁSICOS
Tratar siempre el dolor y no minusvalorar su intensidad.
Explicar al paciente la naturaleza de su dolor, su causa o su mecanismo.
Individualizar el tratamiento según el tipo e intensidad del dolor.
Administrar los analgésicos de manera pautada. Dejar siempre analgesia de rescate. Evitar en lo
posible los términos “si dolor” o “si precisa”.
Explicar y prevenir los efectos secundarios del tratamiento.
Emplear la vía de administración oral siempre que sea posible.
Ajustar la vida media de los fármacos en función del tipo de dolor.
Pactar con el paciente objetivos realistas a la hora de controlar el dolor.
Detectar los posibles factores psicológicos y ambientales que pueden influir en la génesis y
percepción del dolor, ya que pueden dificultar el tratamiento (depresión, ganancias, litigio,
adicción).
Realizar un seguimiento continuo del paciente.
2. ESCALERA ANALGÉSICA DE LA ORGANIZACIÓN MUNDIAL DE LA SALUD Y ASCENSOR ANALGÉSICO (TABLA II)
Tabla II.Escalera analgésica de la Organización Mundial de la Salud.
Fue creada para el tratamiento del dolor oncológico, pero con el tiempo su uso se ha extendido al
tratamiento de otros tipos de dolor. Existen una serie de consejos útiles para el uso de la escalera
analgésica:
Concepto de “ascensor analgésico”: se debe comenzar a emplear el fármaco adecuado de
acuerdo con la intensidad del dolor, sin necesidad de escalonamiento. Recorrer los diferentes
escalones puede provocar un retraso en el control, favoreciendo la refractariedad al
tratamiento adecuado.
Coadyuvantes: son fármacos que se utilizan para el control de otros síntomas asociados o en
aquellos dolores que no responden a los analgésicos convencionales (como el dolor
neuropático). Se deben emplear según el tipo de dolor y los síntomas del paciente,
independientemente del escalón. Cuando se asciende de escalón se debe mantener el
coadyuvante.
3. FÁRMACOS
3.1. Analgésicos no opioides
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [74]
[5] DOLOR Y SEDOANALGESIA
Tienen similar acción farmacológica, eficacia clínica y perfil de efectos adversos, aunque presentan
en distinta proporción propiedades antipiréticas, antiinflamatorias y analgésicas. Están indicados
principalmente en el dolor nociceptivo de intensidad leve-moderada, con componente inflamatorio y para
el que no se haya recibido analgesia previamente. Tienen “techo analgésico”, lo que significa que hay una
dosis a partir de la cual si se incrementa la pauta se aumentan los efectos adversos sin mejoría de la
analgesia. Tienen acción sinérgica con los analgésicos opioides
Paracetamol: carece de actividad antiinflamatoria o toxicidad gastrointestinal por debajo de 2 g
al día. No tiene efecto antiagregante. Tiene un perfil de seguridad muy elevado aunque a dosis
altas puede ser hepatotóxico (ver Capítulo 89. “Intoxicaciones”).
Metamizol (Nolotil®): pirazolona con excelente acción antipirética y analgésica, leve acción
antiinflamatoria. Puede provocar agranulocitosis como reacción adversa idiosincrática, si bien
es muy infrecuente.
Antiinflamatorios no esteroideos (AINE): tienen alta potencia antiinflamatoria. Presentan
numerosos efectos secundarios a nivel gastrointestinal y renal, lo cual limita su empleo en
población anciana, nefrópata, cardiópata, etc. No se deben asociar dos AINE en el mismo
tratamiento (Tabla III).
Tabla III.Fármacos antiinflamatorios no esteroideos más utilizados.
Inhibidores selectivos de la enzima COX-2 (COXIB: etoricoxib y celecoxib): son un subgrupo de
AINE que presentan menos efectos adversos a nivel gastrointestinal y pueden ser de elección
en pacientes con alto riesgo de presentar este tipo de complicación (mayores de 65 años, uso
concomitante de anticoagulantes o corticoides, historia de úlcera gastrointestinal previa). Se
han relacionado, junto con otros AINE no selectivos, con un aumento del riesgo cardiovascular.
La recomendación general es evitar su empleo en pacientes con patología cardiovascular grave
y usar con precaución en pacientes con antecedentes de disfunción de ventrículo izquierdo,
edema, hipertensión y otros factores de riesgo cardiovascular.
Agentes tópicos (ibuprofeno y diclofenaco): se dispensan en gel, crema o spray, y pueden ser
utilizados como parte del tratamiento de algunos tipos de dolor musculoesquelético, siendo
más eficaces en el tratamiento del dolor localizado o en lesiones musculares agudas. No existe
evidencia sobre la eficacia de estos agentes para la lumbalgia aguda o crónica.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [75]
[5] DOLOR Y SEDOANALGESIA
3.2. Opioides y derivados
Actúan principalmente sobre el dolor nociceptivo y en menor proporción sobre el dolor
neuropático. Estos fármacos se unen a los receptores opioides en el SNC para interferir en la activación de
la transmisión y la modulación de los impulsos y la percepción del dolor.
Consideraciones para su uso:
Atendiendo a su potencia analgésica se clasifican en opioides menores y mayores.
Se debe iniciar su administración cuando los analgésicos no opioides hayan fracasado, o
directamente deben pautarse cuando se trate de un dolor moderado-grave.
Usualmente se comienza con opioides menores y se progresa a opioides mayores en
caso de ausencia de respuesta, pero se pueden utilizar estos últimos desde el inicio a
dosis bajas en dolores graves.
No se recomienda la utilización simultánea de diferentes tipos de opioides.
Se pueden asociar opioides menores con otros analgésicos para conseguir mayor
potencia analgésica con menores efectos secundarios, ya que nos permite disminuir la
dosis de los fármacos empleados.
Se deben conocer los efectos adversos, informar a los pacientes de su aparición y
prevenirlos.
Deben tenerse en cuenta los efectos de tolerancia, adicción y dependencia derivados
de su uso.
Se identifican los pacientes que reciben terapia de mantenimiento con opioides como
aquellos que toman al menos 60 mg de morfina oral, 25 μg/h de fentanilo
transdérmico, 30 mg de oxicodona, 8 mg de hidromorfona o una dosis equianalgésica
de otro opioide al día durante una semana o más.
En pacientes en tratamiento con opioides mayores que presentan tolerancia se debe
plantear la rotación de opioide.
Efectos adversos:
Náuseas y vómitos: son muy frecuentes, en especial al inicio del tratamiento, y tienen
rápida tolerancia. Se deben pautar antieméticos de modo preventivo los primeros tres
a cinco días.
Estreñimiento: es el efecto secundario más limitante, siempre ocurre y persiste durante
todo el tratamiento con opioides. Se debe igualmente prevenir con laxantes cuando es
un problema. Existen preparados farmacológicos que combinan la formulación opioide
con un antagonista (naloxona) a dosis bajas, para intentar minimizar este efecto
secundario.
Somnolencia: puede aparecer en algunos casos en los primeros días de tratamiento y
suele ser transitoria. En caso de persistir, se puede plantear la rotación de opioide o
intentar disminuir la dosis.
Sequedad de boca: suele acompañar durante todo el tratamiento, se trata con medidas
físicas y con fármacos que favorecen la salivación.
Otros: retención urinaria, íleo paralítico, sudoración, prurito, etc.
Depresión respiratoria: poco frecuente pero muy grave. Debe tratarse con naloxona y
valorar rotación de opioide, así como ajustar la medicación según las características del
paciente.
Neurotoxicidad inducida por opioide (NIO): abarca alteraciones cognitivas, confusión,
alucinaciones, mioclonías, convulsiones e hiperalgesia. Se produce especialmente con
dosis altas de opioides y tratamientos prolongados, en pacientes con alteraciones
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [76]
[5] DOLOR Y SEDOANALGESIA
cognitivas o delirium previos, deshidratación, insuficiencia renal, empleo de
psicofármacos y edad avanzada. Su tratamiento consiste en hidratación y disminución
de la dosis de opioide; en caso de mal control del dolor, valorar rotación de opioide.
Opioides menores (Tabla IV): pueden emplearse como preparados de liberación retardada o en
combinación con analgésicos de primer escalón. Tienen techo analgésico.
Codeína: tiene potencia analgésica media, actividad antitusígena, antidiarreica y menor
efecto depresor sobre el SNC. Se utiliza en dolor moderadamente intenso, solo o
asociado a AINE o paracetamol para potenciar su efecto. Actualmente está más en
desuso debido a la comercialización de fármacos con mejor perfil analgésico y menores
efectos secundarios.
Dihidrocodeína: sus efectos son similares a la codeína, pero se emplea en forma de
liberación retardada.
Tramadol: además de su afinidad por receptores opioides, inhibe la recaptación de
noradrenalina y serotonina, por lo que es el opioide con mejor perfil para el
tratamiento del dolor neuropático. Su acción no es completamente revertida por la
naloxona. Prácticamente no produce depresión del SNC ni dependencia. Tiene
múltiples vías de administración. Se desaconseja su asociación con inhibidores de la
recaptación de la serotonina (ISRS) por el riesgo de síndrome serotoninérgico.
Tabla IV.Opioides menores
Opioides mayores: indicados para el dolor intenso de carácter nociceptivo, oncológico o no
oncológico, que no responde a analgesia convencional u opioides menores y, a dosis altas, para
el dolor neuropático. No se recomienda el uso concomitante con opioides menores; estos se
deben suspender previamente. Carecen de techo analgésico.
Morfina: fármaco gold standard del tratamiento del dolor moderado-severo de
cualquier origen, del dolor oncológico y del posquirúrgico, entre otros. Disponible para
administración intravenosa (iv), intramuscular (im), subcutánea (sc) y vía rectal, si bien
la vía oral (vo) es de elección en tratamientos prolongados y en pacientes oncológicos.
Oral de liberación inmediata: se utiliza al inicio para titular dosis y como
tratamiento de rescate. Se pauta cada 4 horas. Existen preparados en
comprimidos (Sevredol® 10 y 20 mg) o en solución oral (Oramorph solución® 2,
6 y 20 mg/ml; Oramorph viales® unidosis 10-30 mg/5 ml). Recientemente se ha
comercializado una formulación en pastillas efervescentes (Dolq® comprimidos
efervescentes, 20 mg).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [77]
[5] DOLOR Y SEDOANALGESIA
Oral de liberación lenta: para el tratamiento de mantenimiento. Se administra
cada 12 horas (MST continus® 5, 10, 15, 30, 60, 100, 200 mg) o cada 24 horas
(MST unicontinus® 30, 60, 90, 120, 150, 200 mg). Los comprimidos deben
ingerirse enteros y sin masticar. Cuando esto no sea posible (disfagia, sonda
nasogástrica, etc.), la presentación en cápsulas (Zomorph® cáps. retard 10 y 30
mg) permite abrirlas y mezclar los microgránulos con la comida.
Parenteral (sc, im o iv), epidural e intradural: cloruro mórfico inyectable en
ampollas al 1% y 2%.
Para iniciar el tratamiento en un paciente que nunca ha recibido morfina y titular la
dosis necesaria, empezaremos con morfina de acción inmediata a demanda. Tras 24 horas
se evalúa la dosis total recibida y se pauta esta dosis en presentaciones de liberación
retardada. Mantendremos la morfina de acción inmediata como analgesia de rescate (1/6-
1/10 de la dosis total diaria), que se puede administrar hasta cada media hora si fuera
necesario. Al día siguiente, añadiremos la dosis de rescate usada al total de la de liberación
prolongada pautada. Si la analgesia es insuficiente, y no se puede calcular la dosis requerida
por el método previo, se aumentará la dosis un 30-50% cada 24 horas hasta el control del
dolor.
En el paso de la administración oral a la parenteral y viceversa usaremos la
siguiente equivalencia: 1 vo = 1/2 sc = 1/3 iv = 1 vía rectal.
Puede darse la situación en la que debamos realizar la rotación a un opioide
diferente debido a mala tolerancia, efectos adversos, ineficacia, etc. Se deberán usar dosis
equivalentes consultando las tablas de conversión (Tabla V) y sin olvidar dejar siempre
medicación de rescate.
Tabla V.Equivalencia de opioides.
Meperidina o petidina (Dolantina® 100 mg/2 ml e hidrocloruro de petidina GES 50
mg/ml): agonista puro de receptores μ y ĸ, con propiedades semejantes a la morfina,
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [78]
[5] DOLOR Y SEDOANALGESIA
aunque menos potente, de acción más rápida y duración más corta. Presenta efectos
anticolinérgicos. Está indicado en el dolor intenso (cólico biliar, genitourinario,
gastrointestinal), postoperatorio y, en general, en el manejo del dolor muy agudo. Se
metaboliza en el hígado a normeperidina, metabolito con la mitad de potencia como
analgésico, pero con el doble como estimulante del SNC, por lo que le son atribuidos
algunos efectos tóxicos neurológicos (convulsiones, agitación, irritabilidad, nerviosismo,
temblores). No se recomiendan tratamientos prolongados en el tiempo. Disminuye el
umbral convulsivo y tiene efecto adictivo.
Fentanilo: comparte afinidad por los receptores μ opioides, produciendo analgesia y
sedación, principalmente a nivel del SNC. Sus indicaciones abarcan la analgesia
intraoperatoria y el tratamiento del dolor crónico oncológico y no oncológico, así como
del dolor irruptivo.
Presentación parenteral (Fentanest® 3 ml por ampolla, 0,05 mg/ml):
ampliamente utilizado en anestesiología y en la Unidad de Cuidados Intensivos
(UCI).
Presentación transdérmica: parches que liberan fentanilo a una velocidad
constante durante aproximadamente 72 horas (dosis variable según la
preparación: 12, 25, 50, 75, 100 μg/h en Durogesic®, Fendivia®, Matrifen®,
Fentanilo EFG), aunque algunos pacientes pueden requerir recambio del parche
a las 48 horas. Tarda entre 10-15 horas en alcanzar el nivel analgésico
adecuado. Están indicados en dolor crónico relativamente estable, pacientes
con intolerancia a la vía oral o poca adherencia a la medicación oral.
Desventajas de su uso son la absorción errática según la localización anatómica,
la necesidad de ausencia de vello y las alteraciones en la absorción y
disponibilidad con cambios de temperatura, fiebre, rasurado de la zona, etc.
Presentación transmucosa oral (Actiq® 200-400-600-800-1.200-1.600 μg,
Abstral® 100-200-300-400-600-800 μg, Effentora® 100-200-400-600-800 μg):
muy eficaz para el manejo del dolor episódico de origen oncológico, por su fácil
empleo y rapidez de acción (tarda minutos en hacer efecto). Se recomienda
empezar por la dosis más baja e ir ajustando según las necesidades del
paciente.
Presentación transmucosa nasal: indicada para tratamiento del dolor irruptivo
de origen oncológico. Se emplea con pulverizador y, dependiendo del envase,
se darán de 100 a 400 μg (Pecfent® 100-400 μg, Instanyl® 50-200 μg). Se
recomienda igualmente empezar por la dosis más baja e ir ajustando según el
paciente.
Oxicodona: agonista puro opioide con afinidad por receptores μ y ĸ. Importante
potencia analgésica y alta biodisponibilidad oral (60-87%). Mejora también el dolor
neuropático, pero se considera tratamiento de segunda línea del mismo. Se pueden
encontrar presentaciones de liberación prolongada (OxyContin® y Oxicodona EFG 5, 10,
20, 40 y 80 mg), que se pautan cada 12 horas, y una presentación de liberación
inmediata que permite usarla como rescate (Oxy- Norm® cápsulas 5, 10, 20 mg,
ampolla 10 mg/ml y solución oral 10 mg/ml). Existe una presentación oral de uso cada
vez más extendido que combina oxicodona con naloxona y que se caracteriza por
disminuir la incidencia de efectos secundarios periféricos, principalmente el
estreñimiento (Targin® oxicodona/naloxona 5/2,5 mg, 10/5 mg, 20/10 mg y 40/20 mg).
La dosis diaria máxima es 160 mg de hidrocloruro de oxicodona y 80 mg de naloxona.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [79]
[5] DOLOR Y SEDOANALGESIA
Hidromorfona: agonista de los receptores μ, con una afinidad más baja por los
receptores ĸ. Es cinco veces más potente que la morfina. Se comercializa en
comprimidos de liberación prolongada (Jurnista® 4, 8, 16 y 32 mg, a liberar en 24
horas).
Buprenorfina: agonista-antagonista opiáceo con afinidad por los receptores μ y ĸ. Se
emplea en dolor moderado a intenso. A dosis bajas consigue la mejor relación dosis/
eficacia; a dosis elevadas el efecto puede estar limitado por su papel antagónico sobre
los receptores opiáceos. Causa menor depresión respiratoria que otros opioides, pero
su respuesta a la naloxona es menor. Disponible en presentación transdérmica
(Transtec® 35, 52,5 y 70 μg/h), comprimidos orales (Buprex® 0,2 mg; Suboxone®
comprimidos sublinguales, de 2 mg con 0,5 mg de naloxona y de 8 mg con 2 mg de
naloxona) y por vía intravenosa (Buprex® viales de solución 0,3 mg en 1 ml).
Metadona: agonista de los receptores μ, con potencia ligeramente superior a la
morfina, mayor duración de acción y menor efecto euforizante. Disponible por vía oral
(Eptadone® solución oral 5 mg/ml, 20 mg unidosis o 100 mg unidosis; Metasedin®
comprimidos 5, 30 y 40 mg) e intravenosa (Metasedin® 10 mg/ml). De elección en la
desintoxicación y mantenimiento de usuarios de drogas por vía parenteral (UDVP). Su
empleo en el tratamiento del dolor crónico debe ser realizado por expertos, debido a
su farmacocinética y potenciales efectos adversos.
Tapentadol: analgésico de acción central con un mecanismo de acción dual, como
agonista del receptor opioide μ e inhibidor de la recaptación de noradrenalina, siendo
útil para el dolor tanto nociceptivo como neuropático, con menores efectos adversos y
mejor tolerancia. Posee menor tasa de interacciones con otros fármacos al no
metabolizarse por la vía del citocromo P450, y no está contraindicado en pacientes con
insuficiencia hepática o renal leve-moderada. Se recomienda iniciar a dosis de 50 mg
cada 12 horas, e ir ascendiendo dosis cada tres días, según tolerancia, con dosis
máximas de 250 mg cada 12 horas. Debe evitarse su uso conjunto con inhibidores de la
monoamino-oxidasa (incremento de la señal noradrenérgica y riesgo de crisis
hipertensivas) e ISRS (riesgo de síndrome serotoninérgico). El tapentadol muestra
menor afinidad por el receptor μ que otros agonistas opioides fuertes, lo que debe
tenerse en cuenta a la hora de rotar opioides para evitar la infradosificación. Solo existe
por vía oral (Palexia® 50, 75, 100 mg; Palexia retard® 25, 50, 100, 150, 200, 250 mg;
Yantil® 50, 75 y 100 mg; Yantil retard® 25, 50, 100, 150, 200, 250 mg).
3.3. Coadyuvantes
Son fármacos que se utilizan para aliviar el dolor, solos o asociados con analgésicos, que tratan
síntomas que acompañan al dolor (como el insomnio, la ansiedad y la depresión) o que se utilizan para
reducir los efectos adversos de los analgésicos. En el caso del dolor neuropático, son la primera línea de
tratamiento (Figura 1).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [80]
[5] DOLOR Y SEDOANALGESIA
Figura 1.Algoritmo de tratamiento del dolor neuropático.
Antidepresivos (Tabla VI): la coexistencia de depresión y dolor es muy prevalente, por lo que
en ocasiones se necesita asociar un antidepresivo a los analgésicos. Son útiles para el
tratamiento del dolor incluso en pacientes no deprimidos, a dosis diferentes.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [81]
[5] DOLOR Y SEDOANALGESIA
Tabla VI.Antidepresivos que más frecuentemente se emplean como coadyuvantes.
Antidepresivos tricíclicos: son los coadyuvantes más utilizados en el manejo del dolor
crónico, en especial si es neuropático. El efecto analgésico ocurre a dosis más bajas que
las antidepresivas. Como efectos secundarios, presentan los derivados de su acción
anticolinérgica muscarínica (estreñimiento, somnolencia, sequedad de boca,
alucinaciones y retención de orina), hipotensión ortostática, aumento de presión
intracraneal y arritmias. Hay que tener especial cuidado en pacientes cardiópatas y
ancianos. El fármaco de elección suele ser amitriptilina, a dosis de 25-50 mg/día.
Inhibidores de la recaptación de serotonina y noradrenalina (IRSN): venlafaxina es
efectiva a dosis de 150 mg/día (indicación compasiva); duloxetina tiene utilidad en el
dolor relacionado con la polineuropatía diabética. Ambos son mejor tolerados en
pacientes ancianos o con polifarmacia, aunque con efectos secundarios de tipo
anticolinérgico como los descritos en los tricíclicos.
Antiepilépticos (Tabla VII): indicados para el dolor neuropático, se distinguen dos grupos:
Tabla VII.Anticomiciales que más frecuentemente se emplean como coadyuvantes.
Antiepilépticos clásicos: carbamazepina es el fármaco de elección en la neuralgia del
trigémino y, por paralelismo, en otros dolores similares. Los efectos secundarios son
sedación, náuseas, diplopía, vértigo y ataxia, trastornos hepáticos, hiponatremia,
exantema cutáneo o agranulocitosis.
Nuevos antiepilépticos: oxcarbazepina es un análogo de carbamazepina, más cómodo y
mejor tolerado, con las mismas indicaciones y efectos secundarios más leves, salvo la
hiponatremia, que es más frecuente. Gabapentina es el fármaco más estudiado para el
tratamiento del dolor neuropático. Pregabalina tiene indicaciones más amplias en dolor
neuropático y central, con una relación lineal efecto/dosis. Ninguno de los dos sufre
interacciones relevantes con otros medicamentos, al no tener metabolismo hepático ni
unión a proteínas, y producen efectos secundarios similares (mareo, somnolencia,
edema, sequedad de boca, cefalea, aumento de peso y alteraciones del
comportamiento).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [82]
[5] DOLOR Y SEDOANALGESIA
Corticoides: se emplean por su potente efecto antiinflamatorio. Son muy útiles en metástasis
óseas, compresión medular y nerviosa, hipertensión intracraneal y obstrucción intestinal.
Además, aumentan el apetito y la sensación de bienestar y tienen acción antiemética.
Dexametasona (Fortecortin®) es el corticoide de elección por su potencia, acción prolongada y
escaso efecto mineralocorticoide (para dosis equivalentes de otros corticoides, ver Anexo VI.
“Inmunosupresión y sus complicaciones”).
Neurolépticos: indicados en el dolor neuropático, agitación, delirium, náuseas, vómitos y
síntomas psicóticos. Los más empleados son haloperidol, levomepromazina y clorpromazina.
Benzodiazepinas y miorrelajantes: utilizados en tratamientos breves o casos que asocian
insomnio o ansiedad. No han demostrado eficacia en el tratamiento del dolor crónico e incluso
pueden suponer un riesgo adicional en pacientes ancianos o polimedicados.
Anestésicos locales: provocan un bloqueo reversible de los canales de sodio que evita la
despolarización neuronal y la transmisión del impulso nervioso hacia los centros superiores. Los
parches de lidocaína (Versatis®) son apósitos medicamentosos adhesivos, recortables y
adaptables a la zona anatómica, para el alivio sintomático del dolor neuropático localizado,
siendo el tratamiento de la neuropatía posherpética su principal indicación. Su modo de
empleo es adherirlos a la zona limpia y seca, sin disrupciones cutáneas ni signos de flogosis, con
un máximo de tres parches al mismo tiempo. Se ponen una vez al día durante un total de 12
horas, dejando las otras 12 horas de descanso.
Otros: hay apósitos medicamentosos adhesivos de capsaicina (Qutenza® 179 mg, Hansaterm®)
y cremas tópicas (Capsicin® o Sensedol®) indicados en el dolor moderado-grave en la
neuropatía diabética que no haya respondido a otros tratamientos, si bien la quemazón y los
efectos cutáneos locales pueden limitar su uso.
Toxina botulínica: puede estar indicada en casos de dolor nociceptivo o neuropático localizado.
4. TÉCNICAS COADYUVANTES
En el último escalón se situarían las Unidades de Dolor Crónico. Son unidades multidisciplinares que
cuentan con profesionales de la salud de diferentes especialidades (anestesiólogos, neurólogos, psicólogos,
rehabilitadores y fisioterapeutas) con el objetivo de realizar un tratamiento multimodal del dolor desde la
farmacología, pasando por cambios cognitivo-conductuales, acupuntura y medicina rehabilitadora, hasta
técnicas intervencionistas. Es fundamental el correcto cribado de aquellos pacientes que puedan
beneficiarse de este tipo de manejo. A continuación, resumimos los criterios de derivación a centros o
unidades especializadas en dolor recogidas en el último documento de consenso de Atención Primaria:
Pacientes donde no esté aconsejado el empleo de analgésicos por sus enfermedades
concomitantes, con el objetivo de valorar otras alternativas (técnicas invasivas).
Pacientes con alergias a gran cantidad de fármacos, incluidos analgésicos.
Antecedentes de toxicomanía con dolor intenso no controlable.
Uso de dosis superiores a 90 mg/día de morfina o dosis equianalgésicas de otros opioides
mayores, con dolor de difícil control.
Dolor neuropático, si no se controla con fármacos de 1ª y 2ª línea.
Si al cabo de 6 meses de tratamiento adecuado con un plan integral la intensidad del dolor y/o
funcionalidad no ha alcanzado los objetivos, debe considerarse como un cuadro crónico de
difícil control.
En las Unidades de Dolor se realizan técnicas intervencionistas cuando el empleo de medicamentos
por vía sistémica no resulta útil o suficiente. Las indicaciones más importantes son el dolor radicular
crónico, el dolor facetario, los síndromes miofasciales y el dolor oncológico.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [83]
[5] DOLOR Y SEDOANALGESIA
El abordaje intervencionista presenta dos vertientes: la evaluación diagnóstica y el abordaje
terapéutico. En la mayoría de los casos son necesarias técnicas de imagen como la ecografía o la
radioscopia para localizar las estructuras sobre las que se quiere actuar.
El abordaje intervencionista diagnóstico tiene como objetivo determinar la fisiopatología del
dolor, identificar la estructura anatómica que origina el dolor y las vías de las señales neurales
aferentes. Habitualmente se emplean anestésicos locales.
Los procedimientos terapéuticos se basan en la administración de soluciones farmacológicas o
en la aplicación de diversos procedimientos no farmacológicos sobre estructuras diana, como
son el ganglio de la raíz dorsal, los nervios periféricos o la médula espinal. Ejemplos de
sustancias empleadas son los corticoesteroides, los agentes neurolíticos y la toxina botulínica; y
de técnicas no farmacológicas, la radiofrecuencia pulsada y continua y la neuroestimulación
central o periférica.
V. SEDOANALGESIA
Sedoanalgesia en procedimientos diagnósticos y terapéuticos
1. CONCEPTO
La sedación consiste en el estado de transición entre el individuo consciente y la pérdida de
consciencia. Con mucha frecuencia, la sedación se aplica para procedimientos dolorosos, por lo que suele
llevar asociada analgesia, aplicándose el neologismo de sedoanalgesia.
Los objetivos primarios de la sedación incluyen una adecuada pérdida de la percepción de los
estímulos, con control de la abolición de los reflejos protectores, ausencia de ansiedad, amnesia y
protección frente al dolor y otros estímulos nocivos. Asimismo, la sedoanalgesia constituye una parte
esencial del manejo de los pacientes críticos, proporcionándoles un nivel óptimo de comodidad.
2. TIPOS DE SEDACIÓN
1. SEGÚN LA DURACIÓN
1.1. Sedación de corta duración
Menor de 72 horas; es la ideal.
1.2. Sedación prolongada
Si dura más de 72 horas. Se asocia a aumento de la mortalidad, desconexión dificultosa de la
ventilación mecánica y otras complicaciones.
2. SEGÚN LA PROFUNDIDAD
2.1. Sedación superficial, consciente o ansiolisis
Consiste en una mínima depresión del nivel de consciencia; el paciente conserva los reflejos de
protección de la vía aérea y es capaz de responder a un estímulo verbal o físico. El objetivo es conseguir un
estado de analgesia, bienestar y cierto grado de amnesia para la tolerancia de la exploración o técnica en
cuestión. Es a la que nos referiremos en este capítulo.
2.2. Sedación inconsciente o profunda
Se deprime la consciencia, pudiendo afectarse los reflejos de protección; supone una anestesia
general superficial.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [84]
[5] DOLOR Y SEDOANALGESIA
3. INDICACIONES DE LA SEDACIÓN
La realización de una sedación y su grado dependerán de:
El nivel de ansiedad y de la escasa colaboración del paciente.
La necesidad de inmovilización.
El dolor debido a la patología de base o al procedimiento realizado.
Cada vez es más frecuente el empleo de distintas técnicas de sedación realizadas para la
elaboración de procedimientos diagnósticos y terapéuticos invasivos fuera del área quirúrgica y de la UCI.
Es aconsejable la presencia de un anestesiólogo para la sedación de pacientes más complejos:
Casos en los que se requieran dosis de fármacos muy superiores a las habituales (pacientes con
drogodependencia) o anestesias generales.
Sedaciones de urgencia o sin ayuno cumplido, con riesgo de broncoaspiración.
Pacientes pluripatológicos con grado III-IV de la clasificación de la American Society of
Anesthesiologists (ASA).
Vía aérea difícil.
Pacientes pediátricos y gestantes.
1. PROCEDIMIENTOS QUE PUEDEN REQUERIR SEDOANALGESIA
1.1. Especialidades médicas
Respiratorio: broncoscopias, biopsias.
Digestivo: endoscopias digestivas altas, colangiopancreatografía retrógrada endoscópica
(CPRE), colonoscopias.
Cardiología: implante de marcapasos y desfibrilador automático implantable (DAI),
cardioversión eléctrica.
1.2. Especialidades quirúrgicas
Cirugía plástica: curas de quemaduras o injertos con mala cicatrización, cambios de vendajes.
Cirugía maxilofacial: en asociación a anestesia local, para procesos buco-maxilares como
quistes, extracciones dentarias en deficientes mentales, cardiópatas.
Traumatología: junto con anestesia local en reducciones de fracturas, cambios de yesos,
extracción de material de osteosíntesis.
Neurocirugía: como complemento a la anestesia local para biopsia estereotáxica, evacuación de
hematoma subdural.
Ginecología y obstetricia: exploraciones diagnósticas de esterilidad, técnicas de fertilización,
parto, retención placentaria, drenaje de abscesos.
REQUERIMIENTOS MÍNIMOS PARA LA SEDACIÓN CONSCIENTE EN URGENCIAS
Alcanzar un balance óptimo entre la comodidad del paciente y su seguridad requiere una cuidadosa
dosificación de los fármacos analgésicos y sedantes, así como una apropiada monitorización de los sistemas
nervioso central, cardiovascular y respiratorio, sin olvidar una buena comunicación, tanto con el paciente
como con el cirujano o explorador.
1. ANTES DEL PROCEDIMIENTO
Informar y obtener el consentimiento verbal o por escrito del paciente, o de algún familiar directo
si él no estuviese capacitado.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [85]
[5] DOLOR Y SEDOANALGESIA
Evaluación preanestésica del paciente: historia clínica, alergias y antecedentes médicoquirúrgicos
(experiencias previas de anestesias y/o sedaciones), medicación actual, situación clínica en el momento del
procedimiento y valoración de la vía aérea. Prever factores de riesgo para complicaciones durante la
sedación (Tabla VIII)
Tabla VIII. Factores de riesgo para complicaciones durante la sedoanalgesia.
Periodo de ayuno previo: el riesgo de broncoaspiración se encuentra aumentado si han pasado
menos de seis horas desde la última ingesta, así como en pacientes obesos, embarazadas, ancianos y
diabéticos. Ante procedimientos no urgentes, se recomienda un periodo de ayuno de seis a ocho horas
para sólidos y líquidos espesos, y de dos a tres horas para líquidos claros. Si se trata de una urgencia, la
ingesta de alimentos obliga a una anestesia general con aislamiento de la vía aérea, informando del riesgo
de broncoaspiración.
Evaluación del riesgo anestésico: la tasa de mortalidad se incrementa según el estado físico
preoperatorio, de acuerdo con la clasificación de la ASA.
2. DURANTE EL PROCEDIMIENTO
Monitorización básica: se deberá disponer de electrocardiograma continuo, pulsioximetría (la
hipoxia es el riesgo más importante) y presión arterial no invasiva. En algunas exploraciones, la
monitorización de capnografía resulta muy útil. Es recomendable mantener contacto verbal con el paciente
para valorar de forma constante el nivel de consciencia, así como vigilar la mecánica respiratoria y la
tolerancia del paciente a la técnica para ir modificando la sedación. La monitorización debe mantenerse
hasta la recuperación de la situación basal.
Material necesario: fuente de oxígeno (y acceso a un respirador en caso de urgencia), sistemas de
aspiración, material de intubación, sistemas para canalización de vías periféricas, fluidoterapia y fármacos
para la sedación, así como antagonistas y para la reanimación.
Acceso intravenoso: disponer de una vía venosa segura y comprobar su permeabilidad siempre
antes de cualquier administración farmacológica. Deberá mantenerse hasta la recuperación completa de la
sedación.
Dotación de personal: debido a que toda sedación puede llevar a un estado de depresión
respiratoria y/o cardiocirculatoria, el personal encargado de su administración debería estar entrenado en
el manejo de la vía aérea y la reanimación cardiopulmonar básica y avanzada, así como en el empleo de
dichos fármacos.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [86]
[5] DOLOR Y SEDOANALGESIA
Registro: debe documentarse el procedimiento y se han de registrar las constantes vitales antes,
durante y tras la administración de fármacos, así como antes del alta. Resultan de gran utilidad escalas
como la Richmond Agitation Sedation Scale (RASS) o la de Ramsay.
3. DESPUÉS DEL PROCEDIMIENTO
Monitorización y vigilancia en unidades de despertar: hasta que se cumplan los criterios de alta y
se confirme la ausencia de efectos indeseados (náuseas y vómitos, mareo, dolor, etc.) de los fármacos o del
procedimiento. Si se ha administrado un antagonista por vía intravenosa (naloxona, flumazenilo), deberá
vigilarse al menos dos horas para comprobar que no reaparece la sedación.
Instrucciones sobre los cuidados posquirúrgicos/postsedación: deben administrarse por escrito y
explicarse verbalmente.
Registro: se debe documentar la situación del paciente antes del alta (resulta útil la escala de
Aldrete).
4. CONTRAINDICACIONES
Existen diversas situaciones en las que los riesgos de realizar una sedación superan sus potenciales
beneficios. No debería llevarse a cabo una sedación en los siguientes supuestos:
Negación por parte del paciente.
Falta de experiencia en el manejo de los fármacos sedantes, la vía aérea y/o el aparataje
utilizado.
Alergia o hipersensibilidad a los fármacos.
Incapacidad para monitorizar adecuadamente al paciente durante la intervención.
5. FÁRMACOS UTILIZADOS
El fármaco ideal es el que consigue los objetivos de sedación, con un comienzo de acción rápido,
duración corta, administración fácil y efecto reversible. Existen multitud de fármacos y es importante estar
familiarizados con ellos e individualizar siempre en cada caso, adaptando el grado de sedación y analgesia
necesarias (Tabla IX). De manera general, tendremos en cuenta las siguientes premisas:
En procedimientos no invasivos (por ejemplo, pruebas de imagen), en los que se requiere
inmovilizar al paciente, si este no es colaborador, podremos utilizar midazolam o dosis bajas de
fentanilo intravenoso.
En procedimientos que producen escaso dolor, pero elevada ansiedad (sutura de herida,
extracción de cuerpos extraños, punción lumbar, etc.), se puede combinar anestesia local y
midazolam o fentanilo intravenoso.
En procedimientos que producen dolor intenso y/o mucha ansiedad (reducción de fracturas o
luxaciones, endoscopias, cardioversión, radiología intervencionista, cura de quemaduras) se
suele asociar midazolam a un fármaco hipnótico y fentanilo, o ketamina con midazolam.
Se debe tener en consideración que los pacientes ancianos suelen requerir menores dosis y la
farmacocinética puede verse alterada, teniendo un efecto más prolongado e incluso mayor repercusión
hemodinámica.
Los fármacos se deben dosificar progresivamente y bajo estrecha monitorización para minimizar los
efectos secundarios, especialmente si se utilizan combinaciones (p. ej. benzodiazepinas y opiáceos). En
ocasiones, puede producirse una excesiva sedación con la consiguiente depresión respiratoria. En estos
casos, interrumpiremos la prueba y ventilaremos al paciente manualmente; si fuese necesario, usaremos
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [87]
[5] DOLOR Y SEDOANALGESIA
antagonistas (naloxona y flumazenilo), titulando dosis lentamente. Se debe recordar que pueden precisarse
dosis suplementarias si la vida media del fármaco administrado es mayor que la del antagonista.
Tabla X.Fármacos empleados en sedación superficial.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [88]
[5] DOLOR Y SEDOANALGESIA
Tabla IX.Fármacos empleados en sedación superficial. (Continuación)
6. SEDACIÓN EN SITUACIONES ESPECÍFICAS
1. CARDIOVERSIÓN ELÉCTRICA
El fármaco ideal es el que consigue los objetivos de sedación, con un comienzo de acción rápido,
duración corta, administración fácil y efecto reversible. Existen multitud de fármacos y es importante estar
familiarizados con ellos e individualizar siempre en cada caso, adaptando el grado de sedación y analgesia
necesarias (Tabla IX). De manera general, tendremos en cuenta las siguientes premisas:
2. PROCEDIMIENTOS ENDOSCÓPICOS (RESPIRATORIOS Y DIGESTIVOS)
Los pacientes jóvenes son los que peor suelen tolerar dichas técnicas y los que más se beneficiarán
de la sedación. Se recomienda el uso de midazolam o propofol. En procedimientos prolongados o dolorosos
(CPRE, colonoscopia, tratamiento endoscópico de varices…) debe considerarse la asociación de un opiáceo.
En técnicas de alto riesgo o situaciones de inestabilidad, valorar aislar la vía aérea mediante intubación y
contar con ayuda de un anestesista.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [89]
[5] DOLOR Y SEDOANALGESIA
3. CURAS Y PROCEDIMIENTOS QUIRÚRGICOS
Incluyen desbridamiento de heridas, reducción de fracturas, cambio de apósito en quemados, etc.
Requieren niveles elevados de analgesia. Se recomienda el uso de hipnóticos como ketamina, que genera
una anestesia disociada sin depresión del centro respiratorio (debe asociarse a benzodiazepinas), propofol
y asociación de un opiáceo.
BIBLIOGRAFÍA
Abalo R, Girón R, Goicoechea C, et al. Dolormecum 2015. Barcelona: Ed. Permanyer; 2015.
Agencia Española del Medicamento. Disponible en: http://www.aemps.gob.es/
American Society of Anesthesiologists Task Force on Chronic Pain Management; American Society of
Regional Anesthesia and Pain Medicine. Practice Guidelines for Chronic Pain Management.
Anesthesiology. 2010;112:810-33.
Attal N, Cruccu G, Baron R. EFNS guidelines on the pharmacological treatment of neuropathic pain:
2010 revision. Eur J Neurol. 2010;17:1113-23.
Baron R, Binder A, Biniek R, et al. Evidence and consensus based guideline for the management of
delirium, analgesia and sedation in intensive care medicine. Revisión 2015 (DAS-Guideline 2015).
Intens Care Med.
Borrallo-Pérez JM, Béjar-Delgado A y Grupo de trabajo de analgesia y sedación de la SEMICYUC.
Sedación de corta duración. Med Intensiva. 2008;32(Supl 1):31-7.
Castañeda M, Ruiz MG, Borque JL. Sedación en Urgencias. Servicio de Anestesiología, Reanimación y
Terapia del Dolor. Hospital de Navarra. Capítulo: “Farmacología en Urgencias”. Libro electrónico de
Temas de Urgencias. 1999.
Catalá E. Dolor en el paciente oncológico. En: Gomar C, Villalonga A, Castillo J, et al., editores.
Formación continuada en anestesiología y reanimación. Majadahonda, Madrid: Ergón; 2015. Vol II. pp.
899-904.
Catalá E. Dolor neuropático. En: Gomar C, Villalonga A, Castillo J, et al., editores. Formación continuada
en anestesiología y reanimación. Majadahonda, Madrid: Ergón; 2015. Vol II. pp. 895-8.
Fichas técnicas de fármacos comercializados en territorio español.
López-Andrade A, Prieto M, García MJ, Martín JL. Sedación de pacientes en las técnicas dolorosas
diagnósticas y terapéuticas: supuestos clínicos. Servicio de Anestesiología, Reanimación y Terapéutica
del Dolor. Hospital Virgen de las Nieves de Granada. Documento de consenso de la V Reunión
Científica de la SED y Jornadas de Actualización en Dolor.
Monsegur, J. Sedación: indicaciones y técnicas anestésicas. En: Gomar C, Villalonga A, Castillo J, et al.,
editores. Formación continuada en Anestesiología y Reanimación. Majadahonda, Madrid: Ergón; 2015.
Vol II. pp. 1151-18.
O’Connor AB, Dworkin RH. Treatment of neuropathic pain: An overview of recent guidelines.
Department of Medicine and Departments of Anesthesiology and Neurology, University of Rochester
School of Medicine and Dentistry, Rochester, New York, USA. Am J of Med. 2009;122(10):S22-S32.
Roca G. Orientación diagnóstica y evaluación del paciente con dolor crónico. En: Gomar C, Villalonga A,
Castillo J, et al. Formación continuada en anestesiología y reanimación. Majadahonda, Madrid: Ed.
Ergón; 2015. Vol II. pp. 871-6.
Sánchez J, Tejedor A, Carrascal R. La atención al paciente con dolor crónico no oncológico (DCNO) en
Atención Primaria (AP). Documento de consenso. España 2015.
Temprano I, Álvarez M, Orejas A, Álvarez S. Sedación y analgesia en procedimientos cardiovasculares.
Unidad de Cuidados Intensivos. Hospital de Móstoles, Madrid.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [90]
[6] PRINCIPIOS BÁSICOS EN CUIDADOS PALIATIVOS
6. Principios básicos en cuidados paliativos
Irene Losada Galván.
Medicina Interna
Leticia Sanz Trepiana.
Medicina Interna
Asesora:
Begoña Azcoitia Álvarez.
Médica Adjunta del Equipo de Soporte Hospitalario de Cuidados Paliativos
I. CONCEPTOS
Los cuidados paliativos (CP) representan la parte de la práctica clínica enfocada a mejorar la calidad
de vida de los pacientes y sus familias, promoviendo el bienestar físico, psicológico, social y espiritual.
Pueden aplicarse desde el diagnóstico y de forma paralela a tratamientos “activos” (con intención de
modificar el curso de la enfermedad), aumentando su importancia relativa a medida que avanza la
enfermedad.
Algunas de las características de los CP recogidas por la Organización Mundial de la Salud (OMS)
son:
Proporcionan alivio del dolor y otros síntomas que producen sufrimiento.
Promocionan la vida y consideran la muerte como un proceso natural.
No se proponen acelerar ni retrasar el proceso de morir.
Integran los aspectos psicosociales y espirituales en los cuidados del paciente.
Tienen en cuenta el soporte y los recursos necesarios para ayudar a los pacientes a vivir de la
manera más activa posible hasta su muerte.
Ofrecen apoyo a los familiares y a los allegados durante la enfermedad y el duelo.
Mejoran la calidad de vida del paciente.
Se aplican desde las fases tempranas de la enfermedad junto con otras terapias dirigidas a
prolongar la vida.
Para alcanzar los objetivos mencionados, es fundamental contar con un equipo multidisciplinar
(médico, enfermero, fisioterapeuta, terapeuta ocupacional, psicólogo, trabajador social, voluntarios de
apoyo, etc.).
Se conoce como enfermedad terminal al proceso avanzado, progresivo e incurable, sin tratamiento
específico razonable, con múltiples síntomas intensos, cambiantes y multifactoriales, que causa gran
impacto emocional en el paciente, la familia y el equipo terapéutico, y que tiene un pronóstico de vida
limitado. Los cuidados terminales son una parte importante de los CP, y se refieren al manejo del paciente y
su entorno durante sus últimos días, semanas o meses de vida.
El ámbito de aplicación de los CP incluye a pacientes con enfermedad oncológica y no oncológica
(enfermedad crónica avanzada de un órgano, demencia senil evolucionada o enfermedades degenerativas
del sistema nervioso central −SNC−, ancianos frágiles y comas evolucionados de causas diversas). La
predicción de la supervivencia es importante para poder proporcionar información a pacientes y familiares
y para establecer planes diagnósticos y terapéuticos apropiados.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [91]
[6] PRINCIPIOS BÁSICOS EN CUIDADOS PALIATIVOS
II. CRITERIOS DE TERMINALIDAD
1. EN EL PACIENTE ONCOLÓGICO
Los pacientes oncológicos deben cumplir los siguientes criterios para considerarlos terminales:
Tener una puntuación en la escala Palliative Performance Status (PPS) inferior a 40. La
funcionalidad es el mejor parámetro para predecir la supervivencia, independientemente de la
patología de base.
Padecer una enfermedad oncológica avanzada, progresiva e incurable, con diagnóstico
histológico demostrado. En situaciones especiales, se aceptará la ausencia de diagnóstico
histológico cuando por la situación clínica del paciente no se considere adecuada una
investigación exhaustiva, aunque se deberán haber excluido tumores potencialmente tratables.
Presentar escasa o nula respuesta al tratamiento activo. En ocasiones, se deben emplear
recursos específicos (quimioterapia oral, radioterapia, hormonoterapia, bisfosfonatos,
moléculas en tercera y cuarta línea, etc.) por su impacto favorable sobre la calidad de vida.
Padecer múltiples problemas o síntomas intensos, multifactoriales y cambiantes.
Impacto emocional en el paciente, familia y equipo terapéutico, relacionado con el proceso de
morir.
Pronóstico vital limitado a meses de vida.
La decisión de definir a un paciente como terminal debe ser tomada por especialistas cualificados
con experiencia y estar sujeta a revisión permanente.
2. EN EL PACIENTE NO ONCOLÓGICO
Los pacientes no oncológicos serán considerados terminales si cumplen los siguientes criterios:
Presentan una progresión de la enfermedad documentada por criterios clínicos, de laboratorio
o exploraciones complementarias.
Han precisado varias consultas a urgencias o ingresos hospitalarios en los últimos 6 meses, con
deterioro funcional reciente o dependencia para tres o más actividades básicas de la vida diaria.
Sufren desnutrición o deterioro nutricional, demostrado por una pérdida de peso superior al
10% en los últimos 6 meses o una albúmina sérica inferior a 2,5 g/dL.
Además de los anteriores, existen criterios específicos añadidos para patologías concretas:
Insuficiencia cardiaca (IC):
Clase IV en la escala de valoración funcional de la IC de la NYHA (New York Heart Association)
(ver Capítulo 21. “Insuficiencia cardiaca”): incapacidad para desarrollar cualquier actividad física
sin malestar, con manifestaciones de IC o angina incluso en reposo.
Fracción de eyección ≤ 20%.
Persistencia de síntomas a pesar de tratamiento adecuado con diuréticos, vasodilatadores e
inhibidores de la enzima convertidora de angiotensina (IECA).
IC refractaria y arritmias supraventriculares o ventriculares resistentes al tratamiento
antiarrítmico.
Enfermedad pulmonar (expectativa de vida < 6 meses): los criterios 1, 2 y 3 son obligatorios:
1. Enfermedad pulmonar crónica grave documentada por:
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [92]
[6] PRINCIPIOS BÁSICOS EN CUIDADOS PALIATIVOS
a. Disnea de reposo, sin respuesta a broncodilatadores (BD), con disminución de la
capacidad funcional (permanencia en cama o sentado, fatiga y tos). Una medida
objetiva es un FEV1 < 30% del valor predictivo después del tratamiento con BD,
aunque no es necesaria.
b. Progresión de la enfermedad con hospitalización o incremento de visitas médicas.
Se puede medir con una caída del FEV1 > 40 ml/año, aunque tampoco es necesario
obtenerla.
2. Hipoxemia en reposo, evidenciada por una PaO2 < 55 mm Hg o una saturación de O2 <
88%, o hipercapnia con PaCO2 > 50 mm Hg. Estos valores pueden ser tomados de los
últimos 3 meses.
3. IC derecha o cor pulmonale (no secundario a fallo cardiaco izquierdo o valvulopatía).
4. Taquicardia de reposo > 100 lpm.
Cirrosis hepática:
Estadio C de Child-Pugh (12-15 puntos), no candidato a trasplante (ver Capítulo 57. “Cirrosis
hepática y sus complicaciones”).
Otros aspectos (el pronóstico empeora con la adición de cada uno):
Criterios de laboratorio: actividad de protrombina < 30% junto con albúmina sérica <
2,5 g/dL.
Criterios clínicos:
Ascitis refractaria a restricción sódica y diuréticos.
Peritonitis bacteriana espontánea (mediana de supervivencia al año del 30%).
Síndrome hepatorrenal (supervivencia de días o semanas).
Encefalopatía hepática refractaria a restricción proteica, lactulosa y neomicina.
Sangrado recurrente por varices a pesar de tratamiento.
Empeoran el pronóstico: malnutrición progresiva, pérdida de masa muscular,
alcoholismo activo, carcinoma hepatocelular, antígeno de superficie del virus de la
hepatitis B (HBsAg) positivo.
Insuficiencia renal: filtrado glomerular < 15 ml/min; rechazo, desestimación o futilidad de terapias
de depuración (diálisis, trasplante):
Manifestaciones clínicas de uremia (confusión, náuseas, vómitos refractarios, prurito
generalizado, etc.).
Diuresis < 400 ml/día.
Hipercalemia > 7 mEq/l y que no responde al tratamiento.
Pericarditis urémica, síndrome hepatorrenal o sobrecarga de fluidos intratable.
Coma y estado vegetativo: ver Capítulo 82. “Alteración del nivel de consciencia. Coma”.
Ictus y demencias:
En la Functional Assesment Staging (FAST), una clasificación a partir del nivel 7C (no puede
caminar sin ayuda) apoya la terminalidad.
Presencia en el último año de: neumonía aspirativa, pielonefritis, sepsis, úlceras por presión en
estadio 3-4, fiebre recurrente tras antibiótico, dificultad para deglutir o negativa a comer.
Enfermedad de Parkinson: estadio 5 de la clasificación de Hoehn y Yahr (caquexia, invalidez, que
no pueda permanecer de pie o caminar, o que requiera del constante cuidado de otra persona).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [93]
[6] PRINCIPIOS BÁSICOS EN CUIDADOS PALIATIVOS
Esclerosis lateral amiotrófica (ELA): poliulcerados, deterioro funcional grave, índice de Katz F/G,
índice de Barthel < 20.
Virus de la inmunodeficiencia humana (VIH) y SIDA: recuento de CD4 < 25 células/ mm3, carga
viral > 100.000 colonias/ml, estado funcional < 50 en la escala de Karnofsky.
Tabla I. Comunicación de malas noticias: protocolo de seis etapas de Buckman (SPIKES, por sus siglas en inglés).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [94]
[6] PRINCIPIOS BÁSICOS EN CUIDADOS PALIATIVOS
III. COMUNICACIÓN
La comunicación efectiva permite al paciente tomar decisiones informadas acordes a su realidad
clínica, y al equipo tratante ser consciente de las prioridades y necesidades del paciente y su entorno.
Contribuye a disminuir la ansiedad en el paciente, sus familiares y en el propio profesional. El acceso a la
información es un derecho de todos los pacientes recogido por la ley (Ley 41/2002, de 14 de noviembre,
básica reguladora de la autonomía del paciente y de derechos y obligaciones en materia de información y
documentación clínica), así como el derecho a no ser informado.
Con frecuencia el profesional médico se enfrenta a la necesidad de comunicar malas noticias. La
información ha de ser veraz, comprensible y ha de adaptarse a lo que el paciente sea capaz de integrar en
cada momento, y se debe procurar facilitarla de forma programada para permitir la preparación y el
acompañamiento. Es un proceso dinámico en el que la necesidad de información a lo largo de la
enfermedad es cambiante; suele disminuir para el paciente, pero aumentar para sus familiares. Existen
diferentes propuestas de sistematización de la comunicación de malas noticias, como el protocolo en seis
etapas de Buckman (Tabla I).
En caso de que el paciente se encuentre imposibilitado para expresar sus preferencias en el
momento de la asistencia, habrá que averiguar si realizó algún documento de “instrucciones previas” (IP),
para adecuar la atención a sus deseos. Existen registros de IP que difieren según el lugar de residencia
(registros automatizados online, declaraciones ante notario, etc.). Será necesario preguntar a los familiares
por este tipo de documentos.
Para dar información a familiares, es necesaria la autorización del paciente. Hay que evitar una
“conspiración de silencio”: acuerdo implícito o explícito de alterar la información al paciente por parte de
familiares, amigos y/o profesionales sanitarios, con el fin de ocultar el diagnóstico, pronóstico y/o gravedad
de la situación, cuando el paciente quiere saber lo que le sucede. Se debe abordar de la siguiente forma:
Empatizar con la familia, validar sus necesidades e identificar sus temores.
Explicitar que queremos lo mismo que ellos: lo mejor para el paciente.
Anticipar consecuencias del secretismo.
Sopesar el coste emocional del engaño.
Confrontar opiniones desde la empatía.
Proponer un acuerdo y ofrecernos como mediadores si hay dificultades. Es útil, si el enfermo lo
autoriza, trabajar la información con su familia presente.
IV. EVALUACIÓN Y CONTROL DE LOS SÍNTOMAS
Debe realizarse de forma global, teniendo en cuenta aspectos psicosociales, y reevaluarse en el
tiempo: cambios derivados de la evolución de la enfermedad, efectos adversos del tratamiento
(radioterapia, etc.), vivencias del paciente y cuidadores, entre otros.
1. ESCALAS DE VALORACIÓN. LAS MÁS EMPLEADAS SON:
Escala de Barthel de actividades básicas de la vida diaria (Tabla II): es la más utilizada a nivel
internacional para monitorizar la dependencia funcional del paciente y así poder elaborar planes de
cuidados y rehabilitación.
Escala de valoración funcional de Karnofsky (Tabla III): permite conocer la capacidad del paciente
para realizar actividades cotidianas y constituye un elemento predictor independiente de mortalidad en
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [95]
[6] PRINCIPIOS BÁSICOS EN CUIDADOS PALIATIVOS
patologías oncológicas y no oncológicas. Es útil para la toma de decisiones clínicas. Una puntuación igual o
menor de 50 indica un elevado riesgo de muerte en los 6 meses siguientes.
Tabla II.Escala de Barthel.
Tabla III.Escala de valoración funcional de Karnofsky.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [96]
[6] PRINCIPIOS BÁSICOS EN CUIDADOS PALIATIVOS
Paliative Performance Scale (PPS): modificación de la escala de valoración funcional de Karnofsky.
Cerca del 90% de los pacientes con una puntuación igual o menor de 50 vivirán menos de 6 meses.
2. PRINCIPIOS PARA EL CONTROL EFECTIVO DE SÍNTOMAS
Se recogen en la tabla IV.
Tabla IV.Principios para el control efectivo de síntomas
3. VÍAS DE ADMINISTRACIÓN FARMACOLÓGICA
Se debe elegir la vía oral siempre que sea posible, puesto que es la menos invasiva. La vía
transcutánea no es recomendable, por su absorción errática, dependiente de diferentes parámetros que se
van modificando con la progresión de la enfermedad (adelgazamiento, alteración de la perfusión y cambios
en la temperatura corporal). En caso de perder la vía oral y no ser posible la transcutánea, es de gran
utilidad la vía subcutánea.
4. DOLOR
Requiere un abordaje multidimensional debido a la íntima relación entre aspectos psíquicos, físicos,
sociales y espirituales que lo condicionan, incluyendo medidas farmacológicas, psicoterapéuticas y
rehabilitadoras. (Ver Capítulo 5. “Dolor y sedoanalgesia”).
5. DISNEA
Se deben tratar las causas reversibles de forma específica: broncoespasmo, insuficiencia cardiaca,
infección respiratoria, arritmias cardiacas, anemia, derrame pleural o pericárdico, tromboembolismo
pulmonar o síndrome de vena cava superior. Una vez se aborden dichas causas, se pautará tratamiento
sintomático (Tabla V).
Tabla V.Tratamiento sintomático de la disnea.
6. OBSTRUCCIÓN INTESTINAL
Tratamiento de las causas reversibles: desimpactación de fecaloma, valoración de intervención
quirúrgica (alta tasa de morbimortalidad). Tratamiento sintomático: se expone en la tabla VI.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [97]
[6] PRINCIPIOS BÁSICOS EN CUIDADOS PALIATIVOS
Tabla VI.Tratamiento sintomático de la obstrucción intestinal.
7. DELIRIUM
Requiere tratamiento etiológico y sintomático, siempre que haya agitación, de forma paralela (ver
Capítulo 11. “Síndrome confusional agudo”). Se pueden emplear neurolépticos típicos: haloperidol 1,5-2,5
mg/8 horas vo o sc, con rescates cada 20 o 30 minutos si es necesario (hasta tres dosis); en caso de fracaso,
levomepromazina 12,5 mg/4-12 horas vo o sc, con rescates cada 15 minutos.
8. ASTENIA E HIPOREXIA
Son muy frecuentes, pueden presentarse hasta en el 90% de los casos. Tratamiento de factores
etiológicos: metabólicos (hipercalcemia, hiponatremia, uremia, anemia, hipoxemia), dolor, fármacos,
infecciones, síndromes paraneoplásicos, factores psicológicos (ansiedad, depresión, insomnio), factores
sociales (soledad). Tratamiento sintomático: se expone en la tabla VII.
Tabla VII.Tratamiento sintomático de la astenia y la hiporexia.
9. NÁUSEAS Y VÓMITOS
Tratamiento de las causas precipitantes: obstrucción intestinal, opioides, hipertensión intracraneal,
origen vestibular, etc. Tratamiento sintomático (Tabla VIII).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [98]
[6] PRINCIPIOS BÁSICOS EN CUIDADOS PALIATIVOS
Tabla VIII.Tratamiento sintomático de náuseas y vómitos.
10. DISFAGIA
El tratamiento etiológico y sintomático se refleja en la tabla IX.
Tabla IX.Tratamiento de la disfagia.
11. ESTREÑIMIENTO
Tratamiento etiológico: sedentarismo (causas tratables: dolor, disnea, anemia, anorexia, síndrome
confusional, depresión, etc.), alimentación, causa farmacológica (opioides, neurolépticos, antidepresivos,
anticolinérgicos, etc.), estructural (tumoral, hemorroides) o metabólica (hipotiroidismo). Tratamiento
sintomático (Tabla X).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [99]
[6] PRINCIPIOS BÁSICOS EN CUIDADOS PALIATIVOS
Tabla X.Tratamiento sintomático del estreñimiento.
12. TOS
Se debe tratar la causa: masa tumoral, derrame pleural, broncoespasmo, insuficiencia cardiaca, etc.
Puede precisar tratamiento sintomático (Tabla XI).
Tabla XI.Tratamiento sintomático de la tos.
13. INSOMNIO
Tratamiento etiológico: dolor, delirium, fármacos (corticoides), disnea, náuseas y vómitos, prurito,
ansiedad, depresión, mala higiene del sueño, impacto psicológico de la enfermedad, factores sociales.
Medidas generales: horarios regulares de sueño, evitar estimulantes (cafeína, nicotina), ambiente tranquilo
y agradable, evitar interrupciones de sueño (medicación). Tratamiento farmacológico: se prescribirá si es
preciso a pesar de la corrección de los factores etiológicos (Tabla XII).
Tabla XII.Tratamiento farmacológico en el insomnio.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [100]
[6] PRINCIPIOS BÁSICOS EN CUIDADOS PALIATIVOS
14. ANSIEDAD
Tratamiento psicológico del paciente y su familia. Pueden ser medidas útiles la meditación, los
masajes, la hipnoterapia o la aromaterapia. Tratamiento farmacológico (Tabla XIII).
Tabla XIII.Tratamiento farmacológico de la ansiedad.
15. DEPRESIÓN
Factores de riesgo de depresión: cáncer de páncreas, cáncer primario o metastásico del SNC, dolor,
discapacidad, tratamiento esteroideo, quimioterapia (asparaginasa, interferón, interleucinas, metotrexato
intratecal, vincristina, vinblastina), anfotericina B, radiación cerebral total, alteraciones
endocrinometabólicas, síndromes paraneoplásicos. Factores de riesgo de suicidio: dolor no controlado,
enfermedad avanzada, sexo masculino, depresión, delirium, psicopatología previa, abuso de sustancias,
historia familiar o personal de intento de suicidio, edad avanzada o aislamiento social. El tratamiento de la
depresión se refleja en la tabla XIV.
Tabla XIV.Tratamiento de la depresión.
16. HIPO
Tratamiento de las causas precipitantes: irritación del nervio frénico o vago (esofagitis, distensión
gástrica, obstrucción intestinal, patología biliar o pancreática, bocio, laringitis, etc.), lesiones del SNC
(procesos infecciosos o inflamatorios, lesiones medulares, alteraciones circulatorias, etc.), causas
metabólicas (uremia, hiponatremia, hipocalcemia, etc.), fármacos, cirugía abdominal, psicógeno.
Tratamiento farmacológico: se muestra en la tabla XV.
Tabla XV.Tratamiento farmacológico del hipo.
17. ÚLCERAS
Prevención de úlceras por presión (Tabla XVI). Curas paliativas: incluyen la colocación de un apósito
especial de silicona y la realización de lavados por encima del mismo. Además, se pueden plantear lavados
posteriores con metronidazol y la administración de amoxicilina-clavulánico con el fin de disminuir el olor.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [101]
[6] PRINCIPIOS BÁSICOS EN CUIDADOS PALIATIVOS
Tabla XVI.Prevención de úlceras por presión.
18. PRURITO
Su tratamiento se refleja en la tabla XVII.
Tabla XVII.Tratamiento del prurito.
19. TENESMO VESICAL
En la tabla XVIII se recogen medidas para su tratamiento.
Tabla XVIII.Tratamiento del tenesmo vesical.
20. HIPERCALCEMIA
Factores etiológicos más prevalentes: metástasis osteolíticas (carcinoma de mama y pulmón),
blásticas (próstata), mieloma múltiple, hipercalcemia humoral (secreción de PTH-like en tumores sólidos no
metastásicos y linfomas no Hodgkin) y producción tumoral de calcitriol (enfermedad de Hodgkin y linfomas
no Hodgkin) (ver Capítulo 66. “Trastornos del metabolismo del calcio, fósforo y magnesio”).
21. COMPRESIÓN MEDULAR
(ver Capítulo 80. “Urgencias oncológicas”).
22. CRISIS CONVULSIVAS
(ver Capítulo 86. “Crisis comiciales”).
23. SÍNDROME DE VENA CAVA SUPERIOR
(ver Capítulo 80. “Urgencias oncológicas”).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [102]
[6] PRINCIPIOS BÁSICOS EN CUIDADOS PALIATIVOS
24. HEMORRAGIA
Es importante identificar los pacientes con riesgo hemorrágico elevado, especialmente aquellos con
posibilidad de sufrir un sangrado masivo, como los que padecen cáncer de cabeza y cuello y carcinoma de
pulmón. Las medidas que se han de adoptar en caso de hemorragia aguda se muestran en la tabla XIX.
Tabla XIX.Medidas en caso de hemorragia aguda.
V. VÍA SUBCUTÁNEA
Indicación: si el paciente no puede tomar la medicación por vía oral o si los síntomas no están
suficientemente controlados por esta vía: vómitos, disfagia, oclusión intestinal sin opción a
tratamiento quirúrgico, sedación paliativa, agitación, convulsiones, atención en la agonía. No se
recomienda en caso de anasarca, shock y coagulopatías graves. En la tabla XX se resumen los
fármacos más frecuentemente utilizados.
Tabla XX.Fármacos más utilizados por vía subcutánea en cuidados paliativos.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [103]
[6] PRINCIPIOS BÁSICOS EN CUIDADOS PALIATIVOS
Modo de infusión: en forma de bolos (no más de 2 ml) o infusión continua. Esta última es la de
elección por obtener un efecto continuado y emplear conjuntamente varios fármacos, no
debiendo sobrepasar un ritmo de 2 ml/h.
Material necesario: bomba de infusión, jeringas, aguja de tipo palomilla con aguja metálica 23-
25 G, tiras adhesivas y apósitos transparentes, suero fisiológico o agua para inyección, solución
antiséptica (clorhexidina, povidona yodada), guantes.
Procedimiento: inserción de la palomilla con aguja metálica 23-25 G o un catéter de plástico en
el tejido celular subcutáneo; fijación con un apósito adhesivo transparente para poder
visualizar posibles complicaciones en la zona de punción (edema, infección, etc.). Se
recomienda insertar el dispositivo en la región torácica anterior infraclavicular, en la deltoidea,
en el abdomen o en la cara anteroexterna del muslo.
Infusores: infunden la medicación de forma constante y continua. Tipos: elastoméricos (con
mecanismo de balón), mecánicos (con mecanismo de resorte o de jeringa) y electrónicos (con
mecanismo de tipo peristáltico). Muchos de ellos permiten además la administración de
fármacos en bolos en caso de ser necesario (útiles en el dolor irruptivo), no estando indicada
esta opción si la infusión está compuesta por varios fármacos.
Cómo cargar el infusor: se debe tener en cuenta el flujo de salida medido en ml/h, el tiempo de
autonomía (1, 5 o 7 días, habitualmente) y el volumen total de llenado en ml (Tabla XXI).
Tabla XXI.Cómo cargar un infusor subcutáneo (ejemplo).
Compatibilidad de mezclas: no es conveniente mezclar más de tres fármacos por el riesgo de
precipitación de la solución resultante. La dexametasona y el ketorolaco no deben ser
mezclados con otros fármacos. En la tabla XXII se pueden ver algunos ejemplos de mezclas
compatibles bastante empleadas.
Tabla XXII.Compatibilidad de mezclas de uso frecuente en un infusor subcutáneo.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [104]
[6] PRINCIPIOS BÁSICOS EN CUIDADOS PALIATIVOS
VI. FASE TERMINAL
El pronóstico vital de un enfermo puede estimarse con la siguiente regla, que resulta adecuada
para informar tanto al paciente como a su familia: “Si existe un deterioro de semana en semana, el
pronóstico es habitualmente de semanas; si existe un deterioro de día en día, generalmente será de días”.
La fase terminal es el periodo de tiempo que comienza cuando el deterioro sucede de día en día,
especialmente con pérdida de apetito, de fuerza y del nivel de consciencia. Por tanto, los cambios deben
ser evaluados a diario, siendo los síntomas más claros:
Debilidad profunda: encamamiento, necesidad de asistencia para todo cuidado.
Disminución de la ingesta de comida y bebidas.
Dificultad para deglutir la medicación.
Alteración cognitiva y emocional hiper o hipoactivas: confusión, desorientación, dificultad para
concentrarse, escasa cooperación con el cuidador, silencio.
Emaciación: adelgazamiento patológico.
Si estos cambios suceden bruscamente, deberían considerarse, no obstante, posibles causas
reversibles (cambios de medicación, hipercalcemia, infección, etc.).
Se emplea el término de situación de últimos días (SUD) cuando la fase terminal llega a su fin de
forma evidente con cambios frecuentes y rápidos. La presencia de al menos cuatro de los siguientes signos,
conocidos como signos de Menten, predice el exitus en menos de 4 días: frialdad de extremidades,
livideces, cianosis labial, nariz fría o pálida, estertores premortem, pausas de apnea, anuria (< 300 ml/día),
somnolencia (> 15 h/día).
Se deben tener en cuenta las siguientes recomendaciones:
Elegir el ambiente físico más idóneo para los cuidados del paciente, que respete su privacidad,
sus preferencias y las de su familia: domicilio, centro especializado en cuidados paliativos,
hospital convencional, etc.
Se debe procurar confort (percepción subjetiva de bienestar), tanto del paciente como de la
familia, atendiendo a las necesidades físicas, psicológicas y espirituales.
Interferir lo mínimo imprescindible en la exploración física: se valorará la expresión facial
(dolor), el patrón respiratorio, etc., se realizarán cuidados de la boca y se tendrá en cuenta el
débito intestinal y urinario, además de las zonas relevantes por cada enfermedad.
Prevención de crisis, tratando precozmente cada síntoma y trazando un plan terapéutico para
los síntomas que es previsible que aparezcan (convulsiones, hemorragia, estertores, etc.).
Uso de vía intravenosa si ya estaba disponible. Considerar la vía subcutánea si no se dispone de
intravenosa o es previsible que se pierda.
Mantener el sondaje vesical si lo tuviera previamente. Colocación de sonda en caso de
retención urinaria o movilizaciones dolorosas o incómodas para los cambios. El tratamiento en
la fase terminal se refleja en la tabla XXIII.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [105]
[6] PRINCIPIOS BÁSICOS EN CUIDADOS PALIATIVOS
Tabla XXIII.Tratamiento en la fase terminal.
VII. SEDACIÓN PALIATIVA
Maniobra indicada para controlar un síntoma físico o psicológico refractario a otros tratamientos,
con la intención deliberada de disminuir el nivel de consciencia para aliviar un sufrimiento, habitualmente
en la fase de agonía.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [106]
[6] PRINCIPIOS BÁSICOS EN CUIDADOS PALIATIVOS
1. CONSIDERACIONES ÉTICAS
Obtener el consentimiento del paciente (con antelación), siempre que este pueda darlo, o bien
recabar información acerca de las preferencias del enfermo a través de familiares, por
opiniones expresadas en el pasado.
Debe existir un síntoma refractario, es decir, “que no puede ser adecuadamente controlado a
pesar de los intensos esfuerzos para hallar un tratamiento tolerable en un plazo de tiempo
razonable sin que comprometa la consciencia del paciente”.
Debe haber un objetivo claro de aliviar el sufrimiento. El nivel de consciencia se disminuirá lo
imprescindible para alcanzar la confortabilidad y se ajustarán las dosis en respuesta al alivio
obtenido.
Todo el proceso, los motivos y los participantes, así como las revisiones oportunas, deben
constar en la historia clínica.
2. ABORDAJE
El abordaje de esta fase incluye medidas no farmacológicas y farmacológicas.
No farmacológico:
Procurar un entorno tranquilo y relajado alrededor del paciente. Explicar al paciente y a
la familia los beneficios del sueño y el descanso, para evitar que el enfermo pelee
contra la inducción medicamentosa activando mecanismos de alerta. Evitar
movilizaciones innecesarias, realizando las mínimas imprescindibles (curas de úlceras
malolientes, cambio de pañales o sábanas).
Cuidados de la boca: cacao en los labios, limpieza e hidratación bucal con gasas
mojadas, etc.
Proporcionar siempre privacidad, comprensión, presencia y disponibilidad, tanto al
paciente como a la familia.
Dedicar el tiempo necesario a hablar con la familia para aclarar creencias o juicios de
valor erróneos y dudas. Se debe ofrecer la posibilidad de reevaluar la decisión si la
situación del paciente cambia.
Evaluar sistemáticamente el nivel de sedación del paciente y otros signos clínicos,
además del estado emocional de la familia, anotándolo en la historia clínica.
Farmacológico:
Elegir la vía de administración en función de la situación clínica del paciente, el
fármaco, la rapidez de acción y el tiempo previsto de duración de la sedación.
Mantener el tratamiento analgésico previo, especialmente si el paciente recibía
opioides, ya que su retirada brusca puede precipitar un síndrome de abstinencia, con
agitación secundaria de difícil control.
Simplificar el tratamiento farmacológico previo del paciente, manteniendo únicamente
el tratamiento sintomático.
La dosis de fármaco sedante necesaria para conseguir que el paciente esté en un nivel
II-III de la escala de Ramsay (Tabla XXIV) es la dosis de inducción.
La inducción y los ajustes deben ser supervisados directamente por los profesionales
sanitarios.
Anotar siempre la dosis que ha sido precisa para la inducción, ya que será la dosis de
rescate.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [107]
[6] PRINCIPIOS BÁSICOS EN CUIDADOS PALIATIVOS
Tabla XXIV.Escala de Ramsay.
Si se piensa realizar una sedación intermitente, se deben indicar únicamente las dosis
de rescate.
Los rescates se hacen con el mismo fármaco que se ha empleado para la sedación, para
facilitar el cálculo de las necesidades diarias.
La dosis diaria total del fármaco sedante que precisa cada paciente es la suma de la
dosis basal diaria más las dosis de rescate en las 24 horas previas.
En pacientes con delirium se recomienda emplear como primera opción
levomepromazina, y pasar a midazolam si hay mala respuesta.
Midazolam (ampollas 15 mg/3 ml). Benzodiazepina hidrosoluble, por lo que se puede administrar
por vía subcutánea de forma segura y con menos riesgo de tromboflebitis que por vía endovenosa. Es 2-3
veces más potente que el diazepam. El inicio de acción por vía subcutánea es entre 5-10 minutos, y por vía
endovenosa entre 2-3 minutos. La vida media es de 2-5 horas. La dosis diaria máxima recomendada por vía
parenteral es 160-200 mg, por saturación del sistema GABA. Puede producir agitación paradójica. La
posología aparece en la tabla XXV.
Vía subcutánea:
Administrar un bolo de inducción según la situación del paciente.
Si se piensa en una sedación continua o a ritmo variable, iniciar una infusión continua
subcutánea (ICSC) e indicar la dosis de rescate. Dosis diaria total necesaria para la ICSC = dosis
de inducción × 6.
Vía endovenosa:
Administrar un bolo de inducción según la situación del paciente (diluir una ampolla de 15 mg/3
ml en 7 ml de suero fisiológico, en una jeringa de 10 ml; quedaría una dilución 1 ml = 1,5 mg).
El bolo de inducción se puede repetir cada 5 minutos, bajo supervisión directa de los
profesionales sanitarios, hasta que el paciente alcance un nivel II-III en la escala de Ramsay.
Si se piensa en una sedación continua o a ritmo variable, iniciar una infusión continua
endovenosa (ICEV) e indicar la dosis de rescate. Dosis diaria total necesaria para la ICEV = dosis
de inducción × 6.
En caso de requerir una sedación rápida y profunda (Ramsay V-VI), doblar las dosis recomendadas.
Levomepromazina (ampollas 25 mg/1 ml). Fenotiazina con acción antipsicótica, antiemética y
sedante. Puede producir hipotensión intensa dependiente de dosis. Su vida plasmática es de 15-30 horas.
Puede disminuir el umbral convulsivo (se recomienda asociar benzodiazepinas en los casos de agitación
terminal por edema cerebral). La dosis diaria máxima parenteral recomendada es 300 mg/día.
Está indicada en pacientes con delirium o en aquellos que requieren sedación por otra etiología y
no han respondido a midazolam, o bien si tienen contraindicaciones para benzodiazepinas.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [108]
[6] PRINCIPIOS BÁSICOS EN CUIDADOS PALIATIVOS
Si no ha habido respuesta con midazolam, se recomienda disminuir las dosis del mismo a la mitad
durante las primeras 24 horas, antes de iniciar el tratamiento con levomepromazina, para prevenir
síntomas de deprivación. En los días sucesivos, reducir un 33% de la dosis total cada día, según la evolución.
Tabla XXV.Posología de midazolam y levomepromazina para sedación.
VIII. DUELO
La pérdida de un ser querido constituye un estresor psicosocial grave para cualquier persona. Al
mismo tiempo, es un proceso normal que cumple una función adaptativa y de contribución a la madurez
personal. El duelo normal tiene una gran variabilidad interpersonal, y su intensidad y duración dependerán
de múltiples factores, pudiendo comenzar cronológicamente antes del fallecimiento del ser querido. En la
mayoría de los casos no requiere intervenciones específicas. Sin embargo, se debe permanecer alerta para
intentar prevenir y detectar signos o síntomas compatibles con el duelo complicado. El abordaje específico
del duelo excede el propósito de este manual, por lo que se recomienda la derivación y/o consulta con
especialistas en el caso de sospecha de duelo patológico.
BIBLIOGRAFÍA
Azcoitia B, Bellido S, Carretero Y, García E, Metola A. Sedación paliativa en el paciente con enfermedad
terminal irreversible y síntomas refractarios. Madrid: Protocolo Hospital 12 de Octubre; 2010.
Azcoitia B, Bellido S, Carretero Y, García E, Metola A. Sedación paliativa en el paciente con enfermedad
terminal irreversible y síntomas refractarios. Madrid: Protocolo Hospital 12 de Octubre; 2010.
Baile WF, Buckman R, Lenzi R, Glober G, Beale EA, Kudelka AP. SPIKES-A Six-Step Protocol for
Delivering Bad News: Application to the patient with Cancer. Oncologist. 2000;5(4):302-11.
Buckman R. How to break bad news. A guide for health care professionals. Baltimore: Ed. John
Hopkins; 1992.
Grupo de Trabajo de la Guía de Práctica Clínica sobre Cuidados Paliativos. Guía de Práctica Clínica
sobre Cuidados Paliativos. Madrid: Plan Nacional para el SNS del MSC. Agencia de Evaluación de
Tecnologías Sanitarias del País Vasco; 2008.
Guías de Práctica Clínica en el SNS: OSTEBA Nº 2006/08.
López de Ayala García C, Galea Martín T, Campos Méndez R. Guía Clínica. Seguimiento del duelo en
Cuidados Paliativos. Observatorio Regional de Cuidados Paliativos de Extremadura (Junta de
Extremadura, Servicio Extremeño de Salud - FundeSalud); 2011.
Navarro Sanz JR. Cuidados paliativos no oncológicos: enfermedad terminal y factores pronósticos
[monografía en Internet]. Sociedad Española de Cuidados Paliativos [acceso 8 de diciembre de 2015].
Disponible en: http:// www.secpal.com/CUIDADOS-PALIATIVOS-NO-ONCOLOGICOS-ENFERMEDAD-
TERMINAL-Y-FACTORES- PRONOSTICOS
Porta Sales J, Gómez Batise X, Tuca Rodríguez A. Manual de control de síntomas en pacientes con
cáncer avanzado y terminal. 3ª ed. Institut Català d’Oncologia; 2013.
Riaño Zalbidea V. Cuidados paliativos en el enfermo no oncológico [monografía en Internet]. Paliativos
sin fronteras [acceso 8 de diciembre de 2015]. Disponible en:
http://www.paliativossinfronteras.com/upload/publica/ libros/cuidados-pal-labor-todos/04-CUIDADOS-
PALIATIVOS-EN-ENFERMEDAD-NO-ONCOLOGICA- RIANO-ZALBIDEA.pdf
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [109]
[7] DISNEA E INSUFICIENCIA RESPIRATORIA
7. Disnea e insuficiencia respiratoria
Francisco Javier Teigell Muñoz.
Medicina Interna
Mª Alejandra Duarte Borges.
Medicina Interna
Asesor:
Francisco Javier Castelbón Fernández.
Médico Adjunto de Medicina Interna
I. DISNEA
La disnea (o sensación subjetiva de falta de aire) es uno de los síntomas más frecuentemente
referidos por los pacientes, y puede ser la primera o única manifestación de múltiples enfermedades. La
definición más aceptada en la actualidad es la de la American Thoracic Society, que la describe como la
“experiencia subjetiva de malestar respiratorio que engloba sensaciones cualitativamente distintas y de
intensidad variable”. Existen diferentes tipos de disnea: la ortopnea, que aparece durante el decúbito
supino, y generalmente acompaña a la insuficiencia cardiaca (IC), la parálisis diafragmática y el reflujo
gastroesofágico; la platipnea, que aparece al adoptar la posición vertical, y se asocia a shunt derecha-
izquierda, síndrome hepatopulmonar o pérdida de tono de la musculatura abdominal; la trepopnea, que
aparece durante el decúbito lateral, en relación con hemiparálisis diafragmática, derrame pleural unilateral
o IC; la disnea paroxística nocturna aparece durante el descanso nocturno, obligando al paciente a
incorporarse y permanecer erguido, un síntoma típico de IC; la bendopnea, disnea que aparece al inclinarse
hacia delante (al colocarse los zapatos o calcetines), descrita en 2014 (estudio realizado por la Universidad
de Texas) en pacientes con IC avanzada, que traduce un aumento de las presiones de llenado (su valor
pronóstico no se conoce claramente y su utilidad radica principalmente en casos en los que la valoración de
la ingurgitación yugular sea difícil).
1. Disnea aguda
La disnea aguda aparece en el transcurso de horas o días y representa un motivo de consulta
frecuente en los servicios de urgencias. Es una situación potencialmente grave, por lo que requiere siempre
atención médica urgente y diagnóstico precoz.
El diagnóstico diferencial es muy amplio, e incluye alteraciones de la vía aérea superior, de la pared
torácica, pulmonares, cardiacas, tóxico-metabólicas, neurológicas y otras (Tabla I). No obstante, las causas
más frecuentes de disnea aguda son: IC descompensada, neumonía, agudización de la enfermedad
pulmonar obstructiva crónica (EPOC), tromboembolismo pulmonar (TEP) o exacerbación asmática.
La aproximación al paciente comienza con la valoración de la gravedad, de la necesidad de
oxigenoterapia y soporte ventilatorio, y con una sospecha diagnóstica provisional que oriente las pruebas
complementarias y el tratamiento iniciales. En muchos casos la estabilidad clínica permite esperar los
resultados de dichas pruebas para emitir un diagnóstico más concreto y un tratamiento adecuado.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [110]
[7] DISNEA E INSUFICIENCIA RESPIRATORIA
Tabla I.Causas de disnea aguda.
1.1. Valoración inicial de la gravedad
Las constantes vitales y una exploración física somera permiten identificar rápidamente los
pacientes con signos de gravedad, distrés respiratorio o fracaso respiratorio inminente (Tabla II). En estos
casos lo prioritario es: oxigenoterapia, garantizar un acceso venoso y extracción sanguínea para estudios de
laboratorio, valorar la necesidad de intubación y/o soporte ventilatorio, monitorización cardiorrespiratoria
y una evaluación clínica inicial para descartar causas graves potencialmente reversibles (neumotórax a
tensión, taponamiento cardiaco, cuerpo extraño en la vía aérea superior, anafilaxia y arritmias graves).
Tabla II.Signos de gravedad en la disnea aguda.
1.2. Historia clínica y exploración física
Es fundamental para un enfoque clínico adecuado, aunque en los casos más graves puede ser difícil
de obtener del paciente. Son importantes la cronología, la intensidad y la modalidad de la disnea, los
síntomas acompañantes (fiebre, dolor torácico, tos productiva, hemoptisis y síncope), traumatismo previo,
cirugía o inmovilización recientes, exposición o consumo de tóxicos, alérgenos. Los antecedentes
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [111]
[7] DISNEA E INSUFICIENCIA RESPIRATORIA
personales (EPOC, asma e insuficiencia cardiaca) y el tratamiento habitual orientan al diagnóstico más
probable. La necesidad previa de intubación orotraqueal supone un mayor riesgo de mala evolución. En el
momento del examen físico, además de los signos vitales y de gravedad mencionados, debe realizarse un
examen completo incidiendo en el sistema cardiorrespiratorio. Sin embargo, la sensibilidad y especificidad
de la exploración son limitadas, y la ausencia de signos patológicos no descarta enfermedad subyacente.
1.3. Pruebas complementarias
Se realizarán de forma dirigida, en función de la sospecha clínica, aunque los análisis de laboratorio
básicos, la radiografía de tórax y el electrocardiograma (ECG) están indicados en la gran mayoría de los
casos.
Radiografía de tórax: puede mostrar hallazgos sugerentes de IC, neumonía, derrame pleural,
neumotórax significativo o atrapamiento aéreo (bilateral sugiere asma o EPOC; unilateral,
cuerpo extraño en la vía aérea). Los neumotórax pequeños, las neumonías incipientes, la
mayoría de los pacientes asmáticos y hasta un 20% de las insuficiencias cardiacas pueden
cursar con radiografía normal o no diagnóstica.
ECG: es fundamental en el diagnóstico de isquemia miocárdica aguda (cambios en el ST-T,
aunque en el 20% de los casos es normal). También es de utilidad cuando muestra signos
típicos de TEP (taquicardia sinusal, patrón S1Q3T3, signos de sobrecarga derecha), o de
taponamiento cardiaco (bajos voltajes, alternancia eléctrica), pero es frecuente que estas
entidades cursen con alteraciones inespecíficas.
Pulsioximetría, gasometría arterial y venosa: se realizarán, si es posible, en la situación basal del
paciente (respirando aire ambiente o con su oxigenoterapia habitual). La gasometría arterial es
más fiable y precisa, pero puede ser frecuentemente sustituida por gasometría venosa y
pulsioximetría (ver Apartado “Insuficiencia respiratoria”).
Biomarcadores: la medición de troponinas, péptidos natriuréticos (BNP o NT-proBNP) y dímeros
D es de utilidad, pero no deben solicitarse rutinariamente. Las troponinas (TnT y TnI) son
fundamentales en el diagnóstico del síndrome coronario agudo e infarto miocárdico, pero
pueden ser normales al inicio, o elevarse en otro tipo de situaciones (ver Capítulo 23.
Cardiopatía isquémica). Los péptidos natriuréticos son de utilidad en el diagnóstico de
insuficiencia cardiaca, pero pueden elevarse por otras causas de sobrecarga de volumen (fallo
hepático o renal), TEP e hipertensión pulmonar crónica. Un NT-proBNP inferior a 500 pg/ml
(BNP < 100 pg/ml) tiene un valor predictivo negativo (VPN) superior al 90% para IC; mientras
que si es superior a 2.000 (BNP > 500), su valor predictivo positivo supera el 90% (Tabla III) Los
dímeros D están indicados ante una sospecha de baja-intermedia probabilidad de TEP, por su
elevado VPN en estos casos. No deben emplearse cuando la sospecha es alta.
Tomografía computarizada (TC) torácica y gammagrafía de ventilación-perfusión: la angio-TC
torácica es generalmente de elección para confirmar un diagnóstico de TEP. También es de
utilidad en la insuficiencia cardiaca, neumonía, neoplasia y atelectasia, aunque no suele ser
necesaria. La gammagrafía es una alternativa diagnóstica en el TEP si la radiografía es normal,
en centros donde esté disponible, especialmente si existe contraindicación para la TC (ver
Capítulo 32. “Enfermedad tromboembólica venosa”).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [112]
[7] DISNEA E INSUFICIENCIA RESPIRATORIA
Tabla III.Puntos de corte para BNP y NT-pro-BNP recomendados ante la sospecha de insuficiencia cardiaca (IC).
2. Disnea crónica
Se define como crónica la disnea de duración superior a 4-8 semanas. Sus causas son múltiples,
aunque la mayoría de los casos se deben a IC e isquemia miocárdica, asma, EPOC, enfermedades
intersticiales pulmonares, origen psicógeno o desacondicionamento físico/obesidad. Las causas de la disnea
crónica y sus datos característicos se exponen en la tabla IV.
En ausencia de una enfermedad cardiopulmonar evidente que explique los síntomas, no está claro
cuál es el mejor esquema diagnóstico del paciente con disnea crónica. La valoración clínica (anamnesis y
examen físico) es fundamental para orientar el diagnóstico y elegir adecuadamente las pruebas iniciales,
pero la primera impresión diagnóstica solo permite acertar la etiología en dos tercios de los casos. En
función de la sospecha se propone un estudio en etapas o escalones: valoración clínica, pruebas
complementarias iniciales, estudios más complejos y estudios avanzados.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [113]
[7] DISNEA E INSUFICIENCIA RESPIRATORIA
Tabla IV.Etiología de la disnea crónica y datos característicos.
2.1. Historia clínica
Es importante recoger la cronología de la disnea (tiempo de evolución, progresión), relación con el
esfuerzo, intensidad o grado de disnea (empleando escalas como la Modified Medical Research Council
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [114]
[7] DISNEA E INSUFICIENCIA RESPIRATORIA
[Tabla V], o específicamente en la insuficiencia cardiaca, la New York Heart Association [Tabla VI]),
síntomas asociados (tos, edemas, dolor torácico, artralgias, Raynaud, debilidad muscular), exposición previa
al tabaco e historia ocupacional, o uso de fármacos.
Tabla V. Escala de graduación de la disnea de la Modified Medical Research Council (mMRC).
Tabla VI. Clasificación funcional de la insuficiencia cardiaca según la New York Heart Association (NYHA).
2.2. Examen físico
Se debe realizar una exploración completa, haciendo hincapié en la vía aérea superior y el tórax. La
presencia de alteraciones anatómicas (orofaringe, bocio) o estridor pueden indicar obstrucción de la vía
aérea superior. Las deformidades de la caja torácica indican trastornos ventilatorios (cifoescoliosis,
hiperinsuflación). La presencia de elevación del pulso venoso yugular refleja resistencia aumentada al
llenado del ventrículo derecho. La presencia de sibilancias orienta a obstrucción de la vía aérea o asma
cardial. Los roncus indican obstrucción de la vía aérea por secreciones espesas. Los crepitantes sugieren
ocupación alveolar por moco o agua; cuando son simétricos orientan a IC, cuando están localizados indican
proceso infeccioso/ inflamatorio (foco neumónico y bronquiectasias); los crepitantes finos “en velcro”,
bibasales, son típicos de las enfermedades intersticiales pulmonares. La auscultación cardiaca puede
mostrar arritmias, soplos de valvulopatías o roce pericárdico. La existencia de reflujo hepatoyugular sugiere
insuficiencia cardiaca derecha. Otros datos relevantes son la presencia de ascitis, edemas periféricos o
debilidad muscular.
2.3. Estudios iniciales
Aunque se orientarán en función de la sospecha clínica, los exámenes iniciales incluyen
generalmente análisis básicos de sangre, radiografía de tórax, ECG y posiblemente (según sospecha)
espirometría.
Laboratorio (hemograma, bioquímica y gasometría): permite descartar anemia, causas
metabólicas, hipercapnia o trastornos tiroideos. El péptido natriurético apoya o descarta un
origen cardiogénico. La presencia de D-dímeros normales descarta el tromboembolismo agudo.
Radiografía de tórax: puede mostrar alteraciones anatómicas, masas, signos de EPOC
(atrapamiento aéreo) o insuficiencia cardiaca (cardiomegalia, signos congestivos),
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [115]
[7] DISNEA E INSUFICIENCIA RESPIRATORIA
bronquiectasias, masas, afectación intersticial, enfermedad pleural, etc. No está indicado de
rutina en la sospecha de asma. Una radiografía normal no descarta enfermedad pulmonar
intersticial.
ECG: puede mostrar alteraciones del ritmo o la frecuencia, signos de isquemia o necrosis,
crecimiento o sobrecarga de cavidades, bajos voltajes (obesidad, atrapamiento aéreo, derrame
pericárdico). Un ECG completamente normal con BNP/NT-proBNP bajo hace muy poco
probable un origen cardiaco de la disnea.
Espirometría con/sin test broncodilatador (Tabla VII): si existe una sospecha clara de EPOC o
asma se solicitará de inicio. El patrón obstructivo es típico (aunque no exclusivo) de la EPOC y
del asma. Habitualmente en el asma existe reversibilidad con broncodilatadores, a diferencia
de la EPOC. El patrón restrictivo sugiere enfermedad intersticial pulmonar, enfermedad pleural,
trastornos de la caja torácica, obesidad o enfermedad neuromuscular.
Tabla VII.Interpretación de las pruebas de función respiratoria.
2.4. Estudios de segunda línea
Se realizan de forma dirigida, cuando los estudios iniciales no sean concluyentes pero orienten a
alguna patología. También cuando estos hayan sido negativos, pero persista la clínica y la sospecha de
enfermedad subyacente.
Otras pruebas de función respiratoria: indicados ante la sospecha de enfermedad pulmonar
intersticial, o si los resultados de la espirometría no permiten aclarar el diagnóstico. Si la
sospecha inicial es alta se realizan de inicio junto con la espirometría. Si esta no se realizó
previamente, se solicitará en esta segunda etapa.
Medición de volúmenes pulmonares mediante pletismografía: indicado ante el hallazgo
de una capacidad vital forzada significativamente disminuida, especialmente ante la
coexistencia de un patrón obstructivo, ya que permite diferenciar entre la capacidad
vital disminuida por atrapamiento aéreo (volumen residual [VR] con capacidad
pulmonar total [CPT] aumentados) y la verdadera restricción pulmonar (CPT disminuida
y VR normal/bajo) (Tabla VII). Si se sospecha un origen muscular se solicitarán
presiones inspiratoria y espiratoria máximas, ventilación máxima en un minuto y
espirometría en supino y sedestación. La valoración de la curva flujo-volumen es útil
ante la sospecha de obstrucción de la vía aérea superior.
Test de broncoconstricción: en pacientes con disnea episódica o recurrente, sospecha
de asma y espirometría normal o casi normal. En estos casos se prefiere el test de
broncoconstricción al ensayo terapéutico empírico (Capítulo 29: Asma y enfermedad
pulmonar obstructiva crónica).
Difusión del monóxido de carbono (DLCO): útil en la evaluación de disnea,
especialmente ante la sospecha de enfermedad intersticial pulmonar (patrón
restrictivo, DLCO baja), enfisema o bronquiolitis (patrón obstructivo, DLCO baja) o
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [116]
[7] DISNEA E INSUFICIENCIA RESPIRATORIA
enfermedad vascular pulmonar (espirometría y volúmenes pulmonares normales, DLCO
baja).
TC torácica: se realizará una TC de alta resolución (TACAR) ante la sospecha de enfermedad
pulmonar intersticial (crepitantes secos, patrón restrictivo espirométrico, descenso de la DLCO),
incluso si la radiografía simple es normal, lo que puede suceder en fases iniciales. También es
útil para cuantificar el grado de enfisema en la EPOC. Si se sospecha una masa obstructiva se
indicará una TC torácica con contraste. Ante la posibilidad de TEP crónico (descenso de DLCO,
función pulmonar normal, factores de riesgo) es preciso realizar una angio-TC o,
alternativamente, una gammagrafía de ventilación-perfusión.
Ecocardiograma (ETT): está indicado ante la sospecha de insuficiencia cardiaca o hipertensión
pulmonar, ya sea por hallazgos clínicos, elevación de BNP/NT-proBNP, cardiomegalia,
alteraciones electrocardiográficas o ausencia de diagnóstico tras el estudio previo. Permite
determinar la función sistólica y diastólica, estado de las válvulas, valorar datos de pericarditis
constrictiva y estimar la presión pulmonar.
2.5. Estudios avanzados
Son pruebas complejas indicadas en situaciones concretas, y generalmente precisan de derivación o
consulta al especialista correspondiente. Ante la sospecha de enfermedad intersticial pulmonar está
indicada la realización de broncoscopia con lavado broncoalveolar y/o biopsia transbronquial, o biopsia
pulmonar abierta. Será preciso realizar un cateterismo de cavidades derechas para confirmar una
hipertensión pulmonar sugerida por ETT. El ecocardiograma de estrés y las pruebas de esfuerzo
cardiopulmonar pueden ser útiles en pacientes con disnea de esfuerzo persistente de etiología no aclarada
y que no responden al acondicionamiento físico.
2.6. Disnea crónica con estudio normal
En algunas ocasiones las pruebas mencionadas mostrarán resultados normales o alteraciones leves
e inespecíficas. La mayoría de estos casos se deberán a desacondicionamiento físico u obesidad, quizás con
matices psicógenos (ansiedad y depresión). Se recomienda una explicación detallada del resultado de las
pruebas, un programa de acondicionamiento físico y la reevaluación en 6-12 meses, ya que muy raramente
una causa tratable de disnea puede pasar desapercibida en el estudio inicial.
II. INSUFICIENCIA RESPIRATORIA
1. Concepto y definiciones
Según Campbell y cols. (1965), estamos ante insuficiencia respiratoria (IR) cuando un sujeto en
reposo, respirando aire ambiente y al nivel del mar, tiene una presión parcial de oxígeno arterial (PaO2)
menor de 60 mm Hg, acompañada o no de una presión parcial de dióxido de carbono arterial (PaCO2)
mayor de 45 mm Hg. Niveles inferiores se consideran inadecuados para cubrir las demandas del
metabolismo celular.
La respiración es entendida como una cadena compuesta por distintos eslabones (sistema nervioso
central y periférico, músculos respiratorios, caja torácica, vías respiratorias, parénquima pulmonar, sistema
cardiovascular y hemoglobina) que interaccionan continuamente. Por tanto, la insuficiencia respiratoria
debe de ser considerada un síndrome, y como tal cuenta con múltiples etiologías posibles.
Existen distintos términos que hacen referencia a la utilización de oxígeno y de dióxido de carbono.
La hipoxemia es el descenso de la PaO2 que se sitúa entre 60-79 mm Hg. La hipoxia define un nivel bajo de
aporte de oxígeno a los tejidos en relación con sus necesidades, se correlaciona con PaO2 menor a 60 mm
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [117]
[7] DISNEA E INSUFICIENCIA RESPIRATORIA
Hg. La hipercarbia o hipercapnia es la elevación de la PaCO2 por encima de 45 mm Hg. La disnea es el
síntoma clínico (descrito previamente).
2. Clasificación
2.1. Según su cronología
IR aguda (IRA): instauración en un corto periodo de tiempo, en minutos, horas o días, sin
haberse producido aún mecanismo de compensación.
IR crónica (IRC): de instauración en semanas o meses. Más que el tiempo de evolución, la
existencia de IRC viene marcada por la presencia de mecanismos de compensación para evitar
hipoxia tisular (poliglobulia, vasoconstricción pulmonar, etc.).
IRC agudizada (IRCA): se establece en pacientes con IRC que sufren descompensaciones agudas
de su enfermedad de base, con empeoramiento secundario del intercambio gaseoso (en cifras,
variación de los valores de PaO2 o PaCO2 de más de 5 mm Hg respecto a la situación de
estabilidad).
2.2. Según su mecanismo fisiopatológico
IR hipoxémica o parcial (tipo 1): ocasionada por fallo de la oxigenación. Se define por una PaO2
< 60 mm Hg con PaCO2 normal o baja.
IR hipercápnica, mixta o global (tipo 2): ocasionada por fallo de la ventilación. Coexiste además
de hipoxemia la presencia de hipercarbia. Se define por una PaO2 < 60 mm Hg y una PaCO2 >
45 mm Hg.
2.3. Según el gradiente alvéolo-arterial de oxígeno (A-aO2):
IR con gradiente elevado: afectación de origen intrapulmonar.
IR con gradiente normal: afectación de origen extrapulmonar.
El gradiente alvéolo arterial de oxígeno es un excelente indicador de la eficacia del parénquima
pulmonar en el intercambio gaseoso. Para ello debemos primero calcular la presión alveolar:
PAO2 = [(PB – PH2O) × FiO2] – (PaCO2/R)
Donde PAO2 es la media de PO2 alveolar; PB presión barométrica (760 mm Hg a nivel del mar);
PH2O presión del vapor de agua a 37º (47 mm Hg); FiO2 concentración fraccional de oxígeno inspirado;
PaCO2 es la PCO2 alveolar (se asume que es igual a PCO2 arterial); y R índice de intercambio respiratorio
(cuyo valor es 0,8). En un individuo al nivel del mar respirando aire ambiente (FiO2 del 21%) esta fórmula se
simplificaría en: 149 – (1,25 × PaCO2)
Y finalmente la ecuación:
Gradiente A-aO2 = PAO2 – PaO2
La PaO2 es la presión arterial medida en mm Hg por gasometría arterial. En condiciones normales el
gradiente es de 15-20 mm Hg. Sin embargo, lo más adecuado es ajustarlo de acuerdo a la edad del paciente
con la siguiente fórmula:
A-aO2 = 2,5 + (0,21 × edad).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [118]
[7] DISNEA E INSUFICIENCIA RESPIRATORIA
Aplicar los criterios clasificatorios permite establecer una definición inicial del cuadro clínico:
existencia o no de insuficiencia respiratoria, su cronología, mecanismo fisiopatológico inicial y la existencia
o no de gradiente A-aO2. Partiendo de este punto podremos orientar mejor el abordaje diagnóstico y
terapéutico.
3. Fisiopatología
Existen cinco mecanismos que pueden ocasionar IR (Tabla VIII, Figura 1). Todos ellos pueden
asociarse y aparecer simultáneamente en un enfermo. Sin embargo, la contribución de cada uno es variable
y depende, en cada caso concreto, de la enfermedad de base responsable de la IR.
Figura 1.Diagnóstico fisiopatológico de la hipoxemia.
4. Etiología (Tablas VIII, IX y X)
Tabla VIII.Fisiopatología de la insuficiencia respiratoria.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [119]
[7] DISNEA E INSUFICIENCIA RESPIRATORIA
Tabla IX.Etiología de la insuficiencia respiratoria aguda (IRA).
Tabla X.Causas de agudización de la insuficiencia respiratoria crónica.
5. Diagnóstico (Figuras 2 y 3)
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [120]
[7] DISNEA E INSUFICIENCIA RESPIRATORIA
Figuras 2 y 3.Algoritmos diagnósticos de las insuficiencias respiratorias aguda y crónica.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [121]
[7] DISNEA E INSUFICIENCIA RESPIRATORIA
5.1. Historia clínica y exploración física
(Ver Apartados “Disnea aguda” y “Disnea crónica”), prestando especial atención a los signos y
síntomas de gravedad (Tabla II).
5.2. Pruebas complementarias
Gasometría arterial: establece el diagnóstico y la gravedad de la IR, y facilita su clasificación y
seguimiento. Se realiza respirando aire ambiente o con FiO2 conocida, siempre que sea posible
(las gafas nasales no permiten el cálculo exacto de la FiO2). Además de la oxigenación, informa
sobre la ventilación alveolar (PaCO2) y el equilibrio ácido-base, permitiendo diferenciar entre
procesos agudos, crónicos y crónicos-agudizados:
IR hipercápnica aguda: cursa habitualmente con PaCO2 elevada y acidosis no
compensada (bicarbonato normal/bajo y pH bajo).
IR hipercápnica crónica: cursa habitualmente con PaCO2 elevada en presencia de
acidosis compensada (bicarbonato elevado, pH normalizado).
IR hipercápnica crónica agudizada: cursa habitualmente con PaCO2 elevada en
presencia de acidosis parcialmente compensada (bicarbonato elevado y pH bajo).
La gasometría venosa es menos fiable, pero más fácil de obtener. Combinada con la
pulsioximetría es generalmente suficiente para determinar la situación respiratoria, el estado
ácidobase y descartar una hipercapnia significativa, sobre todo durante la evolución (evitando
repetir las punciones arteriales). Respecto a la gasometría arterial, el pH venoso es 0,03-0,05
unidades más bajo, el bicarbonato 1-2 mEq/l más alto, y la PaCO2 3-8 mm Hg mayor. Otros
datos que podemos extraer:
Gradiente alvéolo-arterial: su aumento indica alteración en la ventilación/perfusión o existencia
de efecto shunt.
Otra forma simplificada de valorar la existencia de shunt es mediante la suma de la PaO2 y la
PaCO2. Un resultado menor a 100 mm Hg sugiere efecto shunt; si es mayor a 120 mm Hg indica
hipoventilación.
Cálculo de la Pa/FiO2 (PaFi): resultado de la división de la presión arterial de O2 entre la
fracción inspirada. Permite monitorizar la gravedad del daño pulmonar y comparar al sujeto
consigo mismo durante la evolución del cuadro.
Pulsioximetría: permite estimar de forma no invasiva la oxigenación arterial, aunque no
sustituye a los datos obtenidos por una gasometría arterial. En condiciones normales una
saturación de oxígeno del 90% y 95% se corresponden con una PaO2 de 60 y 80 mm Hg,
respectivamente. Su fiabilidad disminuye cuando la saturación de oxígeno está por debajo del
70%, hay hipoperfusión periférica grave, anemia extrema, hipotermia, metahemoglobinemia o
ictericia. No es útil ante la sospecha de intoxicación por monóxido de carbono, pues no
diferencia entre oxi- y carboxihemoglobina. En estos casos es necesaria la medición de
carboxihemoglobina arterial (o venosa), pues la PaO2 arterial tampoco se altera (ver Capítulo
89. “Intoxicaciones”).
Laboratorio: generalmente están indicados un hemograma y bioquímica básicos. Los
biomarcadores pueden ser de utilidad en un contexto clínico adecuado (ver Apartado “Disnea
aguda”).
Pruebas de imagen:
La radiografía de tórax, a pesar de ser poco específica y observador dependiente, tiene una
utilidad clara, siendo obligatoria su realización. Se distinguen cuatro patrones radiológicos
básicos: a) normal; b) opacidades pulmonares difusas; c) opacidades pulmonares localizadas; y
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [122]
[7] DISNEA E INSUFICIENCIA RESPIRATORIA
d) patología extrapulmonar (Tabla VII). La ecografía clínica, realizada por personal entrenado,
tiene cada vez más aplicaciones en el ámbito de urgencias. Permite la confirmación de
sospechas diagnósticas (insuficiencia cardiaca, derrame pleural, neumotórax, neumonía,
trombosis venosa profunda) y es útil como guía para la realización de procedimientos invasivos
diagnósticos o terapéuticos (toracocentesis).
Electrocardiograma (ver Apartado “Disnea aguda y crónica”).
Pruebas de función respiratoria: son especialmente útiles en el estudio y seguimiento de la
insuficiencia respiratoria crónica (ver Apartado “Disnea crónica”).
Otras pruebas: dependerán de la sospecha diagnostica (TC torácica, gammagrafía de
ventilación/perfusión y ecocardiografía).
6. Tratamiento
Los objetivos del tratamiento son: corrección de la hipoxemia y de la hipoventilación alveolar,
disminución del trabajo respiratorio, tratar el proceso patológico subyacente y los factores
desencadenantes y prevenir la aparición de complicaciones.
6.1. Medidas generales
En todo paciente se debe: 1) asegurar la permeabilidad de la vía aérea mediante aspiración de
secreciones, retirada de cuerpos extraños, uso de cánula de Guedel o intubación orotraqueal si fuera
necesario (ver Capítulo 2. Técnicas y procedimientos instrumentales); 2) canalizar vía venosa; 3) asegurar
una nutrición e hidratación adecuadas; 4) evitar medicación depresora del sistema nervioso central; 5)
reducir el requerimiento de O2 y la producción de CO2 (reposo, control de la fiebre); 6) asegurar un buen
transporte de O2 (corrección de anemia, control del gasto cardiaco); 7) favorecer la eliminación de las
secreciones respiratorias mediante el drenaje postural, sesiones de fisioterapia o incluso aspiración
mecánica a través del fibrobroncoscopio; 8) profilaxis de la enfermedad tromboembólica venosa y del
sangrado digestivo.
6.2. Tratamiento etiológico
Tanto de la enfermedad subyacente como de los factores desencadenantes.
6.3. Oxigenoterapia
En el tratamiento de la IR lo más importante es corregir la hipoxemia para lograr cuanto antes un
apropiado aporte de oxígeno a los tejidos, y evitar los efectos nocivos de la hipoxia. El objetivo principal es
mantener una PaO2 por encima de 60 mm Hg o una saturación de oxígeno mayor del 90%. No se deben
tolerar valores inferiores a 50 mm Hg, incluso en pacientes con hipercapnia crónica y riesgo de depresión
respiratoria. Los métodos de administración de oxígeno son los siguientes:
Oxigenoterapia de bajo flujo. Se administra mediante gafas nasales. El gas que respira el
paciente es una mezcla entre O2 al 100% y aire ambiente. La FiO2 que proporcionan no es
estable, pues varía en función del patrón ventilatorio del paciente: a mayor ventilación es
menor la FiO2 y al contrario. Son cómodas y permiten la alimentación oral simultánea, pero los
flujos elevados producen efecto irritante local (a partir de 5 l/min). Son el método de elección
en la IRC y son útiles en la IRA leve.
Oxigenoterapia de alto flujo.
Las mascarillas con efecto Venturi (tipo Ventimask®) proporcionan oxígeno a FiO2
elevadas, de forma fiable y constante, independientemente del patrón ventilatorio. Es
necesario asegurarse de que el paciente mantiene, en el transcurso de su evolución,
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [123]
[7] DISNEA E INSUFICIENCIA RESPIRATORIA
una ventilación alveolar adecuada. Es el método de elección en la IRA. Permite alcanzar
FiO2 entre 0,24 y 0,5. Si se usan flujos bajos (< 5 l/min) hay riesgo de reinhalación de
CO2.
Las mascarillas con reservorio presentan una válvula unidireccional, que evita la
reinhalación, y cuya integridad debe ser vigilada. Conectada a una fuente de oxígeno al
100%, permite una FiO2 aproximada de 0,8-0,9.
Existen otros tipos de oxigenoterapia “no convencional” a alto flujo, obteniendo hasta
60 l/min a través de cánulas nasales calefactadas y humidificadas (Optiflow
Fisher&Paykel Anclan, Au®) que incluso permiten bajos valores de continuous positive
airway pressure 1-2 cm H2O y que pueden ser útiles en pacientes con IRCA, aunque su
papel está aún por definir.
Oxigenoterapia crónica domiciliaria. Indicada en pacientes con patologías crónicas que cursen
con IRC. Si se emplea un mínimo de 16-18 horas diarias la oxigenoterapia prolonga la vida,
disminuye el número de ingresos por agudizaciones, desciende la presión de la arteria
pulmonar y mejora las funciones neuropsíquicas de los pacientes. Son candidatos todos los
pacientes que, en situación basal y estable, con tratamiento optimizado presenten una PaO2 ≤
55 mm Hg o SaO2 ≤ 88%. También los pacientes con PaO2 56-59 mm Hg o SaO2 89% si se
acompañan de hipertensión pulmonar, policitemia (hematocrito > 55%) o signos de
insuficiencia cardiaca derecha. En pacientes con PaO2 basal > 60 mm Hg, pero con desaturación
durante el ejercicio o el sueño, podría valorarse el uso de oxigenoterapia portátil o nocturna,
respectivamente. Las fuentes de oxígeno se pueden clasificar en sistemas estáticos y fuentes
portátiles. Los sistemas estáticos son útiles en pacientes que precisen oxígeno a bajo flujo y que
puedan realizar salidas esporádicas sin él. Los concentradores de oxígeno son los prescritos con
más frecuencia para el uso domiciliario, y precisan de conexión a la red eléctrica. Los sistemas
portátiles se utilizan cuando los pacientes no pueden interrumpir la terapia y sin embargo
precisan salir de su domicilio durante horas. Los encontramos de dos tipos: con flujos
continuos, que incluyen cilindros de oxígeno que se pueden transportar con facilidad; o con
tecnología de conservación (“flujo a demanda”), que suministran oxígeno de forma
intermitente cuando el paciente realiza esfuerzo inspiratorio.
6.4. Ventilación mecánica
En situaciones de insuficiencia respiratoria grave, especialmente con fracaso ventilatorio asociado,
puede ser necesario el uso de soporte ventilatorio (invasivo o no invasivo), tanto de manera aguda como
crónica (ver Capítulo 35. “Principios de ventilación mecánica”).
6.5. Otros
En el caso de insuficiencia respiratoria crónica hay que tomar medidas dirigidas a mejorar el
intercambio gaseoso y prevenir complicaciones. Se incluyen el abandono del hábito tabáquico, corrección
de desequilibrios nutricionales, prevención de infecciones (vacunación antineumocócica y antigripal),
manejo de secreciones respiratorias y, por último, considerar rehabilitación respiratoria.
BIBLIOGRAFÍA
Barbara Heil B, Wilson Tang WH. Biomarkers: Their potential in the diagnosis and treatment of heart
failure. Cleveland Clinic J Med. 2015;82(S2):S28-S35.
Ganzo M, Martínez E, Segado A, Maganto A. Interpretación de la gasometría arterial en enfermedades
respiratorias. Medicine. 2015;11(88):5284-8.
Kim HN, Januzzi JL. Natriuretic peptide testing in heart failure. Circulation. 2011;123:2015-19.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [124]
[7] DISNEA E INSUFICIENCIA RESPIRATORIA
Levy BD, Choi AK. Síndrome de insuficiencia respiratoria aguda. Harrison. Principios de Medicina
Interna, 19.º ed. New York (NY): McGraw-Hill; 2016 [consultado 11 Sep 2016]. Disponible en:
http://harrisonmedicina. mhmedical.com/content.aspx?bookid=1717&Sectionid=114931963
Marcos MC, Gómez Punter RM, Diab Cáceres L, Vázquez Espinosa E. Insuficiencia respiratoria crónica.
Tratamiento. Medicine. 2014;11(63):3742-7.
Miller MR, Crapo R, Hankinson J, et al. General considerations for lung function testing. Eur Respir J.
2005;26:153-61.
O’Driscoll B, Howard L, Davison A. BTS guideline for emergency oxygen use in adult patients. Thorax.
2008;63(Suppl VI):vi1-vi68.
Organización médica colegial de España. Guía de buena práctica clínica en Insuficiencia respiratoria.
España. International Marketing & Comunications, S.A.; 2011.
Ortega F, Diaz Salvador, Galdiz J, et al. Oxigenoterapia continua domiciliaria. Arch Bronconeumol.
2014;50(5):185-200.
Parshall MB, Schwartzstein RM, Adams L, et al. An Official American Thoracic Society Statement:
Update on the mechanisms, assessment, and management of dyspnea. Am J Respir Crit Care Med.
2012;185(4):435-52.
Pratter MR, Abouzgheib W, Akers S, et al. An algorithmic approach to chronic dyspnea. Respir Med.
2011;105(7):1014-21.
Schwartzstein RM. Approach to the patient with dyspnea. [Monografía en Internet]. Waltham (MA).
UpToDate, Post TW (Ed); 2015 [consultado 11 Ene 2016]. Disponible en: http://www.uptodate.com/
Schwartzstein RM. Disnea. En: Kasper D, Fauci A, Hauser S, editores. Harrison. Principios de Medicina
Interna, 19 ed. New York, NY: McGraw-Hill; 2016.
Singer AJ, Thode HC Jr, Green GB, et al. The incremental benefit of a shortness-of-breath biomarker
panel in emergency department patients with dyspnea. Acad Emerg Med. 2009;16(6):488.
Stratton S. Acute respiratory failure [monografía en Internet]. London: BMJ Publishing Group Ltd; 2015
[acceso el 10 de febrero de 2016]. Disponible en:
http://bestpractice.bmj.com/bestpractice/monograph/853.html
Thibodeau JT, Turer AT, Gualano SK, et al. Characterization of a novel symptom of advanced heart
failure: Bendopnea. CHF. 2014;2(1):24-31.
Trullàs JC, Casadob J, Morales-Rull JL. Dificultad del diagnóstico de insuficiencia cardiaca en el
paciente con comorbilidad. Rev Clin Esp. 2016;216(5):276-285.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [125]
[8] SÍNCOPE
8. Síncope
Adrián García Villa.
Medicina Interna
Juan Salas Jarque.
Medicina Interna
Asesor:
Alberto Moreno Fernández.
Médico Adjunto de Medicina Interna
I. CONCEPTO
El síncope es una pérdida transitoria de la consciencia debida a una hipoperfusión cerebral global
que asocia una pérdida del tono postural y que se caracteriza por tener inicio rápido, duración corta y
recuperación espontánea completa, sin dejar déficit neurológico tras él ni necesitar ningún tipo de
cardioversión. Es relativamente frecuente, representando hasta el 3% de los motivos de consulta en los
servicios de urgencias. Con el término presíncope se define el estado de enturbiamiento de consciencia e
inestabilidad postural que finalmente no llega a desarrollar completamente un episodio sincopal.
II. FISIOPATOLOGÍA
Los distintos tipos de síncope se caracterizan por una caída de la tensión arterial sistémica que
causa una disminución del flujo sanguíneo cerebral. La cifra de tensión arterial queda determinada por el
gasto cardiaco y por la suma de las resistencias vasculares periféricas, de modo que una reducción de
cualquiera de estos dos factores puede favorecer la aparición de un síncope, si bien a menudo suele
deberse a una combinación de ambos.
III. ETIOLOGÍA
Según los mecanismos fisiopatológicos que producen el síncope se distinguen varias categorías
(Tablas I y II).
1. Síncope reflejo (neuromediado)
Se refiere a aquellas situaciones en las que los reflejos cardiovasculares que normalmente son
útiles para controlar la circulación se vuelven intermitentemente inadecuados en respuesta a un
desencadenante y producen vasodilatación o bradicardia, lo que conlleva una caída en la presión arterial y
en la perfusión cerebral global. Según el desencadenante pueden clasificarse en:
Síncope vasovagal: se desencadena por estímulos emocionales o por estrés ortostático.
Habitualmente se precede de síntomas prodrómicos de activación autónoma (sudoración,
palidez, náuseas).
Síncope situacional: se desencadena por ciertas circunstancias específicas, como la tos, el
estornudo, la estimulación gastrointestinal (tragar, defecar, dolor visceral), tras la micción, el
ejercicio, la ingesta u otras circunstancias (risa, tocar instrumentos de viento, levantar pesas).
Síncope del seno carotídeo: causa rara de síncope (supone aproximadamente el 1%), producido
por hiperactivación vagal tras la presión en la región lateral del cuello. Se diagnostica
reproduciéndolo mediante masaje del seno carotídeo y debe sospecharse cuando se
desencadena con los movimientos bruscos de la cabeza, al afeitarse o en síncopes recurrentes
en pacientes de edad avanzada.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [126]
[8] SÍNCOPE
Formas atípicas: situaciones en que se produce síncope reflejo con desencadenantes inciertos o
incluso sin ellos. El diagnóstico en estos casos se apoya menos en la sola historia clínica y más
en la exclusión de otras causas de síncope (ausencia de cardiopatía estructural) y en la
reproducción de síncopes similares en la mesa basculante.
Tabla I.Clasificación del síncope.
2. Síncope debido a hipotensión ortostática
A diferencia del síncope reflejo, en este caso la actividad simpática eferente está crónicamente
alterada, de forma que la vasoconstricción es deficiente y no se adapta adecuadamente al ortostatismo.
Así, al ponerse de pie, la presión arterial cae y aparece un síncope o un presíncope. Conviene señalar que el
síncope es solo uno de los síntomas que puede expresar una intolerancia ortostática, pudiendo haber otros
como mareo, inestabilidad, palpitaciones, sudoración o alteraciones de la visión y de la audición. Las
distintas causas potencialmente responsables de intolerancia ortostática se detallan en la tabla I.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [127]
[8] SÍNCOPE
3. Síncope cardiaco
Se debe a una disminución repentina del gasto cardiaco, secundaria la mayor parte de las veces a
una arritmia y, en menor medida, a una cardiopatía estructural.
a) Arritmias
Suelen ser arritmias transitorias por lo que son difíciles de diagnosticar. El hecho de que una
arritmia determinada llegue a comprometer de tal forma el gasto cardiaco que induzca el síncope suele
estar relacionado con: una cardiopatía estructural subyacente, la postura (más frecuentemente en
bipedestación que en decúbito), la volemia o la medicación concomitante.
Las bradiarritmias pueden producirse a causa de una alteración en la generación de los impulsos
(por ejemplo, disfunción del nodo sinusal) o en su conducción (por ejemplo, bloqueo auriculoventricular).
En ambos casos puede aparecer un síncope si la frecuencia del marcapasos de escape es insuficiente para
mantener el gasto cardiaco. El síncope por bradicardia suele ocurrir repentinamente, sin síntomas
presincopales, y puede repetirse varias veces al día.
Los síncopes por taquiarritmias suelen ir precedidos de palpitaciones o aturdimiento, pero pueden
ocurrir repentinamente sin síntomas premonitorios. El síncope se desencadena en el inicio de la taquicardia
paroxística, antes de que se desarrolle la compensación vascular. Por regla general la consciencia se
recupera antes de que termine la taquicardia; en caso contrario ya no se considera síncope sino parada
cardiaca.
Diversos fármacos pueden causar bradiarritmias y taquiarritmias. Muchos fármacos antiarrítmicos
pueden producir bradicardia como consecuencia de su efecto sobre la función del nodo sinusal o la
conducción auriculoventricular. El síncope debido a torsades de pointes es relativamente frecuente y puede
precipitarse por la toma de fármacos que alargan el intervalo QT, especialmente en pacientes con síndrome
de QT largo.
b) Enfermedad estructural
Las enfermedades cardiovasculares estructurales pueden causar síncope cuando la demanda
circulatoria sobrepasa la capacidad limitada del corazón para aumentar su gasto cardiaco. El síncope se
relaciona con mayor riesgo de muerte súbita cuando se asocia a situaciones clínicas en que hay una
obstrucción dinámica o fija de la salida del ventrículo izquierdo, cuyas causas más frecuentes son la
estenosis aórtica y la miocardiopatía obstructiva. El tromboembolismo pulmonar también puede ser
responsable de síncope por compromiso de la precarga sobre el ventrículo izquierdo.
IV. ABORDAJE DIAGNÓSTICO
1. Anamnesis
En más del 50% de los casos la diferenciación entre un síncope y cualquier otra entidad responsable
de pérdida de consciencia real o aparente puede obtenerse a partir de una historia clínica detallada, pero a
veces puede ser extremadamente difícil. Se debe responder a las siguientes preguntas:
¿La pérdida de consciencia fue completa?
¿La pérdida de consciencia fue transitoria, de comienzo rápido y duración corta?
¿El paciente se recuperó espontánea y completamente y sin secuelas?
¿El paciente perdió el tono muscular?
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [128]
[8] SÍNCOPE
Si las respuestas a estas preguntas son afirmativas, el episodio tiene una alta probabilidad de ser un
síncope. Si la respuesta a una o más de estas preguntas es negativa, hay que excluir otras formas de
pérdida de consciencia antes de proceder al examen del síncope.
A partir de la evaluación inicial se puede definir la causa del síncope en hasta la mitad de los
pacientes. Las características clínicas que orientan a cada uno de los tipos de síncope se detallan en la tabla
II. La tabla III expone una serie de preguntas de utilidad para la aproximación diagnóstica del episodio.
Tabla II.Características clínicas según el tipo de síncope.
2. Exploración física
Debe estar centrada en los signos vitales, en la exploración cardiológica y en la neurológica. Por
tanto, hay que registrar las constantes vitales y la glucemia capilar. Se debe, asimismo, realizar un examen
físico sistemático en busca de soplos carotídeos, signos de mordedura lingual, auscultación cardiaca
patológica (arritmias, signos de cardiopatía estructural como soplos o tercer o cuarto tono), masas
pulsátiles abdominales, edemas en miembros inferiores, datos de trombosis venosa profunda, ausencia de
pulsos distales y focalidad neurológica.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [129]
[8] SÍNCOPE
Tabla III.Rasgos importantes de la historia clínica en el síncope.
3. Pruebas complementarias
Se deben realizar las siguientes pruebas:
Pruebas básicas. En caso de que el síncope evidencie ser con claridad de etiología
neuromediada o de perfil ortostático, no serán necesarias más pruebas complementarias que
un electrocardiograma (Tabla IV). En función de la anamnesis realizada al paciente se valorará
solicitar otras pruebas como una analítica de sangre con hemograma (para descartar pérdidas
hemáticas) y una radiografía de tórax (buscando signos indirectos de cardiopatía o
tromboembolismo pulmonar).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [130]
[8] SÍNCOPE
Tabla IV.Datos electrocardiográficos que sugieren síncope arrítmico.
Pruebas de ortostatismo. Se trata de pruebas que valoran las variaciones de la presión arterial
y la frecuencia cardiaca como respuesta al cambio desde el decúbito al ortostatismo:
Prueba de ortostatismo activo: está indicada para pacientes que sufren episodios
sincopales en relación con los cambios posturales, ya sea inmediatamente o a los pocos
minutos de haberse incorporado. Se determina repetidamente la tensión arterial y la
frecuencia cardiaca de forma manual, con el paciente en decúbito y tras adoptar el
ortostatismo activo durante los primeros 3 minutos (dado que se han descrito formas
retardadas de hipotensión ortostática, si la historia clínica así lo sugiere, se deberían
prolongar las determinaciones hasta 5 o 10 minutos). Se considera que la prueba es
diagnóstica cuando hay una caída de la tensión arterial con respecto al valor basal en
decúbito mayor de 20 mm Hg de la tensión sistólica o de 10 mm Hg de la diastólica, o si
los valores de la tensión sistólica caen por debajo de 90 mm Hg en valores absolutos;
todo ello necesariamente acompañado de síntomas para considerarse significativo.
Mesa basculante: pretende desencadenar el síncope al inclinar al paciente de forma
pasiva sobre una camilla hasta 60-70 grados. Tiene una baja sensibilidad, por lo que
actualmente su empleo está en desuso. Se reserva para casos de síncopes muy
recurrentes de etiología desconocida y ausencia de criterios de alto riesgo, o una vez
descartada la etiología cardiaca del síncope.
Masaje del seno carotídeo. Debe realizarse bajo monitorización de constantes y
electrocardiográfica, con un acceso venoso y con atropina cargada. Consiste en aplicar una
presión externa sobre la bifurcación de la arteria carótida común, desencadenando un
enlentecimiento de la frecuencia cardiaca, un alargamiento del intervalo PR y una caída de la
tensión arterial (hipersensibilidad del seno carotídeo). Dado que este tipo de respuesta se
observa con relativa frecuencia en individuos añosos o cardiópatas que no han sufrido nunca
un síncope, sus resultados son difíciles de interpretar. Se ha propuesto que para considerar
diagnóstica una respuesta al masaje del seno carotídeo deba reproducirse el síncope,
denominándose entonces síndrome del seno carotídeo y siendo este altamente predictivo de
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [131]
[8] SÍNCOPE
episodios espontáneos de asistolia. Está contraindicado ante accidentes isquémicos transitorios
(AIT) previos, ictus en los últimos 3 meses o presencia de soplos carotídeos (salvo cuando se
descarten estenosis significativas mediante ecografía Doppler).
Monitorización electrocardiográfica. Únicamente es diagnóstica si se reproduce el síncope
durante la monitorización, de ahí que sea difícil obtener registros durante un episodio sincopal
espontáneo. En pacientes con episodios sincopales frecuentes que interfieren sobre su calidad
de vida, o bien en aquellos en que se sospeche un síncope arrítmico, estaría indicada la
monitorización con Holter de 24 o 48 horas (aunque tiene un rendimiento diagnóstico menor
del 5%) o con dispositivos implantables de registro electrocardiográfico.
Estudio electrofisiológico. Es una prueba indirecta cuya interpretación se presta a discusión. No
tiene indicación en pacientes sin cardiopatía estructural y con electrocardiograma normal. Sus
principales objetivos son la detección de una posible bradiarritmia (disfunción sinusal o
trastorno de conducción) o la inducción de taquiarritmias supraventricuales o ventriculares.
Otras pruebas de estudio cardiológico. Ante la sospecha de cardiopatía estructural estaría
indicado completar el estudio mediante una ecocardiografía. Si se sospecha que las arritmias
responsables del síncope pueden estar inducidas por isquemia miocárdica debería realizarse un
cateterismo coronario. Otros estudios como la prueba de esfuerzo o la prueba de adenosina
deberían reservarse para situaciones concretas e interpretarse con precaución. La prueba de
esfuerzo está indicada en el síncope de esfuerzo. En cuanto al test de adenosina, la colocación
de marcapasos en pacientes con hipersensibilidad al trifosfato de adenosina (ATP) y que
presentan pausas mayores de 10 segundos, predice una mejor evolución. Sin embargo, son
necesarios más estudios que aclaren la indicación del test de adenosina en estos pacientes.
Angio-TC de arterias pulmonares. Se realiza si existen datos sugestivos de tromboembolismo
pulmonar como causa del síncope.
Por último, no hay que olvidar que un aparente síncope puede confundirse con otras causas de
pérdida del nivel de consciencia (ver Apartado V. “Diagnóstico diferencial”). Ante la sospecha de etiología
funcional o “pseudosíncope” estaría indiciado solicitar una valoración psiquiátrica, mientras que si se cree
que puede haber un origen neurológico de la pérdida de consciencia, podría plantearse realizar una
ecografía doppler de troncos supraaórticos, una tomografía computarizada (TC) y/o una resonancia
magnética (RM) cerebrales o un electroencefalograma.
V. DIAGNÓSTICO DIFERENCIAL
Se debe realizar el diagnóstico diferencial con las siguientes entidades (Tabla V):
Pseudosíncope psicógeno.
Crisis comicial.
Accidente cerebrovascular (AIT o ictus): puede causar pérdida de consciencia, pero suele
asociar otros signos de focalidad neurológica. Esto es más típico de un ictus de territorio
vertebrobasilar.
Síndrome del robo de la subclavia: consiste en el desvío de flujo sanguíneo hacia el brazo a
través de la arteria vertebral debido a estenosis u oclusión de la arteria subclavia, pudiendo
generar isquemia vertebrobasilar, mareo e incluso síncope, y ocurre cuando se realiza ejercicio
con el cuello o el brazo (lo que cesa el flujo de forma brusca). Habitualmente se debe a
ateroesclerosis.
Otras:
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [132]
[8] SÍNCOPE
Cataplejia: paresia o parálisis desencadenada por emociones. En ella no hay amnesia ni
pérdida de consciencia. Si asociara somnolencia diurna, sería diagnóstico de
narcolepsia.
Drop attack (“caída fulminante”): se puede dar en la enfermedad de Ménière, en crisis
atónicas o en caídas de causa desconocida. No hay pérdida de consciencia, pero el
paciente solo recuerda estar cayendo contra el suelo.
Tóxico-metabólicas: hipoglucemia, hipoxia, intoxicaciones, etc.
Tabla V.Diagnóstico diferencial entre síncope, pseudosíncope y crisis comicial.
VI. ESTRATIFICACIÓN DEL RIESGO
Si no es posible el diagnóstico tras la evaluación inicial, la estratificación del riesgo (Tabla VI)
determinará el ámbito en el que se lleven a cabo los estudios subsiguientes y la necesidad de
monitorización (Figura 1). Para ello se hará hincapié en la historia clínica y en el registro
electrocardiográfico, discerniendo los síncopes de alto riesgo de los de bajo; estos últimos pueden
estudiarse de forma ambulatoria. Los factores de riesgo de mayor peso son la edad avanzada, la cardiopatía
estructural previa (especialmente en forma de arritmias ventriculares y de insuficiencia cardiaca), las
alteraciones electrocardiográficas y la aparición del síncope en reposo (o decúbito supino) y durante el
esfuerzo. Varios estudios han evaluado este riesgo tanto a corto plazo (regla del síncope de San Francisco,
regla ROSE, estudios Boston y STePS) como a largo plazo (grupo de Martin et al., estudios OESIL y EGSYS).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [133]
[8] SÍNCOPE
Sin embargo, las diferentes estrategias propuestas no han sido sometidas a consenso para ser aplicadas de
forma universal y por el momento no reemplazan a la interpretación clínica individualizada de cada caso.
Tabla VI.Criterios de alto riesgo.
Figura 1.Algoritmo diagnóstico en la pérdida transitoria de consciencia.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [134]
[8] SÍNCOPE
VII. TRATAMIENTO
Sus objetivos son prolongar la supervivencia, limitar las lesiones físicas derivadas y prevenir las
recurrencias. A la hora de iniciar un tratamiento específico es necesario conocer la causa y el mecanismo
que provocan un síncope.
1. Tratamiento de los síncopes neuromediados
Las medidas generales son las más importantes: educar al paciente para evitar los
desencadenantes, detectar los síntomas prodrómicos para adoptar el decúbito y evadir las caídas, no tomar
vasodilatadores y evitar la ingesta de alcohol. Son de ayuda las maniobras de contrapresión isométrica
(entrecruzar las piernas o entrelazar las manos y tensar los brazos) y el entrenamiento con mesa basculante
para prevenir las recurrencias.
2. Tratamiento de la hipotensión ortostática
Es útil mantener la hidratación y una ingesta de sal adecuada, dormir con el cabecero de la cama
elevado, usar medias de compresión y ejercitar los músculos de las piernas (natación). Pueden usarse como
adyuvantes fármacos como la midodrina (agonista α-adrenérgico) o la fludrocortisona (mineralocorticoide).
3. Tratamiento de los síncopes cardiacos
Se han de evaluar las diferentes opciones de tratamiento en cada caso, en función de la etiología y
el mecanismo: fármacos, colocación de marcapasos (bloqueos, algunos síncopes neuromediados de perfil
cardioinhibitorio), ablación por catéter (taquiarritmias), implantación de desfibrilador, etc.
BIBLIOGRAFÍA
Akdemir B, Krishnan B, Senturk T, Benditt DG. Syncope: Assessment of risk and an approach to
evaluation in the emergency department and urgent care clinic. Indian Pacing Electrophysiol J.
2015;15(2):103-9.
Bennett MT, Leader N, Krahn AD. Recurrent syncope: differential diagnosis and mangement. Heart.
2015;101(19):1591-9.
Chisholm P, Anpalahan M. Orthostatic hypotension - Pathophysiology, assessment, treatment, and the
paradox of supine hypertension – a review. Intern Med J. 2016 Jul 8. doi: 10.1111/imj.13171. [Epub
ahead of print].
Fragakis N, Antoniadis AP, Saviano M, Vassilikos V, Pappone C. The use of adenosine and adenosine
triphosphate testing in the diagnosis, risk stratification and management of patients with syncope:
current evidence and future perspectives. Int J Cardiol. 2015 Mar 15;183:26
Grupo de Trabajo para el Diagnóstico y Manejo del Síncope de la Sociedad Europea de Cardiología
(ESC), en colaboración con European Heart Rhythm Association (EHRA), Heart Failure Association (HFA)
y Heart Rhythm Society (HRS). Guía de práctica clínica para el diagnóstico y manejo del síncope
(versión 2009). Rev Esp Cardiol. 2009;62(12):1466.
Gutkin M, Stewart JM. Orthostatic circulatory disorders: from nosology to nuts and bolts. Am J
Hypertens. 2016 Apr 1. pii: hpw023. [Epub ahead of print].
Kenny RA, McNicholas T. The management of vasovagal syncope. QJM. 2016 Jun 23. pii: hcw089.
[Epub ahead of print].
Moya-i-Mitjans Á, Rivas-Gándara N, Sarrias-Mercè A, Pérez-Rodón J, Roca-Luque I. Síncope. Rev Esp
Cardiol. 2012;65(8):755-65.
Solbiati M, Sheldon R, Seifer C. Managing syncope in the elderly: the not so simple faint in aging
patients. Can J Cardiol. 2016 Apr 22. pii: S0828-282X(16)30029-0. doi: 10.1016/j.cjca.2016.04.005.
[Epub ahead of print].
Teodorovich N, Swissa M. Tilt table test today - state of the art. World J Cardiol. 2016;8(3):277-82.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [135]
[9] DOLOR TORÁCICO
9. Dolor torácico
Marta Torres Arrese.
Medicina Interna
Álvaro Marchán López.
Medicina Interna
Asesor:
Carlos González Gómez.
Médico Adjunto de Medicina Interna
I. INTRODUCCIÓN
El dolor torácico es una de las consultas más frecuentes en los servicios de Urgencias que abarca
desde causas banales a otras potencialmente mortales (2-10%). El reconocimiento rápido de estas últimas
es el fin primordial de la evaluación del paciente con dolor torácico. Aunque en la mayoría de los casos no
se encuentra una patología orgánica y la causa identificada más frecuente es la osteomuscular, la mitad de
los pacientes con dolor torácico se evalúa como de posible etiología isquémica, confirmándose en tan solo
un 12%. Por otro lado, el 5% de los pacientes dado de alta con el diagnóstico de dolor torácico no
isquémico presenta en realidad un síndrome coronario agudo (SCA).
II. EVALUACIÓN INICIAL
Todo paciente con dolor torácico debe ser valorado inmediatamente de su llegada a Urgencias
como un paciente potencialmente grave de cara a:
1. Descartar datos de gravedad inminente
Inestabilidad hemodinámica (tensión arterial sistólica [TAS] < 90 mm Hg o frecuencia cardiaca
[FC] > 100 lpm).
Hipertensión arterial extrema (TAS > 180 o TAD [diastólica] > 110).
Insuficiencia respiratoria u obstrucción de la vía aérea.
Taquipnea (frecuencia respiratoria [FR] > 30) o bradipnea (FR < 10).
Bajo nivel de consciencia (Glasgow Coma Scale < 12).
2. Identificar etiología isquémica realizando un electrocardiograma
En los casos anteriores la actuación siguiente irá dirigida a:
a) Estabilizar al paciente.
b) Identificar la patología desencadenante del cuadro (descartando siempre las causas
potencialmente letales):
SCA.
Síndrome aórtico agudo.
Tromboembolismo pulmonar (TEP).
Neumotórax a tensión.
Taponamiento cardiaco.
Volet costal.
Mediastinitis.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [136]
[9] DOLOR TORÁCICO
La evaluación inicial debe ser objetiva. Se basa en la anamnesis (Tabla I) y exploración física (Tabla
II); siendo suficiente para orientar la etiología en más del 80% de los casos. Hay que tener en cuenta que
ancianos, diabéticos, o personas con infartos agudos de miocardio (IAM) extensos pueden dar
descripciones atípicas (sudoración, molestias abdominales, astenia, síndrome confusional agudo), así como
que la vivencia del dolor depende de la cultura o del sexo (los hombres lo viven como más intenso
generalmente).
Tabla I.Anamnesis de un paciente con dolor torácico.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [137]
[9] DOLOR TORÁCICO
Tabla II.Exploración física de un paciente con dolor torácico.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [138]
[9] DOLOR TORÁCICO
III. PERFILES CLÍNICOS
1. Isquémico
La isquemia cardiaca cursa habitualmente como un dolor precordial opresivo, distribuido en una
zona más o menos difusa del tórax, siendo la localización del dolor “a punta de dedo” un dato en contra de
etiología isquémica. En ocasiones es referido como una molestia, pesadez, pesar o malestar, más que como
un verdadero dolor, y es muy sugerente el gesto de llevarse el puño al pecho para describirlo (signo de
Levine). Puede presentar irradiación a uno o los dos hombros o brazos, a la mandíbula, y frecuentemente
se acompaña de síntomas vegetativos como náuseas, vómitos, sudoración, sensación presincopal, etc. Su
instauración es progresiva, a lo largo de minutos, mientras que la duración puede ser muy variable, desde
minutos en la angina a varias horas en los infartos. La angina cardiaca se desencadena con los esfuerzos,
mientras que en el SCA a menudo, aunque no siempre, el paciente ha realizado ejercicio físico de cualquier
intensidad en las horas previas.
Angina: se desencadena con la actividad física y cede con el reposo o con vasodilatadores
(nitratos).
Infarto: puede desencadenarse con la actividad física o en reposo. Habitualmente no cede con
el reposo; puede mejorar con nitratos. Con frecuencia descrito como similar, pero de mayor
intensidad, al dolor anginoso habitual.
La exploración física debe estar orientada a detectar la presencia de insuficiencia cardiaca y otras
complicaciones de la cardiopatía isquémica aguda como insuficiencia mitral aguda, rotura ventricular, etc.
2. Aórtico
El dolor debido a disección aórtica se instaura abruptamente, es continuo y se caracteriza por su
intensidad, pudiendo acompañarse, como el isquémico, de cortejo vegetativo. Se irradia a la región
interescapular y su localización puede migrar en función de la progresión de la disección, con aparición de
clínica focal derivada de la oclusión por el flap de ramas de la aorta.
En la exploración física es frecuente la aparición de hipertensión. Puede apreciarse asimetría en los
pulsos periféricos (que puede ser transitoria) y en la tensión arterial entre miembros. Debe valorarse la
presencia de un soplo que indique compromiso de la válvula aórtica.
3. Pleurítico
Está producido por patología pleural y pulmonar. Se trata de un dolor punzante, restringido a una
región pequeña del tórax, frecuentemente costal, que empeora con la tos, la inspiración profunda y, en
ocasiones, con el decúbito del lado afecto, pero no con la digitopresión ni los cambios posturales (pensar
en causas osteomusculares). Mejora con antiinflamatorios.
Pueden escucharse roces pleurales o datos de derrame pleural. Un dolor pleurítico intenso de
instauración súbita con una auscultación pulmonar normal obliga a pensar en TEP.
4. Pericárdico
Puede ser opresivo o punzante, localizado en el centro del tórax, y con irradiación a la espalda o a
los miembros superiores. La instauración puede ser súbita o más larvada, y habitualmente tiene una
duración de horas-días, siendo frecuente la presencia de un cuadro de infección respiratoria/ viriasis en los
días o semanas previos. Empeora con el decúbito y con los movimientos respiratorios, y mejora al inclinar
el tronco hacia delante o con la toma de antiinflamatorios.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [139]
[9] DOLOR TORÁCICO
La aparición en la exploración física de roce pericárdico es rara, aunque muy específica. Deben
buscarse datos de taponamiento cardiaco.
5. Esofágico
Se trata de un dolor, como el isquémico, centrotorácico y opresivo, aunque de instauración más
brusca. Se desencadena con el estrés o la ingesta de alimentos, pudiendo también ser espontáneo, como
en el caso de algunos trastornos de la motilidad esofágicos. Puede acompañarse de náuseas, vómitos,
pirosis o disfagia. La administración de nitratos mejora el dolor, como en el de origen isquémico, pero a
diferencia de aquel, este cede con antiácidos/antisecretores. Debe preguntarse acerca de la ingesta de
cáusticos, cuerpos extraños, realización de endoscopias recientes… que supongan un riesgo mayor de
perforación, en cuyo caso pueden encontrarse datos de neumomediastino (signo de Hamman, crepitación
sincrónica con el latido cardiaco) o de enfisema subcutáneo.
6. Mecánico
Habitualmente de etiología menos grave, deben descartarse las otras causas antes de diagnosticar
un dolor torácico como de origen mecánico. El dolor mecánico típicamente empeora con los cambios de
postura o el movimiento de los miembros, con la digitopresión, y puede hacerlo con la inspiración forzada y
la tos. Mejora con el reposo y con la administración de antiinflamatorios.
En la exploración destaca la reproducción del dolor con la palpación de la estructura afecta
(cartílago, articulación, estructura ósea…). En el síndrome de Tietze se podrá observar hinchazón de la
articulación (costocondral, esternoclavicular, esternocostal) afectada, que suele ser únicamente una. Es
importante descartar deformidades o inestabilidades de la caja torácica, volet, etc. que puedan señalar o
producir compromiso ventilatorio.
7. Neuropático
En ocasiones puede aparecer un dolor neuropático intenso de localización metamérica y que puede
preceder a la aparición de lesiones compatibles con herpes zóster, secundario a radiculopatías, etc.
8. Funcional
De perfil muy variable, típicamente es retroesternal, impide la inspiración profunda, no tiene
relación concreta con el esfuerzo, y es de duración prolongada e intensidad oscilante. Se debe interrogar
por posibles antecedentes psiquiátricos o desencadenantes como el estrés emocional.
Tabla III.Causas de dolor torácico.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [140]
[9] DOLOR TORÁCICO
IV. CAUSAS SEGÚN EL PERFIL CLÍNICO
Las causas según el perfil clínico se describen en la tabla III.
V. PRUEBAS COMPLEMENTARIAS
Se utilizan de cara a no obviar patologías potencialmente graves.
1. El electrocardiograma (Tabla IV)
Tabla IV.El electrocardiograma y la radiografía de tórax en el dolor torácico.
El electrocardiograma (ECG) debe realizarse en los primeros 10 minutos desde la llegada del
paciente a Urgencias.
• Si el ECG es normal:
Reduce notablemente la probabilidad de IAM pero no la anula (si la historia clínica es
compatible el 5% pueden presentar un IAM).
Si la clínica es compatible se debería de valorar el territorio de la circunfleja con las
derivaciones V3r, V4r, V7 y V8, para comprobar que efectivamente el ECG es normal.
No excluye la etiología isquémica, siendo en estas circunstancias más frecuente la angina
inestable.
No excluye entidades de gravedad (como disección aórtica o TEP).
• Si el ECG es anormal nos sirve:
Para diagnóstico:
La presencia de alteraciones electrocardiográficas sugestivas de isquemia (ver Capítulo 23.
“Cardiopatía isquémica”) es el hallazgo con más valor predictivo positivo para el diagnóstico de
la misma.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [141]
[9] DOLOR TORÁCICO
Taquicardia sinusal, BCRD o S1Q3T3 pueden estar presentes en el TEP (ver Capítulo 32.
“Enfermedad tromboembólica venosa”).
Ante un paciente con clínica de dolor torácico que sugiera perfil pericárdico podemos encontrar
una elevación cóncava del segmento ST en todas las derivaciones menos en V1 y aVR, o un
descenso del segmento PR (hallazgo más específico). Si existe un tiempo de evolución de días el
ST puede estar descendido o presentar ondas T negativas (ver Capítulo 25. “Enfermedades del
pericardio”).
Para estratificar el riesgo:
SCA sin elevación del ST: la presencia, extensión y localización de la depresión del segmento ST
u otras anormalidades de la repolarización son factores pronósticos (ver Capítulo 23.
“Cardiopatía isquémica”).
SCA con elevación del ST: precisa de terapia de reperfusión urgente.
2. Radiografía de tórax (ver Tabla IV)
Alrededor del 20% dan información que influye en la terapia. Evalúa causas cardiacas, pulmonares,
pleurales, óseas o mediastínicas.
3. Enzimas de daño miocárdico (ver Capítulo 23. “Cardiopatía isquémica”).
4. Ecocardiograma
Aunque por el momento no se recomienda en las directrices de la American College of
Cardiology/American Heart Association, la ecocardiografía transtorácica (ETT) puede identificar anomalías
de la contractilidad regional a los segundos de producirse la oclusión coronaria. La ausencia de alteraciones
segmentarias de la contractilidad en un paciente con dolor torácico permite razonablemente el alta
hospitalaria. Sin embargo, la presencia de las mismas no es patognomónico y requiere de observación y
estudio más exhaustivo.
Ante un paciente con signos de gravedad y diagnóstico incierto el ETT puede aportar información
de utilidad al valorar datos de taponamiento, TEP masivo, disfunción ventricular, disección aórtica o
contusión cardiaca postraumática.
5. Pruebas para diagnóstico de tromboembolismo pulmonar
Si el paciente se encuentra hemodinámicamente estable se aplican modelos de probabilidad
pretest (criterios de Wells modificados) en dependencia de los cuales se solicita un dímero-D si la
probabilidad es baja o una angio-TAC o gammagrafía de ventilación-perfusión si la probabilidad es media o
alta (ver Capítulo 32. “Enfermedad tromboembólica venosa”).
6. Prueba de estrés miocárdico o coronariografía diagnóstico/terapéutica
Se emplean para diagnóstico y posterior tratamiento de la cardiopatía isquémica. Su utilización
depende del riesgo individual (ver Capítulo 23. “Cardiopatía isquémica”).
VI. ALGORITMO
El algoritmo diagnóstico se describe en la figura 1.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [142]
[9] DOLOR TORÁCICO
Figura 1.Algoritmo diagnóstico del dolor torácico.
BIBLIOGRAFÍA
Amsterdam EA, Wenger NK, Brindis RG, et al. 2014 AHA/ACC Guideline for the Management of
Patients With Non–ST-Elevation Acute Coronary Syndromes: A Report of the American College of
Cardiology/ American Heart Association Task Force on Practice Guidelines. J Am Coll Cardiol.
2014;64(24):e139-e228. DOI: 10.1016/j.jacc.2014.09.017.
Fernández-Bujarrabal Villoslada J. Dolor torácico. Neumología Clínica. 1ª ed. 2010:10-15.
La Combe B, Borie R. Dolor torácico. EMC-Tratado de Medicina. 2012;16(4):1-8 (artículo E-1-0430).
Lee TH. Dolor torácico. En: Longo DL, Kasper DL, Jameson J, et al., eds. Harrison. Principios de
Medicina Interna. 18ª ed. New York, NY: McGrawHill. 2012 [consultado 3 feb 2016]. Disponible en:
http://harrisonmedicina.mhmedical.com/content.aspx?bookid=865&Sectionid=68926388.
Meisel JL. Diagnostic approach to chest pain in adults [sede Web] Jan 2016 May 22, 2014. UpToDate
Waltham, Massachusetts. Disponible en: http://www.uptodate.com/
Meisel JL, Cottrell D. Differential diagnosis of chest pain in adults [sede Web]. Jan 2016 Feb 25, 2015.
UpTo- Date Waltham, Massachusetts. Disponible en: http://www.uptodate.com/
O’Gara PT, Kushner FG, Ascheim DD, et al. 2013 ACCF/AHA Guideline for the Management of ST-
Elevation Myocardial Infarction: A Report of the American College of Cardiology Foundation/American
Heart Association Task Force on Practice Guidelines. J Am Coll Cardiol. 2013;61(4):e78-e140. DOI:
10.1016/ j.jacc.2012.11.019.
Weissman NJ. Transthoracic echocardiography for the evaluation of chest pain in the emergency
department [sede Web]. Jan 2016 Oct 21, 2015. UpToDate Waltham, Massachusetts. Disponible en:
http://www.uptodate.com/
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [143]
[10] DOLOR ABDOMINAL AGUDO
10.Dolor abdominal agudo
Marta Alvarado Blasco.
Medicina Interna
Jorge B. Pérez Torres.
Cirugía General
Asesores: Ana B. Carlavilla. Médica Adjunta de Urgencias. M. Abradelo de Usera. Médico Adjunto de Cirugía General y Aparato
Digestivo
I. INTRODUCCIÓN
El dolor abdominal agudo es un síntoma frecuente; representa el 5-10% de los motivos de consulta
en los servicios de urgencias. Puede ser la expresión de patologías de muy diversa índole (médicas o
quirúrgicas, intraabdominales o extraabdominales, banales o potencialmente graves). El término abdomen
agudo se utiliza para designar todo aquel proceso patológico intraabdominal que cursa con dolor
abdominal intenso y compromiso del estado general del paciente; suele requerir tratamiento quirúrgico.
II. FISIOPATOLOGÍA
Los estímulos responsables del dolor abdominal pueden ser mecánicos (distensión, tracción,
contracción, etc.) o químicos (inflamación, isquemia, etc.).
Las terminaciones nerviosas libres o receptores del dolor del abdomen (distribuidos en la mucosa y
en el músculo liso de las vísceras huecas, la cápsula de vísceras sólidas, el peritoneo parietal, el mesenterio
y la adventicia de los vasos) forman parte de la primera neurona, cuyo cuerpo celular se encuentra en los
ganglios de las raíces dorsales de la médula espinal. El cuerpo de la segunda neurona se halla en el asta
posterior medular y su axón cruza al lado opuesto para constituir el haz espinotalámico. Este establece
conexión con el cuerpo de la tercera neurona a nivel del tálamo y, desde allí, la información se proyecta
hacia la corteza somatosensorial. El aspecto emocional del dolor se produce como consecuencia de las
conexiones establecidas entre las neuronas talámicas, el córtex frontal y el sistema límbico. El peritoneo
visceral y el epiplón carecen de receptores del dolor.
En función del origen del dolor (inflamación del peritoneo parietal, obstrucción de víscera hueca,
etc.), este se presentará de diferente forma (ver Apartado “Calidad del dolor”).
III. ETIOLOGÍA
El dolor abdominal puede deberse a:
a) Procesos intraabdominales. Cualquier estructura localizada en el abdomen puede presentar
patología y, en consecuencia, ser causa de dolor abdominal:
Estómago y duodeno: gastritis aguda, úlcera péptica con penetración o perforación, vólvulo
gástrico, etc.
Intestino delgado: enteritis aguda, enfermedad inflamatoria intestinal, obstrucción,
perforación, isquemia intestinal, divertículo de Meckel, gastroenteritis eosinofílica, etc.
Intestino grueso: apendicitis, colitis infecciosa, enfermedad inflamatoria intestinal, megacolon,
diverticulitis, perforación, oclusión, colitis isquémica, colon irritable, cáncer colorrectal, etc.
Hígado: hepatitis aguda, síndrome de Budd-Chiari, trombosis portal, infarto hepático, absceso
hepático, rotura o necrosis de tumor hepático, etc.
Vías biliares: colangitis, colecistitis aguda, coledocolitiasis, etc.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [144]
[10] DOLOR ABDOMINAL AGUDO
Bazo: rotura del bazo, infarto esplénico, absceso esplénico, etc.
Pared abdominal: hematomas de los músculos de los rectos, etc.
Peritoneo: peritonitis (química, infecciosa), etc.
Mesenterio: linfadenitis mesentérica, etc.
Patología ginecológica: rotura o torsión de quiste ovárico, salpingitis aguda, embarazo
ectópico, rotura uterina, endometriosis, piosálpinx, cáncer de ovario, etc.
Vejiga: litiasis, infecciones, tumores, rotura, etc.
b) Procesos extraabdominales. Muchas patologías localizadas en estructuras no abdominales
pueden provocar un dolor referido en el abdomen:
Tórax: pulmón y pleura (neumonía basal, derrame pleural, neumotórax, infarto pulmonar, etc.),
corazón (infarto agudo de miocardio, pericarditis, miocarditis, endocarditis, etc.), esófago
(rotura de esófago, esofagitis, etc.).
Columna vertebral y sistema nervioso: espondilitis, hernia discal, osteomielitis, tabes dorsal,
radiculopatía, fractura vertebral, infección por el virus del herpes zóster, etc.
Aparato genital masculino: orquitis, epididimitis, etc.
Retroperitoneo: páncreas (pancreatitis, etc.), patología nefrourológica (litiasis renoureterales,
pielonefritis, absceso perirrenal, etc.), rotura o disección de aneurisma abdominal, hematoma
retroperitoneal, fibrosis, etc.
c) Procesos sistémicos:
Intoxicaciones: plomo (cólico saturnino), mercurio, setas, venenos de araña (Latrodectus
mactans), cocaína, anfetaminas, etc.
Fármacos: por su uso (anticolinérgicos, bloqueantes ganglionares, etc.) y por deprivación de
ellos (opiáceos, etc.).
Enfermedades sistémicas, endocrinológicas y hematológicas: insuficiencia suprarrenal (crisis
adrenal), tirotoxicosis, feocromocitoma, alteraciones del metabolismo del calcio
(hipercalcemia, hipocalcemia), uremia, acidosis metabólica (cetoacidosis diabética, acidosis
láctica), porfiria aguda intermitente, hiperlipoproteinemia, crisis hemolíticas (drepanocíticas),
leucemia aguda, hemocromatosis, fiebre mediterránea familiar, lupus eritematoso sistémico,
poliarteritis nodosa, púrpura de Schönlein-Henoch, angioedema (adquirido, hereditario),
anafilaxia, etc.
IV. DIAGNÓSTICO
El dolor abdominal agudo supone un reto desde el punto de vista diagnóstico. Por ello, para lograr
una correcta identificación de los pacientes potencialmente graves, existen dos herramientas
imprescindibles: la anamnesis completa y la exploración física minuciosa.
1. Anamnesis
Es una herramienta fundamental, aunque su calidad varía en función del profesional responsable y
del nivel cultural del paciente. Los datos clave en el enfoque diagnóstico son:
Edad: patologías propias de cada franja etaria; la expresividad de los síntomas puede variar en
los ancianos. Tener más de 65 años hace más probable que la causa del dolor abdominal sea
grave.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [145]
[10] DOLOR ABDOMINAL AGUDO
Sexo: es necesario destacar la importancia de las patologías ginecológicas, el uso de
anticonceptivos y la fecha de última regla (FUR) en la mujer.
Antecedentes familiares: cáncer colorrectal.
Antecedentes personales: factores de riesgo cardiovascular, arritmias cardiacas, estados de
inmunosupresión, cáncer, diverticulosis, hernias, úlceras, colelitiasis, enfermedad inflamatoria
intestinal, toma habitual de fármacos (antiinflamatorios no esteroideos), episodios similares
previos.
Antecedentes quirúrgicos: una cirugía previa puede condicionar la aparición de bridas
intraperitoneales.
Hábitos tóxicos: como el alcoholismo.
La descripción del dolor supone la base de la orientación diagnóstica:
Localización inicial y evolutiva: el dolor abdominal puede presentarse en una única región, en
varias a la vez o de manera difusa. La localización por cuadrantes ayuda a sospechar la
patología subyacente (Tabla I).
Instauración: la forma de instauración del dolor puede ser brusca, aguda o subaguda. Un dolor
intenso y de aparición brusca puede relacionarse con la perforación de una víscera hueca, una
oclusión vascular mesentérica o una torsión ovárica. La pancreatitis y la apendicitis suelen
presentarse de una manera más gradual.
Calidad del dolor: dependerá del origen del mismo:
Dolor visceral o cólico: se debe a la afectación de la cápsula de órganos sólidos o a la
capa muscular de vísceras huecas. Es un dolor de inicio intermitente que se vuelve
constante cuando hay dilatación de la víscera; a menudo se acompaña de síntomas
vegetativos. A pesar de ser difuso y mal delimitado, su localización y caracterización
pueden orientar hacia el origen: hipocondrio derecho (vía biliar), supraumbilical o
periumbilical (intestino delgado), infraumbilical con irradiación lumbar (colon),
suprapúbico (vejiga), flancos con irradicación a genitales (uréteres).
Dolor parietal o somático: se debe a la inflamación del peritoneo parietal. La intensidad
depende del tipo de sustancia que irrite el peritoneo. Provoca un dolor sordo,
sostenido y bien localizado (“a punta de dedo”), que aumenta con el movimiento y las
maniobras de Valsalva. El paciente con peritonitis tiende a estar quieto en la cama. Se
puede desencadenar una defensa muscular en función de la localización del proceso y
de la integridad del sistema nervioso. Ejemplos de este tipo de dolor son los que
aparecen en la peritonitis aguda o en la apendicitis aguda. El dolor relacionado con la
patología vascular intraabdominal suele ser mal localizado y difuso; puede ser agudo e
intenso, o, por el contrario, leve, continuo y aparecer 2 o 3 días antes de que surjan
signos de irritación peritoneal o de shock.
El dolor abdominal relacionado con patología extraabdominal o con causas tóxico-
metabólicas puede tener diversas características. Ejemplos: un dolor abdominal
localizado a nivel de un dermatoma, lancinante, urente, que curse con hiperestesia,
probablemente se deba a una causa neurógena; un dolor abdominal difuso que se
irradie desde los testículos y empeore con la palpación de los mismos probablemente
se deba a patología a este nivel.
No ha sido demostrada la validez orientativa de los términos “lancinante”, “terebrante”, “en
puñalada” y “gravativo”; utilizados clásicamente en la disección del aneurisma aórtico, en el dolor
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [146]
[10] DOLOR ABDOMINAL AGUDO
transfixivo de la pancreatitis aguda, en la úlcera péptica perforada y en el paciente portador de una masa
quística o tumoral, respectivamente.
Tiempo de evolución.
Irradiación: cabe mencionar las irradiaciones típicas de algunos procesos abdominales por su
frecuencia o gravedad:
El dolor irradiado al hipocondrio derecho y a la zona subescapular es típico del cólico
biliar y de la colecistitis.
El “dolor en cinturón” suele aparecer en personas con bajo umbral frente al dolor,
distensión gástrica o intestinal marcada o pancreatitis.
El dolor irradiado a la espalda es característico de procesos biliopancreáticos, úlcera
péptica con signos de penetración o perforación, patología renoureteral o vertebral y
procesos ginecológicos.
La irradiación a la ingle es frecuente en los cólicos renoureterales.
Requieren especial atención los dolores abdominales irradiados a la región sacra,
flancos, genitales y/o cara interna de muslos. Aunque pueden deberse a cólicos
renoureterales, deben hacernos pensar en la posibilidad de un aneurisma de aorta
complicado.
Síntomas y signos acompañantes: anorexia, náuseas, vómitos, fiebre, diarrea, estreñimiento,
ictericia, coluria, acolia, síntomas respiratorios, urinarios o ginecológicos. La relación
cronológica de los vómitos con el dolor abdominal puede orientar hacia la patología
subyacente:
Simultánea: típico de los cólicos nefríticos y biliares.
Precoz (2-3 horas tras el dolor): propio de procesos inflamatorios como la apendicitis
aguda.
Tardía: característica de procesos obstructivos (por neoplasias o bridas); puede orientar
sobre el nivel de la obstrucción.
Alivio y/o empeoramiento: hay que contemplar la modificación del dolor con los cambios
posturales, la ingesta, la defecación o los movimientos respiratorios. Por ejemplo, el dolor
parietal se agrava con los movimientos y la tos (especialmente en el hemiabdomen superior) y
se alivia típicamente con el reposo.
Intensidad del dolor: es una experiencia subjetiva; sin embargo, a menudo se relaciona con la
gravedad del cuadro. El cólico renal, la porfiria, el aneurisma de aorta abdominal y la isquemia
mesentérica aguda pueden cursar con un dolor abdominal desproporcionado a los hallazgos
encontrados en el examen físico.
2. Exploración física
Debe incluir las constantes vitales (tensión arterial, pulso, temperatura, saturación capilar de
oxígeno) y una exploración física general completa (piel, auscultación cardiopulmonar, ángulos
costovertebrales, raquis, pelvis y pulsos arteriales en los miembros inferiores). En el abdomen es necesario
llevar a cabo: inspección, auscultación, palpación y percusión. En ocasiones se deberá realizar examen
rectal, examen genital y/o ginecológico.
Mediante la exploración física se pretende identificar aquellos pacientes que requieran estar en
una unidad de agudos y/o ser valorados de manera inmediata por una especialidad quirúrgica.
Inspección. Es fundamental valorar el estado general del paciente. La inmovilidad sugiere
irritación peritoneal mientras que la inquietud es propia de cólicos biliares o renales. Ante un
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [147]
[10] DOLOR ABDOMINAL AGUDO
paciente pálido y sudoroso, habrá que contemplar la posibilidad de un sangrado activo. Algunos
hallazgos pueden orientar hacia ciertas patologías: cicatrices abdominales por cirugías previas
(obstrucción por bridas), circulación colateral (hipertensión portal), vesículas cutáneas (virus de
la varicela-zóster), equimosis periumbilical −signo de Cullen− o costovertebral −signo de Grey
Turner− (pancreatitis necrohemorrágica), nódulo paraumbilical “de la hermana María José”
(metástasis cutánea de una neoplasia maligna intraabdominal), indicios de un traumatismo
reciente, etc.
Tabla I.Causas de dolor abdominal según su localización por cuadrantes.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [148]
[10] DOLOR ABDOMINAL AGUDO
Auscultación abdominal. Hay que realizarla durante 1 o 2 minutos, siempre antes de la
manipulación abdominal. Es necesario valorar: ruidos metálicos (obstrucción intestinal),
silencio abdominal (íleo paralítico) y soplos (patología arterial).
Palpación abdominal. Se debe realizar con las manos templadas y comenzar por la zona menos
dolorosa, para evitar provocar una contractura de la pared abdominal que dificulte la
exploración de otras áreas. Hay que diferenciar la irritación peritoneal de la contracción
abdominal voluntaria (propia de niños, personas con ansiedad o simplemente incapaces de
relajar el abdomen). La palpación profunda del abdomen puede ser de ayuda para identificar
masas y visceromegalias. Una masa pulsátil debe alertar sobre la existencia de un aneurisma de
aorta. Es necesario explorar los orificios herniarios inguinales para descartar masas a este nivel.
Existen una serie de signos y epónimos que conviene conocer:
Signo de Blumberg: dolor a la descompresión brusca de la pared abdominal. Pone de
manifiesto la existencia de irritación del peritoneo parietal y es típico de la apendicitis si
se localiza en la fosa ilíaca derecha. Percutir suavemente la zona afecta, toser o caer
sobre los talones estando en bipedestación pueden ser maniobras tan útiles como la
descompresión brusca del abdomen para identificar la irritación peritoneal; además,
son menos traumáticas.
Signo de Rovsing: dolor reflejado en la fosa ilíaca derecha al palpar la fosa ilíaca
izquierda. También es propio de las apendicitis aguda, aunque menos frecuente.
Signo del psoas: estando el paciente en decúbito lateral izquierdo, se le pide que
extienda la pierna derecha en dirección a su espalda. En caso de apendicitis retrocecal,
aparece dolor en el punto de McBurney.
Signo de Murphy: dolor a la palpación profunda en el hipocondrio derecho, capaz de
cortar la inspiración; es propio de las colecistitis.
Signo de Courvoisier-Terrier: vesícula biliar palpable debido a su gran distensión.
Sugiere ictericia obstructiva distal, clásicamente tumoración en cabeza pancreática.
Percusión abdominal. El timpanismo indica gas y la matidez la existencia de líquido o
visceromegalias. La ausencia de matidez hepática puede deberse a la presencia de
neumoperitoneo.
Exploración rectal. Permite detectar la existencia de tumoraciones en el canal anal, sangrados
desapercibidos, patología prostática, ocupación del saco de Douglas y patología pélvica o
ginecológica. No se recomienda en el caso de pacientes neutropénicos.
Exploración genital.
Exploración ginecológica. Tiene especial relevancia en mujeres con dolor abdominal
hipogástrico.
3. Pruebas complementarias
Estas pruebas están indicadas cuando por la anamnesis y la exploración física no se ha llegado a un
diagnóstico, o para valorar el grado de repercusión clínica. Han de solicitarse de forma orientada para
confirmar o descartar una sospecha diagnóstica.
3.1. Laboratorio
Hemograma. La cifra de hemoglobina desciende en los sangrados mayores, aunque este
descenso puede tardar hasta 24 horas. La leucocitosis suele estar presente en situaciones
patológicas (infección e inflamación, entre otras), aunque también puede aparecer en
situaciones fisiológicas (embarazo). Asimismo, puede estar ausente, a pesar de existir patología
subyacente, en ancianos, niños e inmunodeprimidos. La leucopenia puede aparecer en el
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [149]
[10] DOLOR ABDOMINAL AGUDO
síndrome de respuesta inflamatoria sistémica o en la sepsis, e indica gravedad. La trombopenia
puede aparecer, entre otras situaciones, en la sepsis y en el hiperesplenismo.
Bioquímica. Se recomienda solicitar glucosa, creatinina e iones. En todo paciente con dolor
abdominal en epigastrio, mesogastrio e hipocondrio derecho, se solicitarán enzimas hepáticas y
pancreáticas. La determinación de enzimas miocárdicas pueden ser útiles si se quiere descartar
un infarto agudo de miocardio.
Gasometría venosa. La acidosis metabólica es un signo de gravedad y puede estar presente en
situaciones de shock, sepsis, cetoacidosis, insuficiencia renal, isquemia intestinal, etc.
Coagulación. Indispensable como parte del estudio preoperatorio en los pacientes que
requieren ser intervenidos. Asimismo, se solicitará a los pacientes anticoagulados y a aquellos
en los que se sospeche sepsis, coagulación intravascular diseminada, etc.
Pruebas cruzadas. En caso de hemorragia digestiva o necesidad de intervención quirúrgica.
Análisis de orina. Puede proporcionar información útil pero es necesario saber interpretarlo. La
presencia de piuria, proteinuria y hematuria sugiere el diagnóstico de infección del tracto
urinario. Sin embargo, estos mismos hallazgos pueden estar presentes en cualquier proceso
inflamatorio que se sitúe cerca de alguno de los uréteres (como la apendicitis). Además, dentro
de la población anciana, es frecuente encontrar piuria moderada. La hematuria es frecuente en
los pacientes con dolor abdominal agudo y no siempre indica nefrolitiasis.
Prueba de embarazo. Hay que descartar, siempre que corresponda, la posibilidad de embarazo
mediante la determinación de Gonadotropina coriónica humana β (β-HCG) en sangre u orina.
Hemocultivos y urocultivo. En caso de fiebre o datos de infección urinaria complicada,
respectivamente.
3.2. Electrocardiograma
Es necesario en aquellos pacientes en los que se quiera descartar isquemia miocárdica como causa
del dolor abdominal y/o arritmias cardiacas potencialmente embolígenas. Algunos procesos abdominales
pueden producir alteraciones electrocardiográficas (negativización de ondas T en la pancreatitis aguda).
3.3. Estudios de imagen
Radiografía de tórax. Realizada en bipedestación e incluyendo las cúpulas diafragmáticas,
permite identificar la existencia de neumoperitoneo o procesos torácicos con dolor irradiado al
abdomen superior (neumonía, derrame pleural).
Radiografía de abdomen. Se desaconseja su realización de forma rutinaria ante todo dolor
abdominal ya que su rendimiento diagnóstico es bajo. Es útil cuando se sospecha la presencia
de cuerpos extraños radioopacos y para detectar signos de perforación y de obstrucción
intestinal, aunque la ausencia de los mismos no excluye el diagnóstico. En la proyección en
decúbito supino, se valorará de manera sistemática: estructuras óseas y musculares, líneas de
grasa de flancos, distribución de gas intestinal, dilatación de asas, aire extraluminal, masas
abdominales, visceromegalias, líquido libre intraperitoneal y calcificaciones. La proyección en
bipedestación es útil para visualizar niveles hidroaéreos y gas extraintestinal. La proyección en
decúbito lateral izquierdo con rayo horizontal sustituye a la anterior en aquellos pacientes que
no pueden adoptar la bipedestación y es la mejor técnica para la visualización del
neumoperitoneo. Los signos característicos de la obstrucción de intestino delgado son: la
distensión de asas (más de 2,5 cm), la presencia de niveles hidroaéreos y el signo de la “pila de
monedas” o “cuentas de rosario”. La presencia de gas intramural (neumatosis) o en territorio
venoso es un signo de isquemia intestinal. El neumoperitoneo es diagnóstico de perforación de
víscera hueca (salvo que el enfermo haya sido sometido a laparoscopia recientemente).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [150]
[10] DOLOR ABDOMINAL AGUDO
Ecografía abdominal. Es una técnica rápida, barata, carente de radiaciones ionizantes y que
puede realizarse en la cabecera del enfermo. Es el estudio de elección en pacientes inestables
con sospecha de patología aórtica, y en aquellos con sospecha de patología de la vesícula biliar,
apendicitis o patología ginecológica. Es útil para detectar algunas colecciones intraabdominales
y para valorar los riñones y el sistema excretor en los cólicos renales complicados. No es útil
para detectar gas libre ni sangrado retroperitoneal. El protocolo FAST (Focused Abdominal
Sonography for Trauma) constituye una de las herramientas básicas en la valoración del
paciente politraumatizado. El registro con doppler ayuda en el diagnóstico de trombosis
venosas (vena porta, venas suprahepáticas, etc.). Se ve limitada en individuos obesos y por la
presencia de meteorismo.
Tomografía computarizada (TC). Es de elección en los pacientes con sospecha de patología
aórtica que se encuentran estables y en aquellos en los que se sospeche perforación visceral,
complicaciones retroperitoneales o isquemia intestinal. Asimismo, se deberá valorar la solicitud
de TC en los pacientes con traumatismo abdominal (cerrado o penetrante) y en los
postoperados con distensión abdominal. Es la mejor técnica para determinar la causa de un
cuadro obstructivo, así como para valorar las complicaciones de las pancreatitis agudas y de la
diverticulitis aguda. Es más sensible que la ecografía para los abscesos interasas y
retroperitoneales. Según las series, establece el diagnóstico definitivo hasta en dos tercios de
los pacientes con dolor abdominal de causa no filiada, sobre todo en ancianos.
Angiografía. Puede ser útil en el diagnóstico y el tratamiento de la isquemia intestinal.
Resonancia magnética (RM) y colangiorresonancia. No son pruebas que se realicen en el
momento agudo. Son útiles para el estudio de la patología biliar y pancreática, cuando la TC o la
ecografía no han sido concluyentes.
3.4. Endoscopia digestiva
Es una prueba indicada ante la sospecha de hemorragia digestiva y contraindicada si existe
perforación. Permite realizar diagnóstico y tratamiento.
3.5. Paracentesis
Indicada en pacientes con ascitis y dolor abdominal, para descartar infección del líquido ascítico.
V. ENTIDADES CLÍNICAS MÁS RELEVANTES
A pesar de que el espectro de posibilidades etiológicas en el dolor abdominal es muy amplio, tan
solo ocho causas son las responsables del 90% de los casos en la práctica clínica habitual. En orden
decreciente de frecuencia son: dolor abdominal inespecífico, apendicitis aguda, colecistitis aguda,
obstrucción intestinal, cólico nefrítico, perforación de víscera hueca, pancreatitis y diverticulitis aguda. Es
importante conocer las causas más frecuentes así como las más graves.
Apendicitis aguda. Es la urgencia quirúrgica más frecuente. La presentación típica incluye un
dolor inicial de tipo visceral localizado en el epigastrio o el mesogastrio que, posteriormente,
tras un intervalo de 3 a 6 horas, se localiza a nivel de la fosa ilíaca derecha y es de
características parietales. Si la apendicitis es retrocecal, puede cursar sin signos peritoneales. Si
es pélvica, puede cursar con síntomas urinarios o diarrea. Se puede acompañar de febrícula,
anorexia, náuseas y vómitos.
Colecistitis aguda. Suele haber antecedentes de cólico biliar o de ingesta de comida grasa
reciente. Cursa con dolor en la línea media superior del abdomen con irradiación al hipocondrio
derecho y la escápula. Se acompaña de náuseas, vómitos, anorexia y fiebre. Puede haber
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [151]
[10] DOLOR ABDOMINAL AGUDO
leucocitosis con neutrofilia y alteración del perfil hepático. El diagnóstico se confirma mediante
ecografía.
Obstrucción intestinal. Los síntomas habituales son dolor abdominal de carácter cólico,
náuseas, vómitos (más precoces cuanto más proximal sea la obstrucción), distensión (mayor
cuanto más distal sea la obstrucción) y dificultad para la emisión de gases y heces. Cuando el
dolor se hace continuo hay que sospechar perforación o compromiso vascular. Inicialmente, los
ruidos hidroaéreos son metálicos y están aumentados; en una fase tardía, estarán ausentes. La
radiografía simple de abdomen es especialmente útil cuando se realiza en bipedestación o
decúbito lateral con rayo horizontal. El dolor abdominal puede ser la primera manifestación de
una patología tumoral, especialmente en pacientes que acuden con obstrucción intestinal
franca.
Dolor abdominal de origen urológico. Una miscelánea de causas urológicas pueden llevar a los
pacientes a consultar por dolor abdominal. Entre ellas se incluyen el cólico renal, las infecciones
del tracto urinario, el escroto agudo y la retención aguda de orina.
Perforación de víscera hueca. Puede deberse a una úlcera péptica, enfermedad inflamatoria
intestinal, diverticulitis y cuadros obstructivos de cualquier etiología. La presentación típica es
un dolor abdominal súbito y de intensidad extrema que se acompaña de un rápido deterioro
del estado general, de íleo paralítico y de signos de peritonismo. Cuanto más distal es la
perforación, mayor es la distensión abdominal que presenta el paciente y mayor es el riesgo de
peritonitis fecaloidea. La TC abdominal permite valorar la causa y la localización de la
perforación.
Pancreatitis aguda. Las causas más frecuentes son la litiasis biliar y el alcohol. Cursa con un
dolor intenso, resistente a los analgésicos habituales, en el epigastrio o el mesogastrio, que se
irradia “en cinturón” hacia la espalda y que se acompaña de náuseas y vómitos. En los casos
más graves puede existir dolor abdominal difuso, distensión abdominal, íleo y signos
peritoneales. Analíticamente existe una elevación de las enzimas pancreáticas. La principal
prueba de imagen es la TC.
Diverticulitis aguda. La localización más frecuente es el sigma. Se suele manifestar como dolor
en el cuadrante inferior izquierdo del abdomen acompañado de náuseas, anorexia, febrícula y
signos de peritonitis focal. Algunos enfermos refieren disuria y polaquiuria como expresión de
irritación vesical por vecindad. La TC es la prueba de imagen inicial cuando haya sospecha de
diverticulitis aguda, especialmente si hay indicios de complicación o antecedentes de
diverticulitis. La ecografía podría ser la prueba de elección inicial en pacientes jóvenes, mujeres
en edad fértil y ante la sospecha de una diverticulitis no complicada.
Úlcera péptica. Dolor epigástrico, urente, que se alivia tras la ingesta de antiácidos o comidas.
Colangitis aguda. La tríada clásica de Charcot (ictericia, fiebre y dolor en hipocondrio derecho)
no siempre está presente. El diagnóstico es eminentemente clínico.
Gastroenteritis aguda. Cursa con náuseas, vómitos, diarrea, dolor abdominal difuso de tipo
cólico y fiebre. La exploración abdominal es anodina salvo por ruidos abdominales aumentados.
Pueden existir signos de deshidratación y niveles hidroaéreos en la radiografía de abdomen.
Enfermedad inflamatoria intestinal (EII). Las complicaciones de la enfermedad de Crohn, que
incluyen oclusión intestinal por edema, formación de abscesos y perforación a peritoneo libre,
se acompañan de dolor abdominal agudo. El megacolon tóxico es la causa más frecuente de
dolor abdominal agudo en la Colitis Ulcerosa.
Síndrome de intestino irritable (SII). Dolor abdominal que se alivia con la defecación y que se
acompaña de un trastorno en la consistencia y/o en la frecuencia de las deposiciones. La
palpación del abdomen puede causar alivio del dolor.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [152]
[10] DOLOR ABDOMINAL AGUDO
Vólvulo de colon. A nivel del ciego, suele asociarse con la presencia de adherencias y se
manifiesta como una obstrucción a nivel del intestino delgado. El vólvulo de sigma es más
frecuente, se relaciona con abuso de laxantes y fármacos con propiedades anticolinérgicas, y
típicamente se manifiesta con una gran distensión asimétrica del abdomen asociada a dolor. Si
aparece fiebre, hipotensión o peritonismo, ha de sospecharse estrangulación.
Hernias de la pared abdominal. Las más frecuentes son las inguinales. Con frecuencia el
paciente refiere padecer un cuadro de varias semanas de evolución de dolor en el hipogastrio
que se exacerba con la tos y el esfuerzo defecatorio. La incarceración de una hernia requiere de
una intervención quirúrgica precoz para evitar las consecuencias de la estrangulación.
Aneurisma de aorta abdominal (AAA). Los factores de riesgo son antecedentes familiares,
edad avanzada y factores de riesgo cardiovascular. La mayoría de los AAA permanecen
asintomáticos hasta su ruptura, momento en el que aparecen las manifestaciones de un shock
hipovolémico. Si la ruptura es hacia el retroperitoneo, el sangrado puede contenerse y el
paciente permanece normotenso en un inicio. Algunos pacientes refieren un cuadro subagudo
de dolor abdominal periumbilical irradiado a flancos o dolor lumbar. Si se presenta como dolor
lumbar y hematuria, puede confundirse con un cólico renoureteral
Isquemia mesentérica. Se debe a la interrupción del flujo vascular (arterial o venoso) del
territorio dependiente de la arteria mesentérica superior. Debe sospecharse en personas con
factores de riesgo que presentan un dolor abdominal de intensidad extrema que contrasta con
la escasa relevancia de los signos exploratorios. La prueba más empleada para el diagnóstico es
la angio-TC. La supervivencia de estos pacientes depende de la rapidez con que se haga el
diagnóstico.
Hemoperitoneo. Dentro de las posibles causas están la rotura de una víscera maciza, la rotura
de un embarazo ectópico, la biopsia hepática percutánea y la rotura de aneurisma abdominal.
Cursa con dolor abdominal, distensión progresiva, signos de irritación peritoneal e inestabilidad
hemodinámica. La principal prueba de imagen es la TC.
Linfadenitis mesentérica. Inflamación de ganglios abdominales por infecciones bacterianas o
víricas. Puede simular una apendicitis. Es un diagnóstico de exclusión.
Dolor abdominal de origen ginecológico. Las patologías ginecológicas agudas que pueden
revestir mayor gravedad son la rotura de un embarazo ectópico, la enfermedad inflamatoria
pélvica, los abscesos tuboováricos, la torsión de la trompa de Falopio, la rotura de un quiste
ovárico y el desprendimiento de la placenta.
Infarto agudo de miocardio. Puede presentarse de una forma atípica hasta en un tercio de los
casos, más frecuentemente en mujeres, ancianos y diabéticos. Puede cursar como dolor en el
piso abdominal superior.
VI. SITUACIONES ESPECIALES
El dolor abdominal es un síntoma frecuente durante el embarazo y, en muchas ocasiones, es
debido a causas fisiológicas (distensión uterina, contracciones de Braxton-Hicks o movimientos fetales). Se
debe sospechar la existencia de patología subyacente ante un dolor localizado en el hemiabdomen superior
o ante un dolor abdominal intenso, brusco, constante y/o asociado a otros síntomas (fiebre, náuseas,
vómitos, diarrea, metrorragia, etc.). Las causas más frecuentes de dolor abdominal en la embarazada se
enumeran en la tabla II.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [153]
[10] DOLOR ABDOMINAL AGUDO
Tabla II.Causas más frecuentes de dolor abdominal en la embarazada.
Es necesario recordar que, durante el embarazo, la posición de las vísceras se modifica, la mayor
laxitud de los tejidos puede enmascarar la irritación peritoneal y que existen cambios en los parámetros de
laboratorio que son fisiológicos (leucocitosis, anemia). La prueba de imagen de elección para la patología
abdominopélvica de la mujer embarazada es la ecografía. Será necesario realizar una interconsulta al
servicio de ginecología ante la sospecha de cualquier patología ginecoobstétrica y para valorar bienestar
fetal.
2. Paciente anciano
En la población anciana, tanto los síntomas como las alteraciones en la exploración física y en los
análisis de sangre son menos expresivos, e incluso pueden no manifestarse. Esto dificulta y retrasa el
diagnóstico, por lo que es más frecuente la aparición de complicaciones. En orden descendente de
frecuencia, las causas más habituales de dolor abdominal en el anciano son: hernias, colecistitis aguda,
obstrucción intestinal, apendicitis aguda, úlcera perforada, isquemia intestinal, vólvulos, diverticulitis
aguda, íleo biliar y rotura de aneurisma aórtico. Se recomienda solicitar una radiografía de tórax y un
electrocardiograma en todos los pacientes ancianos con dolor abdominal.
3. Pacientes oncológicos e inmunodeprimidos
Los pacientes inmunodeprimidos (infectados por el VIH, en tratamiento con quimioterapia,
inmunomoduladores o esteroides) pueden presentar síntomas, signos y alteraciones en las pruebas
complementarias poco floridos. En los pacientes oncológicos en tratamiento, el dolor abdominal puede
deberse a los agentes quimioterápicos (vincristina). En el paciente seropositivo con dolor abdominal, hay
que considerar que pueden ser responsables del cuadro los fármacos antirretrovirales (pancreatitis como
efecto secundario de los mismos), las infecciones oportunistas concomitantes (perforación de intestino
grueso por citomegalovirus), o los tumores asociados al VIH (obstrucción de intestino delgado por sarcoma
de Kaposi).
VII. MANEJO TERAPÉUTICO
1. Actitud inicial
En primer lugar, es preciso detectar aquellos pacientes con criterios de gravedad (Tabla III).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [154]
[10] DOLOR ABDOMINAL AGUDO
Tabla III.Criterios de gravedad en el dolor abdominal.
En la figura 1 se muestra el algoritmo para el manejo del dolor abdominal agudo.
Figura 1.Manejo del dolor abdominal agudo.
Los pacientes inestables deberán ser trasladados a una unidad de agudos. Se realizará una
exploración física inicial. Ante la mínima sospecha de abdomen agudo, se avisará al servicio de cirugía de
guardia. Al mismo tiempo, se indicarán las medidas generales pertinentes (monitorización de constantes y
diuresis, oxigenoterapia, dieta absoluta, reposo, canalización de al menos dos vías de grueso calibre,
sondaje nasogástrico y/o vesical), se llevarán a cabo las medidas de resucitación oportunas, se administrará
la analgesia adecuada y se valorará la administración de antibioterapia según la sospecha clínica. La
ecografía FAST a la cabecera del paciente es útil para valorar la aorta y la presencia de líquido libre. Es
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [155]
[10] DOLOR ABDOMINAL AGUDO
imprescindible realizar unos análisis de sangre completos (incluyendo pruebas cruzadas), un
electrocardiograma y una radiografía de tórax. Asimismo, en toda mujer en edad fértil habrá que solicitar
una prueba de embarazo.
En los pacientes estables se realizará una historia clínica completa, tal y como se ha reflejado es
este capítulo, solicitando las pruebas complementarias de manera dirigida. Se ha de prestar especial
atención a los factores de riesgo, síntomas y signos de las patologías que pueden suponer un riesgo vital
inminente para el paciente (aneurisma de aorta abdominal, síndrome coronario agudo, isquemia
mesentérica aguda, obstrucción intestinal con estrangulación, perforación intestinal, etc.). Una vez que se
han descartado dichas entidades, el diagnóstico se puede orientar en función de la localización
predominante del dolor abdominal y del sexo del paciente, recordando la importancia de la patología
ginecológica en la mujer.
2. Analgesia
La administración de analgésicos no enmascara los signos de irritación peritoneal ni retrasa el
diagnóstico.
3. Valoración del alta hospitalaria
El carácter evolutivo de la presentación de muchas patologías puede conllevar no encontrar
hallazgos relevantes en la valoración inicial de un dolor abdominal. En ocasiones resulta aconsejable
mantener al paciente en un área de observación y repetir el examen clínico y/o las pruebas
complementarias algunas horas después. Con frecuencia, este tiempo de espera permite una mejor
definición de los síntomas y hace posible un diagnóstico. Un gran porcentaje de pacientes quedará
englobado bajo el término de “dolor abdominal inespecífico” y podrá ser dado de alta. A la hora de decidir
el manejo del paciente, se debe tener en cuenta la evolución del dolor durante su estancia en urgencias
(incluyendo la respuesta a la analgesia pautada), los hallazgos en la exploración física seriada y los
resultados de las pruebas complementarias realizadas. Se recomienda dejar por escrito los posibles
síntomas y/o signos ante los cuales deberá consultar de nuevo.
BIBLIOGRAFÍA
Flashar MH, Goldberg E. Acute abdominal pain. Med Clin North Am. 2006;90(3):481-503.
Heading RC. Prevalence of upper gastrointestinal symptoms in the general population: a systematic
review. Scand J Gastroenterol Suppl. 1999;231:3-8.
Longo DL, Kasper DL, Larry Jameson L, Fauci AS, Hauser Sl, Loscalzo J. Harrison principios de medicina
interna. 18ª ed. México: McGraw-Hill; 2012.
Lyon C, Clark DC. Diagnosis of acute abdominal pain in older patients. Am Fam Physician.
2006;74(9):1537- 44.
Macaluso C, McNamara R. Evaluation and management of acute abdominal pain in the emergency
department. Int J Gen Med. 2012;5:789-97.
Montoro MA, Casamayor M. Dolor abdominal agudo. En: Montoro MA, García Pagán JC.
Gastroenterología y hepatología, problemas comunes en la práctica clínica. 2ª ed. España: Jarpyo
Editores; 2012. p. 91-124.
Parker LJ, Vukov LF, Wollan PC. Emergency department evaluation of geriatric patients with acute
cholecystitis. Acad Emerg Med. 1997; 4:51-55.
Sabiston. Tratado de Cirugía: fundamentos biológicos de la práctica quirúrgica moderna. 19ª ed.
Elsevier; 2013.
Schwartz. Principios de Cirugía. 9ª ed. McGraw-Hill; 2010.
Thomas SH, Silen W, Cheema F, Reisner A, Aman S, Goldstein JN, et al. Effects of morphine analgesia
on diagnostic accuracy in emergency department patients with abdominal pain: a prospective,
randomized trial. J Am Coll Surg. 2003;196:18-31.
Yamamoto W, Kono H, Maekawa M, Fukui T. The relationship between abdominal pain regions and
specific diseases: an epidemiologic approach to clinical practice. J Epidemiol. 1997;7:27.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [156]
[11] SÍNDROME CONFUSIONAL AGUDO
11.Síndrome confusional agudo
Beatriz Sánchez Moreno.
Medicina Interna
Asesor:
Alberto Moreno Fernández.
Médico Adjunto de Medicina Interna
I. CONCEPTO
El síndrome confusional agudo (SCA) consiste en una alteración aguda de la consciencia, de curso
fluctuante, que se caracteriza por un déficit de atención, si bien se suele acompañar de disfunción de otras
áreas cognitivas (orientación, memoria, lenguaje y tareas visuoespaciales). Otros términos que a veces se
emplean como sinónimos de SCA son delirium o encefalopatía. La definición según el DSM-5 aparece en la
tabla I.
Tabla I.Criterios diagnósticos de delirium del DSM-5.
Es uno de los problemas más frecuentes en personas con enfermedades médicas, en especial en las
de edad avanzada, afectando aproximadamente a un tercio de los pacientes ingresados con más de 70
años. La prevalencia es variable, según la población estudiada, pudiendo llegar a ser superior al 70% en la
Unidad de Cuidados Intensivos (UCI). A pesar de ello, este trastorno es a menudo infradiagnosticado.
II. ETIOLOGÍA
La patogenia del SCA no está bien dilucidada. Se debe entender como un proceso multifactorial, en
el que participan una suma de factores de riesgo, constituida por factores predisponentes (incrementan la
vulnerabilidad) y precipitantes (inician el síndrome). Cuantos más factores predisponentes estén presentes,
menos precipitantes son necesarios para provocar el trastorno.
Los factores predisponentes más importantes son la edad avanzada y las enfermedades
neurológicas previas (demencia, enfermedad cerebrovascular y de Parkinson), las cuales aparecen en cerca
de la mitad de los pacientes ancianos con SCA. Otros factores son los déficits sensoriales, el deterioro
funcional, la desnutrición y los procesos médicos subyacentes.
Los principales factores precipitantes se recogen en la tabla II, siendo los más comunes en ancianos
la aparición de una enfermedad médica aguda, como las infecciones (el delirium puede constituir la única
manifestación clínica); la polimedicación, el encamamiento, la hospitalización, la retención urinaria y la
impactación fecal, la deshidratación y los trastornos metabólicos. Es habitual que coexistan varios de estos
factores. En jóvenes un desencadenante frecuente es el abuso o deprivación de tóxicos (ver Capítulos 87-
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [157]
[11] SÍNDROME CONFUSIONAL AGUDO
89. “Trastornos relacionados con el consumo de alcohol, Trastornos relacionados con el consumo de drogas
e Intoxicaciones”).
Tabla II.Factores precipitantes del síndrome confusional agudo.
III. CLÍNICA
El rasgo más importante es la alteración de la atención (Tabla I). El SCA tiene un amplio espectro de
manifestaciones clínicas, que va desde formas hipoactivas, más habituales en la población anciana,
pudiendo asociar disminución del nivel de consciencia en forma de somnolencia o letargo, hasta otras
hiperactivas, que cursan con agitación psicomotriz o hipervigilia, como se puede observar en la abstinencia
de alcohol u otros tóxicos. En ocasiones, los pacientes pueden sufrir formas mixtas e incluso fluctuar de una
presentación a otra en cuestión de minutos u horas.
Otros síntomas que frecuentemente coexisten con los anteriormente mencionados son una
inversión en el ciclo sueño-vigilia, trastornos de la percepción como alucinaciones y delirios, disautonomía,
ansiedad, labilidad emocional, irritabilidad e hipersensibilidad al sonido y a la luz.
IV. APROXIMACIÓN DIAGNÓSTICA
Existen dos aspectos importantes: identificar el síndrome y establecer las posibles causas.
1. Diagnóstico sindrómico
El diagnóstico del SCA es clínico, basado íntegramente en la historia clínica y en la exploración
física. El interrogatorio debe dirigirse fundamentalmente a los familiares y cuidadores, quienes pueden
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [158]
[11] SÍNDROME CONFUSIONAL AGUDO
aportar información valiosa acerca de la cronología de los síntomas y de la función cognitiva de base del
paciente. Es necesario evaluar el nivel de consciencia y de atención, para lo que se pueden realizar pruebas
breves, como las que aparecen en la tabla III. También es útil prestar atención al discurso y al lenguaje del
paciente.
Tabla III.Evaluación de la atención.
Se han desarrollado diferentes test diagnósticos a la cabecera del paciente, habiendo obtenido los
mejores resultados con el Confusion Assessment Method, al ser fiable y rápido (Tabla IV). Se puede
complementar con otras herramientas, como el Mini-Mental State Examination (Figura 1) o el IQCODE
(Informant Questionnaire On Congnitive Decline in the Ederly), que no precisa de la atención del paciente
para diagnosticar un deterioro cognitivo previo al episodio.
Tabla IV.Confusion Assessment Method.
2. Diagnóstico etiológico
2.1. Anamnesis
Es clave recoger información acerca de la medicación, el abuso de tóxicos, procesos febriles u otras
enfermedades recientes y antecedentes psiquiátricos del paciente.
2.2. Examen físico
Debe dirigirse a la búsqueda de signos clínicos de enfermedad a cualquier nivel, con especial
atención a las constantes vitales, estado de hidratación, apariencia de la piel, signos de infección y datos de
focalidad neurológica. El examen neurológico puede estar dificultado por la inatención del paciente, si bien
a veces se observan signos inespecíficos como temblor, asterixis, mioclonías multifocales, disartria, etc.,
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [159]
[11] SÍNDROME CONFUSIONAL AGUDO
que pueden orientar hacia un origen tóxico-metabólico del cuadro. Es importante atender a los signos de
disautonomía, que pueden llegar a comprometer la vida del paciente.
2.3. Pruebas complementarias
Prácticamente cualquier evento puede desencadenar un SCA en un paciente predispuesto; sin
embargo, con la valoración clínica inicial, es posible orientar el diagnóstico en la mayoría de los casos,
permitiendo rentabilizar la solicitud de pruebas adicionales (Figura 2).
Los estudios de neuroimagen, como la tomografía computarizada (TC) craneal y el electro-
encefalograma (EEG) no son generalmente necesarios, salvo en casos seleccionados. El patrón EEG más
común en los casos de SCA de causa no comicial consiste en un trazado lento, difuso e inespecífico, aunque
en algunos casos puede sugerir una etiología determinada (por ejemplo, ondas trifásicas en la
encefalopatía hepática).
Figura 1.Mini-Mental State Examination.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [160]
[11] SÍNDROME CONFUSIONAL AGUDO
Figura 2.Algoritmo diagnóstico del síndrome confusional agudo.
3. Diagnóstico diferencial
Ante una alteración del estado mental, especialmente si es brusca, hay que descartar en primer
lugar que se trate de un SCA, antes de considerar otras causas alternativas, ya que podríamos pasar por
alto una enfermedad médica subyacente grave. No debemos olvidar que estas entidades suelen coexistir y
predisponen a su vez al delirium:
3.1. Demencia
El curso es progresivo y sin fluctuaciones tan marcadas. La atención está relativamente conservada.
Los pacientes con demencia vascular a veces tienen un inicio más agudo. La demencia por cuerpos de Lewy
puede ser más difícil de distinguir, debido a la evolución fluctuante y a las alteraciones de la percepción.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [161]
[11] SÍNDROME CONFUSIONAL AGUDO
3.2. Trastornos psiquiátricos
Se confunde especialmente la depresión con el delirium hipoactivo, mientras que la manía o la
esquizofrenia pueden asemejarse a un SCA que curse con agitación psicomotriz y alucinaciones.
3.3. Síndromes focales neurológicos
Los pacientes con afasia de Wernicke pueden parecer confusos, pero su problema está restringido
al lenguaje. De forma similar, los pacientes con amnesia global transitoria padecen una alteración selectiva
de la memoria anterógrada.
3.4. Estatus epiléptico no convulsivo
Es una entidad infradiagnosticada, la cual se debe sospechar en pacientes que presenten
automatismos, hipo incoercible, movimientos oculares tipo nistagmo o focalidad neurológica sin lesión
estructural. También es importante pensar en ella cuando no se consigue detectar la causa del SCA tras las
pruebas iniciales (ver Capítulo 86. “Crisis comiciales”).
V. PRONÓSTICO
El SCA es un factor predictivo independiente de resultados adversos en los pacientes
hospitalizados: incrementa la mortalidad, el riesgo de complicaciones nosocomiales y la estancia
hospitalaria, siendo más probable el desarrollo de un mayor grado de dependencia y la necesidad de
institucionalización al alta. La mortalidad persiste aumentada hasta incluso dos años después del episodio.
El pronóstico es peor en los pacientes con delirium prolongado (semanas e incluso meses), que en aquellos
en los que dura menos de dos semanas, por lo que un objetivo fundamental del tratamiento es reducir la
duración del SCA.
VI. ABORDAJE TERAPÉUTICO
1. Corrección de los factores precipitantes
En muchos casos encontraremos múltiples contribuyentes del delirium, pudiendo obtener buenos
resultados si se actúa sobre varios de ellos. Ciertas etiologías, como la hipoxia o la hipo- glucemia, deben
ser consideradas de inmediato por amenazar la vida del paciente. Se intentarán suspender, en la medida de
lo posible, los medicamentos de mayor riesgo de provocar SCA como benzodiazepinas, opioides o
anticolinérgicos, y emplear alternativas, como, por ejemplo, dexmedetomidina para la sedación de
pacientes críticos.
2. Medidas de soporte (no farmacológicas)
Son la piedra angular del tratamiento del SCA, debiendo llevarse a cabo en todos los pacientes que
lo sufren o que tienen una alta vulnerabilidad para desarrollarlo (Figura 3).
La inmovilización terapéutica no debe emplearse salvo como último recurso, en caso de que el
paciente presente una actitud violenta o para prevenir que se arranque catéteres u otros dispositivos, ya
que puede prolongar el delirium y no disminuye el riesgo de lesiones. Si fuera necesario, se tendrá que
revisar su indicación con frecuencia y habrá que retirarla lo antes posible.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [162]
[11] SÍNDROME CONFUSIONAL AGUDO
Figura 3.Algoritmo terapéutico del síndrome confusional agudo (SCA).
3. Medidas farmacológicas
Es preferible evitar el uso de fármacos, si bien pueden ser necesarios si el comportamiento del
paciente es potencialmente peligroso, interfiere con los cuidados médicos o le genera mucha ansiedad. Hay
poca evidencia al respecto, y no existe ningún fármaco aprobado específicamente para el tratamiento o
prevención del SCA (se utilizan fuera de ficha técnica). La experiencia es mayor con haloperidol,
comenzando a dosis bajas (de 0,5 a 1 mg); no obstante, algunos estudios sugieren que los neurolépticos
atípicos tienen una eficacia similar y podrían ser de elección en casos de parkinsonismo por sus menores
efectos extrapiramidales (Tabla V). De todas formas, el tratamiento antipsicótico no debería mantenerse a
largo plazo, puesto que se ha asociado a mayor riesgo de ictus y a un aumento en la mortalidad en
pacientes con demencia.
Las benzodiazepinas pueden agravar la confusión, debiendo limitarse a casos de abstinencia
alcohólica o de benzodiazepinas (ver los Capítulos 87. “Trastornos relacionados con el consumo de alcohol”
y 19. “Patología psiquiátrica importante para el médico general”).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [163]
[11] SÍNDROME CONFUSIONAL AGUDO
Tabla V.Tratamiento farmacológico del síndrome confusional agudo.
BIBLIOGRAFÍA
American Psychiatric Association. Diagnostic and Statistical Manual. 5th ed. Washington DC: APA
Press; 2013.
Ely EW, Truman B. The Confusion Assessment Method for the ICU (CAM-ICU). Training Manual
[monografía en Internet]. Nashville: Vanderbilt University Medical Center; 2005 [acceso 15 Dic 2015].
Disponible en: http://www.icudelirium.org/docs/CAM_ICU_training_2005.pdf
Inouye SK, Westendorp RGJ, Saczynski JS. Delirium in elderly people. Lancet. 2014;383:911-22.
Josephson SA, Miller BL. Confusión y delirio. En: Longo DL, Fauci AS, Kasper DL, et al, editores.
Harrison. Principios de Medicina interna. 18.a ed. México: McGraw-Hill Interamericana; 2012. [Acceso
8 de diciembre de 2015]. Disponible en:
http://harrisonmedicina.mhmedical.com/content.aspx?bookid=865&Sectionid=68927123.
Lonergan E, Britton AM, Luxenberg J, Wyller T. Antipsychotics for delirium. Cochrane Database Syst Rev.
2007(2);CD005594.
Marcantonio ER. In the clinic. Delirium. Ann Intern Med. 2011;154(11):ITC6-1-16.
National Institute for Health and Care Excellence. Delirium: Prevention, diagnosis and management
[Clinical Guidance 103]. London: Royal College of Physicians (UK); 2010 [acceso 10 Dic 2015].
Disponible en: nice.org.uk/guidance/cg103
Odiari EA, Sekhon N, Han JY, David EH. Stabilizing and managing patients with altered mental status
and delirium. Emerg Med Clin N Am. 2015;33:753-64.
Reade MC, Phil D, Finfer S. Sedation and delirium in the intensive care unit. N Engl J Med.
2014;370:444-54.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [164]
[12] LUMBALGIA
12.Lumbalgia
Isabel de la Cámara Fernández
Reumatología
Rina Aicxa Molina Larios.
Reumatología
Asesora:
Sheila Melchor Díaz.
Médica Adjunta de Reumatología
I. DEFINICIÓN
La lumbalgia es un dolor localizado en la zona del dorso entre la última costilla y la zona glútea, que
puede irradiarse a las extremidades inferiores y que puede deberse a múltiples etiologías. Es un problema
de salud importante, sobre todo, en países industrializados, con una prevalencia que gira alrededor del
70%. Constituye una importante causa de incapacidad laboral entre la población adulta.
II. ETIOLOGÍA
Existen múltiples causas de lumbalgia, la mayoría de ellas benignas y autolimitadas en el tiempo,
pero hay una serie de causas menos frecuentes y asociadas a enfermedades severas que es conveniente
descartar.
Tabla I.Datos de alarma en un paciente con lumbalgia.
Según la etiología del dolor lumbar se puede clasificar de la siguiente manera:
Lumbalgia inespecífica: sin causa aparente, supone un 80% de las lumbalgias. Es un diagnóstico
de exclusión, en ausencia de datos de alarma (Tabla I). Es un proceso benigno, autolimitado y, a
veces, recurrente.
Lumbalgia específica: supone el 20% de las lumbalgias.
Dolor lumbar asociado a radiculopatía o lumbociatalgia: presenta irradiación hacia alguna de las
extremidades inferiores. Es el causado por hernias discales, síndrome de cauda equina, estenosis de canal.
Dolor lumbar secundario:
Grave: aneurisma aórtico, espondilodiscitis, absceso epidural, metástasis vertebrales,
tumores malignos pélvicos/espinales, fractura inestable, síndrome de “cola de caballo”
e infecciones abdominales o pélvicas.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [165]
[12] LUMBALGIA
No grave: espondiloartropatías inflamatorias, aplastamientos vertebrales osteopo-
róticos, enfermedad de Paget, tumores espinales o pélvicos benignos, malformaciones
vasculares, quistes aracnoideos.
III. CLÍNICA
En función del tiempo de evolución hablaremos de lumbalgia aguda si es de menos de 1 a 2
semanas de evolución, lumbalgia subaguda si el dolor se mantiene entre 2 a 12 semanas y lumbalgia
crónica si el dolor persiste más allá de las 12 semanas.
Existen fundamentalmente cuatro perfiles clínicos de dolor lumbar (Tabla II):
Mecánico: empeora con la actividad física, mejora con el reposo.
Inflamatorio: suele tener un inicio insidioso, generalmente aparece antes de los 40 años de
edad, mejora con el ejercicio y empeora con el reposo. Los pacientes suelen presentar dolor
nocturno y rigidez matutina.
Dolor neuropático: se produce como consecuencia de una disrupción o lesión neurológica
somatosensorial a nivel periférico o central, que puede provocar dolor incapacitante,
hinchazón, alteración vasomotora, sudoración anormal y alteración de la función motora.
Descrito como alteraciones sensitivas (disestesia, alodinia), urente, eléctrico, etc.
Dolor referido: en ocasiones la lumbalgia puede corresponder a un dolor referido de otros
órganos y aparatos, por lo que en estos casos los pacientes asocian sintomatología específica
(síndrome miccional en el caso de patología urinaria, flujo vaginal purulento en el caso de
patología ginecológica, clínica gastrointestinal en el caso de patología digestiva, hipertensión
arterial en el caso de patología vascular…).
Tabla II.Clasificación clínica y etiológica del dolor lumbar.
IV. DIAGNÓSTICO
Es fundamental detectar signos de alarma que orientan a una etiología específica del dolor (Tabla I)
a través de:
1. Anamnesis
1.1. Edad y sexo
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [166]
[12] LUMBALGIA
En jóvenes la causa más frecuente es la lumbalgia mecánica o muscular. En pacientes menores de
40 años con dolor de características inflamatorias hay que pensar en espondiloartropatías. En mujeres
posmenopáusicas hay que tener en cuenta la posibilidad de fractura vertebral osteoporótica.
1.2. Profesión
Los trabajos sedentarios y los que suponen esfuerzos físicos importantes predisponen a patología
mecánica. También tienen un papel importante el sobrepeso y la forma física en el caso del dolor mecánico.
1.3. Inicio del dolor
Si es de inicio brusco orienta fundamentalmente a patología mecánica, aunque también puede
tratarse de síndrome aórtico agudo. El dolor inflamatorio suele ser más insidioso.
1.4. Características del dolor
Ver Apartado III. “Clínica” y la tabla II.
1.5. Irradiación
A lo largo de metámeras lumbares o sacras sugiere radiculopatía compresiva. Si es hacia la ingle o
los flancos abdominales orienta a patología urológica (crisis renoureterales).
1.6. Antecedentes patológicos
En pacientes con osteoporosis habría que pensar en fractura vertebral; en pacientes con factores
de riesgo cardiovascular e inicio agudo del dolor hay que descartar patología aórtica; en pacientes con
neoplasia previa, pensar en la posibilidad de metástasis óseas.
1.7. Uso de fármacos
El uso de diversos fármacos puede orientar hacia la etiología de la lumbalgia (hematoma
retroperitoneal en caso de anticoagulantes, fractura osteoporótica en el caso de corticoides, discitis o
absceso vertebral en pacientes con tratamientos inmunosupresores).
2. Exploración física
2.1. Exploración general con constantes vitales
2.2. Inspección
Deformidades espinales, dismetrías, posturas antiálgicas, índice de masa corporal, alteraciones en
la marcha, lesiones cutáneas.
2.3. Palpación
Según dónde se produzca el dolor puede orientar a diferentes patologías, aunque tiene una
especificidad baja: apófisis espinosas (patología mecánica, neoplasia, discitis), entesitis glúteas o
trocantéreas (espondiloartropatías, rocanteritis), puño-percusión renal (cólico renoureteral, pielonefritis,
prostatitis).
2.4. Movilidad de la columna
Flexoextensión, movilidad de articulaciones coxofemorales y sacroilíacas.
2.5. Exploración neurológica exhaustiva
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [167]
[12] LUMBALGIA
Test de Lasègue: orienta a patología radicular. Se considera positivo en caso de dolor agudo
irradiado hacia la pierna en la flexión de cadera/pelvis entre 30º y 60º con la rodilla en extensión. Si el test
de Lasègue es positivo se coloca la pierna en el punto donde aparece el dolor y se realiza flexión dorsal de
pie, siendo el signo de Bragard positivo si se reproduce el dolor.
3. Pruebas complementarias
3.1. Laboratorio
Analítica básica con hemograma, bioquímica, reactantes de fase aguda (proteína C reactiva y
velocidad de sedimentación globular [VSG]) y sistemático de orina. En pacientes de edad avanzada, ante
cualquier dato de alarma o sospecha de infección o tumor, en caso de presencia concomitante de fiebre
y/o dolor de características inflamatorias.
3.2. Pruebas de imagen
No están recomendadas en pacientes con lumbalgia aguda sin signos de alarma
Radiología simple: indicada en los siguientes casos:
Mayores de 50 años.
Antecedentes de neoplasia previa.
Tratamiento crónico con corticoides
Uso de tóxicos (alcohol, usuarios de drogas por vía parenteral).
Historia de traumatismo significativo.
Dolor en reposo, nocturno, rigidez matutina.
Déficit neurológico.
Síndrome constitucional.
Fiebre.
Ausencia de mejoría tras 2-4 semanas de tratamiento conservador adecuado.
Otras pruebas de imagen: en algunas entidades la sensibilidad de la radiografía simple es baja,
por lo que se recomiendan otras pruebas. Por ejemplo, en casos de sospecha de infección o
neoplasia o hernias discales la prueba más indicada es la resonancia magnética nuclear (RMN).
V. TRATAMIENTO Y MANEJO
Recomendaciones generales
Se desaconseja el reposo absoluto durante más de 2 días, ya que puede debilitar al paciente y
producir atrofias musculares.
Los antiinflamatorios no esteroideos (AINE) ayudan a aliviar el dolor desde el inicio de los
síntomas.
Se puede empezar con ejercicios aeróbicos ligeros durante las dos primeras semanas. Los
ejercicios de estiramiento y fortalecimiento se pueden iniciar después de pasadas dos semanas,
en caso de que no haya lesión, ya que pueden empeorar el dolor en fases iniciales.
Se debe fomentar que los pacientes retomen sus actividades habituales lo antes posible.
1. Lumbalgia mecánica aguda o crónica
1.1. Sin compromiso neurológico
Se debe realizar tratamiento conservador, con el cual el 80% de los casos ceden en 4 a 6
semanas.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [168]
[12] LUMBALGIA
Medidas no farmacológicas: calor local, fisioterapia o reposo relativo (evitando encamamiento).
Tratamiento farmacológico: AINE y/o relajantes musculares pautados durante un periodo
máximo de 5 días y después a demanda.
Paracetamol 650-1.000 mg cada 6 u 8 horas.
AINE: con precaución en pacientes con hipertensión arterial, insuficiencia renal,
ancianos, gastritis. Ibuprofeno 400 mg cada 8 horas, diclofenaco 50 mg cada 8 horas,
naproxeno 500 mg cada 12 horas. Se debe valorar la necesidad de asociar un protector
gástrico en estos pacientes.
Inhibidores de la ciclooxigenasa-2: indicado en pacientes con bajo riesgo cardiovascular
y elevado riesgo de gastropatía por AINE. Celecoxib 200 mg cada 12 horas, etoricoxib
90 mg cada 24 horas.
AINE + miorrelajantes: uso controvertido, igual de eficaz que solo AINE. Por ejemplo,
ibuprofeno 600 mg cada 8 horas y diazepam 5 mg cada 12 horas.
Si la intensidad del dolor lo requiere, o los analgésicos convencionales no alivian el dolor, se
puede realizar una escalada analgésica mediante el uso de opiáceos menores como tramadol
50 mg cada 8 horas u otros derivados mórficos.
1.2. Con compromiso neurológico
Ante la presencia de una radiculopatía unilateral sin compromiso vesical se realizará tratamiento
analgésico conservador (ver Apartado 1.1). En caso de radiculopatía con compromiso vesical, anestesia en
“silla de montar” o síntomas neurológicos bilaterales se debe realizar RMN urgente (o tomografía axial
computarizada [TAC]) y valoración por neurocirugía (Tabla III).
Tabla III.Clínica de lesiones de raíces nerviosas lumbares.
2. Lumbalgia inflamatoria
2.1. Sospecha de espondiloartropatía
En un paciente joven, con dolor subagudo o crónico de características inflamatorias. Valorar el
tratamiento sintomático (analgésico, AINE, fisioterapia) y remitir al reumatólogo.
2.2. Sospecha de neoplasia
En un paciente con historia de neoplasia previa, síndrome constitucional, síntomas neurológicos, >
50 años, radiografía sugestiva, VSG > 20. Valorar ingreso hospitalario, estudios de imagen (TAC, RMN,
gammagrafía...) y estudio de extensión y búsqueda de tumor primario.
2.3. Sospecha de infección
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [169]
[12] LUMBALGIA
En un paciente con fiebre, infecciones coexistentes, inmunosupresión, epidemiología compatible,
radiografía sugestiva, VSG > 20. Indicación de ingreso hospitalario, cultivos, estudio analítico, punción-
biopsia.
Tratamiento antibiótico dirigido según el antibiograma (más frecuente: S. aureus en niños y
usuarios de drogas por vía parenteral, gramnegativos en ancianos…), intravenoso durante 4 a 6 semanas
(ver Capítulo 41. “Infección de piel y partes blandas. Osteomielitis”).
2.4. Sospecha de otras patologías
En un paciente con aneurisma de aorta, infecciones o abscesos intraabdominales. Estudios de
imagen (TAC, RM...). Ingreso hospitalario.
BIBLIOGRAFÍA
Airaksinen O, Brox JI, Cedraschi C, et al. European guidelines for the management of chronic
nonspecific low back pain. Eur Spine J. 2006;15(Suppl 2):S192-S300. Doi: 10.1007/s00586-006-
1072-1.
Insausti Valdivia J. Non-specific lower back pain: in search of the origin of pain. Reumatol Clin. 2009;5
(Suppl 2):19-26.
Manual SER de enfermedades reumáticas, 6ª edición; 2014. pp. 102-3.
Pé rez Irazusta I, Alcorta Michelena I, Aguirre Lejarcegui G, et al. Guía de prá ctica clínica sobre
lumbalgia. 2007. Osakidetza. GPC 2007/1. Vitoria-Gasteiz.
Valle Calvet M, Olivé Marquès A. Signos de alarma de la lumbalgia. Seminarios de la Fundación
Española de Reumatología. 2010;11(1):24-7.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [170]
[13] MONOARTRITIS Y POLIARTRITIS
13.Monoartritis y poliartritis
Otto Martín Olivas Vergara.
Reumatología
Marta Torres Arrese.
Medicina Interna
Asesora:
Esther Rodríguez Almaraz.
Médica Adjunta de Reumatología
I. MONOARTRITIS
1. CONCEPTO
La monoartritis es la inflamación de una sola articulación. Suele presentar dolor con el
movimiento, limitación del mismo, tumefacción y/o eritema (estos dos últimos signos son difíciles
de valorar en las articulaciones profundas).
2. ETIOLOGÍA
Según la evolución temporal, la monoartritis se puede clasificar como aguda (inferior a 6
semanas) o crónica (superior a 6 semanas; suele deberse a gota tofácea crónica, artritis por
micobacterias u hongos). En el 16-36% de los casos no se alcanza el diagnóstico etiológico.
Tabla I.Etiología de la monoartritis aguda.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [171]
[13] MONOARTRITIS Y POLIARTRITIS
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [172]
[13] MONOARTRITIS Y POLIARTRITIS
3. DIAGNÓSTICO
Se orienta a través de la historia clínica y exploración. El líquido articular nos servirá para acotar las
posibilidades diagnósticas y descartar artritis séptica.
Figura 1.Algoritmo diagnóstico de la monoartritis aguda
1. Anamnesis
La anamnesis debe dirigirse inicialmente a valorar la emergencia articular, que podría conducir a un
daño permanente de la articulación. Algunos datos relacionados con esta entidad son estado séptico con
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [173]
[13] MONOARTRITIS Y POLIARTRITIS
una articulación caliente y tumefacta, debilidad muscular aguda (a considerar síndrome compartimental,
miopatía periarticular, mielopatía, impotencia por dolor), rubor, parestesias y dolor quemante (que
traduciría componente de neuropatía).
En la anamnesis hay que evaluar:
Síntomas articulares: el tipo de dolor (tiempo de inicio, factores que lo agravan o alivian,
intensidad y duración, afección única o poliarticular). En la artritis inflamatoria el dolor
empeora con el reposo (“rigidez matutina”); en la osteoartritis generalmente se agrava con el
movimiento.
Síntomas sistémicos: fiebre (puede estar presente en infecciones y en artritis inflamatorias
como las microcristalinas), síntomas genitourinarios o gastrointestinales (podrían orientar a
espondiloartropatías o artritis reactivas).
Antecedentes: familiares (artritis psoriásica), consumo de tóxicos (alcohol, drogas por vía
parenteral), viajes, inmunosupresión, contactos sexuales de riesgo.
2. Exploración física
Aúna la exploración sistémica (en busca de aftas orales y/o genitales, psoriasis, hemorragias
subungueales, tofos gotosos, nódulos subcutáneos, exantema, adenopatías y visceromegalias) y la
específica del aparato locomotor (articulación afecta). Hay que distinguir entre procesos articulares,
periarticulares o yuxtaarticulares:
Proceso articular: presenta signos locales (que pueden estar ausentes en articulaciones
profundas como cadera u hombro): tumefacción, calor (palpando con el dorso de la mano),
limitación de la movilidad activa y pasiva (signo más sensible), alineación y estabilidad articular
(signo del cajón, bostezos), derrame (signo más específico) o sinovitis de pequeñas
articulaciones.
Proceso periarticular: en él la limitación de la movilidad es activa, pero se conserva la
movilización pasiva (por ejemplo, en una tendinitis).
Proceso yuxtaarticular: son ejemplos el dolor neuropático y las infecciones locales (celulitis,
abscesos en psoas o retroperitoneales, diverticulitis –puede simular sacrolieítis–).
3. Pruebas complementarias
Estudio de líquido sinovial. Siempre hay que intentar realizar una artrocentesis para establecer
un diagnóstico. La muestra debe obtenerse en condiciones de asepsia. Es importante que la
recogida y el envío se hagan de forma adecuada y rápida (el número de cristales y de células
disminuye pasadas 4 horas). En general, 5 ml son suficientes. Sobre este líquido se debe hacer
estudio de perfil bioquímico, recuento celular y visión microscópica de cristales (además de
tinción de Gram urgente y cultivo, como se detalla en el punto siguiente).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [174]
[13] MONOARTRITIS Y POLIARTRITIS
Tabla II.Características de los derrames sinoviales.
Estudios microbiológicos. Siempre hay que solicitar tinción de Gram urgente en el líquido
sinovial (factible si se dispone de un microbiólogo de guardia) y cultivo del mismo. Se
obtendrán hemocultivos en caso de sospecha de artritis séptica. En alguna ocasión puede ser
conveniente cultivar el líquido en medios especiales para aerobios, anaerobios, micobacterias,
hongos, gonococo (Thayer-Martin) y Brucella spp. En función de la sospecha diagnóstica, se
valorará también el estudio microbiológico de orina, exudados de orofaringe, cérvix uterino,
uretra o piel.
Datos de laboratorio. Hemograma, velocidad de sedimentación globular (VSG), proteína C
reactiva (PCR) y bioquímica con ácido úrico, perfiles renal y hepático y sistemático de orina. Las
cifras de ácido úrico sérico pueden ser normales durante el episodio agudo de gota. Fuera del
evento agudo y para el seguimiento en consulta (en función de la sospecha) solicitaremos
factor reumatoide, anticuerpos antipéptido cíclico citrulinado (anti-CCP), anticuerpos
antinucleares (alta sensibilidad; baja especificidad), serologías (Borrelia spp, Brucella spp, virus
hepatotropos, virus de Epstein Barr [VEB], citomegalovirus [CMV], parvovirus B19), HLA-B27 y
Mantoux. Sin embargo, el valor de estos estudios en el diagnóstico de la monoartritis aguda es
limitado.
Estudios de imagen
Radiografía simple: de poca ayuda en la monoartritis aguda pero importante para
descartar fracturas y otros procesos de curso subagudo-crónico como tumores
primarios o metástasis, osteomielitis, osteonecrosis y artrosis ya establecida.
Inicialmente solo se observa aumento de partes blandas pero en las monoartritis
crónicas puede haber pinzamiento de la interlínea articular, osteopenia subcondral y
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [175]
[13] MONOARTRITIS Y POLIARTRITIS
erosiones. Si hubiera sospecha de condrocalcinosis se habría de buscar calcificaciones
en meniscos, en el ligamento triangular del carpo y en la sínfisis púbica.
Ecografía: es la técnica de elección, aunque no siempre está disponible en Urgencias.
Nos permite ver abscesos, tendinitis, derrame articular y sinovitis (siendo más sensible
que la exploración física), así como dirigir la artrocentesis y guiar la toma de biopsias. Es
especialmente útil para confirmar la presencia de derrame articular y drenarlo en
articulaciones profundas como caderas u hombros.
Tomografía computarizada: útil para guiar la colocación de la aguja en la aspiración de
derrame articular desde áreas de difícil acceso (caderas, sacroilíacas,
esternoclaviculares).
Resonancia magnética (no urgente): indicada en monoartritis persistentes de etiología
no filiada. Útil en el diagnóstico precoz de osteonecrosis, enfermedad de Perthes,
tumores, osteomielitis, lesiones meniscales y ligamentosas e infartos óseos.
Biopsia sinovial (no urgente): normalmente se lleva a cabo guiada por imagen
(tomografía computarizada o ecografía) o por artroscopia. Es útil en monoartritis
crónicas sin diagnóstico filiado (tuberculosis, fúngicas, sarcoidosis, tumores
intraarticulares).
4. TRATAMIENTO
Es importante hacer seguimiento clínico de la monoartritis para no pasar por alto causas menos
probables de entrada. No se debe enmascarar el cuadro con antiinflamatorios no esteroideos (AINE) hasta
tener el diagnóstico definido. Si la intensidad de los síntomas del paciente lo permitiera es preferible tratar
el dolor con analgésicos (codeína o paracetamol).
Tabla III.Tratamiento de las monoartritis.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [176]
[13] MONOARTRITIS Y POLIARTRITIS
II. POLIARTRITIS
1. CONCEPTO
La poliartritis (PA) es un síndrome clínico caracterizado por la inflamación de cuatro o más
articulaciones. En la oligoartritis (OA) solo se afectan dos o tres articulaciones. La importancia de
diferenciar ambos conceptos es relativa. Por tanto, en este capítulo vamos a considerar la PA como la
inflamación de dos o más articulaciones.
2. DIAGNÓSTICO
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [177]
[13] MONOARTRITIS Y POLIARTRITIS
La historia clínica, la anamnesis y la exploración física son importantes para realizar el diagnóstico
diferencial, ya que la sintomatología articular tiene escasa especificidad. Algunos datos importantes en la
anamnesis son la duración de los síntomas, episodios previos de artritis y su distribución. Los síntomas
extraarticulares y las exploraciones complementarias proporcionan datos que ayudan a realizar el
diagnóstico.
Tabla IV.Exploraciones complementarias en las poliartritis agudas (según el cuadro clínico del paciente).
Tabla V.Aproximación diagnóstica.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [178]
[13] MONOARTRITIS Y POLIARTRITIS
3. ENTIDADES CLÍNICAS
Tabla VI.Principales causas de poliartritis y de oligoartritis.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [179]
[13] MONOARTRITIS Y POLIARTRITIS
1. Poliartritis infecciosas
1.1. Bacterianas
Se clasifican como artritis sépticas y se dividen en gonocócicas y no gonocócicas. Este último grupo
comprende numerosos agentes. La infección por Borrelia spp (enfermedad de Lyme) cursa con
sintomatología típica viral en su fase precoz y con un cuadro oligoarticular en la fase tardía. Su diagnóstico
es clínico (eritema crónico migratorio, exposición a la picadura de la garrapata en un área endémica) y
mediante un resultado serológico positivo. Habitualmente se trata con doxiciclina o amoxicilina orales
durante un mes, aunque en algunos casos se precisa terapia endovenosa junto con tratamiento sintomático
(AINE). Los pacientes con afecciones articular y neurológica se tratan según la pauta neurológica. Los casos
refractarios al tratamiento antibiótico se pueden tratar con hidroxicloroquina o someterse a sinovectomía.
1.2. Virales
Son poliarticulares y, a veces, migratorias. El parvovirus B19 puede producir una clínica similar a la
artritis reumatoide, precedida o no de un cuadro pseudogripal. Suele resolverse en pocas semanas aunque
algunos pacientes pueden presentar síntomas durante meses. Se diagnostica mediante la detección en
suero de IgM específica. El tratamiento es sintomático y se realiza con AINE (no hay terapia específica). El
VHB genera una afección simétrica aguda, sobre todo de manos y rodillas. Suele preceder a la ictericia y
remitir al desaparecer esta. La artritis puede recidivar en casos de viremia crónica. El VHC puede asociarse
con crioglobulinemia mixta esencial, caracterizada por artritis, púrpura palpable, afección neurológica y
crioglobulinas en sangre. Para ambas infecciones se ha de disponer tratamiento sintomático y el del virus, si
procediera. El VIH provoca un cuadro oligoarticular en miembros inferiores habitualmente inferior a 6
semanas de duración. El tratamiento es sintomático y en algunos casos se pueden utilizar glucocorticoides,
hidroxicloroquina o sulfasalazina.
Otra entidad que ha incrementado su incidencia es la infección por virus Chikungunya, un alfavirus
transmitido por la picadura de los mosquitos Aedes aegypti y Aedes albopictus. Causa un cuadro febril
agudo caracterizado por rash, cefalea, mialgias y artralgias incapacitantes. El dolor articular es usualmente
simétrico y se localiza en brazos y piernas (en el 90% de los pacientes). Afecta casi siempre a las grandes
articulaciones (las pequeñas y la columna vertebral se ven dañadas en menor medida). Pueden aparecer
edema periarticular, dolor en las entesis, y artritis aguda, en particular en articulaciones interfalángicas,
muñecas y tobillos. Debe sospecharse en pacientes que provengan de zonas endémicas. El diagnóstico se
basa en el cultivo del virus y la determinación de PCR, sobre todo durante los primeros días tras la
infección, puesto que los anticuerpos IgM tardan una semana en aparecer. El tratamiento en esta fase
suele ser sintomático. Sin embargo, hay que considerar que en un 12-60% de pacientes (según las series
consultadas) los síntomas articulares pueden cronificarse y asemejarse a una poliartritis seronegativa. Se ha
planteado el uso de antipalúdicos y de metotrexato en estos casos. (Ver Capítulo 49. “Enfermedades
importadas del viajero y del inmigrante”).
2. Poliartritis postinfecciosas
La artritis de Poncet muchas veces se presenta con síntomas constitucionales como fiebre,
malestar general, anorexia y sudoración nocturna, así como con poliartritis que usualmente compromete
grandes articulaciones. La tuberculosis subyacente produce usualmente afección pulmonar o adenopática.
No suele aislarse en el estudio microbiológico de líquido sinovial.
La fiebre reumática es otra causa bien conocida de artritis postinfecciosa. Es importante
sospecharla en jóvenes con poliartritis migratoria de inicio agudo y con dolor desproporcionado para el
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [180]
[13] MONOARTRITIS Y POLIARTRITIS
grado de sinovitis. Puede asociar afección cardiaca y/o neurológica (corea). Hay que buscar evidencia
serológica de infección estreptocócica (niveles elevados de ASLO o detección de exotoxina de
Streptococcus) y confirmarla con cultivo de exudado faríngeo. Para el diagnóstico se utilizan los criterios de
Jones, que se dividen en criterios mayores (artritis migratoria, carditis y valvulitis, corea de Sydenham,
eritema marginatum y nódulos subcutáneos) y menores (artralgias, fiebre, elevación de reactantes de fase
aguda [PCR/VSG] y prolongación del intervalo PR). Se requieren dos criterios mayores o uno mayor y dos
menores junto con evidencia de infección estreptocócica en los 45 días previos (cultivo faríngeo positivo,
test rápido del antígeno positivo, ASLO elevados, escarlatina reciente). Sin embargo, puede presentarse sin
cumplir todos estos criterios. El tratamiento se realiza con AINE junto con la terapia antibiótica clásica de la
infección estreptocócica (penicilina, amoxicilina).
3. Poliartritis inflamatorias
3.1. Artritis reumatoide
La artritis reumatoide (AR) es más frecuente en mujeres que en hombres. Su inicio suele ser
insidioso aunque puede presentarse como un cuadro agudo. Se caracteriza por afectar a las articulaciones
de forma aditiva y simétrica, y por dañar a las pequeñas articulaciones de manos y pies. También pueden
afectarse las grandes articulaciones de extremidades inferiores y superiores y la columna cervical (es
importante descartar subluxación atloaxoidea). Puede producir daño articular en los primeros 2 años,
causando una gran limitación funcional, y un acortamiento de la esperanza de vida entre 5 y 7 años al
asociarse a arterioesclerosis prematura. Durante su evolución puede presentar afección ocular
(queratoconjuntivis seca, escleritis, escleromalacia), cardiopulmonar (serositis, bronquiolitis, miocarditis),
neuropatía periférica; o asociarse con el síndrome de Felty (esplenomegalia, neutropenia e infecciones de
repetición); con un síndrome de Sjögren secundario; o con vasculitis. El diagnóstico se basa en la clínica, los
test de laboratorio (factor reumatoide, anti-CCP, VSG, PCR, anemia, trombocitosis) y la radiología
(erosiones). El 80% de los pacientes tienen factor reumatoide positivo durante su evolución. Los anti-CCP
son una herramienta diagnóstica sensible y específica en estadios precoces de la enfermedad en pacientes
seronegativos (que no han desarrollado factor reumatoide). Ninguno de los dos marcadores se utiliza en el
seguimiento clínico habitual. Se utilizan AINE o glucocorticoides a dosis bajas y medias como tratamiento
inicial durante la fase aguda o en exacerbaciones, para el control del dolor y la inflamación. En casos de
inicio agresivo y con limitación funcional importante pueden usarse minipulsos de metilprednisolona. Lo
más importante es comenzar precozmente (a lo largo de los tres primeros meses) un tratamiento con
fármacos modificadores de la enfermedad (FAME) para evitar la destrucción articular y la discapacidad. El
FAME de elección es el metotrexato, si bien se utilizan también leflunomida, hidroxicloroquina o
sulfasalazina. Si a pesar de usar dosis plenas hubiera progresión radiológica y empeoramiento clínico, el
siguiente paso sería usarlos en combinación. Si previéramos que la evolución fuera a ser agresiva, habría
que añadir tratamientos biológicos junto a los FAME. Los fármacos inhibidores del factor de necrosis
tumoral (anti-TNF) (infliximab, etanercept, adalimumab, certolizumab pegol, golimumab), tocilizumab y
abatacept son los de primera línea, aunque también se puede usar rituximab. En caso de ineficacia se debe
cambiar el tratamiento a otro fármaco biológico. Los niveles de anticuerpos y de fármacos pueden ayudar
en la elección.
3.2. Lupus eritematoso sistémico (LES)
Alrededor del 70% de los pacientes presentarán episodios de poliartritis similares a los de la AR
durante la evolución de su enfermedad. Esta poliartritis involucra principalmente a las pequeñas
articulaciones de manos y pies. Se diferencia de la AR en que las deformidades articulares se pueden
reducir y en que habitualmente no se producen erosiones (artropatía de Jaccoud). Serositis, rash cutáneo,
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [181]
[13] MONOARTRITIS Y POLIARTRITIS
fiebre, citopenias, hipocomplementemia, afección renal o detección de anticuerpos antinucleares (ANA)
suelen ser claves en el diagnóstico. El tratamiento dependerá del órgano afecto.
3.3. Espondiloartropatías
Este grupo de enfermedades se caracteriza por la presencia del antígeno de histocompatibilidad de
clase I HLA-B27, artritis axial que incluye espondilitis y sacroileítis, afectación inflamatoria ocular y cutánea
y entesopatía (afección tendinosa). El patrón suele ser oligoarticular y asimétrico, con artritis de grandes
articulaciones en miembros inferiores (cadera y rodilla). No suelen presentar títulos positivos de factor
reumatoide ni de ANA. El diagnóstico específico depende de las manifestaciones clínicas que asocien:
3.3.1. Espondilitis anquilosante
El inicio de la espondilitis anquilosante (EA) suele ser insidioso y su afección articular, axial (es el
subtipo con menos afección articular periférica; hombro y cadera se dañan en el 25% de los pacientes).
Puede acompañarse de manifestaciones extraarticulares (oculares, cardiovasculares, pulmonares,
neurológicas y renales). El objetivo del tratamiento es eliminar el dolor y la rigidez y mantener la movilidad
(por ello es importante la terapia física). Los AINE son el escalón inicial, y se recomienda su uso con al
menos 2 diferentes a dosis plenas antes de contemplar una respuesta inadecuada al tratamiento. El
siguiente escalón son los anti-TNF puesto que los FAME y los glucocorticoides parecen tener poca actividad
axial y se utilizan con más frecuencia en caso de afección periférica (metotrexato, sulfasalazina y, con
menor frecuencia, leflunomida).
3.3.2. Artritis psoriásica
Tiene cinco patrones articulares diferentes (uno de ellos, indistinguible de la AR). El más frecuente
es el oligoarticular asimétrico. La dactilitis, los antecedentes personales o familiares de psoriasis cutánea, la
distrofia ungueal y entesopatía son manifestaciones que ayudan en el diagnóstico diferencial. En algunos
pacientes la clínica articular puede preceder a la psoriasis cutánea. No hay datos de laboratorio específicos
para su diagnóstico. El tratamiento es similar al de la AR, con la diferencia de que hay que controlar la
actividad cutánea y articular y no todos los fármacos son igual de eficaces para ambas manifestaciones.
3.3.3. Artritis reactiva
Caracterizada por la tríada de conjuntivitis, uretritis y oligoartritis asimétrica de grandes
articulaciones en miembros inferiores. Estos síntomas pueden no aparecer simultáneamente, lo que limita
el diagnóstico. Sin embargo, las manifestaciones no articulares son claves en él (balanitis circinada,
queratodermia blenorrágica). El inicio de la enfermedad suele ocurrir 1-2 semanas tras desarrollar un
cuadro infeccioso caracterizado por diarrea (causado por Salmonella, Shigella, Campylobacter, Yersinia) o
uretritis (provocado por Chlamydia trachomatis, Ureaplasma urealyticum…). Los AINE se usan en la fase
aguda para el control del dolor y de la inflamación durante, al menos, dos semanas. Solo se indicaría
antibiótico si hubiera evidencia de infección en ese momento (nunca como tratamiento específico de la
artritis). En ocasiones pueden ser útiles las infiltraciones con glucocorticoides. Los FAME (sulfasalazina y
metotrexato) se usan en los casos que no responden a AINE o a infiltraciones locales. Se usan durante 3-6
meses, pudiendo discontinuarse si la clínica remitiera. Se podría plantear el uso de anti-TNF en pacientes
que no hubieran respondido.
3.3.4. Artritis enteropática
Habitualmente poliarticular y asimétrica. Puede preceder a la enfermedad inflamatoria intestinal
(EII) en meses o años. Típicamente produce una artritis no erosiva. La afección periférica suele asociarse a
las exacerbaciones de la EII, y responde al tratamiento de la misma. La artritis axial es independiente de la
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [182]
[13] MONOARTRITIS Y POLIARTRITIS
actividad inflamatoria intestinal y no suele responder bien. La conjunción de espondilitis con dolor
abdominal, eritema nodoso o pioderma gangrenoso suele ser la clave para el diagnóstico. El tratamiento
con AINE (COXIB) debe realizarse con cautela y solo de forma puntual. Se pueden utilizar glucocorticoides
para las exacerbaciones, y FAME como azatioprina y sulfasalazina (que también se usan en la actividad de la
EII) o anti-TNF en los casos refractarios o clínica axial que no responda a AINE.
BIBLIOGRAFÍA
Becker. Clinical manifestations and diagnosis of gout. En: UpToDate, H Ralph Schumacher, MD (Ed),
UpToDate, Waltham, MA, 2015.
Becker. Treatment of acute gout. En: UpToDate, H Ralph Schumacher, MD (Ed), UpToDate, Waltham,
MA, 2015.
Cush JJ, Lipsky PE. Valoración de los trastornos articulares y musculoesqueléticos. En: Longo DL,
Kasper DL, Jameson J, Fauci AS, Hauser SL, Loscalzo J. eds. Harrison. Principios de Medicina Interna,
18e. New York, NY: McGraw-Hill; 2012.
Don L Goldenberg, MD, Daniel J Sexton, MD. Disseminated gonococcal infection. En: UpToDate, Noreen
A Hynes, MD, MPH, DTM&H (Ed), UpToDate, Waltham, MA, 2015.
Don L Goldenberg, MD, Daniel J Sexton, MD. Septic arthritis in adults. Stephen B Calderwood, MD (ed),
UpToDate, Waltham, MA, 2015.
Felson DT. Osteoartritis. In: Longo DL, Kasper DL, Jameson J, Fauci AS, Hauser SL, Loscalzo J. eds.
Harrison. Principios de Medicina Interna, 18e. New York, NY: McGraw-Hill; 2012.
Firestein GS, Budd RC, Harris ED, McInnes IB, Ruddy S. (ed) Kelley`s textbook of Rheumatology. 8ª ed.
Elsevier; 2009.
Gómez Centeno A. Evaluación del paciente con poliartritis. En: Alperi López M, Balsa Criado A, Blanco
Alonso R, Hernández Cruz B, Medina Luezas J, Muñoz Fernández S, Nolla Solé JM, Román Ivorra JA
(ed). Manual SER de Enfermedades Reumáticas. 6ª ed. Madrid: Elsevier. 2014:91-6.
Horcada L, Díaz-Calderón C, Garrido L. Fiebre Chikungunya. Manifestaciones reumáticas de una
infección emergente en Europa. Reumatol Clin. 2015;11(3):161-4.
Kumar A. How to investigate new-onset polyarthritis. Best Pract Res Clin Rheumatol. 2014;28:844-59.
Madoff LC. Artritis infecciosa. In: Longo DL, Kasper DL, Jameson J, Fauci AS, Hauser SL, Loscalzo J.
eds. Harrison. Principios de Medicina Interna, 18e. New York, NY: McGraw-Hill; 2012.
Michael A Becker, MD, Lawrence M Ryan, MD. Clinical manifestations and diagnosis of calcium
pyrophosphate crystal deposition (CPPD) disease. H Ralph Schumacher, MD (Ed). UpToDate, Waltham,
MA, 2015.
Miner J, et al. Chikungunya viral arthritis in the United States a mimic of seronegative rheumatoid
arthritis. Arthritis Rheum. 2015;67(5):1214-20.
Mitchell SR, Beary JF. Monoarthritis/Polyarthritis: Differential diagnosis. En: Paget SA. Manual of
Rheumatology and outpatient orthopedic disorders. 5th ed. LWW. 2005.
Schumacher H, Chen LX. Gota y otras artropatías por cristales. En: Longo DL, Kasper DL, Jameson J,
Fauci AS, Hauser SL, Loscalzo J. eds. Harrison. Principios de Medicina Interna, 18e. New York, NY:
McGraw-Hill; 2012.
Simon M Helfgott, MD. Overview of monoarthritis in adults. Robert H Shmerling, MD (Ed). UpToDate,
Waltham, MA, 2015.
Vela Casampere P. Evaluación del paciente con monoartritis. En: Alperi López M, Balsa Criado A,
Blanco Alonso R, Hernández Cruz B, Medina Luezas J, Muñoz Fernández S, Nolla Solé JM, Román
Ivorra JA (ed). Manual SER de Enfermedades Reumáticas. 6ª ed. Madrid: Elsevier. 2014:85-90.
Weaver S, Lecuit M. Chikungunya virus and the global spread of a mosquito-borne disease. N Engl J
Med. 2015;372:1231-9.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [183]
[14] FIEBRE DE ORIGEN DESCONOCIDO. ALTERACIONES DE LA TERMORREGULACIÓN
14.Fiebre de origen desconocido. Alteraciones de la
termorregulación
Noelia García-Pozuelo Adalia.
Medicina Interna
Blanca Ayuso García.
Medicina Interna
Asesor:
Ángel Luis Coto López.
Médico Adjunto de Medicina Interna
I. CONCEPTO
La fiebre de origen desconocido (FOD) fue definida por Petersdorf y Beeson en 1961 como un
síndrome que incluye: temperatura corporal ≥ 38,3 ºC en varias determinaciones, duración de al menos
tres semanas y diagnóstico etiológico incierto tras una semana de estudio intrahospitalario.
Posteriormente, en 1991, Durack y Street propusieron un nueva definición en la que a lo
anteriormente mencionado se añadía que debía permanecer sin diagnóstico tras tres días de estudios
hospitalarios o en tres consultas ambulatorias (incluyendo la incubación de cultivos microbiológicos
durante al menos 48 horas), clasificándola además según las características del paciente en: clásica,
nosocomial (ausencia de infección o incubación en el momento del ingreso), neutropénica (recuento de
neutrófilos < 500/μl o aparición de fiebre en los próximos tres días) o asociada al virus de la
inmunodeficiencia humana (VIH; requiere estudio ambulatorio durante más de cuatro semanas u
hospitalario durante más de tres días). Sin embargo, estas definiciones están cada vez más en desuso,
pasándose a definir la FOD con un único criterio cualitativo: ausencia de diagnóstico o hipótesis diagnóstica
en un paciente con fiebre (temperatura matutina > 37,2 ºC o > 37,8 ºC a cualquier hora del día) tras un
periodo de investigación razonable con técnicas apropiadas (analíticas, microbiológicas y de imagen
básicas).
Asimismo, la clasificación en cuatro categorías tampoco resulta una herramienta útil, dado que las
tres últimas (nosocomial, neutropénica y asociada al VIH) tienen unas causas definidas aparte, con un
manejo diagnóstico y terapéutico completamente diferente, pasando a ser entidades distintas de la FOD.
Esta, a su vez, pasa a dividirse en cinco grandes categorías según la etiología: infecciosa, tumoral,
inflamatoria no infecciosa (non-infectious inflammatory disease, que incluiría enfermedades
reumatológicas sistémicas, vasculitis, enfermedades granulo- matosas y síndromes autoinflamatorios),
miscelánea y sin diagnóstico.
II. EPIDEMIOLOGÍA
Desde 1990 la cifra de casos ha sufrido un incremento continuo. Ello se debe, por un lado, al avance
y desarrollo de técnicas diagnósticas que permite identificar más precozmente enfermedades que antes se
presentaban como FOD (por ejemplo, tuberculosis extrapulmonar, conectivopatías, tumores sólidos,
abscesos abdominales).
También hay que contar con el aumento de incidencia de la FOD debido al incremento del uso de
antibioterapia empírica y de regímenes agresivos de inmunosupresión, del número de trasplantes, del uso
de hemoderivados, de las estancias hospitalarias largas y del auge de la flora hospitalaria multirresistente.
Además, la facilidad del transporte, con el aumento del acceso a zonas antes no visitadas y del tránsito
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [184]
[14] FIEBRE DE ORIGEN DESCONOCIDO. ALTERACIONES DE LA TERMORREGULACIÓN
migratorio, ha hecho que la distribución de muchas enfermedades restringidas a zonas geográficas haya
cambiado (por ejemplo, malaria, brucelosis, kala-azar, filariasis, esquistosomiasis, etc.).
III. ETIOLOGÍA
En la mayoría de los casos, más que la manifestación de una entidad rara, la FOD es una
manifestación atípica de una enfermedad común. Sus causas pueden variar según el rango de edad. En
mayores de 65 años predominan las enfermedades sistémicas (como enfermedades reumáticas, vasculitis –
especialmente la arteritis de células gigantes–, polimialgia reumática y sarcoidosis), mientras que las
infecciones son el segundo grupo etiológico más frecuente (siendo la tuberculosis la más prevalente). Sin
embargo, en la edad pediátrica suelen ser más prevalentes los procesos virales autolimitados (Tabla I).
Tabla I.Causas de la fiebre de origen desconocido.
IV. DIAGNÓSTICO
1. Anamnesis y examen físico
Es la parte más importante y útil en la evaluación del paciente con FOD, y requiere reevaluaciones
periódicas para detectar signos y síntomas que se presenten con latencia. Todo este proceso irá orientado a
identificar lo que se conoce como pistas potencialmente diagnósticas (potencially diagnostic clues), es
decir, todo signo, síntoma o anomalía que conduce al diagnóstico de la entidad:
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [185]
[14] FIEBRE DE ORIGEN DESCONOCIDO. ALTERACIONES DE LA TERMORREGULACIÓN
Datos epidemiológicos: historia familiar o casos similares en allegados, condiciones sociales,
viajes recientes o no, exposición a animales.
Antecedentes personales: actividad laboral, aficiones, hábitos tóxicos y sexuales, alimentación y
tratamiento farmacológico.
Antecedentes médico-quirúrgicos: incidiendo en la situación inmune del paciente y síntomas
localizadores y/o decisivos. Por el contrario, el grado de fiebre y su respuesta a antipiréticos no
parece tener suficiente especificidad para guiar el diagnóstico.
Exploración física: debe ser igualmente detallada, incluyendo el examen del fondo de ojo y la
exploración del área otorrinolaringológica y de los genitales.
2. Pruebas complementarias
El proceder diagnóstico en el paciente con FOD es progresivo y escalonado, como puede
comprobarse en la figura 1.
Se explican, a continuación, por su interés, las siguientes pruebas complementarias:
2.1. Pruebas de primer nivel
La velocidad de sedimentación globular (VSG), a pesar de ser inespecífica, puede traducir la
magnitud de la gravedad de la causa subyacente. Elevaciones por encima de 100 mm/h
sugieren enfermedad subyacente grave o inflamación significativa (si bien algunas reacciones
por hipersensibilidad a fármacos, las tromboflebitis y la enfermedad renal, sobre todo el
síndrome nefrótico, pueden acompañarse de una elevación significativa de la VSG en ausencia
de infección o malignidad). Valores normales prácticamente descartan un proceso inflamatorio
relevante como causa de la fiebre (con excepciones, como la arteritis de la temporal en algunos
pacientes).
La proteína C reactiva (PCR) puede ser una referencia útil al compararla con la VSG, y es un
indicador más sensible y específico de una respuesta metabólica inflamatoria de fase aguda.
La procalcitonina, aunque puede estar elevada en otros procesos inflamatorios, tiene mayor
especificidad para infección bacteriana.
Intradermorreacción con PPD (Mantoux): puede resultar falsamente negativa en situaciones de
anergia cutánea, como ocurre en la tuberculosis miliar, la sarcoidosis, la enfermedad de
Hodgkin, la malnutrición o el síndrome de inmunodeficiencia adquirida.
2.2. Pruebas de segundo nivel
Ante la ausencia de datos que orienten hacia un diagnóstico, se acudirá a técnicas radiológicas y/o
endoscópicas.
Tomografía computarizada (TC) abdominal: técnica de elección para buscar abscesos ocultos,
neoplasias, adenopatías (como indicador de síndromes linfoproliferativos o enfermedades
granulomatosas) y hematomas. Aunque en ciertos casos la resonancia magnética es más
sensible que la TC (por ejemplo en abscesos raquídeos o pararraquídeos), no suele usarse de
rutina en la evaluación inicial de la FOD.
TC torácica: de gran utilidad en la búsqueda de pequeños nódulos pulmonares o infiltrados no
visualizados en la radiografía, tromboembolismo pulmonar y linfadenopatías hiliares/
mediastínicas. Además, permite localizar lesiones que sean accesibles para la toma de biopsia
por vía endoscópica o transparietal.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [186]
[14] FIEBRE DE ORIGEN DESCONOCIDO. ALTERACIONES DE LA TERMORREGULACIÓN
Ecocardiograma transtorácico: si bien no descarta una endocarditis infecciosa, detecta el 90%
de las endocarditis subagudas y permite también descartar mixomas auriculares (aunque la
técnica de elección para su identificación sea el ecocardiograma transesofágico).
Figura 1.Algoritmo diagnóstico de la fiebre de origen desconocido.
2.3. Pruebas de tercer nivel
Gammagrafía con leucocitos marcados con galio-67 e indio-111: son métodos sensibles de
localización de procesos malignos e inflamatorios, que además abarcan todo el cuerpo. Sin
embargo, son poco específicos al no discriminar el origen de la captación, tienden a
infradiagnosticar conectivopatías, y su realización puede demorarse durante varios días, con el
consiguiente retraso diagnóstico. Su principal utilidad reside en marcar la localización para la
realización de estudios dirigidos como la TC o la toma de muestras, reservándose para aquellos
casos en los que la evaluación inicial ha sido negativa.
La tomografía por emisión de positrones-TC con fluorodesoxiglucosa ha cobrado una
gran relevancia en el estudio de la FOD en los últimos tiempos. Es una prueba con alta
sensibilidad, especificidad y valores predictivos positivo y negativo, siendo útil para el
diagnóstico en hasta dos tercios de los casos, especialmente en aquellos con elevaciones
de la VSG y de la PCR y con fiebre permanente (en casos de fiebre periódica obtiene
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [187]
[14] FIEBRE DE ORIGEN DESCONOCIDO. ALTERACIONES DE LA TERMORREGULACIÓN
resultados favorables en la mitad de los casos, especialmente si se realiza durante el
episodio, facilitando la ampliación de estudios sobre los puntos con captación). Como
ventajas respecto a otras técnicas tiene una alta resolución para infecciones crónicas de
bajo grado, para procesos agudos en el esqueleto central y para vasculitis. Como
desventajas, el aumento de actividad fisiológica en el cerebro y el corazón y la filtración
del captador por los riñones y la vejiga dificultan el diagnóstico de la enfermedad a esos
niveles; además, es una técnica de alto coste relativo (pese al alto coste evitaría la
realización de pruebas innecesarias) y persiste el problema de que no diferencia el origen
infeccioso, inflamatorio o tumoral de la captación. Aunque su uso está ampliamente
aceptado en los algoritmos diagnósticos de la FOD, tanto en pacientes hospitalizados
como ambulatorios, todavía son necesarios estudios de coste-efectividad que avalen su
uso primario frente a otras pruebas.
2.4. Ausencia de diagnóstico o sospecha por pruebas anteriores
Muestras histológicas: punción-aspiración guiada por imagen, biopsia dirigida según la
sospecha clínica o, en casos seleccionados, laparotomía exploradora. En mayores de 55 años
que muestren síntomas y hallazgos de laboratorio orientativos es adecuada la realización de
biopsia a ciegas de ambas arterias temporales. En caso de fiebre persistente, con deterioro del
estado general o mala tolerancia clínica, debe plantearse, por su rentabilidad en este punto, la
biopsia empírica de médula ósea y/o biopsia hepática, siempre y cuando exista una alta
sospecha clínica de afectación a este nivel y ponderando las posibles complicaciones de la
técnica.
Arteriografía: en caso de sospecha de vasculitis sistémica.
Punción lumbar ante la concurrencia de sintomatología neurológica o alteración del nivel de
consciencia, así como pruebas de neuroimagen.
V. PRONÓSTICO
Depende de la causa subyacente. No obstante, en la mayoría de adultos sin diagnóstico tras un
estudio completo el pronóstico suele ser bueno.
VI. TRATAMIENTO
Tratamiento dirigido según la causa subyacente y, si es necesario, asociado a antipiréticos.
Antibioterapia y ciclos de corticoides empíricos: los ensayos terapéuticos con antibióticos o
glucocorticoides no suelen ayudar a establecer un diagnóstico. Además, pueden obstaculizarlo,
al negativizar cultivos microbiológicos y alterar la anatomía patológica de las muestras
obtenidas. Por ello, es preferible recurrir a antipiréticos según las necesidades del paciente
hasta completar el estudio etiológico. La utilización de antibióticos de forma empírica solo se
contempla en caso de deterioro clínico marcado o neutropenia. En cuanto a los ciclos de
corticoides empíricos debe descartarse en primer lugar patología infecciosa subyacente, y están
indicados en caso de sospecha de arteritis de la temporal con signos y/o síntomas oculares y
ante la sospecha de enfermedad de Still con compromiso vital.
En casos seleccionados, con alta sospecha de enfermedades sistémicas inflamatorias cuyo
diagnóstico genético puede demorarse semanas (por ejemplo, fiebre mediterránea familiar), se
han probado con éxito regímenes empíricos con tratamientos biológicos (antagonistas del
receptor de la interleucina-1) o colchicina.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [188]
[14] FIEBRE DE ORIGEN DESCONOCIDO. ALTERACIONES DE LA TERMORREGULACIÓN
En función de la sospecha: viajes recientes a zonas endémicas de microorganismos específicos
(por ejemplo, malaria), deterioro clínico en paciente con sospecha de tuberculosis miliar (aún
sin confirmación microbiológica), retirada de fármacos sospechosos, etc.
En cualquier caso, en pacientes estables en quienes no se ha llegado a un diagnóstico
etiológico, a pesar de un estudio completo y tras una vigilancia de más de seis meses, pueden
indicarse antiinflamatorios no esteroideos (AINE) con la única indicación de control sintomático
de la fiebre, contemplando los corticoides como último recurso. El inicio de cualquier
modalidad de tratamiento empírico no marca el final del estudio diagnóstico, sino que obliga a
reevaluación y a un seguimiento periódico.
VII. ALTERACIONES DE LA TERMORREGULACIÓN
El centro termorregulador del hipotálamo mantiene la temperatura corporal central en 37 ± 0,5 ºC
gracias al balance entre la producción de calor (metabolismo celular) y la pérdida del mismo (vasodilatación
cutánea, sudoración y respiración). Además, la temperatura corporal está sujeta a un ritmo circadiano, con
una variación máxima diaria de 0,5 ºC (mínimo a las 6.00; máximo a las 16.00). Diferentes alteraciones en el
control hipotalámico suponen el desarrollo de las siguientes patologías.
1. HIPOTERMIA
1. Definición
Temperatura corporal que no supera los 35 ºC. Se clasifica en: leve (32 a 35 ºC), moderada (28 a 32
ºC) y grave (por debajo de 28 ºC).
2. Etiopatogenia
La hipotermia se deriva de la alteración en el balance entre la producción de calor corporal y su
pérdida (fundamentalmente a nivel cutáneo y pulmonar). El principal mecanismo en la hipo- termia
accidental es por convección hacia el aire frío circundante, o por conducción hacia el agua. Las causas de
hipotermia no medioambiental están descritas en la tabla II.
Tabla II.Causas de hipotermia no medioambiental.
3. Manifestaciones clínicas
Las manifestaciones clínicas están relacionadas con la etiopatogenia y varían según el grado de
hipotermia; tal y como se describe a continuación:
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [189]
[14] FIEBRE DE ORIGEN DESCONOCIDO. ALTERACIONES DE LA TERMORREGULACIÓN
Leve: taquipnea, taquicardia, ataxia, disartria, confusión, temblor/”tiritona” y “diuresis fría”.
Moderada: bradipnea, disminución del pulso, depresión del sistema nervioso central (SNC) con
letargia e hiperreflexia osteotendinosa, desaparición del temblor, oliguria y alteraciones del
ritmo cardiaco (bradicardia, fibrilación auricular y otras arritmias).
Grave: hipotensión, oligoanuria, edema pulmonar, coma con rigidez muscular y arreflexia,
alteraciones del ritmo cardiaco (arritmias ventriculares y asistolia). La existencia de signos
vitales incongruentes con el grado de hipotermia ha de hacer sospechar una patología
sobreañadida. Así, una taquicardia inconsistente con la temperatura sugiere hipoglucemia,
hipovolemia o intoxicación; la hiperventilación puede indicar una acidosis metabólica
subyacente; y un nivel de consciencia no acorde con el grado de hipotermia apunta hacia un
daño cerebral, infección del SNC o intoxicación. Asimismo, es importante no asumir que la
presencia de arreflexia o parálisis está en relación con la hipotermia hasta que se haya
descartado una lesión medular.
4. Diagnóstico
El diagnóstico se basa en una historia clínica compatible, una exploración física detallada (con
especial atención en los signos vitales, la exploración neurológica y la detección de lesiones cutáneas por
congelación), durante la cual se debe evitar someter al paciente a movimientos bruscos que puedan
precipitar arritmias, y en el registro de una temperatura corporal central inferior a 35 ºC mediante un
termómetro-sonda rectal.
En casos de hipotermia grave, especialmente aquellos con necesidad de intubación orotraqueal, se
puede utilizar una sonda esofágica para obtener un valor aproximado de la temperatura cardiaca. Ambos
métodos pueden ser inexactos, pero ningún otro (timpánico, oral, cutáneo [que no registran medidas por
debajo de 34 ºC]) se ha establecido como válido. Si no fuera posible medir con exactitud la temperatura
corporal se puede realizar una aproximación con los estadios clínicos de Swiss (grado I o leve:
consciente/temblor; grado II o moderada: alteración del nivel de consciencia/ausencia de temblor; grado III
o severa: inconsciente/signos vitales presentes; grado IV o profunda: ausencia de signos vitales), puesto
que la gravedad de la hipotermia determina el manejo posterior.
En casos de hipotermia moderada y grave se deben solicitar pruebas complementarias para
identificar potenciales complicaciones (infecciones, acidosis láctica, rabdomiólisis, diátesis hemorrágica o
edema pulmonar no cardiogénico) y realizar un diagnóstico diferencial con las causas de hipotermia no
medioambiental. Asimismo, es necesario tener en cuenta las alteraciones típicas que se producen
asociadas a la hipotermia y que se describen a continuación:
Hemograma: hemoconcentración (aumento del hematocrito un 2% por cada ºC que desciende
la temperatura), plaquetopenia y leucopenia.
Bioquímica (función renal con electrolitos incluyendo potasio, calcio, creatín fosfocinasa [CK],
lactato): suelen presentar hiperglucemia (inactivación de la insulina < 30 ºC).
Coagulación: los estudios suelen ser normales al realizarse a 37 ºC, aunque in vivo presentan
tiempo parcial de tromboplastina activado alargado.
Gasometría arterial corregida: acidosis metabólica, alcalosis respiratoria o ambas.
Electrocardiograma (ECG): el temblor puede producir irregularidades en la línea de base que
dificultan su valoración. Puede presentar las siguientes alteraciones: prolongación del RR, PR,
QRS y QT, elevación del punto J conocida como “J de Osborn” (más característica en V2-V5, se
correlaciona con el grado de hipotermia), inversión de la onda T, bradicardia sinusal y fibrilación
auricular o ventricular.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [190]
[14] FIEBRE DE ORIGEN DESCONOCIDO. ALTERACIONES DE LA TERMORREGULACIÓN
Radiografía de tórax: detecta la existencia de edema pulmonar o neumonía por
broncoaspiración.
En función de la sospecha: tóxicos en orina, función tiroidea, cortisol basal o pruebas de
neuroimagen.
Las determinaciones analíticas deben reevaluarse cada 4 horas, pues durante el recalentamiento
pueden aparecer alteraciones hidroelectrolíticas.
5. Pronóstico
La mortalidad es aproximadamente de un 40%, conllevando peor pronóstico las hipotermias
asociadas al consumo de etanol, la indigencia, los trastornos psiquiátricos y la edad avanzada.
6. Abordaje terapéutico
El manejo de la hipotermia se basa en los siguientes aspectos:
Evaluación de la permeabilidad de la vía aérea, aporte de oxigenoterapia a alto flujo (FiO2:
50%) o, si es preciso, intubación orotraqueal (bajo nivel de consciencia o distrés respiratorio).
Estabilización hemodinámica con fluidoterapia intravenosa utilizando suero salino calentado a
40-42 ºC (100-200 ml/h), y en caso de hipotensión refractaria iniciar infusión de dopamina (2-5
μg/min). De ser precisa la canalización de una vía venosa central, es preferible un acceso
femoral para evitar desencadenar arritmias por irritación atrial en vías de acceso yugular o
subclavio.
Técnicas de recalentamiento (Tabla III). La velocidad de recalentamiento recomendada es de
0,5 a 2 ºC/h en los procedimientos externos pasivos, y de < 2 ºC/h en los externos y/o internos
activos.
Monitorización ECG, control de las posibles arritmias, teniendo en cuenta que pueden persistir
hasta que el paciente presente una temperatura > 30 ºC y ser refractarias a la desfibrilación
eléctrica y a las medidas farmacológicas. La bradicardia sinusal es fisiológica en la hipotermia,
por lo que solo se plantea la implantación de marcapasos en caso de que persista cuando se
haya alcanzado una temperatura de 32-35 ºC.
Colocación de un sondaje vesical para monitorizar diuresis, sonda nasogástrica para evitar
broncoaspiraciones, pulsioximetría continua y monitorización de la temperatura central
mediante sonda rectal o esofágica.
Dados los efectos neuroprotectores de la hipotermia, las maniobras de resucitación
cardiopulmonar no deben suspenderse hasta que la temperatura corporal alcance los 32-35 ºC.
En caso de no alcanzarse los objetivos de incremento de la temperatura debe plantearse la
existencia de comorbilidades que supongan una menor reserva fisiológica para la producción
endógena de calor y/o causas de hipotermia no accidental. Asimismo, habrán de adoptarse
medidas más agresivas que las requeridas en un principio en función del grado de hipotermia.
Si a pesar de ello no hay respuesta, se recomiendan las siguientes medidas:
Antibioterapia empírica intravenosa de amplio espectro.
Tratamiento de una posible insuficiencia suprarrenal con una dosis única de corticoides
(dexametasona 4 mg intravenosa (iv) —preferible, al no interferir con las
determinaciones analíticas posteriores—, o hidrocortisona 100 mg iv).
Si persiste la alteración del nivel de consciencia considerar la administración de tiamina
100 mg iv, naloxona 0,8-2 mg iv, dextrosa 25 g iv o levotiroxina 250 mcg iv, en caso de
sospecha de coma mixedematoso (previa extracción de estudio de función tiroidea).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [191]
[14] FIEBRE DE ORIGEN DESCONOCIDO. ALTERACIONES DE LA TERMORREGULACIÓN
Tratamiento de las lesiones cutáneas por congelación con analgesia y valoración por parte de
Cirugía Plástica de la necesidad de desbridamiento o amputación.
Tabla III.Técnicas de recalentamiento.
2. HIPERTERMIA
1. Definición
Es una elevación de la temperatura corporal central por encima del rango diurno normal por
alteración en la termorregulación, que condiciona un incremento en la producción de calor corporal y/o
disminución en su disipación. Se considera una hipertermia grave una temperatura > 40 ºC.
2. Etiología
Las principales etiologías que producen hipertermia grave se describen en la tabla IV. Las entidades
más importantes de hipertermia grave son el golpe de calor, el síndrome neuroléptico maligno, la
hipertermia maligna y el síndrome serotoninérgico, cuyas características se resumen en la tabla V.
Tabla IV.Etiología de la hipertermia grave.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [192]
[14] FIEBRE DE ORIGEN DESCONOCIDO. ALTERACIONES DE LA TERMORREGULACIÓN
Tabla V.Diagnóstico diferencial de las etiologías de hipertermia grave.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [193]
[14] FIEBRE DE ORIGEN DESCONOCIDO. ALTERACIONES DE LA TERMORREGULACIÓN
3. Fisiopatología
La elevación de la temperatura corporal central se acompaña de un incremento en la actividad
metabólica y en el consumo de oxígeno. Por otra parte, con una temperatura > 42 ºC las reacciones de
fosforilación oxidativa se alteran y una gran variedad de enzimas cesan su función. Asimismo, se produce
una redistribución del flujo sanguíneo con aumento del mismo a nivel muscular y cutáneo, y el consiguiente
riesgo de fallo multiorgánico (síndrome de distrés respiratorio agudo, fracaso renal agudo, fallo hepático
agudo, rabdomiólisis, crisis comiciales y coagulación intravascular diseminada).
4. Manifestaciones clínicas
Los pacientes presentan taquicardia, taquipnea, amplitud de pulso e hipotensión, a los cuales se
pueden añadir sangrado activo, alteraciones neurológicas (disminución del nivel de consciencia, disartria,
irritabilidad, alteraciones del comportamiento, agitación, ataxia, crisis comiciales o coma), alteraciones
respiratorias (edema pulmonar no cardiogénico) y alteraciones cutáneas (flushing facial por vasodilatación
cutánea, diaforesis o sequedad cutánea en función de la patología subyacente, la rapidez de instauración
del cuadro y el estado de hidratación).
5. Diagnóstico
El diagnóstico es clínico, se basa en una anamnesis detallada con especial atención a la medicación
del paciente, una exploración física rigurosa y el registro de la temperatura corporal central mediante
termómetro-sonda rectal o esofágica. Las pruebas complementarias (Tabla VI) están destinadas a detectar
posibles complicaciones y a determinar la existencia de otras etiologías.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [194]
[14] FIEBRE DE ORIGEN DESCONOCIDO. ALTERACIONES DE LA TERMORREGULACIÓN
Tabla VI.Pruebas complementarias en la hipertermia.
6. Pronóstico
Es en la tabla V donde se informa acerca del pronóstico de las principales entidades causantes de
hipertermia grave.
7. Abordaje terapéutico
El abordaje terapéutico se basa en los siguientes aspectos:
Evaluación de la permeabilidad de la vía aérea, aporte de oxigenoterapia a alto flujo (FiO2:
50%) o, si es preciso, intubación orotraqueal (bajo nivel de consciencia o distrés respiratorio).
Estabilización hemodinámica con administración de bolos de suero salino fisiológico de 250 a
500 ml por vía intravenosa, siendo recomendable la canalización del acceso vascular central
para monitorizar la presión venosa central (PVC; objetivo entre 8-12 mm Hg), debido al elevado
riesgo de desencadenar edema pulmonar no cardiogénico. En caso de no evidenciar una
respuesta adecuada se valorará comenzar con fármacos vasoactivos, debiendo evitarse los
agonistas alfa adrenérgicos por su efecto vasoconstrictor periférico. El objetivo es mantener
una tensión arterial media superior a 60 mm Hg y restaurar así la perfusión y oxigenación
tisular. – Monitorización continua de la temperatura corporal mediante termómetro-sonda
rectal o esofágica, balance hídrico estricto y pulsioximetría.
En la evaluación inicial se debe ubicar al paciente en un lugar más frío, retirar las prendas con
las que esté vestido e iniciar medidas de enfriamiento externo (fundamentalmente
promocionando la pérdida de calor por evaporación, mediante aplicación de paños fríos en el
cuello, axilas e ingles, rociando la piel con agua a 25-30 ºC), con el objetivo de disminuir la
temperatura central a 38-39 ºC (una vez conseguidas estas cifras se interrumpirán las medidas
para evitar hipotermia yatrogénica). La “tiritona” inducida por el enfriamiento por evaporación
debe ser suprimida con la administración de benzodiazepinas (diazepam 5 mg por vía
intravenosa) o, si no se sospecha un síndrome neuroléptico maligno, con clorpromazina 25-50
mg por vía intravenosa.
En la evaluación inicial se debe ubicar al paciente en un lugar más frío, retirar las prendas con
las que esté vestido e iniciar medidas de enfriamiento externo (fundamentalmente
promocionando la pérdida de calor por evaporación, mediante aplicación de paños fríos en el
cuello, axilas e ingles, rociando la piel con agua a 25-30 ºC), con el objetivo de disminuir la
temperatura central a 38-39 ºC (una vez conseguidas estas cifras se interrumpirán las medidas
para evitar hipotermia yatrogénica). La “tiritona” inducida por el enfriamiento por evaporación
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [195]
[14] FIEBRE DE ORIGEN DESCONOCIDO. ALTERACIONES DE LA TERMORREGULACIÓN
debe ser suprimida con la administración de benzodiazepinas (diazepam 5 mg por vía
intravenosa) o, si no se sospecha un síndrome neuroléptico maligno, con clorpromazina 25-50
mg por vía intravenosa.
7.1. Tratamiento farmacológico:
El uso de antitérmicos no está indicado, puesto que el mecanismo de producción de estas
entidades no se debe a un cambio en el punto de ajuste del centro termorregulador.
En el golpe de calor no están indicados ninguno de los tratamientos farmacológicos disponibles.
En el síndrome neuroléptico maligno debe retirarse inmediatamente el fármaco responsable.
En aquellos pacientes que presenten elevaciones significativas de la CK o persistencia de la
hipertermia a pesar de la retirada del fármaco en las primeras 24 horas, el tratamiento
farmacológico podría ser de utilidad, aunque no existe suficiente evidencia al respecto. Los
fármacos disponibles son los siguientes:
Dantroleno (relajante muscular de acción directa): 0,25-2 mg/kg por vía
intravenosa cada 6-12 horas, con un máximo de 10 mg/kg/día, durante 10 días
con posterior reducción gradual.
Bromocriptina (agonista dopaminérgico): 2,5 mg a través de sonda nasogástrica
cada 6-8 horas, con un máximo de 40 mg/día y durante al menos 10 días tras la
estabilización del cuadro, con posterior reducción gradual.
Amantadina (como alternativa a la bromocriptina): 100 mg por vía oral
inicialmente, incrementando hasta un máximo de 200 mg/12 horas.
En caso de ausencia de respuesta a los fármacos, así como en pacientes con catatonía
residual persistente, se puede plantear la terapia electroconvulsiva.
Ante la sospecha de hipertermia maligna, además de interrumpir la administración del
anestésico, ha de administrarse dantroleno en un bolo inicial de 2,5 mg/ kg y sucesivos
bolos de 1 mg/kg hasta corregir los signos agudos (especialmente la hipercapnia). En la
mayoría de los casos la respuesta acontece en minutos. De no ser así, debe replantearse
el diagnóstico. Los calcioantagonistas están contraindicados porque pueden empeorar la
hiperpotasemia.
En caso de síndrome serotoninérgico se recomienda retirar el agente causal, y si existen
datos de gravedad administrar ciproheptadina (antihistamínico con actividad antagonista
5-HT1A y 5-HT2A) a dosis inicial de 12 mg, seguida de 2 mg/8 horas hasta resolución
clínica. La evidencia de su efectividad es limitada.
7.2. Manejo de las posibles complicaciones:
Crisis comiciales: benzodiazepinas de elección (diazepam 5 mg por vía intravenosa).
Rabdomiólisis: hidratación intravenosa enérgica con suero salino fisiológico, junto con la
administración de furosemida, manitol, bicarbonato sódico y disposición de medidas
antihiperpotasemia, con el objetivo de prevenir el fracaso renal inducido por mioglobinuria.
BIBLIOGRAFÍA
Adnet P, Lestavel P, Krivosic-Horber R. Neuroleptic malignant syndrome. Br J Anaesth. 2000;85:129.
Arévalo-Serrano J, López-Matamal B. Hipertermia. En: Rodríguez-García JL, editor. Green Book.
Diagnóstico y Tratamiento Médico. 6ª ed. Madrid: Marbán; 2015. p. 1226-35.
Arévalo-Serrano J, Moya EM, Rodríguez-García JL. Hipotermia. En: Rodríguez-García JL, editor. Green
Book. Diagnóstico y Tratamiento Médico. 6ª ed. Madrid: Marbán; 2015. p. 1236-40.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [196]
[14] FIEBRE DE ORIGEN DESCONOCIDO. ALTERACIONES DE LA TERMORREGULACIÓN
Bleeker-Rovers CP, van der Meer JW, Oyen WJ. Fever of unknown origin. Semin Nucl Med.
2009;39(2):81-7.
Bleeker-Rovers CP, Vos FJ, Mudde AH, et al. A prospective multi-centre study of the value of FDG-PET as
part of a structured diagnostic protocol in patients with fever of unknown origin. Eur J Nucl Med Mol
Imaging. 2007;34(5):694-703.
Bouchama A, Dehbi M, Chaves-Carballo E. Cooling and hemodynamic in heatstroke: practical
recommendations. Crit Care. 2007;11(3):R54.
Bouchama A, Knochel JP. Heat stroke. N Engl J Med. 2002;346:1978-88.
Boyer EW, Shannon M. The serotonin syndrome. N Engl J Med. 2005;352:1112-20.
Brown DJA, Brugger H, Boyd J, Paal P. Accidental Hypothermia. N Engl J Med. 2012;367:1930-8.
Ferda J, Ferdová E, Záhlava J, et al. Fever of unknown origin: A value of F-FDG-PET/CT with integrated
full diagnostic isotropic CT imagine. Eur J Radiol. 2009;73:518-25.
Gafter-Gvili A, Raibman S, Grossman A, et al. [18F]FDG-PET/CT for the diagnosis of patients with fever
of unknown origin. QJM. 2015;108(4):289-98.
Hilmo J, Naesheim T, Gilbert M. “Nobody is dead until warm and dead”: Prolonged resuscitation is
warranted in arrested hypothermic victims also in remote areas- A retrospective study from Northern
Norway. Resuscitation. 2014;85:1204-11.
Knockaert DC, Vanderschueren S, Blockmans D. Fever of unknown origin in adults: 40 years on. J
Intern Med. 2003;253(3):263-75.
Larach MG, Gronert GA, Allen GC, et al. Clinical presentation, treatment, and complications of
malignant hyperthermia in North America from 1987 to 2006. Anesth Analg. 2010;110:498.
Mulders-Manders C, Simon A, Bleeker-Rovers CP. Fever of unknown origin. Clin Med. 2015;15(3):280-
4.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [197]
[15] PATOLOGÍA UROLÓGICA MÁS FRECUENTE
15.Patología urológica más frecuente
Ana Arrébola Pajares
Urología
Santiago Pérez Cadavid.
Urología
Asesor:
Ángel Tejido Sánchez.
Médico Adjunto de Servicio de Urología
I. SÍNTOMAS DEL TRACTO URINARIO INFERIOR
1. CONCEPTO
Se denomina síntomas del tracto urinario inferior (STUI) al conjunto de molestias relacionadas con
la micción. Son comunes en los varones adultos y producen un gran impacto en la calidad de vida. Su
etiología es multifactorial, siendo la primera causa la hiperplasia benigna de próstata (HBP), aunque no
siempre se debe a la obstrucción prostática, ya que existen otras causas que producen estos mismos
síntomas (estenosis de uretra, hiperactividad detrusoriana, infección del tracto urinario y litiasis).
La HBP es una entidad clínico-patológica producida por la hiperplasia glandular y estromal de la
zona transicional de la próstata que provoca un incremento del tamaño de la glándula, obstrucción a la
salida del flujo miccional y síntomas miccionales que, parcialmente, son también debidos a la disfunción
vesical secundaria que produce la obstrucción.
2. CLÍNICA
La clínica miccional se divide en dos tipos de síntomas:
De vaciado: incluyen dificultad para el inicio de la micción, disminución del calibre miccional y
de la fuerza del chorro urinario, chorro entrecortado y esfuerzo miccional.
De llenado: producidos principalmente por la disfunción del detrusor. Con frecuencia
son los más molestos para el paciente. Incluyen aumento de frecuencia miccional (tanto
diurna o poliaquiuria, como nocturna o nicturia), urgencia miccional e incontinencia de
urgencia o continua.
Posmiccionales: consisten en sensación de vaciado incompleto y/o goteo posmiccional.
La HBP en su evolución no controlada puede ocasionar complicaciones, siendo la más frecuente la
retención urinaria que obliga al sondaje vesical de urgencia. Otras complicaciones son hematuria de
repetición por sangrado prostático, infecciones del tracto urinario (ITU) recidivantes, litiasis vesical e
incluso uropatía obstructiva con deterioro secundario de la función renal.
3. APROXIMACIÓN DIAGNÓSTICA
1. Anamnesis
Es fundamental una historia clínica completa con el objetivo de identificar las posibles causas de los
síntomas, incluyendo otras enfermedades que produzcan STUI (especial atención a las enfermedades
neurológicas). Es recomendable además revisar la medicación, los hábitos de vida y los posibles factores
psicológicos.
Se debe interrogar al paciente sobre la calidad miccional y las posibles complicaciones:
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [198]
[15] PATOLOGÍA UROLÓGICA MÁS FRECUENTE
Calidad miccional: el Internacional Prostate Sympton Score (IPSS) (Tabla I) es el test
estandarizado más utilizado mundialmente para evaluar los síntomas de HBP y la eficacia
sintomática del tratamiento. Divide a los pacientes en tres grupos: síntomas leves (0-7 puntos),
síntomas moderados (8-19 puntos) y síntomas severos (20-35 puntos).
Complicaciones: interrogar si el paciente ha experimentado ITU de repetición, hematuria o
episodios de retención aguda de orina.
Tabla I.Internacional Prostate Sympton Score (IPSS)
2. Exploración física
Tacto rectal: fundamental en la valoración de la HBP. Es preciso determinar el volumen y la
consistencia de la próstata. Aunque la determinación del tamaño prostático es explorador-
dependiente, la determinación del volumen ayuda en la elección del tratamiento adecuado.
El volumen prostático se clasifica en 4 grados (correspondiendo el grado I a próstatas pequeñas y el
grado IV a próstatas de gran tamaño). La consistencia de la próstata en pacientes con HBP es firme y
elástica, pudiendo estar agrandada de forma simétrica y lisa.
En caso de consistencia pétrea, asimetría o presencia de nódulos habría que descartar la existencia
de cáncer de próstata.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [199]
[15] PATOLOGÍA UROLÓGICA MÁS FRECUENTE
Exploración abdominal y genital: valorar la presencia de globo vesical y las características del
meato uretral y órganos genitales.
Exploración neurológica básica: determinar el tono muscular, reflejo anal superficial y
bulbocavernoso, así como el tono anal.
3. Bioquímica sanguínea
Es necesario determinar la cifra de creatinina sérica. En algunos casos con obstrucción importante,
tanto aguda como crónica, puede existir hidronefrosis con fracaso renal secundario.
4. Sistemático de orina/tira reactiva
Resulta útil para descartar que la sintomatología no sea secundaria a otras entidades, como por
ejemplo a infección de orina y/o litiasis.
5. Antígeno prostático específico
El antígeno prostático específico (PSA) es un marcador de tejido prostático, y por tanto puede
encontrarse elevado en pacientes con HBP. Su elevación (por encima de 4 ng/ml) puede indicarnos la
presencia de un cáncer de próstata. Además, el valor de PSA se correlaciona con el volumen de la glándula
prostática (nos orienta en el tratamiento a seguir), y con la historia natural de la HBP (a mayor valor de PSA,
mayor probabilidad de presentar complicaciones). Hay que tener en cuenta que no se recomienda la
determinación de PSA con fines de cribado en población general. Solo debe realizarse la determinación de
PSA en aquellos pacientes en los que, en el caso de ser diagnosticados del mismo, se valore un tratamiento
activo, es decir, pacientes con al menos 10-15 años de expectativa de vida susceptibles de tratamiento
curativo o pacientes añosos con síntomas constitucionales susceptibles de tratamiento paliativo.
6. Medición del residuo posmiccional
El residuo posmiccional (RPM) puede ser medido mediante ecografía transabdominal o
cateterización uretral nada más finalizar la micción. Se considera un RPM elevado > 150 ml. Puede deberse
a una afectación de la capacidad contráctil vesical o a obstrucción urinaria.
7. Flujometría
Mide la cantidad de orina que la vejiga del paciente es capaz de expulsar por segundo, la duración
de la micción y cualquier cantidad de flujo intermitente. Se considera normal un flujo máximo por encima
de 15 ml/seg. Un flujo disminuido puede deberse a una afectación de la capacidad contráctil vesical o a
obstrucción urinaria.
8. Estudios de imagen
Si se va a iniciar tratamiento médico, una ecografía para medir el volumen prostático puede ayudar
a elegir el medicamento adecuado. Se debe realizar una ecografía del tracto urinario superior en pacientes
con residuos posmiccionales elevados, síntomas de insuficiencia renal, ITU de repetición, hematuria o
antecedentes de tumores uroteliales o urolitiasis.
4. TRATAMIENTO (Figura 1)
1. Manejo expectante
Indicado en casos de síntomas leves con poca repercusión en la calidad de vida del paciente. Tanto
si se va a realizar un manejo expectante como si se va a iniciar tratamiento médico deben recomendarse
modificaciones en el estilo de vida, como reducir la ingesta de líquidos por la noche, evitar el alcohol y la
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [200]
[15] PATOLOGÍA UROLÓGICA MÁS FRECUENTE
cafeína, evitar el estreñimiento o técnicas de distracción y ejercicios de respiración, entre otras. Además
debe revisarse la medicación habitual del paciente y optimizar su administración (por ejemplo: evitar tomar
diuréticos por la tarde/ noche).
Figura 1.Tratamiento de los síntomas del tracto urinario inferior
2. Fitoterapia
Se han utilizado múltiples extractos de plantas. Sin embargo, todavía no se ha demostrado su
eficacia, y no es posible hacer una recomendación a favor o en contra de su uso. Por ello debe reservarse a
pacientes con sintomatología leve, con poca repercusión sobre su calidad de vida o con contraindicaciones
para el uso de otros tratamientos.
3. Tratamiento médico
Alfa bloqueantes: representan la primera línea de tratamiento. Indicados ante la presencia de
síntomas moderados o severos que afecten la calidad de vida del paciente. Producen un alivio
rápido de la sintomatología, disminuyendo el IPSS sin reducir el volumen prostático. Si tras dos
meses de tratamiento no existe mejoría se aconseja suspender el fármaco. Entre los efectos
secundarios más comunes destacan cefalea, hipotensión ortostática y eyaculación retrógrada.
Comercializados en España: tamsulosina (Omnic®, Urolosin®, Zuantrip®, Sebrane®, Inreq®, 1
comp de 0,4 mg/24 h), silodosina (Urorec®, Silodyx®, 1 comp de 8 mg/24 h), doxazosina
(Carduran neo®, Progandol®, Doxarutis®, 1 comp de 4 u 8 mg/24 h), alfuzosina (Unibenestan®,
Bundisarin®, 1 comp de 10 mg/24 h) y terazosina (Deflox®, Alfaprost®, Magnurol®, Mayul®,
Sutif®, Zayasel®, 2 mg/24 h los primeros 3-4 días, luego 5 mg/24 h). Todos ellos tienen eficacia
clínica similar.
Inhibidores de la 5-alfa reductasa: indicados ante la presencia de síntomas moderados o
severos en pacientes con próstatas de gran volumen (> 40 cc). Disminuyen el volumen
prostático reduciendo el riesgo de retención urinaria y la necesidad de cirugía. Su efecto
máximo tarda en alcanzarse entre seis y 12 meses. La reducción de síntomas depende del
tamaño prostático, no siendo eficaces en próstatas menores de 40 cc. Su uso conlleva una
reducción de la cifra de PSA un 50%, por lo que en pacientes tratados con estos fármacos
debemos duplicar el valor del PSA para calcular el valor real del mismo. Los efectos secundarios
más comunes se centran en la esfera sexual, con disminución de la libido y disfunción eréctil. En
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [201]
[15] PATOLOGÍA UROLÓGICA MÁS FRECUENTE
España están comercializados finasterida (Proscar®, 1 comp de 5 mg/24 h) y dutasterida
(Avidart®, 1 comp de 0,5 mg/24 h).
Combinación de alfa bloqueante + inhibidor de la 5-alfa reductasa: actualmente ya se
comercializan medicamentos que combinan ambos fármacos. Se utilizan en pacientes con
síntomas moderados o severos, con próstatas de un volumen mayor de 40 cc que se
encuentran muy sintomáticos al diagnóstico, o cuando la monoterapia no es suficiente para el
control sintomático. El tratamiento combinado se asocia de manera significativa a un menor
riesgo de retención urinaria y necesidad de cirugía, así como a un mayor alivio sintomático, al
ser comparado con cualquier monoterapia. Hasta la fecha únicamente existe un producto
comercializado en España: Duodart® (dutasterida 0,5 mg/tamsulosina 0,4 mg 1 comp/24 h).
Inhibidores de la 5-fosfodiesterasa: indicados en pacientes con síntomas moderados o severos,
especialmente cuando presentan disfunción eréctil. Diferentes estudios han demostrado que
disminuye la puntuación IPSS, los síntomas de llenado y vaciado vesical, además de mejorar la
calidad de vida. Únicamente Cialis® (tadalafilo 5 mg 1 comp/24 h) ha sido aprobado para los
síntomas del tracto urinario inferior.
Antimuscarínicos: pueden utilizarse en pacientes con síntomas moderados o severos que
presenten principalmente síntomas de llenado. Teóricamente podrían provocar una
disminución de la fuerza de la vejiga y, por tanto, asociarse con una elevación del residuo
posmiccional o con retención urinaria, aunque en los estudios realizados únicamente se ha
observado un ligero incremento en el residuo posmiccional. No obstante, estos fármacos han
de prescribirse con precaución y se recomienda una reevaluación periódica de la puntuación
IPSS y del residuo posmiccional. Los efectos secundarios más comunes son boca seca,
estreñimiento, dificultad para la micción y sensación de mareo. Los antimuscarínicos aprobados
para los síntomas de llenado son: fesoterodina (Toviaz® 1 comp de 4 u 8 mg/24 h), oxibutinina
(Ditropan®, Dresplan® inicialmente 5 mg/día, máx. 20 mg/día), solifenacina (Vesicare® 5 mg una
vez al día, que puede aumentarse a 10 mg una vez al día), tolterodina (Detrusitol®, Urotrol®, 4
mg una vez al día).
Combinación alfa bloqueante + antimuscarínicos: actualmente ya se comercializan
medicamentos que combinan ambos fármacos. El tratamiento combinado es más eficaz en la
reducción de la urgencia, la incontinencia urinaria de urgencia, la frecuencia miccional, la
nicturia y la puntuación IPSS, además de mejorar la calidad de vida. Se utilizan en pacientes con
síntomas moderados o severos en los que la mejoría de los síntomas de llenado ha sido
insuficiente usando cada fármaco en monoterapia. Deben prescribirse con precaución en
pacientes con obstrucción del tracto urinario inferior. Comercializados en España: Vesomni® y
Volutsa® (solifenacina 6 mg/tamsulosina 0,4 mg 1 comp/24 h).
Agonistas β3-adrenérgicos: los receptores β3-adrenérgicos son los predominantes en el
músculo detrusor vesical, y se piensa que su estimulación provoca una relajación del detrusor.
Pueden utilizarse en pacientes con síntomas moderados o severos en los que predominan los
síntomas de llenado vesical. En los estudios realizados el flujo máximo y la presión del músculo
detrusor durante la micción no se ven afectados. Los efectos secundarios más comunes son
hipertensión, infecciones urinarias y cefalea, estando contraindicado su uso en pacientes
hipertensos mal controlados. Comparado con el uso de antimuscarínicos, la proporción de
pacientes con boca seca y estreñimiento es notablemente inferior. Hasta la fecha únicamente
existe un producto comercializado en España: Betmiga® (mirabegrón 50 mg 1 comp/24 h).
4. Tratamiento quirúrgico
Se debe valorar el tratamiento quirúrgico en las siguientes situaciones:
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [202]
[15] PATOLOGÍA UROLÓGICA MÁS FRECUENTE
Clínica severa refractaria al tratamiento médico.
Retenciones agudas de orina recurrentes o refractarias a la retirada de la sonda vesical.
Incontinencia por rebosamiento o dilatación del tracto urinario superior debido a hiperplasia
prostática con o sin insuficiencia renal (retención crónica de orina).
Infecciones del tracto urinario de repetición.
Episodios repetidos de hematuria sin otra causa.
Litiasis vesical.
Deseo del paciente.
II. RETENCIÓN URINARIA
1. CONCEPTO
La retención aguda de orina (RAO) se define como la imposibilidad para realizar la micción a pesar
de encontrarse la vejiga llena.
2. ETIOLOGÍA
La causa más frecuente de retención urinaria es obstructiva, fundamentalmente debida a
hiperplasia prostática en el varón. Además, existen otras causas como son las neurológicas,
medicamentosas e incluso psicógenas.
3. CLÍNICA
La retención aguda de orina se manifiesta por dolor hipogástrico intenso debido a la distensión
vesical, asociado a la imposibilidad para realizar la micción.
1. Anamnesis
Los pacientes refieren incapacidad para orinar a pesar de un deseo miccional intenso, junto con
dolor hipogástrico espontáneo. Existen casos en los que la retención urinaria se trata de un cuadro crónico
debido a residuos posmiccionales elevados. En estos casos los pacientes pueden referir mala calidad
miccional previa e incontinencia urinaria (incontinencia por rebosamiento) sin asociar dolor hipogástrico.
2. Exploración física
La palpación abdominal muestra una masa hipogástrica, intensamente dolorosa de forma
espontánea y a la palpación (que exacerba el deseo miccional), con matidez a la percusión que se
corresponde al globo vesical. La exploración de genitales externos es imprescindible, buscando estenosis de
meato en el varón y prolapsos o masas genitales en la mujer. El tacto rectal en el varón nos informa de las
características prostáticas (tamaño, consistencia y presencia de signos inflamatorios).
3. Pruebas complementarias
Habitualmente no son necesarias en el contexto del manejo en urgencias, salvo que existan dudas
diagnósticas o signos clínicos de insuficiencia renal.
En el caso de dudas en el diagnóstico, el sondaje vesical debe ser la última alternativa. Hay que
tener en cuenta que se trata de un procedimiento incómodo para el paciente, se asocia a yatrogenia (falsas
vías, sangrado, infecciones…) y puede desencadenar una retención tras la retirada de esta.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [203]
[15] PATOLOGÍA UROLÓGICA MÁS FRECUENTE
Si el paciente muestra signos de insuficiencia renal o presenta retención urinaria de gran volumen
la realización de un análisis de sangre puede demostrarnos un deterioro de función renal con elevación de
las cifras de creatinina.
4. DIAGNÓSTICO DIFERENCIAL
Hay situaciones que pueden confundirse con una retención urinaria, tales como un síndrome
miccional severo, la falta de colaboración del paciente en el caso de deterioro cognitivo o bajo nivel de
consciencia o la presencia de oliguria/anuria de otras causas. En este último caso el paciente no orina, pero
tampoco tiene deseo miccional. A la exploración física no se demuestra masa hipogástrica y la ecografía
muestra una vejiga vacía.
Figura 2.Diagnóstico y diagnóstico diferencial de la retención urinaria
5. TRATAMIENTO
El tratamiento de la retención urinaria en urgencias consiste en el drenaje de la vejiga lo más rápido
posible tras confirmar el diagnóstico, mediante sondaje vesical o cistostomía suprapúbica. Habitualmente
el tratamiento de elección es el sondaje vesical, por ser una técnica barata y sencilla que puede realizarse
por un mayor número de profesionales. Las principales contraindicaciones del sondaje vesical son la
infección prostática aguda y la sospecha de rotura uretral postraumática.
El tiempo que debe mantenerse la sonda depende de la historia clínica del paciente. Ante un primer
o segundo episodio de RAO que no ocasione deterioro de la función renal se puede intentar retirar la sonda
pasados 3-7 días, asociando, desde el inicio, un alfa-bloqueante en el caso de los varones para ayudar a que
la retirada sea exitosa. En caso de retención urinaria crónica por residuos posmiccionales elevados,
antecedentes de episodios repetidos de RAO o un único episodio que ocasione deterioro de la función
renal, es necesario mantener la sonda vesical de forma permanente hasta valorar el tratamiento quirúrgico
por parte de un urólogo.
Aunque la administración de antibióticos durante el recambio de sonda vesical es una práctica
común, no existen estudios que hayan valorado su eficacia. Por este motivo parece adecuado limitar esta
práctica a casos seleccionados en los que exista riesgo de sepsis en relación con el recambio: pacientes con
episodio previo de sepsis posrecambio, pacientes con riesgo de endocarditis bacteriana, neutropénicos,
inmunodeprimidos, trasplantados renales o pacientes en los que el recambio haya sido traumático.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [204]
[15] PATOLOGÍA UROLÓGICA MÁS FRECUENTE
III. SÍNDROME DE ESCROTO AGUDO
Se trata de una situación clínica caracterizada por dolor testicular agudo e intenso, en ocasiones
acompañado de signos locales. El diagnóstico diferencial (Tabla II) de las diversas causas que lo originan es
fundamental, puesto que alguna de sus etiologías puede poner en riesgo la viabilidad testicular y requiere
de una rápida actuación.
Tabla II.Diagnóstico diferencial del escroto agudo.
IV. HEMATURIA MACROSCÓPICA
1. DEFINICIÓN
La hematuria se define como la presencia de más de tres hematíes por campo de gran aumento en
orina, cuyo origen puede encontrarse en cualquier punto entre el glomérulo renal y el esfínter urinario
externo, a nivel uretral.
Un número > 100 hemats/campo suele apreciarse a simple vista, denominándose macrohematuria.
2. ETIOLOGÍA
La importancia de la hematuria no depende de su intensidad, sino de la causa que la motiva, pero el
diagnóstico etiológico de la hematuria en urgencias no es un objetivo principal, salvo trastornos
hemodinámicos que pongan en riesgo la vida del paciente.
Deberemos distinguir la hematuria de la uretrorragia, estando el origen de esta última por debajo
del esfínter urinario externo, evidenciándose sangrado a través del meato uretral independientemente de
la micción. Generalmente es de causa yatrogénica.
Las causas etiológicas de la hematuria varían en función de la edad y el sexo, pero tomando como
punto de corte los 40 años, por debajo de esta edad la mayoría de las causas son benignas y/o idiopáticas,
mientras que en los mayores de 40 años adquieren mayor relevancia las neoplasias (Tabla III).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [205]
[15] PATOLOGÍA UROLÓGICA MÁS FRECUENTE
Tabla III.Principales causas de hematuria.
Hay que tener presente las causas de falsas hematurias, como son: hemorragias vaginales,
secundaria a fármacos (rifampicina, metronidazol, fenitoína), alimentos (remolacha, setas, zarzamoras) o
sustancias endógenas como la mioglobinuria, hemoglobina, porfirias, melanina y uratos.
3. CLÍNICA
La hematuria puede acompañarse de otros síntomas o no, en función de su etiología. Cuando se
acompaña de expulsión de coágulos la micción puede resultar dificultosa, llegando incluso a la retención
aguda de orina, requiriendo sondaje uretral para su evacuación y control. La hematuria presente en el seno
de una infección aguda de orina se acompaña de síntomas irritativos (disuria, poliaquiuria, nicturia), siendo
estos predominantes. La asociación de crisis reno-ureteral y hematuria puede ser debida a obstrucción de
la vía urinaria superior por coágulos (generalmente en el seno de una neoformación piélica o ureteral) o a
la hematuria en el seno de una crisis renoureteral litiásica. La hematuria de origen prostático puede o no
asociar clínica de prostatismo (sintomatología obstructiva ± irritativa).
Podemos diferenciar la hematuria según el momento de aparición, cantidad de hematíes y su
duración, lo cual nos ayudará para su evaluación.
1. Según el momento de aparición
Inicial: al iniciar el chorro de la micción y después se aclara la orina espontáneamente. Sugiere
origen uretral o prostático.
Terminal: al final de la micción, a veces incluso como un goteo sanguinolento justo después de
acabar la micción; sugiere origen cercano al cuello vesical.
Total: a lo largo de toda la micción se denomina total; puede proceder del riñón, del tracto
superior o de la vejiga.
2. Según la cantidad de hematíes
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [206]
[15] PATOLOGÍA UROLÓGICA MÁS FRECUENTE
Microscópica: la emisión de hematíes por campo es inferior a 100, visualmente la orina no
cambia de color.
Macroscópica: a partir de 100 hematíes por campo la sangre se hace visible en la orina; 1 ml de
sangre en 1 l de orina hace que esta adopte un color rojizo.
Según la duración
Transitoria: puede producirse por ejercicio intenso, fiebre, actividad sexual o traumatismos. El
diagnóstico es por exclusión. Se produce con más frecuencia entre los 15-40 años y disminuye a
partir de los 50 años. En los pacientes menores de 50 años una segunda tira reactiva negativa
en orina supone una hematuria transitoria y es suficiente para excluir causas graves, salvo que
el paciente presente factores de riesgo de cálculos renales o cáncer de vejiga.
Permanente: hematurias continuas, que no entran en el grupo de transitorias.
4. APROXIMACIÓN DIAGNÓSTICA
Corresponde al especialista determinar el estudio más adecuado. La intensidad del color y la
relación de la hematuria con la micción pueden ocasionalmente orientar la localización de la hemorragia.
Las hematurias totales de color café rojizo y opaco orientan a un origen renal. Las hematurias con sangre
fresca iniciales orientan a vías urinarias bajas.
1. Anamnesis
Se deben recoger los antecedentes personales y familiares, episodios previos, antecedentes
médico-quirúrgicos y urológicos, traumatismo de vías urinarias, ingesta de fármacos. Documentar la
cronología de la hematuria, la presencia de coágulos.
Es importante valorar su intensidad, ante la posibilidad de una hematuria anemizante (Figura 3).
Figura 3.Clasificación de la hematuria
2. Exploración física
Siempre irá encaminada a identificar los signos y su probable asociación a la causa de hematuria.
Incluirá la toma de presión arterial, temperatura, puño-percusión renal, tacto rectal en el hombre, examen
pélvico en la mujer, palpación abdominal para descartar masas abdominales, presencia de globo vesical y/o
masas renales.
No olvidar la inspección macroscópica; al explorar al paciente hay que ver el sangrado.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [207]
[15] PATOLOGÍA UROLÓGICA MÁS FRECUENTE
3. Pruebas complementarias
3.1. Tira reactiva (dipsticks)
Constituye un buen test de despistaje inicial. Este procedimiento detecta tanto la hemoglobina
intraeritrocitaria como la hemoglobina libre y la mioglobina. Se positiviza ante la existencia de más de 5
hematíes por campo en el análisis microscópico del sedimento urinario. Da falsos negativos ante la
presencia de grandes cantidades de vitamina C en la orina y falsos positivos cuando hay hemoglobinuria o
mioglobinuria.
El estudio del sedimento urinario no solo confirma la hematuria, sino que puede orientar sobre su
causa u origen según la morfología que presenten los eritrocitos. (Generalmente no se realiza de
urgencias).
3.2. Análisis de sangre
Hemograma y bioquímica (valorar la función renal, anemización, trombopenia, leucocitosis si hay
sospecha de ITU complicada), estudio de coagulación.
3.3. Pruebas de imagen:
Radiografía de abdomen: si se sospecha enfermedad litiásica.
Ecografía de aparato urinario: en urgencias no suele realizarse de entrada, salvo sospecha de
uropatía obstructiva supravesical y/o mal control de la hematuria. Imprescindible en el estudio
rutinario para descartar neoformaciones vesicales o renales, litiasis y valoración del tamaño
prostático.
Tomografía axial computarizada (TAC) de urgencia: indicada ante la presencia de hematuria
postraumática, hematuria en paciente con antecedentes de poliquistosis hepatorrenal o
angiomiolipomas renales de gran tamaño.
Ante todo paciente con hematuria macroscópica no complicada, en el que se excluya origen
infeccioso o nefrológico, es necesario completar el estudio de forma ambulatoria. La prueba de
mayor rentabilidad diagnóstica es la URO-TAC con fase de eliminación asociada o no a
cistoscopia, según la edad del paciente y los factores de riesgo.
3.4. Otras
Cistoscopia: indicada por el urólogo si las pruebas de imagen resultan no concluyentes o
negativas. Permite valorar la uretra anterior-posterior y la vejiga.
Citología urinaria: carece de utilidad si existe hematuria franca. Alta sensibilidad (98%)
en el diagnóstico del cáncer vesical in situ y de alto grado.
5. CRITERIOS DE INGRESO
Hematuria grave con alteraciones hemodinámicas, retención aguda por coágulos, compromiso
cardiovascular, sepsis, dolor incontrolado, fracaso renal agudo, coagulopatía, vejiga coagulada,
anemización y hematuria macroscópica postraumática.
6. TRATAMIENTO
En general dependerá de la causa misma que cause la hematuria, pero si es monosintomática,
moderada, no anemizante y no provoca dificultad miccional (lo más frecuente) únicamente debemos de
tranquilizar al paciente, indicar ingesta abundante de líquidos y la necesidad de completar el estudio de
forma ambulatoria.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [208]
[15] PATOLOGÍA UROLÓGICA MÁS FRECUENTE
No sondar, salvo sospecha de retención aguda de orina. Si se acompaña de otros síntomas se
realizará tratamiento específico del proceso. En caso de retención urinaria por coágulos se realizará sondaje
vesical con sonda de tres vías realizando un lavado manual y dejando un lavado vesical continuo con suero
frío, que tendrá un efecto vasoconstrictor y evitará la formación de coágulos.
La retención de coágulos en la vejiga puede originar una “vejiga coagulada”, con distensión de la
pared vesical que impide la retracción de vasos vesicales sangrantes, perpetuando el sangrado, situación
que requiere la intervención quirúrgica urgente.
En caso de anemización importante e inestabilidad hemodinámica a veces es necesaria la
exploración bajo anestesia, evacuación de coágulos y resección transuretral (RTU) hemostática.
V. NEFROLITIASIS-CRISIS RENOURETERAL
1. INTRODUCCIÓN Y DEFINICIÓN
La nefrolitiasis constituye la tercera enfermedad urológica más frecuente después de las
infecciones de orina y de la patología prostática. Su forma de presentación más frecuente es el cólico
nefrítico que representa, a su vez, una de las principales urgencias hospitalarias.
Podemos definirlo como un síndrome doloroso, paroxístico, que se produce por alteraciones
mecánicas o dinámicas del flujo urinario que ocasionan una hiperpresión y distensión de la vía urinaria y
que cursa con un intenso dolor renoureteral de carácter agitante.
2. ETIOLOGÍA
Aunque en el 90% de los cólicos nefríticos la causa es litiásica, en un 10% de los pacientes es
provocado por otro motivo que cause una obstrucción intrínseca y/o extrínseca.
Intrínsecas del uréter: coágulos o pus, necrosis papilar, tumoral, estenosis de la unión pielo-
uretral, estenosis de uréter, ureterocele, tuberculosis.
Extrínsecas del uréter: vasculares, procesos benignos del aparato genital femenino, tumores
malignos, enfermedades inflamatorias del tracto gastrointestinal, procesos retroperitoneales
benignos y malignos.
3. CLÍNICA Y DIAGNÓSTICO
A efectos prácticos nos centraremos en estas guías en los cólicos secundarios a litiasis. El cuadro
clínico variará según el tamaño, la localización y la capacidad obstructiva del cálculo.
El dolor del cólico nefrítico, típicamente, es de inicio brusco, con picos de gran intensidad,
localizado al nivel de la fosa renal y/o el flanco, que se suele irradiar a la ingle y/o a los genitales, y no
mejora con los cambios posturales. Generalmente se acompaña de un cortejo vegetativo más o menos
florido (náuseas, vómitos, sudoración y palidez). Otros síntomas menos frecuentes son los irritativos de la
vejiga, típicamente asociados a cálculos al nivel de la unión ureterovesical (frecuencia, urgencia, tenesmo,
sensación de evacuación incompleta) que usualmente conducen a un diagnóstico errado de infección o
retención urinaria.
La litiasis suele producir dolor típicamente al nivel de una de estas cinco zonas, dada la estrechez de
la vía urinaria a uno de estos niveles anatómicos:
Infundíbulo calicial: en consecuencia los cálices individuales se distienden, son dolorosos y
crean hematuria.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [209]
[15] PATOLOGÍA UROLÓGICA MÁS FRECUENTE
Unión pieloureteral: donde el diámetro es de 2-3 mm en comparación con el diámetro piélico,
relativamente amplio (1 cm).
Cruce del uréter iliaco con los vasos iliacos.
Uréter pelviano: donde es cruzado por la arteria uterina y al nivel del ligamento infundíbulo
pélvico, en la mujer, y en el cruce con el deferente en el varón.
Uréter intramural y unión urétero-vesical.
El diagnóstico es principalmente clínico. La valoración inicial de todo paciente que comienza con
una crisis reno-ureteral debe incluir:
Anamnesis y exploración física: debe registrar la existencia de antecedentes familiares y
personales de episodios similares. La presencia de fiebre o anuria nos alertará de la posibilidad
de complicaciones tipo sepsis u obstrucción completa. Las litiasis renales suelen ser
asintomáticas.
Radiografía de abdomen: imprescindible. El 90% de los cálculos son radioopacos, y por lo tanto
visibles. Los cálculos más radiodensos son los de fosfato cálcico (apatita), seguidos de los de
oxalato cálcico. Débilmente cálcicos los de fosfato amónico-magnésico (estruvita) y cistina y
radiotransparentes de ácido úrico.
Análisis de orina: micro o macrohematuria (ausente hasta en un tercio de los casos), y en
ocasiones piuria (inflamatoria o por infección) y cristaluria. El pH urinario es orientativo del tipo
de cálculo.
Análisis de sangre: valorar la función renal y/o datos de infección como recuento leucocitario,
neutrofilia y otros indicadores de sepsis.
Ecografía de aparato urinario: su misión principal es valorar la existencia o no de dilatación de
la vía urinaria y el grado de la misma. Solicitar en casos de dolor refractario al tratamiento
médico, fiebre, deterioro importante de la función renal o riñón único. Tener en cuenta que
puede haber uropatías obstructivas sin dilatación de la vía excretora en los siguientes casos:
rotura fornicial, pelvis intrarrenal, pocas horas transcurridas desde el establecimiento de la
obstrucción, bajo volumen de diuresis debido a la depleción hídrica y error del observador.
TAC abdominal: en caso de cólico complicado o duda diagnóstica. Es la técnica más sensible y
específica.
4. COMPLICACIONES
Aunque la mayoría de los casos se resuelven fácilmente sin repercusiones importantes para el
paciente, hay que tener presente signos y síntomas de alarma que pueden advertir de una complicación.
Fiebre superior a 38,5 ºC y/o signos de sepsis.
Dolor incontrolable con la terapéutica indicada.
Anuria o insuficiencia renal aguda.
Monorreno (se considera complicado por lo que implica).
Grave obstrucción del tracto urinario superior, especialmente en pacientes con litiasis mayor de
10 mm u obstrucción de causa oncológica.
Sospecha de causa vasculorrenal del dolor lumbar y/o infarto renal.
Colecciones renales o perirrenales.
Deterioro clínico del paciente (inestabilidad hemodinámica, hematuria anemizante, hemorragia
retroperitoneal, etc.).
5. DIAGNÓSTICO DIFERENCIAL
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [210]
[15] PATOLOGÍA UROLÓGICA MÁS FRECUENTE
Las principales causas con las que realizar un diagnóstico diferencial las resumimos en la tabla IV.
Tabla IV.Diagnóstico diferencial de cólico renoureteral
6. TRATAMIENTO
El control del dolor es urgente, y no debe demorarse por la realización de pruebas. Una vez
solucionado el episodio de dolor agudo los objetivos fundamentales del son:
Control sintomático: dolor y clínica vegetativa acompañante.
Favorecer la expulsión espontánea del cálculo.
1. Tratamiento sintomático
1.1. Medidas generales
Calor local, evitar una excesiva sobrehidratación durante la fase aguda.
1.2. Analgesia
Antiinflamatorios no esteroideos (AINE): dexketoprofeno, ibuprofeno o diclofenaco,
generalmente por vía parenteral en la fase aguda. Deberán evitarse si existe insuficiencia renal
importante, pudiéndose utilizar en este caso como alternativa el metamizol.
Paracetamol: menor poder analgésico y antiinflamatorio que los previos. Utilizar en
monoterapia si los previos están contraindicados, o en combinación con estos.
Opiáceos: están indicados como tratamiento complementario de los AINE o cuando estos están
contraindicados o no hay respuesta a los mismos. Pueden ser menores (tramadol) o mayores
(morfina). Hay que tener en cuenta el efecto espasmogénico que pueden ejercer estos
medicamentos sobre la vía urinaria, que podría favorecer la impactación del cálculo.
Espasmolíticos: a diferencia de lo que se pensaba antiguamente tienen un papel secundario, no
reconociéndose como terapia de primera línea el uso de espasmolíticos.
2. Tratamiento expulsivo
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [211]
[15] PATOLOGÍA UROLÓGICA MÁS FRECUENTE
Generalmente se indica ante una litiasis < 10 mm y localizada a nivel distal, pudiendo ser indicado
desde urgencias al alta. Pasados 15 días sin expulsión es recomendable suspender el tratamiento y
reevaluar al paciente para evitar daños renales irreversibles. Consiste en AINE combinados con un alfa
bloqueante, siendo el más utilizado la tamsulosina 0,4 mg/24 h.
3. Tratamiento quirúrgico
Derivación de la vía urinaria: descomprimir quirúrgicamente la vía urinaria mediante un catéter
vía endourológica o percutánea.
Extracción de litiasis: endourológicamente mediante fragmentación o extracción con canastillas
o por litotricia extracorpórea por ondas de choque.
BIBLIOGRAFÍA
Albala D, Morey A, Gomella L. Oxford American handbook of Urology. 1.ª ed. Oxford; 2011. pp. 405-18.
Allendorff J, Stelzer K, Kiohler H. Hematuria: diagnostic procedure and therapeutic approaches. Z Arztl
Fortbild (Jena). 1996;90:187-90.
Arribas Rodríguez JM, Pérez-Lanzac de Lorca A, Castiñeiras Fernández J. Síndrome de escroto agudo.
Libro del residente en Urología. 2.a ed. Madrid: Castiñeiras Fernández J; 2007. pp. 159-75.
Bolufer E, Buitrago S. Hematuria. En: Julián Jiménez A, editor. Manual de actuación y protocolos de
urgencias. 3.ª ed. Madrid: Edicomplet; 2010. pp. 901-4.
Davis R, Jones JS, Barocas DA, et al. Diagnosis, evaluation, and follow-up of asyntomatic
microhematuria in adults: AUA GUIDELINE-2012 by the American Urological Association [On line].
https://www.auanet.org/education/clinical-practice-guidelines.cfm
Elizalde Benito A, Úcar Terrén A, Valdivia Uría J. Uropatía obstructiva. Libro del residente en urología.
2.a ed. Madrid: Castiñeiras Fernández J; 2007. pp. 175-97.
Evaluation of the urologic patient. En: Kauvoussi. Campbell-Walsh Urology. 10th ed. Philadelphia:
Elsevier Saunders; 2012. pp. 73-98.
Fumero Arteaga S, Castro-Díaz DM, Rodríguez Hernández P. Oliguria y anuria de origen urológico. Libro
del residente en Urología. 2.a ed. Madrid: Castiñeiras Fernández J; 2007. pp. 133-44.
Gravas S, Bach T, Bachmann A, et al. Guidelines on management of non-neurogenic male lower urinary
tract symptoms (LUTS), incl. benign prostatic obstruction (BPO) (European Association of Urology
guidelines 2015) [On line]. https://www.auanet.org/education/clinical-practice-guidelines.cfm
Gordhan CG, Sadeghi-Nejad. Scrotal pain: Evaluation and management. Korean J Urol. 2015;56:3-11.
Grabe M, Bartoletti R, Bjerklund TE, et al. Guidelines on Urological Infections (European Association of
Urology guidelines 2015) [On line]. https://www.auanet.org/education/clinical-practice-guidelines.cfm
Hernández Hernández D, Bernardez Tesouro R, Castro-Diaz D. Urinary retention. Urologia.
2013;80(4):257- 64.
McConnell JD, Roehrborn CG, Bautista O, et al. Medical therapy of prostatic symptoms (MTOPS)
Research Group. The long-term effect of doxazosin, finasteride, and combination therapy on the clinical
progression of benign prostatic hyperplasia. N Engl J Med. 2003;349:2387-98.
Pearle MS, Goldfarb DS, Assimos DG, et al. Medical management of kidney stones: AUA guideline [On
line]. https://www.auanet.org/education/clinical-practice-guidelines.cfm
Pérez Fentes DA, Blanco Parra MA, Villar Núñez M. Retención urinaria. Libro del residente en Urología.
2.a ed. Madrid: Castiñeiras Fernández J; 2007. pp. 145-58.
Rodgers M, Nixon J, Hempel S, et al. Diagnostic tests and algorithms used in the investigation of
hematuria: Systematic reviews and economic evaluation. Health Technol Assess. 2006;10:iii-iv, xi-259.
Roehrborn CG, Siami P, Barkin J, et al. The effects of combination therapy with dutasteride and
tamsulosin on clinical outcomes in men with symptomatic benig prostatic hyperplasia: 4-year results
from the CombAT study. Eur Urol. 2010;57:123-31.
Spencer Barthold J. Abnormalities of the testis and scrotum and their surgical management. Campbell-
Walsh Urology. 10th edition; 2012. Chapter 132.
Türk C, Knoll T, Petrik A, et al. Guidelines on urolithiasis (European Association of Urology guidelines)
[On line]. https://www.auanet.org/education/clinical-practice-guidelines.cfm
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [212]
[16] PATOLOGÍA OFTALMOLÓGICA
16.Patología oftalmológica
Elena del Fresno Valencia.
Oftalmología
Javier Sambricio García.
Oftalmología
Asesor:
Constantino Reinoso Montalvo.
Médico Adjunto de Oftalmología
I. OJO ROJO
1. Hiposfagma o hemorragia subconjuntival
Se trata de una hemorragia en sábana con bordes definidos, generalmente asintomática. Puede
ocurrir espontáneamente o asociada a maniobras de Valsalva. Es conveniente realizar una medición de la
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [213]
[16] PATOLOGÍA OFTALMOLÓGICA
tensión arterial para descartar patología hipertensiva. El hiposfagma espontáneo no precisa tratamiento ni
valoración oftalmológica.
2. Conjuntivitis
2.1. Alérgica
Inflamación conjuntival secundaria a alérgenos. Generalmente es bilateral y cursa con picor,
escozor y lagrimeo junto a quemosis, edema palpebral y papilas tarsales. Puede asociar otros síntomas
alérgicos. Su tratamiento consiste en colirios de antihistamínicos y estabilizadores de los mastocitos cada
12 horas durante 10-15 días, pudiendo asociar corticoides tópicos o antihistamínicos orales en caso de
conjuntivitis alérgica moderada/severa.
2.2. Adenovírica
Cursa con abundantes secreciones seromucosas, edema palpebral, adenopatía preauricular
palpable, folículos tarsoconjuntivales y enrojecimiento. En ocasiones asocia un cuadro de infección del
tracto respiratorio superior. Es frecuente la historia de contacto con otras personas con conjuntivitis. El
tratamiento es sintomático con lágrimas artificiales, compresas frías, lavados con suero y antiinflamatorios
tópicos. Ante la sospecha de sobreinfección o duda de etiología bacteriana se debe añadir un antibiótico
tópico durante siete días. Se trata de una patología muy contagiosa que suele bilateralizarse en pocos días.
Es necesario extremar las medidas higiénicas para evitar el contagio. El cuadro suele empeorar la primera
semana y puede prolongarse de tres a cuatro semanas.
2.3. Bacteriana
Cuadro de hiperemia conjuntival asociado a secreciones mucopurulentas y quemosis conjuntival.
Su tratamiento consiste en antibióticos tópicos de manera empírica (tobramicina o gentamicina) cuatro
veces al día durante siete días.
3. Epiescleritis y escleritis
Ambas cursan con inyección ciliar sectorial o difusa. No suelen presentar secreciones. Para
diferenciarlas es conveniente instilar una gota de fenilefrina, en caso de epiescleritis se producirá un
blanqueamiento.
3.1. Epiescleritis
Se trata de una patología mucho más leve y más frecuente, caracterizada por dolor ocular leve sin
afectación visual. Aunque se trata de una patología autolimitada, se puede pautar tratamiento con lágrimas
artificiales y antiinflamatorios no esteroideos tópicos (tres veces al día durante siete días) y/o vía oral.
3.2. Escleritis
Patología grave que puede afectar a la visión. Asocia dolor intenso que puede irradiarse, fotofobia y
lagrimeo. Ante su sospecha debe ser derivado a un oftalmólogo. Su tratamiento consiste en
antiinflamatorios no esteroideos orales o corticoides orales.
4. Patología corneal
4.1. Erosión corneal
Lesión epitelial producida por un traumatismo, un cuerpo extraño o lentes de contacto. Cursa con
dolor intenso y sensación de cuerpo extraño. El diagnóstico se realiza con la tinción con fluoresceína y
posterior visualización con luz azul. Su tratamiento consiste en lubricación abundante tópica y antibióticos
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [214]
[16] PATOLOGÍA OFTALMOLÓGICA
tópicos (gentamicina o tobramicina) cuatro veces al día durante siete días para evitar la infección y
analgésicos orales.
4.2. Cuerpo extraño
Comparte la sintomatología con la erosión corneal. Durante la exploración se objetiva la presencia
de un cuerpo extraño corneal. Su tratamiento consiste en la extracción del cuerpo extraño y el tratamiento
de la erosión corneal subyacente.
4.3. Queratitis punteada superficial
Presencia de lesiones punteadas corneales visibles con la tinción con fluoresceína. Cursa con dolor,
lagrimeo y sensación de cuerpo extraño, pudiendo asociar fotofobia y disminución de la agudeza visual. Las
etiologías más frecuentes son: síndrome de ojo seco, queratitis actínica o fotoeléctrica (típica de
soldadores), queratitis por exposición y portadores de lentes de contacto. Tratamiento: lubricantes
(lágrimas artificiales o en forma de geles) de forma abundante; si las lesiones son graves se debe añadir
antibióticos tópicos y analgesia oral.
4.4. Úlcera corneal
Opacidad focal blanquecina corneal. Cursa con fotofobia, dolor moderado/severo, disminución de
la agudeza visual y secreciones. Ante la sospecha de este cuadro el paciente debe ser remitido a un servicio
de oftalmología de forma urgente. El tratamiento se realiza con antibióticos de amplio espectro,
habitualmente quinolonas (ofloxacino o moxifloxacino) de forma tópica cada dos horas.
4.5. Queratitis herpética
Afectación corneal por herpes zóster o herpes simple que se caracteriza por lesiones dendríticas
corneales que se visualizan con tinción con fluoresceína. Ante la sospecha de esta entidad debe ser
derivada a un oftalmólogo. El tratamiento oftalmológico consiste en pomada oftalmológica de aciclovir o
gel oftalmológico de ganciclovir 5 veces al día. Para evitar la sobreinfección se debe añadir un antibiótico
tópico.
5. Uveítis anterior aguda
Inflamación de la úvea anterior (iris y cuerpo ciliar). La mayoría son idiopáticas aunque existen
casos asociados con enfermedades inflamatorias, como la espondilitis anquilosante o la artritis psoriásica, o
enfermedades infecciosas. Cursa con inyección ciliar, dolor, fotofobia y disminución de la agudeza visual,
generalmente unilateral. Habitualmente no presentan secreciones. Ante la sospecha de inflamación del
tracto uveal el paciente debe ser remitido a un oftalmólogo de manera urgente. Su tratamiento consiste en
corticoides tópicos y tratamiento midriático para evitar o liberar sinequias iridianas.
6. Glaucoma agudo
Aumento de la presión intraocular que produce dolor muy intenso, enrojecimiento, midriasis media
arrectiva, náuseas y vómitos, así como disminución de la agudeza visual junto a visión de halos debido al
edema corneal. Se trata de una urgencia oftalmológica que debe ser remitida para valoración. Su
tratamiento consiste en hipotensores tópicos (timolol 0,5%) una gota cada 15 minutos y apraclonidina
(dosis única), corticoides tópicos, acetazolamida oral y/o manitol intravenoso. Si existen vómitos se
asociará metoclopramida.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [215]
[16] PATOLOGÍA OFTALMOLÓGICA
II. ALTERACIONES DE LA AGUDEZA VISUAL
1. Patología macular
El síndrome macular se caracteriza por metamorfopsias, disminución subaguda de la agudeza visual
con afectación predominante de la visión central. Pueden cursar con este síndrome enfermedades como la
degeneración macular asociada a la edad, el edema macular diabético o posquirúrgico o la miopía magna
(secundaria a neovascularización coroidea).
2. Patología vascular
2.1. Obstrucción arterial retiniana
Produce pérdida de visión brusca, indolora y severa, de manera unilateral. El defecto del campo
visual dependerá de la extensión de la retina afectada.
La causa más frecuente es secundaria a émbolos procedentes de patologías carotídeas o cardiacas.
Otra posible causa es la arteritis de células gigantes, que deberá descartarse en todos los >50 años.
Dentro del estudio etiológico se determinará tensión arterial, hemograma, glucemia basal,
hemoglobina glucosilada, estudio de coagulación, perfil lipídico, valoración de la carótida por ecografía
doppler y valoración de patología cardiaca con electrocardiograma.
El tratamiento de esta patología debe realizarse antes de las primeras 24 horas, aunque pasadas
más de dos horas la probabilidad de éxito es casi nula. Se disminuirá la presión intraocular mediante
paracentesis de cámara anterior y acetazolamida oral, entre otras maniobras.
2.2. Obstrucción venosa retiniana
Se trata de un cuadro de pérdida de visión no dolorosa que puede ser altitudinal o completa,
generalmente unilateral. Se produce habitualmente por ateroesclerosis de la arteria central adyacente que
comprime la vena.
Se debe realizar un estudio de los factores de riesgo cardiovascular e hipercoagulabilidad,
realizando una valoración médica completa.
2.3. Aura migrañosa
Síntomas visuales totalmente reversibles (luces parpadeantes, manchas, líneas, pérdida de visión)
asociado a síntomas sensitivos unilaterales. Los síntomas habitualmente duran entre cinco y 60 minutos.
Generalmente preceden a la cefalea (ver Capítulo 81. “Cefaleas y algias craneofaciales”).
3. Desprendimiento de retina y desprendimiento de vítreo posterior
3.1. Desprendimiento de vítreo posterior
Objetos que aparecen en el campo visual referidos como telarañas, moscas o manchas que
cambian de posición con los movimientos oculares. También puede manifestarse con visión borrosa o
destellos. Ante la aparición reciente de estos síntomas el paciente debe ser revisado de forma urgente por
un oftalmólogo para descartar lesiones retinianas.
3.2. Desprendimiento de retina
Defecto del campo visual descrito por el paciente como sombra o cortina que avanza. Ante la
sospecha de esta patología se debe derivar al paciente a un servicio de urgencias oftalmológicas.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [216]
[16] PATOLOGÍA OFTALMOLÓGICA
4. Hemovítreo
Pérdida de visión brusca, no dolorosa o aparición brusca de manchas negras, telarañas o visión
borrosa. Generalmente se produce en personas diabéticas y es secundario a neovascularización retiniana.
5. Patología del nervio óptico
5.1. Neuropatía óptica isquémica anterior no arterítica
Pérdida de visión súbita, indolora, no progresiva de grado moderado. Inicialmente unilateral
aunque puede bilateralizarse. En la exploración se observa defecto pupilar aferente relativo, edema de
papila y hemorragias en llama peripapilares. Es muy importante descartar que no se trate de una NOIA
arterítica mediante la anamnesis y estudio analítico que incluya velocidad de sedimentación globular,
proteína C reactiva y recuento plaquetario (descartar trombocitosis).
5.2. Neuropatía óptica isquémica anterior arterítica
Aparece con la misma sintomatología visual que la forma no arterítica. Debe sospecharse en
pacientes mayores de 50 años con historia de cefaleas previas o simultáneas, claudicación mandibular,
sensibilidad del cuero cabelludo y polimialgias. Se realizarán las mismas pruebas complementarias que las
descritas en la NOIA no arterítica. Ante la sospecha de arteritis de células gigantes se debe comenzar con
tratamiento corticoideo sistémico de forma urgente.
5.3. Neuritis óptica retrobulbar
Debe sospecharse ante la disminución de la agudeza visual en un plazo de horas a días (lo más
frecuente) y ante la falta de hallazgos patológicos en la exploración oftalmológica. Suelen referir dolor a los
movimientos oculares, discromatopsia y defecto pupilar aferente relativo. Esta patología debe ser evaluada
de forma urgente por un neurólogo.
5.4. Papiledema
Se trata de un edema de papila bilateral producido por aumento de la presión intracraneal que
cursa con episodios de pérdida de visión transitorios, sin disminución de la agudeza visual ni dolor.
5.5. Otras neuritis ópticas
Existen otras causa raras de neuritis ópticas menos frecuentes, como las asociadas a procesos
víricos, a tóxicos o déficits nutricionales.
6. Catarata
Pérdida visual lentamente progresiva (meses o años) que afecta a uno o a ambos ojos. La catarata
senil constituye la causa más frecuente de pérdida visual reversible
III. DIPLOPÍA
1. Monocular
La diplopía se mantiene cuando se ocluye el ojo no afectado. Sus causas más frecuentes son errores
de refracción, alineación incorrecta de las gafas, opacidad o irregularidades corneales o catarata.
2. Binocular
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [217]
[16] PATOLOGÍA OFTALMOLÓGICA
La diplopía desaparece cuando se ocluye cualquier ojo. Las causas más frecuentes son parálisis
aisladas del iii, iv o vi par craneal. Otras causas más infrecuentes son la miastenia gravis, la
descompensación de una foria preexistente o enfermedades orbitarias.
Tabla I.Fármacos más utilizados en oftalmología
Tabla II.Criterios de derivación a oftalmología
BIBLIOGRAFÍA
Bengoa A, Gutiérrez E, Pérez E. Atlas urgencias en oftalmología. Hosp. 12 de Octubre. Ed. Glosa; 2001.
Ehlers JP, Shah CP. Manual de oftalmología del Wills Eye Institute. Philadelphia: McGraw Hill; 2007.
Kanski JJ. Oftalmología clínica. 7.ª ed. Windsor: Elsevier; 2012.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [218]
[17] PATOLOGÍA OTORRINOLARINGOLÓGICA. MANEJO DE TRAQUEOTOMÍAS
17.Patología otorrinolaringológica. Manejo de
traqueotomías
Nieves Isabel Rodríguez Lorenzo.
Otorrinolaringología
Gianmarco Narciso Martínez.
Otorrinolaringología
Asesor:
Carlos Almodóvar Álvarez.
Jefe de Servicio de Otorrinolaringología
Otología/neurootología
I. PATOLOGÍA INFLAMATORIA E INFECCIOSA (Tabla I)
Tabla I.Patología otológica inflamatoria e infecciosa
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [219]
[17] PATOLOGÍA OTORRINOLARINGOLÓGICA. MANEJO DE TRAQUEOTOMÍAS
[Nota propia (LJDV): me da la sensación de que aquí han olvidado volcar en la web al menos un par de apartados]
1. Concepto y etiología
El vértigo, que se define como una ilusión de movimiento propio o del ambiente, habitualmente de
giro o rotatorio, constituye uno de los síntomas principales de la patología vestibular, especialmente la
periférica. Cuando la sensación descrita responde más a desequilibrio/inestabilidad (pérdida de control
postural con tendencia a la caída) o a un mareo inespecífico (presentación variable, de difícil definición:
presíncope, confusión, etc.) debemos sospechar otros orígenes. El siguiente esquema resume las
principales etiologías a descartar en el estudio de estos pacientes:
Causas orgánicas:
Vestibulares: periféricas (afección del oído interno, generalmente por una asimetría
funcional repentina, por ejemplo síndrome de Ménière) o centrales (sistema nervioso
central/tronco: esclerosis múltiple, migraña basilar o patología cerebrovascular).
No vestibulares: cardiovasculares (ortostatismo, accidente cerebrovascular y accidente
isquémico transitorio), neurológicas (epilepsia y neuropatías) o medicamentosas
(ansiolíticos, antihipertensivos, etc.).
Causas funcionales/psicogénicas: trastornos de ansiedad/depresivos (sin patrón orgánico,
larga evolución).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [220]
[17] PATOLOGÍA OTORRINOLARINGOLÓGICA. MANEJO DE TRAQUEOTOMÍAS
2. Aproximación diagnóstica
La anamnesis debe ir enfocada al diagnóstico diferencial entre el vértigo periférico, el central y
otras causas de mareo. Ha de interrogarse a cerca de: antecedentes personales (presencia de factores de
riesgo cardiovascular, que obligan a descartar etiología central, anemia, traumatismos, patología cervical,
cardiaca o neurológica), intensidad y naturaleza de la sensación experimentada, duración de la crisis, forma
de presentación, factores desencadenantes y síntomas asociados.
La patología vestibular periférica suele cursar característicamente con sensación de giro de objetos,
de inicio brusco, acompañada de cortejo neurovegetativo, asociando o no sintomatología auditiva
(hipoacusia, acúfenos o aura con plenitud ótica) sin clínica neurológica (no presenta pérdida de fuerza o
sensibilidad, cefalea intensa, alteración de los pares craneales, disfunción piramidal ni pérdida de
conocimiento o falta del control de esfínteres). El diagnóstico diferencial entre vértigo periférico y central
se resume en la tabla II.
Tabla II.Vértigo periférico frente a vértigo central
La exploración física debe incluir toma de constantes, una valoración otológica (otoscopia y signo
de la fístula: aparición de nistagmo al insuflar aire en el oído) y la neurológica básica: pares craneales,
fuerza y sensibilidad, dismetría (maniobra dedo-nariz) y disdiadococinesia. Ha de constatarse si existe o no
nistagmo espontáneo o provocado mediante maniobras posturales como el Dix-Hallpike (positivo si
reproduce la clínica y desencadena un nistagmo posicional) o test de agitación cefálica (pone de manifiesto
nistagmo latente con fase rápida al oído sano). La valoración neurovestibular se completará con las
siguientes pruebas: Romberg (estándar y forzado), de los índices (Barany estático y dinámico) y de la
marcha (estática-Unterberger y dinámica-Babinsky-Weil), todas consideradas positivas si existe
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [221]
[17] PATOLOGÍA OTORRINOLARINGOLÓGICA. MANEJO DE TRAQUEOTOMÍAS
lateralización o lateropulsiones (serán congruentes con vértigo periférico cuando son contrarias a la fase
rápida del nistagmo).
Dentro de las pruebas complementarias en el diagnóstico de vértigo periférico están la
audiometría, potenciales evocados auditivos, videonistagmografía o posturografía dinámica y las pruebas
calóricas, que no se realizarán de manera urgente. Cuando existe sospecha de vértigo central se requerirá
un estudio de imagen. Se ha de tener en cuenta que una tomografía computarizada (TC) craneal sin
alteraciones no descarta esta etiología, dada la baja sensibilidad de la técnica para procesos vasculares
acaecidos en el territorio vertebrobasilar, así como para detectar procesos isquémicos recientes. El estudio
de preferencia es, por tanto, la resonancia magnética (RM).
3. Entidades/patología vestibular periférica
3.1. Vértigo posicional paroxístico benigno
Etiología: cupulolitiasis o canalolitiasis; la ubicación más frecuente es el canal semicircular
posterior. Ocasional antecedente de traumatismo o neuritis vestibular, yatrogenia
(estapedectomía en otosclerosis).
Características: episodios recurrentes de segundos de duración que se desencadenan con el
cambio postural cefálico.
Diagnóstico: Dix-Hallpike positivo.
Tratamiento: maniobras posturales (Epley o Semont) y ejercicios de Brandt-Daroff para
mantenimiento domiciliario (si fallan las maniobras previas). No se utilizan sedantes
vestibulares. Maniobra de Epley:
Se mantiene al paciente en sedestación sobre una camilla, con la cabeza girada 45º
hacia el lado afecto.
Se tumba conservando el giro cefálico, permaneciendo en decúbito supino unos
minutos.
Giro la cefálico 90º contralateral, permanecer unos minutos.
Cambio postural a decúbito lateral hacia el lado sano durante unos minutos. Mientras
tanto se ha de sostener la cabeza del paciente que ha de girar con el cuerpo, hasta
quedar mirando hacia el suelo.
Regresar a la posición de sedestación durante unos minutos.
Nota:es posible que se desencadenen síntomas vertiginosos durante la realización de la maniobra.
3.2. Enfermedad de Ménière
Etiología: hidrops endolinfático idiopático que produce una dilatación del laberinto
membranoso.
Características: episodios recurrentes de minutos a horas de duración, con hipoacusia
fluctuante, acúfenos o aura con plenitud ótica.
Tratamiento: sedantes vestibulares, antieméticos, sedantes en las crisis y dieta hiposódica.
Diuréticos ± betahistina para el mantenimiento.
3.3. Neuritis vestibular
Etiología: lesión inflamatoria del nervio vestibular habitualmente de etiología vírica; puede
existir antecedente de infección viral de vías altas.
Características: episodio único de horas a días de duración, sin afectación auditiva o
neurológica. Habitualmente en adultos jóvenes.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [222]
[17] PATOLOGÍA OTORRINOLARINGOLÓGICA. MANEJO DE TRAQUEOTOMÍAS
Tratamiento: la corticoterapia en los primeros tres días ha demostrado beneficio, no así los
antivirales. Suele requerir ejercicios de rehabilitación vestibular.
3.4. Laberintitis
Etiología: generalmente secundaria a otitis media aguda. Otros: vírica, OMS (otitis media
serosa) y ototóxicos.
Características: episodios de días de duración. Asocia hipoacusia neurosensorial que permanece
tras la resolución del vértigo.
Tratamiento: la forma supurativa o destructiva es la más grave. Requerirá ingreso con medidas
generales (hidratación adecuada, reposo relativo), medicación antivertiginosa, corticoides y
tratamiento etiológico: antibioterapia de amplio espectro (amoxicilinaclavulánico 1 g/8 h o
ceftriaxona 2 g/24 h durante siete días) o antivirales (por ejemplo famciclovir 750 mg/24 h o
valaciclovir 1 g/8 h, siete días).
3.5. Fístula perilinfática
Etiología: puede ser secundaria a otitis media colesteatomatosa, sífilis, barotrauma,
traumatismo penetrante, cirugía otológica o idiopática. Causan una comunicación anormal
entre el espacio perilinfático y el oído medio o el espacio endolinfático.
Características: episodios recurrentes de minutos de duración desencadenados con el Valsalva
o los sonidos fuertes. Signo de la fístula positivo.
Tratamiento: conservador (cabecero cama elevado, laxantes) y específico de la causa.
4. Manejo terapéutico de las crisis
Crisis leves, sin gran afectación del estado general: permiten tratamiento oral con sulpiride
(Dogmatil®) 50 mg/8 h con o sin la asociación de diazepam 5-10 mg/24 h, además de
metoclopramida 10 mg si se asocian náuseas o vómitos.
Deberá tenerse en cuenta que el tratamiento con sedantes vestibulares no ha de mantenerse
de manera crónica.
Crisis severas, con sintomatología incapacitante (imposibilita la tolerancia oral, con cortejo
vegetativo muy intenso): requerirán tratamiento intravenoso que asocie metoclopramida 10
mg, sulpiride 100 mg y diazepam 5-10 mg en suero glucosado 500 cc, a pasar en tres a cuatro
horas. Reevaluación a las cinco a seis horas, repitiendo el ciclo de sedante vestibular y
antiemético si se requiere.
II. PARÁLISIS FACIAL PERIFÉRICA
1. Exploración clínica
La evaluación inicial de los pacientes con parálisis facial deberá incluir: historia clínica detallada,
exploración neurológica completa de todos los pares craneales, otoscopia, acumetría y en casos selectos
pruebas de imagen. Debe tenerse en cuenta la afectación cutánea, los signos de traumatismo o los
hallazgos que orienten a etiología sistémica.
De forma programada se deberá completar el estudio con una audiometría tonal ± estudios
electrofisiológicos.
Para describir el grado de disfunción en cada caso debe hacerse uso de escalas estandarizadas; la
más empleada es la de House-Brackmann: Tabla III.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [223]
[17] PATOLOGÍA OTORRINOLARINGOLÓGICA. MANEJO DE TRAQUEOTOMÍAS
2. Etiologías más comunes (Tabla IV)
2.1. Parálisis facial idiopática (parálisis de Bell)
Es la causa más frecuente, típica entre los 15-45 años, sin diferencia en la incidencia según la raza o
el sexo. Suele ser unilateral y es recurrente en un 10% de los casos. La etiología y fisiopatología
permanecen sin esclarecer, pero se sospecha una infección latente por el virus herpes simplex o un fallo
microcirculatorio de los vasa nervorum. El diagnóstico es clínico por exclusión y no se requiere el empleo de
pruebas de imagen de manera rutinaria.
Tabla III.Escala de House-Brackmann
El tratamiento incluye pauta de corticosteroides orales (por ejemplo prednisona a 1 mg/kg/ día
durante 5 días con pauta descendente de 10 mg cada 3 días) y medidas de protección ocular (lágrimas
artificiales a demanda, pomada lubricante y oclusión ocular nocturnas). El uso de terapia antiviral es
controvertido. El pronóstico suele ser bueno, independientemente de terapia médica, con tasas de
recuperación del 80-90%.
2.2. Síndrome de Ramsay-Hunt
Es la segunda en frecuencia. Asocia otalgia, vesículas en el conducto auditivo externo y la concha,
hipoacusia neurosensorial y vértigo. Su incidencia aumenta en pacientes mayores de 60 años e
inmunocomprometidos, pues se debe a la activación de la infección latente del virus varicela zóster.
El manejo es similar al de la parálisis de Bell, empleándose los corticoides, ya que disminuyen la
neuralgia posherpética, la otalgia y el vértigo, agregando medicación antiviral (Tabla I).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [224]
[17] PATOLOGÍA OTORRINOLARINGOLÓGICA. MANEJO DE TRAQUEOTOMÍAS
Tabla IV.Causas de parálisis facial periférica
2.3. Infecciones bacterianas
Pueden ocurrir en el seno de una otitis media aguda o crónica (simple o colesteatomatosa),
otomastoiditis u otitis externa maligna. La presencia de dehiscencias en el canal de Falopio constituye un
factor de riesgo. La parálisis suele ser incompleta y puede estar acompañada de fiebre, otalgia, otorrea e
hipoacusia. Requiere antibioterapia y corticosteroides parenterales, además de valoración por
otorrinolaringología (ORL) para establecer el tratamiento específico causal.
III. CUERPOS EXTRAÑOS EN EL CONDUCTO AUDITIVO EXTERNO
El tratamiento consistirá en la extracción mediante irrigación, aspiración o instrumental (pinzas,
ganchos) preferiblemente con control otoscópico; a veces se requiere una combinación de ellas. Deben
tenerse presentes las siguientes consideraciones, avisando a ORL cuando se requiera:
Extracción mediante irrigación: instilación de agua tibia a presión en dirección posterosuperior
con jeringa de 100 cc o de 50 cc tras corregir angulación del conducto auditivo externo (CAE) –
tirar del pabellón hacia atrás y arriba–. Contraindicado cuando haya presencia o sospecha de
perforación timpánica, cuerpos higroscópicos que crecen en contacto con el agua y pueden
quedar enclavados (semillas y legumbres), pilas alcalinas (liberan sustancias tóxicas/abrasivas
en contacto con el agua).
Cuerpos extraños animados (insectos): previo a su extracción es necesario matarlos o
inmovilizarlos mediante instilación de soluciones de lidocaína, aceite mineral o alcohol, para
evitar que produzcan daños en el CAE o en la membrana timpánica.
Evitar el empleo de pinzas cuando no se tiene un buen control visual, especialmente ante
cuerpos extraños con aristas o pinchos, vegetales: espigas, espinas, etc.
IV. PATOLOGÍA TRAUMÁTICA
1. Pabellón auricular y conducto auditivo externo
1.1. Seroma y otohematoma
Se producen habitualmente por golpes tangenciales, usualmente repetidos en los seromas. Se da
un aumento de volumen fluctuante, más o menos doloroso, de coloración violácea cuando la colección es
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [225]
[17] PATOLOGÍA OTORRINOLARINGOLÓGICA. MANEJO DE TRAQUEOTOMÍAS
hemática. Requieren aspiración o drenaje y colocación de vendajes compresivos que se adapten a la
superficie cutánea y una cobertura antibiótica de amplio espectro (pseudomonas, flora cutánea habitual,
cocos y bacilos grampositivos) para prevenir la aparición de pericondritis (Tabla I).
1.2. Laceraciones y heridas
Limpieza con antisépticos ± sutura por planos (si existe afección del cartílago las medidas a tomar
serán cobertura antibiótica profiláctica y compresión). En CAE rara vez se requiere sutura; si se observan
escalones subyacentes (óseos o cartilaginosos) habrá que descartar fractura del cóndilo mandibular o de la
base del cráneo. Ante quemaduras, congelaciones y abrasiones químicas: desbridamiento quirúrgico ±
vendajes no compresivos con gasas vaselinadas y cobertura antibiótica local y/o sistémica profiláctica en
función de la afectación.
2. Oído medio
Por diferencias de presión entre la caja y el exterior que la trompa no puede compensar
adecuadamente.
2.1. Barotrauma
Cursa con hipoacusia variable, sensación de taponamiento, otalgia, otorragia leve, acúfenos e
incluso vértigo. A la otoscopia se objetiva retracción timpánica, aumento de la trama vascular y es posible
que se produzcan derrames serosos. Cuando la intensidad es grande y los cambios súbitos (estallidos,
bofetadas, etc.) pueden aparecer hematomas en caja e incluso perforaciones timpánicas. El tratamiento
puede incluir: vasoconstrictores nasales, corticoides tópicos o sistémicos y antiinflamatorios.
2.2. Perforaciones timpánicas
Habitualmente del cuadrante anteroinferior. Debe realizarse una limpieza del CAE mediante control
microscópico, evitar la entrada de agua y si la perforación es grande, hay signos de contaminación o
infección se recomienda cobertura antibiótica sistémica (discutido el uso de tópicos): amoxicilina-
clavulánico 500 u 875 mg/125-8 h durante siete días.
3. Peñasco
3.1. Fracturas temporales
Longitudinales: siguen el eje mayor, con afección habitual de oído medio y CAE. Se sospecha
ante otorragia (80-90%), escalones en CAE y perforación timpánica. Hipoacusia
transmisiva/mixta y posibles otolicuorrea y parálisis facial periférica (20%).
Transversales: usualmente afectan al oído interno y cursan típicamente con hemotímpano,
hipoacusia neurosensorial, parálisis facial (50%) y vértigo periférico.
Oblicuos/mixtos: pueden presentar una combinación de los anteriores.
La confirmación diagnóstica y del tipo de trazo, además de la valoración de afectación de
estructuras adyacentes, se hará mediante realización de TC. En la mayoría el tratamiento es conservador. El
manejo de la parálisis facial es controvertido, indicándose descompresión quirúrgica ante casos inmediatos
totales y prefiriéndose actitud expectante con ciclo corticoideo de inicio en el resto de casos.
3.2. Conmoción laberíntica
No hay fractura del hueso temporal. Cursa con cuadro vestibular periférico, hipoacusia
(neurosensorial) con otoscopia normal ± acúfenos. El pronóstico es variable y tratamiento consiste en
sedantes vestibulares, ansiolíticos y rehabilitación vestibular.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [226]
[17] PATOLOGÍA OTORRINOLARINGOLÓGICA. MANEJO DE TRAQUEOTOMÍAS
Rinología
V. RINOSINUSITIS AGUDA
1. Definición y fisiopatología
El término rinosinusitis hace referencia a la inflamación mucosa de las fosas nasales y senos
paranasales de hasta cuatro semanas de duración. Es una patología común (6-15% de la población), de
prevalencia variable según la estación (mayor en invierno) y los cambios climáticos. Son factores
predisponentes del huésped: condiciones genéticas, alergia, alteraciones inmunológicas y anatómicas,
enfermedades sistémicas y mecanismos neurales. Influyen además factores ambientales: agentes
infecciosos, traumatismos, exposición a químicos, medicación o cambios posquirúrgicos.
Los factores proinflamatorios llevan a edema y obstrucción del complejo osteomeatal,
comprometiendo el drenaje y ventilación de los senos paranasales. Esto provoca una retención de
secreciones con posible colonización bacteriana secundaria.
Se denomina rinosinusitis aguda recurrente cuando ocurren 4 o más episodios en un año, con
resolución total entre ellos.
2. Etiología
La etiología suele ser vírica y en pocos casos puede haber infección bacteriana secundaria (Tabla V).
Tabla V.Frecuencia relativa de microorganismos en rinosinusitis aguda
3. Clínica y diagnóstico
El diagnóstico de la rinosinusitis aguda se puede realizar en función de los signos, síntomas y
exploración física (Tabla VI).
Las pruebas radiológicas, como la TC y la RM no se emplean de rutina, excepto cuando existe
sospecha de una complicación. Las radiografías de senos paranasales no se usan comúnmente debido a su
baja sensibilidad y especificidad. El diagnóstico de confirmación se basa en la aspiración y cultivo de las
secreciones de los senos afectados, sin embargo no se utiliza de manera rutinaria.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [227]
[17] PATOLOGÍA OTORRINOLARINGOLÓGICA. MANEJO DE TRAQUEOTOMÍAS
Tabla VI.Síntomas diagnósticos de rinosinusitis
4. Tratamiento
Figura 1.Tratamiento de rinosinusitis aguda.
4.1 Tratamiento antibiótico
Según recomendaciones recientes de la Sociedad Americana de Enfermedades Infecciosas se
sugiere utilizar amoxicilina/clavulánico en lugar de amoxicilina sola en pacientes de zonas geográficas con
altas tasas de Streptococcus pneumoniae resistente a las penicilinas, infecciones severas, hospitalización,
uso de antibióticos en el último mes o inmunocomprometidos. Los macrólidos no están recomendados
como terapia empírica inicial. Las pautas propuestas son:
Primera línea:
Amoxicilina/clavulánico: 875 mg c/8 h × 7-14 días.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [228]
[17] PATOLOGÍA OTORRINOLARINGOLÓGICA. MANEJO DE TRAQUEOTOMÍAS
Levofloxacino: 500 mg c/24 h × 10 días (alérgicos a betalactámicos).
Segunda línea:
Levofloxacino: 500 mg c/24 h × 10 días.
Moxifloxacino: 400 mg c/24 h × 7-10 días.
Cefuroxima-axetilo: 500 mg c/12 h × 10 días.
Antibiótico dirigido según los cultivos.
5. Complicaciones
Las complicaciones de la rinosinusitis aguda se pueden clasificar según la región anatómica
afectada; principalmente se comprometen la órbita y la fosa craneal anterior, por pérdida de la barrera
anatómica o diseminación hematológica. La sospecha o identificación de complicaciones requiere derivar a
urgencias hospitalarias para evaluación y establecer tratamiento específico. En la siguiente tabla se
presentan las posibles complicaciones y hallazgos clínicos (Tabla VII).
Tabla VII.Hallazgos clínicos en complicaciones de la rinosinusitis aguda
6. Rinosinusitis aguda fúngica fulminante
Causada por hongos de la familia Mucoraceae y Aspergillus spp por invasión directa desde la
mucosa sinonasal o vía vascular hacia la órbita, tejidos blandos y parénquima cerebral. Se suele dar en
pacientes inmunosuprimidos.
La clínica se superpone a la de un episodio agudo simple, aunque puede asociar hallazgos orbitarios
(oftalmoplejía, proptosis y pérdida de la agudeza visual/amaurosis). En la exploración endonasal es habitual
encontrar datos de hipoperfusión/isquemia (zonas blancas) y necrosis (zonas negras) en la mucosa nasal. El
diagnóstico se realiza mediante toma de biopsias examinadas en corte congelado evidenciando invasión
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [229]
[17] PATOLOGÍA OTORRINOLARINGOLÓGICA. MANEJO DE TRAQUEOTOMÍAS
fúngica. Además, se deben obtener muestras para estudio anatomopatológico definitivo (parafina) y
cultivos.
En la TC de senos paranasales se observan hallazgos similares a la rinosinusitis, pero en algunos
casos se puede dar erosión ósea o datos de invasión tisular.
El tratamiento consiste en desbridamiento quirúrgico amplio del tejido afecto, antifúngicos
sistémicos y corrección de la causa subyacente (la supervivencia de estos pacientes está directamente
relacionada con la resolución de la condición predisponente).
VI. EPISTAXIS
Es la urgencia otorrinolaringológica más común, que puede presentarse como patología aislada o
como síntoma de una enfermedad sistémica. Comprende todos los fenómenos hemorrágicos originados en
las fosas nasales. Presenta dos picos de incidencia: menores de 10 y mayores de 40 años. Las causas varían
según la edad y en su mayoría son autolimitadas (Tabla VIII).
Tabla VIII.Clasificación etiológica de las epistaxis
1. Clasificación topográfica
Anteriores (90%): área de Kiesselbach (área septal anteroinferior).
Posteriores (7%): plexo de Woodruff (anastomosis de la arteria esfenopalatina y la arteria
faríngea posterior).
Superior (3%): territorio de las arterias etmoidales anteriores y posteriores.
Difusa.
2. Clínica y aproximación diagnóstica
A la llegada del paciente se deben tomar las constantes vitales e intentar determinar la cuantía del
sangrado. Dependiendo del estado general, se aplicarán protocolos de reposición de volumen intravascular.
En algunos casos será importante distinguir entre epistaxis, sangrado oral, hematemesis o hemoptisis.
Ante un paciente hemodinámicamente estable, la primera medida será adoptar una postura
adecuada: sedestación, inclinar la cabeza hacia adelante y mantener la boca abierta, mientras se realiza
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [230]
[17] PATOLOGÍA OTORRINOLARINGOLÓGICA. MANEJO DE TRAQUEOTOMÍAS
presión bilateral sobre el septum anterior comprimiendo los cartílagos alares digitalmente 10-15 minutos.
Durante esta fase se pueden emplear vasoconstrictores y frío local. Se procederá a obtener pruebas
analíticas y control de coagulación según la necesidad. Si con estas medidas no cede el sangrado debemos
pasar al tratamiento específico.
3. Tratamiento
La clave para el control de las epistaxis es hallar el área de sangrado. Se debe realizar una
rinoscopia anterior limpiando los coágulos retenidos. La endoscopia nasal es de gran utilidad cuando no se
puede identificar el origen (especialmente en epistaxis posteriores).
Una vez encontrado el punto de sangrado, si está accesible, se puede realizar cauterización química
con nitrato de plata o eléctrica, ambas bajo anestesia local. No se realizará la cauterización septal bilateral
por el riesgo de perforación.
Otra alternativa es llevar a cabo un taponamiento anterior unilateral con agentes hemostáticos
reabsorbibles, gasas vaselinadas, esponjas autoexpansibles o dispositivos de neumotaponamiento,
dependiendo de la disponibilidad. En ocasiones será necesario realizar un taponamiento anterior bilateral
para lograr compresión efectiva sobre el área de sangrado. Si se controla, el paciente puede ser dado de
alta y el taponamiento deberá ser mantenido usualmente 48-72 horas, pudiendo prolongarse según el
origen del sangrado. Se requerirá el uso de antibióticos orales si se superan los cuatro días. Otras medidas
generales útiles son reposo relativo, dieta blanda y fría, evitar esfuerzos, elevación del cabecero al dormir y
control estricto de la tensión arterial (Figura 2).
Si persiste la epistaxis a pesar de las medidas previas, se debe pasar a la opción quirúrgica
(taponamiento posterior, cirugía endoscópica o embolización).
Figura 2.Manejo de la epistaxis
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [231]
[17] PATOLOGÍA OTORRINOLARINGOLÓGICA. MANEJO DE TRAQUEOTOMÍAS
Cabeza y cuello
VII. GLÁNDULAS SALIVALES
1. Sialoadenitis supurativa aguda
1.1. Definición y causas
Es la infección, habitualmente bacteriana, de las glándulas salivales. Existen dos factores
protectores para evitar la colonización retrógrada de la flora bacteriana desde la cavidad oral: el flujo salival
normal y las propiedades antimicrobianas de la saliva. La estasis salival por la reducción/obstrucción del
flujo predispone a la infección.
La frecuencia aumenta en mayores de 70 años, personas dependientes (aporte de líquidos
insuficiente), pacientes posquirúrgicos deshidratados (cirugía gastrointestinal y de cadera), polimedicados y
mala higiene oral.
1.2. Clínica y diagnóstico
Se presenta como un aumento de volumen unilateral con descarga purulenta a través del conducto
salival a la digitopresión de la glándula afecta. En la palpación bimanual de los conductos Warthon y Stenon
se puede evidenciar alguna litiasis. Es importante prestar atención a signos sistémicos de deshidratación.
De la secreción drenada se deben tomar cultivos para aerobios y anaerobios. El patógeno aislado
con mayor frecuencia (90%) es el Staphylococcus aureus, seguido de bacterias anaeróbicas (Fusobacterium
y Peptostreptococcus spp).
En el hemograma destaca la leucocitosis con neutrofilia, y en el análisis bioquímico los signos de
deshidratación (la hipernatremia y la elevación de la creatinina). No se necesitan de forma rutinaria
pruebas de imagen, sin embargo, ante la sospecha de absceso (fluctuación a la palpación) o la falta de
respuesta al tratamiento médico en 48-72 horas, la ecografía o TC servirán para descartar complicaciones y
plantear si se requiere tratamiento quirúrgico. La sialografía está contraindicada en la sialoadenitis aguda.
1.3. Tratamiento
El tratamiento inicial se basa en la hidratación con reposición hidroelectrolítica, antibioterapia
empírica con amoxicilina/clavulánico 500 mg c/8 h durante 10 días, calor local, masaje glandular y
sialogogos (se suelen emplear sustancias ácidas como el zumo de limón o el de naranja).
2. Parotiditis vírica
2.1. Definición e incidencia
Causada por el paramyxovirus, es la infección no supurativa más común de las glándulas salivales.
Ha disminuido su incidencia desde la implementación de la vacuna triple vírica; sin embargo, en 2014, se
han reportado más de 3.300 casos en España. Actualmente el grupo etario más afectado son los adultos
jóvenes.
2.2. Clínica
Usualmente se presenta con síntomas prodrómicos que incluyen fiebre, astenia, mialgias, artralgias
y anorexia. Posteriormente aparece aumento de volumen bilateral doloroso en la región parotídea (puede
ser unilateral). Las glándulas submandibulares se afectan en menor medida. Otras manifestaciones incluyen
orquitis, encefalitis, meningitis aséptica, pancreatitis, nefritis e hipoacusia neurosensorial.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [232]
[17] PATOLOGÍA OTORRINOLARINGOLÓGICA. MANEJO DE TRAQUEOTOMÍAS
2.3. Diagnóstico y tratamiento
El diagnóstico de certeza se realiza mediante serología. En la analítica puede haber leucopenia y
elevación de la amilasa salival. El tratamiento se basa en reposo, higiene oral, hidratación y medicación
sintomática. Se debe recordar que es una enfermedad de notificación obligatoria en España.
3. Xerostomía
3.1. Causas
Es un síntoma muy común en la otorrinolaringología, causado por una amplia variedad de
patologías propias de glándulas salivales o sistémicas. También puede tener origen yatrogénico (Tabla IX).
3.2. Consecuencias
La xerostomía puede causar estados inflamatorios en la mucosa orofaríngea, con la siguiente
colonización por flora no saprofita provocando mucositis, estomatitis, micosis, queilitis angular y aumento
de infecciones dentales. Los signos y síntomas más comunes son incremento de la sed, molestias/atrofia
lingual, dolor urente faríngeo, disfonía y disfagia.
Tabla IX.Causas más frecuentes de xerostomía
3.3. Tratamiento
Debe ser el de la causa subyacente, además de instaurar medidas preventivas y paliativas en caso
de que no sea posible corregirla:
Tomas de agua frecuente, sialogogos orales, higiene oral, sustitutos salivales, dieta blanda.
Pilocarpina (aunque debido a los efectos secundarios los pacientes suelen abandonarlo).
Evaluación periódica por el odontólogo.
VIII. FARINGOAMIGDALITIS AGUDA INFECCIOSA
1. Concepto y clasificación
La faringoamigdalitis aguda (FAA) es un proceso que cursa con inflamación de las mucosas de la
faringe y/o amígdalas palatinas. Su etiología más habitual es la infecciosa, y es más común en la infancia. En
función del agente causal las FAA se clasificarán según la tabla X.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [233]
[17] PATOLOGÍA OTORRINOLARINGOLÓGICA. MANEJO DE TRAQUEOTOMÍAS
2. Tratamiento antibiótico de la faringoamigdalitis aguda por Streptococcus del grupo A
El tratamiento antibiótico ha demostrado erradicar el germen y conseguir una reducción del curso
de la enfermedad, de la intensidad de los síntomas, y del contagio. También se asocia a la prevención de
aparición de complicaciones supurativas y no supurativas, aunque no está clara la protección frente a
glomerulonefritis y síndrome PANDAS (desorden neuropsiquiátrico autoinmune asociado a Streptococcus
del grupo A). Por lo tanto, para facilitar la toma de decisiones en el manejo de estos pacientes se han
descrito escalas predictivas, siendo una de las más empleadas la de los criterios Centor (no se deben usar
en inmunosuprimidos) (Tabla XI):
Primera elección: penicilina v (fenoximetilpenicilina) 500 mg/6-8 h, 7-10 días. Equivalencia: 250
mg = 400.000 UI.
Alternativas: penicilina G 1,2 M de UI IM una dosis (si presenta intolerancia oralvómitos),
amoxicilina o cefadroxilo 500 mg/8 h durante 7 días.
Alérgicos a β-lactámicos: josamicina 1 g/12 h 10 días, clindamicina 300 mg/6 h durante 7-10
días (se ha descrito una tasa de resistencia a macrólidos creciente, especialmente los de 14 y 15
átomos, por lo tanto no se recomiendan eritromicina, claritromicina y azitromicina).
Persistencias o casos recurrentes: amoxicilina-clavulánico 875/125 mg/8 h durante siete días,
cefuroxima acetilo 500 mg/12 h durante 7-10 días, clindamicina 300 mg/6 h durante 10 días.
Tabla X.Clasificación etiológica de la faringoamigdalitis aguda
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [234]
[17] PATOLOGÍA OTORRINOLARINGOLÓGICA. MANEJO DE TRAQUEOTOMÍAS
Tabla XI.Criterios de Centor
3. Faringitis micótica
Se da habitualmente en pacientes inmunocomprometidos, siendo también factores de riesgo el
tratamiento con antibioterapia prolongada, el uso de corticoides inhalados, la xerostomía o la radioterapia
previa, entre otros.
Los microorganismos que más habitualmente afectan a la orofaringe son los de la Candida spp.
Cursan con odinodisfagia urente variable, sensación de cuerpo extraño y/o alteración del gusto. A la
exploración son posibles varias formas: muguet clásico (pseudomembranas blanquecinas que se
desprenden al raspado dejando base eritematosa), hiperplásica (placas perladas que se desprenden peor) y
atrófica o eritematosa (placas planas rojizas). Puede invadir también mucosa yugal, lengua, paladar,
hipofaringe, laringe y esófago.
El tratamiento inicial en formas no complicadas será tópico, mejorando la higiene oral y con
enjuagues antifúngicos con nistatina (250-500.000 UI; 2,5-5 ml cada 6-12 h, en adultos o niños mayores de
1 año). En infecciones refractarias, recurrentes o en riesgo de enfermedad sistémica puede agregarse
fluconazol (100-400 mg/24 h) o como alternativa itraconazol (100-200 mg/24 h), en ciclos de 14 días.
4. Entidades específicas más frecuentes causantes de faringoamigdalitis aguda (Tabla XII)
5. Complicaciones de las faringoamigdalitis agudas
5.1. Supurativas
Pueden aparecer en un 1-2% de las FAA bacterianas sin tratamiento o con un antibiótico
inadecuado o mal cumplimiento. Se han descrito por S. pyogenes, pero existe una participación creciente
de otros microorganismos (Fusobacterium spp, S. anginosus, etc.).
Destacan: flemón y absceso periamigdalino, absceso parafaríngeo y retrofaríngeo, otitis media,
sinusitis y adenitis.
Menos frecuentes son las infecciones invasivas con alta morbimortalidad: tromboflebitis de la
vena yugular interna (síndrome de Lemierre), fascitis necrotizante, bacteriemia, abscesos
metastásicos por diseminación hemática o meningitis.
5.1.1. Flemón y absceso periamigdalino
Etiopatogenia: 1.ª fase (flemón): inflamación/edema del velo y pilares amigdalinos; 2.ª fase
(absceso): colección purulenta entre la amígdala y su cápsula, habitualmente polo superior.
Agentes: flora mixta. Frecuente S. pyogenes, S. aureus y anaerobios.
Signos y síntomas: odinofagia intensa, fiebre elevada, pese a tratamiento adecuado. Mala
tolerancia oral. Trismus, abombamiento asimétrico del pilar amigdalino anterior y
desplazamiento contralateral de la úvula. Amígdalas con o sin exudados. Adenopatías
inflamatorias de predominio ipsilateral.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [235]
[17] PATOLOGÍA OTORRINOLARINGOLÓGICA. MANEJO DE TRAQUEOTOMÍAS
Realizar exploración laríngea para descartar la progresión de planos profundos (extensión
parafaríngea); si se confirma la existencia de empastamiento cervical o es sugestiva, habrá que
realizar prueba de imagen (TC).
Tratamiento: punción pilar (negativa: flemón). Si es positiva practicar un drenaje quirúrgico.
Terapia antibiótica: amoxicilina/clavulánico 875/125 mg/8 h, 10 días o clindamicina 300 mg/6 h,
10 días. Los corticoides resultan útiles para el control de la inflamación y el trismus.
5.2. No supurativas: tras episodios de FAA causados por S. pyogenes, poco frecuentes. Son:
escarlatina, síndrome del shock tóxico estreptocócico, PANDAS y, destacando por su importancia, la
glomerulonefritis aguda y la fiebre reumática (que se mantiene como la principal causa de enfermedad
cardiaca adquirida en niños de países en desarrollo).
Tabla XII.Entidades FFA específicas más frecuentes
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [236]
[17] PATOLOGÍA OTORRINOLARINGOLÓGICA. MANEJO DE TRAQUEOTOMÍAS
Laringología
IX. PATOLOGÍA INFECCIOSA/INFLAMATORIA. LARINGITIS
1. Agudas
1.1. Infecciosas: virales (las más frecuentes, habitualmente en el contexto de cuadro catarral;
herpéticas en inmunodeprimidos), bacterianas (primarias o más común por sobreinfección de las víricas),
fúngicas (sospechar en inmunodeprimidos, tras antibioterapia de amplio espectro y corticoterapia
inhalada), granulomatosas (por tuberculosis o sífilis) (ver Tabla XIII).
Tabla XIII.Laringitis agudas más comunes
1.2. No infecciosas: fonotrauma, inhalatorias, térmicas, reflujo gastroesofágico, cáusticas, alérgicas,
medicamentosas y autoinmunes.
2. Crónicas
Laringitis de duración mayor de tres semanas. El síntoma fundamental suele ser disfonía y
sensación de cuerpo extraño; la exploración suele ser inespecífica, afectándose principalmente las cuerdas
vocales. Se han descrito múltiples agentes causales: tabaco, alcohol, reflujo gastroesofágico, insuficiencia
respiratoria nasal, mal uso vocal, inhalación de irritantes, enfermedades sistémicas (amiloidosis y
sarcoidosis) y agentes infecciosos. Su principal diagnóstico diferencial serán las neoplasias laríngeas,
especialmente en fumadores y bebedores importantes.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [237]
[17] PATOLOGÍA OTORRINOLARINGOLÓGICA. MANEJO DE TRAQUEOTOMÍAS
Tratamiento: dirigido a la causa y sintomático (hidratación abundante, humidificadores,
nebulizados, evitar irritantes –cigarrillo–, reposo vocal relativo, analgesia, antiinflamatorios no
esteroideos y antitusígenos).
X. MANEJO DE TRAQUEOTOMÍAS
1. CONCEPTO
El término “traqueotomía” hace referencia a la creación de una apertura en la pared anterior de la
tráquea. Sin embargo, traqueostomía implicaría además abocar el estoma traqueal a la piel cervical
anterior creando una fístula permanente con el exterior. Actualmente se emplean en la práctica médica
diaria como sinónimos.
2. EVALUACIÓN DEL PACIENTE
Existirán dos grandes grupos de pacientes subsidiarios de traqueotomía. El primero incluirá
aquellos casos evaluados de forma urgente, en los que asegurar la vía aérea constituye el aspecto
prioritario. La exploración física dirigida debe incluir la valoración cervicofacial y laríngea (mediante
laringoscopia directa, indirecta y/o nasofibroscopia). Existen una serie de signos y síntomas que sugerirán
obstrucción de la vía aérea superior (Tabla XIV).
Tabla XIV.Signos y síntomas que sugieren obstrucción de la vía aérea superior
En segundo lugar se encontrarán los pacientes en los que la evaluación de la vía aérea no
constituye una urgencia y, por lo tanto, han de ser valorados mediante la realización de una historia clínica
completa con una anamnesis enfocada a descartar traumatismos maxilofaciales/cervicales, intubaciones
previas, antecedentes oncológicos y alteraciones en la voz o en la deglución. Por otro lado, será de gran
importancia la exploración de la vía aérea superior que incluya una evaluación laríngea mediante
laringoscopia indirecta o rinofibrolaringoscopia/ broncoscopia. Adicionalmente se pueden necesitar
pruebas de imagen.
3. INDICACIONES
Cuando sea posible los pacientes con obstrucción de la vía aérea superior deben ser inicialmente
manejados con intubación traqueal. Las principales indicaciones para la realización de una traqueotomía se
resumen en la tabla XV.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [238]
[17] PATOLOGÍA OTORRINOLARINGOLÓGICA. MANEJO DE TRAQUEOTOMÍAS
Tabla XV.Indicaciones de traqueotomía
4. TIPOS DE PROCEDIMIENTOS
1. Cricotiroidotomía o coniotomía
Es la técnica de elección de urgencia, por la mayor facilidad y rapidez respecto a la traqueotomía.
Usualmente se lleva a cabo en la cama del paciente. Se puede realizar de forma percutánea o efectuando
una incisión en la piel para crear una apertura en la membrana cricotiroidea a través de la cual se insertará
un dilatador que permite la colocación de una cánula o tubo endotraqueal.
La cricotiroidotomía es especialmente útil en pacientes con traumatismo facial/cervical severo con
inmovilización cervical, o en presencia de masas cervicales que obstruyan la tráquea (por ejemplo bocio).
Son contraindicaciones relativas de esta técnica la dificultad para identificar las referencias anatómicas (por
ejemplo obesidad), infección, traumatismo o tumor laríngeo y edad menor de 5 años.
La tasa de complicaciones puede llegar hasta el 40%. Comparte con la traqueotomía la posibilidad
de hemorragia, imposibilidad de colocación del tubo y daño de los recurrentes, entre otras. Se debe tener
en cuenta la aparición tardía de estenosis subglótica, que ocurrirá hasta en la mitad de los pacientes. Por lo
tanto, este procedimiento debería ser convertido a traqueotomía reglada de manera precoz.
2. Traqueotomía abierta
2.1. De urgencia
Generalmente se realiza también a pie de cama y es una opción viable cuando existe alguna
contraindicación para realizar una cricotiroidotomía, o como alternativa a ella cuando se dispone de
personal entrenado. En este caso se prefiere la incisión vertical cutánea por el menor riesgo de daño de
estructuras vasculares; aun así, la tasa de complicaciones es 5 veces mayor que en los procedimientos
reglados.
2.2. Reglada
Se puede realizar en quirófano o en la unidad de cuidados intensivos, bajo anestesia general o local.
Para mejorar la exposición, el cuello debe ser hiperextendido. Tras la incisión horizontal cutánea se procede
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [239]
[17] PATOLOGÍA OTORRINOLARINGOLÓGICA. MANEJO DE TRAQUEOTOMÍAS
a la disección por planos vertical, sección o movilización del istmo tiroideo en línea media y apertura
preferentemente del 2.º-3.º anillo traqueal (la elección del nivel en pacientes con tumores laríngeos ha de
individualizarse previniendo el riesgo de carcinomatosis del estoma). Usualmente se empleará un punto de
fijación cutáneo-traqueal (borde inferior de la herida) para estabilizar, facilitar los cambios de cánula y
evitar la formación de falsas vías o el colapso del estoma.
Son casos especiales los pacientes sometidos a una laringuectomía total, en los que la
traqueotomía constituye un procedimiento permanente al separar de manera definitiva la vía aérea de la
digestiva.
3. Traqueotomía percutánea por dilatación
Consiste en la introducción transcervical de una guía hasta la luz traqueal, al nivel del segundo o
tercer anillo, insertando un dilatador que produce una disección roma y progresiva del trayecto hasta
permitir la colocación de la cánula según la técnica de Seldinger modificada. Es una alternativa a la técnica
abierta, empleada preferentemente en áreas de cuidados intensivos por el beneficio logístico al evitar la
movilización del paciente.
Las contraindicaciones absolutas de esta técnica son la presencia de masas cervicales, alteraciones
en la coagulación y traumatismos cervicales. Son malos candidatos pacientes obesos, con referencias
anatómicas pobres.
Es un procedimiento que no está exento de las complicaciones asociadas a todas las traqueotomías,
pero actualmente, la realización bajo control broncoscópico está disminuyendo su incidencia.
5. CUIDADOS Y MANEJO DE LA TRAQUEOTOMÍA
1. Cuidados postoperatorios
Tras el procedimiento el paciente debe ser colocado en posición de semi-Fowler (cabecero a 30º y
rodillas flexionadas a 30º); esta posición facilita la tos, las respiraciones profundas y las aspiraciones
traqueales.
Hasta la cicatrización del estoma se puede emplear suero fisiológico y antisépticos no alcohólicos
para la limpieza; posteriormente será suficiente con agua y jabón, pero siempre habrá que tener
precaución para no instilar cualquiera de ellos a la luz traqueal.
En cuanto a la aspiración de secreciones inicialmente deben ser más frecuentes (de tres a cuatro
veces/día) y luego a demanda según la necesidad y la patología del paciente. Ha de tenerse la precaución
de no realizar aspiraciones bruscas para evitar daños en las paredes traqueales o en la carina con la sonda.
El paso de aire directamente por la tráquea elimina la humidificación, facilitando la formación de tapones
mucosos, por lo tanto, de forma preventiva se pueden usar nebulizados con mascarillas traqueales o
humidificadores ambientales.
2. Tipos de cánulas
La elección de la cánula ha de adecuarse a las características del paciente y su patología. Podemos
clasificarlas según los siguientes parámetros:
Tipo de material:
Metálicas: de plata o acero; se emplean en pacientes estables, pues no poseen balón
de neumotaponamiento ni conector para ventilación mecánica.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [240]
[17] PATOLOGÍA OTORRINOLARINGOLÓGICA. MANEJO DE TRAQUEOTOMÍAS
Plásticas: de silicona (por ejemplo bivonas) o de polivinilo (por ejemplo pórtex). A
diferencia de las anteriores sí tienen conector y pueden, o no, tener balón.
Cánula simple/doble: las cánulas dobles (pieza externa/hembra e interna/macho) mejoran la
seguridad en caso de tapón mucoso, brindando la posibilidad de extracción y limpieza de la
cánula interna sin necesidad de extraer la externa. Existe una tercera pieza, el fiador, que se
empleará dentro de la hembra durante los cambios de cánula para facilitarlos.
Tamaño: una elección adecuada es de especial importancia para evitar decanulaciones
accidentales y erosiones traqueales.
Diámetro: se refiere a la medida en milímetros de la sección interna de la cánula (ID).
Habitualmente se emplea en hombres un 7,5-8 y en mujeres 6,5-7 (la correspondencia
en cánulas de plata suele ser dos números inferior).
Longitud: existen tamaños genéricos (cortos/largos) y dentro de las plásticas la
variedad será mayor, con cánulas de diferentes medidas en su porción horizontal y
vertical y otras de longitud regulable para adaptarse mejor a las características
anatómicas de cada caso.
Balón de neumotaponamiento: al insuflarlo permite evitar el paso de secreciones al árbol
traqueobronquial y ejercer presiones positivas pulmonares durante la ventilación mecánica. Es
importante no superar los 25-30 mm Hg al insuflar el balón para evitar la estenosis traqueal
tardía.
Fenestras: son pequeños orificios en el domo de la cánula que permiten, al ocluir el extremo
proximal, el flujo aéreo a través de la glotis y por lo tanto la fonación. Pueden ser de plástico o
metálicas.
Succión subglótica: esta posibilidad está presente en cánulas plásticas con balón de
neumotaponamiento como medida higiénica adicional y para evitar el paso de secreciones al
árbol traqueobronquial.
3. Cambios de cánula
Para el primer cambio completo se requiere personal entrenado y condiciones
óptimas/controladas: adecuada posición del paciente, asistencia, un repuesto de la cánula con el fiador
lubricado, aspiración y pinza tres ramas o rinoscopio largo que permitan fijar el estoma. Debe realizarse
rápida y cuidadosamente para evitar complicaciones. Se lleva a cabo usualmente entre los tres a cinco días
en traqueotomías abiertas, mientras que en percutáneas se recomienda al menos mantener 7-10 días.
Posteriormente, no suelen ser necesarios los cambios completos diarios (especialmente cuando los
estomas no son estables), siendo suficiente el recambio y limpieza de la camisa.
6. COMPLICACIONES
1. Tempranas
Obstrucción de la cánula: es la complicación más frecuente y usualmente se debe a un tapón
mucoso. Se manifiesta con respiración ruidosa, dificultad para la aspiración y taquipnea. Se
maneja retirando la cánula interna e intentando aspirar; si esto fallara, retirar la pieza en su
totalidad. Se previene con humidificación adecuada, aspiraciones y cambios de cánula interna
frecuentes.
Decanulación accidental-desplazamiento de la cánula: potencialmente fatal, especialmente
cuando los estomas son inestables. Se debe sospechar cuando el paciente presenta distrés
respiratorio o repentinamente puede hablar. Se debe recolocar la cánula; si no se consigue y el
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [241]
[17] PATOLOGÍA OTORRINOLARINGOLÓGICA. MANEJO DE TRAQUEOTOMÍAS
paciente no lo tolera es preferible intentar una intubación orotraqueal para estabilizar la vía
aérea y posteriormente recanalizar el estoma.
Hemorragia: habitualmente suelen ser autolimitadas y de escasa cuantía. Se debe identificar el
origen, siendo lo más frecuente aspiraciones traumáticas, granulomas estomales o
intratraqueales. Cuando provienen de la herida quirúrgica pueden llegar a requerir revisión en
quirófano.
Infección de herida: generalmente se trata de celulitis local y debe ser manejada con higiene
adecuada y antibióticos tópicos o sistémicos.
Enfisema subcutáneo: favorecido por el uso de cánulas sin balón de neumotaponamiento,
suturas traqueales muy ajustadas, tos y obstrucción de la cánula. El signo clave es la presencia
de crepitación cervical, facial o en tercio superior torácico. Se trata de manera conservadora,
con actitud expectante, intentando identificar y corregir la causa.
2. Tardías
Granulomas periestomales o intratraqueales: son manejados dependiendo de su localización
con cauterización, resección quirúrgica o láser.
Disfagia y aspiración: producido por la alteración de reflejos, sensibilidad y fijación de
estructuras durante la deglución. Ocurre especialmente cuando se usa balón de
neumotaponamiento. Las medidas profilácticas incluyen dieta blanda y posición adecuada
durante la ingesta.
Fístula traqueoesofágica: confirmada mediante estudios de tránsito esofágico con contraste
hidrosoluble o visión directa. El tratamiento es quirúrgico.
Ruptura/fístula de la arteria innominada: potencialmente mortal, pero baja incidencia. Se
sospecha por sangrado masivo a través del traqueostoma y con latido de la cánula. Su
tratamiento es quirúrgico urgente.
Estenosis traqueal y traqueomalacia: lo más habitual es que sucedan por el uso de balones de
neumotaponamiento prolongado con presiones de insuflación excesivas, por lo que se
recomienda no superar los 25-30 mm Hg.
Fístula traqueocutánea: ocurre después de la decanulación cuando falla el cierre secundario
del estoma. Se trata con cierre quirúrgico directo o colgajos locales.
Disfonía: se produce habitualmente por hipotonía de las cuerdas vocales por falta de uso. Se
puede resolver cuando el caso lo permita, con la colocación de cánulas fenestradas que
posibilitan la fonación controlada por el paciente.
7. DECANULACIÓN
Una vez resuelta la causa que motivó la traqueotomía, muchos pacientes pueden ser decanulados.
Para plantearlo el requisito principal es comprobar la tolerancia del paciente al cierre del estoma. Esto se
llevará a cabo ocluyendo la cánula con un tapón (contraindicación absoluta en cánulas con balón inflado),
inicialmente en periodos cortos, aumentando el empleo de manera progresiva hasta conseguir un uso
ininterrumpido. Ha de transcurrir un tiempo superior a las 24 horas para la decanulación; esto permite
corroborar que el paciente es capaz de mantener un flujo aéreo naso/orofaríngeo suficiente, deglución
competente y que posee un manejo de secreciones adecuado.
Con la laringoscopia y la fibroscopia a través del estoma se comprueba que el espacio glótico es
suficiente y la ausencia de patología traqueal (valorable hasta la carina) que contraindiquen la
decanulación.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [242]
[17] PATOLOGÍA OTORRINOLARINGOLÓGICA. MANEJO DE TRAQUEOTOMÍAS
El cierre del estoma se lleva a cabo habitualmente por segunda intención, retirando la cánula,
aproximando los bordes cutáneos y realizando una cobertura con gasas y apósitos óptima. Se indicará al
paciente aplicar presión sobre los apósitos al hablar o toser, para reducir el flujo de aire a través del
estoma.
En una media de 7 días la mayoría consigue un cierre total, pero si persistieran poros se podría
plantear un cierre quirúrgico bajo anestesia local o general.
BIBLIOGRAFÍA
Bailey’s Head and Neck Surgery: Otolaryngology. 5th ed. Philadelphia: Lippincott Williams & Wilkins;
2014.
Ballenger’s Otorhinolaryngology Head and Neck Surgery. Shelton, Connecticut: People’s Medical
Publishing House; 2009.
Cummings otolaryngology–head & neck surgery. 6th ed. Philadelphia: Saunders; 2015.
Chan Y, Goddard JC. KJ Lee’s Essential Otolaryngology; Head and Neck Surgery. 11th edition. McGraw-
Hill Education; 2016
McGrath B. National Tracheostomy Safety Project Manual [Internet]. Manchester; 2013. Disponible en:
www. tracheostomy.org.uk
Sahoo, GC. Emergencies in Otorhinolaryngology. 1st ed. New Delhi: Jaypee Brothers Medical Publishers
(P) Ltd; 2014.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [243]
[18] PATOLOGÍAS DERMATOLÓGICAS: EXANTEMAS. URTICARIA Y ANGIODEMAS
18.Patologías dermatológicas: Exantemas. Urticaria y
angiodemas
Ana María Delgado Márquez.
Dermatología
José A. Bastidas Parlanti.
Alergología
Asesores:
Francisco Javier Ortiz de Frutos.
Adjunto de Dermatología
Pilar de Lys Herráez Herrera.
Adjunta de Alergología
I. EXANTEMAS
1. CONCEPTO Y ETIOLOGÍA
Exantema se define como una erupción cutánea eritematosa y difusa, de extensión y distribución
variables, debida a los efectos sistémicos de una noxa sobre la piel. Los términos erupción y rash son
sinónimos de exantema. Se denomina enantema a la erupción de etiología similar que afecta a las
membranas mucosas.
Muchas de estas afecciones aparecen de forma súbita, en ocasiones acompañadas de fiebre y
sintomatología general, por lo que, pese a que muchas de ellas no son urgencias médicas propiamente
dichas, es frecuente encontrarse a pacientes con exantemas en las urgencias hospitalarias.
Ante cualquier exantema es fundamental:
Determinar su posible gravedad (compromiso hemodinámico, destrucción de la barrera
cutánea, síntomas o signos que sugieran disfunción orgánica).
Determinar si el exantema es de causa infecciosa o medicamentosa (las dos etiologías más
frecuentes). En el primer caso, se ha de valorar la necesidad de aislamiento en caso de suponer
riesgo para otros pacientes (sospecha de sarampión, varicela, etc.), y en el segundo, valorar la
interrupción de cualquier fármaco que haya podido desencadenar el cuadro clínico.
Instaurar un tratamiento específico urgente en caso de lograr filiar correctamente la etiología
(sepsis meningocócica, rickettsiosis, necrólisis epidérmica tóxica).
Debido a la multitud de etiologías posibles, y por tratarse de patologías cuya clínica varía en el
tiempo, su diagnóstico específico es complejo, por lo que en la mayoría de los casos lo más importante será
determinar la existencia o no de criterios de gravedad (Figura 1).
A continuación, se ofrece una pauta general de orientación diagnóstica y terapéutica del paciente
con exantema, incidiendo de forma específica en aquellos que más frecuentemente son motivo de atención
urgente.
2. APROXIMACIÓN DIAGNÓSTICA
1. Anamnesis
Se ha de recoger: edad; antecedentes y estado inmunológico; exposición a fármacos, tanto de uso
habitual como de utilización ocasional y/o reciente; antecedente de exposición a alérgenos, animales,
contacto con enfermos, viajes y/o vacunas; prácticas sexuales de riesgo (si se sospecha infección de
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [244]
[18] PATOLOGÍAS DERMATOLÓGICAS: EXANTEMAS. URTICARIA Y ANGIODEMAS
transmisión sexual); pródromos; orden de aparición de los síntomas y su duración; tiempo y forma de
aparición del exantema, así como sus características y evolución; asociación de enantema, y síntomas
asociados.
Figura 1.Esquema del manejo de los exantemas medicamentosos en Urgencias.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [245]
[18] PATOLOGÍAS DERMATOLÓGICAS: EXANTEMAS. URTICARIA Y ANGIODEMAS
2. Exploración física
Exploración general: aspecto general del individuo, constantes vitales, afectación de mucosas
(como criterio de gravedad), datos de afectación de otros sistemas (signos respiratorios y
cardiacos, visceromegalias, presencia de edema, dolor articular, signos neurológicos y
adenopatías).
Exploración dermatológica: con identificación del tipo de lesión elemental (las más frecuentes
se resumen en la tabla I), la distribución (localizado o generalizado, afectación de mucosas y/o
palmas y plantas) y la forma de inicio y progresión (centrípeto, centrífugo, céfalo-caudal,
generalizado o de predominio en los pliegues).
Tabla I.Lesiones cutáneas elementales.
Tras realizar la anamnesis y la exploración física se debe intentar diagnosticar el exantema en
función del aspecto de la erupción y las lesiones elementales que la conforman, aunque dicha clasificación
es controvertida y varía según los autores, muchas veces es necesario esperar a la evolución clínica y a
tener el resultado de determinadas pruebas complementarias para lograr un correcto diagnóstico
definitivo. Los tipos más frecuentes de erupciones cutáneas y etiologías probables se muestran en tabla II.
3. Pruebas complementarias
Aunque realizar una adecuada anamnesis y una completa exploración física son los aspectos más
importantes en la aproximación diagnóstica de un exantema, en ocasiones nos podemos ayudar de pruebas
complementarias.
Se recomienda solicitar una analítica de sangre en todos los exantemas medicamentosos para
valorar los criterios de gravedad.
En el caso de exantemas de etiología infecciosa, en ocasiones una toma de muestra de las lesiones
puede conducir al diagnóstico definitivo (por ejemplo, un cultivo de vesículas en un paciente puede
confirmar que el agente etiológico sea un tipo determinado de virus herpes, o el cultivo de una pústula
determinar qué tipo de bacteria está implicada en la lesión).
La realización de una biopsia podría plantearse ante dudas diagnósticas.
3. DIAGNÓSTICO ETIOLÓGICO Y MANEJO TERAPÉUTICO DE ENTIDADES ESPECÍFICAS
1. Exantemas víricos
Los virus son la causa más frecuente de exantemas en la infancia. Los exantemas víricos se pueden
presentar como máculo-papulosos o vesículo-ampollosos. Generalmente indican primoinfección, y pueden
acompañarse o no de síntomas generales. Las lesiones en las mucosas son frecuentes. En los adultos, la
mayor parte de ellos son inespecíficos pero, debido al carácter benigno y autolimitado, generalmente no es
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [246]
[18] PATOLOGÍAS DERMATOLÓGICAS: EXANTEMAS. URTICARIA Y ANGIODEMAS
necesario conocer el agente etiológico, salvo en situaciones como embarazo o inmunosupresión, en cuyo
caso se puede realizar cultivo vírico de algunas lesiones (vesículas, pústulas) y determinación de serologías
de los virus exantemáticos más frecuentes. Dentro de este grupo, por su frecuencia y fácil diagnóstico se
comentarán las infecciones causadas por los virus herpes.
Tabla II.Clasificación del exantema según lesión elemental y localización.
1.1. Infección por virus herpes simple tipo 1 (VHS-1)
La primoinfección cursa con gingivoestomatitis y faringitis con formación de numerosas vesículas y
aftas. Es más frecuente en niños menores de 5 años. El estado general puede encontrarse afectado, asocia
fiebre, decaimiento, y pueden existir adenopatías regionales.
La reactivación es la forma que más frecuentemente se observa en Urgencias, y se manifiesta como
múltiples vesículas con tendencia a la agrupación sobre una base eritematosa y que posteriormente se
erosionan formando costras. Es posible encontrar afectación del estado general, aunque es más raro. La
reactivación del VHS-1 puede ser el factor desencadenante del eritema exudativo multiforme (véase más
adelante).
En pacientes con dermatosis extensas (por ejemplo, dermatitis atópica) es posible observar la
diseminación de las lesiones, denominándose en este caso erupción variceliforme de Kaposi o eccema
herpeticum. En estos casos se forman erosiones y úlceras que se extienden a gran parte de la superficie
corporal, que supone una situación grave para el paciente.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [247]
[18] PATOLOGÍAS DERMATOLÓGICAS: EXANTEMAS. URTICARIA Y ANGIODEMAS
El diagnóstico es clínico, aunque se puede realizar cultivo vírico como confirmación.
El tratamiento de las lesiones cutáneas consiste en el empleo de fomentos con sustancias
antisépticas y astringentes (por ejemplo, sulfato de zinc diluido al 1/1.000). El empleo de antivíricos orales
se reserva para las formas graves, herpes diseminado o en la primoinfección (por ejemplo, valaciclovir 500
mg/12 h durante 7-10 días). Su utilidad es dudosa pasadas las primeras 48 horas. No se recomienda el uso
de antivíricos tópicos, ya que su utilidad ha sido cuestionada en numerosos estudios.
1.2. Infección por virus de la varicela zóster: varicela y herpes zóster
La primoinfección por virus de la varicela zóster (VVZ) ocasiona la varicela. Su máxima incidencia es
al final del invierno e inicios de la primavera. Es muy contagiosa. El 90% de los casos ocurren antes de los 14
años.
El exantema se compone inicialmente de máculas de intenso color rojo de menos de 0,3 mm de
diámetro, que en 24 horas se convierten en pápulas y vesículas de paredes finas, en número variable. En 2-
3 días aparecen costras, que no dejarán cicatriz salvo en caso de sobreinfección. Dicho exantema es
centrífugo, se inicia en la cabeza y progresa rápidamente en brotes, lo que hace posible observar lesiones
en diferentes estadios evolutivos (imagen en cielo estrellado).
En adultos, la infección es más grave. Puede existir afectación de mucosas, especialmente de la
mucosa oral, y raramente aparece fiebre.
El principal problema son las complicaciones: sobreinfección bacteriana de las lesiones (impétigo,
celulitis), neumonía (varicelosa o bien por sobreinfección bacteriana), hepatitis, alteraciones en la
coagulación (púrpura necrótica) y/o afectación del sistema nervioso (ataxia aguda, encefalitis, síndrome de
Guillain-Barré).
Tabla III.Indicaciones de tratamiento antivírico en infecciones por virus de la varicela zóster.
Tratamiento:
En primer lugar, recordar que la varicela es una enfermedad de declaración obligatoria.
Sintomático (tras descartar posibles complicaciones), utilizando antitérmicos y analgésicos y
mediante la aplicación de fomentos antisépticos (sulfato de zinc).
Agentes antivíricos: el tratamiento específico en principio solo está justificado cuando existen
posibilidades de que el cuadro clínico no se resuelva espontáneamente o de que progrese
(Tabla III).
Aciclovir:
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [248]
[18] PATOLOGÍAS DERMATOLÓGICAS: EXANTEMAS. URTICARIA Y ANGIODEMAS
En pacientes inmunocompetentes: 800 mg por vía oral 5 veces al día. En los primeros
días pueden reducir la gravedad de la enfermedad.
En pacientes inmunodeprimidos o tratados con corticoides (más de 40 g semana
durante más de una semana): 5 mg/kg/8 h por vía intravenosa.
Tras la varicela, el virus queda acantonado en los ganglios espinales sensitivos, donde establece una
infección latente. La reactivación (cuya etiología no está del todo clara: disminución de la inmunidad,
influencia de factores ambientales, etc.) ocasionará el herpes zóster.
El herpes zóster consiste en una erupción vesiculosa sobre un fondo eritematoedematoso,
siguiendo un trayecto metamérico. Como en la varicela, pueden coexistir lesiones en diferentes estadios
evolutivos. Suele asociar sensación de ardor, escozor e hiperalgesia en el territorio afectado, y puede dejar
como secuela, en aproximadamente la mitad de los pacientes, una neuralgia residual de difícil tratamiento.
Las metámeras más frecuentemente afectadas son la rama oftálmica del trigémino (debe descartarse
afectación ocular, ya que puede provocar la pérdida de visión del ojo afectado, por lo que debe
considerarse siempre una emergencia oftalmológica; ver Capítulo 16. “Patología oftalmológica”) y las
metámeras de las raíces D2 a L2. La afectación del VII par craneal produce el síndrome de Ramsay-Hunt.
Tratamiento:
Los antivíricos orales aceleran la curación y reducen la intensidad de la neuritis, de modo que
están indicados en todos los pacientes mayores de 50 años o aquellos con lesiones extensas,
entre otros (Tabla III).
Aciclovir: seguir la misma pauta que en la varicela.
Valaciclovir: 1 g/8 h por vía oral durante 7 días.
Famciclovir: 750 mg al día vía por vía oral durante 7 días, o 250 mg/8 h por vía oral
durante 7 días.
Brivudina: 125 mg al día por vía oral durante 7 días. Está especialmente indicada si hay
afectación renal, y siempre con precaución de que no se estén administrando de forma
concomitante derivados del 5-fluorouracilo.
En pacientes inmunodeprimidos se usará la misma pauta que en caso de varicela. Dicho
tratamiento debe instaurarse lo antes posible (en las primeras 72 horas).
La aplicación de fomentos acelera la curación de las lesiones.
El empleo de analgesia es fundamental, debiendo individualizarse en cada paciente.
Inicialmente se pautará paracetamol 1 g/8 h; utilizar otros analgésicos (gabapentina 300 mg por
la noche, aumentando progresivamente hasta una dosis máxima de 1.800 mg/día fraccionados
en tres dosis por vía oral) o antidepresivos tricíclicos en caso de mal control del dolor.
2. Exantemas bacterianos
Los exantemas bacterianos son menos frecuentes que los de causa vírica, pero en ocasiones
afectan a pacientes inmunodeprimidos y pueden llegar a ser potencialmente mortales, por lo que es
necesario conocerlos. A continuación se describen los más importantes por su gravedad o por su
frecuencia.
2.1. Meningococemia
La púrpura se observa en casi el 90% de los pacientes con sepsis meningocócica. Las lesiones
inicialmente pueden simular un exantema vírico inespecífico (máculas o pápulas eritematosas que
blanquean a la presión) para después hacerse petequiales, irregulares y pequeñas. No se aprecia necrosis.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [249]
[18] PATOLOGÍAS DERMATOLÓGICAS: EXANTEMAS. URTICARIA Y ANGIODEMAS
Afecta al tronco y a las extremidades y, más raramente, zonas acras, cabeza y mucosas. El estado general
está gravemente afectado, con fiebre alta de aparición brusca. La mortalidad es elevada.
2.2. Ectima gangrenoso
Se trata de una gangrena cutánea secundaria a una sepsis bacteriana, generalmente causada por
Pseudomonas aeruginosa. Afecta a pacientes inmunocomprometidos.
En cuanto a la clínica, aparte de la sepsis, consiste en un exantema que aparece de forma brusca
como placas purpúricas de bordes rosados, que crecen rápidamente en extensión y profundidad, dando
lugar a ampollas sanguinolentas y posterior formación de escaras necróticas. Pueden existir lesiones en
diferentes estadios evolutivos, semejando en ocasiones un eritema multiforme, aunque es frecuente la
localización en el periné; respeta las palmas y las plantas.
El diagnóstico específico requiere hemocultivos y cultivo de las flictenas.
El tratamiento consistirá en la cobertura antibiótica adecuada.
2.3. Síndrome de la piel escaldada
Está causado por una exotoxina estafilocócica epidermolítica. En adultos es rara, salvo en la
insuficiencia renal o inmunodepresión.
Por lo que se refiere a la clínica, tras una infección estafilocócica, se presenta de forma súbita con
fiebre y decaimiento. Aparecen máculas de aspecto escarlatiniforme, dolorosas a la palpación y que afectan
a pliegues y zonas periorificiales, sin afectación de mucosas (lo que lo diferencia del síndrome de Stevens-
Johnson y de la necrólisis epidérmica tóxica [NET]). Las lesiones se extienden por toda la superficie
corporal. Las ampollas aparecen en horas y existe signo de Nikolsky (al ejercer una suave presión o roce
sobre la piel sana o eritematosa, pero sin otras lesiones asociadas, se produce un despegamiento de la
misma, dejando una zona erosionada y exudativa; es característico de la NET y del pénfigo vulgar).
Posteriormente, aparece fisurización y descamación laminar extensa. La recuperación sin secuelas se
produce en unas 2 semanas, debiendo vigilarse la sobreinfección y la pérdida de líquidos.
El tratamiento consiste en el empleo de antibióticos antiestafilocócicos en las pautas habituales.
En la fase exudativa (erosiones) se pueden emplear fomentos astringentes como el sulfato de
zinc.
En la fase seca (lesiones residuales, escamocostrosas) se recomienda el empleo de emolientes
como el aceite de vaselina.
Los corticoides, tanto tópicos como orales, no son eficaces.
2.4. Síndrome del shock tóxico
Causado por exotoxinas del Streptococcus pyogenes y del estafilococo. Se inicia con fiebre, mialgias
y alteración del estado general. La afectación multiorgánica y el shock ocurren de forma precoz. El
exantema se inicia en los pliegues y da lugar a una eritrodermia (que semeja una quemadura solar). Suele
respetar la cara, pero afecta a las palmas y las plantas. No existe signo de Nikolsky. El diagnóstico es clínico.
El tratamiento requiere medidas de soporte hemodinámico y antibioterapia empírica precoz (que cubra
tanto estafilococos como estreptococos).
2.5. Roséola sifilítica
La sífilis puede presentar gran variedad de lesiones cutáneas, algunas de muy corta duración. La
roséola sifilítica aparece a los 3 meses del contagio (sífilis secundaria). Es un exantema maculoso, con
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [250]
[18] PATOLOGÍAS DERMATOLÓGICAS: EXANTEMAS. URTICARIA Y ANGIODEMAS
lesiones redondeadas u ovaladas de color asalmonado y localizado en el tórax, abdomen y brazos, con
disposición más o menos simétrica. Puede dejar hipopigmentación residual (collar de Venus). También
pueden aparecer lesiones papulosas, de color rojo oscuro y con un collarete descamativo periférico. Son
más abundantes en el tronco y las raíces de los miembros, la zona anogenital, las palmas, las plantas y la
cara (ver Capítulo 40. “Infecciones de transmisión sexual”).
3. Exantemas medicamentosos o toxicodermias
Las manifestaciones cutáneas son la expresión más frecuente de las reacciones adversas a
fármacos. La mayoría no son graves. Entre los medicamentos más frecuentes destacan: antibióticos,
sulfonamidas, antiinflamatorios no esteroideos (AINE), paracetamol, anticonvulsivantes, alopurinol,
quimioterápicos, inhibidores de la enzima de conversión de la angiotensina (IECA), diuréticos, sin olvidar
productos de herbolario. En general, entre las formas más comunes de presentación cabe mencionar:
Exantema máculo-papuloso (exantema morbiliforme): suele aparecer de 1 a 3 semanas tras el
inicio de la toma del medicamento. Se puede acompañar de fiebre y la clínica es muy polimorfa.
El tratamiento consiste en suspender el fármaco causal. Puede evolucionar a formas graves e
incluso a eritrodermias, pero suelen resolverse con descamación y pigmentación residual.
Exantema fijo medicamentoso: aparece pocas horas después de iniciar la toma del
medicamento y suele ser una lesión única que deja posteriormente una pigmentación residual.
Si el paciente se vuelve a exponer al medicamento, se repite la lesión en la misma localización
Pustulosis exantemática generalizada aguda: es un exantema grave con múltiples pústulas
estériles.
Síndrome de hipersensibilidad medicamentosa ( síndrome DRESS, del inglés drug reaction
with eosinophilia and systemic symptoms): es una reacción grave con un 10% de mortalidad
asociada. Aparece entre 1 semana y 2 meses después de iniciar el fármaco, siendo el más
frecuente la carbamazepina. Suele ir asociado con fiebre y puede ir acompañado de hepatitis,
artralgias, adenopatías o alteraciones hematológicas. Puede evolucionar a una eritrodermia
exfoliativa o hacia formas ampollosas tipo NET. Las alteraciones orgánicas pueden persistir
meses tras la suspensión del fármaco.
En cuanto al manejo y tratamiento (Figura 1), en ocasiones es difícil identificar el medicamento
causante, y la suspensión de este suele ser el tratamiento definitivo.
Los corticoides tópicos pueden ayudar a la resolución de las lesiones cutáneas y el empleo de
emolientes disminuye la descamación y el prurito. En las formas eritrodérmicas o graves se pueden utilizar
corticoides orales.
Tabla IV.Signos de gravedad en exantemas medicamentosos.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [251]
[18] PATOLOGÍAS DERMATOLÓGICAS: EXANTEMAS. URTICARIA Y ANGIODEMAS
En todos los casos, lo importante es reconocer si existen criterios de gravedad (Tabla IV).
4. Eritema exudativo multiforme, síndrome de Stevens-Johnson y necrólisis epidérmica tóxica
El eritema exudativo multiforme se caracteriza por pápulas y placas eritematoedematosas en diana.
Es característica la afectación de las palmas, las plantas y las zonas de extensión articular. En ocasiones,
sobre dichas lesiones se forman vesículas y ampollas. Ante estas lesiones siempre hay que preguntar por
infecciones víricas (pueden aparecer días después o de forma concomitante a un herpes simple) y por los
fármacos que toma el paciente, ya que en ocasiones son de etiología medicamentosa.
El síndrome de Stevens-Johnson (SJS) y la necrólisis epidérmica tóxica (NET) son reacciones
mucocutáneas graves, con mortalidad del 5% y el 35%, respectivamente. Aparecen entre 1 y 3 semanas tras
iniciar la toma del medicamento. En el SJS hay afectación de al menos dos mucosas y un despegamiento de
hasta el 10% de la superficie corporal total. En la NET este porcentaje es >30%. Suelen ir precedidas de
pródromos (fiebre, astenia, anorexia, faringitis, fotofobia, etc.) y 1-2 semanas después aparecen lesiones
ampollosas flácidas, eritema y dolor asociado. El signo de Nikolsky es positivo. Asocian manifestaciones
sistémicas y la mortalidad se debe a complicaciones como sepsis, neumonía, o fallo multiorgánico.
Tratamiento y manejo:
Abordar la causa desencadenante, retirar la medicación relacionada y mantener un estrecho
control hidroelectrolítico. Estos pacientes deben ser tratados como grandes quemados.
Los fomentos antisépticos en piel y mucosas pueden ayudar a la recuperación.
El uso de antibióticos sistémicos se evitará si no hay sospecha de sobreinfección.
La analgesia, e incluso la sedación, pueden ser necesarias.
Prevención de la enfermedad tromboembólica venosa y del ulcus gástrico de estrés con IBP.
El uso de corticoides sistémicos no ha demostrado mejoría en la evolución de estos pacientes.
Otras opciones que se pueden plantear en casos graves son: gammaglobulina humana
intravenosa a dosis elevadas, ciclosporina, plasmaféresis o, incluso, fármacos biológicos.
5. Vasculitis leucocitoclástica o por hipersensibilidad
Las vasculitis pueden ser diagnosticadas por la clínica, y por ello se comentan en este capítulo,
aunque el diagnóstico definitivo siempre será el histológico. Se manifiesta como una púrpura palpable
generalmente en los miembros inferiores, aunque puede asociar lesiones urticariformes, ampollas
hemorrágicas e incluso úlceras y nódulos. Puede asociar fiebre, artritis y afectación de vasos no cutáneos
(neuritis, nefritis). Las causas pueden ser múltiples (fármacos, infecciones, enfermedades sistémicas, etc.).
Siempre hay que descartar afectación renal mediante una analítica de sangre y orina.
El tratamiento consiste en:
Supresión del agente causal y reposo con las piernas elevadas.
Corticoides orales a dosis de 0,5-1 mg/kg/día en ciclos cortos en los casos que presenten
factores de riesgo (alteraciones analíticas, lesiones que comprometan más allá de los miembros
inferiores, lesiones ulceradas o necróticas, afectación sistémica) o tendencia a la progresión.
II. URTICARIA Y ANGIOEDEMA
1. CONCEPTO
La urticaria consiste en una reacción cutánea de tipo vascular con desarrollo de edema en la
dermis, cuyo resultado son los habones. La lesión habonosa se caracteriza por la presencia de un edema
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [252]
[18] PATOLOGÍAS DERMATOLÓGICAS: EXANTEMAS. URTICARIA Y ANGIODEMAS
central o una pápula circunscrita de tamaño variable, casi siempre rodeada por un eritema reflejo
circundante con prurito y escozor asociados. Suelen ser evanescentes y de naturaleza transitoria, con una
duración de entre 1 y 24 horas, tras las cuales la piel vuelve a su apariencia normal. La urticaria puede ir
acompañada o no de angioedema.
El angioedema es un fenómeno similar en la dermis profunda y el tejido celular subcutáneo, con
desarrollo de tumefacción del tejido suprayacente, con afectación fundamentalmente de aquellas zonas
cutáneas más laxas, como labios o párpados. Se manifiesta sin prurito, con sensación de hormigueo, ardor
o dolor, y escaso o nulo eritema; es de resolución más lenta que la urticaria, ya que puede durar hasta 72h.
2. CLASIFICACIÓN (Tabla V)
En función de la duración:
Aguda: aquella que dura menos de 6 semanas, independientemente de su causa.
Crónica: lesiones habonosas recurrentes con una frecuencia mayor de dos veces por semana y
una duración de más de 6 semanas consecutivas.
En función de la existencia o no de factores físicos desencadenantes evidentes:
Espontánea
Inducible.
Tabla V.Clasificación de los distintos tipos de urticaria.
3. ETIOLOGÍA
La urticaria aguda es una enfermedad autolimitada y benigna, que puede llegar a desarrollarla
hasta un 20% de la población general. Las causas de urticaria aguda son varias, aunque en la mayoría de los
pacientes el motivo específico puede no identificarse. Las causas más comunes de urticaria son:
Infecciones, generalmente de origen vírico o bacteriano, sobre todo en niños.
Parásitos como resultado de la sensibilización al nematodo Anisakis simplex, parásito de ciertos
pescados y otras especies marinas.
Reacción alérgica a medicamentos, siendo los antibióticos, y en especial los del grupo de los
betalactámicos (penicilinas y cefalosporinas), los más frecuentemente implicados.
Reacciones alérgicas por ingesta o contacto con alimentos, principalmente leche, huevo, frutos
secos, frutas y pescados.
Por picadura de insectos: como orugas (por ejemplo, procesionaria del pino –Thaumetopoea
pityocampa–) e himenópteros (abejas, avispas, etc.).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [253]
[18] PATOLOGÍAS DERMATOLÓGICAS: EXANTEMAS. URTICARIA Y ANGIODEMAS
4. APROXIMACIÓN DIAGNÓSTICA
1. Historia clínica y exploración física
Es el método diagnóstico más útil. La historia clínica debe ser detallada y exhaustiva, con el fin de
confirmar la existencia de urticaria, más que por su origen. Se deben recoger los siguientes datos:
Características morfológicas de las lesiones: presencia de los típicos habones evanescentes de
menos de 24 horas de duración y/o desarrollo de angioedema.
Duración del proceso: debe indagarse si es un episodio aislado o si el paciente ha presentado
brotes recurrentes, su frecuencia y duración.
Síntomas sistémicos asociados: la presencia de artromialgias, fiebre o síndrome constitucional
(indicativos de una enfermedad subyacente).
Posibles desencadenantes: se identifican solo en el 20% de los casos. Debe investigarse la
exposición previa a fármacos, tanto esporádicos como habituales, alimentos, determinados
factores físicos (exposición solar, frío y/o ejercicio), picaduras de insectos, exposiciones por
contacto, como al látex, etc.
Viajes recientes a países tropicales.
Antecedentes personales de atopia, fármacos de consumo habitual (AINE, anticonceptivos,
vitaminas, laxantes, etc.) y enfermedades concomitantes.
Antecedentes familiares, particularmente en caso de angioedema aislado.
La exploración física debe ser meticulosa, evaluando el aspecto general y confirmando las lesiones
de urticaria o angioedema. Valorar la presencia de bocio o adenopatías. Se debe realizar auscultación
cardiopulmonar, medición de la tensión arterial y el pulso en busca del compromiso de otros aparatos y
sistemas que puedan sugerir una reacción anafiláctica, palpación abdominal buscando masas o
visceromegalias y una inspección completa de la piel para comprobar si existen otras lesiones como
urticaria pigmentosa, vasculitis o signos de dermatomiositis, sobre todo en caso de sospecha de una
urticaria crónica.
2. Pruebas complementarias
El diagnóstico etiológico de la urticaria, sobre todo en las urticarias crónicas, es complejo y poco
rentable, ya que no llega a identificarse la causa en más del 70% de los casos. En el caso de la urticaria
aguda, generalmente no se recomienda realizar pruebas diagnósticas de rutina. Cuando la historia clínica y
la exploración física son indicativas de alguna etiología en concreto, se realizará un estudio dirigido. En el
caso de la urticaria crónica o recurrente, el estudio inicial incluirá: hemograma con velocidad de
sedimentación globular (VSG), bioquímica básica, proteína C reactiva (PCR), análisis de orina y estudio de
factores de complemento en caso de angioedema aislado sin urticaria.
5. ABORDAJE TERAPÉUTICO (Figura 2)
El tratamiento inicial de la urticaria aguda con o sin angioedema, se debería enfocar en el alivio a
corto plazo del prurito, de los habones y del angioedema si está presente. Aproximadamente dos tercios de
los casos de urticaria aguda se resuelven espontáneamente.
Con respecto a la urticaria crónica, ha sido en los últimos años cuando se ha evaluado y establecido
por consenso un nuevo abordaje terapéutico, publicado recientemente en diferentes guías internacionales,
sin grandes variaciones entre ellas. Dicho abordaje se basa en la selección de determinados escalones
terapéuticos en función de la gravedad de la urticaria y su respuesta, cuyo objetivo principal es el control
total de los síntomas. Recientemente se ha aprobado un anticuerpo monoclonal, el omalizumab, como
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [254]
[18] PATOLOGÍAS DERMATOLÓGICAS: EXANTEMAS. URTICARIA Y ANGIODEMAS
tratamiento de elección en pacientes con urticaria crónica refractaria a antihistamínicos a dosis estándar,
con un excelente perfil de eficacia y seguridad en los ensayos clínicos realizados, en los que se ha obtenido
una remisión completa o casi completa en más de dos tercios de los pacientes evaluados.
Figura 2.Algoritmo del manejo de la urticaria.
1. Antihistamínicos
El tratamiento de la urticaria aguda se realiza con antihistamínicos, administrados por vía sistémica
en el Servicio de Urgencias y posteriormente, con el fin de evitar recidivas o cronificación, prescripción
domiciliaria de forma continua hasta que el paciente se encuentre al menos 7-10 días libre de síntomas.
La primera línea terapéutica de elección consiste en emplear antihistamínicos H1 (anti-H1) de
segunda generación no sedante, de forma regular y a dosis convencionales según ficha técnica (Tabla VI).
Tabla VI.Antihistamínicos de segunda generación.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [255]
[18] PATOLOGÍAS DERMATOLÓGICAS: EXANTEMAS. URTICARIA Y ANGIODEMAS
2. Corticoides sistémicos
Según recomendaciones recientes de los consensos internacionales, se aconseja su uso en ciclos
cortos y pautas descendentes: prednisona 0,5 mg/kg/día, aunque no está establecida una dosis
determinada.
En el caso de episodios agudos intensos o exacerbaciones graves de urticaria crónica
(especialmente cuando se acompaña de angioedema) y a la espera de que otros tratamientos controlen la
enfermedad, generalmente se indica prednisona 30-60 mg al día por vía oral durante 5-7 días y
posteriormente reducción progresiva de la dosis en un plazo de 10 días.
3. Adrenalina
A pesar de no ser un tratamiento indicado para la urticaria aguda, ante episodios de sospecha de
anafilaxia que podrían iniciarse con urticaria, estaría indicado su uso (Tablas VII y VIII).
La dosis (ampollas de dilución 1:1.000) es de 0,3-0,5 ml por vía intramuscular en la cara lateral
externa del muslo, que puede repetirse cada 5-15 minutos según sea necesario. La dosis máxima es 1,5 mg.
Tabla VII.Criterios diagnósticos de anafilaxia.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [256]
[18] PATOLOGÍAS DERMATOLÓGICAS: EXANTEMAS. URTICARIA Y ANGIODEMAS
Tabla VIII.Manejo y tratamiento de la anafilaxia.
III. ANGIOEDEMA HEREDITARIO Y ADQUIRIDO
1. CONCEPTO
El angioedema se define como un edema localizado en el tejido subcutáneo y/o submucoso debido
a un incremento temporal de la permeabilidad vascular causado por la liberación de mediadores
vasoactivos. El angioedema puede ir acompañado de urticaria en mecanismos de hipersensibilidad tipo I
(IgE mediado o angioedema histaminérgico); sin embargo, en este capítulo se tratarán el angioedema
hereditario y el adquirido.
2. CLASIFICACIÓN
Actualmente, el angioedema sin habones se divide en dos grandes grupos: angioedema hereditario
(AEH) y angioedema adquirido (AEA).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [257]
[18] PATOLOGÍAS DERMATOLÓGICAS: EXANTEMAS. URTICARIA Y ANGIODEMAS
1. Angioedema hereditario
Es una enfermedad rara autosómica dominante, por déficit del inhibidor de la C1 esterasa (C1-INH).
A su vez, se han descrito dos variedades: el tipo I (85%), con una disminución cuantitativa del C1-INH, lo
que genera una disminución de su actividad funcional, y el tipo II (15%), con niveles normales o elevados de
un C1-INH disfuncional. Recientemente se ha descrito el tipo III, en el que tanto los niveles del C1-INH como
su actividad son normales. Los primeros síntomas se pueden poner de manifiesto en cualquier momento de
la vida y, aunque la mitad de los pacientes suelen debutar en la primera década de la vida, un tercio lo
harán en la segunda década.
2. Angioedema adquirido
A su vez, este se divide en cuatro tipos:
AEA con déficit de C1-INH: se caracteriza por niveles bajos de C1-INH o no funcional, sin
evidencia de herencia. Se asocia fundamentalmente a enfermedades linfoproliferativas,
neoplásicas e infecciosas.
AEA relacionado con la toma de IECA, la cual es responsable de la degradación de la bradicinina
en plasma.
AEA idiopático histaminérgico.
AEA idiopático no histaminérgico.
3. MANIFESTACIONES CLÍNICAS
Se caracteriza por episodios o ataques recidivantes de edema submucoso o subcutáneo en
diferentes localizaciones, tanto a nivel cutáneo (cara, extremidades, tronco, genitales), como en las
mucosas del tracto gastrointestinal y de la vía respiratoria superior (orofaringe, laringe), pudiendo en
ocasiones llegar a comprometer la vida. Los episodios más frecuentes son los cutáneos periféricos y los
abdominales. Suelen ser autolimitados y revierten espontáneamente a las 48-72 horas de su inicio.
Los factores desencadenantes son:
Estrés emocional, ansiedad.
Traumatismos, con un elevado riesgo de desarrollo de angioedema laríngeo en todos los
procedimientos diagnósticos o terapéuticos que supongan un traumatismo de la vía
respiratoria superior (por ejemplo, manipulaciones odontológicas, intubación orotraqueal,
endoscopias, etc.).
Factores hormonales como los estrógenos (embarazo y pubertad) pueden incrementar la
actividad de la enfermedad.
Fármacos: los IECA puede producir un empeoramiento importante de la clínica por su efecto
potenciador de la bradicinina.
Procesos infecciosos, algunos pacientes refieren empeoramiento o aparición de ataques
relacionados.
En la mayoría de los casos no hay un claro factor precipitante.
4. DIAGNÓSTICO
1. Historia clínica y exploración física
Es importante diferenciar el tipo de angioedema según su fisiopatología (histaminérgico frente a
bradicinérgico), además de obtener datos sobre los antecedentes familiares en caso de AEH, edad de
presentación y posibles factores desencadenantes. Realizar un examen físico completo, incluyendo las
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [258]
[18] PATOLOGÍAS DERMATOLÓGICAS: EXANTEMAS. URTICARIA Y ANGIODEMAS
constantes vitales (saturación de oxígeno). En el examen de la vía área superior, extremar la exploración en
busca de edema de labios, lengua y úvula. Llevar a cabo una inspección completa de la piel buscando
urticaria, eritema marginatum u otros signos asociados.
2. Pruebas complementarias
En el caso de un episodio de ataque agudo de angioedema periférico, las pruebas diagnósticas no
están indicadas en la evaluación de rutina en los pacientes que acuden al Servicio de Urgencias.
Si existe afectación orgánica (gastrointestinal, aérea o anafilaxia) considerar la realización de:
hemograma con bioquímica básica, gasometría arterial, marcadores de activación mastocitaria con
medición de la triptasa a la hora y a las 4 horas después del inicio del episodio, electrocardiograma,
radiografía simple de abdomen, ecografía abdominal y/o tomografía computarizada según sea el caso.
5. TRATAMIENTO DEL ANGIOEDEMA EN EL SERVICIO DE URGENCIAS
Asegurar la vía área superior es la prioridad en los ataques agudos. Todos los casos con afectación
laríngea deben ser considerados una urgencia médica, y si hay signos de compromiso importante de la vía
aérea se debe valorar la intubación.
Es importante un abordaje terapéutico específico del ataque agudo del angioedema en el Servicio
de Urgencias (Figura 3 y Tabla IX).
Tabla IX.Fármacos disponibles para el tratamiento del angioedema hereditario por déficit del inhibidor de la C1 esterasa.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [259]
[18] PATOLOGÍAS DERMATOLÓGICAS: EXANTEMAS. URTICARIA Y ANGIODEMAS
Figura 3.Manejo del angioedema en Urgencias.
BIBLIOGRAFÍA
Caballero Molina T, Marcos Bravo C, Piñero Saavedra M, Sala Cunill A. Angioedema. En: Dávila
González I, Jáuregui Presa I, et al. Madrid: Ergon; 2016; p. 769-88.
Caballero T, Baeza ML, Cabañas R, Campos A, Cimbollek S, Gómez-Traseira C, et al. Consensus
statement on the diagnosis, management, and treatment of angioedema mediated by bradykinin. Part
II. Treatment, follow-up, and special situations. J Investig Allergol Clin Immunol. 2011;21(6):422-3.
Caballero T, Baeza ML, Cabañas R, Campos A, Cimbollek S, Gómez-Traseira C, et al. Consensus
statement on the diagnosis, management, and treatment of angioedema mediated by bradykinin. Part
I. Classification, epidemiology, pathophysiology, genetics, clinical symptoms, and diagnosis. J Investig
Allergol Clin Immunol. 2011;21(5):333-47.
Cicardi M, Aberer W, Banerji A, Bas M, Bernstein JA, Bork K, et al. Classification, diagnosis and
approach to treatment in angioedema: Consensus report from the Hereditary Angioedema International
Working Group. Allergy. 2014;69(5):602-16.
Ferner R. Adverse drug reactions in dermatology. Clin Exp Dermatol. 2015;40(2):105-9.
Ferrer Puga M, Veleiro Pérez B, Jáuregui Presa I. En: Dávila González I, Jáuregui Presa I, et al. Madrid:
Ergon; 2016; p. 751-68.
Goldsmith LA, Katz SI, Gilchrest BA, Paller AS, Leffel DJ, Wolff K. Fitzpatrick’s. Dermatology in general
medicine. 8ª ed. New York: McGraw-Hill; 2012.
Pedrosa M, Prieto-García A, Sala-Cunill. Management of angioedema without urticaria in the emergency
department. Ann Med. 2014;46(8):607-18.
Revuz J, Valeryne-Allanore L. Drug reactions. En: Bolognia JL, Jorizzo JL, Rapini RP. Dermatology. 3ª ed.
Elsevier; 2012; p. 335-56.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [260]
[19] PATOLOGÍA PSIQUIÁTRICA IMPORTANTE PARA EL MÉDICO GENERAL
19.Patología psiquiátrica importante para el médico
general
Manuel Nieves Carnicer.
Psiquiatría
Patricia Nava García.
Psiquiatría
Asesor:
Pedro Sanz Correcher.
Médico Adjunto de Psiquiatría
I. ANSIEDAD
1. CONCEPTO
La ansiedad es una reacción fisiológica ante una amenaza (interna o externa). Esta produce una
activación física y psíquica que nos prepara para responder al daño o sufrimiento que se anticipa.
La ansiedad patológica se produce cuando dicha reacción es inadecuada al contexto, supera cierta
intensidad o sobrepasa la capacidad adaptativa del individuo, interfiriendo en su funcionalidad.
Figura 1. Algoritmo diagnóstico: orientación inicial.
2. ANSIEDAD Y URGENCIAS
El papel del médico en urgencias ante un paciente con ansiedad queda resumido en tres
actuaciones fundamentales:
Descartar la presencia de patología orgánica que justifique el cuadro clínico.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [261]
[19] PATOLOGÍA PSIQUIÁTRICA IMPORTANTE PARA EL MÉDICO GENERAL
Identificar uno de los cuadros específicos de ansiedad.
Pautar un tratamiento adecuado y/o derivar al especialista correspondiente.
3. ETIOLOGÍA
Patologías psiquiátricas que cursan con ansiedad (Figura 1).
Patologías orgánicas que cursan con ansiedad e indicadores de organicidad (Tablas I y II).
Tabla I. Causas orgánicas de trastorno mental.
Tabla II. Indicadores de sospecha de organicidad.
4. MANIFESTACIONES CLÍNICAS
Se pueden dividir en dos categorías (Tabla III).
Tabla III. Síntomas de ansiedad: físicos y psicológicos.
5. APROXIMACIÓN DIAGNÓSTICA
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [262]
[19] PATOLOGÍA PSIQUIÁTRICA IMPORTANTE PARA EL MÉDICO GENERAL
La ansiedad, como queda reflejado previamente es un cuadro inespecífico que puede ser nuclear
en ciertas patologías psiquiátricas primarias o acompañante en otras, del mismo modo que en los procesos
orgánicos.
Ante un paciente que presenta ansiedad, se deben realizar una anamnesis y una exploración física
completas. Como pruebas complementarias, en general, se recomienda la realización de una analítica
elemental (hematocrito, glucosa, creatinina, iones y gasometría venosa) y un electrocardiograma. Según la
sintomatología específica, se completará con pruebas más específicas (por ejemplo, perfil tiroideo, calcio
sérico, etc.).
En función de la información obtenida, se realizará una orientación diagnóstica (Figura 1).
6. TRATAMIENTO
El tratamiento del paciente se divide en tres partes.
1. Abordaje del cuadro agudo
En un paciente con una crisis de ansiedad, lo primero será realizar una aproximación empática y
tranquilizadora para intentar rebajar el nivel de angustia. Cuando esto no sea posible o resulte insuficiente,
se procederá al tratamiento farmacológico que, en general, serán benzodiazepinas. Siempre que sea
posible se utilizará la vía oral, puesto que la intramuscular resulta más invasiva y su farmacocinética más
errática. En caso de persistencia de la clínica, podrá repetirse la dosis pasados 30-60 minutos. Atendiendo
al potencial adictivo de esta categoría, resulta recomendable evitar su uso indiscriminado y las pautas fijas
con fármacos de vida media corta (Tablas IV y V).
Tabla IV. Benzodiazepinas en el tratamiento de la ansiedad.
Tabla V. Otros fármacos en el tratamiento de los trastornos de ansiedad.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [263]
[19] PATOLOGÍA PSIQUIÁTRICA IMPORTANTE PARA EL MÉDICO GENERAL
2. Manejo de la patología de base
Una vez realizada la orientación diagnóstica y, en su caso, resuelta la clínica aguda, nos
orientaremos hacia el abordaje de la patología de base del paciente. Si esta es psiquiátrica primaria, se
suele recomendar el tratamiento psicológico combinado, según el caso, con tratamiento farmacológico.
Este último podrá utilizarse para evitar la aparición de ansiedad a lo largo del día, tratarla o prevenirla en
los momentos de exposición cuando esta sea muy incapacitante.
Para prevención o tratamiento en momentos puntuales, se recurrirá generalmente al tratamiento
con benzodiazepinas según ya se ha descrito (Tabla VI). También se podrá utilizar en ocasiones el
propranolol como tratamiento de los síntomas físicos de la ansiedad.
En los trastornos primarios y los casos más complejos, los fármacos más utilizados son los
antidepresivos inhibidores selectivos de la recaptación de serotonina (ISRS), combinados si la clínica es muy
intensa con benzodiazepinas pautadas, que se retirarán en 2-4 semanas, manteniendo el antidepresivo
durante 6-12 meses. Con respecto a la retirada, se recomienda una reducción máxima de un 50% de dosis a
la semana. La introducción y manejo de los antidepresivos (Tabla VII) se aborda más en detalle en el
tratamiento de la depresión.
La pregabalina recibió la indicación como tratamiento en el trastorno de ansiedad generalizada, y
se puede utilizar tanto en monoterapia como en combinación (presenta la ventaja de su menor potencial
adictivo y tolerancia con respecto a las benzodiazepinas).
3. Derivación a psiquiatría
En líneas generales, se recomienda valorar la derivación a psiquiatría cuando exista:
Dificultad o duda diagnóstica (síntomas físicos inespecíficos, somatizaciones, etc.).
Comorbilidad psiquiátrica u orgánica (depresión mayor, dependencia de alcohol y/o abuso de
sustancias).
Ideación suicida (derivación urgente).
En caso de persistencia de ansiedad elevada durante más de 12 semanas de tratamiento
farmacológico y/o psicoterapia de apoyo.
Síntomas muy incapacitantes (adaptación social y/o laboral).
II. DEPRESIÓN
1. CONCEPTO
La depresión es un síndrome con afectación global física y psíquica, en el cual los síntomas
nucleares son los sentimientos o manifestaciones de tristeza y la presencia de anhedonia y/o apatía.
2. DEPRESIÓN Y URGENCIAS
La misión del médico en Urgencias es:
Descartar la presencia de patología orgánica que justifique el cuadro clínico.
Tipificar el cuadro y su gravedad.
Determinar el riesgo de suicidio, así como otros criterios de valoración psiquiátrica urgente.
Pautar un tratamiento adecuado y/o derivar al especialista correspondiente.
3. ETIOLOGÍA
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [264]
[19] PATOLOGÍA PSIQUIÁTRICA IMPORTANTE PARA EL MÉDICO GENERAL
Patologías psiquiátricas que cursan con depresión: trastorno depresivo mayor, distimia,
trastorno bipolar y trastorno adaptativo. También puede aparecer como proceso comórbido
Patologías orgánicas que cursan con depresión e indicadores de organicidad (ver Tabla II en el
Apartado “Ansiedad”).
Tabla VI. Clínica y exploración del trastorno depresivo.
4. APROXIMACIÓN DIAGNÓSTICA
Ante un paciente con síntomas depresivos, inicialmente se debe diferenciar entre emoción
(tristeza) y estado de ánimo (depresión), siendo la primera una reacción afectiva situacional (por ejemplo,
tras un fallecimiento, en el contexto de intoxicación etílica, etc.), y el segundo un estado afectivo
mantenido en el tiempo, que es el que nos ocupa.
En la anamnesis se deben recoger los antecedentes personales, los eventos desencadenantes, la
sintomatología predominante, la repercusión y el curso, que serán elementos clave para la tipificación del
cuadro clínico. Además, hay que evaluar el posible riesgo vital orgánico por deshidratación, desnutrición o
abandono del autocuidado. Respecto a las pruebas que se deben realizar, se pueden seguir las
recomendaciones ya reflejadas en el Apartado “Ansiedad”.
El diagnóstico psiquiátrico de la depresión, en la mayor parte de los casos, lo acabará estableciendo
el especialista de acuerdo con las clasificaciones psiquiátricas internacionales vigentes.
En un momento puntual, para realizar una aproximación diagnóstica, resultará de utilidad conocer
ciertas variables orientativas. Así, antecedentes previos de otros episodios depresivos o de fases maníacas
harán pensar en un trastorno bipolar o un trastorno depresivo recurrente; una forma de aparición más o
menos rápida y ausencia de factores desencadenantes (o desproporcionalidad entre los mismos y la
intensidad del cuadro clínico) hablarán de un episodio depresivo mayor, mientras que un inicio larvado,
junto con factores ambientales desencadenantes y de mantenimiento, y curso largo –de meses o incluso un
periodo más dilatado– y fluctuante apuntan a un trastorno depresivo distímico. De igual forma, la
bradipsiquia y la inhibición psicomotriz nos guiarán hacia un episodio depresivo mayor, así como ideas
deliroides o delirantes de ruina o culpa. Por el contrario, un evento desencadenante único, que se asocia en
el tiempo e intensidad, y en ausencia de antecedentes previos, orientará a un trastorno adaptativo.
En todo paciente con clínica depresiva hay que investigar el riesgo de suicidio (Tabla VII). La
conducta suicida se mueve a lo largo de un espectro que va desde la ideación (idea de la muerte como
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [265]
[19] PATOLOGÍA PSIQUIÁTRICA IMPORTANTE PARA EL MÉDICO GENERAL
descanso, deseos de muerte e ideación suicida) hasta la gradación conductual creciente (amenazas, gestos,
tentativas y suicidio consumado). Hay que investigar sistemáticamente en todo paciente con ánimo
depresivo, la ideación e intencionalidad autolítica, así como los factores de riesgo para la misma.
Tabla VII. Factores de riesgo suicida.
5. MANEJO DEL SÍNDROME DEPRESIVO
En el Servicio de Urgencias se plantea la cuestión de iniciar o no un tratamiento antidepresivo. Si el
paciente presenta un cuadro depresivo leve o moderado y será valorado en breve plazo por otro
profesional que se hará cargo de su tratamiento continuado, resulta recomendable no iniciar en este
momento el tratamiento antidepresivo y que sea su médico de referencia quien lo haga. Si existe
sintomatología ansiosa acompañante, se puede pautar tratamiento ansiolítico. Por otro lado, ante
conocimiento o sospecha de bipolaridad, no es recomendable de inicio el uso de antidepresivos, estando
indicado remitir al paciente al especialista para que decida sobre ello.
En el caso contrario, se puede iniciar el tratamiento antidepresivo para evitar prolongar el
sufrimiento personal y familiar. De primera elección se utilizan los fármacos ISRS. El tiempo de latencia en
el inicio de acción de estos oscila entre 2-6 semanas. Ante una falta total de respuesta pasadas 4 semanas,
se recomienda valorar el cambio a otro antidepresivo, mientras que ante una respuesta parcial parece
indicado mantener o aumentar la dosis del mismo fármaco hasta las 8 semanas. En caso de cambio, se
recomienda iniciar un nuevo ISRS, un inhibidor de la recaptación de serotonina y noradrenalina (IRSN) o un
antidepresivo tricíclico (ADT). Estos últimos actualmente no son de primera línea y, en general, serán de
manejo por parte del especialista en psiquiatría (Tabla VIII).
Es importante informar al paciente y a su familia sobre la naturaleza de la enfermedad si es la
primera vez que consultan por ella, así como de las características del tratamiento (periodo de latencia,
posibles efectos secundarios, etc.).
Se recomienda realizar derivación al especialista en Salud Mental en los siguientes casos:
Riesgo de suicidio o heteroagresividad.
Episodio depresivo grave.
Sospecha de bipolaridad.
Depresión recurrente.
Episodios depresivos prolongados.
Abuso de sustancias.
Negación del trastorno.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [266]
[19] PATOLOGÍA PSIQUIÁTRICA IMPORTANTE PARA EL MÉDICO GENERAL
Tras dos o más intentos fallidos de tratamiento.
Ante dudas diagnósticas o terapéuticas.
La derivación se realizará de forma urgente en caso de que el paciente presente síntomas psicóticos
(ideas delirantes, alteraciones sensoperceptivas), clínica catatoniforme, repercusión grave sobre el
autocuidado o elevado riesgo de suicidio.
Tabla VIII. Antidepresivos de uso frecuente.
III. AGITACIÓN PSICOMOTRIZ
1. CONCEPTO
La agitación psicomotriz es un estado de hiperactividad física y mental descontrolada e
improductiva, de gran intensidad. Se debe diferenciar de la conducta violenta o agresiva, destinada a
causar daño, si bien no son cuadros excluyentes.
Constituye una urgencia psiquiátrica por el riesgo de lesión a uno mismo o a terceros. Ante toda
agitación psicomotriz se debe llevar a cabo un diagnóstico etiológico entre patologías orgánicas,
psiquiátricas y uso de medicamentos o tóxicos.
2. APROXIMACIÓN DIAGNÓSTICA
1. Agitación orgánica
La patología orgánica es la primera que se debe descartar por el riesgo vital que puede suponer. Los
cuadros subyacentes son enfermedades somáticas e intoxicación o abstinencia de fármacos o tóxicos.
La agitación orgánica se presenta en el contexto de un síndrome confusional, caracterizado por
alteración fluctuante del nivel de consciencia, inatención, desorientación temporoespacial, confusión
mental y discurso incoherente. La psicopatología acompañante más habitual son las alucinaciones visuales
(signo bastante específico de organicidad) e ideas delirantes (ocupacionales, de perjuicio, etc.). Conlleva
riesgo de caídas, fuga e interrupción del proceso terapéutico (arrancamiento de sondas o vías, etc.).
Debe sospecharse organicidad en todo cuadro de inicio agudo o subagudo o de aparición en
adultos mayores o pacientes sin antecedentes psiquiátricos.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [267]
[19] PATOLOGÍA PSIQUIÁTRICA IMPORTANTE PARA EL MÉDICO GENERAL
2. Agitación psiquiátrica
Se caracteriza por presentar psicopatología propia de alguna entidad psiquiátrica, como síntomas
psicóticos (alucinaciones auditivas y/o ideas delirantes de perjuicio, megalomaníacas) o alteraciones de la
afectividad (euforia o disforia, irritabilidad). Habitualmente, el nivel de consciencia está preservado, no
existe desorientación temporoespacial y la fluctuación es escasa. Pueden aparecer hostilidad o agresividad,
frecuentemente dirigidas hacia personas concretas o conocidas.
Sospechar en pacientes con antecedentes de patología psiquiátrica y exploración física sin datos
que sugieran organicidad.
3. Agitación mixta
Paciente con diagnóstico psiquiátrico que presenta un componente de organicidad, como patología
somática o intoxicación o abstinencia de alcohol u otros tóxicos.
Se considera que una agitación es de causa psiquiátrica cuando presenta características propias de
esta, no tratándose, por tanto, de un diagnóstico de exclusión. Esto es especialmente relevante en
pacientes con deterioro cognitivo o retraso mental, en los que la agitación psicomotriz puede ser un
indicador de un malestar subjetivo atribuible tanto a una molestia orgánica (fiebre, dolor, estreñimiento,
etc.) como a factores ambientales o sociales.
Para establecer el diagnóstico diferencial se debe realizar toma de constantes vitales, exploración
física completa (incluyendo exploración neurológica) y pruebas de laboratorio: hemograma, bioquímica,
saturación de oxígeno, alcohol en sangre, tóxicos en orina, hormonas tiroideas y análisis de orina. En un
paciente con un cuadro de agitación sin antecedentes psiquiátricos previos, es recomendable realizar una
prueba de imagen (tomografía computarizada [TC] craneal), serologías (sífilis) y medición de vitaminas
(ácido fólico/B12). Ver Capítulo 11. “Síndrome confusional agudo”.
3. ETIOLOGÍA (Tablas IX y X)
4. MANEJO DE LA AGITACIÓN PSICOMOTRIZ EN URGENCIAS
El manejo debe ser inmediato y dirigido a calmar al paciente, minimizar el riesgo de daño a sí
mismo o a otros, facilitar la evaluación diagnóstica completa y permitir el inicio de tratamiento específico.
La contención se puede realizar a varios niveles: verbal, farmacológico y mecánico. En todos los
casos, se debe mantener una distancia de seguridad adecuada con el paciente (distancia de un brazo),
respetando a la vez su espacio personal, y llevar a cabo la valoración en un área privada, libre de objetos
contundentes, manteniendo una vía de salida accesible. En caso de ser preciso, se deberá solicitar la
colaboración del personal de enfermería, celadores y/o seguridad.
Tabla IX. Agitación orgánica frente a agitación psiquiátrica.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [268]
[19] PATOLOGÍA PSIQUIÁTRICA IMPORTANTE PARA EL MÉDICO GENERAL
Tabla X. Causas de agitación psicomotriz.
1. Contención verbal
Es el primer paso en el manejo del paciente agitado. Se debe establecer contacto ocular, pero
evitando mantenerlo para que no resulte retador. Hay que abordar al paciente de forma cordial, en tono
bajo, pero con seguridad y firmeza, escuchándole con interés por su problema, ofreciéndole ayuda y
comprensión. Se recomienda explicar al paciente de forma sencilla y concisa los procedimientos que se van
a seguir y ofrecerle participar en la toma de las decisiones que puedan competerle.
La contención verbal resulta muy útil para explorar el discurso, la lucidez de consciencia y el grado
de comprensión, la presencia de alucinaciones o delirios, la existencia de signos de intoxicación, etc.
En muchas ocasiones, la contención verbal resulta insuficiente para el control del cuadro de
agitación, sobre todo en agitaciones orgánicas en las que está alterada la comprensión.
2. Contención farmacológica
El tratamiento farmacológico debe utilizarse en la mayor parte de los casos, tanto en agitación
orgánica como psiquiátrica. En la actualidad existen tratamientos con diversas vías de administración: oral,
en solución, bucodispersable, inhalada, intramuscular. Hay que considerar siempre ofrecer en primer lugar
tratamiento oral como forma de construir una alianza terapéutica con el paciente. En caso de rechazo al
mismo, se optará por la vía parenteral.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [269]
[19] PATOLOGÍA PSIQUIÁTRICA IMPORTANTE PARA EL MÉDICO GENERAL
Los fármacos que habitualmente se indican en el manejo de la agitación psicomotriz son los
antipsicóticos y las benzodiazepinas.
2.1. Agitación orgánica
Es fundamental el tratamiento de la patología orgánica subyacente. Se debe tener precaución al
administrar un fármaco depresor del sistema nervioso central (SNC) a un paciente médicamente grave,
monitorizando las constantes vitales.
El tratamiento recomendado son los fármacos neurolépticos (orales o intramusculares). De primera
elección son los de alta potencia y, entre estos, por su seguridad y eficacia, el haloperidol es uno de los más
adecuados. Se debe ajustar la dosis según el grado de agitación, la edad y la enfermedad del paciente (5 mg
repetible cada 30-45 minutos, por vía intramuscular, hasta lograr la contención).
Los antipsicóticos clásicos de baja potencia, levomepromazina y la clorpromazina (Sinogan® y
Largactil®, respectivamente) tienen un potente efecto sedante, pero presentan riesgo de hipotensión,
aspiración, delirium anticolinérgico, alteraciones cardiacas, etc., por lo que desaconseja su uso en estos
casos. Otra opción es la clotiapina (Etumina® 40 mg, ½ a 1 comprimido cada 30 minutos o 1 hora repetible
hasta un máximo de 360 mg, es decir, ocho dosis), útil por su gran sedación.
Entre los neurolépticos atípicos, se pueden emplear olanzapina 2,5-15 mg/día, risperidona 2-6
mg/día o quetiapina 50-100 mg/día, con menor riesgo de extrapiramidalismo que el haloperidol, útiles en la
enfermedad de Parkinson.
Las benzodiazepinas deben evitarse en la mayoría de las agitaciones de etiología orgánica, tanto
por su efecto depresor del centro respiratorio, como por su propio efecto sedante, que aumenta la
confusión y, por tanto, la agitación. Únicamente son de elección en el delirium tremens, en el síndrome de
abstinencia de alcohol, benzodiazepinas u opiáceos, en cuadros de origen epiléptico y en algunos tipos de
intoxicaciones por estimulantes (cocaína, anfetaminas, etc.). Cuando se empleen benzodiazepinas en el
tratamiento de estos cuadros clínicos, se debe vigilar el posible riesgo de depresión respiratoria. Para su
uso deben estar disponibles medios de asistencia ventilatoria y flumazenilo (Anexate® 0,2-0,5 mg cada 3-5
minutos hasta mejorar el nivel de consciencia).
2.2. Agitación psiquiátrica
En cuadros de agitación de causa psiquiátrica, sin patología orgánica subyacente que complique el
tratamiento, existe un mayor margen de seguridad.
Agitación leve-moderada, con predominio de sintomatología ansiosa, de etiología no psicótica,
sin sospecha de consumo de alcohol: se consideran las benzodiazepinas como tratamiento de
elección. Las vías sublingual e intramuscular tienen una absorción errática, por lo que se
recomienda la vía oral si el paciente acepta la misma. Se puede administrar lorazepam 2-5 mg
(ausencia de metabolismo hepático, menor riesgo de acumulación).
Agitación intensa, sobre todo si es de origen psicótico o maníaco: se recomiendan
neurolépticos clásicos: haloperidol 5 mg vía im (hasta 4-6 ampollas), cada 30-40 minutos
periodo en el que alcanza su efecto máximo y por tanto se puede repetir la dosis, asociados a
benzodiazepinas (diazepam 10 mg o clorazepato dipotásico 50 mg, vía im). En función de la
intensidad, se puede añadir neurolépticos sedantes como levopremazina 25 mg o
clorpromacina 25 mg. Estos presentan su efecto máximo a las 3-4 horas por lo que no se debe
repetir dosis.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [270]
[19] PATOLOGÍA PSIQUIÁTRICA IMPORTANTE PARA EL MÉDICO GENERAL
Los antipsicóticos atípicos son otros fármacos a considerar, son tan efectivos como el haloperidol y
mejor tolerados. Para la administración vía oral disponemos de risperidona (3-6 mg), quetiapina (200 mg),
olanzapina (10 mg) y aripriprazol (7,5 mg). Estos dos últimos también disponibles vía intramuscular junto
con: olazapina 10 mg, ziprasidona 10-20 mg.
3. Contención mecánica (inmovilización terapéutica)
La inmovilización terapéutica es siempre una medida de última elección, indicada cuando un
paciente agitado o agresivo presenta riesgo de autolesión o heterolesión o para impedir la interrupción del
tratamiento (manipulación de medidas terapéuticas, arrancamiento de vías, en los supuestos legales de
tratamiento forzoso, etc.). Su indicación puede efectuarla cualquier médico, así como el personal de
enfermería, siempre con ratificación por escrito del médico responsable del tratamiento.
Se debe garantizar el respeto a los derechos individuales del paciente, explicando la indicación a
este y a sus familiares. En el supuesto en que los derechos sean vulnerados, se deberá comunicar y solicitar
la autorización de acuerdo a la legalidad vigente.
La contención mecánica tiene que llevarse a cabo en un contexto hospitalario, con material
específico para ello. Para su colocación, se requiere la participación de los profesionales contemplados en
el protocolo correspondiente del hospital.
El paciente debe ser monitorizado a través de control visual permanente y por medio de un
protocolo de cuidados (toma de constantes, temperatura, estado de hidratación, etc.) durante el tiempo
que se mantenga la inmovilización. Los protocolos hospitalarios suelen exigir que sea valorado por el
médico responsable en la primera hora de la colocación de la contención y cada 4 horas desde entonces,
reevaluándose si continúa la indicación de inmovilización en función del estado clínico.
BIBLIOGRAFÍA
American Psychiatric Association. Manual Diagnóstico y Estadístico de los Trastornos Mentales. DSM-5.
5ª edición: Madrid; Panamericana, 2014.
Aranza JR. Guía Práctica de Farmacología del Sistema Nervioso Central. 14ª edición: Pfizer, 2013.
Clasificación Internacional de Enfermedades. CIE-10. 10ª revisión. Modificación Clínica. Edición
Española.
Chinchilla A, Correas J, Quintero FJ, Vega M. Breviario de Urgencias psiquiátricas. 1ª edición: Barcelona;
Elsevier Masson, 2011.
Grupo de Trabajo de la Guía de Práctica Clínica para el Manejo de Pacientes con Trastornos de
Ansiedad en Atención Primaria. Madrid: Plan Nacional para el SNS del MSC. Unidad de Evaluación de
Tecnologías Sanitarias. Agencia Laín Entralgo. Comunidad de Madrid; 2008. Guías de Práctica Clínica
en el SNS: UETS Nº 2006/10.
Grupo de trabajo de la Guía de Práctica Clínica sobre el Manejo de la Depresión en el Adulto. Guía de
Práctica Clínica sobre el Manejo de la Depresión en el Adulto. Ministerio de Sanidad, Servicios Sociales
e Igualdad. Agencia de Evaluación de Tecnologías Sanitarias de Galicia (avalia-t); 2014. Guías de
Práctica Clínica en el SNS: Avalia-t 2013/06.
Lipson-Glick R, Berlin J, Fishkind A, Zeller S. Emergency Psychiatry: Principles and Practice. 1ª edición:
Philadephia; Wolters-Kluwer, Lippincott Williams & Wilkins. 2008.
Richmond JS, Berlin JS, Fishkind AB, et al. Verbal De-escalation of the Agitated Patient: Consensus
Statement of the American Association for Emergency Psychiatry Project BETA De-escalation
Workgroup. West J Emerg Med. 2012;13:17-25.
Sadock BJ, Sadock VA. Kaplan & Sadock: Sinopsis de psiquiatría. 11ª edición. Philadelphia: Wolter
Kluver/Lippincot, Williams & Wilkins, 2015.
Stahl SM. Psicofarmacología Esencial de Stahl: Guía del Prescriptor. 4ª edición: Madrid; Aulamédica,
2012.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [271]
[20] HIPERTENSIÓN ARTERIAL Y RIESGO CARDIOVASCULAR
20.Hipertensión arterial y riesgo cardiovascular
Ana García Santiago
Nefrología
Samara Campos Escudero
Medicina Interna
Julio César Vargas Romero
Medicina Interna
Asesor: Julián Segura de la Morena. Presidente de la SEH-LELHA. Unidad de Hipertensión Arterial. Nefrología
I. DEFINICIÓN Y CLASIFICACIÓN
Según el último informe de la Organización Mundial de la Salud (OMS) publicado en 2013 a nivel
mundial, más de uno de cada cinco adultos tiene la presión arterial (PA) elevada; en países europeos la
prevalencia oscila entre el 30-45%. Si se añade el hecho de que la hipertensión arterial (HTA) duplica el
riesgo de enfermedades cardiovasculares, accidentes cerebrovasculares, insuficiencia renal y arteriopatía
periférica, se calcula que las complicaciones derivadas de la hipertensión son la causa de 9,4 millones de
defunciones cada año en el mundo. Por lo tanto, diagnosticar, tratar y controlar la HTA es una prioridad de
salud mundial.
En la esfera clínica se puede definir la HTA como el nivel de PA en el cual el tratamiento que se
emplea disminuye las cifras de morbilidad y mortalidad por PA. La relación continua existente entre PA y las
complicaciones cardiovasculares (CV) hace difícil la distinción entre normotensión e HTA cuando nos
basamos únicamente en valores de corte de la PA. En la práctica clínica, los valores de corte de la PA (Tabla
I) se utilizan universalmente para simplificar el algoritmo diagnóstico y facilitar la toma de decisiones sobre
el tratamiento.
II. EVALUACIÓN DIAGNÓSTICA
En la evaluación inicial de un paciente con sospecha de HTA se debe confirmar el diagnóstico de
HTA mediante mediciones múltiples, detectar posibles daños en órganos diana, indagar en causas
secundarias de la HTA y evaluar el riesgo cardiovascular (RCV) total. Las causas secundarias de HTA
constituyen en torno al 5-20% de los casos, y se deben sospechar ante una HTA de inicio brusco, cifras
superiores a 180/110 mm Hg, aparición en menores de 30 años o mayores de 50 años, antecedentes
familiares de enfermedad renal y datos sugestivos en la exploración física.
Tabla I. Definición y clasificación de las cifras de presión arterial (mm Hg).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [272]
[20] HIPERTENSIÓN ARTERIAL Y RIESGO CARDIOVASCULAR
1. MEDICIÓN DE LA PRESIÓN ARTERIAL
a. Medición en la consulta
En la actualidad se prefiere el uso de esfigmomanómetros semiautomáticos auscultatorios u
oscilométricos, que se deben calibrar periódicamente y confirmar su precisión. Antes de la
medición de la PA el paciente debe estar sentado y en reposo unos minutos, sin haber bebido o
fumado en los últimos 30 minutos y se debe utilizar un manguito adecuado. En la consulta se
recomiendan tres mediciones (separadas unos minutos), incluyendo ambos brazos en la primera
visita (para detectar posibles diferencias relacionada con enfermedad vascular periférica), durante
dos o tres visitas. Una diferencia significativa > 15 mm Hg y constante de PA sistólica (PAS) entre
ambos brazos se asocia a un incremento del RCV. En la primera visita se deberá realizar también
una medición en bipedestación para el cribado de hipotensión ortostática (reducción de la PAS > 20
mm Hg o de la PA diastólica –PAD– > 10 mm Hg a los 3 minutos de bipedestación), ya que está
relacionado con un peor pronóstico y complicaciones CV. La PA en consulta es generalmente más
alta que la presión automedida o monitorizada de forma ambulatoria, lo que ha de valorarse a la
hora de realizar el diagnóstico de HTA (Tabla II).
Tabla II. Definiciones de hipertensión arterial según los valores de presión arterial medida en consulta y ambulatoria.
b. Medición fuera de la consulta
La PA fuera de la consulta se suele obtener por automedición (AMPA) o monitorización ambulatoria
(MAPA), siendo la correspondencia entre ambas moderada. Estudios recientes indican que la PA
medida en el domicilio se relaciona más estrechamente con el daño sobre órganos diana y que la
predicción de morbimortalidad es significativamente mejor. Para la evaluación inicial del paciente
la AMPA puede ser más adecuada en A. Primaria y la MAPA en especializada (técnica de referencia
fuera de consulta). Las indicaciones clínicas para la medición de la PA fuera de la consulta serían:
Sospecha de HTA de bata blanca (PA alta en la consulta en pacientes asintomáticos y con bajo
RCV) y sospecha de HTA enmascarada (PA normal-alta en la consulta en pacientes
asintomáticos y alto RCV).
Identificación de HTA resistente y falsa.
Sospecha de episodios de hipotensión (sobre todo en ancianos y diabéticos).
Variabilidad acusada de PA en varias consultas o en la misma consulta.
Discordancia entre la PA en consulta y en domicilio y sospecha de HTA nocturna (indicaciones
específicas para MAPA).
MAPA. El paciente lleva un tensiómetro portátil, normalmente en el brazo no dominante, durante
24 horas, con mediciones realizadas en intervalos de 20 minutos durante el día y 30 durante la noche. Se
recomienda no realizar ejercicio extenuante, no moverse durante las mediciones y registrar las horas de
medicación, comida y sueño. La PA disminuye durante la noche entre un 10-20% (definido como dipping).
Se ha objetivado que la incidencia de complicaciones CV es mayor en pacientes con una caída de la PA
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [273]
[20] HIPERTENSIÓN ARTERIAL Y RIESGO CARDIOVASCULAR
nocturna menor que en los pacientes con mayor caída. Las posibles razones para la ausencia de esta caída
nocturna son las alteraciones del sueño, el síndrome de apnea-hipopnea del sueño (SAHS), la obesidad, la
hipotensión ortostática, la disfunción autonómica, enfermedad renal crónica (ERC), la neuropatía diabética
y la edad avanzada.
AMPA. La PA debe medirse diariamente durante 7 días por la mañana y por la noche (en las
condiciones óptimas descritas previamente) anotando los resultados. Permite realizar mediciones en
periodos de tiempo más largos y registrar mayor variabilidad, y además es más barata y más fácil de repetir
que la MAPA. Debe desaconsejarse si va a producir ansiedad en el paciente, ante personalidades y/o
conductas ansiosas/obsesivas o ante posibilidad de que el paciente modifique el tratamiento por sí mismo.
2. ANAMNESIS, EXPLORACIÓN FÍSICA Y PRUEBAS COMPLEMENTARIAS
En la tabla III se muestra la anamnesis, la exploración física y las pruebas complementarias que se
han de realizar cuando se sospecha de HTA.
Tabla III. Anamnesis, exploración física y pruebas complementarias ante la sospecha de hipertensión arterial.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [274]
[20] HIPERTENSIÓN ARTERIAL Y RIESGO CARDIOVASCULAR
III. TRATAMIENTO
1. OBJETIVOS DEL TRATAMIENTO
El nivel óptimo de PA que se debe alcanzar varía en relación a la edad y el RCV total, pero en líneas
generales las recomendaciones serían las señaladas en la tabla IV. Las indicaciones del tratamiento no
farmacológico y farmacológico se resumen en la tabla V.
La hipótesis de la curva en J (defiende que los beneficios de la reducción de la PA a niveles muy
bajos son menores que los obtenidos con reducciones moderadas) ha sido objeto de numerosos estudios
recientes, pero hasta el momento la evidencia es contradictoria.
Tabla IV. Recomendaciones acerca de objetivos del tratamiento antihipertensivo.
Tabla V. Instauración de tratamiento no farmacológico y farmacológico.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [275]
[20] HIPERTENSIÓN ARTERIAL Y RIESGO CARDIOVASCULAR
2. TRATAMIENTO NO FARMACOLÓGICO
Los cambios adecuados en el estilo de vida deben ser la primera medida en instaurarse y se
recomiendan para todos los pacientes con HTA, incluidos los que necesitan tratamiento farmacológico de
entrada (HTA grado 3 y grado 2 con tres o más factores de RCV), ya que ayudan a reducir el número y la
dosis de fármacos antihipertensivos en caso de que sean necesarios. Además contribuyen al control de
otros factores de RCV. Se recomiendan los siguientes cambios en el estilo de vida:
Abandonar el hábito tabáquico.
Moderación en el consumo de alcohol: menos de 20-30 g/día en varones y menos de 10-20
g/día en las mujeres.
Restricción de la ingesta de sal a 5-6 g al día.
Práctica regular de ejercicio que incluya al menos 30 minutos de ejercicio dinámico moderado
5-7 días por semana.
Mayor consumo de fruta, hortalizas y productos lácteos bajos en grasa.
Reducir el peso a un índice de masa corporal (IMC) de 25 y un perímetro abdominal inferior a
102 cm en varones y a 88 cm en las mujeres, siempre que no esté contraindicado.
3. TRATAMIENTO FARMACOLÓGICO
Los últimos estudios y metaanálisis que han analizado esta cuestión han llegado a la conclusión de
que el mayor beneficio del tratamiento farmacológico es la reducción de la PA per se, sin encontrar
diferencias clínicas relevantes entre las distintas clases de fármacos disponibles en la actualidad (aunque
habrá de tenerse en cuenta la variabilidad individual en la respuesta al tratamiento). Se confirma que los
diuréticos, los β-bloqueantes (BB), los antagonistas de los canales de calcio (AC), los inhibidores de la
enzima de conversión de la angiotensina (IECA) y los antagonistas del receptor de la angiotensina II (ARA-II)
son los fármacos adecuados para instaurar y mantener el tratamiento antihipertensivo en monoterapia o
combinados. Recientemente se ha descubierto que los BB no aumentan, e incluso reducen, los episodios de
exacerbación y la mortalidad de los pacientes con enfermedad pulmonar obstructiva crónica (EPOC). Los
fármacos más utilizados en la actualidad en monoterapia son los IECA y ARA-II, por su gran eficacia para
prevenir la proteinuria y en el tratamiento de la insuficiencia cardiaca crónica, sin que se haya demostrado
la mayor eficacia de un grupo sobre otro.
La elección de uno u otro debe individualizarse, tomando en con sideración la gravedad de la HTA,
la comorbilidad, las interacciones farmacológicas, la dosificación, los efectos secundarios y el coste. Existen
preferencias respecto a la elección del fármaco según situaciones clínicas específicas o contraindicaciones
establecidas por diferentes estudios clínicos (Tablas VI y VII).
Monoterapia frente a tratamiento combinado. La monoterapia solo resulta eficaz en un pequeño
número de pacientes hipertensos, requiriendo la mayoría una combinación de al menos dos fármacos para
controlar la PA. Se ha demostrado que la combinación de dos fármacos de dos clases de antihipertensivos
es más eficaz para la reducción de la PA que el aumento de la dosis de un solo fármaco. El uso de
combinaciones de dos fármacos antihipertensivos a dosis fijas en una sola píldora mejora la adherencia y
aumenta el control de la PA. Actualmente se dispone de combinaciones de dos fármacos a distintas dosis
fijas. Es fundamental la valoración de la adherencia al tratamiento antes de incrementar dosis o añadir un
nuevo fármaco.
Si se inicia el tratamiento en monoterapia y no se alcanza el objetivo de PA tras un mes, se
recomienda aumentar las dosis gradualmente o añadir un segundo fármaco; si aún no se alcanza con la
combinación de dos fármacos a dosis máximas, se puede considerar otra combinación de fármacos o añadir
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [276]
[20] HIPERTENSIÓN ARTERIAL Y RIESGO CARDIOVASCULAR
un tercero (la triple terapia siempre deberá constar de un diurético), y si incluso así no se logra el control de
la PA, se valorará remitir al paciente a un especialista en HTA.
Tabla VI. Contraindicaciones para el uso de fármacos antihipertensivos.
Tabla VII. Elección de fármaco según situaciones clínicas específicas.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [277]
[20] HIPERTENSIÓN ARTERIAL Y RIESGO CARDIOVASCULAR
IV. HIPERTENSIÓN EN EL ANCIANO
En pacientes mayores de 65 años los beneficios en cuanto a RCV son claros para recomendar
tratamiento antihipertensivo que reduzca la PAS a 150-140 mm Hg. Todos los fármacos antihipertensivos
están recomendados y pueden usarse para el paciente anciano, aunque son preferibles los diuréticos y los
antagonistas del calcio en caso de HTA sistólica aislada. La medida de la PA en el anciano debe realizarse en
sedestación y bipedestación (por su mayor riesgo de hipotensión postural). Las dosis de inicio y los ajustes
de dosis deben ser más graduales, debido a la mayor posibilidad de efectos indeseables.
Más específicamente, para pacientes ancianos en buen estado con edad menor de 80 años, se
puede considerar el tratamiento antihipertensivo ante valores de PAS ≥ 140 mm Hg, con un objetivo de PAS
< 140 mm Hg siempre que se tolere bien el tratamiento. En el caso de mayores de 80 años con PAS ≥ 160
mm Hg, se recomienda reducir la PAS a 150-140 mm Hg siempre que estén en buena forma física y mental.
Cuando se trate de ancianos frágiles, se recomienda dejar las decisiones sobre el tratamiento
antihipertensivo en manos de su médico, quien debe monitorizar los efectos clínicos del mismo. Se debe
considerar mantener el tratamiento antihipertensivo bien tolerado cuando el paciente tratado llega a los 80
años.
V. HIPERTENSIÓN EN EL EMBARAZO
En el control de la PA en las mujeres gestantes debe tenerse en cuenta un equilibrio entre el
beneficio de reducción de eventos cardiovasculares y el riesgo de hipoperfusión placentaria. Por ello, y por
la falta de estudios en esta población, no existe un consenso en cuanto al objetivo de cifras de PA a partir
de las cuales se debería comenzar tratamiento. Las recomendaciones basadas en opiniones de expertos
indican comenzar el tratamiento con cifras de PA ≥ 150/95 mm Hg, con un objetivo de cifras de PA ≤ 140/90
mm Hg.
Los fármacos antihipertensivos de elección en la mujer gestante son metildopa y labetalol. Se debe
iniciar la metildopa con una dosis inicial de 250 mg dos o tres veces al día, con un incremento gradual a
partir de las 48 horas y una dosis máxima de 1 g/8 horas. El labetalol se inicia a dosis de 100 mg dos veces al
día, pudiendo aumentarse de manera progresiva hasta una máximo de 300 mg/8 horas. En caso de
emergencia (preeclampsia), se puede considerar la administración de labetalol intravenoso o nitroprusiato
en perfusión.
En cuanto a la hidralazina, se recomienda su uso a partir del tercer trimestre solo cuando los
beneficios potenciales justifiquen el riesgo posible sobre el feto. La dosis inicial es de 12,5 mg/6-12 horas,
con un incremento posterior según las necesidades hasta una dosis máxima de 200 mg al día.
VI. HIPERTENSIÓN ARTERIAL RESISTENTE
Se define como la persistencia de cifras de PAS y PAD elevadas (> 140 y 90 mm Hg,
respectivamente) pese al tratamiento de la HTA que incluya cambios en el estilo de vida además de un
diurético y dos fármacos antihipertensivos de clases diferentes a dosis máxima. Es de suma importancia
detectar falsas HTA resistentes y causas desencadenantes (Tabla VIII). Una vez más, el papel de una
correcta anamnesis y de un examen físico meticuloso es de vital importancia.
En estos pacientes se debe considerar la administración de antagonistas del receptor de
mineralocorticoides, amilorida y doxazosina, siempre que no estén contraindicados. Se recomienda la
derivación de estos pacientes a una unidad especializada.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [278]
[20] HIPERTENSIÓN ARTERIAL Y RIESGO CARDIOVASCULAR
Tabla VIII. Causas de hipertensión arterial resistente.
VII. EMERGENCIA Y URGENCIA HIPERTENSIVA
Ante una crisis hipertensiva resulta fundamental descartar la presencia o no de daño orgánico
agudo. El estado clínico es mucho más importante que las cifras de PA en sí. Para ello, será necesario
realizar una anamnesis meticulosa así como examen físico y pruebas complementarias seleccionadas. Esta
se define como elevaciones de la PAS/PAD ≥ 180/120 mm Hg. Se debe distinguir de la pseudocrisis
hipertensiva (elevación asintomática y sin repercusión orgánica de la PA, secundaria a hipoxia, dolor y
sobrecarga de volumen en situaciones de postoperatorio, retención urinaria, dolor intenso, ansiedad o
insomnio), en cuyo caso se debe tratar la causa desencadenante, no las cifras tensionales.
1. EMERGENCIA HIPERTENSIVA
Se define como una crisis hipertensiva que se acompaña de daño orgánico inminente o progresivo
con potencial riesgo vital. Puede aparecer en pacientes con historia previa de HTA o no. Cursa
habitualmente con cefalea, junto con síntomas específicos (dolor torácico, disnea, focalidad neurológica,
etc.) y requiere manejo hospitalario. Estas situaciones clínicas son:
Cambios neurológicos graves: encefalopatía hipertensiva, infarto cerebral y hemorragia
intracraneal.
Afectación cardiovascular: insuficiencia aguda del ventrículo izquierdo, edema agudo de
pulmón, síndrome coronario agudo y disección aórtica.
Daño renal: insuficiencia renal aguda.
Afectación de la retina: retinopatía hipertensiva grado III (hemorragias y/o exudados
bilaterales) o IV (papiledema bilateral). Clásicamente definida como HTA maligna, dado que su
pronóstico era similar al de las patologías tumorales; en la actualidad, con los nuevos fármacos
antihipertensivos, el pronóstico es mucho mejor.
Eclampsia.
2. URGENCIA HIPERTENSIVA
Son subidas importantes, pero aisladas de la PA que no comportan daño orgánico agudo. Cursa de
forma asintomática o paucisintomática (es frecuente la cefalea, en ocasiones también aparecen mareo,
inestabilidad, ansiedad o epistaxis no intensa). La mayoría se asocian a la interrupción o reducción del
tratamiento crónico y a la ansiedad. Deben ser tratadas con la reinstauración o intensificación del
tratamiento hipertensivo y con actuación sobre la ansiedad si existiera. No precisan hospitalización.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [279]
[20] HIPERTENSIÓN ARTERIAL Y RIESGO CARDIOVASCULAR
Una mención especial precisan las situaciones de urgencia hipertensiva en aquellos pacientes que
necesitan una cirugía urgente, presentan hemorragias importantes o se les han realizado suturas vasculares
recientemente. En este caso, por el alto riesgo de sangrado deben ser tratados de una forma más agresiva.
3. MANEJO DE LAS CRISIS HIPERTENSIVAS
El objetivo es diferenciar rápidamente si se trata de una urgencia o de una emergencia, para lo cual
se debe realizar:
Comprobación de la PA: correcta medición de la PA (ambiente tranquilo, sedestación y piernas
descruzadas, tres tomas repetidas), en ambos brazos y midiendo la frecuencia cardiaca.
Anamnesis: indagar sobre HTA previa, tratamientos, transgresiones y modificaciones recientes,
desencadenantes, sintomatología cardiovascular o neurológica, embarazo.
Exploración física: que incluya evaluación neurológica y fondo de ojo.
Pruebas complementarias iniciales: ecocardiograma (ECG), hemograma, bioquímica básica,
sistemático de orina, fondo de ojo y radiología torácica. Debe plantearse la realización de
pruebas adicionales según la sospecha clínica; por ejemplo, tomografía computarizada (TC)
craneal ante la presencia de focalidad neurológica o TC toracoabdominal si se sospecha un
síndrome aórtico agudo).
En la figura 1 se muestra el algoritmo del manejo de las crisis hipertensivas.
Figura 1. Algoritmo de manejo de la crisis hipertensiva.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [280]
[20] HIPERTENSIÓN ARTERIAL Y RIESGO CARDIOVASCULAR
4. TRATAMIENTO DE LA EMERGENCIA HIPERTENSIVA
Requiere ingreso urgente en unidades especializadas dada la amenaza vital potencial y el cambio
pronóstico a largo plazo, además de la regresión del daño orgánico con medidas oportunas. El manejo
terapéutico y la velocidad de descenso de las cifras de PA dependen del tipo de daño orgánico. En general,
se recomienda un descenso cercana al 25% de la PA de manera inmediata (1-2 horas) con una reducción
más cautelosa posteriormente. En el caso de ictus la PA se debe reducir con más cautela o incluso no
tratarse, mientras que en el caso de la disección aórtica y del edema agudo de pulmón la bajada de PA
debe ser mucho más agresiva. El tratamiento específico de las emergencias hipertensivas se describe con
más detalle en sus capítulos correspondientes.
Se debe usar medicación intravenosa inicialmente para producir una disminución de la PA más
controlada y, posteriormente, pautar medicación oral. La elección del fármaco debe hacerse según el tipo
de emergencia hipertensiva y la experiencia del clínico tratante, dado que no existen ensayos clínicos
aleatorizados al respecto (Tabla IX).
Tabla IX. Medicación parenteral en la emergencia hipertensiva.
5. TRATAMIENTO DE LA URGENCIA HIPERTENSIVA
Una vez descartado que se trate de una emergencia hipertensiva, se debe mantener al paciente en
reposo en un lugar tranquilo y valorar la administración de sedación suave (lorazepam 1-2 mg, diazepam 5-
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [281]
[20] HIPERTENSIÓN ARTERIAL Y RIESGO CARDIOVASCULAR
10 mg) si presenta ansiedad o nerviosismo. Si pasados 30 minutos persiste la elevación de la PA, debe
iniciarse el tratamiento hipotensor.
Está contraindicado reducir de forma brusca la PA, por el riesgo de provocar isquemia cerebral,
miocárdica o renal, especialmente en hipertensos crónicos (pues suelen presentar alteraciones de la
autorregulación de la perfusión). El objetivo es llevar la PA a niveles seguros (PA < 210/120 mm Hg) en 2-3
horas, sin intentar normalizar totalmente su valor (lo cual debe alcanzarse en días o semanas). Por ello se
empleará medicación por vía oral.
Si el paciente estaba recibiendo un tratamiento antihipertensivo previo, se debe reinstaurar su
medicación oral (en caso de abandono de la misma), incrementar la dosis, o añadir otro fármaco por vía
oral.
En pacientes sin tratamiento previo, se administrará una dosis oral de alguno de los siguientes
hipotensores: un CA (amlodipino 5-10 mg, manidipino 10-20 mg), un IECA (enalapril 10-20 mg), un BB
(labetalol 100-300 mg, atenolol 50-100 mg) o un agonista α2 (clonidina 0,1-0,2 mg). Si se logra una PA <
210/120 mm Hg, se remitirá al paciente al centro de salud para su control en las siguientes 24 horas (el
objetivo es lograr una PA < 160/100 mm Hg en los días siguientes). Si tras todo lo anterior (incluyendo
varias dosis de medicación por vía oral) persiste una PA > 210/120 mm Hg en el plazo de 2-3 horas, se
considerará el ingreso hospitalario y el inicio de tratamiento parenteral.
En la figura 2 se muestra el algoritmo del manejo de las urgencias hipertensivas.
Figura 2. Algoritmo de manejo de la urgencia hipertensiva.
VIII. RIESGO VASCULAR
La enfermedad cardiovascular (ECV) ateroesclerótica es un trastorno crónico que se desarrolla de
manera insidiosa a lo largo de la vida y suele estar avanzada cuando aparecen los síntomas. Es una de las
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [282]
[20] HIPERTENSIÓN ARTERIAL Y RIESGO CARDIOVASCULAR
principales causas de muerte prematura en Europa, a pesar de que la mortalidad CV ha disminuido
considerablemente en las últimas décadas en muchos países europeos. Se estima que más del 80% de la
mortalidad CV total ocurre actualmente en países en desarrollo. La ECV causa el 42% de todas las muertes
de las mujeres europeas menores de 75 años y del 38% de todas las muertes de varones menores de 75
años.
La ECV se relaciona estrechamente con los estilos de vida y factores de riesgo, en su mayoría
modificables (Tabla X). Las modificaciones en los factores de riesgo son capaces de disminuir la
morbimortalidad por ECV, sobre todo en personas de alto riesgo.
Tabla X. Factores de riesgo cardiovascular principal.
1. MANIFESTACIONES CLÍNICAS
La ECV es la expresión clínica del fenómeno de ateroesclerosis, que ocurre en cualquier territorio
vascular originando así las distintas manifestaciones clínicas (Tabla XI).
Tabla XI. Manifestaciones clínicas de la enfermedad cardiovascular.
2. ESTRATEGIAS Y ESTIMACIÓN DEL RIESGO
El estudio del RCV es una valoración multifactorial, ya que el riesgo del paciente refleja en la
mayoría de las ocasiones el efecto de la combinación de varios factores de riesgo.
Las personas con ECV establecida tienen un riesgo de episodios muy elevado y requieren
intervenciones inmediatas en todos los factores de riesgo, mientras que en las personas aparentemente
sanas debe estimarse el riesgo total con el sistema SCORE. Las sociedades europeas de Hipertensión y
Cardiología recomiendan el uso de la tabla SCORE, que estima el riesgo a 10 años de un primer episodio
ateroesclerótico mortal, como infarto, ictus, aneurisma de aorta, etc. Clasifica al paciente en muy alto
riesgo, alto riesgo, moderado y bajo riesgo (Figuras 3 y 4, Tabla XII; ver Capítulo 73. “Trastornos lipídicos”).
En cambio, es relevante la búsqueda de lesión de órganos diana (incremento de la excreción
urinaria de albúmina, hipertrofia ventricular izquierda) y de enfermedad vascular asintomática en
individuos de un riesgo inicialmente intermedio según la tabla SCORE, pues facilita un mejor enfoque
terapéutico.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [283]
[20] HIPERTENSIÓN ARTERIAL Y RIESGO CARDIOVASCULAR
Las técnicas para la detección de ateroesclerosis subclínica cuyo valor está más demostrado son el
índice brazo-tobillo (ver Capítulo 59. “Patología vascular intestinal”) y la determinación del grosor íntima-
media mediante ecografía carotídea. La ergometría, la determinación de hipertrofia ventricular mediante
ECG y la determinación del calcio coronario por angio-TC solo están indicadas en adultos asintomáticos con
RCV moderado.
Figura 3. Tabla SCORE calibrada para España.
Figura 4. Tabla de riesgo relativo (para jóvenes).
3. MANEJO TERAPÉUTICO
El objetivo de la prevención de la ECV es asistir a los pacientes con bajo riesgo para mantenerlo así
toda la vida y ayudar a disminuirlo en aquellos con riesgo elevado. El manejo de los distintos factores de
riesgo se trata en sus capítulos correspondientes.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [284]
[20] HIPERTENSIÓN ARTERIAL Y RIESGO CARDIOVASCULAR
Tabla XII. Valoración y manejo del riesgo vascular global.
BIBLIOGRAFÍA
European Society of Hypertension-European Society of Cardiology Guidelines Committee. 2003
European Society of Hypertension-European Society of Cardiology guidelines for the management of
arterial hypertension. J Hypertens. 2003;21:1011-53.
Llabrés Díaz J, Blázquez Cabrera JA. Hipertensión arterial en Urgencias. Manejo clínico y terapéutico de
las crisis hipertensivas. Medicine. 2007;9(88):5679-85.
Mancia G, de Backer G, Dominiczak A, Cifkova R, Fagard R, Germano G, et al. Guidelines for the
Management of Arterial Hypertension: The Task Force for the Management of Arterial Hypertension of
the European Society of Hypertension (ESH) and of the European Society of Cardiology (ESC). J
Hypertens. 2007;25:1105-87.
Mancia G, Fagard R, Narkiewicz K, Redón J, Zanchetti A, Böhm M, et al. 2013 ESH/ESC Guidelines for
the management of arterial hypertension: the Task Force for the management of arterial hypertension
of the European Society of Hypertension (ESH) and of the European Society of Cardiology (ESC). J
Hypertens. 2013;31(7):1281-357.
Perk J, de Backer G, Gohlke H, Graham I, Reiner Z, Verschuren M, et al. Guía europea sobre prevención
de la enfermedad cardiovascular en la práctica clínica. Rev Esp Cardiol. 2012;65(10):937.e1-e66.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [285]
[21] INSUFICIENCIA CARDÍACA
21.Insuficiencia cardíaca
Jesús González Olmedo.
Medicina Interna.
Blanca Coto Morales.
Cardiología
Asesora: Laura Domínguez Pérez. Médica Adjunta. Servicio de Cardiología
I. DEFINICIÓN
La insuficiencia cardiaca (IC) es un síndrome clínico caracterizado por síntomas típicos (disnea,
astenia, edemas, etc.) que debe acompañarse de signos, como aumento de la presión venosa yugular,
crepitantes pulmonares, edema periférico, etc., causado por una alteración estructural y/o funcional del
corazón que produce disminución del gasto cardiaco y/o aumento de las presiones intracardiacas en reposo
o con el ejercicio.
II. ETIOLOGÍA
Las principales causas de insuficiencia cardiaca son la enfermedad coronaria y la hipertensión
arterial (HTA), seguidas de valvulopatías y miocardiopatías. Además, ante todo paciente con clínica de
insuficiencia cardiaca o empeoramiento de su clase funcional (Tabla I) se deben buscar los factores
precipitantes o agravantes (Tabla II).
III. CLASIFICACIÓN
Existen diferentes clasificaciones de la insuficiencia cardiaca. Se puede hablar de una clasificación
según su etiología cuando se describe la causa primera de la insuficiencia cardiaca. En otros casos, se
clasifica la insuficiencia cardiaca según la fracción de eyección del ventrículo izquierdo (FEVI):
Insuficiencia cardiaca con FEVI preservada: aquellos con FEVI mayor o igual al 50%.
Insuficiencia cardiaca con FEVI reducida: aquellos con FEVI menor del 40%.
Insuficiencia cardiaca con FEVI en rango medio: aquellos con FEVI entre el 40% y el 49%.
Según la cronología de los síntomas, podemos clasificarla en: insuficiencia cardiaca aguda (por
ejemplo, como consecuencia de un infarto agudo de miocardio) o insuficiencia cardiaca subaguda o crónica
(más frecuente). Tradicionalmente se ha distinguido también entre la insuficiencia cardiaca de bajo gasto
cardiaco (la más frecuente), en contraposición a la insuficiencia cardiaca de alto gasto cardiaco (anemia,
embarazo, hipertiroidismo, sepsis, insuficiencia hepática, fístula arteriovenosa, enfermedad de Paget ósea,
Beri-Beri). En cuanto a la sintomatología se refiere, también podemos hacer distinción entre síntomas de
insuficiencia cardiaca izquierda (relacionados con la congestión pulmonar), insuficiencia cardiaca derecha
(relacionados con congestión hepática, esplácnica, miembros inferiores) e insuficiencia cardiaca
biventricular (Tabla III).
Tabla I. Clasificación funcional de la insuficiencia cardiaca según la New York Heart Association (NYHA).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [286]
[21] INSUFICIENCIA CARDÍACA
Tabla II. Factores precipitantes o agravantes de la insuficiencia cardiaca.
Tabla III. Definición de insuficiencia cardiaca con fracción de eyección (FEVI) reducida, FEVI en rango medio y FEVI preservada.
IV. CLÍNICA
Realizar una buena anamnesis y exploración física es fundamental, ya que muchos de los síntomas
de insuficiencia cardiaca no son específicos, y los más típicos (ortopnea y disnea paroxística nocturna) son
menos frecuentes.
En la tabla IV se muestra un resumen de los principales síntomas y signos.
V. PRUEBAS COMPLEMENTARIAS
Electrocardiograma (ECG): se recomienda la realización de un ECG de 12 derivaciones para
determinar el ritmo y la frecuencia cardiaca, la morfología y duración del complejo QRS y para
detectar otras alteraciones relevantes (datos sugestivos de hipertrofia ventricular y/o de
isquemia). El diagnóstico de insuficiencia cardiaca sistólica es muy improbable (< 2%) en
pacientes con presentación aguda y un ECG completamente normal. En pacientes con
presentación no aguda, un ECG normal tiene un valor predictivo negativo algo menor.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [287]
[21] INSUFICIENCIA CARDÍACA
Radiografía de tórax: se recomienda para detectar o excluir otras patologías que puedan
contribuir a la disnea. También puede valorar el crecimiento de cavidades cardiacas y la
presencia de derrame pleural o signos de congestión (redistribución vascular, edema intersticial
con líneas B de Kerley, borramiento de hilios). Es más útil en pacientes con sospecha de
insuficiencia cardiaca aguda.
Laboratorio: se deberá solicitar hemograma completo, glucosa, perfil renal, hepático y lipídico,
hemoglobina glucosilada (HbA1c), tirotropina (TSH), ferritina y saturación de transferrina.
Tabla IV. Síntomas y signos de insuficiencia cardiaca.
La determinación de marcadores de daño miocárdico, si bien las últimas guías clínicas no indican
realizarla rutinariamente en el estudio inicial de insuficiencia cardiaca, puede ayudar si se sospecha que la
causa inicial ha sido un síndrome coronario agudo (SCA). Pueden estar elevados en la insuficiencia cardiaca
grave o en la insuficiencia cardiaca descompensada en ausencia de SCA, lo que constituye un dato de mal
pronóstico.
La determinación en plasma de niveles de péptido natriurético tipo B (BNP o NT-proBNP) son útiles
por su alto valor predictivo negativo, ya que niveles de BNP < 100 pg/ml o NT-proBNP < 300 pg/ml hacen el
diagnóstico de insuficiencia cardiaca aguda improbable, aunque la presencia de valores elevados no
confirma automáticamente el diagnóstico. En pacientes que presentan formas no agudas, las guías clínicas
de 2016 establecen nuevos valores de corte de NT-proBNP > 125 pg/ml y BNP > 35 pg/ml como dos de las
medidas objetivas para el diagnóstico de insuficiencia cardiaca. En el contexto de la insuficiencia cardiaca
crónica, niveles persistentemente elevados, a pesar de un tratamiento médico óptimo, constituyen un
indicador de mal pronóstico.
Ecocardiograma transtorácico (ETT): fundamental en el estudio diagnóstico y para el enfoque
terapéutico. Permite valorar el tamaño de las cavidades cardiacas, el grosor miocárdico, la
función sistólica y diastólica, la contractilidad, la función valvular, la patología pericárdica, etc.
Otros estudios en pacientes seleccionados: resonancia magnética cardiaca, coronariografía,
tomografía computarizada (TC) coronaria, ecocardiograma transesofágico (ETE),
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [288]
[21] INSUFICIENCIA CARDÍACA
ecocardiograma de estrés (ya sea de ejercicio o farmacológico con dipiridamol o dobutamina),
estudios de perfusión miocárdica, cateterismo cardiaco derecho, ergometría, ergoespirometría.
En la figura 1 se muestra una propuesta de algoritmo diagnóstico ante la sospecha de insuficiencia
cardiaca.
VI. INSUFICIENCIA CARDIACA AGUDA
Se define como la rápida instauración de síntomas y signos secundarios al funcionamiento anómalo
del corazón. Cursa con aumento de la presión capilar pulmonar (PCP) y extravasación de líquido al
intersticio y alveolo pulmonar (edema de pulmón). En algunos casos, la clínica puede estar marcada por
una disminución del gasto cardiaco e hipoperfusión tisular. Constituye un riesgo vital, por lo que es
importante un diagnóstico precoz y la instauración de un tratamiento específico urgente.
Figura 1. Algoritmo diagnóstico ante sospecha de insuficiencia cardiaca aguda.
Puede presentarse de novo o ser una descompensación de una insuficiencia cardiaca crónica;
asimismo, puede estar causada por una disfunción cardiaca primaria o precipitada por factores externos.
1. CLÍNICA
La insuficiencia cardiaca aguda (ICA) no está representada por un grupo homogéneo de pacientes,
sino que dentro de un mismo síndrome se pueden encontrar diferentes situaciones clínicas:
En la mayoría de los casos, los pacientes presentan cifras de tensión arterial sistólica (TAS)
normal (90-140 mm Hg) o elevada (> 140 mm Hg). Tan solo un 5-8% de los pacientes presentan
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [289]
[21] INSUFICIENCIA CARDÍACA
hipotensión arterial (TAS < 90 mm Hg) que se asocia con un peor pronóstico, especialmente
cuando existe hipoperfusión concomitante.
Edema agudo de pulmón: situación clínica en la que se produce una acumulación de líquido en
el espacio intersticial y en los alveolos pulmonares, objetivando por tanto crepitantes, ortopnea
e hipoxemia. Requiere tratamiento farmacológico urgente, oxigenoterapia y en algunos casos
soporte ventilatorio. Puede darse con tensión arterial normal, baja o alta, lo que condicionará
la aproximación terapéutica (Figura 2).
Figura 2. Manejo del edema agudo de pulmón.
Insuficiencia cardiaca de alto gasto: en situaciones de alto gasto cardiaco.
Insuficiencia cardiaca y SCA: según la clasificación de Killip-Kimball (Tabla V).
Tabla V. Clasificación de Killip-Kimball.
Insuficiencia cardiaca derecha: secundaria a disfunción ventricular derecha, que cursa con
edemas periféricos, hepatomegalia y aumento de la presión venosa yugular, en ausencia de
congestión pulmonar.
Shock cardiogénico: es la situación de ICA más grave. Se caracteriza por hipotensión arterial
mantenida (TAS < 90 mm Hg) o una caída de la tensión arterial media > 30 mm Hg, junto con
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [290]
[21] INSUFICIENCIA CARDÍACA
datos de hipoperfusión tisular (extremidades frías, oliguria < 0,5 ml/kg/h y/o alteración del
nivel de consciencia). El diagnóstico final se realiza al objetivar un índice cardiaco disminuido (<
1,8 l/min/m2 sin soporte o < 2-2,2 l/min/m2 bajo soporte), con presiones de llenado adecuadas
o elevadas [presión telediastólica del ventrículo izquierdo > 18 mm Hg (inferida a través de la
mediación de la presión de enclavamiento pulmonar, PCP) o presión telediastólica del
ventrículo derecho > 10-15 mm Hg].
Estas formas clínicas no son excluyentes entre sí, y pueden solaparse.
Actualmente, y de acuerdo con las guías clínicas de la Sociedad Europea de Cardiología, se propone
la clasificación por perfiles clínicos, según la presencia/ausencia de hipoperfusión y/o congestión (Figura 3).
Figura 3. Perfiles clínicos de insuficiencia cardiaca aguda.
Figura 4. Clasificación de Forrester.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [291]
[21] INSUFICIENCIA CARDÍACA
Otra clasificación que también se utiliza es la de Forrester (necesita información obtenida a través
de mediciones invasivas: índice cardiaco y PCP) (Figura 4).
2. BIOMARCADORES COMO FACTORES PRONÓSTICOS EN LA INSUFICIENCIA CARDIACA AGUDA
La certeza diagnóstica de la clínica, la radiografía de tórax y el electrocardiograma es muy limitada
en la insuficiencia cardiaca aguda, ya que los criterios que utilizamos (como por ejemplo los de
Framingham) son criterios adaptados de los que existen para el diagnóstico de la insuficiencia cardiaca
crónica (que ofrecen una baja sensibilidad en el contexto de la insuficiencia cardiaca aguda). Esta
circunstancia es muy relevante, ya que el diagnóstico y tratamiento inicial de la insuficiencia cardiaca aguda
en el servicio de Urgencias va a condicionar los resultados a corto plazo en esta patología (el retraso en el
diagnóstico y en el inicio de tratamiento se asocia con un aumento de la mortalidad intrahospitalaria).
Debido a todo lo anteriormente expuesto, se empezaron a introducir en el diagnóstico ciertos
biomarcadores. De entre los factores predictores diagnósticos descritos por Maisel (edad, antecedentes de
insuficiencia cardiaca, antecedentes de infarto, crepitantes, redistribución vascular, edemas, ingurgitación
yugular y péptidos natriuréticos), los péptidos natriuréticos fueron los predictores más potentes (odds ratio
[OR] 29,6). La combinación, por tanto, del juicio clínico y de los péptidos natriuréticos mejora mucho el
rendimiento diagnóstico.
Es importante, asimismo, estratificar el riesgo de los pacientes y saber cuál es su pronóstico para la
toma de decisiones, fundamentalmente, de si el paciente ingresa o es dado de alta. Según el registro
Epidemiology Acute Heart Failure Emergency (EAHFE), casi un cuarto de los pacientes con diagnóstico de
insuficiencia cardiaca aguda son dados de alta a su domicilio directamente desde la urgencia. Para tomar
este tipo de decisiones nos apoyamos fundamentalmente en escalas de riesgo, muchas de las cuales están
diseñadas a partir de población ingresada y predicen la mortalidad a 30 días. La Emergency Heart Failure
Mortality Risk Grade (EHMRG) predice la mortalidad a 7 días (esta escala no ha sido validada en nuestro
medio). En el registro EAHFE se objetivó una correlación entre la elevación de la troponina y del NT-proBNP
(> 5.180) con la mortalidad a 72 horas y a los 7 días, lo que sugiere que aquellos pacientes con elevación de
la troponina y un NT-proBNP > 5.180 no deberían ser dados de alta. Existen otros biomarcadores en
estudio, como la copeptina y el MR-proADM, que han demostrado una buena capacidad de predicción de
mortalidad a 90 días en los pacientes atendidos por disnea en los Servicios de Urgencias (incluyendo a
aquellos con insuficiencia cardiaca aguda). De hecho, la copeptina y el MR-proADM son los biomarcadores
que mejor predicen la mortalidad a 14 días (que es la que verdaderamente importa cuando nos planteamos
el alta al domicilio desde los Servicios de Urgencias). Hasta que estos biomarcadores sean validados en la
práctica clínica y estén disponibles, se debe seguir apoyando la toma de decisiones en el juicio clínico y en
otros biomarcadores que sí están disponibles (troponina y NT-proBNP). En cuanto a lo que a mortalidad a
un año se refiere, cobrarían especial importancia marcadores como el ST2, junto con la proteína C reactiva.
3. TRATAMIENTO
El manejo inicial de insuficiencia cardiaca aguda debería realizarse siguiendo el algoritmo (figura 5)
Monitorización: control de la tensión arterial, la frecuencia cardiaca, la frecuencia respiratoria y
la saturación de oxígeno al inicio. En los pacientes críticos es imprescindible la monitorización
continua, de modo que en algunos casos se debe recurrir a mecanismos de monitorización
semiinvasiva o invasiva. También ha de monitorizarse la diuresis.
Oxígeno: lo antes posible en pacientes con hipoxemia, para alcanzar saturación de O2 > 95%
(en torno al 90-92% si es un paciente con enfermedad pulmonar obstructiva crónica [EPOC]).
No se debe utilizar sistemáticamente oxígeno en pacientes no hipoxémicos, ya que causa
vasoconstricción y reducción del rendimiento cardiaco.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [292]
[21] INSUFICIENCIA CARDÍACA
Figura 5. Algoritmo de manejo inicial de la insuficiencia cardiaca aguda.
Si existen datos de congestión pulmonar o periférica:
En pacientes en tratamiento crónico de insuficiencia cardiaca, si la descompensación no
es grave, se recomienda no suspender su tratamiento previo con inhibidores de la
enzima de conversión de la angiotensina (IECA) o antagonistas de los receptores de la
angiotensina II (ARA-II) ni el betabloqueante. Si hubiera datos de hipotensión arterial
sintomática o hipoperfusión periférica, deben suspenderse.
Diuréticos de asa: son la piedra angular del tratamiento en pacientes con insuficiencia
cardiaca y signos de sobrecarga de volumen y congestión. En el contexto de la
insuficiencia cardiaca aguda, la vía intravenosa es la más utilizada (ampollas de 20
mg/2ml o 250 mg/25 ml). Si el paciente ya se encontraba bajo tratamiento diurético
previo, la dosis inicial intravenosa debe ser al menos similar a la dosis habitual del
paciente. En el estudio Diuretic Optimization Strategies Evaluation (DOSE), la
administración de 2,5 veces la dosis previa de furosemida produjo una considerable
mejoría de la disnea, mayor pérdida de fluido y mayor cambio en el peso a expensas de
un empeoramiento transitorio de la función renal. En los casos leves se pueden
administrar por vía oral (comprimidos de furosemida de 40 mg). No se ha demostrado
en los estudios realizados mayor eficacia en la administración en bolos o en perfusión
continua. Se debe vigilar la presencia de hipopotasemia, hiponatremia, hiperuricemia o
hipovolemia (sobre todo en tratamientos agresivos).
Otros diuréticos: si hay resistencia al tratamiento, se puede combinar el diurético de
asa con espironolactona (25-50 mg vo) o tiazidas (hidroclorotiazida oral 50-100 mg). Si
no existe insuficiencia renal ni hiperpotasemia, se recomienda la primera, recordando
que su efecto tarda 2 días en aparecer. En caso de alcalosis metabólica secundaria a
diuréticos, podemos emplear acetazolamida (250 mg/24 h vo).
Opiáceos: morfina intravenosa en bolo de 2-5 mg. No se recomienda su uso rutinario.
Puede considerarse con precaución en pacientes con intensa disnea que se encuentran
en situación de edema agudo de pulmón para reducir la ansiedad. Pueden producir
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [293]
[21] INSUFICIENCIA CARDÍACA
náuseas, hipotensión, bradicardia y depresión respiratoria (incrementando el riesgo de
ventilación invasiva). Además, existen controversias acerca de un potencial incremento
en el riesgo de mortalidad en pacientes que han recibido morfina.
Vasodilatadores: son más eficaces en pacientes con hipertensión y deben evitarse en
pacientes con TAS < 90 mm Hg o con hipotensión arterial sintomática. Reducen la
poscarga y la precarga. Se deben utilizar con precaución en pacientes con estenosis
aórtica o mitral significativa. La nitroglicerina (Solinitrina® ampollas 50 mg/10 ml) se
suele emplear en perfusión continua: 25 mg en 250 cc de suero glucosado (SG) 5% o
suero fisiológico (SF) 0,9% o a doble concentración si se quiere infundir menos volumen
(50 mg en 250 cc de SG 5% o SF 0,9%). Dosis: 10-200 mg/min. Se va aumentando el
ritmo de infusión según se requiera, vigilando la aparición de hipotensión arterial.
Puede ocasionar cefalea. El nitroprusiato de sodio (vial de 50 mg) está indicado en
insuficiencia cardiaca hipertensiva. Se diluyen 50 mg en 250 o 500 cc de SG al 5%,
siendo la tasa de infusión inicial 0,3 mg/kg/min, aumentando el ritmo de infusión según
la respuesta, siendo la dosis máxima 5 mg/kg/min. Durante su infusión hay que
monitorizar constantemente los parámetros hemodinámicos, por lo que es
recomendable la monitorización invasiva de la tensión arterial. El nesiritide es un
péptido natriurético recombinante humano con propiedades vasodilatadoras. Fue
aprobado por la Food and Drug Administration (FDA) americana en el año 2001 para el
alivio de la disnea en la insuficiencia cardiaca; sin embargo, presenta evidencia
científica contradictoria y, sobre la base de los resultados del estudio Acute Study of
Clinical Effectiveness of Nesiritide in Decompensated Heart Failure (ASCEND-HF), el uso
de este fármaco no debe recomendarse de forma rutinaria en la insuficiencia cardiaca
descompensada.
Ventilación mecánica no invasiva (VMNI): en pacientes con edema agudo de pulmón
cardiogénico o con ICA hipertensiva que no mejoran con tratamiento diurético. Varios
estudios mostraron una reducción de la tasa de intubación orotraqueal (IOT),
especialmente en pacientes hipercápnicos.
Intubación orotraqueal (IOT) y ventilación mecánica invasiva (VMI): insuficiencia
respiratoria que conlleva hipoxemia, hipercapnia y acidosis. La fatiga física, la
consciencia reducida y la incapacidad de mantener o proteger la vía respiratoria son
otras razones para considerar la IOT.
Tabla VI. Principales fármacos inotrópicos utilizados en la insuficiencia cardiaca aguda.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [294]
[21] INSUFICIENCIA CARDÍACA
Si existen datos de hipoperfusión periférica, agentes inotrópicos y vasoconstrictores (Tabla
VI): el agente inotrópico de elección en el shock cardiogénico es la dobutamina. Si fuese
necesario recurrir a la administración de vasoconstrictores, el fármaco de elección es la
noradrenalina. Dado que el efecto diurético de la dopamina a dosis bajas se encuentra en
entredicho y que este fármaco presenta un mayor riesgo de inducción de arritmias que la
noradrenalina, en la actualidad no se recomienda su uso en el contexto del shock cardiogénico.
VII. INSUFICIENCIA CARDIACA CRÓNICA
1. TRATAMIENTO DE LA INSUFICIENCIA CARDIACA CON FRACCIÓN DE EYECCIÓN REDUCIDA (INSUFICIENCIA CARDIACA
SISTÓLICA)
Los objetivos del tratamiento en pacientes con insuficiencia cardiaca establecida son aliviar los
síntomas (mejora del estado clínico, la capacidad funcional y la calidad de vida), evitar el ingreso
hospitalario y disminuir la mortalidad.
En la figura 6 se muestra el algoritmo de manejo de la insuficiencia cardiaca con FEVI reducida.
Figura 6. Algoritmo de tratamiento de la insuficiencia cardiaca crónica con fracción de eyección disminuida.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [295]
[21] INSUFICIENCIA CARDÍACA
1.1. Medidas no farmacológicas (Tabla VII)
Tabla VII. Medidas no farmacológicas en la insuficiencia cardiaca.
1.2. Medidas farmacológicas
Inhibidores de la enzima de conversión de la angiotensina: se recomienda un IECA para todos
los pacientes con FEVI ≤ 40%, sintomáticos o asintomáticos, para reducir el riesgo de
hospitalización y de muerte prematura. Están contraindicados en los pacientes con
antecedentes de angioedema, estenosis bilateral de las arterias renales, potasio sérico > 5
mmol/l, creatinina (Cr) sérica > 2,5 mg/dL, filtrado glomerular (FG) ≤ 30 ml/ min/l o estenosis
aórtica grave. Se comenzará el tratamiento con las dosis de inicio que se muestran en la tabla
VIII, con control clínico y analítico (función renal e iones) en 1-2 semanas. Si existe buena
tolerancia clínica y no se produce deterioro de las cifras de Cr ni hiperpotasemia, se puede
aumentar la dosis en 2-4 semanas, con control periódico. Si se produce deterioro de las cifras
de Cr o hiperpotasemia, se recomienda reducir la dosis a la mitad y realizar un control estrecho.
Si se objetiva persistencia del deterioro de la función renal e hiperpotasemia, es aconsejable
suspender el tratamiento.
Tabla VIII. Inhibidores de la enzima de conversión de la angiotensina (IECA).
Betabloqueantes: se recomienda su uso en pacientes con una FEVI ≤ 40%, independientemente
de que haya síntomas y de su gravedad; mejoran la función ventricular, reducen el número de
ingresos hospitalarios y aumentan la supervivencia. Están contraindicados en pacientes con
asma, bloqueo auriculoventricular (AV) de segundo o tercer grado, síndrome del seno enfermo
o bradicardia sinusal. Entre sus efectos secundarios potenciales destacan: hipotensión
transitoria, empeoramiento de la insuficiencia cardiaca y bradicardia excesiva. Se recomienda
comenzar el tratamiento con las dosis de inicio que se muestran en la tabla IX, con control
clínico a las 2-4 semanas. Si aparecen signos de descompensación de insuficiencia cardiaca y/o
hipotensión sintomática y/o bradicardia (frecuencia cardiaca <50 lpm), se recomienda disminuir
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [296]
[21] INSUFICIENCIA CARDÍACA
la dosis y revaluar al paciente, suspendiendo su uso si no se toleran y aumentando
progresivamente hasta la dosis óptima o la máxima tolerancia si no aparecen efectos adversos.
Siempre que sea posible, en pacientes hospitalizados se iniciará el tratamiento antes del alta. Es
seguro continuar el tratamiento con betabloqueantes durante un episodio de
descompensación, aunque puede ser necesario reducir la dosis habitual. Se recomienda la
interrupción temporal en pacientes en shock.
Tabla IX. Betabloqueante.
Antagonistas del receptor mineralocorticoideo (aldosterónico): tanto la espironolactona como
la eplerenona bloquean los receptores que fijan la aldosterona y otros corticoides. En pacientes
con síntomas leves de insuficiencia cardiaca (clase funcional II de la New York Heart Association
[NYHA]), dosis óptima de betabloqueante e IECA o ARA-II y una FEVI ≤ 35%, la eplerenona
reduce los ingresos hospitalarios y aumenta la supervivencia (ensayo Eplerenone in Mild
Patients Hospitalization and Survival Study in Heart Failure [EMPHASIS-HF]). En pacientes con
síntomas moderados-graves (clase funcional III-IV de la NYHA), dosis óptima de un
betabloqueante e IECA o ARA-II y una FEVI ≤ 35%, la espironolactona y la eplerenona reducen
los ingresos hospitalarios y aumentan la supervivencia (ensayo Randomized Aldactone
Evaluation Study [RALES] para la espironolactona y EMPHASIS para la eplerenona). Asimismo, la
eplerenona está indicada en el contexto del postinfarto agudo de miocardio cuando la FEVI ≤
40% y el paciente es diabético o ha cursado con insuficiencia cardiaca (estudio Eplerenone Post-
AMI Heart Failure Efficacy and Survival Stud [EPHESUS]), ya que en este grupo de pacientes
reduce la mortalidad, la muerte súbita y la rehospitalización por insuficiencia cardiaca. Están
contraindicados en pacientes con un potasio sérico > 5 mmol/l y creatinina sérica > 2,5 mg/dL.
Entre los efectos secundarios potenciales destacan: el deterioro de la función renal, la
hiperpotasemia (mayor si se asocia a IECA o ARA-II) y la ginecomastia (no con eplerenona). La
tabla X muestra las dosis de inicio recomendadas. Al igual que con IECA y ARA-II, se recomienda
control clínico y analítico (Cr e iones) estrecho tras su inicio y hasta alcanzar la dosis objetivo.
Tabla X. Antagonistas de la aldosterona.
Antagonistas de los receptores de angiotensina II: se recomienda su uso en pacientes con una
FEVI ≤ 40%, como tratamiento alternativo en pacientes que no toleran tratamiento con IECA.
Sin embargo, dados los resultados de los estudios en insuficiencia cardiaca crónica y otros en
disfunción postinfarto, que indican una similar eficacia a los IECA, quizá se podrían haber
recomendado en las guías de práctica clínica como tratamiento inicial al mismo nivel que los
IECA y no solo cuando no es posible usar estos. Mejoran la función ventricular y reducen los
ingresos hospitalarios. Están contraindicados en pacientes con estenosis bilateral de las arterias
renales, potasio sérico ≥ 5 mmol/l, creatinina sérica > 2,5 mg/dL o estenosis aórtica grave. En la
tabla XI se muestran las dosis de inicio y dosis objetivo de los ARA-II.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [297]
[21] INSUFICIENCIA CARDÍACA
Tabla XI. Antagonistas de los receptores de la aldosterona (ARA-II).
Ivabradina: enlentece la frecuencia cardiaca a través de la inhibición del canal If en el nodo
sinusal y, por tanto, solo debe utilizarse en pacientes en ritmo sinusal. Este fármaco demostró
disminución de la hospitalización por insuficiencia cardiaca, así como mejoría de la función del
ventrículo izquierdo y calidad de vida en pacientes sintomáticos a pesar de tratamiento médico
óptimo (IECA, betabloqueantes y antagonistas del receptor mineralocorticoide) con una FEVI ≤
35%, en ritmo sinusal y con una frecuencia cardiaca (FC) ≥ 70 lpm. En aquellos pacientes con FC
> 75 lpm también se observó una disminución de la mortalidad cardiovascular.
Digoxina: en pacientes con insuficiencia cardiaca sintomática y fibrilación auricular (FA) se
puede utilizar digoxina para controlar la respuesta ventricular, aunque se prefieren otros
tratamientos. La digoxina se puede utilizar también en pacientes en ritmo sinusal con
insuficiencia cardiaca sintomática y FEVI ≤ 40%. Se dispone de un único estudio (DIGIS), en el
que se demostró que la digoxina no reduce la mortalidad, pero disminuyó la hospitalización por
insuficiencia cardiaca tras una media de tres años de tratamiento. Un metaanálisis de ensayos a
menor escala indica que la digoxina puede mejorar los síntomas y prevenir el deterioro. Está
contraindicada en pacientes con bloqueo AV de segundo o tercer grado sin marcapasos
permanente, síndromes de preexcitación o evidencia previa de intolerancia a la digoxina. En
pacientes estables en ritmo sinusal no se requiere dosis de carga. Se iniciará el tratamiento con
0,25 mg al día (en pacientes ancianos e insuficiencia renal comenzar con 0,125 mg al día). Como
efectos secundarios: bloqueo AV y sinoauricular, arritmias auriculares y ventriculares,
confusión, anorexia, náuseas, vómitos y alteración de la percepción de los colores. Algunos
fármacos pueden aumentar la concentración de digoxina (amiodarona, diltiazem, verapamilo,
etc.).
Hidralazina y dinitrato de isosorbida: en un estudio aleatorizado y controlado relativamente
pequeño sobre varones exclusivamente (antes de la utilización de IECA o betabloqueantes en
insuficiencia cardiaca) esta combinación de hidralazina y dinitrato de isosorbida produjo una
reducción casi significativa en la mortalidad respecto a placebo. En un estudio aleatorizado y
controlado posterior, agregar hidralazina y dinitrato de isosorbida a la terapia convencional
(IECA, betabloqueante, antagonista del receptor de la aldosterona) redujo la morbilidad y
mortalidad y mejoró los síntomas en afroamericanos con insuficiencia cardiaca. La muestra de
pacientes seleccionada para el estudio, el tamaño relativamente pequeño y la finalización
precoz ha dejado cierta incertidumbre sobre el valor real de esta terapia combinada, sobre
todo en pacientes que no son de raza negra. Se recomienda iniciar el tratamiento con
hidralazina 37,5 mg y dinitrato de isosorbida 20 mg tres veces al día, considerando el aumento
de dosis tras 2-3 semanas de tratamiento hasta una dosis óptima de 75 mg de hidralazina y 40
mg cada 8 horas de dinitrato de isosorbida. Como efectos secundarios cabe mencionar:
hipotensión, mareo, cefalea, artralgias, mialgias, pericarditis, pleuritis, síndrome similar al
lupus.
Diuréticos: no se han estudiado los efectos de los diuréticos en la mortalidad y la morbilidad
sobre pacientes con insuficiencia cardiaca. No obstante, los diuréticos mejoran los síntomas y,
por tanto, se recomienda su uso para pacientes con signos y síntomas congestivos
independientemente de la fracción de eyección. Los diuréticos de asa producen una diuresis
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [298]
[21] INSUFICIENCIA CARDÍACA
más intensa y corta y los diuréticos tiazídicos más moderada y prolongada. Se suelen preferir
los diuréticos de asa a las tiazidas en la insuficiencia cardiaca. Pueden combinarse en casos de
edema resistente y generalmente de forma temporal. El objetivo de los diuréticos es conseguir
y mantener al paciente euvolémico con la menor dosis posible. Se recomienda el control de los
electrolitos y de la función renal. En la tabla XII se muestran los diuréticos de asa y tiazídicos.
Tabla XII. Diuréticos.
Valsartán/sacubitril: los inhibidores del sistema renina angiotensina aldosterona (SRAA) han
sido la base del tratamiento de la insuficiencia cardiaca en las últimas décadas. La inhibición del
SRAA reduce la vasoconstricción, la hipertrofia de miocitos y la fibrosis miocárdica, y esto se
acompaña de mejoría clínica de la supervivencia y clase funcional. Entre los inhibidores SRAA,
los inhibidores de la IECA y los ARA-II han venido siendo de primera elección. Los péptidos
natriuréticos (PN) son secretados por el corazón, los vasos, el riñón o el sistema nervioso
central en respuesta al aumento de tensión parietal del corazón, entre otros estímulos. Además
de su acción natriurética, tienen otros efectos beneficiosos para el corazón como
vasodilatación, inhibición del SRAA, reducción del tono simpático, y son antiproliferativos y
antihipertróficos. Parecía lógico que el beneficio del bloqueo SRAA en la insuficiencia cardiaca
podría ser mayor aumentando los PN. Este fármaco es una combinación fija de valsartán y
sacubitril, un inhibidor de la neprilisina (endopeptidasa neutra que degrada varios péptidos
endógenos vasoactivos, entre ellos los PN). El estudio PARADIGM-HF exploró si la
administración a largo plazo de este fármaco en pacientes con insuficiencia cardiaca crónica y
fracción de eyección deprimida era mejor que el enalapril en cuanto a mortalidad y morbilidad.
El objetivo primario fue el combinado de muerte cardiovascular (CV) u hospitalización por
insuficiencia cardiaca. El estudio se suspendió prematuramente, después de un seguimiento
medio de 27 meses, tras observarse un beneficio manifiesto en el grupo del
valsartán/sacubitril. Las reacciones adversas más comunes observadas durante el desarrollo
clínico fueron: hipotensión, hiperpotasemia e insuficiencia renal. Se observaron muy pocos
casos de angioedema. Existe suficiente evidencia como para reemplazar IECA (o ARA-II) por
valsartán/sacubitril en pacientes con insuficiencia cardiaca con fracción de eyección reducida
que continúan sintomáticos a pesar de dosis optimizadas de IECA (o ARA-II) o que no los
toleran.
Vaptanes: la hiponatremia es una complicación y/o consecuencia de la fisiopatología
subyacente en la insuficiencia cardiaca. Es una de las alteraciones electrolíticas más frecuentes
y un marcador de mal pronóstico. Los antagonistas de los receptores de la vasopresina
(antagonistas del receptor V2: tolvaptán, satavaptán y lixivaptán y antagonistas receptores V1 y
V2: conivaptán) inhiben la reabsorción de agua libre, lo que ayuda a corregir la hiponatremia
ligada a estados de hipervolemia. En el estudio Efficacy of Vasopressin Antagonism in Heart
Failure (EVEREST), en el que se incluyeron pacientes hospitalizados por insuficiencia cardiaca
con FEVI ≤ 40% a los que se les administró tolvaptán frente a placebo, el tolvaptán alivió
algunos síntomas asociados con la insuficiencia cardiaca aguda; sin embargo, no se demostró
beneficio en reducir la mortalidad ni la morbilidad al año asociada con la insuficiencia cardiaca;
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [299]
[21] INSUFICIENCIA CARDÍACA
si bien un subestudio del EVEREST demostró que el tolvaptán podría ser beneficioso en
términos de mortalidad y rehospitalizaciones en pacientes con hiponatremias marcadas (sodio
< 130 mEq/l), aunque son necesarios más ensayos clínicos para confirmar estos hallazgos. En el
momento actual puede plantearse el uso de este fármaco en el contexto de la insuficiencia
cardiaca congestiva en pacientes con hiponatremia importante e hipervolemia, comenzando
con dosis de 15 mg al día. Como efectos secundarios pueden aparecer alteración del perfil
hepático y riesgos intrínsecos de corregir rápidamente la hiponatremia.
1.3. Tratamientos no recomendados
No se recomiendan las tiazolidinedionas o glitazonas, ya que empeoran la insuficiencia cardiaca
y aumentan el riesgo de hospitalización por insuficiencia cardiaca.
No se recomienda utilizar los bloqueantes de los canales de calcio no dihidropiridínicos, ya que
tienen efecto inotrópico negativo y pueden causar empeoramiento de la insuficiencia cardiaca
(formalmente contraindicados con FEVI < 40%).
No se recomiendan los AINE y los inhibidores de la ciclooxigenasa-2 (COX-2) debido a que
pueden inducir empeoramiento de la función renal y de la insuficiencia cardiaca.
No se recomienda añadir un ARA-II a la combinación de un IECA y un antagonista del receptor
de la aldosterona debido al riesgo de insuficiencia renal e hiperpotasemia.
2. TRATAMIENTO DE LA INSUFICIENCIA CARDIACA CON FRACCIÓN DE EYECCIÓN PRESERVADA (INSUFICIENCIA
CARDIACA DIASTÓLICA)
Todavía no ha habido ningún tratamiento que haya demostrado de manera convincente reducir la
mortalidad y la morbilidad en pacientes con insuficiencia cardiaca diastólica.
En dos estudios con una muestra de pacientes muy pequeña se ha demostrado que el verapamilo
puede mejorar la capacidad para hacer ejercicio físico y los síntomas en pacientes con insuficiencia cardiaca
diastólica.
3. OTROS TRATAMIENTOS FARMACOLÓGICOS EN LA INSUFICIENCIA CARDIACA
La serelaxina es un análogo sintético de la relaxina-2, un péptido hormonal responsable en gran
medida de los cambios fisiológicos durante el embarazo a nivel cardiovascular (vasodilatación y aumento
del gasto cardiaco) y renal (aumento del flujo renal). En el ensayo clínico Efficacy and Safety of Relaxin for
the Treatment of Acute Heart Failure (RELAX AHF) (incluye pacientes con insuficiencia cardiaca con fracción
de eyección conservada y baja), la serelaxina mejoró la disnea a los 5 días, aunque la disnea no se modificó
a las 24 horas. No hubo diferencias en las rehospitalizaciones ni en la muerte cardiovascular a 60 días. Sin
embargo, hubo una reducción en la mortalidad de cualquier causa a los 180 días. Se ha sugerido que la
prevención del daño multiorgánico y el alivio de la congestión pudieran redundar en una mejor
supervivencia. Se necesitan más estudios que confirmen las hipótesis lanzadas en este ensayo.
4. DISPOSITIVOS DE TRATAMIENTO NO QUIRÚRGICO EN LA INSUFICIENCIA CARDIACA SISTÓLICA
Procedimientos de revascularización y cirugía: se intentará detectar las entidades susceptibles
de tratamiento quirúrgico y su corrección cuando esté indicado. La coronariografía se
recomienda en pacientes con insuficiencia cardiaca con alto riesgo de enfermedad coronaria
(en pacientes de bajo riesgo se aconsejan pruebas no invasivas de detección de isquemia),
evidencia de valvulopatía significativa o síntomas anginosos. Se debe recodar que, en caso de
indicarse cirugía valvular, la disfunción ventricular es un factor de riesgo importante que
aumenta la morbimortalidad peri y postoperatoria. En la toma de decisión para estas
intervenciones se recomienda el asesoramiento del Heart Team.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [300]
[21] INSUFICIENCIA CARDÍACA
Implante de marcapasos: cuando esté indicado el implante de un marcapasos en pacientes con
insuficiencia cardiaca y en ritmo sinusal, puede ser importante el mantenimiento de una buena
coordinación AV, por lo que se recomienda plantear el uso de dispositivos bicamerales (DDD).
Además, como se explicará en el siguiente punto, si la FEVI < 35% debería valorarse el implante
de un resincronizador.
Terapia de resincronización cardiaca: para plantear esta terapia todos los pacientes deben
tener una expectativa de vida mayor a un año. En los pacientes con FA, si se objetiva un
porcentaje de estimulación < 93-95%, se deberá valorar la realización de una ablación del nodo
AV. Está contraindicada en pacientes con complejo QRS < 130 ms. Indicaciones:
Pacientes sintomáticos a pesar de tratamiento médico óptimo, con FEVI ≤ 35%, con
morfología de bloqueo completo de rama izquierda (BCRI) y ritmo sinusal:
QRS ≥ 150 ms (evidencia IA).
QRS 130-149 ms (evidencia IB).
Pacientes sintomáticos a pesar de tratamiento médico óptimo, con FEVI ≤ 35%, con
morfología distinta al BCRI y ritmo sinusal:
QRS ≥ 150 ms (evidencia IIa B).
QRS 130-149 ms (evidencia IIb B).
Pacientes en FA: se debe considerar en pacientes con FEVI ≤ 35%, complejo QRS > 130
ms y clase funcional NYHA III-IV a pesar de tratamiento médico óptimo (evidencia IIa B).
En pacientes con indicación de implante de marcapasos o de desfibrilador con FEVI ≤
35%, en clase funcional III o IV, independientemente de la duración del complejo QRS,
se aconseja implantar terapia de resincronización concomitante. También podría
considerarse cuando la clase funcional es II.
Desfibrilador automático implantable: en prevención secundaria de muerte súbita para
pacientes con antecedentes de arritmia ventricular con inestabilidad hemodinámica. En
prevención primaria, en pacientes con clase funcional II-IV, FEVI ≤ 35% a pesar de 3 meses de
tratamiento óptimo, con insuficiencia cardiaca de causa no isquémica o de causa isquémica 40
días post-IAM.
Trasplante cardiaco: en pacientes con insuficiencia cardiaca con síntomas graves, sin
comorbilidad importante y sin otras alternativas de tratamiento.
Implante de asistencias ventriculares: es un recurso para los pacientes que no responden a la
terapia habitual. Pueden ser de asistencia izquierda o biventricular. Se usan como puente a
trasplante, puente a decisión quirúrgica, puente a recuperación, y en pacientes seleccionados
como terapia de destino.
5. FIBRILACIÓN AURICULAR EN PACIENTES CON INSUFICIENCIA CARDIACA CON FRACCIÓN DE EYECCIÓN
PRESERVADA, EN RANGO MEDIO Y REDUCIDA
La FA es la arritmia más común en la insuficiencia cardiaca: aumenta el riesgo de complicaciones
tromboembólicas y puede provocar un empeoramiento de los síntomas. Está menos claro que la FA sea un
factor predictor independiente de mortalidad, así como que pueda causar insuficiencia cardiaca sistólica.
5.1. Control de la frecuencia
Para controlar la frecuencia en pacientes con insuficiencia cardiaca con fracción de eyección baja se
prefiere un betabloqueante a la digoxina, ya que esta no controla la frecuencia cardiaca en ejercicio.
Además, los betabloqueantes tienen per se efectos favorables en la insuficiencia cardiaca sistólica. La
combinación de digoxina y betabloqueantes es más efectiva que los segundos en monoterapia para
controlar la frecuencia ventricular en reposo.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [301]
[21] INSUFICIENCIA CARDÍACA
Para los pacientes con insuficiencia cardiaca con fracción de eyección conservada, los bloqueadores
de los canales de calcio (verapamilo y diltiazem) son una alternativa efectiva a los betabloqueantes.
La frecuencia ventricular óptima en pacientes con insuficiencia cardiaca y FA no está clara.
En casos extremos puede ser necesaria la ablación del nodo AV y la implantación de marcapasos.
5.2. Control del ritmo cardiaco
No se ha demostrado que una estrategia de control del ritmo cardiaco (incluida la cardioversión
eléctrica o farmacológica) sea mejor para pacientes con insuficiencia cardiaca crónica que una estrategia de
control de la frecuencia cardiaca para reducir la mortalidad o la morbilidad.
La amiodarona es el único antiarrítmico que debería utilizarse en pacientes con insuficiencia
cardiaca sistólica.
6. MANEJO DE OTRAS COMORBILIDADES EN LA INSUFICIENCIA CARDIACA CON FRACCIÓN DE EYECCIÓN BAJA Y
CONSERVADA
6.1. Déficit de hierro y anemia
Se asocia con más síntomas, peor estado funcional, mayor riesgo de hospitalización por
insuficiencia cardiaca y supervivencia baja. En los casos de anemia por déficit de hierro, este déficit puede
contribuir a la disfunción muscular en la insuficiencia cardiaca. En un estudio aleatorizado y controlado en
el que se incluyeron pacientes con insuficiencia cardiaca sistólica, en clase funcional II-III de la NYHA con
hemoglobina entre 9,5-13,5 mg/dL y ferropenia, se demostró que la terapia con hierro mejoró los
síntomas, la capacidad de ejercicio y la calidad de vida. Por tanto, está indicada la administración de hierro
carboximaltosa en pacientes con insuficiencia cardiaca con FEVI reducida sintomáticos que tengan unos
valores de ferritina < 100 mg/l o de ferritina entre 100-299 mg/l con una saturación de transferrina < 20%.
Se desconoce el efecto de tratar el déficit de hierro en pacientes con insuficiencia cardiaca diastólica.
6.2. Angina
Se han demostrado eficaces en el tratamiento de la angina en la insuficiencia cardiaca sistólica los
betabloqueantes, el amlodipino, la ivabradina y los nitratos. En la insuficiencia cardiaca diastólica se
pueden utilizar diltiazem y verapamilo.
6.3. Enfermedad pulmonar obstructiva crónica y asma
Implican peor estado funcional y pronóstico. Los betabloqueantes están contraindicados en el
asma, pero no en la EPOC, prefiriéndose un antagonista selectivo beta1 (bisoprolol, nevibolol, metoprolol).
El uso de corticoides conlleva retención de agua y sodio, lo que puede empeorar la insuficiencia cardiaca.
6.4. Diabetes mellitus
La metformina debe considerarse el tratamiento de primera línea, salvo contraindicaciones.
Recientemente la empagliflozina, inhibidor del cotransportador sodio-glucosa tipo 2, ha demostrado
reducir la rehospitalización y mortalidad en pacientes con diabetes mellitus y alto riesgo cardiovascular, sin
modificar el riesgo de infarto agudo de miocardio o ictus.
BIBLIOGRAFÍA
Felker GM, Lee KL, Bull DA, Redfield MM, Stevenson LW, Goldsmith SR, et al. Diuretic strategies in
patients with acute descompensated heart failure. N Engl J Med. 2011;364(9):797-805.
Forrester JS, Diamond GA, Swan HJ. Correlative classification of clinical and hemodynamic function
after acute myocardial infarction. Am J Cardiol. 1977;39:137-45.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [302]
[21] INSUFICIENCIA CARDÍACA
García-Aranda Domínguez B, Sanz Trepiana L, Pérez Rial G. Insuficiencia cardiaca. En: Manual de
diagnóstico y terapéutica médica de Hospital Universitario 12 de Octubre. 7ª edición. Madrid; 2012. p.
235-9.
Kelder JC, Cowie MR, McDonagh TA, Hardman SM, Grobbee DE, Cost B, et al. Quantifying the added
value of BNP in suspected heart failure in general practice: an individual patient data meta-analysis.
Heart. 2011;97:959-63.
Kelder JC, Cramer MJ, Verweij WM, Grobbee DE, Hoes AW. Clinical utility of three B-type natriuretic
peptide assays for the initial diagnostic assessment of new slow-onset heart failure. J Card Fail.
2011;17:729-34.
Kirkpatrick JN, Vannan MA, Narula J, Lang RM. Echocardiography in heart failure: applications, utility,
and new horizons. J Am Coll Cardiol. 2007;50:381-96.
Lee DS, Stitt A, Austin PC, Stukel TA, Schull MJ, Chong A, et al. Prediction of heart failure mortality in
emergent care: a cohor study. Ann Intern Med. 2012;156(11):767-75.
Maisel A, Mueller C, Nowak R, Peacock WF, Landsberg JW, Ponikowski P, et al. Mid-region pro-hormone
markers for diagnosis and prognosis in acute dyspnea: results from the BACH (Biomarkers in Acute
Heart Failure) trial. J Am Coll Cardiol. 2010;55:2062-76.
McMurray JJ, Adamopoulos S, Anker SD, Auricchio A, Böhm M, Dickstein K, et al. ESC Guidelines for the
diagnosis and treatment of acute and chronic heart failure 2012. The Task Force for the Diagnosis and
Treatment of Acute and Chronic Heart Failure 2012 of the European Society of Cardiology. Developed
in collaboration with the Heart Failure Association (HFA) of the ESC. Eur Heart J. 2012;33(14):1787-
847.
Nagueh SF, Bhatt R, Vivo RP, Krim SR, Sarvari SI, Russell K, et al Echocardiographic evaluation of
hemodynamics in patients with decompensated systolic heart failure. Circ Cardiovasc Imaging.
2011;4:220-7.
Nohria A, Tsang SW, Fang JC, Lewis EF, Jarcho JA, Mudge GH, et al. Clinical assesment indentifies
hemodynamic profiles that predict outcomes in patients admited with heart failure. J Am Coll Cardiol.
2003;41:1797-804.
Oudejans I, Mosterd A, Bloemen JA, Valk MJ, van Velzen E, Wielders JP, et al. Clinical evaluation of
geriatric outpatients with suspected heart failure: value of symptoms, signs, and additional tests. Eur J
Heart Fail. 2011;13:518-27.
Ponikowski P, Voors AA, Anker SD, Bueno H, Cleland JG, Coats AJ, et al. 2016 ESC Guidelines for the
diagnosis and treatment of acute and chronic heart failure. The Task Force for the Diagnosis and
Treatment of Acute and Chronic Heart Failure of the European Society of Cardiology (ESC). Developed
with the special contribution of the Heart Failure Association (HFA) of the ESC. Eur Heart J.
2016;37(27):2129-200.
Viana Tejedor A. Insuficiencia cardiaca aguda: formas clínicas, diagnóstico y tratamiento. En: Núñez Gil
IJ, Viana Tejedor A. Cardio Agudos, Volumen I. Madrid: Sociedad Española de Cardiología-CTO Editorial;
2015.
Yancy CW, Jessup M, Bozkurt B, Butler J, Casey DE Jr, Drazner MH, et al. 2013 ACCF/AHA Guideline for
the Management of Heart Failure. A Report of the American College of Cardiology
Foundation/American. Heart Association Task Force on Practice Guidelines. Circulation.
2013;128(16):e240-327.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [303]
[22] ARRITMIAS
22.Arritmias
Ana Miguel Gutiérrez.
Cardiología.
Julio César Vargas Romero.
Medicina Interna
Asesor: Adolfo Fontenla Cerezuela. Médico Adjunto Unidad de Arritmias, Cardiología
La despolarización cardiaca es el origen de la contracción miocárdica. El estímulo se origina en el
nodo sinoauricular o sinusal (NS), cuyas células descargan espontáneamente dando lugar a la
despolarización auricular que produce la onda P en el electrocardiograma (ECG). El NS determina la
frecuencia cardiaca debido a que tiene una frecuencia de despolarización más rápida (habitualmente entre
60 y 100 latidos por minuto [lpm]) que el resto de las células con automatismo del corazón. Las aurículas se
activan en sentido craneocaudal y de derecha a izquierda, por lo que la onda p sinusal será positiva en las
derivaciones inferiores (II, III y aVF), I y aVL, y negativa en aVR.
Cuando la activación llega al nodo auriculoventricular (NAV) experimenta un retraso fisiológico de
la conducción, responsable del segmento PR. El impulso continúa a través del haz de His que se bifurca en
dos ramas, derecha e izquierda, que transmiten rápidamente la onda de despolarización hacia el miocardio
a través de las fibras de Purkinje, lo que da lugar a un QRS estrecho (< 120 ms).
Las alteraciones del ritmo cardiaco se denominan arritmias: taquiarritmias si la frecuencia es
superior a 100 lpm y bradiarritmias si es menor de 60 lpm.
I. TAQUIARRITMIAS
1. CONCEPTO
Una taquiarritmia se define como aquel ritmo cardiaco con una frecuencia mayor de 100 lpm en, al
menos, tres latidos consecutivos. Se clasifican según su origen en taquicardias supraventriculares (TSV):
cuando para mantenerse precisan de estructuras localizadas por encima de la división del haz de His, es
decir, las aurículas y el NAV; y taquicardias ventriculares (TV): cuando para su mantenimiento solo precisan
de tejido ventricular.
2. APROXIMACIÓN DIAGNÓSTICA Y TERAPÉUTICA INICIAL
Cualquier taquiarritmia es potencialmente una urgencia vital, por lo que el primer paso ha de ser
una rápida valoración clínica de la situación hemodinámica del paciente. Se debe disponer de
monitorización electrocardiográfica, registro de la tensión arterial, la saturación de oxígeno y canalizar, al
menos, una vía venosa.
1. ANAMNESIS Y EXPLORACIÓN FÍSICA
Se debe realizar una anamnesis breve que recoja algunos datos fundamentales de la historia clínica
del paciente. La existencia de cardiopatía estructural previa y su gravedad es un dato esencial (la
cardiopatía isquémica y las miocardiopatías son situaciones predisponentes al desarrollo de arritmias
ventriculares). Asimismo, hay que interrogar por la presencia de otras enfermedades (enfermedad
pulmonar obstructiva crónica [EPOC], asma, hipertiroidismo), y por el uso de fármacos potencialmente
proarrítmicos (digital, antiarrítmicos, brocodilatadores) o causantes de alteraciones electrolíticas
(diuréticos) que puedan precipitar la aparición de arritmias. Además se preguntará por síntomas graves
(angina, síncope, disnea). En la exploración física hay que buscar signos que reflejen bajo gasto cardiaco o
mala perfusión periférica (obnubilación, palidez, sudoración, frialdad distal) y/o de insuficiencia cardiaca. El
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [304]
[22] ARRITMIAS
pulso venoso yugular puede encontrarse elevado si existe insuficiencia cardiaca; puede mostrar
palpitaciones rápidas y regulares en la base del cuello (“signo de la rana”) en la taquicardia intranodal;
ausencia de onda “a” en la fibrilación auricular y ondas “a” ocasionales de gran amplitud (“ondas a cañón”)
que indican disociación AV en las TV y en el bloqueo AV completo. En la auscultación cardiopulmonar se
buscarán signos de cardiopatía subyacente (soplos, alteraciones de los ruidos cardiacos), signos de
insuficiencia cardiaca izquierda o broncoespasmo.
2. PRUEBAS COMPLEMENTARIAS
2.1. Laboratorio
Se debe realizar un análisis completo para descartar posibles desencadenantes o favorecedores
(alteraciones iónicas y/o del equilibrio ácido base).
2.2. Electrocardiograma
Es el elemento fundamental. Se ha de obtener un ECG de superficie de 12 derivaciones, así como
una tira de ritmo. Se deben valorar, de forma sistemática, tres puntos: la frecuencia cardiaca, la regularidad
y la duración de los complejos QRS (un QRS es ancho si dura más de 0,12 seg) y las ondas P (si están
presentes o no, su morfología, su posición respecto al QRS y la constancia o variabilidad del PR). Supone
una gran ayuda la comparación con ECG previos del paciente, si están disponibles.
Con todo ello el objetivo es identificar si se trata de una TV o de una TSV, ya que difieren tanto en el
tratamiento como en el pronóstico (Figuras 1 y 2).
Figura 1. Taquicardias de QRS estrecho. Diagnóstico diferencial.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [305]
[22] ARRITMIAS
Figura 2. Taquicardias de QRS ancho. Diagnóstico diferencial.
Cuando el QRS es estrecho invariablemente se trata de una TSV, pero si el QRS es ancho es posible
que se trate tanto de una TV como de una TSV. Ante una taquicardia de QRS ancho hay que recordar que la
buena tolerancia clínica no excluye la posibilidad de que se trate de una TV y, en pacientes con cardiopatía
estructural, sobre todo si existe un infarto de miocardio (IAM) previo, toda taquicardia regular de QRS
ancho debe considerarse como TV hasta que se demuestre lo contrario. Ante la duda de si es TSV o TV hay
que tratar la taquicardia como si fuera una TV.
2.3. Pruebas de imagen
Se debe realizar una radiografía de tórax en busca de signos de insuficiencia cardiaca o de
cardiopatía previa (cardiomegalia). El ecocardiograma es una herramienta muy útil que nos orienta en la
posible etiología de la arritmia (cardiopatía isquémica, enfermedad valvular, disfunción ventricular severa,
miocardiopatía infiltrativa, enfermedad pericárdica), en el conocimiento de la repercusión en la función
ventricular que puede tener y nos puede ayudar a tomar una decisión en lo relativo a la estrategia
terapéutica.
3. TRATAMIENTO
El tratamiento inicial se recoge en las figuras 3 y 4 y en la tabla I. Los aspectos específicos se
detallan en los apartados siguientes.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [306]
[22] ARRITMIAS
Figura 3. Algoritmo diagnóstico-terapéutico de las taquiarritmias.
Figura 4. Protocolo de actuación frente a una taquiarritmia con inestabilidad hemodinámica.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [307]
[22] ARRITMIAS
Tabla I. Fármacos antiarrítmicos.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [308]
[22] ARRITMIAS
Tabla I. Fármacos antiarrítmicos. (Continuación)
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [309]
[22] ARRITMIAS
Tabla I. Fármacos antiarrítmicos. (Continuación)
3. CLASIFICACIÓN DE LAS TAQUIARRITMIAS
1. TAQUICARDIAS SUPRAVENTRICULARES
Son aquellas que se originan y mantienen a través de estructuras situadas por encima de la división
del haz de His, es decir, las aurículas y/o el NAV. Suelen presentar un QRS estrecho, ya que la activación
ventricular tiene lugar a través del sistema específico de conducción. Las TSV pueden presentarse como
taquicardias de QRS ancho cuando se asocian a trastornos de conducción por las ramas (aberrancia) o a la
presencia de vías accesorias (preexcitación).
1.1. Taquicardia sinusal
La morfología de la onda P es la del ritmo sinusal. La frecuencia cardiaca se suele encontrar entre
90-120 lpm. Generalmente es secundaria a una causa fisiológica, como la respuesta al ejercicio físico, o
patológica (anemia, fiebre, hipertiroidismo y ansiedad). El tratamiento es el de la causa desencadenante.
1.2. Fibrilación auricular
Figura 5. Fibrilación auricular.
Concepto y epidemiología: la FA es la arritmia sostenida más frecuente y la responsable del
mayor número de hospitalizaciones (entre un 10-40% de pacientes con FA son hospitalizados
cada año). Su prevalencia se estima entre un 1,5-2% (3%) de la población, y se incrementa con
la edad en pacientes con HTA, insuficiencia cardiaca crónica, enfermedad coronaria,
enfermedad valvular, DM, obesidad y enfermedad renal crónica. Su presencia aumenta cinco
veces el riesgo de ictus, tres veces la incidencia de insuficiencia cardiaca y entre 1,5 y 2 veces la
mortalidad por todas las causas en hombres y mujeres. Se caracteriza por una despolarización
auricular desorganizada, con una contracción auricular ineficaz. En el ECG (Figura 5) se
observan ondas de actividad auricular que se caracterizan por ser irregulares, muy rápidas, de
bajo voltaje (ondas f), con una respuesta ventricular irregular (intervalos RR irregulares) y,
generalmente, rápida (salvo en presencia de tratamiento farmacológico o trastorno de
conducción preexistente).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [310]
[22] ARRITMIAS
Clínica y clasificación: en la evaluación clínica se debe incluir los síntomas secundarios a la
propia FA (palpitaciones, astenia, dolor torácico). Una aproximación objetiva la proporciona la
clasificación EHRA (Tabla II), que evalúa los síntomas producidos por la FA que desaparecen
cuando se restaura el ritmo sinusal o se consigue un control efectivo de la frecuencia. Su uso
ayuda a decidir qué estrategia de tratamiento es más recomendable. Además, la pérdida de la
actividad mecánica auricular puede precipitar un deterioro hemodinámico importante en
pacientes con cardiopatía previa, con aparición de síntomas y signos de insuficiencia cardiaca, y
la propia taquicardia mantenida puede llevar a un empeoramiento de la función sistólica
ventricular (taquimiocardiopatía). A todo ello hay que añadir las potenciales complicaciones
cardioembólicas y la consecuente necesidad de tratamiento antitrombótico crónico.
Tabla II. Puntuación de la European Heart Rhythm Association (EHRA).
En la tabla III se muestra la clasificación en función del patrón de presentación y de la cronología.
Tabla III. Clasificación de la fibrilación auricular.
Tratamiento: la actitud en la fase aguda es la descrita previamente para cualquier taquiarritmia
(ver Apartado II. “Aproximación diagnóstica y terapéutica inicial”). A medio-largo plazo se
decidirá entre una estrategia de control del ritmo (tratar de mantener el ritmo sinusal el mayor
tiempo posible) o de control de la frecuencia (mantener al paciente en FA y dirigir los esfuerzos
únicamente a controlar la respuesta ventricular) (Figura 6). Además se debe evaluar el riesgo
de fenómenos tromboembólicos y la indicación de anticoagulación.
Control de frecuencia: en estos pacientes se acepta la FA como ritmo cardiaco de base,
por lo que el objetivo es actuar sobre la frecuencia ventricular. Para ello, una vez
identificados y controlados los factores precipitantes (fiebre, hipoxia, anemia,
enfermedad tiroidea) se valorará el fármaco más adecuado para el control de la
frecuencia ventricular (Figura 7 y Tabla I). Si el tratamiento en monoterapia no es
efectivo resulta útil combinar la digoxina con un calcioantagonista no dihidropiridínico
o con un betabloqueante. Se recomienda reducir la dosis de digoxina en pacientes
tratados con verapamilo, en ancianos y en pacientes con insuficiencia renal. En general
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [311]
[22] ARRITMIAS
no se deben asociar calcioantagonistas y betabloqueantes (salvo en casos
seleccionados y bajo monitorización estrecha). A medio-largo plazo el control de la
frecuencia cardiaca se recomienda en pacientes con todo tipo de FA usando los mismos
fármacos empleados en la fase aguda. En la elección se debe tener en cuenta que los
betabloqueantes y los calcioantagonistas no dihidropiridínicos reducen la frecuencia
tanto en reposo como en ejercicio, frente a la digoxina, que es menos eficaz en el
ejercicio (Figura 8). En pacientes en los que no se consigue control de la respuesta
ventricular a pesar de estas combinaciones, y continúan sintomáticos o desarrollando
taquimiocardiopatía, ha de considerarse la ablación por radiofrecuencia del NAV previo
implante de un marcapasos definitivo.
Figura 6. Elección de la estrategia terapéutica en la fibrilación auricular.
Control del ritmo (Figuras 6 y 9): el objetivo es tanto recuperar como mantener el
ritmo sinusal. Las estrategias de control de ritmo y de frecuencia se asocian a tasas
similares de morbimortalidad, siempre y cuando se realice una buena profilaxis de
fenómenos tromboembólicos. En líneas generales se prefiere intentar una estrategia de
control de ritmo en pacientes jóvenes y/o sintomáticos (a pesar de haber conseguido
un adecuado control de FC de la FA). No obstante, los fármacos antiarrítmicos tienen
efectos adversos que pueden ser potencialmente graves, por lo que la elección de la
estrategia de control del ritmo se debe realizar basándose, en primer lugar, en la
seguridad del paciente. La cardioversión puede ser eléctrica o farmacológica (en el caso
de la CVE el pretratamiento con fármacos antiarrítmicos para aumentar el éxito de
devolver el ritmo sinusal debe ser considerado de forma individual en cada paciente).
En la figura 6 se resumen las indicaciones para seguir esta estrategia. De cara al empleo
de fármacos antiarrítmicos (Tabla I) es fundamental conocer si el paciente presenta
cardiopatía significativa, considerando como tal toda cardiopatía estructural excepto la
cardiopatía hipertensiva con hipertrofia leve-moderada de ventrículo izquierdo y el
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [312]
[22] ARRITMIAS
prolapso de válvula mitral sin insuficiencia mitral significativa asociada. Se ha de
sospechar la presencia de una cardiopatía estructural si hay historia de insuficiencia
cardiaca, existen anormalidades en la exploración cardiovascular (soplos, ingurgitación
yugular) o en las pruebas complementarias (ECG con signos de necrosis, bloqueo de
rama, crecimiento de cavidades o cardiomegalia en la radiografía de tórax,) y se
confirma mediante ecocardiograma. La recurrencia de la FA es frecuente (oscila entre
el 30-50% de los pacientes durante el primer año de seguimiento tras la cardioversión
en función de la cronología de la arritmia y del uso concomitante de fármacos
antiarrítmicos). Los factores que más influyen en este hecho son la edad avanzada, la
presencia de cardiopatía y la dilatación de la aurícula izquierda. Además de tratar los
potenciales factores desencadenantes y la cardiopatía subyacente, debe valorarse la
indicación de tratamiento antiarrítmico prolongado (Tabla I). De forma general, tras un
primer episodio autolimitado de FA y en la FA paroxística poco recurrente y bien
tolerada no se recomienda tratamiento antiarrítmico de mantenimiento, mientras que
en pacientes con episodios de FA frecuentes y mal tolerados, o en aquellos que
presenten descompensación de patología cardiaca asociada a FA, el tratamiento de
mantenimiento estaría indicado (el optar por una estrategia de tratamiento corto
frente a mantenido dependerá de las características de cada paciente). Hay que tener
en cuenta que si el tratamiento con un fármaco antiarrítmico fracasa para el objetivo
de mantener el ritmo sinusal, se puede alcanzar la respuesta clínica adecuada
cambiándolo por otro fármaco antiarrítmico. La ablación con catéter es una opción que
hay que tener en cuenta, especialmente en aquellos pacientes con FA paroxística
sintomática, a pesar del tratamiento farmacológico, en aquellos con FA persistente
sintomática a pesar del tratamiento farmacológico y cardioversión eléctrica (CVE)
(cuando hay posibilidades de mantener el ritmo sinusal en función de la edad, la
cardiopatía de base y el tamaño de las aurículas) y ocasionalmente como primera
opción terapéutica en pacientes seleccionados con FA paroxística sintomática y sin
cardiopatía estructural (habitualmente jóvenes con FA aislada).
Prevenir fenómenos tromboembólicos (Figura 10 y Tabla VI): la FA es la causa más
frecuente de embolismos de origen cardiaco y el 75% de los mismos se manifiestan
como ictus (el 20-30% de los ictus están en relación con FA). El riesgo es mayor al inicio
de la FA y en el periodo de pericardioversión, y es independiente de que la FA sea
paroxística, persistente o permanente. Los pacientes de menos de 65 años con FA
“aislada”, es decir, sin historia clínica previa ni evidencia ecocardiográfica de
enfermedad cardiovascular, tienen un riesgo de ictus o embolismo sistémico bajo
(0,85% al año). Esta probabilidad aumenta según se añaden factores de riesgo, lo que
pone de relieve la importancia de revaluar periódicamente la presencia de factores de
riesgo. Solo el tratamiento antitrombótico ha demostrado reducir la mortalidad
relacionada con la FA. Para la estratificación de riesgo de ictus en pacientes con FA no
valvular (definida como FA en ausencia de estenosis mitral reumática, válvula mecánica
o biológica cardiaca o reparación valvular mitral) se ha propuesto la escala CHA2DS2-
VASC (Tabla IV). En base a esta clasificación se recomienda anticoagular a aquellos
varones con una puntuación mayor o igual a uno y a aquellas mujeres con puntuación
mayor o igual a dos. No se recomienda anticoagulación en varones sin factores de
riesgo o en mujeres con un solo factor de riesgo. El tratamiento con doble terapia
antiagregante (aspirina 75-325 mg/día asociada a clopidogrel 75 mg, más eficaz que en
monoterapia) debe limitarse únicamente a aquellos pacientes con indicación de
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [313]
[22] ARRITMIAS
anticoagulación que rechacen dicho tratamiento, conociendo siempre que dicho
tratamiento aumenta el riesgo de sangrado de forma similar a la anticoagulación y es
menos eficaz frente a la prevención del ictus.
Figura 7. Elección del fármaco para el control de la frecuencia en la fase aguda (FA).
Figura 8. Tratamiento farmacológico para control de frecuencia en la fibrilación auricular (a largo plazo).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [314]
[22] ARRITMIAS
Figura 9. Algoritmo para control de ritmo en la fibrilación auricular.
Tabla IV. Escala de riesgo trombótico CHA2DS2-VASC.
Es fundamental antes de tomar una decisión, en lo relativo al tratamiento antitrom- bótico,
determinar el riesgo hemorrágico del paciente, especialmente de eventos hemorrágicos mayores como la
hemorragia intracraneal (que es la complicación más temida de la anticoagulación y se asocia con una
elevada mortalidad y discapacidad). Para ello, la escala de riesgo hemorrágico HAS-BLED es la más utilizada
(Tabla V). Es obligatoria la revisión periódica del riesgo de sangrado de cada paciente, así como la
corrección de los factores de riesgo de sangrado potencialmente reversibles (HTA, patología
gastrointestinal...). Sin embargo, un elevado riesgo hemorrágico per se no debe considerarse como único
dato para excluir a un paciente del tratamiento anticoagulante.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [315]
[22] ARRITMIAS
Tabla V. Escala de riesgo hemorrágico HAS-BLED.
Tabla VI. Duración recomendada de tratamiento anticoagulante.
El cierre percutáneo de la orejuela izquierda debe valorarse en aquellos pacientes con elevado
riesgo tromboembólico que presenten contraindicación para la anticoagulación prolongada (por ejemplo
por eventos hemorrágicos graves o embolias a pesar de una correcta anticoagulación).
Actualmente existen distintas opciones terapéuticas para llevar a cabo la anticoagulación. Por una
parte contamos con los fármacos inhibidores de la vitamina K, como son el acenocumarol y la warfarina,
aceptándose como rango terapéutico un INR entre 2-3 (entre 2,5-3,5 si el paciente es portador de prótesis
mitral mecánica) y con objetivo de tiempo terapéutico en rango superior al 70% durante el seguimiento.
Además, recientemente se han añadido los denominados nuevos anticoagulantes orales (NACO). Este
grupo lo integran el dabigatrán (inhibidor directo de la trombina), el rivaroxabán, el apixabán y el edoxabán
(inhibidores directos del factor Xa). En relación con los NACO estos ofrecen mayor eficacia (en términos de
reducción de la tasa de accidente cerebrovascular o embolismo sistémico) y mejor perfil de seguridad en
relación con eventos hemorrágicos mayores (presentando dabigatrán, rivaroxabán y edoxabán mayor tasa
de sangrado gastrointestinal) en comparación con warfarina. Están indicados en pacientes con FA no
valvular y no requieren un ajuste periódico de dosis basado en un parámetro de la coagulación, pero deben
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [316]
[22] ARRITMIAS
administrarse con precaución (dosis baja) en pacientes con insuficiencia renal moderada y están
contraindicados en presencia de insuficiencia renal grave.
Figura 10. Tratamiento antitrombótico en la FA.
1.3. Flutter auricular
Concepto: es una arritmia que se caracteriza por un ritmo auricular rápido, regular y
organizado, visible en el ECG en forma de ondas monomorfas sin que exista un segmento
isoeléctrico entre ellas (aspecto de “dientes de sierra”), que se denominan ondas F. Se
producen como consecuencia de la aparición de grandes circuitos de reentrada
(macrorreentradas) a nivel de las aurículas.
Clínica: suele presentarse como una taquicardia regular de QRS estrecho con una respuesta
ventricular en torno a 150 lpm, ya que suele existir bloqueo fisiológico 2:1 a nivel del NAV.
Puede observarse conducción 1:1 en pacientes con vía accesoria con conducción anterógrada
rápida, en situaciones de exceso de catecolaminas o por efecto de fármacos antiarrítmicos
como flecainida (que ralentiza las ondas de flutter y permite la conducción 1:1 a los
ventrículos). Asimismo, puede existir mayor grado de bloqueo (3:1, 4:1.…) bajo tratamiento con
fármacos frenadores del NAV o cuando coexiste enfermedad del sistema intrínseco de
conducción. En algunos casos la respuesta ventricular puede ser irregular, por conducción AV
variable, y en otros el QRS puede ser ancho (vía accesoria, bloqueo de rama preexistente o
funcional).
Clasificación: la forma más frecuente es el flutter típico o ístmico, denominado así por
originarse por un circuito de macrorreentrada alrededor del anillo tricuspídeo. El flutter típico
(Figura 11), a su vez, puede dividirse en común (el circuito recorre el anillo tricuspídeo en
sentido antihorario, con una frecuencia de ondas F de 250-350 lpm, con polaridad negativa en
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [317]
[22] ARRITMIAS
ii, iii, aVF, V5 y V6 y positiva en V1) y en inverso (activación en sentido horario con ondas
positivas en la cara inferior). El flutter atípico no gira alrededor del anillo tricuspídeo, sino de
otras estructuras auriculares o cicatrices previas y pueden presentar una frecuencia auricular
mayor y ondas F con distinta polaridad y, a menudo, “melladas”. La distinción entre ambos
tipos de flutter es importante, ya que tiene implicaciones terapéuticas de cara a plantear la
interrupción del circuito mediante la ablación por catéter. Con cierta frecuencia el flutter
coexiste con fibrilación auricular.
Figura 11. Flutter auricular común.
Tratamiento: es superponible al descrito para la FA, aunque con ciertos aspectos distintivos. En
general la CVE sincronizada es muy eficaz para interrumpirlo, siendo suficiente, generalmente,
energías de 50-100 J. Por el contrario, suele tener mala respuesta a la cardioversión
farmacológica: los fármacos del grupo Ic (flecainida, propafenona), grupo Ia (procainamida,
quinina) y III (amiodarona) tienen una eficacia bastante limitada y presentan riesgo de
proarritmia y efecto inotrópico negativo. Además pueden enlentecer la frecuencia auricular y
favorecer una conducción 1:1 a los ventrículos, por lo que deben utilizarse asociados a
fármacos que controlen la respuesta ventricular, especialmente si se emplea la quinina o la
flecainida. En general esto no es necesario con amiodarona (ya que tiene capacidad intrínseca
frenadora del NAV). Cuando se opta por un control de la frecuencia se pueden emplear los
mismos fármacos descritos para la FA, aunque en general son menos eficaces. Además el flutter
puede aparecer en el contexto de otras patologías, como la exacerbación de la EPOC o la
embolia pulmonar, y el tratamiento adecuado de las mismas es fundamental para el control de
la arritmia. Tras el episodio agudo hay que plantear un tratamiento preventivo de nuevas
recurrencias. La ablación mediante radiofrecuencia de la parte más vulnerable del circuito: el
istmo cavo-triscuspídeo tiene un alto índice de éxito (mayor del 95%) con bajo riesgo de
complicaciones, por lo que se ha convertido en el tratamiento de elección en el flutter típico en
la gran mayoría de los casos. El tratamiento farmacológico tiene un papel muy limitado, tanto
por su escasa eficacia como por sus efectos adversos, entre los que destaca la proarritmia.
Pueden utilizarse fármacos Ic (propafenona, flecainida) y III (amiodarona o sotalol).
En los casos de flutter atípico la ablación es más compleja, puesto que debe delimitarse el
circuito en las aurículas, que habitualmente tiene relación con la presencia de escaras y/o
cicatrices quirúrgicas en las aurículas. En casos no susceptibles de ablación, con mal control de
los síntomas, intolerancia al tratamiento antiarrítmico o comportamiento incesante (pueden
ocasionar disfunción sistólica por taquimiocardiopatía) estaría indicada la ablación del NAV e
implante de un marcapasos definitivo como última opción terapéutica.
Ante todo flutter auricular recurrente o primer episodio sintomático, o en pacientes con
cardiopatía estructural, se recomienda remitir directamente al paciente a una unidad
especializada en arritmias. Por último, aunque el riesgo embólico se supone menor que el de la
FA, se recomienda anticoagulación con las mismas pautas que en esta.
1.4. Taquicardias auriculares
Al igual que el caso del flutter, las taquicardias auriculares solo precisan de tejido auricular para su
mantenimiento. A diferencia de este se originan en zonas concretas de la aurícula, por lo que se denominan
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [318]
[22] ARRITMIAS
de forma más específica “taquicardias auriculares focales”. La frecuencia de las ondas P es variable, entre
130-220 lpm, y su morfología dependerá del punto en el que se origine la despolarización auricular (en
general será negativa en II, III y aVF cuando el origen esté en la parte inferior de la aurícula, o negativa en I
y aVL y positiva en V1 cuando la activación auricular proceda de la aurícula izquierda), siendo la frecuencia
ventricular variable en función de la conducción a los ventrículos. Con maniobras vagales o adenosina/ATP,
al aumentar el grado de bloqueo, se reduce la respuesta ventricular, pero habitualmente no se interrumpe
la taquicardia, lo que resulta útil para el diagnóstico diferencial con otras taquiarrimias supraventriculares
(TSV). Las taquicardias auriculares con frecuencia tienen comportamiento paroxístico o incesante. Pueden
distinguirse dos tipos: unifocal y multifocal.
Taquicardia auricular unifocal: la onda P tiene una morfología constante. El mecanismo de la
misma puede ser por aumento del automatismo (pacientes con neuropatías, intoxicación
digitálica –a menudo con bloqueo AV 2:1 o más avanzado– y también en personas jóvenes sin
cardiopatía) o por pequeños circuitos de reentrada (microrreentradas). El tratamiento agudo se
basa en la corrección de los factores desencadenantes y en aplicar los algoritmos descritos (ver
Apartado II. “Aproximación diagnóstica y terapéutica inicial”). Como tratamiento preventivo
son de elección los calcioantagonistas no dihidropiridínicos y betabloqueantes, pudiéndose
administrar fármacos del grupo Ic o amiodarona como segunda opción. Si el paciente persiste
sintomático a pesar del tratamiento farmacológico debe valorarse la posibilidad de realizar un
estudio electrofisiológico y, mediante radiofrecuencia, tratar de practicar una ablación en el
foco de la taquicardia.
Taquicardia auricular multifocal: se caracteriza por la presencia de ondas P de al menos tres
morfologías diferentes de la sinusal, con intervalos PP irregulares. Aparece en general en
enfermos graves (hipoxia, exacerbaciones de EPOC, alteraciones electrolíticas, uso de
teofilinas). El tratamiento se basa en corregir o mejorar la causa subyacente. Responde mal al
tratamiento antiarrítmico, aunque pueden ser eficaces el sulfato de magnesio o el verapamilo
(contraindicado en pacientes con disfunción ventricular). La CVE no es eficaz y por lo tanto no
está indicada.
1.5. Taquicardias por reentrada intranodal
Es la TSV paroxística más frecuente, especialmente en mujeres de edad media, y la sintomatología
se suele presentar más comúnmente en forma de palpitaciones de inicio y fin brusco que se perciben en el
cuello. Se produce por un mecanismo de reentrada en el NAV, y el sustrato anatómico-funcional es la
existencia de dos vías de conducción a través del NAV, con velocidades de conducción y periodos
refractarios distintos. En la taquicardia por reentrada intranodal (TRIN) común (Figura 12), que es la forma
más frecuente, el estímulo eléctrico se dirige al ventrículo por la vía lenta y vuelve a la aurícula por la vía
rápida. En esta forma en el ECG los QRS y las ondas P retrógradas se superponen, de forma que las ondas P
pueden no ser visibles o deformar ligeramente la porción final del QRS (pseudo-S en II, III y aVF, o pseudo-r´
en V1). El tratamiento agudo (ver Apartado II. “Aproximación diagnóstica y terapéutica inicial”) se basa en
realizar maniobras vagales (maniobra de Valsalva o masaje del seno carotídeo). Si la taquicardia persiste se
puede emplear tratamiento farmacológico para el bloqueo del NAV.
Los fármacos de primera elección son el ATP o la adenosina, por su alta eficacia (superior al 90%) y
la corta duración de su efecto. Además resultan útiles para el diagnóstico diferencial entre las taquicardias
por reentrada AV y las auriculares. El verapamilo intravenoso tiene una eficacia similar y una vida media
más larga, por lo que resulta útil si la taquicardia recurre tras la administración de ATP, o si este está
contraindicado, pero debe evitarse en las taquicardias de QRS ancho por el riesgo de provocar inestabilidad
hemodinámica grave por su efecto inotrópico negativo. Hay que individualizar el tratamiento preventivo en
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [319]
[22] ARRITMIAS
función de la frecuencia y repercusión clínica de los episodios. En algunos casos puede ser suficiente la
realización de maniobras vagales por el paciente o el tratamiento farmacológico solo durante las crisis, sin
precisar tratamiento crónico. En caso de recurrencias frecuentes, que afecten a la calidad de vida o por
elección del paciente, existen dos opciones: los fármacos frenadores del NAV como verapamilo,
betabloqueantes de vida media larga, o antiarrítmicos del grupo Ic (salvo en pacientes con cardiopatía
estructural relevante), ambos grupos disminuyen el número de episodios y la frecuencia de la taquiarritmia,
y la ablación por radiofrecuencia, que se plantea como un tratamiento curativo al eliminar el sustrato.
Actualmente, esta última es la alternativa más empleada y se recomienda ofrecerla a los pacientes dada la
elevada eficacia (mayor del 90%) con baja tasa de complicaciones (menor del 1% de bloqueo del nodo AV).
Figura 12. Taquicardia por reentrada intranodal.
1.6. Taquicardias por vía accesoria
Se producen en presencia de fibras de conducción (bandas de tejido miocárdico) anormales que
conectan eléctricamente las aurículas y los ventrículos. Se trata de trastornos congénitos, por lo que las
arritmias que asocian son más frecuentes en niños y adultos jóvenes que en pacientes de edad avanzada.
La mayoría de las vías accesorias se dan en pacientes sin cardiopatía estructural; sin embargo, en ciertas
cardiopatías son relativamente más frecuentes como en la enfermedad de Ebstein, la miocardiopatía
hipertrófica o la válvula aórtica bicúspide.
Cuando en ritmo sinusal la vía accesoria tiene capacidad de conducción anterógrada origina un
patrón electrocardiográfico de preexcitación: PR corto, onda delta (empastamiento inicial del QRS) y QRS
ancho. Esto se produce porque la vía accesoria conduce más rápidamente que el NAV, por lo que la
activación ventricular se adelanta (preexcitación), originando un intervalo PR corto. Como esta activación
ventricular se lleva a cabo a través de fibras miocárdicas y a través del sistema específico de conducción, la
porción inicial del QRS se ensancha, originando la onda delta. La porción final del QRS es normal porque
depende del sistema de conducción. Si la vía accesoria solo tiene capacidad de conducción retrógrada se
denomina vía oculta: el ECG en ritmo sinusal es normal, pero existe un sustrato para la aparición de
taquicardias. Cuando la vía accesoria interviene en la producción de taquicardias se habla de síndrome de
Wolf Parkinson White (WPW). Los pacientes asintomáticos con patrón de preexcitación en el ECG no
precisan tratamiento, salvo que desempeñen determinadas profesiones (pilotos, conductores profesionales
o deportistas), en los que se recomienda la ablación. El riesgo de presentar arritmias en los pacientes
asintomáticos es de aproximadamente 1,7% al año y el de presentar muerte súbita se estima en 1/1.000
pacientes al año. No obstante, ya que los riesgos de la ablación son actualmente bajos y es un
procedimiento potencialmente curativo, se debe informar al paciente de las opciones terapéuticas.
Taquicardia por reentrada auriculoventricular mediada por vía accesoria
Esta taquicardia es más frecuente en varones, generalmente sin cardiopatía estructural y
clínicamente se suele presentar en forma de palpitaciones de inicio y fin brusco que se perciben
en el tórax. En estas taquicardias la vía accesoria permite constituir un circuito de reentrada en
el que están involucrados la propia vía accesoria, la aurícula, el NAV y el ventrículo. En la forma
típica de taquicardia mediada por vía accesoria, denominada ortodrómica, el NAV conduce
anterógradamente, despolarizando el ventrículo a través del sistema específico de conducción,
por lo que el QRS es estrecho (salvo bloqueo de rama preexistente o desarrollado durante la
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [320]
[22] ARRITMIAS
taquicardia), mientas que la vía accesoria conduce el impulso retrógradamente a la aurícula. En
esta forma en el ECG los QRS y las ondas P retrógradas se pueden superponer (de forma similar
a las taquicardias por reentrada intranodal, aunque el intervalo RP suele ser más largo que en
estas). En la forma antidrómica, muy poco frecuente (generalmente en pacientes con varias
vías), la vía accesoria conduce anterógradamente y produce una taquicardia de QRS ancho que
puede ser indistinguible de una taquicardia ventricular. El tratamiento del episodio agudo de
estas taquicardias en caso de compromiso hemodinámico severo (hipotensión grave, síncope)
es la CVE inmediata (ver Apartado II. “Aproximación diagnóstica y terapéutica inicial”). En
general, si la taquicardia es ortodrómica (QRS estrecho) y bien tolerada se puede tratar de
forma similar a la descrita para la TRIN, con maniobras vagales y/o fármacos frenadores del
NAV (adenosina/ATP). Sin embargo, cualquier frenador del nodo se debe evitar si la taquicardia
presenta un QRS ancho (antidrómica), dada la dificultad del diagnóstico diferencial con la TV y
la posibilidad de provocar inestabilidad hemodinámica, aunque sí pueden intentarse maniobras
vagales o adenosina. Se pueden emplear en cualquier caso antiarrítmicos como la flecainida,
propafenona o amiodarona que actúan sobre la vía accesoria.
En la prevención de recurrencias de taquicardia reentrantes por vía accesoria (orto o
antidrómica), el tratamiento de elección de los pacientes sintomáticos es la realización de un
estudio electrofisiológico que permita la localización anatómica de la vía accesoria y la ablación.
b)
Taquicardias preexcitadas
La presencia de una vía accesoria puede favorecer la conducción rápida a los ventrículos de
cualquier TSV. Dada su frecuencia relativa y el riesgo de transformación en fibrilación
ventricular (FV) hay que resaltar la FA preexcitada. Es una arritmia irregular con QRS ancho y
variable. El tratamiento recomendado, si hay inestabilidad hemodinámica, es la CVE (también
se puede emplear la flecainida o propafenona iv). Se contraindican los frenadores del nodo AV
por el riesgo de favorecer la conducción por la vía accesoria y el potencial riesgo de
degeneración a FV. Tampoco se recomienda la amiodarona por el mismo motivo: tiene un
efecto hipotensor y depresor de la conducción nodal cuando se administra por vía intravenosa,
por lo que se han descrito casos de inducción de FV tras su administración en este contexto.
2. TAQUIARRITMIAS VENTRICULARES
2.1. Concepto y epidemiología
La presencia de tres o más complejos de origen ventricular (frecuencia superior a 100 lpm) se
denomina taquicardia ventricular. Una taquicardia ventricular sostenida se define como aquella cuya
duración es superior a 30 seg o que produce inestabilidad hemodinámica (Tabla VII).
Las taquiarritmias ventriculares (TV) suponen más del 80% de las muertes súbitas (en jóvenes en
relación con canalopatías y miocardiopatías y en adultos en relación con enfermedad coronaria,
valvulopatías y disfunción ventricular). La mayoría se deben a FV, a menudo precedida de una TV. Por ello,
es crucial el diagnóstico diferencial de las TV (potencialmente malignas) frente a otras taquicardias de QRS
ancho benignas (TSV con conducción aberrante) (ver Apartado II. “Aproximación diagnóstica y terapéutica
inicial”).
2.2. Clasificación de las taquicardias ventriculares
Las taquicardias ventriculares pueden ser monomórficas o polimórficas (Tabla VII). Las primeras
tienen una morfología constante mientras que en las segundas la morfología del QRS es cambiante y son
más inestables, teniendo mayor riesgo de degenerar en FV.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [321]
[22] ARRITMIAS
Tabla VII. Clasificación de las taquicardias ventriculares.
Taquicardia ventricular monomorfa sostenida
Su etiología más frecuente es la cardiopatía isquémica crónica (tras un infarto de miocardio)
(Figura 13). Su mecanismo consiste en un fenómeno de macrorreentrada cuyo sustrato es el
tejido fibroso miocárdico (canales de tejido viable que discurren en el interior o los bordes de
una cicatriz de un infarto de miocardio previo). Las formas sostenidas constituyen arritmias
malignas, habitualmente recurrentes, capaces de degenerar en FV y provocar muerte súbita.
Generalmente pueden ser inducibles mediante estimulación eléctrica programada. El
tratamiento del episodio agudo es el descrito en Apartado II. “Aproximación diagnóstica y
terapéutica inicial”. Tras un episodio de TV en pacientes con cardiopatía isquémica crónica, es
importante valorar la función ventricular del paciente, así como la tolerancia clínica a los
episodios. Los betabloqueantes son los únicos fármacos que han demostrado disminuir la
muerte súbita tras un IAM. En estos pacientes se puede plantear la realización de un estudio
electrofisiológico de inducción con eventual ablación, el tratamiento crónico con fármacos
antiarrítmicos y/o el implante de un desfibrilador automático implantable (DAI). El uso de
fármacos antiarrítmicos también se planteará para reducir los choques en pacientes con un
DAI, o junto con betabloqueantes en pacientes con TV no candidatos a implante de un DAI.
Como antiarrítmicos se emplearán amiodarona (de elección si existe disfunción ventricular) o
sotalol, dado su menor efecto proarrítmico, comparado con los fármacos de clase I (el uso
crónico de estos últimos se ha asociado con un incremento en la mortalidad).
Figura 13. Taquicardia ventricular monomorfa sostenida.
Taquicardia ventricular polimorfa
Es una TV rápida, irregular, con complejos QRS de morfología cambiante, cuya frecuencia suele
oscilar entre 200-250 lpm, y que, con frecuencia, degenera en FV. Suele aparecer en el contexto
de isquemia aguda o alteraciones hidroelectrolíticas. También pueden observarse asociadas a la
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [322]
[22] ARRITMIAS
miocardiopatía hipertrófica o al síndrome de Brugada. La TV en torsade des pointes se observa
en pacientes con QT largo congénito o adquirido. En el tratamiento del episodio agudo en los
casos de QT largo adquiridos puede utilizarse sulfato de magnesio (1-2 g iv en al menos 10
minutos, seguido de 200-300 mg por hora durante cuatro a ocho horas), pero no se recomienda
la administración de antiarrítmicos. A veces la torsade de pointes puede producirse o verse
favorecida por bradicardia, por lo que en estos casos puede ser útil la infusión de isoproterenol
o el implante de un marcapasos transitorio o definitivo.
En los pacientes con QT largo congénito que presentan arritmias ventriculares polimórficas
debe plantearse el implante de un DAI.
Taquicardias ventriculares en situaciones especiales
Taquicardias ventriculares en pacientes con miocardiopatía: tanto la miocardiopatía
dilatada como la hipertrófica pueden originar TV no sostenidas y sostenidas. En la
miocardiopatía dilatada aproximadamente el 50% de las muertes ocurren de forma
súbita, posiblemente como consecuencia de arritmias ventriculares. Una variedad
presente en pacientes con dilatación de ventrículo izquierdo y trastornos de
conducción intraventricular es la denominada taquicardia por reentrada rama a rama,
cuyo mecanismo es una macrorreentrada en la que típicamente el brazo anterógrado
es la rama derecha y el brazo retrógrado es la rama izquierda (apareciendo en el ECG
como una taquicardia regular de QRS ancho con bloqueo de rama izquierda [BRI] y eje
izquierdo). La terapia de elección curativa es la ablación por radiofrecuencia de la rama
derecha.
Taquicardias ventriculares idiopáticas: se presentan en pacientes sin cardiopatía
estructural. En general son bien toleradas y tienen buen pronóstico, pero en ciertos
casos pueden provocar síncope o taquimiocardiopatía. Las más frecuentes son las que
se originan en el tracto de salida (aproximadamente el 70%) como consecuencia de la
aparición de focos ectópicos que compiten con el NS. Dentro de estas las que se
originan en el tracto de salida del ventrículo derecho son las más frecuentes (patrón en
ECG de BRI, eje inferior y transición en V3), aunque también pueden aparecer en el
tracto de salida del ventrículo izquierdo (patrón en ECG de BRI (70%) o de BRD (30%),
eje inferior y transición en V1/V2), o en relación con los senos de Valsalva aórticos.
Menos frecuente es otra entidad denominada taquicardia fascicular, que se presenta
en el ECG con un patrón de BRD, eje superior e izquierdo y QRS > 120 ms, aunque
relativamente estrecho (en su variante más frecuente, que es la TV relacionada con la
hemirrama posterior). El tratamiento habitual de elección en los casos sintomáticos son
los betabloqueantes. Si los episodios no se controlan a pesar de tratamiento médico
(betabloqueantes y/o antiarrítmicos) debe plantearse un estudio electrofisiológico
dirigido a la ablación del sustrato (con una tasa de éxito en el caso de las taquicardias
de tracto de salida del ventrículo derecho superiores al 90%, con muy baja tasa de
complicaciones).
Displasia arritmogénica del ventrículo derecho: es más frecuente en varones y se
caracteriza por la sustitución de los cardiomiocitos por tejido adiposo y fibroso. Hasta
en un 50% de los pacientes se produce también afectación del ventrículo izquierdo. El
ECG típico se caracteriza por bloqueo de rama derecha (BRD) con una “muesca” al final
del QRS en precordiales derechas, denominada “onda épsilon”, bajos voltajes y T
negativas también en precordiales derechas. El tratamiento antiarrítmico de elección es
el sotalol o la amiodarona. En los pacientes que presentan arritmias ventriculares
sostenidas debe plantearse el implante de un DAI. La ablación por radiofrecuencia tiene
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [323]
[22] ARRITMIAS
tasas de éxito variables y son frecuentes las recurrencias por el carácter progresivo de
la enfermedad.
Síndrome de Brugada: es una enfermedad genética más frecuente en varones y en el
sudeste asiático, que ocurre en ausencia de cardiopatía estructural y que se debe a una
pérdida de los canales de sodio de la membrana celular. Existen tres patrones clásicos
electrocardiográficos, siendo diagnóstico solo el primero, que consiste en una imagen
de BRD y elevación del segmento ST > 2 mm en forma de “lomo de delfín” con onda T
negativa en las derivaciones V1 a V2 (pudiendo ser este patrón espontáneo o tras un
test de provocación farmacológico). Se asocia a un riesgo aumentado de TV polimorfas
y muerte súbita. Dichos episodios son más frecuentes durante el sueño, episodios
febriles, con el empleo de antiarrítmicos del grupo I, así como con el consumo de
cocaína y alcohol. El único tratamiento eficaz para la prevención de muerte súbita en
estos pacientes es el implante de un DAI.
Ritmo idioventricular acelerado: es un ritmo ventricular con una frecuencia
habitualmente entre 60-100 lpm. Se produce a menudo como signo de reperfusión
coronaria en los IAM. Es especialmente común en los IAM inferoposteriores,
asociándose frecuentemente con bradicardia sinusal. No se asocia a mal pronóstico y
no requiere tratamiento específico. En caso de deterioro hemodinámico se puede
utilizar la atropina iv.
Fibrilación ventricular: es una forma de TV polimórfica en la cual no puede distinguirse
la despolarización de la repolarización miocárdica, y da lugar a una contracción
ventricular ineficaz, con una frecuencia superior a 250 lpm, irregular y de morfología
caótica, sin pulso, que debe tratarse con choque eléctrico no sincronizado.
II. BRADIARRITMIAS
1. CONCEPTO
Las bradiarritmias y los bloqueos de la conducción son una observación clínica frecuente y pueden
ser una reacción fisiológica (por ejemplo en deportistas sanos) o corresponder a un trastorno patológico. Se
definen por la presencia de una frecuencia cardiaca < 60 lpm.
2. PRESENTACIÓN CLÍNICA
La forma de presentación clínica de las arritmias abarca desde signos electrocardiográficos
asintomáticos hasta una amplia variedad de síntomas (mareo, aturdimiento, vértigo, presíncope, síncope,
crisis de Adam-Stokes, fatiga, letargia etc.).
3. CLASIFICACIÓN DE LAS BRADIARRITMIAS
Se clasifican en dos grandes grupos: la disfunción del nódulo sinusal y las alteraciones de la
conducción auriculoventricular.
1. DISFUNCIÓN DE NÓDULO SINUSAL (DNS)
Es un trastorno crónico y progresivo que afecta a la generación del impulso del nódulo sinusal y su
transmisión en el interior de las aurículas, y se produce principalmente en ancianos (Tabla VIII). Las
manifestaciones en el ECG son:
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [324]
[22] ARRITMIAS
Tabla VIII. Causas de disfunción del nódulo sinusal.
1.1. Bradicardia sinusal
Se define por una frecuencia cardiaca < 60 lpm. Habitualmente es más una reacción fisiológica que
un estado patológico. Se aprecia frecuentemente en deportistas, adultos jóvenes en reposo, por la noche y
de forma transitoria por un aumento del tono vagal (Figura 14).
Figura 14. Bradicardia sinusal.
1.2. Bloqueo sinoauricular
Se definen como el retraso o el bloqueo del impulso sinusal a las aurículas. Solo pueden
diagnosticarse por ECG de superficie los bloqueos sinoauriculares de segundo grado (es decir, los
intermitentes). Estos, a su vez, se dividen en dos tipos:
Mobitz I o Wenckebach: la conducción hacia las aurículas se retrasa progresivamente hasta
que se produce una pausa sinusal (intervalo P-P, que es progresivamente más corto hasta que
se produce la pausa).
Mobitz II: la conducción sinoauricular es fija antes del bloqueo completo del estímulo sinusal
(no hay acortamiento progresivo del intervalo PP). La pausa que se origina es el doble al
intervalo PP de base.
1.3. Pausas sinusales o paradas
Las pausas de tres segundos o más se consideran significativas y pueden justificar la implantación
de un marcapasos en los pacientes sintomáticos (Figura 15).
Figura 15. Pausa sinusal.
1.4. Incompetencia cronotrópica
Se define como la incapacidad del corazón de ajustar adecuadamente su frecuencia en respuesta al
aumento de la actividad física. El criterio utilizado es no alcanzar el 80% de la frecuencia cardiaca máxima
esperada (220 menos la edad) en el ejercicio máximo de una prueba de esfuerzo.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [325]
[22] ARRITMIAS
2. BLOQUEO AURICULOVENTRICULAR
Es un trastorno en el que los impulsos auriculares son conducidos con retraso o no son conducidos
a los ventrículos. El bloqueo AV adquirido puede estar causado por diversos trastornos extrínsecos e
intrínsecos (Tabla IX). Se clasifica según criterios electrocardiográficos en bloqueo auriculoventricular (BAV)
de primer (parcial), segundo (intermitente) o tercer grado (completo). Dado que el segmento PR incluye la
conducción auricular, nodal y de sistema ventricular de conducción, muchas veces es difícil determinar por
el ECG de superficie la localización del bloqueo. En función de los registros de electrofisiología intracardiaca
pueden diferenciarse bloqueos suprahisianos (en el nodo AV), intrahisianos (en el haz de His) o infrahisiano
(distales al haz de His).
2.1. Bloqueo auriculoventricular de primer grado
Prolongación anormal del intervalo PR (> 0,2 seg) en forma constante. Todas las ondas P se siguen
de un complejo QRS (Figura 16).
Figura 16. Bloqueo auriculoventricular de primer grado.
2.2. Bloqueo auriculoventricular de segundo grado
En este tipo de bloqueo la conducción a los ventrículos es intermitente y suele seguir un patrón
estable. Se señala con el código X:Y, siendo X el n.º de P totales e Y el n.º de P conducidas a los ventrículos
en una secuencia determinada (ejemplo: en el BAV 3:2 se conducen dos de cada tres ondas P). Puede
dividirse en dos tipos, según los patrones del ECG: tipo Mobitz I o de Wenckebach y tipo Mobitz II.
Tipo Mobitz I: el BAV de segundo grado Mobitz tipo i clásico se caracteriza por una
prolongación progresiva del intervalo PR hasta que una P se bloquea (fenómeno de
Wenckebach). Antes del impulso bloqueado debe haber al menos dos ondas P conducidas (es
decir, un bloqueo AV 3:2) para poder determinar el comportamiento de los intervalos PR.
Puede ser fisiológico durante el sueño, en personas jóvenes o con hipertonía vagal (Figura 17).
Figura 17. Bloqueo auriculoventricular de segundo grado Mobitz I.
Tipo Mobitz II: se define por la aparición de una sola onda P no conducida asociada a intervalos
PR constantes, antes y después de un solo impulso bloqueado. De nuevo precisamos dos ondas
P consecutivas conducidas para hacer el diagnóstico (Figura 18).
Figura 18. Bloqueo auriculoventricular de segundo grado Mobitz II (3:2).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [326]
[22] ARRITMIAS
Bloqueo auriculoventricular 2:1
Hay una onda P conducida que alterna con una onda P bloqueada. En un bloqueo AV 2:1 es
difícil distinguir si el bloqueo AV es de tipo I o tipo II mediante un ECG de superficie (Figura 19).
Figura 19. Bloqueo auriculoventricular 2:1.
Bloqueo auriculoventricular avanzado o alto grado
Se debe a que al menos dos estímulos (ondas P consecutivas) son bloqueadas. Se corresponde
con los BAV 3:1, 4:1 o superiores (Figura 20).
Figura 20. Bloqueo auriculoventricular avanzado.
3. BLOQUEO AURICULOVENTRICULAR DE TERCER GRADO O COMPLETO
Se caracteriza por el fallo de la conducción al ventrículo en cada onda P o cada impulso auricular,
con lo que se produce una disociación AV completa, con unas frecuencias auriculares superiores a las
ventriculares. Puede ser congénito o adquirido. El ritmo de escape ventricular revela la localización
anatómica del bloqueo: un bloqueo AV completo con un ritmo de escape de 40 a 60 lpm y un complejo QRS
estrecho en el ECG de superficie se encuentra generalmente dentro de la unión AV y se observa a menudo
en el BAV congénito (Figura 21). Un complejo QRS ancho asociado a una frecuencia de 20 a 40 lpm implica
generalmente un bloqueo en el sistema de His-Purkinje (Figura 22).
Figura 21. Bloqueo auriculoventricular de tercer grado, con QRS estrecho (suprahisiano).
Figura 22. Bloqueo auriculoventricular de tercer grado, con QRS ancho (infrahisiano).
4. DIAGNÓSTICO Y TERAPÉUTICA INICIAL
La historia clínica es útil para valorar la correlación de los síntomas y el ritmo, la repercusión
hemodinámica y descartar causas reversibles (ver Tablas VIII y IX). El ECG de superficie generalmente
aporta la información necesaria para caracterizar el tipo y localizar el nivel en que se encuentra el bloqueo
(Figura 23). En los pacientes con un BAV intermitente, el registro del ECG Holter y la prueba de esfuerzo son
importantes para establecer una correlación entre los síntomas y el ritmo.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [327]
[22] ARRITMIAS
Tabla IX. Causas de bloqueo auriculoventricular.
Figura 23. Diagnóstico de bradiarritmias.
En la fase aguda una bradiarritmia sintomática con inestabilidad hemodinámica debe ser tratada
con fármacos vagolíticos por vía intravenosa, como la atropina, el isoproterenol, la dopamina (Figura 24) o
colocación de marcapasos temporal transcutáneo y si está disponible de inmediato estimulación por vía
endovenosa. Los pacientes estables deben ser monitorizados continuamente con marcapasos de
estimulación transcutánea para valorar síntomas relacionados con bradicardia, la identificación y el
tratamiento de las causas reversibles.
Figura 24. Manejo de la bradiarritmias.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [328]
[22] ARRITMIAS
El marcapasos permanente es el tratamiento de elección establecido en la mayoría de los casos de
bradiarritmias sintomáticas, una vez descartadas causas corregibles como los fármacos antiarrítmicos o las
alteraciones hidroelectrolíticas (por ejemplo, hiperpotasemia). La indicación depende del tipo y la
localización del bloqueo, los síntomas, el pronóstico y las enfermedades concomitantes (Tablas X y XI).
Tabla X. Indicaciones de marcapasos cardiaco en la disfunción del nódulo sinusal.
Tabla XI. Recomendaciones para el uso de marcapasos cardiaco en el bloqueo auriculoventricular adquirido.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [329]
[22] ARRITMIAS
III. MARCAPASOS: CONCEPTO, INDICACIONES Y DISFUNCIÓN
1. CONCEPTO Y NOMENCLATURA
Los marcapasos son dispositivos diseñados para la corrección de los defectos de conducción
cardiacos, supliendo la función eléctrica fisiológica del corazón. En general, el marcapasos está compuesto
por un generador que se coloca, en la mayoría de los casos, en la región prepectoral izquierda, por debajo
de la clavícula. Dicho generador se conecta a través de unas sondas a las cavidades cardiacas, siendo
variable el número de sondas y cavidades estimuladas.
Todos los marcapasos se nombran con tres letras (AAI, VVI, DDD) dependiendo de su función,
según un código establecido (Tabla XII). Algunos marcapasos tienen la capacidad de variar su frecuencia
adaptándose al ejercicio físico con sensores de actividad. Estos sensores pueden medir la actividad del
paciente y sus variaciones con el ejercicio, aumentando la frecuencia de estimulación. Estos dispositivos
añaden la letra R a su nomenclatura (DDD-R, AAI-R).
2. INDICACIONES
A pesar de la variedad de situaciones clínicas en las que existe indicación para la colocación de un
marcapasos definitivo, existen dos factores generales que siempre hay que considerar: la correlación de los
síntomas y la bradiarritmia, y la localización de la alteración en la conducción (en general se recomienda
colocación de marcapasos en la disfunción sinusal y en el BAV de 2.º grado tipo Wenckebach, solo cuando
son sintomáticos, y en el BAV de 2.º grado (Mobitz-II, 2:1, avanzado) o BAV de 3.er grado, sean sintomáticos
o no (Tablas XI y XII).
Tabla XII. Nomenclatura de marcapasos.
3. DISFUNCIÓN DEL MARCAPASOS
La disfunción del marcapasos es un cuadro que puede ser grave en función del grado de
dependencia del ritmo del paciente a la estimulación por el marcapasos. Globalmente, y de forma
simplificada, la disfunción de marcapasos se puede dividir en:
Defectos de sensado: el marcapasos no es capaz de detectar las despolarizaciones propias del
corazón, no inhibiéndose ante un estímulo natural. Encontraremos estímulos del mismo no
coordinados con el ritmo basal. Si el estímulo del marcapasos coincide con la onda T puede
desencadenar una taquicardia helicoidal o torsade de pointes (fenómeno R sobre T) (Figura 25).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [330]
[22] ARRITMIAS
Figura 25. Defecto de sensado, fenómeno R sobre T y TV.
Sobresensado: el marcapasos interpreta como un latido cardiaco una señal extracardiaca
(potenciales diafragmáticos, interferencias electromagnéticas, etc.) que dan lugar a la
inhibición de la estimulación. No se observan espigas cuando debería haberlas. Puede deberse
a una fractura en el cable de estimulación.
Defectos de captura: el marcapasos genera un estímulo eléctrico de forma correcta, pero dicho
estímulo no se captura por el ventrículo (no genera un QRS) (Figura 26). Estos defectos suelen
producirse por deterioro de las sondas, elevación del umbral de energía necesario para la
estimulación o agotamiento de la batería. El diagnóstico y el tratamiento muchas veces es
complejo, por lo que debe ser realizado en una unidad especializada.
Figura 26. Defecto de captura (espigas no conducidas).
BIBLIOGRAFÍA
Bayés de Luna A. Passive arrhythmias. En: Clinical arrhythmology. 1.ª ed. Oxford: Wiley-Blackwell;
2011.
Camm AJ, Lip GY, de Caterina R, et al. 2012 focused update of the ESC Guidelines for the management
of atrial fibrillation. Eur Heart J. 2013 Sep;34(36):2850-1.
January CT, Wann LS, Alpert JS, et al. 2014 AHA/ACC/HRS Guideline for the management of patients
with atrial fibrillation: Executive Summary. J Am Coll Cardiol. 2014 Dec 2;64(21):2305-7.
Kirchhof P, Benussi S, Kotecha D, Ahlsson A, Atar D, Casadei B, Castella M, Diener HC, Heidbuchel H,
Hendriks J, Hindricks G, Manolis AS, Oldgren J, Popescu BA, Schotten U, Van Putte B, Vardas P. 2016
ESC Guidelines for the management of atrial fibrillation developed in collaboration with EACTS. Euro
Heart J. 2016 Aug 27.
Priori SG, Blomström-Lundqvist C, Mazzanti A, et al. 2015 ESC Guidelines for the management of
patients with ventricular arrhythmias and the prevention of sudden cardiac death. Eur Heart J. 2015
Nov 1;36(41):2793-867.
Vogler J, Breithardt G, Eckardt L. Bradiarritmias y bloqueos de la conducción. Rev Esp Cardiol.
2012;65(7):656-67.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [331]
[23] CARDIOPATÍA ISQUÉMICA
23.Cardiopatía isquémica
María Natalia Tovar Forero.
Cardiología.
Irene Cabrera Rodrigo.
Medicina Interna
Asesor: Roberto Martín Asenjo. Médico Adjunto. Servicio de Cardiología
I. CONCEPTO
La cardiopatía isquémica (CI) es un conjunto de entidades distintas derivadas del desequilibrio
entre la demanda de oxígeno del miocardio y el aporte a través de las arterias coronarias. La enfermedad
arterial coronaria (EAC) es la manifestación más prevalente de las enfermedades cardiovasculares.
II. FISIOPATOLOGÍA
La EAC conlleva un proceso lento y constante por el depósito de lípidos en la pared arterial que
origina un estrechamiento luminal crónico (aterosclerosis) y uno dinámico que origina la oclusión coronaria
parcial o completa de forma súbita y crítica (trombosis, vasoespasmo). En la medida en la que predomine
un proceso u otro, aparecerán las diferentes entidades de la EAC.
La angina estable o cardiopatía isquémica crónica se caracteriza por la aterosclerosis de larga
evolución y obstrucción fija del flujo que desencadena angina con el incremento episódico de
demandas de oxígeno miocárdico.
En el síndrome coronario agudo (SCA) son protagonistas la rotura, ulceración, fisura, erosión o
disección de una placa aterosclerótica que produce la formación de un trombo intraluminal en
una o más arterias coronarias, con la consiguiente reducción del flujo miocárdico o
embolización distal, lo que precipita la oclusión repentina del vaso y la ulterior necrosis
miocárdica. Todo ello dará lugar al infarto de miocardio (IM) de tipo 1. Si la oclusión del vaso
es total, mediada con mayor frecuencia por trombo rico en trombina, dará lugar a un SCACEST,
que conlleva isquemia transmural. Si la oclusión es intermitente o parcial, mediada por un
trombo plaquetario, dará lugar a un SCASEST, con posible isquemia subendocárdica secundaria.
De la misma manera, la angina microvascular o síndrome X cardiaco se manifiesta como
episodios de angina y pruebas de detección de isquemia positivas (focal o difusa), sin lesiones
evidenciables mediante coronariografía en las arterias epicárdicas. El IM de tipo 2 es la necrosis
miocárdica que se produce por el desajuste entre el aporte y la demanda miocárdica de
oxígeno en pacientes con o sin ateroesclerosis coronaria conocida, pero sin inestabilidad de la
placa coronaria. Entre sus mecanismos se incluyen el vasoespasmo arterial coronario, la
disfunción endotelial coronaria, las taquiarritmias, las bradiarritmias, la anemia, la insuficiencia
respiratoria, la hipotensión y la crisis hipertensiva.
El vasoespasmo es reflejo de la disfunción endotelial siendo la causa de la angina variante de
Prinzmetal: se manifiesta como episodios de angina en reposo con elevación transitoria del segmento ST
(isquemia transmural) con arterias coronarias normales o con lesiones no significativas.
La definición universal de IM incluye, además, el IM de tipo 3 con desenlace mortal cuando no se
dispone de biomarcadores, e IM de tipos 4 y 5 relacionados con intervención coronaria percutánea [ICP] y
cirugía de revascularización coronaria [CABG], respectivamente.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [332]
[23] CARDIOPATÍA ISQUÉMICA
III. ETIOLOGÍA
Es preciso identificar los factores de riesgo y desencadenantes que hacen a un paciente vulnerable,
con propensión a generar placas inestables, con riesgo de rotura de las mismas. Conocer e intervenir sobre
esos factores sistémicos nos ayudará a prevenir la incidencia y recurrencia de complicaciones más allá de
los procedimientos revascularizadores y, así, tratar la EAC de forma global.
Existen factores de aterosclerosis establecidos (ver Capítulo 20. “Hipertensión arterial y factores de
riesgo cardiovascular”), cuyo riesgo es acumulativo. Los factores modificables son potencialmente todos,
excepto la edad, el sexo y la historia familiar.
Los factores que incrementen las demandas de oxígeno del miocardio harán evidente el déficit de
suministro, por lo que son factores desencadenantes en la cardiopatía isquémica: la infección, la
tirotoxicosis, la taquicardia, el estrés emocional, la hipertensión arterial (HTA), la estenosis aórtica, la
anemia y la hipoxemia.
Existen otros factores inciertos, con limitada evidencia de reducción del riesgo de EAC con
intervenciones dirigidas sobre ellos. Aunque son muchos los que se investigan, podemos destacar:
hiperhomocisteinemia, hiperuricemia, hiperfosfatemia, factores procoagulantes, marcadores de
inflamación (mieloperoxidasa, leucocitosis, VSG, sICAM-1, sVCAM-1, P y E-selectinas), hipertrofia
ventricular izquierda, alteraciones en el electrocardiograma (ECG) basales o en el ejercicio, calcificación
coronaria o aórtica, etc.
Existen causas de isquemia miocárdica de etiología no aterosclerótica que es aquella que afecta a
las arterias coronarias: arteritis, traumatismo, disección, tromboembolismo coronario, anomalías
congénitas, adicción a cocaína, complicaciones del cateterismo cardiaco, miocardiopatía (hipertrófica o
dilatada) o estenosis aórtica.
IV. CLÍNICA
La presentación clínica es variada, con un espectro que abarca desde la ausencia de síntomas a la
muerte súbita. Como norma general, el síntoma principal que pone en marcha el proceso diagnóstico y
terapéutico de los pacientes es el dolor torácico. El dolor torácico típico se caracteriza por una sensación
retroesternal de presión o pesadez (“angina”) que irradia hacia el brazo izquierdo (menos frecuentemente
hacia ambos brazos o al brazo derecho), el cuello o la mandíbula, y que puede ser intermitente
(normalmente dura varios minutos) o persistente.
También pueden aparecer síntomas adicionales como sudoración, náuseas, disnea y síncope. Las
presentaciones atípicas (sin dolor torácico) incluyen dolor epigástrico, disnea súbita y síncope. Estos
síntomas atípicos se observan más frecuentemente en pacientes ancianos, en mujeres y en pacientes con
diabetes mellitus (DM), enfermedad renal crónica (ERC) o demencia. La exacerbación de los síntomas por el
esfuerzo físico y su alivio en reposo aumentan la probabilidad de isquemia miocárdica. El dolor torácico que
se reproduce cuando se ejerce presión contra el tórax tiene un valor predictivo negativo relativamente alto
para el SCASEST. El alivio de los síntomas tras la administración de nitratos no es específico del dolor
anginoso. El espectro de la EAC abarca diversas entidades clínicas:
Isquemia silente: la ausencia de síntomas (típicos o atípicos) dificulta el diagnóstico; se basará
en signos físicos indirectos (hipotensión, taquicardia) que en ocasiones acompañan y en las
pruebas complementarias..
La angina estable: aparece o se exacerba (de forma predecible) con el ejercicio o el estrés
emocional y cede con el reposo y los nitratos. El patrón de angina en número, frecuencia y
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [333]
[23] CARDIOPATÍA ISQUÉMICA
umbral no debe haber variado en los últimos meses. Según el umbral de esfuerzo que
desencadena la angina, se establece el grado según la clasificación de la Canadian
Cardiovascular Society (CCS) (Tabla I).
Tabla I. Clasificación de la severidad de la angina según la Cardiology Canadian Society.
Síndrome coronario agudo
Un síndrome coronario agudo (SCA) puede ser la angina de nueva aparición (inferior a 2
meses), angina in crescendo (aumento de frecuencia, duración o intensidad en las últimas 4
semanas), angina de reposo y la angina postinfarto agudo de miocardio (post-IAM).
Muerte súbita
Es otra manifestación posible de un SCA. Si se presencia, un monitor con desfibrilador es
fundamental para recuperar potencialmente una fibrilación ventricular.
V. APROXIMACIÓN DIAGNÓSTICA
1. EXPLORACIÓN FÍSICA
La exploración física suele ser normal en los pacientes con sospecha de SCASEST. En caso de que
haya signos de insuficiencia cardiaca o inestabilidad eléctrica, se debe acelerar el diagnóstico y el
tratamiento.
La auscultación cardiaca puede revelar un soplo sistólico producido por regurgitación mitral
isquémica, que se asocia a mal pronóstico o por estenosis aórtica.
En ocasiones un soplo sistólico puede indicar la presencia de una complicación mecánica (como la
rotura de músculo papilar o del septo interventricular) de un IM subagudo y probablemente no detectado.
La exploración física permite identificar signos de dolor torácico producido por otras causas (ver
Capítulo 9. “Dolor torácico”) de origen cardiológico no coronario (como embolia pulmonar, síndromes
aórticos agudos, miopericarditis o estenosis aórtica) o enfermedades extracardiacas (como neumotórax,
neumonía, espasmo esofágico, esofagitis, úlcera gástrica, colecistitis, pancreatitis). Las diferencias en la
presión arterial entre las extremidades superiores y las inferiores o entre los brazos, el pulso irregular, la
distensión yugular venosa, los ruidos cardiacos, el roce pericárdico o el dolor por palpación torácica o
abdominal son hallazgos físicos que apuntan a un diagnóstico alternativo. Otros hallazgos, como la palidez,
la sudoración o el temblor, deben orientar hacia condiciones precipitantes, como la anemia y la
tirotoxicosis.
2. ELECTROCARDIOGRAMA DE 12 DERIVACIONES EN REPOSO
El ECG de 12 derivaciones en reposo es la principal herramienta diagnóstica para la evaluación de
los pacientes con sospecha de SCA. Se debe realizar en los primeros 10 minutos de la llegada del paciente a
Urgencias o, preferiblemente, durante el primer contacto prehospitalario con los servicios médicos de
Urgencias y debe interpretarlo inmediatamente un médico cualificado. Si las derivaciones estándar no son
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [334]
[23] CARDIOPATÍA ISQUÉMICA
concluyentes y el paciente tiene signos o síntomas que indican isquemia miocárdica activa, deben
registrarse derivaciones adicionales posteriores (V7-V9) y precordiales derechas (V3R y V4R).
Un bloqueo completo de la rama izquierda (BCRI) o el ritmo de marcapasos no permiten valorar la
presencia de un IAM anterior, pero la presencia de un BCRI de novo debe hacer sospechar isquemia y es un
dato que puede empeorar el pronóstico. Los criterios de Sgarbossa (Tabla II) pueden ayudar a
diferenciarlos. El bloqueo completo de la rama derecha (BCRD) no interfiere a la hora de valorar un ascenso
del ST.
Tabla II. Criterios de Sgarbossa.
Es preciso realizar registros electrocardiográficos con y sin dolor, así como comparar con
ECG previos del paciente si se dispone de ellos (nos informarán de alteraciones eléctricas de base).
En general, el ECG es más fiable para localizar isquemia transmural (derivaciones con elevación del
ST o T picudas) que subendocárdica, así la alteración de V1-V2: septal; V3-V6: anterior; aVL, I, V4-V6: apical
o lateral; II, III y aVF: cara inferior; V4R, V5R y V6R: ventrículo derecho y V7-V9 (especular en V2): cara
posterior.
Dentro del SCA, en función del ECG inicial, se distinguirán dos diagnósticos de trabajo entre los que
clínicamente no se pueden establecer claras diferencias:
Síndrome coronario agudo sin elevación del ST (SCASEST)
En el contexto del SCASEST, el ECG puede ser normal en más de un tercio de los pacientes, las
alteraciones electrocardiográficas características incluyen:
La depresión del ST (≥ 0,5 mm en dos o más derivaciones contiguas). El número de
derivaciones con descenso del ST y su magnitud es proporcional a la gravedad del
SCASEST.
El descenso transitorio del ST apunta a isquemia subendocárdica (angina inestable); si
persiste, posiblemente sea un IAMSEST.
La elevación transitoria del ST y cambios en la onda T.
El ascenso transitorio del ST se identifica como SCASEST (la angina variante de
Prinzmetal).
En general, no evolucionan con ondas Q patológicas.
Tras la seriación de marcadores de daño miocárdico, el diagnóstico final será de
IAMSEST si se elevan o angina inestable si no existe elevación de los mismos.
Síndrome coronario agudo con elevación persistente del ST (IAMCEST)
Permite clasificar el evento como IAMCEST la elevación del ST > 1 mm en dos o más
derivaciones anatómicas contiguas, o ≥ 2 mm en al menos dos precordiales. Además, pueden
apreciarse ondas T picudas (hiperagudas) y posteriormente en la evolución aparecerá la onda Q
patológica y se invertirá la onda T.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [335]
[23] CARDIOPATÍA ISQUÉMICA
3. MARCADORES DE DAÑO MIOCÁRDICO
Los biomarcadores son un complemento a la valoración clínica inicial y al ECG, orientan el
diagnóstico, la estratificación del riesgo y el tratamiento de los pacientes con sospecha de SCASEST. La
determinación de un biomarcador de daño miocárdico, preferiblemente troponinas cardiacas de alta
sensibilidad, es obligatoria en todos los pacientes con sospecha de SCASEST.
Los más relevantes en la práctica clínica son las troponinas (Tn) T o I, son los biomarcadores más
sensibles y específicos de daño miocárdico, se correlacionan con el pronóstico y la mortalidad a corto y
largo plazo de forma independiente. Si la presentación clínica es compatible con isquemia miocárdica, la
elevación dinámica de troponinas cardiacas permite catalogar el episodio como IAM (Figura 1).
Figura 1. Algoritmo diagnóstico.
En pacientes con IM, los títulos de troponinas cardiacas aumentan rápidamente tras la aparición de
los síntomas (normalmente durante la primera hora si se emplean determinaciones de alta sensibilidad) y
permanecen elevados durante un tiempo variable (normalmente varios días, hasta 2 semanas); en un
SCASEST la elevación es mínima, dura tan solo 24-48 h, pero indica alto riesgo. Es fundamental observar la
curva de troponina. Las determinaciones deben realizarse al ingreso, a las 3-4 h o en caso de nuevo
episodio de dolor torácico grave. Es necesario tener en cuenta que la elevación de troponinas con cinética
compatible con daño miocárdico es diagnóstica de necrosis miocárdica, pero no permite distinguir la
etiología (IAM tipo I, II, III, IV o V). Para ello deberá recurrirse a la anamnesis, ECG y resto de test
complementarios.
Los test de determinación bioquímica no son homogéneos en los laboratorios. En Europa, se
emplean mayoritariamente plataformas para la determinación de troponinas cardiacas, que pueden ser
sensibles (permiten la detección de troponinas cardiacas en un 20-50% de individuos sanos) o
ultrasensibles (detección en un 50-90% de individuos sanos). Siendo las determinaciones ultrasensibles más
recomendables que las de menor sensibilidad, pues aumentan la precisión diagnóstica de IM en el
momento de presentación de los síntomas, especialmente en pacientes atendidos poco después de la
aparición de dolor torácico o con sintomatología atípica, y permiten confirmar o descartar más
rápidamente el diagnóstico de IM.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [336]
[23] CARDIOPATÍA ISQUÉMICA
Entre los múltiples biomarcadores evaluados para el diagnóstico de los SCASEST, solo la creatín-
cinasa (CK), su isoenzima MB (CK-MB) y la copeptina parecen tener importancia clínica. Comparada con la
troponina cardiaca, la CK y la CK-MB muestran una disminución más rápida tras el IM y pueden ser más
útiles para determinar el momento en que se produjo daño miocárdico y detectar el reinfarto precoz. La
determinación de la copeptina (extremo terminal carboxílico de la prohormona vasopresina) permite
cuantificar el nivel de estrés endógeno en distintas afecciones, incluido el IM. Dado que el nivel de estrés
endógeno suele ser invariablemente elevado al inicio del IM, el valor añadido de la copeptina, comparada
con la determinación convencional de troponinas cardiacas (menos sensibles), es considerable, por lo que
podría incluirse en la evaluación del dolor torácico en un futuro próximo.
Existen otras entidades cardiacas no coronarias y no cardiacas que cursan con elevación de Tn,
algunas potencialmente fatales (Tabla III). La curva difiere de la observada en el IAM. En caso de
controversia, los datos clínicos, ECG y ecocardiográficos ayudan a realizar el diagnóstico diferencial. Hay
que tener en cuenta que en estas entidades no coronarias, la elevación de troponina también se asocia a
peor pronóstico, por lo que requiere una evaluación diagnóstica cuidadosa, pero no se deben tratar de
inicio como SCA con terapia antitrombótica ni intervencionismo precoz.
Tabla III. Enfermedades no coronarias con elevación de troponinas.
4. RADIOGRAFÍA DE TÓRAX
En la angina no aporta datos diagnósticos ni ayuda a estratificar el riesgo. Su indicación en la angina
estable es para pacientes con sospecha de insuficiencia cardiaca, enfermedad valvular o enfermedad
pulmonar; se correlacionan con el pronóstico la cardiomegalia, la congestión pulmonar, el crecimiento
auricular y las calcificaciones cardiacas.
5. ECOCARDIOGRAMA TRANSTORÁCICO
Útil en el diagnóstico del SCA al detectar alteraciones de la contractilidad segmentaria, cuya
ausencia hace el diagnóstico menos probable. Determina la función sistólica y diastólica ventricular,
identifica y cuantifica valvulopatías y la presencia de derrame pericárdico. Se debe realizar un
ecocardiograma urgente ante la sospecha de complicaciones mecánicas. También es útil en la
determinación del pronóstico, tanto en la fase aguda como en el seguimiento, aportando datos para la
toma de decisiones (revascularización, prevención de muerte súbita).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [337]
[23] CARDIOPATÍA ISQUÉMICA
6. PRUEBAS DE DETECCIÓN DE ISQUEMIA Y ENFERMEDAD CORONARIA
6.1. Ergometría (prueba de esfuerzo)
Se considera en la mayoría de los casos el método de elección para el cribado de la enfermedad
coronaria, por su disponibilidad y bajo coste. La sensibilidad media de la prueba que es del 65% y la
especificidad del 77%. El paciente es sometido a un esfuerzo progresivo mientras se monitoriza su
frecuencia cardiaca (FC), tensión arterial y registro electrocardiográfico, evidenciando alteraciones
eléctricas y síntomas clínicos que no están presentes en reposo y sí durante el ejercicio.
Como limitaciones a tener en cuenta se encuentran la incapacidad para el ejercicio físico de
determinados pacientes hasta un nivel suficiente para obtener resultados positivos y determinadas
alteraciones del ECG basal que impiden una adecuada interpretación del registro: bloqueo de rama
izquierda, ritmo de marcapasos, síndromes de preexcitación, depresión en reposo del segmento ST
superior a 1 mm (incluyendo hipertrofia VI o tratamiento con digitálicos).
El protocolo más utilizado durante la ergometría convencional para aumentar progresivamente el
esfuerzo es el protocolo de Bruce.
En cuanto a sus indicaciones, permite no solo hacer una valoración diagnóstica de la
enfermedad coronaria, sino también pronóstica en los pacientes con cardiopatía isquémica
conocida, valorar la capacidad funcional del paciente, investigar arritmias durante el ejercicio y
el comportamiento de la tensión arterial.
Si se realiza con fines diagnósticos, la prueba de esfuerzo debe llevarse a cabo sin medicación
antianginosa ni betabloqueantes, para no incurrir en falsos negativos.
Es un procedimiento habitualmente seguro, en ausencia de contraindicaciones (Tabla IV).
Tabla IV. Contraindicaciones de la realización de la prueba de esfuerzo.
Los resultados de la prueba se expresan de la siguiente manera:
Positividad clínica: si desarrollan dolor anginoso típico o signos de disfunción
ventricular izquierda (descenso o falta de progresión de la tensión arterial [TA] con el
ejercicio). Justifica la realización de otras pruebas de detección de isquemia.
Positividad eléctrica: cuando se registran, durante el esfuerzo o en la recuperación,
cambios eléctricos sugerentes de isquemia.
Negativa: cuando se alcanza un nivel de ejercicio significativo y una FC submáxima
(85% de la FC máxima teórica) sin aparición de síntomas clínicos ni cambios eléctricos.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [338]
[23] CARDIOPATÍA ISQUÉMICA
No concluyente: cuando no se alcanza el grado de ejercicio adecuado (estadio I de
Bruce o superar los 5 METS) ni la taquicardización suficiente, por lo que no es posible
descartar si hay isquemia miocárdica subyacente.
Desde el punto de vista pronóstico, existen unos criterios de gravedad que ayudan a
estratificar el riesgo.
6.2. Gammagrafía de perfusión miocárdica (SPECT)
La gammagrafía cardiaca de perfusión permite detectar alteraciones en el flujo coronario mediante
la administración de isótopos intravenosos que son captados por los miocitos de forma proporcional al flujo
coronario. Guarda una sensibilidad y especificidad altas, en torno al 90%.
En cuanto a los métodos para inducir isquemia existen:
Ejercicio físico (ergometría con isótopos), con un cicloergómetro o cinta rodante.
Vasodilatadores como dipiridamol, adenosina o ATP que ejercen una vasodilatación
potente de las arteriolas del árbol coronario con incremento de flujo en las zonas
irrigadas por arterias normales que se traducirá en una mayor captación del isótopo en
dichas áreas, en comparación con los segmentos irrigados por arterias coronarias con
estenosis y, por tanto, con menor captación (flujo) como consecuencia de la
disminución de la reserva coronaria (fenómeno de robo de la arteria coronaria
obstruida). Está contraindicada la administración de dipiridamol en asma, EPOC grave e
hipotensión arterial. Se prefiere la utilización de dichos vasodilatadores cuando exista
limitación al ejercicio físico y en casos de bloqueo de la rama izquierda o portadores de
marcapasos.
Dobutamina: agente simpaticomimético con efecto inotrópico y cronotrópico positivo.
A dosis bajas aumenta la perfusión miocárdica y mejora la contractilidad, con lo que se
investiga la capacidad de reserva contráctil o viabilidad del miocardio. A dosis altas,
aumenta la demanda de oxígeno del miocardio, lo que en presencia de un flujo limitado
por una estenosis, pone de manifiesto la isquemia como una menor captación isotópica
en dicha zona. Está contraindicada en casos de HTA severa, estenosis aórtica grave,
miocardiopatía hipertrófica obstructiva y fibrilación auricular rápida. Dado que los
betabloqueantes antagonizan la acción de la dobutamina, se han de suspender,
sustituyéndolos por otros antianginosos si fuera preciso, antes de realizar la prueba.
Sus indicaciones fundamentales y ventajas son:
Permite el diagnóstico y/o pronóstico de cardiopatía isquémica en las situaciones en las
que la realización de una prueba de esfuerzo convencional no es posible o su resultado
ha sido no concluyente.
Permite obtener información de la localización y la severidad de la isquemia
miocárdica, lo que es de gran utilidad de cara a indicar un procedimiento
revascularizador del vaso causante de la isquemia.
Permite la valoración de la viabilidad miocárdica, en las situaciones en que se plantea la
revascularización de segmentos de miocardio.
Si se realiza sincronizada con el ECG (gated-SPECT), valora el movimiento de las paredes
ventriculares y su engrosamiento sistólico y realiza un cálculo de la fracción de eyección
(FE).
Los resultados de la prueba se expresan de la siguiente manera:
Defecto de captación en las imágenes de esfuerzo que se normaliza en el estudio de
reposo: traduce un territorio isquémico. Son criterios de severidad: defectos extensos
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [339]
[23] CARDIOPATÍA ISQUÉMICA
de perfusión que afecten a más de una región coronaria o a un amplio territorio
correspondiente a la arteria descendente anterior.
Defecto de captación severo, tanto en esfuerzo como en reposo, hace sospechar de
una zona de necrosis (no viable) o de isquemia muy intensa (viable); para su
diferenciación se requiere reinyección (estudio tardío), de forma que, si los defectos
que antes eran persistentes mejoran, se consideran viables.
Ausencia de defectos de perfusión: ausencia de territorio isquémico.
Existen una serie de limitaciones a tener en cuenta:
Empleo de radiación ionizante.
Falsos negativos: en caso de enfermedad severa de tres vasos e isquemia homogénea
en todo el ventrículo izquierdo, no se observarán defectos por comparación entre
segmentos en la gammagrafía de perfusión.
Falsos positivos: pueden observarse defectos septales en ausencia de enfermedad en la
arteria descendente anterior en casos de bloqueo de la rama izquierda. Se puede
producir déficit de captación por atenuación fotónica en la cara inferior en los varones
por el diafragma o en la cara anterior en las mujeres por las mamas, tanto en el
esfuerzo como en el reposo, con motilidad normal de las paredes.
6.3. Ecocardiograma de estrés
El ecocardiograma de estrés tiene como objetivo constatar alteraciones de la contractilidad
regionales originadas por la isquemia. Cuenta con una elevada sensibilidad y especificidad (85%).
Métodos para inducir isquemia (ver “Métodos en gammagrafía”).
En cuanto a las indicaciones del ecocardiograma de estrés son similares a las pruebas
isotópicas. El ecocardiograma de estrés aporta información adicional como la función
diastólica, valoración valvular, pericárdica, etc.
En general, se recomienda emplear la técnica que cuente con mayor disponibilidad y
experiencia en el centro de trabajo.
Los resultados de la prueba se expresan de la siguiente manera:
El test se considera ecocardiográficamente positivo si aparecen alteraciones de la
contractilidad segmentaria que no existían en el examen basal o eran de menor grado.
En el estudio de viabilidad se considera miocardio viable aquel que presentando
alteraciones de la contractilidad en reposo, con dosis bajas de dobutamina, mejora su
contractilidad.
El ecocardiograma de estrés tiene algunas limitaciones y contraindicaciones:
Contraindicaciones ya mencionadas para administrar dobutamina.
Precisa que el paciente posea “buena ventana acústica” para obtener imágenes
completas y de buena calidad.
Dependencia interobservador.
6.4. Angio-TC de arterias coronarias (“coronariografía no invasiva”)
Técnica no invasiva que permite visualizar la anatomía coronaria, las cavidades cardiacas y los
grandes vasos. Facilita el diagnóstico precoz de pacientes afectos de arteriosclerosis, cuantificando la carga
cálcica de las arterias coronarias.
Aporta una serie de ventajas:
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [340]
[23] CARDIOPATÍA ISQUÉMICA
Alto valor predictivo negativo (hasta el 98%): útil para descartar lesiones coronarias en
casos de dolor torácico atípico o resultados dudosos de otras pruebas. Indicado si la
probabilidad pretest de EAC es intermedia.
Valoración en el mismo estudio del resto de estructuras torácicas permitiendo
diagnosticar otras causas de dolor torácico (tromboembolismo pulmonar, disección de
aorta).
Visualización con gran exactitud de los injertos aortocoronarios y de las anomalías
coronarias.
Valoración de las características de la placa de ateroma.
En cuanto a los inconvenientes, destacan:
No permite realizar intervencionismo (prueba exclusivamente diagnóstica).
Empleo de radiación ionizante.
Uso de contraste iodado: limita su uso en caso de alergia o insuficiencia renal
(creatinina > 1,5 mg/dL).
Proporciona información únicamente anatómica, sin conocer la repercusión funcional
de las lesiones.
Calcificación coronaria extensa: limita sustancialmente el análisis de las lesiones
coronarias ya que impide valorar adecuadamente la luz del vaso.
Estenosis intrastent: la valoración de la zona tratada con stent se puede ver interferida
parcialmente por artefactos, si bien, la mejoría tecnológica continua ha permitido
subsanar en parte este problema.
FC mayor de 70 lpm, ectopias u otras arritmias: empeoran de forma significativa la
calidad de la imagen. En general, se administran fármacos para el control de la FC antes
de la prueba.
6.5. Cardiorresonancia magnética de estrés
Permite visualizar imágenes cardiacas de alta resolución con excelente diferenciación tisular sin ser
tan dependiente de la constitución física del paciente como la ecocardiografía ni implicar el uso de
productos radiactivos.
Se analizan los cambios en la motilidad parietal para el estudio de la perfusión miocárdica tras
provocar un estrés con administración de dobutamina o vasodilatadores. Hasta el momento, la
cardiorresonancia es la que ofrece mejor resolución en cuanto a la extensión y el grado de viabilidad
miocárdica, aunque la utilización de esta técnica se encuentra limitada por la disponibilidad y el elevado
coste sanitario, pacientes portadores de objetos metálicos, claustrofobia y tiempos de examen
prolongados, la insuficiencia renal (utilización de gadolinio como contraste), las alteraciones del ritmo
cardiaco (extrasistolia ventricular frecuente...).
6.6. Coronariografía
Permite, mediante la inyección de contraste radiológico, visualizar el contorno de la luz de las
arterias coronarias. La coronariografía permite realizar:
Diagnóstico
Es el único método que permite descartar o confirmar absolutamente la existencia de
enfermedad arterial coronaria epicárdica y es el método de elección para evaluar la anatomía
coronaria y el paso previo a las decisiones terapéuticas de revascularización. Permite conocer la
existencia, extensión, morfología y severidad de las estenosis coronarias, la existencia de
circulación colateral y de fístulas coronarias. La lesión es angiográficamente significativa cuando
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [341]
[23] CARDIOPATÍA ISQUÉMICA
la estenosis luminal que ocasiona es igual o superior al 70%,y en el caso del tronco común
izquierdo cuando es igual o superior al 50%. Para clasificar el flujo postestenosis se emplea la
clasificación TIMI que lo gradúa desde 0 (ausencia de flujo distal a la lesión) hasta 3 (flujo distal
a la lesión normal).
Pronóstico
La presencia de estenosis significativa en el tronco coronario izquierdo, las estenosis en tres de
las arterias principales, en la arteria descendente anterior proximal y la disfunción ventricular
izquierda suponen mal pronóstico con elevada tasa de eventos cardiovasculares.
Tratamiento
Métodos de revascularización endoluminales percutáneos (ICP) mediante angioplastia e
implantación de stents (convencionales o farmacoactivos).
Ventriculografía del ventrículo izquierdo, que permite valorar la FE, contractilidad
regional, aneurismas, insuficiencia mitral, etc.
Medición de presiones intracavitarias (por ejemplo, PTDVI).
Valorar la severidad y significado funcional de lesiones intermedias o dudosas mediante
el empleo de ecografía intracoronaria y guía de presión.
Las indicaciones de la coronariografía se muestran a continuación en la tabla V.
Tabla V. Indicaciones de coronariografía.
Las complicaciones son poco frecuentes y pueden ser causadas por:
Contraste radiológico: fenómenos de hipersensibilidad (que, en general, pueden
controlarse con el empleo previo de esteroides y/o antihistamínicos) y deterioro de la
función renal, sobre todo, en pacientes con diabetes mellitus o insuficiencia renal
previa, pudiendo minimizarse el riesgo de nefrotoxicidad con hidratación abundante.
Punción arterial: las complicaciones vasculares son más frecuentes con la punción
femoral que con la radial (acceso de elección). Entre ellas, destacan hematomas,
pseudoaneurismas, fístulas arteriovenosas, disecciones arteriales, fallos de los
dispositivos de cierre percutáneo, lesiones del nervio femoral e incluso en casos de
punción arterial femoral alta, sangrado con formación de hematoma en el espacio
retroperitoneal.
Intervencionismo coronario: se puede complicar con IAM, disección coronaria,
arritmias, accidente cerebrovascular e incluso muerte.
En la tabla VI se describen criterios que orientan hacia la prueba de detección en cada caso.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [342]
[23] CARDIOPATÍA ISQUÉMICA
Tabla VI. Criterios para orientar la elección de prueba de detección de isquemia.
VI. TRATAMIENTO
1. CARDIOPATÍA ISQUÉMICA CRÓNICA (ESTABLE)
Tras superar la fase aguda de la enfermedad coronaria se establece el diagnóstico de cardiopatía
isquémica crónica. Los objetivos del tratamiento son reducir los síntomas y mejorar el pronóstico
basándose en la modificación de los estilos de vida, el control de los factores de riesgo cardiovascular
(FRCV) y un tratamiento farmacológico óptimo. Para ello es necesario un seguimiento estrecho del paciente
reevaluando la presencia de síntomas isquémicos de novo o progresivos y el deterioro de clase funcional,
con el propósito de ajustar el tratamiento respectivo o valorar la necesidad de pruebas invasivas que
supongan revascularizaciones futuras.
1.1. Medidas dirigidas a mejorar el pronóstico
El abandono del hábito tabáquico, el control estricto de la presión arterial, modificaciones en la
dieta y en la actividad física, al igual que el control del peso corporal, son puntos claves de intervención
sobre el estilo de vida, sobre los que habrá que incidir desde el primer momento del diagnóstico de
cardiopatía isquémica, iniciándose durante la consulta médica o durante el ingreso hospitalario si
corresponde. Esta práctica debe ponerse en marcha desde un abordaje multidisciplinar con cardiólogos,
médicos de cabecera, rehabilitadores, fisioterapeutas y nutricionistas. Como ayuda para el abandono del
tabaco, aparte de los consejos y la motivación, se debe ofrecer de forma sistemática a todos los pacientes
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [343]
[23] CARDIOPATÍA ISQUÉMICA
la terapia de sustitución nicotínica (parches, chicles, sprays) y bupropión, en ausencia de contraindicaciones
específicas. El uso de vareniclina se ha cuestionado recientemente ante un aumento discreto del riesgo
cardiovascular.
1.2. Tratamiento médico específico
Su objetivo es aliviar los síntomas y prevenir nuevos eventos cardiovasculares (Tabla VII).
Tabla VII. Fármacos en cardiopatía isquémica.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [344]
[23] CARDIOPATÍA ISQUÉMICA
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [345]
[23] CARDIOPATÍA ISQUÉMICA
Fármacos antiisquémicos
Nitratos: inducen vasodilatación arteriolar y venosa con lo que mejoran el flujo
coronario y disminuyen la precarga permitiendo una mayor perfusión subendocárdica.
Existen dos tipos, los nitratos de acción corta (sublingual o en aerosol) para el
tratamiento puntual de la angina de esfuerzo o angina ante situaciones determinadas
(posprandial, exposición a temperaturas bajas, actividad sexual, etc.) y de acción
prolongada para profilaxis de episodios anginosos. Su principal inconveniente es el
desarrollo de tolerancia que requiere periodos libres del fármaco, y la aparición de
hipotensión y cefalea, lo que influye en la adherencia al tratamiento. Indicados en
angina vasoespástica o secundaria a consumo de cocaína/anfetaminas. Los nitratos de
acción corta se consideran parte del tratamiento antianginoso de primea línea en
cardiopatía isquémica, mientras que los de acción prolongada forman parte del
tratamiento de segunda línea. Contraindicados en caso de administración de sildenafilo
o vardenafilo en las últimas 24 horas, o de tadalafilo en las 48 horas previas.
Bloqueadores beta: primera línea. Tienen efecto cronotrópico e inotrópico negativo,
enlentecen la conducción auriculoventricular (AV) y la actividad ectópica y mejoran la
perfusión de zonas isquémicas al prolongar la diástole y aumentar la resistencia
vascular en zonas sin isquemia. Por todo esto, controlan la angina y mejoran la
capacidad al ejercicio, reducen el riesgo de muerte cardiovascular (CV) y de IM.
Indicados en angina de esfuerzo, angina inestable y angina microvascular;
contraindicados en angina vasoespástica y en angina inducida por
cocaína/anfetaminas. Se prefieren los bloqueadores beta cardioselectivos como
nebivolol, atenolol, bisoprolol y metoprolol, sobre carvedilol, en pacientes con EPOC o
arteriopatía periférica. Son de elección carvedilol o metoprolol en pacientes con
insuficiencia renal avanzada, ya que su eliminación es por vía hepática.
Bloqueadores de canales de calcio: primera línea. Tanto los dihidropiridínicos
(amlodipino y nifedipino), como los no dihidropiridínicos (verapamilo y diltiazem),
tienen efectos antianginosos; los primeros se centran en la reducción de las resistencias
vasculares sistémicas, mientras que los segundos, además, poseen efecto inotrópico y
cronotrópico negativo. Verapamilo y diltiazem se aconsejan en el tratamiento de la
angina de esfuerzo y angina inestable, cuando por intolerancia o contraindicación no
puedan usarse bloqueadores beta; además, son la primera línea de tratamiento en la
angina vasoespástica y la inducida por cocaína/anfetaminas; no se recomienda su uso
en conjunto con bloqueadores beta por el riesgo de bradicardia o depresión miocárdica
extremas, tampoco su uso en pacientes con disfunción ventricular significativa. Por el
contrario, amlodipino y nifedipino han demostrado un adecuado control de la angina
de esfuerzo cuando se asocian a bloqueadores beta, especialmente en pacientes
hipertensos.
Ivabradina: segunda línea. Inhibidor selectivo de la corriente If del nodo sinusal; actúa
disminuyendo la FC sin efecto inotrópico ni en la TA. Aprobado como apoyo para el
tratamiento betabloqueante, cuando con dosis máximas de este no se consiga reducir
la FC a < 60 lpm o exista contraindicación/intolerancia.
Nicorandil: segunda línea. Nitrato derivado de nicotinamida; usado en prevención y
manejo de la angina como coadyuvante a los tratamientos previos. Puede ocasionar
úlceras orales, intestinales y perineales como efecto secundario.
Ranolazina: segunda línea. Inhibidor selectivo de la corriente tardía de sodio. Aprobado
como tratamiento antianginoso cuando los fármacos de primera línea son insuficientes
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [346]
[23] CARDIOPATÍA ISQUÉMICA
o están contraindicados; su uso disminuye la necesidad de nitratos mejorando los
episodios de angina y la capacidad al ejercicio, observándose mayor beneficio en
aquellos con niveles altos de HbA1c. Puede prolongar el intervalo QT.
Fármacos para prevención de eventos
Antiagregación: los agentes antiplaquetarios tienen un papel fundamental en el control
de los fenómenos trombóticos implicados en la aterogénesis y la aparición de eventos
agudos. El ácido acetilsalicílico (AAS) está indicado en todos los pacientes y de forma
indefinida, si no existe contraindicación específica. Clopidogrel es una alternativa en
estoscasos. No existe evidencia científica suficiente para validar el uso de prasugrel y
ticagrelor en la cardiopatía isquémica estable, por lo que no se recomiendan, aunque
podrían considerarse en casos de trombosis del stent bajo tratamiento con clopidogrel.
El tratamiento antiagregante doble (AAS y clopidogrel) está indicado en pacientes
sometidos a angioplastia electiva y se recomienda mantener un mes en caso de stents
convencionales o 3-6 meses en caso de stents farmacoactivos de nueva generación.
Estatinas: reducen los niveles de colesterol (el objetivo terapéutico en la CI crónica es
LDLc < 70 mm Hg en aquellos pacientes con un LDLc basal mayor de 135 mg/dL, o bien
una reducción del 50% basal si se parte de un LDLc de entre 70 y 135, según las
últimas guías de la ESC) y previenen la progresión de la placa de ateroma, por lo que
están indicadas en todos los pacientes con enfermedad coronaria, tanto en prevención
primaria como secundaria. Los efectos adversos más importantes son la producción de
miopatía y aumento de transaminasas (son recomendables los controles periódicos de
creatina-fosfoquinasa [CPK] y transaminasas). Se debe añadir ezetimibe al tratamiento
con estatinas si, una vez alcanzada su máxima dosis, el LDLc persiste > 70 mg/dL. Se ha
demostrado que atorvastatina a dosis altas de 80 mg al día reduce la incidencia de IM
periangioplastia, por tanto, se recomienda su administración como pretratamiento
ante una ICP electiva; como alternativa está rosuvatatina 20 mg al día.
IECA/ARA II: los IECA reducen el riesgo cardiovascular en la cardiopatía isquémica por lo
que se recomienda su uso en pacientes con hipertensión, diabetes mellitus,
insuficiencia cardiaca o FEVI ≤ 40%, en ausencia de contraindicaciones. Como
alternativa están los ARA II en caso de intolerancia a IECA (tos, angioedema). Deben
usarse con precaución en pacientes con insuficiencia renal y tendencia a la
hiperpotasemia; contraindicados en caso de estenosis de la arteria renal.
Antialdosterónicos: el uso de espironolactona o eplerenona (preferible) se recomienda
en pacientes con IAM previo y FEVI ≤ 35% e insuficiencia cardiaca o diabetes mellitus
asociada cuando, a pesar del tratamiento con IECA y betabloqueadores, persistan los
síntomas. Contraindicados si insuficiencia renal significativa e hiperpotasemia.
Otros
Se debe considerar la utilización de protectores gástricos, preferiblemente inhibidores
de la bomba de protones (IBP), en pacientes con historia de hemorragia gastrointestinal
o con riesgo de presentarla (edad avanzada, anticoagulación crónica, esteroides, AINE e
infección por H. pylori). No hay interacción farmacocinética entre los IBP y los nuevos y
potentes inhibidores del receptor P2Y12, ni tampoco hay evidencias claras de que la
interacción con clopidogrel tenga consecuencias clínicas significativas.
1.3. Revascularización
Se debe llevar a cabo en aquellos pacientes que presenten angina limitante pese al tratamiento
médico óptimo, a los datos de mal pronóstico en las pruebas de detección de isquemia o ante la presencia
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [347]
[23] CARDIOPATÍA ISQUÉMICA
de una nueva o progresiva disfunción ventricular, teniendo en cuenta el balance riesgo-beneficio. Existen
dos abordajes posibles: percutáneo o quirúrgico. Las características clínicas, la anatomía de las lesiones
coronarias, la experiencia local y la preferencia del paciente se deben tener en cuenta a la hora de elegir un
abordaje. En general, para enfermedad de 1-2 vasos y anatomía favorable se prefiere el abordaje
percutáneo por medio del implante de stents; en caso de estar afectado también el tronco común
izquierdo (TCI) o si existe enfermedad de 3 vasos y un riesgo quirúrgico bajo, especialmente en pacientes
diabéticos, estaría indicado el abordaje quirúrgico por medio de bypass aortocoronario. Sin embargo, esta
elección debe tomarse de forma individualizada para cada paciente por parte de un equipo multidisciplinar
Heart-Team.
Existen dos tipos principales de stents, los convencionales Bare Metal Stents (BMS) y los stents
farmacoactivos liberadores de fármacos antiproliferativos Drug Eluting Stents (DES).
Las principales complicaciones del stent son la reestenosis y la trombosis. La reestenosis es un fenómeno
progresivo, que puede manifestarse clínicamente a partir de los 6-9 meses de la implantación de un stent,
habitualmente como angina inestable, estando condicionada por los factores de progresión de la
enfermedad coronaria y siendo más frecuente en los stents convencionales; su aparición ha disminuido tras
la introducción de los DES. La trombosis del stent es un fenómeno agudo que cursa como SCA
generalmente con elevación del ST y que tiene una mortalidad elevada; el riesgo de trombosis es mayor en
los DES, por esta razón requieren doble terapia antiagregante por más tiempo. Según el momento de
presentación puede tratarse de una trombosis aguda (primeras 24 h), subaguda (primer mes), tardía (hasta
el primer año) y muy tardía (después del primer año).
1.4. Seguimiento
Detección de isquemia residual
Independientemente de la presentación de la cardiopatía isquémica (angina estable o SCA), se
debe llevar a cabo un seguimiento estrecho de estos pacientes. Después de un tratamiento de
reperfusión es importante identificar a aquellos con riesgo elevado de episodios futuros e
intervenir para su prevención. A pacientes con SCA previo, sobre los que se ha realizado
angioplastia eficaz de la lesión culpable del evento y de otras lesiones coronarias
funcionalmente significativas (ya sea durante el mismo procedimiento o en sucesivos), no es
necesario realizar un test de detección de isquemia durante el ingreso hospitalario mientras el
paciente se mantenga asintomático. Si por el contrario no se realizó reperfusión de la lesión
culpable o existen dudas sobre la necesidad de tratar otras lesiones, podría ser de utilidad la
realización de una prueba de detección de isquemia, no solo para valorar la presencia de
viabilidad tisular, sino también para dirigir la revascularización. Tras el alta hospitalaria, está
indicada una evaluación precoz del riesgo (pronóstica), habitualmente por medio de ergometría
convencional, a las 4-6 semanas. A los pacientes con cardiopatía isquémica ya conocida, que
comienzan nuevamente con síntomas, se deben realizar pruebas de detección de isquemia
(ecocardiografía de estrés, SPECT miocárdico, RMN cardiaca), para determinar la progresión de
la enfermedad, así como la tolerancia al esfuerzo, que permitan ajustar el tratamiento o
determinar la necesidad de manejo invasivo.
Terapia antiplaquetaria
La continuidad o suspensión de la terapia antiagregante es una decisión que debe tomarse de
forma individualizada; el riesgo de hemorragia severa espontánea, relacionada con cirugía u
otros procedimientos, debe sopesarse con el riesgo de episodios recurrentes de isquemia o
trombosis de stent, secundarios a la interrupción del tratamiento, lo cual se asocia a una
elevada mortalidad; para ello se debe tener en cuenta la localización y gravedad del sangrado
(si se trata de una hemorragia activa), el tipo de cirugía o procedimiento a efectuar (electivo o
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [348]
[23] CARDIOPATÍA ISQUÉMICA
urgente), grado de enfermedad coronaria (sin revascularización, revascularización parcial o
completa) y tiempo transcurrido desde el SCA o desde la última revascularización.
En pacientes que han presentado un SCA (revascularizado o no) las guías clínicas recomiendan
mantener doble antiagregación con AAS y un inhibidor del receptor P2Y12 durante 12 meses,
continuando solo con AAS de forma indefinida como prevención secundaria. Para los pacientes
sometidos a angioplastia electiva, la duración de la doble antiagregación estará determinada
por el tipo de stent implantado (1 mes para stent convencional y 3-6 meses para stent
farmacoactivo). Se debe intentar diferir en la medida de lo posible cualquier intervención con
alto riesgo de sangrado durante el periodo de doble antiagregación. En caso de intervención
urgente con riesgo elevado de sangrado o ante la presencia de hemorragia activa sin
posibilidad de hemostasia dirigida, se deberá considerar la retirada de uno o de los dos
antiagregantes teniendo en cuenta el tipo de stent implantado y el potencial riesgo de isquemia
miocárdica recurrente o fatal. Tras su suspensión, deberá reiniciarse la doble antiagregación
plaquetaria lo antes posible dentro de los límites de seguridad.
En caso de cirugías o procedimientos no urgentes también se deberá tener en cuenta el tiempo
mínimo de suspensión de cada fármaco para disminuir el riesgo de sangrado: AAS: 7-10 días,
prasugrel: 7 días, clopidogrel y ticagrelor: 5 días. Se ha sugerido la posibilidad de cambiar a un
fármaco antiplaquetario reversible y de vida media corta como un inhibidor de la glucoproteína
IIb/IIIa o cangrelor con el propósito de acortar el tiempo sin antiagregación plaquetaria al
periprocedimiento, aunque no existe evidencia clínica actual que apoye esta estrategia.
Anticoagulación crónica
Según las últimas recomendaciones de la ESC, aquellos pacientes con fibrilación auricular e
indicación de anticoagulación crónica a los que se realice revascularización percutánea electiva
deberán mantener la “triple terapia” un mes, reduciendo después el tratamiento a un
antiagregante (ácido acetil-salicílico o clopidogrel) y un anticoagulante oral, régimen que
deberá mantener hasta el mes 12; salvo pacientes cuyo riesgo hemorrágico se estime alto en
contraposición a la posibilidad de síndrome coronario agudo o trombosis del stent, a quien a
partir del sexto mes se indicará únicamente tratamiento anticoagulante oral.
Tras presentar un SCA los pacientes que requieren mantener anticoagulación a largo plazo,
deberán someterse a “triple terapia” con AAS, clopidogrel y anticoagulante oral durante el
menor tiempo posible, determinando el riesgo hemorrágico e isquémico. La necesidad de
anticoagulación oral deberá reevaluarse y solo se mantendrá en caso de una indicación clara
(prótesis valvular mecánica, historia reciente de trombosis relevante o fibrilación auricular con
CHA2DS2-VASc ≥ 2). Se tendrá en cuenta el tipo de stent implantado para acortar la triple
terapia a solo un antiagregante (aspirina o clopidogrel) y anticoagulación durante el primer año,
tras lo cual se podrá suspender por completo la antiagregación y dejar solo con anticoagulación
a los pacientes con bajo riesgo de complicaciones isquémicas coronarias. No se recomienda el
uso de los nuevos antiagregantes en este contexto al no existir evidencia sobre su seguridad.
Sigue siendo discutible el uso de los nuevos anticoagulantes orales (NACO); en caso de ser
necesarios, deberá usarse la dosis más baja aprobada para la prevención del ictus (rivaroxabán
15 mg/día, apixabán 2,5 mcg/12 h, dabigatrán 110 mcg/12 h).
Rehabilitación cardiaca
Recientes estudios han demostrado que la inclusión de pacientes a un programa de
rehabilitación cardiaca después de un SCA ayuda a disminuir la ansiedad y estrés, mejora la
adherencia al tratamiento farmacológico y modifica los estilos de vida, con mayor probabilidad
de mantener a largo plazo estos beneficios; además genera un condicionamiento físico que
contribuye a disminuir el riesgo de mortalidad global y de nuevos eventos cardiovasculares.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [349]
[23] CARDIOPATÍA ISQUÉMICA
Si tras 40 días del evento agudo y con tratamiento óptimo, el paciente persiste con FEVI ≤ 35%,
y sin más opciones de revascularización, se deberá considerar candidato a implante de DAI
(desfibrilador automático implantable) como prevención primaria, asociado o no a
resincronización.
2. SCASEST (ANGINA INESTABLE Y IAMSEST)
2.1. Establecimiento del riesgo
Es necesario estratificar el riesgo de isquemia y hemorragia basándonos en FRCV, anamnesis,
exploración física y resultados de pruebas complementarias (ECG de 12 derivaciones, biomarcadores de
daño miocárdico), con el propósito de establecer el diagnóstico, determinar el pronóstico y guiar el
tratamiento más indicado; las escalas de riesgo GRACE y CRUSADE (disponibles online y en app para
móviles) son útiles en este contexto (Tabla VIII).
Tabla VIII. Estratificación del riesgo en el síndrome coronario agudo sin elevación persistente del ST (SCASEST).
2.2. Tratamiento médico específico
(Ver Tabla VII en páginas anteriores).
El objetivo es disminuir las demandas de oxígeno por parte del miocardio (reduciendo la FC, la
precarga, la poscarga y la contractilidad miocárdica) o aumentando el aporte de O2 (mejoría del flujo
coronario por vasodilatación coronaria o con oxigenoterapia suplementaria).
Medidas generales
Todo paciente con sospecha de SCA deberá ser monitorizado. Se recomienda realización de
ECG a su llegada, que se repetirá según existan variaciones eléctricas o en la clínica. El uso de
oxígeno deberá restringirse para aquellos casos con SaO2 < 90% y/o insuficiencia respiratoria.
Está indicado el uso de nitratos por vía intravenosa para el control de la angina, cifras
tensionales e insuficiencia cardiaca aguda, y su dosis se titulará de acuerdo a la respuesta
clínica con precaución de no producir hipotensión arterial; como coadyuvante para el control
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [350]
[23] CARDIOPATÍA ISQUÉMICA
de los síntomas pueden utilizarse opiáceos por vía intravenosa o subcutánea; en ocasiones, se
requiere administrar ansiolíticos, los cuales deben usarse con precaución por aumentar el
riesgo de depresión respiratoria.
Tratamiento dirigido
Antiagregación: se indica la dosis de carga de AAS (preferible por vía oral) a todo
paciente que no la tomara previamente desde el primer momento del diagnóstico de
SCASEST e independientemente de la estrategia de manejo, a menos que existan
contraindicaciones o indicación clara para su suspensión. Además, se recomienda la
administración de dosis de carga de un inhibidor del receptor P2Y12 si el riesgo
isquémico es moderado o alto; la elección de este segundo antiagregante estará
determinada por el balance riesgo isquemia- hemorragia, prefiriendo el uso de
ticagrelor sobre clopidogrel en pacientes con bajo riesgo hemorrágico y en ausencia de
contraindicaciones; el uso de prasugrel sin conocimiento previo de la anatomía
coronaria no se contempla en este contexto; tampoco es posible realizar aseveraciones
sobre cangrelor (fármaco de reciente aprobación y con poca experiencia de uso clínico).
En caso de haberse administrado carga de clopidogrel y tras conocerse la anatomía
coronaria, podrá realizarse el cambio (switch) desde clopidogrel a ticagrelor o prasugrel
si se considera necesario de acuerdo al riesgo isquémico del paciente. No se
recomienda el switch desde ticagrelor a prasugrel y viceversa, excepto en casos
concretos de trombosis intrastent bajo alguno de esos tratamientos. Los pacientes con
riesgo isquémico bajo pueden esperar a la realización de la coronariografía antes de
decidirse a añadir un segundo antiagregante. Los inhibidores de la GPIIb/IIIa no se
recomiendan de forma sistemática y deberán limitarse a situaciones de rescate o
complicaciones trombóticas durante la angioplastia.
Anticoagulación en fase aguda: pacientes sin indicación de anticoagulación crónica. Se
recomienda iniciar anticoagulación de forma conjunta con la doble antiagregación a los
pacientes con SCASEST de moderado o alto riesgo isquémico, independientemente de
la estrategia de manejo. Se prefiere fondaparinux al tener el mejor perfil de
seguridad/eficacia, aunque puede usarse enoxaparina cuando no se disponga de aquel
o se requiera anticoagulación plena por otras causas (deberá ajustarse a la tasa de
filtración glomerular [TFGe]). El uso de heparina no fraccionada (HNF), con o sin
inhibidor de la GPIIb/IIIa, y de bivalirudina deberá limitarse al laboratorio de
hemodinámica ante el riesgo de sangrado mayor con estos fármacos. Aunque la
duración del tratamiento anticoagulante en el SCASEST es controvertida, se considera
que debe mantenerse durante la fase aguda (8 días) o hasta la revascularización. El
cambio entre anticoagulantes se desaconseja por aumento del riesgo de sangrado.
Pacientes con indicación de anticoagulación crónica: no se recomienda la suspensión
del tratamiento oral con antivitamina K ni hacer puente a anticoagulantes parenterales
antes del procedimiento, por aumento del riesgo de trombosis y hemorragias. Parece
razonable suspender la anticoagulación con NACO en los casos en que se va a realizar
angioplastia ya que no existe evidencia suficiente que avale su seguridad en el contexto
del SCA. Los pacientes que requieran anticoagulación a largo plazo deberán tener el
esquema de “triple terapia” con AAS y clopidogrel, al ser este último el que menor
riesgo de sangrado presenta de los inhibidores del receptor P2Y12 (ver Apartado
“Cardiopatía isquémica crónica”).
Bloqueadores beta: se recomienda su inicio precoz en SCASEST con disfunción
ventricular, una vez estabilizado el paciente y no exista riesgo de desarrollo de shock
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [351]
[23] CARDIOPATÍA ISQUÉMICA
cardiogénico. Para ello se requiere el conocimiento de la función ventricular y descartar
valvulopatía aórtica/pulmonar significativa. En algunos casos puede iniciarse antes, con
precaución, cuando es imprescindible el control de la FC para reducir la isquemia en
curso. Contraindicados en la angina por consumo de cocaína/anfetaminas, ante
sospecha de angina vasoespástica y en situación Killip/KimbalI III y IV (en pacientes
tratados previamente y que se presenten con KK I-II no debe suspenderse).
Bloqueadores de los canales de calcio: los dihidropiridínicos se indican como alternativa
para aquellos pacientes con intolerancia, contraindicación a los betabloqueantes o
como coadyuvantes para el control de los síntomas. Los no dihidropiridínicos son de
elección para tratar la angina vasoespástica o por consumo de cocaína/anfetaminas.
Rara vez se inicia tratamiento con ranolazina e ivabradina para el control de la clínica
anginosa durante la fase aguda de un SCASEST, ya que primero se pretende titular al
alza las dosis de fármacos que han demostrado impacto en la supervivencia y la
disminución de eventos CV futuros como los betabloqueantes.
Estatinas: se debe administrar una estatina a altas dosis de forma precoz a todos los
pacientes, salvo contraindicación (atorvastatina 80 mg/día o rosuvastatina 20 mg/día),
independientemente de los niveles de colesterol, ya que han demostrado ayudar a
estabilizar la placa de ateroma y disminuir la incidencia de IAM e ictus.
Hipolipemiantes no estatínicos: En revisiones posteriores al alta hospitalaria, de no
cumplir los objetivos con respecto al LDLc (véase tratamiento de cardiopatía isquémica
crónica), podría valorarse la adición de ezetimibe a dosis de 10 mg/24 horas.
IECA/ARA II: su inicio precoz tiene efectos beneficiosos sobre la mortalidad
cardiovascular y el remodelado cardiaco. Tras conseguir estabilidad hemodinámica,
deberá iniciarse en todo paciente con FEVI ≤ 40%, insuficiencia cardiaca, diabetes o
HTA; en caso de intolerancia usar ARA II. Si existe contraindicación, considerar el uso de
hidralazina y dinitrato de isosorbide.
Antialdosterónico: deberá iniciarse tratamiento con eplerenona (preferible) o
espironolactona a todo paciente con FEVI ≤ 35% e insuficiencia cardiaca o diabetes, en
ausencia de contraindicaciones.
Inhibidores de la bomba de protones: administrar a todo paciente con doble terapia
antiagregante y elevado riesgo de hemorragia digestiva.
2.3. Revascularización
Se valorará la indicación de una estrategia invasiva y la prontitud con la que debe llevarse a cabo en
función del riesgo isquémico del paciente; los SCASEST de riesgo muy alto, alto y moderado, deberán ser
sometidos a coronariografía y revascularización si procede, por el contrario, los de riesgo bajo y sin
síntomas recurrentes, podrán esperar a la confirmación de isquemia por medio de pruebas no invasivas de
isquemia (preferiblemente pruebas de estrés con imagen) (ver “Algoritmo 2”).
3. SCACEST (IAMCEST)
El tratamiento está dirigido a la apertura inmediata del vaso ocluido sin esperar a la realización de
más pruebas diagnósticas ni a resultados de laboratorio, para ello debe activarse la red de atención
inmediata al IAMCEST (código IAM en la Comunidad Autónoma de Madrid). La localización y el tiempo de
evolución de la oclusión determinarán la extensión de la necrosis miocárdica.
3.1. Tratamiento médico específico
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [352]
[23] CARDIOPATÍA ISQUÉMICA
Medidas generales
Estas medidas no deben retrasar la revascularización urgente de la arteria coronaria culpable,
pero deben adoptarse desde la primera atención al paciente. Es imperativo el control del dolor
para disminuir los efectos de la descarga adrenérgica sobre el trabajo miocárdico; como ya se
expuso en el apartado de SCASEST se puede considerar el uso de nitratos (especialmente si se
asocia HTA o insuficiencia cardiaca) y opiáceos para reducir el dolor y la disnea. Igualmente, la
administración de oxigenoterapia suplementaria se limita a los pacientes con SaO2 < 90%.
Tratamiento dirigido
Antiagregación: se debe administrar doble antiagregación desde el primer contacto
médico con dosis de carga de AAS (preferiblemente por vía oral) y un inhibidor del
receptor P2Y12 como prasugrel, ticagrelor o cangrelor que son fármacos más potentes
y con un inicio de acción más rápido que el del clopidogrel, restringiendo su uso a
aquellos casos en que los previos no estén disponibles, estén contraindicados o cuando
la estrategia de revascularización elegida sea la fibrinólisis. El uso de inhibidores de la
glucoproteína IIb/IIIa (abciximab, tirofibán, eptifibatide), si está indicado, se restringe
para el laboratorio de hemodinámica.
Bloqueadores beta: deberán iniciarse vía oral a partir de las 24 horas del evento agudo,
una vez conseguida estabilidad clínica del paciente. Se podría considerar su uso iv
durante la fase aguda en aquellos pacientes que se presenten hipertensos,
taquicárdicos y sin insuficiencia cardiaca, en ausencia de contraindicaciones.
Bloqueadores de los canales de calcio: son una alternativa al tratamiento
betabloqueante cuando exista intolerancia o contraindicación.
IECA/ARA II: indicado su inicio de forma precoz en aquellos con FEVI ≤ 40%,
insuficiencia cardiaca, diabéticos, hipertensos o con IAM anterior. Como alternativa se
recomienda el uso de un ARA II.
Antialdosterónicos: misma indicación que para el SCASEST.
Anticoagulación en fase aguda: se administrará a criterio del cardiólogo
intervencionista en caso de que se realice angioplastia primaria (bivalirudina, HNF o
HBPM). Si la estrategia elegida es la fibrinólisis, se deberá iniciar anticoagulación y
mantenerla hasta la revascularización invasiva.
Aquellos pacientes sobre los que se decida una estrategia conservadora del SCACEST,
recibirán anticoagulación durante los primeros 8 días del evento con fondaparinux (de
elección) o enoxaparina (esta se prefiere sobre la HNF en pacientes que requieren
anticoagulación plena por otras causas). No existe evidencia científica que avale la
continuidad o el inicio de la terapia anticoagulante con los NACO durante la fase aguda
del SCACEST, por lo que parece razonable revalorar su indicación tras la
revascularización de la lesión culpable. En caso de indicación clara para anticoagulación
crónica deberá iniciarse el esquema de triple terapia expuesto previamente.
Estatinas: misma indicación que en SCASEST.
3.2. Reperfusión
La apertura de la arteria coronaria se realiza por medio de intervención coronaria percutánea
(también llamada “angioplastia coronaria”) o con la administración de un fibrinolítico por vía intravenosa.
Cualquiera que sea el método, este deberá realizarse en las primeras 12 h del inicio de los síntomas,
pudiendo efectuarse hasta pasadas esas 12 h en caso de persistencia de la clínica y/o de los cambios
eléctricos que sugieran isquemia en curso (Figura 2).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [353]
[23] CARDIOPATÍA ISQUÉMICA
Figura 2. Sospecha de síndrome coronario agudo.
Angioplastia primaria
Se considera angioplastia primaria cuando se opta por una estrategia mecánica de reperfusión
sin haber administrado fármacos fibrinolíticos previamente. Es de elección frente a la
fibrinólisis si se lleva a cabo dentro de los tiempos recomendados por las guías clínicas,
especialmente si se realiza en un centro experimentado con un alto volumen de
procedimientos.
La revascularización consiste en la apertura de la arteria responsable del infarto por medio del
inflado intraluminal de un balón y/o el implante de uno o más stents. No existe evidencia actual
que apoye la revascularización de lesiones no culpables en el mismo procedimiento, excepto en
casos de shock cardiogénico o persistencia de la isquemia.
Angioplastia de rescate
Se denomina angioplastia de rescate al uso de la estrategia mecánica de reperfusión tras haber
administrado un fibrinolítico que ha resultado ineficaz.
Terapia fibrinolítica
Los agentes fibrinolíticos (Tabla IX) son la alternativa a la angioplastia primaria cuando no es
posible cumplir con los tiempos estipulados para la revascularización, en ausencia de
contraindicaciones absolutas (Tabla X).
Deberán administrarse conjuntamente carga de AAS y clopidogrel ya que los nuevos
antiagregantes no se han estudiado en este contexto y podrían aumentar el riesgo de
hemorragias graves; además, requiere complementar el tratamiento con anticoagulación
parenteral (fondaparinux, enoxaparina o HNF). Se deberá realizar una coronariografía
preferente en las primeras 24 h tras la fibrinólisis en caso de que esta sea eficaz (descenso del
ST > 50% con respecto al previo y resolución de los síntomas tras los primeros 60 min del inicio
de la infusión) o de forma urgente (angioplastia de rescate) cuando se considere que ha sido
fallida.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [354]
[23] CARDIOPATÍA ISQUÉMICA
Tabla IX. Agentes fibrinolíticos en SCACEST.
Tabla X. Contraindicaciones de la fibrinólisis.
3.3. Pacientes no reperfundidos
La evidencia científica de la que disponemos actualmente demuestra que la revascularización tardía
de una arteria responsable del IAMCEST en pacientes estables no tiene beneficio añadido sobre el
tratamiento médico óptimo. Por tanto, en estos pacientes solo debe considerarse la realización de
angioplastia cuando exista angina recurrente o isquemia residual documentada y viabilidad tisular probada
a partir de una prueba de imagen no invasiva en un territorio miocárdico extenso.
VII. OTRAS CONSIDERACIONES
1. MANEJO DURANTE LA HOSPITALIZACIÓN Y EL ALTA
Pacientes con SCASEST de bajo riesgo requieren ingreso hospitalario en planta de Cardiología para
el tratamiento médico y completar los estudios si procede. Aquellos con SCASEST de riesgo intermedio o
alto riesgo y los que se presentan como SCACEST con o sin reperfusión, deberán ingresar en una unidad
especializada (Unidad Coronaria o Unidad de Cuidados Intensivos) con capacidad de monitorización
continua y atención de las potenciales complicaciones que puedan presentarse durante al menos 24 horas.
A continuación se valorará la indicación de traslado a planta de hospitalización de Cardiología. Se deberá
realizar un análisis de laboratorio completo al momento de la llegada del paciente que incluya hemograma,
bioquímica con función renal y hepática, biomarcadores cardiacos y coagulación. La indicación de una
radiografía de tórax será determinada por el perfil clínico del paciente y la presencia de otras
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [355]
[23] CARDIOPATÍA ISQUÉMICA
comorbilidades. Durante la hospitalización se realizará un acercamiento diagnóstico al perfil metabólico del
paciente, determinando niveles plasmáticos de colesterol, glucemia y HBA1c basales, al igual que se
realizará un seguimiento analítico para valorar potenciales efectos adversos del tratamiento como
deterioro de la función renal o hepática y hemorragias.
2. COMPLICACIONES ASOCIADAS AL SCA
Ver a continuación la tabla XI sobre las complicaciones del síndrome coronario agudo (SCA).
Tabla XI. Complicaciones del síndrome coronario agudo.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [356]
[23] CARDIOPATÍA ISQUÉMICA
3. CIRUGÍA CARDIACA CORONARIA
La indicación de revascularización quirúrgica durante un SCACEST en curso está delimitada por la
imposibilidad de un abordaje percutáneo urgente y el balance riesgo/beneficio de realizar una intervención
quirúrgica mayor sobre un paciente con isquemia miocárdica intercurrente y comorbilidades de base que
determinarán la evolución intra y en el postoperatorio inmediato; por este motivo rara vez se baraja esta
opción. En al menos el 10% de los pacientes con SCASEST se valora la opción quirúrgica; aunque la mayor
dificultad reside en encontrar un equilibrio entre los riesgos isquémicos y hemorrágicos relacionados con el
momento de la cirugía y el tratamiento antitrombótico perioperatorio, no hay que olvidar que estos
pacientes suelen tener un riesgo quirúrgico más elevado. Es, por tanto, imperativo, un estudio minucioso
de cada caso por parte del Heart Team que tendrá en cuenta la situación basal y preferencias del paciente,
el balance riesgo-beneficio y el score SYNTAX (caracteriza angiográficamente la localización y extensión de
las lesiones coronarias).
Ante la necesidad de cirugía coronaria urgente la anticoagulación deberá revertirse con complejos
protrombínicos o vitamina K (según esté indicado). Para cirugías coronarias no urgentes, se mantendrá la
antiagregación con aspirina y se suspenderá el segundo antiagregante como ya se indicó en el apartado de
cardiopatía isquémica crónica. En caso de haberse mantenido la anticoagulación oral durante la fase aguda
del SCA, esta deberá suspenderse al menos 24 horas antes para antagonistas de la vitamina K y 48 horas
para los NACO. Tanto la anti-agregación como la anticoagulación (si se requiere a largo plazo), deberán
iniciarse tan pronto como sea posible.
4. TRATAMIENTO CONSERVADOR DEL SCA
Son candidatos a una estrategia conservadora todos aquellos pacientes sobre los que se no se
identifique beneficio en cuanto a la reducción de complicaciones (por el aumento estimado del riesgo
relacionado con la coronariografía y con la revascularización) o mejoría en la calidad de vida. En ellos el
objetivo primordial es el manejo de los síntomas con tratamiento farmacológico. Habitualmente dentro de
este grupo se encuentran pacientes muy ancianos o frágiles, con comorbilidades limitantes, insuficiencia
renal crónica grave, cáncer avanzado con expectativa de vida corta o riesgo muy alto de complicaciones
hemorrágicas.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [357]
[23] CARDIOPATÍA ISQUÉMICA
Asimismo, existen características anatómicas/funcionales de las arterias coronarias y del miocardio
que pueden indicar una estrategia conservadora sobre una invasiva: enfermedad coronaria no obstructiva
(confirmada por imagen intracoronaria o medición de la reserva fraccional del flujo), arterias coronarias
normales (miocardiopatía de Tako-tsubo, vasoespasmo, enfermedad microvascular, embolia coronaria no
relacionada con EAC), enfermedad coronaria grave y difusa con dificultad para revascularización
percutánea/quirúrgica y ausencia de viabilidad miocárdica en territorios irrigados por coronarias con
enfermedad obstructiva.
BIBLIOGRAFÍA
Braunwald E, Morrow DA. Unstable angina: is it time for a requiem? Circulation. 2013;127:2452-7.
Kirschhof M, Benussi S, Kotecha D, et al. 2016 ESC Guidelines for the management of atrial fibrillation
developed in collaboration with the EACTS. The Task Force for the management of atrial fibrillation.
Developed with the very special contribution of the European Heart Rhythm Association (EHRA) of the
ESC. Endorsed by the European Stroke Organization (ESO). Eur Heart J. (2016) ehw210.
Kristensen SD, Laut KG, Fajadet J, et al. Reperfusion therapy for ST elevation acute myocardial
infarction 2010/2011: current status in 37 ESC countries. Eur Heart J. 2014;35(29):1957-70.
Montalescot G, Sechtem U, Achenbach S, et al. 2013 ESC guidelines on the management of stable
coronary artery disease: the Task Force on the management of stable coronary artery disease of the
European Society of Cardiology. Eur Heart J. 2013;34:2949-3003.
Mueller C. Biomarkers and acute coronary syndromes: an update. Eur Heart J. 2014;35:552-6.
Reichlin T, Twerenbold R, Maushart C, et al. Risk stratification in patients with unstable angina using
absolute serial changes of 3 high-sensitive troponin assays. Am Heart J. 2013;165:371-8, e373.
Reichlin T, Twerenbold R, Reiter M, et al. Impact on myocardial infarction incidence and prognosis. Am J
Med. 2012;125:1205-13, e1201.
Roffi M, Patrono C, Collet J-P, et al. 2015 ESC guidelines for the management of acute coronary
syndromes in patients presenting without persistent ST-segment elevation: Task Force for the
Management of Acute Coronary Syndromes in Patients Presenting without Persistent ST-Segment
Elevation of the European Society of Cardiology. Eur Heart J. 2016;37(3):267-315.
Steg PG, James SK, Atar D, et al. 2012 ESC Guidelines for the management of acute myocardial
infarction in patients presenting with ST-segment elevation: Task Force on the management of ST-
segment elevation acute myocardial infarction of the European Society of Cardiology. Eur Heart J.
2012;33 (20):2569-619.
Thygesen K, Alpert JS, Jaffe AS, et al. Third universal definition of myocardial infarction. Eur Heart J.
2012;33:2551-67.
Thygesen K, Mair J, Giannitsis E, et al. How to use high-sensitivity cardiac troponins in acute cardiac
care. Eur Heart J. 2012;33:2252-7.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [358]
[24] VALVULOPATÍAS
24.Valvulopatías
Elena Puerto García Martín.
Cardiología
Ana Isabel García Gutiérrez.
Cirugía Cardiaca
Coral Arévalo Cañas.
Medicina Interna
Asesor: Carmen Jiménez López-Guarch. Médica Adjunta, Unidad de Imagen Cardiaca. Servicio de Cardiología
I. VALVULOPATÍA MITRAL
A. ESTENOSIS MITRAL
1. INTRODUCCIÓN
La estenosis mitral (EM) es la reducción del área de la válvula mitral que produce una obstrucción
del flujo de sangre desde la aurícula izquierda (AI) al ventrículo izquierdo (VI).
2. ETIOLOGÍA
La primera causa de EM es la enfermedad reumática, que se desarrolla entre 2 y 20 años tras la
enfermedad reumática aguda, y que afecta de forma predominante a mujeres. Otras causas menos
frecuentes que se deben tener en cuenta son: EM de origen congénito (usualmente asociada a cardiopatías
complejas), anillo mitral supravalvular, síndrome carcinoide, lupus, artritis reumatoide, mucopolisacaridosis
o EM secundaria al tratamiento con metisergida.
3. FISIOPATOLOGÍA
El área valvular mitral del adulto es de aproximadamente 5 cm2. Cuando esta se reduce de forma
crónica se activan los mecanismos compensadores y el llenado del VI se mantiene a expensas de un
gradiente de presión diastólico entre la AI y el VI, produciéndose una elevación significativa de presión en la
AI cuando el orificio mitral es inferior a 1,5 cm2. Este incremento de presión se transmite retrógradamente,
produciendo un aumento de presión venocapilar pulmonar que se expresa con la aparición de signos y
síntomas de congestión pulmonar. En las fases más avanzadas de EM puede aparecer hipertensión
pulmonar (HTP) y signos de fallo del ventrículo derecho.
La duración de la diástole y la distensibilidad del VI son imprescindibles en el llenado del VI,
especialmente ante situaciones que dificultan su llenado como la EM, de modo que circunstancias que
provoquen taquicardia pueden contribuir al empeoramiento sintomático.
Los pacientes con EM pueden presentar también un descenso de la fracción de eyección por
disminución de la precarga en el VI, llegando incluso a una hipoperfusión crónica que provoque un
incremento de la resistencia vascular periférica, aumentando de este modo la poscarga y disminuyendo
aún más la fracción de eyección.
4. CLÍNICA
Existe un largo periodo de latencia desde el comienzo de la estenosis hasta la aparición de los
síntomas, aunque en pacientes con EM leve pueden desencadenarse precozmente ante situaciones como
la taquicardia.
Los principales síntomas en la EM más avanzada se deben a la congestión pulmonar (disnea de
esfuerzo, ortopnea y disnea paroxística nocturna). También son característicos, aunque menos frecuentes,
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [359]
[24] VALVULOPATÍAS
otros síntomas debidos al aumento de presiones pulmonares, como la hemoptisis y las infecciones
pulmonares.
En las fases más avanzadas de la valvulopatía predominan los síntomas de insuficiencia cardiaca
derecha secundarios a una HTP mantenida, mejorando en esta fase los síntomas de insuficiencia cardiaca
izquierda.
La dilatación auricular favorece la aparición de fibrilación auricular (FA) y la formación de trombos y
fenómenos tromboembólicos sistémicos. Además, la válvula enferma es más propensa al desarrollo de
endocarditis.
En la exploración física es muy característica la presencia de chapetas malares en las fases
avanzadas de la enfermedad. En el pulso venoso yugular puede observarse una onda “a” prominente por la
contracción vigorosa de la AI para mantener el gradiente transvalvular, siempre y cuando no coexista FA.
A la auscultación destaca soplo mesodiastólico que puede sucederse de un refuerzo presistólico,
irradiado a la axila y auscultándose con mayor intensidad a nivel del ápex, con el paciente en decúbito
lateral izquierdo, que aumenta tras el ejercicio. También puede auscultarse un incremento de intensidad
del primer tono y un chasquido de apertura tras el segundo tono (hallazgo más característico, aunque
desaparece cuando la movilidad valvular disminuye). Su duración y su intensidad se relacionan
directamente con la magnitud de la estenosis. En pacientes con HTP existe un aumento de intensidad del
segundo tono y en muchos casos soplos de insuficiencia tricuspídea (IT) y pulmonar (IP) secundarias (soplo
de Graham-Steel).
La distancia entre el segundo ruido y el chasquido de apertura mitral constituye un buen índice del
grado de estenosis, siendo mayor este cuanto más próximo se encuentra el chasquido del segundo ruido.
5. DIAGNÓSTICO
5.1. Electrocardiograma
En ausencia de FA se observan signos de crecimiento de la AI. La presencia de criterios de
crecimiento ventricular derecho suele ser secundaria a HTP significativa. La existencia de crecimiento
ventricular izquierdo implica siempre una enfermedad asociada.
5.2. Radiografía de tórax
Son frecuentes los signos de crecimiento de la AI, y en fases avanzadas de las cavidades derechas,
así como otros signos de HTP. Pueden existir datos de congestión pulmonar e incluso apreciarse la
calcificación valvular en la EM de larga evolución.
5.3. Ecocardiograma
Es la técnica de elección para establecer el diagnóstico y evaluar la repercusión hemodinámica.
Además, permite la valoración anatómica y funcional, evaluar la función ventricular, estimar las presiones
pulmonares y valorar la presencia de patología valvular concomitante. Se considera que la EM es severa
cuando el área valvular es menor de 1 cm2 o el gradiente transvalvular medio supera los 10 mm Hg.
Se han desarrollado escalas para evaluar la idoneidad anatómica de la válvula de cara a la
realización de una valvuloplastia mitral percutánea (VMP), para ello se evalúan el grosor valvular, la
movilidad, la calcificación, la afectación del aparato subvalvular y las comisuras (score de Wilkins).
Estará indicado realizar un estudio transesofágico cuando el ecocardiograma transtorácico
proporcione una información subóptima sobre la anatomía o el grado de insuficiencia mitral (IM) asociada y
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [360]
[24] VALVULOPATÍAS
como paso previo a la realización de una valvuloplastia percutánea, con el fin de descartar trombos en la AI,
así como de evaluar la anatomía valvular.
Está indicada la repetición de un ecocardiograma transtorácico ante el empeoramiento sintomático
de un paciente diagnosticado de EM. Además, se deberá realizar un seguimiento ecocardiográfico de los
pacientes con EM a pesar de no presentar empeoramiento clínico: cada dos años en pacientes con EM leve
o anual en el caso de EM moderada-severa.
5.4. Ecocardiograma de esfuerzo
El ecocardiograma de esfuerzo es la prueba de elección para valorar la capacidad funcional real en
casos de discrepancia clínico/ecocardiográfica, ya que mide el gradiente valvular y la presión pulmonar,
determinantes de la capacidad funcional. En caso de no ser posible, se puede optar por una ergometría.
5.5. Cateterismo cardiaco
No suele ser necesario recurrir a la evaluación invasiva de la severidad de la EM. Se debe realizar
cuando existe discrepancia entre la clínica y el ecocardiograma. La coronariografía prequirúrgica, al igual
que en el resto de valvulopatías, ha de realizarse en los casos indicados (Tabla I).
Tabla I. Indicaciones de coronariografía prequirúrgica (IC).
6. TRATAMIENTO
El algoritmo terapéutico y de seguimiento se recoge en la figura 1.
6.1. Tratamiento médico
Los pacientes con EM leve asintomáticos no precisan tratamiento. Para controlar los síntomas
secundarios a la congestión pulmonar es recomendable restringir los aportes de sodio en la dieta,
diuréticos y nitratos.
Deben evitarse en lo posible todos los factores desestabilizantes como la taquicardización, la fiebre,
el ejercicio extremo o la anemia. Los fármacos cronotropos negativos (betabloqueantes y antagonistas de
los canales de calcio) pueden mejorar la tolerancia al ejercicio al prolongar la diástole en pacientes que
presentan FA con respuesta ventricular no controlada, así como en pacientes en ritmo sinusal con mala
tolerancia al ejercicio.
La anticoagulación es obligada en pacientes con FA, episodios de embolia sistémica o trombos en la
AI; se recomienda además cuando la AI está dilatada (diámetro mayor de 50 mm). El objetivo es mantener
una razón internacional normalizada (INR) en el límite superior del rango 2-3. Los pacientes con EM no
necesitan realizar prevención para prevenir la endocarditis infecciosa.
6.2. Tratamiento intervencionista
El tipo de tratamiento y el momento en el que debe iniciarse se decidirá en función de las
características clínicas, la anatomía valvular y la experiencia del centro en las distintitas opciones
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [361]
[24] VALVULOPATÍAS
terapéuticas. La intervención solamente debe realizarse en pacientes sintomáticos con EM significativa
(área valvular menor de 1,5 cm² o menor de 1 cm2/m2 de superficie corporal).
Figura 1. Algoritmo terapéutico y de seguimiento de la estenosis mitral.
Valvuloplastia mitral percutánea
Es la técnica de elección cuando no es preciso actuar sobre otras válvulas y la anatomía de la
misma lo permite, ya que ofrece resultados similares a la comisurotomía quirúrgica, pero con
menor morbimortalidad. El riesgo más importante, aunque poco frecuente, es la ruptura de la
válvula, con la consiguiente IM severa aguda que obliga al tratamiento quirúrgico.
Consiste en introducir por vía femoral un catéter provisto de uno o dos balones inflables,
pasando a cavidades izquierdas a través del septo interauricular, por una punción transeptal. Se
infla a nivel del plano valvular mitral, aumentando así el área efectiva de la válvula estenótica.
Se puede ofrecer como tratamiento inicial en pacientes seleccionados con anatomía valvular
favorable, que no presenten IM superior a leve y ausencia de trombos en la AI (Tablas II y III).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [362]
[24] VALVULOPATÍAS
Tabla II. Indicaciones de valvuloplastia mitral percutánea.
Tabla III. Contraindicaciones para la valvuloplastia mitral percutánea.
Comisurotomía quirúrgica
La comisurotomía abierta, aunque en nuestro medio no se realiza habitualmente, es una
técnica de gran interés en centros con gran experiencia reparadora. Existen dos tipos: cerrada
(con el corazón latiendo sin circulación extracorpórea), ya en desuso, y abierta (con el corazón
parado y con circulación extracorpórea).
Recambio valvular protésico
En la práctica diaria, la cirugía consiste en el recambio valvular por prótesis mecánica o
biológica. Se lleva a cabo en los pacientes en los que la valvuloplastia mitral está
contraindicada. Las indicaciones de recambio valvular protésico de describen en la tabla IV. La
supervivencia a largo plazo está relacionada con la edad, la clase funcional, la FA, el grado de
HTP, la función ventricular izquierda preoperatoria y las complicaciones de la válvula protésica.
Tabla IV. Indicaciones de cirugía en la estenosis mitral.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [363]
[24] VALVULOPATÍAS
B. INSUFICIENCIA MITRAL
1. INTRODUCCIÓN
La insuficiencia mitral (IM) consiste en la regurgitación de sangre desde el VI a la AI durante la
sístole, debida a un defecto del cierre de la válvula mitral.
2. ETIOLOGÍA Y TIPOS
Se clasifica, según su mecanismo, en:
2.1. Insuficiencia mitral primaria u orgánica
Se produce por lesiones intrínsecas de los componentes del aparato valvular mitral: válvulas, anillo,
cuerdas tendinosas o músculos papilares.
En función de la forma de presentación se divide, a su vez, en dos tipos:
Insuficiencia mitral aguda
Las causas más frecuentes que la ocasionan son:
Rotura del músculo papilar: se debe sospechar en los pacientes que presentan edema
agudo de pulmón o shock cardiogénico tras un infarto agudo de miocardio.
Endocarditis infecciosa: por destrucción o perforación de las válvulas o por rotura de
cuerdas tendinosas.
Traumatismo.
Insuficiencia mitral crónica
Las causas más comunes son:
Degeneración por déficit fibroelástico: asociada habitualmente a calcificación del
aparato valvular y retracción de los velos. Actualmente es la etiología más frecuente en
los países desarrollados, especialmente en ancianos.
Degeneración mixomatosa: elongación redundante de los velos y cuerdas, que se
traduce en una movilidad excesiva y prolapso de los velos hacia la AI. Puede asociarse a
rotura de cuerdas tendinosas. Es propia de poblaciones más jóvenes.
Enfermedad reumática: por cicatrización y retracción de los velos, especialmente el
posterior, con afectación del aparato subvalvular. Se asocia con fusión comisural y EM.
Aunque su prevalencia ha disminuido en Europa, continúa siendo la etiología más
frecuente en países subdesarrollados.
Endocarditis infecciosa: deformación de la válvula por retracción de las válvulas en la
fase de curación.
Congénita: la forma más común es el cleft o hendidura mitral, que se puede presentar
de forma aislada o asociada a defectos del canal auriculoventricular o comunicación
interauricular.
2.2. Insuficiencia mitral secundaria o funcional
Los componentes del aparato valvular mitral conservan su estructura anatómica, pero existe una
distorsión de la geometría ventricular que impide la coaptación y aposición apropiada de los velos.
Se puede producir por varios mecanismos:
Expansión del anillo mitral secundaria a dilatación del VI.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [364]
[24] VALVULOPATÍAS
Desplazamiento apical del músculo papilar debido al remodelado del VI, que produce tracción
(tethering) del velo al que se encuentra anclado mediante las cuerdas tendinosas y pérdida de
las fuerzas de cierre.
Pérdida del movimiento de contracción anular o esfinteriana por alteraciones de la
contractilidad.
Alteración del cierre por asincronía de la contractilidad.
Las causas más habituales que lo producen son:
Miocardiopatía dilatada de cualquier etiología: por dilatación del VI.
Estimulación ventricular derecha: por asincronía de la contractilidad.
Enfermedad coronaria: por cualquiera de los cuatro mecanismos reflejados previamente.
La IM isquémica crónica, incluida en este grupo, es una entidad dinámica, cuya gravedad aumenta
significativamente cuando se incrementa la poscarga (hipertensión arterial [HTA], ejercicio, etc.). Es una
complicación frecuente tras el infarto agudo de miocardio (20%), más probable en aquellos de localización
inferior por una irrigación más precaria y única del músculo papilar posterior desde la arteria descendente
posterior.
3. FISIOPATOLOGÍA
En la IM el gasto cardiaco disminuye, dado que gran parte del flujo sistólico se dirige hacia la AI.
Cuando la sangre retorna al VI en diástole, provoca una sobrecarga de volumen y un aumento de la
precarga que, de acuerdo con la ley de Frank-Starling, incrementa la contractilidad. Además, según la forma
de presentación, existen dos situaciones fisiopatológicas diferentes:
Insuficiencia mitral aguda: la poscarga del VI es baja debido a que el orificio mitral reduce la
impedancia del VI al vaciamiento, lo que sumado al mayor inotropismo genera un estado
hiperdinámico. El aumento súbito del volumen auricular aumenta la presión capilar pulmonar
favoreciendo la congestión izquierda.
Insuficiencia mitral crónica: el VI se dilata y desarrolla hipertrofia excéntrica para incrementar el
volumen sistólico total y tratar de mantener un flujo anterógrado normal a pesar del flujo
regurgitante que se desvía hacia la AI. La poscarga, conforme el radio del VI aumenta, pasa de
baja a normal. La AI se dilata para evitar que las presiones de llenado del VI elevadas se
transmitan al lecho capilar pulmonar. Si la sobrecarga de volumen progresa, disminuye la
contractilidad, con caída de la fracción de eyección del ventrículo izquierdo (FEVI) y aumento
del volumen regurgitante. En esta fase de descompensación, la poscarga está muy elevada.
4. CLÍNICA
Insuficiencia mitral aguda: el aumento brusco de la presión capilar pulmonar produce
congestión pulmonar, que cursa con disnea de reposo, ortopnea o edema agudo de pulmón,
asociado a signos de disminución del flujo anterógrado, incluido el shock cardiogénico.
Insuficiencia mitral crónica: suele ser asintomática durante años. Los primeros síntomas suelen
ser intolerancia al ejercicio y disnea de esfuerzo, y a medida que progresa aparece astenia,
debilidad y caquexia. Los signos de insuficiencia cardiaca congestiva izquierda como la ortopnea
y la disnea paroxística nocturna se suelen presentar cuando desarrollan disfunción ventricular.
Se puede presentar FA por dilatación de la AI. En los casos de larga evolución puede aparecer
HTP y signos de fallo del ventrículo derecho.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [365]
[24] VALVULOPATÍAS
En la exploración física se evidencia un latido de la punta hiperdinámico y desplazado hacia la
izquierda. El soplo de IM es holosistólico, piante e irradiado a la axila. En la IM aguda el soplo puede ser de
baja intensidad o inaudible por igualación de presiones en las cavidades izquierdas.
5. DIAGNÓSTICO
5.1. Electrocardiograma
Los signos son muy inespecíficos, aunque pueden observarse datos de crecimiento de las cavidades
izquierdas y FA.
5.2. Radiografía de tórax
Muestra cardiomegalia, con dilatación de las cavidades izquierdas en la IM crónica con datos de
congestión pulmonar variables.
5.3. Ecocardiograma
Es el examen principal, que debe incluir la evaluación de la gravedad, los mecanismos implicados, la
función biventricular, el tamaño de la AI y la HTP.
Son datos de severidad: vena contracta 7 mm,> inversión sistólica del flujo en venas pulmonares, volumen
regurgitante > 60 ml y orificio regurgitante efectivo (ORE) > 40 mm2 en la IM primaria o > 30 ml y > 20 mm2
en la secundaria.
El ecocardiograma transesofágico (preferiblemente ecografía tridimensional) puede ayudar a definir el
mecanismo y permite evaluar las posibilidades de reparación quirúrgica en los casos de prolapso valvular
mitral.
La ecocardiografía de esfuerzo permite cuantificar los cambios y la agravación de la IM inducidos por el
ejercicio y la modificación de la función ventricular.
La FEVI < 60% y la dilatación del VI (diámetro telesistólico [DTS] > 40-45 mm) son marcadores de riesgo
perioperatorio de morbilidad y mortalidad.
5.4. Resonancia magnética (RM)
Permite realizar un análisis cuantitativo de la severidad de la IM, y es la prueba de referencia para
determinar la función sistólica ventricular en casos en los que el ecocardiograma no sea definitivo.
5.5. Prueba de esfuerzo cardiopulmonar
La determinación de la capacidad funcional ayuda en la valoración clínica de anamnesis equívocas o
pacientes oligosintomáticos.
La ecocardiografía de ejercicio es la técnica de elección en casos de discordancia clínica/
ecocardiográfica y en los casos de IM isquémica.
5.6. Cateterismo cardiaco
No suele ser necesario. Se deberá realizar si los estudios no invasivos no son concluyentes o son
discordantes con la clínica. Se realizará una coronariografía prequirúrgica cuando esté indicada (Tabla I).
6. TRATAMIENTO
El algoritmo terapéutico y de seguimiento se recoge en la figura 2.
6.1. Tratamiento médico
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [366]
[24] VALVULOPATÍAS
Dirigido a aliviar los síntomas de congestión mediante diuréticos y a disminuir la poscarga mediante
vasodilatadores que aumentan el gasto cardiaco y reducen el flujo regurgitante.
Insuficiencia mitral aguda
Se pueden emplear nitratos intravenosos y diuréticos para reducir la precarga y las presiones
de llenado del VI. Además, en pacientes normotensos o hipertensos el nitropusiato u otros
nitratos intravenosos actúan como vasodilatadores arteriales disminuyendo la poscarga.
Cuando hay hipotensión o shock cardiogénico se pueden añadir inotrópicos (p.ej., dobutamina)
o incluso implantar un balón de contrapulsación intraaórtico como puente a la cirugía.
Insuficiencia mitral crónica
Los vasodilatadores orales, especialmente los inhibidores de la enzima de conversión de la
angiotensina (IECA) o la hidralazina, se reservan para pacientes con insuficiencia cardiaca o FEVI
reducida.
No están indicados en pacientes normotensos, asintomáticos, con función ventricular normal.
Se recomienda el uso de betabloqueantes y espironolactona. En la IM isquémica es
fundamental optimizar el tratamiento de la enfermedad coronaria, incluyendo la
revascularización.
En la IM secundaria a disfunción ventricular, debe establecerse el tratamiento habitual de la
insuficiencia cardiaca (IECA, betabloqueantes, espironolactona, resincronización, etc.). En caso
de disfunción ventricular izquierda con congestión pulmonar, pueden administrarse diuréticos y
digoxina, evitando fármacos depresores de la contractilidad miocárdica. Los pacientes con IM
no necesitan realizar prevención de la endocarditis infecciosa.
Figura 2. Algoritmo terapéutico y de seguimiento de la insuficiencia mitral.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [367]
[24] VALVULOPATÍAS
6.2. Tratamiento intervencionista
Tratamiento quirúrgico
Se puede realizar de tres formas diferentes: reparación valvular, sustitución valvular con
preservación total o parcial del aparato subvalvular mitral y sustitución valvular con resección
completa del aparato subvalvular mitral. Si la válvula es anatómicamente susceptible de
reparación y el equipo quirúrgico tiene experiencia, esta técnica es actualmente de elección,
sobre todo si se debe a prolapso del velo posterior. Se puede considerar en la valvulopatía
reumática si la reparación es duradera y la anticoagulación a largo plazo es cuestionable. En el
resto de los casos se recomienda reemplazo valvular mitral con preservación del aparato
subvalvular cuando sea posible. En la IM isquémica la cirugía debe asociar revascularización
miocárdica si es posible.
Las indicaciones para la cirugía se exponen en la tabla V.
Tabla V. Indicaciones de cirugía en la insuficiencia mitral.
Tratamiento percutáneo
En la actualidad existen distintas técnicas percutáneas como la implantación de un anillo en el
seno coronario que reduce el diámetro del anillo valvular, o el implante de clips que aproximan
los velos valvulares disminuyendo el grado de regurgitación (MitraClip). Esto se debe considerar
en pacientes severamente sintomáticos (a pesar del tratamiento médico óptimo) con IM severa
primaria que tienen una anatomía favorable, una esperanza de vida razonable y un riesgo
quirúrgico prohibitivo por comorbilidades.
II. VALVULOPATÍA AÓRTICA
A. ESTENOSIS AÓRTICA
1. INTRODUCCIÓN
La estenosis aórtica (EAo) causa una obstrucción del flujo de salida de la sangre desde el VI a la
aorta. Es la valvulopatía más prevalente en Europa.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [368]
[24] VALVULOPATÍAS
2. ETIOLOGÍA Y TIPOS
Según la localización de la obstrucción se clasifica en:
2.1. Estenosis aórtica valvular: por afectación de la propia válvula; es el tipo más frecuente.
Sus principales causas son:
Estenosis aórtica degenerativa: se produce por engrosamiento de los velos y depósito de calcio
en las líneas de unión. Es la forma de presentación más común, especialmente en ancianos (2-
7% de la población > 65 años).
Estenosis aórtica congénita: válvulas anormales (unicúspides o bicúspides) que producen
estenosis graves en edades tempranas, o que degeneran precozmente ocasionando síntomas
en la vida adulta. La válvula aórtica bicúspide es la causa más común de estenosis en < 50 años.
Estenosis aórtica reumática: actualmente es rara en países desarrollados. Se genera por fusión
de las comisuras, con un pequeño orificio central. Se suele asociar con insuficiencia aórtica y
afectación valvular mitral.
Otras causas más infrecuentes: enfermedad de Paget, artritis reumatoide, lupus eritematoso
sistémico, enfermedades de depósito (por ejemplo, enfermedad de Fabry), nefropatía terminal.
2.2. Estenosis aórtica subvalvular
Obstrucción del tracto de salida del VI por debajo de la válvula. Puede ser fija (membrana o rodete
fibromuscular) o dinámica, como ocurre en la miocardiopatía hipertrófica.
2.3. Estenosis aórtica supravalvular
Obstrucción en la aorta ascendente por encima de la válvula. Es muy infrecuente y suele
presentarse como rasgo del síndrome de Williams o por depósito de lípidos en la hipercolesterolemia
familiar.
3. FISIOPATOLOGÍA
El área normal de la válvula aórtica es 3-4 cm2. Su reducción, o cualquier estrechamiento a otro
nivel, dificulta el vaciado del VI y la eyección en la aorta, creando un gradiente de presión sistólico entre
ambas cámaras. Como respuesta a este aumento de la poscarga (sobrecarga de presión), el VI experimenta
hipertrofia concéntrica e incrementa la contractilidad para mantener el gasto cardiaco. Este mecanismo
compensador reduce la distensibilidad del VI y origina disfunción diastólica, que aumentará de forma
retrógrada la presión en el lecho pulmonar, produciendo congestión pulmonar y, en casos avanzados, fallo
derecho por HTP.
La entrada en FA puede ocasionar deterioro hemodinámico agudo por pérdida de la contribución
auricular al llenado del VI.
En fases tardías se produce una reducción de la función sistólica del VI y, como consecuencia, una
disminución del volumen de eyección y, por tanto, del gradiente ventrículo-aórtico (EAo de bajo gradiente).
4. CLÍNICA
El curso de la EAo se caracteriza por una fase inicial asintomática, que puede durar años.
Una vez aparecen los síntomas clásicos, generalmente cuando la EAo es severa, la supervivencia
media sin tratamiento se reduce notablemente (angina: 5 años, síncope: 3 años; disnea: 2 años).
4.1. Angina
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [369]
[24] VALVULOPATÍAS
Se debe a isquemia del miocardio hipertrofiado, que por un lado necesita mayores requerimientos
metabólicos, y por otro comprime y dificulta la perfusión de las arterias coronarias intramiocárdicas.
4.2. Síncope
Suele ser de esfuerzo. La obstrucción de salida del VI impide aumentar el gasto cardiaco con el
ejercicio. El mecanismo arritmogénico (bloqueos auriculoventriculares [AV] o taquiarritmias) debe
sospecharse ante síncopes de reposo. Aunque el riesgo de muerte súbita cardiaca en pacientes
asintomáticos es < 1%, se incrementa en la EAo severa sintomática, por hipotensión o arritmias secundarias
a isquemia, fibrosis o disfunción del VI.
4.3. Disnea
La disnea de esfuerzo se debe al aumento de la presión capilar pulmonar por disfunción sistólica
y/o diastólica del VI. Otros síntomas de insuficiencia cardiaca izquierda (disnea de reposo, paroxística
nocturna y ortopnea), insuficiencia cardiaca derecha o bajo gasto son más tardíos y de pronóstico ominoso.
En la exploración física, el pulso arterial es característicamente anácroto (parvus et tardus), de
escasa amplitud. Aunque puede ser normal en pacientes ancianos o hipertensos por pérdida de
distensibilidad arterial.
El impulso apical suele ser sostenido (hipertrofia VI) y no se desplaza. Puede ser doble debido a la
contracción auricular en presencia de fallo diastólico ventricular avanzado. Ocasionalmente se puede
palpar frémito en la base, el hueco supraesternal y las carótidas.
El signo auscultatorio más importante es un soplo sistólico rudo, de baja frecuencia y morfología
romboidal, que comienza poco después del primer ruido y cuya duración se correlaciona con la severidad.
Se localiza en el foco aórtico, y puede irradiarse al hueco supraesternal y a las carótidas, y más raramente al
borde esternal izquierdo y a la punta con una frecuencia alta (fenómeno de Gallavardin). El segundo ruido
suele estar disminuido por fibrocalcificación de los velos o incluso desdoblado paradójicamente por
duración prolongada de la eyección. Puede existir tercer ruido cuando el VI se dilata, y cuarto ruido cuando
se asocia a fallo diastólico avanzado, siempre y cuando se mantenga el ritmo sinusal.
5. DIAGNÓSTICO
5.1. Electrocardiograma
Suele mostrar crecimiento auricular y ventricular izquierdo, con alteraciones secundarias de la
repolarización.
5.2. Radiografía de tórax
La silueta cardiaca puede ser normal, adquirir forma de bota por hipertrofia o cardiomegalia en
fases avanzadas de dilatación del VI. Con frecuencia se observa calcificación valvular y de la raíz aórtica.
5.3. Ecocardiografía
Es el método de elección para establecer el diagnóstico, determinar la causa y valorar la gravedad,
así como la repercusión en el VI (grado de hipertrofia, tamaño y función).
Los hallazgos ecocardiográficos permiten clasificar la EAo según su gravedad:
Leve: área valvular > 1,5 cm2, gradiente medio < 30 mm Hg.
Moderada: área valvular de 1-1,5 cm2, gradiente medio 30-45 mm Hg.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [370]
[24] VALVULOPATÍAS
Severa: área valvular < 1 cm2 (área valvular indexada < 0,6 cm2/m2), velocidad pico > 4m/s,
gradiente medio > 45 mm Hg.
En casos de mala visualización, se puede optar por el ecocardiograma transesofágico
(bidimensional y tridimensional), que permite la medición directa del orificio valvular y la obtención de
gradientes.
La ecocardiografía con dobutamina puede ser útil para evaluar la EAo de bajo flujo/bajo gradiente,
en el contexto de disfunción sistólica del VI, en la que la reducción del área valvular < 1 cm2, con gradiente
medio transvalvular bajo (< 30 mm Hg), puede deberse a que el volumen latido está disminuido.
5.4. Ergometría
Está contraindicada en pacientes con EAo severa sintomática; sin embargo, se recomienda en
pacientes asintomáticos con EAo grave, físicamente activos, para desenmascarar síntomas y estratificar el
riesgo (caída de la tensión arterial [TA]).
5.5. Cateterismo cardiaco
Actualmente no se emplea en la valoración sistemática de la EAo, únicamente se reserva para
aquellos casos en los que existe discrepancia entre los datos clínicos y ecocardiográficos. Se realizará
coronariografía prequirúrgica cuando esté indicada (Tabla I).
6. TRATAMIENTO
El algoritmo terapéutico y de seguimiento se recoge en la figura 3.
6.1. Tratamiento médico
Los pacientes asintomáticos no precisan tratamiento específico, pero se recomienda evitar el
ejercicio extenuante o de competición en casos de EAo moderada-severa. El tratamiento médico no ha
demostrado evitar la progresión. Se limita a aliviar síntomas en los pacientes inoperables o que están
pendientes de intervención quirúrgica.
Deben evitarse vasodilatadores, siendo los IECA o los antagonistas de los receptores de la
angiotensina II (ARA-II) los fármacos de elección en casos de hipertensión arterial.
Si el paciente desarrolla insuficiencia cardiaca se deben emplear diuréticos a dosis bajas para evitar
la hipovolemia. En caso de edema agudo de pulmón, se recomienda usar furosemida y nitroprusiato
intravenoso bajo monitorización hemodinámica invasiva.
Se debe establecer una estrategia de control del ritmo si se presentan arritmias auriculares. En
fases avanzadas con disfunción del VI se puede emplear digoxina, evitando betabloqueantes y
calcioantagonistas. No se requiere prevención de la endocarditis bacteriana.
6.2. Tratamiento intervencionista
Técnicas (Figura 4)
El tratamiento de elección es el reemplazo valvular por una prótesis. La mortalidad
perioperatoria global ronda el 3%, aunque aumenta con la edad, la comorbilidad y la
complejidad de la cirugía. En los pacientes con enfermedad coronaria e indicación de
revascularización debe practicarse la derivación coronaria en el mismo acto quirúrgico.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [371]
[24] VALVULOPATÍAS
Figura 3. Algoritmo terapéutico y de seguimiento de la estenosis aórtica.
Figura 4. Técnica quirúrgica de estenosis aórtica.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [372]
[24] VALVULOPATÍAS
Se ha desarrollado recientemente el implante de prótesis aórticas transcatéter (TAVI) por vía
transarterial (femoral, aórtica, axilar, carotídea) y transapical sin necesidad de circulación extracorpórea,
para intentar mejorar el manejo en pacientes con alto riesgo quirúrgico.
En los niños con EAo congénita el tratamiento de elección es la valvuloplastia percutánea con
balón. En casos muy seleccionados existen otras opciones quirúrgicas como la comisurotomía o la
operación de Ross.
En los adultos, los resultados de la valvuloplastia percutánea son malos, con elevada tasa de
complicaciones (superior al 10%) y aparición habitual de reestenosis en 6-12 meses, por lo que se limita a
su uso como técnica paliativa en pacientes hemodinámicamente inestables, sin posibilidad de intervención
quirúrgica o como puente a la misma.
Indicaciones
Las indicaciones del recambio valvular aórtico se muestran en la tabla VI. En pacientes con
riesgo quirúrgico intermedio o bajo se recomienda la sustitución valvular quirúrgica frente a la
TAVI. Los pacientes con alto riesgo quirúrgico deben ser evaluados por un heart team. Se
recomienda TAVI en pacientes con indicación de recambio valvular con un riesgo quirúrgico
prohibitivo y esperanza de vida > 12 meses y es una alternativa en los pacientes de alto riesgo
quirúrgico.
Tabla VI. Indicaciones de recambio valvular aórtico en la estenosis aórtica.
B. INSUFICIENCIA AÓRTICA
1. INTRODUCCIÓN
La insuficiencia aórtica (IAo) consiste en una regurgitación de sangre desde la aorta al VI en
diástole. La forma aguda y crónica de la IAo son entidades cuyas causas, fisiopatología y presentación son
diferentes.
2. ETIOLOGÍA
Puede deberse a una afectación primaria de la válvula (déficit de coaptación, perforación o
prolapso de los velos) o secundaria a dilatación de la raíz aórtica o aorta ascendente (déficit de coaptación)
(Tabla VII).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [373]
[24] VALVULOPATÍAS
Tabla VII. Etiología de la insuficiencia aórtica.
3. FISIOPATOLOGÍA
La sangre que refluye durante la diástole desde la aorta hacia el VI provoca una disminución del
gasto cardiaco y una sobrecarga de volumen y presión en el VI.
3.1. Insuficiencia aórtica crónica
El principal mecanismo de compensación es la dilatación ventricular, que permite aumentar el
volumen de eyección gracias a una mayor precarga (mecanismo de Frank-Starling), pudiendo mantener el
gasto cardiaco hasta fases avanzadas, a expensas de un incremento de la presión intraventricular que
genera, a su vez, hipertrofia del VI.
3.2. Insuficiencia aórtica aguda
La instauración rápida impide la adaptación ventricular y produce una reducción súbita del gasto
cardiaco y una elevación de la presión diastólica del VI, que retrógradamente produce congestión
pulmonar.
4. CLÍNICA
4.1. Insuficiencia aórtica crónica
Suele ser asintomática durante décadas. Cuando aparece disfunción sistólica del VI, el paciente
desarrolla congestión pulmonar, que se expresa como disnea de esfuerzo que progresa hasta ser de
reposo, asociando ortopnea y disnea paroxística nocturna.
La angina, resultado de la isquemia (baja perfusión coronaria en un ventrículo hipertrófico y
dilatado), es rara, pero los pacientes suelen referir dolor torácico atípico por latido hiperdinámico.
En fases avanzadas pueden aparecer signos de bajo gasto como obnubilación, frialdad, oliguria e
hipoperfusión.
En la exploración física destaca un incremento de la presión diferencial del pulso debido al aumento
de la presión sistólica (alto volumen de eyección) y a la caída de la diastólica (regurgitación al VI).
Periféricamente se refleja con pulso magnus, celer et altus y en ocasiones bisferiens.
El impulso apical es hiperdinámico y se desplaza inferolateralmente debido a la dilatación del VI.
En la auscultación, el segundo ruido está disminuido. Aparece un soplo diastólico, agudo y
decreciente, más audible en el borde esternal superior izquierdo, en apnea postespiración con el paciente
inclinado hacia delante. La duración del soplo indica la gravedad de la IAo, más que la intensidad. Es posible
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [374]
[24] VALVULOPATÍAS
auscultar soplos funcionales: un soplo mesosistólico por hiperaflujo en la válvula aórtica o un segundo
soplo telediastólico en el ápex, por el choque del chorro regurgitante contra la válvula mitral, durante la
contracción auricular, que impide su apertura (soplo de Austin Flint).
4.2. Insuficiencia aórtica aguda
Suele presentarse con clínica súbita de bajo gasto (debilidad, obnubilación, mala perfusión, oliguria,
etc.) acompañada de edema agudo de pulmón.
Si se acompaña de dolor torácico intenso se debe sospechar disección aórtica.
Los signos de circulación hiperdinámica pueden estar ausentes y la presión diferencial es normal o
está ligeramente aumentada.
El soplo protodiastólico suele ser breve por equilibrio precoz de las presiones diastólicas de la aorta
y el VI.
5. DIAGNÓSTICO
5.1. Electrocardiograma
IAo crónica: suele mostrar crecimiento ventricular izquierdo, con alteración marcada de la
repolarización.
IAo aguda: presenta alteraciones de la repolarización inespecíficas.
5.2. Radiografía de tórax
IAo crónica: se evidencia cardiomegalia y desplazamiento inferolateral del ápex, e incluso dilatación
de la raíz aórtica.
IAo aguda: no existe cardiomegalia y destacan signos de congestión pulmonar.
5.3. Ecocardiografía
Es la técnica clave para determinar la causa, el mecanismo y la gravedad de la IAo, así como evaluar
la raíz aórtica y el VI (tamaño y función). Son criterios de severidad: relación jet/TSVI > 65%; inversión
holodiastólica de flujo en la aorta torácica descendente, vena contracta 0,6 cm y volumen regurgitante > 60
ml. La ecografía transesofágica puede ayudar a valorar la anatomía.
5.4. Resonancia magnética cardiaca
En caso de discordancia clínico- ecocardiográfica o visibilidad limitada, se debe recurrir a esta
técnica o, en su defecto, a la aortografía.
5.5. Ergometría
Se realizará esta prueba si existen dudas sobre la presencia de síntomas en los casos de IAo severa.
6. TRATAMIENTO
El algoritmo terapéutico y de seguimiento se muestra en la figura 5.
6.1. Tratamiento médico
El uso de vasodilatadores crónicos, como IECA o dihidropiridinas, para reducir el flujo retrógrado no
ha demostrado cambiar el pronóstico ni demorar la cirugía.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [375]
[24] VALVULOPATÍAS
Su empleo a corto plazo, incluso con inotrópicos y diuréticos, se recomienda en pacientes
pendientes de cirugía con disfunción del VI o con insuficiencia cardiaca severa para mejorar su situación
clínica antes de la intervención.
El tratamiento crónico se reserva para aquellos pacientes que no son candidatos a cirugía pero que
presentan síntomas o disfunción del VI y para pacientes asintomáticos con HTA o con disfunción del VI tras
la intervención.
Figura 5. Algoritmo terapéutico y de seguimiento de la insuficiencia aórtica.
No está indicada la prevención de endocarditis. Los pacientes con IAo severa asintomática pueden
realizar ejercicio, evitando el de tipo isométrico.
6.2. Tratamiento quirúrgico
Insuficiencia aórtica crónica
Los pacientes sintomáticos tienen una tasa de mortalidad anual superior al 10%. Los pacientes
asintomáticos tienen bajo riesgo de desarrollar muerte súbita. Si existe indicación de cirugía por
dilatación de aorta ascendente (mayor de 5,5 cm; mayor de 5 cm con factor de riesgo de
disección, síndrome de Marfan o aumento mayor de 0,3-0,5 cm/año) está indicada la cirugía
valvular en el mismo acto a pesar de ser asintomática. Las indicaciones de la cirugía valvular
aórtica se muestran en la tabla VIII.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [376]
[24] VALVULOPATÍAS
Tabla VIII. Indicaciones de cirugía en la insuficiencia aórtica.
El procedimiento quirúrgico suele ser el recambio valvular por una prótesis, aunque en ocasiones se
puede realizar cirugía reparadora.
Insuficiencia aórtica aguda
En el caso de la IAo aguda severa, está indicado el tratamiento quirúrgico urgente.
III. VALVULOPATÍA TRICUSPÍDEA
A. ESTENOSIS TRICUSPÍDEA
Se trata de una obstrucción al flujo de llenado del VD. Es una valvulopatía poco habitual, cuya
principal etiología es reumática, asociándose frecuentemente a valvulopatías izquierdas. Otras causas
menos frecuentes son las anomalías congénitas, el síndrome carcinoide, las enfermedades de Fabry y de
Whipple y la terapia con metisergida.
Clínicamente suelen predominar los signos y síntomas de las valvulopatías asociadas, siendo la
clínica de insuficiencia cardiaca derecha la principal manifestación de la estenosis tricuspídea (ET), y la
astenia y la fatigabilidad asociadas al bajo gasto cardiaco prácticamente constantes. Existe una discrepancia
entre el grado de disnea y la magnitud del fallo derecho.
En la exploración física son características una onda a gigante, siempre que el paciente se
encuentre en ritmo sinusal, y la ralentización del seno y en el pulso yugular. Frecuentemente pueden estar
presentes signos asociados a insuficiencia cardiaca derecha, como la hepatoesplenomegalia por congestión.
En la auscultación podemos objetivar un chasquido de apertura y un soplo diastólico localizado en el foco
tricuspídeo, que aumenta con la inspiración al aumentar la precarga en las cavidades derechas (signo de
Rivero-Carvallo).
El electrocardiograma muestra signos de crecimiento de la aurícula derecha (AD) en forma de “P
pulmonar’’. En la radiografía de tórax se aprecia dilatación de la AD y de la vena cava superior. El
ecocardiograma valora el grado de afectación valvular y su severidad, además es útil para valorar la
presencia de otras valvulopatías asociadas.
El tratamiento médico se limita a adoptar las medidas que disminuyan la congestión: restricción de
aportes de sodio en la dieta y tratamiento diurético si es preciso. No obstante, el tratamiento definitivo es
la cirugía.
Generalmente, es preferible la comisurotomía abierta. Sin embargo, en ocasiones es necesario
implantar una prótesis valvular, preferiblemente biológica, pues las metálicas tienen altas tasas de
trombosis debido a las bajas presiones del sistema venoso. Otra actuación puede ser la valvuloplastia
percutánea con balón, aunque los resultados a corto plazo no son buenos, generando una IT importante.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [377]
[24] VALVULOPATÍAS
B. INSUFICIENCIA TRICUSPÍDEA
Supone un reflujo de sangre desde el VD a la AD. En la mayoría de los casos se produce como
consecuencia de una dilatación del VD y, por consiguiente, del anillo valvular (como ocurre en cardiopatías
izquierdas, cor pulmonale o hipertensión arterial pulmonar), pero también puede haber una afectación
primaria de la válvula, como en la endocarditis (sobre todo en adictos a drogas por vía parenteral [ADVP]),
siendo otras causas menos habituales la fiebre reumática, la enfermedad de Epstein, el síndrome
carcinoide, el infarto de los músculos papilares de la válvula tricuspídea, los electrocatéteres ventriculares o
fármacos como la fenfluramina.
El reflujo de sangre a la AD supone una disminución del gasto cardiaco, así como una congestión
venosa a nivel sistémico. En la exploración se objetiva distensión de las venas yugulares con una onda v
muy prominente y un seno y profundo (onda de fusión “cv” con abolición del seno x, signo de Lancisi),
reflujo hepatoyugular, hepatomegalia pulsátil, ascitis y edemas (signos derivados de la congestión de origen
derecho). En el borde esternal izquierdo se ausculta un soplo holosistólico que aumenta con la inspiración
(signo de Rivero-Carvallo) y disminuye con la espiración y la maniobra de Valsalva.
El ECG muestra signos electrocardiográficos de crecimiento de las cavidades derechas. En la
radiografía de tórax se observa cardiomegalia como resultado de la dilatación de la AD y el VD por la
sobrecarga de volumen. El ecocardiograma proporciona información sobre la etiología, las posibilidades de
reparación y el grado de repercusión sobre las cavidades derechas. Ante dudas diagnósticas puede ser de
utilidad realizar un ecocardiograma transesofágico, una ecocardiografía tridimensional, una resonancia
magnética o una prueba de esfuerzo en pacientes con insuficiencia tricuspídea severa y mínimos síntomas.
En cuanto al tratamiento médico, este es sintomático para controlar los signos y síntomas
congestivos con restricción salina y diuréticos. Por otro lado, en los casos en los que la IT sea secundaria a
una dilatación del VD, se instaurará un tratamiento de la causa subyacente: si es la hipertensión arterial
pulmonar (grupo 1 de la clasificación Niza), se debe tratar la enfermedad de base con vasodilatadores
pulmonares; en los casos en que la dilatación sea secundaria a una valvulopatía izquierda que requiera
tratamiento quirúrgico, es conveniente reparar la válvula tricuspídea en el mismo acto, si hay dilatación del
anillo (> 40 mm) o evidencia de fallo derecho. Si la IT aislada es severa y sintomática y no responde a
tratamiento óptimo, también está indicada la cirugía. Es preferible, en la mayoría de los casos, la
anuloplastia o la inserción de un anillo protésico. Sin embargo, cuando la IT se debe a un trastorno
intrínseco de la válvula con pérdida de tejido, la sustitución por una prótesis valvular, preferiblemente
biológica, es la técnica de elección. La reoperación para cirugía tricuspídea aislada en la IT severa
sintomática está indicada en pacientes con cirugía previa del lado izquierdo que no tienen HTP severa o
disfunción ventricular derecha significativa.
IV. VALVULOPATÍA PULMONAR
A. ESTENOSIS PULMONAR
Genera una obstrucción del flujo de salida de la sangre desde el VD a la arteria pulmonar,
creándose un gradiente sistólico entre ambas cámaras. El aumento crónico de la poscarga sobre el VD
provoca una hipertrofia compensadora y disminución de su distensibilidad. La etiología más frecuente es
congénita. Cuando es severa produce síntomas de bajo gasto, síncope de esfuerzo, angina e insuficiencia
cardiaca derecha. En la auscultación aparece un chasquido de apertura y un soplo sistólico rudo en el foco
pulmonar que aumenta con la inspiración. El electrocardiograma y la radiografía muestran signos de
crecimiento del VD. La ecocardiografía permite valorar la anatomía y cuantificar la gravedad, así como la
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [378]
[24] VALVULOPATÍAS
función del VD. El tratamiento de elección es la valvuloplastia pulmonar percutánea o el recambio valvular
protésico ante la presencia de síntomas, o si se objetiva severidad.
B. INSUFICIENCIA PULMONAR
Ocasionada por déficit de coaptación de las válvulas pulmonares con regurgitación de sangre desde
la AP al VD en diástole. La causa más común es la dilatación del anillo valvular por HTP, si bien la tetralogía
de Fallot operada representa un grupo etiológico cada vez más numeroso. La sobrecarga crónica de
volumen produce dilatación del VD, que termina por claudicar, generando síntomas de insuficiencia
cardiaca derecha.
A la exploración física se ausculta un soplo diastólico en el foco pulmonar que aumenta con la
inspiración (soplo de Graham-Steele). En el electrocardiograma aparecen signos de sobrecarga del VD y en
la radiografía dilatación de las cavidades derechas. Las técnicas diagnósticas de elección son el
ecocardiograma y la resonancia magnética cardiaca. Esta última permite cuantificar de una manera más
precisa la severidad de la insuficiencia y el grado de dilatación y disfunción del VD.
En los casos ocasionados por aneurisma de la raíz de la AP, el tratamiento es etiológico y está
dirigido a controlar la HTP y la enfermedad de base. Requieren sustitución valvular quirúrgica o percutánea
los pacientes con insuficiencia pulmonar orgánica severa con signos o síntomas de disfunción ventricular
derecha.
Los diuréticos pueden mejorar la congestión sistémica.
V. PRÓTESIS VALVULARES
1. CLASIFICACIÓN
Se dividen, según su composición, en mecánicas y biológicas.
1. MECÁNICAS
El primer modelo de bola enjaulada ha sido reemplazado por las prótesis de disco basculante,
fabricadas con carbón pirolítico, que pueden ser monodisco o bidisco, siendo estas últimas las más
utilizadas por su mejor perfil hemodinámico.
2. BIOLÓGICAS
Tienen un perfil hemodinámico similar a las válvulas nativas, mejor que las mecánicas.
Autoinjerto: válvula del propio individuo (como la válvula pulmonar que sustituye a la aórtica
en la técnica de Ross), con mínima trombogénesis y excelente durabilidad. Existen datos que
sugieren que el autoinjerto puede incluso crecer con el niño.
Homoinjerto: válvula criopreservada de donante cadáver. Si bien su disponibilidad es limitada,
ofrece menor riesgo de trombogénesis y endocarditis. Son de elección en la endocarditis
valvular, especialmente a nivel aórtico con lesiones perivalvulares o sobre una prótesis.
Heteroinjerto: válvulas de otras especies (porcinas o de pericardio bovino o equino). Son las
más utilizadas. Suelen sustentarse sobre un armazón de diversos materiales. Dentro de este
grupo se incluyen las prótesis transcatéter, que están fabricadas con pericardio y van montadas
sobre un stent autoexpansible o que se libera mediante inflado de un balón.
2. ELECCIÓN DEL TIPO DE PRÓTESIS
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [379]
[24] VALVULOPATÍAS
La principal ventaja de las válvulas biológicas sobre las mecánicas es su tasa reducida de
tromboembolia sin necesidad de anticoagulación oral de por vida, salvo cuando se asocia con FA,
enfermedad tromboembólica o hipercoagulabilidad. Aunque con frecuencia se recomienda, no hay
evidencia de que la antiagregación crónica sea beneficiosa si no existe otra indicación para emplearla. Sin
embargo, presentan el inconveniente de su duración limitada. Algunas situaciones favorecen la
degradación de la bioprótesis, como la edad inferior a 40 años, la hipercolesterolemia, la insuficiencia renal
crónica sobre todo en los pacientes en hemodiálisis o el hiperparatiroidismo.
La durabilidad en la práctica de las prótesis mecánicas es ilimitada, pero su mayor riesgo
tromboembólico obliga a mantener una anticoagulación permanente. En general, el valor de INR objetivo
en pacientes con prótesis mecánicas oscila entre 2 y 3,5. En nuestro hospital se mantiene entre 2,5-3,5 los
tres primeros meses en todas las prótesis mecánicas, bajando posteriormente a 2-3 las aórticas aisladas.
Por todo ello, existen datos que favorecen el empleo de uno u otro tipo de prótesis (Tabla IX),
aunque en cualquier caso la decisión del tipo de válvula debe ser un proceso compartido con el paciente e
individualizado. Entre 60 y 70 años cualquiera de las dos es razonable.
Las mujeres jóvenes con deseo genésico y que precisen una prótesis plantean una situación
compleja y hay que individualizar la decisión en cada caso. Por su situación de hipercoagulabilidad,
presentan mayor riesgo de trombosis protésica. Por otra parte, la anticoagulación con dicumarínicos
implica mayor riesgo de hemorragia fetal y embriofetopatía. Además, el deterioro de la prótesis biológica
es elevado en este grupo de edad. Suele preferirse la prótesis biológica o diferir la cirugía hasta después del
parto. A una mujer portadora de prótesis mecánica se le debe recomendar evitar el embarazo.
Tabla IX. Recomendaciones para la elección de prótesis valvular.
3. ANTICOAGULACIÓN EN SITUACIONES ESPECIALES
1. EMBARAZO EN MUJER PORTADORA DE PRÓTESIS MECÁNICA
Durante el primer trimestre se debe sopesar el riesgo fetal y materno para elegir entre antagonistas
de la vitamina K, heparina no fraccionada (HNF) y heparina de bajo peso molecular (HBPM). Si la paciente
rechaza la anticoagulación oral (ACO) durante el primer trimestre se recomienda HNF. No hay datos
definitivos sobre la HBPM en el embarazo. Durante el segundo y el tercer trimestres se recomienda ACO
hasta la semana 35 (INR 2-3), sustituyéndose por heparina sódica intravenosa en la semana 36. Si no hay
sangrado importante, se reinicia la heparina 6 horas tras el parto y la ACO.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [380]
[24] VALVULOPATÍAS
2. PREVIAMENTE A INTERVENCIONISMO
Si el paciente se va a someter a una intervención se recomienda, si es posible, no interrumpir la
ACO y mantener la INR en el rango inferior terapéutico (en torno a 2), lo que permite realizar la mayoría de
las intervenciones quirúrgicas menores con eventuales hemorragias de bajo riesgo. Si el peligro de
sangrado es elevado (cirugía mayor), debe interrumpirse la ACO, sustituirse por heparina sódica (tiempo de
tromboplastina parcial activado [TTPA] objetivo 1,5-2 veces el límite superior normal), que se mantiene
hasta 6 horas antes del procedimiento y se reanuda entre las 6 y 12 horas tras el mismo, junto con la ACO,
en la mayoría de los casos, manteniéndose hasta alcanzar la INR deseada. La HBPM a dosis altas puede ser
una alternativa en casos seleccionados.
3. ANTICOAGULACIÓN EXCESIVA
(Ver Capítulo 77. “Trastornos de la hemostasia. Anticoagulación”).
4. FISIOPATOLOGÍA
Las prótesis mecánicas producen un clic de apertura y cierre sin significado patológico. Suelen ser
levemente restrictivas, generando un soplo audible cuando están abiertas y un gradiente transvalvular que
debe ser evaluado tras cirugía y tomado como referencia para detectar futuras complicaciones. Presentan
insuficiencia fisiológica leve, que permite el lavado de los discos y dificultan la formación de trombos y
pannus.
En el caso de las biológicas, los ruidos cardiacos no están aumentados y no se ausculta soplo.
Suelen tener regurgitación leve central, que es transitoria y se corrige a los pocos días de la cirugía, cuando
los velos se adaptan a la nueva disposición.
La aparición de un nuevo soplo, la amortiguación de los ruidos o la presencia de fenómenos
embólicos sirve para identificar complicaciones.
5. COMPLICACIONES
1. ENDOCARDITIS PROTÉSICA
La endocarditis sobre prótesis valvulares ocurre en el 0,5-1% por paciente/año, constituye el 20%
de todas las endocarditis y tiene mal pronóstico, con una mortalidad en torno al 30%.
Hay que distinguir entre endocarditis protésica precoz (generalmente por microorganismos
adquiridos perioperatoriamente) y tardía (por microorganismos adquiridos de forma secundaria a
bacteriemias, casi un tercio en relación con maniobras instrumentales sanitarias).
Aunque no existe unanimidad en el límite temporal entre endocarditis protésica precoz o tardía, en
la actualidad se establece en el año desde la intervención.
Los microorganismos más frecuentes en la precoz (hasta el 50%) son los estafilococos
(Staphylococcus epidermidis es más frecuente que Staphylococcus aureus), seguidos de hongos y bacilos
gramnegativos. En la tardía son los estreptococos y enterococos. La infección de prótesis mecánicas suele
afectar al anillo y con frecuencia produce la dehiscencia de la prótesis con insuficiencia asociada.
Muy a menudo el diagnóstico es complejo, y está indicado un ecocardiograma transesofágico
siempre que se sospeche endocarditis protésica.
Las indicaciones de cirugía en la endocarditis protésica son similares a las de la endocarditis sobre
válvula nativa, con la peculiaridad de que los casos de endocarditis protésica precoz suelen estar
producidos por microorganismos agresivos y resistentes, por lo que está indicada la cirugía. La intervención
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [381]
[24] VALVULOPATÍAS
incluye la exéresis de todo el material protésico y la colocación de una nueva prótesis, generalmente de
tipo biológico. La endocarditis tardía no estafilocócica sin compromiso hemodinámico puede tratarse de
forma conservadora con seguimiento estrecho.
Para más información, se remite al lector al Capítulo 37. “Endocarditis infecciosa”.
2. TROMBOSIS PROTÉSICA
La trombosis protésica se debe sospechar ante la desaparición o disminución de los ruidos de cierre
de una válvula mecánica, la aparición de un evento embólico o el desarrollo de disnea. El diagnóstico suele
ser ecocardiográfico (generalmente transesofágico), aunque con radioscopia directa también se puede
visualizar el movimiento de los discos. En general, la causa más frecuente es una anticoagulación
inadecuada.
Si existe inestabilidad clínica, el tratamiento es la cirugía inmediata de reemplazo valvular.
Si esta no estuviese disponible, o el riesgo quirúrgico fuese muy alto, la alternativa es la fibrinólisis.
En las prótesis derechas la eficacia de la fibrinólisis es mayor con menor riesgo, por lo que suele preferirse
inicialmente. Si es eficaz, debe seguirse de HNF hasta que la INR sea la deseada. Para trombosis no
oclusivas que ya han producido una embolia, si el riesgo quirúrgico no es excesivo y el trombo es grande
(superior a 10 mm), se recomienda la cirugía y, si es pequeño, puede optimizarse el tratamiento
anticoagulante y seguir estrechamente su evolución hasta su resolución, pero si no se produce, estaría
indicada la intervención. Si aún no se han producido embolias, se intensifica el tratamiento anticoagulante
y únicamente se indica la cirugía ante la persistencia de un trombo grande en pacientes sin alto riesgo
quirúrgico.
3. EMBOLIA
Las prótesis mecánicas, particularmente en posición mitral, son muy embolígenas. El primer mes
tras la intervención es el periodo de mayor riesgo, por lo que se suele iniciar la anticoagulación
precozmente con heparina sódica como puente hasta conseguir niveles de INR apropiados con ACO. A
pesar de pautar un tratamiento anticoagulante correcto, en las prótesis mecánicas la incidencia embólica
anual es del 2-3% en posición mitral y del 1-2% en posición aórtica. Ante la presencia de episodios
embólicos con niveles correctos de anticoagulación, una vez descartada la trombosis protésica, se
recomienda agregar ácido acetilsalicílico (AAS) en dosis bajas (100 mg al día) al tratamiento anticoagulante,
que debe mantenerse en el rango alto del objetivo. También se indica agregar AAS en caso de enfermedad
coronaria inestable (ver Capítulo 23. “Cardiopatía isquémica”).
4. ANEMIA HEMOLÍTICA
Se produce por el choque continuado de hematíes contra la prótesis, y es más acusada con las
mecánicas. No suele tener importancia y no precisa tratamiento. Cuando la hemólisis es clínicamente
importante hay que descartar dehiscencia periprotésica.
5. DISFUNCIÓN PROTÉSICA
La disfunción protésica puede ser consecuencia de diversos procesos, como fallo estructural,
dehiscencia valvular y formación de trombos o pannus.
En fases precoces, sobre todo durante el primer año tras la intervención, se produce por defectos
en la técnica operatoria (dehiscencia de las suturas, fístulas, etc.). En las prótesis biológicas, la causa más
frecuente de disfunción a largo plazo es la degeneración espontánea con perforación o calcificación,
produciéndose regurgitación (suele ser lo predominante), estenosis o ambas cosas. Casi siempre la
instauración es gradual, lo que permite su detección con ecografía antes de que el cuadro clínico sea grave.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [382]
[24] VALVULOPATÍAS
Se recomienda la reintervención ante la presencia de disfunción protésica significativa, sintomática o
asintomática, si la disfunción es grave y existe bajo riesgo para la operación.
6. REGURGITACIÓN O LEAK PARAVALVULAR
Produce soplos de insuficiencia valvular e insuficiencia cardiaca en grado variable. Las causas más
frecuentes son la dehiscencia de suturas y la endocarditis. Suele acompañarse de hemólisis. El tratamiento
médico es el de la insuficiencia cardiaca. La cirugía es el tratamiento definitivo, aunque en caso de
inoperabilidad la opción es el cierre percutáneo. Si la repercusión hemodinámica es ligera puede demorarse
la cirugía, instaurando tratamiento médico y vigilancia clínica y ecocardiográfica estrecha.
6. SEGUIMIENTO
La primera evaluación tras la cirugía se realiza aproximadamente a las 6-12 semanas de la cirugía y
debe incluir historia clínica, exploración física, radiografía de tórax, electrocardiograma y ecocardiograma.
Si el paciente se mantiene asintomático, las revisiones se efectuarán anualmente, realizándose
ecocardiografías en caso de que haya sospecha clínica de complicaciones o disfunción ventricular.
BIBLIOGRAFÍA
Joint Task Force on the Management of Valvular Heart Disease of the European Society of Cardiology
(ESC)1; European Association for Cardio-Thoracic Surgery (EACTS), Vahanian A, Alfieri O, Andreotti F,
Antunes MJ, et al. Guidelines on the management of valvular heart disease (version 2012). Eur Heart J.
2012;33(19): 2451-96.
Nishimura RA, Otto CM, Bonow RO, Carabello BA, Erwin JP 3rd, Guyton RA, et al. 2014 AHA/ACC
guideline for the management of patients with valvular heart disease: a report of the American College
of Cardiology/ American Heart Association Task Force on Practice Guidelines. J Am Coll Cardiol.
2014;63(22):e57-185.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [383]
[25] ENFERMEDADES DEL PERICARDIO
25.Enfermedades del pericardio
Guillermo Alonso Déniz.
Cardiología
Mª del Pilar Hernández Jiménez.
Medicina Interna
Asesor: Carmen Jiménez López-Guarch. Médica Adjunta del Servicio de Cardiología. Unidad de Imagen Cardiaca
I. INTRODUCCIÓN
Se describirán en el presente capítulo las principales entidades que afectan al pericardio, las bases
de su aproximación diagnóstica y el manejo terapéutico. Se distinguen principalmente cuatro síndromes de
afectación pericárdica, que ocurren más frecuentemente en población de edad entre 16 y 65 años, y
varones. La tasa de recurrencia tras un primer episodio es hasta del 30% en los primeros 18 meses. Las
etiologías son variadas, y se distinguen principalmente las infecciosas y las no infecciosas, con un
solapamiento entre las distintas entidades sindrómicas.
1. SÍNDROMES PERICÁRDICOS
Pericarditis aguda (PA). Variantes: incesante, recurrente, crónica.
Miopericarditis y perimiocarditis.
Derrame pericárdico.
Taponamiento cardiaco.
Pericarditis constrictiva.
II. PERICARDITIS AGUDA
Figura 1. Evolución del electrocardiograma en la pericarditis aguda.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [384]
[25] ENFERMEDADES DEL PERICARDIO
Se trata de un proceso inflamatorio del pericardio debido a múltiples etiologías, y constituye hasta
el 5% de las consultas por dolor torácico en Urgencias.
Criterios diagnósticos (al menos dos de cuatro):
Dolor torácico de características pericárdicas (> 85-90%): agudo, a punta de dedo, aumenta con
la tos y la inspiración profunda, mejora con la anteroflexión del tórax (paciente sentado e
inclinado hacia delante).
Auscultación de roce pericárdico (< 30%): áspero, “roce de cuero’’, borde esternal izquierdo.
Alteraciones en el electrocardiograma (ECG) con elevación del segmento ST o descenso del
espacio PR de manera difusa (> 60%) (Figura 1).
Empeoramiento o aparición de derrame pericárdico (> 60%, en general, leve).
Otros datos que apoyan el diagnóstico son la elevación de reactantes de fase aguda (proteína C
reactiva [PCR], velocidad de sedimentación globular [VSG], leucocitosis) y la existencia de hallazgos
inflamatorios en la tomografía computarizada/resonancia magnética nuclear (TC/RMN) cardiaca.
Se pueden encontrar síntomas acompañantes en relación con patología sistémica de base y
aumento de la creatín-cinasa (CPK) y las troponinas en caso de miopericarditis. La radiografía de tórax en
general es normal, y se observa aumento de la silueta cardiaca cuando existe derrame acompañante de
más de 300 ml.
Ante la sospecha de PA, se debe realizar a todos los pacientes: radiografía de tórax + ECG + perfil
cardiaco + ecocardiografía transtorácica (ETT). Tras el diagnóstico, solo precisarán estudio etiológico
aquellos que presenten al menos un factor de riesgo de mal pronóstico (mayor o menor) o se sospeche
enfermedad específica subyacente. La mayoría de los casos son idiopáticos o secundarios a infección vírica,
por lo que no precisan estudio, y se debe instaurar tratamiento y establecer un control evolutivo a los 7
días de forma ambulatoria.
Factores de riesgo mayores: fiebre de más de 38 ºC, curso subagudo, derrame pericárdico por
ETT > 2 cm, taponamiento cardiaco, ausencia de control de síntomas tras tratamiento con
antiinflamatorios no esteroideos (AINE) durante 7 días.
Factores de riesgo menores: miopericarditis, inmunodepresión, traumáticos, anticoagulación.
Sospecha de etiología neoplásica, autoinflamatoria sistémica, bacteriana o tuberculosis.
En estos casos, se procederá al ingreso hospitalario y estudio dirigido en función de la sospecha
(Tabla I).
1. PRINCIPALES ENTIDADES DE AFECTACIÓN PERICÁRDICA
Se describen a continuación de manera breve algunas particularidades de las principales entidades
de afectación pericárdica, que podrían presentarse tanto como PA aislada como con derrame pericárdico o
sin él:
1.1. Pericarditis aguda vírica
Es la causa más frecuente actualmente y, en general, no precisa estudio etiológico. Se suele
acompañar de un cuadro catarral previo o concomitante. Puede ser de utilidad la serología para virus de la
inmunodeficiencia humana (VIH) y de la hepatitis C en función de la sospecha. Para el resto de virus se
prefiere, por su rentabilidad, la determinación de PCR en líquido pericárdico. En el paciente
inmunodeprimido se debe sospechar infección por citomegalovirus o VIH. No se recomienda el tratamiento
con corticoides.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [385]
[25] ENFERMEDADES DEL PERICARDIO
Tabla I. Principales causas de pericarditis aguda y derrame pericárdico, aproximación diagnósticoterapéutica.
1.2. Pericarditis aguda bacteriana
Es indicación de pericardiocentesis diagnóstica (aumento de leucocitos de predominio
polimorfonuclear y glucosa baja) y terapéutica asociada a antibioterapia parenteral tras la recogida de
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [386]
[25] ENFERMEDADES DEL PERICARDIO
hemocultivos y serologías específicas (Coxiella burnetii y Borrelia spp si hay sospecha). En el paciente
inmunodeprimido y en el contexto de cirugía cardiaca se recomienda cobertura para Staphylococcus aureus
y hongos.
1.3. Pericarditis aguda tuberculosa
Es la primera causa en países en vías de desarrollo, pero supone menos del 4% en nuestro medio.
El comportamiento clínico simula a la insuficiencia cardiaca congestiva (ICC). Se recomienda el
estudio inicial con la prueba cutánea de la tuberculina IGRA/Mantoux, cultivo de esputo y TC torácica, y en
líquido pericárdico (predominio mononuclear, menos descenso de glucosa): bacterias ácido-alcohol
resistentes (BAAR) y cultivo, PCR, adenosina-desaminasa (ADA) (> 40 UI/l) e interferón-gamma. Valorar la
realización de una biopsia pericárdica en zonas no endémicas en aquellos derrames que no se resuelven
tras 3 semanas de tratamiento y con estudio negativo para otras causas. Evitar el tratamiento empírico en
regiones no endémicas.
1.4. Pericarditis aguda en insuficiencia renal
Distinguir entre PA urémica, PA dialítica (más allá de la 8ª semana de inicio, previamente 2-21%) y
PA constrictiva. Alta incidencia de PA hemorrágica. Está contraindicado el uso de colchicina.
1.5. Pericarditis aguda en procesos autoinmunes-sistémicos
Su presentación es asintomática o sintomática, se correlaciona con la actividad de la enfermedad
de base. Es más frecuente en el lupus eritematoso sistémico (LES), síndrome de Sjögren, artritis reumatoide
(AR) y esclerodermia, posible en vasculitis, síndrome de Behçet, sarcoidosis y enfermedad intestinal
inflamatoria (EII). Otras causas: fiebres periódicas (aumento de la interleucina-1).
1.6. Síndromes tras lesión cardiaca
Postinfarto agudo de miocardio, pospericardiotomía, postraumático. Mecanismo
predominantemente inmunomediado. Es de difícil diagnóstico por la coexistencia de derrame pleural y
pericárdico asociado a los propios procedimientos, por lo que los criterios diagnósticos difieren
discretamente de los descritos. En posquirúrgicos: tratamiento solo en caso de síntomas.
Pericarditis aguda de etiología neoplásica o sus tratamientos (radioterapia): es importante
por sus implicaciones pronósticas y en la elección del tratamiento, lo que justifica la realización
de pruebas de imagen (TC, cardio-RMN y/o tomografía por emisión de positrones (PET), análisis
del líquido pericárdico con citología y/o biopsia. Dos tercios de los derrames pericárdicos en
pacientes con neoplasia subyacente conocida no son de etiología neoplásica (complicación
infecciosa, tratamiento antineoplásico, etc.).
Los tumores primarios (mesoteliomas) son muy raros y de mal pronóstico. El origen del derrame
pericárdico neoplásico suele ser secundario a cáncer de pulmón, mama, melanoma, linfoma o leucemia. El
estudio de marcadores tumorales en el líquido es controvertido, dada su baja sensibilidad y especificidad, si
bien son útiles para el diagnóstico y, en el caso de los adenocarcinomas, el tratamiento (receptor del factor
de crecimiento epidérmico [EGFR] como diana terapéutica). El tratamiento será el de la causa y se puede
asociar quimioterapia intrapericárdica o radioterapia. Deberán considerarse técnicas quirúrgicas de
descompresión (ventana pericárdica) como medida preventiva en casos de recurrencia y/o control
sintomático/ paliativo.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [387]
[25] ENFERMEDADES DEL PERICARDIO
La radioterapia torácica (linfomas, carcinoma de mama/pulmón) puede producir PA de manera
dosis dependiente hasta en el 20% en los dos primeros años, con posible latencia a 15-20 años
postratamiento. Es de características serohemáticas, con alto riesgo de adherencias.
1.8. Pericarditis aguda en el paciente anciano
La evidencia existente en lo que respecta al paciente anciano con comorbilidad se encuentra
limitada a recomendaciones de expertos. Prestar especial atención a las dosis de medicamentos y los
efectos adversos asociados.
2. TRATAMIENTO
Las bases generales del tratamiento (Tabla II) son:
Reposo relativo, hasta la resolución sintomática y normalización de los datos inflamatorios en
no atletas, con un mínimo de 3 meses en los atletas.
AINE de primera elección, con dosis descendente en la retirada.
Colchicina: se recomienda su asociación desde el primer episodio, ya que disminuye las
recurrencias, incrementa la respuesta al tratamiento y, por tanto, la tasa de remisión.
Los corticoides solo se recomiendan en segunda instancia (si bien presentan efecto más rápido,
se asocian a pericarditis recurrente), a dosis de 0,5 mg/kg/día, con pauta descendente.
El seguimiento se realizará basándose en la clínica y la monitorización de reactantes de fase aguda.
Tabla II. Principales líneas de tratamiento.
3. CLASIFICACIÓN SEGÚN EL CURSO CLÍNICO
3.1. Pericarditis incesante: persistencia de síntomas tras PA durante más de 4-6 semanas con
tratamiento adecuado.
3.2. Pericarditis crónica: persistencia sintomática durante más de 3 meses.
3.3. Pericarditis recurrente: tras la resolución del primer episodio de PA (asintomático durante más
de 4-6 semanas), reaparición de síntomas según los criterios descritos para PA. No se asocia a peor
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [388]
[25] ENFERMEDADES DEL PERICARDIO
pronóstico ni a mayor riesgo de pericarditis constrictiva per se. Se recomienda realizar un estudio etiológico
para el ajuste del tratamiento en función de la causa, e instaurar inicialmente un nuevo tratamiento
estándar durante un mínimo de 6 meses. En caso de ausencia de respuesta, valorar la triple terapia
asociando corticoides (siempre en tuberculosis); además, existen fármacos de tercera línea como los
inmunomoduladores: azatioprina, inmunoglobulina intravenosa, anakinra (antiinterleucina-1). La
pericardiectomía se reserva para casos refractarios al tratamiento médico.
3.4. Miopericarditis: PA que asocia un aumento de marcadores de daño miocárdico, sin
alteraciones de la contractilidad en la ETT/RMN cardiaca.
3.5. Perimiocarditis: PA asociada al aumento de marcadores de daño miocárdico y alteraciones de
la contractilidad (focales o difusas) por ETT/cardio-RMN. Se recomienda en este caso descartar enfermedad
coronaria mediante la realización de una coronariografía, así como una cardio-RMN confirmatoria. Estos
pacientes deberán ingresar en planta con monitorización cardiaca. El tratamiento difiere del clásico de la
PA en: la falta de datos suficientes que apoyen el tratamiento con colchicina, la preferencia de uso de AINE
a dosis menores de las utilizadas en la PA, y la recomendación de reposo relativo de todos los pacientes un
mínimo de 6 meses.
III. DERRAME PERICÁRDICO
Se debe a la acumulación patológica de líquido entre las dos membranas del pericardio. Puede
deberse a inflamación del pericardio (exudado), aumento de la presión venosa sistémica (trasudado),
extravasación de sangre (hemopericardio) o gas (neumopericardio). Se distingue entre agudo, subagudo o
crónico (> 3 meses); leve (< 1 cm), moderado (1-2 cm), grave (> 2 cm) y circunferencial o loculado. Es de
suma importancia la valoración de la repercusión hemodinámica del mismo (ninguna, taponamiento,
derrame efusivo-constrictivo).
Respecto a la etiología, en países desarrollados en más del 50% es idiopática, seguida de infecciosa
(15-30%), neoplásica (10-25%), yatrogénica (15-20%) y secundaria a conectivopatía (5-15%). En países en
vías de desarrollo, en más del 60% de los casos la etiología es tuberculosa (Tabla I).
La presentación clínica depende principalmente de la velocidad de instauración, y con ello de la
capacidad de adaptación de las presiones intracardiacas. Se sospecha derrame pericárdico ante la aparición
de disnea de esfuerzo progresiva, ortopnea, dolor torácico y/o sensación de plenitud. Puede asociar
síntomas secundarios a compresión local (náuseas, disfagia, ronquera, hipo), a la enfermedad subyacente y
otros inespecíficos. La exploración física en los casos sin repercusión hemodinámica suele ser normal, y
sugieren taponamiento cardiaco el aumento de la presión venosa yugular, la disminución de los ruidos
cardiacos, el pulso paradójico y, en las pruebas complementarias, la alternancia eléctrica en el ECG (ver
Apartado IV. “Taponamiento cardiaco”).
El diagnóstico se lleva a cabo por ETT, y en todos los pacientes se debe realizar al menos:
radiografía de tórax, ETT, determinación de reactantes de fase aguda y/o TC/cardio-RM si se sospecha
loculación, masas, engrosamientos pericárdicos o anomalías torácicas.
Es muy importante la filiación etiológica para dirigir el tratamiento. Inicialmente, se realizará un
estudio bioquímico del líquido pericárdico (exudado: proteínas > 3 g/dL, cociente proteínas-líquido
pericárdico/proteínas-suero > 0,5, lactato-deshidrogenasa (LDH) > 200 UI/l, LDH-líquido pericárdico/LDH-
suero > 0,6, recuento celular), menos discriminatoria que en otros líquidos biológicos, con escasa
orientación etiológica en caso de exudado, lo que mantiene la controversia sobre su utilidad diagnóstica. Se
ampliará el estudio con microbiología, citología y otros exámenes adicionales según lo descrito
previamente (sección de PA) dependiendo de la sospecha clínica.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [389]
[25] ENFERMEDADES DEL PERICARDIO
Las indicaciones de pericardiocentesis son:
Taponamiento cardiaco.
Derrame moderado-severo que no responde al tratamiento médico (se correlaciona con el
pronóstico, un tercio evoluciona a taponamiento cardiaco, asociándose asimismo a etiología
bacteriana, tuberculosa y/o neoplásica).
Sospecha de etiología bacteriana o neoplásica.
Se realizará seguimiento ecocardiográfico en derrames moderados-severos por el riesgo ya
mencionado de mala evolución/pronóstico. Moderado: cada 6 meses. Severo: cada 3 meses.
IV. TAPONAMIENTO CARDIACO
1. DEFINICIÓN
Es la situación clínica en la que el derrame pericárdico aumenta la presión intrapericárdica lo
suficiente para generar una disminución del llenado ventricular, de tal manera que produce un deterioro
hemodinámico. Este deterioro hemodinámico presenta una variedad de manifestaciones clínicas que va
desde efectos mínimos hasta el colapso circulatorio y la parada en disociación electromecánica.
2. FISIOPATOLOGÍA
En el taponamiento cardiaco se produce la disminución del llenado de las cavidades cardiacas
secundaria a la compresión que ejerce la acumulación de líquido pericárdico. Los principales determinantes
para que esta situación tenga lugar son, en primer lugar, la presión intrapericárdica, y en segundo, los
mecanismos compensadores.
Presión intrapericárdica. Está influenciada por el volumen del líquido acumulado, por la
velocidad en la que este se acumula y por la rigidez del pericardio. Así, derrames pericárdicos
de pocos mililitros que se instauren de forma brusca (rotura de la pared libre del ventrículo
izquierdo, disección aórtica, procedimientos invasivos) pueden provocar una situación de
colapso circulatorio y muerte en pocos minutos (el pericardio no es capaz de acomodarse al
aumento de volumen). En otros casos, la acumulación de líquido de manera lenta y progresiva
permite cambios compensadores en la relación presión/volumen del saco pericárdico, y por
tanto se producen derrames pericárdicos de gran cuantía sin apenas repercusión
hemodinámica.
Mecanismos compensadores. Principalmente mediados por la estimulación adrenérgica, estos
son: taquicardia, aumento de la contractilidad miocárdica e incremento de las resistencias
vasculares periféricas.
3. CLÍNICA Y DIAGNÓSTICO
Clásicamente se ha descrito la tríada típica: elevación de la presión venosa yugular, hipotensión
arterial y presencia de pulso paradójico. Sin embargo, muchas veces estas características pasan
desapercibidas.
Otros síntomas pueden ser disnea y/u ortopnea en ausencia de edema pulmonar, distensión
abdominal, taquicardia, astenia y/o signos de bajo gasto anterógrado.
4. PRUEBAS COMPLEMENTARIAS
ECG: puede presentarse como taquicardia sinusal, bajos voltajes o alternancia eléctrica. −
Radiografía de tórax: se observa aumento del índice cardiotorácico, con la típica imagen en
tienda de campaña.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [390]
[25] ENFERMEDADES DEL PERICARDIO
ETT: es la herramienta más útil para diagnosticar el derrame pericárdico y valorar el
compromiso hemodinámico. Se debe realizar de forma urgente ante la sospecha de
taponamiento cardiaco. Además, permite evaluar la estrategia terapéutica más conveniente en
cada caso.
TC/RM: es mucho menos accesible que la ETT. Para una correcta evaluación deberían realizarse
con ECG-gating (esto es, la adquisición de las imágenes se sincroniza con el latido cardiaco
mediante ECG). La TC no sincronizada a menudo sobreestima el grado de derrame. No se deben
usar como primera opción.
5. TRATAMIENTO
Medidas generales. Se resumen en la expansión de volumen para intentar aumentar la presión
de llenado de las cavidades derechas. Por esta razón, están contraindicados los diuréticos. Se
pueden usar agentes vasoactivos para intentar mantener la presión de perfusión.
Pericardiocentesis. Es el tratamiento de elección. Mediante punción percutánea, guiada
preferiblemente por ecografía o por fluoroscopia, se accede a la cavidad pericárdica y se extrae
el líquido mediante aspiración. Se recomienda extraer únicamente el líquido suficiente para
mejorar la hemodinámica del paciente (la relación presión-volumen del pericardio presenta
efecto de “última gota”, por lo que los primeros mililitros que se extraen son los que más
descompresión relativa producen). Esto se debe a una complicación rara, pero con importante
impacto clínico, que se conoce como el síndrome de descompresión pericárdica. En los
derrames por hemorragia activa (traumáticos, complicaciones mecánicas, disección aórtica) se
debe extraer solo la cantidad necesaria para recuperar al paciente y poder trasladarlo para
cirugía urgente, ya que la propia presión que ejerce el derrame produce hemostasia.
En los taponamientos se deberá mantener un drenaje pericárdico mediante catéter durante al
menos 24 horas y hasta que el débito diario sea menor de 25 ml/día. Así se disminuyen de manera
apreciable las recidivas.
La Sociedad Europea de Cardiología propone un score a modo de triaje para la toma de decisiones
ante un derrame pericárdico severo sin shock hemodinámico, cuando la pericardiocentesis es obligatoria.
Se reproduce en la figura 2.
V. CONSTRICCIÓN PERICÁRDICA
1. DEFINICIÓN
Se trata de una entidad rara que puede ser consecuencia de casi cualquier patología pericárdica.
Tras un proceso inflamatorio crónico, el pericardio se fibrosa, puede engrosarse e incluso calcificarse,
produciendo así una limitación al llenado ventricular.
La etiología más frecuente en nuestro medio es la idiopática, hasta más de la mitad de los casos,
seguida de la inflamatoria/infecciosa. Aunque existen series que hablan de un aumento de la constricción
secundaria a cirugía cardiaca y radioterapia (hasta casi el 40% y el 20% de los casos, respectivamente), en
las series españolas de mayor número de pacientes estas dos patologías no representan más del 10% de los
casos.
2. CLÍNICA
Se trata de una clínica de instauración generalmente larvada, con predominio de signos y síntomas
de insuficiencia cardiaca derecha. En estadios iniciales presenta edemas en los miembros inferiores,
molestias abdominales y congestión hepática. Posteriormente puede evolucionar a ascitis y anasarca por
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [391]
[25] ENFERMEDADES DEL PERICARDIO
cirrosis cardiaca. En estadios finales de la enfermedad predominan los signos y síntomas de bajo gasto
cardiaco: caquexia, atrofia muscular, etc. En muchas ocasiones se confunde con una enfermedad hepática
primaria, lo cual retrasa su diagnóstico.
Figura 2. Algoritmo de actuación ante el taponamiento cardiaco adaptado de las guías de la Sociedad Europea de Cardiología.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [392]
[25] ENFERMEDADES DEL PERICARDIO
3. EXPLORACIÓN FÍSICA
El signo principal es una elevación marcada de la presión venosa yugular con un descenso rápido y
acusado del seno y. Puede existir signo de Kussmaul (aumento de presión venosa con la inspiración) y hasta
un tercio de los pacientes presentan pulso paradójico, especialmente si se asocia derrame pericárdico.
4. CLASIFICACIÓN
Constricción transitoria. Tras un daño pericárdico, la inflamación activa puede producir
constricción, que se resuelve espontáneamente o con tratamiento médico. Algunos estudios
reportan una prevalencia de hasta el 9% tras un episodio de pericarditis efusiva. La causa más
común es la inflamación pericárdica producida tras la pericardiotomía. En estos casos, los
signos y síntomas de constricción suelen ser leves y pasar desapercibidos.
Pericarditis efusivo-constrictiva. En el síndrome constrictivo, el espacio pericárdico
generalmente se encuentra obliterado. La pericarditis efusivo-constrictiva es un síndrome
clínico y hemodinámico en el cual se produce constricción por la capa visceral del pericardio en
presencia de derrame pericárdico a tensión. Estos pacientes tienen características clínicas
mixtas entre constricción pura y taponamiento cardiaco, aunque generalmente prevalece el
último. La marca distintiva de este síndrome es la persistencia de la elevación de las presiones
en la aurícula derecha una vez se ha reducido la presión intrapericárdica tras la
pericardiocentesis.
Se estima que este síndrome constituye el 1,3% de todos los síndromes pericárdicos, y hasta el
8% en el subgrupo de taponamiento cardiaco. La etiología más frecuente vuelve a ser la
idiopática, seguida de la neoplásica y la posradioterápica.
Constricción crónica. Se define como la constricción persistente después de 3 a 6 meses de
iniciado el proceso. Generalmente no existe inflamación activa (predomina la fibrosis).
5. DIAGNÓSTICO
Ante la sospecha de constricción pericárdica (historia clínica compatible, ICC derecha no explicada,
etc.), el diagnóstico se realiza principalmente a través de técnicas de imagen no invasivas. Se debe solicitar
un hemograma con recuento leucocitario y marcadores de inflamación (principalmente PCR). En la
radiografía de tórax se pueden observar calcificaciones, aunque solo en un 20% de los casos; pero con ella
se detectan otras afectaciones (por ejemplo, derrame pleural). La ETT es una prueba extremadamente útil y
se debe solicitar siempre en estos casos, pues además es capaz de diagnosticar otras patologías que
expliquen la clínica. La TC cardiaca y la cardio-RMN complementan la información del ECG o pueden
confirmar el diagnóstico si este es inconcluso (se prefiere la RM a la TC, dada la ausencia de radiación, la
posibilidad de detectar el componente inflamatorio del pericardio y la mejor evaluación funcional). En la
figura 3 se propone un algoritmo diagnóstico.
6. TRATAMIENTO
Por lo general, se ha considerado la pericardiectomía como el tratamiento de elección de la
constricción pericárdica. Se trata de una cirugía con una mortalidad entre el 6% y el 12%, técnicamente
complicada. Se debe resecar la mayor cantidad de pericardio, aunque si existen adherencias o
calcificaciones importantes esto no siempre es posible.
Esta cirugía consigue la normalización hemodinámica sólo en el 60% de los casos. En las formas
transitorias, o si se demuestra un componente inflamatorio en la cardio-RMN, está indicado tratar con
antiinflamatorios y reevaluar en 3 meses. Las formas leves de constricción no se benefician de la cirugía, y
en las formas muy avanzadas debe individualizarse la indicación, ya que presentan una elevada mortalidad
perioperatoria. En la figura 4 se propone un algoritmo de actuación.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [393]
[25] ENFERMEDADES DEL PERICARDIO
Figura 3. Algoritmo diagnóstico de la constricción pericárdica.
Figura 4. Algoritmo terapéutico de la constricción pericárdica.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [394]
[25] ENFERMEDADES DEL PERICARDIO
BIBLIOGRAFÍA
Adler Y, Charron P, Imazio M, Badano L, Barón-Esquivias G, Bogaert J, et al. 2015 ESC Guidelines for
the diagnosis and management of pericardial diseases. Eur Heart J. 2015;36:2921-64.
Burazor I, Imazio M, Markel G, Adler Y. Malignant pericardial effusion. Cardiol. 2013;124(4):224-32.
Imazio M. Contemporary management of pericardial diseases. Curr Opin Cardiol. 2012;27(3):308-17.
Imazio M, Adler Y. Management of pericardial effusion. Eur Heart J. 2013;34(16):1186-97.
Imazio M, Brucato A, Mayosi BM, Derosa FG, Lestuzzi C, Macor A, et al. Medical therapy of pericardial
diseases: part II: Noninfectious pericarditis, pericardial effusion and constrictive pericarditis. J
Cardiovasc Med (Hagerstown). 2010;11(11):785-94.
Porta-Sánchez A, Sagristà-Sauleda J, Ferreira-González I, Torrents-Fernández A, Roca-Luque I, García-
Dorado D. Pericarditis constrictiva: espectro etiológico, presentaciones clínicas, factores pronósticos y
seguimiento a largo plazo. Rev Esp Cardiol. 2015;68(12):1092-100.
Ristić AD, Imazio M, Adler Y, Anastasakis A, Badano LP, Brucato A, et al. Triage strategy for urgent
management of cardiac tamponade: a position statement of the European Society of Cardiology
Working Group on Myocardial and Pericardial Diseases. Eur Heart J. 2014;35(34):2279-84.
Sabzi F, Faraji R. Predictors of post pericardiotomy low cardiac output syndrome in patients with
pericardial effusion. J Cardiovasc Thorac Res. 2015;7(1):18-23.
Sagristà-Sauleda J, Angel J, Sánchez A, Permanyer-Miralda G, Soler-Soler J. Effusive-constrictive
pericarditis. N Engl J Med. 2004;350(5):469-75.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [395]
[26] SÍNDROME AÓRTICO AGUDO. ENFERMEDAD VASCULAR PERIFÉRICA
26.Síndrome aórtico agudo. Enfermedad vascular
periférica
Marta Torres Arrese.
Medicina Interna
Víctor Manuel Ospina Mosquera.
Cirugía Cardiaca
Isidoro Vargas Ureña.
Cirugía Vascular
Asesor: Ana Isabel Rodríguez Montalbán. Médica Adjunta Cirugía Vascular
I. SÍNDROME AÓRTICO AGUDO
1. DEFINICIÓN
Entidad clínica con elevada morbimortalidad que se caracteriza por la rotura de las capas íntima y
media aórticas. Las entidades clínicas que conforman el síndrome aórtico agudo (SAA) son: el hematoma
intramural (15%), la úlcera penetrante (5%) y la separación de las capas de la pared aórtica o disección
aórtica (80% de los SAA). Dichas entidades pueden derivar en la rotura de la pared aórtica. La aorta
ascendente está afectada en el 60% de los casos.
1. DISECCIÓN AÓRTICA
Interrupción de la capa media causada por una hemorragia intramural que provoca la separación
de las capas de la pared aórtica y la posterior formación de una luz verdadera y una falsa con o sin
comunicación. En un 10% de los casos, la disección aórtica (DAo) puede ocurrir a partir de un hematoma
intramural. Este proceso es seguido por una rotura aórtica en el caso de interrupción de la adventicia o por
la reentrada en la luz verdadera a través de un segundo desgarro de la íntima. Otras complicaciones son
taponamiento, regurgitación de la válvula aórtica, o síndromes de mala perfusión proximal y distal.
Clasificación de la disección aórtica (Tabla I)
La clasificación de la disección se realiza en función de la localización y el tiempo. La
clasificación más empleada es la de Stanford, ya que es la más sencilla.
Tabla I. Clasificación de la disección aórtica.
La mortalidad de los pacientes con el tipo A duplica la mortalidad de los individuos que presentan el
tipo B (25% y 12%, respectivamente). Las complicaciones cardiacas son las más frecuentes. Después de la
rotura aórtica, la insuficiencia aórtica (40-75%) es la segunda causa más común de muerte.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [396]
[26] SÍNDROME AÓRTICO AGUDO. ENFERMEDAD VASCULAR PERIFÉRICA
Epidemiología
En el estudio de Oxford Vascular, la incidencia de la DAo se estima en 6/100.000 personas por
año. Esta incidencia es mayor en varones que en mujeres y aumenta con la edad. El pronóstico
es peor en las mujeres, como resultado de la presentación atípica y el retraso en el diagnóstico.
Factores de riesgo
El factor de riesgo más común asociado es la hipertensión mal controlada.
Otros factores de riesgo son:
Enfermedades con afectación aórtica: aterosclerosis, conectivopatías, infección
local o ciertas vasculitis (arteritis de Takayasu, enfermedad de Behçet).
Enfermedad de la válvula aórtica (válvula aórtica bicúspide).
Cirugía cardiaca previa.
Traumatismo torácico cerrado.
Usuarios de drogas por vía parenteral (UDVP) (cocaína y anfetaminas).
Embarazo.
Tratamiento crónico con inmunosupresores o corticoides.
2. HEMATOMA INTRAMURAL
Colección hemática en la capa media, producida posiblemente por la ruptura espontánea de los
vasa vasorum de la capa adventicia (aunque en ocasiones se asocia a úlcera penetrante). Aparece más
frecuentemente en la aorta descendente y en ancianos.
3. ÚLCERA AÓRTICA PENETRANTE
Lesión ateroesclerótica ulcerada que penetra en la lámina elástica interna, favoreciendo el
desarrollo de un hematoma en la capa media de la pared aórtica. Afecta a pacientes ancianos e
hipertensos, y aparece en sectores de la aorta donde predomina la enfermedad ateroesclerótica, como la
aorta torácica descendente (90% de los casos).
2. DIAGNÓSTICO
Requiere la coexistencia de un cuadro clínico compatible y una prueba de imagen que confirme la
lesión de la pared aórtica. Dada su alta mortalidad, es fundamental que el clínico mantenga un alto nivel de
sospecha para lograr su diagnóstico.
1. CLÍNICA
Las diferentes entidades que conforman el SAA presentan manifestaciones clínicas similares. El
dolor torácico es el síntoma fundamental (85-95%), que suele ser de inicio súbito, de gran intensidad,
lancinante, desgarrante, pulsátil y migratorio. La localización del dolor y otros síntomas asociados puede
indicar el segmento aórtico afectado, y este puede cambiar a medida que progresa la disección y se afectan
otras ramas arteriales. Así, la afectación de la aorta ascendente presenta dolor retroesternal irradiado al
cuello, garganta y mandíbula, mientras que si el dolor se localiza a nivel interescapular o en el abdomen, es
la aorta descendente la afectada con más frecuencia.
1.1. Manifestaciones cardiológicas
La insuficiencia aórtica aparece hasta en el 76% de las disecciones de la aorta ascendente, y se
identifica un soplo diastólico más audible en borde esternal izquierdo (foco aórtico accesorio).
La isquemia miocárdica es infrecuente (10% según las series), y suele ser producida por
compresión coronaria por la falsa luz, o bien, por progresión de la disección hacia los ostium
coronarios. Los hallazgos electrocardiográficos son indistinguibles de los derivados de procesos
coronarios agudos, lo que favorece el error diagnóstico y terapéutico.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [397]
[26] SÍNDROME AÓRTICO AGUDO. ENFERMEDAD VASCULAR PERIFÉRICA
El derrame pericárdico es complicación frecuente de la disección tipo A, y puede producirse por
trasudación directa a través de la falsa luz, que origina un derrame leve, o bien, por rotura
directa hacia el pericardio, con el consiguiente taponamiento, hecho de pronóstico ominoso.
1.2. Síncope
Es un importante síntoma inicial, que ocurre en aproximadamente el 15% de los pacientes con tipo
A y en < 5% de los que presentan el tipo B. Está asociado con un mayor riesgo de mortalidad hospitalaria,
ya que se relaciona a menudo con complicaciones que amenazan la vida, como taponamiento cardiaco o
disección de los troncos supraaórticos.
1.3. Manifestaciones neurológicas
Pueden ser transitorias hasta en el 50% de los casos, y son las únicas manifestaciones clínicas de
SAA hasta en un tercio de las ocasiones, lo que puede enmascarar el diagnóstico. La frecuencia de los
síntomas neurológicos oscila entre 15-40%, y en la mitad de los casos puede ser transitoria. El ictus
isquémico y el accidente isquémico transitorio son las manifestaciones neurológicas más frecuentes
(asociadas sobre todo a disección de tipo A). La afectación de la aorta descendente torácica puede causar
isquemia espinal y producir paraplejia aguda (1%). La neuropatía isquémica cursa con dolor y déficits
motores y sensitivos en las extremidades, se observa en aproximadamente el 10% de los casos. La
ronquera, debido a la compresión del nervio laríngeo recurrente izquierdo, es rara.
1.4. Manifestaciones gastrointestinales
La alteración de la perfusión puede ser intermitente si es causada por el prolapso de la disección, o
persistente por la expansión de la falsa luz y la obliteración de la irrigación arterial de los órganos. La clínica
es frecuentemente insidiosa y los pacientes pueden no manifestar dolor en el 40% de los casos. En
consecuencia, el diagnóstico es con frecuencia demasiado tardío para salvar el intestino y al paciente. Es
esencial mantener un alto grado de sospecha de isquemia mesentérica en pacientes con DAo aguda y dolor
abdominal o aumento de los niveles de lactato. La hemorragia gastrointestinal es rara, pero
potencialmente letal. El sangrado puede ser limitado, como consecuencia de infarto mesentérico, o masivo,
por una fístula aortoesofágica o aortoentérica por rotura de la falsa luz hacia el intestino.
1.5. Insuficiencia renal
Ocurre en el 20% de los pacientes con el tipo A y en el 10% de los pacientes con el tipo B.
Puede ser el resultado de la hipoperfusión renal prolongada, el shock cardiogénico o la
participación de las arterias renales en la disección.
1.6. Derrame pleural
El derrame pleural como consecuencia de la hemorragia aórtica hacia el mediastino y el espacio
pleural es raro, ya que estos pacientes por lo general no sobreviven hasta llegar al hospital. Los derrames
pleurales más pequeños pueden detectarse en el 15-20% de los pacientes y se cree que suelen ser el
resultado de un proceso inflamatorio.
1.7. Complicaciones pulmonares
Las complicaciones pulmonares de la DAo aguda son poco frecuentes. Entre ellas, cabe mencionar
la compresión de la arteria pulmonar y la fístula aortopulmonar (disnea con pulmón blanco unilateral,
hemoptisis masiva).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [398]
[26] SÍNDROME AÓRTICO AGUDO. ENFERMEDAD VASCULAR PERIFÉRICA
2. EXPLORACIÓN FÍSICA
El paciente presenta datos que sugieren gravedad, como palidez, sudoración y taquicardia. La
hipertensión arterial aparece en el 50% de los pacientes, y presentan hipotensión y shock aquellos que
desarrollan taponamiento cardiaco, insuficiencia aórtica severa, isquemia miocárdica o rotura hacia la
cavidad peritoneal. Debido a que la disección puede progresar hacia las arterias braquiales, es precisa la
medición de la tensión arterial (TA) en ambos brazos y, en ocasiones, en ambas piernas. A medida que la
disección afecta a las diferentes ramas arteriales, surgen manifestaciones en distintos órganos y sistemas.
El signo clínico más importante derivado de este hecho es la ausencia, disminución o asimetría de los pulsos
periféricos.
3. TÉCNICAS DIAGNÓSTICAS
3.1. Electrocardiograma
La ausencia de datos de isquemia aguda coincidiendo con dolor de gran intensidad y la presencia de
signos de hipertrofia ventricular izquierda han de hacer pensar en el SAA. Dada la escasa frecuencia de la
coexistencia de SAA con oclusión coronaria, la presencia de un ascenso del segmento ST sugerente de
infarto agudo de miocardio (IAM) debe tratarse como un evento cardiaco primario sin esperar a obtener
pruebas de imagen de la aorta, a menos que el paciente tenga alto riesgo para SAA.
3.2. Radiografía de tórax
El signo radiológico característico es el ensanchamiento mediastínico. Otros signos que pueden
aparecer son el derrame pleural y el desplazamiento del esófago y de la tráquea hacia la derecha y hacia
delante. La cardiomegalia puede sugerir la presencia de derrame pericárdico.
Una radiografía de tórax normal no debe retrasar la realización de técnicas de imagen aórtica
definitivas.
3.3. D-dímeros
Los D-dímeros aumentan en las primeras horas de la DAo, aunque la principal limitación es que no
están elevados en el hematoma intramural o en la úlcera penetrante.
3.4. Técnicas de imagen de elección como screening inicial
La ecocardiografía transtorácica (ETT) posee una sensibilidad y especificidad para la
identificación de la disección de la aorta proximal del 80% y del 96%, respectivamente (si la
ventana acústica lo permite), aunque es de muy escasa utilidad en la identificación de
alteraciones en otros segmentos aórticos, así como en el resto de procesos del SAA.
Puede tratarse de una primera técnica diagnóstica, ya que un diagnóstico positivo favorece la
rapidez en la implantación de la estrategia terapéutica.
Las pruebas aceptadas para screening de síndrome coronario agudo (SCA) son la
ecocardiografía transesofágica, la tomografía computarizada (TC) y la resonancia magnética
(RM). La TC y la RM son superiores a la ETT para la evaluación de la extensión de la DAo aguda y
la participación de las ramas. La elección de la prueba de imagen dependerá de la
disponibilidad de la misma, la situación hemodinámica del paciente y las posibles
contraindicaciones (patología esofágica, alergia al yodo, etc.). Si la sospecha es alta y el estudio
es negativo, se debe plantear la realización de un nuevo estudio.
La ETT con Doppler puede ser de gran interés en el paciente inestable, y se utiliza para
controlar los cambios en el quirófano y en cuidados intensivos. Su utilidad para la
visualización de la aorta torácica distal es limitada, y nula para la aorta abdominal.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [399]
[26] SÍNDROME AÓRTICO AGUDO. ENFERMEDAD VASCULAR PERIFÉRICA
La TC es la técnica de imagen más utilizada para la evaluación del síndrome aórtico
agudo, y en particular para la DAo. Ello se debe a su velocidad, disponibilidad y una
excelente sensibilidad y especificidad > 95%. El estudio comienza con una secuencia sin
contraste para evaluar la existencia de hematoma transmural (que produce una señal
hiperlúcida), para posteriormente realizar el estudio con contraste.
En cuanto a la RM, aunque tiene una sensibilidad y una especificidad del 98%, sus
limitaciones prácticas impiden su uso en la mayoría de los casos. Esta prueba se reserva
para situaciones con dudas diagnósticas y para el seguimiento de disecciones crónicas
tipo B, hematomas y úlceras aórticas.
3. DIAGNÓSTICO DIFERENCIAL
Se establecerá en función de la sintomatología (fundamentalmente dolor torácico muy intenso) y
los hallazgos exploratorios.
Dolor torácico intenso: IAM, tromboembolia pulmonar (TEP), neumotórax espontáneo, ruptura
esofágica.
Dolor abdominal: cólico renal y biliar, obstrucción-perforación intestinal, isquemia mesentérica
de otra etiología.
Dolor de espalda: cólico renal, hernia discal, procesos osteomusculares.
Déficit de pulsos: embolias por otra causa, isquemia arterial aguda de otra etiología.
Déficit neurológico focal: accidente isquémico cerebrovascular primario, síndrome de la cola de
caballo.
4. MANEJO TERAPÉUTICO
Los pacientes con SAA deben ser ingresados en una Unidad de Cuidados Intensivos para una
estrecha monitorización hemodinámica.
1. TRATAMIENTO AGUDO
Se explica en la figura 1 y se basa en el control de la TA, la frecuencia cardiaca y el dolor.
2. TRATAMIENTO DEFINITIVO (TABLA II)
Tabla II. Tratamiento definitivo del síndrome aórtico agudo.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [400]
[26] SÍNDROME AÓRTICO AGUDO. ENFERMEDAD VASCULAR PERIFÉRICA
Figura 1. Tratamiento agudo del síndrome aórtico agudo.
La decisión sobre el manejo quirúrgico o médico en pacientes con DAo aguda se basa en la
localización de la disección y la situación clínica del paciente.
Tratamiento de la DAo tipo A: la cirugía es el tratamiento de elección de cara a salvar la vida del
paciente y evitar cirugías tardías. La mortalidad es del 50% a las 48 horas si no se realiza, y
reduce la mortalidad a 1 mes del 90% al 30%. Cuando hay mala perfusión visceral, los
procedimientos híbridos (cirugía y tratamiento intravascular o fenestración) pueden ser la
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [401]
[26] SÍNDROME AÓRTICO AGUDO. ENFERMEDAD VASCULAR PERIFÉRICA
mejor opción. Situaciones como el coma, el shock secundario a taponamiento pericárdico, la
mala perfusión de las arterias coronarias o periféricas, y los accidentes cerebrovasculares son
factores predictivos importantes para la mortalidad postoperatoria.
Tratamiento de la DAo tipo B: en general, el tratamiento es médico (control del dolor, la
frecuencia cardiaca y la TA), con una estrecha vigilancia para identificar signos de progresión de
la enfermedad y/o mala perfusión. Se recomienda el tratamiento intravascular en las
disecciones tipo B complicadas, y se debe considerar en las no complicadas.
Tratamiento del hematoma intramural: en el tipo A está indicado el tratamiento quirúrgico
emergente o urgente (< 24 horas), dependiendo de los factores de riesgo que presente el
paciente. El componente dinámico de la evolución en el tipo B obliga a un seguimiento estrecho
mediante técnicas de imagen.
Tratamiento de la úlcera penetrante: su objetivo es evitar la ruptura de la aorta y la progresión
a una DAo aguda. Las indicaciones para la intervención son dolor recurrente y refractario, así
como signos de rotura contenida, rápido crecimiento de la úlcera aórtica, hematoma
periaórtico asociado o derrame pleural.
En el caso de la rotura contenida de un aneurisma aórtico, el tratamiento es intravascular
cuando la anatomía es favorable, y guarda una menor morbimortalidad perioperatoria, pero
tiene una mayor tasa de complicaciones tardías. Los casos con rotura libre o hematoma
periaórtico deben considerarse una emergencia quirúrgica. En el resto, el tratamiento puede
diferirse 24 horas hasta la estabilización del paciente. De acuerdo con las series publicadas, el
tratamiento intravascular se prefiere a la cirugía debido tanto a su beneficio en la supervivencia
como al menor riesgo de paraplejia.
3. TRATAMIENTO MÉDICO CRÓNICO Y SEGUIMIENTO
Se basa en el control de la TA y los factores de riesgo cardiovascular. Siempre ha de incluirse en el
tratamiento un betabloqueante, asociado a otros fármacos hipotensores si es preciso.
Se deben llevar a cabo revisiones periódicas con pruebas de imagen (TC, RM y ETT), con un control
más estricto a los 6 meses y posteriormente durante los siguientes 3 años. La revisión debe realizarse con la
misma técnica y tomando las medidas de igual manera en los mismos segmentos anatómicos. Siempre se
debe medir en un plano perpendicular al flujo aórtico.
Debido a la variabilidad de las medidas, se debe considerar significativa una progresión con la TC >
5 mm, aunque en la aorta ascendente y con sincronización electrocardiográfica cambios > 3 mm se
consideran relevantes en patologías como el síndrome de Marfan y la válvula bicúspide.
La ETT puede ser útil en la valoración de la aorta ascendente y la raíz aórtica. Posteriormente, se
mantendrá de forma indefinida una revisión anual.
5. EVOLUCIÓN Y PRONÓSTICO
1. DISECCIÓN AÓRTICA
La mortalidad hospitalaria de la DAo tipo A es del 33%, y la mortalidad quirúrgica del 23%.
La mortalidad de las de tipo A tratadas médicamente a los 30 días es del 85%, frente al 8% de las de
tipo B. Son factores de mal pronóstico la inestabilidad hemodinámica, la afectación de troncos arteriales, la
insuficiencia renal y el sexo femenino.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [402]
[26] SÍNDROME AÓRTICO AGUDO. ENFERMEDAD VASCULAR PERIFÉRICA
2. HEMATOMA INTRAMURAL
Su evolución es dinámica, y puede progresar a disección, a rotura cardiaca o bien reabsorberse de
forma espontánea, pudiendo ocurrir complicaciones hasta 6 meses después del evento agudo, lo que obliga
al seguimiento estrecho de estos pacientes. Su pronóstico, en general, es mejor que el de la disección.
3. ÚLCERA ATEROESCLERÓTICA PENETRANTE
Si es aguda y sintomática, el riesgo de complicaciones es igual o superior al de las otras entidades, y
el riesgo de rotura aórtica oscila del 10% al 40%.
II. ENFERMEDAD VASCULAR PERIFÉRICA
A. ISQUEMIA AGUDA DE LAS EXTREMIDADES
El síndrome de isquemia arterial aguda es la interrupción brusca de la perfusión sanguínea de una
extremidad, y constituye la urgencia vascular más frecuente.
1. ETIOLOGÍA
Existen dos causas principales de isquemia arterial aguda, excluyendo los traumatismos y la
yatrogenia, que son los émbolos y las trombosis arteriales.
Tabla III. Etiología de la isquemia arterial aguda de las extremidades.
Los émbolos proceden normalmente del corazón, a causa de una arritmia o de un defecto
morfológico de la pared ventricular, como un aneurisma. Este émbolo viaja a través del árbol arterial y se
suele alojar en las bifurcaciones arteriales, por ejemplo, en las arterias femoral común y poplítea en las
extremidades inferiores, y en la salida de la arteria humeral profunda en la extremidad superior. Otras
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [403]
[26] SÍNDROME AÓRTICO AGUDO. ENFERMEDAD VASCULAR PERIFÉRICA
causas menos frecuentes son la embolia paradójica, sobre todo en pacientes jóvenes, cuyo origen es una
trombosis venosa profunda acompañada de un foramen oval permeable, las endocarditis y el mixoma
auricular.
La trombosis ocurre in situ como consecuencia de una obstrucción aterosclerótica progresiva,
hipercoagulabilidad, disección arterial, vasoespasmo u oclusión de un bypass (Tabla III).
2. DIAGNÓSTICO
El diagnóstico de la isquemia arterial aguda es fundamentalmente clínico.
Las manifestaciones clínicas clásicas son las seis “P”: dolor (pain), palidez, parestesia, parálisis,
pulso ausente y poiquilotermia. El dolor es el síntoma más frecuente, ya que se observa en el 80% de los
casos, es de aparición brusca y aumenta con el movimiento de la extremidad. La parestesia refleja la
isquemia de los nervios periféricos en sus fases iniciales, mientras que en fases avanzadas se acompaña de
una abolición de la sensibilidad (Tablas IV y V).
Tabla IV. Clasificación clínica de la isquemia arterial aguda de las extremidades.
Tabla V. Diagnóstico diferencial de la isquemia arterial aguda de las extremidades.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [404]
[26] SÍNDROME AÓRTICO AGUDO. ENFERMEDAD VASCULAR PERIFÉRICA
3. EXPLORACIÓN FÍSICA
La exploración de los pulsos permite localizar la lesión. En las extremidades inferiores se deben
explorar todos los pulsos (femoral, poplíteo, tibial posterior y pedio), y en las extremidades superiores, el
subclavio, axilar, humeral, radial y cubital, siempre de manera bilateral.
En la piel se observan cambios de coloración, que inicialmente presenta palidez, seguida de cianosis
con el transcurso del tiempo. La diferencia de temperatura, tanto del sector irrigado como del isquémico en
la misma extremidad, así como con respecto a la extremidad contralateral, es de gran ayuda. Asimismo, se
debe realizar una exploración neurológica minuciosa en busca de alteraciones sensitivo-motoras.
4. PRUEBAS COMPLEMENTARIAS
De forma general, se deben realizar un hemograma completo, una bioquímica que incluya enzimas
musculares (creatina-cinasa [CK] y lactato deshidrogenasa [LDH]), un estudio de coagulación, un
electrocardiograma y una radiografía de tórax.
Se debe realizar una eco-Doppler vascular para la valoración del sector arterial afectado.
La angio-TC, sobre todo a nivel del sector aortoilíaco y femoropoplíteo, con reconstrucción
tridimensional, es de gran utilidad.
La arteriografía continúa siendo la prueba definitiva para localizar con exactitud la obstrucción y
diferenciar entre embolia y trombosis, si esta es preoperatoria; e incluso es diagnóstico- terapéutica en
caso de ser intraoperatoria.
5. TRATAMIENTO
El tratamiento de la isquemia aguda es quirúrgico. El tiempo de la isquemia es el factor pronóstico
aislado más importante para la viabilidad del territorio afectado, y debe ser inferior a 6-8 horas.
Hay distintas modalidades de revascularización: bien de forma percutánea o mediante
trombectomía quirúrgica, bypass y/o reparación arterial. La estrategia terapéutica dependerá del tipo de
oclusión (trombosis/embolia), la duración de la isquemia, las comorbilidades, el tipo de conducto
(arteria/injerto), los resultados y los riesgos relacionados con la terapia.
En cuanto se establece el diagnóstico clínico, deberá iniciarse tratamiento anticoagulante con
heparina no fraccionada. Se recomienda administrar un bolo inicial de 80 UI/kg, seguido de una infusión
continua (18 UI/kg/h) para mantener el tiempo de tromboplastina parcial activado (TTPa) en límites
terapéuticos (1,5-2,5 veces el TTPa control). Si es posible realizar una arteriografía precoz, debe
administrarse el bolo de heparina y esperar a iniciar la infusión continua a su resultado.
No hay que olvidar instaurar un correcto tratamiento analgésico, recurriendo a opiáceos mayores
(cloruro mórfico, etc.) de ser preciso.
B. ISQUEMIA ARTERIAL CRÓNICA
La enfermedad arterial periférica (EAP) de las extremidades inferiores consiste en un conjunto de
signos y síntomas que son el resultado de la estenosis u oclusión de los sectores aortoilíaco,
femoropoplíteo y distal. Su prevalencia aumenta con la edad, siendo del 18% entre las edades de 60-90
años. Se presenta con las siguientes manifestaciones clínicas: enfermedad asintomática, claudicación
intermitente (dolor a la deambulación) o isquemia crítica (dolor de reposo o pérdida de tejido: úlcera o
gangrena).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [405]
[26] SÍNDROME AÓRTICO AGUDO. ENFERMEDAD VASCULAR PERIFÉRICA
1. ETIOLOGÍA
El principal origen de la EAP es la aterosclerosis, y comparte los mismos factores de riesgo que en
otros sectores, es decir, edad avanzada, tabaquismo, diabetes mellitus, etc.
2. APROXIMACIÓN DIAGNÓSTICA
2.1. Anamnesis
La claudicación intermitente es el dolor en un determinado grupo muscular reproducible con el
ejercicio y que mejora con el reposo. Es la manifestación clásica de la EAP. El grupo muscular afectado
durante la marcha se correlaciona con la localización de la lesión vascular. Desde el punto de vista clínico, la
EAP se puede estratificar siguiendo la clasificación de Fontaine, que ofrece información pronóstica y
permite orientar el tratamiento (Tabla VI).
2.2. Exploración física
Se debe realizar una exploración completa: determinación de la TA en ambos brazos, auscultación
(cervical, cardiaca y pulmonar), palpación abdominal en busca de masas pulsátiles compatibles con
aneurismas aórticos (sobre todo en el mesogastrio), palpación de pulsos periféricos (carotídeo, axilar,
humeral, radial, cubital, femoral, poplíteo, pedio y tibial posterior), soplos en las áreas de estenosis,
frialdad distal, mal relleno capilar, cambios cutáneos y ungueales (piel atrófica, brillante) y/o mala
cicatrización de las heridas.
Tabla VI. Clasificación de Fontaine.
2.3. Pruebas complementarias
La decisión de recomendar una intervención quirúrgica o intravascular depende de varios factores:
síntomas, enfermedades concomitantes, localización y gravedad de las lesiones oclusivas. El estudio de
laboratorio inicial es el cálculo del índice tobillo-brazo (ITB: > 0,9 isquemia normal; 0,7 a 0,89 leve; 0,5 a
0,69 moderada y < 0,5 isquemia crítica), con medida de las presiones segmentarias, la claudicometría con
mediciones del ITB antes y después de la misma, la ecografía dúplex, la angio-TC con contraste, la RM) y la
angiografía, esta última con la ventaja de que puede ser tanto diagnóstica como terapéutica.
2.4. Diagnóstico diferencial
Debe establecerse con otras causas de dolor en los miembros inferiores y con otras potenciales
causas de oclusión arterial menos frecuentes que la arterosclerosis, como la displasia fibromuscular,
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [406]
[26] SÍNDROME AÓRTICO AGUDO. ENFERMEDAD VASCULAR PERIFÉRICA
secuelas tardías de traumatismos o radiación, enfermedad de Takayasu, tromboangeítis obliterante
(enfermedad de Buerger), atrapamiento poplíteo o coartación de aorta (Tablas VII y VIII).
Tabla VII. Diagnóstico diferencial de la claudicación intermitente.
Tabla VIII. Diagnóstico diferencial de las úlceras en los miembros inferiores.
3. TRATAMIENTO
El tratamiento médico de la EAP se basa en dos objetivos: disminuir el riesgo cardiovascular del
paciente y mejorar su situación funcional y la clínica asociada a claudicación intermitente.
Para la prevención secundaria de eventos cardiovasculares está indicado el tratamiento con
antiagregantes. El ácido acetilsalicílico (75-100 mg/día) es la primera opción en estos pacientes. Clopidogrel
(75 mg/día) es el tratamiento alternativo.
En estos pacientes se debe añadir una estatina aun teniendo cifras normales de colesterol.
Por otra parte, debería realizarse un programa de ejercicio supervisado como parte del tratamiento
sintomático inicial en todos los pacientes con EAP.
Respecto al tratamiento farmacológico, cilostazol (inhibidor de la fosfodiesterasa) ha demostrado
mejorar significativamente los síntomas en estos pacientes (100 mg/12 h antes de las comidas). Debe
tenerse precaución en pacientes con insuficiencia cardiaca. Otras alternativas con cierto beneficio clínico
serían pentoxifilina y naftidrofurilo.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [407]
[26] SÍNDROME AÓRTICO AGUDO. ENFERMEDAD VASCULAR PERIFÉRICA
Por último, las indicaciones de revascularización dependen de la situación clínica del paciente y del
territorio afectado. De forma general, la principal indicación de revascularización es la isquemia crítica
(grados III y IV de Fontaine). La elección de la técnica quirúrgica (abierta o intravascular) dependerá del tipo
de lesión.
BIBLIOGRAFÍA
Erbel R, Aboyans V, Boileau C, Bossone E, Bartolomeo RD, Eggebrecht H, et al. 2014 ESC Guidelines on
the diagnosis and treatment of aortic diseases. Document covering acute and chronic aortic diseases
of the thoracic and abdominal aorta of the adult. The Task Force for the Diagnosis and Treatment of
Aortic Diseases of the European Society of Cardiology (ESC). Eur Heart J. 2014;35(41):2873-926.
Grupo de Trabajo de la SEC para la guía de la ESC 2014 sobre diagnóstico y tratamiento de la
patología de la aorta, revisores expertos para la guía de la ESC 2014 sobre diagnóstico y tratamiento
de la patología de la aorta, Comité de Guías de la SEC. Comentarios a la guía de práctica clínica de la
ESC 2014 sobre diagnóstico y tratamiento de la patología de la aorta. Rev Esp Cardiol.
2015;68(3):179-84.
Hiratzka LF, Bakris GL, Beckman JA, Bersin RM, Carr VF, Casey DE Jr, et al. 2010
ACCF/AHA/AATS/ACR/ ASA/SCA/SCAI/SIR/STS/SVM Guidelines for the diagnosis and management of
patients with thoracic aortic disease. A Report of the American College of Cardiology
Foundation/American Heart Association Task Force on Practice Guidelines, American Association for
Thoracic Surgery, American College of Radiology, American Stroke Association, Society of
Cardiovascular Anesthesiologists, Society for Cardiovascular Angiography and Interventions, Society of
Interventional Radiology, Society of Thoracic Surgeons, and Society for Vascular Medicine. J Am Coll
Cardiol. 2010;55(14):e27-129.
Tendera M, Aboyans V, Bartelink ML, Baumgartner I, Clément D, Collet JP, et al. Guía de práctica clínica
de la ESC sobre diagnóstico y tratamiento de las enfermedades arteriales periféricas. Rev Esp Cardiol.
2012;65(2):172,e1-57.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [408]
[27] HIPERTENSIÓN PULMONAR
27.Hipertensión pulmonar
Eloy Gómez Mariscal.
Cardiología
Pilartxo Catalán Martín.
Medicina Interna
Asesor: Pilar Escribano Subías. Médica Adjunta de Cardiología. Unidad de Hipertensión Pulmonar
I. CONCEPTO Y CLASIFICACIÓN
La presión arterial pulmonar media (PAPm) se considera normal cuando no excede de 20 mm Hg en
reposo, medida mediante cateterismo cardiaco derecho (CCD). La hipertensión pulmonar (HP) se define
como una PAPm superior a los 25 mm Hg en reposo.
Existe una clasificación clínica de los diferentes tipos de HP en cinco categorías. Dentro de cada
grupo se reúnen las enfermedades que comparten mecanismos fisiopatológicos, presentación clínica u
opciones terapéuticas en la HP que asocian (Tabla I).
Tabla I. Clasificación clínica de la hipertensión pulmonar (Niza, 2013).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [409]
[27] HIPERTENSIÓN PULMONAR
Atendiendo a parámetros hemodinámicos, la HP se clasifica de la siguiente forma: HP precapilar,
HP poscapilar aislada e HP poscapilar combinada (Tabla II).
Tabla II. Clasificación hemodinámica de la hipertensión pulmonar.
Dentro de estos grupos, cabe destacar la hipertensión arterial pulmonar (HAP, grupo 1), que es en
la que se centrará fundamentalmente el capítulo, definida como una elevación de la PAPm ≥ 25 mm Hg en
reposo con presión capilar pulmonar (PCP) ≤ 15 mm Hg (medida por enclavamiento distal del catéter) y
unas resistencias vasculares pulmonares (RVP) > 3 UW (unidades Wood), en ausencia de otras causas de HP
precapilar, como pulmonares (grupo 3) o tromboembólica crónica (grupo 4).
La HP poscapilar de la enfermedad del lado izquierdo del corazón (grupo 2) comprende la HP
poscapilar aislada (PAPm ≥ 25 mm Hg, PCP > 15 mm Hg y gradiente transpulmonar diastólico < 7 mm Hg), y
la HP combinada poscapilar y precapilar (PAPm ≥ 25 mm Hg, PCP > 15 mm Hg y gradiente transpulmonar
diastólico ≥ 7 mm Hg).
II. EPIDEMIOLOGÍA
Los datos en la literatura sobre la incidencia y prevalencia mundial de la HP son escasos. De forma
global, la proporción hombre:mujer es de 1:1,8. La edad media al diagnóstico se sitúa en torno a los 50
años.
Aunque los datos comparativos sobre la prevalencia de los distintos grupos de HP son escasos, la
enfermedad cardiaca izquierda (grupo 2) es la más frecuente. La prevalencia de HP en pacientes con
insuficiencia cardiaca (ICC) crónica aumenta con el deterioro de la clase funcional; también los pacientes
con ICC y función sistólica conservada pueden desarrollar una HP. En las valvulopatías, la HP aumenta
cuanto mayor sea el defecto y los síntomas; se puede encontrar HP en prácticamente todos los pacientes
con valvulopatía mitral sintomática grave y hasta en el 65% de los pacientes con estenosis aórtica
sintomática.
En el grupo HAP (grupo 1), aproximadamente, la mitad de los pacientes tienen HAPI (hipertensión
arterial pulmonar idiopática), HAPH (hipertensión arterial pulmonar hereditaria) o inducida por drogas (en
nuestro medio, por aceite de colza). En el subgrupo de enfermedades asociadas a la HAP (HAPA), la causa
más importante son las enfermedades del tejido conectivo, particularmente la esclerosis sistémica, tanto
por su frecuencia como por su gravedad.
Los pacientes con HP del grupo 3 suelen presentar HP moderada, siendo poco frecuente una HP
severa; esta es habitual en pacientes con fibrosis pulmonar asociada a enfisema.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [410]
[27] HIPERTENSIÓN PULMONAR
En la HP grupo 4 un 0,5-9% de los pacientes que han presentado un tromboembolismo pulmonar
(TEP) agudo desarrollarán HP tromboembólica crónica, pero un 75% de los pacientes con hipertensión
pulmonar tromboembólica crónica (HPTEC) han presentado previamente un TEP; de ellos un 32%
presentaron algún tipo de trombofilia asociada.
En los países emergentes, la HAP asociada a esquistosomiasis y la HP relacionada con grandes
altitudes constituyen un problema importante.
**Los siguientes apartados se referirán fundamentalmente a la HAP; para más información sobre la
patología asociada a la HP grupo 2 (relacionada con enfermedad del corazón izquierdo) y grupo 3
(secundaria a enfermedades pulmonares/hipoxia), ver capítulos correspondientes.
III. MANIFESTACIONES CLÍNICAS DE LA HIPERTENSIÓN ARTERIAL
PULMONAR
Los síntomas de la HP son inespecíficos y se asocian a la progresión del fallo del ventrículo derecho
(VD).
Al inicio, los pacientes suelen estar asintomáticos, gracias al desarrollo de mecanismos
compensadores frente al aumento de las RVP, tales como hipertrofia del VD, dificultando el diagnóstico
precoz de la HP.
Con el tiempo y el progresivo deterioro de la función del VD, comienzan a presentar síntomas con
el ejercicio, y únicamente en estadios avanzados, en reposo: disnea, tos seca, angina y síncope. El síntoma
más frecuente es la disnea de esfuerzo progresiva.
Figura 1. Signos y síntomas de la hipertensión arterial pulmonar.
Los signos que se desarrollarán a medida que la función del VD se deteriore son: refuerzo del
componente pulmonar del segundo ruido cardiaco, soplo de insuficiencia tricuspídea (pansistólico), soplo
de insuficiencia pulmonar (diastólico), ingurgitación yugular, hepatomegalia, ascitis y edemas en miembros
inferiores (Figura 1).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [411]
[27] HIPERTENSIÓN PULMONAR
En el examen físico pueden existir signos que orienten a una entidad específica que cause HP, por
ejemplo, la presencia de telangiectasias, esclerodactilia y úlceras digitales orientarían a una esclerodermia;
las arañas vasculares, atrofia testicular y eritrosis palmar a enfermedad hepática y las acropaquias a una
enfermedad venooclusiva pulmonar (EVOP) o enfermedad intersticial pulmonar.
**¿Cuándo se sospecha de la existencia de una posible HP? Cuando un paciente se presente con
disnea de esfuerzo o síncope con el ejercicio y/o algún signo en la exploración física o en las pruebas
complementarias (ver Apartado “Diagnóstico”) de hipertrofia/disfunción del VD, será prioritario sospechar
la existencia de HP. Asimismo, los pacientes con antecedentes de TEP que desarrollen disnea de esfuerzo o
ICC derecha en cualquier momento de la evolución, deberían someterse a un estudio mediante
ecocardiografía transtorácica para descartar el desarrollo de HPTEC.
IV. DIAGNÓSTICO DE LA HIPERTENSIÓN ARTERIAL PULMONAR
En el diagnóstico de la HAP se ha de partir de la sospecha clínica y seguir un proceso escalonado
para su confirmación, establecer la causa y determinar la gravedad del cuadro para poder planificar el
tratamiento.
1. SOSPECHA DE HIPERTENSIÓN ARTERIAL PULMONAR
Se fundamenta en la presencia de:
1.1. Síntomas y signos
Como ya se ha descrito, los síntomas son generalmente secundarios a disfunción del VD (Figura 1).
1.2. Factores de riesgo de hipertensión arterial pulmonar
Por el riesgo de desarrollo de HAP, se debe buscar la presencia de síntomas en aquellos pacientes
con cardiopatías congénitas (CC) con cortocircuito sistémico-pulmonar, familiares de pacientes con HAP
heredable, infección por el virus de la inmunodeficiencia humana (VIH), hipertensión portal/cirrosis,
enfermedades del tejido conectivo y exposición a anorexígenos u otros tóxicos relacionados con la HAP. De
hecho, se debe realizar un ecocardiograma anual incluso en ausencia de síntomas en aquellos pacientes
con esclerodermia, hipertensión portal y/o cirrosis candidatos a trasplante hepático y en familiares de
pacientes con HAP heredable.
1.3. Detección de la hipertensión arterial pulmonar
Electrocardiograma (ECG). Son sugerentes datos de dilatación de aurícula derecha (AD), eje
derecho y crecimiento del VD, especialmente el patrón tipo A, con R altas o qR en precordiales
derechas, con alteraciones de la repolarización de V1-V4. En fases avanzadas no es infrecuente
el desarrollo de fibrilación auricular y, especialmente, flutter auricular.
Radiografía de tórax. Muestra cambios en el 90% de los pacientes con HAPI en el momento del
diagnóstico. Puede encontrarse dilatación del tronco pulmonar y crecimiento de AD o VD.
Ecocardiograma transtorácico (ETT). Es una prueba diagnóstica fundamental, al permitir
estimar la presión arterial pulmonar (PAP) sistólica y detectar datos indirectos de HAP, que nos
ayudará a establecer la probabilidad de HAP (Tabla III). Además, permite la valoración
pronóstica al informarnos del tamaño y función del VD y presiones de AD, así como descartar la
existencia de CC con shunt sistémico-pulmonar (HP grupo 1), para lo cual habrá que realizar un
test de suero salino agitado. En presencia de shunt estará indicado además realizar un
ecocardiograma transesofágico (ETE). Es importante resaltar que la PAP sistólica no es un
parámetro diagnóstico de HP, solo orientativo.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [412]
[27] HIPERTENSIÓN PULMONAR
Tabla III. Probabilidad ecocardiográfica de HP en pacientes con sospecha clínica y actitud diagnóstica.
Figura 2. Algoritmo diagnóstico de la hipertensión pulmonar.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [413]
[27] HIPERTENSIÓN PULMONAR
2. ALGORITMO DIAGNÓSTICO (FIGURA 2)
Antes de empezar el estudio de la HAP deben descartarse la HP asociada a cardiopatía izquierda
(HP grupo 2), la HP asociada a patología pulmonar y/o hipoxia (HP grupo 3) y la HPTEC (HP grupo 4).
2.1. Descartar hipertensión pulmonar grupo 2 y grupo 3
Se deberá completar el estudio inicial si es preciso con pruebas de función respiratoria, test de
difusión de CO, gasometría arterial y, en caso de precisarse, valorar tomografía axial computarizada de alta
resolución (TACAR) o polisomnografía (Tabla IV).
Tabla IV. Pruebas necesarias para establecer la etiología de la hipertensión pulmonar.
Dentro de este apartado, puede ser complejo el diagnóstico diferencial entre la HAP y la HP
asociada a insuficiencia cardiaca con función sistólica conservada (grupo 2). Existen varios parámetros que
nos pueden ayudar en este diagnóstico diferencial (Tabla V). Cuando a pesar de ello persisten dudas, está
indicado realizar un CCD. Durante el CCD no es infrecuente que casos de HP grupo 2 presenten una PCP <
15 mm Hg debido al tratamiento previo con diuréticos. En estos casos se realizará durante el procedimiento
un test de sobrecarga de volumen para desenmascarar si es una HP grupo 2, o bien, es una verdadera HAP.
Consiste en infundir 500 cc de suero salino fisiológico en 5-10 minutos.
Se considera diagnóstico de HP grupo 2 una PCP > 18 mm Hg sin síntomas o una PCP > 15 mm Hg
con síntomas. No obstante, este resultado no debe utilizarse en solitario para descartar HAP.
Tabla V. Factores que orientan la hipertensión pulmonar secundaria a cardiopatía izquierda.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [414]
[27] HIPERTENSIÓN PULMONAR
2.2. Descartar hipertensión pulmonar tromboembólica crónica (HP grupo 4)
Se realizará con una gammagrafía pulmonar de ventilación/perfusión, que permite un estudio
funcional de la circulación pulmonar. El angio-TAC pulmonar permite un estudio anatómico y no debe
utilizarse como alternativa diagnóstica, ya que puede no detectar casos de HPTEC. En caso de presentar
defectos segmentarios de perfusión sugerentes de HPTEC, se debe remitir a un centro experto para realizar
un estudio de hipercoagulabilidad, angio-TAC pulmonar, CCD y angiografía pulmonar que permitan
confirmar dicho diagnóstico y establecer la actitud terapéutica. Los defectos no segmentarios y dispersos
de la perfusión en la gammagrafía pueden aparecer en la HAP, en la EVOP y en la HP grupo 5.
2.3. Confirmar diagnóstico de la hipertensión arterial pulmonar
Una vez descartadas la HP grupo 2, 3 y 4, deberá realizarse un CCD, que es el examen de referencia
para confirmar el diagnóstico de HAP. El CCD está indicado en todos los pacientes con sospecha de HAP. En
caso de confirmarse, se debe completar el estudio etiológico de la HAP en un centro de referencia (Figura 2
y Tabla IV) para buscar las causas poco comunes de HAP. Hay que tener en cuenta que el diagnóstico de
HAPI es un diagnóstico de exclusión.
3. EVALUACIÓN HEMODINÁMICA DE LA HIPERTENSIÓN ARTERIAL PULMONAR
Se realiza mediante el CCD. Durante el procedimiento se registrarán las presiones pulmonares, las
presiones del VD y la AD, la PCP, el gasto cardiaco, la saturación de oxígeno en la arteria pulmonar y las
resistencias vasculares pulmonares.
También está indicado realizar un test de vasorreactividad pulmonar al diagnóstico en aquellos
pacientes con HAPI, HAPH e HP inducida por tóxicos. Se realizará con óxido nítrico (NO) inhalado, iloprost
inhalado, epoprostenol iv o adenosina iv. Una respuesta aguda positiva se define como la disminución de la
PAPm ≥ 10 mm Hg y una PAPm final ≤ 40 mm Hg sin disminución del gasto cardiaco.
Solo el 10% de los pacientes con HAPI son positivos, y de ellos únicamente el 50% responde a la
terapia con antagonistas del calcio a largo plazo. No se realizará el test ante sospecha de EVOP por el riesgo
de precipitar un edema agudo de pulmón.
Además, el CCD estará indicado repetirlo:
A los 6-9 meses si los parámetros hemodinámicos eran de mal pronóstico en el estudio previo o
para valorar la respuesta a calcioantagonistas en pacientes con test de vasorreactividad
pulmonar positivo.
En el seguimiento siempre que los parámetros no invasivos sean discordantes o aparezcan
datos de alarma clínica.
Antes de iniciar tratamientos con prostanoides o derivación a trasplante.
V. TRATAMIENTO DE LA HIPERTENSIÓN ARTERIAL PULMONAR
Inicialmente habrá que realizar una valoración de la gravedad y pronóstico. Para ello nos
basaremos en parámetros clínicos, pruebas de ejercicio, biomarcadores, así como datos ecocardiográficos y
hemodinámicos (Tabla VI).
Estos parámetros nos permitirán establecer el pronóstico, averiguar cuál es la respuesta a nuestro
tratamiento y saber si se deben hacer cambios en el tratamiento o no.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [415]
[27] HIPERTENSIÓN PULMONAR
El objetivo general del tratamiento es lograr un estadio de riesgo bajo; esto significa lograr que el
paciente se mantenga en la clase funcional de la Organización Mundial de la Salud II (OMS-II), siempre que
sea posible.
La estrategia actual se divide en tres pasos fundamentales: medidas generales, tratamiento de
apoyo y tratamiento específico.
Tabla VI. Parámetros pronósticos en hipertensión arterial pulmonar.
1. MEDIDAS GENERALES
Es importante educar a los pacientes en la práctica de ejercicio físico moderado y rehabilitación
física. Se debe recomendar evitar cirugías electivas por el riesgo aumentado de morbimortalidad; y en el
caso de intervención quirúrgica se prefiere la anestesia epidural a la general siempre que sea posible. Se
debe evitar la gestación ya que conlleva una elevada morbimortalidad materna, especialmente en el
periodo periparto. Asimismo, se debe vacunar de la gripe de forma anual y de la vacuna antineumocócica
cuando corresponda, por el mayor riesgo de infecciones en estos pacientes, especialmente de neumonías
(siendo estas responsables de hasta un 7% de la mortalidad). No hay que olvidar la importancia del apoyo
psicosocial en este tipo de enfermos.
2. TRATAMIENTO DE APOYO
2.1. Anticoagulación oral
Hay una alta prevalencia de lesiones trombóticas vasculares en los estudios post mortem de
pacientes con HAPI; también se han observado anomalías en las vías de la coagulación y fibrinólisis. Estos
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [416]
[27] HIPERTENSIÓN PULMONAR
hallazgos, junto con el aumento de factores de riesgo protrombóticos (ICC, inmovilidad…) son los
fundamentos principales de la anticoagulación oral en la HAP. La evidencia de la anticoagulación oral (en
estudios retrospectivos) se limita a HAPI, heredable y aquella secundaria a drogas/tóxicos (en nuestro
medio el más importante es el aceite de colza, puesto que se continúan diagnosticando casos de este
síndrome). En aquellos pacientes con prostaglandinas iv, debido al riesgo de trombosis del catéter para su
infusión, también se puede indicar si no hay contraindicación. Se desconoce el papel de los anticoagulantes
directos en la HAP. La ratio internacional normalizada (INR) más utilizada es entre 2-2,5.
2.2. Diuréticos
La disfunción del VD conlleva síntomas y signos de congestión sistémica (ascitis, edemas en
miembros inferiores, ingurgitación yugular, congestión hepática). Aunque no existen ensayos clínicos sobre
el uso de diuréticos en la HAP, la experiencia clínica muestra que esta terapia alivia los síntomas de
sobrecarga de fluidos, al disminuir la precarga del VD.
La elección y la dosis del diurético dependerá del médico de HAP, siempre con precaución para no
deplecionar en exceso el VD y evitar que caiga el gasto cardiaco; se debe considerar añadir antagonistas de
la aldosterona como la espironolactona, monitorizando la función renal y los electrolitos en plasma.
2.3. Oxigenoterapia
Aunque se ha demostrado que la administración de O2 reduce las RVP de pacientes con HAP, no
hay datos de ensayos clínicos aleatorizados que indiquen que una terapia de O2 a largo plazo sea
beneficiosa, por lo que las recomendaciones actuales se basan en la evidencia obtenida en pacientes con
enfermedad pulmonar obstructiva crónica (EPOC), aconsejándose oxigenoterapia domiciliaria en aquellos
pacientes con insuficiencia respiratoria basal (pO2 < 60 mm Hg). Se puede considerar el O2 ambulatorio si
hay evidencia de beneficio sintomático y desaturación corregible durante el ejercicio.
2.4. Anemia y perfil férrico
La ferropenia es común en pacientes con HP. Se asocia a la pérdida de capacidad funcional con el
ejercicio e incluso con mayor mortalidad, de forma independiente a la presencia o ausencia de anemia
asociada. Si existe, hay que buscar la causa de la misma y reponer el déficit de hierro, preferiblemente por
vía intravenosa (su absorción por vía oral puede ser menor).
3. TRATAMIENTO ESPECÍFICO
3.1. Antagonistas del calcio
Estará indicado realizar test agudo vasodilatador (test de vasorreactividad pulmonar) en el
momento del diagnóstico y en un centro de referencia en aquellos pacientes con HAPI, HAP heredada e
HAP secundaria a tóxicos (ver Apartado “Diagnóstico”). Los pacientes respondedores son candidatos a
recibir calcioantagonistas. Se eligen según la frecuencia cardiaca basal, siendo los más usados nifedipino,
diltiazem o amlodipino, especialmente los dos primeros, titulándose hasta alcanzar dosis máximas
toleradas. Los factores limitantes más frecuentes para no alcanzar esta dosis son la hipotensión y la
aparición de edema en miembros inferiores. No recibirán tratamiento con calcioantagonistas aquellos
pacientes con test vasodilatador negativo o que no hayan sido sometidos al test de vasorreactividad
pulmonar por los potenciales efectos adversos.
3.2. Inhibidores de la fosfodiesterasa 5 (IPDE5): sildenafilo, taladafilo.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [417]
[27] HIPERTENSIÓN PULMONAR
Son inhibidores de la enzima fosfodiesterasa 5, encargada de la degradación del guanosín
monofosfato cíclico (GMPc), favoreciendo así la vasodilatación pulmonar e inhibiendo la proliferación a
través de la vía óxido nítrico/GMPc.
Se administran por vía oral y su buena tolerancia favorece la adherencia a este tratamiento. En el
caso de angina, no se podría utilizar concomitantemente nitroglicerina u otro vasodilatador por su
potencial hipotensión arterial en su uso combinado.
Sildenafilo: la dosis aprobada es de 20 mg/8 h vía oral; su inconveniente es la escasa duración
del efecto a esta dosis, siendo necesarios ajustes ascendentes de la dosis hasta 40 y 80 mg/8 h
para mantener el mismo efecto. Sus efectos secundarios son leves-moderados, relacionados
con la vasodilatación (cefalea, flushing, epistaxis).
Taladafilo: se administra en dosis única diaria (40 mg/24 h); ha demostrado durabilidad en su
efecto y los efectos secundarios son similares a los de sildenafilo.
3.3. Estimuladores de la guanilato-ciclasa
Riociguat: mientras que los fármacos anteriores actúan inhibiendo la degradación de GMPc,
riociguat es un estimulador de la guanilato ciclasa, aumentando la síntesis del GMPc. Además,
posee efectos antiproliferativos y antirremodelados en estudios preclínicos. No se puede
combinar con los IPDE5, por alto riesgo de hipotensión secundaria. El efecto secundario más
grave descrito es el síncope.
3.4. Inhibidores de la endotelina-1: bosentan, ambrisentan, macitentan.
La activación del sistema de la endotelina ha sido demostrada tanto en plasma como en el lecho
pulmonar en los pacientes con HP.
Bosentan: es un fármaco de administración oral. Su principal efecto secundario (hasta en un
10% de los pacientes) es la hepatotoxicidad, que es dosis dependiente y reversible. Obliga a
control analítico hepático mensual.
Ambrisentan: es también un fármaco de administración oral; es menos hepatotóxico (0,8-3%),
siendo su principal efecto secundario la aparición de edemas periféricos.
Macicentan: no tiene efecto hepatotóxico; su principal efecto secundario es la aparición de
anemia.
3.5. Prostanoides: epoprostenol, iloprost, teprostinil, selexipag.
La prostaciclina es sintetizada fundamentalmente por las células endoteliales y tiene potentes
efectos vasodilatadores. Además, ejerce gran efecto antiagregante y antiproliferativo. Existe disregulación
en el sistema prostaciclina en pacientes con HP, de ahí que los prostanoides (análogos de la prostaciclina)
ejerzan efectos beneficiosos.
Epoprostenol: es el único fármaco que ha demostrado aumentar la supervivencia en la HAPI en
un estudio aleatorizado, manteniendo su eficacia en tratamientos a largo plazo de la HAPI,
HAPA y HPTEC no operable. Se administra por vía intravenosa con una vida media ultracorta (3-
5 minutos), lo que obliga a administrarlo en bomba de infusión continua. La dosis viene
determinada por la tolerancia del paciente debido a sus importantes efectos adversos.
La infusión no debe interrumpirse de forma brusca en ningún momento ya que se puede
producir una HP de rebote con deterioro sintomático e incluso la muerte; ante cualquier fallo
del catéter central o de la bomba de infusión, se puede continuar su administración intravenosa
por vía periférica de forma transitoria. Los efectos secundarios principales son la aparición de
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [418]
[27] HIPERTENSIÓN PULMONAR
cefalea, diarrea y flushing. Entre los efectos adversos que pueden aparecer se encuentran la
infección de la zona de inyección, obstrucción del catéter, fallo de la bomba de infusión e
incluso sepsis (ver Apartado VIII. “Situaciones especiales”).
Iloprost: administración inhalada, con la ventaja teórica de ser selectiva en la circulación
pulmonar y sus efectos adversos son mejor tolerados, si bien precisa ser inhalado 6-9 veces al
día. Sus efectos secundarios más frecuentes son el enrojecimiento y el dolor mandibular.
Teprostinil: existe en diferentes presentaciones: vía oral, intravenosa, inhalada y subcutánea (la
más usada). Ha demostrado un beneficio mayor en los pacientes más comprometidos y en los
que toleraban dosis más elevadas. Su principal limitación es el dolor local en el punto de
infusión subcutáneo. Tampoco debe ser suspendido bruscamente.
3.6. Terapia combinada
Se puede considerar ante una respuesta clínica inadecuada, usando incluso la triple terapia en
centros con experiencia. Es fundamental tener en cuenta las potenciales interacciones entre los fármacos
usados.
3.7. Atrioseptostomía con balón y/o trasplante pulmonar
De forma individualizada, estaría indicado en pacientes con respuesta clínica inadecuada a pesar de
la optimización en la estrategia médica utilizada.
En el seguimiento es importante guiarse por distintos parámetros pronósticos de cara a hacer
modificaciones en el tratamiento. El cateterismo cardiaco derecho debe realizarse siempre previo al inicio
de tratamiento y cuando exista deterioro clínico significativo a lo largo del seguimiento.
VI. PRONÓSTICO DE LA HIPERTENSIÓN ARTERIAL PULMONAR
Respecto a la HAPI, solo con el tratamiento convencional, la esperanza media de vida desde el
momento del diagnóstico era de 2,8 años. Los datos más recientes publicados del registro español de HAP
muestran que con el tratamiento específico de HAP, la supervivencia actual de la HAPI en nuestro país es
del 89% en el primer año, del 77% en el tercer año y del 68% en el quinto año.
Entre los parámetros que nos establecerán el pronóstico de nuestro paciente, se encuentran
aquellos ya descritos por orientar nuestra actitud terapéutica (Tabla VI). Otros parámetros clínicos de mal
pronóstico serán la edad (pacientes jóvenes < 3 años y > 65 años), el sexo masculino, la presencia de
comorbilidades, la causa de la HAP (esclerodermia y portopulmonar), formas rápidamente progresivas,
datos clínicos de congestión derecha o el bajo gasto, y la historia de hemoptisis, síncope o fibrilación
auricular (FA)/flutter auricular.
VII. CARACTERÍSTICAS DE LOS OTROS TIPOS DE HIPERTENSIÓN
PULMONAR
1. HIPERTENSIÓN ARTERIAL PULMONAR – GRUPO 1
La más frecuente de este grupo es la HAPI, cuyo diagnóstico es de exclusión.
1.1. Hipertensión arterial pulmonar asociada a cardiopatías congénitas
Se produce por shunt izquierda – derecha e hiperaflujo y daño endotelial sobre el lecho pulmonar.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [419]
[27] HIPERTENSIÓN PULMONAR
El tratamiento más eficaz es el cierre del shunt cuando es posible, valorando varios parámetros
entre los que destacan que las RVP aún no estén elevadas (RVP < 4 UW/m2, individualizar si RVP 4–8
UW/m2 valorando reversibilidad con test agudo vasodilatador o cierre temporal del shunt con balón).
En casos avanzados, puede darse el síndrome de Eisenmenger, que consiste en una PAP mayor que
la PA sistémica, siendo contraindicación para cierre del shunt.
1.2. Hipertensión arterial pulmonar asociada a enfermedades del tejido conectivo
Puede encontrarse en lupus eritematoso sistémico, enfermedad mixta del tejido conectivo, artritis
reumatoide, dermatomiositis, síndrome de Sjögren y, especialmente, en la esclerosis sistémica. En esta
última entidad está indicado realizar un screening anual con ETT, difusión de CO y biomarcadores.
1.3. Hipertensión portopulmonar
La hipertensión portopulmonar (HPP) consiste en el desarrollo de HP en aquellos pacientes con
hipertensión portal, independientemente de si tienen o no cirrosis. En los candidatos a trasplante hepático
está indicado realizar un screening con ETT anual y derivar a un centro de referencia ante una PAP sistólica
estimada > 50 mm Hg o disfunción del VD. No debe confundirse con el síndrome hepatopulmonar que
consiste en vasodilatación intensa del lecho pulmonar en pacientes con hepatopatía crónica.
1.4. Enfermedad venooclusiva pulmonar y hemangiomatosis capilar pulmonar
Se cree que son dos entidades relacionadas. La hemangiomatosis capilar pulmonar (HCP) se
sospecha que es una reacción angioproliferativa ante la obstrucción poscapilar en la EVOP. A diferencia de
la HAPI, tiene mayor incidencia en varones y su pronóstico es peor.
Se debe sospechar ante una clínica de disnea rápidamente progresiva, tos irritativa, acropaquias y
crepitantes bibasales (inusual en otras formas de HAP).
Además, son muy sugerentes una alteración de la difusión de CO y/o hipoxemia demasiado severas
para el grado de HP en el CCD, así como con la presencia de un patrón reticulonodular en la radiografía de
tórax. En estos casos debe completarse el estudio con un TACAR. El lavado broncoalveolar puede ayudar, y
solo en casos excepcionales se planteará una biopsia pulmonar por su riesgo. Por su posible origen familiar,
se debe hacer estudio del gen EIF2AK4, que es diagnóstico si tiene mutación bialélica. En nuestro país,
existen varios casos familiares en pacientes de etnia gitana, en quienes debuta antes de los 30 años con
una difusión de CO muy baja.
El tratamiento vasodilatador pulmonar debe emplearse con mucho cuidado por el riesgo de inducir
edema agudo de pulmón. El único tratamiento curativo es el trasplante de pulmón, que dada la rápida
evolución de la enfermedad, en ocasiones precisa de membrana de oxigenación extracorpórea (ECMO)
como terapia puente. Fuera de esta opción, la supervivencia es del 30% superado el primer año.
2. HIPERTENSIÓN PULMONAR SECUNDARIA A CARDIOPATÍA IZQUIERDA
Existen una serie de factores que nos van a orientar a esta causa (Tabla V). El tratamiento debe ser
sobre la cardiopatía responsable, ya que no existe evidencia de beneficio con el tratamiento para la HAP.
Para optimizar el tratamiento, si hay dudas sobre el origen de la HP o previo al trasplante, se indicaría un
CCD.
3. HIPERTENSIÓN PULMONAR SECUNDARIA A ENFERMEDAD PULMONAR Y/O HIPOXIA
Se asocia especialmente a EPOC y enfermedades pulmonares intersticiales. El CCD no está indicado
de rutina. El tratamiento es el de la enfermedad pulmonar, incluyendo oxigenoterapia domiciliaria cuando
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [420]
[27] HIPERTENSIÓN PULMONAR
está indicada. El tratamiento para la HAP tampoco está recomendado en ausencia de otra causa
concomitante.
4. HIPERTENSIÓN PULMONAR TROMBOEMBÓLICA CRÓNICA
Ante datos sugerentes de esta entidad, se debe instaurar tratamiento anticoagulante durante 3
meses y luego reevaluar para distinguir de aquellos casos de TEP subagudo. En aquellos casos con HPTEC
está indicada la anticoagulación de por vida, incluso después de la cirugía. Reseñar que alrededor del 50%
de los pacientes con HPTEC no tiene una historia de TEP agudo previo.
El tratamiento de elección es quirúrgico; la HPTEC es la única HP que tiene un tratamiento curativo
mediante endarterectomía pulmonar. Si el paciente no es operable, se podría valorar la realización de
angioplastia con balón de arterias pulmonares y/o tratamiento médico. Por este motivo, es importante una
vez diagnosticados estos casos, remitirlos a un centro con experiencia para decidir cuál es el mejor manejo
por un equipo multidisciplinar.
Dentro del tratamiento médico, se recomienda el empleo de riociguat en aquellos pacientes
sintomáticos con HPTEC persistente o recurrente tras cirugía, o en aquellos no operables una vez valorados
por un equipo experto en HPTEC.
No se debe desestimar a ningún paciente con HPTEC para la cirugía sin antes haber sido valorado en
un centro de referencia.
VIII. SITUACIONES ESPECIALES EN HIPERTENSIÓN ARTERIAL PULMONAR
SEVERA EN URGENCIAS
1. OBSTRUCCIÓN, OCLUSIÓN O INFECCIÓN DEL CATÉTER DE INFUSIÓN DE PROSTAGLANDINAS
Para este tipo de medicación (epoprostenol y treprostinil, los únicos aprobados para infusión iv) se
usan catéteres venosos centrales permanentes, siendo el más usado en nuestro centro el catéter Hickman,
para su infusión continua; habitualmente se suele realizar el acceso a través de la vena subclavia o yugular
derechas. Es importante garantizar que no se suspenda la infusión de estos fármacos ya que, por su corta
vida media, se puede producir un efecto rebote que genere un rápido aumento de las presiones
pulmonares y fracaso agudo del VD.
Entre las complicaciones más frecuentes del empleo de estos catéteres se encuentran la infección,
la obstrucción y la trombosis del catéter. En estos casos, es prioritario canalizar una vía periférica y
comenzar su administración por esta vía, bien con la misma bomba de infusión o bien con una bomba
hospitalaria. Para ello, es recomendable que los pacientes con prostaglandinas intravenosas siempre lleven
consigo un informe actualizado con la dosis para bomba de infusión continua, la dosis para bomba de
infusión hospitalaria y el peso con el que se ha calculado.
Infección del catéter venoso central (CVC): es una complicación bien documentada y a veces
mortal. Existen varios tipos de infección: local (limitada a la piel y tejidos blandos/ infección en el recorrido
tunelizado hasta la vena), bacteriemia asociada a catéter y sepsis asociada a catéter. Siempre debe
sospecharse infección del catéter en pacientes portadores de CVC en tratamiento con prostanoides
sistémicos con fiebre, sin otro foco, a pesar de que no existan signos externos evidentes de infección.
En el caso de sospecha deben extraer hemocultivos x2 del catéter central, interrumpir la infusión
del fármaco e iniciarla a través de acceso venoso periférico (AVP) e iniciar antibioterapia empírica con
vancomicina (1 g cada 12 h) y meropenem (1 g cada 8 h) hasta ajuste según germen y antibiograma; se
deberá extraer el CVC y enviar para cultivo de la punta a microbiología. Posteriormente, se realizarán
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [421]
[27] HIPERTENSIÓN PULMONAR
hemocultivos seriados hasta confirmar la eliminación de la infección y se valorará la recanalización de un
catéter cuando se confirme la eliminación de la misma, dependiendo del germen implicado, y siempre
habiendo pasado un mínimo de 4 días desde el inicio de la terapia antibiótica.
Oclusión del CVC (aposición de la punta del catéter contra la pared del vaso): se sospechará cuando
la bomba alerte presión elevada, sin existir oclusión visible en la alargadera ni en el catéter. Se procederá a
cambiar al paciente de posición y a realizar maniobras de valsalva.
Trombosis del CVC: se sospechará cuando el brazo del catéter esté inflamado.
2. TAQUIARRITMIAS SUPRAVENTRICULARES
Las arritmias ventriculares sostenidas son muy infrecuentes. Sin embargo, las taquiarritmias
supraventriculares (TSV) son un problema creciente, con una incidencia entre el 6-8%. La TSV más
frecuente en estos pacientes es la FA seguida del flutter auricular y la taquicardia por reentrada intranodal
(TRIN).
Debido a que pueden provocar un grave deterioro hemodinámico, se recomienda una estrategia de
control de ritmo con fármacos antiarrítmicos de mantenimiento. Además, se deben evitar aquellos
fármacos frenadores o antiarrítmicos con efecto inotropo negativo. La aparición de TSV es un marcador de
mal pronóstico en estos pacientes.
3. CIRUGÍA NO CARDIACA
Los pacientes con HAP son un grupo de alto riesgo perioperatorio, aunque en la actualidad la
mortalidad parece ser menor, principalmente en cirugía programada que es del 3,7%, que asciende al 15%
para intervenciones urgentes. Por ello se recomienda que la cirugía programada se realice en un centro de
referencia de HAP. Los procedimientos mal tolerados por el paciente con HAP serán la cirugía torácica,
ortopédica, laparoscópica, procedimientos urgentes y los asociados a rápidas pérdidas sanguíneas o larga
duración.
Se deberá garantizar que se mantiene la medicación para HAP en el peri y postoperatorio. Para ello,
las infusiones subcutáneas se cambiarán a infusión intravenosa de epoprostenol o treprostinil por su mejor
absorción garantizada y, en el caso de iloprost inhalado, se deberá disponer de nebulizadores aptos.
Durante el procedimiento se debe evitar el óxido nitroso, el desfluorano y la ketamina porque aumentan
las RVP y se deben adaptar los parámetros ventilatorios a la función del VD, utilizando altas
concentraciones de O2 para promover la vasodilatación pulmonar.
IX. UNIDADES ESPECIALIZADAS MULTIDISCIPLINARES Y CENTROS DE
REFERENCIA
Debido a que la HAP es una entidad poco frecuente, se ha comprobado que los centros con mayor
volumen de pacientes tienden a presentar mejores resultados. Por ello se constituyen centros de referencia
a dos niveles, tanto regional o autonómico como a nivel nacional. Se establecen unos criterios para remitir
a estos centros (Tabla VII).
El Hospital Universitario 12 de Octubre de Madrid cuenta con una Unidad de referencia nacional en
Hipertensión Pulmonar, con un equipo multidisciplinar que engloba a varias especialidades:
(http://www.unidadhp12.es).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [422]
[27] HIPERTENSIÓN PULMONAR
Tabla VII. Indicaciones para la derivación a la Unidad de Referencia en Hipertensión Pulmonar a nivel regional.
BIBLIOGRAFÍA
Escribano Subías P, Barbera Mir JA, Suberviola V. Evaluación diagnóstica y pronóstica actual de la
hipertensión pulmonar. Rev Esp Cardiol. 2010;63:583-96.
Escribano Subías P, Gómez Sánchez MA. Protocolos de Actuación en Hipertensión Pulmonar. Unidad
Multidisciplinar de Hipertensión Pulmonar. Hospital 12 de Octubre. Editorial EDIMSA. 2014.
Galiè N, Humbert M, Vachiery JL, Gibbs S, Lang I, Torbicki A, et al. 2015 ESC/ERS Guidelines for the
diagnosis and treatment of pulmonary hypertension. Eur Heart J. 2015 Aug 29. [Epub ahead of print].
McLaughlin VV, Archer SL, Badesch DB, Barst RJ, Farber HW, Lindner JR, et al. ACCF/AHA 2009 expert
consensus document on pulmonary hypertension. J Am Coll Cardiol. 2009;53(17):1573-619.
Simonneau G, Gatzoulis MA, Adatia I, Celermajer D, Denton C, Ghofrani A, et al. Updated clinical
classification of pulmonary hypertension. J Am Coll Cardiol. 2013;24;62(25 Suppl):D34-41.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [423]
[28] TOS CRÓNICA Y HEMOPTISIS
28.Tos crónica y hemoptisis
Annette Zevallos Villegas.
Neumología
Raúl Martínez Porqueras.
Medicina Interna
Asesor: Ricardo García Luján. Médico Adjunto de Neumología
I. TOS CRÓNICA
1. DEFINICIÓN
La tos es un mecanismo de defensa que puede ser, en condiciones patológicas, indicativo de
enfermedades importantes. Desde un punto de vista clínico, se debe diferenciar entre:
Tos aguda: duración máxima de hasta 4 semanas, relacionada habitualmente con procesos
infecciosos de las vías aéreas superiores o traqueobronquitis. La tos aguda puede persistir y
convertirse en subaguda o crónica.
Tos subaguda: aquella que dura entre 4 y 8 semanas.
Tos crónica: aquella que persiste más de 8 semanas. En este caso, hay que diferenciar entre
específica, si existe una causa conocida, o inespecífica, aquella que no está ligada a un proceso
identificado. La prevalencia de tos crónica es variable, oscila entre 3,3-12%, y tiene cierta
asociación con el hábito tabáquico (multiplica por tres su riesgo) y con la contaminación
ambiental.
2. ETIOLOGÍA
Las causas de la tos crónica son muy variadas, como se recoge en tabla I, y dentro de estas es
importante la identificación de signos de alarma (Tabla II).
Tabla I. Causas de la tos crónica.
Las causas más frecuentes de tos crónica en la población general son las siguientes:
Síndrome de goteo nasal posterior (8-87%): incluye los procesos inflamatorios del área
rinosinusal (rinitis, sinusitis y poliposis). Es la causa más frecuente de tos, sola o asociada a
otras causas. Los síntomas habituales son carraspeo, sensación de ocupación o cuerpo extraño
en la faringe, obstrucción y picor nasal, estornudos, hidrorrinorrea, alteraciones de la olfacción
y voz nasal.
Asma e hiperreactividad bronquial (20-33%). Ver Capítulo 29. “Asma y y enfermedad
obstructiva crónica”.
Reflujo gastroesofágico (RGE) (10-21%).
En más del 25% de los casos la causa de la tos crónica no es única, sino multifactorial.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [424]
[28] TOS CRÓNICA Y HEMOPTISIS
Tabla II. Síntomas de alarma.
3. DIAGNÓSTICO
El protocolo de diagnóstico secuencial de la tos crónica se expone en la figura 1, y consta de tres
fases:
Figura 1. Protocolo diagnóstico secuencial de la tos crónica.
FASE I: DIAGNÓSTICO DE CAUSAS FRECUENTES CON EXPLORACIONES CONVENCIONALES
Se debe plantear siempre en una primera valoración, y normalmente debe realizarse en Centros de
Atención Primaria. Las fases II y III deberían reservarse al ámbito hospitalario.
Anamnesis y exploración física: la historia clínica detallada es el principal método diagnóstico,
y se debe realizar un buen diagnóstico diferencial, sobre todo de las causas más frecuentes
(Tabla III). Hay que recoger la historia de tabaquismo y la toma de fármacos causantes de tos
(nitrofurantoína, colirios, gotas nasales) y en particular de inhibidores de la enzima de
conversión de la angiotensina (IECA), así como los síntomas sistémicos. Si la anamnesis y la
exploración física inicial no orientan a un diagnóstico concreto, y el paciente es fumador o está
recibiendo IECA, se le debe aconsejar que abandone el hábito tabáquico y sustituya los IECA. Si
transcurridas 4 semanas persiste la tos, se realizarán los estudios referidos a continuación.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [425]
[28] TOS CRÓNICA Y HEMOPTISIS
Radiografía de tórax posteroanterior (PA) y lateral: (solo muestra patología en un 4-7% de los
casos) y de los senos paranasales.
Estudios simples de función pulmonar: espirometría con prueba broncodilatadora o
variabilidad diaria de flujo espiratorio máximo.
Atención a síntomas acompañantes de alerta (Tabla II): como hemoptisis (tuberculosis,
carcinoma), síndrome constitucional (carcinoma broncogénico, tuberculosis), expectoración
abundante o purulenta y fiebre (neumonía), disnea súbita (tromboembolismo pulmonar,
neumotórax), paciente inmunocomprometido. En presencia de estos síntomas, se deberían
modificar los pasos del algoritmo diagnóstico realizando las pruebas oportunas para confirmar
la sospecha. Si en esta primera fase la clínica, la exploración física y la radiografía orientan a un
diagnóstico, se puede realizar tratamiento empírico antes de pasar a la siguiente fase. Si no se
realiza el diagnóstico con dichas pruebas, o cuando a pesar de tener un diagnóstico la tos
persiste tras el tratamiento inicial, se debe pasar a la fase II.
Tabla III. Diagnóstico diferencial (basado en la anamnesis) de las tres principales causas de tos crónica.
FASE II: DIAGNÓSTICO DE CAUSAS FRECUENTES CON EXPLORACIONES ESPECIALES
Se aconseja iniciar el estudio con una valoración otorrinolaringológica especializada: realizar
una rinoscopia anterior simple, una radiografía de senos en cuatro proyecciones (valor
predictivo positivo 57-81%; valor predictivo negativo 95-100% para el diagnóstico de sinusitis).
Se debe plantear la realización de una tomografía computarizada (TC) de senos paranasales
(mayor sensibilidad) en casos más concretos ante la posibilidad de sinusitis silente.
Espirometría y prueba broncodilatadora en caso de sospecha de asma. También se puede
realizar la determinación de óxido nítrico en aire espirado (FENO) o pruebas de provocación
bronquial con metacolina o histamina ante la posibilidad de asma o bronquitis eosinófila (un
resultado negativo permite descartar asma; VPP 60-82%).
Realizar una pHmetría de 24 horas en caso de sospecha de RGE (prueba de mayor rendimiento
diagnóstico). La esofagoscopia identifica la esofagitis y sus complicaciones (es clínicamente muy
rentable si el paciente presenta síntomas típicos).
Si tras la realización de dichas pruebas no se obtiene diagnóstico, se debe pensar en un
mecanismo mixto de tos (el 18-62% de los pacientes presentan más de una causa
concomitante) o tos postinfecciosa (puede persistir hasta meses después, aunque lo normal es
la resolución en unas 3 semanas).
FASE III: DIAGNÓSTICO DE CAUSAS INFRECUENTES CON EXPLORACIONES ESPECIALES
Se deben realizar pruebas como TC de tórax o fibrobroncoscopia con el fin de detectar la presencia
de tumores, malformaciones, inhalación de cuerpo extraño, bronquiectasias o enfermedad intersticial.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [426]
[28] TOS CRÓNICA Y HEMOPTISIS
El ecocardiograma detecta malformaciones cardiacas o de los grandes vasos. Se debe valorar la
posibilidad de tos psicógena si el resto de las pruebas son normales.
Es importante destacar que el diagnóstico definitivo de la causa de la tos se establecerá cuando su
tratamiento conlleve la desaparición o una importante mejoría de esta.
Si a pesar de seguir el algoritmo de la figura 1, y haber realizado un tratamiento adecuado, persiste
la tos, se debe pensar en las siguientes causas: baja adhesión al tratamiento, más de una causa productora
de tos que no está siendo tratada, incremento de la tos por fármacos inhalados, evaluación de la eficacia de
tratamiento en un espacio de tiempo corto, tratamiento insuficiente o error en el diagnóstico y manejo por
parte del terapeuta.
4. ABORDAJE TERAPÉUTICO
1. TRATAMIENTO ETIOLÓGICO
Es el factor más importante. Cuando se sospeche síndrome tusígeno por afectación de la vía aérea
superior (goteo nasal posterior) o enfermedad por RGE (ERGE) se debería intentar tratamiento empírico, así
como en la bronquitis eosinofílica previa evaluación de la eosinofilia en el esputo y/o FENO. También se
podrá valorar el inicio con tratamiento empírico en el asma o idealmente evaluar la espirometría, la
reversibilidad broncodilatadora o la prueba de provocación bronquial.
1.1. ERGE
Cambio del estilo de vida (pérdida de peso, reducción de la ingesta de grasas, medidas posturales,
elevación del cabecero de la cama, evitar la cafeína, el tabaco, el alcohol, etc.). Fármacos antisecretores: los
inhibidores de la bomba de protones (por ejemplo, omeprazol 40 mg/24 h, pudiendo llegar hasta 60-80
mg/día), ya que presentan una recomendación consistente, con una evidencia moderada, en comparación
con los anti-H2 (evidencia baja). La mejoría de la tos puede precisar un tratamiento prolongado de hasta 6
meses. Valorar la cirugía antirreflujo en casos refractarios al tratamiento habitual.
1.2. Goteo nasal posterior
El tratamiento de la rinitis postinfecciosa y perenne se fundamenta en el uso de antihistamínicos
(por ejemplo, dexclorfeniramina 2 mg/4-6 h; cetirizina 10 mg/24 h, menos potente pero también menos
sedante) asociados o no a vasoconstrictores (pseudoefedrina 60 mg/12 h por vía oral) que hay que valorar
por su riesgo cardiovascular. En la rinitis moderada o alérgica, se puede asociar tratamiento con esteroides
o cromonas intranasales (por ejemplo, budesonida 100 μg/puls. inhalado 2 veces en cada fosa nasal por la
mañana; cromoglicato disódico 4% inhalado 3-4 veces/día en cada fosa nasal). El uso de anticolinérgicos,
vasoconstrictores, esteroides orales (prednisona 30 mg/24 h) se reservan para casos de rinitis grave o
resistente, incluyendo las vasomotoras.
1.3. Asma y enfermedad pulmonar obstructiva crónica (EPOC)
Ver Capítulo 29. “Asma y y enfermedad obstructiva crónica”.
1.4. Bronquitis eosinofílica
Es un hecho característico (pero no exclusivo) del asma. Se realiza diagnóstico definitivo de
bronquitis eosinofílica no asmática ante un cuadro clínico compatible, ausencia de hiperreactividad
bronquial y una cifra de eosinófilos superior al 3% en el esputo. El tratamiento inicial se realiza con
esteroides inhalados, obteniendo de forma general buena respuesta. De no ser así, se planteará
tratamiento con esteroides orales (prednisona 1 mg/kg/día al inicio, con reducción progresiva hasta cumplir
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [427]
[28] TOS CRÓNICA Y HEMOPTISIS
un total de 4 semanas de tratamiento). El paciente con episodios recurrentes de bronquitis eosinofílica no
asmática tiene mayor riesgo de desarrollar asma u obstrucción crónica al flujo aéreo.
2. TRATAMIENTO SINTOMÁTICO
El tratamiento sintomático se plantea en pocas ocasiones, dado que la posibilidad de determinar la
causa es muy alta y el tratamiento específico es eficaz en el 84-98% de los casos.
Por lo tanto, estaría indicado en los casos en los que la causa no es conocida, el tratamiento
específico no es posible y la tos genera gran malestar para el paciente o tiene riesgo potencial de
complicaciones. Los fármacos opiáceos son los más eficaces (actúan en el centro de la tos, en el bulbo
raquídeo), destacando entre ellos la codeína, en dosis de 15-30 mg/4-6 h por vía oral. El dextrometorfano
(15 mg/6-8 h) también actúa al mismo nivel, pero no es narcótico.
Otros fármacos de elección no opiáceos son: cloperastina, glaucina, viminol, difenhidramina (25-50
mg/4-6 h; antihistamínico con acción anticolinérgica y sedante) y levodropropizina (100 mg/6 h; acción
periférica y alivio a corto plazo), que han demostrado su eficacia en ensayos controlados. La lidocaína por
vía tópica suprime la tos, alterando la sensibilidad de los receptores.
Hay que recordar que el uso de la gabapentina en los casos refractarios ha demostrado una
respuesta positiva en aproximadamente el 60% de los pacientes, y es una recomendación consistente con
evidencia moderada de la misma. Otros fármacos de similares características, sin tanta evidencia, son la
pregabalina, la amitriptilina y el baclofeno.
II. HEMOPTISIS
1. DEFINICIÓN Y CONCEPTO
Se denomina hemoptisis a la expulsión de sangre por la boca mediante la tos y que, por tanto,
procede del árbol traqueobronquial. La definición incluye desde la simple tinción del esputo con estrías de
sangre (denominado esputo hemoptoico), hasta la expectoración de sangre fresca en cantidades masivas.
El concepto actual de la hemoptisis amenazante se define por el riesgo que para la vida del
paciente representa un determinado volumen de hemoptisis, en función de su capacidad funcional
cardiorrespiratoria. Los factores que determinan el carácter amenazante de una hemoptisis son:
Volumen total de sangrado: aunque no hay consenso acerca del volumen o el periodo de
tiempo, en general se establece como un volumen total > 600 ml en 24-48 horas.
Velocidad del sangrado: se considera cuando es mayor de 150 ml/hora.
Capacidad funcional respiratoria previa del paciente: determina la dificultad de expectoración
de la sangre presente en el árbol traqueobronquial.
2. ETIOLOGÍA
Las causas de hemoptisis son muy variadas. En España, las más frecuentes son neoplasias (28%),
bronquitis crónica (19,8%), bronquiectasias (14,5%) y neumonías o abscesos pulmonares (11,5%). En el caso
de hemoptisis amenazante, las principales causas a nivel mundial son las bronquiectasias, tuberculosis,
micetomas, neumonía necrotizante y carcinoma broncogénico.
Hay que considerar que hasta un 30% de los pacientes con hemoptisis no tienen causa identificada,
después de un protocolo diagnóstico adecuado, y se clasifican como hemoptisis idiopática o criptogénica.
En la tabla IV se muestran las principales causas de hemoptisis según el grupo etiológico.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [428]
[28] TOS CRÓNICA Y HEMOPTISIS
Tabla IV. Causas de hemoptisis.
3. DIAGNÓSTICO
1. CONFIRMACIÓN DE LA HEMOPTISIS
En primer lugar, hay que distinguir entre la hemoptisis y el sangrado originado en el tracto
gastrointestinal (hematemesis) o en el área nasofaríngea. En este sentido, las características diferenciales
se recogen en la tabla V. A pesar de estos datos, en ocasiones es difícil determinar el origen del sangrado, y
habrá que considerar la valoración por el especialista de otorrinolaringología y/o realizar un lavado por
sonda nasogástrica para valorar el posible origen del sangrado.
Tabla V. Diagnóstico diferencial entre hemoptisis y hematemesis.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [429]
[28] TOS CRÓNICA Y HEMOPTISIS
2. VALORACIÓN DE LA GRAVEDAD
Como se recoge en la definición, esta se establece según el volumen, la velocidad del sangrado, la
repercusión hemodinámica y la repercusión respiratoria. Lo principal es distinguir entre hemoptisis leve (<
30 ml/día, un esputo hemoptoico equivale a 5 ml), moderada (30-150 ml/día) y amenazante (con los
criterios antes citados), ya que ello determinará la actuación posterior. Solo cuando el paciente con
hemoptisis amenazante llega a la evaluación inicial sin estar sangrando activamente, será aceptable indicar
las medidas diagnósticas que se citan a continuación.
3. APROXIMACIÓN DIAGNÓSTICA INICIAL
3.1. Historia clínica
Deben recogerse una serie de variables que incluyan edad, hábito tabáquico, antecedentes de
patología respiratoria previa (bronquiectasias, EPOC, secuelas de tuberculosis), asociación con síntomas de
bronquitis aguda o exacerbación de bronquitis crónica, antecedentes de enfermedad sistémica (es
importante valorar si el paciente está inmunodeprimido, pues aumenta el riesgo de tuberculosis y
neoplasias) o enfermedad renal (enfermedad de Goodpasture, granulomatosis de Wegener, etc.),
antecedente de traumatismo, atragantamiento (cuerpo extraño) e historia farmacológica.
Hay una serie de factores que incrementan el riesgo de malignidad como causa de la hemoptisis:
edad > 40 años, tabaquismo con índice acumulado mayor de 30 años-paquete y duración de la hemoptisis
mayor de 1 semana o de 30 ml al día.
Tabla VI. Pruebas complementarias iniciales.
3.2. Exploración física
Hay que buscar hallazgos que orienten hacia alguna enfermedad de base (telangiectasias, signos de
trombosis venosa profunda [TVP], soplo cardiaco, signos de insuficiencia cardiaca, etc.).
3.3. Pruebas complementarias iniciales
Se detallan en la tabla VI.
En el caso de que el cuadro clínico no sugiera la posibilidad de un carcinoma broncogénico (Rx de
tórax normal, menor de 40 años, paciente no fumador y hemoptisis de menos de una semana de duración),
o si los datos obtenidos sugieren bronquitis aguda (Figura 2), no serían necesarias pruebas adicionales.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [430]
[28] TOS CRÓNICA Y HEMOPTISIS
Figura 2. Manejo de la hemoptisis leve y moderada.
4. PRUEBAS DIAGNÓSTICAS PARA DETERMINAR ORIGEN Y LOCALIZACIÓN DE LA HEMOPTISIS
4.1. Tomografía computarizada de tórax
Sirve para la detección de lesiones no visibles en la radiografía. Esta técnica es de elección en
pacientes con bajo riesgo de tumor o bronquitis crónica, pero con historia o radiografía sugerente de
bronquiectasias, malformación arteriovenosa, aspergiloma, etc. La prioridad para la realización de esta
prueba la determinará la sospecha clínica y la repercusión pronóstica que de la sospecha clínica se derive.
En el caso del estudio de hemoptisis es preferible la realización de una angio-TC de tórax, ya que,
además de la valoración del parénquima pulmonar, permite detectar los aportes arteriales sistémicos
bronquiales y no bronquiales, así como los orígenes anómalos de los mismos.
4.2. Broncoscopia
Es útil para la localización del punto de sangrado y la visualización de lesiones endobronquiales que
puedan ser la causa de este. Debe realizarse de forma urgente en los casos de hemoptisis amenazante para
la localización del sangrado y el tratamiento posterior, y de forma programada en pacientes que tengan
factores de riesgo para carcinoma broncogénico. En la hemoptisis con riesgo vital, la broncoscopia de forma
precoz está dirigida únicamente a la aspiración del material hemático con el propósito de conseguir una
adecuada ventilación o con el objetivo de proceder a la intubación orotraqueal (IOT) selectiva.
4. TRATAMIENTO
CRITERIOS DE INGRESO SEGÚN LA GRAVEDAD
Criterios de observación: el paciente con hemoptisis debe ser monitorizado clínicamente y, si
no cumple criterios de ingreso, se remitirá a la consulta externa de Neumología para su estudio.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [431]
[28] TOS CRÓNICA Y HEMOPTISIS
El tiempo de observación dependerá de la cuantía de la hemoptisis y el riesgo de hemoptisis
amenazante según su etiología, siendo recomendable de forma general un periodo de 12-24
horas.
Criterios de ingreso en planta: debe realizarse ingreso hospitalario en todos los casos de
hemoptisis persistente de más de 12-24 horas de observación o ante la sospecha por las
pruebas diagnósticas iniciales de patología potencialmente grave subyacente.
Criterios de ingreso en la Unidad de Cuidados Intensivos (UCI): deberían ingresar en esta
unidad todos los casos de hemoptisis amenazante para una correcta monitorización
respiratoria y hemodinámica y un manejo terapéutico inicial adecuado.
1. HEMOPTISIS LEVE-MODERADA
Se realizará tratamiento etiológico.
1.1. Medidas generales
Control de las constantes, dieta absoluta mientras dura la observación clínica y cuantificación del
volumen de hemorragia. El paciente debe permanecer en reposo en cama y en posición de decúbito lateral
ipsilateral del lado del sangrado si se sospecha el origen en función de la historia clínica o los hallazgos
radiológicos.
1.2. Antitusígenos
Debe valorarse su indicación según la relación riesgo-beneficio, ya que la tos es el principal factor
que perpetúa la hemoptisis. Su uso solo está contraindicado en pacientes con EPOC severa, pues puede
provocar un efecto depresor del centro respiratorio con mayor riesgo de hipoventilación. Suele indicarse
codeína 30 mg/6-8 h. Es recomendable la administración conjunta de laxantes para evitar el estreñimiento
secundario a estos fármacos.
1.3. Antibioterapia
Si se sospecha infección respiratoria como desencadenante, se iniciará tratamiento empírico con
amoxicilina/clavulánico 875/125 mg/8 h, levofloxacino 500 mg/24 h o moxifloxacino 400 mg/24 h durante 7
días. Si existe sospecha de tuberculosis, deberían evitarse las quinolonas, pues son fármacos de segunda
línea para esta patología y existe la posibilidad de desarrollar resistencias en caso de monoterapia.
1.4. Transfusión de hemoderivados
En caso de inestabilidad hemodinámica y según el grado de anemización, aunque es excepcional
que en casos de hemoptisis leve o moderada sea necesaria.
2. HEMOPTISIS AMENAZANTE
Es una situación urgente que requiere una evaluación y tratamiento precoces con ingreso en la UCI
(Figura 3). Además de seguir las normas generales de los casos de hemoptisis leve o moderada, en esta
circunstancia es fundamental cumplimentar las siguientes medidas:
2.1. Vía venosa
Debe disponerse de dos accesos venosos periféricos para la administración rápida de líquidos o
hemoderivados en caso de que sean necesarios.
2.2. Valoración de la permeabilidad de la vía aérea
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [432]
[28] TOS CRÓNICA Y HEMOPTISIS
Debe haber disponibilidad inmediata de tubo endotraqueal, equipo de aspiración y medicación
adecuada para la intubación. Si se constata insuficiencia respiratoria severa o incapacidad del paciente para
evacuar la hemorragia mediante la tos, debe procederse a intubación orotraqueal y ventilación mecánica.
Figura 3. Manejo de la hemoptisis amenazante.
2.3. Protección del pulmón no sangrante
En caso de que exista la sospecha de lateralidad del sangrado por pruebas de imagen o este se
establezca mediante una broncoscopia flexible, debería realizarse intubación orotraqueal del pulmón
contralateral al del sangrado, ventilándolo de manera selectiva. En estos casos, el fibrobroncoscopio puede
usarse de guía para introducir el tubo endotraqueal.
2.4. Técnicas endoscópicas
En la mayoría de las ocasiones se usará broncoscopia flexible, reservándose el broncoscopio rígido
para situaciones de riesgo inminente de asfixia, dado que tiene una mayor capacidad de aspiración. Se
puede añadir a la aspiración con broncoscopio el lavado con suero fisiológico frío ± adrenalina (1:10.000), el
bloqueo de la luz bronquial mediante un catéter hinchable tipo Fogarty, la colocación de un tubo de doble
luz o la instilación de sustancias procoagulantes (vasopresina, fibrinógeno, ácido tranexámico, etc.).
2.5. Angiografía con embolización
Se considera el tratamiento sintomático de elección en estos casos. Tiene una tasa inicial de éxito
superior al 80%, tanto en el control inmediato como en el tardío de la hemoptisis amenazante o
recidivante. Su tasa de recurrencias en las primeras semanas es importante (entre un 15-20%),
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [433]
[28] TOS CRÓNICA Y HEMOPTISIS
principalmente si no se trata la causa subyacente. Las complicaciones posibles de la embolización de ramas
arteriales son dolor torácico, disfagia, necrosis de la pared aórtica y bronquial, y embolización de órganos a
distancia. La única contraindicación a la embolización es la presencia de una arteria medular originada en el
mismo vaso que causa la hemoptisis (riesgo de síndrome de sección medular), por lo que en este caso se
valoraría riesgo/beneficio de la técnica. Solo en 4% de los casos la embolización es técnicamente imposible.
2.6. Tratamiento quirúrgico
La resección quirúrgica está reservada para casos con localización concreta del origen del sangrado,
que cumplan criterios de operabilidad y resecabilidad y en los que las medidas previas no han sido eficaces.
Es aconsejable un tratamiento con embolización previo para el control inmediato de la hemoptisis y la
realización de la cirugía de forma programada, ya que tiene menor riesgo de morbimortalidad. La
mortalidad quirúrgica en el tratamiento de la hemoptisis amenazante es del 20%, con una morbilidad del
25-50%, principalmente por empiema y fístula broncopleural.
BIBLIOGRAFÍA
Chun HJ, Byun JY, Yoo SS, Choi BG. Added benefit of thoracic aortography after transarterial
embolization in patients with hemoptysis. AJR Am J Roentgenol. 2003;180(6):1577.
Dave BR, Sharma A, Kalva SP, Wicky S. Nine-year single-center experience with transcatheter arterial
embolization for hemoptysis: medium-term outcomes. Vasc Endovascular Surg. 2011;45(3):258-68.
Dettmar PW, Strugala V, Fathi H, Dettmar HJ, Wright C, Morice AH. The online Cough Clinic: developing
guideline-based diagnosis and advice. Eur Respir J. 2009;34(4):819-24.
Gibson PG, Chang AB, Glasgow NJ, Holmes PW, Katelaris P, Kemp AS, et al. CICADA: Cough in Children
and Adults: Diagnosis and Assessment. Australian cough guidelines summary statement. Diagnosis
and assessment. Australian cough guideliness summary statement. CICADA: Cough in children and
adults. Med J Aust. 2010;192(5):265-71.
Haro Estarriol M, Vizcaya Sánchez M, Jiménez López J, Tornero Molina A. Etiología de la hemoptisis:
análisis prospectivo de 752 casos. Rev Clin Esp. 2001;201:696-700.
Herth F, Ernst A, Becker HD. Long-term outcome and lung cancer incidence in patients with hemoptysis
of unknown origin. Chest. 2001;120(5):1592-4.
Ibrahim WH. Massive haemoptysis: the definition should be revised. Eur Respir J. 2008;32(4):1131-2.
Irwin RS, Baumann MH, Bolser DC, Boulet LP, Braman SS, Brightling CE, et al. Diagnosis and
management of cough executive summary: ACCP evidence-based clinical practice guidelines. Chest.
2006;129 (1 Suppl):1S-23S.
Jean-Baptiste E. Clinical assessment and management of massive hemoptysis. Crit Care Med. 2000
May;28(5):1642-7.
Ketai LH, Mohammed TL, Kirsch J, Kanne JP, Chung JH, Donnelly EF, et al; Expert Panel on Thoracic
Imaging. ACR appropriateness criteria® hemoptysis. J Thorac Imaging. 2014;29(3):W19-22.
Menchini L, Remy-Jardin M, Faivre JB, Copin MC, Ramon P, Matran R, et al. Cryptogenic haemoptysis in
smokers: angiography and results of embolisation in 35 patients. Eur Respir J. 2009;34(5):1031-9.
Morice AH, Fontana GA, Belvisi MG, Birring SS, Chung KF, Dicpinigaitis PV, et al. European Respiratory
Society guidelines on the assessment of cough. Eur Respir J. 2007;29(6):1256-76.
Pacheco A, De Diego A, Domingo C, Lamas A, Gutiérrez R, Naberan K, et al. Tos crónica. Normativa
SEPAR. Arch Bronconeumol. 2015;51:579-89.
Pavord ID, Chung KF. Management of chronic cough. Lancet. 2008;371:1375-84.
Roig J, Llorente JL, Ortega FJ, Orriols R, Segarra A. Normativa sobre el manejo de la hemoptisis
amenazante. Recomendaciones SEPAR. Barcelona: Doyma; 2001.
Savale L, Parrot A, Khalil A, Antoine M, Théodore J, Carette MF, et al. Cryptogenic hemoptysis: from a
benign to a life-threatening pathologic vascular condition. Am J Respir Crit Care Med.
2007;175(11):1181-5.
Schünemann HJ, Jaeschke R, Cook DJ, Bria WF, El-Solh AA, Ernst A, et al. An official ATS statement:
Grading the quality of evidence and strength of recommendations in ATS guidelines and
recommendations. Am J Respir Crit Care Med. 2006;174(5):605-14.
Yanci WS Jr, McCrory DC, Coeytaux RR, Schmit KM, Kemper AR, Goode A, et al. Efficacy and tolerability
of treatments for chronic cough: A systematic review and meta-analysis. Chest. 2013;144(6):1827.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [434]
[29] ASMA Y ENFERMEDAD PULMONAR OBSTRUCTIVA CRÓNICA
29.Asma y enfermedad pulmonar obstructiva crónica
Gabriel José González Salazar.
Alergología
Walther Iván Girón Matute.
Neumología
Estíbaliz Arrieta Ortubay.
Medicina Interna
Asesores: Consuelo Fernández Rodríguez. Jefa de Sección de Alergología. Carlos José Álvarez Martínez. Médico Adjunto de
Neumología
I. ASMA
1. DEFINICIÓN Y FISIOPATOLOGÍA
El asma consiste en episodios recurrentes de sibilancias, disnea, sensación de opresión torácica y
tos, secundarios a un proceso inflamatorio crónico de las vías aéreas que cursa con hiperreactividad
bronquial y obstrucción al flujo aéreo, por lo regular reversible (espontáneamente o con medicación).
Aunque el espectro clínico es muy variable, la presencia de inflamación de la vía respiratoria
(incluida la mucosa nasal) es una característica patológica común (por liberación de mediadores de
mastocitos, eosinófilos, células natural killer [NK] y linfocitos Th2). Los mecanismos por los que se produce
la obstrucción bronquial son: contracción del músculo liso (la más importante y habitualmente reversible
por fármacos broncodilatadores), edema de la vía aérea (la más relevante en las exacerbaciones),
hipersecreción de moco y cambios estructurales en las vías respiratorias (depósito de fibras de colágeno,
fibrosis subepitelial, hiperplasia e hipertrofia del músculo liso bronquial y de las glándulas mucosas con
hipersecreción de moco, proliferación y dilatación de vasos sanguíneos). Todo ello puede, finalmente,
producir obstrucción bronquial persistente.
2. MANIFESTACIONES CLÍNICAS
Sibilancias (el más característico), disnea (el que refleja mayor gravedad), tos y opresión torácica.
Habitualmente son variables, de predominio nocturno y provocados por distintos desencadenantes
(infecciones víricas, alérgenos, humo de tabaco, ejercicio, emociones, etc.). Será también importante
evaluar las variaciones estacionales de los síntomas y los antecedentes familiares o personales de atopia.
Los síntomas pueden presentarse en combinaciones variadas (en conjunto solo aparecen en el 36% de los
asmáticos) y de manera intermitente, y ninguno de ellos es específico del asma (de ahí la necesidad de
incorporar pruebas diagnósticas objetivas que pongan de manifiesto la presencia de obstrucción variable al
flujo aéreo).
3. DIAGNÓSTICO
En la figura 1 se muestra el algoritmo diagnóstico del asma.
1. PRUEBAS DE FUNCIÓN RESPIRATORIA
1.1. Espirometría forzada: es la prueba diagnóstica de primera elección. Los principales parámetros
que se deben determinar son la capacidad vital forzada (FVC) y el volumen espiratorio forzado en el primer
segundo (FEV1). La obstrucción se define como un cociente FEV1/FVC por debajo de 0,7. Un FEV1 reducido
confirma la obstrucción, ayuda a establecer la gravedad e indica un mayor riesgo de exacerbaciones,
aunque muchos enfermos pueden tener una espirometría con valores en el margen de referencia, o incluso
con un patrón no obstructivo (restrictivo) por atrapamiento aéreo.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [435]
[29] ASMA Y ENFERMEDAD PULMONAR OBSTRUCTIVA CRÓNICA
Figura 1. Algoritmo diagnóstico del asma.
1.2. Prueba de broncodilatación: se considera positiva un aumento del FEV1 > 12% y > 200 ml con
respecto al valor basal. Un criterio alternativo es un incremento del flujo espiratorio máximo (PEF) > 60
l/min o > 20%. La reversibilidad también se puede identificar por una mejoría del FEV1 o PEF tras 2 semanas
de tratamiento con glucocorticoides sistémicos (40 mg de prednisona o equivalente) o 2-8 semanas de
glucocorticoides inhalados (1.500-2.000 mg/día de fluticasona o equivalente). Hay que hacer hincapié en
que la reversibilidad de la obstrucción bronquial no está presente en todos los pacientes.
1.3. Monitorización del flujo espiratorio máximo (FEM): es de especial importancia cuando los
valores de la espirometría se encuentran en límites de referencia y la respuesta broncodilatadora es
negativa.
El FEM es el índice (volumen/tiempo) que expresa el mayor flujo que se alcanza al realizar una
maniobra de espiración forzada (utilizando un medidor de pico-flujo o peak flow). La variabilidad diurna del
FEM en pacientes que no han recibido tratamiento, especialmente en mediciones secuenciales durante un
periodo de 2 semanas, es un muy buen indicador del asma y su severidad. El cálculo de la variabilidad se
hace midiendo el FEM al levantarse por la mañana (generalmente, el valor más bajo), y por la tarde (de 19 a
21 horas; el valor más alto); se calculan los índices de variabilidad diurna con la fórmula más empleada para
ello, que es la siguiente:
Variabilidad del FEM (%) = (FEM máximo – FEM mínimo) x 100 / FEM máximo
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [436]
[29] ASMA Y ENFERMEDAD PULMONAR OBSTRUCTIVA CRÓNICA
Se considera variabilidad diurna significativa cuando el índice es igual o superior al 20% en al menos
3 días de la semana durante 2 semanas consecutivas, siendo esta variabilidad altamente sugerente de
asma.
1.4. Prueba de broncoconstricción: puede ser de ayuda en pacientes con sospecha clínica de asma
y función pulmonar normal. Se pueden emplear diversos agentes directos como metacolina o histamina, o
indirectos, como adenosina monofosfato o manitol. La provocación diagnóstica tiene una elevada
sensibilidad, pero una especificidad limitada, por lo que es más útil para excluir que para confirmar el
diagnóstico.
1.5. Fracción exhalada de óxido nítrico (FeNO): prueba no invasiva para cuantificar la inflamación
eosinofílica de las vías aéreas. El procedimiento de determinación ha sido estandarizado y el punto de corte
en adultos se ha establecido en 50 partículas por billón (ppb). Tiene una elevada sensibilidad y especificidad
para el diagnóstico de asma en no fumadores que no utilizan glucocorticoides inhalados.
2. ESTUDIO DE ALERGIA
El objetivo es determinar la existencia de sensibilización a aeroalérgenos que influyan en el
desarrollo del fenotipo de asma alérgica, o que desencadenen exacerbaciones. No se realiza de manera
sistemática, pero sí en los pacientes en los que la historia clínica muestre datos relevantes al respecto.
3. DIAGNÓSTICO DIFERENCIAL
En la tabla I se ofrece un resumen del diagnóstico diferencial del asma.
En lo que se refiere a la tos que persiste durante más de 4 semanas (tos crónica), entre los
diagnósticos alternativos que se deben considerar se encuentran el goteo posnasal causado por
enfermedades de las vías respiratorias superiores (rinitis, sinusitis, pólipos nasales, etc.), el reflujo
gastroesofágico o la toma de fármacos como los inhibidores de la enzima convertidora de la angiotensina
(IECA). Cabe citar, entre otras causas que pueden provocar una tos crónica, la enfermedad pulmonar
obstructiva crónica (EPOC), las bronquiectasias, la bronquitis eosinofílica, la tos postinfecciosa, los tumores
que comprimen y/o irritan la vía respiratoria e incluso la tos psicógena (ver Capítulo 28. “Tos y hemoptisis”).
Tabla I. Diagnóstico diferencial del asma.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [437]
[29] ASMA Y ENFERMEDAD PULMONAR OBSTRUCTIVA CRÓNICA
4. CLASIFICACIÓN DEL ASMA EN EL ADULTO
Según la gravedad clínica (Tabla II): implica tanto la intensidad de los síntomas, como de la
respuesta al tratamiento. Puede variar a lo largo del tiempo, por lo que es necesario reevaluar
periódicamente. Esta clasificación se determina de forma retrospectiva, según el escalón terapéutico
necesario para conseguir el control.
Tabla II. Clasificación de la gravedad del asma en el adulto (antes de recibir tratamiento).
Según el control de los síntomas (Tabla III): el control del asma es el grado en el que las
manifestaciones del asma están ausentes o se ven reducidas al máximo por las intervenciones terapéuticas
y se cumplen los objetivos del tratamiento.
Tabla III. Clasificación del control del asma en el adulto.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [438]
[29] ASMA Y ENFERMEDAD PULMONAR OBSTRUCTIVA CRÓNICA
Si el paciente no recibe tratamiento, estas clasificaciones se deben utilizar como guía para elegir el
tratamiento farmacológico y tomar otras decisiones terapéuticas. Si el paciente está siendo tratado, la
gravedad se determina en función de los requerimientos mínimos de medicación para mantener el control.
5. TRATAMIENTO EN EL PACIENTE ESTABLE
1. TRATAMIENTO FARMACOLÓGICO
Los fármacos empleados se clasifican en:
Medicamentos de mantenimiento: deben administrarse a diario durante periodos
prolongados. Estos incluyen:
Glucocorticoides inhalados (GCI) (beclometasona, budesonida, ciclesonida, fluticasona
o mometasona) o corticoides sistémicos.
Antagonistas de los receptores de los leucotrienos (ARLT): montelukast (en pacientes
de 2 a 5 años, dosis de 4 mg/día; de 6 a 14 años, 5 mg/día; > 15 años 10 mg/día) y
zafirlukast (en > 12 años, 20 mg/2 veces al día).
Agonistas beta-2 adrenérgicos de acción larga (LABA): salmeterol, formoterol o
vilanterol.
Antagonistas de los receptores muscarínicos de acción larga (LAMA): bromuro de
tiotropio, aprobado por la Agencia Europea de Medicamentos como tratamiento de
mantenimiento en asociación con GCI y LABA en pacientes que sufran más de una
exacerbación al año. En estudios recientes otras moléculas de este grupo aprobadas en
el tratamiento de la EPOC, como el bromuro de glicopirronio y el bromuro de aclidinio,
han demostrado su potencial en el tratamiento de pacientes con asma grave.
Anticuerpos monoclonales anti-IgE, en fenotipos de asma específicos.
Cabe destacar que las cromonas y la teofilina de liberación retardada han caído en
desuso por su menor efectividad.
Figura 2. Escalones terapéuticos del tratamiento de mantenimiento del asma del adulto.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [439]
[29] ASMA Y ENFERMEDAD PULMONAR OBSTRUCTIVA CRÓNICA
Medicamentos de alivio o rescate: se utilizan a demanda para tratar o prevenir la
broncoconstricción de forma rápida, y su uso se recomienda en todos los pacientes con
síntomas de asma. Entre ellos se encuentran los agonistas beta-2 adrenérgicos de acción corta
inhalados (SABA), como salbutamol o terbutalina, y los anticolinérgicos de acción corta
inhalados (SAMA), como el bromuro de ipratropio. Los SABA, administrados con una antelación
de unos 10-15 minutos, son los medicamentos de elección para prevenir la broncoconstricción
inducida por el ejercicio.
El objetivo del tratamiento es lograr y mantener el control de la enfermedad, además de
prevenir exacerbaciones, la obstrucción crónica al flujo aéreo y reducir al máximo la
mortalidad. Se clasifica en seis escalones terapéuticos, considerando individualmente la
situación clínica de cada paciente. Si el asma ha estado controlada durante al menos 3 meses,
el tratamiento de mantenimiento puede reducirse progresivamente con el fin de determinar las
necesidades terapéuticas mínimas (Figura 2 y Tabla IV).
Tabla IV. Dosis equivalentes de glucocorticoides inhalados.
Escalón 1: consiste en el uso de SABA inhalados exclusivamente a demanda, en pacientes con
síntomas diurnos ocasionales y leves, sin síntomas nocturnos, asintomáticos entre los episodios y que
mantienen una función pulmonar normal. El uso de un SABA a demanda más de 2 veces a la semana para
tratar los síntomas (sin contar cuando se utilice antes del ejercicio), o el haber tenido exacerbaciones en el
año previo o un FEV1 < 80% indica un control del asma inadecuado.
Escalón 2: para pacientes con asma persistente leve, el tratamiento de elección es un GCI a dosis
bajas utilizado diariamente. Se pueden considerar alternativas los ARLT en pacientes mayores de 2 años en
los que exista contraindicación para el uso de GCI sin historial reciente de exacerbaciones graves o como
prevención en el asma inducida por ejercicio.
Escalón 3: en el asma persistente moderada, el tratamiento de elección es la combinación de un
GCI a dosis bajas con un LABA inhalados, ya que pueden administrarse en un mismo dispositivo. Las
combinaciones comercializadas en España son: fluticasona propionato con salmeterol (Anasma®, Brisair®,
Inaladuo®, Plusvent® y Seretide®), budesonida con formoterol (Duoresp Spiromax®, Bufomix Easyhaler®,
Rilast Turbohaler® y Symbicort Turbohaler®), beclometasona con formoterol (Foster Nexthaler® y Formodual
Nexthaler®), fluticasona propionato con formoterol (Flutiform®), y fluticasona furoato con vilanterol (Relvar
Ellipta®). Los LABA nunca deben utilizarse en monoterapia. Se debe tener en cuenta que a partir de este
escalón de tratamiento las combinaciones budesonida/formoterol o beclometasona/formoterol pueden
utilizarse en terapia MART (maintenance and relief therapy), siendo esta una opción terapéutica que
combina el tratamiento de mantenimiento y de rescate en un único dispositivo de inhalación, con el
objetivo de prevenir las exacerbaciones asmáticas y ofrecer mayor comodidad al paciente.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [440]
[29] ASMA Y ENFERMEDAD PULMONAR OBSTRUCTIVA CRÓNICA
Escalón 4: el tratamiento de elección es la combinación de un GCI a dosis medias con un LABA.
Como alternativa, puede utilizarse la combinación de un GCI a dosis medias con un ARLT.
Escalón 5: se combinan dosis altas de GCI con LABA. Es posible valorar en este nivel tratamientos de
segunda línea, orientados según el fenotipo de asma del paciente:
Asma alérgica mal controlada: complementar el tratamiento con un anticuerpo monoclonal
anti-IgE (omalizumab).
Asma neutrofílica: la administración de azitromicina a dosis bajas durante meses ha
demostrado eficacia.
Asma asociada a obesidad: reducción de peso.
Como novedad incluida en la guía GEMA 4.0, se puede asociar tiotropio a la combinación GCI con
LABA.
Escalón 6: en los pacientes en los que persiste el mal control, a pesar del uso de una combinación
de GCI y LABA a dosis altas, se debe plantear la adición de glucocorticoides orales (a la dosis mínima posible
y en ciclos cortos). Podría considerarse la realización de termoplastia endobronquial y el uso de
triamcinolona intramuscular.
2. OTRAS MEDIDAS TERAPÉUTICAS
Control ambiental.
Inmunoterapia con alérgenos: es un tratamiento eficaz para el asma alérgica bien controlada
con niveles bajos o medios de tratamiento (escalones terapéuticos 2 a 4), siempre que se haya
demostrado una sensibilización mediada por IgE específica frente al alérgeno.
Educación: es fundamental para reducir el riesgo de padecer exacerbaciones, aumenta la
calidad de vida y disminuye los costes sanitarios. El principal objetivo es proporcionar
autonomía al paciente para que mantenga un control óptimo de su enfermedad desde un
manejo autoguiado del asma, es decir, en el que el paciente disponga de conocimientos e
instrucciones individualizadas sobre cómo actuar y cómo modificar su tratamiento ante la
pérdida del control.
Vacunación: debería considerarse la vacunación antigripal anual en pacientes con asma
moderada y grave, y la vacunación antineumocócica según calendario en pacientes con asma
grave.
6. EXACERBACIÓN AGUDA DEL ASMA
Las exacerbaciones (agudizaciones, ataques o crisis de asma) son episodios de empeoramiento de
la situación basal de un paciente asmático que requieren modificaciones en el tratamiento. Desde el punto
de vista clínico, se caracteriza por aumento de los síntomas típicos (disnea, tos, sibilancias y opresión
torácica), cambios en la medicación de alivio o disminución del flujo espiratorio. Ocasionalmente puede ser
la forma de presentación inicial del asma.
Según la rapidez de instauración de la crisis, existen dos tipos:
Crisis de instauración lenta (normalmente en días o semanas): por lo general debido a
infecciones respiratorias altas; el mecanismo fundamental del deterioro es la inflamación.
Crisis de instauración rápida (en menos de 3 horas): se deben a alérgenos inhalados, ingestión
de fármacos (antiinflamatorios no esteroideos o fármacos betabloqueantes), alimentos (por
aditivos y conservantes) o estrés emocional; el mecanismo es el broncoespasmo y, aunque
tiene mayor gravedad inicial, la respuesta al tratamiento es mejor y más rápida.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [441]
[29] ASMA Y ENFERMEDAD PULMONAR OBSTRUCTIVA CRÓNICA
1. EVALUACIÓN DE LA GRAVEDAD
La gravedad de la crisis asmática varía desde leve (incluso puede pasar desapercibida) a ser
potencialmente mortal. Por tanto, es esencial realizar una evaluación rápida de la gravedad del episodio.
1.1. Valoración inicial (evaluación estática)
El objetivo inicial es identificar a los pacientes con factores de riesgo para asma grave (Tabla V),
reconocer datos de compromiso vital (Tabla VI) y medir de forma objetiva el grado de obstrucción al flujo
aéreo mediante la determinación del FEV1 o PEF.
Tabla V. Factores de riesgo de crisis asmática grave.
Tabla VI. Evaluación de la gravedad de la crisis.
Siempre que la situación clínica lo permita, se realizará una breve anamnesis, que orientará sobre
posibles desencadenantes de la sintomatología, duración de la crisis o tratamiento previo. La presencia de
datos de riesgo vital e inminencia de parada cardiorrespiratoria (alteración del nivel de consciencia,
bradicardia, hipotensión, cianosis, tórax “silente” o agitación) obligan a contactar con una Unidad de
Cuidados Intensivos.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [442]
[29] ASMA Y ENFERMEDAD PULMONAR OBSTRUCTIVA CRÓNICA
Medición objetiva del grado de obstrucción al flujo y su repercusión gasométrica.
Peak flow: el registro del flujo espiratorio máximo es de especial utilidad como medida objetiva
de obstrucción al flujo aéreo durante la crisis. Permite determinar la gravedad inicial y objetivar
la respuesta al tratamiento. El valor obtenido se puede comparar con “el mejor” registro del
propio paciente o con valores teóricos de referencia que dependen de la edad, sexo y peso del
paciente (Tabla VII). El porcentaje del PEF sobre el valor teórico, o “el mejor” registro del
paciente, se calcula aplicando la siguiente fórmula:
% PEF teórico o mejor registro = PEF real x 100 / PEF teórico o mejor registro
Saturación periférica de oxígeno (SpO2): se mide mediante pulsioximetría. Se recomienda en la
evaluación inicial, reservando la gasometría arterial para los pacientes con SpO2 inferior al 90%
a pesar de la oxigenoterapia, en los pacientes con signos o síntomas de hipercapnia o en
aquellos con PEF menor del 25% de lo estimado.
La realización de otras pruebas complementarias urgentes, como bioquímica, hemograma,
electrocardiograma y radiografía de tórax, solo está indicada si el paciente presenta síntomas como fiebre,
dolor o disnea intensa que hagan pensar en la existencia de complicaciones (neumotórax o infección
respiratoria).
Tabla VII. Valores teóricos del pico espiratorio del flujo (PEF) en l/min.
1.2. Respuesta al tratamiento (evaluación dinámica)
El objetivo es comparar los cambios conseguidos en el grado de obstrucción al flujo aéreo respecto
a los valores de partida. La respuesta terapéutica inicial a la obstrucción al flujo aéreo se considera el
principal factor pronóstico de la crisis. En un paciente con obstrucción grave, se acepta que la respuesta es
favorable cuando el PEF es superior al 45% del valor teórico a los 30 minutos del comienzo del tratamiento
y el PEF tiene un incremento mínimo de 50 l/min sobre el valor basal predeterminado.
2. TRATAMIENTO FARMACOLÓGICO
En la tabla VIII se muestran los principios básicos de una exacerbación asmática, y en la tabla IX los
fármacos que se emplean en su tratamiento.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [443]
[29] ASMA Y ENFERMEDAD PULMONAR OBSTRUCTIVA CRÓNICA
Tabla VIII. Principios básicos en una exacerbación asmática.
Tabla IX. Fármacos y dosis en el tratamiento de la exacerbación asmática.
2.1. Exacerbación leve
Las crisis más leves pueden tratarse, además de en los servicios de urgencias hospitalarias, en los
centros de atención primaria y en el domicilio por el propio paciente.
El tratamiento se basa en la administración de una agonista beta-2 adrenérgico de acción rápida y
un corticoide por vía oral (vo).
Los agonistas beta-2 adrenérgicos de acción corta inhalados (salbutamol o terbutalina): son los
fármacos broncodilatadores más eficaces y rápidos en el tratamiento de la exacerbación
asmática. El salbutamol se emplea a dosis de 200 a 400 μg (de 2 a 4 inhalaciones) y la
terbutalina a dosis de 500 μg inhalado (Terbasmin® 500 μg, 1 inhalación) o 5 mg nebulizado (0,5
ml diluidos en 4 ml de suero salino fisiológico [SSF]), cada 20 minutos durante la primera hora.
Cuando la respuesta es buena, se continúa con dosis de dos inhalaciones cada 3-4 horas hasta
la remisión de la crisis.
Glucocorticoides sistémicos: excepto en crisis muy leves, deben administrarse siempre y de
manera precoz, especialmente si:
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [444]
[29] ASMA Y ENFERMEDAD PULMONAR OBSTRUCTIVA CRÓNICA
No se consigue una reversión de la obstrucción de las vías respiratorias con agonistas
beta-2 adrenérgicos de acción corta inhalados.
El paciente estaba tomando ya glucocorticoides orales.
El paciente ya ha tratado su exacerbación con otras opciones terapéuticas sin éxito.
Existen antecedentes de exacerbaciones previas que requirieron glucocorticoides
orales.
La dosis diaria es de 0,5-1 mg/kg de peso ideal de prednisona (o su equivalente de otros esteroides)
en una sola dosis al día (preferiblemente matutina), manteniendo dicha dosis entre 5-10 días (sin necesidad
de reducción progresiva de la misma al finalizar su duración).
2.2. Exacerbación moderada-grave
Oxigenoterapia: para mantener una saturación superior al 90%.
Agonista beta-2 adrenérgico de acción corta inhalado (salbutamol o terbutalina): se administra
de forma repetida a intervalos regulares, valorando la respuesta al tratamiento.
Se pueden realizar hasta tres nebulizaciones consecutivas de salbutamol (2,5 mg) cada 20-30
minutos (indicado en crisis graves y en pacientes que no pueden llevar a cabo una adecuada
técnica de inhalación) o 12 pulsaciones (4 cada 10 minutos) si se administran con inhalador
presurizado y en cámara de inhalación. La nebulización continua no ha demostrado mayor
eficacia que la nebulización intermitente, sin embargo, se puede utilizar en casos graves a un
ritmo de 10 mg/h.
La administración parenteral (intravenosa [iv] o subcutánea) de salbutamol no ha evidenciado
diferencias en su eficacia frente a la vía inhalada y presenta potenciales efectos adversos. Por
tanto, solo se recomienda en pacientes bajo ventilación mecánica o en los que no responden al
tratamiento inhalado, siendo imprescindible la monitorización en una unidad de cuidados
intensivos.
Bromuro de ipratropio: se administra nebulizado 0,5 mg diluido en 3 ml de suero salino
fisiológico (Atrovent monodosis® solución inhalatoria de 2 ml con 250 y 500 μg) o en inhalación
(20 μg/pulsación) a dosis de 4-8 pulsaciones con cámara espaciadora cada 20 minutos. Se
administra combinado con salbutamol en la fase inicial de las crisis asmáticas graves, ya que
provoca un incremento significativo de la broncodilatación.
Glucocorticoides sistémicos: se deben administrar precozmente (en la primera hora del
tratamiento de urgencia). La dosis recomendada al inicio es prednisona 40-60 mg/24 h en una
sola toma por vía oral (dada su excelente biodisponibilidad), reservando la vía parenteral para
casos de compromiso clínico o intolerancia oral (por ejemplo, vómitos); en dichas situaciones
puede emplearse también hidrocortisona 100-200 mg/4-6 h iv (400 mg/día).
Los glucocorticoides inhalados se pueden administrar en la primera hora de tratamiento
asociados a los agonistas beta-adrenérgicos nebulizados, tanto en dispositivo de inhalación
(Budesonida Pulmicort® 100, 200 y 400 μg/pulsación) como nebulizados (budesonida ampollas
de 2 ml, 0,5 mg/ml) cada 20 minutos, ya que pueden reducir las necesidades de ingreso. Sin
embargo, su empleo nunca debe sustituir la administración concomitante de corticoides
sistémicos.
Sulfato de magnesio intravenoso: en el caso de pacientes con crisis muy graves y mala
respuesta al tratamiento anteriormente descrito, se puede administrar en dosis única de 1-2 g
(por ejemplo, 1 ampolla de sulfato de magnesio 1,5 g/10 ml diluida en 100 ml de suero salino al
0,9% o glucosado al 5%, administrada en 30 minutos).
Otras medidas:
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [445]
[29] ASMA Y ENFERMEDAD PULMONAR OBSTRUCTIVA CRÓNICA
La adrenalina subcutánea o intramuscular (dosis de 0,3-0,5 ml al 1:1.000) solo está indicada en
caso de exacerbación asmática en el contexto de una anafilaxia.
El heliox puede considerarse en pacientes que no respondan al tratamiento habitual.
Las teofilinas no deben emplearse durante la crisis asmática por su menor eficacia en
comparación con el salbutamol, así como su menor seguridad.
Respecto a los antagonistas de los receptores de leucotrienos o los antibióticos empíricos, no
existen datos que respalden su uso en el tratamiento de las exacerbaciones moderadas-graves
del asma.
3. VENTILACIÓN MECÁNICA
La decisión de proceder a intubación orotraqueal e iniciar ventilación mecánica es clínica (Tabla VI).
En caso de persistencia de insuficiencia respiratoria refractaria o síntomas o signos de exacerbación
grave a pesar del tratamiento, se valorará llevarla a cabo.
El papel de la ventilación mecánica no invasiva (VMNI) en el asma no está tan estudiado como en la
EPOC, pero algunos pacientes podrían beneficiarse de ella.
4. CRITERIOS DE HOSPITALIZACIÓN
Deben ser hospitalizados aquellos pacientes que han recibido un tratamiento adecuado durante 3
horas de estancia en el servicio de urgencias y permanecen sintomáticos, o requieren oxigenoterapia para
mantener una SaO2 superior al 90%, o bien muestran una reducción persistente de la función pulmonar
(PEF inferior al 40%).
En todos los casos en los que no existan criterios de ingreso hospitalario, se recomienda observar al
paciente durante al menos una hora tras la mejoría sintomática para confirmar la estabilidad clínica y
funcional antes del alta. Aunque debe individualizarse en cada paciente, el peak flow al alta debería ser
superior a 200 l/min.
5. CRITERIOS DE ALTA TRAS INGRESO HOSPITALARIO
No hay criterios absolutos para el alta después de una crisis que haya precisado ingreso, aunque se
recomienda proceder a ella si se cumplen los siguientes criterios:
Desaparición o mejoría significativa de la clínica de exacerbación.
PEF superior al 70% de su mejor valor personal en situación estable.
Variabilidad diaria del PEF menor del 20%.
Necesidad de utilizar < 3 veces al día agonistas beta2 adrenérgicos de acción corta a demanda.
Ausencia de disnea significativa al caminar.
Glucocorticoides inhalados ya iniciados.
II. ENFERMEDAD PULMONAR OBSTRUCTIVA CRÓNICA
1. DEFINICIÓN Y EPIDEMIOLOGÍA
La EPOC se caracteriza por la presencia de limitación crónica poco reversible al flujo aéreo asociada
a una reacción inflamatoria crónica debida, principalmente, al humo de tabaco. La obstrucción crónica al
flujo aéreo se define mediante la espirometría con un valor del cociente FEV1 y la FVC posbroncodilatador
con un valor menor de 0,7 (o por debajo del límite inferior de la normalidad en mayores de 60 años).
Dos problemas con frecuencia asociados a la EPOC son el enfisema y la bronquitis crónica (BC). El
enfisema se caracteriza por dilatación no uniforme de los espacios alveolares distales con pérdida de
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [446]
[29] ASMA Y ENFERMEDAD PULMONAR OBSTRUCTIVA CRÓNICA
elasticidad pulmonar, destrucción de los ácinos y ausencia de alteraciones fibróticas. La BC se define por tos
crónica productiva durante más de 3 meses al año durante 2 años consecutivos, en ausencia de otras
neumopatías.
Actualmente, la EPOC es la cuarta causa de muerte en el mundo. En España, la prevalencia es
aproximadamente del 10% y afecta a más de dos millones de personas, aunque solo un 30% están
diagnosticados. Su frecuencia aumenta con la edad, en el sexo masculino y predomina en pacientes de un
nivel socioeconómico bajo, aunque en los últimos años existe un aumento de la incidencia en el sexo
femenino.
Las comorbilidades son muy frecuentes en la EPOC y pueden generar problemas en el diagnóstico y
el tratamiento. Entre las más importantes cabe mencionar: insuficiencia cardiaca (IC), asma bronquial,
síndrome de apnea-hipopnea del sueño (SAHS), cáncer de pulmón, osteoporosis, diabetes mellitus,
cardiopatía isquémica, ansiedad, depresión, arritmias, disfunción muscular esquelética, anemia y obesidad.
2. FACTORES DE RIESGO
Tabaquismo: constituye el factor de riesgo más importante. Su intensidad debe cuantificarse
mediante el índice de años-paquete (número de cigarrillos al día dividido entre 20 y
multiplicado por el número de años que haya fumado). Se considera de riesgo una exposición
de al menos 10 años-paquete.
Exposiciones laborales: el polvo de las minas de carbón y los humos de combustión de
biomasas (un modo de cocinar en algunos países) también constituyen factores de riesgo
independientes para la EPOC.
Infecciones respiratorias de repetición durante la infancia.
Factores genéticos: como el déficit grave de la alfa-1-antitripsina.
3. MANIFESTACIONES CLÍNICAS
1. SÍNTOMAS
Disnea con el ejercicio: es el síntoma principal. Presenta un desarrollo progresivo hasta limitar
las actividades más sencillas de la vida diaria. La escala de disnea más utilizada es la escala
modificada del British Medical Research Council (mMRC) (Tabla X).
Tos: suele ser productiva y de predominio matutino.
Producción de esputo: un volumen mayor de 30 ml en 24 horas sugiere la existencia de
bronquiectasias. Un esputo purulento o un aumento de su volumen de inicio agudo pueden
indicar exacerbación.
Tabla X. Escala de disnea modificada del British Medical Research Council (mMRC).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [447]
[29] ASMA Y ENFERMEDAD PULMONAR OBSTRUCTIVA CRÓNICA
2. EXPLORACIÓN FÍSICA
Puede ser normal. En la EPOC grave, se observa una insuflación del tórax (por aumento del
diámetro anteroposterior). En la auscultación destaca el alargamiento de la espiración con disminución del
murmullo vesicular, junto con presencia de roncus y sibilancias. En fases avanzadas, hay pérdida de peso a
expensas de masa muscular y tejido adiposo; un índice de masa corporal menor de 21 kg/m2 indica mal
pronóstico. Cuando se asocia a hipertensión pulmonar se pueden observar signos de sobrecarga ventricular
derecha, cianosis en los labios y en las zonas acras.
Las acropaquias o hipocratismo digital no son un signo de EPOC y su presencia obliga a identificar
otras causas (cáncer pulmonar, bronquiectasias, etc.).
4. DIAGNÓSTICO
1. PRUEBAS DE FUNCIÓN RESPIRATORIA
Permiten establecer el diagnóstico, seguir la evolución y la respuesta al tratamiento, cuantificar la
gravedad, estimar el pronóstico, así como valorar la gravedad de los episodios de exacerbación.
1.1. Espirometría forzada: el cociente FEV1/FVC posbroncodilatador menor de 0,7 (o del límite
inferior de la normalidad en personas mayores de 60 años) se considera obstrucción al flujo aéreo. A su vez,
el valor de FEV1 es el mejor indicador de la gravedad y se utiliza para la clasificación espirométrica de la
enfermedad (Tabla XI). Otro índice de obstrucción es el índice de Tiffeneau, cociente entre el FEV1 y la
capacidad vital (VC) lenta, que actualmente no se emplea.
Tabla XI. Clasificación espirométrica de la gravedad de la enfermedad pulmonar obstructiva crónica según la Global Initiative for
Chronic Obstructive Lung Disease (GOLD) (FEV1/FVC < 0,7%).
Indicaciones: se recomienda la realización a todos los pacientes con sospecha de EPOC (adultos
mayores de 35 años fumadores o exfumadores con síntomas respiratorios) y en el seguimiento
a largo plazo de forma anual.
Contraindicaciones: las contraindicaciones absolutas de una espirometría son inestabilidad
hemodinámica, embolismo pulmonar (hasta estar adecuadamente anticoagulado), neumotórax
reciente (2 semanas tras la reexpansión), hemoptisis aguda, infecciones respiratorias activas,
infarto de miocardio reciente (7 días), angina inestable, aneurisma de aorta torácico que ha
crecido o de gran tamaño (mayor de 6 cm), hipertensión intracraneal y desprendimiento agudo
de retina.
1.2. Prueba de broncodilatación: establece el grado de reversibilidad y es imprescindible en el
estudio inicial para valorar el grado de obstrucción. Se utiliza para la valoración del fenotipo EPOC-asma
(véase en este capítulo el Apartado V. “Clasificación de la enfermedad pulmonar obstructiva crónica”).
1.3. Volúmenes pulmonares estáticos: se miden habitualmente por pletismografía. Permiten
descartar restricción asociada y valorar el grado de atrapamiento aéreo. Se recomienda su medición en:
EPOC grave o muy grave, EPOC leve o moderada con sospecha de atrapamiento aéreo, enfermedad
restrictiva asociada y valoración preoperatoria de candidatos a resección pulmonar.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [448]
[29] ASMA Y ENFERMEDAD PULMONAR OBSTRUCTIVA CRÓNICA
1.4. Capacidad de difusión del monóxido de carbono (DLCO): esta prueba está indicada en
pacientes con FEV1 inferior al 50%, si se sospecha enfisema y en la valoración preoperatoria de candidatos
a resección pulmonar.
1.5. Función muscular respiratoria: incluye la presión inspiratoria máxima (PIM), la presión
espiratoria máxima (PEM) y la espirometría en decúbito. Está indicada si se sospecha disfunción muscular
respiratoria, parálisis diafragmática o si la disnea es desproporcionada con relación al valor del FEV1.
1.6. Gasometría arterial basal: está indicada en la EPOC grave o muy grave, en EPOC moderada con
saturación de oxígeno (SaO2) < 92% a nivel del mar, y para la prescripción y seguimiento de oxigenoterapia
domiciliaria.
1.7. Pruebas de ejercicio: como la prueba de la marcha de 6 minutos (PM6M), la prueba de
lanzadera, la bicicleta ergométrica o el tapiz rodante. Estas pruebas están indicadas en la valoración del
riesgo quirúrgico en la resección pulmonar, evaluación de la respuesta terapéutica y valoración de la
incapacidad laboral. Además, estas pruebas proporcionan información integrada sobre el impacto funcional
de la enfermedad.
2. OTRAS PRUEBAS RESPIRATORIAS
2.1. Estudio de sueño (oximetría nocturna, poligrafía, polisomnografía): está indicado si se
sospecha la coexistencia de SAHS, hipoventilación alveolar o se sospecha insuficiencia respiratoria (IR)
nocturna (por ejemplo, si existe poliglobulia o signos de IC derecha en ausencia de IR diurna) (ver Capítulo
31. “Trastornos respiratorios durante el sueño”).
2.2. Niveles de alfa-1-antitripsina: debe realizarse en toda EPOC, al menos una vez, especialmente
en pacientes con enfisema que presenten: a) antecedentes mínimos de tabaquismo; b) EPOC prematura
(menores de 45 años); c) antecedentes familiares de neumopatía o familiares directos con déficit de alfa-1-
antitripsina; d) predominio de enfisema en los lóbulos inferiores en la radiografía de tórax o la tomografía
computarizada (TC).
3. EXÁMENES RADIOLÓGICOS
La radiografía de tórax puede ser normal o puede mostrar datos de enfisema (como bullas,
aplanamiento de diafragmas, aumento del espacio retroesternal, atenuación de la trama vascular o
hiperlucidez del parénquima pulmonar). La TC de alta resolución tiene mayor sensibilidad para el
diagnóstico de enfisema; se recomienda en la evaluación de tratamientos quirúrgicos, para identificar
bronquiectasias y ante la sospecha de cáncer de pulmón. Se debe realizar la TC en inspiración y espiración
para valorar traqueomalacia, atrapamiento aéreo y afectación de pequeña vía aérea.
4. EXÁMENES CARDIOLÓGICOS
El electrocardiograma es útil para el estudio de arritmias asociadas. El ecocardiograma
bidimensional valora la disfunción ventricular, las valvulopatías y el diagnóstico de patología cardiaca
asociada; se recomienda en caso de que el paciente presente manifestaciones clínicas o una disnea
desproporcionada a la alteración funcional.
5. CUESTIONARIOS DE CALIDAD DE VIDA
Su objetivo es valorar el impacto de la enfermedad en las actividades cotidianas del paciente, medir
la eficacia del tratamiento o detectar el comienzo de las exacerbaciones. Los más utilizados en la práctica
clínica son el Chronic Obstructive Pulmonary Disease Assessment Test (CAT; disponible en:
http://www.catestonline.org/english/index_SpainUS.htm) y el Cuestionario Clínico para la EPOC (CCQ;
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [449]
[29] ASMA Y ENFERMEDAD PULMONAR OBSTRUCTIVA CRÓNICA
disponible en: http://www.fundacionneumologica.org/asma/CCQ7.htm). En investigación, se utilizan el
Chronic Respiratory Questionnaire (CRQ) y el St. George’s Respiratory Questionnaire (SGQR).
6. ÍNDICE BODE
Se mide a través del índice de masa corporal (IMC) (B), el grado de obstrucción al flujo aéreo con el
FEV1 (O), el grado de disnea mediante el mMRC (D) y la tolerancia al ejercicio con la PM6M (E) con una
puntuación del 0 al 10 (Tabla XII). Este índice permite predecir mejor que el FEV1 el riesgo de muerte en
estos pacientes. Existe otro índice pronóstico, el BODEx, que considera el número de exacerbaciones (Ex)
en sustitución del ejercicio, con una puntuación del 0 al 9 (Tabla XIII); este último se agrupa en cuartiles:
cuartil 1 (0-2 puntos), cuartil 2 (3-4 puntos), cuartil 3 (5-6 puntos), cuartil 4 (7-9 puntos).
Tabla XII. Índice BODE.
Tabla XIII. Índice BODEx.
5. CLASIFICACIÓN DE LA ENFERMEDAD PULMONAR OBSTRUCTIVA CRÓNICA
1. CLASIFICACIÓN SEGÚN LA GUÍA ESPAÑOLA DE MANEJO DE LA EPOC
La guía española de manejo de la EPOC (GesEPOC) reconoce cuatro fenotipos excluyentes entre sí,
por las características clínicas, pronósticas y de respuesta al tratamiento (Figura 3).
Figura 3. Fenotipos clínicos de la enfermedad pulmonar obstructiva crónica según la Guía Española de la EPOC (GesEPOC).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [450]
[29] ASMA Y ENFERMEDAD PULMONAR OBSTRUCTIVA CRÓNICA
EPOC no agudizador, con enfisema o bronquitis crónica.
EPOC mixto con asma, tenga o no agudizaciones frecuentes.
EPOC agudizador con enfisema.
EPOC agudizador con bronquitis crónica.
Para el diagnóstico de identificación de los cuatro fenotipos se deben seguir los pasos de la figura 4.
Figura 3. Fenotipos clínicos de la enfermedad pulmonar obstructiva crónica según la Guía Española de la EPOC (GesEPOC).
Figura 4. Algoritmo diagnóstico de los fenotipos clínicos de la enfermedad pulmonar obstructiva crónica.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [451]
[29] ASMA Y ENFERMEDAD PULMONAR OBSTRUCTIVA CRÓNICA
2. CLASIFICACIÓN SEGÚN LA GLOBAL INITIATIVE FOR CHRONIC OBSTRUCTIVE LUNG DISEASE (GOLD)
Clasifica a los pacientes sobre la base de su sintomatología (bien por el grado de disnea o bien por
la puntuación del CAT), el grado de limitación del flujo aé reo (FEV1) valorado mediante espirometría y el
riesgo de exacerbaciones. Esta se resume en la figura 5.
También se ha identificado el subgrupo de asma-EPOC overlap (ACOS), que se caracteriza por
limitación persistente del flujo aéreo con características asociadas de asma bronquial. Los pacientes con
esta enfermedad presentan características clínicas y funcionales de ambas enfermedades.
Figura 5. Clasificación de la enfermedad pulmonar obstructiva crónica según la GOLD.
6. TRATAMIENTO EN EL PACIENTE ESTABLE
1. NO FARMACOLÓGICO
1.1. Abandono del tabaco: es una medida fundamental, pues mejora la supervivencia y se asocia a
una reducción de la pendiente caída del FEV1. Combinar la farmacoterapia con las medidas de apoyo
mejora la probabilidad de que un paciente deje de fumar. Los tres fármacos más empleados son la
vareniclina, un receptor agonista/antagonista del ácido nicotínico, el bupropión y el tratamiento de
sustitución con nicotina disponible en goma de mascar, parche dérmico, pastilla, aerosol e inhalador nasal.
1.2. Vacunación: en todos los pacientes con EPOC se recomienda la administración anual de la
vacuna antigripal. De la vacuna antineumocócica polisacárida 23 valente se recomienda una sola
administración a todos los pacientes con EPOC mayores de 65 años y su aplicación cada 5 años en los
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [452]
[29] ASMA Y ENFERMEDAD PULMONAR OBSTRUCTIVA CRÓNICA
menores de esa edad. La vacuna conjugada 13 valente se recomienda una sola vez (separada 1 año de la
polisacárida si se hubiera puesto antes).
1.3. Rehabilitación respiratoria: mejora la tolerancia al esfuerzo, la disnea, la calidad de vida, el
índice BODE y la supervivencia, y reduce la frecuencia de exacerbaciones, la utilización de servicios
sanitarios y el número de ingresos. Está indicada especialmente en pacientes con disnea no controlada con
el tratamiento, con mala tolerancia al esfuerzo y con restricción de las actividades.
1.4. Nutrición y actividad física: el paciente con EPOC debe evitar el sedentarismo y hacer ejercicio
físico diario. La nutrición es importante para evitar el sobrepeso y, sobre todo, la desnutrición, ya que
comporta peor pronóstico.
2. TRATAMIENTO FARMACOLÓGICO (TABLA XIV)
La base del tratamiento de la EPOC estable son los broncodilatadores de larga duración (BDLD). El
tratamiento depende de la sintomatología y riesgo (GOLD) y del fenotipo (GesEPOC). El fenotipo no
agudizador se trata con BDLD, en monoterapia o combinados. El fenotipo mixto requiere BDLD combinados
con corticoides inhalados (CI). El fenotipo agudizador con enfisema se basa en BDLD y se añaden CI si no se
consigue el control. Y, por último, el fenotipo agudizador con bronquitis crónica se trata con BDLD, a los
que se añaden CI o inhibidores de la fosfodiesterasa 4 para reducir la frecuencia de exacerbaciones. En
casos con infección bronquial crónica documentada y bronquiectasias, la antibioterapia crónica (bien con
macrólidos o, menos estudiados, con fluorquinolonas) reduce la frecuencia de exacerbaciones.
Tabla XIV. Tratamiento farmacológico de la enfermedad pulmonar obstructiva crónica según los fenotipos y los niveles de gravedad.
2.1. Broncodilatadores
2.1.1. Inhaladores de acción corta: se encuentran los agonistas beta-2 (SABA), que incluyen el
salbutamol (100 μg por pulsación) y la terbutalina (500 μg), y los anticolinérgicos (SAMA) como el bromuro
de ipratropio (20 μg). Son útiles en el rápido control de los síntomas.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [453]
[29] ASMA Y ENFERMEDAD PULMONAR OBSTRUCTIVA CRÓNICA
2.1.2. Inhaladores de acción prolongada: incluye los agonistas beta-2 de vida media larga (LABA)
como el salmeterol y el formoterol, y los de ultra larga como son el vilanterol, el olodaterol y el indacaterol.
Entre los anticolinérgicos de larga acción (LAMA), se encuentran el bromuro de tiotropio, el aclidinio, el
umeclidinio y el glicopirronio. Reducen la sintomatología y el número de exacerbaciones y aumentan la
tolerancia al ejercicio, la función pulmonar y la calidad de vida.
2.1.3. Combinación de glucocorticoides inhalados y agonistas beta-2 de acción prolongada:
mejoran la funció n pulmonar y la sintomatología, además de reducir la gravedad y frecuencia de las
exacerbaciones. Se indica en pacientes con EPOC grave (con dos o más exacerbaciones anuales) o con
fenotipo asma-EPOC. Los pacientes deben enjuagarse la boca después de cada uso para prevenir la
candidiasis oral y la disfonía.
Las diferentes formas de presentación comercializadas actualmente y su posología se muestran en
la tabla XV.
Tabla XV. Posología de algunos broncodilatadores inhalados utilizados en la enfermedad pulmonar obstructiva crónica.
2.2. Metilxantinas: la más utilizada es la teofilina. Es poco eficaz y muy tóxica, con un margen
beneficio/riesgo estrecho, además de múltiples interacciones farmacológicas. Requiere monitorización
durante 1-2 semanas después del ajuste de la dosis y, por lo menos, dos veces al año, intentando mantener
niveles en sangre en el rango 5-15 mg/ml. Una dosis inicial prudente puede ser 200 mg/12 h.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [454]
[29] ASMA Y ENFERMEDAD PULMONAR OBSTRUCTIVA CRÓNICA
2.3. Agentes mucolíticos-antioxidantes: entre ellos se encuentran la carbocisteína y la N-
acetilcisteína. Tienen un efecto modesto en la reducción de las exacerbaciones, menor que el de los
broncodilatadores o corticoides inhalados.
2.4. Inhibidores de la fosfodiesterasa 4 (PDE4): el único comercializado es el roflumilast. Está
indicado en el fenotipo exacerbador con bronquitis crónica. Reduce el número de exacerbaciones, con
efecto modesto en la obstrucción al flujo aéreo o en los síntomas. Hay que vigilar estrechamente al
paciente, pues son frecuentes los efectos secundarios, sobre todo la pérdida de peso y los efectos
gastrointestinales.
2.5. Alfa-1-antitripsina: se recomienda en pacientes con fenotipo homocigoto PiZZ, obstrucción al
flujo aéreo y niveles séricos bajos de esta enzima. Se aconseja al paciente que se vacune contra la hepatitis
B antes de dicho tratamiento de refuerzo.
2.6. Corticosteroides orales: no se recomiendan como terapia de mantenimiento.
2.7. Oxigenoterapia crónica domiciliaria (OCD): se ha demostrado que reduce la mortalidad y
mejora la función física y mental en los pacientes con EPOC e IR. Sus indicaciones se especifican en la tabla
XVI.
Tabla XVI. Indicaciones de oxigenoterapia crónica domiciliaria.
2.8. Ventilación mecánica no invasiva domiciliaria: podría ser beneficiosa en pacientes con IR
hipercápnica y múltiples ingresos con fallo ventilatorio, aunque no hay una clara evidencia de que
pacientes con una EPOC estable se beneficien de VMNI domiciliaria. Otra entidad son los pacientes con
síndrome overlap, de EPOC y SAHS u otra alteración ventilatoria o del centro respiratorio asociada.
2.9. Tratamiento quirúrgico
2.9.1. Trasplante pulmonar: mejora la función pulmonar, la tolerancia al esfuerzo, el intercambio
gaseoso y la calidad de vida y la supervivencia (cuando está bien indicado).
Los criterios de derivación para la valoración inicial del candidato a trasplante en el Hospital 12 de
Octubre son:
FEV1 < 40% o índice BODE > 5, con deterioro clínico-funcional a pesar de: máximo tratamiento
farmacoló gico, abandono del tabaco al menos 6 meses antes, rehabilitació n respiratoria
correcta, OCD y cirugía reductora de volumen (si estuviese indicada).
FEV1 ≥ 40% con frecuentes reingresos por exacerbaciones agudas (> 3 al año) con hipercapnia.
Los criterios de trasplante pulmonar son un BODE ≥ 7 o al menos alguno de los siguientes: FEV1
posbroncodilatador < 20-25%, DLCO < 20%, hospitalizaciones previas con agudización e hipercapnia con
PaCO2O > 55 mm Hg, hipertensión pulmonar o cor pulmonale a pesar de la oxigenoterapia
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [455]
[29] ASMA Y ENFERMEDAD PULMONAR OBSTRUCTIVA CRÓNICA
2.9.2. Bullectomía: en pacientes con bullas que ocupan más de un tercio del hemitórax
acompañadas de evidencia radiológica de compresión del parénquima pulmonar y función pulmonar
relativamente conservada.
2.9.3. Cirugía de reducción de volumen pulmonar (LVRS): indicada en pacientes con enfisema
predominante en los ló bulos superiores y poca capacidad de ejercicio. Las características ideales de los
pacientes candidatos a esta cirugía son:
Edad menor de 75 años.
Disnea severa a pesar del tratamiento médico óptimo y rehabilitación.
Abstinencia de tabaco desde al menos 6 meses antes.
Obstrucción del flujo aéreo con FEV1 entre 20-45%.
DLCO mayor del 20%.
Incremento del volumen residual mayor del 150%.
TC con hiperinsuflación y enfisema heterogéneo con predominio en los lóbulos superiores.
Una PM6M con distancia mayor de 140 metros postrehabilitación.
2.9.4. Válvulas y coils endobronquiales: como con la LVRS, su objetivo es favorecer el colapso de
áreas enfisematosas con hiperinsuflación, mejorando la mecánica diafragmática y el trabajo respiratorio,
pero sin la morbilidad y mortalidad de la LVRS. Puede hacerse con válvulas endobronquiales (Zephyr® o
IBV®) o con coils (PneumRx®). Aunque están aprobados en algunos países, por el momento no existe
evidencia suficiente para su uso fuera de ensayos clínicos.
7. EXACERBACIÓN DE LA ENFERMEDAD PULMONAR OBSTRUCTIVA CRÓNICA
Deterioro de la situación clínica basal del paciente de inicio agudo que cursa con aumento de la
disnea, incremento de la expectoración y/o aumento de la purulencia del esputo (criterios de Anthonissen),
o la combinación de cualquiera de estos tres síntomas, que requiere un cambio terapéutico.
1. ETIOLOGÍA (TABLA XVII)
Tabla XVII. Etiología de la exacerbación aguda de la enfermedad pulmonar obstructiva crónica.
2. VALORACIÓN INICIAL
2.1. Criterios de asistencia hospitalaria
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [456]
[29] ASMA Y ENFERMEDAD PULMONAR OBSTRUCTIVA CRÓNICA
Se deben considerar factores asociados al paciente, la gravedad de la exacerbación, la necesidad de
monitorización, pruebas diagnósticas y tratamiento y el fracaso terapéutico ambulatorio (Tabla XVIII).
Tabla XVIII. Factores asociados a necesidad de asistencia hospitalaria.
2.2. Pruebas complementarias en urgencias
2.2.1. Gasometría arterial. Antes de iniciar el tratamiento (siempre y cuando la situación clínica lo
permita), obtenida de manera basal (si el paciente tiene OCD, extraer bajo su suplemento de oxígeno
habitual). Es importante para valorar la acidosis respiratoria y la hipoxemia.
2.2.2. Pulsioximetría. Identifica la hipoxemia y la respuesta al tratamiento.
2.2.3. Analítica completa. Con hemograma, glucosa, urea, creatinina, sodio, potasio y reactantes de
fase aguda. La determinación de péptido natriurético cerebral (proBNP) puede ayudar a discriminar la
disnea de causa cardiaca.
2.2.4. Radiografía posteroanterior y lateral de tórax. Identifica neumonía, neumotórax, derrame
pleural o IC izquierda.
2.2.5. Tinción de Gram y cultivo de esputo. No se debe solicitar a todos los pacientes con EPOC.
Sus indicaciones aparecen descritas en la tabla XVII.
3. TRATAMIENTO
3.1. Tratamiento ambulatorio
Se debe continuar el tratamiento habitual del paciente. Además, es preciso optimizar el
tratamiento inhalatorio con broncodilatadores de acción corta. Usualmente se prescriben 2-4 inhalaciones
(hasta un máximo de 6) cada 4-6 horas de bromuro de ipratropio (20 μg/pulsación) junto con salbutamol
(100 μg/pulsación) o terbutalina (500 μg/pulsación).
Se debe indicar antibioterapia si existe además esputo purulento, habitualmente durante 5-7 días
(suele prolongarse en caso de Pseudomonas aeruginosa). Algunas opciones posibles son: amoxicilina/ácido
clavulánico 875 mg/125 mg/8 horas, cefditoren 200-400 mg/12 h, levofloxacino 500 mg-750 mg/24 h o
moxifloxacino 400 mg/24 h, durante 5 a 7 días. Se debe considerar el uso de glucocorticoides sistémicos en
pacientes con exacerbación de EPOC grave y en casos de exacerbación leve o moderada con evolución
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [457]
[29] ASMA Y ENFERMEDAD PULMONAR OBSTRUCTIVA CRÓNICA
inicial desfavorable. Se recomienda prednisona 0,5 mg/kg/día (dosis máxima 40 mg/día) o equivalente (5
mg de prednisona equivalen a 4 mg de metilprednisolona o a 20 mg de hidrocortisona), durante 5-10 días.
Se deberá realizar control evolutivo a las 72 horas.
3.2. Tratamiento hospitalario
3.2.1. Antibioterapia
Está indicada cuando existe esputo purulento, en las exacerbaciones graves y cuando se requiera
ventilación mecánica. Los antibióticos recomendados son: levofloxacino 500-750 mg/24 h iv o vo,
moxifloxacino 400 mg/24 h iv o vo, amoxicilina-ácido clavulánico 1-2 g/8 h iv (o 875/125 mg vo), ceftriaxona
1-2 g/12-24 h iv. En caso de sospecha de infección por Pseudomonas spp, se puede utilizar ceftazidima 1-2
g/8 h iv, cefepime 1-2 g/12 h iv, piperacilina-tazobactam 4 g/0,5 g/6-8 h iv o levofloxacino 750 mg iv o vo.
En caso de sospecha clínica y epidemiológica de gripe, es posible añadir oseltamivir 75 mg/12 h vo durante
5 días. La antibioterapia se debe ajustar según criterio médico sobre la base de la respuesta clínica, analítica
y los resultados microbiológicos.
3.2.2. Broncodilatación
Para el manejo sintomático de la disnea, se inicia tratamiento por vía inhalatoria de broncodilatadores de
acción corta. Se comienza con anticolinérgicos tipo bromuro de ipratropio de 500 μg asociado a agonistas
beta-2 de acción corta como salbutamol 2,5-5 mg/6 h. Para la nebulización se diluyen con suero fisiológico
al 0,9% hasta un volumen de 3 ml (algunos preparados ya no precisan esta dilución) y se nebulizan durante
5-10 minutos. Es posible repetir dicha dosis a la hora y a las dos horas si no existiese mejoría. La
nebulización se consigue con cazoletas apropiadas y flujo de aire comprimido (preferiblemente) o de
oxígeno a partir de 8 l/min.
En caso de hipercapnia crónica o patología asociada a hipoventilación nocturna, las nebulizaciones
pueden exacerbar dicha hipercapnia, por lo que no son recomendables. De ser imprescindible, se debe
administrar durante un máximo de 5 minutos con vigilancia clínica.
Otra opción es utilizar inhaladores de dosis medida (MDI) para sustituir las nebulizaciones. Es
importante saber que cada ampolla de nebulización de bromuro de ipratropio contiene 500 μg y cada
pulsación del MDI es 20 μg (la dosis de 500 μg equivale a 25 pulsaciones); lo mismo sucede con el
salbutamol (la dosis de 2,5 mg equivale a 25 pulsaciones).
3.2.3. Glucocorticoides
Se recomienda prednisona de 40 mg (o su equivalente) al día durante 5-10 días, aunque existe evidencia
insuficiente sobre su duración óptima. Es preferible la terapia con metilprednisolona (30-40 mg). La
budesonida nebulizada, aunque costosa, puede ser una alternativa a los glucocorticoides orales.
3.2.4. Oxigenoterapia
Indicada para tratar la IR agudizada. Su administración con mascarillas tipo Venturi permite obtener una
fracción inspiratoria de oxígeno (FiO2) más constante. Tras alcanzar cierta estabilidad en el patrón
respiratorio, puede administrarse mediante gafas nasales.
El objetivo es conseguir una SpO2 entre 88% y 92% para evitar el riesgo de encefalopatía
hipercápnica, puesto que la administración de oxígeno puede asociarse a mayor hipercapnia,
particularmente si los niveles de presión parcial de oxígeno (pO2) o SpO2 son altos, debido a varios
mecanismos (cambios en la distribución ventilación/perfusión, efecto Haldane y, en menor medida,
reducción del estímulo respiratorio e hipoventilación central). En cualquier caso, es necesario mantener un
nivel mínimo de oxígeno (SpO2 en torno al 88 % o pO2 mayor de 50-55 mm Hg) con independencia de la
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [458]
[29] ASMA Y ENFERMEDAD PULMONAR OBSTRUCTIVA CRÓNICA
retención de CO2, y valorar VMNI en caso de que se desencadene acidosis respiratoria (y nunca en esa
situación retirar la oxigenoterapia, permitiendo hipoxemia grave).
3.2.5. Ventilación mecánica no invasiva
Está indicada en el caso de hipercapnia con acidosis respiratoria en la que no exista respuesta rápida al
tratamiento inicial. En caso de disnea con uso de la musculatura accesoria y respiración abdominal con
riesgo de fracaso ventilatorio inminente, puede estar indicada para prevenirlo y evitar la intubación (para
más detalles, ver Capítulo 35. “Principios de ventilación mecánica”).
3.2.6. Ventilación mecánica invasiva
Se valorará en caso de fracaso terapéutico o contraindicación de la VMNI, hipoxemia refractaria, acidosis
severa (pH < 7,25), complicaciones cardiovasculares, fallo multiorgánico o parada respiratoria (para más
detalles, ver Capítulo 35. “Principios de ventilación mecánica”).
3.2.7. Otras medidas complementarias
Pueden destacarse:
Colocar al paciente en sedestación o en decúbito supino con la cabeza elevada a unos 30°.
Diuréticos en caso de datos clínicos de IC.
Prevención con inhibidores de secreción gástrica en pacientes con acidosis respiratoria o
situación de estrés.
Prevención de trombosis venosa profunda con heparinas de bajo peso molecular en pacientes
con escasa movilidad.
Favorecer la movilización y la deambulación precoz una vez estabilizado el paciente, e
incentivar la tos eficaz para conseguir un mejor control de las secreciones.
BIBLIOGRAFÍA
Agusti A, Edwards LD, Celli B, Macnee W, Calverley PM, Mullerova H, et al. Characteristics, stability and
outcomes of the 2011 GOLD COPD groups in the ECLIPSE cohort. Eur Respir J. 2013;42(3):636-46.
Albert P, Agusti A, Edwards L, Tal-Singer R, Yates J, Bakke P, et al. Bronchodilator responsiveness as a
phenotypic characteristic of established chronic obstructive pulmonary disease. Thorax.
2012;67(8):701-8.
Associació Pneumología Sant Pau. Protocolos y Procedimientos del Servicio de Neumología del
Hospital de la Santa Creu i Sant Pau. 2ª ed. Barcelona: Ergon; 2015.
Barnes PJ. Asma. En: Kasper D, Fauci A, Hauser S, Longo D, Larry J, Loscalzo J, editores. Harrison’s
Principios de Medicina Interna. 19ª ed. USA: McGraw-Hill; 2016. pp. 1669-80.
Cataluña JJ, Martínez-García MA, Sánchez L, Perpiña T, Román S. Severe exacerbations and BODE
index: two independent risk factors for death in COPD patients. Respir Med. 2009;103(5):692-9.
Celli BR, Cote CG, Marin JM, Casanova C, Montes-de Oca M, Méndez RA, et al. The body-mass index,
airflow obstruction, dyspnea, and exercise capacity index in chronic obstructive pulmonary disease. N
Engl J Med. 2004;350(10):1005-12.
Desai T, Karlinsky J. EPOC: Manifestaciones clínicas, diagnóstico y tratamiento. En: Crapo J, Glassroth
J, Karlinsky J, Talmadge K. Baum’s Neumología. 7ª ed. Philadelphia: Lippincott Williams & Wilkins;
2007. pp. 231-56.
Domínguez Ortega J, Martín Iglesias A, Martínez Alonso JC, Muñoz Cano R. Tratamiento del asma.
Tratado de Alergología. 2ª ed. Madrid: Ergon; 2015. pp. 681-98.
Entrenas Costa LM, Jurado Gámez B, Jiménez Murillo L, Martín Pérez JM, Calderón de la Barca
Gázquez. Crisis asmática. En: Jiménez Murillo L, Montero Pérez FJ, editores. Medicina de Urgencias y
Emergencias: Guía diagnóstica y protocolos de actuación. 5ª ed. Madrid: Elsevier; 2015.
Global Strategy for the Diagnosis, Management, and Prevention of Chronic Obstructive Pulmonary
Disease. Global Initiative for Chronic Obstructive Lung Disease (GOLD) Updated 2016 [consultado: 25
de agosto de 2016]. Disponible en: http://goldcopd.org/global-strategy-diagnosis-management-
prevention-copd-2016/.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [459]
[29] ASMA Y ENFERMEDAD PULMONAR OBSTRUCTIVA CRÓNICA
Grupo de Trabajo de GesEPOC. Guía de Práctica Cínica para el Diagnóstico y Tratamiento de Pacientes
con Enfermedad Pulmonar Obstructiva Crónica (EPOC)-Guía Española de la EPOC (GesEPOC). Arch
Bronconeumol. 2012;48(1): 2-58.
Grupo de Trabajo de Trasplante Pulmonar. Protocolo PROT-TXP-01. Trasplante Pulmonar. 5ª ed.
Madrid; 2014.
Han M, Lazarus S. COPD: Clinical Diagnosis and Management. En: Courtney-Broaddus V, Mason R,
Ernst J, King T, Lazarus S, Murray J, et al. Murray & Nadel’s Textbook of Respiratory Medicine. 6ª ed.
Philadelphia: Elsevier Saunders; 2016. pp. 767-85.
Horak F, Doberer D, Eber E, Horak E, Pohl W, Riedler J, et al. Diagnosis and management of asthma-
Statement on 2015 (GINA Guidelenes). Wien Klin Wochenschr. 2016 Jul 1 [Epub ahead of print].
Jurado-Gámez B, Torres-Murillo JM, Jiménez-Murillo L, Torres-Degayón V, Berlango-Jiménez A, Muñoz-
Cabera L. EPOC descompensada. En: Jiménez-Murillo L, Montero-Pérez FJ. Medicina de Urgencias y
Emergencias. Guía Diagnóstica y Protocolos de Actuación. 5ª ed. Barcelona: Elsevier; 2015. pp. 254-
60.
Menéndez J. EPOC agudizada. En: Varona-Arche JF, Masa CM, Menéndez JM. Urgencias Médicas:
Claves Diagnósticas y Terapéuticas. Madrid: GSK; 2011. pp. 122-5.
Miravitlles M, Soler-Cataluña JJ, Calle M, Molina J, Almagro P, Quintano JA, et al. Guía Española de la
EPOC (GesEPOC). Tratamiento Farmacológico de la EPOC estable. Arch Bronconeumol. 2012;48:247-
57.
Miravitlles M, Soler-Cataluña JJ, Calle M, Molina J, Almagro P, Quintano JA, et al. Guía Española de la
EPOC (GesEPOC). Update 2014. Arch Bronconeumol. 2014;50(1):1-16.
Nouira S, Marghli S, Belghith M, Besbes L, Elatrous S, Abroug F. Once daily oral ofloxacin in chronic
obstructive pulmonary disease exacerbation requiring mechanical ventilation: a randomised placebo-
controlled trial. Lancet. 2001;358(9298):2020-5.
Plaza Moral V. Comité ejecutivo de la GEMA. Guía Española para el Manejo del Asma (GEMA 4.0). Arch
Bronconeumol. 2015;51(Supl 1): 2-54.
Quince S, Bobolea I, Barranco P. Asma: actualización terapéutica. Med Clin (Barc). 2014;142:317-
22.Reilly JJ, Silverman EK, Shapiro SD. Enfermedad Pulmonar Obstructiva Cronica. En: Kasper D, Fauci
A, Hauser S, Longo D, Larry J, Loscalzo J, editores. Harrison’s Principios de Medicina Interna. 19ª ed.
USA: McGraw-Hill; 2016. pp. 1700-7.
Rodríguez Rodríguez M, Pérez Francés C, Pascual Miravalles MJ. Clínica y diagnóstico del asma.
Tratado de Alergología. 2ª ed. Madrid: Ergon; 2015; pp. 607-21.
Shifren A, Park J, Yusen R. Enfermedad Pulmonar Obstructiva Crónica. En: Shifren A, Lin T. Manual
Washington de Especialidades Médicas. 22ª ed. USA: Wolters Kluwers Health; 2014. pp. 64-72.
Soler J, Martínez MA. Enfermedad Pulmonar Obstructiva Crónica: tratamiento de las exacerbaciones.
En: Álvarez-Sala JL, Casán P, Rodríguez F, Rodríguez JL, Villena-Garrido V. Neumología Clínica. Madrid:
Elsevier; 2010. pp. 197-204.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [460]
[30] BRONQUIECTASIAS
30.Bronquiectasias
Néstor Luis Rodríguez Meleán.
Neumología
Clara Cabañuz Rocatallada.
Medicina Interna
Asesora: María Teresa Martínez Martínez. Médica Adjunta de Neumología
I. INTRODUCCIÓN
Las bronquiectasias (BQ) consisten en dilataciones anormales e irreversibles de los bronquios con
alteración del epitelio ciliar. Son el resultado final de enfermedades diferentes que tienen puntos de
manejo en común. Por lo general, se han diferenciado en BQ debidas a fibrosis quística (FQ) y BQ no FQ,
afectando las segundas a una población heterogénea de pacientes y con etiologías muy diferentes.
Desde la introducción de los antibióticos, la incidencia de las BQ ha ido en descenso. La prevalencia
varía en diferentes poblaciones; en Estados Unidos, por ejemplo, se ha estimado en 52 casos/100.000
adultos y ha aumentado anualmente del 2000 al 2007 un 8,74%, incremento que puede estar relacionado
con la realización de tomografía computarizada (TC) por otros motivos. Son más frecuentes en mujeres, en
población mayor y en asiáticos.
Respecto a la fisiopatología, varios modelos apuntan a que, en personas susceptibles, se desarrolla
una gran respuesta inflamatoria a una infección o lesión pulmonar. Ello provoca un daño estructural de la
vía aérea que permite la estasis mucosa, lo que favorece las infecciones crónicas y que dicho ciclo se
perpetúe. Por lo tanto, el tratamiento ha de estar enfocado a romper este ciclo.
II. ETIOLOGÍA
En la tabla I se resume la etiología de las bronquiectasias.
La frecuencia de las diferentes etiologías en los países desarrollados ha cambiado mucho: han
disminuido las causas postinfecciosas, mientras que las producidas por enfermedades subyacentes que
predisponen a la infección e inflamación bronquial se han incrementado.
Todavía hay un porcentaje considerable de pacientes en los que se desconoce la causa (un 26-53%
según las series). Una historia clínica detallada y la realización de una TC permiten en muchos casos
sospechar la causa e indicar las pruebas diagnósticas necesarias.
Es muy importante la búsqueda sistemática de la etiología, especialmente de las tributarias de un
tratamiento específico, ya que tiene implicaciones clínicas relevantes en el manejo y en el pronóstico.
III. CLÍNICA
1. SÍNTOMAS
Infecciones respiratorias de repetición.
Entre episodios, el paciente está asintomático o tiene expectoración crónica (75-100%)
(mucosa, mucopurulenta o purulenta).
Expectoración hemoptoica o hemoptisis recidivante (51-45%).
Clínica de hiperreactividad bronquial.
Disnea según el grado de afectación de la función pulmonar (72-83%).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [461]
[30] BRONQUIECTASIAS
Dolor torácico de carácter pleurítico por afectación de la pleura visceral (31%).
Astenia y pérdida de peso.
Sinusitis, en especial las debidas a FQ, discinesia ciliar primaria, inmunodeficiencias primarias,
síndrome de Young, síndrome de las uñas amarillas o panbronquiolitis difusa.
Tabla I. Etiología de las bronquiectasias.
2. EXPLORACIÓN FÍSICA
Normal, estertores crepitantes, roncus y/o sibilancias.
En la enfermedad avanzada aparecen acropaquias, caquexia, signos de insuficiencia respiratoria
o cor pulmonale.
IV. DIAGNÓSTICO
Sospechar en adultos no fumadores que presenten: tos productiva, expectoración diaria,
hemoptisis, historia de síntomas de larga data, aislamiento de Pseudomonas aeruginosa en el esputo; y en
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [462]
[30] BRONQUIECTASIAS
pacientes con enfermedad pulmonar obstructiva crónica (EPOC) si la respuesta al tratamiento no es la
adecuada, presentan una lenta recuperación después de las agudizaciones o son exacerbadores frecuentes.
Dado que el concepto de BQ es eminentemente morfológico, la primera aproximación diagnóstica
ha de basarse en técnicas de imagen.
Figura 1. Aproximación diagnóstica de las bronquiectasias.
La radiografía de tórax aporta imágenes inespecíficas, escasa información sobre la extensión de la
enfermedad y un porcentaje no despreciable de falsos positivos y negativos.
Algunos de los signos radiológicos de BQ más destacables al realizar una radiografía de tórax son:
Opacidades lineales paralelas que corresponden a bronquios dilatados con la pared engrosada.
Dan lugar al signo del “raíl de tranvía”.
Imágenes aéreas con pared definida, fina o gruesa, que forman el signo del “anillo de sello” (el
anillo es el bronquio dilatado y el vaso es el sello), o a imágenes quísticas, con o sin nivel
hidroaéreo.
Opacidades tubulares u ovoides (impactos mucoides), que corresponden a bronquios repletos
de moco o líquido. En algunas ocasiones los bronquios, llenos de secreciones, pueden
visualizarse como imágenes lineales densas en forma de “Y”, de “V” o en “dedo de guante”.
El “gold estándar” para el diagnóstico de BQ es la TC de alta resolución sin contraste, con cortes de
1 mm a intervalos de 10 mm, en inspiración máxima. Presenta una sensibilidad y especificidad mayores del
90%.
Permite, además, valorar la extensión y morfología de las BQ (cilíndricas, varicosas o quísticas). Los
criterios diagnósticos de BQ por TC son:
Signos directos: dilatación bronquial con una relación broncoarterial >1-1,5, signo de “anillo de
sello”, falta de afilamiento de los bronquios y visualización de bronquios a 1 cm de la pleura.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [463]
[30] BRONQUIECTASIAS
Signos indirectos: engrosamiento de la pared bronquial, pérdida de volumen lobular, patrón en
mosaico, nódulos en árbol en brote y tapones de moco.
Existen diferencias en la distribución y morfología de las BQ según distintas etiologías, aunque los
hallazgos radiológicos tienen un papel limitado para establecer un diagnóstico etiológico:
Según la localización: campos superiores (tuberculosis y FQ), centrales (aspergilosis
broncopulmonar alérgica, ABPA), unilaterales (sugieren obstrucción local por cuerpo extraño o
tumor endobronquial).
Malformaciones congénitas: situs inversus, traqueobroncomegalia.
Enfisema por déficit de alfa-1-antitripsina.
Micobacterias no tuberculosas (MNT): múltiples nódulos pequeños y “árbol en brote”, de
predominio en la língula y el lóbulo medio.
Además, en todo paciente con BQ se debe realizar:
Espirometría y gasometría arterial basal.
Cultivo de esputo para bacterias, micobacterias y hongos.
Completar el estudio en función de la sospecha clínica (Figura 1).
1. DIAGNÓSTICO DE AGUDIZACIÓN
Presentación de forma aguda y mantenida (al menos 72 horas) de aumento de la tos, cambios en
las características del esputo (incremento del volumen, la consistencia, la purulencia o hemoptisis) y/o
aumento de la disnea no debidos a otras causas.
La agudización puede asociarse a cambios en la densidad bacteriana de la flora colonizadora o a la
adquisición de un microorganismo nuevo.
La agudización grave cursa con taquipnea, insuficiencia respiratoria aguda, insuficiencia respiratoria
crónica agudizada, deterioro significativo de la saturación de oxígeno o de la función respiratoria,
hipercapnia, fiebre de >38 °C, hemoptisis, inestabilidad hemodinámica y/o deterioro del estado cognitivo.
2. COLONIZACIÓN BRONQUIAL
Presencia de una población bacteriana que no induce una respuesta inflamatoria con repercusión
clínica, a excepción de expectoración mucosa.
Se diferencian:
Inicial: primer cultivo positivo en fase estable de un microorganismo no aislado en cultivos
periódicos previos.
Intermitente: cultivos positivos y negativos para un mismo microorganismo, con al menos un
mes de diferencia, en pacientes que no están recibiendo antibiótico contra el mismo. En
general, refleja una colonización crónica con bajos valores cuantitativos, no siempre
detectables en el cultivo de esputo.
Crónica: tres o más cultivos consecutivos positivos para un mismo microorganismo en un
periodo de 6 meses, en muestras separadas entre sí por al menos un mes.
3. INFECCIÓN BRONQUIAL CRÓNICA
Presencia de población bacteriana que induce una respuesta inflamatoria que se manifiesta
clínicamente con expectoración purulenta persistente. Puede acompañarse de infecciones respiratorias de
repetición y afectación sistémica, con febrícula, astenia y/o pérdida de peso.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [464]
[30] BRONQUIECTASIAS
V. TRATAMIENTO
Los objetivos son identificar y tratar las causas específicas para prevenir la progresión de la
enfermedad, mantener y mejorar la función respiratoria, reducir las exacerbaciones y mejorar la calidad de
vida disminuyendo los síntomas (Figura 2).
Figura 2. Aproximación diagnóstica de las bronquiectasias.
1. TRATAMIENTO DE LA AGUDIZACIÓN (TABLAS II Y III)
Tabla II. Criterios de ingreso hospitalario.
Se basará en:
Antibioterapia.
Facilitar la eliminación de las secreciones (ver apartados 7, 8 y 9).
Tratamiento del broncoespasmo asociado (ver apartados 5 y 6).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [465]
[30] BRONQUIECTASIAS
Tabla III. Tratamiento antibiótico en diferentes situaciones clínicas (extraído de Monserrat Vendrell M, et al. 2008).
Respecto a la antibioterapia, se deben tener en cuenta los siguientes aspectos:
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [466]
[30] BRONQUIECTASIAS
Tomar una muestra para cultivo de esputo y, posteriormente, iniciar el tratamiento antibiótico
empírico de forma inmediata, en espera del resultado del cultivo.
Dirigir el tratamiento antibiótico empírico sobre la base de la presencia o no de una
colonización o infección bronquial crónica previa conocida.
Tener en cuenta el riesgo de colonización por P. aeruginosa.
Lugar y vía de administración:
Las agudizaciones leves pueden tratarse ambulatoriamente por vía oral.
La vía intravenosa se utilizará en casos de agudizaciones graves, infección bronquial
crónica por microorganismos resistentes a los antibióticos por vía oral, falta de
respuesta al antibiótico oral y en agudizaciones por Pseudomonas spp en pacientes con
FQ cuando no se haya aislado con anterioridad.
Añadir un antibiótico por vía inhalada al tratamiento antibiótico oral o intravenoso en
las exacerbaciones no ha demostrado aportar beneficios clínicos.
El antibiótico empírico debe modificarse dependiendo del cultivo de esputo y el antibiograma.
Pueden aparecer variantes de un mismo microorganismo, con diferente patrón de sensibilidad frente a los
antimicrobianos. Sin embargo, no siempre hay buena correlación entre la sensibilidad in vitro y la respuesta
al tratamiento. Por otra parte, cuando se utilizan antimicrobianos nebulizados, los criterios de
interpretación del antibiograma deberían adecuarse al hecho de que con esta vía de administración se
alcanzan concentraciones en la mucosa mucho más altas.
Si no hay mejoría clínica, se recomienda usar antibióticos con alto grado de penetración en las
secreciones respiratorias, a dosis elevadas, y administrarlos hasta que el esputo deje de ser purulento,
durante un periodo mínimo de 10 días.
En casos de infección por Pseudomonas spp, se recomienda terapia durante 14-21 días (en la
exacerbación leve, tratar con ciprofloxacino 750 mg/12 horas por vía oral en el domicilio; en la
exacerbación grave, tratar con ceftazidima 2 g/8 horas por vía intravenosa, pudiendo asociar un
aminoglucósido por vía intravenosa si se presentan más de dos resistencias en el antibiograma).
2. TRATAMIENTO DE LA COLONIZACIÓN BRONQUIAL INICIAL
No existe evidencia para indicar tratamiento antibiótico, excepto en el caso del primer aislamiento
de Pseudomonas spp en BQ debidas a FQ, con el objetivo de erradicarla para retrasar la colonización
crónica. Se recomienda la administración de ciprofloxacino oral junto a un antibiótico inhalado
(tobramicina o colistina) durante 2 semanas, o bien dos antibióticos intravenosos durante 14-21 días,
continuando posteriormente en ambos casos con antibiótico inhalado durante 3 meses.
3. INFECCIÓN BRONQUIAL CRÓNICA
El tratamiento se basa en la administración prolongada de antibiótico y en facilitar el drenaje de
secreciones. Se indica cuando la erradicación de bacterias patógenas no es exitosa y el paciente presenta
más de tres exacerbaciones por año que afectan a su calidad de vida. La elección del antibiótico depende
del microorganismo causante de la infección y del antibiograma. La pauta y el tiempo de administración
dependen del control de la infección (obtención y mantenimiento del esputo lo más mucoso posible y
disminución de las agudizaciones). La vía de administración puede ser oral o inhalada. Esta última es de
elección en caso de tres o más exacerbaciones al año, ausencia de respuesta clínica con el antibiótico oral o
de efectos secundarios con el mismo, y en la infección por Pseudomonas spp.
Los antibióticos inhalados deben administrarse con nebulizadores específicos para este fin (Tabla
IV). Pueden producir broncoespasmo, aumento de la disnea o molestias torácicas, que deben controlarse.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [467]
[30] BRONQUIECTASIAS
Se recomienda la administración de un broncodilatador de acción rápida y el drenaje de las secreciones
antes de su administración.
Tabla IV. Antibióticos comercializados para uso nebulizado (extraído de Olveira C, et al. 2014).
4. MACRÓLIDOS
Disminuyen el número de agudizaciones, probablemente por modulación de la respuesta
inflamatoria y la capacidad de interferir con la formación de biopelículas. Se recomienda en pacientes con
afectación funcional severa (o moderada, pero con progresión rápida a pesar del tratamiento adecuado),
infección bronquial crónica por Pseudomonas spp o por otros microorganismos con control clínico difícil a
pesar de un tratamiento adecuado.
El fármaco con el que se dispone de mayor experiencia es la azitromicina a dosis de 250 mg/ diarios
durante 12 meses o 500 mg/3 veces por semana durante 6 meses. Es recomendable el control de la función
hepática en las primeras semanas del tratamiento y a intervalos regulares de 6 meses, así como la
investigación de MNT en secreciones respiratorias antes de iniciar el tratamiento (los pacientes en que se
aíslen MNT no deberían recibir monoterapia con macrólidos).
5. BRONCODILATADORES INHALADOS
Están indicados en pacientes con obstrucción reversible de la vía aérea en la prueba
broncodilatadora con beta-2 agonista o anticolinérgico, así como antes de la realización de fisioterapia y de
la aerosolterapia antibiótica.
6. CORTICOIDES INHALADOS
Podrían estar indicados solo si existe clínica de hiperreactividad bronquial o reversibilidad en la
prueba broncodilatadora, sobre todo combinados con beta-2 agonistas. No se recomienda el uso de
corticoides sistémicos.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [468]
[30] BRONQUIECTASIAS
7. MUCOLÍTICOS
La solución salina hipertónica al 7% nebulizada puede facilitar la expectoración, ya que reduce la
viscosidad del moco. La primera vez que se administre se debe medir el pico flujo espiratorio previo y 5
minutos posterior al tratamiento. La desoxirribonucleasa puede reducir las agudizaciones en la FQ con
afectación pulmonar leve o moderada, pero en BQ no FQ puede aumentar el número de exacerbaciones,
por lo que no se recomienda. La bromhexina puede disminuir la tos y facilitar la eliminación de secreciones.
8. REHABILITACIÓN RESPIRATORIA
Los pacientes deben entrar en programas de rehabilitación respiratoria dirigidos por profesionales
especializados, con el objetivo de facilitar la eliminación de secreciones y mejorar tanto la tolerancia física
como la calidad de vida.
9. FISIOTERAPIA RESPIRATORIA
Es útil en pacientes con hipersecreción bronquial (30 ml/día); existen varias técnicas, aunque no
hay evidencia de cuál es la más efectiva. Se debe realizar 3 veces al día, después del tratamiento
broncodilatador y previamente a los antibióticos inhalados.
10. EJERCICIO
Se recomienda practicar ejercicio moderado a intenso durante 30 mins/día, de 3 a 4 veces/semana.
11. TRATAMIENTO NUTRICIONAL
Este merece especial atención durante las agudizaciones e ingresos. Ofrecer consejo dietético
individualizado. Se recomienda añadir suplementos orales en personas con índice de masa corporal (IMC)
menor de 20 kg/m2.
12. TRATAMIENTO QUIRÚRGICO
12.1. Cirugía
La resección pulmonar se puede considerar en pacientes con afectación localizada, pero con inadecuado
control con el tratamiento médico. Es el único tratamiento curativo, siempre que se descarten las
enfermedades subyacentes que favorecen su aparición. Está indicada con intención paliativa en casos de
hemoptisis grave con embolización inefectiva, o de zonas abscesificadas no curables con antibiótico.
12.2. Trasplante pulmonar
Las indicaciones de derivación a una consulta de trasplante pulmonar son: volumen espiratorio máximo en
el primer segundo (FEV1) inferior al 30% o pérdida rápida de la función pulmonar, exacerbación que precisa
ingreso en la Unidad de Cuidados Intensivos (UCI), aumento de la gravedad y frecuencia de las
exacerbaciones, neumotórax refractario o recurrente, y hemoptisis grave recurrente no controlada con
embolización. Y las de inclusión en lista de espera: insuficiencia respiratoria crónica que precisa
oxigenoterapia, hipercapnia e hipertensión pulmonar. La colonización por microorganismos
multirresistentes es una contraindicación relativa.
VI. COMPLICACIONES
1. HEMOPTISIS
La hemoptisis masiva es una infrecuente pero grave complicación que pone en riesgo la vida del
paciente. Generalmente, se produce en el seno de una agudización. Además de las medidas habituales, se
debe administrar antibiótico intravenoso, así como evitar los fármacos inhalados y la fisioterapia, al menos
durante las primeras 24-48 horas. La embolización de las arterias bronquiales patológicas o la cirugía son el
tratamiento de elección.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [469]
[30] BRONQUIECTASIAS
La cirugía solo está indicada cuando hay riesgo vital y el origen de la hemorragia está bien
localizado en pacientes en los que no pueda controlarse la hemoptisis con las medidas anteriores (ver
Capítulo 28. “Tos crónica y hemoptisis”).
2. INSUFICIENCIA RESPIRATORIA
Requiere oxígeno y ventilación mecánica no invasiva en caso de acidosis respiratoria aguda o
crónica (ver Capítulo 35. “Principios de ventilación mecánica”).
3. AMILOIDOSIS
Debido a la inflamación crónica, existe riesgo de amiloidosis AA (si bien el diagnóstico es
histolólogico, el análisis de orina podría servir de cribado, ya que el 95% de los pacientes tienen
proteinuria).
VII. INMUNOPROFILAXIS
Se aconseja la administración de la vacuna para virus influenza anual, así como la antineumocócica
y la anti-H. influenzae tipo B según el calendario.
BIBLIOGRAFÍA
Gao YH, Guan WJ, Xu G, Tang Y, Gao Y, Lin ZY, et al. Macrolide therapy in adults and children with non-
cystic fibrosis bronchiectasis: A systematic review and meta-analysis. PLoS One. 2014;9(3):e90047.
Goyal V, Chang AB. Combination inhaled corticosteroids and long-acting beta2-agonists for children and
adults with bronchiectasis. Cochrane Database Syst Rev. 2014;6:CD010327.
Grimwood K, Bell SC, Chang AB. Antimicrobial treatment of non-cystic fibrosis bronchiectasis. Expert
Rev Anti Infect Ther. 2014;12(10):1277-96.
Guembe P. Semiología torácica: nódulos y masas pulmonares. Lesión cavitaria y quística. Calcificación
pulmonar. Lesión hiliar. En: Sánchez C, Casanova R, editores. Pedrosa. Diagnóstico por imagen.
Tratado de Radiología clínica. 2ª edición. Madrid: McGraw-Hill Interamericana; 1997; p. 329-71.
Haworth CS, Bilton D, Elborn JS. Long-term macrolide maintenance therapy in non-CF bronchiectasis:
Evidence and questions. Respir Med. 2014;108:1397-408.
Kapur N, Bell S, Kolbe J, Chang AB. Inhaled steroids for bronchiectasis. Cochrane Database Syst Rev.
2009;1:CD000996.
Lee A, Burge A, Holland AE. Airway clearance techniques for bronchiectasis. Cochrane Database Syst
Rev. 2013;5:CD008351.
McShane PJ, Naureckas ET, Tino G, Strek ME. Non-cystic fibrosis bronchiectasis. Am J Respir Crit Care
Med. 2013;188(6):647-56.
Metersky MD. The initial evaluation of adults with bronchiectasis. Clin Chest Med. 2012;33(2):219-31.
Monserrat Vendrell M, De Gracia J, Olveira C, Ángel M, Girón R, Máiz L, et al. Diagnóstico y tratamiento
de las bronquiectasias. Arch Bronconeumol. 2008;44(11):629-40.
Olveira C, Ana Muñoz A, Domenech A. Terapia nebulizada. Arch Bronconeumol. 2014;50(12):535-45.
Pasteur MC, Bilton D, Hill AT; British Thoracic Society Bronchiectasis non-CF Guideline Group. British
Thoracic Society guideline for non-CF bronchiectasis. Thorax. 2010;65 Suppl 1: i1-58.
Pasteur MC, Helliwell SM, Houghton SJ, Webb SC, Foweraker JE, Coulden RA, et al. An investigation into
causative factors in patients with bronchiectasis. Am J Respir Crit Care Med. 2000;162(4 Pt 1):1277-
84.
Shoemark A, Ozerovitch L, Wilson R. Aetiology in adult patients with bronchiectasis. Respir Med.
2007;101(6):1163-70.
Van der Bruggen-Bogaarts BA1, van der Bruggen HM, van Waes PF, Lammers JW. Screening for
bronchiectasis. A comparative study between chest radiography and high-resolution CT. Chest.
1996;109(3):608-11.
Welsh EJ, Evans DJ, Fowler SJ, Spencer S. Interventions for bronchiectasis: an overview of Cochrane
systematic reviews. Cochrane Database Syst Rev. 2015;7:CD010337.
Wilkinson M, Sugumar K, Milan SJ, Hart A, Crockett A, Crossingham I. Mucolytics for bronchiectasis.
Cochrane Database Syst Rev. 2014;5:CD001289.
Wurzel D, Marchant JM, Yerkovich ST, Upham JW, Masters IB, Chang AB. Short courses of antibiotics
for children and adults with bronchiectasis. Cochrane Database Syst Rev. 2011;6:CD008695.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [470]
[31] TRASTORNOS RESPIRATORIOS DURANTE EL SUEÑO: SÍNDROME DE APNEAS-HIPOPNEAS DEL SUEÑO. OTROS
31.Trastornos respiratorios durante el sueño: síndrome
de apneas-hipopneas del sueño. Otros
Irene Cabrera Rodrigo.
Medicina Interna
Adriana Manrique Mutiozábal.
Neumología
Asesora: Eva María Arias Arias. Médica Adjunta de Neumología
I. SÍNDROME DE APNEAS-HIPOPNEAS DEL SUEÑO
1. DEFINICIÓN Y EPIDEMIOLOGÍA
Cuadro de somnolencia excesiva, trastornos cognitivo-conductuales, respiratorios, cardiacos,
metabólicos o inflamatorios secundarios a episodios repetidos de obstrucción de la vía aérea superior (VAS)
durante el sueño.
Estos episodios se miden con el índice de apneas-hipopneas (IAH). Un IAH/índice de alteración
respiratoria (IAR) > 5 asociado a síntomas relacionados con la enfermedad y no explicados por otras causas
confirma el diagnóstico.
Es una enfermedad muy prevalente e infradiagnosticada. Se estima que un 4% de la población
española presenta síndrome de apneas-hipopneas durante el sueño (SAHS) sintomático.
Los tres factores de riesgo más importantes son: índice de masa corporal (IMC) aumentado (> 35),
edad (se triplica su prevalencia en ancianos) y sexo masculino, siendo la relación hombre/mujer de edad
media 3:1, tendiendo a igualarse a partir de la menopausia.
Existen otras variables que influyen en la aparición de SAHS o en su agravamiento: consumo de
alcohol, tabaco, sedantes, hipnóticos, barbitúricos, posición en decúbito supino, factores genéticos,
familiares y raciales.
Con respecto a la clasificación por gravedad se establece en: leve (IAH: 5-15), moderada (IAH: 15-
30) y grave (IAH > 30).
1. DEFINICIONES DE LOS PRINCIPALES EVENTOS RESPIRATORIOS
Apnea obstructiva: ausencia o reducción > 90% de la señal respiratoria medida por termistor,
cánula nasal o neumotacógrafo > 10 segundos de duración en presencia de esfuerzo
respiratorio detectado en las bandas toracoabdominales.
Apnea central: ausencia o reducción > 90% de la señal respiratoria medida por termistor,
cánula nasal o neumotacógrafo > 10 segundos de duración en ausencia de esfuerzo respiratorio
detectado en las bandas toracoabdominales.
Hipopnea: reducción > 30 y < 90% de la amplitud de la señal respiratoria > 10 segundos de
duración o del sumatorio toracoabdominal, que se acompaña de desaturación ≥ 3% y/o
microdespertar en el electroencefalograma.
Esfuerzo respiratorio asociado a microdespertar (ERAM): periodo > 10 segundos de incremento
progresivo del esfuerzo respiratorio que acaba con un microdespertar sin reducción evidente
de la amplitud de flujo.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [471]
[31] TRASTORNOS RESPIRATORIOS DURANTE EL SUEÑO: SÍNDROME DE APNEAS-HIPOPNEAS DEL SUEÑO. OTROS
El IAH es la suma de apneas e hipopneas por hora de sueño (o por hora de registro si se usa la
poligrafía respiratoria).
El IAR consiste en el sumatorio de apneas, hipopneas y ERAM por hora de sueño (o de registro).
2. FISIOPATOLOGÍA
Se sugiere un origen multifactorial. El colapso de la VAS se produce como consecuencia de un
desequilibrio entre fuerzas que tienden a cerrarla y las que la mantienen abierta. Se han identificado
diversos factores que contribuyen a esta situación, como son alteraciones anatómicas y mecánicas de la vía
aérea superior, alteraciones neuromusculares e inestabilidad del centro respiratorio. Los episodios
recurrentes de colapso parcial (hipopnea) o completo (apnea) durante el sueño producen hipoxia y
microdespertares. Estos eventos inducen mecanismos intermedios que favorecen el desarrollo de
enfermedades cardiovasculares y metabólicas.
La obstrucción de la VAS induce esfuerzos inspiratorios ineficaces, generándose presiones
intratorácicas muy negativas que aumentan la presión en el ventrículo izquierdo. Los despertares
condicionan un sueño fragmentado que se asocia a somnolencia diurna, trastornos cognitivos y aumento
de accidentabilidad. La hipoxia aumenta la descarga simpática, los radicales libres, la hipercoagulabilidad y
la inflamación sistémica, favoreciendo la resistencia insulínica y la morbilidad cardiovascular.
3. CLÍNICA Y EXPLORACIÓN FÍSICA
En la anamnesis deben recogerse antecedentes cardiopulmonares de interés, clínica relacionada
con SAHS y horarios de sueño.
Los síntomas y signos más frecuentes del SAHS se dividen en diurnos o nocturnos y se recogen en la
tabla I. Ningún síntoma aislado o en combinación ha demostrado suficiente valor en el diagnóstico, dado
que frecuentemente se encuentran en individuos sanos.
Tabla I. Síntomas y signos frecuentes.
La tríada clínica del SAHS la componen tres síntomas: roncopatía crónica, apneas objetivadas y
excesiva somnolencia diurna (o cansancio en mujeres). Este último es el que marca la intensidad clínica; es
importante realizar una adecuada anamnesis para descartar otras causas de hipersomnia (Tabla II).
Tabla II. Diagnóstico diferencial de hipersomnia.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [472]
[31] TRASTORNOS RESPIRATORIOS DURANTE EL SUEÑO: SÍNDROME DE APNEAS-HIPOPNEAS DEL SUEÑO. OTROS
Existen escalas subjetivas para la medición de hipersomnolencia; el cuestionario de Epworth es el
más utilizado (Tabla III). Es un test autocumplimentado en el que el paciente deberá asignar la posibilidad
de quedarse dormido en diferentes situaciones. Una puntuación ≥ 12 puntos indica hipersomnia patológica.
A pesar de su utilidad en la práctica clínica tiene limitaciones culturales y no está validado en ancianos.
Tabla III. Cuestionario de Epworth.
Son métodos objetivos de medida de hipersomnia:
Test de latencias múltiples del sueño (TLMS): se realiza la mañana siguiente a una
polisomnografía nocturna (PSG) y consiste en cuatro o cinco siestas separadas por dos horas.
Se valora la latencia al sueño en cada siesta y la media global, así como la presencia de sueño
REM.
Test de mantenimiento de la vigilia: es una variante del TLMS cuyo objetivo es evaluar la
capacidad individual de mantenerse despierto. No requiere la realización de PSG la noche
previa. Se emplea para valorar respuesta a un tratamiento o cuando la hipersomnia supone un
peligro para la seguridad personal o pública.
En la tabla IV se enumeran aquellas situaciones de riesgo que pueden asociarse al SAHS y en las
que debería realizarse una anamnesis dirigida.
Tabla IV. Pacientes con alto riesgo de síndrome de apneas-hipopneas del sueño.
La exploración física debe incluir:
Variables antropométricas: IMC, perímetro del cuello e índice cintura/cadera.
Distancia hioides-mandíbula (para valorar cuello corto).
Exploración otorrinolaringológica básica: obstrucción nasal, hipertrofia de amígdalas o úvula,
paladar blando largo, grados de Mallampati, clasificación de Friedman (incluye posición de la
lengua, tamaño amigdalino e IMC), examen del maxilar y mandíbula (retro-micrognatia) y
calidad de la mordida.
Saturación basal de oxígeno.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [473]
[31] TRASTORNOS RESPIRATORIOS DURANTE EL SUEÑO: SÍNDROME DE APNEAS-HIPOPNEAS DEL SUEÑO. OTROS
Tensión arterial.
Auscultación cardiopulmonar.
Se recomienda solicitar a todos los pacientes un perfil analítico que incluya hemograma, bioquímica
básica y perfil lipídico. La radiografía simple de tórax, el electrocardiograma, la espirometría forzada y
niveles de hormonas tiroideas se solicitarán en caso de sospechar enfermedad concomitante.
Clasificación Friedman
4. DIAGNÓSTICO (Figura 1)
Figura 1. Algoritmo de actuación bajo la sospecha del síndrome de apneas-hipopneas del sueño.
El diagnóstico se apoya en datos clínicos y un estudio de sueño que proporcione el IAH. Existen
distintos tipos de estudios según su complejidad (Tabla V).
1. POLISOMNOGRAFÍA CONVENCIONAL
Vigilada por un técnico, es el método de referencia. Consiste en el registro continuo del
electroencefalograma (EEG), electrooculograma (EOG) y electromiograma (EMG) mentoniano (para
identificar las fases de sueño y los microdespertares o arousal), así como pulsioximetría,
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [474]
[31] TRASTORNOS RESPIRATORIOS DURANTE EL SUEÑO: SÍNDROME DE APNEAS-HIPOPNEAS DEL SUEÑO. OTROS
electrocardiograma, flujo aéreo nasobucal mediante cánula nasal y termistor, y bandas toracoabdominales.
Se realiza en horario nocturno o respetando horarios habituales de sueño del sujeto, con un registro
mínimo de 6,5 horas que debe incluir al menos 3 horas de sueño.
Es una técnica cara y técnicamente compleja, no al alcance de todos los centros y que, debido a la
gran demanda, no puede realizarse a todos los pacientes. Con intención de simplificar el proceso
diagnóstico se han desarrollado equipos portátiles que solo registran variables respiratorias.
Tabla V. Clasificación de los estudios de sueño de la American Academy of Sleep Medicine (AASM).
2. POLIGRAFÍA RESPIRATORIA
Indicado en pacientes con sospecha clínica moderada-alta de SAHS. La poligrafía respiratotia (PR)
tiene la ventaja de reducir costes y lista de espera; además, si es domiciliaria, el paciente duerme en su
cama, siendo más representativo el sueño del día a día. Los inconvenientes de la PR son que no evalúa la
calidad del sueño ni permite cuantificar las horas de sueño (no registra variables neurofisiológicas),
infraestima el IAH (al expresar los eventos respiratorios por horas totales de registro en lugar de por horas
de sueño) y no permite evaluar otros trastornos no respiratorios del sueño. Si la PR es negativa y la
sospecha clínica es media o alta se ha de realizar una PSG.
3. ESTUDIOS SUPERSIMPLIFICADOS
Actualmente no están validados como método diagnóstico. La oximetría nocturna registra
desaturaciones en diente de sierra que pueden orientar a la presencia de apneas o hipopneas, pero no
distingue eventos centrales de obstructivos.
Los registros portátiles están indicados en pacientes con alta probabilidad pretest de SAHS. No se
recomiendan si existe comorbilidad cardiovascular o pulmonar severa, trastornos neurológicos o
neuromusculares o si se sospechan otros trastornos de sueño.
5. TRATAMIENTO
Los objetivos del tratamiento serán: conseguir el control de los síntomas (fundamentalmente la
somnolencia), mejorar la calidad de sueño y minimizar el riesgo cardiovascular.
5.1. Medidas generales
Deberá tenerse en cuenta la presencia de factores etiológicos modificables y ofrecer su tratamiento
pertinente.
Medidas higiénicas del sueño. Indicado en todos los pacientes. La causa más frecuente de
somnolencia excesiva es en un sueño irregular e insuficiente. Se aconseja mantener un horario
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [475]
[31] TRASTORNOS RESPIRATORIOS DURANTE EL SUEÑO: SÍNDROME DE APNEAS-HIPOPNEAS DEL SUEÑO. OTROS
fijo, dormir horas suficientes, cenar de manera ligera y esperar al menos 2 horas antes de
acostarse.
Abstinencia de alcohol y tabaco.
Evitar sedantes, especialmente benzodiazepinas.
Pérdida ponderal. En pacientes obesos puede resultar una medida curativa. Recomendar dieta
y ejercicio de forma regular en pacientes con IMC > 25, e incluso valorar cirugía bariátrica en
pacientes con obesidad mórbida.
Medidas posturales, indicadas en casos de SAHS postural, definiéndose el mismo si el IAH en la
posición de decúbito supino es al menos el doble que en decúbito lateral. Deberá evitarse la
posición en decúbito supino aplicando molestias físicas en la espalda (colocación de pelota en
dicha zona). Otra alternativa es elevar el cabecero de la cama unos 30º, pues reduce la
resistencia de la VAS.
Tratamiento de la obstrucción nasal. La congestión nasal (por rinitis fundamentalmente) puede
ser causa de empeoramiento del SAHS o de intolerancia a la presión positiva continua en la vía
aérea (CPAP). Su tratamiento con corticoides nasales puede mejorar el cuadro, administrando
budesonida spray nasal 100 mcg (2 puff en cada fosa nasal, una o dos veces al día). Si
persistieran los síntomas se puede añadir anticolinérgicos nasales o antihistamínicos orales.
5.2. Dispositivos de avance mandibular
Son eficaces en el tratamiento de la roncopatía, del SAHS leve y moderado con bajo IMC y desaturaciones
no importantes y, como segunda elección, en pacientes que no toleran la CPAP nasal, que no son
candidatos a la cirugía o tienen riesgo quirúrgico elevado.
5.3. Presión positiva continua en la vía aérea (CPAP)
Efectos: es el tratamiento de primera elección en la mayoría de los pacientes con SAHS. Actúa
como una prótesis neumática al aplicar una presión positiva continua en la VAS evitando el
colapso y, por consiguiente, las consecuencias fisiopatológicas derivadas del mismo. No solo
corrige las apneas, las hipopneas y el ronquido, sino que también evita las desaturaciones de
oxígeno, los microdespertares electroencefalográficos y normaliza la arquitectura del sueño.
Mejora también la capacidad de atención entre otras variables cognitivas, reduce el riesgo de
accidentes de tráfico y disminuye las cifras de presión arterial en un porcentaje relevante de
sujetos hipertensos con SAHS.
Interfases: existen distintos tipos de mascarillas (nasales, oronasales y olivas nasales) que
buscan la comodidad del paciente, la disminución del espacio muerto y la ausencia de fugas.
Indicaciones (Figura 2): En IAH > 30 debe indicarse CPAP independiente de los síntomas. Para
pacientes con IAH ≥ 5 y < 30 deberá considerarse la repercusión clínica y/o la comorbilidad
asociada. En los pacientes que no toleren o rechacen CPAP, considerar otras opciones como
dispositivo de avance mandibular y cirugía ORL y/o maxilofacial.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [476]
[31] TRASTORNOS RESPIRATORIOS DURANTE EL SUEÑO: SÍNDROME DE APNEAS-HIPOPNEAS DEL SUEÑO. OTROS
Figura 2. Algoritmo terapéutico.
Titulación: cada paciente precisa una presión determinada de CPAP, por lo que esta debe
adecuarse de un modo individualizado. El método más preciso para determinar la presión de
CPAP es la titulación convencional por PSG. Es la técnica que mejor asegura el ajuste de presión
y la corrección de todos los fenómenos patológicos (respiratorios y neurológicos). Por ello, los
pacientes con SAHS que van a ser tratados con CPAP requerirían dos estudios de PSG: uno
diagnóstico y otro de titulación. Para agilizar el proceso se han propuesto estrategias
alternativas al “gold estándar” como las auto- CPAP (APAP). Son CPAP inteligentes que el
paciente utiliza en domicilio durante tres a siete noches y que realizan un test de
reconocimiento respiración a respiración para ajustar la presión según la necesidad del
paciente, y cuentan con una tarjeta de memoria para el análisis de la presión media requerida e
IAH residual. El uso de fórmulas matemáticas puede ser otra opción (Hoffstein: presión = [IMC ×
0,16] + [diámetro de cuello × 0,13] + [IAH × 0,04] – 5,12). También puede titularse con PSG en
noche partida que implica la realización de PSG en la primera parte de la noche (para obtención
de IAH), mientras que en la segunda parte se establece la presión de CPAP de tratamiento, con
el inconveniente de disponer de escasas horas de sueño.
Seguimiento: puesto que no es un tratamiento curativo, debe usarse de forma continuada. El
cumplimiento mínimo que se asocia a una clara mejoría de síntomas es de 3,5 h/noche. La
decisión de retirada del tratamiento en estos casos por mal cumplimiento deberá
individualizarse. – Efectos secundarios: suelen aparecer la primera semana y ser menores y
transitorios. Los más comunes son congestión nasal, irritación cutánea, sequedad faríngea y frío
(mejorables con la introducción de humidificador-calentador), conjuntivitis, epistaxis, ruido e
insomnio.
Contraindicaciones: la única contraindicación absoluta es la fístula de líquido cefalorraquídeo,
usándose con precaución en todas aquellas situaciones que puedan empeorar con la
administración de presión positiva.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [477]
[31] TRASTORNOS RESPIRATORIOS DURANTE EL SUEÑO: SÍNDROME DE APNEAS-HIPOPNEAS DEL SUEÑO. OTROS
5.4. Presión positiva de la vía aérea de dos niveles (BiPAP)
Indicado en pacientes con síndrome de hipoventilación-obesidad puro o asociado a SAHS, o en SAHS severo
que no se controla con CPAP por requerir altas presiones.
5.5. Cirugía
Debe considerarse especialmente en los casos de intolerancia a la CPAP nasal por obstrucción. Se utilizan
diferentes técnicas según la anomalía anatómica que exista: cirugía nasal, palatofaríngea, reductora de la
base de la lengua e incluso cirugía multinivel.
5.6. Oxigenoterapia crónica domiciliaria
Únicamente indicada en casos con insuficiencia respiratoria, en muchos casos se utiliza solo de manera
transitoria al corregirse la hipoxemia con un correcto tratamiento del SAHS.
6. MANEJO DEL SÍNDROME DE APNEAS-HIPOPNEAS DEL SUEÑO EN EL SERVICIO DE URGENCIAS
Todo paciente diagnosticado de SAHS y en tratamiento con CPAP que acude a urgencias debe
traer su CPAP del domicilio.
Si permanece en observación o ingresa, independientemente del motivo, debe mantenerse el
tratamiento.
Si la causa que motiva la visita a urgencias ha desencadenado insuficiencia respiratoria
previamente no presente se debe colocar una conexión de oxígeno a la CPAP que permita el
tratamiento conjunto.
Se deberá valorar el cambio de mascarilla nasal a oronasal si el deterioro clínico provoca
disminución del nivel de consciencia y, con ello, apertura bucal.
Se deberán vigilar los niveles de pCO2. El aumento significativo de pCO2 y la disminución del pH
en la gasometría arterial deberán ser valorados de cara a la indicación de iniciar ventilación
mecánica tipo BiPAP.
Es importante evitar en pacientes con SAHS el tratamiento con sedantes.
II. OTROS TRASTORNOS RESPIRATORIOS DURANTE EL SUEÑO
A. APNEAS-HIPOPNEAS CENTRALES
Disminución del flujo respiratorio, en distinta proporción, producido por ausencia o disminución del
esfuerzo respiratorio, con ausencia de contracción de los músculos respiratorios por déficit en el estímulo
central de los centros respiratorios. Suelen desencadenarse al caer la PaCO2 por debajo de un umbral
apneico. Las apneas-hipopneas centrales (AC) secundarias a insuficiencia cardiaca representan el 40-80%. El
primer paso es optimizar el tratamiento de la enfermedad subyacente y, si persisten las AC, probar la CPAP.
B. RESPIRACIÓN DE CHEYNE-STOKES
Se trata de AC o hipopneas con oscilaciones periódicas en la ventilación, asociadas frecuentemente
a insuficiencia cardiaca (también a ictus y sedación). La ventilación crece y decrece progresivamente hasta
llegar a la AC o hipopnea, reiniciándose el ciclo cada 60-90 segundos, lo que provoca hipoxia intermitente.
Empeora el pronóstico de la insuficiencia cardiaca y aumenta la mortalidad. El tratamiento consiste en
optimizar el tratamiento de la enfermedad subyacente y ensayar con CPAP, aunque los efectos en la
supervivencia no están demostrados.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [478]
[31] TRASTORNOS RESPIRATORIOS DURANTE EL SUEÑO: SÍNDROME DE APNEAS-HIPOPNEAS DEL SUEÑO. OTROS
C. SÍNDROME OVERLAP
Es la concurrencia de SAHS y enfermedad pulmonar obstructiva crónica (EPOC). Presentan mayor
sonmolencia y desaturación nocturna, más riesgo de insuficiencia cardiaca derecha, insuficiencia
respiratoria hipercápnica e hipertensión pulmonar. El tratamiento consiste en oxigenoterapia si cumple
criterios para la misma y ensayar la CPAP para eliminar los eventos obstructivos y las desaturaciones
nocturnas.
D. SÍNDROME DE HIPOVENTILACIÓN-OBESIDAD
El síndrome de hipoventilación-obesidad está definido como la coexistencia de hipoventilación
diurna en vigilia (PaCO2 > 45 mm Hg) y obesidad (IMC ≥ 30), cuando otras causas de hipercapnia han sido
excluidas. Cerca del 90% de los obesos hipercápnicos presentan un SAHS y alrededor del 15% de los
pacientes obesos con SAHS presentan hipercapnia. La medida terapéutica inicial es la pérdida de peso. En
presencia de SAHS se recomienda comenzar tratamiento con CPAP. Sin embargo, en un número de casos
no despreciable, la PaCO2 diurna no se normaliza, y en dicho supuesto sería lógico realizar un cambio a
ventilación mecánica no invasiva (VMNI). La VMNI produce mejoría clínica, gasométrica, de las alteraciones
durante el sueño y descenso del número de días de hospitalización.
E. DESATURACIÓN DURANTE EL SUEÑO ASOCIADA A OTRAS ENFERMEDADES
En los pacientes que padecen EPOC se puede producir desaturación nocturna como consecuencia
de alteraciones en el gradiente alveoloarterial secundario a destrucción parenquimatosa e inflamación
crónica, entre otras.
En aquellos pacientes con trastornos de la pared torácica (cifoescoliosis, toracoplastia, espondilitis
anquilopoyética, etc.) puede existir desaturación durante el sueño por alteraciones en la mecánica
ventilatoria.
En pacientes que sufren enfermedades neuromusculares (esclerosis múltiple, esclerosis lateral
amiotrófica, miastenia gravis, polimiositis, etc.) se puede observar disminución de la saturación nocturna
por alteración en la mecánica ventilatoria, secundario a la debilidad o fatigabilidad de músculos integrantes
del sistema respiratorio, así como alteraciones en la ventilación-perfusión; o hipoventilación nocturna que
se define por pCO2 > 55 mm Hg durante más de 10 minutos en el registro nocturno con capnografía
transcutánea.
BIBLIOGRAFÍA
Gaudette E, Kimoff RJ. Pathophysiology of OSA. Eur Respir Mon. 2010;50: 31-50.
Levy P, Pepin J-L, Tamisier R, Launois-Rollinat S. Outcomes of OSA and indications for different
therapies. Eur Respir Mon. 2010;50:225-43.
Lloberes P, Durán-Cantolla J, Martínez-García MA, Marín JM, Ferrer A, Corral J, et al. Normativa sobre
diagnóstico y tratamiento del síndrome de apneas-hipopneas del sueño. Arch Bronconeumol.
2011;47:143-56.
Malhotra A, Orr JE, Owens RL. On the cutting edge of obstructive sleep apnoea: where next? Lancet
Respir Med. 2015; 3(5):397-403.
Penzel T, Blau A, Schöbel C, Fietze I. Ambulatory diagnosis of OSA and new technologies. Eur Respir
Mon. 2010;50:136-49.
Rabec C, de Lucas Ramos P, Veale D. Complicaciones respiratorias de la obesidad. Arch
Bronconeumol. 2011;47(5):252-61.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [479]
[32] ENFERMEDAD TROMBOEMBÓLICA VENOSA
32.Enfermedad tromboembólica venosa
Pablo Hernández Sanz.
Medicina Interna
Marta Pérez Gallán.
Neumología
Asesores: Roberto del Pozo Rivas. Médico Adjunto de Neumología. María del Carmen Díaz Pedroche. Médica Adjunta de
Medicina Interna
I. DEFINICIÓN Y ETIOPATOGENIA
La enfermedad tromboembólica venosa (ETEV) es la formación de trombos en el territorio venoso
que con frecuencia se fragmentan o desprenden de la pared y acaban albergándose en el territorio arterial
pulmonar. Por tanto, engloba la trombosis venosa profunda (TVP) y el trombo- embolismo pulmonar (TEP).
Ambos procesos están íntimamente relacionados, de manera que el 20-50% de los pacientes con TVP
sintomática demostrada presentan un TEP clínicamente silente y hasta en el 70-80% de los casos de TEP se
demuestra una TVP (asintomática en más de la mitad de ellos).
La TVP puede ocurrir en cualquier localización, pero el 80% de los casos de TEP se asocian a TVP
proximal de la extremidad inferior (venas poplítea, femoral o iliaca). La TVP distal puede resolverse de
forma espontánea (hasta un tercio de los casos), cronificarse o progresar a TVP proximal (en el 20-30% de
los casos). La tromboflebitis superficial de la extremidad inferior puede también progresar a TVP en un
porcentaje muy variable de casos, siendo mayor la incidencia si afecta a la vena safena proximal.
El TEP puede tener, según su tamaño, localización y también en función de la presencia de
patología cardiopulmonar previa, distintas consecuencias:
Hemodinámicas: el aumento de las resistencias vasculares pulmonares (por obstrucción directa
de las arterias pulmonares y vasoconstricción reactiva) puede reducir el gasto cardiaco
derecho, llegando incluso al fracaso ventricular y compromiso del gasto cardiaco izquierdo. Si el
sistema fibrinolítico endógeno no resuelve el trombo, podrá originarse un cuadro de
hipertensión pulmonar crónica secundaria. Solo el 10% de los émbolos causan infarto pulmonar
(gracias a la doble vascularización arterial pulmonar).
Respiratorias: se afecta el intercambio gaseoso por alteración de la relación
ventilación/perfusión (aumento del espacio muerto) y por efecto shunt (se liberan mediadores
inflamatorios que afectan al surfactante pulmonar y favorecen la formación de atelectasias).
1. FACTORES DE RIESGO
La ETEV aparece en la mayoría de los casos en pacientes que presentan uno o varios factores de
riesgo (FR) adquiridos o hereditarios, los cuales están relacionados con uno o varios de los mecanismos
etiopatogénicos de la enfermedad: éstasis venoso, lesión endotelial y/o hipercoagulabilidad. Se clasifican
según el riesgo relativo (RR) u odds ratio (OR) de riesgo protrombótico (Tablas I y II). Además, según la
existencia o no de FR conocidos el TEP se clasifica como:
TEP no provocado, espontáneo o idiopático: aquel que se produce en ausencia de factores de
riesgo conocidos.
TEP provocado o secundario: cuando se asocia a factores de riesgo desencadenantes
temporales o reversibles (como cirugía, traumatismo, inmovilización, gestación o fármacos)
presentes desde 6 semanas a 3 meses antes del diagnóstico. En mujeres fértiles, los
anticonceptivos orales son el factor que más frecuentemente predispone a ETEV.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [480]
[32] ENFERMEDAD TROMBOEMBÓLICA VENOSA
Tabla I. Factores predisponentes para la enfermedad tromboembólica venosa.
II. DIAGNÓSTICO
1. TROMBOEMBOLISMO PULMONAR
La sospecha se establece a través de clínica compatible (Tabla III) en un paciente con factores de
riesgo (de los mencionados previamente), y se confirma con la integración adecuada de las pruebas
complementarias (Figuras 1 y 2).
Clínica: el síntoma más frecuente por el que los pacientes acuden a urgencias es la disnea, que
suele ser de instauración brusca e inexplicable por otras causas, aunque puede estar ausente
en personas mayores. El dolor pleurítico se debe a irritación pleural en embolias distales
(infarto pulmonar), y el dolor torácico anginoso en embolias centrales (refleja isquemia del
ventrículo derecho [VD]).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [481]
[32] ENFERMEDAD TROMBOEMBÓLICA VENOSA
Tabla II. Prevalencia de las trombofilias ordenadas según el riesgo relativo de trombosis.
Tabla III. Síntomas y signos de tromboembolismo pulmonar.
Radiografía de tórax: es esencial para excluir causas alternativas. Puede mostrar alteraciones
inespecíficas, como atelectasias, derrame pleural y cardiomegalia, y es normal hasta en un 20%
de los casos. Signos típicos pero infrecuentes son el aumento unilateral de las arterias
pulmonares (signo de Fleischner), la disminución focal de la vasculatura (signo de Westermark)
o la presencia de una opacidad triangular en la base pulmonar (joroba de Hampton).
Electrocardiograma: es habitual encontrar alteraciones inespecíficas, siendo común la
taquicardia sinusal; la inversión de la onda T de V1 a V4, el bloqueo de rama derecha o el patrón
característico S1Q3T3 como signos de sobrecarga derecha, aparecen con más frecuencia en los
casos graves.
Gasometría arterial: hipoxemia o alcalosis respiratoria por hipocapnia con gradiente alveolo-
arterial elevado.
1.1. Evaluación de la probabilidad clínica
La sospecha clínica es fundamental para el diagnóstico de TEP, pero existe una limitada sensibilidad y
especificidad de los síntomas, signos y pruebas comunes. La combinación de los hallazgos evaluados
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [482]
[32] ENFERMEDAD TROMBOEMBÓLICA VENOSA
(mediante las escalas de probabilidad clínica) permite clasificar a los pacientes con sospecha de TEP en
distintas categorías pretest. Las escalas más comunes son la escala de Wells y la escala de Ginebra, que han
sido validadas (tanto la versión completa como, recientemente, su versión simplificada para facilitar su
adopción en la práctica clínica). Estas escalas son claves en el algoritmo diagnóstico del TEP (Tablas IV y V).
Tabla IV. Escala de Wells (original y simplificada).
Tabla V. Escala de Ginebra (original y simplificada).
1.2. Estudios complementarios
1.2.1. Dímero D (DD)
Se elevan en el plasma por la activación simultánea de la coagulación y la fibrinólisis. Tiene una alta
sensibilidad y un alto valor predictivo negativo para descartar TEP/TVP. Por otro lado, tiene baja
especificidad, ya que se eleva en numerosas enfermedades (cáncer, inflamación, sangrado, traumatismos,
cirugía, etc.). Un valor negativo con una probabilidad clínica baja-intermedia puede excluir el diagnóstico
hasta en el 30% de las sospechas iniciales. En pacientes con alta probabilidad clínica no se recomienda su
realización, puesto que no excluye realizar más pruebas diagnósticas.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [483]
[32] ENFERMEDAD TROMBOEMBÓLICA VENOSA
La especificidad del dímero D disminuye progresivamente con la edad, siendo esta solo del 10% en
mayores de 80 años. La evidencia reciente sugiere, por tanto, usar el “dímero D ajustado a la edad” en los
mayores de 50 años, incrementando así la especificidad en estos del 34% al 46%, conservando una
sensibilidad del 97%.
En ≤ 50 años el punto de corte es: 500 ng/ml.
En > 50 años el punto de corte es: Edad del paciente x 10.
1.2.2. Ecocardiograma
Puede medir el aumento de presión del VD y su disfunción. Algunos hallazgos son el signo de Mc Connell
(depresión de la contractilidad de la pared libre del VD en comparación con el ápex) o el desplazamiento
del anillo tricuspídeo durante la sístole (TAPSE) menor de 16 mm.
La prueba tiene interés en pacientes inestables y de alto riesgo, donde la ausencia de sobrecarga
del VD excluye el TEP como causa del shock y ayuda en el diagnóstico diferencial de otras causas de este
(taponamiento pericárdico, disfunción valvular aguda, disección de la aorta, hipovolemia, disfunción grave
del ventrículo izquierdo [VI]). Consecuentemente, si existe compromiso hemodinámico y signos
inequívocos de sobrecarga/disfunción del VD, en ausencia de angio-TC inmediata, estaría justificada la
terapia de reperfusión. No se recomienda el ecocardiograma de entrada en los pacientes
hemodinámicamente estables por su escasa información diagnóstica (no confirma ni descarta TEP).
1.2.3. Angiografía pulmonar por tomografía computarizada (angio-TC) multicorte
Es el principal medio diagnóstico y el más utilizado. Requiere la administración de contraste yodado y
permite la visualización del trombo hasta niveles subsegmentarios. Según los resultados del estudio PIOPED
II, tiene una sensibilidad del 83% y una especificidad del 96%. El valor predictivo positivo (VPP) varía con la
extensión del TEP y con la probabilidad clínica: una angio-TC positiva tiene un VPP del 96% cuando la
probabilidad clínica de TEP es alta, del 92% cuando es intermedia y solo del 58% cuando es baja. El anterior
estudio también demostró que la angio-TC pulmonar tiene además un alto valor predictivo negativo (VPN)
para descartar TEP en pacientes con probabilidad baja o intermedia (96% y 89%, respectivamente), pero
solo del 60% en los pacientes con probabilidad clínica alta, por lo que una angio-TC negativa en este grupo
de pacientes requiere pruebas diagnósticas adicionales si persiste la sospecha clínica.
1.2.4. Gammagrafía de ventilación/perfusión (V/Q)
Se reserva para pacientes con insuficiencia renal, alérgicos a los contrastes yodados, embarazadas (ver
Apartados “Estrategias diagnósticas en situaciones especiales” y “Embarazo”) y pacientes con mieloma o
paraproteinemia (por los riesgos de radiación/nefrotoxicidad de la angio-TC). Es menos útil en pacientes
con radiografía de tórax patológica o alteraciones pulmonares parenquimatosas, no proporciona
diagnósticos alternativos y no está disponible en todos los centros ni a determinadas horas del día.
El estudio PIOPED II mostró una buena correlación tanto entre los defectos de perfusión de alta
probabilidad gammagráfica con los hallazgos de TEP por angio-TC, como en los estudios normales con
ausencia de TEP por angio-TC. La principal dificultad radica en los estudios con resultados de
baja/intermedia probabilidad, puesto que no son concluyentes.
1.2.5. Ecografía venosa
La compresión venosa a nivel femoral y poplíteo de forma bilateral (cuatro puntos) tiene una sensibilidad
del 90% y una especificidad del 95%. El único criterio diagnóstico válido es la incompleta compresibilidad de
la vena, que indica coágulo, mientras que los criterios de flujo no son fiables. Hasta en un 30-50% de los
pacientes con TEP se demuestra TVP (siendo las TVP proximales las de mayor valor predictivo para TEP). La
sospecha de TEP con ecografía positiva sería suficiente para iniciar la anticoagulación, y es una prueba útil
en embarazadas y en pacientes con gammagrafía no concluyente.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [484]
[32] ENFERMEDAD TROMBOEMBÓLICA VENOSA
1.2.6. Arteriografía pulmonar
Proporciona un diagnóstico de certeza, aunque es poco frecuente su uso en la actualidad por la
disponibilidad de nuevos equipos TC multidetector.
1.3. Algoritmos diagnósticos
La sospecha de TEP se clasifica en TEP inestable, cuando se presenta con shock o hipotensión arterial
(definida por una presión sistólica < 90 mm Hg o caída de la presión sistólica en 40 mm Hg durante > 15
min) y en TEP estable (el resto).
Sospecha de TEP inestable: situación de riesgo que compromete la vida y cuyo diagnóstico
diferencial incluye el taponamiento, el síndrome coronario agudo, la disfunción valvular y la
disección de aorta. Si la angio-TC no está disponible inmediatamente, los signos
ecocardiográficos de sobrecarga derecha son suficientes para iniciar tratamiento de
reperfusión. En pacientes inestables en los que se realiza una coronariografía urgente por
código infarto (ver Capítulo 23. “Cardiopatía isquémica”), y en cuyo estudio no se demuestran
lesiones coronarias, se podría valorar la angiografía pulmonar en ese mismo instante (Figura 1).
Figura 1. Algoritmo diagnóstico en la sospecha de tromboembolismo pulmonar inestable.
Sospecha de TEP estable: en un paciente que acude a Urgencias, lo primero será evaluar las
escalas de probabilidad clínica y realizar la determinación del dímero D cuando esté indicado.
Así, en aquellos con sospecha clínica de TEP improbable o probabilidad baja-intermedia y
dímero D negativo, se descarta el diagnóstico y no se requieren más estudios (el riesgo de ETEV
a los 3 meses es inferior al 1%). Los dímeros D no deben medirse en pacientes de alto riesgo, y
probablemente tampoco en pacientes hospitalizados (mayor tasa de falsos positivos).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [485]
[32] ENFERMEDAD TROMBOEMBÓLICA VENOSA
La angio-TC sería una prueba de segunda línea en pacientes con sospecha clínica de TEP improbable
o baja-intermedia probabilidad y dímeros D elevados, o de primera línea si la sospecha clínica es de TEP
probable o alta probabilidad. Si la angio-TC estuviese contraindicada, se pueden valorar otras pruebas
como la ecografía venosa de los miembros inferiores (MMII) o la gammagrafía de V/Q. Los pacientes con
baja probabilidad pretest y gammagrafía con resultado no concluyente tienen baja prevalencia de TEP (el
VPN aumenta si se descarta TVP mediante ecografía venosa) (Figura 2).
1.4. Estrategias diagnósticas en situaciones especiales
Alergia a contrastes yodados: ante una sospecha clínica de TEP y niveles altos de dímero D, la
ecografía venosa de los MMII debe ser la prueba de imagen inicial, y un resultado positivo es
indicación de tratamiento. Si la ecografía es negativa, puede indicarse la angio-TC en aquellos
pacientes con alergia leve-moderada, previa premedicación con corticoides. En pacientes con
alergia grave, la alternativa es la gammagrafía pulmonar.
Figura 2. Algoritmo diagnóstico en la sospecha de tromboembolismo pulmonar inestable.
Insuficiencia renal: ante una sospecha clínica de TEP y niveles altos de dímero D, la ecografía
venosa de los MMII debe ser la prueba de imagen inicial, y un resultado positivo es indicación
de tratamiento. Si la ecografía es negativa, en los pacientes con insuficiencia renal leve puede
indicarse la angio-TC previa hidratación del paciente, que parece la medida más efectiva para
prevenir la nefropatía inducida por contraste. En el resto de los pacientes está indicada la
realización de una gammagrafía.
Mujeres embarazadas: ver Apartado “Embarazo”.
TC multidetector no concluyente para diagnóstico de TEP: se aconseja mantener tratamiento
anticoagulante con heparina de bajo peso molecular (HBPM) y repetir el estudio radiológico a
las 48 horas.
1.5. Áreas de incertidumbre
La significación clínica del TEP subsegmentario único es cuestionable, pues el VPP es bajo y la variabilidad
entre radiólogos observadores es alta. Parece existir cierto consenso entre expertos en tratar a los
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [486]
[32] ENFERMEDAD TROMBOEMBÓLICA VENOSA
pacientes con reserva cardiopulmonar limitada, pacientes con TVP concomitante (por lo que sería útil
realizar una ecografía venosa de los MMII en estos casos) y pacientes con émbolos subsegmentarios
recurrentes. Tampoco parece clara la decisión de tratar los TEP hallados casualmente en una TC realizada
por otro motivo, salvo si es un hallazgo en un paciente con cáncer o es un TEP casual lobar o proximal.
2. TROMBOSIS VENOSA PROFUNDA
Se dividen en dos grupos:
Distales: trombos que quedarán confinados en las venas profundas de la pantorrilla.
Proximales: son las de mayor riesgo embolígeno e implican afectación de la vena poplítea,
femoral o venas iliacas.
Los síntomas clásicos son edema, dolor, hinchazón, eritema de la extremidad, dilatación venosa
superficial, cordón palpable y aumento de la sensibilidad, no siendo necesaria la correlación entre la
localización de los síntomas y el lugar de la trombosis. Los síntomas son inespecíficos y el signo de Homans
(dolor gemelar a la dorsiflexión del pie) es poco fiable.
En el diagnóstico son útiles los dímeros D, y la confirmación se consigue mediante ecografía venosa
de los MMII (ver Apartado 2.1.2). La flebografía (método de referencia) se reserva para los casos no
concluyentes.
III. EVALUACIÓN PRONÓSTICA Y GRAVEDAD DEL
TROMBOEMBOLISMO PULMONAR
Simultáneamente al diagnóstico de TEP, es preciso realizar una evaluación del pronóstico para la
estratificación del riesgo y la toma de decisiones terapéuticas.
Los pacientes con shock/hipotensión son pacientes de alto riesgo y, si el TEP se confirma, es
indicación de reperfusión primaria y por tanto requiere valoración por la Unidad de Cuidados Intensivos (su
mortalidad es del 15-30%).
En los pacientes con TEP confirmado sin inestabilidad, se debe buscar la presencia de marcadores
de disfunción o daño miocárdico que ayuden a identificar un grupo de pacientes con peor pronóstico (TEP
de riesgo intermedio) que los pacientes que no presentan estos datos (TEP de bajo riesgo). Para ello se
utilizan:
Escala PESI (Pulmonary Embolism Severity Index): es la primera evaluación que se debe realizar.
Clasifica a los pacientes en cinco grupos (o en dos grupos en la nueva versión simplificada
recientemente validada) según el riesgo de mortalidad por cualquier causa en los 30 días del
episodio de TEP (Tabla VI).
Los pacientes de bajo riesgo (PESI I-II o sPESI bajo riesgo) no precisan más estudios y se
benefician de alta precoz y seguimiento de forma ambulatoria. En el resto (PESI III-V o sPESI de
alto riesgo) se deberá realizar un ecocardiograma y la determinación de marcadores
bioquímicos.
Ecocardiograma/angio-TC: valora signos de disfunción del VD, hipertensión pulmonar (HP) y/o
trombos móviles. En la angio-TC se utilizan el cociente entre el diámetro del VD y del VI
(patológico si > 0,9), el reflujo de contraste a la vena cava inferior, el abombamiento del septo,
etc., como marcadores indirectos de disfunción del VD.
NT-proBNP: es liberado por la sobrecarga del VD. Su elevación se asocia a mayor riesgo de
mortalidad en pacientes inestables.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [487]
[32] ENFERMEDAD TROMBOEMBÓLICA VENOSA
Tabla VI. Escala PESI y PESI simplificada (sPESI). Riesgo de mortalidad a los 30 días tras un episodio de tromboembolismo pulmonar.
Troponinas: su elevación se relaciona con isquemia (sin traducir un síndrome coronario agudo)
y es un marcador de mortalidad tanto en pacientes estables como en inestables.
En la tabla VII se muestra la clasificación pronóstica de la mortalidad del TEP.
Tabla VII. Clasificación pronóstica de la mortalidad.
IV. TRATAMIENTO
Tiene como objetivos la estabilización médica del paciente, el alivio de los síntomas, la resolución
de la obstrucción vascular y la prevención de las recurrencias.
1. ESTRATEGIA TERAPÉUTICA (FIGURA 3)
Como ya se ha mencionado, los pacientes de alto riesgo se benefician de reperfusión primaria.
Según guías recientes (CHEST Guideline, 2016; ESC Guidelines, 2014), la fibrinólisis primaria en los pacientes
con riesgo de mortalidad intermedio-alto puede prevenir la inestabilidad hemodinámica que amenaza la
vida. Pero estos beneficios están contrarrestados por el alto riesgo de sangrado mayor o intracraneal, por
lo que no está indicada de forma sistemática en este grupo (considerándose en estos la monitorización
estrecha y la posibilidad de trombólisis si apareciese shock). La embolectomía pulmonar quirúrgica o el
tratamiento percutáneo mediante catéter directo pueden ser alternativas válidas.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [488]
[32] ENFERMEDAD TROMBOEMBÓLICA VENOSA
Asimismo, los resultados de un ensayo clínico (Aujesky, 2011) sugieren que en pacientes con riesgo
de mortalidad bajo, el tratamiento ambulatorio comparado con la hospitalización es igual de eficaz y
seguro, pudiendo considerarse en aquellos con buen soporte social, buen acceso a atención médica y en los
que se espere un apropiado cumplimiento terapéutico.
2. TRATAMIENTO DE SOPORTE
Se debe administrar oxígeno suplementario para conseguir saturaciones superiores al 92%
(además, actúa como vasodilatador pulmonar y puede contribuir a la reducción de la presión de las arterias
pulmonares). La administración de líquidos (< 500 ml) puede ser beneficiosa en pacientes con bajo gasto
cardiaco y normotensión arterial (la expansión de volumen de forma agresiva puede ser perjudicial). La
dopamina o la dobutamina se pueden emplear en pacientes con bajo gasto y normotensión, mientras que
para los pacientes con hipotensión estaría indicada la noradrenalina o la adrenalina. El levosimendán en
algunos estudios parece ser efectivo como ionotropo positivo.
Figura 3. Algoritmo de la estrategia terapéutica.
3. TRATAMIENTO ANTICOAGULANTE
En la mayoría de las ocasiones, los objetivos mencionados se alcanzan con el tratamiento
anticoagulante convencional, que evita la progresión del trombo mientras el sistema fibrinolítico endógeno
resuelve la obstrucción vascular, y solo una minoría de los pacientes requiere el siguiente escalón.
El tratamiento se debe instaurar de forma precoz. Se inicia con heparinas, que han de mantenerse
al menos 5 días y hasta alcanzar una adecuada anticoagulación con los fármacos orales (si son antagonistas
de la vitamina K, hasta alcanzar un cociente internacional normalizado [INR] de 2-3 durante 24 horas,
pudiéndose estos iniciar junto con las heparinas). El tratamiento anticoagulante ha de mantenerse al
menos 3 meses, valorando posteriormente el riesgo de recurrencia para decidir la duración definitiva.
Heparina no fraccionada: en perfusión continua para alcanzar un tiempo de tromboplastina
parcial activado (TTPA) de 1,5-2,5 veces el control (ver Capítulo 77. “Trastornos de la
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [489]
[32] ENFERMEDAD TROMBOEMBÓLICA VENOSA
hemostasia. Anticoagulación”). Está indicada en los pacientes que van a recibir fibrinólisis y en
los que tienen alto riesgo de sangrado.
Heparinas de bajo peso molecular (HBPM)/Fondaparinux: es el tratamiento de elección y se
han de mantener al menos 5 días (enoxaparina/tinzaparina/dalteparina/nadroparina). Alcanzan
concentraciones eficaces en 1 hora. La monitorización (medición de la actividad anti-Xa a las 4
horas de su administración) solo es necesaria en casos de obesidad mórbida (peso > 150 kg),
insuficiencia renal (filtrado glomerular [FG] < 30 ml/min), recidiva bajo tratamiento o
complicaciones hemorrágicas (ver Capítulo 77. “Trastornos de la hemostasia. Anticoagulación”).
Anticoagulantes orales:
Los antagonistas de la vitamina K (acenocumarol, warfarina) deberían iniciarse tan
pronto como fuese posible (incluso desde el diagnóstico, junto con las HBPM),
ajustando la dosis para alcanzar un INR de 2-3.
Los anticoagulantes directos que tienen indicación para ETEV son no inferiores y
presentan menor tasa de sangrado que los antivitamina K. Rápido efecto, que se
alcanza tras 1 a 4 horas de la primera dosis. Están contraindicados en la insuficiencia
renal terminal (FG < 15 ml/min). Fármacos disponibles:
Dabigatrán (150 mg/12 h o 110 mg/12 h en pacientes con edad > 80 años, en
pacientes que estén recibiendo verapamilo o en aquellos con alto riesgo de
sangrado). Está contraindicado en la insuficiencia renal grave (FG < 30 ml/min).
Rivaroxabán (15 mg/12 h durante 3 semanas, posteriormente 20 mg/24 h). En
la insuficiencia renal grave (FG 15-30 ml/min) requiere ajuste de la dosis.
Apixabán (10 mg/12 h durante 1 semana, posteriormente 5 mg/12 h). En la
insuficiencia renal grave (FG 15-30 ml/min) debe usarse con precaución.
Edoxabán (60 mg/24 h). Requiere el ajuste de la dosis (30 mg/24 h) en la
insuficiencia renal moderada (FG 30-50) y grave (FG 15-30 ml/min).
4. TERAPIA DE REPERFUSIÓN
Fibrinólisis: acelera la lisis del coágulo, lo que produce una rápida mejoría hemodinámica. El
beneficio es mayor en las primeras 48 horas, pero es útil hasta 6-14 días. Si de inicio se
administró HBPM/fondaparinux, habrá que esperar 12-24 horas para la trombólisis. Son
preferibles los regímenes acelerados (administración en 2 horas) (Tabla VIII).
Tabla VIII. Fármacos trombolíticos.
Alternativas: la fragmentación mecánica del trombo o la embolectomía pulmonar quirúrgica o
transcatéter son alternativas a la fibrinólisis cuando esta está contraindicada, ha fracasado o
cuando hay trombos cardiacos. Requiere recursos y experiencia del equipo.
5. OTRAS TERAPIAS
Movilización precoz: en varios estudios se ha demostrado que la movilización precoz es segura
en pacientes con TVP proximal, sin aumento del riesgo de TEP ni de recurrencias, disminuyendo
el riesgo de síndrome postrombótico.
Medias de compresión convencional: están indicadas para el síndrome postrombótico. Un
ensayo clínico (Kahn, 2013) puso su efectividad en duda, ya que no mostró beneficios con
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [490]
[32] ENFERMEDAD TROMBOEMBÓLICA VENOSA
respecto a las medias placebo, pero dado que tienen pocos efectos adversos locales, se deben
considerar para su tratamiento.
Filtro de vena cava: existen tanto filtros recuperables (de elección) como definitivos (no
extraíbles). Está indicado cuando existe contraindicación para la anticoagulación o en TEP
recurrentes a pesar de la anticoagulación oral (ACO). Bloquean la migración de los trombos
originados en el sistema venoso profundo. Reducen la mortalidad del TEP, pero aumentan la
recurrencia de TVP y síndrome postrombótico, por lo que habría que reiniciar la
anticoagulación tan pronto como sea posible.
V. SEGUIMIENTO Y DURACIÓN DE LA ANTICOAGULACIÓN
La terapia anticoagulante ha de mantenerse durante 3 meses, momento en el que habrá que
decidir si continuar con la anticoagulación por riesgo de recurrencia o suspenderla (sobre todo en la ETEV
provocada y con alto riesgo hemorrágico). No hay suficiente evidencia para establecer pautas claras, y se
deben valorar los riesgos de sangrado y recurrencia (Tablas IX y X) de forma individual.
Tabla IX. Escala RIETE de riesgo hemorrágico.
1. MARCADORES DE RECURRENCIA INDIVIDUALES
Presentación del evento: en el seguimiento de la ETEV, un metaanálisis (Boutitie, 2011)
observó que la recurrencia suele ocurrir de la misma forma en que se presentó el evento,
apreciación de gran importancia, puesto que la mortalidad del TEP es mayor que la de la TVP.
Dímero D: el ensayo PROLONG demostró que la positividad del dímero D al mes de suspender
la anticoagulación (tras un periodo de tratamiento anticoagulante de 3 meses) se asocia con
mayor riesgo de recurrencia, especialmente en el grupo de mujeres (en los varones no está tan
claro).
Obesidad: el sobrepeso aumenta en un 30% el riesgo de recurrencia.
Sexo: hay mayor incidencia de recurrencias en varones con ETEV no provocada.
Edad: la edad superior a 50 años es un factor débil de recurrencia.
Trombofilia: solo las trombofilias de alto grado (síndrome antifosfolípido) tienen riesgo de
recurrencia elevado, encontrando asociaciones débiles en el resto. A pesar de ello, aunque no
hay acuerdo en la literatura médica, en principio en pacientes con déficit de antitrombina,
déficit de proteína S, déficit de proteína C, detección de anticuerpos antifosfolípido, factor V de
Leiden en homocigosis o factor II G20201A en homocigosis, se recomienda mantener el
tratamiento anticoagulante de forma indefinida.
Recanalización TVP: la recanalización precoz indica que la alta capacidad fibrinolítica del
organismo le va a proteger de nuevos episodios, debiéndose valorar mediante ecografía
Doppler de MMII a los 3 meses en el caso de las TVP.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [491]
[32] ENFERMEDAD TROMBOEMBÓLICA VENOSA
Otros factores: habría que valorar la carga trombótica (no es igual un TEP mínimo que un TEP
acabalgado en las arterias pulmonares), e igualmente la carga familiar (ya que, a día de hoy, no
se conocen todos los factores genéticos predisponentes).
Existen modelos predictores de recurrencias (Score DASH, Canadiense, Viena), que, aunque no
están validados externamente, predicen de forma segura aquellos pacientes en los se podría suspender la
anticoagulación (Tabla X).
Tabla X. Score DASH de recurrencia.
2. PRUEBAS DIAGNÓSTICAS EN EL SEGUIMIENTO
Estudio de hipercoagulabilidad: en pacientes con ETEV recurrente o en TEP de causa
desconocida, se aconseja su realización (anticoagulante lúpico, anticuerpos anticardiolipina,
mutación del factor V de Leiden, déficit de proteínas C y S, déficit de antitrombina III, mutación
del gen de la protrombina 20210A) en el seguimiento de los pacientes antes de suspender el
tratamiento anticoagulante.
Estudio de neoplasia oculta: está dirigida y condicionada a los hallazgos en la anamnesis y
exploración, no debe realizarse de rutina.
Dímeros D: tras completar 3 meses de tratamiento ACO y pasado un mes de su suspensión, su
elevación persistente predice recurrencia, como ya se ha comentado.
Ecocardiograma transtorácico: se recomienda su realización a los 3 meses en el TEP de alto
riesgo (inestabilidad hemodinámica) y antes de retirar la anticoagulación en pacientes con
mayor riesgo de evolución a hipertensión pulmonar tromboembólica crónica (HPTEC) (ver
Apartado VIII).
Ecografía venosa de miembros inferiores: en los pacientes con TVP podría realizarse para
valorar a los 3 meses la existencia de trombosis residual (sería un dato predictor de
recurrencia).
No existen recomendaciones acerca de la realización de pruebas de imagen en el seguimiento
para evaluar la resolución del trombo.
3. DURACIÓN DE LA ANTICOAGULACIÓN
En los pacientes con TEP provocada por factores de riesgo (quirúrgicos y no quirúrgicos), se
sugiere tratamiento anticoagulante durante 3 meses.
En pacientes con TEP no provocada se recomienda tratamiento anticoagulante durante un
mínimo de 3 meses y se sugiere valorar el tratamiento indefinido en función del balance riesgo
recurrencia/riesgo hemorrágico.
En los pacientes que tienen indicación de tratamiento indefinido se recomienda la reevaluación
periódica de esta indicación.
Para los pacientes con un segundo episodio de TVP o TEP no provocada, se recomienda
tratamiento anticoagulante indefinido, reevaluando de forma periódica la indicación.
Los pacientes con TVP proximal o TEP no provocada en los que se decida no continuar la
anticoagulación, serán candidatos a tratamiento con ácido acetilsalicílico 100 mg/día para
reducir el riesgo de recurrencia.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [492]
[32] ENFERMEDAD TROMBOEMBÓLICA VENOSA
VI. SITUACIONES ESPECIALES
1. EMBARAZO
El TEP es la principal causa de muerte materna relacionada con la gestación en países
desarrollados, por lo que su sospecha justifica el empleo de pruebas diagnósticas con el fin de confirmar o
descartar su presencia. El riesgo de TEP es mayor en el posparto, particularmente después de una cesárea.
La clínica es aún más inespecífica que en la población general, pues algunos de los síntomas pueden
acompañar a un embarazo normal. Los más frecuentes serían tos, disnea, dolor torácico y sudoración.
Diagnóstico: el punto de corte del dímero D es el habitual (< 500), aunque este aumenta de
forma fisiológica en el embarazo. Si está aumentado, se recomienda realizar una ecografía de
los MMII como primera prueba de imagen (tras la radiografía de tórax), ya que si resulta
positiva justifica el inicio de la terapia anticoagulante, evitando pruebas adicionales. Si fuese
negativa, se prioriza la gammagrafía de V/Q sobre la angio-TC con protección mamaria en
pacientes con radiografía de tórax normal. Si esta es anormal o si no se dispone fácilmente de
gammagrafía, se debería considerar la angio-TC. Ambas presentan una dosis estimada de
radiación fetal y materna inferior al valor considerado peligroso y son igual de seguras para
descartar TEP.
Tratamiento: es de elección la HBPM ajustada al peso. La heparina no fraccionada (HNF) podría
utilizarse si fuera necesario, debiendo monitorizarse el TTPA. Durante el embarazo se
desaconseja el uso de fondaparinux, antagonistas de la vitamina K (AVK) y anticoagulantes
directos. Tras el parto, el tratamiento con heparina se puede reemplazar por AVK (también en
madres lactantes). El tratamiento anticoagulante debe administrarse hasta al menos 6 semanas
después del parto, con una duración total del tratamiento ≥ 3 meses.
2. CÁNCER
El riesgo medio es cuatro veces superior y depende del tipo de tumor, el grado de extensión y el
tratamiento antineoplásico concomitante. Aunque los mayores números absolutos de episodios de TEV se
producen en pacientes con cáncer de pulmón, colon y próstata, el riesgo relativo es mayor en el mieloma
múltiple y los cánceres cerebral y pancreático (respectivamente 46, 20 y 16 veces mayor frente a controles
sanos). También está aumentado el riesgo de hemorragia. Además, el riesgo de TEV aumenta más de 90
veces en las primeras 6 semanas después de una cirugía de cáncer, y permanece elevado (hasta 30 veces)
entre el 4º y el 12º mes después de la operación.
Diagnóstico: el algoritmo diagnóstico es el mismo. El dímero D negativo tiene el mismo valor
que en el resto, pero en muchos de estos pacientes está aumentado de forma inespecífica.
Tratamiento: se sigue el mismo protocolo de estratificación pronóstica y tratamiento. El
tratamiento anticoagulante de elección durante la fase aguda (7-10 primeros días) son las
HBPM ajustadas al peso (excepto para el TEP de alto riesgo). El tratamiento anticoagulante con
HBPM debe mantenerse un mínimo de 3 meses y se aconseja continuar hasta que el proceso
neoplásico esté curado. Se recomienda el uso de dosis terapéuticas, pudiéndose valorar a partir
de 1 mes de tratamiento reducir la dosis un 25%. En aquellos que presenten episodios de ETEV
bajo dosis de prevención o intermedias de HBPM, deberá aumentarse la terapia a dosis
anticoagulantes; si ocurre con HBPM a dosis plenas, se puede valorar el aumento de la dosis en
un 20-25% o la inserción de un filtro de vena cava. La ETEV incidental (asintomática) en
pacientes con cáncer debe tratarse como un episodio sintomático.
3. EMBOLIA PULMONAR NO TROMBÓTICA
Es rara y su diagnóstico puede ser difícil. Los síntomas son similares a los de la ETEV aguda.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [493]
[32] ENFERMEDAD TROMBOEMBÓLICA VENOSA
En el caso de presentar microémbolos, estos no se detectan en la TC.
Embolia séptica: es relativamente rara y suele asociarse a endocarditis derecha, aunque
también hay otras causas, como tromboflebitis séptica procedente de las amígdalas y las
regiones yugular, dental y pélvica. Es necesario el tratamiento específico del microorganismo
causal.
Embolia pulmonar por material extraño: silicona, catéteres rotos, filtros de vena cava, etc.
Embolia grasa: se produce en casi todos los pacientes con fracturas de cadera o huesos largos y
en los sometidos a colocación de clavos intramedulares o prótesis de cadera y rodilla, aunque
en la mayoría de los casos es autolimitada. Si presenta síntomas, la tríada clásica se caracteriza
por estado mental alterado, dificultad respiratoria y erupción petequial tras un periodo
asintomático de 12-36 horas tras la lesión. El tratamiento es de soporte.
Embolia gaseosa: los émbolos venosos son más comunes que los arteriales, ya que con
frecuencia son complicación de catéteres venosos centrales y de hemodiálisis. El volumen
mortal de inyección de aire varía entre 100-500 ml. La TC puede ser la prueba diagnóstica más
sensible, aunque también se puede diagnosticar mediante radiografía o ecografía. El
tratamiento consiste en colocación en posición de seguridad (decúbito lateral izquierdo en el
embolismo venoso y en decúbito supino en el embolismo arterial), oxigenoterapia a alto flujo,
soporte hemodinámico y expansión de volumen.
Embolia por líquido amniótico: se trata de una complicación rara con alta mortalidad. Ocurre
durante el parto normal o cuando la placenta se altera por cirugía o traumatismo. El
tratamiento es similar a la embolia gaseosa.
Embolia tumoral: es una de las formas más frecuentes, ya que todos los casos de metástasis
pulmonares hematógenas se derivan de fragmentos tumorales acantonados en los vasos
pulmonares. Debido al pequeño tamaño de la mayoría de los fragmentos tumorales, los efectos
atribuibles a la obstrucción de vasos son muy poco aparentes. Cuando los émbolos tumorales
alcanzan un tamaño o número suficiente para comportarse como tromboembolias, las
manifestaciones clínicas, anatomopatológicas y radiológicas pueden ser superponibles a la
ETEV convencional, e incluyen el infarto pulmonar, el cor pulmonale agudo y la hipertensión
pulmonar. Los carcinomas de próstata, digestivos, de hígado y de mama son los más implicados
habitualmente. El tratamiento debe ir dirigido a la enfermedad maligna subyacente.
VII. PREVENCIÓN DE LA ENFERMEDAD TROMBOEMBÓLICA VENOSA
La estratificación del riesgo de ETEV en los pacientes y la adopción de medidas preventivas en cada
caso específico es la vía más efectiva para reducir la morbimortalidad en la ETEV. Se ha demostrado que la
prevención sistemática en los enfermos de alto riesgo es una medida eficaz y segura, con una buena
relación coste-efectividad.
1. INDICACIONES
1.1. Paciente médico hospitalizado
Se recomienda realizar prevención de la ETEV con HBPM o fondaparinux (como alternativa, se puede usar
HNF) durante la hospitalización en todos los pacientes ingresados con enfermedad médica aguda y alto
riesgo de desarrollar una ETEV (Tabla XI), no estando indicada en pacientes con bajo riesgo. Está
contraindicada en pacientes que presentan alto riesgo de sangrado (Tabla XII) o sangrado activo, en cuyo
caso se recomienda la prevención no farmacológica con medidas mecánicas (medias de compresión,
compresión neumática intermitente) (ver Apartado “Medidas de prevención no farmacológica”).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [494]
[32] ENFERMEDAD TROMBOEMBÓLICA VENOSA
Tabla XI. Factores de riesgo para enfermedad tromboembólica venosa de Padua.
Tabla XII. Factores de riesgo de sangrado más identificados.
Recomendaciones específicas:
Insuficiencia cardiaca, enfermedad pulmonar obstructiva crónica descompensada, infección
aguda: se recomienda prevención con HBPM a dosis de alto riesgo en pacientes hospitalizados
mientras estén encamados.
Cáncer: se recomienda prevención con HBPM en pacientes hospitalizados con una enfermedad
médica aguda que estén encamados. En los pacientes ambulatorios no está justificada la
prevención primaria sistemática, aunque estén recibiendo quimioterapia (salvo regímenes con
talidomida o lenalidomida para el mieloma múltiple) o aunque sean portadores de un catéter
venoso central.
Accidente cerebrovascular agudo (ACVA): se recomienda prevención con HBPM en la fase
aguda del ictus (durante 2 semanas), en casos con bajo riesgo de hemorragia intracraneal y
mientras dure la hospitalización; también en caso de paresia de los miembros inferiores,
siempre que se asocie otro FR. No hay evidencia que avale o no el uso de anticoagulantes y/o
antitrombóticos en el ACVA hemorrágico, por lo que solo se indican medidas físicas.
1.2. Paciente quirúrgico hospitalizado
Se proponen los grupos de riesgo reflejados en la tabla XIII. La cirugía de prótesis total de cadera y de
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [495]
[32] ENFERMEDAD TROMBOEMBÓLICA VENOSA
fractura de cadera representa una de las situaciones de mayor riesgo de TVP postoperatoria. El riesgo en la
cirugía ginecológica y urológica es similar al de la cirugía general. Recomendaciones específicas:
Cirugía oncológica: la prevención con HBPM a dosis altas 1 vez al día (o HNF 5.000 UI 3 veces al
día) debe comenzar de 12 a 2 horas antes de la intervención y se debe mantener de 7 a 10 días.
Se ampliará a 4 semanas la duración en caso de cirugía oncológica abdominal o pélvica en
pacientes con alto riesgo de enfermedad tromboembólica y bajo riesgo de hemorragia.
Procedimientos laparoscópicos sin FR: se desaconseja una prevención sistemática distinta de la
movilización intensiva.
Pacientes neuroquirúrgicos: se prefieren medidas físicas sobre los agentes farmacológicos para
evitar complicaciones hemorrágicas; pueden asociarse ambos en los pacientes de alto riesgo.
Tabla XIII. Riesgo de tromboembolismo venoso posquirúrgico.
Politraumatismos: tienen un riesgo moderado-alto de trombosis; en este grupo se recomienda
HBPM y, si existiese contraindicación por riesgo de sangrado, la compresión neumática.
Traumatismos medulares: el periodo de mayor riesgo son las dos primeras semanas. En
ausencia de otros FR, la prevención se debería mantener 3 meses.
1.3. Prevención en situaciones especiales
Embarazo: las recomendaciones son variables y deben individualizarse en cada caso. Se indica
prevención con HPBM a dosis altas: 1) si el paciente tiene alto riesgo de ETEV; 2) si presenta
algún FR (incluida la obesidad) y una enfermedad médica o quirúrgica (por ejemplo, neumonía,
sepsis) o encamamiento, o si presenta dos o más enfermedades durante el ingreso.
Viajes prolongados (> 6 horas): se recomienda la movilización y la contracción periódica de las
piernas, hidratación y evitar llevar ropas ajustadas alrededor de las extremidades y la cintura.
En individuos con FR adicionales, se recomiendan las medias de compresión gradual, y en
sujetos con riesgo trombótico alto está indicado emplear una dosis única de HBPM antes del
viaje. No se ha demostrado la eficacia del ácido acetilsalicílico.
2. MEDIDAS DE PREVENCIÓN NO FARMACOLÓGICA
Medidas generales: se debe promover la movilización precoz del paciente encamado y una
hidratación adecuada.
Medidas de compresión extrínseca: se utilizan, como método único, en los pacientes con
contraindicaciones para los anticoagulantes en dosis preventivas, entre ellos los pacientes con
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [496]
[32] ENFERMEDAD TROMBOEMBÓLICA VENOSA
sangrado activo o con alto riesgo de desarrollarlo (neuroquirúrgicos, con úlcera gastroduodenal
activa, recuento de plaquetas < 50.000/ml, antecedente de sangrado en los 3 meses previos).
También se recomiendan como complemento de la prevención farmacológica en pacientes con
alto riesgo de trombosis. No obstante, están contraindicadas en pacientes con enfermedad
arterial isquémica, neuropatía periférica o dermopatía de las extremidades inferiores.
Compresión neumática intermitente: es el medio de elección. Debe introducirse lo antes
posible y mantenerse con las mínimas interrupciones hasta el alta.
Medias de compresión gradual: en los pocos estudios de calidad realizados en pacientes
quirúrgicos, han demostrado ser efectivas tanto en uso combinado con otros métodos
farmacológicos como de forma aislada (con menor eficacia que los métodos farmacológicos).
En pacientes con enfermedades médicas hay incluso menos estudios y no han demostrado ser
efectivas. En cualquier caso, en pacientes que presenten factores de riesgo para ETEV en los
que la anticoagulación esté contraindicada, se prefiere el uso de métodos mecánicos
(cualquiera de los dos) antes que no realizar ningún tipo de prevención.
3. MEDIDAS DE PREVENCIÓN FARMACOLÓGICA (TABLA XIV)
Heparinas: son de elección las HBPM, pero tanto la HNF como las HBPM han demostrado con
igual eficacia reducir el riesgo de ETEV en pacientes hospitalizados no quirúrgicos. En
situaciones especiales, como la obesidad mórbida, se utilizan dosis superiores a las de alto
riesgo, siendo prudente la monitorización de la actividad anti-Xa.
Fondaparinux: frente a las HBPM ha demostrado igual eficacia en el paciente no quirúrgico y
superioridad en la cirugía mayor ortopédica, con un aumento del riesgo de sangrado mayor (no
complicado). Tiene una dosis fija de 2,5 mg/24 h sc para un peso de 50-100 kg, que debe
ajustarse si hay alteración de la función renal (FG < 30 ml/min). En procedimientos quirúrgicos
se administra en el postoperatorio.
Tabla XIV. Dosis de fármacos para la prevención primaria de la enfermedad tromboembólica venosa.
Anticoagulantes orales directos: inhibidores de los factores Xa (rivaroxabán, apixabán) y IIa
(dabigatrán). En la prevención de ETEV solo están aprobados en pacientes sometidos a cirugía
de reemplazo de cadera o rodilla. Los tres han demostrado que no son inferiores a la HBPM, sin
mayor incidencia de sangrado.
Antagonistas de la vitamina K: no se recomiendan por la latencia del efecto anticoagulante y el
posible efecto protrombótico (por descenso de la proteína C) durante las primeras 36-72 horas;
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [497]
[32] ENFERMEDAD TROMBOEMBÓLICA VENOSA
tienen su papel (con un objetivo de INR 2-3) en pacientes que requieren prevención prolongada
y tienen dificultad para la administración de HBPM.
Ácido acetilsalicílico: no está demostrada su eficacia.
4. INICIO Y DURACIÓN DE LA PREVENCIÓN
La prevención debe mantenerse durante todo el ingreso hasta que se alcance la movilización activa
y persistente del paciente.
En el caso de pacientes quirúrgicos, la duración del tratamiento comprende desde 24 horas antes
de la cirugía hasta completar 35 días con HBPM (o 21 días con fondaparinux) en casos de cirugía ortopédica
mayor, o 28 días en cirugía abdominal mayor por cáncer o en aquellos casos con antecedente de ETEV.
VIII. HIPERTENSIÓN PULMONAR TROMBOEMBÓLICA CRÓNICA (HPTEC)
1. DEFINICIÓN Y EPIDEMIOLOGÍA
Se trata de un incremento de la presión arterial pulmonar (PAP) media ≥ 25 mm Hg, con presión de
oclusión arterial pulmonar ≤ 15 mm Hg en reposo, causada por defectos de perfusión persistentes de las
arterias pulmonares por gammagrafía de V/Q, a pesar de al menos 3 meses con tratamiento anticoagulante
correcto. Aunque dicho tratamiento sea efectivo, más del 50% de los pacientes presentan defectos de
perfusión residual 6 meses después del diagnóstico de TEP. Sin embargo, la mayoría de ellos no
desarrollarán HPTEC manifiesta. La incidencia acumulada es del 0,1-9,1% en los primeros 2 años tras un
episodio de TEP sintomático, pero los datos epidemiológicos disponibles en España demuestran que se
trata de una enfermedad infradiagnosticada y rara, con una incidencia en 2013 de 1,26 casos/millón de
habitantes adultos/ año, y una prevalencia de 8,4 casos/millón de habitantes adultos. No se recomienda
realizar pruebas torácicas de imagen para evaluar la persistencia de trombosis residual, salvo en los casos
que se sospecha HPTEC.
El riesgo de desarrollar HPTEC aumenta en pacientes con ETEV recurrente, TEP de alto riesgo, TEP
idiopático y en los pacientes con hipertensión pulmonar en el diagnóstico inicial de TEP.
2. DIAGNÓSTICO
La primera prueba que se debe realizar para el cribado de HPTEC es la ecocardiografía
transtorácica. Las indicaciones de ecocardiografía en el seguimiento de pacientes con TEP son: 1) síntomas
o signos sugestivos de HPTEC (el más frecuente es la disnea persistente; otros son síncope, hemoptisis o
signos de IC derecha); 2) TEP recurrente; 3) síndrome antifosfolípido; 4) ECG con signos de hipertrofia del
VD; 5) PAP > 50 mm Hg en el ecocardiograma del TEP agudo; 6) TEP de alto riesgo, y 7) signos de HPTEC en
la angio-TC del TEP agudo.
Tras sospechar HPTEC por la clínica, el ecocardiograma y la gammagrafía de V/Q, es necesario
confirmar el diagnóstico mediante el cateterismo cardiaco derecho y evaluar correctamente la localización
de las lesiones trombóticas mediante angio-TC y arteriografía pulmonar (Figura 4).
3. TRATAMIENTO
Es importante que los pacientes con sospecha o diagnóstico de HPTEC sean remitidos a un centro
experto en endarterectomía pulmonar (EP) para su valoración por un equipo multidisciplinar. El
tratamiento de elección es la EP quirúrgica, ya que podría conseguir la curación. Los pacientes no
candidatos a EP o con presencia de HP residual tras la EP pueden beneficiarse de tratamiento específico
para la HP, siendo el riociguat (activador oral de la guanilato ciclasa) el único fármaco estudiado en ensayo
clínico doble ciego y aleatorizado. En estos pacientes se puede valorar también la realización de
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [498]
[32] ENFERMEDAD TROMBOEMBÓLICA VENOSA
angioplastia pulmonar con balón en centros con experiencia, o finalmente el trasplante pulmonar si todos
los tratamientos fracasan. Independientemente de la opción elegida, está indicada la anticoagulación de
por vida (Figura 5).
Figura 4. Algoritmo diagnóstico en la hipertensión pulmonar tromboembólica crónica.
Figura 5. Algoritmo para el tratamiento de la hipertensión pulmonar tromboembólica crónica.
BIBLIOGRAFÍA
Agnelli G, Büller HR, Cohen A, Curto M, Gallus AS, Johnson M. Oral apixaban for the treatment of acute
venous thromboembolism. N Engl J Med. 2013;369(9):799-808.
Aujesky D, Roy PM, Verschuren F, Righini M, Osterwalder J, Egloff M, et al. Outpatient versus inpatient
treatment for patients with acute pulmonary embolism: an international, open-label, randomised, non-
inferiority trial. Lancet. 2011;378(9785):41-8.
Baglin T, Douketis J, Tosetto A, Marcucci M, Cushman M, Kyrle P, et al. Does the clinical presentation
and extent of venous thrombosis predict likelihood and type of recurrence? A patient-level meta-
analysis. J Thromb Haemost. 2010;8(11):2436-42.
Becattini C, Agnelli G, Schenone A, Eichinger S, Bucherini E, Silingardi M, et al. Aspirin for preventing
the recurrence of venous thromboembolism. N Engl J Med. 2012;366(21):1959-67.
Boutitie F, Pinede L, Schulman S, Agnelli G, Raskob G, Julian J, et al. Influence of preceding length of
anticoagulant treatment and initial presentation of venous thromboembolism on risk of recurrence
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [499]
[32] ENFERMEDAD TROMBOEMBÓLICA VENOSA
after stopping treatment: analysis of individual participants’ data from seven trials. BMJ.
2011;342:d3036.
Di Nisio M, van Es N, Büller HR. Deep vein thrombosis and pulmonary embolism. Lancet. 30 Jun 2016.
Grupo de Trabajo de la SEC. Comments on the 2014 ESC Guidelines on the Diagnosis and
Management of Acute Pulmonary Embolism. Rev Esp Cardiol. 2015;68(1):10-6.
Juretschke Moragues MA, Barbosa Ayucar C. Monografia Neumomadrid: Tromboembolismo pulmonar.
Barcelona: Doyma; 2002 [consultado: 20 de febrero de 2016]. Disponible en:
http://neumomadrid.org/ descargas/monog_neumomadrid_iv.pdf.
Kearon C, Akl EA, Comerota AJ, Prandoni P, Bounameaux H, Goldhaber SZ. Antithrombotic therapy for
VTE disease: antithrombotic therapy and prevention of thrombosis, 9th ed: American College of Chest
Physicians Evidence-Based Clinical Practice Guidelines. Chest. 2012;141(2 Suppl):e419S-94S.
Kearon C, Akl EA, Ornelas J, Blaivas A, Jiménez D, Bounameaux H, et al. Antithrombotic therapy for VTE
disease: CHEST Guideline and Expert Panel Report. Chest. 2016;149(2):315-52.
Lozano Olivares J, coordinador. Hipertensión pulmonar tromboembólica crónica. Consejo General de
Colegios Oficiales de Médicos de España y Ministerio de Sanidad, Servicios Sociales e igualdad. 2015
[consultado: 20 de febrero de 2016]. Disponible en:
http://secardiologia.es/images/publicaciones/documentos-consenso/ pas-hipertension-pulmonar-
interactivo.pdf.
Mannucci PM, Franchini M. The real value of thrombophilia markers in identifying patients at high risk
of venous thromboembolism. Expert Rev Hematol. 2014;7(6):757-65.
Olmos VP, Ramos Gallo MJ, Antonio Rebollo M, Ballesteros Ortega D, Iglesias Docampo L, Romera-
Villegas A, et al. Manejo de la enfermedad tromboembólica venosa en pacientes oncológicos: guías de
práctica clínica española. Consenso SEACV-SEOM. Med Clin. 2015;144(Supl 1):3-15.
Otero Candelera R, Grau Segura E, Jiménez Castro D, Uresandi Romero F, López Villalobos JL, Calderón
Sandubete E, et al. Profilaxis de la enfermedad tromboembólica venosa. Arch Bronconeumol.
2008;44(3):160- 9.
Palareti G, Cosmi B, Legnani C, Tosetto A, Brusi C, Iorio A, et al. D-dimer testing to determine the
duration of anticoagulation therapy. N Engl J Med. 2006;355(17):1780-9.
Qaseem A, Chou R, Humphrey LL, Starkey M, Shekelle P; Clinical Guidelines Committee of the American
College of Physicians. Venous thromboembolism prophylaxis in hospitalized patients: a clinical practice
guideline from the American College of Physicians. Ann Intern Med. 2011;155(9):625-32.
Rachel L, Luke H. Developments in the management and treatment of pulmonary embolism. Eur Resp
Rev. 2015;24:484-97.
Reid JH, Coche EE, Inoue T, Kim EE, Dondi M, Watanabe N, et al. Is the lung scan alive and well? Facts
and controversies in defining the role of lung scintigraphy for the diagnosis of pulmonary embolism in
the era of MDCT. Eur J Nucl Med Mol Imaging. 2009;36(3):505-21.
Righini M, Van Es J, den Exter PL, Roy PM, Verschuren F, Ghuysen A, et al. Age-adjusted D-dimer cutoff
levels to rule out pulmonary embolism: The ADJUST-PE Study. JAMA. 2014;311(11):1117-24.
Scottish Intercollegiate Guidelines Network. Prevention and management of venous thromboembolism.
Quick Reference Guide. Edinburgh: 2010 [consultado: 20 de febrero de 2016]. Disponible en:
http://www.sign.ac.uk/ pdf/qrg122.pdf.
Stein PD, Fowler SE, Goodman LR, Gottschalk A, Hales CA, Hull RD, et al. Multidetector computed
tomography for acute pulmonary embolism. N Engl J Med. 2006;354(22):2317-27.
Task Force for the Diagnosis and Management of Acute Pulmonary Embolism of the European Society
of Cardiology (ESC). 2014 ESC Guidelines on the diagnosis and management of acute pulmonary
embolism. Eur Heart J. 2014;35(43):3033-69, 3069a-k.
Tosetto A, Iorio A, Marcucci M, Baglin T, Cushman M, Eichinger S. Predicting disease recurrence in
patients with previous unprovoked venous thromboembolism. A proposed prediction score (DASH). J
Thromb Haemost. 2012;10(6):1019-25.
Uresandi F, Lecumberri R, Monreal M, Escribano P, García-Bragado F, Zamorano JL, et al. Consenso
nacional sobre el diagnóstico, estratificación de riesgo y tratamiento de los pacientes con
tromboembolia pulmonar. Arch Bronconeumol. 2013;49(12):534-47.
Uresandi J, Jiménez D. Actualización del Consenso nacional sobre el diagnóstico, estratificación de
riesgo y tratamiento de los pacientes con tromboembolia de pulmón. Arch Bronconeumol. 2016;52:61-
2.
Uresandi Romero F, Iruin Irulegui G. Enfermedad tromboembólica venosa: prevención y tratamiento.
En: Álvarez-Sala JL, Casán P, Rodríguez F, Rodríguez JL, Villena-Garrido V. Neumología Clínica. Madrid:
Elsevier; 2010. p. 413-22.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [500]
[33] ENFERMEDADES PULMONARES INTERSTICIALES DIFUSAS
33.Enfermedades pulmonares intersticiales difusas
María Emilia Banderas Montalvo.
Neumología
Beatriz Sánchez Moreno.
Medicina Interna
Asesora: Victoria Villena Garrido. Jefa de Sección de Neumología
I. CONCEPTO
Las enfermedades pulmonares intersticiales difusas (EPID) constituyen un grupo heterogéneo de
enfermedades y se caracterizan por afectar principalmente a las estructuras alvéolo-intersticiales
pulmonares, pudiendo extenderse a la pequeña vía aérea y a los vasos pulmonares. Tienen algunas
similitudes en sus manifestaciones clínicas, radiológicas y funcionales, presentándose típicamente con
disnea de esfuerzo, un patrón alveolar y/o intersticial difuso en la radiografía de tórax y una alteración
ventilatoria restrictiva. Pueden evolucionar de manera aguda, subaguda o crónica y se clasifican
dependiendo de si tienen una causa conocida o de si son idiopáticas.
Tabla I. Clasificación de las enfermedades pulmonares intersticiales difusas de la ATS-ERS 2002, modificada en 2012.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [501]
[33] ENFERMEDADES PULMONARES INTERSTICIALES DIFUSAS
Existen pocos datos acerca de la epidemiología de estas enfermedades, y la frecuencia de las
mismas varía de acuerdo a la región estudiada. En España la fibrosis pulmonar idiopática (FPI) es la EPID
más frecuente con una incidencia mundial entre 4,6 y 7,4/100.000 habitantes, pudiendo afectar a unas
7.500 personas aproximadamente en nuestro país. Le siguen en frecuencia la sarcoidosis, la neumonía
organizada criptogenética (NOC) y las EPID asociadas a conectivopatías.
II. CLASIFICACIÓN Y ETIOLOGÍA
Las causas de las EPID son amplias (más de 150), y solo en un 35% se logra obtener una etiología.
Pueden ser causadas por inhalación de polvos, toma de fármacos, asociarse a conectivopatías o a otras
enfermedades, englobándose la mayoría de las EPID en el grupo de idiopáticas. Se clasifican de acuerdo al
consenso de la ATS-ERS de 2002, modificado en el año 2012, en EPID idiopáticas, EPID de causa conocida y
EPID primarias (Tabla I). Es fundamental diferenciar la FPI del resto de EPID idiopáticas.
III. CLÍNICA
1. SÍNTOMAS
Los más frecuentes son la disnea de esfuerzo y la tos seca. La disnea suele ser lentamente
progresiva. Algunas de estas enfermedades, en especial las de presentación aguda-subaguda, pueden
acompañarse de fiebre y sintomatología sistémica: neumonía intersticial aguda, neumonitis por
hipersensibilidad (NH), neumonía organizada criptogenética (NOC), fármacos, eosinofilias pulmonares.
2. EXAMEN FÍSICO
En la FPI, y con menos frecuencia en otras EPID, se pueden auscultar crepitantes de tipo «velcro» al
final de la inspiración y de predominio bibasal, sobre todo en la línea medio-axilar. También se pueden
observar acropaquias en algunos casos. En ocasiones se pueden detectar sibilancias, como es el caso de la
NH y las eosinofilias pulmonares. En fases avanzadas pueden aparecer datos sugerentes de hipertensión
pulmonar (ver Capítulo 27. “Hipertensión pulmonar”).
Se deben buscar además signos extrapulmonares sugestivos o característicos de algunas de las
enfermedades del colágeno antes mencionadas en la tabla I, como nódulos subcutáneos, afectación
articular, queratoconjuntivitis, miositis, etc. En el caso de la sarcoidosis, signos como la uveítis, los nódulos
subcutáneos, la artritis, la afectación neurológica o la hepatoesplenomegalia son muy útiles para el
diagnóstico.
IV. DIAGNÓSTICO (Figura 1)
1. ANAMNESIS
Realizándose una adecuada historia clínica se puede avanzar en el diagnóstico y orientarlo en casi
un tercio de las EPID. Debemos fijarnos en la edad y el sexo. Entre los 20 y 40 años son más frecuentes las
asociadas a enfermedad del colágeno y la sarcoidosis, mientras que la FPI es más frecuente en mayores de
50 años. La linfangioleiomiomatosis se produce mayoritariamente en mujeres. Los antecedentes familiares
son relevantes (FPI, sarcoidosis y microlitiasis alveolar). El tabaco está asociado a algunas de las EPID
idiopáticas (neumonía intersticial descamativa, bronquiolitis respiratoria asociada a enfermedad pulmonar
intersticial, histiocitosis de células de Langerhans) y es un factor de riesgo para la FPI. La historia
ocupacional y la laboral son importantes, sobre todo en neumoconiosis y NH; se debe detallar el tiempo y
el tipo de exposición, recuperando todas las ocupaciones en orden cronológico. Viajes, exposición a otros
tóxicos, antecedentes farmacológicos y otras enfermedades sistémicas constituyen también datos útiles
para el diagnóstico.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [502]
[33] ENFERMEDADES PULMONARES INTERSTICIALES DIFUSAS
Figura 1. Algoritmo diagnóstico de las enfermedades pulmonares intersticiales.
2. PRUEBAS COMPLEMENTARIAS INICIALES
2.1. Pruebas de laboratorio
Es necesario disponer de un hemograma (por ejemplo, en las eosinofilias pulmonares podremos encontrar
eosinofilia en sangre periférica) y de una bioquímica, incluyendo perfil renal y hepático. La elevación de la
lactato deshidrogenasa es inespecífica, pues se halla en muchas de las EPID. Puede ser útil medir el calcio
(hipercalcemia en algunos casos de sarcoidosis) y la calciuria de 24 horas (elevada en la sarcoidosis). En
caso de desaturación por pulsioximetría, hay que realizar una gasometría arterial basal, pues marcará la
gravedad del paciente.
Conviene también solicitar un perfil de autoinmunidad completo, con anticuerpos antinucleares,
anticuerpos extraíbles del núcleo (especialmente anti-Jo-1, anti-Scl 70 y anticentrómero), anti-ADN nativo,
anticuerpos anticitoplasma de neutrófilo, factor reumatoide y anticuerpo anticitrulinado, correlacionando
siempre los resultados con la clínica del paciente, teniendo en cuenta que existen casos en los que las
enfermedades del colágeno comienzan con una EPID.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [503]
[33] ENFERMEDADES PULMONARES INTERSTICIALES DIFUSAS
Se pueden además pedir niveles de enzima convertidora de angiotensina, la cual se puede elevar en
un 40% de los individuos con sarcoidosis. No obstante, tiene un rol limitado en el diagnóstico, puesto que
cuenta con una pobre sensibilidad, una escasa especificidad y hasta un 15% de falsos positivos; podría
tener alguna utilidad en casos con una alta probabilidad pre-prueba de sarcoidosis en los que no se quiere
realizar pruebas más invasivas. Por otra parte, es posible solicitar la detección de precipitinas séricas
cuando existe sospecha de NH (reflejando exposición, no enfermedad).
2.2. Pruebas de imagen
La radiografía de tórax es básica para el diagnóstico inicial y en el seguimiento debido a que la mayoría de
los pacientes tienen una alteración radiológica al momento del diagnóstico. Además, la localización del
patrón intersticial y las imágenes asociadas son una importante ayuda diagnóstica (Tabla II).
Tabla II. Alteraciones en la radiografía torácica en las enfermedades pulmonares intersticiales difusas.
La tomografía computarizada torácica es más sensible que la radiografía para el intersticio
pulmonar, debiendo realizarse una tomografía helicoidal con cortes finos, ya que permite detectar la
enfermedad incluso cuando la radiografía es normal. Valora la extensión de las lesiones parenquimatosas y
su naturaleza y, en algunos casos, puede ser diagnóstica, como en la FPI, en la asbestosis, en la
linfangioleiomiomatosis y en la histiocitosis de células de Langerhans, siendo necesario que se interprete
por radiólogos especializados. Para el resto de EPID es útil como orientación diagnóstica, permitiendo
además valorar cuál es el mejor segmento anatómico para la realización del lavado broncoalveolar y de la
biopsia pulmonar, en caso de ser necesarios. En la tabla III se describen los patrones intersticiales más
frecuentes visualizados en la tomografía computarizada (TC) en algunas EPID.
2.3. Pruebas de función respiratoria
Son fundamentales para el diagnóstico, pronóstico y seguimiento de las EPID. Se debe tener en cuenta que
una exploración funcional normal no excluye el diagnóstico. En la mayoría de las EPID, en la espirometría
forzada, se suele objetivar un patrón sugerente de restricción con disminución de la capacidad vital forzada
(CVF); sin embargo, algunas como la NH, las eosinofilias pulmonares, la sarcoidosis y la
linfangioleiomiomatosis, entre otras, pueden presentar un patrón obstructivo. En la pletismografía se
puede observar una disminución de la capacidad pulmonar total. La difusión puede estar disminuida (es un
indicador muy sensible de la progresión y pronóstico de las EPID). El test de la marcha de los 6 minutos es
igualmente útil para evaluar la evolución y pronóstico.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [504]
[33] ENFERMEDADES PULMONARES INTERSTICIALES DIFUSAS
Tabla III. Patrones radiológicos de algunas enfermedades pulmonares intersticiales difusas, en relación con su histología.
3. PRUEBAS COMPLEMENTARIAS ESPECÍFICAS (ESTUDIO AVANZADO)
Mediante la broncoscopia se pueden realizar diferentes estudios muy importantes para el
diagnóstico de las EPID, como el lavado broncoalveolar, la biopsia transbronquial y la criobiopsia.
El lavado broncoalveolar permite realizar estudio citológico (valorar datos de malignidad),
recuento celular (que puede orientar hacia el diagnóstico de algunas EPID), subpoblaciones linfocitarias o
estudio microbiológico. Puede ser diagnóstico en la proteinosis alveolar y en las eosinofilias pulmonares;
además, ayuda a realizar un diagnóstico diferencial.
En los pacientes con EPID que presentan datos clínicos y radiológicos inconsistentes es
recomendable llevar a cabo una biopsia pulmonar, ya sea de manera quirúrgica o por broncoscopia.
La biopsia tranbronquial (BTB) se realiza guiando la punción de acuerdo a las imágenes de la TC.
Permite diagnosticar procesos neoplásicos, pero también puede ser diagnóstica en sarcoidosis, neumonitis
por hipersensibilidad, eosinofilias pulmonares y linfangioleiomiomatosis, entre otras. Dentro de las EPID
idiopáticas tiene poca utilidad, pues rara vez se obtiene un diagnóstico debido al tamaño de la muestra, a
excepción de la NOC.
La criobiopsia es una técnica viable y con mayor rendimiento diagnóstico para la obtención de
muestras del parénquima pulmonar que la BTB, pues permite conseguir una muestra de mayor tamaño y
mejor preservada para el análisis histopatológico. Es menos invasiva y de menor coste que una biopsia
quirúrgica. Se realiza mediante broncoscopia rígida. El papel de la criobiopsia en el algoritmo diagnóstico de
la FPI y su diagnóstico diferencial con el resto de las EPID aún no está definido.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [505]
[33] ENFERMEDADES PULMONARES INTERSTICIALES DIFUSAS
La biopsia pulmonar quirúrgica es más rentable que la BTB. Es el último paso, si tras las pruebas
anteriores no se ha llegado a un diagnóstico, y en caso de que no haya un tejido afectado más accesible. Se
puede realizar por toracotomía abierta o por videotoracoscopia, dependiendo de la ubicación de la lesión y
de las características del paciente.
4. DIAGNÓSTICO DIFERENCIAL
Es fundamental realizar un adecuado diagnóstico diferencial con diversas patologías que pueden
provocar una radiología o clínica similar a la de las EPID. Entre las alternativas principales a tener en cuenta
se deben distinguir el edema de pulmón (en la insuficiencia cardiaca), las bronquiectasias, las neumonías, la
tuberculosis miliar, la linfangitis carcinomatosa, el carcinoma bronquioloalveolar y síndromes
linfoproliferativos, entre otros.
5. ENTIDADES MÁS RELEVANTES
La FPI es la EPID idiopática más frecuente y la de peor pronóstico. Se describen en este apartado
algunas otras EPID (Tabla IV).
Tabla IV. Características de otras enfermedades pulmonares intersticiales difusas.
5.1. Fibrosis pulmonar idiopática
La FPI se define como una forma específica de neumonía intersticial crónica fibrosante de causa
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [506]
[33] ENFERMEDADES PULMONARES INTERSTICIALES DIFUSAS
desconocida, que afecta sobre todo a adultos sobre los 50 años de edad, se limita al pulmón y se asocia con
un patrón histológico y/o radiológico de neumonía intersticial usual (NIU). Si existe compatibilidad clínico-
funcional con un patrón radiológico de certeza (Tabla V) de NIU, habiendo descartado otras etiologías, se
puede diagnosticar FPI sin necesidad de biopsia. Si los datos previos no se cumplen, o si existe un patrón
radiológico de posible NIU, se debe descartar otra EPID o confirmar la NIU mediante biopsia, antes de
catalogarla como FPI.
Tabla V. Patrones radiológicos de neumonía intersticial usual (NIU).
V. CRITERIOS DE INGRESO
Patrón intersticial pulmonar no conocido con insuficiencia respiratoria aguda, fiebre con
deterioro del estado general y/o inestabilidad hemodinámica.
Sospecha de complicación con compromiso vital.
VI. ABORDAJE TERAPÉUTICO
Depende de la etiología de la EPID. Si existe una causa conocida el tratamiento se debe enfocar a
dicha enfermedad. Para el manejo de las EPID idiopáticas, exceptuando la FPI, el principio básico es
disminuir la inflamación, en general con glucocorticoides y, en ciertos casos, con inmunosupresores. Se
debe insistir en el abandono del hábito tabáquico, sobre todo en las EPID relacionadas con este, como la
bronquiolitis respiratoria con enfermedad pulmonar intersticial y la neumonía intersticial descamativa, en
las que es fundamental suspender la exposición al tabaco.
1. FIBROSIS PULMONAR IDIOPÁTICA
En cuanto al tratamiento farmacológico se han comercializado dos fármacos antifibróticos:
pirfenidona, indicada en FPI de leve a moderada (CVF > 50%), y nintedanib, sin restricción por CVF. La
combinación de azatioprina, N-acetilcisteína y corticoides está contraindicada en el tratamiento de la FPI,
ya que su uso ha demostrado un aumento en la mortalidad y en la tasa de hospitalización.
2. TRATAMIENTO DE COMPLICACIONES Y COMORBILIDADES
El tratamiento se realizará en una unidad especializada en el manejo de EPID. Se debe tener en
cuenta al diagnóstico del paciente, dependiendo de la edad y de otras comorbilidades, la valoración por
una unidad de trasplante pulmonar. Hay que considerar el uso de oxigenoterapia de acuerdo a las
indicaciones de la misma (pO2 menor de 55 mm Hg o menor de 60 mm Hg con hipertensión pulmonar,
poliglobulia o fallo cardiaco derecho). En caso de presentar reflujo gastroesofágico, incluso si es
asintomático, este debe tratarse.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [507]
[33] ENFERMEDADES PULMONARES INTERSTICIALES DIFUSAS
En cuanto a las exacerbaciones se pueden utilizar glucocorticoides, aunque es una recomendación
débil. La ventilación mecánica no invasiva no está indicada en la FPI.
VII. PRONÓSTICO Y SEGUIMIENTO
El pronóstico varía de acuerdo a la etiología de la EPID. En general, las que cursan con fibrosis,
como la FPI y la NINE fibrótica, tienen peor pronóstico, con una supervivencia para la FPI del 50% a los 3-5
años. El pronóstico se ensombrece a mayor disnea, DLCO menor del 40%, saturación menor del 88% en el
test de la marcha de 6 minutos, hipertensión pulmonar y mayor extensión de fibrosis en la TC.
En cuanto al seguimiento depende de la causa, de la situación del paciente, de las comorbilidades y
de la evolución. En el caso de la FPI, de existir una afectación moderada sin limitación para la realización de
ejercicio, se recomienda evaluar al paciente, como mínimo, cada 3-6 meses con pulsioximetría,
espirometría y difusión; la radiografía de tórax y el test de la marcha de 6 minutos son opcionales. Si hay
signos de progresión los intervalos de tiempo entre cada valoración deben ser más cortos, siendo además
conveniente solicitar gasometría arterial, test de la marcha y placa de tórax secuencialmente cada tres
meses, así como tener en cuenta la posibilidad de iniciar oxigenoterapia. No es necesario realizar una TC
torácica periódicamente, solo en caso de sospecha de progresión o complicaciones.
Las principales complicaciones son la insuficiencia respiratoria aguda, las infecciones respiratorias
concurrentes (tener en cuenta la posibilidad de gérmenes oportunistas y tuberculosis) y la hipertensión
pulmonar, que es un dato de gravedad (ver Capítulo 27. “Hipertensión pulmonar”). Además, aumenta el
riesgo de cáncer de pulmón. También se deben considerar el tromboembolismo pulmonar y el neumotórax
como otras posibles complicaciones.
BIBLIOGRAFÍA
American Thoracic Society, European Respiratory Society. American Thoracic Society/European
Respiratory Society international multidisciplinary consensus classification of the idiopathic interstitial
pneumonias. Am J Respir Crit Care Med. 2002;165:277-304.
Ancochea J, de Miguel J. Enfermedades pulmonares intersticiales difusas. Monografías de la Sociedad
Madrileña de Neumología y Cirugía Torácica. [monografía en Internet]*. Volumen XII. Madrid: Ergon;
2008 [consultado 4 Sep 2016]. Disponible en:
http://www.neumomadrid.org/descargas/monog_neumomadrid_xii.pdf
Hernandez-Gonzales F, Lucena C, Ramírez J, et al. Utilidad de la criobiopsia en el diagnóstico de la
enfermedad pulmonar intersticial difusa: análisis de rentabilidad y coste. Arch Bronconeumol.
2015;51(6):261-7.
Mueller-Mang C, Grosse C, Schmid K, Stiebellehner L. What every radiologist should know about
idiopathic interstitial pneumonias. RadioGraphics. 2007;27:595-615.
Raghu G, Anstrom KJ, King TE Jr, et al. Prednisone, azathioprine, and N-acetylcysteine for pulmonary
fibrosis. N Engl J Med. 2012;366(21):1968-77.
Raghu G, Collard H, Egan J, et al. An official ATS/ERS/JRS/ALAT Statement: Idiopathic pulmonary
fibrosis: Evidence-based guidelines for diagnosis and management. Am J Respir Crit Care Med.
2011;183:788-824.
Raghu G, Rochwerg B, Zhang Y, et al. An official ATS/ERS/JRS/ALAT Clinical practice guideline:
Treatment of Idiopathic pulmonary fibrosis. Am J Respir Crit Care Med. 2015;192(2):3-19.
Travis W, Costabel U, Hansell D, King T, Lynch D, Nicholson A, et al. An Official American Thoracic
Society/ European Respiratory Society Statement: Update of the International Multidisciplinary
Classification of Idiopathic Interstitial Pneumonias. Am J Respir Crit Care Med. 2013;188(6):733-48.
Ungprasert P, Carmona E, Crowson C, Matteson E. Diagnostic utility of angiotensin-converting enzyme
in sarcoidosis: A population-based study. Lung. 2016;194:91-5.
Xaubet A, Ancochea J, Bollo E, et al. Normativa sobre el diagnóstico y tratamiento de la fibrosis
pulmonar idiopática. Arch Bronconeumol. 2013;49(8):343-53.
Xaubet A, Cano E. Enfermedades pulmonares intersticiales difusas: etiología, clasificación y
aproximación diagnóstica. En: Álvarez-Sala J, Casan P, Rodríguez de Castro J, Villena V. Neumología
clínica. Barcelona: Elsevier; 2010. pp. 229-35.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [508]
[34] PATOLOGÍA PLEURAL
34.Patología pleural
Luis Alejandro López Yepes.
Neumología
Jaime Laureiro Gonzalo.
Medicina Interna
Asesora: Victoria Villena Garrido. Jefa de Sección de Neumología
I. INTRODUCCIÓN. DEFINICIÓN Y FISIOPATOLOGÍA
El espacio pleural, situado entre la pleura parietal (que recubre la pared torácica) y la visceral (que
recubre el pulmón), está ocupado en el individuo sano por una pequeña cantidad de líquido libre, en torno
a 10-15 ml, resultado del ultrafiltrado de los capilares submesoteliales.
La acumulación de este líquido pleural (LP) en cantidades mayores de lo habitual es lo que se
denomina derrame pleural (DP), y se da por tanto como consecuencia de: 1) un aumento en su formación;
2) una descompensación en el equilibrio de Starling (mecanismo habitual de los trasudados: insuficiencia
cardiaca, síndrome nefrótico, cirrosis hepática, atelectasia, hipoproteinemia); 3) un aumento de la
permeabilidad capilar (mecanismo habitual de los exudados: inflamación, infección, neoplasia,
traumatismo) o, 4) una reducción de su reabsorción en los vasos linfáticos pleurales (traumatismo,
neoplásico, infeccioso).
El DP representa cerca del 10% de todas las enfermedades hospitalarias atendidas en los Servicios
de Neumología y Medicina Interna. En el 75% de los casos, el DP se explica por alguna de las siguientes
cinco causas: insuficiencia cardiaca, cáncer, neumonía, tuberculosis o embolia pulmonar.
II. ETIOLOGÍA
1. TRASUDADO (TABLA I)
Acumulación de líquido en el espacio pleural cuando la superficie de las membranas que lo limitan
no está directamente afectada por el proceso patológico. Se produce como consecuencia de una alteración
de las presiones (hidrostáticas y oncóticas) que regulan el paso de líquido a través de este espacio.
Tabla I. Diagnóstico diferencial del trasudado.
2. EXUDADO (TABLA II)
Causado predominantemente por una inflamación o una infiltración pleural, por alteraciones en el
drenaje linfático (que conllevan un incremento de las proteínas intrapleurales por un aumento en la
permeabilidad capilar) o por un déficit de absorción desde el espacio pleural.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [509]
[34] PATOLOGÍA PLEURAL
Tabla II. Diagnóstico diferencial de exudado.
III. CLÍNICA Y APROXIMACIÓN DIAGNÓSTICA INICIAL
1. ANAMNESIS
Se debe hacer énfasis especial en los antecedentes de exposición al amianto, la toma de
medicamentos y la existencia de otras enfermedades previas o actuales como cardiopatías, tuberculosis,
neoplasias o colagenosis.
La disnea, el dolor torácico pleurítico (inflamación de la pleura parietal) y la tos son los tres
síntomas cardinales del DP. No obstante, un paciente con buena reserva respiratoria previa, con un DP de
pequeño volumen o que se ha formado lentamente, puede estar asintomático.
2. EXPLORACIÓN FÍSICA
Datos como la asimetría en la expansión torácica (menor movimiento inspiratorio en el hemitórax
afectado), la disminución de la transmisión de la voz a través de la pared torácica utilizando la mano
(frémito táctil), la matidez a la percusión sobre el área afectada y la hipofonesis (disminución en intensidad
de los ruidos respiratorios) ayudan en la sospecha de DP.
El roce pleural es un sonido chirriante o frotante que se escucha con los movimientos respiratorios,
predominantemente en la fase espiratoria, en los individuos con una inflamación de la pleura y con escaso
DP (pleuritis “seca”).
3. PRUEBAS DE IMAGEN
3.1. Radiografía simple de tórax
Se necesitan unos 75 ml de líquido pleural para borrar el seno costofrénico posterior, y entre 200 y 500 ml
para el lateral. Los derrames pleurales masivos producen una opacidad completa del hemitórax, con un
desplazamiento del mediastino al lado contrario y, en ocasiones, una inversión del diafragma homolateral.
La ausencia de un desplazamiento contralateral del mediastino suele indicar una atelectasia obstructiva del
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [510]
[34] PATOLOGÍA PLEURAL
pulmón ipsilateral (neoplasia endobronquial) o la fijación del mediastino. No obstante, no todos los
hemitórax opacos corresponden a un DP, y se debe realizar un diagnóstico diferencial con las atelectasias
completas, las neumonías y los tumores pulmonares masivos. El DP también puede adoptar una
distribución atípica, como, por ejemplo, en la región subpulmonar, simulando una elevación del
hemidiafragma. El diagnóstico puede confirmarse con una radiografía de tórax en proyección de decúbito
lateral (puede llegar a discriminar cantidades menores de 10 ml) o con una ecografía torácica. Otro ejemplo
es el “tumor fantasma”, que hace referencia a loculación del líquido pleural en las cisuras interlobulares.
Los DP que se encapsulan pegados a la pared torácica forman ángulos obtusos con esta (en forma de “D”),
con aspecto homogéneo y superficie lisa. Una loculación del líquido en la región colindante al mediastino
simulará una masa pulmonar o paramediastínica. Los derrames que más se loculan son: paraneumónicos,
tuberculosos, hemotórax y, en menor medida, DP malignos y secundarios a embolismo pulmonar.
Finalmente, la calcificación pleural se observa en el empiema tuberculoso y en la asbestosis. La presencia
de nivel hidroaéreo en el espacio pleural puede deberse a una infección pleuropulmonar por gérmenes
formadores de gas, una fístula broncopleural, un hidroneumotórax, un traumatismo o una rotura esofágica.
3.2. Ecografía pleural
En los últimos años la ecografía pleural se ha convertido en una herramienta de suma utilidad para el
diagnóstico y tratamiento de la patología pleural, haciéndose prácticamente imprescindible. Entre sus
ventajas cabe mencionar la ausencia de radiación, su mejor portabilidad, las imágenes en tiempo real y la
capacidad de realizar imagenología dinámica. Sus indicaciones en patología pleural incluyen la detección a
pie de cama del paciente de DP o de neumotórax, dirigir la toracocentesis tanto diagnóstica como
terapéutica, la biopsia pleural (con la disminución de las complicaciones que esto conlleva), y como guía
para la colocación de tubos y drenajes torácicos.
Se pueden detectar características ecográficas del DP sugestivas de DP complicado (presencia de
septos, ecos dentro del derrame) o de malignidad (engrosamientos nodulares en la pleura parietal,
engrosamiento pleural > 1 cm, el signo del remolino o swirling pattern, y metástasis hepáticas).
3.3. Tomografía computarizada (TC) torácica con contraste
Se considera una prueba esencial en la investigación de todo DP cuya causa está sin determinar. Sus
ventajas son numerosas, incluyendo la identificación de derrames pequeños (inferiores a 10 ml),
loculaciones del líquido pleural, engrosamientos de la membrana pleural, lesiones parenquimatosas
pulmonares, adenopatías mediastínicas, nódulos mamarios o anomalías óseas.
IV. ABORDAJE DIAGNÓSTICO
Una vez diagnosticado el DP mediante datos clínicos y radiológicos, el siguiente paso es alcanzar el
diagnóstico etiológico mediante la toracocentesis diagnóstica y demás pruebas complementarias, si se
precisan.
Este abordaje se puede dividir en tres pasos principales:
Diferenciación entre trasudado y exudado según los criterios de Light y los criterios
coadyuvantes (ver Apartado 1.1).
Determinaciones analíticas orientadas al diagnóstico etiológico en el líquido pleural y técnicas
complementarias pertinentes: adenosina desaminasa (ADA), interferón gamma (IFN-γ),
citología, estudio microbiológico, biopsia pleural, fibrobroncoscopia, angio-TC de tórax,
videotoracoscopia (VATS), etc. (Tabla III).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [511]
[34] PATOLOGÍA PLEURAL
Tabla III. Determinaciones y etiología más probable del derame pleural. Bioquímica en líquido pleural.
Detección de criterios pronósticos (pH, glucosa, lactato deshidrogenasa [LDH], Gram y cultivo
de líquido pleural) (ver Apartado 1.3).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [512]
[34] PATOLOGÍA PLEURAL
Las determinaciones habituales que se deben solicitar en el estudio de líquido pleural se resumen
en las Tablas IV y V.
Tabla IV. Determinaciones habituales en toracocentesis diagnóstica y tubos utilizados.
Tabla V. Determinaciones y etiología más probable del derrame pleural. Recuento celular en líquido pleural.
1. TORACOCENTESIS DIAGNÓSTICA
Se debe realizar siempre y cuando existan tres criterios:
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [513]
[34] PATOLOGÍA PLEURAL
Cantidad suficiente de líquido pleural (más de 10 mm de grosor en la radiografía en decúbito
lateral, ecografía o TC torácica).
Ausencia de coagulopatía o trombopenia significativa.
Etiología no secundaria a una insuficiencia cardiaca clara. No obstante, si este se manifiesta de
forma atípica (masivo unilateral, localización izquierda, asociado a fiebre o dolor, sin respuesta
a tratamiento diurético o con una disnea desproporcionada al volumen del derrame), debe
estudiarse también mediante toracocentesis por la probable comorbilidad asociada. Debe
tenerse en cuenta en derrames bilaterales la posibilidad de distinta etiología en cada hemitórax
(síndrome de Contarini).
Sus complicaciones más frecuentes son la reacción vagal (10-14%) y el neumotórax (3-8%). No es
imprescindible hacer una radiografía de tórax tras la toracocentesis, salvo si se sospecha que se han
producido complicaciones. El estudio del líquido pleural permite alcanzar un diagnóstico final confirmativo
o de sospecha en más del 75% de las ocasiones. En el resto de los casos permite la exclusión de causas
concretas, considerándose, según algunos autores, que el DP es idiopático después de dos estudios
pleurales, uno de ellos con biopsia pleural cerrada.
En el análisis del líquido pleural deben valorarse los aspectos que se relacionan a continuación.
Aspecto macroscópico del líquido pleural. Puede ser de utilidad ante determinadas características.
Así, un líquido acuoso sugiere un trasudado, un líquido blanco o lechoso sugiere quilotórax o
pseudoquilotórax y la presencia de pus determina un empiema. Las demás características macroscópicas
son menos específicos (Tabla VI).
Tabla VI. Aspecto macroscópico del líquido pleural.
1.1. Diferenciación entre trasudado y exudado
Todavía siguen vigentes los criterios de Light para discriminar los trasudados de los exudados.
La presencia de uno de estos tres criterios identifica a los exudados:
Cociente proteínas en el líquido pleural/proteínas en suero > 0,5.
Cociente LDH en el líquido pleural/LDH en suero > 0,6.
LDH en líquido pleural superior a dos tercios de su valor normal en suero.
Con estos criterios la sensibilidad es del 95-100% y la especificidad del 70-90%. Si se quiere
evitar una extracción sanguínea simultánea, la combinación de una LDH en el líquido pleural
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [514]
[34] PATOLOGÍA PLEURAL
superior a dos tercios del límite superior de la normalidad sérica teórica y un colesterol mayor
de 60 mg/dL en el líquido pleural, puede suplir a los criterios de Light.
Por otra parte, hay que tener en cuenta que los trasudados pleurales secundarios a fallo
cardiaco pueden pasar a ser exudados por recibir tratamiento diurético y ser mal clasificados
por ese motivo. En estos casos, sugiere causa cardiaca un gradiente de albúmina en suero
menos albúmina en LP superior a 1,2 g/dL, un gradiente de proteínas totales suero-LP superior
a 3,1 g/dL o una elevación de la concentración sérica de NT-proBNP mayor de 100 pg/ml. Igual
ocurre con el hidrotórax ascítico, excepto por los niveles de NT-proBNP (normales).
1.2. Determinaciones analíticas orientadas al diagnóstico etiológico en líquido pleural y técnicas
complementarias pertinentes (Tablas III y IV)
Dentro de estas determinaciones analíticas con orientación etiológica cabe mencionar: triglicéridos y
quilomicrones (quilotórax), colesterol (exudados, pseudoquilotórax), ADA e IFN-γ (tuberculosis pleural),
amilasa (pancreatitis, rotura esofágica), marcadores tumorales, recuento celular absoluto y proporcional, y
citología del LP (neoplasias pleurales). En nuestro hospital se suele utilizar el IFN-γ debido a su mayor
rentabilidad diagnóstica, por lo que no suele solicitarse el ADA de forma rutinaria. Por otra parte, el
diagnóstico de certeza de quilotórax se realiza con la medición de quilomicrones en el LP, aunque, dadas las
dificultades técnicas para esta determinación, el diagnóstico se suele realizar con la medición de
triglicéridos en el LP.
1.2.1. Toracocentesis evacuadora
Es una técnica que puede ser útil para el diagnóstico de síndrome de pulmón atrapado (véase más
adelante), así como para el tratamiento de la disnea del paciente (paliativa en el caso de DP recidivantes sin
importar la etiología) o previa a pleurodesis química. Si se prevé la realización de biopsia pleural ciega
diagnóstica, no se recomienda evacuar el DP por completo (al disminuir la cámara pleural, aumenta el
riesgo de laceración pulmonar). La técnica se realizará con anestesia local y una aguja específica para
toracocentesis evacuadora (disponible en el hospital), compuesta por un tutor metálico y una camisa de
plástico (que quedará dentro de la cavidad pleural) unida a una llave de dos pasos para evitar, en lo posible,
la yatrogenia de un neumotórax; el sistema de evacuación se conectará a su vez a un sistema de vacío.
Debe vigilarse el procedimiento en todo momento y retirar la aguja intrapleural en caso de notar el
parénquima pulmonar reexpandiéndose a medida que el DP se evacúa. La cantidad de líquido extraído
puede ser abundante; el edema pulmonar por reexpansión es una potencial complicación, aunque poco
frecuente; no existe un límite de seguridad, aunque en general no se recomiendan extracciones mayores de
1,5 l si no se utiliza la manometría intrapleural. Algunos autores recomiendan terminar la toracocentesis
ante la aparición de dolor torácico o tos persistente. Los derrames que requieran más de 1-2
toracocentesis/ mes son candidatos a la realización de pleurodesis; no obstante, estaría contraindicada en
el síndrome del pulmón atrapado y en la obstrucción bronquial, ya que requiere que ambas pleuras estén
en contacto. La pleurectomía está reservada para derrames inmanejables como última opción, ya que se
trata de una técnica con múltiples complicaciones.
1.2.2. Biopsia pleural transparietal o con aguja
Está indicada en aquellos pacientes con DP tipo exudado de etiología no conocida con citología negativa del
DP. En nuestro medio, se suelen realizar a la vez tanto la citología del DP como la biopsia pleural si el
diagnóstico pretest es de malignidad. Se deben obtener al menos cuatro fragmentos de pleura parietal para
el estudio anatomopatológico y uno para cultivo de Mycobacterium tuberculosis, en un acto que tan solo
requiere anestesia local y frecuentemente permite un manejo ambulatorio. El rendimiento de esta técnica
aumenta si se dirige con TC torácica o ecografía. Asimismo, aumenta si la afectación pleural es extensa (por
ejemplo, tuberculosis pleural), y disminuye si la afectación es nodular o parcheada (por ejemplo,
neoplasias). Está contraindicada en casos de plaquetopenia inferior a 50.000/μl, infección cutánea de la
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [515]
[34] PATOLOGÍA PLEURAL
zona de incisión, insuficiencia respiratoria (por el peligro de neumotórax) y DP muy pequeño (por el riesgo
que supone poder lesionar una víscera abdominal o el propio pulmón). Las complicaciones son infrecuentes
en manos expertas (menores del 10%): neumotórax principalmente (se recomienda realizar una radiografía
de tórax de control después de la técnica), infección de la cavidad pleural, hemotórax o laceración del
hígado o del bazo. En el caso de estudio no concluyente, debe valorarse la realización de toracoscopia
diagnóstica.
1.2.3. Fibrobroncoscopia
Está indicada si hay síntomas bronquiales (hemoptisis, cambios en la cantidad o aspecto de la
expectoración) o alteraciones radiológicas en el parénquima pulmonar como nódulos, atelectasias o DP
masivo.
1.2.4. Videotoracoscopia (VTA)
El rendimiento diagnóstico para neoplasia supera el 90%, y es especialmente recomendable si hay
antecedentes de contacto con asbesto (riesgo incrementado de mesotelioma). Se puede proceder a una
pleurodesis química (talcaje) en el mismo acto.
1.2.5. Toracotomía
En determinadas situaciones en las que las pruebas menos invasivas no hayan dado un diagnóstico
concluyente, se podría valorar la indicación de toracotomía exploradora diagnóstica.
1.3. Datos pronósticos
Los niveles de pH, glucosa y LDH del líquido definen el pronóstico en los derrames paraneumónicos y en los
malignos. En los DP paraneumónicos, un pH < 7,20, gérmenes en el líquido pleural (Gram y/o cultivo),
glucosa < 60 mg/dL, LDH > 1.000 UI/l se asocian con la necesidad de drenaje torácico ± fibrinolíticos y/u
otras intervenciones quirúrgicas; en los DP malignos, el descenso del pH y de la glucosa se asocia con una
mayor afectación tumoral de la pleura, con lo que aumenta la sensibilidad de la citología, aunque
disminuye la probabilidad de éxito de la pleurodesis (véase más adelante) e implica una menor
supervivencia.
V. TIPOS MÁS FRECUENTES DE DERRAME PLEURAL Y SU ABORDAJE
ESPECÍFICO
En la figura 1 se muestra el algoritmo diagnóstico y el manejo del derrame pleural. Una vez
realizado el diagnóstico etiológico, el abordaje terapéutico se realizará según el tipo de DP.
1. TRASUDADO
Tratamiento etiológico específico (insuficiencia cardiaca congestiva, cirrosis hepática y síndrome
nefrótico).
2. DERRAME PLEURAL PARANEUMÓNICO Y EMPIEMA
Es una de las causas más frecuentes de exudado pleural. Se produce en el contexto de infección
pulmonar (neumonía, absceso pulmonar y bronquiectasias infectadas), y aparece hasta en el 40% de las
neumonías. Suele ser de pequeño tamaño y con resolución espontánea posterior. Generalmente, la
evolución pasa por una fase aguda o exudativa (paraneumónico no complicado) con LP claro con glucosa y
pH normales y sin hallazgos microbiológicos. Puede evolucionar a una fase fibrinopurulenta o de transición,
que se desarrolla en pocas horas en pacientes sin tratamiento antibiótico adecuado (no se debe demorar la
toracocentesis). Esta fase es secundaria a invasión bacteriana del espacio pleural. Se produce acidosis,
aumento de neutrófilos, consumo de glucosa y aumento de la LDH por lisis celular, formación de fibrina y
loculación, que conduce al derrame paraneumónico complicado y el empiema. Este último suele ser de
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [516]
[34] PATOLOGÍA PLEURAL
aparición más tardía, salvo en pacientes inmunodeprimidos. Finalmente, se producirá una fase crónica u
organizativa con engrosamiento pleural (fibrotórax) que puede evolucionar hacia la curación o hasta
formas crónicas de empiema: fístulas, abscesos o empiema necessitatis. Para el manejo del DP
paraneumónico (Tabla VII) es importante valorar:
Características anatómicas del DP: tamaño, loculación y engrosamiento pleural, apoyándonos,
sobre todo, en la ecografía y la TC torácica con contraste intravenoso. Estas técnicas, además,
valoran el engrosamiento de la pleura parietal, lo que en el contexto del DP paraneumónico
sugiere empiema; asimismo, en DP multiloculados o con imposibilidad de colocar tubo de
tórax, permite la colocación de drenajes pleurales de menor calibre que han mostrado ser
efectivos (tipo pig-tail o incluso un pleurecath).
Características bioquímicas (pH y glucosa) y bacteriológicas (Gram y cultivo para bacterias
aerobias, anaerobias y tuberculosis): el pH < 7 es el valor más rentable para el diagnóstico de
derrame paraneumónico complicado ante la ausencia de hallazgos microbiológicos. En
presencia de loculación, el valor del pH puede variar entre las diferentes cámaras. La mayoría
de los antibióticos tienen buena penetrancia pleural (a excepción de los aminoglucósidos, que
deben evitarse en el empiema). La etiología más frecuente se debe a Streptococcus
pneumoniae y Staphylococcus aureus, y menos frecuentemente a bacilos gramnegativos, que
aparecen sobre todo en neumonías nosocomiales. En el caso de empiema, se recomienda
instaurar tratamiento antibiótico con cobertura para anaerobios debido a una importante
incidencia de infecciones mixtas (36-75%), debiéndose mantener este 4-6 semanas.
Tabla VII. Manejo del derrame pleural paraneumónico.
El uso de fibrinolíticos intrapleurales no tiene suficiente evidencia para recomendarse de forma
rutinaria. Están indicados ante derrames pleurales loculados. En todo caso, si se decide su uso debe ser de
manera precoz. No tienen acción fibrinolítica sistémica y su principal contraindicación es la existencia de
fístula a nivel broncopleural. Tras las primeras 24-48 horas de colocar el drenaje pleural, debe reevaluarse
la situación clínica y radiológica. Si no se produce mejoría, se debe sospechar loculación persistente y/o
mala cobertura antibiótica. En el caso de fracaso terapéutico en derrames uniloculados y en derrames
multiloculados debe valorarse el tratamiento mediante videotoracoscopia.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [517]
[34] PATOLOGÍA PLEURAL
3. DERRAME PLEURAL TUBERCULOSO
Aparece en menos del 5% de los casos de tuberculosis, y es la segunda localización extrapulmonar
más habitual y la causa más frecuente de DP en zonas de alta prevalencia de tuberculosis. Suele ser
unilateral en la mayoría de los casos, de escasa o moderada cuantía y hasta en el 80% se asocia infiltrado
pulmonar. Suele presentarse con fiebre, tos no productiva y dolor pleurítico. Normalmente se trata de DP
paucibacilar que se autolimita en el tiempo. Más raro es el desarrollo de empiema tuberculoso crónico tras
la ruptura de una cavidad al espacio pleural con presencia de alta carga bacilar y frecuente evolución a
engrosamiento y calcificación pleural.
El diagnóstico puede ser difícil. Ante la sospecha, se debe solicitar cultivo de esputo para
micobacterias, Mantoux (que suele ser negativo hasta en el 33%), cultivo y baciloscopia del LP. El LP es un
exudado rico en proteínas (casi de manera constante mayor de 3 g/dL y en el 75% mayor de 5 g/dL) y de
predomino mononuclear (aunque en los primeros días pueden tener predominio polimorfonuclear). El 75%
tienen la LDH elevada y la glucosa suele estar disminuida.
El diagnóstico definitivo se obtiene mediante:
Baciloscopia y/o cultivo positivo en LP, con rendimiento menor del 10% y entre 10-50%
respectivamente.
Cultivo positivo o granulomas caseificantes en muestra histológica tras biopsia pleural.
En países con prevalencia media o alta de tuberculosis (como es el caso de España), se recomienda
realizar una biopsia pleural cerrada para el estudio de los DP de más de 2 semanas de evolución, aunque
esta técnica requiere experiencia.
El cultivo tiene una rentabilidad del 40-80% y el estudio histológico objetiva granulomas
caseificantes en el 50-90%. La repetición de la biopsia (hasta en dos ocasiones) o la toma simultánea de
biopsias de distintas localizaciones aumenta la rentabilidad.
Es útil, además, la utilización de parámetros bioquímicos en el LP y pruebas de imagen para
orientar el diagnóstico:
ADA en LP: útil sobre todo en países con alta prevalencia de tuberculosis. Ofrece una alta
sensibilidad, y valores menores de 40 UI/l hacen improbable el diagnóstico. Valores superiores
a 70 UI/l son sugestivos de pleuritis tuberculosa, aunque puede haber falsos positivos en la
mayoría de los empiemas, artritis reumatoide, carcinoma broncoalveolar y mesotelioma.
IFN-γ en LP: mayor rentabilidad que la ADA, con una sensibilidad y especificidad mayores del
94%. El punto de corte en nuestro hospital es de 100 pg/ml.
Reacción en cadena de la polimerasa (PCR) específica para tuberculosis en LP: según los últimos
estudios, tiene una sensibilidad del 46% y una especificidad del 99%. Puede ser útil en
combinación con los anteriores.
TC torácica con contraste intravenoso: engrosamiento pleural, adenopatías, infiltrados
pulmonares.
Como en otras formas de tuberculosis, en el 10-15% no se alcanzará un diagnóstico microbiológico-
histológico definitivo. Dejado a su evolución natural, suele resolverse espontáneamente, aunque el 65% de
los casos desarrollará tuberculosis pulmonar en los siguientes 5 años, por lo que se recomienda tratar a
aquellos pacientes con sospecha clínica alta y datos paraclínicos congruentes. No se recomienda
actualmente asociar corticoides al tratamiento.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [518]
[34] PATOLOGÍA PLEURAL
4. DERRAME PLEURAL MALIGNO
Es una causa muy frecuente de exudado. Es secundario a infiltración pleural, y puede presentarse
como complicación de una neoplasia conocida o ser la primera manifestación de un proceso neoplásico.
Los DP que se producen por complicaciones secundarias al proceso, como son tromboembolismo pulmonar
(TEP), infiltración adenopática, obstrucción bronquial, radioterapia o síndrome de la vena cava superior, y
que por lo tanto no son secundarios a infiltración pleural, se denominan DP paramalignos. El 75% de los DP
malignos están producidos por cáncer de pulmón, mama y linfoma, siendo la causa más frecuente el
adenocarcinoma metastásico; menos frecuentemente mesotelioma, cáncer de ovario y tumores
gastrointestinales (aunque cualquier tumor puede producirlo).
Aunque el pronóstico está en relación con el tipo de tumor y su extensión, en general el DP maligno
implica mal pronóstico.
El diagnóstico requiere hallazgos positivos en la citología del LP y/o en muestras histológicas
pleurales. El estudio del LP suele mostrar exudado (3-10% se comportan como trasudados) más
frecuentemente mononuclear, serohemático y en ocasiones con aumento de eosinófilos.
Niveles de LDH mayores de 1.000 UI/l raramente se ven en otras etiologías diferentes del empiema,
artritis reumatoide y DP maligno. Un 30% tienen pH < 7,30, lo que se correlaciona negativamente con la
supervivencia, así como niveles de glucosa disminuidos. La citología del LP es diagnóstica hasta en el 65%
de los casos, siendo más rentable si se repite la toracocentesis.
Los DP ricos en linfocitos presentan frecuentemente problemas en el diagnóstico diferencial con
linfomas y carcinomas anaplásicos de células pequeñas. En estos casos, el estudio con biología molecular y
la citometría de flujo del LP pueden dar el diagnóstico definitivo. La biopsia pleural debe realizarse si la
primera citología es negativa y persiste la sospecha de etiología tumoral (alta especificidad, aunque la
sensibilidad varía entre 7-70% según el estudio), o debe plantearse una VTA (aclara el diagnóstico en el 95%
de los casos, siendo los estudios previos negativos).
La determinación de marcadores tumorales (MT) puede ayudar en estos pacientes, aunque debe
considerarse que no disponemos de un punto de corte en nuestro centro, que ninguno ha mostrado
utilidad significativa medido de forma aislada y que sirven como coadyuvantes en la orientación
diagnóstica, por lo que únicamente son útiles con valores claramente aumentados y medidos de forma
combinada. Los puntos de corte descritos en la literatura médica para cada MT se exponen en la tabla III.
La TC con contraste aporta importante información, ya que puede identificar un tumor primario
oculto y sugiere malignidad si se evidencia un engrosamiento pleural circunferencial o nodular,
engrosamiento parietal mayor de 1 cm o afectación de la pleura mediastínica. La tomografía por emisión de
positrones (PET) puede ser útil para diferenciar patología benigna de maligna en los casos con citología
negativa y TC que no aporta datos de interés: una PET negativa orientaría a patología benigna y en caso de
captación patológica puede guiar la toma de una muestra histológica.
El mesotelioma maligno se desarrolla 20-40 años tras la exposición al asbesto. El diagnóstico
requiere biopsia pleural con mayor rentabilidad si se realiza por VTA, siendo difícil el diagnóstico diferencial
con adenocarcinoma metastásico.
Los linfomas raramente producen DP aislados sin afectación extrapleural previa, salvo los linfomas
de cavidades, que son infrecuentes y suelen presentarse en el contexto de infección por virus de la
inmunodeficiencia humana (VIH). El 20-30% de los linfomas desarrollan DP; sin embargo, la mayoría de los
DP asociados a linfomas de tipo Hodgkin (LH) son DP paramalignos, y en cambio, los asociados a linfoma no
Hodgkin (LNH) suele ser secundarios a infiltración pleural.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [519]
[34] PATOLOGÍA PLEURAL
Los DP malignos asintomáticos no requieren tratamiento; en los casos de DP sintomáticos, debe
realizarse una toracocentesis evacuadora y posteriormente, dependiendo del pronóstico, la respuesta al
tratamiento sistémico (en linfomas, mama, ovario, células pequeñas, células germinales), la velocidad de
reproducción del derrame y la gravedad de la sintomatología, se valorará una de las siguientes opciones:
Observación.
Toracocentesis evacuadoras de repetición: si la acumulación es lenta y la esperanza de vida
menor de 3 meses.
Drenaje pleural permanente: sobre todo si la acumulación es rápida y hay corta expectativa de
vida y ante la presencia de síndrome del pulmón atrapado u obstrucción bronquial.
Pleurodesis con talco o doxiciclina: indicada si la expectativa de vida es mayor de 3 meses y hay
expansión pulmonar tras toracocentesis evacuadora.
Pleurectomía (parietal y visceral) y decorticación (escisión del tejido fibroso): requiere
toracotomía, con alta morbimortalidad.
Shunt pleuroperitoneal: poco utilizado en nuestro medio.
5. DERRAME PLEURAL POSQUIRÚRGICO
Es frecuente tras cirugía cardiaca, torácica y a veces abdominal. Debe realizarse el diagnóstico
diferencial con complicaciones posquirúrgicas como TEP, neumonía, síndrome de Dressler e insuficiencia
cardiaca congestiva, o con complicaciones quirúrgicas como hemotórax, quilotórax y mediastinitis.
Normalmente es de tamaño pequeño-moderado, tipo exudado serohemático, con LDH elevada y
predominio polimorfonuclear y a veces con aumento de los eosinófilos. La lateralidad del derrame
dependerá de la localización de la intervención.
Se recomienda toracocentesis diagnóstica en derrames grandes (mayores del 25% del hemitórax),
sintomáticos, de aparición tardía (después de 30 días) y ante la sospecha de otra comorbilidad.
En cuanto al tratamiento, si son sintomáticos y abundantes se pueden realizar toracocentesis
evacuadoras de repetición.
6. DERRAME PLEURAL SECUNDARIO A SÍNDROME DEL PULMÓN ATRAPADO
DP secundario a afectación de la pleural visceral con formación de una capa de fibrina que
condiciona una restricción de la expansión pulmonar, generando una presión negativa pleural. Puede ser
secundario a una enfermedad pleural activa (inflamatoria o tumoral) o a un proceso resuelto que dejó una
restricción pleural permanente. El diagnóstico debe sospecharse ante la presencia de DP crónico estable,
DP que tras toracocentesis recurre precozmente (24-48 h) o si no se produce reexpansión pulmonar tras la
colocación de tubo de tórax, y también ante una pérdida de volumen pulmonar del lado del DP (diagnóstico
diferencial con obstrucción endobronquial proximal).
La pleurodesis raramente es efectiva, pues la presión negativa intrapleural mantiene separadas
ambas pleuras; de hecho, la presencia de pulmón atrapado contraindica desde el inicio esta opción
terapéutica.
7. QUILOTÓRAX Y PSEUDOQUILOTÓRAX
Llamamos quilotórax al DP formado por acumulación de quilo en la cavidad pleural.
Anatómicamente, el conducto torácico suele cruzar el mediastino de derecha a izquierda a la altura de D5,
por lo que daños por debajo de ese nivel producen DP derecho y por encima DP izquierdo. La etiología
puede ser traumática (intervenciones quirúrgicas o traumatismos de alta energía que seccionan el
conducto torácico o una de sus ramas) o no traumática (obstrucción extrínseca del conducto torácico,
donde predomina la etiología maligna, como linfomas). El diagnóstico se realiza por toracocentesis con
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [520]
[34] PATOLOGÍA PLEURAL
obtención de LP, cuyo aspecto será quiloso en el 50% de los casos, aunque no se puede descartar ante la
presencia de LP serohemático, turbio y sanguinolento de origen incierto. El diagnóstico de quilotórax
habitualmente se realiza con la medición de triglicéridos en el LP (valores menores de 50 mg/dL lo
excluyen, entre 50 y 110 mg/dL lo dan como posible y > 110 mg/dL lo hacen muy probable). Si se precisa
asegurar el diagnóstico, es necesario objetivar la presencia de quilomicrones en el LP, aunque en la mayoría
de los casos esta determinación no es necesaria. Debe descartarse, en última instancia, la extravasación de
nutrición parenteral desde un acceso venoso central. La respuesta al tratamiento es también orientativa
para el diagnóstico. El tratamiento es polémico por la ausencia de estudios prospectivos, aunque debe
atenderse a las siguientes directrices:
Manejo inicial conservador con:
Drenaje del LP y soporte nutricional (nutrición parenteral parcial o total y/o dieta con
ácidos grasos de cadena media); el 50-80% de los casos se resuelven en 2 o 3 semanas.
La permanencia del drenaje no debe ser prolongada, pues hay riesgo de desnutrición e
inmunodepresión (alto contenido en linfocitos y proteínas).
En causas no traumáticas, será preciso tratar la causa subyacente.
Si no se produce resolución o el drenaje por el tubo de tórax es mayor de 1 litro de quilo al día,
deberá valorarse la sutura quirúrgica (pocas veces se realiza por la dificultad de la técnica y la
localización de la sección del conducto).
En causas tumorales puede ser necesario realizar pleurodesis si no hay respuesta al tratamiento
tumoral, pues no suele resolverse con la ligadura quirúrgica del conducto torácico.
Se denomina pseudoquilotórax a la acumulación de colesterol en el espacio pleural.
Es más raro que el quilotórax, y suele ocurrir en el seno de DP crónicos con pleuras engrosadas y
calcificadas. Las causas más frecuentes son los DP tuberculosos y la artritis reumatoide, aunque su
patogenia es incierta. El LP presenta colesterol mayor de 250 mg/dL, con variabilidad del valor de los
triglicéridos.
8. ENFERMEDAD PLEURAL BENIGNA POR ASBESTO
La exposición al asbesto produce tres tipos de reacciones pleurales benignas (la mayoría tras 20
años o más de la exposición, aunque el DP puede ser de tan solo un año de evolución):
Placas en la pleural parietal. Es la forma más frecuente de afectación pleural. Están en relación
proporcional a la intensidad de la exposición; puede ser útil buscarlas con TCAR (TC de alta
resolución) ante la sospecha de DP asbestósico.
Fibrosis pleural difusa. Afecta a la pleura visceral, y puede producir trastorno ventilatorio
restrictivo y atelectasias redondas por compresión.
DP asbestósico benigno. Suele ser pequeño y unilateral, muchas veces asintomático, pero otras
veces se presenta asociado a reacción inflamatoria con fiebre y dolor pleurítico.
El LP es seroso, serosanguinoliento o hemático, y cumple criterios de exudado. Un tercio de los
pacientes presentan aumento porcentual de los eosinófilos (hasta un 50%). Suele resolverse de manera
espontánea en el curso de unas semanas o meses. Salvo la presencia de calcificación pleural típica, no
existen datos específicos ni en el LP ni en la histología pleural, por lo que el diagnóstico se realizará en
pacientes con antecedentes de exposición y una vez excluidas otras causas, sobre todo malignidad durante
un seguimiento de al menos 3 años. Se recomienda toracoscopia exploradora/diagnóstica en DP
persistentes para descartar mesotelioma.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [521]
[34] PATOLOGÍA PLEURAL
9. HEMOTÓRAX
Viene definido por la presencia en el LP de un hematocrito mayor del 50% de los valores del
hematocrito en sangre periférica. Las etiologías más frecuentes son la traumática y la yatrogénica,
normalmente en el contexto de cirugía torácica, accesos venosos centrales y punciones transpleurales. El
tratamiento en pacientes estables hemodinámicamente y con derrames escasos (pinzamiento del seno
costofrénico) será la observación y fisioterapia respiratoria. En pacientes inestables y/o con derrames de
mayor cuantía, debe colocarse drenaje pleural de calibre grueso, preferiblemente con antibioterapia
preventiva previa. Si el líquido drenado es superior a 1.500 ml o presenta un ritmo mayor de 200 ml/h
durante más de 3 horas, está indicada la toracotomía exploradora diagnóstico-terapéutica urgente, o si el
paciente está estable hemodinámicamente, la VTA para intentar hemostasia. La persistencia de hemotórax
residual mayor de 500 ml, lóculos o coágulos residuales que ocupan al menos un tercio del hemitórax,
tienen riesgo de sobreinfección y a la larga de fibrotórax, por lo que debe valorarse la posibilidad de colocar
drenajes guiados por TC o ecografía y, si no se obtienen resultados satisfactorios, se recurrirá a la instilación
de fibrinolíticos, siempre que se descarte sangrado activo reciente.
10. DERRAME PLEURAL EN ENFERMEDADES DEL TEJIDO CONECTIVO
Sobre todo secundarios a lupus eritematoso sistémico (LES) y artritis reumatoide (AR).
10.1. Hasta el 50% de pacientes con lupus eritematoso sistémico presentarán DP, siendo bilateral
en la mitad de los casos. Suelen cursar con fiebre, tos y dolor pleurítico; en ocasiones se asocia a derrame
pericárdico. Son exudados con pH y glucosa normales y LDH menor de 500 UI/l; es preciso descartar otras
etiologías como la infecciosa, TEP o nefropatía subyacente ante estas determinaciones. La respuesta a
corticoides sistémicos suele ser buena.
10.2. La frecuencia de DP en la artritis reumatoide es más baja, en torno al 5%, aunque es la
manifestación pulmonar más frecuente de esta patología. Muchas veces asintomática, puede coexistir con
pericarditis y nódulos subcutáneos. El LP en ocasiones es purulento (pseudoquilotórax), con pH y glucosa
bajos y aumento de la LDH, de modo que es preciso el diagnóstico diferencial con el DP paraneumónico.
Los títulos de factor reumatoide mayores de 1/320 en el LP sugieren el diagnóstico. No existen estudios que
evalúen la eficacia de corticoides y/o antiinflamatorios no esteroideos (AINE).
11. DERRAME PLEURAL POR FÁRMACOS
Causa infrecuente de DP, asociado o no a neumonitis. La presencia de eosinofilia en sangre y/o LP
puede orientar el diagnóstico, aunque tiene una especificidad y sensibilidad bajas. Entre los agentes más
frecuentemente implicados cabe citar: amiodarona, nitrofurantoína, agentes esclerosantes de varices
esofágicas (causa más frecuente, que suele resolverse en 7 días sin tratamiento específico), metisergida,
bromocriptina y agentes quimioterápicos como bleomicina, procarbazina, metotrexato, mitomicina,
docetaxel o ciclofosfamida.
12. DERRAME PLEURAL IDIOPÁTICO
Su diagnóstico es de exclusión, de acuerdo con el algoritmo diagnóstico (Figura 1). Si existen datos
que orientan a malignidad, es preciso realizar una toracoscopia o una toracotomía. Si no hay criterios de
malignidad, la actitud a seguir será la observación.
En el seguimiento a largo plazo de los DP idiopáticos, solo en el 5-18% de los casos se desarrolla
enfermedad maligna, y el resto se resuelven espontáneamente en unos 5-6 meses sin lograr una filiación
etiológica.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [522]
[34] PATOLOGÍA PLEURAL
Figura 1. Algoritmo diagnóstico y manejo del derrame pleural.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [523]
[34] PATOLOGÍA PLEURAL
VI. NEUMOTÓRAX
Presencia de aire en el interior del espacio pleural con colapso pulmonar secundario y disminución
de la capacidad ventilatoria. El grado de repercusión funcional depende del tamaño y de la reserva
funcional previa del paciente.
1. CLASIFICACIÓN
1. ESPONTÁNEO
Primario. Sin causa precipitante en personas sin patología pulmonar de base, normalmente
secundario a la ruptura de una bulla subpleural. Es más frecuente en varones menores de 40
años, fumadores y de complexión delgada. El pico de incidencia ronda los 20 años.
Secundario. Se produce como complicación de una neumopatía subyacente, sobre todo en el
contexto de enfermedad pulmonar obstructiva crónica (EPOC), cáncer de pulmón, infección por
Pneumocystis jirovecii, tuberculosis y fibrosis quística.
Catamenial. Por endometriosis pleural, suele desarrollarse a las 24-72 h de la menstruación.
2. TRAUMÁTICO
Iatrogénico. Tras manipulación instrumental: broncoscopia, punción guiada por TC,
toracocentesis, biopsia pleural, catéter venoso central o ventilación mecánica.
No yatrogénico. Traumatismo abierto o cerrado.
2. CLÍNICA
Cursa con disnea y dolor torácico pleurítico del lado afectado, aunque un 5-10% son asintomáticos.
La presencia de taquicardia asociada a hipotensión y cianosis sugiere neumotórax a tensión. En la
exploración física destaca hipoventilación de la zona afectada con timpanismo a la percusión e hipofonía.
Puede asociar enfisema subcutáneo (crepitación a la palpación cutánea).
3. DIAGNÓSTICO
Se realiza con radiografía de tórax en inspiración y preferiblemente con el tórax del paciente en
posición erguida si su condición clínica lo permite (la radiografía en espiración forzada puede ser de utilidad
para neumotórax de pequeña cuantía o no detectables en la radiografía en inspiración), donde se observa
la línea blanca de la pleura visceral que representa la división entre tejido pulmonar y aire pleural, y la
ausencia de vasos pulmonares en este espacio. El desplazamiento contralateral de la tráquea y/o el
mediastino no es sensible ni específico para el diagnóstico de neumotórax a tensión, siendo más
importante y orientador valorar la inestabilidad del paciente. La existencia de un nivel hidroaéreo sugiere
hidroneumotórax que, en el caso de ser abundante, debe hacer sospechar la presencia de hemotórax. El
diagnóstico puede ser difícil en pacientes con enfisema de base por la cuantía de sinequias pleurales. Ante
la duda, la TC torácica dará el diagnóstico definitivo, que resulta además útil en pacientes con neumotórax
primario espontáneo de repetición, si se sospecha patología pulmonar subyacente (bullas apicales o
anomalías alveolares con bullas gigantes).
4. TRATAMIENTO
El manejo inicial depende del tamaño y de la clínica asociada. Se recomienda la administración de
oxigenoterapia, lo que facilita la reabsorción del aire pleural. Aquellos pacientes que estén clínicamente
estables y con un neumotórax menor de 2-3 cm entre la pared torácica y el parénquima pulmonar (menor
del 20% del hemitórax) pueden mantenerse en observación, repitiendo una radiografía de tórax a las 6
horas para descartar progresión y cambio en la indicación de drenaje endotorácico (DET). Si existe
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [524]
[34] PATOLOGÍA PLEURAL
estabilidad del neumotórax primario y del paciente, se puede proceder al alta y al seguimiento en
consultas; todo neumotórax secundario requiere hospitalización.
En pacientes con neumotórax grandes y/o inestabilidad clínica se debe proceder a evacuar el aire
del espacio pleural: está indicada la colocación de DET conectado a un sistema con sello de agua (por
ejemplo, Pleurevac®). Se deberá comprobar el funcionamiento del sello de agua para asegurar la
evacuación de aire intratorácico y la correcta transmisión de presiones. Si se detecta un fallo en el sistema,
se debe descartar acodamiento del DET, obstrucción o enclavamiento del DET intratorácico. Se mantendrá
las primeras 24 horas sin conexión a aspiración, pudiendo conectarse después. Una vez no se objetiven
fugas ni nueva cámara de neumotórax tras 12-24 horas de pinzamiento del DET, podrá retirarse. En el caso
de precisar un acto quirúrgico exploratorio, podrá mantenerse sin conectar a aspiración.
Si la fuga persiste tras 3 días con tubo de tórax y la reexpansión es inferior al 90%, se recomienda la
realización de una VTA exploradora. En el mismo acto se intentará observar la presencia de ramilletes
bullosos y resecarlos para evitar recidivas. A su vez, se puede realizar pleurodesis intraoperatoria física o
por abrasión de la pleura parietal. Tras la abrasión de la pleura parietal, el mínimo sangrado del paciente
realizará las funciones de “pegamento” orgánico entre ambas pleuras. Si no es candidato a cirugía puede
optarse por pleurodesis química a través del propio DET (talcaje o pleurodesis con doxiciclina).
5. PREVENCIÓN DE LA RECURRENCIA
En todo paciente debe recomendarse el cese absoluto de la actividad tabáquica, pues es el factor
de riesgo más importante para su recidiva. Debe realizarse intervención quirúrgica (convencional o
videotoracoscópica) o pleurodesis química a través de DET en pacientes con alto riesgo de recurrencia
(Tabla VIII).
Tabla VIII. Indicaciones de cirugía en neumotórax espontáneo.
1. NEUMOTÓRAX PRIMARIO
La recurrencia está en torno al 25-50% en los siguientes 5 años tras el primer episodio y aumenta
hasta el 62% con el segundo episodio. En aquellos pacientes que realizan actividades de riesgo (pilotos de
avión, buceadores, etc.), también es necesaria la realización, en un primer momento, de VTA diagnóstico-
terapéutica.
2. NEUMOTÓRAX SECUNDARIO
El riesgo de recidiva es del 50% a los 3 años, con una mortalidad importante, por lo que se
recomienda intervención en todo paciente una vez resuelto el proceso agudo o durante este. Puede
realizarse con VTA terapéutica (reduce la tasa de recurrencias al 5%) o con pleurodesis química a través de
DET en pacientes que no son subsidiarios de cirugía.
3. NEUMOTÓRAX A TENSIÓN
Es una urgencia vital, secundario al desarrollo de un mecanismo valvular. Si existe inestabilidad
hemodinámica del paciente con riesgo de parada cardiaca, colocar un catéter venoso central en el segundo
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [525]
[34] PATOLOGÍA PLEURAL
espacio intercostal en la línea media clavicular para convertirlo en neumotórax abierto como paso
intermedio a la colocación de tubo de tórax.
BIBLIOGRAFÍA
Clive AO, Jones HE, Bhatnagar R, Preston NJ, Maskell N. Interventions for the management of
malignant pleural effusions: a network meta-analysis. Cochrane Database Syst Rev.
2016;5:CD010529.
Courtney BV, Light RW. Disorders of the Pleura. En: Courtney BV, Mason RJ, Ernst JD, King TE Jr,
Lazarus SC, Murray JF, et al Murray & Nadel´s Textbook of Respiratory Medicine. 6ª edición. New York:
Elsevier; 2016. p. 1396-477.
Cugell DW, Kamp DW. Asbestos and the pleura: a review. Chest. 2004;125(3):1103-117.
Gu Y, Zhai K, Shi HZ. Clinical value of tumor markers for determining cause of pleural effusion. Chin
Med J (Engl). 2016;129(3):253-8.
Guijarro JR, Deu MM, Álvarez Kindelán A. Patología de la pleura. Madrid: Editorial Médica
Panamericana; 2013.
Havelock T, Teoh R, Laws D, Gleeson F; BTS Pleural Disease Guideline Group. Pleural procedures and
thoracic ultrasound: British Thoracic Society Pleural Disease Guideline 2010. Thorax. 2010 Aug;65
Suppl 2:ii61-76.
Heffner JE, Klein JS. Recent advances in the diagnosis and management of malignant pleural
effusions. Mayo Clin Proc. 2008;83(2):235-50.
Jolly EC. Síndromes pleurales. En: Argente HA, Álvarez ME. Semiología Médica: Fisiopatología,
Semiotecnia y Propedéutica: Enseñanza basada en el paciente. Buenos Aires: Editorial Médica
Panamericana; 2005. p. 590-7.
Liang QL, Shi HZ, Qin XJ, Liang XD, Jiang J, Yang HB. Diagnostic accuracy of tumour markers for
malignant pleural effusion: a meta-analysis. Thorax. 2008;63(1):35-41.
Light RW. Trastornos de la pleura y el mediastino. En: Longo DL, Kasper DL, Jameson J, Fauci AS,
Hauser SL, Loscalzo J, editore. Harrison. Principios de Medicina Interna. 19ª edición. New York:
McGraw-Hill; 2016.
Light RW. Pleural disease. 5ª ed. Philadelfia: Lipincott Williams & Wilkins; 2007.
Light RW. Tumor markers in undiagnosed pleural effusions. Chest. 2004;126(6):1721.
Noppen M, De Keukeleire T. Pneumothorax. Respiration 2008; 76(2): 121–27.
Pérez Rodríguez E, Gómez García R. Aproximación al diagnóstico del DP. En: Álvarez-Sala Walther JL,
Casan Clará P, Rodríguez de Castro F, Rodríguez Hermosa JL, Villena Garrido V. Neumología clínica.
Madrid: Elsevier; 2010. p. 657-63.
Pérez Rodríguez E, Villena Garrido V. Enfermedades de la pleura. Monografías Neumomadrid. Madrid:
Ergon; 2003.
Porcel JM, Vives M, Esquerda A, Salud A, Pérez B, Rodríguez-Panadero F. Use of a panel of tumor
markers (carcinoembryonic antigen, cancer antigen 125, carbohydrate antigen 15-3, and cytokeratin
19 fragments) in pleural fluid for the differential diagnosis of benign and malignant effusions. Chest.
2004;126(6):1757-63.
Porcel Pérez JM. Derrame pleural: etiología, patogenia y manifestaciones clínico radiológicas. En:
Álvarez- Sala Walther JL, Casan Clará P, Rodríguez de Castro F, Rodríguez Hermosa JL, Villena Garrido
V. Neumología clínica. Madrid: Elsevier; 2010. p. 649-56.
Rivas de Andrés JJ, Jiménez López MF, Molins López-Rodó L, Pérez Trullén A, Torres Lanzas J.
Diagnóstico y tratamiento del neumotórax espontáneo. Arch Bronconeumol. 2008;44(8):437-48.
Villena Garrido V, Cases Viedma E, Fernández Villar A, de Pablo Gafas A, Pérez Rodríguez E, Porcel
Pérez JM, et al. Normativa sobre el diagnóstico y tratamiento del DP. Actualización. Arch
Bronconeumol. 2014;50(6): 235-49.
Villena Garrido V, Ferrer Sancho J, Hernández Blasco L, de Pablo Gafas A, Pérez Rodríguez E, Rodríguez
Panadero F. Diagnóstico y tratamiento del DP. Arch Bronconeumol. 2006;42(7):349-72.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [526]
[35] PRINCIPIOS DE VENTILACIÓN MECÁNICA. SÍNDROME DE DISTRÉS RESPIRATORIO AGUDO. TRASPLANTE PULMONAR
35.Principios de ventilación mecánica. Síndrome de
distrés respiratorio agudo. Trasplante pulmonar
Jesús Abelardo Barea Mendoza.
Medicina Intensiva
Perla Massiel Valenzuela Reyes.
Neumología
Asesores: Javier Sayas Catalán. Médico Adjunto de Neumología. Ignacio Sáez de la Fuente. Médico Adjunto de Medicina
Intensiva
I. PRINCIPIOS DE VENTILACIÓN MECÁNICA
La ventilación mecánica es una medida de soporte vital, encaminada a suplir el desequilibrio entre
las demandas respiratorias y la capacidad de la musculatura respiratoria.
A. VENTILACIÓN MECÁNICA NO INVASIVA
Permite el empleo de ventilación mecánica mediante sistemas que evitan la rotura de la barrera
glótica, conservando mecanismos de defensa que evitan las complicaciones asociadas a la intubación
orotraqueal.
1. MODALIDADES DE VENTILACIÓN MECÁNICA NO INVASIVA
Existen dos modalidades fundamentales:
La continuous positive airway pressure (CPAP). Se administra una presión positiva continua
sobre la vía aérea.
La bilevel positive airway pressure (BiPAP). Se administran dos presiones: una presión
espiratoria (EPAP) o presión positiva al final de la espiración (PEEP, término utilizado en
ventilación mecánica), y una presión inspiratoria (IPAP). Denominamos presión de soporte a la
diferencia de presión entre EPAP e IPAP (Figura 1).
Figura 1. Modalidad binivel de un ventilador de flujo continuo (derecha) comparada con la modalidad de presión de soporte (PS)
asociada a presión positiva al final de espiración (PEEP).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [527]
[35] PRINCIPIOS DE VENTILACIÓN MECÁNICA. SÍNDROME DE DISTRÉS RESPIRATORIO AGUDO. TRASPLANTE PULMONAR
Existen asimismo otros dos sistemas simplificados, de utilidad en determinadas situaciones:
CPAP de Boussignac. Es un sistema no mecánico de CPAP que emplea el efecto Bernoulli para
generar presión a partir de altos flujos de O2. Su indicación fundamental es el edema agudo de
pulmón, y se usa fundamentalmente en ámbitos extrahospitalarios. Debe evitarse su uso en
pacientes con taquipnea > 25 rpm, dada su incapacidad, en esa situación, para mantener una
presión constante.
Oxígeno de alto flujo por cánula nasal. Es un sistema abierto que permite generar una
pequeña PEEP a nivel orofaríngeo, facilitando también un mayor lavado del espacio muerto
anatómico, entregando flujos altos de aire humidificado activamente y calentado a 37 ºC y
enriquecido con O2. Su indicación está por definir, pero su uso se ha asentado en el tratamiento
de la bronquiolitis en población pediátrica y del fallo hipoxémico de moderada gravedad
(exacerbación de enfermedad pulmonar obstructiva crónica [EPOC], edema cardiogénico y
neumonía).
2. INDICACIONES GENERALES
Está indicado en:
2.1. Insuficiencia respiratoria aguda hipercápnica
Enfermedades obstructivas
EPOC: en la exacerbación de la EPOC que cursa con acidosis respiratoria (pH < 7,35 con
pCO2 > 45 mm Hg), a pesar de un adecuado tratamiento médico inicial. Es una
intervención de primera línea, con el mayor grado de consenso en todas las
recomendaciones.
Fibrosis quística (FQ): las exacerbaciones de FQ manejadas con VMNI presentan menor
mortalidad que aquellas que requieren VM invasiva (VMI), aunque la evidencia
disponible es escasa.
No existe evidencia que permita recomendar su uso rutinario con seguridad en
exacerbaciones asmáticas.
Enfermedades restrictivas
Enfermedades restrictivas extrapulmonares (neuromusculares): aunque la evidencia es
escasa, existe acuerdo en considerar un abordaje inicial del fallo ventilatorio agudo del
paciente neuromuscular con VMNI como primer paso, bajo una estrecha
monitorización.
Síndrome de obesidad-hipoventilación: el uso de VMNI ha demostrado ser eficaz en las
agudizaciones (recomendación grado C). Se debe plantear su utilización a largo plazo.
2.2. Insuficiencia respiratoria no hipercápnica
Edema agudo de pulmón cardiogénico: la VMNI está indicada para su tratamiento
(recomendación grado A). Se considera que el uso de CPAP permite disminuir la necesidad de
intubación orotraqueal y la mortalidad, aunque algunos estudios aportaron información
contradictoria. En esta indicación se recomienda el uso inicial de CPAP, dado que se ha
demostrado equivalente a la ventilación con BiPAP, que podría reservarse a los pacientes con
hipercapnia.
Neumonía adquirida en la comunidad/síndrome de distrés respiratorio del adulto: en casos
seleccionados se podría utilizar VMNI en una Unidad de Cuidados Intensivos, sin demorar la
intubación orotraqueal (IOT) si fuera necesario.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [528]
[35] PRINCIPIOS DE VENTILACIÓN MECÁNICA. SÍNDROME DE DISTRÉS RESPIRATORIO AGUDO. TRASPLANTE PULMONAR
Insuficiencia respiratoria aguda y contraindicación de IOT: podrían beneficiarse de la VMNI en
situaciones de causa reversible como techo de tratamiento, tras una cuidadosa selección del
paciente.
Desconexión de la VMI (weaning o destete).
3. CONTRAINDICACIONES
No demorar la indicación en aquellos pacientes que requieren tratamiento en cuidados intensivos:
Parada respiratoria.
Necesidad de intubación orotraqueal por cualquier causa.
Fallo de más de un órgano (incluyendo respiratorio: infarto agudo de miocardio, oligoanuria...).
Shock o hipotensión grave.
PaO2/FiO2 < 200 mm Hg.
Acidosis grave (pH < 7,25).
Otras contraindicaciones (dificultades técnicas): imposibilidad de ajustar la mascarilla,
traqueotomía, obstrucción de la vía aérea superior, abundantes secreciones, cirugía esofágica
reciente...
4. CRITERIOS DE INICIO
Insuficiencia respiratoria refractaria a medidas convencionales, oxigenoterapia y tratamiento
farmacológico específico.
Disnea no controlada en reposo, utilización de musculatura accesoria y frecuencia respiratoria
mayor a 30 respiraciones por minuto.
Hipercapnia importante y progresiva (PaCO2 > 45 mm Hg) con tendencia a la acidosis
respiratoria (pH < 7,35).
5. MEDIDAS GENERALES PARA EL MANEJO DE LA VENTILACIÓN MECÁNICA NO INVASIVA
5.1. Inicio
Informar y explicar al paciente en qué consiste la técnica. Colocar en posición semisentado, con la cabeza a
45 grados sobre la cama. Monitorizar la frecuencia cardiaca, frecuencia respiratoria y saturación de oxígeno
por pulsioximetría. Escoger la mascarilla adecuada y conectarla al respirador.
5.2. Parámetros de inicio:
CPAP: comenzar con 5 cm de H2O.
BIPAP: en función de las demandas ventilatorias del paciente o de la dificultad para conseguir
una adecuada tolerancia, puede iniciarse con presiones “terapéuticas” (con PEEP 4-6 cm de H2O
y un mínimo de 10 cm de H2O de presión de soporte) o con un incremento progresivo desde
presiones más bajas. Ajustar flujo de O2 o FiO2 a la necesaria para SatO2 entre 88% y 92%.
Previo a la aplicación de la mascarilla se recomienda proteger el puente nasal con un apósito
hidrocoloide para evitar erosiones o úlceras por presión. Fijar la mascarilla con el arnés para evitar las fugas
en la medida de lo posible.
5.3. Mantenimiento
Se debe ir regulando la presión de soporte para obtener un volumen corriente entre 7-8 ml/kg de peso
ideal, una mejoría subjetiva de la disnea, una disminución de la FR al menos en 5 rpm y cese del uso de
musculatura accesoria. El nivel de PEEP/EPAP debe regularse en función de la presencia de eventos
obstructivos, de los esfuerzos ineficaces en los pacientes obstructivos que presentan hiperinsuflación o en
aquellos pacientes más hipoxémicos.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [529]
[35] PRINCIPIOS DE VENTILACIÓN MECÁNICA. SÍNDROME DE DISTRÉS RESPIRATORIO AGUDO. TRASPLANTE PULMONAR
Si presentase desadaptación:
Contracción de esternocleidomastoideo (refleja aumento de la carga inspiratoria): subir IPAP.
Contracción de abdomen (refleja espiración activa): bajar IPAP.
Inspiraciones fallidas: subir EPAP para compensar la autoPEEP.
Si el VC es bajo: ajustar máscara, evitar presión pico mayor de 30 cm de H2O.
Preguntar al paciente por necesidades (posición de la mascarilla, incomodidad, fugas, molestias o
deseos de expectorar) o posibles complicaciones (mayor disnea, distensión abdominal y náuseas). Se debe
realizar una hora después una gasometría arterial. Si en dos a cuatro horas no hay respuesta positiva clínica
o gasométrica después de haber efectuado todos los ajustes y correcciones, considerar cambiar el modo de
VMNI o sopesar la necesidad de IOT y VMI.
5.4. Retirada de la ventilación mecánica no invasiva
No existe un protocolo validado sobre su retirada. Depende de la etiología que genera el fallo ventilatorio.
En general, cuando la causa que motiva el fallo ventilatorio está controlada, se ha resuelto la acidosis
respiratoria (pH > 7,35) y el paciente presenta estabilidad hemodinámica, cardiaca, respiratoria y
neurológica, con requerimientos de FiO2 < 40% puede realizarse una prueba de ventilación espontánea.
Tras un periodo de cuatro a ocho horas en ventilación espontánea debe comprobarse gasométricamente la
tolerancia a la retirada de la VM y valorar su retirada definitiva o progresiva.
B. VENTILACIÓN MECÁNICA INVASIVA
La VMI es una estrategia artificial de soporte vital capaz de remplazar y asistir a los músculos
respiratorios. Durante la VMI se genera una presión positiva desplazando un volumen de aire al interior de
los pulmones. En el transcurso de la VMI la espiración es un proceso pasivo al que contribuyen las fuerzas
elásticas del parénquima pulmonar.
Contrariamente a lo que ocurre en la respiración espontánea, durante la VMI se genera presión
positiva en la vía aérea durante la inspiración. Entender este fenómeno es clave para integrar los cambios
fisiológicos que se producen durante la VMI y sus efectos adversos.
1. INDICACIONES GENERALES
Patología pulmonar:
Tanto en alteraciones de la ventilación como de la oxigenación, como por ejemplo: neumonía,
síndrome de distrés respiratorio del adulto, tromboembolismo pulmonar, atelectasias,
neumopatías, etc.
Patología extrapulmonar:
Afectación de la función ventilatoria por causas extrapulmonares: coma, intoxicación,
neuropatía o miopatías, etc.
Interés en disminuir el consumo de oxígeno y trabajo respiratorio del paciente: shock o
pacientes neurocríticos.
Coma inducido o sedación: cirugía, neurocríticos, procedimientos terapéuticos o diagnósticos.
Los objetivos que se persiguen son:
Controlar la ventilación minuto y la eliminación de CO2.
Mejorar la oxigenación.
Asistir a los músculos respiratorios.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [530]
[35] PRINCIPIOS DE VENTILACIÓN MECÁNICA. SÍNDROME DE DISTRÉS RESPIRATORIO AGUDO. TRASPLANTE PULMONAR
Evitar el daño inducido por la ventilación invasiva: barotrauma, volutrauma, atelectrauma y
biotrauma.
2. CRITERIOS DE INICIO*
Estado mental: agitación o disminución del nivel de consciencia (Glasgow Coma Scale < 8).
Trabajo respiratorio excesivo: taquipnea (>30 rpm), bradipnea, tiraje, asincronía
tóracoabdominal.
Hipoxemia: PaO2 < 60 mm Hg o SpO2 < 90% con aporte de oxígeno.
PaO2/FiO2 < 200.
Hipercapnia progresiva (PaCO2 > 50 mm Hg) o acidosis respiratoria (pH < 7,25).
Shock de cualquier origen con requerimientos de fármacos vasoactivos a dosis importantes.
*Cualquier paciente con sospecha de deterioro de la función respiratoria o indicación de VMI por
otra causa debe ser valorado precozmente por un médico intensivista. El retraso en el establecimiento de la
indicación de VMI o el inicio tardío de la misma empeora el pronóstico de la mayoría de pacientes críticos.
3. MODALIDADES VENTILATORIAS BÁSICAS
Independientemente de la modalidad elegida, actualmente todos los pacientes son ventilados de
forma protectora para evitar el daño inducido por ventilación mecánica (ventilator associated lung injury
[VILI], ver más adelante). Se recomienda de forma genérica el uso de volúmenes corrientes 5-8 ml/kg (peso
ideal) con presiones meseta inferiores a 28-30 cm de H2O. Clásicamente las modalidades más utilizadas son:
Volumen-control: la variable independiente es el volumen corriente, que es ajustado por el
médico. El respirador genera la presión necesaria para suministrar dicho volumen. Las
presiones dependerán (variable dependiente) del volumen pautado y de la dinámica
respiratoria del paciente.
Presión-control: la variable independiente es la presión inspiratoria. Dicha presión se ajustará
por el médico hasta obtener el volumen corriente deseado. En esta modalidad el volumen
administrado dependerá (variable dependiente) de la presión pautada y de la dinámica
respiratoria del paciente.
4. DAÑO INDUCIDO POR VENTILACIÓN MECÁNICA (VENTILATOR-ASSOCIATED LUNG INJURY)
En la VMI el parénquima pulmonar es sometido de forma no fisiológica a importantes cambios en el
ciclo respiratorio. Durante la inspiración, la presión positiva generada por el respirador transmite una serie
de fuerzas sobre el parénquima pulmonar. Dichas fuerzas son capaces de dañar el pulmón.
El VILI se ha estructurado en los siguientes componentes:
Volutrauma: daño inducido cuando los volúmenes suministrados por respiración son excesivos.
Barotrauma: daño inducido cuando se realiza ventilación con presiones elevadas.
Atelectrauma: daño que se da en las regiones alveolares en las que se produce un mecanismo
de apertura y colapso a lo largo del ciclo respiratorio. Este fenómeno se genera en situaciones
de VMI con volúmenes corrientes bajos y/o disminución de la producción de surfactante (por
ejemplo síndrome de distrés respiratorio agudo [SDRA]).
Biotrauma: se produce como resultado de los cambios inflamatorios al nivel del parénquima
pulmonar con liberación de citoquinas y afectación sistémica. Esta respuesta inflamatoria es
estimulada por las agresiones físicas descritas previamente.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [531]
[35] PRINCIPIOS DE VENTILACIÓN MECÁNICA. SÍNDROME DE DISTRÉS RESPIRATORIO AGUDO. TRASPLANTE PULMONAR
Es frecuente que la afectación del parénquima pulmonar sea heterogénea. Como consecuencia,
para un volumen corriente determinado algunas áreas presentarán ciclos de colapsoapertura
(atelectrauma) produciéndose en otras áreas sobredistensión (volutrauma).
La ventilación protectora incluye múltiples estrategias como la ventilación con volúmenes bajos, el
uso rutinario de PEEP o la ventilación con la menor FiO2 posible, y se emplean habitualmente para disminuir
la incidencia de VILI (ver SDRA más adelante). Durante la aplicación de la ventilación protectora se intenta
proteger las áreas sanas evitando la sobredistensión. De forma conjunta se buscará aquella presión que
mantenga la mayor parte de unidades alveolares abiertas (reclutadas) durante todo el ciclo respiratorio
(evitando atelectrauma).
C. VENTILACIÓN MECÁNICA DOMICILIARIA
Existen enfermedades que cursan con insuficiencia respiratoria en algún momento de su evolución,
que tienen indicación de ventilación a largo plazo en el domicilio. Es importante la adaptación inicial al
respirador, el seguimiento clínico del cumplimiento y de las complicaciones, así como el soporte familiar.
1. PROCESOS SUSCEPTIBLES DE VENTILACIÓN MECÁNICA DOMICILIARIA (TABLA I)
Tabla I. Procesos susceptibles de ventilación domiciliaria.
2. INDICACIONES PARA LA VENTILACIÓN MECÁNICA DOMICILIARIA (TABLA II)
Tabla II. Indicación de ventilación mecánica no invasiva a largo plazo.
II. SÍNDROME DE DISTRÉS RESPIRATORIO AGUDO
1. DEFINICIÓN Y FISIOPATOLOGÍA
La definición de SDRA ha sido recientemente modificada (definición de Berlín 2012). Los elementos
principales de la definición vigente incluyen un inicio agudo e hipoxemia progresiva (PaO2/FiO2 < 300 mm
Hg) junto con infiltrados intersticiales bilaterales no explicados por fallo cardiaco izquierdo o sobrecarga de
volumen (Tabla III). Dichos hallazgos tienen lugar en el contexto clínico de un paciente con una patología
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [532]
[35] PRINCIPIOS DE VENTILACIÓN MECÁNICA. SÍNDROME DE DISTRÉS RESPIRATORIO AGUDO. TRASPLANTE PULMONAR
predisponente (Tabla IV). A diferencia de la definición previa, la actual no requiere demostrar la existencia
de una presión capilar pulmonar (PCP) normal.
Tabla III. Criterios diagnósticos de síndrome de distrés respiratorio agudo (definición de Berlín 2012).
La incidencia de SDRA ha variado notablemente en la última década, en parte debido a las nuevas
definiciones del síndrome y en parte a la generalización de las estrategias de ventilación protectora. Los
estudios más recientes en Europa describen una incidencia variable entre 5 y 7,2 casos/100.000 habitantes
y año. En la actualidad la mortalidad global de este síndrome se estima entre un 40-50% (si bien se incluye
en los estudios población muy heterogénea).
El elemento fisiopatológico central es la presencia de un daño alveolar difuso con alteración de la
membrana alvéolo-capilar. De forma subsecuente se produce edema intersticial y alveolar con aumento del
agua extravascular pulmonar (ELWI). Estos cambios se acompañan de una disminución del número de
alvéolos ventilados, disminución de la complianza pulmonar, aumento del trabajo respiratorio e hipoxemia
progresiva. Diversos factores son capaces de iniciar el SDRA actuando como trigger (Tabla IV).
Independientemente del origen del cuadro, el SDRA es una enfermedad sistémica. Las mismas alteraciones
observadas en la circulación pulmonar pueden producirse en otros órganos, siendo el paciente susceptible
del desarrollo de otros fallos orgánicos durante su evolución (fallo hemodinámico, lesión renal aguda,
coagulopatía, etc.).
2. ETIOLOGÍA
Tabla IV. Etiología del síndrome de distrés respiratorio agudo.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [533]
[35] PRINCIPIOS DE VENTILACIÓN MECÁNICA. SÍNDROME DE DISTRÉS RESPIRATORIO AGUDO. TRASPLANTE PULMONAR
3. ABORDAJE TERAPÉUTICO
Las estrategias terapéuticas van encaminadas a ofrecer un soporte respiratorio y hemodinámico,
intentando prevenir el daño pulmonar y las complicaciones.
Por el momento, las intervenciones que han demostrado mejorar el pronóstico de estos pacientes
son las estrategias de ventilación protectora, el uso de relajantes neuromusculares y el decúbito prono
(Figura 2).
1. ESTRATEGIA VENTILATORIA
La estrategia ventilatoria está encaminada a prevenir el VILI. La ventilación protectora ha
demostrado ser eficaz disminuyendo la mortalidad en este grupo de pacientes (estudio ARMA). De las
diferentes modalidades ventilatorias disponibles (volumen control, presión control), ninguna ha
demostrado mejorar el pronóstico de estos pacientes. Independientemente de la modalidad ventilatoria los
parámetros generales son:
Volumen corriente bajo (5-7 ml/kg de peso teórico).
PEEP óptima (incialmente 5 cm de H2O).
Mantener presión de meseta (plateau) por debajo de 30 cm de H2O.
Delta de presión o drive pressure (definida como presión meseta menos PEEP) < 15 cm de H2O.
Objetivo PaO2 55-80 mm Hg y SatO2 88-95%.
Hipercapnia permisiva (pH 7,15-7,20).
Figura 2. Intervenciones terapeúticas en el síndrome de distrés respiratorio agudo.
2. ESTRATEGIAS NO VENTILATORIAS
2.1. Relajación neuromuscular
El uso de la relajación muscular ha sido controvertido. Sin embargo, la evidencia actual (estudio ACURASYS)
apoya el uso precoz de relajantes musculares durante un corto periodo de tiempo en pacientes con SDRA
agudo severo. El uso de relajantes produce mayor adaptación del paciente al respirador, mejor tolerancia
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [534]
[35] PRINCIPIOS DE VENTILACIÓN MECÁNICA. SÍNDROME DE DISTRÉS RESPIRATORIO AGUDO. TRASPLANTE PULMONAR
de modalidades protectoras, así como disminución en la incidencia de complicaciones (barotrauma). El
relajante muscular de elección en nuestro medio es el cisatracurio en perfusión continua.
2.2. Decúbito prono
La ventilación en decúbito prono mejora el reclutamiento alveolar, la relación ventilación/ perfusión y
disminuye el daño asociado a ventilación. Los estudios más recientes han demostrado que mejora la
supervivencia, especialmente en pacientes en los que el prono se realiza de forma precoz (estudio
PROSEVA), así como en pacientes obesos.
La ventilación en decúbito prono es técnicamente compleja y requiere para su realización de un
equipo entrenado para la técnica. Las peculiaridades de la misma conlleva un alto riesgo de complicaciones
si no se lleva a cabo por expertos en unidades apropiadas.
2.3. Oxigenación con membrana extracorpórea
El desarrollo de la oxigenación con membrana extracorpórea (ECMO) ha sido excepcional en los últimos
años, siendo actualmente una estrategia de uso habitual en centros de referencia para insuficiencia
respiratoria grave. Se estima que en 2014 alrededor de 5.000 pacientes recibieron este tipo de tratamiento
en el mundo.
El sistema se compone de dos elementos. Por un lado, una bomba capaz de mover un flujo
continuo de sangre a través a una membrana de oxigenación. El segundo elemento es la propia membrana
de intercambio, en la que se enfrenta la sangre del paciente a un flujo conocido de aire y oxígeno. Para su
uso se requieren accesos vasculares de gran calibre. Existen dos modalidades de ECMO: la ECMO veno-
venosa (la sangre se extrae y se infunde en una vena central) y ECMO veno-arterial (la sangre se extrae de
una vena central y se infunde en una arteria, permitiendo adicionalmente un soporte cardiocirculatorio;
indicado cuando coexiste shock cardiogénico). En el caso de la insuficiencia respiratoria aislada (sin shock
cardiogénico) suelen ser suficientes dos accesos venosos (habitualmente femoral y yugular).
Las principales indicaciones en la insuficiencia respiratoria son el SDRA (infeccioso especialmente),
el trasplante pulmonar, el estatus asmático, la hemorragia alveolar y la contusión pulmonar. Las principales
contraindicaciones son la existencia de enfermedad neoplásica, las lesiones del sistema nervioso central o
la parada cardiaca prolongada. Sin embargo, la indicación y la elegibilidad de pacientes requiere de la
valoración cuidadosa por un equipo con suficiente experiencia. Por esta razón se recomienda la valoración
precoz por centros útiles (equipo ECMO) de aquellos pacientes susceptibles de requerir esta terapia
durante su evolución.
Las complicaciones relacionadas son relevantes, siendo no obstante su incidencia menor en el caso
de los sistemas veno-venosos (insuficiencia respiratoria aislada). La principal complicación es el sangrado
(10-30%); este se asocia a la necesidad de anticoagulación sistémica y a la inserción de las cánulas.
Actualmente la supervivencia de pacientes adultos con ECMO en el contexto de insuficiencia respiratoria es
del 58% al alta hospitalaria (registro ELSO; 2016).
3. EL PAPEL DE LA FLUIDOTERAPIA
Se ha descrito cierta participación del componente hidrostático en la fisiopatología del SDRA. Varios
trabajos han descrito aumentos de las presiones de llenado cardiacas e hipertensión pulmonar en los
pacientes con SDRA. En ese sentido, se ha demostrado que estrategias restrictivas con balances hídricos
negativos se asocian a mejoría en la oxemia junto con un aumento en los días libres de VMI.
Frecuentemente los pacientes que sufren SDRA presentan shock de diversa etiología. Es por eso que el
manejo de la fluidoterapia y el balance hídrico en este grupo de pacientes es especialmente complejo. La
monitorización hemodinámica avanzada es especialmente útil en estos pacientes. Destacan el uso de la
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [535]
[35] PRINCIPIOS DE VENTILACIÓN MECÁNICA. SÍNDROME DE DISTRÉS RESPIRATORIO AGUDO. TRASPLANTE PULMONAR
ecografía pulmonar como punto de atención (point of care) o las técnicas de dilución traspulmonar. La
resucitación guiada por ELWI en este grupo de pacientes se ha asociado a mejores resultados.
4. TRATAMIENTOS EXPERIMENTALES
Existen múltiples estudios encaminados a encontrar una terapia que atenúe la respuesta
inflamatoria en estos pacientes (corticoides, ketoconazol, estatinas, surfactante...). Existen varios ensayos
clínicos en marcha, pero por el momento no hay datos definitivos.
III. TRASPLANTE PULMONAR
El trasplante pulmonar es una alternativa terapéutica que debe ser considerada en pacientes con
enfermedad pulmonar avanzada con deterioro clínico progresivo, a pesar del correcto y exhaustivo
tratamiento médico y/o quirúrgico, en los pacientes que presentan clase funcional III-IV y tengan una
expectativa de vida estimada menor de dos años. El candidato ideal debe ser menor de 65 años y estar libre
de padecer disfunción de otros órganos y manifestaciones extrapulmonares de enfermedades sistémicas.
Cuando un paciente con enfermedad respiratoria crónica grave presenta un deterioro funcional
importante y se pueda predecir que tiene un 50% o menos de posibilidad de sobrevivir en los 2-3 próximos
años, este es el momento de contactar con un centro de trasplante pulmonar.
Las patologías más comunes con indicación de trasplante pulmonar (85% de los casos) son: EPOC,
fibrosis pulmonar idiopática, fibrosis quística, enfisema por déficit de alfa-1-antitripsina e hipertensión
pulmonar idiopática, existiendo criterios específicos de derivación para cada patología, cuyo desarrollo
excede el ámbito de este manual.
BIBLIOGRAFÍA
Amato MB, Meade MO, Slutsky AS, et al. Driving pressure and survival in the acute respiratory distress
syndrome. N Engl J Med. 2015;372(8):747-55.
ARDS Definition Task Force, Ranieri VM, Rubenfeld GD, Thompson BT, et al. Acute respiratory distress
syndrome: The Berlin definition. JAMA. 2012;307(23):2526-33.
ADRS Network. Ventilation with lower tidal volumes as compared with traditional tidal volumes for
acute lung injury and the acute respiratory distress syndrome. N Engl J Med. 2000;342(18):1301-8.
Barrot Cortés E, Sánchez Gómez E. Ventilación mecánica no invasiva. Manual SEPAR de
procedimientos. 2008. Disponible en:
http://issuu.com/separ/docs/procedimientos16?mode=window&backgroundColor=%23222222
Bloomfield R, Noble DW, Webster NR. Prone position for acute respiratory failure in adults. Cochrane
Database Syst Rev. 2015;11:CD008095. DOI: 10.1002/14651858.CD008095
Chacko B, Peter JV, Tharyan P, et al. Pressure-controlled versus volume-controlled ventilation for acute
respiratory failure due to acute lung injury (ALI) or acute respiratory distress syndrome (ARDS).
Cochrane Database Syst Rev. 2015;1:CD008807. DOI: 10.1002/14651858.CD008807
Determann RM, Royakkers A, Wolthuis EK, et al. Ventilation with lower tidal volumes as compared with
conventional tidal volumes for patients without acute lung injury: A preventive randomized controlled
trial. Crit Care. 2010;14(1):R1.
ECLS Registry Report. Extracorporeal Life Support Organization; 2016. Disponible en:
http://www.elso.org
Finfer SR, Vincent JL, Slutsky AS, Ranieri VM. Critical care medicine ventilator-induced lung injury. N
Engl J Med. 2013;22369(28):2126-36.
Frat JP, Thille AW, Mercat A, et al; REVA Group. High-flow oxygen through nasal cannula in acute
hypoxemic respiratory failure. N Engl J Med. 2015;372(23):2185-96.
Gattinoni L, Cressoni M, Brazzi L. Fluids in ARDS: from onset through recovery. Curr Opin Crit Care.
2014;20(4):373-7.
Guérin C, Moss M, Talmor D. A glossary of ARDS for beginners. Intensive Care Med. 2016;42(5):659-
62.
Guérin C, Reignier J, Richard JC, et al; PROSEVA Study Group. Prone positioning in severe acute
respiratory distress syndrome. N Engl J Med. 2013;368(23):2159-68.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [536]
[35] PRINCIPIOS DE VENTILACIÓN MECÁNICA. SÍNDROME DE DISTRÉS RESPIRATORIO AGUDO. TRASPLANTE PULMONAR
Hess DR. Non-invasive ventilation in acute respiratory failure. Respir Care. 2013; 58(6):950-72.
Makdisi G, Wang I-W. Extra Corporeal Membrane Oxygenation (ECMO) review of a lifesaving technology.
J Thorac Dis. 2015;7(7):E166-76.
Papazian L, Forel JM, Gacouin A, et al.; ACURASYS Study Investigators. Neuromuscular blockers in early
acute respiratory distress syndrome. N Engl J Med. 2010;363(12):1107-16.
Prieto I, Temprano S, Barea-Mendoza JA, Viejo R. Oxygen therapy in critical care: A double edged sword.
2014;(August):2035-46.
Rabec C, Rodenstein D, Leger P, et al; SomnoNIV group. Ventilator modes and settings during non-
invasive ventilation: effects n respiratory events and implications for their identification. Thorax.
2011;66(2):170-8.
Rittayamai N, Brochard L. What’s new in ARDS (clinical studies). Intensive Care Med.
2014;40(11):1731-3.
Tonelli AR, Zein J, Adams J, Ioannidis JP. Effects of interventions on survival in acute respiratory
distress syndrome: An umbrella review of 159 published randomized trials and 29 meta-analyses.
Intensive Care Med. 2014;40(6):769-87.
Villar J, Fernández RL, Ambrós A, et al. A Clinical classification of the acute respiratory distress
syndrome for predicting outcome and guiding medical therapy. Crit Care Med. 2015;43(2):346-53.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [537]
[36] BACTERIEMIA Y SEPSIS
36.Bacteriemia y sepsis
Helena Marín Mateos.
Medicina Intensiva
Borja de Miguel Campo.
Medicina Interna
Asesores: Francisco López Medrano. Médico Adjunto de la Unidad de Enfermedades Infecciosas. Renata García Gigorro.
Médica Adjunta de Medicina Intensiva
I. INTRODUCCIÓN
La sepsis es una respuesta inflamatoria e inmunológica deletérea con repercusión sistémica y
disfunción orgánica que el organismo manifiesta ante una infección. Es una patología compleja, con una
alta prevalencia a nivel mundial. La mortalidad es elevada, oscila entre el 25 y el 60% de los casos, y es muy
variable dependiendo del patógeno, el foco de infección y, sobre todo, de la zona geográfica y los recursos
disponibles para su abordaje.
II. DEFINICIONES
En 1992, tuvo lugar la primera Conferencia de Consenso sobre la Sepsis entre la American College
of Chest Physicians y la Society of Critical Care Medicine (ACCP/SCCM). En ella se actualizaron y unificaron
los conceptos de SRIS, sepsis, sepsis grave y shock séptico que en los consensos posteriores entre SCCM y
ESCIM (European Society of Intensive Care Medicine) de 2001 y 2016 se han terminado de perfilar. Este
último consenso, conocido como Sepsis-3 ha supuesto un cambio de paradigma con respecto a los previos,
cobrando mayor importancia la disfunción orgánica frente a la respuesta inflamatoria en el diagnóstico de
esta patología.
Por otro lado, la necesidad de un abordaje terapéutico precoz, riguroso y homogeneizado se ha
visto reflejada en las sucesivas guías internacionales publicadas en 2004, 2008 y, por último, en 2012
conocidas como Surviving Sepsis Campaign (SSC).
Bacteriemia: se define como la presencia de bacterias viables en la sangre. Se denomina
fungemia y viremia en el caso de que los microorganismos viables en sangre sean hongos y
virus, respectivamente.
Síndrome de respuesta inflamatoria sistémica (SRIS): se trata de la respuesta del organismo a
diversos tipos de agresiones, consistente en la liberación de mediadores pro y
antiinflamatorios, y que conlleva la aparición de manifestaciones sistémicas inespecíficas. Su
diagnóstico requiere la presencia de dos o más de los siguientes criterios:
Temperatura > 38 ºC o < 36 ºC.
Frecuencia cardiaca > 90 lpm.
Frecuencia respiratoria > 20 rpm o pCO2 < 32 mm Hg o necesidad de ventilación
mecánica.
Leucocitos > 12.000 o < 4.000 por mm3 o > 10% de cayados.
A pesar de su amplio uso, múltiples análisis estadísticos coinciden en su inespecificidad
y escasa validez a la hora de diferenciar una respuesta inflamatoria adecuada de una
inapropiada ante una infección (sepsis).
Sepsis: disfunción orgánica aguda que entraña compromiso vital, causada por una respuesta
inflamatoria deletérea frente a una infección (clínicamente sospechada o documentada
microbiológicamente).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [538]
[36] BACTERIEMIA Y SEPSIS
Según el último consenso Sepsis-3, la disfunción se define como un incremento ≥ 2 puntos en el
Sequential Organ Failure Assessment Score (SOFA), ampliamente utilizado en las Unidades de Cuidados
Intensivos (UCI); los pacientes sin patología previa se asume que tienen un SOFA de cero puntos (Tabla I).
Puede ser útil para el reconocimiento de la sepsis en pacientes no ingresados en UCI el empleo del quick
SOFA (qSOFA), modelo clínico a pie de cama validado igualmente en Sepsis-3 (Tabla II). Asimismo, reseñar
que en este último documento se ha desechado el término “sepsis grave” por considerarse inespecífico y
redundante, ya que el nuevo concepto de sepsis per se implica disfunción orgánica y, por tanto, riesgo vital.
Tabla I. Sequential Organ Failure Assessment Score (SOFA) para la evaluación de sepsis (Modificado del Consenso Sepsis-3, JAMA,
2016).
Tabla II. Quick SOFA (qSOFA) para la detección a pie de cama de sepsis en pacientes no ingresados en Unidad de Cuidados
Intensivos.
Shock séptico: subtipo de sepsis definido como la coexistencia de hiperlactacidemia (> 2,0
mmol/L) con hipotensión refractaria que requiere el empleo de fármacos vasopresores para
mantener una presión arterial media (PAm) > 65 mm Hg, a pesar de la adecuada resucitación
con fluidoterapia. Es un tipo de shock distributivo, con reducción de las resistencias vasculares
sistémicas y, generalmente, aumento del gasto cardiaco, que entraña una alta mortalidad.
Síndrome de disfunción multiorgánica (SDMO): se trata de un cuadro clínico que se caracteriza
por el deterioro progresivo de dos o más órganos vitales, y en el que la homeostasis del
organismo no es posible sin soporte terapéutico. Es un término ampliamente utilizado a nivel
clínico, si bien no figura entre las últimas definiciones de consenso.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [539]
[36] BACTERIEMIA Y SEPSIS
III. FISIOPATOLOGÍA
1. RESPUESTA INFLAMATORIA DEL HUÉSPED
La sepsis es una respuesta inflamatoria desordenada, no resolutiva y finalmente deletérea que se
pone en marcha cuando el huésped con factores predisponentes sufre una infección o invasión por un
microorganismo patógeno con capacidad para activar dichos mecanismos. En condiciones normales, estos
patógenos son reconocidos por los receptores de las células del sistema inmunitario del huésped. Hay
diversos tipos de receptores encargados de ello como los receptores toll-like o los NOD que detectan una
serie de patrones moleculares asociados a estos patógenos (Pathogen-Associated Molecular Pattern
molecules, PAMP). Tras el reconocimiento de los mismos, se pone en marcha una cascada inflamatoria que
tiene por objetivo la eliminación de dicho organismo invasor y en el que intervienen la inmunidad innata,
neutrófilos, macrófagos, sistema de complemento y numerosas citoquinas, así como, en un segundo
tiempo, la inmunidad adquirida tanto con respuesta humoral como celular. Al mismo tiempo que se activan
estos mecanismos, se inician mecanismos antiinflamatorios compensatorios que buscan frenar y controlar
la respuesta inflamatoria. Cuando estos mecanismos compensatorios o inhibitorios fallan, se produce un
exceso de actividad citotóxica y apoptosis que expone patrones moleculares asociados a daño celular
(denominados Damage- Associated Molecular Pattern molecules, DAMP) que ejercen una actividad
parecida a los PAMP; son reconocidos por los mismos receptores, retroalimentando y perpetuando una
respuesta inflamatoria inadecuada.
2. ALTERACIONES ENDOTELIALES Y MITOCONDRIALES
Por otro lado, esta respuesta inflamatoria participa en la activación de la coagulación mediada por
el factor tisular, se produce una disminución de trombomodulina y de receptores de Proteína C activada
que tiene como consecuencia la disminución de los mecanismos anticoagulantes.
Esto genera, unido a un descenso de la fibrinólisis, un estado protrombótico con formación de
coágulos en la microcirculación que comprometen la oxigenación tisular a pesar de gastos cardiacos
mantenidos.
Esta hipoxia tisular provoca una disfunción mitocondrial y una alteración del aporte y consumo de
oxígeno a nivel celular.
IV. MANIFESTACIONES CLÍNICAS
Son inespecíficas, variables entre individuos y pueden superponerse a las de las enfermedades
subyacentes. Se pueden afectar todos los órganos y sistemas.
De cara al diagnóstico precoz de la sepsis deberemos identificar prioritariamente determinadas
manifestaciones que supongan un compromiso vital potencial y que, además, entrañen mayor riesgo de
disfunción orgánica (respiratorias, hemodinámicas y neurológicas, contempladas en el score qSOFA
anteriormente citado).
A continuación y de forma igualmente importante, podremos determinar otras alteraciones que
también nos ayudarán en la identificación de disfunción orgánica asociada a la infección.
1. MANIFESTACIONES CARDIOVASCULARES Y HEMODINÁMICAS
Las más frecuentes son la disminución de resistencias periféricas con aumento de la frecuencia
cardiaca y del gasto cardiaco secundariamente. Tensiones arteriales sistólicas iniciales menores de 100 mm
Hg o medias menores de 65 mm Hg a pesar de volumen son motivo de aviso precoz a la UCI. La disfunción
sistólica con afectación de la fracción de eyección izquierda (en forma de alteración generalizada y difusa
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [540]
[36] BACTERIEMIA Y SEPSIS
de la contractilidad, sin alteraciones segmentarias) y la disfunción diastólica pueden darse hasta en el 20-
25% de los casos. Ambas disfunciones suelen ser autolimitadas, desapareciendo en los primeros 7-10 días
(su impacto en el pronóstico aún no está aclarado).
2. MANIFESTACIONES PULMONARES Y RESPIRATORIAS
El trabajo respiratorio, con frecuencia respiratoria > 22 rpm, es un dato precoz de disfunción. A
nivel del parénquima se produce una respuesta inflamatoria dentro de los alvéolos y ocupación de los
mismos, lo cual genera alteraciones en la relación ventilación/perfusión. Cuando hay presencia de
infiltrados difusos, afectación de la oxigenación con hipoxemia grave en sangre arterial (PaO2/FiO2 < 300),
en ausencia de insuficiencia cardiaca, lo denominamos SDRA (síndrome de distrés respiratorio del adulto).
Puede estratificarse como leve si la relación PaO2/ FiO2 oscila entre 300-200, moderada entre 200 y 100 y
grave si es menor de 100. La PaO2/FiO2 se calcula dividiendo la presión arterial de oxígeno en mm Hg del
paciente entre la fracción inspirada de oxígeno.
3. MANIFESTACIONES NEUROLÓGICAS
Cualquier alteración neurológica, Glasgow Coma Scale (GCS) < 15, desorientación, agitación o
síndrome confusional es indicador precoz de disfunción orgánica y, por tanto, motivo para valoración por la
UCI. La presentación más común es encefalopatía sin alteraciones electroencefalográficas focales, y menos
frecuente la presentación como focalidad neurológica.
En presencia de disfunción multiorgánica precoz o de shock, es frecuente observar en la evolución
posterior afectación del sistema nervioso periférico, en forma de polineuropatía del enfermo crítico.
4. FIEBRE
Es frecuente pero no constante. Algunos pacientes presentan una temperatura normal e incluso
hipotermia, la cual es factor pronóstico de mala evolución de forma independiente, y es más frecuente en
recién nacidos, ancianos, alcohólicos, urémicos y en sepsis por bacilos gramnegativos (BGN).
5. MANIFESTACIONES MUSCULARES
Las mialgias que acompañan los cuadros febriles infecciosos se deben a un aumento del tono
muscular a través de los nervios somáticos y a lesión directa muscular. Son frecuentes en el tercio proximal
de los muslos. Como en el caso de la polineuropatía, la exacerbación de la respuesta inflamatoria
persistente y la disfunción multiorgánica favorecen el desarrollo posterior de miopatía del enfermo crítico.
6. MANIFESTACIONES ENDOCRINO-METABÓLICAS
Hiperlactacidemia acompañada o no de acidosis metabólica, aumento de lípidos en sangre,
aceleración del catabolismo proteico, hipoalbuminemia e hiperglucemia. La presencia de hipoglucemia,
junto a hipotensión refractaria a vasoactivos debe hacer sospechar insuficiencia suprarrenal relativa
subyacente. Pueden darse situaciones de hipotiroidismo e hipopituitarismo relativos.
7. MANIFESTACIONES HEMATOLÓGICAS
Es frecuente la presencia de leucocitosis con neutrofilia. La leucopenia asocia peor pronóstico. La
trombocitopenia es un hallazgo muy frecuente, asociada o no a coagulación intravascular diseminada (CID),
que debe sospecharse ante la combinación de recuento plaquetario menor a 100.000- 50.000
plaquetas/mm3, aumento del tiempo de protrombina y de los dímeros-D e hipofibrinogenemia.
Clínicamente se manifiesta con fenómenos hemorrágicos (frecuente en piel, mucosas, tracto digestivo,
accesos venosos y arteriales), así como trombóticos a nivel de la microcirculación.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [541]
[36] BACTERIEMIA Y SEPSIS
8. MANIFESTACIONES RENALES
Suele aparecer oliguria e hiperazoemia. El daño renal puede producirse por distintos mecanismos:
necrosis tubular aguda, glomerulonefritis, necrosis cortical, nefritis intersticial, lesión renal secundaria a
fármacos.
9. MANIFESTACIONES DIGESTIVAS
La anomalía principal es la ictericia colestásica que se produce en pacientes con y sin enfermedad
preexistente hepática. El aumento de bilirrubina, fosfatasa alcalina y transaminasas es frecuente; sin
embargo, el fallo hepático agudo es raro y se asocia a peor pronóstico. También pueden producirse
náuseas, vómitos, diarrea, íleo y hemorragia digestiva por úlceras de estrés.
10. MANIFESTACIONES CUTÁNEAS
Son de etiología multifactorial como inoculación local, diseminación hematógena, lesiones por
hipoperfusión como livideces o zonas de necrosis. Pueden orientar el diagnóstico hacia determinados
patógenos: púrpura fulminante (necrosis hemorrágica extensa de predominio en partes acras) por N.
meningitidis, aunque también se ha relacionado con BGN y S. aureus; ectima gangrenoso por embolia
séptica por P. aeruginosa y otros BGN; eritrodermia generalizada en el shock tóxico por S. aureus o por S.
pyogenes.
V. DIAGNÓSTICO
1. DIAGNÓSTICO MICROBIOLÓGICO
Lo más adecuado es extraer cultivos antes de iniciar la terapia antibiótica (siempre y cuando no
suponga una demora > 45 minutos para recibir terapia). Obtener unos cultivos apropiados es fundamental
para confirmar la infección y sus patógenos responsables, y permitir reducir el espectro antibiótico una vez
recibido el antibiograma.
Hemocultivos: es fundamental extraerlos en todos los pacientes con sepsis aunque no exista
fiebre en ese momento (cabe recordar que debe sospecharse bacteriemia clínicamente cuando
el paciente presenta tiritona, aún en ausencia de fiebre). Se deben extraer al menos dos sets de
hemocultivos, cada uno de un lugar de venopunción diferente.
En la tabla III se expone la técnica adecuada para la extracción de los mismos. Si existe un acceso
vascular venoso central de más de 48 horas, se deben extraer muestras de cada una de las luces del mismo
y otra de sangre de venopunción.
Tabla III. Técnica para la extracción de hemocultivos.
Otras muestras: orina, líquido cefalorraquídeo, heridas, secreciones respiratorias u otros
fluidos corporales, deben ser igualmente enviados a Microbiología para cultivo (y extraerlos, si
es posible, antes del inicio del tratamiento antibiótico).
Se recomienda recoger las muestras de exudados purulentos con jeringa y aguja, aspirando
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [542]
[36] BACTERIEMIA Y SEPSIS
preferentemente de zonas profundas (se evitará el uso de torundas ya que disminuyen la
rentabilidad del cultivo).
Si se encuentra disponible, se recomienda realizar tinción de Gram urgente de las muestras
que potencialmente puedan ser el origen de la infección (sobre todo de esputo, de líquido
cefalorraquídeo y de líquido articular), ya que puede aportar información adicional para decidir
la antibioterapia empírica inicial.
Marcadores de infección fúngica: en determinados contextos pueden ser útiles la
determinación de galactomanano (sospecha de aspergilosis) y 1,3-beta-D-glucano (marcador de
infección fúngica invasora, no disponible en todos los centros).
2. BIOMARCADORES
Los más relevantes son la proteína C reactiva (PCR), la procalcitonina (PCT) y el ácido láctico. Los
dos primeros son útiles en la monitorización analítica de la respuesta inflamatoria e infecciosa, siendo
especialmente valiosa la determinación seriada de los mismos (mucho más que una determinación aislada)
para valorar la respuesta al tratamiento prescrito. Esto permite ayudar al clínico en la modificación o
suspensión de la antibioterapia en función de la evolución de sus niveles. Niveles elevados se han asociado
asimismo en múltiples estudios con la posibilidad de desarrollar complicaciones graves. A pesar de su
utilidad, ninguno de estos parámetros debe evaluarse aisladamente (siempre se deben correlacionar con la
clínica y el resto de pruebas).
2.1. Proteína C reactiva
Reactante de fase aguda que se produce en el hígado como respuesta a citoquinas proinflamatorias.
Presenta elevada sensibilidad y especificidad para el diagnóstico de inflamación. Aunque no es específico
de infección, niveles especialmente elevados (> 8-10 mg/dL) se relacionan con etiología infecciosa en la
mayoría de estudios (valores de sensibilidad y especificidad variable, pero por encima del 80%). Su
especificidad disminuye significativamente a la hora de diferenciar la etiología bacteriana, viral o fúngica de
la infección.
2.2. Procalcitonina
Péptido precursor de la calcitonina, secretado por las células claras del tiroides y por células
neuroendocrinas pulmonares. Comienza a elevarse a las 2-4 horas del inicio del cuadro séptico, con un pico
de máxima liberación a las 24 h, manteniéndose elevada hasta la resolución del proceso. Su aumento (>
0,05 ng/ml) orienta hacia un origen bacteriano (tanto más cuanto más incremente su valor). Tiene mayor
sensibilidad y especificidad que la PCR en el diagnóstico de sepsis, y un alto valor predictivo negativo para
descartar la misma. Asimismo, es útil para guiar la antibioterapia: la ausencia de “aclaramiento” (descenso
> 70%) a las 48-72 horas debe hacer pensar en un foco infeccioso no controlado y valorar un cambio de los
antibióticos o realización de una prueba de imagen, drenaje percutáneo o quirúrgico del foco. La
normalización de sus valores puede hacer plantear la suspensión de la antibioterapia, siempre y cuando no
existan otros datos de infección no controlada.
Hay que tener en cuenta que la PCT se puede elevar en otras situaciones como traumatismos,
cirugías, quemaduras, shock cardiogénico, golpe de calor, vasculitis, síndromes paraneoplásicos, terapias
inmunológicas y enfermedad injerto contra huésped, entre otras. Por ello, pese a su utilidad, nunca debe
usarse aisladamente como ya se ha mencionado.
2.3. Ácido láctico
Marcador de hipoxia tisular derivado del metabolismo anaerobio. Su elevación es frecuente en caso de
sepsis o shock séptico (aunque puede también incrementarse en caso de insuficiencia hepática o acidosis
láctica secundaria a toma de metformina, entre otros). Es fundamental su determinación en fases iniciales
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [543]
[36] BACTERIEMIA Y SEPSIS
de la sepsis (en las dos primeras horas) para estratificar el riesgo, ya que se ha descrito como predictor
independiente de mortalidad: niveles intermedios, por encima de 2 mmol/L y especialmente elevados por
encima de 4 mmol/L. Puede ser el único indicador de hipoperfusión en pacientes normotensos. Su
determinación precoz se considera un marcador de calidad en la atención inicial del paciente séptico: ante
un nivel elevado (mayor de 4 mmol/L) la fluidoterapia inicial debe ser prioritaria tal y como se describe en
el apartado de tratamiento. Su disminución en las primeras 24 horas se relaciona con una mejoría
pronóstica de los pacientes sépticos ingresados en la UCI.
Para recoger adecuadamente la muestra, debe evitarse el éstasis venoso (no comprimir el extremo
proximal del brazo). Deben transcurrir como máximo 30 minutos entre la extracción y su análisis.
3. ESTUDIOS DE IMAGEN
Es recomendable realizarlos con prontitud (preferiblemente en las primeras 6-12 horas) de cara a
identificar el foco potencial de la infección. El estudio de elección dependerá de la infección sospechada, si
bien, la ecografía “a la cabecera del enfermo” (para pacientes inestables) y la tomografía computarizada
(tanto por su disponibilidad como por la velocidad de adquisición de las imágenes) suelen ser
habitualmente útiles.
VI. CRITERIOS DE AVISO AL SERVICIO DE MEDICINA INTENSIVA
Al igual que la enfermedad traumática grave o el síndrome coronario agudo, la patología séptica es
una enfermedad tiempo-dependiente. Diversos estudios han demostrado que la activación precoz de
médicos especialistas de Medicina Intensiva y el traslado del paciente, lo antes posible, a unidades de
monitorización continua como la UCI, tienen un impacto positivo en la evolución y supervivencia de los
pacientes graves y potencialmente graves. Por tanto, mientras se ponen en marcha todas las medidas de
soporte indicadas en el Apartado de Abordaje terapéutico, se debería solicitar la valoración urgente por el
intensivista en aquellos pacientes con criterios de sepsis o shock séptico, además de aquellos pacientes
que presenten indicación de intubación orotraqueal y ventilación mecánica.
En general, las indicaciones más frecuentes de intubación orotraqueal en pacientes con sepsis son:
el aumento excesivo e ineficaz del trabajo respiratorio (taquipnea mayor de 25 rpm con utilización de
musculatura accesoria), la insuficiencia respiratoria refractaria al empleo de oxigenoterapia y el deterioro
del nivel de consciencia (indicación absoluta con puntuación en la escala de coma de Glasgow menor de 9
puntos).
VII. ABORDAJE TERAPÉUTICO DE LA SEPSIS
Dado el carácter tiempo-dependiente de esta patología crítica y de acuerdo con las últimas guías
publicadas, el abordaje de la sepsis debe incluir un paquete de medidas o bundle que deberán llevarse a
cabo de la forma más precoz posible para garantizar una adecuada asistencia.
En las primeras 3 horas:
Obtención de cultivos previamente a la antibioterapia, dentro de los primeros 45
minutos.
Medición de ácido láctico, detección de hipoperfusión.
Antibioterapia empírica de amplio espectro en la primera hora.
Fluidoterapia (30 ml/kg de suero salino fisiológico o solución balanceada si hipotensión
o ácido láctico inicial > 4 mmol/L).
En las primeras 6 horas:
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [544]
[36] BACTERIEMIA Y SEPSIS
Si persiste hipotensión o hipoperfusión, canalización de la vía venosa central (VVC) en
la cava superior para medición de la presión venosa central (objetivo 8-12 mm Hg) y la
saturación venosa central de oxígeno (objetivo > 70%).
Iniciar vasopresores ante hipotensión mantenida que no responde a fluidos.
Inicialmente noradrenalina como primera opción.
Reevaluación y remedición de ácido láctico si el inicial estaba elevado.
Para poder cumplir con todas estas medidas, se debe llevar a cabo una adecuada valoración según
el esquema ABCD y una resucitación inicial concomitante con un soporte hemodinámico y respiratorio
adecuados, con el objetivo de detectar problemas o alteraciones fisiológicas que supongan un compromiso
vital para el paciente y solventarlas en el mismo acto médico.
1. VALORACIÓN Y RESUCITACIÓN INICIAL
En el primer contacto con el paciente séptico se debe proceder a la monitorización
electrocardiográfica continua, medición de la presión arterial y de la saturación por pulsioximetría. La
primera prioridad en el paciente con sepsis es la valoración y estabilización de la vía aérea y de la función
respiratoria. Debe valorarse la indicación de intubación orotraqueal y administrarse oxigenoterapia
suplementaria para una saturación arterial adecuada.
Tabla IV. Resumen de objetivos y actuaciones ante pacientes con sepsis.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [545]
[36] BACTERIEMIA Y SEPSIS
A continuación se valorará la situación hemodinámica y la perfusión tisular. En la mayoría de los
casos cifras de PAm < 65 mm Hg pueden suponer un compromiso de la perfusión orgánica, aunque esta
hipoperfusión tisular puede verse incluso con cifras tensionales inicialmente conservadas (por alteraciones
en la microcirculación o disminución del gasto cardiaco). En este caso, como ya se ha descrito, es
recomendable aplicar como referencia la cifra de ácido láctico. Se debe prestar atención a los datos clínicos
como palidez, livideces o retraso en el relleno capilar.
Se recomienda canalizar dos vías venosas periféricas gruesas (calibre 14 o 16 G) e iniciar la
fluidoterapia lo antes posible. En caso de que el paciente cumpla criterios de shock séptico, se recomienda
además canalizar una vía venosa central para guiar la resucitación y cuantificar la diuresis mediante sondaje
vesical.
Figura 1. Algoritmo de abordaje terapéutico de la sepsis.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [546]
[36] BACTERIEMIA Y SEPSIS
Los objetivos y principales actuaciones se resumen en la tabla IV y en la figura 1.
Se recomienda establecer un protocolo de resucitación precoz con objetivos hemodinámicos
cuantitativos a alcanzar y mantener durante las primeras 6 horas, con el objetivo de prevenir la disfunción
multiorgánica:
Mantener una presión venosa central (PVC) entre 8-12 mm Hg.
Mantener una PAm entre 65 y 90 mm Hg.
Diuresis horaria mayor a 0,5 ml/kg/h.
Mantener la saturación venosa central, obtenida de la cava superior (SvcVO2), mayor al 70% y/o
la saturación venosa mixta, obtenida de la arteria pulmonar (SVO2) mayor o igual a 65%. Tanto
la SvcO2 como la SVO2 son indicadores indirectos del gasto cardiaco, de la perfusión tisular y
evalúan la relación aporte/consumo de oxígeno a los tejidos. Sin embargo, estos parámetros
pueden no estar alterados inicialmente en la mayor parte de los pacientes sépticos, por lo que
deberemos tener en cuenta otros datos de posible hipoperfusión como la exploración clínica, la
oliguria o la presencia de lactato elevado. La importancia de estos valores no está en el dato o
cifra puntual, sino en la evolución de los mismos ante las decisiones terapéuticas que tomamos
y las medidas de resucitación que llevamos a cabo. Es importante integrar toda la información
en el contexto clínico del paciente.
Para alcanzar estos objetivos deben seguirse escalonadamente las siguientes líneas de tratamiento:
1.1. Fluidoterapia eficaz
Iniciaremos el tratamiento con la infusión intravenosa de 20-30 ml/kg de cristaloides: 500- 1.000 ml de
suero salino fisiológico al 0,9% en los primeros 30 minutos, logrando un total aproximado de 1.500-2.000
ml en la primera hora (en pacientes ancianos o con cardiopatía de base se recomienda ser más restrictivos
por el riesgo de edema agudo de pulmón).
Posteriormente se recomienda un ritmo de infusión 20-30 ml/kg/día, ajustando en función de la
respuesta clínica y de la consecución de los objetivos ya mencionados. Se puede valorar el empleo de
albúmina (por ejemplo, 1 vial de 50 ml de albúmina al 20% cada 8 horas) en pacientes con grandes
necesidades de cristaloides (con grado de evidencia débil), pero a día de hoy se desaconseja el empleo de
otros coloides (gelatinas, dextranos, almidones) por no haber demostrado beneficio sobre los cristaloides
en múltiples estudios (aumentando la morbimortalidad, sobre todo, por necesidad de tratamiento
sustitutivo renal).
1.2. Vasopresores
Son agentes de segunda línea en el tratamiento del shock séptico. Están indicados en pacientes que no
responden a la fluidoterapia previa (PAm < 65 mm Hg). Se recomienda su administración por catéter
venoso central y bajo monitorización estrecha (monitorización electrocardiográfica, así como arterial
continua mediante empleo de catéteres arteriales). La noradrenalina (NA) es el fármaco de elección (dosis
de inicio de NA de 0,04 μg/kg/min: 8 mg de NA en 250 ml de suero salino fisiológico al 0,9%, comenzando a
un ritmo de 5 ml/h, con incrementos de 5 ml/h cada 5-10 minutos en función de objetivos
hemodinámicos). A día de hoy, no se recomienda el empleo de dopamina como vasopresor (por ausencia
de beneficio sobre NA y mayor morbimortalidad por arritmogenia), reservándose para casos muy concretos
(pacientes con bajo riesgo de arritmia y presencia de bradicardia); tampoco ha demostrado beneficio a
nivel renal (no debe emplearse como nefroprotector). Si se precisase añadir un segundo vasopresor, podría
emplearse adrenalina (> 0,03 μg/kg/min) o vasopresina (0,03 UI/min) en función de la situación clínica y
experiencia de cada centro.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [547]
[36] BACTERIEMIA Y SEPSIS
1.3. Tratamiento inotrópico
Solo debe utilizarse en pacientes en los que se evidencia disfunción miocárdica (elevación de presiones de
llenado o alteración de la FEVI en ecocardiografía) y, además, bajo gasto cardiaco con persistencia de
hipoperfusión pese a una volemia intravascular y tensión arterial adecuadas gracias a las medidas previas
(fluidoterapia y vasopresores). Como agente inotrópico suele emplearse la dobutamina, en dosis inicial 2,5
μg/kg/min, incrementable en 2,5 μg/kg/min cada 30 minutos, hasta un máximo de 20 μg/kg/min (en un
paciente de 70 kg, 250 mg de dobutamina en 250 ml de suero salino fisiológico al 0,9%, a 10 ml/h de forma
inicial). Debe tenerse en cuenta que a bajas dosis puede agravar la hipotensión arterial debido a la
vasodilatación arteriolar. En caso de iniciar tratamiento inotrópico, se recomienda realizar una
monitorización invasiva o mínimamente invasiva del gasto cardiaco (catéter Swanz-Ganz o sistemas como
LiDCO® oVolumeView®).
2. ABORDAJE INFECCIOSO
Extracción de cultivos: debe asegurarse una correcta recolección de muestras microbiológicas,
tal y como se ha explicado, sin retrasar el inicio del tratamiento.
Tratamiento antibiótico: la antibioterapia debe iniciarse dentro de la primera hora desde el
diagnóstico de sepsis o de shock séptico. Cada hora de retraso en la administración de un
antibiótico efectivo se asocia con un incremento notable de la mortalidad.
En la elección del tratamiento empírico inicial se deben tener en cuenta: alergias medicamentosas
del paciente, enfermedades de base, síndrome clínico actual, adecuada penetración del antibiótico en el
foco sospechado, procedencia del enfermo (infección comunitaria o nosocomial, contacto habitual con
medio sanitario), susceptibilidad de los patógenos del área o del hospital (tener presente la posibilidad de
S. aureus oxacilina resistente y BGN productores de betalactamasas de espectro extendido), tratamiento
antibiótico en los 3 meses previos, historial microbiológico del paciente (patógenos previos causantes de
colonización o infección), existencia de neutropenia o posibilidad de infección por hongos. Es necesario
ajustar la dosis del fármaco a la función renal.
Ante una sepsis o shock séptico se deben emplear antibióticos de amplio espectro hasta conocer el
antibiograma del patógeno aislado. En estos pacientes plantearse usar antibióticos de menor espectro o
coste no es una adecuada estrategia inicial. A diario debe reevaluarse la continuación o cambio de
antibioterapia en base a criterios clínicos, microbiológicos y analíticos (en este sentido, la PCR y, sobre
todo, la PCT han demostrado su utilidad para ayudar a decidir la suspensión de la antibioterapia), y valorar
la posibilidad de reducir el espectro antibiótico si procede.
La duración del tratamiento antibiótico dependerá del foco infeccioso de origen y de la evolución
del paciente (ver capítulos correspondientes). Cursos más prolongados se recomiendan para pacientes con
una respuesta más lenta, focos infecciosos de difícil drenaje, microorganismos virulentos (S. aureus, hongos
y algunos virus) e inmunosupresión, incluidos los pacientes neutropénicos; en ellos el tratamiento debe
prolongarse hasta la recuperación de la neutropenia (ver Capítulo 47. “Infecciones en el paciente
inmunodeprimido. Neutropenia febril”).
Búsqueda y drenaje de focos piógenos: es importante definir el foco de la infección en las
primeras 6-12 horas (puede ser útil el empleo de técnicas de imagen tal y como se ha
mencionado). Si este es subsidiario de cirugía o drenaje percutáneo (por ejemplo, colocación de
tubo de tórax en un empiema, drenaje de abscesos, colangiografía transparietohepática en la
sepsis de origen biliar, etc.), se debe intentar realizar en las primeras 6 horas tras el diagnóstico
(una excepción es la pancreatitis necrotizante, en la que se difiere el acto quirúrgico para lograr
mejor diferenciación entre las zonas viables y no viables). Si se sospecha infección de
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [548]
[36] BACTERIEMIA Y SEPSIS
dispositivos (catéter venoso, sonda vesical, dispositivo intravascular), deben retirarse a la
mayor brevedad.
2.1. Sepsis de origen conocido
En cada capítulo correspondiente del Manual se describe el tratamiento antibiótico de las principales
infecciones que pueden producir sepsis.
2.2. Sepsis de origen no filiado
Sepsis de origen en la comunidad
En la terapia empírica inicial se recomienda iniciar el tratamiento con cefalosporina de tercera
o cuarta generación (ceftriaxona 2 g/24 h iv o cefotaxima 2 g/6 h iv) o penicilina + inhibidor de
betalactamasa (piperacilina-tazobactam 4,5 g/6 h iv) o carbapenem (imipenem-cilastatina 500
mg/6 h iv o meropenem 1 g/8 h iv); se puede valorar la administración inicial de
aminoglucósidos (por ejemplo, amikacina a dosis de 15 mg/kg/día iv) por su rápido efecto
bactericida.
Si existe sospecha de implicación de grampositivos resistentes, asociar vancomicina 1-1,5 g/12
h iv (ajustando posteriormente en función de niveles plasmáticos).
Emplear daptomicina 6-10 mg/kg/día en lugar de vancomicina si el paciente tiene shock
séptico, antecedentes de infección previa por S. aureus con una concentración mínima
inhibitoria (CMI) para vancomicina > 1,5 mg/l, empleo reciente de vancomicina (últimos 30
días) o fracaso renal (hay que recordar que la daptomicina no cubre el foco respiratorio al
inactivarse por el surfactante pulmonar).
Sepsis de origen intrahospitalario
Se recomienda asociar vancomicina 1-1,5 g/12 h iv junto con uno de los siguientes antibióticos
con actividad frente a Pseudomonas aeruginosa: penicilinas antipseudomónicas (ceftazidima 2
g/8 h iv o cefepime 2 g/8 h iv o piperacilina-tazobactam 4,5 g/6 h iv) o carbapenems
(meropenem 1 g/8 h iv o imipenem-cilastatina 500 mg/6 h iv). La asociación de dos fármacos
con actividad frente a BGN empleados de manera sistemática parece no aportar mayor
beneficio y sí más riesgo de toxicidad especialmente a nivel renal, por lo que debería reservarse
para pacientes con shock séptico.
Emplear daptomicina 6-10 mg/kg/día en lugar de vancomicina si el paciente tiene shock
séptico, antecedentes de infección previa por S. aureus con una CMI para vancomicina > 1,5
mg/l, empleo reciente de vancomicina (últimos 30 días) o fracaso renal (hay que recordar que
la daptomicina no cubre el foco respiratorio al inactivarse por el surfactante pulmonar).
Si existe sospecha de infección por un BGN productor de betalactamasas de espectro extendido
(BLEE), el betalactámico de elección es un carbapemen.
2.3. Shock séptico de origen no filiado
Recomendamos el siguiente tratamiento empírico: meropenem (1 g/6 h iv) + daptomicina (6-10 mg/kg/día)
+ amikacina (15 mg/kg/día iv). En pacientes con alergia (confirmada o sospechada) a betalactámicos:
tigeciclina (100 mg iv la primera dosis, posteriormente 50 mg/ 12 h iv) + amikacina (15 mg/kg/día iv) +
ciprofloxacino (400 mg/8 h iv); se deberá consultar de manera precoz al Servicio de Alergología para
descartar sensibilización a betalactámicos.
2.4. Sospecha de infección fúngica
La fungemia es la micosis profunda más frecuente en el enfermo crítico. La especie predominante es
Candida albicans. A la hora de seleccionar el fármaco, hay que tener en cuenta el patrón local de
resistencias, la especie predominante, las peculiaridades de algunas especies (C. glabrata generalmente es
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [549]
[36] BACTERIEMIA Y SEPSIS
resistente a los azoles, C. parapsilosis suele serlo a las equinocandinas y C. krusei es siempre resistente a
fluconazol), así como el espectro de acción, farmacocinética y efectos secundarios.
La sepsis por levaduras ha de sospecharse ante la persistencia de fiebre de más de 48 horas a pesar
de tratamiento antibiótico de amplio espectro (incluyendo cobertura frente a S. aureus resistente a
oxacilina), especialmente en pacientes que presentan factores de riesgo para desarrollar fungemia (Tabla
V). Existen también escalas de valoración de riesgo simplificadas como el Candida Score (Tabla VI).
Tabla V. Factores de riesgo para fungemia.
Tabla VI. Candida Score para determinación a pie de cama de riesgo de fungemia.
El tratamiento de la fungemia se pormenoriza en el Capítulo 37 “Endocarditis infecciosa. Infecciones
endovasculares y fungemia”. De manera general, en el paciente séptico con sospecha de infección por
Candida spp, se recomienda emplear de inicio una equinocandina: caspofungina (70 mg iv el primer día,
posteriormente, 50 mg/24 h iv) o anidulafungina (primera dosis, 200 mg iv infundida en 3 horas,
posteriormente 100 mg iv/24 h infundida en 90 minutos) o micafungina (100 mg/24 h iv). En caso de
resistencia, intolerancia o imposibilidad de empleo de equinocandinas, la anfotericina B liposomal (3-5
mg/kg/día) podría ser una alternativa; podría ser de primera elección cuando el foco séptico sea ocular,
urinario o en sistema nervioso central, por presentar mayor biodisponibilidad a dichos niveles.
Una vez identificada la especie, si esta es sensible a fluconazol y el paciente se encuentra
clínicamente estable tras 5-7 días de terapia, se recomienda completar el tratamiento con fluconazol
(primera dosis 800 mg iv, posteriormente 400 mg/24 h iv).
3. SOPORTE HEMATOLÓGICO
3.1. Transfusión de hematíes
En la fase de resucitación (6 primeras horas), puede considerarse la transfusión de hematíes si el enfermo
continúa con SvcO2 < 70 % y presenta niveles de hematocrito < 30%. Fuera de esa fase inicial, solo se
recomienda transfundir si los niveles de hemoglobina (Hb) son < 7 g/dL (salvo en algunas situaciones
extenuantes como isquemia miocárdica, cardiopatía isquémica, hipoxia severa o sangrado agudo), para
conseguir objetivos de Hb entre 7-9 g/dL (valores mayores se han asociado a aumento de morbimortalidad
en numerosos estudios). La eritropoyetina no se ha mostrado útil en este escenario.
3.2. Transfusión de plaquetas
Se recomienda transfusión de plaquetas si: ≤ 10.000 plaquetas/mm3 (en todos los pacientes), o bien ≤
20.000 plaquetas/mm3 si existen factores de riesgo de sangrado (sepsis activa, fiebre > 38 ºC, hemorragia
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [550]
[36] BACTERIEMIA Y SEPSIS
menor reciente, rápido descenso de la cifra de plaquetas o coexistencia de coagulopatía), o bien, ≤
50.000/mm3 si existe sangrado activo o se van a realizar procedimientos quirúrgicos o instrumentales.
3.3. Transfusión de plasma fresco congelado (PFC)
Solo se recomienda la transfusión de PFC en los pacientes con coagulopatía si existe sangrado activo o se
van a realizar procedimientos quirúrgicos o instrumentales (no de rutina).
4. OTROS TRATAMIENTOS A CONSIDERAR
4.1. Empleo de esteroides a bajas dosis
En general, debe evitarse. Utilizar solo en pacientes con shock séptico refractarios a fluidoterapia y
tratamiento vasopresor. En dicho caso, se recomienda hidrocortisona a dosis de 50 mg/6 h o 100 mg/8 h iv.
Este tratamiento debe ser retirado paulatinamente una vez suspendidos los fármacos vasopresores. Se
desaconseja la realización del test de estimulación con ACTH por su escaso valor en estos pacientes.
4.2. Control estricto de la glucemia
Deben aplicarse protocolos específicos (habitualmente con perfusión de insulina) si se detectan glucemias >
180 mg/dL en dos determinaciones consecutivas. El objetivo es mantener una cifra de glucemia entre 140 y
180 mg/dL (objetivos más estrictos conllevan una mayor frecuencia de hipoglucemias graves y no han
demostrado un beneficio añadido). Si es posible, se recomienda evitar glucemias capilares (los valores
pueden no ser fiables).
4.3. Profilaxis de hemorragia digestiva
Con inhibidores de la bomba de protones (de elección) o anti-H2 en pacientes de riesgo (coagulopatía,
hipotensión arterial, ventilación mecánica durante > 48 horas), a las dosis habituales.
4.4. Profilaxis de la enfermedad tromboembólica venosa
Con heparina de bajo peso molecular (HBPM) en todos los pacientes (salvo contraindicación). En fracaso
renal grave (filtrado glomerular < 30 ml/min), se recomienda heparina sódica no fraccionada o HBPM con
medición de niveles de anti-Xa (ver Capítulo 77. “Anticoagulación”). En los pacientes con contraindicación
para anticoagulación (trombopenia, coagulopatía severa, sangrado activo o hemorragia intracerebral
reciente), se recomiendan medias de compresión neumática (las medidas de compresión elástica no son
útiles: solo han demostrado mejorar el síndrome posflebítico), debiendo iniciar terapia farmacológica
cuando desaparezca la contraindicación.
4.5. Terapia sustitutiva renal
En aquellos pacientes con indicación para la misma (ver Capítulo 62. “Fracaso renal agudo”). Las terapias de
hemodiafiltración continua han demostrado no ser inferiores a la hemodiálisis convencional, dado que son
habitualmente mejor toleradas desde el punto de vista hemodinámico.
4.6. Bicarbonato
Únicamente se recomienda cuando el pH ≤ 7,15 (escasa utilidad en los casos debidos a hiperlactacidemia).
Para una corrección rápida inicial podemos administrar 50 ml de bicarbonato 1 Molar iv (1 ml contiene 1
mEq) en 60 minutos. Es necesaria la monitorización del pH para la prescripción de dosis posteriores de
bicarbonato.
4.7. Soporte nutricional
Se recomienda iniciar precozmente (primeras 48 horas de ingreso en la UCI, una vez finalizada la fase de
resucitación inicial) una nutrición oral o enteral (es preferible sobre cualquier solución parenteral, tanto
cristaloides como preparados de nutrición completa).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [551]
[36] BACTERIEMIA Y SEPSIS
4.8. Inmunoglobulina humana inespecífica
No se recomienda ya que no ha demostrado beneficio en pacientes con sepsis.
BIBLIOGRAFÍA
Angus CD, van der Poll T. Severe sepsis and septic shock. Review. N Engl J Med. 2013;360:840.
Bloos F, Marshall JC, Dellinger RP, Vincent JL, Gutiérrez G, Rivers E, et al. Multinational, observational
study of procalcitonin in ICU patients with pneumonia requiring mechanical ventilation: a multicenter
observational study. Crit Care. 2011;15(2):R88.
Caironi P, Tognoni G, Masson S, Fumagalli R, Pesenti A, Romero M. Albumin replacement in patients
with severe sepsis or septic shock. N Engl J Med. 2014;370:1412-21.
Cornely OA, Bassetti M, Calandra T, Garbino J, Kullberg BJ, Lortholary O, et al.; for de ESCMID Fungal
Infection Study Group (EFISG). ESCMID guideline for the diagnosis and management of Candida
diseases 2012: non-neutropenic adult patients. Clin Microbiol Infect. 2012;18(Suppl 7):19-37.
Cuenca-Estrella M, Verweij PE, Arendrup MC, Arikan-Akdagli S, Bille J, Donnelly JP, et al.; for the
ESCMID Fungal Infection Study Group (EFISG). ESCMID guideline for the diagnosis and management of
Candida diseases 2012: diagnostic procedures. Clin Microbiol Infect. 2012;18(Suppl 7):9-18.
De Backer B, Biston P, Devriendt J, Madl C, Chochrad D, Alcolea C, et al. Comparision of Dopamine and
Norepinephrine in the Treatment of Shock. N Engl J Med. 2010;362:779-89.
Dellinger RP, Levy MM, Carlet JM, et al. Surviving Sepsis Campaign: international guidelines for
management of severe sepsis and septic shock: 2012. Crit Care Med. 2013;41:580-619.
Gudiol F, Aguado JM, Almirante B, Bouza E, Cercenado E, Domínguez MA, et al. Diagnosis and
treatment of bacteremia and endocarditis due to Staphylococcus aureus. A clinical guideline from the
Spanish Society of Clinical Microbiology and Infectious Diseases (SEIMC). Enferm Infecc Microbiol Clin.
2015;33(9):625.e1-625.e23.
Holst LA, Haase N, Wetterslev J, Wernerman J, Guttormsen AB, Karlsson S, et al. Lower versus Higher
Hemoglobin Threshold for Transfusion in Septic Shock. N Engl J Med. 2014;371:1381-91.
Lelubre C, Anselin S, Zouaoui Boudjeltia K, Biston P, Piagnerelli M. Interpretation of C-reactive protein
concentrations in critically ill patients. Biomed Res Int. 2013;2013:124021.
León C, Ruiz-Santana S, Saavedra P, Almirante B, Nolla-Salas J, Álvarez-Lerma F, et al.; from the EPCAN
Study Group: A bedside scoring system (Candida score) for early antifungal treatment in non-
neutropenic critically ill patients with Candida colonization. Crit Care Med. 2006;34:730-7.
Leroy G, Lambiotte F, Thévenin D, Lemaire C, Parmentier E, Devos P, Leroy O. Evaluation of Candida
score in critically ill patients: a prospective, multicenter, observational, cohort study. Ann Intensive
Care. 2011;1(1):50.
Myburgh JA, Finfer S, Bellomo R, Billot L, Cass A, Gattas D, et al. Hydroxyethyl Starch or Saline for Fluid
Resuscitation In Intensive Care. N Engl J Med. 2012;367:1901-11.
Norberg A, Christopher NC, Ramundo ML, Bower JR, Berman SA. Contamination rates of blood cultures
obtained by dedicated phlebotomy vs. intravenous catheter. JAMA. 2003;289(6):726.
Pappas PG, Kauffman CA, Andes DR, Clancy CJ, Marr KA, Ostrosky-Zeichner L, et al. Clinical Practice
Guideline for the Management of Candidiasis: 2016 Update by the Infectious Diseases Society of
America. Clin Infect Dis. 2016;62(4):e1-e50.
Perner A, Haase N, Guttormsen AB, Tenhunen J, Klemenzson G, Åneman A. Hydroxyethyl starch
130/0.42 versus Ringer’s acetate in severe sepsis. N Engl J Med. 2012;367:124-34.
Pierrakos C, Vincent JL. Sepsis biomarkers: a review. Crit Care. 2010;14(1):R15. doi: 10.1186/cc8872.
Prkno A, Wacker C, Brunkhorst FM, Schlattmann P. Procalcitonin-guided therapy in intensive care unit
patients with severe sepsis and septic shock -a systematic review and meta-analysis. Crit Care.
2013;17(6):R291.
Reinhart K, Bauer M, Riedemann NC, Hartog CS. New approaches to sepsis: molecular diagnostics and
biomarkers. Clin Microbiol Rev. 2012;25(4):609-34.
Schuetz P, Müller B, Christ-Crain M, Stolz D, Tamm M, Bouadma L, et al. Procalcitonin to initiate or
discontinue antibiotics in acute respiratory tract infections. Cochrane Database of Systematic Reviews.
2012;9:CD007498. doi: 10.1002/14651858.CD007498.pub2.
Singer M, Deutschman CS, Seymour CW, Shankar-Hari M, Annane D, Bauer M, et al. The Third
International Consensus Definitions for Sepsis and Septic Shock (Sepsis-3). JAMA. 2016;315(8):801-
10.
Vázquez-Grande G, Kumar A. Optimizing antimicrobial therapy of sepsis and septic shock: focus on
antibiotic combination therapy. Semin Respir Crit Care Med. 2015;36(1):154-66.
Vincent JL, De Backer D. Circulatory Shock. N Engl J Med. 2013;369:1726-34.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [552]
[37] ENDOCARDITIS INFECCIOSA. INFECCIONES ENDOVASCULARES Y FUNGEMIA
37.Endocarditis infecciosa. Infecciones endovasculares
y fungemia
Elena Arranz Canales.
Medicina Interna
Cristina Castillo Maza.
Medicina Interna
Asesor: Francisco López Medrano. Médico Adjunto de la Unidad de Enfermedades Infecciosas
I. ENDOCARDITIS
1. CONCEPTO
La endocarditis infecciosa (EI) se define como la infección de la superficie endocárdica del corazón,
sus válvulas y de los grandes vasos intratorácicos. Este término también incluye la infección de los
dispositivos intracardiacos. La EI tiene una incidencia estimada de 3-7 casos por 100.000 personas/año, con
una afectación cada vez más frecuente de pacientes con edad avanzada. A pesar de los avances en el
tratamiento médico y quirúrgico, la morbimortalidad de estos pacientes continúa siendo elevada.
Tabla I. Factores epidemiológicos asociados a determinados patógenos.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [553]
[37] ENDOCARDITIS INFECCIOSA. INFECCIONES ENDOVASCULARES Y FUNGEMIA
La historia natural de la enfermedad consiste en la adhesión bacteriana al endotelio, su
proliferación y la formación de vegetaciones típicamente sobre acumulaciones previas de plaquetas y
fibrina. Dichas vegetaciones se asientan sobre zonas dañadas del endotelio, aunque bacterias muy
agresivas (como Staphylococcus aureus), pueden producir endocarditis sobre un endotelio previamente
sano.
2. ETIOLOGÍA
En síntesis, los estreptococos son los microorganismos más frecuentemente implicados en las EI
adquiridas en la comunidad y en las infecciones protésicas tardías, mientras que en las EI nosocomiales o
relacionadas con los cuidados sanitarios, así como en las infecciones protésicas precoces, el
microorganismo causante más común es S. aureus. Sin embargo, la etiología de la endocarditis infecciosa es
variable, dependiendo de varios factores que quedan resumidos en la tabla I.
3. CLÍNICA
Según la localización de la lesión (cavidades izquierdas o derechas), la naturaleza de la válvula
(nativa o protésica) y la agresividad del microorganismo (S. aureus u otro), la clínica es variable. Las
situaciones clínicas en las que hay que sospechar endocarditis aguda se resumen en la tabla II.
Tabla II. Cuándo sospechar endocarditis infecciosa.
La manifestación clínica más frecuente es la fiebre (hasta el 90% de los pacientes la presentan). A
menudo se asocia a anorexia, pérdida de peso, astenia intensa y sudoración nocturna (sobre todo en EI
subaguda), lo que puede hacer confundir el cuadro con un proceso neoplásico. La fiebre puede estar
ausente en pacientes ancianos o en inmunodeprimidos, así como en casos de insuficiencia cardiaca,
insuficiencia renal, enfermedad terminal, tratamiento antibiótico y con algunos microorganismos poco
agresivos. Los soplos cardiacos están presentes hasta en el 85% de los pacientes pero es un dato muy
inespecífico.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [554]
[37] ENDOCARDITIS INFECCIOSA. INFECCIONES ENDOVASCULARES Y FUNGEMIA
Los signos periféricos clásicos son cada vez menos comunes porque el diagnóstico se realiza más
precozmente. Aquellos mediados inmunológicamente y por microembolias son: petequias cutáneas o
conjuntivales, hemorragias «en astilla» subungueales, manchas de Janeway en palmas y plantas, manchas
de Roth en la retina (generalmente cerca del disco óptico) y nódulos de Osler en los pulpejos de los dedos
(en ocasiones al puncionarlos se puede cultivar el microorganismo responsable). Estos signos son más
típicos de las endocarditis subagudas y en las que se afecta a las válvulas del lado izquierdo. No son
exclusivas de la EI, pues pueden aparecer también en el Lupus Eritematoso Sistémico (LES), endocarditis
trombótica no bacteriana, anemia hemolítica y en la infección gonocócica. Asimismo, el debut clínico de
una EI puede deberse a las complicaciones asociadas (ver Apartado 7).
4. DIAGNÓSTICO
El diagnóstico se establece fundamentalmente basado en las manifestaciones clínicas, los
resultados de hemocultivos (HC) y la ecocardiografía.
Hemocultivos
Son imprescindibles para el diagnóstico microbiológico, aunque en un 5-10% de los casos son
estériles. En la EI, la bacteriemia es casi constante, lo que implica que el rendimiento de los HC
no es mayor en los picos febriles que fuera de estos. El aislamiento de bacterias en una sola
botella de hemocultivo debe ser valorada detenidamente antes de asumir el diagnóstico de EI,
sobre todo, si el microorganismo aislado es un potencial contaminante, como la flora saprofita
de la piel (estafilococos coagulasa-negativos (ECN) o Corynebacterium).
Extracción de hemocultivos: deben obtenerse 3 juegos de HC (10 ml de sangre en cada
juego) con un intervalo de 30 minutos (según las guías europeas) entre cada uno de
ellos y, preferiblemente, no de catéteres endovasculares (por el riesgo de
contaminación). A continuación, se debe iniciar tratamiento antibiótico empírico.
Pruebas de laboratorio
En las endocarditis subagudas pueden aparecer alteraciones inespecíficas como anemia de
trastornos crónicos, elevación de la proteína C reactiva o velocidad de sedimentación globular
(VSG), leucocitosis moderada con desviación izquierda, trombopenia,
hipergammaglobulinemia, factor reumatoide positivo o presencia de crioglobulinas séricas,
insuficiencia renal, hematuria o proteinuria.
Radiografía de tórax
Se deben buscar datos de insuficiencia cardiaca y dilatación de cavidades cardiacas secundarias
a la valvulopatía y, en el caso de los UDVP con sospecha de EI de cavidades derechas, la
presencia de embolismo séptico pulmonar (nódulos múltiples de pequeño tamaño y
habitualmente periféricos que pueden cavitarse).
Electrocardiograma
La EI no suele producir alteraciones electrocardiográficas aunque es importante la realización
de un electrocardiograma (ECG) basal para detectar las posibles alteraciones posteriores (por
ejemplo, la aparición de trastornos de la conducción cardiaca, especialmente el bloqueo
auriculoventricular, que sugiere la presencia de un absceso miocárdico con un valor predictivo
positivo del 88%). Asimismo, la aparición de alteraciones sugerentes de isquemia puede reflejar
la existencia de embolismos en las arterias coronarias. Se recomienda la realización de un ECG
diario en las dos primeras semanas, sobre todo, si la afectación es de la válvula aórtica.
Ecocardiograma
Es una prueba fundamental para el diagnóstico y abordaje de los pacientes con EI y debe
realizarse en todos los casos en que se sospeche. La realización de ecocardiograma
transtorácico (ETT) o transesofágico (ETE) depende del tipo de paciente y la situación clínica
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [555]
[37] ENDOCARDITIS INFECCIOSA. INFECCIONES ENDOVASCULARES Y FUNGEMIA
(Figura 1). El ETE es especialmente apropiado para evaluar las válvulas protésicas y los cables de
marcapasos, desfibriladores implantables y resincronizadores, así como la detección precoz de
complicaciones locales y necesidad de cirugía. El ETE es más sensible que el ETT para la
detección de EI, por tanto, debe solicitarse cuando el ETT resulta negativo, pero la sospecha
clínica de endocarditis es alta.
Situaciones especiales:
Falsos negativos: si las vegetaciones son muy pequeñas (< 2 mm) o ya han
embolizado.
Falsos positivos: vegetaciones trombóticas no infecciosas, como en la
endocarditis de Libman-Sacks (lupus eritematoso sistémico), fiebre reumática
aguda, estados de hipercoagulabilidad (síndrome antifosfolípido y
anticoagulante lúpico), neoplasias (endocarditis marántica) y mixoma auricular.
Debe repetirse un ETT una vez finalizada la terapia antimicrobiana para detectar cambios residuales
en las estructuras intracardiacas.
Figura 1. Indicaciones de la ecocardiografía en la sospecha de endocarditis infecciosa.
Criterios de Duke
El diagnóstico de certeza solo se establece cuando las vegetaciones o el material obtenido de
una arteria (émbolos) en la cirugía cardiaca o en la necropsia se someten a un estudio
histológico y microbiológico. Como esto no es factible en la mayoría de los pacientes, se
propusieron los Criterios de la Universidad de Duke, que se consideran de referencia para el
diagnóstico de EI (Tabla III). Combinan criterios clínicos, microbiológicos y ecocardiográficos,
alcanzando una sensibilidad del 80%.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [556]
[37] ENDOCARDITIS INFECCIOSA. INFECCIONES ENDOVASCULARES Y FUNGEMIA
En las guías de 2015 de la European Society of Cardiology (ESC) se añaden a los criterios mayores de
Duke los hallazgos obtenidos con nuevas técnicas de imagen, especificados en la tabla III. De este modo,
cuando el diagnóstico de EI se establece en función de estos criterios clásicos como “posible” o
“improbable” (pero persiste un alto nivel de sospecha clínica) se debe repetir el ecocardiograma y los
hemocultivos, así como realizar pruebas que demuestren la afectación perivalvular (tomografía
computarizada [TC], tomografía por emisión de positrones [PET] o tomografía de emisión por fotón único
con leucocitos marcados) o pruebas para descartar la existencia de eventos embólicos (resonancia
magnética cerebral [RM], tomografía de cuerpo entero o PET).
Tabla III. Criterios de Duke modificados para el diagnóstico de la endocarditis infecciosa.
5. PRONÓSTICO
La tasa de mortalidad hospitalaria de pacientes con EI oscila entre el 15% y el 30%. La identificación
rápida de los pacientes con mayor riesgo permite mejorar la estrategia diagnóstico-terapéutica y cambiar el
curso de la enfermedad. Los factores de mal pronóstico se detallan en la tabla IV.
6. TRATAMIENTO
6.1. Principios generales
El tratamiento de la EI se basa en el uso de antibióticos bactericidas de manera prolongada para asegurar la
eliminación de los microorganismos con lento crecimiento que persisten en las vegetaciones y el biofilm de
válvulas protésicas y dispositivos intravasculares. En el caso de realizar un tratamiento combinado, ambos
antibióticos deben administrarse de forma simultánea para mejorar el efecto sinérgico. El tiempo de
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [557]
[37] ENDOCARDITIS INFECCIOSA. INFECCIONES ENDOVASCULARES Y FUNGEMIA
tratamiento antibiótico se contabiliza a partir del primer día de tratamiento efectivo (primeros
hemocultivos negativos).
Tabla IV. Indicadores de mal pronóstico en pacientes con endocarditis infecciosa.
Si se realiza recambio valvular y el cultivo de la muestra quirúrgica resulta positivo, se considera el
primer día de tratamiento efectivo el de la cirugía. El tratamiento en EI sobre válvula protésica es más largo
(6 semanas) que sobre nativa. Si la válvula nativa precisa recambio valvular, la duración del tratamiento
debe ser el recomendado para EI sobre válvula nativa.
6.2. Tratamiento empírico
Se debe iniciar de inmediato tras la toma de hemocultivos. Además del tipo de válvula, es necesario tener
en cuenta las características del paciente, la antibioterapia previa recibida, lugar de adquisición
(comunitaria, nosocomial o asociado a cuidados sanitarios), así como la epidemiología local, especialmente
el riesgo de resistencia a antibióticos.
Las pautas recomendadas como tratamiento empírico están basadas en un bajo nivel de evidencia,
por lo que se deben consultar con la unidad especializada de forma precoz para la elección de la
antibioterapia empírica más apropiada. La endocarditis sobre válvula natural y la infección tardía sobre
válvula protésica adquirida en la comunidad pueden tratarse con la asociación de cloxacilina 2 g/4 h iv,
ampicilina 2 g/4 h y gentamicina 3 mg/kg/día intravenoso (iv). En caso de riesgo de infección por SARM
(UDVP, infección relacionada con cuidados sanitarios) o de infección por ECN (válvula protésica) puede
emplearse la asociación de daptomicina 10 mg/kg/día iv con cloxacilina 2 g/4 h iv. En los pacientes alérgicos
a penicilinas, daptomicina puede asociarse a fosfomicina 4 g/8 h iv o a gentamicina 3 mg/kg/día iv.
Una vez identificado el microorganismo responsable de la EI, el tratamiento antimicrobiano debe
adaptarse.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [558]
[37] ENDOCARDITIS INFECCIOSA. INFECCIONES ENDOVASCULARES Y FUNGEMIA
6.3. Tratamiento específico según el microorganismo responsable
Las pautas recomendadas para los microorganismos más frecuentes se recogen en la tabla V.
Tabla V. Tratamiento dirigido según el microorganismo aislado.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [559]
[37] ENDOCARDITIS INFECCIOSA. INFECCIONES ENDOVASCULARES Y FUNGEMIA
6.4. Tratamiento parenteral ambulatorio
Para poder llevarlo a cabo y tener un seguimiento estrecho de estos pacientes, es esencial su realización en
unidades especializadas con personal sanitario instruido.
6.5. Anticoagulación y antiagregación
Las recomendaciones para el manejo de la anticoagulación en pacientes con EI están basadas en un bajo
nivel de evidencia, y las decisiones deberían realizarse de forma individualizada por el equipo de EI
especializado. El papel de la terapia puente con heparina no fraccionada o de bajo peso molecular no ha
sido estudiado en pacientes con EI, pero puede tener ventajas razonables en situaciones especiales (como
paciente inestable) antes de una cirugía o para evitar interacciones farmacológicas.
6.6. Indicaciones de cirugía
Como parte del abordaje multidisciplinar, si es posible, se debe consultar todo caso de EI con un Servicio de
Cirugía Cardiaca, dado que sus complicaciones precisan tratamiento quirúrgico en aproximadamente la
mitad de los pacientes. En el caso de pacientes con EI complicada se recomienda remitir precozmente a
centros de referencia con Cirugía Cardiaca. Las indicaciones de cirugía se detallan en la tabla VI.
Tabla VI. Indicaciones para la cirugía en la endocarditis infecciosa.
7. COMPLICACIONES DE LA ENDOCARDITIS INFECCIOSA
7.1. Cardiacas
7.1.1. Insuficiencia cardiaca (42-60%)
Es la complicación más frecuente y es la principal causa de mortalidad. Además, es la principal indicación de
cirugía. En la EI sobre válvula nativa, la insuficiencia cardiaca se produce más frecuentemente cuando
afecta a válvula aórtica. En la mayoría de los casos es consecuencia de la insuficiencia valvular.
El ecocardiograma es de crucial importancia para la evaluación inicial, diagnóstico etiológico (rotura
de cuerda tendinosa, obstrucción por vegetación, rotura o perforación de una valva, fístula cardiaca) y
seguimiento. La medición de la fracción N-terminal del propéptido natriurético de tipo B (NT-proBNP) es
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [560]
[37] ENDOCARDITIS INFECCIOSA. INFECCIONES ENDOVASCULARES Y FUNGEMIA
útil en el diagnóstico y monitorización de la insuficiencia cardiaca. Niveles elevados de NT-proBNP y
troponinas se asocian con mal pronóstico.
7.1.2. Extensión perivalvular
Es la causa más frecuente de infección no controlada y es un signo de mal pronóstico. En una alta
proporción necesitan cirugía. Se produce, sobre todo, cuando afecta a válvula aórtica y es más frecuente en
la EI sobre válvula protésica (56-100%) que sobre válvula nativa (10-40%). Se debe sospechar ante
bacteriemia o fiebre persistente o cuando aparece bloqueo A-V en el ECG.
La ETE es la técnica de elección para el diagnóstico y el seguimiento de todas las complicaciones
perivalvulares. Actualmente, sería de utilidad el PET-TC multicorte.
7.1.3. Otras complicaciones cardiacas son: infarto de miocardio, pericarditis o miocarditis.
7.2. Extracardiacas
7.2.1. Embolismos (20-50%)
El cerebro (65% y de ellos, más del 90% afecta al territorio de la arteria cerebral media) y el bazo son las
ubicaciones más comunes en la EI izquierda, mientras que la embolia pulmonar puede ocurrir en la EI
derecha o EI sobre marcapasos. Los eventos embólicos pueden ser totalmente asintomáticos (hasta un 20-
50%) y el riesgo de repetición es del 6-21%.
Las complicaciones neurológicas (15-30%) se asocian a elevadas morbilidad y mortalidad. El
ecocardiograma es la prueba de elección para predecir los eventos embólicos. Los factores que indican
mayor riesgo de embolia son: el organismo causal (S. aureus, Candida, bacterias del grupo HACEK), el
tamaño y la morfología de las vegetaciones (tamaño mayor de 1 cm y altamente móviles), la válvula
implicada (mitral, multivalvular), un embolismo previo y la precocidad del tratamiento antibiótico (el riesgo
de una nueva embolia es mayor durante los primeros días después de haber comenzado la terapia
antibiótica y posteriormente disminuye rápidamente, en especial transcurridas 2 semanas desde el inicio
del tratamiento aunque el riesgo persiste mientras las vegetaciones continúen presentes).
El diagnóstico de EI e inicio de tratamiento adecuado precoz es la mejor forma de prevenir esta
complicación. Si existe indicación de cirugía, no debe ser retrasada por complicaciones neurológicas una
vez que se ha descartado que estas sean graves (coma, infarto cerebral extenso o hemorragia intracraneal).
No es una contraindicación de cirugía la presencia de microhemorragias cerebrales.
7.2.2. Abscesos viscerales
Son raros, frecuentemente asintomáticos y se producen por émbolos sépticos o por sobreinfección de
infarto visceral previo. El lugar de afectación más frecuente es el bazo y, en el caso de EI derecha, los
pulmones. Producen bacteriemia o fiebre persistente o recurrente, junto con síntomas locales. Las
bacterias más frecuentemente implicadas son S. aureus y estreptococosorales. Responden mal al
tratamiento antibiótico y puede ser necesaria la cirugía o el drenaje percutáneo, según su localización y
comorbilidades del paciente. Preferiblemente el drenaje del absceso se debe realizar antes de la cirugía
valvular.
7.2.3. Aneurismas micóticos
Los aneurismas infecciosos (micóticos, porque su forma recuerda a una seta, no porque estén producidos
por hongos) son secundarios a embolismos arteriales. Frecuentemente son producidos por estreptococo
(50%) y S. aureus (10%). Los aneurismas intracraneales son los más comunes, con alta morbilidad y
mortalidad (60%). Pueden ser clínicamente silentes o producir sintomatología variada (cefalea grave,
déficits neurológicos focales, crisis epilépticas, meningismo…). Su complicación más grave es la hemorragia.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [561]
[37] ENDOCARDITIS INFECCIOSA. INFECCIONES ENDOVASCULARES Y FUNGEMIA
Si existe clínica neurológica o hallazgos sugerentes en TC craneal, se debe solicitar angio-TC, angio-RM o
angiografía para su diagnóstico.
Los aneurismas micóticos viscerales, en cambio, suelen ser asintomáticos hasta su rotura. Algunos
se resuelven con el tratamiento antibiótico, pero otros precisarán cirugía o tratamiento endovascular. Se
debe realizar seguimiento mediante pruebas de imagen durante el tratamiento.
7.2.4. Insuficiencia renal aguda
Es una complicación común (6-30%) y predice mal pronóstico. Las causas suelen ser multifactoriales:
glomerulonefritis, infarto renal secundario a embolismo, hipoperfusión renal secundaria a insuficiencia
cardiaca, sepsis grave o shock cardiogénico tras la cirugía cardiaca, toxicidad antibiótica (especialmente,
aminoglucósidos, vancomicina) o por agentes de contraste utilizados para las pruebas de imagen.
7.2.5. Complicaciones reumáticas
Los síntomas musculoesqueléticos (artralgias, mialgias) son frecuentes durante la EI y las complicaciones
reumáticas pueden ser las primeras manifestaciones de la enfermedad.
La artritis periférica ocurre en un 14% y la espondilodiscitis en un 1,8-15% de los casos. Se debe
realizar RM o TC en pacientes con EI y dolor sugestivo de afectación vertebral. También hay que sospechar
el origen hematógeno de una artritis séptica cuando exista afectación de varias articulaciones
simultáneamente, predomine en articulaciones axiales (sacroilíacas, esternón…) y se cultiven en el aspirado
microorganismos frecuentemente implicados en EI (estafilococos), sobre todo, si no hay antecedente de
traumatismo o cirugía articular reciente que lo justifique. Asimismo, se debe practicar una ecocardiografía
en pacientes con un diagnóstico definitivo de espondilodiscitis piógena para descartar que el origen sea una
EI con embolia séptica vertebral.
8. SEGUIMIENTO
La fiebre puede mantenerse días después de iniciar el tratamiento antibiótico adecuado. La
persistencia de la fiebre más allá de 7-10 días puede relacionarse con tratamiento antibiótico inadecuado,
microorganismos resistentes al tratamiento antibiótico pautado, flebitis, complicaciones locales o
embólicas de EI, infección nosocomial o fiebre medicamentosa. En el abordaje de la fiebre persistente en la
EI se debe realizar cambio de catéteres de acceso venoso, repetición de determinaciones analíticas,
hemocultivos, ecocardiograma y búsqueda de focos infecciosos no controlados intra y extracardiacos. Los
hemocultivos deben repetirse cada 24-48 horas hasta su negativización.
Dado que algunos pacientes reciben tratamiento prolongado con aminoglucósidos, se deberán
monitorizar los niveles plasmáticos de estos antibióticos semanalmente para disminuir el riesgo de
toxicidad. La concentración de gentamicina en valle debe ser menor de 1 mg/l y en pico de 10-12 mg/l.
Todos los pacientes que han presentado un episodio de EI tienen riesgo elevado de recurrencia (2-
6%). Por eso es importante conocer la situación basal en cuanto a la morfología y función valvular,
existencia de vegetaciones y la función ventricular una vez resuelto el cuadro agudo. Para ello está indicada
la realización de un ecocardiograma al finalizar el tratamiento (se debe realizar a los 2, 4 y 8 meses en caso
de afectación perivalvular). Hay que tener en cuenta que la resolución clínica de la EI es más rápida que la
ecocardiográfica, de modo que la persistencia de vegetaciones no es sinónimo de fracaso terapéutico.
En el momento del alta hospitalaria, los pacientes deben ser informados del riesgo de recurrencia y
educados acerca de los signos de alarma (presencia de fiebre, escalofríos u otros signos de infección), así
como de la importancia de prevenir nuevos episodios con la profilaxis antibiótica en situaciones
determinadas (ver Apartado 10) y el mantenimiento de la higiene bucal (revisiones odontológicas
frecuentes) y cutánea (no realización de tatuajes ni piercing).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [562]
[37] ENDOCARDITIS INFECCIOSA. INFECCIONES ENDOVASCULARES Y FUNGEMIA
9. SITUACIONES ESPECIALES
9.1. Dispositivos intracardiacos no valvulares
El aumento del número de pacientes con dispositivos intracardiacos no valvulares (DCNV), marcapasos y
desfibriladores implantables, justifica que cada vez se registren más casos de EI asociada a ellos. Se
distingue entre infección local del reservorio (con signos inflamatorios locales en la bolsa subcutánea del
dispositivo como eritema, dehiscencia de cicatriz, dolor, fluctuación o drenaje purulento) y EI asociada a
DCNV (la infección asienta sobre los electrodos). El principal mecanismo es la contaminación por flora
cutánea en el momento de la implantación, aunque también habría que considerar la infección secundaria
a bacteriemia de un foco infeccioso a otro nivel.
Los factores de riesgo para desarrollarla son insuficiencia renal, empleo de corticoides o
anticoagulantes, insuficiencia cardiaca, formación de hematoma en el sitio de implantación del dispositivo,
diabetes y características del procedimiento (tipo de intervención, uso de profilaxis preoperatoria, fiebre
perioperatoria, experiencia del equipo que implanta el dispositivo). Los microorganismos más frecuentes
(60-80%) son los estafilococos (sobre todo, los coagulasa negativos) y S. aureus.
Se debe sospechar en paciente portador de DCNV con fiebre, síntomas respiratorios (por la
existencia de embolismos pulmonares), reumatológicos, así como cuando se aprecien signos locales de
infección. Ante la sospecha de este tipo de EI, se debe remitir al paciente a una unidad especializada. El
tratamiento se basa en la extracción del DCNV y la administración de antibiótico (según las
recomendaciones recogidas en la tabla V) durante 4-6 semanas.
La prevención de este tipo de infecciones consiste en asegurar que el paciente esté libre de
infección al menos las 2 semanas previas de la implantación de DCNV (a excepción de implantación
urgente) y en la administración de profilaxis antibiótica antes de su colocación con cefazolina o
vancomicina (en el caso de centros con prevalencia de SAOR elevada).
9.2. Endocarditis de cavidades derechas (5-10%)
Esta situación es más frecuentemente observada en pacientes UDVP, sobre todo, con infección
concomitante por virus de la inmunodeficiencia humana (VIH) o inmunosupresión. La válvula tricúspide es
la más frecuentemente afectada.
La forma de presentación es con fiebre elevada y clínica secundaria a embolismo séptico pulmonar
múltiple. El microorganismo más frecuente es S. aureus (60-90%). Otros son Pseudomonas aeruginosa,
otros BGN, Candida e incluso polimicrobianas.
El diagnóstico suele ser posible mediante ETT. El pronóstico es generalmente bueno. En ocasiones,
en pacientes UDVP que rechazan el ingreso para la realización de tratamiento estándar, no presentan
complicaciones y el microorganismo involucrado es S. aureus sensible a oxacilina (SAOS) se puede plantear
una pauta oral con ciprofloxacino (750 mg cada 12 horas) y rifampicina (300 mg cada 12 horas). Para otros
microorganismos distintos al SAOS, el tra tamiento y su duración son iguales que en la endocarditis de
cavidades izquierdas. Se ha aprobado la daptomicina para EI derecha por SAOR y es de elección si la
concentración mínima inhibitoria (CMI) a vancomicina es mayor a 1 mg/l. Dada la alta probabilidad de
recurrencia, sobre todo, debido a la continuidad de consumo de drogas de abuso, la cirugía no suele
indicarse en EI derecha en UDVP.
9.3. Endocarditis infecciosa con hemocultivos negativos
Los HC pueden ser negativos hasta en un 5-10% de los pacientes con diagnóstico establecido de
endocarditis. Las causas más frecuentes son el uso previo de antibióticos, microorganismos no frecuentes y
causas no infecciosas. Para mantener un tratamiento empírico hay que considerar las características
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [563]
[37] ENDOCARDITIS INFECCIOSA. INFECCIONES ENDOVASCULARES Y FUNGEMIA
epidemiológicas y clínicas al igual que al iniciarlo para cubrir los microorganismos más probables (Tabla I).
El diagnóstico y tratamiento de EI con HC negativos se resumen en la tabla VII.
Tabla VII. Endocarditis infecciosa con hemocultivos negativos.
9.4. Endocarditis trombótica no bacteriana
Está asociada con numerosas enfermedades como neoplasias, conectivopatías, enfermedades
autoinmunes, VIH y estados de hipercoagulabilidad. Es muy difícil diferenciar este proceso de EI con
cultivos negativos en la que se ha recibido antibioterapia previa. Se basa en la sospecha clínica, el resultado
negativo de los HC, así como en la EI sin respuesta a la antibioterapia empírica para los microorganismos
más frecuentes. Afecta normalmente a las cavidades izquierdas (mitral más que aórtica), pero las
vegetaciones suelen ser más pequeñas y presenta una afectación bilateral en mayor proporción que la EI. El
ETE es más sensible para el diagnóstico.
9.5. Endocarditis fúngica
Es más frecuentemente observada sobre válvula protésica, en endocarditis en pacientes UDVP y en
pacientes inmunocomprometidos. Candida spp es la etiología más frecuente. Una importante complicación
son los fenómenos de embolia. El diagnóstico microbiológico se realiza mediante HC de repetición o PCR
sobre el material extraído quirúrgicamente. La mortalidad es muy elevada (> 50%) y presentan un riesgo
elevado de recurrencias. Para el tratamiento específico de este tipo de endocarditis se debe remitir al
paciente a un equipo especializado.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [564]
[37] ENDOCARDITIS INFECCIOSA. INFECCIONES ENDOVASCULARES Y FUNGEMIA
10. PROFILAXIS
Las guías de la ESC mantienen la restricción en la indicación de profilaxis antibiótica solo a los
pacientes con muy alto riesgo de adquirir EI (Tabla VIII).
Actualmente la profilaxis está limitada solo a los procesos dentales que precisan la manipulación de
la región gingival o periapical de los dientes o la perforación de la mucosa oral. Esta se realizará con una
sola dosis, 30-60 minutos antes del procedimiento, de amoxicilina o ampicilina 2g vía oral (vo) o en
alérgicos a penicilinas con clindamicina 600 mg vo. La medida de prevención con mayor impacto para la
población general es concienciar a los pacientes de la importancia del mantenimiento de una buena higiene
oral y de la piel y en el “empleo cuidadoso” de catéteres por parte del personal sanitario.
Tabla VIII. Profilaxis de la endocarditis infecciosa: pacientes de alto riesgo.
II. INFECCIONES ENDOVASCULARES
1. CONCEPTO
El desarrollo de las técnicas quirúrgicas y del intervencionismo radiológico ha supuesto una
revolución para el abordaje de la enfermedad arterial y, por lo tanto, el número de pacientes portadores de
prótesis vasculares ha experimentado un importante incremento. Se define como infección endovascular a
aquella que afecta a las prótesis endovasculares aórticas o arteriales periféricas y al bypass axilo-femoral.
La infección de la prótesis es la complicación más grave de estos procedimientos y tiene una mortalidad del
10-25% al mes y del 50% al año, así como un riesgo de amputación de extremidades del 4-14%. Los factores
asociados a infección endovascular se describen en la tabla IX.
Tabla IX. Factores de riesgo de infección de prótesis endovascular.
2. ETIOLOGÍA
La adquisición de la infección se produce con mayor frecuencia en el momento de la intervención.
La infección se puede desarrollar de forma precoz, habitualmente en los primeros días, y el microorganismo
más frecuentemente implicado es S. aureus; o de forma tardía, por micro- organismos más indolentes
como SCN. En algunos casos se puede adquirir por vía hematógena, en el contexto de una bacteriemia
desde un foco infeccioso a distancia.
Otras formas de adquisición son por contigüidad por una infección periprótesis o por formación de
fístulas en comunicación con cavidad intestinal principalmente. La etiología de las infecciones de prótesis
endovasculares son: S. aureus (20-53%), enterobacterias (14-41%), SCN (15%), Pseudomonas aeruginosa,
estreptococos sp y enterococos sp (10-15%), infección polimicrobiana (20%), bacterias anaerobias
facultativas (5%) y fúngica (1-2%).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [565]
[37] ENDOCARDITIS INFECCIOSA. INFECCIONES ENDOVASCULARES Y FUNGEMIA
3. CLÍNICA
La clínica que presentan estos pacientes consiste en síntomas sistémicos como fiebre, deterioro del
estado general, así como la presencia de leucocitosis.
Estos síntomas suelen estar ausentes en las infecciones crónicas. Los pacientes pueden presentar
isquemia aguda de las extremidades en relación con émbolos sépticos desde la prótesis. Los síntomas
locales dependen de la localización de la infección: dolor abdominal, hemorragia digestiva o hemoptisis
secundarias a formación de fístulas aorto-entéricas o aorto-bronquiales, y si sucede afectación local a nivel
de las extremidades, se pueden manifestar mediante equimosis, dehiscencia de la herida quirúrgica o
impotencia funcional de dicha extremidad.
4. DIAGNÓSTICO
El diagnóstico de las infecciones endovasculares consiste en la sospecha clínica, el aislamiento en
HC de microorganismos implicados habitualmente con este tipo de infecciones y la realización de pruebas
de imagen que demuestren dicha infección. El algoritmo diagnóstico queda resumido en la figura 2. Es de
gran importancia el diagnóstico microbiológico para el ajuste posterior de la antibioterapia, por lo que se
debe realizar punción aspiración de aguja fina (PAAF) de colecciones periprotésicas siempre que sea
posible, y cultivo de muestras tomadas durante la cirugía.
Figura 2. Algoritmo diagnóstico ante sospecha de infección de prótesis vascular.
5. TRATAMIENTO
El tratamiento empírico (Tabla X) consiste en antibioterapia eficaz sobre los microorganismos
causantes más frecuentes, así como sobre el biofilm desarrollado sobre la prótesis vascular.
El tratamiento antibiótico empírico solo estará indicado previo a la cirugía en los casos en que la
gravedad e inestabilidad hemodinámica lo exijan. Tras la cirugía, la antibioterapia debe ser ajustada a los
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [566]
[37] ENDOCARDITIS INFECCIOSA. INFECCIONES ENDOVASCULARES Y FUNGEMIA
resultados microbiológicos. Es imprescindible que el paciente sea valorado por un equipo de Cirugía
Vascular con experiencia en el abordaje de este tipo de infecciones, ya que el recambio protésico está
indicado en todos los casos en que sea posible.
La profilaxis mediante la administración de antibioterapia en las primeras 24 horas del
procedimiento en pacientes que van a ser sometidos a cirugía de reconstrucción vascular es la única
medida que ha demostrado efectividad.
Tabla X. Tratamiento empírico de las infecciones endovasculares.
III. CANDIDEMIA
1. INTRODUCCIÓN
Dentro de las infecciones en el hombre causadas por Candida ssp, la candidemia es una de las más
frecuentes en pacientes hospitalizados o críticamente enfermos. Se trata por ello de una entidad con
especial gravedad y que suele tener alta tasa de mortalidad a pesar del tratamiento.
En cuanto a la etiología, existen al menos 15 especies distintas de Candida ssp, pero cerca del 90%
de las infecciones documentadas en el hombre están causadas por C. albicans, C. glabrata, C. tropicalis, C.
parapsilosis y C. krusei. La más frecuente sigue siendo C. albicans (50%), sin embargo, en la actualidad se
está produciendo un aumento de las infecciones producidas por C. parapsilosis y C. glabrata. Otro aspecto
a tener en cuenta, y que empieza a ser un problema global, es la aparición de especies resistentes a los
antifúngicos convencionales.
2. FACTORES DE RIESGO
Se relaciona de forma importante con los cuidados sanitarios (principalmente con la estancia en
Unidades de Cuidados Intensivos y el uso de catéteres intravenosos). Otros factores relacionados vienen
resumidos en la tabla XI.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [567]
[37] ENDOCARDITIS INFECCIOSA. INFECCIONES ENDOVASCULARES Y FUNGEMIA
Tabla XI. Factores de riesgo de candidemia.
3. MANIFESTACIONES CLÍNICAS
En la mayoría de los pacientes con candidemia, la fiebre es el único signo evidente. Se debe realizar
una exploración física completa, incluyendo la inspección cuidadosa de piel y mucosas (aunque es raro,
pueden aparecer lesiones en dichas localizaciones como expresión de la diseminación hematógena). Hay
que sospecharla en todo paciente que presente los factores de riesgo que se han comentado
anteriormente (Tabla XI).
La afectación ocular es muy rara, pero existen casos de coriorretinitis, endoftalmitis y afectación
orbitaria. Se recomienda, por tanto, realizar una exploración oftalmoscópica en la primera semana del
diagnóstico en todos los pacientes. En los pacientes con recuento de neutrófilos < 500 células/ml hay que
diferirla una semana tras la recuperación de la neutropenia.
4. DIAGNÓSTICO
El diagnóstico se realiza mediante métodos directos (aislamiento del microorganismo en
hemocultivos), que constituyen el gold standard. Su sensibilidad ronda el 50% y pueden tardar más de 7
días en positivizar.
Existen métodos indirectos (determinación de antígenos, anticuerpos y de 1,3-beta-D-glucano en
sangre, así como la realización de la reacción en cadena de la polimerasa –PCR–), cuya realización no está
estandarizada en la práctica clínica actual.
Independientemente del resultado de estas pruebas, la existencia de una sospecha clínica elevada
en un paciente con factores de riesgo para candidemia debe ser suficiente para el inicio de tratamiento
empírico específico.
5. TRATAMIENTO
El tratamiento empírico de primera elección en este tipo de infecciones es una equinocandina.
Como excepción, en los pacientes con afectación del sistema nervioso central u oftalmológica
concomitante, se prefiere el uso de fluconazol, ya que las equinocandinas penetran mal en dichos tejidos.
Está indicada la administración de anfotericina B liposomal en caso de resistencia, intolerancia o ausencia
de disponibilidad de los otros antifúngicos. Los antifúngicos y sus dosis se sintetizan en la tabla XII.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [568]
[37] ENDOCARDITIS INFECCIOSA. INFECCIONES ENDOVASCULARES Y FUNGEMIA
Tabla XII. Principales fármacos antifúngicos y dosis recomendadas.
Se deben repetir los HC cada 24-48 horas hasta comprobar la resolución de la candidemia con el
tratamiento.
La duración del tratamiento en todos los casos es de 2 semanas desde la constatación del primer
HC negativo y resolución de los síntomas atribuibles a la candidemia en pacientes sin complicaciones
embólicas. En el caso de pacientes neutropénicos debe mantenerse el tratamiento hasta constatar la
recuperación de la neutropenia.
En el caso de que el paciente evolucione favorablemente, se aísle una especie sensible a fluconazol
y los HC sean negativos de forma repetida tras el inicio del antifúngico, a los 5-7 días se puede completar el
tratamiento por vía oral con fluconazol. Por otro lado, si se aísla C. krusei, el tratamiento para desescalar
será voriconazol.
En pacientes neutropénicos, la restitución de las cifras de neutrófilos ha demostrado mejorar los
resultados del tratamiento, por lo que puede valorarse el uso de factor estimulante de colonias de
granulocitos.
Actitud a seguir en pacientes portadores de catéter venoso central (CVC):
Alrededor del 70% de los casos de candidemia en pacientes no neutropénicos el origen de la
misma está en el CVC. Por tanto, debe retirarse en todos los casos en los que sea posible.
En los pacientes con neutropenia la indicación de retirada no está tan clara, ya que en ellos es
difícil diferenciar si el origen de la infección se encuentra en el CVC o en la afectación del tracto
gastrointestinal y la existencia de mucositis presente en algunos pacientes que reciben
quimioterapia. Debido a ello, la retirada del catéter debe ser considerada de forma individual.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [569]
[37] ENDOCARDITIS INFECCIOSA. INFECCIONES ENDOVASCULARES Y FUNGEMIA
6. PRONÓSTICO
El factor más importante que determina el pronóstico del paciente es iniciar el tratamiento tan
pronto como se sospeche, pues la mortalidad puede alcanzar el 40% si se demora su inicio más de 48 horas.
Otros factores que han demostrado conferir peor pronóstico son la edad avanzada, una puntuación en la
escala Acute Physiology And Chronic Health Evaluation II (APACHE II) elevada y el aislamiento de C.
tropicalis.
7. PROFILAXIS
Aunque se ha ensayado sobre la utilidad de los antifúngicos administrados de forma profiláctica en
pacientes en Unidades de Cuidados Intensivos, su uso no se recomienda de forma sistemática. Lo más
relevante para prevenir su aparición es educar al personal sanitario en la importancia de mantener una
correcta higiene de manos y un adecuado cuidado de los catéteres intravasculares.
BIBLIOGRAFÍA
Baddour LM, Wilson WR, Bayer AS, Fowler VG, Tleyjeh IM, Rybak MJ, et al. Infective Endocarditis in
Adults: Diagnosis, Antimicrobial Therapy, and Management of Complications: A Scientific Statement for
Healthcare Professionals From the American Heart Association. Circulation. 2015;132(15):1435-86.
De Donato G, Setacci F, Galzerano G, Ruzzi U, Borrelli MP, Mazzitelli G, et al. Prosthesis infection:
prevention and treatment. J Cardiovasc Surg, 2014;55:779-92.
Grupo de Trabajo de la Sociedad Europea de Cardiología (ESC) para el manejo de la Endocarditis
Infecciosa. 2015 ESC Guidelines for the management of infective endocarditis. Eur Heart J.
2015;36(44):3075-128.
Kullberg BJ, Arendrup MC. Invasive Candidiasis. N Engl J Med. 2015;373(15):1445-56.
Pappas PG, Kauffman CA, Andes DR, Clancy CJ, Marr KA, Ostrosky-Zeichner L, et al. IDSA Guidelines:
Clinical Practice Guideline for the Management of Candidiasis: 2016 Update by the Infectious Diseases
Society of America. Clin Infect Dis. 2016;62(4):e1-e50.
Revest M, Camou F, Senneville E, Caillon J, Laurent F, Calvet B, et al. Groupe de Rèflexion sur les
Infections de Prothèses vaculaires(GRIP). Medical treatment of prosthetic vascular graft infections:
Review of the literature and proposals of a Working Group. Int J Antimicrob Agents. 2015;46(3):254-
65.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [570]
[38] INFECCIONES DE LAS VÍAS RESPIRATORIAS
38.Infecciones de las vías respiratorias
Olaya Madrid Pascual.
Medicina Interna
Roberto Larrosa Barrero.
Neumología
Asesor: Carlos Álvarez Martínez. Médico Adjunto de Neumología
I. BRONQUITIS AGUDA
1. CONCEPTO Y ETIOLOGÍA
La bronquitis aguda es una patología muy frecuente en Urgencias y Centros de Salud. Se trata de
una inflamación de la mucosa bronquial, generalmente autolimitada. Se considera que la etiología es
infecciosa, pero en menos del 50% de los pacientes se identifica un patógeno, que puede ser tanto un virus
como una bacteria. Muchas veces se produce en el contexto de una infección respiratoria más difusa que
afecta también a la vía aérea superior.
En general, cuando hablamos de bronquitis aguda nos referimos a pacientes sin patología pulmonar
crónica conocida y es importante diferenciarla de las exacerbaciones de bronquitis crónica o de las crisis de
asma bronquial, que pueden tener una presentación similar.
Tabla I. Agentes más frecuentemente implicados en la bronquitis aguda.
2. PRESENTACIÓN CLÍNICA
Los pacientes suelen presentar tos, que puede ser productiva, sibilancias y leve disnea; pueden
presentar febrícula o fiebre. La duración habitual de los síntomas es de una a tres semanas y la resolución
suele ser total pasado este tiempo. En la auscultación podemos encontrar roncus y sibilancias.
El diagnóstico es clínico y la radiografía de tórax está indicada si hay sospecha de neumonía:
taquicardia, taquipnea, fiebre alta, crepitantes o signos de consolidación en la auscultación pulmonar. En
caso de enfermedad previa o edad avanzada hay formas de presentación atípicas, lo que requiere
evaluación individualizada y cuidadosa.
El caso concreto de infección por Bordetella pertussis o tos ferina requiere de alta sospecha clínica
para el diagnóstico, siendo especialmente importante la información epidemiológica. En pacientes adultos
sanos debe sospecharse principalmente si la tos se cronifica; los signos clásicos (paroxismos de tos, estridor
inspiratorio y vómitos postusígenos) tienen un valor diagnóstico solo modesto en esta población. Ante la
sospecha se debe solicitar estudio microbiológico de exudado nasofaríngeo incluida la reacción en cadena
de la polimerasa (PCR) y cultivo. La tos ferina es una enfermedad de declaración obligatoria.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [571]
[38] INFECCIONES DE LAS VÍAS RESPIRATORIAS
La procalcitonina, como marcador específico de infección bacteriana y guía para el tratamiento
antibiótico en las infecciones respiratorias agudas reduce el número de prescripciones antibióticas sin
diferencias en la morbimortalidad, pero todavía se requiere investigación al respecto.
3. TRATAMIENTO
A pesar de la alta frecuencia con que se administran antibióticos en la bronquitis aguda, han
demostrado influir poco en el curso clínico de la enfermedad y no están indicados de forma general
(valoración individualizada en pacientes ancianos y pluripatológicos). Es importante explicar al paciente la
benignidad del cuadro y su resolución esperable en dos o tres semanas.
La principal excepción es la sospecha de infección por B. pertussis. En este supuesto está indicado el
tratamiento con macrólidos (por ejemplo, azitromicina durante 5 días). El tratamiento parece producir
beneficio clínico en el afectado solo en la fase catarral (las primeras dos semanas desde el inicio de la tos
aproximadamente), pero se recomienda el tratamiento antibiótico también ante diagnósticos más tardíos
pues puede disminuir el contagio de la enfermedad. Los regímenes de profilaxis para contactos estrechos
son idénticos al tratamiento estándar.
Es controvertido el uso de broncodilatadores en pacientes sin enfermedad pulmonar subyacente,
pudiendo mejorar los síntomas en algunos pacientes, especialmente si presentan signos de broncoespasmo
en la exploración.
II. NEUMONÍA ADQUIRIDA EN LA COMUNIDAD (NAC) Y NEUMONÍA
ASOCIADA A ENTORNOS SANITARIOS (NAES)
1. DEFINICIONES
1. NEUMONÍA ADQUIRIDA EN LA COMUNIDAD
La neumonía adquirida en la comunidad (NAC) es una enfermedad infecciosa de las vías
respiratorias bajas que afecta al parénquima pulmonar, debida a un microorganismo contraído en el
ámbito extrahospitalario y que se caracteriza habitualmente por síntomas y signos de afectación
respiratoria y sistémica (tos, disnea, expectoración, fiebre…), con evidencia de afectación parenquimatosa
mediante la aparición de infiltrados radiológicos.
2. NEUMONÍA NOSOCOMIAL
Se distinguen tres grandes grupos dentro de la neumonía nosocomial (NN):
2.1. Neumonía asociada a entornos sanitarios o sociosanitaria
La neumonía asociada a entornos sanitarios (NAES) o sociosanitaria es aquella que aparece en pacientes
que han estado hospitalizados más de 48 horas en los 90 días previos, estancia o institucionalización en
residencias u hospitales de cuidados crónicos, receptores de antibióticos habituales o de terapia
intravenosa antibiótica, quimioterapia, diálisis, cura de heridas o Atención Sanitaria Especializada en el
domicilio en los 30 días previos.
Estos pacientes presentan mayores factores de riesgo asociados a patógenos multirresistentes,
especialmente P. aeruginosa por lo que su etiología, pronóstico y manejo en la mayoría de ocasiones está
más relacionado con el resto de NN que con las NAC.
2.2. Neumonía adquirida en el hospital
La neumonía adquirida en el hospital (NAH) se define como aquella de nueva aparición tras 48 horas de
ingreso (ver Capítulo 48. “Infecciones nosocomiales”).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [572]
[38] INFECCIONES DE LAS VÍAS RESPIRATORIAS
2.3. Neumonía asociada a ventilación mecánica
Aquella neumonía que aparece tras 48-72 horas de intubación orotraqueal (ver Capítulo 48. “Infecciones
nosocomiales”) se denomina neumonía asociada a ventilación mecánica (NAVM).
2. ETIOLOGÍA
El aislamiento del microorganismo responsable se alcanza solamente en torno al 10-20% de los
casos. El conocimiento del agente causal es importante para evitar el uso excesivo de antibióticos y sus
efectos adversos, así como para evitar la generación de gérmenes resistentes.
El microorganismo más frecuentemente identificado en general es el Streptococcus pneumoniae.
En aquellos pacientes que requieren ingreso en la Unidad de Cuidados Intensivos (UCI) es frecuente el
hallazgo de S. pneumoniae multirresistente, Legionella spp y Staphylococcus aureus (Tabla II). Existen otros
patógenos, denominados “atípicos” por la mayor dificultad para la obtención de un resultado de forma
rápida, que también causan NAC, como son Mycoplasma pneumoniae, Chlamydophila pneumoniae,
Clamydophila psittaci o Coxiella burnetti.
Tabla II. Agentes causales más frecuentes por gravedad de presentación.
Además de las consideraciones generales epidemiológicas, es necesario tener en cuenta
comorbilidades y factores de riesgo asociados a la presentación clínica. Aunque no existen manifestaciones
específicas para cada agente patógeno, sí hay ciertas características en determinados grupos de riesgo o
patógenos que pueden aportar información y orientación útil en el manejo de un paciente con neumonía.
Ejemplos útiles pueden ser:
Bacteriemia por neumococo en pacientes mayores de 65 años, con consumo de alcohol,
diabéticos o con varias comorbilidades.
Legionella spp puede asociarse con casos de consumo de agua contaminada, gente joven,
fumadores, con asociación de clínica digestiva y neurológica.
M. pneumoniae en pacientes jóvenes, con tratamientos antibióticos previos.
P. aeruginosa en pacientes con enfermedad pulmonar obstructiva crónica (EPOC), fumadores,
con bronquiectasias, con consumo de antibióticos los últimos tres meses o cuatro veces en el
último año o con consumo habitual de corticoides sistémicos.
Broncoaspiración en aquellos pacientes consumidores de alcohol, alteraciones neurológicas,
disfagia o pacientes de residencia o sospecha de NAES.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [573]
[38] INFECCIONES DE LAS VÍAS RESPIRATORIAS
Tabla III. Agentes causales según grupos de riesgo.
3. CLÍNICA
Los principales síntomas y signos que encontramos son los debidos a la afectación del parénquima
y de las vías respiratorias bajas, como son tos, expectoración purulenta, herrumbrosa o hemoptoica, disnea
y dolor torácico pleurítico, pudiendo evidenciarse en la exploración taquipnea así como auscultación
pulmonar normal o con crepitantes, soplo tubárico o egofonía.
A nivel sistémico suele asociar fiebre mayor de 38 ºC e importante afectación del estado general.
Otras manifestaciones pueden ser diarrea, alteración del nivel de consciencia, cefalea, confusión o
descompensación de enfermedades de base, pudiendo objetivarse hiponatremia o hematuria.
Estas manifestaciones más atípicas son cada vez más frecuentes por el aumento de pacientes
ancianos y en los casos con criterios de NAES.
4. DIAGNÓSTICO
1. RADIOGRAFÍA DE TÓRAX
La presencia de un infiltrado asociado a manifestaciones clínicas compatibles con NAC es el patrón
oro para el diagnóstico, por lo que la radiografía de tórax es obligada para poder establecerlo (idealmente
en dos proyecciones). Además, nos aporta información de localización, extensión, posibles complicaciones
(derrame pleural o cavitación), existencia de enfermedades pulmonares asociadas y de evolución de la
NAC. Puede existir empeoramiento radiológico tras el ingreso sin que indique necesariamente fracaso
terapéutico, aunque tiene valor pronóstico negativo. La tomografía computarizada (TC) torácica tiene
mayor sensibilidad y especificidad, pero no es necesaria para el manejo del paciente, salvo en casos de
ayuda en el tratamiento de complicaciones pleurales o búsqueda de diagnósticos alternativos.
2. ECOGRAFÍA TORÁCICA
En manos expertas, tiene una sensibilidad y una especificidad del 94 y 96%, respectivamente,
siendo una técnica más rápida, menos costosa, que evita radiación y que permite visualización y punción de
derrame asociado.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [574]
[38] INFECCIONES DE LAS VÍAS RESPIRATORIAS
3. DATOS DE LABORATORIO
Nos ayudan a conocer el estado del paciente y valorar la gravedad inicial, así como monitorizar la
evolución. En las NAC atendidas en el hospital solicitaremos hemograma, bioquímica con función renal,
hepática, electrolitos, proteína C reactiva (PCR) y, si es posible, procalcitonina (PCT). En función de los
antecedentes del paciente (EPOC, insuficiencia respiratoria crónica, etc.) y la pulsioximetría (SpO2 < 92%),
solicitaremos gasometría arterial.
La PCR es un parámetro que puede resultar útil para la orientación terapéutica en el caso de no
disponer de radiografía de tórax, en casos dudosos o en el resto de infecciones de las vías respiratorias
bajas (exacerbación de EPOC y bronquitis).
En los casos con valores por debajo de 2 mg/dL no se debe indicar tratamiento antibiótico de
rutina, mientras que valores mayores de 10 mg/dL orientan más hacia un proceso neumónico e indicación
de tratamiento antibiótico. Por otra parte, la PCT puede ser útil en cuadros con mayor sospecha de
patógeno bacteriano, así como en la decisión de inicio y de mantenimiento del tratamiento antibiótico,
ayudando a un uso más rentable de los mismos.
En pacientes con NAC estables hospitalizados, valores de PCT por encima de 0,25 ng/ml son
sugerentes de infección bacteriana y de inicio de tratamiento antibiótico, tanto más cuanto mayor sea este
valor.
4. ESTUDIOS MICROBIOLÓGICOS
El diagnóstico microbiológico se obtiene en poco más del 20% en nuestra práctica diaria, en gran
parte por la dificultad de obtener muestras de buena calidad. Los estudios microbiológicos no son
necesarios en los pacientes ambulatorios porque la terapia antibiótica empírica es casi siempre efectiva.
Los estudios microbiológicos en los pacientes con NAES que requieren ingreso se realizan de rutina,
más aún en casos graves o con sospecha de gérmenes resistentes o patógenos atípicos. Deben de
solicitarse lo antes posible, preferiblemente antes de iniciar tratamiento empírico (Tabla IV).
Gram y cultivo de esputo o aspirado bronquial(en pacientes intubados)
La sensibilidad y especificidad diagnóstica es muy variable entre series, influyendo la calidad de
la muestra (procesamiento en menos de 30 minutos, adecuada calidad [menos de 10 células
epiteliales y más de 25 leucocitos polimorfonucleares/campo]), la experiencia del observador y
la administración de tratamiento antibiótico previo. Idealmente deben hacerse cultivos
semicuantitativos siendo 106 UFC/ml el punto de corte para distinguir infección de
colonización. La tinción del mismo puede ayudar en el diagnóstico de algunos casos graves o
con complicaciones, como en M. tuberculosis o Pneumocistis jiroveci, pero no de rutina.
Hemocultivos
Son poco sensibles (10-20%), pero bastante específicos y con valor pronóstico. Su rentabilidad
se reduce a la mitad tras iniciar la toma de antibióticos. El neumococo es el germen aislado en
más de la mitad de los casos de NAC bacteriémica.
Antígenos urinarios
La detección del antígeno de Legionella serogrupo 1 tiene una sensibilidad del 70-90% y una
especificidad del 99%. La excreción del antígeno ocurre desde en el primer día y continúa
incluso hasta dos semanas después.
La detección del antígeno neumocócico en orina tiene una sensibilidad y especificidad
similares, aunque se debe evaluar con cautela en pacientes con EPOC y neumonía o
exacerbación previa. Si está disponible en el centro, resulta útil para dirigir el tratamiento
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [575]
[38] INFECCIONES DE LAS VÍAS RESPIRATORIAS
antibiótico, especialmente considerando la baja rentabilidad que en muchas ocasiones tienen
los hemocultivos. Sería recomendable al menos en determinados pacientes (aquellos con
ingreso en UCI, fracaso del tratamiento antibiótico ambulatorio, presencia de derrame pleural,
leucopenia, paciente esplenectomizado o asplenia funcional y etilismo activo).
Tabla IV. Recomendaciones de técnicas microbiológicas a realizar en paciente con neumonía adquirida en la comunidad.
Líquido pleural
Siempre que ocupe más de 1 cm en la radiografía en posición de decúbito lateral se realizará
toracocentesis para descartar la presencia de empiema. Se hará estudio de bacterias (Gram,
cultivo de aerobios y anaerobios), así como hemograma, estudio bioquímico y pH; si hay
disponibilidad, se realizará antígeno de neumococo. Según sospecha, pueden estudiarse
micobacterias (cultivo y baciloscopia por tinción de Ziehl-Neelsen) u hongos.
Estudios serológicos (M. pneumoniae, C. pneumoniae, Coxiella burnetti, Legionella spp)
Tienen valor epidemiológico, son sensibles y específicos, pero tardíos, siendo poco útiles para el
diagnóstico precoz ya que precisan de seroconversión (elevación 4 veces el título inicial de
anticuerpos). No se recomiendan de forma habitual.
Técnicas invasivas
Se realizan para obtener muestras del tracto respiratorio inferior sin contaminación
orofaríngea, teniendo mayor importancia en pacientes con NN y en el paciente
inmunodeprimido para obtener un diagnóstico etiológico precoz.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [576]
[38] INFECCIONES DE LAS VÍAS RESPIRATORIAS
En la NAC esta técnica estaría indicada en casos de fracaso terapéutico o de gravedad.
Entre las técnicas se encuentran: la punción transtorácica con aguja fina, la fibrobroncoscopia
(pudiendo realizar cultivos de muestras de cepillado bronquial y/o lavado broncoalveolar, cuyos
puntos de corte son 103 y 104 UFC/ml, respectivamente), aspirado bronquial en pacientes
intubados y biopsia pulmonar abierta (reservada para casos excepcionales).
5. ESCALAS PRONÓSTICAS
Tras el diagnóstico sindrómico de la NAC es necesario valorar la gravedad del cuadro y predecir la
posible evolución posterior para determinar dónde debe recibir tratamiento el paciente. Para ello es muy
útil el uso de escalas pronósticas que permiten estimar la probabilidad de muerte y así valorar la decisión
de ingreso hospitalario. Sirven de ayuda al juicio clínico del profesional, quien ha de valorar, además,
condicionantes personales y sociales del paciente (posibilidades de cumplimiento terapéutico, atención
adecuada, necesidad de oxigenoterapia), así como los medios disponibles en el hospital.
Las escalas pronósticas que aportan mejores resultados en su aplicación en Urgencias son:
1. PNEUMONIA SEVERITY INDEX (PSI) O ESCALA DE FINE
Utiliza 20 variables para estratificar a los pacientes en cinco categorías en función del riesgo de
mortalidad a los 30 días.
Se recomienda tratamiento ambulatorio en las clases I-II (salvo que exista hipoxemia), observación
con posibilidad de corta estancia en la clase III e ingreso hospitalario en las clases IV-V.
Una limitación de esta escala es que puede infravalorar la gravedad de la NAC en jóvenes (Tabla V).
Tabla V. Escala de Fine o PSI (Pneumonia Severity Index).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [577]
[38] INFECCIONES DE LAS VÍAS RESPIRATORIAS
2. CURB-65
Escala útil a pie de cama que utiliza cinco variables, asignándose un punto a cada una y
estratificando a los pacientes en tres clases según el riesgo de mortalidad.
La variante CRB-65 puede ser útil en medios donde no se disponga de laboratorio para determinar
la urea. Se recomienda derivación al hospital en caso de puntuación de 1-2 y derivación de forma urgente
en puntuación 3-4 (Tabla VI).
Tabla VI. Escala CURB-65.
3. CRITERIOS SIMPLIFICADOS DE LA NORMATIVA IDSA/ATS
Son los más utilizados para valorar el ingreso en la UCI (Tabla VII).
Tabla VII. Escala de gravedad simplificada para la indicación de ingreso en Unidades de Cuidados Intensivos según las
recomendaciones de la Infectious Diseases Society of America (IDSA/ATS).
6. TRATAMIENTO (Figura 1)
1. MEDIDAS GENERALES
Reposo, aporte hídrico, analgesia y antitérmicos. Oxigenoterapia en caso de SpO2 menor del 90% o
PaO2 inferior a 60 mm Hg. Fisioterapia respiratoria, especialmente en pacientes con EPOC o asmáticos, que
facilite la expectoración eficiente y mejoría de la mecánica de la musculatura respiratoria. En caso de
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [578]
[38] INFECCIONES DE LAS VÍAS RESPIRATORIAS
fracaso ventilatorio se pantearía la necesidad de VMNI (ver Capítulo 35. “Principios de ventilación
mecánica. Síndrome de distress respiratorio agudo. Trasplante pulmonar”).
2. TERAPIA ANTIMICROBIANA
Es el tratamiento fundamental, debe iniciarse de forma empírica y lo antes posible, disminuyendo
la mortalidad si se administra en las 4 primeras horas de la llegada a Urgencias.
Deben tenerse en cuenta la gravedad (medida por las escalas pronósticas) y los factores de riesgo y
ámbito epidemiológico antes mencionados para escoger el antimicrobiano más apropiado. Un esquema
general a seguir descrito en diversas guías es el siguiente (Tabla VIII):
Tabla VIII. Tratamiento de la NAC.
Una pauta segura de duración del tratamiento debe ser de 5-7 días y siempre al menos 3 días más
tras la resolución de la fiebre. Aquellas situaciones en las que conviene prolongar el tratamiento son:
persistencia de la fiebre más de 72 horas, persistencia de algún criterio de inestabilidad clínica, cobertura
inicial inadecuada y aparición de complicaciones extrapulmonares, como meningitis o endocarditis.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [579]
[38] INFECCIONES DE LAS VÍAS RESPIRATORIAS
Figura 1. Algoritmo de manejo de la neumonía adquirida en la comunidad (NAC).
7. EVOLUCIÓN Y COMPLICACIONES
La respuesta al tratamiento debe ser monitorizada mediante vigilancia clínica y de las constantes
vitales. Además, los datos analíticos nos pueden ayudar, como la PCR (cuyo valor a los 3-4 días con un
descenso menor al 40-50% con respecto al primer día aumenta la probabilidad de falta de respuesta o
complicaciones) o la PCT (cuyo valor a los 2-3 días, si se encuentra descendido de un 80-90% del valor
máximo alcanzado o es menor a 0,25 ng/m, permite acortar o reajustar el tratamiento antibiótico).
1. CAMBIO A TRATAMIENTO ORAL
La vía oral es segura y de igual eficacia que mantener el tratamiento intravenoso una vez alcanzada
la estabilidad clínica y mejoría de la fiebre, que se alcanza por lo general en los primeros 3 o 4 días.
2. RADIOLOGÍA DE CONTROL
Aunque es una práctica habitual, no existe evidencia de la utilidad de nuevas radiografías de tórax
en aquellos pacientes que presentan una adecuada evolución clínica y no hay sospecha de complicaciones.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [580]
[38] INFECCIONES DE LAS VÍAS RESPIRATORIAS
Estaría indicada en pacientes fumadores, mayores de 50 años o con persistencia de síntomas, con
el objetivo de comprobar la resolución radiológica y descartar patología subyacente. La resolución
radiológica es más lenta que la clínica, pudiendo tardar 6 semanas o más.
3. NEUMONÍA QUE NO RESPONDE
Incluye aquellas en la que no hay mejoría clínica inicial o presenta deterioro clínico o inestabilidad
en las primeras 72 horas, o bien a la persistencia de imágenes radiológicas tras 4-6 semanas.
La actuación consiste, en primer lugar, en una reevaluación diagnóstica, considerando de nuevo el
diagnóstico de NAC y descartando otras causas no infecciosas (como neoplasias, edema pulmonar, distrés
respiratorio del adulto, eosinofilia pulmonar, neumonía organizada criptogénica o vasculitis). En segundo
lugar, la obtención de nuevas muestras microbiológicas, tanto no invasivas (esputo, hemocultivos) como
invasivas (aspirado bronquial, lavado broncoalveolar, biopsia transbronquial), complementadas por nuevas
técnicas de imagen o incluso TC torácico. Por último, se recomienda modificar la pauta antibiótica a un
espectro mayor que el inicial hasta obtener respuesta de los estudios microbiológicos. Una pauta valida es
un beta-lactámico antipseudomonas (cefepime, ceftazidima, imipenem, meropenem,
piperacilina/tazobactam) + fluoroquinolona. En caso de NAES o colonización por S. aureus, conviene
administrar vancomicina o linezolid. Si existen factores de riesgo para Aspergillus spp (EPOC grave,
inmunodeprimidos, tratamiento con corticoides sistémicos), se debería añadir antifúngico hasta ser
descartada esta causa.
4. NEUMONÍA RECURRENTE
Aquella que aparece después de desaparecer la sintomatología y las alteraciones radiológicas. Las
causas más frecuentes son: EPOC, bronquiectasias, cardiopatía, fibrosis quística, inmunodepresión o
patología inflamatoria no infecciosa como neumonía organizada criptogénica, neumonitis por
hipersensibilidad o neumonías eosinofílicas, entre otras. La reaparición en un mismo lóbulo obliga a
descartar una lesión endobronquial (sospecha de neoplasia).
5. NEUMONÍA NECROTIZANTE Y ABSCESO PULMONAR
Lesión cavitada localizada en el parénquima. El término absceso se reserva para cavitaciones únicas
o predominantes de tamaño mayor a 3 cm de diámetro. La mayoría de los casos se deben a infección por
aspiración de secreciones (colonizadas por microorganismos anaerobios y, frecuentemente,
polimicrobianas) procedentes de la orofaringe.
El cuadro clínico puede ser progresivo e insidioso, de semanas o hasta meses de evolución, con una
importante afectación del estado general, fiebre, sudoración, pérdida de peso y tos productiva con
expectoración purulenta o incluso fétida. La exploración física puede ser inespecífica, aunque puede haber
datos orientativos como boca séptica con piorrea o caries dentales, aliento fétido o desaparición del reflejo
nauseoso.
La distribución de las lesiones en las zonas más declives y la aparición de un nivel hidroaéreo en su
interior suele ser la norma. El diagnóstico diferencial principal debe hacerse con el carcinoma
broncogénico, la tuberculosis (requiriendo aislamiento respiratorio preventivo en caso de alta sospecha
hasta confirmación por baciloscopia), nocardia, endocarditis derecha por S. aureus y hongos. Puede ser
preciso fibrobroncoscopia o punción-aspiración con aguja fina (PAAF) transtorácica para descartar otros
diagnósticos. Estos pacientes requieren ingreso hospitalario y tratamiento con antibióticos de amplio
espectro a altas dosis que cubran gérmenes anaerobios durante tiempo prolongado (al menos hasta la
desaparición de la cavidad), aunque los primeros 15 días deben cubrirse también cocos positivos y bacilos
gramnegativos aerobios, pues suele ser frecuente la flora polimicrobiana.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [581]
[38] INFECCIONES DE LAS VÍAS RESPIRATORIAS
Algunos fármacos válidos pueden ser amoxicilina-clavulánico en monoterapia (de elección),
moxifloxacino en monoterapia o clindamicina asociado a otro antibiótico, como una quinolona. Si se
sospechan gérmenes mutirresistentes, son útiles los carbapenemes o piperacilina/ tazobactam.
8. PREVENCIÓN
En la actualidad se dispone de dos vacunas frente al neumococo.
La vacuna antineumocócica 13 valente conjugada (VC-13, Prevenar 13®) está aprobada e indicada
para la prevención de la enfermedad neumocócica invasiva, neumonía y otitis media aguda causadas por
neumococo en niños de 6 semanas a 17 años, pudiendo administrarse con el resto de vacunas del
calendario vacunal.
En adultos, VC-13 está indicada también en inmunodeprimidos, esplenectomizados, insuficiencia
renal o hepática, alcohólicos o con antecedente de enfermedad neumocócica invasora. Se administra una
vez, con una dosis de recuerdo en los cinco años posteriores de vacuna polisacárida VP-23.
La vacuna polisacárida (VP-23) no está financiada por el Sistema Público de Salud, puede
administrarse simultáneamente con otras vacunas en lugar distinto, pero no debe administrarse durante el
momento agudo de la infección ni antes de dos semanas del inicio del tratamiento inmunosupresor. Se
recomienda su administración (una sola dosis) en los mayores de 65 años, así como en pacientes
inmunodeprimidos y en inmunocompetentes con las comorbilidades recogidas en la tabla IX.
Las recomendaciones en cuanto a la vacuna antigripal se exponen en el Apartado “Gripe”.
Tabla IX. Recomendaciones para el uso de las vacunas antineumocócicas.
Las medidas higiénicas (lavado frecuente de manos, higiene respiratoria) resultan útiles en la
prevención de transmisión de infecciones respiratorias. El tabaquismo es un factor importante en la
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [582]
[38] INFECCIONES DE LAS VÍAS RESPIRATORIAS
morbimortalidad por NAC, por lo que su abandono ha demostrado ser beneficioso y debe establecerse
como un objetivo prioritario en prevención sanitaria.
III. GRIPE
1. CARACTERÍSTICAS GENERALES DE LA GRIPE
La gripe es una infección aguda de las vías respiratorias causada por los virus del género Influenza
(A y B, en función de sus características antigénicas). Suele acompañarse de signos y síntomas de tipo
general, como fiebre, cefalea, mialgias y debilidad. Produce brotes anuales, de extensión e intensidad
variables, que ocasionan importante morbilidad en la población general y mayores tasas de mortalidad en
algunos pacientes de alto riesgo, principalmente como consecuencia de complicaciones pulmonares y
cardiacas.
Los virus de la gripe tienen gran tendencia a presentar cambios en los antígenos de superficie
(hemaglutinina y neuraminidasa) y entre una temporada gripal y la siguiente pueden producirse variaciones
antigénicas menores. Las pandemias tienen relación con variaciones antigénicas mayores, con
consecuencias variables en función del grado de inmunidad de la población frente al nuevo tipo de virus. El
virus de la gripe B, por lo general, produce brotes menos extensos y con una presentación menos grave que
los producidos por el virus A. La vía de transmisión principal son las secreciones respiratorias de personas
con infección aguda, aunque también puede transmitirse por contacto (aproximadamente desde 24 horas
antes del inicio de los síntomas hasta 5 días después).
2. DIAGNÓSTICO
Los test de detección rápida del antígeno en el exudado nasofaríngeo tienen una sensibilidad baja
en adultos (en torno al 55-60%), presentando una especificidad muy alta. En general, se usan como test de
screening dado que son muy rápidos, pero nos dan información limitada, sobre todo cuando el resultado es
negativo, requiriendo realización de RT-PCR como confirmación (sensibilidad y especificidad cercanas al
100%).
Durante un brote de gripe, la mayoría de los diagnósticos puede hacerse de manera clínica y se
reservarán los test diagnósticos para grupos en los que suponga un cambio en la actitud y para vigilancia
epidemiológica (incluyendo las medidas de aislamiento de pacientes ingresados protocolizadas de cada
centro).
3. TRATAMIENTO
En la gripe no complicada que afecta a adultos sanos el tratamiento es sintomático con
antitérmicos y analgésicos (evitar salicilatos, sobre todo en menores por su asociación con el síndrome de
Reye). Es importante disminuir el contacto estrecho con otras personas mientras duren los síntomas y
extremar las medidas de higiene.
En cuanto al tratamiento específico antiviral dirigido a grupos de riesgo (Tabla X), los fármacos con
menos resistencias actualmente son los inhibidores de la neuraminidasa, siendo el más usado oseltamivir
(dosis habitual 75 mg/12 h durante 5 días; requiere ajuste en enfermedad renal). La recomendación general
es el inicio de oseltamivir en las primeras 30 horas desde el inicio de los síntomas pues en este periodo
parece producir una reducción de la duración de los síntomas de aproximadamente un día de promedio.
Está en discusión si el uso de oseltamivir disminuye la frecuencia de complicaciones de la gripe y, ante su
potencial efecto a este respecto, se recomienda su uso en los grupos de pacientes con mayor riesgo de
complicaciones.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [583]
[38] INFECCIONES DE LAS VÍAS RESPIRATORIAS
4. COMPLICACIONES SECUNDARIAS
Principalmente sobreinfección bacteriana en forma de neumonía, otitis media o sinusitis.
La antibioterapia empírica debe cubrir los gérmenes más habitualmente implicados en la NAC,
especialmente, Streptococcus pneumoniae, Streptococcus pyogenes y Staphylococcus aureus, siendo
adecuados amoxicilina-clavulánico, una cefalosporina de tercera generación o una quinolona, combinados
con vancomicina o linezolid si la prevalencia de S. aureus resistentes a oxacilina es alta o se aisla dicho
germen.
Si se precisan broncodilatadores, la vía recomendada será la inhalación, siempre que las
condiciones del paciente lo permitan, pues las nebulizaciones aumentan la transmisión de la infección al
personal sanitario y cuidadores.
Las autoridades sanitarias nacionales e internacionales y las principales Sociedades Científicas de
Neumología y Enfermedades Infecciosas recomiendan fuertemente el uso de la vacuna para prevenir la
gripe, sobre todo en los grupos con especial riesgo de complicaciones (Tabla X) y en los trabajadores de
centros de cuidados y hospitales, dado que los beneficios potenciales superan los riesgos, al ser una vacuna
muy segura. En revisiones sistemáticas y metanálisis de ensayos controlados publicados no se muestran
resultados globales concluyentes sobre su efectividad señalando la necesidad de nuevos estudios
adecuadamente diseñados para aclararlo definitivamente.
Tabla X. Principales grupos de riesgo en la población adulta en los que se plantea el uso de antivirales frente a la gripe.
BIBLIOGRAFÍA
Álvarez-Sala Walther JL, Casan Clarà P, Rodríguez de Castro F, Rodríguez Hermosa JL, Villena Garrido V.
Neumología clínica. 1ª ed. Barcelona: Elsevier; 2010.
Chavez MA, Shams N, Ellington LE, Naithani N, Gilman RH, Steinhoff MC, et al. Lung ultrasound for the
diagnosis of pneumonia in adults: a systematic review and meta-analysis. Respir Res. 2014;15(1):50.
Cillóniz C, Ewig S, Polverino E, et al. Microbial aetiology of community-acquired pneumonia and its
relation to severity. Thorax. 2011;66:340.
Fiore AE, Fry A, Shay D, Gubareva L, Bresee JS, Uyeki TM. Antiviral agents for the treatment and
chemoprophylaxis of influenza - recommendations of the Advisory Committee on Immunization
Practices (ACIP). MMWR Recomm Rep. 2011;60(1):1-24.
Grupo de trabajo de vacunación frente al neumococo en grupos de riesgo 2015 de la Ponencia de
Programas y Registro de Vacunaciones. Comisión de Salud Pública del Consejo Interterritorial del
Sistema Nacional de Salud. Ministerio de Sanidad, Servicios Sociales e Igualdad. 2015. Utilización de
la vacuna frente al neumococo en grupos de riesgo. [Internet]. [acceso 8 de mayo de 2016]. Disponible
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [584]
[38] INFECCIONES DE LAS VÍAS RESPIRATORIAS
en: http://www.msssi.gob.es/profesionales/
saludPublica/prevPromocion/vacunaciones/docs/Neumococo_Gruposriesgo.pdf
Jefferson T, Jones MA, Doshi P, del Mar CB, Hama R, Thompson MJ, et al. Neuraminidase inhibitors for
preventing and treating influenza in adults and children. Cochrane Database of Systematic Reviews.
2014; Issue 4. Art. No.: CD008965. doi:10.1002/14651858.CD008965.pub4.
Menéndez R, Torres A, Aspa J, Capelastegui A, Prat C, Rodríguez de Castro F. Neumonía adquirida en la
comunidad. Nueva normativa de la Sociedad Española de Neumología y Cirugía Torácica (SEPAR). Arch
Bronconeumol. 2010;46(10):543-58.
Poole PJ, Chacko E, Wood-Baker RWB, Cates CJ. Influenza vaccine for patients with chronic obstructive
pulmonary disease. Cochrane Database of Systematic Reviews. 2006; Issue 1. Art. No.: CD002733.
doi:10.1002/14651858.CD002733.pub2.
Prina E, Ranzani OT, Torres A. Community-acquired pneumonia. Lancet. 2015;386(9998):1097-108.
Salih W, Schembri S, Chalmers JD. Simplification of the IDSA/ATS criteria for severe CAP using meta-
analysis and observational data. Eur Respir J. 2014;43(3):842-51.
Scalera NM, File TM. Determining the duration of therapy for patients with community-acquired
pneumonia. Curr Infect Dis Rep. 2013;15(2):191-5.
Schuetz P, Amin DN, Greenwald JL. Role of procalcitonin in managing adult patients with respiratory
tract infections. Chest. 2012;141(4):1063-73.
Schuetz P, Müller B, Christ-Crain M, Stolz D, Tamm M, Bouadma L, et al. Procalcitonin to initiate or
discontinue antibiotics in acute respiratory tract infections. Cochrane Database of Systematic Reviews.
2012; Issue 9. Art. No.: CD007498. doi: 10.1002/14651858.CD007498.pub2.
Smith SM, Fahey T, Smucny J, Becker LA. Antibiotics for acute bronchitis. Cochrane Database of
Systematic Reviews 2014; Issue 3. Art. No.: CD000245.
doi: 10.1002/14651858.CD000245.pub3.
Thomas Roger E, Jefferson T, Lasserson Toby J. Influenza vaccination for healthcare workers who care
for people aged 60 or older living in long-term care institutions [Internet]. Cochrane Database of
Systematic Reviews. 2013; Issue 7. Art. No.: CD005187. doi: 10.1002/14651858.CD005187.pub4.
Woodhead M, Aliyu S, Ashton C, Brown J, Eccles S, Greenwood S, et al. Pneumonia. Commissioned by
the National Institute for Health and Care Excellence (NICE). Diagnosis and management of community-
and hospital-acquired pneumonia in adults. Clinical Guideline 191. Methods, evidence and
recommendation. 3 December 2014. [Internet]. [Acceso 11 de mayo de 2016]. Disponible en:
https://www.nice.org.uk/guidance/cg191/evidence/full-guideline-193389085.
Woodhead M, Blasi F, Ewig S, Garau J, Huchon G, Ieven M, et al. Guidelines for the management of
adult lower respiratory tract infections –full version. Clin Microbiol Infect. France; 2011;17(Suppl 6):E1-
59.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [585]
[39] INFECCIONES DEL TRACTO URINARIO
39.Infecciones del tracto urinario
Noelia García-Pozuelo Adalia.
Medicina Interna
Raúl Benítez Sala.
Urología
Asesora: Ana García Reyne. Médica Adjunta de Medicina Interna
I. INTRODUCCIÓN
La infección del tracto urinario (ITU) constituye la segunda causa más frecuente de infección
extrahospitalaria atendida en hospitales y la causa más común de infección nosocomial (40-60%), sobre
todo cuando se asocia a sondaje vesical. Bajo la definición de ITU se esconden diversos síndromes clínicos
cuyo diagnóstico y tratamiento varían en función de la zona del tracto urinario que esté afectada y el tipo
de paciente (edad, sexo, comorbilidad asociada…).
Esta patología es especialmente frecuente en el sexo femenino. Se estima que entre el 50-80%
sufre al menos un episodio de ITU en su vida, aumentando la prevalencia a partir de la adolescencia
coincidiendo con el inicio de las relaciones sexuales y los embarazos. En el varón es a partir de los 50 años
cuando se objetiva un incremento en el número de casos, probablemente en relación con la patología
prostática o las manipulaciones urológicas. En ancianos de ambos sexos, especialmente en aquellos
hospitalizados y con gran comorbilidad asociada, la bacteriuria tiene una prevalencia elevada (> 25%).
Tabla I. Microoorganismos y porcentaje de sensibilidad a antibióticos en urocultivos recogidos en el Hospital 12 de Octubre de
Madrid durante el año 2015.
Con respecto a la etiología de las infecciones urinarias (en la tabla I quedan reflejados los
aislamientos microbiológicos más frecuentes en nuestro centro), la mayoría son monomicrobianas. En
infecciones urinarias no complicadas (cistitis y pielonefritis aguda), Escherichia coli es el germen más
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [586]
[39] INFECCIONES DEL TRACTO URINARIO
frecuente (80-85%), seguido de Staphylococcus saprophyticus, Klebsiella pneumoniae y Proteus mirabilis. En
pacientes sondados, con manipulación urológica reciente, tratamientos antibióticos previos o en
infecciones nosocomiales, aunque E. coli sigue siendo el más frecuente, aumenta la prevalencia de casos
ocasionados por:
Bacilos gramnegativos diferentes de E. coli, resistentes a antibióticos habituales (Proteus,
Pseudomonas, Enterobacter, Klebsiella, Serratia, Providencia…).
Cepas de enterobacterias (E. coli y Klebsiella) productoras de betalactamasas de espectro
extendido (BLEE), que presentan resistencia a todos los betalactámicos excepto los
carbapenemes y aztreonam, y que además se asocian a resistencias a otras familias de
antibióticos como las quinolonas o el cotrimoxazol. Recientemente, también se han aislado
cepas con carbapenemasas, siendo preciso el desarrollo de nuevas pautas de antibióticos.
Cocos grampositivos como Enterococcus spp o S. aureus.
Candida spp: la candiduria es un hallazgo habitual (particularmente en pacientes diabéticos o
en tratamiento con antibióticos) y en la inmensa mayoría solo representa colonización, siendo
únicamente necesario tratar en caso de neutropenia, necesidad de manipulación urológica,
neonatos y en el trasplante renal.
Polimicrobianas: en caso de sondaje vesical permanente, vejiga neurógena o fístula entero-
vesical o vesicovaginal.
II. BACTERIURIA ASINTOMÁTICA
1. DEFINICIÓN
Bacteriuria significa literalmente bacterias en la orina, pero debido a la dificultad de obtener orina
no contaminada y por lo tanto sin ningún germen, se ha establecido un umbral a partir del cual se
diferencia la bacteriuria significativa (sugerente de infección urinaria) de la contaminación uretral.
La bacteriuria significativa se define como el aislamiento en un urocultivo de un número
determinado de unidades formadoras de colonias (UFC) de un único patógeno en una muestra de orina
recogida adecuadamente. La bacteriuria asintomática es una bacteriuria significativa en pacientes sin
síntomas ni signos de infección urinaria. La definición de bacteriuria significativa depende del tipo de
paciente, de modo que:
Mujeres: se define como el aislamiento de > 105 UFC/ml del mismo patógeno en dos
urocultivos consecutivos. En caso de mujeres embarazadas sería diagnóstico un solo urocultivo
positivo.
Hombres: se requiere > 105 UFC/ml en un único urocultivo.
Pacientes sondados (ambos sexos): la determinación de > 102 UFC/ml de una muestra obtenida
del sondaje.
2. INDICACIONES DE DIAGNÓSTICO Y TRATAMIENTO
Aunque la presencia de bacteriuria es frecuente en pacientes ancianos, sobre todo en mujeres, y
pacientes hospitalizados, la detección y posterior tratamiento solo está indicado en dos situaciones:
Mujeres embarazadas: en el caso de ser positivo se recomienda tratamiento durante 3-7 días,
con seguimiento posterior para detectar recurrencias (ver Apartado IX. “ITU en la
embarazada”).
Pacientes que van a ser sometidos a una resección transuretral de la próstata u otras
intervenciones urológicas en las que se prevé sangrado de mucosas, iniciando el tratamiento
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [587]
[39] INFECCIONES DEL TRACTO URINARIO
antes de la intervención (la noche previa o justo antes de la misma) y retirándolo tras el
procedimiento. Solo en el caso de que el paciente permanezca sondado tras la intervención,
algunos expertos recomiendan mantenerlo hasta su retirada.
No debe realizarse screening ni por tanto tratamiento en: mujeres diabéticas, mujeres
premenopáusicas, ancianos, pacientes con lesión medular y en pacientes sondados, aunque se debe valorar
el tratamiento en aquellas mujeres que tras la retirada de la sonda vesical a las 48 horas persiste la
bacteriuria. En los pacientes trasplantados se recomienda el screening y tratamiento durante el primer mes
tras el trasplante. No existe evidencia actualmente que justifique su realización posteriormente a esta
fecha. En los pacientes con bacteriuria asintomática con indicación de tratamiento, la elección del mismo se
realizará en función del antibiograma y la toxicidad, siendo recomendable efectuar un urocultivo de control
entre 1-2 semanas, una vez completado.
III. CISTITIS AGUDA NO COMPLICADA
1. DEFINICIÓN
Se define como aquella que ocurre en mujeres jóvenes no embarazadas, cuyo riesgo de asociar
complicaciones es muy bajo.
2. CLÍNICA
Se manifiesta con síndrome miccional (disuria, polaquiuria, urgencia miccional), y menos
frecuentemente con tenesmo vesical, dolor suprapúbico, incontinencia urinaria y hematuria. La presencia
de fiebre, dolor en flanco, náuseas y vómitos sugiere posible infección de tracto urinario superior (ver
Apartado V. “Pielonefritis aguda”).
3. DIAGNÓSTICO
Si la historia clínica es sugerente de cistitis no complicada, se procederá al diagnóstico con:
3.1. Anamnesis y exploración física
Se debe preguntar por la posibilidad de embarazo y relaciones sexuales de riesgo. En el examen físico ha de
incluirse la toma de temperatura, signos vitales, exploración abdominal y puño-percusión renal para
descartar afectación del tracto urinario superior. Si la clínica es sugerente de uretritis o vaginitis, conviene
hacer un examen vaginal en busca de signos compatibles o úlceras herpéticas, así como de genitales
externos en varones (ver Capítulo 40. “Enfermedades de transmisión sexual”).
3.2. Tira reactiva
Se pueden emplear como método de screening y, en el caso de clínica compatible con una cistitis simple, el
resultado positivo de una tira reactiva sería suficiente para confirmar el diagnóstico (sobre todo si se
emplean cuando no se tiene acceso a un sistemático de orina). Detectan la existencia de piuria
indirectamente a través de la presencia de estereasa leucocitaria (enzima que poseen los leucocitos), y la
presencia de bacteriuria con la detección de nitritos (estos pueden estar presentes por la reducción
realizada por las enterobacterias de los nitratos en nitritos). La presencia de estereasa leucocitaria tiene
alta sensibilidad (75-96%) y muy alta especificidad (94-98%), por lo que si el resultado es negativo y la
clínica es sugerente se deben realizar otros métodos diagnósticos (sedimento y/o urocultivo). La presencia
de ambos tiene una alta sensibilidad y especificidad para la detección de > 105 UFC/ml de enterobacterias,
pero no detecta la presencia de otros patógenos, de modo que los resultados negativos deben ser
interpretados con precaución. Además, puede haber falsos positivos con la tinción roja de la orina como
ocurre con fármacos o alimentos.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [588]
[39] INFECCIONES DEL TRACTO URINARIO
3.3. Sistemático y sedimento de orina
Se trata de un método diagnóstico muy útil si se interpreta correctamente, dado que en él se pueden hallar
diferentes datos que nos ayuden a diagnosticar una ITU.
Piuria: se define como la presencia de leucocitos en orina en concentración de > 5
leucocitos/campo en orina centrifugada que se correlaciona con una concentración de
bacterias de > 105 UFC/ml. La sensibilidad es del 91% y la especificidad del 97%, aunque el valor
predictivo positivo es del 67%. La piuria está presente en casi todas las mujeres con cistitis, y su
ausencia debe hacernos pensar en otra patología.
Hay que considerar los siguientes falsos negativos:
Obstrucción de la vía urinaria.
Infecciones sin comunicación con la vía urinaria (absceso perirrenal o intrarrenal).
Proteinuria o pH alcalino urinario (alteran la determinación en el análisis urinario).
Fases iniciales de la enfermedad o tratamiento antibiótico previo.
Pacientes neutropénicos.
Hay que considerar también posibles contaminaciones de la muestra que cursarían como
falsos positivos:
Secreciones vaginales (especialmente cuando hay abundantes células epiteliales en la
muestra).
Otras patologías que pueden cursar con piuria (nefrolitiasis, tumores, nefropatías, etc.).
Cuando se detecta un caso de piuria estéril (urocultivo repetidamente negativo) y se
hayan descartado las posibilidades de falsos negativos, se debe plantear la presencia de
infección por Mycobacterium tuberculosis, Chlamydia o Ureaplasma urealyticum.
Bacteriuria: la presencia de bacterias en orina no implica infección urinaria. En ausencia de
piuria, la presencia de bacterias en orina suele deberse a contaminación. No se recomienda el
examen de bacteriuria en sedimento de orina por la imposibilidad de identificar el germen.
Otros: la presencia de hematuria microscópica es habituales en las ITU, y ayuda en el
diagnóstico diferencial porque no aparece en las uretritis ni en las vaginitis. Su persistencia una
vez superada la infección de orina debe hacernos sospechar otros diagnósticos. Los cilindros
leucocitarios son patognomónicos de inflamación del parénquima renal (aunque no
exclusivamente de pielonefritis aguda). Un pH > 8 puede indicar la presencia de gérmenes
productores de ureasa (Proteus…). La hematuria, la piuria y la proteinuria por sí solos son datos
muy inespecíficos para infección urinaria.
3.4. Urocultivo
Indicación: en cistitis aguda no está indicado excepto en casos con síntomas atípicos o en
infecciones complicadas.
Rentabilidad de la muestra: la muestra se puede obtener a través de la micción espontánea,
del sondaje vesical o por punción suprapúbica. Las muestras óptimas son las tomadas en la
primera micción de la mañana, porque durante la noche la orina se concentra más y las
bacterias tienen más tiempo para su replicación.
Técnica de recogida de la muestra (micción espontánea):
Limpiar zona genital, si es mujer abriendo los labios mayores, con solución antiséptica,
y secar después con gasa estéril para eliminar la mezcla de antisépticos de la orina.
Reducir al mínimo el contacto de las mucosas con el chorro de la orina.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [589]
[39] INFECCIONES DEL TRACTO URINARIO
Tomar la muestra de la mitad del chorro.
No demorar el procesamiento de la muestra.
Definición de urocultivo positivo: el número de UFC necesario para que se considere
diagnóstico depende de la situación clínica; en el caso de una cistitis aguda no complicada una
determinación de > 102 UFC/ml sería suficiente.
Falsos negativos: tratamiento antibiótico, infección por microorganismos diferentes a E. coli o
Proteus, fase temprana de la infección, pH urinario bajo u obstrucción uretral.
4. DIAGNÓSTICO DIFERENCIAL
Uretritis/cervicitis infecciosa, vulvovaginitis (ver Capítulo 40. “Enfermedades de transmisión
sexual”) y uretritis traumática (cursa sin piuria y con urocultivo negativo, requiere valoración por
especialista en Urología).
5. TRATAMIENTO (FIGURA 1)
Figura 1. Manejo del paciente con infección urinaria.
5.1. Principios generales
Debe asegurarse una buena hidratación, y en ocasiones puede ser precisa la administración de analgésicos,
aunque el tratamiento antibiótico eficaz controla rápidamente la disuria producida por la infección. El
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [590]
[39] INFECCIONES DEL TRACTO URINARIO
antibiótico apropiado para el tratamiento empírico de las ITU debería tener las siguientes características: 1)
ser activo frente a más del 95% de las cepas de E. coli, ajustándose a los patrones locales de sensibilidad de
los microorganismos; 2) alcanzar concentraciones elevadas y mantenidas en la vía urinaria y en sangre dada
la posibilidad de bacteriemia y 3) respetar la flora rectal y vaginal, para evitar las recurrencias por
enterobacterias colonizadoras.
Prácticamente todos los antibióticos utilizados por vía oral adquieren concentraciones adecuadas
en orina. Si el microorganismo es sensible a las fluorquinolonas o al cotrimoxazol, debe darse preferencia a
estos porque tienen un espectro antimicrobiano más selectivo para microorganismos uropatógenos. Antes
de la elección del tratamiento antibiótico empírico debe tenerse en cuenta: 1) tratamientos antibióticos
previamente recibidos; 2) aislamientos microbiológicos previos y 3) el patrón de resistencias locales.
En general, no es necesario realizar urocultivo de control tras el tratamiento antibiótico para
confirmar erradicación; a menos que la sintomatología persista o recurra a las pocas semanas. En caso de
ser necesario iniciar la antibioterapia por vía parenteral, si el paciente se mantiene 48-72 horas afebril, se
podría completar el ciclo por vía oral según antibiograma.
5.2. Tratamiento antibiótico
Existen varios regímenes terapéuticos indicados para el tratamiento de la ITU no complicada, debiéndose
elegir el antibiótico en función de los estudios de sensibilidad de los microorganismos prevalentes en el
área geográfica. No se recomienda en nuestro medio la utilización de cotrimoxazol, amoxicilina ni de
quinolonas de forma empírica, dado el alto índice de resistencias de los patógenos habituales (ver Tabla I);
principalmente E. coli. Este hecho puede estar relacionado con el gran empleo de estos fármacos, por lo
que se debe intentar evitar su uso como tratamiento empírico de inicio, sobre todo en el caso de que la
cistitis tenga criterios de complicada o en casos de gravedad.
No se recomienda el tratamiento con amoxicilina-ácido clavulánico, al menos como primera opción,
pues se asocia con una frecuencia de reinfecciones aparentemente superior a la observada con el empleo
de cotrimoxazol o fluorquinolonas, debiéndose probablemente este hecho a la mayor actividad de la
amoxicilina sobre la flora anaerobia o microaerófila de la vagina y el colon, que al desaparecer, facilita la
persistencia de E. coli.
Se ha demostrado que ciclos cortos de antibiótico presentan similar eficacia con menos efectos
adversos que las pautas más largas. Los antibióticos recomendados serían: cefalosporinas de 2ª generación
(cefuroxima) o de 3ª generación (ceftibuteno, cefditoren o cefixima) oral durante 3-5 días; fluorquinolona
oral (ciprofloxacino o levofloxacino; no se aconseja moxifloxacino por su escasa eliminación urinaria)
durante 3 días; fosfomicina trometamol 3 g en dosis única (eficacia ligeramente inferior a quinolonas en
cuanto a tasas de erradicación pero con la ventaja de su cómoda administración); o nitrofurantoína
durante 7 días (efectos secundarios frecuentes). Los regímenes de antibióticos más utilizados en las
diferentes entidades quedan reflejados en la tabla II.
Consideraciones importantes:
Ajustar la dosis según función renal.
Se trata de un tratamiento empírico que luego debe ajustarse al antibiograma y al patrón de
resistencia local.
Si el paciente es alérgico a betalactámicos se debe consultar al servicio de alergia de manera
inmediata o diferida según la gravedad (valorar desensibilización).
En el caso de infecciones complicadas (ITU complicada, pielonefritis, prostatitis, orquitis,
epididimitis) se debe consultar al Urólogo de manera diferida o inmediata según la gravedad.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [591]
[39] INFECCIONES DEL TRACTO URINARIO
Tabla II. Tratamiento de las diferentes entidades de infección del tracto urinario.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [592]
[39] INFECCIONES DEL TRACTO URINARIO
IV. CISTITIS AGUDA COMPLICADA
1. DEFINICIÓN
Una infección urinaria complicada es aquella en la que se asocia una condición que aumenta la
probabilidad de fracaso terapéutico, debido a que tienen mayor riesgo de afectación del tracto urinario
superior o infección por patógeno multirresistente (Tabla III).
Tabla III. Factores de riesgo de infección complicada del tracto urinario.
2. CLÍNICA
Suelen cursar con los mismos síntomas que las cistitis no complicadas, sin embargo estos son a
menudo sutiles en los pacientes muy jóvenes o ancianos. La presencia de fiebre elevada, dolor lumbar y
náuseas o vómitos, sugieren una extensión al tracto urinario superior, lo que implicaría medidas
diagnósticas y terapéuticas más agresivas (ver Apartado V. “Pielonefritis aguda”).
3. DIAGNÓSTICO
Se basa en la exploración física, sistemático y sedimento de orina, al igual que en la cistitis simple,
pero en este caso se deberá tomar siempre un urocultivo antes de comenzar el tratamiento. Se puede
valorar según el tipo de paciente la realización de una analítica, puesto que puede ser de ayuda para
detectar afectación parenquimatosa (leucocitosis, PCR y VSG elevadas) o de complicaciones (función renal
e iones).
4. TRATAMIENTO
En estos casos se deben utilizar antibióticos de mayor espectro y durante un tiempo más
prolongado, con las siguientes pautas: cefalosporina de 2ª generación (cefuroxima) o 3ª generación
(ceftibuteno, cefixima, cefditoren) oral durante 7 días; en caso de alergia a betalactámicos, fosfomicina
trometamol en dos dosis de 3 g cada 72 horas o en formulación cálcica 0,5-1 g cada 8 horas durante 7 días,
ajustando el tratamiento posteriormente según el antibiograma.
V. PIELONEFRITIS AGUDA
1. DEFINICIÓN
Es la infección que afecta a la pelvis y al parénquima renal y se suele originar a partir de una
infección del tracto urinario inferior que progresa hasta el superior. La mayoría de las pielonefritis agudas
(PNA) son no complicadas y se producen en mujeres sanas, siendo infrecuente en varones. La PNA
complicada es la progresión a nefritis aguda focal, absceso intrarrenal, absceso perinefrítico, necrosis
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [593]
[39] INFECCIONES DEL TRACTO URINARIO
papilar y pielonefritis enfisematosa. La pielonefritis crónica es una causa rara de enfermedad
tubulointersticial secundaria a la infección de repetición por reflujo vesicoureteral o litiasis.
2. CLÍNICA
La clínica típica cursa con fiebre, dolor lumbar y síntomas de cistitis aguda; esta triada se presenta
en un 60% de los casos. También puede acompañarse de náuseas, vómitos e incluso diarrea. El dolor
lumbar puede irradiarse al abdomen inferior, epigastrio y región inguinal. En ocasiones los síntomas de
infección de las vías bajas pueden preceder a la fiebre y al resto de síntomas de PNA en 1 o 2 días. Hay que
hacer diagnóstico diferencial con cólico renoureteral, abdomen agudo (apendicitis, colecistitis, embarazo
ectópico, diverticulitis, etc.) o enfermedad inflamatoria pélvica.
3. DIAGNÓSTICO
3.1. Anamnesis y exploración física
Es fundamental preguntar por la posibilidad de embarazo y relaciones sexuales de riesgo; en el examen
físico ha de incluirse la toma de temperatura, signos vitales, exploración abdominal y puño-percusión renal.
Se indicará un examen ginecológico si hay signos o síntomas que sugieran vaginitis, uretritis o enfermedad
inflamatoria pélvica. Valorar determinación de procalcitonina en casos de gravedad.
3.2. Hemograma y bioquímica
Se recomienda en casos de sospecha de PNA, donde se puede objetivar leucocitosis con neutrofilia y se
debe valorar la creatinina e iones. El aumento de la VSG y PCR sugieren afectación parenquimatosa. En
pacientes donde el diagnóstico puede resultar más complicado (ancianos paucisintomáticos o síntomas
atípicos) los resultados analíticos pueden ser de mayor utilidad. Valorar determinación de procalcitonina en
casos de gravedad.
3.3. Sistemático y sedimento
Se debe realizar siempre que exista la sospecha de PNA. La presencia de cilindros leucocitarios es
patognomónica de afectación inflamatoria del parénquima renal (aunque no de infección).
3.4. Urocultivo
Es una prueba imprescindible para establecer el diagnóstico. Se considera positivo con un recuento > 104
UFC/ml del mismo microorganismo. La técnica de recogida de la muestra es similar a la expuesta en la
cistitis aguda, así como los posibles falsos negativos.
3.5. Hemocultivo
Alrededor del 20-30% de las PNA cursan con bacteriemia, por lo que resulta conveniente su obtención. Esta
situación es más frecuente en pacientes ancianos, diabetes mellitus, obstrucción vía urinaria e infección por
Serratia o Klebsiella. No hay evidencia de que los hemocultivos positivos conlleven peor pronóstico o
requieran antibioterapia más prolongada.
Tabla IV. Indicaciones de evaluación radiológica en pielonefritis aguda urgente.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [594]
[39] INFECCIONES DEL TRACTO URINARIO
3.6. Pruebas de imagen (Tabla IV)
Radiografía de abdomen: está indicada si se sospecha la existencia de litiasis (90% de los
cálculos son radiopacos) o si el paciente es diabético y presenta pielonefritis grave (permite
descartar la presencia de gas en caso de una pielonefritis enfisematosa). Asimismo, también se
podría observar aumento o deformidad de la silueta renal que sugeriría hidronefrosis, absceso
renal, hematoma o tumor.
Otro dato indirecto es la pérdida de la interfase grasa entre el psoas y el riñón que indicaría
absceso en dicho músculo. En el caso de encontrar algún indicio de estas patologías se
recomienda la realización de otra prueba de imagen (ecografía o TC abdominal).
Ecografía y/o TC abdominal: se requiere una evaluación radiológica para identificar
alteraciones anatómicas que predisponen a la infección, para buscar factores que dificulten la
respuesta a la terapia (cálculos, necrosis papilar u obstrucción) o para buscar alguna
complicación de la PNA (abscesos, pielonefritis enfisematosa). En general, es preferible la TC
abdominal a la ecografía porque es más sensible, tanto para las anomalías renales como para
delimitar la extensión de la enfermedad, llegando a evidenciar abscesos < 2 cm y áreas de
nefritis aguda focal.
4. PIELONEFRITIS COMPLICADA
Es la progresión de la infección del tracto urinario superior a una de las entidades que se describen
y resumen en la tabla V. Generalmente, requieren antibioterapia de forma prolongada (Tabla II) y, en
ocasiones, tratamiento quirúrgico.
Tabla V. Pielonefritis complicada.
5. TRATAMIENTO
Para decidir la pauta de tratamiento antibiótico empírico en la PNA se ha de valorar si el paciente
tiene o no criterios de ingreso hospitalario (Tabla VI) y los posibles microorganismos causales según el tipo
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [595]
[39] INFECCIONES DEL TRACTO URINARIO
de paciente. En caso de que el paciente refiera alergia a betalactámicos, se debe solicitar valoración por
parte del Servicio de Alergia para descartar o confirmar dicha sensibilización. En situaciones de gravedad en
la que se precise el uso de los mismos se podría proceder a desensibilización. Se debe considerar la
valoración por parte del especialista en Urología en el caso de la PNA complicada.
5.1. Pielonefritis sin criterios de ingreso hospitalario
El tratamiento se iniciará con la administración parenteral de una cefalosporina de amplio espectro
(ceftriaxona), y en el caso de alérgicos a betalactámicos se puede utilizar un amino- glucósido, seguido de
un periodo de observación de 24 horas. En ausencia de complicaciones, al alta continuar con una
cefalosporina de 2ª o 3ª generación o una fluorquinolona por vía oral (a pesar de que ha aumentado el
número de cepas de E. coli resistentes a quinolonas, el porcentaje de estas cepas aislados en PNA es algo
inferior al de las cistitis). Algunos estudios, demuestran que si los microorganismos son sensibles, el
tratamiento por vía oral tiene una eficacia similar al parenteral en el caso de las quinolonas y
cefalosporinas.
Tabla VI. Criterios de ingreso en la pielonefritis aguda.
5.2. Pielonefritis con criterios de ingreso
Todas las pautas de tratamiento son por vía intravenosa.
Paciente sin riesgo de infección por microorganismo multirresistente ni criterios de sepsis con
datos de gravedad
Cefalosporinas de 3ª generación (ceftriaxona o cefotaxima), y en caso de alergia a
betalactámicos, aztreonam o un aminoglucósido invenoso o intramuscular en dosis única diaria.
Paciente con riesgo de infección por microorganismos multirresistentes o criterios de sepsis
con datos de gravedad
Monoterapia con un carbapenem (imipenem, meropenem o doripenem) o piperacilina-
tazobactam o combinación de una cefalosporina con actividad antipseudomonas (ceftazidima o
cefepime) asociado a ampicilina. Asimismo, se debe asociar un aminoglucósido si existen
criterios de sepsis o shock séptico. En caso de alergia a betalactámicos, podrían emplearse
amikacina (asociada o no a aztreonam) o fosfomicina (si existe sospecha de infección por
bacilos gramnegativos con resistencia a aminoglucósidos) y un antibiótico activo frente a
Enterococcus (vancomicina o teicoplanina, y si no es posible linezolid o daptomicina).
A partir de la defervescencia, el tratamiento puede continuarse por vía oral con un antibiótico
elegido de acuerdo con el antibiograma hasta completar 7-14 días. En caso de PNA complicada
parece prudente completar 14-21 días de tratamiento.
Es conveniente practicar un segundo urocultivo a las 72 horas de tratamiento antibiótico de
una PNA, sobre todo si persiste la fiebre, existe insuficiencia renal avanzada o se trata de una
PNA complicada, así como a las dos semanas de haber finalizado el tratamiento.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [596]
[39] INFECCIONES DEL TRACTO URINARIO
VI. PROSTATITIS AGUDA
1. INTRODUCCIÓN
Las prostatitis son un conjunto heterogéneo de enfermedades, no siempre infecciosas; la
clasificación más aceptada es la propuesta por el National Institute of Health que se observa en la tabla VII.
La prostatitis aguda o tipo I es una infección aguda de la glándula prostática, casi siempre de origen
bacteriano. Su importancia radica en que puede complicarse rápidamente con sepsis y bacteriemia.
Cualquier infección urinaria febril en un varón debe sugerir a priori una prostatitis aguda, ya que la
glándula prostática actúa como “barrera” anatómica contra una potencial contaminación ascendente de la
vía urinaria (la cistitis con fiebre y la pielonefritis en el varón son excepcionales).
Tabla VII. Clasificación de las prostatitis según el National Institute of Health.
2. ETIOPATOGENIA
Sobre todo, enterobacterias, principalmente E. coli, y en segundo lugar otras como Proteus,
Klebsiella, Enterococcus, Pseudomonas o Serratia; también Staphylococcus. Son factores de riesgo los
antecedentes urológicos o anomalías morfológicas del tracto urinario, sondaje vesical u otras
manipulaciones de las vías urinarias, y estados de inmunodepresión. Otros como traumatismos (montar en
bicicleta o a caballo), deshidratación o abstinencia sexual no están tan claros. En menores de 35 años
también son posibles gérmenes propios de infecciones de transmisión sexual (N. gonorrhoeae, Chlamydia,
Mycoplasma, etc.). En pacientes con SIDA puede verse también gérmenes oportunistas.
La puerta de entrada habitual es la uretra por vía ascendente o bien inoculación directa al realizar
una biopsia transrectal. Otras vías de infección son menos frecuentes.
3. CLÍNICA
La clínica se fundamenta en tres pilares:
Dolor: prostático o perineal, pélvico, escrotal o peneano, hipogástrico o lumbar bajo.
Síntomas del tracto urinario inferior (STUI): sobre todo los de llenado (polaquiuria, urgencia,
incontinencia) y los STUI posmiccionales (sensación de evacuación incompleta, goteo
posmiccional). También micción dolorosa o pruriginosa, hematuria u orina turbia, y STUI de
vaciado (dificultad de inicio, chorro débil…) por obstrucción secundaria a la inflamación de la
uretra prostática.
Afectación general: fiebre elevada, escalofríos y artromialgias, pudiendo complicarse con
sepsis.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [597]
[39] INFECCIONES DEL TRACTO URINARIO
Exploración física: en el tacto rectal la próstata suele estar aumentada de tamaño y
consistencia, caliente y dolorosa; a veces se nota una zona fluctuante sospechosa de absceso.
En ocasiones el tacto rectal es normal. El masaje prostático está contraindicado en la prostatitis
bacteriana aguda por el riesgo de provocar bacteriemia. Hay que descartar la presencia de
globo vesical por retención urinaria. También puede haber lumbalgia a la palpación.
En caso de piospermia o hematospermia hay que descartar una tuberculosis urogenital.
4. PRUEBAS COMPLEMENTARIAS
Un sistemático y sedimento de orina puede mostrar piuria, hematuria y bacteriuria. Un hemograma
suele mostrar leucocitosis o a veces leucopenia. La bioquímica básica no tiene alteraciones específicas; la
PCR no influye en la conducta terapéutica, pero su normalización constituye un marcador evolutivo de
eficacia de la misma. El PSA suele estar elevado por la infección y no tiene valor; tarda al menos 2-3 meses
en estabilizarse desde la resolución de la infección.
Es muy importante tomar cultivos de orina y también de sangre si hay sospecha de bacteriemia,
pues sus resultados nos ayudarán a elegir el mejor tratamiento.
La radiografía simple de abdomen y la ecografía de aparato urinario no suelen aportar datos. En
caso de sospecha de absceso prostático las pruebas de imagen indicadas serían ecografía transrectal o TC
(menos sensible para abscesos de pequeño tamaño).
Para el diagnóstico y diferenciación de las prostatitis crónicas se utiliza la prueba de Stamey-Meares
de los 4 vasos, o la prueba simplificada de dos muestras. Se realizan en las consultas de Urología.
5. TRATAMIENTO
Comienzo con antibioterapia empírica frente enterobacterias, habitualmente parenteral, como
penicilinas de amplio espectro, cefalosporinas de 3ª generación o fluoroquinolonas. Cualquiera de ellos se
puede combinar al inicio con un aminoglucósido. En este punto de la infección, la barrera lipoepitelial
prostática es poco selectiva debido a la inflamación, permitiendo bien el paso de estos fármacos.
Tras 24-48 horas de control de la fiebre y los parámetros de infección, se puede continuar con
antibioterapia oral, dirigida por los resultados de los cultivos si están disponibles: idealmente quinolonas
por su mejor penetración en la próstata, y en segundo lugar el cotrimoxazol; no obstante, se debería evitar
usar levofloxacino para no favorecer la aparición de neumococos resistentes. Se debe mantener el
tratamiento hasta completar 4 semanas para evitar la recaída, la recidiva y el desarrollo de prostatitis
bacteriana crónica. En función de la evolución, el paciente precisará ingreso hospitalario, o bien, solo
observación durante 24-48 horas.
En caso de sondaje vesical previo, manipulación urológica o ingreso reciente, se aconseja inicio con
antibióticos activos frente a Pseudomonas (ceftazidima, cefepime, aminoglucósidos) asociados a ampicilina,
o bien, monoterapia con piperacilina-tazobactam o un carbapenem.
En casos de retención aguda de orina se recomienda generalmente una cistostomía suprapúbica, ya
que un sondaje vesical entraña el riesgo de provocar un shock séptico o la ruptura de un virtual absceso
prostático; no obstante puede intentarse en algunos casos, por parte del urólogo, un sondaje con suma
cautela. Cuando simplemente hay una dificultad miccional sin retención, la asociación de un alfa-
bloqueante (por ejemplo, tamsulosina) puede ayudar a relajar la uretra prostática y permitir la evacuación
de la orina.
En los casos de prostatitis bacteriana crónica los regímenes terapéuticos serán más largos, con
cultivos de control y seguimiento en consultas de Urología. Los pacientes con sospecha de un trastorno
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [598]
[39] INFECCIONES DEL TRACTO URINARIO
urológico subyacente, como hiperplasia benigna de próstata, también deberán ser estudiados por el
urólogo.
6. COMPLICACIONES
Si persisten la fiebre y los síntomas a las 72 horas de tratamiento antibiótico habría que descartar
un absceso prostático, que podría requerir drenaje mediante punción (habitualmente perineal, también
transrectal) o incluso resección transuretral prostática.
La prostatitis también puede asociarse con epididimitis u orquiepididimitis, que en caso de
pacientes jóvenes debe sugerir como etiología un germen de transmisión sexual.
Por último, puede considerarse una complicación también el desarrollo de prostatitis bacteriana
crónica (causa más frecuente de ITU de repetición en el varón). Se manifiesta con dolor y síntomas
urinarios sobre todo de llenado, de al menos 3 meses de evolución. Para el diagnóstico diferencial se
utilizan las pruebas antes mencionadas. El tratamiento de elección son fluoroquinolonas 6-8 semanas, y en
caso de resistencia otros antibióticos durante 8-12 semanas (cotrimoxazol, fosfomicina, doxiciclina,
macrólidos, etc.). Será precisa la realización de cultivos de control (a los 15 días, al mes y a los 6 meses) y
seguimiento en consultas de Urología.
VII. EPIDIDIMITIS Y ORQUITIS
1. DEFINICIÓN
Las epididimitis y orquitis pueden ocurrir de forma aislada o asociada como orquiepididimitis; esta
última habitualmente corresponde a la extensión al testículo ipsilateral de una epididimitis. Casi siempre
son unilaterales. Se diferencian en agudas o crónicas según la duración sea menor o mayor a 6 semanas,
respectivamente.
2. ETIOPATOGENIA
Las epididimitis suelen ser infecciosas, por diseminación retrógrada desde la uretra a través del
conducto deferente. Si progresa al testículo se tratará de una orquiepididimitis verdadera. Casi siempre es
unilateral y aguda.
Desde la pubertad hasta los 35 años suele corresponder a una ITS por Chlamydia trachomatis y/o
Neisseria gonorrhoeae, pudiendo asociarse a uretritis.
En niños prepúberes y en mayores de 35 años (y sobre todo mayores de 50 años) los causantes
suelen ser los uropatógenos habituales, favorecido por malformaciones urogenitales o patología urológica
obstructiva: reflujo de orina colonizada por gérmenes facilitado por el aumento de presión, que vence al
mecanismo antirreflujo del verumontanum.
Otras causas de afectación son traumatismos, enfermedades sistémicas (sarcoidosis, enfermedad
de Behçet, púrpura de Schöenlein-Henoch…) o acúmulo de metabolitos (amiodarona). En epididimitis
crónicas hay que sospechar infecciones sistémicas (tuberculosis o tratamiento con BCG, lúes, brucelosis o
criptococosis).
En cuanto a la orquitis, su principal causa es la infecciosa, habitualmente a raíz de una epididimitis
(orquiepididimitis). La orquitis pura de etiología infecciosa es más infrecuente y de transmisión
hematógena, sobre todo el virus de la parotiditis (orquitis urliana), también virus herpes, ecovirus, virus
Coxsackie, etc.; el CMV puede transmitirse también de forma venérea, sobre todo en SIDA. Por último,
algunos hongos y parásitos, sobre todo, en inmunodeprimidos. También puede haber orquitis secundaria a
enfermedades sistémicas por la implicación de fenómenos autoinmunes.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [599]
[39] INFECCIONES DEL TRACTO URINARIO
3. CLÍNICA
La epididimitis aguda cursa con dolor e inflamación local, solo en el epidídimo o afectando también
al testículo en los casos de orquiepididimitis. El dolor en ambos casos aumenta con la palpación y se alivia
con la elevación del testículo (signo de Prehn positivo). La afectación del cordón espermático provoca un
dolor irradiado a la ingle. También puede haber hidrocele reactivo. Se puede asociar con fiebre, y, por otro
lado, con síndrome miccional o con secreción uretral, debiendo descartar la asociación con uretritis o
prostatitis, según el caso.
4. PRUEBAS COMPLEMENTARIAS
Si se sospecha ITS o asociación de uretritis, en el exudado uretral, recogido mediante hisopo, la
observación de diplococos gramnegativos será diagnóstica de gonococo, mientras que una muestra estéril
con leucocitos hará sospechar uretritis no gonocócica, clamidias en 2/3 de los casos. Otra opción para estos
agentes son pruebas de detección de antígenos o ácidos nucleicos, en secreción uretral u orina (chorro
inicial). Puede estar indicado además descartar infección asociada por otras ITS como VIH, VHB, lúes…,
según la anamnesis.
El urocultivo, de la segunda parte del chorro miccional, en caso de sospecha de uropatógenos
habituales; también para gonococo. Hemocultivos en caso de fiebre, escalofríos, etc.
Si se sospecha tuberculosis urogenital o cuando la evolución con el tratamiento habitual no es
favorable, debe buscarse bacilos de Koch en orina e igualmente descartar una tuberculosis sistémica.
Las pruebas de imagen no suelen ser necesarias inicialmente, salvo duda diagnóstica de otras
causas de dolor escrotal agudo, sobre todo para descartar una torsión del cordón espermático, mediante
ecografía-doppler (o menos frecuentemente gammagrafía con tecnecio).
También en caso de mala evolución o tendencia a la cronicidad, mediante ecografía escrotal se
puede observar la asociación de complicaciones.
5. TRATAMIENTO
El tratamiento del dolor requiere reposo, elevación testicular mediante suspensorio, analgésicos o
AINE y aplicación local de frío.
En sospecha de ITS, para cubrir gonococo y clamidia se recomienda ceftriaxona 250 mg
intramuscular en dosis única, más doxiciclina 100 mg/12 horas durante 10 días (o azitromicina 1 g oral en
dosis única en pacientes que no toleren las tetraciclinas). Alternativa: ceftriaxona más quinolonas con
buena actividad contra clamidias y buena penetración en tracto urogenital, como levofloxacino u
ofloxacino, durante 10 días a las dosis habituales. Si se trata de orquiepididimitis, tratamiento durante tres
semanas.
El estudio y tratamiento de las parejas sexuales de los dos últimos meses es obligatorio, evitando el
coito sin preservativo hasta que el paciente y sus contactos hayan sido tratados. La educación sanitaria de
estos pacientes evitará nuevos episodios.
En sospecha de uropatógenos habituales (según edad, patología urológica conocida o manipulación
reciente de vía urinaria), puede comenzarse tratamiento empírico con cotrimoxazol o quinolonas vía oral,
en las formas leves, o bien en formas graves cefalosporina de 3ª generación parenteral, asociada o no a
aminoglucósidos, continuando posteriormente con quinolonas o cotrimoxazol vía oral cuando haya mejoría
y 24-48 horas de apirexia (si se dispone de cultivos positivos, adecuar el tratamiento al antibiograma). El
tratamiento se puede mantener dos semanas en caso de epididimitis o tres en casos de orquiepididimitis. Si
hay asociación con prostatitis, estará indicado prolongar más el tratamiento.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [600]
[39] INFECCIONES DEL TRACTO URINARIO
En ancianos o portadores de sonda vesical puede estar indicado asociar ampicilina para cubrir
enterococos, o monoterapia con piperacilina-tazobactam o tigeciclina intravenosas. Posteriormente habrá
que ajustar el tratamiento al antibiograma, en cualquiera de los casos.
En los casos sin hallazgo de germen (ni uretritis exudativa ni bacteriuria en orina) el tratamiento
depende del perfil del paciente: en un paciente menor de 35 años sin manipulación endouretral reciente,
puede elegirse tetraciclinas ante la alta probabilidad de infección por clamidias; no obstante, las quinolonas
presentan la ventaja de ser eficaces en ambas situaciones (sospecha de clamidias y sospecha de
enterobacterias).
La orquitis urliana no tiene tratamiento específico, se maneja simplemente con medidas generales.
6. COMPLICACIONES
La resolución clínica suele ser lenta, pudiendo desaparecer el dolor y persistir el engrosamiento
epididimario y/o testicular algunas semanas más. Sin embargo, si persiste la fiebre a los 3 días de
tratamiento correcto, debe descartarse la formación de abscesos, que pueden requerir drenaje o incluso
orquiectomía. También está indicada la exploración quirúrgica urgente si hay dudas sobre torsión testicular
o cáncer.
La epididimitis crónica es secundaria a una infección mal tratada, y se manifiesta por induración
epididimaria y dolor crónicos (mayor de 6 semanas), con oclusión tubular frecuente. También puede ser
secundaria a tuberculosis.
Las recidivas pueden deberse a un mal tratamiento o a una pareja no tratada.
Otras complicaciones son isquemia e infarto testicular, atrofia testicular tardía o infertilidad.
VIII. INFECCIONES URINARIAS ASOCIADAS A CATÉTERES URINARIOS
1. DEFINICIÓN
Son las infecciones en portadores de cualquier tipo de catéter urinario, o que lo han tenido hasta
las últimas 48 horas. La sonda vesical es el tipo de catéter más frecuentemente usado, pero los otros tipos
de catéteres de derivación urinaria, usados por el urólogo, también implican un riesgo de infección, mayor
si cabe, porque la necesidad de su colocación será secundaria a alguna patología urológica que añade algún
factor de riesgo.
La infección urinaria es el tipo de infección nosocomial más frecuente, con o sin catéter, y además
constituye un reservorio importante de microorganismos resistentes y es causa de bacteriemia nosocomial
secundaria. Con el sondaje vesical (u otros catéteres) aumenta el riesgo de infecciones urinarias.
La posibilidad de bacteriuria se relaciona directamente con el tiempo de cateterización (hasta el
100% en sondajes prolongados −a partir de 30 días−). En la mayoría de casos se trata de bacteriuria
asintomática, que no requiere despistaje ni tratamiento salvo excepciones (ver Apartado II). Suele tratarse
de flora habitual del colon, lo más frecuente E. coli; en sondajes prolongados puede haber flora mixta.
La candiduria es más común en pacientes diabéticos y en los que toman algún antibiótico, pero
suele ser una simple colonización y la candidemia es excepcional.
Otros factores de riesgo para contaminación además del tiempo de sondaje son: sexo femenino,
diabetes mellitus, pacientes mayores, estados de inmunodepresión, colonización de bacterias en la bolsa o
mal cuidado de la sonda (manipulaciones sin adecuada asepsia, no mantener un sistema de drenaje
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [601]
[39] INFECCIONES DEL TRACTO URINARIO
cerrado, elevar la bolsa de drenaje por encima del nivel de la vejiga favoreciendo el reflujo de orina hacia el
interior, etc.).
2. CLÍNICA
La presencia aislada de síntomas irritativos como dolor suprapúbico, disuria, etc., ocurre a veces
por mala tolerancia de la sonda o por sondaje traumático, así que por sí solos estos síntomas no son
indicativos de infección. Habrá que comprobar que la sonda está bien colocada y no está obstruida, y si
persisten los síntomas irritativos, sí será más probable que se trate de una ITU.
La presencia de fiebre debe hacer sospechar el diagnóstico pero es imprescindible descartar el
origen de la misma en otro foco para poder establecer el tratamiento más adecuado.
Así, la presencia de fiebre, escalofríos, dolor suprapúbico o pélvico, hematuria, disuria y en
ocasiones dolor en flanco, junto con catéter urinario o retirada del mismo 48 horas antes o menos, debe
hacer sospechar una ITU, debiendo descartar previamente otros focos de infección. En ocasiones no hay
síntomas locales sino disminución del nivel de consciencia, delirios, malestar general, etc., o una
combinación de todos ellos.
A la exploración puede haber dolor a la palpación hipogástrica o en fosas renales, hay que descartar
la presencia de globo vesical por mal funcionamiento de la sonda, y en varones debe descartarse prostatitis
u orquiepididimitis asociada.
3. PRUEBAS COMPLEMENTARIAS
Antes de comenzar con antibioterapia, debe recogerse urocultivo tras retirar la sonda, del chorro
medio de la micción. Si no es posible su retirada, recogerlo tras recambiarla, para cultivar bacterias
procedentes de la vejiga y no las presentes en el biofilm del catéter; debe recogerse a través del puerto de
extracción o en su defecto al salir la orina de la sonda, pero nunca de la bolsa de drenaje que tiene riesgo
de estar contaminada.
El sistemático de orina en un paciente sondado es patológico por defecto, por lo que no es útil en el
diagnóstico. La analítica sanguínea mostrará reactantes de fase aguda elevados.
Si hay fiebre y signos de sepsis conviene tomar muestras para hemocultivo también. Deben
descartarse otros posibles focos como origen del cuadro febril, siendo necesario en ocasiones la realización
de otras pruebas como radiografía de tórax, coprocultivo, etc.
4. TRATAMIENTO
No está indicado el cultivo de orina en ausencia de síntomas, al igual que no está indicado el
tratamiento de la bacteriuria asintomática salvo excepciones:
Embarazadas por el riesgo de complicaciones para el feto.
Antes de intervenciones traumáticas del aparato urinario.
Para intentar erradicar un organismo especialmente virulento que sea prevalente en una
determinada unidad.
Bacteriuria por gérmenes con alta incidencia de bacteriemia, por ejemplo, Serratia marcescens.
En los casos de infección sintomática, lo primero es retirar el catéter si es posible, o al menos
recambiarlo (sobre todo, si lleva puesto más de una semana). Se inicia tratamiento empírico basado en
cultivos previos del paciente o en patrones de susceptibilidad local, por ejemplo, con Cefalosporinas de 3ª
generación para bacilos gramnegativos, o antibióticos que cubran Pseudomonas o cocos grampositivos si se
sospechan estos gérmenes. El tratamiento debe ajustarse cuando estén disponibles los resultados del
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [602]
[39] INFECCIONES DEL TRACTO URINARIO
antibiograma, y mantenerlo de 5 a 21 días según el agente etiológico, las comorbilidades y la respuesta del
paciente.
No está indicado el tratamiento de la candiduria asintomática, pero debe considerarse la retirada
del catéter. En los casos sintomáticos o con candidemia está indicado el tratamiento con antifúngicos
sistémicos.
5. PREVENCIÓN
Ya que la probabilidad de bacteriuria aumenta con el tiempo de cateterización, conviene siempre
una retirada lo más precoz posible, así como evitar su colocación si no es imprescindible.
O bien usar alternativas con menos riesgo: sondaje vesical intermitente, colectores peneanos o
talla vesical en pacientes apropiados. Debe minimizarse el trauma uretral mediante el uso de lubricante y la
sonda de menor calibre posible. El sistema de drenaje debe ser cerrado, y hay que mantener siempre la
bolsa de drenaje por debajo del nivel de la vejiga. La manipulación de la sonda debe hacerse en condiciones
de asepsia.
El principio de retirada precoz se aplica igualmente a otros tipos de catéteres urinarios, pero estará
supeditado a la patología que ha conducido a su colocación.
En los sondajes prolongados debe cambiarse la sonda periódicamente, habitualmente cada mes en
caso de sondas de látex o cada 2 meses las de silicona, como regla general. No está indicada la profilaxis en
los recambios (no hay datos que hablen a favor de la misma). Tampoco está indicada la terapia
antimicrobiana supresora crónica ni los antibióticos o los antisépticos tópicos aplicados en sonda o meato
uretral.
IX. INFECCIÓN DEL TRACTO URINARIO EN LA EMBARAZADA
1. INTRODUCCIÓN
Los cambios morfológicos y funcionales que se producen en el tracto urinario durante la gestación
hacen que la ITU sea la 2ª patología médica más frecuente durante el embarazo. Su incidencia se estima en
un 5-10% y la etiología es similar a la de las mujeres no gestantes con un predominio de los bacilos
gramnegativos (90-85%), siendo el más frecuente E. coli.
Con respecto a la elección del tratamiento antibiótico tendremos en cuenta que el uso de
betalactámicos, fosfomicina-trometamol y nitrofurantoína (categoría A/B de la FDA), cumple con los
criterios de seguridad y eficacia requeridos en la mayoría de los casos. Se debe evitar, sin embargo,
ceftriaxona el día antes del parto por la posibilidad de kernicterus.
Entre los carbapenemas se han visto efectos fetales en animales con imipenem-cilastatina, por lo
que se prefiere utilizar ertapenem, meropenem o doripenem. No se han confirmado los datos de un
estudio retrospectivo de casos y controles que sugirieron un vínculo entre la nitrofurantoína y las
malformaciones congénitas, aunque si existen otras opciones no se debe utilizar en el primer trimestre.
En circunstancias como alergias o infecciones graves puede considerarse el empleo de aztreonam
(categoría A/B) o de aminoglucósidos como gentamicina o tobramicina (categoría C). El trimetroprim
(categoría C) al ser un antagonista del ácido fólico debe evitarse en el primer trimestre de gestación. Las
sulfamidas (categoría C), deben evitarse en el tercer trimestre por riesgo de ictericia, anemia hemolítica y
kernicterus en el recién nacido. También es mejor no utilizar fluoroquinolonas (categoría C), ante sus
posibles efectos en el desarrollo del cartílago fetal.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [603]
[39] INFECCIONES DEL TRACTO URINARIO
2. ENTIDADES CLÍNICAS
Las tres entidades clínicas con mayor repercusión son:
2.1. Bacteriuria asintomática
Su detección y tratamiento son fundamentales durante la gestación, pues se asocia a parto pretérmino,
bajo peso al nacer y elevado riesgo de progresión a pielonefritis aguda y sepsis. Es necesario realizar un
cribado universal mediante la realización de urocultivo entre la 12ª-16ª semanas de gestación (momento
de mayor prevalencia) o en la 1ª visita médica. Los antibióticos más empleados en el tratamiento son:
betalactámicos, nitrofurantoína, ambos en pauta corta de 3-7 días; y fosfomicina-trometamol en dosis
única. El cuadro recurre en un 20-30% de los casos por lo que es necesario un seguimiento, repitiendo el
urocultivo a la semana postratamiento. Si es negativo, se realizarán urocultivos mensuales hasta el parto.
En caso de recurrencia, usar pautas largas y considerar la supresión continua con antibióticos.
2.2. Cistitis aguda
Suele aparecer en el segundo trimestre y no acostumbra a progresar a pielonefritis aguda. El tratamiento es
similar al de la bacteriuria asintomática.
2.3. Pielonefritis aguda
Principal causa de ingreso no obstétrico en la gestante, fundamentalmente en el segundo y tercer
trimestres. La afectación es derecha en un 40% de los casos y bilateral en un 25%. En el 10-20% de los casos
conlleva una complicación grave con el consiguiente riesgo vital tanto materno como fetal.
Debe realizarse diagnóstico diferencial con las siguientes entidades: corioamnionitis, colecistitis,
desprendimiento de placenta, mioma infartado, rotura de quiste ovárico, trabajo de parto y apendicitis.
Con respecto al tratamiento, como primera opción se recomienda tratamiento con betalactámicos
por vía intravenosa (amoxicilina-clavulánico, cefuroxima o ceftriaxona); y en caso de alergia a los mismos
como 2ª opción por vía parenteral: aztreonam, gentamicina o tobramicina y fosfomicina. Si la fiebre ha
descendido a las 48-72 horas, se pasará el tratamiento antibiótico a vía oral según el resultado del
antibiograma hasta completar 14 días de tratamiento.
X. INFECCIÓN URINARIA RECURRENTE
Las infecciones urinarias recurrentes se definen como 3 episodios de infección urinaria en los
últimos 12 meses o dos episodios en los últimos 6 meses. Se clasifican según su patogenia en recidivas y
reinfecciones.
1. RECIDIVAS
Representan un 20% de las recurrencias, se presentan generalmente en las dos primeras semanas
tras la aparente curación de la infección urinaria y son debidas a la persistencia de la cepa original en el
foco de la infección, bien por tratamiento antibiótico inadecuado o demasiado corto, bien por la existencia
de una anomalía genitourinaria o el acantonamiento de las bacterias en un lugar inaccesible al antibiótico.
Incluso pueden aparecer sin causa evidente, en cuya situación se aconseja administrar el antibiótico según
antibiograma durante 4-6 semanas.
Si la infección recidiva con la pauta de 6 semanas y se trata de un niño/a < 5 años, una embarazada
o un paciente con uropatía obstructiva no corregible con riesgo de lesión renal o infecciones urinarias
sintomáticas de repetición, se aconseja profilaxis durante 6-12 meses con las siguientes pautas de
antibióticos (se elegirán en función de la sensibilidad del microorganismo aislado en el último episodio,
evitando en la medida de lo posible el uso de quinolonas dada la posibilidad de generar resistencias): medio
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [604]
[39] INFECCIONES DEL TRACTO URINARIO
comprimido de cotrimoxazol (40 mg de trimetoprim y 200 mg de sulfametoxazol), 100 mg de trimetoprim,
dosis bajas de quinolonas (ofloxacino 200 mg/día o ciprofloxacino 250 mg/día), cefalexina 250 mg/día, 50
mg de nitrofurantoína o fosfomicina-trometamol 3 g cada 7-10 días. La profilaxis se administra por la
noche, y se inicia una vez tratada la última infección. Se requiere la realización de urocultivos de
seguimiento cada 1-2 meses. Si la bacteriuria recidiva y el microorganismo se hace resistente, se cambiará
de antibiótico (Figura 2).
Figura 2. Infección del tracto urinario recurrente-recidiva.
2. REINFECCIONES
Representan un 80% de las infecciones urinarias recurrentes y son nuevas infecciones urinarias
causadas por una cepa distinta. Sin embargo, en mujeres jóvenes sexualmente activas pueden estar
causadas por la misma cepa cuyo reservorio sería el tracto digestivo o bien las propias células uroepiteliales
dónde se crearían biopelículas. Las reinfecciones suelen producirse más tardíamente que las recidivas (en
general, más de dos semanas tras la infección urinaria inicial). También se considera como reinfección
cuando, entre las dos infecciones urinarias, se documenta un urocultivo estéril. En función de las
características del paciente se recomiendan las siguientes medidas (Figura 3):
Mujeres sexualmente activas: se aconseja evitar métodos anticonceptivos con espermicidas. En
estudios recientes se ha demostrado que adquirir el hábito de orinar con frecuencia y realizar
una micción poscoital no disminuyen la incidencia de recurrencias. Si estas son poco frecuentes
(< 3 al año) cada episodio se tratará aisladamente. Si las infecciones recurren > 3 veces al año
se indicará profilaxis antibiótica diaria con dosis bajas de antibióticos como en el caso de las
recidivas durante 6-12 meses, realizando urocultivos de control mensuales. Si las infecciones se
relacionan con la actividad sexual, se aconsejará profilaxis poscoital con las mismas pautas que
en las recidivas.
Mujeres posmenopáusicas: si las recurrencias son sintomáticas y se relacionan con una
anomalía urológica (incontinencia urinaria, cistocele, residuo posmiccional) los esfuerzos
terapéuticos irán encaminados a corregirla; en caso de no ser posible, se aconsejará profilaxis
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [605]
[39] INFECCIONES DEL TRACTO URINARIO
antibiótica durante 6-12 meses. Como alternativa a la profilaxis antibiótica, pueden aplicarse
cremas vaginales de estrógenos, que ha demostrado en algún estudio disminuir la incidencia de
ITU de repetición, sin embargo no se ha comparado con estrategias con antibióticos.
Figura 3. Infección del tracto urinario recurrente-reinfección.
En ambos casos: en pacientes con < 3 episodios al año, se contempla realizar auto-tratamiento
siempre que la paciente tenga un adecuado nivel intelectual para poder establecer el
diagnóstico de cistitis y comprender las instrucciones médicas, siendo preciso control médico
en 48 horas si la evolución no es favorable.
Otras medidas como la administración de arándanos, acidificación urinaria o probióticos
intravaginales no han demostrado eficacia.
BIBLIOGRAFÍA
Arribas Rodríguez JM, Pérez Lanzac de Lorca A, Castiñeiras Fernández J. Síndrome de escroto agudo.
En: Castiñeiras Fernández J, coordinador; Carballido Rodríguez J, Franco de Castro A, Gausa Gascón L,
Robles García JE, Sánchez Chapado M, Server Pastor G, Zuluaga Gómez A, editores. Libro del
Residente de Urología. Asociación Española de Urología; 2007. p. 159-73.
Curtis-Nickel J. Prostatitis and related conditions, orchitis, and epididymitis. En: Wein AJ, Kavoussi LR,
Novick AC, Partin AW, Peters CA, editores. Campbell-Walsh Urology. Vol 1. 10th ed. Estados Unidos:
Elsevier Saunders; 2012. p. 327-56.
Gill BC, Shoskes DA. Bacterial prostatitis. Curr Opin Infect Dis. 2016;29:86.
Gimeno Argente V, Broseta Rico E, Jiménez Cruz JF. Prostatitis y dolor pelviano en el varón. En:
Castiñeiras Fernández J, coordinador; Carballido Rodríguez J, Franco de Castro A, Gausa Gascón L,
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [606]
[39] INFECCIONES DEL TRACTO URINARIO
Robles García JE, Sánchez Chapado M, Server Pastor G, Zuluaga Gómez A, editores. Libro del
Residente de Urología. Asociación Española de Urología; 2007. p. 669-84.
Glaser AP, Shaffer AJ. Urinary tract infection and bacteriuria in pregnancy. Urol Clin N Am.
2015;42:547-60.
Grabe M, Bartoletti R, Bjerklund-Johansen TE, Cai T, Çek M, Köves B, et al. Guidelines on Urological
Infections. European Association of Urology; 2015.
Grigoryan L, Trautner BW, Gupta K. Diagnosis and management of urinary tract infections in the
outpatient setting. A review. JAMA. 2014;312(16):1677-84.
Gupta K, Hooton TM, Naber KG, et al. International clinical practice guidelines for the treatment of
acute uncomplicated cystitis and pyelonefritis in women: A 2010 update by the Infectious Diseases
Society of America and the European Society for Microbiology and Infectious Diseases. Clin Infect Dis.
2011;52:e103.
Hooton TM, Bradley SF, Cardenas DD, et al. Diagnosis, prevention, and treatment of catheter-
associated urinary tract infection in adults: 2009 International Clinical Practice Guidelines from the
Infectious Diseases Society of America. Clin Infect Dis. 2010;50:625.
Hooton TM. Uncomplicated urinary tract infection. N Engl J Med. 2012;366:1028-37.
Kodner CH, Gupton EK. Recurrent urinary tract infection in women: diagnosis and management. Am
Fam Phy. 2010;82;638-43.
Medina Polo J. Estudio prospectivo de tres años de duración de las infecciones en un Servicio de
Urología: factores de riesgo, evaluación microbiológica, resistencia a antibioterapia y evolución
temporal [tesis doctoral]. Madrid: Facultad de Medicina, Departamento de Cirugía. Universidad
Complutense de Madrid; 2015.
Mensa J, Gatell JM, García-Sánchez JE, Letang E, López-Suñé E, Marco F. Guía de terapéutica
antimicrobiana. Editorial Antarés. Barcelona. 2015;492-4, 635-7.
Nicolle LE, Bradley S, Colgan R, et al. Infectious Diseases Society of America guidelinesfor the diagnosis
and treatment of asyntomatic bacteriuria en adults. Clin Infect Dis. 2005;40:643.
Pigrau C, Horcajada JC, Cartón JA, Pujol M. Infección del tracto urinario. Protocolos clínicos de la
SEIMC. 2013. Editorial Salvat.
Schaeffer AJ, Schaeffer EM. Infections of the urinary tract. En: Wein AJ, Kavoussi LR, Novick AC, Partin
AW, Peters CA, editores. Campbell-Walsh Urology. Vol 1. 10th ed. Estados Unidos: Elsevier Saunders;
2012. p. 257-326.
Vidal E, Cervera C, Cordero E, Armiñanzas C, Carratalá J, Cisneros JM, et al. Management of urinary
tract infection in solid organ transplant recipients: Consensus statement of the Group for the Study of
Infection in Transplant Recipients (GESITRA) of the Spanish Society of Infectious Diseases and Clinical
Microbiology (SEIMC) and the Spanish Network for Research in Infectious Diseases (REIPI). Enferm
Infecc Microbiol Clin. 2015; 33(10):679.
Zalmanovici Trestioreanu A, Green H, Paul M, Taphe J, Leibovici L. Antimicrobial agents for treating
uncomplicated urinary tract infection in women. Cochrane Database Syst Rev. 2010;(10).
Zalmanovici Trestioreanu A, Lador A, Sauerbrun-Cutler MT, Leibovici L. Antibiotics for asymtomatic
bacteriuria. Cochrane Database Syst Rev. 2015;4.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [607]
[40] INFECCIONES DE TRANSMISIÓN SEXUAL
40.Infecciones de transmisión sexual
Vanessa Gargallo Moneva.
Dermatología
Mª Pilar Hernández Jiménez.
Medicina Interna
Asesor: Manuel Lizasoain Hernández. Médico Adjunto de la Unidad de Enfermedades Infecciosas
I. INTRODUCCIÓN
Las enfermedades de transmisión sexual corresponden a un amplio grupo de enfermedades entre
las que se incluyen no solo procesos infecciosos sino también neoplasias, trastornos inmunitarios,
traumatismos, etc.
Las infecciones de transmisión sexual (ITS) pueden ser causadas por bacterias, virus, hongos o
parásitos. Su incidencia y expresión clínica dependen de las prácticas y tendencias sexuales. No hay que
olvidar que el hecho de tener una ITS es un importante factor de riesgo para padecer una segunda. No son
infrecuentes las coinfecciones y, además, la disrupción de la barrera epidérmica favorece tanto la
transmisión como el contagio. Por eso, ante cualquier paciente con una ITS, es obligado solicitar serologías
de virus de la hepatitis B (VHB), virus de la hepatitis C (VHC), virus de la inmunodeficiencia humana (VIH) y
sífilis. Se trata de enfermedades con un importante impacto epidemiológico, lo que conlleva la declaración
obligatoria al diagnóstico.
II. APROXIMACIÓN A LAS ÚLCERAS GENITALES
La evaluación de las úlceras genitales es siempre complicada, ya que la etiología puede ser muy
amplia. Siempre se debe establecer el diagnóstico diferencial con causas infecciosas (Tabla I), pero existen
muchas otras causas. La etiología traumática o irritativa es también bastante habitual y se debe realizar una
anamnesis cuidadosa para llegar al diagnóstico. Otras causas comunes pueden ser el exantema fijo
medicamentoso, que da lugar típicamente a una lesión ampollosa que deja una erosión superficial con un
color algo marronáceo. En estos casos, la anamnesis es fundamental. Además hay que tener en cuenta el
eritema exudativo multiforme, el síndrome de Reiter, la enfermedad de Crohn, la enfermedad de Behçet, la
enfermedad de Hailey-Hailey y el pénfigo. En estos casos, es fundamental la exploración de la piel en su
totalidad y ante una anamnesis detallada, ya que rara vez se presentará la úlcera genital como síntoma
único. Por último, ante una úlcera persistente o recurrente sobre una lesión de largo tiempo de evolución,
hay que descartar un carcinoma ulcerado.
Ante úlceras anales o perianales se debe realizar test para sífilis y virus del herpes simple (VHS).
Otras causas más infrecuentes de úlceras en esta localización son el chancroide y la donovanosis. Como
lesiones disruptivas de la barrera protectora de la piel, estas lesiones aumentan el riesgo de transmisión y
adquisición del VIH.
1. HERPES GENITAL
La infección por VHS conlleva cronicidad, con permanencia en el organismo de por vida. El principal
responsable es el VHS-2, aunque las infecciones por VHS-1 están aumentando debido a cambios en los
hábitos sexuales (mujeres jóvenes y hombres que tienen sexo con hombres).
La transmisión ocurre por contacto directo, con un periodo de incubación de 3-7 días. La
primoinfección sintomática se caracteriza por fiebre, aparición de múltiples vesículas genitales, adenopatías
locorregionales dolorosas y disuria, si bien la intensidad de los síntomas es variable y, a veces, inexistente.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [608]
[40] INFECCIONES DE TRANSMISIÓN SEXUAL
Suele seguir a un periodo prodrómico, siendo más intensa y duradera que las reactivaciones (más
frecuentes en VHS-2). Como complicaciones extragenitales (excepcionales en la infección por VHS-1), cabe
destacar la meningitis recurrente de Mollaret en VHS-2 y la proctitis herpética.
Tabla I. Diagnóstico diferencial de las úlceras genitales: características y tratamiento.
No es infrecuente que se produzcan episodios de liberación asintomática del virus, lo que dificulta
establecer el momento del contagio, por lo que el médico debe ser prudente a la hora de informar al
paciente, habida cuenta de las posibles repercusiones en la dinámica de la pareja.
Tratamiento
Siempre se recomienda tratamiento con antivirales orales (Tabla II).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [609]
[40] INFECCIONES DE TRANSMISIÓN SEXUAL
Tabla II. Tratamiento del herpes genital.
2. SÍFILIS
2.1. Concepto
Se trata de una enfermedad secundaria a la infección crónica por Treponema pallidum. Es un proceso
sistémico, con afectación posible de prácticamente cualquier órgano y presentación polimórfica.
La evolución natural de la enfermedad sin tratamiento es, tras un periodo de incubación de
aproximadamente tres semanas (3-90 días), la aparición del chancro de inoculación y de adenopatías
locorregionales, con posterior desarrollo a las 2-8 semanas de las manifestaciones de la sífilis secundaria.
Dos tercios de los pacientes controlan inmunitariamente la enfermedad en este punto; el resto continúa la
evolución hacia una fase latente asintomática que puede durar hasta 10-20 años, y la aparición tardía de
manifestaciones de sífilis terciaria en un 33% de los pacientes.
2.2. Epidemiología
Se trata de una enfermedad de transmisión predominantemente sexual, si bien es posible el contagio
transplacentario, por contacto con lesiones cutáneas (chancro, placas mucosas, exantemas cutáneos y
condilomas planos) o, excepcionalmente, transfusional en fases bacteriémicas. En los últimos 10 años, la
incidencia en España ha ido en aumento, principalmente en varones sexualmente activos.
2.3. Clínica y manejo (Tabla III)
Sífilis primaria. Aparición del chancro (véanse características en tabla I) y adenopatías
bilaterales no dolorosas en la región de inoculación. En ocasiones asocia cuadros de meningitis
o meningoencefalitis. Puede pasar desapercibida, especialmente en mujeres (lesión en cérvix) y
en el caso de prácticas anorrectales.
Sífilis secundaria. Alta variabilidad en su presentación; frecuentemente se presenta como
cuadro constitucional con fiebre, linfadenopatías generalizadas y presencia de manifestaciones
cutáneas.
Lesiones cutáneas: eritematosas máculo-papulosas, de distribución en tronco, raíz de
miembros, afectación palmoplantar, no pruriginosas. Alopecia parcheada. Condilomas
planos en pliegues. Placas mucosas orales (erosiones gris-plata, bordes eritematosos,
no dolorosas).
Más raramente: síntomas neurológicos, hepatitis aguda (patrón colestásico),
glomerulonefritis, artritis y uveítis.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [610]
[40] INFECCIONES DE TRANSMISIÓN SEXUAL
Tabla III. Fases clínicas de la sífilis: diagnóstico y tratamiento.
Sífilis latente. Se distingue una fase precoz (< 1 año) y otra tardía (≥ 1 año, infección latente
persistente o desarrollo en 33% de sífilis tardía), con diferencias en el tratamiento.
Deben buscarse de manera activa signos y síntomas neurológicos que justifiquen el estudio de
neurosífilis subyacente y lesiones cutáneo-mucosas. No es transmisible sexualmente en este
estadio, aunque sí a nivel transplacentario.
Sífilis terciaria
Cardiovascular: aortitis, aneurismas saculares aórticos, enfermedad estenótica
coronaria; rara vez, calcificación lineal en radiografía de tórax.
Gomas: piel y hueso (sífilis benigna tardía). Se incluyen el paladar y el tabique nasal. En
la sífilis congénita, la transmisión es transplacentaria, con manifestaciones a partir de
los 4 meses de edad.
Neurosífilis. Posible desarrollo en cualquier estadio de la enfermedad, más frecuentemente
manifestada como meningitis y meningoencefalitis, posible afectación neurovascular (ictus,
mielitis, afectación de pares craneales), la tabes dorsal (a los 20 años, alteración de la
sensibilidad posicional y dolor profundo → articulación de Charcot, mal perforante plantar) y la
parálisis general progresiva (a los 25-30 años, PARESIS: personalidad, afecto, reflejos exaltados,
eye (pupila de Argyll-Robertson), sensorio, intelecto, ‘speech’).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [611]
[40] INFECCIONES DE TRANSMISIÓN SEXUAL
Son indicaciones de punción lumbar: a) presencia de signos o síntomas neurológicos, otológicos u
oftalmológicos; b) sífilis terciaria previa al inicio del tratamiento; c) fracaso terapéutico (aumento al
cuádruple de títulos en las prueba serológica para la sífilis o en examen de la reagina plasmática rápida
[VDRL/RPR] en más de dos semanas, títulos VDRL/RPR suero ≥ 1:32 sin descenso adecuado en 12-24
meses); d) paciente VIH con sífilis latente tardía asintomático, con CD4 ≤ 350 céls./ml y/o título RPR ≥ 1:32
(en discusión).
2.4. Diagnóstico
Treponema pallidum es una bacteria no cultivable en los medios disponibles. Clásicamente, su diagnóstico
se basaba en la visualización con microscopia de campo oscuro. En la actualidad, el examen directo sigue
siendo de utilidad en fases precoces, en las que la serología es negativa, con visualización de las
espiroquetas presentes en las lesiones de inoculación. Existen también, en función de la disponibilidad del
laboratorio, técnicas de detección por reacción en cadena de la polimerasa (PCR), hibridación in situ,
inmunohistoquímica, etc.
El estudio serológico establece el diagnóstico de presunción en la sífilis. Como principales
limitaciones, no distingue de especies no venéreas de Treponema, habituales en determinadas regiones
endémicas (Latinoamérica). Actualmente se dispone de dos tipos de pruebas:
Treponémicas (TT): FTA-Abs (fluorescent treponemal antibody absorption), TPPA (T. pallidum
particle agglutination assay), TP-EIA (T. pallidum enzyme immunoassay) y MHA-TP
(microhemagglutination test for antibodies to T. pallidum, que es el realizado en nuestro
centro). Positivas a la primera o la segunda semana, con la aparición del chancro. Permanecen
positivas toda la vida, sin modificación en los títulos por el tratamiento. Entrañan el riesgo de
falsos positivos en regiones con baja probabilidad pretest, enfermedades autoinmunitarias y
enfermedad de Lyme.
No treponémicas (NTT): RPR (rapid plasma reagin) y VDRL (Venereal Disease Research
Laboratory). Positivas a los 10-15 días del chancro, a seis semanas de la infección. Alcanzan un
máximo al año o dos años de la infección; luego, incluso sin tratamiento, descienden
progresivamente, manteniendo títulos bajos. Los títulos de manera cuantitativa se
correlacionan con la actividad de la enfermedad y sirven para la monitorización del
tratamiento. Son causa de falsos positivos las infecciones crónicas, VIH, procesos
autoinmunitarios (lupus eritematoso sistémico [LES]), embarazo, neoplasias o la vejez.
Actualmente se utiliza una técnica de cribado u otra (TT, NTT o TT/NTT) en función del centro; en el
nuestro, la prueba realizada con la petición de laboratorio es un test treponémico, que en caso de
positividad se comprueba con RPR cuantitativo. El test realizado en líquido cefalorraquídeo (LCR) es el
VDRL.
2.5. Tratamiento
Se basa principalmente en la utilización de penicilina, ya que es el antibiótico que mayor eficacia ha
demostrado en esta enfermedad. De ahí la importancia del estudio alergológico y la desensibilización en
casos de alergia. Treponema pallidum requiere unos niveles adecuados en sangre y LCR para su
erradicación, así como una permanencia en el tiempo suficiente en relación con su periodo de replicación
(una media de 30-33 horas, más lenta en enfermedad latente). Es de elección la administración parenteral
para asegurar su biodisponibilidad.
Como alternativas al tratamiento con penicilinas (alérgicos, imposibilidad de la administración
intramuscular), se han propuesto tratamientos con ceftriaxona intravenosa o subcutánea y doxiciclina oral
con administración diaria de manera prolongada (10-14 días; 21-28 días en caso de alergia a penicilinas), de
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [612]
[40] INFECCIONES DE TRANSMISIÓN SEXUAL
los cuales se dispone de menor experiencia en cuanto a pautas y eficacia. Es obligado el estudio por el
servicio de alergología en todo paciente alérgico con sífilis, realizándose desensibilización siempre en el
caso de la mujer embarazada y en el paciente VIH.
2.6. Seguimiento
En sífilis temprana, seguimiento clínico y serológico (NTT): 6 y 12 meses; es esperable la
disminución de dos diluciones (× 4) a los 6 meses.
En sífilis latente, seguimiento a 6, 12 y 24 meses.
Un incremento de dos diluciones o más en cualquier momento del seguimiento sugiere
reinfección o reactivación, que precisará tratamiento (tres dosis intramusculares semanales).
Tras neurosífilis, se recomienda estudio de LCR cada seis meses del tratamiento en caso de
pleocitosis hasta la normalización de la celularidad del LCR (mayor sensibilidad), realizando
estudio conjunto de VDRL y proteinorraquia. Se recomienda retratamiento en caso de: a)
ausencia de descenso serológico a los 6 meses; b) ausencia de normalización del LCR a los dos
años.
Es necesario realizar el cribado de VIH en todo paciente diagnosticado de sífilis. En el caso de
coinfección, el manejo general no difiere del del paciente seronegativo. Como particularidades
encontramos clínicamente la posibilidad de chancros múltiples, coexistencia de chancro y exantema
secundario, mayor riesgo de complicaciones neurológicas y peor respuesta al tratamiento. Es fundamental
la exploración neurológica minuciosa en todos los estadios. Algunos autores recomiendan la realización de
punción lumbar en el VIH en fase latente tardía asintomática si CD4 < 350/μl y/o VDRL/RPR sangre > 1:32.
El tratamiento de elección son las penicilinas, con desensibilización en caso de alergia. Los
pacientes VIH pueden presentar falsos negativos y positivos en las serologías (de escasa relevancia), una
mayor lentitud en el descenso de los test serológicos tras el tratamiento y mayor frecuencia de reacción de
Jarisch-Herxheimer (proceso febril agudo pseudogripal [cefalea, mialgias, escalofríos] autolimitado en 24
horas habitualmente, que puede aparecer con el inicio del tratamiento; es importante informar al paciente,
siendo suficiente un manejo sintomático salvo afectación cardiaca o neurológica, en cuyo caso se
recomiendan glucocorticoides). Estos pacientes requieren un seguimiento estrecho postratamiento (en
sífilis temprana: 3, 6, 9, 12, 24 meses; en latente tardía: 6, 12, 18 y 24 meses; en el resto, según se ha
descrito para seronegativos).
III. URETRITIS, EPIDIDIMITIS Y CERVICITIS
Se recomienda realizar, siempre que sea posible, el estudio etiológico para la prevención de
complicaciones, reinfección y transmisión. En cualquier caso, y ante la sospecha clínica, se recomienda
tratamiento empírico, directamente observado al menos en la primera dosis.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [613]
[40] INFECCIONES DE TRANSMISIÓN SEXUAL
El estudio microbiológico se prefiere mediante la realización de técnica de detección de ácidos
nucleicos por PCR (nucleic acid amplification test, o NAAT) por presentar mayor sensibilidad y especificidad
que los cultivos, especialmente en caso de infección por Neisseria y Chlamydia. No excluye la realización de
tinciones sobre la muestra (tinción de Gram, azul de metileno, colorante de Giemsa) que orienten hacia una
u otra etiología. El cultivo se reserva para los casos en los que por fracaso terapéutico se sospeche error en
el diagnóstico o microorganismos resistentes, en cuyo caso se realizará también antibiograma. Las
muestras utilizadas para las técnicas mencionadas serán principalmente exudado o cepillado uretral en el
varón y exudado vaginal y/o cervical en la mujer, siendo posible también el estudio en orina (primera
micción de la mañana). La muestra deberá llegar a microbiología para su procesamiento en menos de tres
horas.
La técnica de triple toma (exudado vaginal/uretral, rectal y faríngeo) solo se indicará en caso de
factor de riesgo exposicional (tipo de práctica) y, sistemáticamente, en caso de abuso sexual.
1. URETRITIS
Es la inflamación de la uretra, y puede ser de causa infecciosa o no infecciosa (irritación química o
traumática, cristales urinarios). Clínicamente se manifiesta por disuria, prurito uretral o excreción uretral.
Es posible la presentación asintomática.
Los principales agentes infecciosos son Chlamydia trachomatis, Neisseria gonorrhoeae (en muchos
casos, asociada a infección por Chlamydia), Mycoplasma genitalium, Trichomonas vaginalis y Haemophilus
spp.
Para el estudio sindrómico, se examinará la presencia de leucocitos en sedimento urinario (>
10/campo) o exudados dirigidos, así como el test de esterasa leucocitaria positivo en la primera orina de la
mañana, asociado a la clínica apoya el diagnóstico.
2. EPIDIDIMITIS
En varones de menos de 35 años sexualmente activos, cabe pensar en etiologías de transmisión
sexual: Chlamydia trachomatis, Neisseria gonorrhoeae y bacilos entéricos (E. coli) en prácticas anales.
Requiere control evolutivo a las 72 horas. En el paciente VIH, se ampliará el diagnóstico diferencial a otras
etiologías: CMV, Salmonella, Ureaplasma, Corynebacterium, Mycoplasma, Haemophilus parainfluenzae,
Toxoplasma, hongos y micobacterias. (Ver Capítulo 39. “Infecciones del tracto urinario”).
3. CERVICITIS
Se trata de un proceso habitualmente asintomático, lo que supone un importante factor de riesgo
de transmisión. Cuando se manifiesta clínicamente, se halla alguno de los siguientes signos: exudado
endocervical visible en el canal o muestra, sangrado con friabilidad al tacto del cérvix o, también, signos
inespecíficos (aumento del flujo, sangrado intermenstrual). Su presencia aumenta el riesgo de transmisión
del VIH.
Los principales agentes etiológicos son Chlamydia trachomatis, Neisseria gonorrhoeae,
Trichomonas spp, vaginosis bacteriana, VHS-2, irritativos.
La infección por Chlamydia trachomatis es la primera causa de ITS. Se recomienda el cribado
anual en mujeres de menos de 25 años sexualmente activas, o en aquellas mayores con
factores de riesgo para su adquisición, dado el alto porcentaje de pacientes asintomáticos y la
fuerte asociación a complicaciones y secuelas en la mujer (enfermedad inflamatoria pélvica
[EIP], embarazo ectópico, infertilidad), aunque actualmente no existen programas de cribado
implantados. La detección sistemática en el tercer trimestre de embarazo y su tratamiento
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [614]
[40] INFECCIONES DE TRANSMISIÓN SEXUAL
previenen asimismo el contagio al recién nacido. Con muestra faríngea y rectal, puede ser útil
en determinados grupos y en función de las prácticas sexuales.
La infección por Neisseria gonorrhoeae constituye la segunda causa de ITS. Se mantienen aquí
las mismas recomendaciones que para C. trachomatis en las mujeres. Dado que la detección
microbiológica en exudado faríngeo ni rectal no se aconseja por su baja rentabilidad
diagnóstica, se optará por la PCR. Dada la alta tasa de resistencia a quinolonas en nuestro
medio y la creciente resistencia a cefalosporinas, se recomienda tratamiento dual con
cefalosporinas asociadas a macrólido, manteniendo sistemas de vigilancia epidemiológica para
la detección precoz de cepas resistentes y consultando en su caso con especialistas en
enfermedades infecciosas.
Respecto a la infección diseminada por gonococo, requiere ingreso y valoración especializada.
Las manifestaciones clínicas posibles son las lesiones cutáneas (acras, pustulosas o petequiales)
o articulares (poliartralgia asimétrica, tenosinovitis o artritis séptica oligoarticular), que
requieren un tratamiento de siete días con posible transición a las 48-72 horas por vía oral en
caso de buena evolución; ocasionalmente, puede complicarse con perihepatitis (síndrome de
Fitz-Hugh-Curtis) y, más raramente, con endocarditis y meningitis, que requieren tratamientos
parenterales prolongados (cuatro semanas y 10-14 días, respectivamente). El diagnóstico se
realizará mediante el aislamiento de la bacteria o detección de su antígeno en los líquidos
biológicos correspondientes.
Tratamiento
Se realizará en todos los casos, independientemente de haberse realizado estudio etiológico. Las pautas
para los tres síndromes clínicos descritos hasta ahora son:
Infección no gonocócica: azitromicina 1 g, vo, en dosis única, o doxiciclina 100 mg, vo, cada 12
horas durante siete días. (Si se sospecha Trichomonas vaginalis, asociar metronidazol 2 g, vo,
en dosis única).
Infección gonocócica: ceftriaxona 250/500 mg, im, más azitromicina 1/2 g, vo, en dosis única.
Dosis única con cefixima/cefditoren 400 mg, vo, si la vía intramuscular resulta inaccesible o se
rechaza.
En tratamiento empírico, utilizar la pauta de infección gonocócica.
IV. VAGINITIS
Consiste en una inflamación de la vagina que se manifiesta por un aumento del flujo vaginal,
prurito y mal olor. Las principales etiologías infecciosas son Trichomonas, la vaginosis bacteriana y la
candidiasis. La cervicitis puede producir un aumento del flujo vaginal indistinguible de estos procesos.
Como etiologías no infecciosas encontramos irritación química, mecánica, alérgica u otras. Ante la sospecha
clínica, son fundamentales la realización de una anamnesis y exploración que orienten hacia una entidad u
otra, el estudio del exudado vaginal (pH, microscopia, solución de hidróxido de potasio (KOH) al 10%,
tinción de Gram y técnicas basadas en PCR) y el consejo hacia la pareja (Tabla IV).
V. PROCTITIS
Se trata de una inflamación del recto que se asocia a dolor, tenesmo o exudado rectal. Los
patógenos de transmisión sexual más frecuentemente involucrados son N. gonorrhoeae, C. trachomatis
(con los serotipos responsables del linfogranuloma venéreo L1, L2, L3), T. pallidum y VHS. Ante un paciente
con síntomas de proctitis aguda, se debe hacer anuscopia, con tinción de Gram de cualquier exudado
obtenido en busca de polimorfonucleados neutrófilos.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [615]
[40] INFECCIONES DE TRANSMISIÓN SEXUAL
Se tomarán muestras para VHS, N. gonorrhoeae, C. trachomatis (con linfogranuloma venéreo [LGV]
de serotipos) y T. pallidum. Si el test para clamidias es positivo, se debe hacer PCR con serotipado para
confirmar el diagnóstico de LGV.
El tratamiento se realiza con ceftriaxona 250 mg, im, en dosis única y doxiciclina 100 mg, vo, dos
veces al día durante siete días.
Tabla IV. Clínica, diagnóstico y tratamiento de las principales vaginitis infecciosas.
VI. ENFERMEDAD INFLAMATORIA PÉLVICA
1. CONCEPTO
Comprende un espectro de procesos inflamatorios del aparato genital femenino alto, con
endometritis, salpingitis, absceso tuboovárico y peritonitis pélvica. Está producida por microorganismos
sexualmente transmisibles (Chlamydia y Neisseria) y otros (flora vaginal: G. vaginalis, anaerobios, bacilos
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [616]
[40] INFECCIONES DE TRANSMISIÓN SEXUAL
gramnegativos (BGN) entéricos, Streptococcus agalactiae; citomegalovirus (CMV), Mycoplasma hominis,
Ureaplasma urealyticum, M. genitalium.
2. DIAGNÓSTICO
Es fundamentalmente clínico. Se sospechará en mujer sexualmente activa con clínica de dolor
abdomino-pélvico en el que se descartan otras causas, y asocia al menos uno de los siguientes criterios: a)
dolor al movimiento del cérvix; b) sensibilidad uterina; c) sensibilidad de anejos. Apoyan el diagnóstico la
presencia de fiebre, secreción vaginal anormal, aumento de VSG o proteína C reactiva, documentación de
infección por Chlamydia o N. gonorrhoeae.
Para estudios más específicos, es posible la realización de una biopsia endometrial, una ecografía
transvaginal y/o una RM pélvica.
3. TRATAMIENTO
Es importante el inicio precoz (disminuye la tasa de complicaciones y secuelas) ante la sospecha, de
forma empírica y de amplio espectro. No es obligatoria la cobertura para anaerobios.
Leve-moderado: oral o intramuscular.
Ceftriaxona 500 mg, im, dosis única y doxiciclina 100 mg/12 h durante 14 días, con o sin
metronidazol 500 mg/12 h durante 14 días.
Grave: intravenoso y hospitalización (cuando no sea posible la exclusión de causas quirúrgicas,
o exista absceso tuboovárico, embarazo, gravedad clínica-fiebre elevada, incapacidad para el
seguimiento o tratamiento oral o falta de respuesta a este). Será posible la transición a vía oral
tras 24-48 horas de evolución favorable.
Cefoxitina 2 g cada 6 horas, iv, con doxiciclina 100 mg, vo/iv, cada 12 horas.
Clindamicina 900 mg cada 8 horas, iv, con gentamicina 2 mg/kg, iv, de carga; luego, 1,5
mg/kg cada 8 horas.
En portadoras de dispositivo intrauterino (DIU), existe riesgo de EIP durante las primeras tres
semanas del implante; después, no precisarán retirada de inicio, y se planteará solo si no evoluciona
favorablemente a las 48-72 horas.
VII. OTRAS INFECCIONES DE TRANSMISIÓN SEXUAL
1. VIRUS DEL PAPILOMA HUMANO
La infección por el virus del papiloma humano (VPH) puede dar lugar a la aparición de verrugas
genitales, frecuentemente por los tipos 6 y 11. Estos genotipos entrañan bajo riesgo oncogénico. Por el
contrario, otros, como el 16 o el 18, son de alto riesgo oncogénico: no producen lesiones verruciformes
pero sí pueden ser el origen de cáncer o lesiones precancerosas a nivel del cérvix, pene, vulva, vagina, ano y
orofaringe.
Cuando la infección produce lesiones genitales, estas son de tipo condiloma de forma acuminada.
El tratamiento de las verrugas genitales externas se puede realizar con podofilotoxina en crema al
0,15%, que se aplicará dos veces al día tres veces por semana, repetibles durante cuatro semanas si no
desaparecen las lesiones, o imiquimod crema al 5%, tres noches a la semana, durante 16 semanas.
Existen dos vacunas frente al VPH que protegen frente al 66% de los cánceres de cérvix: la bivalente
(Cevarix®), que protege frente a los tipos 16 y 18, y la cuadrivalente (Gadasil®), que protege frente al 16, 18,
6 y 11. Se recomienda vacunar a mujeres con cualquiera de las dos vacunas de forma rutinaria entre los 11
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [617]
[40] INFECCIONES DE TRANSMISIÓN SEXUAL
y 12 años, si bien también es aconsejable en mujeres de 13 a 26 años que no han recibido vacunación. Para
los hombres vale la misma recomendación, pero solo utilizando la vacuna cuadrivalente.
Las parejas tienden a compartir los mismos tipos de VPH, y es imposible determinar quién
transmitió la infección inicialmente. Tener VPH no significa que la pareja haya tenido sexo fuera de la
relación.
2. MOLUSCOS
Se trata de una infección producida por un poxvirus que se transmite por contacto directo o
mediante fómites, con un periodo de incubación de entre 2 y 7 semanas. En adultos, el contagio tiene lugar
frecuentemente por vía sexual, con una localización genital o abdominal inferior.
En los niños, esta vía es mucho más rara. Clínicamente son lesiones papulosas, a menudo
agrupadas, de 2-5 mm de color blanco perlado y con un centro umbilicado. Las lesiones se pueden inflamar
como respuesta a la infección. Si bien hay muchas opciones de tratamiento disponibles, desde irritantes
tópicos, como KOH, hasta la simple eliminación por curetaje o extrusión, suelen desaparecer
espontáneamente en el transcurso de un año.
3. PEDICULOSIS PUBIS
Se transmite por contacto íntimo. El principal motivo de consulta es el prurito por hipersensibilidad
a las picaduras. El tratamiento recomendado es permetrina en crema al 1% aplicada a las áreas afectadas,
que se lavarán pasados 10 minutos, o ivermectina 250 μg/kg en una toma y repitiendo la dosis a las dos
semanas.
4. ESCABIOSIS
Producida por el parásito Sarcoptes scabiei, se transmite por contacto estrecho entre personas, no
necesariamente sexual. El prurito, con frecuencia nocturno, y los surcos producidos por los parásitos,
localizados característicamente en muñecas, espacios interdigitales, axila, genitales y aréola mamaria (sin
afectación de la cabeza), son claves en el diagnóstico. El tratamiento es permetrina en crema al 5% aplicado
a todo el cuerpo, excepto la cabeza, con lavado posterior tras 8-14 horas.
Además, las medidas higiénicas son fundamentales. El paciente debe ser aislado, y el tratamiento lo
deben seguir tanto él como los convivientes, ya que puede haber casos de convivientes infectados poco
sintomáticos que sean fuente de reinfestación. Se recomienda también lavar la ropa y las sábanas; en los
objetos que no se puedan lavar, como peluches o zapatillas, la recomendación es dejarlos en una bolsa
cerrada durante al menos 72 horas, ya que la vida del Sarcoptes scabiei fuera de un huésped es de 2-4 días.
VIII. ABUSO O AGRESIÓN SEXUAL
En caso de infección de transmisión sexual en el niño o adolescente, debe investigarse el posible
abuso del menor. Así:
Específicamente en caso de sospecha de abuso o agresión reciente, de menos de 72 horas, está
indicado el traslado para valoración en un centro hospitalario, donde deberá realizarse una
anamnesis completa por la persona más experta, con exploración física detallada por parte de
los servicios de cirugía pediátrica o de ginecología, o de ambos. Es útil la toma de fotografías de
las lesiones, cuidando la privacidad del paciente. Se comunicará con el Grupo de Menores
(GRUME) de la Policía Nacional con el fin de agilizar los trámites legales, la toma de muestras y
el contacto con el médico forense (perito judicial). Para aquellos procesos de más de 72 horas,
la atención no será necesariamente hospitalaria.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [618]
[40] INFECCIONES DE TRANSMISIÓN SEXUAL
En todos los casos se dará parte urgente al juzgado de guardia y se cumplimentarán el registro
de notificación de maltrato y abandono propio de la comunidad autónoma y el anexo de
notificación al trabajador social, con el que se contactará telefónicamente (Samur Social en
noches y festivos), y quien valorará la derivación al centro de intervención de abusos sexuales
infantiles (CIASI) correspondiente. En caso de convivencia con el maltratador, está justificado el
ingreso hospitalario hasta la toma de decisiones.
Habrá de distinguirse entre muestras de interés clínico-asistencial y de interés médico-legal
(que precisan cadena de custodia, y ser recogidas con permiso judicial o por médico forense).
Deberá realizarse un estudio para ITS según lo descrito en apartados anteriores, con la
administración empírica de tratamiento adecuada en función de la edad y peso a las dosis
empleadas (previa consulta al servicio de pediatría). Se informará al respecto al microbiólogo
de guardia.
El abuso o agresión sexual en el adulto precisa un manejo similar al de la infancia (historia clínica
detallada, aviso a trabajador social de guardia, parte judicial y aviso a la Policía Nacional, con cribado para
ITS y envío de muestras al médico forense). En todo paciente susceptible de embarazo, se realizará la
determinación de HCG-β. Las muestras para estudio de ITS siempre serán en triple toma, y se aplicará
tratamiento empírico para Chlamydia, N. gonorrhoeae y Trichomonas; también, test serológicos para VIH
(que incluya cribado de infección aguda), VHB y sífilis. Debe evaluarse el riesgo de exposición al VIH con
vistas a iniciar, si procediera, profilaxis con antirretrovirales lo más temprano posible (menos de 72 horas)
y, en función del estado serológico, vacunación para VHB con o sin inmunización activa (ver Capítulo 50.
“Exposición a material biológico”).
Asimismo, se planteará, en función del caso, la necesidad de valoración por el servicio de
psiquiatría para ofrecer apoyo y tratamiento psicológico. Debe garantizarse un estrecho control clínico y
serológico posterior. Es fundamental la coordinación multidisciplinar.
BIBLIOGRAFÍA
Bennet JE, Dolin R, Blaser MJ. Mandell, Douglas, and Bennett’s Principles and Practice of Infectious
Diseases, 7.ª ed. Churchill Livingstone; 2009.
Bignell C, Unemo M; European STI Guidelines Editorial Board. 2012 European guideline on the
diagnosis and treatment of gonorrhoea in adults. Int J STD AIDS. 2013;24:85-92.
Borrel Martínez JM, et al. Guía de buena práctica clínica en infecciones de transmisión sexual. Madrid:
Ministerio de Sanidad, Política Social e Igualdad.
Centers for Disease Control and Prevention. Sexually Transmitted Diseases Treatment Guidelines,
2015. MMWR Recomm Rep. 2015;64(RR-3):1-137.
Hellín T, Rodríguez-Pichardo A, Ribera E. Enfermedades de transmisión sexual, 2.a ed. En: Bouza E,
coord. Protocolos Clínicos SEIMC. Sociedad Española de Enfermedades Infecciosas y Microbiología
Clínica.
Instituto de Salud Carlos III. Centro Nacional de Epidemiología. Vigilancia Epidemiológica de las
Infecciones de Transmisión Sexual. 1995-2008. 2010. p. 1-3.
Liang Z, Chen YP, Yang CS, et al. Meta-analysis of ceftriaxone compared with penicillin for the
treatment of syphilis. Int J Antimicrob Agents. 2016;47:6-11.
Marques AR, Cohen JI. Herpes simplex. En: Goldsmith LA, Katz SI, Gilchrest BA, Paller AS, Leffell DJ,
Wolff K. Fitzpatricks’s dermatology in general medicine. 8.ª ed. New York: McGraw-Hill; 2012. p. 2367-
82
Stary A, Stary G. Sexually transmited infections. En: Bolognia SL, Jorizzo JL. Schaffer JV. Dermatology.
3.ª ed. Philadelphia: Elsevier Health Science; 2012. p. 1367-90.
Tiplica GS, Radcliffe K, Evans C, Gomberg M, Nandwani R, Rafila A, et al. 2015 European guidelines for
the management of partners of persons with sexually transmitted infections. J Eur Acad Dermatol
Venereol. 2015;29:1251-7.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [619]
[41] INFECCIÓN DE PIEL Y PARTES BLANDAS. OSTEOMIELITIS
41.Infección de piel y partes blandas. Osteomielitis
Laura Corbella Vázquez.
Medicina Interna
Lucía Jorge Huerta.
Medicina Interna
Asesor: Jaime Lora-Tamayo Morillo-Velarde. Médico Adjunto de la Unidad de Enfermedades Infecciosas
I. INFECCIÓN DE PIEL Y PARTES BLANDAS
1. CONCEPTO Y FISIOPATOLOGÍA
Engloba el conjunto de infecciones que afectan desde la piel, constituida por la epidermis, dermis y
tejido celular subcutáneo, hasta los planos musculares profundos (fascia y tejido muscular).
La infección se suele producir por microorganismos del medio o de la microbiota de la piel que
alcanzan los tejidos subyacentes a través de soluciones de continuidad en la barrera cutánea (abrasiones,
cortes, grietas, etc.) y, en menor medida, por vía hematógena desde focos sépticos (más frecuente en
inmunodeprimidos).
2. ETIOLOGÍA
Debe considerarse siempre la participación de Staphylococcus aureus y estreptococos beta-
hemolíticos (típicamente S. pyogenes y S. agalactiae). Considerar S. aureus resistente a oxacilina (SAOR) en
función de los factores de riesgo (Tabla I).
Tabla I. Sospecha de infección por S. aureus resistente a oxacilina (SAOR).
De forma menos frecuente, otros microorganismos pueden producir infecciones de piel y partes
blandas, aunque en estos casos suele haber algún antecedente epidemiológico característico:
Mordeduras:
Humana: gran variedad de estreptococos y de microorganismos anaerobios
(Fusobacterium spp, Bacteroides spp, estreptocococos) y característicamente Eikenella
corrodens.
De perro: Pasteurella multocida, Capnocytophaga canimorsus (potencial sepsis
fulminante en cirróticos).
De gato: Pasteurella multocida.
De rata: infección característica por Streptobacillus moniliformes.
Heridas en contacto con agua salada o con marisco: Vibrio vulnificus (curso fulminante en
cirróticos).
Heridas en contacto con agua dulce: Aeromonas hydrophila.
Piel expuesta a agua de acuario, piel erosionada en piscinas: Mycobacterium marinum.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [620]
[41] INFECCIÓN DE PIEL Y PARTES BLANDAS. OSTEOMIELITIS
Infección de una herida por quemadura: Pseudomonas aeurigonosa, enterobacterias, Candida,
virus del herpes simple (VHS).
Herida por punción en la planta del pie: P. aeruginosa.
Piel erosionada en saunas, jacuzzis: P. aeruginosa (foliculitis difusa).
Manipuladores de carne, pescado o aves de corral: Erysipelothrix rhusiopathiae.
Pacientes hospitalizados e inmunodeprimidos: bacilos gramnegativos.
3. CLÍNICA Y ETIOPATOGENIA
Las manifestaciones clínicas vienen condicionadas por la localización anatómica de la lesión,
aunque cabe considerar su carácter dinámico y potencial propagación a estructuras adyacentes. Según su
localización, se distinguen los siguientes cuadros clínicos (Figura 1):
Figura 1. Localización y etiología fundamental de las infecciones de la piel y partes blandas.
3.1. Afectación cutánea superficial: infecciones de la epidermis y dermis
Sin participación de anejos
Impétigo contagioso: infección más superficial que afecta a la epidermis. La lesión
inicial es una vesícula, aunque normalmente se diagnostica como costras de color
pardo tras su ruptura (en caso de etiología estafilocócica, adquieren un color melicérico
característico). Predomina en zonas periorificiales y las extemidades, sobre piel sana o
dermatosis previa, y cursa con buen estado general.
Ectima: infección de la dermis en forma de úlcera profunda, dolorosa, bien delimitada,
cubierta de una costra adherida habitualmente negruzca con pústulas vecinas. Es más
frecuente en miembros inferiores y cura dejando cicatriz. Debe diferenciarse del ectima
gangrenoso, de aspecto clínico similar, pero que aparece en pacientes neutropénicos
por diseminación hematógena de P. aeruginosa.
Erisipela: infección de la epidermis y dermis superficial, casi siempre producida por S.
pyogenes. Cuadro típico en forma de placa eritematosa, caliente, brillante, dolorosa y
bien delimitada respecto a la piel sana, especialmente en la cara o miembros inferiores.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [621]
[41] INFECCIÓN DE PIEL Y PARTES BLANDAS. OSTEOMIELITIS
Suele tener un inicio brusco con repercusión general (fiebre, malestar) aunque su
extensión a planos profundos o complicaciones es excepcional.
Con participación de anejos
El agente etiológico más frecuente es S. aureus.
Foliculitis superficial: pústula centrada por un pelo, no indurada, sin síntomas
sistémicos.
Forúnculo: infección profunda del folículo piloso en forma de nódulo eritematoso,
caliente, doloroso que puede tener drenaje espontáneo de pus, sin repecursión del
estado general.
Ántrax o carbuno: placa indurada en región pilosa (típicamente en nuca) con varios
folículos en su interior con drenaje de pus (imagen en espumadera). Cursa con fiebre y
malestar general y puede producir bacteriemia.
Hidrosadenitis supurativa: infección de las glándulas sudoríparas apocrinas (axilar,
genital, inguinal) en forma de nódulos dolorosos inflamatorios con cicatrices
hipertróficas previas.
3.2. Afectación cutánea profunda: epidermis, dermis y grasa subcutánea
Celulitis infecciosa: infección de la dermis y tejido celular subcutáneo. Se presenta como una
placa infiltrada, eritematosa, caliente, dolorosa, de bordes mal definidos, especialmente en
miembros inferiores (pie y pierna) y con puerta de entrada vecina (pie de atleta, grietas,
mordeduras). Asocia deterioro del estado general y puede complicarse con sepsis en el 10% de
los casos.
3.3. Afectación fascial y muscular
Fascitis necrotizante estreptocócica: infección y necrosis rápidamente progresiva del tejido
celular subcutáneo y plano fascial profundo. El agente causal más frecuente es S. pyogenes. La
clínica se inicia con dolor desproporcionado a los hallazgos en la exploración física (mínimo
edema o piel sana), con posterior induración de la piel, crepitación o anestesia cutánea
asociado en ocasiones a ampollas hemorrágicas. Sin una actuación precoz, existe alto riesgo de
shock séptico y fallo multiorgánico (mortalidad 30%)
Otros microorganismos pueden dar cuadros clínicos similares:
Gangrena gaseosa: infección por diversas especies de Clostridium productoras de gas
(C. perfringens, C. septicum, C. histolyticum), típicamente a raíz de heridas profundas
que producen interrupción del flujo sanguíneo (ambiente anaerobio) y contaminadas
(tierra, etc).
Gangrena de Fournier: infección necrotizante en la zona perineal caracterizada por
inflamación masiva del escroto y el pene, con extensión al perineo, pared abdominal
y/o extremidades inferiores ocasionada por bacterias aerobias y anaerobias. Acontece
generalmente en pacientes frágiles.
Piomiositis primaria: infección del músculo estriado, típicamente tras un traumatismo menor o
sobreesfuerzo, secundaria a una bacteriemia (habitualmente S. aureus). Cuadro clínico de
fiebre y dolor sordo subagudo, habitualmente en miembros inferiores (cuádriceps, psoas iliaco)
que progresa a la formación de absceso muscular e inflamación local, con potencial riesgo de
mionecrosis y sepsis.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [622]
[41] INFECCIÓN DE PIEL Y PARTES BLANDAS. OSTEOMIELITIS
4. APROXIMACIÓN DIAGNÓSTICA
Las infecciones de piel y partes blandas son inespecíficas desde el punto de vista etiológico por lo
que el diagnóstico se sustenta fundamentalmente en el aspecto clínico de las lesiones (ver Apartado 3). Lo
más importante es determinar la extensión a planos profundos, la afectación sistémica y factores de riesgo
de mala evolución al suponer un cambio en el manejo.
4.1. Anamnesis y exploración física
Debe realizarse una anamnesis detallada, teniendo en cuenta factores predisponentes para padecer estas
infecciones, que se relacionan principalmente con soluciones de continuidad en la piel (pie de atleta,
heridas, cortes, etc.), la dificultad del retorno venoso o linfático (insuficiencia venosa crónica,
linfadenectomía, edemas periféricos, etc.) y las enfermedades debilitantes previas (diabetes,
inmunodepresión, edad avanzada, etc.).
Es importante la exploración física exhaustiva incluyendo la zona genital (gangrena de Fournier) y
buscar una puerta de entrada (pliegues interdigitales de los pies, grietas, etc). Siempre se buscarán signos
de alarma de una infección grave necrotizante (Tabla II). En estos casos, se explorarán los pulsos periféricos
y la presión del compartimento muscular afecto, para valorar la instauración de un síndrome
compartimental y la necesidad de una fasciotomía inmediata.
Tabla II. Síntomas y signos de alarma ante una infección de partes blandas (sospecha de infección necrotizante).
4.2. Pruebas complementarias
El diagnóstico es clínico, por lo que la práctica sistemática de pruebas complementarias no está justificada.
Es muy importante tener presente que ante una alta sospecha de infección necrotizante (Tabla II), se debe
indicar una exploración quirúrgica urgente en ausencia de otras pruebas complementarias (Figura 2).
Datos de laboratorio: en pacientes con fiebre o signos de afectación sistémica, está indicada la
realización de una analítica general básica con reactantes de fase aguda (proteína C reactiva,
VSG), incluyendo creatín-cinasa (CPK), aldolasa, lactato deshidrogenasa (LDH) y calcio. La
elevación de CPK, aldolasa y LDH orienta a necrosis muscular extensa al igual que la
hipocalcemia (fijación del calcio en la necrosis grasa en las fascitis necrotizantes).
Estudios microbiológicos: habitualmente no es necesario la toma de muestras para la
instauración de tratamiento antibiótico (empírico la mayoría de las veces), reservándose los
estudios microbiológicos en caso de afectación sistémica (fiebre), involucración de planos
profundos o datos de alarma, pacientes que requieran ingreso hospitalario, riesgo de infección
por microorganismos resistentes y mala evolución con tratamiento antibiótico empírico.
Hemocultivos: deben recogerse siempre que haya fiebre, sepsis o sospecha de
afectación de planos profundos (positivos 5%).
Punción (lavado/aspiración) del borde activo de la lesión (sensibilidad alrededor del
20%).
Punción de ampollas o vesículas.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [623]
[41] INFECCIÓN DE PIEL Y PARTES BLANDAS. OSTEOMIELITIS
Si se realiza un acto quirúrgico (fascitis, abscesos) deben tomarse cultivos para
aerobios y anaerobios y tinción de Gram.
El aislamiento a partir de torundas de secreciones en úlceras, fístulas, etc., documentan
colonización, pero no indican necesariamente un papel etiológico – evitar su toma
sistemática.
Figura 2. Algoritmo diagnóstico y terapéutico de las infecciones de piel y partes blandas.
Pruebas de imagen: la práctica rutinaria de pruebas de imagen no está indicada en la mayoría
de las ocasiones. Excepciones a esta normal:
Si se sospecha una colección-absceso, la prueba de elección es una ecografía de la zona
afecta.
En caso de sospecha de afectación de planos profundos o crepitación: de elección una
tomografía computarizada (TC) o una resonancia magnética (RM). La TC es la técnica
disponible más sensible para la detección de gas tisular mientras que la RM evalúa
mejor la afectación muscular y fascial. Sin embargo, la realización de pruebas de
imagen no debe retrasar la exploración quirúrgica.
Exploración quirúrgica: indicada ante la existencia de signos de alarma. Se deben tomar
muestras para Gram, cultivo y estudio histológico (trombosis de vasos, vasculitis, necrosis de la
fascia).
4.3. Diagnóstico diferencial
Conviene recordar que la celulitis infecciosa de ambas extremidades inferiores de forma simultánea es una
entidad notablemente infrecuente: debe considerarse antes la posibilidad de dermatitis de éstasis en
pacientes con edemas crónicos, especialmente ante la ausencia de fiebre y dolor. Además, se debe realizar
diagnóstico diferencial con: trombosis venosa profunda, necrólisis tóxica epidérmica o síndrome de Lyell
(secundaria a fármacos), reacción de hipersensibilidad, dermatitis de contacto, pioderma gangrenoso,
panadizo herpético y herpes zóster precoz (antes de aparición de las vesículas) y eritema migrans
(enfermedad de Lyme).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [624]
[41] INFECCIÓN DE PIEL Y PARTES BLANDAS. OSTEOMIELITIS
5. TRATAMIENTO
5.1. Medidas generales
Limpieza de la lesión con suero salino y clorohexidina al 2%. Estabilización hemodinámica en caso de ser
preciso. En la celulitis infecciosa es importante la elevación del miembro afecto y un reposo relativo del
mismo; en casos particulares, puede considerarse la administración de tratamiento antiinflamatorio.
5.2. Antibioterapia (Tabla III)
El tratamiento debe instaurarse empíricamente según el cuadro clínico y los antecedentes epidemiológicos
hasta conocer los resultados microbiológicos en caso de haberse tomado muestras.
Tabla III. Tratamiento antibiótico empírico de la infección de partes blandas.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [625]
[41] INFECCIÓN DE PIEL Y PARTES BLANDAS. OSTEOMIELITIS
De forma empírica, se deberán emplear antibióticos con cobertura frente a cocos grampositivos
teniendo en cuenta el riesgo de SAOR (ver en Tabla III antibióticos con actividad frente a SAOR marcados
con “†”.
La terapia oral está indicada en casos de infecciones leves, reservándose el tratamiento intravenoso
para infecciones moderadas-graves que requieran hospitalización: rápida progresión de la lesión,
afectación del estado general, importante extensión de la infección, respuesta inflamatoria sistémica grave
o comorbilidad (Figura 2).
La duración total del tratamiento es variable en función del cuadro clínico, y puede variar desde los
7-10 días (infecciones no complicadas, pequeña extensión) hasta los 14-21 días (amplia extensión,
afectación del estado general, necesidad de ingreso) o incluso 28 días en celulitis supuradas (abscesos) o
piomiositis. Debe considerarse también el tratamiento de la puerta de entrada, si la hubiera: cura tópica de
las heridas, tratamiento antifúngico tópico para el pie de atleta, etc.
5.3. Tratamiento quirúrgico
En caso de existir abscesos se debe valorar su drenaje. La evidencia de gangrena o infección necrosante
requiere desbridamiento inmediato, extirpando todo el tejido necrótico, incluso con amputaciones
extensas si es necesario y realizando fasciotomía si hay síndrome compartimental. Se debe demorar la
reparación con injertos hasta que esté resuelta la infección y exista tejido de granulación.
II. ÚLCERAS POR PRESIÓN
1. CONCEPTO Y ETIOPATOGENIA
Son lesiones que resultan de la compresión del tejido blando entre una prominencia ósea y una
superficie externa durante un tiempo prolongado, siendo una complicación frecuente, aunque prevenible,
del encamamiento prolongado.
En función del grado de lesión tisular se pueden clasificar en varios estadios (Tabla IV).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [626]
[41] INFECCIÓN DE PIEL Y PARTES BLANDAS. OSTEOMIELITIS
Tabla IV. Estadios de las úlceras por presión.
2. APROXIMACIÓN DIAGNÓSTICA
Aparecen sobre zonas de prominencia ósea (habitualmente en talones, región sacra, trocánter y
maléolo externo), típicamente en pacientes con factores predisponentes externos (presión prolongada y
humedad local) y/o propios (hipoalbuminemia, inmovilización, edad avanzada, diabetes, enfermedad
neurológica-degenerativa, lesiones medulares, neuropatía).
2.1. Sospecha de infección
Sugiere infección signos como aumento de la temperatura local, inflamación del área periulcerosa, mal olor
o secreción purulenta. La infección no siempre se acompaña de fiebre o leucocitosis.
En caso de fiebre se recogerán hemocultivos ante la posibilidad de bacteriemia y sepsis. También
pueden recogerse muestras con torunda, aunque la interpretación de los resultados debe ser cautelosa
(colonización vs. infección). La etiología de la infección suele ser polimicrobiana incluyendo cocos
grampositivos (Staphylococcus, Enterococcus), bacilos gramnegativos (E. coli, Proteus, P. aeruginosa) y
anaerobios (B. fragilis, Peptostreptococcus, Clostridium).
3. TRATAMIENTO Y PREVENCIÓN (TABLA V)
El tratamiento de las úlceras por presión requiere una serie de medidas integradas en la tabla V. Se
debe insistir en las medidas preventivas en todos los pacientes de riesgo, al ser las más coste-efectivas. La
indicación de un tratamiento antibiótico en estas situaciones no es evidente, porque su presión ecológica
es selectiva y normalmente se acompañan de la selección de microorganismos resistentes al tratamiento
prescrito. Por este motivo, el tratamiento fundamental de las úlceras con signos de infección debe ser local
(antisépticos locales ± desbridamiento químico/quirúrgico), y debe reservarse el tratamiento
antimicrobiano a situaciones con afectación sistémica (empeoramiento del estado general, fiebre) o signos
de celulitis cutánea de nueva aparición en torno a la úlcera –ver antibioterapia en tabla III-“Celulitis
infecciosa”–, teniendo en cuenta los aislamientos previos del paciente.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [627]
[41] INFECCIÓN DE PIEL Y PARTES BLANDAS. OSTEOMIELITIS
Tabla V. Manejo de las úlceras por presión.
III. OSTEOMIELITIS
1. CONCEPTO Y CLASIFICACIÓN
La osteomielitis (OM) es la inflamación y destrucción del hueso causada por microorganismos. La
clasificación más útil desde el punto de vista clínico es la patogénica:
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [628]
[41] INFECCIÓN DE PIEL Y PARTES BLANDAS. OSTEOMIELITIS
1.1. OM hematógena
Se produce como resultado de una bacteriemia (documentada o no) a partir de un foco distante. A su vez
conviene distinguir:
OM hematógena de huesos largos: típica de niños y adolescentes, afecta predominantemente
la diáfisis de la tibia y del fémur. Son cuadros típicamente agudos, con síntomas sistémicos
(dolor y fiebre) y aparición de signos inflamatorios locales en la zona del hueso afecto (dolor,
edema, calor local). La etiología más frecuente es S. aureus y S. agalactiae. En muchos casos
pueden curarse con antibióticos y sin cirugía, aunque su cronificación exigirá un manejo
quirúrgico.
OM vertebral (espondilodiscitis infecciosa): típica de pacientes adultos (> 50 años). Aunque la
vía hematógena es la más frecuente, la infección también puede ser posquirúrgica o por
contigüidad de otros focos supurados (ver Apartado 2. “Osteomielitis hematógena:
espondilodiscitis infecciosa”).
1.2. OM posquirúrgica/postraumática
Son las formas más frecuentes como resultado de una fractura abierta y/o tras un tratamiento quirúrgico.
También pueden considerarse en este grupo las OM en el contexto de úlceras de decúbito. Se asocian con
frecuencia a la presencia de cuerpo extraño, material de osteosíntesis. La cirugía es fundamental en el
manejo de estos pacientes.
1.3. OM asociada a prótesis articular
(Ver Apartado 4. “Infección asociada a prótesis articular”).
1.4. OM asociada a insuficiencia vascular (pie diabético)
(Ver Apartado 5. “Osteomielitis asociada a insuficiencia vascular: pie diabético”).
Desde un punto de vista clínico, las osteomielitis pueden clasificarse también en agudas (cuadro
inflamatorio, típicamente hematógeno o posquirúrgico inmediato) y crónicas (cuadros larvados, con
aparición de fístulas, secuestros óseos, ausencia de consolidación, cambios radiográficos).
2. OSTEOMIELITIS HEMATÓGENA: ESPONDILODISCITIS INFECCIOSA
2.1. Etiopatogenia
La vía de acceso microbiana es frecuentemente hematógena. Ocurre habitualmente en mayores de 50 años
y usuarios de drogas por vía parenteral (UDVP). Conviene considerar dos grupos etiológicos:
Osteomielitis vertebral piógena o bacteriana: el microorganismo que predomina es el S. aureus
(50%). En un 5-30% de los casos puede estar causada por bacilos gramnegativos, seguido de
estreptococos (15-30%, típicamente S. agalactiae y también S. viridans, especialmente si
coexiste una endocarditis infecciosa).
Osteomielitis vertebral no piógena: Mycobacterium tuberculosis (mal de Pott), en la que se
encuentra focos de tuberculosis extraespinal en el 30-50% de los casos, presentando curso
subagudo, con afectación predominante de las vértebras dorsales. La espondilodiscitis por
Brucella spp, actualmente muy infrecuente, debe considerarse en pacientes expuestos a
ganado y aquellos con ingesta de lácteos no controlados. La espondilodiscitis fúngica, causada
típicamente por Cándida spp, afecta a pacientes con factores de riesgo clásicos para
candidemia (corticoides, diabetes, nutrición parenteral, presión antibiótica, infección de catéter
venoso, hospitalización…) y suele ocurrir de forma subaguda (de 2 a 15 meses tras la
candidemia).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [629]
[41] INFECCIÓN DE PIEL Y PARTES BLANDAS. OSTEOMIELITIS
2.2. Clínica
La OM vertebral suele debutar con dolor de columna (> 85%), afectándose las vértebras lumbares con
mayor frecuencia (58%), seguida de las torácicas (30%) y las cervicales (11%). El retraso diagnóstico es
frecuente, por lo que el diagnóstico requiere un elevado nivel de sospecha, especialmente en ausencia de
datos inflamatorios. Debe buscarse dolor a la palpación de apófisis espinosas, limitación en la movilidad de
la columna y contractura de la musculatura paraespinal de la zona afecta.
La presentación clínica con signos de afectación sistémica es variable (fiebre en el 60%). Puede
complicarse con cuadros de compresión medular (más frecuente a nivel cervical, por el menor espacio
epidural) o radicular por abscesos epi y subdurales y/o paravertebrales, o con fractura/aplastamiento
vertebral.
2.3. Diagnóstico sindrómico y microbiológico
El diagnóstico es clínico-radiológico (Figura 3). La sospecha clínica puede verse apoyada por los datos
analíticos (presencia de anemia y elevación de reactantes de fase aguda) y debe conducir a la práctica de
una prueba de imagen que confirme el diagnóstico.
Figura 3. Algoritmo diagnóstico de la espondilodiscitis infecciosa.
Las radiografías son normales o muy inespecíficas inicialmente (pérdida de lordosis en la columna
lumbar o cervical). Pasados los primeros 10-21 días, aparecen signos más sugestivos, por este orden:
disminución del espacio intervertebral, rarefacción de los platillos vertebrales, aparición de geodas,
aplastamiento vertebral, artrodesis).
La prueba de elección es la resonancia magnética (RM), muy sensible y específica. La gammagrafía
ósea con tecnecio puede mostrar cambios muy precoces; la técnica con galio o leucocitos marcados
aumenta su especificidad.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [630]
[41] INFECCIÓN DE PIEL Y PARTES BLANDAS. OSTEOMIELITIS
Una vez asumido el diagnóstico sindrómico de osteomielitis vertebral, deben hacerse todos los
esfuerzos por obtener un diagnóstico etiológico, dado lo prolongado del tratamiento y las secuelas
potenciales de la infección. En la medida de lo posible, debe diferirse el inicio del tratamiento antibiótico
hasta obtener un diagnóstico microbiológico:
Se deben realizar hemocultivos seriados aún en ausencia de fiebre (son frecuentes las
bacteriemias intermitentes en este tipo de infección, sensibilidad 50%). Pueden repetirse
hemocultivos en las horas siguientes a una punción vertebral para aumentar la rentabilidad
diagnóstica.
De forma paralela, debe realizarse serología de Brucella spp, y prueba de Mantoux/IGRA.
Si los hemocultivos son negativos, la biopsia guiada por TC es el procedimiento de elección,
siendo lo más rentable la biopsia de colecciones abscesificadas paraespinales (seguido del disco
intervertebral y el platillo vertebral subcondral). Deben enviarse muestras para el cultivo
bacteriano aerobio y anaerobio, así como para hongos y micobacterias, y para anatomía
patológica (confirmación histológica de osteomielitis, hallazgo de granulomas caseificantes en
el caso de etiología tuberculosa).
En el caso de que las muestras de una primera punción sean negativas, debe considerarse
realizar una biopsia quirúrgica, o bien repetir la punción guiada por TC.
2.4. Tratamiento
Debe intentarse la obtención de muestra microbiológica previo al inicio del tratamiento antibiótico,
difiriendo el inicio del mismo a la identificación del microorganismo responsable. Excepciones a esto son las
situaciones de sepsis/shock séptico y la presencia de clínica neurológica en progresión, en cuyo caso debe
plantearse el tratamiento quirúrgico (laminectomía descompresiva y el inicio de antibioterapia empírica.
Nótese que la fiebre por sí misma no es indicación de iniciar un tratamiento antibiótico. Una pauta empírica
razonable podría ser la combinación de cloxacilina (2 g/4 h iv) más ceftriaxona (2 g/24 h iv); si se sospecha
SAOR, puede sustituirse cloxacilina por daptomicina (10 mg/kg/24 h) o vancomicina (1 g/12 h iv).
De acuerdo con lo anterior, el tratamiento antimicrobiano se realizará idealmente de forma dirigida
(Tabla VI). En el caso de las espondilodiscitis piógenas, los antimicrobianos deben mantenerse 6 semanas,
aunque en situaciones de inmunodepresión, grandes abscesos no drenados y en presencia de bacterias
multirresistentes que obliguen a pautas antibióticas subóptimas, puede considerarse un tratamiento más
largo (≥ 8 semanas).
El tratamiento de la espondilitis tuberculosa es el habitual de esta infección (4 fármacos o 3 si se
conoce el patrón de sensibilidad). La duración recomendada es de 6 a 9 meses si puede usarse rifampicina
más isoniazida, y los dos primeros meses, además, pirazinamida. La espondilodiscitis brucelar puede
tratarse con estreptomicina (1 g/24 h im) o gentamicina (5 mg/kg/24 h im) durante 3 semanas más
doxiciclina (100 mg/12 h vo) durante 6 semanas. Alternativamente, puede tratarse con doxiciclina (100
mg/12 h) más rifampicina (600-900 mg/24 h) durante 6 semanas, o cotrimoxazol más rifampicina.
El papel de la cirugía en la espondilodiscitis infecciosa se limita al tratamiento de las complicaciones
(compresión espinal, drenaje de abscesos, inestabilidad...) o al fracaso del tratamiento médico. El drenaje
de abscesos puede considerarse cuando estos son voluminosos y accesibles, especialmente si puede
realizarse de forma percutánea, guiada por TC.
El dolor del paciente mejorará con el tratamiento médico y con el reposo horizontal en cama
durante un periodo variable (aproximadamente dos semanas). La reincorporación del paciente al cabo de
ese tiempo es dependiente del control del dolor y debe considerarse siempre la colocación de un corsé.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [631]
[41] INFECCIÓN DE PIEL Y PARTES BLANDAS. OSTEOMIELITIS
Tabla VI. Tratamiento antibiótico en osteomielitis e infección de prótesis articular.
3. OSTEOMIELITIS POSQUIRÚRGICA/POSTRAUMÁTICA
3.1. Etiopatogenia
Es la causa de infección ósea más frecuente en adultos, habitualmente en el contexto de traumatismos
abiertos y de la cirugía posterior, siendo frecuente la presencia de cuerpos extraños (fragmentos óseos,
material de osteosíntesis, etc.). En este contexto, la etiología subyacente es poco predecible, siendo
frecuente la infección por S. aureus, estafilococos coagulasa-negativos (SCN), y bacilos gramnegativos,
incluyendo P. aerugionosa o Enterobacter cloacae. La OM asociada a infección protésica se abordará en un
apartado distinto.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [632]
[41] INFECCIÓN DE PIEL Y PARTES BLANDAS. OSTEOMIELITIS
3.2. Clínica
La sintomatología suele guardar relación con la virulencia del microorganismo responsable, de forma
parecida a lo que ocurre en la infección de prótesis articular. Así, las infecciones por S. aureus y bacilos
gramnegativos generalmente se acompañan de cuadros más inflamatorios al cabo de pocos días o semanas
de la cirugía (inflamación de la herida quirúrgica, dehiscencia y débito seroso o purulento). Las infecciones
por microorganismos menos virulentos (SCN, Propionibacterium acnes) pueden cursar de forma más sutil y
subaguda, con déficits de consolidación o formación diferida de fístulas.
3.3. Diagnóstico
El diagnóstico sindrómico parte de la sospecha clínica y puede verse confirmado con las pruebas de imagen.
El posterior diagnóstico microbiológico es fundamental dadas las importantes consecuencias terapéuticas
(antibioterapia de larga duración, cirugía agresiva, déficit funcional), y debe fundamentarse en muestras
profundas (biopsia ósea, muestras quirúrgicas).
Diagnóstico sindrómico
Los datos analíticos son inespecíficos, siendo la PCR el marcador más útil (elevado valor
predictivo negativo, utilidad en el seguimiento). El recuento de leucocitos puede ser normal.
Pruebas de imagen
En un contexto posquirúrgico inmediato son poco útiles (cambios posquirúrgicos, infección
demasiado precoz para provocar cambios radiológicos).
La radiografía simple es útil tanto para el diagnóstico como para el seguimiento,
observándose los hallazgos típicos a partir de los 10-21 días de la infección, por lo que
su utilidad es limitada en fases precoces. Los hallazgos típicos incluyen erosión cortical
con destrucción ósea, reacción perióstica, edema de partes blandas, ausencia de
consolidación, o presencia de secuestros.
La ecografía puede ser útil para la detección de colecciones purulentas adyacentes al
foco de osteomielitis.
La resonancia magnética (RM) es muy sensible y detecta cambios precozmente (edema
o destrucción de hueso medular, reacción perióstica y destrucción cortical). Si la RM es
normal, el diagnóstico de OM es improbable. Permite además detectar la afectación
articular o de partes blandas adyacente con mejor sensibilidad que la TC. Es
especialmente útil en la sospecha de OM en el pie. Sin embargo, no es útil en el
seguimiento para evaluar la respuesta a la terapia, dado que el edema óseo persiste
durante meses a pesar de la cura microbiológica.
La tomografía computarizada (TC) es menos sensible que la RM, salvo en el caso del
secuestro óseo. Está indicada cuando no pueda emplearse la RM (por indisponibilidad o
contraindicación) o para guiar la punción-biopsia.
La gammagrafía ósea en tres fases con bisfosfonatos marcados con Tc- 99 m, con
leucocitos marcados con In-111 o con citrato marcado con Ga- 67, presenta una
sensibilidad muy alta en fases tempranas (salvo en áreas de isquemia), con una buena
especificidad (excepto si existen otras alteraciones óseas subyacentes como
traumatismos, artropatía, cirugía reciente, etc.). Pueden ser una buena alternativa a la
RM.
La tomografía por emisión de positrones (PET-TC) puede ser útil para delimitar las
lesiones y visualizar la actividad infecciosa e inflamatoria.
Diagnóstico microbiológico
La rentabilidad de los hemocultivos es muy baja, por lo que solo deben extraerse si hay
fiebre o signos de afectación sistémica.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [633]
[41] INFECCIÓN DE PIEL Y PARTES BLANDAS. OSTEOMIELITIS
Biopsia de hueso: permite la confirmación diagnóstica de osteomielitis y el diagnóstico
microbiológico. En muchas ocasiones puede aprovecharse la propia cirugía terapéutica
para enviar muestras a microbiología. Deben evitarse las muestras superficiales
(biopsia de tejidos blandos, exudado de las fístulas). Puede haber falsos negativos ya
que la afectación ósea habitualmente es parcheada. Debe considerarse el envío de
muestras para cultivo de hongos y micobacterias. La visualización de granulomas con
positividad para la tinción de Ziehl-Neelsen es diagnóstica de tuberculosis.
3.4. Tratamiento
El tratamiento de la osteomielitis posquirúrgica/postraumática y de la osteomielitis crónica es
fundamentalmente quirúrgico. La cirugía servirá, además, en la mayoría de los casos, para la toma de
muestras fiables para microbiología.
El tratamiento antibiótico (Tabla VI) debe quedar dirigido por el resultado de estas muestras, y
complementa la actitud quirúrgica.
OM posquirúrgica/postraumática aguda: cirugía de desbridamiento/ limpieza del foco séptico
y del foco de fractura, con retirada de material desvitalizado y material óseo secuestrado. El
material de osteosíntesis debe retenerse si todavía está cumpliendo su función: si la fractura no
ha consolidado probablemente deba mantenerse; si la fractura ha consolidado y es factible su
retirada, lo ideal es su avulsión.
OM crónica: es una cirugía especializada que no podemos abordar en este capítulo. Supone la
retirada de material extraño, hueso secuestrado o necrótico, la restauración de la
vascularización y relleno de cavidades vacías.
Tras la cirugía, y a la espera de resultados microbiológicos, puede iniciarse una cobertura
antibiótica de amplio espectro (por ejemplo, vancomicina y ceftazidima). La duración posterior del
tratamiento antibiótico es variable, en función de la microbiología, antibioterapia escogida y cuadro clínico.
Habitualmente será de al menos 6-8 semanas.
4. INFECCIÓN ASOCIADA A PRÓTESIS ARTICULAR
4.1. Concepto y etiopatogenia
La infección de prótesis articular supone la colonización del material ortopédico y posterior extensión a las
partes blandas y al tejido óseo circundante. En la fisiopatogenia es fundamental el proceso de adhesión
bacteriana a la prótesis y la formación de biocapas o biofilms. La infección suele adquirirse en el quirófano
o en el postoperatorio inmediato y, con menor frecuencia, por vía hematógena.
El riesgo de infección es mayor en los dos primeros meses tras el implante, aunque se mantiene
durante toda la vida de la prótesis. La probabilidad de infección protésica en el curso de una bacteriemia es
bajo, salvo que se trate de una bacteriemia por S. aureus (30%).
Los factores de riesgo asociados son: el antecedente de una infección “superficial” de la herida
quirúrgica, neoplasia subyacente, las prótesis de revisión o recambio, la diabetes mellitus, la obesidad, la
desnutrición, la artritis reumatoide, el tratamiento con corticoides y la infección urinaria concomitante.
4.2. Clasificación, clínica y diagnóstico microbiológico
Infección posquirúrgica precoz (IPP) (35%): es la que se manifiesta en los primeros 1-3 meses
posimplante. Hay predominio de los signos inflamatorios locales (celulitis, secreción purulenta
de la herida quirúrgica), y puede haber fiebre y síntomas sistémicos (sepsis). El diagnóstico se
basa en el criterio clínico de la herida quirúrgica, con celulitis o supuración de la herida. Las
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [634]
[41] INFECCIÓN DE PIEL Y PARTES BLANDAS. OSTEOMIELITIS
exploraciones complementarias no son de gran ayuda, ya que persisten los cambios
inflamatorios posquirúrgicos analíticos y radiológicos. El cuadro clínico es rápido e inflamatorio
porque la etiología responsable es virulenta: S. aureus, enterobacterias y P. aeruginosa,
típicamente.
Infección posquirúrgica tardía (IPT) (50%): se manifiesta pasado el primer-tercer mes de la
cirugía. La clínica es subaguda y predomina la clínica ortopédica sobre los síntomas de infección
(dolor, aflojamiento protésico), pudiendo existir trayecto fistuloso, ya que frecuentemente son
producidas por flora cutánea con elevada capacidad de adhesión al material extraño pero
escasa virulencia: SCN, P. acnes, y Corynebacterium spp, fundamentalmente.
El diagnóstico diferencial con el aflojamiento aséptico es difícil de establecer. Puede ser útil la
determinación de proteína C reactiva por su elevado valor predictivo negativo. La aparición de cambios en
la Rx simple (radioluminiscencia periprotésica, osteolisis, movilización de componentes protésicos) es
relativamente inespecífica, pero su precocidad sugiere IPT; la reacción periostal es más específica de
infección. La gammagrafía de referencia es la de leucocitos marcados con 111In (sensibilidad 80%). La TC y
la RM son poco útiles para excluir la infección protésica. Los cultivos de exudado de fístula tienen una
dudosa fiabilidad. La artrocentesis para análisis del líquido articular debe plantearse, remitiéndose a
microbiología y recuento celular (la presencia de > 1.700 leucocitos/μL o > 65% PMN es muy sugestivo de
infección). Los cultivos de las muestras quirúrgicas son el procedimiento diagnóstico de referencia. La
observación de falsos negativos se relaciona con la toma previa de antibióticos, por lo que se aconseja
suspender la antibioterapia con un intervalo mínimo de dos semanas antes de la intervención.
Infección hematógena aguda (IHA) (10%): Puede ocurrir en cualquier momento tras la
colocación de la prótesis, y está asociada a bacteriemia (documentada o no). El cuadro clínico
es agudo, y similar al de una artritis nativa (dolor, inflamación local). De hecho, la microbiología
responsable es similar, y justifica la virulencia del cuadro: S. aureus, estreptococos y bacilos
gramnegativos (BGN). El cuadro clínico y finalmente el análisis y cultivo del líquido articular
conducen al diagnóstico.
El diagnóstico microbiológico es fundamental para confirmar el diagnóstico y ofrecer un
tratamiento antibiótico óptimo que complemente el acto quirúrgico terapéutico (ver más abajo). Este
diagnóstico debe cementarse en aislamientos a partir de muestras fiables: líquido articular obtenido por
artrocentesis; hemocultivos (son poco rentables en general, pero deben realizarse siempre que exista
fiebre, sepsis, o sospecha de infección hematógena); y/o muestras intraoperatorias durante el acto
quirúrgico terapéutico (son las más rentables).
La interpretación de los resultados microbiológicos debe contextualizarse en virtud del patógeno
aislado y del tipo de infección:
En infecciones de carácter agudo (IPP e IH), el aislamiento de un microorganismo patógeno en
un cultivo de una muestra fiable bastará para realizar el diagnóstico microbiológico (por
ejemplo, aislamiento de S. aureus del pus observado durante la cirugía de desbridamiento).
En cambio, el aislamiento de SCN obliga a plantearse su papel patógeno vs. su potencial papel
de contaminante habitual. En estos casos, su aislamiento repetido confirma su papel etiológico.
Por este motivo, en el diagnóstico de las IPT se recomienda recoger al menos 5 muestras para
cultivo convencional. El aislamiento de un mismo SCN con idéntico antibiograma en ≥ 2 cultivos
sugiere con fuerza su responsabilidad en la infección.
4.3. Tratamiento
De nuevo, el tratamiento fundamental es quirúrgico. Salvo en situación de sepsis, el tratamiento antibiótico
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [635]
[41] INFECCIÓN DE PIEL Y PARTES BLANDAS. OSTEOMIELITIS
debe diferirse hasta la obtención de un diagnóstico microbiológico fundamentado en muestras fiables. Hay
2 estrategias fundamentales a considerar:
Tratamiento con retención de la prótesis: supone el desbridamiento quirúrgico exhaustivo de
la infección, sin retirada de la prótesis (aunque cambiando los componentes móviles, como las
piezas de polietileno, o la cabeza de las prótesis femorales), seguida de tratamiento antibiótico.
Aunque las posibilidades de curación son menores que con la retirada de la prótesis (40-70%),
ofrece ventajas potenciales atractivas (cirugía menos compleja, menor número de cirugías,
menor pérdida de reserva ósea). Debe reservarse esta opción para casos agudos (IPP e IH), en
que se ofrece un desbridamiento precoz (idealmente < 21 días tras el inicio de los síntomas), en
que la prótesis es estable y la condición de los tejidos circundantes y partes blandas es buena.
El tratamiento antibiótico debe ser óptimo, y administrado durante largo tiempo (las guías
clínicas recomiendan 3-6 meses, aunque hay experiencia con 8 semanas).
Tratamiento con retirada de la prótesis, seguida de tratamiento antibiótico. Las opciones
ortopédicas posteriores son:
Recambio en dos tiempos: tras la retirada de la prótesis y colocación en el mismo acto
quirúrgico de un espaciador de cemento (preserva el espacio articular y puede ser
cargado con antibióticos que difundan altas concentraciones locales), se administran
antibióticos durante 6 semanas, y posteriormente se realiza una nueva cirugía de
reimplante protésico. Curación aproximadamente en el 90%.
Recambio en 1 tiempo: retirada de la prótesis y colocación de un nuevo implante en el
mismo acto quirúrgico, seguida de antibióticos durante 8 semanas. Curación
aproximadamente del 80%.
No volver a colocar una prótesis (artrodesis articular).
Los antibióticos recomendados y sus dosis se recogen en la tabla VI. Frecuentemente aún no se
conoce la etiología en el momento en que se practica la cirugía de desbridamiento o explante protésico;
mientras se espera el resultado de las muestras recogidas en este acto quirúrgico, puede entonces iniciarse
un tratamiento antibiótico de amplio espectro (por ejemplo, vancomicina 1 g/12 h iv combinado con:
ceftazidima 2 g/8 h iv o cefepime 2 g/8 h iv o meropenem 2 g/8 h iv).
5. OSTEOMIELITIS ASOCIADA A INSUFICIENCIA VASCULAR: PIE DIABÉTICO
5.1. Concepto y etiopatogenia
La fisiopatología de la infección del pie diabético es multifactorial: neuropatía periférica (sensitiva, motora y
autonómica), vasculopatía periférica y deficiente cicatrización coexisten ocasionando deformidades
anatómicas y traumatismos inadvertidos donde la sobreinfección es frecuente. Los factores de riesgo para
el desarrollo de un pie diabético son: el antecedente de úlcera o amputación previas, la enfermedad
vascular periférica, las alteraciones estructurales del pie, la presencia de neuropatía periférica, el
tabaquismo, así como el sexo masculino, la diabetes de larga evolución y el mal control glucémico.
Los microorganismos más frecuentemente implicados son los cocos grampositivos, especialmente
S. aureus. Sin embargo, la cronicidad del cuadro clínico y la frecuente prescripción de tratamientos
antibióticos aumentan la frecuencia de bacilos gramnegativos y microorganismos resistentes. La presencia
de isquemia justificará la participación de microorganismos anaerobios.
5.2. Aproximación diagnóstica
En la historia clínica se recogerán datos generales como el tiempo de evolución de la diabetes, control
glucémico, otros factores de riesgo cardiovascular (dislipemia, HTA, tabaquismo) y antecedentes de
enfermedad micro o macrovascular. De forma específica deben recabarse en la anamnesis y exploración
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [636]
[41] INFECCIÓN DE PIEL Y PARTES BLANDAS. OSTEOMIELITIS
física datos de neuropatía periférica, vasculopatía (Tabla VII) y la presencia de úlceras cutáneas y su
gravedad (Tabla VIII).
Tabla VII. Diferencias entre pie neuropático e isquémico.
Tabla VIII. Clasificación de Wagner de las lesiones del pie diabético.
Se deben recoger muestras para estudio microbiológico, recomendándose obtención de muestras
mediante biopsia, curetaje o aspiración (intentar evitar analizar muestras superficiales para evitar falsos
positivos que indiquen colonización). La RM es la prueba ideal para definir lesiones de tejidos blandos y/o la
presencia de osteomielitis.
5.3. Tratamiento
Medidas generales
Incluyen el buen control glucémico y de los factores asociados (deshidratación, edema,
enfermedades asociadas, soporte nutricional). En general, las úlceras de grado 1-2 con
infección leve pueden manejarse de forma ambulatoria. En las infecciones moderadas-graves,
con afectación sistémica, mala respuesta al tratamiento, o ante la imposibilidad de garantizar el
tratamiento adecuado en domicilio está indicado el ingreso hospitalario.
Tratamiento específico
Es especialmente importante reconocer los factores etiopatogénicos implicados en cada
paciente (neuropático, isquémico e infeccioso) y corregirlos de forma específica.
Mecanismo isquémico: el paciente deberá ser valorado por el cirujano vascular para
determinar la necesidad de revascularización.
Mecanismo neuropático: el tratamiento debe incluir cuidados locales (limpieza de la
úlcera y desbridamiento del tejido necrótico) y medidas de descarga de presión que
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [637]
[41] INFECCIÓN DE PIEL Y PARTES BLANDAS. OSTEOMIELITIS
eviten los traumatismos sobre el pie (yesos o fieltros de descarga, calzados especiales,
siliconas, etc.).
Tratamiento antibiótico
Solo indicado en las úlceras con datos de infección. Ante la presencia de celulitis, infección
necrosante u osteomielitis se iniciará terapia empírica tras la obtención de muestras
microbiológicas y posteriormente se ajustará la pauta según el microorganismo aislado y el
antibiograma. Debe considerarse el desbridamiento quirúrgico. Las infecciones superficiales no
tratadas previamente suelen ser producidas por cocos grampositivos aerobios (S. aureus,
Streptococcus), mientras que las úlceras profundas, crónicamente infectadas o tratadas
previamente, suelen tener un origen polimicrobiano incluyendo bacilos gramnegativos
entéricos, enterococos, P. aeruginosa y anaerobios.
La duración del tratamiento antibiótico para infecciones leves (celulitis leve) es de 1-2 semanas
(Tabla III); para infecciones moderadas y severas es de 2-4 semanas, dependiendo del correcto
desbridamiento de la zona y la vascularización local; en el caso de la osteomielitis se requiere tratamiento
durante 4-8 semanas (Tabla VI).
En el caso de que no exista adecuada respuesta al tratamiento antibiótico se debe considerar, si el
estado clínico del paciente lo permite, interrumpir el tratamiento antibiótico y tomar nuevas muestras
microbiológicas pasados 72-96 horas. El factor estimulante de colonias granulocíticas y el oxígeno
hiperbárico pueden prevenir amputaciones en aquellos pacientes con infecciones severas y refractarias.
5.4. Prevención
Además del control estricto metabólico global de la diabetes y de los factores de riesgo cardiovascular, es
conveniente un seguimiento al menos anual (incluso mensual o trimestral en pacientes de alto riesgo) y
una educación para el cuidado de los pies que incluya el uso de calzado adecuado, higiene diaria,
autoexploración frecuente en busca de lesiones y evitar las conductas de riesgo (andar descalzo). Deben
recomendarse los cuidados podológicos a todos los pacientes diabéticos y, de forma obligada, a los que
tengan factores de riesgo de pie diabético.
BIBLIOGRAFÍA
Ariza J, Euba G, Murillo O. Infecciones relacionadas con las prótesis articulares. Enferm Infecc Microbiol
Clin. 2008;26(6):380-90.
Barberán López J. Infecciones de la piel y las partes blandas. En: Farreras/Rozman. Medicina Interna.
17ª ed. Barcelona: Elsevier; 2012;2325-30.
Bernard L, Dinh A, Ghout I, Simo D, Zeller V, Issartel B, et al. Antibiotic treatment for 6 weeks versus 12
weeks in patients with pyogenic vertebral osteomyelitis: an open-label, non-inferiority, randomised,
controlled trial. Lancet. 2015;385(9971):875-82.
Berbari EF, Kanj SS, Kowalski TJ, Darouiche RO, Widmer F, Schmitt SK, et al. 2015 Infectous Diseases
Society of America (IDSA) Clinical Practice Guidelines for the Diagnosis and Treatment of Native
Vertebral Osteomyelitisin Adults. Clinical Infectous Diseases, 2015;61: e26-e46.
Lew DP, Waldvogel FA. Osteomyelitis. Lancet. 2004;364:369-79.
Lipsky BA, Berendt AR, Deery HG, Embil JM, Joseph WS, Karchmer AW, et al. Diagnosis and Treatment
of Diabetic Foot Infections. Clinical Infectious Diseases. 2004;39:885-910.
Rivera R, Llamas R. Infecciones bacterianas cutáneas. En: Iglesias Díez L. Guerra Tapia A, Ortiz Romero
PL. Tratado de Dermatología. 2ª ed. Madrid. Mc Graw Hill. 2004.
Stevens DL, Bisno AL, Chambers HF, Patchen E, Goldstein EJ, Gorbach SL, et al. Practice Guidelines for
the Diagnosis and Management of Skin and Soft Tissue Infections: 2014 Update by the Infectious
Diseases Society of America (IDSA). Clinical Infectous Diseases. 2014;59(2):10-52.
Stevens DL, Eron LJ. Cellulitis and soft-tissue infections. Ann Int Med. 2009;150(1):ITC 11.
Zimmerli W. Vertebral Osteomielytis. N Engl J Med. 2010;362:1022-9.
Zimmerli W. Ed. Bone and joint infections, from microbiology to diagnostics and treatment. Wiley
Blackwell. Oxford. 2015.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [638]
[42] INFECCIONES DEL SISTEMA NERVIOSO CENTRAL
42.Infecciones del sistema nervioso central
Ana Arántzazu Urbanos Núñez.
Neurología
Mikel Mancheño Losa.
Medicina Interna
Asesor: Manuel Lizasoain Hernández. Médico Adjunto de la Unidad de Enfermedades Infecciosas
I. INTRODUCCIÓN
El sistema nervioso central (SNC) se encuentra rodeado por las meninges, tres membranas que
protegen el tejido encefálico y medular de las fuerzas de tracción mecánica y mantienen la homeostasis del
medio interno.
El término meningitis hace referencia a la inflamación de cualquier etiología (infecciosa,
inflamatoria, química) del tejido leptomeníngeo (piamadre y aracnoides) y, por extensión, del líquido
cefalorraquídeo contenido en el espacio subaracnoideo. Clásicamente, las meningitis se clasifican en tres
grandes subgrupos en función de su perfil temporal: meningitis aguda si el cuadro se instaura en unas
horas o pocos días, subaguda si lo hace en menos de cuatro semanas y crónica si el tiempo de evolución es
mayor de cuatro semanas. En la práctica clínica habitual, el diagnóstico diferencial que se plantea ante una
meningitis de evolución subaguda y crónica no difiere sustancialmente. Se considera meningoencefalitis si,
además de las meninges, existe una inflamación concomitante del parénquima cerebral subyacente, y
paquimeningitis aquel proceso inflamatorio en el que se encuentra involucrada la duramadre.
II. ABORDAJE DEL PACIENTE CON SOSPECHA DE INFECCIÓN AGUDA
DEL SISTEMA NERVIOSO CENTRAL
1. CUÁNDO SOSPECHAR UNA INFECCIÓN DEL SISTEMA NERVIOSO CENTRAL. PRESENTACIÓN CLÍNICA
La precocidad en el diagnóstico y el inicio del tratamiento antibiótico en los casos de meningitis
aguda bacteriana son determinantes para el pronóstico vital y funcional del paciente. Para ello, el primer
reto que se plantea es el de identificar y clasificar sindrómicamente al enfermo con sospecha de infección
del SNC.
La historia habitual de la meningitis aguda bacteriana consiste en un cuadro de instauración
hiperaguda o aguda, de entre unas horas y pocos días de evolución, consistente en una
combinación variable de los cuatro síntomas cardinales: fiebre, rigidez de nuca, cefalea y
alteración del nivel de consciencia.
El cuadro clínico es muy similar en la meningitis aguda linfocitaria o aséptica, si bien esta
reviste menos gravedad y conlleva menor afectación del estado general.
La meningitis subaguda o crónica se presenta generalmente como un cuadro insidioso de varios
días o semanas de evolución. Se manifiesta mediante cefalea y febrícula, con o sin compromiso
del nivel de consciencia. También puede asociar otras complicaciones, como neuropatías
craneales, radiculopatías, hidrocefalia arreabsortiva, etc.
Debe sospecharse una meningoencefalitis o encefalitis vírica aguda ante un cuadro febril
acompañado de alteración del nivel de consciencia, disfunción cognitiva aguda, alteraciones
comportamentales y crisis comiciales. Se presenta con mayor o menor grado de implicación
meníngea tanto a nivel clínico como analítico, de manera que el líquido cefalorraquídeo (LCR)
puede ser prácticamente normal. En estos casos, como veremos más adelante, debería iniciarse
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [639]
[42] INFECCIONES DEL SISTEMA NERVIOSO CENTRAL
tratamiento empírico con aciclovir hasta descartar definitivamente una infección herpética
(Figura 1).
Figura 1. Manejo inicial del paciente con sospecha de infección aguda del sistema nervioso central.
Por último, la presencia de fiebre o febrícula, déficit neurológico focal de instauración rápidamente
progresiva, crisis comiciales, datos de hipertensión intracraneal (HTIC) y foco infeccioso activo de
localización otorrinolaringológica (ORL), pulmonar o cardiaca sugiere la existencia de un absceso
cerebral.
2. PROCESO DIAGNÓSTICO
En líneas generales, la atención inicial del paciente con infección del SNC no difiere de la de otro
tipo de enfermedad infecciosa. Debe realizarse una anamnesis detallada en la que se incluyan
antecedentes epidemiológicos, alergias medicamentosas, toma previa de antibióticos y cronología del
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [640]
[42] INFECCIONES DEL SISTEMA NERVIOSO CENTRAL
cuadro, así como una exploración física exhaustiva que incluya fondo de ojo y exploración ORL con
otoscopia. Paralelamente, debe asegurarse la vía aérea, así como la estabilidad hemodinámica del enfermo
mientras se canalizan dos accesos venosos periféricos y se extraen hemocultivos y una analítica básica con
hemograma, estudio de coagulación y bioquímica, que incluirá reactantes de fase aguda (proteína C-
reactiva y procalcitonina). El proceso diagnóstico posterior se detalla en la figura 1 y en los siguientes
apartados.
2.1. Indicaciones de tomografía computarizada craneal urgente
Las guías clínicas vigentes obligan a descartar mediante tomografía computarizada (TC) craneal la presencia
de un proceso expansivo o de aumento de la presión intracraneal antes de realizar una punción lumbar (PL)
en los siguientes supuestos:
Inmunodepresión.
Antecedente de proceso intracraneal de tipo tumor/masa cerebral, ictus o infección focal.
Déficit neurológico focal.
Crisis epilépticas de inicio en la última semana.
Papiledema.
Alteración del nivel de consciencia con la escala de coma de Glasgow (ECG) < 12 puntos.
En el resto de las meningitis agudas adquiridas en la comunidad y no complicadas, la PL debe
realizarse sin demora y sin necesidad de prueba de imagen previa.
2.2. Análisis del líquido cefalorraquídeo
El diagnóstico definitivo de la meningitis purulenta y otros procesos infecciosos del SNC se realiza a través
del análisis del LCR. Como se ha mencionado anteriormente, la presencia de datos semiológicos
(papiledema, rigidez de descerebración, etc.) o la evidencia de HTIC en neuroimagen contraindican la PL
por el riesgo de herniación cerebral que conllevan. Asimismo, infecciones locales en el trayecto de punción,
trombopenia por debajo de 50.000 plaquetas, índice internacional normalizado (INR) superior a 1,7 u otros
trastornos de la coagulación contraindican el procedimiento a menos que se corrijan dichas alteraciones
(transfusión plaquetaria, reversión de anticoagulación, etc.).
Siempre que sea posible, se registrará el aspecto macroscópico del líquido y se medirá la presión de
apertura en decúbito lateral. Cifras por encima de 20 cmH2O se consideran patológicas, y sugieren
meningitis purulenta o inflamación crónica de las meninges. A continuación, debe recogerse la muestra de
LCR en tres tubos secos y estériles: uno de ellos (el menos turbio o hemático) se destinará a
determinaciones citobioquímicas (1-2 ml), y los otros dos, a estudios microbiológicos (10 ml en total).
Veinte gotas equivalen aproximadamente a 1 ml.
En primera instancia se realiza un análisis citobioquímico que orienta la naturaleza del proceso
infeccioso (Tabla I), y posteriormente se lleva a cabo el estudio microbiológico con el fin de tipificar el
agente etiológico y su espectro de susceptibilidad a los distintos antimicrobianos.
De manera rutinaria deben solicitarse tinción y cultivo para bacterias y virus y, según la sospecha
clínica, PCR (reacción en cadena de la polimerasa) para los diferentes microorganismos, tinción y cultivo de
hongos y micobacterias, Venereal Disease Research Laboratory (VDRL), etc. Si la sospecha es de meningitis
no infecciosa, también puede remitirse una muestra al servicio de anatomía patológica para estudio
citológico.
Las características diferenciales del LCR en las distintas infecciones del SNC se detallan en la tabla I.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [641]
[42] INFECCIONES DEL SISTEMA NERVIOSO CENTRAL
Tabla I. Características diferenciales del LCR en las infecciones del sistema nervioso central.
Cabe destacar que el recuento leucocitario y la proteinorraquia pueden verse artefactados por el
antecedente de crisis comiciales o la presencia de abundantes hematíes en la muestra (en caso de punción
traumática o presencia de sangre en el espacio subaracnoideo). Como regla general, se restará 1 mg/dL de
proteinorraquia por cada 1.000 hematíes/ml y 1 leucocito por cada 700-1.000 hematíes/ml, o bien se
aplicará la siguiente fórmula correctora:
3. TRATAMIENTO EMPÍRICO
La mortalidad y las secuelas neurológicas asociadas a la meningitis purulenta o a la
meningoencefalitis herpética aumentan sustancialmente a medida que se retrasa el inicio del tratamiento
antibiótico. Por tanto, es preceptivo comenzar el tratamiento empírico tan pronto como sea considerada la
posibilidad de estos diagnósticos. En general, la situación clínica del paciente permite realizar una correcta
valoración del enfermo y una PL. Sin embargo, en caso de sepsis grave, de retraso en la extracción de la
muestra de LCR o en aquellas situaciones que requieran pruebas de imagen complementarias debe primar
el inicio del tratamiento antibiótico. En cualquiera de los casos, es obligado asegurar el inicio del
tratamiento empírico dentro de los primeros 30 minutos desde que se establece el diagnóstico de
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [642]
[42] INFECCIONES DEL SISTEMA NERVIOSO CENTRAL
presunción. Como se verá más adelante, existen métodos diagnósticos microbiológicos que no se ven
artefactados por la administración de antimicrobianos previamente a la obtención del LCR.
La elección del tratamiento adecuado se hará en función de la sospecha diagnóstica, la edad del
paciente, el patrón local de resistencias y otros factores que se detallan en la tabla II.
III. MENINGITIS BACTERIANA AGUDA
1. ETIOPATOGENIA
La epidemiología de las bacterias productoras de meningitis purulenta muestra una importante
variación geográfica dependiendo del desarrollo sociosanitario de cada región. Pero, además, la frecuencia
con que se aísla cada germen dentro de una misma área geográfica depende de otros factores, como la
edad del paciente y su comorbilidad (Tabla II), así como el mecanismo por el que se adquiere la infección,
siendo las distintas puertas de entrada:
Vía hematógena, a través de bacteriemia o embolismos sépticos.
Por contigüidad, a partir de focos sépticos adyacentes, como los senos paranasales o el oído
medio.
Por inoculación directa, en caso de meningitis postraumática,posquirúrgica o por fístula de LCR.
2. CLÍNICA
La tétrada clásica de cefalea, fiebre, rigidez de nuca y deterioro del nivel de consciencia tiene una
baja sensibilidad para el diagnóstico, ya que ocurre con una frecuencia aproximada de solo el 50%. Sin
embargo, en la inmensa mayoría de los casos de meningitis purulenta sí se encuentran presentes al menos
dos de estos síntomas.
Otros síntomas frecuentes son postración, fotofobia, náuseas y vómitos, focalidad neurológica,
alteraciones comportamentales, crisis comiciales, lesiones cutáneas, etc. Tanto el signo de Kérnig como el
de Brudzinski son muy específicos pero poco sensibles. En ningún caso debería utilizarse su ausencia para
descartar el diagnóstico.
En la meningitis bacteriana cobra especial importancia la monitorización clínica del nivel de
consciencia, cuyo deterioro se ha correlacionado con el mal pronóstico vital del paciente. Para este fin se
acepta el uso de la ECG.
Existen algunas claves en la historia clínica y la exploración física que pueden orientarnos acerca del
agente etiológico, si bien nunca debería modificarse el tratamiento antibiótico empírico en función de estos
hallazgos hasta no haber tipificado el germen:
Streptococcus pneumoniae: otitis media aguda, neumonía (síndrome de Austrian: meningitis,
endocarditis y neumonía por neumococo). Más frecuencia de signos focales y crisis comiciales.
Neisseria meningitidis: odinofagia, exantema (rash) purpúrico en piel y mucosas (aparece en el
50% de los casos, aunque no es específico). La suma de exantema, insuficiencia suprarrenal y
coagulación intravascular diseminada (CID) constituye el síndrome de Waterhouse-
Friderichsen; asplenia, hipogammaglobulinemia o déficit del complemento.
Haemophilus influenzae: epiglotitis, asplenia, hipogammaglobulinemia.
Listeria monocytogenes: neuropatías craneales, signos de romboencefalitis, pacientes mayores
de 50 años, cierto grado de inmunosupresión o enfermedades crónicas debilitantes
(hepatopatía, insuficiencia renal crónica, alcoholismo, diabetes, neoplasia).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [643]
[42] INFECCIONES DEL SISTEMA NERVIOSO CENTRAL
Tabla II. Principales agentes etiológicos y tratamiento empírico en pacientes con meningitis bacteriana.
La expresión clínica del cuadro e, incluso, la propia fiebre pueden estar enmascaradas en pacientes
neutropénicos y en las edades extremas de la vida, en que se presenta como un cuadro de torpeza mental,
confusión, letargia, vómitos, convulsiones u otra focalidad neurológica.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [644]
[42] INFECCIONES DEL SISTEMA NERVIOSO CENTRAL
Conviene estar alerta durante los días posteriores al diagnóstico, ya que la ausencia de mejoría
clínica o la aparición de nueva sintomatología a pesar de estar recibiendo el paciente el tratamiento
antibiótico adecuado puede significar la presencia de alguna de las complicaciones asociadas a la meningitis
purulenta: hidrocefalia comunicante, trombosis séptica de estructuras venosas intracraneales con o sin
isquemia cerebral asociada, infartos cerebrales secundarios a arteritis infecciosa o vasoespasmo,
aneurismas micóticos, ventriculitis o formación de un área de cerebritis o absceso cerebral por extensión
del microorganismo desde el espacio subaracnoideo. Por ello, se recomienda repetir la PL si se observa una
mejoría clínica deficiente en las primeras 48 horas desde el inicio del tratamiento. También estaría indicada
la monitorización del LCR en caso de infección por neumococo resistente a cefalosporinas (sobre todo si se
ha administrado tratamiento esteroideo), infección por bacilos gramnegativos en pacientes neonatos o en
presencia de un dispositivo de derivación de LCR.
3. DIAGNÓSTICO
Como se mencionó anteriormente, las características citobioquímicas del LCR confirman el
diagnóstico de meningitis bacteriana, mientras que el análisis microbiológico tipifica el agente etiológico
causante del cuadro. Para ello se dispone de diferentes técnicas:
Tinción de Gram de LCR: es la medida más rápida para orientar el diagnóstico. Sin embargo, su
sensibilidad es variable dependiendo del microorganismo implicado y de la concentración
bacteriana en LCR.
Cultivo de LCR: es el método de referencia, ya que, además de la tipificación del germen,
permite la realización del antibiograma. Su sensibilidad desciende en pacientes que han
recibido tratamiento antibiótico previo.
PCR de ADN bacteriano: la administración de antimicrobianos previa a la extracción de la
muestra apenas afecta a su sensibilidad. Se encuentra disponible para S. pneumoniae, N.
meningitidis, H. influenzae, L. monocytogenes y E. coli.
Si existe sospecha de meningococcemia, pueden extraerse muestras de exudado de orofaringe
(para cultivo y PCR) y de aspirado de las lesiones cutáneas (para tinción de Gram, cultivo y PCR).
Algunos estudios han demostrado que concentraciones elevadas de lactato en LCR (por encima de
4,2 mmol/l) discriminan con alta sensibilidad y especificidad la meningitis bacteriana. Sin embargo,
actualmente no se recomienda su uso en el caso de pacientes con meningitis purulenta adquirida en la
comunidad; sí podría jugar un papel en el caso de pacientes neuroquirúrgicos.
4. TRATAMIENTO
De acuerdo con las guías clínicas, el tratamiento antibiótico debe iniciarse en los primeros 30
minutos desde la llegada del paciente. Esta premisa también se aplica al ámbito extrahospitalario, de modo
que el inicio de tratamiento empírico está indicado de manera ambulatoria (ceftriaxona 1 g iv o im) si existe
una alta sospecha de enfermedad meningocócica invasiva o si se estima un retraso de 90 minutos o mayor
en el traslado del paciente al hospital. Posteriormente se modificará el tratamiento antibiótico dirigido en
función de los hallazgos microbiológicos (Tabla III y Tabla IV).
En caso de adultos con meningitis neumocócica o en pacientes con antecedentes comiciales en los
que se considere que una crisis podría aumentar su morbilidad, puede plantearse la administración
profiláctica de antiepilépticos (fenitoína en bolo de 18 mg/kg a pasar en 30 minutos bajo monitorización de
frecuencia cardiaca, y continuar 24 horas más tarde con la dosis habitual de 100 mg/8 h o 2 mg/kg/8 h).
Deben emplearse medidas preventivas de HTIC: cabecero a 30°, hipotermia moderada y
mantenimiento de la homeostasis metabólica e hidroelectrolítica (con especial atención al posible
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [645]
[42] INFECCIONES DEL SISTEMA NERVIOSO CENTRAL
desarrollo de un síndrome de secreción inadecuada de hormona antidiurética). Si existe evidencia de
edema cerebral, pueden administrarse agentes hiperosmolares, como el manitol 20% (bolo inicial de 0,5-1
g/kg en 10-15 minutos y repetir cada 4-6 horas), para un objetivo de osmolaridad de 315-320 mOsm/l.
Tabla III. Tratamiento antibiótico dirigido según agente etiológico y patrón de susceptibilidad.
Se han llevado a cabo múltiples estudios prospectivos acerca del beneficio del tratamiento
esteroideo en la meningitis bacteriana. El fundamento teórico es que la respuesta inflamatoria que se
produce en el espacio subaracnoideo durante el proceso de bacteriólisis al inicio del tratamiento antibiótico
agrava sustancialmente la morbimortalidad asociada al cuadro. A pesar de que muchos de estos estudios
no han arrojado resultados concluyentes al respecto y de que un reciente metaanálisis no ha podido
demostrar un beneficio significativo del tratamiento con dexametasona en términos generales,
determinados grupos de población sí podrían beneficiarse de él. En ese sentido, las guías clínicas europeas
(European Federation of the Neurological Societies [EFNS]) y norteamericanas (Infectious Diseases Society
of America [IDSA]) recomiendan asociar dexametasona en dosis de 0,15 mg/kg cada 6 horas durante 2-4
días en todos los casos de adultos inmunocompetentes con posible meningitis neumocócica adquirida en la
comunidad y en niños con posible meningitis por H. influenzae. Esta debe administrarse junto a la primera
dosis de antibiótico o previamente, y siempre y cuando su administración no demore el inicio de la
antibioterapia.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [646]
[42] INFECCIONES DEL SISTEMA NERVIOSO CENTRAL
Tabla IV. Dosis recomendadas para el tratamiento de infecciones de sistema nervioso central.
5. PRONÓSTICO
La mortalidad asociada a la meningitis infecciosa continúa situándose en torno al 10-20%, mientras
que la frecuencia de secuelas neurológicas asciende al 20-40% de los casos. Las más prevalentes son la
sordera neurosensorial por afectación del VIII par craneal (sobre todo en niños con infección por H.
influenzae de tipo b), trastornos cognitivo-conductuales, epilepsia, alteraciones motoras, déficit visual, etc.
Se han descrito los siguientes factores de riesgo de mal pronóstico: edad, signos de sepsis y nivel de
consciencia al diagnóstico, crisis comiciales, neuropatías craneales, recuento leucocitario bajo en LCR y
presencia de cocos grampositivos en el LCR.
6. AISLAMIENTO Y QUIMIOPROFILAXIS
Las medidas de aislamiento y los detalles de la profilaxis posexposición se resumen en la tabla V.
Tabla V. Indicaciones de aislamiento y profilaxis posexposición en la meningitis purulenta.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [647]
[42] INFECCIONES DEL SISTEMA NERVIOSO CENTRAL
IV. MENINGITIS SUBAGUDA O CRÓNICA
El diagnóstico diferencial de las meningitis crónicas es amplio, e incluye etiologías infecciosas y
etiologías no infecciosas (Tabla VI); además, los estudios microbiológicos resultan, en ocasiones, no
concluyentes. A este respecto, es fundamental la realización de una anamnesis y una exploración física
exhaustivas en busca de factores epidemiológicos y de signos y síntomas asociados con etiologías
específicas, ya que podrían proporcionar pistas clave para guiar el estudio diagnóstico y enfocar el
tratamiento empírico.
Tabla VI. Diagnóstico diferencial de meningitis y meningoencefalitis con pleocitosis linfocitaria.
Se debe valorar la situación inmunológica del paciente, ya que en inmunosuprimidos la etiología
infecciosa adquiere especial protagonismo. Otros aspectos importantes que deben quedar reflejados en la
historia clínica son la presencia de clínica constitucional, cambios recientes en la medicación, neurocirugía o
procedimientos invasivos previos y antecedentes epidemiológicos importantes, como infección previa o
contactos con tuberculosis, relaciones sexuales de riesgo (virus de la inmunodeficiencia humana [VIH],
sífilis), viajes a áreas endémicas de infecciones fúngicas (Histoplasma capsulatum), contacto con animales
(Cryptococcus neoformans, Toxoplasma gondii), picaduras (Borrelia burgdorferi) e ingesta de alimentos no
procesados (Brucella, Taenia solium). En la exploración física son especialmente importantes la valoración
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [648]
[42] INFECCIONES DEL SISTEMA NERVIOSO CENTRAL
de un posible foco parameníngeo, presencia de adenopatías, hepatoesplenomegalia, lesiones
cutaneomucosas y alteraciones oculares (uveítis, iridociclitis) o articulares.
Las pruebas de neuroimagen son útiles para descartar lesiones ocupantes de espacio (LOES)
cerebrales (abscesos, neoplasia), focos parameníngeos y complicaciones como el desarrollo de hidrocefalia,
si bien los hallazgos rara vez orientan hacia una etiología específica; también pueden ser útiles a la hora de
identificar áreas de hipercaptación susceptibles de biopsia en el caso de que no se identificara una etiología
específica y se produjera un deterioro clínico progresivo a pesar de tratamiento empírico. La realización de
una radiografía de tórax en pacientes con meningitis crónica adquiere especial importancia, dado que
varias etiologías pueden afectar de manera directa al pulmón (tuberculosis [TBC], infecciones fúngicas
sistémicas, sarcoidosis, neoplasias, etc.).
En caso de ausencia de diagnóstico específico y ante un deterioro neurológico progresivo, hay que
considerar el inicio de tratamiento empírico, que deberá individualizarse según los aspectos clínicos y
epidemiológicos de cada paciente, y que consistirá fundamentalmente en la administración de
antituberculosos, antifúngicos o glucocorticoides. Dada su frecuencia y gravedad, es importante guiar el
tratamiento empírico de una meningitis crónica linfocitaria hacia la tuberculosis, especialmente si presenta
hipoglucorraquia y afectación de pares craneales (PC), y deberá mantenerse un mínimo de seis semanas
antes de asumir un fracaso terapéutico. En principio, y salvo en situaciones de gravedad clínica, el uso
concomitante de tratamiento esteroideo debería evitarse, dado que podría confundir la evaluación de la
respuesta a tratamiento antimicobacteriano. En caso de ausencia de respuesta, habrá que plantear
tratamiento empírico esteroideo o antifúngico, en función de la sospecha etiológica inflamatoria o fúngica
del cuadro.
1. MENINGITIS TUBERCULOSA
1.1. Epidemiología
Constituye la causa principal de meningitis crónica en países con alta prevalencia de tuberculosis. Se puede
producir bien como primoinfección, fundamentalmente en niños, o como reactivación tardía en adultos
cuando se dan condiciones de inmunosupresión (infección por VIH, neoplasias, tratamiento
inmunosupresor, alcoholismo o edad avanzada).
1.2. Clínica
Se sospechará en el paciente que presenta síndrome de meningitis crónica sobre el que se va desarrollando
sintomatología de HTIC (secundaria a hidrocefalia), afectación de PC (especialmente el II y el VI) y, en la fase
más avanzada, estupor, coma y focalidad neurológica por isquemia secundaria a fenómenos vasculíticos.
Hasta en un 50% de los casos puede asociar secreción inadecuada de hormona antidiurética (SIADH) por
afectación hipotalámica. Un tercio de los casos se engloban dentro de un cuadro de afectación
generalizada, por lo que la demostración de tubérculos coroideos o un patrón miliar en la radiografía de
tórax apoyan firmemente la sospecha clínica. De forma ocasional puede presentarse como una meningitis
piógena o una demencia progresiva de meses de evolución.
1.3. Diagnóstico
El gold standard para el diagnóstico es su demostración en cultivo de LCR en medio específico, un método
cuya sensibilidad aumenta hasta el 80% si se cultivan muestras múltiples (se recomienda un mínimo de
tres, extraídas mediante punciones lumbares repetidas). Dado su lento crecimiento (3-6 semanas), en el
momento actual la Organización Mundial de la Salud recomienda como prueba inicial ante la sospecha de
meningitis tuberculosa la realización del test Xpert MTB/Rif®, una PCR en tiempo real con sondas para la
detección de ADN micobacteriano y mutaciones que confieren resistencia a la rifampicina. El resultado se
obtiene en 2 o 3 horas y demuestra una sensibilidad del 80% con respecto al cultivo. La demostración de
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [649]
[42] INFECCIONES DEL SISTEMA NERVIOSO CENTRAL
bacterias ácido alcohol resistentes (BAAR) mediante la tinción de Ziehl-Neelsen del LCR puede ser
diagnóstica, si bien su sensibilidad es baja (30%).
Las características del LCR se expresan en la tabla I. La elevación de la adenosina-desaminasa (ADA)
en LCR por encima de 8 U/l apoya la sospecha clínica (sensibilidad < 59%; especificidad > 96%), si bien su
papel diagnóstico es limitado debido a la heterogeneidad de los estudios disponibles, los diferentes
métodos de laboratorio y su elevación en otras causas de inflamación meníngea. La detección de interferón
gamma en LCR en títulos altos sugiere el diagnóstico. Las pruebas de neuroimagen pueden mostrar
alteraciones típicas, aunque no específicas, tales como engrosamiento e hipercaptación leptomeníngea en
la porción basal, hidrocefalia, lesiones isquémicas y tuberculomas.
1.4. Tratamiento
El tratamiento estándar consiste en una fase de inducción con cuatro fármacos (isoniazida, rifampicina,
pirazinamida y etambutol) durante dos meses, seguido de una fase de mantenimiento con isoniazida y
rifampicina durante 7-10 meses (para detalles y posología, ver Capítulo 45. “Tuberculosis”). Estudios
farmacocinéticos indican que el paso de la barrera hematoencefálica del etambutol es escaso en ausencia
de inflamación, por lo que algunos autores sugieren sustituirlo por una fluoroquinolona (levofloxacino o
moxifloxacino), especialmente en fases no avanzadas de la enfermedad, en que el paso es mucho mayor.
Sin embargo, no existe en el momento actual evidencia clínica suficiente que apoye el uso de un fármaco
sobre otro. Las guías recomiendan el uso concomitante de esteroides en todos los pacientes, ya que han
demostrado disminuir la mortalidad y la gravedad de las secuelas en pacientes sin VIH, pero falta evidencia
que recomiende o desaconseje su uso en pacientes VIH. En pacientes que presentan alteración del nivel de
consciencia o focalidad, se recomienda tratamiento esteroideo por vía iv durante cuatro semanas
(dexametasona 0,4 mg/kg/día la primera semana, 0,3 mg/kg/día la segunda, 0,2 mg/kg/día la tercera y 0,1
mg/kg/día la cuarta), seguido de cuatro semanas de tratamiento por vía oral (4 mg/día y descenso de 1 mg
semanal hasta suspender). En pacientes sin alteraciones neurológicas, el periodo de corticoterapia
intravenosa puede reducirse a dos semanas, seguido de las cuatro semanas por vía oral.
En el futuro, el ácido acetilsalicílico (AAS) podría tener un papel adyuvante, ya que estudios
preliminares apuntan a una disminución de eventos isquémicos y mortalidad global. Tras el inicio del
tratamiento puede aparecer una respuesta paradójica, consistente en un empeoramiento clínico asociado a
la reacción inflamatoria. Aparece de forma típica en pacientes VIH con la reconstitución inmunitaria tras el
inicio de tratamiento antirretroviral de gran actividad (TARGA), aunque también puede aparecer en
pacientes seronegativos. Se recomienda monitorización de respuesta a tratamiento con realización de PL
de control para valorar la normalización de LCR. En casos de hidrocefalia comunicante está indicado el
tratamiento diurético (acetazolamida 10-20 mg/kg/día o furosemida 40 mg/día), valorando la derivación de
LCR en caso de falta de respuesta a tratamiento o de hidrocefalia no comunicante.
1.5. Pronóstico
La meningitis tuberculosa es la forma más grave de infección tuberculosa, con una mortalidad del 25% en
pacientes sin VIH y de hasta el 67% en coinfectados. Aproximadamente la mitad de los supervivientes
sufren secuelas neurológicas. Los factores pronósticos más importantes son el inicio de tratamiento precoz
y la gravedad de presentación al diagnóstico: coma, convulsiones, parálisis de PC y eventos isquémicos.
2. MENINGITIS POR LISTERIA MONOCYTOGENES
Listeria afecta principalmente a neonatos, pacientes con cierto grado de inmunosupresión y
mayores de 50 años (Tabla II). La forma de adquisición en adultos es por ingesta de alimentos
contaminados. La meningitis por Listeria puede cursar como un cuadro subagudo de fiebre y leve
disminución del nivel de consciencia o adquirir un curso fulminante en pocos días. Puede asociar focalidad
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [650]
[42] INFECCIONES DEL SISTEMA NERVIOSO CENTRAL
neurológica por componente encefalítico asociado. Cuando la afectación es puramente encefalítica y afecta
al tronco del encéfalo o cerebelo se denomina romboencefalitis. El curso de dicha entidad es bifásico,
comenzando con fiebre, cefalea y náuseas o vómitos, seguidos a los pocos días de paresia de PC, nistagmo,
ataxia, disminución del nivel de consciencia, crisis epilépticas y hemiparesia por afectación de la vía
piramidal. Listeria puede provocar también un cuadro de cerebritis, con o sin afectación meníngea
asociada, que evoluciona frecuentemente hacia la formación de un absceso cerebral. El diagnóstico se basa
en la demostración de cocobacilos grampositivos en LCR y su aislamiento en cultivo de LCR o hemocultivo.
El tratamiento se realiza con ampicilina y gentamicina durante 21 días. Algunos autores desaconsejan el uso
de gentamicina debido a la alta incidencia de nefro y ototoxicidad, optando por monoterapia con
ampicilina.
3. NEUROSÍFILIS
(Ver Capítulo 40. “Enfermedades de transmisión sexual”).
4. BORRELIOSIS DE LYME
Su agente causal es Borrelia burgdorferi; su vector, las garrapatas del género Ixodes y su reservorio
principal, los pequeños roedores y los ungulados. En España, la mayor parte de los casos se localizan en la
cornisa cantábrica. La manifestación clínica más característica es la presencia de eritema migrans, que
puede aparecer de forma aislada en la primera fase de la enfermedad (fase inicial localizada) o en forma de
lesiones múltiples en la segunda. En la segunda etapa (fase inicial diseminada) pueden existir
meningoencefalitis y meningorradiculitis linfocitaria (síndrome de Bannwarth) con afectación de PC
(parálisis facial periférica, que puede ser bilateral), asociadas a manifestaciones cardiacas y oculares. La
tercera etapa (fase tardía persistente), caracterizada principalmente por la afectación oligoarticular, puede
asociar encefalopatía crónica y polineuropatías. El diagnóstico requiere alta sospecha clínica y se completa
con métodos serológicos. El tratamiento de la meningoencefalitis es ceftriaxona durante 14 a 28 días, y, en
caso de parálisis facial aislada, doxiciclina (100 mg/12 h) o amoxicilina (500 mg/8 h, de elección en
embarazadas y niños) durante 14 días.
5. NEUROBRUCELOSIS
La brucelosis es una infección zoonótica propia del ganado bovino y ocasionada por especies del
género Brucella, entre las cuales B. mellitensis es la más frecuentemente implicada en infección humana. Se
transmite al ser humano tras la ingesta de productos lácteos o cárnicos infectados. Clínicamente tiene una
presentación polimorfa que puede cursar con fiebre y afectación parenquimatosa en múltiples órganos, de
curso agudo o crónico. En el SNC puede cursar con meningitis aguda o crónica, meningoencefalitis,
radiculopatías únicas, múltiples o polirradiculoneuropatía (similar a síndrome de Guillain-Barré), ictus
isquémicos (por afectación meningovascular o cardiogénicos por endocarditis) y mielitis. El LCR presenta un
patrón de pleocitosis linfocitaria con hiperproteinorraquia e hipoglucorraquia. El diagnóstico microbiológico
puede realizarse mediante hemocultivo, cultivo de aspirado de médula ósea en medios bifásicos, test
serológicos (aglutinación en tubo, análisis de inmunoadsorción enzimática ELISA, prueba de Rosa de
Bengala, test de Coombs) o PCR. El tratamiento de primera elección para la neurobrucelosis incluye
ceftriaxona durante un mes asociada a doxiciclina (100 mg/12 h) y rifampicina durante 4-5 meses, debiendo
mantenerse en función de la respuesta clínica y hasta que los parámetros de LCR se normalicen. Otra
posibilidad sería la combinación de cotrimoxazol, doxicilina y rifampicina durante al menos 5-6 meses.
Pueden asociarse esteroides en formas de afectación grave.
6. MENINGITIS CRIPTOCÓCICA
Constituye la infección fúngica del SNC más frecuente en nuestro medio. La afectación del SNC
tiene lugar tras la reactivación de un foco pulmonar latente. Se presenta casi con exclusividad en pacientes
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [651]
[42] INFECCIONES DEL SISTEMA NERVIOSO CENTRAL
con algún grado de inmunodepresión celular (típicamente, VIH con CD4 < 100 céls./μl). Clínicamente suele
cursar como un cuadro de meningitis crónica, aunque en pacientes muy inmunodeprimidos puede
presentarse de forma aguda. Puede cursar con la formación de abscesos o criptococomas. El diagnóstico de
certeza se establece con la visualización directa del hongo en LCR (tinción con tinta china), cultivo o
mediante la demostración del antígeno criptocócico en LCR y suero con técnicas de aglutinación de látex o
ELISA. El tratamiento se basa en anfotericina B liposomal (3-5 mg/kg/día) en combinación con 5-flucitosina
(25 mg/kg/6 h) durante 2 semanas, seguidas de fluconazol (400-800 mg/día) durante 10 semanas. En
pacientes con evidencia de HTIC es fundamental un manejo enérgico de la misma, con realización de PL de
repetición o incluso colocación de una derivación de LCR, que ha demostrado disminuir la morbimortalidad.
La profilaxis secundaria con fluconazol (200-400 mg/día) debe prolongarse durante 6-12 meses o de forma
indefinida, dependiendo de la condición de inmunosupresión subyacente (ver Capítulo 46. “Infección VIH”).
7. NEUROCISTICERCOSIS
Se debe a la infestación del SNC por las formas larvarias de Taenia solium. Su incidencia en nuestro
medio ha experimentado un crecimiento progresivo en los últimos años a causa de la inmigración y los
viajes a zonas endémicas (Centroamérica y Sudamérica, principalmente). La presentación más habitual es
en forma de crisis convulsivas, manifestaciones de HTIC (por efecto masa o desarrollo de hidrocefalia) y
clínica focal dependiendo del número, tamaño, localización de los quistes y magnitud de la respuesta
inflamatoria asociada. La aproximación diagnóstica se basa en el conjunto de datos epidemiológicos,
clínicos, serológicos y radiológicos sugestivos (lesiones quísticas sin escólex, lesiones hipercaptantes,
calcificaciones diseminadas).
El diagnóstico de certeza está definido únicamente por la demostración histológica del parásito, la
objetivación del escólex dentro de un quiste en pruebas de neuroimagen o la visualización del parásito en
el examen de fondo de ojo.
El tratamiento con albendazol (15 mg/kg/día en 2-3 dosis diarias) está indicado en las siguientes
situaciones: quiste parenquimatoso único viable, múltiples quistes parenquimatosos y cisticercosis
subaracnoidea. A los pocos días de iniciado el tratamiento puede advertirse una respuesta paradójica, con
empeoramiento asociado a la respuesta inflamatoria, motivo por el cual está indicado el uso concomitante
de esteroides (prednisona a 1 mg/kg durante 5-10 días y posterior pauta descendente). En casos de
encefalitis, edema cerebral difuso, afectación medular o ante fenómenos vasculíticos asociados, deberá
diferirse el inicio de tratamiento antiparasitario hasta el momento en que la inflamación local esté
controlada con tratamiento esteroideo. El tratamiento no está indicado en pacientes con quistes
calcificados no viables. Antes de iniciar tratamiento debe realizarse un examen de fondo de ojo a todos los
pacientes para descartar afectación ocular (se contraindica tratamiento antiparasitario hasta resección
quirúrgica del quiste). El manejo de las complicaciones incluye tratamiento antiepiléptico y derivación del
LCR o intervención neuroquirúrgica en los quistes que produzcan hidrocefalia obstructiva.
V. MENINGITIS LINFOCITARIA O ASÉPTICA
Hace referencia a un síndrome meníngeo de presentación aguda con pleocitosis linfocitaria y
ausencia de aislamientos bacterianos en tinción de Gram y cultivo de LCR.
1. ETIOLOGÍA
La mayor parte son de etiología vírica, destacando los enterovirus como agente etiológico principal
y continuando en orden descendente de frecuencia con el virus herpes simple de tipo 2 (VHS-2), el virus
varicela-zóster (VVZ) y virus herpes simple tipo 1. Es importante tener en cuenta que la primoinfección por
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [652]
[42] INFECCIONES DEL SISTEMA NERVIOSO CENTRAL
VIH puede presentarse como meningitis aséptica en un 10% de los casos. Otras causas víricas más
infrecuentes, así como causas no víricas, se detallan en la tabla VI.
2. CLÍNICA
La presentación inicial es indistinguible de una meningitis piógena, si bien los síntomas suelen ser
de menor intensidad y la evolución es generalmente favorable. Puede asociar sintomatología vírica
sistémica inespecífica y, en el caso de los enterovirus, alteraciones mucocutáneas específicas (enfermedad
mano-pie-boca, herpangina, exantema). Un deterioro progresivo del nivel de consciencia o la aparición de
convulsiones indicarían evolución a meningoencefalitis.
La meningitis de Mollaret es una forma benigna de meningitis linfocitaria recurrente, con al menos
tres episodios autolimitados de fiebre y meningismo de menos de cinco días de duración, y su agente
etiológico más frecuente es el VHS-2. Pueden llevar asociadas otras manifestaciones neurológicas
transitorias.
3. DIAGNÓSTICO
Las características del LCR se recogen en la tabla I. Está indicada la realización de PCR en LCR para
enterovirus, VHS y VVZ.
4. TRATAMIENTO Y PRONÓSTICO
En el caso de los enterovirus, el tratamiento es exclusivamente sintomático y la evolución resulta
generalmente favorable. En el caso del VHS, estaría indicado el tratamiento con aciclovir, inicialmente
intravenoso (10 mg/kg cada 8 horas) y posteriormente oral, hasta cumplir 14 días de tratamiento. Es
importante mantener una vigilancia estrecha en las primeras 24-48 horas y repetir la PL ante un deterioro
clínico. Si existe duda acerca de la etiología vírica o bacteriana del cuadro (perfil LCR indeterminado),
especialmente en pacientes ancianos, inmunosuprimidos o que hayan tomado antibióticos antes de su
valoración, estaría indicada la cobertura antibiótica empírica hasta la obtención de resultados
microbiológicos (Tabla II).
VI. ENCEFALITIS VÍRICA
1. ETIOPATOGENIA
Al igual que en la meningitis aséptica, el principal agente etiológico de las encefalitis son los virus,
entre los que destaca el VHS-1 como primera causa en casos esporádicos. Otros virus a tener en cuenta son
los enterovirus, el VHS-2, el VVZ, el virus de la parotiditis, el virus de la gripe y los virus transmitidos por
artrópodos (arbovirus). En pacientes inmunosuprimidos cobran importancia otras partículas infecciosas,
como el citomegalovirus (CMV), el virus de Epstein-Barr (VEB), el virus JC y el virus herpes humano 6 (VHH-
6). Se consideran dos mecanismos etiopatogénicos posibles: por afectación parenquimatosa directa del
microorganismo o por una respuesta inmunitaria anómala tras una infección o tras una vacunación. La
invasión de sistema nervioso central puede producirse por vía hematógena o por vía nerviosa (familia
Herpesviridae, rabia), existiendo casi siempre reacción meníngea secundaria.
2. CLÍNICA
El cuadro se define como un síndrome febril asociado a signos de irritación meníngea (cefalea,
rigidez nucal, fotofobia) y datos de afectación difusa y focal del sistema nervioso central. Como datos de
afectación difusa destacan la alteración del nivel de consciencia (desde somnolencia a coma),
desorientación, alteraciones conductuales y de memoria, irritabilidad, agitación o psicosis. La afectación
focal incluye parálisis de PC, afasia, hemiparesia, ataxia, etc. Son frecuentes las crisis comiciales focales o
generalizadas. Puede existir afectación del eje hipotálamo-hipofisario (alteraciones de la termorregulación,
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [653]
[42] INFECCIONES DEL SISTEMA NERVIOSO CENTRAL
diabetes insípida, SIADH). La afectación medular (encefalomielitis) suele cursar con parálisis flácida, nivel
sensitivo y alteración en el control de esfínteres. Ningún síntoma o signo es específico de determinada
etiología. La meningoencefalitis herpética presenta un curso agudo con rápida progresión y afecta
principalmente a lóbulos temporales y frontobasales. En pacientes inmunosuprimidos, el curso suele ser
más prolongado o recurrente. En la encefalitis desmielinizante aguda (posinfecciosa o posvacunal), es
frecuente la presencia de un cuadro pseudogripal que precede en 4-21 días al inicio de la clínica
neurológica.
3. DIAGNÓSTICO
El diagnóstico se apoya en el estudio microbiológico de LCR, las pruebas de neuroimagen y el EEG.
Ante la sospecha de encefalitis aguda, tras descartar mediante prueba de imagen la presencia de una LOE
cerebral, se realizará una PL para estudio de LCR que presentará características superponibles a las de las
meningitis víricas (aunque en pacientes inmunodeprimidos y fases precoces puede ser normal). El LCR
puede presentar un componente hemorrágico (> 500 hematíes/μl) hasta en un 20% de los casos. La PCR,
con una sensibilidad del 98% y una especificidad del 94% para VHS con respecto a la biopsia cerebral, es el
método diagnóstico de elección para las encefalitis víricas. Los hallazgos típicos de la meningoencefalitis
herpética en pruebas de neuroimagen, TC o resonancia magnética (de elección), son, respectivamente,
hipodensidad e hiperintensidad en T2 en región inferomedial de lóbulos temporales, extendiéndose
ocasionalmente hacia la ínsula y la porción basal de los lóbulos frontales, aunque en fases precoces pueden
ser normales. En la meningoencefalitis herpética, el EEG muestra alteraciones focales en uno o ambos
lóbulos temporales desde fases precoces, con enlentecimiento o presencia de complejos punta-onda
periódicos lateralizados (PLED), siendo este último el patrón típico (aunque no patognomónico) de la
enfermedad.
4. TRATAMIENTO
Ante la sospecha de encefalitis herpética, se debe iniciar tratamiento empírico precoz con aciclovir
iv (10 mg/kg cada 8 horas, ajustado a función renal y en perfusión lenta), puesto que reduce la mortalidad y
las secuelas neurológicas. Una vez confirmado el diagnóstico, debe mantenerse durante 14-21 días, repetir
la PCR para VHS en LCR al finalizar tratamiento y ampliar la cobertura siete días más si esta resultara
positiva. Asimismo, son fundamentales las medidas de soporte y el control sintomático (manejo de la HTIC,
reposición hidroelectrolítica, control de la presión arterial, tratamiento antipirético, anticonvulsivo y
analgésico). Ante la sospecha de encefalitis desmielinizante aguda, estaría indicada la administración de
corticoides en dosis altas (bolo de 6-metilprednisolona de 1.000 mg cada 24 horas durante tres días,
seguidos de prednisona a razón de 1 mg/kg durante otros cinco y descenso progresivo en 15 días). Ante la
duda de una posible etiología vírica del cuadro, y a la espera de los resultados microbiológicos del LCR,
estaría indicada la cobertura antibiótica para L. monocytogenes.
5. PRONÓSTICO
En ausencia de tratamiento, hasta el 70% de los pacientes con encefalitis herpética mueren o
sufren secuelas neurológicas graves (amnesia, trastornos de conducta, disfasias, crisis comiciales, etc.),
pero tras la introducción del aciclovir ese porcentaje se ha visto reducido al 30%. Únicamente el 2,5% de los
casos se recuperan sin secuelas.
VII. INFECCIONES FOCALES DEL SISTEMA NERVIOSO CENTRAL
1. ABSCESO CEREBRAL
1.1. Etiopatogenia
Se trata de un proceso supurativo focal del parénquima cerebral que puede estar producido por bacterias,
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [654]
[42] INFECCIONES DEL SISTEMA NERVIOSO CENTRAL
hongos o parásitos. La mayor parte de los pacientes presentan algún factor de inmunosupresión o bien una
ruptura de las barreras protectoras del cerebro (inoculación directa) o un proceso infeccioso local
(propagación por contigüidad) o sistémico (diseminación hematógena). La tabla VII muestra los agentes
etiológicos más frecuentemente implicados. Hasta un 60% presenta un carácter polimicrobiano. En un 20-
30% de los casos no se identifica un foco primario (absceso criptogénico).
Tabla VII. Etiología y tratamiento empírico del absceso cerebral.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [655]
[42] INFECCIONES DEL SISTEMA NERVIOSO CENTRAL
1.2. Clínica
Las manifestaciones clínicas dependerán del foco primario, de la localización y tamaño del absceso, del
grado de HTIC y del estado inmunitario del paciente. El síntoma más frecuente es la cefalea progresiva
seguida por alteración del nivel de consciencia, déficit focal neurológico (hemiparesia, afasia, defectos
campimétricos) y crisis comiciales. La fiebre es inconstante (50%) y de escasa magnitud. Ante un deterioro
clínico agudo con aumento de la cefalea y aparición de signos meníngeos, ha de sospecharse rotura del
absceso al espacio ventricular o subaracnoideo, con desarrollo de meningitis purulenta secundaria. El curso
clínico puede ser agudo y fulminante o bien indolente durante varias semanas, aunque en la mayoría de los
casos la evolución clínica hasta el diagnóstico es inferior a 15 días.
1.3. Diagnóstico
La TC y la RM craneal son las técnicas diagnósticas de elección, ya que aportan información sobre el estadio
evolutivo, número, localización, posibles focos primarios (senos paranasales, oído medio, mastoides) y
detección de complicaciones (efecto masa, rotura a ventrículos, hidrocefalia). La imagen típica es una lesión
hipodensa en TC, hipointensa en RM secuenciada en T1, con restricción a la difusión y con refuerzo en
anillo tras la administración de contraste, generalmente completo, fino y regular. En la fase inicial de
cerebritis, la TC puede ser normal o presentar hipodensidades mal definidas. La RM es más sensible para
detectar abscesos en fase precoz, abscesos de pequeño tamaño (< 1,5 cm) y abscesos localizados en fosa
posterior.
La PL está contraindicada (especialmente en lesiones grandes, con mucho edema, efecto masa y en
aquellas situadas en fosa posterior) por escasa rentabilidad diagnóstica (< 10%) y elevado riesgo de
herniación. El estudio microbiológico se realiza a través de hemocultivos (solo positivos en caso de
mecanismo hematógeno) y cultivo de material obtenido mediante punción estereotáxica del absceso. Debe
realizarse un estudio serológico (VIH, Brucella, Toxoplasma) y antígeno criptocócico según la sospecha
clínica. Las pruebas de laboratorio pueden mostrar leucocitosis y elevación de reactantes.
1.4. Tratamiento
1.4.1. Tratamiento médico
Se debe administrar antibioterapia intravenosa durante 6-8 semanas. Las pautas de antibioterapia empírica
se muestran en la tabla VII. El tratamiento con corticoides únicamente está indicado en casos de HTIC
relacionada con efecto masa del absceso y edema vasogénico importante (dexametasona, con dosis inicial
de 4 mg/6 h). Su uso no debe ser indiscriminado, ya que inhiben el proceso de formación de la cápsula y
disminuyen la penetrancia de algunos antibióticos en el SNC. Puede administrarse tratamiento
anticonvulsivo de forma profiláctica ante la elevada incidencia de crisis epilépticas.
1.4.2. Tratamiento quirúrgico
Todo paciente con sospecha de absceso cerebral debe ser valorado por el servicio de neurocirugía. A pesar
de que los abscesos en fase de cerebritis o de pequeño tamaño pueden resolverse simplemente con
tratamiento antibiótico, debe plantearse la punción-aspiración o la exéresis quirúrgica en todo absceso
cerebral.
Las indicaciones de punción-aspiración más aceptadas son abscesos grandes (de más de 3 cm de
diámetro), localizados en la fosa posterior, adyacentes a la pared ventricular (riesgo de ventriculitis
catastrófica en caso de rotura) o implicación de microorganismos de difícil erradicación (hongos). La
resección quirúrgica se reserva para casos de fracaso de drenaje por aspiración, abscesos multilobulados o
presencia de cuerpos extraños.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [656]
[42] INFECCIONES DEL SISTEMA NERVIOSO CENTRAL
2. TROMBOFLEBITIS SÉPTICA INTRACRANEAL
Se trata de una trombosis de venas corticales y de los senos venosos que puede ocurrir como
complicación de procesos infecciosos locales (SNC, área ORL, celulitis facial). Las manifestaciones clínicas
consisten en cefalea asociada a afectación local en función del seno afectado: en el seno longitudinal
superior destaca la disminución del nivel de consciencia, así como paraparesia y piramidalismo bilateral; en
el seno cavernoso aparecen cefalea frontal, retroorbitaria, ptosis, proptosis, quemosis y afectación de PC
oculomotores; y en el seno lateral, otalgia y afectación de los PC V y VI. El diagnóstico se realiza mediante
RM y angio-RM, y el tratamiento se basa en antibioterapia en función del proceso infeccioso asociado. En
pacientes con trombosis séptica del seno cavernoso debe individualizarse la decisión de iniciar tratamiento
anticoagulante en función del riesgo individual de sangrado, puesto que no existen datos prospectivos al
respecto y, a tenor de los estudios publicados, su uso es controvertido.
3. ABSCESO EPIDURAL Y EMPIEMA SUBDURAL
El absceso epidural está localizado entre la cara interna del cráneo y la duramadre, y el empiema
subdural, entre la duramadre y la aracnoides. Son entidades infrecuentes. Los microorganismos más
frecuentemente implicados son bacilos gramnegativos y cocos grampositivos. Clínicamente cursan con
meningismo, cefalea, fiebre y disminución del nivel de consciencia (mayor en empiema subdural). El
diagnóstico se realiza mediante RM, y la PL está contraindicada. El tratamiento se basa en drenaje
quirúrgico y antibioterapia de amplio espectro con cefalosporinas de tercera generación asociadas a
vancomicina o linezolid y metronidazol durante cuatro semanas.
4. ABSCESO EPIDURAL ESPINAL
Se origina por vía hematógena (70%) o por extensión directa desde una infección local
(osteomielitis, úlceras por decúbito, procedimientos invasivos). Los factores de riesgo son alteraciones
inmunitarias, enfermedades crónicas y consumo de drogas por vía parenteral. Clínicamente, cursan con
dolor local (apofisalgias) y radicular, fiebre y síntomas medulares por efecto compresivo (paraparesia
rápidamente progresiva asociada a alteraciones esfinterianas). Ante la sospecha, debe realizarse una RM
urgente. La PL está contraindicada por riesgo de diseminación. El tratamiento se basa en drenaje quirúrgico
urgente y antibioterapia empírica de amplio espectro con cobertura para Staphylococcus aureus. El
pronóstico funcional depende de la afectación previa a la cirugía, y la mortalidad global alcanza el 20%.
BIBLIOGRAFÍA
Aguilar Rodríguez F, Bisbal Pardo O, Gómez Cuervo C, De Lagarde Sebastián M, Maestro de la Calle G,
Pérez-Jacoiste Asín MA, et al. Manual de Diagnóstico y Terapéutica Médica. Hospital Universitario 12
de Octubre. 7ª ed. MSD; 2012. p. 551-68.
Ballester Joya LA, Capdevila Morell JA. Meningitis bacteriana aguda en adultos. En: Capdevila Morell JA,
coordinador. Protocolos en enfermedades infecciosas. Sociedad Española de Medicina Interna.
Madrid: Elsevier España; 2009. p. 19-32. Disponible en:
https://www.fesemi.org/sites/default/files/documentos/publicaciones/ protocolos-enfermedades-
infecciosas.pdf
Beckham JD, Tyler KL. Encephalitis. En: Bennett JE, Dolin R, Blaser MJ, editores. Mandell, Douglas and
Bennett’s Principles and Practice of Infectious Diseases. 8ª ed. Philadelphia: Elsevier Saunders; 2015.
p. 1144-63.
Brouwer MC, Tunkel AR, McKhann GM, Van de Beek D. Brain abscess. N Engl J Med. 2014;371:447-
56.
Camacho Salas A, González de la Aleja Tejera J, Sepúlveda Sánchez JM. Urgencias en Neurología.
Hospital Universitario 12 de Octubre. 2ª ed. Madrid: Ergon; 2013. p. 272-99.
Chaudhuri A, Martin PM, Kennedy PGE, Seaton RA, Portegies P, Bojar M, et al. EFNS guideline on the
management of community-acquired bacterial meningitis: report of an EFNS Task Force on acute
bacterial meningitis in older children and adults. Eur J Neurol. 2008;(7):649-59.
Fernández-Viladrich P, Cabellos C, Navas E, Martínez Lacasa J, Gatell JM. Infecciones del sistema
nervioso central. En: Aguado JM, Almirante B, Fortún J, editores. Protocolos clínicos SEIMC. Sociedad
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [657]
[42] INFECCIONES DEL SISTEMA NERVIOSO CENTRAL
Española de Enfermedades Infecciosas y Microbiología Clínica; 2002. Disponible en:
https://www.seimc.org/contenidos/ documentoscientificos/procedimientosclinicos/seimc-
procedimientoclinicoii.pdf
Glimåker M, Johansson B, Grindborg Ö, Bottai M, Lindquist L, Sjölin J. Adult bacterial meningitis: earlier
treatment and improved outcome following guideline revision promoting prompt lumbar puncture. Clin
Infect Dis. 2015;(8):1162-9.
Hughes DC, Raghavan A, Mordekar SR, Griffiths PD, Connolly DJ. Role of imaging in the diagnosis of
acute bacterial meningitis and its complications. Postgrad Med J. 2010;(1018):478-85.
Koroshetz WJ, Nath A. Chronic and recurrent meningitis. En: Kasper DL, Hauser SL, Jameson JL, Fauci
AS, Longo DL, Loscalzo J, editores. Harrison’s Principles of Internal Medicine. 19ª ed. McGraw-Hill;
2015. p. 906-11.
Maynard-Smith L, Larke N, Peters JA, Lawn SD. Diagnostic accuracy of the Xpert MTB/RIF assay for
extrapulmonary and pulmonary tuberculosis when testing non-respiratory samples: a systematic
review. BMC Infect Dis. 2014;14:709.
Mensa J, Soriano A, Llinares P, Barberán J, Montejo M, Salavert M, et al. Guía de tratamiento
antimicrobiano de la infección por ‘Staphylococcus aureus’. Rev Esp Quimioter. 2013;26(Supl. 1):1-84.
Pruitt AA. Neurologic infectious disease emergencies. Neurol Clin. 2012;(1):129-59.
Ricard JD, Wolff M, Lacherade JC, Mourvillier B, Hidri N, Barnaud G, et al. Levels of vancomycin in
cerebrospinal fluid of adult patients receiving adjunctive corticosteroids to treat pneumococcal
meningitis: a prospective multicenter observational study. Clin Infect Dis. 2007;(2):250-5.
Siegel JD, Rhinehart E, Jackson M, Chiarello L; Healthcare Infection Control Practices Advisory
Committee. 2007 Guideline for Isolation Precautions: Preventing Transmission of Infectious Agents in
Healthcare Settings.
Solomon T, Michael BD, Smith PE, Sanderson F, Davies NWS, Hart IJ, et al. Management of suspected
viral encephalitis in adults. Association of British Neurologists and British Infection Association National
Guidelines. J Infect. 2012;64:347-73.
Thwaites GE, Van Toorn R, Schoeman J. Tuberculous meningitis: more questions, still too few answers.
Lancet Neurol. 2013;12:999-1010.
Tunkel AR, Hartman BJ, Sheldon LK, Kaufman BA, Roos KL, Scheld WM, et al. Practice guidelines for
the management of bacterial meningitis. Clin Infect Dis. 2004;(9):1267-84.
Van de Beek D, Brouwer MC, Thwaites GE, Tunckel AR. Advances in treatment of bacterial meningitis.
Lancet. 2012;(380):1693-702.
Van de Beek D, Farrar JJ, de Gans J, Mai NT, Molyneux EM, Peltola H, et al. Adjunctive dexamethasone
in bacterial meningitis: a meta-analysis of individual patient data. Lancet Neurol. 2010;(3):254-63.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [658]
[43] INFECCIONES INTRAABDOMINALES. DIARREA POR CLOSTRIDIUM DIFFICILE
43.Infecciones intraabdominales. Diarrea por
Clostridium difficile
Elena Arranz Canales.
Medicina Interna
Nuria Valdeolivas Hidalgo.
Medicina Interna
María García-Conde Delgado.
Cirugía General
Asesores: Julia Origüen Sabater. Médica Adjunta de la Unidad de Enfermedades Infecciosas. Óscar Caso Maestro Médico
Adjunto de Cirugía General y del Aparato Digestivo
I. INTRODUCCIÓN
La infección intraabdominal (IIA) representa un espectro de enfermedades con una localización y
una patogénesis común, pudiendo afectar a la cavidad abdominal, tanto en su compartimento
intraperitoneal como extraperitoneal, y puede manifestarse como una infección contenida o generalizada.
La IIA es la segunda causa más frecuente de infección en pacientes con sepsis grave, shock séptico y muerte
por infección en la Unidad de Cuidados Intensivos (UCI).
La infección puede ser inicialmente localizada, afectando a un órgano, y puede posteriormente
resolverse o contenerse, dando lugar a la formación de abscesos, o generalizarse con la consecuente
aparición de peritonitis o sepsis.
La peritonitis se define como la inflamación del peritoneo, resultado de la contaminación de la
cavidad peritoneal por microorganismos, sustancias químicas irritantes o ambas. Se puede clasificar como
primaria, secundaria y terciaria:
Peritonitis primaria (1%): no está relacionada con la perforación del tubo digestivo y,
generalmente, ocurre en pacientes con enfermedad hepática y ascitis (peritonitis bacteriana
espontánea, PBE), así como nefrópatas (síndrome nefrótico, diálisis peritoneal). Suelen ser
monobacterianas y los gérmenes más frecuentemente implicados son: S. pneumoniae,
estreptococos del grupo A y enterobacterias, en las no asociadas a cirrosis; E. coli y Klebsiella
pneumoniae en las asociadas a cirrosis; microorganismos de la piel (Staphylococcus aureus,
coagulasa negativo y estreptococo del grupo viridans) en las asociadas a diálisis.
Peritonitis secundaria (90%): consecuencia de la contaminación de la cavidad peritoneal por
microorganismos procedentes del tubo digestivo (perforación, necrosis, cirugía, heridas
traumáticas). Los gérmenes más comúnmente implicados son aerobios y facultativos (E. coli,
Enterococcus spp y Klebsiella spp) y anaerobios (Bacteroides fragilis). La mayoría de las
infecciones son polimicrobianas.
Peritonitis terciaria: en pacientes que requieren más de una intervención para el control de la
fuente de la infección, en situación de fallo multiorgánico después de una cirugía abdominal
(debido a translocación bacteriana). Los gérmenes más frecuentes implicados son: estafilococos
coagulasa negativos, enterococos y Candida spp.
El abordaje general de las infecciones intraabdominales consiste en una historia clínica y una
exploración física exhaustiva del paciente, así como en la utilización de las pruebas complementarias
diagnósticas que se necesiten (ver Capítulo 9. “Abdomen agudo”).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [659]
[43] INFECCIONES INTRAABDOMINALES. DIARREA POR CLOSTRIDIUM DIFFICILE
II. APENDICITIS AGUDA
1. CONCEPTO
La apendicitis aguda es la inflamación del apéndice cecal, una de las causas más frecuentes de
abdomen agudo quirúrgico.
2. FISIOPATOLOGÍA
Obstrucción de la luz apendicular (fecalito, hiperplasia linfoide, proceso infeccioso, neoplasias),
compromiso vascular de la pared y sobrecrecimiento bacteriano.
3. CLÍNICA
Dolor abdominal: inicialmente en línea media (sordo y difuso), posteriormente se localiza a
nivel de la fosa ilíaca derecha (FID) (50-60%).
Náuseas o vómitos, anorexia (60-70%).
Febrícula (temperatura > 38 ºC sugiere apendicitis complicada u otra patología).
Puede asociar clínica miccional.
Presentación atípica (25-40%): edades extremas, localizaciones anómalas (retrocecal, pélvica),
mujeres embarazadas (desplazamiento del apéndice por el crecimiento uterino), comorbilidad.
4. DIAGNÓSTICO
El diagnóstico es fundamentalmente clínico (historia clínica y exploración física sugerentes con
hallazgos analíticos compatibles).
Tabla I. Diagnóstico de apendicitis aguda.
4.1. Exploración física
Dolor abdominal a nivel de la FID, defensa y rebote positivo. En casos de apendicitis avanzada puede existir
irritación peritoneal difusa. Los signos clásicos de apendicitis aguda son:
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [660]
[43] INFECCIONES INTRAABDOMINALES. DIARREA POR CLOSTRIDIUM DIFFICILE
Blumberg (dolor a la descompresión en la FID).
Rovsing (dolor en la FID desencadenado con la palpación profunda de la fosa ilíaca izquierda
[FII]).
Psoas (dolor en la FID provocado por la flexión activa o extensión pasiva de la cadera
ipsilateral–apéndice retrocecal).
Obturador (dolor con la rotación interna de la cadera con la rodilla flexionada–apéndice
pélvico).
4.2. Pruebas complementarias (Tabla I)
5. ABORDAJE TERAPÉUTICO
Diagnóstico precoz e intervención quirúrgica urgente.
5.1. Antibioterapia
Ver, al final del capítulo, Apartado VIII. “Tratamiento antibiótico empírico de las infecciones
intraabdominales”.
Apendicitis flemonosas: antibiótico perioperatorio (prevenir la infección de herida quirúrgica y
el absceso intraabdominal posquirúrgico).
Apendicitis perforada o líquido libre intraabdominal: debe mantenerse hasta cumplir un ciclo
terapéutico de 5-7 días.
5.2. Quirúrgico
La apendicectomía es el tratamiento de elección.
La elección de la técnica (laparoscopia frente a la cirugía convencional abierta) es individualizada,
basándose en las características del paciente (hábito constitucional y gravedad del cuadro), en la
experiencia del cirujano y en los medios disponibles. Destaca la utilidad de la laparoscopia en casos de duda
diagnóstica (permite la exploración de la cavidad abdominal), en pacientes obesos o ancianos y mujeres en
edad fértil.
El manejo no quirúrgico de la apendicitis aguda (antibioterapia y reposo digestivo con tratamiento
de soporte) debe limitarse a pacientes seleccionados de elevado riesgo quirúrgico o de largo tiempo de
evolución (> 5 días), con formación de plastrón confirmado por prueba de imagen.
Se debe plantear la apendicectomía diferida a las 6-8 semanas.
En caso de apéndice de aspecto normal, se completa la apendicectomía (permite descartar
apendicitis en la pieza y previene la aparición posterior del cuadro).
III. DIVERTICULITIS AGUDA
1. CONCEPTO
Generalmente, el concepto diverticulitis hace referencia a una inflamación macroscópica
clínicamente evidente de divertículos colónicos. No obstante, es importante saber que pueden aparecer
también divertículos a otros niveles del tubo digestivo y que pueden inflamarse igualmente.
2. ETIOLOGÍA Y FISIOPATOLOGÍA
La prevalencia de la diverticulosis aumenta con la edad (5% en < 40 años, 65% a los 85 años). Hasta
un 15-25% de los pacientes con diverticulosis van a tener algún episodio de diverticulitis aguda (DA) en su
vida.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [661]
[43] INFECCIONES INTRAABDOMINALES. DIARREA POR CLOSTRIDIUM DIFFICILE
Tradicionalmente se ha considerado que la inflamación del divertículo colónico se produce en el
contexto de una microperforación. Los últimos estudios sugieren una etiología inflamatoria similar a la EII o
síndrome de colon irritable, que desencadena isquemia de la pared diverticular y perforación macro o
microscópica.
3. CLÍNICA
Dolor abdominal: síntoma más frecuente, constante y habitualmente localizado en FII. Dolor
hipogástrico o en FID en casos de sigma móvil o diverticulitis derecha.
Náuseas o vómitos (20-62%).
Estreñimiento (50%).
Diarrea (25-35%).
Clínica miccional (10-15%).
Afectación sistémica: fiebre, taquicardia, malestar general.
Fecaluria, neumaturia, piuria (sugieren fístula colovesical).
4. DIAGNÓSTICO
4.1. Exploración física
Dolor abdominal a la palpación (fundamentalmente en FII), defensa a ese nivel y rebote.
Efecto masa palpable (20%).
Peritonismo difuso en casos de peritonitis fecaloidea o purulenta.
4.2. Pruebas complementarias
Laboratorio: Leucocitosis y neutrofilia, elevación de los reactantes de fase aguda (RFA).
Sedimento de orina/urocultivo: piuria estéril (inflamación) o contaminación bacteriana
Pruebas de imagen:
Tomografía computarizada (TC) abdominopélvica con contraste oral e intravenoso (S:
94% y E: 99%). Prueba gold standard que permite diagnosticar el cuadro clínico,
estadificarlo en función de la gravedad y descartar otra patología abdominal.
Ecografía abdominal. Útil en casos en los que la TC esté contraindicada (gestantes,
insuficiencia renal o alergia a contraste iodado). Precisión similar a la TC con
limitaciones (operador dependiente y no permite excluir otras etiologías).
Criterios de imagen: divertículos, engrosamiento de la pared colónica, estriación de la
grasa pericólica, presencia de flemón o absceso, aire extraluminal, estenosis o fístula.
Colonoscopia y enema opaco: contraindicados durante el episodio agudo. Es
obligatorio realizar una colonoscopia a las 6-8 semanas del cuadro para descartar
neoplasias subyacentes.
5. CLASIFICACIÓN
La clasificación de Hinchey se correlaciona con los hallazgos radiológicos y permite estadificar el
cuadro en DA complicada y no complicada para establecer el tratamiento (Tabla II).
DA no complicada: inflamación diverticular sin perforación o absceso.
DA complicada: presencia de perforación y peritonitis, fístula (a órganos adyacentes o piel),
absceso u obstrucción.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [662]
[43] INFECCIONES INTRAABDOMINALES. DIARREA POR CLOSTRIDIUM DIFFICILE
Tabla II. Clasificación de Hinchey y tratamiento.
6. PRONÓSTICO
El 70-100% de los casos de DA no complicada responden al tratamiento médico. El 25% presentan
complicaciones (agudas o crónicas). La peritonitis incrementa la mortalidad hasta un 6% en la peritonitis
purulenta y 35% en la peritonitis fecaloidea.
7. ABORDAJE TERAPÉUTICO
7.1. Diverticulitis aguda no complicada (Hinchey 0 y Ia)
Tratamiento médico (dieta líquida, antibioterapia oral y analgesia).
(Ver Apartado VIII. “Tratamiento antibiótico empírico de las infecciones intraabdominales” al final del
capítulo).
Manejo domiciliario: DA no complicada con estabilidad clínica en pacientes con buena
tolerancia oral y control analgésico, sin fiebre elevada o comorbilidades. Es necesario un
sistema de soporte adecuado para el seguimiento ambulatorio y una buena adherencia
terapéutica por parte del paciente.
Los últimos estudios sugieren la posibilidad de prescindir de los antibióticos (en el contexto de
una etiología exclusivamente inflamatoria).
7.2. DA complicada (Ib, II, III y IV)
Ingreso hospitalario (dieta absoluta y fluidoterapia, analgesia y antibioterapia intravenosa).
Absceso (IB y II): manejo conservador en pacientes clínicamente estables con abscesos < 4 cm.
Drenaje percutáneo en caso de evolución inadecuada o absceso > 4 cm.
Indicación de cirugía
Sepsis y peritonitis difusa (III y IV).
Respuesta inadecuada al tratamiento médico.
Fracaso del drenaje percutáneo de abscesos.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [663]
[43] INFECCIONES INTRAABDOMINALES. DIARREA POR CLOSTRIDIUM DIFFICILE
Fístulas (enterocutánea, colovesical, coloentérica, colovaginal).
Obstrucción intestinal.
Episodios recurrentes.
Opciones quirúrgicas: colostomía de descarga, intervención de Hartmann (sigmoidectomía con
colostomía) y sigmoidectomía con anastomosis primaria con o sin ileostomía de protección.
Se puede plantear la resección electiva del sigma afectado en pacientes seleccionados (por
ejemplo, jóvenes con episodios recidivantes o inmunodeprimidos) una vez superado el episodio
agudo.
IV. PERFORACIÓN DE VÍSCERA HUECA
1. CONCEPTO
Pérdida de la integridad de la pared del tubo digestivo con vertido de aire y/o contenido
intraluminal a la cavidad peritoneal, que desencadena una peritonitis.
2. FISIOPATOLOGÍA
En función de la localización de la perforación y la capacidad de respuesta del tejido circundante, se
producirá una peritonitis difusa con líquido libre intraperitoneal o un proceso localizado con formación de
absceso o fístula.
3. ETIOLOGÍA
Figura 1. Etiología y diagnóstico de la perforación de víscera hueca.
4. DIAGNÓSTICO
4.1. Historia clínica
Orientada a la presencia de factores de riesgo (EII, enfermedad péptica, hábitos tóxicos, AINE o corticoides,
cirugía o endoscopia reciente, traumatismo abdominal). Episodios previos de dolor abdominal.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [664]
[43] INFECCIONES INTRAABDOMINALES. DIARREA POR CLOSTRIDIUM DIFFICILE
4.2. Clínica
Dolor abdominal: síntoma principal. De inicio brusco, intenso y constante, empeora con
movimiento o respiración. Irradiado a espalda u hombros.
Localización en función de la víscera afectada (epigastrio en enfermedad péptica,
hemiabdomen inferior en los casos de apendicitis perforada o diverticulitis).
Náuseas y vómitos.
Progresión a síndrome de respuesta inflamatoria sistémica (SRIS)/sepsis: fiebre, palidez,
taquicardia, hipotensión.
Clínica menos evidente en casos de perforación a retroperitoneo o perforaciones contenidas
con formación de absceso.
4.3. Exploración física
Dolor a la palpación abdominal en la zona afectada, defensa y signos de irritación peritoneal
(localizada o difusa), incluso “vientre en tabla” (defensa involuntaria generalizada del
abdomen).
Tacto rectal doloroso puede indicar presencia de líquido libre en pelvis.
Signos de SRIS (fiebre, taquicardia, taquipnea, hipotensión, alteración del nivel de consciencia).
4.4. Laboratorio
Leucocitosis, neutrofilia y elevación de los RFA. Acidosis metabólica.
4.5. Pruebas de imagen
Radiografía simple
Radiografía simple de tórax centrada en cúpulas, abdomen en bipedestación o abdomen en
decúbito lateral con rayo horizontal. Sensibilidad de 50-70% para detectar neumoperitoneo.
Algunos signos radiológicos de neumoperitoneo son el aire libre subdiafragmático, el signo de
Rigler (visualización de la pared intestinal por presencia de aire en el exterior), el signo del
uraco, el signo de la V invertida (visualización de los ligamentos umbilicales laterales) o la
visualización del ligamento falciforme.
Ecografía abdominal
La ecografía abdominal tiene escaso uso. Permite detectar líquido libre, peristaltismo
disminuido o presencia de abscesos.
TC abdominopélvico
Es una prueba más sensible y específica, permite detectar pequeñas cantidades de aire libre y
localizar el compartimento abdominal en el que se ha producido la perforación. Habitualmente
no permite identificar el punto exacto, pero se observan signos indirectos (engrosamiento de la
pared visceral, fuga de contraste intraluminal, cambio de calibre por obstrucción distal a la
perforación).
5. PRONÓSTICO
En función de la etiología y la gravedad de la extensión peritoneal.
6. ABORDAJE TERAPÉUTICO
6.1. Medidas generales
Dieta absoluta, sueroterapia intravenosa, estabilización hemodinámica y antibioterapia empírica de amplio
espectro (ver Apartado VIII. “Tratamiento antibiótico empírico de las infecciones intraabdominales” al final
del capítulo).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [665]
[43] INFECCIONES INTRAABDOMINALES. DIARREA POR CLOSTRIDIUM DIFFICILE
6.2. Tratamiento específico
La situación clínica y el grado de afectación peritoneal dirigen la actitud a seguir.
Quirúrgico: el objetivo es localizar y reparar la zona de perforación, lavar la cavidad y colocar
drenajes para controlar la contaminación peritoneal.
Conservador: casos seleccionados de perforación localizada con buena tolerancia y sin signos
de gravedad (perforación contenida/absceso, escaso líquido libre, sin signos de peritonitis
difusa). En función de la evolución puede ser necesaria la intervención quirúrgica o drenaje
percutáneo de posibles colecciones.
Perforación yatrogénica secundaria a estudios endoscópicos bajos: habitualmente la
limpieza previa del intestino condiciona la escasa salida de material fecaloideo a la
cavidad peritoneal, por lo que son perforaciones bien toleradas, candidatas a manejo
conservador en función de la situación clínica y la evolución.
En ausencia de clínica, el neumoperitoneo puede estar justificado por cirugía reciente
(especialmente laparoscópica), endoscopia, diálisis peritoneal. En estos casos es
razonable mantener al paciente en observación para valorar el desarrollo de síntomas o
el aumento del volumen del neumoperitoneo.
V. COLECISTITIS AGUDA
1. CONCEPTO
Inflamación de la pared de la vesícula biliar generalmente como complicación de la colelitiasis.
2. FISIOPATOLOGÍA Y ETIOLOGÍA
Litiásica (90%): obstrucción del conducto cístico (litiasis) y éstasis biliar que desencadena la
inflamación de la pared vesicular. Isquemia de la pared secundaria al aumento de la presión
intraluminal, activación de la cascada inflamatoria y colonización bacteriana (hasta en el 80%
de los casos). En casos avanzados se produce gangrena de la pared, perforación de la misma y
peritonitis biliar.
Alitiásica (10%): la colecistitis alitiásica se da en pacientes graves (traumatismos, quemaduras
graves, periodo postoperatorio, enfermedades sistémicas como tuberculosis o sarcoidosis, etc.)
por lesión endotelial e isquémica de la vesícula.
3. CLÍNICA
Dolor abdominal intenso, constante, localizado en hipocondrio derecho y/o epigastrio irradiado
hacia la espalda, de > 6 horas de evolución.
Náuseas y vómitos: 60%.
Masa dolorosa palpable: 20-30%.
Fiebre: 50-60%.
Ictericia: 20% (compresión de la vía biliar/coledocolitiasis).
Episodios previos de cólico biliar.
4. DIAGNÓSTICO
4.1. Exploración física
Dolor y defensa a la palpación en el hipocondrio derecho (HCD). El signo de Murphy (cese brusco de la
inspiración profunda con la palpación subcostal) es relativamente específico. En casos avanzados puede
existir una masa palpable en el HCD o signos de irritación peritoneal.
4.2. Pruebas complementarias
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [666]
[43] INFECCIONES INTRAABDOMINALES. DIARREA POR CLOSTRIDIUM DIFFICILE
Laboratorio: leucocitosis, neutrofilia y elevación de los RFA.
Leve aumento de las enzimas hepáticas (generalmente con patrón de colestasis), bilirrubina (<
5 mg/dL) y amilasa. La alteración marcada del perfil hepático o la bilirrubina deben hacer
sospechar una posible complicación (colangitis/coledocolitiasis o síndrome de Mirizzi
[compresión de la vía biliar producida por la litiasis impactada en el conducto cístico]).
Pruebas de imagen: imprescindibles para confirmar el diagnóstico.
Ecografía abdominal (S: 90-95% y E: 78-80%): Prueba de elección. Las características
ecográficas de la colecistitis son el engrosamiento (> 4 mm), estratificación o edema de
la pared, la presencia de colelitiasis o incluso cálculo enclavado en infundíbulo, Murphy
ecográfico positivo y líquido perivesicular.
TC abdominopélvico: generalmente, no es necesario. Utilidad ante la sospecha de
complicaciones (colecistitis enfisematosa o perforada) o ante dudas diagnósticas.
5. PRONÓSTICO
Puede resolverse sin tratamiento quirúrgico en un plazo aproximado de 10 días. Sin embargo, dada
la elevada incidencia de complicaciones (20%) está indicado el tratamiento definitivo. Mortalidad del 1% en
personas jóvenes, hasta del 10% en pacientes de alto riesgo.
6. ABORDAJE TERAPÉUTICO
Ver la figura 2
Figura 2. Manejo terapéutico de la colecistitis aguda.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [667]
[43] INFECCIONES INTRAABDOMINALES. DIARREA POR CLOSTRIDIUM DIFFICILE
Médico: dieta absoluta, reposición hidroelectrolítica, tratamiento sintomático (analgesia y
antieméticos) y antibioterapia (ver Apartado VIII. “Tratamiento antibiótico empírico de las infecciones
intraabdominales” al final del capítulo).
Quirúrgico: la colecistectomía es el tratamiento definitivo, inmediato o diferido. El tratamiento
quirúrgico en los 7 primeros días del cuadro (preferiblemente en las primeras 72 horas) ha demostrado
mejores resultados. El abordaje laparoscópico es de elección en la mayoría de los casos, aunque dado el
riesgo de complicaciones graves de la cirugía, se debe mantener un umbral bajo para la conversión a cirugía
abierta.
En casos de colecistitis grave o complicada (ver Figura 3), está indicada la cirugía urgente si el
estado del paciente lo permite.
Figura 3. Criterios de colecistitis grave o complicada.
En pacientes de elevado riesgo quirúrgico (edad avanzada, comorbilidad, ASA III-IV) es preferible
mantener una actitud conservadora de forma inicial, valorando la respuesta al tratamiento médico. Si no
existe mejoría o aparecen signos de gravedad, se puede realizar descompresión de la vesícula mediante
colecistostomía percutánea, colangiopancreatografía retrógrada endoscópica (CPRE) o incluso
procedimiento quirúrgico. Resuelto el episodio agudo se valorará de nuevo el riesgo quirúrgico para
plantear el tratamiento definitivo.
Colecistitis enfisematosa: infección de la pared vesicular por gérmenes productores de gas
(Clostridium welchii, Escherichia coli, Clostridium perfringens). Se asocia en la mitad de las
ocasiones a colelitiasis. Aparece típicamente en hombres en la quinta década de la vida y en
pacientes diabéticos (35-50%).
El signo radiológico típico es la presencia de gas en la pared vesicular y puede ser necesaria la
TC abdominal para su diagnóstico. La incidencia de perforación es del 40-60% y la mortalidad es
alta. En el tratamiento es fundamental la colecistectomía precoz.
Colecistitis alitiásica: tiene elevada mortalidad, con alta incidencia de gangrena (50%) y
perforación (10-15%), por lo que es necesario realizar tratamiento urgente mediante
colecistostomía percutánea guiada por imagen. Si el paciente es buen candidato a cirugía o
existen hallazgos que sugieran colecistitis complicada, debe realizarse una colecistectomía
urgente.
VI. COLANGITIS AGUDA O COLANGITIS AGUDA ASCENDENTE
Se trata de la inflamación de la vía biliar secundaria a éstasis de bilis por obstrucción e infección
bacteriana. En ausencia de manipulación previa de la vía biliar o presencia de cuerpo extraño (prótesis
biliares), los principales factores de riesgo son cálculos en la vía biliar (28-70%), seguidos de estenosis
benignas y procesos malignos.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [668]
[43] INFECCIONES INTRAABDOMINALES. DIARREA POR CLOSTRIDIUM DIFFICILE
Estos factores favorecen el acantonamiento de bacterias que ascienden desde el duodeno
principalmente y que posteriormente migrarán al torrente circulatorio originando bacteriemias y formando
parte de una infección, habitualmente polimicrobiana, donde las principales bacterias aisladas son: E. coli
(25-50%), seguida de Klebsiella pneumoniae y otras enterobacterias, enterococos y anaerobios como
Bacteroides y Clostridium. Se puede encontrar colonización por P. aeruginosa en pacientes portadores de
prótesis biliar, aquellos a los que se les ha realizado una endoscopia reciente o han recibido antibioterapia
de amplio espectro, factor que habrá que tener en cuenta a la hora de elegir la terapia antimicrobiana.
Se trata de un proceso potencialmente grave cuya mortalidad varía desde el 11% en casos leves
hasta el 20-30% en casos de colangitis severa.
1. CLÍNICA
La tríada clásica de Charcot: fiebre, ictericia y dolor en hipocondrio derecho aparece solo en el 50-
75% de los casos, siendo más frecuente la aparición de dolor abdominal y fiebre (alta y generalmente
acompañada de escalofríos por episodios de bacteriemia), que ocurre hasta en el 80%. La asociación de
hipotensión y confusión (Pentada de Reynolds) aparece en pacientes con colangitis aguda supurada,
cuadro potencialmente más grave y asociado a una alta mortalidad que favorece el desarrollo de shock
séptico y coagulopatía de consumo. La presencia de hipotensión puede ser el único síntoma de
presentación inicial en pacientes ancianos o en tratamiento con corticoides.
2. DIAGNÓSTICO
El diagnóstico es eminentemente clínico, apoyado por estudios analíticos y pruebas de imagen que
ayudarán a confirmar o a descartar otros procesos con los que es necesario realizar el diagnóstico
diferencial (fugas biliares, diverticulitis aguda, colecistitis, apendicitis, pancreatitis, abscesos hepáticos…)
(Tabla III).
Tabla III. Diagnóstico de colecistitis aguda.
2.1. Pruebas de laboratorio
Analítica: elevación de reactantes de fase aguda (leucocitosis con neutrofilia, PCR) y alteración
de perfil hepático de predominio colestásico (GGT, FA) con elevación de bilirrubina (conjugada).
La aparición de enzimas de citolisis (GOT y GPT) por encima de 1.000 UI sugiere la presencia de
microabscesos hepáticos. La elevación de valores de amilasa 3-4 veces por encima del valor
considerado como normal sugiere pancreatitis asociada.
Cultivos: los hemocultivos son positivos en más del 50% de los casos y deben recogerse
siempre previamente a iniciar antibioterapia empírica de amplio espectro. Si pueden recogerse
cultivos de la vía biliar, estos serán positivos en más del 90%.
2.2. Pruebas de imagen
Ecografía abdominal: primera prueba de imagen a realizar en busca de dilatación de la vía biliar
o cálculos. Si bien su sensibilidad para detectar cálculos en la vesícula es alta, en el caso de
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [669]
[43] INFECCIONES INTRAABDOMINALES. DIARREA POR CLOSTRIDIUM DIFFICILE
coledocolitiasis es solo del 50% y puede no ser concluyente en el caso de cálculos muy
pequeños o de realización precoz, por lo que un resultado normal no descarta el diagnóstico.
Colangio-RM y TC abdominal: superiores a la ecografía para determinar el nivel de la
obstrucción.
Colangiopancreatografía retrógrada endoscópica (CPRE): presenta una sensibilidad mayor del
95% para detectar litiasis en el colédoco. Es por tanto, diagnóstica, terapéutica y reduce la
mortalidad y complicaciones sistémicas. Permite realizar una descompresión de la vía biliar
mediante esfinterotomía y extracción de las litiasis biliares, que resulta eficaz en más del 90%
de los casos, con una tasa de eventos adversos menor del 5% y de mortalidad inferior al 1% en
manos expertas. No obstante, dado que puede presentar algunas complicaciones como
pancreatitis o bacteriemias secundarias, es deseable confirmar la presencia de coledocolitiasis
antes de realizarla.
Ecografía endoscópica: su indicación no está todavía establecida firmemente ya que es una
técnica relativamente invasiva y no permite intervenciones terapéuticas. Su uso queda
reservado para aquellos casos en los que han fallado otras pruebas de imagen.
3. MANEJO Y TRATAMIENTO
Medidas generales: dieta absoluta, monitorización estrecha con reposición hidroelectrolítica y
tratamiento de sepsis.
Tratamiento antibiótico empírico seguido de antibioterapia dirigida en función de los
aislamientos microbiológicos.
De primera elección: piperacilina-tazobactam 4 g/6 h iv o cefalosporina de 3ª
generación (ceftriaxona 2 g/24 h iv o cefotaxima 30 mg/kg/8 h) + metronidazol 500 mg/
8 h iv o carbapenémico (ertapenem 1 g/24 h).
En alérgicos a betalactámicos: consultar precozmente con el servicio de alergia para
valorar uso de los mismos; mientras tanto es posible el uso de una fluorquinolona
(ciprofloxacino 400 mg/12 h iv o levofloxacino 500 mg/24 h iv) + metronidazol 500 mg/
8 h iv o fluorquinolona + tigeciclina (primera dosis 100 mg iv, posteriormente 50 mg/12
h iv).
En caso de sepsis o según comorbilidad (edad, ingreso en los 90 días previos, pacientes
institucionalizados, sospecha de enterobacterias productoras de betalactamasas de
espectro extendido, o pacientes con prótesis o manipulación previa de vía biliar donde
exista necesidad de cubrir empíricamente Pseudomonas): imipenem 1 g/6 h iv o
meropenem 1 g/8 h iv.
En función de la evolución o desarrollo de sepsis se puede valorar añadir un
aminoglucósido por su efecto rápidamente bactericida, como amikacina 1 g/24 h.
Drenaje de la vía biliar: debe ser realizado lo más pronto posible (no existiendo un consenso
claro en los tiempos específicos), siendo de elección la realización de CPRE. Entre el 70-80% de
los pacientes responden de manera adecuada al tratamiento conservador por lo que en estos
casos es razonable retrasar el drenaje de la vía biliar entre 24 y 48 horas. Si la CPRE se retrasa y
el paciente no mejora en las primeras 24 horas, es necesario realizar una descompresión
urgente de la vía biliar. También está indicada en el caso de aparecer síntomas de colangitis
aguda supurada como dolor abdominal persistente, hipotensión refractaria, fiebre mayor de 39
ºC o confusión mental.
La colangiografía transparietohepática (CPTH) queda reservada para aquellos casos en los que la
CPRE fracasa, no se puede realizar o está contraindicada. La cirugía de urgencia hoy día ha sido
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [670]
[43] INFECCIONES INTRAABDOMINALES. DIARREA POR CLOSTRIDIUM DIFFICILE
reemplazada por las anteriores técnicas, por lo que su uso ha quedado relegado a las situaciones en las que
no se pueden realizar o han fracasado.
4. CONSIDERACIONES ESPECIALES Y PREVENCIÓN DE RECURRENCIAS
En mujeres embarazadas el manejo no varía, aunque se tendrá en cuenta la potencial toxicidad
fetal a la hora de elegir tratamiento antibiótico.
En caso de que la colangitis haya sido de causa litiásica, existe riesgo de recurrencia, por lo que se
recomienda realizar colecistectomía; también es común en el caso de las estenosis malignas, siendo la
colocación de un stent lo más habitual, pero su manejo específico depende de las características de cada
paciente. En caso de que haya sido debida a estenosis benigna, será necesaria la reparación (por vía
endoscópica o quirúrgica).
VII. ABSCESOS INTRAABDOMINALES
Los abscesos abdominales pueden clasificarse en abscesos peritoneales y abscesos viscerales, con
etiologías diferentes. El 74% de los abscesos intraabdominales son intra o retroperitoneales (no viscerales)
y lo más frecuente es que se produzcan adyacentes a focos de infección (diverticulitis, apendicitis, etc.) o
como consecuencia de una peritonitis generalizada. Pueden presentarse en diferentes localizaciones, que
vendrán dadas por la configuración de la cavidad peritoneal: subfrénicos, paracólicos, pélvicos,
subhepático, en epiplón menor o entre asas. El absceso intraabdominal espontáneo es una complicación
potencialmente grave en un porcentaje significativo (5,3%) de pacientes con Enfermedad de Crohn.
Respecto a los viscerales, el más frecuente es el absceso hepático, que habitualmente afecta al
lóbulo hepático derecho. Dependiendo de su localización, el mecanismo de formación puede ser resultado
de una contaminación externa o interna (tras una cirugía o una CPRE), contigüidad (ascendente de vía biliar
o de drenaje portal) o diseminación hematógena (bacteriemia, endocarditis).
Generalmente son de origen polimicrobiano, predominando principalmente las enterobacterias,
sobre todo Escherichia coli y, en menor medida, los anaerobios. En los de origen hematógeno, el
microorganismo más frecuentemente aislado es el Staphylococcus aureus y suele ser monomicrobiano.
Klebsiella pneumoniae es la primera causa de absceso hepático piogénico en pacientes asiáticos, asociado
en un 2,3-3,2% a cáncer colorrectal. Esto se debe a un factor de patogenicidad de la cápsula que hace a
este subtipo de Klebsiella especialmente invasora y resistente a la acción del sistema inmune, por lo que en
pacientes de este origen hay que considerarlo.
1. CLÍNICA
El síntoma más frecuente es la presencia de fiebre (90%), generalmente en picos. En gran parte de
las ocasiones es la única clínica referida. Puede acompañarse de dolor abdominal (localizado en función de
la zona o el órgano afectado, incluso pudiéndose irradiar al tórax o los hombros), la presencia de una masa,
distensión y náuseas o vómitos secundarios a un íleo. A veces se presenta de forma más subaguda, como
un síndrome constitucional.
2. DIAGNÓSTICO
La presencia de fiebre sin foco claro en un paciente con factores de riesgo (infección intra-
abdominal o cirugía previas) debe hacernos sospechar este cuadro, que se confirmará con una prueba de
imagen.
2.1. Pruebas de laboratorio
Elevación de los reactantes de fase aguda (leucocitos, neutrófilos, PCR, fibrinógeno) y colestasis disociada
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [671]
[43] INFECCIONES INTRAABDOMINALES. DIARREA POR CLOSTRIDIUM DIFFICILE
en el caso de abscesos hepáticos. Se deberá extraer hemocultivos y cultivos del líquido de los abscesos
cuando sea posible tanto para aerobios como anaerobios (si el paciente está inmunodeprimido, se deben
mandar muestras para cultivo de hongos y micobacterias).
2.2. Pruebas de imagen
Radiología simple: puede sugerir el diagnóstico hasta en la mitad de los casos. Hallazgos
típicos: derrame pleural, atelectasias y elevación diafragmática en los abscesos subfrénicos; la
presencia de burbujas o un nivel hidroaéreo extraluminal; o menos específicos, un patrón de
íleo, un efecto masa con desplazamiento de vísceras o un borramiento de las líneas del psoas.
Ecografía de abdomen (S: 71-93% y E: 87-99%): su utilidad es limitada en algunas
localizaciones, pero resulta especialmente valiosa en el diagnóstico de abscesos hepáticos y
pélvicos.
TC abdominopélvico (S: 95-97% y E: 94-95%): es la mejor prueba de imagen para esta
patología. El aporte de contraste oral permite localizar abscesos entre asas y la presencia de
fístulas, mientras que el contraste intravascular se concentra en la pared de los abscesos y
delimita su localización, aunque existe un 10% de falsos positivos y negativos.
PET-TC y gammagrafía con leucocitos marcados: esta última ha quedado relegada. Puede ser
de utilidad ante un diagnóstico incierto o ante la sospecha de un absceso que no ha podido ser
localizado. Ocasionalmente también ha permitido localizar un foco séptico insospechado fuera
del abdomen.
RM abdominal: prueba menos usada, pero útil en pacientes con enfermedad inflamatoria
intestinal, pues permite evaluar complicaciones asociadas como estenosis, fístulas y abscesos.
3. TRATAMIENTO
El tratamiento de elección y prioritario si el paciente está séptico será el drenaje quirúrgico o
mediante técnicas de radiología intervencionista. Además, se administrará tratamiento antibiótico empírico
hasta que se realice el drenaje (Tabla IV). En abscesos < 3 cm, se podría considerar únicamente tratamiento
médico. Aun así, si técnicamente es posible y no hay diagnóstico etiológico es recomendable el drenaje.
El drenaje percutáneo guiado por ecografía o TC es de elección siempre que se pueda. Si no se
puede realizar o no es efectivo, el drenaje se realizará de forma quirúrgica, incluso practicando
esplenectomía en caso de absceso esplénico si fuera preciso. Una vez tengamos resultados de hemocultivos
o de los cultivos del líquido de los abscesos, deberemos ajustar el tratamiento antibiótico y mantenerlo en
función de la evolución radiológica y de si el drenaje ha sido o no completo, durante 1 a 4 meses.
4. FORMAS ESPECIALES
4.1. Absceso anorrectal
Es una colección de material purulento que surge de las criptas glandulares en el ano o el recto. Se
caracteriza por fiebre y dolor en región perianal con datos de inflamación local y masa fluctuante, y en
algunos casos, salida de material purulento por drenaje espontáneo. En algunos tipos de abscesos no se
ven manifestaciones clínicas y es necesario realizar tacto rectal. La recogida de cultivo solo estará indicada
para distinguir entre un absceso criptoglandular y de la piel perianal, en los pacientes que vayan a ser
tratados con antibioterapia o hayan recibido varios ciclos antibióticos, sospecha de gérmenes resistentes y
en pacientes con enfermedades hematológicas. El tratamiento se basa en el drenaje quirúrgico (la falta de
fluctuación no debe retrasar el drenaje quirúrgico), añadiendo antibiótico solo en pacientes con factores de
riesgo (intensa inflamación, ancianos, diabéticos, inmunocomprometidos, etc.). Está contraindicado la
manipulación del absceso en pacientes neutropénicos.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [672]
[43] INFECCIONES INTRAABDOMINALES. DIARREA POR CLOSTRIDIUM DIFFICILE
Tabla IV. Resumen de los abscesos viscerales abdominales piógenos.
4.2. Absceso hepático amebiano
Entidad causada por Entamoeba histolytica, da lugar generalmente a un absceso único y en el lóbulo
hepático derecho. Debe ser sospechada fundamentalmente en viajeros e inmigrantes de zonas endémicas,
8-20 semanas tras el viaje, aunque se han descrito incluso años después. Se puede manifestar de forma
aguda con fiebre y dolor en hipocondrio derecho, o de forma subaguda como un síndrome constitucional.
Para el diagnóstico es útil realizar serologías y cultivo del líquido drenado. Se trata con metronidazol 1 g
(primera dosis), seguido de 750 mg/8 h vía oral o intravenosa durante 7-10 días, asociado a paramomicina
500 mg/8 h vía oral.
Se debe valorar el drenaje si es de gran tamaño o si no responde al tratamiento.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [673]
[43] INFECCIONES INTRAABDOMINALES. DIARREA POR CLOSTRIDIUM DIFFICILE
4.3. Candidiasis hepatoesplénica
Se debe pensar en ella en pacientes neutropénicos que tras recuperarse del episodio de neutropenia,
continúan con fiebre a pesar de tratamiento antibiótico adecuado, presentan dolor en hemiabdomen
superior y alteración citolítica hepática. El diagnóstico lo ofrecerán las pruebas de imagen (TC, RM
abdominal y PET), aunque son poco útiles en los momentos iniciales, la biopsia hepática. Es preciso un
tratamiento prolongado con anfotericina B (3-5 mg/kg/d) o una equinocandina (micafungina 100 mg/d,
caspofungina 70 mg seguido 50 mg/d o anidulafungina 200 mg seguido de 100 mg/d) y posterior
continuación del tratamiento en forma oral con fluconazol (400 mg/d) hasta resolución radiológica (RM o
PET-TC). La quimioterapia o el trasplante de médula ósea no deben ser retrasados si hay estabilidad clínica,
pero debe mantenerse el tratamiento durante todo el periodo de inmunosupresión. En algunos casos
graves es preciso añadir al tratamiento corticoterapia sistémica, dado que el cuadro se podría considerar en
este caso como un síndrome de reconstitución inmune sistémica (SRIS).
4.4. Absceso hepático en trasplantado hepático
Lo más frecuente es que sean secundarios a problemas de la vía biliar (estenosis del colédoco o trombosis
de la arteria hepática con sobreinfección de infarto hepático). Está causado principalmente por bacilos
gramnegativos, enterococos y anaerobios. Las pruebas de imagen darán el diagnóstico.
El tratamiento se basará en su drenaje y antibiótico. El tratamiento de la causa principal puede
requerir la colocación de una prótesis biliar, su reconstrucción quirúrgica o incluso el retrasplante.
VIII. TRATAMIENTO ANTIBIÓTICO EMPÍRICO DE LAS INFECCIONES
INTRAABDOMINALES (IIA)
1. INDICACIONES Y DURACIÓN DEL TRATAMIENTO ANTIBIÓTICO
El tratamiento antibiótico debe iniciarse una vez que el paciente es diagnosticado de una infección
intraabdominal o una vez que una infección de este tipo se considera probable. El tratamiento antibiótico
es más efectivo cuando, además de la adecuación a la sensibilidad de los patógenos, se inicia de forma
precoz (en menos de 1 hora en casos de sepsis grave o shock séptico; ver Capítulo 36. “Bacteriemia y
sepsis”). Estudios de cohortes en pacientes con sepsis grave han demostrado que por cada hora que se
retrasa el inicio del tratamiento antibiótico adecuado, se incrementa la mortalidad en un 7,6%. Niveles de
fármacos antimicrobianos satisfactorios deben mantenerse durante una intervención para control del foco
infeccioso, por lo que precisa antibioterapia adicional justo antes de iniciar el procedimiento.
Tabla V. Recomendaciones sobre la duración del tratamiento antibiótico en la IIA.
Dado el progresivo aumento del desarrollo de resistencias a antimicrobianos, es importante
desescalar el tratamiento antibiótico según los resultados obtenidos de las muestras microbiológicas y no
debe prolongarse su duración más de 7 días en los pacientes con control de foco infeccioso y respuesta
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [674]
[43] INFECCIONES INTRAABDOMINALES. DIARREA POR CLOSTRIDIUM DIFFICILE
clínica adecuada a antibioterapia empírica (según el último estudio STOP-IT, la terapia antibiótica corta,
reducida a 3-5 días ha demostrado igual efectividad y menor desarrollo de resistencias) (Tabla V).
Tabla VI. Esquema del tratamiento antibiótico empírico de la IIA.
Infecciones derivadas de estómago, duodeno, vía biliar e intestino delgado proximal, contienen
predominantemente microorganismos grampositivos y negativos aerobios y facultativos. Las infecciones
derivadas de intestino delgado distal contienen microorganismos gramnegativos facultativos y aerobios, así
como anaerobios obligados como B. fragillis también frecuentes. La perforación colónica alberga
microorganismos anaerobios facultativos y obligados; estreptococos y enterococos son también frecuentes.
El microorganismo más frecuente es E. coli. Es importante para el tratamiento empírico el conocimiento de
la epidemiología, microbiológica local y resistencias. Además, la cobertura antibiótica empírica (Tabla VI) se
establecerá en función de la gravedad de la IIA (Tabla VII), los factores de riesgo de mala evolución (Tabla
VIII) y la posibilidad de infección por gérmenes poco frecuentes (Figura 4) o microorganismos
multirresistentes (Tabla IX), por lo que es importante determinarlos en nuestra primera valoración.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [675]
[43] INFECCIONES INTRAABDOMINALES. DIARREA POR CLOSTRIDIUM DIFFICILE
Tabla VII. Evaluación de la gravedad de la IIA.
Tabla VIII. Factores de riesgo de mala evolución en la IIA.
Figura 4. Árbol de decisión para el tratamiento antifúngico empírico en la IIA.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [676]
[43] INFECCIONES INTRAABDOMINALES. DIARREA POR CLOSTRIDIUM DIFFICILE
Tabla IX. Factores de riesgo de infección por enterobacterias productoras de ß-lactamasas de espectro extendido (BLEE).
IX. INFECCIÓN POR CLOSTRIDIUM DIFFICILE
Costridium difficile es una bacteria grampositiva anaeróbica productora de toxinas y formadora de
esporas que produce colitis asociada a antibioterapia. Coloniza el tracto intestinal humano después de que
su flora normal haya sido alterada por la toma de antibióticos y libera toxinas (A: enterotoxina y B:
citotoxina) que se unen a los receptores epiteliales de las células intestinales produciendo inflamación,
daño en la mucosa y diarrea.
Pese a ser una infección típicamente nosocomial, cada día se describen más casos de adquisición en
la comunidad. Tanto en presencia como en ausencia de clínica, los pacientes colonizados por C. difficile son
un importante reservorio, transmitiéndose el microorganismo fácilmente por vía fecal-oral mediante la
ingestión de esporas y por lo tanto, rápidamente a través de manos, ropa, utensilios y compañeros de
hospital, presentando los pacientes colonizados un mayor riesgo de desarrollar infección por Costridium
difficile (ICD) que los no colonizados.
Existen algunas cepas asociadas a mayor virulencia y que parecen ser responsables del incremento
dramático en la incidencia, severidad y resistencias al tratamiento de la infección por ICD tanto nosocomial
como asociada a la comunidad, especialmente en pacientes mayores de 65 años. Es el caso de la cepa
hipervirulenta NAP1/B1/027, responsable de grandes brotes en países como Estados Unidos o Canadá y
que, por el momento, no ha afectado de forma significativa a nuestro país.
Potencialmente cualquier antibiótico puede favorecer la ICD habiéndose descrito mayor riesgo con
el uso de algunas familias, que quedan recogidas en la tabla X.
Tabla X. Principales antibióticos asociados a la infección por Costridium difficile.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [677]
[43] INFECCIONES INTRAABDOMINALES. DIARREA POR CLOSTRIDIUM DIFFICILE
La infección por Costridium difficile (ICD) se define como clínica compatible con ICD (diarrea o íleo
paralítico) asociada a una prueba diagnóstica en heces con resultado positivo para la presencia de C.
difficile toxigénico o sus toxinas (sin evidencia de otra causa alternativa de diarrea), o hallazgos
colonoscópicos o histopatológicos sugerentes de colitis pseudomembranosa.
1. CLÍNICA
Puede causar un gran espectro de manifestaciones clínicas que abarcan desde diarrea leve
autolimitada hasta enfermedad fulminante con megacolon tóxico. Para establecer el diagnóstico se
requiere la presencia de manifestaciones clínicas, debido a que existe un porcentaje muy elevado (hasta el
20% de pacientes hospitalizados, pudiendo llegar hasta el 50% en el caso de pacientes procedentes de
residencias o centros de larga estancia) que pueden estar colonizados, siendo posible detectar C. difficile en
las heces sin que produzca ninguna sintomatología.
La sintomatología suele aparecer entre el quinto y décimo día de tratamiento antibiótico y más
raramente después (hasta 10 semanas), siendo la toma previa de antibiótico el principal factor de riesgo.
Otros son: edad mayor de 65, hospitalización reciente y uso de IBP. Es relativamente frecuente que la
leucocitosis pueda preceder hasta 48 horas el inicio de los síntomas, por lo que en pacientes con
leucocitosis inexplicada y especialmente si cumplen algún factor de riesgo, debemos valorar la ICD como
una posibilidad.
Cuadro clínico típico: diarrea acuosa con colitis
Habitualmente asociada a dolor abdominal bajo de tipo cólico, tenesmo, febrícula y náuseas.
Puede cursar con sangre oculta en heces o mucus, siendo la hematoquecia y las melenas raras.
Formas graves:
Íleo paralítico: signos de disfunción severa del tracto gastrointestinal como vómitos y
ausencia de deposiciones combinado con signos radiológicos de distensión intestinal.
Colitis fulminante: diarrea, dolor abdominal difuso, distensión abdominal, fiebre,
hipovolemia, acidosis láctica, hipoalbuminemia, elevación de creatinina y leucocitosis
marcada. Como complicaciones pueden aparecer sepsis, insuficiencia renal, megacolon
tóxico y perforación intestinal.
Se ha propuesto clasificar la gravedad del episodio en función de algunos parámetros clínicos y
analíticos (Tabla XI).
Tabla XI. Clasificación de la infección por Costridium difficile (ICD) en función de la gravedad.
Enfermedad recurrente
Hasta el 20-30% de los pacientes experimentarán una recidiva de la enfermedad. Este alto
índice de recidiva se debe a la persistencia de esporas en el colon que resisten la acción de los
antibióticos activos frente a C. difficile.
El periodo de mayor riesgo es en las 8-10 semanas siguientes a la finalización del tratamiento,
especialmente en aquellos pacientes que no recuperan la microbiota intestinal normal como consecuencia
de la necesidad de continuar bajo tratamiento antibiótico. Las recidivas tempranas se deben a recurrencia
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [678]
[43] INFECCIONES INTRAABDOMINALES. DIARREA POR CLOSTRIDIUM DIFFICILE
de un mismo ribotipo mientras que en pacientes con recaídas tardías pueden sufrir una reinfección por un
ribotipo distinto.
Pacientes con una primera recidiva tienen hasta un 50% de probabilidad de padecer una segunda
recaída y en algunos casos la calidad de vida de los pacientes puede verse gravemente afectada por la
presencia de múltiples recidivas.
En la tabla XII se recogen los principales factores pronósticos que aumentan el riesgo de padecer
una ICD severa, así como de sufrir recurrencia de la enfermedad.
Tabla XII. Factores pronósticos que aumentan riesgo de padecer la infección por Costridium difficile (ICD) severa y/o aumentan
riesgo de recurrencia.
2. DIAGNÓSTICO
Basado en la combinación de clínica compatible y confirmado mediante la evidencia microbiológica
de presencia de C. difficile toxigénico.
2.1. Pruebas de laboratorio
Se debe solicitar una muestra de heces para detección de C. difficile, que en el supuesto de pacientes con
diarrea puede recogerse directamente y en el caso de pacientes con íleo debe ser obtenida mediante
torunda perirrectal. Las pruebas de laboratorio no distinguen entre la diarrea asociada a ICD y la forma
asintomática por lo que solo debe solicitarse en pacientes que tengan diarrea clínicamente significativa.
También debe solicitarse analítica que incluya hemograma y bioquímica.
Con las técnicas de biología molecular (PCR) ha aumentado drásticamente la rapidez y sensibilidad
del diagnóstico. Se suelen utilizar diferentes pruebas diagnósticas combinadas en algoritmos para lograr el
mejor equilibrio entre sensibilidad, especificidad y coste económico. El más usado es un algoritmo
combinado en dos pasos consistente en:
Primer screening mediante técnica de enzimoinmunoensayo o inmunocromatografía que
detecta simultáneamente GDH (glutamato deshidrogenasa, una enzima presente en todas las
especies de Clostridium) con una alta sensibilidad + toxinas A/B de C. difficile, con una
sensibilidad relativamente baja. Si las dos detecciones son negativas, se descarta ICD con alto
valor predictivo negativo, al ser la GDH una prueba muy sensible. Si las dos detecciones son
positivas (GDH y toxina) se obtiene el diagnóstico inmediato de ICD.
Si GDH es positiva y la detección de toxinas negativa, se realiza en segundo lugar PCR que
detecta genes de C. difficile toxigénico descartándose ICD si esta prueba es negativa y
confirmándose con su positividad.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [679]
[43] INFECCIONES INTRAABDOMINALES. DIARREA POR CLOSTRIDIUM DIFFICILE
2.2. Cultivo de heces para microorganismos anaerobios: es un método lento que no se usa de
manera rutinaria para diagnóstico de ICD, siendo útil para el estudio de otras causas de diarrea infecciosa y
para la obtención del antibiograma de C. difficile.
2.3. Pruebas de imagen: la radiografía de abdomen debe realizarse en pacientes con
manifestaciones clínicas de íleo o colitis fulminante para descartar la presencia de megacolon tóxico o
perforación intestinal. La TC de abdomen con contraste es la prueba preferida previa a la cirugía.
2.4. Endoscopia: solo se realiza si se sospecha un diagnóstico alternativo que requiera visualización
directa y/ o biopsia. Puede ser también útil en pacientes con íleo o colitis fulminante en ausencia de diarrea
ya que permite visualizar las pseudomembranas, aunque estas pueden estar ausentes. La biopsia no es
necesaria para el diagnóstico, ayudando en ocasiones a establecer un diagnóstico alternativo
especialmente en pacientes que no están respondiendo clínicamente a una terapia adecuada ante una
presumible infección por ICD.
El diagnóstico diferencial debe incluir causas infecciosas y no infecciosas causantes de diarrea; la
mayoría de las diarreas asociadas a antibioterapia no son atribuibles a ICD y responden a mecanismos
osmóticos mientras que si asocian colitis prácticamente siempre se relacionan con ICD. Algunas entidades
que debemos descartar son la diarrea de origen infeccioso (coprocultivo), diarrea no infecciosa (síndrome
de intestino irritable, enfermedad inflamatoria intestinal, celiaquía y colitis colágena entre otras), abdomen
agudo y shock. Diferenciarlas puede ser especialmente difícil en portadores asintomáticos; en estos casos el
cese de la diarrea en ayunas sugiere diarrea osmótica mientras que la presencia de fiebre y leucocitosis
orienta a ICD u otra causa infecciosa.
3. TRATAMIENTO
3.1. Indicaciones de tratamiento
Manifestaciones típicas y test diagnóstico positivo.
Con los métodos diagnósticos actuales, rápidos y sensibles, es apropiado esperar a la
confirmación diagnóstica para iniciar tratamiento en pacientes con síntomas leves. En caso de
síntomas graves, se debe iniciar tratamiento empírico.
No indicada en pacientes asintomáticos con toxina positiva.
3.2. Medidas generales
Si se confirma el diagnóstico es necesario implementar medidas generales para prevenir la diseminación
intrahospitalaria. Estas incluyen el diagnóstico precoz, educación del personal sanitario, medidas de
aislamiento de contacto adecuadas, limpieza de las superficies en contacto con el paciente con agua y lejía
(una parte de lejía por cada 10 partes de agua), higiene de manos (con agua y jabón, ya que las esporas son
resistentes a la solución hidroalcohólica) y administración correcta de antibióticos.
En caso de brote es necesario implementar medidas específicas. Las medidas adicionales incluyen:
suspender antibioterapia innecesaria, reposición hídrica y electrolítica, evitar fármacos anticinéticos (tipo
loperamida) y revisar necesidad de uso de IBP.
3.3. Tratamiento médico
Existen otros tratamientos que han demostrado eficacia, pero sin la suficiente evidencia como para
recomendar su uso (resinas de unión a toxina, polímeros, nitazoxanida, rifaximina o anticuerpos
monoclonales).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [680]
[43] INFECCIONES INTRAABDOMINALES. DIARREA POR CLOSTRIDIUM DIFFICILE
Tabla XIII. Tratamiento de la infección por Costridium difficile (ICD).
3.4. Tratamiento quirúrgico
En pacientes con ICD fulminante que no responden al tratamiento y que progresan a toxicidad sistémica,
peritonitis, megacolon tóxico o perforación intestinal. Debe realizarse antes de que la colitis se vuelva muy
severa, pues niveles de lactato > 5 mmol/l, shock o fracaso multiorgánico se asocian con elevada
mortalidad quirúrgica.
Hasta ahora la realización de colectomía total o subtotal con ileostomía es la intervención de
elección. Una alternativa puede ser la creación de una ileostomía en asa de derivación combinada con
tratamiento antibiótico (vancomicina intracolónica + metronidazol intravenoso) que parece reducir la
morbimortalidad preservando el colon.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [681]
[43] INFECCIONES INTRAABDOMINALES. DIARREA POR CLOSTRIDIUM DIFFICILE
3.5. Respuesta a tratamiento
Disminución del número de deposiciones y/o mejora en su consistencia combinada con mejoría de
parámetros de severidad de enfermedad (clínicos, radiológicos y analíticos). Se debe evaluar diariamente.
La respuesta clínica puede producirse tan solo después de 3-5 días de tratamiento, sin embargo pueden
transcurrir semanas hasta que la frecuencia y consistencia de las heces se vuelva completamente normal.
No se debe repetir el análisis de heces durante el tratamiento, ni debe realizarse en pacientes
asintomáticos, ya que hasta en un 50% el resultado puede mantenerse positivo hasta 6 semanas después
de haber completado tratamiento.
BIBLIOGRAFÍA
Castón JJ, Porras L, Rivero A, Torres-Cisneros J. Protocolo terapéutico empírico del absceso visceral
abdominal. Medicine. 2010;10(52):3515-7.
Debast SB, Bauer MP, Kuijper EJ, on behalf of the Committee. European Society of Clinical Microbiology
and Infectious Diseases (ESCMID): update of the treatment guidance document for Clostridium difficile
infection. Clin Microbiol Infect. 2014;20(Suppl 2):1-26.
Eckmann C, Dryden M, Montravers P, Kozlov R, Sganga G. Antimicrobial treatment of “complicated”
intra-abdominal infections and the new IDSA Guidelines – A commentary and an alternative European
Approach According to clinical definitions. European Journal of Medical Research. 2011;16:115-26.
Feingold D, Steele SR, Lee S, Kaiser A, Boushey R, Buie WD, et al. Practice parameters for the
treatment of sigmoid diverticulitis. Dis Colon Rectum. 2014;57(3):284-94.
Guiraoa X, Ariasa J, Badía JM, García-Rodríguez JA, Mensa J, et al. Recomendaciones en el tratamiento
antibiótico empírico de la infección intraabdominal. Cirugía Española. 2010;87(2):63-81.
Lübbert C, Wiegand J, Karlas T. Therapy of liver abscesses. Viszeralmedizin. 2014;30:334-41.
Mensa J, Gatell J, García-Sánchez J, Letang E, López-Suñé E, Marco F. Guía de terapéutica
antimicrobiana 2015. 25 ed. Barcelona: Antares; 2015.
Rodríguez García JL. Green Book Diagnóstico y tratamiento médico. 2 ed. Madrid: Marbán libros, SL;
2015.
Sawyer RG, Claridge JA, Natheris AB, Rotstein OD, Duane TM. Trial of Short-Course Antimicrobial
Therapy for Intraabdominal Infection. The New England Journal of Medicine. 2015;372:1996-2005.
Simorov A, Ranade A, Parcells J, Shaligram A, Shostrom V, Boilesen E, et al. Emergent cholecystectomy
is superior to open cholecystectomy in extremely ill patients with acalculous cholecystitis: a large
multicenter outcome study. Am J Surg. 2013;206(6):935-40.
Wu XD, Tian X, Liu MM, Wu L, Zhao S, Zhao L. Meta-analysis comparing early versus delayed
laparoscopic cholecystectomy for acute cholecystitis. Br J Surg. 2015;102(11):1302-13.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [682]
[44] HEPATITIS VIRALES
44.Hepatitis virales
David Rafael de la Cruz Esteban.
Medicina del Aparato Digestivo
Daniel Suárez Pita.
Medicina Interna
Asesora: Raquel Muñoz Gómez. Médica Adjunta de Medicina del Aparato Digestivo. Unidad de Hepatología
I. INTRODUCCIÓN
La hepatitis viral es una infección causada por distintos virus con tropismo por el hepatocito,
caracterizada por la presencia de necrosis e inflamación hepatocelular. Se considera aguda o crónica en
función de si la duración de la misma es menor o mayor de seis meses, respectivamente.
El cuadro clínico y las lesiones histológicas originadas por los diferentes agentes etiológicos son
prácticamente idénticos, existiendo diferencias en el mecanismo de transmisión, el periodo de incubación,
la evolución de la enfermedad y, sobre todo, en los marcadores serológicos que permiten reconocer al
agente responsable.
II. ETIOLOGÍA
En la actualidad se conocen cinco tipos de virus hepatotropos: virus de la hepatitis A (VHA), virus de
la hepatitis B (VHB), virus de la hepatitis D o delta (VHD), virus de la hepatitis C (VHC) y virus de la hepatitis
E (VHE). Existen otros virus que, aunque afecten a otros órganos de forma primaria, también pueden causar
hepatitis aguda. Entre ellos se incluyen el virus de Epstein-Barr (VEB), el citomegalovirus (CMV), el virus
herpes simple (VHS), el virus varicela zóster (VVZ) y el parvovirus B19.
III. EPIDEMIOLOGÍA
Desde el punto de vista epidemiológico, los principales virus hepatotropos pueden agruparse en
función de su principal vía de transmisión. Así, el VHA y el VHE se transmiten fundamentalmente por vía
fecal-oral a través del consumo de agua y alimentos contaminados. Son frecuentes los brotes epidémicos
por estos virus en áreas subdesarrolladas. Se han descrito casos esporádicos de infección por VHE en países
industrializados, sobre todo en pacientes de edad avanzada y con datos de hepatopatía previa. La
transmisión se produce por la ingesta o la manipulación de carne de cerdo u otros animales como el jabalí,
comportándose como una verdadera zoonosis.
El mecanismo principal de transmisión en la infección por el VHB, VHC y VHD es la vía parenteral a
través del uso de jeringuillas contaminadas en usuarios de drogas por dicha vía (UDVP) y de la exposición
accidental en sanitarios. En la actualidad, las transfusiones sanguíneas y las situaciones que propenden a un
uso frecuente de hemoderivados (hemodiálisis, hemofilia, trasplante de órganos, insuficiencia renal
crónica, gammaglobulinas, quimioterapia) suponen un riesgo casi nulo de infección gracias a la inclusión de
pruebas serológicas en los bancos de sangre desde la década de los 90, así como a extremar las medidas
sanitarias para evitar el contagio.
Otras fuentes de transmisión son las vías sexual y vertical, siendo esta especialmente importante en
áreas de alta prevalencia (Asia, África). La infección neonatal por VHB implica riesgo de evolución hacia la
cronicidad hasta en el 90% de los casos.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [683]
[44] HEPATITIS VIRALES
El VHB y el VHC se caracterizan por su tendencia hacia la cronicidad con ulterior desarrollo de
enfermedad hepática, con posibilidad de evolución hacia la cirrosis y la aparición de carcinoma
hepatocelular. La infección por el VHE raramente se cronifica, aunque se han descrito casos en pacientes
inmunodeprimidos.
Tabla I. Características de los virus hepatotropos primarios.
IV. CLÍNICA
En la mayoría de los pacientes la infección aguda es asintomática o cursa con una clínica
inespecífica indistinguible de otras viriasis.
El cuadro clínico típico comienza con una fase prodrómica, caracterizada por síntomas inespecíficos
como deterioro del estado general, fiebre y astenia; síntomas gastrointestinales (anorexia, náuseas, dolor
abdominal, diarrea en la infección por el VHA); o síntomas respiratorios que simulan un cuadro
pseudogripal. Aunque son más frecuentes las formas anictéricas, en la infección por VHA es común la
hepatitis colestásica como forma de presentación. La ictericia aparecería tras el resto de síntomas.
Generalmente la infección aguda por VHC es asintomática. En el caso del VHB y del VHA, la
infección aguda suele pasar desapercibida en niños menores de 5 años, siendo sintomática en adolescentes
y adultos.
Pueden aparecer manifestaciones extrahepáticas derivadas de la formación de inmunocomplejos
tales como artritis, vasculitis, crioglobulinemia, lesiones cutáneas, afecciones renales (glomerulonefritis),
neurológicas (síndrome de Guillain-Barré) y hematológicas (anemia aplásica, trombopenia), entre otras.
Lo más destacable en la exploración física es la ictericia mucocutánea (hepatitis ictérica) y la
hepatomegalia.
En un porcentaje pequeño de casos cursan como formas graves (hepatitis fulminante) y desarrollan
una insuficiencia hepática aguda grave (IHAG), que se define por la presencia de datos clínicos de
encefalopatía hepática y coagulopatía asociada, requiriendo ingreso en la Unidad de Cuidados Intensivos
(UCI) y trasplante hepático en algunas situaciones (ver Capítulo 56. “Hepatitis aguda y fallo hepático
fulminante”). La IHAG es más frecuente en las infecciones por el VHB y el VHE, en el tercer trimestre de
embarazo y en pacientes inmunosuprimidos y con hepatopatía de base.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [684]
[44] HEPATITIS VIRALES
Las hepatitis virales crónicas son asintomáticas, aunque en algunos pacientes pueden manifestarse
clínicamente como astenia prolongada. En ocasiones, la aparición de complicaciones asociadas a la cirrosis
puede ser la forma de diagnóstico de la infección. En otros casos, la sospecha clínica reside en la alteración
de la bioquímica hepática en una analítica de rutina realizada por otros motivos.
V. DIAGNÓSTICO
El diagnóstico de las hepatitis virales se basa en tres puntos fundamentales:
Sospecha clínica y antecedente de exposición al virus.
Alteración de la bioquímica hepática.
La hepatitis aguda se caracteriza por la elevación de las transaminasas en 10-50 veces su valor
normal, con aumento variable de la bilirrubina y de las enzimas de colestasis. La presencia de
coagulopatía, definida por el alargamiento del tiempo de protrombina, es el marcador de
gravedad más fiable.
En la infección crónica se observa una elevación leve-moderada de las transaminasas. En los
casos con enfermedad hepática avanzada pueden apreciarse pancitopenia y coagulopatía en
relación con la cirrosis e hipertensión portal.
Determinación de los marcadores serológicos de infección: nos permiten establecer un
diagnóstico etiológico de la enfermedad.
Tabla II. Interpretación de los marcadores serológicos de la hepatitis.
Detallamos brevemente estos marcadores para cada uno de los agentes responsables.
1. INFECCIÓN POR EL VIRUS DE LA HEPATITIS A
Se basa en la determinación de anticuerpos anti-VHA. La infección aguda se caracteriza por la
presencia de anticuerpos anti-VHA tipo IgM. La detección de anticuerpos anti-VHA de tipo IgG indica
infección pasada o vacunación previa (confieren inmunidad).
2. INFECCIÓN POR EL VIRUS DE LA HEPATITIS B
La infección aguda por el VHB se caracteriza por la detección en suero de anticuerpos anti-HBc tipo
IgM y ADN de VHB. El AgHBs es positivo, aunque en algunos casos puede no detectarse por encontrarnos
durante el periodo de ventana de la infección o mantenerse positivo un corto periodo de tiempo hasta
detectarse ya anti-HBs.
La infección crónica por el VHB se define por la presencia de AgHBs positivo durante más de seis
meses. La historia natural de la infección crónica por VHB es un proceso dinámico en el que se diferencian
cinco fases (Tabla III):
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [685]
[44] HEPATITIS VIRALES
Tabla III. Fases de la infección crónica por el virus de la hepatitis B.
Fase de inmunotolerancia. Se caracteriza por la positividad del antígeno e (AgHBe), niveles
elevados de ADN-VHB en suero, cifras normales de transaminasas, lesión hepática leve o
inexistente y ausencia de progresión o progresión lenta de la fibrosis. Esta fase es más
frecuente en los sujetos con infección neonatal y puede durar entre 10 y 30 años.
Fase inmunorreactiva con AgHBe positivo. Se caracteriza por la positividad del AgHBe, con
niveles de ADN-VHB en suero inferiores a los de la fase inmunotolerante, elevación o
fluctuación de los niveles de transaminasas y necroinflamación hepática moderada-grave, con
progresión de la fibrosis.
Estado de portador inactivo. En esta fase los niveles de ADN-VHB en suero son muy bajos o
indetectables (< 2.000 UI/ml) y las transaminasas son normales. Para clasificar a un paciente
como portador inactivo es necesario un seguimiento mínimo de un año, con determinación
periódica de transaminasas y niveles séricos de ADN-VHB.
Hepatitis crónica con AgHBe negativo. Representa una fase tardía de la enfermedad y se asocia
con predominio de cepas de VHB con mutaciones en las regiones precore o promotor del core,
que reducen la expresión del AgHBe. Es la forma más frecuente en los países mediterráneos. Se
caracteriza por niveles de transaminasas fluctuantes, con periodos de elevación de las mismas
que se siguen de fases de remisión de duración variable y niveles de ADN-VHB también
fluctuantes. Estas fases de remisión se pueden confundir con un estado de portador inactivo.
Por lo tanto, es necesario hacer un seguimiento periódico cada 3-6 meses para realizar un
diagnóstico correcto.
Fase de resolución (remisión). Se produce la pérdida del AgHBs con aparición de anticuerpos
anti-HBc tipo IgG y/o anti-HBs, con ADN-VHB indetectable en suero. Puede persistir una baja
replicación viral con ADN-VHB detectable en los hepatocitos (infección oculta por VHB).
Basándonos en la historia natural de la infección crónica por VHB podemos distinguir dos formas de
hepatitis crónica: hepatitis B AgHBe positivo (cepa salvaje) y hepatitis B AgHBe negativo (cepa mutante
precore), esta última predominante en nuestro medio.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [686]
[44] HEPATITIS VIRALES
El diagnóstico y la clasificación de la fase de la infección crónica por VHB exigen valorar de forma
global varios parámetros:
Niveles de ALT (GPT).
Marcadores serológicos:
AgHBs. La cuantificación del AgHBs puede tener valor en el diagnóstico de portador
inactivo y como marcador pronóstico en la respuesta al tratamiento con interferón.
AgHBe y anti-HBe. Nos determina el tipo de hepatitis crónica (cepa mutante o salvaje)
y la identificación de portador inactivo.
ADN-VHB. Refleja la actividad replicativa del VHB y se monitoriza en la respuesta al
tratamiento.
Lesión histológica hepática. Para su evaluación disponemos de métodos directos, como la
biopsia hepática (BH), e indirectos, como la elastografía hepática (Fibroscan®). La BH sigue
siendo útil en los casos en los que los métodos no invasivos proporcionan información
contradictoria para adoptar decisiones clínicas. La elastografía hepática es una técnica cada vez
más utilizada para la valoración de la fibrosis, pero hay que tener en cuenta que la precisión
diagnóstica y los valores de corte no están claramente establecidos (como lo están en el VHC), y
que la elevación marcada de las transaminasas puede sobreestimar el grado de fibrosis
hepática.
3. INFECCIÓN POR EL VIRUS DE LA HEPATITIS D
El VHD es un virus defectivo. Precisa del VHB para su replicación. Por tanto, su infección siempre
ocurre en asociación con la del VHB. Su diagnóstico se basa en la detección de anticuerpos anti-VHD. En la
práctica clínica, se determinan los anticuerpos anti-VHD totales, y no se diferencia entre IgG e IgM. La
positividad de los mismos indica habitualmente infección por el VHD. En laboratorios especializados puede
determinarse ARN-VHD en caso de duda. Podemos diferenciar dos escenarios posibles:
La coinfección aguda VHB/VHD, que se define por la detección de anticuerpos anti-VHD tipo
IgM, AgHBs positivo y anticuerpos anti-HBc tipo IgM. Se ha demostrado que existe un
incremento del riesgo de desarrollo de hepatitis fulminante pero no de evolución hacia la
cronicidad.
La sobreinfección en portadores crónicos del VHB (AgHBs positivo y anticuerpos anti-HBc tipo
IgG) se caracteriza por la detección del anti-VHD tipo IgM. Puede presentarse como una
hepatitis aguda severa en pacientes portadores del VHB no previamente conocidos o como una
exacerbación de una hepatitis crónica B preexistente. La mayor parte de estos pacientes sufre
progresión hacia la cronicidad de la infección.
4. INFECCIÓN POR EL VIRUS DE LA HEPATITIS C
La infección aguda por el VHC se diagnostica en un paciente con clínica y analítica sugerente de
hepatitis aguda y detección de ARN-VHC en suero. Los anticuerpos anti-VHC pueden tardar en hacerse
positivos hasta seis semanas después de la detección del ARN.
La infección crónica por el VHC se define por la persistencia de ARN-VHC durante más de seis
meses. Esto ocurre en el 50-70% de los casos. No existen marcadores serológicos específicos que nos
permitan diferenciar entre hepatitis aguda y crónica, sino solo el tiempo de evolución. La elastrografía de
transición en la infección crónica por el VHC valora con precisión el estadio de la fibrosis hepática (de F1 a
F4), siendo infrecuente la necesidad de una biopsia hepática.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [687]
[44] HEPATITIS VIRALES
5. INFECCIÓN POR EL VIRUS DE LA HEPATITIS E
El diagnóstico se basa en la detección de anticuerpos tipo IgM anti-VHE o la demostración de ARN-
VHE en suero o heces (útil en pacientes inmunodeprimidos ante la ausencia o aparición tardía de
anticuerpos).
VI. EVOLUCIÓN Y TRATAMIENTO
1. VIRUS DE LA HEPATITIS A
En la mayor parte de los casos de infección por VHA, la enfermedad se resuelve de forma
espontánea. En algunas situaciones puede aparecer un pico de elevación de transaminasas algunas
semanas después del comienzo, cuando el proceso agudo parecía resuelto. No existe ningún tratamiento
específico sino solo medidas de soporte. El desarrollo de hepatitis fulminante es más frecuente en
pacientes de edad avanzada y sujetos con hepatopatía crónica. Ello requiere un diagnóstico precoz y la
derivación a un centro de referencia en trasplante hepático.
2. VIRUS DE LA HEPATITIS B
2.1. Hepatitis aguda
La mayoría (95%) de las hepatitis agudas en adultos inmunocompetentes se resuelven espontáneamente,
por lo que no existe indicación de tratamiento antiviral. Sin embargo, en los casos de hepatitis aguda de
curso grave debe indicarse tratamiento antiviral con entecavir o tenofovir. El tratamiento en estas formas
graves se basa en las medidas de soporte y en considerar si se cumplen los criterios de trasplante hepático
urgente.
2.2. Hepatitis crónica
La progresión a la cronicidad viene determinada fundamentalmente por la edad de adquisición de la
infección. Así, en la infección perinatal, la evolución a la cronicidad alcanza el 90% de los casos,
disminuyendo a un 20% en casos de infección entre 1 y 5 años de edad y siendo cercana al 5% en los casos
de adquisición en la edad adulta.
El 30% de los pacientes con infección crónica desarrollarán cirrosis hepática y el 4-6%, carcinoma
hepatocelular. Es por ello que el objetivo principal del tratamiento es la supresión persistente de la
replicación viral para evitar la progresión hacia la cirrosis, que condicionará el pronóstico. Se ha constatado
regresión de la fibrosis en sujetos bajo tratamiento antiviral, lo cual indica que el control de la infección no
solo frena la progresión de la enfermedad hepática, sino que también permite su retroceso.
El tratamiento de la hepatitis B persigue: a) la inhibición sostenida de la replicación viral,
determinada por el descenso de la carga viral hasta hacerse indetectable (respuesta virológica); la
seroconversión del AgHBe a anti-HBe en caso de cepa salvaje; la seroconversión del AgHBs a anti-HBs, lo
cual se consigue en un porcentaje pequeño de casos; b) respuesta bioquímica, determinada por la
normalización de las transaminasas y c) respuesta histológica.
Las indicaciones de tratamiento son las mismas para pacientes con hepatitis crónica AgHBe positivo
y AgHBe negativo y están basadas en la combinación de tres criterios: niveles de ALT, niveles de ADN-VHB
y lesión hepática valorada por Fibroscan® o BH.
Se debe considerar el tratamiento en aquellos pacientes que presenten un nivel de ADNVHB
superior a 2.000 UI/ml, elevación de los niveles séricos de ALT por encima del valor normal y la existencia
de actividad necroinflamatoria o fibrosis moderada (≥ F2).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [688]
[44] HEPATITIS VIRALES
En pacientes con valores normales de ALT y niveles de ADN-VHB superiores a 2.000 UI/ml, la
indicación de tratamiento lo determinará el grado de lesión hepática.
Los pacientes inmunotolerantes precisan seguimiento periódico y en ellos no está indicado el
tratamiento, aunque se ha de valorar, no obstante, en mayores de 30 años y/o ante historia familiar de
cirrosis o hepatocarcinoma.
Los pacientes con cirrosis compensada o descompensada con ADN-VHB detectable deben iniciar
tratamiento independientemente de los niveles de ALT.
Existen dos tipos de fármacos aprobados para el tratamiento de la hepatitis crónica B: los análogos
de nucleós(t)ido (AN: lamivudina, adefovir, entecavir, telbivudina y tenofovir) y el interferón pegilado
(interferón pegilado α-2a).
El interferón pegilado constituye una estrategia de tratamiento válida en pacientes con AgHBe
positivo con carga viral inferior a 2 x 108 UI/ml y niveles elevados de ALT en suero. La principal
ventaja es la duración finita del tratamiento (48 semanas) y la posibilidad de pérdida del AgHBs
y, por tanto, de curación de la infección. En la actualidad su empleo es escaso por su moderada
eficacia y múltiples efectos secundarios. Su uso está contraindicado en la cirrosis hepática
descompensada.
De los antivirales orales nos vamos a referir solo a entecavir y tenofovir, que constituyen el
tratamiento de elección por su alta potencia antiviral y bajo riesgo de desarrollo de resistencias.
Entecavir (Baraclude®) es un análogo de nucleósido que se administra por vía oral a dosis de 0,5
mg/día, con un buen perfil de seguridad. La probabilidad de resistencias en pacientes no
tratados previamente a largo plazo es del 1,2%, pero son frecuentes en pacientes tratados
previamente con lamivudina.
Tenofovir (Viread®) es un análogo de nucleótido que se administra por vía oral a dosis de 300
mg/día. Se han descrito casos de alteración de la función renal, por lo que debe monitorizarse
la dosis de forma periódica. No se han descrito resistencias con este fármaco. Su dosis debe
ajustarse ante un aclaramiento de creatinina inferior a 50 ml/min. Con una experiencia clínica
ya de 5-8 años, la respuesta virológica (ADN-VHB indetectable) se sitúa por encima del 90%. La
seroconversión del AgHBe a anti-HBe es del 40% y la pérdida del AgHBs se observa en el 10% de
los pacientes con AgHBe positivos.
El tratamiento con antivirales debe mantenerse de forma indefinida. En los pacientes con VHB
salvaje que seroconviertan a anti-HBe debe considerarse retirar el tratamiento un año después
de la misma, así como en aquellos casos en los que se consiga la pérdida del AgHBs.
2.3. Prevención de la reactivación del virus de la hepatitis B en pacientes inmunodeprimidos
Los portadores del VHB que vayan a recibir tratamientos quimioterápicos o inmunosupresores pueden
sufrir una reactivación de la infección por el VHB.
Se debe realizar cribado de la infección por el VHB (AgHBs y anti-HBc) a todo paciente que va a ser
sometido a quimioterapia y/o tratamiento inmunosupresor o biológico. En la tabla IV se muestran los
distintos tratamientos inmunosupresores con diferente potencial de riesgo para reactivación del VHB.
El riesgo de reactivación depende de varios factores: el estado de la infección por el VHB, el tipo de
tratamiento farmacológico utilizado y la enfermedad de base del paciente. El riesgo es más elevado en los
pacientes portadores del AgHBs, aunque también puede ocurrir con menor frecuencia en pacientes AgHBs
negativos con anti-HBc positivo con/sin anti-HBs.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [689]
[44] HEPATITIS VIRALES
Tabla IV. Fármacos inmunosupresores y riesgo estimado de reactivación del virus de la hepatitis B.
El riesgo es especialmente elevado en los sujetos sometidos a trasplante de médula ósea y a
tratamientos quimioterápicos por linfomas (rituximab). No debemos olvidar aquellas enfermedades que
precisan el uso de esteroides y/o anticuerpos antilinfocitarios o anti-TNF.
Se recomienda vacunación frente al VHB en los pacientes seronegativos, pudiendo requerir dosis
más altas de vacuna. La profilaxis está indicada en todos los pacientes portadores del AgHBs que vayan a
recibir terapia biológica, quimioterapia u otro tratamiento inmunosupresor. El tratamiento con AN
(entecavir, tenofovir) se debe iniciar una semana antes previamente al inicio del tratamiento
inmunosupresor y mantenerse al menos 12 meses tras la finalización del mismo o de forma indefinida
dependiendo de la situación basal de la infección por el VHB (hepatitis crónica).
En los pacientes con AgHBs negativo, con Anti-HBc positivo y/o anti-HBs positivo debe
determinarse el nivel de ADN-VHB. Si se detectase replicación, debería realizarse el mismo tratamiento que
en los portadores del VHB. Sin embargo, si la carga viral es indetectable (infección pasada por VHB), se
recomienda hacer un control de niveles de ALT y de carga viral cada 1-3 meses, dependiendo del tipo de
inmunosupresión y de la enfermedad del paciente con el fin de detectar precozmente la reactivación del
VHB, en cuyo caso se debe iniciar tratamiento.
Se recomienda iniciar tratamiento antiviral en pacientes oncohematológicos con AgHBs negativo y
anti-HBc positivo con anti-HBs negativo que van a recibir tratamiento con rituximab y/o tratamientos
antineoplásicos y en los que no se puede asegurar un control estrecho de la carga viral.
3. VIRUS DE LA HEPATITIS D
La erradicación del VHD se consigue con el aclaramiento del AgHB. Este objetivo es alcanzable en
un pequeño porcentaje de casos. El tratamiento con fármacos antivirales frente al VHB se ha demostrado
ineficaz. El único tratamiento aprobado es el interferón pegilado α-2a durante 12-18 semanas. Con ello se
consigue una respuesta viral sostenida (RVS) en solo el 20-30% de los casos.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [690]
[44] HEPATITIS VIRALES
4.1. Hepatitis aguda
La resolución espontánea del VHC se produce solo en el 20-50% de los casos. Es más frecuente en hepatitis
ictéricas, con elevación de transaminasas, en mujeres, en edad joven y en infecciones por genotipo 1. El
fallo hepático agudo se produce en menos del 1% de los casos.
Puede diferirse el tratamiento con antivirales orales de acción directa (AAD) hasta que se confirme
la evolución a la cronicidad o valorar iniciar el tratamiento durante el cuadro agudo. La guía de la
Asociación Europea para el Estudio del Hígado (EASL) recomienda iniciar tratamiento durante el periodo
agudo en pacientes con alto riesgo de transmisión (UDVP, trabajadores sanitarios), en pacientes en que se
prevean complicaciones graves o en aquellos sin factores favorables de curación espontánea.
Las pautas de tratamiento recomendado consisten en la asociación de sofosbuvir y ledipasvir,
sofosbuvir y velpatasvir, o sofosbuvir y daclatasvir durante 8 semanas.
Con el advenimiento de los antivirales orales de acción directa (AAD), la guía de la Asociación
Americana para el Estudio de las Enfermedades del Hígado (American Association for Study of Liver
Diseases, AASLD) recomienda monitorizar al paciente durante seis meses (periodo agudo de la infección). Si
evolucionara hacia la cronicidad, se realizará el mismo tratamiento con AAD que en una hepatitis crónica.
Asimismo, se valorará iniciar tratamiento durante el periodo agudo en los pacientes con alto riesgo de
transmisión (UDVP, trabajadores sanitarios) o en aquellos en que se prevean complicaciones graves.
4. VIRUS DE LA HEPATITIS C
Se recomienda iniciar tratamiento antiviral en pacientes oncohematológicos con AgHBs negativo y
anti-HBc positivo con anti-HBs negativo que van a recibir tratamiento con rituximab y/o tratamientos
antineoplásicos y en los que no se puede asegurar un control estrecho de la carga viral.
4.2. Hepatitis crónica
El VHC constituye la principal causa de hepatopatía crónica en nuestro medio. Tiene una alta tendencia
hacia la cronicidad (50-80%), lo que implica evolución a la cirrosis hepática en un 30% de los casos.
La aparición y desarrollo de los AAD ha supuesto una revolución en el tratamiento de la infección
crónica por VHC, permitiendo estrategias de tratamiento libres de interferón con una eficacia superior al
90% sin apenas efectos secundarios y una duración que varía entre 8, 12, 16 o 24 semanas según el
genotipo viral, las características del paciente y la combinación elegida. Todo paciente con infección crónica
por el VHC debe considerarse potencial candidato a tratamiento con AAD. En la tabla V se resumen las
indicaciones actuales de tratamiento en la hepatitis crónica por VHC.
Previamente al inicio del tratamiento antiviral se estudiarán el genotipo del VHC, la presencia o
ausencia de cirrosis hepática, tratamientos previos recibidos por el paciente y las comorbilidades que
padezca. Se debe prestar especial atención a las posibles interacciones farmacológicas con otros
medicamentos: inductores potentes de la glucoproteína P (fenitoína, carbamazepina, rifampicina),
inhibidores de la HMG-CoA reductasa (estatinas) o aquellos que se metabolicen por la vía del citocromo
CYP3A4/5 (amiodarona). En relación con los fármacos inhibidores de la bomba de protones hay que tener
en cuenta que deben administrarse simultáneamente con el tratamiento antiviral y a dosis que no excedan
los 20 mg de omeprazol, ya que el incremento del pH gástrico disminuye su biodisponibilidad. Hay que
monitorizar los niveles plasmáticos de inmunosupresores.
Las posibles interacciones con otros fármacos pueden consultarse en la ficha técnica del producto y
en el enlace de la Universidad de Liverpool (http://www.hep-druginteractions.org).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [691]
[44] HEPATITIS VIRALES
Existen fármacos cuyo uso conjunto con estos tratamientos queda contraindicado, así como otros
cuya dosis debe ser ajustada con el uso concomitante de los AAD (así, tacrolimus se ajusta con el régimen
3D, y ciclosporina está contraindicada con la combinación grazoprevir/ elbasvir).
Tabla V. Indicaciones de tratamiento en la hepatitis crónica por el virus de la hepatitis C.
Los AAD se pueden clasificar en tres grupos en función de la diana terapéutica sobre la que actúan.
Se describen a continuación de forma breve las características de cada grupo.
Inhibidores de la proteasa NS3/4. Son eficaces frente a los genotipos 1 y 4. Se combinan con
otros antivirales. No deben utilizarse en pacientes con cirrosis descompensada por posible
empeoramiento de la función hepática. Pueden producir fotosensibilidad y elevación de las
cifras de bilirrubina. A este grupo pertenecen simeprevir (SMV), paritaprevir (PTV) y
grazoprevir (GZR).
Inhibidores de la polimerasa NS5B. Son los que presentan mayor potencia antiviral, mayor
barrera genética y mayor espectro pangenotípico. A este grupo pertenece sofosbuvir (SOF,
nucleósido). Sus efectos adversos son escasos. Su eliminación es renal, por lo que no debe
utilizarse en pacientes con filtrado glomerular inferior a 30 ml/min/1,73 m2. Otro inhibidor de la
polimerasa NS5B es dasabuvir (DSV, no nucleósido).
Inhibidores de NS5A. Son fármacos con acción pangenotípica. Sin embargo, presentan una baja
barrera genética (con posibilidad de desarrollo de resistencias). Se administran siempre en
combinación con otros antivirales. A este grupo pertenecen daclatasvir (DCV), ledipasvir (LDV),
velpatasvir (VEL), ombitasvir potenciado con ritonavir (OBV/r) y elbasvir (EBR).
La ribavirina (a dosis de 1000 mg/día [en pacientes con < 75 kg de peso] y 1.200 mg/ día [ante > 75
Kg de peso]) se asocia a los AAD en algunos subgrupos de pacientes, ya que aumenta la eficacia en algunas
poblaciones difíciles de tratar. Su principal efecto adverso es la anemia, que obliga en ocasiones a disminuir
su dosis. Esta también se debe ajustar en función del filtrado glomerular renal.
Las combinaciones actualmente disponibles para el tratamiento de la infección crónica por VHC y
los genotipos para las que son eficaces se indican en la tabla VI.
A continuación se describen algunas consideraciones generales sobre el tratamiento con AAD, ya
que una visión más detallada excede a este capítulo.
Los pacientes naïve no cirróticos con genotipo 1 (GT1) con ARN-VHC < 6 millones UI/ml se
benefician de pautas cortas de 8 semanas de tratamiento con SOF+LDV.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [692]
[44] HEPATITIS VIRALES
En el GT1a, la combinación 3D (OBV/PTV/r+DSV) asocia RBV durante 12 semanas, y en
pacientes cirróticos este tratamiento se prolonga a 24 semanas. También en el GT1a, la
asociación GZR+EBR debe llevar RBV durante 16 semanas en pacientes con ARN-VHC basal >
800.000 UI/ml. La combinación SOF+VEL (pendiente de comercialización) es eficaz en todos los
genotipos y solo precisa asociar RBV en casos de cirrosis descompensada.
El uso de los AAD inhibidores de NS3/A (SMV, PTV, GZR) está contraindicado en pacientes con
cirrosis descompensada (se ha descrito empeoramiento de la función hepática). En estos casos
el tratamiento se realiza con SOF+LDV, SOF+VEL o SOF+DSV asociados a RBV durante 12
semanas (si existiera intolerancia a RBV se prolongaría el tratamiento de la combinación sin
RBV a 24 semanas).
Un 5-10% de los pacientes tratados con AAD presentan fallo al tratamiento, que puede ser
debido a resistencias a los inhibidores de NS5A. El retratamiento de estos pacientes implica no
incluir un fármaco de la familia NS5A. Si la fibrosis hepática fuera leve se recomendaría esperar
al desarrollo de nuevos tratamientos con mayor barrera genética. En pacientes que precisen
retratamiento urgente se aconseja prolongarlo a 24 semanas, asociar RBV y usar un régimen de
tratamiento que incluya SOF.
Se considera respuesta viral sostenida al resultado negativo en la determinación del RNA viral en la
12ª semana postratamiento. Implica la curación de la infección.
Tabla VI. Tratamientos actualmente disponibles en la infección por VHC.
5. VIRUS DE LA HEPATITIS E
No existe un tratamiento específico de la hepatitis aguda por el VHE. Se han descrito casos de
evolución a la cronicidad en pacientes inmunodeprimidos. Ribavirina parece mostrarse eficaz en la hepatitis
crónica por el VHE.
VII. PROFILAXIS
1. PROFILAXIS FRENTE AL VIRUS DE LA HEPATITIS A
La inmunización pasiva con anticuerpos (gammaglobulina) produce una rápida inmunidad de
duración transitoria (1-2 meses). Una dosis de 0,02 ml/kg de peso confiere protección durante
3 meses. Se administrará como profilaxis de preexposición en caso de que no haya sido posible
vacunarse de forma adecuada. Está indicada en niños menores de un año,
inmunocomprometidos o en aquellos que no respondieran a la vacuna o en los que estuviera
contraindicada. Deben extremarse las medidas higiénico-dietéticas (su principal vía de
transmisión es la fecal-oral), siendo esto especialmente importante en áreas endémicas.
La vacuna antihepatitis A (Havrix®, Vaqta®), compuesta por virus inactivados, estimula la
producción de anticuerpos y con ello aporta una protección más duradera. Se administran dos
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [693]
[44] HEPATITIS VIRALES
dosis separadas por un intervalo de 6 meses, alcanzándose una protección superior al 90% con
una duración mayor a 10 años. Si se precisara, se podrían hacer pautas más rápidas de
vacunación (0 y 15 días), recomendadas como profilaxis en caso de viajes a zonas endémicas. Es
útil como medida postexposición para prevenir la infección de los contactos si se aplica durante
la primera semana. En algunas Comunidades Autónomas, como Cataluña, Ceuta y Melilla, está
incluida dentro del calendario de vacunación infantil. Su administración estaría indicada dentro
de los grupos de riesgo para el VHA (Tabla VII).
Tabla VII. Grupos de riesgo que precisan vacunación profiláctica.
2. PROFILAXIS FRENTE AL VIRUS DE LA HEPATITIS B
La prevención pasiva se realiza con gammaglobulina específica hiperinmune que contiene
títulos elevados de anti-HBs. En la actualidad, al disponer de una vacuna frente a la hepatitis B,
la indicación de la gammaglobulina se limita a situaciones especiales: en combinación con la
vacuna en la inmunización de hijos de madres portadoras del VHB, de forma aislada en la
prevención de la recidiva de la infección por el VHB tras el trasplante hepático y, como
profilaxis postexposición, en sujetos no vacunados que han tenido contacto (pinchazo
accidental, contacto sexual…) con un individuo con hepatitis B. Es capaz de prevenirhasta un
75% de las infecciones postexposición, sobre todo si se administra dentro de las primeras 48h.
La profilaxis activa con vacunas recombinantes (Engerix®, HBVaxPro®) consigue una protección
superior al 90%. Valores de anti-HBs superiores a 10 UI/ml tras la vacunación garantizan una
protección prolongada, posiblemente de por vida, en los sujetos sanos vacunados antes de los
40 años. La pauta general de vacunación son tres dosis (0, 1 y 6 meses) por vía intramuscular.
Está incluida dentro del calendario de vacunación infantil. Se debe considerar su administración
en pacientes no vacunados en la infancia pertenecientes a los grupos de riesgo de adquisición
de la infección (Tabla VII). No existen contraindicaciones a la vacuna y puede administrarse en
mujeres gestantes. La tasa de respuesta es menor en inmunodeprimidos, hemodializados,
obesos, neumópatas, cardiópatas o hepatópatas crónicos, recomendándose en estos grupos la
administración de una dosis de recuerdo cuando los títulos de anticuerpos anti-HBs descienden
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [694]
[44] HEPATITIS VIRALES
por debajo de 10 UI/ml. La vacuna es útil tanto en la profilaxis preexposición como
postexposición. La protección existe tras la profilaxis preexposición, a pesar de que los
anticuerpos sean indetectables (se ha comprobado la reaparición o el incremento de los títulos
de anti-HBs después de una exposición al VHB). En general, no parece precisa una dosis de
recuerdo. Como profilaxis postexposición, se recomienda administrar la vacuna de forma
simultánea con la gammaglobulina hiperinmune para obtener de forma rápida títulos elevados
de anti-HBs y lograr una inmunidad persistente.
3. PROFILAXIS FRENTE AL VIRUS DE LA HEPATITIS D
Consiste en la profilaxis de la infección por el VHB.
4. PROFILAXIS FRENTE AL VIRUS DE LA HEPATITIS C
No se ha demostrado la eficacia de la inmunoglobulina en la prevención de la hepatitis C
postransfusional y no se dispone de una vacuna específica eficaz. El riesgo de transmisión sexual y perinatal
del VHC es muy bajo y en la actualidad no se recomienda adoptar medidas profilácticas especiales, a
excepción de los sujetos con anticuerpos frente al virus de la inmunodeficiencia humana (VIH).
5. PROFILAXIS FRENTE AL VIRUS DE LA HEPATITIS E
La prevención de la hepatitis E se basa en mejorar las condiciones generales de higiene y de
potabilización del agua. No hay datos sobre la utilización de la gammaglobulina para prevenir la
postexposición a la hepatitis E. Existe una vacuna eficaz para prevenir hepatitis E comercializada en China.
BIBLIOGRAFÍA
AASLD/IDSA. Hepatitis C guidance: AASLD-IDSA recommendations for testing, managing, and treating
adults infected with hepatitis C virus. Disponible en: http:// www.hcvguidelines.org.
Aggarwal R. Hepatitis E: Historical, contemporary and future perspectives. J Gastroenterol Hepatol.
2011;26:72-82.
Cunha C, Tavanez JP, Gudima S. Hepatitis delta virus: a fascinating and neglected pathogen. World J
Virol. 2015;4:313-22.
De Keukeleire S, Reynders M. Hepatitis E: An underdiagnosed, emerging infection in nonendemic
regions. J ClinTransl Hepatol. 2015;3:288-91.
European Association for the Study of the Liver (EASL). EASL clinical practice guidelines: Management
of chronic hepatitis B virus infection. J Hepatol. 2012;57:167-85.
European Association for the Study of the Liver (EASL). EASL recommendations on treatment of
hepatitis C 2016. J Hepatol. 2016.
Ferenci P, Kozbial K, Mandofer M and Hofer H. HVC targeting of patients with cirrhosis. J Hepatol.
2015;63;1015-22.
Guías AEEH/SEIMC de manejo de la hepatitis C. Disponible en http://www.aeeh.es.
Gutiérrez JA, Lawitz EJ, Poordad F. Interferon-free, direct acting antiviral therapy for chronic hepatitis C.
J Viral Hepat. 2015;22:861-70.
Jeong SH, Lee HS. Hepatitis A: clinical manifestations and management. Intervirology. 2010;53;15-9.
Lampertico P, Maini M, Papatheodoridis G. Optimal management of hepatitis B virus infection-EASL
Special Conference. J Hepatol. 2015;63:1238-53.
Martin P, Lau DT, Nguyen MH, Janssen HL, Dieterich DT, Peters MG, et al. A treatment algorithm for the
management of chronic hepatitis B virus infection in the United States: 2015 update. Clin
Gastroenterol Hepatol. 2015;13:2071-87.
Murali AR, Kotwal V, Chawla S. Chronic hepatitis E: a brief review. World J Hepatol. 2015;7:2194-201.
Noureddin M, Gish R. Hepatitis Delta: Epidemiology, diagnosis and management 36 years after
discovery. Curr Gastroenterol Rep. 2014; 16: 365-72.
Pattullo V. Hepatitis B reactivation in the setting of chemotherapy and immunosuppression- prevention
is better than cure. World J Hepatol. 2015; 7: 954-67.
Terrault NA, Bzowej NH, Chang KM, Hwang JP, Jonas MM, Murad MH. AASLD guidelines for treatment
of chronic hepatitis B. Hepatology. 2016;63:261-83.
World Health Organization. WHO position paper on hepatitis A vaccines. Wkly Epidemiol Rec. 2012;87:
261-76.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [695]
[45] TUBERCULOSIS
45.Tuberculosis
José María Martínez Ávila.
Medicina Interna
Jesús González Olmedo.
Medicina Interna
Asesora: Julia Origüen Sabater. Médica Adjunta de Medicina Interna. Unidad de Enfermedades Infecciosas
I. DEFINICIÓN
La tuberculosis (TB) es la segunda causa infecciosa de muerte en todo el mundo. Se produce por
micobacterias del complejo Mycobacterium tuberculosis (Mycobacterium tuberculosis complex) que incluye
cuatro especies: Mycobacterium tuberculosis, Mycobacterium africanum, Mycobacterium bovis y
Mycobacterium microti. Las cuatro provocan infección en humanos con una clínica similar. La más
frecuente es aquella por M. tuberculosis. La infección por M. africanum es frecuente en África occidental y
su transmisión y manifestaciones clínicas son parecidas. M. bovis causa la mayor parte de las infecciones en
ganado, aunque puede transmitirse a humanos.
Las mayores tasas de incidencia (100/100.000 o mayores) se observan en África subsahariana,
Sudeste asiático y Micronesia. Tasas intermedias (26 a 100 casos/100.000) ocurren en China, América
Central y del Sur, Europa del este y norte de África. Tasas bajas (< 25 casos/100.000 habitantes), en Estados
Unidos, Europa Occidental, Canadá, Japón y Australia. Se notificaron 5.535 casos de TB en España en el año
2013, lo que corresponde a una tasa de incidencia de 11,88 casos por 100.000 habitantes.
II. FISIOPATOLOGÍA
La inhalación de aerosoles portadores de micobacterias puede provocar, a su llegada a los
pulmones, cuatro respuestas posibles según el estado inmunitario del paciente y otros factores como la
carga de bacilos inhalada:
Aclaramiento inmediato de la carga de bacilos inhalada.
Respuesta inmune celular suficiente con persistencia de infección latente.
Respuesta inmune celular insuficiente con establecimiento de tuberculosis activa (TB).
Enfermedad tuberculosa por reactivación tras un periodo de latencia de duración variable
(habitualmente, años).
1. ENFERMEDAD TUBERCULOSA PRIMARIA
Aunque en la mayor parte de los casos la respuesta inmune celular del paciente es capaz de
controlar la proliferación de los bacilos en el tejido pulmonar en 2-10 semanas, algunos factores pueden
provocar que esta respuesta sea insuficiente. En estos casos aparece infección pulmonar activa con focos
de necrosis caseosa y adenopatías regionales por migración de macrófagos activados, portadores de
micobacterias.
2. INFECCIÓN TUBERCULOSA LATENTE
La infección tuberculosa latente (ITBL) es un estado de respuesta inmunitaria persistente a M.
tuberculosis que no se acompaña de manifestaciones clínicas de TB activa. La mayor parte de las personas
son capaces de producir esta respuesta inmunitaria. Se calcula que un tercio de la población mundial
presenta ITBL. No suelen presentar síntomas, si bien tienen un mayor riesgo de presentar TB activa.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [696]
[45] TUBERCULOSIS
3. ENFERMEDAD TUBERCULOSA POR REACTIVACIÓN
La causa más frecuente de TB activa es la reactivación de la infección tuberculosa latente. El riesgo
de reactivación a lo largo de la vida es del 5-10%. Este riesgo es mayor durante los primeros 5 años tras la
infección y en aquellas situaciones en que el estado inmunitario del huésped se vea comprometido.
Tuberculosis en el paciente con infección por el VIH: la inmunodepresión celular que conlleva la
infección por el VIH hace que la TB sea una de las enfermedades diagnósticas de SIDA más frecuentes. La
mayor virulencia de M. tuberculosis respecto a otros patógenos oportunistas que aparecen en la infección
por el VIH determina que los pacientes que desarrollan TB no presenten recuentos de CD4 necesariamente
bajos y que la mayoría no haya padecido hasta el momento otras infecciones definitorias de SIDA.
III. PRESENTACIONES CLÍNICAS
1. SÍNTOMAS SISTÉMICOS DE TUBERCULOSIS
La tuberculosis se acompaña de una respuesta inflamatoria sistémica, por lo que se manifiesta
frecuentemente como fiebre, pérdida de apetito y peso, astenia, sudoración nocturna profusa y malestar
general. Habitualmente estos síntomas son de instauración progresiva a lo largo de varias semanas.
2. TUBERCULOSIS PULMONAR
La presentación clínica más frecuente es la tuberculosis pulmonar. En caso de primoinfección
tuberculosa con adecuada respuesta inmune, la mayor parte de los pacientes se encuentran asintomáticos
o con síntomas muy leves, quedando la enfermedad como ITBL. La magnitud de los síntomas no se
relaciona con la extensión de la enfermedad. Hasta un 5% de los pacientes pueden permanecer
asintomáticos. El síntoma más frecuente es la tos, de más de 2-3 semanas de duración, seca o productiva.
Se puede acompañar de hemoptisis en ocasiones, aunque no de forma constante, y también de disnea o
dolor torácico.
3. TUBERCULOSIS EXTRAPULMONAR
La reactivación tuberculosa extrapulmonar es de frecuencia variable según las poblaciones, aunque
globalmente se sitúa alrededor del 20% en los países desarrollados. Algunas particularidades clínicas y de
diagnóstico y tratamiento se asocian a localizaciones específicas y se discutirán en otros apartados del
capítulo.
3.1. TB ganglionar
Es la forma extrapulmonar más frecuente (30-40% de las formas extrapulmonares). La localización
preferente es en los ganglios linfáticos cervicales y de la región supraclavicular. Se manifiesta como
adenopatías indoloras y de consistencia rígida que crecen gradualmente. Con el tiempo, pueden sufrir
necrosis, fluctuar, fistulizarse y presentar drenaje de caseum al exterior (escrófula).
3.2. TB pleural
Segunda forma extrapulmonar en frecuencia (alrededor del 25% de las formas extrapulmonares; un 5% del
total de los casos de TB). Puede tratarse de derrame pleural aislado como reacción de hipersensibilidad a
antígenos bacterianos en el espacio pleural con escasos bacilos en su interior o, menos frecuentemente,
empiema tuberculoso crónico por ruptura de una caverna al espacio pleural. Suele presentarse como tos
no productiva, dolor torácico, sintomatología general y derrame pleural unilateral.
3.3. TB genitourinaria
Cursa con disuria, hematuria y alteraciones estructurales como uropatía obstructiva, retracciones vesicales,
calcificaciones prostáticas, de vesículas seminales y de conductos deferentes. En la mujer es causa de
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [697]
[45] TUBERCULOSIS
enfermedad pélvica inflamatoria y de esterilidad por estenosis tubáricas. Habrá que sospecharla en
pacientes con estos síntomas que no mejoran con antibioterapia.
3.4. TB del sistema nervioso central
Supone un 1% de todas las formas de TB y aproximadamente un 6% de las presentaciones extrapulmonares
en inmunocompetentes. Se produce por diseminación hematógena y se puede manifestar de varias formas.
La meningitis tuberculosa, la más frecuente, es típica en infección primaria en niños y adultos jóvenes y
como reactivación en inmunosuprimidos. Es de pronóstico fatal sin tratamiento. Se trata de una meningitis
de inicio habitualmente insidioso, con cefalea, disminución del nivel de consciencia y signos de focalidad
neurológica, pudiendo afectar a nervios craneales (óptico y oculomotores son los más frecuentes). Otras
formas de lesión del sistema nervioso central (SNC) son los tuberculomas o conglomerados caseosos, la
aracnoiditis tuberculosa espinal, la hidrocefalia con hipertensión intracraneal y la vasculitis con trombosis e
infartos isquémicos.
3.5. TB osteoarticular
Supone el 10-35% de los casos de TB extrapulmonar. La localización más frecuente es la columna vertebral
(mal de Pott) afectando a la región lumbar y, con menor frecuencia, a la dorsal. Provoca colapso vertebral,
herniación del disco, deformidades y cifosis. Cursa con dolor local y sintomatología general.
3.6. TB pericárdica
Se asocia con tuberculosis en otras localizaciones. Alrededor del 2% de los pacientes con TB pulmonar
presenta pericarditis. Se inicia con una primera fase de granulomas en pericardio seguidos de una reacción
de hipersensibilidad o fase exudativa. En ese momento, existe riesgo de pericarditis constrictiva con fibrosis
y calcificación. Si la instauración es rápida puede dar lugar a taponamiento cardiaco. Debe considerarse la
etiología tuberculosa ante todo derrame pericárdico de aparición insidiosa y de larga evolución que no se
modifica con la administración de AINE.
3.7. Otras formas
La TB laríngea se da en menos del 1% de pacientes con TB y se produce por extensión local procedente del
árbol bronquial. Cursa típicamente con disfonía. Es la forma más contagiosa de la enfermedad, por lo que
habrá que descartar que el paciente sea bacilífero mediante baciloscopias en esputo. La TB gastrointestinal
con localización en la región ileocecal como más frecuente, y la TB ocular con tubérculos coroideos también
pueden presentarse.
4. TUBERCULOSIS MILIAR
Se trata de una enfermedad tuberculosa por diseminación hematógena incontrolada de bacilos. Se
producen pequeños nódulos que se pueden ver en los órganos afectados. El cuadro clínico es variable,
desde una forma aguda con shock séptico y fracaso multiorgánico a una forma insidiosa/ subaguda de
fiebre de origen desconocido. Es característica de la primoinfección en niños y de reactivación en
inmunosuprimidos. Por este motivo, hasta un 50% de estos pacientes pueden tener la prueba cutánea de
tuberculina (PCT) negativa. En la radiografía de tórax es típico el patrón nodular fino o grano de mijo.
5. CONSIDERACIONES ESPECIALES SOBRE EL PACIENTE CON INFECCIÓN POR EL VIRUS DE LA INMUNODEFICIENCIA
HUMANA
La afectación pulmonar exclusiva se da en menos del 50% de los casos. El resto presenta
manifestaciones extrapulmonares o mixtas. El grado de inmunosupresión condiciona la presentación clínica
y radiológica. De esta forma, los pacientes con estado inmunitario conservado tienen una presentación
clínica clásica, con alteraciones variables en las pruebas de imagen, mientras que los pacientes con mayor
grado de inmunosupresión presentan formas diseminadas y extrapulmonares con prueba de tuberculina
negativa (alto grado de anergia cutánea) y pruebas de imagen en ocasiones poco expresivas.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [698]
[45] TUBERCULOSIS
Síndrome inflamatorio de reconstitución inmune asociado a tuberculosis: en los pacientes
infectados por el VIH se observa una reacción paradójica de empeoramiento clínico de algunas infecciones
tras el inicio del tratamiento antirretroviral (TAR) y la recuperación de la inmunidad celular. Es lo que se
conoce como Síndrome Inflamatorio de Reconstitución Inmune (SIRI). Aunque está asociado a muchos
procesos infecciosos, el SIRI asociado a tuberculosis (SIRI-TB) ha sido uno de los más ampliamente
descritos. Su incidencia se sitúa en torno al 15%, aunque es variable según las series. Se puede presentar
como la reaparición o empeoramiento de los signos inflamatorios y síntomas de tuberculosis tras el
comienzo del TAR (SIRI-TB “paradójico” o “reacción paradójica”). También puede presentarse como la
nueva aparición de tuberculosis activa “desenmascarada” por el inicio de tratamiento antirretroviral y la
reconstitución del sistema inmune (SIRI-TB “revelador”). Es más frecuente la primera forma de
presentación. Las manifestaciones clínicas son similares en ambas formas, aunque en el primer caso se
produce un empeoramiento de la clínica previa y, en el segundo, una aparición de síntomas nuevos. Su
presentación se produce antes de los 3 primeros meses de tratamiento (el criterio temporal se considera
necesario para el diagnóstico), con una mediana de aparición de 14 días tras el inicio del TAR. Se deben
excluir otras causas, como toxicidad farmacológica, TB resistente al tratamiento, la presencia de otras
infecciones oportunistas o la mala adherencia al tratamiento. El tratamiento del SIRI-TB se expone en el
Apartado V. “Tratamiento”.
IV. DIAGNÓSTICO
1. DIAGNÓSTICO DE LA INFECCIÓN TUBERCULOSA LATENTE
El objetivo fundamental del diagnóstico de la ITBL es prevenir la reactivación. El bajo riesgo de
reactivación en la población general y los posibles efectos adversos del tratamiento hacen que no sea
recomendable tratar a todas las personas con ITBL. Por ello el diagnóstico debe indicarse solo en aquellos
pacientes en los que el riesgo de reactivación sea elevado y se beneficien, por tanto, de tratamiento.
Diagnóstico y tratamiento en ITBL van ligados, pues solo se realizará detección en aquellos pacientes que se
beneficien de ser tratados.
Descartar tuberculosis activa: los métodos de detección de ITBL son útiles para prevenir el paso de
tuberculosis latente a tuberculosis activa. Por tanto, no tienen utilidad en los casos de enfermedad
tuberculosa activa. Por este motivo, debe descartarse ITBL antes de iniciar su tratamiento y no debe
iniciarse tratamiento de ITBL cuando existan signos o síntomas de tuberculosis activa. Se han propuesto
diversas estrategias para establecer o descartar la sospecha de TB en aquellos pacientes en que se plantea
detectar ITBL. Al tratarse de una estrategia de cribado se buscan una sensibilidad y un valor predictivo
negativo elevados. La combinación de una radiografía de tórax normal y la ausencia de todos los síntomas
de tuberculosis activa (tos, hemoptisis, fiebre, sudores nocturnos, pérdida de peso, dolor torácico, disnea y
fatiga) permiten descartar casi completamente enfermedad tuberculosa activa, por lo que se considera la
estrategia óptima antes de iniciar tratamiento frente a ITBL. La estrategia de detección e indicación de
tratamiento se resume en la figura 1.
Indicaciones de detección y tratamiento de ITBL: los datos disponibles han permitido al grupo de
expertos de la OMS elaborar unas recomendaciones para 15 grupos de personas que presentan riesgo
elevado de reactivación de TB.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [699]
[45] TUBERCULOSIS
Figura 1. Algoritmo de detección de infección tuberculosa latente.
Aunque hay datos que orientan a que existen más grupos en riesgo de reactivación, no hay
evidencia suficiente para realizar recomendaciones firmes. Los pacientes en tratamiento crónico con
terapias inmunosupresoras (glucocorticoides, metotrexato, leflunomida, ciclosporina…) tienen un riesgo de
reactivación del 2-11%, dependiendo del tipo de tratamiento (mayor con glucocorticoides a dosis altas y
leflunomida) y de la dosis administrada. Las guías de tratamiento inmunosupresor recomiendan la
detección en los pacientes que reciben estos tratamientos, especialmente si se prevé la asociación de los
llamados “agentes biológicos” a los inmunosupresores clásicos. Dada la importancia del TNFα (alpha tumor
necrosis factor) en la formación del granuloma, el riesgo de TB es mucho mayor en pacientes en
tratamiento con anti-TNFα. Según el registro BIOBADASER, de la Sociedad Española de Reumatología, la
incidencia de TB entre pacientes en tratamiento con infliximab fue de 1.100 casos por cada 100.000
pacientes en 2001, en comparación con 21 casos por cada 100.000 habitantes en la población general en
España en el año 2000. Por este motivo, a todos los pacientes que vayan a recibir anti-TNFα se les debe
realizar PCT e IGRA (Interferon Gamma Release Assay); y ambos si el primero fuera negativo. La evidencia
es más abundante en lo referente a los anti-TNFα de primera generación (infliximab, etanercept,
adalimumab), pero cada vez hay más datos acerca de que todos los tratamientos biológicos (anti-IL-1, anti-
CD20…) aumentan el riesgo de reactivación. Es importante tener en cuenta esta recomendación, pues cada
vez se extiende más el uso de agentes biológicos.
Aunque tampoco hay evidencia firme, cada vez hay más estudios que revelan que los pacientes
oncológicos presentan mayor riesgo de reactivación independientemente de que reciban quimioterapia o
no. En estos grupos de pacientes se debe individualizar la indicación de detección y tratamiento, teniendo
en cuenta el balance riesgo/beneficio (entre las bondades de la detección y los efectos adversos del
tratamiento) en función de la edad del paciente y de sus comorbilidades.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [700]
[45] TUBERCULOSIS
Tabla I. Grupos de riesgo para la reactivación de la tuberculosis.
Métodos diagnósticos de ITBL: clásicamente la detección de ITBL se ha realizado mediante la
inyección intradérmica de tuberculina (prueba cutánea de tuberculina o PCT) y su valoración tras 72 horas
de la intradermorreacción. La PCT se considera positiva cuando la induración cutánea está por encima de 5
mm. Existen falsos positivos en población vacunada y pacientes infectados por otras micobacterias. En
cualquier caso, la induración por encima de 15 mm se considera diagnóstica de ITBL y, a efectos prácticos,
la induración por encima de 5 mm se considerará diagnóstica en población de riesgo, independientemente
de su estado vacunal. Otra limitación importante de la PCT es que depende del sistema inmunitario del
huésped, por lo que pueden darse falsos negativos en pacientes con la inmunidad celular alterada, lo que
disminuye considerablemente su sensibilidad en un grupo de población con alto riesgo de reactivación. En
pacientes con ITBL de mucho tiempo de evolución pueden aparecer falsos negativos por disminución de la
reactividad (anergia), lo que obliga a la repetición de la PCT pasadas unas semanas para potenciar la
respuesta cutánea (efecto booster).
Existen técnicas que detectan in vitro la respuesta inmune celular, los llamados Interferon Gamma
Release Assays (IGRA). Detectan la liberación de interferón gamma en respuesta a antígenos tuberculosos
específicos. Existen dos técnicas comercializadas: el Quanti FERON-TB-Gold In Tube (Cellestis®) y el T-
SPOT.TB (Oxford Inmunotec®), que no utilizan el PPD como antígeno, sino péptidos sintéticos. Estos
péptidos están ausentes en M. bovis, en la vacuna con bacilos de Calmette-Guérin (BCG) y en la mayoría de
las micobacterias no tuberculosas, lo que aumenta considerablemente la especificidad de la detección,
pues la respuesta solo se produce frente a M. tuberculosis, kansasi, marinum y szulgai.
Los estudios que comparan la sensibilidad y la especificidad de los IGRA frente a PCT no dan
preferencia a ninguno de los dos métodos de detección, por lo que la elección debe ser individualizada. Los
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [701]
[45] TUBERCULOSIS
IGRA son métodos más caros y requieren más trabajo de laboratorio. Sin embargo, pueden ser preferibles a
la PCT en algunos pacientes. Además de los falsos positivos en pacientes vacunados, la PCT tiene un
elevado número de falsos negativos en los pacientes inmunodeprimidos y presenta la dificultad técnica de
requerir una segunda visita para lectura y, en ocasiones, de la necesidad de repetir la prueba para provocar
el efecto booster. Por este motivo, los IGRA podrían ser el método de elección (Tabla II) entre los pacientes
inmunodeprimidos (algunos estudios demuestran mayor sensibilidad entre los receptores de trasplante
hepático, infectados por VIH o portadores de neoplasias hematológicas), los que han recibido vacuna con
BCG y los que no puedan realizar visitas sucesivas para lectura o repetición de PCT.
Tabla II. Posibles candidatos a detección de infección tuberculosa latente mediante IGRA.
Cuando las técnicas IGRA están disponibles, se recomienda su realización sistemática en todos los
pacientes inmunodeprimidos con una prueba de tuberculina negativa. Es decir, se debe hacer una
detección bifásica (Figura 2). Primero la PCT, de menor coste y, en caso de ser negativa, dada la posibilidad
de falsos negativos, se recomienda usar IGRA. Se sugiere iniciar tratamiento incluso en pacientes con
lesiones radiológicas, muy sugestivas de TB antigua, con alto riesgo de reactivación, aunque ambas pruebas
sean negativas.
Figura 2. Estrategia de detección bifásica de infección tuberculosa latente en inmunodeprimidos.
2. DIAGNÓSTICO DE LA TUBERCULOSIS ACTIVA
Diagnóstico de tuberculosis pulmonar
El estudio microbiológico es necesario para el diagnóstico de certeza. Las pruebas
microbiológicas comprenden baciloscopias (tinción para visualización directa de los bacilos),
cultivo y métodos de biología molecular. Las baciloscopias en esputo se realizan mediante
tinción de Zielh-Nielsen y fluorescencia con auramina. Estas pruebas requieren entre 5.000 y
10.000 bacilos/ml en la muestra, por lo que un porcentaje variable de casos tendrán tinción
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [702]
[45] TUBERCULOSIS
negativa. Por tanto, una baciloscopia negativa nunca descarta enfermedad tuberculosa. El
cultivo de esputo para micobacterias es la prueba de referencia con mayor sensibilidad,
identifica el tipo de micobacteria y permite llevar a cabo antibiograma (al menos de fármacos
de primera línea) y descartar resistencias. Como inconveniente, tiene un crecimiento lento
(hasta seis semanas).
Los métodos moleculares o de amplificación de fragmentos genéticos con la reacción en cadena
de polimerasa (PCR) tienen una sensibilidad intermedia con elevada especificidad. Además,
permiten determinar secuencias genéticas que confieren resistencia a diversos fármacos.
Recientemente se ha desarrollado una técnica automatizada (Xpert MTB/RIF) basada en la
plataforma multienfermedad GeneXpert, que permite la realización de técnicas de PCR de
forma simplificada en tiempo real e identificar genes que confieren resistencia a rifampicina.
Puesto que la prevalencia de monorresistencia a rifampicina es baja (1,4%), se debe considerar
el resultado positivo como indicador de multirresistencia (hasta disponer de antibiograma
completo), ya que en la mayor parte de los casos la resistencia a rifampicina coexiste con la
resistencia a isoniazida. La OMS la recomienda como primera prueba en aquellos pacientes en
que se sospecha TB multirresistente y en los pacientes infectados por el VIH.
Pruebas de imagen: la radiografía de tórax sigue siendo la primera prueba que se debe realizar
ante la sospecha de TB pulmonar. Aun así, hay que tener en cuenta que no hay un patrón
patognomónico y que puede ser poco informativa en enfermos inmunodeprimidos. Existen
algunos datos radiológicos orientativos, como la localización más frecuente en lóbulos
superiores y segmentos posteriores, los infiltrados y opacidades parenquimatosas, cavitados o
no, la presencia de niveles hidroaéreos, las adenopatías paratraqueales e hiliares, las
atelectasias, el derrame pleural, la fibrosis o el engrosamiento apical. En ciertas ocasiones, la
tomografía computarizada (TC) torácica puede ser de ayuda.
Tuberculosis extrapulmonar
Estudio anatomopatológico: dada la escasa rentabilidad de los cultivos en la mayor parte de las
localizaciones extrapulmonares (TB pleural, pericárdica, ganglionar), puede precisarse la toma
de biopsia para el diagnóstico. La visualización de granulomas caseificantes (agrupación
organizada de macrófagos o histiocitos formando una estructura cerrada, esférica, con necrosis
caseificante en su interior) en las muestras de biopsia es prácticamente diagnóstica con un
cuadro clínico compatible. Siempre se deben enviar muestras para estudio microbiológico
(tinción, PCR y cultivo).
Estudios de líquidos biológicos: la determinación en líquidos biológicos de
adenosinadesaminasa (ADA, enzima producida por monocitos y macrófagos que se encuentra
elevada en la TB) y de interferón gamma (IFN-γ, citoquina liberada ante la estimulación de
células T sensibilizadas con antígenos de M. tuberculosis) pueden ser útiles para el diagnóstico.
En el caso de la tuberculosis pleural la toracocentesis mostrará un líquido con características de
exudado de predomino linfocitario, con elevación de proteínas, glucosa normal o baja y
elevación de LDH. La detección de niveles de ADA por encima de 45 U/l tiene una sensibilidad
del 92% y una especifidad del 73% para tuberculosis pleural diagnosticada o probable (valor
predictivo positivo [VPP] del 92%). La detección de IFN-γ es la prueba aisladamente más
sensible para el diagnóstico de TB pleural (sensibilidad del 98%), con una especificidad del 77%
y un VPP del 96%. Será necesario realizar cultivo de líquido pleural, aunque su sensibilidad es
baja. Las técnicas de PCR, aunque de sensibilidad relativamente baja (80%), combinadas con
mediciones de IFN-γ tienen un valor predictivo negativo (VPN) y una sensibilidad del 100%.
En la tuberculosis peritoneal, el líquido ascítico presentará elevación de proteínas (> 2,5 g/dL)
con gradiente albúmina sangre-ascitis (GASA) mayor de 1,1 y un recuento celular > 500
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [703]
[45] TUBERCULOSIS
cél/mm3 con predominio de mononucleares. El aumento de ADA (habitualmente > 30 U/l) tiene
elevadas sensibilidad y especificidad (93% y 96%, respectivamente). La detección de IFN-γ
también es útil para el diagnóstico (sensibilidad: 93%; especificidad: 99%). (Ver Capítulo 52.
“Ascitis”).
Aunque los datos son más escasos, en la pericarditis tuberculosa la elevación de IFN-γ es la
prueba más sensible y específica en los estudios publicados (92% y 100%, respectivamente).
También es útil la determinación de ADA (sensibilidad: 87%; especificidad: 89%).
En los casos de tuberculosis genitourinaria, el sedimento de orina muestra piuria estéril (sin
crecimiento de bacterias en urocultivo). Se pueden solicitar baciloscopias en orina, cultivo para
micobacterias y estudios de imagen como TC o urografía.
En la meningitis tuberculosa, el LCR obtenido por punción lumbar presentará pleiocitosis
linfocitaria con proteínas y glucosa disminuida. Los niveles de ADA se encontrarán elevados.
Conforme aumenta el nivel de corte que se utilice (1-4 U/l, 4-8 U/l o > 8 U/l), se incrementa la
especificidad. Sin embargo, también se observan elevaciones en los niveles de ADA en LCR en
otras meningitis bacterianas, por lo que no es de utilidad a la hora de establecer la etiología. El
cultivo en LCR tiene una sensibilidad del 70%. En las primeras fases puede haber predominio de
polimorfonucleares y pruebas de imagen normal. Es necesario hacer pruebas de imagen, siendo
de elección la resonancia magnética (RM) (muestra lesiones captantes de contraste, bien sean
únicas o múltiples). Puede ser oportuna la realización de un fondo de ojo para descartar la
presencia de tuberculomas.
V. TRATAMIENTO
1. PRINCIPIOS GENERALES DEL TRATAMIENTO
El tratamiento actual de la TB se basa en el conocimiento de la enfermedad y en los ensayos
terapéuticos realizados durante más de 30 años por sociedades científicas y organizaciones sanitarias
internacionales. Se considera que un régimen terapéutico reúne condiciones para ser utilizado cuando cura
a más del 95% de los pacientes y ocasiona menos del 5% de intolerancias graves que obliguen a su
modificación.
Debido a la fisiopatología de la enfermedad y la capacidad de las micobacterias para persistir en el
organismo, el tratamiento debe ser prolongado y con varios fármacos, por lo que se establecen dos fases
(inducción y consolidación) para reducir la toxicidad.
1. Medidas de aislamiento y preventivas
El lugar más adecuado para tratar a los pacientes y evitar la transmisión a nuevos contactos será su
domicilio (siempre que ello sea posible), donde deben permanecer hasta que cumplan 2-3 semanas de
tratamiento. Estarán en habitaciones individuales y con mascarilla (tanto en su domicilio como en el
hospital). Los pacientes que cumplan criterios de ingreso hospitalario estarán también en habitaciones
individuales y con la puerta cerrada, idealmente con presión negativa o, en su defecto, en habitaciones bien
ventiladas y que den a un área soleada. Se les restringirán las visitas. El paciente utilizará mascarilla
quirúrgica mientras esté fuera de la habitación. El personal sanitario y los familiares usarán mascarillas de
partículas o, en su ausencia, mascarillas quirúrgicas. Se recomienda mantener el aislamiento domiciliario
como mínimo tres semanas, ampliándose si fuera necesario hasta disponer de tres esputos con
baciloscopia negativa (recogidos en días distintos) junto con una respuesta clínica favorable.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [704]
[45] TUBERCULOSIS
El personal sanitario deberá someterse a la PCT anualmente (siempre y cuando su resultado sea
negativo), si bien la periodicidad debe ser menor en personal con mayor riesgo de exposición
(broncoscopistas, personal de Urgencias, de laboratorio…).
Cuando se diagnostique un caso debe hacerse un estudio de contactos mediante PCT y radiografía
de tórax a todos los contactos cercanos (aquellos con un tiempo de convivencia con el caso mayor a 6 horas
diarias).
La única vacuna disponible hoy en día frente a la TB es la vacuna con bacilos de Calmette- Guérin
(BCG). Esta vacuna es eficaz en la prevención de la tuberculosis meníngea y diseminada en la población
pediátrica pero su utilidad frente a la prevención de la TB pulmonar es discutible. Uno de sus
inconvenientes es la conversión de la prueba de tuberculina en un porcentaje variable de la población
vacunada. Debido a esto y a que en poblaciones con baja incidencia de TB la principal estrategia de
prevención se basa en la detección temprana de contagios a partir de pacientes con enfermedad, no se
recomienda la vacunación sistemática en el momento actual.
2. Criterios de ingreso
El diagnóstico de TB, de sospecha o confirmado, no implica por sí mismo la necesidad de ingreso
hospitalario. La Comunidad Autónoma de Madrid recomienda como criterios de ingreso:
Criterios clínicos:
Enfermedad grave (insuficiencia respiratoria, inestabilidad hemodinámica…).
Afectación del SNC.
Intolerancia digestiva (que impida la absorción del tratamiento).
Comorbilidad grave (cirrosis hepática, enfermedad renal o pulmonar crónica…).
Sospecha de enfermedad por formas resistentes.
Condiciones que comprometan:
Adherencia al tratamiento (patología psiquiátrica, consumo de drogas, ausencia del
cuidador…).
Instauración de medidas preventivas (condiciones de la vivienda, residencias…).
2. FÁRMACOS ANTITUBERCULOSOS
En la tabla III se incluyen los principales fármacos con actividad frente a Mycobacterium
tuberculosis y sus efectos adversos más frecuentes.
3. PAUTAS DE TRATAMIENTO
3.1. Pautas de tratamiento estándar
Todas las guías recomiendan el uso del mismo régimen para el tratamiento de las formas de TB no
resistente, aunque pueden variar en la duración. Por ejemplo, las guías americanas recomiendan prolongar
3 meses más el periodo de consolidación si existen imágenes radiológicas de cavitación o persistencia de
cultivos de esputo positivos.
Los esquemas de tratamiento recomendados generalmente en nuestro medio son los de 6 meses
de duración:
Fase de inducción: 2 meses con rifampicina (R), isoniazida (H), pirazinamida (Z) y etambutol (E).
Se retira etambutol cuando se identifica que el aislamiento microbiológico es sensible al resto
de los fármacos.
Fase de consolidación: 4 meses con R y H.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [705]
[45] TUBERCULOSIS
Tabla III. Fármacos en el tratamiento de la tuberculosis.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [706]
[45] TUBERCULOSIS
3. PAUTAS DE TRATAMIENTO
3.1. Pautas de tratamiento estándar
Todas las guías recomiendan el uso del mismo régimen para el tratamiento de las formas de TB no
resistente, aunque pueden variar en la duración. Por ejemplo, las guías americanas recomiendan prolongar
3 meses más el periodo de consolidación si existen imágenes radiológicas de cavitación o persistencia de
cultivos de esputo positivos.
Los esquemas de tratamiento recomendados generalmente en nuestro medio son los de 6 meses
de duración:
Fase de inducción: 2 meses con rifampicina (R), isoniazida (H), pirazinamida (Z) y etambutol (E).
Se retira etambutol cuando se identifica que el aislamiento microbiológico es sensible al resto
de los fármacos.
Fase de consolidación: 4 meses con R y H.
Las pautas de tratamiento no varían en la edad pediátrica, los lactantes ni las embarazadas (aunque
en estos grupos hay que evitar el uso de aminoglucósidos o protionamida en caso de necesitar del uso de
fármacos de segunda línea).
Tabla IV. Dosificación orientativa de fármacos de primera línea.
La prolongación de los tratamientos implica mayor toxicidad (hepática en el 3-13% de los pacientes
tratados) y falta de adherencia (16-49% de los pacientes no lo completan).
Se han intentado pautas de tratamiento de menor duración (4 meses con moxifloxacino), pero no
han demostrado no inferioridad en los ensayos clínicos realizados, ya que en ellos se objetivaba mayor tasa
de fracaso que con las pautas estándar.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [707]
[45] TUBERCULOSIS
Hay pautas de tratamiento para formas de TB no resistente en las que los fármacos en fase de
consolidación se administran 2-3 veces por semana, adaptando secuencialmente sus dosis. Han
demostrado ser igual de efectivas que las pautas estándar pero en España se utilizan con poca frecuencia.
Se recomienda usar siempre los preparados en combinación fija y tomar toda la medicación en una
sola dosis en ayunas media hora antes del desayuno. Las tablas IV y V muestran la dosificación orientativa
de los fármacos de primera línea y la posología de los preparados en combinación fija para el tratamiento
de la TB.
Tabla V. Posología de preparados en combinación fija para el tratamiento de la tuberculosis.
3.2. Pautas de tratamiento no estándar
En ocasiones están indicadas por varios motivos: intolerancia medicamentosa grave (si bien ante ella suele
ser posible volver a la pauta habitual tras varias semanas), toxicidad, interacciones y aparición de
resistencias.
Las resistencias pueden ser primarias (infección por microorganismos resistentes) o secundarias o
adquiridas (en pacientes que han realizado tratamiento previo de forma incompleta [en monoterapia o
biterapia]).
En cuanto al perfil de resistencias, existen cepas monorresistentes (generalmente resistentes a
isoniazida), multirresistentes (a isoniazida y rifampicina) y cepas extremadamente resistentes (a isoniazida,
rifampicina, quinolonas…).
Debemos sospechar resistencias en pacientes con lesiones extensas y densidad bacilar elevada y,
sobre todo, ante casos de:
Fracaso terapéutico: situación en la que el paciente no mejora clínica ni radiológicamente y
mantiene cultivos positivos con el mismo número de colonias tras 4 meses de tratamiento o en
la que los cultivos vuelven a hacerse positivos tras unos meses de presentar resultados
negativos. Deberá instaurarse retratamiento con 3-4 fármacos no utilizados previamente y a los
que el bacilo sea sensible.
Recaídas en pacientes tratados previamente por enfermedad o ITBL. Cuando el tratamiento
previo fue correcto no suele haber resistencias. Si fue irregular hay que retratar con fármacos
nuevos hasta obtener el perfil de resistencias.
Inmigrantes de países con alta tasa de resistencias.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [708]
[45] TUBERCULOSIS
Contactos de pacientes con formas de TB resistente.
Coinfectados por el VIH.
Las pautas de tratamiento propuestas generalmente se basan en las experiencias y en
recomendaciones de expertos, ya que no se dispone de suficientes estudios aleatorizados que establezcan
cuáles son las más adecuadas. Las más utilizadas se exponen a continuación:
Pacientes con resistencia o toxicidad por isoniazida: se recomienda sustituir este fármaco por E
y prolongar el tratamiento 12 meses (2 m RZE + 10 m RE). Recientemente se ha comprobado la
efectividad de regímenes de 6 meses de duración que sustituyan isoniazida por una
fluoroquinolona (moxifloxacino o levofloxacino).
Pacientes con resistencia o toxicidad por rifampicina: la resistencia aislada a rifampicina es
excepcional. Se recomienda sustituir R por E y mantener el tratamiento 18 meses (2 m HZE + 16
m HE).
Pacientes con resistencia o toxicidad por pirazinamida: se recomienda pauta de tratamiento de
9 meses (2 m HRE + 7 m HR), con eficacia similar a la estándar.
Pacientes con TB multirresistentes: existe menos evidencia en el tratamiento de las formas
multirresistentes. El tratamiento debería dirigirse en función del perfil individual de
resistencias. En ausencia de esta información se puede usar tratamiento empírico, pero ha de
ajustarse tan pronto como se disponga del antibiograma. En nuestro medio, se recomienda la
utilización de un agente inyectable (aminoglucósidos o capreomicina) durante los primeros 6
meses e incluir una fluoroquinolona durante todo el tiempo de tratamiento, así como E si la
cepa fuera sensible. El régimen debe constar al menos de 4 fármacos eficaces. El tratamiento
debe prolongarse hasta cumplir 18 meses de cultivos consecutivamente negativos.
Recientemente se han publicado los resultados de un estudio de cohortes de tratamiento
intensivo de TB multirresistente con siete fármacos durante nueve meses en Bangladesh
(“régimen Bangladesh”), con tasas de curación del 85-89%. Se requieren más estudios que
permitan generalizar los resultados.
3.3. Tratamiento en situaciones especiales
Paciente con infección por el VIH
Se recomienda realizar serología de VIH en todo paciente con diagnóstico de TB. En los
pacientes infectados por el VIH deben tenerse en cuenta tres aspectos esenciales en el
tratamiento de la TB.
Momento de inicio óptimo de tratamiento antirretroviral (TAR) en pacientes infectados
por VIH con TB. Se recomienda iniciar TAR siempre durante el tratamiento de TB
independientemente del recuento de TCD4+, ya que ello disminuye el riesgo de
muerte. El momento óptimo para empezar el TAR depende de dicho recuento. Si es
menor de 50 células/μl debe comenzarse lo antes posible, pudiendo retrasarse (no más
de dos semanas) para disminuir el riesgo de SIRI. Si es mayor de 50 células/μl, podría
demorarse hasta finalizar la fase de inducción (8 semanas). Con estas recomendaciones
se disminuye el riesgo de efectos adversos y el desarrollo de SIRI sin comprometer la
supervivencia.
Pautas de TAR. La principal dificultad en el tratamiento adecuado simultáneo de TB y la
infección por el VIH radica en las posibles interacciones medicamentosas. Estas son
especialmente relevantes en el caso de las rifamicinas por ser potentes inductores del
sistema enzimático CYP3A4. Para el paciente que inicia TAR, la elección del régimen
debe seguir las mismas normas que para la población sin TB y debe incluir, por tanto,
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [709]
[45] TUBERCULOSIS
dos análogos de nucleósidos y un tercer fármaco. El régimen debe construirse de
acuerdo a las siguientes recomendaciones para pacientes que han recibido
previamente TAR y han desarrollado resistencias o intolerancia:
Elección de los inhibidores de la transcriptasa inversa análogos de nucleósidos
(ITIAN). No existe interacción significativa entre los fármacos antituberculosos y
los ITIAN ni hay evidencia de la potenciación de la toxicidad entre ellos. Por
tanto, se puede usar abacavir, tenofovir, emtricitabima o lamivudina sin riesgos
añadidos.
Elección del tercer fármaco. La mayor experiencia y los mejores resultados se
han obtenido con el uso de efavirenz, por lo que es el fármaco de elección. La
dosis de efavirenz es la estándar de 600 mg/día independientemente del peso,
sin necesidad de aumentarla a 800 mg/día. Existe experiencia o evidencia
suficiente para recomendar como pautas alternativas las que incluyan
nevirapina a dosis habituales, raltegravir a dosis de 800 mg cada 12 horas y
maraviroc a dosis de 600 mg cada 12 horas.
Fármacos que no pueden utilizarse. No se pueden coadministrar con
rifampicina los otros no análogos (rilpivirina y etravirina), ningún inhibidor de la
proteasa (potenciado o no con ritonavir) ni elvitegravir. En el caso excepcional
de que un inhibidor de la proteasa fuese la única opción de tratamiento
antirretroviral debe sustituirse rifampicina por rifabutina y realizar el ajuste
correspondiente en las dosis a administrar.
Tratamiento del síndrome inflamatorio por reconstitución inmunológica (SIRI). Es una
complicación frecuente del TAR en pacientes con TB, especialmente en aquellos con
recuentos de TCD4+ muy bajos en los que el TAR se inicia muy precozmente en relación
al inicio del tratamiento antituberculoso. En caso de SIRI se recomienda no interrumpir
el tratamiento antituberculoso ni el TAR. Para el manejo de los síntomas de SIRI pueden
añadirse antiinflamatorios no esteroideos (AINE) en el caso de formas leves-moderadas
o corticoides en las formas moderadas-graves, a dosis de 1,5 mg/kg/día de prednisona
o equivalente durante 14 días, seguidos de 0,75 mg/kg/día durante otros 14 días, según
la respuesta.
Hepatopatía crónica
Se debe intentar el tratamiento estándar, estrechando la vigilancia clínica y analítica. Si existe
hepatopatía avanzada, se debe retirar Z y continuar dos meses con H, R y E y siete meses con H
y R. En casos de hepatitis aguda o hepatopatía crónica en fase terminal se optará por regímenes
en los que no se incluyan fármacos con potencial hepatotoxicidad (fluoroquinolonas,
aminoglucósidos o capreomicina y E o cicloserina).
Insuficiencia renal crónica
Hay que mantener la pauta estándar salvo en pacientes con aclaramiento de creatinina menor
de 30 ml/min o en hemodiálisis. En ellos se recomienda administrar el tratamiento a las mismas
dosis, pero tres veces por semana y después de las sesiones de diálisis.
Formas extrapulmonares
No existen recomendaciones unánimes sobre la duración del tratamiento de las formas
extrapulmonares. En general, se sugiere usar la misma pauta estándar, pero prolongando la
duración del tratamiento. Así, en la meningitis tuberculosa se hacen dos meses de tratamiento
con isoniazida, rifampicina, etambutol y pirazinamida y diez meses con rifampicina e isoniazida
(2 meses HRZE + 10 meses HR); y en la espondilitis tuberculosa con afectación neurológica se
llevan a cabo dos meses con rifampicina, isoniazida, pirazinamida y etambutol y siete meses
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [710]
[45] TUBERCULOSIS
con rifampicina e isoniazida (2 meses HRZE + 7 meses HR). También se recomienda prolongar el
tratamiento en la TB pulmonar de pacientes con silicosis.
Imposibilidad para la administración por vía oral
Hay formulaciones parenterales de H, R y E a dosis equivalentes a las presentaciones orales.
Otra opción es la administración de las formas orales a través de gastrostomía percutánea o
sonda nasogástrica.
Embarazo y lactancia
Debe iniciarse tratamiento siempre que la sospecha de TB sea moderada o alta; está indicado
tratar inicialmente con H, R y E durante 2 meses, manteniendo H y R hasta completar 9 meses.
No existen datos sobre seguridad de Z en el embarazo y, aunque la OMS admite su uso, debería
evitarse en la medida de lo posible. S puede producir sordera en el feto y no ha de utilizarse.
4. TRATAMIENTO ADYUVANTE
4.1. Uso de glucocorticoides
Está indicado el uso de glucocorticoides en las primeras semanas de tratamiento de las formas meníngeas y
en la pericarditis.
Meningitis: dexametasona a dosis de 12 mg/día o prednisona a dosis de 60 mg/día durante 3
semanas y disminuir gradualmente durante las siguientes 3 o 4 semanas.
Pericarditis: 60 mg/día de prednisona durante 4 semanas seguidas de 30 mg/día durante 4
semanas, 15 mg/día durante 2 semanas y 5 mg/día durante la última semana.
Puede considerarse su uso en otras localizaciones (pleural, ganglionar, urinaria, trompas de Falopio,
peritonitis, uveítis, formas miliares con mala evolución y formas muy extensas y diseminadas), aunque su
eficacia aún no está demostrada.
4.2. Uso de piridoxina
La H puede producir neuropatía periférica, por lo que es recomendable la administración profiláctica de
suplementos de piridoxina (10-15 mg/día) en pacientes alcohólicos, desnutridos, embarazadas, diabéticos,
con insuficiencia renal e infectados por el VIH.
4.3. Tratamiento quirúrgico
TB pulmonar: puede emplearse en alguna ocasión como tratamiento coadyuvante en formas de
TB multirresistente con la finalidad de reducir la zona afectada y, por tanto, la densidad bacilar,
lo que permitiría una mejor acción de los fármacos.
TB extrapulmonar: toma de muestras para el diagnóstico o tratamiento de secuelas y
complicaciones.
TB pleural: biopsia pleural o videotoracoscopia para el diagnóstico. Se valorarán toracotomía,
decorticación o toracoplastia si tras 6 meses de tratamiento existen secuelas como empiema o
fístula broncopleural.
TB abdominopélvica (peritoneal, linfática, genitourinaria…): puede estar indicada la cirugía para
la toma de muestras o en el tratamiento de complicaciones (obstrucción intestinal, hemorragia
gastrointestinal, fístulas, drenaje de abscesos, nefrectomía…).
TB meníngea: si existiera hidrocefalia estaría indicada la derivación ventrículo-peritoneal.
Otras: drenaje de abscesos vertebrales, pericarditis constrictiva…
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [711]
[45] TUBERCULOSIS
5. EFECTOS ADVERSOS DEL TRATAMIENTO
5.1. Intolerancia digestiva
Es el efecto adverso más frecuente. Generalmente es suficiente con repartir la medicación en varias tomas
durante unos días. A veces es necesario añadir metoclopramida u omeprazol alejados unas horas de los
antituberculosos para evitar interacciones y manteniéndolos durante poco tiempo. En los casos más graves
habrá que recurrir a la administración parenteral.
5.2. Hepatotoxicidad
En forma de citolisis o colestasis. Generalmente causada por H, R y Z. El fármaco responsable de la
colestasis suele ser la R y los de la citolisis, H y/o Z. La frecuencia y gravedad de la hepatotoxicidad aumenta
en presencia de otros factores como el abuso de alcohol, consumo de drogas, etc. La toxicidad leve se
presenta sin clínica y con un aumento de las transaminasas por debajo de 5 veces sobre su límite superior,
o con una elevación de la fosfatasa alcalina de 3 veces. Ante ella no está indicado suprimir la medicación,
pero hay que aumentar la frecuencia de los controles clínicos y analíticos (Figura 3). En la toxicidad grave,
que se acompaña de clínica de hepatitis y de alteración importante del perfil hepático, y tras descartar
otras causas de hepatitis, debe retirarse la medicación durante una semana o sustituirla por fármacos no
hepatotóxicos. Tras la mejoría clínica y analítica, se reintroduce progresivamente una pauta con fármacos
de primera línea, averiguando el fármaco causante y cambiándolo por otro no hepatotóxico.
Figura 3. Algoritmo de manejo de la hepatotoxicidad.
5.3. Reacciones cutáneas
Las reacciones cutáneas leves como acné, exantema o urticaria son frecuentes en el primer mes. Suelen
responder a tratamiento tópico o antihistamínico. Las graves suelen ser infrecuentes y requieren la retirada
del fármaco y administración de tratamiento corticoideo.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [712]
[45] TUBERCULOSIS
5.4. Fiebre persistente por los fármacos
Tras descartar otras causas de fiebre persistente, debe averiguarse el fármaco causante y sustituirlo por
otro. En ocasiones puede ser necesario asociar corticoides.
5.5. Otros efectos adversos menos frecuentes
Pueden aparecer trombopenia, hemólisis, fracaso renal agudo por R, artralgias o fotosensibilidad por Z,
neuritis óptica por E…
En todos los cambios sucesivos de medicación que se precisen para superar los efectos adversos
debe seguirse estrictamente la recomendación de mantener al menos tres fármacos en la fase de inducción
y dos fármacos en la de consolidación. Siempre es recomendable disponer de un antibiograma adecuado
que oriente los fármacos a elegir. Cuando se reintroduce la R debe hacerse progresivamente a lo largo de
cuatro días (150, 300, 450 y 600 mg, respectivamente) para evitar hemólisis e insuficiencia renal.
6. INTERACCIONES FARMACOLÓGICAS
R es un inductor de isoenzimas del citocromo P450, por lo que disminuye los niveles de los
fármacos que se metabolizan por esa vía. Su efectividad puede verse disminuida por algunos azoles. H
inhibe también algunas isoenzimas del citocromo P450. Es recomendable la monitorización de los niveles
de fenitoína y carbamazepina si se toman conjuntamente con H. En la tabla VI se muestran algunas de
estas interacciones.
Tabla VI. Interacciones más conocidas de rifampicina.
7. CONTROL DEL TRATAMIENTO
Los objetivos más importantes que se plantean una vez instaurado un tratamiento correcto son
asegurar el cumplimiento, evaluar la eficacia curativa, detectar y manejar correctamente la intolerancia, las
interacciones y los efectos secundarios de los fármacos.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [713]
[45] TUBERCULOSIS
Control clínico: debe realizarse a las 2-3 semanas para detectar errores y toxicidad precoz.
Después, cada mes hasta finalizar el tratamiento.
Control analítico: debe incluir hemograma, coagulación y bioquímica con perfil hepático, renal y
ácido úrico. Debe realizarse siempre durante el primer mes de tratamiento. Se repetirán
hemograma y perfil hepático en los meses segundo, cuarto y sexto.
Control microbiológico: baciloscopia y cultivo de esputo a los 2, 4 y 6 meses del inicio del
tratamiento siempre que sea posible la obtención de la muestra.
Control radiológico: se recomienda a los 2 meses y al finalizar el tratamiento de las formas
pulmonares, y siempre que se considere necesario.
En cada visita se debe incentivar el cumplimiento del tratamiento. En aquellos casos con especial
riesgo de abandono, se recomienda potenciar las pautas de tratamiento directamente observado por un
sanitario o parasanitario.
8. TRATAMIENTO DE LA INFECCIÓN TUBERCULOSA LATENTE
8.1. Indicaciones
Como ya se ha mencionado previamente, se ha de tratar a todos los pacientes en los que esté indicada la
detección de ITBL y en los que las pruebas de detección (IGRA o PCT) obtengan un resultado positivo.
El objetivo del tratamiento es evitar la progresión a TB activa. El pilar es el uso de isoniazida 6-12
meses. Los estudios realizados en 1950 han demostrado un beneficio progresivo cuando se administra
durante 9-10 meses, beneficio que se estabiliza si se prolonga la administración del fármaco. Un metanálisis
revela que el riesgo de reactivación de TB es similar en pautas de 6 y de 12 meses.
Algunos estudios muestran un posible beneficio (reducción del número de conversiones) al
administrar H a todos los pacientes VIH+ en países con ingresos bajos y alta prevalencia de VIH, ya que se
ha demostrado un aumento de las conversiones en los primeros meses tras el diagnóstico (aunque no hay
recomendaciones firmes sobre este caso particular).
8.2. Pautas de tratamiento
Las pautas de eficacia comprobada recomendadas por la OMS se resumen en la tabla VII.
Tabla VII. Pautas de tratamiento de la infección tuberculosa latente.
Los estudios que compararon una pauta con otra no demostraron que un tratamiento fuera
superior que otro. Sin embargo, desde el punto de vista de la seguridad, los tratamientos con R durante 3 o
4 meses o rifapentina más H semanales durante 3 meses produjeron menos casos de hepatotoxicidad en
comparación con los tratamientos con H durante 6 y 9 meses, respectivamente.
La principal pauta recomendada es la administración exclusiva de H durante 6-9 meses debido a
que posee la mayor experiencia hasta el momento. Pueden considerarse pautas alternativas basadas en R
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [714]
[45] TUBERCULOSIS
en pacientes que presentan toxicidad por H o en aquellos en los que se sospecha infección por cepas
resistentes a H. Otras pautas aportan facilidad en la administración (como la pauta de rifapentina-H
semanales).
El tratamiento de ITBL no está indicado en contactos de pacientes con TB multirresistente, sino solo
un seguimiento estrecho durante al menos 2 años.
8.3. Seguimiento
Se ha descrito previamente la toxicidad de los diferentes fármacos. Aunque se ha intentado observar la
respuesta al tratamiento mediante la determinación seriada de IGRA, no hay pruebas que confirmen su
eficacia.
Se recomienda el seguimiento periódico mensual de todas las personas que reciben tratamiento de
ITBL.
Al igual que en lo descrito en los pacientes tratados por TB activa, se sugiere la determinación de
transaminasas y bilirrubina al inicio del tratamiento en pacientes en especial riesgo de hepatotoxicidad,
VIH+, mayores de 35 años, mujeres embarazadas y en puérperas durante los primeros 2 meses.
BIBLIOGRAFÍA
Adetifa IM, Ota MO, Jeffries DJ, et al. Interferon-γ ELISPOT as a biomarker of treatment efficacy in latent
tuberculosis infection: a clinical trial. Am J Respir Crit Care Med. 2013;187:439.
Bell L, Breen R, Miller R, Noursadeghi M, Lipman M. Paradoxical reactions and immune reconstitution
inflammatory syndrome in tuberculosis. International Journal of Infectious Diseases. 2015;32:39-45.
Campion E, Getahun H, Matteelli A, Chaisson R, Raviglione M. Latent Mycobacterium tuberculosis
Infection. NEJM. 2015;372(22):2127-35.
Cantini F, Nannini C, Niccoli L, Iannone F, Delogu G, Garlaschi G, et al. Guidance for the management of
patients with latent tuberculosis infection requiring biologic therapy in rheumatology and dermatology
clinical practice. Autoimmunity Reviews. 2015;14:503-9.
Denkinger CM, Pai M, Patel M, Menzies D. Gamma interferon release assay for monitoring of treatment
response for active tuberculosis: an explosion in the spaghetti factory. J Clin Microbiol. 2013;51:607.
Documento de consenso de GeSIDA/Plan Nacional sobre el SIDA respecto al tratamiento antirretroviral
en adultos infectados por el virus de la inmunodeficiencia humana. Actualización de enero de 2016.
Fuentes ZM, Caminero JA. Controversias en el tratamiento de la tuberculosis extrapulmonar. Arch
Bronconeumol. 2006;42(4):194-201.
Getahun H, Matteelli A, Abubakar I, Abdel Aziz M, Baddeley A, Barreira D, Raviglione M. Management of
latent Mycobacterium tuberculosis infection: WHO guidelines for low tuberculosis burden countries.
European Respiratory Journal. 2015;46(6):1563-76.
Getahun H, Matteelli A, Chaisson RE, Raviglione M. Latent Mycobacterium tuberculosis Infection. N
Engl J Med. 2015;372:2127-35.
Gillespie SH, et al. Four-Month Moxifloxacin-Based Regimens for Drug-Sensitive Tuberculosis. N Engl J
Med. 2014;371:1577-87.
González-Martín J, García-García J, Anibarro L, Vidal R, Esteban J, Blanquer R, et al. Documento de
consenso sobre diagnóstico, tratamiento y prevención de la tuberculosis. Enfermedades Infecciosas y
Microbiología Clínica. 2015;28(5):255-74.
González-Martín J, García-García JM, Anibarro L, Vidal R, Esteban J, Blanquer R, et al. Documento de
consenso sobre diagnóstico, tratamiento y prevención de la tuberculosis. Archivos de
Bronconeumología. 2010;46(5):255-74.
Jiang J, Shi H, Liang Q, Qin S, & Qin X. Diagnostic value of interferon-gamma in tuberculous pleurisy: a
metaanalysis. Chest. 2007;131(4):1133-41.
Jick S, Lieberman E, Rahman M, Choi H. Glucocorticoid use, other associated factors, and the risk of
tuberculosis. Arthritis Rheum. 2015;55(1):19-26.
Jick SS, Lieberman ES, Rahman MU, Choi HK. Glucocorticoid use, other associated factors, and the risk
of tuberculosis. Arthritis Rheum. 2006;55:19.
Kalantri Y, Hemvani N, Chitnis D. Evaluation of real-time polymerase chain reaction, interferon-gamma,
adenosine deaminase, and immunoglobulin A for the efficient diagnosis of pleural tuberculosis.
International Journal of Infectious Diseases. 2011;15(4):e226-e231.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [715]
[45] TUBERCULOSIS
Kim H, Hwang S, Ro Y, Jeon C, Ha D, Park S, et al. Solid-organ malignancy as a risk factor for
tuberculosis. Respirology. 2008;13:413-9.
Lawn SD, Zumla AI. Tuberculosis. Lancet. 2011;378:57-72.
Liang Q, Shi H, Wang K, Qin S, Qin J. Diagnostic accuracy of adenosine deaminase in tuberculous
pleurisy: A meta-analysis. Respiratory Medicine. 2008;102(5):744-54.
Longo D, Horsburgh C, Barry C, y Lange C. Treatment of Tuberculosis. New England Journal of Medicine.
2015;373(22):2149-60.
Mir I, Daudén E, Solano-López G, López F, Taxonera C, Sánchez P, Martínez X, García M, et al.
Documento de consenso sobre la prevención y el tratamiento de la tuberculosis en pacientes
candidatos a tratamiento biológico. Arch Bronconeumol. 2016;52:36-45.
Organización Mundial de la Salud. Directrices para la atención de la infección tuberculosa latente.
OMS, Ginebra 2015. http://www.who.int/tb/publications/latent-tuberculosis-infection/en/
Reuter H, Burgess L, van Vuuren W, Doubell A. Diagnosing tuberculous pericarditis. Qjm.
2006;99(12):827-39.
Richeldi L, Losi M, D’Amico R, Luppi M, Ferrari A, Mussini C et al. Performance of Tests for Latent
Tuberculosis in Different Groups of Immunocompromised Patients. Chest. 2009;136:198-204.
Shen Y, Wang T, Chen L, Yang T, Wan C, Hu Q, Wen F. Diagnostic accuracy of adenosine deaminase for
tuberculous peritonitis: A meta-analysis. Archives of Medical Science. 2013;9(4):601-7.
Sociedad Española de Neumología y Cirugía Torácica, Normativa SEPAR: Diagnóstico y tratamiento de
la tuberculosis, 2008.
Su SB, Qin SY, Guo XY, Luo W, Jiang HX. Assessment by meta-analysis of interferon-gamma for the
diagnosis of tuberculous peritonitis. World J Gastroenterol. 2013;19(10):1645-51.
Tuon F, Higashino H, Lopes M, Litvoc M, Atomiya A, Antonangelo L, Leite O. Adenosine deaminase and
tuberculous meningitis-a systematic review with meta-analysis. Scand J Infect Dis. 2010;42(3):198-
207.
Uthman O, Okwundu C, Gbenga K, Volmink J, Dowdy D, Zumla A, Nachega J. Optimal timing of
antiretroviral therapy initiation for HIV-infected adults with newly diagnosed pulmonary tuberculosis: A
systematic review and meta-analysis. Annals of Internal Medicine. 2015;163(1):32-9.
Walker N, Scriven J, Meintjes G, Wilkinson R. Immune reconstitution inflammatory syndrome in HIV-
infected patients. HIV/AIDS (Auckland, N.Z.). 2015;7:49-64.
World Health Organization. Policy statement: automated real-time nucleic acid amplification technology
for rapid and simultaneous detection of tuberculosis and rifampicin resistance: Xpert MTB/RIF system,
2011.
World Health Organization. Systematic screening for active tuberculosis: Principles and
Recommendations. 2013. http://www.who.int/tb/tbscreening/en/
World Health Organization. The use of tuberculosis interferon-gamma release assays (IGRAs) in low-
and middleincome countries. Policy Statement. Geneva, WHO, 2011.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [716]
[46] INFECCIÓN POR VIH
46.Infección por VIH
Clara Cabañuz Rocatallada.
Medicina Interna
Elena de Sautu de Borbón.
Medicina Interna
Asesores: María de Lagarde Sebastián. Médica Adjunta de Medicina Interna. Unidad VIH. Rafael Rubio García. Jefe de Sección
de Medicina Interna. Unidad VIH
I. EPIDEMIOLOGÍA
El virus de la inmunodeficiencia humana (VIH) es un virus RNA perteneciente a la familia
Retroviridae. Existen dos tipos: el VIH-1 (más extendido) y el VIH-2 (cuya infección se sospecha en zonas
endémicas de África Occidental; carecemos de método de medida de su carga viral). El VIH tiene especial
tropismo por los linfocitos TCD4+, además de otras células. Ello origina un deterioro progresivo del sistema
inmunológico en el huésped y condiciona la aparición de infecciones y tumores oportunistas.
El modo de trasmisión más frecuente es la vía sexual y la práctica de mayor riesgo es el coito anal
receptivo. Otras vías de trasmisión son la sangre y sus derivados (transfusión, punción cutánea accidental,
compartir jeringuillas…) y la vertical de madre a hijo.
II. DIAGNÓSTICO Y VALORACIÓN INICIAL
1. DIAGNÓSTICO
Tabla I. Enfermedades indicadoras de infección por VIH asociadas a una prevalencia de VIH no diagnosticado mayor del 0,1%.
Es importante el diagnóstico precoz de la infección puesto que ha demostrado disminuir la
morbilidad, el desarrollo de SIDA, la mortalidad y también la tasa de transmisión y la aparición de nuevos
infectados (Guía de recomendaciones para el diagnóstico precoz de la infección por VIH,
http://www.msssi.gob.es) (Tabla I). Se trata de una prueba voluntaria y confidencial y para hacerla se debe
contar con el consentimiento verbal del paciente. En ella se detectan anticuerpos mediante un test ELISA
(sensibilidad del 99%). Si resultara positivo, posteriormente se haría una prueba de confirmación por
Western-Blot. Los anticuerpos son detectables a las 3-12 semanas de la exposición. Por ello, existe un
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [717]
[46] INFECCIÓN POR VIH
periodo ventana en el que el test ELISA puede resultar un falso negativo. En este caso, la prueba de
elección sería la carga viral (positiva con > 10.000 copias/ml). Los ELISA de tercera y cuarta generación
acortan el periodo ventana al incluir la detección de Ag p24. La técnica de elección para descartar la
infección perinatal es la PCR (reacción en cadena de polimerasa). También existen test rápidos que ofrecen
los resultados en 20 minutos y que también requieren confirmación mediante Western-Blot.
2. CLASIFICACIÓN
Los Centers for Disease Control and Prevention (CDC) clasifican la infección por VIH en base a la
situación inmunológica del paciente y unas categorías clínicas (Tablas II-IV).
Tabla II. Clasificación de los Centers for Disease Control and Prevention para la infección del VIH (CDC, 1993).
Tabla III. Vigilancia de la definición de casos de infección por VIH entre adultos y adolescentes ≥ 13 años (revisión de los CDC, 2008).
3. VALORACIÓN INICIAL
3.1. Anamnesis
Se evaluarán riesgo cardiovascular, comorbilidades, vacunaciones, tratamiento previo de infección
tuberculosa latente, país de origen, viajes, animales domésticos, hábitos sexuales, uso de drogas o tóxicos,
soporte sociofamiliar y medicación concomitante. Ante pacientes con infección por VIH ya conocida es
oportuno detallar los tratamientos previos, su cumplimiento y tolerancia. En mujeres se debe preguntar
sobre uso de anticonceptivos, controles ginecológicos previos y deseo reproductivo.
3.2. Examen físico
Se realizará anualmente y deberá incluir medidas antropométricas (peso, talla, índice de masa corporal
[IMC], circunferencia de cintura), constantes vitales (tensión arterial, frecuencia cardiaca, temperatura) y
examen de piel, orofaringe, corazón, pulmón, abdomen, ganglios linfáticos periféricos, sistema
musculoesquelético, sistema nervioso y zona anogenital.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [718]
[46] INFECCIÓN POR VIH
Tabla IV. Categorías clínicas de la infección por el virus de inmunodeficiencia humana.
3.3. Estudios complementarios (Tabla V)
III. SÍNDROMES Y PROBLEMAS CLÍNICOS ASOCIADOS AL VIH
Para evaluar a un paciente con infección por VIH ya diagnosticada lo primero que se ha de conocer
es su situación inmunovirológica (carga viral plasmática [CVP] y recuento de linfocitos TCD4+). Si es buena
(CVP indetectable durante más de 12 meses y linfocitos TCD4+ > 350/ml), los síndromes clínicos que
desarrollará serán muy similares a los de la población general.
1. FIEBRE DE ORIGEN DESCONOCIDO (FOD)
Ante un paciente con infección por VIH y FOD se realizará una historia clínica detallada, poniendo
especial atención a la medicación y aislamientos previos. Además, se llevará a cabo una exploración física
completa con fondo de ojo. Posteriormente se completará el estudio según lo indicado en la tabla VI.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [719]
[46] INFECCIÓN POR VIH
Tabla V. Exploraciones complementarias en la valoración inicial y seguimiento de los pacientes con VIH.
Dentro de las causas más probables de FOD se encuentran infecciones por micobacterias (la más
común), Pneumocystis jirovecii, citomegalovirus (CMV), micosis endémicas (histoplasmosis,
coccidioidomicosis), leishmaniasis visceral, otros procesos infecciosos (criptococosis, aspergilosis,
toxoplasmosis), neoplasias, fármacos y el síndrome de reconstitución inmune.
2. ADENOPATÍAS
Entre las causas más frecuentes están la linfadenopatía persistente generalizada (que usualmente
se relaciona con la infección aguda y que suele comenzar a las dos semanas de contraer la infección; se
manifiesta con adenopatías axilares, cervicales, occipitales…), infección diseminada por micobacterias,
toxoplasmosis o linfomas (Hodgkin y no Hodgkin). Hay que guiar el estudio en función de la sospecha. En
caso de inmunosupresión severa casi siempre será necesaria una biopsia ganglionar.
3. AFECTACIÓN NEUROLÓGICA Y DETERIORO COGNITIVO
El grado de inmunosupresión (recuento de linfocitos TCD4+) es el factor determinante para el
diagnóstico diferencial en un paciente que presenta alteraciones en la exploración neurológica.
> 500 TCD4+/ml: causas similares a los individuos inmunocompetentes.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [720]
[46] INFECCIÓN POR VIH
200-500 TCD4+/ml: enfermedades motoras y cognitivas asociadas al VIH sin lesiones focales.
< 200 TCD4+/ml: lesiones del sistema nervioso central (SNC), que se clasifican en función de
que produzcan efecto masa o no.
Lesiones con efecto masa: encefalitis por Toxoplasma gondii, linfoma primario del SNC;
otras menos frecuentes son tuberculosis, neurocisticercosis, abscesos cerebrales por
Aspergillus spp, Nocardia spp, Listeria monocytogenes, Staphylococcus spp.
Lesiones sin efecto masa: leucoencefalopatía multifocal progresiva (virus JC),
encefalopatía VIH, encefalitis por CMV.
Tabla VI. Evaluación del paciente con virus de inmunodeficiencia humana con fiebre de origen desconocido.
Figura 1. Algoritmo para el manejo del paciente con VIH con lesión del sistema nervioso central.
En los pacientes con VIH es común la aparición de cambios en la memoria, la capacidad de
concentración y de atención y alteraciones motoras. Cuando ocurren en ausencia de un proceso infeccioso
se clasifican como HAND (HIV-Associated Neurocognitive Disorders), cuyos factores de riesgo son la edad,
un número bajo de linfocitos TCD4+, factores cardiovasculares y enfermedades metabólicas. La terapia
antirretroviral combinada disminuye la prevalencia de los déficits neurocognitivos.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [721]
[46] INFECCIÓN POR VIH
4. AFECTACIÓN RESPIRATORIA
Dentro de las infecciones más comunes están las neumonías bacterianas, la infección por
Pneumocystis jirovecii y la tuberculosis. Se debe considerar también el diagnóstico de gripe. Ante una
neumonía por S. aureus se debe realizar ecocardiograma si se sospecha endocarditis derecha y comenzar
tratamiento empírico.
Ver la figura 2 y la tabla VII a continuación.
Figura 2. Paciente con virus de inmunodeficiencia humana con síntomas pulmonares.
Tabla VII. Patologías pulmonares según el patrón radiológico y la progresión.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [722]
[46] INFECCIÓN POR VIH
5. AFECTACIÓN DEL APARATO DIGESTIVO: DISFAGIA Y DIARREA
5.1. Disfagia
Es un síntoma frecuente. La candidiasis esofágica es su causa principal. Otras infecciones oportunistas que
la provocan son el virus herpes simple (VHS), CMV o Cryptosporidium. Puesto que Candida spp es la
etiología más frecuente se debe iniciar tratamiento empírico con antifúngicos (fluconazol 200 mg/24 h el
primer día seguido de 100 mg/24 h entre 14 y 30 días) ante la presencia de estos síntomas antes de hacer
otras pruebas (radiológicas o endoscópicas).
5.2. Diarrea
Hay que valorar si es aguda (< 2 semanas) o crónica (> 4 semanas) y si afecta predominantemente al
intestino delgado o al grueso (Tabla VIII). El problema del diagnóstico de la causa de la diarrea en los
pacientes con VIH es que son susceptibles de padecer todas las infecciones que afectan a
inmunocompetentes y, además, la multitud de infecciones oportunistas, sin olvidar los efectos adversos
gastrointestinales de su medicación antirretroviral. El número de linfocitos TCD4+ nos ayuda a identificar a
los pacientes con mayor riesgo. Realizaremos el mismo manejo que en un paciente sin VIH para un valor >
200 TCD4+/ml.
Tabla VIII. Causas de la diarrea en la infección por el virus de la inmunodeficiencia humana.
Para el diagnóstico habrá que valorar la realización de hemocultivos, cultivos de heces,
determinación de toxina de Clostridium difficile, estudio de parásitos, antígeno de Giardia lamblia,
bioquímica y grasa fecal o endoscopias.
Se puede hacer un manejo conservador con rehidratación oral y tratamiento sintomático en
pacientes con > 200 TCD4+/ml. El antibiótico empírico debe ir dirigido hacia enteropatógenos
gramnegativos (ciprofloxacino 500 mg/12 h durante 5 días). En caso de alta sospecha de infección
parasitaria se iniciará metronidazol 500 mg/8 h.
6. AFECTACIÓN HEMATOLÓGICA
El SIDA se relaciona con citopenias, cuya incidencia se correlaciona con el grado de
inmunosupresión. El tratamiento consiste en iniciar la terapia antirretroviral y corregir aquellas causas
reversibles.
6.1. Trombopenia
Puede ser la manifestación inicial de infección por el VIH. Hoy en día, con la terapia antirretroviral, la
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [723]
[46] INFECCIÓN POR VIH
trombopenia se asocia a replicación incontrolada del virus y coinfección con virus de hepatitis. Se debe
tanto a una producción inefectiva de plaquetas como a un aumento de su destrucción. También puede ser
secundaria a infecciones, neoplasias, medicamentos o hiperesplenismo.
6.2. Anemia
En la mayoría de los casos es multifactorial y aparece como efecto de infecciones, enfermedades
linfoproliferativas, defectos nutricionales, hemólisis y fármacos. Algunos factores de riesgo de desarrollo de
anemia son un volumen corpuscular medio < 80 fL, un recuento de linfocitos TCD4+ < 200/ml, una carga
viral previa (CVP) > 50.000 copias/ml y el uso de zidovudina (AZT).
6.3. Neutropenia
También es de origen multifactorial, debiéndose al propio VIH, a las infecciones y a la medicación. Solo se
justifica el uso de factores estimuladores de colonias en caso de alto riesgo de infección bacteriana o en
caso de infecciones bacterianas ya documentadas con neutropenia. El derivado del factor estimulante de
colonias granulocíticas (G-CSF) es el de elección.
7. AFECTACIÓN OFTALMOLÓGICA
Las lesiones oftalmológicas más frecuentes en el SIDA son retinopatía por el VIH, retinitis por CMV,
toxoplasmosis, retinitis por virus varicela zóster (VVZ) y VHS, coroidopatía por Pneumocystis jirovecii,
sarcoma de Kaposi, linfoma intraocular y lesiones neurooftalmológicas.
8. AFECTACIÓN RENAL
Los pacientes con VIH tienen riesgo de presentar tanto un daño renal agudo como una enfermedad
renal crónica secundarios a nefrotoxicidad por la medicación (poner especial cuidado en pacientes tratados
con tenofovir [TDF]), nefropatía asociada al VIH (más frecuente en la raza negra), enfermedades por
inmunocomplejos y, menos frecuentemente, microangiopatía trombótica.
Los factores de riesgo para desarrollar daño renal agudo son la edad, diabetes mellitus,
enfermedad renal preexistente, fallo hepático, tratamiento antirretroviral, SIDA, recuento bajo de TCD4+,
alta CVP, coinfección con VHC y crioglobulinemia.
9. AFECTACIÓN DERMATOLÓGICA
Puede aparecer rash como manifestación de la primoinfección por VIH o por otra infección
concomitante, por procesos neoplásicos (sarcoma de Kaposi) y reacciones medicamentosas. Dentro de la
infecciones con afectación cutánea encontramos anginomatosis bacilar, Staphylococcus aureus, Neisseria
gonorrhoeae, sífilis, Helicobacter cinaedi, VHS, VVZ, Parvovirus B19, Crytococcus neoformans, Sporothrix
schenckii, escabiosis, Leishmania, etc.
10. NEOPLASIAS
Estos pacientes sufren un mayor riesgo de cáncer. Los que presentan una mayor frecuencia con
diferencia son los linfomas no Hodgkin (entre los que predominan el linfoma de Burkitt y el linfoma B difuso
de células grandes), el sarcoma de Kaposi y el cáncer de cérvix. Estos tumores han disminuido su incidencia
con el inicio de la terapia antirretroviral. Otros tumores más frecuentes entre los pacientes con VIH en
comparación con la población general son los cánceres de mama, anogenital, colorrectal y de pulmón. Los
tumores no asociados a SIDA no han disminuido su incidencia en la era de la terapia antirretroviral de gran
actividad (TARGA).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [724]
[46] INFECCIÓN POR VIH
Tabla IX. Infecciones oportunistas en el VIH.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [725]
[46] INFECCIÓN POR VIH
IV. TRATAMIENTO ANTIRRETROVIRAL (TAR)
1. OBJETIVOS
Con las terapias actuales no es posible conseguir la curación. Por ello el objetivo del tratamiento
será lograr unos adecuados controles inmunovirológico y clínico para intentar igualar la expectativa de vida
a la de la población general. Se debería ver un aumento de 50-100 linfocitos TCD4+/ml después del primer
año tras el inicio del TAR. A pesar de la supresión virológica, este aumento no se produce en algunos
pacientes muy inmunodeprimidos.
Respecto a la CVP, el objetivo está en conseguir niveles inferiores a 20-50 copias/ml. La respuesta
virológica es la reducción de la CVP en más de un logaritmo (1 log) a las cuatro semanas del inicio del TAR y
que sea indetectable (< 50 copias/ml) tras 16-24 semanas de tratamiento.
2. EVALUACIÓN PREVIA AL INICIO DEL TRATAMIENTO ANTIRRETROVIRAL
Tabla X. Evaluación previa al inicio del tratamiento antirretroviral.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [726]
[46] INFECCIÓN POR VIH
3. ¿CUÁNDO INICIAR EL TRATAMIENTO ANTIRRETROVIRAL?
Se recomienda la administración del TAR a todos los pacientes con infección por VIH para evitar la
progresión de la enfermedad, disminuir la transmisión del virus y limitar el efecto nocivo sobre posibles
comorbilidades coexistentes.
Figura 3. Algoritmo de tratamiento antirretroviral.
4. FAMILIAS DE FÁRMACOS ANTIRRETROVIRALES
4.1. Inhibidores de la transcriptasa inversa análogos de nucleósidos (ITIAN)
En España hay comercializados seis ITIAN: AZT (o ZDV), ddI, d4T, 3TC, FTC y ABC. También se dispone de un
análogo de nucleótido (TDF).
El uso de AZT, ddI y d4T es excepcional debido a su mayor toxicidad. Las combinaciones de ITIAN de
elección son las formadas por TDF/FTC y por ABC/3TC.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [727]
[46] INFECCIÓN POR VIH
TDF/FTC frente a ABC/3TC:
TDF/FTC debe evitarse en pacientes con insuficiencia renal. En todos los pacientes se debe
controlar periódicamente la función renal (filtrado glomerular estimado, proteinuria…) debido
al riesgo de tubulopatía por depósito de TDF en las células del túbulo renal. Se ha desarrollado
una nueva formulación de tenofovir (tenofovir alafenamida [TAF]), no inferior en eficacia a TDF
y con menor nefrotoxicidad (apto para FG > 30 ml/min) y menor reducción de la densidad
mineral ósea que TDF. Ambas formulaciones de tenofovir son activas frente a VHB.
ABC/3TC se debe evitar en pacientes con CVP elevada (más de 100.000 copias/ml) cuando se
combina con un ITINN o un IP/r distinto de LPV/r.
Cuando se prescriba ABC se deben tomar las medidas necesarias para tratar de minimizar todos
los factores de riesgo cardiovascular modificables.
4.2. Inhibidores de la transcriptasa inversa no nucleósidos (ITINN)
En España hay cuatro ITINN comercializados: NVP, EFV, ETR y RPV. Son inductores de algunos isoenzimas
del citocromo p450. Por ello hay que tener cuidado con las interacciones farmacológicas.
EFV está contraindicado durante el primer trimestre de la gestación. Por ello deben
considerarse otras opciones en mujeres que no utilicen métodos anticonceptivos. EFV puede
empeorar alteraciones neuropsiquiátricas previas no estabilizadas y hay que tener precaución
al usarlo en pacientes que realicen tareas peligrosas si presentan somnolencia, mareos o
trastornos de la concentración. No es infrecuente la aparición de exantema.
RPV no puede usarse conjuntamente con IBP. No se aconseja su uso en pacientes con CVP >
100.000 copias/ml. Debe tomarse con una comida copiosa (> 400 Kcal).
NVP se ha relacionado con el desarrollo de hepatitis aguda. No se recomienda su uso en pautas
de inicio de TAR.
4.3. Inhibidores de la proteasa potenciados con ritonavir (IP/r)
Los IP/r tienen que administrarse con dosis bajas de RTV o COBI para ver potenciado su efecto. En la
actualidad hay seis IP/r disponibles en la clínica: ATV, DRV, LPV, FPV, SQV y TPV (solo en pacientes
pretratados). Son inductores e inhibidores del citocromo p450, por lo que hay que ser precavido con las
interacciones farmacológicas.
LPV se comercializa en comprimidos coformulados con RTV. Más recientemente se ha incorporado
COBI como potenciador de ATV o DRV, también en coformulaciones.
Se caracterizan por una elevada barrera genética que dificulta la selección de mutaciones de
resistencia (MR), aun en situaciones desfavorables como la baja adherencia. Presentan peor perfil
metabólico que otros antirretrovirales y el desarrollo de dislipemia es frecuente (siendo menor con ATV y
DRV).
4.4. Inhibidores de la integrasa (INI)
Los INI disponibles en la clínica son tres: RAL, EVG y DTG. El primer miembro de esta familia fue RAL, con un
perfil de tolerabilidad muy favorable (en caso de insuficiencia renal o hepática) y escasas interacciones con
otras familias de fármacos. No se ha seleccionado ninguna mutación de resistencia a DTG en ninguno de los
tres ensayos clínicos en fase III de inicio de TAR. Ello hace pensar que DTG presenta una elevada barrera
frente a las mutaciones, superior a la de otros INI, aunque esto se habrá de confirmar cuando se disponga
de mayor experiencia y seguimiento. EVG debe usarse potenciado con COBI. Existe una coformulación con
TAF recientemente comercializada.
¿Qué combinación de antirretrovirales debe usarse?
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [728]
[46] INFECCIÓN POR VIH
El tratamiento inicial debe combinar tres fármacos que incluyan dos ITIAN asociados a un INI, a un
ITINN o a un IP/r. Con las combinaciones actuales se puede conseguir una CVP inferior a 50 copias/ml a las
48 semanas en más del 75% de los casos.
Habrá que valorar el estudio de resistencias. Es necesario revisar la medicación concomitante del
paciente y tener en cuenta las posibles interacciones farmacológicas, sobre todo, al usar ITINN e IP/r.
Existen aplicaciones informáticas actualizadas para consultar posibles interacciones (por ejemplo, la de la
Universidad de Liverpool).
Tabla XI. Combinaciones de tratamiento antirretroviral recomendadas de inicio (modificado del Documento de Consenso de GeSIDA/
Plan Nacional sobre el SIDA respecto al tratamiento antirretroviral en adultos infectados por el VIH, actualizado a enero de 2016).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [729]
[46] INFECCIÓN POR VIH
5. ADHERENCIA Y TOLERABILIDAD
La adherencia incorrecta es la primera causa de fracaso terapéutico. Hay que revisar la adherencia
al tratamiento ante cualquier aumento de CVP. Para comprobar esto podemos valernos de los registros de
retirada de medicación de farmacia. Se recomiendan pautas basadas en IP/r ante pacientes con alta
sospecha de tener dificultades en el cumplimiento terapéutico.
Asimismo, habrá que evaluar periódicamente la tolerancia al tratamiento. Los nuevos fármacos son
mucho mejor tolerados. Por ello es cada vez más infrecuente el abandono del TAR a causa de los efectos
secundarios. Podría justificarse un cambio en el tratamiento ante ciertos efectos adversos, y más si
impidieran el correcto cumplimiento del TAR (ver Apartado 6. “Cambio de tratamiento antirretroviral”).
6. CAMBIO DE TRATAMIENTO ANTIRRETROVIRAL
6.1. Cambio de tratamiento antirretroviral en pacientes con carga viral suprimida
Ver a continuación la tabla XII.
Tabla XII. Recomendaciones sobre el uso de tratamiento antirretroviral.
Tras el cambio de un TAR, hay que repetir una determinación de la CVP a las 4 semanas para
confirmar que se mantiene la supresión virológica.
6.2. Fracaso virológico (FV)
Se define como la presencia de CVP > 50 copias/ml en dos determinaciones consecutivas una vez
transcurridas 24 semanas del inicio del TAR (si la CVP basal fuese muy elevada, este periodo puede
prolongarse hasta 48 semanas, sobre todo, si se usan IP/r). El FV puede ocurrir con o sin selección de
mutantes resistentes (MR). Habremos de analizar la causa del fracaso (adherencia, interacciones
farmacológicas, intolerancia, toxicidad). Hay que realizar un estudio de resistencias; idealmente, el
genotipo debe proceder de una muestra con virus sometido a presión selectiva del fármaco en el seno del
fracaso (ya que de esta manera se selecciona la mutante resistente), o bien, realizar el estudio lo antes
posible. Se debe cambiar de TAR precozmente para evitar la acumulación de mutaciones de resistencia.
Este cambio debe llevarse a cabo por personal experto en VIH.
Una situación diferente es la de los repuntes virológicos transitorios o blips, que son valores de
CVP detectables entre 50 y 200 copias/ml, con recuentos previos y posteriores < 50 copias/ml. Los blips
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [730]
[46] INFECCIÓN POR VIH
aislados no tienen repercusión clínica pero los blips frecuentes se han asociado a mayor riesgo de FV y
aparición de MR. En presencia de blips se recomienda evaluar la adherencia y la barrera genética del TAR.
6.3. Fracaso inmunológico
Incapacidad para obtener un recuento adecuado de TCD4+ a pesar de mantener una CVP < 50 copias/ml. Se
observa en pacientes que han padecido una inmunosupresión prolongada. Ante él no se recomienda
modificar el TAR.
7. TRATAMIENTO EN CIRCUNSTANCIAS ESPECIALES
7.1. Infecciones oportunistas (IO)
En muchas ocasiones dependemos de la regeneración del sistema inmune para el control de las infecciones
oportunistas, pero debemos tener en cuenta el riesgo de efectos adversos y de síndrome inflamatorio por
reconstitución inmunológica (SIRI). Ante pacientes con IO (salvo en la tuberculosis y en la meningitis
criptocócica) hay que iniciar TAR dentro de los primeros 15-30 días tras el comienzo del tratamiento de la
infección (ver Apartado VI. “SIRI [Síndrome Inflamatorio de Reconstitución Inmunológica]”).
7.2. Embarazo
Se debería realizar una serología de VIH a toda mujer embarazada y, si fuera negativa, repetirla en el tercer
trimestre. Si resultase positiva se tendría que iniciar el TAR en todas las gestantes con el objetivo de llegar
a la concepción con CVP indetectable.
La elección de tratamiento se realizará teniendo en cuenta:
Estudio de resistencias.
Seguridad de los fármacos antirretrovirales (FAR).
Si no hubiera resistencias, el TAR de elección sería TDF o ABC + 3TC o FTC + LPV/r o ATV/r. En
caso contrario podrán recibir cualquiera de los FAR tras una valoración individualizada.
Si en el momento del parto la paciente no hubiera recibido TAR o lo hubiera tomado durante poco
tiempo (con una CVP > 1.000 copias/ml o desconocida), se indica una cesárea electiva y tratamiento con
ZDV por vía intravenosa intraparto, asociando nevirapina (NVP) oral al menos 2 horas antes del parto
(especialmente cuando no pudiera practicarse la cesárea y el parto tuviera que llevarse a cabo por vía
vaginal).
La lactancia materna está contraindicada.
7.3. Hepatopatía por VHB y VHC
La hepatotoxicidad asociada al TAR es más frecuente en pacientes coinfectados. Sin embargo, salvo los
dideoxinucleósidos (d-AN) y NVP (que pueden causar fallo hepático agudo y toxicidad crónica), los FAR
utilizados actualmente presentan bajo riesgo de hepatotoxicidad. En pacientes con hepatopatía crónica y
función hepática conservada (incluyendo cirrosis grado A de la escala de Child) se puede utilizar cualquier
FAR (a excepción de NVP).
En caso de insuficiencia hepatocelular, los INI son de elección (puesto que no precisan ajuste de
dosis). Los IP/r presentan mayor margen terapéutico que los ITINN.
Coinfección por VHB: TDF suprime el VHB en la inmensa mayoría de los pacientes. Por tanto,
en estos se debe iniciar el TAR incluyendo TDF junto a FTC o 3TC.
Coinfección por VHC: a excepción de sofosbuvir, los antivirales de acción directa (AAD)
actualmente utilizados (simeprevir, daclatasvir, ledipasvir, paritaprevir, ombitasvir y dasabuvir)
presentan interacciones farmacocinéticas significativas con los FAR, lo que obliga a ajustes de
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [731]
[46] INFECCIÓN POR VIH
dosis o contraindica la coadministración. Antes de prescribir un tratamiento con AAD en un
paciente que recibe TAR, se debe consultar con un experto y usar herramientas que
proporcionen información actualizada de interacciones farmacológicas (como, por ejemplo, la
de la Universidad de Liverpool).
7.4. Insuficiencia renal
En cada revisión o ante cualquier cambio clínico se debe prestar especial atención a la función renal ya que
en muchas ocasiones obliga a ajuste de dosis y/o incluso cambio de TAR.
Precisan ajuste de dosis todos los ITIAN, excepto ABC.
No se requiere ajuste de dosis en ITINN, IP, ENF (enfuvirtida) ni INI (RAL o DTG).
Hay que hacer ajuste de dosis en pacientes con enfermedad renal crónica avanzada (ERCA)
siguiendo las recomendaciones de la ficha técnica de cada medicamento (por ejemplo, TDF), teniendo en
cuenta las posibles interacciones entre los diferentes fármacos. Se desaconseja el uso de coformulaciones
debido a la dificultad para el ajuste de dosis.
7.5. Infección aguda
A los síntomas que ocurren durante los primeros 30 días tras el contagio se los considera infección aguda.
No debe confundirse con la infección reciente (pacientes diagnosticados en los primeros 6 meses de la
infección). En más de la mitad de los casos se caracteriza por un síndrome febril agudo autolimitado.
Las pruebas de ELISA de cuarta generación (que detectan Ac y Ag p24) acortan el periodo de
ventana y permiten el diagnóstico durante la infección aguda en un 80-90% de los casos. Ante ella se debe
iniciar el TAR lo antes posible. Las recomendaciones y las pautas de inicio son las mismas que en el caso de
la infección crónica.
7.6. Neoplasias
En el caso de sarcoma de Kaposi o linfomas no Hodgkin, el TAR es un pilar fundamental del tratamiento.
Ante el resto de las neoplasias ha de empezarse el TAR tan pronto como sea posible. Los FAR de elección en
caso de coadministración de quimioterapia han de ser RAL o DTG por su excelente tolerancia y mínimas
interacciones.
8. PROFILAXIS POSTEXPOSICIÓN
Se consideran fluidos potencialmente infecciosos la sangre, el semen, las secreciones vaginales, la
leche materna y los líquidos cefalorraquídeo, pleural, peritoneal, pericárdico, amniótico y sinovial. También
los tejidos, órganos, cultivos celulares y los concentrados de virus de laboratorio. No se consideran
infecciosos el sudor, el esputo, la orina, las heces, el vómito, las secreciones nasales, la saliva ni las
lágrimas, a menos que contengan sangre visible.
Habitualmente distinguimos entre exposición ocupacional y exposición no ocupacional. En ambos
casos, si fue a través de una herida o contacto con conjuntiva, debe realizarse lavado con agua y jabón y
desinfectar con un antiséptico.
Debemos valorar cuidadosamente el riesgo de contagio. Si el paciente o persona fuente es VIH+
conocido, se debe completar cuál es su situación virológica (muy bajo riesgo en pacientes con CVP
indetectable) y cuál fue la situación de riesgo. Existen documentos específicos (por ejemplo, Documento de
Consenso sobre Profilaxis Postexposición de GeSIDA) que nos pueden ayudar en la valoración del riesgo
para decidir si está indicado iniciar profilaxis o no.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [732]
[46] INFECCIÓN POR VIH
En caso de que esté indicado iniciar profilaxis, esta se debe comenzar antes de 24 horas y mejor
antes de 2 horas. No se recomienda su inicio pasadas más de 72 horas. Las pautas recomendadas son
TDF/FTC + RAL o DRV/r o ATV/r, priorizando el INI frente al IP.
Hay que valorar infecciones por otras ETS y/o enfermedades transmisibles por vía parenteral,
derivar al paciente a Medicina Preventiva (si no se confirma el contagio no es necesaria una valoración por
Unidad de VIH) y realizar serología a las 6 semanas y repetirla a los 3 meses (ver Capítulo 50. “Exposición a
material biológico”).
V. SIRI (SÍNDROME INFLAMATORIO DE RECONSTITUCIÓN INMUNE)
1. DEFINICIÓN Y EPIDEMIOLOGÍA
En el contexto de la infección por VIH, definimos SIRI como el conjunto de alteraciones
inflamatorias que suceden como consecuencia de una respuesta paradójica del sistema inmunológico tras
el inicio del TAR. Puede ser general, estar en relación con infecciones oportunistas preexistentes,
exacerbación de enfermedades autoinmunes o de neoplasias.
La incidencia se ha estimado entre un 7 y 13% según diferentes series actuales (algunas más
antiguas la estiman en un 30%).
2. FACTORES DE RIESGO
Recuento bajo de linfocitos TCD4+ y aumento rápido tras inicio del TAR.
CVP elevada y disminución rápida tras inicio del TAR.
Infección tuberculosa.
Meningitis criptocócica.
3. CRITERIOS DIAGNÓSTICOS
No existen criterios diagnósticos aceptados universalmente. La mayoría de los pacientes
cumplen las siguientes condiciones:
Respuesta inflamatoria exagerada y atípica en tejidos y órganos afectados.
Asociación temporal entre el inicio del TAR y el de las manifestaciones clínicas (mediana
de aparición de 48 días [29-99]).
Recuento bajo de TCD4+ previo al inicio del TAR (< 100 células/mL). En el caso de
tuberculosis se han descrito casos de SIRI en pacientes con > 200 CD4/mL.
Respuesta inmunovirológica al TAR (aumento de TCD4+ y disminución de la CVP).
Descartar sobreinfección bacteriana, microorganismos multirresistentes, reacciones de
hipersensibilidad, interacciones farmacológicas que disminuyan niveles de fármacos.
4. CARACTERÍSTICAS CLÍNICAS
En general, mala evolución y aparición de nuevas lesiones a pesar de tratamiento adecuado.
M. avium complex: linfadenitis generalizada.
M. tuberculosis: fiebre, linfadenopatías intratorácicas con o sin infiltrados radiológicos
pulmonares, linfadenopatías cervicales y derrame pleural.
Las manifestaciones clínicas se correlacionan con la positivización del Mantoux. La enfermedad
extratorácica es menos frecuente. Destacan las manifestaciones intraabdominales (37%) y otras
menos comunes: meningitis con cultivos negativos, empeoramiento paradójico de
tuberculomas cerebrales, cerebritis localizada, vasculitis del SNC, hipertensión intracraneal
(HTIC), afectación hepatoesplénica y disfunción renal aguda.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [733]
[46] INFECCIÓN POR VIH
C. neoformans: se establecen dos patrones. El precoz cursa con manifestaciones clínicas de un
síndrome neurológico infeccioso, cultivos de LCR o sangre positivos; el tratamiento antifúngico
está indicado (se diferencia de la clásica meningitis criptocócica por mayor presión de apertura
en la PL, mayor glucorraquia y pleocitosis del LCR; la distinción entre ambas es importante
porque el SIRI se beneficia del tratamiento con corticoides mientras que la meningitis empeora
con ellos). El tardío (hasta 15 meses tras inicio de TAR) tiene una afección predominantemente
linfadenopática. También puede cursar como meningitis aséptica, HTIC y masas cerebrales
inflamatorias.
P. jirovecii: fiebre, insuficiencia respiratoria e infiltrados pulmonares parcheados. Antes del
diagnóstico de SIRI deben excluirse resistencia a cotrimoxazol, sobreinfección bacteriana y
toxicidad inducida por fármacos.
CMV: se diferencian dos vertientes: temprana (3 primeros meses), con retinitis de novo; y
tardía, con uveítis y vitritis por restauración inmunológica. Se ha descrito la pancolitis grave
perforante.
VHB y VHC: clínica de hepatitis aguda. Se recomienda no suspender el tratamiento para VHB
una vez que se inicia TAR (en general, se hará con TDF/FTC); no hay datos para VHC.
Virus JC: el único tratamiento eficaz es el TAR, pero se han descrito el comienzo y el
empeoramiento de déficits neurológicos poco después su inicio como una forma inflamatoria
de leucoencefalopatía multifocal progresiva.
Otros SIRI de etiología infecciosa: síndromes dermatológicos exuberantes (VVZ, VHS, Moluscum
contagiosum, Leishmania major), peritonitis granulomatosa (Microsporidium), Strongyloides
spp, Schistosoma spp, etc.
Otros de etiología no infecciosa:
SIRI autoinmune. Se han documentado tras inicio del TAR casos de artritis reumatoide,
lupus eritematoso sistémico, polimiositis, enfermedad de Still del adulto, síndrome de
Guillain-Barré, enfermedad de Graves-Basedow, policondritis recidivante…
SIRI tumoral. Principalmente, sarcoma de Kaposi. Otros: enfermedad de Castleman,
linfoma no Hodgkin, linfoma primario de cavidades.
5. MANEJO TERAPÉUTICO
5.1. Tratamiento preventivo
Para prevenir el desarrollo de SIRI hay que valorar la endemicidad de las enfermedades infecciosas,
identificar coinfecciones múltiples, diagnosticar las IO subclínicas en los individuos marcadamente
inmunodeprimidos (por ejemplo, examen de fondo de ojo en pacientes con TCD4+ < 100/mL para descartar
retinitis por CMV).
De forma ideal, se recomienda el comienzo de TAR a los 10 o a los 14 días de inicio del tratamiento
de la IO y, preferentemente, antes de los 28 días en los pacientes con IO diferentes a la tuberculosis y a la
meningitis criptocócica, siempre que no haya complicaciones clínicas que lo limiten.
En la tuberculosis (TB) se recomienda iniciar TAR siempre durante el tratamiento antituberculoso,
independientemente del recuento de células TCD4+, puesto que disminuye el riesgo de muerte. El
momento óptimo sí depende del recuento de células TCD4+:
TCD4+ < 50/mL: debe iniciarse lo antes posible y no más tarde de las dos primeras semanas.
Si TCD4+ es > 50/mL: puede retrasarse el inicio del TAR hasta finalizar la primera fase del
tratamiento antituberculoso (8 semanas). Se están realizando estudios que sugieren que es
posible iniciar el TAR tras finalizar tratamiento de TB con un recuento mayor a 350 TCD4+/mL.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [734]
[46] INFECCIÓN POR VIH
No se conoce el momento óptimo de inicio en el caso de meningitis tuberculosa.
Intentar incluir rifampicina en tratamiento de TB y usar un TAR sin problemas de interacciones.
EFV se considera el fármaco de elección (mayor experiencia y mejores resultados). RAL, DTG
(ajustado a doble dosis), MVC (maraviroc), NVP podrían ser alternativas.
No pueden utilizarse RPV, ETV, EVG/c ni IP/r (en caso de no haber alternativa a los IP/r, habría
de usarse rifabutina).
En caso de SIRI no debe interrumpirse el tratamiento antituberculoso ni el TAR. Pueden añadirse
AINE ante formas leves-moderadas o corticoides en las formas moderadas-graves.
En pacientes con meningitis criptocócica se recomienda diferir el inicio del TAR hasta 5 semanas
por riesgo de mayor mortalidad asociada con un inicio precoz del mismo (especialmente en pacientes con
menos de 5 células/mL en el LCR o incremento de la presión intracraneal).
5.2. Tratamiento del SIRI constituido
Existe consenso en mantener TAR en lo posible (se ha de suspender en los casos en los que el SIRI amenace
la vida del paciente). Debe mantenerse el tratamiento específico ya iniciado para la IO. Para el tratamiento
del SIRI han demostrado eficacia los AINE, los bloqueantes del TNF-a y rituximab (hay estudios con
montelukast). Pero los datos más claros de eficacia del tratamiento antiinflamatorio coadyuvante en el SIRI
obedecen a los corticoides (particularmente, prednisolona), que deben reservarse para los casos más
graves, puesto que aumentan el riesgo de reactivar otras infecciones latentes.
6. PRONÓSTICO
El SIRI puede ser mortal (media del 4%, mayor en meningitis criptocócica), pero en la mayoría de los
casos las manifestaciones son leves y corregibles (en menos del 10% de los pacientes es necesario
suspender el TAR o utilizar corticoides).
VI. ABREVIATURAS UTILIZADAS EN EL TEXTO Y NOMBRES
COMERCIALES DE LOS FÁRMACOS ANTIRRETROVIRALES (®) MÁS
USADOS (POR ORDEN ALFABÉTICO)
NOMENCLATURA PARA EL TRATAMIENTO ANTIRRETROVIRAL:
Fármacos separados por “/”: disponible en coformulación.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [735]
[46] INFECCIÓN POR VIH
BIBLIOGRAFÍA
Beatty GW. Diarrhea in patients infected with HIV presenting to the emergency department. Emerg Med
Clin North Am. 2010;28(2):299-310.
Becker KN, Becker NM. Ocular manifestations seen in HIV. Dis Mon. 2014;60(6):268-75.
Dieterich DT, Wilcox CM. Diagnosis and treatment of esophageal diseases associated with HIV
infection. Practice Parameters Committee of the American College of Gastroenterology. Am J
Gastroenterol. 1996;91(11):2265-9.
Grupo de expertos de la Secretaría del Plan Nacional sobre el SIDA (SPNS), Grupo de Estudio de SIDA
(GeSIDA), Sociedad Española de Medicina y Seguridad del Trabajo (SEMST), Sociedad Española de
Medicina Preventiva, Salud Pública e Higiene (SEMPSPH), Asociación Española de Especialistas en
Medicina del Trabajo (AEEMT), Sociedad Española de Salud Laboral en la Administración Pública
(SESLAP), Asociación Nacional de Médicos del Trabajo en el Ámbito Sanitario (ANMTAS), Sociedad
Española de Infectología Pediátrica (SEIP), Sociedad Española de Medicina de Urgencias y
Emergencias (SEMES) y Grupo de Estudio de Hepatitis Víricas-SEIMC (GEHEP). Documento de
consenso sobre profilaxis postexposición ocupacional y no ocupacional en relación con el VIH, VHB y
VHC en adultos y niños (actualización de marzo de 2015). Disponible en: http://www.gesida-
seimc.org/guias_clinicas.php?mn_MP=406&mn_MS=410
Guidelines of European AIDS Clinical Society (EACS), 8.0, October 2015.
Hoffmann C, Rockstroh JC. HIV 2015/2016. Hamburg: Medizin Fokus Verlag. 2015.
Hot A, Schmulewitz L, Viard JP, Lortholary O. Fever of unknown origin in HIV/AIDS patients. Infect Dis
Clin North Am. 2007;21(4):1013-32.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [736]
[46] INFECCIÓN POR VIH
Insight Start Study Group, Lundgren JD, Babiker AG, Gordin F, Emery S, Grund B, et al. Initiation of
antiretroviral therapy in early asymptomatic HIV infection. N Engl J Med. 2015;373:795-807.
Ministerio de Sanidad, Servicios Sociales e Igualdad, Plan Nacional sobre Sida, Guía de
recomendaciones para el diagnóstico precoz de VIH en el ámbito sanitario, 2014. Disponible en:
http://www.gesida-seimc.org/guias_clinicas.php?mn_MP=406&mn_MS=410
Müller M, Wandel S, Colebunders R, et al. Immune reconstitution inflammatory syndrome in patients
starting antiretroviral therapy for HIV infection: a systematic review and meta-analysis. Lancet Infect
Dis. 2010;10:251.
Murdoch DM, Venter WD, Feldman C, van Rie A. Incidence and risk factors for the immune
reconstitution inflammatory syndrome in HIV patients in South Africa: a prospective study. AIDS.
2008;22:601.
Panel de expertos de GeSIDA. Documento de prevención y tratamiento de infecciones oportunistas y
otras coinfecciones en pacientes con infección por VIH (actualización de mayo de 2015). Disponible
en: http://www. gesida-seimc.org/guias_clinicas.php?mn_MP=406&mn_MS=410
Panel de expertos de GeSIDA y Plan Nacional sobre el SIDA. Documento de consenso de GeSIDA/Plan
Nacional sobre el SIDA respecto al tratamiento antirretroviral en adultos infectados por el virus de la
inmunodeficiencia humana (actualización de enero de 2016). Disponible en: http://www.gesida-
seimc.org/guias_clinicas.php?mn_MP=406&mn_MS=407
Temprano Anrs Study Group, Danel C, Moh R, Gabillard D, Badje A, Le Carrou J, et al. A Trial of Early
Antiretrovirals and Isoniazid Preventive Therapy in Africa. N Engl J Med. 2015;373:808-22.
T.r.k ME, Yen NTB, Chau TTH, Mai NTH, Phu NH, Mai PP, et al. Timing of Initiation of Antiretroviral
Therapy in Human Immunodeficiency Virus (HIV)-Associated Tuberculous Meningitis. Clinical Infectious
Diseases. 2011; 52:1374-83.
Wilcox CM, Karowe MW. Esophageal infections: etiology, diagnosis, and management.
Gastroenterologist. 1994;2(3):188-206.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [737]
[47] INFECCIONES EN EL PACIENTE INMUNODEPRIMIDO. NEUTROPENIA FEBRIL
47.Infecciones en el paciente inmunodeprimido.
Neutropenia febril
Jesús González Olmedo.
Medicina Interna
Denis Zafra Torres.
Hematología y Hemoterapia
Asesores: Carmen Díaz Pedroche. Médica Adjunta de Medicina Interna. Carlos Juan Lumbreras Bermejo. Jefe de Servicio de
Medicina Interna
I. INTRODUCCIÓN
El espectro de pacientes inmunodeprimidos es cada vez más amplio debido, entre otros motivos, al
incremento del número de receptores de trasplantes, a la mayor supervivencia de los enfermos con
inmunodeficiencias congénitas y al uso creciente de fármacos inmunosupresores en el tratamiento de
enfermedades autoinmunes y del cáncer. La extensión de este campo sobrepasa los límites de este
capítulo, por lo que nos centraremos en el manejo de la neutropenia febril y en las principales infecciones
del paciente trasplantado. Los pacientes inmunodeprimidos se caracterizan por su susceptibilidad a
infecciones producidas por organismos con baja tasa natural de virulencia en inmunocompetentes.
En la tabla I se recogen las infecciones más frecuentes según el tipo de inmunodepresión.
II. NEUTROPENIA FEBRIL
Las complicaciones infecciosas continúan siendo una causa importante de morbilidad y mortalidad
en los pacientes que desarrollan neutropenia (habitualmente como consecuencia del tratamiento
inmunosupresor que reciben para su enfermedad de base).
Hasta un 50% de los pacientes con neoplasias de órgano sólido y más de un 80% de los pacientes
con neoplasias hematológicas sufrirán fiebre durante más de un ciclo de neutropenia asociada a
quimioterapia. Solo un 20-30% de estos casos tendrán una causa infecciosa documentada, siendo los focos
clínicos más frecuentes el tracto gastrointestinal, el pulmón y la piel. La bacteriemia solo aparecerá en un
10-25% de los pacientes, con mayor frecuencia en el seno de neutropenias profundas y prolongadas.
La epidemiología de los aislamientos microbiológicos ha ido cambiando a lo largo de las últimas
décadas. Entre 1960 y 1980 las infecciones bacterianas por gramnegativos (en particular, Pseudomonas
aeruginosa) eran las predominantes. En los años 90 las infecciones por grampositivos ocuparon los
primeros puestos debido al desarrollo de dispositivos intravasculares y al uso de profilaxis antibiótica
dirigida preferentemente frente a gramnegativos. Actualmente, en la mayoría de los centros, el aislamiento
de estafilococos coagulasa negativos es el más frecuente, seguido por enterobacterias y bacilos
gramnegativos no fermentadores (Pseudomonas aeruginosa, Stenotrophomonas spp…). Es infrecuente que
los hongos (Candida spp, Aspergillus spp…) sean los responsables de una fiebre precoz en un paciente
inmunodeprimido, siendo más típica su aparición en neutropenias profundas y prolongadas en pacientes
que han recibido antibioterapia previa.
Por tanto, la mayoría de los pacientes que desarrollan fiebre durante la neutropenia no tendrán
foco clínico ni aislamiento microbiológico. No obstante, todos ellos deben recibir tratamiento
antimicrobiano urgentemente (en las primeras dos horas y tras la recogida de muestras microbiológicas)
por el riesgo de rápida progresión a sepsis grave que existe en esta situación.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [738]
[47] INFECCIONES EN EL PACIENTE INMUNODEPRIMIDO. NEUTROPENIA FEBRIL
Tabla I. Infecciones más frecuentes según el tipo de inmunosupresión.
1. DEFINICIONES
Los siguientes conceptos son importantes:
Fiebre: una única toma de temperatura oral mayor o igual a 38,3 ºC o mayor o igual a 38 ºC
durante más de una hora.
Neutropenia: cifra de neutrófilos menor a 500 células/mm3 o que se prevé que disminuya por
debajo de 500 en las siguientes 48 horas. Se considera neutropenia profunda el recuento de
neutrófilos menor a 100 células/mm3 y neutropenia funcional al déficit cualitativo en pacientes
con un número de neutrófilos normales (siendo común al diagnóstico de neoplasias
hematológicas).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [739]
[47] INFECCIONES EN EL PACIENTE INMUNODEPRIMIDO. NEUTROPENIA FEBRIL
2. ESTRATIFICACIÓN DEL RIESGO
En las últimas décadas se ha introducido la individualización del riesgo como un factor clave en el
manejo de un episodio de neutropenia febril. La estratificación del riesgo determinará el tipo de
tratamiento antibiótico empírico inicial, su vía de administración, la duración del mismo y la necesidad de
ingreso hospitalario.
La mayoría de los expertos consideran como pacientes de alto riesgo:
Neutropenia (actual o inminente) profunda (< 100 células/mm3) y prolongada (> 7 días).
Asociación de comorbilidad importante:
Inestabilidad hemodinámica.
Mucositis oral o gastrointestinal que impida la deglución o provoque diarrea
importante.
Síntomas gastrointestinales: diarrea, vómitos, dolor abdominal…
Cambios de nueva aparición en el estado neurológico.
Infección de catéter intravascular.
Enfermedad pulmonar crónica de base, insuficiencia respiratoria, nuevos infiltrados
radiológicos a nivel pulmonar.
Insuficiencia hepática (definida como aumento de las transaminasas por encima de cinco veces
su valor normal) o insuficiencia renal (definida como un aclaramiento de creatinina menor de
30 ml/min).
Los pacientes que con más frecuencia desarrollan neutropenia febril de alto riesgo son aquellos que
reciben quimioterapia de inducción en el tratamiento de la leucemia mieloide aguda o por ser receptores
de trasplante alogénico de médula ósea.
Se consideran pacientes de bajo riesgo:
Neutropenia esperada menor de 7 días, sin comorbilidad y con función renal estable y
adecuada. Suelen ser pacientes bajo quimioterapia para neoplasias de órgano sólido.
De forma adicional a estas definiciones clínicas se puede considerar el score MASCC (Multinational
Association for Supportive Care in Cancer risk index score) para la estratificación del riesgo en la
neutropenia febril. Los pacientes de alto riesgo tienen una puntuación menor de 21 y los de bajo riesgo
mayor o igual a 21 (Tabla II).
Tabla II. Score MASCC (Multinational Association for Supportive Care in Cancer risk index score).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [740]
[47] INFECCIONES EN EL PACIENTE INMUNODEPRIMIDO. NEUTROPENIA FEBRIL
3. APROXIMACIÓN DIAGNÓSTICA
La fiebre en el paciente neutropénico puede ser el único signo de una infección subyacente grave.
Y, a la vez, la ausencia de fiebre no descarta una infección subyacente importante. Es necesario ser
sistemático en la evaluación inicial del paciente con neutropenia febril y elaborar una historia clínica
completa.
3.1. Anamnesis
Comorbilidad previa (enfermedad pulmonar, insuficiencia renal, diabetes mellitus,
cardiopatía…).
Anamnesis completa por órganos y aparatos.
Situación de la neoplasia (remisión completa o parcial, recidiva o progresión).
Pauta de quimioterapia recibida.
Profilaxis antimicrobiana previa.
Episodios previos de neutropenia febril y documentación microbiológica.
Transfusión de hemoderivados.
3.2. Exploración física
Prestar especial atención a:
Piel y mucosas: celulitis, úlceras, erupciones herpéticas…
Cavidad oral: mucositis, abscesos…
Senos paranasales.
Fondo de ojo.
Región perirrectal y periné: está contraindicada la realización de tacto rectal.
Puntos de inserción de catéteres venosos, sondas, heridas quirúrgicas…
3.3. Pruebas complementarias en la evaluación del paciente con neutropenia febril
Hemograma y bioquímica (perfil renal, perfil hepático…).
Hemocultivos: al menos dos pares.
Si el paciente fuera portador de catéter venoso central, recoger un hemocultivo de cada luz y
uno periférico de venopunción simultáneamente.
Si no fuera portador de catéter venoso central, recoger dos hemocultivos de diferentes
venopunciones.
Recoger otros cultivos solo si existiera clínica sugerente de su foco.
Radiografía de tórax: debe hacerse de forma rutinaria en la evaluación inicial aun en ausencia
de semiología respiratoria. Suele ser normal; los infiltrados suelen aparecer cuando el paciente
se recupera de la neutropenia.
TC de tórax: se recomienda en pacientes con clínica respiratoria que tengan una radiografía de
tórax normal y que sufran una neutropenia de alto riesgo para infección fúngica invasiva
(leucemia mieloide aguda, trasplante alógenico de precursores hematopoyéticos), y también en
pacientes con neutropenia febril persistente y/o recidivante, aunque sea de bajo riesgo.
TC de otras áreas (craneal, abdominal…) si hubiera indicación clínica.
Los marcadores analíticos de inflamación como la proteína C reactiva (PCR) o la procalcitonina
son de menor utilidad en el paciente neutropénico. No hay evidencia suficiente para
recomendar su uso como guía de la pauta de tratamiento antimicrobiano.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [741]
[47] INFECCIONES EN EL PACIENTE INMUNODEPRIMIDO. NEUTROPENIA FEBRIL
4. PROFILAXIS ANTIMICROBIANA EN NEUTROPENIA FEBRIL (TABLA III)
Tabla III. Profilaxis a seguir en pacientes inmunodeprimidos según las recomendaciones de las Guías de la National Comprehensive
Cancer Network (NCCN) y de la Infectious Diseases Society of America (IDSA).
4.1. Profilaxis antibiótica
La infección bacteriana es la principal causa de morbilidad y mortalidad en el paciente con neutropenia
debida a quimioterapia. Distintos metaanálisis señalan que la profilaxis antibiótica con fluoroquinolonas
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [742]
[47] INFECCIONES EN EL PACIENTE INMUNODEPRIMIDO. NEUTROPENIA FEBRIL
reduce la mortalidad en pacientes neutropénicos de riesgo intermedio y alto, así como las incidencias de
fiebre y bacteriemia. Se debe considerar la profilaxis con fluoroquinolonas en pacientes de alto riesgo con
neutropenia esperada profunda y prolongada. Para ello se evaluaron levofloxacino y ciprofloxacino,
resultando equivalentes. Sin embargo, se prefiere levofloxacino en situaciones con riesgo aumentado de
infección por estreptococos del grupo viridans asociada a mucositis. No se recomienda asociar agentes
activos frente a grampositivos, pero sí poner en marcha estrategias de monitorización de aparición de
bacilos gramnegativos resistentes a fluoroquinolonas.
La cuestión del inicio y fin de la profilaxis antibiótica no ha sido sistemáticamente estudiada.
Algunos clínicos comienzan el tratamiento profiláctico el primer día de inicio de la quimioterapia y otros al
día siguiente a la administración de la última dosis de quimioterapia, finalizando la profilaxis tras la
recuperación de la neutropenia (por encima de 500 células/mm3) o al instaurar tratamiento antibiótico
empírico inicial por aparición de fiebre.
4.2. Profilaxis antifúngica
La infección fúngica invasiva es la principal causa de muerte en pacientes con neoplasias hematológicas.
Actualmente, Aspergillus spp es la primera causa de infección fúngica invasiva en el paciente hematológico,
debido al uso extendido de profilaxis antifúngica contra Candida spp. Es importante tener en cuenta las
interacciones entre la quimioterapia administrada y los antifúngicos empleados.
Infecciones por Candida spp: se recomienda profilaxis con fluconazol en pacientes
neutropénicos de alto riesgo. Las candidiasis invasivas son raras en pacientes neutropénicos de
bajo riesgo, por lo que no se recomienda su uso de forma rutinaria.
Infecciones por Aspergillus spp: la profilaxis con posaconazol ha demostrado ser superior frente
a fluconazol e itraconazol en la prevención de infección fúngica invasiva, y significativamente
mejor en la prevención de aspergilosis pulmonar invasiva. Se aconseja profilaxis con
posaconazol en pacientes con neutropenia febril de alto riesgo (leucemia mieloide aguda y
trasplante alogénico de precursores hematopoyéticos).
4.3. Profilaxis antivírica
Se recomienda en pacientes neutropénicos con riesgo intermedio y alto y en aquellos con episodios previos
de infección por virus herpes simple (VHS), aunque su riesgo sea bajo. El agente sugerido es aciclovir (400
mg/12 h).
5. TRATAMIENTO
Debe basarse en la estratificación de riesgo del paciente, en el foco clínico infeccioso más probable,
en el uso previo de antibióticos, en los aislamientos microbiológicos anteriores, en las alergias del paciente
y en el patrón de resistencias del centro hospitalario.
5.1. Pacientes de bajo riesgo
Es posible seguir tratamiento ambulatorio si se cumplieran criterios clínicos y sociales (apoyo
familiar, acceso al hospital en menos de una hora…).
No se recomienda tratamiento oral en pacientes que recibían profilaxis con fluoroquinolonas.
La administración de la primera dosis de antibiótico (oral o endovenosa) ha de ser en el
hospital. El paciente ha de quedar bajo observación durante 12-24 horas.
Pautas:
Ciprofloxacino (750 mg/ 12 h, oral) + amoxicilina/clavulánico (875/125 mg/8 h, oral), es
la pauta más estudiada.
Moxifloxacino (400 mg/24 h, oral).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [743]
[47] INFECCIONES EN EL PACIENTE INMUNODEPRIMIDO. NEUTROPENIA FEBRIL
Ante alergia a penicilinas: ciprofloxacino (750 mg/12 h, oral) + clindamicina (600 mg/8
h, oral).
Seguimiento estrecho tras el alta (diario durante las primeras 72 horas).
Se ingresará al paciente y se instaurará tratamiento como si fuera de alto riesgo ante
persistencia o reaparición de la fiebre a los 3-5 días del inicio del tratamiento, cultivos positivos,
intolerancia oral, deterioro clínico…
5.2. Pacientes de alto riesgo
Se les ingresa para tratamiento hospitalario.
Monoterapia con antibiótico antipseudomónico:
Meropenem (1 g/8 h, intravenoso) o imipenem/cilastina (500 mg/6 h, intravenoso):
opción más usada en nuestro medio.
Piperacilina/tazobactam (4,5 g/6-8 h, intravenoso).
Cefepima (2 g/8 h, intravenoso): un metaanálisis asoció su uso a mayor mortalidad en
comparación con los otros dos betalactámicos mencionados. La Food Drug
Administration (FDA) lo sigue considerando un fármaco de primera elección.
Ceftazidima (2 g/8 h, intravenoso): de utilidad más limitada por carecer de actividad
frente a grampositivos y gramnegativos resistentes. Hay menor evidencia clínica para
su uso que con las otras tres opciones.
No se recomienda la combinación con aminoglucósidos de forma rutinaria, aunque
puede ser una opción válida en función de las resistencias existentes.
Solo se recomienda cobertura empírica inicial contra cocos grampositivos (vancomicina 15-20
mg/kg de peso/12 h, intravenoso) si existiera sospecha de infección asociada a catéter o de piel
y partes blandas, y también ante pacientes hemodinámicamente inestables o ante el
crecimiento de cocos grampositivos en hemocultivos (hasta su identificación definitiva). Hay
que replantear su indicación a los 2-3 días de su inicio empírico en caso de ausencia de
documentación microbiológica.
Linezolid (600 mg/12 h, oral) y daptomicina deberían limitarse a situaciones específicas
que incluyan infecciones causadas por microorganismos resistentes a vancomicina
(enterococos) o a pacientes en los que la vancomicina sea peor opción (endocarditis
y/o bacteriemia complicada por Staphylococcus aureus oxacilín-resistente [SAOR)].
Es necesario ampliar la cobertura antibiótica en función de los aislamientos previos y del perfil
de resistencias (vancomicina ante SAOR, carbapenémico ante bacilos gramnegativos con
betalactamasas de espectro extendido [BLEE], carbapenémicos en perfusión extendida
asociados a colistina y/o aminoglucósidos ante gramnegativos productores de
carbapenemasas). Puede usarse tigeciclina, pero nunca en monoterapia.
Ante alergia a betalactámicos, usar aminoglucósido, aztreonam y vancomicina ± tigeciclina.
Ante estos pacientes debe insistirse, aun así, en la desensibilización a betalactámicos dada la
gravedad de la situación clínica.
Hay que valorar el inicio de tratamiento antifúngico (azol, equinocandina o anfotericina B
liposomal) si persistiera la fiebre al cuarto día del inicio de la cobertura antibiótica,
especialmente en pacientes que no han recibido profilaxis antifúngica.
El tratamiento antibiótico empírico inicial en el paciente neutropénico febril con datos de
inestabilidad hemodinámica debería incluir:
Antipseudomónico + vancomicina + aminoglucósido + fluconazol/equinocandina (si no
estuviera bajo profilaxis antifúngica).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [744]
[47] INFECCIONES EN EL PACIENTE INMUNODEPRIMIDO. NEUTROPENIA FEBRIL
La Tabla IV recoge las modificaciones de la cobertura antibiótica en función del foco clínico.
Tabla IV. Cobertura antibiótica según el foco clínico.
III. INFECCIONES EN EL PACIENTE TRASPLANTADO
1. TRASPLANTE DE ÓRGANO SÓLIDO
El desarrollo de las terapias inmunosupresoras ha disminuido la incidencia de rechazo en el
trasplante de órgano sólido pero también ha aumentado la susceptibilidad de los trasplantados a
desarrollar infecciones oportunistas y neoplasias. El perfil de infecciones oportunistas adquiridas también
ha cambiado gracias al desarrollo de profilaxis eficaz frente a agentes como Pneumocystis jirovecii o
citomegalovirus (CMV).
El riesgo de infección tras el trasplante cambia con el paso del tiempo y depende de factores
epidemiológicos (infecciones derivadas del donante, infecciones derivadas del receptor, infecciones
nosocomiales y adquiridas en la comunidad) y del tratamiento inmunosupresor.
La gran mayoría de las infecciones aparecerán en los primeros seis meses posteriores al trasplante,
siendo consecuencia en su mayoría del propio acto quirúrgico y del uso de una potente terapia
inmunosupresora en el postrasplante inmediato. Se distinguen tres subperiodos:
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [745]
[47] INFECCIONES EN EL PACIENTE INMUNODEPRIMIDO. NEUTROPENIA FEBRIL
1.1. Primer mes postrasplante
Aúna tres grandes grupos de infecciones:
Infecciones derivadas del receptor: aquellas presentes en el receptor en el momento del
trasplante, que aparecen o empeoran con el inicio de la terapia inmunosupresora. Incluyen
aquellas infecciones nosocomiales que han tenido riesgo de contraer los pacientes con un
ingreso prolongado antes del trasplante (Pseudomonas aeruginosa, enterococo resistente a
vancomicina, Aspergillus spp…).
Infecciones derivadas del donante: es fundamental un adecuado cribaje del donante para
evitarlas. Ejemplos: bacterianas, CMV, VHS, VIH, tuberculosis, leishmaniasis, enfermedad de
Chagas…
Infecciones relacionadas con el acto quirúrgico y el postoperatorio: generalmente producidas
por bacterias nosocomiales (S. aureus, enterobacterias, P. aeruginosa…). Se pueden
subclasificar en infecciones directamente relacionadas con la cirugía y el postoperatorio
(infecciones de la herida, de las anastomosis, asociadas a catéter, urinarias, neumonías…) y las
que se relacionan con problemas que afectan al injerto (colangitis, absceso hepático,
traqueobronquitis…).
En este periodo tiene lugar la máxima incidencia de infección por Candida spp (generalmente no
suele ser C. albicans).
1.2. Del segundo al sexto mes postrasplante
Las infecciones de este periodo suelen deberse a una inmunosupresión máxima y se producen por
microorganismos oportunistas. El perfil de las infecciones que aparezcan dependerá de la profilaxis
recibida.
Infecciones virales latentes reactivadas o transmitidas a través del injerto: CMV, VHB, VHC, VVZ,
VEB.
Infecciones por microorganismos intracelulares: Mycobacterium tuberculosis, Listeria
monocytogenes, Toxoplasma gondii, Leishmania spp.
Infecciones tardías del injerto: generalmente relacionadas con problemas técnicos de las
anastomosis no resueltos. Por ejemplo, colangitis agudas de repetición (en el trasplante
hepático), pielonefritis agudas (en el trasplante renal).
1.3. Del sexto mes en adelante
El riesgo de infección disminuye mucho a partir de los seis meses postrasplante. No obstante, los
receptores de órgano sólido tienen siempre un riesgo mayor de padecer infecciones por microorganismos
de la comunidad (virus respiratorios, neumococo…) que la población general. Las infecciones crónicas
virales (CMV, VHB, VHC, VEB, VIH) pueden causar daño del injerto en algunos pacientes (por ejemplo,
cirrosis por VHC en receptores de trasplante hepático, daño vascular acelerado por CMV en receptores de
trasplante cardiaco) y aumentar el riesgo de desarrollo de neoplasias (síndromes linfoproliferativos,
cánceres de piel y anogenital…). Un pequeño porcentaje de trasplantados, especialmente aquellos con
mayores requerimientos de inmunosupresión, seguirán teniendo un riesgo elevado de infecciones
oportunistas (Mycobacterium tuberculosis, Pneumocystis jirovecii, Cryptococcus neoformans…).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [746]
[47] INFECCIONES EN EL PACIENTE INMUNODEPRIMIDO. NEUTROPENIA FEBRIL
2. TRASPLANTE DE PROGENITORES HEMATOPOYÉTICOS (TPH) (TABLA V)
Tabla V. Trasplante de progenitores hematopoyéticos.
2.1. Tipos de TPH
Autólogo: células obtenidas del propio paciente.
Alogénico: células obtenidas de un donante sano.
Hermano HLA idéntico.
Hermano gemelo univitelino (TPH singénico).
Otro familiar parcialmente compatible.
No emparentado (donante altruista).
2.2. Fuentes de los progenitores hematopoyéticos
Médula ósea (requiere anestesia general o epidural).
Sangre periférica (ahora, más extendida).
Sangre de cordón umbilical (limitada por la escasa celularidad que obtiene).
2.3. Fases del TPH e infecciones más frecuentes en el paciente trasplantado
Acondicionamiento (de mayor o menor intensidad en función de las características del paciente
y de la enfermedad).
Mieloablativo: dosis altas de quimioterapia ± radioterapia con la finalidad de eliminar
toda la celularidad neoplásica y no del paciente, creando espacio medular para los
nuevos progenitores hematopoyéticos. Inmunosupresión para evitar el rechazo.
Intensidad reducida: potentes inmunosupresores para facilitar el implante y progresiva
sustitución de la hematopoyesis del paciente por la del donante.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [747]
[47] INFECCIONES EN EL PACIENTE INMUNODEPRIMIDO. NEUTROPENIA FEBRIL
Fase preinjerto: desde el día de infusión de células hematopoyéticas (día 0) hasta
aproximadamente el día +30, en el que se resuelve la aplasia medular.
Fase postinjerto: progresiva recuperación de cifras de neutrófilos.
Fase tardía: periodo de reconstitución inmune.
A lo largo de las distintas fases hay que administrar las siguientes profilaxis:
Antibacteriana: ciprofloxacino 500 mg/12 horas.
Antifúngica: fluconazol 200-400 mg/24 horas en el trasplante autólogo durante la neutropenia
si hubiera mucositis, y en el trasplante alogénico durante la neutropenia y hasta al menos 75
días después del trasplante. Considerar posaconazol ante enfermedad injerto contra huésped
(EICH).
Antivírica: aciclovir 800 mg cada 12 horas.
Ante infección por VHS, prolongarla en función del riesgo.
Ante infección por VVZ, considerar mantenerla al menos un año después del trasplante
alogénico y entre medio y un año después del autólogo.
Ante infección por CMV en trasplante alogénico hay que monitorizar la infección
mediante determinación de PCR de CMV hasta 1 mes postrasplante o hasta la retirada
de la inmunosupresión.
Contra Pneumocystis jirovecii: trimetoprim/sulfametoxazol 160/800 mg, tres veces por semana
(lunes, miércoles y viernes). Mantenerlo 3-6 meses después de trasplante autólogo.
Mantenerlo durante al menos 6 meses tras trasplante alogénico y mientras dure el tratamiento
para evitar enfermedad injerto contra huésped.
3. ENTIDADES CLÍNICAS RELEVANTES EN EL PACIENTE TRASPLANTADO
3.1. Enfermedad por citomegalovirus (CMV)
La infección por citomegalovirus (CMV) es la complicación infecciosa más frecuente en el paciente receptor
de órgano sólido. El CMV es responsable de “efectos directos” (síndrome viral, hepatitis, colitis,
neumonitis…) y de “efectos indirectos” (rechazo, disfunción del injerto, desarrollo de otras infecciones…). El
CMV humano infecta en torno al 30-80% de la población de nuestro medio. Tras la primoinfección, se
adquiere el estado de infección latente debido al control que ejerce la inmunidad. Es fundamental conocer
los test diagnósticos apropiados para el manejo de la infección y enfermedad por el CMV en pacientes
inmunocomprometidos. Disponemos de las siguientes herramientas diagnósticas:
Serología: detecta anticuerpos IgM e IgG frente al CMV, lo que permite diferenciar entre
infección aguda y crónica. Solo es útil para determinar el riesgo de adquisición de infección por
el CMV en el receptor de órgano sólido procedente del donante.
Carga viral: cuantificada mediante reacción en cadena de la polimerasa (PCR). Permite
diagnosticar enfermedad activa, monitorizar pacientes con riesgo de enfermedad por el CMV y
monitorizar la respuesta al tratamiento.
Antigenemia: permite la detección rápida y directa de proteínas del CMV (pp65) en leucocitos
de sangre periférica. Pierde sensibilidad cuando el recuento de neutrófilos es menor de 1.000
células/mm3. La afectación del sistema nervioso central (incluyendo coriorretinitis) y
gastrointestinal (colitis, gastritis…) por CMV suele cursar con antigenemia negativa.
Otras: examen histológico de muestras, cultivo…
Las estrategias para prevenir la infección por CMV en el receptor de órgano sólido son dos:
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [748]
[47] INFECCIONES EN EL PACIENTE INMUNODEPRIMIDO. NEUTROPENIA FEBRIL
Profilaxis universal con valganciclovir oral: se prefiere en pacientes con alto riesgo de padecer
enfermedad por CMV (receptores de trasplante de pulmón e intestino, receptores
seronegativos frente al CMV que reciben un órgano procedente de un donante seropositivo,
pacientes bajo terapias que incluyan agentes deplectores de linfocitos). La duración de la
profilaxis que se recomienda es de 6-12 meses para trasplantes de intestino y pulmón y de 3-6
meses para la situación donante positivo/receptor negativo para trasplantes de riñón, corazón
e hígado.
Estrategia de tratamiento anticipado: indicada en el resto de pacientes (receptores
seropositivos para CMV sin otros factores adicionales). En este grupo se recomienda
monitorizar la carga viral con PCR y tratar cualquier valor positivo durante 14-21 días con la
intención de anticiparse a la aparición de la enfermedad.
En la enfermedad por CMV se recomienda ganciclovir intravenoso o valganciclovir como primera
línea de tratamiento. Se prefiere valganciclovir, salvo en casos graves o en aquellos en los que no pueda
usarse la vía oral. Una estrategia alternativa de tratamiento sería una terapia secuencial, comenzando con
ganciclovir intravenoso y posteriormente con valganciclovir oral. Se debería sospechar resistencia a
ganciclovir ante la persistencia o incremento de la carga viral o la progresión clínica de la enfermedad tras
tres semanas de tratamiento adecuado. Foscarnet sería una terapia empírica alternativa de tratamiento si
se sospechara resistencia a ganciclovir (hay que tener en cuenta su nefrotoxicidad).
3.2. Infecciones pulmonares
Son una de las complicaciones infecciosas más graves en el paciente trasplantado. Se indica la realización
precoz de TC torácico y de broncoscopia ante la sospecha clínica de infección pulmonar. Además, deben
llevarse a cabo las siguientes pruebas: hemocultivos, antigenuria de Legionella en orina, test rápido y
cultivo de virus respiratorios en momentos de epidemia (virus Influenza A, B y VRS), antigenemia del CMV,
Mantoux, galactomanano en suero y, siempre que sea posible, broncoscopia con lavado broncoalveolar
para tinción de Gram, cultivo de bacterias, BAAR y cultivo de micobacterias, tinción y/o PCR para P. jirovecii,
cultivo de hongos y galactomanano.
Debe iniciarse un tratamiento antimicrobiano empírico precoz en función de los factores de riesgo
individuales. Han de usarse, sobre todo en los primeros meses tras el trasplante, fármacos que cubran P.
aeruginosa (carbapenémico + fluoroquinolona). El tratamiento empírico cubrirá otras posibilidades en
función de las características clínicas y radiológicas: vancomicina o linezolid ante riesgo de neumonía por
SAOR; cotrimoxazol intravenoso ante riesgo de infección por P. jirovecii; ganciclovir ante la posibilidad de
neumonitis por CMV; oseltamivir ante posibilidad de infección por virus Influenza.
Hay que recordar también la posibilidad de que el cuadro de fiebre e infiltrados pulmonares no sea
de etiología infecciosa (por ejemplo, en casos de toxicidad pulmonar por fármacos inmunosupresores
[sirolimus, everolimus, micofenolato]).
3.3. Infecciones del sistema nervioso central
En el paciente inmunodeprimido se iniciará antibiótico intravenoso de amplio espectro con meropenem (2
g/8 h), vancomicina (15-20 mg/kg de peso/12 h) y ampicilina (2 g/4 h, ante la posibilidad de infección por
Listeria monocytogenes). En función del curso clínico y de las características del LCR se asociarán
tratamiento antituberculoso o aciclovir (ante sospecha de meningoencefalitis herpética) o antifúngicos
(ante sospecha de infección por Cryptococcus spp o Aspergillus spp).
El manejo de estas infecciones se desarrolla más ampliamente en el Capítulo 42. “Infecciones del
sistema nervioso central”.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [749]
[47] INFECCIONES EN EL PACIENTE INMUNODEPRIMIDO. NEUTROPENIA FEBRIL
3.4. Infecciones gastrointestinales
Se solicitará coprocultivo (Salmonella, Campylobacter…), determinación de toxina del C. difficile y carga
viral de CMV en pacientes trasplantados que sufran diarrea. La carga viral del CMV puede ser negativa
incluso ante sospecha de colitis por CMV. En estos casos se recomienda solicitar una colonoscopia con
toma de biopsias sobre las que se realice PCR y cultivo para virus. En casos de dolor abdominal y sospecha
de infección intraabdominal se valorará llevar a cabo una prueba de imagen (ecografía, TC…).
3.5. Infecciones urinarias
Dentro de este grupo destacan las pielonefritis agudas en pacientes con trasplante renal. Hay que descartar
alteraciones anatómicas de la vía urinaria en caso de pielonefritis agudas de repetición en estos pacientes.
Se ha identificado al virus BK (Polyomavirus) asociado a nefropatía y obstrucción ureteral en receptores de
trasplante renal, por lo que su monitorización es muy recomendable en ellos. Por el momento no se
dispone de un tratamiento antiviral efectivo y solo se recomienda disminuir el tratamiento inmunosupresor
ante su detección.
BIBLIOGRAFÍA
Carreras i Pons E. Manual de Trasplante Hemopoyético. Collbató: Antares. 4ª ed.
Fishman J.A. Infection in Solid-organ Transplant Recipients. New England Journal of Medicine.
2007;357:2601-14.
Freifeld AG, Bow EJ, Sepkowitz KA, et al. Clinical practice guideline for the use of antimicrobial agents
en neutropenic patients with cancer: 2010 uptade by The Infecious Diseases Society of America. Clin
Infect Dis. 2011;52:e56-93.
Lumbreras C, Manuel O, Len O, Berge I, Sgarabotto D, Hirsc HH. Study group of Infection in
Compromised Hosts. Cytomegalovirus. Infection in solid organ transplant recipients. Clin Microbio
Infect. 2014;20(Suppl 7):19-26.
Maschmeyer G, Carratalà J, Buchheidt D, Hamprecht A, Heussel CP, Kahl C, et al. Diagnosis and
antimicrobial therapy of lung infiltrates in febrile neutropenic patients (allogeneic SCT excluded):
updated guidelines of the Infectious Diseases Working Party (AGIHO) of the German Society of
Haematology and Medical Oncology (DGHO). Ann Oncol. 2015;26(1):21-33.
National Comprehensive Cancer Network Guidelines Version 2.2015. Prevention and Treatment of
Cancerrelated Infections.
Origüen Sabater J, Gil Niño J. Infecciones en el paciente inmunodeprimido. En: Aguilar Rodríguez F,
Bisbal Pardo O, Gómez Cuervo C, et al., editores. Manual de Diagnóstico y Terapéutica Médica. Hospital
Universitario 12 de Octubre. 7ª ed. Madrid: MSD; 2012. p. 607-17.
Villafuerte-Gutiérrez P, Villalón L, Losa J, Henríquez-Camacho C. Treatment of febrile neutropenia and
prophylaxis in hematologic malignancies: a critical review and Update. Advances in Hematology. 2014.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [750]
[48] INFECCIONES NOSOCOMIALES
48.Infecciones nosocomiales
Laura Corbella Vázquez.
Medicina Interna
Francisco Trapiello Valbuena.
Medicina Interna
Asesor: Mario Fernández Ruiz. Médico Adjunto de Medicina Interna. Unidad de Enfermedades Infecciosas
I. INFECCIÓN DEL TRACTO URINARIO
1. EPIDEMIOLOGÍA Y FACTORES DE RIESGO
La infección del tracto urinario (ITU) es una de las más prevalentes en el medio hospitalario y
supone cerca del 20% del total de infecciones nosocomiales. Su mortalidad atribuible es baja pero su
principal complicación asociada, la bacteriemia secundaria, aparece en el 5% de los casos (hasta el 15% de
las bacteriemias nosocomiales tienen su origen en el tracto urinario). Además, constituye una causa
frecuente de prescripción inapropiada de antibióticos. El principal factor de riesgo para su adquisición es la
presencia de sondaje vesical (SV), identificable en más del 95% de las ITU nosocomiales. La incidencia de
bacteriuria por cada día de SV oscila entre el 3 y el 8%, de forma que a las dos semanas está presente en el
50% de los pacientes y al cabo de 30 días esta prevalencia alcanza el 100%.
A consecuencia de los cambios acontecidos en el Sistema de Salud en los últimos años, el paciente
portador de SV ya no es exclusivo del medio hospitalario. Por ello, sujetos institucionalizados o
ambulatorios con SV de larga evolución pueden presentar cuadros similares a la ITU nosocomial. Esta
circunstancia ha motivado la introducción del término más genérico de ITU asociada al cuidado sanitario.
Otros factores de riesgo para su desarrollo son el sexo femenino, la edad avanzada, el deterioro de la
función renal, el uso de sistemas colectores abiertos, la presencia de diabetes mellitus, malformaciones
urológicas, la colonización previa del meato uretral y disfunciones esfinterianas de naturaleza neurológica.
De forma análoga a la ITU comunitaria, Escherichia coli es el microorganismo identificado con más
frecuencia, si bien su importancia relativa es menor en las formas nosocomiales. También destacan Proteus
spp y otros bacilos gramnegativos (BGN) entéricos, Pseudomonas aeruginosa, Enterococcus spp y Candida
spp. La mayor parte de las bacteriurias asociadas al SV de corta duración (menos de un mes) son
monomicrobianas (BGN y enterococos). Por el contrario, en el 75% de las ITU asociadas a SV prolongados
puede aislarse la flora polimicrobiana que procede de la microbiota fecal y cutánea del propio paciente,
entre la que figuran patógenos más infrecuentes como Providencia spp y Morganella morganii. Otra
diferencia respecto a la ITU comunitaria reside en el perfil de resistencia a antibióticos.
Entre las cepas de E. coli aisladas en nuestro centro a lo largo del año 2014 las tasas de resistencia
fueron del 20% para amoxicilina/ácido clavulánico, del 30% para fluoroquinolonas y de alrededor del 10%
para cefalosporinas de 3ª generación debido a la expresión de β-lactamasas de espectro extendido (BLEE)
(Tabla I). Esta tendencia es aún más relevante para K. pneumoniae, pues hasta el 40% de los aislamientos
en casos de bacteriemia fueron resistentes a las cefalosporinas de 3ª generación. Por otra parte,
aproximadamente la tercera parte de los aislamientos de P. aeruginosa mostraron resistencia a
carbapenémicos y empiezan a identificarse con frecuencia creciente cepas extremadamente resistentes
(solo sensibles a colistina). Por último, parte de estos microorganismos tienen capacidad productora de
biofilms en superficies artificiales como la sonda vesical, por lo que la retirada de este dispositivo puede
resultar imprescindible para el tratamiento de la ITU nosocomial.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [751]
[48] INFECCIONES NOSOCOMIALES
Tabla I. Factores predictores de aislamiento de enterobacterias productoras de BLEE en pacientes con infección del tracto urinario
asociada a sondaje vesical.
2. DIAGNÓSTICO
De forma convencional la bacteriuria (o candiduria) significativa queda definida por la presencia de
más de 105 unidades formadoras de colonias (UFC) por ml, si bien recuentos menores (103 UFC/ml) en
portadores de SV pueden considerarse significativos siempre que se aíslen en cultivo puro.
Idealmente la muestra debería obtenerse a través de una sonda colocada recientemente (habría
que evitar procesar las muestras recogidas directamente de la bolsa colectora). Menos de la tercera parte
de los pacientes con bacteriuria asociada a SV tienen algún tipo de sintomatología. Para evitar la
administración innecesaria de tratamiento antibiótico y la emergencia de resistencias, es fundamental
diferenciar la simple colonización (bacteriuria asintomática) de la verdadera infección, solicitando estudios
diagnósticos en virtud de la sospecha clínica y no de forma rutinaria. Sin embargo, la expresión clínica de la
ITU en el portador de SV puede ser atípica e inespecífica, particularmente en el anciano frágil con
comorbilidad, circunstancia que obliga a mantener un índice de sospecha elevado y a excluir causas
alternativas (Tabla II).
El síndrome miccional (disuria, polaquiuria o urgencia), la fiebre o la leucocitosis tienen escaso valor
en el paciente con SV, así como la presencia aislada de piuria, sedimento patológico, alteraciones en el olor
o turbidez de la orina. No obstante, la ausencia de piuria en un paciente con fiebre y bacteriuria asociada a
SV sugiere que la ITU probablemente no sea causante de la sintomatología.
Tabla II. Espectro de presentación clínica de la infección del tracto urinario nosocomial.
3. TRATAMIENTO
No existe indicación para la detección ni el tratamiento de la bacteriuria asintomática asociada al
SV. Se maneja mediante la retirada o el recambio de la sonda. Las situaciones que justifican el tratamiento
son la gestación y la manipulación urológica inminente (sobre todo, si se prevé sangrado de mucosas).
Otras indicaciones de tratamiento, aunque con menor grado de evidencia, son las anomalías anatómicas de
la vía urinaria (uropatía obstructiva, catéter ureteral o nefrostomía) y la inmunodepresión grave. Se
recomienda igualmente el tratamiento de las bacteriurias persistentes tras la retirada de la sonda, así como
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [752]
[48] INFECCIONES NOSOCOMIALES
las originadas por bacterias productoras de ureasa (Corynebacterium urealyticum, Proteus spp) y por cepas
con elevada incidencia de bacteriemia (Serratia marcescens). En estas circunstancias el tratamiento debe
estar dirigido por el antibiograma.
Ante la sospecha clínica de ITU nosocomial (particularmente en presencia de signos sugerentes de
bacteriemia o sepsis) se tendrá que iniciar tratamiento empírico antes de obtener el resultado
microbiológico. Para ello es conveniente considerar los aislamientos previos del paciente, la ecología propia
del centro y la presencia de factores de riesgo específicos para microorganismos resistentes (ver Tabla I).
Entre las pautas más apropiadas en nuestro medio figuran las cefalosporinas de 3ª generación, las
penicilinas con actividad antipseudomónica (piperacilina/tazobactam) y los carbapenémicos.
Cabe destacar que antibióticos como daptomicina, moxifloxacino y tigeciclina son de reducida
utilidad para el tratamiento de la ITU nosocomial dada su escasa eliminación en orina. El resultado del
urocultivo estará disponible en 24-48 horas, permitiendo el ajuste del régimen en función de los hallazgos
(Tabla III). La duración óptima del tratamiento antibiótico en la ITU nosocomial no está bien establecida; las
pautas de 7 días parecen adecuadas en la mayor parte de los casos. Las pautas más largas (10-14 días) se
reservan en caso de mala evolución inicial o en presencia de anomalías anatómicas de la vía urinaria.
Tabla III. Actuación ante una infección del tracto urinario grave (sospecha de sepsis) asociada a sondaje vesical.
4. PREVENCIÓN
Las medidas con mayor impacto sobre la incidencia de ITU nosocomial pasan por reducir tanto la
realización de SV (limitándolo a las indicaciones bien establecidas que recoge la tabla IV) como su duración
(reevaluando de forma diaria su necesidad y retirando la sonda de forma precoz). Entre las alternativas al
SV para reducir la bacteriuria figuran el uso de sistemas de recolección externa (“condones”), el sondaje
intermitente y los dispositivos de drenaje a nivel suprapúbico.
Para la realización del sondaje es preciso mantener condiciones asépticas durante todo el
procedimiento, utilizando material estéril. Se recomienda seleccionar sondas del menor calibre posible y
preferiblemente de silicona, ya que han demostrado ser más resistentes a la formación de biofilms que las
de látex, además de obstruirse con menos frecuencia. El sistema de drenaje debe permanecer cerrado, y la
bolsa de recolección ha de mantenerse en todo momento por debajo del plano de la vejiga del paciente
(para evitar el reflujo de orina almacenada).
El uso de sondas recubiertas de antibiótico o de plata, la profilaxis con derivados del arándano o
con sales de metenamina, la irrigación del catéter con antibióticos y las estrategias de recambio rutinario
no han demostrado eficacia en la reducción a largo plazo de la incidencia de ITU nosocomial. Por último, el
uso de profilaxis antibiótica antes o durante el sondaje, así como en el momento de su recambio o retirada,
tampoco ha demostrado reducir de forma significativa el riesgo de infección, pero sí incrementar las tasas
de resistencia bacteriana, por lo que no puede recomendarse de forma sistemática.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [753]
[48] INFECCIONES NOSOCOMIALES
Tabla IV. Principales indicaciones para el sondaje vesical.
II. INFECCIÓN ASOCIADA AL CATÉTER INTRAVASCULAR
1. EPIDEMIOLOGÍA Y CONCEPTO
La mayor parte de los pacientes hospitalizados son sometidos a algún tipo de cateterización
intravenosa a lo largo de su ingreso. La infección asociada al catéter (IAC) constituye una de las principales
complicaciones de estos procedimientos y representa una causa relevante de morbimortalidad e
incremento de la duración del ingreso y sus costes. La mayoría de los estudios epidemiológicos realizados
en nuestro medio se limitan a pacientes ingresados en Unidades de Cuidados Intensivos (UCI), con una
incidencia global de 2,93 episodios por cada 1.000 días de inserción de catéter venoso central (CVC). No
obstante, la IAC también se presenta con frecuencia en plantas de hospitalización convencional. En nuestro
centro el 40% de las bacteriemias de adquisición nosocomial detectadas a lo largo de los años 2013 y 2014
estuvieron relacionadas con los catéteres intravasculares. La mortalidad atribuible a la IAC oscila entre el 3
y el 25%, en función de la virulencia del microorganismo implicado (mayor en el caso de Staphylococcus
aureus), de la gravedad de la enfermedad de base y del tipo de abordaje terapéutico.
Hay varios conceptos diferentes en relación con la IAC:
Colonización del catéter intravascular: crecimiento significativo de un microorganismo (cultivo
cuantitativo o semicuantitativo) en la punta del catéter, el segmento subcutáneo o la luz, en
ausencia de signos de infección sistémica (sepsis) o de infección local en el punto de inserción.
Infección del punto de inserción: documentada desde un punto de vista clínico (presencia de
signos locales en el punto de entrada del catéter: eritema, induración, calor o exudado
purulento) o microbiológico (si además existiera un cultivo positivo en una muestra obtenida
del punto de inserción, en ausencia de bacteriemia concomitante).
Bacteriemia (o fungemia) relacionada con el catéter intravascular (diagnóstico tras su retirada):
aislamiento del mismo microorganismo (iguales especie y antibiograma) en el hemocultivo
obtenido por venopunción periférica y en el cultivo (cuantitativo o semicuantitativo) de la
punta del catéter, en un paciente con cuadro clínico de sepsis y ausencia de un foco alternativo
de infección.
Bacteriemia (o fungemia) relacionada con el catéter intravascular (sin retirada del catéter):
cuadro clínico de sepsis, en ausencia de un foco alternativo de infección, en el que se aísla el
mismo microorganismo (iguales especie y antibiograma) en hemocultivos simultáneos
cuantitativos obtenidos a través del catéter y mediante venopunción periférica en una
proporción igual o superior a 5:1, o bien con diferencia horaria significativa en los hemocultivos
diferenciales.
Bacteriemia (o fungemia) probablemente relacionada con el catéter intravascular (sin cultivo
del catéter): cuadro clínico de sepsis, en ausencia de un foco alternativo de infección, con
positividad del hemocultivo y en el que se documenta la desaparición de la sintomatología en
las primeras 48 horas desde la retirada del catéter.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [754]
[48] INFECCIONES NOSOCOMIALES
Bacteriemia (o fungemia) relacionada con los líquidos de infusión: cuadro clínico de sepsis, en
ausencia de un foco alternativo de infección, con aislamiento del mismo microorganismo
(iguales especie y antibiograma) en el líquido de infusión y en los hemocultivos obtenidos por
venopunción periférica.
2. ETIOLOGÍA Y PATOGENIA
La mayor parte de las IAC son de naturaleza estafilocócica (más del 60%). Los estafilococos
coagulasa-negativos (ECN), particularmente S. epidermidis, son los microorganismos más frecuentes gracias
a su gran capacidad de adherencia y colonización de las superficies plásticas y a sus escasos requerimientos
nutricionales. En nuestro centro la resistencia a meticilina en aislamientos de ECN alcanzó el 83% en el año
2014. Entre los cocos grampositivos destacan igualmente S. aureus (con un 25% de cepas resistentes a
meticilina) y Enterococcus spp (con un 1,5% de cepas resistentes a vancomicina). La incidencia de BGN
(como E. coli, Klebsiella spp o Serratia spp) es mayor entre los portadores de CVC permanentes y en los
insertados por vía femoral. Además, estos microorganismos constituyen una causa relevante de
bacteriemia relacionada con el líquido de infusión (Enterobacter spp, Burkholderia cepacia complex o
Citrobacter freundii). El aislamiento de Candida albicans y Candida parapsilosis es frecuente, sobre todo, en
pacientes con nutrición parenteral total.
Tabla V. Factores de riesgo para el desarrollo de infección asociada a catéter.
Tabla VI. Catéteres intravasculares más utilizados.
En la patogenia de la IAC se reconocen tres mecanismos posibles:
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [755]
[48] INFECCIONES NOSOCOMIALES
Colonización extraluminal del catéter desde el punto de inserción por la flora cutánea: es el
mecanismo predominante en los catéteres insertados hace menos de 14 días. Su incidencia se
puede reducir aplicando medidas de asepsia estricta durante su colocación y mantenimiento.
Colonización endoluminal del catéter a partir de las conexiones o de la infusión de líquidos
contaminados (este último mecanismo es más infrecuente). Supone la vía de infección más
descrita en los catéteres de larga duración (más de 14 días), ya sean tunelizados o no.
Siembra hematógena de la punta del catéter desde un foco séptico a distancia. La incidencia de
IAC depende de factores relacionados con el huésped y el dispositivo implantado (Tabla V y VI).
3. DIAGNÓSTICO
Los hallazgos clínicos tienen escasa relevancia a la hora de establecer el diagnóstico de IAC. Los
signos locales de infección en el punto de entrada del catéter, su trayecto subcutáneo o el reservorio (en
dispositivos totalmente implantados) tienen una elevada especificidad, si bien aparecen en menos del 5%
de los casos. Por otra parte, el signo más sensible de infección sistémica (fiebre sin focalidad aparente) es
muy poco específico. Por ello el diagnóstico siempre se fundamenta en los hallazgos microbiológicos. Ante
la sospecha de IAC, y de forma previa al inicio de la antibioterapia, se deben extraer dos o tres
hemocultivos seriados, de los que al menos uno de ellos debe ser obtenido mediante punción directa de
una vena periférica y el resto a través del catéter. En presencia de un catéter con varias luces se deberían
obtener idealmente muestras a través de cada una de ellas. Si esto no fuera posible, sería preferible
emplear la luz distal.
Como principio general, el diagnóstico de IAC es muy improbable en caso de resultado negativo de
los hemocultivos extraídos a través del catéter (elevado valor predictivo negativo). Si el plan terapéutico
inicial incluye la conservación del dispositivo, se puede recurrir a la toma de muestras (mediante frotis) de
la conexión y de la piel que rodea el punto de inserción, ya que su cultivo presenta igualmente un elevado
valor predictivo negativo (próximo al 99%).
Entre las técnicas microbiológicas útiles para el diagnóstico de IAC se encuentran:
Hemocultivos cuantitativos. Se basa en el principio de que la concentración de colonias
bacterianas o fúngicas es mayor en la sangre extraída a través del catéter intravascular (al ser
este el foco primario de infección) con respecto a la obtenida por venopunción periférica. Por
ello, la existencia de una relación 5:1 o superior en el recuento de los cultivos obtenidos de una
y otra forma es considerada diagnóstica.
Hemocultivos diferenciales. En base al mismo principio, el tiempo hasta que los hemocultivos se
hacen positivos en los sistemas automatizados de lectura será menor en la sangre extraída a
través del catéter en caso de que este sea el foco primario de la infección, considerándose
como significativa una diferencia mayor o igual a 2 horas.
La sensibilidad y especificidad de estos dos criterios superan el 80% en relación con el método
diagnóstico de referencia (que implica la retirada y cultivo del catéter).
4. TRATAMIENTO
El abordaje terapéutico de la IAC reposa en tres pilares: manejo del catéter intravascular implicado,
administración de tratamiento antibiótico y diagnóstico y tratamiento de las complicaciones asociadas
(locales o sistémicas). La simple colonización de la punta del catéter intravascular en ausencia de
crecimiento en los hemocultivos extraídos de forma simultánea a su retirada no requiere tratamiento
antibiótico, si bien se debe extremar la vigilancia clínica y, en ciertas situaciones (aislamiento de S. aureus),
proceder a la extracción de nuevos hemocultivos al cabo de unos días.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [756]
[48] INFECCIONES NOSOCOMIALES
4.1. Manejo del catéter
Los catéteres venosos periféricos se deben retirar siempre. En el caso de que el dispositivo implicado sea un
CVC de corta duración (menos de 14 días), tanto de inserción periférica (PICC) como central, se debe
proceder a su retirada precoz y cultivo de la punta en cualquiera de las siguientes circunstancias:
Presencia de sepsis grave o shock séptico.
Signos de infección local en el punto de inserción.
Sospecha de complicaciones locales (tromboflebitis séptica) o a distancia (endocarditis
infecciosa, osteomielitis o embolismos sépticos).
Prótesis valvular u otro dispositivo intravascular (incluyendo marcapasos).
En los demás casos se puede mantener el catéter hasta la confirmación microbiológica de la
infección. Una vez establecido el diagnóstico de IAC siempre se debe retirar el catéter. Solo ante
microorganismos de muy bajo potencial patógeno (ECN, Streptococcus spp, Corynebacterium spp) o
marcada limitación para la canalización de un nuevo acceso venoso, se puede plantear una estrategia de
conservación del catéter, que implica la administración de tratamiento antibiótico sistémico y local
mediante el sellado del catéter.
Una alternativa para intentar salvar el acceso vascular es su recambio sobre guía metálica (técnica
de Seldinger), aceptable cuando la sospecha de la infección sea baja y no esté confirmada de forma
concluyente (por ejemplo, una bacteriemia por un microorganismo típicamente asociado a IAC, pero sin
crecimiento diferencial en los hemocultivos). En este caso se debe cultivar el catéter recambiado. De
confirmarse su infección, es recomendable la retirada definitiva del catéter y la inserción de uno nuevo en
una localización diferente. El recambio sobre guía está contraindicado en presencia de sepsis o signos
locales de infección (ver Figura 1 en Apartado 4.2. “Tratamiento antibiótico empírico”).
En infecciones asociadas a catéteres venosos permanentes (tunelizados o totalmente implantados
con reservorio) hay que individualizar de forma cuidadosa la decisión sobre su retirada, teniendo en cuenta
el estado general del paciente (habitualmente oncológico o en hemodiálisis), las posibilidades de
canalización de nuevos accesos y los riesgos inherentes al propio proceso quirúrgico de retirada. Como se
ha indicado, en esta situación la infección suele ser intraluminal, por lo que una alternativa consiste en el
tratamiento local mediante sellado del catéter con antibiótico. El sellado del catéter tiene por objetivo
alcanzar concentraciones intraluminales del antibiótico que superen entre 100 y 1.000 veces la
concentración mínima inhibitoria (CMI) del microorganismo (Tabla VII). De este modo se pretende un
marcado efecto bactericida a nivel local, minimizando la toxicidad sistémica. La respuesta difiere según el
microorganismo implicado, siendo en general exitosa en infecciones por ECN (con tasas de curación de
hasta el 80%) y mucho menos eficaz en el caso de S. aureus, P. aeruginosa y Candida spp, en los que solo se
recomienda esta estrategia en casos muy excepcionales (estabilidad clínica y dificultad marcada para la
obtención de un acceso alternativo). El sellado ha de mantenerse durante el mayor número de horas
diarias (mínimo de 8 horas diarias).
Como norma general, debe cambiarse la solución al menos cada 48 h; en pacientes ambulatorios
con CVC femorales el cambio ha de realizarse cada 24 h, y después de cada sesión en pacientes en
hemodiálisis periódica. La duración total del tratamiento será de 7-14 días (4 semanas en la infección por S.
aureus). El sellado del catéter no exime de la necesidad de tratamiento antibiótico sistémico para la
bacteriemia, se mantendrá de forma simultánea durante 7-14 días. El sellado antibiótico no tiene sentido
en catéteres temporales ni tampoco en dispositivos con menos de 14 días desde su implantación (ya que en
tales casos la infección suele ser extraluminal).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [757]
[48] INFECCIONES NOSOCOMIALES
Tabla VII. Soluciones empleadas en el sellado antibiótico del catéter intravascular.
4.2. Tratamiento antibiótico empírico
Figura 1. Algoritmo de abordaje diagnóstico y terapéutico inicial de la infección asociada a catéter.
Es necesario considerar varios aspectos tales como la gravedad del cuadro, la epidemiología propia
del centro y los factores de riesgo específicos del paciente para determinados microorganismos. Dada la
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [758]
[48] INFECCIONES NOSOCOMIALES
prevalencia en nuestro hospital de cepas de S. aureus y ECN resistentes a meticilina, toda pauta empírica
deberá incluir la administración de vancomicina (15 mg/kg de peso/8-12 horas durante las primeras 24
horas, con ajuste a partir de la tercera dosis para obtener un nivel valle de 15-20 ng/ml) o daptomicina (6
mg/kg/día). Si existiera una elevada sospecha inicial de S. aureus como causante del cuadro, habría que
considerar añadir al tratamiento empírico cloxacilina (2 g/4 h) por su gran efecto bactericida frente a cepas
sensibles a meticilina, o bien emplear alternativamente daptomicina a dosis elevadas (8-10 mg/kg/día). En
ocasiones puede ser preciso asociar cobertura frente a BGN y valorar también añadir un antifúngico ante la
posibilidad de IAC por Candida spp (Figura 1).
Las equinocandinas (anidulafungina, caspofungina o micafungina) constituyen el antifúngico de
elección, aunque fluconazol puede ser una alternativa válida en pacientes que permanezcan
hemodinámicamente estables y que no hayan tenido exposición a antifúngicos a lo largo de los 3 meses
previos o aislamientos previos de C. glabrata o C. krusei. No está indicada la administración de agentes
trombolíticos como terapia adyuvante de forma rutinaria.
Tabla VIII. Tratamiento antibiótico de la infección asociada al catéter según el microorganismo.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [759]
[48] INFECCIONES NOSOCOMIALES
4.3. Tratamiento antibiótico dirigido
Una vez recibido el resultado de los hemocultivos se podrá ajustar el tratamiento antibiótico inicial (Tabla
VIII). La duración debe ser individualizada en función del microorganismo implicado, la presencia de
factores de riesgo y la velocidad de aclaramiento de la bacteriemia (Tabla IX); se considera como primer día
de tratamiento la fecha a partir de la cual se obtienen los primeros hemocultivos negativos.
Tabla VIII. Tratamiento antibiótico de la infección asociada al catéter según el microorganismo.
La mayor parte de las IAC por ECN no requieren administración de antibiótico una vez retirado el
catéter y en ausencia de factores de riesgo (dispositivos intravasculares), excepto en caso de fiebre o
bacteriemia persistentes (circunstancias que justificarían un ciclo de 5-7 días de tratamiento).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [760]
[48] INFECCIONES NOSOCOMIALES
Una excepción sería la infección por Staphylococcus lugdunensis, cuya capacidad de producir
complicaciones sépticas y endocarditis lo asemejan más a S. aureus que al resto de los ECN. En el caso de S.
aureus la retirada del catéter debe ser la norma (particularmente en los de corta duración), con extracción
de hemocultivos de control en 48-72 horas y realización de un ecocardiograma (que deberá ser
transesofágico en caso de bacteriemia persistente, presencia de dispositivos intravasculares de cualquier
tipo o en pacientes en hemodiálisis crónica). Si la cepa de S. aureus aislada es sensible a meticilina, el
tratamiento empírico inicial debe ser modificado a cloxacilina de forma precoz.
Tabla IX. Duración del tratamiento antibiótico en la infección asociada a catéter.
4.4. Diagnóstico y tratamiento de las complicaciones
La persistencia tanto de bacteriemia o fungemia como de fiebre al cabo de 72 horas de la retirada del
catéter y del inicio del tratamiento obliga a descartar la presencia de complicaciones sépticas locales o a
distancia.
Tromboflebitis séptica: es más frecuente en IAC por S. aureus o Candida spp. Si tiene lugar en
las venas periféricas produce signos inflamatorios locales (calor, eritema, supuración) o
regionales (cordón palpable), mientras que si se asocia a un CVC puede presentarse en forma
de dolor y tumefacción en el cuello y en la extremidad ipsilateral, o bien mediante embolismos
sépticos (de localización pulmonar en la mayor parte de las ocasiones). El diagnóstico se realiza
mediante una ecografía en modo Doppler o una tomografía computarizada (TC) con contraste.
El tratamiento implica la retirada del catéter, la prolongación del tratamiento antibiótico
parenteral durante al menos 4-6 semanas (ver Tabla IX) y tratamiento anticoagulante con
heparina (cuestionable en las tromboflebitis periféricas y yugulares, donde se limita a casos con
evidencia de extensión del trombo). Habría que considerar también la valoración quirúrgica en
los casos de evolución tórpida.
Endocarditis infecciosa: también es más frecuente en infecciones por S. aureus, particularmente
en presencia de prótesis valvulares cardiacas o valvulopatías predisponentes (ver Capítulo 37.
“Endocarditis infecciosa. Infecciones endovasculares y fungemia”). Por este motivo es necesario
solicitar un ecocardiograma en todo paciente con IAC por S. aureus una vez transcurridos 5-7
días desde el diagnóstico de la bacteriemia (si se llevara a cabo más precozmente podría
asociarse a un resultado falsamente negativo). En caso de que otros agentes estuvieran
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [761]
[48] INFECCIONES NOSOCOMIALES
implicados en la IAC, la sospecha debería orientar la solicitud de otros estudios diagnósticos
para no hacerlos de forma rutinaria.
Metástasis sépticas a distancia: pueden producir osteomielitis, abscesos viscerales o
vertebrales o endoftalmitis. Se recomienda la realización sistemática de un examen de fondo
de ojo a todo paciente con candidemia (aun asintomático) para descartar la presencia de
coriorretinitis.
5. PREVENCIÓN
Dos intervenciones que han demostrado un mayor impacto en la reducción de la IAC son la
aplicación de medidas estrictas de asepsia durante la inserción del catéter y su manipulación, y su
indicación correcta (hay que reevaluar diariamente su necesidad y retirarlo tan pronto como deje de ser
imprescindible).
Es preciso revisar a diario el estado del punto de inserción para detectar la aparición de signos
locales de infección, y cambiar los apósitos al menos una vez a la semana. Si se empleara un conector sin
aguja, antes de la conexión de cualquier infusión este debe ser desinfectado con una toallita impregnada en
clorhexidina. Es recomendable el cambio rutinario de los catéteres venosos periféricos cada 72-96 horas
para evitar el desarrollo de flebitis (aunque esta práctica no parece ser superior al recambio basado en
indicación clínica). Sin embargo, esta actitud no se recomienda por regla general en los CVC excepto si se
hubiera insertado uno de forma urgente sin mantener una técnica estéril (en cuyo caso sería necesaria una
nueva inserción de forma programada al cabo de 48 horas). Tampoco estaría indicado el cultivo rutinario de
la punta de todos los CVC una vez retirados por cualquier motivo, salvo si existiera sospecha de IAC. Los
baños con clorhexidina o el uso de catéteres impregnados en antibióticos o antisépticos pueden ayudar a
disminuir la incidencia de IAC, sobre todo en pacientes ingresados en Unidades de Cuidados Intensivos.
III. INFECCIÓN DEL SITIO QUIRÚRGICO
1. DEFINICIÓN Y FACTORES DE RIESGO
La infección del sitio quirúrgico (ISQ) es aquella que tiene lugar en la zona de la intervención en un
plazo de hasta 30 días desde su realización (hasta un año en caso de implante de material protésico). Según
los estudios más recientes constituyen actualmente la primera causa de infección nosocomial en orden de
frecuencia (28% del total), si bien la incidencia de esta complicación varía notablemente en función de la
técnica quirúrgica y de las características del paciente. Su aparición implica un aumento de la mortalidad,
de la duración del ingreso hospitalario (7-10 días adicionales de media) y de los costes atribuibles. Con
arreglo al nivel de afectación pueden clasificarse en:
Infecciones incisionales superficiales: limitadas a piel y tejido celular subcutáneo.
Infecciones incisionales profundas: afectan a fascia y planos musculares.
Infecciones del órgano/espacio quirúrgico: si existiera compromiso de los órganos o cavidades
que fueron manipulados durante la intervención.
Entre los factores de riesgo para el desarrollo de una ISQ figuran:
Factores relacionados con el paciente: edad, malnutrición, diabetes, obesidad, hábito
tabáquico, duración de la estancia hospitalaria previa a la intervención, colonización por
diversos microorganismos (particularmente, S. aureus resistente a meticilina),
inmunodepresión, presencia de otras infecciones concurrentes.
Factores relacionados con la intervención: tipo de herida quirúrgica (Tabla X), duración del
procedimiento, técnica empleada (abierta o mínimamente invasiva), características del
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [762]
[48] INFECCIONES NOSOCOMIALES
quirófano, implante de cuerpos extraños o de material protésico, medidas inadecuadas de
antisepsia o profilaxis antibiótica, requerimientos transfusionales, factores relacionados con la
técnica quirúrgica (mala hemostasia, fallo en el cierre de espacios profundos, trauma tisular).
Factores relacionados con el microorganismo: cuantía del inóculo bacteriano y virulencia del
patógeno.
A partir de estos factores se han diseñado diversas escalas de predicción del riesgo de ISQ. La más
difundida es la del NNISS (National Nosocomial Infection Surveillance System), que asigna un punto a cada
una de las siguientes variables: elevado riesgo preoperatorio en la escala de la American Society of
Anesthesiologists (ASA ≥ 3), herida quirúrgica contaminada o sucia y duración de la intervención por encima
del percentil 75 del tiempo habitualmente empleado para ese procedimiento. El empleo de laparoscopia
resta un punto en el score final.
Tabla X. Clasificación de las heridas quirúrgicas.
2. ETIOLOGÍA
El agente etiológico de la mayoría de las ISQ procede de la flora endógena del propio paciente.
Globalmente, S. aureus, ECN, Enterococcus spp, E. coli, P. aeruginosa, Enterobacter spp y K. pneumoniae
son los microorganismos identificados con más frecuencia, si bien su distribución relativa varía en función
del tipo de cirugía y de la microbiología del centro donde tiene lugar la intervención quirúrgica. Así, los
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [763]
[48] INFECCIONES NOSOCOMIALES
cocos grampositivos (particularmente S. aureus) predominan en las infecciones de cirugías limpias, en tanto
que las heridas contaminadas suelen infectarse por flora mixta polimicrobiana (enterobacterias, P.
aeruginosa y anaerobios).
Los estreptococos del grupo B pueden estar presentes tras intervenciones obstétricas y
ginecológicas. Las infecciones muy precoces y rápidamente progresivas (menos de 24 horas desde la
intervención) sugieren la implicación de Clostridium perfringens o de estreptococos del grupo A. Algunas
ISQ pueden presentar una fuente exógena a través de la colonización o infección del personal sanitario, del
instrumental, del quirófano o del material implantado durante la intervención.
3. ABORDAJE DIAGNÓSTICO Y TERAPÉUTICO
Las ISQ deben sospecharse ante la aparición de signos locales de inflamación (exudado purulento a
través de la incisión o del drenaje quirúrgico) o de manifestaciones sistémicas (fiebre y leucocitosis).
Pueden cursar sin alteraciones analíticas relevantes.
El diagnóstico etiológico se establece a partir del estudio microbiológico (tinción de Gram y cultivo)
del exudado de la herida. Debe obtenerse la muestra en condiciones asépticas, preferentemente mediante
aspirado con jeringa del lecho de la herida, biopsia por punción, o bien durante una reintervención
quirúrgica. La interpretación clínica de las muestras obtenidas con torunda de los márgenes externos de la
herida se ve dificultada por la presencia de numerosos falsos positivos (colonización o contaminación), por
lo que esta técnica debe evitarse.
Entre las pruebas de imagen, la TC es la de elección para la visualización de gas ectópico o de
abscesos viscerales profundos.
4. TRATAMIENTO
Se basa en el control del foco, con el abordaje quirúrgico apropiado (limpieza y desbridamiento de
tejidos necróticos, eliminación de cuerpos extraños o drenaje de abscesos o colecciones), particularmente
en las ISQ incisionales profundas y de órgano/espacio. Hay que asociar antibioterapia empírica dirigida de
acuerdo a los hallazgos microbiológicos previos, a las características clínicas del paciente y al perfil de
resistencias del propio centro. El tratamiento antibiótico suele ser suficiente en las infecciones incisionales
superficiales.
5. PREVENCIÓN
5.1. Medidas preoperatorias: minimización de la estancia hospitalaria prequirúrgica; control de los
niveles de glucemia en pacientes diabéticos; interrupción del consumo de tabaco (al menos en los 30 días
previos a la intervención); identificación y tratamiento de las infecciones activas concurrentes, demorando
la intervención hasta alcanzar su control; y reducción, en la medida de lo posible, del uso de esteroides u
otra medicación inmunosupresora.
5.2. Preparación del paciente: en cirugía de colon o cistectomía abierta, preparación digestiva con
solución de polietilenglicol, afeitado del vello con máquina inmediatamente antes de la intervención solo si
se considerase imprescindible (evitando el rasurado, que causa microabrasiones cutáneas) y asepsia
correcta de la piel (con povidona yodada al 10%, gluconato de clorhexidina jabonosa al 4% o solución
alcohólica de clorhexidina al 0,5%). Los resultados sobre la aplicación de oxigenoterapia a alto flujo
perioperatoria son controvertidos.
5.3. Profilaxis antibiótica: la 1ª dosis se debe administrar 60 minutos antes de la incisión quirúrgica;
se ha de repetir una 2ª dosis intraoperatoria al cabo de 3 horas en intervenciones muy prolongadas o si
existiera mucha pérdida hemática durante el procedimiento (esta última dosis no sería necesaria si
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [764]
[48] INFECCIONES NOSOCOMIALES
emplearan vancomicina o gentamicina gracias a su efecto postantibiótico). En cualquier caso, la profilaxis
se debe interrumpir en las primeras 24 h tras la intervención. Las pautas de elección suelen basarse en
cefalosporinas de 1ª o 2ª generación (Tabla XI), evitando el empleo rutinario de vancomicina (excepto en
pacientes con hipersensibilización a β-lactámicos). La detección sistemática del estado de portador nasal de
S. aureus está indicada en pacientes que van a someterse a cirugía cardiaca electiva, con descolonización
mediante mupirocina tópica al 2% (dos aplicaciones diarias durante 5 días). Es aconsejable la consulta de
las guías específicas para cada tipo de intervención.
Tabla XI. Profilaxis antibiótica según el tipo de cirugía.
5.4. Medidas intra y postoperatorias
Control de las condiciones ambientales del quirófano (ventilación, reducción de la circulación del personal);
técnica quirúrgica aséptica y cuidadosa (con minimización de daño tisular y de implante de cuerpos
extraños); mantenimiento de la normotermia; cierre primario de la herida (o por segunda intención en caso
de contaminación franca del lecho quirúrgico); utilización de sistemas de drenaje cerrados; protección de
las heridas con cierre primario con un apósito estéril no oclusivo durante las primeras 24-48 horas y uso de
técnicas estériles durante la manipulación y cura posterior de la herida.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [765]
[48] INFECCIONES NOSOCOMIALES
IV. NEUMONÍA NOSOCOMIAL
1. CONCEPTO Y EPIDEMIOLOGÍA
La neumonía nosocomial (NN) es la segunda infección nosocomial en frecuencia y la asociada a
mayor mortalidad (20-50%). Existen varios conceptos diferentes:
Neumonía adquirida en el hospital (NAH): se da en el paciente no ventilado a partir de las
primeras 48 horas de ingreso hospitalario (tras excluir que la infección no estuviera ya presente
o en periodo de incubación en el momento del ingreso). La incidencia de la NAH oscila entre 5 y
10 episodios por cada 1.000 ingresos. Tiene una mortalidad del 10%.
Neumonía asociada a ventilación mecánica (NAVM): aquella diagnosticada una vez
transcurridas al menos 48 horas desde la intubación orotraqueal (IOT) y el inicio de la
ventilación mecánica invasiva (VMI). La incidencia global es del 10 al 20%, con una incidencia
diaria del 3% a lo largo de los 5 primeros días de VMI. Tiene una mortalidad superior al 30%. En
algunos pacientes puede verse precedida por una traqueobronquitis asociada a ventilación
mecánica (fiebre, leucocitosis y secreciones bronquiales purulentas con un recuento bacteriano
significativo en el aspirado endotraqueal [AET], en ausencia de un infiltrado radiológico de
nueva aparición).
Neumonía asociada a cuidados sanitarios: en pacientes hospitalizados durante más de 48 horas
en los 3 meses previos; institucionalizados o con estancia en un Centro de Cuidados Crónicos; o
que han recibido a lo largo del mes previo alguna sesión de hemodiálisis, quimioterapia,
antibioterapia parenteral, cura de heridas o atención sanitaria especializada en su domicilio. En
muchos casos su comportamiento es similar a la NN más que a la neumonía adquirida en la
comunidad, excepto en aquellos pacientes con buena situación funcional, en los que es menos
frecuente la implicación de microorganismos multirresistentes (salvo del Staph. aureus).
2. ETIOLOGÍA Y FACTORES DE RIESGO
La flora orofaríngea se va modificando a lo largo de la hospitalización por efecto de la alcalinización
del pH gástrico (administración de inhibidores de la bomba de protones), el uso de sondas nasogástricas, la
presión antibiótica y la malnutrición, de tal forma que la colonización por BGN pasa a ser la norma a los
pocos días del ingreso (ver Tabla XI). La microaspiración es el principal mecanismo etiopatogénico. Entre
sus factores de riesgo figuran las situaciones de bajo nivel de consciencia, alteración del reflejo deglutorio,
manipulaciones de la vía aérea, edad avanzada, gravedad de la enfermedad de base, antibioterapia previa y
larga duración del ingreso hospitalario. La adquisición puede producirse, más excepcionalmente, tras la
inhalación de aerosoles aéreos o acuosos (por Legionella spp o Chlamydophila pneumoniae), o bien por
diseminación hematógena desde un foco a distancia (por S. aureus o BGN).
Los microorganismos más frecuentes varían en función de las series y los diferentes centros
hospitalarios, predominando generalmente S. aureus, seguido de P. aeruginosa, Klebsiella spp, E. coli,
Acinetobacter spp y Enterobacter spp. Todos ellos causan el 80% de las NN.
La incidencia relativa de microorganismos resistentes depende de la presencia de factores de riesgo
(Tabla XII). S. aureus (y, en particular, cepas resistentes a meticilina), es el responsable del 20-40% de las
NAVM, especialmente en pacientes con factores específicos de riesgo (diabetes mellitus, enfermedad renal
crónica sometida a diálisis, colonización nasal o ingreso previo en un Centro de Cuidados Crónicos).
Se distinguen dos grupos de presentación de la NN:
NN de presentación precoz (menos de 5 días de hospitalización): suele estar originada por
microorganismos que ya estaban presentes en el momento del ingreso, como Streptococcus
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [766]
[48] INFECCIONES NOSOCOMIALES
pneumoniae, Moraxella catarrhalis, Haemophilus influenzae, S. aureus sensible a meticilina,
BGN no resistentes (E. coli, Klebsiella spp, Enterobacter spp, Proteus spp, Serratia marcescens) o
flora anaerobia (en particular, tras una cirugía abdominal reciente).
NN de presentación tardía (≥ 5 días de hospitalización): hay que considerar la implicación de
microorganismos gramnegativos con mecanismos adicionales de resistencia, como
enterobacterias (E. coli y K. pneumoniae) y BGN no fermentadores (A. baumannii,
Stenotrophomonas maltophilia y, en especial, P. aeruginosa, que es el agente más
frecuentemente identificado en la NAVM).
Tabla XII. Factores de riesgo para microorganismos específicos en la neumonía nosocomial.
3. DIAGNÓSTICO
La definición comúnmente aceptada de NN exige la aparición de un infiltrado pulmonar nuevo (o la
progresión de uno preexistente) acompañado de al menos dos de los siguientes signos: fiebre (> 38 ºC) o
hipotermia (< 35,5 ºC); leucocitosis (> 10.000/mm3) o leucopenia (< 4.000/ mm3); y presencia de
secreciones respiratorias purulentas. Para mayores de 70 años, la alteración del estado mental también
debería estar incluida en esta definición.
En cuanto a las pruebas de laboratorio, la procalcitonina (PCT), que puede ser normal si no hay
síndrome de respuesta inflamatoria sistémica (SRIS) acompañante, tiene un papel importante durante el
seguimiento y en la determinación de la respuesta y la duración del tratamiento antibiótico, siendo
superior su valor pronóstico al de la proteína C reactiva.
El diagnóstico etiológico se alcanza en menos del 50% de las NN, proporción aún más reducida en
pacientes no intubados (mayor dificultad en la obtención de muestras respiratorias de calidad). Aunque la
rentabilidad de los hemocultivos suele ser baja, en las neumonías por S. aureus o S. pneumoniae es
aceptable, por lo que se recomienda su obtención de forma sistemática (en caso de existir bacteriemia, la
mortalidad se duplica). La detección en orina (mediante enzimoinmunoensayo o inmunocromatografía) del
antígeno neumocócico y de L. pneumophila (serogrupo 1) presenta buena especificidad, con una
sensibilidad algo menor.
La demostración de bacterias en la tinción de Gram de un esputo de buena calidad, según los
criterios de Murray (más de 25 polimorfonucleares y menos de 10 células epiteliales por campo de 100
aumentos) se correlaciona, de forma aproximada, con un recuento bacteriano superior a 10 UFC/ml.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [767]
[48] INFECCIONES NOSOCOMIALES
En el caso de NAH, se debería reservar la broncoscopia con cepillado bronquial con catéter
protegido (CBCP]) o lavado broncoalveolar (LBA) ante mala respuesta clínico-radiológica al cabo de 72
horas de tratamiento antibiótico empírico (ver Figura 1). En pacientes sometidos a IOT, se considera
específico un recuento significativo en el cultivo de las muestras distales obtenidas mediante CBCP (> 10
UFC/ml) o LBA (> 10 UFC/ml), así como la demostración de más de 2-5% de gérmenes intracelulares en los
macrófagos o neutrófilos recuperados del LBA. Muestras del LBA con una proporción de células epiteliales
superior al 1% sugieren contaminación por la flora del tracto respiratorio superior.
Se debe realizar toracocentesis con cultivo de líquido pleural en presencia de un derrame
significativo.
En huéspedes inmunodeprimidos podrían justificarse exploraciones específicas, como la
determinación de galactomanano en suero o LBA, la detección de Pneumocystis jirovecii en LBA (mediante
las tinciones de plata-metenamina o azul de toluidina, o la detección con técnicas de reacción en cadena de
polimerasa [PCR]), o bien, la antigenemia p65 o PCR para el diagnóstico de citomegalovirus (ver Capítulo 47.
“Infecciones en el inmunodeprimido. Neutropenia febril”).
4. TRATAMIENTO
4.1. Tratamiento antibiótico empírico
La precocidad y adecuación del tratamiento antibiótico disminuyen la mortalidad en la NN. Por ello debe
iniciarse y de forma empírica tras considerar las características del paciente y de su entorno
epidemiológico, precedido de la obtención de muestras microbiológicas (hemocultivos, tinción de Gram y
cultivo de esputo y AET en pacientes intubados). La pauta empírica se elige en función de factores de riesgo
para microorganismos específicos (con arreglo a los que se establecen diferentes grupos de pacientes [ver
Tabla XII]) y de la gravedad del cuadro (Tabla XIII).
Tabla XIII. Criterios de gravedad de la neumonía nosocomial.
En todo tratamiento empírico es fundamental considerar la tasa de resistencias del centro y del
entorno. De este modo se pueden distinguir tres grupos de pacientes (Tabla XIV).
Grupo I: NN grave de presentación precoz, y NN no grave sin factores de riesgo para
microorganismos específicos, de presentación precoz o tardía: requiere cubrir los denominados
agentes centrales o core (S. pneumoniae, H. influenzae, S. aureus sensible a la meticilina y
enterobacterias como S. marcescens y Klebsiella spp) para lo cual se puede recurrir a la
monoterapia con un β-lactámico o una quinolona respiratoria.
Grupo II: NN no grave con factores de riesgo para microorganismos específicos, precoz o tardía:
será necesario asociar un tratamiento específico en función del factor de riesgo que presente el
paciente. Las quinolonas respiratorias (con la adición de rifampicina en casos graves) han
desplazado a los macrólidos como tratamiento de elección ante la sospecha de infección por
Legionella. Por otra parte, linezolid ha demostrado ser superior en la erradicación
microbiológica a los glucopéptidos (vancomicina o teicoplanina) en las NN por S. aureus
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [768]
[48] INFECCIONES NOSOCOMIALES
resistente a meticilina, especialmente en aquellos pacientes con insuficiencia renal, aunque no
hay diferencias en términos de mortalidad. En el caso de enterobacterias productoras de BLEE
el tratamiento debe incluir un carbapenémico, preferentemente asociado a una quinolona o a
un aminoglucósido (por ejemplo, amikacina). La implicación de A. baumannii o de
enterobacterias productoras de carbapenemasas obliga al uso combinado de regímenes
basados en colistina, amikacina, tigeciclina y, en ocasiones, carbapenémicos en perfusión
extendida (en función de la CMI del microorganismo aislado).
Tabla XIV. Tratamiento por grupo de presentación y sospecha etiológica.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [769]
[48] INFECCIONES NOSOCOMIALES
Grupo III: NN grave de presentación precoz o tardía con factores de riesgo para
microorganismos específicos: es preciso recurrir a la terapia combinada con un β-lactámico con
acción antipseudomónica y un aminoglucósido o una quinolona (ciprofloxacino o
levofloxacino), considerando igualmente la necesidad de cobertura específica frente a S. aureus
resistente a meticilina. En la mayoría de estudios se prefiere el uso de aminoglucósidos frente a
quinolonas como segundo agente debido a que así se evita la selección de resistencias por
parte de las quinolonas, con mejor cobertura frente a los gramnegativos. Una dosis total en las
primeras 24 horas mejora la eficacia y minimiza la toxicidad. Algunos estudios han sugerido la
utilidad de la colistina nebulizada asociada al tratamiento sistémico en pacientes con NAVM por
A. baumannii o P. aeruginosa multirresistente.
4.2. Tratamiento antibiótico de continuación
Quedará condicionado por la respuesta clínico-radiológica al tratamiento empírico inicial en las primeras
48-72 horas y por los resultados microbiológicos (Figura 2). No es recomendable efectuar cambios en la
antibioterapia durante las primeras 48-72 horas, excepto en caso de deterioro clínico franco o recepción de
resultados microbiológicos. La mejoría radiológica suele demorarse respecto a la clínica.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [770]
[48] INFECCIONES NOSOCOMIALES
Si la evolución fuera favorable y existiera un aislamiento microbiológico significativo (sin
demostración de Pseudomonas spp) se debería ajustar el tratamiento antibiótico al antibiograma y
simplificar la pauta hacia la monoterapia. Ante el aislamiento de Pseudomonas spp se recomienda
mantener la doble terapia para evitar la aparición de resistencias. Se ha de individualizar la duración total
del tratamiento en estos casos.
Se pueden utilizar pautas cortas (7 días) en ausencia de complicaciones locales (empiema pleural) o
sistémicas (bacteriemia). Se deben usar pautas largas (14-21 días) en pacientes inmunodeprimidos e
infecciones por S. aureus, Pseudomonas spp o A. baumannii, así como en las neumonías necrotizantes o
con cavitación. Algunos estudios sugieren utilizar la PCT (procalcitonina) en el seguimiento con el fin de
acortar las pautas de tratamiento (una vez su valor se haya normalizado). En caso de tratamiento
combinado, se debe mantener 3-5 días, y si existiera buena respuesta y el microorganismo responsable
fuera sensible al β-lactámico empleado, se podría continuar en monoterapia con el mismo hasta completar
las 2-3 semanas.
Figura 2. Algoritmo del abordaje diagnóstico y terapéutico de la neumonía nosocomial.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [771]
[48] INFECCIONES NOSOCOMIALES
La ausencia de respuesta al tratamiento (definida por la no mejoría o el empeoramiento al cabo de
48-72 horas de la fiebre, la leucocitosis, la purulencia de las secreciones o la función respiratoria) obliga a
ampliar el diagnóstico diferencial, incluyendo entidades de etiología no infecciosa, patógenos no
convencionales o el desarrollo de complicaciones locales o a distancia (Tabla XV). En esta situación se ha de
considerar la realización de una fibrobroncoscopia con obtención de muestras respiratorias distales
mediante CBCP o LBA (Figura 2). La TC y la gammagrafía pulmonar permiten descartar complicaciones y
otras causas de fiebre. Un resultado negativo en el AET en pacientes aún no sometidos a tratamiento
antibiótico (ausencia de células inflamatorias y de gérmenes en el cultivo) presenta un valor predictivo
negativo elevado (94%) para el diagnóstico de NAVM, por lo que permite la retirada segura de la pauta
empírica inicial y obliga a excluir otros diagnósticos alternativos.
Tabla XV. Causas de ausencia de respuesta al tratamiento empírico inicial.
5. PREVENCIÓN
Una de las actuaciones con mayor impacto sobre la incidencia de NAVM pasa por reducir en lo
posible la indicación de IOT (empleo de ventilación mecánica no invasiva) y la duración de la VMI
(protocolos de extubación temprana).
Otras medidas incluyen el empleo prioritario de la vía orotraqueal para la intubación, la higiene de
manos en cualquier manipulación de la vía aérea, la elevación del cabecero de la cama 30-45º, el empleo
de tubos endotraqueales recubiertos de plata que previenen la formación de biofilms, la higiene periódica
de la cavidad oral con solución antiséptica basada en clorhexidina, o la aspiración continua de las
secreciones subglóticas. La administración de profilaxis antibiótica por vía tópica (descontaminación oral
selectiva) o sistémica (descontaminación digestiva selectiva) ha demostrado su utilidad en algunos ensayos
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [772]
[48] INFECCIONES NOSOCOMIALES
clínicos a la hora de reducir la incidencia de NAVM, si bien su uso no se ha generalizado y no existe
adecuada evidencia en cuanto a su impacto a largo plazo sobre la aparición de resistencias bacterianas.
BIBLIOGRAFÍA
American Thoracic Society and The Infectious Diseases Society of America. Guidelines for the
management of adults with Hospita-acquired, Ventilator-associated, and Healthcare-associated
Pneumonia. Am J Respir Crit Care Med. 2005;171:388-416.
Brayzler DW, Dellinger EP, Olsen KM, et al. Clinical Practical Guidelines for antimicrobial prophylaxis in
surgery. Am J Heatlh Syst Pharm. 2013;70(3):195-283.
Chastre J, Blasi F, Masterton G, et al. European perspective and update on the management of
nosocomial pneumonia due to methicillin-resistant Stafilococcus aureus after more than 10 years of
experience with linezolid. Clin Microbial Infect. 2014;20(Suppl 4):19-36.
Crawford T, Rodvold KA, Solomkin JS. Vancomycin for Surgical Prophylaxis? Clinical Infectous Diseases.
2012;54:1474-9.
Denis GA, Relich RF. Antibiotic Resistance in Nosocomial Respiratory Infections. Clin Lab Med.
2014;34:257-70.
Gudiol F, Aguado JM, Almirante B, Bouza E, Cercenado E, Domínguez MA, et al. Diagnosis and
treatment of bacteremia and endocarditis due to Staphylococcus Aureus. A clinical guideline from the
Spanish Society of Clinical Microbiology and Infectious Diseases (SEIMC). Enferm Infecc Microbiol Clin.
2015;33:625-48.
Hooton TM, Bradley SF, Cardenas DD, Colgan R, Geerlings SE, Rice JC, et al. Diagnosis, prevention and
treatment of catheter-associated urinary tract infection in adults: 2009 International Clinical Practice
Guidelines from the Infectious Diseases Society of America. Clin Infect Dis. 2010;50:625-63.
Justo JA, Bookstaver PB. Antibiotic lock therapy: review of technique and logistic challenges. Infect Drug
Resist. 2014;7:343-63.
Liu C, Bayer A, Cosgrove SE, Daum RS, Fridkin SK, Gorwitz RJ, et al. Clinical Practice Guidelines by the
Infectious Diseases Society of America for the Treatment of Methicillin-Resistant Staphylococcus
Aureus Infections in Adults and Children. Clin Infect Dis. 2011;52:1-38.
Nair GB and Niederman MS. Nosocomial Pneumonia: Lessons Learned. Crit Care Clin. 2013;29:521-
46.
O’Grady NP, Alexander M, Burns LA, Dellinger EP, Garland J, Heard SO, et al. Guidelines for the
prevention of intravascular catheter-related infections. Clin Infect Dis. 2011;52:1-22.
Rodríguez-Baño J, Cisneros JM, Cobos-Trigero N, Fresco G, Navarro-San Francisco C, Gudiol C, et al.
Diagnosis and antimicrobial treatment of invasive infections due to multidrug-resistant
Enterobacteriaceae. Guidelines of the Spanish Society of Infectous Diseases and Clinical Microbiology.
Enferm Infecc Microbiol Clin. 2015;33(5):337.e1–337.e21.
Schweizer M, Perencevich E, McDanel J, Carson J, Formanek M, Hafner J, et al. Effectiveness of a
bundled intervention of decolonization and prophylaxis to decrease Gram positive surgical site
infections after cardiac or orthopedic surgery: systematic review and meta-analysis. Biomedical Journal.
2013;346:f2743. doi: 10.1136/bmj.f2743.
Tenke P, Kovacs B, Bjerklund-Johansen TE, Matsumoto T, Tambyah PA, Naber KG. European and Asian
guidelines on management and prevention of catheter associated urinary tract infections. Internal
Journal of Antimicrobial Agents. 2008;31S:68-78.
Young PY, Khadaroo RG. Surgical Site Infections. Surg Clin N Am. 2014;94:1245-64.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [773]
[49] ENFERMEDADES IMPORTADAS DEL VIAJERO Y DEL INMIGRANTE
49.Enfermedades importadas del viajero y del
inmigrante
Laura Corbella Vázquez.
Medicina Interna
María Espinosa Díaz.
Medicina Interna
Asesor: Juan María Herrero Martínez. Médico Adjunto de Medicina Interna
I. INTRODUCCIÓN
La especialidad de Medicina Tropical se centra en dos tipos de pacientes: pacientes nacionales que
viajan a un país tropical o subtropical donde la prevalencia de determinadas enfermedades es endémica, y
pacientes inmigrantes procedentes de dichos países. La expresión en inglés visiting friends and relatives
(VFR) hace referencia a un subtipo especial de inmigrantes. Son aquellos que residen en un país y que se
desplazan temporalmente a sus países de origen, en viajes habitualmente de larga duración y hacia ámbitos
rurales. Suelen tener una baja percepción de susceptibilidad a la enfermedad y por ello están más
expuestos a las distintas dolencias endémicas de sus territorios natales.
En los últimos años, como fruto de la globalización, se ha producido un incremento en los viajes
internacionales a todos los continentes. Se debe estar alerta ante el aumento de patología importada, pero
sin olvidar que la atención a la población inmigrante constituye una oportunidad muy valiosa para la
detección y prevención de patologías más comunes y menos “exóticas”.
1. ANAMNESIS
1.1. Historia de vacunación
La vacunación contra los virus de la hepatitis A y B (VHA y VHB) y la fiebre amarilla es muy efectiva, y
prácticamente descarta dichas infecciones. La vacuna contra la fiebre tifoidea y la inmunización pasiva con
inmunoglobulina frente al VHA tienen una efectividad cercana al 70%, por lo que estas patologías no deben
descartarse aunque el paciente haya tomado la profilaxis (Tabla I).
1.2. Quimioprofilaxis recibida
Es de interés especialmente si el paciente ha viajado a una zona endémica para malaria y otras
enfermedades transmitidas por artrópodos. Es necesario saber, en el caso de la malaria, la quimioprofilaxis
realizada (fármaco, dosis, duración, cumplimiento, fecha de la última toma), y tener en cuenta que dicha
profilaxis no protege totalmente y que el grado de cumplimiento correcto suele ser bajo. Asimismo, se
recogerá en la historia el uso de barreras de protección frente a las picaduras.
Tabla I. Eficacia y duración de algunas vacunas en el viajero inmunocompetente.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [774]
[49] ENFERMEDADES IMPORTADAS DEL VIAJERO Y DEL INMIGRANTE
1.3. Tipo de viajes realizados
Se registrarán el destino, el itinerario y los medios de transporte empleados en el último viaje o los
realizados durante al menos el último año (se han notificado brotes de enfermedades infecciosas en
cruceros, trenes y vuelos); también el propósito del viaje (para definir el grado de contacto con las personas
autóctonas del país [mayor en viajes de cooperación y en los VFR]), el alojamiento, las actividades
realizadas (especialmente si han tenido lugar en el medio rural), las bebidas y alimentos consumidos, el
contacto con animales y los contactos sexuales (que se dan hasta en el 50% de los jóvenes que viajan al
trópico) (Tabla II).
Tabla II. Exposiciones específicas y enfermedades infecciosas asociadas*.
1.4. Clínica
Se consideran aquí síntomas (inicio, duración, evolución [empeoramiento o mejoría tras alguna medida]) y
exposición a diferentes elementos (es de ayuda calcular el periodo de incubación) (Tabla III).
2. EXPLORACIÓN FÍSICA
En la tabla IV se resumen los principales hallazgos y su significado. Es importante explorar oídos,
dientes y senos paranasales (las otitis, los abscesos dentarios y las sinusitis son causa de fiebre sin foco y
deben ser descartados antes de iniciar un estudio exhaustivo de fiebre en el viajero). Las adenopatías son
útiles para el diagnóstico. La existencia de fiebre con estado mental alterado es una emergencia que
requiere manejo especializado. Por último, siempre se ha de realizar una exploración genital.
3. PRUEBAS COMPLEMENTARIAS
Tras hacer una historia clínica que nos permita tener una adecuada orientación, se han de solicitar
las pruebas complementarias de forma dirigida (en primer lugar, para comprobar y estudiar el diagnóstico
sindrómico y, posteriormente, para confirmar la etiología).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [775]
[49] ENFERMEDADES IMPORTADAS DEL VIAJERO Y DEL INMIGRANTE
Tabla III. Periodos de incubación para enfermedades infecciosas del viajero.
4. VALORACIÓN INICIAL
Valorar signos de gravedad clínica. El paciente deberá ser hospitalizado inmediatamente ante
manifestaciones neurológicas, distrés respiratorio, hipotensión arterial o hemorragias
mucocutáneas o viscerales.
Valorar la necesidad de medidas de aislamiento. Se han de instaurar en pacientes con
manifestaciones hemorrágicas que hayan llegado en los últimos 21 días de un área en la que se
hayan notificado casos de fiebre vírica hemorrágica durante los últimos cinco años; y también
en aquellos que hayan tenido contacto con fluidos corporales de personas o animales
potencialmente infectados por los virus de la fiebre de Crimea-Congo, Ébola, Marburgo o Lassa,
aunque no tengan signos de hemorragia.
Valorar la necesidad de tratamiento empírico. Se tiene que considerar, sobre todo, en casos de
malaria y de leptospirosis. Todo paciente procedente de un área endémica para malaria debe
someterse a pruebas para descartar dicha infección (ver Apartado IV. “Fiebre”). Si la
probabilidad de malaria fuera alta (esplenomegalia o plaquetas por debajo de 150.000/mm3 o
hemoglobina inferior a 12 g/dL), no hubiera diagnóstico alternativo y no se pudieran realizar las
pruebas diagnósticas, se tendría que iniciar tratamiento antimalárico empírico. Hay que valorar
la necesidad de tratamiento empírico frente a leptospirosis ante todo viajero con fiebre,
antecedente de contacto con agua dulce (en actividades deportivas y de aventura) y clínica
compatible (cefalea, mialgias, vómitos, dolor abdominal o ictericia).
II. CRIBADO EN EL INMIGRANTE ASINTOMÁTICO
Los inmigrantes asintomáticos procedentes de países en vías de desarrollo con relativa frecuencia
presentan enfermedades infecciosas no diagnosticadas, tanto ubicuas (por ejemplo, infección por VIH)
como asociadas a determinadas áreas geográficas (es el caso de la enfermedad de Chagas); el riesgo de
padecer distintas enfermedades va a estar determinado por el área geográfica de procedencia y la ruta
migratoria, el grupo étnico y el estado de salud, entre otros. La importancia de identificar estas infecciones
en fase asintomática o paucisintomática radica en el potencial riesgo de morbilidad e incluso de mortalidad
asociado a las mismas; además, en el caso de algunas enfermedades, la importancia de su identificación se
extiende al campo de la Salud Pública. Por tanto, el cribado del inmigrante asintomático debe realizarse de
forma precoz (durante el primer contacto con el sistema sanitario) y ajustarse a sus características
epidemiológicas (especialmente al área de procedencia [Tabla I]), mereciendo una especial atención las
mujeres gestantes.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [776]
[49] ENFERMEDADES IMPORTADAS DEL VIAJERO Y DEL INMIGRANTE
Tabla IV. Exploración física en el viajero.
Es importante recordar que la valoración global del paciente en este grupo de población ha de ir
dirigida a la búsqueda no solo de procesos infecciosos, sino también de entidades no infecciosas de especial
prevalencia: debe descartarse la existencia de abuso de alcohol y otros hábitos tóxicos, así como otros
problemas de salud mental y situaciones sociales de riesgo. Se recomienda una exploración física completa,
sin olvidar el estado nutricional, la búsqueda de lesiones cutáneas y el examen bucodental y ginecológico; y
también la realización de analítica de sangre (bioquímica básica y hemograma), sistemático de orina y test
de embarazo en mujeres en edad fértil, y valorar asimismo una radiografía de tórax, además de las pruebas
microbiológicas expuestas en la tabla V.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [777]
[49] ENFERMEDADES IMPORTADAS DEL VIAJERO Y DEL INMIGRANTE
Tabla V. Propuesta de cribado de enfermedades infecciosas importadas en el inmigrante asintomático.
1. ENFERMEDAD DE CHAGAS
1.1. Etiopatogenia y clínica
La tripanosomiasis americana o enfermedad de Chagas es una zoonosis causada por Trypanosoma cruzi, un
protozoo endémico de América Central y del Sur. España es el segundo país con mayor número de
inmigrantes infectados. El ser humano se contagia a través del contacto de mucosas o de heridas cutáneas
con heces de insectos hematófagos triatómidos (chinches), y también por vía oral, por vía maternofetal,
por transfusiones de sangre o trasplante de órganos de donantes infectados o por accidentes de
laboratorio.
Su curso se divide en dos fases: aguda y crónica. La fase aguda aparece tras un periodo de
incubación de 5-12 días. Es asintomática en la mayoría de los casos, pero también puede asociar un cuadro
febril, malestar general y anorexia, en ocasiones acompañados de exantema morbiliforme,
hepatoesplenomegalia o adenopatías generalizadas. En el punto de entrada de la piel se puede observar
una induración con edema y eritema (chagoma) y con linfadenopatía local. Si el contagio se produce a
través de la conjuntiva, es típico, aunque infrecuente, encontrar edema palpebral y periorbicular unilateral
indoloro (signo de Romaña). La fase aguda es autolimitada, si bien raramente puede evolucionar hacia
miocarditis o meningoencefalitis, que pueden ser mortales. La fase crónica suele ser asintomática (fase
crónica indeterminada) durante muchos años (e, incluso, de por vida) aunque se pueden dar reactivaciones
con clínica similar a la de la fase aguda en pacientes inmunodeprimidos.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [778]
[49] ENFERMEDADES IMPORTADAS DEL VIAJERO Y DEL INMIGRANTE
Hasta en un 20-30% de los casos ocurren complicaciones tardías (fase crónica sintomática), que
pueden ser cardiacas, digestivas o mixtas. La afección cardiaca consta de arritmias, miocardiopatía dilatada
o fenómenos tromboembólicas. Se manifiestan con alteraciones en el registro del electrocardiograma (el
signo electrocardiográfico más frecuente es el bloqueo de rama derecha), insuficiencia cardiaca o ictus. A
nivel digestivo pueden desarrollarse megaesófago (con disfagia, odinofagia, dolor torácico, regurgitación
[con el riesgo de broncoaspiración que ello supone]) o megacolon (con dolor abdominal y estreñimiento
crónico [con riesgo de volvulación, obstrucción o sepsis secundaria]).
1.2. Diagnóstico
Durante la fase aguda y las reactivaciones, el diagnóstico se basa en la detección del parásito a través del
examen microscópico de sangre periférica (microhematocrito o técnica de Strout) o mediante técnicas de
biología molecular (reacción en cadena de polimerasa [PCR]). En las reactivaciones se puede hallar al
parásito en las biopsias de tejidos.
En la fase crónica, el diagnóstico es serológico, siendo necesarios dos test positivos dirigidos frente
a antígenos diferentes. Habitualmente se emplean enzimoinmunoanálisis de adsorción (ELISA),
inmunofluorescencia indirecta, inmunocromatografía o hemaglutinación indirecta. Se indica el estudio en
pacientes procedentes de áreas endémicas o que hayan recibido transfusiones sanguíneas o trasplantes en
dichas áreas, y en hijos de madres infectadas.
Se recomienda realizar registro de electrocardiograma y ecocardiograma transtorácico en el
momento del diagnóstico y, más adelante, cada 2-5 años, en función del grado de afectación inicial. Se
llevarán a cabo otras pruebas (electrocardiografía Holter, manometría, tránsito baritado
esofagogastroduodenal, enema opaco, etc.) en función de los síntomas que presente el paciente.
1.3. Tratamiento
Es controvertido, dados la escasez de estudios clínicos y los frecuentes efectos secundarios de los fármacos
disponibles. Actualmente debe indicarse siempre en caso de infección aguda o congénita (donde tiene una
eficacia del 90%), en la reactivación en pacientes inmunodeprimidos y en menores de 18 años. Debe
ofrecerse a mujeres en edad fértil y a adultos de hasta 50 años en fase crónica indeterminada o con
cardiopatía leve (con alteraciones electrocardiográficas y también, si bien esto es más discutido, con
cardiomegalia pero sin insuficiencia cardiaca). La eficacia del tratamiento es menor en mayores de 50 años.
No está indicado en pacientes con cardiopatía chagásica avanzada, insuficiencia cardiaca congestiva o
megaesófago. Está contraindicado en el embarazo y en las insuficiencias renal y hepática graves.
Se realiza con benznidazol (5 mg/kg/día en adultos, divididos en 2-3 dosis, durante 60 días) o
nifurtimox. El benznidazol es de primera línea por su mejor perfil de eficacia-seguridad. Debe hacerse una
analítica, con hemograma y bioquímica renal y hepática, antes del inicio del tratamiento y periódicamente
durante el seguimiento para atender a la aparición de posibles complicaciones o efectos secundarios. En
ausencia de un método de referencia (gold standard) que indique curación, se evalúa la respuesta al
tratamiento mediante la desaparición de los anticuerpos IgG (lo que puede tardar años o, incluso, no llegar
a suceder nunca). La determinación de PCR después del tratamiento es útil para detectar fracasos
terapéuticos, si bien la parasitemia puede fluctuar, por lo que un valor negativo no indicaría curación. Las
manifestaciones cardiacas y digestivas requieren manejo multidisciplinar en el que participen cardiólogos,
médicos del aparato digestivo y/o cirujanos generales.
III. EOSINOFILIA
La eosinofilia (más de 500 eosinófilos/μl) es un hallazgo frecuente en inmigrantes y viajeros
procedentes de países tropicales. Aunque las posibles causas subyacentes son diversas (inmunológicas,
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [779]
[49] ENFERMEDADES IMPORTADAS DEL VIAJERO Y DEL INMIGRANTE
farmacológicas, neoplásicas, etc.), en este grupo debe descartarse, en primer lugar, la etiología infecciosa, y
en especial las infecciones por helmintos. Resulta de especial interés el estudio de la infección por
Strongyloides stercoralis en estos pacientes, dado el riesgo asociado de desarrollar un síndrome de
hiperinfestación bajo determinadas circunstancias (ver el apartado siguiente). En ausencia de una evidencia
sólida en el abordaje de estos pacientes, la figura 1 ofrece un posible algoritmo diagnóstico.
Es importante tener en cuenta que pueden coexistir varias parasitosis responsables de la
eosinofilia, por lo que se deberá realizar un control a los 2-3 meses del tratamiento específico y, en caso de
no resolverse, continuar el estudio diagnóstico. Por otra parte, en muchas ocasiones, a pesar de un estudio
exhaustivo no se logra conocer la causa de la eosinofilia; en estos casos puede estar indicado el tratamiento
antihelmíntico empírico. La ausencia de respuesta al mismo debe hacer plantear la búsqueda de causas no
infecciosas responsables de la alteración hematológica (Figura 1).
1. ESTRONGILOIDIASIS
1.1. Etiopatogenia y clínica
Causada por Strongyloides stercoralis, es endémica de América del Sur y del Sudeste asiático. El contagio se
produce a través de la penetración de la larva a través de la piel, pudiendo provocar el cuadro de larva
currens, con trayectos lineales muy pruriginosos en las zonas de acceso, que desaparecen en 72 horas.
Menos frecuentemente se adquiere tras la ingesta de alimentos contaminados con la larva. Habitualmente
la infección es asintomática, con posibilidad de autoinfestación (puede permanecer en el huésped durante
décadas y producir autoinfestaciones frecuentes). La ausencia de eosinofilia no es rara, e incluso resulta
habitual en el caso de hiperinfestación/diseminación. En caso de provocar síntomas, estos pueden ser
gastrointestinales inespecíficos, respiratorios (incluyendo neumonía eosinofílica o síndrome de Löffler, que
se produce por una reacción de hipersensibilidad por la migración de la larva a través de los tejidos) y
dermatológicos (como exantemas).
Figura 1. Algoritmo diagnóstico de la eosinofilia.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [780]
[49] ENFERMEDADES IMPORTADAS DEL VIAJERO Y DEL INMIGRANTE
En el caso de pacientes inmunodeprimidos (p. ej., en tratamiento esteroideo, y raramente sin
embargo en pacientes con virus de la inmunodeficiencia humana [VIH], en los que se puede dar en el seno
de una reconstitución inmunitaria) o coinfectados por HTLV-1 (human T-cell lymphotropic virus 1) puede
darse un síndrome de hiperinfestación local o de estrongiloidiasis diseminada. En ella se produce una
diseminación de las larvas a través del intestino delgado a otros órganos (riñones, hígado, piel y tejido
subcutáneo, ganglios linfáticos, SNC y meninges) que da lugar a hemorragias. A su paso por la pared
intestinal pueden transportar bacterias, generando bacteriemias y sepsis por bacilos gramnegativos. Es un
cuadro infrecuente pero con una mortalidad de hasta el 85%.
1.2. Diagnóstico
La serología (ELISA) es un método muy sensible para el diagnóstico de estrongiloidiasis, aunque puede
haber falsos positivos por reacciones cruzadas con otros nematodos. El examen directo de las heces tiene
una baja sensibilidad, siendo útil sin embargo para descartar la presencia de otros parásitos intestinales. La
técnica de cultivo de heces en para detección de Strongyloides en tres o más muestras de heces aumenta
considerablemente la sensibilidad. Muchos autores recomiendan el empleo de serología y la búsqueda del
parásito en heces de forma combinada para establecer el diagnóstico.
1.3. Tratamiento
El tratamiento de la estrongiloidiasis consiste en administrar ivermectina 200 μg/kg/día durante uno o dos
días consecutivos por vía oral (medicamento extranjero). En el caso de síndrome de hiperinfestación, debe
prolongarse durante 7-10 días y asociar antibioterapia de amplio espectro. Se debe procurar administrar el
tratamiento antihelmíntico antes de la inmunosupresión.
2. ESQUISTOSOMIASIS
2.1. Etiopatogenia y clínica
También llamada bilharziasis, se produce por trematodos del género Schistosoma. Las personas se infectan
cuando las cercarias (formas larvarias del parásito liberadas por caracoles de agua dulce), penetran en la
piel durante el contacto con aguas infestadas. Es endémica en África, y áreas de la península arábiga, Asia y
Sudamérica (focos en Venezuela, Brasil, Surinam e islas del Caribe). Las especies patógenas para el hombre
son S. mansoni, S. haematobium y S. japonicum (y, con menor frecuencia, S. intercalatum y S. mekongi). La
infección tiene un curso insidioso, de tal forma que hasta casi el 95% de los pacientes está asintomático u
oligoasintomático. En la infección aguda puede producirse inicialmente el llamado “prurito del nadador”.
Consiste en un rash papular pruriginoso con eritema y eosinofilia tras el baño que dura 24-72 horas y que
se debe a la penetración de la cercaria a través de la piel. Las semanas posteriores a la exposición se
produce una reacción de hipersensibilidad a la migración del parásito a través de los tejidos, con fiebre
(esquistosomiasis aguda o fiebre de Katayama), anorexia, cefalea, adenopatías, hepatomegalia, urticaria,
dolor abdominal, diarrea y tos seca, acompañada de eosinofilia e hipergammaglobulinemia.
El cuadro clínico suele durar una semana, y en esta fase temprana la serología puede ser negativa y
no existe liberación de huevos del parásito a heces ni a orina. En la fase crónica, los huevos inducen
inflamación granulomatosa con fibrosis. Puede así producir fibrosis hepática periportal con hipertensión
portal, habitualmente sin datos de disfunción hepática (causada fundamentalmente por S. mansoni y S.
japonicum); diarrea crónica y/o suboclusión intestinal; enfermedad genitourinaria, con hematuria
recurrente e indolora los primeros meses o años de la infección, y posteriormente con hidronefrosis y
carcinoma de vejiga (S. haematobium); y afectación neurológica y pulmonar por embolización de los
huevos que se encuentran depositados en los plexos venosos, causando meningoencefalitis (más frecuente
en S. japonicum), mielitis transversa o hipertensión pulmonar.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [781]
[49] ENFERMEDADES IMPORTADAS DEL VIAJERO Y DEL INMIGRANTE
2.2. Diagnóstico
El diagnóstico se realiza mediante la observación de los huevos en orina o semen (S. haematobium) o en
heces. La serología es útil, aunque no permite distinguir infección activa o pasada. En ocasiones puede ser
útil la biopsia rectal o la realización de cistoscopia.
2.3. Tratamiento
El tratamiento de elección es el praziquantel (PZQ) a dosis de 40 mg/kg/día en toma única o repartida en
dos. En el caso de infección por S. japonicum o S. mekongi suele emplearse una dosis de 60 mg/kg/día
repartida en tres tomas. En la fiebre de Katayama se recomienda tratamiento con prednisona (20-30
mg/día) durante al menos cinco días junto al PZQ. Se debe repetir otra dosis de este a las 6-8 semanas. En
caso de neuroesquistosomiasis o mielitis, los esteroides se administran en dosis inicialmente más elevadas
(1,5-2 mg/kg/día), y prolongando su disminución progresiva de 2 a 6 meses.
2.4. Seguimiento
La serología no es útil para el seguimiento. Se recomienda reevaluar la eosinofila, así como una nueva
determinación de parásitos en orina o heces a los 3-6 meses postratamiento, comprobando su viabilidad.
IV. FIEBRE
La fiebre es, después de la diarrea, el motivo de consulta más frecuente en pacientes procedentes
de regiones tropicales. Puede deberse a patógenos tanto habituales en todos los continentes como
endémicos. Estos pacientes deben abordarse con una anamnesis y exploración física exhaustivas, según lo
expuesto en la introducción del capítulo, que nos permitirán elaborar un diagnóstico diferencial razonado.
Merece la pena hacer hincapié en la importancia de la detección del paciente grave y de enfermedades
potencialmente mortales pero curables si se instaura un tratamiento de manera precoz, tales como la
malaria, la fiebre tifoidea o la meningitis bacteriana. Se deben valorar también causas no infecciosas. A
continuación se desarrollan algunas de las entidades más importantes.
1. MALARIA
La malaria o paludismo es una enfermedad producida por protozoos del género Plasmodium,
transmitida a través de la picadura de la hembra del mosquito Anopheles en regiones tropicales (se pueden
consultar las áreas endémicas de malaria actualizadas en la dirección web http://
www.cdc.gov/malaria/travelers/country_table/a.html). Además, se han descrito casos de transmisión
vertical, por transfusiones de sangre, trasplantes de órganos y a través de jeringuillas compartidas.
Cinco especies causan enfermedad en el ser humano: P. falciparum, P. vivax, P. malariae, P. ovale
(P. ovale wallikeri y P. ovale curtisi) y P. knowlesi. La principal especie causante de malaria importada en
nuestro país es P. falciparum (90%) que, además, junto con P. knowlesi, es responsable de los cuadros más
graves. P. vivax y P. ovale tienen la particularidad de poder permanecer en estado latente dentro de los
hepatocitos en forma de hipnozoítos, con capacidad de producir reactivaciones incluso varios años después
de la infección inicial. El periodo de incubación suele ser de 7-14 días, aunque puede ser mucho más
prolongado (como en el caso de toma concomitante de algunos antibióticos o de quimioprofilaxis frente a
malaria, o en el caso de especies distintas de P. falciparum).
La enfermedad se debe a la parasitación directa sobre los hematíes y a la modificación de su
membrana, con los consecuentes fenómenos de citoadherencia y hemólisis que darán lugar a las
manifestaciones clínicas y analíticas.
1.1. Clínica
El único dato necesario para sospechar una malaria es la estancia en un área endémica.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [782]
[49] ENFERMEDADES IMPORTADAS DEL VIAJERO Y DEL INMIGRANTE
La clínica de la malaria es inespecífica, siendo frecuente la presencia de fiebre, así como de cefalea,
artromialgias, astenia, síntomas digestivos (dolor abdominal, náuseas, vómitos, diarrea) y tos seca. En la
exploración física, junto con la fiebre, podemos encontrar esplenomegalia, así como hepatomegalia, palidez
e ictericia. Analíticamente son características las alteraciones en el hemograma (trombocitopenia en el 80-
85% de los casos, anemia, leucopenia) y en la bioquímica (elevación de lactato-deshidrogenasa [LDH] y de
bilirrubina, hipoglucemia, acidosis).
La malaria es una enfermedad potencialmente mortal. En la malaria grave se produce un deterioro
clínico rápido que conduce al fallecimiento si no se instaura un tratamiento precoz. Las embarazadas, los
niños, los inmunodeprimidos y los viajeros no semiinmunes son los grupos de mayor riesgo. Ante un
paciente con malaria (confirmada o sospechada) debemos buscar activamente datos de gravedad (Tabla
VI). Por otra parte, la denominada malaria complicada corresponde a un cuadro de malaria con mala
evolución por motivos diferentes a la propia infección por Plasmodium. Las dos causas principales de
malaria complicada son la sobreinfección bacteriana y la rotura esplénica. La presencia de leucocitosis,
poco frecuente en la malaria, debe hacernos sospechar una malaria complicada.
Tabla VI. Criterios de gravedad de la malaria importada (SEMTSI 2014).
Los pacientes que han padecido malaria previamente pueden presentar un cierto grado de
inmunidad durante 1-2 años que los protege frente a episodios graves posteriores: son los llamados
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [783]
[49] ENFERMEDADES IMPORTADAS DEL VIAJERO Y DEL INMIGRANTE
semiinmunes. En estos pacientes es más frecuente la ausencia de fiebre (incluso pueden permanecer
asintomáticos), así como la presencia de infecciones submicroscópicas.
Las infecciones submicroscópicas son aquellas que muestran microscopia negativa y prueba de
biología molecular positiva; en general, las encontramos en individuos semiinmunes que permanecen
asintomáticos, aunque también podemos verlas en viajeros que han recibido profilaxis antimalárica y
pueden producir clínica o alteraciones analíticas.
1.2. Diagnóstico
La malaria es una enfermedad potencialmente mortal en cuestión de horas y precisa un diagnóstico y
tratamiento urgentes. A continuación se describen las técnicas para dicho diagnóstico.
Diagnóstico microscópico
Las técnicas microscópicas permiten identificar la presencia de parásitos en sangre y aportan
información sobre la especie de Plasmodium y la parasitemia, con valor pronóstico.
Gota gruesa: tiene una elevada sensibilidad (95% en un primer examen), detectando
hasta 5-20 parásitos/μl (parasitemias del 0,0001%). En caso de resultar negativa, debe
repetirse en nuevas muestras a las 12-24 horas y a las 48 horas para excluir el
diagnóstico. Su realización requiere microscopistas expertos. Permite evaluar la
respuesta al tratamiento.
Frotis de sangre periférica: es menos sensible que la gota gruesa (precisa más de 1-500
parásitos/μl), pero tiene la ventaja de permitir una mejor identificación de la especie.
Pruebas de diagnóstico rápido
Los test de diagnóstico rápido (TDR) se basan en la detección rápida de antígenos parasitarios
(en general se emplea un kit con un antígeno específico de P. falciparum [HRP-2] y otro
panmalárico común a todos los Plasmodium [aldolasa o LDH]) mediante técnicas
inmunocromatográficas. Las principales ventajas de esta prueba son su sencillez y rapidez
(menos de 20 minutos). Su sensibilidad disminuye en malaria no Falciparum y con parasitemias
bajas (menos de 100 parásitos/μl). El tratamiento con algunos antibióticos como quinolonas,
cotrimoxazol, macrólidos, clindamicina o tetraciclinas puede disminuir la parasitemia. Por
tanto, debe realizarse siempre de forma paralela una técnica microscópica. Pueden
permanecer positivos hasta 3-4 semanas después de un tratamiento eficaz, por lo que no es útil
en la evaluación de la respuesta al tratamiento. Tampoco permiten la cuantificación de la
parasitemia.
Biología molecular
La PCR (polymerase chain reaction) específica de especie detecta parasitemias muy bajas (0,001
parásitos/μl) con una sensibilidad y especificidad cercanas al 100%. Permite una mejor
caracterización de especie y detección de infecciones mixtas respecto a las otras técnicas.
Además, descubre infecciones submicroscópicas e infección en gestantes con secuestro
placentario de parásitos. Sin embargo, conlleva una mayor demora en el resultado (entre 6 y 24
horas), no distingue entre parásitos viables y no viables, su coste es elevado y queda
normalmente restringida a laboratorios de referencia.
Ante un paciente procedente de un área endémica que refiera fiebre u otra clínica compatible, el
objetivo en las tres primeras horas es conocer si padece o no malaria y, en caso afirmativo, si se debe a P.
falciparum y cuantificar la parasitemia. Solicitaremos las pruebas diagnósticas de manera urgente,
independientemente de la presencia o ausencia de fiebre en ese momento, combinando un TDR con
técnicas microscópicas. Es importante recordar que el principal factor asociado a mal pronóstico es el
retraso en el diagnóstico. La profilaxis no descarta una infección malárica, que además puede presentar
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [784]
[49] ENFERMEDADES IMPORTADAS DEL VIAJERO Y DEL INMIGRANTE
periodos de incubación más largos y con una clínica más larvada. El resultado negativo de las pruebas no
excluye el diagnóstico y, en caso de una alta sospecha clínica, será precisa su repetición en dos ocasiones
más, a las 12-24 horas y a las 48 horas (Figura 2). Asimismo, ante la sospecha de malaria, de cara a la
valoración pronóstica y a descartar complicaciones, se deben realizar una analítica de sangre, incluyendo
hemograma, bioquímica (glucemia, creatinina, perfil hepático y ácido láctico), gasometría y coagulación,
test de embarazo en mujeres en edad fértil y hemocultivos.
1.3. Tratamiento
El retraso en el diagnóstico no debe demorar el inicio de tratamiento antimalárico empírico si la
probabilidad de malaria es alta y el paciente está grave.
Las pautas de tratamiento antimalárico se exponen en la tabla VII. Debido a que muchos de estos
fármacos son teratógenos, las mujeres embarazadas requieren consideraciones especiales.
Malaria con criterios de gravedad
En pacientes con malaria con criterios de gravedad debe iniciarse el tratamiento antimalárico
por vía intravenosa lo más precozmente posible. El artesunato es el fármaco de elección. Se
deberá mantener el tratamiento por vía intravenosa al menos durante las primeras 24 horas,
con paso posterior a una pauta oral. Estos pacientes requieren ingreso en una Unidad de
Cuidados Intensivos, con monitorización de constantes vitales, presión venosa central, diuresis,
nivel de consciencia y glucemia, así como tratamiento de soporte. El manejo de líquidos debe
ser cauteloso debido a la predisposición a desarrollar edema pulmonar no cardiogénico, que
aporta mayor gravedad al cuadro. En caso de sepsis o sospecha de sobreinfección, la
antibioterapia empírica debe incluir cobertura frente a bacterias gramnegativas (ceftriaxona
por vía intravenosa a una dosis de 2 g/24 h) (Tabla VIII).
Malaria sin criterios de gravedad
En estos casos está indicado el tratamiento por vía oral. Dado que son frecuentes las náuseas y
los vómitos, siempre que sea preciso se administrarán antieméticos (no debe combinarse
metoclopramida con atovacuona). En caso de intolerancia oral, aun en ausencia de datos de
gravedad, se seguirán las pautas de tratamiento intravenoso hasta recuperar la tolerancia. Se
debe asegurar una hidratación adecuada. Especialmente en casos de malaria por P. falciparum,
durante las primeras horas se debe reevaluar repetidamente la aparición de datos de gravedad.
Algunas pautas generales a seguir en el tratamiento antimalárico son:
En caso de P. falciparum se recomiendan las combinaciones con artemisinas.
En el resto de las especies, el tratamiento de elección es la cloroquina. Se han descrito
resistencias a este fármaco en P. vivax en personas procedentes del Sudeste asiático y
Oceanía, y en P. malariae en pacientes procedentes de Indonesia; estos casos se
tratarán como P. falciparum.
En P. vivax o P. ovale debe añadirse al tratamiento primaquina para eliminar los
hipnozoítos hepáticos y lograr una cura radical.
Las infecciones mixtas que incluyen P. falciparum deben recibir tratamiento contra esta
especie. Si la infección mixta incluye P. vivax o P. ovale, se añadirá primaquina.
Si el paciente ha tomado profilaxis antipalúdica, se debe emplear un antimalárico
diferente.
Se debe realizar un seguimiento clínico, microbiológico y analítico de todos los casos. Ha de tenerse
en cuenta que una malaria inicialmente no grave puede adquirir en su evolución criterios de gravedad,
especialmente al comienzo del tratamiento y en las infecciones por P. falciparum, pudiendo aparecer
complicaciones incluso días después de iniciado el tratamiento. Los criterios de ingreso hospitalario se
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [785]
[49] ENFERMEDADES IMPORTADAS DEL VIAJERO Y DEL INMIGRANTE
exponen en la tabla VIII. El tratamiento ambulatorio se puede plantear en infecciones por P. vivax, P.
malariae y P. ovale, siempre y cuando estén garantizados el seguimiento ambulatorio para controles
clínico, microbiológico y analítico, una correcta tolerancia y adherencia al tratamiento, y la posibilidad de
volver a Urgencias en caso de empeoramiento.
Tabla VII. Tratamiento de la malaria.
Figura 2. Algoritmo de tratamiento de la malaria.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [786]
[49] ENFERMEDADES IMPORTADAS DEL VIAJERO Y DEL INMIGRANTE
Se debe realizar un seguimiento clínico, microbiológico y analítico de todos los casos. Ha de tenerse
en cuenta que una malaria inicialmente no grave puede adquirir en su evolución criterios de gravedad,
especialmente al comienzo del tratamiento y en las infecciones por P. falciparum, pudiendo aparecer
complicaciones incluso días después de iniciado el tratamiento. Los criterios de ingreso hospitalario se
exponen en la tabla VIII. El tratamiento ambulatorio se puede plantear en infecciones por P. vivax, P.
malariae y P. ovale, siempre y cuando estén garantizados el seguimiento ambulatorio para controles
clínico, microbiológico y analítico, una correcta tolerancia y adherencia al tratamiento, y la posibilidad de
volver a Urgencias en caso de empeoramiento.
Tabla VIII. Criterios de ingreso hospitalario en pacientes con malaria.
La microscopía es el único método microbiológico fiable para controlar la eficacia del tratamiento:
Malaria con criterios de gravedad: realizar gota gruesa a las 12, 24 y 48 horas, y diariamente
hasta su negativización. La elevación de la parasitemia más allá de las 36-48 horas del inicio del
inicio del tratamiento, una disminución de la misma inferior a un 25% a las 48 horas o la
persistencia de formas asexuadas más allá del día 3 (en caso de temperatura > 37,5 °C) o del día
7 (en afebriles) indica fracaso terapéutico. Aunque no hay consenso y dependerá también de la
evolución clínica y analítica, puede ser recomendable repetir la gota gruesa a los 7 y 28 días
(detección de recrudescencias) tras la finalización del tratamiento.
Malaria sin criterios de gravedad: realizar gota gruesa entre los días 3 y 7 y a los 28 días. En
caso de fracaso terapéutico o recidiva se contactará con un especialista en Enfermedades
Infecciosas. Se debe vigilar analíticamente el desarrollo de hemólisis durante las primeras
cuatro semanas postratamiento si se ha empleado artesunato intravenoso (Figura 2).
2. FIEBRE TIFOIDEA
2.1. Epidemiología y clínica
Esta causada por cuatro serotipos de bacterias tifoparatíficas del género Salmonella: S. enterica typhi y S.
enterica paratyphi A, B y C. Los cuadros clínicos más graves (y más frecuentes) se deben a S. enterica typhi y
a S. enterica paratyphi A. Es endémica en el subcontinente indio, el Sudeste asiático, Rusia, Centroamérica,
América del Sur y África. El reservorio es el ser humano. Existen portadores asintomáticos, en los que la
bacteria persiste en la vía biliar, que diseminan la infección a través de heces y orina. El contagio se produce
mediante la ingesta de agua y de alimentos contaminados. El periodo de incubación es de dos semanas (5-
21 días), con un cuadro súbito de fiebre y de malestar general, con dolor abdominal, estreñimiento (aunque
en ocasiones puede haber diarrea), un exantema característico (“roséola tifoídica”, 30%), alteraciones
neurológicas (cefalea, apatía, confusión intermitente, bajo nivel de consciencia), cuadros psicóticos
(ocasionalmente), bradicardia relativa y hepatoesplenomegalia. Son características la normalidad del
hemograma (o disminuciones moderadas de cualquiera de las tres series), hipertransaminasemia leve y
datos de coagulación intravascular diseminada (aunque, habitualmente, sin relevancia clínica). Suele
autolimitarse a tres semanas, pero puede complicarse (perforación intestinal [que suele aparecer a partir
de la segunda semana], hemorragia digestiva, colecistitis subclínica, miocarditis, neumonía lobar).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [787]
[49] ENFERMEDADES IMPORTADAS DEL VIAJERO Y DEL INMIGRANTE
2.2. Diagnóstico
Se realiza mediante el aislamiento del microorganismo en hemocultivos (sensibilidad del 40-80%
[bacteriemias intermitentes]). El cultivo de médula ósea tiene una sensibilidad del 75%. El test de Widal
usado en el diagnóstico serológico tiene bajas sensibilidad y especificidad.
2.3. Tratamiento y prevención
Se debe iniciar tratamiento empírico inicial ante la sospecha clínica, puesto que la mortalidad sin
tratamiento alcanza el 10%. Son de elección las cefalosporinas de tercera generación, la azitromicina y las
fluoroquinolonas. Suele haber resistencias a fluoroquinolonas en Asia del Sur, por lo que hay que evitarlas.
Pueden añadirse corticoides en caso de enfermedad grave. Los pacientes convalecientes pueden eliminar
bacterias en heces durante meses, por lo que se recomienda extremar las medidas de higiene. El
tratamiento de los portadores asintomáticos puede realizarse con ciprofloxacino durante 28 días, o bien
con cotrimoxazol. La vacunación debe ofrecerse a los viajeros a zonas endémicas, pero su eficacia es
moderada (< 60-70%) y no protege frente a todos los serotipos. Por ello la medida preventiva más
importante es evitar el consumo de agua o de alimentos sospechosos.
3. ENFERMEDADES VÍRICAS IMPORTADAS
Se suelen transmitir por la picadura de un artrópodo, y la mayoría son zoonosis. Habitualmente
cursan con un síndrome febril leve autolimitado, aunque en algunas ocasiones pueden desarrollar
manifestaciones muy graves. Suelen clasificarse en tres grandes síndromes, aunque pueden superponerse
(Tabla IX): I) fiebre, artralgia y rash (FAR); II) encefalitis (encefalitis japonesa, encefalitis de San Luis); y III)
fiebres hemorrágicas. A continuación desarrollaremos las más importantes.
3.1. Dengue
Es la segunda causa de fiebre en el viajero transmitida por un vector. Existen cuatro serotipos entre los que
no existe protección cruzada (DENV 1-4). Se transmiten por mosquitos del género Aedes (principalmente
por A. aegypti), que viven en domicilios y sus alrededores y pican durante el día. El periodo de incubación
es de siete días (3-14 días). La clínica más habitual es la de un cuadro pseudogripal de fiebre bifásica con
artromialgias, cefalea retroorbitaria y pulsátil, exantema maculopapular confluente con posibles petequias
y prurito (que, en general, aparece entre el tercer y el quinto día), linfadenopatía y eritema faríngeo. El
dengue clásico se suele acompañar de leucopenia, trombocitopenia, aumento de LDH e
hipertransaminasemia, y se autolimita en 4-7 días. No obstante, puede evolucionar a dengue hemorrágico,
siendo esto más frecuente si se produce una nueva infección por un serotipo diferente (por ello es poco
frecuente en viajeros). El dengue hemorrágico cursa con un cuadro clínico inicial similar al del dengue
clásico. Tras un periodo inicial de 4-7 días presenta una mejoría clínica seguida de (normalmente a partir
del quinto día) manifestaciones hemorrágicas, hemoconcentración (elevación del hematocrito > 20%),
leucopenia y trombocitopenia, shock y distrés respiratorio (secundarios al aumento de permeabilidad
capilar y al fallo multiorgánico). El diagnóstico suele ser clínico y su confirmación se lleva a cabo mediante el
aislamiento del virus en suero o tejidos con PCR o detección antigénica (en fases iniciales), y la
determinación de anticuerpos IgM e IgG específicos (una vez superada la fase febril). El tratamiento es
únicamente sintomático y de soporte. El dengue hemorrágico precisa ingreso en la Unidad de Cuidados
Intensivos (la fase de shock dura habitualmente 24-48 horas; se recomienda evitar la sobrecarga de
volumen durante la recuperación).
3.2. Chikunguña
Tras la picadura del mosquito (que suele ser Aedes aegypti) y un periodo de incubación de 4-8 días,
sobreviene un cuadro agudo de fiebre con artralgias invalidantes, mialgias, cefalea, fotofobia, vómitos,
adenopatías y rash predominantemente troncular. Puede haber fenómenos hemorrágicos leves.
Habitualmente se resuelve en 5-7 días, pero hasta en el 12% se desarrollan artralgias crónicas muy
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [788]
[49] ENFERMEDADES IMPORTADAS DEL VIAJERO Y DEL INMIGRANTE
limitantes. Se han descrito casos de meningoencefalitis en neonatos y ancianos. Hay que hacer diagnóstico
diferencial con el dengue y el virus de Zika (con quienes comparte vector y distribución geográfica y cuya
clínica es muy superponible). Se ha de determinar PCR en suero en caso de presentar menos de 48-72
horas desde el inicio de la clínica, y realizar serología (IgM por ELISA) posteriormente. El tratamiento es
sintomático. Hay que evitar usar antiinflamatorios hasta que no se haya descartado el dengue para no
favorecer las manifestaciones hemorrágicas que este pudiera causar.
Tabla IX. Enfermedades víricas importadas.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [789]
[49] ENFERMEDADES IMPORTADAS DEL VIAJERO Y DEL INMIGRANTE
3.3. Zika
También se transmite por la picadura del mosquito Aedes spp. Sin embargo, se han documentado
transmisiones placentaria y sexual y por transfusiones. La infección es asintomática en el 80% de los
pacientes, y aquellos que desarrollan clínica sufren un cuadro leve con fiebre, rash maculopapular,
artralgias y conjuntivitis, que se resuelve en menos de una semana. Es generalmente benigno, aunque se ha
descrito una posible asociación con síndrome de Guillain-Barré y con microcefalia (en fetos de mujeres
embarazadas infectadas). El diagnóstico se realiza con la determinación de PCR en suero y tejidos durante
la fase inicial (o en sangre de cordón y tejido placentario en casos de neonatos en los que se sospecha
infección), y con serología en fases más tardías. El tratamiento es de soporte, evitando el uso de
antiinflamatorios hasta descartar la existencia de dengue.
3.4 Fiebre amarilla
Tras la picadura del mosquito Aedes spp y un periodo de incubación de 3-6 días sobreviene un cuadro
agudo de fiebre, mialgias, malestar general, cefalea, náuseas y vómitos e inyección conjuntival. Se resuelve
espontáneamente a los 3-4 días en la mayoría de los casos, pero hasta en un 15% de los pacientes, a las 24
horas de esta mejoría inicial se produce una fase “tóxica” de incremento de la fiebre con bradicardia
relativa, ictericia, dolor abdominal y diarrea junto con fracaso renal, trombocitopenia y coagulopatía (que
favorecen las manifestaciones hemorrágicas). La mortalidad de este cuadro, con tratamiento, alcanza el 20-
30%. El diagnóstico se realiza mediante PCR durante los primeros días de la enfermedad o por serología
tras la fase inicial. No hay tratamiento específico, sino únicamente de soporte. Puede prevenirse mediante
la administración de una vacuna de virus vivos atenuados.
3.5 Ébola
Hay cinco tipos de virus del Ébola, cuatro de los cuales producen enfermedad en el ser humano: Zaire,
Sudán, Taï-Forest y Bundibugyo. Se desconoce el reservorio natural, aunque se sospecha que son los
murciélagos y otros mamíferos pequeños. Se contagia por contacto con fluidos (u objetos contaminados)
de personas infectadas a través de mucosas y lesiones cutáneas o de forma percutánea. No hay evidencia
de que se transmita por el aire. El periodo de incubación es de 8-10 días (2-21 días), tras el que aparece un
cuadro agudo de fiebre con postración que se sigue, varios días después, de cefalea, exantema
micropapular, inyección conjuntival, mialgias, vómitos y diarrea sanguinolenta. El 46-71% de los casos son
asintomáticos. Los fenómenos hemorrágicos tienen lugar a partir del tercer día de la enfermedad y se dan
hasta en el 30-70% de los pacientes e incluyen hemorragia digestiva y/o urinaria. Pueden aparecer también
complicaciones pulmonares. Se acompaña habitualmente de leucopenia, seguida por leucocitosis con
linfocitos atípicos, trombocitopenia, coagulopatía, elevación de transaminasas y trastornos
hidroelectrolíticos asociados a vómitos y diarrea. En los casos severos se produce shock hipovolémico con
fallo multiorgánico. El diagnóstico se realiza mediante la determinación de PCR o del antígeno vírico en
fluidos contaminados. Hay que tener en cuenta que en los primeros 3-5 días de la infección puede haber
falsos negativos, por lo que el paciente debe permanecer ingresado si existiera una alta sospecha. La
mortalidad global oscila entre el 30 y el 90% en función de las distintas epidemias y los distintos subtipos.
En la última epidemia de África, en 2014, la mortalidad llegó al 74%. El tratamiento es sintomático, de
soporte. Se debe mantener al paciente en aislamiento estricto y hay que informar a las autoridades locales
ante la sospecha de un caso. Se recomienda consultar protocolos específicos al respecto (Tabla IX).
4. RICKETTSIOSIS
Las rickettsias constituyen un grupo heterogéneo de pequeños cocobacilos y bacilos gramnegativos
de metabolismo intracelular obligado. Tienen distribución mundial. Muchos de ellos son transmitidos por
vectores como garrapatas, ácaros, pulgas o piojos. Sus reservorios habituales son los mamíferos y, en
algunos casos, el hombre. El género Rickettsia produce las fiebres manchadas y los tifus; Orientia, la fiebre
de los matorrales: Coxiella burnetii, la fiebre Q.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [790]
[49] ENFERMEDADES IMPORTADAS DEL VIAJERO Y DEL INMIGRANTE
Las fiebres manchadas en general se transmiten por la picadura de garrapatas. Tras un periodo de
incubación de 5-7 días (3-14 días) aparecen fiebre, mialgias, cefalea, linfadenopatías y rash. En ocasiones se
identifican una o varias de las llamadas “manchas negras” (pequeñas úlceras en el lugar de la inoculación).
En nuestro medio la más frecuente es la fiebre botonosa o fiebre manchada mediterránea, causada por
Rickettsia conorii. Habitualmente tiene un curso leve, aunque puede ser fatal en ancianos o si se retrasa el
tratamiento. Otras fiebres manchadas son la fiebre de las montañas rocosas (Rickettsia rickettsii, en
Estados Unidos, que suele ser severa y no produce mancha negra), y la fiebre por picadura de garrapata
(endémica en África), entre otros.
Los tifus se dividen en epidémico (Rickettsia prowazekii) y endémico (Rickettsia typhi). Tras un
periodo de incubación de 1-2 semanas aparecen fiebre con mialgias, conjuntivitis, postración y rash
maculopapular (generalmente, al final de la primera semana). No existe “mancha negra”. El tifus epidémico
se contagia entre dos personas tras la picadura del piojo. Es endémico en áreas montañosas africanas, Asia
y América Central y del Sur, y tiene una mortalidad de en torno al 10-40% sin tratamiento. El tifus endémico
se transmite por la picadura de la pulga de la rata.
La fiebre de los matorrales, causada por Orientia tsutsugamushi, se transmite por la picadura de
ácaros, y es endémica de zonas rurales y suburbanas de Asia y Australia. En ella se desarrolla una lesión
ulcerosa seguida de un cuadro clínico similar a un tifus. Es frecuente la asociación de una neumonitis, con
alta mortalidad.
La fiebre Q está causada por Coxiella burnetti. Su reservorio está en los ganados ovino y caprino. Se
contagia a través de la inhalación de aerosoles, contacto de fómites infectados o consumo de lácteos no
pasteurizados. Puede ser asintomática. El cuadro clínico queda conformado, habitualmente, por hepatitis
y/o neumonitis o endocarditis con hemocultivos negativos.
El diagnóstico de las rickettsiosis se realiza habitualmente por serología, o bien mediante
determinación de PCR o cultivo celular (en caso de que estén disponibles). En el caso de la fiebre Q, los
anticuerpos de la fase II están inicialmente más elevados que los de fase I (en la fase crónica, sus títulos se
invierten). El tratamiento se realiza con doxicilina o fluoroquinolonas, pudiendo asociarse hidroxicloroquina
en la fiebre Q crónica.
5. ENFERMEDADES PRODUCIDAS POR ESPIROQUETAS
Las fiebres recurrentes son enfermedades causadas por espiroquetas del género Borrelia. Pueden
transmitirse por garrapatas del género Ornithodoros (Borrelia hispanica en nuestro medio) o a través de
piojos (Borrelia recurrentis, más frecuente en áreas de África y América del Sur). El periodo de incubación
es de siete días (2-18 días), tras el que sobreviene un episodio febril agudo con cefalea, mialgias y malestar
general que se autolimita en una semana. Aparecen recidivas en los 5-9 días siguientes, en general más
leves que el primer episodio. Puede haber miocarditis, hepatitis, meningitis, neumonitis y coagulación
intravascular diseminada. La mortalidad sin tratamiento es mayor en el caso de la fiebre recurrente
epidémica transmitida por piojos, pero tanto en ella como en la transmitida por garrapatas la mortalidad se
reduce a menos del 2-5% con el tratamiento adecuado (tetraciclinas, eritromicina).
La leptospirosis es una zoonosis distribuida mundialmente. Las especies más importantes son
Leptospira interrogans y Leptospira weilii. Su reservorio son mamíferos pequeños o grandes (roedores y
ganado, especialmente). El contagio suele producirse a través del contacto directo con agua dulce
contaminada con la orina del animal infectado. Por ello, habitualmente las personas expuestas son poceros,
trabajadores de campos de arroz o viajeros que han practicado actividades recreativas acuáticas. El periodo
de incubación es de 2 a 30 días y la enfermedad presenta tres fases. Durante los primeros 5-7 días se
produce una fase “septicémica”, con fiebre elevada (de patrón clásico bifásico), cefalea, mialgias,
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [791]
[49] ENFERMEDADES IMPORTADAS DEL VIAJERO Y DEL INMIGRANTE
conjuntivitis no purulenta (25%) y hasta fenómenos de vasculitis. En los siguientes 4-30 días se produce la
respuesta inmunitaria, desaparece la fiebre y se origina leptospiruria, que causa insuficiencia renal por
daño tubular. Durante esta fase tiene lugar el síndrome de Weil, con rabdomiólisis, meningitis aséptica
(80%), hepatitis ictérica (el fallo hepático es poco habitual), insuficiencia renal no oligúrica e incluso
afección pulmonar con hemorragia alveolar y miocarditis (esta fase tiene una mortalidad del 5-30%).
Finalmente existe una fase de convalecencia en la que se excretan las bacterias en orina durante meses. En
caso de curación no hay secuelas. El diagnóstico se basa en la sospecha clínica: fiebre, cefalea, mialgias en
las pantorrillas y proteinuria de aparición brusca en paciente con antecedente epidemiológico sugieren
fuertemente el diagnóstico; conjuntivitis, meningismo y hepatitis tienen elevado valor confirmatorio. Se
confirma mediante el cultivo del microorganismo. Este es lento y requiere medios especiales, por lo que
tiene una baja sensibilidad; son de elección los hemocultivos en las fases iniciales (fase septicémica) y de
orina en fases posteriores (a partir de la segunda semana). La PCR permite el diagnóstico temprano, pero
no está disponible en todos los centros. La serología tiene sensibilidad y especificidad cercanas al 90% (IgM
detectable a partir del quinto-séptimo día del inicio de los síntomas). La microscopía de orina en campo
oscuro es poco sensible. El tratamiento de elección es la doxicilina (200 mg/día durante siete días) en las
formas leves, pero en las graves se han de emplear ceftriaxona, cefotaxima, penicilina G o doxiciclina junto
con el adecuado tratamiento de soporte. Hay que recordar que las penicilinas y las cefalosporinas no tienen
actividad contra rickettsias en caso de plantearnos un diagnóstico diferencial con ellas en ausencia de
confirmación de leptospirosis.
V. SÍNDROMES DIGESTIVOS
1. DIARREA DEL VIAJERO
La diarrea del viajero es la enfermedad más frecuente en viajeros internacionales, pudiendo afectar
al 30-70% de esta población. Las áreas geográficas de mayor riesgo son las regiones tropicales o
subtropicales con pobres medidas de higiene. La infección generalmente se transmite a través de agua y
alimentos contaminados. La etiología bacteriana es la más frecuente (80-90%), encabezada por Escherichia
coli enterotoxigénico (Tabla X).
Tabla X. Etiología de la diarrea del viajero.
El cuadro de diarrea, de instauración brusca y gravedad variable, puede asociar náuseas, vómitos,
dolor abdominal, fiebre o deposiciones sanguinolentas. Sin tratamiento, la diarrea suele autolimitarse en 2
a 7 días. En el caso de la diarrea por parásitos, la instauración suele ser más gradual y la evolución más
prolongada. Es importante la reposición hidrosalina mediante rehidratación oral. El uso de antibióticos
acorta el tiempo de enfermedad, siendo recomendable en caso de interferencia con las actividades o datos
de gravedad. Se pueden administrar desde la primera deposición diarreica, empleándose ciprofloxacino
500 mg en dosis única o cada 12 horas durante 1-3 días en función de la respuesta. En el Sudeste asiático
existe una alta prevalencia de cepas de Campylobacter resistentes a quinolonas, siendo de elección la
azitromicina (500 mg/24 h de 1 a 3 días). Puede asociarse loperamida al tratamiento antibiótico al inicio del
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [792]
[49] ENFERMEDADES IMPORTADAS DEL VIAJERO Y DEL INMIGRANTE
cuadro, aunque no se recomienda en casos de diarrea sanguinolenta o fiebre. En caso de persistencia de la
diarrea u otros síntomas gastrointestinales durante más de 14 días, nos debemos plantear:
Infección persistente o coinfección por un segundo microorganismo (descartar infección por
VIH):
Parásitos: deben ser la principal sospecha; de ellos, Giardia lamblia es el más
frecuentemente identificado (puede valorarse su tratamiento empírico [metronidazol
250 mg/8 h durante 7-10 días o tinidazol 2 g en dosis única] en caso de estudios
microbiológicos negativos) (Tabla X).
Diarrea por Clostridium difficile secundaria al tratamiento antibiótico o a la profilaxis
antimalárica.
Algunos casos de diarrea persistente debidos al denominado esprúe tropical,
consistente en un cuadro de malabsorción y déficit de folato y vitamina B12, de
etiología desconocida y buena respuesta al tratamiento con tetraciclinas.
Patología intestinal previa no conocida y desenmascarada por el proceso infeccioso agudo:
Celiaquía.
Enfermedad inflamatoria intestinal.
Cáncer colorrectal.
Síndrome de intestino irritable posinfeccioso: constituye un diagnóstico de exclusión.
2. AMEBIASIS
Entamoeba histolytica, de distribución mundial, es altamente prevalente en el subcontinente indio,
Extremo Oriente, África, México y otras partes de Centroamérica y Sudamérica, constituyendo la segunda
causa de muerte por parasitosis intestinal a nivel mundial. La infección se adquiere con la ingesta de quistes
que contaminan el agua y los alimentos. También puede producirse transmisión de quistes o trofozoítos
por vía sexual oral/anal. Su nombre hace referencia a su capacidad para producir daño tisular, habiéndose
descrito la trogocitosis amebiana (ingesta de fragmentos de células vivas que conducirá a la muerte celular)
como uno de los principales mecanismos de lesión. El 90% de los infectados permanecen asintomáticos,
mientras que en el 10% restante se producirá invasión intestinal por trofozoítos, habitualmente entre una y
tres semanas tras la infección (dentro de los cinco primeros meses en el caso del absceso amebiano),
aunque puede presentarse hasta años después de la infección. La colitis amebiana se manifiesta
generalmente con diarrea sanguinolenta y dolor abdominal; algunas complicaciones, como la perforación o
la sobreinfección bacteriana de las úlceras, ensombrecen el pronóstico. En casos cronificados pueden
formarse amebomas, pudiendo simular un cáncer de colon. También puede producirse diseminación
extraintestinal, más frecuentemente al hígado a través del sistema portal, con formación del absceso
hepático amebiano, en general sin colitis concurrente. Menos frecuentemente se produce afectación
pulmonar, cardiaca o del sistema nervioso central.
2.1. Diagnóstico
E. histolytica es morfológicamente indistinguible de E. dispar, E. moshkovskii y E. bangladeshi que, en
general, se consideran comensales, aunque existen dudas sobre un posible papel patogénico de las dos
últimas. Esto, junto con su baja sensibilidad, hace de la microscopía una herramienta con valor diagnóstico
limitado. El diagnóstico mediante detección antigénica o PCR permite diferenciar E. histolytica de E. dispar
y E. moshkovskii; se trata de pruebas con gran sensibilidad y especificidad. Estas pruebas diagnósticas
suelen realizarse sobre muestras de heces o de material aspirado de abscesos. La serología posee también
una alta sensibilidad y especificidad, si bien puede ser negativa durante los primeros días y no diferencia
infección presente de infección pasada, por lo que es más útil fuera de áreas endémicas.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [793]
[49] ENFERMEDADES IMPORTADAS DEL VIAJERO Y DEL INMIGRANTE
2.2. Tratamiento
El tratamiento de la amebiasis sintomática implica dos pasos: en primer lugar se debe administrar un
agente amebicida (metronidazol 500 o 750 mg/8 h durante 10 días; o alternativamente se puede emplear
tinidazol 2 g/24 h durante 5 días); y, en segundo lugar, un agente quisticida luminal (paromomicina 25-35
mg/kg/día dividido en tres dosis durante 7-10 días; o como alternativas se pueden emplear furoato de
diloxanida 500 mg/8 h durante 10 días o yodoquinol 650 mg/8 h durante 20 días). En portadores
asintomáticos se recomienda un tratamiento quisticida.
VI. SÍNDROME RESPIRATORIO
En nuestro medio, las causas más frecuentes de síndrome respiratorio en pacientes inmigrantes y
viajeros son las mismas que en población general. No obstante, se debe tener en cuenta el antecedente
epidemiológico de riesgo para pensar en otras etiologías una vez han sido evaluadas las más habituales. La
tuberculosis se aborda en un capítulo al respecto en este manual (ver Capítulo 45. “Tuberculosis”). En este
apartado desarrollaremos los síndromes respiratorios provocados por agentes “tropicales”, como las
micosis endémicas. Otras parasitosis que lo desarrollan son la hidatidosis, la paragonimiasis y los ya
descritos síndrome de hiperinfestación por Strongyloides stercoralis y la fiebre de Katayama.
1. HISTOPLASMOSIS
Está producida por Histoplasma capsulatum. La variante H. capsulatum var. capsulatum es
endémica de América, Asia y este de África, y causa infección pulmonar aguda o crónica, linfadenopatía
hiliar, pericarditis y manifestaciones articulares. En el caso de pacientes inmunodeprimidos se genera una
histoplasmosis diseminada, que cursa con un síndrome linfoadenopático con hepatoesplenomegalia e
infiltración cutánea (pápulas ulceradas) y de médula ósea (pancitopenia). La variante H. capsulatum var.
duboisii es endémica del este y centro de África y habitualmente origina una forma local de infección ósea,
ganglionar o cutánea que, en ocasiones, se disemina para afectar fundamentalmente al pulmón y al tracto
gastrointestinal.
2. BLASTOMICOSIS
Es una infección sistémica causada por Blastomyces dermatitidis, endémico de Norteamérica,
África, India y Oriente Medio. En ella predomina la afección pulmonar y cutánea, en forma de nódulos que
posteriormente se ulceran y pueden llegar a causar necrosis ósea.
3. COCCIDIOIDOMICOSIS
Viene provocada por Coccidioides immitis, hongo endémico de regiones áridas de América.
Inicialmente afecta al pulmón y posteriormente se disemina a meninges, articulaciones y piel.
4. PARACOCCIDIOIDOMICOSIS
Está generada por Paracoccidioides brasiliensis. Es una enfermedad granulomatosa que ha tenido
brotes episódicos en América del Sur y Central. Presenta una forma aguda, con fiebre, pérdida de peso,
hepatoesplenomegalia y un cuadro poliadenopático, con infrecuente afección pulmonar; y una forma
crónica, en la que existen disnea y tos, lesiones ulcerosas mucocutáneas y pérdida de peso, que evoluciona
a una fase de fibrosis pulmonar.
El diagnóstico se realiza mediante la visualización del hongo en los tejidos infectados. La
histoplasmosis se puede diagnosticar en nuestro medio mediante serología y PCR. El tratamiento de las
micosis endémicas se hace con anfotericina B liposomal, a la que habrá que añadir fluconazol en la
meningitis por coccidioidomicosis. En la histoplasmosis ha de mantenerse itraconazol durante tres meses
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [794]
[49] ENFERMEDADES IMPORTADAS DEL VIAJERO Y DEL INMIGRANTE
tras la mejoría clínica con anfotericina B liposomal. Las secuelas crónicas de la paracoccidioidomicosis
pueden necesitar tratamientos médico y quirúrgico dependiendo de cronología, localización, etc.
VII. SÍNDROME NEUROLÓGICO
En este apartado se describen las principales meningitis a considerar en un paciente con factores de
riesgo (no se abordan otras enfermedades como la rabia o el tétanos por superar el propósito de esta
obra). La criptococosis y la tuberculosis producen habitualmente meningitis aguda (ver Capítulo 46.
“Infección por VIH”).
1. ENFERMEDAD MENINGOCÓCICA EPIDÉMICA
Está producida por Neisseria meningitidis del grupo A. Es endémica, con brotes epidémicos cada 2-
10 años, en el llamado “cinturón de la meningitis”, que se extiende por el África subsahariana desde
Senegal hasta Etiopía. Se recomienda la vacunación si se viaja a una región endémica o con brote
epidémico activo (ver Capítulo 42. “Infecciones del sistema nervioso central”).
2. CISTICERCOSIS
Se produce por enquistamiento de larvas del cestodo Taenia solium en los tejidos, con nódulos
subcutáneos o intramusculares y afección del sistema nervioso central (que da lugar a meningitis, lesión
ocupante de espacio, epilepsia e hidrocefalia). El diagnóstico se realiza mediante examen de heces,
serología y/o estudio radiológico con TAC o RM. La serología puede dar falsos positivos por reacción
cruzada con Taenia saginata y Echinococcus spp. El tratamiento de la neurocisticercosis es complejo, por lo
que debe buscarse la opinión de expertos; el más importante y primero a instaurar es el antiepiléptico; el
antiparasitario está indicado en algunas formas de la enfermedad (puede hacerse con PZQ 50 mg/kg/día
repartido en tres dosis durante 15 días, y/o albendazol 15 mg/kg/día repartido en tres dosis, durante 14-28
días), asociado a dexametasona para disminuir la reacción inflamatoria producida por la muerte del
parásito.
3. MENINGOENCEFALITIS POR AMEBAS
Es una enfermedad muy rara y con elevada mortalidad. Está causada por Naegleria fowleri, y se
produce tras la invasión amebiana del sistema nervioso central a través de la lámina cribosa tras bañarse en
aguas dulces. Causa una encefalitis aguda con necrosis del sistema nervioso central. Es necesario hacer un
diagnóstico diferencial con la meningitis bacteriana. Acanthamoeba spp provoca una encefalitis
granulomatosa crónica en pacientes inmunocomprometidos.
VIII. FILARIASIS (Tabla XI)
1. FILARIASIS LINFÁTICAS
Son un conjunto de enfermedades causadas por tres especies distintas de filarias con diferente
distribución geográfica: Wuchereria bancrofti, Brugia malayi y Brugia timori. Se transmite a través de la
picadura de un mosquito; el insecto inocula larvas que a su vez migran a los ganglios linfáticos, donde se
desarrollan hasta convertirse en gusanos adultos capaces de sobrevivir durante años. Habitualmente, en la
filariasis linfática se produce una fase aguda con fiebre, cefalea y mialgias, acompañadas de
orquitis/orquiepididimitis y/o celulitis con linfangitis, y una fase crónica (que se desarrolla tras varios
episodios agudos continuos), con hidrocele y linfedema (elefantiasis), generalmente asimétrico. En
ocasiones producen eosinofilia pulmonar tropical, con tos y sibilancias nocturnas. El diagnóstico se realiza
mediante la visualización de las microfilarias en sangre. El tratamiento de elección es dietilcarbamazina
(DEC) en dosis de 6 mg/kg/día en tres dosis durante 12 días con doxicilina 100-200 mg/día durante 6-8
semanas (con el que se trata la bacteria endosimbionte Wolbachia spp). En pacientes con elevada carga
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [795]
[49] ENFERMEDADES IMPORTADAS DEL VIAJERO Y DEL INMIGRANTE
parasitaria se recomienda iniciar tratamiento con una dosis baja e ir aumentándola progresivamente. Como
alternativa se puede usar albendazol 400 mg en dosis única en combinación con ivermectina 150-200
mg/kg, también en dosis única.
Tabla XI. Microfilarias.
2. ONCHOCERCA VOLVULUS
Endémica del oeste de África y transmitida por moscas que habitan en los ríos, produce patología
cutánea y ocular (“ceguera de los ríos”). Se diagnostica mediante la visualización de la forma adulta en el
oncocercoma o de la microfilaria en la biopsia cutánea, o bien mediante exploración oftalmológica. Se trata
con ivermectina 150 mg/kg en dosis única, y se repetirá cada 6-12 meses hasta que el paciente quede
asintomático, junto con doxicilina 100-200 mg/día durante 6-8 semanas (tratamiento de la bacteria
endosimbionte Wolbachia spp). Previamente a su inicio debe descartarse siempre una infección
concomitante por Loa loa, puesto que la DEC usada en el tratamiento de esta última aumenta la toxicidad
ocular y el riesgo de ceguera. El tratamiento de la coinfección es complejo, y se recomienda disminuir lo
máximo posible la carga parasitaria de Loa loa con albendazol 400 mg/día durante tres semanas, para
después tratar O. volvulus con ivermectina, asociada o no a doxicilina.
3. LOA LOA
Es endémica del centro de África y se transmite por la picadura del tábano Chrysops. La migración
de la larva produce un angioedema transitorio llamado “de Calabar”. El diagnóstico se establece mediante
la visualización de la filaria en sangre (periodicidad diurna). El tratamiento se hace con DEC 9 mg/kg/día en
tres dosis durante 12 días. Al igual que en las filariasis linfáticas, en sujetos con moderada carga parasitaria
se recomienda una pauta escalonada de DEC o bien comenzar tratamiento con albendazol (400 mg/día
durante cuatro semanas) para disminuir la carga parasitaria, seguido posteriormente de DEC. No es
necesaria la terapia con doxiciclina, pero sí descartar siempre la presencia de O. volvulus antes del inicio del
tratamiento, puesto que los pacientes con Loa loa tratados con ivermectina corren riesgo elevado de sufrir
encefalopatía. Puede considerarse el uso de corticoides para reducir la reacción inmunitaria producida por
la muerte de las microfilarias (prednisolona 20 mg/día tres días antes y una vez iniciado el tratamiento).
BIBLIOGRAFÍA
Ali IKM. Intestinal amebae. Clin Lab Med. 2015;35:393-422.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [796]
[49] ENFERMEDADES IMPORTADAS DEL VIAJERO Y DEL INMIGRANTE
Bakajika DK, Nigo MM, Lotsima JP, et al. Filarial antigenemia and Loa loa night blood microfilaremia in
area without bancroftian filariasis in the Democratic Republic of Congo. Am J Trop Med Hyg.
2014;91(6):1142-8.
CDC. Yellow Book 2016.
Connor BA. Chronic diarrhea in travelers. Curr Infect Dis Rep. 2013;15:203-10.
Chikeka I, Dumler JS. Neglected bacterial zoonoses. Clin Microbiol Infect. 2015; 21(5):404-15.
Danso-Appiah A, Donegan PL, Sinclair S, Utzinger J. Drugs for treating Schistosoma mansoni infection.
Cochrane Review. 2013;2:1-177.
Dengue: Guías de atención para enfermos en las Américas. Organización Panamericana de la Salud,
2010.
Díaz-Menéndez M, Norman F, Monge-Maillo B, et al. La filariasis en la práctica clínica. Enferm Infecc
Microbiol Clin. 2011;29(Suppl 5):27-37.
Kramer CV, Zhang F, Sinclair D, Olliaro PL. Drugs for treating urinary schistosomiasis. Cochrane Review.
2014;8:1-201.
Monge-Maillo B, López-Vélez R, Norman FF, Ferrere-González F, Martínez-Pérez A, Pérez-Molina JA.
Screening of imported infectious diseases among asymptomatic sub-Saharan African and Latin
American immigrants: a public health challenge. Am J Trop Med Hyg. 2015;92:848-56.
Morillo CA, Marín-Neto JA, Avezum A, et al. Randomized trial of benznidazole for chronic Chagas
cardiomyopathy. N Engl J Med. 2015;373:1295-306.
Muñoz J, Rojo-Marcos G, Ramírez-Olivencia G, Salas-Coronas J, Treviño B, Pérez Arellano JL.
Diagnóstico y tratamiento de la malaria importada en España: recomendaciones del Grupo de Trabajo
de Malaria de la Sociedad Española de Medicina Tropical y Salud Internacional (SEMTSI). Enferm
Infecc Microbiol Clin. 2015;33(6):e1-13.
Pérez-Arellano JL, Carranza-Rodríguez C. Estrategias de cribado en población inmigrante recién llegada
a España. Enferm Infecc Microbiol Clin. 2016;34(1):45-52.
Pérez-Arellano JL, Pardo J, Hernández-Cabrera M, Carranza C, Angel-Moreno A, Muro A. Manejo práctico
de una eosinofilia. An Med Intern (Madrid). 2004;21:244-52.
Pritt BS, Clark CG. Amebiasis. Mayo Clin Proc. 2008;83(10):1154-60.
Ralston KS, Solga MD, Mackey-Lawrence NM, Somlata, Bhattacharya A, Petri WA Jr. Trogocytosis by
Entamoeba histolytica contributes to cell killing and tissue invasion. Nature. 2014;508(7497):526-30.
Ramírez-Olivencia G, Cuesta MA, Bravo A, et al. Imported strongyloidiasis in Spain. Int J Infec Dis.
2014;18:32-7.
Rojo-Marcos G, Cuadros-González J. Malaria y protozoos intestinales. Enferm Infecc Microbiol Clin.
2016;34(3):191-204.
Rougeron V, Feldmann H, Grard G, et al. Ebola and Marburg haemorrhagic fever. J Clin Virol.
2015;64:111-9.
Salas-Coronas J, Cabezas-Fernández MT, Vázquez-Villegas J, Soriano-Pérez MJ, Lozano-Serrano AB,
Pérez- Camacho I, et al. Evaluation of eosinophilia in immigrants in Southern Spain using tailored
screening and treatment protocols: a prospective study. Travel Med Infect Dis. 2015;13: 315-21.
Shah N, DuPont HL, Ramsey DJ. Global etiology of travelers’ diarrhea: Systematic review from 1973 to
the present. Am J Trop Med Hyg. 2009;80(4):609-14.
Torrús D, Carranza C, Ramos JM, Rodríguez JC, Rubio JM, Subirats M, et al. Diagnóstico microbiológico
de la malaria importada. Enferm Infecc Microbiol Clin. 2015;33(Supl 2):40-46.
WHO. Guidelines for the treatment of malaria. 3rd edition. World Health Organization; 2015.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [797]
[50] EXPOSICIÓN A MATERIAL BIOLÓGICO
50.Exposición a material biológico
Alejandra Morales Cartagena.
Medicina Interna. Unidad de Enfermedades Infecciosas
Manuel Valdivia Guijarro.
Medicina Preventiva
Asesora: Carmen Muñoz Ruipérez. Jefa de Sección de Medicina del Trabajo. Prevención de Riesgos Laborales
I. INTRODUCCIÓN
Los accidentes biológicos constituyen el riesgo laboral más frecuente en el personal sanitario. Un
accidente biológico es la exposición laboral a agentes biológicos (material potencialmente infeccioso:
sangre y fluidos) por vía percutánea (pinchazos o cortes con objetos afilados) o por contacto con mucosas o
piel no íntegra (agrietada, erosionada o con dermatitis), que conlleva un riesgo para el trabajador de
contraer una infección por los virus de la hepatitis B (VHB), de la hepatitis C (VHC) o de la inmunodeficiencia
humana (VIH). Aunque existen otros virus y microorganismos transmisibles por estas vías, su contagio es
mucho menos probable.
La mejor forma de prevenir la transmisión ocupacional es evitar la exposición, considerando que
todos los pacientes son potencialmente infecciosos, y debiendo extremar la precaución en el manejo de
sangre y fluidos corporales (líquido cefalorraquídeo [LCR], pleural, peritoneal, sinovial y amniótico, semen,
secreciones vaginales y leche materna), y también de las muestras de laboratorio que contienen virus.
Existe riesgo de contagio con otros fluidos (secreciones nasales, saliva, esputo, lágrimas, orina, sudor, heces
y vómito) cuando están contaminados con sangre.
1. MEDIDAS DE PRECAUCIÓN UNIVERSALES
Vacunación contra la hepatitis B: indicada en todos los trabajadores que realicen su actividad
en el medio sanitario y se encuentren en contacto directo o indirecto con sangre u otros
fluidos.
Lavado de manos antes y después de cada actividad (aunque se hubieran utilizado guantes).
Cobertura de lesiones cutáneas (cortes, heridas, etc.) con apósitos impermeables antes de
iniciar la actividad.
Desinfección y esterilización de todos los objetos contaminados de acuerdo con las normas
específicas de cada centro.
2. ELEMENTOS DE PROTECCIÓN BARRERA
Dependerán del procedimiento que se vaya a realizar.
Guantes. Se usarán siempre que exista contacto con piel no intacta o mucosas del paciente, y
también al manejar sangre o fluidos contaminados u objetos, materiales o superficies
contaminadas o presumiblemente contaminadas por material orgánico o inorgánico
potencialmente dañino. Deben utilizarse guantes en todo procedimiento invasivo.
Batas, mascarillas y protectores oculares. Indicados en casos en los que se prevea la aparición
de salpicaduras de sangre u otros fluidos (endoscopias, aspiración de secreciones, manipulación
de equipos de fisioterapia respiratoria, hemorragias importantes…).
3. MANEJO DE OBJETOS PUNZANTES O CORTANTES
Los trabajadores deberán poner especial atención en el manejo de agujas, lancetas, hojas de bisturí
y cualquier otro objeto cortante o punzante, durante y tras su uso. Las agujas, una vez utilizadas, nunca
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [798]
[50] EXPOSICIÓN A MATERIAL BIOLÓGICO
deben ser reencapuchadas ni sometidas a manipulación alguna. Se deben desechar estos objetos en
envases apropiados inmediatamente después de su uso.
4. REDUCIR PROCEDIMIENTOS DE RIESGO
Unificar extracciones de sangre. Evitar en la medida de lo posible las técnicas quirúrgicas en las que
no se visualice de forma directa la aguja o el bisturí. Se evitarán también los procedimientos de sutura
entre dos cirujanos en los que se pierda de vista la punta de los dedos. Actualmente en el Hospital 12 de
Octubre, debido a la introducción de los dispositivos de seguridad biológica (Orden 827/2005, de 11 de
mayo, de la Consejería de Sanidad y Consumo de la Comunidad de Madrid, por la que se establecen e
implantan los procedimientos de seguridad y el sistema de vigilancia frente al accidente con riesgo
biológico en el ámbito sanitario de la Comunidad de Madrid), el accidente biológico más habitual es el
ocurrido en quirófanos por agujas de sutura, constituyendo el objeto más frecuentemente implicado en los
accidentes biológicos penetrantes.
II. ACTUACIÓN ANTE UNA EXPOSICIÓN ACCIDENTAL
1. ACTUACIÓN INMEDIATA
La actuación ante una exposición accidental queda detallada en la tabla I.
Tabla I. Actuaciones inmediatas ante una exposición accidental.
Asistencia: durante el horario laboral el paciente deberá acudir cuanto antes tras el accidente al
Servicio de Prevención de Riesgos Laborales. En el Hospital 12 de Octubre, fuera de este horario deberá ser
atendido en el Servicio de Urgencias (Medicina Interna).
2. VALORACIÓN DEL RIESGO Y MEDIDAS GENERALES
2.1. Evaluación de la exposición
Exposiciones de riesgo. Percutánea, contaminación de mucosas, conjuntivas y piel no intacta,
lesión por mordedura humana que resulta en una herida abierta.
Materiales de riesgo. La sangre y los fluidos corporales que contengan sangre son los de mayor
riesgo. Otros potencialmente infecciosos: semen, secreciones vaginales, leche materna, LCR,
líquidos sinovial, pleural, peritoneal, pericárdico y amniótico. También es de riesgo el contacto
directo con el virus en el laboratorio.
Tipo de vehículo. Aguja hueca (mayor riesgo), aguja maciza, bisturí, etc.
Gravedad. Profundidad del pinchazo, cantidad de fluido en la exposición mucocutánea. La
situación de mayor riesgo se produce tras la punción con aguja hueca contaminada con sangre
de una persona infectada.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [799]
[50] EXPOSICIÓN A MATERIAL BIOLÓGICO
2.2. Evaluación de la presencia de infección en el paciente fuente
Revisar la historia clínica.
En caso de desconocer la situación serológica (o que la última serología sea de hace más de dos
meses) se solicitarán, previa autorización del paciente (oral o por escrito), las siguientes determinaciones:
Serología VIH (ELISA): se recomienda realizar una prueba de 4ª generación (incluye la detección
de anticuerpos y de antígeno p24). En caso de ser positiva, solicitar carga viral. Será importante
conocer el tipo de tratamiento antirretroviral (TAR), si lo recibe, la historia farmacológica y los
motivos de posibles cambios de tratamiento (resistencias o intolerancia) del paciente fuente.
VHB: solicitar antígeno AgHBs.
VHC: anticuerpos (Ac) anti-VHC. Considerar solicitar carga viral del VHC en caso de
inmunodepresión avanzada o presencia de otras enfermedades que se asocien con la
posibilidad de un falso negativo de la serología.
Se deberá considerar como infectado en caso de no dar consentimiento o si la fuente es
desconocida.
2.3. Evaluación de la susceptibilidad del trabajador expuesto
Según los resultados de la fuente se solicitarán al trabajador expuesto (tras consentimiento informado):
Si la fuente es positiva para el VIH: serología urgente de VIH (ELISA), prueba de 4ª generación
recomendada.
Si la fuente es positiva para el AgHBs: determinar título de Ac anti-HBs en el trabajador (en las
primeras 24 horas tras el accidente).
Si la fuente es positiva para el VHC: hacer serología de VHC en el trabajador.
Si la fuente es desconocida o no es posible obtener sus datos serológicos, se solicitarán al
trabajador expuesto: serología VIH (ELISA), título de anti-HBs y serología de VHC.
2.4. Otras consideraciones y pruebas complementarias
Se debe mantener la confidencialidad del trabajador accidentado.
Solicitar hemograma completo y bioquímica general que incluya enzimas hepáticas y
parámetros de función renal.
En casos de exposición no ocupacional por contacto sexual, incluir pruebas diagnósticas de
otras infecciones de transmisión sexual (sífilis, gonococo y Chlamydia) y valorar tratamiento
empírico de uretritis bacteriana en caso de que no se pudiera garantizar el seguimiento
(ceftriaxona 500 mg intramuscular [im] u otra cefalosporina de 3ª generación, en dosis única, y
azitromicina 1-2 g vía oral [vo] en dosis única).
En la exposición parenteral es recomendable conocer el estado vacunal del tétanos (del caso
expuesto) y vacunar o usar una dosis de recuerdo en caso necesario (esta medida no es
específica para el accidente biológico en el ámbito sanitario).
Prueba de embarazo: debe realizarse siempre que vaya a instaurarse terapia con fármacos
antirretrovirales en una mujer en edad fértil con posibilidades de estar embarazada.
Todos los pacientes que vayan a iniciar un tratamiento de profilaxis postexposición (PPE) deben
firmar un documento de consentimiento informado.
Informar sobre el cuadro clínico de la primoinfección por VIH, así como de posibles síntomas de
hepatitis aguda (en el caso de VHB y VHC) e indicar que deben consultar de inmediato en caso
de presentar síntomas compatibles.
Ofrecer apoyo psicológico.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [800]
[50] EXPOSICIÓN A MATERIAL BIOLÓGICO
3. SEGUIMIENTO
Las actuaciones deben iniciarse lo antes posible, preferiblemente antes de las 4-6 horas del
accidente y siempre antes de las 72 horas, manteniendo el seguimiento serológico durante un mínimo de
seis meses (24 semanas) y de 12 meses en caso de coinfección VIH + VHC. Algunos autores recomiendan
ampliar el seguimiento a un año, incluso en casos de exposición única al VIH, por riesgo de seroconversión
tardía. Durante este periodo, sobre todo durante las primeras 12 semanas, deberán seguirse las
recomendaciones para evitar una posible transmisión secundaria (ver más adelante).
III. EXPOSICIÓN AL VIRUS DE LA HEPATITIS B
1. GENERALIDADES
Las personas con infección previa por VHB son inmunes a la reinfección y no precisan profilaxis
postexposición (PPE). En las medidas a adoptar será necesario tener en cuenta la serología de la fuente y el
estado de vacunación, así como la respuesta a la vacuna del trabajador expuesto. Se considera que el
trabajador es susceptible de infección por el VHB cuando no está vacunado o cuando, estando vacunado,
presente un título de Ac anti-HBs < 10 mUI/ml posvacunales.
2. SEGUIMIENTO
Determinación de anti-HBs de uno a dos meses después de la última dosis de la vacuna. No es
valorable si se ha recibido IGHB (inmunoglobulina de la hepatitis B) en los tres o cuatro meses previos.
Tabla II. Profilaxis postexposición ocupacional y no ocupacionala al virus de la hepatitis B.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [801]
[50] EXPOSICIÓN A MATERIAL BIOLÓGICO
3. EDUCACIÓN Y CONSEJOS SANITARIOS
Las personas anti-HBs negativas que han sufrido una exposición a AgHBs no necesitan tomar
precauciones especiales para prevenir la transmisión secundaria durante el periodo de seguimiento: no es
necesario modificar las prácticas sexuales, evitar el embarazo o interrumpir la lactancia. Sin embargo, se
debe evitar donar sangre, plasma, tejidos, órganos o semen.
4. ESTRATEGIAS DE PROFILAXIS
Estrategias de profilaxis posexposición ocupacional y no ocupacional al VHB se detallan en tabla II.
IV. EXPOSICIÓN AL VIRUS DE LA HEPATITIS C
La incidencia media de seroconversión después de una exposición percutánea con una fuente
positiva para el VHC es del 1,8% (0-7%). Es infrecuente a través de exposición mucosa y no está descrito en
contacto con piel intacta. No existe una profilaxis efectiva frente al VHC, pues la cinética viral demuestra
que debe haber ya una infección establecida para que el tratamiento sea eficaz. Por ello es importante el
seguimiento de estos pacientes para poder diagnosticar cuanto antes una posible infección aguda por el
VHC, en cuyo caso el tratamiento puede ser más eficaz.
Seguimiento cuando la fuente es positiva para el VHC:
Determinación basal, a los 4 y a los 6 meses de anti-VHC y de transaminasas.
Confirmar resultados positivos mediante técnica de inmunoblot o determinación cuantitativa
del ARN-VHC.
Informar al trabajador de los síntomas sugestivos de infección aguda por VHC, e indicar que
deberá consultar en caso de que aparezcan.
No es necesario que tome precauciones especiales para evitar la transmisión secundaria
durante el periodo de seguimiento, salvo que no podrá donar sangre, plasma, tejidos u órganos
(aunque algunos autores recomiendan empleo de preservativo en las relaciones sexuales
durante los primeros 6 meses de seguimiento).
Si existe coinfección VHC y VIH se debe prolongar el seguimiento a 12 meses.
Si la fuente es anti-VHC negativo no es necesario tomar ninguna medida.
V. EXPOSICIÓN AL VIRUS DE LA INMUNODEFICIENCIA HUMANA
1. EXPOSICIÓN OCUPACIONAL
1.1. Riesgo de transmisión
El riesgo de transmisión del VIH tras exposición percutánea a sangre infectada es del 0,3% (IC 95%: 0,2% al
0,5%). Tras la exposición de mucosas el riesgo se reduce al 0,09% (IC 95%: 0,006% al 0,5%), siendo incluso
menor cuando el contacto es con piel no intacta. Los factores asociados a un mayor riesgo de transmisión
del VIH son: la profundidad del pinchazo, que la sangre sea visible en el dispositivo y que este haya sido
recién extraído de una vena o arteria de una fuente con carga viral elevada y bajo recuento de CD4.
1.2. Pautas de actuación
Seguir las pautas recomendadas anteriormente (ver Apartado II. “Actuación ante una
exposición accidental”).
Evaluar la situación del paciente fuente:
Si es positivo para el VIH (pero no era conocido previamente), valorar el tipo de
accidente (Tabla III) y, en caso de indicación, iniciar profilaxis lo antes posible
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [802]
[50] EXPOSICIÓN A MATERIAL BIOLÓGICO
(preferentemente en las primeras cuatro a seis horas, y siempre dentro de las primeras
72 h posexposición). No está indicada después de 72 horas. Su duración será de 28 días.
En el caso de que la fuente tenga infección conocida por el VIH, es fundamental
conocer la carga viral y el recuento de CD4, el tipo de TAR y si lo recibe, así como la
historia farmacológica y los motivos de cambio de tratamiento (resistencias,
intolerancia o toxicidad) del paciente fuente.
Si no se conoce su situación serológica, se le considerará como fuente desconocida.
Si es negativo para el VIH, no será necesario hacer nada más.
Tabla III. Recomendación de profilaxis postexposición ocupacional para el virus de la inmunodeficiencia humana.
1.3. Pauta de profilaxis postexposición recomendada
Según el Documento de Consenso sobre Profilaxis postexposición ocupacional y no ocupacional de GeSIDA
(marzo de 2015) se recomienda utilizar preferentemente una pauta convencional con tres fármacos:
tenofovir (TDF) + emtricitabina (FTC), a ser posible en combinación coformulada de un comprimido al día,
asociados a raltegravir (RAL), un comprimido dos veces al día.
El Servicio de Prevención de Riesgos Laborales del Hospital 12 de Octubre recomienda una pauta
con dolutegravir (DTG) en lugar de RAL asociado a TDF + FTC, debido a sus escasas interacciones
farmacológicas, a una mejor adherencia al tratamiento (una dosis al día) y a una mayor eficacia en
pacientes naive (pacientes que no han recibido TAR previamente). En mujeres embarazadas es preferible
utilizar TDF/FTC + lopinavir potenciado con ritonavir (LPV/r).
En caso de duda sobre la indicación de la PPE se recomienda administrar la primera dosis de forma
inmediata y valorar su continuidad en las 24-72 horas posteriores por un experto en infección por el VIH.
1.4. Seguimiento
A toda persona que haya sido evaluada tras una exposición ocupacional o no ocupacional al VIH debe
ofrecérsele un plan de seguimiento clínico y analítico, información y apoyo psicológico. Además, también se
deben valorar otras enfermedades que compartan las mismas vías de transmisión que el VIH.
El inicio de la PPE nunca debe demorarse, aunque no se disponga en el momento de los resultados.
Si posteriormente se confirma que la fuente es negativa para el VIH se suspenderá la PPE. El seguimiento
de los pacientes es de 24 semanas (6 meses), salvo en casos de exposición a una fuente coinfectada VIH +
VHC, en cuyo caso se deberá realizar una nueva serología frente al VIH a los 12 meses (Tabla IV). En los
laboratorios donde dispongan de determinación combinada de antígeno/anticuerpo para el VIH de 4ª
generación, el seguimiento podría reducirse a la determinación basal, a las 6 semanas y a los 4 meses
postexposición.
Las personas que han sufrido una exposición accidental deben ser informadas sobre los signos y/o
síntomas de la infección aguda por el VIH. En caso de presentarlos, se realizará una carga viral del VIH,
independientemente del tiempo transcurrido desde la exposición accidental.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [803]
[50] EXPOSICIÓN A MATERIAL BIOLÓGICO
Los pacientes que inicien PPE, además, deben ser informados de los efectos secundarios del TAR,
de las posibles interacciones medicamentosas y de la necesidad de tener una buena adherencia al mismo.
Los efectos secundarios más frecuentes de la PPE son náuseas, astenia y mal estado general, que
aparecen hasta en el 75% de los pacientes en algunas series. Las anomalías de laboratorio son más
infrecuentes (< 10%) y se suelen resolver al acabar la PPE. Los efectos secundarios leves son la causa más
frecuente de abandono de la PPE.
Se debe advertir al trabajador accidentado que durante el periodo de seguimiento, sobre todo
durante las primeras 12 semanas, deberá evitar una posible transmisión secundaria del VIH o de otras
infecciones: uso correcto del preservativo en todas las relaciones sexuales, no compartir jeringuillas, evitar
el embarazo y la lactancia. Tampoco se podrán realizar donaciones de sangre, semen u órganos.
Tabla IV. Cronograma del seguimiento.
2. EXPOSICIÓN NO OCUPACIONAL
2.1. Riesgo de transmisión
La probabilidad de transmisión del VIH depende del tipo de exposición, de la infectividad de la persona
fuente (carga viral y recuento de CD4) y de otros factores añadidos (agresión sexual, presencia de otras
infecciones de transmisión sexual, heridas o lesiones en el área genital expuesta y aparición de sangrado o
menstruación; tabla V).
Tabla V. Probabilidad estimada por acto de adquirir la infección por el virus de la inmunodeficiencia humana de una fuente
infectada, según la ruta de exposición.
2.2. Pautas de actuación
Es importante recoger la historia sexual del paciente junto con el despistaje de enfermedades de
transmisión sexual e informar de los métodos para la prevención de la transmisión del VIH en las relaciones
sexuales y otras prácticas de riesgo.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [804]
[50] EXPOSICIÓN A MATERIAL BIOLÓGICO
Se debe considerar la PPE teniendo en cuenta el nivel de riesgo, la vía de exposición y las prácticas
sexuales de riesgo de la persona fuente (Tabla VI). También debe tenerse en cuenta el TAR recibido por la
persona fuente en el caso de infección por el VIH conocida, y la existencia de factores de riesgo añadidos.
En cualquier caso, el inicio de la PPE es una decisión que debe tomarse de forma individualizada,
debiendo cumplir siempre las siguientes condiciones:
Consulta en las primeras 72 horas tras la exposición que permita inicio precoz de la PPE (igual a
la PPE ocupacional).
Ausencia de contraindicaciones para tomar tratamiento antirretroviral.
Exposición excepcional.
Garantía de seguimiento clínico y analítico del paciente.
Tabla VI. Recomendación de profilaxis del virus de la inmunodeficiencia humana postexposición no ocupacional.
2.3. Pauta de profilaxis postexposición no ocupacional recomendada
La PPE recomendada en caso de exposición no ocupacional es la misma que en la ocupacional.
Como pautas alternativas se pueden utilizar TDF/FTC con darunavir/ritonavir (DRV/r),
atazanavir/ritonavir (ATV/r), DTG, elvitegravir/cobicistat (EVG/COBI) o rilpivirina (RPV). En general, en las
pautas preferentes no se recomienda el uso de inhibidores de la transcriptasa inversa no nucleósidos de 1ª
generación –efavirenz (EFV) y nevirapina (NVP)– como tercer fármaco, por sus efectos adversos y mayor
riesgo de resistencias primarias. EFV además puede ser teratogénico, por lo que no se debe usar en
mujeres embarazadas o con exposición sexual con riesgo de embarazo.
2.4. Seguimiento
El inicio, la duración y el seguimiento son superponibles a los casos de exposición ocupacional. En el caso de
exposición por vía sexual se debe solicitar serología de sífilis y descartar otras infecciones de transmisión
sexual (considerar la prescripción de profilaxis antibiótica con dosis única de ceftriaxona 500 mg por vía
intramuscular o azitromicina 1-2 g por vía oral, si no se puede garantizar un adecuado seguimiento) y
realizar un test de embarazo en mujeres en edad fértil.
BIBLIOGRAFÍA
Polo R, Lozano F, González P. Documento de Consenso sobre profilaxis postexposición ocupacional y
no ocupacional en relación con el VIH, VHB y VHC en adultos y niños. (Actualización marzo de 2015).
Disponible en URL: http://www.gesida.seimc.org.
Protocolo de actuación ante exposición accidental a material biológico por vía percutánea, mucosa o
piel no íntegra. Servicio de Prevención de Riesgos Laborales. Hospital 12 de Octubre. Madrid. 2012.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [805]
[51] ICTERICIA
51.Ictericia
María Teresa Álvarez-Nava Torrego.
Medicina del Aparato Digestivo
Juan Salas Jarque.
Medicina Interna
Asesora:
Sonia Sáenz-López Pérez.
Médica Adjunta de Medicina del Aparato Digestivo
I. DEFINICIONES Y FISIOPATOLOGÍA
Se denomina ictericia a la coloración amarillenta de la piel y de las mucosas debida al depósito de
bilirrubina sérica. Se aprecia mejor en la periferia de la conjuntiva ocular y en la mucosa oral (del paladar
duro y sublingual, sobre todo). La ictericia clínica suele aparecer con concentraciones de bilirrubina
mayores a 2 mg/dL.
La bilirrubina es el metabolito principal que resulta del catabolismo del grupo hemo de la
hemoglobina (Hb). Un 85% procede de la destrucción de hematíes; el 15% restante, de la eritropoyesis
ineficaz y de la degradación de proteínas tisulares que contienen dicho grupo bioquímico en su estructura.
Su concentración plasmática normal es menor de 1 mg/dL.
Hay dos tipos de bilirrubina: directa o conjugada (hidrosoluble, se conjuga en el hígado mediante la
enzima uridinadifosfato-glucuroniltransferasa [UDP-GT]), que se excreta por la vía biliar y forma parte de la
circulación enterohepática), y no conjugada o indirecta (liposoluble, forma hasta el 96% de la bilirrubina en
condiciones normales). La bilirrubina directa tiñe las heces (pleiocromía) y la orina en caso de aumentar su
eliminación por vía renal (coluria).
La colestasis es la dificultad de llegada de la bilis al duodeno debida a una alteración en la síntesis
de la misma (colestasis intrahepática) o a una obstrucción en el flujo de salida (colestasis extrahepática). La
colestasis hace que no haya pigmentos biliares en la luz intestinal y que, por tanto, no exista una
pigmentación de las heces (hipo o acolia), que se reabsorban las sales biliares hacia la circulación general y
que, como consecuencia, aparezcan prurito (por irritación de las terminaciones nerviosas) y coluria (por
aumento del paso de la bilirrubina conjugada hacia la orina).
II. ETIOPATOGENIA
En función de dónde se encuentre la alteración del metabolismo de la bilirrubina (síntesis,
excreción), aumentarán las fracciones directa, indirecta o ambas (Tabla I).
1. Hiperbilirrubinemia no conjugada
Considerada como una bilirrubinemia indirecta por encima del 85% (la total no suele ser mayor de
3-4 mg/dL). Puede deberse a un aumento de la producción o déficit en la captación o en la conjugación de
la bilirrubina por el hígado. Las causas más frecuentes son la hemólisis, la ictericia neonatal y el síndrome
de Gilbert. La enfermedad de Crigler-Najjar es una causa rara de hiperbilirrubinemia indirecta.
Hemólisis. Además de hiperbilirrubinemia no conjugada, se manifiesta con reticulocitosis y
disminución de haptoglobina. La concentración de hierro suele estar aumentada por su
liberación desde los hematíes lisados. Si la hemólisis es intravascular, puede aparecer
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [806]
[51] ICTERICIA
hemoglobinuria. La eritropoyesis ineficaz (primaria o secundaria a déficit vitamínico, trastornos
hematológicos o intoxicación por plomo) presenta una concentración normal de haptoglobina.
Tabla I. Causas de hiperbilirrubinemia.
Ictericia neonatal (bilirrubinemia < 5 mg/dL). Se debe a falta de maduración de la UDP-GT. En
ocasiones remite con la suspensión de la lactancia materna, que contiene inhibidores de la
enzima. En el neonato, otras entidades que eleven intensa y duraderamente la bilirrubina (> 20
mg/dL) pueden causar kernícterus por su depósito en los ganglios basales.
Síndrome de Gilbert (bilirrubinemia < 5 mg/dL). Trastorno hereditario autosómico recesivo
debido a déficit parcial de la enzima UDP-GT. Afecta al 2-5% de la población general. No cursa
con clínica, salvo por la ictericia, y el resto de la bioquímica hepática no sufre alteraciones. Se
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [807]
[51] ICTERICIA
desencadena en situaciones de estrés (ayuno, infecciones, agresiones quirúrgicas, consumo de
etanol). Es benigno y no requiere tratamiento.
Enfermedad de Crigler-Najjar. Se trata de un trastorno hereditario autosómico recesivo. Existen
dos tipos: en el tipo I la actividad de la enzima UDP-GT se encuentra ausente mientras que en el
tipo II está muy reducida. En el tipo I, los pacientes suelen fallecer durante el primer año de
vida por kernícterus, y el único tratamiento es el trasplante hepático. En el de tipo II, además de
fototerapia se puede usar fenobarbital como inductor de la actividad de la UDP-GT. Para
establecer un diagnóstico diferencial entre ambos, se ha de valorar el efecto del ensayo con
fenobarbital.
2. Hiperbilirrubinemia mixta
Ictericia hepatocelular debida al fracaso global de la función hepática, que afecta a todos los pasos
del metabolismo de la bilirrubina, aumentando ambas fracciones de la misma (la directa oscila entre el 15%
y el 50%). La historia clínica orienta hacia la causa del daño hepatocelular. En la bioquímica se observa
predominio de las enzimas de citólisis sobre las de colestasis (lesión hepatocitaria). La administración de
vitamina K no corrige la coagulopatía.
3. Hiperbilirrubinemia conjugada
Bilirrubinemia directa superior al 50%. Puede manifestarse con colestasis o sin ella.
3.1. Sin colestasis o metabólicas
El síndrome de Dubin-Johnson y la enfermedad de Rotor son dos trastornos autosómicos recesivos
benignos que no requieren tratamiento y en los que se ve afectada la excreción de la bilirrubina hacia el
canalículo biliar. El primero cursa, además, con alteración en la eliminación urinaria de coproporfirinas y del
aclaramiento de bromosulftaleína, y con pigmentación negra de los hepatocitos en la biopsia (técnicas
usadas en el diagnóstico diferencial).
3.2. Con colestasis
Colestasis intrahepática: La interrupción del flujo biliar se encuentra en el parénquima
hepático. Existen varias causas:
Trastornos infiltrativos difusos: en ellos es típico el patrón bioquímico de colestasis
disociada. En ella la bilirrubina no aumenta pero sí existe incremento de las enzimas
gamma-glutamil-transferesa (GGT) y fosfatasa alcalina (FA).
Inflamación de los conductillos biliares: causada, entre otras, por cirrosis biliar primaria
(enfermedad de etiología desconocida, de patogenia autoinmunitaria;
patológicamente, cursa con inflamación portal y periportal que progresa hacia una
cirrosis; presenta anticuerpos antimitocondriales [AMA] en la mayoría de los casos; el
único fármaco aprobado para su tratamiento antes del trasplante es el ácido
ursodeoxicólico [AUDC], a dosis de 15 mg/kg/día repartido en 3 o 4 tomas) o colangitis
esclerosante primaria (también de índole autoinmunitaria [se asocia a colitis ulcerosa
en el 70% de los casos]; es característica la distorsión arquitectural de las vías biliares
(tanto intra- como extrahepáticas), con arrosariamiento de las mismas en las pruebas
de imagen; presenta ANCA (anticuerpos anticitoplasma de neutrófilo) en el 80%; de
evolución crónica; puede asociar la aparición de colangiocarcinoma; su tratamiento
definitivo es el trasplante hepático).
Síndrome de Stauffer: colestasis paraneoplásica reversible no relacionada con la
existencia de lesiones metastásicas hepáticas, sino con la producción de citocinas por
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [808]
[51] ICTERICIA
parte del tumor primario. El tumor más frecuentemente asociado a este síndrome es el
de riñón.
Colestasis extrahepática. La interrupción del flujo se encuentra en el trayecto de salida de la vía
biliar extrahepática, por lo que tiende a cursar con dilatación retrógrada de esta. Las causas
más frecuentes son la coledocolitiasis, los tumores, las enfermedades inflamatorias de la vía
biliar y los procesos que ejercen compresión extrínseca sobre el árbol biliar.
III. APROXIMACIÓN DIAGNÓSTICA
1. Anamnesis
1.1. Antecedentes personales
Se debe interrogar acerca de la exposición a tóxicos hepáticos (alcohol, fármacos o productos de
herbolario, setas, exposición a tóxicos ambientales), consumo de drogas por vía parenteral, antecedente de
transfusión de hemoderivados, historia previa de enfermedades autoinmunitarias, contactos
epidemiológicos, virus de la inmunodeficiencia humana (VIH), embarazo, etc. La historia familiar de ictericia
o hepatopatía puede orientar a hiperbilirrubinemia hereditaria o hepatopatía genética. En la vejez, los
procesos obstructivos del árbol biliar (ya sea por cáncer o por litiasis) son más frecuentes.
1.2. Inicio y curso
El curso varía según la etiología: en las hepatitis agudas es brusco y progresivo, mientras que en la
coledocolitiasis es brusco y oscilante; en las neoplasias de la encrucijada biliopancreática resulta insidioso y
progresivo (sobre todo en las neoplasias de la cabeza de páncreas); en la obstrucción por litiasis móvil y en
las ictericias de causa hereditaria suele ser intermitente, y puede coincidir con la ingesta en el primer caso y
situaciones de ejercicio, en caso de ayuno y fiebre en el segundo caso.
1.3. Clínica
La presencia de dolor abdominal (generalmente, en el hipocondrio derecho o en el epigastrio
irradiado a hipocondrio derecho, de tipo cólico), fiebre y antecedente de cirugía biliar o edad avanzada
orientan a proceso obstructivo de la vía biliar por litiasis. Si el dolor abdominal se acompaña de síndrome
constitucional, debe pensarse en una neoplasia. Los cuadros pseudogripales (anorexia, mialgias, malestar
general) sugieren hepatitis viral. El prurito puede aparecer en cualquier forma de colestasis, aunque es un
síntoma típico de la cirrosis biliar primaria y la colestasis benigna del embarazo, pudiendo preceder a la
ictericia en estos casos. Si la ictericia va acompañada de hemorragia digestiva, conviene descartar neoplasia
de la ampolla de Vater. Se debe pensar en hepatopatía subyacente si se observan síntomas en relación con
hipertensión portal.
2. Exploración física
La presencia de dolor a la palpación en hipocondrio derecho junto con fiebre alta y tiritona e
ictericia (tríada de Charcot) orienta a colangitis, que también puede acompañarse de confusión mental e
hipotensión o shock (péntada de Reynolds) en casos de mayor gravedad. La evidencia de masa palpable
sugiere neoplasia. Se debe pensar en hepatopatía subyacente si se observan datos de hipertensión portal
clínicamente significativa (ascitis, circulación colateral, etc.) o estigmas de hepatopatía (arañas vasculares,
eritema palmar, asterixis, ginecomastia). Ciertos signos físicos pueden indicar hepatopatías específicas,
como la hiperpigmentación en la hemocromatosis, los xantomas en la cirrosis biliar primaria y el anillo de
Kaiser-Fleischer en la enfermedad de Wilson.
3. Pruebas complementarias
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [809]
[51] ICTERICIA
3.1. Datos de laboratorio
Los análisis esenciales en el paciente con ictericia incluyen sistemático de sangre y bioquímica: la
concentración sérica de bilirrubina (total y fraccionada), FA, transaminasas y tiempo de protrombina. En
caso de hiperbilirrubenemia de predomino indirecto y ausencia de alteración de los niveles séricos de
transaminasas y FA, se deben sospechar procesos de hemólisis o trastornos del metabolismo de la
bilirrubina (ver Capítulo 74. “Trastornos de la serie roja”). Si se trata de hiperbilirrubinemia mixta o directa,
se debe sospechar patología hepatobiliar, motivo de estudio en el presente capítulo. En el tinte ictérico,
una elevación predominante de la FA respecto a las transaminasas orienta a obstrucción biliar o colestasis
intrahepática. La elevación predominante de las transaminasas (aspartato-aminotransferasa [AST] y
alaninaaminotransferasa [ALT]) respecto a la FA indica que la ictericia se debe a una enfermedad
hepatocelular intrínseca. Se conoce como colestasis disociada la elación de la FA y la GGT con niveles
normales de bilirrubina, y es debida a colestasis intrahepática. La prolongación de la actividad de
protrombina indica un déficit de producción de factores de la coagulación por parte del hígado y una
deficiencia de vitamina K, que requiere para su absorción una circulación enterohepática intacta.
3.2. Pruebas de imagen
La ecografía es la prueba imagen inicial, ya que es rápida, segura y relativamente barata. La
sensibilidad para detectar alteraciones en el árbol biliar es del 82-95%. Es la prueba de imagen de elección
para valorar la vesícula biliar. Detecta bien colelitiasis y lesiones ocupantes de espacio (LOS) mayores de 1
cm. Puede tener limitaciones en la observación del colédoco distal y páncreas por interposición de gas
intestinal en línea media y en pacientes obesos. Debe realizarse siempre en casos de colestasis,
especialmente si se sospecha obstrucción de la vía biliar.
En un segundo tiempo se puede emplear la tomografía computarizada (TC), técnica no invasiva, con
menor dependencia del explorador que la ecografía y que está menos limitada por la anatomía del
paciente. Las principales desventajas son el mayor coste que la ecografía y que requiere el empleo de
radiación y contrastes yodados, con el consiguiente riesgo de nefrotoxicidad y reacciones alérgicas. Su
sensibilidad y especificidad son similares a las de la ecografía en la detección de obstrucción biliar y detecta
LOS mayores de 5 mm, aunque la ecografía detecta mejor la presencia de litiasis y valora mejor la vesícula
biliar.
La colangiorresonancia magnética (CRM) es una variante de la resonancia magnética, que no
precisa contraste intravenoso yodado ni radiación y obtiene imágenes del árbol biliar con mayor precisión
que la TC y la ecografía. Se trata de una prueba no invasiva con especificidad y sensibilidad y coste similares
respecto a los de la colangiografía retrógada endoscópica (CPRE). Como inconvenientes destacan que
requiere de la colaboración del paciente y que está contraindicada en caso de claustrofobia y la presencia
de dispositivos metálicos. Puede pasar por alto alteraciones en conductos biliares de pequeño tamaño al
igual que el resto de pruebas de imagen.
La CPRE es una técnica endoscópica que consiste en el acceso a través del duodeno a la ampolla de
Vater, lo que permite su visualización directa (papilitis, ampuloma) y la administración de contraste en el
árbol biliar, así como en el conducto pancreático, obteniéndose imágenes radiológicas. Es la técnica más
precisa para el diagnóstico. Pero dado que se trata de una prueba invasiva, con riesgo de complicación de
0,2% al 3% (hemorragia, perforación, colangitis y pancreatitis) y con un coste mayor que el resto de las
pruebas de imagen, se utilizará únicamente en el diagnóstico para aquellos casos en los que no se obtiene
un diagnóstico etiológico definitivo mediante otras pruebas complementarias, cuando se sospeche
colangitis esclerosante primaria (pues se considera el “gold standard” en el diagnóstico de esta patología) o
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [810]
[51] ICTERICIA
en algunos casos de alta sospecha de causa obstructiva de la vía biliar que requiera terapéutica. La principal
indicación de la CPRE es la posibilidad de realizar terapéutica en el mismo acto.
La sensibilidad y especificidad de la ecoendoscopia (EE) son similares a las de la CPRE para la
detección de litiasis biliar, pero con menor tasa de complicaciones, y también en la detección de patología
ampular y colangiocarcinomas proximales. Permite, además, la punción de lesiones sospechosas, si bien
esto incrementa el riesgo de complicación. Tiene, no obstante, una mayor limitación a la hora de valorar la
vía biliar intrahepática y no ofrece las posibilidades terapéuticas de la CPRE. Frente a las pruebas de imagen
comentadas, tiene una sensibilidad y especificidad mayor en el diagnóstico de obstrucción biliar y patología
ampular; sin embargo, entraña mayor riesgo de complicaciones por ser un procedimiento invasivo que
requiere sedación y cuenta con una menor disponibilidad.
3.3. Biopsia hepática
Proporciona información precisa sobre los detalles de la arquitectura lobulillar hepática y resulta
más útil en pacientes con ictericia persistente no diagnosticada para el diagnóstico de enfermedades
colestásicas intrahepáticas. No obstante, puede ser completamente normal en la obstrucción biliar aguda.
Se asocia a una tasa baja de complicaciones (hemorragia y perforación, con una necesidad de
hospitalización del 1% y tasa de mortalidad del 0,01%). Está contraindicada en caso de dilatación de la vía
biliar intrahepática, ascitis y alteración de los factores de coagulación.
4. Algoritmo diagnóstico (Figura 1)
La integración entre la anamnesis, exploración física y pruebas bioquímicas permite estimar la
probabilidad de ictericia obstructiva.
En el paciente asintomático, con exploración física anodina y concentración sérica de transaminasas
y FA normal, es poco probable la existencia de hepatopatía colestásica o la obstrucción biliar. Se deben
realizar pruebas encaminadas a descartar procesos de hemólisis o trastornos del metabolismo de la
bilirrubina (I).
Si, por el contrario, se sospecha obstrucción del árbol biliar, se planteará un estudio de imagen u
otro en función de la probabilidad de obstrucción y de la necesidad de una actitud terapéutica. Como ya se
ha comentado, la ecografía es la prueba de imagen inicial de elección, aunque puede considerarse realizar
TC en primer lugar en casos de gravedad (shock, sospecha de perforación) o en caso de limitaciones
anatómicas para la ecografía (obesidad, cirugías previas).
Si la probabilidad clínica de obstrucción de la vía biliar es elevada y la ecografía no muestra
dilatación de la vía biliar, se debe realizar otra prueba diagnóstica, preferiblemente una EE por su mayor
sensibilidad y especificidad. Sin embargo, se optará antes por otra prueba de imagen como la TC o,
preferiblemente, la CRM, dependiendo de la disponibilidad del centro, la edad y comorbilidades del
paciente. Se reservará en estas situaciones la EE para casos en los que estas pruebas radiológicas tampoco
muestren dilatación de la vía biliar ni causa obstructiva.
Si la probabilidad de obstrucción biliar es baja y no se identifica dilatación ni obstrucción biliar en
las pruebas de imagen, se debe plantear el diagnóstico diferencial de hepatopatías colestásicas. Cabe
reseñar que en algunos casos de alta probabilidad de obstrucción biliar en los que no se identifica causa
obstructiva en las pruebas radiológicas iniciales, puede estar indicada la CPRE antes que otros estudios
diagnósticos, sobre todo teniendo en cuenta la gravedad, situación clínica y antecedentes del paciente, ya
que ofrece posibilidad terapéutica en el mismo acto.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [811]
[51] ICTERICIA
Figura 1. Algoritmo de diagnóstico de la ictericia.
IV. TRATAMIENTO
1. Tratamiento etiológico
1.1. Obstrucción biliar
Mediante técnicas endoscópicas y radiológicas se puede realizar la desobstrucción biliar. La CPRE es
la técnica de primera elección y permite la realización de esfinterotomía endoscópica, esfinteroplastia,
extracción de los cálculos biliares, dilatación de estenosis en el árbol biliar, colocación de endoprótesis, etc.
La colangiografía transparietohepática (CTPH) es una técnica que complementa a la CPRE. Es especialmente
útil cuando el nivel de obstrucción biliar es proximal y, por tanto, no es accesible endoscópicamente, y
resulta una técnica alternativa cuando existen alteraciones anatómicas que no permiten o dificultan la
realización de la CPRE (cirugías previas como la anastomosis en Y de Roux, divertículos yuxtapapilares, etc.).
Permite la colocación de drenajes externos e internos y la dilatación de estenosis. Existe una tasa de
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [812]
[51] ICTERICIA
complicaciones en torno al 3-10%, incluyendo sangrado, sepsis, fuga biliar, neumotórax, reacción
vasovagal, fístula arteriovenosa y reacción al contraste. En ocasiones puede ser necesario el tratamiento
quirúrgico, sobre todo en casos de fracaso de los procedimientos anteriores y de colecistitis aguda
asociada.
1.2. Hepatopatía colestásica
El tratamiento óptimo va dirigido a la causa subyacente. En el caso de la cirrosis biliar primaria,
incluso en aquellos pacientes asintomáticos, el ácido ursodesoxicólico (AUDC) ha demostrado efectos
favorables a largo plazo, especialmente en estadios precoces de la enfermedad en aquellos pacientes que
presentan mejoría bioquímica durante el primer año de tratamiento. Sin embargo, no ha probado beneficio
en el alivio del prurito en esta enfermedad. Las dosis recomendadas son de 13-15 mg/kg/día. En los últimos
años han surgido nuevos tratamientos alternativos en pacientes con respuesta subóptima a AUDC, como
los fibratos (fenofibrato 160 mg/día, bezafibrato 400 mg/día) en uso combinado con AUDC.
2. Medidas generales
En lactantes se debe usar fototerapia para evitar neurotoxicidades. La hiperbilirrubinemia en
adultos no requiere tratamiento, pero sí medidas de soporte para prevenir o tratar las complicaciones
derivadas de la misma. Puede producir nefrotoxicidad mediante un mecanismo similar al de otros
pigmentos como la mioglobina, y puede llegar a provocar necrosis tubular aguda por precipitación de la
bilis al formar cilindros intratubulares y por citotoxicidad directa sobre las células epiteliales. En caso de
riesgo de nefrotoxicidad (a partir de 15-20 mg/dL de bilirrubina en sangre), es útil asegurar una buena
perfusión renal a través de una adecuada hidratación del paciente y la alcalinización de la orina con
bicarbonato sódico.
En los casos en que el flujo de bilis está reducido, puede existir malabsorción de vitaminas
liposolubles (A, D, E, K), por lo que se recomienda la exposición a la luz solar y se debe considerar la
administración de suplementos. Las dosis recomendadas son: calcio (1.000- 1.200 mg/día, vo), vitamina D
(400-800 UI/día, vo), vitamina A (100.000 UI/mes, im, 25.000- 50.000 UI/semana, vo), vitamina E (200
mg/día, vo), vitamina K (10 mg semana, im). Puede existir coagulopatía, observándose prolongación de la
actividad de protrombina, que puede deberse a un déficit de producción de factores por parte del hígado y
a un déficit de vitamina K por malabsorción debido a afectación de la circulación enterohepática. La
administración de vitamina K parenteral normaliza por lo general un tiempo de protrombina alargado en
pacientes con obstrucción biliar, pero no en pacientes con enfermedad hepatocelular.
3. Tratamiento sintomático
Para el tratamiento del prurito se recomiendan medidas tópicas, como el uso de jabones suaves y la
hidratación cutánea con cremas o vaselina líquida. Se utilizan resinas fijadoras de los ácidos biliares, que
evitan su absorción en la luz intestinal, como la colestiramina (Lismol®, Resincolestiramina® 4 g) en dosis de
4-6 g 30 minutos antes de las comidas, o antes y después del desayuno sin dosis vespertina; o el colestipol
(Colestid® 5 g) entre 15 y 30 g al día, siguiendo la misma pauta que la colestiramina. Suelen ser bien
toleradas, aunque pueden producir molestias digestivas y estreñimiento. Se pueden emplear
antihistamínicos con principal efecto sedante, como la hidroxicina (Atarax® comp. 25 mg/6-8 horas) o la
difenhidramida (Benadryl® comp. 25-50 mg/6-8 horas).
También pueden emplearse fármacos inductores enzimáticos en casos refractarios a los
tratamientos anteriores: el fenobarbital (200 mg al día), que ha resultado menos efectivo que otros
fármacos en los estudios prospectivos, y la rifampicina, de uso limitado por su potencial hepatotóxico (en
dosis entre 300 y 450 mg/día o 10 mg/kg/día). También se usan en casos de prurito intratable antagonistas
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [813]
[51] ICTERICIA
opioides, como la naloxona, que podría ser una opción útil en pacientes ingresados por prurito intratable
(en infusión iv 0,2 μg/kg/min, precedida de un bolo de 0,4 mg iv), y la naltrexona, que permite realizar
tratamiento por vía oral (25 mg el primer día seguido de 50 mg/d).
V. SITUACIONES ESPECIALES
1. Ictericia en el embarazo
Las entidades que pueden producir ictericia en el embarazo se deben a causas no relacionadas con
el embarazo que son las mismas que en la población general (ver Apartado II. “Etiopatogenia”) y las
relacionadas con el embarazo que se exponen a continuación
1.1. Hiperemesis gravídica
Es una entidad propia del tercer trimestre y generalmente autolimitada. Puede acompañarse de
alteración del perfil hepático, sobre todo como elevación de las transaminasas, pero es rara la ictericia.
1.2. Colestasis intrahepática benigna del embarazo
Se manifiesta en forma de prurito asociado a elevación de los ácidos biliares por encima de 10
μm/l. Suele aparecer a finales del segundo trimestre y en el tercer trimestre del embarazo. La causa no está
clara, pero se ha relacionado con mutaciones que causan una mayor sensibilidad a los efectos inhibidores
de los estrógenos en la formación de bilis. El tratamiento de elección es AUCD en dosis de 10-15 mg/kg de
peso corporal, ya que ha demostrado reducir el prurito y los niveles de ácidos biliares. No obstante, la
resolución de esta entidad se produce tras el parto.
1.3 Hígado graso agudo del embarazo
Consiste en una esteatosis microvesicular de los hepatocitos que sucede en la segunda mitad del
embarazo, sobre todo en el tercer trimestre. Es una entidad rara pero grave, ya que puede derivar en fallo
hepático fulminante. Los síntomas pueden variar desde náuseas, vómitos o dolor abdominal a
encefalopatía hepática e ictericia. Puede asociar alteraciones analíticas, como elevación de transaminasas,
hiperbilirrubinemia menor de 5 mg/dL, coagulopatía e hipoglucemia. Las pruebas de imagen del
parénquima hepático suelen mostrar datos de infiltración grasa. El parto temprano es esencial para su
resolución, y debe considerarse el trasplante hepático en casos de fallo hepático agudo.
1.4. Preeclampsia
Es una entidad multisistémica que se caracteriza por hipertensión y proteinuria, y también pueden
aparecer edemas. En un 10-20% puede haber afectación hepática, sobre todo en forma de elevación de las
transaminasas, si bien es rara la ictericia. Cuando se acompaña de convulsiones, se conoce como eclampsia.
El síndrome de hemólisis, elevación de las enzimas hepáticas y trombocitopenia (HELLP) pertenece al
mismo espectro patológico y es especialmente grave. El tratamiento en todos estos casos es provocar el
parto lo antes posible.
2. Virus de la inmunodeficiencia humana
En los pacientes con infección por VIH, hay que añadir al diagnóstico diferencial factores propios de
la enfermedad, como fármacos antirretrovirales (atazanavir) y antituberculosos (que generalmente
producen colestasis intrahepática), y los atribuibles a la inmunosupresión (linfoma, sarcoma de Kaposi e
infección por micobacterias atípicas y otros patógenos oportunistas).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [814]
[51] ICTERICIA
Existe una entidad, conocida como colangiopatía del sida, de aparición tardía en el curso de la
enfermedad y con una inmunosupresión severa, con niveles de CD4 por debajo de 100. Se asocia muchas
veces con infecciones oportunistas por citomegalovirus, Cryptosporidium o micobacterias. Se caracteriza
por dolor en el hipocondrio derecho, fiebre y colestasis con marcado aumento de la FA y, con menor
frecuencia, ictericia. La CPRE es el procedimiento diagnóstico fundamental y se pueden observar estenosis
papilar, estenosis larga de colédoco y colangitis esclerosante en el examen endoscópico. Además, la CPRE
ofrece posibilidades terapéuticas como la esfinterotomía endoscópica.
3. Ictericia en el postoperatorio
Suele ser multifactorial. Existen procesos favorecedores de su aparición: fármacos hepatotóxicos,
en particular los anestésicos, nutrición parenteral, transfusiones de sangre, infecciones y sepsis, deterioro
de la perfusión hepática por bajo gasto durante el procedimiento y después de la intervención. Se utiliza la
expresión colestasis posoperatoria benigna para un síndrome autolimitado de 1-2 semanas de
hiperbilirrubinemia sin otras alteraciones bioquímicas de lesión hepatocelular o disfunción sintética.
4. Trasplante hepático
El diagnóstico diferencial de la ictericia en el receptor de trasplante hepático debe incluir: lesión
hepatocelular por mala conservación del órgano, rechazo, obstrucción de los conductos biliares, hepatitis
virales (CMV), toxicidad por fármacos inmunosupresores (azatioprina), trastornos linfoproliferativos,
recaída de enfermedad (colangitis esclerosante primaria, hepatitis B, hepatitis C, etc.) y hepatitis fibrosante
en pacientes con infección por VHC.
BIBLIOGRAFÍA
Costi R, Gnocchi A, Di Mario F, Sarli L. Diagnosis and management of choledocholithiasis in the golden
age of imaging, endoscopy and laparoscopy. World J Gastroenterol. 2014;20(37):13382-401.
Deepak J, Andra J, Alberto Q, Rachel HW, Michael AH. Liver disease in pregnancy. Lancet.
2010;375:594-605.
European Association for the Study of the Liver. EASL Clinical Practice Guidelines: Management of
cholestatic liver diseases. J Hepatol. 2009;51:237-67.
Fabris L, Cadamuro M, Okolicsanyi L. The patient presenting with isolated hyperbilirrubinemia. Dig Liver
Dis. 2009;41(6):375-81.
Greenberger NJ, Paumgartner G. Enfermedades de la vesicular biliar y las vías biliares. En: Longo DL,
Fauci AS, Kasper DL, Hauser SL, Jameson JL, Loscalzo J, editores. Harrison. Principios de Medicina
Interna. 18ª ed. México: McGraw-Hill Interamericana; 2012.
Krier M, Ahmed A. The Asymptomatic outpatient with abnormal liver function tests. Clin Liver Dis.
2009;13(2):167-77.
Lidofsky SD. Ictericia. En: Sleisenger & Fordtran’s. Enfermedades digestivas y hepáticas. 8ª edición.
Madrid: Elsevier España. 2008; p. 301-16.
O’Brien CB. The hospitalized patient with abnormal liver function tests. Clin Liver Dis. 2009;13(2):179
Saini S. Imaging of the hepatobiliary tract. N Eng J Med. 1997;336:1889-94.
Williams EJ, Green J, Beckingham I, Parks R, Martin D, Lombard M. Guidelines on the management of
common bile duct stones (CBDS). Gut. 2008;57(7):1004-21.
Wolkoff AW. Hiperbilirrubinemias. En: Longo DL, Fauci AS, Kasper DL, Hauser SL, Jameson JL, Loscalzo
J, editores. Harrison. Principios de Medicina Interna. 18ª ed. México: McGraw-Hill Interamericana.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [815]
[52] ASCITIS
52.Ascitis
Laura Santos Santamaría.
Medicina del Aparato Digestivo
Noelia García-Pozuelo Adalia.
Medicina Interna
Asesora:
Ana Martín Algíbez.
Médica Adjunta de Medicina del Aparato Digestivo
I. CONCEPTO
Se denomina ascitis a la acumulación patológica (mayor de 25 ml) de líquido ascítico (LA) en la
cavidad peritoneal. Las causas más frecuentes son la cirrosis hepática (80%), la patología tumoral (10%) y la
insuficiencia cardiaca (3%). Hasta en un 5% hay más de una causa. Estos casos se denominan ascitis mixtas.
II. ETIOPATOGENIA
Distintos mecanismos pueden provocar ascitis. En función del mecanismo que la cause, dividimos a
la ascitis en ascitis con hipertensión portal (HTP) y sin hipertensión portal (Tabla I).
Tabla I. Causas de ascitis*.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [816]
[52] ASCITIS
III. CLÍNICA
1. Anamnesis
2. Exploración física
Ante la sospecha de ascitis, se ha de llevar a cabo una exploración que permita responder a las
siguientes preguntas.
2.1. ¿Hay matidez cambiante a la percusión?
La matidez cambiante se detecta en flancos con el paciente en decúbito supino (positiva con más
de 500-1.000 ml de LA) y desaparece al pasar al paciente a decúbito lateral (positiva con más de 1.500 ml
de LA). Estos hallazgos tienen una sensibilidad y especificidad que oscilan entre el 50-94% y 29-82%,
respectivamente. Su sensibilidad es menor en el paciente obeso, donde se recomienda el uso de pruebas
de imagen complementarias.
2.2. ¿Hay estigmas cutáneos que sugieran cirrosis?
Arañas vasculares (cara, cuello, región anterior del tórax; más raras por debajo del ombligo) y
eritema palmar (eminencia hipotenar > tenar). Son difíciles de detectar en pieles pigmentadas.
La presencia de circulación colateral en la pared abdominal sugiere HTP en caso de que el flujo se
aleje del ombligo, mientras que indica obstrucción de la cava si se acerca a este.
2.3. ¿Tiene signos que sugieran presión venosa central elevada?
Debe explorarse, sobre todo, la presión venosa yugular (ver Capítulo 21. “Insuficiencia cardiaca”).
En algunos casos se debe valorar la existencia de insuficiencia cardiaca derecha o de ingurgitación yugular,
como por ejemplo:
En pacientes alcohólicos, por la posibilidad de sufrir miocardiopatía dilatada como causa
principal o sobreañadida de la ascitis.
Coexistencia de hepatopatía con hipertensión pulmonar, insuficiencia renal o ascitis a tensión.
2.4. ¿Tiene signos que sugieran patología tumoral?
Hay que buscar masas abdominales y adenopatías a cualquier nivel. Las metástasis umbilicales (que
en su mayoría se deben a neoplasias de estómago y colon), aunque poco frecuentes, son fácilmente
accesibles para la biopsia y, de resultar positivas, confirman la etiología tumoral. Son indispensables un
tacto rectal y una exploración pélvica en la búsqueda de masas o procesos infecciosos
2.5. ¿Tiene otras manifestaciones sistémicas?
Edemas a otros niveles, anasarca, fiebre.
2.6. ¿Cuál es la intensidad de la ascitis?
Se distinguen tres grados de ascitis en función de su intensidad. La validez de esta clasificación no
se ha establecido todavía a pesar de que es ampliamente utilizada.
Grado 1: ascitis mínima, solo detectable mediante ecografía.
Grado 2: ascitis moderada. Se manifiesta por malestar abdominal que no interfiere con las
actividades de la vida diaria.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [817]
[52] ASCITIS
Grado 3: ascitis intensa o a tensión. Se manifiesta con distensión abdominal importante o a
tensión, y se caracteriza por malestar abdominal intenso, en ocasiones asociado a disnea, que
interfiere de forma importante con las actividades diarias del paciente. Cada uno de estos
grados se puede acompañar de edemas en las extremidades inferiores.
IV. DIAGNÓSTICO
Tras sospechar la ascitis, es necesario confirmar su presencia e identificar su causa (Figura 1).
1. Pruebas de laboratorio
Siempre se solicitarán hemograma, bioquímica básica, estudio de coagulación y analítica de orina
(con determinaciones de sistemático y sedimento, iones y creatinina). Con ello se valorarán la presencia de
citopenias que orienten a la existencia de HTP, alteraciones de la bioquímica hepática, datos de
insuficiencia hepática (albúmina, bilirrubina, protrombina) y datos de la función renal.
2. Estudios de imagen
El diagnóstico de ascitis suele ser evidente mediante la anamnesis y la exploración física. En caso de
duda, la ecografía abdominal permite confirmar o descartar fácilmente su presencia. Además, aporta
información sobre el patrón ecográfico del hígado, posibles lesiones focales hepáticas, datos compatibles
con hipertensión portal, afectación vascular (trombosis portal o de las venas suprahepáticas) o lesiones
sugerentes de neoplasias en otras localizaciones. Se realizará de forma urgente en caso de duda diagnóstica
(es capaz de detectar cantidades de 100 ml de LA o mayores). Si la semiología es muy sugestiva, se hará de
forma programada como parte del estudio etiológico dirigido. En el estudio inicial no existe indicación de
otras pruebas de imagen en ausencia de una ecografía abdominal patológica.
Figura 1. Diagnóstico diferencial de ascitis.
3. Paracentesis diagnóstica
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [818]
[52] ASCITIS
Es la técnica fundamental para identificar la causa de la ascitis y para descartar o confirmar la
existencia de peritonitis bacteriana espontánea. Debe realizarse en toda ascitis de reciente comienzo o que
requiera ingreso hospitalario, y también en aquellas que empeoren o en las que se modifique el contexto
clínico etiológico. Se recomienda solicitar las determinaciones que figuran en la tabla II (ver Capítulo 2.
“Técnicas y procedimientos instrumentales”) y tener en cuenta las siguientes particularidades:
3.1. ¿Qué aspecto tiene el LA?
Habitualmente es cristalino, de color amarillo transparente o amarillo claro. Sin embargo, tiene
otros aspectos en ciertas etiologías.
Lechoso: puede confundir entre pus y LA con triglicéridos. Si los triglicéridos en LA superan los
200 mg/dL, el líquido tiene un aspecto lechoso. La ascitis quilosa es la entidad más
característica en la que se encuentra un LA lechoso.
Rosa o hemático: los principales diagnósticos diferenciales que plantea el LA hemático son
cirrosis, punción de vaso colateral (en paracentesis previas) y patología tumoral
(principalmente, hepatocarcinoma). Es de ayuda saber que si el sangrado se debe a una
paracentesis traumática a menudo la sangre coagula y tiñe el LA de forma heterogénea,
mientras que en sangrados no traumáticos o por paracentesis traumáticas antiguas el LA está
teñido de forma homogénea y no coagula (coaguló tiempo atrás y el tinte proviene del trombo
diluido). En los LA hemáticos hay que corregir el número de leucocitos y neutrófilos con la
siguiente fórmula: restar un polimorfonuclear (PMN) por cada 250 hematíes, o un leucocito por
cada 750 hematíes. Si el sangrado es antiguo, la muerte de los PMN hace que el resultado sea
negativo.
3.2. ¿Existe infección en el LA?
Para saberlo es preciso hacer un recuento leucocitario precoz (en menos de una hora; existen
incluso tiras reactivas que permiten hacerlo en 90-120 segundos) para valorar la necesidad de tratamiento
antibiótico en todo paciente con 250 PMN/mm3 o más (diagnóstico de peritonitis bacteriana espontánea
[PBE]; ver Capítulo 54. “Hepatopatía crónica. Cirrosis hepática y sus complicaciones”). Si la población
dominante es mononuclear, hay que sospechar otras causas, como carcinomatosis o tuberculosis (TBC). En
el paciente cirrótico solo se justifica la presencia de más de 500 leucocitos/mm3 por infección y también
por incremento de la diuresis (pero solo si se hubiera cuantificado la diuresis previamente al episodio,
predominaran linfocitos normales y no hubiera otros datos que apuntaran a otras posibles causas).
Diferenciación entre PBE y perforación gastrointestinal cuando el recuento de PMN bilirrubina en LA
es ≥ 250 células/mm3
Si se cumplieran dos o más de los siguientes criterios, se habría de hacer una valoración clínica para
solicitar un TAC abdominopélvico de forma urgente para descartar una perforación intestinal.
Proteínas totales > 1 g/dL.
Glucosa < 50 mg/dL.
LDH mayor del límite superior en suero.
3.3. ¿Hay hipertensión portal?
Un gradiente albúmina sérica-albúmina ascítica (GASA) mayor de 1 tiene una gran precisión (hasta
del 97%) para determinar HTP, incluso en el contexto de infección, diuresis intensa y tratamiento con
albúmina intravenosa (Tabla I). Las tomas de las muestras para la determinación de albúmina sérica y
ascítica deberían realizarse dentro de la misma hora para evitar fluctuaciones que proporcionen un GASA
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [819]
[52] ASCITIS
falsamente alterado, puesto que hay situaciones especiales que lo modifican; puede estar falsamente
elevado en la ascitis quilosa y encontrarse falsamente disminuido en:
Insuficiencia cardiaca bajo tratamiento con diuréticos (a diferencia de la cirrosis).
Cirróticos con albúmina sérica ≤ 1,1 mg/dL (< 1% de casos).
Situaciones de hipotensión arterial por disminución de la presión portal.
Situaciones de hipergammaglobulinemia (globulina sérica > 5 g/dL o 50 g/l), en las que debe
corregirse mediante la siguiente fórmula:
IGASA corregido = GASA no corregido × 0,16 × (globulina sérica [g/dL] + 2,5)
Tabla II. Mediciones realizadas en líquido ascítico.
4. Laparoscopia
Está indicada en aquellos casos en que no se obtiene un diagnóstico con las pruebas mencionadas,
sobre todo ante sospecha de enfermedad peritoneal. Resulta de gran utilidad en la ascitis tuberculosa y
carcinomatosa.
V. ENTIDADES CLÍNICAS
En la tabla III aparecen detalladas las características analíticas del LA según la etiología. A
continuación se enumeran las diferentes causas de ascitis.
1. Ascitis como descompensación de hepatopatía crónica
(Ver Capítulo 57. “Hepatopatía crónica. Cirrosis hepática y sus complicaciones”).
2. Ascitis de origen neoplásico
Supone menos del 10% de los casos de ascitis. Los principales mecanismos son: carcinomatosis
peritoneal, metástasis hepáticas masivas, hepatocarcinoma, obstrucción linfática por un proceso
neoformativo y el síndrome de Budd-Chiari de origen neoplásico. Es un error tomar como sinónimos ascitis
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [820]
[52] ASCITIS
maligna y carcinomatosis peritoneal (esta solo es uno de los mecanismos que originan ascitis de causa
neoplásica). El LA se puede producir por trasudación (en relación con HTP secundaria a infiltración tumoral
del hígado, del eje espleno-portal o de las venas suprahepáticas), por exudación por parte del peritoneo
(ante invasión tumoral [como es el caso de la carcinomatosis peritoneal]) o por un mecanismo mixto
(cuando además de infiltración hepática masiva existe carcinomatosis peritoneal). El estudio citológico del
LA tiene una sensibilidad cercana al 100% en la carcinomatosis peritoneal; sin embargo, esta sensibilidad
disminuye notablemente cuando es otro tipo de mecanismo el productor de la ascitis (metástasis hepáticas
masivas, hepatocarcinoma, etc.). La citometría de flujo y el estudio inmunohistoquímico pueden aumentar
la sensibilidad. Recientemente se ha propuesto la medición de CEA en el líquido ascítico como una prueba
útil para la detección de ascitis neoplásica; sin embargo, su sensibilidad y especificidad son limitadas y su
relevancia en el diagnóstico diferencial resulta incierta. Aunque también se ha hablado de la medición de
CA-125 y de diferentes proteínas expresadas por las células tumorales, por el momento no se plantea su
uso debido a su escasa relevancia clínica.
3. Ascitis tuberculosa
Aparece en el contexto de una TBC peritoneal, siendo una entidad poco frecuente, ya que
representa únicamente del 4 al 10% de las formas extrapulmonares de TBC. Más del 90% de los pacientes
con TBC peritoneal tiene ascitis en el momento de la presentación. La afectación peritoneal por TBC es más
frecuente en pacientes alcohólicos, con infección por VIH, con cirrosis hepática, con diabetes mellitus, con
cáncer, tras tratamiento con inhibidores del factor de necrosis tumoral α (anti-TNF-α) y sometidos a diálisis
peritoneal. El LA se produce por exudación de material proteináceo de los nódulos o tubérculos. Puede
debutar clínicamente con dolor abdominal y fiebre, por lo que habrá que hacer diagnóstico diferencial con
la PBE.
La baciloscopia en el LA tiene una sensibilidad muy baja (0-2%) debido a la reducida concentración
de micobacterias. El cultivo de Löwenstein tendría una sensibilidad de aproximadamente el 60-80% en caso
de cultivarse 1 l de LA. Las muestras habitualmente procesadas son de 50 ml, por lo que esta sensibilidad
disminuye notablemente. Por ello deben obtenerse tres muestras para hacer baciloscopia y cultivo de
micobacterias. Otros análisis de laboratorio del LA útiles en el diagnóstico de ascitis de origen tuberculoso
son las determinaciones de adenosina-desaminasa (ADA), de interferón γ (IFN-γ) y del ARN bacteriano
mediante reacción en cadena de la polimerasa (PCR). La determinación de ADA supone una herramienta
indirecta para el diagnóstico de ascitis tuberculosa, con una sensibilidad de 100% y una especificidad de
97% cuando su valor es superior a 36-40 UI/l (el punto óptimo de corte se sitúa en 39 UI/l). En pacientes
cirróticos, la sensibilidad disminuye al 30% debido a la pobre respuesta inmunitaria humoral y celular que
presentan. Una cifra de IFN-γ superior a 3,2 UI/ml tiene una sensibilidad y especificidad próximas al 100%.
El papel de la PCR en el LA no está bien establecido; sin embargo, en algunos estudios su sensibilidad ha
sido del 100%.
La presencia de un valor positivo en la prueba de Mantoux puede apoyar este diagnóstico (es
positivo en el 70% de los casos, pero un resultado negativo no excluye ascitis tuberculosa). Más
recientemente se ha incluido la utilización de IGRA (Interferon Gamma Release Assays) dentro del
diagnóstico de infección tuberculosa.
La TAC abdominal puede orientar hacia un diagnóstico de TBC peritoneal. Los hallazgos más
frecuentes son la presencia de ascitis, de implantes peritoneales y de linfadenopatías con centro necrótico
de forma característica.
El estudio histológico y el cultivo de las biopsias peritoneales (obtenidas por laparoscopia o
laparotomía exploradora) tienen una sensibilidad cercana al 100%, por lo que se consideran las técnicas de
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [821]
[52] ASCITIS
elección para el diagnóstico. Se debe recurrir a ellas si la sospecha de esta entidad es alta y el resto de
determinaciones han resultado negativas.
4. Ascitis cardiaca
Supone menos del 5% de los casos de ascitis. Las patologías responsables son la insuficiencia
cardiaca (la más frecuente), la pericarditis constrictiva y la valvulopatía tricúspide. El análisis del LA suele
demostrar un GASA mayor de 1,1 g/dL con proteínas elevadas (a diferencia de la cirrosis hepática, que
suele presentar cifras de proteínas bajas en LA). Recientemente se han publicado estudios que proponen la
medición de metabolitos del péptido natriurético cerebral (NT-proBNP) en el LA para confirmar o descartar
el diagnóstico de ascitis secundaria a insuficiencia cardiaca.
5. Ascitis pancreática
Se debe a la rotura del conducto pancreático principal o de un pseudoquiste, o bien a fístulas
pancreatoperitoneales. Estas situaciones pueden acaecer en el seno de pancreatitis agudas graves,
pancreatitis crónicas y traumatismos pancreáticos (espontáneos o yatrogénicos [por ejemplo, tras una
ecoendoscopia con punción]). La determinación de amilasa en el LA no se realiza de forma rutinaria, sino
ante la sospecha de este tipo de ascitis o cuando las pruebas realizadas han sido negativas para detectar
otras causas. Su valor suele ser mayor a 2.000 UI/l, y al menos cinco veces superior a la cifra sérica (que
habitualmente se encuentra elevada en estos casos). La combinación de GASA menor de 1,1 g/dL, proteínas
totales en LA mayores de 3 g/dL y amilasa elevada en LA es diagnóstica de esta entidad. Se debe hacer
diagnóstico diferencial con la perforación intestinal (en la que la cifra de amilasa en el LA también puede
ser alta) y con la PBE (dada la predominancia de neutrófilos en el LA).
La realización de una colangiopancreatografía retrógrada endoscópica (CPRE) suele mostrar la fuga
de contraste desde el conducto pancreático principal o desde un pseudoquiste pancreático, y permite
realizar tratamiento endoscópico mediante la colocación de prótesis. La colangiorresonancia magnética
puede ser de utilidad para evaluar afectaciones de conductos secundarios, y en pacientes no candidatos a
una CPRE en los que se puede plantear la utilización de octreótido junto con diuréticos.
6. Ascitis quilosa
Es una causa poco frecuente de ascitis. Se produce ante la rotura de vasos linfáticos que contienen
quilo, que puede ocurrir ante infiltración neoplásica o infecciosa (parásitos o micobacterias), cirrosis (por
aumento de la presión en el sistema linfático), sección yatrogénica durante una intervención,
traumatismos, anomalías congénitas, radioterapia sobre el abdomen, pericarditis constrictiva y pancreatitis
(aguda o crónica). El aspecto del LA es turbio o lechoso. Ante un contenido elevado de leucocitos o de
células tumorales, puede aparecer un líquido pseudoquiloso (turbio). Los hallazgos típicos en el análisis del
LA incluyen triglicéridos mayores de 200 mg/dL y una cifra de proteínas y GASA variables (según la causa).
La tinción con rojo de Sudán detecta la presencia de glóbulos de grasa. En caso de ascitis quilosa se deben
hacer los exámenes de rutina realizados en toda ascitis, además de estudios dirigidos según la sospecha
etiológica (TBC, malignidad, rotura traumática, etc.).
7. Ascitis nefrogénica
Aparece en pacientes en hemodiálisis o con síndrome nefrótico (y es más frecuente en niños). En
estos dos casos, normalmente existe una segunda causa de ascitis (generalmente cirrosis de origen
alcohólico o por infección crónica por VHC). Se suele observar un GASA menor de 1,1 g/dL y proteínas bajas
en LA.
8. Ascitis biliar
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [822]
[52] ASCITIS
Puede producirse por una perforación biliar (rotura de la vesícula o de la vía biliar) o por una
duodenal. La peritonitis biliar ocurre como consecuencia del efecto irritativo de la bilis en la cavidad
peritoneal (Tabla III).
Tabla III. Ascitis: entidades clínicas, diagnóstico y tratamiento.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [823]
[52] ASCITIS
9. Otras entidades
Se pueden incluir aquí el síndrome de Budd-Chiari, mixedema, diálisis peritoneal, enfermedades del
tejido conectivo (serositis, lupus eritematoso sistémico, etc.), síndrome de hiperestimulación ovárica,
síndrome hemofagocitíco y síndrome de POEMS (polineuropatía, organomegalia, endocrinopatía,
componente M, skin).
VI. TRATAMIENTO
1. Medidas generales
En la mayoría de los casos se indica restricción de sodio (800 mg al día, que equivalen a 2 g de
NaCl) y/o tratamiento diurético. La respuesta a los diuréticos suele ser mala en casos de ascitis
no relacionados con HTP; no obstante, la pauta a seguir es la misma (ver Capítulo 57.
“Hepatopatía crónica. Cirrosis hepática y sus complicaciones”).
La realización de paracentesis evacuadoras está indicada en ascitis a tensión, ascitis moderada
que no responde al tratamiento médico o en aquella que provoca malestar importante al
paciente por ocupación abdominal, disnea, etc.
2. Tratamiento específico
El tratamiento de la causa responsable de la ascitis es el pilar fundamental en la ascitis no
relacionada con hepatopatía crónica (ver Tabla III).
BIBLIOGRAFÍA
Becker G, Galandi D, Blum HE. Malignant ascites: systematic review and guideline for treatment. Eur J
Cancer. 2006;42:589.
EASL clinical practice guidelines on the management of ascites, spontaneous bacterial peritonitis, and
hepatorenal syndrome in cirrhosis. European Association for the Study of the Liver. J Hepatol. 2010;53:
397-417.
Feldman M, Friedman LS, Brandt LJ. Ascitis y peritonitis bacteriana espontánea. En: Sleisenger y
Fordtran. Enfermedades digestivas y hepáticas. 9ª ed. Elsevier: 2010. p. 1517-42.
Runyon BA, AASLD. Introduction to the revised American Association for the Study of Liver Diseases
practice guideline management of adult patients with ascites due to cirrhosis 2012. Hepatology.
2013;57:1651.
Sheer TA, Joo E, Runyon BA. Usefulness of serum N-terminal-ProBNP in distinguishing ascites due to
cirrhosis from ascites due to heart failure. J Clin Gastroenterol. 2010;44:e23.
Steinemann DC, Dindo D, Clavien PA, Nocito A. Atraumatic chylous ascites: systematic review on
symptoms and causes. J Am Coll Surg. 2011;212:899.
Torresini RJ, Prolla JC, Diehl AR, et al. Combined carcinoembryonic antigen and cytopathologic
examination in ascites. Acta Cytol. 2000;44:778.
Urrunaga NH, Singal AG, Cuthbert JA, Rockey DC. Hemorrhagic ascites. Clinical presentation and
outcomes in patients with cirrhosis. J Hepatol. 2013;58:1113.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [824]
[53] HEMORRAGIA DIGESTIVA
53.Hemorragia digestiva
Estibaliz Arrieta Ortubay.
Medicina Interna
María Algara San Nicolás.
Medicina del Aparato Digestivo
Asesora:
Carmen Yela San Benardino.
Medicina del Aparato Digestivo.
I. CONCEPTO
La hemorragia digestiva (HD) consiste en la pérdida de sangre a cualquier nivel del tubo digestivo.
Se puede manifestar clínicamente como:
Hematemesis: vómito de sangre roja, parcialmente digerida o “en posos de café”.
Melenas: heces negras, pastosas y malolientes, como la “pez” o el “alquitrán”.
Hematoquecia: sangre oscura y coágulos mezclados con las heces.
Rectorragia: sangre roja o coágulos frescos no mezclados con las heces.
Sangrado microscópico evidenciado con anemia ferropénica o test de sangre oculta en heces
positivo.
Síntomas secundarios a pérdida de sangre previos a objetivarse el sangrado: mareo, síncope,
disnea o angina.
Según su origen, la HD se puede clasificar en:
Hemorragia digestiva alta (HDA): por encima del ángulo de Treitz (esófago, estómago y
duodeno). Se manifiesta como hematemesis con o sin melenas, o rectorragia si HDA masiva.
Hemorragia digestiva baja (HDB): entre el ángulo de Treitz y el ano. Se manifiesta como
hematoquecia, rectorragia o, en caso de tránsito lento, melenas.
Hemorragia digestiva oculta: es la pérdida de sangre a través del tubo digestivo que no
modifica las características macroscópicas de las heces. Se reconoce por la presencia de anemia
ferropénica o el resultado positivo de los exámenes químicos o inmunológicos de detección de
sangre en heces.
Hemorragia digestiva de origen incierto: en ella no se identifica el lugar del sangrado tras la
realización de las pruebas diagnósticas habituales (endoscopia alta y baja y estudio radiológico
del intestino delgado). Puede presentarse como un sangrado visible o como una HD oculta.
II. MANEJO INICIAL
Es una patología potencialmente grave, por lo que el abordaje inicial cobra especial importancia. Es
obligatorio: 1) confirmar que se trata de una HD; 2) valorar la cuantía del sangrado y su repercusión
hemodinámica; y 3) llevar a cabo maniobras de resucitación. Posteriormente se procederá a investigar la
fuente del sangrado para plantear la mejor opción terapéutica y su manejo ulterior. Se deben priorizar las
medidas de reanimación sobre cualquier otro punto siempre que el paciente lo requiera por su situación
hemodinámica.
1. Confirmación de la hemorragia digestiva
La emisión de sangre por la boca puede originarse, además de en el tubo digestivo, en el aparato
respiratorio, en la propia boca, en la faringe o en la nariz. Incluso puede proceder del estómago pero ser
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [825]
[53] HEMORRAGIA DIGESTIVA
sangre deglutida de origen respiratorio u oral. Practicar un aspirado gástrico a través de una sonda
nasogástrica (SNG) puede confirmar la hemorragia si se observan restos hemáticos. Sin embargo, la última
guía de la Sociedad Europea de Endoscopia no lo recomienda de forma sistemática, y solo habrá de llevarse
a cabo en casos seleccionados (en caso de duda o para ayudar a decidir la actitud a seguir en pacientes con
comorbilidades importantes).
Figura 1. Plan asistencial. Valoración inicial del paciente con hemorragia digestiva alta.
La presencia de sangre roja o agua de lavar carne que no se aclara tras varios lavados indica
sangrado activo. El lavado en posos de café indica un sangrado alto reciente pero no activo. El lavado
bilioso excluye prácticamente el sangrado alto activo. Un lavado gástrico limpio no excluye el origen alto de
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [826]
[53] HEMORRAGIA DIGESTIVA
la HD, ya que la SNG puede estar mal colocada o puede haber edema alrededor de una úlcera (por ejemplo,
edema pilórico alrededor de una úlcera bulbar).
Se debe hacer un tacto rectal a todo paciente con sospecha de HD. Las melenas orientan hacia
HDA, aunque el origen puede ser bajo (intestino delgado, colon derecho) si existe un tránsito lento. La
rectorragia y la hematoquecia suelen orientar a HDB, y sin embargo pueden aparecer en HDA masiva
debido a un tránsito rápido. El tratamiento con algunos fármacos (hierro, bismuto) y determinados
alimentos pueden teñir las heces de color verde-negruzco, lo que no se debe confundir con la existencia de
melenas. Se considera tacto rectal negativo la presencia de heces normales. Una ampolla vacía no descarta
la existencia de sangrado (Figura 1).
En la evaluación inicial es prioritario conocer la situación hemodinámica del paciente. Se deben
determinar la frecuencia cardiaca (FC), la tensión arterial (TA) y la perfusión periférica a todo paciente con
sospecha de HD. También es importante valorar la saturación de oxígeno y el nivel de consciencia. La
repercusión hemodinámica del sangrado depende tanto de la cantidad de sangre perdida como de la
rapidez con la que se produce dicha pérdida (Tabla I).
Tabla I. Valoración de la cuantía de la hemorragia.
2. Valoración de la cuantía y repercusión hemodinámica
3. Resucitación hemodinámica
Medidas generales. Para llevar a cabo una adecuada reposición de la volemia se ha de disponer
de buenos accesos venosos: al menos dos vías periféricas de grueso calibre (16 G) o bien una
vía periférica y una central. Sin embargo, la canalización de esta última no debe retrasar el
inicio de la resucitación si se dispone ya de un acceso periférico. En todo paciente con HD se
necesita una correcta monitorización de la diuresis, especialmente en aquellos con
inestabilidad hemodinámica, en los que se prefiere usar un sondaje vesical. Se extraerán
muestras de sangre para determinar hemograma completo (“en mano” si fuera posible,
especialmente en las hemorragias graves), bioquímica general (con determinación de urea),
coagulación, gasometría venosa y pruebas cruzadas (isogrupo sanguíneo AB0). Si la hemorragia
fuera cuantiosa, se habrían de reservar 4 unidades de concentrados de hematíes.
Reposición de la volemia, inicialmente mediante cristaloides (suero salino fisiológico [SSF] al
0,9% o solución láctica de Ringer) a un ritmo adecuado para evitar la hipoperfusión (objetivo:
tensión arterial sistólica [TAS] > 90 mm Hg), y derivados sanguíneos si fuera necesario (shock
hemorrágico). Hay que tener precaución con la reposición, ya que una expansión plasmática
excesiva podría favorecer la recidiva hemorrágica. Por ejemplo, en un sangrado por varices
esofagogástricas no es recomendable continuar con la administración de volumen cuando la TA
sistólica sea superior a 90 mm Hg, para evitar así un aumento de la presión portal. Se debe
administrar oxigenoterapia en los pacientes con HD, pudiendo necesitar intubación orotraqueal
en casos de shock hipovolémico, bajo nivel de consciencia o hematemesis masiva. Los
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [827]
[53] HEMORRAGIA DIGESTIVA
pacientes con HD grave o masiva que no respondan a medidas iniciales deben ingresar en una
unidad de cuidados intensivos (UCI) o de hemorragia digestiva (UHD) si estuviera disponible.
Transfusión de concentrados de hematíes en función de los resultados de las pruebas
cruzadas. En casos de extrema urgencia se iniciará inmediatamente la transfusión de sangre de
isogrupo o, excepcionalmente, de grupo 0–. En pacientes con hemorragia masiva y shock se
recomienda administrar conjuntamente concentrados de hematíes y cristaloides hasta lograr su
estabilización. Por el contrario, en los pacientes estables se aconseja una estrategia
transfusional restrictiva, trasfundiendo únicamente con niveles de hemoglobina (Hb) inferiores
a 7 g/dL con el objetivo de mantenerlos entre 7 y 9 g/dL. Se debe considerar la transfusión ante
niveles de Hb menores de 9 g/dL en ancianos o en aquellas personas con patología
cardiovascular o respiratoria. Es importante recordar que los valores iniciales de Hb o
hematocrito (Hto) pueden no reflejar adecuadamente la intensidad de la pérdida hemática por
aparecer normales en una primera determinación hasta que se produce el fenómeno de
hemodilución.
Corrección de los trastornos de la coagulación. La corrección de la hemostasia se realizará
mediante vitamina K, plasma fresco congelado (PFC) o concentrados de complejo
protrombínico (CCP) en pacientes con coagulopatía, o bien mediante plaquetas ante trombo-
penias inferiores a 50.000/mm3 y/o disfunción plaquetaria (antiagregación, uremia) con
sangrado activo. En pacientes politransfundidos se debe administrar una unidad de PFC por
cada 4 concentrados de hematíes. En los pacientes bajo tratamiento anticoagulante el manejo
dependerá de la repercusión hemodinámica del sangrado y del tipo de anticoagulante
administrado: Ante antagonistas de la vitamina K (warfarina y acenocumarol), se administrará
vitamina K (por vía oral o intravenosa) y/o PFC/CCP en función de la repercusión hemodinámica
de la hemorragia y del valor del INR (International Normalized Ratio) (Tabla II).
Tabla II. Manejo de la anticoagulación con antagonistas de vitamina K en la hemorragia digestiva.
En el caso de los nuevos anticoagulantes orales (NACO: dabigatrán, rivaroxabán, apixabán), se
dispone en la actualidad de antídoto para el primero de ellos, dabigatrán. Se trata de un anticuerpo
monoclonal llamado idarucizumab [Praxbind®] (ver Capítulo 77. “Trastornos de la hemostasia.
Anticoagulación”). Rivaroxabán y apixabán no disponen todavía de un antídoto específico que contrarreste
su efecto anticoagulante. En cualquier caso, se debe suspender el fármaco y priorizar el soporte
hemodinámico hasta su eliminación (su vida media oscila entre 6 y 18 horas). En caso de inestabilidad
hemodinámica, si bien su eficacia no está claramente demostrada, se puede considerar el uso de PFC o CCP
o bien plantear una hemodiálisis urgente en el caso de NACO con eliminación renal (dabigatrán). Hay que
valorar hacer un lavado por SNG si la toma de la medicación ha sido en las dos horas previas al sangrado.
Por último, en caso de HD moderada o grave en pacientes anticoagulados con heparina no
fraccionada se debe antagonizar el efecto de la heparina con sulfato de protamina (aplicando dosis
repetidas de 20 mg en infusión lenta hasta el cese de la hemorragia o la corrección del tiempo de cefalina o
tiempo de tromboplastina parcial activada [TTPa]).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [828]
[53] HEMORRAGIA DIGESTIVA
En cualquier paciente bajo tratamiento anticoagulante hay que valorar el balance riesgo/ beneficio
de mantener la anticoagulación. Se recomienda, como medida general, suspender la anticoagulación con
dicumarínicos y mantener dosis plenas de heparina de bajo peso molecular (HBPM) durante la fase aguda
de la hemorragia.
III. HEMORRAGIA DIGESTIVA ALTA
1. ETIOLOGÍA (ver Tabla III)
Tabla III. Causas de hemorragia digestiva alta.
2. DIAGNÓSTICO
1. Anamnesis
Episodios previos de HDA. Hasta el 60% de los pacientes con historia previa de hemorragia
sufrirán un sangrado desde la misma lesión.
Enfermedades asociadas. Se debe investigar sobre enfermedades que sugieran o predispongan
a una etiología concreta y sobre comorbilidades o situaciones que condicionen el manejo de la
hemorragia (patologías sensibles a la hipoxemia o a la sobrecarga de volumen [enfermedades
cardiorrespiratorias o enfermedad renal crónica], alteraciones de la hemostasia o
predisposición a broncoaspiración [demencia, encefalopatía hepática]).
Tabla IV. Antecedentes que orientan hacia el origen del sangrado.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [829]
[53] HEMORRAGIA DIGESTIVA
Síntomas digestivos previos: epigastralgia o malestar abdominal, pirosis, náuseas y vómitos,
disfagia, regurgitación.
Fármacos o tóxicos que predispongan al sangrado, se asocien a él o faciliten: antiinflamatorios
no esteroideos (AINE), corticoides, anticoagulantes, antiagregantes, alcohol o tabaco.
Situaciones de estrés: quemaduras, traumatismo craneoencefálico, sepsis, broncoaspiración
(Tabla IV).
Tabla IV. Antecedentes que orientan hacia el origen del sangrado.
2. Exploración física
Valorar constantes vitales, estado de volemia y nivel de consciencia.
Identificar signos clínicos que orienten a la enfermedad subyacente (como estigmas de
hepatopatía crónica [arañas vasculares, eritema palmar, ascitis], equimosis o petequias
[enfermedad hematológica], anomalías vasculares [enfermedad de Rendu-Osler]).
Descartar complicaciones: un dolor abdominal agudo con datos de irritación peritoneal
(“vientre en tabla”) debe hacernos sospechar perforación.
3. Pruebas complementarias
Estudios básicos. En todos los pacientes son necesarios hemograma, coagulación, bioquímica
general con perfil hepático y urea, y pruebas cruzadas. Se valorarán electrocardiograma (ECG) y
radiografía de tórax (si esta incluyera las cúpulas diafragmáticas, podría ayudar a descartar
neumoperitoneo).
Endoscopia digestiva alta. Permite diagnosticar el origen de la hemorragia en el 95% de los
casos, realizar maniobras terapéuticas y establecer el pronóstico y la probabilidad de
resangrado. Se realizará de forma urgente si hay inestabilidad hemodinámica o signos de
sangrado activo, en las primeras 12 horas si el origen bajo sospecha está relacionado con la
hipertensión portal (HTP), y en las primeras 24 horas en los demás casos. En ausencia de
contraindicación (intervalo QT prolongado), se recomienda administrar eritromicina (250 mg
por vía intravenosa) 30 o 120 minutos antes de la endoscopia, ya que se ha demostrado que
mejora significativamente la visualización endoscópica y reduce la necesidad de una segunda
exploración endoscópica, la duración de la estancia hospitalaria y la necesidad de transfusión.
Las principales complicaciones de esta técnica son:
Menores: espasmo glótico, faringitis, síndrome de Mallory-Weiss, traumatismo dental.
Mayores: perforación digestiva, aspiración broncopulmonar, bacteriemia, endocarditis
y arritmias.
Actualmente no existen contraindicaciones absolutas para llevar a cabo una
endoscopia digestiva alta pero no se recomienda en los pacientes con shock hipovolémico
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [830]
[53] HEMORRAGIA DIGESTIVA
inadecuadamente resucitados, en las perforaciones de víscera hueca (a menos que la
exploración se realice como parte del tratamiento) ni en pacientes con aneurisma disecante de
aorta ni con subluxación atloaxoidea. Se debe tener especial precaución en los pacientes con
infarto agudo de miocardio revascularizado en las últimas semanas, con cirugías
toracoabdominales recientes y en los que no colaboren en la realización de la técnica.
Otras pruebas diagnósticas
Angio-TAC. Presenta una alta sensibilidad, cercana al 100%, en la HD aguda masiva, por
lo que se puede utilizar tras un estudio endoscópico no diagnóstico o en aquellos
pacientes en los que esté contraindicada la gastroscopia. A pesar de que su sensibilidad
disminuye notablemente en sangrados moderados, en un alto porcentaje de ellos
muestra signos indirectos que sugieren el origen y la causa del sangrado. Tiene la
ventaja adicional de no precisar preparación especial y de poder realizarse urgente.
Arteriografía. En la actualidad su papel diagnóstico ha sido sustituido por la TAC. Sin
embargo, a diferencia de esta, no solo permite localizar el punto de sangrado activo,
que debe ser de mayor cuantía, sino que además puede hacer maniobras terapéuticas
(inyección intraarterial de vasopresina, embolización de arterias sangrantes). Sus
principales indicaciones son la hemorragia activa persistente en la que no se ha podido
demostrar el origen del sangrado en endoscopia, la recidiva del sangrado grave o el
segundo resangrado tras tratamiento endoscópico en pacientes con elevado riesgo
quirúrgico.
Gammagrafía con hematíes marcados con tecnecio 99 (99Tc). Detecta sangrados de escasa
cuantía (0,1 ml/min) y es más sensible que la arteriografía a la hora de localizar hemorragias
activas. Sin embargo, no permite realizar maniobras terapéuticas y no se suele hacer de manera
urgente en la fase aguda de la hemorragia.
Cápsula endoscópica. Es cómoda para el paciente y visualiza la mayor parte de la mucosa del
intestino delgado. No hace maniobras terapéuticas ni toma biopsias, y es útil en la hemorragia
de origen oculto.
Enteroscopia. Examina todo el duodeno y el yeyuno proximal. Con ella se pueden hacer
maniobras terapéuticas y tomar biopsias (p. ej., en caso de haber visualizado una lesión en el
intestino delgado con la cápsula endoscópica).
Estudios radiológicos con bario. Prácticamente están en desuso en la actualidad.
A. HEMORRAGIA DIGESTIVA ALTA NO ASOCIADA A HIPERTENSIÓN PORTAL
El 80-90% de las HDA son de causa no varicosa. La úlcera péptica sigue siendo la etiología más
frecuente (30-55% del total de las hemorragias; a pesar de haber disminuido la prevalencia de infección por
Helicobacter pylori [HP], esta proporción se mantiene por el envejecimiento de la población y por el
aumento del consumo de AINE).
1. Úlcera péptica
1.1. Factores predisponentes (Tabla IV)
Consumo de AINE: inhiben la ciclooxigenasa 1 (COX-1), encargada de sintetizar las
prostaglandinas que reparan la mucosa intestinal y conservan su integridad. Los más
gastrolesivos son el naproxeno y la indometacina (el ibuprofeno es el menos gastrolesivo; el
diclofenaco y el ketoprofeno entrañan riesgo intermedio). La infección por HP, los
glucocorticoides, el alcohol y los anticoagulantes aumentan su poder gastroerosivo.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [831]
[53] HEMORRAGIA DIGESTIVA
Edad: se considera un factor de riesgo independiente. Más del 60% de los casos ocurren por
encima de los 60 años.
Figura 2. Plan asistencial en la hemorragia digestiva alta no asociada a hipertensión portal.
Infección por HP: produce una gastritis activa crónica. El 10% de los infectados desarrollará
úlcera péptica. Se estima que el 80-90% de los pacientes con úlcera duodenal tienen infección
por HP, aunque la incidencia de la infección está disminuyendo en los países desarrollados (su
prevalencia actual es menor [50-75%]).
Estrés: en hospitalizados con enfermedades graves. Son más frecuentes en pacientes con
enfermedades respiratorias y coagulopatía. La mortalidad del sangrado por úlceras de estrés es
más elevada.
Secreción ácida: como único factor causal es raro (en algunas ocasiones sí puede ser causa
única; por ejemplo, en el síndrome de Zollinger-Ellison [hipersecreción de gastrina debida
generalmente a un gastrinoma]).
1.2. Estratificación del riesgo de sangrado
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [832]
[53] HEMORRAGIA DIGESTIVA
Para determinar la gravedad de la HDA, la necesidad transfusional, el riesgo de recidiva
hemorrágica y la mortalidad, hemos de considerar elementos clínicos, de laboratorio y endoscópicos.
Actualmente se recomienda el uso de escalas pronósticas que aúnan estos elementos (puntación de
sangrado de Glasgow-Blatchford [GBS] y escala de Rockall) para predecir estos riesgos. El GBS puede
utilizarse antes de la gastroscopia (los pacientes con puntación de 0 podrían ser dados de alta sin su
realización; en el resto de los pacientes se habría de llevar a cabo en las primeras 24 horas, ya que
proporciona los datos pronósticos más fiables). La clasificación de Forrest, la más utilizada, predice de
forma efectiva el riesgo de recidiva hemorrágica y la necesidad de tratamiento endoscópico (Tablas V-VII).
Tabla V. Puntuación de sangrado de Glasgow-Blatchford.
Tabla VI. Escala de Rockall.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [833]
[53] HEMORRAGIA DIGESTIVA
Tabla VII. Clasificación de Forrest.
Los pacientes jóvenes sin signos de sangrado activo o reciente en las endoscopias pueden ser dados
de alta precozmente. Por el contrario, los pacientes con factores de riesgo deben quedarse ingresados al
menos durante las primeras 72 horas después del episodio de sangrado, que es cuando existe un mayor
riesgo de recidiva hemorrágica.
1.3. Tratamiento
Tratamiento médico. El tratamiento con inhibidores de la bomba de protones (IBP) previo a la
endoscopia reduce la frecuencia de estigmas endoscópicos de alto riesgo y, por tanto, la
necesidad de tratamiento endoscópico. Sin embargo, su administración no debe retrasar la
gastroscopia. Se recomienda disponer un bolo intravenoso de 80 mg de omeprazol,
pantoprazol o esomeprazol seguido de una perfusión continua del mismo compuesto disuelto
en suero fisiológico a 8 mg/h (precipitan en sueros glucosados). La perfusión ha de cambiarse
cada 12 horas. Para prepararla, por ejemplo, se han de diluir 2 viales de pantoprazol (40 mg) en
500 ml de SSF al 0,9% y se han de pasar en 12 horas; posteriormente, se diluyen 3 viales en
otros 500 ml de SSF al 0,9%, que se administrarán a lo largo de las siguientes 12 horas. Tras la
gastroscopia se debe continuar con la perfusión continua de IBP durante 72 horas en pacientes
con estigmas endoscópicos de alto riesgo (correspondientes a los estadios de Forrest Ia, Ib, IIa y
IIb) y mantener dieta absoluta durante las primeras 24 horas por si fuera necesario repetir la
endoscopia. Pasadas las 72 horas se puede proceder al alta con IBP cada 24 horas por vía oral.
En los pacientes con estigmas endoscópicos de bajo riesgo (estadios de Forrest III y IIc) puede
reiniciarse la dieta, suspenderse la perfusión e indicarse al alta IBP cada 24 horas por vía oral.
Se debe mantener el tratamiento antisecretor (generalmente con IBP a dosis estándar [cada 24
horas]) durante 6 semanas ante una úlcera duodenal y durante 8 semanas ante una úlcera
gástrica). Los pacientes en tratamiento con ácido acetilsalicílico (AAS) o AINE requerirán
tratamiento de mantenimiento.
Tratamiento endoscópico. La hemostasia endoscópica está indicada en úlceras en estadios de
Forrest I y IIa al reducir la incidencia de resangrado, la necesidad de cirugía urgente y la
mortalidad. Cuando hay un coágulo adherido a la lesión (Forrest IIb), se recomienda movilizarlo
y hacer tratamiento endoscópico sobre dicha lesión si hubiera un sangrado activo o un vaso
visible. Los métodos de hemostasia utilizados son: 1) térmicos: aplicación de calor sobre el
vaso; 2) de inyección (más utilizados): vasoconstrictores (adrenalina diluida en una proporción
de 1:1.000), esclerosantes (polidocanol), adhesivos (cianoacrilato) o trombosantes (trombina o
goma de fibrina); 3) mecánicos: clips hemostáticos, bandas o endolazos (endoloops); y 4)
aerosoles hemostáticos tópicos. Para lograr la máxima eficacia se han de combinar dos técnicas,
y una de ellas será la inyección de adrenalina. En caso de recidiva se indica una segunda
gastroscopia y la repetición de tratamiento endoscópico. Si no fuera posible o fallara, se habría
de considerar la cirugía o la embolización mediante arteriografía (en caso de alto riesgo
quirúrgico). Los factores que aumentan el riesgo de recidiva son: presencia de shock, Hb baja
con requerimiento de transfusión, hemorragia activa en la endoscopia, úlceras de diámetro
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [834]
[53] HEMORRAGIA DIGESTIVA
superior a 2 cm y localización de las úlceras en la curvatura menor del estómago o en la cara
superior o posterior del duodeno. No se recomienda una gastroscopia rutinaria de control
(second look) a las 24 horas.
Tratamiento quirúrgico. Debe considerarse en los siguientes casos: 1) hemorragia masiva con
shock refractario sin opción a tratamiento endoscópico; 2) fracaso del segundo intento de la
endoscopia terapéutica; 3) recidiva hemorrágica grave, una vez valorado un segundo intento
endoscópico.
Angiografía terapéutica. Consiste en la embolización selectiva mediante angiografía y está
indicada en casos de tratamiento endoscópico ineficaz (especialmente en pacientes de alto
riesgo quirúrgico).
1.4. Prevención de recidiva a largo plazo
Erradicación de Helicobacter pylori. En todo paciente con HDA por úlcera péptica se debe
investigar la presencia de infección por HP y tratarla en caso de confirmarse. Para ello se
recomienda biopsiar la mucosa gástrica durante la endoscopia (aunque un resultado negativo
en una prueba realizada durante la fase aguda no descarta la infección). Por ello, dada la alta
prevalencia de la infección, se habría de confirmar el resultado negativo mediante un segundo
test en diferido (test del aliento con urea marcada con C13). Una vez completado el ciclo
antibiótico, es obligatorio confirmar su erradicación. El tratamiento se resume en la tabla VIII.
La triple terapia se recomienda en áreas con baja resistencia a claritromicina. Sin embargo, en
nuestro medio se sugiere la pauta cuádruple concomitante como tratamiento de primera línea,
pudiendo realizarse también terapia cuádruple clásica o secuencial de entrada. Tras el fracaso
de un primer tratamiento que incluya claritromicina o de una cuádruple terapia, se
recomiendan pautas que contengan quinolonas.
Tabla VIII. Tratamiento de infección por Helicobacter pylori.
AINE, antiagregantes y anticoagulación. Se recomienda suspender el antiinflamatorio. Si no
fuera posible, se debe valorar su sustitución por un inhibidor de COX-2 (celecoxib) y mantener
IBP durante su administración. En pacientes con doble antiagregación se ha observado mayor
riesgo trombótico que hemorrágico si se demora su reintroducción. Por tanto, se aconseja
reiniciar el tratamiento de manera precoz (alrededor del quinto día del episodio hemorrágico).
Se ha de individualizar la decisión de reintroducir la anticoagulación. Se recomienda iniciarla
con HBPM o con heparina sódica en casos de alto riesgo (prótesis metálicas), con posterior
paso a anticoagulación oral.
2. Síndrome de Mallory-Weiss
Consiste en laceraciones de la mucosa de la unión gastroesofágica cuyo sangrado cede
espontáneamente en la mayoría de los casos. Generalmente existe el antecedente de vómitos con arcadas
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [835]
[53] HEMORRAGIA DIGESTIVA
intensas. Si en la endoscopia se halla una lesión sangrante, se puede tratar con métodos térmicos, de
inyección o colocando bandas elásticas. Si el paciente no ha sangrado durante la endoscopia y no padece
otras patologías, se puede dar de alta en un periodo breve de tiempo.
3. Lesiones agudas de la mucosa gastroduodenal
Gastropatía o gastritis hemorrágica y erosiva es la denominación utilizada para designar las
hemorragias y erosiones subepiteliales que se identifican en la endoscopia. Se asocian con la ingesta de
AINE (más frecuentemente), con enfermedades relacionadas con el estrés o con quemaduras extensas y
con el consumo de alcohol. La terapia endoscópica en general es infructuosa. Además de las medidas
generales y del tratamiento de la causa subyacente, se pueden utilizar anti-H2, IBP o sucralfato.
B. HEMORRAGIA DIGESTIVA ALTA ASOCIADA A HIPERTENSIÓN PORTAL (HTP)
La HDA por HTP puede ser secundaria a rotura de varices esofagogástricas o ectópicas o a
gastropatía de la HTP. La HDA es la complicación más grave de los pacientes con cirrosis hepática y HTP, ya
que la mortalidad global a las 6 semanas oscila entre el 10 y el 20%. Por tanto, es importante identificar los
factores de mal pronóstico, de fracaso terapéutico y de mortalidad con el fin de optimizar el manejo de
estos pacientes.
Tabla IX. Clasificación endoscópica de las varices esofágicas.
Tabla X. Factores de mal pronóstico en la hemorragia digestiva alta por hipertensión portal.
Se considera fracaso en el control de la hemorragia a todo sangrado no controlado en los primeros
cinco días o a la aparición de recidiva tras haberse detenido inicialmente la hemorragia durante dicho
periodo. Se define por la aparición de hematemesis o aspirado nasogástrico hemático pasadas dos horas
del inicio del tratamiento (farmacológico o endoscópico), por la presencia de shock hipovolémico o por la
caída de Hb en 3 g/dL en un periodo de 24 horas sin transfusión. Esto conlleva la necesidad de un cambio
en el tratamiento. El fracaso en la prevención de la recidiva hemorrágica se define por un nuevo episodio
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [836]
[53] HEMORRAGIA DIGESTIVA
de hematemesis o melena (con caída de 3 g/dL de Hb) más allá de los 5 días iniciales y siempre una vez que
se haya controlado el sangrado (Tablas IX y X).
Las varices esofágicas están presentes en el 50% de los pacientes en el momento del diagnóstico, y
las gástricas, en el 20%. El mejor método para cuantificar el riesgo de HDA por varices esofágicas es el
gradiente de presión venosa hepática (GPVH), medido por estudio hemodinámico. Se considera HTP un
GPVH mayor de 5 mm Hg y es clínicamente significativa si supera los 10 mm Hg.
1. Hemorragia por varices esofágicas
Es la causa más frecuente de HDA en pacientes cirróticos con HTP. Se trata de una situación grave
con alta mortalidad que debe ser tratada con rapidez.
1.1. Tratamiento de la hemorragia aguda
Incluye medidas de reanimación, fármacos vasoactivos, terapia endoscópica, taponamiento
esofágico y derivaciones portosistémicas. Ninguno es totalmente eficaz, por lo que se combinan con
frecuencia. El tratamiento combinado farmacológico y endoscópico controla el episodio agudo en un 90%
de los casos y previene de la recidiva precoz en el 80% de los pacientes.
Medidas generales. El primer paso es la estabilización hemodinámica del paciente (ver
Apartado II. “Manejo inicial”) y la prevención de las complicaciones que puedan
desencadenarse.
Infecciones bacterianas: constituyen un factor independiente de mortalidad y de
fracaso terapéutico en el control de la hemorragia. Se recomienda el tratamiento
antibiótico durante 7 días en todo paciente cirrótico con hemorragia digestiva, con o
sin ascitis, mediante una quinolona (norfloxacino, 400 mg/día) o una cefalosporina de
tercera generación (ceftriaxona, 1 g/24 h por vía intravenosa; indicada en aquellos con
estadio funcional C de Child-Pugh o que estuvieran previamente con profilaxis con
quinolonas y en hospitales con alta tasa de resistencia a quinolonas). Si el paciente
tiene ascitis se le debe practicar siempre una paracentesis diagnóstica para descartar
peritonitis bacteriana espontánea (PBE).
Insuficiencia renal aguda: también se considera un factor independiente de
mortalidad. Para reducir su incidencia se debe realizar una reposición de volumen
adecuada y evitar diuréticos y fármacos nefrotóxicos.
Encefalopatía hepática: se puede prevenir mediante la administración de rifaximina o
lactulosa por vía oral o a través de sonda nasogástrica. El laxante puede administrarse
en forma de enema, aunque su eficacia no está claramente demostrada.
Deprivación alcohólica: en pacientes en que se sospeche alcoholismo activo se evitará
la deprivación alcohólica mediante el uso de benzodiazepinas pautadas o bien a
demanda en función de la clínica y grado de ansiedad (p. ej., lorazepam, 1-2 mg cada 4
horas como máximo). Para evitar el desarrollo de síndrome de Wernicke- Korsakoff, se
administra tiamina (Benerva® en ampollas de 100 mg) a una dosis de 100 mg/8-12 h
por vía intravenosa o intramuscular durante 3-5 días (siempre antes de aportar suero
glucosado).
Tratamiento farmacológico. Su objetivo es provocar una vasoconstricción esplácnica que
reduzca el flujo sanguíneo portal y la presión a la que está sometida la variz. Los fármacos
empleados son somatostatina y terlipresina. Este último es el único que ha demostrado
aumentar la supervivencia, pero debe evitarse ante cardiopatía isquémica inestable o
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [837]
[53] HEMORRAGIA DIGESTIVA
vasculopatía periférica. Deben emplearse inmediatamente ante la sospecha de hemorragia y
mantenerse durante 5 días (Tabla XI).
Figura 3. Plan asistencial en la hemorragia digestiva alta por hipertensión portal.
Tabla XI. Tratamiento farmacológico en hemorragia digestiva por hipertensión portal.
Tratamiento endoscópico: se debe efectuar endoscopia digestiva alta durante las primeras 12
horas a todos los pacientes que presenten HDA por HTP siempre que se garantice la seguridad
en su realización (si fuera necesario, en una UCI o en una UHD [en función de su
disponibilidad]). Durante la endoscopia se evalúa la existencia de varices esofágicas, su tamaño
y los signos de alarma de sangrado (Tabla IX), así como la presencia de varices esofagogástricas
o gástricas aisladas y de gastropatía de la HTP. Se asume que la hemorragia es varicosa ante la
presencia de sangrado activo, coágulo adherido, mamila con fibrina o restos hemáticos sin otra
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [838]
[53] HEMORRAGIA DIGESTIVA
causa que lo justifique. La ligadura con bandas elásticas es el tratamiento endoscópico de
elección en la hemorragia por varices. Se reserva la terapia esclerosante mediante inyección
intravaricosa de polidocanol o etanolamina para los casos en la que la ligadura sea
técnicamente difícil. En un 10-20% de las ocasiones el tratamiento inicial falla. En estos casos se
deberá intentar una segunda endoscopia. Si esta no fuera capaz de controlar el sangrado o se
produjera una nueva recidiva, se deberían utilizar otros tratamientos como los que se describen
a continuación.
Derivación portosistémica percutánea intrahepática (DPPI o TIPS): colocación de una prótesis
metálica recubierta en el parénquima hepático que comunica la vena porta derecha con la vena
hepática derecha. Está indicada si existiera un fallo en el control de la hemorragia, si fracasara
la segunda endoscopia terapéutica o si la recidiva fuera grave (prácticamente, ha desplazado a
la cirugía). No se puede realizar en pacientes con trombosis portal completa o con hepatopatía
muy avanzada (Child C > 14 puntos). Actualmente se recomienda la implantación precoz de un
TIPS (durante las primeras 72 horas de la hemorragia) en pacientes considerados de alto riesgo
para fracaso terapéutico (Child C < 14 puntos y Child B con sangrado activo en el momento de
la gastroscopia) y tras iniciar el tratamiento farmacológico y endoscópico, puesto que ello se
asocia a un marcado descenso de la mortalidad y del fracaso en el control de la hemorragia. Si
el paciente presentara un resangrado durante los primeros 5 días tras el primer tratamiento, se
debería llevar a cabo un nuevo tratamiento endoscópico si fuera posible, valorando colocar un
TIPS en los episodios de mayor gravedad.
Sondas-balón (Sengstaken-Blakemore, Minnessotta, Linton): se emplean en caso de
hemorragias masivas incoercibles de probable origen esofágico y ante fracaso del tratamiento
combinado como puente a tratamientos definitivos. La más empleada es la sonda de
Sengstaken-Blakemore, con un balón esofágico y otro gástrico que comprimen las varices y
evitan su sangrado. No se deben mantener durante más de 24-48 horas. Después de su
colocación hay que comprobar mediante endoscopia el cese del sangrado. Son muy eficaces en
el control de la hemorragia, pero llevan asociado un elevado riesgo de complicaciones, como
broncoaspiración o isquemia esofágica. Por ello, estos pacientes tienen indicación de
intubación orotraqueal y deben estar ingresados en una UCI o una UHD.
Prótesis metálicas autoexpansibles: los estudios sugieren que pueden ser igual de eficaces y
más seguras que los balones en sangrados refractarios a tratamiento endoscópico.
1.2. Profilaxis del sangrado por varices
Profilaxis primaria: se debe realizar una endoscopia de cribado para la detección de varices en
todos los pacientes con cirrosis. Hay dos modalidades terapéuticas indicadas en la profilaxis
primaria: los betabloqueantes no selectivos (BBNS) y la ligadura endoscópica de las varices con
bandas elásticas. La indicación y la elección del tratamiento dependerán del tamaño de las
varices, de la presencia de signos de sangrado y de la función hepática (Child-Pugh).
Sin varices: la exploración se ha de repetir cada 2 o 3 años; el tratamiento profiláctico
no está indicado.
Varices pequeñas (F1) sin signos de alarma (RC–) y con buena función hepática (Child
A): el uso de BBNS es opcional; debería repetirse el seguimiento en 1 o 2 años.
Varices pequeñas (F1) pero con signos de alarma (RC+) o hepatopatía avanzada (Child B
o C): se recomienda el uso de BBNS, no siendo necesario hacer más endoscopias para
evaluar la presencia de varices.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [839]
[53] HEMORRAGIA DIGESTIVA
Varices grandes (F2 o F3): se recomienda el uso de BBNS o hacer ligadura con bandas
elásticas (en función de la experiencia del centro, la elección del paciente, las
contraindicaciones y los efectos secundarios).
Los betabloqueantes no selectivos utilizados son el propranolol, el nadolol y el
carvedilol (con acción anti-α1 adrenérgica y actualmente considerado más efectivo para
disminuir el GPVH). Las dosis iniciales se deben incrementar cada 2 o 3 días hasta alcanzar
la dosis máxima tolerada o reducir la frecuencia cardiaca a 55 lpm. En aquellos centros con
disponibilidad para medir el GPVH, el objetivo es una disminución de un 20% del basal o
conseguir que este sea de 12 mm Hg o inferior. La caída de un 10% de la presión venosa
hepática basal o un GPVH de 12 mm Hg o inferior tras la administración de propranolol
endovenoso permitirá identificar a los pacientes respondedores a betabloqueantes. Los
efectos adversos más habituales son hipotensión y ortostatismo, debiéndose prestar
atención a la aparición de broncoespasmo, insuficiencia cardiaca o angina. Conviene
monitorizar la función renal por la disminución de flujo sanguíneo que producen (Tabla XII).
Tabla XII. Betabloqueantes no selectivos en profilaxis de hemorragia digestiva por hipertensión portal.
Profilaxis secundaria: hay que abordarla en todos los pacientes que han sufrido una
hemorragia por varices. Debe comenzarse tan pronto como sea posible a partir del sexto día de
la HD. Es de elección el tratamiento combinado con ligadura y BBNS. El procedimiento de la
ligadura se debe repetir cada 2-4 semanas hasta la erradicación de las varices, con controles
posteriores cada 6 o 12 meses. En aquellos casos en los que no se pueda hacer ligadura
endoscópica se recomienda tratamiento con BBNS en monoterapia; y, a la inversa, en aquellos
con intolerancia al tratamiento farmacológico se puede intentar la ligadura endoscópica como
única opción.
En los casos en los que fracasara el tratamiento para la prevención del sangrado se habría de
plantear la colocación de un TIPS (o de una derivación quirúrgica en pacientes con buena función hepática
[Child A o B] si aquel no estuviera disponible). El trasplante hepático en pacientes candidatos obtiene
buenos resultados a largo plazo, teniendo que usar el TIPS como tratamiento puente.
Los BBNS deben utilizarse con precaución en pacientes con ascitis refractaria. Hay que vigilar
estrechamente TA, función renal y niveles de natremia, reduciendo la dosis o suspendiéndolos ante TAS por
debajo de 90 mm Hg, Na+ < 130 mEq/l o fracaso renal agudo.
2. Hemorragia por varices gástricas
Las varices gástricas aparecen en el 20% de los pacientes con cirrosis y son más frecuentes en casos
de HTP segmentaria (p. ej., trombosis portal o esplénica). Presentan menos tendencia a sangrar aunque,
cuando lo hacen, la hemorragia es más severa y acarrea mayor mortalidad. Su manejo inicial no varía
respecto al del sangrado por varices esofágicas (Tabla XIII).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [840]
[53] HEMORRAGIA DIGESTIVA
Tabla XIII. Clasificación de las varices gástricas.
El tratamiento endoscópico suele ser más complejo porque la localización de las varices dificulta su
abordaje. El tratamiento de elección en varices esofagogástricas aisladas (IGV) o varices esofagogástricas de
tipo 2 (GOV-2) es la inyección intravaricosa de un pegamento tisular llamado N-butil-cianoacrilato
(Glubran®). En caso de no poder realizarla, se podría intentar la esclerosis de las varices, aunque los
resultados esperables son peores. Si no se logra controlar el sangrado se debe proceder a la colocación de
un TIPS o a la derivación quirúrgica. En pacientes con varices esofagogástricas de tipo 1 (GOV-1) se puede
efectuar ligadura con bandas o tratamiento con pegamento tisular.
Respecto a la profilaxis primaria, todos los pacientes con varices gástricas deben recibir tratamiento
con BBNS. Para la profilaxis secundaria se deben utilizar también BBNS unidos al tratamiento endoscópico
con pegamento tisular, ligadura con bandas (en el caso de varices GOV-1) o TIPS.
3. Hemorragia por gastropatía de la hipertensión portal (HTP)
La gastropatía de la HTP es una lesión de la mucosa gástrica caracterizada por dilatación de
capilares y vénulas de la mucosa y submucosa gástrica sin fenómenos erosivos o inflamatorios que
endoscópicamente se manifiesta como un patrón mucoso en mosaico o en piel de serpiente de aspecto
congestivo. Se clasifica en leve o severa, en función de la ausencia o presencia de “manchas rojo-cereza”. Se
manifiesta como HD. Su presentación más frecuente es en forma de pérdida crónica de sangre y anemia,
siendo muy baja la incidencia de hemorragia aguda; cuando esta se produce, su manejo inicial es
superponible al de la hemorragia varicosa. El tratamiento endoscópico se realiza mediante
electrofulguración con argón-plasma, y actualmente se recomienda mantener el tratamiento con fármacos
vasoactivos tras el procedimiento. La profilaxis secundaria se debe hacer con BBNS. No existe evidencia
para recomendar profilaxis primaria. El tratamiento de las pérdidas sanguíneas crónicas se lleva a cabo con
suplementos de hierro por vía oral y BBNS. En caso de mal control se debe plantear la realización de un
shunt portosistémico.
IV. HEMORRAGIA DIGESTIVA BAJA
Se denomina tradicionalmente hemorragia digestiva baja a aquella cuyo origen se encuentra en un
punto distal al ángulo de Treitz. Es más frecuente que la HDA, con una incidencia anual de 25-33 casos por
cada 100.000 habitantes. Su curso clínico suele ser más leve, con una mortalidad en torno al 2-5%, menor
riesgo de shock hipovolémico y menores necesidades transfusionales. Se trata de un problema frecuente
que supone un 20-25% de los ingresos por hemorragia digestiva, con ligero predominio en varones y edad
avanzada (edad media de aparición: 75 años). Se autolimita hasta en un 80% de los casos. En función de su
tiempo de evolución, se puede clasificar en aguda (menos de tres días) o crónica (días o semanas) y, en
función de la cuantía de la hemorragia, en leve, moderada, grave o masiva.
1. ETIOLOGÍA
Su forma de presentación más frecuente es la rectorragia, seguida de hematoquecia y diarrea
sanguinolenta. No hay que olvidar que hasta el 13% de las hemorragias que se presentan como sangrados
digestivos bajos corresponden a HDA. La etiología de la HDB varía en función del grupo de edad. En adultos,
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [841]
[53] HEMORRAGIA DIGESTIVA
las principales causas de HDB son el sangrado diverticular, seguido de la colitis isquémica y las
angiodisplasias. Globalmente, las causas más frecuentes son las siguientes (Tabla XIV):
Tabla XIV. Principales causas de HDB según el grupo de edad.
1. Diverticulosis
Es la causa más frecuente de HDB debido a su alta prevalencia, aunque solo el 3-5% de los
pacientes con divertículos la sufren. Son más frecuentes en el colon izquierdo; sin embargo sangran más los
pacientes afectados del colon derecho (ocasionándose el sangrado por la erosión de una arteria en el fondo
del divertículo). Generalmente la hemorragia es autolimitada pero recurre hasta en el 25% de los casos.
2. Angiodisplasias
Son ectasias vasculares que se distribuyen de forma difusa en la mucosa y la submucosa de la pared
intestinal, localizándose preferentemente en ciego, colon ascendente e íleon distal. Causan generalmente
sangrados venosos autolimitados pero que recurren en el 80% de los casos. Pueden asociarse a
enfermedades sistémicas, como estenosis aórtica o insuficiencia renal crónica, entre otras.
3. Colitis isquémica (ver Capítulo 59. “Patología vascular intestinal”).
4. Hemorroides
Son la causa más frecuente de rectorragia fresca, típicamente de pequeña cuantía, indolora y que
acontece al final de la deposición.
5. Pólipos y poliposis
Son lesiones mucosas únicas o múltiples que se proyectan hacia la luz intestinal. Su sangrado se
produce por la erosión de su superficie.
6. Sangrado pospolipectomía
Puede clasificarse en agudo o inmediato (durante el mismo procedimiento) o tardío (en relación a
la caída de la escara necrótica), que se presenta hasta 7 días después del procedimiento.
7. Neoplasia colorrectal
Su sangrado se produce por la erosión de la superficie tumoral y por fragilidad vascular.
8. Otras causas:
Divertículo de Meckel: es la causa más frecuente de HDB en niños y jóvenes. Se debe a la
ulceración péptica de la mucosa.
Enfermedad inflamatoria intestinal.
Enterocolitis infecciosa: destacan las causadas por Salmonella spp, Campylobacter spp, Yersinia
spp, Escherichia coli o Clostridium difficile, y también las virales (especialmente por CMV).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [842]
[53] HEMORRAGIA DIGESTIVA
Fármacos: AINE, anticoagulantes orales.
Trastornos de la coagulación.
Vasculitis: lupus eritematoso sistémico, panarteritis nodosa, granulomatosis eosinofílica con
poliangeítis (antigua vasculitis de Churg-Strauss).
2. DIAGNÓSTICO
La historia clínica y el examen físico son esenciales para confirmar la presencia de hemorragia
digestiva y para valorar su magnitud y la repercusión clínica. El paciente hemodinámicamente estable, con
hemorragia limitada y sin enfermedad asociada grave podrá ser evaluado de manera diferida.
1. Anamnesis
Se recogerán antecedentes familiares (cáncer colorrectal, cáncer de endometrio, síndrome de
Lynch), personales (edad, consumo de alcohol, fármacos ulcerógenos, antibióticos o anticoagulantes,
radioterapia, procedimiento endoscópico o polipectomía previa, enfermedad inflamatoria intestinal [EII],
patología cardiaca, hepática o renal) y datos sobre la enfermedad actual (magnitud, características y tiempo
de evolución del sangrado).
Las manifestaciones de la HDB dependen de la velocidad del sangrado y del tipo de lesión
subyacente. Cuanto más distalmente se localice o cuanto mayor sea la velocidad de tránsito, más roja será
la sangre eliminada. Por ello, ante una hematoquecia precedida de melenas o rectorragia franca
acompañadas de inestabilidad hemodinámica es obligatorio descartar HDA mediante la colocación de
sonda nasogástrica para hacer lavado. Si se acompañara de fiebre, diarrea con sangre, moco o pus, debe
descartarse diarrea infecciosa o EII. Heces acintadas, cambios en el hábito intestinal o síndrome
constitucional pueden orientar hacia patología neoplásica.
2. Exploración física
Es obligatorio llevar a cabo una exploración anal externa y un tacto rectal para valorar las
características de los restos fecales de la ampolla rectal y descartar lesiones ocupantes de espacio o
patología perianal. Hemos de prestar atención a la presencia de estigmas de hepatopatía crónica,
telangiectasias en labios y mucosas (enfermedad de Rendu-Weber-Osler), melanosis cutánea o mucosa
(poliposis intestinal), dermatitis herpetiforme (enfermedad celiaca), arritmias, soplos cardiacos y masas
abdominales (neoplasias, enfermedad diverticular o enfermedad de Crohn complicadas).
3. Colonoscopia
La eficacia diagnóstica de la colonoscopia en la HDB es del 53-97%. Su tasa de complicaciones es
baja (2%) y ofrece posibilidad terapéutica. Por tanto, es de elección como exploración inicial. Se aconseja
proceder previamente a una preparación del colon con una solución de polietilenglicol (no hay evidencia de
que dichas preparaciones reactiven ni aumenten el sangrado digestivo). Si existiera sospecha clínica de
obstrucción intestinal o de perforación, sería necesario realizar una radiografía de abdomen antes que la
endoscopia. En casos leves y limitados puede realizarse de manera electiva (más allá de las primeras 24
horas), mientras que en las formas más graves se recomienda su realización de manera precoz (a las 12-24
horas). Si sospechamos patología anorrectal, puede plantearse la realización de una rectosigmoidoscopia.
Ante una HDB grave o con inestabilidad hemodinámica es necesario estabilizar al paciente antes del
procedimiento endoscópico. En caso de no ser posible su estabilización por sangrado activo, la endoscopia
deberá llevarse a cabo bajo el soporte de una UCI o de un quirófano, con la monitorización adecuada
(existen riesgos en la sedación de estos pacientes, y también complicaciones hemodinámicas durante la
endoscopia).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [843]
[53] HEMORRAGIA DIGESTIVA
4. Angiografía
Presenta una sensibilidad del 47%. Para mostrar el origen de la HDB debe existir un sangrado con
flujo superior a 0,5 ml/min. Está indicada si la HDB permanece activa con el paciente inestable o si la
colonoscopia no es diagnóstica. Permite establecer el diagnóstico etiológico, la localización de la lesión y
también efectuar tratamiento mediante embolización (inyección de Gelfoam®). Para ello se introduce
contraste selectivamente en las arterias mesentéricas superior e inferior y los vasos celiacos hasta localizar
el punto de sangrado. Puede haber complicaciones hasta en el 11% de los casos (trombosis arterial,
embolización, fracaso renal, vasoconstricción de territorios vasculares como el coronario o el cerebral).
5. TAC
Puede realizarse como técnica previa a arteriografía por su disponibilidad, pero nunca sustituirla
puesto que no ofrece la realización de tratamiento. No precisa preparación previa, es rápida y presenta una
tasa de detección de lesiones del 50-86%. Es de elección ante la sospecha de fístula aortoentérica y
también ante colitis isquémica.
6. Técnicas de Medicina Nuclear
Permiten establecer la localización del sangrado, pero no su etiología. La gammagrafía con
hematíes marcados con 99mTc es la prueba de elección ante la sospecha de divertículo de Meckel.
7. Endoscopia alta
Puesto que en el 10-15 % de las HDB el origen del sangrado se encuentra en tramos altos, la
gastroscopia estará indicada en las HDB con lavado por SNG positivo y en las hemorragias graves o masivas,
bien antes o bien después de la realización de una colonoscopia sin lesiones.
8. Cápsula endoscópica y enteroscopia de doble balón
La primera obtiene imágenes del intestino delgado sin que se puedan tomar biopsias ni realizar
tratamiento; antes de llevarla a cabo se requiere una prueba de imagen que descarte contraindicaciones
para su realización (y, ante la duda, incluso se puede introducir una cápsula Patency® como sonda de
exploración para evitar complicaciones). La segunda se practica mediante un endoscopio que tiene un
balón en su extremo distal y otro en un sobretubo, con acceso alto o bajo en función del punto del intestino
delgado que se quiera alcanzar; con ella sí es posible tomar biopsias y el tratamiento de distintas lesiones.
9. Cirugía
Debe valorarse cirugía urgente en caso de hemorragia persistente, inestabilidad hemodinámica a
pesar de tratamiento médico intensivo, recidiva precoz grave, requerimientos transfusionales elevados (>6
unidades de hematíes en las primeras 24 h) o fracaso del tratamiento endoscópico con o sin embolización.
3. TRATAMIENTO
1. Manejo inicial
Toda HDB es una urgencia médica. En caso de inestabilidad hemodinámica, serán necesarias
maniobras inmediatas de reanimación, como se detalla al inicio del capítulo. Se deben canalizar dos vías
periféricas y obtener pruebas cruzadas y analítica completa con coagulación. Es recomendable la corrección
de los trastornos de la coagulación en pacientes tratados con anticoagulantes que sufran una hemorragia
aguda. Puede ser necesaria la transfusión de hemoderivados previamente a la realización de la endoscopia
para minimizar el riesgo de complicaciones y optimizar la hemostasia durante el procedimiento. Tras la
estabilización hemodinámica se deberá confirmar la presencia de HDB, estableciendo su cuantía y
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [844]
[53] HEMORRAGIA DIGESTIVA
características (se realizará tacto rectal y, en casos de hemorragia masiva o inestabilidad hemodinámica, se
colocará una SNG para descartar que el origen sea alto).
El manejo inicial de la HDB varía según el tipo de sangrado y la estabilidad hemodinámica.
Paciente con hemorragia aguda sin repercusión hemodinámica, hemorragia limitada o con
sangrado crónico: se realizará el estudio de manera electiva.
Paciente hemodinámicamente inestable o con sangrado masivo: si a pesar de maniobras de
reanimación persiste con inestabilidad hemodinámica puede requerir ingreso en UCI. La prueba
inicial de elección es la colonoscopia de urgencia (o gastroscopia si la sospecha es sangrado
alto), para lo que es necesaria la estabilidad hemodinámica. Si la hemorragia se detiene, se hará
una colonoscopia con preparación adecuada. Si la hemorragia persistiera tras la colonoscopia
urgente (ya fuera por fracaso del tratamiento endoscópico o porque no se hubiera identificado
punto de sangrado), se pueden llevar a cabo TAC abdominal urgente o angiografía (que podría
acompañarse de embolización arterial), colonoscopia de emergencia o cirugía dirigida.
2. Tratamiento específico
Aunque el 80% de las HDB se autolimitan, presentan una alta recidiva (esto depende de su
etiología). Por ello, aunque fuera de manera electiva, debería completarse el estudio.
La técnica de hemostasia endoscópica estará determinada por el tipo de lesión causante de la HDB.
Los métodos más usados en la práctica habitual son los métodos de inyección (adrenalina diluida 1:10.000,
etanolamina, etoxiesclerol), los métodos térmicos (termocoagulación y coagulación con argón-plasma
[APC)] y los métodos mecánicos (clips, bandas elásticas y endolazos). La inyección de adrenalina diluida se
usa frecuentemente asociada a la inyección de otra sustancia esclerosante o método mecánico, como los
hemoclips, debido a que su efecto se debe a vasoconstricción local (y resulta ser transitorio). Suele ser el
método de elección en el sangrado tras polipectomía o en sangrados diverticulares. La APC es eficaz para el
tratamiento de las angiodisplasias y de la proctitis actínica, tanto en el control del sangrado agudo como en
su recurrencia. El sangrado por hemorroides generalmente responde a tratamiento médico, pudiéndose
plantear de manera diferida la ligadura de las mismas o la cirugía.
La actitud a tomar ante la recidiva hemorrágica dependerá de la naturaleza y la localización de la
lesión, así como de la situación y características de cada paciente. Las alternativas en los pacientes en los
que fracasa el tratamiento endoscópico son la cirugía y la embolización arterial por vía percutánea.
Las indicaciones de intervención son la hemorragia masiva, el sangrado persistente que requiera
más de 4-6 unidades de sangre en 24 horas, la persistencia de la hemorragia durante 72 horas o antes de
que requiera 10 unidades y la recidiva grave ocurrida en los 7 días tras su tratamiento. Las resecciones
segmentarias a ciegas no deben realizarse por la alta morbimortalidad y el riesgo de resangrado que
conllevan. Por otro lado, en ocasiones se puede plantear cirugía electiva en pacientes con HDB recidivante
tras fracaso del manejo médico y endoscópico, como p.ej. divertículos y angiodisplasias (Figura 4).
V. HEMORRAGIA DE ORIGEN INCIERTO
Representa el 1-2% de todas las HD. Hasta en el 75%, el origen del sangrado se encuentra en el
intestino delgado. En el 10% de los casos no se identificará la causa.
La etiología, al igual que en el colon, depende del grupo de edad. Las angiodisplasias son la causa
más frecuente en el anciano. Debido a la mayor rentabilidad que ofrece el estudio endoscópico, estaría
indicada su repetición para, posteriormente, valorar hacer otras pruebas diagnósticas (Figura 5).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [845]
[53] HEMORRAGIA DIGESTIVA
Figura 4. Manejo de la hemorragia digestiva baja.
Figura 5. Manejo de la hemorragia de origen incierto.
VI. HEMORRAGIA DIGESTIVA OCULTA
Se define como la existencia de un test de sangre oculta en heces positivo o anemia ferropé nica sin
evidencia de sangrado macroscópico. Son múltiples las causas de hemorragia digestiva oculta, destacando
la enfermedad celiaca, patología péptica, EII o patología tumoral. Las exploraciones iniciales son el estudio
de los tramos accesibles por endoscopia. Después se continuará o no el estudio en función de la historia
clínica y de las pruebas analíticas.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [846]
[53] HEMORRAGIA DIGESTIVA
Se utilizan dos tipos de test para el estudio de sangre oculta en heces (SOH): cromogénico e
inmunológico. Este último es más sensible y no precisa la realización de una dieta específica durante los
días previos, pero es más caro. Existen tres posibles escenarios:
Paciente con anemia o síntomas gastrointestinales y test positivo para SOH: realizar
colonoscopia; si esta resultara negativa, se llevará a cabo gastroscopia; si también fuera
negativa, se procederá a un estudio del intestino delgado (TAC, RM, cápsula endoscópica,
enteroscopia de doble balón)
Paciente con test positivo para SOH, sin anemia y sin síntomas gastrointestinales: colonoscopia;
si resultara negativa, no precisaría más estudio.
Paciente con anemia ferropénica pero con test para SOH negativo: también se recomienda
realizar gastroscopia y colonoscopia salvo ante hematuria importante y mujeres jóvenes pre-
menopáusicas asintomáticas, con déficit de hierro moderado y sin antecedente de malignidad.
BIBLIOGRAFÍA
Barkun AN, Bardou M, Kuipers EJ, Sung J, Hunt RH, Martel M, et al. International consensus
recommendations on the management of patients with nonvariceal upper gastrointestinal bleeding.
Ann Intern Med. 2010; 152: 101-13.
Barnert J, Messmann H. Management of lower gastrointestinal tract bleeding. Best Pract Res Clin
Gastroenterol. 2008;22(2):295-312.
Bosch J, Abraldes JG, Albillos A, et al. Hipertensión portal: recomendaciones para su evaluación y
tratamiento: documento de consenso auspiciado por la Asociación Española para el Estudio del Hígado
(AEEH) y el Centro de Investigación Biomédica en Red de Enfermedades Hepáticas y Digestivas
(CIBERehd). Gastroenterol Hepatol. 2012; 35: 421-50.
De Franchis R. Revising consensus in portal hypertension: report of the Baveno V consensus workshop
on methodology of diagnosis and therapy in portal hypertension. J Hepatol. 2010; 53: 762-8.
De Franchis R, Baveno VI Faculty. Expandin consensu in portal hypertension: report of the Baveno VI
Consensus Workshop: stratifying risk and individualizing care hypertension. J Hepatol. 2015; 63:743.
Feu Caballé F, Saperas Franch E. Hemorragia digestiva baja. Resumen de las recomendaciones
terapéuticas con nivel de evidencia científica y grado de recomendación. Gastroenterol. 2008;22:295.
Garrido A, Rincón JP, Martínez JL. Hemorragia digestiva baja. Medicine. 2000;14: 734- 41.
Gisbert JP, Calvet X, Bermejo F, et al. III Spanish consensus conference on Helicobacter pylori infection.
Gastroenterol Hepatol. 2013; 36:340-74.
GraInek IM et al. Diagnosis and management of nonvariceal upper gastrointestinal hemorrhage:
European Society of Gastrointestinal Endoscopya (ESGE) Guideline. Endoscopy. 2015; 47:a1.
Green BT. Lower gastrointestinal bleeding-management. Gastroenterol Clin North Am. 2005;34:665-7.
Hwang JH, Fisher DA, Ben-Menachem T, et al. The role of endoscopy in the management of acute non-
variceal upper GI bleeding. Gastrointest Endos. 2012; 75:1132.
Jensen DM, Machicado GA, Jutabha R, Kovacs TOG. Urgent colonoscopy for the diagnosis and
treatment of severe diverticular hemorrhage. N Engl J Med. 2000;342:78-82.
Laine L, Jensen DM. Management of patients with ucler bleeding. Am J Gastroenterol. 2012; 107:345.
Lanas A, Calvet X, Feu F, Ponce J, Gisbert JP, Barkun A. Primer consenso español sobre el tratamiento
de la hemorragia digestiva por úlcera péptica. Med Clin (Barc). 2010;135: 608-11.
Marín JC, Rodríguez S. Técnicas endoscópicas para la prevención de la hemorragia pospolipectomía.
GH Continuada;6(2).
Radaelli F, Dentali F, Repici A, Amato A, Paggi S, Rondonotti E, Dumonceau JM. Mangement of
anticoagulation in patients with acute gastrointestinal bleeding. Dig Liver Dis. 2015;47(8):621-7.
Raju GS, Gerson L, Das A, Lewis B. American Gastroenterological Association (AGA). Institute technical
review on obscure gastrointestinal bleeding. Gastroenterology. 2007;133:1697-717.
Rockey DC. Occult and obscure gastrointestinal bleeding: causes and clinical management. Nat Rev
Gastroenterol Hepatol. 2010;7:265-79.
Romero LN, Mariela Montes A, Montes SV, Vizcaíno AV. Hemorragia digestiva baja: revisión. Revista de
Posgrado de la VI Cátedra de Medicina. 2006;156.
Villanueva C, Colomo A, Bosch A, et al. Transfusib strategies for acute upper gastrointestinal bleeding.
N Engl J Med. 2013; 368:11.
Zuccaro G. Management of the adult patient with acute lower gastrointestinal bleeding. Am J
Gastroenterol. 1998;93(8).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [847]
[54] DIARREA AGUDA Y CRÓNICA
54.Diarrea aguda y crónica
María Teresa Álvarez-Nava Torrego.
Medicina del Aparato Digestivo
Beatriz Sánchez Moreno.
Medicina Interna
Asesor:
Gonzalo Jesús Gómez Gómez.
Médico Adjunto Medicina del Aparato Digestivo
I. DIARREA
La diarrea se define como el aumento de volumen, fluidez o frecuencia de las deposiciones en
relación con el hábito intestinal normal de cada individuo, consistiendo generalmente en tres o más
deposiciones líquidas diarias (> 200 g al día). Debe distinguirse de dos entidades: la pseudodiarrea, en la
que se eliminan heces pequeñas y frecuentes (como en el síndrome del intestino irritable o en la proctitis),
y la incontinencia fecal, en la que se evacúa de forma involuntaria el contenido del recto.
En función de la duración del cuadro, se clasifica en diarrea aguda (menos de 14 días), diarrea
persistente o subaguda (entre 2 y 4 semanas) y diarrea crónica (más de 4 semanas).
En función del mecanismo fisiopatológico predominante, se clasifica en:
Diarrea acuosa:
Diarrea osmótica: se debe a solutos osmóticamente activos que apenas se absorben,
por lo que la presión osmótica en la luz intestinal es mayor que la plasmática,
provocando una secreción rica en agua, con escaso contenido en sodio (Na fecal < 60
mEq/l) e hiato osmolar en heces (290 – 2 [Na heces + K heces]) mayor de 125
mOsm/kg. El pH fecal suele ser bajo (< 5) por la fermentación bacteriana de los hidratos
de carbono. El volumen de las heces es generalmente menor de 1 l/día y cede con el
ayuno o cuando se suspende la ingesta del soluto no absorbible.
Diarrea secretora: por una disminución de la absorción o un aumento de la secreción
intestinal de líquidos y electrolitos (frecuentemente coinciden ambos). El hiato osmolar
en heces es menor de 50 mOsm/kg y son ricas en sodio (Na fecal > 90 mEq/l). Suelen
ser heces voluminosas (> 1 l/día) y generalmente persiste la diarrea pese al ayuno.
Diarrea exudativa o inflamatoria: por alteración de la integridad de la mucosa intestinal debida
a inflamación, ulceración o necrosis. Las heces suelen presentar moco, leucocitos (pus) y sangre
(oculta o visible).
Diarrea esteatorreica o esteatorrea: debida a una alteración en la digestión o absorción de
grasas. Las heces presentan 7-14 g de grasa al día.
Diarrea motora: secundaria a alteraciones de la motilidad intestinal, bien por aumento del
peristaltismo (se reduce el tiempo de contacto entre contenido intraluminal y epitelio
intestinal, por lo que el colon recibe más agua de la que puede absorber), bien por reducción
del mismo (condiciona un sobrecrecimiento bacteriano, que puede desencadenar diarrea).
II. DIARREA AGUDA
1. Concepto
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [848]
[54] DIARREA AGUDA Y CRÓNICA
Diarrea de duración inferior a 2 semanas. Se calcula que hay unos 2.000 millones de casos anuales a
nivel mundial, y es más frecuente en menores de 5 años. Generalmente son cuadros de naturaleza benigna
y autolimitada, aunque es una causa de morbimortalidad importante, sobre todo en países en desarrollo.
2. Etiología
Más del 90% se debe a agentes infecciosos, la mayoría virales, transmitidos por vía fecal-oral.
También pueden provocarla fármacos, tóxicos, alergias y otros trastornos (Tabla I). Por otra parte, la
diarrea puede ser un síntoma de otras enfermedades intraabdominales o sistémicas.
Tabla I. Etiología de la diarrea aguda.
3. Clínica
Se describen dos síndromes clínicos:
Acuoso: heces líquidas de gran volumen, que se pueden acompañar de vómitos. Producido por
toxinas bacterianas o patógenos capaces de adherirse al intestino. Suele requerir únicamente
terapia de soporte.
Inflamatorio o disentería: deposiciones frecuentes de escaso volumen y sanguinolentas,
acompañadas de dolor abdominal y fiebre, con leucocitos y sangre en heces. Producido por
microorganismos invasores. Suele beneficiarse de tratamiento antibiótico.
En ocasiones aparecen complicaciones extraintestinales secundarias (Tabla II). Además, puede
predisponer al desarrollo de síndrome de intestino irritable.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [849]
[54] DIARREA AGUDA Y CRÓNICA
Tabla II. Manifestaciones extraintestinales de la diarrea aguda y su etiología.
4. Aproximación diagnóstica
La anamnesis y el examen físico resultan indispensables para orientar el diagnóstico, evaluar la
gravedad y determinar la necesidad de más estudios (Figura 1).
Figura 1. Algoritmo diagnóstico-terapéutico en el paciente con diarrea aguda.
4.1. Historia clínica
Se debe recabar la siguiente información:
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [850]
[54] DIARREA AGUDA Y CRÓNICA
Características de la diarrea: duración (si es persistente, pensar en infección parasitaria),
frecuencia, volumen y aspecto de las deposiciones, además de síntomas acompañantes.
Factores de vulnerabilidad del huésped: edades extremas, inmunosupresión, fármacos como
inhibidores de la bomba de protones (IBP) y antibióticos, entre otros; cirugía o radioterapia
previa. Las enfermedades subyacentes, como la diabetes mellitus (DM), cardiopatías,
insuficiencia renal o cirrosis, pueden complicar el manejo y predisponer a la sepsis.
Factores epidemiológicos:
Alimentos y tiempo entre la ingesta y el desarrollo de síntomas (Tabla III).
Afectación de otros miembros de la familia o brote epidémico.
Prácticas sexuales de riesgo (infecciones de transmisión sexual, parásitos).
Viajes recientes (diarrea del viajero).
Lugar en el que se desarrolla la diarrea (domicilio, institución, hospital).
Tabla III. Intoxicaciones alimentarias.
4.2. Exploración física
Se deben valorar datos de deshidratación: hipotensión arterial u ortostatismo (descenso de 10 mm
Hg con la bipedestación), taquicardia y sequedad de piel y mucosas. Asimismo, hay que determinar la
presencia de fiebre y explorar el abdomen (una masa dolorosa en la fosa ilíaca derecha puede sugerir ileítis
terminal), buscando signos de peritonismo que puedan indicar necesidad de cirugía. También es
recomendable realizar una inspección anal y un tacto rectal.
4.3. Pruebas complementarias
Pruebas básicas: se realizarán en diarreas de más de 48-72 horas de duración o con datos de
gravedad. Incluyen:
Hemograma, bioquímica (glucosa, creatinina e iones) y gasometría venosa (acidosis
metabólica por pérdida de bicarbonato en heces).
Radiografía de abdomen simple y en bipedestación o en decúbito lateral con rayo
horizontal: si se sospecha íleo o megacolon.
Pruebas dirigidas: serán necesarias en diarreas en las que existan criterios de gravedad.
Heces:
Leucocitos y sangre oculta: su presencia apoya una etiología bacteriana.
Lactoferrina y calprotectina: su positividad indica presencia de neutrófilos. Son
más sensibles que las anteriores.
Coprocultivo: habitualmente resulta negativo, siendo más rentable en caso de
diarrea inflamatoria o cuando los leucocitos en heces son positivos. Además, se
recomienda su realización en inmunosuprimidos, pacientes con comorbilidades
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [851]
[54] DIARREA AGUDA Y CRÓNICA
y manipuladores de alimentos. Su rendimiento es menor en pacientes que
llevan más de 72 horas hospitalizados.
Otros estudios microbiológicos: en función de los datos clínico-
epidemiológicos, se solicitarán estudios de huevos y parásitos (viajeros,
inmigrantes, inmunosuprimidos y homosexuales; se deben enviar muestras 3
días consecutivos), detección de toxina de Clostridium difficile (especialmente
en pacientes hospitalizados o que han tomado antibióticos), examen con
microscopio de campo oscuro (si se sospecha Vibrio), cultivos especiales,
reacción en cadena de la polimerasa (PCR), ELISA, etc.
Sangre: hemocultivos en caso de fiebre, y serologías (útiles cuando se sospecha
amebiasis, Campylobacter o Yersinia).
Pruebas endoscópicas: en casos de diarrea sin un patógeno identificable, que no
mejora después de tratamiento empírico, o bien si se sospecha una etiología no
infecciosa, como un brote de enfermedad inflamatoria intestinal (EII). Puesto que la
mayoría de los procesos afectan de forma difusa al colon, suele bastar con una
rectosigmoidoscopia con toma de biopsias. La colonoscopia completa es preferible para
patología del íleon terminal o del colon proximal, o bien para diarrea asociada a sida
(una proporción de infecciones y linfomas pueden afectar solo al colon derecho o al
íleon). En algunos casos, puede ser útil realizar una endoscopia alta con aspiración del
contenido duodenal o biopsias.
Tomografía computarizada (TC) abdominal: cuando se incluyen otras patologías
intraabdominales en el diagnóstico diferencial (colitis isquémica, diverticulitis, etc.).
5. Tratamiento
El manejo de la diarrea aguda depende de la gravedad. Debe indicarse ingreso hospitalario en los
siguientes casos: deshidratación grave, repercusión sistémica importante (inestabilidad hemodinámica,
sepsis), vómitos incoercibles, diarrea con riesgo vital (botulismo, cólera), hemorragia y asociación de
factores de riesgo.
5.1. Medidas generales
El tratamiento fundamental, que debe llevarse a cabo en todos los pacientes, es reponer el déficit
de líquidos y electrolitos, preferiblemente por vía oral. En los casos leves, puede bastar con el aporte
exclusivo de líquidos (incluyendo bebidas deportivas, caldos, etc.). Cuando la diarrea es grave, se requieren
soluciones de rehidratación oral, como la estándar recomendada por la Organización Mundial de la Salud
(OMS) (3,5 g de cloruro sódico, 2,5 g de bicarbonato sódico, 1,5 g de cloruro potásico y 20 g de glucosa por
litro de agua), ingiriendo 2-3 litros al día a pequeños sorbos. La rehidratación intravenosa (Ringer lactato®)
debe emplearse en caso de intolerancia por vómitos o de deshidratación intensa.
En cuanto a la dieta, si se tolera la vía oral no es necesario el reposo intestinal. Se recomienda
aportar las calorías suficientes para favorecer la renovación de los enterocitos en forma de féculas hervidas
(patatas, arroz, avena, trigo), galletas saladas, plátanos, etc. Una vez que las deposiciones sean más
formadas, debe reintroducirse la dieta normal, evitando los alimentos ricos en grasas y la leche de forma
temporal (suele puede producirse un déficit transitorio de lactasa).
5.2. Tratamiento sintomático
Los antidiarreicos reducen la frecuencia y el volumen de las deposiciones, por lo que pueden ser
útiles en la diarrea secretora. Sin embargo, están contraindicados en la diarrea provocada por gérmenes
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [852]
[54] DIARREA AGUDA Y CRÓNICA
enteroinvasores ya que, al producir estasis intestinal, pueden favorecer la invasión tisular o retrasar su
aclaramiento, agravando o prolongando el cuadro. También se desaconsejan en pacientes con EII, colitis
pseudomembranosa (por riesgo de megacolon tóxico) y dilatación del intestino, así como en niños,
ancianos e inmunosuprimidos.
El fármaco más empleado es la loperamida (Fortasec®: dosis inicial de 4 mg, seguida de 2 mg
después de cada deposición, hasta un máximo de 16 mg diarios durante 2 días). El subsalicilato de bismuto
tiene una eficacia menor, pero es útil en la prevención y tratamiento de la diarrea del viajero.
En caso de vómitos, se pueden emplear antieméticos como la metoclopramida (Primperan ®, 10
mg/8 h vo/im/iv). El dolor abdominal de tipo cólico puede responder a espasmolíticos como la
butilescopolamina (Buscapina®, 10-20 mg/6-12 h vo/iv/im/sc), si bien también pueden aumentar el riesgo
de megacolon tóxico.
Los probióticos pueden ser beneficiosos en algunos casos de diarrea aguda, como en la diarrea por
antibióticos y en niños (ver más adelante, en el Apartado 5.2. “Diarrea crónica”).
5.3. Antibioterapia
No se recomienda su uso rutinario. Se debe instaurar tratamiento antibiótico empírico en los
siguientes casos:
Diarrea moderada-grave en pacientes mayores de 65 años, aquellos con enfermedad
subyacente grave o portadores de prótesis intravasculares, o en inmunosuprimidos (trasplante,
tratamiento corticoideo, DM, VIH, neoplasias).
Diarrea del viajero moderada-grave.
Considerar en diarrea grave.
Considerar en diarrea invasiva, fiebre > 38,5 °C y sangrado deposicional.
Considerar en manipuladores de alimentos y trabajadores sanitarios.
El tratamiento empírico puede realizarse con una quinolona oral (ciprofloxacino 500 mg/12 h,
norfloxacino 400 mg/12 h o levofloxacino 500 mg/24 h) durante 3-5 días. En situaciones en las que se
sospeche la infección por Escherichia coli enterohemorrágica (diarrea sanguinolenta sin fiebre), hay que
evitar administrar antibióticos por el riesgo de inducir síndrome hemolítico urémico. Si se sospecha
infección por Campylobacter, con mayor probabilidad de resistencia a quinolonas, se recomienda tratar con
macrólidos (azitromicina 500 mg/24 h durante 3 días o eritromicina 500 mg/12 h durante 5 días).
El tratamiento antibiótico dirigido depende del patógeno aislado en las muestras obtenidas (Tabla
IV). En pacientes inmunodeprimidos, con mayor riesgo de infecciones por gérmenes oportunistas, se
recomienda tratamiento dirigido durante más tiempo, en ocasiones de por vida.
6. Diarrea del viajero
Afecta a personas que viajan a países en vías de desarrollo, tras la ingesta de alimentos o bebidas
contaminadas, bien durante el viaje o al poco tiempo de regresar. Entre los factores de riesgo para
desarrollarla, se encuentran la inmunosupresión, la diabetes mellitus, la hipoclorhidria y la EII. La
antibioterapia reduce la duración del cuadro, pero se debe sopesar su uso debido a los efectos secundarios
y la aparición de resistencias; en general, se recomienda tomar quinolonas orales en casos graves. La
rifaximina (antibiótico de pobre absorción intestinal) es una opción alternativa, pero tiene una alta tasa de
resistencias. Además, se puede emplear subsalicilato de bismuto en cuadros leves-moderados.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [853]
[54] DIARREA AGUDA Y CRÓNICA
Tabla IV. Tratamiento antibiótico dirigido de la diarrea infecciosa.
III. DIARREA CRÓNICA
1. Conceptos
Diarrea crónica: se considera que la diarrea es crónica cuando su duración es superior a 4
semanas. Es un síntoma relativamente frecuente que afecta aproximadamente a un 3-5% de la
población general.
Malabsorción: alteración en la absorción de la mucosa de los nutrientes. El cuadro clínico
clásico consiste en deposiciones abundantes, pastosas y espumosas, distensión abdominal y
desnutrición. Generalmente se manifiesta como cuadro de diarrea crónica acuosa que puede ir
asociada a otros síntomas gastrointestinales, anemia y otras alteraciones de laboratorio.
Maldigestión: se define como la alteración en la hidrólisis de los nutrientes.
2. Clasificación y etiología
La diarrea crónica se puede clasificar en función de su mecanismo fisiopatológico predominante
(Tabla V). No obstante, esta clasificación tiene poca aplicabilidad en la práctica clínica, debido a que, en la
mayoría de los casos, la diarrea crónica está causada por varios mecanismos fisiopatológicos. Desde el
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [854]
[54] DIARREA AGUDA Y CRÓNICA
punto de vista práctico, tiene mayor interés distinguir entre diarrea con datos de organicidad o de perfil
funcional (Tabla VI).
Tabla V. Causas de diarrea crónica según su mecanismo fisiopatológico.
Tabla VI. Características de la diarrea funcional y orgánica.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [855]
[54] DIARREA AGUDA Y CRÓNICA
Tabla VII. Características de la diarrea según la localización de las lesiones.
La historia clínica también puede orientar sobre la localización más probable de las lesiones, en
intestino delgado, colon derecho o izquierdo (Tabla VII), que puede ayudar a orientar la causa de la diarrea.
3. Aproximación diagnóstica
3.1. Historia clínica
Se debe interrogar al paciente tanto sobre los síntomas digestivos como sobre los síntomas
sistémicos acompañantes:
Características de las heces (líquidas, pastosas, oleosas, presencia de productos patológicos,
volumen de las heces).
Frecuencia y patrón de las deposiciones: en caso de presentar patrón nocturno, orienta
especialmente a diarrea de perfil orgánico.
Inicio y curso de la diarrea: si el inicio es abrupto, deben considerarse diarreas de origen
infeccioso en primer lugar, pero también se han de tener en cuenta otro tipo de diarreas
orgánicas que pueden iniciarse de manera brusca (EII, colitis microscópica, colitis isquémica,
fármacos, etc.). Además, se debe recoger el patrón (continuo o intermitente) y la duración del
cuadro clínico.
Otros síntomas digestivos asociados: dolor abdominal y su localización, presencia de tenesmo y
urgencia defecatoria (afectación rectal) y/o flatulencia (malabsorción de carbohidratos).
Presencia de síntomas y/o signos sistémicos asociados referidos: fiebre, pérdida de peso, aftas
mucosas, lesiones cutáneas, etc., que orientan a origen orgánico.
Factores epidemiológicos: se deben registrar los viajes previos, la ingesta de agua o alimentos
potencialmente contaminados, familiares con síntomas similares, profesión (personal sanitario,
trabajadores de guarderías, etc.), toma de antibióticos (factor de riesgo para colitis
pseudomembranosa) u otros fármacos (puede ser un efecto secundario), hábitos sexuales
(proctitis asociada a gonorrea, clamidia, sífilis y amebiasis en caso de relaciones sexuales anales
de riesgo), consumo de drogas (colitis isquémica por cocaína) y alcohol. Resulta especialmente
útil realizar una cuidadosa anamnesis de los fármacos que toma el paciente y el periodo en el
que han sido introducidos.
Factores agravantes: relación con la ingesta y/o mejoría con el ayuno (orienta hacia un origen
orgánico), relación con el estrés (suele orientar hacia un origen funcional).
Antecedentes personales de interés: enfermedades endocrinometabólicas (DM,
hipertiroidismo), cirugías abdominales (síndrome del intestino corto tras resecciones masivas,
síndrome de Dumping y cuadros de malabsorción o maldigestión tras gastrectomía, etc.),
radioterapia (enteritis actínica), trasplante de médula ósea (enfermedad de injerto contra
huésped), etc.
Antecedentes familiares (EII, cáncer de colon, enfermedad celíaca, etc.).
3.2. Exploración física
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [856]
[54] DIARREA AGUDA Y CRÓNICA
La presencia de alteraciones en la exploración física sugiere un origen orgánico. Además, permite
valorar la gravedad y el grado de repercusión de la diarrea, y también orientar hacia la causa de la misma.
Se debe evaluar:
Tensión arterial y temperatura.
Piel y mucosas: se deben buscar signos de deshidratación y de desnutrición, además de otras
alteraciones como aftas bucales, eritema nodoso y pioderma gangrenoso (EII), dermatitis
herpetiforme (enfermedad celíaca), eritema necrolítico migratorio (glucagonomas),
hiperpigmentación (esprúe celíaco, enfermedad de Whipple o síndrome de Addison), palidez,
glositis y queilitis (déficit de hierro, de vitamina B12 y/o de ácido fólico por síndromes
malabsortivos), crisis de rubefacción (síndrome carcinoide, vipomas o feocromocitomas), etc.
Presencia de adenopatías.
Palpación tiroidea.
Auscultación cardiaca (taquicardia o soplo en el hipertiroidismo o síndrome carcinoide).
Palpación abdominal: masa palpable en los flancos o en la fosa ilíaca derecha (ileítis por
enfermedad de Crohn o causas infecciosas), hepatomegalia (metástasis hepáticas, amiloidosis),
ascitis (enteropatía pierde-proteínas).
Exploración neurológica: neuropatía periférica o demencia (pelagra por déficit de niacina y
otros síndromes malabsortivos por déficit de vitamina B12 y ácido fólico), desorientación,
nistagmo y oftalmoplejia (enfermedad de Whipple), disautonomía (DM y amiloidosis).
Extremidades: artritis (EII, enfermedad de Whipple, vasculitis y algunas infecciones), edemas
(enteropatía pierde-proteínas), acropaquias (hepatopatías, EII).
Inspección y tacto anorrectal: heces impactadas (diarrea por rebosamiento), hipotonía del
esfínter anal (incontinencia fecal), enfermedad perianal (fístulas, fisuras, úlceras o abscesos en
la enfermedad de Crohn).
3.3. Pruebas complementarias
Análisis de sangre: la analítica inicial debe incluir hemograma completo, proteína C reactiva,
velocidad de sedimentación, electrolitos, función renal, hepática y tiroidea, parámetros de
coagulación, albúmina y colesterol. El aumento de reactantes de fase, la presencia de datos de
malnutrición o de anemia orientan hacia un origen orgánico y aconsejan continuar realizando
exploraciones complementarias.
Determinaciones especiales:
Anticuerpos antitransglutaminasa y antiendomisio IgA, para el diagnóstico de
enfermedad celíaca (hasta un 5% de los pacientes celíacos presentan déficit de IgA y
por tanto falsa negatividad de la serología).
Otras determinaciones dirigidas por la anamnesis y la exploración: gastrina
(enfermedad ulceropéptica grave y diarrea acuosa), péptido intestinal vasoactivo,
calcitonina, anticuerpos antinucleares (si se sospecha vasculitis o esclerodermia),
anticuerpos anticitoplasma de neutrófilos (colitis ulcerosa), inmunoglobulinas,
serologías (VIH, Entamoeba histolytica).
Análisis de orina: se pueden solicitar ácido 5-hidroxiindolacético, ácido vanilmandélico y
metanefrina e histamina si se sospecha síndrome carcinoide, feocromocitoma y mastocitosis,
respectivamente.
Análisis de heces:
Inspección de heces en busca de productos patológicos.
pH: un pH bajo (< 5,3) es sugestivo de malabsorción de carbohidratos.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [857]
[54] DIARREA AGUDA Y CRÓNICA
Sodio, potasio e hiato osmolar fecal: el escaso contenido en sodio (Na fecal < 60 mEq/l)
y el hiato osmolar elevado (> 125 mOsm/kg) son típicos de diarreas osmóticas, como en
la malabsorción de carbohidratos; el sodio elevado (Na fecal > 90 mEq/l) con hiato
osmolar bajo (< 50 mOsm/kg) suele deberse a diarreas secretoras.
Osmolaridad fecal.
Sangre oculta en heces.
Leucocitos: diarrea inflamatoria.
Calprotectina fecal: es una proteína de unión al zinc y al calcio presente en neutrófilos y
monocitos, por lo que es un marcador de su actividad, y su valor en heces se
incrementa en caso de inflamación intestinal. Presenta un elevado valor predictivo
negativo, siendo de especial interés para descartar organicidad.
Prueba de Van de Kamer (cuantitativa): los valores superiores a 7 g de grasa por 100 g
de heces indican esteatorrea.
Coprocultivo: existen agentes que pueden causar diarrea persistente en personas
inmucompetentes (Yersinia, Mycobacterium tuberculosis) y en inmunosuprimidas
(Campylobacter, Salmonella).
Toxina de Clostridium difficile: se debe solicitar en caso de factores de riesgo para
colitis pseudomembranosa (toma de antibióticos, ancianos, inmunosuprimidos).
Parásitos en heces: sobre todo en caso de viajes recientes u otros factores de riesgo. Se
puede solicitar la detección del antígeno específico de Giardia lamblia en caso de existir
factores de riesgo (déficit de IgG, contacto con niños, etc.).
α1-antitripsina: se encuentra elevada en pacientes con enteropatía pierde-proteínas.
Determinación de quimotripsina y elastasa fecal: permite valorar la función pancreática
exocrina, pues se encuentran disminuidas en caso de insuficiencia.
Análisis de laxantes.
Estudios radiológicos:
Radiografía simple de abdomen: permite identificar el luminograma, calcificaciones
pancreáticas (pancreatitis crónica) y niveles hidroaéreos (suboclusión intestinal).
Tránsito gastrointestinal: si se sospecha afectación de intestino delgado; esta técnica ha
quedado parcialmente desplazada por la resonancia magnética del intestino (entero-
RM) y la entero-TC.
Ecografía, TC o RM abdominal: permiten valorar patología estructural a nivel del área
pancreatobiliar (pancreatitis crónica, neoplasia), enteritis y/o colitis (EII), adenopatías
(linfoma, tuberculosis, otras infecciones), etc.
Gammagrafía con leucocitos marcados: determina áreas abdominales con captación y
por tanto sospechosas de inflamación.
Estudios endoscópicos:
Colonoscopia: en algunos casos, la sigmoidoscopia puede ser suficiente para el
diagnóstico. La colonoscopia completa permite también valorar el colon derecho y el
íleon terminal si se realiza ileoscopia. La visualización directa de la mucosa permite
evaluar la presencia de datos de inflamación, úlceras y masas. La toma de biopsias es
obligada, dado que puede aportar el diagnóstico definitivo incluso en patologías en las
que no existan alteraciones macroscópicas en la mucosa (enfermedad de Whipple,
colitis microscópicas, estadios iniciales de EII, amiloidosis y algunas infecciones). Se
recomienda su realización en pacientes mayores de 40 años o con datos de
organicidad.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [858]
[54] DIARREA AGUDA Y CRÓNICA
Gastroscopia con toma de biopsias: es especialmente útil en el diagnóstico de cuadros
de malabsorción como la enfermedad celíaca y otras patologías, como la enfermedad
de Crohn, el linfoma intestinal, la gastroenteritis eosinofílica, la
hipogammaglobulinemia, la abetalipoproteinemia, la amiloidosis, la enfermedad de
Whipple, etc. Además, el aspirado duodenal puede servir para el diagnóstico de
patologías infecciosas, como determinadas parasitosis y tuberculosis.
Cápsula endoscópica y/o enteroscopia: no se recomienda de rutina, pero puede ser útil
para la evaluación de la enfermedad del intestino delgado cuando otras investigaciones
no son concluyentes. La cápsula endoscópica tiene la desventaja de que no permite la
toma de biopsias.
Pruebas funcionales:
Prueba del hidrógeno espirado: si se sospecha intolerancia a la lactosa, fructosa,
sorbitol o sobrecrecimiento bacteriano.
Prueba de absorción de la D-xilosa: valora la integridad absortiva de la mucosa
intestinal.
Prueba de la secretina: evaluación de la secreción exocrina pancreática. Se considera el
gold standard, pero es poco empleada en la práctica clínica por su complejidad.
Prueba del aliento con triglicéridos mixtos marcados con C13 (trioleína C13): es una
técnica eficaz, fácil y rápida para evaluar la insuficiencia pancreática exocrina. Permite
evaluar la eficacia y realizar un ajuste más preciso de los requerimientos reales de
enzimas pancreáticas.
4. Diagnóstico diferencial
La información recogida debe ser suficiente para distinguir entre una diarrea de perfil orgánico o
funcional, lo que es fundamental para seleccionar las pruebas complementarias que se han de solicitar
(Figura 2).
Figura 2. Algoritmo diagnóstico de la diarrea crónica.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [859]
[54] DIARREA AGUDA Y CRÓNICA
Diarrea crónica con características sugestivas de un origen funcional. La ausencia de síntomas y
signos de alarma, la normalidad del examen físico y la inexistencia de alteraciones en la analítica elemental
generalmente sugieren un origen funcional. No hay que olvidar que existen diarreas de base orgánica que
pueden ser clínicamente indistinguibles de un cuadro funcional. Se deben tener en cuenta, especialmente
cuando la diarrea es acuosa, cuatro entidades: colitis microscópica, enfermedad celíaca, malabsorción de
ácidos biliares e intolerancias a lactosa, fructosa o sorbitol. Dentro del grupo de origen funcional, merece
especial mención el síndrome del intestino irritable con predominio de diarrea, que asocia dolor o malestar
abdominal que precede a la deposición y se alivia tras la misma, y que cumple los criterios de Roma III
(Tabla VIII).
Tabla VIII. Criterios diagnósticos del síndrome del intestino irritable (Roma III).
Diarrea crónica con características de organicidad. Existen una serie de síntomas y signos referidos
(diarrea nocturna o que persiste con el ayuno; heces voluminosas, esteatorreicas o con productos
patológicos; coexistencia de fiebre, pérdida de peso y otros síntomas sistémicos; etc.), alteraciones en el
examen físico (masa abdominal palpable, hepatomegalia, adenopatías, aftas y otras lesiones
mucocutáneas) y alteraciones analíticas (anemia, macrocitosis, hipoprotrombinemia, hipoalbuminemia,
hipocolesterolemia, anomalías electrolíticas) que deben hacer sospechar un origen orgánico de la diarrea.
En estos casos, se han de solicitar más pruebas complementarias, según la sospecha clínica, para completar
el diagnóstico.
5. Tratamiento
El objetivo del tratamiento es controlar la diarrea, independientemente de su etiología, y conseguir
a la vez mantener una adecuada hidratación, el equilibrio electrolítico y el estado de nutrición, previniendo
además posibles complicaciones.
5.1. Medidas generales
La mejoría sintomática puede conseguirse, en teoría, disminuyendo las secreciones endógenas,
enlenteciendo el tránsito gastrointestinal y mejorando la absorción de solutos. Como consejo práctico, se
recomienda la reducción e incluso la eliminación de alimentos que contengan lactosa, bebidas con cafeína,
productos dietéticos con edulcorantes osmóticamente activos (sorbitol, manitol) y medicamentos con
sorbitol.
5.2. Tratamiento sintomático
Está indicado en tres situaciones: cuando, a pesar de las exploraciones realizadas, no se ha
conseguido llegar a un diagnóstico etiológico; cuando no existe tratamiento específico de la causa o
cuando, de haberlo, la respuesta al mismo es insuficiente.
Los objetivos son aumentar la consistencia de las heces, disminuir la frecuencia de las deposiciones
y aliviar los síntomas asociados.
Las opciones terapéuticas son varias:
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [860]
[54] DIARREA AGUDA Y CRÓNICA
Sustancias absorbentes como la fibra dietética (salvado de trigo, metilcelulosa, Plantago
ovata): actúan como coloides hidrófilos que solidifican las heces mediante la absorción de agua
en la luz intestinal. Pueden modificar la consistencia de la deposición pero no disminuyen el
peso de la misma. Podrían ser, por tanto, especialmente útiles en algunos pacientes con diarrea
funcional.
Derivados opiáceos (loperamida −Fortasec®−, codeína, difenoxilato): retrasan el vaciamiento
gástrico, inhiben la secreción gástrica, biliar y pancreática, estimulan la absorción intestinal de
agua y electrolitos y reducen el peristaltismo intestinal. No deben utilizarse ante sospecha de
oclusión intestinal, insuficiencia hepática grave ni en las exacerbaciones de colitis ulcerosa o
enfermedad de Crohn, por el riesgo de precipitar un íleo o una dilatación aguda intestinal. El
fármaco de elección es la loperamida, que carece de efectos secundarios a nivel del sistema
nervioso central.
Análogos de la somatostatina (octreótido): disminuyen las secreciones intestinales y solo
deben ser utilizados en diarreas secretoras graves incontrolables por otros métodos (síndrome
del intestino corto, diarreas hormonales, síndrome de Dumping posgastrectomía, proctocolitis
actínica).
Resincolestiramina: quelante de los ácidos biliares, que impide la acción irritante de estos
sobre la mucosa del colon. Además de estar indicado en el síndrome poscolecistectomía o tras
la resección del íleon terminal, ha resultado ser útil en el tratamiento de la diarrea idiopática.
La dosis recomendada es de 4-12 g/día.
Probióticos: son microorganismos vivos que confieren un beneficio a la salud del huésped.
Existen diversos preparados farmacéuticos comercializados que incluyen distintas
combinaciones de cepas de probióticos. Las especies de Lactobacillus y Bifidobacterium son las
usadas más frecuentemente. Los probióticos estimulan los mecanismos inmunitarios de la
mucosa intestinal, incrementan la función de la barrera intestinal y ofrecen protección frente a
la colonización e invasión por microorganismos patógenos. Estos fenómenos reducen la
incidencia y gravedad de la diarrea. En este sentido, han demostrado utilidad en el tratamiento
de la diarrea aguda (siendo mayor su beneficio en las gastroenteritis virales que en las
infecciones bacterianas o parasitarias), en la prevención de la diarrea aguda (tanto de la infantil
como en la del adulto en algunas situaciones específicas, como evitar la diarrea asociada a los
antibióticos y la diarrea por Clostridium difficile en adultos hospitalizados), en el síndrome del
intestino irritable con predominio de diarrea (en esta entidad también pueden mejorar otros
síntomas como la distensión abdominal, la flatulencia y el dolor) y en otro tipo de diarreas de
perfil funcional. Existe menos evidencia sobre su beneficio en el alivio de los síntomas de
intolerancia a la lactosa y sobrecrecimiento bacteriano. Por otro lado, los probióticos pueden
ser efectivos en la pouchitis (para prevenir brotes iniciales y como tratamiento de
mantenimiento de la pouchitis con actividad inflamatoria leve).
5.3. Tratamiento empírico
Se puede realizar cuando hay alta sospecha diagnóstica, como en los siguientes ejemplos:
Metronidazol (250-500 mg/8 h durante 7-10 días), ante un brote previo conocido de giardiasis.
Resincolestiramina (4-12 g/día), en la diarrea tras resección ileal.
Antibióticos intraluminales (metronidazol 500 mg/8 h vo o rifaximina 200 mg/6 h o 400 mg/8 h
vo durante 7-10 días), en cuadros recurrentes de sobrecrecimiento bacteriano.
Sospecha de intolerancia a la lactosa que mejora al retirarla de la dieta.
5.4. Tratamiento específico
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [861]
[54] DIARREA AGUDA Y CRÓNICA
Muchas de las enfermedades que cursan con diarrea crónica tienen un tratamiento específico
eficaz, como en los siguientes casos:
Antibióticos en la enfermedad de Whipple (ceftriaxona 2 g/día o meropenem 3 g/día iv, seguido
de cotrimoxazol 160-800 mg/12 h vo durante 12 meses).
Dieta exenta de gluten en la enfermedad celíaca.
Suplementos de enzimas pancreáticas (Kreon®) en la insuficiencia pancreática exocrina (ver
Capítulo 58. “Pancreatitis”).
Aminosalicilatos, fármacos inmunosupresores y biológicos en la EII (ver Capítulo 55.
“Enfermedad inflamatoria intestinal”).
Budesonida (9 mg/día durante 6 semanas inicialmente, manteniendo posteriormente 3-6
mg/día durante 24 semanas) y aminosalicilatos (3-4 g/día durante 3-6 meses) en caso de falta
de respuesta a budesonida, en la colitis microscópica.
Indometacina en la diarrea que acompaña al carcinoma medular de tiroides y a la proctocolitis
actínica.
BIBLIOGRAFÍA
Camilleri M, Murray JA. Diarrea y estreñimiento. En: Longo DL, Fauci AS, Kasper DL, Hauser SL,
Jameson JL, Loscalzo J, editores. Harrison. Principios de Medicina Interna. 18ª ed. México: McGraw-Hill
Interamericana; 2012 [acceso 16 de enero de 2016]. Disponible en:
https://harrisonmedicina.mhmedical.com/Content. aspx?bookid=865§ionid=68928222.
Drossman DA, Camilleri M, Mayer EA, Whitehead WE. American Gastroenterology Association technical
review on irritable bowel syndrome. Gastroenterology. 2002;123:2108-31.
DuPont HL. Acute Infectious Diarrhea in Immunocompetent Adults. N Eng J Med. 2014;370(16):1532-
40.
Fine KD, Schiller LR. American Gastroenterology Association technical review on the evaluation and
management of chronic diarrhea. Gastroenterology. 1999;116:1464-86.
Guarner F, Kahn A, Garisch J, Eliakim R, Gangl A, Thomson A, et al. World Gastroenterology
Organization Global Guidelines: probiotics and prebiotics October 2011. J Clin Gastroenterol.
2012;46:468-81.
Guerrant RL, Van Gilder T, Steiner TS, Thielman NM, Slutsker L, Tauxe RV, et al. Practice Guidelines for
the Management of Infectious Diarrhea. Clin Infect Dis. 2001;32(3):331-51.
Guía Práctica de la Organización Mundial de Gastroenterología. Diarrea aguda en adultos y niños: una
perspectiva mundial. Febrero de 2012 [acceso 20 de enero de 2016]. Disponible en:
http://www.worldgastroenterology. org/UserFiles/file/guidelines/acute-diarrhea-spanish-2012.pdf.
LaRocque RC, Ryan ET, Calderwood SB. Diarreas infecciosas agudas e intoxicación alimentaria por
bacterias. En: Longo DL, Fauci AS, Kasper DL, Hauser SL, Jameson JL, Loscalzo J, editores. Harrison.
Principios de Medicina Interna. 18ª ed. México: McGraw-Hill Interamericana; 2012 [acceso 16 de
enero de 2016]. Disponible en:
http://harrisonmedicina.mhmedical.com/Content.aspx?bookid=865&Sectionid=68937602.
Li Z, Vaziri H. Treatment of chronic diarrhea. Best Pract Res Cl Ga. 2012;26:677-87.
Schiller LR. Chronic diarrhea. Gastroenterology. 2004;127:287-93.
Schiller LR. Definitions, pathophysiology, and evaluation of chronic diarrhea. Best Pract Res Cl Ga.
2012;26:551-62.
Schiller LR, Sellin JH. Diarrhea. En: Feldman M, Friedman LS, Brandt LJ, editores. Sleisenger and
Fordtran’s gastrointestinal and liver disease: pathophysiology, diagnosis, management. Philadelphia:
Saunders Elsevier; 2010. p. 211-32.
Thielman NM, Guerrant RL. Acute Infectious Diarrhea. N Eng J Med. 2004;350:38-47.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [862]
[55] ENFERMEDAD INFLAMATORIA INTESTINAL
55.Enfermedad inflamatoria intestinal
María Algara San Nicolás.
Medicina del Aparato Digestivo
Adrián García Villa.
Medicina Interna
Asesora:
Ángeles Masedo González.
Médica Adjunta de Medicina del Aparato Digestivo
I. INTRODUCCIÓN
La enfermedad inflamatoria intestinal (EII), es un proceso inflamatorio crónico del tubo digestivo,
que intercala periodos de actividad y otros de remisión. La etiología es desconocida, interviniendo factores
genéticos, inmunológicos y ambientales. Dentro de la EII, se incluyen la enfermedad de Crohn (EC), la colitis
ulcerosa (CU), la colitis no clasificada (supone el 10% de los casos, afectando al colon y con características
clínicas, radiológicas, endoscópicas e histológicas que no permite diferenciar entre CU y EC) y la colitis
indeterminada (término anatomopatológico cuando coexisten características histológicas de EC y CU en la
misma pieza quirúrgica tras colectomía).
Antes de profundizar en las enfermedades, es necesario conocer algunos conceptos básicos:
Brote: periodo en el que un paciente con EII padece síntomas y signos dependientes de la
reactivación de su enfermedad.
Remisión: disminución (denominada remisión parcial) o desaparición (remisión completa) de
los síntomas y signos de la enfermedad.
Curación mucosa: desaparición de las lesiones intestinales en la endoscopia.
Recidiva: reaparición de sintomatología después de un periodo de quiescencia o inactividad de
la enfermedad.
Recurrencia: reaparición de la enfermedad después de una resección quirúrgica curativa en la
EC. Puede ser endoscópica y/o clínica.
Corticodependencia: se da cuando no es posible reducir la dosis de prednisolona por debajo de
10 mg/día (o 3 mg/día de budesonida) en los primeros 3 meses de tratamiento esteroideo, o
cuando reaparecen los síntomas antes de los 3 meses de suspender los corticoides.
Corticorrefractariedad: enfermedad que se mantiene en actividad a pesar de corticoides a
dosis plenas (1 mg/kg/día).
II. APROXIMACIÓN DIAGNÓSTICA
Para el diagnóstico de la EII no existe un “patrón de oro” sino que debe establecerse a través de la
combinación de los datos obtenidos de la historia clínica, pruebas de laboratorio, radiología, endoscopia y
la histología, siendo necesario excluir otras causas, principalmente las infecciones.
Aunque la forma de presentación es muy heterogénea, debe sospecharse EII ante la aparición
crónica o recurrente de episodios de diarrea, rectorragia, dolor abdominal, tenesmo o urgencia defecatoria,
presencia de lesiones perianales o de ciertas manifestaciones extraintestinales (MEI). Tanto la clínica como
la exploración física, se explican detalladamente más adelante.
1. Anamnesis
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [863]
[55] ENFERMEDAD INFLAMATORIA INTESTINAL
Deben recogerse antecedentes familiares de enfermedades digestivas (EII, enfermedad celíaca,
cáncer colorrectal), toma de fármacos (especialmente los AINE por su capacidad de producir enteritis o
colitis y los antibióticos por la colitis pseudomembranosa), hábito tabáquico y otras drogas, factores
epidemiológicos de colitis infecciosas (viajes al extranjero, intoxicaciones alimentarias o casos en
convivientes) y resto de antecedentes personales. En cuanto a la historia actual: duración del cuadro y
características del mismo o episodios similares previos, MEI asociadas. En los casos con diagnóstico
establecido de EII, la anamnesis irá dirigida a determinar si el cuadro que presenta el paciente es por un
brote de la EII u otra patología concomitante, establecer la gravedad del mismo, la necesidad de
tratamiento intravenoso y de ingreso hospitalario.
2. Exploración física
Deben descartarse signos de irritación peritoneal, obstrucción intestinal o la presencia de masas
abdominales que sugieran una complicación intraabdominal grave (abscesos, perforación intestinal...). Hay
que explorar la zona perianal.
3. Pruebas de laboratorio
Se realizará hemograma, bioquímica con reactantes de fase aguda (VSG, fibrinógeno, PCR), función
hepática, renal e iones. Estudio nutricional y perfil férrico, ácido fólico, vitamina B12, proteínas totales.
Son útiles para el diagnóstico diferencial: hormonas tiroideas, anticuerpos antitransglutaminasa,
inmunoglobulinas y autoinmunidad.
4. Estudios microbiológicos
Coprocultivo y toxina de Clostridium difficile (TCD), deben realizarse al diagnóstico de la EII y en los
pacientes con brote grave, antes del inicio de antibioterapia. Los parásitos se realizarán al diagnóstico de la
enfermedad, ante la sospecha clínica o factores epidemiológicos que lo justifiquen.
5. Calprotectina en heces
Heterodímero de proteína presente en el citoplasma de los neutrófilos, por lo que constituye un
biomarcador al aumentar sus niveles en procesos inflamatorios/infecciosos. Su determinación permite
distinguir entre diarrea orgánica y funcional, detectar actividad inflamatoria, predecir aparición de brotes y
monitorización del tratamiento. Es más específico de intestino que la VSG y la PCR. Los niveles son: < 50
μg/g normal, 50-100 μg/g test débilmente positivo y > 100 μg/g resultado positivo.
6. Pruebas endoscópicas
Ante la sospecha de una EII, la primera prueba endoscópica a realizar es una ileocolonoscopia con
toma de biopsias de todos los tramos (íleon, colon ascendente, colon transverso, colon descendente y
recto). Existen distintos índices que evalúan la actividad endoscópica siendo los más utilizados en la
práctica clínica el Índice de Mayo para la CU y el SES-CD en la EC (Tablas I y II).
Tabla I. Índice de Mayo para la colitis ulcerosa.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [864]
[55] ENFERMEDAD INFLAMATORIA INTESTINAL
Tabla II. Índice de SES-CD para la enfermedad de Crohn.
La EC y CU presentan hallazgos endoscópicos diferentes (Tablas III y IV).
Se considera enfermedad de Crohn definida la presencia de granulomas junto a otro criterio o, en
ausencia de granulomas, la existencia de tres criterios; se define la enfermedad probable con dos criterios
en ausencia de granulomas (Tabla IV).
Se solicitará una recto-sigmoidoscopia urgente en los casos de brote grave para evaluar la presencia
y gravedad de las lesiones rectales y tomar muestras para descartar infección por citomegalovirus (CMV),
con mínima insuflación de aire por el riesgo de perforación.
En EC con síntomas altos es preciso realizar una gastroscopia con biopsias, aunque no existan
lesiones macroscópicas. También estaría indicada en la colitis inclasificable, para descartar lesión gástrica
que indicaría EC.
La cápsula endoscópica es especialmente útil en alta sospecha de EC con ileocolonoscopia,
gastroscopia y entero-RMN normales, en EC conocida cuando existe discordancia entre la clínica y las
pruebas analíticas/endoscópicas habituales y en colitis inclasificable.
Tabla III. Criterios diagnósticos de Lennard-Jones para colitis ulcerosa.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [865]
[55] ENFERMEDAD INFLAMATORIA INTESTINAL
Tabla IV. Criterios diagnósticos de Lennard-Jones para la enfermedad de Crohn.
La enteroscopia por pulsión y de doble balón, permiten alcanzar yeyuno e íleon proximal y distal,
por boca o por ano respectivamente, permitiendo la detección de lesiones de EC no visibles o no accesibles
por otros métodos y en determinadas situaciones su tratamiento (por ejemplo, dilatación de estenosis
cortas)
La ecoendoscopia baja está indicada para el estudio de la enfermedad perianal (EPA).
7. Radiodiagnóstico
Ayuda a determinar la localización, la extensión, la presencia de actividad inflamatoria y en la EC, el
patrón clínico. Además de permitir descartar complicaciones y valorar la respuesta al tratamiento.
7.1. Radiografía de tórax
Necesaria antes de iniciar tratamiento inmunosupresor (IS) o biológico, para determinar posibles
cambios morfológicos que sugieran enfermedad tuberculosa.
7.2. Radiografía simple de abdomen
Debe realizarse en todo paciente que ingrese por EII o complicaciones relacionadas. En caso de
afectación extensa de colon, se recomienda su realización cada 24-48 horas. En la CU puede ayudar a
determinar la extensión proximal de la colitis, observando pérdida de la haustració n, edema mucoso y
ausencia de heces en el tramo afecto, y para descartar megacolon tóxico. En la EC para descartar
complicaciones como presencia de niveles hidroaéreos si existe obstrucción o pseudo-obstrucción
intestinal o aire libre si existe perforación intestinal.
7.3. Ecografía abdominal
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [866]
[55] ENFERMEDAD INFLAMATORIA INTESTINAL
Permite evaluar la presencia de complicaciones (masas o abscesos) y recientemente gracias a la
utilización de contraste, se detecta la actividad inflamatoria y su extensión. Además, al ser una prueba
inocua y de gran disponibilidad, es muy útil en el seguimiento de los pacientes y la monitorización del
tratamiento.
7.4. La tomografía axial computarizada (TC) abdominal
Es la prueba de elección ante sospecha de complicación.
7.5. Enterorresonancia magnética (entero-RM): evalúa la extensión y actividad de la EII, además de
aportar información extramural. En la EC, la RM pélvica es fundamental para el estudio de la EPA.
Es importante tener en cuenta que los pacientes con EII, son pacientes jóvenes, con una
enfermedad crónica y con múltiples complicaciones en su evolución, por ello y ante el desarrollo de
técnicas menos invasivas, el uso de pruebas con radiación ionizante debe limitarse para evitar yatrogenia.
8. Histología
A través de los criterios de Lennard-Jones, que recoge criterios clínicos, radiológicos, endoscópicos
y anatomopatológicos, se puede definir la presencia de EII (Tablas III y IV). La tabla V recoge de forma
resumida las principales diferencias entre ambas entidades y la tabla VI las MEI.
Debido a la evolución crónica e impredecible de la EII, al realizarse el diagnóstico es necesario
solicitar una serie de estudios complementarios, encaminados a descartar contraindicaciones y prevenir
complicaciones al inicio del tratamiento con IS y biológicos. Aunque algunas ya se han nombrado, este
estudio incluiría: Mantoux-Booster, placa de tórax, serologías virales (VHA, VHB, VHC, VIH, VEB, VVZ, CMV)
y revisión del calendario vacunal (existen guías que recogen la obligatorias y las que puede recibir el
paciente bajo tratamiento), la tiopurina S-metiltransferasa (TPMT) (< 5 UI contraindica el uso de tiopurinas)
y autoinmunidad (ANA, anti-DNA).
Tabla V. Principales diferencias diagnósticas entre colitis ulcerosa y enfermedad de Crohn.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [867]
[55] ENFERMEDAD INFLAMATORIA INTESTINAL
Tabla VI. Manifestaciones extraintestinales de las enfermedades inflamatorias intestinales.
Las MEI subrayadas presentan curso paralelo a la enfermedad y se manejan con el tratamiento de
la enfermedad inflamatoria intestinal (EII); el resto requieren tratamiento específico y son independientes
del curso de la EII.
III. DIAGNÓSTICO DIFERENCIAL
El diagnóstico diferencial debe realizarse con todas las enfermedades que cursen con cuadro clínico
similar (dolor abdominal, diarrea o rectorragia):
Patología funcional, destacando por frecuencia el síndrome de intestino irritable: con
normalidad en las pruebas complementarias y ausencia de datos de alarma.
Causas de ileítis aguda: apendicitis, patología ginecológica (tubo-ovaritis, enfermedad
inflamatoria pélvica) e ileítis infecciosas (Yersinia, tuberculosis, amebiosis).
Colitis isquémica: pacientes de edad avanzada con factores de riesgo cardiovascular.
Colitis infecciosas: que típicamente producen colitis agudas autolimitadas. Los gérmenes más
frecuentes son: Yersinia, Shigella, Campylobacter, Giardia, Chlamydia o Clostridium difficile. En
pacientes inmunodeprimidos, además de los previos pueden producirse por gérmenes
oportunistas: criptosporidios, Mycobacterium avium o CMV.
Proctitis infecciosas: gérmenes de transmisión sexual que pueden presentar un cuadro similar a
la CU (herpes simple, Neisseria gonorrhoeae, Treponema pallidum).
Colitis por fármacos (AINE, quimioterápicos).
Neoplasias digestivas, sobretodo el adenocarcinoma de colon y el linfoma intestinal.
Cuando la afectación se limite únicamente al colon, será necesario realizar el diagnóstico diferencial
entre EC y CU (Tabla V). Otras: enfermedad celíaca, vasculitis, diverticulitis, colitis microscópica (linfocítica y
colágena), colitis actínica.
IV. COLITIS ULCEROSA
Se caracteriza por afectación de la mucosa del intestino grueso. La inflamación se inicia en el recto
y se extiende de forma continua y proximal hasta el ciego.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [868]
[55] ENFERMEDAD INFLAMATORIA INTESTINAL
El intestino delgado no está habitualmente afecto excepto en las colitis extensas graves, en las que
puede afectarse el íleon terminal (ileítis por reflujo).
La enfermedad cursa en forma de brotes de actividad, durante los cuales el grado de inflamación
aumenta, siendo imprevisible el número, gravedad y periodicidad de estos. Estos brotes de actividad se
siguen de periodos de remisión de duración variable, bien espontáneos o inducidos por el tratamiento.
I. CLÍNICA
La intensidad de los síntomas depende de la extensión y la gravedad de la inflamación. La principal
manifestación clínica es la diarrea con secreción de moco y sangre, acompañada frecuentemente de
síndrome rectal (tenesmo, urgencia deposicional) y, en menor medida y habitualmente de forma leve, de
dolor abdominal de tipo cólico o retortijón. Las deposiciones frecuentemente son nocturnas. En los
enfermos con proctitis, es frecuente el estreñimiento mientras que en afectaciones más extensas es más
probable que se produzca diarrea sanguinolenta. Los síntomas generales como astenia, fiebre o pérdida de
peso son menos frecuentes que en la enfermedad de Crohn.
Tan solo el 15% de los pacientes presenta una colitis grave al inicio. El megacolon tóxico es una
complicación muy grave presente en el 5% de las crisis, que puede estar precipitado por alteraciones
electrolíticas y por narcóticos. Consiste en una dilatación de más de 6 cm del colon transverso asociado a
manifestaciones clínicas de toxicidad sistémica definidas según los criterios de Jalan, de tal manera que
aquella existiría si se cumplen tres de las siguientes condiciones: fiebre de más de 38,5 ºC, taquicardia
superior a 120 lpm, leucocitosis mayor de 10500/mcL, anemia; y además una de las siguientes:
deshidratación, trastornos hidroelectrolíticos, distensión abdominal, hipotensión, alteración de la
consciencia. Si se presenta en el seno de un brote grave de CU, habitualmente se indica la intervención
quirúrgica porque las posibilidades de perforación son muy elevadas. Si el megacolon es la forma de debut,
puede tratarse durante 48-72 horas de modo intensivo y, si el paciente empeora o surge alguna
complicación como perforación o hemorragia, debe ser intervenido.
La perforación es la complicación local más peligrosa y los signos físicos de peritonitis no siempre
son evidentes. La enfermedad puede acompañarse de MEI (Tabla VI).
Existe asimismo un aumento del riesgo de adenocarcinoma colorrectal, sobre todo en formas
extensas y de larga evolución. Por ello, para estos pacientes, existen recomendaciones específicas para
cribado y el intervalo entre las colonoscopias de vigilancia de cáncer colorrectal.
II. EXPLORACIÓN FÍSICA
Aparecerá afectación del estado general y de las constantes vitales de forma variable. Los signos
físicos de la proctitis incluyen sensibilidad del conducto anal y presencia de sangre en el tacto rectal. En
formas más extensas el paciente refiere dolor con la palpación directa sobre el colon. Los individuos con
colitis tóxica presentan dolor intenso, hemorragia y timpanismo abdominal, pudiendo existir signos de
peritonitis si ha ocurrido perforación. Es necesario hacer una exploración detallada de la cavidad oral, ojos,
piel y articulaciones.
III. VALORACIÓN DE LA ACTIVIDAD
Habitualmente las manifestaciones clínicas tienen buena correlación con la intensidad de la
inflamación. Para estadificar la gravedad se utilizará la clasificación de Montreal (Tabla VII), que define la
actividad de la enfermedad en cuatro grupos (inactiva, leve, moderada y grave) y determinará el manejo
terapéutico y el seguimiento.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [869]
[55] ENFERMEDAD INFLAMATORIA INTESTINAL
De forma práctica en la clínica, y para valorar la actividad de los brotes, se puede utilizar el índice
de Truelove-Witts modificado (Tabla VIII), si bien esta escala, aunque frecuentemente utilizada en su forma
semicuantitativa, no ha sido validada y debe usarse con prudencia.
Tabla VII. Clasificación de Montreal para la colitis ulcerosa.
Tabla VIII. Índice de Truelove-Witts modificado.
IV. TRATAMIENTO DE LA COLITIS ULCEROSA
Sus objetivos son controlar los brotes de actividad, mantener la remisión de la enfermedad libre de
esteroides, disminuir la necesidad de hospitalizaciones y cirugías, mejorar la calidad de vida de los
pacientes y desde la introducción de las terapias biológicas, cambiar el curso natural de la enfermedad y la
curación de la mucosa.
Hay que indicar el ingreso hospitalario a aquellos pacientes que cumplen los criterios de la tabla IX
por el elevado riesgo de colectomía.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [870]
[55] ENFERMEDAD INFLAMATORIA INTESTINAL
Tabla IX. Criterios de ingreso en la colitis ulcerosa.
1. Medidas generales a tener en cuenta independientemente del tipo de enfermedad
inflamatoria intestinal
Se debe evitar el uso de AINE, fármacos antidiarréicos y espasmolíticos, por el riesgo de
desarrollar megacolon tóxico.
Se recomienda la anticoagulación profiláctica con heparina de bajo peso molecular
(enoxaparina 20 mg o 40 mg cada 24 h subcutáneo) en todos los brotes graves y en brotes leves
o moderados si el paciente presenta otros factores de riesgo (inmovilidad, obesidad, etc.),
incluso si presentan rectorragia.
Si se sospecha complicación séptica o en caso de megacolon tóxico, debe realizarse cobertura
empírica frente a bacilos gramnegativos y anaerobios (ciprofloxacino 400 mg/12 h o ceftriaxona
1 g/24 h asociado a metronidazol 500 mg/8 h), siempre previa realización de coprocultivos y
TCD.
Adecuado soporte nutricional, siempre que sea posible se recomienda la nutrición por vía oral,
pudiendo asociar suplementos de nutrición enteral. La nutrición parenteral está indicada en
casos de intolerancia digestiva, obstrucción o perforación intestinal, fístulas de gran débito y
megacolon tóxico.
Deben vigilarse y corregirse las posibles alteraciones hidroelectrolíticas como la hipopotasemia
y de forma específica, el magnesio en caso de tratamiento con ciclosporina A (CsA).
Durante el tratamiento con sulfasalazina y metotrexato (MTX) se deben administrar
suplementos de ácido fólico.
Durante el tratamiento con corticoides se debe administrar calcio con vitamina D3.
En la EC es frecuente el déficit de vitamina B12 y vitaminas liposolubles que se deben corregir.
La anemia ferropénica es un problema frecuente. Se debe iniciar tratamiento con hierro (oral
excepto en caso de intolerancia o falta de respuesta) o transfusión de hemoderivados.
Las guías clínicas de EII recomiendan realizar profilaxis de infección por Pneumocystis jiroveci
(trimetroprim-sulfametoxazol 160/800 mg, un comprimido 3 veces por semana) siempre que se
mantenga el tratamiento con corticoides a dosis mayores de 20 mg durante al menos 3
semanas, y durante el tratamiento concomitante con dos o más IS y/o fármacos biológicos.
La elección del tratamiento se basa en dos factores primordiales definidos por la clasificación de
Montreal: la gravedad y la extensión de la enfermedad. Ambos determinan los fármacos a utilizar y su vía
de administración (tópica o sistémica).
2. Inducción de la remisión
2.1. Brote de colitis ulcerosa leve-moderado
Proctitis: un supositorio de 1 g de mesalazina al día es el tratamiento de elección (distribuye el
fármaco de manera más efectiva y son mejor tolerados). Es igual de eficaz en dosis única que
fraccionada. Los enemas o la espuma de mesalazina son una alternativa. La combinación de
mesalazina tópica y oral o corticoides tópicos es más eficaz que cualquiera de ellos por
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [871]
[55] ENFERMEDAD INFLAMATORIA INTESTINAL
separado, por lo que es la opción al escalar en el tratamiento. La proctitis refractaria puede
requerir IS y/o agentes biológicos.
Figura 1. Manejo del brote leve-moderado de colitis ulcerosa.
Colitis izquierda o extensa: el tratamiento de elección es el enema de mesalazina de 1 g al día
asociado a mesalazina oral ≥ 2 g al día (la remisión clínica se alcanza tanto con 2,4 g/día como
con 4 g/día, aunque es más rápida con esta última dosis).
Otros tratamientos (corticoides/aminosalicilatos tópicos o aminosalicilatos orales en monoterapia)
son menos eficaces. Si no existe respuesta a mesalazina, hay que asociar corticoides orales de baja
biodisponibilidad, como budesonida MMX (9 mg/día) o dipropionato de beclometasona (5 mg/día), o
sistémicos, como prednisona (0,75-1 mg/kg/día).
Ante fracaso de las medidas terapéuticas previas, son de elección los corticoides orales clásicos a
dosis plenas (1 mg/kg/día) de prednisona o equivalente, siempre en dosis única y preferentemente por la
mañana. Cuando no se obtenga respuesta (corticorresistencia) en un tiempo que varía según la gravedad
del brote (entre una y dos semanas), se debe indicar tratamiento como un brote grave. Además,
aproximadamente un cuarto de los pacientes que responden van a presentar corticodependencia, por lo
que requerirán tratamiento específico de mantenimiento.
2.2. Brote de colitis ulcerosa grave
Requieren ingreso hospitalario y colaboración desde el principio con el cirujano. Los fármacos de
elección en este escenario son los corticoides sistémicos por vía endovenosa, a dosis de 1 mg/kg de
prednisona diaria o equivalente.
Dado que se trata de pacientes con altas probabilidades de requerir terapia de rescate con
biológicos o IS, se solicitará el estudio complementario necesario de cara al inicio de dicho tratamiento
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [872]
[55] ENFERMEDAD INFLAMATORIA INTESTINAL
(serologías, PPD…), así como radiografías simples de abdomen seriadas para diagnosticar precozmente
complicaciones (perforación cólica o megacolon tóxico) y una rectoscopia con biopsia para descartar
sobreinfección por CMV. En estos pacientes la colonoscopia completa está contraindicada.
La respuesta a los corticoides debe valorarse continua y específicamente tras los tres primeros días
de tratamiento. La persistencia de un elevado número de deposiciones (más de seis diarias) con sangre,
junto a niveles elevados de PCR (más de 45 mg/dL) a las 72 horas, permite predecir con gran exactitud y
precozmente la corticorrefractariedad. En los pacientes corticorrefractarios las diferentes opciones de
tratamiento (biológicos, CsA o colectomía) deben comentarse con el paciente. La decisión de iniciar
tratamiento biológico o CsA, dependerá de varios factores, como la experiencia del centro, la disponibilidad
de niveles de ciclosporina, la realización previa al tratamiento biológico de Mantoux-Booster o Quantiferón
y placa de tórax, así como si el paciente ha recibido previamente o no IS, es decir, si es naïve o no.
Figura 2. Manejo del brote grave de colitis ulcerosa.
3. Terapias de rescate
La ciclosporina endovenosa se usa a dosis de 2-4 mg/kg/día repartidos en dos dosis (ajustando
en función de los niveles en sangre recomendándose entre 150-250 ng/ml), debiendo
prolongarse el tratamiento un mínimo de 7 y un máximo de 14 días. Durante el tratamiento
deben mantenerse los corticoides intravenosos a dosis plenas. En el caso de haber alcanzado
respuesta clínica con CsA endovenosa se debe continuar el tratamiento vía oral a dosis de 4-8
mg/kg, introduciendo en este momento azatioprina (AZA) o 6-mercaptopurina (6-MP) y
disminuyendo progresivamente los corticoides hasta 20 mg/día. Tras 3 meses se suspende la
CsA y se prosigue la retirada de corticoides. Se evitará en caso de fracaso previo de tiopurinas,
hipertensión arterial grave, insuficiencia renal o imposibilidad de medir niveles de CsA.
Infliximab se usa a dosis estándar (Tabla X). Se aconseja administrar un IS desde el inicio para
incrementar la eficacia y disminuir las reacciones a la infusión. Está contraindicado en caso de
infección tuberculosa latente, insuficiencia cardiaca congestiva y enfermedad desmielinizante.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [873]
[55] ENFERMEDAD INFLAMATORIA INTESTINAL
La colectomía constituye una alternativa en el brote grave corticorrefractario, sobre todo en
caso de falta de respuesta o contraindicación a la terapia de rescate. Estaría especialmente
indicada ante una historia prolongada de colitis ulcerosa mal controlada y/o la presencia de
displasia en controles previos, siendo a veces necesaria ante la aparición de un megacolon
tóxico o una hemorragia masiva.
En hospitales de tercer nivel con experiencia está aceptado un segundo tratamiento de rescate
antes de la cirugía.
En caso de que se confirme la infección por CMV, se debe añadir ganciclovir endovenoso al
tratamiento (mínimo de una semana, seguido de valganciclovir oral durante 2-3 semanas).
Tabla X. Fármacos anti-TNF alfa: presentaciones, dosis y pautas.
4. Tratamiento de mantenimiento
Figura 3. Tratamiento de mantenimiento en la colitis ulcerosa según la gravedad del brote y la extensión.
Una vez inducida la remisión clínica, es preciso seguir tratamiento de mantenimiento de la
remisión, que se mantendrá indefinidamente y que dependerá de la gravedad del brote, extensión y del
fármaco utilizado para conseguir la remisión y la respuesta clínica.
4.1. Tras brote leve-moderado
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [874]
[55] ENFERMEDAD INFLAMATORIA INTESTINAL
En la proctitis cuya remisión se ha alcanzado con supositorios de mesalazina, estos se
mantendrán 3 veces en semana durante 6 meses y posteriormente se suspenderán (única
situación donde el tratamiento no es indefinido), salvo si presenta brotes repetidos, en cuyo
caso se mantendrán indefinidamente.
En la CU izquierda-extensa, si la remisión se alcanza con aminosalicilatos o corticoides de baja
disponibilidad, tras el descenso progresivo y la suspensión de los mismos, se continuará
mantenimiento con mesalazina. En caso de haber requerido corticoides sistémicos, se utilizarán
IS igual que en la corticodependencia. Los pacientes con CU moderada, activa, refractaria a
tiopurinas deben de ser tratados con terapia anti-TNFα, aunque debe considerarse la
colectomía.
4.2. Tras brote grave
Controlado con corticoides: se indicarán tiopurinas asociado o no a salicilatos. Se realizará
vigilancia estrecha porque en caso de nuevo brote o pérdida de eficacia de las tiopurinas, será
necesario añadir anti-TNFα.
Corticorrefractario: el tratamiento de mantenimiento dependerá del fármaco empleado para
lograr la remisión.
Remisión obtenida con CsA. Esta no deberá prolongarse más de seis meses por riesgo
de nefrotoxicidad irreversible, por eso después de la remisión si el paciente es naïve a
AZA/6-MP, se mantendrá indefinidamente bajo este tratamiento. En caso de no
mantener la remisión, se considerará biológico o cirugía, según factores individuales. En
los pacientes no naïve a AZA, el mantenimiento se podrá realizar con un biológico.
Remisión obtenida con IFX. En caso de que no haya recibido previamente IS, se iniciará
AZA o 6-MP indefinidamente; si no se mantiene la remisión, se plantearán los
biológicos o la cirugía de manera personalizada. Si el paciente ya había recibido
previamente inmunosupresores se continuará con el biológico y, en caso de pérdida de
respuesta, se planteará la intensificación del biológico o el cambio de biológico si
persiste la pérdida de respuesta.
Debido a que se han descrito casos de linfoma hepatoesplénico de células T en hombres jóvenes
que recibían terapia combinada (biológico y tiopurínicos), actualmente se recomienda limitar a un año el
tratamiento combinado, y tras este periodo de tiempo podría plantearse la utilización de monoterapia en
pacientes en remisión clínica, biológica y con curación de las lesiones mucosas.
En la actualidad existen tres fármacos anti-TNFα admitidos como tratamiento en la CU: IFX
(Remicade®), adalimumab (Humira®) y golimumab (Simponi®). Recientemente han sido aprobados por la
Agencia Europea del Medicamento dos fármacos biosimilares de IFX (Remsima®, de los laboratorios
Celltrion, e Inflectra®, de los laboratorios Hospira), que empezaron a comercializarse en febrero de 2015 y
tienen las mismas indicaciones y vía de administración que IFX (Tabla X). El IFX es el único anti-TNFα
admitido en el tratamiento del brote grave de CU corticorrefractaria como alternativa a la CsA.
4.3. Corticodependencia y corticorrefractariedad
CU corticodependiente: está indicado el inicio de IS (AZA y 6-MP). El efecto de estos fármacos
tarda aproximadamente 3 meses, por lo que se deben mantener los corticoides durante este
tiempo. Como alternativa está indicado el tratamiento con anti-TNFα, en monoterapia o
asociado a IS.
CU corticorrefractaria: el tratamiento de mantenimiento dependerá del fármaco empleado
para lograr la remisión, pudiendo ser los IS o los anti-TNFα como se describe previamente.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [875]
[55] ENFERMEDAD INFLAMATORIA INTESTINAL
Tabla XI. Indicaciones quirúrgicas
V. ENFERMEDAD DE CROHN
Se caracteriza por la inflamación transmural y discontinua del tracto gastrointestinal, en cualquier
segmento desde la boca a la región perianal (aunque el recto suele estar respetado). La afectación más
frecuente es la localización íleocecal (40%) e íleon (30%). La afectación aislada del colon (20%) o de tramos
proximales del tubo digestivo (5-10%) es menos frecuente.
I. CLÍNICA
Son más heterogéneas que en la CU, están condicionadas por la localización y la presencia de
complicaciones. Las manifestaciones más frecuentes incluyen: la diarrea (que suele de mayor cuantía que
en la CU y sin sangre), dolor abdominal (de predominio en fosa ilíaca derecha (FID) tipo cólico y que
empeora con las comidas) y pérdida de peso. Con cierta frecuencia, asocian síntomas sistémicos como
malestar general, anorexia o fiebre.
Como manifestaciones menos frecuentes, puede existir clínica de afectación digestiva alta como
disfagia, dispepsia, vómitos de retención o epigastralgia por afectación esofagogástrica y/o duodenal.
Dentro de las complicaciones, se sospechará obstrucción o subobstrucción intestinal secundaria a
estenosis luminal con dolor abdominal tipo cólico, ausencia de deposición o de emisión de gases e incluso
náuseas y vómitos. Presencia de abscesos o complicaciones sépticas intraabdominales con un abdomen
agudo con peritonitis. La EPA, presente en el 30% de pacientes con EC, ocasiona dolor local y supuración
por la presencia de fisuras, fístulas o abscesos perianales o perineales y estenosis anal.
Las MEI que se asocian a la EC pueden consultarse en la tabla VI. Los pacientes con enfermedad
perianal tienes más riesgo de padecer MEI.
II. EXPLORACIÓN FÍSICA
Los datos de la exploración física suelen ser más llamativos que en la CU. Además de la exploración
general y de la toma de constantes y el peso, es preciso realizar una exploración detallada en busca de MEI,
así como inspección anal y tacto rectal. En la auscultación, los ruidos hidroaéreos pueden estar aumentados
en caso de oclusión-suboclusión intestinal, o ausentes ante la presencia de íleo paralítico. La palpación
abdominal suele ser dolorosa, sobre todo en FID, pudiéndose palpar íleon engrosado, masa abdominal o
incluso peritonismo. En la inspección anal es importante descartar la presencia de pliegues perianales
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [876]
[55] ENFERMEDAD INFLAMATORIA INTESTINAL
engrosados, hemorroides, fisuras, fístulas y abscesos. En el tacto rectal es posible evidenciar sangrado
rectal o la presencia de pus por descarga de las fístulas.
III. VALORACIÓN DE LA ACTIVIDAD
La clasificación de Montreal (Tabla XII) define el patrón de la enfermedad según su extensión y
comportamiento. Es importante reseñar, que la enfermedad evoluciona con el tiempo, pudiendo cambiar
de un patrón a otro o presentarse dos patrones simultáneamente, y que esta clasificación tiene
implicaciones pronósticas y terapéuticas.
Tabla XII. Clasificación de Montreal de la enfermedad de Crohn.
En la EC, la actividad inflamatoria, la gravedad clínica y los hallazgos endoscópicos o radiológicos,
muchas veces presentan peor correlación, por ello, se dispone de múltiples índices que valoran las distintas
situaciones clínicas. Entre ellos, destacar el CDAI (Crohn Disease Activity Index); es un índice clínico validado
que mide la actividad de la EC, sin embargo, su uso en la clínica diaria no es adecuado, utilizándose en los
ensayos clínicos.
En la práctica clínica habitual, se diferencia entre: brote leve, paciente ambulatorio, capaz de tener
una alimentación oral, sin síntomas de deshidratación, toxicidad, fiebre ni complicaciones
intraabdominales. Brote moderado, paciente con febrícula, pérdida de peso, dolor abdominal o sensibilidad
a la exploración abdominal, náuseas o vómitos sin hallazgos obstructivos o anemia significativa. En el brote
grave existe fiebre alta, vómitos persistentes, obstrucción intestinal, peritonismo, caquexia o absceso
abdominal.
La EPA incluye fisuras, úlceras perianales, pliegues cutáneos, fístulas y abscesos, por lo que es
necesario un estudio completo mediante RM pélvica, ecoendoscopia o incluso exploración bajo anestesia,
para realizar una adecuada evaluación y clasificación de la enfermedad. Es más frecuente en el EC que
afecta al colon.
Al diagnóstico de la EC, además, hay que tener en cuenta ciertos factores cuya presencia implican
un peor pronóstico y por ello, un manejo terapéutico más agresivo. Estos factores son: edad < 40 años,
hábito tabáquico, requerimiento de múltiples ciclos de corticoides, afectación extensa del ID, afectación
rectal, fenotipos estenosantes y fistulizantes, EPA compleja, resecciones previas y presencia de úlceras
profundas en la colonoscopia.
IV. TRATAMIENTO DE LA ENFERMEDAD DE CROHN
Los objetivos son los ya mencionados en la CU, y la elección del tratamiento debe realizarse de
manera individualizada, en función de las características de cada paciente, considerando la localización, el
fenotipo y la gravedad de la enfermedad, así como las MEI, complicaciones asociadas o EPA.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [877]
[55] ENFERMEDAD INFLAMATORIA INTESTINAL
1. Medidas generales
Las medidas generales descritas para la CU también deben emplearse en EC (ver Apartado “Colitis
Ulcerosa”, punto IV.1).
2. Inducción de la remisión
2.1. Enfermedad íleocecal/ileal
Figura 4. Manejo de la enfermedad de Crohn ileal e ileocecal.
Brote leve y moderado: generalmente es de manejo ambulatorio. La budesonida oral
(Intestifalk®, Entocord®) a 9 mg/día durante 6-8 semanas, es el tratamiento de elección. Se
recomienda descenso de 3 mg en 3 mg cada 2 semanas o 9 mg cada 48 horas durante 4
semanas y suspender. En caso de falta de respuesta a las 2 semanas, está indicado el
tratamiento con prednisona o equivalente, por vía oral, a dosis de 1 mg/kg al día, con reducción
progresiva de la dosis, hasta su supresión. En caso de ausencia de respuesta en 2-4 semanas o
empeoramiento clínico, se considerará manejo como brote grave.
Brote grave: es indicación de ingreso hospitalario e inicio de corticoides intravenosos (1 mg/kg
al día). En caso de deterioro clínico o falta de respuesta a las 4 semanas, está indicado el
tratamiento a dosis de inducción con anti-TNFα. La terapia combinada de anti-TNFα e IS ha
demostrado mayor eficacia que el anti-TNFα en monoterapia. Por ello, la terapia combinada
estará indicada en: pacientes que presentan brote grave corticorrefractario, que sufren brote
grave bajo tratamiento IS, con intolerancia/contraindicación a los corticoides o pacientes con
factores de mal pronóstico (edad joven, patrón fistulizante o estenosante, afectación extensa).
En caso de brote grave con falta de respuesta al tratamiento médico, está indicada la cirugía.
2.2. Enfermedad colónica
a) Brote leve
Se recomienda el tratamiento con mesalazina, a las dosis comentadas en la CU. En caso de
persistencia de la clínica puede utilizarse dipropionato de beclometasona (Clipper®) a dosis de 5-10 mg
durante 4 semanas y si no hay respuesta utilizar corticoides por vía oral a dosis de 1 mg/kg al día.
b) Brote moderado
Se recomienda el uso de corticoides sistémicos por vía oral a dosis de 1 mg/kg al día, en pauta
decreciente habitual. El uso de metronidazol (500 mg cada 8 horas), se debe reservar ante la sospecha de
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [878]
[55] ENFERMEDAD INFLAMATORIA INTESTINAL
complicación séptica, sobrecrecimiento bacteriano y EPA. En caso de refractariedad o contraindicación al
uso de corticoides, la indicación es anti-TNFα asociado o no a tiopurinas.
c) Brote grave
Es criterio de ingreso hospitalario. El tratamiento no difiere del de la afectación ileal. La cirugía se
indicará para el tratamiento de las complicaciones y la enfermedad que no responde al tratamiento
médico, que en la EC será lo más conservadora posible.
Figura 5. Manejo de la enfermedad de Crohn de colon.
2.3. Localizaciones especiales
Afectación extensa de intestino delgado: cuando afecta a más de 100 cm. Supone un factor de
mal pronóstico y frecuentemente se asocian a déficit nutricionales. Es indicación de inicio
precoz de anti-TNFα.
Afectación gastroduodenal y esofágica: el tratamiento con inhibidores de la bomba de
protones mejora la sintomatología. También constituye un factor de mal pronóstico y, por
tanto, indicación de inicio precoz de anti-TNFα.
3. Tratamiento de mantenimiento
3.1. Tras brote leve-moderado
EC ileal o ileocecal, la eficacia de la mesalazina para esta indicación es discutido. La indicación
es iniciar tratamiento de mantenimiento con tiopurinas.
EC de colon, los brotes leves en los que se alcanza la remisión con aminosalicilatos, se
continuará con estos. En caso contrario, y en brotes moderados, se utilizarán
inmunosupresores. Los pacientes con EC moderada refractaria a tiopurinas o pacientes que
además presenten factores de mal pronóstico, deben de ser tratados con terapia combinada
con tiopurinas y anti-TNFα.
3.2. Tras brote grave
a) Controlado con corticoides
En aquellos pacientes con respuesta a corticoides, se indicarán tiopurinas. Se realizará vigilancia
estrecha porque en caso de nuevo brote o pérdida de eficacia de las tiopurinas, será necesario añadir anti-
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [879]
[55] ENFERMEDAD INFLAMATORIA INTESTINAL
TNFα. En los pacientes con factores de mal pronóstico, de entrada, se planteará terapia combinada IS y
anti-TNF α.
b) Corticorrefractario
Está indicado el inicio de anti-TNFα en monoterapia o asociado a IS en función del paciente.
En conclusión, en los pacientes con EII grave o factores de mal pronóstico, está indicado comenzar
de manera precoz con tratamientos más agresivos, siendo la combinación de anti-TNFα y tiopurinas de
elección, planteando una desescalada posterior (top-down). En el resto de pacientes, se recomienda
realizar una escalada rápida en el tratamiento (step-up acelerado) en función de la evolución clínica, para
minimizar el riesgo de progresión de la enfermedad.
3.3. Corticodependencia y corticorrefractariedad
EC corticodependiente: está indicado el inicio de IS (AZA y 6-MP). El efecto de estos fármacos
tarda aproximadamente 3 meses, por lo que se deben mantener los corticoides durante este
tiempo. Como alternativa está indicado el tratamiento con anti-TNFα, en monoterapia o
asociado a IS. El MTX está indicado en caso de intolerancia o contraindicación a tiopurinas.
Debe administrarse asociado a ácido fólico para disminuir la toxicidad.
EC corticorrefractaria: está indicado el inicio de anti-TNFα en monoterapia o asociado a IS. En el
caso de brote grave corticorrefractario, puede usarse la CsA en perfusión iv.
4. Tratamiento de la enfermedad perianal
Figura 6. Manejo de la enfermedad perianal.
En la EPA simple el tratamiento se basará en antibioterapia, metronidazol (750-1.500 mg/ 24 h) +/-
ciprofloxacino (500 mg/12 h) que puede mantenerse hasta 6 meses si es efectivo.
Si no hay respuesta al tratamiento antibiótico, existen recidivas precoces o frecuentes, o se trata de
EPA compleja, se debe pautar tratamiento IS (AZA/6-MP) en combinación con tratamiento quirúrgico
(sedales de drenaje). Los fármacos anti-TNFα pueden usarse como tratamiento de segunda línea, que
deben mantenerse al menos un año, por la alta tasa de recidiva tras su suspensión precoz.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [880]
[55] ENFERMEDAD INFLAMATORIA INTESTINAL
Las indicaciones quirúrgicas son el drenaje de abscesos, la fistulectomía en ausencia de afectación
rectal o colocación de sedales de drenaje si existe proctitis.
5. Indicaciones quirúrgicas en la enfermedad de Crohn
Tabla XIII.
VI. SITUACIONES ESPECIALES
1. Masa o absceso abdominal
Suelen originarse por microperforaciones generalmente en íleon terminal. El síntoma más
frecuente es el dolor abdominal, aunque en pacientes inmunosuprimidos puede no estar presente o
presentarse de manera atípica. El diagnóstico se realiza mediante prueba de imagen (ecografía, entero-RM
o TC). Si el paciente se encuentra estable, y el absceso es de pequeño tamaño, puede intentarse
tratamiento médico con antibióticos de amplio espectro (ertapenem, cefalosporinas de 3ª generación o
quinolona asociados a metronidazol) y drenaje percutáneo guiado por TC, que supone el tratamiento de
elección. La falta de respuesta o el deterioro clínico a pesar de tratamiento conservador, sería indicación de
cirugía.
2. Fístulas (no perineales)
Es una complicación tan frecuente en la EC (13-48% de los pacientes) que define un patrón de la
enfermedad. La prueba de imagen de elección en la entero-RM, siendo necesario además descartar la
presencia de absceso o estenosis asociados. El curso clínico depende de la localización y complejidad de las
fístulas. Se clasifican en internas cuando comunican dos vísceras entre sí, o externas, cuando comunican
víscera con la piel. La enfermedad fistulizante es indicación de tratamiento con IS en monoterapia o
asociado a anti-TNFα. La cirugía se reserva para los casos refractarios, abscesos o perforación.
3. Suboclusión intestinal
Los episodios de obstrucción/suboclusió n intestinal son secundarios a la presencia de zonas estenó
ticas, habitualmente en el intestino delgado. Las estenosis son la complicación más frecuente, y pueden
deberse a la propia actividad inflamatoria, componente fibrótico o a ambas. Las causadas por inflamación
responden a tratamiento médico, mientras que la estenosis fibrótica, no mejora con tratamiento médico y
constituye una indicación quirúrgica, aunque actualmente, se propone tratamiento endoscópico para
estenosis cortas y accesibles, siendo la cirugía para las refractarias, complejas o no accesibles.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [881]
[55] ENFERMEDAD INFLAMATORIA INTESTINAL
4. Enfermedad inflamatoria intestinal y embarazo
La actividad inflamatoria durante el embarazo se asocia a mayor riesgo de prematuridad. Por ello,
se debe planificar la gestación, eligiendo un momento de inactividad de la enfermedad, aunque una tercera
parte de ellas presentarán exacerbación durante el embarazo. Se deben suspender 6 meses antes MTX,
talidomida, y entre 3 y 6 meses metronidazol y ciprofloxacino. La CsA debe evitarse. Las tiopurinas no
deben suspenderse por su seguridad y el riesgo de recaída. Los fármacos biológicos hay que mantenerlos
hasta el tercer trimestre del embarazo. Respecto a las pruebas diagnósticas, la ecografía, gastroscopia y
rectosigmoidoscopia son razonablemente seguras y pueden realizarse si son necesarias. La colonoscopia
completa, aunque probablemente segura, debe evitarse y pocas veces estaría justificada. La lactancia
materna se contraindica durante el tratamiento con metronidazol, quinolonas, CsA y MTX.
5. Enfermedad inflamatoria intestinal y displasia
Tanto en la CU como en la EC coló nica está aumentado el riesgo de CCR. Son factores de riesgo
establecidos la duración de la enfermedad (mayor de 8 años), la extensión, la historia familiar de CCR y la
coexistencia de CEP. La displasia es la lesión precursora bien sobre mucosa plana o bien elevada (displasia
asociada a lesión o masa). Se debe programar a todos los pacientes con CU y EC de colon (excepto proctitis
ulcerosa) una pancolonoscopia de cribado a los 8 años desde el inicio de los síntomas y posteriormente con
una periodicidad cada 1-3 años (según los hallazgos) y en la CEP al diagnóstico con periodicidad anual. Las
colonoscopias se realizarán en periodos de remisión clónica y endoscópica, siempre que sea posible. Los
aminosalicilatos a dosis de 1,2-2 mg tienen un efecto protector sobre el desarrollo de CCR.
VII. MANEJO DEL PACIENTE CON ENFERMEDAD INFLAMATORIA
INTESTINAL EN EL SERVICIO DE URGENCIAS
1. Anamnesis
Interrogar al paciente para esclarecer si el cuadro que presenta es compatible con un brote de su
enfermedad u otro proceso. En caso de tratarse de un brote, determinar la gravedad del mismo (Tablas VIII
y IX) y la necesidad de ingreso hospitalario o, por el contrario, si la situación clínica lo permite, realizar
manejo ambulatorio.
2. Exploración física
Constantes vitales y temperatura. Exploración abdominal para descartar complicaciones como
perforación abdominal, masa abdominal, signos de irritació n peritoneal, datos de obstrucción o
suboclusión intestinal. Debe realizarse tacto rectal e inspección anal por si existieran complicaciones
sépticas a este nivel.
3. Pruebas complementarias
Analítica urgente completa con hemograma, reactantes de fase aguda, perfil renal e iones, y
coagulación. La presencia de leucocitosis, trombocitosis, aumento de fibrinógeno, PCR o VSG son
indicadores de actividad inflamatoria y deberá́ intensificarse el tratamiento. Radiografía de abdomen, para
descartar complicaciones. En caso de sospecha de patología séptica intraabdominal se solicitará una prueba
de imagen urgente (ecografía abdominal y/o TC abdominal). Solicitar coprocultivo y TCD en todos los
pacientes con brote moderado-grave, factores de riesgo para colitis pseudomembranosa, y las muestras se
recogerán antes del inicio de la antibioterapia.
4. Tratamiento
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [882]
[55] ENFERMEDAD INFLAMATORIA INTESTINAL
Se ajustará en función de la gravedad del brote y del tratamiento de mantenimiento del paciente
de acuerdo a los algoritmos explicados previamente.
BIBLIOGRAFÍA
Biancone L, Michetti P, Travis S, Escher JC, Moser G, Forbes A, et al. European evidence based
Consensus on the management of ulcerative colitis: Special situations. J Crohn´s Colitis. 2008;2(1):63-
92.
Conductas de actuación en la enfermedad inflamatoria crónica intestinal, 6ª ed., 2014.
Dignass A, Eliakim R, Magro F, Maaser C, Chowers Y, Geboes K, et al. Second European evidence-
based Consensus on the diagnosis and management of ulcerative colitis: Definitions and diagnosis.
Journal of Crohn’s and Colitis. 2012.
Dignass A, Lindsay JO, Sturm A, Windsor A, Colombel J-F, Allez M, et al. Second European evidence-
based Consensus on the diagnosis and management of ulcerative colitis: Current management.
Journal of Crohn’s and Colitis. 2012.
Dignass A, van Assche G, Lindsay JO, Lémann M, Söderholm J, Colombel J-F, et al. for the European
Crohn’s and Colitis Organisation (ECCO). The second European evidence-based consensus on the
diagnosis and management of Crohn’s disease: Current management. Journal of Crohn’s and Colitis.
2010;4:28-62.
Gomollón F, García-López S, Sicilia B, Gisbert JP, Hinojosa J y en representación del Grupo Español de
Trabajo de Enfermedad de Crohn y Colitis Ulcerosa o Spanish Group for Working on Crohn’s Disease
and Ulcerative Colitis (GETECCU). Therapeutic guidelines on ulcerative colitis: a GRADE methodology
based effort of GETECCU. Gastroenterol Hepatol. 2012.
Gomollón F, Rubio S, Charro M, García-López S, Muñoz F, Gisbert JP y Domènech E, en representación
de GETECCU. Recomendaciones del Grupo Español de Trabajo de Enfermedad de Crohn y Colitis
Ulcerosa (GETECCU) sobre el uso de metotrexato en la enfermedad inflamatoria intestinal.
Gastroenterol Hepatol. 2015;38(1):24-30.
Jonathan S, Levine MD and Burakoff R. Extraintestinal manifestations of inflammatory bowel disease.
Gastroenterology & Hepatology. 2011;7:235241.
Manual de manejo rápido del paciente con colitis ulcerosa. 1a ed., 2014.
Panaccione R, Colombel J-F, Louis E, Peyrin-Biroulet L, and Sandborn WJ. Evolving Definitions of
Remission in Crohn’s Disease. Inflamm Bowel Dis. 2013;19(8).
Stange EF, Travis SPL, Vermeire S, Reinisch W, Geboes K, Barakauskiene A, et al. for the European
Crohn’s and Colitis Organisation (ECCO). European evidence-based Consensus on the diagnosis and
management of ulcerative colitis: Definitions and diagnosis. Journal of Crohn’s and Colitis. 2008.
Van Assche G, Dignass A, Panes J, Beaugerie L, Karagiannis J, Mathieu Allez, et al. for the European
Crohn’s and Colitis Organisation (ECCO). The second European evidence-based consensus on the
diagnosis and management of Crohn’s disease: Definitions and diagnosis. Journal of Crohn’s and
Colitis. 2010;4:7-27.
Van Assche G, Dignass A, Reinisch W, van der Woude CJ, Sturm A, de Vos M, et al. The second
European evidence based Consensus on the diagnosis and management of Crohn’s disease: Special
situations. J Crohn´s Colitis. 2010;4(1):63-101.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [883]
[56] HEPATITIS AGUDA Y FALLO HEPÁTICO FULMINANTE
56.Hepatitis aguda y fallo hepático fulminante
Rubén Viejo Moreno.
Medicina Intensiva
Alba San Bruno Ruz.
Medicina del Aparato Digestivo
Elena Arranz Canales.
Medicina Interna
Asesoras:
Elena Gómez Domínguez.
Médica Adjunta de Medicina del Aparato Digestivo
Noelia Lázaro Martín.
Médica Adjunta de Medicina Intensiva
I. HEPATITIS AGUDA
A. CONCEPTO
La hepatitis aguda hace referencia al daño o inflamación del hígado de menos de 6 meses de
duración. Se caracteriza por aumento de las cifras de transaminasas con o sin ictericia, la presencia de
síntomas inespecíficos y, en los casos más graves, la aparición de fallo hepático (coagulopatía y
encefalopatía). La elevación de transaminasas (transaminasa glutámico oxalacética −GOT− y transaminasa
glutámico-pirúvica –GPT) > 10 veces por encima del límite superior de la normalidad (LSN) y de fosfatasa
alcalina (FA) < 3 veces el LSN sugieren la existencia de una hepatitis aguda. Valores hasta 300 U/l son
inespecíficos y pueden aparecer en cualquier trastorno hepático.
B. ETIOLOGÍA Y DIAGNÓSTICO
Ver la figura 1 a continuación.
Figura 1. Evaluación de la hepatitis aguda.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [884]
[56] HEPATITIS AGUDA Y FALLO HEPÁTICO FULMINANTE
1. ANAMNESIS
La historia clínica detallada es fundamental para establecer el diagnóstico y la etiología. Debe
incluir un amplio cuestionario tanto de índole personal como familiar (Tabla I).
Tabla I. Datos de la anamnesis de utilidad en el diagnóstico de la hepatitis aguda.
2. EXPLORACIÓN FÍSICA
Puede ser normal, aunque es frecuente detectar hepatomegalia dolorosa, ictericia y, en los casos
de fallo hepático, ascitis y esplenomegalia.
3. PRUEBAS COMPLEMENTARIAS
a) Bioquímica, hemograma y estudio de coagulación
El grado de elevación de las transaminasas puede orientar al diagnóstico etiológico, aunque no se
correlaciona con la gravedad (Tablas II y III). Las elevaciones por encima de 50-100 veces el valor de
referencia se producen, casi exclusivamente, en los trastornos asociados a la lesión hepatocelular extensa,
como la lesión hepática isquémica o lesiones hepáticas inducidas por toxinas o fármacos. En las infecciones
virales agudas el incremento suele oscilar entre 10 y 50 veces. En las restantes causas de lesión hepática
aguda las enzimas no están tan elevadas (5-10 veces la normalidad), aunque hay excepciones, como algún
caso de obstrucción aguda biliar, si bien los datos clínicos, la ecografía y el perfil bioquímico evolutivo (con
descenso brusco de transaminasas y progresivo patrón colestásico), sugieren el diagnóstico. En la hepatitis
alcohólica aguda, la elevación de las transaminasas suele ser inferior a 10 veces el límite máximo normal.
Enfermedades no hepáticas, como algunos procesos musculares, el infarto agudo de miocardio o procesos
gripales también pueden ocasionar la elevación aguda de cifras de transaminasas, sobre todo de GOT. La
alteración en las pruebas de función hepática (hiperbilirrubinemia, coagulopatía e hipoalbuminemia)
indicará el grado de gravedad. El signo más fiable es el alargamiento del tiempo de protrombina, que no
responde a la administración parenteral de vitamina K.
b) Serología de virus hepatótropos
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [885]
[56] HEPATITIS AGUDA Y FALLO HEPÁTICO FULMINANTE
El diagnóstico serológico de una infección aguda por el virus de la hepatitis A (VHA) y B (VHB) es
claro, pero el de la hepatitis aguda por el virus de la hepatitis C (VHC) puede plantear dificultades porque
los marcadores de infección no diferencian entre infección aguda y crónica. Ante un paciente con
marcadores de infección de VHC (anti-VHC y ARN-VHC), clínica de hepatitis aguda y antecedentes
epidemiológicos compatibles podemos hacer el diagnóstico de hepatitis aguda por VHC. En casos
sospechosos, debe investigarse la posibilidad de una hepatitis aguda E determinada por la detección de
anticuerpos frente al virus de la hepatitis E (VHE), totales y/o de clase IgM, que se aclaran de forma precoz.
Tabla II. Patrones bioquímicos en la hepatitis aguda.
Tabla III. Causas de elevación aguda de transaminasas.
c) Otras pruebas de laboratorio
Pueden ser de utilidad los marcadores de otros agentes infecciosos, fundamentalmente los virus
herpes simple tipos 1 y 2, citomegalovirus y virus de Epstein-Barr, el estudio de autoinmunidad,
proteinograma, recuento de inmunoglobulinas A, G y M, ceruloplasmina y cupruria en 24 horas, serología
de enfermedad celiaca, hormonas tiroideas, cortisol, perfil férrico y porfirias.
d) Pruebas de imagen
La ecografía abdominal debe realizarse de forma sistemática ante la sospecha o la evidencia clínica
de hepatitis aguda, a pesar de su escasa especificidad. Permite descartar otras alteraciones hepáticas y
ascitis de escasa cuantía.
Su mayor rentabilidad consiste en el estudio del árbol biliar (inflamación o litiasis) y, en la
modalidad eco-Doppler, identificar el síndrome de Budd-Chiari o la trombosis del eje esplenoportal. Las
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [886]
[56] HEPATITIS AGUDA Y FALLO HEPÁTICO FULMINANTE
técnicas colangiográficas (colangiorresonancia y colangiopancreatografía retrógrada) estarán indicadas en
la sospecha de obstrucción biliar aguda. La obtención de biopsia hepática se reservara casi exclusivamente
para los casos de hepatitis aguda de causa desconocida.
C. HEPATITIS AGUDA VÍRICA
El 90% de los casos de hepatitis aguda es de etiología viral (ver Capítulo 44. “Hepatitis virales”).
D. HEPATITIS AGUDA ALCOHÓLICA
1. CONCEPTO
La hepatitis alcohólica (HA) es un síndrome clínico caracterizado por inflamación, daño
hepatocelular y fibrosis que se produce en el contexto de consumo reciente de grandes cantidades de
alcohol.
La HA generalmente se da en pacientes que cumplen los criterios diagnósticos de consumo de
alcohol abusivo o conducta adictiva. Aunque se presenta de forma aguda, en la mayoría de los casos se
trata de la exacerbación de una hepatopatía crónica alcohólica subyacente no diagnosticada previamente.
Los factores de riesgo para desarrollo de dicha entidad son: el consumo de alcohol (> 60 g/d en
varones, > 20 g/d en mujeres), el patrón de consumo (más riesgo los pacientes que presentan consumo de
grandes cantidades de forma prolongada, fuera de comidas), tipo de alcohol (cerveza y licores), sexo
femenino, obesidad, coinfección viral (particularmente por VHC) y sobrecarga férrica, además de raza y
factores genéticos.
2. DIAGNÓSTICO
El diagnóstico de HA se basa en los antecedentes de consumo excesivo de alcohol, cuadro clínico y
alteraciones analíticas compatibles.
El cuadro clínico consiste habitualmente en ictericia progresiva, fiebre, astenia, pérdida de peso y
hepatomegalia dolorosa. Asimismo, se puede presentar como descompensación hepática (ascitis,
encefalopatía hepática [EH], hemorragia digestiva aguda [HDA]). En la mayoría de las ocasiones, las
semanas previas, los pacientes han disminuido o abandonado la ingesta de alcohol. Hasta un 90% de los
pacientes asocian malnutrición proteico-calórica.
Se debe descartar infección concurrente en todos los casos, aunque no presente datos clínicos
sugerentes. Esto es especialmente importante en los pacientes con formas severas de HA, que la
desarrollaran en el 40%. Para ello, se debe realizar extracción de hemocultivos, urocultivo, cultivo de
líquido ascítico si presentase ascitis y radiografía de tórax al ingreso. Asimismo, se deben descartar
disfunción de otros órganos relacionada con la ingesta de alcohol (cardiopatía alcohólica, neuropatía
alcohólica, pancreatitis crónica...).
Respecto a las alteraciones analíticas, la mayoría de los pacientes presentan elevación de
transaminasas 2-6 veces el valor normal, con un ratio GOT/GPT > 2 raramente visto en otras etiologías
(siendo > 3 muy sugestivo de hepatopatía alcohólica) y una elevación de bilirrubina > 4 veces el valor
normal. Frecuentemente se observa leucocitosis con neutrofilia. Asimismo, es importante evaluar función
renal (síndrome hepatorrenal [SHR] hasta en un 30%), alteraciones iónicas y alteración de la coagulación.
La realización de pruebas de imagen solo es útil para excluir otras causas de enfermedad hepática.
El diagnóstico definitivo lo establece la biopsia hepática, pero dado los riesgos que esta conlleva en estos
pacientes (con ascitis, coagulopatía), solo se recomienda en pacientes con afectación severa en los que la
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [887]
[56] HEPATITIS AGUDA Y FALLO HEPÁTICO FULMINANTE
etiología no queda clara (20% de los pacientes con historia de abuso de alcohol tienen una 2ª o coexistente
etiología), a fin de administrar el tratamiento más específico. Además, la biopsia nos da información del
pronóstico y datos histológicos que sugieren una mayor respuesta al tratamiento corticoideo.
3. PRONÓSTICO
La HA severa tiene una supervivencia al mes de 50-65% sin tratamiento. Existen varios scores que
establecen la gravedad y el pronóstico de la HA, que nos ayudan en el manejo del paciente (Tabla IV). El
índice pronóstico más utilizado y validado es el índice de Maddrey modificado (mDF), que establece la
indicación de tratamiento en los casos severos (mDF ≥ 32) y/o con EH.
Tabla IV. Estratificación pronóstica de hepatitis aguda.
Respecto a los indicadores de mal pronóstico, la no disminución de al menos el 25% de los niveles
de bilirrubina al 7º día, predice mala respuesta al tratamiento y por lo tanto peor pronóstico. Existe un
grupo de pacientes con HA grave (40%), llamados “no respondedores”, con mala respuesta al tratamiento
corticoideo, que pueden ser identificados con un índice de Lille (> 0,45) a la semana del inicio de
tratamiento. Estos pacientes tienen un mayor riesgo de infecciones y el tratamiento corticoideo no les
aporta ningún beneficio, por lo tanto, debería ser retirado y considerar tratamientos alternativos.
4. TRATAMIENTO
Ver la figura 2 a continuación.
a) Medidas generales
Si inestabilidad hemodinámica o complicación, considerar ingreso en la Unidad de Vigilancia
Intensiva.
Tratamiento del fallo hepático, hipertensión portal, así como disfunción de otros órganos si
existieran: manejo de ascitis, encefalopatía y SHR.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [888]
[56] HEPATITIS AGUDA Y FALLO HEPÁTICO FULMINANTE
Tratamiento de infecciones intercurrentes.
Prevenir la insuficiencia renal: evitar nefrotóxicos, contrastes iodados.
Aportes de vitaminas del complejo B, ácido fólico y reposición iónica.
Tratamiento del síndrome de abstinencia con benzodiazepinas de corta duración (lorazepam)
aunque exista riesgo de desencadenar encefalopatía.
Gastroprotección (IBP, anti-H2), sobre todo, si corticoterapia o ingreso en UVI.
Figura 2. Algoritmo de manejo de la hepatitis alcohólica.
b) Abstinencia con apoyo multidisciplinar médico-psicologicosocial
Es la piedra angular del tratamiento, ha demostrado mejorar supervivencia en todos los estadios de
enfermedad hepática por alcohol. La abstinencia no garantiza la recuperación completa: solo el 27% de los
pacientes alcanzan la normalización histológica, 18% progresan a cirrosis y el resto presenta cambios
histológicos persistentes hasta 18 meses después. Después de un episodio de HA la abstinencia debe ser
total ya que existe un riesgo significativo de recidiva para cualquier cantidad de alcohol ingerida.
Actualmente la recomendación es el uso de baclofeno (iniciar 5 mg/8 h e incrementar si buena
tolerancia a 10 mg/8 h de forma indefinida) para conseguir mantener la abstinencia indefinidamente.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [889]
[56] HEPATITIS AGUDA Y FALLO HEPÁTICO FULMINANTE
c) Aporte nutricional
Casi el 100% de pacientes con HA presentan diferentes estadios de desnutrición proteicocalórica,
que se correlacionan con la severidad y el pronóstico del cuadro. Debe alcanzarse un aporte proteico de 1,5
mg/kg (incluso en pacientes con encefalopatía) y 40 kcal/kg, añadiendo aportes nutricionales si hiciera
falta. En pacientes con HA grave puede ser necesario un tratamiento agresivo con nutrición enteral o
parenteral.
d) Corticoterapia
Aumenta la supervivencia a corto plazo en pacientes con HA grave. Las indicaciones actuales son:
MDF ≥ 32, GAHS ≥ 9, MELD ≥ 21 o EH.
Está contraindicado si MDF < 32 (donde la supervivencia es mayor del 90% y los corticoides
aumentan las complicaciones) y en pacientes con cualquier índice de MDF con pancreatitis aguda, SHR o
hepatitis crónica por VHB (no evaluada en los estudios realizados la corticoterapia en estos pacientes).
Según estudios recientes, la infección y/o la hemorragia digestiva concomitante no son contraindicaciones
absolutas de tratamiento. Antes del inicio de corticoterapia, es obligado descartar la coexistencia de
infección asintomática, y en el caso de que existiera, se debe iniciar tratamiento antibiótico precoz.
Se recomienda prednisolona (no tiene paso hepático) a dosis de 40 mg/24 h durante 28 días, con
reducción posterior a lo largo de 2-4 semanas (por ejemplo, disminuir 10 mg/d cada 4 días hasta 10 mg/d,
disminuyendo 5 mg/d cada 3 días). Si el índice de Lille es > 0,45 a la semana de tratamiento, debería ser
suspendido en ese momento, sin esperar a completar 4 semanas.
e) Pentoxifilina
Inhibidor de la fosfodiesterasa que también tiene acción anti-TNF. Presenta beneficios en la
supervivencia de pacientes con MDF > 32, más en relación con una disminución del riesgo de desarrollar
SHR que con la mejoría de la función hepática, a dosis de 400 mg tres veces al día vía oral durante 28 días.
Sin embargo, sus beneficios actualmente están en duda, dado los resultados de un reciente ensayo
aleatorizado (STOPAH), aunque dicho ensayo demuestra limitaciones significativas. Está indicado en
pacientes donde los corticosteroides no pueden ser utilizados. No ha demostrado beneficio en asociación
con corticoterapia, ni en pacientes no respondedores a esta.
f) Asociación N-acetilcisteína y corticoterapia
Ha demostrado aumentar la supervivencia a corto plazo con respecto a la corticoterapia sola, así
como una menor frecuencia de SHR y de infecciones. Es probable que exista un efecto sinérgico con
corticoterapia, sin embargo, son necesarios estudios adicionales.
g) GCSF
Existen datos de beneficio de su uso asociado al tratamiento estándar de HA en la supervivencia,
pero son necesarios más estudios.
h) Dispositivo Extracorpóreo de Asistencia Hepática (ELAD): en el que se usan hepatocitos
humanos derivados de líneas celulares. Este dispositivo ha demostrado un aumento de supervivencia
respecto a medidas convencionales, pero son precisos más estudios.
i) Trasplante hepático
Se requieren seis meses de abstinencia para su indicación. Los resultados del trasplante en un
estudio recientemente realizado en pacientes con HA grave sin respuesta a corticoterapia es excelente, con
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [890]
[56] HEPATITIS AGUDA Y FALLO HEPÁTICO FULMINANTE
una supervivencia a los seis meses de 66% frente al 23% sin trasplante. Sin embargo, esta medida
actualmente no está aceptada, por lo que los pacientes que no recuperan la función hepática en los
primeros tres meses, a pesar de la abstinencia y un tratamiento médico correcto, es improbable que
sobrevivan hasta poder ser incluidos en lista de trasplante hepático.
E. DAÑO HEPÁTICO AGUDO EN PACIENTES CON HEPATOPATÍA CRÓNICA.
ACUTE ON CHRONIC LIVER FAILURE (ACLF)
1. CONCEPTO
El término fallo hepático agudo sobre crónico, Acute on Chronic Liver Failure en inglés (ACLF), es
una entidad de reciente diagnóstico y cada vez más reconocida, de la que no existe una definición
universalmente aceptada. Las definiciones de consenso establecen el ACLF como el síndrome que define a
un subgrupo de pacientes cirróticos que desarrollan fallo orgánico tras su ingreso en un hospital con o sin
un factor precipitante identificable y con alta mortalidad a corto plazo.
La prevalencia de ACLF en pacientes hepatópatas hospitalizados con descompensación aguda
(encefalopatía, hemorragia…) es del 30%. Las características de estos pacientes son diferentes en
Occidente, donde es particularmente frecuente en cirrosis alcohólica (50-70%) o asociada a hepatitis C, y
donde los principales desencadenantes son las infecciones bacterianas y los tóxicos (consumo activo de
alcohol). Sin embargo, en Oriente, es frecuente sobre cirrosis asociada a infección por virus de hepatitis B
(VHB) y el principal desencadenante es la etiología viral (reactivación de la infección por VHB u otras
infecciones virales, como la hepatitis E).
La existencia de fallo orgánico se establece según los criterios diagnósticos del score original CLIF-
SOFA o su versión simplificada CLIF-C OF (Tabla V), y se han establecido distintos grados de ACLF.
ACLF grado 1:
Pacientes con fallo renal únicamente.
Pacientes con fracaso de un órgano (coagulopatía, fallo hepático, insuficiencia respiratoria o
fallo hemodinámico) con Creatinina de 1,5-1,9 mg/dL y/o EH I-II.
Pacientes con EH con creatinina 1,5-1,9 mg/dL.
ACLF grado 2: fallo de dos órganos o sistemas.
ACLF grado 3: fallo de tres o más órganos o sistemas.
Tabla V. Score CLIF Consortion Organ Failure.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [891]
[56] HEPATITIS AGUDA Y FALLO HEPÁTICO FULMINANTE
2. CLÍNICA
El cuadro clínico consiste habitualmente en ictericia progresiva, fiebre, astenia, pérdida de peso,
hepatomegalia dolorosa, aunque en la mayoría de los casos se presenta como una descompensación
hepática. La mitad de los pacientes con ACLF no tenían historia previa de descompensación aguda o habían
desarrollado la primera descompensación en los 3 meses previos al diagnóstico de ACLF.
3. DIAGNÓSTICO
Analíticamente estos pacientes presentan criterios de síndrome de Respuesta Inflamatoria
Sistémica (aumento de PCR, leucocitosis), independientemente de etiología infecciosa como
desencadenante.
Es importante identificar la gravedad del cuadro como se indicó anteriormente, mediante la
identificación de daños a nivel de los distintos órganos. El fracaso orgánico más común en pacientes con
ACLF es la insuficiencia renal (56%), seguido de fallo hepático (44%), coagulopatía (28%), encefalopatía
(24%), fallo hemodinámico (17%) y respiratorio (9%). El fracaso hemodinámico y respiratorio solo asociado
a pacientes más graves (ACLF 3). Por otro lado, está indicada la identificación del factor precipitante si
existiera, dado que el tratamiento cambia su pronóstico.
Los eventos precipitantes más frecuentes asociados a ACLF son infecciones bacterianas (30%), el
alcoholismo activo (25%) o la reactivación aguda de hepatitis B, pero en el 40% de los casos el evento
precipitante no se identifica, aunque esto no supone un aumento de gravedad ni mortalidad.
Las infecciones bacterianas más frecuentes son la peritonitis bacteriana espontánea y la neumonía.
Por este motivo, las pruebas diagnósticas deben ir encaminadas a descartar estas patologías (hemocultivos,
serologías, radiografía de tórax, paracentesis diagnóstica si ascitis...).
4. MANEJO Y TRATAMIENTO
El principio fundamental es una identificación temprana del ACLF, su severidad (CLIF-C ACLF score)
y tratamiento precoz de sus posibles factores desencadenantes para prevenir la progresión del síndrome.
En los pacientes con descompensación aguda hepática es importante, una vez descartado el síndrome
ACLF, evaluar gravedad (CLIF-C AD score) que va a indicarnos su probabilidad de progresión a ACLF y, por lo
tanto, nos va a guiar en el manejo de estos pacientes (Figura 3).
En general, los pacientes con ACLF deben ser tratados en una unidad especial o UCI para una
monitorización y manejo más estrecho, y los posibles candidatos a trasplante hepático deben ser
trasladados a su centro de referencia. Se debe de realizar el tratamiento específico dirigido a la disfunción
orgánica que se presente. En el caso de ACLF secundario a reactivación de infección por VHB, debería ser
iniciado el tratamiento antiviral con análogos de nucleótidos de forma precoz, ya que ha demostrado
mejoría pronóstica.
Los sistemas de soporte hepático extracorpóreo (MARS), utilizados como terapia puente a
trasplante o mientras el evento precipitante se resuelve, han sido ampliamente utilizados en pacientes con
ACLF, demostrando eficacia en el soporte de pacientes con encefalopatía y fracaso renal, pero no
mejoraron su supervivencia. Actualmente se encuentran en estudio la administración de GCSF y el
trasplante de células (hepatocitos o células madre).
El trasplante es el tratamiento de elección. No obstante, debe tenerse en cuenta que no todos
pacientes son candidatos (edad avanzada, alcoholismo activo o enfermedades concomitantes), o que la
presencia y severidad de la disfunción orgánica pueda impedir el trasplante. La supervivencia al año es de
aproximadamente 80% tras el trasplante, comparado con los no trasplantados que es del 50%. Solo un
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [892]
[56] HEPATITIS AGUDA Y FALLO HEPÁTICO FULMINANTE
tercio de los candidatos al trasplante alcanzan este, por lo que actualmente se está considerando el
trasplante de donante vivo.
5. PRONÓSTICO
La importancia de la identificación precoz de estos pacientes y su manejo, radica en el mal
pronóstico de esta entidad, que se correlaciona con el grado de ACLF: ACLF-1 se asocia a una tasa de
mortalidad a los 28 días del 22%, ACLF-2 del 32% y ACLF-3 del 73%. Aunque el grado inicial de ACLF se
correlaciona con el pronóstico, el determinante más importante es la evolución clínica durante la
hospitalización, que puede predecirse según el cambio en la puntuación de los scores (CLIF-C ACLF score)
con respecto al ingreso.
Figura 3. Algoritmo de manejo del paciente cirrótico con descompensación aguda.
F. HEPATITIS AUTOINMUNE
La hepatitis autoinmune (HAI) es una enfermedad muy heterogénea que debe sospecharse en
cualquier paciente con una hepatitis aguda o crónica, sobre todo si presenta hipergammaglobulinemia.
La prevalencia es de 15 a 25 casos por 100.000 habitantes en Europa. Puede debutar a cualquier
edad (distribución bimodal, con un pico en la adolescencia y otro entre la 4ª y la 6ª décadas) y afecta a
ambos sexos aunque es más frecuente en mujeres (3:1).
1. CLÍNICA
La presentación clínica de la HAI es heterogénea y su curso clínico suele caracterizarse por periodos
fluctuantes de mayor o menor actividad. Lo más frecuente es que comience de forma insidiosa, con
síntomas inespecíficos (astenia, dolor abdominal en hipocondrio derecho, anorexia, pérdida de peso,
náuseas, etc.), de tal modo que un tercio de los pacientes adultos y la mitad de los niños tienen cirrosis en
el momento del diagnóstico. Aproximadamente en un 25% de los pacientes debuta como una hepatitis
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [893]
[56] HEPATITIS AGUDA Y FALLO HEPÁTICO FULMINANTE
aguda. En estos casos puede tratarse de una exacerbación de una HAI crónica no diagnosticada
previamente o un debut agudo de la HAI (sin hallazgos histológicos de enfermedad hepática crónica).
La HAI puede asociarse a otras enfermedades autoinmunes, las más frecuentes son la tiroiditis
autoinmunes, la diabetes mellitus tipo 1 y el síndrome de Sjögren. En ocasiones puede coexistir con otras
enfermedades hepáticas colestásicas (cirrosis biliar primaria o colangitis esclerosante primaria), lo que se
conoce como “síndrome de overlap”.
2. DIAGNÓSTICO
El diagnóstico es clínico, se basa principalmente en la presencia de autoanticuerpos,
hipergammaglobulinemia y biopsia típica o compatible.
a) Laboratorio: lo más frecuente es una elevación de GPT y GOT.
Recientemente se ha visto que la GGT (sin elevación de FA) también puede estar elevada, y que
además se puede usar como un predictor independiente de la respuesta al tratamiento. Hasta en el 85% de
los pacientes con HAI se observa elevación de inmunoglobulina G (con IgA e IgM normales), aunque este
porcentaje es menor en pacientes que debutan con una hepatitis aguda. El nivel de inmunoglobulinas es un
importante marcador para la monitorización de respuesta al tratamiento y su normalización es un indicador
de remisión de la enfermedad.
b) Autoanticuerpos circulantes: los autoanticuerpos no órgano-específicos están presentes en la
mayoría de los pacientes con HAI. Se usan para subclasificar la HAI en tres subgrupos: HAI-1 (ANA y/o SMA
positivos), HAI-2 (anti-LKM1, anti-LKM3 y/o anti-LC-1) y HAI-3 (anti-SLA/LP). Solo se consideran específicos
de la HAI los anticuerpos anti-SLA, identificados en aproximadamente el 10-30% de los casos.
c) Histología: la biopsia hepática es esencial para establecer el diagnóstico y para determinar la
gravedad de la enfermedad, así como la necesidad de tratamiento.
El Grupo Internacional de Hepatitis Autoinmune propuso un sistema de puntuación para facilitar el
diagnóstico, que consta de 13 ítems, el cual es engorroso y poco utilizado en la práctica clínica diaria. Por
este motivo, recientemente se ha desarrollado un nuevo sistema de puntuación más simplificado (Tabla
VI), que, además, goza de una mayor especificidad y predictibilidad que el anterior. Solo tiene en cuenta
cuatro parámetros: autoanticuerpos, concentración de IgG, exclusión de una hepatitis vírica y criterios
histológicos.
Tabla VI. Criterios diagnósticos simplificados del Grupo Internacional de Hepatitis Autoinmune.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [894]
[56] HEPATITIS AGUDA Y FALLO HEPÁTICO FULMINANTE
3. TRATAMIENTO
El objetivo del tratamiento inmunosupresor es la normalización de los cambios serológicos,
inmunológicos e histológicos, además de prevenir la progresión de la enfermedad. Todos los pacientes con
HAI activa deben ser tratados. Solamente aquellos pacientes con remisión espontánea pueden no recibir
tratamiento, aunque deben continuar con seguimiento estrecho.
El tratamiento consta de dos fases: inducción y mantenimiento, y se basa clásicamente en el uso de
corticoides y azatioprima. El tratamiento de inducción se realiza con prednisona (0,5-1 mg/kg). A las dos
semanas, se añade azatioprina (50 mg/día) si los niveles de bilirrubina son inferiores a 6 mg/dL), y se va
aumentando progresivamente la dosis. Solo puede retirarse el tratamiento de mantenimiento tras al
menos 3 años de tratamiento inmunosupresor y al menos 2 años de respuesta completa (normalización de
las transaminasas y niveles de IgG).
Los pacientes con HAI aguda severa deben tratase con dosis elevadas de corticoesteroides
intravenosos (> 1 mg/kg), tan pronto como sea posible. La ausencia de respuesta en los primeros 7 días de
tratamiento debe considerase una emergencia y el paciente debe ser trasladado a un centro de referencia
de trasplante hepático.
Los tratamientos alternativos en la HAI (budesonida, micofenolato, ciclosporina, etc.), tienen una
evidencia científica escasa basada fundamentalmente en series de casos con falta de estudios aleatorizados
y controlados, y estarían indicados en pacientes en los que fracasa el tratamiento estándar o existe
intolerancia o contraindicación para su uso.
G. HEPATITIS MEDICAMENTOSA/DAÑO HEPÁTICO INDUCIDO POR FÁRMACOS
(DILI)
La hepatotoxicidad por fármacos (Drug Induced Liver Injury o DILI) podría definirse como aquella
lesión hepática inducida por medicamentos o hierbas de uso medicinal que conlleva una disfunción
hepática. Es la causa más frecuente de retirada de un fármaco una vez comercializado y representa una de
las causas más frecuentes de fallo hepático fulminante (FHF).
La incidencia de DILI se ha estimado en 20 casos por cada 100.000 habitantes al año, si bien es un
problema creciente y probablemente infradiagnosticado, pues solo una pequeña parte de las hepatopatías
tóxicas se informan a las agencias de control del medicamento.
Los fármacos que producen con mayor frecuencia hepatotoxicidad son los antibióticos,
anticonvulsivantes y antiinflamatorios no esteroideos. Se ha considerado factores de riesgo para el
desarrollo de hepatotoxicidad una edad superior a 50 años, la polimedicación, el consumo habitual de
alcohol y la presencia de una hepatopatía subyacente.
1. TIPOS DE DAÑO HEPÁTICO INDUCIDO POR DROGAS
Existen varios tipos de hepatotoxicidad, clásicamente diferenciados en:
Dosis-dependiente: este tipo de daño hepático es predecible y ocurre en la mayoría de
pacientes expuestos a partir de un rango terapéutico. El más frecuente. Normalmente tiene un
periodo de latencia más corto y suele ser reversible tras suspender el fármaco. El ejemplo
clásico es el paracetamol.
Dosis independiente o idiosincrásica: es una reacción adversa imprevisible teniendo en cuenta
la acción farmacológica del medicamento, no tiene relación con la dosis y tiene un periodo de
latencia variable desde unos días hasta 12 semanas. En ocasiones continúa incluso después de
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [895]
[56] HEPATITIS AGUDA Y FALLO HEPÁTICO FULMINANTE
retirar el fármaco y puede ser fatal si persiste el consumo una vez ha comenzado la reacción.
Solo supone un 0,7% de los casos de hepatotoxicidad.
En función del perfil bioquímico, se ha descrito distintos patrones de afectación hepática:
hepatocelular, colestásico y mixto, diferenciados por el cociente GPT/fosfatasa alcalina (Tabla VII). Hay que
tener en cuenta que el mismo fármaco puede producir distintas alteraciones bioquímicas y que el patrón
no es estático y puede modificarse con el tiempo. Además, el DILI puede ser clasificado en inmune y no
inmune, considerándolo inmune cuando se presenta como una reacción de hipersensibilidad con fiebre,
rash, eosinofilia y autoanticuerpos.
Tabla VII. Patrones de afectación hepática según el perfil enzimático.
2. CLÍNICA
Las manifestaciones clínicas del DILI son muy variables, desde síntomas inespecíficos como astenia,
anorexia o náuseas hasta síntomas específicos relacionados con una hepatitis aguda o fallo hepático
fulminante como dolor en el hipocondrio derecho, ictericia, ascitis y encefalopatía. En ocasiones, pueden
asociarse manifestaciones de hipersensibilidad como fiebre y exantemas que ayudarán en el enfoque
diagnóstico.
3. DIAGNÓSTICO
DILI es una entidad a considerar en el estudio de un caso de hepatitis aguda y, en menor medida,
en casos de hepatopatía crónica o cirrosis de causa no aclarada. Es un diagnóstico de exclusión, ya que no
se dispone de pruebas complementarias específicas. En primer lugar, es necesario realizar una anamnesis
exhaustiva que incluya de forma detallada el consumo de fármacos, hierbas medicinales y drogas de abuso
durante los últimos 3 meses, la duración y dosis del tratamiento, el tiempo transcurrido desde el inicio del
tratamiento y la aparición del cuadro, la gravedad de la reacción y revisar documentación acerca de casos
previos de hepatotoxicidad con el mismo fármaco.
Es fundamental descartar otras causas alternativas de afectación hepática, mediante un estudio
que incluya una ecografía abdominal con Doppler, serologías virales (VHB, VHC, VHA, VHE, CMV, EBV) y un
estudio metabólico y de autoinmunidad (ANA, AMA, AML y anti-LKM).
La realización de una biopsia hepática no suele ser necesaria, pero puede ser de utilidad en
pacientes seleccionados para descartar otras causas de hepatopatía. Además, el estudio
anatomopatológico puede proporcionarnos información sobre una posible progresión de la hepatopatía y
la presencia de fibrosis o cirrosis.
Aunque su utilidad es limitada en la práctica clínica habitual y ninguna de ellas establece una
relación de causalidad de forma definitiva, existen escalas que nos permiten apoyar el diagnóstico de DILI;
las más difundidas son la RUCAM-CIOMS (1989) y la escala de María y Victorino (1997).
4. TRATAMIENTO
El tratamiento del DILI incluye la retirada inmediata del o de los fármacos sospechosos e instaurar si
procede medidas de soporte. No existe un tratamiento etiológico específico salvo los casos de intoxicación
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [896]
[56] HEPATITIS AGUDA Y FALLO HEPÁTICO FULMINANTE
por paracetamol (N-acetil cisteína) o por valproato (L-carnitina). La N-acetil cisteína se debe administrar en
primeras 8 horas tras la ingesta para poder evitar la toxicidad hepática, pero puede ser eficaz aunque se
administre hasta 36 horas postingesta.
La dosis inicial es de 140 mg/kg y posteriormente 70 mg/kg/4 horas hasta un total de 17 dosis
dependiendo de los niveles plasmáticos de paracetamol. En el caso del metotrexato, debe utilizarse ácido
fólico para evitar la citotoxicidad de este.
Se pueden usar corticoides asociados si aparecen manifestaciones de hipersensibilidad sistémica,
pero no hay estudios controlados que prueben la eficacia de este medicamento. Si predomina la clínica de
colestasis puede usarse ácido ursodesoxicolólico en dosis de 15 mg/kg al día, para disminuir la
sintomatología y en caso de prurito asociado puede administrarse resincolestiramina, a dosis de 4-8 g/día,
con incremento gradual si se precisa.
Lo más frecuente es que tras la retirada del fármaco se observe una mejoría progresiva del perfil
hepático. Sin embargo, la recuperación puede tardar en aparecer, incluso en algunos casos, como
amoxicilina-clavulánico o fenitoína típicamente puede cursar con un empeoramiento inicial.
Se debe evitar reintroducir el fármaco posteriormente pues se puede desarrollar una lesión
hepática más severa. En casos graves de DILI, con coagulopatía (INR > 1,5) o encefalopatía, el paciente debe
ser trasladado a un centro de referencia de trasplante hepático.
5. PRONÓSTICO
En la mayoría de los casos de DILI, el pronóstico es favorable con la retirada del fármaco, siendo
infrecuente la progresión de la hepatopatía y el desarrollo de fibrosis o cirrosis. Un patrón hepatocelular, el
valor elevado de bilirrubina y el sexo femenino son factores asociados a un peor pronóstico.
El fallo hepático por paracetamol tiene mejor pronóstico que el fallo hepático secundario a DILI
idiosincrásico. Por otro lado, se ha visto, que los casos de DILI que se acompañan de reacciones de
hipersensibilidad como rash cutáneo, eosinofilia o linfoadenopatias suelen tener un curso más benigno y
mejor supervivencia.
La mayoría de personas sin enfermedad hepática previa que sobreviven a una hepatitis tóxica
recuperan totalmente la función hepática; solo un 10% evoluciona a la cronicidad. La preexistencia de
hepatopatía previa posiblemente tiene mayor efecto sobre la capacidad de recuperación que sobre la
predisposición a desarrollar este tipo de reacciones.
H. RELACIÓN ENTRE DILI Y HAI
En algunos pacientes la exposición a fármacos puede desencadenar fenómenos autoinmunes que
produzcan afectación hepática o desenmascarar una hepatopatía autoinmune. La relación es compleja y no
está completamente entendida.
Se presentan tres escenarios posibles:
DILI inmunomediado (IM-DILI): DILI con un fuerte componente inmunoalérgico que mimetiza
una HAI.
HAI con DILI: son pacientes con HAI conocida, inactiva o controlada con tratamiento
inmunosupresor. Al entrar en contacto con un fármaco se produce una reactivación de la HAI.
HAI inducida por DILI (DI-HAI): paciente predispuestos a HAI o HAI con bajo grado de actividad,
no diagnosticada. Tras la exposición a un fármaco, se produce un primer brote de hepatitis
autoinmune.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [897]
[56] HEPATITIS AGUDA Y FALLO HEPÁTICO FULMINANTE
Algunos de los fármacos implicados en este tipo de patología han sido minociclina, alfametildopa,
nitrofurantoína, efarivenz o los anti-TNF alfa (infliximab).
En ocasiones, es muy difícil diferenciar un DILI inmunomediado de una auténtica HAI y en estos
casos solo pueden ser diferenciadas tras un tiempo de seguimiento. En el IM-DILI la respuesta al
tratamiento con esteroides es completa y se mantiene la remisión tras la suspensión del mismo, mientras
que en la DI-HAI es necesario tratamiento de mantenimiento con inmunosupresores durante un largo
periodo de tiempo (Tabla VIII).
Tabla VIII. Diferencias entre DI-AIH y IM-DILI.
I. HEPATITIS ISQUÉMICA
Debido a su compleja vascularización y su alta actividad metabólica, el hígado es un órgano
particularmente susceptible a las alteraciones circulatorias.
1. CONCEPTO
Se trata del daño hepático difuso secundario a hipoxia hepática, ya sea por hipoperfusión (lo más
frecuente), pero también se pude presentar en pacientes sin registro de hipotensión. Se da en el 0,5-1,5%
de los pacientes críticos y es más frecuente en pacientes con edad avanzada.
2. ETIOLOGÍA
Inestabilidad hemodinámica de cualquier etiología.
Crisis drepanocítica y trombosis de la arteria hepática en trasplantados hepáticos o en
pacientes con trombosis portal previa.
Enfermedades respiratorias en las que se produce hipoxia.
3. CLÍNICA
Los pacientes suelen estar asintomáticos o presentar síntomas inespecíficos como náuseas,
vómitos, hiporexia, malestar y dolor en hipocondrio derecho.
Por otro lado, dado que acontece en el contexto de una insuficiencia cardiaca, respiratoria o
hemodinámica, la clínica será predominantemente la de esta. En muchas ocasiones estos pacientes puede
desarrollar alteración del estado mental, que suele estar más en relación con la hipoperfusión cerebral por
la causa desencadenante que con el desarrollo de EH en el contexto de fallo hepático.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [898]
[56] HEPATITIS AGUDA Y FALLO HEPÁTICO FULMINANTE
4. DIAGNÓSTICO
a) Laboratorio
Se produce un aumento rápido de las enzimas de citolisis (25-250 veces el límite superior de la
normalidad) y masivo de LDH entre el primer y el tercer día del evento precipitante. Niveles tan elevados de
transaminasas con ratio GPT/LDH < 1,5 es muy sugestivo de hepatitis isquémica, pero no son
patognomónicos. Los niveles de bilirrubina raramente superan cuatro veces el límite alto de la normalidad y
la FA no suele doblar sus valores máximos. Tras la resolución del cuadro isquémico, las enzimas hepáticas
vuelven a la normalidad en 7-10 días. Pueden objetivarse además alteraciones analíticas en relación con
afectación de otros órganos por hipoperfusión, especialmente insuficiencia renal secundaria a necrosis
tubular aguda. La coagulación habitualmente no suele estar alterada.
b) Eco-Doppler hepático
Se realiza para valorar las arterias y venas hepáticas, así como descartar factores precipitantes. El
diagnóstico consiste en cuadro clínico compatible con las alteraciones analíticas antes descritas. Es
necesaria la realización del diagnóstico diferencial con otras patologías, entre ellas sobredosis por
paracetamol, tóxicos hepáticos y hepatitis virales.
5. TRATAMIENTO Y PRONÓSTICO
Habitualmente no precisa tratamiento específico, salvo la resolución del cuadro precipitante. La
hepatitis isquémica es una causa frecuente de daño agudo severo y está asociado a una alta mortalidad
intrahospitalaria (aproximadamente del 50%). Lo más importante es el reconocimiento de esta patología
incluso cuando no exista hipotensión documentada. Si desaparece la causa originaria, el pronóstico de la
hepatitis isquémica es favorable, incluso con reversibilidad de las alteraciones histológicas. El pronóstico
vital de una hepatitis isquémica viene determinado por la enfermedad que la haya originado, junto a la
duración de la isquemia hepática y el empeoramiento progresivo de la función hepática. La mayoría (80%)
de los fallecimientos son debidos a problemas cardiopulmonares.
J. INFARTO HEPÁTICO
Cuadro poco frecuente dada la vascularización dual del hígado. Se diferencia de la hepatitis aguda
en que la isquemia en este caso es focal. Está descrita tras trombosis de la arteria hepática sobre todo en
trasplante hepático, colocación de TIPS, yatrogenia durante una cirugía biliar, embolia, embarazo,
hipercoagulabilidad y quimioembolización de la arteria hepática.
Puede ser asintomático y detectarse solo en una prueba de imagen o presentarse mediante
ictericia, dolor en hipocondrio derecho o epigastrio, fiebre, náuseas o vómitos. Las transaminasas se elevan
transitoriamente, muchas veces hasta niveles muy altos y suele asociar leucocitosis. En el diagnóstico
diferencial por imagen hay que diferenciarlo de tumores o abscesos piógenos siendo excepcional la
necesidad de biopsia para el diagnóstico. Debe realizarse un eco-Doppler hepático para valorar la
integridad de la arteria hepática y ante la sospecha de oclusión de esta, realizar una angiorresonancia
magnética o una arteriografía.
En general, no se dispone de un manejo específico sino de la enfermedad responsable; la
anticoagulación puede estar indicada en casos individualizados. El pronóstico dependerá de la reserva
hepática del paciente.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [899]
[56] HEPATITIS AGUDA Y FALLO HEPÁTICO FULMINANTE
K. COLANGITIS ISQUÉMICA
La colangiopatía isquémica se caracteriza por daño focal o difuso de los conductos biliares mayores
secundario a la afectación del flujo sanguíneo en la arteria hepática.
1. CLÍNICA
Las manifestaciones pueden variar desde el cuadro clínico asintomático hasta una sepsis severa,
siendo muy frecuente la ictericia y la fiebre. Se presenta como colestasis y puede asociar sobreinfección
(colangitis o abscesos hepáticos).
2. DIAGNÓSTICO Y TRATAMIENTO
El diagnóstico debe ser considerado en un contexto clínico, analítico y radiológico en un paciente
que ha presentado una situación predisponente. Es importante la realización de un diagnóstico diferencial
de colangitis esclerosante primaria, colangiocarcinoma difuso y colangitis relacionada con enfermedad IgG4
(Figura 4).
Figura 4. Algoritmo diagnóstico de colangiopatía isquémica.
El tratamiento de esta enfermedad consiste en el tratamiento de la enfermedad desencadenante o
de sus secuelas. Este tratamiento es individualizado (Tabla IX).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [900]
[56] HEPATITIS AGUDA Y FALLO HEPÁTICO FULMINANTE
Tabla IX. Tratamiento de colangiopatía isquémica.
II. FALLO HEPÁTICO FULMINANTE (FHF)
A. CONCEPTO
Síndrome clínico, súbito y grave, caracterizado por la necrosis hepática masiva, que condiciona el
desarrollo precoz de importantes complicaciones, siendo la coagulopatía (INR > 1,5) y la EH el común
denominador resultante de la disfunción hepatocelular que define al FHF. El fallo hepático agudo (FHA)
acontece dentro de las primeras 28 semanas desde el inicio de los síntomas, mientras que una evolución
superior a lo previo, o la presencia de cirrosis, orientan hacia FHA sobre un fallo hepático crónico (Tabla X).
Tabla X. Clasificación de O ‘Grady del fallo hepático agudo.
B. EPIDEMIOLOGÍA Y ETIOLOGÍA
La incidencia del FHF es 1-6 casos por millón de habitantes/año en países desarrollados, siendo
propio de jóvenes (mediana 38 años), raza blanca (74%) y predominio femenino (73%).
La etiología de FHF varía según la zona geográfica y el nivel socioeconómico, si bien la causa más
frecuente en el mundo es secundaria a fármacos (antituberculosos, halotano, antitiroideos, ácido
valproico…).
En Estados Unidos, así como en el Noroeste de Europa, el mayor número de casos se produce como
consecuencia de intoxicaciones autolíticas por paracetamol. En España la etiología viral es la causa más
frecuente, sobre todo por VHB, seguida de los fármacos y los tóxicos. No obstante, existen otras muchas
causas, pero se debe tener en cuenta que hasta un 30-35% de los casos, tras sus estudio etiológico, no se
les identifica causa (Tabla XI).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [901]
[56] HEPATITIS AGUDA Y FALLO HEPÁTICO FULMINANTE
Tabla XI. Etiología del fallo hepático fulminante.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [902]
[56] HEPATITIS AGUDA Y FALLO HEPÁTICO FULMINANTE
C. CLÍNICA
El curso clínico suele ser insidioso, con síntomas inespecíficos: malestar general, astenia, náuseas,
vómitos, anorexia, fiebre, dolor abdominal, etc. Posteriormente, aparece ictericia y EH a partir de la cual
pueden aparecer complicaciones letales como: edema cerebral, hipertensión intracraneal (HIC), coma,
coagulopatía y trombopenia severas, hemorragia activa, alteraciones hemodinámicas, fracaso renal agudo,
sepsis e incluso, fracaso multiorgánico (FMO) y muerte.
D. DIAGNÓSTICO
Los criterios diagnósticos de FHF son: la ausencia de enfermedad hepática o bien hepatopatía
crónica previa compensada, presencia de EH, protrombinemia menor de 40% o INR > 1,5 y evolución < 28
semanas.
1. ANAMNESIS
Dirigida a averiguar la etiología del FHF. La presencia de un síndrome gastroentérico puede orientar
a intoxicación por setas o la aparición de rash sobre origen farmacológico. Se debe insistir sobre la posible
exposición a tóxicos, uso de drogas, realización de viajes u origen del paciente, infecciones crónicas, etc. Es
importante conocer el tiempo de latencia hasta la aparición de síntomas ya que puede orientar la gravedad
y el pronóstico.
2. EXPLORACIÓN FÍSICA
En la exploración física es frecuente encontrar alteraciones cognitivas, ictericia, fetor hepático,
sangrados por mucosas o por puntos de punción, petequias, ascitis, esplenomegalia, hepatomegalia y
ascitis en el Budd-Chiari.
La palpación de un hígado pequeño y duro refleja una necrosis hepática masiva siendo un signo de
mal pronóstico. La presencia de anillo de Kayser-Fleischer orienta hacia enfermedad de Wilson.
3. PRUEBAS COMPLEMENTARIAS
3.1. Determinaciones de laboratorio
Nos permiten orientar la etiología, el diagnóstico y la severidad del cuadro. Se debe incluir
hemograma, grupo sanguíneo, coagulación con determinación de factores (fundamental factor V),
bioquímica (que incluya iones, perfil hepático, amilasa, urea, amonio), gasometría arterial, lactato, análisis
toxicológico, niveles de paracetamol, alfa amanitas en orina si existe sospecha de intoxicación por setas,
serologías virales y estudio de autoinmunidad. En mujeres se debe realizar un test de embarazo.
Si se sospecha enfermedad de Wilson se debe hacer determinación de ceruloplasmina plasmática y
niveles de cobre en orina.
3.2. Pruebas de imagen
La ecografía abdominal permite valorar signos de hepatopatía crónica, lesiones ocupantes de
espacio y permeabilidad de los vasos hepáticos que pueden condicionar las actitudes terapéuticas. Si no es
concluyente y la valoración clínica lo indica, es recomendable realizar una TC abdominal. En aquellos
pacientes que presentan deterioro neurológico y coagulopatía severa concomitante está indicado realizar
una TC cerebral para descartar sangrado intracraneal o datos de HIC que pueda condicionar el pronóstico e
incluso contraindicar el trasplante hepático.
3.3. Biopsia hepática
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [903]
[56] HEPATITIS AGUDA Y FALLO HEPÁTICO FULMINANTE
Presenta un elevado riesgo de sangrado y su rentabilidad es baja para detectar la causa, por ello es
poco frecuente su práctica.
Puede estar indicada cuando se sospecha etiología autoinmune, enfermedad metastásica, linfoma
o hepatitis por herpes priorizando la vía transyugular.
E. COMPLICACIONES
La necrosis celular masiva se acompaña de una respuesta inflamatoria sistémica que puede
conllevar a la presencia de múltiples complicaciones, las cuales condicionarán el pronóstico.
1. COMPLICACIONES NEUROLÓGICAS
a) Encefalopatía hepática: se produce por la acumulación en el cerebro de neurotoxinas por
incapacidad de aclaramiento hepático y de la existencia de shunts portosistémicos, siendo el amonio la
sustancia más nociva para el cerebro. Cuanto más precoz es su aparición, peor suele ser el pronóstico.
Diversos factores extrahepáticos, como la administración de fármacos sedantes (benzodiazepinas),
la hipoxia, la insuficiencia renal aguda, diuréticos, laxantes osmóticos o infecciones pueden contribuir a su
desarrollo. Clínicamente es similar a encefalopatías de otras causas, con un curso a veces fluctuante. El
grado de encefalopatía tiene valor pronóstico.
b) Edema cerebral: se produce tanto por mecanismo vasogénico como citotóxico. Es raro en la
encefalopatía grado I y II, está presente en el 25-35% en grado III y 75% en grado IV. Es más frecuente en
pacientes con curso hiperagudo o agudo y encefalopatía grado IV. Es la causa principal de muerte en el FHF
y se debe a HIC, condicionando la misma en hasta el 50% de los pacientes con curso fulminante no
trasplantados.
Las manifestaciones clínicas de la HIC son inespecíficas, además los datos más característicos
(cefalea, vómitos, papiledema, hipertensión, bradicardia) suelen estar ausentes en estos pacientes o ser
difíciles de detectar al estar muchos de ellos ingresados en UCI, sedados y con ventilación mecánica. La
medición invasiva de la presión intracraneal (PIC) con objetivo < 20 mm Hg, presión de perfusión cerebral >
60 mm Hg y consumo cerebral de oxígeno debe considerarse en pacientes con EH grado III o IV.
2. ALTERACIONES DE LA HEMOSTASIA
a) Alteraciones de la coagulación: secundarias a la disminución de la síntesis hepática (factores I, II,
V, VII, IX y X), de proteasas inhibidoras de la coagulación (proteína C, proteína S y antitrombina III) y de
vitamina K.
Un factor V < 17%, un factor VII < 8% y un INR < 4, son signos de mal pronóstico. Asimismo, hay un
aumento de la fibrinólisis y una mayor predisposición para desarrollar coagulación intravascular diseminada
(CID) secundaria al propio FHF. El factor V es el de mayor valor pronóstico (niveles < 20% se asocian a
mayor mortalidad y niveles > 50% en el seno de una insuficiencia hepática aguda suponen un riesgo muy
bajo de evolución a EH y FHF).
b) Trombopenia y trombopatía: es frecuente como consecuencia de hiperesplenismo y/o
disminución de la síntesis de trombopoyetina por enfermedad hepática.
3. COMPLICACIONES RESPIRATORIAS
a) Hiperventilación: debida a hiperventilación central neurógena y acidosis metabólica. El
desarrollo de normo o hipercapnia en un paciente previamente hipocápnico sugiere agotamiento de los
músculos respiratorios o depresión del centro respiratorio.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [904]
[56] HEPATITIS AGUDA Y FALLO HEPÁTICO FULMINANTE
b) Hipoxemia: de origen multifactorial (atelectasias, infección, shunt secundario a la hepatopatía,
edema pulmonar cardiogénico y no cardiogénico –SDRA– en el 40% de los casos, hemorragia alveolar),
agrava el edema cerebral y suele ser el precipitante del FMO.
4. ALTERACIONES HEMODINÁMICAS
a) Shock distributivo: vasodilatación sistémica, en relación con el acumulo de toxinas endógenas,
un descenso en las resistencias vasculares sistémicas, hipotensión arterial y un incremento compensador
del gasto cardiaco resultando una situación hiperdinámica.
b) Arritmias cardiacas y alteraciones electrocardiográficas: lo más frecuente es la taquicardia
sinusal, aunque pueden aparecer arritmias secundarias a alteraciones hidroelectrolíticas o neurológicas.
c) Alteraciones hemodinámicas secundarias al edema cerebral: crisis hipo e hipertensivas bruscas,
episodios de taquicardia, bradicardia sinusal o alteraciones de la repolarización.
5. INSUFICIENCIA RENAL AGUDA
Presente en el 50% de los FHF y en mayor porcentaje en edades avanzadas y los casos secundarios
a intoxicación por paracetamol. Su origen es multifactorial (deshidratación, síndrome hepatorrenal, tóxicos,
necrosis tubular aguda…), aunque la causa más frecuente es el SHR.
Es un factor de mal pronóstico. Es más adecuada la medición de creatinina que de urea (con síntesis
hepática disminuida en esta situación), pero dado que la hiperbilirrubinemia interfiere en la determinación
de esta dando un valor falsamente disminuido, la monitorización de la diuresis es el mejor indicador de
disfunción renal.
6. ALTERACIONES HIDROELECTROLÍTICAS Y METABÓLICAS
a) Hipoglucemia: las hipoglucemias ocurren en el 40% de los pacientes con FHF aunque también
puede ser un signo indirecto de sepsis, por lo que se recomienda seguimiento estrecho de la misma con
controles frecuentes para niveles de 80-200 mg/dL.
b) Alteraciones del equilibrio ácido-base: lo más frecuente es la alcalosis respiratoria por
hiperventilación, pero el trastorno más importante es la acidosis metabólica (la acidosis láctica implica muy
mal pronóstico).
c) Trastornos hidroelectrolíticos: las alteraciones hidroelectrolíticas son muy frecuentes y de origen
multifactorial. Puede aparecer hipocaliemia, hiponatremia, hipofosfatemia y alteraciones del calcio. La
causa de la hiponatremia es dilucional, consecuencia del exceso de agua libre. La hipofosfatemia es
frecuente en FHF secundarios a sobredosis de paracetamol y si presentan fracaso renal agudo. Es
conveniente corregir precozmente la hipofosfatemia porque puede provocar alteraciones musculo-
esqueléticas y empeoramiento de la EH.
d) Otros: aumento de ácidos grasos y disminución del colesterol plasmático, hiperamoniemia y
aumento de aminoácidos no ramificados en plasma, alteración de la concentración de fármacos.
7. COMPLICACIONES INFECCIOSAS
Existe riesgo elevado de infecciones como consecuencia inmunosupresión funcional por disfunción
de las células de Kupffer, monocitos, polimorfonucleares y deficiencias del complemento.
Las complicaciones infecciosas pueden ser:
a) Bacterianas: prevalencia del 80%.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [905]
[56] HEPATITIS AGUDA Y FALLO HEPÁTICO FULMINANTE
Los gérmenes grampositivos están implicados en el 70% de los casos (el más frecuente S. aureus,
seguido de S. epidermidis y estreptococos). El diagnóstico se ve dificultado por la escasa rentabilidad de los
cultivos, la frecuente ausencia de fiebre y leucocitosis y porque el FHF tiene un patrón hemodinámico
similar al de un shock séptico.
b) Fúngicas: 30% de los casos.
Los patógenos más frecuentes son Cándida sp y , generalmente aparecen a partir de la segunda
semana de hospitalización empeorando severamente el pronóstico e incrementando la mortalidad hasta el
100% si no son tratados adecuadamente.
c) Otras
Puede existir hipertensión portal y ascitis, así como alteración de enzimas pancreáticas, aunque sin
importancia clínica ni pronóstica en general.
F. PRONÓSTICO
La supervivencia de los pacientes trasplantados alcanza el 79% al año y el 72% a los 5 años del THO,
mientras que la mortalidad global de los no trasplantados puede ascender hasta el 80%.
Los factores de mal pronóstico clásicos se representan en la tabla XII, y se corresponde con el grado
de encefalopatía, la edad del paciente, la etiología del fracaso agudo, APACHE II > 15, el grado de necrosis
del parénquima hepático, los niveles séricos de factor V, protrombina, bilirrubina y creatinina, entre otros.
Sin embargo, existen también otros factores relacionados con buen pronóstico como son: intervalo corto
entre el inicio de la ictericia y la aparición de encefalopatía, edades comprendidas entre los 10 y 40 años
(encontrándose supervivencias superiores al 50% sin THO en las desarrolladas por intoxicación por
paracetamol), VHA, hígado de shock o del embarazo.
Tabla XII. Factores de mal pronóstico en el fallo hepático fulminante.
G. TRATAMIENTO
Los pacientes con FHF deben ser ingresados de forma precoz en una UCI, idealmente en un centro
con programa de trasplante hepático. Igualmente, será fundamental conocer la etiología del cuadro a la
hora de guiar la planificación del tratamiento.
1. MEDIDAS DE SOPORTE
a) Medidas generales
Monitorizar tensión arterial, frecuencia y ritmo cardiaco, frecuencia respiratoria, temperatura,
diuresis, saturación de oxígeno y estado mental. Si existe fracaso cardiaco o renal es conveniente
monitorización hemodinámica invasiva.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [906]
[56] HEPATITIS AGUDA Y FALLO HEPÁTICO FULMINANTE
b) Complicaciones neurológicas
Hay que evitar y corregir aquellos factores que puedan agravar o desencadenar la encefalopatía.
Prevenir el sobrecrecimiento bacteriano y la producción o el acúmulo de amonio mediante las mismas
medidas utilizadas en la hepatopatía crónica (ver Capítulo 57. “Hepatopatía crónica”). En las encefalopatías
grado I-II, la administración de N-acetil-cisteína (NAC) independientemente de la causa, puede mejorar el
pronóstico de estos pacientes. En encefalopatías grado III-IV se recomienda proceder a la intubación
endotraqueal y sedación, generalmente mediante propofol, el cual puede disminuir la PIC a la vez de
presentar efecto anticonvulsionante evitando las benzodiazepinas. La hiperamonemia > 200 μml/l o niveles
entre 150-200 μml/l mantenidos pueden inducir hipertensión intracraneal (HIC). La monitorización de la PIC
no presenta efectos beneficiosos sobre mortalidad y es muy controvertida dado el elevado riesgo
hemorrágico de estos pacientes.
Se recomienda mantener amoniemias < 100 μml/l, PIC < 20 mm Hg y tensión arterial media (TAM) >
70 mm Hg. En caso de HIC se debe considerar la relajación neuromuscular, la administración de agentes
osmóticos (salino hipertónico: 3 ampollas. ClNa al 20% en 100 cc de SSF en 15-30 minutos y solo en
ausencia de respuesta valorar la hiperventilación moderada. Se debe perseguir un medio osmótico en
sangre favorable mediante natremias de 145-150 mmol/l. Finalmente, considerar el uso de barbitúricos en
la HIC refractaria con tiopental. No se recomienda el uso de corticoides. La terapia de depuración
extrarrenal veno-venosa puede facilitar el aclaramiento de amonio disminuyendo el riesgo de HIC. El
tratamiento de elección para las crisis comiciales es fenitoína y dosis bajas de benzodiazepinas. Se debe
realizar electroencefalograma en pacientes con crisis así como en los pacientes con encefalopatía.
c) Alteraciones de la hemostasia
Se suele administrar vitamina K 10 mg iv cada 12 horas. En general, no se debe administrar
plaquetas de forma profiláctica excepto en recuentos < 10.000 o previo a la realización de procedimientos
invasivos al igual que el plasma. Se recomiendan niveles de fibrinógeno > 100 mg/dL. La profilaxis de
sangrado digestivo es una indicación para estos pacientes (ranitidina 50 mg iv c/8 h o pantoprazol 40 mg iv
c/24 h).
d) Alteraciones respiratorias
El deterioro del nivel de consciencia en encefalopatías avanzadas (III-IV) es la causa más frecuente
de intubación endotraqueal en estos pacientes. Otras causas son hipoxemia, sangrados digestivos, etc.
e) Alteraciones hemodinámicas
La hipotensión en el FHA es frecuente y puede deberse tanto a pérdidas de volumen (vómitos,
ascitis…), así como consecuencia de una baja ingesta oral.
A ello se añade una situación de resistencias vasculares periféricas disminuidas que acentúan la
hipotensión. Se debe prestar especial cuidado a la resucitación con volumen para mantener una adecuada
volemia y no sobrecargar, considerando usar sistemas de monitorización hemodinámica, bien sea mediante
termodilución transcardiaca o transpulmonar que permitan guiar la optimización de la volemia en
pacientes inestables.
En casos de hipotensión refractaria a volumen, la noradrenalina es el fármaco vasopresor de inicio
pudiendo añadirse vasopresina o su análogo terlipresina (induce menor isquemia miocárdica que la
anterior), todos ellos en perfusión continua. La ausencia de respuesta a fluidos y vasopresores puede
traducir un estado de insuficiencia suprarrenal relativa en la que la administración de hidrocortisona podría
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [907]
[56] HEPATITIS AGUDA Y FALLO HEPÁTICO FULMINANTE
justificarse. En caso de hipertensión no se deben usar fármacos con acción vasodilatadora sistémica, que
pueden originar hipotensión severa.
f) Insuficiencia renal aguda
Mantener un adecuado volumen intravascular y una presión arterial media > 70 mm Hg son las dos
medidas para su prevención junto con la restricción o eliminación de agentes nefrotóxicos.
El reemplazo renal con terapias de diálisis continuas es de elección ya que permite una mayor
estabilidad metabólica y hemodinámica utilizándose terapias en torno a los 35 ml/kg/h.
g) Alteraciones hidroelectrolíticas y metabólicas
Se recomienda vigilar cuidadosamente el mantenimiento de la homeostasis metabólica. El estado
nutricional así como los niveles de glucosa (mantener glucemias mayores de 100 mg/dL), fosfato, potasio y
magnesio deben ser monitorizados y sus alteraciones corregidas. La hiponatremia suele ser dilucional,
aunque no se recomienda la restricción hídrica por el riesgo de hipovolemia, por lo que se debe de tratar
con salino hipertónico.
Hay que considerar, en primer lugar, la administración de nutrición enteral con 35-40 kcal/kg/día y
restricción proteica (0,6-1 g/kg/día) debido a su estado hipercatabólico, valorándose el uso de nutrición
parenteral si la primera está contraindicada (encefalopatía III-IV), es mal tolerada o se muestra insuficiente
para el aporte de los requerimientos nutricionales utilizando fórmulas con mayor proporción de
aminoácidos ramificados. El aporte energético debe ser mixto, con predominio de hidratos de carbono.
Debe aumentarse el aporte de vitaminas y de oligoelementos.
h) Complicaciones infecciosas
Se debe mantener una estrecha vigilancia de posibles focos y signos de infección, y obtener de
forma frecuente muestras para cultivos de secreciones, orina, sangre o cualquier foco sospechoso para
detectar infecciones precozmente. La administración de antibióticos profilácticos no ha demostrado
disminuir las tasas de infecciones en estos pacientes ni mejorar la mortalidad, por lo que quizá deberían
reservarse para los pacientes de mayor riesgo de encefalopatía, de fracaso orgánico o en los subsidiarios a
trasplante. Sin embargo, el tratamiento empírico debería iniciarse ante progresión de encefalopatía, signos
del síndrome de respuesta inflamatoria sistémica (SIRS) o hipotensión mantenida.
2. ETIOLÓGICO
a) Intoxicación por paracetamol: Es importante obtener los niveles plasmáticos y valorar estos en
función del tiempo de la ingesta (los resultados pueden comprobarse en el normograma de Rumack). Esto
permite evaluar el riesgo del sujeto de presentar un daño hepático significativo. Se recomienda administrar
carbón activado en las primeras 4 horas mientras que la NAC presenta efecto protector administrado
dentro de las primeras 8 horas tras la ingesta (ver Capítulo 89. “Intoxicaciones”). En estos pacientes, no se
debe administrar AINE o aminoglucósidos por el potenciado riesgo de nefrotoxicidad.
b) Intoxicación por setas
Si se conoce o sospecha intoxicación por setas, se recomienda valorar la administración de
penicilina G y silibinina (30-40 mg/kg/día vo o iv, durante 3-4 días). El carbón activado precoz vía oral
también puede ser utilizado para quelar la toxina. Generalmente se emplea también NAC, aunque sin
suficiente evidencia científica. En estos casos el paciente debe de ser valorado para trasplante hepático
pues generalmente es el único procedimiento eficaz.
c) Hepatitis vírica
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [908]
[56] HEPATITIS AGUDA Y FALLO HEPÁTICO FULMINANTE
Si la etiología herpética es conocida o sospechada, el paciente debe recibir tratamiento con
aciclovir (5-10 mg/kg/8 h durante 7-14 días). Como profilaxis de FHF en pacientes con antígeno de
superficie positivo para la hepatitis B que van a recibir tratamiento quimioterápico, se recomienda
administrar análogos de nucleósidos antes y durante seis meses tras la finalización de dicho tratamiento
para evitar la reactivación de la hepatitis.
d) Hepatitis autoinmune (HAI)
Desarrollado previamente.
3. SISTEMAS DE SOPORTE HEPÁTICO ARTIFICIAL
Tabla XIII. Indicaciones de la terapia MARS en el fallo hepático fulminante del Hospital 12 de Octubre.
Tabla XIV. Criterios de trasplante hepático.
Se han desarrollado tres tipos de terapia con asistencia hepática extracorpórea; no obstante, la
terapia MARS® (Molecular Adsorbent Recirculating System) es la que cuenta con un mayor grado de
desarrollo para su aplicación clínica y está disponible en nuestro centro (Tabla XIII). Es un sistema de
hemodiafiltración extracorpórea que utiliza como baño dializador la albúmina y permite sustituir la función
de detoxificación hepática. El uso de este sistema ha demostrado reducir los niveles de sustancias tóxicas
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [909]
[56] HEPATITIS AGUDA Y FALLO HEPÁTICO FULMINANTE
(bilirrubina, creatinina, urea, amonio…), el edema cerebral y facilita la estabilidad hemodinámica y renal de
estos pacientes.
Con las ventajas descritas, podría ser útil su uso hasta la llegada del órgano donante, no obstante a
día de hoy, no hay estudios que hayan demostrado mejorar la supervivencia de estos pacientes y con el
estudio más reciente y riguroso (FULMAR), que falló en el mismo sentido.
Las contraindicaciones son: shock refractario a vasopresores, hemorragia no controlable con las
medidas de tratamiento habituales, coagulopatía grave, trombocitopenia severa, paciente con expectativa
de vida inferior a 24 horas.
4. TRASPLANTE HEPÁTICO URGENTE
Es el único tratamiento con eficacia probada sobre la supervivencia de los pacientes. Dado el
limitado número de donantes y los estrictos criterios que se deben cumplir para ser candidato (Tabla XIV),
únicamente existe una tasa de trasplante del 15%. La inclusión en lista debe ser precoz.
BIBLIOGRAFÍA
Arroyo V, Moreau R, Jalan J, Ginés P. Acute-on-chronic liver failure: A new síndrome that will re-classify
cirrosis. Journal of Hepatology. 2015;62:131-43.
Bañares R, Vega Catalina M, Vaquero J. Molecular Adsorbent Recirculating System and Bioartificial
Devices for Liver Failure. Clin Liver Dis. 2014;945-56.
Bernal W, Wendon J. Acute Liver Failure. N Engl J Med. 2013;2525-34.
Blasco S, Masegosa J, Gutiérrez ML, Alonso S, Fernández CM. Acute-on-chronic liver failure:
Pathogenesis, prognostic factors and management. World Journal of Gastroenterology. 2015;21:
12125-40.
Buffet, C. Elevación de transaminasas en hepatología. EMC-Tratado de Medicina. 2014;18(4).
Castiella A, Zapata E, Lucena MI, Andrade RJ. Drug-induced autoinmune liver disease: a diasgnostic
dilema of an increasngly reported disease. WJH. 2014;6(4):160-8.
Devarcbhavi H. An Update on Drug Induced Liver Injury. J Clin Exp Hepatol. 2012;2:247-59.
EASL Clinical Practical Guidelines: Management of Alcoholic Liver Disease. Journal of Hepatology.
2012;57:399-420.
European Association for the Studio of the Liver. J Hepatol. 2015;63:971-1004.
Kodali S, McGuire B.M. Diagnosis and Management of Hepatic Encephalopathy in Fulminant Hepatic
Failure. Clin Liver Dis. 2015;565-76.
Leise MD, Poterucha JJ, Talwalkar JA. Drug-Induced Liver injury. Mayo Clin Porc. 2014;89(1):85-106.
Martínez J, Tejedor M, Martín RM, Albillos A. Enfermedades hepáticas de causa cardiovascular.
Medicine. 2012;11:601-7.
Mathurin P, Lucey MR. Management of alcoholic hepatitis. Journal of Hepatology. 2012;S39-S45.
Pérez Moreno JM, Aguilar-Reina J. Estudio diagnóstico del paciente con hepatitis aguda. GH
continuada. 2006;5(2).
Plessier A, Rautou PE, Valla DC. Management of hepatic vascular diseases. Journal of Hepatology.
2012;S25-S38.
Potts JR, Verma S. Alcoholic hepatitis: diagnosis and management in 2012. Expert Reviews.
Gastroenterol Heptatol. 2012;6:695-710.
Singanayagam A, Bernal W. Update on acute liver failure. Curr Opin Crit Care. 2015;21:134-41.
Thursz MR, Richardson P, Allison M, Austin A, Bowers M, et al. Prednisolone or Pentoxifylline for
Alcoholic Hepatitis. New England Journal of Medicine. 2015;372:1619-28.
Willars C. Update in intensive care medicine: acute liver failure. Initial management, supportive
treatment and who to transplant. Curr Opin Crit Care. 2014;202-9.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [910]
[57] HEPATOPATÍA CRÓNICA. CIRROSIS HEPÁTICA Y SUS COMPLICACIONES
57.Hepatopatía crónica. Cirrosis hepática y sus
complicaciones
Miguel Telmo Galovart Araguas.
Medicina del Aparato Digestivo
Mario Aramberri del Vigo.
Medicina Interna
Daniel Suárez Pita.
Medicina Interna
Asesora:
María Luisa Alonso Manzano.
Médica Adjunta de Medicina del Aparato Digestivo
I. HEPATOPATÍA CRÓNICA Y CIRROSIS
1. DEFINICIÓN
La hepatopatía crónica se define como la alteración persistente (>6 meses) de los tests de función
hepática asociada a grados variables de necrosis hepatocelular, infiltrado inflamatorio y fibrosis hepática.
La cirrosis hepática es el estadio final en la evolución de la hepatopatía crónica y se caracteriza por
la progresiva fibrosis del parénquima con distorsión de la arquitectura hepática y formación de nódulos de
regeneración. Una vez alcanzado este estadio aparecen las complicaciones características secundarias a la
hipertensión portal (HTP) y a la disfunción hepatocelular (Figura 1).
Figura 1. .Evolución de la cirrosis
2. ETIOLOGÍA
Existe una amplia variedad de causas de hepatopatía crónica y cirrosis (Tabla I). En nuestro medio
más del 90% de los casos se deben al alcohol, a la infección por el virus de la hepatitis C (VHC) y a la
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [911]
[57] HEPATOPATÍA CRÓNICA. CIRROSIS HEPÁTICA Y SUS COMPLICACIONES
enfermedad grasa hepática no alcohólica (EGHNA). A nivel mundial tiene gran relevancia la enfermedad por
el virus de la hepatitis B (VHB) por su alta prevalencia en países en desarrollo.
En los próximos años veremos un cambio epidemiológico con descenso de la incidencia de la
enfermedad por VHC, tras la aparición de los nuevos tratamientos antivirales, y un progresivo aumento de
casos de hepatopatía asociada a la EGHNA.
Tabla I. Etiología de la hepatopatía crónica y cirrosis.
3. DIAGNÓSTICO (Figura 2)
1. ANAMNESIS
El interrogatorio deberá ser exhaustivo indagando sobre el historial farmacológico (actual y
pasado), factores metabólicos (dislipemia, diabetes mellitus, obesidad), hábito alcohólico, factores de
riesgo para hepatitis virales (recepción de hemoderivados, uso de drogas por vía parenteral, tatuajes,
conductas sexuales de riesgo), consumo de suplementos nutricionales o productos de herbolario,
tratamientos alternativos, historia familiar y viajes o procedencia geográfica.
También hemos de enfocar la anamnesis hacia posibles episodios previos de descompensación en
forma de ascitis, ictericia, edemas, hemorragia digestiva, encefalopatía, etc.
2. EXPLORACIÓN FÍSICA
En la mayoría de las ocasiones será anodina en los estadios iniciales. Deberá prestarse especial
atención a estigmas de hepatopatía avanzada y cirrosis (hepatomegalia, esplenomegalia, ascitis, ictericia,
asterixis, arañas vasculares, eritema palmar, ginecomastia, Caput medusae, atrofia muscular de
extremidades, pérdida del vello, tendencia a la hipotensión).
3. TEST DE LABORATORIO
El estudio básico incluye las enzimas de citólisis (GOT/AST y GPT/ALT), colestasis (GGT, FA) y la
bilirrubina sérica total, según predominen unas u otras podremos orientar la etiología. La alteración en los
marcadores de síntesis hepática (albúmina y tiempo de protrombina) sugieren una enfermedad
evolucionada con afectación de los mecanismos de síntesis hepática. Otro aspecto a valorar será la
presencia de trombopenia asociada o no a pancitopenia, característica de la cirrosis hepática con
hiperesplenismo (HE). Esta primera aproximación nos podrá orientar sobre si estamos ante una
hepatopatía crónica o ante una cirrosis ya establecida.
Se iniciará el estudio etiológico solicitando serologías virales, perfil lipídico, perfil férrico,
ceruloplasmina, inmunoglobulinas e inmunidad no órgano específica y hepática (Tabla II).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [912]
[57] HEPATOPATÍA CRÓNICA. CIRROSIS HEPÁTICA Y SUS COMPLICACIONES
Figura 2. Sistemática de estudio.
Tabla II. Características del diagnóstico según la patología.
4. PRUEBAS DE IMAGEN
La ecografía abdominal es el pilar en el estudio de la hepatopatía tanto como abordaje inicial como
para el control evolutivo. Permite el diagnóstico de hepatopatía crónica y cirrosis, así como de la presencia
de HTP. Puede orientar hacia la etiología subyacente, como por ejemplo en el caso de la EGHNA. Otro
aspecto fundamental es su papel en la detección precoz del carcinoma hepatocelular (ver Apartado VIII.
“Carcinoma hepatocelular”).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [913]
[57] HEPATOPATÍA CRÓNICA. CIRROSIS HEPÁTICA Y SUS COMPLICACIONES
Otras pruebas a valorar, como la tomografía computarizada (TC) y la resonancia magnética (RM),
podrán aportar información complementaria y su indicación será individualizada según el contexto clínico.
En el control de los grados iniciales de fibrosis actualmente se emplea la elastografía de transición
(FibroScan®). Esta técnica está basada en el grado de propagación de las ondas a través del parénquima
siendo esta proporcional al grado de fibrosis. Respecto a los valores y sus puntos de corte solamente existe
un claro consenso en el seguimiento de la hepatopatía por VHC; en otras patologías sus resultados nos
orientarán en torno al grado de fibrosis en máximos y mínimos.
5. BIOPSIA HEPÁTICA
Se trata del “Gold Standard” para la filiación etiológica, si bien, en muchas ocasiones se puede
llegar al diagnóstico por otros medios. Se realiza bien por vía percutánea, transyugular o quirúrgica. Se
recurrirá a la biopsia hepática en el caso de que la alteración del perfil hepático sea persistente y no se
llegue al diagnóstico por otras vías, para estadificación de determinadas enfermedades hepáticas crónicas o
para el diagnóstico de enfermedades sistémicas o lesiones hepáticas ocupantes de espacio (Tabla III).
La complicación más frecuente es el sangrado que puede ser leve (1/500) o grave (1/2.500 a
1/10.000) en caso de hemorragia intraperitoneal y necesidad de transfusión, hospitalización o tratamiento
quirúrgico. La tasa de mortalidad es de 1/10.000. Otras complicaciones posibles son: perforación de víscera
hueca, pneumotórax, hemotórax, peritonitis biliar, sobreinfección, hemobilia y muy raramente
taquiarritmia ventricular (en las biopsias transvenosas).
Tabla III. Indicaciones de la biopsia hepática percutánea.
Tabla IV. Contraindicaciones para la biopsia hepática percutánea.
4. TRATAMIENTO
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [914]
[57] HEPATOPATÍA CRÓNICA. CIRROSIS HEPÁTICA Y SUS COMPLICACIONES
El tratamiento etiológico y control de los factores de riesgo en fases iniciales puede revertir la
fibrosis o, al menos, enlentecer su progresión, de ahí la importancia del estudio etiológico.
5. SEGUIMIENTO
En los pacientes con hepatopatía crónica se debe realizar un seguimiento periódico que variará en
función de la etiología. Asimismo, con los pacientes cirróticos, una vez realizado el estudio etiológico y
establecido el grado funcional, se debe establecer un seguimiento de carcinoma hepatocelular, de profilaxis
de sangrado variceal y del resto de complicaciones.
6. PRONÓSTICO
Para definir la gravedad y el pronóstico en la cirrosis la clasificación de Child-Pugh (Tabla V)
continúa siendo la más empleada.
Tabla V. Clasificación de Child-Pugh.
Tabla VI. Escala MELD.
II. COMPLICACIONES DE LA CIRROSIS HEPÁTICA
A. ASCITIS
Es la complicación más frecuente. El 50-60% de los pacientes con cirrosis en fase compensada
presentarán su primer episodio en los 10 años iniciales de seguimiento. Está asociada a un peor pronóstico,
marcando una mortalidad al año del 15% y a los cinco del 50%, por lo que el trasplante hepático debe ser
considerado como una opción de tratamiento.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [915]
[57] HEPATOPATÍA CRÓNICA. CIRROSIS HEPÁTICA Y SUS COMPLICACIONES
1. FISIOPATOLOGÍA
El mecanismo fundamental es la hipertensión portal (HTP) secundaria a la distorsión de la
arquitectura sinusoidal ocasionada por la cirrosis hepática. Desencadena la liberación de sustancias
vasodilatadoras (óxido nítrico, etc.) que provoca una dilatación de la circulación arterial visceral, con una
reducción secundaria de la resistencia vascular sistémica, con el consiguiente estímulo de los sistemas
renina-angiotensina-aldosterona, simpático y de hormona antidiurética, que conlleva una mayor
reabsorción renal de sodio con expansión del volumen extracelular, acumulándose en el abdomen y en los
miembros inferiores.
2. DIAGNÓSTICO
(ver Capítulo 52. “Ascitis”)
En los pacientes con cirrosis establecida deberá analizarse el líquido ascítico mediante paracentesis
en los siguientes casos:
Primer episodio de ascitis clínica.
Empeoramiento de ascitis o necesidad de ingreso por otra complicación de la cirrosis.
Sospecha de infección del líquido ascítico.
Sospecha de etiología distinta a la HTP.
3. TRATAMIENTO
a) Primera línea
Deberá realizarse una restricción moderada de la sal en la dieta, 4,6-6,9 g diarios; esto equivale a
no añadir sal a los alimentos y evitar comidas preparadas. Restricciones más estrictas pueden ser
contraproducentes.
En pacientes con hábito alcohólico documentado, deberá insistirse en el abandono del mismo.
En pacientes con grado 2 de ascitis está indicado el inicio de tratamiento con diuréticos; son de
elección los antagonistas de la aldosterona, muestran gran efectividad dado el hiperaldosteronismo
existente en la cirrosis, asociados a diuréticos de asa. La pauta habitual de inicio sería 100 mg de
espironolactona y 40 mg de furosemida diarios en el desayuno. Se aumentará secuencialmente en caso de
falta de respuesta hasta una dosis máxima de 400 mg de espironolactona y 160 mg de furosemida,
manteniendo un ratio 100:40 mg. Debe evitarse la administración de diuréticos de asa por vía intravenosa,
ya que pueden desencadenar una reducción aguda del filtrado glomerular y consecuentemente
desencadenar un fracaso renal agudo que derive en un síndrome hepatorrenal.
El objetivo será conseguir una pérdida de peso de 0,5 kg por día en aquellos pacientes con ascitis
sin edemas en miembros inferiores; en el caso de presentar edemas en extremidades, como máximo diario,
se procurará 1 kg.
Los efectos secundarios más frecuentes son la insuficiencia renal prerrenal por depleción del
volumen intravascular, hiponatremia, hipopotasemia (furosemida), hiperpotasemia (espironolactona),
encefalopatía hepática, acidosis o alcalosis metabólica, ginecomastia y calambres musculares (a veces por
hipomagnesemia). Deberá suspenderse el tratamiento diurético en los siguientes supuestos: fracaso renal
prerrenal, encefalopatía hepática, peritonitis bacteriana espontánea, hiponatremia < 120 mEq/L,
hiperpotasemia > 6 mEq/L, hipopotasemia < 3 mEq/L o en caso de calambres musculares.
De presentarse ginecomastia dolorosa puede sustituirse espironolactona por amiloride (10-40 mg
diarios).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [916]
[57] HEPATOPATÍA CRÓNICA. CIRROSIS HEPÁTICA Y SUS COMPLICACIONES
En pacientes con cirrosis es frecuente la hiponatremia dilucional definida como niveles de sodio <
130 mEq/L en situaciones de sobrecarga de volumen. Es un indicador de mal pronóstico. Suele ser una
alteración crónica, bien tolerada y que no precisa de un tratamiento específico. No debe intentarse una
corrección rápida mediante el uso de soluciones hipertónicas pues guarda mayor riesgo de complicaciones
que de beneficio. Está indicada la restricción hídrica con cifras de sodio sérico menores de 130 mEq/L. Por
debajo de 125 mEq/L puede plantearse el uso de inhibidores del receptor V2 de la vasopresina (tolvaptán).
Se comenzará con una dosis de 15 mg por día, inicialmente a nivel hospitalario, con monitorización
frecuente de los niveles de sodio sérico.
En pacientes con ascitis a tensión (grado 3), se realizará paracentesis evacuadora y extracción de la
mayor cantidad posible de líquido ascítico. En extracciones mayores de 5 L para prevenir la disfunción
circulatoria posparacentesis, que puede desencadenar fracaso renal, hiponatremia y síndrome
hepatorrenal, se realizará expansión del volumen intravascular mediante la administración de albúmina
humana (8 g/L, un vial de 50 ml al 20% por cada 1,25 litros de líquido ascítico extraído). En el caso de
extracciones menores pueden emplearse expansores sintéticos (dextrano 70:8 g por litro de ascitis) o
albúmina.
Está contraindicado el uso de AINE, ya que pueden precipitar un fracaso renal además de anular la
respuesta al tratamiento diurético, así como la administración de fármacos inhibidores de la enzima
convertidora de angiotensina y los antihipertensivos antagonistas de los receptores de la angiotensina II
(IECA/ARA-II). Respecto al uso de betabloqueantes, no existe consenso sobre su efecto en esta fase de la
enfermedad.
b) Segunda línea
La ascitis puede ser refractaria al tratamiento diurético por dos motivos: por ausencia de respuesta
al tratamiento diurético (ascitis resistente) o por presentarse complicaciones relacionadas con ello de
forma reiterada (ascitis intratable). En este grupo de pacientes donde la mediana de supervivencia es de 6
meses, deberá plantearse la inclusión en lista de espera para trasplante hepático, pues es la única medida
que puede incrementar la supervivencia. Hasta entonces contamos con las siguientes opciones
terapéuticas:
Paracentesis terapéutica periódica con administración de albúmina.
Deberá mantenerse la restricción de sodio y los diuréticos si no hay contraindicaciones.
Derivación portosistémica intrahepática transyugular (TIPS).
Logra un aumento de la natriuresis secundario a la reducción del gradiente de presión portal con la
consiguiente disminución de actividad del sistema renina-angiotensina-aldosterona. Se trata de una terapia
puente en pacientes candidatos a trasplante hepático, a considerar también cuando no es posible realizar
paracentesis periódicas. Aumenta la supervivencia libre de trasplante, disminuye la mortalidad por causa
hepática, las recidivas de ascitis y la tasa de síndrome hepatorrenal. No obstante, aumenta el riesgo de
encefalopatía hepática.
No se puede recomendar en pacientes con enfermedad hepática muy avanzada (Child: > 11;
bilirrubina: > 5 mg/dL; INR: > 2; episodios repetidos de encefalopatía hepática: > 2 West-Haven o
persistente), de edad avanzada, con infección activa, insuficiencia renal progresiva o comorbilidad severa
cardiaca o respiratoria.
La realización de shunt peritoneo-venoso prácticamente se ha abandonado en la actualidad por la
alta tasa de complicaciones. Se ha recogido en estudios y en guías clínicas la utilidad de la midodrina, si
bien no se emplea de rutina en nuestro medio.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [917]
[57] HEPATOPATÍA CRÓNICA. CIRROSIS HEPÁTICA Y SUS COMPLICACIONES
B. PERITONITIS BACTERIANA ESPONTÁNEA
La peritonitis bacteriana espontánea (PBE) se define como la infección del líquido ascítico sin un
origen intraabdominal claro que lo justifique. Se produce por un mecanismo conocido como traslocación
bacteriana, por el cual las bacterias entéricas cruzan la barrera mucosa intestinal, invaden los ganglios
mesentéricos alcanzando finalmente, por vía hematógena, el líquido ascítico. Se trata de una complicación
frecuente en pacientes cirróticos con ascitis con una prevalencia del 3% en pacientes ambulantes y del 10%
en pacientes hospitalizados. Los principales microorganismos implicados son bacterias entéricas
gramnegativas (E. coli), siendo los cocos grampositivos más frecuentes en pacientes hospitalizados. Los
factores de riesgo son todas aquellas situaciones que deprimen la actividad del sistema mononuclear-
fagocítico: hipovolemia, hemorragia digestiva, vasoconstricción esplácnica, alcoholismo, etc.
1. CLÍNICA
Depende del grado de evolución del cuadro, pudiendo ser asintomática. La manifestación más
frecuente es la fiebre (80%), siendo también habitual la presencia de otros signos de inflamación sistémica
(hipotermia, leucocitosis, taquicardia o taquipnea), así como signos o síntomas locales de peritonitis (dolor
abdominal, diarrea, vómitos, íleo), empeoramiento de la función hepática, encefalopatía hepática (EH),
shock, fracaso renal o hemorragia digestiva.
2. DIAGNÓSTICO
Se basa en el recuento de polimorfonucleares (PMN) y el cultivo del líquido ascítico. Se debe
realizar una paracentesis diagnóstica para descartar PBE en todo paciente ascítico (Figura 3) que ingresa en
un hospital o presenta cualquiera de las manifestaciones clínicas descritas previamente.
Es diagnóstica una cifra igual o superior a 250 PMN/mm³. En pacientes con ascitis hemorrágica (>
10.000 hematíes/mm³) hay que restar 1 PMN por cada 250 hematíes. Han de inyectarse inmediatamente
tras la obtención del líquido ascítico al menos 10 ml en frascos de hemocultivos para bacterias aerobias y
anaerobias. La frecuente presencia de bacteriemia justifica la extracción de hemocultivos aún en ausencia
de fiebre.
Figura 3. Algoritmo diagnóstico de manejo de la peritonitis bacteriana espontánea.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [918]
[57] HEPATOPATÍA CRÓNICA. CIRROSIS HEPÁTICA Y SUS COMPLICACIONES
3. TRATAMIENTO
Medidas generales: es necesario vigilar los parámetros hemodinámicos, valorando la necesidad
de fluidoterapia IV y, en caso de shock, de fármacos vasoactivos. Deben evitarse causas que
favorezcan la aparición de EH y maniobras que puedan deteriorar la función renal, como la
administración de fármacos nefrotóxicos (AINE, aminoglucósidos, etc.) o diuréticos. En caso de
ascitis a tensión, puede realizarse paracentesis evacuadora de pequeño volumen (< 4 litros) con
reposición de albúmina.
Tratamiento antibiótico empírico (Tabla VII): debe iniciarse inmediatamente tras el
diagnóstico de PBE, sin esperar a los resultados de cultivo de líquido ascítico y en aquellos
pacientes con < 250 PMN/mm³ con signos o síntomas de infección abdominal a la espera del
cultivo.
Tabla VII. Tratamiento de la peritonitis bacteriana espontánea.
No está indicada la realización de una nueva paracentesis diagnóstica si la evolución es favorable.
Sin embargo, ante la sospecha de una respuesta inadecuada se realizará una nueva paracentesis a las 48
horas.
Si el número de PMN no ha descendido al menos en un 25%, se debe asumir la presencia de una
bacteria resistente a la antibioterapia. Por lo tanto, será necesario modificar el tratamiento antibiótico o
descartar la presencia de peritonitis secundaria. En este caso el tratamiento debe prolongarse hasta que los
signos clínicos de infección hayan desaparecido y el contaje de PMN en líquido ascítico se haya
normalizado.
Profilaxis del síndrome hepatorrenal (SHR): hasta el 30% de los pacientes con PBE desarrollan
síndrome hepatorrenal (SHR), siendo el fracaso renal el principal predictor de supervivencia. Se
recomienda la infusión de albúmina a dosis de 1,5 g/kg en las 6 primeras horas tras el
diagnóstico y 1 g/kg/24 h a las 48 horas en pacientes con insuficiencia hepática grave
(bilirrubina sérica > 4 mg/dL) o con signos de deterioro de la función renal (nitrógeno ureico en
sangre [BUN] > 30 mg/dL o creatinina sérica > 1 mg/dL).
PROFILAXIS DE LA PERITONITIS BACTERIANA ESPONTÁNEA:
Se ha asociado recientemente el uso de los inhibidores de la bomba de protones al desarrollo de
PBE, por lo que es recomendable ajustar estrictamente su uso a las indicaciones de los mismos.
1. PRONÓSTICO
La mortalidad de la PBE oscila alrededor del 20%, mientras que la supervivencia al año tras el
primer episodio es muy baja (30-50%), por lo que todo paciente que se recupere de una PBE debe ser
considerado como potencial candidato a trasplante hepático.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [919]
[57] HEPATOPATÍA CRÓNICA. CIRROSIS HEPÁTICA Y SUS COMPLICACIONES
Tabla VIII. Indicaciones de profilaxis de la peritonitis bacteriana espontánea.
2. PERITONITIS BACTERIANA SECUNDARIA
Se trata de la infección del líquido ascítico secundario a una perforación visceral o a un absceso de
un órgano abdominal. Se debe sospechar en aquellos casos que se presentan con signos o síntomas
abdominales muy localizados, ausencia de respuesta al tratamiento de PBE, un recuento de PMN en líquido
ascítico muy elevado (habitualmente > 10.000/mm³) o un cultivo de líquido ascítico polimicrobiano.
El diagnóstico viene dado por: a) la presencia en líquido ascítico de dos o más de los siguientes
hallazgos: glucosa < 50 mg/dL, proteínas > 1 g/dL, LDH > límite superior de la normalidad de LDH en plasma;
b) un aumento del antígeno carcinoembrionario 5 ng/ml o de la FA > 240 U/l en líquido ascítico, sugestivo
de perforación intestinal; c) hallazgos en la radiografía simple, ecografía, tomografía o gammagrafía con
leucocitos de perforación, abscesos o colecciones abdominales como causa de la peritonitis.
Habitualmente requiere tratamiento quirúrgico y antibioterapia de amplio espectro con cobertura
para gérmenes anaerobios.
C. HIDROTÓRAX HEPÁTICO
Se define como la existencia de un derrame pleural mayor de 500 cc en un paciente cirrótico con
HTP, tras exclusión de otras causas que lo justifiquen. Suele deberse a defectos en la pared diafragmática y
presentarse junto con ascitis. En el 85% de los casos estará en el hemitórax derecho, si bien, puede ser
bilateral o izquierdo.
1. CLÍNICA
Clínicamente se puede manifestar como disnea de esfuerzo, ortopnea y trepopnea, con tos seca
y/o dolor pleurítico, o bien, puede ser asintomático.
2. DIAGNÓSTICO
Debe realizarse una toracocentesis, debiendo ser los datos bioquímicos coherentes con un
trasudado, el gradiente entre albúmina plasmática y el líquido pleural debe ser mayor de 1,1 g/dL. Deberán
excluirse otras causas de derrame pleural.
3. TRATAMIENTO
Las medidas iniciales comprenderán restricción de sodio en la dieta y diurético con pautas similares
al manejo de la ascitis. Puede realizarse una toracocentesis evacuadora para alivio sintomático. Está
contraindicada la colocación de un tubo de drenaje pleural, por presentar una muy alta frecuencia de
complicaciones y riesgo de mortalidad.
Deberá valorarse la inclusión del paciente en lista de espera para trasplante hepático.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [920]
[57] HEPATOPATÍA CRÓNICA. CIRROSIS HEPÁTICA Y SUS COMPLICACIONES
En caso de refractariedad una opción a valorar sería la realización del TIPS, si bien, todavía no está
completamente demostrada su efectividad.
Puede infectarse generando un empiema bacteriano espontáneo. Se diagnostica con un número
absoluto de polimorfonucleares mayor a 250 con cultivo positivo, o mayor de 500 con cultivo negativo. Los
gérmenes implicados con más frecuencia son enterobacterias o cocos grampositivos. El tratamiento será
antibioterapia con cefalosporinas de tercera generación.
D. SÍNDROME HEPATOPULMONAR
Se define como la hipoxia arterial secundaria a dilataciones vasculares en el parénquima pulmonar
que condicionan un shunt derecha-izquierda en pacientes con enfermedad hepática crónica y/o HTP.
Suele afectar a pacientes con alto grado de disfunción hepatocelular (más frecuente en cirrosis
grado C de Child y en lista de espera para trasplante).
1. CLÍNICA
Es muy característico el síndrome de platipnea-ortodeoxia (disnea y desaturación en bipedestación
con mejoría en decúbito), si bien, no es patognomónico; la manifestación clínica más frecuente es la disnea
de esfuerzo, con cianosis, arañas vasculares y la aparición de acropaquias.
2. DIAGNÓSTICO
Para realizar el diagnóstico deberá tomarse una gasometría arterial en decúbito y en bipedestación
para demostrar la ortodeoxia, una radiografía de tórax y test de fisiología respiratoria, en el que lo
esperable es una reducción en la tasa de difusión de CO. Las técnicas más empleadas son la ecocardiografía
con contraste y la gammagrafía con macroagregados de albúmina marcados con tecnecio 99, siendo esta la
más específica. En raras ocasiones es necesaria la realización de una arteriografía pulmonar.
3. TRATAMIENTO
El tratamiento de elección en caso de disnea progresiva y/o hipoxemia es el trasplante hepático.
E. ENCEFALOPATÍA HEPÁTICA
La encefalopatía hepática (EH) se define como la disfunción cerebral producida por insuficiencia
hepatocelular y/o shunts protosistémicos, manifestada por un amplio espectro de alteraciones
neuropsiquiátricas.
Se produce como consecuencia del paso al sistema nervioso central de sustancias tóxicas y
productos nitrogenados producidos por bacterias intestinales que, al disminuir el metabolismo hepático,
alcanzan la circulación sistémica. Constituye una de las complicaciones más frecuentes en los pacientes
cirróticos, implicando un mal pronóstico (supervivencia al año de un 40%), por lo que supone una
indicación para valorar al paciente como candidato a trasplante hepático.
1. CLÍNICA
La EH se presenta como un deterioro cognitivo-conductual que oscila entre alteraciones leves de la
consciencia y el coma. En etapas iniciales se expresa únicamente como un deterioro de la calidad de vida
sin alteraciones clínicas aparentes (EH mínima), detectándose únicamente mediante pruebas psicométricas
específicas que ponen de manifiesto sutiles alteraciones neuropsicológicas o neurofisiológicas.
Para establecer el grado de EH se utiliza generalmente la clasificación de West-Haven (Tabla IX)
aunque para grados avanzados también puede usarse la clasificación de Glasgow.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [921]
[57] HEPATOPATÍA CRÓNICA. CIRROSIS HEPÁTICA Y SUS COMPLICACIONES
Tabla IX. Grados de encefalopatía hepática según la clasificación de West-Haven.
2. DIAGNÓSTICO
Es un diagnóstico fundamentalmente clínico que se realiza en el contexto de insuficiencia hepática
y/o shunts portosistémicos ante la presencia de signos y síntomas inespecíficos, entre los que cabe
destacar la discalculia por ser uno de los más precoces y la asterixis o flapping por ser de los más comunes.
La determinación de niveles de amonio en sangre no es necesaria en aquellos casos en los que el
diagnóstico sea evidente, siendo improbable la presencia de EH si los niveles de amonio son normales (solo
un 10% de EH presentan amoniemia normal). Tampoco se recomiendan las determinaciones seriadas
puesto que no se correlacionan sus niveles con el grado de EH.
El electroencefalograma es poco sensible (principalmente en estadios iniciales) y poco específico en
el estudio de la EH, muy sujeto a la interpretación individual.
Un enfoque inicial debe incluir una evaluación de la función hepática y un estudio detallado de los
posibles factores desencadenantes o contribuyentes.
Tabla X. Factores precipitantes de encefalopatía hepática por orden de frecuencia.
Una vez alcanzado el diagnóstico es conveniente caracterizar la EH en función del tipo, grado, curso
temporal y factor precipitante (Tabla X y XI).
Tabla XI. Clasificación de la encefalopatía hepática.
Dado que las alteraciones son inespecíficas e indistinguibles de otras encefalopatías es necesario
hacer un diagnóstico diferencial con lesiones estructurales intracraneales, otras encefalopatías
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [922]
[57] HEPATOPATÍA CRÓNICA. CIRROSIS HEPÁTICA Y SUS COMPLICACIONES
metabólicas/tóxicas y trastornos neuropsiquiátricos. Todo esto justifica la realización de una exploración
física detallada que incluya tacto rectal y lavado por SNG para descartar hemorragia gastrointestinal,
paracentesis diagnóstica en presencia de ascitis, analítica completa con análisis de orina y TC craneal ante
la presencia de coma, estupor, focalidad neurológica o signos de irritación meníngea.
3. TRATAMIENTO
Medidas generales: cualquier paciente con EH debe ser ingresado, a excepción del grado I con
hepatopatía conocida y episodios previos si el desencadenante es tratable ambulatoriamente y
el cuadro revierte en menos de 24 horas. Puede ser necesaria la colocación de una sonda
nasogástrica (SNG) y vesical en grados III y IV, monitorizar la saturación de oxígeno e incluso
valorar la necesidad de intubación endotraqueal. Se deben evitar los sedantes, siendo
preferible el uso de contenciones mecánicas en caso de agitación.
Tratamiento de la causa desencadenante: hasta el 90% de los pacientes mejoran tras tratar el
factor desencadenante, siendo de especial interés en los casos de hemorragia digestiva la
colocación de una SNG y la administración de enemas para evitar la formación de productos
nitrogenados. Hay que combatir el estreñimiento intensamente con laxantes orales y/o
enemas.
Medidas específicas
Dieta: deberá contener entre 1,2 y 1,5 g/kg/día de proteínas y habrá de administrarse
por vía oral, enteral o parenteral según el nivel de consciencia. Se recomienda incluir
complejos vitamínicos y suplementos de zinc. La restricción proteica ha demostrado ser
perjudicial.
Laxantes (disacáridos no absorbibles): está demostrada la eficacia de dos compuestos
diferentes: lactulosa (Duphalac®) y lactitol (Emportal®).
Además de su efecto catártico, actúan modificando la flora local y acidificando el medio
intestinal, lo que inhibe la síntesis y difusión del amoníaco. Se recomienda iniciar el
tratamiento con laxantes una vez se ha corregido la causa precipitante. La dosis diaria
recomendada de lactulosa es aquella que alcance el objetivo de conseguir 2-3
deposiciones blandas al día, y suele variar entre 45 y 90 g/día. En casos de hemorragia
digestiva o bajo nivel de consciencia, se recomienda la administración de enemas (200
g de lactulosa en 800 ml de agua cada 8 horas) hasta la resolución del episodio.
Antibióticos poco absorbibles: la rifaximina a dosis de 400 mg/8 horas es el antibiótico
con mejor perfil de eficacia/seguridad de todos los disponibles para el tratamiento de
la EH, siendo su principal inconveniente su alto coste. Las reacciones adversas más
frecuentes son el mareo, la cefalea o la distensión abdominal. Otros antibióticos como
la paramomicina o la neomicina son fármacos más baratos como alternativa a la
rifaximina, pero están cayendo en desuso por el riesgo de efectos adversos graves
como la ototoxicidad o la nefrotoxicidad.
Oclusión de shunts portosistémicos espontáneos: deben llevarse a cabo por medio de
radiología intervencionista en centros experimentados, tras el fracaso del resto de
medidas.
Medidas que aún no han demostrado eficacia: se están estudiando otras alternativas
para el tratamiento de la EH como la dieta rica en aminoácidos ramificados, los
probióticos, la L-ornitina-fenilacetato y la L-ornitina-L-aspartato, el gliceril-fenilbutirato,
los inhibidores de la glutaminasa, la albúmina iv, los laxantes no disacáridos o el
flumazenilo, sin resultados concluyentes hasta el momento, pudiendo ser de utilidad en
un futuro próximo.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [923]
[57] HEPATOPATÍA CRÓNICA. CIRROSIS HEPÁTICA Y SUS COMPLICACIONES
4. PROFILAXIS
Profilaxis primaria: no se recomienda la profilaxis primaria de EH en pacientes cirróticos ni en
pacientes a los que se les ha realizado un TIPS.
Profilaxis secundaria: se aconseja mantener tratamiento crónico con lactulosa tras un primer
episodio de EH. En caso de nueva recidiva la adición de rifaximina a dosis de 400 mg/8 horas ha
demostrado ser el agente más eficaz para prevenir nuevos brotes de EH.
F. SÍNDROME HEPATORRENAL
Se trata de una complicación grave y se define como el deterioro de la función renal en ausencia de
una causa identificable en un paciente con enfermedad hepática avanzada con HTP. El SHR es un trastorno
funcional y, por tanto, potencialmente reversible. Puede aparecer en insuficiencias hepáticas graves de
curso agudo además de en la enfermedad crónica.
1. FISIOPATOLOGÍA
Se produce por una intensa vasodilatación periférica que origina una hipovolemia arterial efectiva,
generándose una respuesta adaptativa que estimula los sistemas vasoconstrictores y antinatriuréticos
(sistema simpático, sistema renina-angiotensina, sistema arginina-vasopresina). Estos cambios ocasionan
una vasoconstricción renal y un descenso del filtrado glomerular produciéndose el SHR.
2. CLÍNICA
Presentación clínica similar a otras causas de fracaso renal. Se clasifica en dos tipos según la
intensidad y la progresión:
SHR tipo 1: se produce un importante deterioro de la función renal rápidamente progresivo con
oliguria, natriuria descendida (< 10 mEq), elevación de los niveles de creatinina, urea y potasio
e hiponatremia dilucional. En general, está precedido por un acontecimiento desencadenante
como una hemorragia o una infección. Mal pronóstico en ausencia de tratamiento con una
mortalidad del 80% a dos semanas.
SHR tipo 2: tiene una evolución más indolente y lentamente progresiva y es característico de
pacientes con ascitis refractaria. Cursa con un aumento moderado de la creatinina sérica. Los
pacientes con SHR tipo 2 pueden evolucionar a un SHR tipo 1.
3. DIAGNÓSTICO
Es de exclusión, por lo requiere descartar otras causas de fallo renal (shock, nefrotoxicidad por
fármacos o contrastes, glomerulopatías, etc.).
Recientemente se han actualizado los criterios de insuficiencia renal aguda (Tabla XII) en el paciente
cirrótico y consecuentemente del SHR de cara a intentar un diagnóstico y tratamiento precoz. Esta nueva
definición del International Club of Ascites (ICA-AKI) (Tabla XIII) se basa en un incremento ≥ 0,3 mg/dL en
menos de 48 horas o un incremento ≥ 50% de la creatinina basal ocurrido en los últimos 7 días.
Tabla XII. Criterios de insuficiencia renal aguda en cirrosis (ICA-AKI).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [924]
[57] HEPATOPATÍA CRÓNICA. CIRROSIS HEPÁTICA Y SUS COMPLICACIONES
Tabla XIII. Criterios síndrome hepatorrenal según el International Club of Ascites (ICA).
4. TRATAMIENTO (FIGURA 4)
Medidas generales: los paciente con SHR tipo I requieren hospitalización debiendo valorarse su
ingreso en una Unidad de Cuidados Intensivos. Una vez diagnosticado debe iniciarse
tratamiento de forma inmediata para evitar su progresión. Se han de monitorizar de manera
estricta las constantes vitales, controlar la función renal y hepática y vigilar la aparición de
posibles complicaciones intercurrentes. Debe optimizarse el balance de líquidos para evitar una
sobrecarga de volumen o un empeoramiento de la hiponatremia. La monitorización de la PVC
se considera útil, pero no obligatoria. Deben suspenderse los diuréticos, por lo que, en caso de
ascitis de gran volumen o ascitis refractaria deberá realizarse paracentesis evacuadora con
reposición de albúmina. En caso de sobrecarga de volumen se podrá emplear furosemida
intravenosa, estando contraindicada la administración de antagonistas de la aldosterona.
No hay evidencias concluyentes acerca de la conveniencia de mantener o suspender el tratamiento
betabloqueante en pacientes en profilaxis del sangrado variceal.
Tratamiento farmacológico: el tratamiento de elección son los fármacos vasoconstrictores
asociados a albúmina. El más empleado es terlipresina (Glypressin®), un análogo de la
vasopresina. En los estudios ha demostrado una eficacia entre un 40-60% en el tratamiento del
SHR tipo 1. Se iniciará tratamiento con terlipresina iv (1 mg/4-6 h) asociando albúmina (1 g/kg
de peso durante el primer día, máximo de 100 g/día, posteriormente a dosis de 20- 40 g/día). Si
durante el seguimiento no se produce un descenso > 25% de los niveles de creatinina
plasmática en 3 días, se podrá aumentar la dosis a 2 mg cada 4 horas. Su administración ha de
prolongarse al menos 7 días, momento en que se valorará su suspensión en caso de no
producirse un descenso > 25% en creatinina plasmática. En caso de buena respuesta se
mantendrá durante 15 días.
La recidiva del SHR debe tratarse de la misma manera. Su administración está contraindicada en
paciente con antecedentes de cardiopatía isquémica y siempre han de vigilarse complicaciones isquémicas
sean a nivel coronario o periférico.
Existe escasa evidencia de su utilidad en el SHR tipo 2; según algunos estudios puede lograr una
mejoría de la función renal hasta en el 50% de los pacientes pero que empeora al suspender el tratamiento.
En Unidades de Cuidados Intensivos se emplea con buenos resultados noradrenalina. Hasta el momento,
aunque existen estudios a favor de la eficacia de otros vasoconstrictores, como los análogos de
somatostatina (Octreotide) y los agonistas alfa adrenérgicos (Midodrina), no existe suficiente evidencia.
Derivación portosistémica intrahepática transyugular (TIPS): algunos estudios demuestran una
mejoría de la función renal en el SHR tipo 1. Existen múltiples contraindicaciones (Child-Pugh: >
12; bilirrubina: > 5 mg/dL, EH) y complicaciones respecto a esta técnica por lo que permanece
como un tratamiento de segunda línea en pacientes tras fracaso del tratamiento
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [925]
[57] HEPATOPATÍA CRÓNICA. CIRROSIS HEPÁTICA Y SUS COMPLICACIONES
vasoconstrictor y su indicación debe ser individualizada. También se ha planteado su eficacia en
la ascitis refractaria en pacientes con SHR tipo 2 en algunos estudios.
Terapias de sustitución renal: la hemodiálisis (HD) puede valorarse en aquellos pacientes no
respondedores, en lista de espera para trasplante hepático y que reúnan criterios para su
realización. Las indicaciones habituales para HD como la hiperpotasemia grave, la acidosis
metabólica intratable o la sobrecarga de volumen son poco frecuentes en el SHR, sobre todo,
en estadios iniciales. Existen otros métodos como los de diálisis con albúmina (MARS,
Prometheus) que se pueden emplear como puente al trasplante. Si bien son eficaces, existen
escasos estudios y están disponibles en pocos centros.
Trasplante hepático: es el tratamiento definitivo para el SHR con una supervivencia del 65% en
el SHR tipo 1. La indicación del trasplante doble hepatorrenal se restringirá a aquellos pacientes
con necesidad de terapia renal sustitutiva durante más de 8 semanas. El tratamiento con
vasoconstrictores del SHR previo al trasplante parece que mejora los resultados tras el mismo.
5. PRONÓSTICO
El pronóstico sin tratamiento es malo a corto plazo con una supervivencia de 1 mes en el SHR tipo 1
y de 6 meses en el SHR tipo 2. Los pacientes que desarrollan un SHR deben ser valorados para trasplante.
6. PROFILAXIS
Administración de albúmina en pacientes con PBE y tras paracentesis evacuadoras.
La administración de pentoxifilina en pacientes con hepatitis aguda alcohólica disminuye la
incidencia de SHR y aumenta la supervivencia.
Figura 4. Algoritmo de manejo de insuficiencia renal aguda y SHR.
G. CARCINOMA HEPATOCELULAR
La incidencia del carcinoma hepatocelular (CHC) continúa en ascenso y actualmente a nivel global
es el sexto cáncer más frecuente y la tercera causa de muerte por cáncer. La cirrosis de cualquier etiología
constituye el principal factor de riesgo en su desarrollo (hasta un 80% de CHC asientan sobre hígados
cirróticos). Respecto a su etiología se observa una clara distribución geográfica. En los países desarrollados
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [926]
[57] HEPATOPATÍA CRÓNICA. CIRROSIS HEPÁTICA Y SUS COMPLICACIONES
predomina el alcohol y la infección por VHC mientras que en Asia y África fundamentalmente se producen
por hepatitis B. Por ello son fundamentales las estrategias de vigilancia en los pacientes con cirrosis que
permitan un diagnóstico precoz.
1. DIAGNÓSTICO
Los programas de vigilancia se basan en la ecografía abdominal con una sensibilidad del 58-89% y
una especificidad superior al 90% y ha de realizarse cada 6 meses (excepto en lesiones < 1 cm y en el
seguimiento tras resección o tratamientos locorregionales). La utilización de la alfafetoproteína como
técnica de cribado aislada no se recomienda por su baja sensibilidad ni tampoco asociada a la ecografía.
Lesiones < 1cm: se valorará el crecimiento y cambios en sus características realizándose
seguimiento cada 3-4 meses durante 1 año y posteriormente cada 6 meses. b)
Lesiones > 1 cm: habrá de completarse el estudio mediante otras técnicas (TC multidetector o
RM con contraste dinámico). Si la lesión presenta las características radiológicas típicas
(hipervascularidad en la fase arterial con lavado en la fase venosa portal o tardío), se podrá
establecer el diagnóstico de CHC en las lesiones > 2 cm. En contextos subóptimos y lesiones
entre 1-2 cm se recomienda una estrategia más conservadora completándose el estudio con
otra prueba de imagen (TC o RM, según que técnica se emplease en primer lugar). El
diagnóstico anatomopatológico se realizará en lesiones de características atípicas o con
pruebas de imagen no concluyentes.
2. TRATAMIENTO Y PRONÓSTICO
Se recomienda el estadiaje del Barcelona-Clinic-Liver-Center (BCLC) (Figura 5) que aporta
información pronóstica y permite la asignación al tratamiento. Se basa en el estadio tumoral, la función
hepática, el estado general y variables que se ha visto se relacionan con la respuesta terapéutica (HTP,
bilirrubina, presencia de síntomas).
Estadio muy precoz-0 (lesión única < 2 cm, grado funcional A de Child y buen estado general) y
precoz-A (lesión única < 5 cm o 3 lesiones < 3 cm, grado funcional A-B de Child).
Resección quirúrgica: reservada para pacientes con función hepática conservada y sin
HTP significativa (gradiente de presión venosa hepática [GPVH] < 10 mm Hg) o recuento
de plaquetas > 100.000/mm³.
Trasplante hepático: constituye el tratamiento de elección en pacientes con elevado
GPVH o hiperbilirrubinemia en ausencia de comorbilidad o contraindicaciones para el
mismo. Se acepta el tratamiento locorregional, fundamentalmente con
radiofrecuencia, si la lista de espera es superior a 6 meses.
Radiofrecuencia (RF): es el tratamiento estándar para pacientes no aptos para cirugía.
Se considera un tratamiento seguro y bien tolerado con un índice de complicaciones
muy inferior (2-10%) a los tratamientos convencionales. En un 20-30% puede aparecer
dolor y fiebre, que constituyen el síndrome postablación, así como hemorragia,
infección, lesión biliar, etc.
Inyección de etanol: en tumores < 2 cm, BCLC de 0, parece que alcanza respuestas
similares a RF. Se emplea fundamentalmente en aquellos pacientes en los que la
ablación por RF no es viable técnicamente (10-15%).
Otros tratamientos ablativos como las microondas y la crioablación están en fase de
investigación.
Estadio intermedio-B (tumores de gran tamaño o multifocales, grado A-B de Child,
asintomático, sin invasión vascular macroscópica o diseminación extrahepática).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [927]
[57] HEPATOPATÍA CRÓNICA. CIRROSIS HEPÁTICA Y SUS COMPLICACIONES
El tratamiento de elección continúa siendo la quimioembolización transarterial (TACE/
QETA). Se trata de un tratamiento paliativo que ha demostrado un incremento en la
mediana de supervivencia de 16 a 20 meses. El efecto adverso más frecuente (60-80%)
es el síndrome posquimioembolización. Cursa con molestias en hipocondrio derecho,
náuseas y vómitos, fiebre con alteración del perfil hepático e hiperbilirrubinemia. Suele
ser autolimitado y resolverse en una semana. Además, pueden producirse otras
complicaciones de mayor gravedad como isquemia hepática, formación de abscesos,
daño de la vía biliar, fallo renal, etc.
Existen otros tratamientos como la radioterapia interna con microesferas de vidrio 131I
o 90Y o la radioterapia externa conformacional.
Estadio avanzado-C (invasión vascular, afectación extrahepática o clínica tumoral importante,
grado A-B de Child).
Sorafenib (Nexavar®), un inhibidor múltiple de tirosina quinasas con acción
antiangiogénica, continúa siendo el tratamiento de elección. Se emplea en pacientes
con buena función hepática (Child A) y tumores avanzados (BCLC-C) o en aquellos con
progresión a pesar de tratamientos locorregionales. Existen una amplia variedad de
efectos adversos asociados a sorafenib fundamentalmente cutáneos (21-40%) como
xerosis, alopecia, síndrome mano-pie, etc. También son frecuentes los efectos
gastrointestinales y cardiovasculares. En la mayoría de casos se podrán manejar con
tratamiento sintomático requiriendo en los casos más graves el ajuste de dosis de
sorafenib.
Actualmente hay una gran variedad de estudios en marcha en la búsqueda de nuevos
fármacos.
Estadio-D (pacientes con grave deterioro del estado general y/o grado C de Child).
Figura 5. Clasificación BCLC de carcinoma hepatocelular.
III. TRASPLANTE HEPÁTICO
1. INCLUSIÓN EN LISTA DE ESPERA
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [928]
[57] HEPATOPATÍA CRÓNICA. CIRROSIS HEPÁTICA Y SUS COMPLICACIONES
Deben ser evaluados para trasplante hepático ortotópico (THO) aquellos pacientes con cirrosis
hepática con disfunción hepática avanzada (MELD ≥ 15) o que presente una complicación mayor (ascitis,
hemorragia variceal, EH, SHR, SHP grave).
2. INDICACIONES
Las más frecuentes continúan siendo la cirrosis hepática secundaria a VHC y alcohol (necesario 6
meses de abstinencia). Otra indicación frecuente es el CHC siempre que cumpla los criterios de Milán (1
nódulo < 5 cm o 3 nódulos < 3 cm, sin invasión vascular ni manifestaciones extrahepáticas). En algunos
casos de tumores que exceden los criterios de Milán se puede plantear el trasplante tras tratamiento
locorregional. La insuficiencia hepática aguda también constituye otra importante indicación para
trasplante.
La aparición de los nuevos tratamientos antivirales contra el VHC ha cambiado de forma importante
el planteamiento de manejo de esta infección en los candidatos a THO. Previamente los tratamientos
basados en interferón estaban contraindicados en muchos de los candidatos por la comorbilidad e
importantes efectos secundarios asociados. Hoy en día no hay consenso sobre cuándo tratar. En general se
prefiere el tratamiento previo al trasplante si la situación del paciente lo permite.
Esta decisión deberá ser individualizada de acuerdo a lista de espera de cada centro, la priorización
en ella y la situación funcional del paciente.
3. PRIORIZACIÓN EN LA LISTA DE ESPERA
En los pacientes que presenten una insuficiencia hepática aguda se emplean los criterios del King’s
College para definir la necesidad de trasplante.
La priorización en los pacientes con hepatopatía crónica se realiza basándose en el índice MELD.
Existen una serie de situaciones clínicas en las que este índice no refleja de forma adecuada el pronóstico y
que constituyen excepciones al MELD (carcinoma hepatocelular, síndrome hepatopulmonar, colangitis
esclerosante primaria/secundaria, síndrome de Caroli, estenosis postTHO, síndrome de Budd-Chiari,
colangiocarcinoma, fibrosis quística, prurito refractario, etc.). Sobre cómo priorizar a estos pacientes no hay
consenso y deberán ser evaluados de forma individualizada.
4. CONTRAINDICACIONES
Infección sistémica: constituye una contraindicación absoluta.
Edad: en ausencia de comorbilidad importante la edad (> 70 años) no se considera una
contraindicación.
Obesidad: todo paciente obeso debe ser sometido a consejo dietético previo al trasplante. La
obesidad grado 3 (IMC > 40) se considera contraindicación relativa.
Hipertensión portopulmonar: es una comorbilidad frecuente en los candidatos y que debe ser
valorada; en casos graves puede suponer una contraindicación al trasplante.
Tumores extrahepáticos: la presencia de tumores extrahepáticos no tratados se considera
contraindicación absoluta. En pacientes que han recibido tratamiento con intención curativa se
puede plantear el trasplante aunque el margen de tiempo de vigilancia no está definido y se
deberá individualizar según el tipo de tumor.
VIH: no se considera contraindicación si la infección está controlada (CD4 > 100 y CV
indetectable).
Colangiocarcinoma: constituye una contraindicación absoluta, excepto en estadios muy
precoces.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [929]
[57] HEPATOPATÍA CRÓNICA. CIRROSIS HEPÁTICA Y SUS COMPLICACIONES
BIBLIOGRAFÍA
Angeli P, Ginès P, Wong F, Bernardi M, Boyer TD, Gerbes A, et al. Diagnosis and management of acute
kidney injury in patients with cirrhosis: revised consensus recommendations of the International Club of
Ascites. J Hepatol. 2015;62(4):968-74.
Bai M, Qi XS, Yang ZP, Yang M, Fan DM, Han GH. TIPS improves liver transplantation-free survival in
cirrhotic patients with refractory ascitis: an updated meta-analysis. World J Gastroenterol. 2014;
20(10):2704-14.
D’Amico G, García-Tsao G, Pagliaro L. Natural history and prognostic indicators of survival in cirrhosis: a
systematic review of 118 studies. J Hepatol. 2006;44(1):217-31.
EASL Clinical Practice Guidelines: Liver transplantation. J Hepatol. 2015.
European Association for Study of Liver, European Organisation for Research and Treatment of Cancer.
EASLEORTC clinical practice guidelines: management of hepatocellular carcinoma. Eur J Cancer.
2012;48(5): 599-641.
European Association for the Study of the Liver. EASL clinical guidelines on the management of ascites,
spontaneus bacterial peritonitis, and hepatorrenal syndrome on cirrosis. Journal of Hepatology.
2010;53:397-417.
Krier M, Ahmed A. The asymptomatic patient with abnormal liver function tests. Clin Liver Dis.
2009;13(2): 167-77.
Martin P, DiMartini A, Feng S, Brown R, Fallon M. Evaluation for liver transplantation in adults: 2013
practice guideline by the American Association for the Study of Liver Diseases and the American
Society of Transplantation. Hepatology. 2014;59(3):1144-65.
Reig M, Matilla A, Bustamante J, Castells L, de La Mata M, Delgado M, et al. Recommendations for the
management of Sorafenib in patients with hepatocellular carcinoma. Gastroenterol Hepatol.
2010;33(10):741-52.
Rockey DC, Caldwell SH, Goodman ZD, Nelson RC, Smith AD; American Association for the Study of
Liver Diseases. Liver Biopsy. Hepatology. 2009;49(3):1017-44.
Runyon BA. American Association for the Study of Liver Diseases. Management of adult patients with
ascites due to cirrosis: Update 2012.
Vilstrup H, Amodio P, Bajaj J, Cordoba J, Ferenci P, Mullen KD, et al. Hepatic Encephalopathy in Chronic
Liver Disease: 2014 Practice Guideline by AASLD and EASL. Hepatology. 2014;60:715.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [930]
[58] PANCREATITIS
58.Pancreatitis
Esteban Romero Romero
Medicina del Aparato Digestivo
Ángel Torralba Morón
Medicina Interna
Asesor:
Andrés J. del Pozo García
Médico Adjunto de Medicina del Aparato Digestivo
I. PANCREATITIS AGUDA
1. CONCEPTO
La pancreatitis aguda (PA) se define como un proceso inflamatorio del páncreas con compromiso
variable de estructuras anatómicas adyacentes o de órganos a distancia. Es una de las patologías digestivas
más frecuentes, con una incidencia según algunas series de 73,4 por cada 100.000 habitantes a nivel
mundial. Se han identificado dos fases de la pancreatitis aguda: la temprana, durante la primera semana,
que se caracteriza por el síndrome de respuesta inflamatoria sistémica (SRIS) con o sin fallo multiorgánico;
y la tardía, pasada la primera semana, que se caracteriza por las complicaciones locales.
2. ETIOLOGÍA
La principal causa de la PA es la litiasis biliar (40-70%), por lo que se recomienda la realización de
una ecografía abdominal en el momento del diagnóstico en todos los pacientes para identificar colelitiasis.
En los casos en los que no se demuestre la presencia de colelitiasis y la sospecha de etiología biliar es alta,
se deben considerar otras pruebas de imagen, como la colangiopancreatorresonancia magnética (CPRM) o
la ultrasonografía endoscópica (USE).
La segunda causa más frecuente es el consumo de alcohol (25-35%) y suele encontrarse en el
contexto del enolismo crónico. Se debe considerar esta etiología cuando el paciente tiene una historia de
consumo de alcohol importante (más de 50 g/día) durante más de 5 años.
En tercer lugar, se encuentra la pancreatitis poscolangiopancreatografía retrógrada endoscópica
(CPRE), procedimiento tras la cual aparece en el 2-4%; es más común cuando se realiza terapéutica
endoscópica (por la esfinterotomía) y cuando se agrupan varios factores predisponentes propios del
paciente, como el sexo femenino, la edad por debajo de 60 años, la ausencia de dilatación de vía biliar o la
sospecha de disfunción del esfínter de Oddi, con factores determinantes de dificultad técnica (opacificación
del Wirsung, precorte o canulación difícil).
Otras causas menos frecuentes son la hipertrigliceridemia (donde los valores deben sobrepasar los
1.000 mg/dL), medicamentosas (teniendo en cuenta la azatioprina y la 6-mercaptopurina), infecciosas,
otras causas metabólicas (hipercalcemia e hiperparatiroidismo), autoinmunes, tumorales, etc. (Tabla I).
3. SIGNOS Y SÍNTOMAS
El principal síntoma es el dolor abdominal, de instauración rápidamente progresiva y
frecuentemente posprandial, descrito generalmente en epigastrio o hemiabdomen superior, intenso y
continuo que puede irradiarse a espalda, tórax o flancos. El dolor suele empeorar en decúbito supino.
Puede asociar náuseas o vómitos. En los casos graves puede acompañarse de datos de afectación sistémica,
como taquicardia, taquipnea, agitación, fiebre e incluso, shock y coma.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [931]
[58] PANCREATITIS
A la exploración física se evidencia dolor a la palpación en hemiabdomen superior, con signos de
defensa en los casos graves. En menos del 1% de los casos se puede observar equimosis en uno o ambos
flancos (signo de Grey-Turner) o periumbilical (signo de Cullen), que se producen por extravasación de
exudado en la pancreatitis hemorrágica y que suelen asociarse a mal pronóstico. La ictericia puede
objetivarse en casos de coledocolitiasis o compresión extrínseca del colédoco por el edema pancreático. Es
posible palpar una masa epigástrica cuando se desarrollan complicaciones locales como los pseudoquistes.
Menos frecuentemente aparecen paniculitis, tromboflebitis de miembros inferiores o poliartritis. Es
característica la disminución de ruidos hidroaéreos o incluso el silencio auscultatorio abdominal,
relacionado con el frecuente íleo paralítico secundario.
Tabla I. Etiología de la pancreatitis aguda.
4. DIAGNÓSTICO
Además del dolor abdominal típico de la PA, el diagnóstico se apoya en los hallazgos de pruebas de
laboratorio y de imagen.
1. Pruebas de laboratorio
1.1. Amilasa sérica
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [932]
[58] PANCREATITIS
Tabla II. Causas de hiperamilasemia.
Es el parámetro más utilizado para orientar el diagnóstico. Aunque no existe consenso acerca de
sus valores de corte, en la práctica clínica habitual se considera que debe estar elevada más de tres veces
por encima del valor normal. Sus valores no se correlacionan con la gravedad de la enfermedad y no es útil
para establecer el pronóstico. Aumenta en las primeras horas desde la aparición de los síntomas, y puede
mantenerse elevada hasta 3-5 días. Puede tener cifras normales en los casos de pancreatitis por alcohol o
hipertrigliceridemia. Puede estar elevada en situaciones diferentes a la pancreatitis, como
macroamilasemia, disminución del filtrado glomerular, enfermedades de las glándulas salivales y otros
procesos abdominales extrapancreáticos como apendicitis aguda, colecistitis, obstrucción o isquemia
intestinal, úlcera péptica o procesos ginecológicos. En estos casos puede ser útil la medición de la isoenzima
pancreática de la amilasa (P-isoamilasa), que representa el 35-50% de la amilasa sérica y permite así
diferenciarla de la amilasa salival. Si persiste elevada durante varias semanas, se debe considerar el
desarrollo de complicaciones (Tabla II).
1.2. Lipasa sérica
Más específica que la amilasa, se mantiene elevada durante más tiempo tras el inicio de los
síntomas (8-14 días), por lo que se considera también más sensible y se prefiere ante la amilasa para el
diagnóstico. También puede estar elevada por causas extrapancreáticas abdominales y en la
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [933]
[58] PANCREATITIS
macrolipasemia. Se deben considerar niveles superiores a los habituales en pacientes diabéticos (más de 5
veces el valor normal) por causas que aún no están aclaradas.
1.3. Otros productos pancreáticos
Pueden elevarse la fosfolipasa A, la carboxipeptidasa, la colipasa y la tripsina. Se está estudiando el
péptido de activación de tripsinógeno y el tripsinógeno-2 urinario como marcadores de pancreatitis aguda,
que también ofrecerán valor pronóstico ya que forman parte de la patogenia de esta entidad.
1.4. Amilasuria
Útil cuando los niveles de amilasa y lipasa son poco expresivos.
2. Pruebas de imagen
2.1. Radiografía simple de tórax y abdomen
De poca utilidad en el diagnóstico de PA, se utilizan para descartar la presencia de derrame pleural
u otros datos de distrés respiratorio agudo, lo que confiere peor pronóstico. La radiografía de abdomen
suele ser anodina, aunque en algunos casos puede observarse dilatación de un asa de intestino delgado
(asa centinela) secundaria al íleo paralítico o la interrupción brusca del gas colónico en el ángulo esplénico
(signo del colon cortado) por oclusión espástica a este nivel por extensión de la inflamación pancreática a
través del ligamento mesocólico.
2.2. Ecografía abdominal
Puede observarse la glándula pancreática con disminución de la ecogenicidad y engrosamiento
difuso de la misma, en algunas ocasiones con líquido libre peripancreático. Presenta la limitación de la baja
visibilidad secundaria al meteorismo, que impide muy frecuentemente la valoración adecuada de la línea
media. Su utilidad recae en la visualización de colelitiasis, coledocolitiasis, dilatación de la vía biliar intra- o
extrahepática para el diagnóstico etiológico.
2.3. Tomografía computarizada
La TC presenta una sensibilidad y especificidad del 90% para el diagnóstico. No se recomienda su
realización de rutina, salvo ausencia de mejoría clínica en las 48-72 horas desde la presentación de los
síntomas, una vez instaurado tratamiento conservador, ya que los cambios morfológicos no suelen ser
visibles precozmente y podría infraestimar el pronóstico. Debe realizarse también cuando se sospechen
complicaciones locales, como la necrosis pancreática, que del mismo modo solo se hace patente tras las
primeras 48-72 horas del inicio del cuadro.
2.4. Colangiopancreatorresonancia magnética
La CPRM presenta una sensibilidad y especificidad comparables con la TC para el diagnóstico e
identificación de complicaciones, aunque la TC identifica mejor la necrosis. Como ventajas, no implica el
uso de radiación ionizante ni de contraste iodado, y además puede identificar litiasis de hasta 3 mm de
diámetro en el interior de la vía biliar, así como disrupción del Wirsung.
2.5. Ultrasonografía endoscópica
La USE presenta también una sensibilidad y especificidad muy elevada para el diagnóstico de litiasis
de pequeño tamaño, superando incluso las de la CPRM, aunque debe reservarse para casos donde la
sospecha de etiología biliar es alta sin haber sido objetivada mediante otras pruebas de imagen, ya que se
trata de un procedimiento invasivo.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [934]
[58] PANCREATITIS
5. VALORACIÓN DE LA GRAVEDAD
Aunque existen otras clasificaciones, la que mejor define los criterios de gravedad de la pancreatitis
aguda es la clasificación de Atlanta revisada de 2013 (Tabla III). Según esta, se clasifica en:
Pancreatitis aguda leve: autolimitada, se caracteriza por la ausencia de fallo orgánico o
complicaciones locales. Tras 48 horas de ingreso, estos pacientes presentan mejoría
significativa, permitiendo generalmente el inicio precoz de la nutrición enteral.
Tabla III. Clasificación de Atlanta revisada de 2013.
Pancreatitis aguda moderadamente grave: es aquella en la que se presentan complicaciones
locales y/o fallo orgánico durante menos de 48 horas de duración. Entre las complicaciones
locales se incluyen las colecciones de líquido peripancreático y la necrosis pancreática y/o
peripancreática. La necrosis pancreática se define como áreas focales o difusas de parénquima
no viable, mayores de 3 cm de tamaño o del 30% del total del páncreas. El fallo orgánico se
calcula con la escala de Marshall modificada, según la cual es necesaria una puntuación igual o
mayor a 2, considerando la afectación del sistema respiratorio, renal o cardiovascular. Este
puntuación puede resultar complicada de calcular, por lo que algunas guías clínicas
recomiendan seguir utilizando la antigua definición de fallo orgánico de la clasificación de
Atlanta de 1993, que consiste en: sangrado digestivo estimado mayor de 500 ml/24 h, shock
definido como tensión arterial sistólica menor o igual a 90 mm Hg, presión parcial arterial de
oxígeno (PaO2) menor o igual a 60% y creatinina sérica mayor o igual a 2 mg/dL.
Tabla IV. Escala de Marshall modificada.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [935]
[58] PANCREATITIS
Pancreatitis aguda grave: se define por la presencia de fallo orgánico que persiste durante más
de 48 h. Cuando el fallo orgánico es persistente, suelen desarrollarse una o más complicaciones
locales. La mortalidad en estos casos se encuentra entre el 36% y el 50% (Tabla IV).
Tabla IV. Escala de Marshall modificada.
6. PREDICTORES DE GRAVEDAD
Se han utilizado múltiples escalas para predecir la gravedad de la PA. Estas suelen ser engorrosas y
requieren de al menos 48 horas para ser precisas, momento en el cual la gravedad de la enfermedad suele
ser evidente (Ranson, APACHE II, etc.). El sistema BISAP, el más sencillo para calcular, no ha demostrado ser
superior que el resto. Sin embargo, existen hallazgos clínicos en el momento de la valoración inicial que
predicen aún mayor riesgo para el desarrollo de una enfermedad grave; entre ellos se incluyen factores
propios del paciente como la edad, la obesidad y la presencia de comorbilidades, factores clínicos como la
presencia del SRIS, hallazgos de laboratorio (aumento del hematocrito, nitrógeno ureico sanguíneo [BUN] y
creatinina) y radiológicos (derrame pleural, infiltrados pulmonares y colecciones peripancreáticas).
Tabla V. Factores predictores de gravedad en la pancreatitis aguda.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [936]
[58] PANCREATITIS
A pesar de lo anteriormente mencionado, algunos autores aún recomiendan el cálculo de por lo
menos una escala pronóstica en el momento del diagnóstico inicial (Tablas V-IX).
Tabla VI. Sistema BISAP*.
Tabla VII. Criterios de Ranson*.
Tabla VIII. Índice de gravedad radiológica.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [937]
[58] PANCREATITIS
Tabla IX. Escala APACHE II (Acute Phisiology and Chronic Evaluation)*.
7. TRATAMIENTO
El diagnóstico de PA requiere de ingreso hospitalario en todos los casos. Los pilares fundamentales
son las medidas de soporte, en donde se incluye la hidratación del paciente, el control del dolor y la
nutrición. El uso de antibióticos solo está indicado en situaciones especiales.
1. Monitorización
Los pacientes que presenten un SRIS sostenido deben ser valorados para ingreso en una unidad de
vigilancia intensiva o de cuidados intermedios.
2. Hidratación
Actualmente existe controversia acerca de la fluidoterapia intensiva y su papel en la PA. En las
últimas guías clínicas se recomienda la hidratación agresiva, administrando un volumen de 250-500
ml/hora de solución cristaloide, a menos que exista alguna comorbilidad que lo contraindique
(cardiovascular, renal, etc.), manteniéndola en las primeras 12-24 horas. No se ha demostrado su utilidad
más tardíamente. Una vez iniciada, debe valorarse cada 6 horas para su ajuste; el objetivo principal es el
descenso del hematocrito, el BUN y la creatinina. Sin embargo, estas recomendaciones se basan en
estudios en animales y en datos indirectos como que los pacientes con BUN elevado al ingreso o a las 24
horas tienen peor evolución. Recientes estudios multicéntricos prospectivos han encontrado (de modo
independiente) mayores complicaciones locales y sistémicas cuando se administran por encima de 4.100 ml
de fluidos en las primeras 24 horas, por lo que recomiendan seleccionar muy bien a los pacientes y
monitorizarlos estrechamente. Algunos autores recomiendan el uso de solución láctica de Ringer sobre el
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [938]
[58] PANCREATITIS
suero salino fisiológico al 0,9%, ya que estabiliza el pH, y la acidosis contribuye a la activación del
tripsinógeno, lo que hace al acino pancreático más susceptible de daño celular. Otros autores recomiendan
este tipo de fluidoterapia solo en casos de deshidratación o shock, y, cuando estos no estén presentes,
administrar menos volumen (130-150 ml/hora). Una vez que se consigue una presión arterial media de 65
mm Hg y una diuresis de 0,5 ml/kg/hora, se puede suspender la fluidoterapia intensiva y administrar el
volumen necesario para mantener estos valores.
3. Manejo del dolor
Debe administrarse el fármaco necesario para un adecuado control analgésico, ya que este no
dificulta el diagnóstico ni el manejo. Suelen utilizarse el metamizol y/o opiáceos (morfina, meperidina o
hidromorfina). En casos de dolor refractario se puede usar su administración con bomba de infusión o,
incluso, valorar analgesia vía epidural. El control del dolor contribuye al inicio de la nutrición enteral precoz.
4. Nutrición
Actualmente se promueve el inicio de la nutrición enteral de la manera más precoz posible, ya que
esto contribuye a disminuir las complicaciones infecciosas, mientras que el reposo intestinal se asocia a
atrofia vellositaria que predispone a la translocación bacteriana. La nutrición enteral precoz disminuye
también la estancia hospitalaria, la morbilidad y la mortalidad. En casos de PA leve se recomienda la
nutrición por vía oral inmediatamente (se prefiere una dieta baja en grasas) si el paciente no presenta
náuseas ni vómitos (o íleo paralítico) y el dolor abdominal está adecuadamente controlado. Se debe evitar
la nutrición parenteral total si es posible, mucho menos fisiológica y con frecuentes complicaciones
infecciosas por la propia manipulación y acceso venoso, o hidroelectrolíticas. Si no puede utilizarse la vía
oral, se prefiere administrar nutrición enteral a través de una sonda nasoyeyunal para evitar la fase de
activación gástrica, aunque algunas guías clínicas establecen que también puede recurrirse a la vía
nasogástrica, ya que su colocación es más sencilla y suele ser más cómodo para el paciente.
5. Antibioterapia
No se recomienda el uso de antibióticos de manera profiláctica en la PA. Su uso se reserva para los
casos de necrosis infectada, que debe ser sospechada en pacientes con necrosis pancreática o
extrapancreática que empeoran o no mejoran en 7-10 días desde el inicio del cuadro clínico. La fiebre o la
elevación de reactantes de fase aguda deben ser interpretadas cuidadosamente, ya que pueden formar
parte del proceso inflamatorio en ausencia de infección. Si se sospecha necrosis infectada, por lo antes
mencionado, se puede iniciar antibioterapia empírica con carbapenems, quinolonas o metronidazol. Por
otro lado, puede plantearse previo al uso de antibióticos, la realización de una punción-aspiración con
aguja fina guiada por tomografía computarizada (TC-PAAF) para tinción de Gram y cultivo de la muestra; de
esta forma, se puede administrar un agente específico, pero es mejor evitar la manipulación que dicha
técnica conlleva en pacientes con necrosis conocida que asocian datos clínicos (fiebre, mala evolución,
SRIS) y bioquímicos (leucocitosis, elevación de reactantes de fase aguda) compatibles y en los que se
evidencian datos radiológicos altamente sugestivos de infección (gas intranecrosis). Se deben utilizar
antibióticos en caso de infecciones extrapancreáticas, como colangitis, infecciones asociadas al catéter,
bacteriemia, infecciones del tracto urinario o neumonía.
6. Cirugía
En casos de PA leve de origen biliar, en pacientes con colelitiasis, se debe realizar colecistectomía
durante el mismo ingreso para evitar la recurrencia. En los casos de PA necrotizante, se debe diferir la
colecistectomía hasta que disminuya la inflamación y se resuelvan o estabilicen las colecciones. La
presencia de pseudoquistes asintomáticos o necrosis pancreática o extrapancreática no necesitan
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [939]
[58] PANCREATITIS
intervención quirúrgica de entrada. Si existe necrosis infectada que no responde adecuadamente al
tratamiento conservador, el desbridamiento quirúrgico, endoscópico o radiológico debe retrasarse al
menos 4 semanas para permitir la formación de una pared fibrosa alrededor de la misma, la llamada
walled-off necrosis (WON).
7. Técnicas de desbridamiento de la necrosis mínimamente invasivas
Son de elección antes de la cirugía siempre que sea posible. Se pueden realizar por vía radiológica
colocando catéteres de drenaje por vía percutánea, o por vía endoscópica, actualmente la preferida al ser
menos agresiva, permitiendo el drenaje de colecciones a cavidad gástrica mediante la implantación de una
prótesis o, incluso la necrosectomía endoscópica. En todos los casos, se debe individualizar el manejo,
incluso utilizándose estas técnicas de manera combinada.
8. CPRE
Se debe realizar en las primeras 24 horas desde el ingreso cuando se asocia a colangitis. Debe
evitarse de manera precoz en los casos en los que no se sospecha obstrucción biliar, ya que la manipulación
papilar y la administración de contraste pueden empeorar el cuadro. No debe realizarse para el diagnóstico
de litiasis biliar; se prefiere en estos casos la USE o la CPRM.
9. Otros
Se deben tratar situaciones como la hipertrigliceridemia con medidas higiénico-dietéticas, y, si
fuera necesario, con fibratos o gemfibrozilo. En los casos en los que la hipertrigliceridemia sea la causea de
la PA, se puede plantear disminuir sus niveles séricos con plasmaféresis.
8. COMPLICACIONES
1. Colecciones líquidas agudas peripancreáticas
Se forman como consecuencia de la inflamación glandular y suelen ser asintomáticas. Aparecen
generalmente antes de la cuarta semana de la aparición del cuadro, no tienen pared definida y su
contenido es líquido. No suelen precisar tratamiento.
2. Necrosis pancreática y peripancreática
Ya descrita previamente, se define como áreas focales o difusas de parénquima no viable, mayores
de 3 cm de tamaño o del 30% del total del páncreas. Se debe considerar la necrosis infectada ante la
ausencia de mejoría tras el inicio de la sintomatología pasados 7-10 días. Si se sospecha la necrosis
infectada se puede iniciar antibioterapia empírica o, en su defecto, la realización de TC-PAAF y obtener
muestras para su estudio microbiológico. Si no se evidencia mejoría con el tratamiento conservador y no
puede diferirse su drenaje, se puede plantear el desbridamiento radiológico endoscópico y, en segunda
línea, el quirúrgico.
3. Pseudoquiste pancreático
Se trata de colecciones más maduras y evolucionadas, con pared propia definida. Son de contenido
líquido rico en enzimas y jugo pancreático, sin necrosis en su interior. Se desarrolla típicamente a partir de
la cuarta semana desde el inicio del cuadro de PA. Pueden desarrollarse también como consecuencia del
trauma pancreático. Se diagnostican con pruebas de imagen convencional (ecografía, TC, RM). En los casos
donde es asintomático y no se asocia a pseudoaneurisma, se puede plantear el manejo expectante, con
pruebas de imagen cada 3-6 meses. Clásicamente se ha recomendado el drenaje cuando su diámetro es
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [940]
[58] PANCREATITIS
mayor a los 6 cm; actualmente se reserva el drenaje en caso de desarrollar síntomas o si se asocia a
pseudoaneurisma. Se puede plantear el drenaje radiológico o endoscópico y, si estos fallasen, el quirúrgico.
4. Walled-off necrosis (WON)
Colecciones fluidas heterogéneas de contenido líquido y sólido, con una pared bien definida que la
encapsula y que suele formarse también tras la 4ª semana desde el inicio del cuadro clínico. Deben tratarse
cuando se sospeche necrosis infectada como se describe previamente o si se asocia a pseudoaneurisma, y
debe procurarse que se encuentre adecuadamente encapsulada para plantear su drenaje, si la situación del
paciente lo permite. Se prefiere el drenaje radiológico y endoscópico frente al quirúrgico.
5. Pseudoaneurisma
Se desarrollan en alrededor de un 10% de los pacientes con colecciones pancreáticas encapsuladas
por afectación de las adventicias arteriales. Si se rompen, pueden producir hemorragias masivas y fatales,
que pueden manifestarse como una hemorragia digestiva alta en caso de estar en comunicación con el
conducto de Wirsung. Si está presente, se recomienda la embolización previa al desbridamiento de las
colecciones encapsuladas.
6. Ruptura del conducto de Wirsung
Suele producirse por erosión secundaria a necrosis o por yatrogenia tras exploraciones
endoscópicas. Puede formar colecciones pancreáticas o extravasarse y producir ascitis pancreática. Si falla
el tratamiento conservador, puede plantearse la colocación de una prótesis pancreática por vía
endoscópica o el tratamiento quirúrgico.
7. Trombosis venosa portoesplenomesentérica
Se observa hasta en el 50% de los casos de PA necrotizante, y es excepcional ante la ausencia de
necrosis. Puede resolverse espontáneamente tras la resolución de la PA. Se debe plantear la
anticoagulación en casos de alteración de la función hepática o isquemia intestinal.
8. Síndrome compartimental
Secundario a la hipertensión intraabdominal, es una complicación poco común y que confiere mal
pronóstico a la PA. Suele aparecer en pacientes críticos y los síntomas son inespecíficos (malestar general,
astenia, dolor y distensión abdominal, disnea, etc.). Debe sospecharse en pacientes con mal estado general,
distensión abdominal, empeoramiento progresivo respiratorio con aumento de los requerimientos
ventilatorios y oliguria. Las pruebas de imagen aportan poco para el diagnóstico. Es necesaria la medición
de la presión intraabdominal, que debe estar por encima de los 15 mm Hg. Se deben administrar medidas
generales de soporte. Debe valorarse la descompresión abdominal quirúrgica en estos pacientes, en
especial en aquellos que presentan una presión abdominal por encima de 25 mmHg.
9. Hemosuccus pancreaticus
Se trata del sangrado desde el conducto pancreático, y es una causa rara de hemorragia digestiva
alta. Puede producirse por inflamación local con o sin relación con un pseudoquiste pancreático asociada a
la liberación de elastasa. Su tratamiento suele ser la implantación endoscópica de una prótesis pancreática.
II. PANCREATITIS CRÓNICA
1. CONCEPTO
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [941]
[58] PANCREATITIS
La pancreatitis crónica (PC) es un proceso progresivo de necroinflamación, fibrosis y alteraciones
morfológicas de la glándula pancreática que provocan en ella un daño estructural permanente, lo que se
traduce en un deterioro progresivo de sus funciones exocrina y endocrina. Puede dividirse de acuerdo con
su morfología subyacente en PC de conductos grandes o PC de conductos pequeños, con o sin
calcificaciones.
2. ETIOLOGÍA
1. Abuso de alcohol
El abuso de alcohol es la causa más frecuente en los países desarrollados. No obstante, se estima
que debe existir una susceptibilidad individual, ya que solo un 5-10% de los bebedores de riesgo desarrollan
pancreatitis crónica. El tabaco parece acelerar el desarrollo y progresión de la PC, y recientemente se ha
revelado en un estudio multicéntrico con más de 1.000 pacientes como un factor de riesgo independiente y
dosisdependiente de PC; también aumenta el riesgo de desarrollar cáncer de páncreas.
2. Obstrucción ductal
La obstrucción de los ductos pancreáticos secundaria a calcificaciones, tumores o traumatismos
pancreáticos puede producir PC. La obstrucción secundaria a disfunción del esfínter de Oddi también se ha
asociado a PC, aunque no se sabe a ciencia cierta si es un factor causal. También se ha descrito obstrucción
al flujo en la papila minor en el páncreas divisum, aunque no sin controversia.
3. Fármacos
Inhibidores de la enzima convertidora de la angiotensina (IECA), estatinas, azatioprina, esteroides,
lamivudina, hidroclorotiazida, interferón, ácido valproico o anticonceptivos orales.
4. Pancreatitis autoinmune
Cumple criterios radiológicos, serológicos e histológicos característicos. El parámetro analítico con
mayor valor diagnóstico es la elevación sérica de inmunoglobulina 4 (IgG4). De hecho, hay quien considera
esta afectación pancreática dentro del espectro de la enfermedad asociada a IgG4, y no una verdadera
forma de PC. Presenta buena respuesta al tratamiento con esteroides.
5. Pancreatitis hereditaria
Suele presentar historia familiar (transmisión autosómico dominante [AD] con penetrancia del 80%)
y desarrollarse antes de los 20 años; asocia un marcado mayor riesgo de desarrollo de cáncer de páncreas.
6. Pancreatitis tropical
De causa desconocida, es propia de ciertas zonas tropicales, donde supone la causa más frecuente
de PC.
7. Secundaria a procesos sistémicos
Mutaciones en el gen de la fibrosis quística (CFTR), lupus eritematoso sistémico,
hipertrigliceridemia, hipercalcemia, etc.
8. Pancreatitis crónica idiopática
Guarda posible relación con ingesta subrepticia de alcohol, hipersensibilidad a escasa cantidad de
etanol, traumatismos inadvertidos, mutaciones en el gen del tripsinógeno catiónico.
3. TIPOS DE PANCREATITIS CRÓNICA
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [942]
[58] PANCREATITIS
Aunque las características clínicas, funciones y morfológicas suelen ser similares en los pacientes
con PC, ciertos hallazgos clínicos e histológicos permiten establecer esta clasificación:
1. PC calcificante
Típica en consumidores de tabaco y alcohol, y en causas hereditarias. Predomina el dolor
abdominal, los brotes de pancreatitis aguda, la calcificación de la glándula pancreática y la insuficiencia
pancreática endocrina y exocrina.
2. PC obstructiva
Secundaria a obstrucción ductal, causa atrofia de la célula acinar. Genera menos dolor abdominal,
pero puede debutar con síntomas de pancreatitis aguda. Los cambios histológicos y funcionales pueden
revertir si se trata precozmente la causa de la obstrucción ductal.
3. Pancreatitis del surco
Afecta el surco formado entre la cabeza del páncreas, el duodeno y el colédoco. Típica en
alcohólicos, cursa con intenso y recurrente dolor abdominal y pérdida ponderal. La forma superficial se
localiza en el surco y no causa estenosis de los ductos pancreáticos. La forma penetrante se extiende al
parénquima pancreático y afecta al conducto de Santorini y al colédoco, pero no al conducto pancreático
principal. Su tratamiento definitivo es la intervención de Whipple o duodenopancreatectomía cefálica.
4. PC autoinmune
Con sus propias características radiológicas e histológicas, no suelen presentar calcificaciones, con
imagen típica sausage-like, y en algunos casos (pancreatitis autoinmunitaria [PAI] de tipo I, asociada a IgG4),
responden bien a corticoides.
4. CLÍNICA
1. Dolor abdominal
Es el síntoma más frecuente y que más afecta a la calidad de vida de los pacientes. Inicialmente
cursa en brotes y posteriormente se hace continuo con episodios de exacerbación. Típicamente, es un
dolor epigástrico, irradiado a la espalda “en cinturón” y empeora con la ingesta. Puede asociar náuseas o
vómitos. Excepcionalmente, el dolor está ausente. En ocasiones puede desaparecer tras muchos años de
evolución (“páncreas quemado”).
2. Malabsorción
Se produce cuando hay una pérdida de la función exocrina del páncreas superior al 90% o cuando la
capacidad secretora del páncreas exocrino cae por debajo del 10%. La malabsorción grasa es la primera en
manifestarse, mediante esteatorrea. Existe malabsorción de vitaminas liposolubles (ADEK), vitamina B12 y
oligoelementos (Mg, Zn), aunque es raro que estos déficits provoquen manifestaciones clínicas.
3. Diabetes mellitus (DM)
Se denomina de tipo 3c y se debe a la pérdida de la función endocrina del páncreas. Es más
frecuente en formas evolucionadas y calcificantes, y en pacientes con antecedentes familiares de DM-2. La
duodenopancreatetomía cefálica, a diferencia de resecciones pancreáticas más amplias, no aumenta el
riesgo de DM.
4. Complicaciones de la PC
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [943]
[58] PANCREATITIS
Pseudoquistes, fístulas, trombosis esplénica e hipertensión portal secundaria, obstrucción biliar o
duodenal (por compresión debida a fibrosis o pseudoquistes), agudizaciones, ascitis pancreática, derrame
pleural, gastroparesia y cáncer de páncreas.
5. DIAGNÓSTICO
Precisa de la combinación de datos clínicos y analíticos, pruebas de imagen y test funcionales. Los
datos típicos incluyen: dolor abdominal, presencia de calcificaciones pancreáticas, esteatorrea y diabetes.
Sin embargo, esta combinación solo suele verse en fases muy avanzadas de la enfermedad. El diagnóstico
diferencial incluye enfermedades que provocan dolor en el hemiabdomen superior, como el cáncer de
páncreas, el cólico biliar, la enfermedad ulcerosa péptica o el síndrome del intestino irritable.
1. Datos de laboratorio
Amilasa y lipasa: normales o ligeramente elevadas, suelen estar descendidas en fases
avanzadas de la enfermedad. No se correlacionan con la gravedad ni con el pronóstico de la PC.
Hemograma, bioquímica hepática e iones: suelen ser normales. La elevación de enzimas de
colestasis puede indicar compresión del colédoco intrapancreático.
VSG, IgG4, factor reumatoide y autoanticuerpos (ANA y AML): elevados en la PC autoinmune
de tipo 1.
Marcadores nutricionales: pueden presentar niveles disminuidos en casos de malabsorción
secundaria a la maldigestión provocada por la disfunción pancreática exocrina avanzada
(prealbúmina, RBP, Mg, ADEK).
Elastasa fecal: valores disminuidos son indicativos de insuficiencia pancreática exocrina. Sus
niveles se correlacionan con el grado de insuficiencia, si bien pueden hallarse niveles normales
cuando hay insuficiencia pancreática leve-moderada (escasa sensibilidad en formas no graves).
Estudios genéticos: se indican si se sospecha PC hereditaria. Los genes implicados son el CTFR
(regulador de la conductancia transmembrana de la fibrosis quística), SPINK-1 (codifica al
inhibidor de la tripsina) y PRSS-1: mutaciones en este último pueden ser diagnósticas de formas
hereditarias de PC, mientras que el estudio de los otros dos no se realiza de forma rutinaria.
2. Pruebas funcionales
Determinación de grasa en heces de 72 horas (test de Van de Kamer): es el método de
referencia (gold-standard) para el diagnóstico de disfunción exocrina. Valores de más de 7 g
diarios de grasa son diagnósticos de malabsorción grasa.
Estimulación con secretina-colecistocinina (CCK) y análisis posterior de un aspirado de jugo
duodenal (test endoscópico): comprueba la respuesta pancreática exocrina. Es útil en
pacientes con síntomas compatibles y prueba de imagen no diagnóstica, si bien se usa poco por
ser farragoso y precisar la intubación duodenal.
Test de aliento con triglicéridos marcados con carbono-13 radiactivo (C-MTG): tras administrar
C-MTG, se mide el porcentaje de CO2 en aliento marcado con 13C, que es proporcional a la
cantidad de grasa digerida. Alternativa al test de cuantificación fecal de grasa para el
diagnóstico de insuficiencia pancreática exocrina, con sensibilidad (S) y especificidad (E) del
91%, aunque bastante menor en formas leves. Baja disponibilidad.
Test de tolerancia a la glucosa: pretende evaluar la función pancreática endocrina.
3. Pruebas de imagen y endoscópicas
La presencia de calcificaciones, atrofia pancreática o dilatación y arrosariamiento del conducto
pancreático principal (CPP) orientan al diagnóstico de PC.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [944]
[58] PANCREATITIS
Radiografía abdominal: poco sensible. La presencia de calcificaciones en el CP, es muy
específica de PC, siendo más frecuentes en las causas etílica, tropical y autoinmune.
Ecografía abdominal: S del 60-70% y E del 80-90%. Solo detecta estadios muy avanzados de PC.
TC abdominal: similar S y E a la ecografía, ya que solo es útil en estadios avanzados. Es la mejor
técnica de imagen para detectar y localizar calcificaciones pancreáticas.
CPRM: prueba más sensible para detectar fases precoces de PC, incluso formas segmentarias.
La inyección de secretina mejora la sensibilidad de esta prueba.
CPRE: desde el punto de vista diagnóstico, dada su menor agresividad, ha sido desplazada por
la CPRM y la ecoendoscopia. No obstante, conserva gran valor terapéutico en el manejo de las
complicaciones y en casos de duda diagnóstica.
Ultrasonografía endoscópica: la prueba más sensible para el diagnóstico de PC, aunque es muy
dependiente del explorador. La presencia de cuatro o más de los siguientes signos es altamente
sugestiva de PC: calcificaciones, cálculos intraductales, dilatación o irregularidad del CPP, focos
hiperecogénicos periductales o presencia de quistes. Permite realizar diversas maniobras
terapéuticas.
6. TRATAMIENTO
1. Medidas generales
El tratamiento de la PC es sintomático. Deben descartarse complicaciones tratables que causen los
síntomas y evitar o controlar los factores etiológicos. La endoscopia y la cirugía se reservan para
complicaciones o situaciones concretas.
2. Tratamiento del dolor
Se genera dolor por aumento de la presión intrapancreática por obstrucción ductal, por neuropatía
y por cambios hormonales (aumento de CCK, que supone un estímulo para la secreción pancreática). Las
medidas terapéuticas incluyen:
Dieta pobre en grasas: disminuye la estimulación de la secreción pancreática, pero sin embargo
optimiza la absorción del tratamiento enzimático sintético sustitutivo, por lo que no deben
suspenderse por completo a no ser que incrementen el dolor o la esteatorrea.
Analgesia: con paracetamol, antiinflamatorios no esteroideos (AINE) o metamizol y
progresando a opioides débiles como tramadol en caso de mal control. La pregabalina parece
ser el mejor coadyuvante, aunque también pueden utilizarse gabapentina, antidepresivos
tricíclicos o inhibidores selectivos de la recaptación de serotonina. Los opioides mayores, como
la morfina oral, suponen el tercer escalón terapéutico.
Enzimas pancreáticas: pretenden disminuir la secreción pancreática, sustituyendo su función y
disminuyendo así el dolor, aunque tal eficacia analgésica es controvertida; debe hacerse un
intento terapéutico para el control del dolor durante al menos dos meses. Los preparados
enzimáticos deben tener una cubierta no entérica para permitir su liberación duodenal, y ser
administradas junto a un inhibidor de la secreción gástrica.
Antioxidantes: parecen mejorar el control del dolor al reducir el estrés oxidativo que participa
en la patogénesis de la PC. Existen compuestos farmacológicos de uso corriente en algunos
países (no disponible en España).
Octreotida: disminuye la secreción de CCK y, por tanto, la secreción pancreática. Se utiliza
cuando fracasan otros tratamientos, como uso compasivo, a dosis iniciales de 100 μg cada 8
horas subcutáneos, aumentando progresivamente la dosis hasta 200 μg cada 8 horas en caso
de buena respuesta. No obstante, las últimas recomendaciones del Club Español Pancreático,
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [945]
[58] PANCREATITIS
principal grupo de investigación y aspectos clínicos sobre el páncreas en España, no recomienda
su utilización como terapia contra el dolor.
Tratamiento endoscópico: utilizado ante fracasos del tratamiento médico y cuando existe
obstrucción de los conductos pancreáticos, con el fin de disminuir la presión en su interior.
Incluye la esfinterotomía, extracción de litiasis, colocación de endoprótesis y dilatación de
estenosis.
Tratamiento intervencionista: mediante punción guiada por TC o ecoendoscopia, siendo esta
última más segura, eficaz y duradera; permite el bloqueo nervioso o neurólisis del plexo celiaco,
con disminución generalmente temporal del dolor.
Tratamiento quirúrgico: incluye diversas técnicas de desobstrucción de los conductos
pancreáticos y de resección pancreática. Según diversos estudios, los tratamientos de
descompresión quirúrgicos (derivaciones pancreatoentéricas) parecen más eficaces y
duraderos que los endoscópicos, si bien para ser técnicamente factibles precisan de una
dilatación suficiente del conducto de Wirsung. Las técnicas de resección incluyen la
pancreatectomía, la duodenopancreatectomía cefálica, resecciones pancreáticas más amplias,
la esplacniectomía toracoscópica, la colocación de drenajes, etc. La cirugía también permite la
ablación del plexo celiaco.
3. Tratamiento de las complicaciones
Esteatorrea: la absorción grasa mejora con la administración de enzimas pancreáticas, con una
dosis inicial de 500 UI/kg de lipasa antes de cada comida. La respuesta se evalúa determinando
la disminución de la esteatorrea y la ganancia de peso del paciente. La falta de eficacia puede
precisar aumentar la dosis o cambiar de preparado, descartar otras causas de malabsorción, un
sobrecrecimiento bacteriano o reemplazar la grasa de la dieta por triglicéridos de cadena media
(poco factible en la práctica). También pueden precisarse suplementos nutricionales o inhibir la
excesiva acidificación duodena l con IBP.
DM: habitualmente precisa insulina. Dado que se ven afectadas las células α, productoras de
glucagón, existe mayor riesgo de hipoglucemias, por lo que los objetivos de control de glucemia
han de ser más laxos.
Prevención del cáncer de páncreas: su incidencia es aproximadamente del 5% en pacientes con
PC de más de 20 años de evolución. El riesgo es mayor en las PC de inicio temprano: la
hereditaria y la tropical. El tabaquismo se relaciona con el desarrollo de cáncer de páncreas. En
la actualidad, no existe evidencia para justificar el cribado de cáncer de páncreas en los
pacientes con PC. Parece que el empleo de metformina en pacientes con diabetes
pancreatopriva disminuye el riesgo de cáncer.
Pseudoquistes, fístulas, compresiones pancreáticas y otros: pueden drenarse, corregirse,
extirparse, “baipasearse”, etc., mediante técnicas quirúrgicas, endoscópicas o mediante
radiología intervencionista (Figura 1).
4. Tratamiento específico de la PC autoinmune
Corticoterapia: utilizada en los episodios de exacerbación. Se administran 30 mg diarios de
prednisolona durante 2 semanas. Posteriormente, se reduce la dosis de 5 en 5 mg cada 1-2
semanas hasta llegar a los 15 mg. Por último, se rebaja la dosis 2,5-5 mg cada 2-8 semanas
hasta suspender el tratamiento. A veces, se producen recurrencias al finalizar el tratamiento
esteroideo,
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [946]
[58] PANCREATITIS
Azatioprina: se utiliza como tratamiento de mantenimiento a dosis de 2 mg/kg/ día,
debiéndose comprobar previamente una concentración adecuada de tiopurina metiltransferasa
(TPMT).
Figura 1. Abordaje diagnóstico-terapéutico de la pancreatitis crónica.
BIBLIOGRAFÍA
Alarcón C, Bisbal O. Pancreatitis. En: Aguilar F, Bisbal O, Gómez C, et al., editores. Manual de
diagnóstico y terapéutica médica. 7ª ed. Madrid: MSD; 2012. p. 815-32.
Banks PA, Bollen TL, Dervenis C, et al. Classification of acute pancreatitis-2012: revision of the Atlanta
classification and definitions by international consensus. Gut. 2013;62:102-11.
Conwell DL, Lee LS, Yadav D, et al. American Pancreatic Association Practice Guidelines in Chronic
Pancreatitis: evidence-based report on diagnostic guidelines. Pancreas. 2014;43:1143-62.
De-Madaria E, Abad-González Á, Aparicio JR, et al. The Spanish Pancreatic Club´s recommendations for
the diagnosis and treatment of chronic pancreatitis: part 2 (treatment). Pancreatology. 2013;13:18-28.
Easler J, Muddana V, Furlan A, et al. Portosplenomesenteric venous thrombosis in patients with acute
pancreatitis is associated with pancreatic necrosis and usually has a benign course. Clin Gastroenterol
Hepatol. 2014;12(5):854.
El Hamel A, Parc R, Adda G, et al. Bleeding pseudocysts and pseudoaneurysms in chronic pancreatitis.
Br J Surg. 1991;78(9):1059.
Kiviluoto T, Schröder T, Kivilaakso E, Lempinen M. Acute haemorrhage associated with pancreatic
pseudocyst and chronic pancreatitis. Ann Chir Gynaecol. 1984;73(4):214-8.
Lindkvist B, Phillips ME, Domínguez-Muñoz JE. Clinical, anthropometric and laboratory nutritional
markers of pancreatic exocrine insufficiency: prevalence and diagnostic use. Pancreatology.
2015;15:589-97.
Martínez J, Abad-González A, Aparicio JR, et al. The Spanish Pancreatic Club recommendations for the
diagnosis and treatment of chronic pancreatitis: part 1 (diagnosis). Pancreatology. 2013;13:8-17.
Nadkarni NA, Khanna S, Vege SS. Splanchnic venous thrombosis and pancreatitis. Pancreas.
2013;42(6):924.
Tenner S, Baillie J, DeWitt J, Vege SS. American College of Gastroenterology Guideline: management of
acute pancreatitis. Am J Gastroenterol. 2013; 108:1400-15.
Yokoe, Takada T, Mayumi T, et al. Japanese guidelines for the management of acute pancreatitis:
Japanese Guidelines 2015. J Hepatobiliary Pancreat Sci. 2015;22:405-32.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [947]
[59] PATOLOGÍA VASCULAR INTESTINAL
59.Patología vascular intestinal
Laura Santos Santamaría.
Medicina del Aparato Digestivo
Diana Paredes Ruiz.
Medicina Interna
Marina Pérez-Flecha González.
Cirugía General y del Aparato Digestivo
Asesora:
Mercedes Pérez Carreras.
Médica Adjunta de Medicina del Aparato Digestivo
I. INTRODUCCIÓN
La isquemia intestinal define el cuadro clínico-patológico que aparece cuando el flujo sanguíneo del
territorio mesentérico es insuficiente para los requerimientos del intestino. En función del vaso afectado
(arterial o venoso), del área del intestino lesionado (delgado o colon) y del tiempo de instauración (agudo,
subagudo o crónico), la isquemia intestinal puede dividirse en tres entidades clínicas:
Colitis isquémica (CI).
Isquemia mesentérica arterial: aguda (IMAA) y crónica (IMC) o angina intestinal
Isquemia mesentérica venosa: trombosis venosa mesentérica (TVM) aguda y crónica.
Las formas arteriales son más frecuentes que las venosas. Las formas agudas son una urgencia vital,
por lo que es fundamental sospechar estos cuadros en el servicio de urgencias. En la tabla I se exponen las
distintas formas y frecuencias de aparición de la isquemia intestinal.
Tabla I. Tipos de isquemia intestinal y frecuencias de aparición.
II. COLITIS ISQUÉMICA
1. CONCEPTO
La CI representa el trastorno vascular intestinal más frecuente (Tabla I). Aparece cuando el colon se
ve privado del flujo vascular como consecuencia de alteraciones en la circulación sistémica o de cambios
anatómicos o funcionales en los vasos mesentéricos locales. La irrigación del colon viene dada por dos
grandes sistemas vasculares: la arteria mesentérica superior (AMS), que proporciona flujo al colon derecho
y transverso, y la arteria mesentérica inferior (AMI), que irriga el colon izquierdo. Existe además un sistema
de arcadas (arteria marginal de Drumond y arco de Riolano) que garantiza el aporte de flujo sanguíneo en
condiciones de isquemia al colon derecho, ángulo esplénico y unión rectosigmoidea. Aunque la CI puede
afectar a cualquier segmento colónico, incluido el recto, la falta de desarrollo de este sistema de arcadas
vasculares hasta en un tercio de la población hace que estas tres zonas del colon sean las más vulnerables a
la isquemia (Figura 1).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [948]
[59] PATOLOGÍA VASCULAR INTESTINAL
Figura 1. Anatomía vascular del colon.
2. ETIOPATOGENIA
La isquemia del colon puede producirse por dos mecanismos:
Oclusivo. Es consecuencia de la obstrucción mecánica de ramas vasculares que irrigan el colon,
ya sea por una embolia, una trombosis o un traumatismo, como sucede durante la cirugía de
reconstrucción aórtica. La oclusión de pequeños vasos puede deberse a síndromes de
hipercoagulabilidad o a vasculitis.
No oclusivo. La isquemia puede aparecer de forma espontánea (generalmente en pacientes
con factores de riesgo cardiovascular como diabetes, hipertensión arterial o en diálisis) o por
vasoconstricción esplácnica reactiva a situaciones de bajo gasto cardiaco (shock, insuficiencia
cardiaca, hemorragia, deshidratación) o de secuestro vascular hacia órganos vitales (como
puede suceder durante el ejercicio intenso). Se han implicado también en la CI no oclusiva
sustancias como la cocaína, especialmente cuando la isquemia afecta a jóvenes (Tabla II).
Tabla II. Causas de colitis isquémica.
Cuando la isquemia afecta a un vaso de calibre grueso, la lesión intestinal suele ser transmural,
produciéndose una necrosis gangrenosa; cuando tiene su origen en vasos de menor calibre, los cambios
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [949]
[59] PATOLOGÍA VASCULAR INTESTINAL
afectan a la mucosa o se extienden hasta la muscular, dando lugar a un infarto mucoso o mural,
respectivamente, siendo la evolución menos grave.
3. CLÍNICA
La presentación y el patrón evolutivo de la CI varían en función de la causa, extensión de la oclusión
vascular, tiempo de isquemia del colon, segmento afectado y posibles comorbilidades (Tabla III).
Tabla III. Formas clínicas y patrones evolutivos de la colitis isquémica.
Formas leves (no gangrenosas). Suelen manifestarse por la siguiente tríada: 1) dolor abdominal
de inicio brusco, localizado en cuadrante inferior e izquierdo y de intensidad levemoderada; 2)
urgencia para defecar; y 3) emisión de sangre roja-brillante, hematoquecia o diarrea
sanguinolenta, generalmente a las 12-24 horas del inicio del dolor. En ocasiones puede
presentarse como un cuadro de diarrea indolora, con o sin sangre, similar al de una
gastroenteritis infecciosa. Estas formas de CI leve suelen cursar como una colopatía reversible o
una colitis transitoria, con restitución total en el 80% de los casos. El 20% restante evoluciona
hacia la CI segmentaria crónica o colitis persistente, que suele manifestarse con diarrea con
sangre, episodios de fiebre alta con leucocitosis y síntomas de oclusión intestinal, debidos un
patrón ulcerativo crónico de causa isquémica que afecta a un segmento intestinal y que cursa
de forma asintomática, hasta producir una estenosis cicatricial.
Formas graves (gangrenosas). Se asocian a una mortalidad del 50% y son más frecuentes
cuando la isquemia afecta al colon derecho. Cursan con fiebre de más de 38 °C, anorexia,
náuseas, vómitos, distensión abdominal por íleo paralítico, hipotensión y obnubilación. Un 10-
15% de los pacientes presentan signos de peritonitis al inicio del cuadro. La rectorragia es
mucho menos frecuente en estas formas (<30%) y suele acompañarse de anemización
importante. La evolución natural es hacia la perforación con peritonitis, sepsis y fracaso
multiorgánico. La denominación “colitis fulminante” incluye un subgrupo de pacientes con CI
gangrenosa que debuta con síntomas graves (diarrea profusa, fiebre, hipotensión,
obnubilación, deshidratación, hipoalbuminemia, alteraciones hidroelectrolíticas, leucocitosis y
anemia), y que evoluciona rápidamente hacia la perforación y peritonitis. Su mortalidad es muy
elevada si no se actúa de forma urgente.
La presencia de comorbilidades, la afectación aislada del colon derecho, los signos de peritonismo y
la persistencia de síntomas durante más de dos semanas son factores de gravedad y criterios de mal
pronóstico de la CI.
4. DIAGNÓSTICO (FIGURA 2)
Laboratorio. No existen marcadores analíticos específicos de CI. Puede aparecer leucocitosis
moderada, anemia leve (en las CI transitorias) o severa (en las formas gangrenosas), elevación
de enzimas (lactato-deshidrogenasa [LDH], creatina-cinasa [CPK], fosfatasa alcalina), acidosis
metabólica y alteraciones hidroelectrolíticas por deshidratación. La elevación de enzimas, la
hipoalbuminemia y la acidosis metabólica son indicadores de mal pronóstico y sugestivas de
necrosis gangrenosa.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [950]
[59] PATOLOGÍA VASCULAR INTESTINAL
Figura 2. Diagnóstico y tratamiento de la colitis isquémica (CI) basados en la gravedad.
Radiografía simple de abdomen. Inespecífica en las formas de CI leve (asas dilatadas, pérdida
de haustración y engrosamiento parietal en forma de impresiones dactilares [thumbprinting]) y
neumatosis intestinal en las formas de CI grave o neumoperitoneo en casos de perforación.
Colonoscopia. Es la prueba de elección en caso de sospecha de CI, ya que es la única que ofrece
el diagnóstico de certeza. Permite valorar el estado de la mucosa del colon y tomar biopsias,
tanto para la confirmación histológica como para descartar otras causas de colitis (Tabla IV).
Debe realizarse precozmente (antes de las 48 horas), a ser posible sin preparación (las
soluciones de polietilenglicol pueden agravar la isquemia) y con mínima insuflación (para evitar
elevar la presión intraabdominal y empeorar la hipoperfusión sanguínea intestinal). Las lesiones
isquémicas siguen un patrón de distribución típicamente segmentario, con la mucosa rectal
generalmente preservada. Los hallazgos más típicos incluyen eritema, edema, úlceras,
superficiales y profundas, y nódulos violáceos, sugestivos de gangrena. Con frecuencia, estos
cambios afectan a un segmento del colon, que aparece flanqueado por áreas de mucosa
indemne. La colonoscopia está contraindicada en caso de existir peritonismo y deberá
interrumpirse si se observan imágenes de gangrena, por el elevado riesgo de perforación.
Tabla IV. Diagnóstico diferencial de la colitis isquémica.
Tomografía axial computarizada (TC) abdominal (con contraste oral e intravenoso): en
ocasiones es la prueba inicial que establece la sospecha de CI y es de elección cuando la
colonoscopia esté contraindicada. Permite conocer la extensión y la severidad de la CI (según el
engrosamiento de la pared intestinal), identificar signos que predicen el infarto transmural del
colon (líquido libre peritoneal, neumatosis intestinal, gas en el territorio venoso portal) y
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [951]
[59] PATOLOGÍA VASCULAR INTESTINAL
descartar otras etiologías distintas a la CI (Tabla IV). Debe realizarse siempre que se sospeche
una colitis moderada o grave y en aquellos casos con CI aislada del colon derecho en los que el
clínico precise del estudio de los vasos mesentéricos para distinguir la CI de la IMAA.
Resonancia magnética (RM) y angio-RM: útiles en pacientes con riesgo de nefrotoxicidad por el
contraste yodado y cuando se precisen controles radiológicos repetidos para ver la evolución
del cuadro isquémico.
Arteriografía mesentérica: podría plantearse de forma excepcional en aquellos casos en que
persistan dudas de si se trata de una IMAA y no de una CI del colon derecho, a pesar de que el
TC no detecte oclusión vascular.
5. TRATAMIENTO (FIGURA 2)
El manejo de estos pacientes dependerá de la gravedad del episodio. La mayoría de las CI se
resuelven espontáneamente, sin requerir tratamiento específico ni hospitalización (CI transitoria o
colopatía isquémica). Los pacientes con síntomas graves deben ser ingresados para poder actuar en caso de
aparecer complicaciones o una CI irreversible.
5.1. Tratamiento médico
Se aplica a los pacientes sin signos de peritonitis al ingreso:
Medidas generales:
Dieta absoluta (para disminuir los requerimientos intestinales de oxígeno)
Fluidoterapia (hidratación)
Sonda nasogástrica y/o sonda rectal (descompresión intestinal)
Control de factores precipitantes: optimizar la función cardiaca (control de las
situaciones de bajo gasto, retirada de fármacos vasopresores)
Nutrición enteral o parenteral: en situaciones de malnutrición, diarrea profusa, ausencia de
mejoría clínica en 24-72 horas, casos en los que se prevea un tiempo prolongado de
recuperación y en aquellos con elevado riesgo quirúrgico por enfermedades graves asociadas.
Antibioterapia: indicada en casos de CI moderada y severa, en los que se recomienda la
asociación de ceftriaxona (2 g/24 h, iv) y metronidazol (500 mg/8 h, iv) durante 7 días. El uso de
antibióticos de amplio espectro previene los fenómenos de translocación bacteriana y acorta el
tiempo de evolución del cuadro. El empleo de corticoides está contraindicado, salvo en los
casos en que la causa de CI sea una vasculitis, ya que pueden enmascarar la aparición de signos
de peritonismo.
Monitorización de la evolución: incluye exploraciones abdominales, radiografías simples de
abdomen, controles analíticos frecuentes e incluso TC o RM abdominal, para poder conocer el
patrón evolutivo del episodio de CI.
5.2. Tratamiento quirúrgico
Debe considerarse en pacientes con CI severa, especialmente cuando exista sospecha de necrosis
intestinal. Las siguientes situaciones constituyen indicación de cirugía urgente:
Hemorragia masiva
Signos de peritonismo
Colitis fulminante universal, con o sin megacolon tóxico
Deterioro de la situación clínica
Neumatosis intestinal o gas en el territorio portal en las pruebas de imagen Otras indicaciones
en las que se debe considerar la laparotomía son:
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [952]
[59] PATOLOGÍA VASCULAR INTESTINAL
Sepsis persistente y refractaria al tratamiento médico
Aparición de signos sugestivos de infarto intestinal en cualquier momento de la evolución
(marcada leucocitosis, íleo, hipotensión o acidosis metabólica)
CI pancolónica o limitada al colon derecho
Ausencia de respuesta al tratamiento médico tras 2-3 semanas o una colopatía pierde proteínas
Neumoperitoneo visible en las pruebas de imagen
Evidencia endoscópica de gangrena
5.3. Seguimiento endoscópico
Aunque las guías de práctica clínica recomiendan la realización de una colonoscopia de control a las
2-3 semanas desde el inicio del cuadro, probablemente esta no sea imprescindible en las formas leves (no
gangrenosas), dado que la mayoría de ellas curan de forma espontánea. Sin embargo, la persistencia de
una colitis ulcerativa segmentaria sintomática tras 2-3 semanas del episodio agudo obliga a realizar un
seguimiento endoscópico para determinar si la enfermedad se resuelve, evoluciona a colitis persistente o
se complica con una estenosis. En este último caso, y siempre que la estenosis sea sintomática, se
considerará la dilatación endoscópica o quirúrgica.
5.4. Valoración de factores predisponentes
Se debe realizar una evaluación cardiológica durante el ingreso para descartar alteraciones que
predispongan a eventos embólicos. En pacientes menores de 60 años se realizará siempre estudio de
hipercoagulabilidad.
III. ISQUEMIA MESENTÉRICA ARTERIAL AGUDA
1. CONCEPTO
La IMAA se produce por un déficit de aporte sanguíneo en el territorio de la AMS que ocasiona
lesiones en el intestino delgado y el colon derecho. Representa aproximadamente un tercio de todas las
formas de isquemia intestinal (Tabla I) y suele afectar a pacientes de edad avanzada, en la séptima o la
octava década de la vida. Su incidencia ha aumentado en los últimos años debido al progresivo
envejecimiento de la población y a la mayor supervivencia de los enfermos con patología o factores de
riesgo cardiovascular. Se asocia a una elevada mortalidad (60-70%), y solo un diagnóstico y tratamiento
precoces pueden reducir significativamente estas cifras.
2. ETIOPATOGENIA
Las lesiones intestinales aparecen inicialmente en la mucosa y submucosa, en forma de edema y
hemorragia, y pueden evolucionar a formas transmurales, con ulceraciones, necrosis, perforación y
peritonitis en caso de persistir la obstrucción arterial.
La IMAA puede producirse por distintos mecanismos:
Embolia de la AMS (50%): consecuencia de la impactación de un trombo procedente de la
aurícula o ventrículo izquierdos en el punto donde la arteria presenta un estrechamiento
anatómico, en localizaciones variables. Una minoría de los émbolos (15%) obstruye la AMS en
su origen, produciendo una extensa afectación intestinal.
Trombosis de la AMS (10-15%): en personas de edad avanzada con aterosclerosis de las ramas
de la AMS. Se conoce también como “isquemia aguda sobre crónica”.
Isquemia mesentérica no oclusiva (IMNO) (20-30%): deriva del compromiso del flujo sanguíneo
intestinal en ausencia de obstrucción anatómica, como consecuencia de una vasoconstricción
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [953]
[59] PATOLOGÍA VASCULAR INTESTINAL
mesentérica grave. Se produce por la liberación de sustancias vasoactivas en el contexto de un
bajo gasto (infarto agudo de miocardio, arritmias, insuficiencia cardiaca, sepsis, shock), o bien
tras cirugía cardiaca o abdominal mayor. Es una entidad típica de pacientes ingresados en una
unidad de cuidados intensivos. Excepcionalmente, el consumo de tóxicos con actividad
simpática, como la cocaína o los ergotamínicos, puede producir vasoconstricción visceral
aislada y desencadenar IMNO.
Otros mecanismos (5%): embolias de colesterol, vasculitis (panarteritis nodosa, la más
frecuente), traumatismos o lesiones por radiación.
3. CLÍNICA
El síntoma predominante es el dolor abdominal de aparición brusca e intensidad desproporcionada
con respecto a los pocos hallazgos en la exploración abdominal. Al inicio del cuadro suele ser un dolor
cólico localizado en epigastrio o mesogastrio, haciéndose continuo y difuso cuando la viabilidad del
intestino se ve comprometida. Puede aparecer distensión abdominal, vómitos y, con menos frecuencia,
diarrea. En el caso de la IMNO, la clínica puede ser inespecífica (distensión abdominal, hemorragia
digestiva) o estar ausente, y puede pasar desapercibida por la gravedad de las enfermedades subyacentes.
La presencia de signos de irritación peritoneal debe alertar de la evolución de la isquemia intestinal hacia el
infarto y la perforación.
4. DIAGNÓSTICO (FIGURA 3)
El pronóstico del paciente con una IMAA depende de que el clínico establezca el diagnostico de
sospecha antes de que la isquemia evolucione hacia el infarto intestinal, lo que puede suceder a partir de
las 24 horas del inicio del dolor abdominal.
4.1. Sospecha clínica
La aparición de clínica compatible con IMAA en un paciente con factores de riesgo vascular puede
ayudar a establecer el diagnóstico. Además, algunos factores vasculares de riesgo sugieren el mecanismo
causal de la IMAA (Tabla V).
Tabla V. Factores de riesgo de isquemia mesentérica aguda.
Arritmias en la auscultación cardiaca, historia previa o concomitante de embolismo en otras
localizaciones: sugieren embolia arterial mesentérica.
Historia previa de angina intestinal, trombosis en otras localizaciones, dolor de instauración
más larvada: sugieren trombosis arterial mesentérica.
Sepsis, situaciones de bajo gasto cardiaco: sugieren IMNO.
4.2. Laboratorio
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [954]
[59] PATOLOGÍA VASCULAR INTESTINAL
No hay marcadores serológicos específicos. Puede aparecer leucocitosis con desviación izquierda,
elevación de algunas enzimas (CPK, fosfatasa alcalina, LDH, amilasa) y acidosis metabólica. La elevación de
los dímeros D puede apoyar la sospecha de IMAA.
4.3. Radiografía simple de abdomen
Aunque puede ser normal en las primeras horas, es útil para identificar complicaciones tardías:
neumoperitoneo por perforación, engrosamiento y dilatación de asas, o imágenes de impresiones
dactilares en caso de infarto intestinal. Permite también excluir otras causas de dolor abdominal.
Sin embargo, tanto la analítica como la radiografía de abdomen pueden ser inespecíficas,
especialmente al inicio del cuadro. Por ello, ante la sospecha clínica de IMAA debemos realizar una prueba
de imagen.
4.4. Arteriografía mesentérica
Es considerada la prueba de elección en aquellos centros que dispongan de esta técnica y en
función de la experiencia angiográfica del radiólogo vascular. Permite establecer el diagnóstico de IMAA,
distinguir la causa (embolia, trombosis, IMNO) y su localización, perfundir agentes terapéuticos
intraarteriales (vasodilatadores y trombolíticos), y disponer de un mapa vascular para conocer la presencia
o no de colaterales y establecer un plan quirúrgico.
4.5. TC abdominal (con contraste oral e intravenoso)
En la mayoría de los casos, las alteraciones son inespecíficas y tardías. Los hallazgos de mayor
especificidad son: gas intramural (neumatosis), edema de pared y ausencia de realce vascular de la pared
intestinal. En algunos casos permite el diagnóstico etiológico, sin tener que recurrir a la arteriografía. Signos
radiológicos como la neumatosis o presencia de gas en el territorio portal presagian un pronóstico muy
grave.
4.6. Eco-Doppler abdominal
Se trata de una técnica poco invasiva que, en manos expertas, puede ser útil para explorar las
porciones proximales de los vasos esplácnicos mayores (tronco celíaco y origen de la AMS) y para detectar
flujo y signos de daño de las asas intestinales; sin embargo, carece de utilidad para detectar estenosis de
vasos no principales y en el diagnóstico de IMNO.
Debe realizarse el diagnóstico diferencial con otras causas de dolor abdominal agudo como son la
obstrucción intestinal, la perforación de víscera hueca, la pancreatitis aguda y la disección o rotura de un
aneurisma de aorta.
5. TRATAMIENTO (FIGURA 3)
Incluye medidas generales (dirigidas a estabilizar la situación clínica y hemodinámica del paciente) y
medidas específicas para cada una de las formas clínicas de IMAA.
5.1. Tratamiento médico
Medidas generales:
Sonda nasogástrica para descompresión intestinal.
Estabilización hemodinámica, reposición hidroelectrolítica y restauración del equilibrio
ácido-base. Evitar fármacos vasopresores.
Monitorización de la diuresis, tensión arterial y frecuencia cardiaca.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [955]
[59] PATOLOGÍA VASCULAR INTESTINAL
Figura 3. Algoritmo diagnóstico y terapéutico de la isquemia mesentérica arterial aguda.
Antibioterapia de amplio espectro: para prevenir los efectos de la translocación bacteriana
secundaria a la isquemia intestinal. Se recomiendan pautas que cubran gérmenes anaerobios y
gramnegativos como son: ertapenem (1 g/12-24 h, iv); piperacilina-tazobactam (4-0,5 g/6-8 h,
iv); amoxicilina-clavulánico (2-0,2 g/6-8 h, iv); asociación de cefotaxima (1-2 g/8 h, iv, o
ceftriaxona (2 g/24 h, iv) con metronidazol (500 mg/8 h, iv), clindamicina 600 mg/8 h, iv) o
tigeciclina (dosis de carga de 100 mg, iv, seguida de 50 mg/12 h, iv) como alternativa en
alérgicos a betalactámicos.
Anticoagulación: con perfusión intravenosa de heparina sódica durante 7-10 días y
posteriormente cumarínicos durante 3-6 meses (de por vida en caso de hipercoagulabilidad o
fibrilación auricular). Existe controversia sobre el momento de iniciar la anticoagulación,
pudiendo iniciarse la perfusión en el momento del diagnóstico de IMAA, o bien retrasarla hasta
48 horas después de la embolectomía o de la reconstrucción arterial, debido al riesgo de
hemorragia intestinal o intraperitoneal.
5.2. Tratamiento quirúrgico
Debe indicarse cuando exista sospecha de infarto intestinal establecido. El propósito de la cirugía es
evaluar la viabilidad del intestino, resecar el tejido necrótico y repermeabilizar el vaso obstruido, en
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [956]
[59] PATOLOGÍA VASCULAR INTESTINAL
aquellos casos en que sea posible. En ocasiones se precisa una segunda laparotomía de reevaluación
(second look) de la viabilidad del intestino a las 24-48 horas.
5.3. Tratamiento específico
Dependerá de la causa de la IMAA:
Embolia arterial. El tratamiento depende de la localización del émbolo, de que la oclusión sea
total o parcial y de que aparezcan signos de peritonitis. La laparotomía es obligada en caso de
peritonitis, obstrucción completa y embolia mayor, con el fin de repermeabilizar el vaso
(embolectomía) y resecar el tejido necrótico. En casos de obstrucción parcial, embolia menor o
embolia mayor en pacientes con alto riesgo quirúrgico y en ausencia de peritonitis, la infusión
arterial de vasodilatadores (papaverina), trombolíticos (urocinasa) o la anticoagulación
sistémica constituyen una alternativa a la cirugía, especialmente cuando el tiempo de evolución
sea menor de 12 horas. Se recomienda una nueva laparotomía pasadas 12-24 horas para
reevaluar la viabilidad intestinal tras la revascularización, con el fin de evitar resecciones
innecesarias.
Trombosis arterial. En presencia de peritonitis, se realizará laparotomía con el fin de efectuar la
revascularización (trombectomía y derivación mediante injerto vascular o derivación [bypass]) y
resecar el tejido necrótico. En ausencia de peritonitis, o cuando el riesgo quirúrgico sea alto,
puede indicarse la perfusión de agentes trombolíticos o un procedimiento de revascularización
no quirúrgico (angioplastia percutánea con o sin colocación de un stent). En ausencia de signos
de isquemia intestinal avanzada y en pacientes seleccionados, hemodinámicamente estables y
con circulación colateral bien replecionada en el estudio angiográfico, puede mantenerse una
actitud expectante bajo anticoagulación sistémica.
IMNO. Es fundamental la corrección de los factores desencadenantes. Se puede realizar
infusión intraarterial de drogas vasodilatadoras (papaverina) durante la arteriografía. La
aparición de peritonitis constituye indicación de cirugía.
5.4. Tratamiento a largo plazo y medidas preventivas
Superado el cuadro agudo, deberá iniciarse una estrategia de reducción del riesgo cardiovascular
con antiagregantes y estatinas, valorándose de forma individual la anticoagulación a largo plazo.
IV. ISQUEMIA MESENTÉRICA CRÓNICA: ANGINA INTESTINAL
1. CONCEPTO
La IMC o angina intestinal se caracteriza por la aparición de episodios de dolor abdominal agudos y
recurrentes, secundarios a un flujo esplácnico insuficiente durante los períodos en los que se incrementan
las demandas intestinales, típicamente p osprandiales.
Aparece en pacientes con marcada arterioesclerosis y representa menos del 5% de los casos de
isquemia intestinal (Tabla I). La formación de circulación colateral hace que se trate de un proceso
indolente y que no aparezcan síntomas hasta que al menos dos de los tres vasos principales, tronco celiaco
(TC), AMS y AMI presenten una estenosis severa. Aunque la IMC no es una patología urgente, cuando un
paciente con arterioesclerosis y dolor posprandial crónico acude al servicio de urgencias porque el dolor se
ha hecho continuo y de mayor intensidad se debe sospechar una trombosis arterial aguda y tomar
decisiones diagnósticas y terapéuticas urgentes (véase el apartado sobre la IMAA).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [957]
[59] PATOLOGÍA VASCULAR INTESTINAL
2. ETIOPATOGENIA
Las placas de arteriosclerosis en el origen de los segmentos proximales del TC, AMS y AMI son la
causa más frecuente de IMC. Otras menos habituales son vasculitis y otras lesiones vasculares (Tabla VI).
Tabla VI. Etiología de la isquemia mesentérica crónica.
3. CLÍNICA
Se manifiesta en forma de episodios recurrentes de dolor abdominal cólico o sordo, que aparecen
típicamente tras las comidas (especialmente las ricas en grasas), disminuyendo en intensidad a las 2-3
horas de la ingesta. Suele localizarse en epigastrio/mesogastrio, pudiendo irradiarse a la espalda. Con
frecuencia se asocia a pérdida de peso progresiva (el enfermo evita comer por el dolor) y, en ocasiones, a
distensión abdominal, diarrea y malabsorción. En caso de producirse la oclusión del TC, pueden aparecer
náuseas, vómitos y saciedad precoz (por gastroparesia), ulceraciones en la mucosa gástrica de etiología
isquémica (no asociadas a Helicobacter pylori y que no mejoran con inhibidores de la bomba de protones) o
colecistitis alitiásica (por discinesia vesicular). Conforme progresa la oclusión vascular, el dolor abdominal
llega a hacerse continuo y puede acabar en IMAA por formación de un trombo.
4. DIAGNÓSTICO (FIGURA 4)
Requiere un alto índice de sospecha. Debe sustentarse en tres criterios: 1) clínica compatible; 2)
exclusión de otras causas de dolor abdominal típicamente posprandial, como la úlcera péptica, la colelitiasis
o la pancreatitis crónica, y de síndrome constitucional, como el cáncer pancreático; y 3) demostración
angiográfica de obstrucción de al menos dos de los tres vasos esplácnicos principales.
Exploración física: suele ser anodina (abdomen blando y no doloroso o con distensión leve),
pudiendo auscultarse un soplo en epigastrio. En ocasiones llama la atención el estado de
caquexia.
Laboratorio: las pruebas de laboratorio son inespecíficas. Pueden existir datos de malnutrición.
Radiografía simple de abdomen: puede ser normal o presentar calcificaciones vasculares en el
territorio esplácnico.
Endoscopia digestiva alta: el hallazgo de ulceraciones gástricas es inespecífico, pero puede
ayudar al diagnóstico.
Eco-Doppler abdominal: permite identificar estenosis en arterias esplácnicas (el aumento de
velocidad sistólica máxima en la AMS y TC mayor a 275 y 200 cm/s, respectivamente, indica
estenosis de al menos el 70% con alta sensibilidad y especificidad). Aunque es una técnica muy
útil para descartar una IMC (valor predictivo negativo del 99%), algunas limitaciones de la
técnica, como la obesidad, la interferencia por el gas abdominal y la experiencia del operador,
obligan a realizar una arteriografía si el diagnóstico es equívoco.
Angio-TC abdominal y angio-RM: visualizan las estenosis vasculares y permiten determinar
limitaciones anatómicas para una angiografía posterior.
Arteriografía mesentérica: es la prueba diagnóstica de elección.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [958]
[59] PATOLOGÍA VASCULAR INTESTINAL
Considerando que hasta el 18% de los individuos mayores de 65 años de la población general
pueden presentar una estenosis significativa del TC o de la AMS en ausencia de IMC, la detección por
arteriografia, eco-Doppler, angio-TC o angio-RM de una estenosis significativa en al menos dos grandes
vasos esplácnicos, junto con el hallazgo de circulación colateral, no se considera suficiente para establecer
el diagnóstico de IMC en ausencia de manifestaciones clínicas.
5. TRATAMIENTO (FIGURA 4)
Figura 4. Algoritmo diagnóstico y terapéutico en la isquemia mesentérica crónica.
En la mayoría de los casos, el tratamiento no es urgente, salvo que aparezca una trombosis arterial
aguda. Se debe llevar a cabo una terapia definitiva para paliar los síntomas y prevenir la recidiva. La
elección del tipo de tratamiento de revascularización, quirúrgico o por radiología vascular intervencionista,
dependerá de la edad y comorbilidades del paciente, número, severidad y localización de los vasos
ocluidos.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [959]
[59] PATOLOGÍA VASCULAR INTESTINAL
V. ISQUEMIA MESENTÉRICA VENOSA: TROMBOSIS VENOSA
MESENTÉRICA
1. CONCEPTO
La TVM se debe a la obstrucción trombótica de la circulación venosa esplácnica, cuya consecuencia
es un aumento en la presión venosa y un defecto de la perfusión arterial que puede llevar al infarto
intestinal. En la mayoría de los casos afecta a yeyuno e íleon (trombo en la vena mesentérica superior) y
raramente involucra al colon (trombo en la vena mesentérica inferior). Representa el 5-10% de las
enfermedades isquémicas intestinales y la edad media de aparición es entre 30 y 60 años (Tabla I).
2. ETIOPATOGENIA
La obstrucción de la circulación venosa mesentérica por formación de un trombo produce un
aumento de la presión venosa y de las resistencias vasculares, así como una disminución en la presión de
perfusión arterial. Como consecuencia de ello, se produce una lesión intestinal similar a la descrita para la
IMAA, en la que las alteraciones aparecen inicialmente en la mucosa y submucosa, en forma de edema y
hemorragia, pudiendo evolucionar a formas transmurales, con ulceraciones, necrosis, perforación y
peritonitis, en caso de persistir la isquemia. Si la oclusión es rápida y completa, puede no haber tiempo
suficiente para el desarrollo de circulación colateral.
La TVM puede ser primaria, cuando se debe a un trastorno de coagulación, o secundaria a procesos
abdominales locales agudos o crónicos, como la propia hipertensión portal. La TVM es la presentación
clínica inicial del 25-78% de trastornos mieloproliferativos, fundamentalmente de la Policitemia Vera y de la
Trombocitosis Esencial. Menos del 10% de las TVM son idiopáticas (Tabla VII).
Tabla VII. Etiología de la trombosis venosa mesentérica*.
3. CLÍNICA
En función de la localización, extensión y rapidez en la formación del trombo, la TVM se clasifica en
aguda, subaguda y crónica. Las formas agudas se comportan como la IMAA, mientras que las subagudas y
crónicas son frecuentemente silentes debido a la formación de circulación colateral, que evita la necrosis
transmural intestinal.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [960]
[59] PATOLOGÍA VASCULAR INTESTINAL
TVM aguda: cursa con dolor abdominal en epigastrio-mesogastrio, que puede acompañarse de
náuseas, vómitos y diarrea, en ocasiones con sangre. El cuadro clínico es indistinguible del
producido por una IMAA, pudiendo evolucionar al infarto intestinal y muerte si no se sospecha
en el servicio de urgencias. En la tabla VIII se exponen diferencias entre IMAA y TVM aguda.
TVM subaguda: se caracteriza por dolor abdominal inespecífico y difuso de 1-2 semanas de
evolución. Puede evolucionar a la forma aguda o a la crónica, según la localización y extensión
del trombo venoso.
TVM crónica: puede ser indolora y debutar como una hemorragia digestiva por varices esófago-
gástricas e incluso detectarse en una TC abdominal realizado por otro motivo.
Tabla VIII. Características diferenciales entre la trombosis venosa mesentérica aguda e isquemia mesentérica aguda embólica.
4. DIAGNÓSTICO
La ausencia de síntomas, signos y marcadores de laboratorio específicos y la variabilidad en la
evolución de la enfermedad hacen que el diagnóstico de la TVM aguda sea difícil. El amplio uso de la TC
abdominal ha contribuido al diagnóstico de formas asintomáticas.
Laboratorio: en el caso de la TVM aguda puede aparecer leucocitosis, acidosis metabólica,
aumento de enzimas intestinales y de los dímeros D, de forma similar a la IMAA. Pueden existir
alteraciones hematológicas y bioquímicas relacionadas con el mecanismo causal de la
trombosis (trombofilias, cirrosis hepática, etc.).
Radiografía simple de abdomen: puede detectar engrosamiento de la pared intestinal por
congestión y edema de asas intestinales y formación de impresiones dactilares en caso de TVM
aguda e infarto intestinal.
TC abdominal (con contraste oral e intravenoso): es la prueba diagnóstica de elección. Permite
el diagnóstico en más del 90% de los casos, establece la extensión de la trombosis, identifica
causas locales y complicaciones como la gangrena o perforación intestinal y diferencia la forma
aguda de la crónica, al identificar circulación colateral.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [961]
[59] PATOLOGÍA VASCULAR INTESTINAL
Angio-RM: debe considerarse en casos de insuficiencia renal para evitar la toxicidad del
contraste yodado.
Arteriografía mesentérica: permite diferenciar la trombosis venosa de las formas arteriales de
isquemia intestinal y proporciona el acceso para el tratamiento endovascular.
Laparoscopia: es útil para confirmar el diagnóstico de TVM e intervenir de forma urgente a
pacientes con dolor abdominal de origen incierto con sospecha de isquemia intestinal.
En las formas idiopáticas de TVM debe realizarse estudio de trombofilias, incluyendo la
determinación de la mutación V617F en el gen Janus kinase 2 (JAK2), presente en el 95% de los
pacientes con Policitemia Vera y en el 50-60% de los casos de Trombocitosis Esencial y
Mielofibrosis Primaria. Su determinación permite establecer el diagnóstico de síndrome
mieloproliferativo, sin necesidad de realizar una biopsia de médula ósea.
En las formas crónicas de TVM se debe realizar una gastroscopia para detectar varices esófago-
gástricas, y una colangio-RM para evaluar una posible colangiopatía de la hipertensión portal
por desarrollo de colaterales alrededor de los ductos biliares.
5. TRATAMIENTO (FIGURA 5)
Se dirige a evitar la extensión del trombo, prevenir el infarto intestinal y disminuir el riesgo de
recurrencia.
TVM aguda y subaguda: fluidoterapia intravenosa, antibióticos de amplio espectro y
anticoagulación (heparina sódica en perfusión durante 7-14 días para mantener un INR
(international normalized ratio) entre 2 y 2,5 veces por encima de lo normal; posteriormente,
cumarínicos durante al menos 6 meses e indefinidamente en los casos de trombofilia). En caso
de existir sospecha de peritonitis, debe realizarse laparotomía exploradora y resección del
intestino infartado. Si existen áreas de dudosa viabilidad, pueden inyectarse sustancias
vasodilatadoras (papaverina) y realizar una trombectomía. La cirugía de revisión en las 12-48
horas posteriores a la cirugía permite rescatar intestino de dudosa viabilidad en la primera
intervención y puede evitar con ello un síndrome de intestino corto.
TVM crónica: individualizar la decisión de anticoagular 3-6 meses en función de los síntomas,
localización, extensión de la trombosis y riesgo de sangrado (especialmente en pacientes con
cirrosis hepática). En caso de hemorragia por varices esófago-gástricas, debe procederse a su
tratamiento endoscópico (esclerosis, ligadura, inyección de cianoacrilato) o derivación vascular
(comunicación portosistémica intrahepática transyugular, o TIPS [transjugular intrahepatic
portosystemic shunt]).
6. PRONÓSTICO
La mortalidad de la TVM es del 10-20%, llegando hasta el 75% en los casos que cursan con infarto
intestinal. El inicio precoz de la anticoagulación sistémica y el creciente uso de la TC abdominal han
mejorado su pronóstico. La principal causa de muerte en las formas agudas de TVM es la sepsis con fallo
multiorgánico. El pronóstico a largo plazo de las formas crónicas está determinado por la enfermedad
subyacente.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [962]
[59] PATOLOGÍA VASCULAR INTESTINAL
Figura 5. Algoritmo terapéutico de la trombosis venosa mesentérica.
BIBLIOGRAFÍA
Acosta S, Björck M. Modern treatment of acute mesenteric ischaemia. Br J Surg. 2014: 1;101:e100-8.
Brandt LJ, Boley SJ. American Gastroenterological Association medical position statement: guidelines
on intestinal ischemia. Gastroenterol. 2016;118:951-3.
Brandt LJ, Feuerstadt P, Longstreth GF, Boley SJ. American College of Gastroenterology ACG clinical
guideline: epidemiology, risk factors, patterns of presentation, diagnosis, and management of colon
ischemia (CI) Am J Gastroenterol. 2015;110:18-44.
Brandt LJ, Feuerstadt P. Isquemia intestinal. En: Sleisenger y Fordtran. Enfermedades digestivas y
hepáticas. 9ª ed. Madrid: Elsevier; 2010. p. 2027-48.
Kumar S, Sarr MG, Kamath PS. Mesenteric venous thrombosis. N Engl J Med. 2001;345:1683-8.
Montoro Huguet MA, García Egea J, Fabregat G. Isquemia intestinal. En: Montoro Huguet MA, García
Pagán JC, editores. Gastroenterología y hepatología. Problemas comunes en la práctica clínica. 2ª ed.
Madrid: Jarpyo; 2012. p. 383-410.
Montoro Huguet MA, Sánchez Puértolas AB, Sanz P. Colitis isquémica. En: Montoro Huguet MA, García
Pagán JC, editores. Gastroenterología y hepatología. Problemas comunes en la práctica clínica. 2ª ed.
Madrid: Jarpyo; 2012. p. 411-33.
Russell CE, Wadhera RK, Piazza G. Mesenteric venous thrombosis. Circulation. 2015;131:1599-603.
Singal AK, Kamath PS, Tefferi A. Mesenteric venous thrombosis. Mayo Clin Proc. 2013;88:285-94.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [963]
[60] OBSTRUCCIÓN INTESTINAL Y ESTREÑIMIENTO
60.Obstrucción intestinal y estreñimiento
Alejandro Salagre García.
Medicina del Aparato Digestivo
Álvaro Marchán López.
Medicina Interna
Cristina Cobo Vázquez.
Cirugía General y del Aparato Digestivo
Asesores:
Iago Justo Alonso.
Médico Adjunto Cirugía General y del Aparato Digestivo
Constanza Ciriza de los Ríos.
Médica Adjunta Medicina del Aparato Digestivo
I. INTRODUCCIÓN
Una de las funciones del aparato digestivo es la propulsión de los alimentos y la materia fecal a lo
largo del tubo digestivo, y su expulsión a través del ano. Este proceso puede verse dificultado o impedido
por diversas causas; en este capítulo se recogen las alteraciones del tránsito en los segmentos distales del
tubo digestivo, el intestino delgado y el colon. Las causas de esas alteraciones pueden ser secundarias a un
obstáculo mecánico, que puede encontrarse dentro de la luz intestinal, ser intrínseco o extrínseco a la
pared del tubo digestivo, o ser consecuencia de un trastorno funcional primario o secundario, en cualquier
punto de la longitud del intestino.
II. EVALUACIÓN INICIAL Y APROXIMACIÓN DIAGNÓSTICA
La valoración inicial del paciente que refiere enlentecimiento del tránsito intestinal debe estar
dirigida a detectar signos de alarma que sugieran un cuadro orgánico que puede degenerar en patología
urgente o tumoral, y a diferenciarlo del estreñimiento primario o idiopático.
1. Anamnesis
Debe realizarse una historia detallada del cuadro, incluidas frecuencia y características de las
deposiciones (puede emplearse la escala de Bristol, que tiene buena correlación con el tiempo de tránsito
colónico), aparición de productos patológicos en heces, alternancia con diarrea, presencia de dolor
abdominal, fiebre, náuseas o vómitos y empleo de laxantes. Un cuadro instaurado recientemente sugiere
una etiología secundaria a modificaciones dietéticas o farmaco- lógicas, obligando a descartar origen
orgánico. Además, es necesario recoger los siguientes datos: medicación previa y cambios recientes en la
prescripción farmacológica, consumo de tóxicos, antecedentes quirúrgicos, enfermedades sistémicas
(endocrinológicas, neurológicas, neoplasias, trastornos psiquiátricos), antecedentes familiares de cáncer
del tubo digestivo o enfermedad inflamatoria intestinal, anamnesis por aparatos (pérdida de peso, astenia,
anorexia, intolerancia digestiva o de otro cuadro sistémico).
2. Exploración física
La exploración física completa ayuda a detectar enfermedades sistémicas que puedan estar
ocasionando un cuadro de estreñimiento.
Exploración abdominal: debe inspeccionarse el abdomen en busca de cicatrices quirúrgicas
previas, masas y asimetrías. En la auscultación, la ausencia de ruidos o la aparición de ruidos de
tono metálico orientan hacia un cuadro de obstrucción intestinal. La palpación abdominal
puede revelar la presencia de una masa tumoral que origine el cuadro, hernias o eventraciones,
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [964]
[60] OBSTRUCCIÓN INTESTINAL Y ESTREÑIMIENTO
así como la presencia de cicatrices previas. La presencia o ausencia de dolor, su intensidad y el
área de focalización orientan sobre su etiología.
Examen anorrectal: a la inspección pueden encontrarse fístulas, fisuras, hemorroides, rectocele
o prolapsos. El examen digital anorrectal permite la evaluación anatómica y funcional del canal
anal. Entre las alteraciones anatómicas, se pueden palpar hemorroides internas, estenosis,
tumores anorrectales y heces impactadas en la ampolla rectal. Desde el punto de vista
funcional, el tacto rectal proporciona información sobre el tono del canal anal. El tono
esfinteriano puede orientar hacia trastornos neuromusculares (hipotonía) o hacia fisuras
(hipertonía). Colocando la mano en el abdomen del paciente y pidiéndole que realice
contracciones voluntarias del esfínter o maniobras defecadoras, podemos aproximar nuestro
diagnóstico hacia trastornos de hipomotilidad, disfunción del suelo pélvico o disinergia
defecadora.
3. Pruebas complementarias
Deben realizarse de forma urgente en caso de sospecha de obstrucción intestinal, así como en
cuadros de estreñimiento con criterios de alarma, sin que esté clara su sistematización en estreñimiento de
instauración crónica o subaguda sin signos de alarma.
Laboratorio: debe estar orientado a la sospecha clínica. En caso de sospecha de patología
urgente, debe considerarse solicitar hemograma (detección de anemia y signos indirectos de
ferropenia), coagulación (función hepática e imprescindible para candidatos quirúrgicos) y
bioquímica con parámetros de función renal e iones en suero. Si se sospecha sufrimiento
intestinal, deberían incluirse lactato-deshidrogenasa (LDH), amilasa y gasometría venosa para
valoración de pH y exceso de bases. En caso de estreñimiento de instauración larvada puede
valorarse la determinación de hormonas tiroideas.
Radiografía de abdomen: en ausencia de datos de alarma, su utilidad se limita a la detección
de impactación fecal no objetivada en el tacto rectal. Debe realizarse en todo paciente con
datos de alarma, siendo hallazgos que orientan hacia obstrucción intestinal la ausencia de gas
distal, la dilatación de asas con imagen de “pila de monedas” en el intestino delgado, la
presencia de niveles hidroaéreos, o de un parada (stop) intestinal. La radiografía simple de
abdomen permite además evaluar la funcionalidad de la válvula ileocecal, el diagnóstico de
megacolon (síndrome de Ogilvie) o de vólvulo intestinal/colónico (imagen de “grano de café” o
de “pico de loro”, con la punta apuntando hacia el hipocondrio derecho en el vólvulo de sigma,
o hipocondrio derecho en el vólvulo cecal). Permite descartar, aunque con baja sensibilidad, la
presencia de perforación: neumoperitoneo. La radiografía abdominal forma parte del estudio
del tiempo de tránsito colónico con marcadores radioopacos para el estudio reglado del
estreñimiento de origen funcional. Podría tener su aplicación dinámica con contraste baritado
en el estudio del estreñimiento crónico.
Tomografía computarizada (TC) abdominal: está indicada su realización urgente ante el
diagnóstico de sospecha de obstrucción; también es útil en el estudio programado de
estreñimiento con cuadros suboclusivos. Permite valorar la etiología y la localización de la
obstrucción de manera más precisa, además de la presencia de complicaciones como
inflamación, isquemia, perforación o diseminación tumoral.
Otras pruebas como el enema de bario o la colonoscopia pueden ayudar al diagnóstico
etiológico de cuadros de obstrucción o estreñimiento, pero son de menor interés en la
evaluación urgente para determinar la gravedad y el manejo inicial del paciente. Ante un
paciente valorado en urgencias que no presenta datos clínicos o en las pruebas
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [965]
[60] OBSTRUCCIÓN INTESTINAL Y ESTREÑIMIENTO
complementarias de alarma, es razonable iniciar medidas higiénicas contra el estreñimiento,
añadiendo en su caso laxantes, y remitirlo al alta para su seguimiento y estudio ambulatorio.
III. OBSTRUCCIÓN INTESTINAL
La obstrucción intestinal consiste en la detención completa y persistente del contenido intestinal en
algún punto del tubo digestivo debido a una causa mecánica. Puede asociar o no alteraciones vasculares. Es
importante distinguir el nivel de la obstrucción, que puede ser alto (intestino delgado) o bajo (colon o
recto).
1. Obstrucción de intestino delgado
Supone casi el 80% de las causas de obstrucción. La etiología puede ser sospechada en base a los
antecedentes del paciente en muchos casos. En la radiografía de abdomen podrán apreciarse niveles
hidroaéreos a nivel de intestino delgado, con dilatación del mismo con imagen de “pila de monedas”. Este
signo radiológico no es patognomónico de obstrucción, por lo que debe acompañarse de un cuadro clínico
compatible. Sus causas pueden ser:
1.1. Extraluminales
Adherencias: son la causa más frecuente (60%) de obstrucción del intestino delgado. Ocurren
fundamentalmente en pacientes con antecedentes de procedimientos quirúrgicos abdominales
o pélvicas, aunque también existen bridas congénitas. Solo el 2-5% de los pacientes requerirán
adhesiólisis; el resto pueden responder bien al manejo conservador con descompresión
intestinal y reposo digestivo.
Hernias: suponen la tercera causa (10%) de las obstrucciones de intestino delgado, y son las
que más complicaciones pueden producir en caso de incarceración (isquemia, necrosis,
perforación). Ocurren en sitios de debilidad muscular de la pared abdominal, como la región
inguinal, crural o paraestomal. Se puede intentar la reducción de una hernia inguinal
incarcerada dentro de las primeras 4-6 horas siempre que no existan datos sugestivos de
complicación vascular. Posteriormente, el tratamiento siempre será quirúrgico. Las hernias
crurales incarceradas son indicación de cirugía de entrada.
Carcinomatosis peritoneal: suelen estar precedidas de uno o varios episodios de suboclusión,
aunque también ocurren de manera aguda por volvulaciones sobre metástasis. Los tumores
con mayor propensión a causar implantes peritoneales múltiples proceden de colon, ovario,
páncreas y estómago. No existe un consenso sobre la estrategia óptima de tratamiento, que
deberá individualizarse cuidadosamente. Pueden ser útiles el manejo médico con reposo
digestivo y descompresión intestinal asociando fármacos anticolinérgicos y glucocorticoides
que reduzcan las secreciones, los movimientos peristálticos y el edema. La cirugía paliativa
puede beneficiar a algunos pacientes; sin embargo, se asocia con altas tasas de mortalidad y
periodos prolongados de hospitalización.
1.2. Intrínsecas de la pared intestinal
Tumores: suponen el 20% de las obstrucciones de intestino delgado. Puede tratarse de
tumores primarios o de metástasis (p. ej., de melanoma, cáncer de pulmón, mama, cuello
uterino, colon y sarcoma).
Enfermedad inflamatoria intestinal: la enfermedad de Crohn causa hasta el 5% de las
obstrucciones. Puede ser secundaria a la inflamación y el edema agudo de la pared intestinal,
pudiendo, en estos casos, responder a tratamiento médico conservador. También puede
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [966]
[60] OBSTRUCCIÓN INTESTINAL Y ESTREÑIMIENTO
deberse a estenosis fibrosa en cuadros crónicos, y precisar intervención quirúrgica o dilatación
endoscópica.
1.3. Endoluminales
Se incluyen bezoar, cálculo biliar, cuerpo extraño, etc. Se trata de causas más raras, que en caso de
obstrucción intestinal requieren su extracción quirúrgica.
2. Obstrucción de intestino grueso
Suponen el 20-25% de las obstrucciones intestinales. Pueden deberse a una causa mecánica o
funcional. Las imágenes radiológicas mostrarán dilatación y niveles en intestino grueso con ausencia de gas
distal. En el caso de presentar una válvula ileocecal eficaz, no existirá dilatación de intestino delgado, lo que
conlleva mayor riesgo de perforación. En caso contrario, la dilatación se hará extensiva al intestino delgado
y mostrará niveles hidroaéreos en dicho espacio y la mencionada imagen de “pila de monedas”. Requerirán
tratamiento quirúrgico con más frecuencia que las obstrucciones de intestino delgado.
2.1. Obstrucción intestinal mecánica
Se produce por la oclusión de la luz intestinal parcial o completa que conlleva aumento del
peristaltismo.
Intraluminal: se estima que el 2-5% de los pacientes con cáncer colorrectal debutan con una
obstrucción completa. Las neoplasias (incluidos depósitos secundarios) pueden ser causa de
obstrucción de colon hasta en el 30% de los casos. En función de los hallazgos intraoperatorios
y del nivel de obstrucción, puede realizarse una resección de colon segmentaria o total,
asociando o no un estoma, o tan solo la realización de un estoma de derivación. Es causa de
controversia el papel de la prótesis endoluminal en colon izquierdo y sigma, asociando cirugía
precoz.
Extraluminal: los vólvulos causan cerca del 5% de las obstrucciones de colon. Debido a la
anatomía del intestino grueso, pueden ocurrir a nivel de sigma o de ciego. El primero es mucho
más frecuente (casi el 75%) y se asocia a dolicosigma, a pacientes ancianos con estreñimiento
crónico y neurofármacos que alteran la motilidad intestinal. La radiología muestra una imagen
característica en forma de “grano de café”, de “pico de loro” o de “tubo doblado” con ausencia
de gas distal. Tras la estabilización médica, el tratamiento se basa en la descompresión
endoscópica salvo en el caso de que exista necrosis de la mucosa intestinal. Muchos de los
pacientes requerirán una intervención quirúrgica programada tras un estudio completo, dado
que hasta el 50% pueden llegar a recidivar. El vólvulo cecal es mucho más infrecuente, ocurre
en pacientes más jóvenes y, aunque se ha descrito la devolvulación endoscópica, requieren
frecuentemente intervención quirúrgica urgente para su resolución. Su etiopatogenia suele
conllevar una causa intrínseca, como pólipos o tumores, que hacen de eje de la rotación, pero
se han descrito casos de hiperlaxitud cecal. La colonoscopia está indicada cuando el
tratamiento no ha sido quirúrgico.
2.2. Obstrucción intestinal adinámica o pseudoobstrucción
Está causada por la ausencia de contractilidad intestinal de causa primaria o secundaria con
alteración neuropática o miopática.
Pseudoobstrucción colónica aguda (síndrome de Ogilvie): se produce una obstrucción de colon
derecho y ciego en ausencia de causa obstructiva. Ocurre hasta en el 95% de los casos en
relación con una patología subyacente desencadenante (traumatismos, infecciones, patología
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [967]
[60] OBSTRUCCIÓN INTESTINAL Y ESTREÑIMIENTO
cardiaca o abdominal, enfermedades neurológicas, alteraciones metabólicas o tratamiento con
opioides). Una imagen radiológica con dilatación cecal mayor de 9 cm presenta un riesgo mayor
de perforación y obliga a valorar intervención quirúrgica. El tratamiento en ausencia de
dilatación cecal importante y de dolor intenso incluye medidas generales como la suspensión
de fármacos precipitantes si es posible, la corrección de las patologías subyacentes o trastornos
hidroelectrolíticos, así como la adecuada hidratación, reposo digestivo y descompresión
mediante sonda nasogástrica y/o rectal si la dilatación alcanza el colon sigmoideo. Se debe
descartar la infección por Clostridium difficile.
La neostigmina está indicada en el caso de pacientes que no respondan al tratamiento
conservador en 24-48 horas y diámetro cecal de mayor de 9 cm. Es de elección salvo
contraindicaciones (hipersensibilidad, bradicardia, infarto agudo de miocardio reciente,
peritonitis, obstrucción mecánica del tránsito gastrointestinal o genitourinario). Se administran
1,5-2 mg en inyección intravenosa lenta durante cinco minutos, con monitorización continua de
los signos vitales y electrocardiograma durante 30 minutos y la evaluación clínica continua
durante 15 a 30 minutos. Debe disponerse de atropina en la cabecera de la cama para tratar la
posible bradicardia asociada. También puede utilizarse eritromicina en dosis de 250 mg en 250
ml de suero salino fisiológico intravenoso cada 8 horas durante tres días, aunque su acción
procinética se localiza más en el tracto digestivo alto. La prucaloprida es un agonista altamente
selectivo del receptor de serotonina 5-HT4 y que, por tanto, actúa estimulando la motilidad
intestinal, sobre todo a nivel del colon. Debido a esta gran afinidad por el receptor 5-HT4, no
presenta los efectos cardiovasculares de otros procinéticos como la cisaprida. La
descompresión endoscópica debe considerarse en casos de alto riesgo de perforación con
fracaso de las medidas conservadoras y del tratamiento farmacológico. No está exenta de
complicaciones, y la dilatación puede recidivar hasta en un 40% de los casos. La cecostomía
percutánea o cirugía se reserva para los casos en que no funcionen las medidas anteriores, o en
caso de sospecha de perforación o peritonitis.
Pseudoobstrucción colónica crónica: se caracteriza por estreñimiento de tránsito lento con o
sin dilatación del colon. El megacolon puede ser congénito (enfermedad de Hirschsprung,
ausencia de células ganglionares de los plexos submucoso de Miessner y mientérico de
Auerbach) o adquirido. El megacolon adquirido aparece como complicación de las múltiples
causas de estreñimiento existentes, y es la causa más frecuente la infección por Trypanosoma
cruzi (enfermedad de Chagas).
IV. ESTREÑIMIENTO
1. Concepto
El estreñimiento es la dolencia digestiva más frecuente en la población general, con una
prevalencia estimada del 15%. No se trata, por tanto, de una enfermedad en sí misma, sino que es un
síntoma que puede acompañar a diversas situaciones clínicas o patológicas. Se caracteriza por la dificultad
o la escasa frecuencia en relación con las deposiciones, a menudo acompañadas por un esfuerzo excesivo
durante la defecación o por sensación de evacuación incompleta. En la mayoría de los casos no tiene una
causa orgánica subyacente y es considerado un trastorno funcional intestinal. Frecuentemente lleva
implícito un importante componente subjetivo basado en la impresión del propio paciente. De acuerdo con
los criterios de Roma III, el estreñimiento funcional requiere la presencia durante los tres meses anteriores
de dos o más de las siguientes circunstancias:
Esfuerzo defecatorio (≥ 25% deposiciones)
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [968]
[60] OBSTRUCCIÓN INTESTINAL Y ESTREÑIMIENTO
Deposiciones duras o caprinas (≥ 25% deposiciones)
Sensación de evacuación incompleta (≥ 25% deposiciones)
Obstrucción defecatoria (≥ 25% deposiciones)
Maniobras manuales para la defecación (≥ 25% deposiciones)
Menos de tres deposiciones por semana
Los síntomas deben haber comenzado un mínimo de 6 meses antes del diagnóstico, no existir
diarrea si no es tras la toma de laxantes y no cumplirse criterios de síndrome del intestino irritable.
2. Etiología y clasificación
2.1. Causas secundarias de estreñimiento
El hábito dietético incorrecto es junto con el uso de fármacos la causa más frecuente. El resto de las
causas más frecuentes se recogen en la tabla I. Cabe mencionar de manera independiente el síndrome del
intestino irritable o colon espástico, pues constituye una de las causas más frecuentes. Cursa con dolor y
distensión abdominal, y alteración del ritmo deposicional en forma de estreñimiento, de diarrea o de
ambos.
Tabla I. Causas secundarias de estreñimiento.
2.2. Estreñimiento crónico funcional idiopático
Cuando se han descartado causas secundarias y criterios de alarma. Como ya se ha comentado,
viene definido por los criterios de Roma III. Según los mecanismos fisiopatológicos implicados, el
estreñimiento funcional se clasifica en tres grupos:
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [969]
[60] OBSTRUCCIÓN INTESTINAL Y ESTREÑIMIENTO
Trastornos de la defecación (defecación disinérgica, disfunción del suelo pélvico)
Estreñimiento con transito colónico lento
Estreñimiento con tránsito colónico normal
El diagnóstico de estos subtipos fisiopatológicos precisa de técnicas diagnósticas funcionales
complementarias. En pacientes que presentan un tránsito normal, es posible que el estrés psicosocial
juegue un papel importante; no obstante, en ocasiones presentan alteraciones de la motilidad colónica y de
la sensibilidad rectal que podrían estar implicadas.
Tras descartar datos de alarma y causas secundarias (estreñimiento crónico idiopático), se debe
iniciar un tratamiento médico basado en la educación, cambio de hábitos dietéticos y administración de
fibra soluble (15-25 g/día). En la gran mayoría de los casos (90%), el estreñimiento mejora con hidratación
abundante, ejercicio y fibra en la dieta. Debe realizarse una reevaluación a las 4-6 semanas y, si no hay
mejoría, escalonar el tratamiento utilizando laxantes osmóticos, como el polietilenglicol (PEG). En caso de
refractariedad, se ha de continuar el estudio.
3. Evaluación secundaria
Está indicada en los pacientes con estreñimiento crónico idiopático que no responden al manejo
conservador con educación, dieta, fibra y laxantes. Permite clasificar el cuadro en relación con el tránsito
colónico y la presencia o no de trastornos de la defecación. A pesar de todo, solo en un 30% de los
pacientes con estreñimiento grave se llega a identificar una causa.
Medición del tránsito del colon/tiempo de tránsito colónico: sencilla, reproducible, inocua y
fiable. El tiempo de tránsito colónico debe de ser menor a 3 días. Se realiza una radiografía de
abdomen tras 5 días de la ingesta de material radioopaco. La retención de más del 20% de los
marcadores indica un tránsito prolongado. Puede mostrar retraso del tránsito colónico
proximal o una progresión normal con detención en el rectosigma (retraso del vaciamiento). Se
puede realizar el mismo estudio con radioisótopos o con la cápsula smart pill (de mayor costo).
Estudios de motilidad: la manometría anorrectal permite registrar las presiones a lo largo del
canal anal y del recto, valorar la sensibilidad rectal e identificar la integridad de los reflejos
rectoanales (reflejo inhibidor anorrectal, reflejo de Valsalva, etc.). Dicho registro puede hacerse
tanto en reposo como durante la maniobra defecatoria espontánea o provocada tras la
distensión de un balón intrarrectal. Esta prueba es útil para el diagnóstico de la disinergia
esfinteriana, junto con el test de expulsión del balón. La defecografía y la resonancia magnética
pelviana dinámica valoran la dinámica de defecación y permiten identificar anomalías como
rectocele, prolapso o invaginación. La resonancia tiene la ventaja de no utilizar radiación
ionizante y ser menos dependiente del operador que la videofluoroscopia.
Perfil psicológico: trastornos de la alimentación, estrés psicosocial.
4. Tratamiento
Educación sanitaria y dietética: asegurar una ingesta hídrica adecuada (de al menos 2 l/día) y
realizar ejercicio físico moderado. Se recomienda aumentar el consumo diario de fibra
(verduras, fruta, pan integral, salvado de trigo) a 20-25 g/día, preferiblemente soluble, para
contribuir a aumentar el volumen fecal. En un ensayo clínico, la ingesta de tres ciruelas secas
diarias (100 g/día) se ha mostrado más eficaz que los laxantes. Este tratamiento debe
instaurarse de forma gradual y sus efectos beneficiosos pueden tardar hasta un mes en
aparecer. El aumento de la fibra en la dieta puede ocasionar flatulencia y dolor abdominal, lo
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [970]
[60] OBSTRUCCIÓN INTESTINAL Y ESTREÑIMIENTO
que hace que algunos pacientes no lo toleren, especialmente en los que se sospeche síndrome
del intestino irritable con estreñimiento.
Fármacos laxantes: se utilizan especialmente en los estreñimientos con tránsito lento.
Inicialmente se debe comenzar con laxantes formadores de masa o fibra (grado de evidencia B)
durante 4-6 semanas para evaluar su eficacia. Si no es suficiente o el paciente no lo tolera, se
suelen utilizar laxantes osmóticos (grado de evidencia A). Este tipo de laxantes contienen iones
no absorbibles o moléculas que retienen agua en la luz intestinal. Los más utilizados son el PEG,
la lactulosa y las sales de magnesio. El PEG es más eficaz que la lactulosa en el control de los
síntomas y produce menos efectos secundarios, por lo que debe considerarse como fármaco de
primera elección; además tiene buen perfil de seguridad. Los laxantes estimulantes, entre los
que se incluyen los difenilmetanos (fenolftaleína, bisacodilo, picosulfato sódico) y las
antraquinonas (sen, cáscara sagrada, Aloe vera) son útiles para el tratamiento del
estreñimiento (grado de evidencia B), aunque menos eficaces para controlar el dolor y la
distensión abdominal. Su perfil de seguridad es menor que el de los laxantes osmóticos, por lo
que se deben utilizar con mucha precaución en ancianos y en pacientes con insuficiencia
cardiaca, o con tratamiento diurético o con corticoides. Los lubricantes o emolientes no
cuentan con una evidencia consistente para ser recomendados en el estreñimiento crónico,
aunque pueden ser útiles en combinación. Las soluciones evacuantes a base de PEG suelen
utilizarse de manera excepcional, en cuadros severos resistentes a las medidas habituales.
Enemas (salinos, de fosfato o aceite mineral) y supositorios (glicerina, bisacodilo): son
esenciales en el tratamiento del estreñimiento complicado con impactación fecal, en algunos
casos de defecación obstructiva y como complemento de otras medidas terapéuticas en casos
de estreñimiento grave con importante alteración del tránsito intestinal para conseguir la
limpieza del colon distal.
Otros fármacos: se ha de valorar su utilización si las medidas anteriores no son satisfactorias,
individualizando en cada caso el balance riesgo/beneficio. La prucaloprida (1-2 mg/ día) es un
procinético útil en el tratamiento del estreñimiento funcional que no responde a otras medidas
farmacológicas. Aunque en menor medida, también mejora el dolor y la distensión con un buen
perfil de seguridad. Se puede utilizar en pacientes ancianos con estreñimiento refractario. La
linaclotida (145 μg/día) es un secretagogo que está aceptado para el síndrome del intestino
irritable con estreñimiento y en el estreñimiento crónico idiopático (no en España). Es el
fármaco de elección en pacientes con dolor o hinchazón abdominal y estreñimiento cuando la
fibra dietética y los laxantes han fracasado. Los resultados y el riesgo-beneficio a largo plazo
están aún por determinar. Otro secretagogo es la lubiprostona (no comercializada en España).
La inyección de toxina botulínica en el músculo puborrectal puede ser útil en algunos casos de
defecación disinérgica.
Biorregulación (biofeedback): se basa en la reeducación de los músculos estriados del suelo
pélvico y del esfínter anal externo. Tiene su principal utilidad en los trastornos de la defecación
(disinergia defecatoria o anismo) y en la disfunción del suelo pélvico. Cuando únicamente existe
disfunción del suelo de la pelvis, estas técnicas consiguen hasta un 80% de resultados positivos.
La principal limitación de la biorregulación es la reducida accesibilidad, así como la falta de
estandarización en cuanto a su uso. Sus resultados pueden evaluarse mediante manometría
anorrectal.
Terapia psicológica: algunos tipos de tratamientos psicológicos, como la terapia
cognitivoconductual y la hipnosis, pueden ser útiles para controlar el dolor abdominal, además
de disminuir el nivel de estrés en pacientes con dolor abdominal y estreñimiento crónico.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [971]
[60] OBSTRUCCIÓN INTESTINAL Y ESTREÑIMIENTO
Tratamiento quirúrgico: es excepcional y debe ser la última opción para el estreñimiento
refractario que no responde a otras medidas. La técnica utilizada debe individualizarse en
función del perfil del paciente, e iniciarse por procedimientos menos agresivos, en pacientes
con vida social activa (neuromodulación de raíces sacras), pasando por procedimientos
intermedios (colectomía segmentaria, colectomía total, proctocolectomía total) hasta técnicas
paliativas (estomas, apendicecostomía para irrigación intestinal).
V. ESTREÑIMIENTO EN EL ANCIANO E IMPACTACIÓN FECAL
El estreñimiento constituye un problema muy frecuente en la población anciana, ya que además de
menoscabar en gran medida su calidad de vida ejerce un notable impacto en los costes sanitarios. La edad
avanzada, el sexo femenino, el sedentarismo y el bajo nivel cultural y económico se asocian con frecuencia
al estreñimiento. La escasa ingesta calórica e hídrica también ha sido asociada al estreñimiento en
pacientes ancianos. Hay que tener en cuenta que los pacientes en tratamiento con opioides pueden ver
enlentecido su tránsito intestinal (no se recomiendan los aportes de fibra en estos casos).
La impactación fecal es frecuente en los pacientes con una movilidad reducida y con alteración de
la percepción sensorial. Cuando se sospecha, ha de realizarse un tacto rectal; si con este no se evidencian
heces en la ampolla rectal, se ha de realizar una radiografía de abdomen para descartar impactación en el
rectosigma. Cuando sea posible, se ha de intentar la desimpactación manual, seguida de un enema con
aceite mineral (evitando inicialmente los enemas de fosfato de sodio, que pueden causar alteraciones
hidroelectrolíticas). Una vez realizada la desimpactación, se han de eliminar en la medida de lo posible los
fármacos que favorezcan el estreñimiento e instaurar una dieta baja en residuos, con el objetivo de que el
paciente efectúe al menos una deposición cada 48 horas. A tal fin, pueden utilizarse laxantes osmóticos
(PEG, lactulosa o sorbitol). Si aun con ellos no se consigue una evacuación en 48 horas, pueden utilizarse
supositorios de bisacodilo o enemas (Figura 1, Tabla II).
Figura 1. Aproximación diagnóstica.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [972]
[60] OBSTRUCCIÓN INTESTINAL Y ESTREÑIMIENTO
Tabla II. Principales fármacos en el estreñimiento.
BIBLIOGRAFÍA
American Gastroenterology Association. American Gastroenterological Association Medical Position
Statement on Constipation. Gastroenterology. 2013;144(1):211-7.
Azpiroz Vidaur, F. Trastornos de la motilidad intestinal. En: Rozman C, editor. Farreras-Rozman
Medicina Interna. 17ª ed. Barcelona: Elsevier España; 2012.
Bordeianou L, Dante D. Epidemiology, clinical features, and diagnosis of mechanical small bowell
obstruction in adults. UpToDate. [Internet]. Disponible en:
http://www.uptodate.com/contents/epidemiology-clinicalfeatures- and-diagnosis-of-mechanical-small-
bowel-obstruction-in-adults?
Dante D, Bordeianou L. Overview of mechanichal colorectal obstruction. UpToDate. [Internet].
Disponible en: http://www.uptodate.com/contents/overview-of-mechanical-colorectal-obstruction.
Evers BM. Intestino delgado. En: Townsend CM, Beauchamp RD, Evers BM, Mattox KL, editores.
Tratado de Cirugía. 18ª ed. St. Louis: WB Saunders; 2008. cap. 48.
Ford AC, Suares NC. Effect of laxatives and pharmacological therapies in chronic idiopathic
constipation: systematic review and meta-analysis. Gut. 2011; 60(2):209-18.
Fry DR. Colon y recto. En: Townsend CM, Beauchamp RD, Evers BM, Mattox KL, editores. Sabiston
Tratado de Cirugía. 18ª ed. Barcelona: Elsevier España; 2009. p. 1348-430.
Lembo A. Constipation. En: Feldman M, Friedman LS, J. Brandt L, editores. Gastrointestinal and liver
disease. 10ª ed. Elsevier Saunders; 2016. p. 270-96.
Parrilla Paricio P, Targarona Soler EM. Abdomen agudo. En: Rozman C, editor. Farreras-Rozman
Medicina Interna. 17ª ed. Barcelona: Elsevier España; 2012.
Shah BJ, Rughwani N, Rose S. In the clinic: constipation. Ann Intern Med. 2015;162(7):ITC1.
Stern T, Davis AM. Evaluation and treatment of patients with constipation. JAMA. 2016;315(2):192-3.
Townsend, CM. Sabiston Tratado de Cirugía. 18ª ed. Barcelona: Elsevier España; 2009. p. 1278-330.
Wald A. Management of chronic constipation in adults. [Consultado 15 de febrero de 2016]. Disponible
en: http://www.uptodate.com/contents/management-of-chronic-constipation-in-adults.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [973]
[61] ALTERACIONES DEL SISTEMÁTICO Y SEDIMENTO DE ORINA. APROXIMACIÓN DIAGNÓSTICA A LA HEMATURIA Y LA
PROTEINURIA
61.Alteraciones del sistemático y sedimento de orina.
Aproximación diagnóstica a la hematuria y la
proteinuria
Candela Moliz Cordón
Nefrología
Borja de Miguel Campo
Medicina Interna
Asesor:
Manuel Praga Terente
Jefe de Servicio de Nefrología
I. ANÁLISIS DE ORINA
La orina es el producto orgánico formado mediante la filtración y procesamiento del plasma
sanguíneo en los riñones, con posterior eliminación a través del sistema excretor urinario.
1. Características macroscópicas
1.1. Volumen
Oscila entre 600 y 2.000 ml/día (gracias a la gran capacidad del riñón de ajustar el volumen urinario
para mantener un volumen circulatorio adecuado). Múltiples factores condicionan esta variabilidad como la
ingesta de líquidos, la temperatura, la sudoración y las pérdidas de líquidos (vómitos, diarrea), entre otros.
Una disminución del volumen urinario por debajo de 400 ml en 24 horas se denomina oliguria; si es inferior
a 100-50 ml, lo consideraremos anuria.
1.2. Color
Normalmente es de color amarillo claro, pero este puede estar afectado por el grado de
concentración, pigmentos, colorantes, sangre y pH. Es más clara cuanto más diluida, y más oscura cuanto
más concentrada. El color ámbar de la orina se debe a pigmentos (principalmente urocromo). La coloración
roja puede deberse a hematuria (1 ml de sangre puede teñir de rojo 1 litro de orina), porfirinas, ingesta de
remolacha y fármacos. La presencia de bilirrubina conjugada (coluria) da lugar al típico “color coca-cola”
que también puede observarse en las hematurias macroscópicas de origen glomerular (la forma de
diferenciarlas se explica en el apartado de hematuria). Otras alteraciones menos frecuentes son orina
blanca (piuria, cristales de fosfato, propofol), verde (azul de metileno, amitriptilina, propofol, infección por
Pseudomonas), negra (hemoglobinuria, alcaptonuria, ocronosis), naranja (eritromicina, rifampicina,
nitrofurantoína) o marrón oscuro (levodopa, melanosarcoma). Es importante preguntarse qué curso
presenta la alteración en la coloración: persistente o intermitente (porfiria), en reposo o con el ejercicio.
1.3. Transparencia
La orina normal es limpia y transparente. Si no se conserva en condiciones adecuadas, se deterioran
sus características (entre ellas, su transparencia). Se puede enturbiar por la precipitación de cristales o
sales, presencia de microorganismos, células sanguíneas o epiteliales del tracto urinario, proteínas o lípidos.
La formación de espuma al agitarla traduce la existencia de sales biliares o proteínas.
2. Características bioquímicas y microscópicas: tira de orina
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [974]
[61] ALTERACIONES DEL SISTEMÁTICO Y SEDIMENTO DE ORINA. APROXIMACIÓN DIAGNÓSTICA A LA HEMATURIA Y LA
PROTEINURIA
2.1. Densidad y osmolaridad
El valor de la densidad puede oscilar entre 1.003 y 1.025 g/l, y el valor de la osmolaridad, entre 50 y
1.400 mOsm/kg (su interpretación debe relacionarse con el contexto clínico del paciente). La medición de la
densidad y la osmolaridad es importante para estudiar la capacidad del riñón de concentrar o diluir la orina
y conocer el estado de la volemia (densidad y osmolaridad elevadas en un contexto de deshidratación
siempre que el riñón preserve la capacidad de concentrar la orina). En condiciones normales se
correlacionan, pero la densidad aumenta en relación con la osmolaridad por la presencia de sustancias de
alto peso molecular (proteínas o azúcares) y disminuye por la urea.
2.2. pH
Su rango oscila entre 4,5 y 8. La tendencia habitual es mantener un pH ligeramente ácido, de entre
5 y 6. Un pH alcalino (> 7) sugiere infección por gérmenes que desdoblan la urea (Proteus mirabilis,
Klebsiella), dieta vegetariana, diuréticos, vómitos, fármacos (protectores gástricos), tratamientos para
alcalinizar la orina (acetazolamida, bicarbonato), consumo de bebidas isotónicas. Un pH ácido (< 5) se
asocia a acidosis metabólica, aumento del catabolismo (fiebre, desnutrición), ingesta de carne y algunas
enfermedades metabólicas (fenilcetonuria, alcaptonuria).
2.3. Glucosa
La presencia de glucosa en orina depende de la glucemia y de la función renal. La glucosa se filtra
en el glomérulo, pero se absorbe totalmente en el túbulo proximal siempre y cuando los niveles de glucosa
en sangre sean menores de 180 mg/dL; a partir de dicha cantidad se sobrepasa la capacidad de absorción
del túbulo proximal y aparece glucosuria. Otras causas pueden ser enfermedades que afecten al túbulo
proximal, de forma aislada como en la glucosuria renal (en que cursa con glucemia normal) o como parte
del síndrome de Fanconi (en donde se presenta hipofosfatemia, hipouricemia, aminoaciduria y acidosis
tubular).
2.4. Nitritos
Algunas bacterias (enterobacterias) transforman los nitratos a nitritos y su presencia debe hacernos
sospechar una infección urinaria. Hay que tener en cuenta que no todas las bacterias producen nitritos (los
grampositivos, Pseudomonas spp, Neisseria spp, y las micobacterias no los producen), se necesitan 4 horas
para la conversión (en casos de incontinencia no se producirán nitritos) y la presencia de ácido ascórbico
evita la transformación. Por ello, la negatividad de nitritos en orina no descarta la infección si hay síntomas
que sugieran su presencia.
2.5. Esterasa leucocitaria
Su detección orienta a la presencia de piuria, que puede estar en relación con la infección, pero
también con otros procesos (nefritis intersticial, tuberculosis renal o litiasis).
2.6. Cuerpos cetónicos
Son resultado del metabolismo incompleto de los lípidos. Aparecen en un contexto de ayuno
prolongado, cetoacidosis diabética y alcohólica. Su presencia siempre es patológica.
2.7. Pigmentos y sales biliares
La bilirrubina conjugada en el hígado es hidrosoluble, y es esta fracción la que podemos cuantificar
en la orina (debe ser inferior a 0,2 mg/dL en condiciones normales). El urobilinógeno es resultado del
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [975]
[61] ALTERACIONES DEL SISTEMÁTICO Y SEDIMENTO DE ORINA. APROXIMACIÓN DIAGNÓSTICA A LA HEMATURIA Y LA
PROTEINURIA
metabolismo bacteriano de la bilirrubina en el intestino, y que, en un pequeño porcentaje, se absorbe y
retorna a la circulación portal, excretándose posteriormente en la orina. En la orina podemos encontrar:
Bilirrubina y urobilinógeno: aumento de producción de bilirrubina o enfermedad hepática no
obstructiva.
Solo bilirrubina: enfermedades obstructivas hepáticas y cuando se administra tratamiento
antibiótico que erradica la flora intestinal.
Solo urobilinógeno: hemólisis.
2.8. Proteínas
Ver más adelante Apartado “Proteinuria”.
2.9. Pigmentos hemáticos
Ver más adelante Apartado “Hematuria”.
3. Sedimento urinario
Es la fracción sólida tras la centrifugación de la orina y está compuesta por células, cristales y
microorganismos. El procedimiento para su obtención consiste en recoger una muestra de orina
(preferiblemente la primera del día); a continuación se centrifuga, se desecha el sobrenadante y se toma
una muestra del precipitado o sedimento para su visualización directa al microscopio. Permite detectar
anomalías no valoradas mediante tiras reactivas. En pacientes sanos es escaso, aunque podemos encontrar
cristales, bacterias, células epiteliales y cilindros.
3.1. Hematíes
Normalmente en los análisis de urgencia no se detallan sus alteraciones morfológicas. Ver más
adelante Apartado “Hematuria”.
3.2. Leucocitos
Suelen ser polimorfonucleares. Su presencia es normal de forma aislada, y la contaminación de la
muestra es una causa frecuente. Denominamos piuria la presencia de más de 10 leucocitos por campo;
traduce inflamación del aparato urinario que puede estar o no en relación con causas infecciosas. La piuria
sin bacteriuria (piuria estéril) obliga a descartar litiasis, neoplasia genitourinaria, nefropatía intersticial
inmunoalérgica, glomerulonefritis rápidamente progresiva (GNRP), poliquistosis renal e infecciones por
Mycobacterium tuberculosis, Mycoplasma, Ureaplasma, micosis, Chlamydia spp o virus de la varicela-
zóster.
3.3. Eosinófilos
No se realiza de rutina por requerir tinciones especiales. Se relaciona con nefritis intersticial aguda,
ateroembolismo de colesterol y GNRP, entre otros.
3.4. Células epiteliales
Su presencia es normal, aunque en número aumentado pueden sugerir necrosis tubular aguda o
pielonefritis.
3.5. Cilindros
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [976]
[61] ALTERACIONES DEL SISTEMÁTICO Y SEDIMENTO DE ORINA. APROXIMACIÓN DIAGNÓSTICA A LA HEMATURIA Y LA
PROTEINURIA
Habitualmente no se suelen registrar en los análisis de urgencia. Representan los moldes de las
nefronas y pueden ser de distintos tipos:
Hialinos: agregados mucoproteicos semitransparentes e incoloros (compuestos por proteína de
Tamm-Horsfall). En condiciones normales pueden aparecer entre 0-5 por campo. Se pueden
asociar a orinas concentradas, tratamiento con diuréticos o fracaso renal agudo.
Granulosos: compuestos por células epiteliales degeneradas, leucocitos, eritrocitos, albúmina y
grasas. Representan degradación celular. Pueden aparecer en personas sanas y en numerosas
patologías (necrosis tubular, pielonefritis, glomerulonefritis [GN] y nefritis intersticial aguda).
Céreos: de color amarillo cristalino. Traducen un túbulo dilatado y atrófico, propio de fases
finales de la insuficiencia renal.
Leucocitarios: presentes en pielonefritis aguda, GN y nefritis intersticial.
Hemáticos: localizan a nivel glomerular la fuente de la hematuria. Se ven en GN y vasculitis.
Epiteliales: asociados a necrosis tubular aguda y GN.
Grasos: asociados al síndrome nefrótico, GN y poliquistosis renal.
Pigmentarios: hiperbilirrubinemia y hemoglobinuria, entre otros.
3.6. Cristales
La orina normal contiene cristales y componentes amorfos que precipitan al enfriarse. Con pH ácido
precipitan los cristales de ácido úrico, oxalato cálcico, urato sódico y uratos amorfos. Con pH alcalino, los
cristales de urato amónico, trifosfatos, fosfato cálcico, fosfatos amorfos y carbonato cálcico. A veces
pueden detectarse cristales de cistina (cistinuria), estruvita (asociada a gérmenes que desdoblan urea como
Proteus o Klebsiella), tirosina (necrosis hepática masiva) o leucina. Es importante valorar si su presencia se
asocia a insuficiencia renal aguda, como en el caso de fracaso renal agudo por aciclovir o en el síndrome de
lisis tumoral (ver Capítulo 80. “Urgencias oncológicas”).
3.7. Bacterias
Su presencia puede deberse a contaminación de la muestra o a infección, por lo que es importante
valorar el contexto clínico.
II. APROXIMACIÓN DIAGNÓSTICA DE LA HEMATURIA Y LA
PROTEINURIA
1. Hematuria
1.1. Concepto
Se considera normal la presencia de 1-3 hematíes por campo de gran aumento en el microscopio,
aunque la persistencia de esta discreta hematuria a lo largo del tiempo puede ser patológica. Por encima de
esta cantidad se considera siempre como patológica y debe ser estudiada. La hematuria macroscópica, que
altera el color normal de la orina, se traduce en el sedimento en un incontable número de hematíes por
campo.
Es importante conocer las características de la hematuria y las del paciente, ya que, por ejemplo, la
hematuria transitoria es común en adultos jóvenes en relación con ejercicio intenso, fiebre, infección o
traumatismo y no tiene significación patológica. En adultos de más de 50 años puede ser secundaria a un
proceso tumoral (vejiga, riñón, próstata).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [977]
[61] ALTERACIONES DEL SISTEMÁTICO Y SEDIMENTO DE ORINA. APROXIMACIÓN DIAGNÓSTICA A LA HEMATURIA Y LA
PROTEINURIA
1.2. Etiología
Según su origen, las causas de hematuria se dividen en renales o extrarrenales; y, dentro de las
causas renales, en glomerulares y extraglomerulares (Tabla I).
Tabla I. Causas de hematuria.
1.3. Evaluación del paciente con hematuria (Figura 1)
Historia clínica: la anamnesis y la exploración física deben ser exhaustivas. Se debe visualizar la
orina del paciente, comprobar la existencia de hematuria y describirla. La presencia de sangre
roja brillante, acompañada o no de coágulos, sugiere una causa urológica (ver Capítulo 15.
“Patología urológica más frecuente”), mientras que la presencia de orinas oscuras (color “coca-
cola”) sugiere un origen glomerular. Deben tenerse en cuenta las manifestaciones clínicas
acompañantes de la hematuria (Tabla II).
Tira reactiva: método semicuantitativo utilizado como test inicial que detecta el grupo hemo
(hemoglobina intrahematíe, hemoglobina libre, mioglobina). Es positivo cuando existen más de
5 hematíes por campo de gran aumento y siempre debe comprobarse con estudio con
microscopio óptico (sedimento urinario). Los falsos positivos (tira reactiva positiva con
microscopia óptica sin hematuria) son debidos a la presencia de hemoglobina libre (hemólisis
intravascular), mioglobina (rabdomiólisis) o pH muy alcalino. Los falsos negativos son
excepcionales (grandes cantidades de vitamina C en la orina).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [978]
[61] ALTERACIONES DEL SISTEMÁTICO Y SEDIMENTO DE ORINA. APROXIMACIÓN DIAGNÓSTICA A LA HEMATURIA Y LA
PROTEINURIA
Figura 1. Algoritmo diagnóstico de la hematuria.
Tabla II. Situaciones más frecuentes asociadas a hematuria.
Confirmar la hematuria: para ello es imprescindible la visualización del sedimento con
microscopia óptica, ya que permite diferenciar la hematuria de otras causas que cambien la
coloración de la orina: si el color rojo se observa en el sedimento, ello indica la presencia de
hematíes; por el contrario, si se encuentra en el sobrenadante, puede deberse a presencia de
hemoglobina o mioglobina libre (tira positiva para grupo hemo), porfirinas, fármacos u otros
colorantes (tira negativa para grupo hemo). El sedimento permite, además, cuantificar el
número de hematíes y conocer sus características (dismórficos y en qué porcentaje), así como
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [979]
[61] ALTERACIONES DEL SISTEMÁTICO Y SEDIMENTO DE ORINA. APROXIMACIÓN DIAGNÓSTICA A LA HEMATURIA Y LA
PROTEINURIA
analizar el resto de los elementos de la orina. Existen datos que orientan a patología
glomerular: cilindros hemáticos, hematíes dismórficos y/o proteinuria > 500 mg/día.
Pruebas complementarias: además de confirmar la hematuria mediante la tira y el sedimento,
debe realizarse un hemograma, un estudio de coagulación, una determinación de la creatinina
plasmática y una prueba de imagen (generalmente una ecografía). Los estudios posteriores
estarán orientados según la sospecha inicial (Tabla III).
Si a pesar de un estudio completo no se llega a un diagnóstico etiológico, es importante un
seguimiento periódico con la realización de análisis de orina y citologías cada 6 meses, y ecografía,
cistoscopia y/o urografía intravenosa anuales (según los factores de riesgo del paciente), durante 3 años.
Tabla III. Causas y estudio de hematuria.
2. Proteinuria
2.1. Concepto
En condiciones normales el riñón filtra proteínas de bajo peso molecular (microglobulina β2,
cadenas ligeras) y una pequeña cantidad de macromoléculas como la albúmina. La mayor parte se
reabsorbe en el túbulo contorneado proximal, lo que da lugar a una excreción de proteínas en orina menor
a 150 mg/día, de los cuales 10-15 mg son albúmina, siendo la mayoría proteínas secretadas por el túbulo
(Tamm-Horsfall). Por tanto, una proteinuria mayor de 150 mg/día debe de ser estudiada. La albuminuria
debe ser menor a 30 mg/día. Es importante recordar que los análisis de orina de urgencia solo miden
albúmina y pueden no detectar proteinuria de otros tipos. La proteinuria no es un dato aislado; siempre
debe estudiarse e interpretarse en el contexto general del paciente.
2.2. Clasificación
Según el origen de la proteinuria:
Proteinuria glomerular: es consecuencia del aumento de la permeabilidad de la pared
capilar glomerular, que permite la filtración de proteínas de alto peso molecular. Puede
ser selectiva (entre el 80% y el 90% corresponde a albúmina) o no selectiva (albúmina,
transferrina, IgG). Si aparece en una sola determinación, suele asociarse a ejercicio,
estrés, fiebre, convulsiones o gestación (proteinuria transitoria); o en jóvenes, asociada
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [980]
[61] ALTERACIONES DEL SISTEMÁTICO Y SEDIMENTO DE ORINA. APROXIMACIÓN DIAGNÓSTICA A LA HEMATURIA Y LA
PROTEINURIA
a la deambulación (proteinuria ortostática), que estaría ausente en la primera micción.
En caso de que sea persistente, suele responder a patología glomerular o sistémica.
Proteinuria tubular: producida por una alteración en la reabsorción tubular de
proteínas de bajo peso molecular, fisiológicamente filtradas. Aparece en enfermedades
tubulointersticiales o glomerulopatías avanzadas con daño en este compartimento.
Proteinuria por sobrecarga: tiene lugar en patologías con aumento de producción de
proteínas de bajo peso molecular que sobrecargan los mecanismos de reabsorción o
bien que son tóxicas para el epitelio tubular (cadenas ligeras del mieloma múltiple,
mioglobina en la rabdomiólisis, hemoglobina libre en la hemólisis intravascular). No se
detecta en la tira de orina.
Según sus características cuantitativas:
Normoalbuminuria y microalbuminuria: la primera se define como la excreción
urinaria de albúmina inferior a 30 mg/día o mg/g de creatinina; y para la segunda, de
entre 30 y 300 mg/día o mg/g de creatinina. No se detecta en tiras de orina habituales,
por lo que son necesarios métodos de detección más sensibles. La cuantía de la
albuminuria, incluso en los rangos de normo- y microalbuminuria, ha demostrado ser
un factor de riesgo cardiovascular y constituir un riesgo de progresión de la nefropatía
diabética.
Proteinuria no nefrótica: valores de proteinuria inferiores a 3,5 g/24 h.
Proteinuria en rango nefrótico: valores por encima de 3,5 g/24 h. Puede estar
integrada en un síndrome nefrótico completo (hipoalbuminemia, hiperlipidemia,
edema) o presentarse como una manifestación aislada sin síndrome nefrótico. Esto
ocurre característicamente en las enfermedades causadas por hiperfiltración
glomerular (glomerulopatía de la obesidad, reducción de masa renal, reflujo
vesicoureteral, cicatrización de procesos glomerulares previos).
2.3. Aproximación diagnóstica
La proteinuria se mide por métodos semicuantitativos, cuantitativos y cualitativos. La integración
de todos ellos ayuda al diagnóstico.
Semicuantitativos (tira reactiva): método de cribado (screening). Solo mide albúmina y no
detecta albuminuria inferior a 300 mg/día. Mide la cantidad de proteínas en cruces de 1 a 4
(Tabla IV). Puede haber falsos positivos (uso de radiocontrastes yodados, orinas muy alcalinas,
hematuria, orinas concentradas o presencia de antisépticos) y falsos negativos (orinas muy
diluidas).
Tabla IV. Equivalencia de cruces en tira de orina y proteinuria estimada.
Cuantitativos: son los métodos más seguros. Deben realizarse en todo paciente con proteinuria
persistente. El método por excelencia es la determinación de la proteinuria en orina de 24
horas, que detecta todos los tipos de proteínas y los cuantifica en g/24 h. Dada la incomodidad
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [981]
[61] ALTERACIONES DEL SISTEMÁTICO Y SEDIMENTO DE ORINA. APROXIMACIÓN DIAGNÓSTICA A LA HEMATURIA Y LA
PROTEINURIA
de recogida de la muestra, se puede estimar en una muestra aislada mediante el cociente
proteínas/creatinina en orina (expresado en g/g) o el cociente albúmina/ creatinina en orina
(expresado en mg/g). Su resultado es equivalente a los gramos de proteínas en 24 horas (así, un
cociente albúmina/creatinina de 4.500 mg/g equivaldría a 4,5 g de proteinuria en 24 horas).
Cualitativos: permiten identificar el tipo de proteína. Son la electroforesis, la
inmunoelectroforesis y la inmunofijación. En la figura 2 se muestra el algoritmo diagnóstico de
la proteinuria.
Figura 2. Algoritmo diagnóstico de la proteinuria.
III. GRANDES SÍNDROMES GLOMERULARES
1. Síndrome nefrítico
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [982]
[61] ALTERACIONES DEL SISTEMÁTICO Y SEDIMENTO DE ORINA. APROXIMACIÓN DIAGNÓSTICA A LA HEMATURIA Y LA
PROTEINURIA
El síndrome nefrítico se caracteriza por una inflamación glomerular que se traduce clínicamente en
hematuria (micro- o macroscópica), proteinuria (generalmente no nefrótica), oliguria, edemas, hipertensión
arterial y deterioro de la función renal. La presentación clásica ocurre en la GN posestreptocócica,
especialmente en niños. Las causas más frecuentes son GN primarias y secundarias. Siempre requiere
valoración por el servicio de nefrología.
2. Síndrome nefrótico
2.1. Concepto
El síndrome nefrótico (SNo) es la consecuencia clínica de un daño glomerular que ocasiona el
aumento de la permeabilidad de la pared capilar glomerular a las proteínas. Todas las alteraciones que se
describen son consecuencia directa de la pr oteinuria masiva. Se caracteriza por la péntada formada por
proteinuria (> 3,5 g/24 h), hipoalbuminemia (< 3 g/ dL), lipiduria, hiperlipidemias y edemas. Puede aparecer
proteinuria nefrótica aislada en pacientes con hiperfiltración o en la diabetes mellitus. Es la indicación más
frecuente de biopsia en España.
2.2. Etiología
En la infancia, la causa más frecuente es la nefropatía de cambios mínimos; en adultos, la causa
más frecuente es la nefropatía diabética (no suele biopsiarse). En nuestro medio, la causa más frecuente de
síndrome nefrótico biopsiada es la GN membranosa, seguida de la nefropatía de cambios mínimos y la
glomeruloesclerosis focal y segmentaria (Tabla VI).
Tabla V. Manejo agudo del síndrome nefrótico.
2.3. Clínica
Consecuencia directa de la proteinuria:
Edemas: es el signo clínico más llamativo y el motivo principal de consulta. Es un
edema blando, con fóvea, que predomina en zonas declives y periorbitaria. Puede
progresar hasta desarrollar edema genital, ascitis, derrame pleural o anasarca. La
aparición de derrame pleural es infrecuente a menos que coexistan insuficiencia
cardiaca o insuficiencia renal.
Hiperlipidemia: en un 80-85% de los pacientes se trata de hipercolesterolemia. Para
que aparezca hipertrigliceridemia debe existir una albúmina de menos de 2 g/dL. Puede
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [983]
[61] ALTERACIONES DEL SISTEMÁTICO Y SEDIMENTO DE ORINA. APROXIMACIÓN DIAGNÓSTICA A LA HEMATURIA Y LA
PROTEINURIA
aumentar el riesgo de eventos cardiovasculares y acelerar la progresión del daño
glomerular. Aparece lipiduria con cilindros grasos en la orina.
Trombosis: estado de hipercoagulabilidad con mayor incidencia de fenómenos
tromboembólicos (sobre todo en territorio venoso). Son más frecuentes en los
primeros meses del SNo. Suele afectar a territorio venoso profundo de miembros
inferiores o a vena renal, e incluso puede ocasionar tromboembolismo pulmonar. La
mayor incidencia se da en la GN membranosa. Son criterios de alto riesgo para la
aparición de trombosis el sufrir un SNo de largo tiempo de evolución, albuminemia de 2
g/dL, proteinuria > 10 g/24 h, antitrombina < 75% del valor normal y la hipovolemia.
Infecciones: especialmente en niños y por gérmenes encapsulados. Se debe
fundamentalmente a pérdida de factores del complemento e IgG. Es típica la peritonitis
bacteriana por S. pneumoniae e infecciones de partes blandas muy edematosas
(típicamente, S. pyogenes y gramnegativos, y más raras las causadas por estafilococos).
Anemia: por déficit de transferrina y de eritropoyetina (en ocasiones también concurre
un fracaso renal asociado).
Fracaso renal: no forma parte del síndrome como tal, pero puede aparecer asociado a él. Suele
ser secundario a hipovolemia (más frecuente en ancianos y secundario al tratamiento diurético
intensivo). El tratamiento con antiinflamatorios no esteroideos (AINE), inhibidores de la enzima
conversora de la angiotensina (IECA) o antagonistas de los receptores de la angiotensina II
(ARA-II) así como el edema del intersticio renal y la trombosis renal bilateral son también causa
de fracaso renal asociado a síndrome nefrótico.
2.4. Aproximación diagnóstica
Anamnesis y exploración física.
Pruebas complementarias: en todo paciente con sospecha de SNo es importante solicitar una
analítica completa con hemograma, bioquímica, coagulación y gases venosos; sedimento
urinario con iones, orina de 24 horas y ecografía renal. De forma orientada en función de la
historia clínica: serología de virus de la hepatitis C (VHC), virus de la hepatitis B (VHB), virus de
la inmunodeficiencia humana (VIH) y sífilis; crioglobulinas; inmunoelectroforesis en sangre y
orina (sospecha de amiloidosis y mieloma múltiple); anticuerpos antinucleares (ANA), anti-DNA
y complemento (sospecha de lupus); y antiestreptolisina O (ASLO) en caso de sospecha de GN
posestreptocócica.
Biopsia renal: se realiza en todos los adultos con SNo. Hay que recordar que no toda
proteinuria en rango nefrótico es un síndrome nefrótico y que, por tanto, no habrá que biopsiar
a los pacientes con proteinuria nefrótica por diabetes o hiperfiltración.
2.5. Tratamiento
Tratamiento general del SNo
Proteinuria: el objetivo principal es disminuirla. En sujetos con función renal normal, se
recomienda seguir dietas normoproteicas (0,8-1 g/kg/día), ya que la hiperproteica no
mejora la hipoalbuminemia y produce hiperfiltración y daño glomerular, mientras que
la hipoproteica favorece la desnutrición. El tratamiento farmacológico consiste en el
bloqueo del eje renina-angiotensina-aldosterona para reducir la presión
intraglomerular y, con ello, la proteinuria. Para ello se pueden usar IECA o ARA II. Es
importante hacer hincapié en que el inicio de tratamiento con IECA y/o ARA II se debe
realizar una vez que el paciente haya pasado la fase aguda del cuadro, debido a que
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [984]
[61] ALTERACIONES DEL SISTEMÁTICO Y SEDIMENTO DE ORINA. APROXIMACIÓN DIAGNÓSTICA A LA HEMATURIA Y LA
PROTEINURIA
durante esta existe una hipovolemia intravascular relativa, por lo que estos fármacos
pueden ocasionar un deterioro agudo de la función renal. La acción antiproteinúrica de
estos agentes se puede potenciar con la dieta baja en sal y con la asociación de
diuréticos (tiazidas, antialdosterónicos). Tras el inicio del tratamiento con IECA/ARA II,
es necesario un control analítico estricto, vigilando la función renal y las cifras de
potasio.
Edemas: en primer lugar es necesario realizar una dieta pobre en sal (2-4 g/24 h); solo
se indicará restricción hídrica si existiera anasarca o hiponatremia. En situación de
anasarca también se recomienda reposo en decúbito o en sedestación, e incluso
medias elásticas hasta la raíz del muslo, acompañado de medidas antitrombosis. El
tratamiento farmacológico se basa en diuréticos de asa, a dosis doble o tripe de lo
habitual (furosemida 40-200 mg/24 h). Se pueden asociar tiazidas (hidroclorotiazida
12,5-50 mg/día) y/o diuréticos ahorradores de potasio (espironolactona 25-400 mg/
día) si la respuesta diurética es insuficiente, monitorizando estrechamente la función
renal, hiponatremia o hiperpotasemia. En casos refractarios, que se acompañen de
hipoalbuminemia severa (< 2 g/dL), se puede intentar tratamiento con albúmina (un
vial de 50 ml albúmina al 20%, que contiene 10 g de albúmina, con furosemida
intravenosa asociada). En aquellos casos en que los que el mal manejo del volumen o el
fracaso renal supongan un riesgo vital, puede ser necesaria la hemodiálisis.
Hiperlipidemia: medidas dietéticas; en ocasiones se precisan estatinas para conseguir
una LDL por debajo de 100 mg/dL (reduciendo la dosis a la mitad para evitar efectos
secundarios). Con la corrección del Sno se moderará la dislipidemia.
Trombosis: no se recomienda profilaxis de forma primaria; sin embargo, se debe iniciar
en pacientes de alto riesgo trombótico (véase más arriba, dentro del Apartado 2.3.
“Clínica”, el párrafo relativo a trombosis) o cuando la hipoalbuminemia sea inferior a 2
g/dL. Es necesario iniciar tratamiento anticoagulante en pacientes que sufran un
fenómeno tromboembólico, con heparina sódica o de bajo peso molecular
inicialmente, para después continuar con anticoagulantes orales durante al menos 3
meses y/o hasta que la albúmina sea superior a 2,5 mg/dL.
Infecciones: cualquier infección debe tratarse de forma precoz y agresiva. En adultos
no hay evidencia sobre el uso de medidas profilácticas de forma general. Se debe
indicar vacunación antineumocócica en pacientes de alto riesgo.
Tratamiento específico: se debe realizar un diagnóstico exacto de la causa del SNo (Tabla VI)
para hacer un tratamiento dirigido. De aquí la importancia de la biopsia renal en muchos casos.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [985]
[61] ALTERACIONES DEL SISTEMÁTICO Y SEDIMENTO DE ORINA. APROXIMACIÓN DIAGNÓSTICA A LA HEMATURIA Y LA
PROTEINURIA
Tabla VI. Etiología del síndrome nefrótico.
BIBLIOGRAFÍA
Althof S, Kindler J, Heintz R. El sedimento urinario: atlas, técnica de estudio y valoración. 6.ª ed.
Madrid: Médica Panamericana; 2003.
Baños-Laredo ME, Núñez-Álvarez CA, Cabiedes J. Análisis de sedimento urinario. Reumatol Clin.
2010;6(5):268-72. – Davis R, Jones J
S, Barocas DA, Castle EP, Lang EK, Leveillee RJ, et al. American Urological Association. Diagnosis,
evaluation and follow-up of asymptomatic microhematuria (AMH) in adults: AUA guideline. J Urol.
2012;188(6 Suppl):2473-81.
Hernando L, Arias M, Egido J, Lamas S, Praga M, Aljama P, editores. Nefrología clínica (4ª ed.). Madrid:
Médica Panamericana; 2013.
Israni AK, Kasike BL. Laboratory assessment of kidney disease: glomerular filtration rate, urinalysis,
and proteinuria. En: Taal MR, Chertow GM, Marsden PA, Skorecki K, Yu ASL, Brenner BM. Brenner &
Rector’s the kidney. 9ª ed. Philadelphia: Elselvier Saunders; 2012. p. 869-93.
Lin J, Denker BM. Hiperazoemia y anomalías urinarias. En: Longo DL, Kasper DL, Jameson JL, Fauci AS,
Hauser SL, Loscalzo J. Harrison. Principios de Medicina Interna. 18ª ed. México DF: McGraw-Hill
Interamericana; 2012. p. 334-40.
Mark A, Perazella MD, The urine sediment as a biomarker of kidney disease. Am J Kidney Dis.
2015;66(5): 748-55.
Niemi MA, Cohen RA. Evaluation of microscopic hematuria: a critical review and proposed algorithm.
Adv Chronic Kidney Dis. 2015;22(4):289-96.
Praga M, Gutiérrez E, Morales E, Hernández E, Sevillano AM, Auñón P, et al. Enfermedades de sistema
nefrourinario. Medicine. Unidad temática 82. Junio 2015.
Sharp VJ, Barnes KT, Erickson BA. Assessment of asymptomatic microscopic hematuria in adults. Am
Fam Physician. 2013;88(11):747-54.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [986]
[62] FRACASO RENAL AGUDO
62.Fracaso renal agudo
Mónica Milla Castellanos
Nefrología
Irene Losada Galván
Medicina Interna
Asesor:
Eduardo Gutiérrez Martínez
Médico Adjunto de Nefrología
I. DEFINICIÓN
El fracaso renal agudo (FRA) es el síndrome caracterizado por el deterioro brusco, en días o
semanas, de la tasa de filtrado glomerular (TFG), con o sin disminución del volumen urinario. Se produce un
acúmulo consecuente de productos nitrogenados en sangre, fundamentalmente urea y creatinina, lo que
puede alterar el volumen extracelular y el equilibrio electrolítico, situación que puede llegar a ser
potencialmente reversible. Puede afectar tanto a individuos con función renal normal como a pacientes con
enfermedad renal crónica (ERC).
Se considera un factor de riesgo mayor para complicaciones no renales y contribuye de manera
independiente a la mortalidad.
A falta de elementos más precisos y precoces para el diagnóstico de FRA (actualmente se está
investigando en varios biomarcadores), se utiliza la creatinina sérica (Crs) y la estimación del filtrado
glomerular mediante la fórmula CKD-EPI (Chronic Kidney Disease Epidemiology Collaboration) para el
diagnóstico y estratificación del FRA (Tabla I, disponible también en aplicaciones y calculadoras online).
Tabla I. Estimación del filtrado glomerular mediante la fórmula CKD-EPI.
II. APROXIMACIÓN DIAGNÓSTICA (Tabla II)
Ante todo deterioro de función renal, se debe intentar aclarar el tipo de insuficiencia renal
(cronología, gravedad) y su etiología, para poder dirigir un tratamiento precoz que permita mejorar el
pronóstico. En ocasiones, especialmente en el FRA en el ámbito hospitalario, la etiología puede ser
multifactorial. Las principales herramientas serán una historia clínica detallada, una exploración física
minuciosa y pruebas complementarias escalonadas según los resultados previos.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [987]
[62] FRACASO RENAL AGUDO
Tabla II. Enfoque diagnóstico del fracaso renal agudo.
Se pueden distinguir varios tipos de diagnósticos:
Diagnóstico sindrómico: pretende confirmar que el deterioro se ha producido agudamente.
Solo el conocimiento de la función renal previa permite el diagnóstico de certeza, si bien
existen indicadores que pueden orientar hacia la cronicidad (Tabla III).
Tabla III. Datos de cronicidad.
Diagnóstico funcional: es importante clasificar a los pacientes según la gravedad funcional,
puesto que ha demostrado tener valor pronóstico. Actualmente se recomienda el uso de la
clasificación AKIN, del Acute Kidney Injury Network (Tabla IV), que debe aplicarse una vez se
haya optimizado el estado de volemia y descartado uropatía obstructiva cuando el criterio
únicamente sea la oliguria.
Tabla IV. Clasificación AKIN del fracaso renal agudo.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [988]
[62] FRACASO RENAL AGUDO
Diagnóstico fisiopatológico: se trata de dilucidar el mecanismo principal de daño para
distinguir entre FRA prerrenal, parenquimatoso u obstructivo.
Tabla IV. Clasificación AKIN del fracaso renal agudo.
1. ANAMNESIS
Se debe realizar una minuciosa anamnesis recabando la siguiente información:
Antecedentes personales: con especial incidencia en aquellos que constituyan un factor de
riesgo para el desarrollo de insuficiencia renal, como diabetes, enfermedad vascular periférica,
hipertensión arterial (HTA), enfermedad coronaria, ictericia o hepatopatía.
Clínica sugerente de causas obstructivas: molestias en la región suprapúbica, dolor en flanco,
nicturia, polaquiuria, urgencia o retraso miccional (infecciones del tracto urinario, cólicos
renoureterales, enfermedad retroperitoneal, neoplasias, patología prostática).
Procesos actuales que orienten hacia causas prerrenales: diarrea, vómitos, hemorragia, tercer
espacio (pancreatitis, íleo intestinal), hipotensión, disminución del volumen circulante eficaz
(estados edematosos).
Situaciones de riesgo de nefrotoxicidad: tratamientos farmacológicos, pruebas con contraste,
tratamiento con quimioterapia que sugiera un síndrome de lisis tumoral o una nefropatía úrica
aguda, sospecha de toxicidad por pigmentos en los casos de rabdomiólisis (convulsiones,
ejercicio físico excesivo, isquemia de extremidades) o hemólisis, además de pruebas
endovasculares intervencionistas que pudieran haber ocasionado un ateroembolismo de
colesterol.
Datos que hagan sospechar patología isquémica: dolor en flanco en el caso de oclusión arterial
o venosa aguda.
Datos que orienten hacia enfermedades sistémicas: inspección de la piel en busca de lesiones
como nódulos subcutáneos, livedo reticularis, púrpura palpable o isquemia digital que orienten
a vasculitis o ateroembolia; erupción en alas de mariposa típica del lupus eritematoso sistémico
(LES); impétigo en pacientes con glomerulonefritis postinfecciosa; erupción maculopapular en
el caso de nefritis intersticial inmunoalérgica (NIIA); presencia de uveítis (síndrome de Behçet),
sinusitis (enfermedad de Wegener), sordera (síndrome de Alport), coexistencia de dificultad
respiratoria en los síndromes renopulmonares; estigmas de hepatopatía crónica; clínica
neurológica para el diagnóstico de púrpura trombótica trombocitopénica/síndrome hemolítico
urémico (PTT/SHU); antecedentes de infecciones por virus de la inmunodeficiencia humana
(VIH), de la hepatitis C (VHC) o B (VHB); dolores óseos en el anciano que orienten a mieloma
múltiple.
Evaluación cardiovascular: en busca de arritmias que sugieran embolismo, presencia de
hipertensión arterial o enfermedad ateromatosa generalizada.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [989]
[62] FRACASO RENAL AGUDO
2. EXPLORACIÓN FÍSICA
En el examen físico se debe explorar diversos aspectos:
Situación volémica: prestando atención a signos de depleción hídrica (taquicardia, hipotensión,
pérdida en la turgencia de la piel o lentitud en el relleno capilar, ortostatismo) y de insuficiencia
cardiaca. La monitorización invasiva hemodinámica es imprescindible en los pacientes críticos.
La aparición de edemas sin otros datos de insuficiencia cardiaca debe orientar hacia síndrome
nefrótico o hepatopatía.
Examen general: en busca de soplos que sugieran enfermedad vascular (carotídeos,
abdominales), auscultación cardiaca, auscultación pulmonar, aneurismas palpables, masas
asociadas a procesos tumorales, hepatopatía, presencia de lesiones cutáneas (púrpura, rash,
livedo reticularis); signos de neuropatía periférica como marcador de fases avanzadas de la
diabetes, en el seno de la compresión nerviosa en un síndrome compartimental que puede
acompañarse de FRA por rabdomiólisis, en la intoxicación por metales pesados o en la discrasia
de células plasmáticas (síndrome POEMS).
Fondo de ojo: donde se pueden ver lesiones de retinopatía hipertensiva, diabética, cristales de
colesterol, signos de endocarditis o signos de HTA maligna (hemorragias, exudados o edema de
papila).
Presencia de uropatía obstructiva: globo vesical o hipertrofia de próstata; se debe verificar la
permeabilidad de la sonda urinaria.
3. PRUEBAS COMPLEMENTARIAS
3.1. Orina
El análisis de la orina es fundamental e indispensable en todo paciente con FRA (Tabla V). Se debe medir el
volumen urinario, no siendo necesario el sondaje siempre que sea posible realizar un correcto balance
hídrico, salvo en pacientes críticos. El volumen de orina es de poca utilidad en el diagnóstico diferencial; sin
embargo, la anuria sugiere una obstrucción completa del tracto urinario, una complicación grave de un FRA
prerrenal o parenquimatoso (necrosis cortical o glomerulonefritis necrotizante) o bien una causa vascular
aguda.
Osmolaridad, sodio urinario y excreción fraccional de sodio (EFNa): estos tres parámetros serán
de gran utilidad para diferenciar si el FRA se ha establecido originando una situación de
necrosis tubular aguda (NTA), si bien no deben ser usados aisladamente.
La EFNa mide el porcentaje de sodio filtrado que es excretado finalmente en la orina, y se emplea
como marcador de pérdida o conservación de la capacidad para concentrar la orina por parte del túbulo.
Para su cálculo se aplicará la siguiente fórmula:
Por ello, en los FRA prerrenales, en los que la vasoconstricción disminuye el filtrado glomerular y el
túbulo reabsorbe agua y sodio para recuperar la volemia, se obtendrán orinas concentradas (osmolaridad >
400 mOsm/kg), con concentraciones de Cru elevada, eliminación de sodio baja (< 20 mEq/l) y EFNa < 1%. En
la uropatía obstructiva, las glomerulonefritis o la nefropatía por pigmentos también se pueden obtener
excreciones bajas, así como en las patologías vasculares, en la toxicidad por contrastes y en las patologías
que inducen una disminución del volumen circulante eficaz. En las situaciones de NTA, con alteración de la
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [990]
[62] FRACASO RENAL AGUDO
función tubular, la orina tiene osmolaridad baja (< 350 mOsm/kg), con Cru disminuida y sodio elevado (> 40
mEq/l), con excreción fraccional superior al 3%. El tratamiento con diuréticos, la glucosuria o la orina
alcalina también pueden ocasionar EFNa elevadas, a pesar de tratarse de situaciones prerrenales.
Sistemático de orina y sedimento (ver Capítulo 61. “Alteraciones del sistemático y sedimento
de orina”):
Fracaso prerrenal: la proteinuria es oscilante (+ o ++), con sedimento anodino
(ocasionales cilindros hialinos y células epiteliales).
NTA: la proteinuria suele ser menos cuantiosa (+) y en el sedimento se encuentran
células epiteliales, cilindros hialinos (formados por la precipitación de la proteína de
Tamm-Horsfall) y granulares.
Tabla V. Fracaso renal agudo según parámetros urinarios.
Procesos glomerulares y vasculitis: la proteinuria es elevada (+++ o ++++, más de 1 g en
orina de 24 horas) con sedimento activo (cilindros hemáticos, hematíes dismórficos y
hematuria macro o microscópica).
NIIA: se suele observar leucocituria y eosinofiluria, siendo la proteinuria variable. La
eosinofiluria también puede aparecer en los casos de ateroembolismo de colesterol y
en algunos casos de LES.
Litiasis: se pueden encontrar cristales de fosfato, ácido úrico y oxalato cálcico, además
de hematuria.
Rabdomiólisis: la positividad para sangre de la tira reactiva sin hallazgo de hematíes en
el sedimento orienta hacia la presencia de mioglobinuria o hemoglobinuria.
Otros: en el síndrome de lisis tumoral se pueden encontrar cristales de ácido úrico. En
la intoxicación por etilenglicol, administración de dosis masivas de vitamina C o en
pacientes con bypass yeyuno-ileal es posible hallar cristales de oxalato cálcico.
Tira urinaria: solo detecta albúmina, por lo que puede existir una discordancia entre la
determinación cualitativa y la cuantitativa, como ocurre de manera muy especial en la
afectación renal por mieloma múltiple o en la nefropatía por cadenas ligeras, situaciones en las
que la determinación cualitativa es negativa mientras que en la orina de 24 horas puede existir
una cuantificación elevada.
3.2. Hemograma, bioquímica y gasometría venosa
Inicialmente se debe solicitar hemograma y estudio bioquímico completo con perfil hepático, iones
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [991]
[62] FRACASO RENAL AGUDO
(incluidos calcio y fósforo), urea, lactato-deshidrogenasa (LDH), ácido úrico y gasometría venosa. Se
observará un aumento de la creatinina sérica y de la urea, debido al descenso del aclaramiento. En función
de la sospecha etiológica se deberá completar el estudio con proteinograma, inmunoelectroforesis en
sangre y orina, extensión de sangre periférica para descartar la presencia de esquistocitos, serología viral
(VIH, VHC, VHB), paratohormona (PTH), estudio de autoanticuerpos (ANA, ANCA, antimembrana basal
glomerular), complemento, factor reumatoide, cuantificación de inmunoglobulinas y hormonas tiroideas.
3.3. Pruebas de imagen
Se debe solicitar una prueba de imagen en la mayoría de los pacientes con FRA, con el objetivo de excluir la
uropatía obstructiva aguda y buscar signos que indiquen ERC.
Ecografía renal: es la prueba de elección en la mayoría de los casos. Es de gran utilidad, dado su
bajo coste y la ausencia de radiaciones ionizantes. Informa del tamaño renal, del grosor
cortical, de las diferencias de densidad corticomedular y tiene alta sensibilidad para el
diagnóstico de patología obstructiva. Las principales limitaciones son su incapacidad para
localizar el punto de la obstrucción en obstrucciones recientes o en casos de fibrosis
retroperitoneal en la que los uréteres y la pelvis quedan atrapados e impiden la dilatación del
sistema excretor.
Ecografía doppler renal: evalúa la vascularización arterial y venosa renal. Generalmente, la NTA
produce un patrón de reducción de flujo intrarrenal con aumento de los índices de resistencia
(IR) por encima de 0,75. Los IR están disminuidos en los casos de obstrucción vascular.
Radiografía simple de abdomen: es capaz de localizar litiasis radioopacas y permite valorar las
siluetas renales y calcificaciones vasculares.
Tomografía computarizada (TC) de abdomen (con o sin contraste): es más eficaz que la
ecografía en los casos de obstrucción ureteral, ya que puede localizar mejor el lugar y valorar la
presencia de patología retroperitoneal.
Angiografía renal: indicada en los casos de oclusión vascular.
Pielografía retrógrada o anterógrada: se usa para el diagnóstico y la localización de la
obstrucción, pudiendo resolverse con la colocación de un stent ureteral (casos excepcionales) o
una nefrostomía percutánea en el mismo acto.
3.4. Biopsia renal
Será necesaria en aquellos casos en los que se hayan excluido causas pre y posrenales y la etiología no esté
clara. En términos generales está indicada en los casos de FRA con sospecha de causa glomerular, vasculitis,
enfermedad sistémica, rechazo del aloinjerto, NTA que no se recupera en 3-4 semanas, NIIA con mala
evolución tras la retirada del fármaco y el tratamiento con esteroides y FRA de origen incierto. Además de
permitir el diagnóstico, es útil para establecer el pronóstico y decidir las opciones terapéuticas.
Contraindicaciones: alteraciones no corregibles de la hemostasia, riñones pequeños que orienten a IRC
avanzada, HTA grave que no se controla con medicación, quistes bilaterales múltiples, tumor, hidronefrosis,
infección renal o perirrenal activa y falta de cooperación del paciente. Complicaciones: el sangrado es la
complicación más frecuente (hasta un 12% de los pacientes tienen hematuria macroscópica autolimitada
que cede con el reposo) y puede llegar a ocasionar una hemorragia grave que requiera una nefrectomía.
Para evitarlo o minimizarlo, el paciente deberá guardar reposo 24 horas tras el procedimiento. Otras
complicaciones son fístula arteriovenosa, que se resuelve de forma espontánea en la mayoría de las
ocasiones, y la infección.
4. DIAGNÓSTICO ETIOLÓGICO
Una vez dilucidado el mecanismo, se persigue averiguar el proceso concreto para dirigir el
tratamiento. En la tabla VI se resumen algunas características de las entidades causantes de FRA.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [992]
[62] FRACASO RENAL AGUDO
Tabla VI. Diagnóstico del fracaso renal agudo.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [993]
[62] FRACASO RENAL AGUDO
III. ETIOPATOGENIA
1. CAUSAS PRERRENALES
Constituyen la causa más frecuente de FRA (Tabla VII). Implican una respuesta apropiada a
múltiples situaciones que conllevan a hipoperfusión renal. La función tubular es típicamente normal. La
reabsorción renal de sodio y agua se incrementan y, en consecuencia, se encuentra bajo contenido de
sodio de la orina (< 10 mmol/l) y una orina concentrada (osmolaridad urinaria > 500 mOsm/kg). Las
presiones de filtrado glomerular y la TFG son mantenidas por la vasodilatación arteriolar aferente y la
vasoconstricción arteriolar eferente. Esta situación es reversible en el momento inicial, pero puede
evolucionar hacia la NTA si no se resuelven los factores desencadenantes.
Tabla VII. Causas de fracaso renal agudo prerrenal.
2. CAUSAS PARENQUIMATOSAS
Su origen es secundario a modificaciones hemodinámicas que producen isquemia prolongada (NTA
isquémica) o agresiones tóxicas (NTA nefrotóxica). Ambos tipos de agresiones producen un deterioro
brusco de las funciones renales, condicionado por la lesión anatómica de las diferentes estructuras,
glomérulos, túbulos, intersticio y vasos. El curso típico de la NTA no complicada es la recuperación a lo largo
de 2 a 3 semanas. Sin embargo, daños renales superpuestos pueden alterar el curso. En la tabla VIII se
exponen las causas parenquimatosas y en la tabla IX las de la NTA.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [994]
[62] FRACASO RENAL AGUDO
Tabla VIII. Causas parenquimatosas.
Tabla IX. Causas de necrosis tubular aguda.
3. CAUSAS POSRENALES
Las causas posrenales (Tabla X) difieren según la edad. En la infancia predominan las anomalías
anatómicas; en la edad adulta, las litiasis; y en pacientes mayores, la hiperplasia prostática y neoplasias
pélvicas. La mayoría de las causas son susceptibles de tratamiento, y el pronóstico es generalmente bueno,
dependiendo de la enfermedad subyacente. El origen de la obstrucción puede ser intrarrenal (tubular),
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [995]
[62] FRACASO RENAL AGUDO
aumentando la presión intratubular, que si es lo suficientemente alta, puede oponerse a la presión de
filtración glomerular y disminuir la TFG; o extrarrenal (a nivel de la pelvis renal, uréteres, vejiga o uretra),
provocando una obstrucción aguda que ocasiona un aumento retrógrado de la presión y compromete el
filtrado glomerular. El volumen urinario es variable. Ante toda anuria brusca o periodos alternativos de
anuria/poliuria se debe descartar un FRA obstructivo. El flujo urinario normal o elevado no lo excluye. La
ecografía abdominal es la primera prueba diagnóstica que debe realizarse para descartar dilatación de las
vías urinarias o retención aguda de orina.
Tabla X. Principales causas de fracaso renal agudo obstructivo.
IV. TRATAMIENTO
Es fundamental conocer los factores de riesgo y las medidas más importantes para su prevención
(Tabla XI). El objetivo de estas medidas es preservar la función renal, prevenir las complicaciones del FRA
(sobrecarga de volumen y alteraciones del equilibrio ácido-base y eletrolíticas) y evitar que el paciente
precise diálisis crónica. Para identificar los pacientes de riesgo hay que valorar adecuadamente la función
renal previa. La disminución del volumen es el factor de riesgo más importante para el desarrollo del FRA,
así que una adecuada reposición intravenosa puede prevenirlo. La reposición de fluidos debe hacerse
cuidadosamente, en paralelo con las pérdidas, siendo fundamental la exploración física.
Tabla XI. Actitudes terapéuticas para minimizar la incidencia de fracaso renal agudo en el medio hospitalario.
1. TRATAMIENTO FARMACOLÓGICO DEL FRACASO RENAL AGUDO EN LA FASE DE INSTAURACIÓN
El FRA prerrenal es, en la mayoría de los casos, secundario a un problema no renal. El tratamiento
debe iniciarse corrigiendo la causa que lo originó. Los diuréticos del asa aumentan la diuresis en el FRA
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [996]
[62] FRACASO RENAL AGUDO
establecido. Puede valorarse su utilización después de haber conseguido un volumen circulante y una
presión arterial adecuada. Son útiles en el tratamiento de la sobrecarga de volumen e hiperpotasemia
asociados al FRA oligúrico.
2. ASPECTOS PRÁCTICOS DEL TRATAMIENTO DEL FRACASO RENAL AGUDO EN LA FASE DE EVOLUCIÓN
Ante un paciente con disminución de la diuresis y deterioro de la función renal, una vez cumplida la
evaluación diagnóstica, hay que realizar una serie de actuaciones destinadas a evitar el daño tisular. Se
deben suspender todos los posibles fármacos nefrotóxicos; en el caso de los antibióticos se deberá analizar
la posible toxicidad renal intentado una alternativa terapéutica que garantice la cobertura microbiana y
minimice la posible toxicidad. El control de los niveles circulantes de fármacos puede limitar la toxicidad. La
normalización de la volemia debe ir acompañada de una composición adecuada del medio interno. Salvo en
casos extremos de hipopotasemia, nunca debe reponerse potasio en esta fase. El uso del bicarbonato debe
considerarse cuando el pH sanguíneo sea menos de 7,2. Otro factor importante para conseguir una
perfusión renal eficaz es una función cardiaca adecuada, por lo que se debe optimizar la presión arterial y el
gasto cardiaco con un adecuado volumen circulante o fármacos vasoactivos si es necesario. La medición de
la presión venosa central (PVC) puede ser necesaria en ambas fases. La anemia puede ser otra complicación
durante el curso del FRA, y debe tratarse cuando haya sintomatología o posibles riesgos, valorando la
transfusión de hematíes o factores estimulantes de la eritropoyesis.
3. TRATAMIENTO DIALÍTICO
Se dispone de tres grupos de técnicas para la depuración extrarrenal.
La diálisis peritoneal es la más biocompatible ya que utiliza como dializador al propio peritoneo,
pero es menos eficaz que las otras técnicas. En la actualidad está en desuso para el FRA pero es útil en
pacientes pediátricos o en situaciones que no son de emergencia.
La hemodiálisis intermitente permite una elevada y rápida depuración de toxinas de forma
discontinua y produce cambios bruscos del volumen circulante, lo que puede conllevar hipotensión o
arritmias cardiacas, por lo que no es la técnica más adecuada en pacientes críticos o inestables.
Por último, la hemofiltración o la hemodiafiltración veno-venosa continua, de elección en pacientes
críticos, permiten mayor balance negativo y eliminan más cantidad de mediadores de inflamación.
4. INDICACIONES DE DIÁLISIS EN EL FRACASO RENAL AGUDO
Está indicada en casos de sobrecarga de volumen con edema agudo de pulmón, hiperpotasemia,
acidosis metabólica o hiponatremia graves siempre que no respondan al tratamiento médico habitual. Otra
indicación es la uremia grave, manifestada con vómitos, alteraciones neurológicas, diátesis hemorrágica o
pericarditis.
5. TRATAMIENTO DEL FRACASO RENAL AGUDO OBSTRUCTIVO
Se debe colocar una sonda vesical en casos de patología prostática. Cuando exista globo vesical, se
debe drenar la vejiga de forma intermitente para evitar la hematuria ex vacuo. En obstrucciones de causa
ureteral colocará un catéter doble J, un catéter interno-externo o una nefrostomía. Solo en aquellos casos
en los que la desobstrucción sea imposible o las alteraciones clínicas del paciente fueran una amenaza para
su vida, estaría indicada la utilización de medidas de apoyo, como la diálisis, mientras se da una solución a
la obstrucción.
6. TRATAMIENTO DEL FRACASO RENAL AGUDO EN FASE DE RECUPERACIÓN
Cuando las estructuras renales vuelven progresivamente a la normalidad, el organismo elimina gran
cantidad de metabolitos tóxicos produciendo una poliuria osmótica, especialmente en los de causa
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [997]
[62] FRACASO RENAL AGUDO
obstructiva, con una pérdida importante de agua y electrolitos y la consiguiente reducción del volumen
circulante, hipotensión e hipoperfusión renal, pudiendo aparecer hipopotasemia. Se debe realizar un
estrecho control de las pérdidas para realizar una reposición adecuada.
V. SITUACIONES ESPECIALES
1. NEFROTOXICIDAD POR CONTRASTES YODADOS
Los factores de riesgo son la diabetes mellitus, la insuficiencia renal, el mieloma múltiple, las
situaciones de hipoperfusión renal y dosis elevadas de contraste. Tras el uso del contraste, aparece oliguria
en 24-48 horas y deterioro de la función renal en 3-5 días, iniciándose después la recuperación, que se
suele alcanzar en 2 semanas. La prevención se debe hacer con hidratación con 1000 ml de suero salino
fisiológico (SSF) al 0,9%, 12 horas antes (esta medida es la más importante) y 12 horas después de la
prueba, y N-acetilcisteína 1.200 mg de la misma manera. En situaciones de sobrecarga hídrica se puede
valorar disminuir la hidratación. Se deben suspender los antiinflamatorios no esteroideos (AINE) y los
diuréticos 24 horas antes y reintroducirlos 24 horas después de la administración del contraste. La
metformina se debe suspender la mañana de la prueba y reintroducirla una vez confirmado que no se ha
producido FRA por el riesgo de acidosis láctica. Se realizará un control bioquímico en 24-48 horas después
del contraste.
2. NEFRITIS INTERSTICIAL INMUNOALÉRGICA
Se caracteriza por la presencia de infiltrados inflamatorios y edema en el intersticio, generalmente
asociada a un deterioro agudo de la función renal. Los fármacos más frecuentemente implicados son los
AINE, b-lactámicos, quinolonas, diuréticos, cotrimoxazol y alopurinol. El deterioro de la función renal
coincide temporalmente con el fármaco. Los pacientes pueden presentar rash cutáneo, fiebre, eosinofilia,
leucocituria y microhematuria. Se debe realizar el diagnóstico diferencial con el ateroembolismo de
colesterol o con la nefritis intersticial inducida por agentes infecciosos. El tratamiento es la suspensión del
fármaco y la administración de esteroides, a dosis de 1 mg/kg/día durante al menos 6-8 semanas, asociada
inicialmente a pulsos de metilprednisolona para acelerar la recuperación de la función renal y evitar el
desarrollo de fibrosis. En ocasiones es imprescindible realizar una biopsia renal para llegar al diagnóstico.
3. ENFERMEDAD ATEROEMBÓLICA
Su patogenia se basa en el impacto de cristales de colesterol procedentes de placas de ateroma de
grandes arterias que se difunden por el torrente circulatorio y se depositan en vasos arteriales distales a
nivel renal, ocular, cerebral, pancreático, intestinal, piel y dedos de los pies, donde se observa livedo
reticularis. Se ven más afectados los varones, mayores de 60 años, fumadores, dislipémicos, diabéticos e
hipertensos.
Puede aparecer de forma espontánea o después de un procedimiento intervencionista, o en
pacientes con antecedente de infarto del miocardio o en quienes estén anticoagulados. Pueden presentar
FRA, microhematuria, leucocituria, proteinuria leve, eosinofilia e hipocomplementemia. El diagnóstico se
puede obtener con la presencia de cristales en la piel, músculo, fondo de ojo o riñón.
El tratamiento se basa en evitar el cuadro controlando los factores de riesgo cardiovascular (tensión
arterial y placa de ateroma) y evitando que el paciente se exponga a factores desencadenantes del cuadro
(anticoagulantes, intervencionismo endovascular). La otra parte del tratamiento consiste en disminuir la
isquemia en los órganos afectos para mejorar su disfunción. Se utilizan los esteroides, que pretenden
mejorar el componente inflamatorio periémbolo aumentando el flujo distal a la obstrucción vascular y
reduciendo el daño isquémico; los análogos de las prostaglandinas, que tienen actividad vasodilatadora y
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [998]
[62] FRACASO RENAL AGUDO
antiagregante, con mejoría de las lesiones cutáneas y del dolor, y las estatinas a altas dosis. Hasta el
momento ningún tratamiento ha demostrado una eficacia elevada.
4. FRACASO RENAL AGUDO Y ENFERMEDADES HEPÁTICAS
Este tipo de pacientes son susceptibles de desarrollar FRA prerrenal por pérdida de volumen (uso
excesivo de diuréticos o hemorragias), redistribución del volumen al tercer espacio o cardiopatía.
Se debe ser muy cuidadoso con el uso de fármacos nefrotóxicos y con la realización de paracentesis
evacuadoras cuantiosas sin la correcta reposición con albúmina.
El síndrome hepatorrenal (SHR) es un cuadro de FRA oligúrico que acontece en pacientes con
enfermedad hepática avanzada. Fisopatológicamente se caracteriza por una intensa vasoconstricción renal
que produce disminución del filtrado glomerular y vasodilatación a nivel esplácnico. Como consecuencia se
produce una disfunción circulatoria grave caracterizada por hipotensión arterial y estimulación intensa del
sistema renina-angiotensina-aldosterona (SRAA), del sistema simpático y de la hormona antidiurética.
Generalmente cursa con hiponatremia y sodio urinario muy bajo (< 10 mEq/l), ya que la capacidad del riñón
para excretar sodio y agua se ve reducida. El diagnóstico se establece cuando la creatinina es mayor de 1,5
mg/dL y se han descartado otras causas. Existen dos tipos: el SHR tipo 1 es un fallo renal grave y
rápidamente progresivo y el SHR tipo 2 se presenta con un deterioro moderado de la función renal y
lentamente progresivo. Los análogos de la vasopresina (por ejemplo, terlipresina) pueden tener un efecto
beneficioso en la evolución del SHR.
En ocasiones el uso de dopamina a dosis vasodilatadora puede tener un efecto beneficioso en los
FRA oligoanúricos. Puede haber también FRA en el curso del trasplante hepático y en el contexto de sepsis,
inestabilidad hemodinámica, toxicidad por inmunosupresores como tacrolimus, fracaso del injerto hepático
o multifactorial.
5. FRACASO RENAL AGUDO POR DAÑO VASCULAR MICROSCÓPICO
Las microangiopatías trombóticas se definen como una lesión histológica en las arteriolas y
capilares que se caracteriza por engrosamiento e inflamación de la pared vascular y presencia de trombos
plaquetarios que ocluyen las luces vasculares. Existen dos entidades clínicas: a) la púrpura trombótica
trombocitopénica (PTT), consecuencia de una deficiencia de la actividad del ADAMTS13, enzima encargada
de fragmentar los multímeros del factor de Von Willebrand; b) el síndrome hemolítico urémico (SHU), que
se clasifica en SHT típico, en el que el 90% de los casos son causados por una infección entérica a partir de
alimentos contaminados, y SHU atípico, cuyo diagnóstico es de exclusión, que se debe a una disregulación
de la vía alterna del complemento sobre las superficies celulares. Existen también causas secundarias.
Desde un punto de vista bioquímico se observa anemia hemolítica microangiopática no inmune (elevación
de LDH, descenso de haptoglobina y esquistocistos en la extensión de sangre periférica con Coombs
negativo), trombocitopenia e insuficiencia renal aguda.
6. FRACASO RENAL AGUDO ASOCIADO A INHIBIDORES DE LA ENZIMA CONVERTIDORA DE ANGIOTENSINA Y
ANTAGONISTAS DE LOS RECEPTORES DE ANGIOTENSINA II
Los IECA y ARA-II son fármacos que impiden la vasoconstricción de la arteriola eferente y reducen la
presion intraglomerular y el filtrado glomerular. La elevación de la creatinina aparece a los pocos días de la
introducción del fármaco. Se debe descartar la presencia de estenosis arterial renal bilateral, aunque la
mayoría de las veces el deterioro de la función renal se debe al efecto hipotensor por existir afectación de
pequeño vaso. Se debe vigilar la hiperpotasemia.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [999]
[62] FRACASO RENAL AGUDO
7. FRACASO RENAL AGUDO ASOCIADO A ANTIINFLAMATORIOS NO ESTEROIDEOS
Supone una causa común de FRA, debido al alto consumo de estos medicamentos. El FRA puede ser
debido a una reducción de la TFG en algunas situaciones clínicas como la enfermedad ateroesclerótica
cardiovascular en pacientes de edad avanzada, la insuficiencia renal crónica previa, los estados de
hipoperfusión renal (uso de diuréticos, hipotensión) y los estados de sodio ávido (cirrosis, síndrome
nefrótico e insuficiencia cardiaca congestiva). Hay poca evidencia de que los AINE alteren la función renal
en individuos por lo demás sanos. El daño es reversible en 2 a 7 días desde la suspensión del fármaco,
aunque con menor frecuencia puede originar NTA o NIIA. Otros efectos secundarios incluyen retención de
sodio, lo que puede exacerbar una insuficiencia cardiaca congestiva o HTA, hiponatremia e hiperpotasemia.
8. FRACASO RENAL AGUDO ASOCIADO A PIGMENTOS DEL GRUPO HEMO
La lesión renal se debe a la depleción de volumen, vasoconstricción renal, citotoxicidad directa,
coagulación intravascular diseminada y formación intraluminal de cilindros. La depleción de volumen en la
rabdomiólisis se debe al secuestro de grandes cantidades de líquido (hasta 15-20 l) en el músculo
lesionado. La depleción de volumen activa el sistema nervioso simpático y el sistema renina-angiotensina,
lo que se traduce en vasoconstricción renal. Por su pequeño tamaño, estos pigmentos son filtrados en el
glomérulo y ocasionan citotoxicidad directa en las células epiteliales. Son capaces de formar cilindros
intratubulares al precipitarse con la proteína de Tamm-Horsfall y ocasionar una NTA.
Hemoglobinuria. Estados donde circula la hemoglobina libre. Si la hemólisis es leve, la hemoglobina
liberada se une a la haptoglobina circulante. Con la hemólisis masiva, la haptoglobina se “agota”. Entre las
diferentes causas se incluyen la transfusión de sangre de un grupo incompatible, la anemia hemolítica
autoinmune, la malaria, el deficit de glucosa-6-fosfatodeshidrogenasa, la hemoglobinuria paroxística
nocturna y las toxinas (dapsona, venenos).
Rabdomiólisis. El trauma muscular es la causa más frecuente. Otras causas de lesión muscular
incluyen el ejercicio intenso, convulsiones, abuso del alcohol, consumo de drogas, isquemia aguda de
extremidades e inmovilidad prolongada (coma, caídas). En los músculos esqueléticos confinados a
compartimentos rígidos, el edema celular después de una lesión puede provocar un aumento de las
presiones intracompartimentales, lo que impide la circulación microvascular local, dando lugar a un
síndrome compartimental. La terapia con estatinas puede estar asociada a rabdomiólisis. El riesgo aumenta
con el tratamiento concomitante de fibratos, ciclosporina o eritromicina. La rabdomiólisis se caracteriza por
un FRA oligúrico con signos de depleción de volumen intravascular. La EFNa será baja. La orina se tiñe de
color marrón-rojizo con positividad en la tira reactiva para el grupo hemo pero ausencia de hematíes en el
sedimento. A nivel bioquímico se encontrará creatina-fosfocinasa (CPK) elevada, hiperpotasemia,
hiperfosfatemia, hiperuricemia y tendencia a la hipocalcemia con presencia de acidosis láctica. El
tratamiento se basa en la hidratación del paciente y alcalinización de la orina para minimizar el daño
tubular.
9. FRACASO RENAL AGUDO ASOCIADO A NEOPLASIAS
Los pacientes con cáncer son propensos al FRA como consecuencia de su enfermedad subyacente y
tratamiento pero también presentan FRA prerrenal debido a la alta frecuencia de náuseas, vómitos, y
diarrea.
Síndrome de lisis tumoral. Necrosis de gran número de células tumorales, típicamente después de
la quimioterapia. Puede liberar grandes cantidades de contenido intracelular nefrotóxico (ácido úrico,
fosfato, xantina) a la circulación. Por lo general ocurre después del tratamiento de los linfomas y leucemias
pero puede ocurrir de forma espontánea en pacientes con tumores de rápida división celular e incluso en
tumores sólidos. Se presenta como un FRA oligoanúrico y se debe sospechar en pacientes con niveles altos
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1000]
[62] FRACASO RENAL AGUDO
de LDH, fósforo, ácido úrico y potasio. Las medidas preventivas incluyen el uso de altas dosis de alopurinol,
hidratación y alcalinización urinaria. La rasburicasa es eficaz en la reducción de los niveles de ácido úrico en
suero en 24 horas, considerándose indicada en pacientes de alto riesgo.
Hipercalcemia. La depleción de volumen secundaria a la hipercalcemia o bien el daño directo de
ésta puede causar lesión renal aguda.
Infiltración renal. La infiltración renal directa de los riñones por tumores no es infrecuente, pero
rara vez provoca insuficiencia renal. El FRA puede aparecer en linfomas o leucemias de crecimiento lento,
cuando el paciente presenta un FRA no oligúrico, sedimento de orina normal y riñones aumentados de
tamaño en la ecografía. La función renal puede mejorar dependiendo de la capacidad de respuesta del
tumor al tratamiento. No hay que olvidar la obstrucción del tracto urinario relacionada con el tumor.
Agentes quimioterapéuticos. El cisplatino se asocia comúnmente con un FRA no oligúrico
afectando al túbulo proximal y distal. Analíticamente destaca la hipomagnesemia y la hipopotasemia.
BIBLIOGRAFÍA
Campistol JM, Arias M, Ariceta Iraola G, Blasco M, Espinosa Román L, Espinosa M, Grinyó JM, et al.
Actualización en síndrome hemolítico urémico atípico: diagnóstico y tratamiento. Documento de
consenso. Nefrología 2015;35(5): 421-447.
Chawla LS, Eggers PW, Star RA, Kimmel PL. Acute kidney injury and chronic kidney disease as
interconnected syndromes. N Engl J Med. 2014;371:58-66.
Feehally J, Floegue J, Johnson R. Comprehensive clinical nephrology. 4a ed. Philadelphia: Mosby
Elsevier; 2011.
González Monte E. Nefropatías intersticiales. Nefrología al día. 2012;6:0.
Hernando Avendaño L, Jiménez Murillo P, Arias Rodríguez M, Caramelo Díaz C, Egido de los Ríos J,
Lamas Pérez S. Nefrología clínica. 3a ed. Madrid: Editorial Médica Panamericana; 2008.
Levey AS, Stevens LA, Schmid CH, Zang Y, Castro AF, Feldman HI et al. A new equation to estimate
glomerular filtration rate. Ann Intern Med. 2009;150:604-12.
Sevillano Á, Hernández E, Caro J, Molina M, Gutiérrez E, Morales E, et al. Ateroembolia de colesterol y
tratamiento combinado con esteroides e iloprost. Nefrologia. 2012;32(6):824-8.
Tenorio Cañamás MT, Galeano Álvarez C, Rodríguez Mendiola N, Liaño García F. Diagnóstico diferencial
de la insuficiencia renal aguda. NefroPlus. 2010;3(2):16-32.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1001]
[63] ENFERMEDAD RENAL CRÓNICA
63.Enfermedad renal crónica
Paola Rodríguez Ramos
Nefrología
Estíbaliz Arrieta Ortubay
Medicina Interna
Asesor:
Enrique Morales Ruiz
Médico Adjunto de Nefrología
I. CONCEPTO
1. CONCEPTO Y ESTADIOS
La enfermedad renal crónica (ERC) es la disminución clínicamente significativa, irreversible y
progresiva del número de nefronas funcionantes, con independencia de la causa. En condiciones normales,
el riñón se encarga de regular el medio interno, excretar productos del metabolismo nitrogenado y
sintetizar hormonas, además de otras funciones metabólicas. En la ERC se produce una pérdida progresiva
de dichas funciones y la aparición de manifestaciones clínicas secundarias. Así, la ERC en el adulto se define
por la presencia de alteraciones en la estructura o función renal (puesta de manifiesto por alteraciones en
el sedimento, pruebas de imagen o histología) con o sin disminución del filtrado glomerular (FG) o bien por
un FG menor de 60 ml/min, sin otros signos de lesión renal. Estas anomalías deben persistir durante al
menos tres meses.
Tradicionalmente, la ERC se ha clasificado en cinco estadios en función del FG; sin embargo, la
organización internacional Kidney Disease: Improving Global Outcomes (KDIGO) propone establecer una
nueva clasificación pronóstica, basada en categorizar la albuminuria (cociente albúmina/creatinina) en
cualquiera de los cinco estadios con el objetivo de identificar a un subgrupo de pacientes con mayor riesgo
de progresión de la enfermedad renal y más morbimortalidad cardiovascular (Tablas I y II).
2. MEDICIÓN DEL FILTRADO GLOMERULAR
La valoración del FG es el mejor índice para evaluar la función renal, varía en función de la edad, el
sexo y la masa corporal del individuo. El FG puede ser estimado por métodos directos a través de la
medición de sustancias exógenas como la inulina (considerada método de referencia); sin embargo, es de
difícil realización en la práctica clínica diaria. Habitualmente se utilizan métodos indirectos para su
estimación a través de sustancias endógenas como la creatinina. La concentración de creatinina sérica no
debe utilizarse de modo aislado para estimar el FG, ya que esta se puede realizar a través del cálculo de
creatinina a partir de la creatinina sérica y su excreción en orina de 24 horas. Sin embargo, en la actualidad
se recomienda la estimación del FG a través de ecuaciones que combinan la información que proporciona
la creatinina sérica con otras variables demográficas y antropométricas, evitando la colección de orina de
24 horas: MDRD-4 IDMS, MDRD-6 y CKD-EPI (Tabla III). Desde hace unos años se aconseja el uso de esta
última ecuación (CKD-EPI), ya que mejora la capacidad predictiva del FG, aunque apenas está disponible en
la práctica clínica habitual. Recientemente se ha sugerido el uso de cistatina C para calcular el FG. Este
marcador endógeno se modifica menos respecto a las variables que influyen en la creatinina sérica y parece
predecir mejor las complicaciones cardiovasculares y la mortalidad. En la actualidad, las guías
(organización) KDIGO reconocen su utilidad en pacientes con un FG entre 45 y 59 ml/min, sin marcadores
de lesión renal, en las que sea preciso el diagnóstico de ERC.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1002]
[63] ENFERMEDAD RENAL CRÓNICA
Tabla I. Clasificación, plan de actuación y sintomatología de la enfermedad renal crónica.
Tabla II. Pronóstico de la enfermedad renal crónica por IR y categorías de albuminuria.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1003]
[63] ENFERMEDAD RENAL CRÓNICA
Tabla III. Determinación del filtrado glomerular.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1004]
[63] ENFERMEDAD RENAL CRÓNICA
II. APROXIMACIÓN DIAGNÓSTICA
1. HISTORIA CLÍNICA
Ante todo paciente con deterioro de la función renal es esencial realizar una buena historia clínica.
En ella se recogerán antecedentes familiares de nefropatía hereditaria o de malformaciones urológicas y
antecedentes personales considerados factores de riesgo para desarrollar una nefropatía, hipertensión
arterial (HTA), diabetes mellitus (DM), anomalías en el análisis de orina, problemas con el embarazo
(preeclampsia o abortos de pocas semanas), etc. Es importante descartar el consumo de fármacos
nefrotóxicos o exposición laboral a metales pesados e hidrocarburos y se debe interrogar específicamente
sobre síntomas como nicturia (tras descartar síndrome prostático), orinas espumosas, prurito,
manifestaciones gastrointestinales (anorexia, náuseas, vómitos), síndrome anémico, alteraciones
neurológicas (síndrome de piernas inquietas, parestesias distales por polineuropatía urémica, calambres),
dolores óseos y fracturas patológicas por la osteodistrofia renal (Tabla IV).
Tabla IV. Trastornos asociados a la enfermedad renal crónica.
2. EXPLORACIÓN FÍSICA
Debe registrarse el peso, la talla y posibles malformaciones o trastornos del desarrollo. Es necesario
realizar un cribado de HTA, examen del fondo de ojo (retinopatía hipertensiva o diabética), exploración
cardiovascular completa, palpación abdominal (buscando masas o riñones palpables) y descartar datos de
sobrecarga de volumen. Asimismo, deben buscarse lesiones de rascado, hiperpigmentación cutánea,
hematomas, fetor urémico o signos de malnutrición.
3. PRUEBAS COMPLEMENTARIAS
3.1. Laboratorio
Bioquímica completa (incluidas las concentraciones de calcio, fósforo y hormona paratiroidea [PTH]),
hemograma, gasometría venosa, determinación de proteinuria, iones en orina y estudio del sedimento
urinario en todos los pacientes. En caso de anemia, se solicitará perfil férrico, vitamina B12, ácido fólico y
estudio electroforético en suero y orina, si se acompaña de hipercalcemia. Se aconseja ampliar el estudio
con serologías de hepatitis B, C e infección por VIH y panel de autoinmunidad ante sospecha de
enfermedad sistémica. En general, se observará un incremento en las cifras de creatinina (Cr) y urea, así
como una disminución del FG, calculado por cualquiera de las fórmulas mencionadas (Tabla III). Se pueden
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1005]
[63] ENFERMEDAD RENAL CRÓNICA
encontrar otras alteraciones como hiponatremia o hipernatremia (al perder el riñón la capacidad de
manejar el agua corporal correctamente), hiperpotasemia (suele manifestarse en fases avanzadas de la
enfermedad, salvo en la nefropatía diabética, que aparece antes por la presencia de un hipoaldosteronismo
hiporreninémico y en la nefropatía intersticial crónica por la pobre respuesta del túbulo a la acción de la
aldosterona), acidosis metabólica, hiperfosfatemia con hipocalcemia (aunque el calcio puede ser normal en
relación con hiperparatiroidismo secundario e incluso elevado si aparece un hiperparatiroidismo terciario),
hiperuricemia (aumenta según progresa la ERC), alteraciones del perfil lipídico, anemia normocítica-
normocrómica (debido principalmente al déficit de eritropoyetina) o alteración del tiempo de hemorragia o
Ivy (en relación con la trombopatía urémica).
3.2. Pruebas de imagen
La ecografía es un estudio obligado para comprobar la existencia de dos riñones, valorar la simetría y
morfología, medir su tamaño y descartar una obstrucción de la vía urinaria. Un tamaño renal pequeño (< 9
cm, según la superficie corporal) puede sugerir cronicidad e irreversibilidad de la enfermedad. Un tamaño
renal normal favorece el diagnóstico de un proceso agudo; sin embargo, la poliquistosis renal, la
amiloidosis o la diabetes pueden cursar con riñones de tamaño normal o aumentado. La asimetría renal
(una diferencia de tamaño entre ambos riñones superior a 2 cm) puede deberse a patología vascular de la
arteria renal, reflujo vesicoureteral o diversos grados y formas de agenesia o hipoplasia renal unilateral.
La ecografía-Doppler es útil para el diagnóstico de la estenosis unilateral o bilateral de la arteria
renal. Se pueden emplear otras técnicas de imagen como la angiografía digital, la tomografía
computarizada (TC), la gammagrafía renal de perfusión o la angiorresonancia magnética (angio-RM).
3.3. Biopsia renal
Se realizará en casos seleccionados con criterios específicos y en estadios iniciales de ERC, ya que la biopsia
de un riñón atrófico supone un mayor riesgo y suele aportar poca información sobre el diagnóstico
etiológico de la patología renal.
4. DIAGNÓSTICO DIFERENCIAL ENTRE FRACASO RENAL AGUDO Y ENFERMEDAD RENAL CRÓNICA
Es muy importante diferenciar entre fracaso renal agudo (FRA) o una verdadera ERC, ya que el
primer caso resulta reversible con medidas terapéuticas apropiadas. Aunque no siempre resulta sencillo,
existen ciertos parámetros que ayudan a diferenciarlas (Tabla V).
Tabla V. Datos que sugieren cronicidad en un fracaso renal agudo.
5. DIAGNÓSTICO ETIOLÓGICO DE LA ENFERMEDAD RENAL CRÓNICA
Es importante establecer la etiología debido a que algunas causas son tratables, de modo que se
puede paliar la progresión de la ERC o recuperar parte de la función renal. Asimismo, es importante
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1006]
[63] ENFERMEDAD RENAL CRÓNICA
diagnosticar enfermedades sistémicas con afectación de la función renal de cara a un tratamiento
específico, así como la identificación de enfermedades de origen hereditario para realizar un consejo
genético adecuado. Existen diversas causas de ERC según el grupo de edad (Figura 1). Por último, se debe
tener en cuenta que determinadas enfermedades renales pueden recidivar tras el trasplante. En función de
la sospecha etiológica se realizará un estudio dirigido (Tabla VI).
Tabla VI. Características que orientan a la etiología de la enfermedad renal crónica.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1007]
[63] ENFERMEDAD RENAL CRÓNICA
Figura 1. Diagnóstico etiológico de la enfermedad renal crónica.
III. PROGRESIÓN DE LA ENFERMEDAD RENAL CRÓNICA. CRITERIOS DE
DERIVACIÓN A NEFROLOGÍA
Existen una serie de factores que determinan tanto la aparición como la progresión de la ERC,
siendo los más importantes la edad superior a 60 años, los antecedentes familiares de enfermedad renal, la
DM, la enfermedad cardiovascular, el hábito tabáquico y la obesidad (Tabla VII). La intervención sobre
aquellos factores modificables ayudará a retrasar la progresión de la ERC.
La evolución de la ERC puede ser variable entre los pacientes que la padecen; sin embargo, la
mayoría presenta un empeoramiento progresivo de la función renal hacia la enfermedad renal terminal.
Esta evolución se aprecia tanto en aquellas enfermedades renales en las que el proceso patológico sigue
actuando, como en otras entidades en las que, a pesar de desaparecer el mecanismo patogénico, la
reducción de la masa de la nefrona funcionante condiciona una serie de cambios hemodinámicos
compensatorios que da lugar a una esclerosis glomerular progresiva. Este fenómeno se conoce como teoría
de la hiperfiltración.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1008]
[63] ENFERMEDAD RENAL CRÓNICA
La presencia de albuminuria se considera signo de daño renal y sistémico, y como se comentó
anteriormente, se trata de un factor de progresión renal muy importante, además de un marcador
independiente de riesgo cardiovascular global. Por todo ello, es fundamental su monitorización junto con la
función renal, al menos de manera anual, aunque puede ser semestral en los pacientes de alto riesgo
(Tabla II). En la actualidad se admiten como válidas para la medida de la albuminuria y/o proteinuria: la
orina de 24 horas y el cociente de proteína (o albumina)/creatinina de una sola micción. La seriación
periódica de otros parámetros clínicos (síntomas urémicos, balance hídrico) y analíticos (Cr, urea, sodio,
potasio, hemograma, hierro, ferritina, calcio, fósforo, PTH) también son de utilidad en el seguimiento de la
ERC y sus complicaciones.
La derivación del paciente con ERC a Nefrología se realizará en función del estadio de la
enfermedad, la velocidad de progresión, el grado de albuminuria, la presencia de signos de alarma y la
situación funcional del paciente (Tabla VIII). Estos criterios de derivación serán más “laxos” en la población
anciana, en mayores de 80 años, ya que, por lo general, la progresión de la enfermedad es poco frecuente y
más lenta.
Tabla VII. Factores de riesgo de progresión de la enfermedad renal crónica.
Tabla VIII. Criterios de derivación al Servicio de Nefrología.
IV. MANEJO DE LA ENFERMEDAD RENAL CRÓNICA
1. TRATAMIENTO CONSERVADOR (MÉDICO)
1.1. Descartar factores evitables o reversibles
La progresión de la ERC suele ocurrir por actividad de la enfermedad renal primaria y los mecanismos de
progresión natural de la misma. Cuando se detecten criterios de progresión, siempre habrá que descartar
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1009]
[63] ENFERMEDAD RENAL CRÓNICA
factores potencialmente reversibles de agudización, como uropatía obstructiva, depleción de volumen,
inestabilidad hemodinámica, uso de antiinflamatorios no esteroideos (AINE), antibióticos nefrotóxicos o
contrastes radiológicos.
1.2. Cómo prevenir o retrasar la progresión de la enfermedad renal crónica
La base de la prevención de la progresión de la ERC es el manejo integral del paciente, que se sustenta en
medidas dietéticas, cambios en el estilo de vida y control estricto de los factores de riesgo CV (Tabla IX).
Tabla IX. Medidas para prevenir la progresión de la enfermedad renal crónica.
Dieta: se recomienda disminuir la ingesta diaria proteica a aproximadamente 0,8 g/kg/ día en
pacientes con FG < 30 ml/min/1,73m2, ya que disminuye la pérdida del FG. Se ha evidenciado
que la baja ingesta proteica también enlentece la progresión de la proteinuria incluso en
aquellos pacientes que tienen proteinurias inferiores a 1 g/día. Hay que tener especial cuidado
con las restricciones dietéticas en pacientes con ERC avanzada, ya que en esta población la
malnutrición es frecuente por diversas causas (anorexia, acidosis, resistencia a la insulina,
inflamación y pérdida urinaria de proteínas).
Hipertensión arterial: el control de la tensión arterial (TA) es uno de los objetivos principales
para evitar la progresión natural de la ERC. Las recomendaciones generales sobre el objetivo
para el control tensional en pacientes con ERC aconsejan cifras inferiores a 140/90 mm Hg en
pacientes con cociente albúmina/creatinina < 30 mg/g, y una TA < 130/80 mm Hg en pacientes
con un cociente albúmina/creatinina > 30 mg/g (incluyendo pacientes con albuminuria elevada
o proteinuria). Cuanto mayor sea la proteinuria, mayor será el beneficio de controlar la TA.
Merece la pena reseñar que los objetivos de TA mencionados anteriormente no se
recomiendan para todo tipo de pacientes. Mantener una TA sistólica entre 130-140 mm Hg es
aceptable, por ejemplo, para pacientes ancianos (frágiles), aquellos que presentan enfermedad
cardiovascular evidente o intolerancia a un control más estricto de la TA (astenia, síntomas
ortostáticos, dolor torácico o incluso aumento de creatinina sérica).
Existe consenso sobre la necesidad de utilizar fármacos que bloqueen el sistema renina-
angiotensina- aldosterona (SRAA), bien mediante los inhibidores de la enzima convertidora de
la angiotensina (IECA) o los antagonistas de los receptores de angiotensina-II (ARA-II), debido a
sus efectos nefroprotectores adicionales. No existe evidencia contundente para recomendar el
doble bloqueo del eje SRAA (uso de IECA y ARA-II) para prevenir la progresión de la ERC, pero sí
de sus posibles efectos secundarios, como deterioro agudo de la función renal o
hiperpotasemia. No hay que olvidar que la misma ERC se asocia a una mayor resistencia al
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1010]
[63] ENFERMEDAD RENAL CRÓNICA
tratamiento antihipertensivo, por lo que el tratamiento combinado (> 2 fármacos) debe
considerarse la norma cuando la tensión arterial sistólica (TAS) está por encima de 20 mm Hg
del límite recomendado con un solo fármaco.
Dislipidemia: los pacientes con ERC y FG < 60 ml/min/1,73m2 se consideran de muy alto riesgo
cardiovascular. El patrón lipídico típico de estos pacientes es una disminución del HDL-
colesterol, junto con hipertrigliceridemia y aumento del colesterol total, principalmente del
LDL-colesterol. Aparte de modificaciones dietéticas y cambio en el estilo de vida, la mayoría de
los pacientes requerirán fármacos hipolipemiantes. Las estatinas siguen siendo el fármaco de
elección, y se debe intentar evitar aquellas de eliminación renal. Los fibratos están
contraindicados en la ERC avanzada, ya que aumentan el riesgo de miopatía, especialmente si
se asocian a estatinas. También se ha demostrado que el uso de fibratos puede producir un
deterioro agudo de la función renal, sobre todo en pacientes con ERC previa, y en algunos casos
este deterioro puede no ser reversible.
Hiperglucemia: el control de la glucemia es uno de los objetivos primordiales para prevenir la
progresión de la ERC. Se recomienda un objetivo de hemoglobina glucosilada (HbA1c) < 7%. Hay
que tener en cuenta que el riesgo que presenta la hipoglucemia grave en pacientes con ERC es
muy alto (favorecido por cambios en la ingesta debidos a hiporexia, y cambios en los horarios
de comidas por la diálisis). En estos pacientes, así como en aquellos ancianos y en pacientes
débiles se recomienda un objetivo de HbA1c más laxo, entre 7,5% y 8%. En cuanto a los
antidiabéticos orales, hay que tener especial cuidado con la metformina, ya que se elimina
principalmente por la orina, y los pacientes con deterioro de la función renal son más
susceptibles a la acidosis láctica. Si se utiliza este fármaco, debe disminuirse la dosis al 50% con
un FG entre 30 y 45 ml/min/1,73 m2, y debe suspenderse en pacientes con un FG inferior a 30
ml/min/1,73 m2.
Obesidad: la obesidad produce una serie de cambios hemodinámicos, funcionales y
estructurales en el riñón que pueden favorecer la ERC. Los mecanismos por los cuales la
reducción de peso mejora la función renal son varios: mejor control de la TA, mejora del perfil
lipídico y de la glucemia, reversión de la hiperfiltración glomerular e inhibición del sistema
renina-angiotensina. Los cambios en la fisiología renal inducidos por la obesidad son
reversibles, por lo que la disminución de peso puede mejorar la función renal de los obesos,
sobre todo en estadios iniciales de la ERC .
Tabaquismo: el tabaco promueve la progresión de todas las causas de enfermedad renal, de
forma dosis-dependiente; quizás aún más en personas de raza negra. Se asocia a un mayor
riesgo de hiperfiltración glomerular y proteinuria.
Tratamiento de los trastornos hidroelectrolíticos y del equilibrio ácido-básico
Retención de agua y sodio: en los estadios iniciales de la ERC (leve-moderada) no suele ser
necesario modificar la ingesta de sal, salvo en situaciones específicas (síndrome nefrótico,
insuficiencia cardiaca o síndrome hepatorrenal). En estadios más avanzados, la ingesta
recomendada de sal es de aproximadamente 4-6 g de sal al día, produciendo una disminución
de la TAS 4-5 mm Hg.
Con FG < 10-15 ml/min/1,73 m2, es fundamental mantener una restricción hídrica (en
función de las pérdidas insensibles, que se estiman en 500 ml, y la diuresis del paciente). Si a
pesar de lo anterior el paciente continúa con datos de sobrecarga hidrosalina, se deben añadir
fármacos diuréticos. Los diuréticos de elección son los diuréticos de asa, entre los que están la
furosemida (Seguril®), con una dosis inicial de 40-80 mg, o la torasemida (Dilutol®) (mayor
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1011]
[63] ENFERMEDAD RENAL CRÓNICA
biodisponibilidad), con una dosis inicial de 10-20 mg; con incremento posterior según la
respuesta y el grado de insuficiencia renal.
Otra opción son los diuréticos tiazídicos (que potencian a los diuréticos de asa), entre
los que está la clortalidona (Higrotona®), con dosis inicial de 50 mg; sin olvidar que son
ineficaces de forma aislada con FG < 25-30 ml/min/1,73 m2. Otro grupo de fármacos, los
diuréticos ahorradores de potasio (amilorida, triamtereno y los antagonistas de la aldosterona
–espironolactona y eplerenona–), se deben manejar con cautela por el riesgo de
hiperpotasemia, sobre todo cuando se utilizan en pacientes diabéticos y que reciben
tratamiento combinado con IECA o ARA-II.
Hiperpotasemia: el riesgo de hiperpotasemia aumenta de forma significativa cuando la tasa de
FG es menor de 20 ml/min/1,73 m2. Se recomienda reducir la ingesta de potasio a < 60
mEq/día, con restricción de verduras (evitar la ingesta de tomate y patatas), frutas y frutos
secos. Se utilizan resinas de intercambio iónico (poliestirensulfonato cálcico –Resincalcio®
sobres– en dosis de 10-40 g/día), asociado a laxantes para evitar el estreñimiento. El uso de
bicarbonato oral y diuréticos también favorece el control de la hiperpotasemia.
Acidosis metabólica: la prevalencia y gravedad de la acidosis aumenta a medida que empeora
la ERC. La acidosis metabólica inhibe el anabolismo proteico, empeora la hiperpotasemia y
acelera la pérdida de masa ósea (actuando el hueso como amortiguador). Se recomienda el
tratamiento con bicarbonato oral en pacientes con concentraciones séricas < 22 mEq/l. Hay que
tener en cuenta que los suplementos de bicarbonato (que contienen sodio) pueden empeorar
la hipertensión y la sobrecarga de volumen.
Magnesio: se produce hipermagnesemia con un aporte excesivo de magnesio (con la
administración de antiácidos que contengan magnesio o con la aplicación de enemas). La
eliminación renal de magnesio se afecta con los diuréticos ahorradores de potasio.
Hiperuricemia: no existe evidencia suficiente que sustente o rechace el uso de fármacos
hipouricemiantes para frenar la progresión de la ERC. Se recomienda tratamiento de la
hiperuricemia sintomática en pacientes con ERC para obtener niveles de ácido úrico < 7 mg/dL.
Algunos autores recomiendan el tratamiento de la hiperuricemia asintomática con alopurinol
en los pacientes con ERC (especialmente con concentraciones de ácido úrico superiores a 8
mg/dL), ya que podría disminuir el riesgo cardiovascular y frenar la progresión de la ERC.
1.4. Tratamiento de las alteraciones hematológicas
La anemia de la ERC es una de complicaciones que influye significativamente en la sintomatología y la
calidad de vida del paciente, y a su vez tiene un impacto decisivo en el pronóstico de la ERC. Suele ser de
origen multifactorial, asociada a inflamación crónica, déficit de hierro y deficiencia relativa de
eritropoyetina. La anemia asociada a ERC suele ser normocítica y normocrómica en su origen.
Existen tres aspectos fundamentales para la evaluación de la anemia en la ERC, que son:
1) Realizar un adecuado diagnóstico diferencial y descartar causas secundarias (déficit de hierro,
vitamina B12 y/o ácido fólico); 2) suplementar farmacológicamente el hierro, de ser necesario, y 3) emplear
agentes estimuladores de la eritropoyesis en pacientes con una hemoglobina (Hb) < 11 g/dL (aunque no
existe un consenso claro sobre cuándo debe iniciarse). Se ha evidenciado que pacientes sintomáticos o con
cardiopatía isquémica pueden beneficiarse de un tratamiento más precoz. Las cifras de hemoglobina
objetivo se sitúan en 10-11,5 g/dL, evitando cifras superiores por su asociación a mayor mortalidad
cardiovascular (Figura 2).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1012]
[63] ENFERMEDAD RENAL CRÓNICA
Hierro: se debe suplementar hierro cuando se evidencie su déficit (ferritina < 500 ng/ml o
saturación de transferrina < 20%). Se comenzará el tratamiento con hierro oral, y si aparece
intolerancia digestiva o no existe respuesta a la ferroterapia oral, se valorará la administración
de hierro intravenoso.
Agentes estimuladores de la eritropoyesis (EPO): se debe considerar el inicio de tratamiento
con eritropoyetina recombinante humana cuando se ha corregido el déficit de hierro y otras
posibles causas subyacentes; siempre se deben tener en cuenta sus beneficios (disminuir la
necesidad de transfusiones sanguíneas y mejorar los síntomas relacionados con la anemia) y
sus posibles riesgos (aumento del riesgo de accidente cerebrovascular [ACV], pérdida del
acceso vascular, crisis epilépticas e hipertensión). La monitorización de los marcadores férricos
se realizará cada mes al inicio del tratamiento con EPO y cada 3 meses al estabilizarse la
hemoglobina. La concentración de Hb debe medirse cada 1-2 semanas tras el inicio de
tratamiento con EPO, o después de cada modificación del tratamiento (aumento o disminución
de dosis), hasta que se estabilice la Hb y la dosis de EPO. El objetivo es un aumento de 1-2 g/dL
de hemoglobina al mes hasta alcanzar el objetivo. Si este incremento es > 2,5 g/dL al mes, se
disminuirá la dosis semanal en un 25-50%, y si es < 0,7 g/dL en 2-4 semanas, la dosis semanal
deberá aumentarse un 50%.
Transfusiones sanguíneas: se recomienda evitar las transfusiones sanguíneas por sus riesgos
generales, pero especialmente en aquellos pacientes en lista de espera de trasplante renal,
para evitar la alosensibilización. Solamente debe considerarse cuando existe una disminución
brusca de los niveles de Hb (hemorragia gastrointestinal aguda o tras cirugía) o cardiopatía
isquémica.
Figura 2. Algoritmo para el manejo de la anemia en la enfermedad renal crónica.
1.5. Tratamiento de las alteraciones del metabolismo mineral y óseo
Las alteraciones del metabolismo óseo y mineral pueden comenzar en los grados iniciales de la ERC
avanzada y aumentan a medida que la enfermedad progresa. Las alteraciones observadas se caracterizan
por una hiperfosfatemia por disminución de la excreción renal (que se acentúa generalmente a partir del
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1013]
[63] ENFERMEDAD RENAL CRÓNICA
estadio 3) y déficit de vitamina D3, al estar disminuida la activación renal de la misma. En este contexto, se
produce un hiperparatiroidismo secundario y enfermedad ósea renal (Figura 3).
Figura 3. Diferentes formas de enfermedad ósea renal.
En la evaluación de estos pacientes hay que determinar niveles séricos de calcio, fósforo, vitamina
D, PTH intacta y bicarbonato. La frecuencia de la monitorización dependerá del estadio de la ERC (Tabla X).
El objetivo del tratamiento de las alteraciones del metabolismo calcio-fósforo en la ERC es evitar la
hiperfosforemia, la hipocalcemia y la hipovitaminosis D; para evitar el aumento progresivo y descontrolado
de la PTH y el desarrollo incluso de un hiperparatiroidismo grave o terciario. Los valores recomendados se
observan en la tabla XI.
Déficit de vitamina D: la deficiencia de vitamina D se debe reponer siguiendo las estrategias
recomendadas en la población general. Las dosis exactas no están bien definidas, pero se han
establecido entre 300 y 800 UI/día, considerándose un máximo de 2.000 UI/día (60.000
UI/mes). En España se utilizan varios preparados, entre los que cabe mencionar calcidiol
(Hidroferol®) en ampollas de 16.000 UI, que se pueden administrar de forma quincenal o
mensual, ajustando según los niveles de calcio y fósforo plasmáticos.
Control de la hiperfosfatemia (quelantes del fósforo): suele ser necesario su uso a partir del
estadio 3 de la ERC (FG < 60 ml/min/1,73 m2). Existen preparados con contenido cálcico
(administrados fuera de la comida pueden aportar calcio) y sin él (Tabla XII).
Otros: existen otros fármacos, como un análogo de la vitamina D, el paricalcitol (Zemplar®) y un
calcimimético (Mimpara®). Ambos tienen como objetivo la disminución de la PTH, indicado en
pacientes con tratamiento renal sustitutivo (TRS).
Tabla X. Intervalo de medida de hormona paratiroidea, calcio y fósforo según el estadio de enfermedad renal crónica.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1014]
[63] ENFERMEDAD RENAL CRÓNICA
Tabla XI. Valores bioquímicos recomendados.
Tabla XII. Fármacos para el tratamiento de la hiperfosfatemia.
2. TRATAMIENTO RENAL SUSTITUTIVO
A pesar de todos los esfuerzos para optimizar el manejo de la ERC, muchos de los pacientes
requerirán TRS. La decisión de inclusión de un paciente en programa de diálisis debe valorarse en una
consulta especializada de ERC avanzada (ERCA) con el soporte de una consulta de enfermería especializada,
de forma individualizada, en función de las condiciones psíquicas, clínicas y la capacidad de adaptación del
paciente y su familia. Cuando se decida un manejo conservador de la ERCA (alta mortalidad a corto plazo,
poca posibilidad de mejoría en calidad de vida, pacientes muy ancianos o que no deseen comenzar TRS),
debe coordinarse un manejo domiciliario multidisciplinar (nefrólogo, médico de atención primaria y
equipos de soporte domiciliario), para facilitar el bienestar del paciente, minimizando el impacto físico y
familiar de su condición de salud.
El inicio óptimo del TRS es aquel que se realiza de forma planificada. La falta de previsión en tal
inicio aumenta innecesariamente la morbilidad, las infecciones y el número de hospitalizaciones (por uso
de catéteres para hemodiálisis). Se debe plantear el inicio de TRS cuando el FG sea < 15 ml/min/1,73 m 2 o
antes, si aparecen signos y síntomas de uremia (pericarditis o encefalopatía urémica), dificultad para el
control de la TA, sobrecarga de volumen, hiperpotasemia grave, acidosis metabólica grave o
empeoramiento del estado nutricional. Por norma general, se iniciará TRS con la modalidad elegida cuando
el FG esté situado entre 8 y 10 ml/ min/1,73 m2 y es imprescindible con FG < 6 ml/min/1,73 m2.
Existen tres opciones de tratamiento renal sustitutivo actualmente, que son:
Hemodiálisis crónica: se realiza a través de una fístula arteriovenosa o a través de un catéter
venoso central (temporal o permanente; en la vena yugular, subclavia o femoral).
Habitualmente, se pautan tres sesiones semanales de 4 horas de duración cada una, ajustando
en función de las características del paciente.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1015]
[63] ENFERMEDAD RENAL CRÓNICA
Diálisis peritoneal ambulatoria: utiliza el peritoneo como membrana dializante. Se implanta un
catéter peritoneal y se puede realizar de forma manual o automatizada. La elección de esta
técnica depende de la situación social, laboral y familiar del paciente y de sus condiciones
clínicas.
Trasplante renal: es la opción ideal (especialmente de forma anticipada y de un donante vivo).
Permite la recuperación de la calidad de vida del paciente, no olvidando los riesgos que
conlleva la inmunosupresión (infecciones, neoplasias). En los últimos años hay una mayor
supervivencia del injerto renal con nuevos fármacos inmunosupresores.
BIBLIOGRAFÍA
Bover J, Cebolla J, Escalada J, Esmatjes E, Fácila L, Gamarra J, et al. Documento de consenso sobre la
enfermedad renal crónica. 2012.
Choi M, Fried L. Chronic kidney disease and progression. NephSAP. Am Soc Nephrol. 2015;14:4.
Gorostidi M, Santamaría R, Alcázar R, Fernández-Fresnedo G, Galcerán JM, Goicoechea M, et al.
Documento de la Sociedad Española de Nefrología sobre las guías KDIGO para la evaluación y el
tratamiento de la enfermedad renal crónica. Nefrología. 2014;34(3):302-16.
Kidney Disease: Improving Global Outcomes (KDIGO) Anemia Work Group. KDIGO Clinical Practice
Guideline for Anemia in Chronic Kidney Disease. Kidney Inter. 2012;2(Suppl):279-335.
Parikh S, Haddad N, Hebert L. Retarding progression of kidney disease. En: Johnson RJ, Feehally J,
Floege J, editores. Comprehensive Clinical Nephrology. 5ª edición. Philadelphia: Saunders; 2015.
Tomlinson L, Wheeler D. Clinical evaluation and management of chronic kidney disease. En: Johnson
RJ, Feehally J, Floege J, editores. Comprehensive Clinical Nephrology. 5ª edición. Philadelphia:
Saunders; 2015.
Torregrosa JV, Cannata Andia J, Bover J, Caravaca F, Lorenzo V, Martín de Francisco AL, et al.
Recomendaciones de la Sociedad Española de Nefrología para el manejo de las alteraciones del
metabolismo óseo-mineral en los pacientes con enfermedad renal crónica (SEN-MM). Nefrología.
2011;31(Suppl 1):3-32.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1016]
[64] TRASTORNOS DEL EQUILIBRIO ÁCIDO-BASE
64.Trastornos del equilibrio ácido-base
Beatriz Redondo Navarro.
Nefrología
Pilartxo Catalán Martín.
Medicina Interna
Asesora:
Mª Esther González Monte.
Médica Adjunta de Nefrología
I. CONCEPTO
El pH (potencial de hidrogeniones) se define como el logaritmo negativo en base de 10 de la
actividad de los iones hidrógeno (pH = – log10 [aH+]). Es una forma de medir la concentración de
hidrogeniones (H+), iones tan activos que pequeñas variaciones en su concentración alteran de forma
significativa las reacciones enzimáticas celulares. Por ello, para un correcto mantenimiento de la
homeostasis del organismo, se requiere un pH estable entre 7,35-7,45. Para lograr esto, existen
mecanismos o sistemas compensadores, llamados sistemas tampón o búfer, los cuales captan o liberan H+
en respuesta a pequeñas variaciones del pH. Estos sistemas son intracelulares (proteínas, hemoglobina,
fosfatos, carbonatos) y extracelulares. Entre estos últimos, el fundamental es el sistema
bicarbonato/dióxido de carbono (HCO3-/CO2), que reacciona con los H+ mediante la siguiente fórmula:
H+ + HCO3- ↔ H2CO3 ↔ H2O + CO2
Por ello, la regulación última del pH depende del riñón y del pulmón, que mantienen la
concentración de bicarbonato y de dióxido de carbono, respectivamente, dentro de unos estrechos límites.
La disminución del pH por debajo de 7,35 se denomina acidosis y la elevación por encima de 7,45,
alcalosis. La acidosis puede deberse a una disminución del bicarbonato (acidosis metabólica) o a una
elevación de la presión parcial de dióxido de carbono (pCO2) (acidosis respiratoria). A su vez, la alcalosis
puede ser consecuencia de una elevación del bicarbonato (alcalosis metabólica) o a un descenso de la pCO2
(alcalosis respiratoria). La aparición de cualquiera de estos trastornos activa los mecanismos reguladores
descritos anteriormente para mantener el pH en el rango de la normalidad. La compensación respiratoria
de los trastornos metabólicos es rápida, aunque no es máxima hasta transcurridas 12-24 horas, mientras
que la compensación renal de los trastornos respiratorios es más lenta, ya que se inicia entre 6-12 horas
tras la aparición del trastorno, alcanzándose la respuesta máxima días o semanas después.
II. INTERPRETACIÓN GASOMÉTRICA
Una correcta valoración de la situación clínica del paciente es suficiente para sospechar la presencia
del trastorno ácido-base asociado al cuadro clínico al que nos enfrentemos. La realización de una
gasometría es el siguiente paso; suele recogerse a partir de una muestra de sangre arterial, aunque el uso
de sangre venosa es también correcto siempre que no se demore su utilización para evitar la alteración de
los distintos parámetros gasométricos.
Para la correcta identificación de los trastornos ácido-base es aconsejable seguir una sistemática
habitual:
Comprobar el valor del pH: los valores considerados normales se detallan en la tabla I.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1017]
[64] TRASTORNOS DEL EQUILIBRIO ÁCIDO-BASE
Tabla I. Valores normales para las variables del equilibro ácido-base en sangre arterial y venosa.
Examinar cambios direccionales de pCO2 y HCO3- con respecto a su valor normal. La respuesta
compensadora fisiológica debe tener idéntica dirección a la del componente alterado (Tabla II).
Tabla I.
Evaluar el grado de compensación: nunca se alcanza un pH normal en un paciente por medio
únicamente de la compensación, puesto que este mecanismo compensatorio se agota y con el
tiempo puede llegar a detenerse. En la tabla III se detallan los grados de compensación que se
consideran adecuados para cada trastorno del equilibrio ácido-base.
Calcular el hiato aniónico (ver Apartado II.2.).
Descartar la existencia de un trastorno ácido-básico mixto: un trastorno mixto es aquel en el
que coexisten simultáneamente dos anomalías primarias del equilibrio ácido-base. Se sospecha
cuando las alteraciones de la pCO2 y el HCO3- van en distinto sentido, o cuando la magnitud de
una compensación está fuera de los límites esperados para un trastorno primario según lo
descrito en la tabla III.
Tabla III. Compensaciones adecuadas en los trastornos ácido-base.
III. ACIDOSIS METABÓLICA
1. Concepto
La acidosis metabólica es un trastorno caracterizado por un descenso primario de la concentración
plasmática de HCO3 -, que tiende a la disminución del pH arterial, desencadenando una hiperventilación
compensadora con descenso de la pCO2.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1018]
[64] TRASTORNOS DEL EQUILIBRIO ÁCIDO-BASE
2. Etiopatogenia
Tres son los posibles orígenes de una acidosis metabólica: 1) la amortiguación con HCO3 - de un
ácido no volátil añadido al organismo; 2) la pérdida de HCO3 - en los líquidos corporales, y 3) la adición
rápida al LEC (líquido extracelular) de soluciones sin HCO3 - (acidosis por dilución).
A efectos prácticos, se clasifican según el cálculo del AG o hiato aniónico, basado en el principio de
electroneutralidad, el cual representa el conjunto de aniones no medidos de forma habitual
(fundamentalmente albúmina, fosfatos y sulfatos):
AG = [Na+] – ([Cl-] + [HCO3])
Su valor normal se encuentra en 12 ± 2 mmol/l. Por tanto, tendremos un AG aumentado con la
adición de ácidos (y sus aniones correspondientes) orgánicos, y disminuido cuando desciendan los aniones
no determinados, distintos del Cl- y el HCO3 - (principalmente albúmina). La hipoalbuminemia es una
situación muy frecuente en la práctica clínica y es útil corregir el valor del AG según la siguiente fórmula:
AG corregido = AG calculado + 0,25 x (4,4 – albúmina sérica en g/dL)
Las acidosis con AG aumentado (o normoclorémicas) se producen por aumento en la
producción/ganancia de ácidos. Las acidosis metabólicas con AG normal suelen estar causadas por pérdida
de HCO3 - con hipercloremia (la cual garantiza la electroneutralidad).
Tabla IV. Clasificación de la acidosis metabólica.
3. Clínica
La causa subyacente del trastorno ácido-base es la responsable del cuadro clínico, aunque, en
general, pueden observarse síntomas directos en varios niveles:
3.1. Aumento de esfuerzo ventilatorio y, en acidosis graves (pH < 7,20), respiración de Kussmaul.
3.2. Cardiovasculares: hipotensión, shock y edema pulmonar (por disminución de las resistencias
vasculares periféricas), depresión de la contractilidad cardiaca (con menor respuesta a las catecolaminas si
el pH < 7,25) y arritmias ventriculares (si el pH < 7,15).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1019]
[64] TRASTORNOS DEL EQUILIBRIO ÁCIDO-BASE
3.3. Óseo: debido, entre otros motivos, al efecto tamponador del hueso en el caso de acidosis
crónicas, ya que puede haber desmineralización ósea.
3.4. Neurológicos: cefalea, confusión, deterioro del nivel de consciencia y crisis comiciales. Son
menos llamativas que en las acidosis respiratorias.
3.5. Alteraciones electrolíticas: hiperpotasemia, hipercalcemia.
4. Clasificación (Tabla IV)
4.1. Acidosis metabólica hiperclorémica (con AG normal) (Tabla V)
Tabla V. Clasificación de la acidosis metabólica hiperclorémica.
Pérdidas intestinales: suelen asociar hipopotasemia y depleción de volumen. La diarrea es la
causa más frecuente de este tipo de acidosis. En el caso de las ileostomías, la pérdida de HCO3 -
es mayor cuanto más reciente es su creación. En las derivaciones intestinales, la acidosis en las
anastomosis ureterocólicas suele ser más grave que las utereroileales. En su tratamiento se
debe tener en cuenta la cantidad de Cl- y K+ en los sueros de reposición.
Tabla VI. Acidosis tubulares renales.
Pérdidas renales: acidosis tubulares renales (Tabla VI). Deben sospecharse cuando se eliminan
las causas no renales (por ejemplo, diarrea).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1020]
[64] TRASTORNOS DEL EQUILIBRIO ÁCIDO-BASE
Acidosis por dilución: la expansión rápida del LEC con líquidos sin HCO3 - provoca dilución del
contenido plasmático y una acidosis leve que se corrige rápidamente mediante generación
renal de HCO3 -.
Ganancia de ácidos: la administración de nutrición parenteral con aminoácidos sin
administración concomitante de álcalis (lactato, acetato) puede producir acidosis metabólica.
Es excepcional en pacientes sin insuficiencia renal.
4.2. Acidosis metabólica normoclorémica (con AG elevado)
Acidosis láctica: la concentración normal de lactato en plasma es de 0,5-1,5 mEq/l. La acidosis
láctica se caracteriza por valores de lactato sérico superiores a 4 mEq/l. Entre las causas
principales cabe mencionar la sobreproducción bacteriana intestinal (obstrucciones, isquemia),
la hipoxia tisular (shock, intoxicación por monóxido de carbono), la insuficiencia hepatocelular y
ciertos fármacos (metformina, nitroprusiato, isoniazida, inhibidores de la transcriptasa inversa).
Su diagnóstico es de exclusión y el tratamiento es el de la enfermedad de base.
Cetoacidosis diabética: para su diagnóstico es importante la presencia de hiperglucemia junto
con la acidosis, y suele acompañarse de alteraciones electrolíticas (hipopotasemia,
hipomagnesemia), que se deben considerar al establecer el tratamiento. El uso de bicarbonato
queda reservado para acidosis graves (pH < 7).
Cetoacidosis alcohólica: se produce en pacientes con larga evolución de abuso enólico junto
con disminución de la ingesta y, en algunas ocasiones, con historia de náuseas y vómitos. En
este contexto, el acúmulo de cetoácidos se debe a una gluconeogénesis baja y a la consecuente
lipólisis acelerada. La glucemia varía entre 50-250 mg/dL. Puede transformarse en un trastorno
mixto si se acompaña de vómitos (alcalosis metabólica). El tratamiento consiste en la reposición
de volumen, vitamina B1 y glucosa, así como de los déficits electrolíticos asociados.
Cetoacidosis de ayuno: sucede por producción de cetoácidos debida al aumento del
metabolismo de las grasas; la integridad de la liberación de insulina controla la lipólisis y no hay
acidosis importante. El HCO3 - suele ser > 18 mEq/l y no requiere tratamiento específico.
Intoxicación por alcoholes: el etilenglicol es un componente de los anticongelantes y
disolventes y la grave toxicidad se produce por sus metabolitos activos, principalmente los
ácidos glicólico, glioxílico y oxálico. La toxicidad provoca edema cerebral difuso, depresión del
sistema nervioso central (SNC), acidosis metabólica severa, nefrotoxicidad con necrosis tubular
aguda por depósitos de cristales de oxalato cálcico e hipocalcemia (la cual se debe tener en
cuenta en la corrección de la acidosis). A nivel cardiaco, puede provocar arritmias e
insuficiencia cardiaca. La intoxicación aguda por metanol cursa con una acidosis metabólica
severa por la transformación del metanol en formaldehído y ácido fórmico. A altas dosis
provoca depresión miocárdica, afectación de la retina, obnubilación, convulsiones y coma. El
metanol no se ha descrito como tóxico renal directo, pero puede provocar insuficiencia renal
aguda por rabdomiólisis. En la intoxicación inicial de ambos puede haber un pH normal, aunque
es más típico un hiato osmolal > 25 mOsm/kg (diferencia entre la osmolalidad medida del suero
y la osmolalidad calculada) por las características de estas moléculas. El tratamiento se basa en
la sueroterapia, administración de fomepizol (un inhibidor de la enzima alcohol
deshidrogenasa) y, en el caso de que hubiera insuficiencia renal o pH < 7,20, valorar la
realización de hemodiálisis.
Intoxicación por salicilatos: se trata de un trastorno complejo en el que, aparte de la acidosis
metabólica por la ganancia de ácidos, sucede alcalosis respiratoria por hiperventilación. El
manejo consiste en el tratamiento de soporte, la administración de bicarbonato para alcalinizar
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1021]
[64] TRASTORNOS DEL EQUILIBRIO ÁCIDO-BASE
la orina (excepto si existe alcalosis respiratoria) y, si los niveles plasmáticos de salicilato son
superiores a 90 mg/dL o hay clínica grave, hemodiálisis.
5. Tratamiento
El tratamiento de base de la acidosis metabólica es el de la causa subyacente, de modo que se
deben corregir los déficits de volumen y electrólitos. Es imprescindible monitorizar el K+ y el Ca2+
plasmáticos. En general, se tratan aquellas acidosis agudas que no tengan una fuente “potencial” de
producción de álcali, como es el caso de la acidosis de la enfermedad renal crónica (ERC), las intoxicaciones
y en caso de las pérdidas digestivas y renales. En el resto de los casos, se debe manipular el bicarbonato en
el contexto agudo solo si el pH afecta de manera adversa a la función de los órganos, si el pH < 7,15. En
cuanto a las acidosis crónicas, su tratamiento sí es beneficioso y, en el caso de la ERC puede preservar la
función renal y aminorar la pérdida de masa ósea.
El déficit de bicarbonato se calcula según la siguiente fórmula, suponiendo que el volumen de
distribución del bicarbonato (agua corporal total) representa el 60% del peso del paciente:
Déficit de bicarbonato = 0,6 x Peso (kg) x ([HCO3-] deseado – [HCO3-] medido)
Como norma general, la reposición se debe hacer de forma lenta, corrigiendo aproximadamente la
mitad del déficit en las primeras 24 horas (variará según la gravedad del cuadro clínico), monitorizando de
cerca el estado volémico del paciente y la evolución gasométrica.
Existen varios preparados de bicarbonato que se administran por vía intravenosa u oral (Tabla VII).
Se prefiere el uso de bicarbonato 1 M en casos graves o en pacientes con sobrecarga de volumen. Debe
administrarse por una vía distinta al resto de fármacos para evitar su precipitación.
Tabla VII. Formas de presentación del bicarbonato.
Su administración debe ser cuidadosa, y se debe vigilar la aparición de las posibles complicaciones:
sobrecarga de volumen y/o de sodio (cuando se requieren grandes cantidades de bicarbonato sódico en
pacientes con disfunción miocárdica o insuficiencia renal); hipopotasemia, hipofosfatemia, hipocalcemia y
tetania; alcalosis de rebote (por exceso de corrección intravenosa de bicarbonato o por persistencia de
hiperventilación al corregir más rápido el pH del LEC que el del líquido cefalorraquídeo); arritmias cardiacas
(si se perfunde rápidamente por un catéter central y la perfusión no es diluida), e hipoventilación.
IV. ALCALOSIS METABÓLICA
1. Concepto y fisiopatología
La alcalosis metabólica se caracteriza por una elevación del pH debida al aumento primario de la
concentración plasmática de bicarbonato y, de forma compensadora, un incremento de la pCO2. Para su
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1022]
[64] TRASTORNOS DEL EQUILIBRIO ÁCIDO-BASE
desarrollo se requiere una causa inicial (bien por pérdidas digestivas o renales de H+ o por un aporte
excesivo de bicarbonato) y un factor de mantenimiento que evite que se elimine el exceso de bicarbonato.
Un riñón sano es capaz de eliminar el exceso de HCO3 - plasmático, por lo que el factor de mantenimiento
de la alcalosis suele afectar directa o indirectamente a la función renal. Los tres mecanismos son:
Coexistencia de disminución del volumen circulante eficaz: ya sea total o relativo; en ella, los
mecanismos de compensación de reabsorción tubular de sodio se acompañan de reabsorción
de bicarbonato. La corrección de la hipovolemia disminuirá la activación del sistema renina-
angiotensina-aldosterona y corregirá la alcalosis, y al utilizarse el cloro como anión alternativo
en la reabsorción de sodio, se permite la excreción del exceso de bicarbonato por la orina
(alcalosis cloro-sensible). En este caso, la reexpansión de volumen sin aporte de cloro no
corregiría la alcalosis.
Hiperaldosteronismo (no secundario a hipovolemia): en este caso, la inadecuada actividad
mineralocorticoidea inicia y mantiene la alcalosis al incrementar la excreción distal de H+, con la
consiguiente regeneración de HCO3- . No hay respuesta a la expansión de volumen en este caso.
Hipopotasemia grave (K+ < 2 mEq/l): puede ser una consecuencia de la alcalosis metabólica,
pero participa en su mantenimiento, dado que favorece la excreción distal de H+ y, por tanto, la
regeneración de HCO3-.
2. Clínica
No hay síntomas ni signos específicos de alcalosis metabólica. En casos moderados ([HCO- 3] < 40
mEql/l), el paciente suele estar asintomático. En casos más graves (pH > 7,55), pueden observarse
alteraciones del SNC (confusión, estupor, convulsiones e hipoventilación), alteraciones relacionadas con la
hipocalcemia (arritmias cardiacas con prolongación del intervalo QT, tetania, calambres musculares,
parestesias) y la hipopotasemia (debilidad muscular, hiperreflexia y disminución de la contractilidad
miocárdica). Además, puede haber síntomas y signos asociados a la deshidratación (astenia, ortostatismo).
Figura 1. Etiología de la alcalosis metabólica.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1023]
[64] TRASTORNOS DEL EQUILIBRIO ÁCIDO-BASE
3. Diagnóstico etiológico
La etiología de la alcalosis metabólica (Figura 1) puede deducirse habitualmente de la historia
clínica, deteniéndonos en la presencia o no de hipertensión o edemas, y la concentración urinaria de cloro
(Cl0), puesto que la concentración de sodio urinario es inconstante en la alcalosis al excretarse junto con el
exceso de bicarbonato. Las causas más frecuentes son los vómitos y el uso de diuréticos. Si el origen no es
obvio, se debe sospechar vómitos o ingesta de diuréticos de forma subrepticia, o una de las causas de
hiperaldosteronismo.
La Cl0- sirve para orientar el diagnóstico etiológico, ya que permite diferenciar dos entidades:
Alcalosis con depleción de cloro (sensible al cloro): en la que Cl0- < 25 mEq/l. Aparece en
situaciones de contracción de volemia (vómitos, diarrea, sudor, diuréticos). Suele ser más leve y
responde a la reposición con suero salino fisiológico.
Alcalosis sin depleción de cloro (resistente al cloro): es el caso del exceso de
mineralocorticoides. En este caso, Cl0-- > 40 mEq/l y no responde a la expansión de volumen.
Figura 1. Etiología de la alcalosis metabólica.
4. Tratamiento
Se deben tratar tanto las causas específicas como los mecanismos de mantenimiento, teniendo
como objetivo alcanzar una cifra de pH < 7,55 y HCO3 - < 40 mEq/l.
4.1. Alcalosis con depleción de cloro
Se corregirá la depleción de volumen mediante administración de suero salino al 0,9%. Si existe
hipopotasemia, esta se debe reponer, ya sea por vía oral con cloruro potásico (KCl) o añadido a los sueros.
Nunca se repondrá con citrato o acetato potásico (BOI-K®), ya que se transforma en HCO3 - y agravaría la
alcalosis. El aporte de volumen debe ajustarse estrechamente en función de la tensión arterial, la diuresis y
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1024]
[64] TRASTORNOS DEL EQUILIBRIO ÁCIDO-BASE
el riesgo de sobrecarga hídrica. En el caso de que el aporte de volumen se vea limitado por la sobrecarga
hídrica, puede intentarse reposición de cloro por vía oral con KCl siempre que no haya peligro de
hiperpotasemia. Además, hay que corregir la causa (suspender el diurético, tratamiento de los vómitos,
antagonistas H2 o inhibidores de la bomba de protones en portadores de sonda nasogástrica para reducir la
pérdida de H+).
4.2. Alcalosis sin déficit de cloro
El tratamiento depende de la causa. En los pacientes con hiperaldosteronismo se tratará su causa
(cirugía si existe un adenoma suprarrenal, diuréticos ahorradores de K+ como amiloride o espironolactona)
junto con restricción de sodio y dieta libre de potasio. En los estados edematosos (insuficiencia cardiaca,
síndrome nefrótico o cirrosis), en los que la alcalosis se asocia al tratamiento diurético, se intentará retirar
o disminuir la dosis en la medida de lo posible. Cuando estos pacientes presentan una alcalosis grave (pH >
7,6) o asocian una acidosis respiratoria crónica (la hipoventilación compensadora por el incremento del pH
puede provocar hipoxemia) se puede emplear acetazolamida a dosis de 250 mg/24-48 h, ya que aumenta la
excreción renal de HCO3 -; para valorar su efectividad se monitorizará el pH urinario, ya que no será útil con
pH > 7. Como efectos adversos puede causar hipopotasemia y un aumento transitorio de la pCO2. La
infusión de HCl se reserva para casos graves (pH > 7,7) y estos pacientes deben ser ingresados en una
unidad de cuidados intensivos.
V. ACIDOSIS RESPIRATORIA
1. Concepto y fisiopatología
Es el proceso fisiopatológico consistente en la disminución del pH sanguíneo (pH < 7,35) debido a
un aumento primario de la pCO2 (hipercapnia), que produce un incremento variable secundario del HCO3 -
compensador. El principal mecanismo que regula la presión parcial arterial de CO2 (PaCO2) es la ventilación
alveolar. Esta está controlada por dos estímulos diferentes: la hipercapnia y la hipoxia. La hipercapnia
(menor eliminación de CO2 debida, generalmente, a una alteración en la ventilación alveolar efectiva:
hipoventilación) es el estímulo más potente de la ventilación en condiciones normales. El aumento de la
pCO2 produce un descenso en el pH que es detectado por los quimiorreceptores de la médula,
provocándose un aumento de la ventilación. La hipoxia, a su vez, estimula los receptores situados en el
bulbo carotídeo al alcanzar la presión parcial arterial de oxígeno (PaO2) valores de 50-60 mm Hg. Sin
embargo, en pacientes con hipercapnia crónica, el estímulo principal es la hipoxia, que es capaz de producir
un aumento en la ventilación con niveles de PaO2 < 80 mm Hg.
2. Clasificación
Dependiendo del tiempo de instauración de la acidosis respiratoria, esta puede ser aguda o crónica.
Cuando la instauración es aguda, la compensación metabólica (renal) es escasa, puesto que se basa en los
tampones intracelulares (hemoglobina, proteínas), estando así el organismo desprotegido (solo aumenta el
bicarbonato 1 mEq por cada 10 mm Hg que se incrementa la pCO2), siendo la respuesta renal de
eliminación de H+ tardía; sin embargo, si la hipercapnia se mantiene, se estimulará la secreción renal de H+,
con la consiguiente regeneración de bicarbonato y la reabsorción de bicarbonato en el túbulo proximal,
tendiendo a la normalización del pH. Esta respuesta comienza a los 3-5 días, y produce un aumento de
bicarbonato de 3-5 mEq por cada 10 mm Hg que aumenta la pCO2.
3. Etiología
Ante un paciente con acidosis respiratoria, se deben buscar causas de hipoventilación (Tabla VIII).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1025]
[64] TRASTORNOS DEL EQUILIBRIO ÁCIDO-BASE
4. Clínica
4.1. Acidosis respiratoria aguda A nivel neurológico, produce diversos síntomas como cefalea, visión
borrosa, agitación y ansiedad. Conforme aumenta su gravedad, pueden aparecer temblores, asterixis,
delirio, somnolencia y finalmente el coma. Los síntomas se deben al aumento del flujo cerebral secundario
al descenso del pH cerebral que produce hipertensión intracraneal y papiledema (encefalopatía
hipercápnica). A nivel cardiaco, produce hipotensión arterial por vasodilatación arteriolar y favorece la
aparición de arritmias, tanto supraventriculares como infraventriculares, por favorecer el mecanismo de
reentrada, y bajar el umbral para la fibrilación ventricular.
Tabla VIII. Etiología de la acidosis respiratoria.
4.2. Acidosis respiratoria crónica
El paciente puede mantener un pH normal por los mecanismos compensadores renales, y estar
asintomático, aunque la hipercapnia crónica favorece la instauración de cor pulmonale, y por consiguiente,
signos y síntomas de congestión sistémica. La respuesta a las catecolaminas se encuentra reducida en la
acidosis de cualquier causa. Además, favorece la aparición de hiperpotasemia por la salida de potasio al
espacio extracelular.
5. Diagnóstico
El diagnóstico se realiza mediante la gasometría arterial. Un pH bajo en presencia de hipercapnia es
diagnóstico de acidosis respiratoria. La historia clínica y la exploración física son fundamentales para
orientar el diagnóstico etiológico (Tabla VIII). El gradiente alvéolo-arterial de oxígeno (presión parcial
alveolar de oxígeno [PAO2]-PaO2) puede ser de utilidad para diferenciar las alteraciones tanto
intrapulmonares como extrapulmonares. El gradiente siempre está alterado en las alteraciones
pulmonares, pero también puede estarlo en las extrapulmonares. Sin embargo, un gradiente normal
prácticamente excluye una enfermedad pulmonar intrínseca.
6. Tratamiento
El pronóstico de la acidosis respiratoria grave lo va a determinar la hipoxemia, y no la hipercapnia,
por lo que el objetivo fundamental es mantener una oxigenación adecuada sin empeorar la hipercapnia.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1026]
[64] TRASTORNOS DEL EQUILIBRIO ÁCIDO-BASE
El manejo de la acidosis respiratoria depende de la causa, la severidad y del tiempo de instauración
(aguda o crónica).
6.1. Acidosis respiratoria aguda
Para disminuir la pCO2 se necesita aumentar la ventilación alveolar mediante el control de la
enfermedad subyacente (por ejemplo, broncodilatadores en la crisis asmática) o mediante la utilización de
la ventilación mecánica (no invasiva/invasiva), cuando esté indicada. Se considerará el uso de ventilación
mecánica en el caso de hipoxia severa refractaria, hipercapnia progresiva sintomática, agotamiento o
depresión del centro respiratorio (ver Capítulo 35. “Ventilación mecánica”). El papel del bicarbonato no
está bien definido si no existe acidosis metabólica asociada; su administración puede conllevar un aumento
de la pCO2 y mayor acidemia tisular, ya que se combina con los H+ de los tejidos produciendo más CO2, que
no será posible eliminar por la hipoventilación. Además, puede favorecer la sobrecarga hídrica, y si se
corrige la hipercapnia, llevar a una alcalosis metabólica. Por todo ello, en las acidosis respiratorias puras, el
bicarbonato no está indicado.
6.2. Acidosis respiratoria crónica
Hay que tratar la enfermedad de base. Si existe hipoxemia severa (PaO2 < 55-60 mm Hg) se
empleará oxigenoterapia, que aumenta la supervivencia y disminuye la severidad del cor pulmonale
(reduce la vasoconstricción pulmonar). Hay que emplearlo con precaución, puesto que un aporte excesivo
disminuye el principal estímulo ventilatorio de estos pacientes, que es la hipoxia, intentando mantener una
saturación de O2 del 88-92%, dado que es precisamente la hipoxia mantenida la que reduce la
supervivencia
VI. ALCALOSIS RESPIRATORIA
1. Concepto
Elevación del pH sanguíneo debido a una reducción primaria de la PaCO2 (hiperventilación
alveolar), que produce una disminución secundaria del bicarbonato de forma compensadora.
La hiperventilación puede estar provocada por hipoxemia (que estimula el centro respiratorio), así
como por otros desencadenantes como la anemia grave o la hipotensión, ya que la disminución del aporte
de oxígeno a los quimiorreceptores de los grandes vasos produciría una hiperventilación secundaria.
La hipocapnia provoca una vasoconstricción cerebral que puede conllevar hipoxia y,
consecuentemente, los síntomas característicos de la hiperventilación.
Es el trastorno del equilibrio ácido-base más frecuente.
2. Etiología
La causa más habitual de alcalosis respiratoria continúa siendo la crisis de ansiedad (Tabla IX).
3. Clínica
Es variable, aunque es más evidente en las situaciones agudas, en las que el cuadro clínico es
característico, con la aparición de parestesias acras y periorales, hormigueos, sensación de
entumecimiento, mareo y, en los casos más severos, tetania. Tanto la propia alcalosis como el descenso
acompañante del calcio iónico conducen a un aumento de la excitabilidad neuromuscular, provocando los
síntomas anteriormente descritos. Si la situación se agrava, puede aparecer síncope y aturdimiento (por
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1027]
[64] TRASTORNOS DEL EQUILIBRIO ÁCIDO-BASE
descenso del flujo cerebral debido a la vasoconstricción por la hipocapnia), e incluso arritmias cardiacas. En
la exploración física destaca la taquipnea.
Tabla IX. Causas de la alcalosis respiratoria.
4. Diagnóstico
El diagnóstico se basa en la confirmación mediante gasometría arterial de hipocapnia con pH
elevado. Los niveles sanguíneos de lactato pueden estar elevados y los de calcio iónico disminuidos.
5. Tratamiento
El de la causa subyacente y sintomático. Se debe tranquilizar al paciente, evitando la
hiperventilación secundaria a la ansiedad. Los síntomas, en crisis de ansiedad, pueden aliviarse haciendo
respirar al paciente en un sistema de bolsa cerrado o mediante la administración de sedación suave con
benzodiazepinas. La sedación más profunda puede estar indicada en los casos extremos. Si la
hiperventilación se debe a hipoxemia se debe administrar oxigenoterapia.
VII. TRASTORNOS MIXTOS
Son aquellos en los que existen de forma simultánea dos o más alteraciones del equilibro
ácidobase. No debe confundirse con la respuesta compensadora, según las directrices que se han descrito
en Apartado II. “Interpretación gasométrica”.
1. Acidosis respiratoria con acidosis metabólica
Surge cuando se combina un descenso de los valores de bicarbonato sérico con una elevación de la
pCO2. Las principales causas son aquellas en las que coexiste, de forma aguda o crónica, hipoventilación
junto con entidades desencadenantes de acidosis metabólica (parada cardiorrespiratoria, edema agudo de
pulmón, insuficiencia respiratoria hipercápnica con insuficiencia renal avanzada, diarrea, etc.). El pH
disminuye considerablemente incluso con alteraciones moderadas de la pCO2 y el HCO3, y el tratamiento
consiste en corregir primero la alteración respiratoria y, si fuera necesario, tratar el componente
metabólico junto con la patología de base.
2. Acidosis metabólica con alcalosis respiratoria
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1028]
[64] TRASTORNOS DEL EQUILIBRIO ÁCIDO-BASE
Es típica de la intoxicación por salicilatos, la intoxicación alcohólica, la sepsis y la insuficiencia
hepática asociada a insuficiencia renal. El pH puede ser normal o cercano a la normalidad, puesto que, en
cierto modo, se aumenta la compensación de cualquiera de los trastornos aislados. El tratamiento se
enfoca a la enfermedad de base y el problema acido-básico no suele requerir tratamiento.
3. Acidosis respiratoria con alcalosis metabólica
Representa uno de los trastornos mixtos más frecuentes. El escenario principal es un paciente
hipoventilador crónico que recibe tratamiento diurético o presenta síndrome emético. El pH puede ser
normal o bajo; gasométricamente se manifiesta como una elevación de la pCO2 y un aumento del
bicarbonato mayor de lo esperable únicamente por mecanismo compensador.
4. Alcalosis metabólica con alcalosis respiratoria
Ocurre cuando se combina un aumento del bicarbonato sérico con una disminución de la pCO2; por
ejemplo, una crisis de ansiedad en un paciente que toma diuréticos de forma crónica.
5. Acidosis y alcalosis metabólicas
Se producen al combinar una acidosis metabólica (cetoacidosis diabética, alcohólica o insuficiencia
renal crónica) con una situación que provoque alcalosis metabólica, como por ejemplo los vómitos
incoercibles.
BIBLIOGRAFÍA
Al-Jaghbeer M, Kellum JA. Acid-base disturbances in intensive care patients: etiology, pathophysiology
and treatment. Nephrol Dial Transplant. 2015;30(7):1104-11.
DuBose TD Jr. Acidosis and alkalosis. En: Longo DL, Fauci AS, Kasper DL, Hauser SL, Jameson JL,
Loscalzo J, editores. Harrison’s principles of internal medicine. Vol. 1. 18ª ed. New York: McGraw-Hill;
2012; p. 363-71.
Kaehny WD. El paciente con un trastorno ácido-base. En: Schrier RW. Manual de Nefrología. 8ª ed.
Philadelphia: Wolters Kluwer Health; 2015; p. 62-78.
Kraut JA, Madias NE. Diferential diagnosis of nongap metabolic acidosis: value of a systematic
approach. Clin J Am Soc Nephrol. 2012;7(4):671-9.
Rose BD. Post TW. Electrolitos y equilibrio ácido-base. 6ª ed. Madrid: Marbán; 2009; p. 1204-13.
Schrier RW. Trastornos renales e hidroelectrolíticos. 7ª ed. Philadelphia: Lippincott Williams & Wilkins;
2010; p. 86-121, 131-4.
Williams MH Jr, Shim CS. Ventilatory failure. Etiology and clinical forms. Am J Med. 1970;48(4):477-83.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1029]
[65] TRASTORNOS DEL EQUILIBRIO HIDROELECTROLÍTICO. SÍNDROME DE SECRECIÓN INADECUADA DE HORMONA
ANTIDIURÉTICA. FLUIDOTERAPIA
65.Trastornos del equilibrio hidroelectrolítico.
Síndrome de secreción inadecuada de hormona
antidiurética. Fluidoterapia
María Soledad Librizzi.
Endocrinología y Nutrición
Pilar Auñón Rubio.
Nefrología
Ángel Torralba Morón.
Medicina Interna
Asesores:
Miguel León Sanz.
Jefe de Sección de Endocrinología y Nutrición
Florencio García.
Médico Adjunto de Nefrología
I. ALTERACIONES EN EL EQUILIBRIO DEL SODIO Y DEL AGUA
A. CONCEPTO Y FISIOPATOLOGÍA
El agua corporal total está compuesta por el líquido intracelular y el extracelular. A su vez, este
último incluye los compartimentos intravascular e intersticial. En condiciones normales, el agua corporal
total supone el 60% del peso corporal en los varones y el 50% en las mujeres, del cual dos tercios
corresponden al compartimento intracelular y un tercio al extracelular.
La osmolaridad es la concentración de solutos por litro de solución. La osmolalidad es la
concentración de solutos por kilogramo de agua. El valor de la osmolaridad plasmática es similar al de la
osmolalidad (osmolaridad plasmática = osmolalidad plasmática × 0,93). En la práctica clínica se utiliza el
término osmolaridad plasmática, aunque el plasma no esté compuesto exclusivamente por agua.
Figura 1. Mecanismos de regulación de la volemia y osmolalidad plasmática.
En el compartimento extracelular, el sodio (Na+), la glucosa y la urea son los osmoles más
importantes (partículas osmóticamente activas), por lo que la osmolalidad plasmática (Osmp) se calcula con
la siguiente fórmula:
Osmp = 2 (Na+ [mEq/l]) + Glucosa (mg/dL) / 18 + Urea (mg/dL) / 5,6
La Osmp se debe mantener constante, y existe un equilibrio osmótico entre los compartimentos
intracelular y extracelular. Para mantener este equilibrio, se debe regular la ganancia y pérdida de agua y
de osmoles. El aumento de la Osmp estimula la sed y la liberación de la hormona antidiurética (ADH),
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1030]
[65] TRASTORNOS DEL EQUILIBRIO HIDROELECTROLÍTICO. SÍNDROME DE SECRECIÓN INADECUADA DE HORMONA
ANTIDIURÉTICA. FLUIDOTERAPIA
mientras que el descenso de la Osmp actúa en sentido inverso. En presencia de ADH, el riñón reabsorbe
agua produciendo una orina hiperosmolar, mientras que en ausencia de ADH el riñón excreta más agua,
produciendo una orina hipoosmolar (Figura 1). Los valores normales de Osmp oscilan entre 275-290
mOsm/kg y los de osmolalidad urinaria (Osmo) entre 50-1.200 mOsm/kg.
La hipernatremia y la hiponatremia son alteraciones en el balance del sodio y el agua, aunque en la
mayoría de las situaciones clínicas representan un trastorno en el balance de agua.
B. HIPONATREMIA
1. Concepto y etiología
Se define como un descenso del sodio plasmático (Nap) por debajo de 135 mEq/l, generalmente
acompañado por una disminución de la Osmp (hiponatremia hipoosmolar). Es la alteración electrolítica más
frecuente, tanto en el paciente hospitalizado como en el ambulatorio. La clasificación más utilizada y más
sencilla se realiza en función del estado del volumen del paciente (Tabla I).
La hiponatremia isoosmolar puede deberse a la presencia de cationes distintos del Nap
(intoxicación por litio, hiperpotasemia, hipermagnesemia, hipercalcemia) o por una
cuantificación de la natremia falseada por un exceso de lípidos o proteínas en plasma o tras la
instilación de soluciones con glicina en la resección transuretral de próstata o vejiga.
La hiponatremia hiperosmolar se debe a la presencia de otros osmoles (hiperglucemia,
inmunoglobulinas, manitol).
2. Aproximación diagnóstica
2.1. Manifestaciones clínicas
Se deben al edema neuronal secundario al paso de agua al interior celular por el descenso de la
Osmp. La gravedad sintomática depende más de la rapidez de instauración que del grado de hiponatremia.
Tabla I. Causas de hiponatremia-hipoosmolaridad.
En la hiponatremia de instauración aguda los pacientes presentan náuseas y malestar general a
medida que disminuye la concentración plasmática de sodio por debajo de 125 mEq/l. Entre 115 y 125
mEq/l suele aparecer cefalea, letargia y obnubilación, y por debajo de 115 mEq/l convulsiones y coma
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1031]
[65] TRASTORNOS DEL EQUILIBRIO HIDROELECTROLÍTICO. SÍNDROME DE SECRECIÓN INADECUADA DE HORMONA
ANTIDIURÉTICA. FLUIDOTERAPIA
(Tabla II). En la hiponatremia crónica pueden aparecer trastornos en la marcha, déficits cognitivos, además
de un aumento en el riesgo de caídas, osteoporosis y fracturas.
Tabla II. Manifestaciones clínicas de hiponatremia.
2.2. Diagnóstico etiológico (Figura 2)
Anamnesis y exploración física: es esencial realizar una precisa historia clínica, haciendo
hincapié en la presencia de vómitos, diarrea, consumo excesivo de agua (potomanía), resección
transuretral reciente, antecedentes de insuficiencia cardiaca, cirrosis hepática, insuficiencia
suprarrenal o hipotiroidismo. Además, es fundamental interrogar acerca de fármacos que
puedan producir hiponatremia (Tabla III), algunos de ellos utilizados frecuentemente, como el
omeprazol (el mecanismo no está claro, aunque se cree que podría ser por excesiva pérdida de
sodio en orina). Se deben excluir causas de síndrome de secreción inadecuada de ADH (SIADH)
(Tabla IV). Además, se debe valorar el estado del volumen extracelular, buscando la existencia
de signos de depleción (hipotensión arterial, disminución de la presión venosa central (PVC),
sequedad de piel y mucosas –signo del pliegue–, oliguria, taquicardia), o de sobrecarga de
volumen (ingurgitación yugular, edemas, ascitis y aumento de peso).
Figura 2. Algoritmo para el manejo de pacientes hospitalizados con hiponatremia.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1032]
[65] TRASTORNOS DEL EQUILIBRIO HIDROELECTROLÍTICO. SÍNDROME DE SECRECIÓN INADECUADA DE HORMONA
ANTIDIURÉTICA. FLUIDOTERAPIA
Tabla III. Causas de hiponatremia inducidas por drogas.
Tabla IV. Causas de síndrome de secreción inadecuada de vasopresina (SIADH).
Pruebas complementarias: se debe descartar, en primer lugar, la posibilidad de una
pseudohiponatremia, por ejemplo por hiperglucemia (por cada incremento en 100 mg de la
glucemia por encima de 100 mg/dL, el sodio plasmático disminuye 1,6 mEq/l), o por
hiperlipidemia o hiperproteinemia.
Debemos solicitar:
Gasometría venosa: determinadas alteraciones del equilibrio ácido-base pueden
orientar el diagnóstico (la alcalosis metabólica con hipopotasemia se asocia a vómitos o
diuréticos; la acidosis metabólica e hiperpotasemia acompañan a la insuficiencia renal y
suprarrenal).
Sodio urinario (Nao) y densidad en orina: refleja de forma aproximada la Osmo. Si el
Nao es menor de 20 mEq/l sugiere depleción del volumen circulante eficaz. Los
pacientes con SIADH, insuficiencia suprarrenal, hipotiroidismo, reajuste del osmostato
o uso de diuréticos presentarán una natriuria elevada (en general, mayor de 40 mEq/l).
Asimismo, una Osmo baja (menor de 100 mOsm/kg) apoya el diagnóstico de polidipsia
primaria o reajuste del osmostato hipotalámico, mientras que un valor mayor aparece
cuando está alterada la excreción de agua (SIADH, hipotiroidismo, insuficiencia
suprarrenal).
Osmolaridad plasmática: la mayoría de los casos cursan con hipoosmolaridad y se
deben descartar causas de pseudohiponatremia cuando en una hiponatremia la Osmp
esté normal o elevada.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1033]
[65] TRASTORNOS DEL EQUILIBRIO HIDROELECTROLÍTICO. SÍNDROME DE SECRECIÓN INADECUADA DE HORMONA
ANTIDIURÉTICA. FLUIDOTERAPIA
3. Tratamiento (Figura 2)
El tratamiento de la hiponatremia depende de la repercusión clínica y de su causa. Así, en pacientes
con depleción de volumen, la corrección se basará en la administración de suero salino, y en pacientes
euvolémicos el tratamiento será la restricción hídrica. Si el estado de hidratación no está claro (euvolemia
frente a hipovolemia) se puede hacer una prueba terapéutica: los pacientes hipovolémicos responderán
tras la infusión de sodio (suero salino fisiológico [SSF] 0,9%) con un aumento de la natremia, mientras que
los pacientes con SIADH no mejorarán, e incluso podrían empeorar. Por esta razón es muy importante
medir el Nap a las 6 horas de iniciar el tratamiento. En pacientes hipervolémicos, el tratamiento es el de la
causa subyacente (Figura 2).
El tratamiento agresivo con suero salino hipertónico (Tabla IV) solo se empleará en la hiponatremia
sintomática de instauración aguda o cuando el Nap sea inferior a 110-115 mEq/l (hiponatremia grave), ya
que pueden producirse daños neurológicos irreversibles.
Tabla V. Contenido de sodio en las distintas soluciones (mEq en 1.000 ml).
Generalmente, se recomienda detener esta corrección rápida al cesar los síntomas que amenacen
la vida o al alcanzar una natremia de seguridad entre 120-125 mEq/l. Es importante tener en cuenta que la
corrección excesivamente rápida de la hiponatremia, sobre todo si es de curso crónico, puede empeorar la
situación neurológica por la aparición de una mielinólisis central pontina (disartria, paresia fláccida, disfagia
y coma), secundaria a deshidratación neuronal. Esta complicación es más frecuente en pacientes ancianos,
malnutridos, alcohólicos, con enfermedades del sistema nervioso central (SNC), hipoxemia o en pacientes
posquirúrgicos.
El déficit de sodio se calcula según la siguiente fórmula:
Na+ a administrar (mEq) = 0,6* × Peso corporal (kg) × (Nap deseado – Nap actual)
* 0,5 en la mujer.
Como regla general, el Nap no debe aumentar más de 0,5 mEq/l/h. Como orientación, se debe
reponer en 12 horas la mitad de los mEq calculados, realizando controles analíticos periódicos (cada 4-8
horas). El resto del déficit se corregirá en las 24-36 horas siguientes. En pacientes con síntomas graves, y
sobre todo cuando el curso es agudo, se puede incrementar más rápidamente, hasta 1 mEq/l/h en las 3-4
primeras horas. El aumento total no debe ser superior a 8-10 mEq/l/día.
Además de corregir la natremia, se debe tratar la causa subyacente. Así, si se debe a hipotiroidismo
o insuficiencia suprarrenal, se administrará el tratamiento hormonal específico. El SIADH es un diagnóstico
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1034]
[65] TRASTORNOS DEL EQUILIBRIO HIDROELECTROLÍTICO. SÍNDROME DE SECRECIÓN INADECUADA DE HORMONA
ANTIDIURÉTICA. FLUIDOTERAPIA
de exclusión, en el cual la restricción hídrica es el pilar del tratamiento. El grado de restricción hídrica puede
calcularse mediante la fórmula de Furst (ver algoritmo). En caso de no observar mejoría tras esta medida,
podría ser recomendable la valoración del caso por un especialista.
Los antagonistas del receptor de ADH, como el tolvaptán (antagonista específico del receptor V2)
por vía oral, se utilizan para el tratamiento del SIADH. La experiencia clínica es limitada y su uso debería
restringirse a especialistas habituados en el uso de esta medicación.
C. HIPERNATREMIA
1. Concepto y etiología
Es una elevación del Nap por encima de 145 mEq/l e implica siempre una situación de
hiperosmolaridad. Puede producirse por pérdida de agua libre o retención excesiva de sodio (Tabla VI). La
hipernatremia persistente no existe en sujetos normales, ya que el aumento del Nap y de la Osmp estimula
los osmorreceptores hipotalámicos produciendo sed y liberación de ADH, lo que conduce a la retención de
agua, con normalización de la natremia. Por ello, la hipernatremia solo se produce en situaciones de falta
de acceso al agua (niños que no demandan agua, ancianos en los que está disminuido el estímulo de la sed,
o adultos con disminución del nivel de consciencia). Es una situación menos frecuente que la hiponatremia,
pero en general la gravedad del paciente es mayor.
Tabla VI. Causas de hipernatremia.
2. Aproximación diagnóstica
2.1. Manifestaciones clínicas
Los síntomas más precoces son somnolencia, debilidad e irritabilidad, apareciendo posteriormente
temblor, convulsiones, coma e incluso la muerte en los casos graves. Los síntomas derivan de la salida de
agua de las neuronas, provocada por el aumento de la Osmp. La disminución del volumen cerebral puede
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1035]
[65] TRASTORNOS DEL EQUILIBRIO HIDROELECTROLÍTICO. SÍNDROME DE SECRECIÓN INADECUADA DE HORMONA
ANTIDIURÉTICA. FLUIDOTERAPIA
ocasionar la ruptura de vasos, apareciendo hemorragias subaracnoideas e intraparenquimatosas que
pueden dejar déficits neurológicos irreversibles.
2.2. Diagnóstico etiológico (Figura 3)
Figura 3. Algoritmo diagnóstico y tratamiento de la hipernatremia.
Anamnesis y exploración física: en la anamnesis se deben buscar situaciones que incrementen
las pérdidas de agua (gastrointestinales, fiebre, quemaduras), así como interrogar por causas
de diabetes insípida (Tabla VII). Además de las alteraciones neurológicas, los pacientes
hipernatrémicos pueden mostrar signos de expansión o depleción de volumen según el
mecanismo subyacente. Dado que el origen más frecuente de la hipernatremia es la pérdida de
agua libre, los pacientes mostrarán signos de deshidratación cutánea, disminución de la PVC e
hipotensión ortostática. Los pacientes con sobrecarga de sodio pueden presentar edema
periférico y/o pulmonar. Por otra parte, hay que recordar que en cualquier forma de diabetes
insípida es infrecuente la hipernatremia debido a la eficacia del mecanismo de la sed. Estos
pacientes presentarán polidipsia, poliuria y nicturia en lugar de síntomas de hiperosmolaridad.
La excepción a esto se da en pacientes con diabetes insípida adípsica, con pérdida del
mecanismo de la sed.
Pruebas complementarias: la causa de la hipernatremia habitualmente se encuentra al hacer la
anamnesis. Si la causa no es obvia, es importante la determinación de la osmolaridad
plasmática y urinaria para orientar el diagnóstico.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1036]
[65] TRASTORNOS DEL EQUILIBRIO HIDROELECTROLÍTICO. SÍNDROME DE SECRECIÓN INADECUADA DE HORMONA
ANTIDIURÉTICA. FLUIDOTERAPIA
Tabla VII. Causas de diabetes insípida.
3. Tratamiento
El tratamiento de la hipernatremia depende de la repercusión clínica y del trastorno subyacente.
Es importante tener en cuenta que la corrección excesivamente rápida de la hipernatremia, sobre todo si
es de curso crónico, puede producir la aparición de edema cerebral, convulsiones, lesiones neurológicas
graves y muerte. Para reducir este riesgo, se aconseja que la concentración plasmática de sodio se
reduzca lentamente, a menos que el paciente presente síntomas.
El déficit de agua (agua libre que es necesario aportar para alcanzar la concentración de Nap
deseada) se calcula según la siguiente fórmula:
Déficit de agua (l) = 0,6* × Peso corporal (kg) × [(Nap actual / Nap deseado) – 1]
Déficit de agua (l) = 0,6* × Peso corporal (kg) × [(Nap actual / 140) –1]
* 0,5 en la mujer
Al déficit total calculado habrá que añadirle las pérdidas insensibles (de 800 a 1.000 ml/ día). El
déficit de agua calculado debe administrarse en, al menos, 48-72 horas. El descenso de los niveles de Nap
no debe superar 0,5 mEq/h (hasta 1 mEq/h en las primeras horas) y no más de 10 mEq/l al día. Es
importante monitorizar la diuresis diaria para ajustar los aportes.
En los pacientes con hipernatremia que presenten signos de deshidratación, hipotensión o
insuficiencia renal aguda, el déficit de agua y sodio se corregirá inicialmente con SSF (0,9%). Una vez
lograda la estabilidad hemodinámica, el déficit hídrico restante se repondrá mediante la ingesta oral de
agua libre o, si el paciente no es capaz de beber, mediante suero hipotónico (glucosado al 5% o
glucosalino). En caso de déficit grave en pacientes con trastorno hemodinámico, ancianos o cardiópatas, se
aconseja la monitorización de la PVC para evitar la sobrecarga de volumen.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1037]
[65] TRASTORNOS DEL EQUILIBRIO HIDROELECTROLÍTICO. SÍNDROME DE SECRECIÓN INADECUADA DE HORMONA
ANTIDIURÉTICA. FLUIDOTERAPIA
En los pacientes con exceso de volumen se debe valorar el uso de diuréticos y reponer agua en
forma de suero glucosado al 5%. Si en estos casos existe insuficiencia renal con falta de respuesta al
tratamiento diurético, se debe considerar la hemodiálisis. En el caso específico de la diabetes insípida
central, el tratamiento es la administración de desmopresina, y en la diabetes insípida nefrogénica es: dieta
pobre en sal, administración de diuréticos (amiloride/tiazida) y corrección de los trastornos metabólicos
subyacentes.
II. ALTERACIONES DEL POTASIO
A. FISIOPATOLOGÍA (Figura 4)
El potasio (K+) es el principal catión intracelular, de manera que se encuentra en un 98% en el
compartimento intracelular, mientras que el K+ plasmático representa únicamente un 2% del K+ corporal
total.
El mantenimiento de este equilibrio es crucial para conservar la normal excitabilidad de las
membranas celulares, fundamental para la transmisión neuromuscular; además, el K+ es esencial para otras
funciones celulares como la síntesis de proteínas y glucógeno.
La homeostasis del potasio es el resultado de la ingesta, la eliminación y la redistribución
transcelular, y en ella intervienen distintos factores.
La ingesta de potasio en la dieta occidental es de aproximadamente 1 mEq/kg de peso/día. Ante un
aporte de potasio, la regulación se realiza en dos fases: una primera respuesta rápida de redistribución al
interior de la célula, y una segunda fase definitiva en la nefrona distal (túbulos contorneado distal y
colector cortical) que ajusta la eliminación renal de potasio a las entradas.
Figura 4. Homeostasis del potasio.
B. HIPOPOTASEMIA
1. Concepto y etiología
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1038]
[65] TRASTORNOS DEL EQUILIBRIO HIDROELECTROLÍTICO. SÍNDROME DE SECRECIÓN INADECUADA DE HORMONA
ANTIDIURÉTICA. FLUIDOTERAPIA
Se define como una concentración plasmática de potasio inferior a 3,5 mEq/l. Puede clasificarse en
leve (3-3,5 mEq/l), moderada (2,5-3 mEq/l) y grave (< 2,5 mEq/l).
2. Causas (Tabla VIII)
Tabla VIII. Causas de hipopotasemia.
Puede deberse a una disminución en los aportes, una redistribución al interior de la célula o un
aumento en las pérdidas de potasio.
La ingesta deficitaria es rara como causa única, ya que el riñón es capaz de adaptarse y disminuir la
excreción urinaria a < 15 mEq de K+ al día.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1039]
[65] TRASTORNOS DEL EQUILIBRIO HIDROELECTROLÍTICO. SÍNDROME DE SECRECIÓN INADECUADA DE HORMONA
ANTIDIURÉTICA. FLUIDOTERAPIA
Las causas más frecuentes en nuestro medio son un incremento en las pérdidas (digestivas o
renales), como ocurre con la toma de diuréticos, los vómitos y la diarrea.
Otro grupo importante lo representan los estados de hiperaldosteronismo, ya sean primarios o
secundarios, en los que existe un aumento en la eliminación renal de potasio.
También son frecuentes las hipopotasemias transitorias por desplazamiento del potasio al interior
de la célula, en las situaciones primarias de alcalosis o al corregir con insulina una hiperglucemia en el
paciente diabético.
3. Clínica
Dependerá del grado de hipopotasemia (suele aparecer a partir de 3-2,5 mEq/l), así como de la
velocidad de instauración.
Las manifestaciones clínicas son principalmente cardiacas y neuromusculares, y se deben a la
hiperpolarización de la membrana celular:
Neuromusculares: astenia, debilidad y calambres en los miembros inferiores (MMII), mialgias,
parálisis fláccida ascendente, rabdomiólisis, compromiso de la musculatura respiratoria.
Digestivas (músculo liso): estreñimiento, íleo paralítico.
Cardiacas: cambios en el electrocardiograma (ECG) (aplanamiento e inversión de onda T, onda
U prominente, descenso del segmento ST, prolongación del intervalo QT), arritmias con
especial riesgo si existe cardiopatía subyacente (extrasístoles auriculares y ventriculares,
taquicardia ventricular, bloqueo auriculoventricular [AV], fibrilación ventricular), aumento de la
toxicidad por digital.
Renales: diabetes insípida nefrogénica (defecto en la concentración urinaria, poliuria y
polidipsia), nefritis tubulointersticial y quistes renales (hipopotasemia crónica), aumento de la
producción de amonio (puede agravar la encefalopatía hepática).
4. Diagnóstico (Figura 5)
Anamnesis (vómitos, diarrea, toma de diuréticos, laxantes, bicarbonato, insulina, antecedentes
familiares) y exploración física (tensión arterial, estado de volemia).
Analítica (creatinina sérica, K+, Na+, Mg2+, creatina-cinasa, hemograma, gasometría venosa,
iones en orina, osmolaridad urinaria y plasmática, renina, aldosterona).
ECG.
La respuesta renal (K+ urinario), las cifras de tensión arterial y la presencia de acidosis o alcalosis
metabólica son fundamentales a la hora de evaluar una hipopotasemia.
Un valor de K+ urinario < 15 mEq/l en una orina aislada indica una respuesta renal adecuada y
orienta a pérdidas extrarrenales, mientras que un K+ urinario > 15 mEq/l sugiere una pérdida renal.
El K+ urinario puede verse afectado por el estado de concentración o dilución de la orina (un
paciente puede tener un K+ en orina > 15 mEq/l pese a tener pérdidas extrarrenales, dada la alta
concentración de K+ en orina debida al hiperaldosteronismo secundario a la hipovolemia), por lo que
resulta útil corregirlo a la reabsorción de agua en el túbulo colector, mediante el cálculo del gradiente
transtubular de potasio (TTKG):
TTKG = [Ku × Osmp] / [Kp × Osmu]
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1040]
[65] TRASTORNOS DEL EQUILIBRIO HIDROELECTROLÍTICO. SÍNDROME DE SECRECIÓN INADECUADA DE HORMONA
ANTIDIURÉTICA. FLUIDOTERAPIA
Ku: potasio urinario; Osmp: osmolaridad plasmática; Kp: potasio plasmático; Osmu: osmolaridad
urinaria.
Si el TTKG < 4: ausencia de actividad mineralocorticoide en el túbulo distal (hipopotasemia no
mediada por aldosterona).
Si el TTKG > 7: presencia de actividad mineralocorticoide en el túbulo distal (hipopotasemia
mediada por aldosterona).
Figura 5. Algoritmo diagnóstico de la hipopotasemia.
En cuanto al equilibrio ácido-base, en la mayoría de las ocasiones la hipopotasemia se acompañará
de alcalosis metabólica (que además supone un factor que contribuye a perpetuar la hipopotasemia). Las
causas de hipopotasemia con acidosis metabólica se reducen a las pérdidas digestivas bajas (diarrea,
adenoma velloso, laxantes), las acidosis tubulares proximal de tipo 2 (o toma de acetazolamida) y distal de
tipo 1, las tubulopatías proximales por fármacos y la cetoacidosis diabética.
5. Tratamiento
Irá dirigido a corregir el déficit, minimizar las pérdidas y tratar la causa subyacente.
La intensidad en la reposición dependerá de la gravedad de la hipopotasemia, la presencia de
manifestaciones clínicas y la agudeza del trastorno. En hipopotasemias graves debe hacerse monitorización
electrocardiográfica del paciente.
Se ha de tener en cuenta:
Por cada disminución de 1 mEq/l en el potasio plasmático existirá un déficit de 200 mEq/l en las
reservas de potasio corporal total, hasta que la potasemia sea inferior a 2 mEq/l.
La hipomagnesemia es una causa de hipopotasemia refractaria, de forma que estará indicada
su reposición, así como su administración empírica, en hipopotasemias graves.
En presencia de un trastorno del equilibrio ácido-base, se corregirá antes el déficit de potasio
(la corrección previa de la acidosis puede agravar la hipopotasemia).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1041]
[65] TRASTORNOS DEL EQUILIBRIO HIDROELECTROLÍTICO. SÍNDROME DE SECRECIÓN INADECUADA DE HORMONA
ANTIDIURÉTICA. FLUIDOTERAPIA
Si la causa es un desplazamiento transcelular de potasio, prestar especial atención para evitar
reposición excesiva de potasio.
Vía oral:
Indicada en hipopotasemias leves-moderadas, asintomáticas.
Existen distintas preparaciones, la más útil el cloruro potásico (Potasion® 600 mg = 8 mEq), de
elección en la mayoría de las hipopotasemias, a excepción de aquellas con acidosis metabólica.
En esos casos se prefiere el uso de bicarbonato potásico + ácido ascórbico (BoiK® 1 comprimido
= 10 mEq), bicarbonato potásico + ácido ascórbico + ácido aspártico (BoiK aspártico® 1
comprimido = 25 mEq) o citrato potásico (Acalka® 1 comprimido = 10 mEq). Evitar estas últimas
en caso de alcalosis, ya que pueden agravarla.
Vía intravenosa:
De elección en las hipopotasemias graves (< 2,5 mEq/l), sintomáticas o en pacientes
digitalizados con K+ < 3 mEq/l, y en aquellos pacientes que no toleran la vía oral.
Se administra cloruro potásico diluido en SSF 0,9% (no en suero glucosado, pues estimula la
liberación de insulina, pudiendo agravar considerablemente la hipopotasemia). A través de vía
venosa periférica no superar una concentración superior a 20-40 mEq/l, ni una velocidad
superior a 10-20 mEq/h, por riesgo de irritación local y flebitis. En caso de requerir
concentraciones superiores de potasio, se utilizará una vía venosa central, que permite la
administración de hasta un máximo de 100 mEq/l y una velocidad de infusión máxima de 20-40
mEq/h (evitar que la punta del catéter alcance la aurícula por el riesgo de arritmias). En caso de
riesgo de arritmias ventriculares malignas en hipopotasemias graves puede administrarse 10
mEq de ClK en 100 cc de SSF 0,9% en 10 minutos seguidos de 10 mEq en otros 10 minutos.
La administración de altas concentraciones de K+ de forma rápida requiere un manejo muy
cuidadoso y una monitorización muy estrecha, preferiblemente en la unidad de vigilancia
intensiva (UVI).
C. HIPERPOTASEMIA
1. Concepto
Se define como una concentración plasmática de potasio mayor de 5,5 mEq/l. Se clasifica en leve
(5,5-6 mEq/l), moderada (6-7 mEq/l) y grave (> 7 mEq/l).
Puede deberse a un aumento en los aportes (excepcional como causa única, ya que normalmente
está asociado a un defecto en la excreción renal), una disminución en su eliminación o una redistribución
hacia el exterior de la célula. Generalmente existe más de un factor contribuyente.
La causa más frecuente en nuestro medio es la combinación de insuficiencia renal y fármacos, lo
que ha hecho que aumente su prevalencia, especialmente en población anciana o con una situación de VEC
disminuido (ICC o cirrosis) que reciben inhibidores de la enzima de conversión de la angiotensina (IECA),
antagonistas de los receptores de la angiotensina II (ARA-II) o diuréticos ahorradores de potasio.
Es, por tanto, en muchos casos un trastorno resultado de una prescripción inadecuada y
consecuentemente evitable.
2. Causas (Tabla IX)
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1042]
[65] TRASTORNOS DEL EQUILIBRIO HIDROELECTROLÍTICO. SÍNDROME DE SECRECIÓN INADECUADA DE HORMONA
ANTIDIURÉTICA. FLUIDOTERAPIA
Tabla IX. Causas de hiperpotasemia.
3. Clínica
Las manifestaciones clínicas vienen dadas por la alteración en la función neuromuscular derivada
del papel del potasio en los potenciales de membrana. Existe escasa correlación entre la clínica y las cifras
de potasio. La acidosis, la hiponatremia y la hipocalcemia pueden agravar la situación. En los pacientes en
diálisis, la debilidad en las extremidades inferiores y la dificultad para la marcha pueden ser signos de
hiperpotasemia grave. La velocidad en la instauración marca la gravedad más que las cifras de potasio.
Alteración neuromuscular: parestesias, debilidad, parálisis fláccida.
Alteración en la conducción cardiaca:
K+ ≈ 6,5 mEq/l: ondas T picudas.
K+ > 7 mEq/l: espacio PR prolongado, ensanchamiento del complejo QRS, desaparición
de onda P.
K+ > 8 mEq/l: patrón de onda sinusoidal (fusión del complejo QRS con la onda T),
arritmias ventriculares (fibrilación ventricular [FV], taquicardia ventricular [TV]),
asistolia.
4. Diagnóstico (Figura 6)
Una vez descartada pseudohiperpotasemia por salida de potasio de las células sanguíneas
inmediatamente antes o después de la venopunción (torniquete apretado, muestra hemolizada,
leucocitosis > 70.000/mm3 o trombocitosis > 600.000/mm3), la anamnesis suele ser suficiente para llegar a
un diagnóstico etiológico.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1043]
[65] TRASTORNOS DEL EQUILIBRIO HIDROELECTROLÍTICO. SÍNDROME DE SECRECIÓN INADECUADA DE HORMONA
ANTIDIURÉTICA. FLUIDOTERAPIA
Figura 6. Algoritmo diagnóstico de la hiperpotasemia.
Si bien el cálculo del TTKG es muy orientativo para conocer el efecto de la aldosterona en la
excreción renal de potasio, no suele ser necesario para identificar la causa de la hiperpotasemia en la
mayoría de los casos.
Anamnesis (dieta, antecedentes de enfermedad renal, diabetes mellitus, toma de fármacos,
antecedentes familiares) y exploración física (estado de volemia, hiperpigmentación, fuerza
muscular).
Analítica (glucosa, creatinina sérica, K+, Na+, Ca2+, CK, hemograma, gasometría venosa, iones en
orina, osmolaridad urinaria y plasmática).
ECG.
5. Tratamiento (Tabla X)
La hiperpotasemia es el trastorno hidroelectrolítico más grave, ya que puede ocasionar arritmias
potencialmente letales, por lo que constituye una emergencia médica. Requiere monitorización
electrocardiográfica del paciente.
Los objetivos del tratamiento son estabilizar la membrana de las células miocárdicas previniendo
efectos arritmogénicos de la hiperpotasemia, promover el paso del potasio sérico al interior de las células y
forzar su eliminación. Simultáneamente, se ha de investigar y tratar la causa subyacente (suspender
fármacos, corregir la insuficiencia renal y la acidosis, utilizar fludrocortisona en la insuficiencia suprarrenal).
Hiperpotasemia leve (5,5-6 mEq/l):
Restricción de potasio en la dieta.
Resinas de intercambio iónico.
Diuréticos del asa.
Hiperpotasemia moderada (6-7 mEq/l):
Insulina + glucosa.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1044]
[65] TRASTORNOS DEL EQUILIBRIO HIDROELECTROLÍTICO. SÍNDROME DE SECRECIÓN INADECUADA DE HORMONA
ANTIDIURÉTICA. FLUIDOTERAPIA
Salbutamol nebulizado o subcutáneo.
Bicarbonato sódico solo si hay acidosis metabólica.
Diuréticos del asa.
Hiperpotasemia grave (> 7 mEq/l o alteraciones en el ECG):
Gluconato cálcico.
Insulina + glucosa.
Salbutamol nebulizado o subcutáneo.
Bicarbonato sódico solo si hay acidosis metabólica.
Diuréticos del asa.
Tratamiento a largo plazo (hiperpotasemias crónicas):
Restricción del potasio en la dieta.
Valorar la suspensión de fármacos.
Resinas de intercambio iónico.
Diuréticos del asa.
Fludrocortisona si hay insuficiencia suprarrenal.
Diálisis en caso de insuficiencia renal.
Tabla X. Tratamiento de la hiperpotasemia.
III. FLUIDOTERAPIA
1. INTRODUCCIÓN
La fluidoterapia tiene como principal objetivo el mantenimiento de la adecuada perfusión y
oxigenación de los tejidos, así como la recuperación y el mantenimiento del equilibrio
hidroelectrolítico y de la volemia cuando esto sea necesario. El agua corporal total es de
aproximadamente 600 ml/kg (60% del peso corporal), con variaciones individuales que dependen
de la edad, la proporción de tejido adiposo y muscular o el estado de salud. Dos tercios del agua
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1045]
[65] TRASTORNOS DEL EQUILIBRIO HIDROELECTROLÍTICO. SÍNDROME DE SECRECIÓN INADECUADA DE HORMONA
ANTIDIURÉTICA. FLUIDOTERAPIA
corporal total corresponden al líquido intracelular (LIC), y un tercio al líquido extracelular (LEC). En
este último, un cuarto es líquido intravascular y tres cuartos, líquido intersticial.
2. NECESIDADES DIARIAS DE AGUA Y SOLUTOS
1. Necesidades diarias de agua
El cálculo de los requerimientos diarios de agua puede aproximarse mediante la fórmula de
Holliday-Segar, válida para pacientes pediátricos y adultos. Una aproximación más sencilla, válida solo para
adultos, es un requerimiento de agua de 35 ml/kg/día (Tabla XI). Las necesidades basales de líquidos
pueden variar en diferentes situaciones. Así, la fiebre, la sudoración o la hiperventilación aumentan las
necesidades diarias de agua, mientras que la hipotermia, la humedad ambiental o la sedación disminuyen
las necesidades diarias de agua.
Tabla XI. Necesidades diarias de agua (fórmula de Holliday-Segar).
2. Necesidades diarias de electrolitos
Durante periodos de ayuno deben aportarse 2 g/kg/día de glucosa, valorándose el inicio de
nutrición enteral, preferiblemente y siempre que sea posible, o parenteral si se prevé un ayuno de más de 7
días. En la tabla XII se reflejan las necesidades diarias de electrolitos.
Tabla XII. Necesidades diarias de electrolitos.
3. Pérdidas diarias de agua y electrolitos
Las pérdidas diarias de agua pueden dividirse en pérdidas sensibles (heces, orina y sudor) e
insensibles (respiración y transpiración), tal y como se refleja en la tabla XIII. El ayuno provoca una pérdida
de agua de unos 80 ml/h de ayuno. La perspiración o evaporación insensible provoca una pérdida de unos
10 ml/kg/día de agua en condiciones normales.
Tabla XIII. Pérdidas diarias de agua.
3. INDICACIONES DE LA FLUIDOTERAPIA INTRAVENOSA
Aquellas situaciones de ausencia de nutrición oral o enteral, alteración de la volemia o del
equilibrio hidroelectrolítico.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1046]
[65] TRASTORNOS DEL EQUILIBRIO HIDROELECTROLÍTICO. SÍNDROME DE SECRECIÓN INADECUADA DE HORMONA
ANTIDIURÉTICA. FLUIDOTERAPIA
1. Ayuno o dieta absoluta.
2. Depleción del líquido extracelular:
Pérdidas digestivas: vómitos, diarrea, fístulas, débitos por sondas de drenaje, etc.
Pérdidas renales: poliuria osmótica, tubulopatías, diabetes insípida, etc.
Tercer espacio: íleo paralítico, aumento de permeabilidad vascular, pérdida de presión
oncótica, etc.
3. Depleción salina
Diuréticos, nefropatías, pérdidas digestivas, insuficiencia adrenal aguda, etc.
4. Depleción hídrica
Sudoración profusa, taquipnea, síndrome hiperosmolar, cetoacidosis diabética, etc.
5. Trastornos hidroelectrolíticos
Que precisen corrección con fluidos intravenosos.
6. Shock hipovolémico
Hemorrágico, deshidratación, quemaduras, etc.
7. Shock distributivo
Séptico, anafiláctico, neurogénico.
4. TIPOS DE FLUIDOS PARA LA ADMINISTRACIÓN INTRAVENOSA (Tabla XIV)
Tabla XIV. Tipos de fluidos intravenosos.
1. Soluciones cristaloides
Permiten mantener el equilibrio hidroelectrolítico, expandir el volumen intravascular y, si contienen
glucosa, aportar energía. Respecto al plasma, pueden ser hipo-, iso- o hipertónicas (Tablas XV- XVIII).
Los compuestos multielectrolíticos (Ringer y Ringer lactato), por sus características, son muy
adecuados para sueroterapia de mantenimiento y postoperatorio inmediato.
2. Soluciones alcalinizantes (Tabla XIX)
3. Soluciones acidificantes (Tabla XX)
4. Soluciones coloides (Tablas XXI a XXIII)
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1047]
[65] TRASTORNOS DEL EQUILIBRIO HIDROELECTROLÍTICO. SÍNDROME DE SECRECIÓN INADECUADA DE HORMONA
ANTIDIURÉTICA. FLUIDOTERAPIA
Contienen partículas de alto peso molecular, por lo que actúan como expansores plasmáticos.
Mantienen efectos hemodinámicos más duraderos y rápidos que las soluciones cristaloides. Pueden ser
naturales (albúmina) o artificiales (dextranos, derivados de la gelatina y hidroxietilalmidones).
Tabla XV. Soluciones hipotónicas
Tabla XVI. Soluciones isotónicas.
Tabla XVII. Soluciones hipertónicas.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1048]
[65] TRASTORNOS DEL EQUILIBRIO HIDROELECTROLÍTICO. SÍNDROME DE SECRECIÓN INADECUADA DE HORMONA
ANTIDIURÉTICA. FLUIDOTERAPIA
Tabla XVIII. Composición de las diferentes soluciones cristaloides.
Tabla XIX. Soluciones alcalinizantes.
Tabla XX. Soluciones acidificantes.
5. NORMAS GENERALES PARA EL USO DE FLUIDOTERAPIA INTRAVENOSA
La administración de fluidoterapia intravenosa debe individualizarse en función de las
características clínicas del paciente y el cuadro clínico que presenta.
1. Indicación del volumen y tipo de soluciones
Se realizará tras la valoración de los siguientes aspectos:
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1049]
[65] TRASTORNOS DEL EQUILIBRIO HIDROELECTROLÍTICO. SÍNDROME DE SECRECIÓN INADECUADA DE HORMONA
ANTIDIURÉTICA. FLUIDOTERAPIA
Estimación de las necesidades diarias del paciente de agua, electrolitos y glucosa.
Estimación de las pérdidas de agua y electrolitos (vómitos, diarrea, débitos intestinales, etc.).
Seleccionar la fluidoterapia que más se asemeje a las pérdidas.
Considerar patologías asociadas para ajustar el volumen que se va a administrar (insuficiencia
renal, insuficiencia cardiaca, insuficiencia hepática, etc.).
Seleccionar el fluido que se va a administrar y la velocidad de infusión.
Estimar los líquidos intravenosos utilizados para administración de medicación.
Tabla XXI. Coloides naturales.
Tabla XXII. Coloides artificiales.
Tabla XXIII. Características de los diferentes coloides.
2. Monitorización (Tabla XXIV)
A través de parámetros clínicos, analíticos o hemodinámicos, permite ajustar la composición y el
ritmo de infusión de la sueroterapia.
2.1. Signos clínicos
Diuresis, frecuencia cardiaca, tensión arterial, signos de hipovolemia (sequedad cutaneomucosa,
pliegue cutáneo, sed), signos de hipervolemia (ingurgitación yugular, edemas, crepitantes pulmonares) y
aumento de las pérdidas por sondas, ostomías, fístulas, etc.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1050]
[65] TRASTORNOS DEL EQUILIBRIO HIDROELECTROLÍTICO. SÍNDROME DE SECRECIÓN INADECUADA DE HORMONA
ANTIDIURÉTICA. FLUIDOTERAPIA
Tabla XXIV. Monitorización hemodinámica para el balance de fluidos.
2.2. Datos analíticos
Función renal, iones, gasometría, lactato, osmolaridad plasmática, relación nitrógeno ureico
sanguíneo [BUN]/creatinina sérica. Este último parámetro es un marcador de deshidratación del individuo:
< 15 equivale a hidratación suficiente, > 20 indica bajo volumen intravascular.
2.3. Parámetros hemodinámicos
Requieren una monitorización invasiva para su medición (presión venosa central, presión capilar
pulmonar, índice cardiaco, saturación venosa mixta de O2).
BIBLIOGRAFÍA
Grant P, Ayuk J, Bouloux PM, Cohen M, Cranstons I, Murray RD, et al. The diagnosis and management
of inpatient hyponatraemia and SIADH. Eur J Clin Invest. 2015;45(8):888-94.
Overgaard-Steensen D, Ring T. Clinical review: practical approach to hyponatraemia and
hypernatraemia in critically ill patients. Crit Care. 2013;17(1):206.
Rodrigo Casanova MP, García Peña JM, Lomillos Rafols V, De Luis Cabezón N, Aguilera Celorrio L.
Fluidoterapia perioperatoria. Rev Esp Anestesiol Reanim. 2010;57(9):575-85.
Runkle I, Villabona C, Navarro A, Pose A, Formiga F, Tejedor A, et al. Tratamiento de la hiponatremia
secundaria al síndrome de secreción inadecuada de la hormona antidiurética: algoritmo
multidisciplinar español. Nefrología. 2014;34(4):439-50.
Sánchez R, Partida M. Fluidoterapia y principios de nutrición. En: Aguilar F, Bisbal O, Gómez C, de
Lagarde M, Maestro G, Pérez-Jacoíste MA, Pérez L, Vila J; editores. Manual de diagnóstico y terapéutica
médica. 7ª ed. Madrid: MSD; 2012. p. 941-62.
Sequeira P, Rodríguez D. Alteraciones en el metabolismo del potasio. En: Arias M. Nefrología Clínica.
Hernando. 4ª edición. Madrid: Editorial Médica Panamericana; 2014. p. 101-12.
Spasovski G, Vanholder R, Allolio B, Annane D, Ball S, Bichet D, et al. Clinical Practice guideline on
diagnosis and treatment of hyponatraemia. Eur J Endocrinol. 2014;170(3):G1-47.
Vila Santos J, Apaza Chávez J. Trastornos del equilibrio hidroelectrolítico. En: Aguilar F, Bisbal O, Gómez
C, de Lagarde M, Maestro G, Pérez-Jacoíste MA, editores. Manual de diagnóstico y terapéutica médica.
7ª ed. Madrid: MSD; 2012. p. 911-26.
Weiner ID, Lindas SL, Wingo CS. Disorders of Potassium Metabolism. En: Floege J, Johnson RJ, Feehally
J. Comprehensive Clinical Nephrology, 4ª edición. St. Louis, MO: Elsevier, Inc.; 2010. p. 118-29.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1051]
[66] TRASTORNOS DEL METABOLISMO DEL CALCIO, FÓSFORO Y MAGNESIO
66.Trastornos del metabolismo del calcio, fósforo y
magnesio
María Soledad Librizzi.
Endocrinología y Nutrición
Juan Salas Jarque.
Medicina Interna
Hernando Trujillo Cuéllar.
Nefrología
Asesores:
Sonsoles Guadalix Iglesias.
Médica Adjunta de Endocrinología y Nutrición
Eduardo Hernández Martínez.
Médico Adjunto de Nefrología
I. ALTERACIONES EN EL METABOLISMO DEL CALCIO
A. FISIOPATOLOGÍA
El calcio se encuentra en la sangre unido en un 40% con proteínas plasmáticas (principalmente
albúmina) y en un 10% con pequeños aniones (fosfato, citrato, sulfato, lactato). El 50% restante circula
libremente en forma iónica (Ca2+), siendo esta la única que atraviesa membranas. Estas proporciones se
modifican en función del pH (la alcalosis aumenta la unión del calcio a la albúmina, disminuyendo el calcio
iónico) y de la concentración de aniones (la elevación de la fosfatemia reduce el calcio iónico).
La calcemia total varía en función de la albúmina plasmática; así, por cada 1 g/dL que se modifica la
albúmina, la calcemia total varía 0,8 mg/dL en la misma dirección. Para corregir el calcio total en función de
la albuminemia se puede emplear la siguiente fórmula:
Ca corregido = Ca medido + 0,8 x (4,4 – albuminemia)
O la simplificada:
Ca corregido = Ca medido + (4 – albuminemia)
Una alternativa es medir el calcio iónico, especialmente en pacientes con alteración del pH, ya que
en estos la calcemia total puede ser normal y no serlo el calcio iónico.
La calcemia está regulada por la parathormona (PTH), el calcitriol (metabolito de la vitamina D) y la
calcitonina (en menor medida).
La liberación de PTH por las glándulas paratiroides aumenta al descender el calcio iónico plasmático
por medio de receptores sensores de calcio. La hipomagnesemia también estimula la liberación de PTH,
pero si es grave y crónica la inhibe, al igual que la hipermagnesemia. El calcitriol promueve la
mineralización ósea, y aumenta las concentraciones de calcio y fosfato en plasma. La vitamina D
(colecalciferol) se obtiene de la dieta y de la producción cutánea (requiere exposición a la luz ultravioleta),
es transformada en el hígado en calcidiol (25-hidroxicolecalciferol) y este, en el riñón, en calcitriol (1,25-
dihidroxicolecalciferol), el metabolito activo. Este último paso es catalizado por la alfa-1-hidroxilasa renal,
que es estimulada por la PTH y por los descensos en la calcemia y la fosfatemia, pudiendo afectarse su
función en pacientes con insuficiencia renal crónica.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1052]
[66] TRASTORNOS DEL METABOLISMO DEL CALCIO, FÓSFORO Y MAGNESIO
B. HIPERCALCEMIA
Se define como la concentración de calcio plasmático total superior a 10,5 mg/dL o de calcio iónico
superior a 5,25 mg/dL (1,3 mmol/l). Debe diferenciarse de la pseudohipercalcemia, es decir, un calcio
plasmático total aumentado con calcio iónico normal, cuyas principales causas son la hiperalbuminemia
(deshidrataciones) y, rara vez, los mielomas productores de para- proteínas transportadoras de calcio.
1. ETIOLOGÍA
El hiperparatiroidismo (primera causa en pacientes ambulatorios) y las neoplasias (primera causa
en pacientes hospitalizados) representan el 90% de los casos de hipercalcemia (Tabla I).
Tabla I. Etiología de la hipercalcemia.
2. CLÍNICA
Los pacientes con hipercalcemia leve (< 12 mg/dL) pueden estar asintomáticos o referir síntomas
inespecíficos. La hipercalcemia moderada (12-14 mg/dL) suele tolerarse bien si es crónica, pero de forma
aguda puede causar síntomas importantes. La hipercalcemia grave (> 14 mg/dL) puede ser letal, ya que
conlleva riesgo de parada cardiaca y coma (Tabla II).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1053]
[66] TRASTORNOS DEL METABOLISMO DEL CALCIO, FÓSFORO Y MAGNESIO
3. DIAGNÓSTICO (FIGURA 1)
En primer lugar, hay que descartar que se trate de una pseudohipercalcemia corrigiendo la
calcemia total según la albuminemia (véase la fisiopatología) o midiendo el calcio iónico. En segundo lugar,
debe confirmarse la hipercalcemia con una nueva determinación y revisar los valores en análisis previos, si
estuvieran disponibles. Una hipercalcemia crónica con valores menores de 11 mg/dL en un paciente
asintomático, con una exploración física normal, orienta hacia un hiperparatiroidismo primario. Valores
superiores a 13 mg/dL en un paciente sintomático son más sugestivos de malignidad.
Tabla II. Presentación clínica de la hipercalcemia.
Una vez confirmada la hipercalcemia, se debe determinar si está mediada por la parathormona
midiendo la PTH intacta y la función renal (para descartar hiperparatiroidismo secundario).
Valores de PTH elevados o en el límite alto de la normalidad: indican hiperparatiroidismo
primario (en ausencia de toma crónica de litio) o, menos frecuentemente, hiper- calcemia
hipocalciúrica familiar, que cursa con excreción fraccional de calcio < 1%.
Valores bajos de PTH: obligan a buscar otras causas. Para ello, se realizarán otras
determinaciones:
PTHrP: puede ser útil para el diagnóstico de hipercalcemia tumoral en pacientes con neoplasia
conocida.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1054]
[66] TRASTORNOS DEL METABOLISMO DEL CALCIO, FÓSFORO Y MAGNESIO
Metabolitos de la vitamina D: la elevación del calcidiol (25[OH]D) indica intoxicación por este o
por vitamina D; sin embargo, el ascenso del calcitriol (1,25[OH]2D) puede deberse a
intoxicación por este, a producción extrarrenal (enfermedades granulomatosas y linfoma) o a
un aumento de la producción renal (inducible por PTH pero no por PTHrP).
Fosfatemia: será baja o en el límite bajo de la normalidad en caso de estar aumentada la PTH o
PTHrP, y normal o elevada ante un aumento de los metabolitos de la vitamina D,
inmovilización, tirotoxicosis, síndrome de leche-alcalinos y enfermedad ósea metastásica.
Concentraciones plasmáticas de cloruro y bicarbonato: son útiles en el diagnóstico del
hiperparatiroidismo primario (Cl > 103 mEq/l y leve acidosis metabólica) y el síndrome de leche-
alcalinos (cifras menores de Cl y alcalosis metabólica).
Calciuria: es alta en el hiperparatiroidismo y en la hipercalcemia secundaria a malignidad, y
baja en el síndrome de leche-alcalinos, en el consumo de diuréticos tiazídicos y en la
hipercalcemia hipocalciúrica familiar.
Radiografías óseas: la presencia de osteítis fibrosa es muy específica del hiperparatiroidismo
primario, pero solo se observa en el 5% de los casos.
Figura 1. Algoritmo de la hipercalcemia.
4. TRATAMIENTO (TABLA III)
Consiste en la reducción del calcio plasmático y en el tratamiento de la enfermedad causal. Los
pacientes con hipercalcemia hipocalciúrica familiar no suelen requerir tratamiento, de ahí la importancia de
establecer correctamente el diagnóstico.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1055]
[66] TRASTORNOS DEL METABOLISMO DEL CALCIO, FÓSFORO Y MAGNESIO
Tabla III. Tratamiento de la hipercalcemia.
C. HIPOCALCEMIA
Concentración de calcio plasmático total inferior a 8,0 mg/dL o de calcio iónico inferior a 4,65
mg/dL (0,8 mmol/l).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1056]
[66] TRASTORNOS DEL METABOLISMO DEL CALCIO, FÓSFORO Y MAGNESIO
1. ETIOLOGÍA
La hipocalcemia puede ocurrir por una insuficiente producción de PTH (hipoparatiroidismo
primario) o una deficiencia de vitamina D, que desencadena una elevación compensadora de la PTH
(hiperparatiroidismo secundario).
Esto nos permitirá clasificar las hipocalcemias en aquellas que cursan con PTH baja y aquellas con
PTH alta (Tabla IV).
Tabla IV. Etiología de la hipocalcemia.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1057]
[66] TRASTORNOS DEL METABOLISMO DEL CALCIO, FÓSFORO Y MAGNESIO
2. CLÍNICA
Las manifestaciones clínicas dependen del grado de hipocalcemia y de la rapidez con que se
instaura; así, las hipocalcemias crónicas suelen ser asintomáticas hasta que aparece algún factor
desencadenante (tratamiento con diuréticos del asa, estrés, hiperventilación, embarazo, lactancia, vómitos,
periodos de rápido crecimiento, anticomiciales, tratamiento estrogénico, glucocorticoides, administración
de potasio y magnesio).
Tetania: es la manifestación más característica y se fundamenta en un aumento de la
irritabilidad neuromuscular. Inicialmente es leve, con hormigueo peribucal, parestesias de
manos y pies, debilidad muscular proximal y calambres; posteriormente aparecen espasmo
carpopedal, laringoespasmo y convulsiones focales o generalizadas, que se deben diferenciar
de la contracción muscular generalizada que ocurre en la tetania grave. Existen también
manifestaciones autonómicas como sudoración, broncoespasmo y cólico biliar. Se presenta con
calcemias inferiores a 7-7,5 mg/dL (< 4,3 mg/dL de calcio iónico) de instauración aguda. La
hipocalcemia y la alcalosis actúan de forma sinérgica en la generación de la tetania. La
exploración física puede revelar una tetania latente con los signos de Trousseau (inducción de
espasmo carpopedal mediante la compresión con el esfigmomanómetro por encima de la
presión sistólica durante 3 minutos) y Chvostek (contracción de la musculatura facial ipsilateral
al percutir sobre el nervio facial delante del pabellón auricular).
Convulsiones: la hipocalcemia puede facilitar crisis generalizadas tonicoclónicas, de ausencia y
focales.
Manifestaciones cardiovasculares: la hipotensión puede complicar la hipocalcemia aguda,
especialmente la inducida por ácido etilendiaminotetracético (EDTA) o citrato, llegando incluso
a reducir la contractilidad cardiaca y producir un fallo cardiaco congestivo; la disfunción
miocárdica se resuelve al reponer el calcio. Además, la hipocalcemia prolonga el intervalo QT
en el electrocardiograma y se asocia a despolarización precoz y arritmias como la torsade de
pointes. La hipocalcemia también reduce la sensibilidad a la digoxina (efecto opuesto a la
hipercalcemia).
Papiledema: ocurre en la hipocalcemia grave y puede acompañarse de hipertensión
intracraneal.
Manifestaciones psiquiátricas (reversibles): inestabilidad emocional, ansiedad y depresión;
menos frecuentemente, confusión, alucinaciones y psicosis.
3. DIAGNÓSTICO (FIGURA 2)
En primer lugar, debe verificarse que se trata de una verdadera hipocalcemia, ajustando la cifra de
calcio plasmático total según la albuminemia (véase la fisiopatología) o determinando el calcio iónico.
Algunos contrastes con gadolinio pueden interferir con los ensayos colorimétricos usados para medir la
calcemia; este efecto desaparece rápidamente con la excreción urinaria del contraste, pero puede ser más
prolongado en pacientes con insuficiencia renal.
En segundo lugar, se recomienda confirmar la hipocalcemia con una segunda determinación. La
extracción de la muestra de sangre debe ser muy cuidadosa, evitando la estasis vascular (uso de
torniquetes), y procesando la muestra rápidamente. Además, es conveniente revisar calcemias previas.
Una vez confirmada la hipocalcemia se determinarán:
PTH: es la determinación analítica más útil en los pacientes con hipocalcemia. Debe medirse
simultáneamente a la calcemia. En presencia de hipocalcemia, una PTH baja, e incluso normal,
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1058]
[66] TRASTORNOS DEL METABOLISMO DEL CALCIO, FÓSFORO Y MAGNESIO
apoya el diagnóstico de hipoparatiroidismo; también puede observarse en la hipomagnesemia
o en la rara hipocalcemia autosómica dominante (mutación activadora del sensor del calcio).
Fosforo: una hipocalcemia persistente junto a hiperfosfatemia, en ausencia de enfermedad
renal o destrucción tisular, es virtualmente diagnóstica de hipoparatiroidismo o
pseudohipoparatiroidismo; debe acompañarse de hipofosfaturia. La hipofosfatemia suele
indicar un exceso de PTH, es decir, un hiperparatiroidismo secundario a un déficit de vitamina
D. Asimismo, la fosfatemia suele ser normal o baja en caso de hipomagnesemia.
Magnesio: concentraciones plasmáticas < 1 mg/dL se asocian a hipocalcemia, aunque esta
también puede observarse con cifras normales e hipermagnesemia grave (> 6 mg/dL). En caso
de hipomagnesemia, la hipermagnesuria orienta a pérdidas renales.
Metabolitos de la vitamina D: la determinación de calcidiol (25[OH]D) es más representativa
de la disponibilidad de vitamina D que la de calcitriol (1,25]OH]2D). El calcidiol es bajo en el
déficit de vitamina D, mientras que el calcitriol puede ser normal o alto, ya que el
hiperparatiroidismo secundario estimula a la alfa-1-hidroxilasa renal. Por el contrario, los
pacientes con hipoparatiroidismo pueden tener un calcidiol normal y bajas concentraciones de
calcitriol.
Creatinina: su elevación es diagnóstica de insuficiencia renal. En esta, se combinan cifras
normales o bajas de calcidiol, calcitriol bajo, PTH alta y fósforo alto (única entidad en la que el
hiperparatiroidismo secundario cursa con fosfatemia elevada).
Fosfatasa alcalina: suele hallarse elevada en la osteomalacia y menos frecuentemente en
pacientes con metástasis osteoblásticas.
Calciuria: es baja en pacientes con hipoparatiroidismo o deficiencia de vitamina D.
Figura 2. Algoritmo de la hipocalcemia.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1059]
[66] TRASTORNOS DEL METABOLISMO DEL CALCIO, FÓSFORO Y MAGNESIO
4. TRATAMIENTO (TABLA V)
Tabla V. Tratamiento de la hipocalcemia.
II. ALTERACIONES EN EL METABOLISMO DEL FÓSFORO
A. FISIOPATOLOGÍA
El 85% del fósforo corporal se encuentra formando parte de la hidroxiapatita del hueso. El 14% se
localiza en el espacio intracelular, formando parte del trifosfato de adenosina (ATP), fosfolípidos de
membrana y ácidos nucleicos. Solo el 1% del fósforo corporal total se encuentra en el líquido extracelular,
por lo que el fósforo plasmático no siempre refleja la cantidad de fósforo corporal total. El fósforo existe en
diferentes formas, tanto en el espacio extracelular como dentro de las células, predominantemente como
H2PO4 - o NaHPO4 -. Estos aniones en conjunto son conocidos como fosfato. Las concentraciones de fosfato
en plasma y líquido intracelular se expresan en términos de fósforo elemental. En el plasma,
aproximadamente el 12% del fósforo se encuentra unido a proteínas. El fósforo se absorbe en el intestino
delgado proximal, siendo su absorción estimulada por la 1,25 hidroxivitamina D. La excreción del fósforo es
por vía renal y está mediada por la PTH y el factor de crecimiento fibroblástico-23 (FGF-23). El fósforo se
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1060]
[66] TRASTORNOS DEL METABOLISMO DEL CALCIO, FÓSFORO Y MAGNESIO
filtra libremente a través del glomérulo, es excretado entre el 5% y el 20% y el resto, reabsorbido. La
reabsorción renal de fósforo en el túbulo proximal es la principal reguladora de su homeostasis. Las
concentraciones normales de fósforo oscilan entre 2,5 y 4,5 mg/dL.
B. HIPERFOSFATEMIA
1. DEFINICIÓN
Concentración plasmática de fósforo superior a 5 mg/dL.
2. ETIOLOGÍA
El objetivo principal al estudiar un paciente con hiperfosfatemia es elucidar la causa por la cual la
movilización de fósforo al espacio extracelular está excediendo la capacidad del riñón para excretarlo o si
la capacidad del riñón para excretar fósforo se encuentra disminuida. Existen varios escenarios en los que
estas circunstancias pueden ocurrir: carga aguda de fósforo, redistribución aguda al espacio extracelular,
insuficiencia renal aguda/enfermedad renal crónica o aumento primario de la reabsorción tubular de
fósforo (Tabla VI).
Tabla VI. Principales causas de hiperfosfatemia.
Por otro lado, se ha descrito hiperfosfatemia espuria en el contexto de hiperglobulinemia (mieloma
múltiple, macroglobulinemia de Waldenström, gammapatía monoclonal), hemólisis, hiperbilirrubinemia y
dosis altas de anfotericina B liposomal.
3. CLÍNICA
La hiperfosfatemia induce la formación de complejos insolubles de fosfato cálcico, lo que produce
hipocalcemia y calcificaciones en tejidos blandos. Las manifestaciones son más graves cuanto más brusca e
intensa es la hiperfosfatemia. Las principales manifestaciones son náuseas, vómitos, debilidad, calambres,
tetania, convulsiones, insuficiencia renal por nefrocalcinosis acelerada, prolongación del intervalo QT,
arritmias y calcifilaxia.
4. TRATAMIENTO
El tratamiento de la hiperfosfatemia debe encaminarse a la causa. La hiperfosfatemia aguda se
trata forzando la diuresis con suero salino (3-6 l/día). Esta medida puede disminuir también la calcemia, de
modo que es preciso monitorizar los niveles de calcio. La acetazolamida (15 mg/kg/4 h) favorece la
excreción renal de fósforo, y su uso está descrito en la calcinosis tumoral. Hay que valorar la hemodiálisis
en casos de hiperfosfatemia grave con hipocalcemia o insuficiencia renal avanzada.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1061]
[66] TRASTORNOS DEL METABOLISMO DEL CALCIO, FÓSFORO Y MAGNESIO
El objetivo del tratamiento de la hiperfosfatemia crónica en casos de insuficiencia renal avanzada es
mantener los valores de fósforo plasmático en rangos de normalidad. Las principales medidas incluyen
restricción de fósforo en la dieta, el uso de quelantes de fósforo, diálisis eficiente para remover el fosfato y
el control del hiperparatiroidismo grave para evitar mayor movilización de fósforo desde el hueso (ver
Capítulo 63. “Enfermedad renal crónica”).
C. HIPOFOSFATEMIA
1. DEFINICIÓN
Concentración plasmática de fósforo menor de 2,5 mg/dL.
2. ETIOLOGÍA (TABLA VII)
Tabla VII. Principales causas de hipofosfatemia.
Existen tres mecanismos primarios por los cuales se puede producir hipofosfatemia: aumento de su
excreción renal, disminución en la absorción intestinal y redistribución aguda al espacio intracelular. Por
otro lado, puede producirse hipofosfatemia espuria en el contexto de paraproteínas que interactúan con la
medición del fósforo. Para lograr establecer un diagnóstico adecuado es necesario realizar una historia
clínica detallada, conocer los antecedentes familiares y evaluar la capacidad que tiene el túbulo renal para
manejar el fósforo.
La excreción fraccional de fósforo puede calcularse en una muestra de orina al azar. Una excreción
fraccional mayor del 5% es compatible con un aumento renal en la excreción de fósforo, mientras que una
menor del 5% sugiere que la hipofosfatemia puede ser secundaria a redistribución interna o disminución en
la absorción intestinal.
Fórmula para calcular la excreción fraccional de fósforo:
EFPO4 = [UPO4 x PCr x 100] / [PPO4 x UCr]
UPO4: fósforo en orina; PCr: creatinina en plasma; PPO4: fósforo en plasma; UCr: creatinina en orina.
3. CLÍNICA
Los niveles de fosfato sérico no reflejan con exactitud las reservas corporales totales de fósforo, por
lo que el grado de hipofosfatemia no siempre se correlaciona con los síntomas. La hipofosfatemia suele
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1062]
[66] TRASTORNOS DEL METABOLISMO DEL CALCIO, FÓSFORO Y MAGNESIO
clasificarse en moderada (1-2,5 mg/dL) o grave (< 1 mg/dL). La mayoría de los pacientes hipofosfatémicos
presentan cifras moderadamente bajas y se encuentran asintomáticos. Cuando la fosfatemia disminuye por
debajo de 1 mg/dL suelen aparecer manifestaciones clínicas: debilidad, rabdomiólisis, resistencia a la
insulina, convulsiones, encefalopatía, mielinólisis pontina central, hemólisis, insuficiencia respiratoria por
debilidad de la musculatura respiratoria, insuficiencia cardiaca y arritmias.
4. TRATAMIENTO
La hipofosfatemia moderada asintomática suele responder a la corrección de la causa, como por
ejemplo en la cetoacidosis diabética, el déficit de vitamina D o la secundaria a fármacos o diarrea crónica.
En algunas ocasiones es necesaria la administración de suplementos de fosfato por vía oral (si los valores de
fósforo plasmático están entre 1 y 2 mg/dL). Se recomienda una dosis de 2,5-3,5 g de fósforo elemental al
día en 3-4 tomas. La leche de vaca, como medida complementaria, es un buen suplemento de fósforo, ya
que contiene 1 g por litro.
La hipofosfatemia grave (menor de 0,5 mg/dL o en niveles mayores pero con complicaciones
neuromusculares, cardiopulmonares o hematológicas) es rara, y requiere reposición con monofosfato
sódico (ampollas de 10 ml con 1 mmol por ml; 10 mmol por ampolla) a una dosis de 0,25-0,50 mmol/kg de
peso, en 500 ml de suero salino fisiológico en 6 horas. Dosis de hasta 40 mmol de monofosfato sódico
administradas en un máximo de 20 mmol por hora han demostrado ser seguras. Se puede repetir la dosis
hasta alcanzar niveles plasmáticos de 1 mg/dL. El fósforo (intravenoso) puede producir hipocalcemia,
hiperpotasemia, hiperfosfatemia y acidosis metabólica, por lo que se realizará una monitorización estricta
de sus niveles cada 6 a 12 horas. Se recomienda telemetría continua.
III. ALTERACIONES EN EL METABOLISMO DEL MAGNESIO
A. FISIOPATOLOGÍA
El magnesio (Mg) es el segundo catión intracelular más abundante. Un 50-60% se encuentra en el
hueso, y la mayor parte del resto en el interior de las células. Solo el 1% del Mg corporal es extracelular (por
ello esto no refleja su contenido corporal total). La equivalencia para el Mg es la siguiente:
24 mg = 1 mmol = 2 mEq
De modo que 2,4 mg/dL equivalen a 1 mmol/l o 2 mEq/l. Sus concentraciones séricas oscilan entre
1,4 y 2,0 mEq/l (1,7-2,3 mg/dL).
Está en gran variedad de alimentos (sobre todo, vegetales verdes). Alrededor del 40-50% se
absorbe en el intestino mediante la vitamina D. Su excreción es renal. El riñón puede reabsorberlo en
situaciones de déficit, siendo este el principal mecanismo de su homeostasis.
Interviene como cofactor enzimático en múltiples rutas metabólicas intracelulares (síntesis proteica
y de ADN), así como en procesos de transmisión bioeléctrica muscular y nerviosa, de manera que también
está relacionado con la vasomoción, la tensión arterial y la conducción cardiaca.
La concentración extracelular elevada de Mg reduce la actividad del sistema nervioso y la
contracción del músculo esquelético. La concentración reducida de Mg incrementa la irritabilidad del
sistema nervioso, provoca una vasodilatación periférica y arritmias cardiacas.
B. HIPERMAGNESEMIA
Concentración sérica de Mg superior a 2 mEq/ (2,4 mg/dL o mayor).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1063]
[66] TRASTORNOS DEL METABOLISMO DEL CALCIO, FÓSFORO Y MAGNESIO
1. ETIOLOGÍA
La causa más frecuente es la insuficiencia renal. La hipermagnesemia es infrecuente en personas
con función renal normal (Tabla VIII).
Tabla VIII. Causas de hipermagnesemia.
2. CLÍNICA (TABLA IX)
La mayor parte de los pacientes sufren hipermagnesemia crónica asintomática (niveles < 3 mEq/l o
< 3,6 mg/dL), apareciendo la clínica a partir de 4 mEq/l (4,8 mg/dL). Algunos factores aumentan la
cardiotoxicidad del magnesio, como la hipocalcemia, hiperpotasemia, acidosis y la intoxicación digitálica.
Tabla IX. Manifestaciones clínicas en hipomagnesemia e hipermagnesemia.
3. TRATAMIENTO
El tratamiento depende del grado de insuficiencia renal del paciente, de los niveles séricos de Mg y
de las manifestaciones clínicas.
La hipermagnesemia crónica asintomática de la insuficiencia renal avanzada no requiere
tratamiento, sino solo prevención (evitar medicaciones con Mg y monitorizar niveles en pacientes con
aportes parenterales [nutrición]). En enfermos con función renal normal, basta con identificar la causa de la
hipermagnesemia y suspender el aporte del Mg, aunque pueden usarse diuréticos (de asa o tiazídicos) para
forzar su eliminación.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1064]
[66] TRASTORNOS DEL METABOLISMO DEL CALCIO, FÓSFORO Y MAGNESIO
En los pacientes con ERC (enfermedad renal crónica) moderada o fracaso renal agudo (FRA) leve se
ha de realizar una hidratación intravenosa enérgica en combinación con diuréticos de asa, recurriendo a la
diálisis si estas medidas no fueran eficaces, principalmente a la hemodiálisis.
Se comenzará diálisis en los casos de filtrado glomerular (FG) < 15 ml/min o de fracaso renal agudo
(FRA) moderado-severo. Cuando existan alteraciones neuromusculares o cardiacas importantes, se iniciará
inmediatamente tratamiento intravenoso con gluconato cálcico al 10% (10-20 ml diluidos en 100-250 cc de
suero glucosado al 5% a pasar en 5-10 minutos).
C. HIPOMAGNESEMIA
Concentración sérica de magnesio inferior a 1,4 mEq/l (1,7 mg/dL).
1. ETIOLOGÍA (TABLA X)
Suele deberse a pérdidas excesivas de Mg desde el intestino o el riñón. La excreción fraccional de
Mg (EFMg, calculada de forma análoga a la EFNa [ver Capítulo 65. “Trastornos del equilibrio
hidroelectrolítico. SIADH. Fluidoterapia”]) y la magnesiuria de 24 horas son herramientas útiles que orientan
hacia el origen de las pérdidas. Una EFMg menor del 1% y una magnesuria de 24 horas menor de 20 mg
apuntarían a pérdidas extrarrenales. Una EFMg mayor del 3% y una magnesiuria de 24 horas mayor de 40
mg indicarían pérdidas renales.
Tabla X. Causas de hipomagnesemia.
Elevadas concentraciones de etanol en sangre alteran directamente la reabsorción tubular de Mg.
En pacientes diabéticos, la glucosuria con diuresis osmótica conlleva también la pérdida de este ion. Existe
una entidad denominada depleción de Mg normomagnesémica que cursa con concentraciones séricas
normales pero disminución de las reservas tisulares de Mg. Se sospecha en el contexto de una hipocalcemia
concomitante y puede mejorar con la administración de Mg.
2. CLÍNICA (TABLA IX)
A menudo, la hipomagnesemia se acompaña de otras alterac hidroelectrolíticas como hipocalcemia
o hipopotasemia. Se ha de sospechar esta entidad cuando dichas alteraciones sean de difícil control.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1065]
[66] TRASTORNOS DEL METABOLISMO DEL CALCIO, FÓSFORO Y MAGNESIO
3. TRATAMIENTO
La vía de reposición y la dosis de Mg dependen del grado de función renal del paciente (se
recomienda ser cauto en pacientes con enfermedad renal avanzada), de los niveles séricos de Mg y de las
manifestaciones clínicas. Siempre se tratará de corregir la causa subyacente. Recordemos que 1 mmol de
Mg equivale a 2 mEq o a 24 mg de Mg de elemental.
En la hipomagnesemia leve asintomática se usarán sales de magnesio por vía oral. La dosis diaria
para pacientes con función renal normal es de 240 a 1.000 mg (20-80 mEq o 10-40 mmol), repartida en
varias tomas. Tienen una biodisponibilidad limitada y su principal efecto secundario es la diarrea, que
puede atenuarse usando sales de cloruro, gluconato o lactato (de liberación más sostenida).
Los pacientes que sufren hipomagnesemia grave sintomática requieren la administración
intravenosa de sulfato de Mg. Para ello, se administrará una ampolla de Sulmetin® (10 ml de sulfato de Mg
al 15% [1,5 g], diluidos en 100 cc de suero glucosado al 5%, a pasar en 15 minutos), seguidos de una
perfusión de mantenimiento que contenga 6 g de sulfato de Mg (4 ampollas de Sulmetin®) diluidos en
1.000 cc de suero glucosado al 5% a pasar en 24 horas durante 3-7 días con el fin de replecionar las
reservas intracelulares de Mg. Los pacientes con insuficiencia renal suelen requerir menores dosis de
mantenimiento para evitar el desarrollo de hipermagnesemia. Es necesaria una monitorización clínica y
analítica de estos pacientes (los niveles séricos han de permanecer por debajo de 2,5 mEq/l [3 mg/dL]).
BIBLIOGRAFÍA
Bollerslev J, Rejnmark L, Marcocci C, Shoback DM, Sitges-Serra A, van Biesen W, et al. European
Society of Endocrinology Clinical Guideline: Treatment of chronic hypoparathyroidism in adults. Eur J
Endocrinol. 2015;173:G1-20.
Bringhurst F, Demay MB, Krane SM, Kronenberg HM. Bone and mineral metabolism in health and
disease. En: Kasper D, Fauci A, Hauser S, Longo D, Jameson J, Loscalzo J, editores. Harrison’s
Principles of Internal Medicine, 19ª edición. New York, NY: McGraw-Hill; 2015. Disponible en:
http://accessmedicine.mhmedical. com/content.aspx?bookid=1130&Sectionid=79753494. Accessed
January 11, 2016.
Chang WT, Radin B, McCurdy MT. Calcium, magnesium, and phosphate abnormalities in the emergency
department. Emerg Med Clin North Am. 2014;32:349-66.
De Baaji JHF, Hoenderop JGJ, Bindels RJM. Magnesium in man: implications for health and disease.
Physiol Rev. 2015;95:1-46.
García Esparza D, Ortiz Imedio J. Trastornos del metabolismo del calcio, fósforo y magnesio. En: Aguilar
F, Bisbal O, Gómez C, de Lagarde M, Maestro G, Pérez-Jacoíste MA, et al, editores. Manual de
diagnóstico y terapéutica médica. 7ª ed. Madrid: MSD; 2012. p. 927-40.
Geerse DA, Bindels AJ, Kuiper MA, Roos AN, Spronk PE, Schultz MJ. Treatment of hypophosphatemia in
the intensive care unit: a review. Crit Care. 2010;14(4):R147.
Holick MF. Vitamin D Deficiency. N Engl J Med. 2007;357(3):266-81.
Howard SC, Jones DP, Pui CH. The tumor lysis syndrome. N Engl J Med. 2011;364:1844-54.
Imel EA, Econs MJ. Approach to the hypophosphatemic patient. J Clin Endocrinol Metab.
2012;97(3):696-706.
Kerr S, Kindt J, Daram SR. Hypophosphatemia associated with paraproteinemia: a case report and
review of the literature. WMJ 2007;106(8):490-3.
Lane JW, Rehak NN, Hortin GL, Zaoutis T, Krause PR, Walsh TJ. Pseudohyperphosphatemia associated
with high-dose liposomal amphotericin B therapy. Clin Chim Acta. 2008;387(1-2):145-9.
Larner AJ. Pseudohyperphosphatemia. Clin Biochem. 1995;28(4):391-3.
Minisola S, Pepe J, Piemonte S, Cipriani C. The diagnosis and management of hypercalcaemia. BMJ.
2015;350:h2723.
Musso CG. Magnesium metabolism in health and disease. Int Urol Nephrol. 2009;41:357-62.
Prié D, Friedlander G. Genetic disorders of renal phosphate transport. N Engl J Med. 2010;362:2399-
409.
Shoback D. Hypoparathyroidism. N Engl J Med. 2008;359:391-403.
Trujillo-Cuéllar H, Sierra-Lara Martínez JD, Osorno-Solís L. Alteraciones del metabolismo mineral y óseo
asociadas a la enfermedad renal crónica. Revista Médica. 2015;6(2):151-60.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1066]
[67] FLUIDOTERAPIA Y PRINCIPIOS DE NUTRICIÓN
67.Fluidoterapia y principios de nutrición
Raúl Martínez Porqueras.
Medicina Interna
Milagros Sierra Bracamonte.
Endocrinología y Nutrición
Asesores:
Miguel de León Sanz.
Jefe de Sección de Endocrinología
María de los Ángeles Valero Zanuy.
Médica Adjunta de Endocrinología
I. FLUIDOTERAPIA
La fluidoterapia tiene como objetivo la recuperación y el mantenimiento del equilibrio
hidroelectrolítico alterado y el mantenimiento de la volemia para la adecuada perfusión y entrega de
oxigeno a los tejidos.
El agua corporal supone 600 ml/kg de peso, con variaciones individuales que dependen de la edad
(a menor edad hay mayor agua corporal), la proporción de tejido adiposo, el tejido muscular y el estado de
salud. Las concentraciones de los diferentes iones disueltas en los líquidos corporales se muestran en la
tabla I.
A. NECESIDADES DIARIAS DE AGUA Y ELECTROLITOS
1. NECESIDADES DIARIAS DE AGUA
El cálculo de los requerimientos diarios de agua se puede realizar a través de la ecuación de
Holliday-Segar (Tablas II y III). Una aproximación más sencilla es un requerimiento diario de agua de 35
ml/kg/día. Existen situaciones en las que se precisa variar las necesidades basales de líquidos (Tabla IV).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1067]
[67] FLUIDOTERAPIA Y PRINCIPIOS DE NUTRICIÓN
2. NECESIDADES DIARIAS DE GLUCOSA Y ELECTROLITOS
Durante periodos de ayuno breve (menores de 24 horas) se deben aportar al menos 2 g/kg/día de
glucosa para disminuir la neoglucogénesis hepática. Si el aporte de glucosa exógeno es inferior, se produce
un balance nitrogenado negativo. Si se prevé un ayuno de más de 7-10 días, se debe valorar el inicio de
nutrición artificial. Las necesidades de electrolitos se exponen en la tabla V.
3. CÁLCULO DE LA PÉRDIDA DE AGUA Y ELECTROLITOS SEGÚN LA SITUACIÓN CLÍNICA (TABLAS VI Y VII)
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1068]
[67] FLUIDOTERAPIA Y PRINCIPIOS DE NUTRICIÓN
B. INDICACIONES DE LA FLUIDOTERAPIA INTRAVENOSA
La fluidoterapia está indicada en todas aquellas situaciones en las que existe alteración de la
volemia, del equilibrio hidroelectrolítico o de ambos.
Ayuno superior a 24-48 horas o situaciones en las que existe disminución de la ingesta (disfagia,
postoperatorio, etc.).
Depleción del líquido extracelular:
Pérdidas digestivas (vómitos, diarrea, fístula enterocutánea, débito elevado por sonda
nasogástrica [SNG]).
Tercer espacio (ascitis, íleo paralítico, edemas).
Alteraciones renales (glomerulonefritis, poliuria osmótica, diabetes insípida).
Depleción hídrica por aumento de las pérdidas: sudoración excesiva, diabetes insípida,
cetoacidosis diabética, síndrome hiperosmolar, taquipnea en ventilación mecánica.
Depleción salina por diuréticos, nefropatías (pérdida de sal), pérdidas digestivas, insuficiencia
adrenal aguda.
Trastornos hidroelectrolíticos.
Shock hipovolémico: hemorragia, deshidratación, quemaduras, etc.
Shock distributivo: séptico, anafiláctico, neurogénico.
C. TIPOS DE FLUIDOS PARA ADMINISTRACIÓN INTRAVENOSA (Tablas VIII a XIV)
Se utilizan distintos fluidos intravenosos para cubrir los requerimientos de agua. Según la situación
clínica, se pueden administrar soluciones hipotónicas, isotónicas o hipertónicas.
Las soluciones más utilizadas son las isotónicas. De estas, los cristaloides merecen especial
mención. Entre los cristaloides es importante diferenciar las soluciones que se utilizan para reponer
pérdidas y las que son de mantenimiento.
La solución de reposición ideal es el lactato de Ringer, que es equivalente al plasma en sodio,
potasio, cloro y bicarbonato. El suero fisiológico (NaCl 0,9%), que es la solución más utilizada en el ámbito
hospitalario, tiene mayor cantidad de sodio y cloro que el plasma. La solución ideal para el mantenimiento
es el glucosalino, agregando suplementos de potasio.
En la tabla VIII se describen las principales soluciones utilizadas para fluidoterapia, así como sus
características e indicaciones.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1069]
[67] FLUIDOTERAPIA Y PRINCIPIOS DE NUTRICIÓN
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1070]
[67] FLUIDOTERAPIA Y PRINCIPIOS DE NUTRICIÓN
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1071]
[67] FLUIDOTERAPIA Y PRINCIPIOS DE NUTRICIÓN
D. NORMAS GENERALES PARA EL USO DE FLUIDOTERAPIA INTRAVENOSA
1. INDICACIONES DE VOLUMEN Y TIPO DE SOLUCIONES
No existe un protocolo general para la administración de fluidoterapia, de modo que se debe
individualizar en función de las características del paciente y el cuadro clínico. Se han de tener en cuenta
diversos aspectos:
Estimación de las necesidades básicas diarias de agua, electrolitos y glucosa (35 ml/ kg de agua,
2 mEq/kg de sodio, 1 mEq/kg de potasio y 2 g/kg de glucosa al día).
Estimación de pérdidas de agua y electrolitos (vómitos, diarrea, SNG, ostomías, etc.).
Considerar patologías asociadas: insuficiencia cardiaca, insuficiencia renal, insuficiencia
hepática. Se debe ajustar especialmente el volumen para evitar la sobrecarga.
Selección del fluido que se va a administrar y la velocidad de reposición.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1072]
[67] FLUIDOTERAPIA Y PRINCIPIOS DE NUTRICIÓN
2. MONITORIZACIÓN
2.1. Signos clínicos: diuresis, frecuencia cardiaca, presión arterial, temperatura, estado de alerta y
otros signos de hipovolemia (sequedad de piel y mucosas, presencia de pliegue cutáneo y/o sed) o
hipervolemia (ingurgitación yugular, crepitantes pulmonares, aparición de tercer ruido cardiaco y/o
edemas) y pérdidas extras por sondas, ostomías, fístulas, etc.
2.2. Datos de laboratorio:
Función renal: urea, creatinina en sangre.
Iones: sodio, potasio, cloro en sangre y orina.
Gasometría arterial.
Relación nitrógeno ureico sanguíneo (BUN)/creatinina: marcador de hidratación del individuo;
si son menores de 15 equivalen a hidratación suficiente, mientras que índices inferiores a 20
indican bajo volumen intravascular.
Osmolaridad plasmática: especialmente indicada en casos de deshidratación.
2.3. Monitorización invasiva de parámetros hemodinámicos: presión venosa central, presión capilar
pulmonar, índice cardiaco, lactato.
II. PRINCIPIOS DE NUTRICIÓN
A. VALORACIÓN DEL ESTADO NUTRICIONAL
A todos los pacientes hospitalizados se les debe realizar al ingreso y reevaluar cada 7 días o cuando
se produzca un cambio en su estado clínico o nutricional. La valoración nutricional puede consistir
inicialmente en un cribado o screening de riesgo nutricional. Aquellos pacientes que se identifican como en
situación de riesgo, deberían ser sometidos a una valoración más completa con énfasis en el aspecto
nutricional.
1. MÉTODOS DE CRIBADO NUTRICIONAL
Su objetivo es detectar a los pacientes que están en riesgo de malnutrición o la padecen con el
objeto de implementar medidas de soporte nutricional para reducir las complicaciones y acelerar la
recuperación. Existen varias herramientas de cribado, de modo que se puede utilizar cualquiera de las
validadas. La Sociedad Europea de Nutrición Parenteral y Enteral (ESPEN) recomienda el Nutritional Risk
Screening-2002 (NRS-2002) para pacientes ingresados en el hospital.
2. VALORACIÓN NUTRICIONAL COMPLETA
En aquellos pacientes con cribado nutricional positivo, se debe realizar una valoración nutricional
completa. Esta incluye:
Historia clínica: se debe prestar atención a la existencia de patología crónica de base,
antecedentes quirúrgicos (especialmente sobre el tracto digestivo), medicamentos que
interfieran con el apetito, la absorción y el metabolismo de los nutrientes, nivel
socioeconómico, organización doméstica y de las comidas y el estado mental. Se debe estimar
la ingesta alimentaria (recordatorio de la ingesta de las últimas 24 horas). Se han diseñado una
serie de cuestionarios que permiten valorar el estado nutricional de una forma ágil y fiable sin
invertir mucho tiempo. El NRS-2002 está diseñado como herramienta de cribado de
desnutrición en individuos hospitalizados.
Exploración física: Se deben obtener los siguientes parámetros antropométricos:
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1073]
[67] FLUIDOTERAPIA Y PRINCIPIOS DE NUTRICIÓN
Peso y talla: son indicadores a largo plazo del estado nutricional. El peso es un
indicador indirecto de la masa proteica y de las reservas energéticas. Se debe tener en
cuenta el estado de hidratación (edemas y ascitis enmascaran posibles pérdidas de
masa corporal).
Pérdida de peso (Porcentaje de pérdida de peso = [Peso habitual – Peso actual] x 100 /
Peso habitual) (Tabla XV).
Índice de masa corporal (IMC): es una forma de expresar el peso en relación con la talla
[IMC = Peso (kg) / Talla (m2)]. Para la interpretación del resultado, véase la tabla XVI.
Pruebas de laboratorio:
Proteínas plasmáticas: conviene resaltar que la albúmina se considera un buen
parámetro de morbilidad y mortalidad, pero un mal parámetro nutricional, debido a
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1074]
[67] FLUIDOTERAPIA Y PRINCIPIOS DE NUTRICIÓN
que la alteración de sus concentraciones séricas se debe mucho más a cambios de
distribución corporal, síntesis y degradación que a una ingesta nutricional insuficiente
(Tablas XVII y XVIII).
Otros parámetros analíticos: colesterol plasmático total (desnutrición < 120 mg/dL),
hemoglobina (la existencia de anemia hace sospechar determinados déficits
nutricionales como ácido fólico en alcohólicos o vitamina B12 y hierro en
malabsorción), creatinina, 3-metilhistidina, etc.
Evaluación del estado inmunitario: el recuento linfocitario también permite clasificar la
desnutrición.
Métodos de composición corporal: los más utilizados son impedanciometría corporal,
absorciometría de fotones y técnicas de imagen (tomografía computarizada y resonancia
magnética).
B. TRASTORNOS NUTRICIONALES
La desnutrición es el estado corporal debido a una deficiencia o exceso de energía, proteínas y
otros nutrientes, causa efectos adversos medibles en la composición y función de los tejidos/ órganos y en
el resultado clínico. Recientemente, la ESPEN ha establecido nuevos criterios diagnósticos de la
desnutrición (Tabla XIX).
Desde el punto de vista etiopatogénico, la desnutrición en los adultos puede deberse a tres causas:
en primer lugar, a una disminución de la ingesta, como ocurre en la anorexia nerviosa (starvation-related
malnutrition). En segundo lugar, a la presencia de una enfermedad aguda, en la cual existe un aumento de
la respuesta inflamatoria debido al estrés; es lo que ocurre en los enfermos quemados, politraumatizados,
sépticos o con traumatismo craneoencefálico grave (acute disease o injury-related malnutrition). Por
último, la desnutrición puede aparecer en presencia de una enfermedad crónica con un grado
leve/moderado de respuesta inflamatoria; se presenta en enfermedades crónicas como nefropatía,
hepatopatía, enfermedad pulmonar, enfermedades cardiacas, cáncer de páncreas, artritis reumatoide,
obesidad y diabetes mellitus (chronic disease-related malnutrition).
C. SOPORTE NUTRICIONAL
Consiste en la administración de nutrientes y de otras sustancias terapéuticas coadyuvantes
necesarias con el propósito de mejorar o mantener el estado nutricional del paciente. El soporte nutricional
(SN) está indicado en todo paciente en el que no se puede asegurar la ingesta vía oral durante un periodo
prolongado. Según las distintas guías, el tiempo puede variar entre 5 y 7 días. Se puede iniciar antes en
pacientes desnutridos o con riesgo de desnutrición.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1075]
[67] FLUIDOTERAPIA Y PRINCIPIOS DE NUTRICIÓN
A continuación, se describen una serie de situaciones clínicas que requieren soporte nutricional
(Tabla XX) y una serie de patologías de riesgo desde el punto de vista nutricional.
D. TIPOS DE SOPORTE NUTRICIONAL
Se clasifican de acuerdo con la vía de administración (Figura 1):
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1076]
[67] FLUIDOTERAPIA Y PRINCIPIOS DE NUTRICIÓN
1. NUTRICIÓN ENTERAL (NE)
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1077]
[67] FLUIDOTERAPIA Y PRINCIPIOS DE NUTRICIÓN
Modalidad de SN mediante la cual se administra una fórmula enteral por vía digestiva, ya sea por
sonda u ostomía, o incluso por vía oral. Frente a la nutrición parenteral (NP), la nutrición enteral (NE) es
más fisiológica, fácil de preparar y administrar, tiene un coste menor, menor incidencia y gravedad de las
complicaciones y preserva mejor la función e integridad intestinal.
1.1. Indicaciones
Pacientes candidatos a SN que tienen un aparato digestivo funcionalmente útil, o con alguna
alteración pero que permite la suficiente digestión y absorción de nutrientes (Tabla XXI).
1.2. Fórmulas de nutrición enteral
Son soluciones químicamente definidas constituidas por una mezcla de macronutrientes y
micronutrientes. Son nutricionalmente completas. La composición en vitaminas y minerales suele cumplir
las recomendaciones establecidas para la dieta oral (RDI, recommended dietary intake) en volúmenes de
1.000 a 2.000 ml de fórmula de NE (Tabla XXII). Existen una serie de fórmulas especiales para determinadas
patologías (insuficiencia renal, insuficiencia respiratoria aguda y crónica, insuficiencia hepática, diabetes
mellitus e intolerancia hidrocarbonada, estrés hipermetabólico, inmunodepresión, cáncer).
1.3. Vías de administración
La vía de elección dependerá de la patología de base, la duración prevista del tratamiento
nutricional y del riesgo de aspiración. El acceso más fisiológico es el oral, pero si este no es posible se
utilizan sondas u ostomías (Tabla XXIII).
1.4. Formas de administración
Alimentación por SNG o gastrostomía: se inicia con bolos de 50-100 ml/3 h, respetando la
noche. Se aumenta 50 ml cada uno o dos aportes hasta un máximo de 350-500 ml/3-4 h, o
hasta completar las necesidades nutricionales. Tras cada bolo se deben administrar 50-100 ml
de agua para evitar la obstrucción de la sonda. Se debe elevar la cabecera de la cama 30o
durante la administración de la NE y 2 horas después para disminuir el riesgo de reflujo y
aspiración.
Alimentación por sonda nasoduodenal o yeyunostomía: se recomienda infundir el preparado
de forma continua (bomba de infusión o caída por gravedad), comenzando a 25-50 ml/h. Si se
tolera, a las 12-24 h se aumenta 25-50 ml/h y se continúa con esta pauta de ascenso cada 12-24
h, hasta cubrir los requerimientos nutricionales. La velocidad de infusión máxima oscila entre
100-150 ml/h.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1078]
[67] FLUIDOTERAPIA Y PRINCIPIOS DE NUTRICIÓN
1.5. Control de los pacientes con sondas de alimentación
Se deben lavar una vez al día las ventanas nasales, aplicar vaselina en los labios y cepillar
frecuentemente los dientes; además, si la situación clínica lo permite, deben masticar chicles, chupar
caramelos o hacer enjuagues con elixires. Es posible que el paso de alimentación sea simultáneo con el de
fármacos. Hay que conocer qué medicamentos pueden triturarse y su interacción con la alimentación.
1.6. Complicaciones
Pueden clasificarse en cuatro grupos: gastrointestinales, metabólicas, infecciosas y mecánicas
(Tabla XXIV).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1079]
[67] FLUIDOTERAPIA Y PRINCIPIOS DE NUTRICIÓN
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1080]
[67] FLUIDOTERAPIA Y PRINCIPIOS DE NUTRICIÓN
2. NUTRICIÓN PARENTERAL
Modalidad de SN que permite administrar nutrientes directamente al torrente sanguíneo.
2.1. Indicaciones
Pacientes candidatos a SN cuyo tracto digestivo no funciona adecuadamente o no puede ser
utilizado con seguridad. Para comenzar con nutrición parenteral (NP) se requiere que el paciente esté
hemodinámicamente estable.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1081]
[67] FLUIDOTERAPIA Y PRINCIPIOS DE NUTRICIÓN
2.2. Composición de las fórmulas de nutrición parenteral
Están compuestas por macronutrientes (glucosa, lípidos y aminoácidos), micronutrientes (vitaminas
y minerales) y electrolitos en un volumen decidido por quien hace la prescripción.
2.3. Tipos de nutrición parenteral
Según el tipo de acceso al torrente circulatorio utilizado, existen dos tipos de NP:
Nutrición parenteral total o central (NPT): cuando los nutrientes se infunden a través de una
vía venosa central de alto flujo. Permite administrar soluciones de alta osmolaridad (> 900
mOsm/l). En general, cubren todos los requerimientos energéticos y proteicos. Cuando se
prevé una duración del SN menor de 30 días se administra a través de catéteres venosos
centrales (CVC) transitorios (los accesos vasculares más frecuentes son las venas subclavia y
yugular) o insertado a través de una vía periférica (PICC, peripherally inserted central catheter;
por ejemplo, Drum). Cuando la duración es mayor de 30 días se usan CVC tunelizados
permanentes (tipo Hickman) o reservorios subcutáneos.
Nutrición parenteral parcial o periférica (NPP): cuando se administra a través de una vía
venosa periférica. La osmolaridad máxima tolerada es de 600-900 mOsm/l, en general, no son
nutricionalmente completas (exceptuando en individuos con requerimientos energéticos
bajos). Está indicada en:
Desnutrición moderada y/o estrés metabólico leve que requiere SN inferior a 10 días.
Como complemento de dieta oral/enteral insuficiente o limitada.
Como alternativa transitoria en pacientes que requieren NPT y no disponen de accesos
centrales.
Transición de NP a NE u oral. Está contraindicada en situaciones de restricción de
volumen como la insuficiencia renal o cardiaca, o en la hepatopatía crónica con ascitis.
La complicación más frecuente es la tromboflebitis.
Está contraindicada en situaciones de restricción de volumen como la insuficiencia renal o cardiaca,
o en la hepatopatía crónica con ascitis. La complicación más frecuente es la tromboflebitis.
2.4. Complicaciones (Tabla XXV)
Existen complicaciones mecánicas e infecciosas propias de la colocación de la vía venosa central
(para más información, ver Capítulo 2. “Técnicas y procedimientos instrumentales”).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1082]
[67] FLUIDOTERAPIA Y PRINCIPIOS DE NUTRICIÓN
BIBLIOGRAFÍA
Benito C, Perales N. Principios básicos de fluidoterapia. Barcelona: Fresenius Kabi; 2010.
Boullata J, Gilbert K, Saks G, Labossiere RJ, Crill C, Goday P, et al. ASPEN clinical guidelines: parenteral
nutrition ordering, order review, compounding, labeling, and dispensing. 2014. JPEN J Parenteral
Enteral Nutrition. 2014;38(3):334-77.
Cederholm T, Bosaeus I, Barazzoni R, Bauer J, Van Gossum A, Klek S, et al. Diagnostic criteria for
malnutrition – An ESPEN Consensus Statement. Clin Nutr. 2015;34(3):335-40.Kondrup J. Clinical
Guidelines for Nutrition Screening 2002. Clin Nutr. 2010; 22(4): 415-21.
León M. Principios de nutrición clínica. En: Rodés J, Carné X, Trilla A, editores. Manual de terapéutica
médica. Barcelona: Masson; 2002; p. 765-80.
Lobo DN. Fluid, electrolytes and nutrition: physiological and clinical aspects. Proc Nutr Soc.
2004;63(3):453- 66.Luque-Ramírez M, Sánchez A. Nutrición clínica: evaluación del estado nutricional.
En: Sancho JM, Varela C, De la Calle H, Balsa JA, editores. Manual de diagnóstico y terapéutica en
Endocrinología y Nutrición. Madrid: Novo Nordisk; 2004; p. 238-49.
Mueller C, Compher C, Druyan ME, American Society for Parenteral and Enteral Nutrition (ASPEN)
Board of Directors. ASPEN clinical guidelines: nutrition screening, assessment, and intervention in
adults. JPEN J Parenter Enteral Nutr. 2011;35(1):16-24.
Padhi S, Bullock I, Li L, Stroud M; National Institute for Health and Care Excellence (NICE) Guideline
Development Group. Intravenous fluid therapy for adults in hospital: summary of NICE guidance. BMJ.
2013;347:f7073.
Van Bokhorst-de van der Schueren MA, Guaitoli PR, Jansma EP, de Vet HC. Nutrition screening tools:
does one size fit all? A systematic review of screening tools for the hospital setting. Clin Nutr.
2014;33(1):39-58.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1083]
[68] ENFERMEDADES DEL TIROIDES
68.Enfermedades del tiroides
Milagros Sierra Bracamonte.
Endocrinología y Nutrición
Olaya Pascual Madrid.
Medicina Interna
Asesora:
Sonsoles Guadalix Iglesias.
Médica Adjunta de Endocrinología
I. EVALUACIÓN DE LA MORFOLOGÍA Y FUNCIÓN TIROIDEA
1. FISIOLOGÍA
La glándula tiroidea es ligeramente más grande en el hombre que en la mujer, aumenta de tamaño
con la edad y disminuye con el aumento de la ingesta de yodo. Existen dos hormonas activas, tiroxina (T4) y
triyodotironina (T3); su secreción está regulada por la tirotropina u hormona estimulante del tiroides (TSH),
de origen hipofisario, que además produce hipertrofia e hiperplasia del tejido tiroideo, por lo que su
inhibición puede tener implicaciones terapéuticas. El 80% de la T3 se produce en tejidos extratiroideos (casi
todos los tejidos de la economía, principalmente hígado y riñón), la mayoría de forma intracelular mediante
un proceso de desyodación de la T4 y es la que realmente tiene la actividad biológica. El paso
extraglandular de T4 a T3 está regulado por factores hormonales, nutricionales y patológicos con
diferencias de unos tejidos a otros e independencia del eje hipotálamo-hipofisario-glandular. Esto tiene
importancia a la hora de paliar parcialmente los efectos del hipotiroidismo, y se ve afectada por fármacos y
diversas enfermedades. También por desyodación de la T4 se produce triyodotironina reversa (rT3) que es
biológicamente inactiva.
La T4 y la T3 circulan en más del 99% unidas a proteínas transportadoras: globulina fijadora de
tiroxina (TBG), transtiretina (TTR), albúmina y lipoproteínas. La variación de la concentración de estas
proteínas transportadoras tiene gran influencia en las concentraciones totales de T3 y T4, no afectando a la
proporción de hormona libre.
2. EVALUACIÓN INICIAL
1. ANAMNESIS
Es fundamental preguntar por los síntomas básicos de hiper e hipofunción tiroidea. Además hay
que conocer el curso de la enfermedad, la ingesta diaria de yodo, fármacos bociógenos (amiodarona,
fenitoína, carbamazepina, andrógenos, estrógenos, etc.), antecedentes de radiación de cabeza y cuello en
la infancia y antecedentes familiares de patología tiroidea.
2. EXPLORACIÓN FÍSICA
La exploración de la glándula tiroidea debe atender a la forma (difuso, nodular), consistencia y
adherencia a planos profundos, tamaño, dolor, soplo tiroideo (enfermedad de Graves) y presencia de
adenopatías cervicales.
3. PRUEBAS COMPLEMENTARIAS
Hormonas tiroideas: útiles para la detección de enfermedad tiroidea y para el seguimiento de
la respuesta al tratamiento.
TSH (0,5-5 μUI/ml): alta sensibilidad pero poca especificidad. Útil para identificar
hipertiroidismo e hipotiroidismo, incluso en estadios subclínicos, y para monitorizar el
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1084]
[68] ENFERMEDADES DEL TIROIDES
tratamiento siendo la determinación de elección en ambos casos. La secreción de TSH
es pulsátil aumentando un 50-100% por la tarde y tiene tendencia a aumentar con la
edad (ver Tabla I).
T4 total (T4T) (5-12 μg/dL): tiene buena correlación con la T4 libre (T4L), salvo si se
producen alteraciones de las proteínas transportadoras (ver más adelante).
T4L (0,7-1,8 ng/dL): debe determinarse ante el hallazgo de una TSH alterada
confirmando el diagnóstico de hiper-hipotiroidismo e indicando la severidad. No se ve
afectada por los frecuentes cambios en las proteínas transportadoras, por lo que es la
más útil y fiable.
T3 total (T3) (75-195 ng/dL): útil en los casos con sospecha de hipertiroidismo (TSH
suprimida), con T4L normal, debido a la existencia de casos de tirotoxicosis por T3,
sobre todo en el seno de enfermedad de Graves y adenoma/bocio multinodular tóxico
(BMNT).
T3L (2-5,8 ng/dL): útil en los casos de sospecha de hipertiroidismo y síndrome
eutiroideo enfermo, en los casos de T4L normal. Los niveles estarán elevados en el
hipertiroidismo y disminuidos en el síndrome eutiroideo enfermo.
El screening (Figura 1) se realizará con la TSH salvo en pacientes ingresados,
aquellos que estén tomando fármacos que alteren las determinaciones de TSH o sospecha
de afectación central, donde se solicitará también T4 y T3 según cada caso.
Está indicado el cribado en: embarazadas, pacientes con clínica compatible,
fármacos que alteren la función tiroidea, alteraciones hipotalámica o pituitaria, bocio,
enfermedades autoinmunes, tratamiento previo con radioyodo, antecedentes familiares de
patología tiroidea, alteraciones de laboratorio (hiperlipidemia, hiponatremia, aumento de
CPK, anemia), fibrilación auricular o taquicardia sinusal y derrame pleural o pericárdico.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1085]
[68] ENFERMEDADES DEL TIROIDES
Para monitorizar el tratamiento la TSH tendrá valor a partir de las 4-6 semanas,
momento en que alcanza su estado estacionario. Si necesitamos hacerlo antes deben
solicitarse T4L y T3.
Anticuerpos antitiroideos: no se recomienda medirlos de rutina.
Anti-tiroperoxidasa (Ac-anti-TPO) y anti-tiroglobulina (Ac-anti-TG): elevados de manera
constante en la tiroiditis autoinmune, aunque también se elevan en la enfermedad de
Graves y en la población general. Los Ac-anti-TPO pueden predecir la evolución del
hipotiroidismo subclínico a sintomático. Los Ac-anti-TG solo se utilizan en el
seguimiento del carcinoma diferenciado de tiroides.
Anti-receptor de TSH (Ac-anti-R-TSH): pueden ser estimuladores (específicos de la
enfermedad de Graves), bloqueantes o neutrales (en la enfermedad de Graves y
tiroiditis autoinmune). Existen dos posibles determinaciones:
Thyroid-stimulating inmunoglobulin (TSI) (determinación usada en nuestro
centro): mide la respuesta efectora y es más específico de la enfermedad de
Graves.
TSH binding inhibitor inmunoglobulin (TBII) de nueva generación, es más
sensible aunque menos específico para la enfermedad de Graves.
Tiroglobulina (TG): antes de ser secretadas las hormonas tiroideas se hidrolizan de la TG y una
pequeña cantidad de esta proteína es también secretada a la sangre. Es útil en el seguimiento
del cáncer de tiroides y en el diagnóstico diferencial de la tirotoxicosis facticia y la tiroiditis,
donde ocurre una elevación importante por la destrucción del folículo tiroideo.
Ecografía tiroidea: es el estudio de imagen de elección para el tiroides. Las principales
indicaciones para la realización de la ecografía tiroidea son: presencia de bocio, palpación de
nódulo tiroideo, valoración de incidentalomas tiroideos, realización de punción y aspiración con
aguja fina (PAAF) y seguimiento de bocio, nódulo tiroideo y cáncer de tiroides.
Gammagrafía tiroidea con Tc-99 o I-123: valora el estatus funcional de la glándula. Está
indicada para el estudio del nódulo tiroideo, clasificándolos en calientes (hipercaptante),
indeterminados y fríos (hipocaptante). También es útil en el estudio de bocios nodulares con
sospecha de autonomía y diagnóstico diferencial del hipertiroidismo. Es una técnica de imagen
en dos dimensiones, por lo que el tejido normal puede superponerse al alterado; así un tercio
de los nódulos pequeños presentan un efecto de relleno apareciendo como normocaptantes
(debemos considerarlos como fríos). Su interpretación está interferida por la administración
previa de yodo (fármacos, contrastes yodados...) que inhibe la captación tiroidea del yodo
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1086]
[68] ENFERMEDADES DEL TIROIDES
radiactivo. En estos casos se debe esperar un plazo mínimo de 6 semanas para solicitarlo y que
sea valorable. Está contraindicada en lactancia y embarazo; en estos casos se puede valorar la
opción de ecodoppler.
Estudio histopatológico: suele realizarse con PAAF sobre nódulos, masas tiroideas y
adenopatías locorregionales. Puede guiarse por palpación, aunque en su gran mayoría se guía
por ecografía. Las complicaciones son raras, siendo las más frecuentes el dolor local y los
hematomas.
3. ALTERACIÓN DE LAS DETERMINACIONES FUNCIONALES TIROIDEAS EN LA ENFERMEDAD NO
TIROIDEA
Valorar la función tiroidea en el paciente crítico resulta difícil, puesto que las distintas pruebas
pueden presentar anomalías que en estabilidad clínica no se suelen correlacionar con patología
endocrinológica. Las alteraciones analíticas varían desde ligeras desviaciones de la normalidad, hasta
importantes alteraciones en los niveles de hormonas tiroideas. A estas alteraciones se les engloba en el
denominado síndrome del enfermo eutiroideo.
Estas anomalías deben considerarse en el contexto de las reacciones que coordinan la respuesta del
huésped ante cualquier agresión externa, por lo cual no se recomienda solicitar un perfil tiroideo si no se
tiene una alta sospecha de patología subyacente.
A continuación, en las tablas II y III se describen las alteraciones más frecuentes que se producen
en estos pacientes:
4. ALTERACIÓN TIROIDEA SECUNDARIA A FÁRMACOS
Distintos fármacos pueden afectar a cualquiera de los procesos metabólicos de síntesis, regulación,
transporte o excreción de las hormonas tiroideas, produciendo clínica hiper o hipotiroidea o alteraciones
aisladas en las pruebas de función tiroidea sin repercusión clínica. A continuación desarrollamos las
alteraciones tiroideas más frecuentes relacionadas con fármacos (Tablas IV, V y VI).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1087]
[68] ENFERMEDADES DEL TIROIDES
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1088]
[68] ENFERMEDADES DEL TIROIDES
II. BOCIO
1. CONCEPTO Y ETIOPATOGENIA
El término bocio se refiere al aumento de la glándula tiroides a más del doble de su tamaño, o que
pesa más de 40 gramos. El 90% desciende en el mediastino anterior. El 20% de bocios son retroesternales,
no palpables en el cuello. Puede ser secundario a múltiples etiologías (Tabla VII).
El yodo es un componente esencial de las hormonas tiroideas, y un aporte insuficiente lleva a
déficit de producción de estas, con un aumento compensatorio de la TSH y desarrollo de bocio simple. El
bocio es inicialmente difuso, aunque con el tiempo puede volverse un bocio multinodular (BMN), pues unos
folículos proliferan más que otros. Este aumento de replicación tiroidea favorece las mutaciones en el
receptor de la TSH produciendo nódulos autónomos con riesgo de desarrollar BMN tóxico (BMNT) y
tirotoxicosis por yodo (muchas veces tras la administración de contrastes yodados). Sin embargo, con el
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1089]
[68] ENFERMEDADES DEL TIROIDES
desarrollo de campañas de profilaxis con yodo en los países desarrollados el déficit de yodo es raro. En el
BMN el riesgo de cáncer sobre alguno de los nódulos es similar al del nódulo tiroideo solitario.
2. CLÍNICA
Dependerá del tamaño, localización y funcionalidad. La mayoría de los pacientes con bocio
eutiroideo pequeño tiene un curso benigno y asintomático.
Funcional (ver hipo-hipertiroidismo).
Inflamatoria: en algún caso de tiroiditis (ver tiroiditis).
Compresión de estructuras cervicales: es rara porque el tiroides tiene un crecimiento
excéntrico, siendo más frecuente el desplazamiento de estructuras cervicales por bocios de
crecimiento asimétricos (a veces visible en la radiografía de tórax). Suele desarrollarse de
manera lenta e insidiosa, salvo en los casos de bocio de crecimiento rápido, donde habrá que
descartar linfoma, cáncer de tiroides anaplásico o una hemorragia intratiroidea. La
sintomatología más frecuente es secundaria a compresión traqueal: disnea de esfuerzo o
postural, tos nocturna. Menos frecuentemente puede producirse estridor, sibilancias, disfagia,
parálisis de una cuerda vocal, síndrome de Horner, parálisis del nervio frénico o afectación de
los vasos cervicales. Además, puede producirse crecimiento de uno de los lóbulos hacia el
interior del tórax (bocio retroesternal), donde la mayoría ocupa el mediastino anterolateral
pudiendo producir clínica compresiva de estructuras intratorácicas.
3. DIAGNÓSTICO
Solicitar pruebas de función tiroidea y ecografía cervical. La gammagrafía tiroidea está indicada en
caso de nodularidad (ver estudio de nódulo tiroideo), TSH normal-disminuida o en el diagnóstico diferencial
de enfermedad de Graves y tiroiditis. El BMNT se presenta con una o varias áreas de aumento de captación
de radioyodo con inhibición o atenuación en el resto de la glándula. Ante la sospecha de clínica compresiva
o bocio retroesternal debe realizarse tomografía computarizada o resonancia magnética que incluya cuello
y tórax, y solicitar una espirometría que muchas veces es patológica aun en pacientes asintomáticos y con
escasa afectación en las pruebas de imagen.
4. TRATAMIENTO
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1090]
[68] ENFERMEDADES DEL TIROIDES
1. TRATAMIENTO DEL BOCIO NO TÓXICO
Cirugía (tiroidectomía total o subtotal): quizás el tratamiento de elección para bocios
eutiroideos con clínica compresiva, retroesternales grandes, aunque sean asintomáticos, o
bocios de crecimiento rápido. La decisión de intervenir se basará en la clínica y en las pruebas
de imagen y función respiratoria.
2. BOCIO MULTINODULAR TÓXICO
Además del tratamiento sintomático con betabloqueantes, por ejemplo propranolol 10-80 mg/24
h, existen 3 alternativas:
Tratamiento con tionamidas: de elección en ancianos, cardiópatas o hipertiroidismo
moderado-severo. Se recomienda comenzar con dosis de metimazol 10 mg/24 h, salvo en casos
de hipertiroidismo severo que comenzaremos con 20-30 mg/24 h. El objetivo es mantener al
paciente eutiroideo para posteriormente realizar tratamiento definitivo con radioyodo o
cirugía. En pacientes jóvenes sin patología cardiaca no es necesario el pretratamiento con
antitiroideos.
Radioyodo: recupera la función tiroidea del 85-100% de los pacientes, con menos incidencia de
hipotiroidismo que en la enfermedad de Graves, aunque aumenta en pacientes pretratados con
fármacos antitiroideos.
Cirugía: se prefiere si existen síntomas compresivos, necesidad de resolución rápida de la
clínica hipertiroidea y en presencia de nódulos fríos.
Otras opciones: inyección de etanol en los nódulos funcionantes o el tratamiento con láser.
III. NÓDULO TIROIDEO
La nodularidad tiroidea es muy frecuente, y su prevalencia está entre el 5-30% de la población,
dependiendo de si existe deficiencia de yodo. La prevalencia es mayor en mujeres y aumenta con la edad (a
partir de los 60 años). Entre los pacientes con un nódulo palpable el 20-48% tiene otros nódulos al realizar
la ecografía cervical. La importancia del nódulo tiroideo es que el 5-15% oculta un cáncer (Tabla VIII). Los
incidentalomas tienen el mismo riesgo de malignidad que un nódulo palpable solitario, al igual que la
presencia de múltiples nódulos (BMN). En las glándulas con varios nódulos se recomienda biopsiar aquellos
con características ecográficas de malignidad, más que el nódulo dominante, aunque no hay consenso al
respecto.
1. DIAGNÓSTICO
1. HISTORIA CLÍNICA Y EXPLORACIÓN FÍSICA
El crecimiento rápido, la presencia de adenopatías, masa fija y síntomas compresivos (disfonía,
disfagia...) sugieren malignidad (Tabla IX).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1091]
[68] ENFERMEDADES DEL TIROIDES
2. HORMONA ESTIMULANTE DEL TIROIDES
Una TSH baja orienta a un nódulo hiperfuncionante, por lo que se solicitará una gammagrafía
tiroidea; si se demuestra un nódulo caliente no se requerirá citología. Una TSH alta o normal, con un patrón
ecográfico sospechoso, es indicación directa de biopsia.
3. ECOGRAFÍA TIROIDEA
Debe solicitarse ante todo nódulo palpable, incidentaloma, BMN y en pacientes con factores de
riesgo de cáncer tiroideo. Según el patrón ecográfico se determinará el riesgo de malignidad y se decidirá el
manejo clínico. A continuación se resumen las nuevas recomendaciones de la guía de la Sociedad
Americana de Tiroides (ATA) 2015 para el nódulo tiroideo (Tabla X).
4. GAMMAGRAFÍA
Está disminuyendo su uso; actualmente está indicada en nódulos con TSH baja o con citología
folicular y en BMN. Los nódulos malignos son fríos o indeterminados, por lo que no está indicada la
citología en los calientes.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1092]
[68] ENFERMEDADES DEL TIROIDES
5. PUNCIÓN ASPIRACIÓN CON AGUJA FINA
Indicada en nódulos fríos en la gammagrafía y en función del tamaño y patrones ecográficos.
6. OTRAS DETERMINACIONES
Calcitonina: útil en la valoración de cáncer medular de tiroides (niveles > 100 pg/ml son muy
sugestivos). Su uso en el cribado es controvertido, pero podría usarse en pacientes con
antecedentes familiares de cáncer medular o MEN 2.
Anticuerpos antitiroideos: no se recomiendan de rutina.
Tiroglobulina: no aporta información en el diagnóstico de malignidad, aunque sí en el
seguimiento del cáncer diferenciado de tiroides. Si se solicita deben pedirse además Ac-anti-TG.
Tomografía por emisión de positrones (PET): dado el aumento del uso de la PET, la detección
de nódulos tiroideos por este método resulta cada vez más frecuente. Se recomienda la
realización de una PAAF en los casos de captación focal del nódulo, actividad metabólica y
tamaño (mayor de 1 cm). Si la captación es difusa y los signos ecográficos y analíticos son
compatibles con una tiroiditis linfocitaria crónica, no precisa seguimiento.
2. MANEJO
El manejo va a depender de los patrones ecográficos y resultados citológicos según la clasificación
de Bethesda. A continuación presentamos un resumen de las recomendaciones de la ATA 2015 (Figura 2).
IV. TIROIDITIS
Con el término tiroiditis nos referimos a un grupo de trastornos caracterizados por algún grado de
inflamación tiroidea; tienen un espectro clínico amplio, sus principales características, así como los
tratamientos empleados se resumen en la tabla XI.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1093]
[68] ENFERMEDADES DEL TIROIDES
V. HIPERTIROIDISMO
1. ETIOLOGÍA
1. HIPERTIROIDISMO ASOCIADO A HIPERFUNCIÓN DE LA GLÁNDULA TIROIDES (CAPTACIÓN AUMENTADA DE
RADIOYODO)
Sustrato autoinmune: enfermedad de Graves-Basedow (más frecuente en jóvenes).
Tejido tiroideo autónomo: adenoma tóxico o BMNT (más frecuente en ancianos).
Otros: hiperproducción de TSH, hipertiroidismo mediado por la hormona gonadotropina
coriónica.
2. HIPERTIROIDISMO NO ASOCIADO A HIPERFUNCIÓN DE LA GLÁNDULA (CAPTACIÓN DE RADIOYODO AUSENTE)
Tiroiditis (Tabla XI).
Ingesta de hormona tiroidea exógena (yatrogénico, intencional, facticio).
Ectópico (struma ovarii, carcinoma folicular metastásico).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1094]
[68] ENFERMEDADES DEL TIROIDES
2. CLÍNICA
La relación entre la expresividad de la clínica y los niveles de hormona tiroidea no es
necesariamente lineal, influyendo tanto el tiempo de instauración como la edad del paciente. En pacientes
jóvenes predominan los síntomas neurológicos y en ancianos los cardiovasculares.
En la enfermedad de Graves-Basedow la presentación suele ser florida con bocio difuso,
oftalmopatía y dermatopatía infiltrativa, con un curso clínico que puede ser fluctuante. En el BMNT y
adenoma tóxico predominan los síntomas cardiovasculares. En general, la sintoma- tología local y la fiebre
orientan a tiroiditis (Tabla XII).
3. DIAGNÓSTICO
La prueba inicial de despistaje es la medición de TSH, en caso de estar suprimida se deben
determinar T3 y T4 libres, y si estas están elevadas confirman el diagnóstico de hipertiroidismo primario; si
la sospecha es alta o hay dificultades en el seguimiento puede plantearse realizar ambas mediciones en la
misma analítica. Ante niveles normales o elevados de TSH habrá que descartar principalmente adenoma
hipofisario productor de TSH.
La enfermedad de Graves y el BMNT típicamente provocan elevaciones de T3 mayores que de T4. El
diagnóstico de enfermedad de Graves a veces es clínicamente evidente con oftalmopatía, bocio grande no
nodular e hipertiroidismo moderado-severo; no obstante, si el diagnóstico no es evidente en relación con la
forma de presentación la solicitud de Ac-anti-R-TSH es muy útil, puesto que de ser positiva permite
confirmar el diagnóstico.
4. TRATAMIENTO
En este apartado nos centramos en el hipertiroidismo causado por la enfermedad de Graves,
puesto que el tratamiento del adenoma tóxico, BMNT y el nódulo tiroideo se explican en otros apartados.
El tratamiento consiste en el control de síntomas con betabloqueantes y medidas inclinadas a
disminuir la síntesis de hormona tiroidea: antitiroideos, yodo radiactivo o cirugía. La decisión entre una de
estas tres estrategias debe ser personalizada en función de las características, situación y preferencias de
cada paciente.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1095]
[68] ENFERMEDADES DEL TIROIDES
1. BETABLOQUEANTES
Considerar en todos los pacientes con hipertiroidismo sintomático y sin contraindicación,
especialmente en ancianos, con taquicardia y enfermedad cardiovascular (Tabla XIII).
2. ANTITIROIDEOS DE SÍNTESIS (ATS) O TIONAMIDAS
Inhiben la función de la tiroperoxidasa, reduciendo la oxidación y organificación del yoduro.
Presentan una latencia de efecto de varias semanas y la mayoría de los pacientes no alcanza el estado
eutiroideo hasta 4-6 semanas tras su inicio. Se recomienda realización de hemograma y perfil hepático
previo al inicio del tratamiento. Los efectos secundarios más frecuentes son exantema, urticaria, fiebre y
artralgias. Pueden resolverse espontáneamente o tras la sustitución del fármaco por otro antitiroideo.
Algunos efectos secundarios poco frecuentes, pero graves, son la hepatitis, síndrome similar al lupus
eritematoso sistémico (SLE) y agranulocitosis (< 1%). Deben entregarse a los pacientes instrucciones sobre
los principales síntomas de la agranulocitosis (faringitis, fiebre, úlceras bucales) y la necesidad de
interrumpir el tratamiento y consultar inmediatamente si se producen (Tabla XIV).
3. YODO-131
Puede utilizarse como tratamiento inicial o para las recidivas tras un intento con antitiroideos. Está
contraindicado durante el embarazo o si existen deseos gestacionales en los 6 meses siguientes, o durante
la lactancia. Se deben pretratar con ATS aquellos pacientes con aumento del riesgo de complicaciones por
exacerbación del hipertiroidismo (ancianos, patología cardiaca) y para reducir el pequeño riesgo de crisis
tirotóxica que entraña, suspendiéndose en los días previos a la administración del yodo. Es esencial el
seguimiento posterior, dado el riesgo de presentar hipotiroidismo a corto y largo plazo. La oftalmopatía de
Graves clásicamente era una contraindicación para el tratamiento con yodo, recomendándose actualmente
una actuación cuidadosa valorando añadir corticoides.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1096]
[68] ENFERMEDADES DEL TIROIDES
4. CIRUGÍA
El tratamiento quirúrgico tiene especial interés en pacientes jóvenes con bocio muy voluminoso, en
el embarazo, en los que se quiere evitar la exposición al yodo radiactivo o que tengan riesgo de efectos
adversos con los ATS, así como ante la presencia de oftalmopatía severa. Antes de la cirugía debe realizarse
un control estricto de la tirotoxicosis con antitiroideos, seguido de la administración de yoduro potásico,
con el fin de evitar una crisis tirotóxica y reducir la vascularización de la glándula. Como principales
complicaciones posquirúrgicas se encuentran el hipoparatiroidismo con hipocalcemia (se deben
monitorizar niveles de calcio y PTH en el postoperatorio), parálisis del nervio laríngeo recurrente y la
recidiva del hipertiroidismo en casos de tiroidectomías subtotales. En tiroidectomías totales el tratamiento
sustitutivo con levotiroxina debería iniciarse antes del alta en pacientes eutiroideos; si el paciente persiste
hipertiroideo debería esperarse hasta que los niveles de hormonas tiroideas sean normales, realizando
seguimiento estrecho.
5. CRISIS TIRÓTOXICA O TORMENTA TIROIDEA
Se trata de un trastorno poco frecuente pero de extrema gravedad caracterizado por
manifestaciones graves y multiorgánicas de tirotoxicosis. Tiene una elevada mortalidad si no es reconocido
y tratado de manera agresiva. Requiere de una alta sospecha clínica. Los criterios que definen su
diagnóstico se exponen en la tabla XV. Posibles precipitantes en pacientes con hipertiroidismo previo son la
suspensión brusca de los fármacos, las cirugías, las enfermedades agudas, el parto y raramente tras
administración de radioyodo e incluso contrastes yodados. El tratamiento requiere soporte y vigilancia
intensiva y terapias destinadas a reducir la síntesis de hormona tiroidea y sus efectos (Tabla XVI).
6. HIPERTIROIDISMO SUBCLÍNICO
Hablamos de hipertiroidismo subclínico ante la presencia de TSH baja (< 0,5 mU/l) con T3 y T4
normales. Es una entidad clínicamente relevante, pues se ha relacionado con un aumento de mortalidad en
relación con enfermedad coronaria, aumento de frecuencia de fibrilación auricular y de insuficiencia
cardiaca, así como efectos deletéreos en el metabolismo óseo.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1097]
[68] ENFERMEDADES DEL TIROIDES
En general la indicación de tratamiento depende de la edad, la comorbilidad y el grado de
supresión de la TSH, siguiendo los mismos esquemas de tratamiento que para el hipertiroidismo franco
(Tabla XVII).
VI. HIPOTIROIDISMO
Hablamos de hipotiroidismo cuando existe disminución de la concentración de hormonas tiroideas.
El hipotiroidismo primario (es el más común) se caracteriza por niveles de TSH altos; el hipotiroidismo
secundario o terciario, en cambio, lo hacen por la disminución de TSH y hormona liberadora de tirotropina
(TRH) respectivamente.
1. ETIOLOGÍA
La deficiencia de yodo sigue siendo la causa más frecuente de hipotiroidismo a nivel mundial. En
áreas en las que hay suficiente yodo son más frecuentes la enfermedad autoinmunitaria (tiroiditis de
Hashimoto) y las causas yatrógenas (tratamiento del hipertiroidismo)
1. HIPOTIROIDISMO PRIMARIO
Tiroiditis crónica autoinmune o enfermedad de Hashimoto: causa más común en zonas no
deficitarias de yodo.
Iatrógeno: quirúrgico, tratamiento con antitiroideos, radioyodo o radioterapia. Como efecto
secundario de diferentes fármacos (ver apartado específico).
Déficit de yodo (bocio endémico): causa más común de hipotiroidismo y bocio en zonas con
deficiencia de yodo.
Enfermedades infiltrativas: tiroiditis de Riedel, enfermedades por depósito. Infecciones.
Hipotiroidismo congénito.
Hipotiroidismos transitorios: tiroiditis silente o posparto, tiroiditis granulomatosa, interrupción
del tratamiento sustitutivo tiroideo, pacientes con enfermedad de Graves tras tratamiento con
radioyodo, o tras tiroidectomía subtotal.
2. HIPOTIROIDISMO SECUNDARIO O TERCIARIO
Hipopituitarismo. Enfermedades hipotalámicas. Debe sospecharse hipotiroidismo central cuando
exista enfermedad hipotalámica o hipofisaria conocidas, ante lesiones en el espacio hipofisario y cuando las
manifestaciones clínicas sugestivas de hipotiroidismo se asocien con otros déficits hormonales.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1098]
[68] ENFERMEDADES DEL TIROIDES
2. CLÍNICA
Las manifestaciones clínicas del hipotiroidismo dependerán tanto del grado de déficit hormonal
como de la duración, la velocidad de instauración y la edad de la persona afectada (Tabla XVIII).
3. DIAGNÓSTICO
1. PRUEBAS DE LABORATORIO
1.1. Hormonas tiroideas
Puesto que el 95% de los casos de hipotiroidismo son causados por hipotiroidismo primario, la
medición de TSH es el método de despistaje. En caso de encontrarse elevada se debe medir T4L, y si esta
está disminuida tenemos el diagnóstico de hipotiroidismo primario. Si la TSH es normal pero existe alta
sospecha de hipotiroidismo, debe repetirse la medición junto con T4L, para descartar hipotiroidismo
central.
1.2. Anticuerpos antiperoxidasa
Dada su alta prevalencia en la población general no son muy útiles en el diagnóstico etiológico del
hipotirodisimo. No obstante, en casos de hipotiroidismo subclínico, tiroiditis silente o posparto tienen valor
pronóstico para el desarrollo de hipotiroidismo franco.
2. PRUEBAS DE IMAGEN
Ver el apartado específico.
4. TRATAMIENTO
El tratamiento sustitutivo se precisa siempre, salvo en hipotiroidismo transitorio o causado por
algún fármaco que pueda retirarse. Es necesario descartar insuficiencia suprarrenal previo al inicio de la
sustitución con levotiroxina, sobre todo ante hipotiroidismo central o síndrome poliglandular autoinmune.
La dosis estándar de levotiroxina es de unos 1,2-1,4 mcg/kg/día, pudiendo iniciarse a dosis plenas en
personas jóvenes sin enfermedades cardiovasculares. En pacientes mayores de 50-60 años sin evidencia de
enfermedad coronaria se suele empezar con 50 mcg al día, y si existe enfermedad coronaria la dosis inicial
no sobrepasa los 12,5-25 mcg diarios, con monitorización estrecha de posibles síntomas anginosos. La dosis
de mantenimiento se ajustará cada 4-8 semanas según los niveles de TSH, o con los niveles de T4L en caso
de hipotiroidismo central. En caso de requerir administración parenteral de levotiroxina debe reducirse la
dosis a un 70-80% de la dosis oral.
5. COMA MIXEDEMATOSO
Es una emergencia médica con una mortalidad de hasta el 40%. Consiste en la deficiencia grave de
hormonas tiroideas, que provoca típicamente disminución del nivel de consciencia e hipotermia. Otras
manifestaciones clínicas son hipoventilación con insuficiencia respiratoria global, bradicardia, hipotensión e
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1099]
[68] ENFERMEDADES DEL TIROIDES
hiponatremia. Si el resultado del valor de hormonas tiroideas está rápidamente disponible debe extraerse
una muestra para el diagnóstico, pero nunca a coste de retrasar el tratamiento. Se debe iniciar tratamiento
empírico sin esperar a la confirmación, y debería realizarse en la unidad de cuidados intensivos. Como
medidas generales se debe asegurar el soporte ventilatorio, el manejo de la hipotermia, el tratamiento de
la hipotensión y las alteraciones iónicas según se precise.
La sustitución hormonal precisa la administración de levotiroxina intravenosa con dosis de carga de
200-400 mcg, continuando a dosis de 50-100 mcg/día hasta que el paciente pueda usar la vía oral. En
ocasiones se recomienda añadir también T3 (liotironina). Previo a su administración se debe administrar
hidrocortisona intravenosa a dosis de 100 mg/8 h, suspendiéndose posteriormente si se descarta
insuficiencia suprarrenal concomitante.
6. HIPOTIROIDISMO SUBCLÍNICO
Hablamos de hipotiroidismo subclínico ante la presencia de hormonas tiroideas normales y TSH
aumentada. La prevalencia se estima entre el 4-15% aproximadamente. Las causas subyacentes pueden ser
similares a las del hipotiroidismo franco, y de haber síntomas también son superponibles al hipotiroidismo.
Se postula que para pacientes ancianos los límites altos de la normalidad de la TSH puede que sean más
laxos; en pacientes embarazadas, en cambio, los límites son más bajos y es necesario usar valores de TSH
específicos para cada trimestre.
En general, se suele recomendar tratar a pacientes con TSH > 10 mU/l. Con valores de TSH de entre
4,5 y 10 mU/l no se recomienda tratar de manera rutinaria. Se debe valorar de manera individualizada
iniciar tratamiento si hay síntomas, anticuerpos antiTPO o factores de riesgo cardiovascular (si bien el
equilibrio es estrecho, pues tanto el hipotiroidismo como el hipertiroidismo aumentan el riesgo de
problemas cardiacos), en ancianos en general se tiende a ser conservador. En caso de no iniciar tratamiento
se recomienda seguimiento cada 6 meses aproximadamente dado el riesgo de pasar a hipotiroidismo
franco.
BIBLIOGRAFÍA
Bahn Chair RS, Burch HB, Cooper DS, et al. Hyperthyroidism and other causes of thyrotoxicosis:
management guidelines of the American Thyroid Association and American Association of Clinical
Endocrinologists. Thyroid. 2011;21(6):593–646.
Bahn RS, Castro MR. Approach to the patient with nontoxic multinodular goiter. J Clin Endocrinol
Metabol. 2011;96(5):1202-12.
Biondi B, Bartalena L, Cooper DS, et al. The 2015 European thyroid association guidelines on diagnosis
and treatment of endogenous subclinical hyperthyroidism. Eur Thyroid J. 2015;4(3):149–63.
Cooper DS, Doherty GM, Haugen BR, et al. Revised American Thyroid Association Management
guidelines for patients with thyroid nodules and differentiated thyroid cancer. Thyroid.
2010;10(11):1167-214.
Corrales JJ, Alonso N, Cantón A, et al. Guía clínica del diagnóstico y tratamiento de la disfunción
tiroidea sub-clínica. Endocrinol Nutr. 2007;54(1):44-52.
Garber JR, Cobin RH, Gharib H, et al. Clinical practice guidelines for hypothyroidism in adults:
cosponsored by the American Association of Clinical Endocrinologists and the American Thyroid
Association. Endocr Pract. 2012;18(6):988–1028.
Gharib H, Papini E, Paschke R, et al. American association of Clinical Endocrinologists, Associazione
Medici Endocrinologi, and European Thyroid Association medical guidelines for clinical practice for the
diagnosis and management of thyroid nodules. J Endocrinol Invest. 2010;33(Suppl 5):1-50.
Pearce EN, Farwell AP, Braverman LE. Thyroiditis. N Engl J Med. 2003;348(26):2446-55.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1100]
[69] PATOLOGÍA SUPRARRENAL
69.Patología suprarrenal
Juan Carlos Romero Rodríguez.
Endocrinología y Nutrición
Pilartxo Catalán Martín.
Medicina Interna
Asesora:
María Calatayud Gutiérrez.
Médica Adjunta de Endocrinología
I. SÍNDROME DE CUSHING
1. DEFINICIÓN Y ETIOLOGÍA
El síndrome de Cushing (SC) engloba todo el conjunto de signos y síntomas resultantes de la
exposición prolongada a niveles inapropiadamente elevados de glucocorticoides.
En general su etiología se puede dividir en causas hormona adrenocorticotropa (ACTH)
dependientes o independientes; las más comunes se describen en la tabla I.
2. CLÍNICA
No existen signos ni síntomas patognomónicos del SC. Dentro de la historia clínica siempre se debe
descartar la exposición crónica a esteroides (SC yatrógeno) y prestar atención especial a situaciones
causantes del llamado síndrome “pseudocushing” (SSC) como son la obesidad, la depresión, el alcoholismo,
la diabetes mellitus mal controlada o el embarazo.
Las manifestaciones clínicas son muy variables y se pueden dividir en específicas o inespecíficas
(estas últimas mucho más frecuentes, pero menos discriminatorias); se describen en la tabla II.
3. DIAGNÓSTICO
1. POBLACIÓN A ESTUDIAR
Se debe estudiar a todo paciente que presente:
Signos y síntomas de sospecha de SC.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1101]
[69] PATOLOGÍA SUPRARRENAL
Pacientes con comorbilidades asociadas inusuales para su edad o de difícil explicación o control
(diabetes mellitus, hipertensión arterial, osteoporosis en pacientes jóvenes).
Todos los pacientes con incidentalomas suprarrenales.
Niños con retraso en el crecimiento y aumento de peso inexplicable.
2. PRUEBAS DIAGNÓSTICAS
No existe un test con marcada superioridad sobre otro, en general se cree que el diagnóstico es
más probable cuando existe más de un test patológico en más de una ocasión. Se desaconseja estudiar a
pacientes durante fase de inestabilidad/estrés importante o enfermedad aguda.
Se recomienda un estudio sucesivo, mediante pruebas escalonadas en las siguientes fases: cribado,
confirmación, evaluación de dependencia/independencia de ACTH y estudio morfológico/por imágenes.
2.1. Pruebas de cribado/diagnóstico sindrómico
2.1.1. Determinación de cortisol libre urinario de 24 horas: de elección como test inicial de
cribado, se requieren valores tres a cuatro veces por encima del límite alto de la normalidad en al menos
dos ocasiones para confirmar diagnóstico. Deben considerarse ciertas situaciones de falsos resultados. En la
tabla III se describen algunas de ellas.
2.1.2. Test de supresión con 1 mg de dexametasona nocturna (test de Nugent): valores de cortisol
matutino (entre las 8:00 h y las 9:00 h), previa administración de 1 mg oral de dexametasona (DXM) antes
de dormir (23:00 h). Valores por debajo de 1,8 μg/dL descartan hipercortisolismo. Se deben considerar
situaciones especiales en los resultados para todas las pruebas que utilizan DXM, las cuales se describen en
la tabla III.
2.1.3. Determinación de cortisol en saliva nocturno: test poco invasivo que se puede realizar en el
ámbito domiciliario. Los valores dependen de los límites establecidos por cada laboratorio y deben
estandarizarse.
2.2. Pruebas de confirmación
Se puede optar por repetir cortisol libre urinario (CLU), cortisol en saliva nocturno u optar por otras
pruebas como:
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1102]
[69] PATOLOGÍA SUPRARRENAL
2.2.1. Determinación de cortisol sérico nocturno: valores por debajo de 1,8 μg/dL en pacientes
dormidos descartan hipercortisolismo, mientras que por encima de 7,5 μg/dL en pacientes despiertos
sugieren hipercortisolismo.
2.2.2. Test de supresión con dosis bajas de dexametasona (test de Liddle “débil”): consiste en la
administración de dosis de 0,5 mg de DXM cada seis horas durante dos días (se inicia a las 12:00 h del
primer día). Al tercer día se miden niveles de cortisol a las 8:00 h (dos horas tras la última toma de DXM);
valores por debajo de 1,8 μg/dL descartan hipercortisolismo.
2.3. Diagnóstico etiológico
Consiste en demostrar la causa/fuente del síndrome de Cushing. Se dispone de las siguientes
pruebas:
2.3.1. Determinación de hormona adrenocorticotropa basal: extraído a las 8:00 h
ACTH inferior a 5 pg/ml: orientan a SC ACTH independiente (suprarrenal).
ACTH por encima de 15 pg/ml: orientan a SC ACTH dependiente (hipofisario/ectópico).
ACTH en niveles intermedios (5-15 pg/ml) obligan a estímulo con hormona estimuladora de
corticotropina.
2.3.2. Diagnóstico del síndrome de Cushing hormona adrenocorticotropa dependiente: el objetivo
principal es distinguir una fuente de ACTH hipofisaria frente a una ectópica. Se pueden utilizar las siguientes
pruebas:
Supresión con dosis altas (“fuerte”) con dexametasona: similar a la supresión “débil” con la
diferencia de la dosis total (8 mg de DXM: 2 mg cada seis horas), también se puede utilizar una
sola dosis de 8 mg de DXM la noche previa. Se considera positiva una supresión superior al 50%
del valor de cortisol basal.
Prueba de hormona estimuladora de corticotropina: se administra hormona estimuladora de
corticotropina (CRH) intravenosa (100 mcg en una sola dosis o 1 mcg/kg) y se miden valores de
ACTH y cortisol (a las 8:00 h). En caso de origen hipofisario existirá aumento de cifras de ACTH
y/o cortisol del 50% y 20% respectivamente, respecto a sus basales.
Cateterismo de senos petrosos inferiores: prueba invasiva que determina concentraciones de
ACTH en senos petrosos inferiores y en sangre periférica basales y tras la administración de
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1103]
[69] PATOLOGÍA SUPRARRENAL
CRH. Indicada en caso de que las pruebas dinámicas y los resultados radiológicos no sean
concluyentes, o en ausencia de imagen compatible con adenoma en la resonancia magnética
(RMN) hipofisaria.
2.4. Diagnóstico por pruebas de imagen
Permiten una confirmación de localización de la fuente de producción de ACTH. Deben ser
consideradas como el último paso de diagnóstico y no deben realizarse antes de las pruebas funcionales.
Síndrome de Cushing hormona adrenocorticotropa-dependiente: RMN hipofisaria. Hasta en el
40% de los casos existe la posibilidad de una prueba de imagen normal. La presencia de una
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1104]
[69] PATOLOGÍA SUPRARRENAL
imagen igual o mayor a 6 mm (sugerente de adenoma) confirma el diagnóstico y descarta la
necesidad de otras pruebas
Síndrome de Cushing hormona adrenocorticotropa-independiente: se recomienda
inicialmente una tomografía computarizada (TC) abdominal, dejando como segunda alternativa
a la RMN abdominal debido a su mayor coste. Ayudan fundamentalmente a diferenciar
adenomas de otras lesiones.
Síndrome de Cushing con sospecha de fuente de hormona adrenocorticotropa ectópica: se
utilizan como pruebas de localización: TC, tomografía por emisión de positrones (PET)-TC, RMN
y gammagrafía con octreótido, según la sospecha de la fuente ectópica. Existen un 10-15% de
casos en los cuales no se llega a localizar la fuente ectópica de producción.
En la figura 1 se describe un algoritmo diagnóstico propuesto para el SC.
4. TRATAMIENTO
1. SÍNDROME DE CUSHING HORMONA ADRENOCORTICOTROPA-DEPENDIENTE
1.1. Tratamiento quirúrgico
En casos de confirmación de adenoma. De elección se utiliza la vía transesfenoidal.
1.2. Tratamiento médico
Como adyuvancia a otras técnicas (cirugía, radioterapia, otras) o cuando las mismas no están
indicadas, no son posibles o no han sido curativas. Se dispone de las siguientes alternativas:
Agentes inhibidores de la esteroidogénesis:
Ketonoconazol: dosis totales 400-1.600 mg/día, vía oral. De primera elección entre los
fármacos disponibles para el tratamiento médico.
Metirapona: dosis totales 500-6.000 mg/día, vía oral. De primera o segunda línea,
utilizado solo o en combinación con ketoconazol (esta última alternativa de elección en
SC florido).
Mitotano: dosis totales 250-8.000 mg/día, vía oral. De uso más extenso en el carcinoma
suprarrenal avanzado (inextirpable, metastásico o recidivante).
Etomidato: de uso intravenoso, dosis usuales: bolo inicial de 3-5 mg, seguido de
infusión continua a 0,03-0,10 mg/kg/hora. Logra disminuir los niveles de cortisol sérico
en horas, por lo tanto es de elección cuando se quiere conseguir un control inmediato
del hipercortisolismo. Requiere monitorización respiratoria.
Antagonistas del receptor de glucocorticoides: mifepristona. Dosis totales: 300-1.200 mg/día,
vía oral. Útil en pacientes con hipercortisolismo y diabetes mellitus mal controlada.
Agentes que modulan la secreción de hormona adrenocorticotropa: se ha descrito control
parcial del hipercortisolismo con el uso de agonistas dopaminérgicos (cabergolina –dosis
totales: 1-7 mg/semana-vía oral–) y análogos de somatostatina (pasireótido –dosis totales: 600-
900 μg/día-vía intramuscular–).
1.3. Radioterapia (convencional/estereotáxica)
Indicada en casos de recurrencia o contraindicación quirúrgica. Precisa asociar tratamiento médico,
ya que su efecto tarda años en corregir el hipercortisolismo.
1.4. Adrenalectomía bilateral
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1105]
[69] PATOLOGÍA SUPRARRENAL
Se prefiere la vía laparoscópica. De elección en casos en los cuales no se ha alcanzado curación por
cualquiera de las otras vías, o cuando se busca un control inmediato del hipercortisolismo. Requiere
cobertura esteroidea residual de mantenimiento de por vida.
2. SÍNDROME DE CUSHING HORMONA ADRENOCORTICOTROPA-INDEPENDIENTE
2.1. Adrenalectomía
De elección en adenomas o carcinomas (si son resecables). Se debe realizar cobertura esteroidea
durante la cirugía y tras la misma a dosis sustitutivas hasta comprobar una recuperación de la glándula
contralateral (la cual suele estar atrófica).
3. SÍNDROME DE CUSHING POR HORMONA ADRENOCORTICOTROPA-ECTÓPICA
3.1. Tumores resecables
Si la fuente ectópica es resecable es el tratamiento de elección.
3.2. Tumores irresecables
En la mayoría de los casos (ya sea por falta de localización, por situación clínica o por metástasis
múltiples) no es posible la resección del tumor de base. Para el control del hipercortisolismo se deben
utilizar fármacos inhibidores de la esteroidogénesis solos o en combinación con análogos de la
somatostatina. La adrenalectomía bilateral puede estar indicada.
II. INSUFICIENCIA SUPRARRENAL
1. DEFINICIÓN
La insuficiencia suprarrenal (IS) es un trastorno que se caracteriza por un déficit de
glucocorticoides, al que se puede asociar en ocasiones un déficit de mineralocorticoides y/o andrógenos
adrenales.
2. CLASIFICACIÓN Y ETIOLOGÍA
Se describen en la tabla IV.
1. INSUFICIENCIA SUPRARRENAL PRIMARIA/ENFERMEDAD DE ADDISON
Puede aparecer tras la ausencia o destrucción de las glándulas suprarrenales, o tras un bloqueo en
la producción hormonal. Existe déficit de glucocorticoides y mineralocorticoides. Para que existan
manifestaciones clínicas de la enfermedad tiene que haberse producido al menos una destrucción del 90%
de la superficie glandular. Su principal causa es la enfermedad autoinmune.
2. INSUFICIENCIA SUPRARRENAL CENTRAL
Existe un déficit de ACTH con disminución progresiva de la síntesis de cortisol; sin embargo, no
existe déficit de mineralocorticoides. Su principal causa es la supresión del eje hipotalámico- hipofisario-
suprarrenal (HHS) por la administración crónica de esteroides.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1106]
[69] PATOLOGÍA SUPRARRENAL
3. CLÍNICA
Los síntomas y signos clínicos asociados a la IS dependen del grado de afectación suprarrenal y de la
preservación o no del eje mineralocorticoide. Generalmente se instauran de manera lenta y suelen
aparecen coincidiendo con situaciones de estrés físico o enfermedades intercurrentes.
1. INSUFICIENCIA SUPRARRENAL PRIMARIA CRÓNICA
1.1. Por déficit de glucocorticoides
Síntomas generales: astenia, anorexia, debilidad, pérdida de peso, mialgias.
Síntomas gastrointestinales: dolor abdominal, náuseas, vómitos, diarrea, estreñimiento.
Alteraciones analíticas: hipoglucemia (raro), hiponatremia.
1.2. Por déficit de mineralocortiocoides
Síntomas generales: hipotensión ortostática, mareos, síncopes.
Alteraciones analíticas: hiperpotasemia, acidosis metabólica.
1.3. Signos por exceso de hormona adrenocorticotropa
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1107]
[69] PATOLOGÍA SUPRARRENAL
Hiperpigmentación cutánea (principalmente en codos, rodillas, surcos palmoplantares, mucosa
oral y cicatrices).
1.4. Signos/síntomas por déficit de andrógenos
Disminución de la libido y vello corporal (axilar y púbico); más acentuado en mujeres.
2. INSUFICIENCIA SUPRARRENAL CENTRAL CRÓNICA
Síntomas similares a los de la afectación primaria debidos al déficit de glucocorticoides con mayor
frecuencia de hipoglucemia y menor frecuencia e intensidad de los síntomas gastrointestinales. No
aparecerá la hiperpigmentación cutánea ni los signos/síntomas asociados al déficit de mineralocorticorides.
Existe además la posibilidad de afectación de otras líneas del eje hipofisario o aparición de síntomas
neurológicos por efecto de masa (cefalea, alteraciones visuales).
3. INSUFICIENCIA SUPRARRENAL AGUDA (CRISIS SUPRARRENAL)
Es una emergencia médica que suele presentarse de forma súbita. Casi la mitad de los pacientes
con insuficiencia suprarrenal primaria (ISP) comienzan en forma de crisis suprarrenal. Los factores
predisponentes más comunes suelen ser: infecciones, cirugía, traumatismos o cualquier otra situación de
estrés importante. La manifestación clínica predominante suele ser el shock, aunque la presentación suele
ser más insidiosa en la mayoría de casos: astenia, anorexia, dolor abdominal, náuseas, vómitos, fiebre,
hipotensión arterial y síncope. Suelen además existir alteraciones hidroelectrolíticas acompañantes:
hiponatremia, hiperpotasemia, acidosis metabólica, hipoglucemia, anemia, linfocitosis y eosinofilia.
4. DIAGNÓSTICO
1. TEST BASALES
Cortisol basal: es la prueba de elección como despistaje de IS. Es esencial su extracción entre
las 8:00 h y las 9:00 h. Valores por debajo de 3,6 μg/dL confirman el diagnóstico. Cifras por
encima de 18 μg/dL lo descartan. Valores intermedios requieren otras pruebas. Se deben tener
en cuenta ciertas situaciones en las cuales existen cifras de cortisol basal falsamente
disminuidas (hipotiroidismo, enfermedad hepática, sepsis y síndrome nefrótico) o elevadas
(hipertiroidismo, embarazo y uso de anticonceptivos orales).
Hormona adrenocorticotropa basal: útil en el diagnóstico etiológico; se encontrarán cifras
elevadas (por encima del doble del rango de la normalidad) en la ISP, mientras que en la IS
central (ISC) se encontrarán cifras normales o bajas. Se debe realizar su extracción entre las
8:00 h y 9:00 h, conservando la muestra en tubo EDTA en una bandeja en hielo.
2. TEST DINÁMICOS
Test de hipoglucemia insulínica: test “gold estándar” para el diagnóstico de IS. Consiste en
evaluar la respuesta del cortisol a la hipoglucemia inducida por la insulina (se administran dosis
entre 0,1 y 1,15 UI/kg IV).
Test de estímulo con hormona adrenocorticotropa a dosis estándar: se determinan
mediciones de cortisol basal, a los 30 y/o 60 minutos tras la administración de ACTH sintética IV
o IM (Synacthen®) a dosis estándar: 250 μg en una inyección. Cifras de cortisol por encima de 18
μg/dL y por encima de 23 μg/dL descartan una ISP y una ISC respectivamente. Debido a su
simplicidad y fácil interpretación es el test más utilizado en la actualidad. En la figura 2 se
describe un algoritmo diagnóstico sugerido en caso de sospecha de IS.
5. TRATAMIENTO
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1108]
[69] PATOLOGÍA SUPRARRENAL
En todos los casos se recomienda la mínima dosis de esteroides tolerada adecuadamente por el
paciente que permita evitar sus probables efectos adversos.
1. TRATAMIENTO DE LA INSUFICIENCIA SUPRARRENAL CRÓNICA
1.1. Insuficiencia suprarrenal primaria
1.1.1. Terapia con glucocorticoides
Hidrocortisona (Hidroaltesona®, comprimidos de 20 mg): terapia de elección, por ser el
esteroide más fisiológico. Se recomiendan dosis totales de entre 15-25 mg/día. Se prefiere
dividir la dosis total en dos a tres tomas diarias, simulando el ritmo circadiano de cortisol (dos
dosis: 2/3 al levantarse y 1/3 en la merienda; o tres dosis: 1/2 al levantarse, 1/4 al mediodía y
1/4-1/5 en la merienda). En la actualidad también existen preparados comerciales con
hidrocortisona de liberación prolongada (Plenadren®, comprimidos de 5 y 20 mg), que permiten
una única administración en la mañana (20 mg antes de levantarse), sin embargo por ahora no
están comercializados en España.
Otros glucocorticoides: se utilizan como alternativas algunos glucocorticoides de vida media
larga, como la dexametasona; la dosis diaria habitual es de 0,5 mg (0,25 a 0,75 mg) en una sola
toma, o la prednisona en dosis diaria habitual de 5 mg (2,5 a 7,5 mg) en una sola toma. Son
útiles en pacientes que no toleren adecuadamente la hidrocortisona o en situaciones en las que
se requiera además un poder antiinflamatorio asociado.
1.1.2. Terapia con mineralocorticoides: indicada únicamente en pacientes con ISP. Fludrocortisona:
es el único preparado disponible (Astonin®, Florinef®, comprimidos de 0,1 mg); dosis diaria habitual de 0,1
mg (0,05 a 0,2 mg) en una sola toma al levantarse. Se suelen requerir dosis de 0,2 mg en pacientes tratados
con glucocorticoides de vida media larga.
1.1.3. Monitorización y seguimiento del tratamiento: se basa en:
Seguimiento de signos/síntomas: secundarios al déficit o exceso de gluco/mineralocorticoides
administrados.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1109]
[69] PATOLOGÍA SUPRARRENAL
Glucocorticoides: si existen síntomas de déficit se puede aumentar su dosis, pero si los mismos
no mejoran se reanudará la dosis previa y se buscarán otras causas posibles. La aparición de
signos de exceso de glucocorticoides obliga la disminución de la dosis de esteroides. Los
pacientes deben ser instruidos sobre la necesidad de aumentar las dosis en situaciones de
estrés.
Mineralocorticoides: en caso de hipotensión ortostática, taquicardia, hiperpotasemia se debe
valorar aumentar las dosis y disminuirla en casos de aparición de signos de sobredosificación
(hipertensión arterial, edemas, hipopotasemia). No se requiere aumento de dosis de
mineralocorticoides en caso de situaciones de estrés.
Parámetros hormonales: no parecen de utilidad para el ajuste del tratamiento: la medición de
ACTH (que resultará elevada en el paciente normosustituido) podría ser útil ante la sospecha de
sobredosificación (donde se encontraría baja o suprimida) y las curvas de cortisol deben ser
solicitadas únicamente en base a sospecha clínica.
Medición de la actividad (o concentración) de renina plasmática (ARP-CRP): puede ser útil para
el ajuste del tratamiento con mineralocorticoides; se recomienda mantenerla en el límite alto o
inmediatamente por encima.
2. DIFERENCIAS EN EL TRATAMIENTO DE LA INSUFICIENCIA SUPRARRENAL CENTRAL
Se requieren dosis generalmente menores de glucocorticoides: 10 a 15 mg diarios de
hidrocortisona. En caso de existir otros déficits hormonales, el de glucorticotides debe ser el primero en
sustituirse para evitar una crisis.
3. TRATAMIENTO DE LA INSUFICIENCIA SUPRARRENAL AGUDA (CRISIS SUPRARRENAL)
3.1. Medidas de emergencia
3.1.1. Fluidoterapia y normas generales
Extracción de sangre para determinación analítica: hemograma, bioquímica, gasometría
venosa, cortisol basal y ACTH; previos a la administración de corticoides.
Sueroterapia: 2.000 a 3.000 cc de suero salino fisiológico en un día. Si el paciente está en
shock: 1.000 cc en la primera hora, 500 cc en la segunda hora y luego según la evolución
hemodinámica o la presión venosa central. Administrar además suero glucosado para evitar la
aparición de hipoglucemia.
3.1.2. Glucocortidoides
Hidrocortisona: inicialmente bolo de 100 mg IV y luego en perfusión continua (200-300 mg en
suero glucosado al 5% a un ritmo de 10 mg/h) o en bolos IV/IM de 100 mg cada seis a ocho
horas.
Se puede utilizar también dexametasona: inicialmente bolo de 4 mg IV, y luego cada 12 horas.
3.2. Otras medidas
Corrección de factores precipitantes, corrección de hiponatremia, etc.
3.3. Tras estabilización del paciente:
Continuar con perfusión de suero salino fisiológico a menor velocidad de perfusión en las
siguientes 24-48 horas.
Disminuir gradualmente dosis de glucocorticoides hasta dosis de mantenimiento oral en los
siguientes 3 a 4 días.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1110]
[69] PATOLOGÍA SUPRARRENAL
Iniciar sustitución de mineralocorticoides (fludocortisona): 0,1 mg diarios vía oral, cuando se
detenga la perfusión se suero salino y la dosis de hidrocortisona (o equivalente) sea inferior a
50 mg diarios.
Confirmar el diagnóstico de IS con prueba de estímulo con ACTH (si el paciente no está
diagnosticado).
Determinar el tipo y causa de la IS.
En las Tablas V y VI se describen ciertas consideraciones especiales a tomar en cuenta en el
tratamiento de los pacientes con IS.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1111]
[69] PATOLOGÍA SUPRARRENAL
6. OTRAS CONSIDERACIONES
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1112]
[69] PATOLOGÍA SUPRARRENAL
1. SUPRESIÓN DEL EJE HIPOTALÁMICO-HIPOFISIARIO-SUPRARRENAL EN PACIENTES QUE RECIBEN TRATAMIENTO
CRÓNICO CON ESTEROIDES
El tratamiento crónico con esteroides puede producir una supresión del eje HHS. La dosis recibida,
el momento de la toma y la duración del tratamiento son los factores principales que determinan la
probabilidad de supresión del eje HHS en pacientes tratados con esteroides. Otros factores relacionados
son la potencia del esteroide (riesgo mayor con esteroides más potentes como beclometasona,
triamcinolona o budesonida), la edad del paciente (mayor en jóvenes) y ciertas situaciones especiales (por
ejemplo al utilizar la vía tópica se debe considerar la aplicación en el cuero cabelludo y en los pliegues, el
tratamiento de superficies extensas y los vendajes oclusivos como situaciones de riesgo mayor).
Atendiendo a estos tres parámetros el riesgo de presentar supresión del eje HHS se clasifica en
probable, intermedio/incierto e improbable. En la tabla VII se definen las situaciones probables y las
actitudes recomendadas.
2. RECOMENDACIONES GENERALES DE DESCENSO PROGRESIVO DE ESTEROIDES EN PACIENTES CON TRATAMIENTO
CRÓNICO
Se exponen en la tabla VIII.
III. HIPERALDOSTERONISMO
1. INTRODUCCIÓN
La hipersecreción de aldosterona es la causa más frecuente de hipertensión arterial (HTA)
secundaria (5-13%), aunque es una entidad que continúa siendo infradiagnosticada.
2. ETIOLOGÍA
Ver la tabla IX.
Hiperaldosteronismo primario: el defecto primario es una hipersecreción de aldosterona por
un trastorno intrínseco suprarrenal
Hiperaldosteronismo secundario: el defecto primario es una hipersecreción de renina
(estímulo del eje renina-angiotensina-aldosterona) por un proceso extrínseco a la glándula
suprarrenal.
Hipersecreción de otros corticoides con actividad mineralocorticoide.
Síndrome de Liddle: trastorno autosómico dominante que consiste en una mutación con
ganancia de función de los canales de sodio del túbulo colector.
Hipersecreción de aldosterona por un trastorno intrínseco suprarrenal.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1113]
[69] PATOLOGÍA SUPRARRENAL
3. CLÍNICA
Hipertensión arterial e hipopotasemia: combinados es altamente sugestivo de
hiperaldosteronismo, aunque la caliemia puede ser normal hasta en más del 50% de los
pacientes.
Cuando la causa es un adenoma la concentración plasmática de aldosterona suele ser mayor, la
hipopotasemia más severa y la edad más joven (< 50 años) al diagnóstico, en comparación con
la hiperplasia adrenal bilateral idiopática.
Alcalosis metabólica: mediada por aumento de la excreción renal de hidrogeniones al nivel del
túbulo distal secundario a la hipopotasemia y a la acción de la aldosterona.
Hipernatremia e hipomagnesemia, así como intolerancia a la glucosa: infrecuente.
Tasa de morbimortalidad cardiovascular elevada en comparación con pacientes de la misma
edad y sexo con hipertensión arterial esencial y cifras tensionales similares.
Ausencia de edemas, debido al fenómeno de “escape de la aldosterona”, inhibición en la
síntesis de renina, estímulo de la secreción de péptidos natriuréticos y poliuria tras aumento de
2,5-3 kg de peso corporal (aproximadamente).
4. DIAGNÓSTICO
1. ESTUDIO INICIAL/DESPISTAJE
Se recomienda el screening de hiperaldosteronismo primario (HP) en aquellos grupos de pacientes
con alta prevalencia de HP (ver Tabla X).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1114]
[69] PATOLOGÍA SUPRARRENAL
Cociente renina/aldosterona en plasma (CRA): es la determinación más fiable durante el
despistaje. En caso de que este sea no concluyente se debe repetir la medición. Los puntos de
corte de esta ratio dependen de las unidades utilizadas, del laboratorio de cada centro y de si
se determina la actividad de renina plasmática o la concentración de renina plasmática.
En el hiperaldosteronismo primario habrá un aumento en la concentración de aldosterona, con
una concentración de renina disminuida o suprimida. En el hiperaldosteronismo secundario, sin
embargo, la renina es la responsable del aumento de la aldosterona, por lo que se encontrará
aumentada. Diferentes situaciones y fármacos pueden interferir en los resultados del cociente
renina/ aldosterona (CRA).
En la tabla XI se especifican las condiciones en las que se debiera medir este cociente, y en la
tabla XII se especifican los fármacos antihipertensivos que no interfieren en su medición, y que
por lo tanto podrían utilizarse durante el estudio inicial/despistaje.
2. DIAGNÓSTICO DE CONFIRMACIÓN
Los pacientes con positividad en la medición del CRA deben ser sometidos a uno de los cuatro test
de los que se dispone para confirmar la existencia de HP. Ninguno se considera “gold estándar”; se elegirá
en función de las características del enfermo, del coste o de la disponibilidad del centro.
2.1. Sobrecarga oral de sodio
Se administra una dieta de 6 g de sodio/día durante tres días. Posteriormente, se realiza la
medición del nivel de aldosterona en orina de 24 horas el tercer y el cuarto día después del inicio de la
dieta. Cifras > 12-14 mg/día de concentración de aldosterona son altamente sugestivas de HP.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1115]
[69] PATOLOGÍA SUPRARRENAL
2.2. Infusión de 2 l suero salino fisiológico
Durante cuatro horas. Concentraciones de aldosterona > 10 ng/dL en plasma es altamente
sugestivo de HP.
2.3. Test de supresión con fludrocortisona
Administración de 0,1 mg de este fármaco cada seis h durante cuatro días; concentraciones de
aldosterona en plasma el cuarto día > 6 ng/dL confirma HP.
2.4. Prueba del captopril
Ausencia supresión de la aldosterona en plasma tras al menos una hora de la toma del fármaco
sugiere HP.
3. DIAGNÓSTICO DE LOCALIZACIÓN
Una vez que el diagnóstico bioquímico de HP ha sido establecido, es necesario realizar pruebas
complementarias para identificar si el problema es unilateral (adenoma suprarrenal,más raramente
carcinoma o hiperplasia unilateral) o bilateral (hiperplasia adrenal bilateral idiopática), de gran importancia
de cara al tratamiento.
3.1. Pruebas de imagen
Se realizará TC de suprarrenales a todos los pacientes con HP confirmado, preferible a la RMN
(menor resolución espacial). Los hallazgos guiarán el plan terapéutico en cada caso.
Nódulo hipodenso entre 1-2 cm: adenoma.
Normales o cambios nodulares: hiperplasia adrenal idiopática.
Sin embargo, como todo método diagnóstico, la TC no está exenta de limitaciones: microadenomas
interpretados como hiperplasia idiopática, áreas de hiperplasia interpretadas como microadenomas (con
posteriores tratamientos inadecuados) y macroadenomas no funcionantes; por ello, la cateterización de las
venas suprarrenales por personal experto es de gran ayuda de cara a planificar un correcto tratamiento.
3.2. Cateterización de las venas suprarrenales
Es un procedimiento complementario que mide la concentración local de aldosterona. Determina la
uni/bilateralidad (adenoma: lateralización; hiperplasia adrenal bilateral: no lateralización) de la
hipersecreción de aldosterona y planifica así el tratamiento, de hasta en 1/3 de los pacientes en los que se
sospecha enfermedad unilateral por TC, en realidad se trata una hiperplasia bilateral, de ahí la importancia
de la cateterización de las venas suprarrenales antes de realizar tratamiento quirúrgico. Es de especial
interés en el caso de pacientes que sean candidatos a tratamiento quirúrgico y en los que la TC sea normal
o con alteraciones bilaterales o unilaterales en pacientes mayores de 35 años (a más edad, más
probabilidad de que el adenoma no sea funcionante) (ver Figura 3).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1116]
[69] PATOLOGÍA SUPRARRENAL
5. TRATAMIENTO
El objetivo terapéutico, independientemente de la causa, es prevenir los riesgos de la HTA, la
hipopotasemia, la toxicidad renal y el daño cardiovascular; el exceso de aldosterona por sí mismo produce
hipertrofia del ventrículo izquierdo y aumenta el riesgo de ictus, infarto agudo de miocardio y fibrilación
auricular.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1117]
[69] PATOLOGÍA SUPRARRENAL
1. ADENOMA PRODUCTOR DE ALDOSTERONA
El tratamiento de elección es la adrenalectomía laparoscópica, con una tasa de mejoría en los
niveles de potasio y en las cifras de tensión arterial en alrededor del 100% de los pacientes y en > 50% se
logra una curación de la HTA. Previo a la cirugía hay que corregir la hipopotasemia y la HTA con fármacos
antagonistas de la aldosterona. Tras la intervención se recomienda medir la concentración de aldosterona
en los días posteriores para asegurar la curación, eliminar los aportes de potasio y reducir los fármacos
antihipertensivos conforme sea posible. Es fundamental monitorizar estrechamente los niveles de potasio,
puesto que en ocasiones puede aparecer una hiperpotasemia debida a hipoaldosteronismo transitorio
secundario a cierto grado de atrofia en la función de la otra glándula suprarrenal. Este estado de
“hipoaldosteronismo transitorio” puede prolongarse hasta tres semanas después de la intervención, por lo
que se recomienda una dieta rica en sodio para prevenir la hiperpotasemia.
2. HIPERPLASIA ADRENAL BILATERAL IDIOPÁTICA
El tratamiento es médico mediante fármacos antagonistas de la aldosterona (espironolactona,
eplerenona); en caso de intolerancia se administrará amiloride/triamterene, aunque estos últimos no
antagonizan los efectos de aldosterona (ver Tabla XIII).
IV. HIPOALDOSTERONISMO
Debe sospecharse ante un paciente con hiperpotasemia persistente en ausencia de insuficiencia
renal crónica o toma de diuréticos ahorradores de potasio. Asociado a hiponatremia y disminución de la
volemia.
Existen tres tipos de hipoaldosteronismo de acuerdo a los niveles de aldosterona, renina y su
cociente:
1. HIPOALDOSTERONISMO HIPORRENINÉMICO
Es consecuencia de un fallo en los mecanismos que estimulan la síntesis de aldosterona, como es la
renina. Existe hiperpotasemia junto con acidosis metabólica hiperclorémica (anión GAP normal). No es
frecuente la existencia de hiponatremia, por mecanismos compensadores. Esta situación también es
conocida como acidosis tubular renal tipo IV y su causa más frecuente es la nefropatía diabética, por lesión
en el aparato yuxtaglomerular renal que sintetiza la renina. Otras causas son las nefropatías túbulo-
intersticiales crónicas, la nefroangioesclerosis hipertensiva, el virus de la inmunodeficiencia humana, la
cirrosis hepática, así como los fármacos nefrotóxicos (antiinflamatorios no esteroideos, inhibidores de la
enzima de conversión de la angiotensina [IECA], antagonistas de los receptores de angiotensina II) y
anticalcineurínicos (ciclosporina).
El déficit de secreción de aldosterona responde adecuadamente a estímulos no dependientes de
renina, como son la administración de ACTH o potasio (estimulan directamente la aldosterona).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1118]
[69] PATOLOGÍA SUPRARRENAL
A diferencia de otros tipos de hipoaldosteronismo, se acompaña de HTA hasta en 50% de los casos.
El tratamiento indicado es la fludrocortisona (mineralocorticoide) a dosis de 0,05- 0,2 mg/día. En
los pacientes con HTA su administración no sería beneficiosa (riesgo elevado de hiperpotasemia), por lo
que se recomienda una dieta pobre en potasio y un diurético tiazídico.
2. HIPOALDOSTERONISMO HIPERRENINÉMICO
Consecuencia de un déficit primario en la secreción de aldosterona, con un aumento
compensatorio en la secreción de renina. La causa más frecuente es la insuficiencia suprarrenal primaria,
en la que hay un déficit de aldosterona y cortisol (ver apartado correspondiente).
Otras causas menos frecuentes son:
Hiperplasia suprarrenal congénita (formas clásicas): grupo de enfermedades de herencia
autosómica recesiva, consistentes en la presencia de defectos en alguna de las enzimas
implicadas en la síntesis de esteroides y el consiguiente cúmulo de los metabolitos previos al
defecto enzimático. El déficit más frecuente es el de la enzima 21-hidroxilasa. Puede ser desde
asintomático hasta formas graves que comienzan en el periodo neonatal con acidosis
metabólica, deshidratación hiponatrémica, hiperpotasemia y virilización en niñas por
acumulación de precursores androgénicos.
Farmacológico: heparina sódica y heparinas de bajo peso molecular, por efecto tóxico directo
en la capa glomerulosa de la glándula adrenal, dosis-independiente.
Enfermos críticos con hipotensión mantenida.
3. PSEUDOHIPOALDOSTERONISMO (RESISTENCIA A LA ALDOSTERONA)
Cursan habitualmente con hipercalemia, acidosis metabólica e hipertensión pierde-sal o
hipertensión arterial hipervolémica. Puede ser congénito o adquirido:
Congénito tipo 1 o tipo 2 (síndrome de Gordon).
Adquirido: diuréticos ahorradores de potasio (espironolactona, eplerrenona, amiloride y
triamterene). Antibióticos como el trimetroprim-sulfametoxazol o la pentamidina, dosis
dependiente, por el efecto inhibitorio en el canal de sodio del túbulo colector (lugar donde
actúa la aldosterona reabsorbiendo sodio).
V. FEOCROMOCITOMA
1. CONCEPTO
Es un tumor neuroendocrino productor de catecolaminas que procede de las células cromafines del
sistema nervioso simpático. El 90% se localiza en la médula adrenal y el resto en el tejido cromafín
extraadrenal (ganglios simpáticos extraadrenales paravertebrales de tórax, abdomen o pelvis), llamados
paragangliomas.
Es una causa rara de HTA secundaria (< 0,2%). La edad más frecuente al diagnóstico es entre los 40-
50 años y no hay diferencias por sexo.
2. CLASIFICACIÓN
Esporádicos: lo más frecuente.
Hereditarios: hasta en un 30% de los pacientes existe un trastorno hereditario, entre los que
destacan, todos ellos con herencia autosómica dominante: MEN tipo 2, neurofibromatosis (NF)
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1119]
[69] PATOLOGÍA SUPRARRENAL
tipo 1 y síndrome de Von-Hippel-Lindau (VHL). En este grupo los feocromocitomas tienden a ser
bilaterales y son más frecuentes los paragangliomas.
3. CLÍNICA
La sintomatología es consecuencia de la hipersecreción de catecolaminas (adrenalina,
noradrenalina y dopamina). Se caracteriza por ser episódica (en forma de crisis paroxísticas) con tendencia
a agravarse con el tiempo.
Tríada clásica: cefalea, sudoración y taquicardia: un 50% tiene hipertensión arterial paroxística.
La mayoría de los pacientes no presentan esta tríada, aunque si se presenta la especificidad es
> 90%. También se puede objetivar papiledema, pérdida de peso, poliuria y polidipsia,
estreñimiento severo, crisis de pánico (sobre todo si son productores de adrenalina), aumento
de la velocidad de sedimentación globular, eritrocitosis y resistencia a la insulina (efecto directo
catecolaminérgico). De forma menos frecuente hipotensión ortostática (por depleción de
volumen), cardiomiopatía similar a Takotsubo (comienza como una insuficiencia cardiaca que
empeora con el beta-bloqueo) y crisis paroxísticas hipertensivas en diferentes situaciones
(inducción de la anestesia, cirugías, determinados alimentos que contengan tiramina y
fármacos) (ver Tabla XIV).
Asintomáticos: debido al mayor uso de las pruebas de imagen, especialmente la TC, se
diagnostican más incidentalomas suprarrenales, de los cuales hasta un 5% corresponden a
feocromocitomas en pacientes asintomáticos.
4. DIAGNÓSTICO
1. INDICACIONES
Debe sospecharse en pacientes con uno o más de los siguientes:
Clásica tríada de cefalea + sudoración + palpitaciones, con o sin hipertensión.
Crisis adrenérgica durante anestesia, cirugía, angiografía o parto o provocada por fármacos
mencionados en la tabla XIV.
HTA de difícil manejo, hipertensión en pacientes menores de 20 años o HTA en pacientes con
diabetes mellitus con características atípicas.
Trastornos hereditarios que aumenten el riesgo de padecerlo (MEN 2, NF tipo 1 y VHL).
Incidentaloma adrenal con o sin hipertensión arterial.
Cardiomiopatía dilatada idiopática.
Crisis de pánico súbitas.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1120]
[69] PATOLOGÍA SUPRARRENAL
El screening no está indicado en pacientes con HTA asintomáticos. Las patologías que forman parte
del diagnóstico diferencial se exponen en la tabla XV.
2. TEST BIOQUÍMICOS
El objetivo es demostrar la presencia de exceso de catecolaminas. La prueba de elección varía
según la probabilidad pretest (ver Tabla XVI).
2.1. Alta probabilidad
Determinación de metanefrinas fraccionadas en plasma, justificada por su elevada sensibilidad (S
99%).
2.2. Baja probabilidad
Determinación de catecolaminas y metanefrinas fraccionadas en orina de 24 horas; ofrece mayor
especificidad con aceptable sensibilidad (se evitaría la alta tasa de falsos positivos en una población de bajo
riesgo).
Para confirmar el diagnóstico el resultado de las determinaciones hormonales debe ser al menos el
doble que el límite superior del rango de referencia.
De ser posible se recomienda la suspensión de cualquier medicación al menos dos semanas previas
a la realización de la prueba. Sin embargo, si el paciente precisa continuar con el tratamiento
antihipertensivo, los diuréticos, los inhibidores de la enzima de conversión de la angiotensina (IECA), los
antagonistas del calcio, el minoxidil y los bloqueadores alfa o beta han mostrado mínima interferencia en
las determinaciones.
Existen diversas situaciones clínicas y fármacos que pueden alterar el resultado de las
determinaciones de los parámetros estudiados y que deberían solventarse antes de iniciar el estudio (ver
Tabla XVII).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1121]
[69] PATOLOGÍA SUPRARRENAL
3. PRUEBAS FUNCIONALES
Indicadas en caso de sospecha de falso positivo o resultados borderline en las determinaciones de
metanefrinas y catecolaminas.
3.1. Test de supresión con clonidina
Fármaco alfa-adrenérgico de acción central que inhibe la liberación neuronal de catecolaminas,
pero no las producidas por un feocromocitoma. Se administra 0,3 mg vía oral, y se determinan las
catecolaminas tres horas antes y después de la misma; si se produce supresión (niveles < 500 pg/ml) se
descarta el feocromocitoma. Contraindicada en pacientes hipotensos.
4. Técnicas de imagen para localización del tumor
Debe realizarse una vez llevado a cabo el diagnóstico bioquímico de feocromocitoma, nunca antes.
4.1. Tomografía computarizada abdominopélvica
Es la prueba de elección, por su alta resolución espacial en el tórax, el abdomen y la pelvis.
4.2. Resonancia magnética abdominopélvica
Se reserva para gestantes, niños o pacientes en los que sea necesaria la mínima radiación.
Aproximadamente, entre el 9% y el 23% de los tumores son extraadrenales, pero el 95% se localiza en el
abdomen y en la pelvis.
4.3. Gammagrafía con 123-yodo-metayodobencilguanidina
Se realizará en caso de alta sospecha clínica y bioquímica sin hallazgos en la TC/RMN, dada su alta
sensibilidad. También es válida en la detección de tumores múltiples.
4.4. PET-TC FDG
Similar a la anterior. Puede presentar mayor sensibilidad que la gammagrafía para el diagnóstico de
enfermedad metastásica.
5. TEST GENÉTICO
Indicada la realización de las mutaciones más frecuentes en pacientes con feocromocitoma
bilateral, paragangliomas, historia familiar, feocromocitoma en < 45 años y/o clínica compatible con
síndrome hereditario.
5. TRATAMIENTO
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1122]
[69] PATOLOGÍA SUPRARRENAL
El tratamiento de elección siempre que sea posible es quirúrgico. En líneas generales la presencia
de un feocromocitoma productor de catecolaminas aumenta la morbilidad y mortalidad cardiovascular.
1. MANEJO PREOPERATORIO
1.1. Medidas generales
Dieta rica en sal: 5 g/día. Debe iniciarse después del segundo-tercer día de inicio del alfa-
bloqueo (ver más adelante).
Ingesta hídrica abundante: para prevenir la hipotensión ortostática secundaria al alfa-bloqueo y
la posible hipotensión posquirúrgica.
Suero salino fisiológico: de dos a tres litros previos a la cirugía (precaución en los pacientes con
insuficiencia cardiaca o renal).
1.2. Medidas farmacológicas
1.2.1. Bloqueo alfa adrenérgico: el objetivo es controlar la hipertensión arterial y aumentar el
volumen circulante, además de contrarrestar la liberación masiva de catecolaminas durante la cirugía. Se
debe empezar 7-14 días antes de la cirugía. A destacar:
Fenoxibenzamina (Dybenziran®, Dibenyline® cáps. 10 mg): ha sido el más empleado. Bloqueante
alfaadrenérgico no selectivo. Dosis de 5-10 mg/12 horas, aumentando 20-30 mg/día cada dos a
tres días, con una dosis máxima de 1 mg/kg/ día. No comercializado en España, debe solicitarse
a través de las oficinas de medicamentos extranjeros.
Doxazosina (2-8 mg/día), prazosina (2-5 mg/8 h), terazosina (2-5 mg/24 horas): son
bloqueantes selectivos α1 sin efecto α2. Producen menos hipotensión ortostática y menos
taquicardia refleja en el postoperatorio, puesto que el bloqueo alfa es incompleto. Su acción es
menos duradera y permite un ajuste más rápido de dosis.
Monitorización y objetivos del alfa-bloqueo: se deben hacer mediciones de la frecuencia cardiaca
(FC) y de la tensión arterial (TA) en bipedestación y sedestación 2 veces al día. Los objetivos prequirúrgicos
son: TA < 130/80 mm Hg sentado y tensión arterial sistólica > 90 mm Hg en bipedestación.
1.2.2. Bloqueo beta adrenérgico: siempre después del tercer día recibiendo alfa-bloqueo (nunca
antes por riesgo de precipitar crisis hipertensiva). Habitualmente se suelen asociar al bloqueo alfa 2-3 días
antes de la cirugía. Los más usados son propranolol (40 mg/8 h) o atenolol (25-50 mg/día).
Objetivo del beta bloqueo: controlar la taquicardia refleja inducida tras el bloqueo alfa, con el
objetivo de mantener la FC entre 60-70 lpm sentado y 70-80 lpm en bipedestación.
1.2.3. Otras alternativas:
Antagonistas del calcio: pueden ser utilizados junto con los alfa 1-bloqueantes en caso de no
lograr el control de la TA con los mismos. Puede ser un régimen alternativo al bloqueo alfa en
aquellos casos en los que la hipertensión preoperatoria sea leve o en los pacientes con
hipotensión ortostática severa bajo tratamiento alfabloqueante.
Inhibidores de la síntesis de catecolaminas (metirosina): inhibe la enzima tirosina-hidroxilasa,
que es el paso limitante en la síntesis endógena de catecolaminas. De esta forma facilita el
control de la presión arterial antes y durante la cirugía, especialmente durante la inducción de
la anestesia y la manipulación del tumor. Este fármaco cruza la barrera hematoencefálica y
puede producir efectos secundarios importantes, por lo que debe utilizarse con precaución y
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1123]
[69] PATOLOGÍA SUPRARRENAL
solo cuando otros agentes hayan sido ineficaces, o en pacientes en los que se prevé una
marcada manipulación o destrucción tumoral, junto con los bloqueadores alfa.
2. CIRUGÍA
La vía laparoscópica es actualmente el procedimiento de elección en los tumores únicos con un
diámetro < 6 cm. Se recomienda adrenalectomía parcial (con conservación de la corteza suprarrenal) como
prevención de la insuficiencia suprarrenal en casos de afectación bilateral.
3. MANEJO POSTOPERATORIO
Monitorización estrecha de la tensión arterial, frecuencia cardiaca y glucemia en las primeras 24-48
horas posquirúrgicas, por el riesgo de hipertensión, hipotensión e hipoglucemia. Se debe mantener una
infusión intravenosa de suero fisiológico y suero glucosado durante las primeras 24 horas. En caso de:
Hipotensión arterial posquirúrgica: la reposición de volumen es el tratamiento de elección.
Hipoglucemia: aparece en el 10-15% de los casos y ocurre porque se suprime la inhibición de la
secreción de insulina mediada por catecolaminas. Se trata con una infusión intravenosa de
glucosa.
4. SEGUIMIENTO
Se recomienda la medición de metanefrinas fraccionadas en plasma/orina posquirúrgico para
asegurar la curación; se recomienda esta medición a partir de las dos a cuatro semanas de la intervención.
Puesto que un 10% de los feocromocitomas pueden ser malignos (presencia de metástasis en tejido
no cromafín) con aparición de metástasis hasta 20 años después del diagnóstico y que se han descrito
recidivas o aparición de nuevos tumores a largo plazo, debe mantenerse seguimiento anual.
VI. INCIDENTALOMA ADRENAL
1. DEFINICIÓN Y EPIDEMIOLOGÍA
El incidentaloma adrenal (IA) se define como cualquier masa adrenal igual o mayor a 1 cm de
diámetro descubierta de manera incidental en cualquier estudio de imagen, en ausencia de síntomas o
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1124]
[69] PATOLOGÍA SUPRARRENAL
signos clínicos sugerentes de enfermedad adrenal. Se excluyen como definición a aquellas masas
descubiertas en pacientes oncológicos estudiados durante procesos de estadiaje tumoral.
El IA es una entidad cuya incidencia ha aumentado en las últimas décadas, como resultado de los
avances en los métodos radiológicos de imagen. Tiene una prevalencia variable: entre el 1% y el 8% según
las series (hasta en el 4% de los TC/RMN abdominales). Es más frecuente en población de edad avanzada.
2. ETIOLOGÍA
Se describe en tabla XVIII.
3. DIAGNÓSTICO
Ante el diagnóstico de un IA se deben resolver dos preguntas esenciales: si existe actividad
hormonal y si existe sospecha de malignidad. Para responder a estas inquietudes se sugieren los siguientes
estudios:
1. ESTUDIO DE FUNCIONALIDAD HORMONAL
La mayoría de los IA son no funcionantes, sin embargo hasta un 10-15% de los casos presentan
funcionalidad. Aunque los IA por definición acontecen en pacientes asintomáticos, se debe interrogar a
todos los pacientes sobre síntomas de hiperfunción; en caso de estar presentes se completará el estudio en
función de la sospecha clínica. En el resto se debe realizar despistaje de:
1.1. Hipercortisolismo
Debe descartarse en todos los pacientes con un IA. La prueba de elección es la supresión nocturna
con 1 mg de DXM, siendo útiles también el CLU de 24 horas o las concentraciones de ACTH y
dehidroepiandrosterona sulfato cuando el test inicial resulta alterado.
El pseudocushing (SSC) constituye la anormalidad hormonal más frecuente asociada al IA, y se
define como toda aquella situación de hipercortisolismo sin una clara expresividad clínica, pero que, sin
embargo, conlleva un riesgo aumentado de eventos cardiovasculares (hipertensión arterial, diabetes
mellitus, osteoporosis y fracturas vertebrales). Los criterios de diagnóstico no están totalmente
establecidos, sin embargo cifras de cortisol basal tras una supresión nocturna con 1 mg de dexametasona
elevadas, asociadas al menos a algún otro parámetro alterado (CLU de 24 horas elevado y ACTH basal
disminuida) parecen tener la mayor rentabilidad diagnóstica.
1.2. Feocromocitoma
Debe ser descartado en todos los pacientes con IA. La prueba de elección inicial depende del nivel
de sospecha clínica; en aquellos pacientes con baja sospecha se sugieren metanefrinas o catecolaminas
fraccionadas en orina de 24 horas; si la sospecha es alta se sugiere la detección de metanefrinas
fraccionadas en plasma.
1.3. Hiperaldosteronismo
Debe ser descartado en pacientes con hipertensión arterial y/o hipopotasemia. La prueba de
elección inicial sugerida es la medición de concentraciones de aldosterona plasmática y ARP (o CRP). Una
ratio aldosterona/renina elevada obliga a la realización de otras pruebas confirmatorias/de localización.
1.4. En pacientes con masas bilaterales se debe descartar una posible insuficiencia suprarrenal,
determinando cifras de cortisol basal y realizando un test de estímulo con 250 μg de ACTH; además de
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1125]
[69] PATOLOGÍA SUPRARRENAL
descartar la posibilidad de una hiperplasia suprarrenal congénita, determinando cifras de 17-OH-
progesterona.
2. ESTUDIO POR MÉTODOS DE IMAGEN
Se recomienda como prueba inicial la tomografía computarizada de abdomen sin contraste. En los
casos dudosos se pueden utilizar otras pruebas de confirmación (TC con contraste, RMN, PET/TC,
gammagrafías, otras).
3. PUNCIÓN-ASPIRACIÓN CON AGUJA FINA
Únicamente sirve para diferenciar lesiones primarias de metastásicas (no diferencia adenomas de
carcinomas suprarrenales), por lo que su utilidad parece reducida a pacientes con antecedentes de
neoplasias conocidas; antes de realizarla se debe descartar la presencia de un feocromocitoma, por la
posibilidad de desencadenar una crisis catecolaminérgica.
En la tabla XIX se enumeran algunas características diferenciales de los diferentes tipos de IA.
4. TRATAMIENTO
1. QUIRÚRGICO
En general se recomienda en todas las masas hiperfuncionantes, unilaterales, de gran tamaño y/o
que tengan características sugestivas de malignidad.
2. MANEJO DEL SSC
Actualmente no existe un claro consenso. Se sugiere una estrategia inicial conservadora,
reservando el tratamiento quirúrgico a aquellos casos con pobre control o empeoramiento de las
comorbilidades médicas asociadas o en pacientes jóvenes. Se debe realizar cobertura esteroidea en
pacientes sometidos a cirugía, considerando la posibilidad de desarrollo de una insuficiencia suprarrenal
por supresión de la ACTH.
5. SEGUIMIENTO
En aquellos pacientes que no cumplen criterios quirúrgicos se recomienda realizar controles por
métodos de imagen: al inicio a los tres a seis meses; posteriormente de forma anual durante uno a dos
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1126]
[69] PATOLOGÍA SUPRARRENAL
años en función de las características de la lesión, además de determinaciones hormonales anuales hasta
cuatro o cinco años tras el diagnóstico.
En la figura 4 se exponen las recomendaciones de manejo del IA.
BIBLIOGRAFÍA
Bornstein S, Allolio B, Arlt W, et al. Diagnosis and treatment of primary adrenal insufficiency: An
Endocrine Society Clinical Practice Guideline. J Clin Endocrinol Metab. 2016;101(2):364-89.
De Miguel Novoa P, Torres E, Palacios N, et al. Guía para el diagnóstico y tratamiento de la
insuficiencia suprarrenal en el adulto. Endocrinol Nutr. 2014;61(1):1-35.
Funder J, Carey R, Fardella C, et al. Case Detection, diagnosis, and treatment of patients with primary
aldosteronism: An Endocrine Society Clinical Practice Guideline. J Clin Endocrinol Metab. 2008;93(9):
3266-81.
Lenders J, Duh Q, Eisenhofer G, et al. Pheochromocytoma and paraganglioma: An Endocrine Society
Clinical Practice Guideline. J Clin Endocrinol Metabol. 2014;99(6):1915-42.
Santos S, Santos E, Gaztamide S, Salvador J. Diagnóstico y diagnóstico diferencial del síndrome de
Cushing. Endocrinol Nutr. 2009;56(2):71-84.
Nieman L, Biller B, Findling M, et al. Treatment of Cushing’s syndrome: An Endocrine Society Clinical
Practice Guideline. J Clin Endocrinol Metab. 2015;100(8):2807-31.
Nieman L, Biller B, Findling W, et al. The diagnosis of Cushing’s syndrome. J Clin Endocrinol Metabol.
2008;9(5):1526-40.
Terzolo M, Stigliano A, Chiodini I, et al. AME position statement on adrenal incidentaloma. Eur J
Endocrinol. 2011;164:851.
Young W, Kaplan N, Kebebew E. The adrenal incidentaloma. En: UpToDate, Basow DSN, editor.
UpTpDate, Waltham, MA; 2014.
Zeiger M, Thompson G, Duh Q, et al. American Association of Clinical Endocrinologists and American
Association of Endocrine Surgeons Medical Guidelines for the management of adrenal Incidentalomas.
Endocr Pract. 2009;15(Suppl 1):1-20.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1127]
[70] DIABETES MELLITUS. MANEJO A LARGO PLAZO
70.Diabetes mellitus. Manejo a largo plazo
Irene Losada Galván.
Medicina Interna
Laura Pérez-Olivares Martín.
Endocrinología y Nutrición
Asesora:
Elena García Fernández.
Médica Adjunta de Endocrinología y Nutrición
I. DEFINICIÓN
La diabetes mellitus (DM) se define como el conjunto de trastornos metabólicos que tienen como
nexo común la hiperglucemia crónica que resulta de defectos en la síntesis-secreción de insulina, en su
acción sobre los tejidos o en ambos. Esta situación se asocia a: a) manifestaciones clínicas por la propia
hiperglucemia; b) complicaciones agudas potencialmente mortales; c) complicaciones crónicas macro y
microvasculares; d) otras alteraciones (susceptibilidad a infecciones, complicaciones gestacionales,
psicológicas, sociolaborales, etc.). La Organización Mundial de la Salud (OMS) vaticina un aumento de
proporciones epidémicas en su prevalencia. En 2014 se estimaba que aproximadamente 422 millones de
personas tenían diabetes, con una prevalencia del 8,5%, el doble de lo calculado en 1980. En España se
estima que es del 13,8%.
II. TIPOS DE DIABETES MELLITUS
Diabetes mellitus tipo 1 (asociada a la destrucción de la célula beta, que usualmente cursa con
deficiencia absoluta de insulina).
Autoinmune. Subtipo LADA (Latent Autoinmune Diabetes of the Adult).
Idiopática.
Diabetes mellitus tipo 2 (asociada a un defecto progresivo de la secreción de insulina y a un
estado de insulinorresistencia).
Diabetes gestacional (aquellas formas de diabetes que son diagnosticadas durante la
gestación).
Tipos específicos de diabetes asociada a otras causas (ADA) (Tabla I).
III. ETIOPATOGENIA
1. DIABETES MELLITUS TIPO 1
La DM tipo 1 (DM1) representa el 5-10% de los casos registrados. Supone un déficit absoluto de
insulina por la destrucción de las células beta pancreáticas. Se precisa insulinoterapia para evitar el
desarrollo de complicaciones metabólicas crónicas y la muerte. Presenta una herencia poligénica (riesgo del
6% en hermanos afectos), con una fuerte asociación con el complejo mayor de histocompatibilidad (HLA
DQ y DR).
DM tipo 1A o autoinmune. En ella están implicadas la inmunidad celular (linfocitos T y
macrófagos) y la humoral (anticuerpos antiinsulina, anti-ácido glutámico decarboxilasa [anti-
GAD65], antitirosina fosfatasa IA-2, antitransportador de zinc 8). Entre el 50-60% debutan antes
de los 18 años. Pueden asociar otras patologías autoinmunes.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1128]
[70] DIABETES MELLITUS. MANEJO A LARGO PLAZO
DM tipo 1B o idiopática. Cursa con insulinopenia y tendencia a la cetoacidosis sin mediación
autoinmune. Es más frecuente en pacientes de origen africano y asiático. Presentan menor
prevalencia de complicaciones crónicas.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1129]
[70] DIABETES MELLITUS. MANEJO A LARGO PLAZO
2. DIABETES MELLITUS TIPO 2
La DM tipo 2 (DM2) representa el 90-95% de los casos registrados. Combina en grado variable un
defecto en la secreción de la insulina y la resistencia a su acción en los tejidos periféricos. No suele
presentar cetosis, salvo en determinadas situaciones (infección o enfermedades graves). Su herencia es
poligénica, con mayor influencia genética que en la DM1 (un progenitor afecto aumenta el riesgo al 40%;
dos progenitores afectos a un 60%). Constituyen un factor de riesgo para su desarrollo: la obesidad, los
antecedentes familiares, la etnia (mayor riesgo en afroamericanos, hispanos, asiático-americanos, indio-
americanos), el sexo femenino y las situaciones de insulinorresistencia (síndrome de ovario poliquístico).
IV. CLÍNICA
La sintomatología clásica de la hiperglucemia con insulinopenia (clínica cardinal) consiste en:
poliuria (la glucemia plasmática > 180 mg/dL provoca glucosuria, la cual se asocia con diuresis osmótica e
hipovolemia), polidipsia (por aumento de la osmolalidad plasmática secundaria a la hiperglucemia y a la
hipovolemia) y polifagia con pérdida de peso. Otras manifestaciones de la hiperglucemia son visión borrosa
por pseudomiopía diabética (como consecuencia de cambios osmóticos que afectan al cristalino y al humor
vítreo) y mayor riesgo de infecciones.
Diabetes mellitus de tipo 1. Sus formas de presentación clínica son: cetoacidosis diabética
(CAD) y, menos frecuentemente, glucemia elevada en una analítica realizada por otro motivo.
Los pacientes suelen presentar un índice de masa corporal (IMC) normal o bajo.
Diabetes mellitus de tipo 2. Sus formas de presentación pueden ser: asintomática (hallazgo
casual de hiperglucemia en una analítica realizada por otro motivo), descompensación
hiperglucémica hiperosmolar no cetósica y, menos frecuentemente, cetoacidosis diabética
(CAD). El 80-90% de los pacientes son obesos.
V. DIAGNÓSTICO
En la tabla II se describen las indicaciones de cribado y en la tabla III se detallan los criterios y test
diagnósticos.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1130]
[70] DIABETES MELLITUS. MANEJO A LARGO PLAZO
VI. EVALUACIÓN INICIAL Y MANEJO DE LA DIABETES
Los pacientes con DM deberán recibir cuidados médicos por parte de un equipo multidisciplinario
experto en diabetes que incluya personal médico, de Enfermería, de Nutrición y Salud Mental. Los
pacientes, además, deberán asumir un papel activo en el manejo de su enfermedad.
1. EVALUACIÓN INTEGRAL DEL PACIENTE DIABÉTICO
Historia médica: edad, fecha y características de inicio de la diabetes (asintomático,
cetoacidosis...), hábitos dietéticos y de ejercicio físico, historia de tabaquismo, consumo de
alcohol u otras sustancias, comorbilidades, otros factores de riesgo cardiovascular (FRCV) como
hipertensión arterial, dislipemia, problemas psicosociales, screening de depresión (escala PHQ-
2 y PHQ-9 [si la PHQ-2 fuera positiva]), screening de distrés asociado a la DM (Problem Areas In
Diabetes [PAID-1] o Diabetes Distress Screening [DDS]), enfermedades dentales, educación
diabetológica recibida, grado de autocuidado de su enfermedad (cumplimiento dietético,
número de controles de glucemia capilar realizados diariamente), regímenes de tratamiento
previos y respuesta de la hemoglobina glucosilada (HbA1c), hipoglucemias (número, causas
percibidas/desapercibidas, severas, nocturnas) y complicaciones metabólicas crónicas.
Exploración física: talla, peso, IMC, perímetro de la cintura abdominal, tensión arterial,
palpación tiroidea, examen dermatológico (acantosis nigricans, dermopatía diabética,
lipohipertrofias, etc.) y exploración de los pies (vascular y neurológica).
Laboratorio: nivel de HbA1c de los últimos tres meses, perfil lipídico, perfil hepático, relación
albúmina/creatinina en una muestra de orina de una micción, creatinina, filtrado glomerular
estimado (FGe; CKD-EPI o MDRD) y tirotropina (TSH) en DM1 y, entre los DM2, en varones y en
las mujeres con dislipemia o mayores de 50 años. En el momento del diagnóstico de la DM1 se
solicitarán anticuerpos antiperoxidasa, antitiroglobulina y antitransglutaminasa. Se repetirán
posteriormente solo si se considera clínicamente indicado.
Se derivará a Oftalmología. Otras derivaciones que pueden ser necesarias durante el
seguimiento son: planificación familiar en mujeres en edad reproductiva (el embarazo en una
mujer con DM debe ser planificado y el nivel de HbA1c aconsejado debe ser < 6,5%), evaluación
por Odontología para un correcto cuidado dental (enfermedad periodontal diabética,
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1131]
[70] DIABETES MELLITUS. MANEJO A LARGO PLAZO
infecciones dentarias…) y también por Podología. Se derivará a Psiquiatría por depresión,
ansiedad, trastornos de la conducta alimentaria asociados a la diabetes (diabulimia), fobia a las
agujas, fobia a las hipoglucemias, falta de aceptación de la enfermedad, etc. En pacientes con
diabetes se ha demostrado una asociación entre depresión y mortalidad por todas las causas.
Deberá evaluarse la función cognitiva y la presencia de depresión en pacientes con DM
mayores de 65 años.
2. VALORACIÓN DE LAS COMPLICACIONES METABÓLICAS CRÓNICAS
Como consecuencia del mal control glucémico crónico se pueden desarrollar: complicaciones
macrovasculares (enfermedad cerebrovascular, enfermedad cardiovascular y enfermedad vascular
periférica) y microvasculares (retinopatía, neuropatía y nefropatía). El inicio de la DM2 es insidioso y
muchas veces asintomático, por lo que cualquier complicación puede estar presente en el momento del
diagnóstico.
2.1. Retinopatía
Es la causa de ceguera más frecuente en adultos entre 20 y 74 años en el mundo occidental. Afecta
al 25-35% de los diabéticos. Su prevalencia se relaciona estrechamente con la duración de la diabetes y el
riesgo está aumentado en pacientes con hiperglucemia crónica, nefropatía e hipertensión.
Es asintomática hasta estadios avanzados, en los que se manifiesta como disminución de la agudeza
visual por presencia de edema macular, desprendimiento de retina o hemorragia vítrea.
Se recomienda realizar un fondo de ojo a los 5 años del diagnóstico a los pacientes con DM2 y a los
5 años a los pacientes con DM1. Posteriormente se debe repetir anualmente o antes según el grado de
retinopatía. El embarazo se asocia con una rápida progresión de la retinopatía diabética, por lo que las
mujeres con DM1 o DM2 con deseo gestacional deberán ser aconsejadas acerca del posible desarrollo o
progresión de esta entidad. Se recomienda la valoración oftalmológica en cada trimestre con un
seguimiento estrecho posterior hasta un año tras el parto.
El control glucémico intensivo, al igual que el de otros factores como la HTA, la dislipemia (con, por
ejemplo, el uso de fibratos en retinopatías no proliferativas leves) ha demostrado prevenir y/o retrasar su
progresión. Cabe destacar que la existencia de retinopatía no contraindica el uso de ácido acetilsalicílico.
2.2. Neuropatía
Existen distintos tipos de neuropatías dependiendo de las fibras nerviosas afectadas (Tabla IV). El
50% de los pacientes que acuden a una consulta de Endocrinología por primera vez presentan neuropatía
por DM subclínica. Es muy importante su diagnóstico en esta fase para poner en marcha medidas
educacionales que eviten el desarrollo de úlceras. Para su diagnóstico clínico se emplean distintos test de
screening (Tabla V: test de Michigan).
La optimización del control glucémico previene o retrasa el desarrollo de esta patología en la DM1 y
enlentece la progresión en la DM2. Para su manejo se realizan dos aproximaciones: en primer lugar, el
control glucémico que previene o retrasa y su desarrollo. En segundo lugar, el manejo del dolor (la queja
más frecuente y limitante), para el cual disponemos de fármacos como pregabalina, duloxetina o
tapentadol, entre otros.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1132]
[70] DIABETES MELLITUS. MANEJO A LARGO PLAZO
Neuropatías difusas
Neuropatías motoras proximales. Comienzan de forma aguda o gradual con dolor en los
muslos, caderas o nalgas y se sigue de una importante debilidad de los músculos
proximales de las extremidades inferiores, con incapacidad para incorporarse desde la
posición de sentado (maniobra de Gowers positiva). Presentan fasciculaciones
musculares espontáneas o provocadas por la percusión. En el electromiograma (EMG)
se detecta una plexopatía lumbosacra.
Polineuropatía simétrica distal (DSPN). Es la neuropatía más frecuente. Su inicio es
insidioso, aunque ocasionalmente puede ser agudo, y desencadenado por estrés o por
el inicio del tratamiento de la DM. Los pacientes presentan pérdida progresiva de
sensibilidad, de comienzo distal, seguida de debilidad muscular en los casos más
severos. Es subclínica en el 85% de los casos, descubriéndose en la exploración; en el
resto se manifiesta por la presencia de dolor o hiperalgesia (neuropatía de fibra corta)
y/o de pérdida de sensibilidad térmica, táctil y presora (neuropatía de fibra gruesa) en
las extremidades inferiores y en las manos.
Neuropatías focales
Mononeuropatías. Su inicio suele ser agudo, se asocian a dolor y afectación motora en
el territorio del nervio afecto. Dañan más frecuentemente a los pares craneales
oculomotores y a los nervios del tronco. Pueden coexistir mononeuropatías en varias
localizaciones. Se suelen resolver en 6-8 semanas.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1133]
[70] DIABETES MELLITUS. MANEJO A LARGO PLAZO
Síndromes de atrapamiento. Aparecen en un tercio de los diabéticos. Comienzan de
forma lenta y progresiva. Suelen afectar a los nervios mediano, cubital, radial, femoral,
laterales cutáneos del muslo, peroneos, plantares laterales y medianos. Para su
diagnóstico se emplean las pruebas de Tinel y Phalen en la muñeca o sus equivalentes
en otras zonas.
Neuropatía autonómica (Tabla VI) Se presenta en forma insidiosa, puede afectar a múltiples
órganos y se diagnostica por exclusión.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1134]
[70] DIABETES MELLITUS. MANEJO A LARGO PLAZO
2.3. Nefropatía
Ocurre en un 20-40% de los pacientes y es la principal causa de insuficiencia renal terminal. Para su
detección precoz deben determinarse anualmente el ratio albúmina/creatinina en la orina de una micción
(UACR) y estimarse el filtrado glomerular (FGe; MDRD o CKD-EPI) en la DM2 desde el diagnóstico, en la
DM1 a partir de los 5 años del diagnóstico y en todos los pacientes con DM e hipertensión arterial.
Factores como el ejercicio, la fiebre, la insuficiencia cardiaca congestiva, la hiperglucemia, la
menstruación y la hipertensión arterial pueden alterar el valor de UACR independientemente de la función
renal. Debido a esta variabilidad, deberán obtenerse al menos dos de tres test alterados (UARC > 30 mg/g)
recogidos en un periodo de 3 a 6 meses antes de considerar que el paciente tiene albuminuria.
A considerar que:
Si UACR persistentemente incrementado (30-299 mg/g): es un indicador temprano de
enfermedad renal y un FRCV establecido.
Si UACR > 300 mg/g: está asociado a retinopatía y apoya el diagnóstico de nefropatía diabética.
Si UACR < 300 mg/g, con disminución del FGe y sin retinopatía: se deben valorar otras causas
de afectación renal.
En la tabla VIII se describen las indicaciones para el manejo de la nefropatía diabética.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1135]
[70] DIABETES MELLITUS. MANEJO A LARGO PLAZO
2.4. Enfermedad cardiovascular (ECV)
Es la mayor causa de morbimortalidad en pacientes diabéticos. Es común la coexistencia de otras
condiciones (por ejemplo, hipertensión y dislipemia).
Enfermedad arterial periférica
El 40-70% de las amputaciones no traumáticas de miembros inferiores son por DM. Tras una
amputación, la incidencia de una nueva úlcera o de una nueva amputación es del 50% en los
próximos cinco años. El cribado de la enfermedad arterial periferica (EAP) valora la existencia
de claudicación intermitente, la palpación de pulsos distales (tibiales posteriores y pedios
bilaterales) y el índice tobillo/brazo (ITB), que se han de estudiar anualmente.
El ITB resulta de la relación entre la tensión arterial a nivel maleolar y en el brazo. Se debe
realizar en: pacientes sintomáticos, pacientes asintomáticos mayores de 50 años y pacientes
asintomáticos menores de 50 años con otros factores de riesgo cardiovascular. Permite
clasificar la EAP en 4 grados:
Mayor de 1,3: no interpretable
Entre 0,9 y 1,3: normal
Entre 0,41 y 0,9: enfermedad arterial periférica leve-moderada
Menor o igual a 0,4: enfermedad arterial periférica severa.
En caso de obtener un resultado no interpretable o patológico deberá completarse el
estudio con una ecografía Doppler arterial de miembros inferiores.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1136]
[70] DIABETES MELLITUS. MANEJO A LARGO PLAZO
Enfermedad cardiovascular aterosclerótica: enfermedad coronaria
Aproximadamente el 80% de los pacientes con DM2 sufren complicaciones cardiovasculares en
las que la lesión predominante es el fenómeno aterotrombótico. El 70% de las muertes por
aterotrombosis son cardiacas y se empiezan a producir en la cuarta década de la vida. La
proteinuria multiplica por quince el riesgo de desarrollar una enfermedad coronaria.
La tasa de mortalidad por infarto agudo de miocardio (IAM) en pacientes diabéticos es casi el
doble que en los no diabéticos, tanto durante la fase aguda como en el periodo precoz y tardío
debido a un mayor riesgo de insuficiencia cardiaca y de muerte súbita y una mayor probabilidad
de reinfarto precoz.
Como consecuencia de la neuropatía los pacientes pueden presentar síntomas atípicos durante
el síndrome coronario agudo e isquemia silente. Se debe realizar un test de isquemia
miocárdica a los pacientes con síntomas típicos o atípicos para cardiopatía isquémica y a
aquellos con alteraciones electrocardiográficas sugestivas. No se recomienda en pacientes
asintomáticos con ECG normal.
Enfermedad cerebrovascular
La DM es un importante factor de riesgo para el infarto cerebral isquémico. En pacientes con
accidente cerebrovascular agudo (ACVA) la prevalencia de la DM conocida es del 20% y de la no
conocida, del 6-42%.
El control glucémico estricto no ha demostrado reducir la incidencia de ACVA. Sin embargo, el
control tensional lo reduce hasta en un 44%.
Detección precoz de enfermedad aterotrombótica subclínica
Puesto que la mortalidad por causas cardiovasculares y cerebrovasculares es muy alta, se
aconseja intentar que la enfermedad aterotrombótica se diagnostique en fase precoz. Existen
métodos no invasivos para ello como la determinación del score de calcio coronario, la
determinación del grosor íntima-media carotídeo (ecografía carotídea), la valoración de las
calcificaciones en la aorta lumbosacra (radiografía; método Kauppila) y la medición de la
velocidad de la onda de pulso.
2.5. Pie diabético (PD)
Las úlceras en los pies y las amputaciones (consecuencia de la neuropatía diabética o de la
enfermedad arterial periférica) son frecuentes y representan una causa importante de morbilidad y
mortalidad. Son factores de riesgo de PD: la amputación y úlceras previas, la neuropatía periférica, la
deformidad del pie, la enfermedad arterial periférica, la disminución de la agudeza visual, la nefropatía
diabética, el mal control glucémico y el hábito tabáquico. Se realizará un examen anual del pie que incluirá
la inspección completa de la piel y de posibles deformidades, la palpación de los pulsos distales (pedios y
tibiales posteriores) y la exploración de la sensibilidad. La clasificación de las úlceras diabéticas se detalla en
la tabla IX.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1137]
[70] DIABETES MELLITUS. MANEJO A LARGO PLAZO
VII. VALORACIÓN DE OTRAS COMORBILIDADES ASOCIADAS A LA
DIABETES
Aumento de la incidencia de hepatopatía crónica no alcohólica y carcinoma hepatocelular. Las
intervenciones que mejoren el perfil metabólico son beneficiosas en los pacientes diabéticos
con enfermedad hepática grasa.
Síndrome de apnea del sueño, con una prevalencia en la población con DM2 del 23%.
La DM2 se asocia con mayor riesgo de cáncer de páncreas, hepático, del endometrio, de colon,
del recto, de la mama y de la vejiga.
Riesgo aumentado de fractura de cadera en pacientes con DM1 y DM2 en ambos sexos. La DM1
se asocia a osteoporosis, aunque en la DM2 el riesgo aumentado de fractura existe a pesar de
la densidad mineral ósea aumentada. En pacientes con DM2 y con riesgo de fractura
aumentado, deben evitarse las tiazolidinedionas y los inhibidores del cotransportador sodio-
glucosa.
Los niveles de testosterona en los hombres diabéticos son menores que en los hombres no
diabéticos. A pesar de ello no se recomienda la terapia de reemplazo en pacientes
asintomático.
La enfermedad periodontal es más severa, aunque no es más prevalente.
Riesgo aumentado de deterioro cognitivo y demencia.
VIII. OBJETIVOS Y ESTRATEGIAS DE CONTROL
1. PREDIABETES
Retrasar y prevenir la aparición de diabetes mediante:
Consejo dietético para adoptar una dieta equilibrada con el objetivo de lograr una pérdida de al
menos el 7% del peso corporal (en caso de presentar sobrepeso u obesidad). Algunos estudios
recientes apoyan el papel de la dieta mediterránea (relativamente rica en grasas
monoinsaturadas) como medida para prevenir la DM2.
Actividad física: realización de al menos 150 min/semana de ejercicio de intensidad moderada,
alcanzando el 50-70% de la frecuencia cardiaca máxima (por ejemplo, caminar a paso ligero),
repartidos en al menos tres días a la semana, evitando estar más de dos días consecutivos sin
actividad".
La consideración de tratamiento con metformina en pacientes prediabéticos con IMC > 35
kg/m2, menores de 60 años o con historia de diabetes gestacional o aumento progresivo de la
HbA1c a pesar de las medidas higiénico-dietéticas.
El seguimiento para el diagnóstico precoz de la DM debe ser al menos anual en pacientes de
alto riesgo (Tabla II) y cada cuatro años en el resto de pacientes a partir de los 40 años,
determinando una glucemia basal plasmática. Se debe realizar también despistaje y
tratamiento de otros FRCV.
2. CONTROL GLUCÉMICO
El control glucémico estricto ha demostrado prevenir la enfermedad microvascular, si bien su papel
para la prevención de la enfermedad cardiovascular (ECV) no está tan bien definido. El objetivo del control
glucémico viene determinado actualmente por la hemoglobina glucosilada (HbA1c), aunque en los últimos
años han surgido nuevos parámetros a considerar (tiempo en rango). El valor objetivo de los mismos varía
en función de las características del paciente.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1138]
[70] DIABETES MELLITUS. MANEJO A LARGO PLAZO
Los pacientes con DM de larga duración, historia de hipoglucemias severas, ateroesclerosis severa o
edad avanzada, se beneficiarán de unos objetivos glucémicos menos estrictos.
Autocontrol glucémico (glucemia capilar)
Ha de integrarse en un plan global de automanejo y adaptarse a las necesidades del paciente
en cada momento. El número de determinaciones diarias y el momento de las mismas varían
en función del tipo de DM, el tratamiento hipoglucemiante, la estabilidad del control y las
características del paciente (Tabla X).
Debe instruirse a los pacientes sobre cómo ajustar la ingesta, el ejercicio o la terapia
farmacológica según el tipo de glucemias y así conseguir objetivos concretos. Especialmente en
pacientes tratados con insulina es importante informar acerca de la prevención y el tratamiento
de las hipo e hiperglucemias asintomáticas. En los pacientes con DM1 existe correlación entre
el número de determinaciones diarias y los mejores objetivos de HbA1c alcanzados. En los
últimos años se han introducido los sistemas de monitorización continua de glucosa (CGM),
especialmente indicados para los pacientes con DM1.
Hemoglobina glucosilada (HbA1c)
Es una medida ponderada de los niveles de glucemia medios de los últimos 120 días (vida
media aproximada del hematíe) y tiene un alto valor predictivo de posibles complicaciones de
la DM.
Los niveles de glucemia de los días más cercanos a la determinación contribuyen en un
mayor porcentaje que los más lejanos (la glucemia media de los 30 días más cercanos a la
extracción contribuye aproximadamente al 50% de la HbA1c , mientras que la glucemia media
entre 90 y 120 días antes de la extracción contribuye solo en un 10%). Expresada en porcentaje,
se correlaciona con los valores medios y de glucemia basal según la tabla XI. Los objetivos
varían en función de las características del paciente y se recogen en la tabla XII.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1139]
[70] DIABETES MELLITUS. MANEJO A LARGO PLAZO
Existen limitaciones para su interpretación en caso de alteraciones en el recambio de hematíes. Así,
en situaciones de recambio rápido (hemólisis, sangrado, tratamiento con eritropoyetina [EPO],
hemodiálisis) se infraestima la cifra de HbA1c . En situaciones de bajo recambio (anemias por déficit de
ácido fólico, vitamina B12, esplenectomizados) existen cifras más elevadas de HbA1c que corresponden al
mayor tiempo de exposición a glucosa de los hematíes.
De forma general, se persiguen objetivos de HbA1c por debajo del 7%. Sin embargo, se establecen
objetivos superiores al 7% en pacientes con DM de muy larga evolución, historia de hipoglucemias severas,
arterioesclerosis avanzada y edad avanzada/fragilidad, por riesgo de hipoglucemias severas.
La HbA1c no es una buena medida de la variabilidad glucémica o la presencia de hipoglucemias. En
pacientes con tendencia a la variabilidad (DM1 o DM2 con deficiencia insulínica severa), el control
glucémico se evalúa combinando los resultados de la HbA1c con las cifras y horarios de los autocontroles
glucémicos.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1140]
[70] DIABETES MELLITUS. MANEJO A LARGO PLAZO
IX. TRATAMIENTO
1. TRATAMIENTO NO FARMACOLÓGICO (MODIFICACIÓN DEL ESTILO DE VIDA)
1.1. Dieta: ver Apartado VIII. “Objetivos y estrategias de control”.
1.2. Actividad física: ver Apartado VIII. “Objetivos y estrategias de control”. Las contraindicaciones
para el ejercicio son HTA o DM descompensadas, neuropatías autonómica o periférica severas, retinopatía
proliferativa y antecedentes o presencia de úlceras en los pies.
1.3. Abandono del hábito tabáquico, incluyendo el uso de cigarrillos electrónicos.
2. TRATAMIENTO FARMACOLÓGICO
2.1. Insulina (Tabla XIII)
Forma de administración: las insulinas de acción rápida y ultrarrápida deben administrarse por
vía subcutánea en el abdomen. Las intermedias y lentas en brazos, muslos o nalgas. Debe
rotarse el lugar de la inyección para evitar la aparición de lipodistrofias que alteren la absorción
de la insulina.
Factores modificadores de la absorción: lugar de administración (más rápida en el abdomen y
más lenta en muslos, brazos y nalgas), flujo sanguíneo (absorción mayor con el masaje o la
exposición de la zona a agua caliente [ducha o baño]), dosis (absorción más lenta a mayor
volumen inyectado) y profundidad (absorción mayor a más profundidad).
Tipos de insulina (Tabla XIV)
Basal: suple la producción continua de insulina por parte del páncreas y controla la
producción hepática de la glucosa.
Glargina: se administra en una sola dosis diaria.
Detemir: puede administrarse en una sola dosis pero generalmente se
administra en dos debido a su vida media. La dosis suele repartirse en 2/3 por
la mañana y 1/3 por la tarde.
NPH: se administra en dos dosis (2/3 por la mañana y 1/3 por la tarde).
Glargina U300 y degludec: insulinas ultralentas, recientemente
comercializadas. Tienen mayor vida media (36 h y 42 h, respectivamente) y
permiten la administración más flexible. Presentan una menor tasa de
hipoglucemias nocturnas y una mayor estabilidad glucémica.
Preprandial: controla la elevación de glucemia tras cada ingesta.
Insulina regular (Actrapid®).
Insulina ultrarrápida (lispro, aspart, glulisina).
2.2. Otros agentes hipoglucemiantes
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1141]
[70] DIABETES MELLITUS. MANEJO A LARGO PLAZO
Indicados exclusivamente en la DM2 (ver resumen de las características en las tablas XV y XVI). Se
debe tener en cuenta la existencia de múltiples formulaciones combinadas.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1142]
[70] DIABETES MELLITUS. MANEJO A LARGO PLAZO
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1143]
[70] DIABETES MELLITUS. MANEJO A LARGO PLAZO
Sensibilizadores a la acción de la insulina
Biguanidas:
Metformina: antidiabético oral de primera elección. Su principal efecto
secundario es la intolerancia digestiva (diarrea, meteorismo...), por lo que se
debe iniciar a dosis bajas e ir incrementándolas progresivamente. Los datos
actuales indican que el riesgo de acidosis láctica asociada a metformina es bajo.
No obstante, debe evitarse en pacientes con alto riesgo de acidosis láctica (ERC
avanzada, alcoholismo, insuficiencia respiratoria, administración de
radiocontraste, sepsis). El uso de metformina debe ser reevaluado cuando se
alcanza un FGe de 45 ml/min/1,73 m2 y hay que reducir su dosis a un máximo
de 1.000 mg/día. Deberá interrumpirse el tratamiento con FGe de 30
ml/min/1,73 m2. Tras dos o tres años de tratamiento con metformina se debe
monitorizar la concentración de vitamina B12, puesto que puede interferir con
su absorción.
Glitazonas o tiazolidinedionas:
El único disponible en el mercado es la pioglitazona. Puede existir aumento de riesgo
de cáncer de vejiga en los pacientes tratados con este fármaco, por lo que no debe
utilizarse en pacientes con cáncer de vejiga activo, considerando la relación de
riesgo/beneficio en aquellos con historia previa (sin actividad), teniendo en cuenta que
el riesgo de desarrollar cáncer de vejiga aumenta con la dosis acumulada. Se han
comunicado casos de hepatotoxicidad diferida varios meses después del inicio del
tratamiento, por lo que se recomienda monitorización de la función hepática
periódicamente.
Reguladores de la secreción de insulina
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1144]
[70] DIABETES MELLITUS. MANEJO A LARGO PLAZO
Sulfonilureas. Las sulfonilureas estimulan las células beta del páncreas a secretar
insulina, y por este motivo pueden provocar hipoglucemia. Su posología es
generalmente una o dos veces al día, antes de las comidas. Todas las sulfonilureas
tienen efectos similares sobre los niveles de glucosa en la sangre, pero difieren en los
efectos secundarios, la frecuencia con que se toman y las interacciones con otros
fármacos.
Aumentan la secreción de insulina mediante la estimulación directa de la célula, por lo
que requieren la presencia de cierta reserva pancreática (DM2 de corta evolución) y
pueden producir hipoglucemias. Algunas producen aumento de peso y conllevan mayor
riesgo de hipoglucemias (glibenclamida > gliclazida > glimepirida). Disminuyen
incidencia de complicaciones microvasculares. De eliminación renal en su mayoría.
Glinidas: Pueden ser utilizadas en pacientes en los que presentan insuficiencia renal
leve-moderada.
Inhibidores de α-glucosidasa: acarbosa y miglitol. Estos medicamentos ayudan a reducir los
niveles de glucosa en la sangre mediante el retraso de la digestión/absorción de carbohidratos
en el intestino. Su acción ralentiza el aumento de los niveles posprandiales de glucosa en la
sangre. Los principales efectos secundarios incluyen gases y diarrea.
Incretín-miméticos o terapias basadas en GLP-1 (glucagón-like peptide) (Tabla XVI).
Análogos de GLP-1 (administración subcutánea). En algunos casos es necesaria la
titulación de dosis durante el primer mes para minimizar las náuseas, efecto adverso
que presenta fenómeno de taquifilaxia. No producen hipoglucemias, salvo si se
administran junto con sulfonilureas o insulina, debiendo disminuir la dosis de las
mismas.
Inhibidores de DPP-4 (administración oral): Disminuyen la HbA1C sin causar
hipoglucemias. Funcionan impidiendo la degradación de las incretinas activas del
intestino (GIP y GLP-1) que son liberadas tras la comida, estimulando el páncreas a
producir insulina. En consecuencia, se aumenta la liberación de insulina a partir de las
células beta cuando los niveles de glucosa son elevados. Los inhibidores DPP-4 no
tienden a causar aumento de peso. El metabolismo de la saxagliptina está mediado
principalmente por el citocromo P-450, por lo que puede tener interacciones con
inductores potentes del CYP 3A4. No es necesario ajuste de dosis con digoxina, pero
cuando sitagliptina es usada concomitantemente con digoxina se recomieda vigilar los
pacientes con riesgo de toxicidad por digoxina. Estos fármacos pueden ser utilizados en
caso de insuficiencia renal, incluyendo moderada y severa (ver tabla). Ver ajuste de
dosis para pacientes con alteración de la función renal en la tabla XVII).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1145]
[70] DIABETES MELLITUS. MANEJO A LARGO PLAZO
Inhibidores del cotransportador renal de sodio y glucosa 2 (SGLT2)
Disminuyen la reabsorción de la glucosa filtrada en el glomérulo, produciendo glucosuria y un
discreto efecto diurético. Se han comunicado casos de cetoacidosis diabética euglucémica en
pacientes en tratamiento con estos fármacos, sin haberse dilucidado claramente el mecanismo
subyacente. Debido a su mecanismo de acción, es frecuente la aparición de infecciones
genitourinarias.
No se recomienda su uso en pacientes con sospecha de DM1 ni en pacientes con riesgo
aumentado de cetoacidosis (aquellos con reserva baja de células beta, restricción de ingesta,
reducción súbita de insulina, cirugía, abuso de alcohol, etc.).
Cuando se inicia tratamiento con este grupo farmacológico se debe indicar a los pacientes que,
en caso de sentir molestias abdominales, náuseas, vómitos, anorexia, polidipsia o confusión,
deben suspender el fármaco y acudir al Servicio de Urgencias (descartar CAD). Se debería
interrumpir también el tratamiento en pacientes que hayan sido hospitalizados por
procedimientos de cirugía mayor o enfermedades agudas graves, pudiendo restablecerlo al
alta.
2.3. Elección del tratamiento farmacológico
Ha de tenerse en cuenta el objetivo individualizado de la HbA1c según el paciente, eficacia, coste,
efectos adversos potenciales, cambios en el peso, riesgo de hipoglucemia y las preferencias del paciente.
Diabetes mellitus de tipo 1
La pauta de elección es la insulinoterapia intensiva bolo-basal, que consiste en la
administración de una insulina de acción intermedia, lenta o ultralenta, junto con bolos de
insulina rápida o ultrarrápida antes de las comidas.
La terapia de "infusión continua subcutánea de insulina" (ICSI) se indica ante pacientes con alta
motivación o altos conocimientos en el manejo de la diabetes, en aquellos que no alcancen el
objetivo terapéutico con una pauta de insulina subcutánea de bolo-basal, que presenten
hipoglucemias recurrentes desapercibidas, que tengan requerimientos diarios de insulina muy
bajos (< 20 UI/día), que tengan fobia a las agujas, que sean atletas de competición, y también
ante el mal control glucémico durante el embarazo o previamente al mismo para planificarlo
correctamente.
Se realiza a través de microinfusoras de insulina que dispensan insulina ultrarrápida a los
pacientes durante las 24 horas del día y a un ritmo programado por el endocrinólogo. A través
de las microinfusoras, los pacientes se autoadministran, además, bolos de insulina ultrarrápida
preprandiales (según la cantidad de hidratos de carbono que vayan a ingerir) y correctores
(según su glucemia capilar y su sensibilidad a la insulina en un momento determinado). La
cantidad de insulina que debe administrarse en estos bolos se indica mediante unos
dispositivos denominados “calculadores de bolos” (programados por el Servicio de
Endocrinología).
Todo paciente diabético en terapia ICSI posee un informe en el que se detalla la programación
de la microinfusora y la pauta alternativa de insulina subcutánea pinchada (bolo-basal) que se
debe administrar en caso de no poder mantenerse la microinfusora en funcionamiento. Cuando
estos enfermos acudan al Servicio de Urgencias se les debe solicitar este documento.
Diabetes mellitus de tipo 2
ADO: metformina es el ADO de elección en ausencia de intolerancia o contraindicación.
Debe añadirse un segundo agente oral, análogo de GLP-1 o insulina en caso de no
alcanzarse los objetivos de HbA1c tras tres meses de tratamiento, o bien de inicio en
caso de HbA1c ≥ 9%.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1146]
[70] DIABETES MELLITUS. MANEJO A LARGO PLAZO
Las recomendaciones generales se pueden encontrar en la figura 1, expresadas sin
orden de preferencia particular.
Insulina: indicada en pacientes recién diagnosticados, con pronunciada hiperglucemia
(≥ 300-350 mg/dL o/y una HbA1c ≥ 10-12%) o en pacientes que no alcanzan objetivos de
HbA1c a pesar del tratamiento con otros agentes hipoglucemiantes y en situaciones de
estrés (infecciones, cirugías, corticoterapia, hospitalización…). No debería retrasarse su
uso, teniendo presente que puede tratarse de una medida transitoria. Resulta clave
ajustar la complejidad y la intensidad del tratamiento a las necesidades metabólicas y a
las características del paciente (objetivos metabólicos y capacidad de adherencia y
cumplimento del mismo) (Figura 2).
Como terapia inicial (en monoterapia o combinada con ADO no secretagogos):
se busca aumentar la sensibilidad a la insulina. Posteriormente, cuando la
glucemia basal sea < 130 mg/dL o cuando la necesidad de insulina sea igual o
menor a 12 UI/día se puede sustituir el tratamiento por ADO.
En combinación con ADO o agonistas GLP-1: si no se alcanzan los objetivos de
tratamiento, se recomienda añadir insulina basal y suspender ADO
secretagogos (sulfonilureas, glinidas) por riesgo de hipoglucemias.
En monoterapia: en situaciones de estrés y en caso de persistir mal control a
pesar de las combinaciones descritas previamente. Se suspende ADO y se inicia
terapia insulínica intensiva con insulina basal y corrección prandial.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1147]
[70] DIABETES MELLITUS. MANEJO A LARGO PLAZO
Ajustes: suelen hacerse de 2 en 2 o hasta de 4 en 4 unidades, cada 2-3 días. Las
insuficiencias renal y hepática pueden disminuir los requerimientos de insulina
basal. La actitud ante la hiperglucemia predesayuno debe ser la siguiente: se
debe medir la glucemia a las 2-3 a.m. y a las 5 a.m. Si se detecta hipoglucemia
nocturna (fenómeno de Somogy), se reducirá la dosis nocturna. Si la glucemia a
las 2-3 a.m. es normal y posteriormente elevada (fenómeno del alba), se puede
retrasar la administración de insulina intermedia o cambiar la insulina
intermedia por un análogo lento (que permite el aumento de dosis nocturna
con menor riesgo de hipoglucemia).
3. EVALUACIÓN Y CONTROL DE FRCV
Se recomienda realizar el cálculo individualizado del riesgo cardiovascular de cada paciente según
las escalas validadas como la de la American College of Cardiology/American Heart Association, dado que el
riesgo de cada paciente determina la estrategia de control a seguir (ver Capítulo 20. “Hipertensión arterial y
riesgo vascular”).
3.1. Obesidad
La pérdida de peso en pacientes con sobrepeso u obesidad ha demostrado mejorar el control
glucémico y disminuir o retrasar la progresión de pre-DM a DM2. Estos beneficios se consiguen con una
pérdida del 5% del peso corporal, si bien se recomienda una pérdida mantenida de al menos el 7%. El
efecto sobre el control glucémico es mayor en las fases iniciales de la enfermedad, en relación con la
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1148]
[70] DIABETES MELLITUS. MANEJO A LARGO PLAZO
disfunción reversible de la secreción de insulina por las células β. Se recomienda monitorizar el IMC en cada
visita de control del paciente con DM.
Medidas no farmacológicas
En pacientes motivados se puede alcanzar una pérdida de peso en torno al 5% mediante dietas
con déficit energético aproximado de 500-750 kcal/día, aumento de la actividad física y
programas de mantenimiento a largo plazo. Una dieta hipocalórica puede reducir la HbA1c por
debajo del 6,5% y la glucemia basal por debajo de 126 mg/dL, en ausencia de medidas
farmacológicas.
Farmacológicas
Es importante tener en cuenta el efecto sobre el peso antes de prescribir cualquier tratamiento
a un paciente con diabetes. Los hipoglucemiantes asociados a la pérdida de peso son:
metformina, inhibidores de alfa-glucosidasa, análogos de GLP-1 e inhibidores de
cotransportadores sodio-glucosa 2 (Tablas XV y XVI). Los inhibidores de la dipeptidil peptidasa-
4 (DPP-4) tienen un efecto neutro sobre el peso. Algunos fármacos frecuentemente empleados
para tratar otras patologías pueden favorecer la ganancia de peso (antipsicóticos atípicos,
antidepresivos, glucocorticoides, anticonceptivos orales que contengan progestágenos,
anticomiciales, antihistamínicos, anticolinérgicos).
En EEUU existen cinco fármacos aprobados para el tratamiento de la obesidad. De ellos, el
único aprobado en España es orlistat. Está indicado en pacientes con IMC ≥ 28 kg/m2 con
comorbilidades asociadas o pacientes con IMC ≥ 30 kg/m2 motivados para la pérdida de peso.
orlistat es un inhibidor de la lipasa que produce una pérdida media de peso de entre 2,5 y 3,4
kg al año de tratamiento. Solo se puede mantener durante 12 meses. Durante los primeros tres
meses de tratamiento se debe monitorizar el IMC mensualmente y suspender el tratamiento en
caso de pérdida de peso menor del 5% y/o problemas de intolerancia o seguridad. Se deberá
aconsejar un método anticonceptivo a las mujeres en edad fértil por desconocerse los posibles
efectos sobre el feto.
Quirúrgicos
La cirugía bariátrica se debe considerar en adultos con IMC > 35 kg/m2 y DM2, especialmente si
esta última es de difícil control y asocia comorbilidades. Estos pacientes precisarán de control
estrecho posteriormente a la cirugía, al menos una vez al año. Algunos estudios pequeños
muestran beneficios en cuanto al control glucémico en pacientes con DM e IMC de 30-35
kg/m2, sin que pueda establecerse claramente la indicación por el momento.
3.2. Hipertensión arterial
El objetivo de tensión arterial (TA) en pacientes diabéticos debe ser < 140/90 mm Hg; pudiendo
establecerse en < 130/80 mm Hg en aquellos con expectativa de vida larga, enfermedad renal crónica
(ERC), albuminuria y/o HTA con algún otro FRCV asociado (como dislipemia, tabaquismo u obesidad).
Además de las medidas higiénico-dietéticas, la terapia de elección inicial es un IECA (o ARA-II) (ver Capítulo
20. “Hipertensión arterial y riesgo vascular”).
3.3. Dislipemia
Se recomiendan cambios en el estilo de vida ligados a la reducción de ingesta de grasas (saturadas y
trans) y colesterol, aumentar la ingesta de ácidos omega 3 y de fibra, así como aumentar la actividad física y
perder peso (si estuviera indicado).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1149]
[70] DIABETES MELLITUS. MANEJO A LARGO PLAZO
La indicación de terapia farmacológica con estatinas, así como la potencia de las mismas, se
establece en función de la edad y los FRCV. Su uso está contraindicado en el embarazo (Tabla XVIII) (ver
Capítulo 73. “Trastornos lipídicos”).
3.4. Antiagregantes
Se recomienda el uso de ácido acetilsalicílico (AAS) 100 mg/día en prevención secundaria y en
prevención primaria si el RCV > 10% a los 10 años. Esto incluye a la mayoría de hombres y mujeres ≥ 50
años con un FRCV añadido a la DM. Puede considerarse clopidogrel 75 mg/día como alternativa en caso de
alergia al AAS o úlcera gastroduodenal. El uso de AAS está contraindicado en menores de 21 años por
asociarse al síndrome de Reye.
3.5. Vitaminas
El objetivo de los niveles sanguíneos de vitamina D debe estar por encima de los 30 ng/ml. Hay que
valorar inicia tratamiento por debajo de este número en función de la edad, la época del año y los niveles
previos. Se indica la suplementación farmacológica con niveles inferiores a 20 ng/ml.
Hay que monitorizar la vitamina B12, especialmente si el paciente está en tratamiento con
metformina.
3.6. Vacunación
Se recomienda la vacunación contra el virus de hepatitis B en pacientes entre 19 y 59 años
(pudiendo considerarse su administración también a partir de los 60 años), ya que la incidencia de su
infección se encuentra aumentada en DM1 y DM2. Se recomienda la vacunación anual contra el virus de la
gripe y antineumocócica en mayores de 65 años.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1150]
[70] DIABETES MELLITUS. MANEJO A LARGO PLAZO
X. DIABETES GESTACIONAL
La diabetes gestacional se define como toda intolerancia a los hidratos de carbono diagnosticada
por primera vez durante el embarazo, independientemente de la necesidad de tratamiento insulínico, del
grado de trastorno metabólico o de su persistencia una vez finalizada la gestación. Constituye la alteración
metabólica que más frecuentemente se asocia al embarazo, afectando al pronóstico de la madre y al de su
futuro hijo. Además, aumenta el riesgo de desarrollar DM2 a lo largo de la vida.
1. DIAGNÓSTICO
Según las guías de la ADA de 2016 hay dos estrategias para el diagnóstico de la diabetes
gestacional:
El diagnóstico puede ser realizado a través de dos distintas estrategias, que deben ser realizadas
entre las semanas 24-28 en mujeres embarazadas sin diagnóstico previo de diabetes.
La primera, consiste en una sola etapa, con una prueba de tolerancia oral a glucosa con una carga
de 75 g; y la segunda estrategia consiste en dos etapas, con un carga oral de glucosa de 50 g (sin ayunas)
seguida de una prueba de tolerancia oral a la glucosa con una carga de 100 g.
En la primera estrategia, la DM gestacional es confirmada si los niveles de glucosa en sangre son
superiores a:
92 mg/dL en ayunas.
180 mg/dL tras 1 hora.
153 mg/dL tras 2 horas.
En la segunda estrategia, si el nivel de glucosa en plasma tras 1 hora de recibir la carga de 50 g es ≥
a 140 mg/dL, se debe proceder a la prueba de tolerancia oral a la glucosa con una carga de 100 g.
El diagnóstico de DM gestacional se confirma si al menos dos de los siguientes valores de glucosa
en sangre son alcanzados o superados:
En ayunas: 95 mg/dL (Carpenter/Coustan) o 105 mg/dL (NDDG).
Tras 1 hora: 180 mg/dL (Carpenter/Coustan) o 190 mg/dL (NDDG).
Tras 2 horas: 155 mg/dL (Carpenter/Coustan) o 165 mg/dL (NDDG).
Tras 3 horas: 140 mg/dL (Carpenter/Coustan) o 145 mg/dL (NDDG).
Para mujeres embarazadas con factores de riesgo, se deben realizar pruebas en la primera visita
prenatal, utilizando criterios diagnósticos estándares.
Para mujeres con diabetes mellitus gestacional, se recomienda llevar a cabo las pruebas para
diabetes persistente entre 6-12 semanas posparto utilizando la prueba de tolerancia oral a la glucosa y
criterios diagnósticos estándares.
Las mujeres con una historia de diabetes gestacional deben ser sometidas a pruebas diagnósticas
de diabetes al menos a cada 3 años.
Las mujeres con historia de diabetes gestacional diagnosticadas con pre-diabetes deben realizar
cambios en su estilo de vida o tratamiento profiláctico con metformina.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1151]
[70] DIABETES MELLITUS. MANEJO A LARGO PLAZO
2. MANEJO
En el 80% de los casos es posible controlar la glucemia con cambios en la alimentación y estilo de
vida. En caso de precisar tratamiento farmacológico, el más empleado es la insulina. Todas las insulinas se
clasifican como categoría B en el embarazo (excepto glargina, glulisina y degludec, que se clasifican como
categoría C).
Existen estudios que demuestran eficacia y seguridad a corto plazo de metformina y glibenclamida
en el embarazo (ambas de categoría B). Sin embargo, ambas atraviesan la placenta y no se dispone de
datos de seguridad sobre los efectos en el feto a largo plazo. Los objetivos de control glucémico en la mujer
embarazada con DG son:
En ayunas ≤ 95 mg/dL.
1 hora posprandial ≤ 140 mg/dL.
2 horas posprandial ≤ 120 mg/dL.
Si no es posible alcanzar estos objetivos sin hipoglucemias significativas, se establecerán objetivos
de glucemia más elevados individualizando en cada caso. Hay que tener en cuenta que durante el primer
trimestre existe mayor riesgo de hipoglucemia y que las necesidades de insulina decrecen rápidamente tras
el alumbramiento. Existe también mayor riesgo de cetoacidosis con niveles de glucemia menos elevados.
3. SEGUIMIENTO
A las 6-12 semanas posparto se debe realizar un test diagnóstico para descartar la DM2,
preferiblemente una sobrecarga oral (SOG, 75 g), aplicando los criterios diagnósticos para la población
general no gestante y realizando un seguimiento cada 1-3 años (con cualquiera de los métodos
diagnósticos: HbA1c, glucemia en ayunas, SOG: 75 g).
XI. DIABETES ESTEROIDEA
Uno de los efectos adversos más conocidos de la terapia con glucocorticoides (GC) es su efecto
deletéreo sobre el metabolismo de los hidratos de carbono. Exacerban la hiperglucemia en la práctica
totalidad de los pacientes con DM previa o precipitan la aparición de DM esteroidea en los pacientes sin
DM previa pero predispuestos a ella. La prevalencia de la DM esteroidea varía entre el 5 y el 25%, aunque
probablemente esté infradiagnosticada.
Los GC más utilizados son los de acción intermedia (prednisona y metilprednisolona). Tienen un
pico de acción a las 4-8 horas y una duración de aproximadamente 12-16 horas. La hiperglucemia inducida
por GC se caracteriza por una ausencia o mínima elevación de la glucemia en ayunas, con aumento de las
glucemias posprandiales, especialmente después de la comida. Esto supone hiperglucemia por la tarde y
noche.
1. DIAGNÓSTICO
El diagnóstico se establece igual que para la DM de otras etiologías. Sin embargo, en los pacientes
que reciben una única dosis matutina de GC de acción intermedia, las glucemias que ofrecen mayor
sensibilidad para el diagnóstico son la glucemia posprandial de la comida y la preprandial de la cena. Por
tanto, en este grupo de pacientes se deben monitorizar estas GC durante los 2-3 primeros días de
tratamiento.
2. MANEJO
El uso de agentes hipoglucemiantes orales queda reservado para las hiperglucemias leves (< 200
mg/dL) en pacientes sin diabetes conocida o con diabetes conocida y adecuadamente controlada.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1152]
[70] DIABETES MELLITUS. MANEJO A LARGO PLAZO
En el resto de situaciones la insulina es el tratamiento de elección. En pacientes sin tratamiento
previo con insulina puede comenzarse una dosis de NPH/NPL/bifásica (mezcla de insulinas de acción
intermedia y rápida) antes del desayuno. Estos preparados son los de elección, ya que mimetizan el perfil
de acción hiperglucemiante de los corticoides de acción intermedia. En los pacientes con corticoides de
larga duración son preferibles los análogos de insulina de larga duración: una dosis de insulina glargina,
glargina U 300 o degludec o dos dosis de insulina detemir; o bien la administración de dos dosis de insulina
NPH/NPL. Esto último es de elección en pacientes que reciben dos o más dosis de GC de acción intermedia,
debiendo distribuir la dosis de insulina total en 2/3 antes del desayuno y 1/3 antes de la cena. La
estimación de dosis se realizará en base a la tabla XIX.
XII. DIABETES EN EL ANCIANO
El envejecimiento poblacional, unido a la alta prevalencia de la DM en nuestro medio, resulta en un
incremento significativo de pacientes con DM a partir de la séptima década de la vida. La evidencia
científica en estos grupos de edad es escasa, aunque se admite que los objetivos han de ser diferentes a los
de la población general. Las estrategias terapéuticas han de tener en cuenta el riesgo aumentado de
hipoglucemias inadvertidas, de caídas, etc., así como el recorte de los beneficios a largo plazo por tratarse
de pacientes que en muchos casos han superado su esperanza de vida, o bien se encuentran en situación
de fragilidad importante (deterioro cognitivo, movilidad reducida, etc.). Existe cierto consenso en cuanto al
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1153]
[70] DIABETES MELLITUS. MANEJO A LARGO PLAZO
aumento del umbral de objetivos de glucemia y HbA1c, así como la retirada de fármacos en prevención
primaria en determinadas situaciones (Tabla XX).
BIBLIOGRAFÍA
American Diabetes Association. Management of hyperglycemia in type 2 diabetes, 2015: A patient-
centered approach. Diabetes Care. 2015;38:140-9.
American Diabetes Association. Standards of medical care in diabetes 2016. Diabetes Care. 2016;39
Suppl 1:S1-S112.
Arrieta F, Iglesias P, Pedro-Botet J, et al. Diabetes mellitus y riesgo cardiovascular: recomendaciones
del Grupo de Trabajo Diabetes y Enfermedad Cardiovascular de la Sociedad Española de Diabetes
(SED, 2015). Clin Invest Arterioscl. 2015;05:002.
Bennett WL, Maruthur NM, Singh S, et al. Comparative effectiveness and safety of medications for type
2 diabetes: an update including new drugs and 2-drug combinations. Ann Intern Med.
2011;154(9):602-13.
Inzucchi SE, Bergenstal RM, Buse JB, et Al. Management of hyperglycaemia in type 2 diabetes: A
patient-centered approach. Position statement of the American Diabetes Association (ADA) and the
European Association for the Study of Diabetes (EASD). Diabetologia. 2012;55:1577-96.
Kasper DL, Braunwald E, Fauci AS, et al. Harrison's principles of internal medicine. En: Jameson L,
Isselbacher KJ, editores. 18th ed. Ed. McGraw-Hill; 2011.
Menéndez Torre E, Tartón García T, Ortega Millán C, et al. Recomendaciones 2012 de la Sociedad
Española de Diabetes sobre la utilización de tiras reactivas para la medición de glucemia capilar en
personas con diabetes. Av Diabetol. 2012;28(1):3-9.
Mezquita-Raya P, Reyes García R, Moreno Pérez O, et al. Documento de posicionamiento: evaluación y
manejo de la hipoglucemia en el paciente con diabetes mellitus. Grupo de Trabajo de Diabetes Mellitus
de la Sociedad Española de Endocrinología y Nutrición. Endocrinol Nutr. 2013;60(9):517.e1-517.e18.
Mikhail N. Place of sodium-glucose co-transporter type 2 inhibitors for treatment of type 2 diabetes.
World J Diabetes. 2014;5(6):854-9.
Phung OJ, Scholle JM, Talwar M, Coleman CI. Effect of noninsulin antidiabetic drugs added to
metformin therapy on glycemic control, weight gain, and hypoglycemia in type 2 diabetes. JAMA. 2010
Apr 14;303(14):1410-8.
Saigí I, Pérez A. Manejo de la hiperglucemia inducida por corticoides Rev Clin Esp. 2010;210(8):397-
403.
Skyler JS, Bergenstal R, Bonow RO, et al. American Diabetes Association; American College of
Cardiology Foundation; American Heart Association. Intensive glycemic control and the prevention of
cardiovascular events: Implications of the ACCORD, ADVANCE, and VA Diabetes Trials: A position
statement of the American Diabetes Association and a scientific statement of the American College of
Cardiology Foundation and the American Heart Association. Diabetes Care. 2009;32:187-92.
Soriguer F, Goday A, bosch-Comas A, et al. Prevalence of diabetes mellitus and impaired glucose
regulation in Spain: the Di@bet.es Study. Diabetologia. 2012;55(1):88-93.
Type 1 diabetes through the life span: A position statement of the American Diabetes Association.
Diabetes Care. 2014;37:2034-54.
Wei N, Zheng H, Nathan DM. Empirically establishing blood glucose targets to achieve HbA1c goals.
Diabetes Care. 2014;37:1048-51.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1154]
[71] COMPLICACIONES AGUDAS DE LA DIABETES
71.Complicaciones agudas de la diabetes
Carlos Patricio Silva Vaca.
Endocrinología
Noelia García-Pozuelo Adalia.
Medicina Interna
Asesora:
Elena García Fernández.
Médica Adjunta de Endocrinología
I. CETOACIDOSIS DIABÉTICA Y SÍNDROME HIPERGLUCÉMICO
HIPEROSMOLAR
1. ETIOPATOGENIA
La cetoacidosis diabética (CAD) y el síndrome hiperglucémico hiperosmolar (SHH), también llamado
hiperglucemia no cetósica, son dos de las complicaciones más importantes de la diabetes mellitus (DM).
La cetoacidosis diabética está asociada característicamente con la DM tipo 1, pero también puede
ocurrir en la de tipo 2 bajo condiciones de estrés extremo (infección grave, traumatismo o isquemia
cardiaca) y con menor frecuencia como debut (síndromes con tendencia a la acidosis, Ketone Prone
Diabetes).
La CAD es más frecuente en pacientes jóvenes (< 65 años), mientras que el SHH aparece
predominantemente en individuos > 65 años. La mortalidad en las crisis hiperglucémicas se debe
principalmente a las enfermedades precipitantes y raramente a las complicaciones metabólicas de la
hiperglucemia o la cetoacidosis. El pronóstico de una crisis hiperglucémica es significativamente peor en los
extremos de edad y ante la presencia de coma e hipotensión.
A veces, es difícil distinguir entre el debut de una DM tipo 1 o 2, por lo que, dado el potencial riesgo
de la CAD, debería iniciarse el tratamiento con insulina indistintamente en todo paciente con estado
catabólico, cetonuria o acidosis.
Las causas fundamentales son una deficiencia en la secreción de insulina con o sin aumento de la
resistencia a la misma y un exceso de hormonas contrainsulares (glucagón, catecolaminas y cortisol), lo que
estimula la lipólisis, incrementando la llegada al hígado de ácidos grasos libres y su transformación en
cuerpos cetónicos (acetoacético y betahidroxibutírico).
Parece que, para inhibir la lipólisis, la concentración de insulina necesaria es una décima parte de la
requerida para producir la captación periférica de glucosa, por tanto, la reserva insulínica de pacientes con
DM tipo 2 suele ser suficiente para bloquear la lipólisis y, por tanto, la formación de cetoácidos, pero no
para impedir la hiperglucemia.
Las crisis hiperglucémicas son estados proinflamatorios que generan elevación de las citoquinas y
de los factores procoagulantes, como TNF-alfa y la proteína C reactiva (PCR), lo que explica la asociación
con la hipercoagulabilidad. Estos factores vuelven a sus niveles normales 24 horas después del inicio de la
terapia insulínica y la remisión de la hiperglucemia.
La razón por la que la hiperglucemia es menor en la CAD que en el SHH es porque la acidosis
produce síntomas antes que la hiperosmolaridad, por ello los pacientes con CAD acuden a consulta antes.
Por otra parte, los pacientes con CAD tienden a ser más jóvenes y suelen tener una tasa de filtrado
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1155]
[71] COMPLICACIONES AGUDAS DE LA DIABETES
glomerular mayor, con mayor capacidad para excretar la glucosa por orina, limitando el grado de
hiperglucemia.
Los factores precipitantes de la CAD y del SHH se recogen en la tabla I.
2. DIAGNÓSTICO
Aunque la tabla II recoge los criterios diagnósticos propuestos por la American Diabetes Association
(ADA) para diferenciar entre la CAD y el SHH, así como los diferentes grados de este último, en más de un
tercio de los pacientes pueden superponerse algunos de los hallazgos. Tanto la CAD como el SHH son
emergencias médicas que deben ser identificadas y tratadas de forma precoz.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1156]
[71] COMPLICACIONES AGUDAS DE LA DIABETES
1. HISTORIA CLÍNICA
La CAD generalmente se desarrolla rápidamente, en unas 24 horas, mientras que en el SHH los
síntomas aparecen de forma insidiosa con poliuria, polidipsia y pérdida de peso varios días antes y
posteriormente van apareciendo los síntomas neurológicos que incluyen letargia, síntomas neurológicos
focales y muy raramente coma.
El dolor abdominal asociado a náuseas y vómitos se correlaciona con la gravedad de la acidosis
metabólica, pero no con la hiperglucemia o deshidratación, por lo que aparece de forma casi exclusiva en la
CAD. Se cree que es debido a un retraso en el vaciamiento gástrico o íleo paralítico inducido por la acidosis
y las alteraciones electrolíticas. Es preciso buscar otras causas si se presenta en ausencia de acidosis
metabólica grave o persiste tras la resolución de la misma.
La existencia de estupor o coma en un paciente con SHH en ausencia de una elevación de la
osmolalidad efectiva (> 320 mOsm/kg) requiere la consideración inmediata de otras causas de deterioro
neurológico. La disminución del nivel de consciencia también puede ocurrir en pacientes con CAD que
presentan un menor grado de hiperosmolalidad si existe acidosis severa.
2. EXPLORACIÓN FÍSICA
Una evaluación inicial debe centrarse en reconocer: a) signos vitales básicos, b) datos de depleción
de volumen (sequedad cutáneo mucosa, presión venosa yugular baja, hipotensión), c) nivel de consciencia
(desde la obnubilación hasta el coma e incluir en el caso de SHH síntomas neurológicos focales o crisis
comiciales), d) posibles precipitantes.
Los pacientes con CAD pueden desprender un olor afrutado por la exhalación de acetona y
presentar respiración de Kussmaul (patrón de respiraciones profundas que reflejan hiperventilación) como
mecanismo compensador de la acidosis. Por la vasoconstricción periférica (hallazgo frecuente) la fiebre es
rara incluso en presencia de infección.
3. EXPLORACIONES COMPLEMENTARIAS
La evaluación inicial de laboratorio de un paciente en el que se sospecha CAD o SHH debe incluir la
determinación de:
Glucemia plasmática.
Electrolitos en suero (calcular el anión GAP), nitrógeno ureico en sangre (BUN) y creatinina
plasmática.
Hemograma completo con recuento diferencial.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1157]
[71] COMPLICACIONES AGUDAS DE LA DIABETES
Sistemático y sedimento de orina y medición de cuerpos cetónicos en tira de orina.
Osmolalidad plasmática.
Cuerpos cetónicos en plasma (si los cuerpos cetónicos en orina son positivos).
Gasometría arterial si el bicarbonato sérico está sustancialmente disminuido o si se sospecha
hipoxia.
Electrocardiograma.
Otros exámenes adicionales como la radiografía de tórax, el urocultivo, los hemocultivos y los
cultivos de esputo, deben ampliarse según la clínica (Tabla III). La HbA1c no es útil para determinar el grado
de control previo puesto que los niveles tan elevados de glucemia que existen durante el episodio de CAD
glicosilan la hemoglobina, alterando su valor total (ver Capítulo 70. “Diabetes mellitus. Manejo a largo
plazo”).
4. HALLAZGOS DE LABORATORIO
La hiperglucemia y la hiperosmolalidad son los dos hallazgos de laboratorio principales en pacientes
con CAD o SHH; los pacientes con CAD también presentan una acidosis metabólica con anión GAP elevado.
El impacto de la hiperglucemia, el déficit de insulina, la diuresis osmótica y la ingesta de líquidos en cada
individuo determinan hallazgos de laboratorio variables, en función de su importancia relativa.
4.1. Bioquímica
Glucemia
La concentración de glucosa en plasma frecuentemente excede los 1.000 mg/dL en el SHH,
pero suele ser menor de 800 mg/dL y con frecuencia entre 350-500 mg/dL aproximadamente
en la CAD. En algunas situaciones especiales como desnutrición o embarazo, o si el tratamiento
con insulina se inicia antes de la llegada a Urgencias, la glucosa puede estar solo levemente
elevada (cetoacidosis euglucémica). Estos pacientes igualmente precisan insulina para corregir
la acidosis.
Cuerpos cetónicos
En la CAD se producen y se acumulan tres cuerpos cetónicos: el ácido acetoacético (el único
cetoácido verdadero), el ácido betahidroxibutírico (un hidroxiácido formado por la reducción
del ácido acetoacético) y la acetona (se deriva de la descarboxilación del ácido acetoacético).
La acetona es una cetona verdadera, pero químicamente se comporta de forma neutra.
Osmolalidad plasmática
Los pacientes con síntomas neurológicos suelen presentar cifras de 320 a 330 mOsm/kg (Tabla
III). La hiperosmolaridad en el SHH se debe más a la diuresis osmótica producida por la
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1158]
[71] COMPLICACIONES AGUDAS DE LA DIABETES
glucosuria, que conlleva pérdida de sodio y potasio, que a la propia hiperglucemia. Esto explica
que los pacientes con insuficiencia renal crónica avanzada puedan presentar hiperglucemias
severas con escasos síntomas neurológicos.
La osmolalidad plasmática efectiva es la fracción de la osmolalidad total que se genera por las
sales de sodio y glucosa (Tabla III). El valor del sodio empleado es el medido en el plasma y no
el corregido.
Sodio sérico
Es variable, refleja el balance entre la dilución del sodio debida a la salida del agua intracelular y
la concentración debida a la diuresis osmótica inducida por la glucosuria. La mayoría de los
pacientes con CAD y SHH tienen una hiponatremia leve. Sin embargo, los pacientes con SHH
que tienen una importante diuresis osmótica pueden tener niveles normales o incluso elevados
de sodio (a pesar de la hiperglucemia severa), por lo que a menudo tienen síntomas
neurológicos.
Hay que corregir los niveles de sodio (Tabla III) añadiendo 1,6 mg/dL a la cifra medida por cada
100 mg/dL de glucosa por encima de 100 mg/dL.
Pseudohiponatremia/Pseudohipercloremia
Algunos pacientes con diabetes descontrolada desarrollan una marcada hiperlipidemia y
presentan un suero lipémico.
En función del tipo de analizador utilizado, la hiperlipidemia puede generar artefactos en la
medición de electrolitos. Desplaza el agua y reduce su fracción en el plasma por debajo del
valor normal (93%), analizándose así menos agua y electrolitos, generando
pseudohiponatremia. En relación a la concentración del cloro, ocurre un efecto contrario, lo
que se traduce en una hipercloremia marcada.
Potasio sérico
Tanto en la CAD como en el SHH suele haber un déficit de potasio de 3 a 5 mEq/kg debido,
sobre todo, a las pérdidas por la diuresis osmótica. A pesar de ello, el potasio sérico es normal
al ingreso o está incluso elevado en un tercio de pacientes, por varios mecanismos: el agua sale
de las células para tratar de compensar la hiperosmolaridad plasmática arrastrando el potasio,
la existencia de un déficit de insulina (que promueve la captación de potasio por las células) y el
intercambio por hidrogeniones a través de bombas de membrana para compensar la acidosis.
El tratamiento con insulina vuelve a introducir el potasio dentro de las células y puede causar
hipopotasemia severa, sobre todo, en pacientes que parten de unos niveles normales o bajos,
por lo que es esencial su monitorización y añadir al tratamiento aportes de potasio
intravenosos.
Fosfato sérico
Los pacientes con hiperglucemia descontrolada típicamente presentan un balance de fosfato
negativo debido a la ingesta reducida, al movimiento de fosfato al espacio extracelular
secundario, a la acidosis metabólica y a la fosfaturia causada por la diuresis osmótica. A pesar
de la depleción de fosfato, su concentración inicial suele ser normal o incluso alta puesto que,
tanto la deficiencia de insulina como la acidosis metabólica, determinan su movimiento fuera
de las células al igual que por la contracción del volumen extracelular. Este movimiento
transcelular es revertido y presenta el verdadero estado del balance del fosfato
desenmascarado después del tratamiento con insulina y fluidos.
Creatinina sérica
La mayoría de los pacientes presentan elevaciones agudas del BUN y la concentración de la
creatinina sérica, lo que refleja un descenso en la tasa de filtrado glomerular inducida por la
hipovolemia. Inicialmente la creatinina se eleva de forma desproporcionada a la caída del
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1159]
[71] COMPLICACIONES AGUDAS DE LA DIABETES
filtrado glomerular.
Cuando existe cetoacidosis, la creatinina sérica puede estar falsamente elevada si se utilizan
ciertos análisis colorimétricos para su determinación debido a los altos niveles de acetoacetato.
Sin embargo, actualmente la mayoría de los laboratorios utilizan análisis enzimáticos que no se
ven afectados por este artefacto.
Amilasa y lipasa
Aunque la pancreatitis aguda puede precipitar una CAD, la amilasa y la lipasa pueden estar
elevadas en ausencia de la misma, por lo que el diagnóstico de pancreatitis aguda debe basarse
en la clínica y en los hallazgos de la tomografía computarizada (TC) abdominal.
No está clara la fuente de estas enzimas; parece que la amilasa es con más frecuencia de origen
salival, pero también puede ser pancreática.
El aumento de la amilasa se correlaciona con el pH y la osmolalidad plasmática, mientras que el
incremento de la lipasa se correlaciona solamente con la osmolalidad plasmática. Los valores se
normalizan dentro de las primeras 24 horas iniciales.
Perfil lipídico
La insulina es antilipolítica y su déficit se combina con niveles elevados de hormonas lipolíticas
(catecolaminas, GH, ACTH y glucagón), lo que conduce al acúmulo de ácidos grasos libres y
aumento sérico de colesterol y triglicéridos, pudiendo encontrarse incluso suero lipémico.
4.2. Hemograma
La mayoría de los pacientes con crisis hiperglucémicas presentan leucocitosis. La leucocitosis es
proporcional al grado de cetonemia y se correlaciona con la secreción de cortisol y catecolaminas. Sin
embargo, si es mayor de 25.000 células por microlitro o presenta más del 10% de cayados, es sugerente de
infección. Existirá elevación del hematocrito por la hemoconcentración.
4.3. Cuerpos cetónicos en orina
En la CAD se producen dos cetoácidos (ácido betahidroxibutírico, más abundante, y ácido
acetoacético) y una cetona neutra (acetona). Las tiras reactivas urinarias no reaccionan con los derivados
del ácido betahidroxibutírico, por lo que es posible un falso negativo. Ante esta posibilidad una solución es
añadir a la muestra de orina unas gotas de peróxido de hidrógeno (agua oxigenada) lo que lo convierte en
acetoacetato. Fármacos que lleven el grupo sulfhidrilo, como captopril o penicilamina, pueden dar falsos
positivos.
4.4. Gasometría arterial
El bicarbonato sérico en la CAD está muy disminuido mientras que en el SHH se encuentra normal o
ligeramente disminuido. En la CAD existe siempre una acidosis metabólica con anión GAP elevado (suele ser
mayor de 20) por acúmulo de cetoácidos.
3. DIAGNÓSTICO DIFERENCIAL
Debe hacerse junto con otras causas de cetoacidosis en las que la glucemia suele estar baja
(alcohólica o por inanición), acidosis con anión GAP elevado, sin elevación de cuerpos cetónicos (ver
Capítulo 64. “Interpretación gasométrica. Trastornos del equilibrio ácido-base”) y otras causas de
encefalopatía metabólica (Tabla IV).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1160]
[71] COMPLICACIONES AGUDAS DE LA DIABETES
4. TRATAMIENTO
El tratamiento para la CAD y el SHH es similar (Figura 1). En ambos casos es importante identificar y
tratar el factor precipitante.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1161]
[71] COMPLICACIONES AGUDAS DE LA DIABETES
1. MEDIDAS GENERALES
Asegurar un adecuado acceso venoso, si es posible mediante catéter venoso central de
inserción periférica (por ejemplo, drum) o vía venosa central para poder medir la presión
venosa.
Control estricto y horario de la glucemia y diuresis, y cada 2-4 horas control de iones, gases
venosos y osmolalidad.
Valoración por la Unidad de Cuidados Intensivos (UCI) en caso de hipotensión, anasarca,
comorbilidad que dificulte el manejo, enfermedad grave como desencadenante o mala
evolución.
2. FLUIDOTERAPIA
El déficit medio de fluidos es de 3 a 6 litros en la CAD y de 8 a 10 litros en el SHH. El objetivo del
tratamiento es reponer el líquido extracelular sin producir edema cerebral a causa la reducción demasiado
rápida de la osmolalidad.
La reposición debe hacerse en aproximadamente 24 horas.
En las primeras dos horas:
Se iniciará con suero salino isotónico que corrige la depleción del volumen más
rápidamente que el hipotónico, disminuye la osmolaridad y reduce la concentración de
glucosa por dilución. Además, aumentan las pérdidas urinarias al mejorar la perfusión
renal.
Si no existe insuficiencia cardiaca, el ritmo debe ser de aproximadamente 1.000 ml/h.
Se infundirá lo más rápidamente posible en los pacientes en situación de shock.
A partir de las primeras dos horas:
El tipo de suero para continuar con la reposición depende del estado de hidratación, los
niveles de sodio en sangre y la diuresis.
Natremia normal o elevada, se cambiará a suero salino hipotónico al 0,45%.
Si el sodio sérico está bajo, se puede continuar con suero salino al 0,9%.
Si se requieren aportes de potasio superiores a 40 mEq/l, es preferible utilizar suero
salino hipotónico, pues la adición de esos mEq de potasio al suero isotónico, crearía un
fluido hipertónico que no corregiría la hiperosmolaridad.
Ritmo: el ritmo adecuado es de 250 a 500 ml/h (debe individualizarse en función de la
edad y comorbilidades del paciente). En pacientes con insuficiencia renal o cardiaca la
reposición debe ser más cuidadosa para evitar yatrogenia y a veces requiere el manejo
en la UCI.
Se añadirá suero glucosado al 5% al tratamiento cuando se alcancen glucemias de 200
mg/dL en CAD y de 250-300 mg/dL en el SH. Mantener esas cifras de glucemia hasta
que mejore la hiperosmolalidad, el nivel de consciencia y el paciente esté estable.
3. POTASIO
El cambio en la distribución del potasio corporal revierte rápidamente tras la administración de
insulina con una caída brusca en las concentraciones séricas, siendo esencial la monitorización durante el
tratamiento. Para prevenir la hipopotasemia deben añadirse 20 a 30 mEq/l a la sueroterapia en cuanto el
potasio sérico disminuya por debajo de 5,3 mEq/l y la diuresis sea adecuada (> 50 ml/h), para mantener
unos niveles séricos de 4 a 5 mEq/l. Si el potasio está por debajo de 3,3 mEq/l, debe retrasarse o
suspenderse la perfusión de insulina para evitar posibles arritmias, paro cardiaco o debilidad de la
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1162]
[71] COMPLICACIONES AGUDAS DE LA DIABETES
musculatura respiratoria. En estos pacientes lo más urgente es la reposición del potasio, aportando de 20 a
30 mEq/h en suero salino hipotónico al 0,45% para no agravar la situación hiperosmolar.
4. INSULINOTERAPIA
Tras el inicio de la reposición del volumen, la única indicación para retrasar la insulinoterapia es la
existencia de un potasio sérico menor de 3,3 mEq/l, ya que este induciría el paso del potasio al espacio
intracelular y agravaría la hipopotasemia.
La infusión continua intravenosa de insulina regular es el tratamiento de elección del SHH y la CAD
moderada o grave (50 UI de insulina regular en 500 ml de suero salino fisiológico para tener una dilución de
0,1 UI/ml).
Se iniciará a un ritmo de 0,14 UI/kg/h o con un bolo de 0,1 UI/kg, seguido de una perfusión a 0,1
UI/kg/h. Las dosis más altas en general no producen un efecto hipoglucemiante más prominente,
posiblemente porque los receptores de la insulina están completamente saturados.
El ritmo de descenso de la glucemia deseado es de 50-70 mg/dL/h. En caso de no alcanzarse, se
debe valorar si hay algún problema en el acceso venoso, y doblar la velocidad de la perfusión cada hora
hasta que se consiga un descenso estable en la glucemia plasmática.
En pacientes con SHH la caída en la glucemia puede ser más pronunciada con la reposición del
volumen debido a la gran hemoconcentración. Cuando la glucemia alcanza los 200 mg/dL en la CAD o 250 a
300 mg/dL en el SHH, debe añadirse al tratamiento suero glucosado al 5%, a un ritmo de 125-250 ml/h y
reducir la perfusión de insulina a 0,02-0,05 UI/kg/h (para 70 kg: 1,4 a 3,5 UI/h = 14 a 35 ml/h de la
perfusión). La reducción en este punto de la glucemia por debajo de 200 mg/dL en la CAD y por debajo de
250 mg/dL en el SHH, puede provocar el desarrollo de edema cerebral. El objetivo es mantener la glucemia
en 200 mg/dL en la CAD y entre 200 y 300 mg/dL en el SHH hasta que se resuelva la crisis hiperglucémica.
Si nos encontrarnos fuera del medio hospitalario o es imposible canalizar una vía venosa, existiría la
posibilidad de iniciar el tratamiento de la CAD con insulina rápida intramuscular o subcutánea, pero la
absorción es errática en pacientes en situación de shock, por lo que la vía intravenosa será siempre
preferible.
El tratamiento con análogos de insulina de acción rápida por vía subcutánea cada 1-2 horas, ha
demostrado ser efectivo y seguro en la CAD leve, pero en la práctica clínica habitual se sigue prefiriendo la
insulina regular intravenosa por su efecto más controlable (Figura 1).
5. BICARBONATO
El bicarbonato en las indicaciones para la CAD son controvertidas y no hay evidencias claras de sus
beneficios, ya que puede conllevar importantes efectos indeseados: a) puede aumentar la pCO2 (ya que la
acidosis estimula la hiperventilación) y producir una caída paradójica del pH cerebral (el CO2 es muy
liposoluble y atraviesa fácilmente la barrera hematoencefálica), provocando un deterioro neurológico; b)
puede ralentizar la recuperación de la cetosis, ya que algunos estudios en animales sugieren que el
bicarbonato estimula la cetogénesis hepática; c) puede conducir a una alcalosis metabólica postratamiento,
ya que la metabolización de los cetoácidos tras el tratamiento con insulina genera bicarbonato que
espontáneamente corrige la acidosis. Por tanto, el tratamiento con bicarbonato deber reservarse para:
Pacientes con pH arterial < 6,9, pues existe riesgo de depresión miocárdica, vasodilatación
cerebral, coma y complicaciones gastrointestinales.
Pacientes con hiperpotasemia grave.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1163]
[71] COMPLICACIONES AGUDAS DE LA DIABETES
Si el pH es < 6,9, se administrarán 100 mEq de bicarbonato sódico (bicarbonato 1 Molar, vial de 250
mEq/250 ml, 1 mEq/ml), diluido en 400 ml de agua estéril o de suero salino hipotónico al 0,45% con 20 mEq
de cloruro potásico a pasar en 2 horas. Se repetirá la misma infusión cada 2 horas hasta que el pH sea > 7,0.
Conforme la concentración de bicarbonato aumenta puede disminuir el potasio sérico y se puede
necesitar su reposición de forma más enérgica.
6. FOSFATO
Al igual que ocurre con el potasio, hay un déficit total enmascarado que se pone de manifiesto con
el tratamiento insulínico. La hipofostatemia suele ser asintomática y autolimitada. Solo debe plantearse el
tratamiento, añadiendo 20-30 mEq/l de fosfato potásico (fosfato monopotásico ampollas 1 M de 10 ml) a
los sueros en:
Pacientes con cifras de fosfato sérico menores de 1,0 g/dL, especialmente si existe disfunción
cardiaca, anemia hemolítica y/o depresión respiratoria.
5. MONITORIZACIÓN GENERAL
La glucemia debe medirse inicialmente cada hora hasta que el descenso sea estable, mientras que
los electrolitos, la urea, la creatinina y el pH venoso (en el caso de una CAD) debe medirse cada 2-4 horas
dependiendo de la severidad de la crisis aguda y de la respuesta clínica.
Se recomienda la utilización de una tabla con un formato prediseñado con todos estos parámetros
para facilitar la visualización y la evaluación de la evolución del cuadro clínico del paciente.
En la CAD no es necesario repetir la gasometría arterial dado que el pH venoso (0,03 unidades por
debajo del arterial) es adecuado para evaluar la respuesta al tratamiento y evitar el dolor y las
complicaciones potenciales de varias punciones arteriales repetidas.
La crisis hiperglucémica se considera resuelta cuando:
La glucosa capilar se mantiene por debajo de 200 mg/dL en la CAD o entre 250 y 300 mg/dL en
el SHH.
En la CAD se ha corregido la acidosis:
el anión GAP es < 12 mEq/l,
el bicarbonato sérico es ≥ 18 mq/l,
el pH venoso es > 7,35.
En el SHH el paciente está mentalmente alerta y la osmolalidad plasmática es < 315 mOsm/kg.
El paciente es capaz de tolerar la alimentación por vía oral.
Si el paciente no es capaz de alimentarse por vía oral, es preferible continuar con la perfusión. En
pacientes diabéticos ya insulinizados se iniciará el tratamiento con insulina subcutánea a su dosis habitual.
En pacientes sin tratamiento previo con insulina se iniciará un régimen multidosis a 0,5-0,8 UI/kg/día
dividido en insulina basal y bolos preprandiales de insulina rápida o ultrarrápida a las dosis habituales (ver
Capítulo 70. “Diabetes mellitus. Manejo a largo plazo”).
La perfusión intravenosa de insulina debe continuar hasta 2 horas después de iniciar la insulina
subcutánea, pues su suspensión brusca puede conducir a la recurrencia de la hiperglucemia y la
cetoacidosis.
6. COMPLICACIONES DEL TRATAMIENTO
Las más frecuentes son la hipoglucemia y la hipopotasemia.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1164]
[71] COMPLICACIONES AGUDAS DE LA DIABETES
La hiperglucemia se produce por la interrupción de la perfusión de la insulina sin haber iniciado
previamente el tratamiento con insulina subcutánea.
El edema cerebral es casi exclusivo en pacientes menores de 20 años, sobre todo, niños. Los
síntomas suelen aparecen a las 12-24 horas del inicio del tratamiento. La cefalea es la primera
manifestación, seguida de letargia y deterioro neurológico progresivo con convulsiones, incontinencia
urinaria, alteraciones pupilares, bradicardia y paro respiratorio. Estos síntomas pueden progresar si se
produce una herniación del tronco del encéfalo, llegando a ser tan rápido que no alcance a desarrollarse
papiledema.
Tiene una mortalidad del 20-40%. Es imprescindible la monitorización continua del estado
neurológico del paciente para realizar un diagnóstico y tratamiento precoces.
Las medidas preventivas para reducir el riesgo de edema cerebral son:
La reposición gradual del déficit de agua y sodio en pacientes con estado hiperosmolar. Se inicia
con suero salino al 0,9% a un ritmo de 1.000 ml/h, pero sin sobrepasar los 50 ml/kg en las
primeras 4 horas (3.500 ml en un paciente de 70 kg).
La administración de bicarbonato sódico únicamente en los casos indicados previamente.
Una vez instaurado el edema cerebral, el tratamiento se basa en la administración de manitol (0,25
a 1 g/kg) y suero salino hipertónico al 3% (5 a 10 ml/kg en 30 minutos) para inducir un movimiento
osmótico de agua fuera del cerebro. Estas recomendaciones se basan en la experiencia clínica en pacientes
pediátricos dada la falta de evidencia en adultos.
Hipoxemia y edema pulmonar no cardiogénico durante el tratamiento de la CAD, atribuidos a una
reducción en la presión oncótica que produce paso de agua del intersticio pulmonar a los alveolos. Los
pacientes con CAD que presentan un gradiente alveolo-arterial elevado, objetivado en la gasometría, o
crepitantes en la exploración física presentan un mayor riesgo de desarrollar un edema agudo de pulmón.
II. TRATAMIENTO DE LA HIPERGLUCEMIA EN PACIENTE
HOSPITALIZADO
1. INTRODUCCIÓN
La hiperglucemia no controlada, además de ser un marcador de gravedad, ocasiona importantes
efectos adversos, que influyen tanto en el pronóstico como en un aumento de la mortalidad, del riesgo de
infección y de la estancia hospitalaria. Las principales causas de un control glucémico deficiente en el
paciente hospitalizado son: a) inercia clínica: tolerancia de la hiperglucemia como medida de seguridad
frente a la hipoglucemia; b) falta de consideración del tratamiento previo del paciente; c) infrautilización de
perfusiones de insulina iv; d) sobreutilización de pautas deslizantes de insulina: corrección empleando
únicamente insulina rápida correctora sin insulina basal (deben evitarse dado su riesgo de hiper e
hipoglucemia).
2. OBJETIVOS DE CONTROL GLUCÉMICO
El control glucémico estricto en el paciente crítico (glucemias < 110 mg/dL), aumenta el riesgo de
hipoglucemia y conlleva mayor morbimortalidad. Los objetivos glucémicos deseados se describen en la
tabla V.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1165]
[71] COMPLICACIONES AGUDAS DE LA DIABETES
3. TRATAMIENTO
1. PACIENTES EN TRATAMIENTO CON ANTIDIABÉTICOS ORALES (ADO)
Lo ideal en pacientes bajo tratamiento con ADO es la suspensión de los mismos durante la estancia
hospitalaria, dado el riesgo de descontrol glucémico o acidosis láctica. En el caso de hospitalización
ambulatoria o ingresos de pacientes no quirúrgicos, se puede continuar el tratamiento previo, tomando en
consideración las contraindicaciones de los diferentes fármacos (ver Capítulo 70. “Diabetes mellitus.
Manejo a largo plazo”).
2. PACIENTES CON INSULINOTERAPIA SUBCUTÁNEA PREVIA
2.1. Pacientes con ingesta limitada
Si tratamiento insulínico previo con buen control: continuar con el 80% de la dosis de insulina
detemir o glargina, o con el 50-80% en el caso de insulina NPH.
Si se inicia tratamiento con insulina: insulina basal 0,2 UI/Kg/día + bolos correctores con
insulina ultrarrápida cada 4-6 horas (Tabla VI).
2.2. Pacientes con adecuada ingesta oral
Si tratamiento insulínico previo con buen control: continuar tratamiento habitual.
Inicio de tratamiento insulínico:
Cálculo de la dosis de insulina (Figura 2).
Se deberá distribuir la dosis total de insulina calculada en un 50% de la insulina basal y
el otro 50% en bolos preprandiales (desayuno, comida y cena). Los ajustes posteriores
se realizarán con las siguientes indicaciones:
Si solo está alterada la glucemia basal, se debe aumentar un 20% la insulina
basal.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1166]
[71] COMPLICACIONES AGUDAS DE LA DIABETES
Si solo está alterada la glucemia preprandial de una comida, hay que aumentar
un 10-20% la dosis del bolo prandial de la comida anterior.
Si todos los controles glucémicos están alterados, se deben sumar todas las
dosis correctoras del día previo y añadir un 50% del total necesitado a la
insulina basal.
Si presentara una glucemia basal < 70 mg/dL o durante todos los controles
glucémicos, se debe reducir un 20% la insulina basal.
En caso de que se objetivara una glucemia preprandial o antes de acostarse <
70 mg/dL, hay que reducir un 10-20% la dosis del bolo prandial de la comida
anterior.
3. INSULINOTERAPIA INTRAVENOSA
La insulinoterapia intravenosa se recomienda en pacientes con riesgo de cetosis:
Diabetes mellitus tipo 1.
Diabetes mellitus tipo 2 de más de 10 años de evolución con requerimientos de insulina desde
al menos 5 años.
Índice de masa corporal (IMC) < 25.
Historia de cetoacidosis, patología en las siguientes situaciones: paciente crítico, ayuno,
perioperatorio de cirugía mayor y descompensación hiperglucémica por tratamiento
corticoideo o nutrición parenteral.
3.1. Recomendaciones generales
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1167]
[71] COMPLICACIONES AGUDAS DE LA DIABETES
Se calcula la dosis de insulina diaria total a 0,3 UI/kg/día. La dosis de insulina intravenosa diaria
total será el 80% de la dosis calculada anteriormente. Dicha cantidad se divide entre cuatro para calcular la
cantidad de insulina intravenosa que se va administrar en cada 500 ml de suero glucosado (500 ml de SG al
5% cada 6 horas). En caso de que haya una limitación del volumen a administrar se contactará con el
Servicio de Endocrinología.
3.2. Ajuste de dosis
Se debe monitorizar la glucemia cada 6 horas antes de la perfusión de cada 500 ml de suero
glucosado al 5% y aplicar la pauta correctora modificada en función de la cantidad de insulina recibida al día
(Tabla VII).
3.3. Tratamiento de las hipoglucemias
Suspender la infusión de insulina. Administrar glucosa intravenosa (25-50 ml de SG al 50%) y
repetir en 10-20 minutos si continuara siendo menor de 60 mg/dL.
Una vez que la glucemia sea superior a > 100 mg/dL, se debe restaurar la infusión de insulina
con el algoritmo que se muestra en la figura 1.
III. HIPOGLUCEMIA
1. CONCEPTO
La hipoglucemia es un síndrome clínico debido a múltiples causas, no un diagnóstico en sí mismo.
Se debe definir por la presencia de la triada de Whipple:
Síntomas de hipoglucemia
Adrenérgicos o neurogénicos: se inician con niveles de glucosa plasmática < 60 mg/dL,
siendo la respuesta protectora inicial que induce la ingesta de hidratos de carbono. Se
manifiesta con ansiedad, sensación de calor, sudoración, hambre, taquicardia,
hormigueo y temblor.
Neuroglucopénicos: consecuencia de la deprivación de la glucosa al sistema nervioso
central. Las manifestaciones principales son: fatiga, mareo, cefalea, alteraciones
visuales, dificultad para hablar o concentrarse. Se inicia un déficit cognitivo con
glucemias plasmáticas < 35 mg/dL, observándose síntomas más severos como
obnubilación o letargia con glucosas de < 45-50 mg/dL, y coma cuando se alcanzan
cifras < 30 mg/dL, llegando a convulsiones o muerte con glucemias < 20 mg/dL.
Baja concentración de glucosa (glucosa en plasma venoso < 50 mg/dL o < 70 mg/dL si se trata
de un paciente diabético).
Mejoría de los síntomas tras la normalización en los niveles de glucemia.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1168]
[71] COMPLICACIONES AGUDAS DE LA DIABETES
2. ETIOLOGÍA
La búsqueda de la causa de la hipoglucemia en el paciente adulto debe realizarse en base al tipo de
paciente ya sea aparentemente sano, medicado o enfermo (Tablas VIII y IX).
3. DIAGNÓSTICO
Salvo en pacientes tratados con insulina o fármacos secretagogos de insulina, la aparición de la
hipoglucemia es un evento clínico raro. El proceso diagnóstico comienza con una anamnesis detallada en la
que se incluyan las características de los episodios sintomáticos, la duración, los síntomas específicos, los
factores desencadenantes, los fármacos y las comorbilidades.
Para considerar que la clínica se ha producido por una hipoglucemia deberá desaparecer en un
máximo de 10-15 minutos tras la corrección de la glucemia. En caso contrario, se deberán descartar otras
alteraciones metabólicas (insuficiencia suprarrenal), déficits neurológicos o coma poshipoglucémico por
edema cerebral.
Dentro del estudio etiológico se debe realizar una serie de análisis para detectar si existe
hiperinsulinismo endógeno.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1169]
[71] COMPLICACIONES AGUDAS DE LA DIABETES
Individuo previamente sano con hipoglucemia: determinación de la glucosa plasmática durante
el episodio, insulina, péptido C, proinsulina, betahidroxibutirato y agentes hipoglucemiantes
orales en plasma y orina.
Casos no concluyentes o en pacientes en los que no aparecen episodios espontáneos: está
indicada la realización del “test de ayuno de 72 horas” bajo el siguiente protocolo (Tabla X):
Anotar la fecha y la hora de la última ingesta. Suspender todas las medicaciones no
imprescindibles, solo se permitirán líquidos sin calorías y sin cafeína.
Asegurar una actividad física normal.
Recoger muestras de sangre cada 6 horas para glucosa, insulina, péptido C y proinsulina
hasta que la glucosa plasmática sea menor de 60 mg/dL. A partir de este momento, la
frecuencia de recogida de sangre será cada 2 horas (es posible durante este tiempo la
toma de glucosa capilar por reflectómetro, aunque estas cifras no determinan el fin de
la prueba).
Finalizar el test cuando la glucosa plasmática sea < 45 mg/dL; si es < 55 mg/dL
coincidiendo con signos o síntomas de hipoglucemia; si existe clínica neurológica
independientemente de la glucemia o se cumplen 72 horas desde su inicio.
Al finalizar el test, se recoge una muestra sanguínea para determinar sulfonilureas y
betahidroxibutirato. Se administra 1 mg de glucagón intravenoso para determinar la
glucemia a los 10, 20 y 30 minutos posglucagón.
4. TRATAMIENTO
El tratamiento del episodio agudo de hipoglucemia en pacientes con adecuado nivel de consciencia
se debe realizar mediante la ingesta oral de 10 g de glucosa (2 sobres o 2 cucharadas soperas de azúcar
disueltas en un vaso de agua, 175 ml de zumo o refresco).
En pacientes con alteración del nivel de consciencia hay que administrar 20-40 ml de glucosa al 50%
(Glucosmon®). En el medio extrahospitalario, una alternativa es la administración de glucagón 1 mg por vía
intramuscular o subcutánea. La mejoría del nivel de consciencia debe ser clara en menos de 10-15 minutos,
de no ser así se deberá repetir la dosis de glucosa intravenosa cada 15 minutos puesto que pueden persistir
síntomas de hipoglucemia una vez que esta se ha corregido, así evitaremos la administración de dosis
elevadas de glucosa.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1170]
[71] COMPLICACIONES AGUDAS DE LA DIABETES
Se deben repetir glucemias capilares cada 10 minutos y, si la glucemia se mantiene < 70mg/dL, se
deberá repetir la administración de glucosa. En caso de que la glucemia sea > 70 mg/dL, si el paciente tiene
un nivel de consciencia adecuado, se deben administrar 10 g de hidratos de carbono de absorción lenta (4
galletas, 20 g de pan o 250 ml de leche) para evitar nuevas hipoglucemias.
Si el paciente requiere ayuno prolongado o se prevé que la causa de la glucemia persistirá en el
tiempo (en caso de ADO –sulfonilureas y repaglinida pueden persistir hasta 48 horas– o insulinas de acción
larga), se debe iniciar fluidoterapia con suero glucosado al 5% o al 10% hasta que desaparezca la
hipoglucemia y mantener controles glucémicos cada 1-2 horas hasta obtener dos determinaciones
superiores a 150 mg/dL.
En hipoglucemias de difícil recuperación se pueden administrar 100 mg de hidrocortisona
intravenosa cada 6-8 horas ante la posibilidad de que se trate de una insuficiencia suprarrenal aguda.
El tratamiento de la hipoglucemia fuera del episodio agudo dependerá de la patología que la
produzca.
BIBLIOGRAFÍA
Alfaro Martínez JJ, Mora Escudero I. Hipoglucemia. Medicine. 2012;11(18):1089-95.
Cryer PE, Axelrod Ll, et al. Evaluation and management of adult hypoglycemic disorders: An Endocrine
Society Clinical Practice Guideline. J Clin Endocrinol Metabol. 2009;94(3):709-28.
Kitabchi AE, Umpierrez GE, Murphy M, Kreisberg R. Hyperglycemic Crises in Adult Patients with
Diabetes: A consensus statement from the American Diabetes Association. Diabetes Care.
2006;29(12):2739-48.
Martens P, Tits J. Approach to the patient with spontaneous hypoglycemia. Eur J Med. 2014;25:415-
21.
Menéndez Torre E, Tartón García T, Ortega Millán C, Fornos Pérez JA, García Mayor R, López Fernández
ML. Recomendaciones 2012 de la Sociedad Española de Diabetes sobre la utilización de tiras
reactivas para la medición de glucemia capilar en personas con diabetes. Av Diabetol. 2012;28(1):3-9.
Murad MH, Coto-Yglesias F, et al. Drug-induced hypoglycemia: a systematic review. J Clin Endocrinol
Metabol. 2009;94(3):741-5.
Organización Mundial de la Salud. Informe mundial sobre la diabetes. Abril de 2016. Disponible en
http://www.who.int/diabetes/global-report/es/
Protocolo de manejo del paciente diabético no crítico en Urgencias y planta de Hospitalización.
Hospital Universitario 12 de Octubre. Madrid.
Standards of medical care in diabetes 2016. Diabetes Care. 2016;39(S1):S1-S105.
Umpierrez G, Korytkowski M. Diabetic emergencies -ketoacidosis, hyperglycaemic hyperosmolar state
and hypoglycaemia. Nat Rev Endocrinol. 2016;12(4):222-32.
Umpierrez GE, Hellman R, et al. Management of hyperglycemia in hospitalized patients in non-critical
care setting: An Endocrine Society Clinical Practice Guideline. J Clin Endocrinol Metabol.
2012;97(1):16-38.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1171]
[72] OSTEOPOROSIS
72.Osteoporosis
Jaime Laureiro Gonzalo.
Medicina Interna
Juan Carlos Romero Rodríguez.
Endocrinología y Nutrición
Asesor:
Guillermo Martínez Díaz-Guerra.
Médico Adjunto de Endocrinología
I. CONCEPTO Y CLÍNICA
La osteoporosis es la enfermedad ósea más común, es una patología sistémica esquelética
caracterizada por una baja masa ósea y deterioro de la microarquitectura del tejido óseo que compromete
la resistencia del hueso y aumenta la susceptibilidad a fracturas. Es una enfermedad silenciosa hasta que se
complica con fracturas por fragilidad (caídas desde la propia altura o traumatismos leves), afectando
típicamente a vértebras, cadera y antebrazo distal (fractura de Colles). También se asocia con dolores
óseos, deformidad ósea y pérdida de altura.
Afecta a una gran parte de la población, a ambos sexos, a todas las razas y su prevalencia aumenta
en la población anciana. En torno a una de cada dos mujeres caucásicas y uno de cada cinco hombres
padecerán una fractura por fragilidad en algún momento de su vida.
II. APROXIMACIÓN DIAGNÓSTICA
Los principales factores de riesgo de fractura ósea osteoporótica son: la edad (> 65 años), el sexo
femenino y la densidad mineral ósea (DMO), destacando también el antecedente de fractura por fragilidad.
Otros factores a tener en cuenta son: el antecedente de fracturas por fragilidad en un familiar de primer
grado, el tabaquismo, la ingesta alcohólica excesiva, peso corporal bajo (índice de masa corporal [IMC] < 19
kg/m2), así como el grupo de osteoporosis secundarias (debidas a una enfermedad y sus tratamientos:
artritis reumatoide, cirrosis, hipogonadismo, menopausia precoz, malabsorción, enfermedad inflamatoria
intestinal o el uso de corticoides).
Teniendo en cuenta los factores de riesgo de mayor valor predictivo se han elaborado escalas de
puntuación para valorar el riesgo de padecer osteoporosis y otras para valorar el riesgo de fractura
osteoporótica. Destaca el índice FRAX®; un algoritmo publicado por la Organización Mundial de la Salud
(OMS) que calcula el riesgo a 10 años de fractura por fragilidad. Este proporciona dos valores: fractura de
cadera y fractura osteoporótica mayor (fractura clínica vertebral, de húmero, de radio distal, además de
cadera); si bien, aplicado en la población española proporciona un riesgo de fractura mayor muy inferior al
que corresponde por lo que actualmente no sería recomendable en nuestro medio.
1. DENSITOMETRÍA ÓSEA
El término densitometría ósea engloba el conjunto de pruebas invasivas que miden la DMO, siendo
la técnica de “absorciometría por rayos X con doble nivel de energía X (DXA)” el procedimiento óptimo para
estimar el riesgo de fractura, recomendándose explorar al menos dos regiones (el fémur proximal y la
columna lumbar).
Los resultados de las mediciones de la DMO se expresan mediante el índice T (T-Score) o el índice Z
(Z-Score). En la tabla I se recogen los criterios diagnósticos de la OMS para diferenciar los distintos tipos de
enfermedad ósea en base a criterios densitométricos.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1172]
[72] OSTEOPOROSIS
No existen criterios universalmente aceptados sobre cuándo realizar una densitometría. Se
recomienda realizarla en mujeres mayores de 65 años (no hay límite superior establecido) o en aquellas por
debajo de esa edad, pero con algún factor de riesgo de osteoporosis. En varones y mujeres
premenopáusicas no se recomienda, excepto si existen factores predisponentes o sospecha de
osteoporosis secundaria. El intervalo de tiempo que debe transcurrir para la realización de un control
densitométrico, en general, no debe de ser inferior a uno o dos años.
2. PRUEBAS DE LABORATORIO
Se recomiendan las siguientes pruebas de laboratorio: hemograma, función renal y hepática, calcio
(junto con albúmina), fosfatasa alcalina, hormonas tiroideas, niveles de 25-OH vitamina D, proteinograma y
calciuria de 24 horas.
Actualmente se discute la conveniencia de determinar la hormona paratiroidea (PTH) y los
marcadores de remodelación ósea, ya que estos últimos no son útiles para el diagnóstico y no se
recomiendan de forma sistemática en la evaluación de un paciente con osteoporosis, aunque podrían ser
útiles para predecir pacientes con mayor de riesgo de fractura. Sí que han demostrado ser útiles para
valorar la respuesta precoz al tratamiento.
Existen ciertos casos particulares, en los cuales las recomendaciones pueden ser diferentes
requiriendo una ampliación del estudio (Tabla II).
Osteoporosis en la mujer premenopáusica: en función de los síntomas o signos, se planteará
ampliar el estudio (descartar otras comorbilidades asociadas, p. ej., enfermedad celíaca).
Osteoporosis en el varón: a los estudios básicos (si no hay una causa evidente como
corticoterapia crónica) se añadirá la cuantificación de testosterona sérica. Además, de forma
dirigida, se podrá plantear ampliar el estudio.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1173]
[72] OSTEOPOROSIS
3. RADIOGRAFÍA SIMPLE
A pesar de no ser un método sensible ni específico para valorar los cambios de masa ósea, se
recomienda la realización de una radiografía simple de la columna dorsal y de la columna lumbar (dos
proyecciones) en pacientes que presenten:
Dolor raquídeo.
Cifosis significativa.
Fractura pasados los 50 años.
Historia compatible con fractura no documentada previamente.
Disminución de la talla (2 cm de estatura o 4-6 cm de la talla recordada en la juventud).
Tratamiento corticoideo de riesgo (≥ 7,5 mg diarios de prednisona o equivalente durante más
de tres meses, o a cualquier dosis y duración en mujeres posmenopáusicas y varones > 50
años).
Valores densitométricos de osteoporosis (T-Score ≤ -2,5 DE), debido al carácter asintomático de
muchas de las fracturas.
III. TRATAMIENTO Y PREVENCIÓN
1. MEDIDAS NO FARMACOLÓGICAS
Las siguientes medidas generales se recomiendan a todos los pacientes:
Evitar caídas y mejorar el soporte muscular incentivando el apoyo postural.
Realizar ejercicio físico regularmente.
Evitar el consumo de tóxicos (alcohol y tabaco).
Ingerir niveles adecuados de calcio y vitamina D; en general, se recomienda que los aportes de
dichos micronutrientes estén incluidos en la dieta habitual, reservando los aportes
farmacológicos a aquellos pacientes en los que no se puedan asegurar las cantidades diarias
necesarias (ver el siguiente Apartado “Medidas farmacológicas”).
2. MEDIDAS FARMACOLÓGICAS
En condiciones generales se acepta el inicio del tratamiento farmacológico en los siguientes casos:
Pacientes que han sufrido una fractura por fragilidad.
Osteoporosis densitométrica.
Osteopenia densitométrica y factores importantes de riesgo sobreañadidos (ver Apartado II.
“Aproximación diagnóstica”).
Existe una gran variedad de fármacos aprobados para el tratamiento de la osteoporosis. Cabe
destacar que en todos los pacientes sometidos a tratamiento farmacológico se deben prescribir, además,
suplementos de calcio y vitamina D que cubran las necesidades diarias:
Calcio:
1.000 mg diarios para hombres entre 50 y 70 años.
1.200 mg diarios para hombres mayores de 70 años y mujeres mayores de 50 años.
Vitamina D:
800-1.000 UI diarias.
Se recomienda mantener los niveles séricos de 25-OH vitamina D no inferiores a 20 ng/ml (valores
óptimos inmediatamente por encima de 30 ng/ml).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1174]
[72] OSTEOPOROSIS
2.1. Fármacos antirresortivos
Bisfosfonatos: aprobados tanto como para la prevención como para el tratamiento de la
osteoporosis.
Se dispone en el mercado de las siguientes alternativas: alendronato, risedronato, ibandronato,
zoledronato; en distintas presentaciones y pautas de administración (oral/intravenosa;
diaria/semanal/mensual/anual). Son considerados como el primer escalón de tratamiento de la
osteoporosis. Se deben considerar ciertos efectos secundarios derivados de su uso (sobre todo,
gastrointestinales de tipo dispépticos si se utilizan por vía oral) y la imposibilidad de su uso en
pacientes con enfermedad renal sobreañadida (no se aconsejan, en general, en pacientes con
un filtrado glomerular estimado [FGe] por debajo de 30 ml/min). Tampoco están indicados
durante el embarazo y la lactancia; y deben utilizarse con precaución en pacientes con
hipocalcemia (la cual debe corregirse antes de administrarlos).
Se han comunicado, además, casos de osteonecrosis de mandíbula (de mayor incidencia en
pacientes con antecedentes de neoplasias, tratados por vía intravenosa durante largos
periodos de tiempo), y fracturas atípicas de fémur que obligan a detener su uso (sin embargo,
cabe señalar que el riesgo en general es bajo).
Cuando se utilizan por vía oral se recomienda tomarlos al menos 30-60 minutos antes del
desayuno, con agua (no con otros líquidos), evitando tumbarse tras su ingesta debido al riesgo
de esofagitis asociada (Figura 1).
Agonistas/antagonistas de estrógenos (moduladores selectivos de los receptores
estrogénicos)
Aprobados para la prevención y el tratamiento de la osteoporosis posmenopáusica. Se dispone
en el mercado de dos opciones: raloxifeno y bazedoxifeno.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1175]
[72] OSTEOPOROSIS
Deben considerarse los efectos secundarios derivados de su uso: sofocos, calambres y edema
de los miembros inferiores, síntomas dispépticos y aumento de la incidencia de trombosis
venosa profunda.
Terapia hormonal sustitutiva (estrógenos/progestágenos)
Aprobada para el tratamiento de la osteoporosis posmenopáusica. Se dispone de múltiples
presentaciones (oral, transdérmica, intravaginal); con múltiples pautas individualizadas para
cada paciente.
No se consideran actualmente como fármacos de primera línea, principalmente teniendo en
cuenta la posibilidad de aparición de efectos secundarios importantes (aumento de riesgo de
eventos cardiovasculares: infarto de miocardio, tromboembolismo pulmonar, trombosis venosa
profunda, ictus; cáncer); de tal manera que se reservan únicamente para aquellas pacientes en
las cuales no se disponga de otras opciones terapéuticas.
Inhibidores del RANK/RANKL (denosumab)
Anticuerpo monoclonal aprobado para el tratamiento de varios tipos de osteoporosis
(posmenopáusica, en el varón, formas secundarias). Puede utilizarse como fármaco de primera
o segunda línea. Se utiliza por vía subcutánea en dosis semestrales.
Es importante vigilar en el varón en el contexto de ablación hormonal por cancer de próstata la
aparición de hipocalcemia y tratar posibles deficiencias de 25-OH vitamina D. Se ha descrito
también la posibilidad de osteonecrosis de mandíbula y fracturas atípicas del fémur (de menor
incidencia que con el uso de bisfosfonatos), así como reacciones cutáneas. Se puede utilizar en
pacientes con enfermedad renal crónica.
Ranelato de estroncio
De uso por vía oral, en dosis diarias. Se considera un fármaco de segunda línea en casos de
osteoporosis severa con alto riesgo de fractura en mujeres posmenopáusicas y hombres
adultos, cuando no se dispone de otras opciones terapéuticas.
Debido al riesgo de aparición de eventos cardiovasculares secundarios importantes, estarían
contraindicados en pacientes con hipertensión arterial (HTA) mal controlada, antecedentes de
cardiopatía isquémica, enfermedad arterial periférica o eventos cerebrovasculares.
2.2. Fármacos osteoformadores
Hormona paratiroidea (teriparatida [1,34 PTH])
Aprobada para el tratamiento de todos los tipos de osteoporosis (posmenopáusica, del varón,
formas secundarias). Uso en primera o segunda línea de tratamiento. Se prefiere, sobre todo,
en pacientes con osteoporosis severa con alto riesgo de fractura. De uso por vía subcutánea en
dosis diarias por un tiempo máximo de 18-24 meses (en la práctica común se suele seguir
tratamiento secuencial con algún fármaco antirresortivo).
Dentro de sus efectos adversos se han descrito náuseas, mareo, vértigos y calambres; pero, en
general, tiene una buena tolerancia. Está contraindicada en pacientes con antecedentes de hipercalcemia,
metástasis u otras enfermedades óseas (por ejemplo, enfermedad de Paget).
En la tabla III se resumen las diferentes vías de administración, dosis, sitios de acción e indicación
de los principales fármacos utilizados en el tratamiento de la osteoporosis.
2.3. Otras alternativas de tratamiento
En casos de fracturas sintomáticas se puede utilizar calcitonina para el control agudo del dolor,
además del apoyo de medidas ortopédicas. En aquellas situaciones en las cuales la fractura
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1176]
[72] OSTEOPOROSIS
pueda asociarse a un compromiso vital o sea de muy difícil manejo se puede utilizar la
cifoplastia/vertebroplastia, siendo esta última más eficaz y segura.
3. RECOMENDACIONES GENERALES DE ELECCIÓN DE TRATAMIENTO Y SEGUIMIENTO
3.1. Elección inicial del fármaco
Debería ser individualizada, teniendo en cuenta los siguientes escenarios:
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1177]
[72] OSTEOPOROSIS
Paciente con riesgo elevado de fractura (equivalente a 2 o más fracturas vertebrales):
inicialmente teriparatida (podría utilizarse también si T-score < 3,5-4 en ausencia de fracturas)
durante 24 meses, seguida de bisfosfonatos (se podrían utilizar también fármacos de primera
línea si existe contraindicación para teriparatida). Y se puede usar denosumab como primera
línea de tratamiento.
Paciente joven con riesgo moderado de fractura vertebral y poco riesgo de fractura de cadera
(osteoporosis densitométrica exclusivamente en la columna en ausencia de fracturas):
raloxifeno/bazedoxifeno en mujeres o bisfosfonatos en el resto de la población.
Cualquier otra situación: bisfosfonatos o denosumab.
Se debe considerar, además, que los fármacos que se administran con mayores intervalos de
tiempo se prefieren para pacientes de edad avanzada y polimedicados con el objetivo de
alcanzar una mayor adherencia.
3.2. Duración del tratamiento
La duración exacta del tratamiento debe ser individualizada para cada tipo de paciente. Está
justificada la interrupción del fármaco elegido cuando se hayan alcanzado los objetivos terapéuticos, por
pérdida de eficacia o por aumento del riesgo de aparición de efectos adversos.
Una situación especial es la que se presenta con el uso de bisfosfonatos, que no deberían ser
utilizados durante más de 5 años seguidos (3 años en el caso de zolendronato), salvo algunas situaciones
clínicas especiales. En el algoritmo de la figura 1 se exponen recomendaciones propuestas para el uso de
bisfosfonatos a largo plazo.
Algo similar ocurre con el uso de denosumab, se debe reevaluar la posibilidad de continuar o no
con él en los 5 años siguientes a su inicio; transcurrido dicho tiempo existen dos opciones: si el riesgo de
fractura es elevado, se debe mantener o iniciar tratamiento con teriparatida o ranelato de estroncio; en
cambio si el riesgo de fractura es bajo, se puede optar por tomar un periodo de “vacaciones terapéuticas”.
Sin embargo, se debería iniciar en ese momento tratamiento con otro antirresortivo de menor potencia
(por ejemplo, raloxifeno/bazedoxifeno o bisfosfonatos a la mitad de su dosis habitual).
3.3. Recomendaciones en el seguimiento
Se recomienda la valoración anual del paciente identificando ciertos parámetros de riesgo (mala
adherencia terapéutica, pérdida de talla entre los controles efectuados, aparición de efectos secundarios
del fármaco elegido, evaluación de la tendencia de marcadores de recambio óseo); además, se
recomiendan densitometrías de control cada 1-2 años; siempre individualizando el seguimiento para cada
tipo de paciente.
BIBLIOGRAFÍA
Adler A, Fuleihan G, Bauer D, Camacho P, Clarke B, Cline G, et al. Managing Osteoporosis in Patients
on Long-Term Bisphosphonate Treatment: Report of a Task Force of the American Society for Bone
and Mineral Research. J Bone and Min Res. 2016;31(1):16-35.
Guías de práctica clínica en la osteoporosis posmenopáusica, glucocorticoidea y del varón. Sociedad
Española de Investigación Ósea y del Metabolismo Mineral. 3ª versión, actualizada en 2014.
Disponible en: http://www.seiomm.org/uploads/sfMedia/guia-seiomm_v4_2014_c.pdf
National Osteoporosis Foundation. Clinician’s Guide to Prevention and Treatment of Osteoporosis.
Washington, DC: National Osteoporosis Foundation; 2013. Disponible en:
http://nof.org/files/nof/public/content/file/2791/upload/919.pdf
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1178]
[73] TRASTORNOS LIPÍDICOS
73.Trastornos lipídicos
Marta de Castro Martínez.
Medicina Interna
Julio César Vargas Romero.
Medicina Interna
Asesor: Agustín Blanco Echeverría. Medicina Interna. Unidad de Lípidos y Riesgo Vascular
I. INTRODUCCIÓN
Los lípidos en el plasma son transportados por las lipoproteínas plasmáticas debido a su
insolubilidad en el plasma. Las lipoproteínas plasmáticas se clasifican en función de su densidad: alta (high
density lipoproteins [HDL]), baja (low density lipoproteins [LDL]), intermedia (intermediate density
lipoproteins [IDL]) y muy baja (very low density lipoproteins [VLDL]). Los quilomicrones se originan en el
intestino y están formados principalmente por los lípidos de la dieta y pequeñas cantidades de proteínas.
Tabla I. Clasificación de las hiperlipemias primarias.
El mecanismo causal principal de la enfermedad ateroesclerótica es el colesterol unido a
lipoproteínas de baja densidad (c-LDL). La relación causal del c-LDL con la aterosclerosis está claramente
demostrada, siendo la enfermedad cardiovascular (ECV) la principal causa de muerte y discapacidad en las
sociedades más desarrolladas.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1179]
[73] TRASTORNOS LIPÍDICOS
II. CONCEPTO Y CLASIFICACIÓN
1. CONCEPTO
La dislipemia es una alteración de la concentración plasmática de colesterol y/o triglicéridos (TG).
Aunque las concentraciones plasmáticas dependen de la edad, del sexo y de la raza, de manera general
consideraremos como patológicas unas cifras plasmáticas de colesterol total y de TG ≥ 200 mg/dL (los
niveles óptimos se consideran < 150 mg/dL), y de colesterol unido a lipoproteínas de alta densidad (c-HDL)
< 40 mg/dL en el varón y < 50 mg/dL en la mujer, precisando de una evaluación de los niveles de c-LDL en
función del riesgo cardiovascular (RCV) individual.
2. CLASIFICACIÓN
Dislipemias primarias: son dislipemias de causa genética. Son alteraciones genéticas únicas o
anormalidades poligénicas originadas por mutaciones en uno o más genes que intervienen en
la síntesis y/o metabolismo de las lipoproteínas. Se clasifican según el tipo de lipoproteína
alterada y su repercusión clínica (Tabla I). Debe sospecharse una dislipemia primaria en
presencia de enfermedad ateroesclerótica prematura, de depósitos lipídicos (xantomas o arco
corneal en personas < 45 años) y cuando existen antecedentes familiares de dislipemia.
Dislipemias secundarias: las causas más frecuentes son la diabetes mellitus (DM) y las
asociadas al incremento del RCV (DM y el síndrome metabólico [SM]) (Tabla II). (Ver Capítulo
20. “Hipertensión arterial y riesgo cardiovascular”).
Tabla II. Causas de hiperlipemia secundaria.
III. APROXIMACIÓN DIAGNÓSTICA
El cribado de dislipemia poblacional está indicado a partir de los 20 años, realizando una
determinación cada cinco años. La edad a partir de la cual los pacientes no se benefician del cribado no está
establecida. Debe prestarse especial atención a los individuos de alto riesgo (Tabla III).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1180]
[73] TRASTORNOS LIPÍDICOS
Se debe medir la cifra de colesterol total, c-LDL, c-HDL y TG tras ayuno nocturno de 12 horas. La
determinación en ayunas de 12 horas, es fundamentalmente por los triglicéridos, aunque actualmente se
sabe que la hipertrigliceridemia posprandial incrementa también el RCV.
Tabla III. Individuos de alto riesgo en los que se debe realizar el cribado de la dislipemia.
El diagnóstico de dislipemia debe basarse en al menos dos análisis compatibles en un periodo de 2-
3 semanas en situación basal (en ausencia de enfermedad aguda, infección, cirugía o cambio reciente de
dieta). Si existe una diferencia en ambas determinaciones mayor de 30 mg/dL, debe hacerse un tercer
análisis. En los pacientes hospitalizados (incluyendo los eventos coronarios agudos) solo se consideran
válidas las determinaciones en las primeras 24 horas.
El valor de c-LDL puede estimarse a partir del colesterol total y del c-HDL mediante la fórmula de
Friedewald:
c-LDL = colesterol total – [TG (mg/dL)/5 + c-HDL]
Los TG divididos entre 5 representan el colesterol de las VLDL, por lo que este método no es válido
si la cifra de TG es superior a 200 mg/dL. En los pacientes con hipertrigliceridemia moderada-grave o con
SM se deberá determinar también el colesterol no-HDL (incluye LDL, IDL, VLDL). En estas situaciones el
colesterol no-HDL se convierte en el marcador principal de RCV.
Otras determinaciones que se deben incluir en el perfil lipídico de los pacientes con alto RCV son las
determinaciones de las apolipoproteínas A y B (Apo-A y Apo-B) y la lipoproteína(a) [Lp(a)] (una forma
especial de LDL). La Lp(a) se conforma en el espacio extracelular por la unión de la Apo-A con la Apo-B100
de las LDL. El aumento de su nivel es independiente de la dieta y tiene un origen genético. Es un factor de
RCV independiente y se asocia a la calcificación valvular aórtica. Actualmente los inhibidores de las PCSK9
son los únicos que pueden disminuir los niveles de la Lp(a), aproximadamente un 30%, por mecanismos no
suficientemente conocidos. Existen fármacos en desarrollo, oligonucleótidos antisentido, específicamente
diseñados para disminuir los niveles de la Lp(a).
IV. OBJETIVOS TERAPÉUTICOS
El objetivo final es evitar la aparición de cualquier evento cardiovascular.
1. OBJETIVOS PRIMARIOS
Los esfuerzos terapéuticos deben ir dirigidos a conseguir unos niveles de c-LDL adecuados en
función del riesgo individual. Cuanto más disminuyan los niveles de c-LDL, mayor mejoría pronóstica se
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1181]
[73] TRASTORNOS LIPÍDICOS
obtiene. Por cada 39 mg/dL (1 mmol/l) de reducción en los niveles de c-LDL, la incidencia de enfermedad
cardiovascular aterosclerótica (ECVA) disminuye aproximadamente en un 22%.
Una excepción es la existencia de niveles de TG ≥ 500 mg/dL, en los que el objetivo primario debe
ser el control rápido de la hipertrigliceridemia mediante un fibrato, con ácidos grasos omega 3 o incluso
aféresis para evitar el desarrollo de pancreatitis aguda. En estos pacientes los objetivos de tratamiento,
además de controlar los niveles de los TG, deben ser el colesterol no-HDL o la Apo-B.
2. OBJETIVOS SECUNDARIOS
Se ha observado que aumentan el RCV:
Niveles bajos de c-HDL y de Apo-A1.
Niveles elevados de TG, fibrinógeno, homocisteína, Apo-B y lipoproteína(a)
La hipercolesterolemia familiar o la elevación de la proteína C reactiva (PCR) ultrasensible.
La tríada lipídica aterogénica o dislipemia diabética: elevación de los TG, reducción de HDL y
aumento de LDL.
Por ello, como objetivos secundarios deben conseguirse cifras de colesterol total < 200 mg/dL, TG <
150 mg/dL, c-HDL ≥ 40 mg/dL en el varón y ≥ 50 mg/dL en la mujer y colesterol no-HDL (colesterol total – c-
HDL) que no superen en 30 mg/dL al objetivo de c-LDL. Los niveles objetivo del resto de factores no están
bien determinados.
Tanto el colesterol no-HDL como la Apo-B pueden ser considerados posibles objetivos terapéuticos,
especialmente en sujetos con DM2, SM o dislipemia combinada (la determinación de la Apo-B no está
disponible en todos los centros de salud y es menos económica que la del colesterol no-HDL).
Tabla IV. Grupos de riesgo cardiovascular.
No se ha demostrado el rendimiento clínico de ulteriores ajustes del tratamiento hipolipemiante
para uno o más de los objetivos secundarios en los pacientes con RCV muy alto una vez alcanzado el
objetivo de c-LDL.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1182]
[73] TRASTORNOS LIPÍDICOS
Los niveles elevados de homocisteína se asocian con la elevación del RCV; sin embargo, la
disminución de sus niveles con ácido fólico o vitamina B, no reduce el RCV.
3. EVALUACIÓN DEL RIESGO CARDIOVASCULAR
Es el primer paso en la planificación terapéutica dado que nos delimitará los objetivos de c-LDL Para
ello, hay que considerar tanto la existencia de ECV o sus equivalentes (prevención secundaria) como la
existencia y número de factores de RCV sin ECV asociada (prevención primaria).
Existen diferentes guías para la evaluación del RCV. Cada una ofrece una escala para valorar el
mismo, se asigna al paciente a uno de los cuatro grupos de riesgo (Tabla IV) y, en función de ello, se
establecen unos objetivos de tratamiento (Tabla V). En nuestro medio son adecuadas la escala SCORE (ver
Capítulo 20. “Hipertensión arterial y riesgo cardiovascular”) y la escala de las guías de la Sociedad Europea
de Cardiología publicadas en el año 2011.
Las tablas de las recientes guías americanas no deberían utilizarse ya que su población no es
extrapolable a la población española.
Tabla V. Objetivos terapéuticos e indicación del tratamiento.
V. TRATAMIENTO
1. MODIFICACIONES EN EL ESTILO DE VIDA Y SUPLEMENTOS
Las modificaciones en el estilo de vida son la primera actuación que debe llevarse a cabo en todo
paciente, independientemente de que reciba tratamiento farmacológico. Debe hacerse hincapié en
mantener el peso ideal, realizar ejercicio aeróbico regular, abandonar el consumo de tabaco y moderar o
suprimir el consumo de alcohol, especialmente si existe hipertrigliceridemia.
En cuanto a la dieta, las grasas no deben representar más del 35% del aporte calórico diario, de las
cuales < 7% deben corresponder a grasas saturadas. Los ácidos grasos saturados (AGS) son el factor
dietético con mayor impacto en las concentraciones de c-LDL con aumento de 0,8-1,6 mg/dL de c-LDL por
cada 1% de energía adicional derivada de las grasas saturadas. Si el 1% de la energía derivada de los AGS se
sustituyese por ácidos grasos monoinsaturados (AGMI), el c-LDL disminuiría 1,6 mg/dL. Por otro lado, los
hidratos de carbono tienen un efecto neutral en el c-LDL y son una de las alternativas para sustituir la grasa
saturada de la dieta. Asimismo, puede recomendarse al paciente la ingesta de 5-10 g de fibra soluble al día
y de 2-3 g/d de fitoesteroles como terapia coadyuvante. Combinando estas medidas se puede alcanzar
hasta un 20% de reducción en los valores basales de c-LDL.
2. INICIAR TRATAMIENTO HIPOLIPEMIANTE
Los pasos sucesivos serían:
Decidir si el paciente precisa tratamiento con estatina según el nivel de riesgo y la cifra de LDL.
Asignar el objetivo de c-LDL que se debe alcanzar (Tabla V).
Calcular el porcentaje de reducción que se precisa para alcanzar dicho objetivo en función de la
cifra inicial (Tabla VI).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1183]
[73] TRASTORNOS LIPÍDICOS
Tabla VI. Porcentaje de reducción para alcanzar los objetivos de c-LDL.
En caso de que precise estatina, elegir la más adecuada para conseguir la reducción porcentual
requerida (Tablas VII y VIII).
Tabla VII. Dosis diaria (mg) y eficacia comparativa de las distintas estatinas.
Tabla VIII. Intensidad del tratamiento con estatinas.
Ajustar la dosis y vigilar posibles problemas de toxicidad.
Valorar la necesidad de tratamientos combinados o alternativos (Figura 1).
3. FÁRMACOS HIPOLIPEMIANTES (VER FIGURA 1)
3.1. Estatinas
Son los fármacos más útiles y prácticos para reducir el c-LDL, han demostrado disminuir la morbimortalidad
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1184]
[73] TRASTORNOS LIPÍDICOS
cardiovascular (tanto en prevención primaria como secundaria), siendo de primera elección. Actúan
inhibiendo de forma parcial, competitiva y reversible la enzima hidroxi-metil-glutaril coenzima A (HMG-
CoA) reductasa, produciendo una disminución de la biosíntesis del colesterol intrahepático, un aumento en
la extracción del c-LDL de la sangre y una disminución de la concentración de LDL circulante y otras
lipoproteínas que contienen Apo-B.
Figura 1. Tratamiento farmacológico de inicio.
La reducción de c-LDL obtenida no es igual para todas las estatinas (Tablas VII y VIII) y es
dependiente de la dosis en todas ellas.
Las estatinas difieren en su farmacocinética y en su unión a proteínas. La mayoría se metabolizan
vía citocromo P450 mediante metabolismo hepático, excepto pravastatina, rosuvastatina y pitavastatina.
Atorvastatina, fluvastatina y pitavastatina son de elección en pacientes con insuficiencia renal grave.
No existe una clara indicación para la elección de cada estatina; sin embargo, antes del inicio de
tratamiento es recomendable relacionar la potencia con los objetivos del tratamiento.
Se han observado casos de diabetes en pacientes tratados con estatina más allá de lo esperado y
con una tendencia estadísticamente significativa. Dicho efecto secundario parece estar relacionado con el
grado de inhibición de la HMG-CoA reductasa, siendo, por tanto, más frecuente con el uso estatinas de
elevada potencia. Sin embargo, su uso no está contraindicado en pacientes de alto riesgo (parece que
pivastatina es la que confiere menor “riesgo diabetógeno”).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1185]
[73] TRASTORNOS LIPÍDICOS
Al inhibir a la HMG-CoA reductasa se potencia la absorción de colesterol en la dieta, por ello es
recomendable su combinación con fármacos que la inhiban como son ezetimiba o las resinas, ejerciendo así
un efecto sinérgico.
Los efectos secundarios más frecuentes de las estatinas son:
Miopatía (< 0,1%). Es el efecto adverso asociado más importante, que puede progresar a
rabdomiolisis, fracaso renal y muerte, donde la elevación de la creatina fosfoquinasa (CPK) es el
primer y mejor marcador. La existencia de dolor muscular, debilidad y emisión de orinas
oscuras, deben hacernos sospechar una miositis, siendo necesaria la determinación urgente de
los niveles de la CPK. La monitorización de la CPK debe relacionarse con la clínica, ya que es
inútil la determinación rutinaria de dichos niveles. La definición habitual de elevación tolerable
es de hasta cinco veces el límite superior de la normalidad en dos ocasiones.
La miopatía ocurre con más frecuencia en pacientes polimedicados (atención a ciclosporina,
gemfibrozilo, macrólidos, antifúngicos e inhibidores de la proteasa), ancianos (especialmente
en mujeres) y pacientes con insuficiencia renal.
La combinación de estatinas con fibratos aumenta el riesgo de miopatía. Este riesgo es mayor
con gemfibrozilo que con el resto de fibratos y se debe evitar esta asociación (el riesgo con
fenofibrato y bezafibrato es menor). En aquellos pacientes con un episodio de miositis o que
hayan presentado una elevación de la CPK de hasta 10 veces superior a los valores basales
(excluyendo hipotiroidismo, traumatismo o ejercicio vigoroso) se puede intentar, una vez
normalizados los valores, un ensayo con pravastatina o fluvastatina con seguimiento estrecho.
Las mialgias (sin elevación de la CPK) ocurren hasta en un 5-10% de los pacientes. Estos
pacientes pueden continuar con el tratamiento si los síntomas son tolerables, alentados por el
enorme beneficio que supone la reducción en el RCV. En caso contrario, se debe suspender el
tratamiento o intentarlo con otros fármacos (atorvastatina, rosuvastatina, pitavastatina) y
administrarlos en días alternos.
Hipertransaminasemia (0,5-2%). Es dependiente de la dosis y suele resolverse con la reducción
de la misma o incluso manteniendo el propio tratamiento. Si se incrementan los valores por
encima de tres veces el límite superior de la normalidad medido en dos ocasiones (intervalo de
días o de unas semanas), es necesario retirar el fármaco. La progresión a fallo hepático es rara.
La clínica remite en pocos días, pero la normalización de los valores enzimáticos puede durar
semanas. Una vez resuelto el cuadro clínico no suele recurrir con la reinstauración del
tratamiento a dosis más bajas.
Los pacientes con SM y esteatosis hepática y ligeras elevaciones de las transaminasas que
precisen tratamiento con estatinas deben someterse a controles frecuentes para ver la
tolerancia y la eficacia, sin que su uso esté contraindicado. En la tabla IX se describen las
recomendaciones para monitorizar el tratamiento.
3.2. Resinas de intercambio catiónico
Las resinas de intercambio catiónico impiden la absorción intestinal de colesterol e interrumpen
parcialmente su circulación enterohepática. La consecuencia final es el descenso de la concentración
plasmática de colesterol total (20% sobre los niveles basales) y de c-LDL (del 18 al 25%). El c-HDL aumenta
del 3 al 5%, pero también aumentan los triglicéridos plasmáticos (del 0 al 10%). Asimismo, reducen los
niveles de glucosa y de hemoglobina glucosilada en pacientes con hiperglucemia y diabetes, aunque el
mecanismo por el que lo realizan no está claro. Son útiles en el tratamiento combinado con estatinas o en
monoterapia si los TG plasmáticos son inferiores a 200 mg/dL, en los niños y en aquellos que tan solo
requieren una pequeña reducción en las cifras de c-LDL.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1186]
[73] TRASTORNOS LIPÍDICOS
Están indicadas en caso de intolerancia a estatinas y asociadas a estas para conseguir reducciones
adicionales de c-LDL no conseguidas con el uso exclusivo de estatinas.
La dosis diaria de colesevelam es de 4 a 6 comprimidos de 625 mg (2,50 a 3,75 g/día),
administrados por vía oral una o dos veces al día. La dosis diaria máxima es de 6 comprimidos. En relación a
colestiramina, la dosis recomendada es de 3-4 sobres de 4 g al día, administrada por vía oral
Tabla IX. Recomendaciones para monitorizar lípidos y enzimas durante el tratamiento.
Como efectos secundarios son frecuentes, incluso a bajas dosis, la elevación de los triglicéridos
plasmáticos, la intolerancia digestiva y el estreñimiento. Colesevelam (en España requiere visado) es mejor
tolerado que colestiramina; ambos se pueden dar junto con estatinas. Las contraindicaciones para su uso
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1187]
[73] TRASTORNOS LIPÍDICOS
son cifras de TG > 400 mg/dL y la disbeta-lipoproteinemia. Presentan interacciones, pueden disminuir la
absorción de otros fármacos y de las vitaminas liposolubles de los alimentos, excepto colesevelam. Por ello,
deben administrarse una hora después o cuatro horas antes de la toma de fármacos y alimentos.
3.3. Fibratos
Aumentan la acción de los receptores activados de la proliferación de los peroxisomas (PPAR alfa),
activándose la lipoproteína lipasa (LPL). Reducen los TG en el 20-35%, el c-LDL en el 5-20% y aumentan el c-
HDL en el 10-35%. Son los fármacos hipotrigliceridemiantes más potentes. Su gran porcentaje de unión a la
albúmina hace que eleven los niveles plasmáticos de múltiples fármacos.
Los fibratos disponibles son fenofibrato (dosis de 145 mg a 250 mg/día), gemfibrozilo (dosis de 600
mg/12 h, 900 mg/24 h, dosis máxima de 1.500 mg/día), bezafibrato (200 mg/8 h y presentación retard 400
mg/día). Se deben administrar tras las comidas, a excepción de las formas retard, con las que se realiza una
sola toma nocturna.
Se encuentran indicados en los pacientes con hipertrigliceridemia primaria con niveles de TG > 500
mg/dL y en los pacientes con dislipemia aterogénica (TG elevados, c-HDL bajo y partículas LDL pequeñas y
densas), diabéticos y/o con SM asociado a estatinas. Los efectos adversos más frecuentes son: digestivos
(náuseas, diarrea, dispepsia, distensión o dolor abdominal), hepatotoxicidad (elevación reversible de las
transaminasas), miopatía (favorecida por la coexistencia de insuficiencia renal y/o la administración
concomitante de estatinas) y citopenias sanguíneas. Es importante señalar que gemfibrozilo compite con
las estatinas por el catabolismo hepático en mayor medida que otros fibratos, lo que determina un
potencial superior de interacciones farmacocinéticas y efectos adversos.
Están contraindicados en presencia de hepatopatía o insuficiencia renal grave, litiasis biliar y junto
con el empleo de inhibidores de la monoaminooxidasa.
3.4. Ácido nicotínico o niacina
Vitamina hidrosoluble del grupo B. Reduce en un 20% el colesterol total, el c-LDL y los TG. Es el fármaco que
más incrementa los valores plasmáticos de c-HDL (20%) y el único que reduce los niveles de Apo-A.
Se ha retirado del mercado por su ineficacia para disminuir la morbimortalidad cardiovascular en
diferentes estudios.
3.5. Ezetimiba
Impide la absorción tanto del colesterol de la dieta como el biliar a través de la inactivación de la NPCL-1.
No altera la absorción de sales biliares ni de vitaminas liposolubles. Disminuye el colesterol plasmático en
un 16-18%. Este efecto sería aditivo al obtenido con las estatinas, con lo que se obtiene hasta un 60% de
descenso en el c-LDL, de tal manera que su principal indicación es el uso combinado con dichos fármacos
en la hipercolesterolemia grave de pacientes de alto riesgo en los que no se consiguen los objetivos de c-
LDL. Puede emplearse en monoterapia si existe intolerancia a las estatinas, excepto si existe insuficiencia
hepática moderada o severa.
Las dosis recomendadas diarias son de 10 mg/día, por la mañana o noche, sin relación con las
comidas. Puede administrarse con cualquier estatina a cualquier dosis de la misma. Los excelentes
resultados en el descenso de c-LDL asociados a estatinas se han confirmado (además se acompañan de una
mayor reducción del RCV) en el estudio IMPROVE-IT, ratificándose la teoría lipídica de que cuanto más bajo
es el nivel de LDL, es mejor. Especial beneficio se ha observado en los pacientes diabéticos.
No han sido descritos efectos adversos graves, siendo el más frecuente la elevación moderada de
las enzimas hepáticas y las mialgias.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1188]
[73] TRASTORNOS LIPÍDICOS
3.6. Inhibidores de la proproteína convertasa subtilisina/kexina tipo 9
La proproteína convertasa subtilisina/kexina tipo 9 (PCSK9) se une a los receptores de las LDL (R-LDL) en la
superficie de los hepatocitos para estimular la degradación de los R-LDL en el hígado con el consiguiente
aumento de los niveles séricos de c-LDL. Los inhibidores de la PCSK9 son los primeros en su clase, son
anticuerpos monoclonales humanizados que al inhibir la unión de la PCSK9 al R-LDL aumentan el número
de R-LDL disponibles para eliminar el LDL, reduciendo así los niveles de c-LDL.
A nivel europeo están aprobados evolucumab y alirocumab por la Agencia Europea de
Medicamentos (EAM). En España están comercializados bajo el nombre de Rapatha® y Praluent®,
respectivamente. Dichos fármacos causan grandes reducciones en los niveles de c-LDL, en comparación con
el placebo (39% a 62% de reducción para alirocumab y 47% a 56% para evolocumab).
Está indicado en adultos con hipercolesterolemia primaria (familiar heterocigótica y no familiar),
adultos con dislipidemia mixta como complemento a la dieta, pacientes que no consiguen alcanzar los
niveles objetivo de c-LDL con la dosis máxima tolerada de estatina, pacientes intolerantes a las estatinas o
existe contraindicación para su uso, tanto solo como en combinación.
Únicamente evolocumab está indicado en la hipercolesterolemia familiar homocigótica en adultos y
adolescentes a partir de 12 años en combinación con otros tratamientos hipolipemiantes.
Posología: alirocumab (Praluent®) 75 mg administrado por vía subcutánea, una vez cada dos
semanas hasta 150 mg cada dos semanas, y evolocumab (Repatha®) 140 mg cada dos semanas o 420 mg
por vía subcutánea una vez al mes; ambas dosis son clínicamente equivalentes. No se ha establecido
todavía el efecto de Rapatha o de Praluent sobre la morbilidad y sobre la mortalidad cardiovascular.
Los efectos adversos más frecuentes de evolocumab fueron nasofaringitis, infección respiratoria del
tracto superior, dolor de espalda, artralgia, gripe y náuseas. Con alirocumab se produjeron reacciones
locales en la zona de inyección, signos y síntomas del tracto respiratorio superior y prurito.
Se debe usar con precaución en pacientes con insuficiencia renal grave (eGFR < 30 ml/min/ 1,73 m2)
y en pacientes con insuficiencia hepática grave (clase C de la escala Child-Pugh) ya que no han sido
estudiados. No se recomienda su utilización durante el embarazo y la lactancia.
3.7. Ácidos grasos omega 3
La ingesta de estos ácidos grasos a través del pescado azul, aceite de pescado o cápsulas de aceite de
pescado concentrado tiene la capacidad de reducir el nivel de los TG. Sus componentes principales son
eicosapentaenoico (EPA) y docosahexaenoico (DHA). Son fármacos seguros, eficaces y bien tolerados.
Su principal papel terapéutico está en el tratamiento de la hipertrigliceridemia grave, con valores
superiores a 500 mg/dL. La dosis diaria de los ácidos grasos omega 3 es de 2 a 4 cápsulas de 1 g (2-4 g/d),
administrados por vía oral una vez al día. La dosis diaria máxima es de 4 g. Pueden asociarse o no a fibratos.
3.8. Mipomersen
Mipomersen es un ologoneuclótido no codificante que inhibe la síntesis de la Apo-B, así como de las
lipoproteínas que la contienen, disminuyendo así su concentración plasmática, en particular las LDL.
Alcanza todos los tejidos del organismo, excepto el musculoesquelético.
A nivel hepático (donde alcanza la mayor concentración) inhibe el ácido ribonucleico (ARN)
mensajero de la Apo-B. No tiene efectos sobre las isoenzimas del citocromo p450, por lo que no presenta
interacciones significativas con otros medicamentos.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1189]
[73] TRASTORNOS LIPÍDICOS
Su principal indicación es la hipercolesterolemia familiar homocigota o las formas heterocigotas
graves en las que no se logran objetivos terapéuticos de c-LDL, a pesar de la terapia con estatinas a
máximas dosis toleradas.
Se administra por vía subcutánea a dosis de 200 mg semanales. Su vida media es dependiente de la
dosis; sin embargo, oscila entre 23 a 46 días. A nivel analítico se observa una reducción de los niveles de c-
LDL, colesterol no-HDL y Apo-B, permaneciendo sin cambios los valores de los triglicéridos y del HDL.
Entre los efectos adversos más frecuentes destacamos reacciones en el sitio de inyección, tales
como cambio en la coloración de la piel, enrojecimiento, cuadros pseudogripales, que ocurren en el 30-50%
de los pacientes, y la elevación de las transaminasas tres o más veces por encima del valor normal, aunque
varía en los distintos estudios. Se ha descrito también un aumento del tejido graso en el hígado. Este
medicamento ha sido aprobado en enero de 2013 por la Food and Drug Administration (FDA), en cambio
hasta el momento no ha sido aprobado por la EMA.
3.9. Lomitapide
Lomitapide es un inhibidor selectivo de la proteína de transferencia microsomal (PTM). Es una proteína de
transferencia lipídica intracelular que se encuentra en la luz del retículo endoplásmico y es la responsable
de unir y transportar las moléculas lipídicas individuales entre las membranas. La PTM desempeña una
función clave en el ensamblaje de las lipoproteínas que contienen la Apo-B en el hígado y en el intestino. La
inhibición de la PTM reduce la secreción de lipoproteínas y las concentraciones en sangre de los lípidos
transportados por las lipoproteínas, como el colesterol y los TG.
Está indicado como complemento a una dieta baja en grasas y a otros medicamentos
hipolipemiantes, con o sin aféresis de las LDL, en pacientes adultos con hipercolesterolemia familiar
homocigótica. Disminuye el c-LDL un 30-50%, los triglicéridos un 31-45%, la Apo-B entre un 41-49% y la
lipoproteína(a) en un 15-19%.
Desde un punto de vista práctico se sugiere comenzar con la dosis de 5 mg de lomitapide una vez al
día (2 h después de la cena) y titular la dosis cada 4 semanas según su tolerancia (máximo 60 mg/día).
Está contraindicado en pacientes con insuficiencia hepática moderada o grave, no está
recomendado en personas menores de 18 años y en los pacientes con enfermedad renal terminal
sometidos a diálisis no deben sobrepasarse los 40 mg diarios.
Las reacciones adversas más frecuentes que se han descrito son de tipo gastrointestinal (diarrea,
náuseas, dispepsia y vómitos). Está aprobado por la EMA y por la FDA.
3.10. Nuevos agentes en el manejo de la dislipidemia
Oligonucleótido antisentido APOC3 (Volanesorsen®): el gen APOC3 codifica la apolipoproteína
C-III, pieza clave en la regulación del metabolismo de la lipoproteína y de los niveles de TG en el
plasma. El oligonucleótido antisentido APOC3 (fase III) está basado en el bloqueo del ARN
mensajero del APOC3, aunque el gen sea transcrito, la proteína que codifica no es sintetizada.
Es de administración subcutánea una vez por semana y está indicado en el síndrome de
quilomicronemia familiar y reduce los TG entre un 20% y un 86%.
Terapia génica: alipogen tiparvovec (Glybera®) contiene una variante del gen de la LPL humana,
unida a un vector. El vector está formado por una cubierta proteínica derivada del virus
adenoasociado de serotipo 1 (AAV1).
Fue aprobado por la EMA para pacientes adultos con diagnóstico de deficiencia de LPL,
confirmado mediante una prueba genética adecuada y que hayan presentado ataques graves o
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1190]
[73] TRASTORNOS LIPÍDICOS
múltiples de pancreatitis, a pesar de seguir una dieta baja en grasas. Se administra mediante
una única serie de inyecciones intramusculares en las piernas. La dosis en cada punto de
inyección es de 1,5 x 1012 cg/kg de peso.
El receptor de peroxisoma-proliferador-activado (PPAR alfa, delta y gamma): aleglitazar (fase
III) es un agonista dual PPAR alfa/delta/gamma que alcanza una concentración pico a las 3
horas de su administración, con una vida media que varía entre 5 y 16 horas. Este fármaco
incrementó los niveles de c-HDL en forma dependiente de la dosis hasta un 28% y redujo la
concentración de TG hasta un 38%, asociado con la disminución dependiente de la dosis de la
hemoglobina glucosilada (HbA1c) en -0,85%.
Inhibición de la diacilglicerol aciltransferasa-1 (DGAT1): esta enzima está implicada en la
absorción de la grasa dietética desde el intestino delgado y en la síntesis de los TG. El objetivo
potencial para el tratamiento del síndrome de quilomicronemia familiar y la
hipertrigliceridemia en general. Pradigastat (fase III) es un inhibidor de la DGAT1 oral. Redujo
los TG en ayunas hasta en un 70%, sin mayores problemas de seguridad.
4. ASOCIACIONES DE FÁRMACOS
Estatinas + resinas de intercambio catiónico: esta asociación reduce el c-LDL en un 10-20%. No
hay estudios de la combinación de estos últimos con otros fármacos. Esta combinación reduce
la aterosclerosis (evaluada mediante angiografía coronaria).
Estatinas + ezetimibe: es la combinación de elección en pacientes de alto riesgo cardiovascular
que no alcancen los objetivos de reducción del c-LDL. En el estudio IMPROVE-IT se ha
demostrado que esta combinación disminuye los eventos CV y la mortalidad.
Estatinas + fibratos: es una combinación útil en la dislipemia aterógena y en el SM. Está
contraindicada la asociación con gemfibrozilo, por el alto riesgo de rabdomiolisis.
Estatinas + ácidos grasos omega 3: indicados en dislipemia mixta.
Fibratos + ácidos grasos omega 3: para el tratamiento de la hipetrigliceridemia.
BIBLIOGRAFÍA
Alegría-Ezquerra E, et al. La guía europea de dislipemia. Fortalezas y debilidades. Rev Esp Cardiol Supl.
2015;15(A):14-7.
Anguita M, et al. Comentarios a las guías de práctica clínica sobre manejo de las dislipemias de la
Sociedad Europea de Cardiología y la Sociedad Europea de Aterosclerosis 2011. Un informe del Grupo
de Trabajo del Comité de Guías de Práctica Clínica de la Sociedad Española de Cardiología. Rev Esp
Cardiol. 2011:64(12):1090-5.
Bays, et al. National Lipid Association Annual Summary of Lipidology 2015. J Clin Lipidol. 2014;8(6S).
Blom DJ, Hala T, Bolognese M, et al. A 52-week placebo-controlled trial of evolocumab in
hyperlipidemia. New Eng J Med. 2014;370(19):1809-19.
Jarcho JA, Keaney JF Jr. Proof That Lower Is Better--LDL Cholesterol and IMPROVE-IT. N Engl J Med.
2015;372(25):2448-50.
Kamstrup PR, Tybjaerg-Hansen A, Steffensen R, Nordestgaard BG. Genetically elevated lipoprotein(a)
and increased risk of myocardial infarction. JAMA. 2009;301:2331.
Robinson JG, Farnier M. Efficacy and Safety of Alirocumab in Reducing Lipids and Cardiovascular
Events. New Eng J Med. 2014;370:1809-19.
Santos RD and Maranhao RC. What is new in familial hypercholesterolemia? Curr Opin Lipidol.
2014;25:183-8.
Stone NJ, Robinson JG, Lichtenstein AH, et al. 2013 ACC/AHA guideline on the treatment of blood
cholesterol to reduce atherosclerotic cardiovascular risk in adults: a report of the ACC/AHA Task Force
on Practice Guidelines. Circulation. 2014;129(25 Suppl 2):S1-45.
The Task Force for the management of dyslipidaemias of the European Society of Cardiology (ESC) and
the European Atherosclerosis Society (EAS). ESC/EAS Guidelines for the management of dyslipidemias.
Eur Heart J. 2011;32:1769-818.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1191]
[74] TRASTORNOS DE LA SERIE ROJA
74.Trastornos de la serie roja
Teresa Díaz Rueda.
Hematología y Hemoterapia
María Alejandra Duarte Borges.
Medicina Interna
Asesora:
Sandra Gómez Rojas.
Médica Adjunta de Hematología y Hemoterapia
I. ANEMIA
1. CONCEPTO
La anemia se ha definido clásicamente como un descenso de la masa eritrocitaria habitual,
disminuyendo la capacidad de transportar oxígeno a las células para satisfacer las necesidades del
organismo. Estas necesidades pueden cambiar conforme a ciertos parámetros, como la altitud sobre el
nivel del mar, el tabaquismo, el sexo o la edad, variando con ello las cifras normales de hemoglobina (Hb),
que es el mejor parámetro para evaluar la existencia y el grado de anemia.
Se acepta que existe anemia cuando la Hb es menor de 13 g/dL en el varón y de 12 g/dL en la
mujer, mientras que en el embarazo se define por Hb < 11 g/dL en el primer trimestre, < 10,5 g/dL en el
segundo trimestre y < 10 g/dL en el posparto. Esto es debido a que, en mujeres sanas sin ferropenia, las
concentraciones de Hb cambian durante el embarazo para adaptarse al aumento de la volemia materna y a
las necesidades de hierro del feto.
Se habla de pseudoanemia cuando un aumento del volumen plasmático condiciona una
disminución de la Hb de carácter dilucional (por ejemplo, embarazo, insuficiencia cardiaca, esplenomegalia
masiva, mieloma múltiple, macroglobulinemia, hipoalbuminemia, etc.). Por el contrario, las situaciones que
disminuyen el volumen plasmático aumentan falsamente la hemoglobina (hemoconcentración).
2. FISIOPATOLOGÍA Y CLÍNICA
Para evitar la hipoxia tisular, el organismo pone en marcha una serie de mecanismos
compensadores que favorecen la oxigenación celular, y que son responsables de las manifestaciones
clínicas (síndrome anémico). Los signos y síntomas dependen del grado, la rapidez de instauración y la
etiología de la anemia.
Entre los mecanismos compensadores, está el aumento de 2,3-difosfoglicerato en los eritrocitos,
que disminuye la afinidad de la Hb por el oxígeno y facilita su liberación; además, existe un incremento de
eritropoyetina, que se traduce en un mayor estímulo medular para la producción de la serie roja. Por otra
parte, la hipoxia favorece una redistribución del volumen sanguíneo hacia los órganos vitales (como el
sistema nervioso central), produciendo vasoconstricción en otras áreas como la piel y el riñón.
Si la anemia es muy aguda (en hemorragias), puede dar lugar a un shock hipovolémico. Cuando es
crónica, el volumen plasmático aumenta progresivamente, produciéndose una primera fase de adaptación,
con un descenso no proporcional de la Hb por hemodilución. Por ello, en pacientes de edad avanzada y/o
cardiópatas, se debe tener en cuenta que la transfusión de concentrados de hematíes aumenta
rápidamente la volemia y puede precipitar insuficiencia cardiaca.
Las manifestaciones más frecuentes del síndrome anémico son:
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1192]
[74] TRASTORNOS DE LA SERIE ROJA
Astenia, que puede acompañarse de disnea u ortopnea.
Palidez mucocutánea, por vasoconstricción.
Taquicardia, palpitaciones y soplo sistólico funcional (más intenso a mayor rapidez de
instauración): por aumento del débito cardiaco, generalmente con Hb < 7 g/dL.
Pérdida de memoria, cambios de humor, cefalea, vértigo, insomnio, acúfenos, incapacidad para
concentrarse; con Hb < 3 g/dL puede darse hipoxia cerebral o un estado de coma.
3. ETIOLOGÍA
Desde el punto de vista etiológico, las anemias pueden clasificarse en dos grupos: aquellas en las
que la producción medular está conservada (regenerativas) y aquellas debidas a insuficiencia medular, en
las que hay un defecto en la eritropoyesis en distintas etapas madurativas (arregenerativas). La diferencia
entre ambas se establece en función del número de reticulocitos, parámetro fundamental en el estudio de
la anemia (Tabla I).
4. DIAGNÓSTICO
1. ANAMNESIS Y EXPLORACIÓN FÍSICA
Hay que preguntar acerca de hemorragias, tanto agudas como crónicas (ginecológicas,
gastrointestinales, urológicas); fármacos u otros tóxicos (especialmente alcohol y AINE), hábitos dietéticos,
antecedentes personales (enfermedad hepática, renal, endocrinológica, reumatológica, etc.), infecciones
recientes, historial de transfusiones y antecedentes familiares en el caso de anemias de larga evolución.
También es importante buscar síntomas acompañantes que se puedan deber a la causa subyacente, como
síndrome constitucional o fiebre.
2. HEMOGRAMA
Hb y hematocrito (Hto): el Hto indica el porcentaje volumétrico que ocupan los eritrocitos en la
sangre y suele ser aproximadamente el triple de la cifra de Hb, si bien esta relación puede
aumentar en la aglutinación de hematíes, la hemólisis intravascular y la sepsis por Clostridium.
Volumen corpuscular medio (VCM): tamaño medio de los hematíes, siendo lo normal 80-100
fl. En función del VCM, se establece una clasificación morfológica de la anemia en tres grupos
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1193]
[74] TRASTORNOS DE LA SERIE ROJA
(normocítica, microcítica y macrocítica), la cual es la más utilizada para dirigir el diagnóstico
etiológico (Figuras 1-3).
Amplitud de distribución eritrocitaria (ADE) (en inglés, red-cell distribution width [RDW]):
informa de la variabilidad en el tamaño de los hematíes (anisocitosis). Suele oscilar en torno a
13 ± 1,2%.
Hemoglobina corpuscular media (HCM): cantidad de Hb que porta cada eritrocito. Disminuye
en la anemia ferropénica (hipocromía) y en las talasemias, mientras que aumenta en patologías
como la esferocitosis o la macrocitosis de cualquier origen. La concentración de HCM (CHCM)
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1194]
[74] TRASTORNOS DE LA SERIE ROJA
informa sobre la relación entre Hb y Hto y suele mantenerse estable, incluso en presencia de
hipocromía (salvo en ciertas entidades, como la esferocitosis congénita), por lo que su utilidad
clínica es menor.
Recuento de plaquetas: las alteraciones del mismo se pueden asociar a desórdenes causantes
de anemia, bien sea trombopenia (anemia aplásica, hiperesplenismo, sepsis, déficit de ácido
fólico o vitamina B12, etc.), bien trombocitosis (ferropenia, infecciones, entidades inflamatorias
o neoplásicas).
Serie blanca: en general, si la anemia va acompañada de leucopenia (± trombopenia) suele
traducir un defecto medular, con hematopoyesis ineficaz.
3. RETICULOCITOS
Se trata de eritrocitos inmaduros, más grandes que los hematíes maduros. Su recuento permite
dividir las anemias en regenerativas o arregenerativas. En anemias graves, el porcentaje puede estar
sobreestimado, ya que procede del referido a una cifra normal de hematíes, siendo necesaria una
corrección. Es recomendable, por tanto, valorar la cifra absoluta y el índice de producción reticulocitaria
(IPR):
4. FROTIS DE SANGRE PERIFÉRICA
Confirma los hallazgos del hemograma, aportando además valiosa información sobre la morfología
eritrocitaria (Tabla II):
Policromasia: presencia de reticulocitos.
Anisocitosis: variación en el tamaño de los hematíes.
Poiquilocitosis: formas anormales de los hematíes.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1195]
[74] TRASTORNOS DE LA SERIE ROJA
5. PERFIL FÉRRICO (TABLA III)
Sideremia o hierro plasmático: valores normales en torno a 50-150 μg/dL. Disminuye en la
ferropenia y la anemia de enfermedades crónicas; aumenta en la hemocromatosis y la anemia
sideroblástica.
Ferritina sérica: entre 30 y 400 ng/ml en mayores de 50 años (en mujeres de 16-50 años, 15-
150 ng/ml). Su nivel se correlaciona con los depósitos de hierro. Por encima de 100 ng/l, rara
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1196]
[74] TRASTORNOS DE LA SERIE ROJA
vez existe ferropenia. Hay que tener en cuenta que es un reactante de fase aguda, por lo que
puede estar elevada en diferentes situaciones, como en la anemia de trastornos crónicos,
hepatopatía o cualquier estado inflamatorio.
Transferrina: en torno a 200-360 mg/dL. Transporta hierro en el plasma. Su síntesis aumenta
cuando hay déficit de hierro.
Capacidad total de fijación del hierro (CTFH) (en inglés, total iron binding capacity [TIBC]):
mide indirectamente los niveles de transferrina, puesto que determina la cantidad de hierro
precisa para saturar la transferrina plasmática.
Índice de saturación de la transferrina: cociente entre sideremia y CTFH, multiplicado por 100.
Receptor soluble de la transferrina: depende de la cantidad de precursores eritroides y del
hierro tisular. Su incremento es proporcional a la magnitud de la deficiencia de hierro. Su
concentración no aumenta en procesos inflamatorios, a diferencia de la ferritina.
6. OTRAS DETERMINACIONES BIOQUÍMICAS
Lactato deshidrogenasa (LDH), bilirrubina indirecta y haptoglobina si se sospecha hemólisis;
vitamina B12 y ácido fólico en anemia megaloblástica; hormonas tiroideas, andrógenos o corticoides si se
sospechan alteraciones hormonales, etc.
7. BIOPSIA DE MÉDULA ÓSEA
Indicada en casos de anemia normocítica con reticulocitos bajos sin una causa identificable (ver
Figura 2), o en casos de anemia asociada a otras citopenias.
II. PRINCIPALES TIPOS DE ANEMIA
A. Anemia ferropénica
Considerada un problema de salud global, es la principal causa de anemia a nivel mundial,
afectando a más de 2.000 millones de personas. En España presenta una incidencia variable, siendo
aproximadamente del 20% en mujeres en edad fértil y del 10-15% en adolescentes.
1.1. Definición
Se incluye dentro de las anemias arregenerativas y se caracteriza por ser microcítica e hipocroma.
Como su nombre indica, está presente en estados de déficit de hierro, en los que este resulta insuficiente
para satisfacer las necesidades individuales. Tanto el desarrollo del déficit como su velocidad de aparición
varían según el nivel de los depósitos iniciales, lo que depende de múltiples factores, como el sexo (menor
nivel en la mujer), la edad (adulta) y la relación entre absorción y pérdida.
1.2. Etiología (Tabla IV)
1.3. Clínica
Además del síndrome anémico, es posible hallar manifestaciones clínicas directamente
relacionadas con la ferropenia, como estomatitis angular, molestias linguales y atrofia papilar, sequedad de
boca, caída del cabello, coiloniquia (uñas en cuchara), fragilidad ungueal, pica (ingestión compulsiva de
arcilla, hielo, tierra), pirosis, síndrome de piernas inquietas, cefalea, menor tolerancia al ejercicio, etc. Del
mismo modo, podremos encontrar una exacerbación sintomática de procesos subyacentes: angina
(enfermedad coronaria), disnea (insuficiencia cardiaca), confusión (demencia)...
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1197]
[74] TRASTORNOS DE LA SERIE ROJA
1.4. Diagnóstico
1.4.1. Historia clínica y exploración física
Antecedentes personales y familiares, modo de vida, hábitos dietéticos y tóxicos, medicación
habitual. Tiempo de evolución. Es importante insistir en la búsqueda de posibles pérdidas hemáticas, con
especial énfasis en el tracto digestivo.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1198]
[74] TRASTORNOS DE LA SERIE ROJA
1.4.2. Pruebas complementarias
Aparte de los estudios iniciales (hemograma, reticulocitos, frotis de sangre periférica (SP) y perfil
férrico [Figura 4]), se solicitarán otras pruebas más específicas dirigidas a identificar la etiología, según los
hallazgos clínico-analíticos:
Pérdidas hemorrágicas de origen digestivo: panendoscopia oral, colonoscopia, enema opaco
(ver Capítulo 53. “Hemorragia digestiva”).
Pérdidas hemorrágicas genitourinarias: examen urológico y/o ginecológico completo.
Síndromes de malabsorción: descartar gastritis atrófica, enfermedad celíaca, infección por H.
pylori (test del aliento), resecciones gástricas o de intestino delgado.
Hemólisis intravascular: valorar la presencia de prótesis valvulares, hemoglobinuria paroxística
nocturna (HPN).
1.5. Tratamiento
La aproximación dependerá de la gravedad y la causa. De esta forma, en pacientes
hemodinámicamente inestables, con evidencia de daño orgánico secundario, se debe transfundir de forma
urgente (ver Capítulo 78. “Hemoterapia”), mientras que los pacientes con anemia compensada se pueden
tratar de forma conservadora con sustitución de hierro. La indicación de tratar con hierro incluye a los
pacientes con anemia ferropénica y a aquellos con ferropenia sin anemia.
1.5.1. Ferroterapia
La primera decisión radica en la vía de administración, oral o intravenosa, la cual dependerá de
varios factores: tiempo de aparición, coste, disponibilidad y tolerancia. Los preparados de hierro
intravenoso están indicados principalmente en pacientes que no lo toleren por vía oral por sus efectos
adversos (sobre todo ancianos y mujeres embarazadas), en aquellos con patología gastrointestinal
subyacente (como enfermedad inflamatoria intestinal, cirugía gástrica previa, síndromes de malabsorción)
o con enfermedad renal crónica, y en los que ha fracasado la vía oral.
Hierro oral: los preparados se pueden ver en la tabla V. En pacientes de edad avanzada son
recomendables los preparados de sales ferrosas, debido a su mejor absorción. Se aconseja
acompañar con zumo de naranja (o 50-100 mg de ácido ascórbico), 30 minutos antes del
desayuno, para mejorar la tolerancia y potenciar la absorción. En algunos casos, se puede
plantear dar dosis elevadas en días alternos.
La dosis diaria es variable:
Pacientes con anemia ferropénica: 150-200 mg de hierro elemental al día.
Pacientes con déficit de hierro sin anemia: 30-50 mg de hierro elemental al día
(una vez normalizada la Hb).
Precauciones: no dar con las comidas, administrar separado de alimentos (incluyendo
café y té) y de medicamentos que contengan calcio.
Efectos secundarios: sabor metálico, náuseas, flatulencia, estreñimiento, diarrea,
epigastralgia, vómitos. Heces de coloración negro/verdosa.
Monitorización: analítica a las 2-4 semanas de iniciado el tratamiento (un aumento de 2
g/dL de Hb se considera una respuesta adecuada).
Tiempo de tratamiento: entre 6-8 semanas para mejorar la cifra de Hb; hasta 6 meses
para reponer los depósitos de hierro.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1199]
[74] TRASTORNOS DE LA SERIE ROJA
Hierro intravenoso (Tabla VI):
Dosis: hay fórmulas para cada preparado que permiten el cálculo de la dosis total a
administrar. No existe evidencia de que dosis > 1.000 mg de hierro elemental tengan
beneficio.
Premedicación: valorar en pacientes con asma, alergia a más de un medicamento o
artritis inflamatoria. Se recomienda administrar 125 mg de metilprednisolona antes de
la infusión.
Monitorización: pasadas 4 semanas de la administración. Reticulocitos: aumento en 7-
10 días. Hb: aumento de 2 g/dL en 3 semanas.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1200]
[74] TRASTORNOS DE LA SERIE ROJA
B. Anemia de trastornos crónicos
2.1. Definición y etiología
También se denomina anemia de estados inflamatorios, ya que es secundaria a una enfermedad
sistémica o inflamación crónica. Ocupa el segundo lugar de prevalencia a nivel mundial, tras la anemia
ferropénica, siendo la más frecuente en pacientes hospitalizados. Se ha relacionado con múltiples
trastornos, incluyendo infecciones, neoplasias (hematológicas o tumores sólidos), patologías autoinmunes
(artritis reumatoide, lupus eritematoso sistémico, vasculitis), lesiones tisulares extensas (quemaduras,
fracturas, úlceras), insuficiencia renal crónica e insuficiencia cardiaca, entre otros.
Entre los mecanismos relacionados con su aparición, encontramos una alteración en la homeostasis
del hierro (deficiencia funcional por bloqueo del mismo en el sistema reticuloendotelial), una reducción de
la síntesis de eritropoyetina (EPO) y de la proliferación de progenitores de la serie roja, así como una
reducción de la vid a media de los eritrocitos.
2.2. Clínica
Relacionada con el trastorno orgánico subyacente, solapada con el síndrome anémico. En general,
la anemia es leve-moderada e insidiosa. Existe una variante aguda, que se relaciona con un evento en
particular (cirugía, trauma, infarto de miocardio, sepsis).
2.3. Diagnóstico
El objetivo principal será diferenciarla de la anemia ferropénica (ver Tabla III).
Hemograma: suele ser una anemia normocítica (aunque a veces es microcítica) y
normocrómica, con reticulocitos bajos. Puede acompañarse de alteración de otras líneas
celulares (neutrofilia, trombocitosis).
Bioquímica: elevación de reactantes de fase aguda (proteína C reactiva, velocidad de
sedimentación globular). Niveles de EPO disminuidos.
Otras pruebas (según la sospecha): autoinmunidad, imagen, microbiología, histología…
Raramente es necesaria una biopsia de médula ósea (aumento de los depósitos de hierro y
disminución de sideroblastos).
2.4. Tratamiento
Radica en el tratamiento del proceso inflamatorio o maligno subyacente.
Transfusión: se reserva para casos de riesgo vital o síndrome anémico muy sintomático (ver
Capítulo 78. “Hemoterapia”).
Agentes estimulantes de la eritropoyesis (ver Apartado 3.3): podrían ser beneficiosos en
pacientes con niveles de EPO <500 mU/ml.
Hierro sustitutivo: si coexiste ferropenia; principalmente se plantea en pacientes que estén
recibiendo tratamiento con EPO, para obtener valores de saturación de transferrina > 20% y de
ferritina > 100 ng/ml.
C. Anemia en la insuficiencia renal
Es un hallazgo bastante frecuente en pacientes con enfermedad renal crónica y se asocia con un
aumento del riesgo cardiovascular y de la morbimortalidad. Su presencia tiene una importante relación con
la disminución de la tasa de filtrado glomerular, estimándose que aproximadamente el 90% de los
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1201]
[74] TRASTORNOS DE LA SERIE ROJA
pacientes con filtrado < 20 ml/min presentarán anemia. Del mismo modo, a mayor edad, mayor es la
incidencia.
3.1. Etiopatogenia
Está determinada por la interacción de los siguientes factores:
Inhabilidad del organismo para producir EPO, considerado el más relevante.
Estado inflamatorio crónico presente en los pacientes con enfermedad renal, con pérdida
funcional de hierro (no disponible para la eritropoyesis).
Pérdidas hemáticas crónicas, secundarias a diálisis (principalmente hemodiálisis).
3.2. Diagnóstico
Descartar la existencia de otros factores potencialmente reversibles, realizando un estudio
completo que incluya: hematología, perfil férrico, niveles de EPO, búsqueda de pérdidas hemáticas, niveles
de vitamina B12 y ácido fólico.
3.3 Tratamiento
Las herramientas de las que disponemos incluyen:
Transfusiones: solo indicadas en pacientes sintomáticos, en caso de cirugía mayor y
complicaciones hemorrágicas (ver Capítulo 78. “Hemoterapia”).
Agentes estimulantes de la eritropoyesis: las indicaciones para su uso incluyen: Hb < 10 g/dL,
en ausencia de ferropenia (ferritina > 100 ng/ml) o tras corrección previa de la misma; ausencia
de antecedente de accidente isquémico vascular o de patología neoplásica maligna de base. El
objetivo será alcanzar cifras de Hb entre 11 y 12 g/dL. Incluyen:
Epoetina alfa (Eprex®/Epopen®): hemodiálisis (HD)/prediálisis: 50 UI/kg tres veces por
semana. Diálisis peritoneal (DP): 50 UI/kg dos veces por semana. Mantenimiento: HD,
dosis semanal total entre 75-300 UI/kg; prediálisis, 17-33 UI/kg tres veces por semana;
DP, 25-50 UI/kg dos veces por semana. Se recomienda suspender el tratamiento si la
cifra de hematocrito es > 40%, y reiniciarlo si es < 36% (usando el 75% de la última
dosis).
Epoetina beta (NeoRecormon®): 20 UI/kg tres veces a la semana por vía subcutánea, o
40 UI/kg tres veces a la semana por vía intravenosa. Dosis máxima: 720 UI/kg/ semana.
Mantenimiento: la mitad de la dosis anterior; ajuste posterior cuando se alcance la
estabilidad. Administrar cada dos semanas. Se recomienda suspender el tratamiento si
la cifra de hematocrito es > 40%, y reiniciarlo si es < 36% (usando el 75% de la última
dosis).
Darbepoetina alfa (Aranesp®): HD/DP: 0,45 μg/kg/semana. Prediálisis: 0,75 μg/kg cada
dos semanas. Mantenimiento: HD/DP, una vez por semana o cada dos semanas;
prediálisis, una vez al mes. Si la cifra de hematocrito es > 36%, se recomienda
suspender; si desciende por debajo de dicho valor, reiniciar con el 75% de la dosis
previa.
Es importante resaltar que estos datos son orientativos y recomendamos que su indicación sea
realizada por el especialista tratante. Vía de administración: intravenosa en pacientes en hemodiálisis,
subcutánea en pacientes en prediálisis o diálisis peritoneal.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1202]
[74] TRASTORNOS DE LA SERIE ROJA
D. Anemia megaloblástica
4.1. Definición
Se debe a una alteración en la maduración de los precursores hematopoyéticos por una síntesis
defectuosa del ADN, comprometiendo a todas las series celulares. Es característica la existencia de anemia
con macrocitosis (VCM > 100 fl), produciéndose asimismo una mielopoyesis ineficaz con hemólisis
intramedular.
4.2. Etiología
En casi todos los casos su origen radica en un déficit de B12 (cobalamina) y/o folato (Tabla VII).
Déficit de vitamina B12: como los requerimientos diarios son bajos (mínimo 2 μg/dL) y el
organismo presenta depósitos de hasta 5 mg, su aparición es insidiosa (hasta 3-4 años desde el
inicio del déficit). Actualmente, se considera que la causa más frecuente de este déficit es la
malabsorción, como ocurre en casos de aclorhidria, en los que disminuye la secreción ácida,
reduciendo la liberación de la vitamina B12 de las proteínas de los alimentos.
Déficit de folato: se manifiesta a los 3-4 meses de iniciado el déficit, debido a la existencia de
depósitos pequeños (5-10 mg) en relación con los requerimientos diarios (200-400 μg).
4.3. Clínica
Alteraciones hematológicas: síndrome anémico (astenia, disnea, mareo, palpitaciones, etc.),
síntomas derivados de la pancitopenia.
Manifestaciones neurológicas: relacionadas exclusivamente con el déficit de cobalamina.
Incluyen parestesias, ataxia, debilidad, alteración de la memoria, cambios en la personalidad,
neuropatía periférica, disfunción autonómica... Es característica la degeneración combinada
subaguda de la médula espinal, con afectación piramidal y de cordones posteriores, poco
frecuente en la actualidad.
Los síntomas neurológicos y hematológicos no tienen correlación; pueden existir alteraciones
neurológicas importantes sin anemia, y viceversa.
4.4. Diagnóstico
Hemograma: anemia con elevación de volumen corpuscular medio y cifra de reticulocitos
normal o baja. Frotis de SP (Tabla II).
Bioquímica: aumento de LDH y bilirrubina indirecta, por eritropoyesis ineficaz.
Niveles de cobalamina: por debajo de 148 pmol/l (200 pg/ml) tienen una alta sensibilidad para
el diagnóstico del déficit. En el embarazo descienden los niveles de forma habitual, de manera
que cifras de 110-148 pmol/l (150-200 pg/ml) pueden ser fisiológicas (valorar déficit en función
de la sintomatología y la presencia de anticuerpos anti-factor intrínseco). Niveles de folato, de
forma paralela: existe déficit si < 3 ng/ml.
Determinación de metabolitos intermediarios en sangre: la homocisteína está elevada en las
deficiencias de ambas vitaminas, mientras que el ácido metilmalónico solamente aumenta en
la de vitamina B12. Se deben determinar cuando existe alta sospecha clínica de déficit
vitamínico con niveles indeterminados en suero.
Valorar la posibilidad de anemia perniciosa y solicitar pruebas dirigidas al diagnóstico
etiológico:
Anticuerpos anti-factor intrínseco y anti-células parietales: los anticuerpos anti-factor
intrínseco tienen una sensibilidad en torno al 70%, con una especificidad alta, del 95%,
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1203]
[74] TRASTORNOS DE LA SERIE ROJA
mientras que los anticuerpos anti-células parietales tienen una sensibilidad del 90%,
pero con una especificidad del 50%, por lo que no son concluyentes para el diagnóstico
de anemia perniciosa y algunas guías desaconsejan su uso.
Endoscopia digestiva alta: no se recomienda su realización de forma rutinaria, excepto
en los casos de coexistencia con anemia ferropénica o sintomatología específica que
haga sospechar gastritis crónica atrófica (con riesgo leve de progresión a malignidad).
4.5. Tratamiento
Identificar y tratar la causa de la deficiencia.
Como no se suele disponer del diagnóstico del déficit de forma inmediata, se iniciará tratamiento
combinado o con cobalamina en primer lugar, ya que el uso exclusivo de ácido fólico puede empeorar las
manifestaciones neurológicas debidas al déficit de vitamina B12. Una vez conocido el déficit concreto se
tratará solamente este.
4.5.1. Déficit de vitamina B12
Vitamina B12 parenteral o intramuscular:
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1204]
[74] TRASTORNOS DE LA SERIE ROJA
Pacientes sin clínica neurológica: 1 mg, tres veces en semana, durante dos semanas;
después, continuar con 1 mg cada tres meses hasta la corrección de la causa. En caso
de anemia perniciosa, el tratamiento se debe mantener de por vida.
Pacientes con clínica neurológica: dosis inicial de 1 mg/día durante siete días; después,
seguir con 1 mg/semana hasta que mejoren los síntomas neurológicos. Más adelante,
continuar con 1 mg cada dos meses, durante al menos seis meses.
Vitamina B12 por vía oral: dosis diarias de 1-2 mg han demostrado ser tan efectivas como la vía
intramuscular, incluso en pacientes con anemia perniciosa. Se recomienda tratamiento
profiláctico con 400 μg/día de ácido fólico.
4.5.2. Déficit de folato:
Ácido fólico: 5 mg/día por vía oral durante cuatro meses; posteriormente, se continuará con el
tratamiento si no se logra corregir la causa del déficit.
La profilaxis con dosis menores de ácido fólico se lleva a cabo en situaciones especiales, como
anemias hemolíticas crónicas, trastornos hematológicos hiperproliferativos, gestación, hemodiálisis y toma
de antagonistas del ácido fólico.
4.5.3. Monitorización:
Vigilar cifras de potasio (riesgo de hipopotasemia) y ácido úrico (puede aumentar).
Recuperación de cifras de LDH y bilirrubina indirecta.
Elevación de reticulocitos a los 7 días y de hemoglobina tras 6-8 semanas; si no se produce
respuesta hematológica en este periodo, se debe replantear el diagnóstico o valorar la
coexistencia con otros déficits.
E. Anemia hemolítica
5.1. Concepto y clasificación
Se produce una disminución en la vida media del eritrocito, la cual, en condiciones normales, se
sitúa en aproximadamente 120 días. Dado que la destrucción de los hematíes se produce fuera de la
médula, se estimula la eritropoyesis, con incremento de reticulocitos. De este modo, puede existir
hemólisis sin anemia o hemólisis compensada, ya que la médula ósea tiene la capacidad de aumentar la
producción eritrocitaria entre cinco y ocho veces (en adultos y niños, respectivamente).
La hemólisis o destrucción prematura del hematíe se puede deber a defectos propios del mismo
(corpusculares) o a causas extrínsecas (extracorpusculares). Con la excepción de la HPN, las anemias
hemolíticas (AH) corpusculares suelen ser hereditarias (Tabla I).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1205]
[74] TRASTORNOS DE LA SERIE ROJA
Aparte de esta división etiológica, las AH también se pueden clasificar, según el lugar de hemólisis,
en extravasculares, cuando existe una exacerbación de la eliminación fisiológica de los hematíes (en el
sistema mononuclear-fagocítico [SMF]), e intravasculares, cuando se produce su rotura en el interior de los
vasos. En toda AH existe un componente mixto, pero puede predominar uno u otro mecanismo (Tabla VIII).
5.2. Clínica
Las manifestaciones clínicas del síndrome hemolítico dependen de su rapidez de instauración.
AH aguda (crisis hemolítica): dolor abdominal o lumbar, fiebre, malestar general, taquicardia,
fatiga muscular, palidez intensa o ictericia y coloración oscura de la orina. Si es muy intensa
puede manifestarse como shock e insuficiencia renal.
AH crónica: hay tiempo para que se pongan en marcha mecanismos de adaptación, dando
lugar a un síndrome anémico de intensidad variable, que se puede acompañar de ictericia o
esplenomegalia. Muchos casos son hereditarios, mostrando complicaciones derivadas de la
hipoxia crónica (en niños puede producir alteraciones del desarrollo), la eritropoyesis
aumentada (sobrecarga férrica, consumo de ácido fólico, deformación ósea en niños) y el
hipercatabolismo de la Hb (litiasis biliar, etc.). Los cuadros hemolíticos crónicos pueden,
además, descompensarse por tres mecanismos: crisis de aplasia selectiva de la serie roja, por
infección por parvovirus B19; crisis de anemia megaloblástica, por consumo de ácido fólico; o
reagudización o crisis hemolítica, con empeoramiento de la anemia y de los parámetros de
hemólisis por hiperesplenismo (a veces asociado a leucopenia y trombopenia).
5.3. Diagnóstico (Figura 5)
5.3.1. Sospecha de hemólisis
Historia clínica: particularmente relevante si se sospecha una AH congénita; preguntar por la
edad de aparición, ictericia neonatal, historia familiar de anemia, relación con toma de
alimentos, origen étnico (talasemia y esferocitosis hereditaria en el área mediterránea, anemia
falciforme y déficit de glucosa-6-fosfato deshidrogenasa en individuos de raza negra, etc.).
También es importante investigar sobre la toma de fármacos y enfermedades previas
(valvulopatía cardiaca, hepatopatía, infecciones, etc.).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1206]
[74] TRASTORNOS DE LA SERIE ROJA
Laboratorio: ciertos datos deben hacernos sospechar la presencia de hemólisis (Tabla IX). Otras
pruebas (descenso de hemopexina o de Hb glucosilada, medición de estercobilinógeno fecal)
son menos específicas o no se usan de forma rutinaria. Lo mismo ocurre con la determinación
de la vida media eritrocitaria (mediante cromo marcado), que si bien es la única prueba
confirmatoria de hemólisis, no suele emplearse en la práctica por cuestiones técnicas (requiere
isótopos radioactivos, mediciones durante al menos 20 días, etc.).
5.3.2. Frotis de sangre periférica (SP)
Una vez establecida la sospecha de AH mediante las determinaciones anteriores, es conveniente
realizar un frotis de SP, que si bien no es diagnóstico por sí mismo, puede confirmar los hallazgos del
hemograma e informar sobre la morfología eritrocitaria, aportando datos complementarios sobre el posible
origen de la anemia (Tabla II).
5.3.3. Test de Coombs directo
Prueba de gran utilidad en el algoritmo diagnóstico de la AH, ya que, si resulta positivo, orientará a
un origen inmune de la misma, mientras que, si es negativo, aunque la etiología inmune no queda
totalmente descartada, se deben buscar otras posibles causas de hemólisis.
Ante una AH de mecanismo inmune habrá que considerar diversas entidades (Figura 6): puede
tener un origen aloinmune (según las características del paciente, especialmente si ha recibido
transfusiones recientes) o, lo que es mucho más frecuente, ser de tipo autoinmune (ver Tabla X).
Si, por el contrario, se llega a la conclusión de que la hemólisis es no inmune, se deberá pensar en
otros trastornos (Figura 7), entre los cuales siempre hay que recordar la microangiopatía, siendo de vital
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1207]
[74] TRASTORNOS DE LA SERIE ROJA
importancia descartar la existencia de púrpura trombótica trombocitopénica/ síndrome hemolítico
urémico, cuyo diagnóstico depende de criterios clínicos, sin que exista ninguna prueba confirmatoria (ver
Capítulo 76. “Trombocitopenia. Trombocitosis. Pancitopenia”).
5.3.4. Otras pruebas
En caso de sospecha de AH congénita: electroforesis de Hb, test enzimáticos o para diagnóstico
de membranopatías.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1208]
[74] TRASTORNOS DE LA SERIE ROJA
En caso de sospecha de HPN: citometría de flujo (ver Capítulo 76. “Trombocitopenia.
Trombocitosis. Pancitopenia”).
5.4. Tratamiento
Dependiendo de la etiología, se pueden llevar a cabo actuaciones específicas (Tabla XI), siempre
teniendo en cuenta unos principios generales:
Corrección de la causa subyacente, si se conoce.
Tratamiento de soporte: hidratación adecuada, vigilancia del equilibrio ácido-base, de la
función renal, etc.
Corticoterapia: especialmente en caso de sospecha de origen inmune.
La esplenectomía puede estar indicada en casos graves y en algunas AH congénitas.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1209]
[74] TRASTORNOS DE LA SERIE ROJA
Limitar al máximo las transfusiones. La decisión de transfundir no debe estar basada solo en la
cifra de Hb; hay que tener en cuenta la situación clínica del paciente, su edad, las
comorbilidades y la velocidad de instauración de la anemia (ver Capítulo 78. “Hemoterapia”).
En caso de decidir transfundir, se debe premedicar con corticoides (prednisona 1-2 mg/kg) y
administrar muy lentamente.
III. ERITROCITOSIS (POLICITEMIA)
1. CONCEPTO
Exceso de la masa eritrocitaria total del organismo. Se sospecha cuando la cifra de Hb supera 18,5
g/dL en el hombre o 16,5 g/dL en la mujer, y/o cuando el Hto es mayor del 52% o del 48%,
respectivamente. La eritrocitosis conlleva un incremento secundario de la viscosidad de la sangre,
aumentando así el riesgo de trombosis y la morbimortalidad cardiovascular.
2. CLASIFICACIÓN
Policitemia relativa: secundaria a un descenso del volumen plasmático. Incluye la enfermedad
de Gaisböck o policitemia espuria, la cual se asocia con frecuencia al síndrome metabólico.
Policitemia absoluta: existe un aumento real de la masa celular eritrocitaria. Puede ser:
Primaria: si el defecto se encuentra a nivel de la medula ósea, por una mutación
heredada o adquirida en los progenitores hematopoyéticos. Aquí se encuadra la
policitemia vera (PV), perteneciente al grupo de neoplasias mieloproliferativas
crónicas, en la cual se produce pancitosis (no solo eritrocitosis) por afectación de la
célula madre pluripotencial, en relación con mutaciones en el gen JAK2.
Secundaria: si hay algún factor externo que estimula la eritropoyesis (dependientes de
eritropoyetina [EPO]). Se incluyen en este grupo la insuficiencia respiratoria, patologías
cardiacas, alteraciones renales o la administración de EPO exógena. La obesidad, el
consumo de alcohol, el hábito tabáquico o la hipertensión arterial son algunos factores
relacionados con su aparición.
3. ETIOLOGÍA (Tabla XII)
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1210]
[74] TRASTORNOS DE LA SERIE ROJA
4. CLÍNICA
Inespecífica. Pueden darse síntomas relacionados con el estado de hiperviscosidad, incluyendo
mialgias, debilidad, fatiga, cefalea, visión borrosa o amaurosis, parestesias, alteración del comportamiento
(enlentecimiento), etc. En la PV es típica la aparición de prurito, sobre todo con el contacto con agua
caliente.
5. DIAGNÓSTICO
Tras su identificación, por lo general de forma incidental, se recomienda confirmar el diagnóstico
tras un intervalo mínimo de una semana, preferiblemente un mes. Las pruebas diagnósticas iniciales
incluirán:
Anamnesis y exploración física: preguntar por hábitos tóxicos y fármacos (tiazidas, esteroides,
testosterona). Se deben buscar síntomas y signos compatibles con patología cardiaca o
respiratoria, así como indagar acerca de antecedentes de nefropatía. El examen físico ha de ser
completo, incluyendo pruebas neurológicas. La presencia de eritrosis franca y, especialmente,
de esplenomegalia orienta hacia la sospecha de PV.
Análisis: hematología completa, perfil férrico, niveles de vitamina B12 y folato. Función renal y
hepática. Saturación arterial de oxígeno.
Pruebas de imagen: radiografía de tórax, ecografía abdominal.
Cifra de EPO (al menos dos determinaciones): su valor disminuido apoya el diagnóstico de PV,
mientras que si está aumentada o normal pensaremos en causas secundarias. En función de
dicho resultado, es posible establecer un algoritmo diagnóstico (Figura 8).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1211]
[74] TRASTORNOS DE LA SERIE ROJA
6. TRATAMIENTO
Dependerá de la causa subyacente.
BIBLIOGRAFÍA
Adamson JW. Ferropenia y otras anemias hipoproliferativas. En: Longo DL, Kasper DL, Jameson J, et al,
editores. Harrison. Principios de Medicina Interna. 18.ª ed. New York, NY: McGraw-Hill; 2012.
Disponible en: http://harrisonmedicina.mhmedical.com/content.aspx – Bain BJ. Diagnosis from the
blood smear. N Engl J Med. 2005;353(5):498-507.
British Committee for Standards in Haematology: UK guidelines on the management of iron deficiency
in pregnancy; 2011.
Camaschella C. Iron-deficiency anemia. N Engl J Med. 2015;372:1832-43. DOI:
10.1056/NEJMra1401038
Cullis J. Diagnosis and management of anaemia of chronic disease: Current status. Br J Haematol.
2011;154: 289-300.
DeLoughery T. Microcytic anemia. N Engl J Med. 2014;371:1324-31. DOI: 10.1056/NEJMra1215361
Hoffbrand A. Anemias megaloblásticas. En: Longo DL, Kasper DL, Jameson J, et al, editores. Harrison.
Principios de Medicina Interna. 18.ª ed. New York, NY: McGraw-Hill; 2012. Disponible en: http://
harrisonmedicina.mhmedical.com/content.aspx
Hunt A, Harrington D, Robinson S. Vitamin B12 deficiency. BMJ. 2014;349:g5226. DOI:
10.1136/bmj.g5226
Jackups R, Sanfilippo K, Wang T, Blinder M. Hematologic disorders and transfusion therapy. En: Godara
H, Hirbe A, Nassif M, et al, editores. The Washington manual of medical therapeutics. 34th ed.
Lippincott Williams & Wilkins; 2014. p. 760-73.
Keohane C, McMullin M, Harrison C. The diagnosis and management of erythrocytosis. BMJ.
2013;347:f6667. DOI: 10.1136/bmj.f6667.
Koury MJ, Rhodes M. How to approach chronic anemia. Hematology. Am Soc Hematol Educ Program.
2012;2012:183-90. DOI: 10.1182/asheducation-2012.1.183
Kutuby F, Wang S, Desai V, Lerma E. Anemia of chronic kidney disease. Dis Month. 2015;61:421-4.
McMullin M, Bareford D, Campbell P, et al. Guidelines for the diagnosis, investigation and management
of polycythaemia/erythrocytosis. Br J Haematol. 2005;130:174-95.
Sans-Sabrafen J, Besses Raebel C, Vives Corrons JL. Hematología Clínica. 5.ª ed. Elservier; 2007.
Sanz MA, Carreras E. Manual práctico de hematología clínica. 5.ª ed. Editorial Antares; 2015.
Stabler S. Vitamin B12 deficiency. N Engl J Med. 2013;368:149-60. DOI: 10.1056/NEJMcp1113996
World Health Organization. Haemoglobin concentrations for the diagnosis of anaemia and assessment
of severity. Vitamin and Mineral Nutrition Information System. Geneva, World Health Organization;
2011 (WHO/ NMH/NHD/MNM/11.1).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1212]
[75] TRASTORNOS DE LA SERIE BLANCA
75.Trastornos de la serie blanca
María del Pilar Hernández Jiménez.
Medicina Interna
José María Sánchez Pina.
Hematología y Hemoterapia
Asesora:
Rosa Ayala Díaz.
Médica Adjunta de Hematología y Hemoterapia
I. INTRODUCCIÓN
La serie blanca es el conjunto de células hematopoyéticas encargadas de la inmunidad en el
organismo. Se compone de grupos celulares con especialización en distintos tipos de defensa frente a
agentes externos e internos. Los granulocitos-monocitos (sistema reticuloendotelial), primera línea de
inmunidad, son, junto con los linfocitos, los principales efectores. Eosinófilos y basófilos representan
fracciones minoritarias con funciones en muchos casos aún desconocidas, en relación con fenómenos de
hipersensibilidad y reacción frente a cuerpos extraños. Mediante la liberación de citocinas y factores
inflamatorios, se produce la interacción que coordina el conjunto de participantes. La fracción evaluable en
sangre periférica es una representación incompleta de la distribución real de estas células en el cuerpo,
entre la médula ósea, el sistema ganglionar y los tejidos.
Las alteraciones de la serie blanca son extremadamente frecuentes en la práctica clínica, dada la
reactividad de este compartimento en relación con múltiples procesos sistémicos. En este capítulo se
estudiarán los trastornos de esta serie desde un punto de vista práctico, atendiendo al exceso o descenso
de sus distintas poblaciones.
II. LEUCOCITOSIS
Se define de manera arbitraria como la presencia en sangre periférica de una cifra de leucocitos por
encima de 10.000/mm3. Cuando dicha cifra supera los 50.000/mm3 se denomina reacción leucemoide, y
presenta una significación clínica y una aproximación diagnóstica específica. La leucocitosis se puede
producir a expensas de las distintas poblaciones leucocitarias, aunque la más frecuente es la neutrofilia,
seguida de la linfocitosis.
En todos los casos, el primer paso será la comprobación de los datos analíticos, así como la
realización de una anamnesis y una exploración completas y dirigidas en función de la sospecha etiológica,
que condicionarán el proceder diagnóstico-terapéutico subsiguiente
1. NEUTROFILIA
Se define como un recuento absoluto de neutrófilos mayor de 7.500/mm3 en adultos.
1.1. Causas (Tabla I)
Se conoce como reacción leucemoide la existencia en sangre periférica de más de 50.000
leucocitos/mm3; suele conllevar un incremento considerable en la cifra de neutrófilos. Puede ocurrir tras
infecciones graves, vasculitis, hemólisis severa, hemorragias, cetoacidosis o quemaduras. Es imprescindible
realizar un frotis de sangre periférica, donde se suele observar una serie mieloide madura con un muy
pequeño componente inmaduro, junto con granulación tóxica, vacuolas y cuerpos de Döhle. Esta prueba
ayuda a distinguir la reacción leucemoide del síndrome mieloproliferativo crónico (SMPc), ya que este
último generalmente se presenta como una neutrofilia sin causa aparente, mantenida en el tiempo, que se
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1213]
[75] TRASTORNOS DE LA SERIE BLANCA
acompaña de esplenomegalia, siendo habitual observar en sangre periférica un aumento de formas más
inmaduras (blastos, promielocitos) y, ocasionalmente, basofilia.
La asociación de anomalías en otras series orientará el diagnóstico:
Anemia: infección e inflamación crónicas, anemia hemolítica, malignidad.
Aumento del hematocrito: policitemia vera.
Descenso de plaquetas: sepsis, coagulación intravascular diseminada, síndrome hemolítico
urémico/púrpura trombótica trombocitopénica.
Trombocitosis: infección, inflamación, malignidad, reconstitución medular. Trombocitemia
esencial.
Reacción leucoeritroblástica (presencia de células inmaduras de las series mieloide y eritroide
en sangre periférica): shock séptico, infiltración medular (por fibrosis, neoplasia,
granulomatosis).
1.2. Aproximación diagnóstica
La mayoría de las causas son abordables por la anamnesis y la exploración física inicial, atendiendo
especialmente a infecciones, antecedentes familiares, enfermedades previas, alteraciones metabólicas,
estrés, fármacos y tóxicos, así como sintomatología general junto con organomegalias, asplenia y fiebre. En
la bioquímica, será importante valorar datos que apoyen la reactividad del proceso, como los reactantes de
fase aguda. Si no hay datos que hagan sospechar la existencia de una causa que lo origine, o la cifra de
leucocitos es exagerada, se solicitará un estudio morfológico de sangre periférica. En función de los valores
y del frotis de sangre periférica:
Se debe pensar en una causa reactiva cuando el número total de leucocitos sea menor de
50.000/mm3 y los neutrófilos sean maduros, presenten granulaciones tóxicas y vacuolas
(también en monocitos), con cuerpos de Döhle o trombocitosis asociada.
Sin embargo, los datos que podrían sugerir etiología neoplásica serán un recuento leucocitario
mayor de 50.000/mm3, la asociación de basofilia, eosinofilia, dacriocitos o displasia, y que el
aumento sea prolongado en el tiempo.
2. MONOCITOSIS
Puede acompañar a la neutrofilia, y refleja una activación crónica del sistema fagocítico-
mononuclear. Con cifras por encima de 1.000/mm3, de forma mantenida, se recomienda la búsqueda de
mielodisplasia/neoplasia hematológica.
2.1. Causas (Tabla II)
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1214]
[75] TRASTORNOS DE LA SERIE BLANCA
Se tratará de una monocitosis reactiva cuando sea transitoria, con elementos maduros y cambios
reactivos (vacuolas, etc.). Sin embargo, apoyará un origen neoplásico el hecho de que la monocitosis sea
persistente, con existencia de promonocitos, blastos o displasia en la extensión de sangre periférica.
3. LINFOCITOSIS
Se define en adultos arbitrariamente como un recuento absoluto de linfocitos mayor de
4.000/mm3, siendo las causas principales las reactivas y, dentro de estas, las secundarias a viriasis.
3.1. Causas (Tabla III)
3.2. Aproximación diagnóstica (Figura 1)
Se realizará la historia clínica atendiendo sobre todo a los antecedentes infecciosos cercanos que
orienten a infección vírica, a la edad y a la existencia de un cuadro constitucional con presencia de síntomas
B (fiebre, sudoración nocturna, pérdida de peso). De la misma manera, se llevará a cabo la exploración
física, en la que se ha de tener especial cuidado al valorar la existencia de hepatoesplenomegalia y
adenopatías. Los datos analíticos más relevantes son el tiempo de evolución de la linfocitosis, la elevación
de la lactato-deshidrogenasa (LDH) sin alteración de otras enzimas y la existencia de otras citopenias o
coagulopatía.
Cuando, tras realizar la historia clínica y cotejar otros datos analíticos, no se explique la causa, se
recomienda solicitar un estudio morfológico (frotis), que orientará la etiología del proceso:
Pleomórfico: indica reactividad a un proceso infeccioso, inflamatorio, estrés, etc. La presencia
de linfocitos activados y en apoptosis es muy sugestiva de síndrome mono- nucleósico.
Monomórfico: la morfología nuclear y citoplasmática, característica de determinados procesos
linfoproliferativos, ayuda a orientar el estudio. Indica la necesidad de realizar una citometría de
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1215]
[75] TRASTORNOS DE LA SERIE BLANCA
flujo para confirmar la clonalidad y el tipo de síndrome linfoproliferativo (SLP). La existencia de
un cuadro leucoeritroblástico acompañante sugiere la extensión medular del proceso.
El estudio de citometría de flujo permite sospechar, valorando el porcentaje de las poblaciones
linfocitarias, y posteriormente confirmar, mediante la restricción de cadenas ligeras, la clonalidad de la
linfocitosis. Mediante el estudio de los antígenos de superficie (inmunofenotipo) es posible reconocer el
tipo de proceso linfoproliferativo. Cuando dicho estudio no es capaz de distinguir el tipo de SLP, se recurre
al estudio citogenético, que podrá identificarlo gracias a mutaciones características de estos procesos. En el
caso de sospechar un síndrome linfoproliferativo T, la clonalidad se puede demostrar mediante estudios de
biología molecular, con los reordenamientos en el T cell receptor (TCR).
4. BASOFILIA
Se define como la existencia de una cifra de basófilos mayor de 200/mm3. Entre sus causas se
encuentran hipersensibilidad, déficit de hierro e inflamación crónica; ocasionalmente, se puede dar en
infecciones (gripe, varicela). Se recomienda la búsqueda de una neoplasia subyacente (SMPc), por ser muy
raro su origen reactivo.
5. EOSINOFILIA
Se distinguen tres formas en función de los valores sanguíneos, así como de la presencia o no de
afectación tisular secundaria (predominantemente piel, pulmón, tubo digestivo, sistema nervioso y
corazón).
Eosinofilia: ≥ 500/mm3; se divide en leve (500-1.500), moderada (1.500-5.000) y grave (>
5.000).
Hipereosinofilia: ≥ 1.500/mm3. Suelen existir manifestaciones de daño orgánico.
Síndrome hipereosinofílico (SHE): grupo de entidades con las siguientes características
comunes:
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1216]
[75] TRASTORNOS DE LA SERIE BLANCA
≥ 1.500/mm3 en al menos dos ocasiones.
Signos de disfunción orgánica atribuible a la eosinofilia.
Exclusión de otras causas.
Distinguimos entre:
SHE primario: aquel asociado a neoplasia hematológica.
SHE secundario: relacionado con causas alérgicas, parásitos, fármacos, etc.
SHE idiopático: sin causa determinada tras un estudio diagnóstico completo.
5.1. Causas (Tabla IV)
5.2. Aproximación diagnóstico-terapéutica
Es fundamental la recogida de la historia farmacológica, de exposición ambiental, alimentaria,
profesional y de viajes, así como de contacto con animales (perro, gato, cerdo, etc.). Preguntar por
síntomas de daño orgánico: fiebre y síntomas generales, exantema, prurito, afectación nasal, tos, disnea,
congestión torácica, diarrea, mialgias, síntomas neurológicos, adenopatías o hepatoesplenomegalia,
disfunción cardiaca o miocarditis, etc.
Una eosinofilia transitoria, con historia de contacto con fármacos, trasfondo alérgico o sospecha de
infección parasitaria, apoya una naturaleza reactiva. Por el contrario, la eosinofilia persistente, con
presencia de células inmaduras, otras citopenias asociadas y displasia, orientan hacia una etiología
neoplásica (si bien es rara).
Los pacientes con eosinofilia leve, sin daño orgánico secundario ni factores de riesgo para infección
parasitaria o enfermedad sistémica asociada, solo precisan observación (evolución clínica y analítica cada 6
meses). Estos casos, que representan hasta un 2-10% de la población, suelen ser secundarios a alergias,
atopia, fármacos, de origen familiar, etc.
Requerirán estudio etiológico, por tanto, aquellos pacientes que presenten:
Más de 500/mm3 y daño orgánico.
Entre 500-1.500/mm3 con historia de viajes a zonas endémicas, síntomas o hallazgos clínicos
asociados a la eosinofilia.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1217]
[75] TRASTORNOS DE LA SERIE BLANCA
Todos aquellos que presenten > 1.500/mm3 en dos o más ocasiones. En caso de enfermedad
aguda con hipereosinofilia > 100.000/mm3, se requiere ingreso e inicio de corticoterapia si
existiera daño orgánico, junto con ivermectina 200 μg/kg/día durante 2 días.
Manejo recomendado:
Estudio inicial: hemograma y frotis de sangre periférica. Perfil renal, hepático, sistemático y
sedimento de orina. Vitamina B12. Radiografía de tórax en todos los casos. Serología de
Strongyloides. Poblaciones linfocitarias. Troponina: si está elevada, realizar un
electrocardiograma (ECG) y un ecocardiograma transtorácico.
En pacientes seleccionados: tratamiento con ivermectina empírica. Prueba de Mantoux.
Estudio de parásitos en función de la sospecha y la exposición:
Serologías: Toxocara (solo útil en niños), Trichinella, Schistosoma (también
estudio del parásito y huevos en orina), filarias.
Heces (tres muestras): huevos y parásitos; permite detectar Strongyloides (solo
huevo y larva), Ancylostoma y Necator, Fasciola, Clonorchis, etc.
Es posible también llevar a cabo el estudio tisular en función de las
manifestaciones clínicas.
Otras serologías: virus de la inmunodeficiencia humana (VIH) y virus
linfotrópicos de células T humanas (HTLV) 1 y 2.
Inmunoglobulinas, niveles de triptasa (si hay sospecha de mastocitosis), cortisol basal
(sospecha de insuficiencia suprarrenal), anticuerpos antinucleares (ANA), antígeno
nuclear extraíble (ENA) y anticuerpos anticitoplásmicos de neutrófilos (ANCA).
Sospecha de linfoma: tomografía computarizada (TC), toracoabdominopélvica, biopsia
de adenopatía. Si existe sospecha de neoplasia hematológica, realizar un estudio de
médula ósea.
La Organización Mundial de la Salud (OMS) incluye dentro de los trastornos proliferativos
hematológicos una categoría asociada a eosinofilia, y distingue tres entidades en función del estudio
genético, según presenten mutaciones en los factores PDGFRA (1), PDGFRB (2) o FGFR1 (3).
Ensayo con suspensión farmacológica si se sospecha toxicidad.
Estudio de médula ósea (indicaciones):
Más de 100.000/mm3.
Más de 1.500/mm3 y daño orgánico sin otra causa conocida subyacente.
Alteraciones en el frotis sugestivas de proceso hematológico subyacente.
III. LEUCOPENIA
Se define de manera arbitraria como la presencia en sangre periférica de una cifra de leucocitos por
debajo de 4.000/mm3, primordialmente a expensas de linfocitos y/o neutrófilos.
1. NEUTROPENIA
Se denomina de este modo a la disminución de neutrófilos por debajo de 1.500/mm3 (1.800 en
mayores de 10 años y 1.200 en personas de raza negra), y se clasifica como: leve (1.000- 1.500/mm3),
moderada (500-1.000/mm3) y grave (< 500/mm3; algunos autores consideran neutropenia grave cifras
menores de 100/mm3). Por debajo de 500/mm3 se pierde el control de la flora endógena, y con cifras
inferiores a 200/mm3 no se inicia el proceso inflamatorio. Como resultado, existe una mayor predisposición
a infecciones graves por hongos y bacterias.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1218]
[75] TRASTORNOS DE LA SERIE BLANCA
1.1. Causas (Tablas V y VI)
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1219]
[75] TRASTORNOS DE LA SERIE BLANCA
La agranulocitosis es muy rara, y consiste en la desaparición absoluta de los neutrófilos en sangre
periférica, debido a una reacción idiosincrática a un fármaco administrado a dosis habituales. Se produce
mediante dos mecanismos:
Inmune: está mediada por anticuerpos, en los que el fármaco actúa como hapteno (por
ejemplo, propiltiouracilo, flecainida, metamizol). Su inicio es brusco. Recurre en caso de
reintroducción del fármaco.
Mielotoxicidad directa: se origina una supresión de células hematopoyéticas medulares
mieloides (por ejemplo, fenotiazinas, procainamida o clozapina). Su inicio es algo más larvado.
Es muy característica la presencia de úlceras necróticas no purulentas en las regiones orofaríngea,
anal y vaginal, con o sin fiebre. Cuando se acompaña de fiebre, suele ser secundaria a infección por bacilos
gramnegativos entéricos y cocos grampositivos de la piel. No se acompaña de otras citopenias; se puede
realizar un estudio de médula ósea si existen dudas diagnósticas, el cual puede ayudar además a predecir la
duración de la neutropenia. El manejo consiste en la retirada de los fármacos potencialmente causantes y
en cobertura antibiótica para neutropenia febril si existiera, así como medidas generales en el paciente
neutropénico y uso de factores estimuladores de colonias. (Ver Capítulo 47. “Infecciones en el paciente
inmunodepremido. Neutropenia febril”).
Mientras que la agranulocitosis se suele presentar como neutropenia febril o sepsis, la neutropenia
dosis-dependiente habitualmente es leve y asintomática, salvo en el caso de fármacos quimioterápicos.
1.2. Aproximación diagnóstica (Figura 2)
Al realizar la anamnesis de un paciente con neutropenia, se debe indagar sobre su historia familiar,
etnia, antecedentes de infecciones previas (a qué edad aparecieron y su gravedad), fármacos, síntomas
cíclicos y existencia de sintomatología constitucional. Si no es grave y el paciente no presenta datos de
alarma, se puede repetir el hemograma en 1-2 semanas para confirmar el resultado. En la exploración
física, habrá que buscar la presencia de úlceras en mucosas, adenopatías y organomegalias.
En cuanto a los estudios de laboratorio, habrá que realizar un hemograma y un frotis de sangre.
Uno de los datos más importantes será establecer la duración de la neutropenia. En la bioquímica habrá
que incluir vitamina B12, ácido fólico y cobre. También habrá que realizar serología de VIH y estudio de
autoinmunidad sin anticuerpos antineutrófilo (no se recomienda, dada la alta tasa de falsos positivos).
Se realizará finalmente un estudio de médula ósea en ausencia de datos que orienten a una causa,
si se acompaña de otras citopenias no explicadas o según los hallazgos del frotis (elementos inmaduros o
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1220]
[75] TRASTORNOS DE LA SERIE BLANCA
displasia). También se puede solicitar una citometría de sangre periférica para descartar leucemia de
linfocitos grandes granulares cuando haya datos sugerentes en el frotis.
2. LINFOPENIA
Se define como un recuento de linfocitos menor de 1.000/mm3. En la evaluación inicial se debe
atender a la edad, cronología de la linfopenia, antecedentes infecciosos de repetición y factores de riesgo
para infección por VIH, junto con la existencia de organomegalias o linfadenopatías.
Si no se determina la causa, se recomienda la realización de un estudio de poblaciones linfocitarias,
para determinar el compartimento disminuido, así como la cuantificación de inmunoglobulinas. Debe
considerarse el trasplante de médula ósea en los trastornos de inmunodeficiencia primaria.
2.1. Causas (Tabla VII)
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1221]
[75] TRASTORNOS DE LA SERIE BLANCA
BIBLIOGRAFÍA
Aspectos diagnósticos y terapéuticos de la hematopoyesis y de la patología leucocitaria. Neoplasias
hematológicas. En: Burgaleta C, Alegre A. Manual del Médico Residente en Hematología y
Hemoterapia. Madrid: Sociedad Española de Hematología y Hemoterapia/Editores médicos; 2015. p.
73-180.
Boxer LA. How to approach neutropenia. Hematology Am Soc Hematol Educ Program. 2012;2012:174-
82.
Bron D. Approche rationnelle d’une hyperleucocytose. Rev Med Brux. 2013;34(4):339-422.
Chabot-Richards DS, George TI. Leukocytosis. Int J Lab Hematol. 2014;36(3):279-88.
Gibson C, Berliner N. How we evaluate and treat neutropenia in adults. Blood. 2014;124(8):1251-8.
Gotlib J. World Health Organization-defined eosinophilic disorders: 2015 update on diagnosis, risk
stratification, and management. Am J Hematol. 2015;90(11):1077-89.
Holland SM, Gallin JI. Trastornos de los granulocitos y monocitos. En: Longo DL, Fauci AS, Kasper DL, et
al, editores. Harrison. Principios de Medicina interna. 18ª ed. México: McGraw-Hill Interamericana;
2012. p. 472-85.
Kaushansky K, Lichtman MA, Prchal JT, Levi MM, Press OW, Burns LJ, et al, editores. Williams
Hematology. 9ª edición. New York: McGraw-Hill Education; 2016.
Roufosse F, Weller PF. Practical approach to the patient with hypereosinophilia. J Allergy Clin Immunol
[Internet]. 2010;126(1):39-44.
Sanz MÁ, Carreras E, editores. Manual Práctico de Hematología Clínica. 5ª edición. Barcelona Antares;
2015.
Swerdlow SH, Campo E, Harris NL, Jaffe ES, Pileri SA, Stein H, et al. WHO Classification of tumours of
haematopoietic and lymphoid tissues. 4ª edición. Lyon: International Agency for Research on Cancer;
2008.
Valent P, Klion AD, Horny HP, Roufosse F, Gotlib J, Weller PF, et al. Contemporary consensus proposal
on criteria and classification of eosinophilic disorders and related syndromes. J Allergy Clin Immunol.
2012;130(3):607-12.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1222]
[76] TROMBOCITOPENIA. TROMBOCITOSIS. PANCITOPENIA
76.Trombocitopenia. Trombocitosis. Pancitopenia
Gonzalo Carreño Gómez-Tarragona.
Hematología y Hemoterapia
Mikel Mancheño Losa.
Medicina Interna
Asesor:
Carlos Grande García.
Médico Adjunto de Hematología y Hemoterapia
I. TROMBOCITOPENIA
1. DEFINICIÓN
Disminución del número de plaquetas por debajo de 150 x 109/l. Se puede clasificar como leve (> 50
x 10 /l), moderada (entre 20-50 x 109/l) y grave (< 20 x 109/l).
9
2. ETIOLOGÍA
En función del mecanismo que la origina, existen diferentes tipos de trombocitopenia (Tabla I).
3. CLÍNICA
Los recuentos de plaquetas mayores de 100 x 109/l no se suelen asociar a sangrado y, por tanto, el
estudio de trombocitopenia por encima de esa cifra suele carecer de relevancia clínica. La púrpura, los
hematomas espontáneos y la hemorragia prolongada postraumática aparecen de forma progresiva
conforme el recuento de plaquetas cae por debajo de 50 x 109/l.
El riesgo hemorrágico depende del recuento de plaquetas (mayor si es inferior a 20 x 109/l) y
además de otros parámetros, como la existencia de trombocitopatía asociada (antiagregantes, insuficiencia
renal, etc.), la presencia de manifestaciones hemorrágicas en el momento de la evaluación (mayor si hay
sangrado mucoso), la eventual coexistencia de otro defecto hemos- tático y el origen de la trombocitopenia
(mayor si es por fallo medular).
4. APROXIMACIÓN DIAGNÓSTICA
Dado que las causas de trombocitopenia son múltiples, su diagnóstico diferencial es complejo. Sin
embargo, una buena historia clínica y un análisis básico, al que es indispensable añadir un frotis de sangre
periférica (SP), pueden ofrecer un diagnóstico preciso (Figura 1).
1. ANAMNESIS
Edad, sexo, antecedentes personales o familiares de diátesis hemorrágica, localización y gravedad
de las manifestaciones hemorrágicas, embarazo (trombocitopenia dilucional, síndrome HELLP), consumo de
alcohol (puede producir trombocitopenia tanto por toxicidad directa como por desnutrición o por
hiperesplenismo en el caso de enfermedad hepática), transfusiones (trombocitopenia aloinmune), cirugía o
vacunaciones recientes, virus, síntomas de infección, desnutrición, consumo de fármacos o complementos
alimenticios (ver Tabla I; cabe destacar la trombocitopenia inducida por heparina).
2. EXPLORACIÓN FÍSICA
Evaluación de las manifestaciones hemorrágicas (púrpura, hematomas, hemorragias en mucosas),
búsqueda de adenopatías (procesos linfoproliferativos, infecciones, enfermedades autoinmunes),
esplenomegalia (trombocitopenia por hiperesplenismo secundario a neoplasias hematológicas o
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1223]
[76] TROMBOCITOPENIA. TROMBOCITOSIS. PANCITOPENIA
hepatopatía), signos de trombosis (orientan a coagulación intravascular diseminada [CID], hemoglobinuria
paroxística nocturna [HPN] o trombocitopenia inducida por heparina [TIH]), datos de infección, anomalías
esqueléticas asociadas a trombocitopatías congénitas, desnutrición, manifestaciones neurológicas
(microangiopatías trombóticas), etc.
3. EXTENSIÓN DE SANGRE PERIFÉRICA
Descartar pseudotrombocitopenia, síndrome mielodisplásico u otros procesos clonales
hematológicos, microangiopatías trombóticas, etc.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1224]
[76] TROMBOCITOPENIA. TROMBOCITOSIS. PANCITOPENIA
4. OTRAS PRUEBAS
Estudio de coagulación (descartar CID, síndrome antifosfolípido por presencia de
anticoagulante lúpico, etc.).
Serologías de virus de la inmunodeficiencia humana (VIH) y virus de la hepatitis C (VHC), así
como de otros virus (virus de la hepatitis B [VHB], virus de Epstein-Barr [VEB], citomegalovirus
[CMV], parvovirus B19).
Autoinmunidad (anticuerpos antinucleares, test de Coombs directo para descartar síndrome de
Evans, búsqueda de anticuerpos antiheparina y antifactor 4 plaquetario en TIH).
Estudios de trombocitopatía.
Pruebas de función tiroidea (el hipertiroidismo aumenta el consumo y el hipotiroidismo
disminuye la producción).
Ecografía o tomografía computarizada (TC) abdominal (hepatopatía, procesos malignos, etc.).
5. TRATAMIENTO
El tratamiento de las trombocitopenias se basa en el de la causa subyacente. Es fundamental
valorar el riesgo hemorrágico del paciente y considerar la retirada tanto de aquellos fármacos con posible
implicación en la trombocitopenia como de aquellos que alteran la función plaquetaria (antiagregantes) o
que aumentan el riesgo de sangrado (anticoagulantes).
En cuanto a la transfusión de plaquetas, esta es más eficaz en el caso de trombocitopenias de causa
central, siendo su eficacia limitada en aquellas causadas por destrucción periférica. Está contraindicada en
microangiopatías trombóticas. Se indica en función de las cifras plaquetarias, las manifestaciones
hemorrágicas y otros factores concomitantes (ver Capítulo 78. “Hemoterapia”). Se recomienda una buena
coordinación con los anestesistas y los cirujanos de cara a realizar procedimientos invasivos.
6. ENTIDADES CLÍNICAS
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1225]
[76] TROMBOCITOPENIA. TROMBOCITOSIS. PANCITOPENIA
1. PSEUDOTROMBOCITOPENIA
La presencia de plaquetas gigantes o de agregados plaquetarios puede infravalorar el recuento
automatizado de plaquetas. La existencia de criptoanticuerpos dependientes de ácido
etilendiaminotetraacético (EDTA) puede desencadenar la formación de agregados plaquetarios o el
fenómeno de satelitismo plaquetario, contabilizándose una falsa trombocitopenia. Es fácil de objetivar con
un frotis de SP.
2. TROMBOCITOPENIA INMUNE
Antes conocida como púrpura trombocitopénica idiopática (PTI).
2.1. Definición y etiopatogenia
Es una de las causas más comunes de trombocitopenia. Se debe a la producción de anticuerpos
antiplaquetarios, responsables, por un lado, de la destrucción periférica de las plaquetas por el sistema
mononuclear fagocítico y, por otro, de la disminución de su producción a nivel central. Se puede distinguir
entre PTI primaria, no asociada a ninguna otra enfermedad, y PTI secundaria, asociada a otras alteraciones
inmunológicas (enfermedades reumatológicas, inmunodeficiencias, procesos linfoproliferativos).
2.2. Clínica
Viene determinada por la cifra de plaquetas, y se puede presentar con petequias y sangrado de
mucosas; son muy raros los sangrados intracraneales. Aunque el acrónimo PTI se mantiene por su
importancia histórica, el término adecuado es trombocitopenia inmune, dado que no todos los pacientes
presentan clínica purpúrica ni su causa es idiopática. En los niños generalmente es una enfermedad
autolimitada y dos terceras partes se recuperan espontáneamente en el plazo de 6 meses, mientras que en
el adulto suele tener un curso crónico, con una duración mayor de un año.
2.3. Diagnóstico
De exclusión. El recuento plaquetario ha de ser < 100 x 109/l. Se debe solicitar hemograma con
reticulocitos y extensión de SP, estudio de coagulación, bioquímica de sangre y orina, dosificación de
inmunoglobulinas (previamente al inicio del tratamiento con gammaglobulinas intravenosas), test de
Coombs, anticuerpos antinucleares y serologías para VIH, VHC y VHB. Otros estudios que se pueden
plantear son la detección de anticuerpos antifosfolípido, anticuerpos antitiroideos y pruebas de función
tiroidea, así como el test del aliento para detectar infección por Helicobacter pylori. No se recomienda la
solicitud de anticuerpos antiplaquetarios (por falsos positivos y negativos).
El estudio de médula ósea (MO) se reserva para casos refractarios a la primera línea de
tratamiento, antes del inicio de la segunda línea. Puede valorarse su realización en mayores de 60 años.
2.4. Tratamiento
La indicación de tratamiento viene marcada tanto por las cifras de plaquetas como por la presencia
o no de clínica hemorrágica. El tratamiento de primera elección se basa en glucocorticoides, a los que
pueden añadirse inmunoglobulinas en caso de manifestaciones hemorrágicas importantes (Figura 2).
Los pacientes refractarios o con pérdida de respuesta pueden ser sometidos a esplenectomía y, en
caso de contraindicación, ser tratados con agentes trombopoyéticos como romiplostim o eltrombopag. En
caso de sangrado visceral muy grave, además de los pulsos de corticoides y el uso de inmunoglobulinas,
puede plantearse la transfusión de plaquetas (tras las inmunoglobulinas), ya que proporcionan soporte
hemostático inmediato, a pesar de su rápida destrucción. También debe valorarse el uso de
antifibrinolíticos.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1226]
[76] TROMBOCITOPENIA. TROMBOCITOSIS. PANCITOPENIA
3. MICROANGIOPATÍAS TROMBÓTICAS (MAT)
Cuadros caracterizados por anemia hemolítica microangiopática (con esquistocitos en la extensión
de SP y test de Coombs directo siempre negativo), trombocitopenia y afectación de al menos un órgano
(Tabla II). Se trata de un grupo complejo de enfermedades de causa multifactorial (Tabla III), entre las
cuales destacamos las que se describen a continuación.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1227]
[76] TROMBOCITOPENIA. TROMBOCITOSIS. PANCITOPENIA
3.1. Púrpura trombótica trombocitopénica (PTT)
Se trata, junto a la leucemia mieloide aguda promielocítica, de una de las mayores urgencias en
Hematología. Se caracteriza, además de por la anemia hemolítica y la trombocitopenia, por producir
alteraciones neurológicas y daño en otros órganos, aunque inusualmente presenta afectación renal. Se
debe a la deficiencia (congénita o adquirida) de ADAMTS13, enzima encargada de degradar los multímeros
del factor de von Willebrand. Estos se acumulan, incrementando el riesgo de formación de trombos
plaquetarios en los pequeños vasos. Su tratamiento se basa en el recambio plasmático, además de en la
inmunosupresión en los casos adquiridos.
3.2. Síndrome hemolítico urémico (SHU)
MAT caracterizada por deterioro de la función renal. Es más frecuente en niños y suele estar
precedida de diarrea hemorrágica, dado que está mediada por la toxina Shiga producida por Escherichia
coli O157H7 y Shigella dysenteriae tipo I. El tratamiento es de soporte. Cabe mencionar el SHU atípico,
causado por deficiencias en el sistema del complemento, para cuyo tratamiento, además de la
plasmaféresis, está indicado el uso de eculizumab, inhibidor de C5 también empleado en el tratamiento de
la hemoglobinuria paroxística nocturna.
4. TROMBOCITOPENIA INDUCIDA POR HEPARINAS (TIH)
Se distinguen dos tipos: la tipo I, por acción directa de la heparina sobre las plaquetas,
generalmente leve; y la tipo II, de mecanismo inmune, clínicamente significativa. Dado que el diagnóstico
es difícil, se han desarrollado scores (ver Capítulo 77. “Trastornos de la hemostasia. Anticoagulación”).
II. TROMBOCITOSIS
1. DEFINICIÓN
Exceso de plaquetas en sangre periférica (SP), en concreto cuando se encuentran por encima de
450 x 109/l.
2. ETIOLOGÍA
Aunque existen trombocitosis congénitas (secundarias a mutaciones en el gen de la
trombopoyetina y su receptor MPL), estas son una rareza, ya que la inmensa mayoría son adquiridas.
Dentro de las adquiridas, se diferencian dos tipos:
Trombocitosis primarias, autónomas o clonales, que son aquellas debidas a neoplasias,
síndromes mieloproliferativos y mielodisplásicos.
Trombocitosis secundarias o reactivas, que se dan en ausencia de procesos mieloproliferativos
o mielodisplásicos (Tabla IV). Suponen más del 85% de las trombocitosis adquiridas, incluso en
aquellos casos con cifras superiores a 1.000 x 109/l plaquetas.
Cabe destacar que existen también causas de falsa trombocitosis: de esta manera, en la
crioglobulinemia mixta, los fragmentos de crioglobulinas se agregan, dando errores de medida cuando la
muestra baja de los 30 °C; además, en ocasiones los fragmentos celulares pueden ser medidos como
plaquetas en leucemias, linfomas, anemias hemolíticas o quemados graves.
3. CLÍNICA
Sea primaria o secundaria, toda trombocitosis puede tener manifestaciones hemorrágicas,
trombóticas o vasomotoras (cefalea, síntomas visuales, dolor torácico atípico, disestesias acrales,
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1228]
[76] TROMBOCITOPENIA. TROMBOCITOSIS. PANCITOPENIA
eritromelalgia). Es importante reseñar que estos síntomas son mucho más frecuentes en las trombocitosis
clonales o primarias, por lo que su presencia orienta hacia su diagnóstico.
Debe prestarse especial atención a los síntomas y signos que permiten diferenciar una
trombocitosis reactiva de una primaria: esplenomegalia, en el caso de síndromes mieloproliferativos;
síndrome anémico y clínica compatible con ferropenia (ver Capítulo 74. “Trastornos de la serie roja”);
fiebre, con proteína C reactiva (PCR) elevada, en los procesos inflamatorios o infecciosos, etc.
Por otra parte, hay que señalar que la trombocitosis puede ser causa de pseudohiperpotasemia sin
repercusión clínica.
4. APROXIMACIÓN DIAGNÓSTICA
Dado que la mayoría de las trombocitosis son secundarias, es primordial realizar el diagnóstico
diferencial de estas frente a la trombocitosis de origen clonal.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1229]
[76] TROMBOCITOPENIA. TROMBOCITOSIS. PANCITOPENIA
Anamnesis: traumatismo o cirugía recientes, esplenectomía, historia compatible con proceso
infeccioso, antecedentes o síntomas relacionados con sangrados, trombosis o ferropenia;
diagnóstico previo de enfermedad hematológica, proceso autoinmune, pérdida de peso,
hiporexia, fatiga o cualquier signo que apoye una enfermedad neoplásica, medicación habitual,
etc.
Exploración física: esplenomegalia, palidez mucocutánea, signos de infección o enfermedad
inflamatoria, etc.
Pruebas complementarias: el frotis de SP es fundamental, puesto que puede aportar datos que
dirijan al diagnóstico de anemia (microcitosis, hipocromía), asplenia (cuerpos de Howell-Jolly),
infección (granulación tóxica, desviación izquierda), mielodisplasia o neoplasia
mieloproliferativa crónica (displasia, plaquetas gigantes).
Otras pruebas incluyen:
PCR, velocidad de sedimentación, ferritina, fibrinógeno.
Si, a pesar de estas pruebas, no se encuentra la causa de la trombocitosis, se podrá
ampliar el estudio con técnicas de biología molecular en SP (reordenamiento BCR/ ABL
o mutaciones en JAK2, MPL, CALR, etc.) o con estudio completo de médula ósea (MO).
5. TRATAMIENTO
En caso de que la trombocitosis sea secundaria a una causa subyacente, el tratamiento debe ir
dirigido a tratar dicha causa. Si la trombocitosis es de origen clonal, se deberá realizar una estratificación
del riesgo tanto trombótico como hemorrágico (en caso de trombocitosis extremas). En función del mismo,
se decidirá comenzar tratamiento citorreductor, asociado o no a antiagregantes (no se pautarán con cifras
> 1.000 x 109/l).
III. PANCITOPENIA
1. INTRODUCCIÓN
El término pancitopenia hace referencia a la presencia simultánea de anemia, leucopenia y
trombocitopenia. En la valoración de un paciente que se presenta con pancitopenia de novo, es útil pensar
en términos fisiopatológicos a la hora de guiar el abordaje diagnóstico. A este respecto, un paciente puede
presentar disminución de las tres líneas celulares por mecanismo periférico (hiperesplenismo, infecciones y
enfermedades inmunomediadas) o central, bien porque la médula ósea (MO) haya sido reemplazada
(mielofibrosis, enfermedades infiltrativas), se encuentre ausente (aplasia medular) o sea ineficiente
(síndromes mielodisplásicos [SMD], estados carenciales). El abordaje diagnóstico es, por tanto, extenso y
debe incluir una historia clínica detallada, en la que se haga especial hincapié en la presencia de
sintomatología sugestiva de enfermedades sistémicas, procesos infecciosos, estado nutricional, ingesta de
fármacos, drogas y exposición a tóxicos ambientales.
2. ETIOLOGÍA (Tabla V)
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1230]
[76] TROMBOCITOPENIA. TROMBOCITOSIS. PANCITOPENIA
3. APROXIMACIÓN DIAGNÓSTICA
1. ANAMNESIS Y EXPLORACIÓN FÍSICA
La gravedad de las manifestaciones clínicas dependerá del grado de las citopenias y de la velocidad
de instauración; el paciente puede presentar manifestaciones típicas de un síndrome anémico (palidez,
astenia, ortostatismo, palpitaciones, disnea de esfuerzo) junto con manifestaciones hemorrágicas
(fundamentalmente a expensas de sangrados mucosos, equimosis e hipermenorrea en mujeres
premenopáusicas) e infecciones recidivantes, que pueden orientar acerca del tiempo de evolución del
cuadro clínico. La exploración física debe ser exhaustiva, con especial atención a la presencia de
hepatoesplenomegalia, adenopatías periféricas y signos sugestivos de un proceso sistémico subyacente.
2. PRUEBAS COMPLEMENTARIAS
2.1. Laboratorio
Hemograma con extensión de sangre periférica (SP) y reticulocitos. Con la determinación de
reticulocitos se puede orientar la etiología de la pancitopenia hacia causas de mecanismo
central (reticulocitopenia) o periférico (reticulocitosis). En la extensión de SP se pueden
apreciar elementos que sugieran el diagnóstico, como la presencia de displasia (SMD),
neutrófilos hipersegmentados (déficit de vitamina B12 y folato), hallazgos compatibles con
mieloptisis (mielofibrosis, enfermedades infiltrativas) y presencia de células neoplásicas
(blastos, células peludas, células linfomatosas).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1231]
[76] TROMBOCITOPENIA. TROMBOCITOSIS. PANCITOPENIA
Bioquímica. Estudio completo con perfil férrico, vitamina B12, ácido fólico, perfil hepático,
perfil renal, marcadores de hemólisis, espectro electroforético y cuantificación de
inmunoglobulinas, perfil tiroideo y estudio de coagulación.
Inmunología. Si se sospecha conectivopatía, se realizará un estudio dirigido (panel de
autoinmunidad, fracciones del complemento, test de Coombs, factor reumatoide, etc.).
2.2. Microbiología
Serologías víricas, incluyendo virus hepatotropos, VIH, VEB, CMV y parvovirus B19.
2.3. Imagen
Ecografía abdominal para valorar la presencia de esplenomegalia o datos sugestivos de hepatopatía
crónica e hipertensión portal. Radiografía de tórax para valorar adenopatías mediastínicas.
2.4. Estudio de médula ósea (MO)
En función de la sospecha diagnóstica (en todas las enfermedades hematológicas), y en aquellos
pacientes que presenten pancitopenia grave y persistente de etiología no aclarada tras una aproximación
diagnóstica no invasiva inicial, habrá que realizar un estudio de MO con aspirado (valoración de la
morfología celular) y biopsia (valoración de la arquitectura y celularidad). Además, se podrán procesar las
muestras para estudio citogenético y microbiológico (Mycobacterium tuberculosis, Leishmania spp) según
la orientación diagnóstica.
4. MANEJO CLÍNICO
En pacientes con pancitopenia de origen central, la urgencia con la que debe programarse el
estudio morfológico de MO depende de la gravedad del cuadro clínico, que está determinada
fundamentalmente por el grado de citopenias (requerimientos transfusionales, plaquetopenia < 20.000
céls./mm3, neutropenia < 500 céls./mm3) y los hallazgos morfológicos de la extensión de SP. Otros factores
que se deben tener en cuenta son una rápida progresión del cuadro, alteraciones de la coagulación y
ausencia de etiología clara.
5. ENTIDADES ESPECÍFICAS
1. APLASIA MEDULAR
1. 1. Definición
Enfermedad de la célula madre multipotencial definida por la presencia de pancitopenia en SP y
una MO hipocelular en la que no se aprecia mielodisplasia significativa, infiltración medular o fibrosis. Es
una entidad infrecuente pero potencialmente mortal. La aplasia medular adquirida se presenta con mayor
frecuencia en adultos jóvenes entre 15-25 años, y existe un segundo pico de incidencia algo menor después
de los 60 años. Se puede presentar de forma repentina, en cuestión de días, o de forma insidiosa, a lo largo
de semanas o meses.
1.2. Etiopatogenia
Habitualmente se trata de un trastorno adquirido, aunque existen algunas formas asociadas a
enfermedades congénitas. Se estima que en la mayor parte de los casos el mecanismo fisiopatológico de
daño medular es inmunomediado y se atribuye a una respuesta anómala mediada por una población
oligoclonal de linfocitos T autorreactivos que sucede en individuos genéticamente susceptibles y que
conlleva la sobreproducción de citocinas inductoras de la apoptosis de la célula madre multipotencial.
Aunque en la mayoría de los casos (hasta el 80%, según las series) no se encuentra un factor
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1232]
[76] TROMBOCITOPENIA. TROMBOCITOSIS. PANCITOPENIA
desencadenante, se han hallado múltiples asociaciones clínicas (Tabla VI). Es importante distinguir la
aplasia medular yatrogénica, de carácter inevitable y predecible, que ocurre tras la administración de
quimioterapia citotóxica intensa y/o radioterapia.
1.3. Criterios diagnósticos y clasificación pronóstica
La anemia aplásica se define por la presencia de hipocelularidad en la biopsia de MO, siendo < 25%
(o entre 25-50 % con < 30% de células hematopoyéticas), y dos o más citopenias. Se considera anemia
aplásica grave cuando, además, presenta dos de las siguientes características: neutrófilos ≤ 500/μl,
plaquetas < 20.000/μl o reticulocitos absolutos ≤ 20.000/μl. Se considera muy grave cuando cumple
criterios de anemia aplásica grave y además presenta neutrófilos ≤ 200/μl. Se considera menos grave o
moderada cuando cumple criterios de anemia aplásica, pero no los criterios previos, y los neutrófilos son >
500/μl. Además de valorar causas secundarias, debe completarse un estudio con citometría de flujo para
descartar hemoglobinuria paroxística nocturna (HPN) y estudio citogenético en MO para descartar SMD con
hipocelularidad medular. En pacientes menores de 40 años, habría que realizar un test de fragilidad
cromosómica para descartar anemia de Fanconi.
1.4. Tratamiento
El tratamiento depende de la gravedad de la pancitopenia, siendo conservador en casos leves, con
tratamiento de soporte y, si lo hubiera, etiológico. El tratamiento de la aplasia grave en pacientes menores
de 40 años con donante familiar HLA-idéntico es el trasplante de progenitores hematopoyéticos (TPH), con
hasta un 90% de curación. En mayores de 40 años, o en ausencia de donante familiar, el tratamiento de
primera línea es la terapia inmunosupresora con globulina antitimocítica y ciclosporina A. Si no hay
respuesta, se puede plantear un segundo ciclo de tratamiento inmunosupresor o TPH de donante no
emparentado en pacientes candidatos.
2. SÍNDROMES MIELODISPLÁSICOS (SMD)
2.1. Definición
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1233]
[76] TROMBOCITOPENIA. TROMBOCITOSIS. PANCITOPENIA
Grupo heterogéneo de neoplasias mieloides clonales caracterizado por alteraciones morfológicas y
funcionales de las diferentes series hematopoyéticas, dando como resultado una hemopoyesis ineficaz con
citopenias de grado variable (a pesar de presentar una MO generalmente normo o hipercelular). Presentan
un curso clínico variable y con una clara tendencia a evolucionar a leucemia mieloide aguda. La edad media
de aparición es 75 años y la incidencia global es mayor en varones que en mujeres.
2.2. Etiología
La mayor parte (90%) son primarios o idiopáticos, a consecuencia del daño acumulado con la edad
en la célula madre hematopoyética (mutaciones espontáneas, cambios epigenéticos y alteraciones en el
microambiente medular), que promueve su replicación o le confiere una ventaja proliferativa, dando lugar
a la aparición de un clon patológico. Existen algunas enfermedades congénitas que predisponen a padecer
SMD (anemia de Fanconi, neurofibromatosis, etc.). Los SMD secundarios se presentan en pacientes que
han recibido quimioterapia (agentes alquilantes, inhibidores de la topoisomerasa II), radioterapia o que han
estado expuestos a hidrocarburos volátiles como el benceno.
2.3. Clínica
Las manifestaciones clínicas dependen del número y grado de citopenias derivadas de la
insuficiencia medular crónica. La citopenia más común es la anemia, habitualmente normocítica o
macrocítica, con un índice reticulocitario bajo para el grado de anemia.
2.4. Diagnóstico (Tabla VII)
Ante la presencia de una o varias citopenias constantes de origen no aclarado y datos de
mielodisplasia en el frotis de SP, se realizará un aspirado de MO para estudio morfológico y citogenético.
Previamente se deben descartar otras causas de mielodisplasia como déficits nutricionales (vitamina B12,
ácido fólico, hierro, cobre), exceso de zinc, algunos fármacos (metotrexato, azatioprina, micofenolato de
mofetilo, eritropoyetina, etc.), exposición a tóxicos (alcohol, arsénico, metales pesados), infecciones víricas
(VIH, VHC, VHB, parvovirus B19, CMV) y citopenias inmunomediadas.
2.5. Tratamiento
El tratamiento depende del pronóstico individual, teniendo en cuenta el grupo de riesgo del SMD
(definido por el número de citopenias, la cantidad de blastos y la citogenética), la probabilidad de respuesta
al tratamiento, la comorbilidad y el estado funcional del paciente.
El objetivo de tratamiento en pacientes de bajo riesgo es mejorar la calidad de vida, reduciendo la
clínica derivada de las citopenias y la necesidad de soporte transfusional. En pacientes de alto riesgo, el
objetivo es modificar la evolución natural de la enfermedad para prolongar la supervivencia.
En todos los pacientes se debe considerar tratamiento de soporte con transfusiones periódicas,
quelantes de hierro si existe sobrecarga férrica, vacunación contra el virus de la gripe y el neumococo y
diagnóstico y tratamiento precoz de los procesos infecciosos.
En pacientes asintomáticos con SMD de bajo riesgo, se realizará una monitorización clínico-
analítica estrecha para valorar la progresión de la enfermedad. En pacientes sintomáticos con SMD de
riesgo bajo o intermedio en los que predomina la anemia, se instaurará tratamiento con agentes
estimulantes de eritropoyesis si presentan déficit de eritropoyetina, y con lenalidomida si presentan un
síndrome de del(5q) aislado. Si fracasa dicho tratamiento, se valorará instaurar un tratamiento de soporte,
la inclusión en un ensayo clínico o el inicio de tratamiento con agentes hipometilantes (azacitidina,
decitabina), inmunosupresores (globulina antitimocítica [ATG], ciclosporina) o lenalidomida.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1234]
[76] TROMBOCITOPENIA. TROMBOCITOSIS. PANCITOPENIA
En pacientes de alto riesgo, con buena situación funcional y con disponibilidad de donante, el
tratamiento de elección es el TPH alogénico. En aquellos que no dispongan de donante, se optará entre
tratamiento hipometilante o quimioterapia intensiva. En pacientes con SMD de alto riesgo y no candidatos
a tratamiento intensivo, se valorará tratamiento hipometilante o exclusivo de soporte.
2.6. Pronóstico (Tabla VIII)
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1235]
[76] TROMBOCITOPENIA. TROMBOCITOSIS. PANCITOPENIA
3. HEMOGLOBINURIA PAROXÍSTICA NOCTURNA
3.1. Definición y etiopatogenia
Se trata de una enfermedad clonal de las células progenitoras hematopoyéticas originada por una
mutación somática en el gen PIG-A, que condiciona la ausencia de fosfatidil-inositolglucano del grupo A,
necesario para la fijación de numerosas proteínas de membrana a la superficie celular, como CD55 y CD59,
reguladoras de la acción del complemento. Como consecuencia, las células son altamente susceptibles a la
acción lítica del complemento, produciéndose hemólisis intravascular, así como pancitopenia de grado
variable y episodios recurrentes de trombosis venosas y arteriales. Se trata de una enfermedad muy
infrecuente que debuta generalmente entre los 30 y los 50 años de edad y presenta una distribución
homogénea en ambos sexos.
3.2. Clínica
Se caracteriza por hemólisis intravascular crónica que cursa con brotes desencadenados por el
sueño, situaciones inflamatorias (infecciones, transfusiones, cirugías, estrés) y tras repleción férrica en
pacientes con ferropenia. De este modo, los pacientes presentan anemia, ictericia leve, hemoglobinuria,
hemosiderinuria, ferropenia y deterioro de la función renal (necrosis tubular aguda en crisis hemolíticas
intensas y daño crónico por hemólisis persistente). Por otra parte, sufren un componente variable de
insuficiencia medular, asociándose ocasionalmente a aplasia medular y SMD. Los fenómenos trombóticos
son más frecuentes en el territorio venoso, y pueden aparecer en lugares inusuales, como venas
suprahepáticas, vena porta y senos venosos cerebrales. Como consecuencia de una depleción de óxido
nítrico (NO) por la hemoglobinemia, pueden aparecer distonías de musculatura lisa (durante las crisis) y
disfunción eréctil. Además, se puede desarrollar hipertensión pulmonar de origen tromboembólico y por la
depleción de NO en el territorio vascular pulmonar.
3.3. Diagnóstico
La prueba diagnóstica de elección es la citometría de flujo, que mostrará un déficit de CD55 y CD59
sobre hematíes, granulocitos y/o monocitos.
3.4. Tratamiento
Además del tratamiento de soporte, en pacientes sintomáticos con hemólisis importante o con
complicaciones derivadas (trombosis, daño renal, pulmonar, musculatura lisa, etc.) está indicado el
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1236]
[76] TROMBOCITOPENIA. TROMBOCITOSIS. PANCITOPENIA
tratamiento con eculizumab, anticuerpo monoclonal que inhibe la activación final del complemento. En
pacientes que asocian aplasia medular grave está indicado el TPH, único tratamiento curativo de la
enfermedad.
4. LINFOHISTIOCITOSIS HEMOFAGOCÍTICA (HLH) O SÍNDROME HEMOFAGOCÍTICO
4.1. Definición y etiopatogenia
Se trata de una entidad rara pero potencialmente mortal, que tiene su origen en una alteración de
la función de los linfocitos NK y T citotóxicos, lo cual conlleva una activación incontrolada de las células
presentadoras de antígeno (histiocitos, macrófagos) y de los linfocitos T, dando lugar a una respuesta
inflamatoria exagerada con hiperproducción de citocinas proinflamatorias (interferón-gamma, factor de
necrosis tumoral-alfa [TNF-α] e interleucinas 1, 6, 10, 12, 18) que, en última instancia, conduce a daño
tisular y disfunción orgánica.
Puede ser primaria (de origen genético y aparición en la edad pediátrica) o secundaria (reactiva) a
procesos infecciosos, autoinmunes o tumorales. En adultos, generalmente se identifica una convergencia
de factores externos desencadenantes y enfermedades predisponentes de base (Tabla IX).
Entre los desencadenantes, destacan las infecciones víricas, ya sea como primoinfección en
pacientes sanos o reactivación en inmunodeprimidos, y tiene un papel primordial la familia de virus herpes
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1237]
[76] TROMBOCITOPENIA. TROMBOCITOSIS. PANCITOPENIA
(sobre todo VEB); también puede desencadenar el síndrome la infección por M. tuberculosis, y, con mucha
menor frecuencia, por otras bacterias, parásitos y hongos. Entre los desencadenantes no infecciosos, se
han descrito casos en relación con la administración de algunos fármacos, vacunas o poscirugía.
En cuanto a las enfermedades predisponentes, destacan las neoplasias hematológicas, con una
prevalencia de hasta el 20% en algunos tipos específicos de linfomas B (formas intravasculares o aquellos
que se presentan sin adenopatías periféricas) y de células T. También se asocia con enfermedades
autoinmunes, infecciones víricas crónicas (principalmente VIH) y pacientes trasplantados.
Aunque el perfil epidemiológico de la enfermedad en adultos no está bien definido, parece ser algo
más frecuente en varones (8:3), la edad media de presentación es de 50 años y la mitad de los casos
descritos en la literatura médica provienen de países asiáticos.
4.2. Manifestaciones clínicas
Clínicamente se caracteriza por un cuadro de instauración aguda o subaguda (1-4 semanas)
dominado por fiebre alta persistente (> 38,5 °C), hepatoesplenomegalia, adenopatías y afectación
multiorgánica progresiva, precisando soporte en unidades de cuidados intensivos hasta en el 40% de los
casos. Afectación órganoespecífica:
Cutánea: pueden aparecer lesiones inespecíficas como exantema, edemas, petequias o
púrpura; es importante valorar la presencia de nódulos subcutáneos tipo paniculitis por su
estrecha relación con un linfoma de células T subyacente.
Hepática: muy frecuente, puede variar desde una leve alteración de las pruebas de función
hepática hasta un fallo hepático fulminante.
Pulmonar: también frecuente, con eventual desarrollo de distrés respiratorio e insuficiencia
respiratoria aguda.
Gastrointestinal: hasta un 20% de los pacientes asocian síntomas inespecíficos (diarrea,
náuseas, vómitos y dolor abdominal), aunque se han descrito presentaciones graves como
hemorragia intestinal, pancreatitis o colitis ulcerosa (importante descartar CMV).
Neurológica: es heterogénea y puede incluir coma, convulsiones, meningitis, encefalomielitis,
hemorragia cerebral, alteraciones psiquiátricas, etc. Es importante descartar procesos
asociados como malaria o linfoma cerebral primario.
Renal: también se ha descrito insuficiencia renal o desarrollo de síndrome nefrótico,
requiriendo diálisis el 50% de los casos.
Hematológica: incluye crecimiento de órganos linfopoyéticos, citopenias y coagulación
intravascular diseminada.
4.3. Diagnóstico
El diagnóstico se basa en la coexistencia de hallazgos clínicos, analíticos e histológicos, aunque
ninguno de ellos es patognomónico. La Sociedad del Histiocito estableció unos criterios diagnósticos (Tabla
X), ampliamente utilizados en adultos; sin embargo, su sensibilidad y especificidad no han sido evaluadas.
Es fundamental distinguir si el cuadro clínico del paciente se debe a una HLH o a una presentación agresiva
de las enfermedades vinculadas a ella. Es muy sugestiva de HLH la evidencia de hemofagocitosis junto con
valores muy alterados de hipofibrinogenemia, hipertrigliceridemia e hiperferritinemia (> 10.000 mg/ml).
4.3.1. Estudios de laboratorio
Además de las alteraciones antes mencionadas, es posible encontrar bicitopenia o pancitopenia,
que pueden ser graves; alteración del perfil hepático, coagulopatía con incremento de dímeros- D (> 10.000
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1238]
[76] TROMBOCITOPENIA. TROMBOCITOSIS. PANCITOPENIA
ng/dL), lactato deshidrogenasa (LDH) elevada, hiponatremia y aumento de reactantes de fase aguda (PCR,
velocidad de sedimentación globular [VSG], hiperferritinemia).
4.3.2. Inmunología
Elevación del CD25 soluble y actividad disminuida de los linfocitos NK. Son pruebas no disponibles
en la mayoría de los hospitales, pero que se pueden solicitar en laboratorios de referencia.
4.3.3. Hallazgos histológicos
Demostración de hemofagocitosis en MO (preferentemente) o en órganos reticuloendoteliales. No
es una condición imprescindible para su diagnóstico y puede estar presente y aumentada de forma
fisiológica en múltiples situaciones (infecciones, enfermedades autoinmunes, transfusiones), por lo que su
hallazgo debe interpretarse en el contexto clínico del paciente.
4.3.4. Estudios microbiológicos
Debe realizarse un estudio dirigido a descartar factores infecciosos desencadenantes en todos los
pacientes, especialmente víricos, mediante estudios serológicos, cultivos microbiológicos de SP y otras
muestras en función de la sintomatología, y pruebas específicas según la sospecha clínica y el contexto
epidemiológico del paciente.
4.4. Tratamiento
El tratamiento de la HLH reactiva se basa en un abordaje triple con medidas de soporte vital,
tratamiento del factor desencadenante (principalmente infecciones) y supresión de la respuesta
inflamatoria exagerada o la proliferación celular descontrolada (neoplasias) con fármacos
inmunosupresores o citotóxicos, respectivamente. Se han utilizado glucocorticoides a dosis altas (pulsos de
metilprednisolona), inmunosupresores (ciclosporina A, metotrexato, ciclofosfamida), inmunoglobulinas
intravenosas, plasmaféresis, terapias biológicas (anti-TNF, anti- CD20, anti-IL1r, anti-IL-6) y quimioterapia
(regímenes que incluyen etopósido), en función de la enfermedad de base del paciente. Sin embargo, la
ausencia de ensayos clínicos aleatorizados y controlados en adultos hace que en el momento actual las
decisiones terapéuticas se basen en recomendaciones de expertos y experiencia clínica personal.
4.5. Pronóstico
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1239]
[76] TROMBOCITOPENIA. TROMBOCITOSIS. PANCITOPENIA
La mortalidad global alcanza el 41%. El pronóstico varía según la enfermedad de base, y es peor en
neoplasias que en primoinfecciones víricas y enfermedades autoinmunes. Los principales factores
pronósticos identificados en adultos son la edad elevada al diagnóstico y la presencia de trombopenia
grave. Existen dos picos de mortalidad, uno en las primeras semanas de enfermedad, por disfunción
multiorgánica, y otro tardío, relacionado con la toxicidad de los tratamientos, con infecciones en el seno de
neutropenia prolongada y con la aparición posterior (5-16 semanas) de una neoplasia hematológica
agresiva en pacientes que sobreviven a una HLH catalogada inicialmente como idiopática. Las recaídas no
son infrecuentes, y pueden acontecer en el seno de la retirada o disminución del tratamiento inductor
inicial; es fundamental, por tanto, la valoración cuidadosa de cada nuevo episodio febril en estos pacientes.
BIBLIOGRAFÍA
Brito-Zerón P, Bosch X, López-Guillermo A, Fraile G, Khamashta MA, Ramos-Casals M. Síndrome
hemofagocítico. En: Cervera R, Espinosa G, Ramos-Casals M, et al, editores. Enfermedades
autoinmunes sistémicas. Diagnóstico y tratamiento. 5ª edición. Madrid: Editorial Médica
Panamericana; 2015; p. 308-24.
Burgaleta C, Alegre A. Manual del Médico Residente en Hematología y Hemoterapia. Madrid: Sociedad
Española de Hematología y Hemoterapia; 2015.
George JN, Nester CM. Syndromes of thrombotic microangiopathy. N Engl J Med. 2014;371(19):1847-
8.
Greinacher A. Heparin-induced thrombocytopenia. N Engl J Med. 2015;373(19):1883-4.
Hoffman R, Benz EJ, Silberstein LE, Heslop H, Weitz J, Anastasi J. Hematology Basic Principles and
Practice. 6ª edición. Elsevier; 2013.
Jarque I, Palau J, Sanz MA. Trombocitopenias. En: Sanz MA, Carreras E. Manual Práctico de
Hematología Clínica. 5ª edición. Barcelona: Antares; 2015; p. 457-60.
Rondeep S, Stanley L. Consultative hematology. En: Kaushansky K, Lichtman MA, Prchal JT, Levi MM,
Press OW, Burns LJ. Williams Hematology. 9ª edición. New York: Mc Graw-Hill Education; 2016; p. 41-9.
Sans-Sabrafen J, Besses Raebel C, Vives Corrons JL. Hematología clínica. 5ª edición. Madrid: Elsevier;
2006.
Schafer AI. Thrombocytosis. N Engl J Med. 2004;350(12):1211-9.
SEHH. Directrices de diagnóstico, tratamiento y seguimiento de la PTI: Documento de Consenso.
Madrid: Prodrug multimedia; 2011.
Steensma DP. Myelodysplastic syndromes: Diagnosis and treatment. Mayo Clin Proc. 2015;90(7):969-
83.
Vallejo C. Aplasia medular adquirida. En: Sanz MA, Carreras E. Manual Práctico de Hematología Clínica.
5ª edición. Barcelona: Antares; 2015; p. 85-96.
Villegas A, Arrizabalaga B, Bonanad S, Colado E, Gaya A, González A y Grupo de Trabajo de HPN de la
Sociedad Española de Hematología y Hemoterapia. Consenso español para el diagnóstico y
tratamiento de la hemoglobinuria paroxística nocturna. Med Clin (Barc). 2016;146(6):278.e1-e7.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1240]
[77] TRASTORNOS DE LA HEMOSTASIA. ANTICOAGULACIÓN
77.Trastornos de la hemostasia. Anticoagulación
José González Medina.
Hematología y Hemoterapia
Juan Ortiz Imedio.
Medicina Interna
Asesoras:
Nerea Castro Quismondo, Mª Ángeles Martín Mola.
Médicas Adjuntas. Hemostasia. Hematología y Hemoterapia
I. HEMOSTASIA
1. CONCEPTO
Se denomina hemostasia al conjunto de mecanismos que mantienen la sangre en estado líquido en
el interior de los vasos y que, ante una lesión endotelial, conservan la integridad del sistema vascular,
previniendo la pérdida de sangre mediante la formación de un tapón hemostático y su regulación.
2. FISIOLOGÍA DE LA HEMOSTASIA
En el proceso de hemostasia normal, se pueden diferenciar varias etapas, que se desarrollan
simultáneamente:
Hemostasia primaria: se activa por alteración endotelial o exposición subendotelial. Se produce
vasoconstricción y formación del tapón plaquetario (adhesión, activación y agregación). Implica
interacción entre las plaquetas, la matriz extracelular, las macromoléculas (como el factor de
von Willebrand) y la pared vascular.
Hemostasia secundaria: comienza sobre la membrana plaquetaria en presencia de fosfolípidos
de carga negativa y calcio. Consta de tres fases: iniciación, amplificación y propagación. In vivo,
la unión entre el factor tisular y el factor VII activado (FVIIa) es el mecanismo más importante
de iniciación (Figura 1).
Fibrinólisis: se produce remodelación y limitación del tapón de fibrina por acción de la plasmina
y se forman productos solubles de degradación. Los principales agentes son el activador del
plasminógeno tisular (tPA) y urinario (utPA). Intervienen también los factores de contacto,
precalicreína y cininógeno de alto peso molecular.
El mantenimiento del equilibrio hemostático corresponde a los inhibidores de la coagulación:
proteína C, proteína S, antitrombina, trombomodulina e inhibidor de la vía extrínseca (TFPI); asimismo,
existen moléculas que previenen una fibrinólisis precoz: inhibidor del activador del plasminógeno (PAI-1),
alfa-2 antiplasmina e inhibidor de la fibrinólisis activado por trombina (TAFI).
La coagulación, como mecanismo de defensa, está íntimamente ligada a la inflamación. La
activación endotelial y la expresión de factor tisular produce un desequilibrio procoagulante. Se sabe que la
trombina estimula la producción de moléculas proinflamatorias, aumentando la permeabilidad endotelial y
la producción de interleucina-6 (IL-6) por los monocitos, los cuales también pueden expresar el factor
tisular. Por último, el depósito de fibrina en los sitios de infección evita la propagación de la enfermedad de
su lugar original. La separación en dos vías (intrínseca y extrínseca), mediante pruebas in vitro, es útil en el
cribado inicial de los desórdenes de la coagulación, aunque actualmente el concepto más aceptado in vivo
se basa en un modelo celular.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1241]
[77] TRASTORNOS DE LA HEMOSTASIA. ANTICOAGULACIÓN
3. APROXIMACIÓN DIAGNÓSTICA: DIÁTESIS HEMORRÁGICA
La diátesis o predisposición hemorrágica puede ser hereditaria o adquirida. Se observa en una gran
variedad de enfermedades, e incluso la pueden producir algunos fármacos.
1. ANAMNESIS
En cuanto a antecedentes personales, se debe interrogar al paciente sobre historia previa de
sangrado, edad y forma de aparición, cuantía y si requirió tratamiento. Se indagará también acerca de
patologías concomitantes y uso de fármacos y/o productos de herbolario, así como de la historia obstétrica
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1242]
[77] TRASTORNOS DE LA HEMOSTASIA. ANTICOAGULACIÓN
y quirúrgica, extracciones dentales y traumatismos, haciendo énfasis en las complicaciones hemorrágicas.
Se recogerán, además, los antecedentes familiares de sangrado hasta tres o más generaciones.
2. EXPLORACIÓN FÍSICA
Exploración cutánea: petequias sugestivas de proceso vascular o plaquetario; y más
inespecíficamente: equimosis, púrpura y hematomas. En las mucosas: epistaxis, gingivorragia, menorragia,
hemorragias digestivas y hematuria. Valorar, asimismo, posibles hemorragias a nivel musculoesquelético,
retroperitoneal e intraabdominal.
3. PRUEBAS DE LABORATORIO
3.1. Pruebas de cribado (Figura 2)
Hemograma: se debe repetir para confirmar las alteraciones.
Tiempo de protrombina (TP) (rango: 10-14 segundos, depende del laboratorio): se utiliza para
detectar anomalías en la vía extrínseca y se prolonga por déficit o inhibición de factores VII, X,
V, protrombina (II) y fibrinógeno. De ellos, VII, X y protrombina dependen de la vitamina K.
Puede representarse como porcentaje (actividad de protrombina) o como INR (international
normalized ratio). El INR se utiliza como monitorización de antagonistas de la vitamina K, como
acenocumarol o warfarina.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1243]
[77] TRASTORNOS DE LA HEMOSTASIA. ANTICOAGULACIÓN
Tiempo de tromboplastina parcial activada (TTPa) (rango: 26-39 segundos, depende del
laboratorio): tiempo de coagulación en presencia de fosfolípidos, un activador de factores de
contacto y calcio. Se denomina “parcial” porque solo lleva la parte lipídica de la tromboplastina.
Valora la vía intrínseca e identifica la deficiencia de todos los factores de coagulación (salvo VII
y XIII), la presencia de inhibidores, anticoagulante lúpico y alteraciones del fibrinógeno. Se
emplea en la monitorización de la terapia con heparina.
Tiempo de trombina (TT) (rango: 14-20 segundos, depende del laboratorio): tiempo de
coagulación en presencia de trombina exógena. Mide la fibrinoformación. Se prolonga en la
hipofibrinogenemia, la disfibrinogenemia, en presencia de inhibidores de trombina (heparina,
dabigatrán, argatrobán) y de productos de degradación del fibrinógeno.
3.2. Pruebas específicas de hemostasia primaria
Si la historia clínica y el examen físico, el recuento plaquetario y las pruebas de cribado orientan a
un trastorno de la hemostasia primaria, se deben realizar las siguientes pruebas:
Tiempo de obturación (PFA-100) (rango normal colágeno/ADP: 71-118 segundos,
colágeno/epinefrina: 94-193 segundos): valora la hemostasia primaria global in vitro. Se utiliza
para el estudio de trombocitopatías y de la enfermedad de von Willebrand (EvW). Su resultado
se ve modificado por trombocitopenia y anemia, lo que limita su uso en estos casos. También
se puede alterar en la cirrosis, la uremia, deficiencias graves de glicoproteínas y por fármacos,
sobre todo antiagregantes y antiinflama- torios no esteroideos (AINE).
Tiempo de hemorragia (método de Ivy): valora la hemostasia primaria de manera global in
vivo, ya que mide el tiempo en que deja de sangrar una pequeña incisión realizada al paciente.
Se trata de una técnica invasiva, difícil de estandarizar, de baja reproducibilidad y sensibilidad.
Actualmente está en desuso.
Agregación plaquetaria: es el método específico más extendido para el estudio de la función
plaquetaria. Se debe realizar ante la sospecha de trombocitopatía o EvW.
Determinación del factor de von Willebrand (FvW): se determinan la carga antigénica y sus
aspectos funcionales, como la actividad como cofactor de ristocetina o su capacidad de unión al
factor VIII (FVIII). También puede estudiarse su capacidad de formar multímeros. Se debe
realizar siempre que se sospeche una alteración de la hemostasia primaria (ver más adelante
Apartado “Enfermedad de von Willebrand”).
Tromboelastografía y test de generación de trombina (TGT): están todavía en fase de
estandarización y desarrollo. Son pruebas globales de hemostasia.
3.3. Pruebas específicas de hemostasia secundaria
Tiempo de reptilasa (TR): al igual que el TT, mide la fibrinoformación. Se diferencia de este en
que no es sensible a la heparina.
Fibrinógeno (rango: 200-560 mg/dL): puede ser calculado (derivado) o cuantificado
directamente (coagulativo) por el método de Clauss, el cual mide el tiempo que tarda en
transformarse a fibrina al añadir trombina.
Corrección de TP y/o TTPa con plasma normal al 50%: diferencia el déficit de factores (corrige
al añadirle plasma normal) de la presencia de inhibidores (no corrige).
Determinación de factores de coagulación: se expresa como porcentaje de actividad respecto
a una curva de referencia.
Detección de anticoagulante circulante: anticoagulante lúpico.
3.4. Otras pruebas
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1244]
[77] TRASTORNOS DE LA HEMOSTASIA. ANTICOAGULACIÓN
Dímero D: producto circulante de la degradación de fibrina. Es muy sensible pero poco
específico. Se utiliza en el diagnóstico y seguimiento de la coagulación intravascular diseminada
(CID), y permite descartar trombosis venosa profunda (TVP) en caso de baja probabilidad
pretest, por su alto valor predictivo negativo. Aumenta con la edad, las neoplasias, el
embarazo, la inflamación y las infecciones.
Factor XIII: participa en la estabilización de la fibrina. Su déficit no altera la vía intrínseca ni
extrínseca, produce hemorragias tardías.
Alfa-2-antiplasmina: los defectos congénitos son muy raros e implican tendencia hemorrágica.
II. TRASTORNOS DE LA HEMOSTASIA
1. DIÁTESIS HEMORRÁGICA
1.1. Trastornos hemorrágicos hereditarios
Enfermedad de von Willebrand: diátesis hemorrágica hereditaria más frecuente. La forma
adquirida es menos habitual. Se produce por un déficit cuantitativo o cualitativo de la síntesis
del FvW. Se hereda de forma autosómica dominante, excepto la tipo 3, que es de herencia
autosómica recesiva o por doble heterocigoto.
Se clasifica en:
Tipo 1 (70-80%): por deficiencia parcial cuantitativa (tipo 1C: aclaramiento del FvW
aumentado).
Tipo 2 (20%): por deficiencias cualitativas (2A, 2M y 2N por pérdida de función y 2B por
ganancia de función).
Tipo 3 (muy infrecuente): por deficiencia completa.
Fisiopatología: el FvW interviene en la adhesión y agregación plaquetaria,
primordial en la hemostasia primaria. Circula unido al FVIII y le protege de su degradación
proteolítica. Se sintetiza en las células endoteliales y megacariocitos. Se libera en respuesta
a diversos estímulos fisiológicos y farmacológicos, incluyendo trombina, fuerzas de
cizallamiento y desmopresina. Su forma multimérica (o de alto peso molecular) es óptima
para su funcionamiento, y está regulada por la metaloproteasa ADAMTS13.
Las manifestaciones hemorrágicas dependen de la gravedad del déficit.
Predominan las hemorragias mucocutáneas (epistaxis, sangrado cutáneo por heridas
menores, sangrados de la cavidad oral), hemorragias tras extracciones dentales o cirugías,
posparto, menorragias o, incluso, sangrados del sistema nervioso central (menos
frecuentes).
El diagnóstico se basa en la historia hemorrágica personal y/o familiar, con cifra de
plaquetas normal o levemente disminuida (tipo 2B), TTPa normal o alargado, tiempo de
obturación prolongado, función plaquetaria normal y disminución de FvW y/o FVIII. Se
confirma mediante pruebas funcionales que miden la actividad del FvW como cofactor de la
ristocetina (FvW: RCo), así como mediante su detección cuantitativa directa (FvW: Ag).
El tratamiento está orientado a detener la hemorragia o prevenirla en caso de
cirugía o procedimientos invasivos:
Hemorragias leves (especialmente en la cavidad oral), extracciones dentarias, cirugía
menor: se pueden emplear hemostáticos locales y antifibrinolíticos como ácido
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1245]
[77] TRASTORNOS DE LA HEMOSTASIA. ANTICOAGULACIÓN
tranexámico (15-25 mg/kg/8-12 h por vía oral; 10 mg/kg/8-12 h por vía intravenosa);
este último está contraindicado en la hematuria. También se utiliza desmopresina
(DDAVP), cuya administración aumenta la concentración plasmática de FvW y FVIII
circulante; la dosis es 0,3 μg/kg por vía intravenosa (diluido en 50-100 ml de suero
salino fisiológico [SSF] al 0,9%, a pasar en 30 minutos). Se produce taquifilaxia después
de la tercera dosis consecutiva. Está contraindicada en niños menores de 2 años por el
riesgo de hiponatremia y es poco recomendable en pacientes cardiópatas o con
antecedentes cerebrovasculares por el riesgo protrombótico.
Cirugía mayor, pacientes en los que la desmopresina es ineficaz o está contraindicada:
se utilizan concentrados de FvW y FVIII derivados del plasma inactivado (Wilate®).
Hemofilia: las hemofilias A y B, de herencia ligada al cromosoma X, se caracterizan por un
defecto cuantitativo del factor VIII y IX, respectivamente. La hemofilia A afecta a 1 de cada
5.000 varones, y la B, a 1 de cada 30.000. Se producen aproximadamente un 30% de casos
esporádicos de ambas. Se clasifican, según el nivel de los factores, en grave (< 1%), moderada
(1-5%) o leve (> 5%).
La aparición de manifestaciones clínicas está en función del grado de deficiencia.
Las manifestaciones más frecuentes son hemartrosis, hematomas musculares y sangrado
tardío persistente tras traumatismos o cirugías. En un menor porcentaje de pacientes,
puede aparecer sangrado intracraneal, gastrointestinal o hematuria. Las formas leves
asintomáticas se diagnostican por alteraciones en estudios rutinarios o preoperatorios
(TTPa alargado).
El diagnóstico se sospecha en todo varón con clínica hemorrágica típica y/o
antecedentes familiares de hemofilia, con un TTPa alargado que corrige al añadir plasma
normal. Se confirma con la determinación de los factores VIII y IX, excluyendo
razonablemente otras causas de alargamiento del TTPa (inhibidores, heparina, deficiencia
de otros factores). El diagnóstico diferencial en el caso de hemofilia A se debe hacer con la
EvW 2N.
Tratamiento:
Hemorragias leves en mucosas (cavidad oral, epistaxis, menorragias): se utilizan
hemostáticos locales, antifibrinolíticos como el ácido tranexámico o desmopresina por
vía intravenosa.
Hemorragia grave o cirugía mayor: se emplean factores derivados del plasma humano o
recombinantes a partir de ingeniería genética (por ejemplo, ReFacto AF®). Es
importante tener en cuenta la probabilidad de desarrollar inhibidores frente al FVIII o
FIX (15-30% en la hemofilia A y 1-4% en la hemofilia B). Se recomienda administrar el
mismo concentrado de factor a cada paciente.
Prevención en hemofilia grave: consiste en la administración de concentrado de factor
de forma periódica.
Otras alteraciones congénitas de la coagulación:
Defectos del fibrinógeno: afibrinogenemia (ausencia completa), hipofibrinogenemia
(deficiencia parcial) y disfibrinogenemia (alteración cualitativa). En el caso de la
afibrinogenemia, se puede realizar profilaxis con infusiones periódicas de concentrado.
Se recomienda la administración de concentrado cuando la cifra de fibrinógeno es
inferior a su rango hemostático (50-100 mg/dL). La disfibrinogenemia es una causa rara
de trombofilia.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1246]
[77] TRASTORNOS DE LA HEMOSTASIA. ANTICOAGULACIÓN
Deficiencia de otros factores de coagulación (II, V, VII, X, XI): se han descrito déficits
aislados o combinados. La clínica hemorrágica es variable, y generalmente está en
relación con el grado de deficiencia. El tratamiento se basa en la administración de
concentrado de factor específico o plasma fresco congelado.
Trombopenia (ver Capítulo 76. “Trombocitopenia. Trombocitosis. Pancitopenia”).
Trombocitopatías congénitas: son anomalías de la función plaquetaria. Las entidades mejor
caracterizadas y con clínica hemorrágica predecible son el síndrome de Bernard- Soulier y la
trombastenia de Glanzmann, ambas de herencia autosómica recesiva y muy raras. Las
alteraciones más frecuentes se deben a defectos de la secreción plaquetaria, con clínica y
expresión en el laboratorio variables; en algunas ocasiones se requieren para su diagnóstico
técnicas no disponibles de forma habitual en el laboratorio.
1.2. Trastornos hemorrágicos adquiridos
Trastornos de la pared vascular: se produce púrpura u otras hemorragias en enfermedades con
formación de inmunocomplejos (viriasis, rickettsiosis, gammapatías monoclonales), escorbuto
(déficit de vitamina C), síndrome de Cushing, envejecimiento (púrpura senil) y vasculitis
(púrpura de Schönlein-Henoch).
Trombocitopenia (ver Capítulo 76. “Trombocitopenia. Trombocitosis. Pancitopenia”).
Disfunción plaquetaria adquirida: puede ser secundaria a fármacos (antiagregantes, AINE,
nitratos, calcioantagonistas o heparina), circulación extracorpórea, hepatopatía, uremia,
paraproteinemia o síndrome mieloproliferativo.
Déficit de vitamina K: la vitamina K es un cofactor necesario para la síntesis de los factores II,
VII, IX y X, y de las proteínas C y S. Su aporte proviene fundamentalmente de la dieta, aunque
también la genera la flora intestinal bacteriana. Su déficit, cuyas causas se muestran en la tabla
I, puede producir clínica hemorrágica variable, objetivándose en el estudio de coagulación un
alargamiento del TP y, posteriormente, del TTPa, con un descenso variable de los factores
dependientes de la vitamina K.
El tratamiento del déficit (no por antagonistas de la vitamina K) consiste en la
administración de 2-10 mg de vitamina K (fitomenadiona, Konakion®) cada 24 horas por vía
oral; en caso de malabsorción, pueden emplearse las vías subcutánea o intravenosa (diluir
en 50-100 ml de SSF y administrar en infusión lenta, no mayor de 1 mg/min).
En caso de hemorragia intensa o necesidad de corrección inmediata, se
administrará complejo protrombínico o, en su defecto, plasma fresco congelado, si no se
dispone del complejo o no precisa reversión urgente.
Hepatopatías: las hepatopatías crónicas y la insuficiencia hepática aguda se asocian con
cambios considerables en la hemostasia (Tabla II). Frente a la consideración clásica de que la
hepatopatía suponía una diátesis hemorrágica, actualmente se propone la existencia de una
hemostasia “reequilibrada”, en la que los factores antitrombóticos son compensados por otros
protrombóticos. Sin embargo, se trata de un equilibrio frágil, y son frecuentes las
complicaciones hemorrágicas y trombóticas en estos pacientes.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1247]
[77] TRASTORNOS DE LA HEMOSTASIA. ANTICOAGULACIÓN
Además, se sabe que las determinaciones habituales (TP, INR, TTPa, fibrinógeno,
recuento plaquetario) solo reflejan una parte del sistema hemostático, no prediciendo
adecuadamente el riesgo de sufrir episodios hemorrágicos o trombóticos. Las nuevas
técnicas que estudian globalmente la coagulación, como el test de generación de trombina
en presencia de trombomodulina y la tromboelastografía, podrían ofrecer una visión más
precisa, pero no están estandarizadas ni disponibles para el uso clínico diario.
Actualmente, se recomienda evitar el uso preventivo de hemoderivados para
corregir las alteraciones de la coagulación antes de la realización de una cirugía o
procedimiento invasivo; por el contrario, las transfusiones deben guiarse por la aparición de
fenómenos hemorrágicos. Esta política se ha demostrado segura en el trasplante hepático
(con mínimos requerimientos de hemoderivados), y debería extenderse a otros
procedimientos habituales (biopsias, toracocentesis y cirugías menores). Como excepción a
esta norma, se considera prudente corregir el alargamiento del TP y la trombocitopenia <
50.000/mm3 en intervenciones de alto riesgo (por ejemplo, la colocación de un monitor de
presión intracraneal en un paciente con fallo hepático agudo). Asimismo, se debe actuar
sobre aquellos factores que alteran el equilibrio hemostático, como la insuficiencia renal
(por disfunción plaquetaria), las infecciones bacterianas (por producción de factores
inhibidores de la coagulación) o las situaciones de aumento de la presión portal (por
ejemplo, la transfusión excesiva de hemoderivados en el sangrado por varices). Se
encuentran en estudio fármacos como la desmopresina, los antifibrinolíticos (ácidos
tranexámico y épsilon aminocaproico) y el factor VIIa recombinante.
Por otro lado, se recomienda no reducir la profilaxis tromboembólica con heparina
de bajo peso molecular (HBPM) cuando esté indicada, incluso en presencia de alteraciones
de las pruebas de coagulación. Las HBPM se han demostrado seguras en la prevención y
tratamiento de los episodios trombóticos venosos en pacientes cirróticos (incluyendo la
trombosis portal), asumiendo sus posibles efectos adversos (trombocitopenia inducida por
heparina, citólisis, osteopenia) y una escasa utilidad de la monitorización con actividad anti-
Xa por infraestimación de su efecto. Los antagonistas de la vitamina K, sin embargo, se han
asociado con un excesivo número de complicaciones hemorrágicas, por lo que se
desaconseja su uso. Los anticoagulantes orales de acción directa (ACOD) ofrecen una
interesante alternativa terapéutica, aunque todavía deben desarrollarse estudios
específicos.
Coagulación intravascular diseminada (CID): consiste en una activación generalizada de la
coagulación, que provoca una extensa formación de fibrina intravascular, especialmente en
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1248]
[77] TRASTORNOS DE LA HEMOSTASIA. ANTICOAGULACIÓN
vasos de pequeño y mediano calibre. La trombosis microvascular generalizada conduce al fallo
orgánico y al consumo masivo de plaquetas y factores de la coagulación, con riesgo de
hemorragias graves. La CID puede presentarse como complicación de múltiples enfermedades
(Tabla III).
Las manifestaciones clínicas más frecuentes son las hemorragias en cualquier
localización (más restringidas a la piel y las mucosas en la CID crónica). Los fenómenos
microtrombóticos pueden dar lugar a necrosis cutánea generalizada (purpura fulminans) y
fallo multiorgánico: insuficiencia renal aguda, disfunción hepática, insuficiencia suprarrenal
aguda, síndrome de distrés respiratorio agudo (SDRA), alteraciones del sistema nervioso
central y shock. También pueden producirse trombosis de grandes vasos y embolia
cerebral.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1249]
[77] TRASTORNOS DE LA HEMOSTASIA. ANTICOAGULACIÓN
El diagnóstico debe basarse en la sospecha clínica, con el apoyo de las pruebas de
laboratorio. Por orden de frecuencia, se han descrito las siguientes alteraciones:
trombocitopenia (98%), elevación de productos de degradación del fibrinógeno (PDF) y
dímeros D, alargamiento de TP y TTPa (50-60%) y descenso del fibrinógeno (40%). Se
recomienda el uso de sistemas de puntuación como el de la ISTH (International Society on
Thrombosis and Haemostasis), que presenta alta sensibilidad y especificidad para el
diagnóstico de CID (Tabla IV); al ser un proceso dinámico, pueden ser necesarias varias
determinaciones antes de confirmar dicho diagnóstico. Existen otras patologías, con
alteraciones analíticas similares, con las que debe realizarse el diagnóstico diferencial
(Tabla V).
El tratamiento de la CID es el de la causa subyacente; sin embargo, algunos casos
pueden requerir medidas específicas. No se deben transfundir hemoderivados en función
únicamente de las alteraciones de las pruebas de laboratorio, sino que han de reservarse
para aquellos pacientes con sangrado activo o con riesgo de desarrollarlo durante un
procedimiento invasivo (Tabla VI). Debe monitorizarse la respuesta al tratamiento
empleado con nuevas determinaciones de laboratorio.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1250]
[77] TRASTORNOS DE LA HEMOSTASIA. ANTICOAGULACIÓN
En pacientes con predominio de fenómenos trombóticos, ha de considerarse la
administración de HBPM o heparina no fraccionada (HNF) a dosis terapéuticas, con
individualización de las dosis valorando la función renal y el riesgo hemorrágico. En los
casos en que coexista un alto riesgo hemorrágico, se recomienda valorar la reposición de
los factores deficientes. El empleo de anticoagulantes fisiológicos, como la antitrombina o
la proteína C activada recombinante, no ha demostrado beneficios. Asimismo, en pacientes
críticos, no sangrantes, en situación de CID, se recomienda la administración de profilaxis
tromboembólica con HBPM.
Inhibidores adquiridos de los factores de la coagulación: se trata de anticuerpos
dirigidos contra uno o varios factores de la coagulación, interfiriendo con su actividad, y
manifestándose clínicamente en forma de hemorragias, que pueden ser graves. El más
frecuente y estudiado es el dirigido contra el FVIII (hemofilia A adquirida). Se identifica
una causa subyacente en la mitad de los casos, y las más frecuentes son: embarazo y
puerperio (típicamente primíparas en el segundo o tercer mes), edad avanzada, artritis
reumatoide (AR), lupus eritematoso sistémico (LES), neoplasias sólidas y hematológicas,
y fármacos (penicilina, sulfamidas, fenitoína, interferón, fludarabina). Se observa un
alargamiento exclusivo del TTPa que no se corrige en la mezcla con plasma normal. El
tratamiento consiste en el control del sangrado mediante el uso de agentes bypass, que
sortean el efecto inhibidor (factor VIIa recombinante, concentrado de complejo
protrombínico activado) y la eliminación del inhibidor mediante la administración de
inmunosupresores (glucocorticoides, ciclofosfamida, rituximab, inmunoglobulinas).
Fármacos: además de los anticoagulantes y fibrinolíticos, existen otros fármacos que
pueden provocar coagulopatía, como: coloides, L-asparaginasa, antiepiléppticos,
antibió́ticos (rifampicina, isoniazida, betalactámicos, ciprofloxacino) y contrastes
yodados.
2. TROMBOFILIA
2.1. Concepto: estado de predisposición a la trombosis producido por trastornos de la coagulación
genéticos o adquiridos. Los defectos hereditarios se asocian generalmente a tromboembolismo venoso. El
trastorno adquirido más importante, el síndrome antifosfolípido, se asocia a trombosis arterial y venosa.
2.2. Etiología
Hereditaria: la incidencia en pacientes que han sufrido enfermedad tromboembólica venosa
(ETEV) oscila entre un 20-40%. Agrupa una serie de mutaciones genéticas que se traducen en
una alteración de los mecanismos anticoagulantes naturales.
Factor V Leiden: es el defecto hereditario más frecuente. Se produce por una mutación
puntual en el gen del factor V, que se traduce en una resistencia del factor Va a la
inactivación por la proteína C activada. El riesgo de trombosis venosa en heterocigotos
es 5-7 veces mayor que en no portadores con otros factores de riesgo (cirugías,
anticonceptivos hormonales, gestación). En homocigotos, el riesgo está aumentado de
30 a 100 veces. El diagnóstico se realiza mediante reacción en cadena de la polimerasa
(PCR).
Mutación G20210A del gen de la protrombina: tiene una prevalencia en caucásicos del
1-3%. Se asocia a un aumento de los niveles de protrombina. El riesgo de trombosis
venosa en heterocigotos es de 2-8 veces más, siendo mayor en homocigotos con otros
factores de riesgo. El diagnóstico se realiza mediante PCR.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1251]
[77] TRASTORNOS DE LA HEMOSTASIA. ANTICOAGULACIÓN
Déficit de proteínas C y S: la proteína C y su cofactor, la proteína S, son proteínas
dependientes de la vitamina K que se sintetizan en el hígado y participan en la
inactivación de los factores Va y VIIIa, lo que disminuye la formación de trombina. Estas
deficiencias se heredan de forma autosómica dominante con penetrancia incompleta.
Los heterocigotos con déficit parcial de proteína C tienen un riesgo de trombosis
venosa 6-10 veces mayor que los no portadores, y los heterocigotos con déficit parcial
de proteína S, en torno a 2 veces mayor. Las formas homocigotas con niveles
indetectables se manifiestan como púrpura fulminante neonatal. En pacientes con
déficit de proteína C o S, la toma de dicumarínicos puede provocar necrosis cutánea.
Los niveles de proteína C y S pueden variar según la edad y se alteran durante los
episodios agudos de enfermedad y/o trombosis.
El diagnóstico de déficit de proteína C se realiza midiendo su funcionalidad, mediante
un test cromogénico, o su concentración en plasma. El déficit de proteína S se
diagnostica midiendo la proteína S libre. Debe realizarse y confirmarse pasado el
episodio agudo de trombosis, en ausencia de tratamiento anticoagulante.
Déficit de antitrombina (AT): la antitrombina es una proteína plasmática de síntesis
hepática que actúa como anticoagulante natural inhibiendo la trombina, FXa, FIXa, FXIa
y FXIIa. El déficit de antitrombina se hereda de forma autosómica dominante y, de las
trombofilias congénitas, es la de mayor riesgo trombótico, aumentando 10 veces el
riesgo. Los estados homocigotos producen muertes intrauterinas o trombosis graves
perinatales. El diagnóstico se realiza mediante pruebas funcionales como cofactor de
heparina o mediante su medición antigénica.
Otros trastornos genéticos: existen otros trastornos de menor relevancia clínica y
frecuencia, como la mutación del gen de la metilen-tetrahidrofolato-reductasa (MTHFR
C677T), que en homocigosis incrementa la susceptibilidad de desarrollar
hiperhomocisteinemia, en particular cuando las concentraciones de folato son bajas. A
pesar de ello, no se recomienda su cribado, ya que el 42% de la población es portadora
en estado heterocigoto.
La homocistinuria clásica se produce por deficiencia de cistationina-ß-sintasa, que da
lugar a hiperhomocisteinemia y aumento de la metionina plasmática.
Adquirida: se deben distinguir los factores de riesgo clínicos de enfermedad tromboembólica
(ver Capítulo 32. “Enfermedad tromboembólica venosa”) de las alteraciones adquiridas del
sistema de la coagulación, que se describen a continuación:
Síndrome antifosfolípido (SAF): patología de origen autoinmune caracterizada por
episodios tromboembólicos (arteriales, venosos o de pequeño vaso) y/o morbilidad en
el embarazo, en presencia de anticuerpos antifosfolípidos. Puede ocurrir de forma
aislada o en el seno de una enfermedad autoinmune, especialmente el LES; también se
ha descrito su asociación a infecciones, fármacos y neoplasias. Para realizar el
diagnóstico de SAF, debe cumplirse al menos un criterio clínico mayor junto con un
criterio de laboratorio (Tabla VII). Además de los episodios tromboembólicos y la
morbilidad en el embarazo, existen otras manifestaciones de la enfermedad (Tabla
VIII). El manejo del síndrome antifosfolípido consiste en el tratamiento y prevención de
los eventos trombóticos (Tabla IX).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1252]
[77] TRASTORNOS DE LA HEMOSTASIA. ANTICOAGULACIÓN
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1253]
[77] TRASTORNOS DE LA HEMOSTASIA. ANTICOAGULACIÓN
Un pequeño grupo de pacientes desarrolla una forma particularmente grave de
la enfermedad, denominada SAF catastrófico, que se puede desencadenar por
infecciones, cirugías o interrupción de la terapia anticoagulante. Se presenta con
manifestaciones trombóticas difusas y fracaso multiorgánico. Para su diagnóstico, debe
existir un antecedente de SAF o anticuerpos antifosfolípido, desarrollarse tres o más
nuevas trombosis orgánicas en el plazo de una semana, confirmarse la presencia de
microtrombos en una biopsia y descartarse otras causas de trombosis multiorgánica o
microtrombosis. El manejo debe ser agresivo, dada su alta mortalidad (30%), y ha de
basarse en el tratamiento de cualquier posible infección precipitante, anticoagulación
con heparina, administración de esteroides a dosis altas (1 g de metilprednisolona iv/24
h durante 3 días, seguido de esteroides orales o parenterales a una dosis equivalente a
1 mg/kg/día de prednisona) y plasmaféresis, con o sin la adición de inmunoglobulinas.
Déficit adquirido de proteína C: se asocia a hepatopatías, sepsis, CID, SDRA, periodo
postoperatorio y utilización de fármacos (ciclofosfamida, metotrexato, 5-fluorouracilo
[5-FU] y L-asparaginasa). Se ha demostrado beneficioso el uso de concentrado de
proteína C en la sepsis meningocócica complicada con purpura fulminans y CID.
Déficit adquirido de proteína S: puede producirse en el embarazo, CID, enfermedad
tromboembólica aguda, infección por virus de la inmunodeficiencia humana (VIH),
hepatopatías y administración de fármacos (anticonceptivos orales y L-asparaginasa).
Hiperhomocisteinemia: la homocisteína es un producto intermedio del metabolismo
de la metionina a cisteína. Su concentración total es producto de una compleja
interacción entre múltiples factores genéticos y ambientales. Los déficits de folato,
vitaminas B6 y B12, más frecuentes en las personas mayores, son la principal causa de
hiperhomocisteinemia. Otras causas son insuficiencia renal crónica, hipotiroidismo,
fármacos, hábito tabáquico y edad.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1254]
[77] TRASTORNOS DE LA HEMOSTASIA. ANTICOAGULACIÓN
La hiperhomocisteinemia es un factor de riesgo independiente de enfermedad
vascular cerebral, periférica, coronaria y de enfermedad tromboembólica, aunque no
tan importante como los factores de riesgo tradicionales. Se aconseja una adecuada
ingesta de vitaminas B, ya sea en la dieta o con suplementos.
2.3. Estudio de trombofilia
Actualmente no existe consenso sobre las indicaciones para realizar el estudio de trombofilia. En
general, se recomienda solicitar estudio de trombofilia genética a los siguientes pacientes: < 50 años con un
primer episodio de trombosis venosa sin factores desencadenantes, trombosis venosas de repetición,
trombosis en territorios venosos inusuales (cerebral, portal, mesentérico, hepático o renal), trombosis
venosa durante la gestación, puerperio o en relación con la toma de anticonceptivos hormonales, y
trombosis venosa con historia familiar en primer grado de ETEV idiopática. En caso de trombosis arterial en
pacientes jóvenes, mujeres con una o más pérdidas fetales o trombosis venosa en localizaciones inusuales,
se aconseja realizar además estudio de trombofilia adquirida.
El estudio de trombofilia se debe efectuar al menos 3 meses después del episodio agudo.
III. ANTICOAGULACIÓN
El tratamiento anticoagulante implica siempre un riesgo hemorrágico, por lo que antes de iniciarlo
se debe valorar la indicación y el balance beneficio/riesgo para el paciente. El nivel de anticoagulación
deseado dependerá del riesgo hemorrágico y trombótico de cada paciente, por lo que el tratamiento debe
ser individualizado.
A continuación, se describen los fármacos anticoagulantes disponibles de uso habitual.
A. ANTICOAGULANTES PARENTERALES
1. HEPARINA NO FRACCIONADA (HNF)
Es una mezcla heterogénea de glucosaminoglicanos sulfatados de carga negativa. La heparina se
une a la antitrombina (AT) por medio de un pentasacárido, produciendo un cambio conformacional en su
centro activo que la convierte en un inhibidor muy rápido de la trombina (FIIa) y de otros factores activados
(FXa, FIXa, FXIa, FXIIa). Al inactivar la trombina, se inhibe la activación plaquetaria mediada por esta y se
previene la formación de fibrina. La trombina y el factor Xa son los más sensibles a la inactivación (la
trombina es 10 veces más sensible que el factor Xa).
La heparina sódica se administra por vía intravenosa, y en bolo el efecto anticoagulante es
inmediato. En el sistema circulatorio se une de manera inespecífica a: proteínas plasmáticas (puede
modificar su efecto anticoagulante, contribuyendo a la variabilidad en la respuesta a la heparina entre
pacientes, así como a la aparición de resistencia a la heparina), células endoteliales y macrófagos
(mecanismo de aclaramiento de heparina), factor plaquetario 4 (FP4) y plaquetas. No atraviesa la barrera
placentaria y no se excreta en la leche materna. La vida media oscila entre 30 minutos y 3 horas. La
eliminación se realiza por unión a células endoteliales y macrófagos y, en menor medida, por vía renal.
El control de su efecto se realiza mediante determinación del TTPa. La pauta habitual para su
administración es una perfusión de 24.000 UI en 500 ml de suero glucosado al 5% a 18 UI/kg/h. Se
recomienda comenzar con 21 ml/h para pacientes con peso entre 60 y 80 kg, o bien con 24 ml/h entre 81 y
95 kg. Si se requiere un efecto anticoagulante inmediato, se podrá administrar un bolo inicial de 80 UI/kg.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1255]
[77] TRASTORNOS DE LA HEMOSTASIA. ANTICOAGULACIÓN
El efecto ha de medirse a las 6 horas de haber iniciado la perfusión y se continuará con controles
cada 6 horas hasta alcanzar el rango deseado (TTPa 1,5-2,5 veces el basal). Posteriormente, los controles se
harán diariamente (Tabla X).
En ocasiones, pueden requerirse dosis inusualmente altas para alcanzar el rango terapéutico o
incluso puede no alcanzarse. Esta resistencia a la heparina puede deberse a: déficit de antitrombina
(solicitar su determinación para descartarlo), aumento de proteínas plasmáticas que se unen a heparina,
aumento del fibrinógeno y del factor VIII, trombocitosis o aumento del aclaramiento de la heparina.
Complicaciones de su uso:
Hemorragia: Se debe detener la perfusión de heparina. En caso de hemorragia vital, si se acaba de
dar un bolo de heparina intravenosa, se administrará 1 mg de protamina por cada 100 UI de HNF. Si
ha pasado media hora, reducir la dosis a la mitad. En cualquier otro caso, y cuando la HNF se pone
en perfusión continua, se administrarán 20 mg de protamina. Hacer control de TTPa a los 15
minutos. Se puede repetir la dosis hasta que cese el sangrado o se corrija el TTPa (no sobrepasar los
100 mg de sulfato de protamina).
Trombocitopenia inducida por heparina (TIH):
o Tipo I: mecanismo no inmune. Se observa un leve descenso de la cifra de plaquetas en los
primeros dos días tras la exposición a heparina. Revierte espontáneamente sin necesidad
de suspender la heparina.
o Tipo II: mecanismo inmune, por formación de anticuerpos anti-FP4 unidos a heparina, que
dan lugar a activación y agregación plaquetaria, así como producción de factor tisular y
daño endotelial. Se observa un descenso del recuento de plaquetas > 50% o entre 20.000-
100.000/mm3 en los 5-15 días tras el inicio de la heparina, o inmediatamente si ha habido
una exposición a ella en los 100 días previos. Puede aparecer trombosis venosa o arterial.
Ante la sospecha de TIH, se debe suspender la heparina y solicitar determinación de anticuerpos
anti-FP4-heparina. Para evaluar la probabilidad de TIH, se sugiere utilizar el score de las 4T
(trombocitopenia, tiempo, trombosis y otra etiología para trombocitopenia; Tabla XI).
Se iniciará anticoagulación con otros fármacos, como argatrobán o fondaparinux (véase más
adelante). La introducción de acenocumarol o warfarina se realizará a dosis bajas cuando el recuento de
plaquetas sea > 150.000/mm3, solapando los primeros días con el anticoagulante elegido para evitar
necrosis cutánea. Se podrá suspender el otro anticoagulante cuando el INR esté en rango terapéutico dos
días consecutivos.
Osteopenia: inhibe la formación de osteoblastos y activa los osteoclastos.
Citólisis hepática: aumento moderado de las enzimas hepáticas, que revierte totalmente con la
suspensión del tratamiento.
Reacciones alérgicas, urticaria.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1256]
[77] TRASTORNOS DE LA HEMOSTASIA. ANTICOAGULACIÓN
2. HEPARINAS DE BAJO PESO MOLECULAR (HBPM)
Las HBPM se obtienen de la despolimerización de la HNF. Ejercen su acción a través de la unión a
antitrombina aunque, por su menor tamaño, tienen menos capacidad para catalizar la inhibición de la
trombina (FII). Su efecto anticoagulante se debe principalmente a que promueven la inactivación del factor
Xa (su relación anti-Xa/anti-IIa varía entre 2/1 y 7/1).
Su unión a proteínas y células es relativamente baja, lo que les confiere mejores propiedades
farmacocinéticas y farmacodinámicas que la HNF; su respuesta es más predecible y su vida media más
larga, por lo que generalmente no precisan control de laboratorio.
Su administración es por vía subcutánea, con una biodisponibilidad cercana al 100%. La vida media
es de 3-6 horas, con un pico de actividad anti-Xa a las 3-5 horas de la administración. Su eliminación es
principalmente renal. Si el aclaramiento de creatinina (ClCr) es de 30-50 ml/ min, valorar reducir la dosis un
20-40%, sobre todo en pacientes ancianos o con factores de riesgo hemorrágico. Con ClCr < 30 ml/min, se
recomienda sustituir por HNF. Se administran en dosis fijas para profilaxis, mientras que las dosis
terapéuticas se ajustan al peso (Tabla XII).
La monitorización de su efecto a dosis terapéutica generalmente no es necesaria, salvo en
situaciones especiales: insuficiencia renal, obesidad y gestación. Se realiza con la determinación de la
actividad anti-Xa a las 4 horas de la administración de la HBPM (Tabla XIII).
Las complicaciones son: sangrado, reacciones alérgicas y necrosis en el punto de punción. La
incidencia de TIH y osteopenia es mucho menor que con la HNF.
Para la reversión del efecto anticoagulante, se pueden administrar 20 mg de sulfato de protamina
(aunque solo neutraliza el 60% de la actividad anti-Xa), con control del TTPa a los 15 minutos. En caso de
hemorragia vital, se puede usar FVIIa recombinante (NovoSeven®) a dosis de 90 μg/kg iv, valorando el
riesgo-beneficio.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1257]
[77] TRASTORNOS DE LA HEMOSTASIA. ANTICOAGULACIÓN
3. FONDAPARINUX (ARIXTRA®)
Heparinoide, pentasacárido sintético inhibidor selectivo del factor Xa, que actúa a través de la
unión a antitrombina. Se administra por vía subcutánea, con una rápida absorción y un efecto
anticoagulante predecible por su baja unión a proteínas plasmáticas. La vida media es de 17-21 horas y se
elimina por vía renal, por lo que se contraindica su uso si el ClCr < 30 ml/min. También está contraindicado
en el embarazo.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1258]
[77] TRASTORNOS DE LA HEMOSTASIA. ANTICOAGULACIÓN
Se administra a dosis fijas de 2,5 mg/24 h para prevención de tromboembolismos, y ajustado al
peso en caso de tratamiento: peso < 50 kg, 5 mg/24 h; peso 50-100 kg, 7,5 mg/24 h; peso > 100 kg, 10
mg/24 h.
No forma complejos con FP4 y no tiene reacción cruzada con anticuerpos antiheparina, por lo que
se puede emplear en caso de TIH.
No tiene antídoto específico. En caso de sangrado incoercible, se empleará plasma fresco
congelado o FVIIa recombinante.
4. ARGATROBÁN
Inhibidor directo de la trombina de bajo peso molecular. Se administra por vía intravenosa y su vida
media es de 45 minutos. Se metaboliza en el hígado a través del sistema enzimático del citocromo P450
3A4/5, por lo que se debe utilizar con precaución en pacientes con disfunción hepática.
Se utiliza como anticoagulante en caso de trombocitopenia inducida por heparina. La dosis inicial
en pacientes adultos sin insuficiencia hepática en la TIH es de 2 μg/kg/min, en perfusión continua. En
pacientes con disfunción hepática moderada (clase B de Child- Pugh), sometidos a cirugía cardiaca o en
estado crítico, se recomienda una dosis inicial de 0,5 μg/kg/min.
El control de su efecto se realiza mediante el TTPa. El intervalo objetivo es de 1,5-3 veces el valor
basal, sin exceder los 100 segundos. El primer control se debe realizar a las 2 horas de haber iniciado la
perfusión. Tras dos TTPa consecutivos dentro del intervalo deseado, se harán controles diarios. El
argatrobán prolonga también el TP, por lo que se alterarán la actividad de protrombina y el INR. No tiene
antídoto específico.
B. ANTICOAGULANTES ORALES
1. ANTAGONISTAS DE LA VITAMINA K
Ejercen su acción a través de la inhibición de la conversión de la vitamina K en su forma activa,
impidiendo la carboxilación de los factores que dependen de la vitamina K (factores II, VII, IX y X, y
proteínas C y S). El descenso de los factores depende de la vida media de cada uno de ellos, siendo el factor
VII y la proteína C los que descienden más rápidamente, por lo que inicialmente puede existir una
hipercoagulabilidad transitoria al disminuir la proteína C.
Los fármacos de este grupo son el acenocumarol (Sintrom®) y la warfarina (Aldocumar®). Su
metabolismo es hepático, vía citocromo P450, por lo que interaccionan con múltiples fármacos y con
alimentos y, consecuentemente, requieren un control estrecho de su efecto. El control se realiza a través
del INR, que debe estar entre 2-3 para la mayoría de las patologías, y entre 2,5-3,5 en algunas patologías de
mayor riesgo.
En cuanto a las dosis, se recomienda comenzar con 2-3 mg/día de acenocumarol o 5 mg de
warfarina. En caso de pacientes ancianos o mayores de 65 años con insuficiencia cardiaca congestiva o
estasis hepática, se recomienda empezar con 1 mg/día de acenocumarol o 2,5 mg de warfarina. Asociar
HBPM a dosis terapéuticas si se requiere anticoagulación inmediata.
Inicialmente, se aconseja realizar controles diarios hasta lograr el rango adecuado, aumentando el
intervalo entre controles progresivamente. Más adelante, los controles se realizarán mensualmente si se
mantiene estable el INR. Ante una sobredosificación, la actitud variará en función del INR y la presencia de
sangrado (Tabla XIV).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1259]
[77] TRASTORNOS DE LA HEMOSTASIA. ANTICOAGULACIÓN
Las complicaciones son: la hemorragia, relacionada con la intensidad de la anticoagulación, la
asociación con otros fármacos (como AINE) y las patologías previas del paciente; la necrosis cutánea por
trombosis de las vénulas y capilares del tejido celular subcutáneo en pacientes con déficit de proteína C o S,
o en caso de síndrome antifosfolípido (requiere suspender el fármaco, administrar vitamina K y reanudar la
anticoagulación con heparina); y la alopecia, que es relativamente frecuente con el acenocumarol.
Están contraindicados durante la gestación, en el primer trimestre por teratogenia y en el tercero
por riesgo de sangrado en el parto.
2. ANTICOAGULANTES ORALES DIRECTOS (ACOD)
Los ACOD están indicados en la prevención de ictus y embolismo sistémico en pacientes con
fibrilación auricular (FA) no valvular, en el tratamiento agudo de la TVP y el embolismo pulmonar (EP) y en
su prevención secundaria, así como en la prevención primaria de trombosis en pacientes sometidos a
cirugía de reemplazo total de cadera o rodilla. Están contraindicados en pacientes con prótesis valvulares
cardiacas.
2.1. Dabigatrán (Pradaxa®)
Inhibidor directo de la trombina. Es un profármaco que se administra por vía oral y se transforma
en su forma activa en el plasma y el hígado. Tiene una vida media de 12-17 horas y una concentración
máxima (Cmáx) a las 2 horas de su administración. Se une a proteínas plasmáticas en un 35%. Su eliminación
es renal (80%) y hepática (20%).
No precisa monitorización de laboratorio. En el estudio de coagulación se puede observar
alargamiento del TTPa y del TT. Un TT normal excluye la presencia de dabigatrán en plasma.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1260]
[77] TRASTORNOS DE LA HEMOSTASIA. ANTICOAGULACIÓN
La dosis terapéutica recomendada es de 150 mg/12 h. Se aconseja reducir la dosis a 110 mg/12 h
en: pacientes > 80 años, o bien de 75-80 años si presentan factores de riesgo hemorrágico (tratamiento con
antiagregantes o AINE, peso < 50 kg); tratamiento concomitante con verapamilo y ClCr 30-50 ml/min con
factores de riesgo hemorrágico.
La dosis profiláctica, según la ficha técnica, en cirugía electiva de reemplazo de cadera o rodilla es
de 220 mg/24 h, administrándose una primera dosis de 110 mg entre 1-4 horas después de la cirugía si se
ha asegurado una correcta hemostasia, y continuando con 220 mg/día. En pacientes ≥ 75 años o con ClCr
30-50 ml/min, se recomienda una primera dosis de 75 mg y continuar con 150 mg/día.
Está contraindicado si el ClCr < 30 ml/min. No se recomienda su uso en cirrosis grado B o C de Child.
2.2. Rivaroxabán (Xarelto®)
Inhibidor directo del factor Xa. Tiene una vida media de 5-13 horas y una Cmáx a las 1,5-3 horas. Se
une a proteínas plasmáticas en un 95%. De la dosis administrada, se metaboliza en el hígado
aproximadamente el 66% (después la mitad se elimina por vía biliar y la otra mitad por vía renal) y el 33%
se excreta por vía renal directamente, como metabolito activo.
No precisa monitorización de laboratorio. El TP es la prueba más sensible.
La dosis terapéutica recomendada es de 20 mg/24 h. Es aconsejable reducir la dosis a 15 mg/24 h si
el ClCr es de 30-50 ml/min. Con ClCr de 15-29 ml/min, se debe utilizar con precaución, a dosis de 15 mg/24
h. En el tratamiento de un episodio agudo de TVP y/o EP, se administran 15 mg/12 h durante las tres
primeras semanas y, posteriormente, 20 mg/día.
La dosis profiláctica en cirugía electiva de reemplazo de cadera o rodilla es de 10 mg/24 h,
comenzando en las 6-10 horas poscirugía si se ha asegurado una correcta hemostasia.
Está contraindicado si el ClCr < 15 ml/min, en la insuficiencia hepática asociada a coagulopatía y en
la cirrosis grado B o C de Child.
2.3. Apixabán (Eliquis®)
Inhibidor directo del factor Xa. Vida media de 8-15 horas y una Cmáx a las 1-3 horas. Se une un 87% a
proteínas plasmáticas y la eliminación por vía renal es solo del 30%, mientras que por vía biliar es del 70%.
No precisa monitorización de laboratorio. El TP es la prueba más sensible.
La dosis terapéutica recomendada es de 5 mg/12 h. Se aconseja la reducción de dosis a 2,5 mg/12 h
en: pacientes ≥ 80 años, peso < 60 kg, ClCr 15-30 ml/min y creatinina ≥ 1,5 mg/dL.
En el tratamiento de un episodio agudo de TVP y/o EP, se administran 10 mg/12 h los primeros 7
días y, posteriormente, 5 mg/12 h. Tras cumplir 6 meses de tratamiento, si se decide continuar con el
mismo, la dosis será de 2,5 mg/12 h. La dosis profiláctica en cirugía electiva de reemplazo de cadera o
rodilla es de 2,5 mg/12 h, comenzando en las 12-24 horas poscirugía.
Está contraindicado en pacientes con hepatopatía asociada a coagulopatía y riesgo clínicamente
elevado de sangrado. No se recomienda su uso en pacientes con insuficiencia hepática grave ni en
pacientes con un ClCr < 15 ml/min.
2.4. Edoxabán (Lixiana®)
Se trata de un inhibidor directo del factor Xa. Tiene una vida media de 9-10 horas y una Cmáx a las
1-2 horas. Se une a proteínas plasmáticas en un 40-59% y la eliminación por vía renal es de un 40%.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1261]
[77] TRASTORNOS DE LA HEMOSTASIA. ANTICOAGULACIÓN
No precisa monitorización de laboratorio. En el estudio de coagulación se puede observar
alargamiento del TP.
La dosis terapéutica es de 60 mg/24 h. Se recomienda reducir a 30 mg/24 h si el paciente presenta
ClCr de 15-50 ml/min, peso < 60 kg y toma simultáneamente fármacos inhibidores de la glucoproteína-P
(ciclosporina, eritromicina, ketoconazol, dronedarona). Está contraindicado en pacientes con hepatopatía
asociada a coagulopatía y riesgo clínicamente elevado de hemorragia, así como en aquellos con un ClCr <
15 ml/min.
El manejo de las complicaciones hemorrágicas derivadas del uso de ACOD se basa en la suspensión
del fármaco y en la instauración de medidas de soporte (hemostasia local, transfusión de hemoderivados,
carbón activado si han pasado menos de 4 horas desde la administración). En caso de hemorragia grave, se
puede administrar complejo protrombínico o FVIIa recombinante, aunque con poca evidencia.
Actualmente, se están desarrollando antídotos específicos para revertir su efecto anticoagulante:
para la reversión del dabigatrán, un fragmento de anticuerpo monoclonal humanizado llamado
idarucizumab (Praxbind®, ya disponible en España); y para la reversión de los inhibidores del factor Xa, una
forma recombinante de factor Xa denominada andexanet-alfa (también es activo frente a HBPM y
fondaparinux).
IV. MANEJO PERIOPERATORIO EN PACIENTES QUE RECIBEN
TRATAMIENTO ANTICOAGULANTE
El manejo del tratamiento anticoagulante en el periodo perioperatorio depende del riesgo
individual de sufrir ETEV y hemorragia. Se deben valorar los factores de riesgo trombótico y hemorrágico
derivados de la patología del paciente, así como los que se derivan de la intervención y del propio
tratamiento anticoagulante empleado en el periodo perioperatorio, tratando de estratificar los riesgos.
Dependiendo de la indicación para la anticoagulación y la comorbilidad asociada, se puede estratificar a los
pacientes en función del riesgo tromboembólico tras suspender la anticoagulación en alto, moderado o
bajo (Tabla XV).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1262]
[77] TRASTORNOS DE LA HEMOSTASIA. ANTICOAGULACIÓN
Debe tenerse en cuenta la probabilidad de sangrado asociado a cada procedimiento. Se consideran
cirugías de alto riesgo hemorrágico: cirugía intracraneal o raquídea, cirugía mayor abdominal, cirugía de
aneurismas, bypass aortocoronario, bypass arterial periférico, cirugía de próstata y vejiga, cirugía
ortopédica (prótesis de cadera o rodilla), cirugía torácica y cardiaca, nefrectomía (en general, cualquier
cirugía mayor que dure más de 45 minutos). También son procedimientos de alto riesgo hemorrágico:
colonoscopia con polipectomía, implantación de marcapasos y biopsia renal y hepática.
Los pacientes con alto o moderado riesgo trombótico que se someten a cirugía de alto riesgo
hemorrágico deben recibir la máxima protección antitrombótica que permita su riesgo hemorrágico.
1. MANEJO DE ANTICOAGULACIÓN PERIOPERATORIA EN PACIENTES QUE RECIBEN ANTAGONISTAS DE LA VITAMINA K
Se recomienda suspender el antagonista de la vitamina K 5 días antes en caso de warfarina y 3 días
antes en caso de acenocumarol. Si el INR persiste elevado (> 1,5) 24 horas antes de la cirugía o
procedimiento, se valorará administrar vitamina K oral (5-10 mg).
Durante la interrupción temporal de la anticoagulación oral, en pacientes con riesgo alto o
moderado de tromboembolismo, se recomienda el empleo de HBPM o HNF a dosis terapéuticas como
puente. En pacientes con bajo riesgo, se aconseja la administración de HBPM a dosis profilácticas.
Si se emplea HBPM a dosis terapéutica como puente, se recomienda administrar la última dosis 24
horas antes de la cirugía. Si se emplea HBPM a dosis profiláctica, es aconsejable administrar la última dosis
12 horas antes de la cirugía. En caso de estar recibiendo HNF, se detendrá su administración 4-6 horas
antes del procedimiento.
Si se trata de cirugía mayor u otro procedimiento de alto riesgo de sangrado, se recomienda
retrasar el inicio de la dosis terapéutica de HBPM o HNF hasta las 48-72 horas poscirugía y asegurar una
hemostasia correcta. Se puede iniciar la administración de HBPM profiláctica a partir de las 12-24 horas tras
la cirugía. En caso de cirugía menor o procedimiento invasivo de bajo riesgo, se recomienda reintroducir la
HBPM a dosis terapéutica al día siguiente del procedimiento, si existe una adecuada hemostasia.
La reintroducción del antagonista de la vitamina K se puede hacer a partir de las 24 horas en cirugía
menor o procedimientos de bajo riesgo, si la hemostasia es correcta, y a partir de las 48-72 horas si el
riesgo hemorrágico es mayor.
Si el paciente que recibe antagonistas de la vitamina K precisa una cirugía o procedimiento urgente,
se recomienda administrar vitamina K intravenosa (5-10 mg). Si precisa una reversión inmediata de la
anticoagulación, se puede administrar plasma fresco congelado o complejo protrombínico, además de la
vitamina K.
2. ANTICOAGULACIÓN PERIOPERATORIA EN PACIENTES QUE RECIBEN ANTICOAGULANTES DE ACCIÓN DIRECTA
El tiempo de suspensión previo a cirugías o procedimientos en el caso de ACOD depende de la
función renal del paciente y del riesgo hemorrágico del procedimiento (Tabla XVI). La reintroducción del
anticoagulante oral se puede hacer a partir de las 24 horas en cirugía menor o procedimientos de bajo
riesgo si la hemostasia es correcta, y a partir de las 48-72 horas si el riesgo hemorrágico es mayor.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1263]
[77] TRASTORNOS DE LA HEMOSTASIA. ANTICOAGULACIÓN
En caso de precisar reversión urgente del efecto de los ACOD, se dispone de un antídoto específico
(idarucizumab para dabigatrán; otros están en desarrollo). Se recomienda retrasar la cirugía hasta que los
parámetros de laboratorio sean normales, o al menos hasta que hayan pasado 12 horas desde la última
dosis del fármaco. Si la intervención no se puede demorar, también se puede contemplar el uso de
complejo protrombínico, a dosis de 20-30 UI/kg, o factor VIIa recombinante, a dosis de 90 μg/kg.
BIBLIOGRAFÍA
Ageno W, Gallus AS, Wittkowsky A, Crowther M, Hylek EM, Palareti G; American College of Chest
Physicians. Antithrombotic therapy and prevention of thrombosis, 9th Edition: American College Of
Chest Physician Evidence-based clinical practice guidelines. Oral anticoagulant therapy. Chest.
2012;141(2 Suppl):e44S-88S.
Arruda VR, High KA. Trastornos de la coagulación. En: Kasper D, Fauci A, Hauser S, Longo D, Jameson
JL, Loscalzo J. Harrison. Principios de Medicina Interna. 18ª ed. Madrid: McGraw-Hill; 2012; p. 973-82.
Cosmi B. Current management of heparin-induced thrombocytopenia. Expert Rev Hematol.
2015;8(6):837-49.
Daniels PR. Periprocedural management of patients taking oral anticoagulants. BMJ.
2015;351:h2391.
Garcia DA, Baglin TP, Weitz J, Samama MM. Antithrombotic therapy and prevention of thrombosis, 9th
Edition: American College Of Chest Physician Evidence-based clinical practice guidelines. Parenteral
anticoagulants. Chest. 2012;141(2 Suppl):e24S-43S.
Greinacher A. Heparin-induced thrombocytopenia. N Engl J Med. 2015;373:252-61.
Hernández-Zamora E, Zavala-Hernández C, Quintana-González S. Enfermedad de von Willebrand,
biología molecular y diagnóstico. Cirugía y Cirujanos. 2015;83(3):255-64.
Hoffman M, Monroe III D. A Cell-based model of hemostasis. Thromb Haemost. 2001;85:958-65.
Konkle B. Trastornos de las plaquetas y de la pared vascular. En: Kasper D, Fauci A, Hauser S, Longo
D, Jameson JL, Loscalzo J. Harrison. Principios de Medicina Interna. 18ª ed. Madrid: McGraw-Hill;
2012; p. 965-73.
Marder VJ, William CA, Bennet JS, Schulman S, White GC. Hemostasis and Thrombosis. Basic Principles
and Clinical Practice. 6ª edición. Philadelphia: Lippincott Williams & Wilkins; 2013.
Potze W, Porte RJ, Lisman T. Management of coagulation abnormalities in liver disease. Expert Rev
Gastroenterol Hepatol. 2015;9(1):103-14.
Ruiz-Irastorza G, Crowther M, Branch W, Khamashta MA. Antiphospholipid syndrome. Lancet.
2010;376(9751):1498-509.
Sanz MA, Carreras E. Manual Práctico de Hematologia Clínica. 5ª edición. Molins de Rei: Antares;
2015.
Wada H, Thachil J, Di Nisio M, Mathew P, Kurosawa S, Gando S, et al. Guidance for diagnosis and
treatment of disseminated intravascular coagulation from harmonization of the recommendations from
three guidelines. J Thromb Haemost. 2013;11:761-7.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1264]
[78] HEMOTERAPIA
78.Hemoterapia
Mario Rodríguez Rodríguez.
Hematología y Hemoterapia
Asesora: Médica Adjunta.
Laura Montejano Ortega.
Banco de Sangre. Hematología y Hemoterapia
I. GRUPOS SANGUÍNEOS
En función de los antígenos de superficie de los hematíes, los diferentes grupos sanguíneos se
clasifican en:
Sistema ABO: los antígenos A y B son codificados por los genes A y B, respectivamente,
mientras que el gen O es un alelo silencioso. Los anticuerpos de este sistema (Tabla I) se
expresan de forma natural y son clínicamente significativos, ya que pueden causar reacciones
hemolíticas transfusionales, así como enfermedad hemolítica del recién nacido (EHRN).
Sistema Rh: el antígeno D determina el grupo Rh (positivo en el 85% de la población, negativo
en el 15% restante). También forman parte de este sistema los antígenos E, e, C y c. Los
anticuerpos no son producidos de forma natural, sino por sensibilización en el seno de una
transfusión sanguínea, gestación, etc. Son también clínicamente significativos, ya que pueden
provocar reacciones transfusionales y EHRN.
Otros grupos sanguíneos con anticuerpos clínicamente significativos son los sistemas Kell,
Duffy y Kidd. Se producen por sensibilización.
Existen además antígenos de alta frecuencia (presentes en más del 99% de la población), frente a
los cuales se pueden desarrollar anticuerpos, lo cual plantea problemas muy importantes a la hora de hallar
donantes compatibles.
II. ASPECTOS GENERALES DE LA DONACIÓN
La única fuente disponible de hemoderivados para la transfusión es la donación. Un colectivo de
donantes lo suficientemente numeroso y concienciado es el primer elemento para garantizar la seguridad
transfusional. Esta donación es altruista, anónima, no remunerada y voluntaria.
Todos los aspectos relacionados con la donación (incluidos los criterios de selección y rechazo de
donantes) y la transfusión de hemoderivados están recogidos en el Real Decreto 1088/2005.
En cada donación se extraen unos 450 ml de sangre total, o bien componentes específicos por
aféresis. De una sola unidad de sangre total se pueden obtener un concentrado de hematíes, un pool de
plaquetas y una unidad de plasma, mediante centrifugación y filtración. A todas las donaciones se les
realizarán las siguientes pruebas: grupo ABO, escrutinio de anticuerpos irregulares y detección de sífilis,
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1265]
[78] HEMOTERAPIA
virus de las hepatitis B (VHB) y C (VHC) y virus de la inmuno- deficiencia humana (VIH) 1 y 2, así como otros
test según el contexto epidemiológico (paludismo, enfermedad de Chagas, virus linfotrópico de células T
humanas [HTLV], etc.).
III. ASPECTOS PRETRANSFUSIONALES
Toda transfusión ha de ser indicada por un facultativo e ir acompañada de:
Una solicitud en la que conste una correcta identificación del receptor y del médico prescriptor,
así como el motivo de la transfusión.
Una muestra de sangre del receptor en un tubo de ácido etilendiaminotetraacético (EDTA),
identificada de forma inequívoca.
Consentimiento informado (en caso de que el paciente se niegue, también debe firmar un
consentimiento de denegación).
1. PRUEBAS PRETRANSFUSIONALES REALIZADAS EN EL BANCO DE SANGRE
Antes de la administración de hemoderivados, es necesario realizar pruebas de compatibilidad,
salvo en casos de extrema urgencia, en los que se debe reflejar por escrito en la solicitud.
Grupo ABO (hemático y sérico) y grupo RhD.
Escrutinio de anticuerpos antieritrocitarios (prueba de Coombs indirecta).
Prueba de Coombs directa: en pacientes con sospecha de anemia hemolítica autoinmune.
Pruebas cruzadas: se enfrenta el suero del paciente con los hematíes de la bolsa que se va a
transfundir; solo se realizarán en pacientes con anticuerpos antieritrocitarios positivos y/o con
prueba de Coombs directa positiva.
Otras pruebas: fenotipo (en pacientes con anticuerpos antieritrocitarios y en
politransfundidos), elución de anticuerpos (en casos con prueba de Coombs directa positiva),
autoadsorción de anticuerpos (en pacientes con autoanticuerpos, para descartar la presencia
de aloanticuerpos).
Las pruebas pretransfusionales se realizarán cada 72 horas en trasplantados, embarazadas o
transfundidos en los últimos 3 meses.
2. OTROS ASPECTOS PRETRANSFUSIONALES
Recomprobación del grupo ABO y Rh del receptor, con una nueva muestra de sangre extraída
en la cabecera del paciente.
Comprobación del hemoderivado: aspecto externo, integridad y caducidad.
Identificación activa e inequívoca del receptor.
IV. TRANSFUSIÓN DE CONCENTRADOS DE HEMATÍES
Concentrado de hematíes (CH): a partir de centrifugación de sangre total o bien por eritroaféresis.
Volumen de 200-300 ml y contenido en hemoglobina (Hb) superior a 40 g.
1. INDICACIONES DE TRANSFUSIÓN DE CONCENTRADOS DE HEMATÍES
1.1. Anemia aguda
Generalmente por hemorragia aguda. Las pérdidas son de sangre total, por lo que su corrección
debe hacerse con distintos componentes para, en primer lugar, mantener la volemia y, por otra parte, el
transporte de oxígeno mediante CH (Tabla II).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1266]
[78] HEMOTERAPIA
1.2. Anemia preoperatoria e intraoperatoria
No existe un valor de Hb por debajo del cual no se pueda practicar una anestesia general o regional.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1267]
[78] HEMOTERAPIA
Los pacientes normovolémicos, sin signos de descompensación cardiopulmonar, que han de ser
intervenidos en un corto plazo de tiempo, solo serán transfundidos si la Hb es < 7 g/dL,
preferentemente durante la cirugía o en el postoperatorio inmediato.
En pacientes con síntomas de enfermedad vascular (cerebral o coronaria) o respiratoria
crónica, está justificada la transfusión preoperatoria para aumentar la Hb por encima de 8,5
g/dL.
1.3. Anemia postoperatoria
En pacientes con enfermedad vascular o respiratoria crónica, mayores de 70 años o sépticos, es
prudente mantener la Hb entre 9-10 g/dL; en el resto, pueden ser suficientes niveles en torno a 7-8 g/dL.
1.4. Anemia crónica en pacientes adultos (Tabla II).
2. CONTRAINDICACIONES
Anemias carenciales (déficit de hierro, vitamina B12 o ácido fólico), salvo que sean sintomáticas y
requieran tratamiento inmediato. Los CH tampoco deberían usarse como expansores plasmáticos.
3. DOSIFICACIÓN
Cada CH eleva la Hb alrededor de 1 g/dL o un 3% el hematocrito. Se administrará la dosis mínima
para eliminar la sintomatología; en muchas ocasiones, un único concentrado alivia la sintomatología y
permite continuar con el tratamiento etiológico. En pacientes añosos o con patología cardiovascular, es
aconsejable no transfundir más de una unidad de forma sucesiva.
4. ADMINISTRACIÓN
Se iniciará lentamente, a un ritmo de 10 gotas/min, vigilando la aparición de posibles efectos
adversos en los primeros 5-10 minutos. Después, se aumentará el ritmo de transfusión hasta 30-60
gotas/min. Habitualmente, un CH se transfundirá en 1-2 horas. En pacientes cardiópatas, oligoanúricos, de
edad avanzada y en casos de anemia intensa, será necesario disminuir el ritmo, no sobrepasando nunca las
4 horas.
V. TRANSFUSIÓN DE PLAQUETAS
Concentrado de plaquetas: a partir de sangre total, de unas cinco donaciones, o bien de
plaquetoaféresis de un único donante.
1. INDICACIONES DE TRANSFUSIÓN DE PLAQUETAS (TABLA II)
2. CONTRAINDICACIONES
Púrpura trombótica trombocitopénica, trombocitopenia de origen inmune (púrpura
trombocitopénica idiopática), trombocitopenia inducida por heparina.
3. DOSIFICACIÓN
Cada concentrado eleva el recuento, generalmente, en 30.000-50.000 plaquetas/mm3.
4. ADMINISTRACIÓN
No son necesarias pruebas de compatibilidad eritrocitaria si únicamente van a ser transfundidas
plaquetas. Es recomendable premedicar con 1 ampolla de dexclorfeniramina (Polaramine®). La transfusión
se realizará, por lo general, en 20-30 minutos; nunca deberá exceder las 4 horas por riesgo de
contaminación bacteriana.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1268]
[78] HEMOTERAPIA
VI. TRANSFUSIÓN DE PLASMA FRESCO CONGELADO
Plasma fresco congelado (PFC): a partir de donación de sangre total o de plasmaféresis. Es una
fuente fundamental de factores de coagulación, albúmina, inmunoglobulinas (Ig), etc.
1. INDICACIONES DE TRANSFUSIÓN DE PLASMA FRESCO CONGELADO (TABLA II)
2. DOSIFICACIÓN
Dependerá de la causa y del estado del paciente. La dosis habitual de restauración de factores de
coagulación es de 10-20 ml/kg de peso, con lo que aumentaría en un 20% la concentración de factores. Es
importante realizar un control postransfusional mediante actividad de protrombina y tiempo de
tromboplastina parcial activada (TTPa).
3. ADMINISTRACIÓN
No son necesarias pruebas cruzadas, pero sí compatibilidad ABO. El PFC deberá ser transfundido
inmediatamente después de su descongelación; de no ser así, podrá ser conservado entre 1-6 °C durante
un máximo de 24 horas. La transfusión se iniciará lentamente a un ritmo de 10 gotas/min, vigilando la
aparición de posibles efectos adversos, y aumentando después el ritmo hasta unas 125 gotas/min. Una
unidad de PFC de 300 ml se transfundirá en 20-30 minutos. En pacientes cardiópatas, oligoanúricos, de
edad avanzada, etc., el ritmo de transfusión se disminuirá, no excediendo nunca las 2 horas.
VII. REACCIONES ADVERSAS A LA TRANSFUSIÓN
Ante la sospecha de una reacción transfusional aguda, se debe interrumpir inmediatamente la
infusión del producto hemoderivado, verificar la correcta identificación del producto y del paciente, evaluar
el estado clínico del enfermo y notificar dicha sospecha de reacción al servicio de transfusión, al que se
remitirá una muestra de sangre del paciente, el producto hemoderivado y la documentación.
1. COMPLICACIONES AGUDAS
1.1. Reacción transfusional hemolítica aguda
Los hematíes transfundidos son destruidos de forma aguda por anticuerpos presentes en el plasma
del receptor. La principal causa es incompatibilidad ABO; otra posible causa es la aloinmunización del
paciente.
Clínica: fiebre, escalofríos, taquicardia, hipotensión, shock, dolor torácico, dolor lumbar,
hemorragia, coagulación intravascular diseminada, hemoglobinuria, hiperbilirrubinemia
indirecta.
Tratamiento: detener la infusión de inmediato. Iniciar sueroterapia para remontar la
hipotensión y mantener buen ritmo de diuresis, usando fármacos vasoactivos si fuera preciso.
Valorar el uso de diuréticos. Reponer factores de coagulación si fuera preciso.
1.2. Reacción transfusional febril no hemolítica
Está producida por citocinas liberadas en el producto transfundido durante el periodo de
almacenamiento.
Clínica: fiebre, con o sin tiritona, hasta 2 horas después de la transfusión. No se acompaña de
hipotensión.
Tratamiento: interrumpir la infusión hasta descartar otras reacciones graves, administrar
antitérmicos.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1269]
[78] HEMOTERAPIA
1.3. Reacción transfusional alérgica
Se debe a la presencia en el producto hemoderivado de sustancias a las que el paciente es alérgico,
como fármacos o ciertas proteínas.
Clínica: desde manifestaciones cutáneas hasta reacciones anafilácticas, aunque generalmente
son leves.
Tratamiento: interrumpir la transfusión; antihistamínicos, corticoides y adrenalina si fuera
preciso. Es importante descartar déficit de IgA, ya que precisará productos deficitarios en IgA o
lavados en suero salino.
1.4. Lesión pulmonar aguda producida por transfusión (TRALI)
Se debe a anticuerpos antineutrófilo presentes en el producto hemoderivado. Los neutrófilos se
aglutinan y quedan atrapados en la microcirculación, dañan el endotelio de los capilares pulmonares y
aumentan su permeabilidad, produciéndose daño alveolar.
Clínica: insuficiencia respiratoria aguda e infiltrados pulmonares bilaterales durante o en las 6
horas siguientes a una transfusión de hemoderivados.
Tratamiento: detener la infusión e iniciar oxigenoterapia; en ocasiones se precisa intubación
orotraqueal y ventilación mecánica. Administrar sueroterapia si hubiera deterioro
hemodinámico. No hay evidencia para el uso de corticoides.
1.5. Aloinmunización frente a antígenos eritrocitarios inducida por la transfusión
Durante una transfusión se administran al paciente factores extraños a su organismo (antígenos
eritrocitarios), lo cual puede inducir la formación de aloanticuerpos. Por lo general, no afectará a la
transfusión en curso, pero sí a transfusiones posteriores, pudiendo causar reacciones hemolíticas
inmediatas o retardadas.
1.6. Aloinmunización frente a antígenos plaquetarios
Los pacientes pueden desarrollar aloanticuerpos frente al sistema HLA (antígenos de
histocompatibilidad) de las plaquetas transfundidas o frente a antígenos plaquetarios específicos,
presentando refractariedad a la transfusión de plaquetas; habrá que administrarles plaquetas HLA
compatibles.
1.7. Contaminación bacteriana
Excepcionalmente, los productos hemoderivados pueden contener bacterias procedentes de la piel
del donante, habitualmente bacilos gramnegativos o cocos grampositivos. Dan lugar a un cuadro de sepsis
con fiebre, escalofríos e hipotensión. Es necesario interrumpir la transfusión, tomar cultivos del producto
transfundido y del paciente, dar soporte hemodinámico y administrar tratamiento antibiótico empírico
para cubrir grampositivos y Pseudomonas aeruginosa.
1.8. Sobrecarga circulatoria
Se trata interrumpiendo la transfusión y administrando oxigenoterapia y furosemida.
2. COMPLICACIONES RETARDADAS
2.1. Reacción hemolítica retardada
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1270]
[78] HEMOTERAPIA
En ocasiones, pacientes ya inmunizados presentan un título tan bajo de aloanticuerpos que no es
detectable en las pruebas pretransfusionales. Tras la transfusión, aumenta el título de aloanticuerpo,
produciéndose una reacción hemolítica a las 2-3 semanas.
2.2. Púrpura postransfusional (PPT)
Generalmente en mujeres ya sensibilizadas frente al antígeno plaquetar HPA-1. Da lugar a una
trombocitopenia grave con púrpura a los 3-10 días de la transfusión de plaquetas. El tratamiento incluye el
uso de esteroides, inmunoglobulinas e incluso plasmaféresis. Será necesario administrar plaquetas HPA-1
negativas.
2.3. Enfermedad de injerto contra huésped (EICH)
Es una complicación excepcional, producida por linfocitos T del donante en pacientes con
inmunosupresión grave. Se manifiesta a los 10-15 días de la transfusión con erupción cutánea, diarrea,
hepatitis, fiebre y pancitopenia.
2.4. Transmisión de agentes infecciosos
A pesar de las actuales medidas de seguridad, existe riesgo de transmisión de infecciones:
1/400.000 para VIH, 1/250.000 para VHC y 1/100.000 para VHB.
2.5. Sobrecarga de hierro secundaria a politransfusión
Complicación propia de pacientes incluidos en programas de transfusión crónica. Se produce un
acúmulo de hierro a nivel orgánico, especialmente en el hígado y el corazón, siendo necesario un
seguimiento periódico de los niveles de ferritina, así como resonancia magnética hepática y/o cardiaca para
medir los depósitos cuando sea preciso. El tratamiento será con quelantes del hierro (deferoxamina,
deferiprona, deferasirox).
VIII. AFÉRESIS
El objetivo fundamental de los procedimientos de aféresis terapéutica (citaféresis y plasmaféresis)
es la eliminación de determinadas células sanguíneas o componentes plasmáticos, cuya acumulación
excesiva se considera causa o determinante de síntomas de ciertas patologías. Durante este proceso, se
separan los distintos componentes sanguíneos en función de su densidad, tamaño y peso mediante un
proceso de centrifugación. De esta manera, se forma una capa eritrocitaria, una capa leucoplaquetaria y
otra capa constituida por plasma, siendo posible la extracción de uno de los componentes de forma
selectiva.
Dentro de las aféresis terapéuticas, la más frecuentemente realizada es la plasmaféresis/ recambio
plasmático, en la cual se extrae un importante volumen de plasma del paciente, que es sustituido con PFC o
con albúmina, dependiendo de la patología presentada por el paciente.
1. INDICACIONES (TABLA III)
Categoría I: patologías en las que la plasmaféresis está aceptada como tratamiento de primera
línea, en solitario o asociada a otros tratamientos.
Categoría II: patologías en las que la plasmaféresis está aceptada como tratamiento de segunda
línea, en solitario o asociada a otros tratamientos.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1271]
[78] HEMOTERAPIA
BIBLIOGRAFÍA
Añón JM, García A, Quintana M, González E, Bruscas MJ. Lesión pulmonar aguda producida por la
transfusión. Med Intensiva. 2010;34(2):139-49.
Comisión de transfusión del Hospital 12 de Octubre. Guía de transfusión, indicaciones y uso de los
hemoderivados. 2ª edición. Madrid; 2015.
Kelton JG, Heddle NM, Blajchman MA. Transfusión sanguínea, bases teóricas y aplicación clínica.
Barcelona: Doyma; 1986.
Ortiz P, Mingo A, Lozano M, Vesga MA, Grifols JR, Castrillo A, et al. Guía sobre la transfusión de
componentes sanguíneos. Med Clin. 2005;125(10):389-96.
Sociedad Española de Transfusión Sanguínea y Terapia Celular. Guía sobre la transfusión de
componentes sanguíneos y derivados plasmáticos. 4ª edición. Barcelona; 2010.
Szczepiorkowski ZM, Winters JL, Bandarenko N, Kim HC, Linenberger ML, Marques MB, et al. Apheresis
Applications Committee of the American Society for Apheresis. Guidelines on the use of therapeutic
apheresis in clinical practice. Evidence-based approach from the Apheresis Applications Committee of
the American Society for Apheresis. J Clin Apher. 2010; 25(3):83-177.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1272]
[79] ADENOPATÍAS. ESPLENOMEGALIA. ESPLENECTOMÍA
79.Adenopatías. Esplenomegalia. Esplenectomía
Clara Cabañuz Rocatallada.
Medicina Interna
Amaia López de Lacalle Juega.
Hematología y Hemoterapia
Asesores:
Carlos Grande García.
Médico Adjunto de Hematología y Hemoterapia
Juan María Herrero Martínez.
Médico Adjunto de Medicina Interna
I. ADENOPATÍAS
1. INTRODUCCIÓN
Las adenopatías se definen como un aumento del tamaño o una consistencia alterada de los
ganglios linfáticos. En general, se considera normal un tamaño menor de 1 cm, pero varía en función de la
localización del ganglio y la edad del paciente.
Es un hallazgo tan frecuente que hasta un 50% de los pacientes evaluados por otras causas tienen
adenopatías cervicales. Si la causa no está clara, el proceso diagnóstico tiene que ser rápido y no se debe
administrar ningún tratamiento empírico (solo en caso de compromiso de la vía aérea podría estar
justificada la administración de corticosteroides).
Las adenopatías periféricas sin clara causa tras una historia clínica dirigida suponen un dilema en la
práctica habitual. Por un lado, hay causas graves que pueden producirlas, aunque es lo más infrecuente;
por otro lado, para el diagnóstico de certeza, habitualmente es necesaria una biopsia, que es un
procedimiento invasivo, injustificado en la mayoría de los casos.
2. ETIOLOGÍA
Existen diferencias según la epidemiología; así, en países con alta prevalencia de tuberculosis (TB),
esta es la primera causa de adenopatías cervicales. El 75% de las adenopatías son localizadas y más del 50%
se detectan en la región de la cabeza y el cuello, y suelen estar causadas por una enfermedad específica en
la región que recoge ese drenaje linfático. El 25% son generalizadas y son un signo dentro de una
enfermedad sistémica de base.
A grandes rasgos, es posible agrupar la etiología según el acrónimo CHICAGO:
Cáncer: neoplasias hematológicas como linfomas (Hodgkin y no-Hodgkin), leucemias,
macroglobulinemia de Waldenström, mastocitosis sistémica. Metástasis (dependerá de la
localización).
Hipersensibilidad (síndromes de hipersensibilidad): enfermedad del suero. Fármacos
(difenilhidantoína, carbamazepina, primidona, sales de oro, alopurinol, indometacina, atenolol,
captopril, sulfasalazina, hidralazina, cefalosporinas). Enfermedad de injerto contra huésped,
posvacunal.
Infecciones: víricas (virus de Epstein-Barr [VEB], virus de la inmunodeficiencia humana [VIH],
citomegalovirus [CMV], adenovirus, virus varicela-zóster [VVZ], hepatitis virales), bacterianas
(infecciones cutáneas por estafilococos y estreptococos, enfermedad por arañazo de gato,
chancroide, TB, micobacterias atípicas, clamidias, sífilis, fúngicas (histoplasmosis,
coccidioidomicosis), protozoos (toxoplasmosis), helmintos (filariasis).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1273]
[79] ADENOPATÍAS. ESPLENOMEGALIA. ESPLENECTOMÍA
Conectivopatías: lupus eritematoso sistémico (LES), artritis reumatoide (AR), dermatomiositis,
enfermedad mixta del tejido conectivo, síndrome de Sjögren.
Atípicos (enfermedades linfoproliferativas atípicas): enfermedad de Castleman, granulomatosis
con poliangeítis (Wegener).
Granulomatosas: TB, histoplasmosis, silicosis, beriliosis, enfermedad por arañazo de gato.
Otras: enfermedad de Kikuchi, enfermedad de Rosai-Dorfman, enfermedad de Kawasaki.
Adenopatías localizadas: casi siempre son manifestación de una enfermedad a nivel local (Tabla I).
Adenopatías generalizadas: como etiologías más frecuentes cabe mencionar la infección por VIH,
TB ganglionar, mononucleosis infecciosa, LES y síndromes de hipersensibilidad. Etiologías infrecuentes son
la enfermedad de Castleman, la enfermedad de Kikuchi, la enfermedad de Kawasaki o el linfoma T
angioinmunoblástico.
3. APROXIMACIÓN DIAGNÓSTICA (Figura 1)
Se debe realizar una anamnesis dirigida y una exploración física minuciosa ante la presencia de
linfadenopatías, para establecer en qué casos es preciso realizar un estudio etiológico.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1274]
[79] ADENOPATÍAS. ESPLENOMEGALIA. ESPLENECTOMÍA
Especial importancia tienen la edad, los factores epidemiológicos (exposición a animales, ingesta de
carne poco cocinada, viajes, etc.), el tiempo de evolución y los síntomas acompañantes (síndrome
constitucional, prurito generalizado, etc.). En cuanto a la exploración física, se debe describir con detalle:
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1275]
[79] ADENOPATÍAS. ESPLENOMEGALIA. ESPLENECTOMÍA
Localización anatómica y si son localizadas o generalizadas (afectación de dos o más
localizaciones anatómicas, incluido el anillo de Waldeyer y las epitrocleares).
Tamaño (en general, son patológicas si son mayores de 1 cm, pero este criterio varía en función
de la localización y la edad).
Consistencia (duras, blandas) y movilidad (adheridas a planos profundos, móviles). −
Hepatoesplenomegalia, lesiones cutáneas, etc.
1. EXPLORACIONES COMPLEMENTARIAS
En el caso de que la anamnesis y la exploración física orienten a un proceso sistémico o malignidad
se debe comenzar el estudio diagnóstico.
1.1. Estudio básico inicial
Hemograma, bioquímica completa que incluya lactato deshidrogenasa (LDH), proteinograma,
serologías (prueba serológica para la sífilis [VDRL] y prueba de la reagina plasmática rápida [RPR], VIH,
toxoplasma, VEB, CMV), prueba de Mantoux, anticuerpos antinucleares (ANA) y anti-DNA, beta-2-
microglobulina, radiografía de tórax y valorar ecografía abdominal.
1.2. Pruebas de imagen
Ayudan a determinar el tamaño de la adenopatía, a distinguir masas no linfáticas y a seleccionar la
adenopatía de mayor tamaño como paso previo al estudio histológico.
Ecografía: las características ecográficas que orientan a malignidad son: ratio eje largo/eje
corto < 2, hipoecogenicidad en comparación con los tejidos adyacentes, ausencia de hilio,
índices de resistencia y pulsatilidad elevados cuando se valora con ecografía Doppler.
Tomografía computarizada (TC): puede ayudar en la detección de adenopatías de localización
profunda.
Tomografía por emisión de positrones (PET): no está establecida su utilidad en la valoración de
adenopatías, pero puede ser de ayuda cuando la sospecha de malignidad es alta y no se ha
llegado a un diagnóstico a pesar de un estudio histológico inicial, o cuando se trata de
adenopatías poco accesibles para su estudio histológico.
2. DIAGNÓSTICO HISTOLÓGICO
Es el método de referencia para la evaluación de adenopatías (Tabla II).
2.1. Punción-aspiración con aguja fina (PAAF)
Actualmente es una prueba de utilidad limitada, ya que el escaso material que permite obtener, en
la mayoría de casos, resulta insuficiente para llegar a un diagnóstico etiológico, lo que obliga a repetir la
biopsia y produce retrasos en el diagnóstico. Podría ser útil en sospechas de recidiva tumoral en pacientes
con neoplasia conocida. Una alternativa de probada eficacia es la biopsia con aguja gruesa (BAG).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1276]
[79] ADENOPATÍAS. ESPLENOMEGALIA. ESPLENECTOMÍA
Limitaciones:
La principal: que la muestra no sea significativa.
Elevada tasa de falsos negativos en el linfoma de Hodgkin y clasificación incompleta en el caso
de linfomas no-Hodgkin.
Podría mejorar la sensibilidad si se hace guiada por ecografía.
2.2 Biopsia ganglionar
Prueba de gran rentabilidad diagnóstica, sobre todo si se realiza guiada por imagen (TC o ecografía),
lo que permite, además, la posibilidad de realizar una BAG y obtener un diagnóstico definitivo en la
mayoría de los casos.
Es imprescindible su realización cuando se sospecha un linfoma.
Debe elegirse la adenopatía de mayor tamaño y de características patológicas.
Si no es diagnóstica y persisten las adenopatías, debe repetirse.
4. TRATAMIENTO
El tratamiento será el de la enfermedad de base.
II. ESPLENOMEGALIA
1. CONCEPTO
Tradicionalmente, el método de referencia para el diagnóstico de esplenomegalia se consideraba el
peso del bazo, el cual, para un adulto sano, es de aproximadamente 150 gramos. No obstante, dado que
esto solo se podía establecer tras realizar una esplenectomía, se propuso un nuevo criterio diagnóstico, el
diámetro cráneo-caudal esplénico, dato objetivo y de fácil estudio.
De esta manera, hoy en día la esplenomegalia se puede definir mediante parámetros clínicos y
radiológicos. Por un lado, a través del hallazgo de un bazo palpable en la exploración física, lo que requiere
un aumento en torno al 40% de su tamaño normal (12 cm x 7 cm x 3,5 cm) y, por otro lado, mediante
pruebas de imagen abdominal que permiten un diagnóstico más precoz, así como un seguimiento
evolutivo.
Por último, se habla de esplenomegalia masiva en aquellos casos en los que el bazo sobrepase la
línea media umbilical o el polo inferior del bazo se introduzca en la pelvis.
2. FISIOPATOGENIA
El bazo está compuesto por la pulpa roja (relacionada con el sistema circulatorio y su función
depurativa o de filtración) y la pulpa blanca (unida al sistema inmune) y desempeña múltiples funciones
fisiológicas:
Inmunidad humoral y celular: es el órgano linfoide más grande del organismo y alberga el 25%
de la masa linfoide.
Filtro o depuración de las células envejecidas, algunas bacterias y proteínas anómalas.
Hematopoyesis extramedular: es fisiológica en los primeros meses de la vida fetal, y es
consecuencia del fracaso u ocupación medular que desplaza la hematopoyesis normal en los
adultos.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1277]
[79] ADENOPATÍAS. ESPLENOMEGALIA. ESPLENECTOMÍA
Equilibrio homeostático: regulación del flujo espleno-portal gracias a su capacidad de albergar
gran volumen sanguíneo. La esplenomegalia se puede producir por diferentes mecanismos
fisiopatogénicos, que son comunes para determinadas enfermedades (Tabla III).
3. APROXIMACIÓN DIAGNÓSTICA (Figura 2)
El diagnóstico diferencial de la esplenomegalia es muy extenso, por lo que una anamnesis
cuidadosa y dirigida, una exploración física minuciosa y los estudios analíticos iniciales pueden ayudar a
orientar los posibles diagnósticos.
Anamnesis: interrogar al paciente sobre antecedentes familiares, consumo de tóxicos, factores
de riesgo para enfermedades infecciosas (viajes recientes, prácticas sexuales de riesgo,
contacto con animales), síndrome constitucional, factores de riesgo para enfermedad
trombótica, traumatismos recientes.
Exploración física: se realizará en decúbito supino y, para no obviar una esplenomegalia
masiva, se comenzará la palpación en la fosa ilíaca izquierda y se avanzará hacia el cuadrante
superior izquierdo. La posición en decúbito lateral derecho y la inspiración profunda facilitan la
detección de la esplenomegalia. Además, se realizará una valoración de otros estigmas o
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1278]
[79] ADENOPATÍAS. ESPLENOMEGALIA. ESPLENECTOMÍA
hallazgos que puedan orientar el diagnóstico, como adenopatías (síndrome linfoproliferativo
crónico), palidez o ictericia (anemia ± hemólisis) o estigmas de hepatopatía.
Pruebas complementarias: han de realizarse una serie de pruebas iniciales (Figura 2). El frotis
puede aportar información fundamental en determinadas ocasiones (presencia de linfocitos
atípicos en síndromes linfoproliferativos, esferocitos y reticulocitosis en la anemia hemolítica
autoinmune, mielemia y dacriocitos en la mielofibrosis, cuadro leucoeritroblástico en la
infiltración medular metastásica, granulación tóxica con presencia de cayados en infecciones,
etc.). Posteriormente, se valorará la realización de una prueba de imagen (ecografía, TC, etc.)
para el estudio de neoplasias, patología hepática con hipertensión portal o colecciones
infecciosas. Se considerará, además, la posibilidad de practicar una biopsia dirigida (adenopatía,
lesiones sugerentes de malignidad, etc.) en el caso de haberse detectado alguna anomalía. Si
todos estos estudios resultan negativos, se podrá plantear la realización de un estudio de
médula ósea (anatomopatológico y microbiológico) y como último recurso se valorará, siempre
y cuando el beneficio supere al riesgo, la realización de una esplenectomía.
4. TRATAMIENTO
El de la causa subyacente. Las indicaciones de la esplenectomía se detallan más adelante (Tabla IV).
5. COMPLICACIONES
Rotura o infarto esplénico.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1279]
[79] ADENOPATÍAS. ESPLENOMEGALIA. ESPLENECTOMÍA
Hiperesplenismo: situación en la que el bazo secuestra y destruye mayor cantidad de células
debido al aumento del flujo sanguíneo o por producción de anticuerpos dirigidos frente a las
células sanguíneas. La tríada típica consiste en esplenomegalia, citopenias por destrucción
aumentada de una o más series hematopoyéticas y médula normocelular con aumento del
recambio celular (presencia de reticulocitos, plaquetas inmaduras, cayados y
polimorfonucleares inmaduros en sangre periférica).
Hipoesplenismo funcional: disminución de las funciones esplénicas por infartos esplénicos
sucesivos (típico en la anemia drepanocítica).
III. ESPLENECTOMÍA. HIPOESPLENISMO
1. INDICACIONES
Las causas más frecuentes de esplenectomía son el traumatismo con rotura esplénica y las lesiones
yatrogénicas en cirugías abdominales. En algunas enfermedades hematológicas puede estar indicada en
situaciones de hiperesplenismo no controlable con citopenias relevantes (Tabla IV). En todas ellas siempre
se deberá realizar un balance riesgo/beneficio individualizado y, en los casos en los que sea posible, se
realizará la esplenectomía por vía laparoscópica.
2. REPERCUSIONES FUNCIONALES
Tanto la esplenectomía como la asplenia funcional o congénita producen un estado de
hipoesplenismo o disminución de las funciones desempeñadas por el bazo, lo que provoca un estado de
vulnerabilidad frente a determinadas infecciones. Esto se debe, por un lado, a la menor producción de
anticuerpos IgM e IgG, que origina una menor eliminación de bacterias recubiertas por dichas
inmunoglobulinas y, por otro lado, a la deficiente actividad fagocítica frente a microorganismos
encapsulados.
El riesgo de infección se relaciona con la edad (es más elevado cuanto mayor es la edad), el motivo
de la esplenectomía (superior en inmunodeficiencias, linfomas y talasemias, y menor en la esplenectomía
traumática) y el tiempo transcurrido desde la cirugía (máximo durante los 2-3 primeros años).
3. MANEJO DEL PACIENTE ESPLENECTOMIZADO
1. EDUCACIÓN DEL PACIENTE Y SUS ALLEGADOS CERCANOS
Es fundamental la correcta concienciación, tanto del paciente como de sus convivientes más
cercanos, sobre la mayor vulnerabilidad a las infecciones de los pacientes esplenectomizados. Se debe
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1280]
[79] ADENOPATÍAS. ESPLENOMEGALIA. ESPLENECTOMÍA
insistir en el cumplimiento estricto de los calendarios vacunales, además de la consulta precoz ante
cualquier síntoma infeccioso al centro sanitario más cercano.
Por otro lado, los individuos esplenectomizados deberán recibir consejos y recomendaciones
especiales si van a realizar viajes a zonas endémicas para enfermedades como malaria o meningococo
serogrupo A, y se desaconsejarán los viajes a áreas endémicas de Babesia.
2. PREVENCIÓN DE LA SEPSIS EN EL PACIENTE ESPLENECTOMIZADO
El riesgo de sepsis y de mortalidad por esta causa es de 50 a 600 veces más alto que en la población
general; muchas infecciones ocurren en los dos primeros años postesplenectomía, pero permanece algún
grado de riesgo a lo largo de la vida. Streptococcus pneumoniae es el causante hasta en un 50% de los
casos, aunque algunas series de pacientes recientes sugieren que tras la vacunación de estos pacientes con
VNC13 + VNP23 podría estar cambiando la epidemiología y ser más frecuentes los bacilos gramnegativos.
Como causantes, también destacan cepas invasivas de Haemophilus influenzae y, en menor porcentaje,
Salmonella spp, Escherichia coli, Pseudomonas aeruginosa y Capnocytophaga canimorsus.
Se han ensayado estrategias de prevención basadas en:
Profilaxis antibiótica: a día de hoy, no se aconseja la quimioprofilaxis universal (algunos autores
defienden su indicación en la prevención secundaria tras sepsis por germen encapsulado, niños
menores de 5 años o en adultos durante los 3 años siguientes a la esplenectomía).
Autoadministración de antibióticos y consulta temprana a urgencias en caso de fiebre.
Inmunoprofilaxis.
3. INMUNOPROFILAXIS
En el bazo se producen la mayoría de anticuerpos IgM necesarios para la opsonización de gérmenes
encapsulados.
Se recomienda vacunar 15 días antes de la esplenectomía (si no es posible, retrasar la vacuna hasta
2 semanas después) frente a los microorganismos que aparecen en la tabla V (además de las
recomendadas para la población general, por lo que habrá que revisar todo el calendario vacunal).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1281]
[79] ADENOPATÍAS. ESPLENOMEGALIA. ESPLENECTOMÍA
4. MANEJO DE EPISODIOS FEBRILES EN PACIENTES ESPLENECTOMIZADOS (FIGURA 3)
BIBLIOGRAFÍA
Bazemore AW, Smucker DR. Lymphadenopathy and malignancy. Am Fam Physician.
2002;66(11):2103-10.
Dubin LG, Schaffner W. Clinical practice. Care of the asplenic patient. N Engl J Med. 2014;371(4):349-
56.
Fijten GH, Blijham GH. Unexplained lymphadenopathy in family practice. An evaluation of the probability
of malignant causes and the effectiveness of physicians’ workup. J Fam Pract. 1988;27(4):373-6.
Habermann TM, Steensma DP. Lymphadenopathy. Mayo Clin Proc. 2000;75(7):723-32.
Khanna R, Sharma AD, Khanna S, Kumar M, Shukla RC. Usefulness of ultrasonography for the
evaluation of cervical lymphadenopathy. World J Surg Oncol. 2011;9:29.
Kim DK, Bridges CB, Harriman KH; Advisory Committee on Immunization Practices. Recommended
Immunization Schedule for Adults Aged 19 Years or Older: United States, 2016. Ann Intern Med.
2016;164(3):184-94.
Leone G, Pizzigallo E. Bacterial infections following splenectomy for malignant and nonmalignant
hematologic diseases. Mediterr J Hematol Infect Dis. 2015;7(1):e2015057.
Mohseni S, Shojaiefard A, Khorgami Z, Alinejad S, Ghorbani A, Ghafouri A. Peripheral lymphadenopathy:
approach and diagnostic tools. Iran J Med Sci. 2014;39(2 Suppl):158-70.
Nasuti JF, Yu G, Boudousquie A, Gupta P. Diagnostic value of lymph node fine needle aspiration
cytology: an institutional experience of 387 cases observed over a 5-year period. Cytopathology.
2000;11(1):18-31.
Pozo AL, Godfrey EM, Bowles KM. Splenomegaly: Investigation, diagnosis and management. Blood Rev.
2009;23(3):105-11.
Spelman D, Buttery J, Daley A. Guidelines for the prevention of sepsis in asplenic and hyposplenic
patients. Inter Med J. 2008;38(5):349-56.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1282]
[80] URGENCIAS ONCOLÓGICAS
80.Urgencias oncológicas
Beatriz Gil Haro.
Oncología Radioterápica
Gustavo Ruiz Ares.
Oncología Médica
Asesores:
María Ángeles Cabeza Rodríguez.
Médica Adjunta de Oncología Radioterápica
Guillermo de Velasco Oria de Rueda.
Médico Adjunto de Oncología Médica
I. COMPRESIÓN MEDULAR
1. Generalidades
La compresión de la médula espinal (CM) es la segunda complicación neurológica en los pacientes
oncológicos, siendo su incidencia del 5%. Es una urgencia médica, ya que un retraso en el manejo
terapéutico puede suponer déficits neurológicos irreversibles, implicando un empeoramiento en la calidad
de vida y una disminución de la supervivencia.
2. Fisiopatología y etiología
La CM se produce por un compromiso del saco dural y sus contenidos, causado por una masa
tumoral de origen primario o metastásico. Puede desarrollarse de tres formas:
Lesiones extradurales-epidurales: son las más frecuentes (85%). Se producen por crecimiento
de una metástasis ósea en el espacio epidural. El compromiso ocurre comúnmente por
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1283]
[80] URGENCIAS ONCOLÓGICAS
afectación del cuerpo vertebral, mientras que en un porcentaje menor la neoplasia se localiza
paravertebralmente.
Lesiones intradurales-extramedulares: secundarias a diseminación leptomeníngea.
Lesiones intradurales-intramedurales: son las menos frecuentes. Tienen muy mal pronóstico.
La fisiopatología de la CM se describe en la figura 1.
La localización más frecuente es en la columna dorsal (60-70%), seguida de la lumbosacra (20-30%)
y la cervical (10%). Cualquier tumor puede causar CM, aunque los tumores de mama, pulmón y próstata
son los más comunes.
3. Clínica
La presentación clínica de la CM varía en función de la localización, severidad y duración de la
compresión. Entre la sintomatología destaca:
3.1. Dolor
Aparece en el 83-95% de los casos. Generalmente precede en semanas a los síntomas neurológicos.
Se localiza en el segmento afecto, es de intensidad progresiva y puede empeorar con los movimientos
(sugiriendo en este caso inestabilidad ósea), con la posición de decúbito y con las maniobras de Valsalva.
Puede presentarse al principio como un dolor radicular. En las lesiones intradurales-intramedulares no
suele aparecer dolor. En algunos casos se describe el signo de L’hermitte (sensación breve tipo descarga
eléctrica que ocurre al flexionar el cuello).
3.2. Déficit motor
Es el segundo síntoma más frecuente, ocurriendo en el 60-85% de los casos.
Generalmente se produce debilidad simétrica en extremidades inferiores, de inicio proximal, con
paraparesia, claudicación y compromiso progresivo de la deambulación hasta la paraplejia. Puede aparecer
hiperreflexia o hipertonía y las lesiones radiculares pueden venir acompañadas de atrofia.
3.3. Alteraciones sensitivas
Aparecen aproximadamente en el 50% de los pacientes al diagnóstico. Se describen de forma más
común como hipoestesia o parestesias distales en miembros inferiores que ascienden hasta alcanzar el
nivel medular de la lesión.
3.4. Disfunción autonómica (impotencia, incontinencia urinaria y fecal)
Se describe en un 40-60% de los pacientes. Aparece de forma tardía, implicando un grado avanzado
en la lesión medular, excepto en lesiones a nivel del cono medular, donde constituye un síntoma precoz.
3.5. Ataxia
La ataxia de la marcha en el contexto de un paciente oncológico con dolor de espalda debe plantear
la sospecha de CM.
4. Diagnóstico
Ante la sospecha clínica, las primeras maniobras diagnósticas serán la anamnesis y la exploración
neurológica. Posteriormente, se realizarán pruebas de imagen para confirmar el cuadro.
4.1. Radiografía simple
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1284]
[80] URGENCIAS ONCOLÓGICAS
Es el estudio más sencillo. Puede detectar anomalías como el colapso del cuerpo vertebral o la
erosión del pedículo con radiculopatía asociada en el 75-83% de los casos. No debe emplearse como
screening ya que presenta hasta un 20% de falsos negativos.
4.2. Resonancia magnética nuclear (RMN)
Es la prueba de imagen de elección. Debe realizarse lo antes posible si hay sospecha clínica. Posee
una sensibilidad del 93% y una especificidad del 97% para la detección de CM. Un signo característico es la
hiposeñal en T2 comprimiendo el saco tecal. Es de gran utilidad para la planificación terapéutica, tanto
quirúrgica como radioterápica.
4.3. Tomografía computarizada (TC)
Se puede realizar cuando no se dispone de RMN o está contraindicada, superando a esta última en
la valoración del grado de destrucción y estabilidad de la columna.
4.4. Mielografía-TC
Muy poco empleada hoy en día. Ofrece información indirecta y parcial y tiene riesgos importantes.
4.5. Gammagrafía ósea
Posee más sensibilidad que la radiografía simple, pero menos especificidad. No se encuentra
disponible como prueba de imagen urgente, pero conviene su realización posteriormente, ya que permite
diagnosticar otras metástasis óseas en caso de estar presentes.
En todos los casos debe realizarse un diagnóstico diferencial con abscesos, hematomas,
hemangiomas, hernias discales, secuelas de tratamientos antitumorales y síndromes paraneoplásicos.
5. Pronóstico
Los pacientes se clasifican en tres grupos pronósticos según la escala pronóstica de MESCC (Tablas I
y II), que se utilizan para guiar la decisión y el esquema terapéutico a seguir.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1285]
[80] URGENCIAS ONCOLÓGICAS
El factor pronóstico principal es el grado de déficit neurológico establecido en el momento del
diagnóstico y el tiempo transcurrido desde el inicio de la clínica hasta llevar a cabo un tratamiento. Si previo
al tratamiento se ha producido paraplejia y han transcurrido más de 24 horas, la posibilidad de
recuperación de la función neurológica es mínima (10-15%). Otros factores pronósticos a tener en cuenta
son la rapidez de instauración del cuadro y su duración, la presencia de colapso vertebral, la localización de
la CM (peor a nivel cervical y torácico), la afectación multinivel, la disfunción vesical o intestinal, la
extensión sistémica de la enfermedad neoplásica y la histología tumoral. Se consideran histologías
favorables los tumores de mama, de próstata, linfomas, mielomas y seminomas, y desfavorables los
carcinomas no microcíticos de pulmón, sarcomas, melanomas, tumores renales y de origen desconocido.
6. Abordaje terapéutico
El objetivo fundamental es el control de la función neurológica del paciente junto con la
disminución del dolor. El tratamiento debe individualizarse, eligiéndose en función del pronóstico, número
y localización de las lesiones, la histología de las mismas, la clínica neurológica y la velocidad de
instauración del cuadro. Asimismo, debe llevarse a cabo de forma multidisciplinar, incluyendo las siguientes
opciones (Figura 2).
6.1. Medidas generales
Reposo, profilaxis tromboembólica con heparinas de bajo peso molecular, analgesia, sondaje
vesical si retención urinaria y prevención del estreñimiento.
6.2. Corticoesteroides
Se deben iniciar de forma precoz ante la sospecha de una CM. El fármaco más utilizado es la
dexametasona, debido a su reducida actividad mineralocorticoide, elevada acción antiinflamatoria y
prolongada vida media (36-54 horas). Se administra de forma inicial una dosis de 10 mg en bolo iv, seguida
de una dosis de mantenimiento de 16 mg cada 24 horas iv repartidos cada 6-8 horas. Una vez se estabilice
la clínica neurológica puede iniciarse una reducción progresiva de la dosis (aproximadamente reducir 1/3
de la dosis cada 3-4 días) y cambiar la administración a la vía oral.
Los posibles efectos secundarios se pueden consultar en Anexo VI. “Inmunosupresión y sus
complicaciones”.
6.3. Radioterapia
La radioterapia (RT) es el pilar fundamental del tratamiento en la mayoría de los casos, siendo de
elección en pacientes no candidatos a cirugía. Debe iniciarse lo antes posible. Al administrarse junto con
corticoides consigue descomprimir las estructuras nerviosas por su efecto citorreductor tumoral, disminuir
el déficit neurológico (45-60%), revertir la paresia (10-20%) y controlar el dolor. No hay claro consenso
sobre la dosis y el fraccionamiento a llevar a cabo, debiendo individualizarse en función del tipo histológico
y pronóstico de cada paciente.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1286]
[80] URGENCIAS ONCOLÓGICAS
El estándar suele ser una dosis total de 30 Gy, en 10 sesiones. En pacientes con paraplejia
instaurada > 48 horas, bajo performance status (PS) o mal pronóstico en términos de supervivencia, podría
administrarse una sesión única de 8 Gy.
6.4. Cirugía
Mediante esta técnica se consigue mejorar o aliviar el dolor, descomprimir de forma inmediata la
médula espinal, estabilizar la columna y llegar a un diagnóstico histopatológico de la lesión.
Existen indicaciones específicas para el tratamiento quirúrgico (Tabla III). Se recomienda llevar a
cabo la cirugía en las primeras 24 horas tras el diagnóstico, seguida de RT a las 2 semanas, ya que se han
demostrado resultados superiores con el tratamiento combinado.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1287]
[80] URGENCIAS ONCOLÓGICAS
6.5. Quimioterapia
La quimioterapia (QT) se considera uno de los tratamientos de elección en caso de tumores
altamente quimiosensibles como los linfomas, tumores germinales o carcinoma microcítico de pulmón,
sobre todo en niños o pacientes jóvenes, en los que la RT puede ocasionar alteraciones en el crecimiento y
aumentar el riesgo de segundos tumores. Valorar en aquellos adultos que hayan sido tratados previamente
con RT en la misma localización o en los que no sean candidatos a RT o cirugía.
II. METÁSTASIS CEREBRALES
1. Concepto
Las metástasis cerebrales son el tumor intracraneal más común en los adultos, constituyendo más
del 50% de todos los tumores cerebrales. En pacientes con neoplasias sistémicas, pueden aparecer en el
10-30% de los adultos y el 6-10% de los niños. Son la complicación neurológica más frecuente en los
pacientes oncológicos.
2. Etiopatogenia
En los adultos, los carcinomas son los responsables de la mayor parte de las metástasis cerebrales,
siendo más frecuentes las metástasis del cáncer de pulmón, mama y melanoma. Son poco probables en
tumores de próstata, orofaringe y piel. En los niños, la etiología más frecuente son los sarcomas,
neuroblastomas y tumores de células germinales.
Por lo general, ocurren a través de diseminación hematógena, con predilección por los hemisferios
cerebrales. Suelen asociar edema vasogénico perilesional por la interrupción de la barrera
hematoencefálica.
3. Clínica
Son sintomáticas en el 70% de los casos. Entre la sintomatología destacan:
3.1. Cefalea (40-50%)
Es el síntoma más frecuente, fundamentalmente en el caso de lesiones múltiples o localizadas en la
fosa posterior. Puede acompañarse de náuseas y vómitos.
3.2. Déficit neurológico (20-40%)
Lo más común es la hemiparesia, pero puede variar en función de la localización de la metástasis.
3.3. Disfunción cognitiva (30-35%)
Incluye alteraciones de la memoria, cambios en el estado de ánimo y en la personalidad.
3.4. Crisis comiciales (10-20%)
Se producen por el desarrollo de actividad cerebral anómala. Pueden aparecer en forma de crisis
parciales o generalizadas. Más comunes en pacientes con lesiones múltiples o con histología de melanoma.
3.5. Accidente cerebrovascular (5-10%)
Causado por sangrado de la metástasis, hipercoagulabilidad, invasión o compresión de una arteria
por el tumor o embolización por las células tumorales. Las metástasis más propensas al sangrado son las
debidas a melanoma, coriocarcinoma, carcinoma tiroideo y carcinoma renal.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1288]
[80] URGENCIAS ONCOLÓGICAS
4. Diagnóstico
Las metástasis cerebrales deben diferenciarse de los tumores cerebrales primarios, procesos
infecciosos, enfermedades inflamatorias y degenerativas, accidentes cerebrovasculares, fenómenos
paraneoplásicos y efectos secundarios de algunos tratamientos, como la radionecrosis.
En la mayor parte de los casos, se diagnostican tras conocer el tumor primario, hablando de
metástasis metacrónicas. En un porcentaje menor, son la primera manifestación de la enfermedad
oncológica o se presentan al mismo tiempo, denominándose metástasis sincrónicas.
Las pruebas complementarias para su diagnóstico son las siguientes:
Tomografía axial computarizada (TC)
Es la técnica más empleada debido a su accesibilidad. Las lesiones de pequeño tamaño
requerirán la administración de contraste intravenoso adicional.
Resonancia magnética (RM)
Es el estudio de elección debido a su elevada sensibilidad. Los signos radiológicos que pueden
ayudar a diferenciar las metástasis cerebrales de otras lesiones del sistema nervioso central son
la presencia de lesiones múltiples, los márgenes circunscritos y la asociación de edema
vasogénico perilesional. El uso de espectroscopia puede contribuir a esclarecer la naturaleza
biológica de la lesión, ya que permite diferenciar entre parénquima cerebral normal, edema,
necrosis tumoral o desmielinización.
PET-TC
Puede emplearse en el estudio de tumor primario desconocido o para localizar enfermedad
metastásica a otro nivel.
Biopsia
Se llevará a cabo cuando haya dudas acerca del diagnóstico; es especialmente importante
tenerlo en cuenta en pacientes con lesión única.
Punción lumbar
Puede realizarse cuando existe sospecha de diseminación metastásica leptomeníngea.
5. Pronóstico
Se encuentra relacionado con la edad, el PS, la histología del tumor primario y la existencia o no de
enfermedad extracerebral.
En la figura 3 se muestra un esquema de los factores pronósticos realizado por el Radiation Therapy
Oncology Group (RTOG).
Es fundamental distinguir entre metástasis cerebrales únicas o múltiples en los pacientes nivel I y II.
De esta forma, podemos considerar pacientes de bajo riesgo (supervivencia esperada mayor de seis meses)
a aquellos que presenten nivel I con tres o menos lesiones y nivel II con lesión única. De lo contrario, serán
considerados de alto riesgo con una supervivencia inferior a los seis meses.
Teniendo en cuenta la histología tumoral, el pronóstico empeora en el caso de tumores con menos
sensibilidad a la radioterapia, como melanoma, sarcoma y carcinoma renal.
6. Abordaje terapéutico
El objetivo principal es la mejoría de la calidad de vida. El manejo está compuesto por terapias
sintomáticas y definitivas.
6.1. Terapias sintomáticas de soporte
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1289]
[80] URGENCIAS ONCOLÓGICAS
Corticoesteroides
Constituyen un tratamiento fundamental en pacientes con metástasis cerebrales que presentan
edema sintomático. Su mecanismo de acción se relaciona con la disminución de la
permeabilidad de los capilares del tumor. El más utilizado es la dexametasona. Se recomienda
iniciar el tratamiento con una dosis de carga de 10 mg en bolo vía iv y, posteriormente, una
dosis de mantenimiento de 16 mg vía oral en 24 horas, repartidos cada 4, 6 u 8 horas.
Cuando existe riesgo de herniación pueden ser necesarias medidas urgentes para reducir el edema
cerebral (manitol). La supresión de tratamiento corticoideo debe ser gradual, siendo recomendable
retirarlo completamente siempre que sea posible.
Anticomiciales
No se recomiendan de forma preventiva, sino en casos de crisis epilépticas al diagnóstico o que
aparezcan durante el tratamiento de las metástasis. El fármaco más utilizado es el
levetiracetam.
6.2. Terapias definitivas
Están basadas en la cirugía y la radioterapia. La elección en cada caso dependerá de la localización,
tamaño y número de metástasis cerebrales, edad, PS, control del tumor primario y existencia de
enfermedad extracerebral.
Radioterapia holocraneal
Indicada en pacientes con metástasis cerebrales múltiples y/o afectación extracerebral no
controlada, como tratamiento paliativo. Tiene como finalidad mejorar la función neurológica y,
en determinados pacientes, prolongar la supervivencia. Se objetiva mejoría clínica en el 50-90%
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1290]
[80] URGENCIAS ONCOLÓGICAS
de los casos, apareciendo la misma entre 1 a 3 semanas tras el inicio de la radioterapia. Las
posibles toxicidades agudas de este tratamiento incluyen astenia, somnolencia, cefalea,
náuseas, vómitos, eritema y alopecia.
Los efectos a largo plazo pueden incluir alteraciones en la conducta y disminución de la capacidad
intelectual. Por este motivo, en pacientes de clase pronóstica I se puede valorar realizar un tratamiento
sobre la metástasis con margen (hipofraccionamientos o RT estereotáxica). Durante la irradiación es
recomendable mantener la terapia corticoidea debido a que puede aumentar el edema cerebral.
Radiocirugía
Consiste en la administración de una dosis elevada de radiación sobre un área cerebral. Los
candidatos a esta técnica son aquellos pacientes que presentan buen estado general, un
máximo de 3-4 lesiones y un diámetro de las mismas menor de 35 mm. En evaluaciones
retrospectivas, obtiene resultados similares a la cirugía, con la ventaja de poder tratar
metástasis no accesibles a esta última.
Se ha descrito cefalea, crisis comiciales, náuseas, vómitos, alopecia e hidrocefalia como
complicaciones agudas. De forma tardía puede desarrollarse una pseudoprogresión en las pruebas de
imagen que es preciso conocer para su manejo terapéutico específico.
Cirugía
Puede ser una opción terapéutica en pacientes con una a tres metástasis cerebrales, PS ≥ 70 y
tumor primario controlado. Entre sus beneficios se encuentra la mejoría de los síntomas
neurológicos, la posibilidad de obtener histología en caso de ser necesaria e incluso el aumento
de la supervivencia (los últimos estudios han demostrado un aumento de hasta 14 meses en
casos seleccionados). El uso de RT holocraneal o focal posquirúrgica parece disminuir la recidiva
tumoral.
Quimioterapia
Puede valorarse su empleo en el caso de tumores primarios quimiosensibles.
III. SÍNDROME DE VENA CAVA SUPERIOR
1. Concepto
Se define el síndrome de vena cava superior (SVCS) como el conjunto de signos y síntomas que
ocurren por obstrucción de la vena cava superior (VCS).
2. Etiopatogenia
El SVCS se produce por un déficit en el retorno del flujo sanguíneo de la VCS al corazón, bien por
invasión de la misma o por compresión debida a un proceso adyacente. La causa más frecuente son los
procesos neoplásicos –los cuales suponen hasta un 80% de los casos– principalmente el carcinoma de
células no pequeñas (50%), el carcinoma epidermoide de pulmón (25%) y el linfoma no Hodgkin (10%). En
un porcentaje menor, puede deberse a una trombosis asociada a catéter venoso central, suponiendo una
causa indirectamente relacionada con el proceso oncológico subyacente. Entre las causas no malignas,
pueden incluirse la fibrosis mediastínica, alteraciones vasculares, procesos infecciosos y algunos tumores
benignos.
3. Clínica
Se basa en los signos y síntomas secundarios a la obstrucción venosa central.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1291]
[80] URGENCIAS ONCOLÓGICAS
La disnea es lo más frecuente (54%), seguida de tos, dolor torácico, cefalea y disfagia. Entre los
signos que aparecen, destacan el edema facial y de miembros superiores, la ingurgitación yugular y, menos
frecuentemente, la plétora facial. Existe una “triada clásica” caracterizada por edema en esclavina, cianosis
facial y circulación colateral toracobraquial. La clínica empeora con los cambios posturales, principalmente
con el decúbito, la maniobra de Valsalva y la flexión ventral del tronco.
En la mayoría de los casos, los síntomas se desarrollan gradualmente a lo largo de varias semanas.
Si la obstrucción de la VCS aparece de forma súbita, se puede producir edema cerebral con riesgo de
fallecimiento del paciente.
4. Diagnóstico
Está basado fundamentalmente en la clínica y las pruebas de imagen radiológicas.
4.1. Radiografía de tórax
Permite observar anomalías hasta en el 80% de los casos, siendo las más frecuentes
ensanchamiento mediastínico superior (35-65%), masa hiliar derecha (12-40%) y derrame pleural
(generalmente derecho).
4.2. TC de tórax con contraste intravenoso
Es la prueba más útil. Aporta información sobre el nivel de la obstrucción y la extensión de la
misma, permite identificar si existe trombosis asociada y muestra la presencia de adenopatías o masa
mediastínica, así como la afectación de otras estructuras.
4.3. Resonancia magnética
Indicada en casos de alergia al contraste intravenoso.
4.4. Flebografía
Se usa en casos excepcionales, en SVCS asociado a trombosis.
5. Abordaje terapéutico
Se basa en la corrección de los síntomas mediante el manejo del proceso de base (Figura 4). El SVCS
no es una urgencia vital, por lo que se debe intentar conseguir un diagnóstico histopatológico, en caso de
carecer de él, antes de iniciar el tratamiento.
5.1. Medidas generales
Elevación del cabecero y oxigenoterapia.
Valorar el uso de diuréticos y la restricción dietética de sal, para intentar reducir el edema. En
caso de emplearlos, vigilar la aparición de trombosis secundaria por deshidratación.
Corticoesteroides (el más utilizado es la dexametasona) para disminuir la posible inflamación
tumoral.
5.2. Terapia endovascular (stent)
Indicada en casos de SVCS de etiología maligna o benigna refractaria o en pacientes con
compromiso hemodinámico. Ofrece un alivio sintomático rápido, puede realizarse aun cuando no se
disponga de diagnóstico etiológico y no invalida la utilización de otros tratamientos posteriores. Está
contraindicada en oclusión completa y enfermedad cardiaca crónica.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1292]
[80] URGENCIAS ONCOLÓGICAS
5.3. Quimioterapia
Es de elección en los tumores quimiosensibles (carcinoma microcítico de pulmón, linfomas y
tumores de células germinales). La remisión de la sintomatología se consigue a los 5-10 días.
5.4. Radioterapia
Reduce los síntomas en las primeras 72 horas. Se puede aplicar en monoterapia o combinada con
QT. Es de elección en los tumores menos quimiosensibles.
5.5. Fibrinólisis
Se emplea en el SVCS trombótico. Se recomienda la anticoagulación durante 3-6 meses tras un
episodio de trombosis para prevenir la progresión y recurrencia, aunque la duración exacta ofrece
controversia. En casos de trombosis asociada a catéter, considerar la retirada del mismo y el inicio de
anticoagulación.
IV. SÍNDROME DE LISIS TUMORAL
1. Concepto
El síndrome de lisis tumoral (SLT) es un conjunto de alteraciones causadas por una destrucción
masiva de células y la liberación de su contenido al torrente circulatorio. Se caracteriza por hiperuricemia,
hiperfosfatemia, hipocalcemia e hipercalemia.
El SLT suele ocurrir después del inicio del tratamiento quimioterápico en neoplasias de alto índice
proliferativo (por ejemplo, leucemias agudas linfoblásticas, linfomas de alto grado y tumores germinales),
con gran carga tumoral o alta sensibilidad al tratamiento.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1293]
[80] URGENCIAS ONCOLÓGICAS
2. Fisiopatología
La masiva destrucción celular produce la liberación de potasio, fósforo, ácidos nucleicos y del
producto del catabolismo de estos últimos, ácido úrico. La elevada cantidad de estos metabolitos
sobrepasa los mecanismos homeostáticos encargados de su procesamiento, causando inicialmente
alteraciones analíticas, seguidas de clínicas.
La primera alteración bioquímica que se suele observar es la hipercalemia. Puede aparecer en
las primeras 6 horas después de iniciar la QT y puede ser extremadamente grave, provocando
arritmias y muerte súbita.
Simultáneamente, como consecuencia directa de la hiperuricemia, los cristales de ácido úrico
precipitan en los túbulos renales, particularmente en el medio ácido de los túbulos distales,
disminuyendo la excreción renal y provocando fracaso renal agudo.
La hiperfosfatemia conduce a un aumento del producto calcio-fósforo, existiendo el riesgo de
que el fosfato cálcico precipite en los tejidos, con la consiguiente disminución del calcio en
sangre (hipocalcemia). Si la cristalización se produce en el parénquima renal, será otro factor
que contribuirá al empeoramiento de su función.
La insuficiencia renal, además, provoca acidosis metabólica, lo que acelera la cristalización del
ácido úrico en los túbulos renales, desencadenando una cascada fuera de control.
3. Diagnóstico
Véase la tabla IV a continuación.
4. Factores de riesgo
Con el objeto de identificar a los pacientes con riesgo de sufrir SLT y, de esta manera, dirigir las
medidas preventivas necesarias, se utiliza una clasificación que los divide en tres grupos de riesgo, en
función del tipo de neoplasia, la carga tumoral y la sensibilidad al tratamiento (Tabla V). Se han descrito
otros factores de riesgo como edad avanzada, deshidratación, daño renal previo o hiperuricemia. Evaluar y
estratificar a los pacientes según su riesgo de sufrir SLT es la medida más importante que permitirá decidir
qué tipo de medidas preventivas deben aplicarse.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1294]
[80] URGENCIAS ONCOLÓGICAS
5. Abordaje terapéutico
5.1. Tratamiento preventivo
Tiene como objetivo disminuir la formación de ácido úrico, favorecer su degradación y aumentar su
excreción renal. Las medidas se indicarán según el riesgo de padecer SLT (ver Tabla V).
Monitorización: balance hídrico, hemograma, electrolitos, LDH, función renal, pH urinario,
electrocardiograma (ECG). La frecuencia variará desde cada 6 a cada 24 horas según el riesgo
de cada paciente.
Hidratación: 3 litros/m2/día de solución glucosalina, sin aportes de potasio, con el objetivo de
conseguir diuresis de al menos 100 cc/m2/hora. Si bien se puede considerar el uso de
furosemida para lograr dicho objetivo, se debe tener en cuenta que puede promover la
cristalización del ácido úrico en los túbulos renales.
Alcalinización de la orina: es una medida tradicionalmente recomendada pero controvertida.
Su indicación se basa en que, a mayor pH, el ácido úrico es más soluble, pero sus precursores
(xantina e hipoxantina) son menos solubles y puede favorecer el depósito de fosfato cálcico,
pudiendo precipitar en el parénquima renal. En las últimas guías del British Committee for
Standards in Haematology (2015) desaconsejan esta medida.
Alopurinol: es un inhibidor competitivo de la xantina oxidasa, enzima que metaboliza las
purinas hacia ácido úrico. La dosis es 300 mg/día por vía oral, debe iniciarse 1 o 2 días antes de
comenzar el tratamiento y mantenerse hasta 7 días después de su finalización. Precisa ajuste
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1295]
[80] URGENCIAS ONCOLÓGICAS
en caso de insuficiencia renal. Hay que tener cuidado con el uso concomitante de otros
fármacos que utilicen esta vía metabólica (6-mercaptopurina, metotrexato).
Rasburicasa: transforma el ácido úrico en alantoína, sustancia más soluble en orina y por tanto
eliminada por el riñón con mayor facilidad. La dosis es 0,2 mg/kg/día, desde el día anterior a la
QT y hasta 5-7 días en total, dependiendo de la evolución del paciente. Se puede utilizar en
pacientes con riesgo intermedio en vez de alopurinol en caso de insuficiencia renal o
hiperuricemia persistente. Está contraindicada en pacientes con déficit de glucosa-6-fosfato-
deshidrogenasa.
5.2. Tratamiento del SLT establecido
Requiere un manejo entre oncólogos/hematólogos, nefrólogos e intensivistas.
Intensificar monitorización (cada 4-6 horas, durante un mínimo de 72 horas y hasta 24-48
horas tras corregirse).
Mismas medidas de hidratación y utilización de rasburicasa para la profilaxis.
Corrección de las alteraciones metabólicas (ver Capítulo 65. “Trastornos hidroelectrolíticos”).
La hipocalcemia solo se debe corregir si es sintomática, para lo que se puede administrar
gluconato cálcico. Se puede repetir la misma dosis si no se observan cambios en el ECG pasados
5 a 10 minutos.
En cuanto a la hiperfosfatemia, si mediante hidratación no se ha conseguido disminuirla, es
difícil controlarla sin diálisis. El uso de hidróxido de aluminio ha sido descrito pero su acción es
corta y pobremente tolerada, por lo que no se recomienda.
Terapia renal sustitutiva: en caso de disminución de diuresis, que no mejora con hidratación
intensiva ni furosemida, valorar la posibilidad de obstrucción urinaria. Si se descarta, considerar
hemodiálisis aguda si:
Potasio > 7 mEq/L.
Hipocalcemia sintomática.
Fósforo > 10 mg/dL.
Ácido úrico >10 mg/dL.
Creatinina > 10 mg/dL.
Hipertensión arterial grave que no responde al tratamiento.
Sobrecarga de volumen sintomática.
V. MUCOSITIS
1. Definición
La mucositis es una reacción inflamatoria que se produce en la mucosa del tracto gastrointestinal,
secundaria a la acción de la QT y la radiación ionizante. La cavidad oral es muy sensible a los efectos tóxicos
directos e indirectos de dichos tratamientos y es la mucosa que se afecta con mayor frecuencia.
Su incidencia varía según la dosis y el tipo de tratamiento administrado: en pacientes tratados con
altas dosis de RT (por ejemplo, cuando se da con intención radical en cabeza y cuello) y de QT (en
trasplantes hematopoyéticos) puede llegar al 85%, mientras que, en los pacientes que están recibiendo una
dosis estándar de QT, puede llegar al 40%.
2. Fisiopatología
La QT y la RT producen daños en el ácido desoxirribonucleico (ADN) y en otras estructuras de las
células epiteliales basales, de la submucosa y endoteliales, generando radicales libres. Esto lesiona las
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1296]
[80] URGENCIAS ONCOLÓGICAS
membranas celulares y origina una reacción inflamatoria, que a su vez provoca la pérdida de la integridad
de la mucosa, produciendo así ulceración y atrofia.
3. Etiología y factores predisponentes
Varios factores delimitan la extensión y la severidad de la mucositis:
Tipo de quimioterapia: las drogas dirigidas a alterar la replicación del ADN son las que producen
mucositis con mayor frecuencia (alquilantes, antraciclinas, antimetabolitos y taxanos). Algunos
fármacos –por ejemplo, metotrexato o etopósido– potencian su efecto tóxico debido a que se
secretan por la saliva. Fármacos dirigidos contra dianas moleculares también pueden producir
mucositis oral, como, por ejemplo, afatinib, everolimus, temsirolimus, sunitinib, etc.
Dosis de RT acumulada: mayor riesgo con RT hiperfraccionada.
Combinación de quimioterápicos y/o tratamiento concurrente con RT: elevan el riesgo de
mucositis.
Estado previo de la cavidad oral: falta de higiene, caries y enfermedad periodontal.
Edad: los jóvenes tienen una mayor tasa de recambio celular y, por tanto, son más susceptibles
al efecto citotóxico de la RT y de la QT.
4. Clínica
El inicio de la mucositis es muy variable y, aunque típicamente se desarrolla entre 5-7 días tras la
administración del tratamiento, puede aparecer en las primeras 24 horas. Al principio se observa un
eritema con sensación levemente dolorosa, que puede evolucionar a úlceras difusas con dolor intenso, lo
que puede condicionar incluso incapacidad para la deglución. Según su gravedad se puede clasificar en
cinco grados (Tabla VI). Si no se producen complicaciones, la mucositis es un proceso autolimitado que cura
en una o dos semanas. Sin embargo, puede sobreinfectarse por hongos (Candida albicans) o bacterias, y ser
la puerta de entrada de infecciones, especialmente cuando se asocia a neutropenia.
La QT puede inducir la reactivación de la infección por virus herpes simple (VHS), prolongando la
clínica y exacerbando los síntomas.
5. Prevención
Se han estudiado una serie de estrategias para prevenir o minimizar la mucositis inducida por los
tratamientos oncológicos. Aunque la calidad de la evidencia de los ensayos es limitada, las guías prácticas
recomiendan:
Protocolos de cuidado oral: tienen como objetivo reducir la carga microbiana. Incluyen
generalmente una combinación de cepillado de los dientes, uso de hilo dental y de enjuagues
bucales y evaluación por un dentista para eliminar posibles focos de infección o traumatismo.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1297]
[80] URGENCIAS ONCOLÓGICAS
En cuanto a los tipos de enjuagues, se sugiere que los de clorhexidina podrían ser beneficiosos
en pacientes que reciben RT para tratar tumores de cabeza y cuello. En los que reciben QT, por
evidencia insuficiente o conflictiva, no recomiendan ninguno por encima de otro (solución
salina, bicarbonato de sodio, enjuagues bucales mixtos, clorhexidina).
Crioterapia: la aplicación de hielo sobre la mucosa oral durante la infusión de la QT parece
reducir la mucositis al producir vasoconstricción local. Su uso es recomendado en pacientes en
tratamiento con 5-fluorouracilo en bolo y altas dosis de melfalán.
Factor estimulante de queratinocitos (palifermina): reduce tanto la severidad como la duración
de los síntomas. Se recomienda en pacientes que recibirán tratamiento con altas dosis de QT
seguido de trasplante autólogo de progenitores hematopoyéticos. Debido a su alto coste su uso
no está extendido.
Terapia láser de baja energía: podría ser beneficiosa en pacientes con QT en altas dosis previo a
trasplante, pero –dado que requiere un equipamiento costoso y personal especializado– su uso
también está restringido.
6. Abordaje terapéutico
El tratamiento de la mucositis establecida es sintomático y debe estar centrado en una higiene
bucal meticulosa y tratamiento analgésico.
Hidratación abundante y dieta blanda, libre de especias y comidas calientes, saladas o ácidas.
En casos leves pueden ser útiles los complejos hiperproteicos. En casos de odinofagia intensa
(grado ≥ 3) se utilizará nutrición parenteral.
Analgesia: en los casos leves puede ser suficiente un tratamiento tópico mediante enjuagues
(lidocaína viscosa). En los casos más graves se debe pautar analgesia sistémica, tanto para
control del dolor basal como de las exacerbaciones con la ingesta. En caso de dificultad para la
deglución de comprimidos, valorar el uso de fentanilo transdérmico para pacientes
ambulatorios y de perfusión de morfina para el ámbito hospitalario.
Tratamiento de las infecciones:
Fúngicas: la candidiasis oral se puede tratar con nistatina tópica (Mycostatin®). En casos
de candidiasis grave, con afectación esofágica o con neutropenia o fiebre asociadas,
tratar con fluconazol oral 100 mg cada 24 horas. Se recomienda profilaxis con
posaconazol en pacientes de alto riesgo (leucemia mieloide aguda, QT a alta dosis,
neutropenia prevista de más de 14 días).
Víricas: en caso de sospecha de infección por VHS o varicela-zóster, tratar con aciclovir,
famciclovir o valaciclovir. Se recomienda profilaxis con aciclovir en pacientes de alto
riesgo (leucemia mieloide aguda, QT a alta dosis, tratamiento con bortezomib).
Bacterianas: si se sospecha infección bacteriana, se deben utilizar antibióticos que
cubran gérmenes anaerobios (amoxicilina-clavulánico, clindamicina, moxifloxacino). En
caso de neutropenia febril grado IV de alto riesgo con mucositis, considerar asociar un
glucopéptido, daptomicina o linezolid si en el centro sanitario hay antecedentes de
aislamientos de Streptococcus viridans resistentes a penicilina.
Si la mucositis es severa puede requerir hospitalización. Los criterios de ingreso son:
Mucositis grado 3-4.
Neutropenia u otras toxicidades concomitantes.
Mal control del dolor.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1298]
[80] URGENCIAS ONCOLÓGICAS
VI. EMESIS INDUCIDA POR QUIMIOTERAPIA
1. Definición
La emesis constituye un efecto secundario del tratamiento quimioterápico con una importante
repercusión en la calidad de vida del paciente. Es una respuesta involuntaria del organismo dividida en dos
fases distintas: náusea (sensación de malestar epigástrico con ganas de vomitar) y vómito (expulsión
violenta del contenido gástrico a través de la boca). Sin tratamiento antiemético adecuado, hasta el 80% de
los pacientes tratados con QT podrían experimentar náuseas o vómitos.
2. Fisiopatología
El vómito es un reflejo controlado por el cerebro y se desencadena por múltiples estímulos
aferentes dirigidos hacia el centro del vómito (localizado en la médula espinal), que pueden originarse en la
faringe, tracto gastrointestinal (vía vagal aferente), zona gatillo quimiorreceptora (en el área postrema) y en
la corteza cerebral. Activado el reflejo, el impulso viajará desde el centro del vómito por las vías eferentes a
las glándulas salivales, músculos abdominales, centro respiratorio y nervios craneales.
El tracto gastrointestinal, la zona gatillo quimiorreceptora y el centro del vómito poseen numerosos
receptores de neurotransmisores (principalmente de serotonina y dopamina), que pueden ser activados
por la QT o sus metabolitos. Otros receptores involucrados se encuentran localizados en los centros
vestibulares del sistema nervioso central. Cada antiemético tiene la función de bloquear un tipo de
receptor, pudiendo actuar de forma sinérgica cuando se combinan.
3. Clasificación
La emesis por QT se puede clasificar en:
Emesis aguda: ocurre minutos u horas desde la administración de la QT y generalmente se
resuelve dentro de las primeras 24 horas.
Emesis retardada: ocurre a partir de las 24 horas de la administración de la QT.
Emesis anticipatoria: sucede antes del segundo o siguientes ciclos de QT.
Emesis irruptiva: ocurre a pesar del tratamiento preventivo y precisa de medicación de rescate.
Emesis refractaria: se desencadena en varios ciclos de QT pese a medicación preventiva y de
rescate.
4. Factores predictivos
Una serie de factores, dependientes tanto del paciente como del esquema quimioterápico
utilizado, van a influir en el riesgo de desarrollar emesis (Tablas VII y VIII). En caso de administrar
asociaciones de fármacos, se considera su poder emetógeno en función del citostático de mayor riesgo.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1299]
[80] URGENCIAS ONCOLÓGICAS
5. Diagnóstico
Ante un paciente con QT que presente emesis, no hay que olvidar que pueden existir otras causas
que la justifiquen: oclusión o suboclusión intestinal, otros fármacos, alteraciones metabólicas, metástasis
cerebrales, hipertensión intracraneal, etc.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1300]
[80] URGENCIAS ONCOLÓGICAS
Junto con una anamnesis adecuada, es importante revisar la pauta antiemética prescrita y su
cumplimiento. El examen físico y la analítica, además de intentar descartar otras causas, deben tener el
objeto de evaluar la repercusión general (deshidratación, volemia, alteraciones iónicas y de la función
renal, etc.). Otras pruebas complementarias se solicitarán en función de la sospecha clínica.
6. Abordaje terapéutico
6.1. Tratamiento preventivo
Una adecuada profilaxis es el mejor tratamiento de la emesis por QT, y se pautará en función del
riesgo emetógeno de los fármacos antitumorales (Tabla IX).
6.2. Tratamiento de rescate
El principio general del tratamiento de rescate es añadir un fármaco de diferente clase a los que se
utilizaron en la profilaxis. Se puede elegir entre los siguientes, sin preferencia de orden:
Corticoides:
Dexametasona 12 mg/día iv/oral.
Antidopaminérgicos:
Metoclopramida 10-40 mg iv/oral, cada 4-6 h.
Haloperidol 0,5-2 mg iv/oral, cada 4-6 h.
Antagonistas de la serotonina:
Ondansetrón 16 mg/día iv/oral.
Granisetrón 1-2 mg/día oral.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1301]
[80] URGENCIAS ONCOLÓGICAS
Benzodiazepinas: se puede valorar su uso en el caso de la emesis anticipatoria, la noche antes
del tratamiento, pudiendo combinarlo asimismo con terapia conductual.
Lorazepam, 0,5-2 mg/6 horas iv/sc/oral.
Antipsicóticos atípicos:
Olanzapina 10 mg/día oral, 3 días. Antes de administrar la próxima dosis de
quimioterapia, se debe considerar subir la pauta profiláctica a una de mayor riesgo.
Antes de administrar la próxima dosis de quimioterapia, se debe considerar subir la pauta
profiláctica a una de mayor riesgo.
VII. NEUTROPENIA FEBRIL
Ver Capítulo 47. “Infecciones en el paciente inmunodeprimido. Neutropenia febril”.
VIII. HIPERCALCEMIA
Ver Capítulo 66. “Trastornos del metabolismo del calcio, fósforo y magnesio”.
BIBLIOGRAFÍA
Basch E, Prestrud AA, Hesketh PJ, Kris MG, Feyer PC, Somerfield MR, et al. Antiemetics: American
Society of Clinical Oncology clinical practice guideline update. J Clin Oncol. 2011;29(31):4189-98.
Blázquez Arroyo M. Mucositis. Manual de Urgencias Oncológicas del Hospital Universitario 12 de
Octubre. Madrid. 2015:53-60.
Cairo MS, Coiffier B, Reiter A, Younes A. Recommendations for the evaluation of risk and prophylaxis of
tumour lysis syndrome (TLS) in adults and children with malignant diseases: an expert TLS panel
consensus. Br J Haematol [Internet]. 2010;149(4):578-86. Disponible en:
http://www.ncbi.nlm.nih.gov/pubmed/20331465
Coiffier B, Altman A, Pui C-H, Younes A, Cairo MS. Guidelines for the management of pediatric and adult
tumor lysis syndrome: an evidence-based review. J Clin Oncol [Internet]. 2008;26(16):2767-78.
Disponible en: http://www.ncbi.nlm.nih.gov/pubmed/18509186.
Elad S, Raber-Durlacher JE, Brennan MT, Saunders DP, Mank AP, Zadik Y, et al. Basic oral care for
hematologyoncology patients and hematopoietic stem cell transplantation recipients: a position paper
from the joint task force of the Multinational Association of Supportive Care in Cancer/International
Society of Oral Oncology (MASCC). Support Care Cancer [Internet]. 2015;23(1):223-36. Disponible en:
http://www.pubmedcentral.nih.
gov/articlerender.fcgi?artid=4328129&tool=pmcentrez&rendertype=abstract
Ettinger D, et al. Antiemesis. Versión 2.2015. National Comprehensive Cancer Network. 2015.
George R, Jeba J, Ramkumar G, Chacko AG, Tharyan P. Interventions for the treatment of metastatic
extradural spinal cord compression in adults. Cochrane Database Syst Rev. 2015;9:CD006716.
Gralla RJ, Roila F, Tonato M. MASCC/ESMO Antiemetic Guideline 2013. Multinatl Assoc Support Care
Cancer. 2013;4(1):1-21.
Hesketh PJ, Bohlke K, Lyman GH, Basch E, Chesney M, Clark-Snow RA, et al. American Society of
Clinical Oncology. Antiemetics: American Society of Clinical Oncology Focused Guideline Update. J Clin
Oncol. 2016 Feb 1;34(4):381-6.
Howard SC, Jones DP, Pui C-H. The tumor lysis syndrome. N Engl J Med [Internet]. 2011;364(19):1844-
54. Disponible en:
http://www.pubmedcentral.nih.gov/articlerender.fcgi?artid=3437249&tool=pmcentrez&rendertype=a
bstract
Iglesias Docampo L. Emesis por quimioterapia. Manual de Urgencias Oncológicas del Hospital
Universitario 12 de Octubre. Madrid. 2015:45-51.
Jones GL, Will A, Jackson GH, Webb NJA, Rule S. Guidelines for the management of tumour lysis
syndrome in adults and children with haematological malignancies on behalf of the British Committee
for Standards in Haematology. Br J Haematol [Internet]. 2015;169(5):661-71. Disponible en:
http://www.ncbi.nlm.nih.gov/pubmed/25876990
Kamar FG, Posner JB. Brain metastases. Semin Neurol. 2010;30(3):217-35.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1302]
[80] URGENCIAS ONCOLÓGICAS
Khan UA, Shanholtz CB, McCurdy MT. Oncologic mechanical emergencies. Emerg Med Clin North Am.
2014;32(3):495-508.
Kocher M, Wittig A, Piroth MD, Treuer H, Seegenschmiedt H, Ruge M, et al. Stereotactic radiosurgery for
treatment of brain metastases. A report of the DEGRO Working Group on Stereotactic Radiotherapy.
Strahlenther Onkol. 2014;190(6):521-32.
Lalla R V, Bowen J, Barasch A, Elting L, Epstein J, Keefe DM, et al. MASCC/ISOO clinical practice
guidelines for the management of mucositis secondary to cancer therapy. Cancer [Internet].
2014;120(10):1453-61. Disponible en:
http://www.pubmedcentral.nih.gov/articlerender.fcgi?artid=4164022&tool=pmcentrez&rendertype=a
bstract
Laufer I, Rubin DG, Lis E, et al. The NOMS framework: approach to the treatment of spinal metastatic
tumors. Oncologist 2013;18:744-51.
Lechuga Vázquez C, Murillo González M. Indicaciones de radioterapia urgente. Conceptos básicos del
tratamiento radioterápico en situaciones urgentes en el paciente oncológico. Manual de Urgencias
Oncológicas del Hospital Universitario 12 de Octubre. Madrid. 2015:253-64.
Lin X, DeAngelis LM. Treatment of Brain Metastases. J Clin Oncol. 2015;33(30):3475-84.
Loblaw DA, Mitera G, Ford M, Laperriere NJ. A 2011 updated systematic review and clinical practice
guideline for the management of malignant extradural spinal cord compression. Int J Radiat Oncol Biol
Phys. 2012;84(2):312-7.
Muñoz Sánchez-Miguel C. Síndrome de lisis tumoral. Manual de Urgencias Oncológicas del Hospital
Universitario 12 de Octubre. Madrid. 2015:87-94.
Peterson DE, Bensadoun R-J, Roila F. Management of oral and gastrointestinal mucositis: ESMO
Clinical Practice Guidelines. Ann Oncol [Internet]. 2011;22(Suppl 6):vi78-84. Disponible en:
http://www.pubmedcentral.nih.gov/articlerender.fcgi?artid=3662500&tool=pmcentrez&rendertype=a
bstract
Roila F, Molassiotis A, Herrstedt J, Aapro M, Gralla RJ, Bruera E, et al. 2016 MASCC and ESMO
guideline update for the prevention of chemotherapy- and radiotherapy-induced nausea and vomiting
and of nausea and vomiting in advanced cancer patients. Ann Oncol. 2016 Sep;27(suppl 5):v119-
v133.
Ryu S, Yoon H, Stessin A, Gutman F, Rosiello A, Davis R. Contemporary treatment with radiosurgery for
spine metastasis and spinal cord compression in 2015. Radiat Oncol J. 2015;33(1):1-11.
Savage P, Sharkey R, Kua T, Schofield L, Richardson D, Panchmatia N, et al. Malignant spinal cord
compression: NICE guidance, improvements and challenges. QJM. 2014;107(4):277-82.
Sociedad Española de Oncología Radioterápica. Manual Práctico de Oncología Radioterápica. Abbvie.
2013.
Wilson LD, Detterbeck FC, Yahalom J. Clinical practice. Superior vena cava syndrome with malignant
causes. N Engl J Med. 2007;356:1862-9.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1303]
[81] CEFALEAS Y ALGIAS CRANEOFACIALES
81.Cefaleas y algias craneofaciales
Emilio Gómez Cibeira.
Neurología
Blanca Ayuso García.
Medicina Interna
Asesor:
Antonio Martínez Salio.
Médico Adjunto de Neurología
I. INTRODUCCIÓN
Las cefaleas son una causa frecuente de consulta médica y, aunque en su mayoría son cefaleas
primarias (sin alteración estructural identificable, principalmente migraña, cefalea tensional y cefalea en
racimos), es de crucial importancia detectar las cefaleas secundarias a otros procesos que pueden suponer
un riesgo vital importante.
II. APROXIMACIÓN DIAGNÓSTICA
En la evaluación de una cefalea es fundamental reconocer las cefaleas secundarias, por lo que el
proceso diagnóstico debe dirigirse en este sentido.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1304]
[81] CEFALEAS Y ALGIAS CRANEOFACIALES
1. ANAMNESIS
El interrogatorio incluirá: antecedentes personales y familiares, edad de inicio e historia natural
(brotes, remisiones), perfil temporal (al despertar, al final del día, interrupción del sueño), forma de
instauración (súbita, gradual; Tabla I), duración, horario de aparición o empeoramiento, localización
(unilateral frente a bilateral, ocular o retroocular, paranasal, a punta de dedo, en cinta, distribución
trigeminal), cualidad (pulsátil, opresiva, urente, sorda, punzante), intensidad, síntomas acompañantes
(vegetativos, focalidad neurológica, así como datos que sugieran infección local o sistémica,
inmunosupresión o comorbilidad de riesgo), factores que agravan o alivian el dolor y respuesta a fármacos.
Si hay antecedentes de cefalea se indagará sobre posibles cambios en su patrón habitual.
2. EXPLORACIÓN FÍSICA
Es fundamental determinar las constantes vitales, realizar una exploración general básica y una
exploración neurológica completa en busca de focalidad motora, sensitiva o cerebelosa y signos
meníngeos, y que incluya la evaluación de los pares craneales y de la función visual (con campimetría por
confrontación). Además, se debe realizar un fondo de ojo y búsqueda de puntos dolorosos a nivel de senos
frontales y maxilares, articulación temporomandibular y arterias temporales.
3. PRUEBAS COMPLEMENTARIAS
Su necesidad viene determinada por la sospecha diagnóstica tras la anamnesis y la exploración
física, así como por la presencia de síntomas de alarma (Tabla II).
Puede solicitarse un analítica sanguínea completa si se sospecha patología sistémica asociada, que
incluya la velocidad de sedimentación globular (VSG) y la proteína C reactiva (PCR) (sobre todo en > 50 años
con cefalea subaguda para descartar arteritis de la temporal) y una glucemia en todo paciente diabético. Se
solicitará una tomografía computarizada (TC) craneal ante la presencia de síntomas o signos de alarma y
previamente a la realización de una punción lumbar.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1305]
[81] CEFALEAS Y ALGIAS CRANEOFACIALES
Se puede realizar una punción lumbar de urgencia sin TC si no hay focalidad neurológica, el fondo
de ojo muestra pulso venoso, ausencia de papiledema y el paciente no presenta alteración de la
consciencia. Y es primordial realizarla si se sospecha meningitis o, si siendo la TC normal, hay alta sospecha
de hemorragia subaracnoidea o hipertensión intracraneal (HTIC).
La resonancia magnética (RM) no se realiza de urgencia por rutina, y su uso se reserva para
descartar la trombosis de senos venosos con TC craneal normal, lesión de fosa posterior, seno cavernoso o
silla turca, delimitación de la obstrucción si existe hidrocefalia y ante la sospecha de hipopresión licuoral.
III. CLASIFICACIÓN SEGÚN PERFIL TEMPORAL
Ver Figura 1 y Tabla I.
1. CEFALEAS SÚBITAS NO RECURRENTES
Son aquellas que aparecen de forma brusca y alcanzan su intensidad máxima en menos de un
minuto. Engloban con mayor frecuencia una patología neurológica grave.
1.1. Hemorragia subaracnoidea
La hemorragia subaracnoidea (HSA) hay que sospecharla en toda cefalea de inicio súbito, muy
intensa (“la más intensa de mi vida”), de localización variable, tras un esfuerzo físico o tensión emocional,
asociada a náuseas y vómitos y con alteración del nivel de consciencia. La causa más frecuente es la ruptura
de un aneurisma sacular. Hasta un 20% son precedidas de una hemorragia centinela manifestada como una
cefalea autolimitada (ver Capítulo 85. “Enfermedad cerebrovascular”).
1.2. Ictus
La cefalea es más frecuente e intensa en los hemorrágicos (55%, sobre todo, en los de localización
occipital, cerebelosa y lobares extensos) que en los isquémicos (20%, más común en los corticales y los
extensos) o que en los accidentes isquémicos transitorios (AIT) (ver Capítulo 85. “Enfermedad
cerebrovascular”).
1.3. Disecciones arteriales cervicales (carótida/vertebral): espontáneas o por traumatismos leves
Hasta en un tercio de los casos se manifiesta por la tríada del síndrome de Horner: carotidinia o
dolor hemicraneal y focalidad neurológica cerebral o retiniana (ver Capítulo 85. “Enfermedad
cerebrovascular”).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1306]
[81] CEFALEAS Y ALGIAS CRANEOFACIALES
2. CEFALEAS AGUDAS DE RECIENTE COMIENZO
Son cefaleas de inicio insidioso, que tardan horas o días en instaurarse.
2.1. Secundarias a infección intracraneal
Típicamente presentan cuadro clínico de fiebre, cefalea, meningismo y un grado variable de
alteración del estado mental y/o focalidad neurológica (ver Capítulo 42. “Infecciones del sistema nervioso
central”).
2.2. Secundaria a trombosis de senos venosos o venas cerebrales
(Ver Capítulo 85. “Enfermedad cerebrovascular”).
2.3. Arteritis de la temporal
Se trata de una vasculitis sistémica cuyo síntoma de inicio más frecuente es la cefalea y que ha de
descartarse en todo paciente mayor de 55 años (pico de incidencia entre los 70 y 80 años).
Los síntomas clásicamente asociados a la enfermedad son: cefalea (70-90%; típicamente unilateral
de localización frontotemporal, con instauración gradual o repentina e intensa, de tipo sordo y de
predominio nocturno; en un 40% hay hipersensibilidad del cuero cabelludo), polimialgia reumática (40-
60%), claudicación mandibular (muy sugestiva, pero infrecuente), síntomas visuales (amaurosis fugax en el
10%, diplopía, pérdida de agudeza visual, alucinaciones) y constitucionales, como febrícula, anorexia,
astenia y pérdida de peso.
En la exploración física deben palparse las arterias temporales (un 50% presentan alteraciones, con
hipersensibilidad, engrosamiento y ausencia de pulso al tacto) e incluir una valoración del fondo de ojo.
Para el cribado se determinará la VSG (> 50 mm/hora en un 97% de casos, si bien, es normal hasta en el
17% de los mismos); no hay límites establecidos, aunque el límite de normalidad orientativo sería: la edad
dividida entre 2 para los varones y la edad más 10 dividida entre 2 para las mujeres ([edad + 10]/2), con un
papel menos establecido para la PCR.
El tratamiento se iniciará tan pronto como se sospeche (prevención de ceguera ipsi y contralateral,
dado que el riesgo de recidiva contralateral es del 100% sin tratamiento) y se confirmará el diagnóstico a
posteriori con biopsia de la arteria temporal (lo antes posible tras el inicio del tratamiento, intentando no
demorarla más de 10 días). En ausencia de complicaciones isquémicas, se iniciará tratamiento con
prednisona 40-60 mg/día, iniciando la reducción de dosis en 4 semanas si se ha obtenido remisión clínica y
analítica, a razón de 10 mg semanales, y alcanzando en 3-4 meses la dosis de mantenimiento (alrededor de
10 mg/día). A partir del segundo año, se inicia una reducción muy paulatina de la dosis hasta su supresión.
Si existen alteraciones visuales o isquémicas relacionadas, se emplearán dosis altas de metilprednisolona
de 1.000 mg/día intravenosa (iv) durante 3 días, seguidas de tratamiento oral, como se menciona en las
formas no complicadas (ver Capítulo 16. “Patología oftalmológica”). En todos los pacientes es
recomendable asociar a ácido acetilsalicílico 100 mg/día, excepto si existe contraindicación. En el
seguimiento hay que vigilar y prevenir complicaciones del tratamiento esteroideo (ver Anexo VI.
“Inmunosupresión y sus complicaciones”). Se recomienda la realización de una tomografía axial
computarizada (TAC) o resonancia magnética nuclear (RMN) para valorar la extensión de la afectación
arterial (estenosis, disección, aneurismas), especialmente de grandes vasos. Se propone la utilización de la
tomografía por emisión de positrones (PETTAC), que puede detectar actividad metabólica además de
alteraciones morfológicas.
2.4. Secundaria a trastornos de la homeostasia
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1307]
[81] CEFALEAS Y ALGIAS CRANEOFACIALES
Principalmente dos entidades: la asociada al SAHS (típicamente matutina) y las atribuidas a crisis de
hipertensión arterial (justifica la cefalea con cifras de tensión arterial sistólica [TAS] de 160 mm Hg y tensión
arterial diastólica [TAD] > 120 mm Hg). Otras menos frecuentes ocurren en situaciones de hipoxia o
hipercapnia, en la preeclampsia/eclampsia y en la anemia, entre otras.
2.5. Secundaria a ingesta o abstinencia de sustancias
Se descartará consumo de drogas y fármacos o suspensión de los mismos. Son más susceptibles los
pacientes con algún tipo de cefalea primaria.
2.6. Secundaria a hipotensión intracraneal (hipovolemia de líquido cefalorraquídeo [LCR])
Característicamente ortostática (aparece a los pocos minutos de ponerse en pie y mejora poco
después de tumbarse), focalizada u holocraneal y resistente a analgésicos. Suele acompañarse de náuseas,
vómitos, meningismo y, en algunos casos, de focalidad neurológica (hipoacusia, diplopía en ortostatismo
por tracción del VI par).
La causa principal es la cefalea pospunción lumbar (PL) (10-30% de las PL), apareciendo
generalmente en las primeras 12-24 h y resolviéndose de media en 4-8 días. Otras menos frecuentes son
las fístulas de LCR posquirúrgicas o postraumáticas, así como la forma espontánea en mujeres en torno a
los 40 años con evidencia de presión disminuida del LCR (< 6 cm H2O en sedestación) o hallazgos
compatibles en realce meníngeo.
El tratamiento consiste en reposo en decúbito supino, hidratación y analgesia (es especialmente
útil cafeína en dosis de 500 mg vía oral o iv, repitiendo la dosis transcurridos 45 minutos si no ha cedido el
dolor) y, si es resistente, el tratamiento consistirá en la colocación de un parche epidural de sangre
autóloga.
2.7. Secundaria a traumatismo craneoencefálico
Es normal tras un traumatismo craneoencefálico (TCE) y su duración es variable. Se puede
acompañar de mareo, dificultad de concentración e insomnio durante los siete primeros días tras el TCE.
Requiere la realización de una prueba de imagen ante focalidad neurológica, deterioro del nivel de
consciencia o factores que favorezcan complicaciones (paciente anciano, alcohólico o anticoagulado,
individualizando en el paciente antiagregado).
2.8. Otras
Secundaria a trastornos oculares y ORL: ver Capítulo 16. “Patología oftalmológica” y
Capítulo 17. “Patología otorrinolaringológica”.
Secundaria a alteraciones cervicales: la anteriormente conocida como cefalea secundaria a
alteraciones cervicales no es una causa válida de cefalea cervicogénica y, realmente, se trata de
una cefalea tensional con contractura e hipersensibilidad de la musculatura cervical.
Secundaria a disfunción de la articulación temporomandibular (ATM) o síndrome de Costen: es
causa frecuente de cefalea hemicraneal. Cursa con dolor a la movilización o palpación de la
ATM y de la musculatura masticatoria, y con restricciones y ruidos (clic o crepitantes) durante
los movimientos masticatorios.
Su tratamiento es sintomático, con AINE, calor local y dieta blanda durante una o dos semanas, con
control posterior por la Unidad de Cirugía Maxilofacial.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1308]
[81] CEFALEAS Y ALGIAS CRANEOFACIALES
3. CEFALEAS AGUDAS RECURRENTES
En su mayoría son cefaleas primarias, cuyo diagnóstico es clínico y se basa en los criterios
diagnósticos de la International Headache Society (IHS).
3.1. Migraña
Concepto: constituye la cefalea primaria más frecuente en Urgencias. La prevalencia es mayor
en la mujer y se inicia antes de los 30 años de edad (hay que dudar del diagnósticoen cefaleas
que debutan en mayores de 45 años sin antecedentes previos de migraña). Existen con
frecuencia antecedentes familiares, sobre todo maternos.
Orientación diagnóstica: se debe preguntar por factores precipitantes, siendo los más típicos
hormonales, emocionales, cambios de presión atmosférica, inicio o abandono de fármacos y
algunos alimentos.
Clínica
Ataques sin aura: son los más frecuentes y caracterizan a la migraña sin aura o común
(Tabla III). La intensidad y características del dolor no difieren de las de los ataques con
aura.
Ataques con aura (Tabla IV): hasta en el 10-20% se puede preceder o acompañar de
síntomas de origen cortical, lo que se conoce como aura. La forma más común es la
visual, seguida de la sensitiva y la del lenguaje. Pueden coexistir distintas formas de
aura en un mismo paciente y en un mismo ataque. En este último caso sigue un patrón
temporal secuencial (visual-sensitiva-alteración del lenguaje). Se debe hacer
diagnóstico diferencial con los AIT y con las crisis epilépticas focales (va a favor de aura
el inicio progresivo y la presencia de síntomas no adscribibles a un territorio concreto).
Aura sin cefalea: en pacientes migrañosos de larga evolución, aunque es infrecuente.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1309]
[81] CEFALEAS Y ALGIAS CRANEOFACIALES
Complicaciones de la migraña
Migraña crónica: es aquella en la que el número de ataques se incrementa hasta
superar una frecuencia de más de 15 días al mes durante un periodo de más de tres
meses y que, al menos durante ocho días al mes, presenta características de cefalea
migrañosa. Es, junto con la cefalea tensional, la causa más frecuente de cefalea crónica
diaria. Son factores de riesgo para su desarrollo el abuso de medicación (sobre todo
opioides), obesidad, consumo de cafeína y estrés.
Estatus migrañoso: se define como un ataque de migraña (con o sin aura) de más de 72
horas de duración a pesar de instaurar un tratamiento adecuado. Es infrecuente como
inicio de una migraña no conocida, apareciendo en pacientes migrañosos previos. Son
factores de riesgo el abuso de medicación, el estrés emocional, la depresión, la
ansiedad y la interrupción del tratamiento profiláctico. Aunque excepcional, el estatus
migrañoso refractario al tratamiento convencional puede ser la única manifestación de
un estatus epiléptico no convulsivo, por lo que en estos casos es recomendable la
realización de un electroencefalograma (EEG).
Infarto migrañoso: la migraña se asocia a un incremento del riesgo de ictus isquémico,
siendo este mayor en la migraña con aura, en fumadores, mujeres y con la toma de
anticonceptivos orales (estando contraindicados en la migraña con aura, en la migraña
sin aura en mujeres ≥ 35 años o en < 35 años con al menos un factor de riesgo
cardiovascular asociado).
Tratamiento de la migraña
Tratamiento sintomático agudo
En los ataques leves los AINE orales son una buena opción, teniendo cada uno
sus características particulares en cuanto a su acción se refiere. En los ataques de
intensidad moderada-severa los triptanes son la terapia de elección si no existen
contraindicaciones (se debe intentar no usar más de dos dosis de los mismos en 24
horas). El tratamiento debe iniciarse a ser posible en los primeros 15 minutos del
ataque. Todos los fármacos utilizados en el tratamiento de la migraña, incluyendo los
triptanes, han demostrado mayor eficacia cuanto antes sean administrados y, de
hecho, el retraso en el inicio del tratamiento se asocia a un mayor riesgo de recurrencia
en las primeras 24 horas.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1310]
[81] CEFALEAS Y ALGIAS CRANEOFACIALES
La respuesta terapéutica óptima es aquella que permite aliviar el dolor y volver
a las actividades diarias en menos de dos horas. Es de suma importancia hacer
comprender al paciente que no siempre la primera elección de tratamiento o la
monoterapia será lo más efectivo en su caso, se necesita en ocasiones recurrir a la
combinación de varias estrategias farmacológicas. En cuanto a la disponibilidad de los
diferentes AINE y triptanes, así como las características particulares de cada uno, se
resumen en la tabla V.
Respecto al tratamiento del ataque de migraña en el ámbito de la urgencia
hospitalaria, lo normal es que el paciente migrañoso haya tomado su medicación
habitual para los ataques, sin éxito. Debido a los vómitos o a una ingesta oral reducida
por náuseas, el paciente puede llegar con depleción de volumen, por este motivo el
primer paso terapéutico será la rehidratación intravenosa y el tratamiento de las
náuseas/vómitos con bloqueantes dopaminérgicos (clorpromazina o metoclopramida
iv), los cuáles poseen un triple efecto como antiemético, sedante y controlador del
dolor. El siguiente paso debe ser ubicar al paciente en el lugar más tranquilo y oscuro
posible para evitar el empeoramiento de la sonofobia/fotofobia. Finalmente, se debe
administrar lo más rápido posible un tratamiento específico para el ataque (Tabla V).
Tratamiento preventivo
Está indicado en las siguientes circunstancias: cuando el número de ataques es
≥ 4/mes; cuando el tratamiento sintomático agudo es ineficaz, presenta efectos
secundarios intolerables, está contraindicado o se usa con demasiada frecuencia;
cuando las migrañas son muy incapacitantes; cuando se presentan frecuentes
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1311]
[81] CEFALEAS Y ALGIAS CRANEOFACIALES
complicaciones del tipo estatus, infarto o aura persistente, o preferencia personal del
paciente.
Conviene que el médico comunique al paciente expectativas realistas de la
eficacia de estos tratamientos, ya que, en la mayoría de los casos, el tratamiento
preventivo reduce la recurrencia de la migraña no mucho más de un 50% de cómo lo
venía presentando. Igualmente también es importante saber y comunicar al individuo
que la eficacia máxima puede demorarse entre 2 y 6 meses desde el inicio del
tratamiento.
Entre las opciones farmacológicas de primera elección se encuentran los
antiepilépticos: ácido valproico (inicio a 250 mg/24 h hasta 500 mg/24 h), topiramato
(inicio a 25 mg por la noche hasta 50 mg/12 h) y zonisamida (inicio 25 mg/noche hasta
100 mg/noche); los betabloqueantes: metoprolol (100-200 mg/24 h) y propranolol (20-
40 mg/8 h); y flunarizina (5 mg/noche).
En ocasiones, es necesaria la combinación de varios fármacos preventivos
entre sí. Se recomienda mantener el tratamiento alrededor de 6-9 meses. Otro
tratamiento cada vez más usado en la profilaxis de la migraña y con muy buenos
resultados es la inyección de toxina botulínica en músculos pericraneales. También es
necesario informar al paciente migrañoso de los beneficios que puede ofrecer la
realización de ejercicio habitual, una correcta higiene de sueño y una alimentación
equilibrada.
3.2. Cefaleas trigémino-autonómicas
Las cefaleas trigémino-autonómicas (CTA) constituyen un grupo infrecuente de cefaleas primarias
caracterizadas por dolor estrictamente unilateral localizado en la distribución de la primera rama del nervio
trigémino (V1) y asociado a sonofobia/fotofobia y síntomas autonómicos (lagrimeo, inyección conjuntival,
edema palpebral/periorbitario, sudoración facial, rinorrea, congestión nasal y síndrome de Horner), todo
ello ipsilateral al dolor, durante los ataques (no en los periodos intercrisis). Los distintos tipos se diferencian
entre sí en la duración y frecuencia de los ataques (a medida que la frecuencia aumenta, la duración del
ataque disminuye). La importancia de diagnosticar correctamente estos síndromes reside en su excelente,
aunque selectiva, respuesta al tratamiento (Tabla VI).
Un porcentaje no despreciable de este tipo de cefaleas, en ocasiones, corresponde a causas
secundarias como disecciones arteriales (carotidea y cervical) o tumores (orbitarios, hipofisarios), siendo
obligado en un primer diagnóstico la realización de pruebas de imagen del tipo de la resonancia magnética
(RM) que incluyan estructuras intracraneales y vasos extracraneales.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1312]
[81] CEFALEAS Y ALGIAS CRANEOFACIALES
3.3. Neuralgia
Consiste en ataques paroxísticos de dolor muy intenso, lancinante o eléctrico, de inicio y
finalización bruscos, de segundos a dos minutos de duración, unilateral, localizado en el área de
distribución sensitiva de un nervio.
Neuralgia del nervio trigémino
Afecta al área de distribución sensitiva del nervio trigémino (rama maxilar o V2 junto con V3
son las más frecuentemente afectadas, mientras que V1 solo está involucrada en el 4% de los
casos). Los ataques de dolor se desencadenan típicamente por estímulos cutáneos sobre la
boca o la nariz (lavarse los dientes, masticar, afeitarse). Es típico un periodo de refractariedad
breve durante el que un nuevo estímulo es incapaz de evocar otro ataque. La frecuencia de los
ataques es variable, desde unos pocos al día hasta varios centenares. Presentan periodicidad
concentrándose en periodos de varias semanas separados por fases de remisión de unos 6
meses-1 año. Existen dos formas:
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1313]
[81] CEFALEAS Y ALGIAS CRANEOFACIALES
Idiopática: más prevalente en mujeres mayores de 40 años. Los pacientes no presentan
síntomas de focalidad neurológica en la exploración física (no hay hipoestesia facial ni
debilidad de los músculos masticatorios y el reflejo corneal está conservado).
Actualmente se conoce que el 85% de las formas consideradas idiopáticas son debidas
a una anomalía vascular (arteria cerebelosa superior o antero-inferior aberrante) que
produce compresión sobre la raíz del nervio trigémino. Esta compresión neurovascular
puede demostrarse mediante RM cerebral.
Sintomáticas: en ellas existe una lesión estructural subyacente distinta a la compresión
neurovascular. Se debe sospechar ante una neuralgia del trigémino que asocia déficits
neurológicos, si existe afectación bilateral o de V1, y en menores de 40 años. Las causas
más comunes son los tumores del ángulo pontocerebeloso (schwannoma vestibular) y
la esclerosis múltiple. Es necesaria la realización de RM cerebral.
El tratamiento agudo ambulatorio inicial debe sustentarse en la medicación oral. El fármaco de
primera elección es carbamaczepina a dosis inicial de 100 mg/12 h, obteniendo buena respuesta
habitualmente con dosis de 100-200 mg/8 h, pudiendo escalar hasta un máximo de 1.200 mg/día si la
respuesta es insuficiente. Se recomiendan controles hematológicos y hepáticos en los primeros meses, así
como la monitorización de niveles si se manejan dosis por encima de 600 mg. Como mejor alternativa
contamos con oxcarbazepina (inicio a 300 mg/12 h y mantenimiento a 600-1.200 mg/24 h en dos tomas) y
el acetato de eslicarbazepina (400-1.200 mg en dosis única); y ya en segunda línea baclofeno, lamotrigina o
lacosamida. En casos refractarios se plantearía cirugía sobre la compresión neurovascular, siempre que la
haya.
En el tratamiento sintomático agudo en Urgencias durante los ataques más severos está indicada
la fenitoína intravenosa. La administración de una dosis de carga intravenosa (14 mg/kg) de fenitoína alivia
el dolor durante 24-48 horas y permite el inicio de un tratamiento oral alternativo. La dosis de carga debe
diluirse en 250 cc de suero salino fisiológico (SSF) al 0,9% y administrarse en no menos de 30 minutos con
control electrocardiográfico. Otras opciones son sumatriptán subcutáneo a dosis de 3 mg y lidocaína
intranasal al 8%. El tratamiento oral se mantiene solo durante los periodos de ataques y después se intenta
retirar o mantener a dosis mínimas.
Neuralgia herpética aguda y posherpética
Las formas craneales de la infección por el virus herpes zóster (HZ) son el HZ oftálmico y el
óptico (ver Capítulo 16. “Patología oftalmológica”, Capítulo 17. “Patología
otorrinolaringológica” y Capítulo 18. “Patología dermatológica”).
La infección aguda del nervio trigémino casi siempre afecta a la división oftálmica. El dolor en esta
fase es intenso y puede requerir la administración de AINE convencionales e incluso analgésicos opioides.
Los antivíricos, gabapentina/pregabalina y prednisona, pueden disminuir el dolor durante esta etapa. La
neuralgia posherpética (NPH) es la complicación más frecuente del HZ craneal. Se define como un
síndrome doloroso neuropático unilateral que persiste o se desarrolla más allá de los 3 meses después de
que el rash vesicular haya desaparecido. La intensidad del dolor es variable, así como la calidad (quemante,
lancinante, cortante, profunda). El dolor puede ser intermitente o continuo. Puede manifestarse en forma
de alodinia. En el tratamiento, como terapia de primera línea puede utilizarse gabapentina a dosis inicial de
900 mg/día, fraccionada en tres tomas, que puede incrementarse gradualmente hasta la dosis de 1.800
mg/día; la pregabalina a dosis inicial de 150 mg/día, en dos tomas, con incremento gradual de dosis hasta
600 mg/día, es una alternativa. Otra buena opción terapéutica inicial son los parches tópicos de lidocaína al
5% y amitriptilina a dosis de 10-75 mg/noche.
3.4. Otras cefaleas agudas recurrentes
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1314]
[81] CEFALEAS Y ALGIAS CRANEOFACIALES
Existen cefaleas primarias asociadas a la tos, al ejercicio físico o a la actividad sexual. Ante un
paciente con una cefalea de estas características es importante descartar causas secundarias y diferenciarlo
de las crisis de migraña que pueden desencadenarse con el ejercicio.
4. CEFALEAS SUBAGUDAS PROGRESIVAS
Constituidas en su mayor parte por cefaleas secundarias a lesiones orgánicas que producen un
síndrome de hipertensión intracraneal.
4.1. Síndrome de hipertensión intracraneal
El síndrome de hipertensión intracraneal (HTIC) puede deberse a distintas causas (Tabla VII).
Se produce un incremento de la presión intracraneal, que se manifiesta como cefalea, que puede
ser holocraneal o localizada, no suele ser pulsátil, y suele ir asociada a náuseas/vómitos “en escopetazo”
que empeoran con la actividad física o con las maniobras que aumentan la presión intracraneal (maniobra
de Valsalva, toser, estornudar, inclinarse hacia delante, tumbarse o hipercapnia nocturna, motivo por el
que puede despertar al paciente); puede agravarse por la mañana. También puede acompañarse de paresia
del VI nervio craneal (incluso bilateral) por compresión durante su trayecto, produciendo una diplopía
binocular horizontal. Si progresa el cuadro puede llegar a aparecer alteración del nivel de consciencia como
resultado de una incipiente herniación cerebral transtentorial (ver Capítulo 82. “Alteración del nivel de
consciencia. Coma”).
Para el diagnóstico es obligada la realización de una exploración neurológica que incluya el fondo
de ojo para valorar la existencia de papiledema y confirmar la ausencia de pulso venoso. Asimismo, es
necesaria la realización de un estudio de neuroimagen y, si este resulta normal, debe procederse a la
realización de una punción lumbar (PL) para medir la presión de apertura (> 20 cm H2O) y estudiar el LCR. El
tratamiento inicial del paciente con HTIC consiste en estabilizar las constantes y la vía aérea. A
continuación, deben adoptarse medidas posturales que faciliten el retorno venoso craneal como elevar la
posición de la cabeza 30º y no usar la postura en Trendelenburg. Deberá tratarse etiológicamente la HTIC
cuando sea posible (drenaje de hematomas, antibioterapia en casos de infección, resección tumoral, etc.).
El tratamiento sintomático consiste en instaurar medidas que disminuyan la propia HTIC y
controlen el edema cerebral. La hiperventilación produce vasoconstricción cerebral dando lugar a una
disminución del flujo sanguíneo cerebral y de la presión intracraneal (PIC). Los agentes osmóticos, como el
manitol, deben ser usados con precaución debido a la diuresis osmótica e hipovolemia secundaria,
indeseable en pacientes con HTIC. Si se administran, debe garantizarse un control estricto del balance
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1315]
[81] CEFALEAS Y ALGIAS CRANEOFACIALES
hídrico del paciente intentando mantener un estado de euvolemia. La infusión se realiza por vía
intravenosa, preferentemente en bolo inicial de 0,75 g/kg al 20% en 20 minutos (para un paciente de 70 kg
sería la dosis de 250 ml ya que esta equivale a 50 g), seguido de 125 ml/6 horas, y disminuyendo la
frecuencia progresivamente a cada 8 horas, cada 12 horas y cada 24 horas hasta suspender. No es
recomendable mantener esta terapia más allá de tres días consecutivos por los efectos adversos
mencionados. La dexametasona se administra con dosis de carga de 10 mg, seguido de 4 mg cada 6 horas,
hasta respuesta, después se pasa a la vía oral y se reduce hasta retirar si es posible en 7 días. Solo se
emplea en el edema vasogénico asociado a tumores y abscesos, pero está contraindicado en ictus y
traumatismo craneoencefálico.
Si el control de la HTIC es subóptimo con la terapia osmótica, el siguiente paso debe ser la
inducción del coma farmacológico.
4.2. Hipertensión intracraneal idiopática o pseudotumor cerebri
Es típico de mujeres obesas en edad fértil (20-44 años). Puede asociarse a toma de fármacos
(tetraciclinas, corticoides, vitamina A, etc.). Clínicamente se caracteriza por cefalea (síntoma más
frecuente), grave en intensidad, que puede ser de calidad pulsátil, de horas de duración y con frecuencia
diaria, acompañada de datos de HTIC, náuseas/vómitos, tinnitus pulsátil (sincrónico con el pulso),
oscurecimientos visuales transitorios (descritos como visión borrosa mono/binocular de menos de 30
segundos de duración), fotopsias y pérdida de visión.
El papiledema bilateral, las alteraciones visuales (alteraciones campimétricas como aumento del
punto ciego y déficit inferonasal con preservación de la agudeza visual en el optotipo en fases iniciales) y la
anteriormente citada paresia del VI nervio craneal son frecuentes en la exploración neurológica. Para el
diagnóstico se requiere estudio de neuroimagen con despistaje de causas secundarias de HTIC, así como
aumento de la presión del LCR (> 20 cm H2O). El tratamiento inicial se basa en la pérdida de peso y, dentro
de las medidas farmacológicas, se incluyen acetazolamida (250 mg/día y posteriormente cada 12 horas),
furosemida o topiramato, pudiendo requerir la realización de derivación de LCR en los casos más graves.
5. CEFALEAS CRÓNICAS
5.1. Migraña crónica: ver “Complicaciones de la migraña” previamente.
5.2. Cefalea tensional
Es la cefalea más prevalente de todas. Es más frecuente en mujeres y no tiene el carácter familiar
de la migraña. Se instaura de forma insidiosa, es opresiva (no pulsátil), de intensidad leve-moderada,
bilateral en el 90%, localizándose en la región frontotemporal u occipitocervical. Los pacientes la describen
como “un casco que me oprime la cabeza”. Muchos aquejan hormigueos en la superficie craneal y en
ocasiones existe contractura de músculos pericraneales a la palpación. Suelen consultar por una cefalea
cotidiana durante periodos de semanas, meses e incluso años. El dolor empeora con el transcurso del día,
la falta de sueño o el estrés físico o emocional. No suele empeorar con la maniobra de Valsalva, ni se
acompaña de síntomas neurológicos, aunque es frecuente encontrar insomnio, depresión, ansiedad y
sensación de mareo inespecífica.
En el tratamiento agudo suele ser suficiente con analgésicos simples como paracetamol en dosis de
0,5-1 g, AINE tipo ibuprofeno 600 mg o naproxeno sódico 550 mg. Es importante evitar las asociaciones de
analgésicos con cafeína, benzodiazepinas, barbitúricos, etc., para prevenir el abuso de fármacos. La
angustia del paciente y el carácter inespecífico de la cefalea hacen que sea necesaria en muchos casos la
práctica de estudios de neuroimagen de complacencia con fines placebo.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1316]
[81] CEFALEAS Y ALGIAS CRANEOFACIALES
En los casos crónicos, de larga evolución o afectación general importante, se recomienda el
tratamiento profiláctico, comenzando a ser beneficioso al mes del inicio y debiendo mantenerse durante
3-6 meses, retirándolo posteriormente de modo escalonado. El más establecido es amitriptilina (10 mg en
dosis única nocturna, subir a 25 mg, se puede llegar a 75 mg). La alternativa es sertralina 50 mg/día y
citalopram 10 mg/día. Son de utilidad medidas que disminuyan el estrés, incluyendo el uso de
benzodiazepinas si es necesario.
5.3. Cefalea por abuso de medicamentos
La cefalea por abuso de medicamentos (CAM) es una cefalea crónica no primaria que está presente
más de 15 días al mes, con un abuso regular (> 10 días/mes) de fármacos durante más de tres meses.
Normalmente, aunque no siempre, se resuelve en dos meses tras la retirada de medicamentos. Lo habitual
es que una cefalea primaria (migraña o tensional) se cronifique en relación al abuso de fármacos (sobre
todo, por automedicación). Su presencia se asocia a una reducción en la efectividad de los tratamientos
preventivos, así como a la tolerancia, habituación y dependencia a la medicación.
El manejo del cuadro se basa en una adecuada explicación al paciente de su problema,
promocionar hábitos de vida saludables y suspender el medicamento al que se atribuye esta cefalea (salvo
si asocia benzodiazepinas que se deben retirar lentamente si hiciera falta). Concomitante a esto, es
necesario iniciar tratamiento preventivo para la cefalea primaria de base que tuviese el paciente.
BIBLIOGRAFÍA
Becker WJ. Acute Migraine Treatment. Continuum. 2015;21:953-72.
Bermejo, F. Neurología Clínica Básica. 2ª edición. España: Zoompin; 2012.
Boseh Gil JÁ, Solans Laqué R, Gil Aguado A, Gónzalez-Gay Mantecón MÁ, Cid Xutglá MC, Álvarez de
Mon M, Ingelmo Morín M, et al. En: Farreras-Rozmán, editores. Farreras-Rozmán, Medicina Interna. Vol.
1. 16ª edición. España: Elsevier; 2010: 1118-35.
Headache Classification Committee of the International Headache Society (IHS). The International
Classification of Headache Disorders. 3rd edition (beta version). Cephalalgia. 2013;33:629.
Silberstein SD. Preventive Migraine Treatment. Continuum. 2015;21:973-89.
Valle Arcos MD, Hernández Gallego J. Cefaleas. En: A. Camacho Salas, J. González de la Aleja Tejera,
JM Sepúlveda Sánchez, editores. Urgencias en Neurología. 2ª ed. España: Ergón, 2012:110-25.
Weyand CM, Goronzy JJ. Giant-Cell Arteritis and Polymialgia Rheumatica. N Engl J Med. 2014;371:50-7.
Zarranz JJ. Neurología. 5ª edición. España: Elsevier; 2013.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1317]
[82] ALTERACIÓN DEL NIVEL DE CONSCIENCIA. COMA
82.Alteración del nivel de consciencia. Coma
Diego Barragán Martínez.
Neurología
Elena de Sautu de Borbón.
Medicina Interna
Asesora:
Sara Llamas Velasco.
Médica Adjunta de Neurología
I. CONCEPTO
Al igual que la uremia implica un fallo renal, la alteración del nivel de consciencia supone un fallo en
la función cerebral, y es uno de los problemas que comporta una mayor dificultad clínica. En esta situación
el tiempo para actuar suele ser escaso y las causas múltiples, lo que hace de este problema un verdadero
desafío para el médico.
La consciencia se define como el “estado de pleno conocimiento de uno mismo y de sus relaciones
con el entorno”. Esto es, sin embargo, difícil de valorar clínicamente, por lo que para ser operativos, a pie
de cama, queda definido por el grado de respuesta del paciente al examinador. Pese a que con esto se
facilita la valoración clínica del coma, es posible que un paciente esté consciente aunque no responda al
examinador, por ejemplo, si está paralizado o voluntariamente decide no responder. Por lo tanto,
determinar el estado de consciencia puede suponer un ejercicio técnicamente complejo.
La consciencia tiene dos componentes principales, el contenido y el nivel de vigilia o alerta, y un
fallo en cualquiera de ellos puede derivar en una alteración de la primera:
La corteza cerebral procesa, integra y contextualiza la información que recibe, dando lugar al
contenido de la consciencia, y, si bien lesiones circunscritas podrán originar déficits focales en
este (por ejemplo, una disfasia), rara vez darán lugar a una disminución del nivel de
consciencia, pues para esto último es necesario un daño difuso de este sistema.
La alerta (o nivel de vigilia) es la situación en que se está despierto. Su localización anatómica
es el sistema reticular activador ascendente (SRAA), una red neuronal que se sitúa en el
tegmento pontino, mesencéfalo, hipotálamo posterior y tálamo, y que proyecta a la corteza
cerebral para inducir y mantener su actividad.
En la alteración del nivel de consciencia hay un fallo en la respuesta a estímulos junto a una
dificultad para alertar (“despertar”) al paciente, siendo el coma un grado tan profundo que supone una
ausencia de respuesta con incapacidad de alertar al paciente. Términos como estupor, letargia y
obnubilación, que definen niveles intermedios entre la consciencia y el coma, deberían ser evitados sin una
mayor descripción, dada su ambigüedad.
II. ETIOLOGÍA
El abordaje diagnóstico inicial va encaminado a diferenciar si la causa es un proceso difuso o bien
una alteración estructural. Esta tarea se ha visto enormemente facilitada desde la introducción de las
pruebas de neuroimagen en los servicios de urgencias, que son capaces de descartar gran parte de las
causas estructurales de coma en poco tiempo. Sin embargo, cuando la neuro-imagen no revela la causa, no
existe una determinación o procedimiento aislado más eficaz que una evaluación clínica minuciosa. Con los
datos que se hayan obtenido en la anamnesis y la exploración, se debería poder clasificar al paciente en
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1318]
[82] ALTERACIÓN DEL NIVEL DE CONSCIENCIA. COMA
uno de los dos tipos fisiopatológicos principales del coma, que se exponen a continuación. Cada uno incluye
patologías concretas (Tabla I), y si se logra catalogar al paciente en uno de ellos, se habrá acotado el
diagnóstico diferencial y se podrá realizar un estudio y tratamiento más dirigidos.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1319]
[82] ALTERACIÓN DEL NIVEL DE CONSCIENCIA. COMA
1. LESIÓN CEREBRAL DIFUSA
Supone la principal causa de disminución del nivel de consciencia, siendo las alteraciones tóxico-
metabólicas las más frecuentes dentro del grupo. En los trastornos difusos el coma suele ser de
instauración progresiva y puede acompañarse de mioclonías positivas, negativas (asterixis o flapping
tremor), temblor y crisis epilépticas. Lo más habitual es la ausencia de sintomatología focal neurológica,
salvo etiologías concretas como las alteraciones de la glucemia y la natremia, que sí pueden producirla. Los
reflejos y funciones del tronco cerebral estarán preservados y el patrón respiratorio puede ser variable.
2. LESIÓN ESTRUCTURAL FOCAL O MULTIFOCAL
Pueden ser hemisféricas o troncodiencefálicas:
Lesiones hemisféricas: el coma suele ser de instauración progresiva, si bien la clínica focal
inicial se puede instaurar de manera súbita, especialmente si se trata de infartos o
hemorragias. Suele tratarse de lesiones de tamaño suficiente como para que se den signos
focales neurológicos, frecuentemente asimetrías en la motricidad y desviación de la mirada
conjugada. Si la lesión crece, la disminución del nivel de consciencia progresará y aparecerán
otros signos secundarios a herniación, como asimetría pupilar, respuestas motoras patológicas,
alteración en los reflejos troncoencefálicos, alteraciones ventilatorias y autonómicas.
Lesiones troncodiencefálicas: si la lesión afecta directamente al SRAA (infarto, hemorragia) el
coma puede aparecer desde el primer momento, o más progresivamente si se afecta por
compresión (tumores, abscesos). En esta topografía, lesiones de menor tamaño podrán
producir sintomatología más florida, y en caso de lesiones compresivas, su comportamiento
será similar al descrito a nivel hemisférico.
III. CLÍNICA
Lo primero que se ha de tener en cuenta es que la valoración clínica inicial debe ir encaminada a la
estabilización del paciente (ver Apartado VI.1. “Actitud inmediata ante un paciente en coma”). Una vez
estabilizado, la anamnesis y la exploración deberían ayudar a distinguir, en primer lugar, si el paciente
presenta una verdadera disminución del nivel de consciencia o bien sufre otros trastornos como la
catatonía, el mutismo acinético o el síndrome de cautiverio, o bien si se trata de un cuadro conversivo (ver
Apartado IV.2. “Diagnóstico diferencial”). En segunda instancia, hay que tratar de discernir si se trata de un
daño difuso o de un daño estructural, y en este último caso, a qué nivel. Esta distinción servirá de ayuda
para orientar las medidas diagnósticas y terapéuticas que seguidamente se adoptarán. Por último, es
posible encontrar datos de especial valor para el diagnóstico etiológico, aunque para establecerlo
definitivamente son precisas las pruebas complementarias (ver Apartado IV.1. “Pruebas
complementarias”).
1. ANAMNESIS
Es la parte más importante en la valoración de cualquier paciente con disfunción del sistema
nervioso y, dado que en estos casos el enfermo no suele participar, es importante la entrevista con
familiares, cuidadores y personal médico de emergencias que puedan conocerla, aunque no es raro en
estos pacientes que falte por completo. Esta información, al ser obtenida de manera indirecta, debe ser
interpretada con cautela. Puede ser útil revisar los efectos personales del paciente en busca de
documentos identificativos, informes médicos y hojas de tratamiento.
Es importante indagar en los antecedentes del paciente, ya que el coma puede complicar la
evolución de muchos procesos (diabetes, insuficiencia hepática, renal, respiratoria), y/o puede suponer su
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1320]
[82] ALTERACIÓN DEL NIVEL DE CONSCIENCIA. COMA
estadio final. Hay que tratar de conocer también los fármacos y tóxicos que consuma el paciente de manera
habitual y que en sobredosis puedan originar una disminución del nivel de consciencia (Tabla I. Tóxicos).
En ausencia de antecedentes que justifiquen la alteración del nivel de consciencia, se deben buscar
otros datos.
Escenario: el lugar y las circunstancias donde se encontró al paciente pueden aportar pistas
sobre la etiología del cuadro. Por ejemplo, si el paciente se encontraba en casa, resulta útil
saber si había braseros o envases de medicamentos. O si el paciente fue encontrado en la vía
pública, si había indicios de violencia, de traumatismo o de consumo de tóxicos.
Constantes: cuando el paciente es hallado, la determinación de constantes vitales (tensión
arterial, frecuencia cardiaca, temperatura, glucemia capilar) no solo es importante para su
estabilización hemodinámica, sino que también puede resultar orientativa en cuanto a la
etiología del cuadro (Tabla II).
Comienzo: el lapso de tiempo desde que el paciente fue visto consciente por última vez hasta
que entró en coma también puede ser de ayuda. Un coma de instauración súbita generalmente
responde a un daño encefálico primario, y orienta fundamentalmente a infartos y hemorragias,
aunque en estas últimas, al igual que en otros cuadros compresivos, el inicio puede ser más
gradual. La oclusión de estructuras vasculares o la obstrucción al drenaje de líquido
cefalorraquídeo (LCR) por una lesión compresiva pueden también disminuir el nivel de
consciencia de manera aguda. Inicios más larvados y fluctuantes orientan más bien a etiologías
metabólicas o tóxicas, pero se debe tener en cuenta que hay tóxicos de acción muy rápida
como el alcohol metílico, y otros, como la cocaína y el éxtasis, que asocian complicaciones
vasculares de patocronia aguda.
Síntomas y signos acompañantes: la semiología focal como la hemiparesia, la desviación
oculocefálica, la disfasia o las crisis focales orientan a una fisiopatología preferentemente
estructural, mientras que las alteraciones del comportamiento, la confusión y las crisis
generalizadas lo hacen hacia un daño difuso. Síntomas sistémicos como el dolor torácico, la
disnea o palpitaciones pueden referir a un origen cardiogénico (shock, cardioembolia), mientras
que síntomas como la cefalea o los vómitos sugieren una elevación de la presión intracraneal
(hemorragia, meningitis), así como la presencia de fiebre sugiere procesos infecciosos.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1321]
[82] ALTERACIÓN DEL NIVEL DE CONSCIENCIA. COMA
2. EXPLORACIÓN FÍSICA GENERAL
Se debe realizar una exploración física convencional, en la que se buscarán pistas que nos orienten
el diagnóstico etiológico.
Inspección: la equimosis periorbitaria bilateral (signo de ojos de mapache) o un hematoma bajo
la apófisis mastoides (signo de Battle) son sugestivos de fractura de la base craneal. Hay que
revisar la piel en busca de lesiones petequiales (sepsis meningocócica, coagulación
intravascular diseminada) o signos de venopunción, así como la cavidad bucal en busca de
restos de vómito o mordeduras.
Fondo de ojo y otoscopia: en el fondo de ojo se puede encontrar edema de papila en casos de
encefalopatía hipertensiva, o hemorragia vítrea en la hemorragia subaracnoidea (síndrome de
Terson). La otoscopia busca un hemotímpano que sugiera una fractura de la base de cráneo.
Patrón respiratorio: aunque clásicamente se habla de unos patrones respiratorios bien
definidos, en la práctica clínica no son frecuentes y su valor localizador es limitado. Observando
la respiración espontánea del paciente se puede hallar:
Hipoventilación: suele aparecer en pacientes intoxicados por opiáceos, sedantes o en el
coma hipotiroideo. La respiración apnéustica consiste en la presencia de pausas
respiratorias en inspiración completa, que ocasionalmente aparecen también al final de
la espiración. Tiene un importante valor localizador para el daño protuberancial, y más
raramente se puede encontrar en casos de encefalopatía metabólica o meningitis.
Cuando hay lesiones del bulbo raquídeo el patrón de hipoventilación suele ser irregular,
denominándose respiración atáxica o de Biot, que asociará otros signos de afectación
bulbar, augurando con frecuencia una parada respiratoria.
Hiperventilación: la hiperventilación en un paciente en coma suele responder a
patología sistémica más que neurológica, como un edema agudo de pulmón,
cetoacidosis diabética o encefalopatía hepática. La hipertensión intracraneal (HIC), de
cualquier etiología, producirá hiperventilación, así como las lesiones troncoencefálicas
altas. En este caso suele aumentar con estímulos dolorosos, que además desencadenan
respuestas motoras patológicas.
Respiración periódica: la respiración de Cheyne-Stokes consiste en un patrón periódico
en el que la amplitud de la inspiración aumenta de forma regular para posteriormente
disminuir de manera igualmente regular hasta alcanzar una apnea que dura varios
segundos, tras la cual se inicia un nuevo ciclo. Es un patrón respiratorio inespecífico que
aparece en lesiones difusas de ambos hemisferios, pero su presencia indica que los
reflejos respiratorios troncoencefálicos están intactos. Es frecuente encontrarla,
además, en pacientes ancianos o con insuficiencia cardiaca, especialmente durante el
sueño. Si no aparece pausa de apnea se denomina simplemente respiración periódica.
Signos meníngeos: no solo orientan hacia una neuroinfección, sino también hacia otros
procesos irritativos de las meninges como la hemorragia subaracnoidea o la carcinomatosis
meníngea. En el coma profundo pueden estar ausentes.
3. EXPLORACIÓN NEUROLÓGICA
La exploración neurológica tiene como objetivo fundamental establecer la topografía de la lesión, o
al menos poder hacer una distinción entre una lesión focal, multifocal y difusa. Además, servirá de
referencia para el seguimiento posterior y para establecer un pronóstico.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1322]
[82] ALTERACIÓN DEL NIVEL DE CONSCIENCIA. COMA
Tanto por la rapidez necesaria para adoptar medidas diagnósticas y terapéuticas como por la
escasez de respuestas que se encontrarán, la exploración neurológica del paciente en coma debería poder
llevarse a cabo en pocos minutos. Sus componentes fundamentales se explican a continuación.
Nivel de consciencia
Valorar el grado de pérdida de consciencia en un paciente aporta información
fundamentalmente pronóstica. Para ello es preciso determinar la intensidad de estímulo
necesaria para obtener una respuesta, así como la calidad de respuesta conseguida, atendiendo
especialmente a la respuesta verbal, ocular y motora. Se aplicarán estímulos en orden creciente
de intensidad (auditivos, táctiles, luminosos y nociceptivos), hasta conseguir la mejor respuesta.
Si se logra alertar al paciente, se valorará su capacidad de respuesta verbal a preguntas
sencillas (nombre, edad, mes del año) y su capacidad de obedecer órdenes sencillas (abrir y
cerrar los ojos, hacer un puño con la mano), así como el tiempo que consigue mantenerse
alerta. En caso de no poder alertar al paciente, se valorará con qué estímulo se logran
respuestas y qué tipo de respuestas oculares y motoras se consiguen.
Existen varias escalas que pretenden de una manera sencilla y rápida proporcionar esta valoración
pronóstica. La escala de coma de Glasgow (Tabla III), que se concibió para pacientes con traumatismo
craneal, tiene la ventaja de ser globalmente conocida, pero se ha visto que, utilizada en el servicio de
urgencias, tiene solo un moderado acuerdo interobservador. Esta escala es además poco precisa en
pacientes intubados y carece de un examen de las funciones del tronco, valores que se añaden en la escala
FOUR, full outline of unresponsiveness (Tabla IV). En cualquier caso, hay que tener en cuenta que ninguna
escala es adecuada para todos los pacientes, y por tanto, suele ser más útil describir qué estímulos originan
o no respuestas y la clase de respuestas que se observan. A la hora de describir los hallazgos es importante
evitar el uso de términos ambiguos como obnubilación, estupor, letargia, etc., ya que cada uno comprende
un amplio abanico de respuestas entre las que puede existir solapamiento.
Pupilas
Se debe explorar el tamaño, la simetría (hasta un 20% de pacientes sanos tienen una diferencia
de 1 mm entre ambas pupilas) y la respuesta fotomotora (directa y consensuada). Las
anomalías pupilares son indicativas de un daño estructural que afecta a su inervación simpática
(pupilodilatadora) o parasimpática (pupiloconstrictora), o que involucra directamente al ojo o al
nervio óptico, y por tanto, su exploración tendrá un importante valor localizador. Como
excepción, se pueden encontrar las pupilas de la hipotermia, la encefalopatía
hipóxicoisquémica, y las pupilas tóxico-farmacológicas. El coma metabólico suele respetar la
función pupilar hasta estadios avanzados. En la tabla V se muestran los posibles hallazgos
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1323]
[82] ALTERACIÓN DEL NIVEL DE CONSCIENCIA. COMA
pupilares en
un paciente en coma y su valor diagnóstico.
Movimientos oculares
En el paciente en coma se debe evaluar la posición de la mirada en reposo, la presencia de
movimientos oculares espontáneos y los reflejos oculocefálicos (ROC) y oculovestibulares
(ROV).
En posición de reposo y en ausencia de lesión estructural, el paciente debería permanecer con los
ojos cerrados, y al levantarle pasivamente los párpados, se observarían los ojos en posición media y
conjugada. También es posible hallar movimientos oculares de tipo roving. La tabla VI muestra diferentes
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1324]
[82] ALTERACIÓN DEL NIVEL DE CONSCIENCIA. COMA
patrones de alteración en la posición primaria de la mirada y movimientos oculares espontáneos que se
pueden encontrar en el paciente en coma, con su valor diagnóstico.
Los ROC se exploran realizando movimientos de rotación cefálica pasiva, rápidos, hacia la derecha,
izquierda, arriba y abajo. En ausencia de lesión estructural troncoencefálica, se observará una desviación
ocular conjugada en el sentido opuesto al giro cefálico. Resulta confuso saber si el llamado “signo de los
ojos de muñeca” consiste en la presencia o ausencia de ROC, por lo que se recomienda hablar de
“maniobra de los ojos de muñeca” para referirse a la maniobra en sí, en vez de a su resultado. Hay que
saber que el control voluntario de la mirada supera esta respuesta refleja, y por tanto, no se encontrará
este reflejo en el paciente consciente. No se debe realizar esta maniobra sin haber descartado antes
inestabilidad cervical. En este caso, se colocará un collarín cervical y se evaluarán los ROV en vez de los
anteriores. Para explorar los ROV se flexiona el cuello 30 grados sobre la horizontal y se instilan en el
conducto auditivo externo de 10 a 50 ml de suero salino frío, previa otoscopia para descartar perforación
timpánica. Si el tronco está indemne se apreciará una desviación lenta y conjugada de la mirada hacia el
lado irrigado, pero no nistagmo, que indicaría una función cortical preservada y por tanto un proceso
diferente al coma (ver Apartado IV.2. “Diagnóstico diferencial”) o un coma poco profundo. Una lesión
estructural a nivel troncoencefálico producirá una respuesta ausente o desconjugada de los ROC o los ROV,
mientras que su normalidad será indicativa de integridad.
Reflejo corneal
Se realizará preferentemente con un hisopo de algodón, una gasa o una gota de suero salino al
0,9%, estimulando el limbo corneal, y no directamente sobre la córnea. La respuesta normal
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1325]
[82] ALTERACIÓN DEL NIVEL DE CONSCIENCIA. COMA
consiste en un cierre de ambos párpados con supraversión de la mirada (fenómeno de Bell).
Esta respuesta supone la indemnidad de la vía aferente (V nervio craneal) y eferente (III y VII
nervios craneales), así como sus conexiones troncoencefálicas. Una lesión a cualquiera de estos
niveles alterará la respuesta. El reflejo corneal puede estar abolido en pacientes ancianos,
diabéticos, bajo tratamiento sedante o portadores habituales de lentes de contacto.
Reflejo nauseoso y tusígeno
Se puede explorar el reflejo nauseoso estimulando con un depresor lingual la pared posterior
de la orofaringe, y el tusígeno mediante la aspiración de secreciones en el paciente intubado.
Su presencia indica integridad de los nervios craneales IX y X (bulbo raquídeo).
Respuestas musculoesqueléticas
Se valorará inicialmente la presencia de movimientos espontáneos del paciente y su simetría.La
movilización espontánea asimétrica de un hemicuerpo es indicativa de daño en la vía piramidal
y por tanto de un coma estructural. Movimientos anormales como el temblor y las mioclonías
suelen aparecer en pacientes con daño cerebral difuso, generalmente tóxico-metabólico.
En ausencia de movimientos espontáneos, se valorará el tono muscular y la respuesta motora ante
estímulos nociceptivos. Al aplicar estímulos dolorosos conviene comenzar en un lado, ejerciendo presión en
el lecho ungueal, el arco supraorbitario o la articulación temporomandibular, para valorar la lateralización
de la respuesta. A continuación se debe repetir el estímulo en el otro lado, ya que una respuesta
localizadora requiere que el brazo contralateral cruce la línea media hacia el estímulo, y porque una lesión
focal en las vías sensitivas, tanto cerebrales como medulares, puede anular las respuestas a estímulos en
ese hemicuerpo. Si no se encuentran respuestas motoras, hay que aplicar un estímulo más intenso en la
línea media, presionando con los nudillos contra el esternón del paciente. Es importante valorar además la
asimetría en las respuestas. Por ejemplo, una hemihipotonía, valorada al dejar caer las extremidades contra
gravedad, o una hemiparesia, detectada por respuestas asimétricas al dolor, son indicativas de una lesión
estructural.
Clásicamente se han descrito las posturas reflejas en decorticación y descerebración, con una
intención localizadora. Hoy en día se sabe que su valor localizador es escaso, al igual que no son indicadores
fiables de etiología. Además, el patrón motor es variable, de manera que suele ser más útil simplemente
describir los movimientos observados, en vez de intentar encuadrarlos en uno de estos patrones. Lo que sí
es posible extraer de este tipo de reflejos es que indican mayor profundidad del coma y por lo tanto peor
pronóstico, tanto si están presentes desde el inicio como si aparecen en la evolución.
Respecto a los reflejos de estiramiento muscular, suelen estar hipoactivos en el paciente en coma,
pero, más que su actividad, se debe valorar su simetría. Los reflejos cutáneos también suelen ser
hipoactivos, y ocasionalmente se puede encontrar una respuesta cutaneoplantar extensora bilateral en
ausencia de lesión estructural, con lo que de nuevo resultan más interesantes las respuestas asimétricas.
IV. DIAGNÓSTICO
1. PRUEBAS COMPLEMENTARIAS
El objetivo de las pruebas diagnósticas iniciales en el paciente en coma es identificar las condiciones
tratables. La recuperación depende en gran medida del tratamiento precoz, por lo que las pruebas deben
realizarse rápidamente en función de la evaluación clínica previa. Una vez descartadas estas opciones, el
estudio se orientará a identificar la etiología del cuadro.
Laboratorio
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1326]
[82] ALTERACIÓN DEL NIVEL DE CONSCIENCIA. COMA
Pruebas básicas: hemograma, perfil hepático, amonio, iones, calcio, magnesio, fósforo,
glucosa, urea, creatinina, lactato, osmolaridad, gases arteriales, coagulación y tóxicos
en orina.
Pruebas adicionales: hormonas tiroideas, cortisol, hemocultivos, urocultivo, porfirinas
en orina, metales pesados en sangre y orina, frotis, anticuerpos antifosfolípido,
carboxihemoglobina, etc.
Neuroimagen
La tomografía computarizada (TC) craneal permite determinar cambios estructurales
intracraneales y por su rapidez y accesibilidad suele ser la prueba de elección en la
evaluación inicial del paciente en coma. Por ejemplo, permite identificar infartos
cerebrales, hemorragias intracraneales, masas cerebrales, edema e hidrocefalia aguda,
entre otros.
La resonancia magnética (RM) permite ver alteraciones de forma más precoz en
determinadas patologías: encefalitis vírica, encefalomielitis aguda diseminada,
isquemia cerebral aguda, leucoencefalopatía posterior reversible, trombosis de senos
venosos cerebrales o vasculitis del sistema nervioso central (SNC). También permite
detectar lesiones para las que la TC presenta baja sensibilidad, como las del daño
axonal difuso. En caso de tener disponibilidad de RM urgente, esta será más útil que la
TC para el diagnóstico del ictus en fase aguda, mediante secuencias de difusión. Sin
embargo, no suele ser la primera prueba que se efectúa, debido a su menor
disponibilidad y al tiempo necesario para su realización, que requiere una mayor
estabilidad del paciente.
El doppler trascraneal resulta útil para descartar patología vascular cerebral y
especialmente en el diagnóstico de muerte cerebral.
La tomografía por emisión de positrones (PET) permite dar una aproximación sobre la
integridad funcional del tejido, pues se puede ver un patrón diferente de función
metabólica en los distintos estados de consciencia.
Punción lumbar
Se realizará cuando no se tenga claro el diagnóstico o ante la sospecha de infección del SNC,
efectuando siempre una prueba de neuroimagen previa. Habrá que medir la presión de
apertura del LCR, realizar un estudio citobioquímico (células, glucosa y proteínas),
microbiológico, espectrometría del centrifugado si es preciso (para diferenciar una hemorragia
subaracnoidea de una punción traumática) y citología si existe sospecha de neoplasia.
Electroencefalograma
Es útil para detectar patología comicial, especialmente un estado epiléptico no convulsivo,
para el diagnóstico diferencial y como marcador pronóstico. También puede ser de ayuda para
monitorizar los efectos del tratamiento. Los potenciales evocados somatosensoriales
proporcionan un pronóstico más definitivo.
2. DIAGNÓSTICO DIFERENCIAL
Existen ciertas patologías que semiológicamente pueden confundirse con el coma, pero que
requieren de unas medidas diagnósticas y terapéuticas específicas:
Estado vegetativo persistente: denota la recuperación de la situación de coma ante la
aparición de periodos de “ojos abiertos” en un paciente que no responde. Los pacientes en esta
situación no presentan evidencia de consciencia de sí mismos o de su entorno,pero mantienen
la regulación vegetativa del tronco cerebral (ciclos vigilia-sueño, función cardiopulmonar y
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1327]
[82] ALTERACIÓN DEL NIVEL DE CONSCIENCIA. COMA
regulación autonómica visceral). El término estado vegetativo persistente se reserva para
pacientes que permanecen en ese estado durante al menos 30 días.
Estado de mínima consciencia: existe una mínima consciencia propia o del entorno. Como el
estado vegetativo, el estado de mínima consciencia a menudo existe como un estado de
transición que surge durante la recuperación del coma o durante el empeoramiento de la
enfermedad neurológica progresiva. En algunos pacientes, sin embargo, puede ser una
condición permanente. Los criterios para su diagnóstico clínico incluyen la evidencia limitada
pero claramente discernible de consciencia del “yo” o ambiental de forma reproducible o
sostenida, valorada al cumplir uno o más de los siguientes puntos: 1) respuesta a órdenes
simples; 2) respuestas “sí/no” gestuales o verbales; 3) verbalización inteligible; 4)
comportamiento intencionado incluyendo movimientos o comportamientos afectivos en
relación con estímulos relevantes.
Mutismo acinético o coma vigil: describe una condición de silencio, una apariencia de
inmovilidad que caracteriza a ciertos estados subagudos o crónicos de alteración de la
consciencia donde el ciclo sueño-vigilia se recupera pero la evidencia de actividad mental sigue
siendo ausente y hay una falta de actividad motora por lesión prefrontal en las áreas
responsables de iniciar el movimiento.
Síndrome del cautiverio o locked in: describe un estado en el que el paciente presenta parálisis
de las cuatro extremidades y los pares craneales inferiores. Sin embargo, el estado de alerta no
se ve afectado. No pueden responder a la mayoría de los estímulos pero suelen conservar el
control de los movimientos oculares verticales y la apertura de los párpados. Pueden aprender
a responder al examinador mediante parpadeos, como un código.
Muerte cerebral: se define como la pérdida irreversible de todas las funciones del cerebro,
incluido el tronco, por lo que el organismo no es capaz de mantener la homeostasia respiratoria
y cardiovascular. Es necesaria la evaluación de la historia clínica, de los estudios
neurorradiológicos y de las pruebas de laboratorio para evitar variables de confusión (debe
haber una situación de normotermia, normotensión, equilibrio electrolítico y ausencia de
drogas). El diagnóstico de muerte cerebral requiere dos circunstancias indispensables: la
primera, que el daño sea por una causa estructural conocida o un daño metabólico irreversible
conocido; la segunda, que las estructuras vitales del cerebro necesarias para mantener la
consciencia y la supervivencia vegetativa independiente estén dañadas sin posibilidad alguna
de reparación. Los criterios de muerte cerebral se describen en la tabla VII.
Inconsciencia psicógena: dentro de este cuadro se pueden encontrar las reacciones de
conversión, las convulsiones psicógenas, la depresión con síntomas psicóticos y la simulación. El
diagnóstico debe realizarse con mucho cuidado y después de demostrar que el paciente tiene
un correcto funcionamiento de los hemisferios y del tronco cerebral, porque en ocasiones
pueden tener también enfermedades somáticas que confundan el diagnóstico. Estos pacientes
suelen presentar una aparente inconsciencia con ojos cerrados, existiendo una resistencia
activa a la apertura de los párpados, con un patrón respiratorio normal o con taquipnea. El ROV
con agua helada produce nistagmo contralateral en lugar de desviación tónica de los ojos hacia
el oído estimulado, existe resistencia pasiva al movimiento de las extremidades, los reflejos
osteotendinosos pueden ser normales o estar abolidos de forma voluntaria y los reflejos
plantares son invariablemente flexores.
Catatonía: la catatonía es un trastorno del comportamiento, de fisiopatología desconocida, que
se caracteriza por una incapacidad para moverse con normalidad. Puede ocurrir en el contexto
tanto de enfermedades psiquiátricas (trastorno bipolar, depresión, trastornos psicóticos) como
médicas (patología infecciosa, metabólica, neurológica). Asocia síntomas típicos como el
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1328]
[82] ALTERACIÓN DEL NIVEL DE CONSCIENCIA. COMA
negativismo, mantenimiento de posturas, flexibilidad cérea, catalepsia, ecolalia y ecopraxia.
Puede presentar también otros que planteen un diagnóstico diferencial con el coma, como la
acinesia, el mutismo o la rigidez. El diagnóstico es íntegramente clínico y las pruebas
complementarias irán orientadas a descartar otros procesos. Una prueba terapéutica con
benzodiazepinas puede apoyar el diagnóstico. El tratamiento, aparte del de soporte y el de la
enfermedad de base, se basa en benzodiazepinas y terapia electroconvulsiva.
V. PRONÓSTICO
El pronóstico tras una situación de coma es variable y difícil de precisar. El paciente puede fallecer,
permanecer en un estado vegetativo persistente, presentar un deterioro funcional de diverso grado o una
recuperación neurológica completa.
Además de referirse a la esperanza de vida, también es importante, de cara a los familiares de los
pacientes, determinar la probabilidad del retorno a la plena consciencia y a las funciones voluntarias.
Los clínicos basan sus aproximaciones atendiendo a guías clínicas y a estudios prospectivos,
considerando entre otros la causa del daño cerebral, la duración del episodio, la edad del paciente, la
presencia de comorbilidad, la neuroimagen, los signos neurológicos y los marcadores electrofisiológicos.
Desafortunadamente, los indicadores radiológicos y bioquímicos en general han proporcionado
predicciones menos precisas.
Se pueden considerar datos de mal pronóstico: la etiología isquémica frente a la traumática, la
ausencia de respuesta motora, la pérdida del reflejo pupilar a la luz, la hipotensión, la hipoxia, la HIC y la
edad avanzada.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1329]
[82] ALTERACIÓN DEL NIVEL DE CONSCIENCIA. COMA
VI. ABORDAJE TERAPÉUTICO
El coma supone una verdadera urgencia médica que amenaza la vida del paciente, por lo que se
requiere un diagnóstico y manejo tempranos. El desafío radica en la amplia diversidad etiológica del coma y
el escaso tiempo que posee el médico para establecer los juicios diagnósticos y terapéuticos apropiados.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1330]
[82] ALTERACIÓN DEL NIVEL DE CONSCIENCIA. COMA
Se requiere un enfoque sistemático que permita dirigir los esfuerzos diagnósticos y terapéuticos a
lo largo de las vías adecuadas.
En primer lugar, es importante realizar una interpretación lo más exacta posible de un número
limitado de signos físicos que reflejan la integridad o defecto de los distintos niveles del cerebro, y en
segundo lugar, si es una disfunción estructural o metabólica la que mejor explica el patrón y la evolución de
estos síntomas.
1. ACTITUD INMEDIATA ANTE UN PACIENTE EN COMA
En la figura 1 se describe el manejo inicial del paciente en coma. En caso de requerir perfusión
continua de antídotos, se administrará naloxona 2 mg en 500 ml de suero glucosado 5%, a 100 ml/hora,
ajustando según la respuesta clínica y suspendiéndose en caso de agitación o convulsiones. Además,
flumazenilo 2,5 mg en 500 ml, a 20-100 ml/hora.
2. TRATAMIENTO ESPECÍFICO SEGÚN LA ETIOLOGÍA
Una vez estabilizado el paciente y con una mayor información acerca de la etiología del cuadro, se
procederá al tratamiento etiológico:
Tratamiento de la HIC: ver Capítulo 81. “Cefaleas y algias craneofaciales”.
Tratamiento de las crisis comiciales: ver Capítulo 86. “Crisis comiciales”.
Tratamiento del proceso infeccioso: ver Capítulo 42. “Infecciones del sistema nervioso central”.
Es importante la extracción de cultivos y el inicio lo más precoz posible de la antibioterapia
empírica y antiviral si fuese necesario.
Tratamiento quirúrgico: se debe considerar ante un hematoma subdural, epidural o
intraparenquimatoso, así como ante una hemorragia subaracnoidea secundaria a rotura de un
aneurisma, hidrocefalia obstructiva, absceso cerebral de gran tamaño, lesiones ocupantes de
espacio de otro origen y traumatismo craneoencefálico grave, entre otros.
Tratamiento de las alteraciones metabólicas: se procederá a la corrección de la hipoglucemia,
acidosis metabólica o respiratoria, estados hiperosmolares, alteraciones electrolíticas, etc.
Tratamiento de los trastornos psiquiátricos.
BIBLIOGRAFÍA
Bodart O, Laureys S, Gosseries O. Coma and disorders of consciousness: scientific advances and
practical considerations for clinicians. Semin Neurol. 2013;33(2):83-90.
Edlow JA, Rabinstein A, Traub SJ, Wijdicks EF. Diagnosis of reversible causes of coma. Lancet.
2014;384(9959):2064-76.
Ghoshal S, Greer DM. Why is diagnosing brain death so confusing? Curr Opin Crit Care.
2015;21(2):107-12.
Guldenmund P, Stender J, Heine L, Laureys S. Mindsight: diagnostics in disorders of consciousness.
Crit Care Res Pract. 2012;2012:624724.
Jox RJ, Bernat JL, Laureys S, Racine E. Disorders of consciousness: responding to requests for novel
diagnostic and therapeutic interventions. Lancet Neurol. 2012;11(8):732-8. Erratum in: Lancet Neurol.
2012;11(10):841.
Murcia FJ, Villarejo A. Alteraciones del estado mental. En: Camacho A, González de la Aleja J,
Sepúlveda JM. Urgencias en neurología. Hospital Universitario 12 de Octubre. 2ª ed. Madrid: Ergon;
2013. p. 84-109.
Posner JB, Saper CB, Schiff ND, Plum F. Plum and Posner’s diagnosis of stupor and coma. 4ª ed. New
York: Oxford University Press; 2007.
Sivilotti ML. Flumazenil, naloxone and the ‘coma cocktail’. Br J Clin Pharmacol. 2016;81(3):428-36.
Stevens RD, Cadena RS, Pineda J. Emergency Neurological Life Support: Approach to the Patient with
coma. Neurocrit Care. 2015;23 Suppl 2:69-75.
Tijero B, Zarranz D, Zarranz JJ. Trastornos de la vigilancia. En: Zarranz JJ. Neurología. 5ª ed. Barcelona:
Elsevier; 2013. p. 137-59.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1331]
[83] DEMENCIA Y OTROS TRASTORNOS NEURODEGENERATIVOS. ENFERMEDAD DE PARKINSON
83.Demencia y otros trastornos neurodegenerativos.
Enfermedad de Parkinson
Mª Paz Guerrero Molina.
Neurología
Ana Simarro García.
Neurología
María Espinosa Díaz.
Medicina Interna
Asesor:
Alejandro Herrero San Martín.
Médico Adjunto de Neurología
I. DEMENCIA
1. INTRODUCCIÓN
La demencia se define como un deterioro de las funciones cognitivas, que afecta a una o más áreas
o dominios, entre los que se encuentran la memoria, el aprendizaje, las funciones ejecutivas y motoras, el
lenguaje, la percepción, la atención compleja o el comportamiento social, y que supone un decremento con
respecto al nivel de funcionamiento cognitivo previo. Además, estas alteraciones cognitivas deben tener
una repercusión funcional, interfiriendo con el normal desempeño de las tareas habituales de la vida diaria
o repercutiendo sobre el grado de independencia del individuo que la padece de forma permanente y no
pudiendo ser atribuido a otro trastorno (incluidos trastornos psiquiátricos, entre los que destaca la
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1332]
[83] DEMENCIA Y OTROS TRASTORNOS NEURODEGENERATIVOS. ENFERMEDAD DE PARKINSON
pseudodemencia depresiva). La prevalencia de demencia en mayores de 64 años es de un 5-10%, y
aumenta de manera exponencial con la edad. En la mayoría de los casos el deterioro se produce de manera
progresiva a lo largo de varios años. No obstante, en ocasiones tiene lugar un deterioro marcado de forma
subaguda (normalmente menos de dos años), denominándose en ese caso demencia rápidamente
progresiva, siendo característica esta evolución de la enfermedad de Creutzfeldt-Jakob, si bien podemos
encontrarla también en demencias secundarias a causas tratables o en casos atípicos de demencias
primarias. Los criterios diagnósticos de demencia propuestos en el DSM-V se exponen en la tabla I.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1333]
[83] DEMENCIA Y OTROS TRASTORNOS NEURODEGENERATIVOS. ENFERMEDAD DE PARKINSON
Dentro del espectro de pérdida progresiva de funciones cognitivas encontramos un estado
intermedio entre lo que se considera el envejecimiento “fisiológico” o no patológico y la demencia: el
deterioro cognitivo leve. Se trata de una situación de pérdida de funciones cognitivas que no es lo
suficientemente severa como para requerir ayuda en la realización de las actividades básicas e
instrumentales de la vida diaria, manteniendo la independencia funcional y sin afectación significativa de la
esfera social. En mayores de 64 años la prevalencia de deterioro cognitivo leve es de un 10-20%,
tratándose de una situación que puede preceder y progresar a cualquier tipo de demencia, o mantenerse
relativamente estable a lo largo del tiempo. Los criterios para el diagnóstico de deterioro cognitivo leve
propuestos en el DSM-V se exponen en la tabla I.
2. ETIOLOGÍA
En función de la etiología las demencias pueden ser primarias o secundarias. Es importante hacer
hincapié en este segundo grupo, ya que en ocasiones subyacen causas tratables y nos encontramos ante
cuadros de demencia potencialmente reversibles (Tabla II).
3. APROXIMACIÓN DIAGNÓSTICA
El diagnóstico de demencia se basa en criterios clínicos (Tabla I), por lo que no se recomienda el
cribado en población asintomática, sino la evaluación del paciente que consulta por quejas cognitivas y/o
de conducta.
En primer lugar es necesario realizar un diagnóstico sindrómico, basado en una evaluación
sistemática a partir una detallada historia clínica, exploración sistémica, neurológica general y cognitiva.
Posteriormente se solicitarán las pruebas diagnósticas recomendadas en las guías de buena práctica clínica
para detectar entidades potencialmente tratables y establecer el diagnóstico de presunción.
1. DIAGNÓSTICO SINDRÓMICO
1.1. Historia clínica
Debe ser detallada, a ser posible por el propio paciente. No obstante, en este tipo de patología es
fundamental la información aportada por un acompañante o cuidador fiable, y siempre debe ser
contrastada en la medida de lo posible.
Es importante evaluar la comorbilidad, que ha de ser considerada como posible causa o agravante
de los síntomas. Debemos obtener información acerca de:
Antecedentes familiares de enfermedades neurodegenerativas.
Factores de riesgo cardiovascular y enfermedades previas.
Hábitos tóxicos (alcohol y drogas).
Fármacos, con especial atención a benzodiazepinas, barbitúricos, opiáceos, anticolinérgicos,
ácido valproico o litio.
Situación basal previa y el grado de repercusión de los síntomas en sus actividades habituales
de la vida diaria, funcionamiento social y laboral.
Descripción cronológica de los síntomas, con forma de inicio (aguda, subaguda, insidiosa) y
evolución (progresiva, fluctuante o estacionaria).
Preguntar acerca de problemas de memoria: olvidos frecuentes y relevantes o preguntas
reiterativas.
Abordar dificultades en otras esferas cognitivas diferentes a la memoria: lenguaje (fluencia,
presencia de parafasias y coherencia), funciones ejecutivas (planificación y secuenciación de
tareas), función visuoespacial (cálculo de distancias y orientación espacial), etc.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1334]
[83] DEMENCIA Y OTROS TRASTORNOS NEURODEGENERATIVOS. ENFERMEDAD DE PARKINSON
Preguntar acerca de síntomas neuropsiquiátricos (trastorno del ánimo, alucinaciones, ideación
delirante) y alteraciones conductuales (agresividad, desinhibición y abandono de la higiene
personal).
1.2. Exploración general
Signos de afectación cardiorrespiratoria, hepática, metabólica, etc.
1.3. Exploración neurológica sistemática
Sin olvidar los aspectos clave de una exploración sistemática, realizando especial hincapié en
funciones superiores, pares craneales, sistema motor y sensitivo, así como en la búsqueda de estigmas
parkinsonianos o signos de motoneurona, a menudo asociados a los procesos neurodegenerativos.
1.4. Test cognitivos breves
Las baterías neuropsicológicas están indicadas en los siguientes casos:
Dudas diagnósticas, sobre todo en estadios iniciales en los que el paciente o el informador
refieren cambios en el funcionamiento intelectual, pero la evaluación cognitiva grosera es
normal. Si existen dudas diagnósticas o persisten las quejas del paciente es conveniente realizar
un seguimiento longitudinal y repetir la evaluación clínica y cognitiva a los 6-12 meses.
Evaluación de pacientes con síntomas cognitivos asociados a trastornos del estado del ánimo.
Sospecha de simulación.
Seguimiento o monitorización del deterioro cognitivo en los pacientes con demencia
establecida.
El test más empleado es el Mini-Mental State Examination (ver la figura 1 del Capítulo 11), cuyo
punto de corte se establece en 24 puntos, aunque presenta ciertas limitaciones, ya que no explora todos
los dominios cognitivos y disminuye su rendimiento cuando se aplica en fases iniciales de demencia, en
demencias no corticales y en sujetos de bajo nivel sociocultural. Estas limitaciones han dado lugar a la
búsqueda de nuevas herramientas como el Montreal Cognitive Assessment (test MOCA), el test del reloj, el
Memory Impairment Screen (MIS) o el test de las fotos.
Hay que tener en cuenta que la realización de los test durante la hospitalización puede ofrecer
información limitada por los factores asociados al ingreso.
2. DIAGNÓSTICO ETIOLÓGICO
La importancia de investigar la etiología de la demencia radica en la posibilidad de tratar procesos
potencialmente reversibles, así como ofrecer el tratamiento más indicado en función de la sospecha
neuropatológica, minimizando efectos adversos y evitando tratamientos innecesarios. Las pruebas
complementarias de rutina, actualmente recomendadas por las guías de práctica clínica, son las siguientes:
Laboratorio: debe incluir hemograma, velocidad de sedimentación globular y perfil bioquímico
con glucemia, perfil renal con urea y creatinina, perfil hepático (transaminasa glutámico-
pirúvica, transaminasa glutámico oxalacética, gamma glutamil transpeptidasa, fosfatasa alcalina
y bilirrubina), electrolitos (sodio, potasio, calcio y fósforo), colesterol, vitamina B12 y hormona
estimulante de tiroides (TSH). La determinación de ácido fólico y las serologías de sífilis y de
virus de la inmunodeficiencia humana (VIH) no se realizan de rutina, sino que se individualizan
en función de la sospecha clínica, así como la determinación de metales pesados.
Neuroimagen: su utilidad radica en descartar causas potencialmente tratables (hematoma
subdural crónico, hidrocefalia a presión normal o tumores), generalmente mediante tomografía
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1335]
[83] DEMENCIA Y OTROS TRASTORNOS NEURODEGENERATIVOS. ENFERMEDAD DE PARKINSON
computarizada (TC) craneal. La resonancia magnética (RM) cerebral no está indicada de forma
habitual para el diagnóstico de demencia, pero permite valorar mejor el patrón de atrofia en
enfermedades neurodegenerativas (es utilizada como marcador de riesgo para determinadas
patologías, como la atrofia del hipocampo en la enfermedad de Alzheimer [EA]), es más
sensible que la TC craneal para detectar daño vascular y es aconsejable en cuadros clínicos con
presentación atípica.
Otras pruebas reservadas para situaciones específicas:
Punción lumbar: se recomienda ante cuadros atípicos, en casos de demencia
rápidamente progresiva o, en general, cuando se sospecha una demencia secundaria
(infección del sistema nervioso central [SNC], serología luética positiva,
inmunodepresión, sospecha de vasculitis del SNC, paraneoplásica, hidrocefalia a
presión normal...). También es recomendable en casos de demencia de inicio precoz
(menores de 55 años). Por otra parte, con el uso cada vez más extendido de los
biomarcadores en el líquido cefalorraquídeo (LCR) (proteína tau y beta-amiloide) para
el diagnóstico diferencial entre los principales procesos neurodegenerativos primarios,
esta técnica
se emplea más frecuentemente en el diagnóstico general de la demencia.
Electroencefalograma (EEG): se recomienda cuando se sospecha un estatus no
convulsivo, encefalopatía tóxico-metabólica, encefalitis o enfermedad de Creutzfeldt-
Jakob.
Tomografía por emisión de positrones/tomografía por emisión de fotón único
(PET/SPECT): se recomienda cuando existen dudas diagnósticas y también es útil como
biomarcador por imagen en el diagnóstico diferencial de las demencias primarias, ya
que muestra patrones típicos de alteración metabólica (en la PET) o de perfusión (en la
SPECT), en los distintos tipos de demencias primarias (por ejemplo alteración en la
corteza temporoparietal bilateral en la EA, en la corteza frontal en la demencia
frontotemporal, patrón multifocal asimétrico en la demencia vascular y ausencia de
alteraciones en la pseudodemencia).
Test neuropsicológicos: (ver Apartado 1.4).
Biomarcadores:
En los últimos años las líneas de investigación en demencia han ido encaminadas a
descubrir biomarcadores capaces de predecir, en fases presintomáticas, el riesgo de
enfermedad y ayudar a desenmascarar su etiopatogenia. Existen varios tipos de
biomarcadores (bioquímicos, genéticos y de neuroimagen) que en los últimos tiempos
se han introducido como parte de los criterios diagnósticos, aunque, de momento, se
encuentran limitados al ámbito experimental o de unidades especializadas.
Bioquímicos: destaca la disminución de β-amiloide 42, aumento de proteína tau
fosforilada e incremento del cociente proteína tau/amiloide en el líquido
cefalorraquídeo en la EA.
Genéticos: útiles en menores de 65 años. Se han descrito mutaciones en tres
genes, el gen de la proteína precursora del amiloide, presenilina 1 y presenilina
2, los tres en relación con agregación de β-amiloide, y por tanto en casos de
demencia tipo Alzheimer.
Neuroimagen: bien a través de los distintos patrones metabólicos y de
perfusión anteriormente señalados en pruebas de medicina nuclear, bien a
través de radiotrazadores que se unen de forma específica a fibrillas de la
proteína Aβ-amiloide presentes en las placas neuríticas de la EA (PET amiloide).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1336]
[83] DEMENCIA Y OTROS TRASTORNOS NEURODEGENERATIVOS. ENFERMEDAD DE PARKINSON
3. DIAGNÓSTICO DIFERENCIAL
En los ensayos clínicos publicados hasta el momento, la prevalencia de demencias tratables varía
entre un 7% y un 23 % del total de casos. De todas ellas, las más frecuentes son secundarias a fármacos o a
trastornos del estado de ánimo (pseudodemencia). Se exponen a continuación (Tabla III) las principales
características, por un lado de las demencias primarias y por otro de las tratables (Tabla IV).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1337]
[83] DEMENCIA Y OTROS TRASTORNOS NEURODEGENERATIVOS. ENFERMEDAD DE PARKINSON
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1338]
[83] DEMENCIA Y OTROS TRASTORNOS NEURODEGENERATIVOS. ENFERMEDAD DE PARKINSON
II. TRATAMIENTO FARMACOLÓGICO
1. TRATAMIENTO DE LOS SÍNTOMAS PRIMARIOS DE LA DEMENCIA PRIMARIA
1.1. Enfermedad de Alzheimer
Inhibidores de la acetilcolinesterasa (IACE): los IACE de uso actual son el donepezilo, la
rivastigmina y la galantamina; indicados para las formas leves-moderadas de la enfermedad.
Los tres se dosifican escalonadamente, incrementado la dosis de forma gradual. Si apareciese
algún efecto adverso se recomienda continuar el ascenso a intervalos de seis u ocho semanas
hasta alcanzar la dosis máxima que tolere el paciente, dentro de los rangos terapéuticos
establecidos. Los IACE producen una mejoría cognitiva equivalente al empeoramiento que se
produce durante 3 a 12 meses de evolución natural. Este grupo de fármacos también ha
demostrado su utilidad en la demencia por cuerpos de Lewy y en la demencia asociada a la
enfermedad de Parkinson (Tabla V), contribuyendo principalmente al manejo de los síntomas
neuropsiquiátricos asociados a estos procesos.
Memantina: se trata de un antagonista del N-metil-D-aspartato indicado en pacientes con EA
moderada a severa (Tabla V).
1.2. Demencia vascular
No existe tratamiento específico, por lo que las actuaciones deben centrarse en la prevención de la
misma, modificando hábitos de vida y con el tratamiento de los factores de riesgo. Una vez iniciado el
deterioro cognitivo, la progresión se relaciona principalmente con la recurrencia de los infartos cerebrales.
Los IACE no han demostrado beneficio en el tratamiento de estos pacientes, si bien a menudo son
utilizados en estos casos, dada la frecuente asociación entre la patología vascular y la demencia tipo
Alzheimer en las series neuropatológicas.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1339]
[83] DEMENCIA Y OTROS TRASTORNOS NEURODEGENERATIVOS. ENFERMEDAD DE PARKINSON
1.3. Demencia por cuerpos de Lewy y demencia asociada a la enfermedad de Parkinson
Está indicado el tratamiento con IACE, ayudando, entre otros, al control de las alteraciones
comportamentales.
1.4. Demencia frontotemporal
No se ha demostrado beneficio ni con los IACE ni con memantina, ocasionando incluso un
agravamiento de los síntomas neuropsiquiátricos en estos pacientes.
2. TRATAMIENTO DE LOS SÍNTOMAS SECUNDARIOS DE LA DEMENCIA
La aparición de síntomas de índole psiquiátrica superpuestos al cuadro de demencia es frecuente,
suponiendo un deterioro de la calidad de vida del paciente. Se deben investigar las causas precipitantes,
considerar modificaciones ambientales y estrategias no farmacológicas, en particular en la agitación.
Cuando sea necesaria la instauración de un tratamiento farmacológico debe realizarse con la menor dosis
posible y con un aumento lento de la misma, prestando especial atención a los efectos adversos. Una vez
controlados los síntomas se debe considerar periódicamente la disminución de la dosis o la retirada del
medicamento.
2.1. Depresión
Ocurre en un 15-20% de los pacientes con EA en algún momento de la enfermedad. Si requiere
tratamiento farmacológico, los que más evidencia clínica han demostrado son los inhibidores selectivos de
la recaptación de serotonina (ISRS), manteniéndolos como mínimo de cuatro a seis semanas para evaluar
su eficacia. Otro fármaco útil es la venlafaxina (inhibidor de la recaptación de serotonina y noradrenalina).
Los antidepresivos tricíclicos deben evitarse por su efecto anticolinérgico, así como la paroxetina, por ser el
ISRS con mayor efecto anticolinérgico.
2.2. Ansiedad
Puede acompañar a la EA, sobre todo en los estadios precoces. Pueden resultar útiles las
benzodiazepinas de forma puntual, teniendo en cuenta el posible efecto paradójico que pueden tener en
estos pacientes; o la trazodona (dosis de inicio 100-150 mg al día, repartido en tres tomas después de las
comidas o en una sola toma nocturna. Dosis de mantenimiento 200-300 mg al día, hasta un máximo de 600
mg al día).
2.3. Trastorno del comportamiento
Primero se debe investigar la existencia de factores precipitantes como malestar físico, excesiva
estimulación ambiental o ambiente inadecuado. Cuando son leves, las medidas no farmacológicas son de
elección. Si precisan tratamiento farmacológico se recomienda comenzar con ISRS. Si no fueran eficaces
estaría indicado iniciar tratamiento con antipsicóticos, siendo de elección actualmente los neurolépticos
atípicos como la quetiapina con escalada lenta. Si se necesita un tratamiento más incisivo habrá que iniciar
risperidona a bajas dosis, aunque conlleve mayor efecto parkinsonizante. En la demencia por cuerpos de
Lewy deben evitarse los neurolépticos convencionales y es de utilidad la rivastigmina (ver Capítulo 11.
“Síndrome confusional”).
2.4. Ideas delirantes
Solo deben tratarse cuando perturban de manera significativa al paciente, al cuidador o cuando
tienen un impacto claro en la calidad de vida del paciente.
2.5. Insomnio
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1340]
[83] DEMENCIA Y OTROS TRASTORNOS NEURODEGENERATIVOS. ENFERMEDAD DE PARKINSON
Se debe manejar con medidas ambientales, manteniendo al paciente despierto durante el día y
reduciendo la ingesta de líquidos a la hora de acostarse; la exposición adecuada a la luz del día puede
ayudar a restablecer el ritmo circadiano natural y mejorar el ciclo sueño-vigilia. Cuando estas medidas
fallan, deben emplearse medidas farmacológicas, existiendo únicamente escasa evidencia para la
trazodona a dosis de 50-100 mg/24 h.
3. CUIDADOS PALIATIVOS
Es importante consensuar el plan de cuidados de los estadios finales de la enfermedad con el
propio paciente y los familiares. Por ello es necesario plantear estas dudas mientras el paciente presente
capacidad de decisión. En las guías actuales se aconseja la alimentación por vía artificial (sonda
nasogástrica) solo cuando la disfagia es transitoria, estando desaconsejada cuando la disfagia o la oposición
a la alimentación son manifestaciones avanzadas de la enfermedad.
4. NUEVOS TRATAMIENTOS FARMACOLÓGICOS
En los últimos años se han puesto en marcha numerosos ensayos clínicos con el objetivo de frenar
la enfermedad actuando sobre los depósitos de tau o amiloide cerebral. Los resultados de algunos de estos
ensayos han demostrado una disminución de la carga lesional, aunque sin una repercusión clínica
acompañante.
III. OTROS TRASTORNOS NEURODEGENERATIVOS: ENFERMEDAD DE
PARKINSON
1. INTRODUCCIÓN
La enfermedad de Parkinson (EP) es una enfermedad neurodegenerativa frecuente que afecta al
1% de la población mayor de 65 años. Dentro del espectro de trastornos extrapiramidales, es importante
diferenciar el concepto de parkinsonismo, el cual engloba diferentes entidades clínicas, entre ellas la EP
idiopática que, a su vez, constituye el 80% del total de parkinsonismos.
El diagnóstico de parkinsonismo se basa en la presencia obligada de bradicinesia asociada al menos
a una de las siguientes manifestaciones: temblor de reposo, rigidez o inestabilidad postural. Una vez
establecido el diagnóstico de parkinsonismo es necesario determinar si se trata de una EP o de un
parkinsonismo atípico, entre los que destacan los parkinsonismos secundarios (ver más adelante).
La EP, que suele comenzar alrededor de los 60 años, se caracteriza por un inicio insidioso y
asimétrico, y con un empeoramiento progresivo de las manifestaciones motoras, características
diferenciales con los parkinsonismos atípicos, comentados más adelante.
2. ETIOLOGÍA
La base de la disfunción de la EP es la alteración de la aferencia dopaminérgica en la vía
nigroestriada que resulta de la degeneración de la pars compacta de la sustancia negra.
La enfermedad es, probablemente, el resultado de la interacción entre factores genéticos y
ambientales. Existen varios genes implicados identificados hasta el momento: algunos con herencia
autosómica dominante (alfa-sinucleína, LRRK2, VPS35, EIF4G1...) y otros con herencia autosómica recesiva
(DJ1, PINK1, parkina...). El componente hereditario es mayor cuando la enfermedad se desarrolla en
menores de 50 años.
3. APROXIMACIÓN DIAGNÓSTICA
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1341]
[83] DEMENCIA Y OTROS TRASTORNOS NEURODEGENERATIVOS. ENFERMEDAD DE PARKINSON
1. APROXIMACIÓN CLÍNICA Y ETIOLÓGICA
El diagnóstico de la EP es clínico y los síntomas cardinales son: bradicinesia, temblor de reposo,
rigidez e inestabilidad postural. La bradicinesia/acinesia es un criterio diagnóstico obligatorio. El inicio es
asimétrico (generalmente, primero confinado a un brazo) e insidioso con evolución progresiva a lo largo de
años. Existen determinados síntomas que pueden preceder en años al desarrollo de clínica motora, como
depresión/ansiedad, estreñimiento, anosmia y trastorno de conducta del sueño REM, etc., englobados bajo
el término de síntomas premotores de la enfermedad.
También existen criterios de exclusión de la EP que apoyan el diagnóstico de parkinsonismo atípico
o secundario: inicio simétrico, rápida progresión (dependencia grave en menos de cinco años), ausencia de
respuesta a dopamina, demencia severa y precoz, alteración postural y caídas en el primer año,
disautonomía precoz, disfunción bulbar y/o piramidalismo o afectación cortical (apraxia, alteración
sensitiva, etc.).
Dentro de los parkinsonismos secundarios es importante mencionar, por su elevada incidencia, el
atribuible a fármacos (Tabla VI). Deberemos considerar no solo el potencial parkinsonizante del fármaco,
sino también el tiempo durante el que ha sido administrado. En estos casos el parkinsonismo está
dominado por la bradi/acinesia y tiene un inicio subagudo a lo largo de varias semanas, resolviéndose
normalmente en los primeros seis meses si se interrumpe el tratamiento causante. Hay que recordar que el
parkinsonismo farmacológico puede clínicamente ser idéntico a la EP típica, por lo que ante la sospecha
diagnóstica deberemos revisar atentamente la medicación del paciente. También existen parkinsonismos
secundarios a otras etiologías (infecciosa, tóxico-metabólica o estructural) (Tabla VII).
De los parkinsonismos atípicos conviene señalar determinadas asociaciones características (Fig. 1):
Parkinsonismo vascular: alteración precoz de la marcha con marcha parkinsoniana y
“parkinsonismo de la mitad inferior del cuerpo”, factores de riesgo vascular y afectación
vascular en neuroimagen.
Parálisis supranuclear progresiva (PSP): alteración de la marcha y caídas en el primer año,
sacadas oculares verticales lentas con parálisis supranuclear de la mirada vertical, retrocollis y
disfunción frontal precoz.
Atrofia multisistema (AMS): disfunción autonómica precoz, con signos cerebelosos y
piramidales.
Degeneración corticobasal (DCB): distonía en una extremidad ± mioclonías estímulosensibles y
afectación cortical (mano “alien”, apraxia, etc).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1342]
[83] DEMENCIA Y OTROS TRASTORNOS NEURODEGENERATIVOS. ENFERMEDAD DE PARKINSON
2. PRUEBAS COMPLEMENTARIAS
El diagnóstico de EP es clínico, por lo que la mayoría de pruebas complementarias se plantean en
caso de duda diagnóstica. Algunas pruebas analíticas y de neuroimagen son necesarias para descartar un
parkinsonismo secundario.
Laboratorio: debe incluir hemograma y bioquímica (perfil renal, perfil hepático, electrolitos–
sodio, potasio, calcio y fósforo– y perfil tiroideo básico). En jóvenes es importante solicitar
ceruloplasmina en plasma y cobre en orina de 24 horas para descartar enfermedad de Wilson.
En función de la sospecha clínica y antecedentes epidemiológicos, pueden solicitarse niveles de
manganeso o carboxihemoglobina, e incluso serologías y punción lumbar si se sospecha
etiología infecciosa.
Neuroimagen (TC craneal y RM cerebral): no muestran alteraciones características en la EP. La
utilidad de la TC reside en detectar algunos parkinsonismos secundarios (hidrocefalia a presión
normal, tumores o microangiopatía isquémica). La mayor resolución de la RM cerebral permite
detectar hallazgos característicos en los parkinsonismos atípicos, tales como atrofia
mesencefálica o frontal en en la PSP, atrofia pontina y cerebelosa en la AMS o atrofia parietal
asimétrica en la DCB.
Respuesta a la levodopa (hasta un máximo de 1 g diario durante dos meses): mayor validez en
pacientes con EP avanzada y teniendo en cuenta que algunos parkinsonismos atípicos pueden
presentar alguna mejoría inicialmente.
Test olfatorio: puede detectar la anosmia como signo precoz en EP.
Test de función autonómica: estudios urodinámicos y test de hipotensión ortostática.
SPECT (DaT-SCAN): emplea un radioligando que se une selectivamente al transportador
cerebral de dopamina (DAT) en el estriado, resultando en una reducción de su captación en la
EP y en los parkinsonismos atípicos (PSP, AMS y DCB), permitiendo diferenciarlo de otras
entidades como el parkinsonismo farmacológico o del temblor esencial principalmente, en los
que la prueba no muestra anormalidades.
Ecografía-doppler transcraneal: puede detectar hiperecogenicidad de la sustancia negra del
mesencéfalo en más del 90% de los pacientes con EP.
Test genéticos: útiles en formas juveniles o con agregación familiar de EP.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1343]
[83] DEMENCIA Y OTROS TRASTORNOS NEURODEGENERATIVOS. ENFERMEDAD DE PARKINSON
IV. TRATAMIENTO
Actualmente contamos con varias opciones terapéuticas sintomáticas para la EP, tanto
farmacológicas como quirúrgicas. El objetivo a largo plazo es mejorar la calidad de vida y mantener el grado
de independencia del paciente el mayor tiempo posible.
Es por ello que la terapia debe ser multidisciplinar y asociar, además del tratamiento farmacológico,
un adecuado programa de tratamiento rehabilitador, ocupacional y en muchas ocasiones psiquiátrico y/o
psicológico.
1. TRATAMIENTO FARMACOLÓGICO (TABLA VIII)
1.1. Levodopa
Es la terapia más efectiva en cuanto a los síntomas motores se refiere. En los últimos años parece
existir un cambio de mentalidad en cuanto al momento de inicio del tratamiento con L-dopa,
aconsejándose en la actualidad no retrasar su uso si se considera necesario, siempre y cuando se mantenga
a la dosis mínima efectiva para evitar complicaciones motoras. El desarrollo de las complicaciones motoras
parece estar en relación no con el tiempo desde el inicio del tratamiento con L-dopa, sino con la evolución
intrínseca de la enfermedad. Se utiliza asociado a un inhibidor de la dopa-decarboxilasa periférica,
reduciendo así los efectos adversos, como la carbidopa (Sinemet®) o benserazida (Madopar®). Para
prolongar el efecto de este se puede asociar a los inhibidores de la catecol-o-metil-transferasa (COMT),
como entacapona (disponible como principio activo aislado o combinado con levodopa-carbidopa). No
debe suspenderse de forma brusca (ver Apartado 5.1). Como efectos adversos pueden presentar náuseas y
vómitos (normalmente desaparecen en una o dos semanas), hipotensión ortostática, alucinaciones o
somnolencia diurna.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1344]
[83] DEMENCIA Y OTROS TRASTORNOS NEURODEGENERATIVOS. ENFERMEDAD DE PARKINSON
1.2. Agonistas dopaminérgicos
Son el tratamiento más efectivo para los síntomas motores después de la levodopa, y raramente
ocasionan fluctuaciones motoras. Suelen usarse en la terapia inicial, siendo desaconsejado su uso en
pacientes con deterioro cognitivo por la aparición de alucinaciones como efecto adverso. En nuestro medio
están disponibles: el pramipexol y el ropirinol (ambos por vía oral), la rotigotina (transdérmica) y la
apomorfina (subcutánea). Es necesario vigilar la aparición de alteraciones del control de impulsos en estos
pacientes: hipersexualidad, juego patológico, trastornos alimentarios, actitudes repetitivas...
1.3. Amantadina
Con un mecanismo de acción desconocido, habitualmente se emplea para controlar discinesias en
pacientes con terapia dopaminérgica.
1.4. Inhibidores de la monoamino oxisasa B
En monoterapia o tratamiento adyuvante. A las dosis prescritas no requieren restricciones
dietéticas. Incluso asociado a ISRS muy raramente provocará una crisis serotoninérgica, si bien su uso
concomitante está contraindicado. En nuestro medio están disponibles rasagilina y selegilina.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1345]
[83] DEMENCIA Y OTROS TRASTORNOS NEURODEGENERATIVOS. ENFERMEDAD DE PARKINSON
1.5. Anticolinérgicos
Usados principalmente en pacientes jóvenes con predominio de temblor. Sus efectos adversos más
comunes son boca seca, glaucoma de ángulo agudo, estreñimiento, retención urinaria, alteración de
memoria, confusión y alucinaciones. En nuestro medio están disponibles el trihexifenidilo, la benzotropina
y la prociclidina.
2. TERAPIAS AVANZADAS
Solo están disponibles en centros de referencia y son beneficiarios de este tipo de tratamiento los
pacientes con importantes fluctuaciones motoras o con efectos adversos de la medicación inasumibles.
2.1. Terapias de infusión continua
Apomorfina (de colocación subcutánea) o levodopa-carbidopa (Duodopa®). Esta última inyecta
dopamina a través de una sonda de localización duodenal, por lo que es importante revisar el trayecto de la
sonda en pacientes con este dispositivo que presenten síntomas abdominales, aunque estos puedan
parecer banales.
2.2. Estimulación cerebral profunda
Se considera en pacientes con fluctuaciones motoras importantes no controlables con fármacos y
sin deterioro cognitivo. Por medio de electrodos de localización profunda se consigue la estimulación a
determinada frecuencia y voltaje del núcleo subtalámico o globo pálido interno (diana terapéutica escogida
en función de las características clínicas del paciente).
3. MODIFICACIONES TERAPÉUTICAS DE LAS COMPLICACIONES MOTORAS EN FASES AVANZADAS DE LA EP
Respuesta insuficiente: ocurre en pacientes que han tenido una respuesta previa adecuada a
agonistas dopaminérgicos o a L-dopa y experimentan un deterioro mantenido de su movilidad.
Es necesario descartar la existencia de factores farmacocinéticos que interfieran con la
absorción de los fármacos. Una vez descartado, la opción sería incrementar la dosis y/o
disminuir los intervalos de entre dosis.
Deterioro fin de dosis (wearing-off): aparece cuando disminuye el tiempo de beneficio
aportado por cada dosis de L-dopa, lo que se soluciona disminuyendo el intervalo entre dosis o
asociando entacapona a las dosis de levodopa.
Fenómeno on-off: consiste en periodos impredecibles de acinesia grave de inicio y final rápidos,
que duran más de 30 minutos. Son difíciles de tratar, y a menudo exigen terapias avanzadas.
Discinesias: se clasifican según su relación con la toma de L-dopa en: a) discinesias en los
“periodos on” o “pico dosis”: coreicas, son las más frecuentes y aparecen cuando las
concentraciones son más elevadas, mejorando por tanto con el descenso de la dosis; b)
discinesias bifásicas: consisten en la aparición de movimientos involuntarios que preceden o
siguen al efecto terapéutico de L-dopa y reaparecen cuando los efectos de la medicación están
en descenso; fundamentalmente en miembros inferiores y acompañados de signos de
parkinsonismo en el resto del cuerpo; suelen manifestarse como corea, pero también como
movimientos alternantes rítmicos, balismos o distonías; c) distonía en fase off: aparece en los
momentos en que los pacientes presentan signos marcados de parkinsonismo, son
especialmente frecuentes por la mañana y predominan en miembros inferiores, siendo
dolorosas; pueden mejorar administrando L-dopa de liberación retardada nocturna.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1346]
[83] DEMENCIA Y OTROS TRASTORNOS NEURODEGENERATIVOS. ENFERMEDAD DE PARKINSON
V. CONSIDERACIONES PARA EL MANEJO DE LA ENFERMEDAD DE
PARKINSON EN LA URGENCIA/HOSPITALIZACIÓN
El paciente con trastornos parkinsonianos que llega a la urgencia por complicaciones de su
enfermedad usualmente lo hace por síntomas motores (hipercinéticos o bradicinéticos) o por alteraciones
neuropsiquiátricas, exacerbados por un cambio de medicación, ya sea a la baja o al alza. Si esto ocurre, el
procedimiento más sensato es volver a la pauta de tratamiento anterior a la última modificación.
Destacamos las más importantes:
1. SÍNDROME NEUROLÉPTICO MALIGNO-LIKE (ACINESIA-HIPERPIREXIA)
Se produce ante la supresión dopaminérgica brusca por retirada del tratamiento habitual o por la
aparición de un proceso intercurrente, en algunas ocasiones banal. Se caracteriza por periodos de off
mantenidos, con elevación de la temperatura corporal y elevación de la creatín-cinasa (CK). Para evitar esta
entidad grave provocada por la retirada de la medicación es importante mantener el tratamiento,
administrándolo por sonda nasogástrica si fuese necesario. En el caso de estar desencadenada por un
proceso intercurrente puede ser refractario a la medicación
dopaminérgica y los esfuerzos deben estar encaminados a tratar la condición de base, además de continuar
con su tratamiento habitual.
Si el paciente presenta una condición que conlleva dieta absoluta (por ejemplo, intervención
quirúrgica) tendremos que sustituir el tratamiento por dosis equivalentes de rotigotina en parches (hasta
un máximo de 16 mg) o en forma de apomorfina subcutánea. Para ello es necesario calcular la dosis total
de levodopa de todo el tratamiento antiparkinsoniano (incluyendo inhibidores de la monoamino oxidasa,
agonistas, etc.) y posteriormente dividirlo por el factor de conversión correspondiente, que será 30 en el
caso de los parches de rotigotina o 10 para la apomorfina (ver Tabla IX).
2. PSICOSIS
Suele comenzar con trastornos del sueño como pesadillas, terrores nocturnos o sueños vívidos, a
los que se añaden posteriormente alucinaciones visuales, pudiendo evolucionar a un estado confusional
con rasgos paranoides. La aparición a veces coincide con cambios en la dosis de los fármacos (aumento de
dosis). Se deben buscar posibles factores desencadenantes (ver Capítulo 11. “Síndrome confusional”). Si los
síntomas son leves se intentará disminuir los fármacos añadidos a L-dopa: en primer lugar los
anticolinérgicos y si persisten continuar con la amantadina; posteriormente los agonistas dopaminérgicos
(descenso lento para no provocar un síndrome de abstinencia por retirada), siguiendo con los inhibidores
de la COMT; y por último el descenso de dosis de L-dopa. Si persisten las alucinaciones e interfieren con la
calidad de vida del paciente se añadirá un neuroléptico atípico en dosis bajas si el paciente no presenta
demencia asociada, o un IACE si presenta demencia asociada a la EP o demencia por cuerpos de Lewy (ver
sección de tratamiento de la demencia).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1347]
[83] DEMENCIA Y OTROS TRASTORNOS NEURODEGENERATIVOS. ENFERMEDAD DE PARKINSON
3. DISAUTONOMÍA
Muchos de estos pacientes pueden ser derivados al servicio de urgencias por síncopes de
repetición. En el caso de poner de manifiesto la hipotensión ortostática, esta puede ser debida a una
manifestación de la enfermedad avanzada o fruto de la medicación antiparkinsoniana (principalmente
agonistas dopaminérgicos). Para tratarla primero hemos de retirar los fármacos que puedan contribuir al
descenso de la tensión arterial e instaurar medidas conservadoras (aumento de la ingesta de sal y líquidos,
medias de compresión). Si es necesario usaremos
fármacos como fludrocortisona, midodrina, droxidopa o vasopresina, siendo de elección la domperidona
(10 mg tres veces al día) cuando la hipotensión es debida al tratamiento con agonistas dopaminérgicos.
BIBLIOGRAFÍA
Ali K, Morris HR. Parkinson’s disease: chameleons and mimics. Pract Neurol. 2015;15:14-25.
Barahona-Hernando R, Domínguez Rubio R, Romero Delgado F, et al. Diagnóstico precoz y pronóstico
de la demencia. Empleo y utilización de pruebas complementarias. Medicine. 2015;11(72):4334-9.
Edwards M, Stamelou M, Quinn N, Bhatia KP. Parkinson ́s Disease and other movement disorders.
Oxford Specialist Handbooks. 2nd ed. Nueva York: Oxford university Press; 2016.
Fox SH, Lang AE. ‘Don’t delay, start today’: delaying levodopa does not delay motor complications.
Brain. 2014;137(Pt 10):2628-30.
Langa KM, Levine DA. The diagnosis and management of mild cognitive impairment: a clinical review.
JAMA. 2014;312(23):2551-61.
López-Álvarez J, Agüera-Ortiz LF. Nuevos criterios diagnósticos de la demencia y la enfermedad de
Alzheimer: una visión desde la psicogeriatría. Psicogeriatría. 2015;5(1):3-14.
McConathy J, Sheline YI. Imaging biomarkers associated with cognitive decline: A review. Biological
Psychiatry. 2015;77:685-92.
Kuruppu DK, Matthews BR. Young-onset dementia. Semin Neurol. 2013;33(4):365-85.
Ngo J, Holroyd-Leduc JM. Systematic review of recent dementia practice guidelines. Age and Ageing.
2015;44:25-33.
Paterson RW, Takada LT, Geschwind MD. Diagnosis and treatment of rapidly progressive dementias.
Neurol Clin Pract. 2012;2(3):187-200.
Postuma RB, Berg D, Stern M, et al. MDS Clinical Diagnostic Criteria for Parkinson’s Disease. Mov
Disord. 2015;30(12):1591-9.
Rosenbloom MH, Atri A. The evaluation of rapidly progressive dementia. Neurologist. 2011;17(2):67-
74.
Schapira A. Oxford neurology Library. Parkinson ́s disease. 1st. Nueva York: Oxford university Press;
2010.
Tomlinson CL, Stowe R, Patel S. Systematic review of levodopa dose equivalency reporting in
Parkinson’s
disease. Mov Disord. 2010;25(15):2649-53.
Waters CH, editor. Diagnosis and management of Parkinson ́s disease. 6th ed. Nueva York:
Professionals
Communications; 2008.
Weingarten CP, Sundman MH, Hickey P, et al. Neuroimaging of Parkinson’s disease: Expanding views.
Neurosci Biobehav Rev. 2015;59:16-52.
Williams DR, Litvan I. Parkinsonian syndromes. Continuum. 2013;19(5):1189-212.
Wu CK, Hohler AD. Management of orthostatic hypotension in patients with Parkinson’s disease. Pract
Neurol. 2015;15:100-4.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1348]
[84] MIELOPATÍAS, NEUROPATÍAS PERIFÉRICAS Y MIOPATÍAS
84.Mielopatías, neuropatías periféricas y miopatías
Yerko-Pétar Ivánovic Barbeito.
Neurología
Diana Paredes Ruiz.
Medicina Interna
Asesora:
Cristina Domínguez González.
Médica Adjunta de Neurología
I. CONCEPTO
Se debe diferenciar entre la clínica de los síndromes medulares (sistema nervioso central, SNC), que
presentan reflejos de estiramiento muscular (REM) exaltados, respecto a los cuadros restantes periféricos,
descritos en este capítulo como neuropatías periféricas y miopatías, que manifiestan REM disminuidos. Las
quejas somáticas serán en todo caso dos: pérdida de fuerza y alteración de la sensibilidad/dolor, en el
tronco o en las extremidades, sin afectación del territorio facial*.
*Tanto en neuropatías periféricas agudas disinmunes como en miopatías puede haber afectación facial.
II. APROXIMACIÓN DIAGNÓSTICA
Se debe conocer la anatomía para entender la patología. En el caso de la exploración del sistema
nervioso, la afectación de médula, raíz, plexo, nervio periférico, unión neuromuscular o músculo, tendrá
unas características clave que seguiremos como síntomas guía.
Tras describir un diagnóstico sindrómico debemos establecer el diagnóstico topográfico (Figura 1),
para el que la exploración neurológica será clave. El diagnóstico etiológico implica el conocimiento de la
noxa que provoca la lesión a estudio (se realiza generalmente durante el ingreso del paciente con estudio
ampliado de pruebas complementarias).
Toda historia clínica debe responder a las siguientes cuestiones:
¿Es un cuadro central o periférico?
Si estamos ante un cuadro central, ¿es cerebral o medular?
Si estamos ante un cuadro periférico, ¿está afectada una raíz, nervio, unión neuromuscular o
músculo?
1. ANAMNESIS
Debe considerarse la edad, los antecedentes familiares y personales (con especial atención al riesgo
cardiovascular y a la anticoagulación, historia de traumatismos recientes, infecciones más o menos
recientes y antecedentes oncológicos, entre otros).
La patocronia es clave. La instauración brusca/abrupta de la clínica neurológica es sugerente de
etiología vascular; lo agudo no brusco sugiere etiología compresiva (medular o radicular tras esfuerzo por
tumoración o herniación discal); lo subagudo y progresivo puede implicar patología degenerativa vertebral,
enfermedad desmielinizante o tumores. Los cuadros fluctuantes son en ocasiones definitorios de patología
de la unión neuromuscular si se demuestra fatigabilidad (miastenia gravis y síndrome de Eaton Lambert). La
intolerancia al ejercicio o aparición episódica de los síntomas en relación con el esfuerzo pueden
relacionarse con miopatías metabólicas.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1349]
[84] MIELOPATÍAS, NEUROPATÍAS PERIFÉRICAS Y MIOPATÍAS
El patrón de pérdida de fuerza y/o alteración de la sensibilidad serán relevantes para determinar
la topografía de la lesión. Un trastorno de la integración sensorial (agnosia) nos indica lesión hemisférica
cerebral y nos alejará de la topografía medular/periférica; una lesión medular puede presentar disociación
de las sensibilidades primarias epicrítica y protopática (en la figura 2 se muestran las principales vías
nerviosas de la anatomía transversal medular), mientras que una lesión de la raíz, plexo o nervio siempre
afectará a ambas. Será clave también si la afectación presenta un “nivel vertical”, con afectación
hemicorporal (respetando la cara, que implicaría afectación hemiférica o troncoencefálica); o un “nivel
horizontal” (para y tetraparesia), o sigue la distribución de un dermatoma (si se afecta la raíz) o territorio de
un nervio periférico concreto. El dolor neuropático (típico de cuadros periféricos) se describe como urente,
quemante y punzante, y es raro en los cuadros centrales, salvo en los infartos talámicos donde puede
desarrollarse hiperpatía talámica. El dolor de origen talámico es fácilmente diferenciable del dolor
periférico por la afectación hemicorporal (cara y extremidades ipsi- laterales). La Tabla I recoge los
síndromes medulares y sus principales etiologías.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1350]
[84] MIELOPATÍAS, NEUROPATÍAS PERIFÉRICAS Y MIOPATÍAS
La Tabla II detalla las características de lesión en 1ª y 2ª motoneuronas.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1351]
[84] MIELOPATÍAS, NEUROPATÍAS PERIFÉRICAS Y MIOPATÍAS
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1352]
[84] MIELOPATÍAS, NEUROPATÍAS PERIFÉRICAS Y MIOPATÍAS
2. EXPLORACIÓN FÍSICA
Debe comenzarse con una exploración de rutina por aparatos y sistemas. La presencia de dolor
interfiere con la valoración real de la fuerza y la sensibilidad, algo especialmente importante en lesiones
nerviosas como las radiculopatías (ciatalgia), siendo precisa en ocasiones la analgesia previa a la
exploración. La presencia de patología osteomuscular o cutánea puede enmascarar los resultados de la
exploración, y debe considerarse en las opciones diagnósticas.
2.1. Exploración motora (Tabla III)
La afectación de la musculatura proximal y simétrica de las cuatro extremidades es sugestiva de
afectación muscular.
La debilidad proximal asimétrica monomélica orienta hacia la afectación de un plexo.
En la debilidad distal asimétrica, con monoparesia, consideramos la implicación del nervio
periférico.
La debilidad exclusivamente distal de cuatro extremidades, simétrica, orienta a una probable
polineuropatía, si bien cuando esta es asimétrica la primera posibilidad es una mononeuritis
múltiple.
Cuando la debilidad incluye la musculatura distal y la proximal de manera difusa el diagnóstico
diferencial se amplía y puede estar en relación tanto con polirradiculoneuropatías como con
miopatías.
Los músculos flexores del cuello y flexores de la cadera están afectados precozmente en la
miopatía inflamatoria y en la miastenia.
En los casos de alteración de la transmisión neuromuscular, el síntoma fundamental será la
fatigabilidad. Así, deben buscarse síntomas y signos que indiquen su presencia (aparición de
debilidad en un músculo basalmente normal, tras la repetición de una actividad): más de 10
flexiones del cuello en decúbito supino, levantarse y sentarse sin apoyo de brazos de una silla
baja (25-40 cm) más de 10 veces, mantener la mirada vertical en supraversión durante al
menos 30 segundos, etc.
El dolor muscular o mialgia es un síntoma muy frecuente e inespecífico. Sin debilidad será
excepcional que esté en relación con una enfermedad muscular primaria.
La miotonía consiste en la dificultad para relajar el músculo tras una contracción muscular
sostenida. Si se demuestra con la percusión del músculo se denomina miotonía mecánica. Es un
signo muy específico de algunas entidades y, por tanto, su presencia será clave en el
diagnóstico diferencial.
2.2. Exploración de los reflejos de estiramiento muscular (Tabla IV).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1353]
[84] MIELOPATÍAS, NEUROPATÍAS PERIFÉRICAS Y MIOPATÍAS
En las lesiones periféricas estarán disminuidos o abolidos. Típicamente esta hipo/arreflexia suele
asociarse a atrofia muscular e hipotonía, e incluso fasciculaciones como manifestación clínica de
denervación crónica.
2.3. Exploración sensitiva
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1354]
[84] MIELOPATÍAS, NEUROPATÍAS PERIFÉRICAS Y MIOPATÍAS
Cuando hay síntomas sensitivos son de gran valor localizador. Pueden presentarse como
síntomas negativos (hipo o anestesia) o como síntomas positivos (parestesias o dolor
neuropático). La distribución de la hipo o anestesia permite localizar la lesión a nivel radicular
(cuando sigue la distribución de un dermatoma) o al nivel del nervio periférico (Figura 3). Las
parestesias, sin embargo, tienen poco valor localizador, puesto que generalmente exceden del
territorio cutáneo asociado a la raíz o nervio afectado.
La radiculopatía se presenta con dolor y parestesias, que característicamente son irradiadas, y
puede asociarse a déficit sensorial en un dermatoma específico. Se agrava con Valsalva o con
los movimientos raquídeos que aumenten la tensión neural (maniobras de Lasègue y de
Bragard). Mejora con el reposo y el decúbito.
Las polineuropatías dan síntomas sensitivos distales en las cuatro extremidades, generalmente
simétricos; de naturaleza negativa (hipoestesia, hipoalgesia) o positiva (parestesias, disestesias,
alodinia, hiperalgesia), clásicamente denominados “en guante y calcetín”.
Las mononeuropatías dan síntomas sensitivos y motores según el territorio cutáneo y de los
músculos inervados por cada nervio en particular.
3. DIAGNÓSTICO TOPOGRÁFICO (VER FIGURA 1)
3.1. Lesión del sistema nervioso central (Ver Capítulo 85.“Enfermedad Cerebrovascular”)
Abarca hemisferios cerebrales, troncoencéfalo y médula espinal, mostrando como clínica motora la
debilidad piramidal (evidenciable con maniobras antigravitatorias) por afectación de 1ª motoneurona, con
hiperreflexia y reflejo cutáneo plantar extensor (Babinski). La clínica sensitiva (epicrítica, protopática,
integrada) dependerá de la localización de la lesión. La localización de ambas manifestaciones sensitivo-
motoras dependerá del nivel de la lesión.
a. Hemisferios cerebrales y troncoencéfalo
Las alteraciones hemisféricas producen habitualmente pérdida de fuerza contralateral (debilidad
piramidal o de 1ª motoneurona) y se suelen asociar a otros déficits neurológicos, como son las
alteraciones sensitivas contralaterales, del lenguaje o disfasias (en caso de localizarse en el
hemisferio dominante, habitualmente el izquierdo), agnosias (asomatognosia –no reconocimiento
de su propio cuerpo– y anosognosia –no reconocimiento de la enfermedad–) en el caso de lesiones
hemisféricas no dominantes en la región parietal, y las alteraciones visuales contralaterales
(hemianopsias y cuadrantanopsias).
La afectación troncoencefálica cursa generalmente con afectación de pares craneales, ipsilaterales
a la lesión, y con afectación contralateral de vías largas (motoras o sensitivas de extremidades). La
afectación cerebelosa es ipsilateral a la lesión; en las lesiones de los hemisferios cerebelosos tendremos la
clínica típica de dismetría, disdiadococinesia, Stewart Holmes o rebote, penduleo de extremidades y
disartria escándida, mientras que en las lesiones vermianas la clínica será predominantemente de ataxia
truncal.
Médula espinal
La médula espinal es la estructura del SNC contenida dentro del canal vertebral. Está formada
por múltiples vías ascendentes (preferencia sensitiva) y descendentes (preferencia motora) que
acaban uniéndose para dar lugar a las raíces nerviosas que conformarán los nervios periféricos
(cervicales superiores y torácicos por debajo de T2), y se reunirán en la región cervical y la
lumbosacra en plexos.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1355]
[84] MIELOPATÍAS, NEUROPATÍAS PERIFÉRICAS Y MIOPATÍAS
En primer lugar debemos conocer la anatomía medular (Figura 2), la cual presenta una distribución
más o menos homogénea a lo largo de su recorrido. Se extiende desde el foramen magno, caudal al bulbo,
hasta el nivel vertebral L1-L2, inferior al cual se encuentran el cono medular y caudal a él, las
prolongaciones de las raíces lumbo-sacras (cola de caballo). Por este motivo, toda lesión compresiva por
encima de L1-L2 va a ser causante de un síndrome medular (Tabla I), y toda lesión por debajo de ese nivel
de un síndrome de cola de caballo o de cono medular (Tabla V). La médula se divide en 8 segmentos
cervicales, 12 torácicos o dorsales, 5 lumbares, 5 sacros y uno coccígeo.
Así, la clínica va a depender de dos factores:
Topografía transversal medular de la lesión (Figura 2).
Nivel medular: las lesiones por encima de C5 provocan alteraciones sensitivo-motoras
de las 4 extremidades, las lesiones inferiores a T1 solo en los miembros inferiores y las
lesiones por encima de T6 implican un mayor riesgo de disautonomías severas. Los
reflejos cutáneo-abdominales (evocados al estimular con un objeto punzante la piel
adyacente al ombligo alejándose de este, dando lugar a un desplazamiento del mismo
por contracción de la musculatura abdominal ipsilateral) estarán presentes en lesiones
inferiores a T1. La presencia de un nivel sensorial permite establecer la localización de
la lesión (aproximadamente la mamila se corresponde con T5, el ombligo con T10 y la
región inguinal con L1: la figura 3 recoge la distribución de los dermatomas). La
indemnidad del reflejo bulbocavernoso en el hombre, o clitoridoanal en la mujer
(contracción súbita del esfínter anal al pellizcar el glande o el clítoris) indica integridad
de la vía sacra.
La mielopatía aguda es una entidad clínica grave que exige reconocimiento y tratamiento precoz,
mejorando así el pronóstico funcional del paciente. Debe ser sospechada ante todo paciente con
antecedentes de neoplasia, traumatismo, enfermedad infecciosa reciente o uso de anticoagulantes, que
refiera pérdida de fuerza, sensibilidad o alteraciones esfinterianas de instauración aguda. La Tabla VI
recoge las principales etiologías de mielopatía según su curso clínico. De manera inicial puede no
presentarse la clínica completa, por lo que estos pacientes precisan de un seguimiento clínico estrecho, con
exploraciones frecuentes dirigidas.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1356]
[84] MIELOPATÍAS, NEUROPATÍAS PERIFÉRICAS Y MIOPATÍAS
Debemos prestar atención a los siguientes cuatro puntos:
Nivel del trastorno motor (Figura 2).
Existencia de un nivel sensitivo cutáneo, si bien este puede modificarse y no ser del todo
congruente hasta establecerse completamente la lesión medular (Figura 3).
Considerar la posibilidad de abolición de reflejos en la fase de shock medular (hipo/arreflexia y
disfunción hipotónica esfinteriana), que puede tardar de horas a semanas en recuperarse,
momento en el que aparece el piramidalismo (datos de primera motoneurona).
Pérdida de tono esfinteriano anal (reflejo bulbocavernoso/clitoridoanal).
Desde el punto de vista etiológico y de manejo terapéutico podemos diferenciar entre mielopatías
compresivas y no compresivas; si bien en los dos casos puede requerirse el uso de esteroides
(dexametasona 10 mg IV en bolo al inicio y 4 mg cada 8 horas de mantenimiento) para controlar el edema
asociado. Las primeras requieren valoración por el neurocirujano u oncólogo radioterapeuta según su
naturaleza, mientras que las segundas se tratarán en función de su etiología (antibiótico, vitaminas…).
3.2. Lesión del sistema nervioso periférico
El sistema nervioso periférico comprende: raíces dorsales y ventrales, ganglio raquídeo posterior,
nervio espinal (formado por la unión ambas raíces), plexos nerviosos (formados por la unión de varios
nervios espinales) y nervio periférico.
Las manifestaciones clínicas del sistema nervioso periférico se caracterizan por síntomas motores
(hipoarreflexia, fasciculaciones, atrofia), sensitivos (incluyendo dolor) y autonómicos. Los trastornos de la
unión neuromuscular y las miopatías, en cambio, no cursan con alteraciones de la sensibilidad.
Radiculopatías
Clínicamente suelen comenzar con dolor y parestesias en el dermatoma correspondiente.
Mientras que el dolor adquiere un carácter bastante difuso, las parestesias tienen mucho más
valor localizador. Además del dolor y las parestesias puede haber trastornos objetivables
sensitivos, motores y de los reflejos (en las Tablas VII y VIII se exponen las radiculopatías
cervicales y lumbares, respectivamente).
Destacaremos la cervicobraquialgia y la lumbociatalgia por ser frecuente motivo de consulta:
Cervicobraquialgia: la espondiloartrosis y las hernias discales cervicales (C5-C6
afectando la raíz C6, o C6-C7 afectando C7) son las etiologías más frecuentes tras las
causas mecánicas. Se manifiesta con dolor cervical irradiado al hombro y al brazo, con
congruencia anatómica de la raíz afectada, en especial en los episodios paroxísticos, si
bien el valor localizador se pierde con la cronificación del proceso. La exploración
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1357]
[84] MIELOPATÍAS, NEUROPATÍAS PERIFÉRICAS Y MIOPATÍAS
motora será más fiable que la sensitiva dada la superposición de inervación cutánea de
diferentes territorios.
En caso de radiculopatía los REM se encontrarán disminuidos o abolidos. La maniobra de Spurling
con Valsalva simultáneo, inclinando ligera y lateralmente la cabeza hacia el lado afecto, con compresión
axial, puede desencadenar la clínica. En contraposición a lo anterior, la abducción del brazo afecto,
colocando la mano sobre la cabeza, alivia significativamente el dolor en caso de radiculopatía cervical. No
es infrecuente la presencia de una contractura cervical antiálgica. En el caso de hernias centrales podrá
existir compromiso medular (la hiperreflexia y el hallazgo de un signo de Hoffman –el estímulo brusco de
flexión de la falange distal del tercer dedo produce un cierre en garra– sugieren compromiso de la vía
piramidal).
La radiografía simple cervical nos ayudará en el diagnóstico, si bien los hallazgos radiológicos
pueden no correlacionarse con la gravedad de la clínica. Está indicada la realización de una resonancia
magnética (RM) si los síntomas no se resuelven en 4-6 semanas, o si existen déficits neurológicos. El estudio
electrofisiológico mediante electromiograma o electroneurograma tiene utilidad tras dos o tres semanas de
clínica neurológica franca. Se deben considerar en el diagnóstico diferencial causas neurológicas no
radiculares (zóster, atrapamiento de nervios periféricos, traumatismos, síndrome de dolor regional
complejo), causas osteomusculares como patología del manguito de los rotadores o epicondilitis y causas
vasculares. El tratamiento debe reunir medidas farmacológicas (paracetamol, antiinflamatorios no
esteroideos [AINE], tramadol, miorrelajantes) y físicas (educación postural y rehabilitación), al menos de
cuatro a seis semanas, salvo la aparición de déficits neurológicos.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1358]
[84] MIELOPATÍAS, NEUROPATÍAS PERIFÉRICAS Y MIOPATÍAS
Lumbociatalgia (ver Capítulo 12. “Lumbalgia”): su etiología más frecuente son las
hernias discales posterolaterales, por este orden: L5-S1 (comprometiendo la raíz S1),
L4-L5 (raíz L5) y L3-L4 (raíz L4). Los cambios espondilóticos lumbares también pueden
provocar compresión radicular. El dolor empeora con la actividad física, Valsalva y
flexión anterior del tronco (a diferencia de la estenosis de canal lumbar) y se irradia por
la cara posterolateral de la pierna. La maniobra de Lasègue/Lazarevic flexionando
pasivamente la cadera en decúbito, con el miembro inferior en extensión de rodilla y
tobillo a 90º, puede reproducir el dolor referido desde los 30º a 70º. La maniobra de
Bragard aumenta la tensión neural al hacer flexión dorsal pasiva del tobillo, sobre el
Lasègue. Si existe compromiso radicular los REM se encontrarán abolidos o
disminuidos, y existirá un déficit para la marcha de talones (si se afecta la raíz L5) o
puntillas (S1 afectada). El signo de Patrick diferencia la artropatía de cadera y se realiza
con rotación externa de cadera, con flexión en rodilla y con el muslo flexionado sobre la
cadera, lo que desencadenaría dolor, especialmente en la región inguinal.
El tratamiento debe reunir medidas farmacológicas (paracetamol, AINE, tramadol y miorrelajantes)
y físicas, evitando el reposo absoluto, siendo clave la movilización. Debe solicitarse una RM y valoración por
especialista si existen déficits neurológicos o ausencia de mejoría tras 4-6 semanas de tratamiento
conservador optimizado. El uso de corticoides puede ser de interés en cuadros de dolor incoercible. La
cirugía se reserva para casos donde el dolor no responde al tratamiento conservador o en casos con déficit
neurológico grave (síndrome de cola de caballo).
Plexopatías
Se producen por la lesión de varios nervios espinales. Pueden afectar a la región cervical baja
(C5-T1 o plexo braquial) o a la región lumbar y sacra (L1-S4 o plexo lumbosacro), afectando a
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1359]
[84] MIELOPATÍAS, NEUROPATÍAS PERIFÉRICAS Y MIOPATÍAS
los miembros superiores e inferiores respectivamente. Es clínicamente difícil de distinguir de la
lesión de múltiples raíces.
Neuropatías
Existen varias formas clínicas: las mononeuropatías y las polineuropatías.
Mononeuropatías: consisten en la lesión o disfunción de un único nervio periférico. Las
más frecuentes son las neuropatías por atrapamiento; las más habituales se recogen en
la tabla IX. Ocurren en estructuras anatómicas donde el nervio es más susceptible a la
compresión. Inicialmente se manifiestan con dolor y parestesias, pudiendo evolucionar
a debilidad, y en los casos más avanzados a atrofia muscular. La mononeuropatía
múltiple (multineuritis) consiste en la afectación sucesiva y asimétrica de nervios
periféricos, siendo la vasculitis la etiología más frecuente a considerar.
Polineuropatías: se caracterizan por una combinación variable de alteraciones de tipo
sensitivo, motor o autonómico debido a una afectación bilateral y simétrica de los
nervios periféricos, con mayor afectación clínica distal (manos y pies). Se asocian a
procesos metabólicos del tipo diabetes mellitus, alcoholismo e insuficiencia renal, entre
otras, pudiendo suceder de manera aguda en procesos inflamatorios/infecciosos
sistémicos.
3.3. Unión neuromuscular
Las enfermedades de la placa motora producen pérdida de fuerza pura, sin afectación sensitiva. La
más característica es la miastenia, y destaca la fluctuación de los síntomas con fenómeno de fatigabilidad.
3.4. Miopatías (Tabla X)
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1360]
[84] MIELOPATÍAS, NEUROPATÍAS PERIFÉRICAS Y MIOPATÍAS
Se produce una pérdida de fuerza progresiva, rara vez aguda (salvo algunas miopatías tóxicas), de
predominio proximal en cintura escapular o pelviana (muestran generalmente signo de Gowers, al trepar
sobre su cuerpo el paciente para pasar del decúbito a la bipedestación). En ningún caso se acompaña de
pérdida de sensibilidad o alteración autonómica, si bien pueden aparecer mialgias espontáneas o a la
palpación. Los REM sí pueden encontrarse hiporreactivos o abolidos si la debilidad es intensa.
III. ENTIDADES CLÍNICAS
1. SÍNDROME DE GUILLAIN-BARRÉ
1.1. Concepto
El epónimo síndrome de Guillain-Barré (SGB) se emplea para describir un gran grupo de
polirradiculoneuropatías inmunomediadas. El SGB clásico, también denominado polirradiculoneuropatía
desmielinizante inflamatoria aguda (AIDP, por sus siglas en inglés), es la forma más frecuente (85-90% en
nuestro medio). Su clínica principal es una debilidad progresiva, de inicio distal y en los miembros
inferiores, pudiendo progresar a una tetraplejía flácida e insuficiencia respiratoria. En el 50-70% de los
casos se encuentra un antecedente infeccioso, más frecuentemente respiratorio o gastrointestinal, entre
una y cuatro semanas antes del inicio de los síntomas neurológicos. Entre los microorganismos más
frecuentemente asociados encontramos el Campylobacter jejuni, citomegalovirus, virus de Epstein Barr y
Mycoplasma pneumoniae. Asimismo, el virus de la inmunodeficiencia humana (VIH) puede provocar un SGB
como manifestación de primoinfección. Existen formas distintas a la AIDP: neuropatía axonal motora aguda
(AMAN), neuropatía axonal sensitivo-motora aguda (AMSAN), síndrome Miller-Fisher o encefalitis de
Bickerstaff, entre otros. La fisiopatogenia se basa en una reacción autoinmune secundaria a reacciones
cruzadas (agente infeccioso-estructuras propias del SN), con formación de anticuerpos por parte de los
linfocitos contra epítopos de la mielina o axones. Si bien la forma más frecuente de SGB es desmielinizante
(AIDP), las formas axonales (AMAN, AMSAN), que pueden conservar los reflejos, tienen mucho peor
pronóstico, siendo el Campylobacter jejuni el agente infeccioso más frecuentemente implicado en estos
cuadros.
1.2. Clínica
Los primeros síntomas pueden ser un dolor lumbar intenso de perfil radicular (radiculitis inicial).
Posteriormente aparecen parestesias (“hormigueos”) en la planta de los pies y debilidad de inicio distal en
los miembros inferiores, simétrica y ascendente en el transcurso de horas o días, que podrá llegar a afectar
a los miembros superiores. Asociado a ello, se van perdiendo los REM de distal a proximal (primero los
aquíleos).
La severidad y progresión de la pérdida de fuerza es variable, pero una vez el paciente pierde la
deambulación se debe vigilar el compromiso de la musculatura respiratoria, instaurando si precisa
ventilación mecánica. El síndrome de Miller-Fisher es una variante de SGB que presenta oftalmoplejía y
ataxia, con afectación motora de pares craneales y sensitiva de extremidades.
1.3. Diagnóstico (Tabla XI)
En el diagnóstico diferencial se deben incluir otras entidades que pueden producir una tetraparesia
progresiva como: el déficit agudo severo de vitamina B1, la intoxicación por arsénico, n-hexano
(esnifadores de pegamento), vasculitis, enfermedad de Lyme, porfirias, sarcoidosis, síndromes
paraneoplásicos, miopatías agudas, mielitis transversas, polineuropatía del enfermo crítico o patología de la
unión neuromuscular.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1361]
[84] MIELOPATÍAS, NEUROPATÍAS PERIFÉRICAS Y MIOPATÍAS
El diagnóstico de presunción se hace a través de la historia clínica y la exploración neurológica,
apoyándose en las siguientes pruebas complementarias:
Punción lumbar: se evidencia un aumento de proteínas en el líquido cefalorraquídeo (0,45 a
2,0 g/l) sin aumento de celularidad, que suele ser menor a 10 cél/mm3 (hiperproteinorraquia
sin pleocitosis). Esta disociación albúmino-citológica aparece desde los 7 días de inicio del
cuadro en el 50-66% de los casos, y en más del 75% desde la tercera semana. En el caso de más
de 15 cél/mm3 debe descartarte infección por el VIH.
Estudios neurofisiológicos: aportan información diagnóstica (formas axonales y
desmielinizantes, motoras y sensitivas) y pronóstica. En los primeros días no muestran
alteraciones evidentes. La onda F (mide conducciones motoras proximales) puede encontrarse
prolongada a partir de los tres días del inicio de la clínica.
Inmunología: la determinación de anticuerpos antigangliósido, si son positivos, ayuda a
establecer el origen disinmune de una polineuropatía, y en algunos casos a diferenciar subtipos.
1.4. Tratamiento
Soporte vital: monitorización cardiaca y de constantes vitales (temperatura, tensión arterial,
saturación de O2, Peak flow) para valoración de la disautonomía y datos de afectación
ventilatoria (un 30% de los pacientes precisan ventilación mecánica). Ante cualquier indicio de
fallo respiratorio (peak flow < 200 ml; debilidad en flexión musculatura cervical en decúbito
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1362]
[84] MIELOPATÍAS, NEUROPATÍAS PERIFÉRICAS Y MIOPATÍAS
supino) está indicada la vigilancia en la Unidad de Cuidados Intensivos (UCI). Para el manejo de
la hipertensión arterial y taquicardia pueden ser necesarias grandes dosis de antihipertensivos
y betabloqueantes (labetalol, esmolol, nitroprusiato).
Tratamiento específico: se realiza cuando el paciente pierde la deambulación autónoma o
presenta dificultad respiratoria. Consiste en administración de inmunoglobulinas intravenosas
(2 g por kg de peso repartidos entre tres y cinco días), siendo la plasmaféresis equivalente
según un metanálisis de 2014 (Hughes et al). Es conveniente la cuantificación de los niveles de
IgA antes de iniciar el tratamiento para evitar reacciones alérgicas en pacientes con
agammaglobulinemia A.
Otras medidas: se debe realizar tromboprofilaxis mientras el paciente no deambule e iniciar la
rehabilitación de forma precoz (las ortesis pueden ser útiles para prevenir retracciones
aquíleas).
1.5. Evolución y pronóstico
En la evolución suele existir un empeoramiento progresivo las dos semanas iniciales, tras las cuales
sigue un proceso de estabilización y posterior mejoría en unas 4 semanas desde el inicio de la clínica,
quedando déficits importantes en un 10% de los casos. El mal pronóstico vital está relacionado con las
alteraciones autonómicas y la necesidad de intubación. El pronóstico a medio-largo plazo dependerá de la
gravedad de la debilidad, la velocidad de instauración de la clínica y la evolución en las primeras semanas.
2. MIASTENIA GRAVIS
2.1. Concepto
La miastenia gravis (MG) es un trastorno autoinmune debido a la existencia de anticuerpos
circulantes que bloquean la transmisión neuromuscular a nivel postsináptico, impidiendo la correcta
contracción muscular y provocando el fenómeno característico de fatigabilidad.
2.2. Clínica
Se caracteriza por un cuadro fluctuante de debilidad y fatigabilidad (aparece con la actividad y
mejora con el reposo), con empeoramiento vespertino, de preferencia proximal, conservando reacciones
pupilares, sensibilidad y reflejos. En la mayoría de los pacientes (> 60%) los síntomas iniciales afectan a los
músculos oculares en forma de ptosis y diplopía intermitente, si bien la mitad de estos desarrollarán
posteriormente miastenia generalizada. El comienzo en forma de afectación bulbar o afectación exclusiva
de extremidades aparece en torno al 15% y 5% respectivamente.
Las maniobras que fatigan grupos musculares específicos pueden ser de gran utilidad para
reproducir la clínica: hacer que el paciente mantenga la mirada elevada durante 30 segundos puede
provocar ptosis y posterior diplopía al explorar las versiones de la mirada; hacer que cuente hasta 30 sin
descanso en voz alta puede provocar disartria o disfonía.
2.3. Diagnóstico
Test del hielo: con un 80% de sensibilidad, consiste en mejorar la transmisión de la unión
neuromuscular por la disminución de la temperatura. Se aplica en las formas oculares, con la
colocación de hielo (dentro de guante de exploración) sobre el párpado superior, durante dos
minutos. Al retirarlo, se explora inmediatamente la motricidad ocular y la ptosis.
Test de edrofonio (Anticude®): inhibidor de la enzima acetilcolinesterasa que degrada la
acetilcolina de la hendidura sináptica, con la consecuente mayor activación de los receptores
musculares y desaparición rápida de la clínica miasténica, principalmente la ocular. Hace efecto
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1363]
[84] MIELOPATÍAS, NEUROPATÍAS PERIFÉRICAS Y MIOPATÍAS
en 30 segundos y su vida media es corta (5-10 minutos), por lo que su efecto es transitorio. Se
debe evitar en caso de enfermedad cardiaca y bronquial. La bradicardia grave y el síncope son
efectos posibles, por lo que se debe disponer de monitorización cardiaca y atropina como
antídoto. Es posible que esta prueba no esté disponible en breve en España por agotarse la
producción del edrofonio.
Determinación de anticuerpos contra el receptor de la acetilcolina (Ac AChR): la presencia de
anticuerpos en un paciente con un cuadro clínico compatible confirma el diagnóstico, pero su
ausencia no lo excluye. Se detectan hasta en el 80-90% de los pacientes con MG generalizada,
pero solo en un 40-55% de los que presentan síntomas exclusivamente oculares. La ausencia de
timoma y Ac AChR negativos tienen un valor predictivo negativo del 99,7%. Existen otros
anticuerpos relacionados con la enfermedad, como son los antiMuSK, que aparecen en el 38-
50% de las miastenias generalizadas con Ac AChR negativos, y se asocian con formas de
presentación atípicas.
Pruebas electrofisiológicas: con una sensibilidad del 75-95%, la estimulación nerviosa
repetitiva a bajas frecuencias (2 a 3 Hz) produce un decremento progresivo de la amplitud de
los potenciales evocados musculares. Presenta una alta rentabilidad en músculos proximales,
como el trapecio, orbicular de los ojos o deltoides. La electromiografía de fibra aislada, con una
sensibilidad en torno al 90%, produce un aumento del Jitter (retraso o ausencia de contracción
muscular tras estimulación del nervio).
Otras pruebas: es obligado realizar una tomografía computarizada torácica para valorar la
presencia de patología tímica, que desempeña un importante papel en la génesis de la
respuesta inmune, siendo anormal hasta en el 75% de los pacientes (85% hiperplasia tímica;
15% timoma). Se recomienda estudio de función tiroidea y autoinmunidad por su asociación
con hipertiroidismo (3-8% de los casos) y otras enfermedades autoinmunes (lupus eritematoso
sistémico y artritis reumatoide).
2.4. Tratamiento
Existen cuatro modalidades de tratamiento: 1) sintomático; 2) inmunosupresor; 3)
inmunomodulador de acción rápida; y 4) quirúrgico (timectomía). Sobre estas modalidades el tratamiento
debe ser individualizado según el grado (ocular frente a generalizado) y la severidad de la MG. Debe
prestarse atención en la prescripción de ciertos medicamentos que pueden exacerbar los síntomas de la
MG: benzodiazepinas, betabloqueantes, calcioantagonistas y aminoglucósidos, entre otros.
Inhibidores de la colinesterasa (sintomático): el bromuro de piridostigmina (Mestinón®) es el
de uso más habitual. La dosis inicial en adultos es de entre 30 y 60 mg, pudiendo administrarse
cada cuatro horas si fuera necesario. Los efectos secundarios más frecuentes son las molestias
gastrointestinales, las náuseas, los vómitos, la diarrea, la sudoración y el aumento de
secreciones bronquiales y bradicardia.
Corticoesteroides (inmunosupresor): principalmente la prednisona. Está indicado cuando los
síntomas generalizados u oculares no están suficientemente controlados con los inhibidores de
la colinesterasa. Habitualmente se inicia a dosis elevadas (entre 1 y 1,5 mg/kg/ día) durante
varios meses. Inicialmente pueden producir un empeoramiento transitorio de la debilidad
que incluso requiera ingreso y control de la función respiratoria.
Inmunosupresores ahorradores de corticoides: necesarios cuando son imprescindibles dosis
altas de corticoides para controlar los síntomas. Tardan varios meses en comenzar el efecto. La
azatioprina es el más utilizado, pero puede tardar hasta seis meses en hacer efecto; también se
emplean el micofenolato mofetil y la ciclosporina, esta última de acción más rápida. Las
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1364]
[84] MIELOPATÍAS, NEUROPATÍAS PERIFÉRICAS Y MIOPATÍAS
terapias biológicas como el rituximab se reservan para casos refractarios a la terapia
inmunomoduladora optimizada.
Inmunoglobulinas/plasmaféresis (inmunomodulador de acción rápida): indicadas en la crisis
miasténica, pretimectomía o como terapia puente hasta conseguir el efecto de los
inmunomoduladores crónicos. Existen distintas pautas de administración de inmunoglobulinas
intravenosas (IgIV), siendo las más utilizadas dosis de 2 g/kg repartidos en tres a cinco días en
las agudizaciones, y 1 g/kg al mes como mantenimiento. La plasmaféresis se realiza en cinco
ciclos (3-5 litros en cada sesión) en 7-14 días. Ambas son igual de efectivas, aunque se prefieren
las IgIV por su mejor perfil de efectos adversos.
Timectomía: se realiza siempre que haya timoma o en pacientes entre los 15 y 60 años con
miastenia generalizada seropositiva sin buen control clínico a pesar del tratamiento. Según
recomendaciones de expertos debe realizarse en los tres primeros años tras el inicio de la
clínica. El beneficio máximo se obtiene con la exéresis de un timoma (menos claro en el caso de
hiperplasia tímica), si bien la mejoría puede observarse incluso años después de la intervención.
2.5. Manejo en situaciones especiales
Crisis miasténica: es una exacerbación aguda de la MG lo bastante grave como para requerir
soporte ventilatorio. Sus principales indicativos son la debilidad de la musculatura cervical y un
peak flow inferior a 200 l/min. Como factor desencadenante podemos encontrar una infección,
intervenciones quirúrgicas, empeoramiento inducido por corticoides o exposición a
determinados fármacos. El tratamiento debe hacerse en una UCI, con asistencia ventilatoria.
Están indicadas las IgIV (2 g/kg repartidos en tres a cinco días) o plasmaféresis.
Crisis colinérgica: una administración excesiva de inhibidores de la colinesterasa puede
incrementar la debilidad. La presencia de signos de hiperactividad colinérgica, como salivación
excesiva, fasciculaciones, aumento de las secreciones bronquiales y calambres abdominales,
contribuirá al diagnóstico diferencial de una crisis miasténica. Debe retirarse la medicación
durante dos o tres días y reintroducirla posteriormente a dosis más bajas.
Embarazo: en general, la miastenia suele empeorar en el primer trimestre del embarazo y las
tres a cuatro primeras semanas posparto. Se han empleado con seguridad los corticoides, Ig o
plasmaféresis. No deben usarse dosis excesivas de inhibidores de la colinesterasa, ya que
pueden inducir contracciones uterinas. Deben evitarse los inmunosupresores por su potencial
teratogénico.
Cirugía: antes de cualquier procedimiento quirúrgico debe asegurarse que el paciente está bien
controlado clínicamente. En caso de empeoramiento posterior, se reajustará su medicación.
Durante la intervención quirúrgica se evitarán los bloqueantes neuromusculares.
Bajo nivel de consciencia: no existen formulaciones intravenosas para los inhibidores de la
colinesterasa. Si fuera necesario, se podrán administrar por vía intramuscular o por sonda
nasogástrica.
3. BOTULISMO
Está causado por una toxina producida por Clostridium botulinum que actúa inhibiendo la liberación
de acetilcolina en las terminaciones nerviosas periféricas a nivel presináptico. En los adultos la toxina se
ingiere con los alimentos contaminados, generalmente conservas. La clínica comienza a las 12-48 horas de
la ingesta con síntomas digestivos (dolor abdominal, náuseas y vómitos). Posteriormente aparecen los
síntomas anticolinérgicos (xerostomía, oftalmoplejía, midriasis arreactiva, visión borrosa por alteración de
la acomodación), junto con afectación motora (parálisis flácida descendente y simétrica, ptosis, diplopía,
disfagia). La debilidad de la musculatura oculomotora es precoz, y descendente, desde craneal a caudal, al
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1365]
[84] MIELOPATÍAS, NEUROPATÍAS PERIFÉRICAS Y MIOPATÍAS
contrario que en el SGB. Finalmente la debilidad se generaliza y produce una insuficiencia respiratoria. El
tratamiento comprende lavado gástrico, medidas de mantenimiento y antitoxina botulínica (antitoxina
bivalente A-B equina, un vial, 250 ml IV). En niños no se emplea la antitoxina equina, se trata con Ig humana
antitoxina botulínica (50 mg/kg en una sola dosis, administrada en los 7 días siguientes al comienzo d e la
clínica).
BIBLIOGRAFÍA
Camacho Salas A, González de la Aleja Tejera J, Sepulveda JM. Urgencias en neurología. Hospital
Universitario 12 de Octubre. 2.ª ed. Madrid: Ergon; 2013.
Chamberlain MC. Neoplastic myelopathies. Continuum (Minneap Minn). 2015;21(1 Spinal Cord
Disorders):132-45. 1.
Cho TA. Spinal cord functional anatomy. Contin Lifelong Learn Neurol [Internet]. 2015;21(1 Spinal Cord
Disorders). Disponible en:
http://journals.lww.com/continuum/Fulltext/2015/02000/Spinal_Cord_Functional_ Anatomy.6.aspx
Daroff RB, Jankovic J, Mazziotta JC, Pomeroy SL. Bradley’s neurology in clinical practice. Vol 2. 7th ed.
Elsevier; 2016.
Greenberg BM, Frohman EM. Immune-mediated myelopathies. Continuum (NY). 2015;21(1):121-31.
Hughes RA, Swan AV, van Doorn PA. Intravenous immunoglobulin for Guillain-Barré syndrome.
Cochrane Database Syst Rev. 2014:CD002063.
Lewis SL. Disorders that strike a cord. Continuum (Minneap Minn). 2015;21(1 Spinal Cord
Disorders):11-2.
Tavee JO, Levin KH. Myelopathy due to degenerative and structural spine diseases. Continuum
(Minneap Minn). 2015;21(1 Spinal Cord Disorders):52-66.
Tarulli AW. Disorders of the cauda equina. Continuum (Minneap Minn). 2015;21(1 Spinal Cord
Disorders):146-58.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1366]
[85] ENFERMEDAD CEREBROVASCULAR
85.Enfermedad cerebrovascular
Sara Vila Bedmar.
Neurología
Ana María Castaño León.
Neurocirugía
Ángel Torralba Morón.
Medicina Interna
Asesores:
Jaime Díaz Guzmán.
Médico Adjunto de Neurología.Unidad de Ictus
Luis Jiménez Roldán.
Médico Adjunto de Neurocirugía
I. ICTUS ISQUÉMICO
1. APROXIMACIÓN DIAGNÓSTICA Y TERAPÉUTICA INICIAL
1. CONCEPTO
El término ictus (golpe, en latín) describe el carácter brusco y súbito del cuadro clínico debido a una
alteración del flujo sanguíneo cerebral. Se clasifica en ictus isquémico y hemorrágico, en función de la
naturaleza de la lesión.
Por otro lado, en función de la duración de la sintomatología se distingue entre accidente
isquémico transitorio (AIT) e ictus establecido. El AIT se define como un breve episodio de disfunción
neurológica causado por isquemia focal cerebral o retiniana, en la que los síntomas clínicos duran menos
de una hora y no hay evidencia en la neuroimagen de infarto agudo cerebral. El ictus establecido se
produce cuando la isquemia cerebral es lo suficientemente prolongada en el tiempo como para producir un
área de necrosis tisular.
2. FISIOPATOLOGÍA
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1367]
[85] ENFERMEDAD CEREBROVASCULAR
La fisiopatología del ictus isquémico es un proceso complejo que incluye una cascada de
alteraciones bioquímicas que comienzan tan solo unos 15 segundos después de iniciarse la hipoperfusión
cerebral. En ausencia de flujo sanguíneo cerebral se estima que cada minuto se pierden del orden de
2.000.000 neuronas. El concepto de área de penumbra isquémica se refiere a aquellas regiones cerebrales
que, a pesar de haber sido sometidas a un descenso relativo del flujo sanguíneo cerebral, mantienen aún la
viabilidad neuronal y son, por tanto, recuperables. Las características fisiopatológicas del ictus isquémico
dependen de varios factores, entre los que destacan el mecanismo y el tamaño del mismo y el estado de la
circulación colateral. Esto se explica debido a que el sistema de colaterales arteriales puede garantizar en
algunos casos un flujo sanguíneo cerebral mínimo que prolongue un estado de penumbra reversible en la
fase aguda de un ictus isquémico. Los tres principales sistemas de colaterales son las ramas de ambas
arterias carótidas (interna y externa) que comunican la circulación extra e intracraneal, el sistema de vasos
comunicantes del polígono de Willis y las arterias leptomeníngeas, capaces de garantizar en parte una
irrigación retrógrada (Figura 1).
3. ETIOLOGÍA. CLASIFICACIÓN SEGÚN MECANISMO ETIOPATOGÉNICO
Infarto aterotrombótico. Ateroesclerosis de arteria grande extra o intracraneal. Infarto
generalmente de tamaño medio-grande, de topografía cortical o subcortical y localización
carotídea o vertebrobasilar (Tabla I). El mecanismo último del infarto puede ser, a su vez:
Trombótico: oclusión in situ intravascular.
Embólico, en forma de embolia arterio-arterial desde la placa de ateroma (por ejemplo
de arteria carótida interna a cerebral media).
Hemodinámico, en casos de estenosis hemodinámicamente significativas responsables
de una hipoperfusión cerebral, hecho que se favorece en situaciones de bajo gasto (por
ejemplo hipotensión arterial, bradicardia). En estos casos los infartos suelen localizarse
en los denominados “territorios frontera” (Tabla II). Su diagnóstico requiere cumplir
alguno de los criterios siguientes, en ausencia de otra etiología:
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1368]
[85] ENFERMEDAD CEREBROVASCULAR
Presencia de ateroesclerosis clínicamente generalizada (cardiopatía isquémica
o enfermedad arterial periférica).
Ateroesclerosis con estenosis mayor o igual al 50%, de la arteria extracraneal o
intracraneal de gran calibre correspondiente a la localización del ictus, en
ausencia de otra etiología.
Ateroesclerosis con estenosis inferior al 50% en la arteria extracraneal o
intracraneal de gran calibre correspondiente a la localización del ictus, en
ausencia de otra etiología y en presencia de al menos dos de los siguientes
factores de riesgo cardiovascular (FRCV): edad superior a 50 años, hipertensión
arterial (HTA), diabetes mellitus, tabaquismo o hipercolesterolemia.
Infarto cardioembólico. Infarto generalmente de tamaño medio-grande, de topografía cortical
y en el que se evidencia una cardiopatía estructural y/o arritmia de carácter potencialmente
embolígeno. Presenta características clínicas propias (Tabla III). Se debe sospechar en ausencia
de otra etiología y con presencia de alguna de las siguientes cardiopatías embolígenas:
fibrilación auricular crónica o paroxística, trombo o tumor intracardiaco, estenosis mitral
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1369]
[85] ENFERMEDAD CEREBROVASCULAR
reumática, prótesis mecánica (mitral > aórtica), endocarditis, enfermedad del nodo sinusal,
infarto agudo de miocardio (IAM) reciente (< 3 meses), aneurisma ventricular izquierdo o
acinesia después de un IAM, hipocinesia o discinesia cardiaca global, miocardiopatía dilatada
con fracción de eyección del ventrículo izquierdo < 35%.
Infarto lacunar. Enfermedad oclusiva de pequeño vaso arterial. Infarto de pequeño tamaño en
el territorio de una arteria perforante cerebral que suele ocasionar clínicamente un síndrome
lacunar. Estos infartos se definen por la ausencia de clínica cortical: desviación oculocefálica,
hemianopsia, afasia, negligencia, etc. (Tabla IV). La causa más importante es la
microateromatosis favorecida por la hipertensión arterial de larga evolución y/o mal
controlada. Otras causas menos frecuentes son la embolígena, arteriopatías inflamatorias o no
inflamatorias y los tóxicos.
Infarto cerebral de causa inhabitual. Infarto de cualquier tamaño, características y localización
secundario a una causa diferente a la aterotrombótica, cardioembólica y lacunar. Son más
frecuentes en niños y adultos jóvenes. Las causas poco frecuentes de ictus isquémico pueden
clasificarse en varios subgrupos etiológicos (Tabla V). La disección de la arteria carótida es una
de las vasculopatías no ateroescleróticas que más frecuentemente provocan ictus en adultos
jóvenes. Es típico en los segmentos extracraneales de la arteria carótida interna. La causa
puede ser espontánea, traumática o en relación con enfermedades como la displasia
fibromuscular, la neurofibromatosis o los síndromes de Marfan o Ehlers-Danlos. La tríada
clásica, presente solo en un tercio de los casos, incluye síndrome de Horner, carotidinia y
focalidad neurológica cerebral o retiniana (por trombos liberados desde la pared disecada). En
las disecciones de la arteria vertebral el dolor se localiza en la parte posterior del cuello. En un
10-20% de los casos existe afectación de varios vasos.
Infarto cerebral de causa indeterminada. Son aquellos infartos en los que tras un adecuado
estudio diagnóstico no se ha identificado una causa responsable (“criptogénico”) o aquellos en
los que coexiste más de una etiología. Se están desarrollando clasificaciones etiológicas que
permiten ponderar cada una de las posibles causas que concurren en un mismo paciente, de
cara a establecer un marco probabilístico de la etiología del ictus (definida, probable, posible).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1370]
[85] ENFERMEDAD CEREBROVASCULAR
4. CLÍNICA
La presentación clínica de un ictus isquémico depende del territorio vascular afectado y del
mecanismo del ictus (Tablas I a IV). La clasificación más empleada del ictus isquémico desde un punto de
vista clínico-topográfico es la propuesta a partir del Oxfordshire Community Project, distinguiéndose: 1)
infarto completo de la circulación anterior (TACI); 2) infarto parcial de la circulación anterior (PACI); 3)
infarto lacunar (LACI); y 4) infarto de circulación posterior (POCI).
5. DIAGNÓSTICO
Como norma general aquellos pacientes de cualquier edad, con un déficit neurológico focal agudo
de naturaleza vascular, de menos de seis horas de evolución y situación previa de independencia (o
dependencia leve de causa no neurológica), deben ser considerados y manejados como código ictus* por el
Servicio de Neurología.
*Código ictus: protocolo de actuación en aquellos pacientes con sospecha de ictus isquémico en los que por tiempo de evolución se
podría administrar a priori un tratamiento recanalizador (fibrinólisis intravenosa y/o tratamiento endovascular). Para que se active un código ictus
deben cumplirse los siguientes criterios: 1) déficit neurológico focal; 2) tiempo de evolución inferior o igual a ocho horas (salvo que se sospeche
territorio vertebrobasilar, donde se permiten hasta 12 horas); y 3) paciente previamente independiente o parcialmente dependiente por causa no
neurológica: puntuación en escala de Rankin de 0-3 (ver tratamiento).
5.1 Anamnesis
En un paciente que acude o es llevado a urgencias con motivo de síntomas neurológicos de inicio
súbito es obligado determinar con certeza la hora de inicio de los mismos, o en su defecto la hora en la que
fue visto por última vez asintomático, a través del paciente y de sus familiares o testigos del cuadro. Se
debe intentar dilucidar, en la medida de lo posible, la naturaleza de los síntomas: forma de inicio, síntomas
previos, secuencia de aparición, etc., así como la situación basal física y cognitiva del paciente.
5.2. Exploración física
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1371]
[85] ENFERMEDAD CEREBROVASCULAR
Lo primero a valorar es el nivel de consciencia del paciente y, si está deteriorado, asegurar el
control de la vía aérea y la estabilidad hemodinámica (valoración conjunta si es preciso con la UCI).
Inicialmente hay que registrar las constantes vitales, incluyendo glucemia capilar y temperatura. En todos
los pacientes se debe realizar una exploración general y dirigida, buscando posibles signos de cardiopatía,
vasculopatía periférica, estigmas cutáneos de endocarditis, etc. Se realizará una exploración neurológica
completa buscando signos de focalidad que permitan orientar topográficamente el cuadro (Tablas II y III).
La escala de valoración National Institutes of Health Stroke Scales (NIHSS) permite estimar la gravedad del
ictus y monitorizar la evolución del cuadro, especialmente en los ictus de territorio anterior (Tabla VI).
5.3. Pruebas complementarias
A todo paciente con sospecha de ictus en urgencias se le debe realizar inmediatamente una
analítica completa que incluya hemograma, ionograma, glucosa plasmática, pruebas de función hepática,
renal y coagulación; electrocardiograma (ECG), radiografía de tórax y tomografía computarizada (TC)
cerebral. La TC cerebral es la técnica de elección en la fase aguda, ya que permite diferenciar las lesiones
isquémicas de las hemorrágicas y de procesos estructurales (abscesos, tumores). En los ictus isquémicos
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1372]
[85] ENFERMEDAD CEREBROVASCULAR
suele ser normal en las primeras 24 horas, aunque existen una serie de signos radiológicos precoces de
isquemia cerebral (pérdida de la diferenciación entre sustancia gris y blanca, atenuación del núcleo
lenticular, borramiento de surcos corticales, etc.). A partir de las 24-48 horas, a veces antes, puede
detectarse el infarto como un área hipodensa. Los infartos lacunares pueden no detectarse en la TC debido
a su pequeño tamaño. El estudio debe completarse con alguna técnica de neuroimagen vascular con el
objetivo de valorar la permeabilidad de las arterias y detectar oclusiones arteriales, como doppler de
troncos supraaórticos- transcraneal, angio-TC o angio-resonancia magnética nuclear (RMN). Esto
permitirá seleccionar aquellos pacientes candidatos a tratamiento endovascular (ver más adelante). En
casos seleccionados (por ejemplo ictus del despertar) se puede valorar realizar de forma urgente una RMN
multimodal con secuencias avanzadas (difusión-perfusión) o una TC-perfusión que informa de la integridad
estructural del cerebro y la perfusión cerebral relativa. Estas técnicas permiten estimar el área de tejido
isquémico cerebral potencialmente salvable (concepto de penumbra isquémica) y seleccionar aquellos
pacientes que en teoría podrían beneficiarse de un tratamiento de reperfusión.
6. ABORDAJE TERAPÉUTICO
6.1. Medidas generales
Vía aérea permeable: No está indicada la administración rutinaria de oxígeno. Se deben aspirar
secreciones, colocar tubo Guedel y/o proceder a intubación orotraqueal si el nivel de
consciencia lo requiere.
Cabecero incorporado a 30º en pacientes con bajo nivel de consciencia, riesgo de aspiración o
signos de hipertensión intracraneal.
Control hidroelectrolítico: se ha de mantener un balance hídrico adecuado utilizando
soluciones salinas isotónicas (unos 2.000 cc cada 24 horas puede ser una pauta adecuada). Se
deben evitar las soluciones glucosadas (hipotónicas), a menos que exista hipoglucemia, ya que
facilitan el desarrollo de edema cerebral.
Control de la hiperglucemia: se debe controlar de forma estricta la glucemia en la fase aguda
del ictus, manteniendo cifras inferiores a 150 mg/dL.
Control de la temperatura: la fiebre es un factor independiente de mortalidad y mal pronóstico
neurológico. Se debe garantizar una temperatura por debajo de 37,5 ºC con antitérmicos (por
ejemplo paracetamol). La causa más frecuente es la infección respiratoria por broncoaspiración
transcurridas las primeras 24 horas. La antibioticoterapia precoz y dirigida mejora el pronóstico.
Profilaxis de enfermedad tromboembólica venosa con movilización precoz, medias de
compresión y heparinas de bajo peso molecular si no existen contraindicaciones.
Control de la tensión arterial (TA): durante la fase aguda es conveniente mantener cifras
moderadamente elevadas de TA. Se recomienda tratamiento antihipertensivo urgente en ictus
isquémicos con cifras de TA sistólica > 220 y/o TA diastólica > 120 mm Hg procurando un
descenso gradual, ya que disminuciones de TA rápidas pueden disminuir la perfusión sobre la
zona de penumbra y aumentar el territorio infartado. Los pacientes que van a recibir
tratamiento trombolítico deben mantener cifras de TA por debajo de 185/105 mm Hg. Se
recomiendan los siguientes fármacos: labetalol (10 mg) y urapidilo (25 mg) monodosis por vía
intravenosa, pudiendo repetir la misma dosis cada 10 minutos hasta en tres ocasiones si la TA
persiste elevada. En caso de control subóptimo estaría indicado la administración continuada
de estos fármacos mediante perfusión (ver Capítulo 20. “Hipertensión y riesgo cardiovascular,
crisis hipertensiva”). Se desaconseja el uso de nifedipino o captopril sublingual por el riesgo de
inducir hipotensión brusca.
6.2. Tratamiento específico de la isquemia cerebral en fase aguda
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1373]
[85] ENFERMEDAD CEREBROVASCULAR
Terapias de reperfusión (Figura 2).
Fibrinólisis intravenosa:
El activador tisular del plasminógeno recombinante, o rtPA, es un fármaco de
naturaleza enzimática cuyo mecanismo de acción es la transformación de
plasminógeno en plasmina, que promueve la disgregación del trombo formado. El rtPA
está indicado en el tratamiento del ictus isquémico de menos de cuatro horas y media
de evolución desde el inicio de los síntomas, en ausencia de contraindicaciones (Tabla
VII). La dosis empleada es de 0,9 mg/kg (máximo de 90 mg) administrando un bolo
inicial del 10% de la dosis total en un minuto, y el resto en infusión durante 60 minutos,
por vía intravenosa. La probabilidad de mejoría neurológica se estima en uno de cada 7
pacientes tratados, pero es muy variable y está claramente condicionada por diferentes
factores (edad, comorbilidades, tipo y mecanismo de ictus…), siendo más desfavorables
los resultados cuanto más tarde se inicie el tratamiento, y en casos de oclusión de gran
vaso demostrada (por ejemplo trombo en la carótida distal o arteria cerebral media en
su origen). El principal riesgo del tratamiento son los eventos hemorrágicos a cualquier
nivel, incluyendo el sangrado intracraneal. La cuidadosa selección de los pacientes
candidatos a este tratamiento, y el exhaustivo control de la TA previamente y durante
la infusión (cada 15 minutos) son dos factores determinantes para prevenir esta
complicación. Se debe sospechar la presencia de transformación hemorrágica durante
la fibrinólisis cuando aparece deterioro neurológico, cefalea intensa, vómitos o
elevación aguda de la TA. Ante la sospecha se debe detener la infusión de rtPA, realizar
TC craneal urgente y analítica con estudio de coagulación.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1374]
[85] ENFERMEDAD CEREBROVASCULAR
Tratamiento endovascular:
Las nuevas evidencias (estudios MR CLEAN, ESCAPE, EXTEND-IA, SWIFT PRIME y
REVASCAT) han demostrado el beneficio del tratamiento endovascular y, en concreto,
de la trombectomía mecánica con dispositivos de tipo stent. Esto ha supuesto la
renovación y actualización de los protocolos de actuación terapéutica previos. La
conclusión de estos estudios es que la trombectomía mecánica posterior al tratamiento
estándar (fibrinólisis intravenosa) en pacientes adecuadamente seleccionados aumenta
significativamente la probabilidad de recanalización arterial y el grado de
independencia. Son candidatos a trombectomía mecánica con el máximo nivel de
evidencia y recomendación los pacientes que cumplen de forma simultánea todos los
siguientes criterios:
Edad ≥ 18.
Previamente independientes: escala modificada de Rankin (EmR) = 0-1 (Tabla).
Tiempo de evolución desde el inicio hasta punción femoral menor de 6 horas.
Puntuación en escala NIHSS igual o superior a 6.
Oclusión aislada de arteria carótida interna distal o cerebral media proximal.
TC basal sin alteraciones.
Tratados previamente con fibrinólisis intravenosa según protocolo en las
primeras 4,5 horas sin lograrse recanalización.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1375]
[85] ENFERMEDAD CEREBROVASCULAR
En otras circunstancias diferentes a las previamente detalladas podría existir beneficio del
tratamiento, siendo necesaria la valoración individualizada del caso por un equipo multidisciplinar para
determinar la decisión final. Algunas situaciones habituales y las recomendaciones son las siguientes:
Tiempo de evolución desconocido o superior a seis horas: el tratamiento podría indicarse si se
demuestra por técnicas de imagen multimodal (ver apartado de pruebas complementarias) que
el volumen de tejido irreversiblemente dañado es pequeño y existe tejido recuperable.
Oclusión de la arteria basilar: en estos casos la ventana temporal es de 12 horas y se
prolonga hasta 24 horas si el curso es fluctuante o progresivo.
Edades extremas (más de 80 años y menos de 18): no suponen un criterio de exclusión
para el tratamiento si es técnicamente posible.
Situaciones especiales como el embarazo, el cáncer, la endocarditis infecciosa o la
alergia a contrastes deben someterse a una valoración individualizada, pudiéndose
llevar a cabo el tratamiento con medidas específicas cuando se estime un beneficio
superior al riesgo asociado.
Las contraindicaciones de la trombectomía mecánica se detallan en la tabla IX.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1376]
[85] ENFERMEDAD CEREBROVASCULAR
Tratamientos antitrombóticos: La prevención secundaria de la enfermedad cerebrovascular
con tratamiento antitrombótico puede establecerse desde la fase aguda del ictus. En pacientes
sometidos a tratamiento con fibrinólisis intravenosa el uso posterior de antiagregantes o
anticoagulantes se retrasará 24 horas, previa realización de TC de control que descarte
complicaciones hemorrágicas.
Antiagregación. El comenzar la administración de ácido acetilsalicílico (AAS) a dosis de
300 mg al día en las primeras 48 horas tiene un efecto beneficioso (modesto) en la
evolución de los pacientes a los 6 meses, así como en la reducción de recidivas
precoces y de mortalidad. El clopidogrel 75 mg al día es una buena alternativa al AAS
100 mg, sobre todo en ictus aterotrombóticos.
Anticoagulación. La anticoagulación en fase aguda no se recomienda en términos
generales, ya que no ofrece beneficio en la evolución y se asocia a un claro incremento
en el riesgo de transformación hemorrágica clínicamente relevante. Existen situaciones
en las que se acepta la anticoagulación desde la fase aguda, por considerar su potencial
beneficio superior al perfil de riesgos, entre las que se incluyen:
AIT o ictus leve de clara etiología cardioembólica o protrombótica (por ejemplo
estado de hipercoagulabilidad), con excepción de la endocarditis infecciosa.
Ictus vertebrobasilar progresivo (si el tratamiento endovascular está
contraindicado) y cuadros fluctuantes de perfil tromboembólico
(recomendación de expertos, limitado nivel de evidencia).
En el resto de casos la anticoagulación debe posponerse unos días; este periodo dependerá del
tamaño del ictus y de la etiología del mismo, factor que condiciona a su vez el riesgo de recurrencia.
En general se recomienda comenzar tratamiento anticoagulante con heparina sódica o de bajo
peso molecular, en función del cuadro clínico y de la valoración individualizada del riesgo hemorrágico. Lo
antes posible se iniciará terapia anticoagulante oral, bien con dicumarínicos (acenocumarol), bien con
anticoagulantes directos: dabigatrán, apixabán, ribaroxabán o edoxabán (ver Capítulo 77. “Trastornos de la
hemostasia. Anticoagulación”).
Estatinas. Las estatinas han demostrado tener un efecto protector en el ictus isquémico, de tal
manera que su administración precoz puede asociarse a una mejor evolución clínica (efecto
pleiotrópico). Su retirada en caso de que el paciente las tomara previamente a sufrir el ictus
isquémico es un factor independiente de mal pronóstico. El fármaco más habitualmente
empleado es atorvastatina 80 mg al día.
Neuroprotección. Se han estudiado múltiples agentes farmacológicos denominados
neuroprotectores que teóricamente podían disminuir los daños causados por la interrupción
del flujo sanguíneo cerebral, inhibiendo mediadores bioquímicos responsables de la afectación
por isquemia-reperfusión. Sin embargo, su efecto beneficioso no se ha confirmado en los
estudios clínicos, por lo que no
7. TRATAMIENTO DE LAS COMPLICACIONES
7.1. Edema cerebral (swelling) e hipertensión intracraneal
El edema cerebral se puede desarrollar a partir de las primeras 24 horas. En ocasiones puede ser
incluso más precoz y conllevar importante deterioro clínico-radiológico (“infarto maligno”).
7.1.1. Tratamiento
Médico:
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1377]
[85] ENFERMEDAD CEREBROVASCULAR
Medidas generales comunes a todos los ictus isquémicos, restricción hídrica moderada
y uso de manitol (bolo inicial de 0,75 g/kg al 20% en 20 minutos [250 ml en un paciente
de 70 kg], seguido de 125 ml/6 horas, con posterior disminución gradual de la dosis y
suspensión en dos a tres días). Se puede combinar inicialmente con furosemida (40 mg
en bolo). Los corticoides no tienen ninguna utilidad en estos casos.
Es cuestionable la inducción de coma barbitúrico e hiperventilación, lo que precisaría
ingreso en la Unidad de Cuidados Intensivos (UCI).
Quirúrgico:
La craniectomía descompresiva se emplea como medida terapéutica de rescate en los
casos de ictus malignos seleccionados cuidadosamente, existiendo evidencia firme de
su efecto sobre la disminución de mortalidad debido al mejor control de la presión
intracraneal secundaria al edema del tejido isquémico. Técnicamente consiste en la
realización de una craniectomía (sin reposición de hueso en esta fase) fronto-temporo-
parietal del lado afecto, junto con una adecuada descompresión de la fosa craneal
temporal basal y ampliación dural. Esto permite al cerebro inflamado expandirse sin
ocasionar herniaciones profundas que pongan en peligro la vida del paciente. En
general, se considera indicada en las primeras 48 horas tras el inicio de los síntomas
isquémicos en pacientes ≤ 60 años, sin comorbilidades importantes, que desarrollan
deterioro del nivel de consciencia junto a hallazgos radiológicos que indiquen alta
probabilidad de progresión a infarto maligno. En la TAC se consideran signos
radiológicos de alarma una hipodensidad franca en la TAC inicial (en las primeras seis
horas de los síntomas), la afectación de más de un tercio del territorio de la arteria
cerebral media y la desviación de la línea media. En el caso de la RMN cerebral un
volumen ≥ 80 ml de territorio cerebral con restricción en la secuencia de difusión en la
RMN inicial se considera factor de riesgo para desarrollar edema cerebral.
En el caso de infartos cerebelosos con efecto masa (desplazamiento troncoencefálico,
oclusión o deformación del IV ventrículo con o sin hidrocefalia triventricular y
compromiso de cisternas perimesencefálicas) y deterioro del nivel de consciencia se
considera indicada la craniectomía suboccipital urgente con o sin derivación ventricular
externa.
7.2. Crisis comiciales
Los pacientes con ictus pueden sufrir crisis comiciales. En estos casos una única crisis es indicación
de tratamiento anticomicial por elevado riesgo de recurrencia (ver Capítulo 86. “Crisis comiciales”). El
tratamiento con fármacos antiepilépticos de forma preventiva en pacientes con ictus que no han sufrido
crisis no está indicado.
7.3. Transformación hemorrágica
Se define como la aparición de una o más áreas hemorrágicas en un territorio cerebral previamente
infartado o en otras zonas (Tabla X). Esta complicación es más frecuente en ictus isquémicos extensos de
mecanismo embólico, y en aquellos pacientes sometidos a fibrinólisis intravenosa o en tratamiento
anticoagulante desde la fase aguda (ver indicaciones). La transformación hemorrágica de un infarto no
siempre conlleva un deterioro clínico, y en algunos casos es un hallazgo radiológico que no obliga a realizar
cambios terapéuticos más allá de una vigilancia clínico-radiológica adecuada.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1378]
[85] ENFERMEDAD CEREBROVASCULAR
8. ISQUEMIA CEREBRAL TRANSITORIA
En el caso de los AIT el enfoque clínico es idéntico a lo previamente descrito para ictus isquémicos
agudos (anamnesis y exploración). Sin embargo, por la naturaleza transitoria del cuadro es frecuente tener
que hacer diagnóstico diferencial de cuadros comiciales, migrañas, crisis hipoglucémicas y cuadros
psicofuncionales, entre otros. En todo paciente con AIT en urgencias se debe solicitar valoración por
Neurología y realizar una analítica completa, ECG, TC craneal y estudio neurovascular.
El manejo posterior diagnóstico y terapéutico depende de las características del paciente,
incluyendo su edad, la etiología del mismo y el riesgo de recurrencia estimado según criterios clínicos
(Tabla XI). En algunos casos se requiere ingreso hospitalario, como en los pacientes en los que se estima
alto riesgo de recurrencia.
2. EVALUACIÓN SECUNDARIA: DIAGNÓSTICO Y TRATAMIENTO A LARGO PLAZO
Tras la fase aguda se debe intentar filiar la etiología del ictus, de cara a administrar el mejor
tratamiento posible (ver Apartado 3. “Etiología. Clasificación según mecanismo etiopatogénico”).
1. PRUEBAS COMPLEMENTARIAS
1.1. Dúplex de troncos supraórticos (TSA)
Rápida y sencilla, es la técnica de elección para la evaluación del segmento extracraneal de las
arterias carótidas y vertebrales. Debe realizarse lo antes posible en el ictus isquémico. Mediante doppler
permite detectar alteraciones del flujo en estenosis superiores al 50%, presentando una elevada
sensibilidad y especificidad en estenosis superiores al 70%. En ocasiones no permite distinguir entre
estenosis crítica y oclusión. Su sensibilidad es menor para evaluar la estenosis de las arterias vertebrales.
Mediante ecografía permite valorar la morfología de los ejes vasculares, así como la existencia de placas y
su caracterización.
1.2. Doppler transcraneal
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1379]
[85] ENFERMEDAD CEREBROVASCULAR
Evalúa el estado de la circulación en los segmentos proximales de las arterias intracraneales.
Presenta una alta sensibilidad para identificar estenosis intracraneales superiores al 60%, permitiendo
conocer el estado de la circulación colateral y detectar microembolias cerebrales en la fase aguda de
isquemia cerebral, por lo que es conveniente realizarlo precozmente si está disponible. Siempre debe
realizarse antes un estudio de TSA. También permite detección de shunts derecha-izquierda,
monitorización de eventos embólicos, vasoespamo cerebral, de procedimientos cardiovasculares,
valoración de reserva hemodinámica y la monitorización de la recanalización en la fibrinólisis. Puede usarse
como tratamiento coadyuvante en la fibrinólisis intravenosa (sonotrombólisis).
1.3. RMN cerebral
Permite identificar lesiones isquémicas pocos minutos después de su inicio, por lo que cada vez se
usa más en fase aguda. Más allá de esta fase, tiene gran utilidad por ser más sensible que la TC para la
detección de lesiones isquémicas, sobre todo en la fosa posterior, infartos lacunares y edema cerebral.
Mediante angio-RMN puede evaluarse el estado de la circulación intra y extracraneal, estudio que debe
realizarse lo antes posible ante la sospecha de una disección carotídea o vertebral (la secuencia de elección
para ello es T1 con supresión grasa).
1.4. Ecocardiograma transtorácico
Se recomienda ante la sospecha de etiología cardioembólica, ictus en paciente joven, ictus y fiebre
(sospecha de endocarditis infecciosa), arritmia embolígena no conocida previamente y en pacientes en los
que no se ha aclarado la causa con otras pruebas complementarias.
1.5. Ecocardiograma transesofágico
Más sensible para detectar anomalías del septo interauricular (foramen oval permeable,
aneurismas), trombos en la aurícula izquierda, vegetaciones valvulares y lesiones ateroescleróticas en la
aorta ascedente y patología del cayado aórtico.
1.6. Holter-ECG de 24 horas
Puede detectar el 2% de las arritmias embolígenas no identificadas mediante ECG convencional. En
casos muy seleccionados hay que recurrir a monitorización prolongada.
1.7. Electroencefalograma
Tiene utilidad si es preciso el diagnóstico diferencial con crisis comiciales o cuando se sospeche
afectación tóxico-metabólica en el paciente con ictus y alteración del nivel de consciencia.
1.8. Angiografía digital arterial
Tiene indicación (al margen de la terapéutica endovascular en fase aguda) en: a) estenosis de
troncos supraaórticos subsidiarias de tratamiento quirúrgico o intravascular; b) diagnóstico de arteriopatías
inflamatorias o no inflamatorias; c) diagnóstico y tratamiento de aneurismas cerebrales, malformaciones
arteriovenosas y fístulas durales.
1.9. Otros
En los pacientes con ictus de origen desconocido y/o con datos clínicos que lo apoyen, debe
considerarse la realización de las siguientes pruebas complementarias:
Estudios microbiológicos: serologías para lúes, virus de la inmunodeficiencia humana (VIH),
virus de la hepatitis C, virus de la hepatitis B, Borrelia, Brucella y tuberculosis (TBC).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1380]
[85] ENFERMEDAD CEREBROVASCULAR
Estudio inmunológico: anticuerpos antinucleares, anticuerpos extraíbles del núcleo,
anticuerpos anticitoplasma del neutrófilo, complemento, FR, anti-ADN, crioglobulinas, proteína
C reactiva, velocidad de sedimentación globular.
Estudio de hipercoagulabilidad: proteínas C y S, antitrombina III, anticoagulante lúpico,
mutaciones relacionadas con factor V de Leyden o gen de la protrombina, etc. Se recomienda
realizar el estudio de causas de hipercoagulabidad no determinadas genéticamente de forma
diferida, a partir de las ocho semanas del ictus.
Estudio genético: estudio de mutaciones propias de enfermedades que pueden asociar un
mayor riesgo de ictus (por ejemplo enfermedad de Fabry, CADASIL, enfermedades
mitocondriales, etc.).
Punción lumbar: ante sospecha de arteritis o hemorragia subaracnoidea o patologías
inflamatorias.
Biopsia cutánea (por ejemplo sospecha de CADASIL) o muscular (por ejemplo sospecha de
enfermedad mitocondrial).
2. TRATAMIENTO A LARGO PLAZO
Debe ejercerse un control estricto sobre los factores de riesgo cardiovascular y sobre los hábitos de
vida que suponen un riesgo para el desarrollo de enfermedad ateroesclerótica (tabaquismo, sedentarismo,
etc.). En cuanto al tratamiento médico-quirúrgico deben considerarse:
2.1. Antiagregación
Eficaz en la prevención secundaria del ictus aterotrombótico o lacunar. El AAS (300 mg/día) es el
agente de elección, siendo el clopidogrel (75 mg/día) una buena alternativa y el agente de elección en caso
de arterioesclerosis generalizada. Otros antiagregantes menos utilizados y con indicaciones más
restringidas son ticlopidina, triflusal o dipiridamol. La doble antiagregación con AAS y clopidogrel durante
tres meses ha demostrado superioridad frente a la angioplastia en el tratamiento de la estenosis arterial
intracraneal aterotrombótica > 70%. También se emplea este régimen durante tres a seis meses tras la
colocación de stent carotídeo.
2.2. Estatinas
La atorvastatina a dosis de 80 mg/día en fase aguda ha demostrado eficacia frente a placebo en la
prevención secundaria de recurrencias de ictus aterotrombótico.
2.3. Anticoagulantes
(Tabla XII). Deben utilizarse en aquellas situaciones de riesgo de ictus cardioembólico o
protrombótico (cardiopatía o arritmia embolígenas, situaciones trombofílicas, etc.). En función de las
comorbilidades y características de cada paciente han demostrado eficacia en la prevención a largo plazo
del ictus cardioembólico los siguientes anticoagulantes orales: warfarina y acenocumarol, dabigatrán,
rivaroxabán, apixabán y edoxabán. Existen otros compuestos en estudio, como betrixabán.
2.4. Endarterectomía carotídea (EC)
Indicada en: a) estenosis carotídea sintomática > 70%, preferentemente en las dos primeras
semanas del ictus, si este es leve o moderado; b) estenosis carotídea sintomática entre 50-69% en
pacientes de riesgo quirúrgico bajo; y c) estenosis carotídea asintomática > 70%, en pacientes
seleccionados y de riesgo quirúrgico bajo. El tratamiento perioperatorio con antiagregantes y estatinas
mejora los resultados de la intervención quirúrgica.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1381]
[85] ENFERMEDAD CEREBROVASCULAR
2.5. Angioplastia carotídea percutánea (AC)
Se plantea como una alternativa a la EC en pacientes que rechazan la cirugía, presentan alto riesgo
quirúrgico, dificultad para el acceso quirúrgico (radioterapia cervical, lesiones distales), estenosis carotídea
no ateroesclerótica y reestenosis carotídea. Ante estenosis carotídea de etiología aterotrombótica, la EC ha
demostrado superioridad sobre la AC en diversos estudios publicados hasta la actualidad.
II. HEMORRAGIA INTRAPARENQUIMATOSA
1. CONCEPTO Y ETIOLOGÍA
La hemorragia intracerebral (HIC) es una colección de sangre dentro del parénquima cerebral,
producida por una rotura vascular. Supone un 10-15% de todos los ictus, y condiciona un peor pronóstico
que los ictus isquémicos. Es más frecuente a medida que avanza la edad, en hombres y en población negra
y japonesa. Su factor de riesgo más importante es la HTA. La HIC puede ser espontánea, cuando se produce
sin traumatismo previo; primaria, cuando se debe a la rotura de un vaso normal o cuya pared se ha
debilitado por procesos degenerativos secundarios a la HTA o la angiopatía amiloide; o secundaria, cuando
se asocia a otros procesos estructurales vasculares.
HIC espontánea hipertensiva: es la más frecuente, y más aún en fumadores. Provoca sangrados
habitualmente en áreas profundas, de tamaño variable, que alcanzan su máximo tamaño en
minutos u horas.
Angiopatía amiloide: más frecuente en ancianos. Los depósitos de amiloide provocan
hemorragias lobares espontáneas. Suelen ser recurrentes y se asocian a demencia.
Infarto hemorrágico: una complicación del ictus isquémico, típicamente de mecanismo
embólico, o de la trombosis de senos venosos.
Malformaciones vasculares: Son propias de pacientes más jóvenes que las hipertensivas.
Pueden deberse a roturas de aneurismas, malformaciones arteriovenosas, cavernomas,
angiomas venosos, malformaciones durales o telangiectasias.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1382]
[85] ENFERMEDAD CEREBROVASCULAR
Tumores intracranales: menos del 10% de las causas de HIC. Pueden ser primarios (gliomas,
adenomas de hipófisis, más raro en meningiomas) o metastásicos (coriocarcinoma, melanoma,
pulmón, riñón, tiroides).
Coagulopatías: tratamiento con anticoagulantes orales o heparina (mayor riesgo en
tratamientos prolongados, antiagregación asociada, edad avanzada, HTA, leucoaraiosis severa y
angiopatía amiloide; son sangrados de crecimiento lento pero de mayor tamaño final que los
secundarios a HIC hipertensiva, con alta mortalidad), agentes fibrinolíticos (mayor riesgo si
existe crisis hipertensiva, angiopatía amiloide y enfermedad cerebrovascular crónica-
leucoaraiosis relevante) y situaciones de diátesis hemorrágica.
Otros: fármacos y tóxicos (fundamentalmente, simpático-miméticos, vasoconstrictores de uso
tópico, cocaína y abuso de alcohol), vasculitis, algunas infecciones del sistema nervioso central
(SNC) y la HIC traumática.
2. APROXIMACIÓN DIAGNÓSTICA
2.1. Clínica
La HIC es más frecuente durante la actividad física, provoca un déficit neurológico que progresa
durante horas, por crecimiento del hematoma. Presenta síntomas específicos en función de la localización
del sangrado. Suele provocar síntomas de hipertensión intracraneal: alteración del nivel de consciencia,
cefalea, náuseas y vómitos, aumento de la presión arterial. Las crisis comiciales son más frecuentes en
hematomas lobares. La anamnesis debe ir encaminada a considerar traumatismo craneoencefálico previo
(difícil en pacientes hallados solos con alteración del nivel de consciencia), tiempo de inicio de los síntomas,
presencia de FRCV, consumo de fármacos o tóxicos y cirugías recientes.
2.2. Pruebas complementarias
Ante todo paciente con focalidad neurológica aguda debe realizarse inmediatamente una analítica
completa con hemograma, coagulación, iones, glucosa, funciones renal y hepática, TC craneal, ECG y una
radiografía de tórax.
La TC craneal es la prueba de elección ante la sospecha inicial de una HIC, ya que la clínica no
suele permitir distinguir entre ictus isquémicos y hemorrágicos en pacientes con focalidad
neurológica aguda. La TC detecta los hematomas en su fase aguda, definiendo su tamaño y
localización, así como posibles complicaciones: signos de herniación, sangrado intraventricular
e hidrocefalia secundaria. Mediante administración de contraste (angio-TC) mejora la detección
de anomalías subyacentes, como malformaciones vasculares (por ejemplo rotura
aneurismática), presencia de tumores u otras lesiones estructurales.
La RMN craneal tiene la misma sensibilidad que la TC para detectar sangrados agudos, pero
mucha menor disponibilidad en urgencias. Es más sensible para detectar hemorragias antiguas
y microhemorragias (secuencias eco de gradiente) y para definir el tiempo de evolución de la
hemorragia, así como detectar y caracterizar sangrados localizados en la fosa posterior. Es
imprescindible su realización para completar el estudio en casos de sospecha de existencia de
una lesión subyacente que haya causado la HIC, como malformaciones o aneurismas. En estos
casos puede ser necesario repetir el estudio transcurridas de cuatro a seis semanas, si en el
inicial la persistencia del sangrado impide la valoración adecuada del parénquima subyacente.
La arteriografía debe ser considerada cuando existe una sospecha alta, clínica o radiológica, de
causa secundaria (malformación, aneurisma) que no haya sido identificada mediante TC o
RMN. Es la técnica de elección en los casos de sospecha de vasculitis y puede ser negativa en
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1383]
[85] ENFERMEDAD CEREBROVASCULAR
los angiomas cavernosos. En cambio, su rendimiento es mínimo en caso de sospecha de
hematoma hipertensivo.
3. TRATAMIENTO
3.1. Tratamiento médico
3.1.1. Medidas generales
La atención debe realizarse en un hospital donde se disponga de valoración por neurocirugía y
traslado a una UCI durante las 24 horas del día. Debe asegurarse la estabilidad hemodinámica y protegerse
la vía aérea, planteando la intubación ante hipoxemia o hipercapnia refractarias o bajo nivel de consciencia
con riesgo de broncoaspiración. Se revertirá la anticoagulación si procede, se mantendrá la euvolemia y se
corregirán las alteraciones electrolíticas. Debe tratarse la hipertermia, y considerar las complicaciones
infecciosas asociadas. La tromboprofilaxis debe realizarse con medias de compresión, preferiblemente
medias de compresión neumática intermitente. La anticoagulación profiláctica, con heparina de bajo peso
molecular (HBPM), puede iniciarse a las 48 horas del ictus hemorrágico, si no hay sospecha de crecimiento
o recurrencia del sangrado intracraneal.
3.1.2. Medidas específicas
Deberá mantenerse la TA por debajo de 180 mm Hg, empleando preferiblemente enalapril, o
labetalol o urapidil por vía intravenosa, y la glucemia por debajo de 155 mg/dL (evitando los sueros
glucosados en lo posible). Debe tratarse también la hipertensión intracraneal, que se debe al efecto masa y
a la hidrocefalia, mediante las mismas medidas que las empleadas en el ictus isquémico.
3.2. Tratamiento quirúrgico
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1384]
[85] ENFERMEDAD CEREBROVASCULAR
Resumen de manejo en la figura 3. A la hora de considerar la indicación del tratamiento quirúrgico
debemos diferenciar en un primer momento, según la localización de los hematomas intracerebrales, dos
grandes grupos:
3.2.1. Hematomas supratentoriales
En este grupo están incluidos los hematomas lobares, de ganglios basales (putaminales) y los
talámicos. El fundamento de la evacuación quirúrgica del hematoma se basa en los beneficios obtenidos
por la disminución de la presión intracraneal y la reducción del efecto deletéreo del hematoma sobre el
parénquima vecino sano (por efecto masa local y el efecto citotóxico de los productos de degeneración de
la sangre). En los últimos años se han realizado estudios donde se emplea la craniectomía con/sin
evacuación del hematoma en pacientes con bajo nivel de consciencia y hematomas voluminosos, para el
control de la presión intracraneal refractaria a tratamiento médico. Otra alternativa, sin evidencia
suficiente aún para su recomendación generalizada, es la evacuación endoscópica mínimamente invasiva
del hematoma. A pesar de ello, el tratamiento quirúrgico continúa siendo controvertido debido a que los
ensayos clínicos aleatorizados realizados al respecto no han demostrado un beneficio claro de la
evacuación del hematoma intracerebral. En nuestro medio se siguen las siguientes recomendaciones:
Pacientes con hematomas < 20 cc o sin deterioro del nivel de consciencia (Glasgow Coma Scale
[GCS] 13-15) se deben manejar de forma conservadora.
Pacientes con hematomas > 20 cc con deterioro del nivel de consciencia (GCS 6-12) se pueden
considerar candidatos a la evacuación quirúrgica del hematoma si tenían buena situación basal
en cuanto a comorbilidad (la edad es un criterio relativo). No se considera indicado la
evacuación profiláctica de hematomas > 3 cm si la situación clínica es buena.
Pacientes con muy mala situación neurológica (GCS < 6 o puntuación motora dentro del GCS ≤
3) rara vez se consideran candidatos a procedimiento quirúrgico.
En los hematomas asentados en el tálamo o con extensión mesencefálica no se considera
indicado el tratamiento quirúrgico.
Los pacientes con hematomas (generalmente putaminales), que asocian extensión ventricular
con hidrocefalia secundaria que condiciona deterioro del nivel de consciencia, se pueden
beneficiar de la colocación de un drenaje ventricular externo si tenían buena situación basal.
3.2.2. Hematomas infratentoriales
Se incluyen los hematomas de los hemisferios y vermis cerebeloso y los hematomas
troncoencefálicos. La evidencia científica es más homogénea al respecto del beneficio de la evacuación
quirúrgica de los hematomas en esta localización. De forma general se consideran las siguientes
indicaciones:
Los hematomas que asientan en el tronco del encéfalo no se consideran quirúrgicos, dado el
improbable beneficio de la evacuación quirúrgica del hematoma en dicha localización.
Los hematomas cerebelosos se deben evacuar si asocian signos radiológicos de alarma como es
el diámetro > 4 cm, la compresión del IV ventrículo, la hidrocefalia supraventricular o la
deformación-desplazamiento troncoencefálico, incluso en pacientes con buen nivel de alerta,
dado el riesgo elevado de deterioro. En ausencia de estos signos de alarma se deben intervenir
aquellos hematomas que ocasionen deterioro del nivel de consciencia (GCS < 14). La cirugía
consiste en una craniectomía de fosa posterior y evacuación del hematoma con/sin colocación
de drenaje ventricular externo. No se considera indicado el tratamiento quirúrgico en aquellos
pacientes con comorbilidades graves, GCS 3 o ausencia de reflejos troncoencéfalo.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1385]
[85] ENFERMEDAD CEREBROVASCULAR
III. HEMORRAGIA SUBARACNOIDEA
1. DEFINICIÓN
Se trata de la hemorragia que se produce debajo de la cubierta aracnoidea de la superficie cerebral,
y que se extiende por las cisternas y surcos cerebrales.
2. EPIDEMIOLOGÍA
Es el subtipo de accidente cerebrovascular más infrecuente (5%), pero de enorme relevancia
sociosanitaria debido a la mortalidad y morbilidad asociadas: el 30% de los pacientes que llegan a ser
atendidos en el hospital fallecen debido a la HSA y/o sus complicaciones, y el 50% de los supervivientes
presentará discapacidad grave. A diferencia del ictus isquémico, la incidencia de la HSA permanece
invariable en 6-8 casos/100.000 habitantes-año en nuestro medio. La edad de presentación más frecuente
en la HSA es alrededor de los 55 años.
3. ETIOLOGÍA
Las principales causas de HSA aparecen en la tabla XIII. La etiología más frecuente de HSA es la de
origen traumático; sin embargo, el objeto de este capítulo es la HSA espontánea y, en concreto, la
secundaria a rotura de aneurisma cerebral por tener una fisiopatología específica. La localización del
aneurisma roto con mayor frecuencia es en el territorio carotídeo (85-95%), siendo los más habituales en
orden descendente de frecuencia los de la arteria comunicante anterior, la arteria comunicante posterior y
la arteria cerebral media. En el 5-15% restante de los casos de HSA el aneurisma asienta en circulación
posterior (punta de la arteria basilar y menos frecuentemente en la arteria vertebral). En el 20-30% de los
casos de HSA se evidencian aneurismas múltiples.
4. FISIOPATOLOGÍA
Tras la rotura del aneurisma cerebral la hemorragia ocupa y se extiende por el espacio aracnoideo,
en el que se encuentran las ramas de las principales arterias cerebrales. Desde este momento inicial
podemos diferenciar tres mecanismos de daño cerebral:
4.1. Daño cerebral precoz
La salida de sangre al espacio subaracnoideo determina un incremento instantáneo de la presión
intracraneal, que produce una disminución del flujo sanguíneo cerebral. Por otro lado, el sangrado produce
por sí mismo una caída del flujo sanguíneo cerebral y además se ocasiona una respuesta fisiológica normal
de la arteria ante la ruptura mediante vasoconstricción. Por último, el intento de reparación del sangrado
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1386]
[85] ENFERMEDAD CEREBROVASCULAR
por los elementos formes del torrente sanguíneo y sistema de coagulación determina una obstrucción
intraluminal. Todo ello hace que se produzca una disminución del flujo sanguíneo cerebral que determina
una situación de isquemia.
4.2. Respuesta y complicaciones sistémicas tras HSA
En más de la mitad de los pacientes tras la HSA se ha descrito el síndrome de respuesta inflamatoria
sistémica consistente en taquicardia, taquipnea, hipertermia y leucocitosis como manifestación de la
activación del sistema adrenérgico. Entre las complicaciones sistémicas asociadas a HSA destacan las
siguientes:
Cardiovasculares: alteraciones en el electrocardiograma (50-100%), trastorno de la motilidad
cardiaca (miocardio contundido, 10-50%).
Hidroelectrolíticas: hiponatremia (35%).
Pulmonares: edema agudo de pulmón neurogénico (25%).
Trombosis venosa profunda de los miembros inferiores (15%).
Hemorragia del tracto gastrointestinal (4%).
4.3. Daño cerebral isquémico diferido
Aunque la definición de este proceso ha sido y es controvertida, actualmente se entiende por daño
cerebral isquémico diferido el deterioro del nivel de consciencia y/o nueva focalidad que no puede ser
explicada por el desarrollo de hidrocefalia, resangrado, crisis, exceso de sedación o causas sistémicas.
Aunque tradicionalmente la lesión isquémica diferida era atribuida al vasoespasmo (fomentado por los
productos de degeneración de la hemoglobina y estrés oxidativo), recientemente se han añadido otros
posibles factores contribuyentes como el trastorno en la autorregulación de la pared arteriolar, una
respuesta inflamatoria o un desequilibrio de la actividad fibrinólisis-coagulante (microtrombosis).
5. CLÍNICA
5.1. Síntomas
El síntoma más frecuente es la cefalea (97%), de localización variable, inicio brusco y elevada
intensidad descrita habitualmente como “el peor dolor de cabeza que he tenido en mi vida”. En ocasiones
se desencadena tras un esfuerzo físico o maniobra de Valsalva. Se acompaña con frecuencia de vómitos y
foto-sonofobia. Se denomina “cefalea centinela” a aquel episodio de cefalea de las mismas características
que precede en horas o días, con resolución parcial o total, y se relaciona con micro-roturas del aneurisma
o crecimiento del mismo. La cefalea centinela es descrita por hasta el 30-60% de los pacientes
diagnosticados de HSA aneurismática. Hasta una cuarta parte de los pacientes experimentan pérdida del
nivel de consciencia transitoria o no que se relaciona con el aumento de presión intracraneal inicial.
También pueden contribuir en los casos más graves la hidrocefalia, las crisis epilépticas, los hematomas
cerebrales, o la isquemia difusa. Con frecuencia el paciente asocia dolor cervical e incluso lumbar por
irritación meníngea por la HSA.
5.2. Signos a la exploración física
Nivel de consciencia: se debe explorar siguiendo la Glasgow Coma Scale (GCS). Es importante
estimar el grado clínico de cada paciente, ya que existe una buena correlación entre la
evolución final y el grado clínico inicial; la escala de situación clínica más empleada en el
contexto de HSA son la de la Asociación Mundial de Sociedades Neuroquirúrgicas (WFNS)
reflejada en la tabla XIV. Las puntuaciones superiores (WFNS III-V) constituyen un factor de
riesgo de mal pronóstico.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1387]
[85] ENFERMEDAD CEREBROVASCULAR
Meningismo: a través de los signos clásicos de Kerning y Brudzinski. Sin embargo, los signos de
irritación meníngea suelen aparecer a las 6-24 horas del inicio del cuadro.
Focalidad neurológica: derivada del efecto masa de hematomas secundarios a la rotura del
aneurisma o efecto local de aneurisma roto sobre estructuras vecinas (afectación de pares
oculomotores principalmente).
Hemorragia ocular: tres tipos de hemorragia ocular (subhialoidea o prerretiniana, retiniana y
vítrea) han sido descritas en relación con HSA de forma individual o en combinación en el 20-
40% de los casos. Exigen examen del fondo del ojo.
6. DIAGNÓSTICO
La prueba complementaria de elección para el diagnóstico de la HSA es la TC cerebral y para el
diagnóstico etiológico (aneurisma roto) es la arteriografía cerebral.
6.1. TC cerebral
Puede detectar HSA si se realiza en las primeras 48 horas tras la hemorragia con un 95% de
sensibilidad. La HSA aparece hiperdensa en la TAC, y su distribución puede orientar la localización del
aneurisma que se sospecha. La TC también es eficaz para detectar hidrocefalia, edema cerebral o isquemia
o hematomas intracraneales. La cantidad de HSA cisternal y cortical se gradúa siguiendo la escala de Fisher
(Tabla XV), que es además un elemento predictor de desarrollo de vasoespasmo.
6.2. La angio-TC
Es una prueba complementaria a la TC convencional que ha demostrado una sensibilidad menor
para detectar la presencia de aneurismas cerebrales que la arteriografía cerebral, pero dada su
disponibilidad y rapidez se debe realizar a todo los pacientes con sospecha de HSA de origen aneurismático.
Sin embargo, un estudio angio-TC negativo no descarta la presencia de aneurisma cerebral si la sospecha es
alta.
6.3. Arteriografía cerebral
Es el estudio de elección para comprobar la existencia, determinar las características geométricas
(diámetro y cuello) y detectar la presencia de signos de rotura de los aneurismas cerebrales. Se considera
completa cuando se han rastreado los 4 vasos principales cerebrales (los 2 sistemas carotídeos y
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1388]
[85] ENFERMEDAD CEREBROVASCULAR
vertebrales). Esta prueba se deberá realizar lo antes posible tras la hemorragia, si bien no se aconseja
realizar en las primeras seis horas del sangrado, pues parece que aumenta el riesgo de resangrado.
También resulta de enorme utilidad en la planificación del tratamiento quirúrgico (dominancia,
colateralidad).
6.4. Punción lumbar
Es altamente sensible para detectar de HSA, pero solo debe realizarse si la sospecha clínica es
elevada y la TC resultó negativa. En caso de HSA el LCR es hemático y la presión de apertura elevada. A
diferencia de una punción lumbar traumática, la sangre no se coagula y el teñido hemático no se aclara en
los sucesivos tubos. La presencia de xantocromía es diagnóstica de HSA, aunque también existen
infrecuentes falsos positivos. Se recomienda utilizar trocar fino y obtener una muestra de volumen escaso
puesto que, aunque es infrecuente, la disminución de presión intracraneal con la evacuación de LCR puede
favorecer resangrado precoz.
6.5. RMN cerebral
No detecta la HSA aguda en las primeras 24-48 horas, pero la secuencia FLAIR es la de mayor
utilidad para los casos con HSA subaguda dado la probable negatividad de la TC cerebral.
7. TRATAMIENTO
Los pacientes con HSA aneurismática deben ser tratados en centros especializados dotados de UCI,
Servicio de Neurocirugía y disponibilidad de tratamiento endovascular y microquirúrgico. Aunque, en
general, se recomienda que todos los pacientes diagnosticados de HSA aneurismática sean admitidos en
camas de hospitalización en UCI, esta condición es indispensable en los peores grados clínicos WFNS III-V.
Los objetivos fundamentales del tratamiento médico de la HSA son:
Prevención del riesgo de resangrado: reposo en cama, evitar oscilaciones de la presión arterial
sanguínea y exclusión precoz del aneurisma.
Prevención de la aparición de isquemia cerebral: evitar hipovolemia/hipotensión y
administración de betabloqueantes del calcio (nimodipino) como profilaxis del vasoespasmo.
7.1. Medidas generales
El paciente permanecerá en reposo en la cama con el cabecero a 30º, con monitorización de
constantes vitales, en dieta absoluta y debe evaluarse de forma horaria el nivel de consciencia, la situación
pupilar y la aparición de focalidad neurológica.
Asegurar una ventilación y oxigenación adecuada (PO2 alrededor de 80-100 mm Hg o
saturación de oxígeno igual o superior al 95%, y pCO2 alrededor de 35-45 mm Hg). Valorar la
necesidad de ventilación mecánica según el nivel de consciencia (GCS inferior o igual a 8) o la
función respiratoria.
Control de la presión arterial: es muy importante evitar tanto la hipertensión como la
hipotensión arterial. La presión arterial media (PAM) objetivo es 90-110 mm Hg (en pacientes
con aneurisma no excluido la PA objetivo será PAM 90 mm Hg, reservando cifras superiores
para los pacientes con aneurisma excluido y con factores de riesgo de vasoespasmo o evidencia
del mismo de forma precoz). En caso de presión arterial sistólica (PAS) > 140 mm Hg se debe
excluir causas desencadenantes de la HTA, como el mal control del dolor, hipertensión
intracraneal, agitación e hipoxia, en cuyo caso habría que tratar las mismas. En su ausencia se
pueden emplear fármacos antihipertensivos, siendo de elección el labetalol (efecto β1-
bloqueante selectivo causará una reducción del gasto cardiaco, sin provocar vasoconstricción
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1389]
[85] ENFERMEDAD CEREBROVASCULAR
cerebral) y los calcioantagonistas, especialmente el nimodipino (previene el vasoespasmo
cerebral). Los diuréticos están contraindicados al causar depleción del volumen intravascular.
Fluidoterapia: el control de líquidos y electrolitos debe ser estricto, evitando siempre la
hipovolemia y la hemoconcentración. La administración de líquidos puede reducir la viscosidad
sanguínea y mejorar la perfusión cerebral. Se recomiendan 3 litros de suero isotónico (en
combinación o no con coloides) al día (salvo contraindicación por comorbilidad asociada) y
evitando si es posible soluciones hiposmolares (sueros glucosados). Se debe evitar la
hiponatremia, que en el contexto de la HSA suele ser debida al síndrome pierde sal con mayor
frecuencia que el síndrome de secreción inadecuada de la hormona antidiurética y puede
empeorar el edema cerebral.
Tratamiento antiemético, analgésico (metamizol, paracetamol y opioides), laxantes y
protección gástrica.
Profilaxis de la trombosis venosa profunda mediante la colocación de medias neumáticas
durante las primeras 48 horas, pudiendo iniciarse heparinas de bajo peso molecular
posteriormente, salvo que se prevea procedimiento quirúrgico.
7.2. Tratamiento etiológico: exclusión del aneurisma
7.2.1. Técnica microquirúrgica
Consiste en la realización de una craneotomía pterional (acceso para los aneurismas más
frecuentes) y disección de la aracnoides hasta evidenciar el aneurisma roto y su relación con las ramas
arteriales vecinas. El aneurisma se interrumpe de la circulación colocando un clip quirúrgico en el cuello del
aneurisma, aunque dependiendo de la complejidad del mismo y su relación con ramas arteriales próximas
la técnica microquirúrgica puede ser variable y muy compleja. Aunque hoy en día se recomienda cirugía
temprana (0-3 días) en aquellos pacientes en mejor grado clínico (WFNS I-III), en la decisión también
influyen otros factores como la edad, las enfermedades concomitantes, la localización, el tamaño, la
complejidad del aneurisma y la disponibilidad de medios. Tradicionalmente los pacientes en mal grado
clínico inicial (grados IV-V) no eran intervenidos de forma precoz, sino de forma diferida. Sin embargo,
existen trabajos recientes con resultados favorables para la cirugía precoz en este grupo de pacientes, por
lo que no debe ser el único criterio.
7.2.2. Técnica endovascular
Mediante acceso femoral arterial se excluye el aneurisma de la circulación mediante su
embolización con coils. Resulta más apropiado el tratamiento endovascular en el caso de pacientes con mal
grado clínico inicial, comorbilidades, alto riesgo quirúrgico (especialmente los de circulación posterior) e
inoperabilidad por consideraciones anatómicas. La embolización no está indicada en el caso de aneurismas
con cuellos anchos, presencia concomitante de hematomas intraparenquimatosos que requieren
evacuación urgente ni en el caso de los aneurismas de arteria cerebral media.
En el International Subarachnoid Aneurysm Trial se comparó el tratamiento microquirúrgico y
endovascular para pacientes con aneurismas rotos en los que existían dudas sobre el mejor tratamiento,
demostrando mejores resultados en el caso de la técnica endovascular. No obstante, el estudio ha sido
criticado por los criterios de inclusión elegidos, y por tanto la extrapolación de los resultados es muy difícil
de realizar debido a la heterogeneidad de las poblaciones incluidas en cada serie. Por lo general, hay que
individualizar cada caso teniendo en cuenta los resultados de los diferentes tratamientos en cada centro, y
por ello suelen tomarse las decisiones en equipos multidisciplinares.
7.3. Tratamiento de las complicaciones
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1390]
[85] ENFERMEDAD CEREBROVASCULAR
7.3.1. Resangrado
Tras un primer episodio de HSA existe un riesgo de resangrado de un 3-4% en las primeras 24
horas, seguido de un riesgo acumulativo entre un 1-2%/día durante las primeras 4 semanas. Es la
complicación más grave, puesto que asocia un elevado riesgo de mortalidad (70%), mayor que el primer
episodio de sangrado. Se manifiesta clínicamente como un empeoramiento brusco con deterioro del nivel
de consciencia frecuentemente. La TC cerebral demostraría aparición de nuevos focos de HSA. El mejor
tratamiento dada la gravedad de esta complicación, una vez que acontece, es su prevención mediante el
reposo en cama, control estricto de las oscilaciones de PA y con la exclusión precoz del aneurisma de la
circulación cerebral. El uso de fármacos antifibrinolíticos es controvertido debido a los estudios publicados
más antiguos en los que su administración se relacionó con efectos adversos isquémicos, si bien en ese
periodo el uso de calcioantagonistas para la profilaxis del vasoespasmo no estaba sistematizado. En los
estudios recientes donde emplean tandas cortas y precoces de medicación en espera del procedimiento de
exclusión del aneurisma, se han obtenido mejores resultados en la reducción del riesgo de resangrado sin
asociar mayor riesgo de isquemia cerebral. Se puede administrar ácido épsilon-aminocaproico o ácido
tranexámico.
7.3.2. Vasoespasmo
Previamente se ha considerado que el déficit isquémico diferido en la fisiopatología de la HSA
aneurismática y el vasoespasmo es uno de los múltiples factores implicados en el desarrollo del mismo. El
vasoespasmo angiográfico es la reducción significativa del calibre arterial cerebral y tiene un pico de
incidencia alrededor del 7.° día, con una resolución gradual entre la 2.º y 4.º semana siguientes. La
incidencia estimada de vasoespasmo angiográfico es de aproximadamente 2/3 de los pacientes, de los
cuales 1/3 desarrollará síntomas isquémicos (deterioro, nuevo déficit). Una atención especial se debe
prestar a los pacientes no explorables debido a que se encuentren bajo sedación y ventilación mecánica. En
estos casos, la realización de ecografía doppler transcraneal y TC de perfusión cerebral de forma frecuente
pueden detectar datos indirectos de vasoespasmo o alteración diferida de la perfusión cerebral. La
mortalidad asociada al vasoespasmo es del 7% en la actualidad.
Profilaxis: la profilaxis del desarrollo del vasoespasmo se basa en mantener a los pacientes en
normovolemia y en la administración de calcioantagonistas (nimodipino). Existen varios
estudios que demuestran que el nimodipino reduce la incidencia de déficits neurológicos
isquémicos y mejora la evolución neurológica a los tres meses. Se recomienda nimodipino oral
(60 mg cada 4 horas, 21 días) y, en los casos en los que no se puede administrar medicación vía
oral, el nimodipino intravenoso ha demostrado eficacia similar, pero se asocia a mayor riesgo
de hipotensión arterial.
Tratamiento: una vez diagnosticado el vasoespasmo las medidas terapéuticas serán óptimas en
situación de aneurisma tratado, puesto que implican aumento del resangrado si no se
encuentra excluido. El tratamiento se basa en la terapia “triple H”: hipertensión (PAS > 150 mm
Hg), hemodilución (hematocrito alrededor del 30%) e hipervolemia (presión venosa central 5-
10 mm H2O). No existen estudios aleatorizados que demuestren su beneficio, y no está exenta
de riesgos (edema cerebral, edema agudo de pulmón e isquemia miocárdica), lo cual impide su
recomendación sistematizada. Actualmente se considera una opción razonable el tratamiento
con fármacos vasoactivos (noradrenalina, dopamina) y cristaloides/coloides. De las «tres H» se
considera menos apropiada la hemodilución, porque el hematocrito objetivo podría
comprometer la oxigenación cerebral, aun mejorando las características reológicas. Ante el
fracaso de la terapia triple H, o en presencia de contraindicación absoluta para la misma, está
indicado el tratamiento endovascular que puede consistir en la infusión intraarterial de
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1391]
[85] ENFERMEDAD CEREBROVASCULAR
vasodilatadores (nimodipino, nicardipino o verapamilo; la papaverina se encuentra en desuso)
o en la angioplastia con balón en casos seleccionados.
7.3.3. Hidrocefalia
La dilatación ventricular puede aparecer en el periodo agudo entre un 20-40% de los casos. Si el
grado clínico es aceptable (WFNS I-III) y no existe deterioro neurológico se puede adoptar una actitud
conservadora, ya que en la mayoría de los casos ocurre una resolución espontánea. Si existe deterioro
clínico se aconseja un drenaje ventricular externo, asumiéndose un aumento del riesgo de meningitis y de
resangrado. Si el paciente se encuentra en grados WFNS IV-V se recomienda drenaje externo
independientemente de la presencia o no de hidrocefalia en la TC inicial. Si la dilatación ventricular se
desarrolla de forma diferida y ocasiona un deterioro clínico consistente en los síntomas propios de la
hidrocefalia normotensa (ataxia de la marcha, incontinencia esfinteriana, deterioro cognitivo) se tratará
mediante la colocación de una derivación ventriculoperitoneal.
7.3.4. Convulsiones
Las crisis epilépticas pueden aparecen en el contexto de HSA con una frecuencia entre el 3-30% y
pueden contribuir al resangrado del aneurisma cerebral. No existe evidencia para recomendar el uso de
antiepilépticos como prevención de crisis comiciales, pero sí cuando el paciente presenta una crisis para
que no reaparezcan. No existe evidencia tampoco para mantener el tratamiento anticomicial a largo plazo,
salvo antecedente de epilepsia previo o hematomas intraparenquimatosos o infartos tras HSA. El fármaco
con la mejor relación beneficio-riesgo es el levetiracetam.
7.3.5. Hiponatremia
Aparece hasta en el 10-30% de los casos en relación con natriuresis elevadas (síndrome pierde sal)
y en menor medida a síndrome de secreción inapropiada de hormona antidiurética. Se debe tratar
mediante sueros hipertónicos y evitar la restricción hídrica.
IV. TROMBOSIS VENOSA CEREBRAL
1. CONCEPTO Y ETIOLOGÍA
La trombosis venosa cerebral (TVC) es una oclusión trombótica de las venas y/o senos venosos que
se encargan del drenaje venoso del encéfalo. Presenta múltiples causas (Tabla XVI) y puede tratarse de un
cuadro clínico muy grave. La etiología más frecuente en niños es la infecciosa, a partir de infecciones
sinusales y óticas. En los adultos es predominante la etiología secundaria a estados de hipercoagulabilidad,
como el embarazo, el puerperio o el uso de anticonceptivos.
2. APROXIMACIÓN DIAGNÓSTICA
1. MANIFESTACIONES CLÍNICAS
El inicio clínico suele ser subagudo, aunque puede comenzar de forma súbita o crónica. La cefalea
es el síntoma más frecuente y precoz, suele ser difusa, progresiva, muy intensa y acompañada de signos y
síntomas de hipertensión intracraneal. Puede acompañar pérdida visual transitoria o permanente,
focalidad neurológica fluctuante o alternante, disminución del nivel de consciencia o crisis comiciales. La
TVC profunda puede cursar como un coma de inicio agudo y alta gravedad. La trombosis del seno
cavernoso suele manifestar exoftalmos no pulsátil y sin soplos, quemosis conjuntival, edema palpebral y
dolor ocular con oftalmoplejía por afectación de los nervios oculomotores (III, IV y VI), cuyo recorrido
atraviesa el seno cavernoso.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1392]
[85] ENFERMEDAD CEREBROVASCULAR
2. PRUEBAS COMPLEMENTARIAS
El método de elección para el diagnóstico y seguimiento de la TVC es la RMN y la angio-RMN
cerebral. La TC craneal puede mostrar signos indirectos como edema, infarto o realce con contraste de la
hoz y el tentorio, como consecuencia de venas colaterales ingurgitadas. En la TC sin contraste el “signo de
la cuerda” se corresponde con la hiperdensidad de la vena trombosada; en la TC con contraste se puede
observar el “signo del delta vacío”, que se define como una hiperdensidad de forma triangular (contraste
retenido), delimitando una zona hipodensa que corresponde con el trombo en el seno sagital superior (solo
se observa en un 30% de los casos). Puede utilizarse la angiografía cerebral cuando las anteriores no sean
diagnósticas y exista una sospecha fundada. El estudio de líquido cefalorraquídeo está indicado ante
pacientes con síntomas de hipertensión intracraneal, sospecha clínica y pruebas de neuroimagen normales.
Confirmará la elevación de la presión y permite completar el estudio etiológico cuando se sospeche una
causa inflamatoria, infecciosa o tumoral. Los D-dímeros se elevan en esta situación clínica.
3. TRATAMIENTO
Se debe iniciar tratamiento con heparina sódica o HBPM, aunque existan lesiones hemorrágicas
asociadas (en estos casos se prefiere la HBPM). Posteriormente, se iniciará anticoagulación oral durante
tres a seis meses, o más tiempo según la causa subyacente, que también deberá tratarse. En casos graves
seleccionados puede considerarse el uso de agentes trombolíticos locales en el seno trombosado o la
trombectomía mecánica por neurorradiólogos expertos. Para la hipertensión intracraneal puede utilizarse
acetazolamida y punciones lumbares evacuadoras o colocación de sistema drenaje de LCR si fuera preciso.
BIBLIOGRAFÍA
Abilleira S, Cardona P, Ribó M, et al. Outcomes of a contemporary cohort of 536 consecutive patients
with acute ischemic stroke treated with endovascular therapy. Stroke. 2014;45:1046-52.
Berkhemer OA, Fransen PS, Beumer D, et al. A randomized trial of intraarterial treatment for acute
ischemic stroke. N Engl J Med. 2015;372:11-20.
Campbell BCV, Mitchell PJ, Kleinig TJ, et al. Endovascular therapy for ischemic stroke with perfusion-
imaging selection. N Engl J Med. 2015;372:1009-18.
Charpentier C, Audibert G, Guillemin F, et al. Multivariate analysis of predictors of cerebral vasospasm
occurrence after aneurysmal subarachnoid hemorrhage. Stroke. 1999;30:1402-1408.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1393]
[85] ENFERMEDAD CEREBROVASCULAR
Easton D, Saver JL, Alberts GW, et al. Definition and evaluation of transient ischemic attack. A Scientific
Statement for Healthcare Professionals from the American Council J. Heart Association/American
Stroke Association. Stroke. 2009;40:2276-93.
Fisher CM, Kistler JP, Davis JM. Relation of cerebral vasospasm to subarachnoid hemorrhage visualized
by computerized tomographic scanning. Neurosurgery. 1980;6:1-9.
Gallego JA, et al. Guía para el tratamiento preventivo del ictus isquémico y AIT (I). Actuación sobre los
factores de riesgo y estilo de vida. Neurología. 2012;27(9):560-74.
Gallego JA, et al. Guía para el tratamiento preventivo del ictus isquémico y AIT (II). Actuación sobre los
factores de riesgo y estilo de vida. Neurología. 2014;29(3):168-83.
Gonzalez J, Rodriguez M, Sepulveda JM. Urgencias en Neurología, Hospital Universitario 12 de Octubre.
Madrid: Jarpyo editores; 2006.
Goyal M, Demchuk AM, Menon BK, et al. Randomized assessment of rapid endovascular treatment of
ischemic stroke. N Engl J Med. 2015;372:1019-30.
Hemphill JC, Greenberg SM, Anderson CS, et al. Guidelines for the management of spontaneous
intracerebral hemorrhage. A Guideline for Healthcare Professionals From the American Heart
Association/American Stroke Association. Stroke. 2015;46(7):2032-60. – Hernesniemi J, Koivisto T.
Comments on “The impact of the International Subarachnoid Aneurysm Treatment Trial (ISAT) on
neurosurgical practice”. Acta Neurochir (Wien). 2004;146(2):203-8.
Jauch EC, Saver JL, Adams HPJ, et al. Guidelines for the early management of patients with acute
ischemic stroke: a guideline for healthcare professionals from the American Heart
Association/American Stroke Association. Stroke. 2013;44:870-947.
Kidwell CS, Jahan R, Gornbein J, et al. MR RESCUE Investigators. A trial of imaging selection and
endovascular treatment for ischemic stroke. N Engl J Med. 2013;368:914-23.
Lagares A, Cicuendez M, Ramos A, et al. Acute perfusion changes after spontaneous SAH: A perfusion
CT study. Acta Neurochir (Wien). 2012;154(3):405-11.
Lagares A, Gómez PA, Alén JF, et al. Hemorragia subaracnoidea aneurismática: guía de tratamiento del
Grupo de Patología Vascular de la Sociedad Española de Neurocirugía. Neurocirugía. 2011;22:93-115.
Lagares A, Gómez PA, Lobato RD, et al. Prognostic factors on hospital admission after spontaneous
subarachnoid haemorrhage. Acta Neurochir (Wien). 2001;143(7):665-72.
Leciñana MA, Díaz-Guzmán J, Egido JA, et al. Endovascular treatment in acute ischaemic stroke. A
stroke care plan for the region of Madrid. Neurologia. 2013;28:425-34.
Leciñana MA et al. Guidelines for treatment of acute ischaemic stroke. Neurologia. 2014;22:102-22
Leciñana MA, Fuentes B, Ximénez-Carrillo Á, et al. A collaborative system for endovascular treatment of
acute ischaemic stroke: the Madrid Stroke Network experience. Eur J Neurol. 2015. DOI:
10.1111/ene.12749. PubMed PMID: 26073869.
Molyneux AJ, Kerr RS, Yu LM, et al. International subarachnoid aneurysm trial (ISAT) of neurosurgical
clipping versus endovascular coiling in 2143 patients with ruptured intracranial aneurysms: A
randomised comparison of effects on survival, dependency, seizures, rebleeding, subgroups, and
aneurysm occlusion. Lancet. 2005;366(9488):809-17.
Ohkuma H, Manabe H, Tanaka M, Suzuki S. Impact of cerebral microcirculatory changes on cerebral
blood flow during cerebral vasospasm after aneurysmal subarachnoid hemorrhage. Stroke.
2000;31:1621-1627.
Pérez-Núñez A, Alday R, Rivas JJ, et al. Tratamiento quirúrgico de la hemorragia intracerebral
espontánea. Parte II: Hemorragia infratentorial. Neurocirugía. 2008;19:101-112.
Pérez-Núñez A, Lagares A, Pascual B, et al. Tratamiento quirúrgico de la hemorragia intracerebral
espontánea. Parte I: Hemorragia supratentorial. Neurocirugía. 2008;19:12-24.
Protocolo para el tratamiento endovascular en el ictus isquémico agudo. Documento de consenso,
Plan de Atención del Ictus de la Comunidad de Madrid. Asociación Madrileña de Neurología 2015.
Roda JM, Conesa G, Díez Lobato R, et al. Hemorragia subaracnoidea aneurismática. Introducción a
algunos de los aspectos más importantes de esta enfermedad. Neurocirugia. 2000;11(3):156-168.
Saver JL, Goyal M, Bonafe A, et al. Stent-retriever thrombectomy after Intravenous t-PA vs. t-PA Alone in
Stroke. N Engl J Med. 2015;372:2285-95.
Steiner T, et al. European Stroke Organisation (ESO) guidelines for the management of spontaneous
intracerebral hemorrhage. World Stroke Organization. 2014;9:840-55.
Van Gijn J, Rinkel GJ. Subarachnoid haemorrhage: diagnosis, causes and management. Brain.
2001;124 (Pt 2):249-78.
Vergouwen MD et al. Microthrombosis after aneurysmal subarachnoid hemorrhage: An additional
explanation for delayed cerebral ischemia. J Cereb Blood Flow Metab. 2008;28(11):1761-70.
Wijdicks EFM, Sheth KN, Carter BS, et al. Recommendations for the management of cerebral and
cerebellar infarction with swelling. A statement for healthcare professionals from the american heart
association/american stroke association. Stroke. 2014;45(4):1222-38.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1394]
[86] CRISIS COMICIALES
86.Crisis comiciales
Lorena García Vasco.
Neurología
Coral Arévalo Cañas.
Medicina Interna
Asesora:
Rosa Ana Saiz Díaz.
Médica Adjunta de Neurología. Unidad de Epilepsia
I. CONCEPTO
Se define como crisis epiléptica la aparición de signos y síntomas transitorios debidos a una
descarga anormal, sincronizada y excesiva de neuronas corticales. Se considera epilepsia a la alteración
cerebral caracterizada por la predisposición permanente para generar crisis y por las consecuencias
neurobiológicas, cognitivas, psicológicas y sociales derivadas de esta condición; en ciertos casos su
diagnóstico es posible tras una crisis no provocada aislada. Por lo tanto, se puede considerar a un paciente
como epiléptico si ha sufrido un único episodio comicial y, además, presenta una alteración cerebral
mantenida capaz de inducir nuevas crisis. La epilepsia no es una enfermedad única, sino un conjunto de
síndromes, siendo el concepto de síndrome epiléptico el resultado de la conjunción de diferentes criterios:
tipo de crisis, tipo de anomalías en el electroencefalograma (EEG), edad de inicio, factores precipitantes,
etiología, localización del foco, pronóstico y tratamiento. Si la causa está bien determinada, se denomina
enfermedad epiléptica.
La epilepsia afecta en torno al 1-3% de la población de forma bimodal, con dos picos, uno en la
infancia y otro en la senectud, estimándose que el 10% de la población general puede presentar una crisis a
lo largo de su vida.
Las crisis comiciales son, por lo general, autolimitadas. Su duración es aproximadamente de 1-2
minutos y pueden seguirse de un periodo variable de depresión cerebral llamado periodo poscrítico que
puede ser focal (debilidad en las extremidades o “parálisis de Todd”, afasia, alteraciones sensitivas) o difuso
(somnolencia, agitación).
II. CLASIFICACIÓN DE LAS CRISIS COMICIALES
La clasificación clásica de las crisis epilépticas está en constante proceso de renovación, con
propuestas de cambio en los últimos años, si bien se mantiene en vigor la clasificación que, de manera
práctica, las divide en: crisis generalizadas, crisis parciales o focales, y crisis no clasificables.
1. CRISIS GENERALIZADAS
La crisis se origina en algún punto de la red neuronal y rápidamente se propaga por esta al resto de
la corteza, englobando ambos hemisferios cerebrales. Actualmente se admite que este tipo de crisis
pueden ser asimétricas y que una crisis generalizada no necesariamente debe incluir la totalidad de la
corteza cerebral. Dentro de este tipo de crisis se distinguen:
Crisis tónico-clónicas: cuya clínica típica consiste en una pérdida súbita de la consciencia
seguida de una fase tónica de 10-30 segundos, movimientos clónicos de las cuatro
extremidades de predominio proximal, que van disminuyendo en frecuencia y aumentando en
amplitud, para finalmente seguirse de un periodo de confusión poscrítico.
Crisis de ausencia: se caracterizan por un mínimo componente motor.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1395]
[86] CRISIS COMICIALES
Típicas: consisten en una pérdida de la consciencia de segundos de duración, y se
pueden acompañar de automatismos simples (parpadeo, muecas faciales), con inicio y
fin bruscos, sin periodo poscrítico y con un EEG típico, con descargas generalizadas de
punta-onda a 3 Hz. Son típicas de la infancia y la adolescencia.
Atípicas: su principal diferencia con respecto a las típicas es que el trastorno de la
consciencia suele ser menor y presentan un inicio y un fin menos repentinos.
Ausencia con características especiales: crisis de ausencia mioclónicas y ausencia con
mioclonías palpebrales.
Crisis mioclónicas: consisten en sacudidas musculares súbitas, breves e irregulares que pueden
ser focales, axiales o generalizadas. Son más comunes en la infancia y la adolescencia.
Constituyen el único tipo de crisis generalizadas en las que el nivel de consciencia no está
alterado.
Crisis clónicas: consisten en movimientos clónicos de las cuatro extremidades, a menudo
asimétricos e irregulares.
Crisis tónicas: se caracterizan por una contracción muscular mantenida de corta duración axial
o de las extremidades.
Crisis atónicas (astáticas): consisten en una pérdida brusca del tono muscular, que ocasiona
caídas y el consiguiente riesgo de traumatismo. Son más frecuentes en niños.
2. CRISIS PARCIALES O FOCALES
La crisis se origina en algún punto de la red neuronal y se limita a un hemisferio. La última
clasificación propone no subdividir este apartado; sin embargo, se mantiene la descripción por razones
operativas y conceptuales.
Simples: cursan sin alteración del nivel de consciencia. Los síntomas o signos presentados se
correlacionan con el área cortical donde se origina la descarga, y se subdividen, de este modo,
en motoras, sensitivas, autonómicas o psíquicas. La crisis parcial simple sin síntomas motores
se denomina aura, y puede preceder a crisis parciales complejas o generalizadas.
Complejas: producen alteración del nivel de consciencia. Pueden presentarse como alteración
aislada del nivel de consciencia o comenzar desde una crisis parcial simple. Suele existir
confusión poscrítica, de duración variable. Son frecuentes los automatismos (actos
estereotipados simples o complejos, como chupeteo, toqueteo de la ropa o frotamiento de las
manos).
Secundariamente generalizadas: son crisis generalizadas que evolucionan tras una crisis parcial
simple o compleja.
3. CRISIS NO CLASIFICABLES
III. ETIOLOGÍA
Se deben diferenciar factores etiológicos, como causa directamente responsable de las crisis, y
factores precipitantes, que son los que facilitan la aparición de crisis en una persona predispuesta
(privación de sueño, estrés, fiebre, procesos sistémicos, tóxicos, menstruación). Según el mecanismo que
desencadena las crisis, se distinguen tres tipos de epilepsias:
1. IDIOPÁTICAS/GENÉTICAS
Son aquellas en las que no se encuentra una causa subyacente, salvo una presumible
predisposición genética. La exploración y las pruebas de neuroimagen son normales, con patrones EEG
característicos. Su aparición y curso clínico dependen de la edad y, en general, tienen buen pronóstico.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1396]
[86] CRISIS COMICIALES
2. SINTOMÁTICAS
Se deben a un trastorno subyacente conocido del sistema nervioso central (SNC), ya sea congénito
o adquirido (enfermedades cerebrovasculares, degenerativas, tumores, traumatismo craneoencefálico
[TCE], infecciones, malformaciones, etc.). La exploración y la neuroimagen suelen ser anormales, con un
pronóstico peor que las anteriores. La edad de aparición de las crisis orienta a las etiologías más probables
(Tabla I).
3. PROBABLEMENTE SINTOMÁTICAS
Aquellas en las que se sospecha la existencia de un trastorno del SNC que no puede determinarse
con los medios diagnósticos disponibles.
IV. APROXIMACIÓN DIAGNÓSTICA
En la valoración de una posible crisis epiléptica en el Servicio de Urgencias se seguirán estos pasos:
1. ANAMNESIS
El diagnóstico de una crisis es clínico, con una especificidad del 70-80%, mayor cuanto más
exhaustiva y minuciosa sea la historia clínica, que será la herramienta diagnóstica principal y permitirá
hacer el diagnóstico diferencial con otras entidades como el síncope o las crisis psicógenas. Hay que tener
en cuenta que, ante la duda, es mejor esperar a un segundo episodio antes de establecer el diagnóstico.
¿Es una crisis epiléptica? Es fundamental el interrogatorio, tanto al paciente como a los
testigos presenciales si los hubiese. Es de gran utilidad solicitar a familiares y al personal del
hospital que, en caso de presenciar una sospecha de crisis, graben en vídeo el episodio para
valorarlo con objetividad. En cuanto a la anamnesis, es prioritario conocer:
Antes del episodio: interrogar sobre síntomas que orienten hacia la presencia de aura
epiléptica (fenómeno subjetivo y estereotipado de características sensoriales,
psíquicas, autonómicas o epigástricas que precede a la crisis y que el paciente
reconoce, como, por ejemplo, fenómenos de déjà vu) y situación en que se inició el
episodio (vigilia, sueño, cambios posturales).
Durante el episodio: interrogar sobre el inicio (comportamientos extraños,
automatismos, movimientos focales) y su secuencia, así como otras manifestaciones:
grito inicial, cianosis labial, trastornos motores (simétricos o no), sensitivos, vegetativos
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1397]
[86] CRISIS COMICIALES
o cognitivos. La desconexión del medio (incluida la amnesia del episodio) va a favor de
crisis epiléptica. La presencia de relajación de esfínteres y mordedura lingual son
hallazgos inespecíficos. Puede ser útil pedir a los familiares que imiten los movimientos
del paciente. También se debe preguntar sobre la duración de los síntomas (que
generalmente suele ser inferior a 2 minutos) y la velocidad de instauración.
Después del episodio: conocer si el paciente permaneció inconsciente después del
evento, confuso, o con focalidad neurológica, definiendo un estado poscrítico que
orienta hacia una crisis epiléptica.
¿Hay antecedentes o desencadenantes? Indagar sobre la existencia de episodios previos que
hayan podido pasar desapercibidos (incluidos sucesos durante el sueño), así como recabar
otros antecedentes que puedan estar relaciondos con crisis (patología perinatal, infecciones,
ictus, traumatismo cerebral, convulsiones febriles, historia familiar de epilepsia). Preguntar
también por la existencia de factores predisponentes (Tabla II).
En todo paciente epiléptico conocido en el que no se haya detectado un factor desencadenante
evidente o si, a pesar del mismo, hay un cambio en el contexto clínico o tipo de crisis epiléptica, se
procederá al diagnóstico como en un primer episodio de crisis para descartar patologías agudas
potencialmente graves.
2. EXPLORACIÓN FÍSICA
Esta debe ser sistemática e incluir una exploración neurológica completa, y es importante conocer
el tiempo transcurrido desde la crisis. En un periodo inmediato puede existir confusión poscrítica (apoya el
diagnóstico de crisis epiléptica), meningismo y datos localizadores, como disfasia o paresia postictal de
Todd, que se suele resolver en las primeras 48 horas. Se pueden observar signos físicos que son el resultado
de una crisis, como mordedura de la lengua, TCE, luxación del hombro, etc., así como otros datos que
sugieran causas de crisis agudas sintomáticas, como fiebre, irritación meníngea o alteración del nivel de
consciencia más allá de la crisis. Monitorizar la tensión arterial y el ritmo cardiaco puede ser útil para el
diagnóstico diferencial con eventos de origen vegetativo o cardiogénico.
3. PRUEBAS COMPLEMENTARIAS
Aportan información básica para determinar la etiología y establecer un diagnóstico sindrómico
que permita elegir el tratamiento más adecuado.
Analítica: hemograma y bioquímica general, incluyendo tóxicos para despistaje de crisis
sintomática aguda. En caso de pacientes epilépticos, determinar los niveles de fármacos para
valorar el cumplimiento terapéutico. En el periodo poscrítico inmediato puede encontrarte
leucocitosis, elevación de creatina-cinasa (CPK) y acidosis metabólica con lactato elevado.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1398]
[86] CRISIS COMICIALES
Electrocardiograma (ECG): contribuye al diagnóstico diferencial con síncopes y alteraciones del
ritmo cardiaco, que pueden contraindicar la administración de fármacos antiepilépticos (FAE)
como fenitoína o carbamazepina.
Neuroimagen: se debe realizar una prueba de neuroimagen (resonancia magnética [RM]
preferiblemente, o tomografía computarizada [TC] urgente que descarte lesiones estructurales
groseras que obliguen a un manejo específico) a todo paciente adulto no epiléptico conocido
con una primera crisis no sintomática aguda. La información proporcionada tiene valor tanto
diagnóstico como pronóstico, ya que en presencia de lesiones estructurales el riesgo de
recurrencia es mayor y apoya la instauración de tratamiento con FAE. En pacientes con
diagnóstico previo de epilepsia sin sospecha de proceso agudo asociado, no es necesaria su
realización, salvo que exista un cambio en la semiología, duración o frecuencia de las crisis,
infección por el virus de la inmunodeficiencia humana (VIH) o inmunosupresión, antecedente
de cáncer, o estado poscrítico prolongado.
Punción lumbar: no es una prueba de rutina, salvo si hay sospecha de infección del SNC,
hemorragia subaracnoidea o pacientes VIH e inmunodeprimidos con crisis de etiología
desconocida, una vez descartada lesión estructural por neuroimagen. Puede aparecer
pleocitosis leve en el líquido cefalorraquídeo (LCR) tras una crisis prolongada o en el seno de un
estatus epiléptico.
EEG: permite apoyar el diagnóstico, pero en ningún caso excluirlo ante un EEG normal. Ayuda a
determinar el tipo de crisis (incluso de síndrome epiléptico) y el riesgo de recurrencia, y puede
mostrar alteraciones sugerentes de lesiones focales subyacentes. La sensibilidad es mayor
dentro de las primeras 48 horas tras la crisis, y el rendimiento aumenta con la repetición de los
estudios. Las indicaciones de EEG urgente se resumen en la tabla III.
4. DIAGNÓSTICO DIFERENCIAL
Se recoge en la tabla IV, que detalla los siguientes:
Síncope (ver Capítulo 8. “Síncope”): durante un síncope pueden aparecer movimientos
involuntarios, que ocurren con mayor frecuencia si el paciente permanece incorporado, debido
a la hipoperfusión cerebral. Estos movimientos suelen ser de tipo clónico-mioclónico, con una
duración menor que en la crisis epiléptica (15 segundos) y de características no tan amplias,
rítmicas y sincrónicas como en esta. Comienzan tras la pérdida de consciencia y la caída, a
diferencia de las crisis. La presencia de incontinencia de esfínteres no es un factor
diferenciador, pues pueden darse en ambos casos. En el síncope, la recuperación es completa
de forma rápida, y la desorientación y la somnolencia posterior son breves (menos de 5
minutos).
Crisis psicógena: predominan en el sexo femenino, entre los 20-30 años y en pacientes con
comorbilidad psiquiátrica. Suelen durar más de 2 minutos, a diferencia de las crisis, con fases
de intensificación y cese de movimientos de forma repetitiva, acompañado en ocasiones de
llantos y vocalizaciones. Los movimientos son descoordinados, con ojos cerrados (ofreciendo
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1399]
[86] CRISIS COMICIALES
oposición a su apertura) y no existe periodo confusional poscrítico. Pueden suponer un reto
diagnóstico, y es de gran utilidad la realización de un EEG.
V. TRATAMIENTO
1. MEDIDAS GENERALES
Ante una crisis comicial se debe: 1) asegurar el entorno del paciente (evitar traumatismos, no
introducir nada en la boca), colocándolo posteriormente en decúbito lateral; 2) mantener la vía aérea
permeable; 3) canalizar dos vías venosas periféricas; 4) iniciar medicación inmediata si procede; 5)
descartar causas que requieran tratamiento urgente (hipoglucemia, hipoxia, hipertensión intracraneal,
intoxicaciones, infección del SNC, eclampsia).
En función de la causa de las crisis, su frecuencia y su dificultad de control, se valorará el ingreso
hospitalario.
En caso de un paciente epiléptico conocido que presenta una crisis de características similares a las
suyas habituales, una vez valorados los factores concomitantes que puedan estar influyendo (mal
cumplimiento terapéutico, desencadenantes como tóxicos, privación de sueño, interacciones, etc.), no es
necesario mantenerlo en observación durante 24 horas.
En caso del paciente no epiléptico, se seguirá el algoritmo expuesto en la figura 1.
2. TRATAMIENTO FARMACOLÓGICO
2.1. Indicaciones
Tras una primera crisis, el tratamiento farmacológico se ha de individualizar:
En el caso de crisis sintomáticas agudas, el tratamiento es el de la causa que las provoca,
aunque puede ser necesario iniciar un FAE de forma transitoria si las crisis no se controlan
fácilmente.
Si se trata de una primera crisis no provocada, en general, no es necesario tratamiento, excepto
si existe alguno de los datos resumidos en la tabla V. En función de la situación clínica,
sospecha diagnóstica y demora en las consultas de especialista ambulatorias, se puede aplazar
la decisión de inicio de tratamiento ante una primera crisis no provocada, no siendo en
ocasiones adecuado iniciarlo de forma urgente. Las últimas evidencias demuestran que el inicio
de tratamiento tras una primera crisis reduce el riesgo de recurrencia en los siguientes 2 años
(periodo de mayor riesgo), pero no mejora la calidad de vida ni el pronóstico de remisión o de
desarrollo de epilepsia a largo plazo.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1400]
[86] CRISIS COMICIALES
2.2. Medidas generales
Mantener un estilo de vida saludable, realizando actividad física regular y evitando factores
desencadenantes como alcohol, tóxicos, estrés emocional y privación de sueño. En el caso de epilepsias
fotosensibles, se recomienda evitar destellos luminosos, mantener una distancia de al menos 2 metros de
pantallas de televisión y videojuegos, así como no emplearlos en la oscuridad.
2.3. Fármacos antiepilépticos (FAE)
Como norma general, se debe iniciar tratamiento en monoterapia a dosis bajas, para minimizar los
efectos secundarios, con incrementos graduales. Se debe elegir el fármaco en función del tipo de crisis
(Tabla VI), la edad, el perfil de efectos secundarios y la comorbilidad. La dosis de mantenimiento será la
mínima dosis eficaz que controle las crisis. Si el fármaco prescrito no es efectivo o aparece toxicidad, se
valorará introducir de forma progresiva un segundo FAE hasta alcanzar dosis terapéuticas y retirar
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1401]
[86] CRISIS COMICIALES
lentamente el primero, intentando evitar en la medida de lo posible la politerapia. Los principales FAE y sus
indicaciones se resumen en la tabla VII.
Datos útiles a la hora de escoger entre diversos FAE:
Paciente migrañoso: topiramato, zonisamida.
Mujer en edad fértil: lamotrigina, carbamazepina. Evitar ácido valproico y fenobarbital.
Personas obesas: topiramato, zonisamida. Evitar ácido valproico.
Pacientes ancianos, pluripatológicos: levetiracetam, lamotrigina.
Crisis de ausencias típicas: ácido valproico, etosuximida. Evitar carbamazepina, fenitoína.
Mioclonías: ácido valproico, clonazepam. Evitar carbamazepina, fenitoína, lacosamida. −
Fotosensibilidad: ácido valproico.
Síndrome de West: corticotropina (ACTH), esteroides, vigabatrina.
Eclampsia: sulfato de magnesio.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1402]
[86] CRISIS COMICIALES
2.4. Interacciones farmacológicas
Se debe tener en cuenta que algunos FAE tienen características inductoras (carbamazepina,
fenitoína, fenobarbital) y otros inhibidoras (ácido valproico) sobre otros medicamentos que son
metabolizados por el citocromo P450.
2.5. Niveles plasmáticos
Es útil su determinación para el ajuste de dosis, descartar toxicidad y comprobar el cumplimiento
terapéutico. No obstante, hay que tener en cuenta que puede haber pacientes correctamente controlados
con niveles fuera del rango teórico ideal. La extracción debe realizarse en valle, es decir, 8-12 horas tras la
última dosis (primera hora de la mañana en ayunas). Los niveles plasmáticos y posología de los FAE (vo e iv)
se resumen en las Tablas VIII y IX.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1403]
[86] CRISIS COMICIALES
2.6. Epilepsia y conducción
Según se recoge en el Boletín Oficial del Estado (BOE), todo paciente con epilepsia que haya sufrido
una crisis comicial convulsiva o con pérdida de consciencia no podrá conducir un vehículo particular hasta
completar al menos un año libre de crisis. En caso de crisis exclusivamente durante el sueño (crisis
morfeicas), se ha de constatar que durante al menos un año solo presenta este tipo de crisis y solo durante
el sueño. En el caso de conductores profesionales, se exigen al menos diez años libres de crisis y sin
tratamiento antiepiléptico. Para más información, en función del contexto y el tipo de crisis, se recomienda
consultar: http://boe.es/diario_boe/txt.php?id=BOE-A-2010-13946.
VI. ESTATUS EPILÉPTICO
Tradicionalmente se considera estatus epiléptico aquella crisis que dura más de 30 minutos o crisis
encadenadas sin recuperación del nivel de consciencia entre ellas durante el mismo periodo de tiempo.
Desde un punto de vista operativo, se debe iniciar tratamiento urgente en las crisis convulsivas de duración
mayor de 5-10 minutos, así como determinar la causa que lo produce (en pacientes con epilepsia conocida,
la principal causa es la interrupción del tratamiento o cambios recientes en este). Existen diversas
clasificaciones en función del tipo de crisis. Una aproximación práctica basada en su semiología las divide
en estatus epiléptico convulsivo y estatus epiléptico no convulsivo.
1. ESTATUS EPILÉPTICO CONVULSIVO
Es, fundamentalmente, tónico-clónico generalizado. Es una urgencia neurológica con alta
morbimortalidad (que depende de la causa desencadenante, la duración, la edad y la patología
concomitante).
Se divide en varias fases:
Estatus epiléptico en desarrollo o inminente: convulsiones tónico-clónicas generalizadas (CTCG)
que se prolongan durante más de 5 minutos o crisis intermitentes sin recuperación del nivel de
consciencia entre las mismas durante más de 15 minutos. Se ha de iniciar tratamiento con FAE
intravenosos, aun asumiendo que en algunos casos las crisis podrían cesar espontáneamente.
Estatus epiléptico establecido: crisis continuas o intermitentes sin recuperación de la
consciencia entre ellas durante más de 30 minutos.
Estatus epiléptico refractario: aquel que se prolonga más de 60 minutos o no responde a dos o
tres líneas de tratamiento intravenoso.
Estatus epiléptico superrefractario: aquel que persiste tras 24 horas o más tras el inicio de
agentes anestésicos o recurre tras su intento de descenso o retirada.
Todo estatus epiléptico convulsivo requiere tratamiento rápido y agresivo, como se detalla en la
figura 2.
2. ESTATUS EPILÉPTICO NO CONVULSIVO (ENC)
Se caracteriza por un cambio en el nivel de alerta del paciente, que puede variar desde la alteración
de la conducta hasta el coma, sin signos clínicos motores evidentes (puede haber movimientos sutiles),
durante más de 30 minutos, asociado a alteraciones epileptiformes en el EEG. Necesita un alto índice de
sospecha y es fundamental un EEG urgente para su diagnóstico. Los principales tipos y su tratamiento son:
Estatus epiléptico no convulsivo (ENC) parcial complejo: es el más frecuente. Se produce
alteración variable de la consciencia (desde confusión hasta coma), y se puede acompañar de
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1404]
[86] CRISIS COMICIALES
mínimos automatismos motores y dificultad en el lenguaje si afecta al hemisferio dominante. El
tratamiento es similar al del estatus convulsivo (Figura 2).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1405]
[86] CRISIS COMICIALES
ENC de ausencias: puede presentarlo un paciente con una epilepsia generalizada idiopática y de
novo. Este último aparece principalmente como cuadro de desconexión/confusión en ancianos,
asociado a retirada brusca de fármacos psicotropos (benzodiazepinas, sobre todo). Se trata
restituyendo el tratamiento interrumpido previo más benzodiazepinas por vía oral (o a bajas
dosis por vía intravenosa). Si no responde, emplear ácido valproico.
ENC sutil: es un estatus refractario que aparece tras CTCG o estatus convulsivos que no han
respondido al tratamiento o si este ha sido insuficiente. Requiere ingreso en la unidad de
cuidados intensivos (UCI) para tratamiento con agentes anestésicos.
VII. SITUACIONES ESPECIALES
1. ENFERMEDAD GASTROINTESTINAL
Puede existir retraso en la absorción de los FAE. Ajustar la dosis en función de la clínica y los niveles
del fármaco en sangre, incluso cambiar a vía intravenosa si es preciso.
2. ENFERMEDAD HEPÁTICA
Elegir FAE que no interfieran con el metabolismo hepático y que tengan escasa unión a proteínas
plasmáticas (por ejemplo, levetiracetam, topiramato, lacosamida). Evitar las benzodiazepinas (pueden
precipitar una encefalopatía hepática en pacientes que estaban previamente compensados), el
fenobarbital, la fenitoína y el valproato (ya que por su marcada unión a proteínas plasmáticas, en caso de
hipoalbuminemia aumenta la fracción libre del fármaco).
3. INSUFICIENCIA RENAL
Se deben ajustar las dosis de todos los FAE, porque se altera la unión a proteínas plasmáticas y la
eliminación renal de los que no se unen a proteínas. Los fármacos de elección son los excretados por
biotransformación hepática (ácido valproico, lamotrigina, benzodiazepinas). En caso de hemodiálisis,
cuanto mayor es la unión a proteínas plasmáticas, menor es la efectividad con que se dializan. Por ello,
dada su baja unión a proteínas, requieren administración suplementaria tras la hemodiálisis: levetiracetam,
topiramato, fenobarbital y primidona.
4. INFECCIÓN POR VIH
Los FAE inductores enzimáticos disminuyen la efectividad de los antirretrovirales. El levetiracetam
puede ser una alternativa en casos de interacciones que comprometan la eficacia de los fármacos.
5. ENFERMEDAD CARDIOVASCULAR
La administración de fenitoína en infusión en pacientes con enfermedad cardiaca puede causar
arritmias o hipotensión, y está contraindicada en pacientes con enfermedad miocárdica grave, bradicardia
sinusal y bloqueos aurículo-ventriculares de segundo y tercer grado, siendo la alternativa en estos casos el
ácido valproico. Posibles interacciones:
Los fármacos inductores enzimáticos interaccionan con los calcioantagonistas y algunos
antiarrítmicos, y también aumentan el metabolismo de los dicumarínicos.
El ácido valproico y los nuevos FAE no interaccionan con los anticoagulantes.
Las concentraciones plasmáticas de digoxina pueden disminuir con la administración de
fenitoína o topiramato.
La hiponatremia por diuréticos puede incrementarse en casos de toma de carbamazepina u
oxcarbazepina y eslicarbazepina.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1406]
[86] CRISIS COMICIALES
Los salicilatos pueden incrementar los niveles de ácido valproico o fenitoína por
desplazamiento de su unión a proteínas o inhibición de su metabolismo.
6. PROCEDIMIENTOS QUIRÚRGICOS
Los pacientes que antes de la intervención tomaban antiepilépticos por vía oral que disponen de
presentación parenteral deben cambiar a esta vía de administración hasta que toleren de nuevo la vía oral.
Si están siendo tratados con fármacos sin presentación parenteral, lo indicado es que previamente a la
cirugía se administre una dosis superior a lo normal y continuar con la vía oral lo antes posible. Si se prevé
ayuno prolongado, se debe sustituir el fármaco que tomaba por otro de administración parenteral, con una
dosis de carga previa a la cirugía.
7. EMBARAZO
Se recomienda mantener el tratamiento que mejor controle las crisis a la menor dosis posible,
prefiriendo la monoterapia. El ácido valproico es el que mayor riesgo teratógeno posee, por lo que debe
evitarse en las mujeres en edad fértil. La lamotrigina y la carbamazepina son los fármacos con menor
incidencia de malformaciones congénitas. Se recomienda aportar suplementos de ácido fólico. En caso de
crisis aguda, sobre todo si se trata de un estatus, se controlará como si se tratase de una no gestante. En el
control de la eclampsia se emplea sulfato de magnesio por vía intravenosa.
8. ADULTOS MAYORES DE 65 AÑOS
Pueden debutar epilepsias focales, principalmente por causa vascular y patologías degenerativas.
No se debe olvidar la posibilidad de aparición de estatus no convulsivo. Suelen presentar una respuesta
excelente al tratamiento, generalmente a dosis bajas de FAE, que deben mantenerse dada la elevada tasa
de recurrencia de crisis en este subgrupo (hasta del 90%) durante semanas o meses en el contexto de
patología aguda, individualizando el resto de casos según su contexto clínico y social. Como primera
elección en estos pacientes: levetiracetam (permite el ascenso rápido de dosis, con excelente tolerancia y
bajo potencial de interacciones), lamotrigina (escaso potencial de interacciones; requiere ascenso lento
gradual cada 2 semanas y su principal efecto adverso es el exantema cutáneo) y lacosamida.
BIBLIOGRAFÍA
Berg AT, Berkovic SF, Brodie MJ, Buchhalter J, Cross JH, van Emde Boas W, et al. Revised terminology
and concepts for organization of seizures and epilepsies: Report of the ILAE Commission on
Classification and Terminology, 2005-2009. Epilepsia. 2010;51(4):676-85.
Gómez L, Vilaplana L, Sancho J. Tratamiento de la epilepsia. Medicine. 2015;11(73):4374-84.
Krumholz A, Wiebe S, Gronseth GS, Gloss DS, Sánchez AM, Kabir AA, et al. Evidence-based guideline:
management of an unprovoked first seizure in adults. Neurology. 2015;84:1705-13.
Perrig S, Jallon P. Is the first seizure truly epileptic? Epilepsia. 2008;49(Supl 1):2-7.
Rodríguez JL, Aguilera M, Arévalo J. Diagnóstico y tratamiento médico. 2ª ed. Madrid: Marbán; 2015; p.
515-34.
Saiz RA, De la Peña P. Crisis comiciales. Urgencias en Neurología. 2ª ed. Madrid: Ergon; 2013; p. 59-
80.
Trinka E, Cock H, Hesdorffer D, Rossetti AO, Scheffer IE, Shinnar S, et al. A definition and classification
of status epilepticus: report of the ILAE task force on classification of status epilepticus. Epilepsia.
2015;56(10):1515-23.
Trinka E. What is the evidence to use new intravenous AEDs in status epilepticus? Epilepsia.
2011;52(Supl.8): 35-8.
Shorvon S. Super-refractory status epilepticus: an approach to therapy in this difficult clinical situation.
Epilepsia. 2011;52(Supl 8):53-6.
Wiebe S, Téllez-Zenteno JF, Shapiro M. An evidence-based approach to the first seizure. Epilepsia.
2008;49 (Supl 1):50-7.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1407]
[87] TRASTORNOS RELACIONADOS CON EL CONSUMO DE ALCOHOL
87.Trastornos relacionados con el consumo de alcohol
Jorge D. Gil Niño.
Medicina Interna
Samara Campos Escudero.
Medicina Interna
I. INTRODUCCIÓN Y DEFINICIONES
Desde el punto de vista clínico actualmente se utilizan las definiciones enmarcadas en las diferentes
propuestas del manual Diagnostic and Statistical Manual of Mental Disorders (DSM), concretamente DSM-
V, de reciente aparición.
De las definiciones anteriores del DSM-IV, el DSM-V ha sustituido abuso y dependencia por una
única definición, la de trastorno por consumo de alcohol, que sería el que aparece por un consumo de
alcohol propiciando problemas psicológicos, de comportamiento y psicosociales. El diagnóstico se establece
mediante un patrón problemático de consumo de alcohol que conlleva un deterioro o un malestar
clínicamente significativo, manifestado por al menos 2 de los criterios definidos (Tabla I) durante un
periodo de 12 meses.
Además, a partir de esta clasificación se puede estadificar la gravedad actual de la siguiente forma:
grado leve de dos a tres síntomas; grado moderado de cuatro a cinco síntomas; y grado severo de seis o
más síntomas.
Consumo de riesgo
Aunque existen factores de riesgo individuales (intrínsecos) para el desarrollo de patología orgánica
relacionada con el alcohol, hay que definir esta situación. Es aquella en la que existe riesgo para desarrollar
problemas relacionados con el tóxico según la cantidad ingerida.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1408]
[87] TRASTORNOS RELACIONADOS CON EL CONSUMO DE ALCOHOL
Es un concepto difícil de consensuar entre las diferentes sociedades científicas. El National Institute
on Alcohol Abuse and Alcoholism lo clasifica según el número de unidades de bebida estándar (UBE = 8-13 g
de alcohol puro) ingeridas:
Consumo de riesgo (riesgo de problemas por el alcohol): mujeres y varones > 65 años
más de 7 UBE por semana o más de 3 al día, varones < 65 años más de 14 UBE por
semana o más de 4 al día y cualquiera que consuma más 8 UBE en un periodo de varias
horas al menos una vez al mes.
Consumo episódico intenso (binge drinkins, asocian mayor riesgo cardiovascular y
daños por intoxicación aguda): mujeres y varones > 65 años 4 o más UBE en una
ocasión, varones < 65 años 5 o más UBE en una ocasión.
En la tabla II se expone la graduación de las bebidas alcohólicas más frecuentes.
II. DIAGNÓSTICO DE TRASTORNOS RELACIONADOS CON EL ALCOHOL
Anamnesis
Se debe interrogar por el consumo presente y pasado y por antecedentes familiares de consumo de
alcohol. Hay que cuantificar la cantidad de alcohol ingerida investigando sobre el consumo de riesgo. Para
el screening de trastornos relacionados con el consumo de alcohol existen diferentes cuestionarios, más
eficaces que las preguntas referidas a cantidad y frecuencia, los más utilizados en la actualidad son el CAGE
(es especialmente útil en las situaciones en las que la probabilidad de abuso es alta, como servicios de
urgencias) o el AUDIT-C (versión comprimida del cuestionario AUDIT con similar sensibilidad y especificidad,
86% y 78% respectivamente) (Tablas III y IV).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1409]
[87] TRASTORNOS RELACIONADOS CON EL CONSUMO DE ALCOHOL
Exploración física
Existen datos que nos hacen sospechar la presencia de consumo de alcohol, como temblor,
hipertensión, taquicardia, datos de neuropatía periférica y si existe daño hepático avanzado, estigmas de
hepatopatía crónica (eritema palmar, hipertrofia parotídea, contractura de Dupuytren, arañas vasculares y
telangiectasias).
Pruebas complementarias
En los estudios analíticos básicos podemos encontrar lo siguiente: macrocitosis (cierto grado de
anemia y trombopenia por toxicidad del propio alcohol, déficit de ácido fólico o por el desarrollo de
hipertensión portal), el 30% de los consumidores crónicos de alcohol presenta dislipidemia, especialmente
hipertrigliceridemias, pues es característico el aumento de GGT aislado > 50 U/l. La relación GOT/GPT > 2 es
muy sugestiva de consumo crónico.
La transferrina deficiente en carbohidratos (CDT) es una isoforma de la transferrina que aumenta
su concentración conforme se incrementa el consumo de alcohol. Es un marcador altamente específico (72-
99%) y con una sensibilidad variable (31-81%). Se consideran indicativos valores absolutos por encima de
20 U/l (varones) y 25 U/l (mujeres), y valores relativos los mayores del 6%. Los valores se normalizan a las 2
semanas de abstinencia, y aumentan tras una semana de consumo diario mayor a 40 g/día, por lo que
puede ser útil para la monitorización del tratamiento. La hepatopatía crónica ya establecida (sobrecarga
férrica) y la cirrosis biliar primaria son causas de falsos positivos.
III. TRASTORNOS RELACIONADOS CON EL CONSUMO AGUDO DE
ALCOHOL
La intoxicación etílica aguda es el trastorno relacionado con el alcohol más frecuentemente
atendido en Urgencias. Hay diferentes factores que pueden influir en la severidad de la intoxicación, como
la cantidad y concentración de alcohol ingerido, el peso corporal y la tolerancia al alcohol.
Los criterios diagnósticos establecidos por DSM-V son actualmente:
Ingesta reciente de alcohol.
Cambios comportamentales o psicológicos problemáticos y clínicamente significativos
(comportamiento sexual o agresivo inapropiado, labilidad del humor, juicio deteriorado) que
aparecen durante, o poco tiempo después, de la ingestión de alcohol.
Uno (o más) de los siguientes signos o síntomas que aparecen durante, o poco tiempo después,
de la ingestión de alcohol: habla farfullante, descoordinación, marcha inestable, nistagmo,
deterioro de la atención o memoria, estupor o coma
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1410]
[87] TRASTORNOS RELACIONADOS CON EL CONSUMO DE ALCOHOL
Los signos o síntomas no son atribuibles a otro problema médico y no se explican mejor por
otro trastorno mental, incluida la intoxicación por otra sustancia.
La sintomatología se relaciona con la concentración sanguínea de alcohol (Tabla V); sin embargo,
en personas con consumo crónico los síntomas son impredecibles y pueden mostrar escasos signos de
intoxicación, aunque sus concentraciones sanguíneas sean elevadas.
Las manifestaciones clínicas de la intoxicación alcohólica y sus complicaciones son debidas al
efecto tóxico del alcohol sobre los diferentes órganos. El principal riesgo vital es la depresión respiratoria.
Entre las más importantes se encuentran las cardiovasculares (taquicardia, vasodilatación periférica con
hipotensión) que pueden contribuir a la hipotermia e hipotensión y a la aparición de arritmias. Los efectos
gastrointestinales incluyen náuseas y vómitos que pueden ocasionar alteraciones hidroelectrolíticas,
diarrea, dolor abdominal por gastritis aguda, ulcus o pancreatitis aguda.
Otros problemas a tener en cuentas son el riesgo de broncoaspiración y neumonía y la aparición de
rabdomiólisis aguda (tanto por la agitación como por traumatismos musculares).
El tratamiento se fundamenta en la vigilancia respiratoria, especialmente en intoxicaciones graves,
evitando el desarrollo de aspiraciones. La canalización de una vía venosa periférica y la administración de
fluidos intravenosos y suplementos vitamínicos es el tratamiento desoporte. Además, hay que tener en
cuenta el control metabólico (puede aparecer hipoglucemia, hipopotasemia, hipomagnesemia,
hipocalcemia, hipofosfatemia, hipocloremia, cetoacidosis y acidosis láctica). Si existe agitación se puede
controlar con el uso de sedantes (cuidado con las
benzodiazepinas y los antipsicóticos, ya que pueden empeorar la depresión respiratoria). El lavado gástrico
por sonda y el carbón activado no tienen utilidad (no presenta circuito enterohepático), y se debe usar
únicamente en casos de sospecha de intoxicación concomitante por otros tóxicos.
Existe una forma clínica especial, denominada intoxicación idiosincrásica (coloquialmente
“borrachera patológica”), que ocurre generalmente en personas abstemias o con alguna patología de
sistema nervioso central (SNC) previa. Cursa típicamente con alteraciones graves del comportamiento, con
violencia extrema, a la toma de dosis bajas de alcohol con amnesia lacunar asociada.
IV. TRASTORNOS RELACIONADOS CON EL CONSUMO CRÓNICO DE
ALCOHOL
En este apartado existen múltiples patologías. La mayor parte de ellas desarrolladas en otros
apartados del presente manual (Tabla VI). Por lo tanto, nos centraremos en el desarrollo de la
encefalopatía de Wernicke.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1411]
[87] TRASTORNOS RELACIONADOS CON EL CONSUMO DE ALCOHOL
1. Encefalopatía de Wernicke
Se trata de la forma aguda del síndrome neurológico de Wernicke-Korsakoff determinado por el
déficit de tiamina (vitamina B1). La mayoría de los estudios que intentan describir la prevalencia de esta
enfermedad son series de autopsias, con gran variabilidad en la demostración de lesiones características,
que relatan que la prevalencia en población general oscila de 0,5-2,8%, siendo mayor entre los
consumidores crónicos de alcohol.
Las prevalencia es mayor en varones, aunque parece que existe mayor susceptibilidad en mujeres
al valorar de forma comparada estudios de prevalencia de la enfermedad frente a la de la dependencia
alcohólica en el sexo femenino.
En los últimos años se ha evidenciado la aparición de la enfermedad en otros contextos clínicos
distintos que producen dicho déficit vitamínico (Tabla VII).
La fisiopatología de la enfermedad se basa en la utilidad de dicha vitamina en el metabolismo
energético celular como cofactor de múltiples enzimas. Las formas activas de la tiamina se desarrollan
gracias a cambios químicos mediados por el magnesio.
El mecanismo por el cual en alcohólicos se desarrolla es múltiple: la ingesta deficitaria, la
malabsorción intestinal y el descenso en los niveles de reserva hepáticos.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1412]
[87] TRASTORNOS RELACIONADOS CON EL CONSUMO DE ALCOHOL
Las lesiones son más evidentes en la región periventricular del 3.º y 4.º ventrículo, con evidencia de
mayor pérdida neuronal en el tálamo medial. La afectación de los cuerpos mamilares es muy específica en
las formas crónicas, pero poco habitual en las formas agudas de encefalopatía de Wernicke.
1.1. Manifestaciones clínicas
Las más características son las siguientes: encefalopatía, afectación oculomotora y ataxia. Esta
tríada clásica solo se manifiesta en un tercio de los pacientes, presentado el resto de pacientes dos o solo
una manifestación. La manifestación más frecuente es la encefalopatía, después la afectación oculomotora
y finalmente la ataxia.
Encefalopatía: caracterizada por cuadro confusional, predominando la inatención y la
desorientación, y en ocasiones asociado a situaciones de deprivación y agitación psicomotriz.
Sin embargo, la afectación del nivel de consciencia es excepcional (< 5%), apareciendo
especialmente en aquellos cuadros que se dejan evolucionar sin tratar
Afectación oculomotora: la más frecuente es el nistagmo, sobre todo el horizontal, y
posteriormente el vertical. Mucho más inhabitual el rotatorio. La parálisis del músculo recto
lateral es la forma de oftalmoplejía más frecuente y suele ser bilateral. Suele ser más habitual
las formas conjugadas, aunque también se han descrito parálisis aisladas. Existen alteraciones
de la movilidad pupilar e incluso anisocoria.
Ataxia de la marcha: de mecanismo multifactorial (polineuropatía, afectación cerebelosa y
disfunción vestibular). El espectro de manifestación es amplio desde el aumento de la base de
sustentación, la marcha a pasos cortos y finalmente la ataxia franca con incapacidad para la
marcha. La afectación vestibular parece el mecanismo fundamental de la ataxia. La afectación
cerebelosa se restringe al vermis anterior y superior, lo que explica la rara aparición de disartria
asociada.
Otras alteraciones fuera de las manifestaciones clínicas clásicas más infrecuentes son la
hipotensión, la hipotermia, la malnutrición proteinocalórica, la neuropatía periférica (especialmente de
miembros inferiores con debilidad, parestesias y dolor), afectación cardiovascular (rara en contraposición al
Beri-Beri) cuya forma más característica es taquicardia, insuficiencia cardiaca de alto gasto y anormalidades
en el electrocardiograma.
La persistencia en el tiempo del déficit de tiamina y la encefalopatía de Wernicke (EW) conducen al
desarrollo del síndrome de Korsakoff, caracterizado fundamentalmente por déficit de memoria
anterógrada y retrógrada, que se intenta suplir por parte del paciente mediante la confabulación. Este
síndrome constituye una forma de daño irreversible a pesar del tratamiento con tiamina, por lo que es
importante el tratamiento precoz de la EW.
1.2. Diagnóstico
No existen pruebas complementarias que confirmen el diagnóstico, siendo este eminentemente
clínico. Actualmente no se requiere cumplir las tres manifestaciones de la tríada clásica, ya que estos
criterios poseen una sensibilidad pobre en torno al 22%. Actualmente, se han propuesto los criterios de
Caine (que consideran el diagnóstico al cumplir 2 de los siguientes criterios):
Sospecha de déficit dietético.
Trastornos oculomotores.
Disfunción cerebelosa-ataxia.
Estado mental alterado o déficit mnésico moderado.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1413]
[87] TRASTORNOS RELACIONADOS CON EL CONSUMO DE ALCOHOL
Con estos criterios la sensibilidad asciende hasta el 85%, pero sigue teniendo una especificidad
pobre, siendo más rentable desde el punto de vista diagnóstico en pacientes alcohólicos que en otros
pacientes.
En las pruebas de laboratorio los niveles plasmáticos de tiamina no tienen utilidad, ya que la
normalidad de estos no excluye la enfermedad.
El uso de la resonancia magnética cerebral puede tener algo más de utilidad. Se restringe a
situaciones en las que existan dudas en el diagnóstico y para excluir otras causas alternativas. Las lesiones
más típicas en la fase aguda no son características de la enfermedad (aumento de la señal T2 y FLAIR en
regiones periventriculares), con una sensibilidad que se sitúa en torno al 50%. Dichas lesiones desaparecen
a las 48 h de haber comenzado con el tratamiento.
En pacientes con daño crónico (síndrome de Korsakoff) existe un hallazgo más específico que es la
atrofia de los cuerpos mamilares, estando presente en el 80% de los pacientes con consumo crónico de
alcohol y antecedentes de EW.
Un dato de apoyo al diagnóstico es la prueba “ex juvantibus”, se refiere a mejoría sintomática tras
el tratamiento con tiamina.
1.3. Tratamiento:
Hay que actuar con determinación al tratarse de una urgencia médica, con el objetivo de intentar
evitar la aparición de daño neurológico irreversible. La confirmación del diagnóstico no debe retrasar el
tratamiento.
Recordar que es muy importante la administración de tiamina antes de cualquier suplementación
con hidratos de carbono (solución de glucosa intravenosa), ya que puede precipitar la encefalopatía en
pacientes de riesgo.
Existen dos tipos diferentes de posología en función del objetivo:
Dosis profilácticas: se usa en pacientes con riesgo de EW, pero que aún no presentan la
enfermedad, y que además presentan un proceso intercurrente agudo que aumente la
demanda (infecciones, proceso quirúrgico, hospitalización). En este caso las dosis son menores:
entre 200-300 mg iv al día durante tres días, con posterior suplementación por vía oral.
Dosis terapéuticas: se recomienda el uso de 500 mg de tiamina tres veces al día durante dos
días y posteriormente 250 mg al día durante 5 días más.
Posteriormente hay que mantener una suplementación oral profiláctica prolongada, ya que existe
riesgo de que en el futuro inmediato del paciente existan nuevos déficits que puedan precipitar otra vez la
enfermedad. Esta requiere la ingesta diaria de 60 mg de tiamina a la que se añaden complementos
vitamínicos que llevan otros suplementos del grupo B, así como electrolitos (como Mg, K y Zn). Como
ejemplos se dispone de Hidroxil B1-B6-B12® (250 mg por comprimido) o Becozyme C Forte® (15 mg por
comprimido).
2. Neuropatía periférica
De predominio axonal, aunque puede ser también desmielinizante en pacientes con déficit
nutricional asociado. Suele ser distal y simétrica, pudiendo afectar tanto a las fibras sensoriales, como a las
motoras o autonómicas. No presenta tratamiento específico. Mejora con la abstinencia alcohólica.
3. Degeneración cerebelosa
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1414]
[87] TRASTORNOS RELACIONADOS CON EL CONSUMO DE ALCOHOL
Puede aparecer como consecuencia del daño directo por alcohol, ayudado por déficits
nutricionales, especialmente la tiamina. Su único tratamiento es la abstinencia alcohólica. Sin embargo, una
vez establecida la sintomatología en forma de ataxia, generalmente es irreversible.
V. SÍNDROME DE ABSTINENCIA ALCOHÓLICA
Se trata de un conjunto de síntomas que aparecen como consecuencia de la retirada completa o de
la disminución de la ingesta de alcohol, en pacientes con consumo crónico del mismo.
Fisiopatología
La abstinencia alcohólica se entiende hoy día como una situación de disregulación entre el sistema
de neurotransmisores GABA y el sistema NMDA al nivel del SNC. Los pacientes con consumo crónico de
alcohol presentan una inhibición en la expresión y en la activación de receptores GABA, ya que el efecto
inhibitorio de este neurotransmisor lo realiza en ellos el alcohol. Además, el consumo crónico produce una
regulación “al alza” de los receptores del sistema NMDA.
En el momento de la disminución de la dosis, o interrupción del consumo de alcohol, se
produce un desbalance con excesiva estimulación del sistema NMDA que produce una gran
actividad catecolaminérgica que termina produciendo la clínica de abstinencia.
Clínica
Esta comienza a las 6-12 horas de la reducción o de la suspensión del consumo de alcohol, y la
sintomatología varía y va en progresión según el tiempo de la última ingesta:
En las primeras 6-36 horas desde la suspensión de la ingesta predominan síntomas de
ansiedad y nerviosismo, con insomnio, temblor, cefalea, palpitaciones, sudoración
profusa, náuseas, vómitos o diarrea. A la exploración física es habitual la presencia de
taquicardia e hipertensión arterial.
Entre las 12-36 horas existe el riesgo máximo de aparición de convulsiones, que
ocurren en el 10% de los pacientes con síndrome de abstinencia. Generalmente son
crisis únicas, de perfil clínico tónico-clónico y rara vez progresan a estatus comicial. Un
tercio de los pacientes que desarrollan crisis comiciales terminan en situación de
delirium tremens. Generalmente, no requieren tratamiento anticomicial, salvo que el
paciente tenga otros
factores epileptógenos asociados.
En las primeras 12-48 horas puede aparecer el cuadro de alucinosis alcohólica, que se
caracteriza por alteraciones de la percepción, siendo más frecuentes las de tipo visual,
siendo raras las auditivas. Este cuadro cursa sin alteración del juicio, sin presentar
delirio ni desorientación.
Finalmente el delirium tremens, que ocurre entre las 72-96 horas desde el abandono,
siendo la forma más grave de este proceso. Ocurre en alrededor del 10% de los
pacientes con abstinencia. Obedece a una situación de hiperactividad del sistema
nervioso vegetativo, produciendo fiebre, severa taquicardia e hipertensión. Se
acompaña de agitación, alucinaciones y desorientación (la situación de delirium es
imprescindible para establecer el diagnóstico). Es un cuadro que presenta una alta
mortalidad (en torno al 40%), pero con un manejo médico adecuado dicha reducción
pasa al 5%. El cuadro de delirium tremens es más frecuente cuando han pasado más de
dos días de la interrupción del consumo, siendo además más habitual en mayores de 30
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1415]
[87] TRASTORNOS RELACIONADOS CON EL CONSUMO DE ALCOHOL
años, en aquellos que ya han tenido episodios previamente, en pacientes que
presentan al diagnóstico niveles altos de etanol en sangre, historia previa de crisis
comiciales y comorbilidad asociada.
Como se puede intuir, el espectro clínico de la enfermedad es continuo y las manifestaciones se
suelen solapar, y el curso clínico agravarse según nos alejamos del momento de la última ingesta, para lo
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1416]
[87] TRASTORNOS RELACIONADOS CON EL CONSUMO DE ALCOHOL
cual se recomienda el uso de escalas estandarizadas para optimizar el tratamiento, la respuesta y el lugar
para la desintoxicación. La herramienta más utilizada es la escala CIWA-Ar (Tabla VIII).
Manejo del síndrome de abstinencia alcohólica
Diferenciando según la escala de gravedad anteriormente comentada, se puede estratificar a los
pacientes para manejo ambulatorio que serían leves (sin clínica abstinencial o aquellos con una puntuación
CIWA-Ar < 15 puntos y que sean capaces de cumplir el tratamiento oral, con adecuado apoyo familiar y
compromiso para el seguimiento diario en la unidad correspondiente y sin comorbilidad subyacente que
complique el manejo ambulatorio), y que se atienden en unidades especializadas.
Y los de manejo hospitalario, que serían todos los demás y cuyo seguimiento sería el siguiente:
Medidas generales: adecuada hidratación y reposición hidroelectrolítica, tiamina
intravenosa y aporte calórico adecuado. Hay que manejar las posibles complicaciones
asociadas al consumo crónico como hemorragia digestiva, pancreatitis, ascitis y
encefalopatía hepática, y descartar otras entidades que puedan mimetizarse con el
delirium tremens como las infecciones del SNC o las complicaciones hemorrágicas
intracraneales.
Tratamiento específico: las benzodiazepinas deben ser la primera línea en el
tratamiento del proceso. Se pueden usar por cualquier vía, pero preferiblemente en
primera instancia es recomendable el uso de la vía oral. Además del control
sintomático, el objetivo de este tratamiento es evitar la progresión y el desarrollo de
formas más graves (crisis comiciales y delirium tremens). Las más utilizadas en nuestro
medio son lorazepam, diazepam y clorazepato dipotásico. El mecanismo de estos
fármacos se basa en la estimulación de la vía GABA, con disminución de la actividad
neuronal y catecolaminérgica. Hay que tener especial precaución con los efectos de
excesiva sedación y depresión respiratoria, especialmente en pacientes cirróticos y con
patología respiratoria previa. Estos efectos son más acusados con el diazepam y el
clorazepato, ya que presentan metabolitos activos y una vida media más larga, siendo
más fácilmente controlado con lorazepam (sin metabolismo hepático, con vida media
corta y sin metabolitos activos posteriores). Aunque la administración oral es la
preferible, siempre hay que tener canalizada una vía periférica para la posible escalada
terapéutica.
Respecto la pauta de administración, hay varios patrones: por un lado la pauta a dosis fija, por otro
la pauta establecida según síntomas (symptom-triggered therapy) y la pauta de choque (dosis de carga).
Habiéndose realizado diferentes ensayos clínicos que comparan los diferentes métodos, la
estrategia de tratamiento establecida por síntomas ha presentado menos dosis total de fármacos, así como
de duración de ingreso, reduciendo costes sin tener repercusión sobre la morbimortalidad. Por lo tanto,
hoy en día se recomienda el uso de esta pauta en unidades hospitalarias en las que exista un personal de
enfermería entrenado en el uso de escalas de síntomas.
Para ello, lo recomendable es utilizar las escalas estandarizadas (CIWA-Ar). Para pacientes con
formas graves de deprivación alcohólica que requiere ingreso en la UCI e intubación orotraqueal, se
recomienda el uso de otras escalas como la Richmond Agitation-Sedation Scale.
Programa basado en síntomas: como se ha comentado, las guías clínicas
basadas en ensayos recomiendan este programa. Dicho programa hace
referencia a la administración de fármacos según las escalas de síntomas
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1417]
[87] TRASTORNOS RELACIONADOS CON EL CONSUMO DE ALCOHOL
utilizadas en varias ocasiones durante el ingreso. Se requiere el apoyo del
personal de enfermería que lo implemente. Restringido generalmente a
circunstancias ideales.
Programa fijo: uso de dosis de fármacos a dosis fijas a intervalo fijo, con
reducción progresiva diaria, y dirigida según los síntomas y los efectos de
sedación. Actualmente, sigue siendo la pauta más utilizada. En el protocolo de
actuación de nuestro centro sigue siendo la pauta de elección (Tablas IX y X).
Programa dosis de carga: consiste en el uso desde el inicio de dosis altas de
benzodiazepinas, posteriormente se mantiene la misma dosis que el día inicial,
pero repartida en 4 tomas en el segundo día, con un descenso posterior del
20% en los días siguientes. Menos utilizada por el riesgo de sedación e
intubación orotraqueal.
Existen otros tratamientos dentro del apartado:
Neurolépticos: los únicos aceptados como adyuvantes, aunque no se deben usar de
forma rutinaria. Se deberían reservar para controlar la alucinosis alcohólica y la
agitación asociada al delirium tremens; sin embargo, estos fármacos bajan el umbral
convulsivo, por lo que el paciente debe ser pretratado con benzodiazepinas, y de
elección usar el tiapride.
Agonistas alfa-2 de efecto central, como la clonidina. Pueden mejorar algunos
síntomas leves, pero no existen datos para su uso sistemático y no previenen ni las
convulsiones ni el delirium tremens.
Anticomiciales: especialmente la carbamazepina. Presenta datos favorables en algunos
estudios respecto al control de los síndromes leves-moderados, pero no para su uso
sistemático; no posee evidencia suficiente respecto a formas graves.
Fenobarbital y propofol: son fármacos restringidos para uso en la unidad de cuidados
intensivos. Se reserva para aquellos pacientes con delirium tremens refractario al
tratamiento convencional (> 10 mg lorazepam o > 50 mg de diazepam en la primera
hora). Parece que presentan un efecto sinérgico con las benzodizepinas al abrir los
canales de cloro. Requieren intubación orotraqueal del paciente.
VI. DESHABITUACIÓN ALCOHÓLICA
El término deshabituación hace referencia al conjunto de medios terapéuticos que facilitan que el
paciente aprenda a vivir bien en abstinencia. El proceso de deshabituación alcohólica debe ser dirigido por
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1418]
[87] TRASTORNOS RELACIONADOS CON EL CONSUMO DE ALCOHOL
personal especializado mediante un abordaje multidisciplinar (médicos, psicólogos, trabajador social). La
parte central del tratamiento consiste en utilizar métodos cognitivo-conductuales, asociados a la terapia
farmacológica (ambas herramientas unidas son más efectivas para conseguir la deshabituación). El contacto
con el personal de tratamiento ambulatorio se ha de mantener un mínimo de 6 meses y preferentemente
todo un año tras el inicio de la abstinencia. Este procedimiento no debe realizarse con el paciente
ingresado en un centro hospitalario, a menos que existan síntomas de abstinencia moderados-severos o
comorbilidad médica que lo justifique.
Respecto al arsenal farmacológico existen dos tipos de fármacos, los que inhiben el deseo de
consumir (anticraving) y los que intentan disuadir el consumo (aversivos o interdictores).
Fármacos anticraving
Naltrexona (Revia®): es un antagonista opioide, que parece actuar modulando la
liberación de dopamina en las áreas de recompensa cerebrales. Dicha acción
incrementaría la capacidad de mantener el control sobre la ingesta una vez iniciado el
consumo (efecto anti-priming), no siendo útil en condiciones de abstinencia. Se
administra en dosis de entre 50-100 mg al día en una sola toma cada 24 horas o en una
dosis inyectable mensual de 380 mg. Está contraindicado si existe insuficiencia renal
grave y no se recomienda en pacientes con hepatopatía crónica, ni en pacientes en
tratamiento con opiáceos.
Acamprosato (Campral®): actúa produciendo una reducción de la transmisión
glutamatérgica, a nivel de los receptores NMDA. De menor uso y eficacia. Reservado
para pacientes que no pueden usar otros fármacos.
Fármacos aversivos o interdictores
Disulfiram (Antabus®): inhibe la acetaldehído-deshidrogenasa, provocando que ante la
ingesta alcohólica se alcancen niveles altos de acetaldehído en sangre. Este último
produce una reacción ante el consumo de alcohol caracterizada por vasodilatación,
rubefacción, hipotensión, palpitaciones, disnea, ansiedad, cefalea, náuseas y vómitos.
Esta reacción es dosis-dependiente, se inicia rápidamente después de la ingesta y suele
durar unas horas. El disulfiram se prescribe generalmente en dosis de 250 mg/día en
una sola toma, preferiblemente supervisada. Constituyen contraindicaciones absolutas
los antecedentes de cardiopatía, psicosis o embarazo.
Otros fármacos
Anticonvulsivantes: topiramato demostró ser eficaz para reducir el craving. También la
oxcarbamazepina, la gabapentina o la pregabalina demostraron una eficacia algo
menor en este mismo apartado.
Oxibato sódico: estructura similar a la del GABA, debido a su acción gabaérgica, se ha
considerado como un tratamiento sustitutivo para la dependencia al alcohol.
BIBLIOGRAFÍA
Cassidy EM, O’Sullivan I, Bradshaw P, et al. Symptom-triggered benzodiazepine therapy for alcohol
withdrawal syndrome in the emergency department: a comparison with the standard fixed dose
benzodiazepine regimen. Emerg Med J. 2012;29:802.
Galvin R, Bråthen G, Ivashynka A, et al. EFNS guidelines for diagnosis, therapy and prevention of
Wernicke encephalopathy. Eur J Neurol. 2010;17:1408.
Monte Secades R, Rabuñal Rey R. Guía de práctica clínica: tratamiento del síndrome de abstinencia
alcohólica. 2.ª edición. Galicia Clin. 2011;72(2):51-64.
Schuckit MA. Recognition and management of withdrawal delirium (delirium tremens). N Engl J Med.
2014;371:2109-13.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1419]
[88] TRASTORNOS RELACIONADOS CON EL CONSUMO DE DROGAS
88.Trastornos relacionados con el consumo de drogas
Cristina Castillo Maza.
Medicina Interna
Íñigo Gredilla Zubiria.
Medicina Interna
Asesor: Salvador Mateo Álvarez. Servicio de Medicina Interna, Profesor de Toxicología en la UCM
I. INTRODUCCIÓN
En la última década se ha producido un cambio en el patrón de consumo de las drogas recreativas,
con un drástico descenso del consumo de heroína y un progresivo incremento del de cocaína, éxtasis y
derivados. Además, continúan apareciendo en el “mercado” nuevas drogas que se están popularizando en
los ambientes de consumo habituales. Según el Observatorio Español sobre Drogas, las drogas más
consumidas en la población española de entre 15 y 64 años son el alcohol y el tabaco, seguidas del
cannabis, los hipnosedantes, la cocaína, el éxtasis, las anfetaminas, los alucinógenos y la heroína (en ese
orden). En el año 2013, la cocaína fue la droga más frecuentemente implicada en la admisión a Urgencias,
seguida por el cannabis y la heroína. Como otro cambio destacable respecto a años previos, las nuevas
drogas han sufrido un repunte al alza en cuanto a motivar visitas a Urgencias, sobre todo los derivados de
las anfetaminas. Los consumos de todas las sustancias son más prevalentes en varones, con la excepción de
los hipnosedantes, cuyo uso es más frecuente en mujeres.
En la actualidad, es característico el policonsumo de drogas (legales e ilegales), cada vez más
frecuente (el 50% de los consumidores de sustancias psicoactivas utiliza dos o más de ellas, estando el
alcohol presente en más del 90% de los policonsumos). Esto aumenta los riesgos, problemas asociados y
dificulta su tratamiento.
Los principales trastornos médicos relacionados con el consumo de drogas comprenden las
intoxicaciones agudas y los problemas relacionados con el abuso, la dependencia y la abstinencia de dichas
sustancias. En relación con el manejo inicial, ver Capítulo 89. “Intoxicaciones”.
II. CANNABIS
Se trata de la droga ilegal más consumida en España. Es un derivado de la planta Cannabis sativa,
cuyos brotes florecidos, hojas hembras (marihuana) y resina (hachís y aceites de hachís) son ricos en
cannabinoides (principio activo). La vía de consumo principal es la fumada (porros), aunque también se
consume por vía oral, en forma de infusiones, pasteles o tartas (lo cual suele ocasionar intoxicaciones más
graves).
Sus efectos aparecen pocos minutos después de fumar y duran unas 2-3 horas. La intoxicación
aguda por cannabis puede producir acción depresora del sistema nervioso central (SNC) y alteraciones de la
percepción (se trata de un alucinógeno menor), y sus principales manifestaciones clínicas son taquicardia,
hiperemia conjuntival, sequedad de mucosas, náuseas, vómitos y aumento del apetito. Sus metabolitos se
acumulan en los depósitos grasos del organismo (lipofilia) y se eliminan lentamente por las heces y la orina,
pudiendo detectarse en esta última hasta una semana después de su consumo. De modo que su detección
en orina no implica necesariamente relación con la intoxicación aguda.
Sus principales complicaciones (que, aunque poco frecuentemente, pueden motivar asistencia en
Urgencias) son las crisis de pánico y la psicosis aguda, que solo requieren sedación con benzodiazepinas
(diazepam o clorazepato dipotásico vía oral –vo– o intramuscular –im–). Las intoxicaciones son raras, a
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1420]
[88] TRASTORNOS RELACIONADOS CON EL CONSUMO DE DROGAS
pesar de su elevado consumo (aunque puede verse en niños o tras ingestas orales masivas), y pueden
conducir a coma hipotónico con depresión respiratoria (no existe antídoto antagonista). El uso crónico
puede producir complicaciones pulmonares (similares al tabaco), alteraciones de la memoria (se ha
demostrado disminución del tamaño de la amígdala y el hipocampo en pruebas de imagen de
consumidores crónicos, sobre todo si se inicia el consumo a edades tempranas), de la atención, de las
hormonas sexuales (ginecomastia, alteración de la espermatogénesis), disminución de los niveles de sodio y
potasio (lo que predispone a la aparición de arritmias en torsión de puntas), así como el controvertido
síndrome amotivacional. En cuanto a la abstinencia, puede producir un leve síndrome de unos 3-4 días de
duración consistente en irritabilidad, astenia e insomnio. Aunque se ha ensayado con diversos fármacos
para tratarlo (bupropión, acetilcisteína, agonistas de los receptores de cannabinoides, etc.) hacen falta más
estudios para recomendar su uso en este contexto.
III. COCAÍNA
Alcaloide extraído de las hojas de la planta Erithroxylum coca, que se consume fumado como base
libre (crack), o disuelto en ácido clorhídrico (clorhidrato de cocaína, forma más utilizada, inhalada –
esnifada–, fumada o intravenosa). La cocaína es, tras el cannabis, la droga ilegal más consumida en España
y su volumen de consumo se encuentra a la cabeza en los países europeos. A pesar de ello, en los últimos
años se observa cómo se ha modificado la tendencia ascendente que venía manifestándose desde hacía
una década y que alcanzó su máximo nivel en el año 2009. Su sobredosis es potencialmente mortal y es la
causa más frecuente de muerte relacionada con drogas en la actualidad.
Fumada y por vía parenteral presenta un inicio de acción muy rápido (1-2 minutos), con efecto
máximo a los 60 minutos. Por vía intranasal el inicio de acción es más tardío (por su efecto vasoconstrictor
local), de unos 20 minutos, con máximo efecto a las 2-3 horas. Su metabolismo depende de las
colinesterasas plasmáticas y hepáticas, y sus metabolitos (la mayoría inactivos: benzoilecgonina) son
detectables en orina más de 48 horas tras consumos puntuales y más de una semana tras consumos
crónicos.
Existen circunstancias que aumentan el riesgo derivado de su consumo, como la disminución de la
actividad de las colinesterasas (niños, embarazo, ancianos, hepatopatías, etc.), el consumo de alcohol
(induce metabolitos activos –cocaetileno, con mayor vida media–) o el virus de la inmunodeficiencia
humana (VIH). Además, con frecuencia está adulterada con sustancias que pueden potenciar sus efectos
como efedrina, cafeína, anfetaminas, quinina, estricnina y levamisol. Este último se ha relacionado con
vasculitis cutáneas anticuerpo anticitoplasma de neutrófilos positivos, leucoencefalopatía o agranulocitosis.
1. Efectos de la cocaína
Es un potente estimulante del SNC, produce un bloqueo de la recaptación presináptica de aminas y
ocasiona efectos catecolaminérgicos (alfa y beta), dopaminérgicos y serotoninérgicos. También bloquea los
canales de sodio (efecto anestésico local y antiarrítmico tipo I). Otro efecto potencialmente peligroso es la
capacidad de inducir agregación plaquetaria y aumentar la producción de tromboxano (predisponiendo,
por tanto, a eventos cardiovasculares agudos).
La cocaína produce un aumento de la autoestima y de la confianza, euforia, locuacidad y excitación
(anorexia e insomnio). Sus efectos son de escasa duración, genera ansiedad por repetir el consumo y una
fuerte dependencia psicológica (craving), más acusada con la cocaína base o crack. Induce tolerancia con
rapidez, haciendo muy variable e impredecible la dosis tóxica (de 12 a 15 g vía oral –hojas de coca–, de 20 a
100 mg intranasal, de 10 a 50 mg iv y de 50 a 200 mg inhalada).
2. Intoxicación aguda
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1421]
[88] TRASTORNOS RELACIONADOS CON EL CONSUMO DE DROGAS
La intoxicación aguda origina un cuadro caracterizado por nerviosismo, midriasis, hipertensión
arterial (HTA), hipertermia, taquicardia, agitación psicomotriz, sudoración y palidez, al que pueden añadirse
las siguientes complicaciones:
En el SNC: insomnio, hiperreflexia, acatisia, distonías (crack dancers), discinesias bucolinguales
(“boca torcida”), convulsiones (por lo general aisladas y autolimitadas, si son múltiples existe
alto riesgo de hipertermia y muerte), ictus isquémico o hemorrágico y delirio alucinatorio
característico (microzoopsias: percepción táctil y visual de insectos).
Cardiovasculares: arritmias (taquicardia supraventricular paroxística [TSVP], taquicardia
ventricular [TV], fibrilación ventricular [FV], fibrilación auricular [FA]), síndrome coronario
agudo (infarto agudo de miocardio [IAM], espasmo coronario, disección aórtica), muerte súbita.
Al parecer, ciertos grupos son más vulnerables a estas entidades, aun sin presentar factores de
riesgo cardiovascular (embarazadas, infectados por VIH, consumo concomitante de alcohol).
Respiratorias: (más frecuentes en fumadores de crack): neumotórax y neumomediastino,
broncoconstricción, edema pulmonar (cardiogénico o no), vasoespasmo profundo (simula
tromboembolia pulmonar [TEP] en la gammagrafía pulmonar) y daño inflamatorio agudo
(infiltrados alveolares con fiebre y eosinofilia), hemorragia alveolar, neumonías intersticiales.
Digestivos: isquemia e infarto mesentérico, perforación gastrointestinal, hepatitis aguda (de
causa isquémica, pues no ha demostrado hepatotoxicidad directa en humanos).
Otros: bruxismo, necrosis de tejidos blandos (tabique nasal, puntos de punción), hipertermia,
rabdomiólisis, fracaso renal, coagulación intravascular diseminada, infarto renal y testicular,
trombosis venosa, abruptio placentae, aborto espontáneo, prematuridad.
2.1. Tratamiento
No existe antídoto, por lo que el tratamiento de su intoxicación consiste en medidas básicas de
soporte vital, monitorización electrocardiográfica (ECG), canalización de vía periférica y vigilancia del nivel
de consciencia, así como asegurar la correcta reposición de volumen y la prevención del fracaso renal
agudo (FRA) con fluidoterapia intravenosa. En casos graves, considerar el ingreso en la unidad de cuidados
intensivos (UCI). A continuación se detalla el tratamiento de las potenciales complicaciones:
Agitación: de elección benzodiazepinas (diazepam 5-10 mg iv, repetible cada 4 h).
Neurolépticos en caso de delirio alucinatorio intenso. (Ver Capítulo 19. “Patología psiquiátrica
importante para el médico general: agitación psicomotriz”).
Convulsiones: si son aisladas y autolimitadas, no requieren tratamiento. En caso de status,
tratamiento enérgico con diazepam (5-10 mg iv repetibles hasta cada 10-60 min, máximo 3
mg/kg/24 h), seguido de perfusión de fenitoína (15- 20 mg/kg) y/o fenobarbital (10 mg/kg).
(Ver Capítulo 86. “Crisis comiciales”).
Hipertermia: tratamiento inmediato con sedación y medidas físicas de enfriamiento,
idealmente en menos de 30 minutos, pudiendo requerir relajantes neuromusculares (UCI). Los
antitérmicos no son eficaces.
Rabdomiólisis: sueroterapia y bicarbonato para alcalinizar la orina (2-5 mEq/kg iv en infusión
lenta 4-8 h; por vía oral inicialmente 4 g seguidos de 1-4 g/4 h).
HTA: dada la corta semivida de la cocaína, suele resolverse espontáneamente; sin embargo, en
ocasiones puede condicionar una emergencia hipertensiva. En principio, se debe tratar con
benzodiazepinas (diazepam 5-10 mg iv repetibles) y si ello no fuera suficiente,
calcioantagonistas por vía oral (amlodipino 10 mg o nifedipino 10 mg). En situaciones graves y
mantenidas se puede usar nitroprusiato sódico (0,15-0,3 mg/kg/min) o fentolamina (5-20 mg iv
repetibles cada 2-4 h). El uso de betabloqueantes es controvertido, si bien no se recomienda
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1422]
[88] TRASTORNOS RELACIONADOS CON EL CONSUMO DE DROGAS
por su efecto vasoconstrictor, que puede precipitar isquemia coronaria y periférica, aunque
bajo estrecha vigilancia y tras administrar un agente bloqueador alfa (como la fentolamina),
pueden administrarse.
Dolor torácico: es el motivo de consulta más frecuentemente asociado al consumo de cocaína.
En el 6-8% de los casos se evidencia elevación enzimática (IAM), pero en general son síndromes
coronarios de baja mortalidad (al ser más frecuente en varones jóvenes sin otros factores de
riesgo cardiovascular [FRCV], salvo el tabaco). El riesgo de IAM es mayor en la primera hora tras
el consumo, por lo que debe interrogarse acerca del mismo (y solicitar metabolitos en orina si
existe sospecha). El ECG presenta menor sensibilidad y especificidad en este contexto (alta
incidencia de repolarización precoz en pacientes varones jóvenes, además son frecuentes los
IAM con ECG normal o con alteraciones inespecíficas de la repolarización). La creatina-cinasa
(CPK) y la mioglobina son poco específicas (aumento de actividad muscular, rabdomiólisis). La
fracción MB de la creatina-cinasa (CK-MB) también pierde algo de especificidad en esta
población y la troponina mantiene su especificidad. Las complicaciones son relativamente
infrecuentes (4-17% arritmias ventriculares, 5-7% insuficiencia cardiaca, 2% mortalidad). En
estos pacientes deben evitarse los betabloqueantes y los bloqueantes mixtos (en el momento
agudo), como se comentó previamente. Sí están indicados a largo plazo siempre que se
garantice que el paciente no recae en el consumo. La anticoagulación debe ser valorada con
cautela por el riesgo de hemorragia intracraneal y disección aórtica asociados al uso de cocaína.
Para ampliar el diagnóstico y manejo del síndrome cororario agudo con o sin elevación del
segmento ST, ver Capítulo 23. “Cardiopatía isquémica”.
Arritmias: la cocaína es una sustancia arritmogénica debido a que bloquea los canales de sodio
(prolonga el complejo QRS y el intervalo QT) e induce un estado hiperadrenérgico. Deben
evitarse los antiarrítmicos del grupo I (quinidina, lidocaína, flecainida. Potencian sus efectos). Se
recomienda el uso de benzodiazepinas.
Ingesta oral:
Mulas (body packer): transportan gran cantidad de droga (potencialmente letal) en
paquetes ocultos en el tracto intestinal. El tratamiento en asintomáticos es la
observación con medidas de soporte y monitorización ECG; si aparecen
manifestaciones graves de intoxicación (status epiléptico, arritmias, abdomen agudo) u
obstrucción intestinal está indicada la laparotomía urgente.
Body stuffers (ingesta precipitada por temor a ser detenidos, menor cantidad pero peor
envuelta): medidas de soporte, lavado gástrico, carbón activado (1 mg/kg) y
tratamiento sintomático según lo expuesto anteriormente.
3. Síndrome de abstinencia y deshabituación
La interrupción brusca del consumo de cocaína no produce un cuadro de abstinencia “física” típica
y no suele motivar la visita a los servicios de Urgencias ni requiere tratamiento farmacológico. Genera
alteraciones del estado de ánimo (disforia, depresión), deseo de droga (craving), irritabilidad, astenia o
agitación psicomotriz. Su deshabituación requiere un abordaje multidisciplinar usualmente ambulatorio
(salvo casos seleccionados que precisen ingreso hospitalario). Se utilizan psicoterapia, antidepresivos
tricíclicos, bromocriptina y están contraindicados los inhibidores de la monoaminoxidasa (IMAO) (por el
riesgo de crisis HTA).
IV. ANFETAMINAS Y DERIVADOS DE SÍNTESIS
Grupo de compuestos estructuralmente relacionados con la efedrina que incluyen la anfetamina
(alfa-metilfeniletilamina, speed), la metanfetamina (cristal, crack) y sus derivados de síntesis
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1423]
[88] TRASTORNOS RELACIONADOS CON EL CONSUMO DE DROGAS
(metilendioximetanfetamina [MDMA] –éxtasis–, etilendioxianfetamina [MDA], metilendioxietilanfetamina
[MDEA], etc., componentes habituales de las llamadas drogas de diseño o pastillas) que presentan
importante efecto estimulante del SNC al inhibir la recaptación de monoaminas (efecto catecolaminérgico,
dopaminérgico y serotoninérgico).
Se absorben bien por todas las vías, aunque predomina su consumo por vía oral e intranasal. Sus
efectos comienzan 30-60 minutos tras la ingesta y alcanzan los máximos a las 2 horas, pudiendo persistir
más de 6 horas. Presentan metabolismo hepático y eliminación urinaria de metabolitos (detectables hasta
2-4 días tras el consumo).
1. Intoxicación por anfetaminas y derivados
Producen locuacidad, lucidez, euforia, anorexia, resistencia al sueño y la fatiga, piloerección,
temblor, hiperreflexia, midriasis, inquietud, diaforesis, bruxismo, sequedad oral, náuseas y vómitos. Los
compuestos de síntesis (tipo éxtasis) tienen además propiedades entactógenas (facilitadoras de las
relaciones interpersonales) y alucinógenas.
2. Complicaciones agudas
Del SNC: hiperactividad con coreoatetosis, delirium, psicosis aguda anfetamínica (crisis de
pánico con gran agitación, ideas paranoides y alucinaciones). Raramente convulsiones,
hemorragia intracraneal, vasculitis cerebral.
Cardiovasculares: HTA, taquicardia y arritmias, raramente IAM. Al igual que con la cocaína,
evitar durante la intoxicación aguda el uso de betabloqueantes.
Otras: deshidratación y alteraciones hidroelectrolíticas, hipertermia (golpe de calor),
rabdomiólisis, fracaso renal agudo, disfunción hepática, edema pulmonar, coagulopatía,
hiponatremia por síndrome de secreción inadecuada de vasopresina (SIADH) e ingesta
compulsiva de líquidos (éxtasis).
Trastornos psiquiátricos: fenómenos psicóticos atípicos, despersonalización, celotipias,
flashbacks, ansiedad, crisis de pánico, síndromes depresivos y alteraciones del sueño.
2.1. Tratamiento
Valoración inicial, indicando si es preciso soporte vital con monitorización ECG, pulsioximétrica y de
diuresis, asegurando el aporte de líquidos. Está indicado el lavado gástrico y el uso de carbón activado, la
diuresis forzada y la sedación con benzodiazepinas. El abordaje de las principales complicaciones debe
realizarse de manera similar al de las intoxicaciones por cocaína (véase el apartado anterior).
Agitación intensa: lorazepam 2-4 mg iv o diazepam 5-10 mg iv. Estas dosis se pueden repetir
cada 8 a 10 minutos si se precisa. Las restricciones físicas no son deseables. Los pacientes que
luchan contra las restricciones físicas experimentan contracciones musculares isométricas que
se pueden asociar con acidosis láctica, hipertermia, colapso cardiaco repentino y muerte.
Psicosis aguda: haloperidol (10 mg/6 h, ampollas im; máximo 30 mg/6 h). Las benzodiazepinas
son igualmente otra línea de tratamiento disponible.
Hipertermia maligna (temperatura mayor de 41,1 ºC): complicación potencialmente mortal
que requiere diagnóstico y tratamiento precoz, inicialmente con hidratación y medidas físicas
(incluyendo el uso de sueros fríos intravenosos o lavados vesicales con agua fría). Si existe
hipotensión refractaria a fluidos, valorar el uso de drogas vasoactivas e ingreso en la UCI. Se ha
utilizado el dantroleno (1-3 mg/kg en bolo, repetibles cada 10 a 15 minutos, hasta un máximo
de 10 mg/kg) para el control sintomático en casos graves (aunque no hay ensayos controlados);
así como intubación con sedorrelajación muscular para disminuir el riesgo de rabdomiólisis.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1424]
[88] TRASTORNOS RELACIONADOS CON EL CONSUMO DE DROGAS
Hipertensión arterial: al igual que con la cocaína, está contraindicado el uso de
betabloqueantes. Se recomiendan fármacos vasodilatadores (nitroglicerina) y antagonistas
alfaadrenérgicos (doxazosina).
Arritmias: siempre que se asocien a agitación, se recomienda el uso de benzodiazepinas.
3. Uso crónico
Cada vez más frecuente, se ha relacionado con la aparición de trastorno psicótico, esquizofrenia y
manía. Pueden inducir la muerte neuronal al activar circuitos intracelulares, pero este mecanismo no es
bien conocido (se cree que se debe a un mal procesamiento de la dopamina).
4. Abstinencia
Incluye anhedonia, irritabilidad, hiperfagia, insomnio o hipersomnia, falta de concentración, y
agitación o inhibición psicomotriz. Estos síntomas aparecen de forma precoz al cesar el consumo y suelen
desaparecer a las 2 semanas.
V. ALUCINÓGENOS
Grupo heterogéneo de sustancias que comparten la capacidad de inducir importantes alteraciones
en la percepción y los procesos del pensamiento. Asimismo, presentan efectos simpaticomiméticos leves.
Los alucinógenos de mayor difusión en España son la dietilamida del ácido lisérgico (LSD, tripi o ácido), de
mayor potencia alucinógena, y los hongos de las familias Psilocibe, Conocybe y Stropharia (setas mágicas),
estructuralmente relacionados entre sí (indolalquilaminas). Aunque existen cientos de sustancias naturales
y sintéticas con potencial alucinógeno, a efectos prácticos nos centraremos en las señaladas anteriormente.
El LSD se presenta en forma de sellos (papel secante impregnado) o comprimidos y se absorbe bien
por cualquier vía (predomina la oral o la sublingual). Presenta metabolización hepática y eliminación
urinaria (24 horas postingesta), pudiendo durar su acción más de 8 horas. Los hongos se consumen por vía
oral, con efectos similares a la LSD pero con menor potencia.
En general, estas sustancias no producen dependencia, y sus principales complicaciones médicas
son:
Crisis de pánico (mal viaje): reposo en lugar tranquilo y administración de benzodiazepinas
(diazepam 5-10 mg iv). − Reacciones psicóticas agudas: haloperidol 10 mg/6 h.
Accidentes (traumatismos): motivados por las alteraciones conductuales que puede producir
su consumo.
Flashbacks (instauración transitoria de los efectos alucinógenos que puede ocurrir incluso años
después del último consumo), habitualmente precedidos por algún desencadenante (consumo
de otros tóxicos –especialmente cannabis–, o situaciones de estrés).
Las complicaciones graves, cardiovasculares y la hipertermia derivadas de su acción
simpaticomimética suelen ser poco frecuentes y aparecer en el seno de consumo de cantidades muy
elevadas (> 400 microgramos).
VI. OPIOIDES
Grupo de sustancias naturales o sintéticas derivadas del opio, extraído del jugo de la adormidera
(Papaver somniferum); la heroína (derivado semisintético de la morfina, principal alcaloide natural del opio)
es el más utilizado con fines recreativos. En la última década se ha producido una importante disminución
de su consumo, así como el progresivo abandono de la vía intravenosa a favor de su uso fumado, debido
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1425]
[88] TRASTORNOS RELACIONADOS CON EL CONSUMO DE DROGAS
principalmente a la mayor percepción de peligrosidad de esta sustancia entre sus consumidores. La
metadona (opioide sintético utilizado en el tratamiento de la dependencia a la heroína) ocasiona episodios
agudos de intoxicación con relativa frecuencia.
La heroína se consume principalmente por vía intravenosa, fumada e intranasal, alcanzando pico
sérico de forma inmediata, atravesando rápidamente y en gran proporción la barrera hematoencefálica.
Presenta una vida media de 2-5 horas, metabolismo hepático y excreción urinaria durante 2-3 días tras su
consumo. La metadona presenta una vida media considerablemente mayor (24-36 horas).
Los opioides actúan sobre los receptores del sistema opioide endógeno (mu, kappa y delta), y
existen sustancias agonistas puras (morfina, heroína, metadona, fentanilo, etc.), antagonistas puras
(naloxona y naltrexona) y agonistas parciales (buprenorfina, pentazocina). Los agonistas en general
producen analgesia, sedación, miosis, depresión respiratoria y estreñimiento; comparten una gran
capacidad para generar tolerancia de forma precoz y ocasionar dependencia con un síndrome de
abstinencia grave.
1. Complicaciones del consumo de opioides
Derivadas de la vía de administración (intravenosa): infecciones cutáneas, endocarditis
derecha, transmisión de virus de las hepatitis B y C (VHB, VHC) y virus de la inmunodeficiencia
humana (VIH).
Intoxicación aguda y sobredosis: cuadro potencialmente mortal, frecuente tras periodos de
abstinencia, por diferentes “purezas” en la composición de la heroína o por la combinación con
otros sedantes (alcohol y benzodiazepinas).
2. Intoxicación aguda
2.1. Diagnóstico
La tríada clásica consistente en depresión respiratoria (< 12 respiraciones/minuto, lo más
específico), disminución del nivel de consciencia y miosis (que puede faltar en consumos concomitantes de
otras sustancias, hipoxia o hipoglucemia o en casos de consumo de meperidina o propoxifeno), con
evidencia circunstancial de consumo, obliga a sospechar intoxicación. Puede ser de utilidad valorar la
respuesta a la naloxona (aunque la falta de respuesta no descarta intoxicación). Si coexisten tos o dificultad
respiratoria, debe realizarse una radiografía torácica.
2.2. Complicaciones
Hipotensión, hipotermia, bradicardia, náuseas, vómitos, arritmias (especialmente con el consumo
de fármacos que alargan el intervalo QT: metadona, propoxifeno y oxicodona), edema agudo de pulmón no
cardiogénico de aparición tardía (2 a 24 horas postexposición), rabdomiólisis, neumonías aspirativas, coma,
encefalopatía anóxica, síndrome serotoninérgico (meperidina), etc.
2.3. Tratamiento
Se dirigirá a conseguir una adecuada ventilación, por la posible depresión respiratoria. Se asegurará
la vía aérea (cánula de Guedel, intubación orotraqueal), ventilación y administración de oxígeno, si fuera
necesario. En caso de depresión grave del nivel de consciencia y de la respiración, se administrará el
antídoto, naloxona (amp 0,4 mg/1 ml, dosis de 0,1 a 0,2 mg se puede repetir cada 2-5 minutos si no hay
respuesta). Dado que sus efectos son mucho más breves que los de la heroína, debe mantenerse la
observación durante, al menos, 6-8 horas (hasta 24-48 horas en caso de intoxicación por metadona). En
caso de que la disminución del nivel de consciencia o la depresión respiratoria reaparezca, valorar inicio de
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1426]
[88] TRASTORNOS RELACIONADOS CON EL CONSUMO DE DROGAS
perfusión intravenosa de naloxona, por ejemplo, 2 mg en 500 ml de SSF o S. Glucosa al 5% para obtener
una concentración de 0,02 mg/ml. El ritmo de perfusión depende de la respuesta (se sugiere iniciar con 2/
de la dosis inicial efectiva). Se debe sospechar consumo concomitante de otros tóxicos en caso de
respuesta parcial o incompleta a la naloxona. Si aparecen arritmias en torsión de puntas o ensanchamiento
del complejo QRS, está indicado el uso de bicarbonato (1 a 2 mEq/kg de bicarbonato de sodio por vía
intravenosa en ausencia de contraindicaciones).
3. Abstinencia
Aparece a las 6-12 horas tras el último consumo (en compuestos de vida media corta tipo heroína)
y dura hasta 5-8 días (pico máximo de síntomas a las 36-72 horas). En el caso de la metadona, el inicio del
síndrome es más tardío. Este consta de: agitación, ansiedad, insomnio, lagrimeo, rinorrea, piloerección,
diaforesis, midriasis, mialgias, temblores, diarrea, náuseas, vómitos, dolor abdominal (que puede simular
un abdomen agudo quirúrgico) e incluso hipertermia, escalofríos y convulsiones.
3.1. Tratamiento
Se basa en la utilización de agonistas opioides en dosis descendentes. El más utilizado es la
metadona (dosis inicial ajustada según el consumo habitual de heroína: 1 mg de metadona por cada 2 mg
de heroína pura/día –considerando una pureza del 10%–; usualmente 30-80 mg/día fraccionados en dos
tomas durante 2 días, disminuyendo posteriormente un 10% cada día). La indicación de este tratamiento
debe controlarse desde un programa de desintoxicación reglado, nunca desde el Servicio de Urgencias, a
excepción de que el paciente precise ingreso por cualquier enfermedad grave. Otras pautas (clonidina,
pautas “cortas” y “ultracortas”) son menos recomendables y actualmente están en desuso.
4. Dependencia
Su abordaje debe realizarse siempre desde programas multidisciplinares de desintoxicación. La
estrategia más utilizada se basa en el uso de agonistas (metadona) en una sola dosis diaria durante largos
periodos. Se debe mantener la misma dosis en caso de admisión a Urgencias o ingreso hospitalario por
cualquier otro motivo (consultando la dosis con el Centro de Atención a las Drogodependencias de
referencia). Se deben considerar las potenciales interacciones de la metadona con los fármacos que se
suelen administrar durante el ingreso (rifampicina, fenitoína y antivirales como nevirapina o efavirenz –
consultar el apéndice de interacciones medicamentosas–).
VII. SUSTANCIAS EMERGENTES
Cada día surgen en el mercado nuevas sustancias derivadas o similares a las drogas clásicas con
vistas a facilitar su tráfico, su comercialización o dificultar su ilegalización. Entre las más conocidas en la
actualidad están las que se comentan a continuación, pero existen otras muchas.
Gamma-hidroxibutirato (GHB): derivado hidroxilado del ácido γ-aminobutírico (GABA), potente
depresor del SNC (denominado éxtasis líquido, sin fundamento bioquímico alguno). Se presenta
como líquido incoloro, que se administra por vía oral. Sus efectos (impredecibles, con gran
variabilidad intraindividual e interindividual) comprenden estados de euforia y excitación,
alucinaciones, síndrome confusional, hipotonía muscular, coma, depresión respiratoria y
muerte. Pequeños incrementos de dosispueden inducir importantes intoxicaciones. No existe
antídoto, y el manejo de la intoxicación aguda se basa en el soporte vital, con particular
atención al estado ventilatorio.
Ketamina (keta, special K): fármaco anestésico disociativo, su uso recreativo (generalmente
por vía intranasal u oral) produce euforia, alucinaciones, estimulación simpática, incoordinación
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1427]
[88] TRASTORNOS RELACIONADOS CON EL CONSUMO DE DROGAS
motora, alteraciones cognitivas y confusión. Son frecuentes los malos viajes (crisis de pánico,
episodios psicóticos agudos), así como los flashbacks. Su tratamiento es puramente sintomático
y de soporte.
Poppers: sustancias vasodilatadoras (nitrito de amilo, butilo o isobutilo),
metahemoglobinizantes, volátiles y muy inflamables, usadas por vía inhalada. De efecto
inmediato y corta duración (< 2 minutos), provocan euforia, relajación muscular (esfinteriana) y
pueden prolongar e intensificar el orgasmo. Pueden causar mareo, cefalea, hipotensión,
taquicardia, palpitaciones, disnea y, en casos graves, cianosis intensa (metahemoglobinemia,
cuyo tratamiento es azul de metileno 1-2 mg/kg en 100 ml de suero glucosado a pasar en 10
minutos). Riesgo de hipotensión grave si se asocia a sildenafilo (Viagra®) y similares.
Drogas de asalto: cada vez con mayor frecuencia se producen casos de robo, violación,
secuestro, etc., en los que se utiliza una sustancia (por lo general con potencial depresor del
SNC, alucinógeno y/o amnésico) para doblegar la resistencia de la víctima. Las más utilizadas
son (habitualmente en combinación con el alcohol) hipnosedantes tipo benzodiazepinas, GHB,
ketamina, anticolinérgicos (como la escopolamina –burundanga– y la atropina) y otros
alucinógenos (fenotiazinas). Tratamiento: soporte vital, valorando lavado gástrico y uso de
carbón activado. En caso de intoxicación por anticolinérgicos (midriasis, taquicardia, sequedad
de boca, delirium, alucinaciones, coma) considerar el empleo de fisostigmina (0,5-2 mg iv a
pasar lentamente, valorando la respuesta clínica).
Cannabinoides sintéticos (spice o K2): se consumen por vía inhalada. Causan resultados muy
similares a la intoxicación por cannabis, pero producen con mayor frecuencia efectos
simpaticomiméticos, comportamiento agresivo y alucinaciones. Se han reportado casos de
daño renal agudo con su uso. El examen de tóxicos en orina será típicamente negativo para
cannabis.
Sales de baño (mefedrona, metilenodioxipirovalerona y metilona, son formas de la llamada
“droga caníbal”): compuestos sintéticos derivados de las catinonas de la planta de kath (Catha
edulis) con efectos simpaticomiméticos. Su uso provoca euforia, aumento de la sociabilidad,
incremento de la sensibilidad sensorial, de la energía y el apetito sexual. Las complicaciones
más frecuentes son la agitación y la psicosis. Pueden observarse cambios en la piel (exantema,
decoloración azulada), así como en el olor corporal. El tratamiento es de soporte (sedación con
benzodiazepinas y asegurar la correcta hidratación, principalmente).
BIBLIOGRAFÍA
Andrabi S, Greene S, Moukaddam N, Li B. New drugs of abuse and withdrawal syndromes. Emerg Med
Clin North Am. 2015;33(4):779-95.
Baptiste G, Alexopoulos A, Masud T, Bonsall J. Systemic levamisole-induced vasculitis in a cocaine user
without cutaneous findings: A consideration in diagnosis. Case Rep Med. 2015;2015: 1-3.
Bechtel LK, Holstege CP. Criminal poisoning: Drug-facilitated sexual assault. Emerg Med Clin N Am.
2007;25:499-525. – Blaho K, Merigian K, Winbery S, Geraci S, Smartt C. Clinical pharmacology of
lysergic acid diethylamide: case reports and review of the treatment of intoxication. Am J Ther.
2016;4(5-6):211-21.
Chan WL, Dines AM, Lipi M, Wood DM, Dargan PI. Limited evidence for the safety of β-blockers for
cocaineassociated chest pain. Am J Emerg Med. 2013;31(6):988-9.
Cole JC, Sumnall HR. Altered states: The clinical effects of Ecstasy. Pharmacol Therapeut.
2003;98(1):35-55. – Greene SL, Kerr F, Braitberg G. review article: amphetamines and relates drugs of
abuse. Emerg Med Australas. 2008;20(5):391-402.
Jones J, Weir W. Cocaine-associated chest pain. Med Clin North Am. 2005;89(6):1323-42.
Lorenzo P, Lizasoain I. Características farmacológicas de las drogas recreativas (MDMA y otras
anfetaminas, Ketamina, GHB, LSD y otros alucinógenos). Adicciones. 2003;15:supl 2.15.
Mokhlesi B, Leikin JB, Murray P, Cordbridge TC. Adult toxicology in critical care, Part I General approach
to the intoxicated patient. Chest. 2003;123(2):577-92.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1428]
[88] TRASTORNOS RELACIONADOS CON EL CONSUMO DE DROGAS
Mokhlesi B, Leikin JB, Murray P, Cordbridge TC. Adult toxicology in critical care, Part II: Specific
poisonings. Chest. 2003;123(3):897-922.
Newton T, Kalechstein A, Duran S, Vansluis N, Ling W. Methamphetamine abstinence syndrome:
Preliminary findings. Am J Addict. 2004;13(3):248-55.
Observatorio Español de la Droga y las Toxicomanías (OEDT). Informe 2015. Alcohol, tabaco y drogas
ilegales en España. Observatorio español sobre drogas. Informe del plan nacional sobre Drogas.
Ministerio de Sanidad, Servicios Sociales e Igualdad. Madrid; 2015.
Observatorio Español de la Droga y las Toxicomanías (OEDT). Consumo percepciones y opiniones ante
las drogas (Edades). Informe 2013. Ministerio de Sanidad, Servicios Sociales e Igualdad. Madrid;
2013.
Pendergraft W, Herlitz L, Thornley-Brown D, Rosner M, Niles J. Nephrotoxic effects of common and
emerging drugs of abuse. Clin J Am Soc Nephrol. 2014;9(11):1996-2005.
Tyagi M, Weber J, Bukrinsky M, Simon G. The effects of cocaine on HIV transcription. J NeuroVirol.
2016;22(3):261-74.
Winstock A, Barratt M. The 12-month prevalence and nature of adverse experiences resulting in
emergency medical presentations associated with the use of synthetic cannabinoid products. Hum
Psychopharmacol. 2013;28(4):390-3.
Yap M, Whittle S, Yücel M, Sheeber L, Pantelis C, Simmons J, et al. Interaction of parenting experiences
and brain structure in the prediction of depressive symptoms in adolescents. Arch Gen Psychiatry.
2008;65(12):1377.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1429]
[89] INTOXICACIONES
89.Intoxicaciones
Ana Sánchez Morla.
Medicina Interna
Nuria Valdeolivas Hidalgo.
Medicina Interna
Lucía Jorge Huerta.
Medicina Interna
Asesor Alberto Moreno Fernández.
Médico Adjunto de Medicina Interna
I. INTRODUCCIÓN
Un tóxico es cualquier sustancia que, al entrar en contacto con el organismo, produce un efecto
perjudicial a través de una reacción química. Prácticamente cualquier sustancia puede ser tóxica a una
dosis determinada. Atendiendo a la población global, se estima que en España se producen hasta 120.000
intoxicaciones al año (aproximadamente el 2% de todas las urgencias médicas), siendo más frecuentes en la
infancia, en la mayoría de los casos accidentales, producidas en el domicilio, con productos de uso
doméstico o medicamentos.
En cuanto a la etiología de las intoxicaciones atendidas en Servicios de Urgencias de adultos, la
principal causa es la tentativa de suicidio con medicamentos (50,2%), seguida de intoxicaciones etílicas
agudas y sobredosis por drogas ilegales. Asimismo, cabe destacar los accidentes laborales y enfermedades
profesionales de origen tóxico (de declaración obligatoria), siendo en este caso los más frecuentes los
causados por metales e hidrocarburos.
II. MANEJO GENERAL DE LAS INTOXICACIONES
1. Aproximación diagnóstica
1.1. Anamnesis
Pueden producir un amplio abanico de manifestaciones clínicas con afectación de todos los órganos
y sistemas, por lo que una buena anamnesis es el pilar básico del diagnóstico; es fundamental obtener
información sobre el tipo de tóxico, la cantidad, la vía de administración, el intento de eliminación del
mismo y la sintomatología. Si es posible, debe realizarse directamente al paciente y, en caso de que este se
encuentre inconsciente, de manera indirecta a todas aquellas personas que puedan aportar información,
especialmente si estuvieron presentes en el momento en que se produjo la intoxicación.
Es frecuente que los síntomas se agrupen en determinados síndromes que pueden orientar hacia el
agente causal de la intoxicación (Tabla I).
Una vez conocido el presunto tóxico, en España se puede solicitar información al Instituto Nacional
de Toxicología y Ciencias Forenses las 24 horas del día (teléfono de información general 915 620 420 o de
información solo para médicos 914 112 676).
1.2. Exploración física
Ha de ser completa, incluyendo exploración cardiovascular y neurológica, especialmente en los
casos de coma (ver Capítulo 82. “Alteración del nivel de consciencia. Coma”). En muchas ocasiones, nos
ayuda a orientar el diagnóstico y a calibrar la gravedad de la intoxicación.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1430]
[89] INTOXICACIONES
1.3. Pruebas complementarias
Analítica: básica que incluya hemograma, bioquímica con glucemia, creatinina, ionograma,
equilibrio ácido-básico y coagulación. En función de la sospecha, debemos solicitar también
valores específicos como gasometría arterial, calcemia, creatinina fosfocinasa (CPK),
osmolaridad, etc.
Análisis toxicológicos: de manera urgente, solo en casos graves (con sospecha de etiología
tóxica), cuando conocer la concentración del tóxico en sangre tiene interés terapéutico
(paracetamol, litio, metanol, etilenglicol) o implicaciones médico-legales (algunos casos de
intoxicación etílica). Puede ser útil la determinación de un panel general de tóxicos en orina,
que en nuestro hospital incluye: cocaína, cannabis, opiáceos, metildioximetanfetamina
(MDMA), benzodiazepinas, antidepresivos tricíclicos y barbitúricos, aunque estos deben
interpretarse con cautela en función del posible consumo crónico y fenómenos de tolerancia.
Radiografía de tórax: en pacientes expuestos a gases y vapores irritantes, si presentan signos o
síntomas de insuficiencia respiratoria y en todos los casos de intoxicaciones graves para
descartar complicaciones (broncoaspiración, neumonía, atelectasia, etc.).
Radiografía de abdomen: útil en la ingesta de cáusticos, sospecha de ingesta de sustancias
radioopacas (hierro, arsénico o mercurio) o presencia de drogas ilegales ocultas en el tubo
digestivo (body-packers).
Electrocardiograma (ECG): en casos graves y sospecha de intoxicaciones por sustancias
cardiotóxicas (digoxina, antiarrítmicos, antidepresivos tricíclicos y cocaína).
2. Tratamiento inicial del paciente expuesto de forma aguda a un tóxico
Se debe realizar una valoración rápida y global del paciente, con particular vigilancia del control e
inicio de las medidas básicas de soporte de las constantes vitales. La aproximación a la atención del
paciente intoxicado incluye las siguientes medidas:
A (Airway): mantener la permeabilidad de la vía aérea.
B (Breathing): mantener la función respiratoria.
C (Circulation): asegurar el soporte hemodinámico.
D (Decontamination): descontaminación.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1431]
[89] INTOXICACIONES
E (Enhanced elimination): favorecer la eliminación del tóxico.
F (Focused therapy, antidotal therapy): antídoto, si existe.
G, H (Get help): obtener ayuda.
Las medidas de soporte vital son la base del tratamiento de todas las intoxicaciones, y en gran
número de ellas el único posible, por lo que la determinación del agente tóxico causal no debe demorar
nunca el inicio de las mismas. Siempre debe tenerse en cuenta que, si bien el 80% de las intoxicaciones son
leves, hasta el 5% de los pacientes pueden requerir ingreso en una Unidad de Cuidados Intensivos (UCI).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1432]
[89] INTOXICACIONES
Se debe asegurar la permeabilidad de la vía aérea y el control cervical, mantener la función
respiratoria y el soporte hemodinámico. A la hora de valorar el sistema nervioso central, debemos
descartar particularmente dos situaciones:
Coma: en caso de etiología no filiada, se puede realizar un ensayo con glucosa intravenosa
acompañado de 100 mg de tiamina; en caso de respuesta negativa y si existe sospecha clínica,
hacer un ensayo terapéutico de forma sucesiva con naloxona (0,4-0,8 mg iv o im) y/o flumazenil
(0,25-0,50 mg iv).
Convulsiones: se administrará tratamiento sintomático con benzodiazepinas como primera
elección. Ejemplo: diazepam (10-20 mg iv). Ver Capítulo 86. “Crisis comiciales”.
Independientemente de la etiología, tipo y número de agentes involucrados, se puede utilizar el
Poisoning Severity Score (PSS) (Tabla II) para establecer la gravedad inicial del cuadro clínico. Esta escala
tiene la ventaja de que es aplicable en todo tipo de intoxicación, en adultos y niños, y que la graduación de
la gravedad se basa exclusivamente en los síntomas y signos observados, sin tener en cuenta parámetros
como cantidades ingeridas o niveles en plasma o suero.
3. Tratamiento específico
3.1. Descontaminación
En caso de contacto ocular, se debe proceder a la irrigación continua con suero salino fisiológico
(SSF) o agua durante 15 minutos, sin intentarse ningún tipo de neutralización. En caso de contacto cutáneo
(con solventes orgánicos o pesticidas), se realizará un lavado riguroso con agua y jabón y la retirada de la
ropa que llevara el paciente en el momento de la exposición. La persona que realiza la descontaminación
debe protegerse con guantes.
3.2. Disminuir la absorción
En caso de ingesta oral. Es un tema controvertido, ya que, si bien estas medidas disminuyen la
absorción del tóxico, no hay estudios que demuestren que este proceso conlleve una reducción de la
morbimortalidad. Por este motivo, se debe realizar solo a aquellos pacientes que puedan obtener mayor
beneficio:
Presentación precoz (antes de 2 horas).
Ingestión de un tóxico en una cantidad que pueda causar toxicidad.
No presentan factores clínicos de riesgo que contraindiquen la medida.
No debe realizarse si el agente ingerido es claramente no tóxico, si se considera que ya se ha
absorbido de manera completa o si el tóxico no es subsidiario de descontaminación mediante
estas técnicas.
Medidas físicas:
Lavado gástrico con el objetivo de aspirar fragmentos de pastillas u otras toxinas del estómago.
A pesar de ser una técnica muy extendida, actualmente no se recomienda su uso rutinario
debido a lo dudoso de su beneficio y el riesgo de complicaciones importantes. Muy raramente
puede ser útil en pacientes que han ingerido gran cantidad de un tóxico en un tiempo menor de
una hora, y se puede realizar en pacientes en coma, previa intubación, o en pacientes con
riesgo de convulsiones, previo tratamiento. Está contraindicado en caso de vía aérea
desprotegida, ingestión de cáusticos o hidrocarburos y en pacientes con riesgo de hemorragia
gastrointestinal o perforación. Se realiza mediante una sonda multiperforada de 12-13 mm por
vía orogástrica, realizando primero una aspiración y posteriormente irrigando con suero salino
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1433]
[89] INTOXICACIONES
(250 ml) en cada lavado parcial y aspirando hasta que el retorno salga limpio. Cuando se realiza,
debe ir seguido de la administración de carbón activado, excepto en el caso de tóxicos no
absorbibles.
Medidas farmacológicas:
Vaciado gástrico usando:
Carbón activado: su uso está indicado cuando la ingestión del tóxico ha ocurrido en
menos de 2 horas, aunque los beneficios de la administración más tardía no pueden
excluirse. Está contraindicado en situaciones de disminución del nivel de consciencia
(riesgo de aspiración), presentación tardía, necesidad de endoscopia, toxinas no
absorbibles (alcoholes, derivados del petróleo, algunos pesticidas, sales de hierro y
litio), obstrucción intestinal y disminución de la peristalsis. Los principales efectos
secundarios son dolor abdominal, náuseas, vómitos, estreñimiento y diarrea
(especialmente si se ha administrado con catártico, ver más adelante). Se realiza
mediante la administración de 50 g disueltos en 200-250 ml de agua, siempre junto con
un catártico inicialmente (como sorbitol); no se recomiendan las dosis repetidas de
forma rutinaria.
Multidosis de carbón activado: indicado en tóxicos que retornan al tubo digestivo por
excreción biliar (carbamazepina, digoxina, amatoxinas, fenobarbital, dapsona, quinina,
teofilina). Las contraindicaciones son obstrucción intestinal (absoluta) y disminución de
la peristalsis (relativa). La forma de administración es 0,5 g/kg/3 h, y no está indicada
en este caso la administración concomitante de un catártico.
Eméticos: hasta hace unos años era de elección, pero ya no se recomienda su uso
rutinario, puesto que son menos eficaces que el carbón activado, tienen
efectossecundarios impredecibles, aumentan el riesgo de efectos adversos, pueden
retrasar la administración de otros métodos de descontaminación más efectivos y
tienen mayor riesgo de aspiración. En caso de administrarse, puede utilizarse jarabe de
ipecacuana (de elección) en dosis de 30 ml en 200 ml de agua, pudiendo repetirse a los
30 minutos si no se produce el vómito, o mediante apomorfina (0,1 mg/kg sc) como
alternativa si el paciente se niega a tomar la ipecacuana. Solo administrar en caso de
ingesta muy reciente (primera o segunda hora postingesta), estando contraindicados
en pacientes con bajo nivel de consciencia o riesgo de convulsiones, en ingesta de
cáusticos, disolventes o hidrocarburos, coingesta de objetos cortantes, shock o diátesis
hemorrágica, y pacientes debilitados (ancianos, embarazadas o todos aquellos para los
que el vómito pueda suponer un riesgo).
Catárticos (citrato de magnesio, sulfato de magnesio, sorbitol o manitol): su uso en
monoterapia está contraindicado. Se utilizan combinados con carbón activado y en una
única administración.
Irrigación intestinal con solución balanceada de polietilenglicol: no se recomienda su
uso rutinario, excepto en intoxicaciones por sustancias no absorbibles por el carbón
activado (sales de hierro y litio), fármacos de liberación retardada con cubierta entérica
(teofilina, antiarrítmicos), productos muy tóxicos (arsénico o paraquat) o en envases
herméticos (body packers de heroína, cocaína o pilas). Se realiza mediante la
administración de solución evacuante Bohm®, 20 g disueltos en 250 ml de agua, por vía
oral o por sonda nasogástrica (SNG), cada 15 minutos, hasta un total de 2-3 l durante 3
horas.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1434]
[89] INTOXICACIONES
Dilución: nunca se debe neutralizar la toma de ácido con una base y viceversa. Está
indicado en caso de ingesta de cáusticos, mediante la administración de agua o leche,
siendo poco eficaz si no es en los primeros minutos (ver Apartado IV. “Agentes
cáusticos”).
Eliminación endoscópica o quirúrgica: está indicada en la ingestión de conglomerados
de pastillas, cuerpos extraños o metales pesados. La cirugía urgente puede ser
necesaria en caso de paquetes de droga que puedan romperse.
3.3. Excreción del tóxico
Depuración renal: tóxicos con excreción renal que estén parcialmente ionizados en solución.
Está contraindicada en la insuficiencia renal, el edema pulmonar y cerebral o el shock. Se debe
colocar un catéter que mida la presión venosa central y establecer control horario de la
diuresis. Sus complicaciones más frecuentes son los trastornos hidroelectrolíticos y el edema
agudo de pulmón. Cabe destacar:
Diuresis forzada neutra: indicada en 2,4 diclorofenoxiacético (herbicida), Amanitas,
bromo, litio, metotrexato, paraquat (herbicida) y talio. Se realiza mediante 500 ml de
suero glucosalino isotónico + 10 mEq cloruro de potasio (KCl), en perfusión intravenosa
continua, cada 2 horas. Repetir este ciclo las veces que sea necesario, y si la diuresis es
< 250 ml/h añadir 20 mg de furosemida intravenosa, ajustando el volumen de líquidos
para evitar hipovolemia o hipervolemia. Realizar control de ionograma cada 8 horas.
Diuresis forzada alcalina: indicada en 2,4 diclorofenoxiacético, barbitúricos de acción
larga, metotrexato y salicilatos. Se realiza mediante 500 ml de suero bicarbonato sódico
1/6 M, en perfusión intravenosa continua durante 4 horas + 500 ml de suero glucosado
5% + 10 mEq KCl en perfusión intravenosa continua durante las primeras 2 horas y 500
ml de suero glucosalino + 10 mEq KCl en perfusión intravenosa continua durante la
tercera y la cuarta horas.
Diuresis forzada ácida: no se recomienda.
Depuración extrarrenal: indicada en intoxicaciones graves en ausencia de respuesta a las
medidas de soporte general, complicaciones graves e insuficiencia renal o hepática que
aumenten el riesgo de complicaciones.
Hemodiálisis: considerar su uso cuando el aclaramiento mediante hemodiálisis sea
significativamente mayor que al aclaramiento endógeno y el paciente sufra un
deterioro progresivo. Su uso queda limitado a barbitúricos, bromuros, alcoholes
(etanol, isopropranolol, acetona, metanol, etilenglicol con desarrollo de acidosis), litio,
procainamida, teofilina, salicilatos, metales pesados, tricloroetanol, atenolol y sotalol.
Hemoperfusión: no está disponible en todos los centros, pero en general, si se dispone
de ella, su uso es preferible a la hemodiálisis. En el caso de la teofilina, su aclaramiento
es claramente superior mediante hemoperfusión que con hemodiálisis, aunque se
asocia a mayor tasa de complicaciones. Se puede usar también en el caso de
barbitúricos (fenobarbital, primidona), hipnóticos sedantes, fenitoína, teofilina,
disopiramida, cloranfenicol, Amanita, carbamazepina, valproico, procainamida, cafeína,
dapsona, metotrexato, fenilbutazona, tetraclorato de carbono y paraquat. En ambos
casos, se requiere habitualmente anticoagulación con heparina, por lo que pacientes
con hemorragias activas y coagulopatía no serían candidatos a estos procedimientos.
Como efectos secundarios, puede inducir hipotensión (por lo que esta puede ser
también una contraindicación), sangrado por la anticoagulación, hipotermia,
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1435]
[89] INTOXICACIONES
embolismos de aire y las complicaciones derivadas de obtener un acceso venoso
central.
Hemofiltración: se utiliza para la eliminación de aminoglucósidos, vancomicina y
metales; no elimina de manera efectiva tóxicos unidos fuertemente a proteínas. Puede
ser beneficioso también en intoxicaciones por drogas con amplio volumen de
distribución, que se unen fuertemente a tejidos y con baja transferencia
intercompartimental (procainamida).
Exanguinotransfusión: está raramente indicada, aunque puede ser útil en el caso de
hemólisis masiva (clorato de sodio o arsénico), metahemoglobinemia,
sulfahemoglobinemia o toxicidad neonatal.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1436]
[89] INTOXICACIONES
3.4. Terapia dirigida mediante antídoto específico (Tabla III)
Si existe. Los antídotos no están libres de efectos secundarios y, por tanto, su uso debe estar
siempre justificado tanto por la sospecha clínica como por el estado del paciente.
4. Aspectos legales
4.1. Paciente que ingresa cadáver o fallece en urgencias
Si se conoce o sospecha que la intoxicación es la causa de la muerte, existe obligación legal de
comunicarlo al Juzgado de Guardia para la realización de una autopsia médico-legal, ya que no se debe
firmar un certificado de defunción en el que la causa fundamental de la muerte sea una intoxicación.
4.2. Intoxicación por terceras personas
Como en el supuesto anterior, existe obligación legal de comunicarlo al Juzgado de Guardia, en este
caso mediante el parte de lesiones (Tabla IV) correspondiente.
4.3. Intoxicaciones con intención autolítica
Una vez aplicado el tratamiento correspondiente, y aunque la intoxicación sea leve, debe realizarse
una valoración psiquiátrica previa al alta. En caso de que el paciente se niegue a recibir tratamiento, se
evalúa el grado de afectación de las funciones superiores del enfermo, de tal manera que, si se considera
que está capacitado para tomar decisiones, debe respetarse su criterio; en caso contrario, debe obtenerse
el consentimiento de los familiares y, si no es posible, actuar según el criterio, actuar según el criterio que
el facultativo considere adecuado.
4.4. Sospecha de conducción bajo los efectos de un tóxico o prueba de alcoholemia positiva
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1437]
[89] INTOXICACIONES
Si el paciente se somete voluntariamente, se puede proceder a la extracción de una muestra de
sangre (obteniéndose dicho consentimiento por escrito); en caso de que el paciente se niegue, el
facultativo solo realizará dicha extracción si es por orden judicial (Tabla V).
III. INTOXICACIONES MEDICAMENTOSAS
1. Analgésicos
1.1. Paracetamol (acetaminofeno)
Constituye una de las principales causas de sobreingesta medicamentosa. Se considera tóxica la
toma de 7,5 a 10 g de paracetamol de modo agudo, la ingesta de 200 mg/kg en 24 horas o de más de 150
mg/kg/día en 48 horas.
Hay una serie de factores que facilitan la toxicidad hepática del paracetamol, entre los que se
incluye el uso concomitante de fármacos inductores de CYP2E1 como algunos anticomiciales
(carbamazepina, fenitoína) o tuberculostáticos (rifampicina, isoniazida), la malnutrición o la edad avanzada.
En alcohólicos crónicos, se produce mayor toxicidad en los casos de ingesta de dosis supraterapéuticas
repetidas de modo crónico. La ingesta alcohólica simultánea disminuye la capacidad tóxica del
paracetamol.
Clínica:
Periodo inicial (0-24 horas): en general, el paciente está asintomático, aunque puede
cursar con náuseas, vómitos, epigastralgia, malestar y diaforesis. Las transaminasas
suelen ser normales. Solo un pequeño porcentaje de pacientes pasa al periodo
siguiente, ya que el resto presenta una evolución favorable sin toxicidad hepática.
Periodo intermedio (24-72 horas): el paciente puede continuar asintomático o
presentar dolor en el hipocondrio derecho. Es característica la elevación de las
transaminasas, normalmente a las 36 horas, con pico a los 3-4 días. Puede
acompañarse de coagulopatía e hiperbilirrubinemia. Se produce afectación renal en
menos del 2% de los casos y el porcentaje aumenta en los casos de afectación hepática.
También se han descrito efectos en el miocardio, el páncreas, series hematológicas o
inestabilidad hemodinámica. Desde este periodo se puede evolucionar a la normalidad
en pocos días o hacia el siguiente periodo, con fracaso hepático.
Periodo tercero (72 horas-5 días): es el periodo de mayor mortalidad y de máxima
hepatotoxicidad, ya que se puede producir insuficiencia hepática aguda.
Periodo curativo (5-7 días hasta 2 semanas): si se supera el fracaso hepático, la
reversibilidad es total, regenerándose el tejido hepático.
Diagnóstico: el análisis de la concentración sérica de paracetamol es fundamental para el
diagnóstico y para determinar la necesidad de tratamiento. Se debe realizar entre las 4 y 24
horas postingesta. Antes de las 4 horas carece de valor pronóstico, puesto que la absorción no
es completa, y pasadas las 24 horas se habrá metabolizado. En función de los niveles, y
basándose en el Nomograma de Rumack-Matthew (Tabla VI), se decidirá el tratamiento. Se
recomienda monitorizar los niveles hasta su negativización. Se solicitará el perfil hepático al
inicio para tener valores basales. Se debe monitorizar este, así como la glucemia, la coagulación
y la gasometría venosa (al menos cada 12 horas si hay alteraciones).
Tratamiento (Tabla VII)
La descontaminación digestiva se debe hacer con carbón activado en las primeras 4 horas
postingesta.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1438]
[89] INTOXICACIONES
El antídoto específico es la N-acetilcisteína (NAC). Se debe dar en las primeras 6-8 horas tras la
ingesta, aunque se puede iniciar hasta pasadas 36 horas. Se administrará cuando los niveles de
paracetamol superen la línea de tratamiento del Nomograma de Rumack-Matthew (Tabla VI y Figura 1).
Existen dos pautas para administrar NAC, la oral y la parenteral (Tabla VIII), aunque ninguna de
ellas ha demostrado superioridad en los ensayos clínicos. La administración intravenosa se recomienda en
casos con fracaso hepático o si hay síntomas digestivos. Hay que considerar que hasta un 10-20% de los
pacientes presentan reacciones alérgicas a NAC parenteral. En caso de coagulopatía y/o encefalopatía, se
ha de solicitar la valoración por la Unidad de Cuidados Intensivos (UCI) y el equipo de trasplante hepático.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1439]
[89] INTOXICACIONES
La duración del tratamiento, tanto intravenoso como oral, debe ser al menos de 21 horas. En ese
momento, se deben cuantificar los niveles de paracetamol y las enzimas hepáticas. En caso de que los
niveles del fármaco sigan siendo detectables o haya alteración de la función hepática, se recomienda seguir
con la pauta oral como viene especificado, o continuar en caso de protocolo intravenoso a dosis de 6,25
mg/kg/h. Reevaluar cada 12 horas. Se debe mantener el tratamiento hasta que no se detecten niveles del
fármaco y haya descenso significativo de las transaminasas. Se podría suspender la pauta oral antes de las
72 horas si se cumplen estos criterios.
1.2. Salicilatos
El fármaco más usado de este grupo es el ácido acetilsalicílico, aunque también se incluyen otros
como acetilsalicilato de lisina.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1440]
[89] INTOXICACIONES
En función de la cantidad ingerida en dosis única, se puede clasificar en: intoxicación leve, si la
ingesta < 150 mg/kg; intoxicación moderada, cuando se ingieren 150-300 mg/kg; intoxicación grave si > 300
mg/kg o intoxicación letal si > 500 mg/kg.
Clínica: las manifestaciones más precoces son náuseas, vómitos, sensación de calor,
rubefacción y sudoración (son mecanismos para contrarrestar la formación de calor originada
por el fármaco a nivel metabólico). También se producen acúfenos e hipoacusia. A medida que
aumenta la concentración, aparecen síntomas neurológicos como consecuencia de la
estimulación a nivel central del salicilato, como alteraciones neurosensoriales, hiperventilación
con la consiguiente alcalosis respiratoria, cefalea, vértigo y febrícula. En casos más graves,
puede presentarse agitación, confusión, alucinaciones, hiperreflexia y convulsiones, a los que
podría seguir una fase de coma. De forma excepcional, puede producirse edema agudo de
pulmón no cardiogénico o insuficiencia renal (por deshidratación, tubulopatía o rabdomiólisis).
Hay un aumento de la demanda de glucosa, que puede inducir hipoglucemias o incluso
hipoglucorraquia sin hipoglucemia sérica. En relación con las alteraciones ácido-básicas,
inicialmente se objetiva alcalosis respiratoria, seguida de acidosis metabólica con anión gap
elevado (por aumento de los ácidos orgánicos producidos por alteración en el metabolismo y
por la acumulación del propio salicilato) y en fases finales acidosis respiratoria.
Diagnóstico: deben solicitarse niveles de salicilatos a las 6 horas postingesta del fármaco para
tener una aproximación de la toxicidad (Figura 2). Los niveles plasmáticos no se corresponden
de una forma precisa con la toxicidad debido a que, cuando hay acidemia, los salicilatos pasan
al espacio intracelular, aumentando el daño tisular, aunque descendiendo los niveles
plasmáticos. Se debe por ello repetir los niveles a las 6 horas para comprobar su posible
incremento y valorarlos junto con la acidemia. Niveles por encima de 40 mg/dL suelen conllevar
toxicidad y por encima de 65 mg/dL el paciente debe ser valorado por la UCI.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1441]
[89] INTOXICACIONES
Tratamiento: la descontaminación digestiva se debe hacer con carbón activado hasta 2 horas
tras la ingesta. Este periodo se puede prolongar varias horas debido al retraso de la absorción
habitual en el ácido acetilsalicílico en sobredosis o en el caso de haber ingerido pastillas con
cubierta entérica. Se puede plantear una segunda dosis a las pocas horas para evitar la
desadsorción.
Para el aumento de la excreción se emplea la alcalinización de la orina, con el objetivo de alcanzar
un pH urinario de 7,5-8 en intoxicaciones moderadas-graves (salicilemia > 50 mg/dL). Además, esta técnica
disminuye la acidemia en sangre, con la consiguiente salida del fármaco del espacio tisular. Se debe
monitorizar gasométricamente para suspender el tratamiento cuando se alcance un pH arterial > 7,55 y
tener un control de los niveles de potasio. Se inicia con un bolo de bicarbonato 1 M de 1 mg/kg.
Posteriormente, se prepara una infusión de 100 ml de bicarbonato sódico 1 M en perfusión de 4 horas.
Simultáneamente, por otra vía se administran 500 ml de suero glucosado 5% + 20 mEq de potasio. Se
repetirá este ciclo las veces que sean necesarias, añadiendo bolos horarios de 10-20 mEq de bicarbonato 1
M si el pH urinario < 7,5. La alcalinización debe evitarse si existen signos de edema pulmonar o cerebral. Se
suspenderá cuando la salicilemia baje de 35-40 mg/dL y el paciente esté asintomático.
La hemodiálisis debe considerarse en casos de insuficiencia renal o cardiaca graves, acidosis o
toxicidad sobre el sistema nervioso central (SNC) refractarias a tratamiento, o salicilemia > 100 mg/dL. En
casos de deterioro neurológico brusco o convulsiones, administrar 50 ml de glucosa hipertónica (al 33%)
aunque la glucemia sérica sea normal. Está contraindicada la acetazolamida.
1.3. Antiinflamatorios no esteroideos
Clínica: manifestaciones gastrointestinales (vómitos, diarrea), hematológicas (discrasias y
hemorragia), renales (retención hidrosalina, insuficiencia renal, nefritis intersticial
inmunoalérgica o necrosis papilar), cardiacas (descompensación de insuficiencia cardiaca [IC]),
neurológicas (mareo, visión borrosa, somnolencia), obstétricas (retraso del parto o riesgo de
hemorragia) e hipersensibilidad (exacerbación en pacientes con tríada ASA –asma, poliposis
nasal, intolerancia a antiinflamatorios no esteroideos [AINE]–).
Tratamiento: descontaminación digestiva con carbón activado y medidas de soporte.
2. Anticonvulsivos
2.1. Ácido valproico
El rango terapéutico del fármaco es de 50-100 mg/ml. La toxicidad del fármaco se objetiva con
niveles superiores, y normalmente con cifras > 180 mg/ml hay afectación del SNC, aunque no hay una clara
correlación entre la concentración plasmática y los efectos clínicos. A menudo se producen picos tardíos en
plasma (hasta 18 horas postingesta), por lo que debe dejarse al paciente en observación seriando los
niveles plasmáticos hasta que se inicie el descenso de estos.
Clínica: los síntomas más frecuentes son los que afectan al SNC, que incluyen desde
somnolencia hasta coma, así como agitación, mioclonías, temblores, etc. Se puede producir
edema cerebral desde las 12-48 horas postingesta y su aparición no tiene una clara relación con
la dosis ingerida. La aparición de hiperamoniemia puede darse en intoxicaciones agudas o
crónicas, sin correlacionarse necesariamente con una alteración del perfil hepático o con los
niveles de ácido valproico. A nivel digestivo, se suele producir una elevación reversible de las
transaminasas, y en ocasiones pancreatitis o hepatitis rápidamente progresivas. A nivel
analítico, aparece hipernatremia, acidosis metabólica con anión gap elevado, hipocalcemia,
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1442]
[89] INTOXICACIONES
trombopenia y raramente leucopenia y anemia. Hay casos con inestabilidad hemodinámica,
fracaso renal o hipertermia.
Tratamiento: es fundamental el tratamiento de soporte. La descontaminación digestiva debe
hacerse solamente con carbón activado en las 2 horas postingesta. La naloxona a dosis de 0,01
mg/kg en caso de depresión respiratoria tiene cierto efecto. Como la hiperamoniemia y la
hepatotoxicidad pueden estar en parte mediadas por el déficit de L-carnitina, se recomienda su
uso en esos supuestos y en los pacientes con afectación del nivel de consciencia. Se aconseja su
empleo intravenoso con dosis de carga de 100 mg/kg, con un máximo de 6 g, seguida de 15
mg/kg/4 h. En casos de niveles elevados de ácido valproico pero sin afectación clínica, se
recomienda su uso de modo preventivo por vía oral a dosis de 3 g en 4 tomas al día. La
hemodiálisis se puede plantear con niveles > 300 mg/ml, aunque su beneficio es controvertido.
2.2. Carbamazepina
El rango terapéutico está comprendido entre 4-10 mg/ml y su toxicidad se inicia con valores > 12
mg/ml. Se debe establecer una diferencia entre consumidores habituales y aquellos que la ingieren por
primera vez, ya que la carbamazepina (CBZ) induce su propio metabolismo y en pacientes que la toman de
modo crónico se requieren dosis mucho mayores para producir toxicidad. Hay que tener en cuenta la toma
de otros fármacos que puedan ser inductores o inhibidores de su metabolismo. Se recomienda realizar una
seriación de los niveles, ya que el pico puede aparecer hasta días después de la ingesta.
Clínica: suele producir síntomas cardiovasculares y neurológicos. En intoxicaciones leves:
somnolencia, midriasis, nistagmo, ataxia, movimientos coreoatetósicos, disartria y taquicardia.
En intoxicaciones moderadas: depresión del nivel de consciencia, prolongación del intervalo PR,
el complejo QRS y el intervalo QT. En intoxicaciones graves: coma, convulsiones, hipotensión y
arritmias. También son frecuentes síntomas en relación con el síndrome anticolinérgico (íleo
paralítico o retención aguda de orina) e hiponatremia por síndrome de secreción inapropiada
de hormona antidiurética (SIADH).
Tratamiento: descontaminación digestiva con carbón activado; se aconseja administrar
múltiples dosis por la recirculación enterohepática del fármaco (ver Apartado “Multidosis de
carbón activado” al inicio del capítulo). Tratamiento de soporte. En caso de arritmias, valorar
bicarbonato intravenoso, y en caso de crisis comiciales, benzodiazepinas.
2.3. Barbitúricos (fenobarbital)
Son intoxicaciones graves, pero cada vez menos frecuentes. Los efectos tóxicos se producen con
niveles > 50 mg/l, caracterizados por ataxia y depresión progresiva del SNC que llega hasta el coma,
depresión respiratoria, fracaso hemodinámico, depresión miocárdica, hipotermia, íleo paralítico,
epidermólisis (lesiones cutáneas bullosas) y rabdomiólisis. Sus efectos se potencian con el alcohol. Su
efecto sobre el SNC es reversible. Para el tratamiento, es útil el carbón activado (incluso dosis repetidas), la
diuresis forzada con alcalinización de la orina, la hemodiálisis (en especial los de vida media más larga como
el fenobarbital) y la hemofiltración en los de vida media más corta.
2.4. Fenitoína
Su efecto es principalmente a nivel del SNC y, en función del grado de intoxicación, produce
diferente sintomatología; hay una buena correspondencia entre los niveles del fármaco y el grado de
intoxicación (Tabla IX). Puede producir toxicidad cardiovascular (hipotensión, bradiarritmia, asistolia), pero
solo en administraciones intravenosas. Su tratamiento se basa en descontaminación digestiva con carbón
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1443]
[89] INTOXICACIONES
activado (en ocasiones se podría plantear la posibilidad de múltiples dosis) y tratamiento de soporte. No
son útiles las técnicas de diuresis forzada ni hemodiálisis.
3. Psicofármacos
3.1. Benzodiazepinas
Actualmente constituyen la causa más frecuente de intoxicación medicamentosa. La ingesta
exclusiva de benzodiazepinas (BDZ) rara vez produce un cuadro grave, a menos que se asocie con otras
sustancias.
Clínica: la ingesta de 15-20 veces la dosis terapéutica produce deterioro del nivel de
consciencia, ataxia, disartria, nistagmo y, ocasionalmente, excitación paradójica. Si se supera
100 veces la dosis terapéutica, asocia efectos cardiovasculares como hipotensión. En casos
graves (normalmente cuando se asocia con otros fármacos o alcohol), puede haber depresión
respiratoria con broncoaspiración e inestabilidad hemodinámica.
Diagnóstico: se detecta en orina, pero su cuantificación no es relevante. Se requiere una
evaluación de la situación respiratoria con pulsioximetría y radiografía de tórax si hay sospecha
de broncoaspiración.
Tratamiento: descontaminación digestiva con carbón activado solo en las primeras horas
postingesta. El tratamiento es de soporte, con especial atención a la situación respiratoria, ya
que si es necesario se debe proceder a la intubación orotraqueal. El antídoto es el flumazenil
(Anexate®), que está indicado en caso de coma o depresión respiratoria. Se administra un bolo
de 0,2 mg iv a pasar en 30 segundos, se espera un minuto y si no hay respuesta, se repite cada
2-3 minutos hasta una dosis máxima de 2-3 mg. Su efecto desaparece a los 50 minutos, por lo
que hay que mantenerse vigilante pasado este periodo. En caso de ingesta de BZD de vida
media larga, insuficiencia hepatocelular o ancianos, se debe valorar administrar una perfusión a
ritmo de 0,1-0,4 mg por hora. Está contraindicado en caso de convulsiones. Se debe evitar en
pacientes con epilepsia previa, ingesta de proconvulsivos o pacientes con dependencia a
benzodiazepinas.
3.2. Antidepresivos tricíclicos
El efecto principal de los antidepresivos tricíclicos (ADT) se debe al bloqueo presináptico de
neurotransmisores en el SNC (noradrenalina [NA] y serotonina), pero también tiene actividad
anticolinérgica, antagonista α-1-adrenérgico, bloqueante de canales del Na+, antagonista de receptores de
la histamina y del ácido γ-aminobutírico (GABA). A todo ello debe la clínica producida en su intoxicación. Se
considera ingesta tóxica aquella superior a 20 mg/kg, y de carácter grave a la superior a 40 mg/kg.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1444]
[89] INTOXICACIONES
Clínica: se presenta entre 1 y 6 horas tras la ingesta y produce: afectación del SNC, con
deterioro del nivel de consciencia, agitación y convulsiones; afectación cardiaca con aparición
de hipotensión y arritmias (la más frecuente es la taquicardia sinusal, pero puede aparecer
taquicardia ventricular o fibrilación ventricular), y síndrome anticolinérgico (ver Tabla I).
Diagnóstico: se puede detectar en sangre y orina, pero su valor plasmático tiene utilidad
limitada debido a que la concentración se modifica con el pH, el volumen de distribución y la
variabilidad individual. El electrocardiograma (ECG) es el elemento de mayor valor pronóstico;
así, el ensanchamiento del complejo QRS por encima de 100 ms, las alteraciones en el complejo
QRS o la aparición de onda R mayor de 3 mm en aVR son predictores de convulsiones y
arritmias. Se debe repetir cada hora hasta la resolución del cuadro clínico.
Tratamiento: tratamiento de soporte y monitorización cardiaca. Descontaminación digestiva
con carbón activado. En casos graves, se pueden administrar dosis repetidas de carbón
activado. El bicarbonato sódico se considera de elección cuando haya hipotensión, alteraciones
en el ECG o arritmias (la acidosis aumenta la fracción libre de fármaco en sangre). Se inicia con
un bolo de 1-2 mEq/kg con monitorización cardiaca. Si hay cambios en el ECG tras su infusión,
se debe dejar una perfusión de 150 mEq en 4 horas disueltos en 1 l de suero glucosado al 5%.
Se suspenderá cuando alcance un pH de 7,5-7,55. En caso de persistencia de las arritmias a
pesar del bicarbonato, se puede emplear sulfato de magnesio o lidocaína. Si aparecen
convulsiones, administrar diazepam. Si se produce hipotensión a pesar de la fluidoterapia
intensa, el fármaco de elección es la noradrenalina. Están contraindicados los antiarrítmicos
clase IA (procainamida) y IC (flecainida), así como el Anexate® y la fisostigmina. Valorar el
ingreso en la UCI en casos graves. Se puede plantear la emulsión lipídica (ver Apartado
“Calcioantagonistas”) en casos graves refractarios a las medidas planteadas anteriormente.
Evolución: valorar el alta si tras 6 horas de observación el paciente persiste asintomático, sin
alteraciones analíticas ni en el ECG. Si ha precisado tratamiento, debe permanecer en
observación 12-24 horas tras su suspensión.
3.3. Inhibidores de la recaptación de serotonina
Son los antidepresivos más seguros. La ingesta de hasta 30 veces la dosis diaria de inhibidores de la
recaptación de serotonina (ISRS) apenas da síntomas; si la cantidad ingerida alcanza 50-75 veces la dosis
diaria, se producen síntomas leves como somnolencia, taquicardia, náuseas, vómitos y temblor. En casos
graves, en los que se haya ingerido hasta 150 veces la dosis diaria o se haya asociado a otros fármacos, se
produce agitación, arritmias y convulsiones (sobre todo con citalopram y escitalopram). Se puede
desencadenar un síndrome serotoninérgico, principalmente cuando se asocian al menos dos ISRS (ver
Tabla I). El tratamiento se basa en medidas de soporte, descontaminación digestiva con carbón activado y,
en caso de convulsiones, benzodiazepinas. En casos de síndrome serotoninérgico grave, se puede emplear
ciproheptadina 12 mg vo. Si el paciente está asintomático, debe permanecer 6 horas en observación. Si la
ingesta es superior a 150 veces la dosis diaria, seguirá en observación durante 24 horas aunque el paciente
esté asintomático.
3.4. Neurolépticos (antipsicóticos)
Es un grupo heterogéneo de fármacos que, en casos de sobredosis, pueden producir síntomas poco
específicos. Se recomienda descontaminación digestiva con carbón activado, aunque en los neurolépticos
de primera generación no se ha demostrado un claro beneficio.
Pueden producir síntomas neurológicos como alteración del nivel de consciencia, que se manejará
con tratamiento de soporte, o convulsiones, que se tratarán con diazepam; síndrome anticolinérgico (véase
el manejo al comienzo del capítulo); alteraciones en el ECG y arritmias (en la prolongación del intervalo QT,
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1445]
[89] INTOXICACIONES
valorar la hipomagnesemia y la hipopotasemia asociadas y la corrección de las mismas; en arritmias
ventriculares, administrar sulfato de magnesio; en la hipotensión, sueroterapia y, si es preciso, usar
noradrenalina), y síndrome neuroléptico maligno (ver Capítulo 14. “Fiebre de origen desconocido.
Alteraciones de la ermorregulación”). Los síntomas extrapiramidales como distonías o acatisia se pueden
producir con cualquier dosis del fármaco. Para su tratamiento, se emplea difenhidramina (Benadryl® 25-50
mg iv administrados en varios minutos) o biperideno (Akinetón® 2 mg iv o im, que se puede repetir cada 30
minutos hasta dosis de 8 mg en 24 horas).
3.5. Litio
Su margen terapéutico es muy estrecho debido a que los niveles terapéuticos (0,7-1,2 mEq/l) están
muy cerca de los niveles tóxicos (a partir de 1,6 mEq/l). El riesgo de intoxicación es mayor en pacientes que
lo toman de manera crónica (sobre todo en ancianos), en los que puede precipitarse por deshidratación,
insuficiencia renal o asociación con otros fármacos (inhibidores de la enzima de conversión de la
angiotensina [IECA] o AINE).
Clínica:
Intoxicación leve: letargia, debilidad, temblor fino distal, náuseas, vómitos y diarrea.
Intoxicación moderada: temblor grosero, ataxia, lentitud, confusión, hiperreflexia,
clonus y alteraciones inespecíficas en el ECG.
Intoxicación grave: convulsiones, coma, shock, fasciculaciones, arritmias y muerte.
También puede generar hipernatremia por diabetes insípida (sobre todo intoxicación
crónica), alteraciones del tiroides y de la paratiroides.
Diagnóstico: se considera intoxicado aquel con síntomas y litemia > 1,2 mEq/l o cuando existan
niveles > 1,6 mEq/l. En ocasiones, los niveles no se corresponden con la clínica debido a su
lenta absorción por el SNC. Se deben seriar los niveles hasta alcanzar el pico de litemia. Se
pueden producir falsos positivos si se envía la muestra en tubo con heparina de litio.
Tratamiento: no está indicado el carbón activado. Se recomienda el lavado intestinal total con
solución Bohm® hasta 12 horas postingesta en caso de haber tomado comprimidos de
liberación retardada. Es fundamental la hidratación hasta conseguir euvolemia y normalización
de la natremia. La hemodiálisis es el tratamiento de elección en: litemia > 3,5 mEq/l,
independientemente de la clínica; litemia > 2 mEq/l con síntomas neurológicos, en situaciones
donde esté limitada la reposición de volumen (IC) o en las que esté limitada la eliminación del
fármaco (insuficiencia renal). Tras la diálisis es esperable un efecto rebote por la salida del litio
intracelular al espacio extracelular, por lo que se requerirá una segunda sesión. Existe una
relación entre el tiempo de litemia elevada y las secuelas neurológicas a largo plazo, por lo que
no debe retrasarse la diálisis en caso de que esté indicada.
4. Antiarrítmicos
4.1. Calcioantagonistas
Hay dos tipos de calcioantagonistas, los dihidropiridínicos (amlodipino, nifedipino, etc.) y los no
dihidropiridínicos (diltiazem y verapamilo). La intoxicación por los primeros produce hipotensión y
taquicardia refleja; los segundos ocasionan hipotensión, inotropismo negativo y bradicardia. No obstante, a
medida que las dosis aumentan, la especificidad de grupo se pierde y las dihidropirinas pueden tener efecto
en la contractilidad y conducción cardiaca. Se consideran dosis tóxicas entre 5 y 10 veces la dosis diaria.
Clínica: principalmente, toxicidad cardiológica (hipotensión, bradicardia, ritmos nodales
rápidos, asistolia) pero también síntomas neurológicos (deterioro del nivel de consciencia,
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1446]
[89] INTOXICACIONES
convulsiones), gastrointestinales (náuseas, vómitos, íleo paralítico, isquemia intestinal) y
metabólicos (hiperglucemia y acidosis láctica).
Tratamiento: vigilancia estrecha con reevaluaciones frecuentes, ya que los pacientes pueden
deteriorarse de modo brusco. Descontaminación digestiva con carbón activado. El tratamiento
varía en función de la gravedad del paciente:
Paciente asintomático: si el ECG es normal, se puede dar el alta tras 6-8 h de
observación.
Intoxicación leve-moderada: suele cursar con hipotensión y bradicardia leve. Hay una
serie de medidas recomendadas que se deben aplicar de modo escalonado, pasando a
la siguiente si pasados 15 minutos no ha sido efectiva la medida empleada:
De inicio, expansión de la volemia con 500-1.000 ml de suero salino fisiológico
(SSF) 0,9% en 1 hora y atropina (0,5-1 mg iv, que se repite cada 3 minutos hasta
una dosis de 3 mg). Si persiste la clínica, comenzar tratamiento con cloruro de
calcio al 10%, 10-20 ml iv, o gluconato de calcio, 30-60 ml iv. Se pueden repetir
los bolos cada 20 minutos o iniciar perfusión (cloruro de calcio 0,2-0,4 ml/kg/h;
gluconato de calcio 0,6-1,2 ml/kg/h).
Glucagón intravenoso (introduce el monofosfato de adenosina cíclico [AMPc]
en las células), en situaciones de mala respuesta a los tratamientos previos.
Debe reconstituirse el preparado comercial en polvo para administrar por vía
intramuscular, sustituyendo el diluyente comercial por suero salino para su
administración intravenosa. La dosis es de 3 mg en 1 minuto, que se puede
aumentar si es necesario a 5 mg el bolo y perfusión continua a 5 mg/h.
Insulina, si no hay respuesta. Administrar en bolo intravenoso a dosis de 0,1
UI/kg seguido de perfusión de 0,2-0,3 UI/kg/h asociado a suero glucosado 5-
10%.
Fármacos vasoactivos (noradrenalina, isoprenalina) o colocación de un
marcapasos temporal en el caso de fracaso de los tratamientos previos.
Intoxicación grave: se caracteriza por presentar hipotensión y bradicardia grave. Se
aplicarán las mismas medidas que en casos moderados pero de modo simultáneo.
Valorar contactar con la UCI.
Si las terapias anteriores fracasan, está indicado emplear emulsiones lipídicas, que en estudios
preliminares han demostrado ser beneficiosas en pacientes hemodinámicamente inestables con
intoxicación por fármacos lipofílicos como calcioantagonistas o betabloqueantes. Se recomienda un bolo
inicial de 1,5 ml/kg (basado en el peso ideal) de emulsión lipídica al 20% durante 1 minuto, seguido de una
perfusión a 0,25 ml/kg/min hasta conseguir la mejoría hemodinámica (normalmente, 30-60 minutos). Si no
es efectivo, se puede repetir el bolo hasta 3 veces en caso de parada cardiaca o aumentar la perfusión a 0,5
ml/kg/min en la hipotensión refractaria. Se han objetivado hipertrigliceridemia, embolismo graso e
infecciones como efectos adversos. Puede alterar algunos resultados analíticos.
4.2. Betabloqueantes
Clínica: a nivel cardiovascular, se observa hipotensión y bradicardia, que puede progresar a
shock cardiogénico o todo tipo de arritmias. En el ECG pueden aparecer signos de intoxicación
entre 20 minutos y 3 horas tras la ingesta. El alargamiento del complejo QRS > 120 ms o del
intervalo QT son signos de gravedad. A nivel neurológico, pueden producir somnolencia,
agitación, alucinaciones, convulsiones y coma. También se puede observar broncoconstricción,
acidosis láctica, hiperpotasemia (por insuficiencia renal aguda), hipocalcemia e hipoglucemia.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1447]
[89] INTOXICACIONES
Tratamiento: descontaminación digestiva con carbón activado. Si aparece broncoespasmo,
administrar beta-2 agonistas, y si se producen convulsiones, benzodiazepinas. Desde el punto
de vista cardiológico, el tratamiento se divide en función de la gravedad del paciente:
Asintomático: mantener en observación durante 12 horas con control analítico y de
ECG.
Intoxicación leve-moderada: suele cursar con hipotensión y bradicardia leve. Se debe
actuar de modo escalonado, progresando al siguiente paso en caso de ausencia de
respuesta cada 15 minutos (ver Apartado 4.1. “Calcioantagonistas”). Se debe recordar
que en caso de arritmias se valorará tratamiento con bicarbonato o sulfato de
magnesio.
Intoxicación grave: hipotensión y bradicardia graves. Se emplearán de modo
simultáneo las terapias anteriores. Se podrían administrar emulsiones lipídicas (ya
explicadas en el apartado anterior).
4.3. Digoxina
Su intoxicación es frecuente por su estrecho margen terapéutico (0,8-2,2 ng/ml), alcanzado cifras
tóxicas con rangos por encima de 2,5 ng/ml. Para medir los niveles deben haber pasado 6 horas tras la
ingesta oral o al menos 4 horas tras la administración intravenosa. Los niveles no se corresponden
completamente con el grado de intoxicación.
Se puede producir una intoxicación por ingesta aguda masiva (más rara) o más frecuentemente por
sobredosificación en pacientes que lo toman de manera habitual (en general, por insuficiencia renal). Hay
ciertas situaciones que incrementan su toxicidad, como hipopotasemia, hipomagnesemia, hipercalcemia,
hipoxia, cardiopatía isquémica, hipotiroidismo o determinados fármacos (amiodarona, betabloqueantes,
calcioantagonistas, etc.).
Clínica: síntomas digestivos como náuseas, vómitos o dolor abdominal (más frecuente en
intoxicaciones agudas), síntomas neurológicos como síndrome confusional, cefalea o
convulsiones (más habituales en la intoxicación crónica), alteraciones visuales como visión
amarillenta, escotomas o ceguera. Las alteraciones cardiacas son las más graves, ya que
producen casi todo tipo de arritmias, desde extrasístoles hasta fibrilación ventricular,
incluyendo arritmias más específicas como ritmo acelerado de la unión auriculoventricular (AV)
o taquicardia ventricular bidireccional.
Tratamiento: descontaminación digestiva con carbón activado. La mayoría de los casos no
necesitan tratamiento, salvo hidratación y corrección de la función renal. En caso de
intoxicación aguda grave, valorar la indicación de anticuerpos antidigoxina (Fab; Digibind® vial,
38 mg). Esta terapia se recomienda en arritmias que conlleven riesgo vital, datos de disfunción
de algún órgano o hiperpotasemia > 5,5 mEq/l. Se debe disolver la dosis en SSF y pasar en 30
minutos, apreciándose los efectos en 1 hora. La dosis del antídoto se obtiene al multiplicar por
0,8 la dosis ingerida de digoxina (en mg). Si se desconoce la dosis ingerida, se utilizarán 480 mg
de antídoto. Hasta su cálculo y preparación se puede emplear atropina o se puede colocar un
marcapasos temporal. La respuesta al tratamiento se monitorizará con ECG, no con niveles de
digoxina.
5. Isoniazida
En la intoxicación aguda se produce alteración del nivel de consciencia y convulsiones, pudiendo
llegar a estatus convulsivo (mayor probabilidad cuanto mayor es la dosis ingerida). En intoxicaciones
crónicas se observa hepatotoxicidad y neuropatía periférica. La descontaminación se debe hacer de modo
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1448]
[89] INTOXICACIONES
precoz (1-2 horas postingesta) con carbón activado, y solo en casos muy graves con lavado gástrico. Si hay
presencia de convulsiones, se debe emplear piridoxina intravenosa a dosis de 1 g por cada gramo ingerido
de isoniazida a pasar en 5 minutos (si se desconoce la dosis tóxica, administrar 5 g) asociado a
benzodiazepinas. Con el tratamiento adecuado y en ausencia de complicaciones, el pronóstico es bueno
tras 24-48 horas. Si el paciente está asintomático a las 6 horas postingestión, es poco probable que
desarrolle complicaciones.
6. Antidiabéticos orales
Ver Capítulo 71. “Complicaciones agudas de la diabetes”, Apartado “Hipoglucemia”.
7. Anticoagulantes orales
Ver Capítulo 77. “Trastornos de la hemostasia. Anticoagulación”, Apartado “Anticoagulación”.
IV. AGENTES CÁUSTICOS
Son intoxicaciones frecuentes por su fácil acceso y uso cotidiano (doméstico). Normalmente
aparecen tras la ingestión, accidental o voluntaria con finalidad autolítica, de ácidos fuertes, como el
clorhídrico o el sulfúrico (sospechar con la ingestión de limpiadores domésticos, tintes del pelo, líquido de
baterías o productos industriales) o de bases fuertes como hidróxido de sodio o potasio (desatascadores,
pilas de botón o limpiadores de hornos), carbonato de sodio (detergentes de lavavajillas), amoniaco o
hipoclorito sódico (lejía).
Ocasionan lesiones en el tracto digestivo y a veces en el tracto respiratorio por su capacidad para
emitir vapores (especialmente al mezclar dos o más productos domésticos, como ocurre con la lejía y el
amoniaco), llegando a producir neumonitis química y síndrome de dificultad respiratoria aguda (SDRA). De
manera general, la ingesta de álcalis origina lesiones más graves (mayor riesgo de perforación por
licuefacción pero con menor afectación gastroduodenal por neutralización parcial) que la ingesta de ácidos
(daño por coagulación, especialmente a nivel del estómago, con menor ingesta total por causar dolor al
contacto con la orofaringe).
Clínica: varía desde pacientes asintomáticos hasta aquellos que muestran intensa odinofagia,
disfagia, sialorrea e incluso hematemesis. La ronquera o estridor sugiere implicación de la
laringe y la epiglotis (compromiso de la vía respiratoria) o la aspiración del cáustico. No existe
una buena correlación entre los síntomas y la gravedad y en ningún caso la ausencia de lesiones
orofaríngeas descarta la presencia de lesiones esofagogástricas graves. Puede haber
hipocalcemia, hipomagnesemia, hemólisis y acidosis metabólica.
Valoración inicial (Figura 3): lo primero es asegurar la vía aérea y la estabilidad hemodinámica.
El lavado por sonda nasogástrica, la inducción del vómito, el intento de dilución con agua y el
uso de sustancias neutralizantes están contraindicados. El carbón activado es inútil y dificulta la
endoscopia. La endoscopia digestiva es siempre necesaria, ya que define la gravedad de las
lesiones y el manejo. Se debe practicar el estudio en las primeras 6-24 horas tras la ingesta
(cuando más tarde se realice, más se incrementa el riesgo de perforación yatrogénica) y se
debe realizar siempre y cuando se haya descartado perforación digestiva. Por ello, el primer
paso es hacer radiografías de tórax y abdomen para descartar perforación (mediastinitis,
peritonitis). En caso de sospecha de perforación que no se detecte en la radiografía simple, se
realizará una tomografía computarizada (TC) con contraste hidrosoluble pero no estudios
baritados, ya que interfieren en la endoscopia y pueden originar neumonitis o peritonitis
química en caso de perforación. Igualmente, debe valorarse la afectación de la vía área superior
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1449]
[89] INTOXICACIONES
mediante laringoscopia directa, especialmente si hay datos clínicos que lo sugieran (estridor,
disfonía) y valorar edema de glotis que requiera intubación orotraqueal o traqueostomía. La
clasificación endoscópica de las lesiones agudas inducidas por cáusticos es la de Zargar: grado
0, ninguna lesión; grado I, edema y eritema; grado IIA, úlceras superficiales (erosión); grado IIB,
úlceras profundas; grado III, necrosis focal, y grado IV, necrosis extensa y/o perforación. Se
relacionan directamente con la evolución y orientan el tratamiento.
Tratamiento: está indicado el uso de inhibidores de la secreción gástrica, siendo de elección los
inhibidores de la bomba de protones (IBP) por vía oral o intravenosa según la gravedad. Se
debe administrar analgesia adecuada (generalmente cloruro mórfico). El uso de corticoides es
controvertido; tienen un potencial efecto antiinflamatorio y disminuyen el riesgo de estenosis
posterior pero no parecen estar indicados de forma generalizada, ya que disminuyen la
cicatrización de las lesiones y aumentan el riesgo de infección. No obstante, deben valorarse en
lesiones graves (grados IIb y III de Zargar) por su posible efecto beneficioso. Los antibióticos
solo se aconsejan en caso de que se demuestren microperforaciones o complicaciones y en
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1450]
[89] INTOXICACIONES
aquellos casos en los que se usen corticoides (será de elección una antibioterapia de amplio
espectro como amoxicilina/ácido clavulánico). El manejo estará condicionado según la
gravedad de las lesiones:
Lesiones de grados 0, I y IIA: pueden ser dados de alta con IBP a dosis altas por vía oral
durante 7 días (omeprazol 20 mg/12 h) y dieta líquida, con progresión a dieta completa
durante las 24-48 horas siguientes.
Lesiones de grados IIIB y III: tienen un elevado riesgo de desarrollar estenosis y
complicaciones (máximo riesgo de perforación en las primeras 48 horas), por lo que
requieren hospitalización para vigilancia y soporte nutricional parenteral (está
contraindicada la nutrición enteral por sonda nasogástrica (SNG), ya que aumenta el
riesgo de perforación). Se deberá mantener al paciente en observación e iniciar
tolerancia en 48 horas si es capaz de tragar saliva. La alimentación oral se introducirá
en cuanto sea posible.
Lesiones de grado IV: está indicada la cirugía urgente (también si existe perforación,
mediastinitis o peritonitis). La ingestión de pilas planas tiene el peligro de liberar su
contenido cáustico y causar perforación, por lo que debe intentarse su extracción
endoscópica, y si no es posible, hacer seguimiento radiológico e intervenir si aparecen
complicaciones.
Secuelas: hasta un tercio de los pacientes tienen posteriormente estenosis esofágicas tardías
(entre 1 y 3 meses después) y existe un aumento del riesgo de cáncer epidermoide de esófago
de entre 30 y 100 veces hasta 40 años después del episodio. Por ello, está indicado realizar una
endoscopia en un segundo tiempo de control (generalmente a partir de los 3 meses) e iniciar el
cribado mediante endoscopia a partir de los 15-20 años de la ingesta. En caso de estenosis
como complicación tardía, el tratamiento de elección es la dilatación endoscópica con balón
junto con la administración intralesional de corticoides, valorando la colocación de
endoprótesis en caso de fracaso de las dilataciones.
V. INTOXICACIÓN POR GASES
1. Gases no irritantes
1.1. Monóxido de carbono (Figura 4)
Es responsable de más del 50% de las intoxicaciones por gases, siendo la principal causa de muerte
por inhalación de gases, especialmente durante el invierno. El monóxido de carbono (CO) es un gas
inodoro, incoloro e insípido que se produce en todas las combustiones incompletas (braseros de leña,
incendios, gases del tubo de escape de motores de explosión y calentadores de gas). Un mecanismo
habitual de intoxicación es por mala combustión de calderas o estufas de gas en estancias mal ventiladas.
Su absorción es rápida por vía pulmonar, y su acción tóxica se basa en una combinación de efectos
hipóxicos debido a la formación de carboxihemoglobina (COHb; efecto principal), cuya afinidad por la
hemoglobina (Hb) es 200 veces superior a la del oxígeno, lo que conlleva una disminución de la Hb efectiva
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1451]
[89] INTOXICACIONES
para transportar oxígeno; y a toxicidad celular directa (unión a metaloproteasas, que produce acidosis
metabólica y aumento de óxido nítrico, que desencadena vasodilatación y síncope).
Clínica: depende de las tasas en sangre de COHb:
Menor del 10%: el paciente permanece asintomático.
Entre 15 y 25%: cefaleas, mareo y náuseas.
Entre 30 y 40%: dificultad respiratoria, debilidad en las extremidades, confusión
mental, alteraciones visuales.
Entre 45 y 60%: acidosis metabólica por hipoxia tisular, color rojo cereza en piel y
mucosas, edema pulmonar, síncope y coma.
Mayor del 60%: parada cardiorrespiratoria. Debido a la unión con la mioglobina puede
facilitar la aparición de rabdomiólisis, isquemia miocárdica y arritmias fatales.
Síndrome neurológico tardío: consiste en la aparición de trastornos neuropsiquiátricos
diversos (deterioro cognitivo, parkinsonismo, psicosis) al cabo de días o semanas
después de la intoxicación y tras haberse constatado la recuperación clínica y la
normalización de COHb. Presenta una frecuencia variable que puede llegar al 10%. Su
mecanismo se desconoce, pero se ha sugerido toxicidad directa por CO, que consiste en
desmielinización a nivel de los ganglios basales o de la sustancia blanca profunda
(alteraciones visualizadas en pruebas de imagen cerebral). Esta sintomatología es
reversible en el 50-75% de los casos en el periodo de un año.
Diagnóstico: la sospecha suele establecerse por factores ambientales y epidemiológicos, y es
habitual la presencia de varias personas afectadas. Se confirma con la medición de niveles de
COHb de una muestra de sangre venosa o arterial; en este sentido, valores superiores al 3-4%
en no fumadores y superiores al 10% en fumadores se consideran patológicos. La presión
parcial de oxígeno y la pulsioximetría (excepto algunos modelos especiales) muestran valores
falsamente normales (determinan saturación global de la Hb sin diferenciar si es por CO o por
oxígeno), por lo que su uso no es fiable. Es necesaria la determinación directa de la saturación
arterial de oxígeno mediante gasometría. Esta es igualmente utilizada para determinar niveles
de ácido láctico, en intoxicaciones leves o moderadas de CO (COHb < 20%). Si existe acidosis
láctica, sobre todo con niveles de ácido láctico > 10 mmol/l, se debe sospechar intoxicación
conjunta de CO y cianuro (cointoxicación frecuente por inhalación de humo de incendio; ver
Apartado “Cianuros” más adelante).
Tratamiento: salir de la zona de exposición y administrar oxígeno a alto flujo de forma precoz,
normalmente mediante mascarilla con reservorio para conseguir una fracción inspiratoria de
oxígeno (FiO2) del 100%, hasta que los niveles de COHb estén por debajo del 3% y el paciente
esté asintomático (lo que suele tardar unas 6 horas por la semivida de eliminación del CO). La
simple sospecha de intoxicación justifica la administración de oxígeno a alto flujo, cuyo objetivo
es desplazar el CO de sus lugares de unión, y no solo la corrección de una posible hipoxemia
coexistente, por lo que se debe mantener elevada la FiO2 durante todo el tiempo (incluidos los
casos que requieran ventilación) con monitorización periódica de los niveles de COHb cada 4
horas. Si aparecen signos de fatiga con hipoxemia y desaturación a pesar del reservorio, se
valorará proceder a intubación y ventilación mecánica (que reduce la vida media de la COHb a
90 minutos). La oxigenoterapia hiperbárica a 3 atmósferas se valorará en los siguientes casos,
teniendo en cuenta la disponibilidad de una cámara hiperbárica cercana y la seguridad y
estabilidad hemodinámica del traslado: sintomatología neurológica grave (por ejemplo, coma o
disminución del nivel de consciencia en el rescate o durante la evolución); COHb > 30-40%;
acidosis grave con lesión de órgano vital (isquemia cardiaca o cerebral); embarazadas con COHb
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1452]
[89] INTOXICACIONES
> 20% o > 15% si hay datos de sufrimiento fetal; y en la refractariedad a tratamiento con O2
normobárico (definida por la persistencia de síntomas a las 4-6 horas).
1.2. Cianuros
La intoxicación por cianuro se produce habitualmente por inhalación de sus derivados gaseosos
(ácido cianhídrico, cianógeno y derivados halogenados), que puede ocurrir en trabajadores de la plata,
combustión de plásticos o moquetas artificiales, por el humo de incendios (intoxicación mixta por CO y
cianuro) o por fármacos como el nitroprusiato sódico. El cianuro es un gas incoloro con olor a almendras
amargas, que inhibe la citocromooxidasa mitocondrial, generando hipoxia celular grave con acidosis láctica
secundaria.
Clínica: aparece en el curso de la primera hora tras la intoxicación, se caracteriza por
hiperventilación refleja debida a la acidosis metabólica (que puede ser mal interpretada como
ansiedad), así como síntomas inespecíficos derivados de la anerobiosis (cefalea, náuseas,
vómitos, disminución del nivel de consciencia, letargia) y fallo multiorgánico (insuficiencia renal
y hepática, coagulación intravascular diseminada [CID]). Es típico el olor del paciente o del
aliento a almendras amargas y la coloración rojo cereza de la piel.
Diagnóstico: aunque se pueden determinar los niveles de cianuro o tiocianato (metabolito
intermedio del cianuro) en sangre, orina, contenido gástrico y tejidos (niveles de tiocianato
entre 20 y 30 mg/dL se consideran peligrosos y superiores a 100 mg/dL se consideran letales),
su resultado no suele estar disponible en el plazo de la toma de decisiones. Ante la sospecha, se
debe realizar una gasometría con ácido láctico; así, niveles de ácido láctico ≥ 10 mmol/l
presentan una buena sensibilidad y especificidad para intoxicación por cianuro (traducción de
la grave hipoxia celular) y tienen buena correlación con la gravedad. En general, esta
intoxicación debe sospecharse en un trabajador de la industria química o con antecedentes de
incendio en una industria de material plástico o poliuretano, que sufre de forma súbita un
desvanecimiento y presenta al ingreso acidosis láctica que no responde de forma rápida a la
oxigenoterapia.
Tratamiento: es importante desnudar al paciente y lavarle con agua y jabón neutro para
disminuir la absorción de cianuros por vía cutánea. Se aplicarán medidas generales de soporte
(oxigenoterapia al 100%, soporte hemodinámico y corrección de la acidosis con bicarbonato) y
se valorará el empleo de antídotos que generen compuestos estables y atóxicos con el cianuro.
Actualmente, el antídoto de elección es la hidroxicobalamina (vitamina B12) intravenosa a dosis
de 70 mg/kg (la dosis estándar para adultos es de 5 g iv (CyanoKit©), que al unirse al cianuro
genera cianocobalamina (compuesto neutro y atóxico que se elimina por vía renal) con pocos
efectos adversos (el más típico es color rojo anaranjado de la orina), por lo que puede
administrarse a pacientes críticos. Su uso está indicado en intoxicaciones graves (rápido
descenso del nivel de consciencia, inestabilidad hemodinámica, lactato > 7,5 mmol/l). También
puede usarse conjuntamente (o según su disponibilidad) el tiosulfato sódico (12,5 g iv en 50 ml
a pasar en 10 minutos; si el paciente no mejora en 30 minutos, se puede administrar una dosis
extra de 6,25 g), que reacciona con el cianuro para crear tiocianato (compuesto atóxico de
eliminación renal), aunque su efecto es menor.
2. Gases irritantes (ácido sulfhídrico, fluoruros, cloruros, amoniaco)
La exposición a gases irritantes debe sospecharse cuando exista contacto con descomposición de
materia orgánica como alcantarillas, pozos negros o estiércoles líquidos (exposición a ácido sulfhídrico); en
trabajadores de la industria del vidrio, cerámica o petróleo (derivados fluorados) o en contacto con
fertilizantes; en la desinfección de piscinas o mezclas domésticas con lejías y amoniaco (derivados
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1453]
[89] INTOXICACIONES
clorados). Todos ellos se caracterizan por producir profundas y extensas lesiones en la mucosa de las vías
aéreas que pueden alcanzar los alveolos y generar edema agudo de pulmón según la intensidad y duración
de la exposición; son especialmente agresivos los gases hidrosolubles (amoniaco, ácido sulfhídrico y cloro),
ya que producen marcados signos de irritación de las mucosas de las vías respiratorias altas y edema de
glotis (estridor). La manifestación que domina el cuadro clínico es la insuficiencia respiratoria aguda, que
suele acompañarse de irritación de las mucosas (lagrimeo, tos, estornudos) o a veces quemaduras graves
de la piel. El tratamiento general es sintomático (no existen antídotos) y consiste en corregir la hipoxemia
(puede ser necesario soporte ventilatorio), tratamiento broncodilatador y corticoides en caso de
broncoespasmo, prevención antibiótica y analgesia. Debe mantenerse al paciente en observación durante
al menos 8-12 horas por el riesgo de aparición de SDRA tardío.
VI. INTOXICACIÓN POR HUMO
Los síntomas consisten en tos, expectoración de esputo negruzco (que pueden permanecer hasta 2
semanas después), disfonía, disnea, estridor, broncoespasmo y edema pulmonar. Las complicaciones
respiratorias pueden aparecer hasta 3 días más tarde. En la exploración hay que valorar las fosas nasales
para buscar las vibrisas chamuscadas, un signo de exposición intensa y de gravedad. El tratamiento se basa
en medidas de soporte respiratorio con aspiración frecuente de las secreciones y administración de oxígeno
humidificado. La broncoscopia puede ser necesaria para eliminar detritos endotraqueales. Los pacientes
asintomáticos y no pertenecientes a grupos de riesgo solo precisan 4-6 horas de observación.
VII. INTOXICACIÓN POR SETAS
Se producen por la ingesta accidental de especies venenosas confundidas con las comestibles. Es
frecuente que aparezcan varios casos simultáneamente en otoño. Desde el punto de vista clínico, estas
intoxicaciones se clasifican en dos grandes grupos según el periodo de latencia (mayor o menor de 6 horas),
lo cual ayuda a la orientación diagnóstica. Es importante la identificación de la especie por un micólogo
experto (enviar fotografías al Instituto Nacional de Toxicología y Ciencias Forenses y conservar las setas en
nevera envueltas en papel, nunca en bolsa de plástico).
1. Síndromes de aparición precoz (< 6 horas): toxicidad leve (Figura 5)
1.1. Síndrome muscarínico
Se debe al efecto de la muscarina de los hongos del tipo Clitocybe e Inocybe. Cursa con síndrome
colinérgico (ver Tabla I), que aparece entre 15 minutos y 2 horas después de la ingesta. El tratamiento
comprende medidas generales de sostén (el cuadro cede espontáneamente en unas horas) y en casos
graves el uso de atropina (0,5-1 mg iv, que se puede repetir cada 5-10 minutos hasta el control de la
frecuencia cardiaca o la broncorrea).
1.2. Síndrome micoatropínico (neurológico o glutamatérgico)
Producido por Amanita muscaria o Amanita panthera. Tras 30 minutos-3 horas, producen dolor
abdominal y síndrome anticolinérgico (ver Tabla I) con clínica neurológica variable, predominando los
efectos gabaérgicos en los adultos (vértigo, somnolencia, delirio y alucinaciones) y los glutaminérgicos en
los niños (hiperactividad, hiperreflexia, mioclonías y convulsiones). El cuadro se autolimita en pocas horas.
El tratamiento comprende las medidas generales de sostén, lavado con carbón y administración de
diazepam en caso de agitación (0,5 mg/kg iv; 3 dosis en 4 horas). En casos graves (convulsiones intratables
o arritmias con compromiso hemodinámico), está indicado administrar fisostigmina (bolo de 1 mg iv con
monitorización electrocardiográfica, que puede repetirse cada 5 minutos; en casos graves, infusión
continua a 4 mg/h).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1454]
[89] INTOXICACIONES
1.3. Síndrome gastrointestinal puro
Se debe a “hongos irritantes” como el Entoloma lividum. Poseen sustancias que inflaman la mucosa
digestiva entre 30 minutos y 3 horas tras la ingesta, provocando un corto cuadro gastrointestinal de
resolución espontánea (12- 48 horas).
1.4. Síndrome pseudoantabus, acetaldehídico o copriniano
Consiste en un efecto “disulfiram” (flushing, vómitos, taquicardia, cefalea, ansiedad, dolor torácico,
etc.) si hay toma de alcohol en las horas siguientes a la ingesta de Coprinus atramentarius, al inhibir la
aldehído deshidrogenasa. Este efecto aparece a los 30-60 minutos del consumo de etanol y siempre que la
seta se haya ingerido en un plazo inferior a 5 días. El cuadro clínico suele ser leve y autolimitado tras 3-6
horas. El tratamiento es sintomático y de mantenimiento, y está prohibida la ingesta de alcohol durante 4-5
días.
1.5. Síndrome alucinatorio
Por consumo de hongos importados como droga recreativa que provocan hiperactividad simpática
y un cuadro neuropsíquico de confusión, debilidad y alucinaciones visuales, auditivas y táctiles; el paciente
puede desarrollar hipertermia y convulsiones. Estos síntomas aparecen a los 30 minutos de su ingestión y
suelen desaparecer a las 6-8 horas. El tratamiento es el de las complicaciones y el uso de sedantes
(diazepam).
2. Síndromes de aparición tardía (> 6 horas): toxicidad grave (Figura 6)
2.1. Síndrome faloidiano
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1455]
[89] INTOXICACIONES
La Amanita phalloides es la más peligrosa, ya que causa alrededor del 90% de las muertes por setas.
Genera gran toxicidad y necrosis celular a través de toxinas (amatoxinas), especialmente sobre hepatocitos,
túbulos renales y epitelio intestinal al presentar circulación enterohepática. Una ingesta de 10 mg (menos
de una seta) puede producir fallo hepático fulminante.
Clínica: se distinguen varias fases en la evolución:
Periodo de incubación o latencia (8-12 horas postingesta): asintomático. El inicio de los
síntomas antes de 6 horas no descarta síndrome faloidiano, ya que pueden haberse
ingerido conjuntamente otras setas que generen síntomas antes.
Periodo coleriforme o fase intestinal (12-24 horas postingesta): gastroenteritis grave
(dolor abdominal, diarrea profusa, náuseas, vómitos y alteraciones hidroelectrolíticas
por deshidratación).
Fase de mejoría aparente (24-36 horas): resolución del cuadro de gastroenteritis y
alteraciones hidroelectrolíticas pero puede haber alteración del perfil hepático.
Fase de agresión visceral o hepatorrenal (48-72 horas tras la ingesta): empeoramiento
del estado general con datos de insuficiencia hepática grave que puede llevar al fallo
hepático fulminante (ictericia, hepatomegalia blanda y dolorosa,
hipertransaminasemia, hiperbilirrubinemia, coagulopatía, hipoglucemia), y de
insuficiencia renal (hipovolemia, hipoperfusión, nefritis tubulointersticial). La
mortalidad se estima en el 30%.
Fase de recuperación (a partir del 5-7º día): si se supera la fase anterior se constata un
descenso progresivo de las enzimas hepáticas y recuperación de la actividad de
protrombina. Puede haber recuperación completa o desarrollarse una hepatitis crónica.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1456]
[89] INTOXICACIONES
Diagnóstico: se puede utilizar inmunoanálisis para detectar amatoxinas en la orina o el aspirado
gástrico, teniendo en cuenta que 48 horas después de la ingestión perdería fiabilidad para
descartar el envenenamiento. No hay relación entre la concentración y el pronóstico. Esta
técnica solo está disponible en centros especializados, por lo que muchas veces el diagnóstico
será clínico y por reconocimiento de la seta por un micólogo experto (si se posee el ejemplar).
Tratamiento: debe ser lo más precoz posible y no hay que retrasarlo a la espera de
confirmación diagnóstica. Se fundamenta en tres pilares:
Medidas de soporte: fluidoterapia, corrección de las alteraciones hidroelectrolíticas,
vitamina K (se recomiendan ampollas de vitamina K: 10 mg iv/día). La insuficiencia
renal aguda puede requerir hemodiálisis. La aparición de fallo hepático implica un
manejo intensivo que puede incluir el trasplante hepático.
Aumentar la eliminación de las amatoxinas del tubo digestivo y del organismo: se
procede a la colocación de una sonda nasogástrica o nasoduodenal para aspiración
continua con administración repetida de carbón activado a 0,5 g/kg (máximo 50 g) cada
4 horas durante 72 horas (tiempo máximo de recirculación enterohepática de
amatoxina); si hay náuseas o vómitos, administrar ondansetrón (8 mg iv), evitando
otros antieméticos y espasmolíticos; diuresis forzada neutra (ver Apartado “Excreción
del tóxico”).
Antídotos (inhiben la circulación enterohepática de toxinas y/o desplazan la amanitina
de su unión a proteínas, permitiendo la eliminación renal): silibinina (Legalon SIL®) a
dosis de 20-50 mg/kg/día iv distribuida en cuatro infusiones de 2 horas de duración
durante 3-5 días; si no se dispone de silibinina, dar como segunda opción penicilina G
sódica 0,3-1 millón/kg/día (máximo 40 millones/día) en perfusión continua intravenosa
o distribuida en dosis cada 4 horas. Si se detecta afectación hepatocelular, algunos
autores proponen el uso de N-acetilcisteína (perfusión intravenosa secuencial: 150
mg/kg en 1 hora; después, 12,5 mg/kg/h durante 4 horas; posteriormente, 6,25
mg/kg/h durante 16 horas y suspender).
2.2. Síndrome orelaniano (orellánico, cortinarínico)
Producido por Cortinarius orellanus. La clínica se inicia tardíamente (no antes del tercer día) con
anorexia, náuseas, diarrea, dolor abdominal y síntomas neuromusculares como parestesias o mialgias.
Después de una media de 9 días, y según la susceptibilidad del individuo, este puede presentar nefritis
tubulointersticial, que en la mitad de los casos, y tras días o semanas del consumo de la toxina, puede
evolucionar a insuficiencia renal crónica. El tratamiento es sintomático y de mantenimiento, incluyendo las
técnicas de depuración extrarrenal.
2.3. Síndrome giromitriano
Producido por Gyromitra esculenta, y también por Morchella esculenta (colmenilla) si se consume
cruda. El cuadro clínico aparece a las 5-8 horas y se presenta como un síndrome gastrointestinal. Sin
embargo, lo más típico son los trastornos del sistema nervioso central (SNC), como cefalea, ataxia, vértigo,
nistagmo y disartria. En los casos leves cede tras 1-3 días mientras que en los graves puede aparecer
hepatitis, fallo hepático, convulsiones y coma. El tratamiento consiste en una descontaminación
gastrointestinal precoz con carbón activado y medidas de soporte según los síntomas. Si existen
convulsiones, además de benzodiazepinas, se debe administrar vitamina B6 (Benadon® ampollas 300 mg; 25
mg/kg/6 h iv en perfusión continua durante 15-30 minutos), ya que las convulsiones se producen por
bloqueo neuronal de la piridoxina.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1457]
[89] INTOXICACIONES
VIII. MORDEDURAS Y PICADURAS DE ANIMALES
1. Serpientes
Las especies de serpientes que habitan en la península ibérica son trece, y se dividen en víboras y
culebras; solo cinco de ellas son venenosas: a) Víboras: Vipera aspis (víbora áspid, la más peligrosa; habita
en zonas montañosas de los Pirineos, Montseny y cordillera cantábrica), V. latasti (en casi toda España,
excepto en el Norte) y V. seoaeni (Galicia y cornisa cantábrica); pueden inocular veneno con enzimas
proteolíticas, coagulantes y anticoagulantes. b) Culebras: Malpolon monsepessulanus (“culebra bastarda” o
de Montpellier; la de mayor tamaño y más agresiva; habita en toda la península ibérica) y Macroprotodon
cucullatus (“culebra de cogulla”, en Baleares y mitad sur de la Península), ambas poco venenosas.
Diagnóstico: de la mordedura (en caso de no observarse, no se puede descartar inoculación de
veneno mientras no haya ausencia de síntomas en una hora). Con fines pronósticos y
terapéuticos, las mordeduras se clasifican en cuatro grados:
Grado 0 (sin envenenamiento): ausencia de reacción local y general (marca de
colmillos, sin inoculación de veneno).
Grado I (envenenamiento leve): equimosis y edema local moderado sin síntomas
generales.
Grado II (envenenamiento moderado): reacción local intensa (equimosis,
tromboflebitis y denopatías) y manifestaciones generales leves (náuseas, vómitos o
diarrea).
Grado III (envenenamiento grave): reacción local intensa que supera la extremidad (en
este punto también se tienen en cuenta las mordeduras en la cara y el cuello) y
manifestaciones generales graves (coagulación intravascular diseminada [CID],
rabdomiólisis, fracaso renal agudo y alteraciones neurológicas).
Tratamiento: se procederá en todos los casos a inmovilización y liberación de la extremidad
(quitar anillos, pulseras, etc.), aplicación de frío local, desinfección, analgesia potente y
prevención antitetánica según el estado inmune y antibiótica (amoxicilina/ácido clavulánico).
Los casos locales graves y aquellos con manifestaciones sistémicas (grados II y III) requieren
ingreso y valorar el uso de suero antiofídico polivalente (Viper Fav®; puede provocar una
reacción inmunológica inmediata o tardía, por lo que su uso debe estar justificado). Si se
administra, se deben emplear corticoides en pauta descendente durante 3 semanas (iniciar con
1 mg/kg/día de metilprednisolona) y antihistamínicos por el riesgo de hipersensibilidad. Se
deberá mantener al paciente en observación al menos 6-12 horas en asintomáticos o 2 días en
sintomáticos para valorar la progresión, aunque las molestias pueden persistir durante varias
semanas.
2. Arañas
Las arañas de nuestro entorno son poco venenosas, salvo algunas excepciones. La Latrodectus
tredecimguttatus (viuda negra) posee una potente neurotoxina con efecto colinérgico, cuya picadura
provoca un leve edema local doloroso que raramente puede evolucionar a escara necrótica y adenopatías
regionales. En casos graves, aparecen síntomas sistémicos con contracturas musculares y signos
muscarínicos (ver Tabla I). Suele mejorar espontáneamente en menos de 7 días y el tratamiento consiste
en la desinfección local y medidas sintomáticas; en caso de contracturas o espasmos musculares se puede
utilizar diazepam, gluconato cálcico o metocarbamol. La picadura de tarántula produce un cuadro clínico
leve con edema, eritema, linfangitis y pequeña necrosis, sin repercusión sistémica. El tratamiento se basa
en la desinfección local y medidas sintomáticas.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1458]
[89] INTOXICACIONES
3. Otros animales venenosos
En general, las picaduras de otros animales, bien insectos (abejas y avispas, mosquitos, tábanos,
escalopendras), arácnidos (garrapatas, escorpiones) o animales acuáticos (medusas, peces venenosos),
originan una lesión en la zona de inoculación con inflamación local, con escasa repercusión sistémica (salvo
casos de shock anafiláctico, ver Capítulo 4. “Shock”). Requieren un manejo sintomático, habitualmente
mediante desinfección de la piel, antihistamínicos orales en caso de prurito y analgesia convencional para
el dolor. Como recomendación, se tendrán en cuenta los siguientes aspectos según el agente causal:
Abejas y avispas: alivio sintomático con calor local (la toxina es termolábil) y extracción del
aguijón de las abejas con pinzas.
Garrapata: eliminar la garrapata aplicando aceite o alcohol, agarrándola con unas pinzas lo más
cerca posible de la piel y aplicando una tracción constante en perpendicular a la superficie
cutánea (no retorcer ni dar tirones). Si quedasen restos, no retirar (se eliminarán solos). Se
valorará prevención con doxiciclina (200 mg vo, dosis única) en aquellos casos de riesgo de
zoonosis (borreliosis de Lyme, fiebre botonosa mediterránea), especialmente si ha habido
contacto con ciervos o perros de caza.
Escorpión: si el dolor es muy intenso está aprobado el uso de mepivacaína subcutánea local.
Medusas: limpieza de los restos con suero salino o agua marina, retirando los filamentos con
pinzas, rascado con el borde de una tarjeta o con celofán (evitar la aplicación de agua dulce).
Peces venenosos (pez araña, pez escorpión, cabracho): calor local (baño local a 50 °C durante
15-30 minutos), extracción del aguijón y revisar la inmunidad antitetánica.
IX. INSECTICIDAS
Los que más frecuentemente producen intoxicaciones son los organofosforados (paratión,
malatión, gas sarín) y los carbamatos, que se encuentran en los insecticidas habituales usados en
agricultura.
Son sustancias muy lipofílicas que se absorben bien por piel, mucosas y vía intestinal o respiratoria,
apareciendo los síntomas en las primeras 3-4 horas. Su mecanismo de acción se basa en la inhibición de la
acetilcolinesterasa (solo es reversible en el caso de los carbamatos), generando síndrome colinérgico (ver
Tabla I). Los casos más graves en los que predominan los signos nicotínicos y del SNC (ataxia, convulsiones,
fasciculaciones) suelen deberse a organofosforados, ya que los carbamatos atraviesan mal la barrera
hematoencefálica y suelen tener menor toxicidad. La parálisis muscular es lo que marca el pronóstico, ya
que puede producir parada respiratoria. Algunos autores han definido un síndrome intermedio que aparece
en un 8% de los intoxicados (generalmente los más graves) a los 2-3 días de la intoxicación y tras haber
superado la fase colinérgica. Se caracteriza por la afectación muscular respiratoria proximal de las
extremidades y flexores del cuello, que puede persistir varios días o semanas y acompañarse de
insuficiencia ventilatoria. También se han descrito manifestaciones tardías a las 2-3 semanas de la
exposición, como la neuropatía retardada de tipo periférico y trastornos neuropsiquiátricos, que pueden
tardar meses o años en revertir, en ocasiones de forma incompleta, y que no responden a la atropina ni a
las oximas.
Diagnóstico: se realiza indirectamente a través de la actividad de la colinesterasa plasmática o
intraeritrocitaria (esta se correlaciona mejor con la gravedad), que suelen estar disminuidas,
aunque sus niveles no se correlacionan bien con la gravedad clínica, siendo más importante
seguir la curva de colinesterasas.
Tratamiento: debe incluir:
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1459]
[89] INTOXICACIONES
Medidas de soporte y descontaminación: si se precisa intubación utilizar bloqueantes
neuromusculares no desponlarizantes como el rocuronio (nunca utilizar succinilcolina).
Es muy importante la retirada de la ropa y el lavado de la piel con agua jabonosa para
disminuir la absorción cutánea.
Disminuir la absorción: lavado gástrico y carbón activado a dosis altas (dosis de 50 g
repetidas durante las primeras 3 horas en las primeras 24 horas).
Antídotos:
Atropina a dosis altas (presentación en ampollas de 1 mg/ml): 2 mg iv seguidos
por bolos de 1 mg cada 3-5 minutos hasta que desaparezcan los signos
muscarínicos y/o aparezca atropinización (sequedad de boca y midriasis). De
ser preciso, puede continuarse en perfusión continua durante 24-48 horas (50
mg en 500 ml de suero salino a pasar entre 0,02 y 0,08 mg/kg/h). En el caso de
los carbamatos, dado que inhiben de forma reversible la colinesterasa, solo se
requiere atropina durante 12 horas.
Pralidoxima (reactivador de la colinesterasa): neutraliza los síntomas
nicotínicos y mejora la fuerza muscular, por lo que se usa como tratamiento de
las fasciculaciones y la debilidad. Debe administrarse conjuntamente con
atropina y de forma precoz (utilidad discutible después de 24 horas tras la
intoxicación). Está indicada principalmente en los organofosforados (en los
carbamatos, se regenera de forma rápida y espontánea). Dosis inicial de 15-30
mg/kg en 250 ml de suero salino 0,9% en 30 minutos, seguida de infusión
continua de 0,5 g/h, sin sobrepasar los 4 g/día. Debe mantenerse hasta 24
horas después de la desaparición de los síntomas.
X. RATICIDAS
Se clasifican en tres grupos: gaseosos (ácido cianhídrico y bromuro de metilo), minerales (arsénico y
talio) y orgánicos (anti-vitamina K). Una de las intoxicaciones más habituales y que cuenta con un
tratamiento específico es la intoxicación por los anti-vitamina K (rodentecidas warfarínicos y
superwarfarínicos), que se produce por su ingestión accidental o con fines suicidas. Inhiben la síntesis
hepática de los factores de coagulación dependientes de la vitamina K (II, VII, IX y X), por lo que su toxicidad
se manifiesta por hemorragias.
Se absorben con facilidad en el tubo digestivo en menos de 6 horas pero el paciente suele estar
asintomático o con mínima clínica digestiva en las primeras 48 horas, iniciando posteriormente una diátesis
hemorrágica en forma de petequias, equimosis, epistaxis, gingivorragias o hematuria, con riesgo de
hemorragias internas. Por ello, tras confirmarse la ingesta y que se trata de un anti-vitamina K (se intentará
identificar el producto a través de contactos o testigos), se deben establecer controles de tiempo de
protrombina cada 12-14 horas y dejar al paciente en observación durante 48-72 horas para vigilar los signos
de sangrado y/o anemia. El tratamiento se basa en la descontaminación digestiva con carbón activado y el
inicio de vitamina K. En caso de coagulopatía sin riesgo de sangrado, se acepta una dosis inicial de 10 mg de
vitamina K por vía oral con control del INR en las siguientes 24 horas. Si el tiempo de protrombina es
inferior al 10% y/o existe sangrado activo, se continuará con vitamina K intravenosa (preferiblemente
fitomenadiona, 10 mg/12 h) y transfusión de plasma fresco o complejo de protrombina (Octaplex®).
XI. HERBICIDAS
El Paraquat® y el Diquat® se utilizan para destruir la maleza y se desnaturalizan al contacto con la
tierra. Se absorben por la piel intacta y por vía digestiva (el 10% de la dosis ingerida) y se eliminan por vía
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1460]
[89] INTOXICACIONES
renal en 3 días. Los síntomas iniciales son digestivos (por efecto cáustico) y pueden mejorar de forma
espontánea en las primeras 24 horas, con desarrollo posterior de síntomas de la vía área superior (dolor
bucofaríngeo, tos irritativa, dificultad para la deglución con desarrollo de placas blanquecinas en la mucosa
orofaríngea) y a partir de las 72 horas, de necrosis hepatorrenal (ictericia y anuria) e insuficiencia
respiratoria con dificultad respiratoria, que origina el fallecimiento al cabo de 5-7 días. Los supervivientes
pueden quedar con secuelas pulmonares (fibrosis). El tratamiento incluye lavado gástrico con carbón
activado y diuresis forzada neutra (ver Apartado “Excreción del tóxico”) para eliminar el tóxico, siendo
ineficaz el uso de la hemodiálisis y la hemoperfusión por el elevado volumen de distribución. Ningún
fármaco ha demostrado su capacidad como antídoto aunque el uso de ciclofosfamida (1 g/día durante 2
días) en combinación con metilprednisolona (1 g/día durante 3 días) parecen aumentar la supervivencia y
disminuir la fibrosis pulmonar, por lo que es aconsejable su utilización en casos moderados y/o graves,
mientras no se disponga de otras alternativas.
XII. METALES
1. Plomo (saturnismo)
La intoxicación crónica por plomo es la enfermedad profesional por metales con repercusión
sistémica más frecuente en España. Puede ocurrir por exposición mantenida profesional, generalmente por
vía inhalatoria (por ejemplo, soldadores, chapistas, pintores, trabajadores de fábricas de plomo, artesanos
en contacto con esmaltes de cerámica y vidrio, recuperadores de baterías); y también por vía digestiva a
través del consumo de agua contaminada (canalizaciones antiguas de plomo) o de alimentos envasados en
latas de conserva.
Clínica: los síntomas dependen de la localización del depósito del metal: a nivel digestivo causa
los “cólicos saturninos” (asemeja a un abdomen agudo por el dolor y los vómitos, pero cursa sin
fiebre ni peritonismo), el ribete gingival o de Burton, disgeusia y anorexia; en el sistema
nervioso puede causar cefalea, síndrome confusional y neuropatía de predominio motor.
Diagnóstico: es necesario un alto índice de sospecha, ya que muchos síntomas son
inespecíficos (síndrome constitucional, anemia y dolores abdominales). Para una aproximación
inicial, serán datos sugestivos unos niveles de coproporfirina en orina > 300 mg/24 h y el
punteado basófilo de los hematíes. La presunción se corrobora con la concentración de plomo
en sangre (normal hasta 40 mg/dL), que es superior a 80 mg/dL en la mayoría de los casos; en
caso de duda, se puede realizar una prueba de descarga con edetato cálcico disódico (EDTA)
positiva si tras administrar 1 g de EDTA en 500 ml de SSF por vía intravenosa en 2 horas se
obtiene una plumbemia superior a 1.000 mg/24 h.
Tratamiento: en intoxicaciones con niveles moderadamente altos (40-60 mg/dL) estando el
paciente asintomático, es de elección la monoterapia con EDTA, que actúa como quelante del
plomo (1 g/12 h iv diluido en 500 ml de SSF al 0,9% a pasar en 6 horas durante 5 días). Si la
intoxicación cursa con niveles altos (60-80 mg/dL) y el paciente tiene síntomas, el tratamiento
recomendado es dimercaprol (4 mg/kg/4 h im) iniciando a partir de la segunda dosis
tratamiento combinado con EDTA (50 mg/kg/día), manteniendo ambos durante 2 a 7 días
según la respuesta clínica. En caso de encefalopatía, se utilizará el esquema previo con mayor
dosis de EDTA (75 mg/kg; máximo 3 g). En ambos casos debe monitorizarse la función renal y
conseguir una buena hidratación para evitar la lesión tubular inducida por liberación de plomo.
El cólico saturnino puede tratarse con infusión de gluconato cálcico.
2. Mercurio
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1461]
[89] INTOXICACIONES
Los casos más habituales descritos de exposición a altas dosis de mercurio se han producido por la
rotura accidental en la boca de termómetros de mercurio metálico (esta circunstancia es menos frecuente
en la actualidad, ya que no se utilizan estos dispositivos), por exposición profesional (por ejemplo,
inhalación de vapores de mercurio en los empastes dentales con amalgama de mercurio, de las lámparas
fluorescentes, mina de oro, sales mercuriales en la industria química) o por consumo de peces con altas
concentraciones de mercurio (pez espada, atún, tiburón, lubina), casi en su totalidad en forma de
metilmercurio (especialmente en países asiáticos). El mercurio metálico (termómetros) es prácticamente
inabsorbible por vía digestiva y no produce casi ningún síntoma digestivo, aunque se debe vigilar la
aparición de síntomas respiratorios a pesar de que la ingesta haya sido oral (puede absorberse por vía
respiratoria si se ha calentado). En estos casos no suele ser necesario realizar análisis de mercurio en sangre
u orina y no requiere tratamiento (solo dieta rica en residuos para favorecer la eliminación por heces). Por
vía inhalatoria puede producir neumonitis intersticial y edema pulmonar. La intoxicación crónica cursa con
gingivitis, cambio de carácter, temblor y alteración renal (síndrome nefrótico y tubulopatía). Para el
tratamiento en casos agudos graves con repercusión sistémica (frecuente en la intoxicación inhalatoria o
por ingesta de sales mercuriales) se administra dimercaprol en pauta descendente (5 mg/kg/4 h durante 2
días; 2,5 mg/kg/6 h durante 2 días; 2,5 mg/kg/12 h durante 7 días). También se puede usar D-penicilamina.
3. Arsénico
El medio habitual de contagio es por vía digestiva o inhalatoria, a través de raticidas o herbicidas,
en trabajadores del vidrio o con conservantes de madera, o a veces por ingestión de agua contaminada. En
la intoxicación aguda se producen síntomas locales (vómitos y diarrea si la ingesta ha sido oral), es
característico el aliento aliáceo (con olor a ajo), que en los casos más graves puede progresar a
hepatotoxicidad y arritmias cardiacas. En la intoxicación crónica es característica la dermatitis, la
polineuropatía sensitivo-motora, alteraciones hematológicas y digestivas. El tratamiento en casos agudos
se hace mediante la administración de dimercaprol (3 mg/kg/4 h durante 2 días, luego cada 6 horas un día
seguido de cada 12 horas una semana).
XIII. INTOXICACIONES POR SUSTANCIAS INDUSTRIALES Y DERIVADOS
1. Alcoholes y glicoles
Son causa de acidosis metabólica con anión gap elevado (valor normal: 10 ± 2). Además, si se
sospecha intoxicación por alcoholes, debe calcularse el osmol gap (OG = osmolaridad medida (por el
laboratorio) – osmolaridad calculada ([2 x Na+] + [Glucosa / 18] + [BUN / 2,8]), siendo sus valores normales
de 10 ± 6 mOsm/kg. Un OG elevado (desequilibrio osmolar) es un potencial indicador de ingesta de
alcoholes tóxicos. Tres alcoholes pueden originar intoxicaciones letales: etilenglicol, metanol y alcohol
isopropílico. Los tres generan un OG elevado pero solamente el metanol y el etilenglicol originan acidosis
con anión gap elevado.
1.1. Alcohol etílico o etanol
(Ver Capítulo 87. “Trastornos relacionados con el consumo de alcohol”).
1.2. Alcohol metílico (metanol o alcohol de quemar)
Se utiliza sobre todo como alcohol de quemar, anticongelante o disolvente. Es inodoro y volátil a
temperatura ambiente. Se absorbe por vía gastrointestinal, por la piel y por las vías respiratorias. Dosis
bajas (50-250 ml) fácilmente alcanzan niveles potencialmente letales (niveles > 1 g/l). Su ingestión causa
acidosis metabólica a través de la acción de sus metabolitos formaldehído y ácido fórmico, que derivan de
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1462]
[89] INTOXICACIONES
la acción de la enzima ADH (alcohol deshidrogenasa). Además, son dañinos para el nervio óptico y para el
SNC, siendo esta su principal toxicidad.
Clínica: aparece en las primeras 24 horas con cefalea, confusión, alteraciones visuales y dolor
abdominal. Uno de sus órganos diana es la retina (hiperemia del nervio óptico en el fondo de
ojo), hasta producir ceguera irreversible con midriasis arreactiva. Es frecuente la presencia de
hemorragia subaracnoidea y puede desembocar en coma y crisis comiciales. Analíticamente
hay alteración del perfil hepático y acidosis metabólica grave con anión gap y OG elevados (la
normalidad de este último no lo descarta).
Tratamiento: medidas de soporte, con especial atención a la corrección total de la acidosis con
bicarbonato. El objetivo es conseguir disminuir la producción de metabolitos tóxicos de
metanol por la ADH mediante su inhibición directa (fomepizol) o desviación de su génesis
mediante el uso de etanol (al tener 10 veces más de afinidad por la ADH). Habitualmente, el
tratamiento se basa en la administración de etanol en perfusión intravenosa si la metanolemia
es superior a 0,2 g/l o si existe sospecha y no hay niveles séricos disponibles (bolo de 1,1 ml/kg
de etanol en 250 ml de suero glucosado (SG) al 5% a pasar en 30 minutos, con perfusión
posterior de mantenimiento de 0,1 ml/kg/h en 100 ml de SG al 5% para mantener los niveles de
etanol entre 1 y 2 g/l; mejor usando una vía central debido a la tendencia a flebitis). La vía oral
se puede utilizar con las mismas diluciones. Otro antídoto disponible, de primera elección para
algunos autores por ser menos tóxico que la perfusión de etanol, es el fomepizol (bolo de carga
de 15 mg/kg, seguido de 4 dosis de 10 mg/kg/12 h iv; después dosis de 15 mg/kg/12 h iv hasta
llegar a concentraciones de metanol < 0,2 g/l), aunque su uso suele ser más restringido por la
menor disponibilidad y precio. La hemodiálisis está indicada con pH arterial < 7,2; desequilibro
osmolar > 20 mOsm/kg; metanolemia > 0,5 g/l; cuando existan trastornos visuales o
disminución del nivel de consciencia (todo ello hasta que la metanolemia sea < 0,1 g/l). Debe
administrarse además ácido folínico (50 mg/4 h iv) durante varios días para catabolizar el ácido
fórmico.
1.3. Etilenglicol
Se utiliza como anticongelante de vehículos y como disolvente. Solo se absorbe por vía digestiva, y
su ingestión causa acidosis metabólica con anión gap elevado debido a la producción de diversos ácidos
(glicólico y oxálico) que generan lesiones graves del SNC, corazón, pulmones y riñones. Es tóxico en dosis
tan bajas como 50-100 ml (niveles mayores de 0,5 g/l) y es potencialmente mortal con la ingestión de más
de 100 ml.
Clínica: en 12-24 horas aparece insuficiencia cardiaca por depresión miocárdica y dificultad
respiratoria, y en 48 horas fracaso renal oligúrico por necrosis tubular aguda, junto con
depresión progresiva del nivel de consciencia (embriaguez hasta la progresión a sedación y
coma). El diagnóstico se facilita por la observación de cristales de oxalato en la orina (que
explica en parte la insuficiencia renal), y es bastante habitual la presencia de hipocalcemia. Se
confirma el diagnóstico al detectar etilenglicol en sangre, y es importante emprender
inmediatamente el tratamiento y no esperar a la medición de las concentraciones de
etilenglicol.
Tratamiento: es superponible al referido para el metanol, con las mismas dosis farmacológicas
e indicaciones para la perfusión de etanol, fomepizol y hemodiálisis. Prestar atención a la
hipocalcemia. Deben añadirse además piridoxina (100 mg/6 h iv) y tiamina (100 mg/6 h iv)
durante 2 días.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1463]
[89] INTOXICACIONES
XIV. INTOXICACIÓN POR DISOLVENTES ORGÁNICOS Y SUS VAPORES
Habitualmente se trata de intoxicación por hidrocarburos lineales (gas metano, propano y
tetracloruro de carbono) o aromáticos (benceno y tolueno) que se encuentran en disolventes, barnices o
pegamentos, en el gas natural o industrial y en derivados del petróleo (gasolina o queroseno). La
intoxicación se adquiere habitualmente por vía inhalatoria y más raramente por vía digestiva (con fines
autolíticos o accidental) en el ámbito industrial, aunque pueden utilizarse como drogas de abuso
(inhalación de pegamento). Los síntomas suelen ser hiperreactividad del SNC con alucinaciones, seguido de
disminución variable del nivel de consciencia que puede llegar al coma, ataxia, arritmias e insuficiencia
hepática y renal grave con grado variable de neumonitis química. El tratamiento se basa en medidas
generales (no existen antídotos específicos) y se debe administrar oxígeno al 100% (en intoxicaciones por
vía inhalatoria). En los casos de consumo oral no se recomienda el uso de carbón activado. La
administración precoz de acetilcisteína intravenosa podría disminuir las complicaciones hepatorrenales en
el caso de intoxicación por tetracloruro de carbono (hidrocarburo halogenado), por lo que estaría indicado
en pacientes graves intoxicados por dicho compuesto.
BIBLIOGRAFÍA
Holstege CP, Borek HA. Toxidromes. Crit Care Clin. 2012;28:479-98.
Erickson TB, Thompson TM, Lu JJ. The approach to the patient with an unknown overdose. Emerg Med
Clin North Am. 2007;25:249-81.
Munné P, Arteaga J. Asistencia general al paciente intoxicado. Anales Sis San Navarra. 2003;26(Supl
1):21-48.
Teijera R. Aspectos legales de la atención toxicológica. Anales Sis San Navarra. 2003;26(Supl 1) 275-
80.
Persson HE, Sjöberg GK, Haines JA, Pronczuk de Garbino J. Poisoning severity score: Grading of acute
poisoning. J Toxicol Clin Toxicol. 1998;36(3):205-13.
Osés I, Burillo-Putze G, Nogué S, Pinillos MA. Intoxicaciones medicamentosas (I). Psicofármacos y
antiarrítmicos. Anales Sis San Navarra. 2003;26(Supl 1):49-63.
Munné P, Sáenz Bañuelos JJ, Izura JJ, Burillo-Putze G, Nogué S. Intoxicaciones medicamentosas (II).
Analgésicos y anticonvulsivantes. Anales Sis San Navarra. 2003;26(Supl 1):65-97.
Jang DH, Spyres MB, Fox L, Manini AF. Toxin-induced cardiovascular failure. Emerg Med Clin North Am.
2014;32(1):79-102.
Wiener SW. Toxicologic acid-base disorders. Emerg Med Clin North Am. 2014;32(1):149-65.
López AM, Hendrickson RG. Toxin-induced hepatic injury. Emerg Med Clin North Am. 2014;32(1):103-
25.
McKay Jr CA. Toxin-induced respiratory distress. Emerg Med Clin North Am. 2014;32(1):127-47.
Ruha AM, Levine M. Central nervous system toxicity. Emerg Med Clin North Am. 2014;32(1):205-21.
Hampson NB, Piantadosi A, Thom SR, Weaver LK. Practice recommendations in the diagnosis,
management, and prevention of carbon monoxide poisoning. Am J Respir Crit Care Med.
2012;18(186):1095-101.
Benítez-Macías JF, García-Gil D, Brun-Romero FM, Nogué-Xarau S. Actualización clínica: Intoxicaciones
agudas por setas. Rev Clin Esp. 2009;209(11):542-9.
Nogué S, Dueñas A, Marruecos L, Nolla J. Sección XVIII: Toxicología. En: Farreras/Rozman. Medicina
Interna. 17ª ed. Barcelona: Elsevier; 2012. p. 2381-413.
Matamala B, Monsalvo R, Valenzuela JC, Arévalo J, Rodríguez-García JL. Intoxicaciones agudas. En:
DTM: Diagnóstico y Tratamiento Médico. 2ª ed. Madrid: Marban; 2011. p. 1901-9.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1464]
[90] ANEXO I. VALORES DE REFERENCIA DE LABORATORIO
90.Anexo I. Valores de referencia de laboratorio
Mauricio César Escobar Porcel
Servicio de Bioquímica Clínica
Daniel Párraga García
Servicio de Bioquímica Clínica
Asesora: Rosa Cornejo González
Servicio de Análisis Clínicos
I. INTRODUCCIÓN
En las tablas siguientes (Tablas I-XII) se presentan los valores de referencia de los parámetros
bioquímicos que se determinan en el Hospital Universitario 12 de Octubre. Dichos valores dependen de la
población y del método empleado, por lo que son susceptibles de cambiar si lo hace el instrumental del
laboratorio. La mayoría de las determinaciones en sangre se realizan en suero, aunque hay casos en los que
se utiliza plasma (muestras recogidas en tubos con ácido etilendiaminotetraacético [EDTA], fluoruro o
heparina de litio en el caso de determinaciones de urgencia).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1465]
[90] ANEXO I. VALORES DE REFERENCIA DE LABORATORIO
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1466]
[90] ANEXO I. VALORES DE REFERENCIA DE LABORATORIO
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1467]
[90] ANEXO I. VALORES DE REFERENCIA DE LABORATORIO
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1468]
[90] ANEXO I. VALORES DE REFERENCIA DE LABORATORIO
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1469]
[90] ANEXO I. VALORES DE REFERENCIA DE LABORATORIO
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1470]
[90] ANEXO I. VALORES DE REFERENCIA DE LABORATORIO
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1471]
[90] ANEXO I. VALORES DE REFERENCIA DE LABORATORIO
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1472]
[90] ANEXO I. VALORES DE REFERENCIA DE LABORATORIO
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1473]
[90] ANEXO I. VALORES DE REFERENCIA DE LABORATORIO
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1474]
[90] ANEXO I. VALORES DE REFERENCIA DE LABORATORIO
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1475]
[90] ANEXO I. VALORES DE REFERENCIA DE LABORATORIO
II. INFORMACIÓN AL PACIENTE PARA LA RECOGIDA DE MUESTRAS
Para un buen resultado es imprescindible el exacto cumplimiento de todas las normas.
1. Orina
1.1. Primera orina de la mañana
Se le facilitará un sistema para la recogida de orina en la consulta peticionaria. No utilizar ningún
otro recipiente para recogerla. Al levantarse y, antes de orinar, lavar los genitales con agua abundante sin
jabón y secar con una toalla limpia. Para evitar que la orina toque la piel si es un hombre retirar la piel del
pene hacia atrás; si es una mujer, separar con la mano los labios de los genitales. Recoger solo orina
intermedia, eliminando la primera y la última parte siempre que el médico no indique lo contrario. Recoger
la orina directamente en el recipiente que facilita la consulta peticionaria. Procurar no tocar con la mano el
interior del vaso. Llenar los tubos con la orina del vaso y después tirar la cantidad sobrante y el vaso. Cerrar
los tubos y llevarlos el mismo día a la recogida de muestras. Las mujeres han de procurar no hacerse el
análisis durante la menstruación, ni los 3 o 4 días antes o después de tenerla. Si se toma cualquier
medicación es muy importante decir cuál es. En los niños pequeños debe extremarse la limpieza de los
genitales y la zona perianal. Colocar la bolsa correctamente y vigilar cada 30 minutos la emisión de orina.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1476]
[90] ANEXO I. VALORES DE REFERENCIA DE LABORATORIO
No mantener la bolsa instalada más de una hora. Tan pronto como se haya obtenido la muestra retirar la
bolsa y guardarla en la nevera hasta su envío a la recogida de muestras.
1.2. Orina de 24 horas
Al levantarse el día anterior al de la entrega de la orina, orine directamente en el inodoro y, a partir
de ese momento, recoja en uno o varios frascos de plástico de 2 litros (comprados previamente en la
farmacia) toda la orina que haga, incluida la primera del día siguiente. La orina se guardará en el frigorífico.
Si durante este periodo tuviera que hacer deposición, intentar orinar antes en el recipiente para evitar
pérdidas. Hay que tener presente que esta prueba solo es válida si se recoge correctamente toda la orina.
Mezclar bien toda la orina de 24 horas, medir el volumen exacto y anotarlo en el volante de petición.
Trasvasar parte de esta orina a los tubos que previamente le habrán entregado en la consulta peticionaria.
Cerrar bien los tubos y entregarlos en la recogida de muestras.
1.3. Catecolaminas, ácido vanilmandélico y ácido indolacético
Tres días antes de la recogida de la orina, y durante la recolección de la misma, deben eliminarse
de la alimentación los siguientes productos: verduras, hortalizas, frutos cítricos, plátanos, piña, frutos
secos, chocolate, té, café y todos aquellos productos en cuya composición pueda figurar la vainilla, como
pueden ser galletas, helados, flanes o pasteles. Asimismo, se suprimirá la medicación o, en el caso de no ser
posible, se informará de la misma en el volante de petición.
Para la recogida de la orina el paciente orinará a las ocho de la mañana tirando esa muestra. A
partir de este momento y hasta las ocho de la mañana del día siguiente recogerá toda la orina. En la
recogida de muestras se le suministrará un frasco que contiene un ácido, por lo que se recomienda no
orinar directamente. Se recogerá la orina en otro envase y se traspasará al contenedor suministrado. La
orina debe guardarse en un sitio fresco durante la recogida.
1.4. Oxálico
Dos días antes de la recogida de la orina y durante la recolección de la misma deben eliminarse de
la alimentación la vitamina C y los alimentos que la contengan. El método de recogida es igual que el
descrito para la determinación de catecolaminas (ver arriba).
1.5. Porfirinas
Antes de comenzar la recogida de orina de 24 horas se deberá echar en el envase en el que se va a
recoger el contenido de la bolsa adjunta para su correcta conservación. Hay que proteger el envase de la
luz, bien sea con papel de aluminio o con una bolsa negra y mantenerlo en un lugar fresco durante la
recogida. El paciente orinará a las ocho de la mañana tirando esa muestra. A partir de este momento y
hasta las ocho de la mañana siguiente recogerá toda la orina en dicho envase.
1.6. Xilosa
El enfermo debe estar en ayunas. Se administra la mitad de su peso (kg) en gramos de xilosa
disuelta en un vaso de agua (por ejemplo: si pesa 56 kg se le darían 28 g de xilosa). En niños por debajo de
15 kg se dan 5 g de xilosa. Para la obtención de la muestra se debe proceder según se explica a
continuación:
Adultos: se extrae plasma en un tubo malva (EDTA) a los 60 minutos y otro a los 120 minutos
tras la ingestión de xilosa. A los 120 minutos se llevan los tubos a la recogida de muestras. Se
recoge toda la orina de 5 horas desde la ingesta de xilosa.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1477]
[90] ANEXO I. VALORES DE REFERENCIA DE LABORATORIO
Niños: se extrae plasma en un tubo malva (EDTA) a los 60 minutos tras la ingesta de xilosa. No
se recoge orina.
2. Heces
2.1. Sangre oculta en heces
La determinación se realizará en una o tres muestras de días diferentes, según indicación clínica en
el volante de petición. El paciente recogerá uno o tres tubos de buffer en la recogida de muestras junto con
las instrucciones sobre su recogida. Una vez recogidas las muestras se entregarán los tubos, junto con el
volante, en la recogida de muestras.
2.2. Grasa en heces
Pedir en la recogida de muestras un recipiente previamente pesado. Seguir una dieta grasa durante
6 días que consistirá en añadir a la alimentación normal 50 g de mantequilla. En los 3 últimos días de la
dieta recoger en el recipiente pesado las heces completas de esos 3 días. Mantener las heces en nevera
durante su recogida, hasta que se entreguen en la recogida de muestras.
3. Semen
3.1. Control posvasectomía
Deberá tener un periodo de abstención sexual entre 3 y 5 días. El primer control se deberá realizar
a los 4 meses tras la intervención quirúrgica y después de haber tenido, al menos, 24 eyaculaciones.
Recoger toda la muestra directamente sin preservativo y mediante masturbación sobre el envase indicado
por el médico peticionario (envase estéril de boca ancha). La muestra se deberá transportar manteniendo
el envase envuelto y protegiéndola de los cambios de temperatura (mantenerla a temperatura ambiente y
en invierno transportar debajo del abrigo o en el bolsillo). Se entregará el recipiente en la consulta de
seminogramas. No deberá transcurrir más de una hora entre la recogida y la entrega de la muestra. Si prevé
un tiempo mayor de transporte, la recogida se deberá realizar en el hospital en el lugar indicado por el
personal de recogida de muestras. En este caso deberá llegar media hora antes de la cita. El envase deberá
estar bien cerrado y etiquetado con nombre y apellidos. En el caso de que se realicen controles posteriores
deberá cumplir las mismas condiciones.
3.2. Estudios seminales por causa distinta a vasectomía
Deberá tener un periodo de abstención sexual entre 3 y 5 días. Deberá comunicar cualquier
intervención quirúrgica, tratamiento o enfermedad reciente. Se seguirán las mismas indicaciones que para
el control posvasectomía.
BIBLIOGRAFÍA
Gary L, Howovitz MD. Tietz textbook of clinical chemistry and molecular diagnostics. 5th ed. Chapter 5.
Establisment and use of reference values. Elsevier; 2012. pp. 95-118.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1478]
[91] ANEXO II. MONITORIZACIÓN DE FÁRMACOS
91.Anexo II. Monitorización de fármacos
Isabel Gómez Valbuena.
Farmacia
Alba Fernández del Pozo.
Bioquímica Clínica
Asesor: Aitor Delmiro Magdalena.
Médico Adjunto de Bioquímica Clínica
La monitorización estará justificada en las siguientes circunstancias:
Fármacos cuyo margen terapéutico es estrecho, es decir, cuando el nivel que produce la
respuesta eficaz se encuentra cercano al que produce toxicidad.
Fármacos para los que existe una gran variabilidad intra e interindividual. La administración de
la misma dosis resultará ineficaz para algunos pacientes, mientras que producirá efectos
tóxicos en otros. Esta variabilidad en la respuesta depende principalmente de factores
farmacocinéticos que alteran los procesos de absorción, distribución y eliminación y, por tanto,
la relación entre la dosis que se administra y el nivel que se alcanza. El fármaco no unido a
proteínas o eritrocitos (libre) es el disponible para la distribución y eliminación, por lo que los
cambios en estas uniones tendrán una gran influencia en estos procesos y se deberán tener en
cuenta para una valoración correcta de los niveles. Depende también de factores
farmacodinámicos, que alteran la sensibilidad del organismo al fármaco y, por tanto, la relación
entre los niveles plasmáticos y los efectos.
En general, monitorizaremos los niveles de un fármaco cuando exista falta de respuesta con dosis
adecuadas, sospecha de toxicidad, para vigilar el cumplimiento terapéutico y para controlar cambios
fisiológicos (patrón genético, edad, hábitos dietéticos, ingesta de alcohol o hábito de fumar; las diferencias
son particularmente importantes entre el niño, el adulto, el anciano y en el embarazo), patológicos
(alteraciones en la función renal, hepática o cardiaca), o yatrogénicos (interacciones entre fármacos
administrados simultáneamente), que puedan afectar a los niveles de los fármacos.
La monitorización también resulta útil en aquellos casos en los que la eficacia o toxicidad son
difíciles de valorar clínicamente. Esto ocurre en los fármacos que se utilizan con fines profilácticos
(prevención de crisis comiciales con antiepilépticos, prevención del rechazo de un trasplante). También se
monitorizan fármacos cuando la valoración clínica es compleja (depresión), o los efectos tóxicos son muy
inespecíficos o difíciles de medir (náuseas y vómitos o arritmias con digoxina).
Para llevar a cabo la monitorización de niveles de fármacos es preciso que esté definido su
intervalo terapéutico óptimo, es decir, aquel en el que la mayor parte de los pacientes van a presentar una
buena respuesta sin toxicidad, y que está comprendido entre la concentración efectiva mínima y la
concentración tóxica mínima. Este intervalo óptimo es el que se utiliza como punto de referencia para
ajustar la dosis cuando no se dispone de criterios clínicos, o antes de disponer de ellos. Se debe interpretar
con flexibilidad, ya que cada paciente va a requerir un nivel diana, en función de sus características
individuales. A diferencia del intervalo óptimo, que es poblacional, el nivel diana es específico para cada
paciente e incluso para cada situación.
El término nivel se utiliza en monitorización de fármacos para referirse no a cualquier
concentración, sino a la concentración de muestras extraídas en las condiciones concretas en las que se
estableció el intervalo óptimo, que suele ser en estado de equilibrio (cuando han trascurrido entre cinco y
siete semividas de eliminación del fármaco; en este estado la concentración corporal del fármaco está en
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1479]
[91] ANEXO II. MONITORIZACIÓN DE FÁRMACOS
equilibrio con la dosis del fármaco administrada y la eliminación del mismo) y en unas condiciones
adecuadas de extracción de la muestra, según sea el objeto de la monitorización. En un ciclo de dosificación
óptimo la concentración sanguínea valle es la más baja conseguida justo antes de la siguiente dosis, y esta
no debería ser más baja de la concentración efectiva mínima. La concentración pico es la más alta
conseguida dentro del ciclo de dosificación, y no debería ser mayor de la concentración tóxica mínima.
Para realizar la medición de niveles es preciso conocer los siguientes datos:
Tiempo que lleva el paciente tomando la misma dosis.
Fármacos coadministrados y situación clínica.
Fecha y hora de administración de la última dosis.
Fecha y hora de extracción de la muestra.
En la tabla I se detallan las características farmacocinéticas y los rangos terapéuticos y tóxicos de
los fármacos que se determinan en la unidad de monitorización de fármacos del servicio de bioquímica, así
como en el servicio de inmunología de nuestro hospital.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1480]
[91] ANEXO II. MONITORIZACIÓN DE FÁRMACOS
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1481]
[91] ANEXO II. MONITORIZACIÓN DE FÁRMACOS
BIBLIOGRAFÍA
Hammett-Stabler CA, Dasgupta A. Therapeutics Drug Monitoring Data. A Concise Guide. Washington,
DC: AACC PRESS (American Association for Clinical Chemistry); 2007.
Hiemke C, Baumann P, Bergemann N, et al. AGNP Consensus Guidelines for Therapeutic Drug
Monitoring in Psychatry: Update 2011. Pharmacopsychiatry. 2011;44:195-235.
Schulz M, Iwersen-Bergmann S, Andresen H, Schmoldt A. Therapeutic and toxic blood concentrations of
nearly 1,000 drugs and other xenobiotics. Critical Care. 2012;16(4):R136-R136.
Van Hal SJ, Paterson DL, Lodise TP. Systematic review and meta-analysis of vancomycin-induced
nephrotoxicity associated with dosing schedules that maintain troughs between 15 and 20 milligrams
per liter. Antimicrob Agents Chemother. 2013;57(2):734-44.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1482]
[92] ANEXO III. FÁRMACOS Y EMBARAZO
92.Anexo III. Fármacos y embarazo
Siria Pablos Bravo.
Farmacia
Raquel Moreno Vidal.
Ginecología y obstetricia
El embarazo supone una etapa diferente en cuanto al tratamiento farmacológico. Los cambios
fisiológicos y farmacocinéticos producidos en la gestante, junto con la actuación de la barrera placentaria,
hacen que el uso de fármacos durante el embarazo confiera una situación especial de uso de estos. Para
ello, es fundamental conocer las categorías de uso según la FDA durante la gestación:
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1483]
[92] ANEXO III. FÁRMACOS Y EMBARAZO
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1484]
[92] ANEXO III. FÁRMACOS Y EMBARAZO
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1485]
[92] ANEXO III. FÁRMACOS Y EMBARAZO
(1) Paracetamol: recientes estudios indican que puede haber riesgo fetal con un uso prolongado en
la madre o en casos en los que existe variabilidad genética. Evitar su uso frecuente durante la gestación.
(2) Antiinflamatorios no esteroideos (AINE): riesgo en el primer y tercer trimestre. En fechas
próximas al parto puede provocar el cierre del ducto arterioso (categoría D). Inhiben el trabajo del parto y
pueden prolongar la gestación.
(3) Ácido acetilsalicílico: a dosis bajas es compatible con el embarazo; a dosis analgésicas es de
categoría D si se utiliza en el tercer trimestre (como el resto de AINE).
(4) Analgésicos opioides: categoría D administrado en periodos prolongados y a altas dosis a
término.
(5) Penicilinas: riesgo bajo durante todo el embarazo, excepto con ampicilina y amoxicilina, que su
exposición en primer y tercer trimestre pueden provocar fisuras orales.
(6) Eritromicina: el uso de su sal de estolato ha mostrado hepatotoxicidad en embarazadas.
(7) Metronidazol: según estudios publicados, a dosis antiinfecciosas no parece constituir un riesgo
significativo de
malformaciones del feto. Sin embargo, el fabricante lo contraindica en el primer trimestre.
(8) Fluconazol: parece ser teratógeno durante el primer trimestre a dosis diarias de 400 mg/24 h o
mayores. La experiencia a dosis más pequeñas sugiere que el riesgo de efectos adversos es bajo.
(9) Fluoroquinolonas: durante años han sido contraindicadas debido al posible daño en el cartílago
fetal. Actualmente determinados autores afirman que no hay relación directa entre su uso y este daño.
(10) Anticomiciales: las gestantes epilépticas deben saber que existe riesgo si se suspende el
tratamiento. Se deben administrar a la dosis mínima posible e informar del riesgo de malformaciones. Se ha
recomendado la administración de suplementos de ácido fólico al inicio del embarazo.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1486]
[92] ANEXO III. FÁRMACOS Y EMBARAZO
(11) Inhibidores selectivos de la recaptación de serotonina (ISRS) y venlafaxina: riesgo durante el
tercer trimestre (riesgo D en la segunda mitad del embarazo).
(12) Se recomienda el uso de insulina para la diabetes tipo 1 y 2 durante el embarazo y para la
diabetes gestacional si el tratamiento dietético no tiene éxito.
(13) Antipsicóticos atípicos: se recomienda 4 mg/día de ácido fólico, ya que se puede tener mayor
riesgo de defectos del tubo neural debido a una ingesta inadecuada de folatos y obesidad.
(14) Clorpromazina: uso ocasional y en dosis bajas es seguro. No obstante, el uso próximo al parto
debería evitarse debido al riesgo de hipotensión materna y efectos adversos en el recién nacido.
(15) Diuréticos: usar solo en casos graves. Riesgo D (excepto acetazolamida) si se utiliza para la
hipertensión gestacional debido a la hipovolemia materna característica de esta enfermedad.
(16) β-bloqueantes: riesgo durante el segundo y tercer trimestre. Se deben suspender de dos a tres
días antes del parto, si es posible, para evitar el riesgo de bradicardia, hipotensión y depresión respiratoria
fetal.
(17) Inhibidores de la enzima de conversión de la angiotensina (IECA) y antagonistas de los
receptores de la angiotensina ii (ARA-II): riesgo durante el segundo y tercer trimestre. Se deben utilizar a la
menor dosis posible y vigilar de forma minuciosa los niveles de líquido amniótico y el bienestar fetal.
(18) Las embarazadas asmáticas deben tratarse correctamente. El asma descontrolado es más
peligroso para la madre y el feto que los efectos secundarios que pudieran derivar del uso adecuado de la
medicación.
(19) Budesonida: parenteral parece ser teratógena en animales. En humanos no parece que la
forma inhalada represente un riesgo significativo de defectos congénitos (inhalada riesgo B; oral riesgo C).
(20) Colestiramina y colestipol: el uso prolongado puede causar una reducción de la absorción
intestinal de vitaminas liposolubles (A, D, E y K). El tratamiento hipocolesterolemiante se podría suspender
durante la gestación, ya que esto no debería tener efectos en el tratamiento a largo plazo de la
hiperlipidemias.
(21) Glucocorticoides: a dosis bajas son relativamente seguros para el feto. Se consideran categoría
D si se utilizan durante el primer trimestre. Los más seguros son la prednisona y la prednisolona.
(22) Benzodiazepinas: uso prolongado durante la gestación puede producir dependencia en el
neonato.
(23) Sulfasalazina: riesgo D si se administra al final de la gestación.
BIBLIOGRAFÍA
Bengoa Gorosabel MA, Onis Gonzalez E, Alfayate Miguélez S. Vacunas y embarazo. 2015. Disponible
en: https://www.aepap.org/sites/default/files/vacunacion_en_el_embarazo_def.pdf
Briggs GG, Freeman RK, Yaffe SJ. Drugs in pregnancy and lactation: A reference guide to fetal and
neonatal risk. 9th ed. Lippincott Williams & Wilkins; 2011.
Orueta Sánchez R, López Gil MJ. Manejo de fármacos durante el embarazo. 2011. Disponible en:
http://www.msssi.gob.es/biblioPublic/publicaciones/recursos_propios/infMedic/docs/EmbarazoVol35
n4.pdf
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1487]
[93] ANEXO IV. FÁRMACOS USADOS EN PERFUSIÓN CONTINUA INTRAVENOSA
93.Anexo IV. Fármacos usados en perfusión continua
intravenosa
Andrea Lázaro Cebas.
Residente Farmacia Hospitalaria
Asesora: Carmen García Muñoz.
Farmacéutica Adjunta Farmacia Hospitalaria
En la tabla I se exponen las perfusiones más frecuentemente usadas en perfusión continua en la
práctica clínica.
Dobutamina: puede ser necesario utilizar diluciones más concentradas (máximo 5 mg/ml). Aunque
teóricamente no tiene techo, la dosis máxima recomendada es de 20 μg/kg/min, y de forma excepcional
hasta 40 μg/kg/min. Incompatible con el bicarbonato sódico y otras soluciones alcalinas (como furosemida
o fenitoína sódica).
Dopamina: aumentar la dosis a razón de 1-4 μg/kg/min cada 10-30 min hasta obtener los efectos
terapéuticos deseados. La dosis máxima recomendada es de 20 μg/kg/min, pudiéndose administrar dosis
de 50 μg/kg/min o superiores en situaciones graves, comprobando frecuentemente la respuesta presora y
la diuresis. Es incompatible con bicarbonato sódico y con otras soluciones alcalinas. En caso de sobredosis
hay que detener la infusión. Hay que emplear la vía venosa central, ya que es irritante y para evitar
extravasaciones.
Isoproterenol (isoprenalina): puede producir reacciones alérgicas graves y broncoespasmo, ya que
contiene como excipiente metabisulfito de sodio (E-223). Como antídoto pueden emplearse β-bloqueantes.
Noradrenalina: 8 mg de L-norepinefrina bitartrato (presentación comercial) equivalen a 4 mg de L-
norepinefrina base. En el caso del shock séptico se deben ajustar las dosis alrededor de 0,5 μg/kg/min
(hasta un máximo de 1 μg/kg/min). No se debe suspender bruscamente la perfusión. La extravasación
puede causar necrosis y/o gangrena por vasoconstricción local.
Labetalol: betabloqueante muy útil en las crisis hipertensivas (embarazo, postinfarto agudo de
miocardio [IAM], feocromocitoma). Puede producir hipotensión, bloqueo cardiaco e insuficiencia cardiaca
congestiva. Suele producir hipotensión ortostática hasta varias horas después de suspender la perfusión. Su
uso está recomendado bajo monitorización electrocardiográfica. Se puede emplear sin diluir en bolos
lentos de hasta 50 mg (1/2 amp = 10 ml) repetibles cada 5 min (máximo de 200 mg). Si aparece bradicardia
grave se usará atropina.
Nitroglicerina: iniciar a 10 μg/min y aumentar de 10 en 10 μg cada 2-3 min hasta conseguir la
respuesta esperada. La dosis máxima es de 400 μg/min (en ocasiones superior). Monitorizar la tensión
arterial (TA). Puede aparecer tolerancia a su efecto a las 24-48 h de su administración continuada. Se
adhiere a los envases y sistemas de cloruro de polivinilo, por lo que es preciso utilizar polietileno o vidrio
(Viaflo®).
Nitroprusiato: en general la dosis de 3 μg/kg/min implica reducción de la TA diastólica del 30-40%
respecto al valor previo al tratamiento. Monitorizar la TA; no administrar más de 24 h (transformación en
tiocianato). Si fuera imprescindible continuar la infusión puede ser útil administrar vitamina B12 para evitar
que el cianuro formado pase a los tejidos.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1488]
[93] ANEXO IV. FÁRMACOS USADOS EN PERFUSIÓN CONTINUA INTRAVENOSA
Urapidilo: se pueden administrar bolos de 25 mg en 20 seg repetidos cada 5 min (máximo 3 bolos
pudiendo ser el 3.º de 50 mg). Es incompatible con el bicarbonato sódico y otras soluciones alcalinas.
Nimodipino: si no es posible coinfusión con suero fisiológico/suero glucosado (SF/SG) administrar
de manera directa por vía central. La infusión debe iniciarse como máximo 4 días después de la hemorragia.
No hay que emplear equipos de infusión que contengan PVC.
Flecainida: Recomendado su uso bajo monitorización electrocardiográfica durante administración.
Para suspender disminuir la infusión 20%/h y suspender a la 4.ª hora. La dosis máxima acumulativa las
primeras 24 h es de 600 mg. En pacientes con insuficiencia renal reducir dosis a la mitad.
Amiodarona: se comienza con una dosis inicial de 5 mg/kg (aproximadamente 300 mg) que puede
repetirse de dos a tres veces en 24 h. Dosis máxima: 1.200 mg/24 h. Es incompatible con equipo médico o
productos sanitarios que contengan material plástico de tipo di-2-etilhexil ftalato.
Verapamilo: habitualmente se administra en bolo, de 5-10 mg (0,075-0,15 mg/kg) a pasar en 5 min,
pudiéndose repetir a los 30 min. Es aconsejable la monitorización electrocardiográfica y es incompatible
con soluciones alcalinas.
Diazepam: se recomienda administrar intravenoso (IV) en bolo o intramuscular (IM). No infundir a
más de 5 mg/min ni administrar a pacientes con hipoventilación grave (pCO2 > 50). No sobrepasar los 3
mg/kg/d. Considerar el uso de flumazenilo si hay depresión importante del sistema nervioso central (no
recomendado en pacientes con estatus epiléptico por riesgo de aparición de convulsiones bruscas).
Ácido valproico: si existe tratamiento previo por vía oral emplear la misma dosis administrada, a
razón de 0,5-1 mg/kg/h. Pacientes > 65 años: 15-20 mg/kg.
Morfina: la posología es muy variable, debiéndose individualizar en función de la clínica y el uso
previo de opioides.
Remifentanilo: la dosis de mantenimiento varía entre 0,05 y 2 μg/kg/min en función de anestésicos
empleados junto con remifentanilo. El efecto del remifentanilo desaparece a los 5-10 min de finalizada la
administración. Deben monitorizarse las funciones respiratoria y cardiaca. Es compatible con ringer lactato
y propofol.
Midazolam: con una sedación prolongada puede aparecer tolerancia. Se recomienda monitorizar la
función respiratoria y cardiaca. Es incompatible con el bicarbonato sódico y otras soluciones alcalinas.
Propofol: en inducción de anestesia administrar bolos de 20-40 mg cada 10 seg (1,5-2,5 mg/kg)
hasta que aparezcan signos de inducción de anestesia. La solución contiene un 10% de lípidos, por lo que
debe ser desechada junto con la línea de administración a las 12 h de haber sido preparada. Usar bolsas de
PVC o frascos de vidrio.
Clonidina: se irá modificando según las necesidades y los parámetros hemodinámicos (frecuencia
cardiaca y TA media). Se debe tener la precaución de no retirar bruscamente por el riesgo de desarrollar
crisis hipertensiva de rebote.
Dexmedetomidina: la dosis máxima es de 1,4 μg/kg/h. Se emplea solo en la unidad de cuidados
intensivos por personal entrenado. Se puede combinar con propofol o midazolam hasta que se alcancen
niveles clínicos de dexmedetomidina.
Rocuronio: en intubación traqueal; IV en bolo: 0,6 mg/kg, mantenimiento: 0,15 mg/kg o 0,075-1
mg/kg si hay anestésicos volátiles. Se recomienda monitorizar de manera continua el bloqueo
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1489]
[93] ANEXO IV. FÁRMACOS USADOS EN PERFUSIÓN CONTINUA INTRAVENOSA
neuromuscular. En reversión o sobredosificación puede administrarse sugammadex o inhibidores de la
acetilcolinesterasa (edrofonio, neostigmina…).
Cisatracurio: en intubación traqueal: IV; en bolo: 0,15 mg/kg; mantenimiento: 0,03 mg/kg. Se
recomienda monitorizar de manera continua el bloqueo neuromuscular. En reversión o sobredosificación
pueden administrarse inhibidores de la acetilcolinesterasa (edrofonio, neostigmina, etc.). Incompatible con
soluciones alcalinas.
Flumazenilo: posee una vida media más corta que la mayoría de las benzodiazepinas, por lo que se
aconseja poner perfusión tras la dosis de carga (bolo 0,2 mg IV, pudiendo repetir bolos de 0,1 mg cada 60
seg hasta 1 mg). La supresión brusca del efecto de las benzodiazepinas puede dar lugar a convulsiones en
los pacientes epilépticos.
Naloxona: en principio se administra IV en bolos de 0,4 a 2 mg (1-5 ampollas), vía IM o subcutánea
si la vía IV es imposible. Si no revierte la intoxicación por opioides se procede a la perfusión. Tiene una corta
vida media de eliminación. Puede provocar un síndrome de abstinencia. Una dosis igual a la mitad del bolo
administrado al inicio debe administrarse 15 min tras el inicio de la perfusión para evitar una caída de los
niveles de naloxona.
N-acetilcisteína: se recomienda iniciar dentro de las primeras 8 h tras la ingestión de paracetamol.
Diluir en SG al 5%, pero si este estuviera contraindicado puede diluirse de manera excepcional en SF.
Furosemida: puede emplearse en casos de ICC severa o edema asociado a insuficiencia renal
crónica. La dosis máxima recomendada es de 80-160 mg/h.
Heparina sódica: antes de la perfusión hay que administrar un bolo inicial de 5.000 UI y titular
según el tiempo de cefalina (tiempo de tromboplastina parcial activada). Antídoto: sulfato de protamina.
Somatostatina: en hemorragia por varices emplear un bolo inicial de 250 μg. En fístulas
pancreáticas emplear dosis de 1,75 μg/kg/h (mitad de dosis) los dos últimos días del tratamiento para
evitar efecto rebote. Incompatible con soluciones alcalinas.
Pantoprazol: emplear perfusión durante un máximo de 72 h. Cinco viales de pantoprazol en 500 ml
de SF/SG al 5% cada 24 h. Por problemas de estabilidad cambiar la perfusión cada 12 h (2,5 viales en 250
ml).
Ranitidina: se emplea en perfusión continua en profilaxis de hemorragia gastrointestinal
debida a úlcera de estrés.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1490]
[93] ANEXO IV. FÁRMACOS USADOS EN PERFUSIÓN CONTINUA INTRAVENOSA
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1491]
[93] ANEXO IV. FÁRMACOS USADOS EN PERFUSIÓN CONTINUA INTRAVENOSA
BIBLIOGRAFÍA
Álvarez Arroyo L, Arrufat Goterris G, Barceló Campomar C, et al. Guía de administración de
medicamentos vía parenteral versión 1.0. Servicio de Farmacia. Hospital Universitario Son Espases,
Palma de Mallorca. Disponible para Android, iPhone, iPad en: http://bit.ly/1cKU2Jf
Centro de información online de medicamentos de la AEMPS-CIMA [base de datos en Internet]. Fichas
técnicas medicamentos [consultado 10 enero 2016]. Disponible en:
http://www.aemps.gob.es/cima/fichasTecnicas.do?metodo=detalleForm
Chamorro C, Romera MÁ. Grupo de Trabajo de Analgesia y Sedación de la SEMICYUC. Estrategias de
control de la sedación difícil. Med Intensiva. 2008;32 Supl 1:31-7.
Gaspar Carreño M, Torrico Martín F, Novajarque Sala L, et al. Medicamentos de administración
parenteral: recomendaciones de preparación y estabilidad. Farm Hosp. 2014;38(6):461-7.
Lexicomp® OnlineTM. Monografías de medicamentos [consultado 24 enero 2016]. Disponible en:
http://online.lexi.com/lco/action/home
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1492]
[94] ANEXO V. ENFERMEDADES DE DECLARACIÓN OBLIGATORIA
94.Anexo V. Enfermedades de declaración obligatoria
Sara de Miguel García.
Medicina Preventiva
Asesoras:
Felisa Jaén Herreros.
Jefa de Sección de Medicina Preventiva
M.ª Inmaculada Sanz Gallardo.
Médica Adjunta de Medicina Preventiva
El Sistema de Enfermedades de Declaración Obligatoria (EDO) constituye una pieza clave dentro de
la Red de Vigilancia Epidemiológica de la Comunidad de Madrid. Su finalidad es la detección precoz de
problemas de salud para facilitar la toma de medidas encaminadas a proteger la salud de la población y
minimizar los riesgos que supone la aparición de determinadas enfermedades en colectivos.
El Real Decreto 2210/1995, de 28 de diciembre, crea la Red Nacional de Vigilancia Epidemiológica y
establece un Programa nacional de vigilancia de las enfermedades transmisibles. La Orden 445/2015, de 9
de marzo, modifica la lista de Enfermedades de Declaración Obligatoria (Tabla I) y sus modalidades de
notificación.
¿Quién notifica una EDO? Están obligados a declarar todos los médicos en ejercicio en la
Comunidad de Madrid, tanto del sector público como privado, ajustándose a las modalidades de
notificación reguladas en cada caso. La información epidemiológica tiene su origen fundamental en la labor
asistencial.
¿Qué se notifica? La aparición de cualquier incidencia que afecte o pueda afectar a la salud de la
Comunidad. Se notifican las EDO (Tabla I) y las situaciones epidémicas y brotes, independientemente de su
etiología (Tabla II).
¿Dónde se notifica? La notificación se realiza a los Servicios de Salud Pública del Área
correspondiente o, en su defecto, al Servicio de Epidemiología del Instituto de Salud Pública de la
Comunidad de Madrid, siendo recomendable informar al Servicio de Medicina Preventiva del hospital. La
notificación de cualquier enfermedad de declaración urgente da lugar a una investigación epidemiológica
por parte de los Servicios de Salud Pública, y a la toma de medidas de control si procediera.
¿Cómo se notifica? La información necesaria para notificar cada EDO está contenida en formularios
que debe cumplimentar el médico notificador. Existen EDO con formularios de declaración específicos y
otras que se notifican en el formulario general. Se puede acceder a estos formularios llamando al Servicio
de Medicina Preventiva del hospital o a través del Portal de Salud de la Comunidad de Madrid.
En la Comunidad de Madrid, en la práctica habitual, se recogen las EDO en dos modalidades de
notificación:
Declaración urgente con envío de datos epidemiológicos básicos: enfermedades que deben
notificarse a los Servicios de Salud Pública de Área el mismo día en el que se sospecha el caso y
con carácter de urgencia tan pronto como se detecte su existencia (teléfono: 061), con
posterior envío del formulario cumplimentado. Los brotes o las situaciones epidémicas también
son de notificación obligatoria y urgente en la Comunidad de Madrid, independientemente de
su etiología.
Declaración semanal y envío de datos epidemiológicos básicos: casos nuevos de las EDO
detectados durante la semana epidemiológica en curso.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1493]
[94] ANEXO V. ENFERMEDADES DE DECLARACIÓN OBLIGATORIA
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1494]
[94] ANEXO V. ENFERMEDADES DE DECLARACIÓN OBLIGATORIA
BIBLIOGRAFÍA
Comunidad de Madrid. Manual de notificación. Sistema de Enfermedades de Declaración Obligatoria.
Documento de Salud Pública n.º 69. Madrid: Comunidad de Madrid. Consejería de Sanidad; 2007.
Decreto 184/1996, de 19 de diciembre, por el que se crea la Red de Vigilancia Epidemiológica de la
Comunidad de Madrid. Boletín Oficial de la Comunidad de Madrid, n.º 2, (3-1-1997).
Orden SSI/445/2015, de 9 de marzo, por la que se modifican los anexos i, ii y iii del Real Decreto
2210/1995, de 28 de diciembre, por el que se crea la Red Nacional de Vigilancia Epidemiológica,
relativos a la lista de enfermedades de declaración obligatoria, modalidades de declaración y de
enfermedades endémicas de ámbito nacional. Boletín Oficial del Estado, n.º 65, (17-03-2015).
Portal de Salud de la Comunidad de Madrid [sede Web]. Madrid: Comunidad de Madrid [acceso 9 de
febrero de 2016]. Enfermedades de Declaración Obligatoria. Disponible en:
http://www.madrid.org/cs/Satellite?c=PTSA_Generico_FA&cid=1142337084999&language=es&page
id=1142337086965&pagename=PortalSalud%-
2FPTSA_Generico_FA%2FPTSA_pintarGenericoIndice&pv=1142337079090&vest=1159289986941.
Real Decreto 2210/1995, de 28 de diciembre, por el que se crea la Red Nacional de Vigilancia
Epidemiológica. Boletín Oficial del Estado, nº 21, (24-1-1996).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1495]
[95] ANEXO VI. INMUNOSUPRESIÓN Y SUS COMPLICACIONES
95.Anexo VI. Inmunosupresión y sus complicaciones
María Martín López.
Reumatología
Francisco Trapiello Valbuena.
Medicina Interna
Asesora: Eugenia Enríquez Merayo.
Médica Adjunta de Reumatología
I. GLUCOCORTICOIDES
Los glucocorticoides (GC) son una parte esencial en el manejo de procesos de origen
inflamatorio/autoinmune, tanto por vía sistémica como local mediante infiltraciones. Es importante
conocer sus posibles efectos adversos para tratar de prevenirlos o minimizarlos.
1. Clasificación (Tabla I).
2. Efectos secundarios de los glucocorticoides
La mayoría de efectos adversos se relacionan con la dosis y el tiempo de tratamiento, e incluso
dosis bajas durante un tiempo mantenido también pueden llevar a la aparición de los mismos
(fundamentalmente relacionados con la supresión del eje hipotálamo-hipofisario-suprarrenal [HHS]).
Osteomusculares: miopatía, osteoporosis, osteonecrosis y retraso de crecimiento.
Endocrinometabólicos: síndrome de Cushing, diabetes mellitus, dislipidemia, ganancia
ponderal, hipopotasemia y lipodistrofia.
Cardiovasculares: hipertensión arterial, insuficiencia cardiaca, arteriosclerosis, inducción de
arritmias (en pulsoterapia) y edema.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1496]
[95] ANEXO VI. INMUNOSUPRESIÓN Y SUS COMPLICACIONES
Cutáneos: fragilidad cutánea y capilar, hirsutismo, acné, alopecia y púrpura.
Oftalmológicos: glaucoma, catarata subcapsular y coriorretinopatía serosa.
Gastrointestinales: ulcus péptico, perforación visceral (divertículos) y esteatosis hepática.
Potencia toxicidad digestiva con antiinflamatorios no esteroideos.
Neuropsiquiátricos: euforia, insomnio, ansiedad, psicosis inducida, acatisia, atrofia cerebral,
hipertensión intracraneal.
Sistema inmunológico: infecciones comunes y oportunistas, tuberculosis, Pneumocystis
jirovecii, herpéticas. Puede disminuir la respuesta a las vacunas.
Sistema reproductivo: irregularidad menstrual, disminución de la fertilidad.
Supresión del eje HHS: se produce en pacientes con dosis suprafisiológicas durante más de tres
semanas, en caso de suspensión brusca de GC o situación de estrés. La disminución de GC para
evitar la supresión del eje se muestra en la tabla II.
3. Recomendaciones generales para uso y manejo
Informar al paciente sobre los posibles efectos secundarios antes de iniciar el tratamiento.
Utilizar la mínima dosis eficaz en terapias crónicas y evaluar de forma periódica su posible
disminución o retirada.
Valorar el riesgo/beneficio, sobre todo en embarazadas (a dosis altas favorece prematuridad y
retraso de crecimiento) y en niños (es preferible una dosis puntual con infiltración o bolos y
monitorizar el crecimiento).
Se recomienda administrar por la mañana y a poder ser en dosis única para minimizar la
supresión del eje HHS.
Profilaxis de osteoporosis con suplementos de calcio/vitamina D y bifosfonatos en pacientes
que inician prednisona ≥ 7,5 mg/día o equivalente durante ≥ 3 meses, o en pacientes con
factores de riesgo para desarrollar osteoporosis (ver Capítulo 72. “Osteoporosis”).
Utilizar inhibidores de la bomba de protones si se asocian con antiinflamatorios no esteroideos
(o usar inhibidores de la ciclooxigenasa-2).
Profilaxis con sulfametoxazol-trimetoprim 800/160 mg (Septrin forte®), tres días por semana, en
tratamientos prolongados con dosis > 15 mg/día de prednisona o equivalente.
En situaciones de estrés médico o quirúrgico, para evitar insuficiencia suprarrenal, administrar
dosis adicional de 50-100 mg de hidrocortisona intravenosa (iv) dos horas antes de la cirugía y
después cada ocho horas iv hasta alcanzar la tolerancia oral.
II. FÁRMACOS MODIFICADORES DE LA ENFERMEDAD NO BIOLÓGICOS
Los fármacos inmunosupresores o inmunomoduladores constituyen la base fundamental del
tratamiento de las enfermedades inflamatorias crónicas de base inmunológica. No actúan de forma
selectiva sobre una citoquina o receptor, sino que intervienen al nivel de distintos componentes de la
cascada inflamatoria y respuesta inmune (Tablas III, IV y V).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1497]
[95] ANEXO VI. INMUNOSUPRESIÓN Y SUS COMPLICACIONES
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1498]
[95] ANEXO VI. INMUNOSUPRESIÓN Y SUS COMPLICACIONES
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1499]
[95] ANEXO VI. INMUNOSUPRESIÓN Y SUS COMPLICACIONES
III. FÁRMACOS MODIFICADORES DE LA ENFERMEDAD BIOLÓGICOS
Los fármacos biológicos actúan de forma específica para neutralizar la acción de diversas moléculas
o funciones celulares que desempeñan un papel relevante en la patogenia de las enfermedades
inflamatorias. Las dianas terapéuticas son citocinas, receptores de citocinas u otras moléculas que se
expresan en la superficie de células del sistema inmune que tienen una actividad proinflamatoria (TNF-alfa,
IL-1, IL-6, IL12/IL23, BAFF, CD20 en linfocitos B, CD80/CD86 en linfocitos T) (Tablas VI y VII).
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1500]
[95] ANEXO VI. INMUNOSUPRESIÓN Y SUS COMPLICACIONES
1. Consideraciones comunes a todas las terapias biológicas
Antes del tratamiento:
Aspectos clínicos: descartar infección activa, cáncer, enfermedad desmielinizante, citopenias,
insuficiencia cardiaca, contacto reciente con tuberculosis (profilaxis con isoniazida 9 meses o
rifampicina 4 meses).
Pruebas complementarias: hemograma, bioquímica, serologías del virus de la hepatitis B (VHB)
y C (VHC), radiografía de tórax, Mantoux y booster.
Medidas preventivas: vacuna antineumocócica y antigripal. Valorar vacuna contra VHB,
antimeningocócica y Haemophilus según comorbilidad. Valorar tratamiento antiviral si el VHB
es positivo (remitir al especialista). Evitar vacunas con gérmenes atenuados o vivos. Educar al
paciente en síntomas de alarma, medidas higiénico-dietéticas, planificación de la gestación, etc.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1501]
[95] ANEXO VI. INMUNOSUPRESIÓN Y SUS COMPLICACIONES
Situaciones clínicas especiales: desaconsejar embarazo y lactancia. Suspender en cirugía mayor
electiva, de 2 a 8 semanas antes, según biológico, y reanudar tras la cicatrización. Población
inmigrante: evaluación de infecciones poco frecuentes en nuestro medio.
Durante el tratamiento:
Aspectos clínicos: aparición de infecciones, citopenia grave, cáncer, enfermedad
desmielinizante o neuritis óptica. Aparición o empeoramiento de neumopatía o insuficiencia
cardiaca.
Pruebas complementarias: hemograma y bioquímica mensual los tres primeros meses,
posteriormente cada tres a seis meses.
Suspensión temporal: si infección o cirugía mayor electiva, en periodo perioperatorio. Valorar
en embarazo o lactancia.
Suspensión definitiva: si aparece cáncer, enfermedad desmielinizante, citopenia grave,
neumopatía intersticial nueva o empeoramiento, eventos graves en relación con fármaco.
IV. INMUNOGLOBULINAS INTRAVENOSAS
Las inmunoglobulinas humanas policlonales inespecíficas (Flebogamma®, Privigen®, Endobulin®) se
emplean en una gran variedad de entidades clínicas que incluyen: inmunodeficiencias primarias
(hipogammaglobulinemias congénitas o adquiridas) o secundarias, trasplante de células hematopoyéticas,
infecciones intercurrentes graves en huéspedes inmunocomprometidos o en pacientes con trastornos
inflamatorios y mediados por mecanismos autoinmunes (inmunomodulador).
La dosis varía según la enfermedad a tratar; como tratamiento sustitutivo, en estados de
inmunodeficiencia primaria o secundaria, se emplean dosis bajas (200-400 mg/kg/mes), mientras que en
otras entidades, como la púrpura trombocitopénica idiopática, la enfermedad de Kawasaki o el síndrome
de Guillain-Barré, se administran dosis mayores (400 mg/kg o 1-2 g/kg repartidos en dos a cinco días).
Fuera de ficha técnica se han usado en anemia hemolítica autoinmune, polimiositis, etc.
Entre sus efectos secundarios destacan: síndrome pseudogripal con la infusión (disminuir
velocidad), riesgo de hipotensión y episodios tromboembólicos (aumenta viscosidad sanguínea); además,
reduce la eficacia de la vacunación con virus vivos (esperar tres meses). Usar con precaución en el
embarazo (clase C) y la lactancia. No administrar en insuficiencia renal crónica estadio IV o V.
BIBLIOGRAFÍA
Álvaro-Gracia Álvaro JM, García Arias M. Fármacos modificadores de la enfermedad.
Inmunosupresores. En: Alperi López, M, editora. Manual SER de enfermedades reumáticas. 6.ª ed.
Barcelona: Elsevier; 2014. pp. 163-72.
Hoes JN, Jacobs JW, Boers M, et al. EULAR evidence based recommendations on the management of
systemic glucocorticoid therapy in rheumatic diseases. Ann Rheum Dis. 2007;66:1560-7.
Medina Luezas, JA. Glucocorticoides. En: Alperi López M, editora. Manual SER de enfermedades
reumáticas. 6.ª ed. Barcelona: Elsevier; 2014. pp.157-62.
Saag KG, Furst DE. Major side effects of systemic glucocorticoids [monografía en internet]. Wolters
Kluver Health CS: Uptodate 2014 [consultado 9 enero 2015]. Disponible en: http://www.uptodate.com
Sanmartí R, García Rodríguez S, Álvaro-Gracia JM, et al. Actualización 2014 del Documento de
Consenso de la Sociedad Española de Reumatología sobre el uso de terapias biológicas en la artritis
reumatoide. Reumatol Clin. 2015;11(5):279-94.
SanMartí Sala R. Fármacos biológicos y otras dianas terapéuticas. En: Alperi López M, editora. Manual
SER de enfermedades reumáticas. 6.ª ed. Barcelona: Elsevier; 2014. pp. 173–82.
Van der Goes MC, Jacobs JWG, Bijlsma JWJ. Towards a fer treatment with glucocorticoids: Via patient
and rheumatologist perspectives to recommendations on monitoring for adverse events. Clin Exp
Rheumatol. 2011;29 (Suppl. 68):S116-20.
Manual de Diagnóstico y Terapéutica Médica – Hospital Universitario 12 de Octubre [1502]
También podría gustarte
- Cuadro Historia Del DX FTDocumento1 páginaCuadro Historia Del DX FTStephany Rendón100% (1)
- Hoja de Salud Depilacion LaserDocumento1 páginaHoja de Salud Depilacion LaserCarlos HernándezAún no hay calificaciones
- Consentimiento Informado Cancer de PielDocumento2 páginasConsentimiento Informado Cancer de PielBaldur SernaAún no hay calificaciones
- Informe - Caso de Fobia Social Desde El Modelo Conigtivo ConductualDocumento11 páginasInforme - Caso de Fobia Social Desde El Modelo Conigtivo ConductualYulieth Paola Salas MachucaAún no hay calificaciones
- Examen - (ACDB1-15%) (SUP1) Actividad Suplementaria - Analice Los Criterios Diagnósticos de Los Trastornos Alimentarios y de La Ingestión de AlimentosDocumento4 páginasExamen - (ACDB1-15%) (SUP1) Actividad Suplementaria - Analice Los Criterios Diagnósticos de Los Trastornos Alimentarios y de La Ingestión de AlimentosBryan RuizAún no hay calificaciones
- Ejemplos de Trastornos de La Personalidad ExtrañaDocumento2 páginasEjemplos de Trastornos de La Personalidad ExtrañaEdwin Rodrigo Sulca Huaynate100% (1)
- TDH en Los NiñosDocumento7 páginasTDH en Los Niñosluisa reyesAún no hay calificaciones
- Enfoque de Riesgo CVDocumento11 páginasEnfoque de Riesgo CVRoberto Páez BravoAún no hay calificaciones
- 01 Diabetes Gestacional - ResDocumento8 páginas01 Diabetes Gestacional - ResYennyHerreraQuirozAún no hay calificaciones
- El Rol Del Fonoaudiólogo en La DegluciónDocumento2 páginasEl Rol Del Fonoaudiólogo en La DegluciónMaría Eloísa García AbelloAún no hay calificaciones
- Ponencia Guadilla Marisa Jornada - OctubreDocumento15 páginasPonencia Guadilla Marisa Jornada - OctubreMia CuentaAún no hay calificaciones
- Maniobras de Reposición CanalicularDocumento5 páginasManiobras de Reposición Canalicularjuan jorqueraAún no hay calificaciones
- Anorexia NerviosaDocumento15 páginasAnorexia NerviosaMaría Yojaira Barrera RomeroAún no hay calificaciones
- Hoja de Triaje ActualDocumento2 páginasHoja de Triaje ActualXiomara TrujilloAún no hay calificaciones
- TriageDocumento21 páginasTriageAlexis ORhpositivoAún no hay calificaciones
- Enfermedades Priónicas PDFDocumento15 páginasEnfermedades Priónicas PDFEliana CamargoAún no hay calificaciones
- Epoc - 2023Documento34 páginasEpoc - 2023Luis VasquezAún no hay calificaciones
- Sindrome de Oht.Documento2 páginasSindrome de Oht.Aylin Revilla VargasAún no hay calificaciones
- El AbortoDocumento11 páginasEl AbortoAna GerreroAún no hay calificaciones
- Evaluacion Por Hipotesis Diagnostic A de Deficit AtencionalDocumento2 páginasEvaluacion Por Hipotesis Diagnostic A de Deficit AtencionalMiguel Angel FloresAún no hay calificaciones
- Neuro - Esquemas para ExamenDocumento6 páginasNeuro - Esquemas para Examennolas16100% (3)
- Sindrome Piramidal y Evento Cerebro VascularDocumento9 páginasSindrome Piramidal y Evento Cerebro VascularSara Lisbeth Mora LedesmaAún no hay calificaciones
- AcidosisDocumento10 páginasAcidosisAriangel Zurita BustamanteAún no hay calificaciones
- Tratamiento Post QuirúrgicoDocumento2 páginasTratamiento Post QuirúrgicoDiegoAún no hay calificaciones
- EGAN'S Fundamentals of Respiratory Care 12th Ed (1) (1) .En - EsDocumento21 páginasEGAN'S Fundamentals of Respiratory Care 12th Ed (1) (1) .En - EsHelí Ricardo Carmona0% (1)
- SRQ Cuestionario AutorreporteDocumento2 páginasSRQ Cuestionario AutorreporteLaly Huarca CcansayaAún no hay calificaciones
- Enfermedades Mentales HereditariasDocumento2 páginasEnfermedades Mentales HereditariasnicolasAún no hay calificaciones
- Enfermedad de AlzheimerDocumento6 páginasEnfermedad de AlzheimerDamián GalindoAún no hay calificaciones
- HEMORRAGIASDocumento11 páginasHEMORRAGIASYuli Esquivel RodrigezAún no hay calificaciones
- Lectura 1. RESUMEN DEPRESIÓNDocumento10 páginasLectura 1. RESUMEN DEPRESIÓNliongadoAún no hay calificaciones