Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Taller N 2 Agroforestal
Cargado por
Daniel RodriguezDescripción original:
Título original
Derechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
Taller N 2 Agroforestal
Cargado por
Daniel RodriguezCopyright:
Formatos disponibles
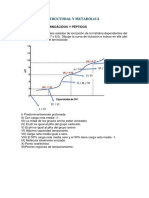
TALLER N° 2
AMINOÁCIDOS Y PUNTO ISOELÉCTRICO
1. Escribir la forma que presenta cada uno de los siguientes aminoácidos a pH 7:
isoleucina (Pka:2,36 y 9,68)
tirosina (Pka: 2,2; 9,11 y 10,07)
treonina (Pka: 2,11; 9,62 y 13,6)
glutámico (Pka: 2,19; 9,67 y 4,25)
arginina (Pka: 2,17; 9,04 y 12,48).
2. Escribir los posibles estados de ionización de los siguientes aminoácidos:
• Ácido glutámico
• Histidina
• Serina
b) Calcular el punto isoeléctrico de cada uno de ellos.
3. Dado el siguiente tripéptido: DKAYM
a) Escribir las diferentes formas de ionización
b) Indicar la estructura que predomina a pH 4.
c) Calcular el pI del tripéptido
d) Indicar la carga del péptido a pH 4 y 12.
4. Se preparó un tampón 30mM a pH semejante al que existe en el interior de la célula hepática
(6,65), para lo cual se utilizó histidina:
a) ¿Cuántos gramos de histidina son necesarios para preparar el tampón? (pm=155,2)
b) ¿Cuáles son las concentraciones de las especies iónicas presentes en la solución tampón?
5. Se llevó a cabo una electroforesis sobre papel de una mezcla de Gli, Ala, Glu, Lis, Arg. Indicar su
estado de ionización y su movilidad electroforética a pH=2, pH=6 y pH=9.
6. Se realiza una cromatografía de intercambio iónico en columna, rellena con una resina de
cargada positivamente. Se le añade una mezcla de Lis, Arg,Asp, Glu, Tir y Ala a pH=10. Predecir el
orden de elución de los aminoácidos por tratamiento de la resina con disoluciones a pH
sucesivamente decrecientes.
7. De un hidrolizado proteico se han separado los siguientes péptidos, de los que se han valorado
los pKa de sus grupos ionizables, obteniéndose los siguientes valores:
Asp-Gli (2.2; 4.5;9.1)
Ala-Lis-Ala (3.3;8.0;10.6)
Gli-Glu-Lis-Ala (3.3;4.1;8.2;10.5)
Calcular su pI e indicar el pH al que debería realizarse una electroforesis para separarlos.
También podría gustarte
- Taller N 2 AgroforestalDocumento2 páginasTaller N 2 AgroforestalhenryAún no hay calificaciones
- Problemas Ionizacion Aminoacidos 10-11 Con Respuestas-1Documento5 páginasProblemas Ionizacion Aminoacidos 10-11 Con Respuestas-1Manuel Jaen CardenasAún no hay calificaciones
- Ejercicios IonizacionDocumento1 páginaEjercicios IonizacionEmilio LasherasAún no hay calificaciones
- Biomoléculas 1Documento11 páginasBiomoléculas 1MaximimilianoAún no hay calificaciones
- AMINOACIDOS (Recuperado)Documento54 páginasAMINOACIDOS (Recuperado)nathaloaAún no hay calificaciones
- Problemario Aa y ProteínasDocumento8 páginasProblemario Aa y ProteínasalescrialferAún no hay calificaciones
- Guía de Ejercitación AMINOÁCIDOSDocumento1 páginaGuía de Ejercitación AMINOÁCIDOSn9mdjtrtsmAún no hay calificaciones
- Problemas Sobre Equilibrios Acido - Base y AminoacidosDocumento5 páginasProblemas Sobre Equilibrios Acido - Base y AminoacidosFanita Alarcon TourisAún no hay calificaciones
- Taller Aminoácidos y Péptidos 2022Documento4 páginasTaller Aminoácidos y Péptidos 2022zero kiryuuAún no hay calificaciones
- AMINOÁCIDOS Y PROTEÍNAS (Ejercicios)Documento2 páginasAMINOÁCIDOS Y PROTEÍNAS (Ejercicios)Jorge Villaroel100% (1)
- Sem 2Documento4 páginasSem 2Joel Paucar SincheAún no hay calificaciones
- Qui024 - Ejercicios de Aminoácidos y Péptidos - Semprim2015-3Documento12 páginasQui024 - Ejercicios de Aminoácidos y Péptidos - Semprim2015-3Milton Paredes Avalos100% (1)
- Curva ProteinasDocumento32 páginasCurva ProteinasBenjamin HonorioAún no hay calificaciones
- Amino Ácid OsDocumento3 páginasAmino Ácid OsMarivel Huancollo PalominoAún no hay calificaciones
- Taller de BioquímicaDocumento14 páginasTaller de BioquímicaDaniel MancillaAún no hay calificaciones
- Biomoléculas IDocumento6 páginasBiomoléculas IJuanma AlfaroAún no hay calificaciones
- Ejercicios Aminoacidos y SecuenciacionDocumento4 páginasEjercicios Aminoacidos y SecuenciacionDaniel Gomez GalindoAún no hay calificaciones
- Sem2 AminoacidosDocumento6 páginasSem2 AminoacidosDanny D RbAún no hay calificaciones
- AminoacidosDocumento6 páginasAminoacidosKarianny TorresAún no hay calificaciones
- Problemas Aa Resueltos PDFDocumento5 páginasProblemas Aa Resueltos PDFcgilgasAún no hay calificaciones
- 2 Clase20problemas20aminoacidos1Documento14 páginas2 Clase20problemas20aminoacidos1Valentina Gariazzo PalmaAún no hay calificaciones
- ProteinasDocumento11 páginasProteinasclaroquesicampeon12Aún no hay calificaciones
- Cuestiones Tema2 Aminoacidos PeptidosDocumento3 páginasCuestiones Tema2 Aminoacidos PeptidosLaura Heras EchavarríaAún no hay calificaciones
- Taller Aminoácidos y Proteínas.Documento2 páginasTaller Aminoácidos y Proteínas.niccol alvaradoAún no hay calificaciones
- Guía ProteínasDocumento10 páginasGuía ProteínasCecilia Arellano RamirezAún no hay calificaciones
- Ejer Cici OsDocumento3 páginasEjer Cici OsStephany BqAún no hay calificaciones
- Taller No 9. ProteínasDocumento2 páginasTaller No 9. ProteínasSantiago Loaiza PerezAún no hay calificaciones
- 1 GUIA DE EJERCICIOS Estructura ProteinasDocumento2 páginas1 GUIA DE EJERCICIOS Estructura ProteinasValeria QuirozAún no hay calificaciones
- Ejercicios Aminoácidos Y ProteínasDocumento2 páginasEjercicios Aminoácidos Y ProteínasMel GonzalezAún no hay calificaciones
- PROBLEMAS Bioquimica LenhingerDocumento8 páginasPROBLEMAS Bioquimica LenhingermarinaftvAún no hay calificaciones
- Ejercicio 1 y 2Documento2 páginasEjercicio 1 y 2JuliaLojánAún no hay calificaciones
- Problemas Aa. Peptidos. ProteínasDocumento3 páginasProblemas Aa. Peptidos. ProteínasCarolinaAún no hay calificaciones
- Conceptos Fundamentales BohinskiDocumento16 páginasConceptos Fundamentales BohinskiAzael CandiaAún no hay calificaciones
- Todos Los ReasDocumento52 páginasTodos Los ReasJohanna CastilloAún no hay calificaciones
- 2 Parcial 2016Documento1 página2 Parcial 2016Martin RodriguezAún no hay calificaciones
- 01 Conceptos Básicos, Bioenergética y MembranaDocumento4 páginas01 Conceptos Básicos, Bioenergética y MembranaBraulio LimaAún no hay calificaciones
- 1taller Problemas PHDocumento6 páginas1taller Problemas PHangelica galvezAún no hay calificaciones
- SOLUCIONES Taller Aminoácidos y Péptidos - 2021Documento14 páginasSOLUCIONES Taller Aminoácidos y Péptidos - 2021Facundo SoriaAún no hay calificaciones
- Bioquímica Preguntas (Temas 1-6)Documento26 páginasBioquímica Preguntas (Temas 1-6)Mar Carrasco CarrascoAún no hay calificaciones
- Guia Macromoleculas KineDocumento4 páginasGuia Macromoleculas KineChristian Mandiola QuililongoAún no hay calificaciones
- Palafox Luna Act08 BQ 2023Documento4 páginasPalafox Luna Act08 BQ 2023Aiden PalafoxAún no hay calificaciones
- Serie de Problemas - QaiiDocumento10 páginasSerie de Problemas - QaiiJuan José MendozaAún no hay calificaciones
- Problemario Bioquimica 2011Documento15 páginasProblemario Bioquimica 2011Daniel PAún no hay calificaciones
- Protein AsDocumento14 páginasProtein AsjulianAún no hay calificaciones
- Taller de AminoacidosDocumento18 páginasTaller de AminoacidosCARLOS GREGORIO PADILLA PAJOYAún no hay calificaciones
- Taller No. 2 - Medio Acuoso y Soluciones Buffer - Prof. Jorge LeyvaDocumento2 páginasTaller No. 2 - Medio Acuoso y Soluciones Buffer - Prof. Jorge LeyvaSofia Rodríguez0% (1)
- Taller Final ORG2 2015-1Documento3 páginasTaller Final ORG2 2015-1Maria CamilaAún no hay calificaciones
- Comportamiento +ícido-Base de Amino+ícidos y P+®ptidosDocumento8 páginasComportamiento +ícido-Base de Amino+ícidos y P+®ptidosAbel Valenzuela GarcíaAún no hay calificaciones
- Clase Práctica No.8 Cap. I. Aminoácidos y PéptidosDocumento4 páginasClase Práctica No.8 Cap. I. Aminoácidos y PéptidosAiden PalafoxAún no hay calificaciones
- Hoja Problemas T 1 - BQ1Documento2 páginasHoja Problemas T 1 - BQ1tusclasesparticulares060Aún no hay calificaciones
- Repartido 1-A.a 2015 ArregladoDocumento5 páginasRepartido 1-A.a 2015 ArregladoOscar MuñozAún no hay calificaciones
- Parcial Bioquimica 1Documento5 páginasParcial Bioquimica 1Alejo MuñozAún no hay calificaciones
- Enumadj 15Documento2 páginasEnumadj 15Juan AAún no hay calificaciones
- Deberes de Aminoácidos y PéptidosDocumento2 páginasDeberes de Aminoácidos y PéptidosLaura Heras EchavarríaAún no hay calificaciones
- Guia de Estudio 1Documento5 páginasGuia de Estudio 1Daniela Avendaño0% (1)
- Estatus ácido-base: Conceptos, desequilibrios e interpretaciónDe EverandEstatus ácido-base: Conceptos, desequilibrios e interpretaciónAún no hay calificaciones
- Acceso a Universidad para Mayores de 25 años. Biología 2013-2017.: Solucionario Pruebas 2013-2017De EverandAcceso a Universidad para Mayores de 25 años. Biología 2013-2017.: Solucionario Pruebas 2013-2017Aún no hay calificaciones
- Casos de estudio de termodinámica: Solución mediante el uso de ASPENHYSYSDe EverandCasos de estudio de termodinámica: Solución mediante el uso de ASPENHYSYSCalificación: 4.5 de 5 estrellas4.5/5 (7)