Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Estado Gaseoso
Cargado por
Bejarano AndresDerechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
Estado Gaseoso
Cargado por
Bejarano AndresCopyright:
Formatos disponibles
CAPTULO
Profesor:
Tema
Julio Oria
ESTADO GASEOSO
INTRODUCCIN :
* Vivimos
en el fondo de un ocano de aire, cuya composicin porcentual en volumen es
aproximadamente: 78% de N2, 21% de O2 y 1% de otros gases (H2, CO2 , etc.).
Los gases desempean, un papel importante en nuestra vida diaria, debido a que tienen
mltiples usos y aplicaciones. Por ejemplo:
* El gas domstico como fuente de energa.
* El oxigeno vital para los seres vivos.
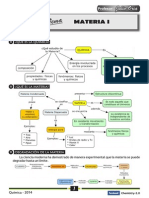
: Llamado tambin estado catico, es el estado de agregacin molecular de
* laCONCEPTO
materia, donde las molculas constituyentes estn en constante movimiento catico (al
azar), debido a su alta energa cintica interna.
GAS : Es un fluido que toma la forma y ocupa en su
* totalidad
el volumen del recipiente que lo contiene.
Sus molculas estn separadas debido a que la fuerzas
de repulsin intermolecular son mucho mayores que
las de atraccin (cohesin), por eso los gases carecen
de forma y volumen definido.
FR
FA
FA
FR
FA <<< FR
FA : Fuerza de atraccin intermolecular
FR : Fuerza de repulsin intermolecular
GAS
GENERALES :
* -PROPIEDADES
Cuentan con densidades mucho menores que los slidos y
lquidos.
- Cuando se encuentran confinados en el mismo recipiente se mezclan homogneamente, es
decir son miscibles entre s.
- Poseen la propiedad de la isotropa, la cual indica que las propiedades fsicas y mecnicas
son iguales en cualquier direccin con la que se les mida.
- Son compresibles, es decir, el volumen que ocupa un gas se puede reducir fcilmente
mediante la accin de una fuerza externa, esto se explica debido a la existencia de
grandes espacios intermoleculares.
- Se pueden expandir, un gas ocupa todo el volumen del recipiente que lo contiene debido a
que sus molculas poseen una alta energa cintica traslacional.
- Difusin, consiste en que las molculas gaseosas se trasladan a travs de otro cuerpo
material (gas, lquido o slidos) debido a su alta energa cintica y alta entropa.
- Atmlisis, es la separacin de los componentes de una mezcla gaseosa por difusin a travs
de una membrana porosa, el ms ligero se difunde a travs de la membrana porosa y el
ms pesado no puede difundirse a travs de la membrana porosa.
- Efusin, consiste en la salida de las molculas gaseosas a travs de orificios pequeos
practicados en la pared del recipiente que contiene el gas, debido a una variacin de
presin a temperatura constante.
P
P
Embolo
mvil
Compresin
Difusin
Expansin
Qumica - 2013
El gas domstico contiene principalmente
propano (C3H8), pero el olor se debe a la
presencia de mercaptanos (compuestos de azufre)
1
Chemistry-2.0
Qumica
Julio Oria
DE ESTADO :
* ElFUNCIONES
comportamiento de una determinada cantidad de gas
(n), es independiente de su composicin qumica y se puede
describir mediante el uso de 3 parmetros termodinmicos
que son: P, V y T.
*
*
Presin (P) :
Los gases ejercen presin sobre cualquier superficie
con la que entran en contacto, debido al constante movimiento de sus
molculas e incesantes choques que ejercen sobre estas superficies.
La presin de un gas se manifiesta en diferentes direcciones con igual
intensidad en cualquier parte interior del recipiente que lo contiene.
Es decir, los gases ejercen presin isotrpica al recipiente que los
contiene. Es decir, ejercen la misma presin en todas direcciones.
Volumen (V) :
El gas debido a su alta energa cintica ocupa todo el volumen del recipiente
3
que lo contiene. Unidades: L, mL, m , etc.
Temperatura (T) :
Es la medida de la energa cintica media (promedio) de las molculas
gaseosas, debido a la constante agitacin que estas experimentan. En las leyes del estado
gaseoso se utilizan solo escalas absolutas, en el S.I. La temperatura se mide en Kelvin (K).
Unidades: K,C
* Para lectura absoluta: K = C + 273,15
* Para variacin: C = K
Nmero de moles (n) :
LEYES EMPRICAS DE LOS GASES :
m
M
g
g/mol
El descubrimiento de estas relaciones cuantitativas, se dio de la mitad del siglo XVII y la
mitad del siglo XIX. Para una determinada masa gaseosa y en condiciones moderadas,
manteniendo constante una de las variables fsicas (P, V o T) es posible demostrar una relacin
sencilla entre las otras dos.
Ley de Boyle (Proceso Isotrmico) :
En 1961, Robert Boyle, hizo un
sencillo experimento vertiendo
mercurio en el extremo abierto
de un tubo en forma de J, observando
que a medida que iba adicionando ms
mercurio, la presin sobre el gas
aumentaba, haciendo que su volumen
disminuya
Qumica - 2013
2
Chemistry-2.0
Qumica
Julio Oria
P.V = K
Grficas del Proceso Isotrmico
P
PV
PV
T3
Isoterma
T2
Isoterma
Isoterma
T1
T2
Isoterma
T1
0
Se cumple: T3 > T2 >T1
T3
T2
T1
T3
T2
T1
T3
1/V
0
P
Se cumple: T3 > T2 >T1
Se cumple: T3 > T2 >T1
Se cumple: T3 > T2 >T1
Ley de Charles (Proceso Isobrico) :
En 1787 el fsico Francs Jacques Alexandre Charles,
pionero en los globos aerostticos y llenos con hidrgeno, hizo una de las primeras
observaciones cuantitativas de los gases a presiones fijas, concluyendo que el volumen de un
gas guarda una relacin directa con su temperatura.
Cuando se sumerge en nitrgeno lquido un
globo lleno de aire (-196C) , el globo se
contrae. Despus de que se saca el globo
del nitrgeno lquido, regresa a su tamao
original. Un gas se contrae cuando se
enfra y se expande cuando se calienta.
P1
V =K
T
P1
P2
P2
P3
P3
Isobara
Isobara
-273,15
T (C)
Grficas del Proceso Isobarico
Ley de Gay-Lussac (Proceso Isocrico) :
Se cumple: P3 > P2 >P1
Joseph Louis Gay-Lussac (1802)
P
P =K
T
V1
V2
V1
V2
V3
V3
Isocora
-273,15
Grficas del Proceso Isocrico
Qumica - 2013
T (K)
Se cumple: P3 > P2 >P1
Isocara
T (C)
Se cumple: V3 > V2 >V1
T (K)
Se cumple: V3 > V2 >V1
3
Chemistry-2.0
Qumica
ECUACIN COMBINADA :
La ley de Boyle (V 1/P) y la Ley de Charles (V T) pueden combinarse y expresarse en un solo
enunciado: el volumen ocupado por una cantidad dada de un gas es proporcional a la temperatura
absoluta dividida entre la presin ( V T/P). Puede escribir esta ecuacin como:
Para m= cte
(n= cte)
P.V = K
T
LEY DE AVOGADRO :
A presin y temperatura constante, el volumen de un gas ideal vara
directamente con su cantidad de sustancia (n).
Para T, P= cte
Julio Oria
V =K
n
LEY DE LOS GASES IDEALES :
P.M = T.R.D
P.V = R.T.n
D: Densidad (g/L)
P.V.M = R.T.m
m: masa (g)
MEZCLA DE GASES :
Qumica - 2013
4
Chemistry-2.0
Qumica
Julio Oria
Es un
Qumica - 2013
5
Chemistry-2.0
También podría gustarte
- Resistencia A La Compresión Del Concreto 2%Documento10 páginasResistencia A La Compresión Del Concreto 2%Bejarano AndresAún no hay calificaciones
- Informe Laboratorio 11-04-2022-TovarDocumento19 páginasInforme Laboratorio 11-04-2022-TovarBejarano AndresAún no hay calificaciones
- Veran: CicloDocumento1 páginaVeran: CicloBejarano AndresAún no hay calificaciones
- Lista de Precios - 2023-06-14T102024.220Documento100 páginasLista de Precios - 2023-06-14T102024.220Bejarano AndresAún no hay calificaciones
- Algebra AduniDocumento48 páginasAlgebra AduniBejarano AndresAún no hay calificaciones
- PC02 ValDocumento14 páginasPC02 ValBejarano AndresAún no hay calificaciones
- INGENIERO QUIMICO - YanDocumento13 páginasINGENIERO QUIMICO - YanBejarano AndresAún no hay calificaciones
- Oficio #410 SUNAFIL Despidos Sindicato UTP (R)Documento1 páginaOficio #410 SUNAFIL Despidos Sindicato UTP (R)Bejarano AndresAún no hay calificaciones
- Proyecto de Inversion Parte II en El Marco Invierte PeDocumento19 páginasProyecto de Inversion Parte II en El Marco Invierte PeBejarano AndresAún no hay calificaciones
- Estudio HídricoDocumento14 páginasEstudio HídricoBejarano AndresAún no hay calificaciones
- Simulacion y Control ProcesosDocumento18 páginasSimulacion y Control ProcesosBejarano AndresAún no hay calificaciones
- Proyectos e IngenieriaDocumento47 páginasProyectos e IngenieriaBejarano AndresAún no hay calificaciones
- 10.2.1 Informe EMS2Documento38 páginas10.2.1 Informe EMS2Bejarano AndresAún no hay calificaciones
- Estado Del Arte Rev 4fDocumento10 páginasEstado Del Arte Rev 4fBejarano AndresAún no hay calificaciones
- Introduccion Al Bombeo HidraulicoDocumento25 páginasIntroduccion Al Bombeo HidraulicoBejarano AndresAún no hay calificaciones
- Annotated-Estado Del Arte Rev 4fDocumento10 páginasAnnotated-Estado Del Arte Rev 4fBejarano AndresAún no hay calificaciones
- Semana 08 - Plantilla de Proyecto de InvestigaciónDocumento7 páginasSemana 08 - Plantilla de Proyecto de InvestigaciónBejarano AndresAún no hay calificaciones
- Matriz ComunicacionesDocumento2 páginasMatriz ComunicacionesBejarano AndresAún no hay calificaciones
- Banco de Quimica 2Documento75 páginasBanco de Quimica 2Bejarano AndresAún no hay calificaciones
- Flujo Permanente y Uniforme en CanalesDocumento8 páginasFlujo Permanente y Uniforme en CanalesBejarano AndresAún no hay calificaciones
- El Yodo 2015 MarDocumento27 páginasEl Yodo 2015 MarBejarano AndresAún no hay calificaciones
- Estados de Agregacion - Temperatura y PresionDocumento4 páginasEstados de Agregacion - Temperatura y PresionBejarano AndresAún no hay calificaciones
- Capitulo 01 - Materia IDocumento10 páginasCapitulo 01 - Materia ILuisFernandoQuispeLevaAún no hay calificaciones
- Perfiles de AluminioDocumento14 páginasPerfiles de AluminioJuan David Loaiza PerugacheAún no hay calificaciones
- Fase 3 Grupo 337Documento11 páginasFase 3 Grupo 337Johan DiazAún no hay calificaciones
- Cemento Tipo VDocumento13 páginasCemento Tipo VAlexander GuerraAún no hay calificaciones
- Quimicacontextualiterceraunidad 091023220703 Phpapp02Documento105 páginasQuimicacontextualiterceraunidad 091023220703 Phpapp02Cesar DoAún no hay calificaciones
- Taller de REDOXDocumento1 páginaTaller de REDOXFernanda BaezaAún no hay calificaciones
- MorterosDocumento7 páginasMorteroserickAún no hay calificaciones
- Especificaciones Tecnicas RepresaDocumento35 páginasEspecificaciones Tecnicas RepresaJoseph MorenoAún no hay calificaciones
- Diagrama Balance Masa y Energia Proceso Product. BioetanolDocumento2 páginasDiagrama Balance Masa y Energia Proceso Product. BioetanolEduardo Bohórquez VargasAún no hay calificaciones
- Vocabulary of Matter and ForcesDocumento4 páginasVocabulary of Matter and ForcesSonia Navarro FloresAún no hay calificaciones
- Ciencias 8voDocumento153 páginasCiencias 8vonahuelymartinAún no hay calificaciones
- Capitulo 6 Intemperismo, Erosion y Formaciond de SuelosDocumento6 páginasCapitulo 6 Intemperismo, Erosion y Formaciond de SuelosAldoElwisPortoLopezAún no hay calificaciones
- MC 2014 08313 en EsDocumento8 páginasMC 2014 08313 en EsMelissa Quiroz PaezAún no hay calificaciones
- Reemplazo de Deshidratadores de Glicol Con Deshidratantes DesecantesDocumento11 páginasReemplazo de Deshidratadores de Glicol Con Deshidratantes DesecantesivarclAún no hay calificaciones
- Memoria Descriptiva Local SacuyoDocumento5 páginasMemoria Descriptiva Local SacuyoAlex Tom Quispe ApazaAún no hay calificaciones
- Tipo de ResiduosDocumento2 páginasTipo de ResiduosNicoll Patricia Moran MendozaAún no hay calificaciones
- Informe #3 - Efecto Del Ion ComúnDocumento28 páginasInforme #3 - Efecto Del Ion ComúnAlan TorrezAún no hay calificaciones
- Aislación Hidrófuga: CorreoDocumento3 páginasAislación Hidrófuga: CorreoJhonatan TorresAún no hay calificaciones
- Ficha Técnica Termoplac® Pasta ProDocumento1 páginaFicha Técnica Termoplac® Pasta ProcelectricAún no hay calificaciones
- Carbones Informe CenizasDocumento14 páginasCarbones Informe CenizasKaren PortilloAún no hay calificaciones
- Estructuras MetálicasDocumento96 páginasEstructuras MetálicasDaniel Mauricio SalgueroAún no hay calificaciones
- Formato Guía para El Transporte de Sustancias QuímicasDocumento11 páginasFormato Guía para El Transporte de Sustancias QuímicasNicole Rebolledo TatisAún no hay calificaciones
- Curriculum Iintol (Rev End - May 2017)Documento21 páginasCurriculum Iintol (Rev End - May 2017)Jose HuescaAún no hay calificaciones
- Ejercicios Prueba de EvaporaciónDocumento3 páginasEjercicios Prueba de EvaporaciónLennin Trujillo0% (1)
- FICHA TECNICAbloqueador FPS 100Documento1 páginaFICHA TECNICAbloqueador FPS 100Sandra BlasiAún no hay calificaciones
- SIG-GHSE-PRO04 Procedimiento de Segregación de Residuos Sólidos r.01Documento5 páginasSIG-GHSE-PRO04 Procedimiento de Segregación de Residuos Sólidos r.01Estalin Wilfredo Pari LlashagAún no hay calificaciones
- Chambi Hualpa Betzy (A)Documento9 páginasChambi Hualpa Betzy (A)Betzy Chambi HualpaAún no hay calificaciones
- FISICOQUIMICA Ejercicos 2Documento20 páginasFISICOQUIMICA Ejercicos 2Marco Antonio Hipòlito Gutierrez100% (2)
- La Subrasante (Subgrade)Documento29 páginasLa Subrasante (Subgrade)glampreavAún no hay calificaciones
- Parte I de Practica 2 AQDocumento7 páginasParte I de Practica 2 AQSantiago Kuri RiosAún no hay calificaciones