Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Manual de Tecnicas Basicas de Diagnostico Patologico en Peces PDF
Cargado por
jaime_andresTítulo original
Derechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
Manual de Tecnicas Basicas de Diagnostico Patologico en Peces PDF
Cargado por
jaime_andresCopyright:
Formatos disponibles
MANUAL de
TCNICAS BSICAS de
DIAGNSTICO PATOLGICO
en PECES
Versin: Junio 2005
V Curso de Ictiopatologa Prctica para Piscicultores
Situacin Sanitaria Actual del Cultivo de la Dorada y Lubina
Dr. Francesc Padrs
Servicio de Diagnstico Patolgico en Peces
Facultad de Veterinaria
Universidad Autnoma de Barcelona
Carlos Zarza
Servicio de Patologa de Peces
SKRETTING
Manual de Tcnicas Bsicas de Diagnstico Patolgico en Peces - 2005
Prlogo
El presente manual es una gua bsica sobre el diagnstico patolgico de las
enfermedades de los peces dirigida a los responsables de salud de las granjas u otras
personas interesadas en el tema .
Para elaborar el texto, se ha recopilado informacin procedente de los manuales de
los cursos previos y, adems, se ha incluido el conocimiento prctico de campo,
adquirido por los autores en el da a da en los ltimos aos, una informacin que
muchas veces no se recoge los libros y que puede resultar muy til.
No se pretende que se sigan todos los protocolos al pie de la letra, sino que cada
persona en cada situacin concreta adapte paras s las tcnicas que crea conveniente
y le resulten ms eficaces.
El diagnstico de las enfermedades de los peces puede resultar complicado y
enigmtico en ocasiones, pero la clave est en el conocimiento y experiencia. As que
a practicar...
19 de junio 2005
Manual de Tcnicas Bsicas de Diagnstico Patolgico en Peces - 2005
INDICE
1.- Bases Diagnsticas en Patologa de Peces ........................................................ 4
1.1.- Conceptos generales ............................................................................................ 4
1.2.- Filosofa del diagnstico ........................................................................................ 6
1.3.- El proceso de diagnstico ..................................................................................... 9
1.4.- Fuentes de informacin ....................................................................................... 12
2.- Epidemiologa en Sanidad Pisccola .................................................................. 15
2.1.- Qu entendemos por epidemiologa? ............................................................... 15
2.2.- Conceptos bsicos de epidemiologa .................................................................. 16
2.3.- Patrones de enfermedad ..................................................................................... 16
2.4.- Deteccin de enfermedad ................................................................................... 17
2.5.- Muestreos ............................................................................................................ 18
2.6.- Investigando las causas de enfermedad ............................................................. 23
3.- Protocolos de Diagnstico .................................................................................. 24
3.1.- Informacin bsica y situacin epidemiolgica general ..................................... 24
3.2.- Historia clnica y anamnesis ................................................................................ 24
3.3.- Examen in situ ..................................................................................................... 26
3.4.- Seleccin y envo de muestras .......................................................................... 33
3.5.- Anlisis directo de los peces ............................................................................... 35
3.6.- Pruebas rpidas directas...................................................................................... 41
3.7.- Anlisis complementarios..................................................................................... 44
3.8.- Diagnstico e interpretacin de los resultados..................................................... 57
4.- El Diagnstico en Planta ..................................................................................... 58
4.1.- Niveles de diagnstico en planta ........................................................................ 58
4.2.-Telediagnstico ................................................................................................. 59
5.- Anexo I: Ejemplo de Historia Clnica ................................................................. 60
6.- Anexo II: Ejemplo de Ficha de identificacin de Lesiones .............................. 62
Manual de Tcnicas Bsicas de Diagnstico Patolgico en Peces - 2005
1.- BASES DIAGNSTICAS EN PATOLOGA DE PECES
1.1.- CONCEPTOS GENERALES
Qu entendemos como diagnstico patolgico en peces?
El diagnstico patolgico en peces lo podemos definir como todas aquellas
actuaciones que llevamos a cabo con el fin de identificar y si es posible comprender
las causas de un determinado problema en una poblacin de peces. Entre las causas
de estos problemas podemos tener un abanico amplsimo que incluye desde agentes
biolgicos (virus, bacterias, parsitos, hongos) a agentes no infecciosos (neoplasias,
malformaciones, manejo, agentes fsico qumicos, alimentacin) que pueden actuar
solos o combinados entre s (lo ms habitual) provocando en muchos casos sinergias
que son precisamente las causantes de los problemas.
El diagnstico como herramienta de prevencin
La gestin sanitaria de una explotacin acucola se debe basar fundamentalmente en
la prevencin de los procesos patolgicos. Prevenir es siempre mejor que curar. De
esta manera no slo pretendemos evitar las mortalidades sino tambin, reducir costes
en tratamientos (que tambin son muy limitados), prdidas de rendimientos
productivos (el pez enfermo no come), no aumentar nuestro coste de produccin y por
ltimo evitar las prdidas de valor comercial de nuestro producto.
La prevencin dentro del proceso de produccin debe ser parte fundamental de la
misma, es decir, una rutina ms en el da a da. Junto con las herramientas de
diagnstico, otros elementos bsicos que se debern incluir en un programa de
prevencin sern las medidas higinico-sanitarias, estrategias de inmunoprofilaxis
mediante vacunacin y empleo de inmunoestimulantes adecuadas a cada situacin y
riesgo, la aplicacin correcta de los tratamientos teraputicos y un manejo ptimo de
las condiciones de cultivo y alimentacin. Nunca debemos olvidar que cada una de las
partes es igual de importante y, por lo tanto, el xito en el control de las enfermedades
en una explotacin pisccola radicars gestionar de forma eficaz todas y cada una de
ellas.
El diagnstico entendido como medida de prevencin debe realizarse de la forma ms
rpida y eficaz, antes de la expresin de la enfermedad, pues de su eficacia va a
depender el xito de las medidas de control que vamos a aplicar.
Necesidades de diagnstico: Urgencia / Con Previsin
Los procesos de diagnstico pueden realizarse de dos formas: De urgencia o
improviso o con previsin.
Manual de Tcnicas Bsicas de Diagnstico Patolgico en Peces - 2005
a) De Urgencia: Siempre vienen precedidos por alertas
- Uno o varios parmetros zootcnicos se encuentran modificados con respecto
a las previsiones tericas: Aumento del consumo de oxigeno, reduccin del
ndice de conversin, reduccin de los crecimientos esperados
- Aumento anormal de la mortalidad
- Cambios de comportamiento o de aspecto de los peces.
Resultado: Medidas urgentes y muchas veces precipitadas
b) Con previsin: A raz de la implantacin de un plan de control sanitario.
- Deteccin precoz de problemas como resultado de la realizacin peridica de
controles.
Resultado: Aplicacin de medidas de control antes de la expresin de
la patologa
Evidentemente, la deteccin precoz de patgenos mediante los controles sanitarios es
un mecanismo muy eficaz para identificar el desarrollo de una patologa antes de que
ste llegue a suponer problemas severos y nos permitir actuar de una forma rpida y
eficaz.
mortalidad
Plan de control
tiempo
Tiempo de reaccin
Nivel de deteccin
Manual de Tcnicas Bsicas de Diagnstico Patolgico en Peces - 2005
En el ejemplo A, la deteccin de la patologa tiene lugar a partir de que la mortalidad
cruza el umbral del nivel de deteccin de la patologa y como consecuencia de
necesitar un cierto tiempo de reaccin (debido a la logstica a utilizar), los niveles de
mortalidad pueden ser muy altos.
En el ejemplo B, el establecimiento de un muestreo peridico permite detectar la
patologa antes de que sta cruce el umbral del nivel de deteccin y por lo tanto, con
un mismo tiempo de reaccin, la patologa puede ser controlada de forma efectiva,
antes de que alcance niveles difcilmente controlables
Por ello hemos de tener siempre en mente que el xito o fracaso de la gestin
sanitaria en nuestra instalacin depender de esta trada de actuaciones
PREVENCIN DETECCIN PRECOZ INTERVENCION RPIDA
Diagnstico en planta y diagnstico en laboratorio especializado
Si el tiempo de reaccin desde que detectamos el problema hasta que se apliquen las
medidas de control va a ser ms o menos constante, muchas veces la efectividad de
estas medidas radicar en detectar la causa del problema lo ms rpido posible desde
su aparicin en la granja.
Existen laboratorios especializados en enfermedades de peces donde podemos enviar
una muestra para la realizacin del diagnstico, pero muchas veces se puede perder
un tiempo vital hasta que obtenemos el resultado definitivo. Por ello, siempre es
recomendable realizar un primer diagnstico presuntivo a pie de planta que nos
permitir aplicar unas primeras medidas teraputicas.
Esto es especialmente importante en las enfermedades bacterianas agudas, como la
Pasteurelosis, de rpida progresin. El esperar varios das una confirmacin puede
hacer que los peces reduzcan considerablemente su apetito, con lo que resultar ms
difcil un tratamiento por va oral.
Siempre ser recomendable enviar la muestra al laboratorio para la confirmacin del
diagnstico, pero cuanto ms podamos hacer en la granja, mejor. Ms adelante
revisaremos los protocolos de diagnstico bsicos, y gran parte de ellos se pueden
realizar de forma sencilla a pie de granja.
1.2.- FILOSOFA DEL DIAGNSTICO
Cmo reconocer e identificar los problemas patolgicos?
En el proceso de identificacin y reconocimiento de los problemas patolgicos es
importante recordar que:
Hemos de evitar que los rboles nos impidan ver el bosque
Manual de Tcnicas Bsicas de Diagnstico Patolgico en Peces - 2005
Es decir, que nunca un resultado de una prueba puede ser considerado un
diagnstico sin antes haber estado evaluado y a ser posible, acompaado por otras
pruebas diagnsticas.
Es demasiado frecuente encontrar que en el anlisis de los problemas patolgicos los
resultados de los anlisis son tomados como valores absolutos, sin tener en cuenta lo
que pueden significar.
Nunca hay que confiarse
Por muy clara que veamos la solucin a nuestro problema, siempre hay que realizar
todo el proceso de diagnstico, de forma sistemtica y completa y hasta el final, sin
olvidarnos ninguna prueba. Con la emocin del momento, es relativamente sencillo
que se nos puedan pasar cosas por alto y confundirnos de diagnstico. Y por tanto de
tratamiento.
Por ello recomendamos realizar un acercamiento mucho ms cauto y prudente a los
problemas. Frecuentemente los problemas patolgicos en centros de acuicultura,
ncleos zoolgicos o en el medio natural suelen ser complejos, multifactoriales y de
explicacin compleja.
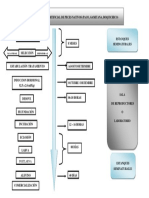
Nuestra experiencia indica que es recomendable realizar los acercamientos a estos
problemas mediante lo que podramos decir un doble sistema de entrada
(ANAMNESIS) y de salida (INTERPRETACIN de resultados y DIAGNSTICO)
Intentamos representar este proceso mediante varios crculos concntricos que
representan el proceso por el cual podemos obtener un diagnstico final de forma ms
precisa. Cada uno de los crculos representa los contextos o planos sobre los cuales
vamos a tener que analizar y procesar:
A: El contexto informativo general
B: El contexto del sistema particular
C: El contexto de la poblacin afectada
D: El contexto del individuo / rganos y sistemas
B
A
ENTRADA =
SALIDA =
ANAMNESIS
ANALISIS Y
DIAGNSTICO
Manual de Tcnicas Bsicas de Diagnstico Patolgico en Peces - 2005
Como esto puede sonar a filosofa barata y para entendernos, la descripcin de este
proceso la realizaremos a partir de un supuesto prctico:
Supongamos el caso particular de una piscifactora de engorde de trucha en la que se
detectan mortalidades anormales durante el verano. Para adentrarnos en el problema,
que debemos hacer?. Ir directamente a mirar peces muertos? NO!! GRAVE ERROR!!
Por qu puede ser un grave error? Porque posteriormente la evaluacin del problema
la realizaremos prcticamente en base a solo lo que hayamos podido encontrar en
esos peces. Evidentemente, es fcil que podamos encontrar algo anormal en esos
peces e incluso identificar la presencia de agentes extraos en ellos (parsitos, lo ms
habitual). El problema posiblemente aparecer cuando queramos atribuir la mortalidad
a uno o varios de esos agentes. En este caso, estaramos haciendo un diagnstico
real o buscando una especie de chivo expiatorio? Desgraciadamente an siguen
realizndose diagnsticos errneos de esta manera, con los graves problemas que
esto comporta ya que posiblemente los tratamientos planteados con este diagnstico
equivocado no sean efectivos y a veces incluso contraproducentes.
Por ello siempre es preciso abordar los problemas en patologa de peces con una
mentalidad abierta, sin juicios previos (aunque evidentemente podamos tener
sospechas previas) e intentando primero de todo obtener informacin y analizar cada
uno de los contextos que hemos indicado antes.
A: El contexto informativo general
Primero deberemos tener en cuenta lo que sera el contexto informativo general, es
decir, es muy importante estar al da y obtener informacin reciente sobre la
epidemiologa de las enfermedades que afectan a cada tipo de cultivo, tanto en la
zona geogrfica concreta, cuenca del ro, zona martima, comunidad, pas, etc.
Evidentemente esto no lo podemos hacer de forma puntual, sino que entra dentro de
lo que consideramos como formacin / informacin continuada.
Hay que recordar que slo podremos encontrar aquello que conocemos, en este
sentido es MUY importante y recomendable que los tcnicos que tengan que realizar
funciones de diagnstico puedan disponer del tiempo y de los medios necesarios para
ponerse al da de estos temas, sea leyendo libros y artculos especializados,
acudiendo a seminarios, congresos, reuniones, a travs de foros en internet y sobre
todo manteniendo un contacto permanente y fluido con otros tcnicos y especialistas
en patologa de peces.
Asimismo es importante conocer datos recientes sobre la situacin de los cauces
fluviales o zonas marinas (disponibilidad y calidades de agua), situacin meteorolgica
(lluvias torrenciales, vientos, sequa), etc.
Con todos estos datos y sin darnos cuenta nos iremos haciendo a la idea de ese
contexto general y podremos tener ya algunas orientaciones sobre determinados
parmetros que pueden (o no) modular el desarrollo del problema detectado.
Manual de Tcnicas Bsicas de Diagnstico Patolgico en Peces - 2005
B: El contexto del sistema en particular
El paso siguiente es considerar el contexto del sistema en particular, es decir, el centro
de produccin. En este paso es preciso conocer (mejor si ya lo conocemos de
antemano) datos sobre el tipo de produccin, sistema, tecnologa aplicada e historial
sanitario del centro, con el objetivo de valorar a posteriori los riesgos y puntos crticos
que puede presentar esta explotacin.
C: El contexto de la poblacin afectada
Una vez nos hayamos familiarizado con las caractersticas del centro, es el momento
de pasar al nivel siguiente, el contexto de la poblacin afectada. En este punto es
necesario obtener datos sobre qu parte o partes del sistema se encuentran
afectados. Es posible que el problema pueda expresarse solamente en unos
estanques/ tanques/jaulas determinados, en una especie en particular (si coexisten en
el sistema dos o ms especies), en un rango de edad especfico, en peces de una
determinada procedencia, en peces que han sido alimentados o han recibido un
manejo especial, etc.
D: El contexto particularizado de los peces afectados
Una vez tenemos acotada de forma mas precisa cmo se distribuye el problema en el
centro, pasamos a la parte final, lo que seria el corazn del problema, que sera el
contexto particularizado de los peces afectados. En este punto es preciso obtener el
mximo posible de datos para que se puedan analizar posteriormente.
Generalmente es lo que conocemos como fase analtica y en la que tendremos que
seleccionar las pruebas, lo que conocemos propiamente como TCNICAS DE
DIAGNSTICO que pueden aplicarse en funcin de parmetros como informacin
aportada, especificidad, sensibilidad, capacidad diagnstica de los resultados y coste
econmico.
El primer anlisis de datos se puede obtener a partir de lo que conocemos
habitualmente como historial clnico o ficha del caso. Esta ficha o historial puede ser
general o adaptada para cada tipo de instalacin. De la misma manera pueden idearse
fichas similares para la recopilacin de datos sobre los contextos de sistema y de
poblacin afectada. Evidentemente, cada tcnico podr confeccionar las suyas a partir
de su propia experiencia. Al final de este tema incluimos un ejemplo de lo que
podramos considerar como un historial-tipo y al que se pueden aadir los datos
obtenidos de las distintas pruebas diagnsticas realizadas (por ejemplo, tipo dossier).
1.3.- EL PROCESO DE DIAGNSTICO
Como hemos comentado anteriormente, ahora slo queda proceder con los protocolos
de diagnstico correspondientes a las tcnicas diagnsticas seleccionadas y esperar a
conocer los resultados. La descripcin pormenorizada de estas tcnicas de
diagnstico y de sus protocolos sern tratadas ms adelante.
Manual de Tcnicas Bsicas de Diagnstico Patolgico en Peces - 2005
Con estos resultados habremos obtenido una serie de inputs o informaciones y a
partir de aqu entramos en la segunda parte, lo que sera la segunda parte del
trayecto (hacia fuera de la diana virtual que hemos esquematizado al principio de
este apartado) Se trata de analizar e interpretar estos datos, valorarlos, razonarlos y
ponderarlos.
Con ello se deber llegar al elemento final, EL DIAGNSTICO.
El diagnstico es sin duda la parte ms difcil de todo este proceso. En la primera parte
pueden seguirse unas guas ms o menos completas. Sin embargo, en el diagnstico,
la utilizacin de guas o cuadros es mucho ms compleja y depende en buena manera
de la habilidad y experiencia del tcnico encargado de emitir este diagnstico.
Adems, es probable que no se dispongan de elementos de juicio suficientes para
emitir un diagnstico suficientemente claro.
Nuestra experiencia demuestra que uno de los aspectos que pueden mejorar las
habilidades diagnsticas es mejorar el conocimiento de la epidemiologa aplicada a la
ictiopatologa. Por ello hemos incluido un apartado especfico sobre Epidemiologa en
este bloque con el objetivo de intentar llenar algunas lagunas sobre determinados
conceptos epidemiolgicos y su tratamiento, que creemos son importantes a la hora
de recoger y valorar la informacin as como en la realizacin de un diagnstico.
Evidentemente tambin es muy importante tener una base lo ms amplia posible sobre
conocimientos de patologa de peces. Estos conocimientos los podemos adquirir a
travs de varios canales: Cursos, libros, revistas, internet. Los veremos en el apartado
final de este captulo.
Identificacin de los trastornos de salud vs diagnstico del problema
Hemos comentado antes que muchas veces las patologas en las explotaciones
acucolas son procesos multifactoriales y complejos y no siempre es fcil llegar a un
diagnstico definitivo. Siempre se requerir esfuerzo, tiempo y prctica para dominar
todas las tcnicas que requiere el arte del diagnstico.
Desde nuestro punto de vista, no es tan importante el qu es, sino reconocer si lo
que vemos es normal o no. Al piscicultor, que est cada da trabajando con los
peces, le puede costar diagnosticar una enfermedad, pero no reconocer si sus
animales estn enfermos o no, y qu pasos debe dar para a partir de ese momento
para llegar al diagnstico final. Esa identificacin de los transtornos de salud, ser
clave en el diagnstico rpido. Y por ello determinante en el proceso de prevencin.
Una vez detectado el problema, podr l mismo aplicar las tcnicas correspondientes
o enviar una muestra a un laboratorio especializado. Esa reaccin rpida es lo
fundamental. Ms delante repasaremos cmo podemos reconocer la presencia de
enfermedad en los peces.
El concepto de mortalidad natural
Es frecuente que en conversaciones entre colegas salga el trmino de mortalidad
natural, en referencia a aquellas mortalidades que se asumen como normales en
una determinada explotacin.
10
Manual de Tcnicas Bsicas de Diagnstico Patolgico en Peces - 2005
Nuestra opinin es que se trata de un trmino utilizado incorrectamente ya que si bien
en todas las poblaciones existen unas ciertas mortalidades en cada uno de los rangos
de edad, estas mortalidades dependen totalmente de cada una de las circunstancias
de cada poblacin.
Para poner un ejemplo, si comparamos la mortalidad neonatal humana entre la
existente en pases desarrollados y la que existe en pases del tercer mundo veremos
que puede existir un abismo en cuanto al porcentaje sobre nacimientos. Podramos
denominar a esta mortalidad como natural cuando en uno y otro lugar son bien claras
las causas de esta mortalidad? O ms bien hemos de hablar de tasa de mortalidad
de referencia para cada pas?.
De una forma parecida, cada una de las explotaciones tiene unas tasas de mortalidad
basales que dependern siempre de las circunstancias propias de la empresa y de
su capacidad de gestin. Si las asumimos como naturales podemos caer en el error
de pensar que son invariables y no mejorables.
Con esta informacin, podra ser cero la mortalidad natural en una piscifactora?
Las infecciones latentes y las dificultades de diagnstico
Por desgracia para nosotros y a pesar de lo que podamos pensar, el sector de la
sanidad en piscicultura supone solamente una infinitsima parte (en trminos de
inversin, personas trabajando, instalaciones disponibles, informacin generada, etc.)
de lo que representa la sanidad en otros sectores, como la produccin bovina, de
cerdos, de aves, y no digamos la sanidad en animales domsticos (y no hablemos de
la humana) Por ello, el trabajo en patologa de peces supone muchas veces una lucha
constante entre el desaliento que produce esa sensacin de desconocimiento sobre
muchos aspectos de la patologa de los peces y el estmulo que ofrece un campo de
estudio tan abierto.
A pesar de lo que podemos aportar en este curso y en el trabajo diario, son muchos
los aspectos que desconocemos sobre etiologa, patogenia, epidemiologa, prevencin
y tratamiento de las enfermedades de peces. Rara vez disponemos de enciclopedias
de todo el saber o recetas mgicas donde podamos tener mtodos operativos
precisos con resultados garantizados.
Uno de estos problemas derivados de esta falta de conocimientos son las infecciones
latentes. Como infeccin latente o encubierta, en un sentido laxo, podemos incluir a
aquellas infecciones por organismos biolgicos cuyo nivel de presencia es difcilmente
detectable por la tcnicas de diagnstico empleadas. Por ello, de nuevo hay que
reafirmar en que un diagnstico nunca debe basarse en el resultado de una nica
prueba diagnstica sino en el razonamiento de todos aquellos datos disponibles sobre
el contexto total que rodea a un grupo de peces.
Un ejemplo claro est en la deteccin de Photobacterium damselae ssp piscicida. Si
bien el diagnstico sobre casos clnicos reales es relativamente fcil mediante las
tcnicas habituales (cultivo), la deteccin de animales portadores en infecciones
latentes, subclnicas o encubiertas es muy difcil y en muchos casos slo las tcnicas
ms sensibles (moleculares o inmunolgicas) son capaces de detectarlas (aunque con
problemas de especificidad y sensibilidad debido a lo fino de la propia metodologa).
11
Manual de Tcnicas Bsicas de Diagnstico Patolgico en Peces - 2005
En muchos de estos casos se ha demostrado que nicamente un test de estrs
previo podr identificar positivamente la existencia de infecciones latentes en
poblaciones de doradas o lubinas.
1.4.- FUENTES DE INFORMACIN
En este apartado recopilamos libros y revistas cientficas especializadas en patologa
de peces y acuicultura, as como enlaces de internet que consideramos pueden
resultar de inters para el conocimiento de este tema tan amplio.
LIBROS
Manual on Hatchery Production of Sea bass and Gilthead Sea bream. FAO, 1999
Aquaculture for veterinarians: Fish husbandry and medicine. Editor Lydia Brown.
Pergamon Press 1993. (Tambin en castellano: Editorial Acribia)
Fish Disease. Diagnosis and Treatment. Noga, E.J. Iowa State University Press /
Ames. 2000
Fish Medicine. Stoskopf, Michael K. W.B. Saunders Company cop. 1993
Manual on Hatchery Production of Sea bass and Gilthead Sea bream. FAO, 1999
Fish Pathology. editor Ronald J. Roberts. Churchill Livingstone. 2001
Fish Diseases and Disorders: Volumes 1, 2& 3. CABI Publishing. 1995, 1998, 1999
What should I do. A practical guide for the marine fish farmer . Bruno D.W.,
Alderman, D.J. and Scholtfeldt H.J. European Association of Fish Pathologists. (En
ingls y castellano).
Bacteria from Fish and Other Aquatic Animals: A Practical Identification Manual.
Buller, N.B. CABI Publishing. 2004
Systemic Pathology of Fish. Ferguson, Hugh W. Ames, Iowa Iowa State University
Press 1989
Applied Fish Pharmacology. Treves-Brown, K.M. Springer, 2000
Anaesthetic and Sedative Techniques for Aquatic Animals 2nd ed. Lindsay G.
Ross and Barbara Ross, Blackwell Science, 1999.
International Aquatic Animal Health Code. O.I.E. 2004
Diagnostic Manual for Aquatic Animal Diseases. O.I E. 2003
Applied Veterinary Epidemiology and the Control of Disease in Populations.
Toma, B. et al. Maisons-Alfort AEEMA. 1999.
12
Manual de Tcnicas Bsicas de Diagnstico Patolgico en Peces - 2005
REVISTAS CIENTFICAS
Aquaculture
http://www.elsevier.com/wps/find/journaldescription.cws_home/503302/description
Aquaculture International
http://www.ingentaconnect.com/content/klu/aqui
Bulletin of the European Association of Fish Pathologists
http://www.eafp.org/bulletin.html
Diseases of Aquatic Organisms
http://www.int-res.com/journals/dao/
Fish & Shellfish Immunology
http://www.elsevier.com/wps/find/journaldescription.cws_home/622832/description
Journal of Aquatic Animal Health
http://afs.allenpress.com/afsonline/?request=index-html
Journal of Fish Biology
http://www.blackwell-synergy.com/loi/jfb
Journal of Fish Diseases
http://www.blackwell-synergy.com/servlet/useragent?func=showIssues&code=jfd
ENLACES DE INTERNET
Agencia Espaola del Medicamento
http://www.agemed.es/
Agencia Europea de Evaluacin de Medicamentos
http://www.emea.eu.int/
Departamento de pesca de la FAO
http://www.fao.org/fi/default.asp
Diccionario de Bacteriologa Veterinaria
http://www.bacterio.cict.fr/bacdico/garde.html
Taxonoma Bacteriana
http://www.bacterio.cict.fr/index.html
Revista AquaTIC
http://www.revistaaquatic.com/
Observatorio Espaol de Acuicultura
http://www.observatorio-acuicultura.org/
Portal de la Piscicultura en Espaa
http://www.mispeces.com/
13
Manual de Tcnicas Bsicas de Diagnstico Patolgico en Peces - 2005
Federacin Europea de Productores Acucolas
http://www.feap.info/feap/
European Aquaculture Society
http://www.easonline.org/
Asociacin Europea de Patlogos de Peces
http://www.eafp.org/
Organizacin Internacional de Epizootias
http://www.oie.int/aac/eng/en_fdc.htm
AquaFeed
http://www.aquafeed.com/
Aqua-Flow
http://www.aquaflow.org/
IntraFish
http://www.intrafish.com/
UF / IFAS
http://edis.ifas.ufl.edu/
Bases de datos de peces
http://www.fishbase.org/search.cfm
Instituto Nacional de Meteorologa
http://www.inm.es/
Buscadores cientficos
http://www.ncbi.nlm.nih.gov/
Buscadores generales
http://www.google.com/
http://www.yahoo.com/
14
Manual de Tcnicas Bsicas de Diagnstico Patolgico en Peces - 2005
2.- EPIDEMIOLOGA EN SANIDAD PISCCOLA
2.1.- QU ENTENDEMOS POR EPIDEMIOLOGIA?
La epidemiologa es el estudio del estado de salud de las poblaciones o, ms
concretamente, el estudio de la enfermedad y de los factores que determinan su
presentacin y frecuencia en una poblacin. Su objetivo final va a ser la prevencin de
la enfermedad y su control en caso de que sta aparezca.
En el caso de una enfermedad infecciosa o transmisible, existe una interaccin entre el
agente, la poblacin y el ambiente donde vive esa poblacin, que determinar las
caractersticas epidemiolgicas de esa enfermedad. Es lo que se conoce como teora
multifactorial de causa.
Raza
Sexo
Edad
Resistencia
Tropismo
POBLACIN
AGENTE
AMBIENTE
Manejo
Climatologa
Vectores
Las bacterias o parsitos viven en equilibrio con sus huspedes, los peces, y, en
situaciones normales, no va a existir enfermedad. En la piscicultura intensiva, los
factores estresantes son los que frecuentemente van a desplazar la balanza en favor
de los agentes infecciosos y desencadenarn las enfermedades.
Muchos de los problemas patolgicos que nos vamos a encontrar en las instalaciones
pisccolas van a ser resultado de diferentes interacciones entre estos factores
determinantes.
Existen diferentes aproximaciones a las investigaciones epidemiolgicas que,
tradicionalmente, se han denominado tipos de epidemiologa. Estos tipos son
epidemiologa descriptiva, analtica, experimental, operacional, terica...
Sea cual sea el tipo de epidemiologa que apliquemos, el hecho de trabajar con
poblaciones implica necesariamente que los resultados obtenidos deben ser
expresados numricamente. De ello deriva la importancia de la cuantificacin en
epidemiologa.
15
Manual de Tcnicas Bsicas de Diagnstico Patolgico en Peces - 2005
2.2.- CONCEPTOS BSICOS EN EPIDEMIOLOGA
Proporcin y ratio
Existen algunos valores bsicos comnmente utilizados en epidemiologa y que por su
inters deben ser conocidos. Se trata de dos fracciones o medidas relativas: la
PROPORCION y la RATIO.
En la proporcin (o tasa), el numerador forma parte del denominador y en la ratio (o
razn) el denominador no incluye el numerador.
Si a y b son dos poblaciones distintas, la PROPORCIN viene definida por la razn: a/
(a+b), mientras que la RATIO viene definida por la razn a/b.
Ejemplo. Supongamos una poblacin de 8 tiburones de puntas negras (por que no?)
en un acuario de exhibicin, en los cuales tenemos 3 machos y 5 hembras, la
PROPORCION de hembras en el conjunto ser 5/(3+5)= 5/8= 0.625 o 62.5%. En
cambio, la RATIO de hembras respecto a los machos ser de 5/3= 1.6 (la ratio no se
expresa en %)
Descriptores de medida de enfermedad: Prevalencia e incidencia
Con frecuencia prevalencia e incidencia se utilizan como sinnimos y de forma
incorrecta. Sin embargo, cada uno expresa una condicin distinta:
PREVALENCIA indica el nmero de casos de una determinada enfermedad en una
determinada poblacin de riesgo durante un periodo de tiempo (puntual o intervalo).
Es una medida esttica que nos indica la probabilidad que tiene un determinado
animal de esa poblacin de estar infectado.
Por el contrario, INCIDENCIA indica el nmero de nuevos casos de una determinada
enfermedad en una determinada poblacin durante un determinado intervalo de
tiempo. Es una medida dinmica de la velocidad a la que nuevos animales van
enfermando.
Existen tambin otros muchos descriptores de enfermedad, tales como, morbilidad,
mortalidad, tasa de ataque, tasa de mortalidad, tasa de mortalidad especfica, tasa de
letalidad, etc. Las definiciones de todas ellas las podemos encontrar en la bibliografa
recomendada.
2.3.- PATRONES DE ENFERMEDAD
Segn el tipo de presentacin de una enfermedad en una poblacin con relacin al
tiempo, se puede establecer la siguiente clasificacin:
- Endemia (o enzoota): presencia de una enfermedad a niveles constantes a lo largo
del tiempo (incidencia ms o menos estable), o presentacin habitual de la misma en
una poblacin. No se refiere a la cantidad de individuos afectados, si no a la
constancia en la proporcin de individuos.
- Epidemia (o epizoota): presencia de una enfermedad por encima de su nivel
normal o endmico (aumento importante de la incidencia), o partiendo de un nivel nulo
de enfermedad.
- Las pandemias (o panzootas) son epidemias a gran escala que afectan a una zona
muy amplia (diferentes pases)
16
Manual de Tcnicas Bsicas de Diagnstico Patolgico en Peces - 2005
- Presentacin espordica: aparicin irregular y casual de una enfermedad
(incidencia baja)
2.4.- DETECCIN DE ENFERMEDAD
Los mtodos de diagnstico de las enfermedades no son siempre perfectos (o ms
bien dicho, prcticamente no existen mtodos perfectos), por eso a veces se pueden
cometer errores. Cabe la posibilidad de que la prueba clasifique como positivo a un
animal sano (falso positivo), o que lo clasifique como negativo cuando realmente est
enfermo (falso negativo).
Estos errores se pueden cuantificar comparando los mtodos de diagnstico
disponibles con la situacin verdadera (revelada con un test de referencia o golden
standard)
Positivo
Prueba
Negativo
Enfermedad
Positivo
Negativo
Verdaderos positivos
Falsos positivos
VP
FP
Verdaderos
negativos
Falsos negativos
VN
FN
La eficacia de nuestro test se puede expresar mediante las siguientes medidas:
Sensibilidad:
la proporcin de verdaderos positivos que detecta el test
respecto al total de enfermos
Se = VP / (VP+FN)
Especificidad:
la proporcin de verdaderos negativos que detecta el test
respcto al total de sanos
Ep = VN / (VN+FP)
Valor predictivo de los positivos: la probabilidad de que un individuo diagnosticado
como positivo realmente lo sea o
la proporcin de verdaderos positivos respecto al
total de positivos que detecta el test
VP+ = VP / (VP+FP)
Valor predictivo de los negativos: la probabilidad de que un individuo diagnosticado
como negativo realmente lo sea o
la proporcin de verdaderos negativos respecto al
total de negativos que detecta el test
VP- = VN / (VN+FN)
17
Manual de Tcnicas Bsicas de Diagnstico Patolgico en Peces - 2005
2.5.- MUESTREOS
A diferencia de otras especies, en ictiopatologa muchas veces nos tenemos que
enfrentar con el estudio de grandes poblaciones de peces. El estudio de poblaciones
reducidas, en las que podemos tomar datos de todos y cada uno de los componentes,
es muchas veces un lujo y slo se produce en algunos casos en la clnica de especies
ornamentales o en los acuarios de exhibicin en especies de alto valor biolgico o
econmico. Por ello muchas veces debemos seleccionar una parte reducida de esa
poblacin para analizarla. Es lo que habitualmente denominamos como muestra.
Cuando realizamos un estudio a partir de una muestra, los valores obtenidos son una
estimacin de lo que realmente sucede en la poblacin. Sin embargo, despus de
obtener estos datos nos puede surgir una pregunta: los resultados obtenidos a partir
de esta muestra pueden ser extrapolados la poblacin general? O, en otras palabras,
sern el reflejo de lo que pasa en esta poblacin? Si la respuesta es no, habremos
hecho un trabajo en vano, por lo cual es importante seleccionar previamente una
muestra adecuada.
Cules son las propiedades que ha de tener una muestra?
La estimacin obtenida a partir de la muestra ha de ser exacta y precisa.
La exactitud nos da una idea de cuanto se acerca nuestra estimacin a los valores
reales en la poblacin. Para que esta estimacin sea lo ms exacta posible, la muestra
ha de ser representativa de la poblacin. Esto lo conseguiremos mediante la seleccin
aleatoria. El muestreo aleatorio nos asegura que cada individuo de la poblacin a
estudiar tiene las mismas posibilidades de ser seleccionado.
Ejemplo: Hacer estudios de prevalencia de enfermedades diagnosticadas en nuestro
Servicio de Diagnstico no sera correcto, pues las muestras que nos remiten no son
representativas de la poblacin general, ya que la mayora provienen de peces
sintomticos que no se han recogido de forma aleatoria.
La precisin nos da una idea de la dispersin obtenida en nuestra estimacin
respecto al verdadero valor en la poblacin. Esta precisin viene determinada por el
tamao de la muestra de tal manera que, aumentando el numero de individuos
muestreados aumentaremos tambin el nivel de precisin, y al revs.
Cmo seleccionamos la muestra?
Bsicamente existen dos mtodos principales para realizar un muestreo:
1. - No probabilstico, intencionado o dirigido: la seleccin de la muestra se realiza por
conveniencia del investigador
2. - Probabilstico: la seleccin se realiza mediante un proceso aleatorio o al azar.
MUESTREOS NO PROBABILSTICOS
Aqu, el encargado de seleccionar las muestras las recoge en funcin de unos
determinados parmetros que esta persona considera importantes. En este caso se
18
Manual de Tcnicas Bsicas de Diagnstico Patolgico en Peces - 2005
pierde representatividad en el muestreo pero se gana tiempo en el procesado de las
muestras ya que normalmente el nmero de muestras a recoger es menor.
En algunos casos este tipo de muestreo intencionado es muy adecuado, como el que
se realiza normalmente para la deteccin de una enfermedad, por ejemplo, en caso
de sospechar de un brote de Vibriosis en lubina. El tcnico evidentemente recoger
peces sintomticos (peces con hemorragias en piel y rganos internos) El resultado
de ese estudio posiblemente pueda confirmar la presencia de Listonella anguillarum y
por lo tanto del brote de Vibriosis, aunque no va a permitir determinar qu cantidad de
poblacin se encuentra afectada. Seguramente si calculramos la prevalencia a partir
de estas muestras tendramos una sobrestimacin de la misma.
Aunque parezca extrao, no es aconsejable en estos casos seleccionar peces que
presenten una sintomatologa muy acusada o avanzada. Frecuentemente esos peces
presentan problemas secundarios (infecciones por bacterias oportunistas como alguna
Pseudomonas, Aeromonas o algunas vibrionceas, dependiendo del medio) que nos
podrn dificultar mucho el diagnstico.
MUESTREOS PROBABILSTICOS
a) Muestreo aleatorio simple
Las muestras se seleccionan al azar de una poblacin, cada miembro de la cual tiene
las mismas posibilidades de ser elegido. Es imprescindible tener una lista de todos los
individuos de la poblacin, lo que se conoce como marco del muestreo. Este mtodo lo
aplicaramos en el caso de considerar que toda la poblacin sea homognea o
uniforme.
Ejemplo: Tenemos en una explotacin mayorista de peces ornamentales un stock de
neones repartidos en doce tanques a los que queremos chequear de una determinada
enfermedad (por ejemplo, presencia del microsporidio Pleistophora). Cada tanque esta
numerado del uno al doce y el modelo de muestreo nos dice que es necesario
chequear cuatro de los doce tanques. Lo que podemos hacer para seleccionar estos
tanques es utilizar tablas de nmeros aleatorios o bien aplicar la funcin matemtica
random existente en muchos programas informticos. Lo mismo se puede aplicar a
peces, asignando un nmero a cada uno (aunque esto lo reservaramos tal vez para el
caso de tener peces de alto valor, como en el caso de reproductores o peces de
exhibicin.
b) Muestreo aleatorio sistemtico
Cuando no disponemos del marco del muestreo, se puede aplicar un mtodo
sistemtico, que ms o menos viene a ser seleccionar animales mediante un
determinado orden preestablecido, aunque iniciado al azar. Por ejemplo, podemos
recoger peces a intervalos determinados (lubinas) durante todo el proceso de
clasificacin de una jaula. Sin embargo, cuando se utiliza este mtodo es muy
importante que se muestree durante todo el proceso. Si se recogen peces slo en la
primer parte del muestreo corremos el riesgo de que la muestra contemple los
primeros peces recogidos y que siempre suelen ser los que se dejan coger mas
fcilmente (peces enfermos).
19
Manual de Tcnicas Bsicas de Diagnstico Patolgico en Peces - 2005
c) Muestreo aleatorio estratificado
En este caso realizamos un muestro aleatorio dentro de unos estratos de la poblacin
que se han definido previamente. Un estrato sera un subgrupo dentro de la poblacin
ms homogneo respecto a unas caractersticas concretas, como la edad, origen,
peso.
Existen tambin otros modelos ms complicados, aunque a efectos prcticos slo se
requieren en el caso de estudios epidemiolgicos determinados.
Qu tamao de muestra necesitamos?
La respuesta a esta pregunta es compleja, pues cada tipo de estudio epidemiolgico
tiene unas necesidades tamao de muestra especficas derivadas de los clculos
estadsticos a aplicar. Tambin depende de criterios especficos en cada caso, como
la prevalencia esperada, nivel de confianza del test, poblacin de muestreo, etc.
Existe un software informtico especfico que podemos utilizar para realizar el clculo
del tamao de la muestra, como el STATCALC o WINEPISCOPE.
Podemos expresar algunos casos prcticos sencillos, pero muy frecuentes, en los que
se puede obtener un nmero de muestra concreto.
a) Confirmaciones rutinarias de enfermedad
El primer caso es el de confirmaciones de rutina de existencia de una determinada
enfermedad en una explotacin ante unos determinados problemas. Cuntas
muestras hemos de recoger? En general, consideraremos que es razonable
seleccionar un nmero mnimo de:
Peces mayores de 100-150 gramos
Juveniles (5-150 gramos)
Alevines y larvas (<5 gramos)
5 ejemplares
10 ejemplares
20 ejemplares
Considerando siempre que se recogen peces que se consideran enfermos o
representativos del problema que estamos observando (muestreo dirigido). Con este
nmero de ejemplares y utilizando las tcnicas diagnsticas adecuadas en la mayor
parte de los casos se llega a comprobar la enfermedad.
b) Deteccin de la presencia de enfermedad en una poblacin
Este es el supuesto de un estudio de control sanitario en el que consideramos una
poblacin de peces en la que queremos comprobar la presencia / ausencia de una
determinada enfermedad. En este caso, el tamao de muestra va a depender de:
a) El tamao de poblacin
b) Prevalencia supuesta de la enfermedad
c) Nivel confianza del test
20
Manual de Tcnicas Bsicas de Diagnstico Patolgico en Peces - 2005
En este caso, suponiendo que la tcnica diagnstica tiene una sensibilidad total, nos
aseguramos que recogiendo ese nmero de muestras y con un nivel n de confianza
determinado detectaremos al menos un pez enfermo, en el caso de que exista
enfermedad.
Para calcular al tamao de la muestra podemos utilizar una complicada frmula o, ms
fcilmente, utilizar las tablas apropiadas. A continuacin resumimos una de ellas, con
un nivel de confianza del 95% (uno de los ms razonables).
P
0.1%
0.5%
1%
10%
100
----95
25
500
--349
224
28
1000
950
450
258
28
5000
2253
563
289
28
Tamao de la poblacin
10000 25000 50000
2587
2822
2906
580
591
595
294
295
296
28
28
28
100000
2950
596
296
28
500000
2985
597
296
30
1.106
2990
598
296
30
Como comprobamos en la tabla, a medida que la poblacin a examinar se hace
mayor, el nmero de peces a muestrear se reduce proporcionalmente. Evidentemente,
a menor prevalencia supuesta de la enfermedad, mayor esfuerzo de muestreo se
deber realizar.
c) Medida de la prevalencia de una enfermedad en una poblacin
En el caso de que queramos determinar la prevalencia de una enfermedad en una
poblacin el tamao de la muestra va a depender de:
a)
b)
c)
d)
El tamao de poblacin
Prevalencia esperada de enfermedad
La precisin o error
Nivel confianza del test
Tambin podemos aplicar la frmula adecuada o una serie de tablas que nos van a
relacionar el tamao de la muestra a elegir, con la precisin deseada y la prevalencia
esperada. Si desconocemos este ltimo valor, se asumir una prevalencia del 50% y
escogeremos el mayor tamao de muestra.
As, para un tamao grande de poblacin y con un nivel de confianza del 95%:
Prevalencia esperada
10%
20%
30%
40%
50%
60%
70%
80%
90%
10%
35
61
81
92
96
92
81
51
35
Precisin absoluta deseada
5%
138
246
323
369
384
369
323
246
138
21
1%
3457
6147
8067
9220
9604
9220
8067
6147
3457
Manual de Tcnicas Bsicas de Diagnstico Patolgico en Peces - 2005
Si nuestra poblacin total de animales es pequea, aplicaremos la siguiente frmula
una vez obtenido el tamao de la muestra requerido a partir de las tablas:
1/n=1/nt+1/N
donde
n: tamao de la muestra
nt: numero obtenido en la tabla
N: tamao de la poblacin
Errores en la toma de muestras
En un estudio epidemiolgico podemos encontrar dos tipos de errores, errores
aleatorios o errores sistemticos (sesgos). La suma de ambos nos da el error total
producido en el estudio. Ambos tipos se pueden producir en las diferentes fases del
estudio, al muestrear, al observar o medir los datos y al procesarlos.
En el muestreo podemos provocar un error aleatorio al escoger un tamao de muestra
inadecuado (imprecisin); o un error sistemtico o sesgo al no utilizar la seleccin
aleatoria de las muestras (no representatividad).
En nuestros estudios epidemiolgicos ser muy importante no sesgar las muestras
mediante malas prcticas de muestreo. Aqu exponemos algunos ejemplos de los
sesgos ms frecuentes en la toma de muestras:
1. Recoger peces mediante salabre si antes no se han concentrado:
- Los peces no son tontos y huyen cuando ven el salabre. Si vamos recolectando
peces de esta manera es muy probable que estemos seleccionando peces con
problemas en la natacin, peces enfermos, peces deformes, peces con problemas
en la visin, etc
- Si utilizamos un salabre de malla ancha podemos estar seleccionado solo los
peces grandes.
2. Recoger peces slo del fondo, de superficie, cerca de la entrada de agua o cerca
del sumidero: Seguro que recogemos peces enfermos o con problemas.
En ambos casos la muestra no ser representativa de la poblacin total.
Para evitar estos errores (por otra parte MUY frecuentes) recomendamos agrupar los
peces antes de tomar la muestra. En tanques es posible hacerlo mediante redes. Es
muy importante que esta operacin se haga de forma correcta, impidiendo que se
escapen peces. Una vez esta concentrada TODA la poblacin a muestrear (y los
peces estn bien concentrados) coger un salabre mas pequeo y recoger una
submuestra generosa en nmero. Hay que ir con cuidado que al concentrar los
peces no se estratifiquen por pesos. De estas submuestra la volvemos a concentrar y
cogemos al azar el nmero de ejemplares necesarios.
Evidentemente estas son las recomendaciones tericas, pero es muy importante
indicar que en muchos casos las operaciones de concentracin de los peces y toma
de muestras aleatoria tienen una logstica muy complicada (sobre todo en tanques
grandes, estanques de grandes dimensiones y en especial en jaulas en mar abierto),
lo que muchas veces dificulta o impide la realizacin de muestreos en condiciones.
22
Manual de Tcnicas Bsicas de Diagnstico Patolgico en Peces - 2005
2.6. INVESTIGANDO LAS CAUSAS DE ENFERMEDAD
Podemos determinar la existencia de relaciones entre la presencia de un problema o
patologa y la presencia o ausencia de determinados factores?. Efectivamente, existen
una serie de estudios analticos que nos pueden indicar si hay relacin entre un
determinado factor y el desarrollo de una determinada enfermedad. Generalmente
estas relaciones se establecen a travs de una serie de estudios estadsticos
realizados a partir de modelos de estudio predeterminados.
Existen dos tipos de estudios analticos, los estudios observacionales y los estudios
experimentales.
En los estudios observacionales slo se observa y no existe intervencin del
experimentador. Los grupos se distribuyen a posteriori y no de forma aleatoria. Existen
tres tipos: transversales, casos-controles y de cohortes.
En los estudios experimentales existe una distribucin a priori y de forma aleatoria
por parte del experimentador. Existen tres tipos: ensayos clnicos, pruebas de campo y
ensayo comunitario de intervencin.
No es objetivo de este curso el explicar para que sirven, como se estructuran y como
se realizan. Para ello es aconsejable consultar con un especialista en epidemiologa o
bien consultar las obras y referencias citadas en la bibliografa.
23
Manual de Tcnicas Bsicas de Diagnstico Patolgico en Peces - 2005
3.- PROTOCOLOS GENERALES DE DIAGNSTICO
De forma terica, en el proceso de diagnstico se pueden definir diferentes niveles de
actuacin aunque, en la prctica, muchas veces se realizar de forma conjunta.
Niveles de actuacin
1
2
3
4
5
6
7
8
Informacin bsica y situacin epidemiolgica general
Historia clnica y anamnesis
Examen "in situ"
Seleccin y envo de muestras
Anlisis directo de los peces
Pruebas rpidas directas
Anlisis complementarios
Diagnstico e interpretacin de los resultados
3.1.- INFORMACIN BSICA Y SITUACIN EPIDEMILOGICA GENERAL
Como comentamos al principio del manual en el apartado del contexto informativo
general, slo reconocemos aquello que conocemos. Por ello es fundamental adquirir
una serie de conocimientos bsicos si nos vamos a enfrentar con un problema
patolgico en una explotacin acucola. Esta informacin y formacin continuada
deber ser tanto sobre enfermedades de peces en particular, como de los sistemas de
cultivo en general. Sin olvidarnos de la biologa, nutricin y alimentacin, hidrologa,
etc.. Hay que estar siempre muy al da !
Fuentes de informacin? Como ya comentamos antes, cursos, congresos, libros,
revistas e internet (imprescindible en los tiempos que corren)
3.2.- ANAMNESIS E HISTORIA CLNICA
El primer paso a dar cuando nos enfrentamos ante el problema, es recopilar la mayor
cantidad de informacin posible sobre el mismo y registrarla en una ficha o historial
clnico para su posterior anlisis. Nuestra experiencia nos dice que, la mayora de
veces, esos datos sern imprescindibles para llegar a la causa final del problema. Al
final del manual incluimos un modelo de ficha clnica.
A la hora de obtener la informacin necesaria es fundamental la aportacin del
personal que est cada da en contacto con los animales: Piscicultor, alimentador,
buzo o cuidador. Ellos, que saben cual el estado normal de los peces, pues los
observan cada da, saben cmo se comportan y como se alimentan. Cualquier
desviacin de esa normalidad nos debe ser notificada inmediatamente.
24
Manual de Tcnicas Bsicas de Diagnstico Patolgico en Peces - 2005
La formacin y educacin en salud del personal de la granja es fundamental dentro del
programa rutinario de gestin sanitaria. Haciendo una comparacin con un las filas de
un ejrcito, ellos son la vanguardia, la primera lnea del frente. Normalmente sern
los primeros en detectar que existe un problema.
Aqu mostramos un ejemplo de una lista de preguntas a realizar durante nuestra
anamnesis:
Sobre la instalacin y el problema observado:
-
Caractersticas del sistema de cultivo: Jaulas, esteros.
Localizacin geogrfica.
Situacin dentro de la granja de las unidades afectadas
Historiales de enfermedades previas
Especies afectadas: Si tenemos ms de una en nuestra instalacin
Rango de tallas afectadas: Tamao, edad
Alimentacin: Tipo y pautas
Problema especfico que se ha observado: Mortalidad, mal crecimiento, anorexia
Desde cundo se observa ese problema
Da donde ha comenzado el problema: Sndrome del fin de semana
Condiciones ambientales y climatologa previa al problema.
Historial previo de situacin de estrs: Movimientos, clasificaciones
Tratamientos teraputicos y vacunaciones administradas
Temperatura: Niveles de riesgo, variaciones bruscas
Evolucin en el tiempo de la mortalidad: Aguda, crnica, intermitente.
Sobre los peces:
-
Respuesta a estmulos: Alimentacin, captura
Distribucin de los peces en el agua: Aislados, en grupo, en superficie
Alteraciones de la natacin: Ataxia, errtica, en crculos, rascado
Alteraciones de la actividad respiratoria: Rpida, lenta
Alteraciones en el aspecto externo
Se observa alguna lesin interna
Y finalmente:
Alguna sospecha por parte los cuidadores de los animales?
Parece una lista demasiado amplia, pero hay que insistir y no debemos preocuparnos
por bombardear a preguntas para obtener los datos que creamos necesarios para
realizar nuestro diagnstico. Aunque nosotros realizaremos nuestras tcnicas de una
forma ordenada, sistemtica y completa, es fundamental que antes de empezar a
examinar los peces tengamos una idea en mente del problema al que nos
enfrentamos.
25
Manual de Tcnicas Bsicas de Diagnstico Patolgico en Peces - 2005
3.3.- EXAMEN IN SITU
Cuando sea posible, siempre es recomendable examinar a los peces directamente en
el medio donde se encuentren. Es este captulo veremos cmo vamos a manipular los
peces para su posterior anlisis, segn si los podemos sacrificar o no y cmo vamos a
identificar los trastornos de salud mediante nuestra anamnesis previa y la observacin
clnica de los peces en el agua
Manipulacin de los animales
La manipulacin que realizaremos sobre los peces es distinta segn si:
a) El pez va a ser sacrificado.
b) El pez no va a ser sacrificado.
MANIPULACIN CON SACRIFICIO
Si el pez va a ser o puede ser sacrificado para su anlisis, entonces hay que proceder
lo antes posible al sacrificio del mismo. El sacrificio de los animales puede realizarse
de diversas formas:
-
Mediante una sobredosis de anestsico: Pueden utilizarse los mismos anestsicos
que indicamos en el apartado siguiente, en dosis altas de sacrificio. En algunos
casos (sobre todo si no se conoce bien este procedimiento) se deben aplicar a
continuacin otros mtodos para asegurar la muerte clnica del pez y evitar que el
pez despierte en el caso que hayamos utilizado una dosis o un tiempo incorrecto.
Mediante decapitacin, seccionando la mdula espinal a la salida del crneo. Esta
operacin puede realizarse mediante un instrumento afilado, como un cuchillo,
bistur, tijeras En estos casos es aconsejable sedar primero los peces con una
dosis baja de anestsico.
Mediante concusin: golpeando la base del crneo mediante un golpe seco contra
una superficie roma y dura (canto de una mesa, madera)
Por fro: inmersionando los peces en agua cercana a 0C.
Cada uno de estos mtodos presenta una serie de ventajas en inconvenientes:
En el caso de la sobredosis de anestsico: Es el mtodo recomendado para
asegurar un sacrificio ajustado a los cnones de tica en el manejo animal. Los
animales mueren sin sufrimiento en un plazo de tiempo razonablemente corto.
Tambin se evitan algunas alteraciones debidas al manejo (hemorragias). Como
inconvenientes tiene el precio del anestsico (poco significativo si se usan productos
asequibles como el fenoxietanol o el aceite de clavo) y que algunos parsitos se
pueden llegar a desprender durante el proceso de la anestesia y pueden llegar a ser
pasados por alto.
En los casos de concusin y decapitacin: Son un mtodo rpido y econmico si se
efectan con rapidez y eficacia, aunque son menos recomendables desde el punto de
vista del bienestar animal, especialmente en el caso de que no ser suficientemente
diestro. Combinados con anestesia suelen ser ms indicados. Estas tcnicas producen
artefactos en las muestras para histopatologa (telangiectasias debido a la dilatacin
de vasos debida a la sobrepresin sangunea ejercida durante la operacin de
sacrificio.
26
Manual de Tcnicas Bsicas de Diagnstico Patolgico en Peces - 2005
El sacrificio por fro (aadiendo hielo al agua o refrigerando sta) es el mtodo
utilizado habitualmente en explotaciones comerciales ya que permite sacrificar gran
cantidad de peces en poco tiempo, disminuyendo relativamente el estrs y permitiendo
bajar rpidamente la temperatura del pescado para asegurar la calidad nutricional y
sanitaria de los mismos. Este mtodo se basa en que al ser los peces organismos
poiquilotermos, al disminuir la temperatura ambiente tambin disminuye su
metabolismo.
Tambin existen otros sistemas menos utilizados como el sacrificio con dixido de
carbono (aadiendo bicarbonato) o mediante electrocucin, mtodos ms cruentos
aunque en algunos casos tambin son prcticos
Una vez hayamos comprobado la muerte de los animales podremos empezar con el
resto de protocolos de diagnstico.
MANIPULACION SIN SACRIFICIO
Cuando debamos obtener muestras de animales que no van a ser sacrificados hemos
de considerar que su manejo debe de ser especialmente cuidadoso, ms an es
especies clsicamente sensibles como la mayora de los peces ornamentales marinos
y algunas especies comerciales como las lubinas. A continuacin indicamos algunas
de las medidas que hemos de tomar:
-
Sedacin y/o anestesia:
Para asegurar una buena manipulacin de los animales es muy importante
tranquilizarlos o anestesiarlos previamente. Con ello evitaremos la produccin
de lesiones al manejarlos (recordemos que son extremadamente resbaladizos),
podremos obtener ms fcilmente muestras de sangre o biopsias y evitaremos
en parte la generacin de respuesta de estrs debida al manejo y que puede
comprometer seriamente su recuperacin posterior. Ms adelante explicamos
de forma resumida qu anestsicos podemos utilizar.
Manejo: Para manejar los animales hemos de tener en cuenta que su piel es
mucho ms sensible que la de los mamferos debido a la presencia de moco, la
delgadez de la epidermis y la falta de queratina. Por ello, durante la manipulacin
de los peces los peores enemigos son: las abrasiones de la piel, la prdida de
moco y la deshidratacin.
- Para evitar las abrasiones es aconsejable o bien manipular los peces con
guantes de plstico o ltex. En caso de no disponer de ellos, recomendamos
humedecer las manos unos 30 segundos con el fin de reblandecer la queratina
de la piel de la mano y hacerla menos spera. Personalmente recomiendo este
tipo de manejo para especies muy resbaladizas (anguila, trucha) cuyo manejo
con guantes puede verse dificultado. Sin embargo, el uso de guantes es
recomendable por motivos higinicos y para la prevencin de algunas de las
escasas zoonosis transmisibles en peces como las Micobacteriosis.
- Para evitar la prdida de moco evitaremos realizar las operaciones de manejo
sobre superficies rugosas o absorbentes. Buscaremos superficies lisas,
impermeables y a poder ser no duras. Hemos de evitar en lo posible el uso de
esponjas, bayetas, toallas o papeles y utilizar plsticos y bases de goma.
Evidentemente estas superficies son ms resbaladizas pero a su vez son
menos traumticas
-
27
Manual de Tcnicas Bsicas de Diagnstico Patolgico en Peces - 2005
Para evitar la deshidratacin es necesario mantener hmeda la superficie del
pez. Como norma general hemos de evitar trabajar en ambientes con aire
acondicionado ya que resecan con mayor facilidad al pez. Tambin es
conveniente humedecer cada 2-3 minutos el cuerpo del pez e incluso puede
rodearse al mismo con un plstico fino (tipo plstico transparente de uso
alimentario) para evitar su desecacin si la operacin va a durar varios
minutos.
En algunas especies (por ejemplo en el rodaballo) es especialmente
beneficioso tapar los ojos a los peces con un plstico para facilitar su
tranquilizacin.
SEDACIN Y ANESTESIA
Existen distintos productos que podemos utilizar para sedar o anestesiar a los peces.
Generalmente el mismo tipo de producto anestsico tiene propiedades de sedacin,
utilizado a dosis menores o con menores tiempos de induccin. Normalmente estos
productos se aaden al mismo agua.
Para una correcta anestesia o tranquilizacin hemos de considerar los siguientes
puntos:
- Hemos de sedar /anestesiar los peces en un pequeo volumen de agua y dejar un
recipiente con suficiente cantidad de agua sin anestsico para su recuperacin.
- La recuperacin en el caso de anestesia por inhalacin (anestsico en el agua) la
recuperacin se realiza de forma rpida despus de transferir los peces a agua sin
anestsico. Se puede forzar esta recuperacin forzando la natacin a
contracorriente, ponindolos debajo de un chorro de agua o un burbujeo fuerte.
- La solucin anestsica debe estar a la misma temperatura que el agua de origen.
- El anestsico debe mezclarse de forma eficiente con el agua (muchos anestsicos
son bastante hidrfobos)
- Hemos de observar los distintos movimientos de los peces durante la induccin, lo
que nos indicar el plano de sedacin o anestesia que se encuentra. Estos
comportamientos se definen en la siguiente tabla:
ESTADIO
I
II
PLANO
1
ESTADO
Sedacin ligera
Sedacin profunda
Anestesia ligera
Anestesia profunda
COMPORTAMIENTO
Tras un pequeo periodo de aparente
excitacin,
los
peces
reducen
sus
movimientos.
Los peces estn prcticamente quietos y slo
responden a estmulos fuertes. La analgesia
es ligera
Los peces empiezan a perder el equilibrio,
pero luchan por no ponerse de costado. La
analgesia es total
Los peces se echan de costado, al levantarlos
la cola y las aletas caen hacia abajo.
Respiracin espordica
Completa ausencia de tono muscular y
respuesta a estmulos.
III
Anestesia quirrgica
IV
Colapso medular (eutanasia)
28
Cese de la respiracin durante varios minutos.
Paro cardaco.
Muerte del animal
Manual de Tcnicas Bsicas de Diagnstico Patolgico en Peces - 2005
Para las manipulaciones habituales como por ejemplo para la toma de sangre es
suficiente con una anestesia ligera. Para la toma de biopsias recomendamos una
anestesia profunda o quirrgica.
Los productos utilizado ms habitualmente son MS-222, Benzocaina, Quinaldina,
Fenoxietanol y aceite de clavo (eugenol). Las dosis y tiempos de induccin son
extremadamente variables entre especies, tallas y dependiendo del plano de anestesia
que queramos conseguir, por lo que vamos a expresar slo valores orientativos en el
siguiente cuadro. Para ms detalles recomendamos las obras de de Ross & Ross
(1999), Noga (1996) y Stoskopff (1992).
PRODUCTO
MS-222
Benzocana
Quinaldina
Fenoxietanol
Aceite de clavo
DOSIS ORIENTATIVAS
10-250 mg/L
10-500 mg/L
1-100 mg/L
0.1-0.4 mg/L
0.1-0.5 mg/L
BIOPSIAS
La toma de muestras de tejidos vivos a partir de peces tranquilizados o anestesiados
no es tan difcil ni infrecuente en la prctica clnica.
Las biopsias ms habituales son las de piel y aletas debido a su fcil accesibilidad y a
que son relativamente poco agresivas. Generalmente se realizan mediante las
tcnicas de raspado de piel y aletas y la excisin de trozos de aleta. La tcnica del
raspado de piel es la misma que se describe ms adelante, con la salvedad de que
debe realizarse de forma ms cuidadosa y no agresiva que sea posible. En el caso de
las aletas normalmente pueden cortarse sin ms problemas (no suele haber sangrado
en los telesteos si no se cortan desde la base).
Otra tcnica de biopsia que puede realizarse sin demasiado problema es la biopsia
branquial. Con el animal suficientemente sedado o anestesiado, y mediante unas
tijeras finas podemos cortar una pequea porcin de filamentos branquiales a nivel del
tercio proximal del arco branquial. Debido a que se trata de un rgano fuertemente
vascularizado, despus de la excisin la branquia seccionada suele sangrar.
Personalmente utilizo una ligera cauterizacin con un instrumento metlico fino
(frceps, pinzas) calentado moderadamente con un mechero, para cortar la
hemorragia, aadiendo sobre esa zona una pomada drmica mezclada con antibitico
(sulfamidas) en polvo para evitar en lo posible la infeccin en esa herida. Sin embargo,
en muchos de los casos, la herida coagula rpidamente si ms en contacto con el
agua.
Una vez obtenidas, la biopsias de piel o branquia pueden mantenerse durante un corto
tiempo en solucin salina o suero fisiolgico, aunque deben ser siempre examinadas
lo antes posible. Tambin es posible obtener muestras de rganos internos mediante
laparatoma, aunque esta tcnica es ms complicada y no es el objeto de este curso.
29
Manual de Tcnicas Bsicas de Diagnstico Patolgico en Peces - 2005
Identificacin de los trastornos de salud
Como vamos a reconocer que existe una enfermedad en nuestra explotacin? Slo
por que existe mortalidad? NO, GRAVE ERROR: No siempre tenemos que esperar a
que aparezcan la bajas para poder detectar que existe un problema en mi granja.
Como comentamos antes, la experiencia de los cuidadores o alimentadores en el da a
da, siendo capaces de detectar si un pez esta enfermo o normal, es fundamental en
este punto.
HISTORIAL PREVIO
Periodos estacionales de riesgo
En la mayora de explotaciones, la temperatura es fundamental en el
desencadenamiento de las enfermedades. Cada patologa, vrica, bacteriana o
parasitaria, tiene su poca del ao de riesgo. Debemos conocerlas, no slo para poder
estar preparados y saber cundo debemos extremar las medidas de prevencin de
nuestros peces, sino tambin para establecer un diagnstico correcto.
Ejemplo: Si estamos en el mes de enero, con 12C en el agua, y al analizar unas
doradas de nuestras jaulas encontramos unos bazos granulomatosos, podemos estar
ante un brote de Pasteurelosis?
Por otro lado, y si es posible, cuando llegan los momentos ms crticos del ao no est
dems reforzar la comunicacin con nuestros colegas vecinos (otros piscicultores) o
consultar a patlogos expertos para ver como est la situacin de esa enfermedad
concreta tan grave, si la tenemos cerca y estar preparados.
Variaciones medioambientales
Algunas instalaciones estn muy expuestas a las variaciones medioambientales, como
el cultivo en jaulas flotantes en el mar: Fuertes corrientes, temporales, ... Estas
alteraciones muchas veces van ser las responsables de problemas
mecnico/traumticos, que pueden derivar en heridas y contaminaciones por bacterias
Por otro lado, las variaciones de temperatura bruscas, principalmente en primavera y
otoo, suelen desencadenar muchos problemas patolgicos.
Ejemplos:La Vibriosis por Listonella anguillarum en la lubina aparece ms
frecuentemente en primavera, con las variaciones al alza de la temperatura, y la
Pasteurelosis en otoo, con las variaciones a la baja..
El famoso estrs que sufren los peces durante un trabajo rutinario, como un
movimiento o transporte, muchas veces va a desencadenar un problema patolgico
debido a la inmunodepresin consecuente. Es importante destacar que cuanto ms
severa es una situacin estresante, ms tardarn los peces en recuperarse (de 1 a 3
semanas) Durante todo ese periodo la poblacin ser ms susceptible de padecer
infecciones y enfermedades.
30
Manual de Tcnicas Bsicas de Diagnstico Patolgico en Peces - 2005
ALTERACIONES DE LOS PARMETROS PRODUCTIVOS
Es importante recordar que los peces enfermos no suelen comer, y pierden el apetito.
La monitorizacin de los parmetros productivos, como el crecimiento y la conversin,
es fundamental a la hora de detectar un problema.
Si en los muestreos mensuales nos damos cuenta que los peces no han crecido como
deberan, quizs sea una buena idea chequear bien los lotes, por si hubiera algn
problema patolgico subyacente.
CAMBIOS DE COMPORTAMIENTO
Distribucin de los peces en el agua
Los peces en las unidades de cultivo suelen nadar en grupo. Si vemos algunos
aislados y que nadan de forma separada, quizs estn enfermos. Si los peces estn
en superficie boqueando, con los oprculos muy abiertos y en cabecera del estanque
puede ser sintomtico que de que les falta oxgeno (por ejemplo, niveles bajos de
oxgeno en el estanque o por qu no, una parasitosis severa branquial)
Tipo de natacin
Un pez enfermo normalmente nadar de forma lenta y errtica. SI nada en espiral
puede indicar que problema del sistema nerviosos central (por ejemplo, si se trata de
una jaula de lubinas, una posible infeccin por rickettsias e incluso un caso de necrosis
nerviosa viral) Si se rasca contra las paredes de la red o el estanque podra tratarse
de un problema parasitario externo.
Actividad respiratoria
Normalmente los peces afectados por un problema infecciosos suelen tener su
actividad respiratoria ms reducida que sus compaeros sanos. Por otro lado, si
necesita aumentar su aporte de oxgeno sanguneo estar hiperventilando (por
ejemplo, bajn de oxgeno en la unidad o infeccin severa bacteriana branquial )
MORTALIDAD
No slo hay que darse cuenta de que se mueren los peces, sino de cmo se mueren.
Tenemos que estudiar la evolucin en el tiempo de esta mortalidad. Si de un da para
otro nos aparecen mil peces muertos, no existe ningn proceso infeccioso que de un
da para otro tenga ese patrn. Este tipo de mortalidades suelen ser debidas a
alteraciones medioambientales o problemas de estrs sobreagudos (falta de oxgeno,
temporales, accidentes) En general, los procesos agudos suelen estar causados por
virus y algunas bacterias; y los procesos crnicos sern debidos a parsitos y
bacterias. De todas formas es necesario conocer la epidemiologa de cada
enfermedad y saber cul es el patrn de mortalidad caracterstico que que suele
provocar.
31
Manual de Tcnicas Bsicas de Diagnstico Patolgico en Peces - 2005
Distribucin normal de los patgenos en una poblacin
En una poblacin de peces de cultivo tenemos una distribucin normal de tallas, donde
encontraremos una mayora de peces normales, y una serie de cabezas y colas
cuyo nmero normalmente depender de lo bien que est clasificado ese lote.
De la misma manera, encontraremos una relacin con el nivel de agentes infecciosos
que conviven de forma habitual con la poblacin. As en las cabezas su nmero ser
mucho menor que el que podemos encontrar en las colas. Este hecho es fundamental
a la hora de interpretar un hallazgo en nuestro proceso de diagnstico.
Distribucin normal de protozoos ciliados parsitos en una poblacin de doradas
32
Manual de Tcnicas Bsicas de Diagnstico Patolgico en Peces - 2005
3.4.- SELECCIN Y ENVO DE MUESTRAS
Con toda la informacin que estamos recogiendo en la anamnesis y con el examen in
situ, ya podemos seleccionar algunos ejemplares de peces para su anlisis. Hemos
visto que NUNCA esta seleccin se debe hacer al azar, sino que deberemos recoger
peces enfermos y, en su defecto, recin muertos. Es un muestreo siempre DIRIGIDO.
Normalmente en esta muestra se podr detectar la causa de la patologa.
A veces, segn el tipo de instalacin, como las jaulas flotantes, puede ser difcil
recoger las muestras si los peces no estn claramente enfermos. A veces lo ms
fcil es echar un poco de pienso y cogerlos Eso es un error fatal ! En esta muestra,
los peces estarn sanos (recordad la distribucin normal mencionada antes) y
podemos no encontrar el origen del problema. Perderemos un tiempo precioso para
iniciar el tratamiento. Por ello insistimos: Hay que recoger las muestras de forma
correcta y utilizando todo el tiempo que sea necesario. De los bien que se haga
depender el xito de todo el anlisis posterior.
Por otro lado es importante conocer la forma de enviar las muestras segn el tipo de
anlisis a realizar.
No debemos olvidar enviar una historia clnica y, si es posible, AVISAR al laboratorio
donde vamos a enviar ka muestra.
Vivos
Examen directo
+++
Refrigerados
(4C)
++
Congelados
Toxicologa
+++
++
+++
Parasitologa
+++
++
++
++
++
Bacteriologa
+++
++
Virologa
+++
+++
++
Bioqumica,
hematologa
serologa, biologa
molecular
+++
Depende
depende
Depende
Histopatologa
+++
++
+++
Microscopa
electrnica
+++
+++
33
Fijados en
Glutaraldehdo
-
Fijados en
Formol
+
Manual de Tcnicas Bsicas de Diagnstico Patolgico en Peces - 2005
Envos de muestras: Normas generales
La mejor forma de enviar muestras es siempre peces vivos. Si estos peces se han de
transportar durante distancias largas o periodos largos de tiempo antes de llegar al
laboratorio, los peces deben embalarse en buenas condiciones. Estos son algunos
consejos:
-
Deben situarse en bolsas de plstico resistente (si pueden ser dobles, mejor) que
estarn convenientemente identificadas con el nmero de la unidad de cultivo.
Estas bolsas deben llenarse con 1/3 parte de agua (a poder ser, la misma donde
estn los peces)
Las 2/3 partes restantes deben ser llenadas con oxgeno (si se hace con aire, el
oxgeno en agua bajar de forma extremadamente rpida).
Debemos sellar convenientemente la bolsa y depositarla en un contenedor
adecuado. Las cajas de porex suelen ser muy adecuadas por ser relativamente
baratas, resistentes y aislantes. El contenedor puede ser rellenado con virutas o
con papeles para que quede bien encajada.
Pondremos algunas bolsas con hielo encima y debajo de la bolsa con peces para
evitar las subidas de temperatura (importante en verano) o bien bolsas de "calor
qumico" si se prevn temperaturas por debajo de las ptimas de los peces
(especialmente especies tropicales en envos en invierno).
El volumen mximo de biomasa de peces a transportar debe ser como norma no
superior a 1/4 parte del volumen de agua.
No deben enviarse de esta forma peces con peso superior a los 250 gramos ya
que soportan mal este tipo de transporte. Hay que ir con mucho cuidado con enviar
peces enfermos puesto que es posible que no soporten el viaje y lleguen muertos
Si se puede, los peces deben estar en ayunas 24/48 horas para evitar que se
ensucie el agua de transporte.
Para enviar peces refrigerados, utilizaremos las mismas bolsas de plstico donde
introduciremos los peces, SIN AGUA. Las cerraremos bien y las colocaremos en las
cajas de porex o contenderos estanco adecuado. Alrededor colocaremos hielo picado
en otra bolsa o placas congeladoras. Importante: Que no contacten nunca los peces
con el agua. Este ser el sistema de eleccin para peces grandes y enfermos.
O2
h
Envo de peces vvos
Envo de peces refrigerados
34
Manual de Tcnicas Bsicas de Diagnstico Patolgico en Peces - 2005
3.5.- ANLISIS DIRECTO DE LOS PECES
Observacin externa
La observacin externa de un animal puede ser realizada de mltiples formas. Sin
embargo es importante que siempre tengamos en cuenta lo siguiente:
-
Es conveniente que anotemos los parmetros biomtricos ms importantes de los
animales examinados (de todos ellos o de algunos) sobre todo especie, peso, talla
(longitud total, longitud estndar), sexo (si es reconocible), grupo de edad (si se
conoce), origen o estirpe. Estos datos pueden llegar a tener un valor importante
para el estudio epidemiolgico.
Hemos de anotar el aspecto externo y la presencia de cualquier alteracin
observada: Malformaciones, lceras, erosiones, etc. Ms adelante en el captulo
revisaremos las alteraciones ms importantes.
En ocasiones es bastante til utilizar una ficha en la que podemos indicar sobre un
esquema la localizacin y extensin de las alteraciones, como la que presentamos
al final del manual.
35
Manual de Tcnicas Bsicas de Diagnstico Patolgico en Peces - 2005
Necropsia
La necropsia en los peces es el proceso por el cual examinamos mediante una
diseccin sistematizada el aspecto de los rganos internos de los peces. Durante este
proceso podemos aprovechar tambin para incluir la toma de muestras para otras
pruebas. Importante recordar: Hay que ser siempre sistemtico, ordenado y completo.
Atencin : ALGUNAS CONSIDERACIONES PREVIAS
Sin embargo es importante en este punto considerar un aspecto muy importante en el
proceso de necropsia y toma de muestras. Este aspecto particular es la AUTOLISIS y
la HETEROLISIS
La AUTOLISIS es el proceso natural de degradacin de los tejidos despus de la
muerte del animal. Esta degradacin est principalmente determinado por la liberacin
de las propias enzimas (fosforilasas, catepsinas, lipasas, proteasas, etc) de las clulas
del pez que autodegradan los tejidos. El problema es que en los peces este proceso
tiene lugar con una sorprendente RAPIDEZ, debido principalmente que al ser
poiquilotermos, sus carga enzimtica est adaptada a trabajar a la mismas
temperaturas que vive el pez. En cambio, en las aves y mamferos, al ser
homeotermos, despus de la muerte la temperatura corporal disminuye de los 37-40C
hasta temperatura ambiente, lo que hace que disminuya la actividad de los enzimas de
estos animales. Por ello, una vez muerto, la temperatura de los peces sigue siendo la
misma que antes de su muerte, con lo cual no hay cambio de actividad. Por poner un
ejemplo, lo que pasa en los peces es lo mismo que si dejamos un cadaver de un perro
en pleno mes de agosto al sol a 40C: el ritmo en que tarda ese perro en corromperse
sera relativamente similar al de un pez a 20-25C. Adems, es importante aadir que
a ms temperatura, los enzimas actan con mayor rapidez. De ah la importancia de
tomar las muestras tan rpidamente y conservar los peces en hielo. A este fenmeno
hay que aadir que en los peces las proteasas se liberan muy rapidamente de las
vsceras debido a su estructura menos compacta. Adems, el descenso del pH tisular
post-mortem activa an ms la actividad de las proteasas. Por ello la evisceracin
rpida de los peces aumenta mucho la vida til del pescado. Es MUY importante que
tengamos siempre en cuenta estas consideraciones ya que de ello depende en buena
parte que las muestras que podamos obtener tengan una calidad suficiente y no nos
den problemas de falsas lecturas
La HETEROLISIS es el proceso de destruccin del los rganos y tejidos debido a la
accin de microorganismos. En condiciones normales, los microorganismos tienen
dificultad en penetrar en estos tejidos debido a la existencia de barreras fsicas (piel).
Sin embargo, en los peces estas barreras son mucho menos gruesas y adems son
muy alterables debido a la autolisis, como hemos indicado anteriormente. Por ello, la
contaminacin bacteriana y el expolio en los distintos tejidos es mucho ms fcil que
ocurra en los peces una vez muertos. Un caso particularmente dramtico es el tubo
digestivo, el cual contiene habitualmente una microbiota endgena bastante
importante. Como hemos indicado anteriormente, el tubo digestivo y los rganos
internos son muy ricos en proteasas que se liberan de inmediato, afectando
seriamente la integridad de estos rganos, dejando escapar rpidamente los
microorganismos del tubo digestivo, los cuales pueden sembrar por completo y de
forma rpida toda la cavidad abdominal y sus rganos. Algunos autores afirman que
incluso este proceso puede darse durante la agona de los peces. Este fenmeno
adquiere importancia capital en la toma de muestras para microbiologa ya que de no
36
Manual de Tcnicas Bsicas de Diagnstico Patolgico en Peces - 2005
tener cuidado en recoger peces vivos o recin muertos y refrigerarlos de forma
inmediata se pueden cometer errores graves al sembrar a partir que rganos que se
habrn contaminado previamente, enmascarando el verdadero origen del problema.
Este problema sigue siendo an relativamente habitual.
PROCEDIMIENTO DE LA NECROPSIA
Para la realizacin de la necropsia realizaremos las siguientes operaciones:
1- Extraccin del ojo(s) de su(s) rbita(s) y examen interno
2- Separacin del oprculo y exposicin de branquias
3- Apertura de la cavidad abdominal
4- Apertura y exposicin del cerebro
5- Observacin de la musculatura
Como se indicar ms adelante, esta tcnica debe ser modificada si se desean obtener
muestras para pruebas complementarias, especialmente en el caso de bacteriologa.
Material necesario:
Para la realizacin de la necropsia es conveniente utilizar el siguiente material:
- Base de diseccin: Es importante que sea de un material mnimamente rgido, no
poroso, no absorbente, de fcil limpieza y desinfeccin. Nuestra experiencia con
cubetas metlicas y planchas de ltex nos ha dado muy buenos resultados
- Tijeras: Es recomendable tener un juego de tres tijeras: pequeas (de unos 8 cm
aprox.), medianas (mejor curvas, de aprox. 16 cm) y unas tijeras grandes y fuertes (e.g.
"tijeras de pescadero") para el oprculo y los huesos duros de peces de gran tamao.
- Pinzas: Es suficiente con unas pinzas de dientes de ratn y unas pinzas ms finas de
superficie de contacto estriada. Pueden ser tambin de utilidad unas pinzas
hemostticas para separar rganos y tejidos.
- Bistur con hojas de recambio, aunque debido a la menor consistencia de los rganos y
tejidos en los peces nuestra experiencia nos demuestra que hojas de afeitar, cutters o
de cualquier otro tipo son muy tiles para realizar secciones de forma rpida y fcil.
Protocolo de necropsia:
Este es un protocolo general de necropsia. Es vlido para la mayora de los peces
aunque las mltiples morfologas que pueden presentar pueden hacer variar la forma de
realizarlo
Con el animal recostado sobre su lado derecho, realizaremos la necropsia siguiendo los
siguientes pasos:
1.- Extraccin del globo ocular de la rbita. Lo observaremos y realizaremos una incisin
en su plano medio para evidenciar su interior. Nos fijaremos en su forma, la presencia
de la retina y el cristalino, su aspecto y la presencia de alteraciones como masas
anormales de tejido, sangre, burbujas de aire, opacidad de crnea o de cristalino, etc.
37
Manual de Tcnicas Bsicas de Diagnstico Patolgico en Peces - 2005
2.- Separacin de oprculo y observacin de branquias. Procederemos a cortar el
oprculo, observando tambin su cara interna. Procederemos posteriormente a observar
cada uno de los arcos branquiales observando su color, aspecto y presencia de
formaciones extraas.
3.- Apertura de la cavidad abdominal. Para la apertura de la cavidad abdominal,
procederemos del modo siguiente:
- Realizaremos una incisin a nivel del ano (recomendamos con tijeras),
dirigindonos en unos 45 grados y en direccin craneal hacia la lnea lateral del
ejemplar, siguiendo la incisin cranealmente ms o menos a nivel de esta lnea lateral
hasta llegar a la regin branquial.
- A continuacin, volveremos al ano y realizaremos una incisin en direccin
craneal en la lnea media ventral hasta llegar a la base de las branquias.
- Realizaremos una tercera incisin uniendo los dos cortes en la zona branquial y
podremos levantar la pared abdominal.
Al levantarla, observaremos si hay adherencias y el aspecto que presenta la cara interna
del abdomen. Reconoceremos todos y cada uno de los rganos internos, su color y
aspecto. Retiraremos la vejiga natatoria para exponer mejor el rin. Tambin podemos
cortar a nivel de esfago e intestino posterior y extraer el paquete visceral para su mejor
examen. En este punto observaremos y anotaremos cualquier lesin que aparezca.
Ms adelante del captulo comentaremos las ms importantes que podemos encontrar.
38
Manual de Tcnicas Bsicas de Diagnstico Patolgico en Peces - 2005
4.- Apertura del crneo y exposicin del sistema nervioso central.
Esta tcnica es bastante variable segn la especie y la localizacin del cerebro en sta.
La apertura puede iniciarse por una incisin entre las narinas, para seguir de forma
simtrica hacia la zona superior de cada una de las rbitas oculares. Desde esta zona
hay que seguir cortando el crneo en direccin caudal hasta llegar a la zona de
separacin entre crneo y tronco y unir las dos incisiones paralelas. Posteriormente y
haciendo palanca con las pinzas, levantar cuidadosamente para exponer el encfalo.
39
Manual de Tcnicas Bsicas de Diagnstico Patolgico en Peces - 2005
5- Observacin de la musculatura
Es conveniente tambin levantar la piel de la regin media para observar el aspecto de
la musculatura. Una seccin transversal de la cola del pez puede ser tambin til para
examinar la musculatura. Esta maniobra puede realizarse tambin al inicio del proceso
de la necropsia
Reconocimiento de enfermedad: Diagnstico diferencial de lesiones
CAMBIOS DE FORMA Y COLOR: Deformidades, melanosis (oscurecimiento),
aclaracin, hinchazn, dilatacin abdominal, adelgazamiento
ALTERACIONES EN PIEL: Manchas de color, despigmentacin, hiperpigmentacin,
prdida de escamas, presencia de hemorragias petequiales (puntiformes) y equimosis
(extendidas), burbujas, fornculos, nodulaciones, masas algodonosas y filamentosas,
erosiones, lceras, parsitos macroscpicos.
ALTERACIONES DE LAS ALETAS: Deshilachamiento, erosiones, prdida parcial o total
ALTERACIONES DE LOS OJOS: Manchas de color en la superficie, opacidad corneal,
burbujas, exoftalmia (inflamacin), endoftalmia (hundimiento), masas extraas en el
interior
ALTERACIONES DE LAS BRANQUIAS: Ausencia de arcos y/o filamentos, palidez
(anemia), inflamacin, exceso de mucosidad, hemorragias, manchas de color (blanco,
amarillo, negro, ...), erosiones, necrosis.
ALTERACIONES INTERNAS: Lquido en cavidad abdominal (ascitis), lquido en tubo
digestivo, inflamacin , congestin, hemorragias, nodulaciones, abscesos, granulomas,
parsitos macroscpicos.
40
Manual de Tcnicas Bsicas de Diagnstico Patolgico en Peces - 2005
3.6. - PRUEBAS DIAGNSTICAS RPIDAS
Adems de la necropsia, puede hacerse una observacin con lupa binocular de los
rganos, adems de una serie de pruebas directas que son de realizacin fcil y rpida
que son muy tiles en el diagnstico patolgico en peces, sobre todo en planta. Estas
pruebas son las siguientes:
-
RASPADOS DE PIEL
PREPARACIN EN FRESCO DE BRANQUIA
"SQUASHES" DE TEJIDO: Cerebro y rganos internos
IMPRONTAS DE BRANQUIA
IMPRONTAS DE TEJIDOS
PREPARACIONES DE LQUIDO BILIAR Y ASCTICO
PREPARACIONES DE CONTENIDO INTESTINAL
PREPARACIONES DE MUSCULATURA
Raspados de piel
En los raspados de piel podremos detectar la presencia de ectoparsitos como
protozoos ciliados, monogenea, bacterias, hongos etc. El procedimiento es bastante
simple.
a/ Raspar la superficie del cuerpo y de las aletas del pez a examinar usando una hoja de
bistur o simplemente mediante un portaobjetos. Aconsejamos realizar esta maniobra en
direccin crneo-caudal ya que en direccin contraria podemos levantar demasiadas
escamas (en los peces que las posean) que pueden enmascarar la observacin,
especialmente si no se tiene una cierta experiencia.
b/ Depositar y extender bien el material obtenido sobre un portaobjetos. Cubrir el
material con un cubreobjetos. Con una pipeta o similar, introducir por capilaridad
solucin salina o suero fisiolgico hasta que ocupe la totalidad del espacio por debajo
del cubreobjetos. En caso de no disponer, utilizar agua corriente. Si se utiliza agua
marina, el lquido se evapora rpidamente y se forman cristales de sal que entorpecen la
observacin.
c/ Observar al microscopio, trabajando con el condensador bastante cerrado. Se
observarn de forma normal mucus, clulas epiteliales aisladas o en grupo y escamas.
41
Manual de Tcnicas Bsicas de Diagnstico Patolgico en Peces - 2005
Preparaciones en fresco de branquia
Esta sencilla tcnica puede darnos, con un mnimo de experiencia, bastante informacin
acerca del estado y las patologas de un rgano diana como la branquia.
a/ Tomar uno de los arcos branquiales y separar parte de los filamentos del eje del arco
hasta que se individualicen los distintos filamentos.
b/ Repartir los diferentes filamentos sobre un portaobjetos (que no queden uno sobre
otro), cubrir con un cubreobjetos e introducir solucin salina de la misma forma que
describimos en el raspado de piel.
c/ Observar al microscopio, trabajando con el condensador bastante cerrado.
Observaremos tanto el interior de las branquias como su contorno y las zonas
adyacentes. Podemos ayudarnos de soluciones de lugol para identificar parsitos como
Oodinium y Amyloodinium.
"Squashes de tejido
Esta tcnica est especialmente indicada para la deteccin de parsitos en los rganos.
a/ Cortar una seccin fina y de pequeo tamao del tejido a examinar.
b/ Cubrir con un cubreobjetos haciendo presin suave hasta que vemos que el tejido se
expande e introducir solucin salina de la misma forma que describimos en el raspado
de piel.
c/ Observar al microscopio
42
Manual de Tcnicas Bsicas de Diagnstico Patolgico en Peces - 2005
Improntas de branquia y tejidos
En estas muestras se pueden observar la presencia de parsitos y bacterias en los
diferentes tejidos.
a/ Cortar un trozo pequeo del rgano o branquia a examinar y con unas pinzas
presionar varias veces con este trozo sobre la superficie de un portaobjetos, hasta que
veamos que deja una huella.
b/ Dejar secar al aire o secar a la llama
c/ Teir con las coloraciones habituales. Particularmente rpidas son las tinciones de
Giemsa, Diff-Quick y especialmente la tincin de GRAM
d/ Observacin al microscopio. A 1000x aumentos, si existe una infeccin bacteriana
activa, las bacterias puedes ser observadas claramente. Hay que prestar atencin a su
morfologa, tamao y disposicin dentro de los rganos.
Ejemplos de bacterias que se pueden observar:
GRAM negativa, bacilos muy largos, formaciones en red: Tenacibaculum maritimum
GRAM negativa, bacilos muy cortos, tincin bipolar, agrupados, intracelulares:
Photobacterium damselae sp piscicida.
GRAM negativa, bacilos largos, forma de coma: Vibrios
43
Manual de Tcnicas Bsicas de Diagnstico Patolgico en Peces - 2005
Preparaciones de lquido biliar, asctico y contenido intestinal
Tambin el examen del lquido asctico, bilis o contenido intestinal pueden aportar
informacin. En lquido asctico podremos observar la presencia de clulas inflamatorias,
macrfagos con bacterias, bacterias libres, hongos, etc. En la bilis y contenido intestinal
podremos observar la presencia de parsitos (sobre todo mixosporidios) y algunos
microorganismos (aunque considerando siempre la posibilidad de contaminacin
retrgrada de la bilis procedente del tubo digestivo)
Ambos lquidos pueden recogerse mediante una puncin con aguja. El lquido asctico lo
trataremos como si fuera para realizar una extensin de sangre mientras que el lquido
biliar lo depositaremos en un portaobjetos, pondremos un cubreobjetos y lo
examinaremos directamente al microscopio.
Para el examen del contenido intestinal, cortaremos una seccin del intestino y
realizaremos un raspado de la mucosa, depositando este material en un portaobjetos, lo
cubriremos y examinaremos.
Preparaciones de musculatura
Para los casos de control de parsitos en musculatura podemos aprovechar la tcnica
que se utiliza para el control de Triquinas en el msculo de cerdo. Consiste en dos
placas de cristal (placas de triquina) que se unen a presin con unos tornillos. La
muestra de musculatura se introduce entre ambos cristales y se hace presin con los
tornillos para que se extienda bien. Observando esta placa en la lupa se puede observar
la presencia de quistes de parsitos, nematodos, etc.
Otra forma ms sencilla consiste en cortar un trocito pequeo de msculo donde
sospechemos que estn los parsitos y lo colocaremos entre dos portaobjetos o entre
un porta y un cubreobjetos. Examinaremos a condensador cerrado.
3.7.- ANALISIS COMPLEMENTARIOS
En los protocolos de diagnstico muy frecuentemente necesitaremos de otros tipos de
estudios ms particularizados con el objetivo de evidenciar la implicacin de agentes
biticos o abiticos en el proceso patolgico detectado.
Sin embargo, el objetivo de este manual no es explicar todas y cada una de las
tcnicas disponibles en cada especialidad, sino sencillamente indicar cules son,
para qu nos pueden servir y sobre todo cmo hemos de proceder para poder
obtener las muestras correctamente, en las mejores condiciones posibles y
remitirlas adecuadamente a los laboratorios de referencia que disponemos. Uno
de los problemas ms habituales es que una muestra recogida de forma inadecuada
suele ser no apta para su estudio, lo que hace que aparte de que se pierde tiempo y
dinero, puede inducir a error en el diagnstico, lo que es peor.
Es muy importante seleccionar adecuadamente qu tipo de anlisis necesitamos en
cada caso y an ms importante es la correcta evaluacin de los resultados obtenidos
de stos. Recordemos: NUNCA debemos considerar que un resultado de una prueba
puede tener un valor diagnstico absoluto.
44
Manual de Tcnicas Bsicas de Diagnstico Patolgico en Peces - 2005
ANLISIS DE AGUA
Hay mltiples parmetros que es necesario controlar en el agua, aunque algunos
deben ser comprobados con mayor frecuencia y precisin dependiendo de nuestras
condiciones de trabajo y el riesgo existente. Algunos de estos parmetros son
habitualmente controlados en las instalaciones, mientras que otros deben ser remitidos
a centros especializados (generalmente son las muestras de toxicologa).
Los parmetros que es necesario controlar con mayor detalle son: Oxgeno y
Temperatura
Son los parmetros ms necesarios de controlar con mayor detalle. En estos dos
casos hay que procurar obtener varias lecturas durante el da y ms frecuentemente
an si se sospecha que pueden haber oscilaciones. En estos casos lo ideal es tener
mediciones constantes y registradas acopladas a un sistema informtico de anlisis de
datos y conexin de alarmas.
La falta de oxgeno ha sido tradicionalmente una de las mayores causas de mortalidad
y de generacin de problemas debido principalmente a que los episodios de hipoxia
pueden desarrollarse de forma relativamente rpida y si no se efectan los controles
oportunos pueden quedar sin deteccin
Las oscilaciones de temperatura son tambin un fenmeno muy habitual que afecta
seriamente a los peces. En general podemos decir que los cambios de temperatura si
son suficientemente bruscos, afectan a la salud del pez reduciendo la respuesta de
sus sistemas de defensa y alterando su metabolismo durante varios das. Adems hay
que aadir que la temperatura es uno de los factores ms importantes en la
epizootiologa de las enfermedades de los peces
Otros parmetros a controlar de forma peridica sern:
- pH, salinidad, amoniaco, nitritos, nitratos y reserva alcalina
- materias en suspensin, fosfatos, DBO, conductividad, potencial redox, dureza
- saturacin de gases, cloro libre
- carga microbiana del agua: coliformes, mesfilos y estreptococos fecales
Tambin hemos de considerar los anlisis especiales de agua como el de la
presencia y niveles de productos teraputicos (formol, sulfato de cobre, cloro, perxido
de hidrgeno) o de txicos (herbicidas, pesticidas organoclorados,
organofosforados, cianuros, tensoactivos, metales pesados, fenoles, PCBs etc.)
Toma de muestras de agua
En los casos concretos de la temperatura y el oxgeno, las muestras se toman in situ
mediante termmetros / termgrafos y sondas de oxgeno (oxmetros). En el caso
particular del oxgeno es de vital importancia el realizar un mantenimiento adecuado
de los mismos y calibrarlos peridicamente (aunque parezca una tontera, este es un
punto MUY importante y en la prctica se observan todava errores demasiado
frecuentemente).
Para los parmetros indicados posteriormente (pH, salinidad, amoniaco, nitritos y
reserva alcalina) y para buena parte de los descritos posteriormente (cloro, dureza
45
Manual de Tcnicas Bsicas de Diagnstico Patolgico en Peces - 2005
total y fosfatos) o bien se utilizan aparatos especficos (pHmetro,, salinmetro,
densmetro) o bien suelen utilizarse kits comerciales. Estos kits suelen dar bastante
buenos resultados (aunque a veces poco precisos) y son bastante prcticos y rpidos
de utilizar, por lo que se adaptan bien a la prctica diaria de la empresa. Tambin se
pueden determinar mediante valoraciones qumicas, aunque estas tcnicas
generalmente son de difcil realizacin en el centro de trabajo y suelen reservarse a los
laboratorios de referencia. El resto de parmetros pueden determinarse de la siguiente
forma:
En todos los casos es importante que la muestra de agua a recoger sea representativa
de lo que queremos analizar. Tengamos siempre presentes:
- El tiempo: Los sistemas acuticos son dinmicos y lo que en un momento est en
el agua, al cabo de un tiempo corto puede haberse eliminado por el recambio del
agua o haberse degradado.
- Localizacin: La muestra ha de tomarse a distintos niveles (entrada de agua,
salida de agua, distintos tanques, distintas unidades de cultivo, etc)
- Profundidad. Sobre todo cuando se trate de analizar sistemas en grandes masas
de agua (por ejemplo jaulas o estanques ) es importante recordar el fenmeno de
la estratificacin del agua y tenerlo en cuenta a la hora del muestreo del agua.
La cantidad y la forma de conservacin de las muestras de agua pueden variar
notablemente segn el laboratorio y las tcnicas de deteccin empleadas. Aunque la
tendencia es la de utilizacin de tcnicas "miniaturizadas" donde es suficiente un
volumen de muestra pequeo, nuestro consejo es ser generosos con la cantidad de
muestra remitida (1-2 litros de agua suelen ser suficientes en todos los casos para cada
una de las muestras)
Hemos de considerar los siguientes aspectos ya que son de absolutamente
necesarios para poder garantizar por parte nuestra la fiabilidad de los resultados del
anlisis:
-
Recipientes a utilizar: A poder ser, deben utilizarse recipientes limpios, estriles,
opacos y fciles de identificar. Mejor si son de cristal, especialmente en el caso de
determinacin de derivados de petrleo, aunque los envases de Polietileno son
menos frgiles. Como frecuentemente no se dispone del recipiente ideal, hay que
procurar que al menos est limpio.
Llenado de los recipientes: Debe realizarse en el interior del agua y llenarlo hasta
arriba. Esta tcnica se utiliza para evitar la presencia de aire en contacto con el agua
que pueda modificar sobre todo los valores de gases disueltos.
Rotulacin de los frascos: tiene que ser clara, y marcada en el frasco (no en el
tapn).Utilizar marcadores resistentes al agua.
Envo: De forma rpida y mantenida en refrigeracin (4C)
46
Manual de Tcnicas Bsicas de Diagnstico Patolgico en Peces - 2005
TECNICAS BACTERIOLGICAS
Las tcnicas bacteriolgicas o microbiolgicas que habitualmente se precisan en
patologa de peces tienen por objetivo el aislamiento e identificacin a partir de las
muestras de microorganismos (generalmente bacterias) potencialmente implicados en
problemas patolgicos. Tambin comprenden la realizacin de antibiogramas para
comprobar la sensibilidad de esas bacterias de distintos antibiticos.
Las tcnicas ms habituales se basan en la siembra en medios de cultivo adecuados a
partir de las muestras y la comprobacin de la presencia o ausencia de crecimiento de
los microorganismos potencialmente presentes en esa muestra. Posteriormente, los
microorganismos que crecen en estos medios de cultivo se identifican a travs de
distintas pruebas bioqumicas, serolgicas y/o moleculares.
Consideraciones al interpretar los resultados de la microbiologa
La importancia de la contaminacin: El hecho de realizar una siembra a partir de
una muestra de bazo, rin o piel significa que nosotros queremos saber si en esa
muestra existen bacterias que al ser sembradas en un medio de cultivo se revelan en
forma de colonias macroscpicas. En condiciones normales, los rganos internos de
los peces sanos no pueden contener microorganismos y por lo tanto, si obtenemos
crecimiento el razonamiento lgico es pensar en que en esos peces existe una
infeccin que hace que los microorganismos responsables de la misma se encuentren
en ese rgano. Sin embargo la relacin crecimiento / infeccin no es siempre
verdadera. La observacin de crecimiento a partir de la siembra tambin se puede dar
por la existencia de contaminacin. Esta contaminacin puede proceder de:
a) Heterolisis: El estado de la conservacin de la muestra no es adecuada ya
que se ha permitido que bacterias del exterior o del tubo digestivo contaminen
los rganos seleccionados. En el caso de la siembra a partir de heridas
exteriores o lceras, la contaminacin casi siempre proviene de la misma
microbiota del agua.
b) Contaminacin iatrognica: Corresponde a la contaminacin producida por
una necropsia mal realizada y/o por la manipulacin incorrecta de las muestras,
sin guardar la debida asepsia. Por ello, si en la necropsia pensamos en tomar
muestras para microbiologa hemos de tener mucho cuidado con la esterilidad
del material y de no contaminar los rganos durante el proceso de la necropsia
(por ejemplo, romper el tubo digestivo y vaciar su contenido sobre los rganos
abdominales).
La eleccin del medio adecuado: Cada medio de cultivo presenta unas
caractersticas especficas que permiten el crecimiento de los microorganismos de una
forma ms o menos selectiva. Siempre hemos de utilizar medios generales como el
TSA (Tripicasa Soja Agar, con sal para peces marinos), MA (agar marino) o medios
generales enriquecidos como el AS (agar sangre) Una inadecuada eleccin del medio
puede dar como consecuencia la ausencia de crecimiento y por tanto un falso no
aislamiento. Por ejemplo, en el caso de las Flexibacteriosis es necesario utilizar
medios especficos (FMM) ya que no suelen crecer en los medios generales.
47
Manual de Tcnicas Bsicas de Diagnstico Patolgico en Peces - 2005
La eleccin de la muestra: En la mayora de los procesos infecciosos por bacterias
existen fases en las cuales el germen puede ser aislado de forma ms o menos fcil.
En las fases de diseminacin o septicmicas es cuando estos microorganismos
pueden ser aislados de forma ms fcil. Sin embargo, en fases muy iniciales o en
fases crnicas pueden acantonarse o disminuir su viabilidad, aunque seguir
presentando sintomatologa o eliminando toxinas. Por ejemplo, en las fases crnicas
de Pasteurelosis, la bacteria queda acantonada en el interior de macrfagos y es
difcilmente cultivable. En el caso de Pseudomonas anguilliseptica en muchos casos
se acantona slo a nivel del sistema nervioso central, no pudiendo ser cultivable a
partir de rin, bazo o hgado.
El uso de antibiticos y desinfectantes: En algunos casos las muestras pueden
proceder de peces que han sido tratados previamente, con lo cual disminuimos la
viabilidad de las bacterias debido al poder bactericida y/o bacteriosttico de los
antibiticos, transformndolos en no cultivables.
Toma de muestras microbiolgicas
Para el envo de muestras de peces al laboratorio de referencia de microbiologa hemos
de procurar enviar peces moribundos o muertos recientemente y que no presenten
externamente signos de autolisis o heterolisis (hinchamiento abdominal por
fermentacin). Los peces deben ser enviados en hielo o refrigerados para evitar el
crecimiento de contaminacin bacteriana.
Sin embargo, tambin podemos procesar los peces y realizar siembras con un equipo
mnimo.
-
Para la toma de muestras necesitaremos la presencia de una llama para poder
trabajar alrededor de la misma en unas mnimas condiciones de esterilidad (pueden
utilizarse mecheros de alcohol o incluso un "camping-gas"), instrumental para
recoger la muestra (asa de platino, asas de plstico estriles, pipetas Pasteur
estriles, hisopos estriles o cualquier otro instrumento afn) y medio de cultivo.
Para iniciar la operacin de toma de muestras, podemos desinfectar la piel del pez
mediante una solucin de hipoclorito o amonio cuaternario, o simplemente retirar el
moco de la zona de incisin mediante un pao o papel absorbente.
A continuacin, procederemos a la apertura de la cavidad abdominal tal y como se
describe en el apartado referente a la necropsia, teniendo la precaucin de utilizar
las tijeras y pinzas desinfectadas pasndolas por alcohol y dejndolo quemar o bien
puede incidirse solamente por su lado ventral para mejorar las condiciones de
esterilidad (en estos casos, unos mondadientes estriles suelen ir bien como
"retractores" abdominales).
Cuidaremos de no puncionar por error los intestinos puesto que facilitara mucho la
contaminacin de la muestra, tal y como hemos indicado anteriormente. Una vez
hemos expuesto los rganos internos, procederemos a la toma de muestras.
Generalmente se toman muestras de rin craneal (pronfrico) y bazo por sus
caractersticas de rganos filtradores y hemopoyticos en los que se reflejan la
mayora de enfermedades bacterianas. Particularmente es preferible sembrar de
rin craneal ya que es un rgano separado de la cavidad abdominal y es menos
48
Manual de Tcnicas Bsicas de Diagnstico Patolgico en Peces - 2005
susceptible a contaminacin procedente del tubo digestivo. Pueden utilizarse
tambin el hgado, cerebro o cualquier otro rgano que pueda presentar lesiones.
En el caso de tomar muestras estos rganos o de lesiones la piel recordemos que
hemos de tener en cuenta que nos encontraremos con importante contaminacin
bacteriana secundaria.
Para tomar muestras de rin craneal pueden traccionarse el paquete visceral con
unas pinzas estriles, punzando si es preciso la vejiga natatoria y dejando al
descubierto el rin. Con el asa de platino al rojo o un escalpelo estril, incidiremos
en la zona media del rin sobre la capa fibrosa que recubre a ste para permitir el
paso libre al parnquima renal. A continuacin, con la punta del instrumento de
recogida (la misma asa, o otra de plstico o una pipeta estril, entraremos en este
corte para recoger una muestra de rin. Debe irse con cuidado de no tocar el resto
de rganos de la cavidad abdominal al entrar o salir de ella.
Inoculacin de medios
Para la inoculacin de placas con los medios utilizamos la misma tcnica en estra que
para otros casos. En casos de mltiples muestras, podemos dividir las placas en
"porciones". Tambin podemos hacer las siembras en tubos con medio lquido ("caldo")
para despus pasarlo a medio slido en placas. Los medios ms frecuentemente
utilizados en peces marinos son los siguientes:
- Medios generales: Agar Marino (MA), Agar sangre (AS), Tripticasa Soja Agar (TSA)
- Medios especficos: TCBS (Vibrios), FMM (Flexibacter maritimus)
Estos medios se pueden realizar ms o menos fcilmente o bien pueden ser adquiridos
ya preparados. En algunos casos, algunos laboratorios prefieren utilizar otros medios
menos habituales y que suelen dar buenos resultados.
Incubacin
En general se consideran temperaturas de incubacin aceptables entre 15 y 30 grados,
siendo 20 y 25 grados las ms aceptables. En caso de no tener estufa, puede dejarse a
temperatura ambiente, aunque los resultados son mucho menos fiables. Normalmente,
si existe una infeccin bacteriana activa, en 24-48 horas ya tendremos un crecimiento
significativo, aunque es recomendable dejar las placas incubando al menos una
semana, pues existen algunos patgenos que crecen ms lentamente, como
Pseudomonas angulliseptica o Tenacibaculum maritimum.
Identificacin y antibiograma
Una vez obtenemos en las placas sembradas, podemos enviar la placa a un
laboratorio de microbiologa para la identificacin del agente en cuestin mediante
tcnicas bioqumicas (API), serolgicas y/o moleculares.
El antibiograma est casi siempre ligada a la identificacin bacteriana, aunque muchas
veces es lo que realmente desea conocer el responsable de los peces. La tcnica
utilizada es la misma que podemos utilizar para diagnstico en otras especies.
49
Manual de Tcnicas Bsicas de Diagnstico Patolgico en Peces - 2005
TECNICAS VIROLOGICAS
Las tcnicas de deteccin virolgica son tal vez el grupo de tcnicas ms complejas,
laboriosas y de elevado coste econmico que requieren de un laboratorio y personal
sumamente especializado (bastante escasos) en este tipo de determinaciones. En este
apartado no abordaremos los protocolos utilizados en el diagnstico virolgico y solo
indicaremos algunos consejos para a la toma de muestras para virologa.
Toma de muestras para virologa
La toma de muestras para virologa frecuentemente debe realizarse aparte de las
tcnicas habituales. Este hecho es debido a las especiales condiciones del muestreo
virolgico. Se debe evitar la contaminacin cruzada por poner en contacto material
infectivo, sobre todo si se muestrean varios grupos, ya que dara lugar a resultados
equvocos.
Las muestras pueden consistir en ejemplares vivos remitidos directamente al laboratorio
de diagnstico virolgico o bien muestras de peces muertos refrigerados o de rganos
como rin, bazo y/o encfalo (ms de 1 g). Estas muestras deben ser recogidas
aspticamente y en envases esterilizados. Posteriormente han de enviarse refrigeradas
en hielo a una temperatura inferior a 10 grados y deben poder ser procesadas antes de
las 48 horas, avisando al laboratorio del envo de las muestras. En el caso de alevines
muy pequeos, pueden ser considerados como rganos. Pueden ser remitidos sin
cabeza ni cola la mayora de las veces.
ANLISIS PARASITOLOGICO
Para la deteccin de parsitos se emplean casi todas las tcnicas diagnsticas que
comentamos en este manual. Normalmente, en nuestro examen directo de los peces y
con las pruebas rpidas ya realizamos un anlisis parasitolgico. Preliminar. Despus,
tambin se pueden utilizar microscopa ptica y electrnica, tcnicas inmunolgicas e
incluso moleculares
Cualquier organismo parasitario que encontremos y queramos enviar a un laboratorio
especializado deber ser conservado en un bote con alcohol 70% y convenientemente
rotulado.
MICOLOGIA
Existen comparativamente pocos grupos de hongos patgenos en peces y su
diagnstico puede realizarse de forma ms o menos fcil mediante tcnicas que no
requieren su cultivo. De todas formas como medio general puede utilizarse el medio de
Sabouraud con adicin de antibitico como medio base para el aislamiento de hongos.
Saprolegniales: Diagnstico directo por raspados de piel y observacin de la morfologa
de hifas y conidios. Puede intentarse su cultivo en caamn.
Ichyhyophonus, Exophiala, Phoma: Diagnstico directo por squashes de tejido o por
histopatologa.
50
Manual de Tcnicas Bsicas de Diagnstico Patolgico en Peces - 2005
HISTOPATOLOGIA
Esta tcnica nos permite visualizar en secciones de tejido las lesiones ocasionadas en
los diferentes procesos patolgico y a partir de la visualizacin de un tipo u otro de
lesin, determinar su naturaleza. Para ello es necesario una larga experiencia en
diagnstico para poder discernir entre los distintos cuadros patolgicos que pueden
aparecer.
Toma de muestras para histopatologa (Microscopa ptica)
Si se desean tomar muestras para histopatologa es MUY IMPORTANTE que sean
muestras a partir de peces vivos, moribundos o muertos MUY RECIENTEMENTE, ya
que como hemos comentando anteriormente respecto a la autolisis en peces, los
procesos de alteracin de las estructuras del pez son extremadamente rpidas y
pueden comprometer seriamente la calidad de la muestra, transformndola en muestra
no apta.
Por ello es muy importante fijar rpidamente la muestra y que esta muestra tenga el
mximo contacto posible con la solucin fijadora. Es MUY importante que las
muestras se remitan en recipientes con ABUNDANTE FIJADOR, ya que de lo contrario
la fijacin es deficiente. Como mnimo hay que poner 3 partes de fijador por cada parte
de muestra, siendo lo ideal una relacin de 9:1.
Si se envan peces enteros es muy necesario que se tome la precaucin de abrir el
abdomen y revertir las muestras al exterior para mejorar la fijacin. Esta prctica incluye
tambin a peces pequeos, ya que normalmente se les fijan mal los rganos
abdominales. Tambin es recomendable pinchar o retirar la vejiga natatoria para que el
fijador pueda acceder al rin. Es importante incluir en la muestra tanto tejido sano como
tejido alterado. Tambin es necesario indicar que lesiones avanzadas como ulceras o
tejidos que presenten un grado de alteracin avanzado no suelen ser buenas muestras
para el diagnstico, ya que en estas muestras frecuentemente slo se observan
procesos degenerativos terminales o infecciones secundarias que enmascaran el origen
inicial del problema.
Para fijar las muestras, los fijadores ms habituales son Formol al 10% tamponado (el
que recomendamos) y Formol salino. La formulacin para preparar estos fijadores es:
Formol al 10% tamponado
Formol comercial (37-40%): 100 ml
Agua destilada: 900 mL
Fosfato monosdico (monohidrato): 4 g
Fosfato disdico (anhidro): 6 g
(Si usamos agua del grifo y tiene suficiente contenido en sales, puede usarse sin
necesidad de aadir tampn.).El formol salino se prepara con agua de mar filtrada (con
agua limpia es suficiente) en lugar de agua destilada.
Las muestras fijadas tambin permiten realizar sobre ellas las mismas tcnicas que las
que describimos en las preparaciones en fresco. Tambin hemos de tener en cuenta
que algunos parsitos (sobre todo los monogenea, los coppodos y los ispodos)
pueden desprenderse de los tejidos o de la superficie de piel y branquias cuando se
sumergen las muestras en el fijador, por lo que es interesante pipetear los fondos de los
recipientes y observar el contenido de este arrastre al microscopio. Recordemos que
51
Manual de Tcnicas Bsicas de Diagnstico Patolgico en Peces - 2005
precisamente el formol es uno de los antiparasitarios utilizados con mayor frecuencia.
Recordemos tambin utilizar botes de plstico (mejor que los de cristal) de cierre
hermtico (o de lo contrario corremos el riesgo de que tengan prdidas durante el
transporte, nos lleguen las muestras secas y con el cartn de la caja empapado de
formol. Las muestras deben fijarse unas 48 horas antes de su procesado. Tambin es
preferible mantener las muestras en un lugar fresco y alejado de la luz directa.
Toma de muestras para Microscopa Electrnica
En ocasiones es necesario realizar estudios ms precisos para conocer con ms detalle
el carcter de las lesiones o de los agentes patgenos que se encuentran en estas
lesiones. Por ello puede ser necesario utilizar el microscopio electrnico (de transmisin
y/o barrido). No nos extenderemos comentando el procesado de las muestras para
estas tcnicas ya que son las mismas que se utilizan para otro tipo de muestras, sino
que slo indicaremos como se debe proceder para obtener muestras para esta tcnica.
Las muestras para microscopio electrnico deben tomarse muy rpidamente y a partir
solo de material muy fresco. Es importante indicar las muestras de tejidos deben ser
porciones muy pequeas (si es posible porciones de menos de 1 milmetro cbico) y
fijarlas muy rpidamente en el fijador para microscopio electrnico. Existen distintos
tipos de fijadores para este tipo de estudios, aunque nosotros siempre utilizamos el
glutaraldehido como fijador de eleccin, siguiendo este protocolo:
Solucin fijadora de glutaraldehido: Glutaraldehido al 2%. La muestras se fijan en esta
solucin a 4C durante 1-2 horas. Posteriormente se lavan con tampn fosfato, tampn
de Sorenson, tampn Millonig, tampn cacodilato o con tampones similares,
conservndose en tampn hasta que tiene lugar la postfijacin con tetraxido de osmio
al 1% (en tampn) y conservndose en tampn de nuevo hasta su transporte hasta el
laboratorio de referencia.
HEMATOLOGIA
El estudio de la sangre puede ser tambin bastante til para el diagnstico. A partir de
una muestra de sangre pueden realizarse determinaciones como hematocrito,
extensiones sanguneas, hemograma, bioqumica sangunea y serologa. La mayora de
estas pruebas necesitan del conocimiento de los valores habituales (y su rango de
variacin) para poder ser comparadas. Debido al menor nmero de datos que se
poseen sobre especies de peces en comparacin con la especie humana y otros
vertebrados, su utilizacin es a veces de poca significacin diagnstica.
Toma de muestras
Para tomar muestras de sangre utilizamos el mismo tipo de agujas y jeringas que se
utilizan en medicina veterinaria, adaptndolas al tamao del pez y cantidad de sangre a
recoger. Nuestra experiencia indica que es til (si se puede) utilizar una aguja y jeringa
heparinizadas para evitar la rpida coagulacin de la sangre.
En general y de forma habitual se toma muestras de sangre a partir de:
- vena caudal
- corazn (ventrculo o seno venoso)
- arteria aorta dorsal (menos frecuente)
- Seccin de pednculo caudal
52
Manual de Tcnicas Bsicas de Diagnstico Patolgico en Peces - 2005
Extraccin de sangre de la vena caudal
Incidir en la zona ventral de la cola, justo despus de la aleta anal y en direccin dorsal
avanzar hasta contactar con la columna vertebral, rotar ligeramente la aguja y recoger la
sangre. Tambin puede incidirse en unos 60 grados desde una zona prxima a la lnea
lateral.
Extraccin de sangre del corazn
Incidir en la zona ventral de la regin de transicin entre cabeza y cola, entre las aletas
pectorales y la zona de los oprculos. Rpidamente se llega al ventrculo de donde se
puede recoger sangre de forma fcil. Si se incide ligeramente por delante de la aleta
pectoral se consigue tomar sangre del seno venoso.
Extraccin de sangre de la arteria aorta dorsal
Abrir la boca del pez e incidir en la zona ms caudal de la insercin dorsal de los arcos
branquiales.
Seccin del pednculo caudal
Para los peces que por su tamao no es posible sacar sangre de las otras formas
descritas y pueden sacrificarse, puede seccionarse el pednculo caudal (despus de
anestesiar al pez), secar la superficie de corte y recoger la sangre que sale de la aorta
dorsal y vena caudal seccionadas.
53
Manual de Tcnicas Bsicas de Diagnstico Patolgico en Peces - 2005
Conservacin de muestras de sangre
Tras retirar la aguja, la sangre puede ser recogida en tubos sin anticoagulante y dejarlas
coagular en un lugar fresco para separar el suero o bien recoger en tubos con
anticoagulante (en general, EDTA o heparina, segn el tipo de anlisis a realizar) y
mantener a 4 grados.
Extensiones sanguneas
Depositar una gota pequea de sangre fresca en un portaobjetos (fresca o con
anticoagulante) y aplicar otro portaobjetos en ngulo agudo, dejar extender la gota de
sangre por el lado del segundo portaobjetos y con un movimiento rpido realizar una
extensin de la gota de sangre. Despus se seca al aire y teir con las tcnicas
habituales como Giemsa, May-Grnwald-Giemsa o Diff-Quick.
En este tipo de muestras es posible evidenciar la existencia de parsitos, morfologas
extraas o cuerpos raros en las clulas sanguneas. Pueden realizarse contajes semicuantitativos de los diferentes tipos celulares presentes, aunque a veces es necesario
estar habituado o contar con la ayuda de un experto para diferenciar cada tipo celular.
Hematocrito
Se debe llenar el 70-80% de un tubo capilar heparinizado o con EDTA y despus sellar
ambos bordes con plastilina o similar. Centrifugar durante 4-5 minutos a unos 12.000 g y
calcular el porcentaje de la columna roja con el del total de sangre. El valor calculado es
el PCV (Packed Cell Volume) o hematocrito.
Hemograma, bioqumica sangunea
Estas tcnicas son bastante especializadas y suelen estar solamente al alcance de
determinados laboratorios. No obstante, describiremos brevemente qu tcnicas se
utilizan habitualmente.
- Hemograma: La determinacin cuantitativa de los elementos celulares
presentes en sangre Se realiza utilizando las mismas tcnicas descritas para
vertebrados terrestres (contajes en cmara de recuento de diversos tipos).
Frecuentemente esta tcnica se encuentra con el problema de la enorme
variabilidad individual, variabilidad segn condiciones del medio y la falta de
valores de referencia suficientemente establecidos para las diferentes especies.
- Bioqumica sangunea: Son mltiples los parmetros que pueden determinarse
en una muestra de sangre. Desafortunadamente, hasta el momento estas
tcnicas son de escasa utilizacin diagnstica en la clnica habitual, quedndose
frecuentemente limitadas a los trabajos de investigacin. Posiblemente en el
futuro estas tcnicas puedan tener una mayor implantacin en patologa de
peces
TECNICAS INMUNOLGICAS
Las tcnicas inmunolgicas se basan en la utilizacin de anticuerpos especficos para
demostrar la presencia de un agente vrico, bacteriano, parasitario etc. Frecuentemente
54
Manual de Tcnicas Bsicas de Diagnstico Patolgico en Peces - 2005
se utilizan como complemento a el resto de tcnicas anteriormente comentadas. Entre
las tcnicas utilizadas habitualmente para el diagnstico en peces podemos destacar:
Tcnicas de aglutinacin
Bastante sencillas y utilizados sobre todo para el diagnstico bacteriano. Se basan en
poner en contacto las bacterias de una colonia con un suero en el que existen
anticuerpos especficos contra esa bacteria. En el caso de que los anticuerpos
reconozcan a los antgenos bacterianos, se producir una aglutinacin visible a simple
vista. Esta tcnica se puede realizar sobre un portaobjetos o sobre otra base similar
sobre la cual se coloca una muestra de colonia y a continuacin se le aade el suero,
observndose o no aglutinacin (que puede ser fuerte o dbil) a los pocos minutos. Esta
tcnica depende de que el suero utilizado tenga suficiente cantidad de anticuerpos (ttulo
alto). Existen ya bastantes kits comerciales en el mercado que utilizan esta tcnica para
la identificacin rpida. Tambin pueden obtenerse en el mercado antisueros
monoclonales o policlonales para la realizacin de esta y otras tcnicas.
Tcnicas de ELISA
Utilizadas para la cuantificacin de anticuerpos en sangre o presencia de antgenos en
extractos celulares. Esta tcnica se basa en la adsorcin mediante incubacin de
partculas antignicas vricas, bacterianas, etc. (en el caso de querer detectar
anticuerpos en suero) o de anticuerpos (en el caso de querer detectar partculas
antignicas) y posterior fijacin en pocillos de placas de microtitulacin. A continuacin
se lavan con soluciones tampn y se incorporan las soluciones a testar (suero con
anticuerpos o soluciones con el antgeno) Se volver a lavar con soluciones tampn y si
el antgeno o anticuerpo ha reconocido a su homlogo unido al pocillo, no se perder al
lavar. Para revela la existencia de esta unin utilizaremos anticuerpos contra el antgeno
o contra la fraccin Fc de los anticuerpos de la especie de pez de la que testamos el
suero. Estos anticuerpos estn conjugados con una enzima o con un sistema
amplificador (por ejemplo avidina-biotina o otro anticuerpo contra el anticuerpo anterior).
Al final de la cadena est un enzima fijado a uno de los componentes amplificadores que
al ponerlo en contacto con una sustancia (sustrato) se observa la existencia de reaccin
por un cambio de color que se puede cuantificar. Estas tcnicas ELISA son
generalmente las utilizadas en el anlisis virolgico y son las tcnicas obligatorias para
el anlisis de VHS y IHN. Los protocolos de realizacin pueden variar bastante segn el
tipo de determinacin a realizar.
Tcnicas de inmunofluorescencia
Directa e indirecta (FAT e IFAT) sobre improntas de rganos y/o tejidos celulares o bien
en suero. Utilizada para el diagnstico de BKD y la mayora de las virosis.
Tcnicas de inmunohistoqumica
Se basan en la deteccin en cortes histolgicos de los antgenos o estructuras
especficas de pared o membrana de distintos agentes patgenos en peces. Para
detectar estos antgenos o estructuras se utilizan anticuerpos monoclonales o
policlonales o bien sustancias especficas como las lectinas. En el caso que exista
reconocimiento, la unin se revela mediante el uso de un segundo anticuerpo marcado
o bien marcando el primero de los anticuerpos o sustancia especfica. Los marcadores
55
Manual de Tcnicas Bsicas de Diagnstico Patolgico en Peces - 2005
pueden ser sustancias fluorescentes, complejo avidina-biotina o con un enzima
acoplado a un sistema revelador (cromgeno).
TCNICAS MOLECULARES
Estas tcnicas son bastante recientes y derivan en su mayora de las tcnicas de PCR
(Polymerase Chain Reaction). Se basan en el la deteccin de la presencia del DNA del
agente patgeno mediante su multiplicacin del DNA o RNA en varios ciclos mediante
una polimerasa y en la posterior identificacin mediante la utilizacin de sondas
especficas. Son tcnicas complicadas pero que se estn poniendo a punto para los
diferentes patgenos. Una de las mejores ventajas de esta tcnica es su alta
sensibilidad pero su utilizacin para diagnsticos de rutina es an limitada, pero puede
tener una importancia cada vez mayor en el futuro.
TEST DE STRESS
Estos test se utilizan de experimental para comprobar la resistencia de los peces a
condiciones extremas y de esta forma asegurar la calidad de los grupos de peces, o
bien, se utilizan para detectar portadores asintomticos (carriers) e suelen dar negativo
a las otras tcnicas.
En el primero de los casos, se utiliza especialmente en el cultivo larvario y consiste en
exponer a las larvas/juveniles a altas salinidades (55-65 por mil) y medir la supervivencia
a intervalos de tiempo regulares.
En el segundo de los casos se somete a los peces a un cambio sbito de temperatura y
se les administran inmunodepresores (p. ej. prednisolona) y se les muestrea unos das
despus para ver si los test habituales dan positivo.
RADIOLOGIA
Se utiliza especialmente en el diagnstico de malformaciones en juveniles.
Particularmente sensibles para esta tcnica se han demostrado las placas de
mamografa
CONSIDERACIONES PRCTICAS SOBRE LOS ANLISIS COMPLEMENTARIOS
La gran mayora de tcnicas indicadas anteriormente son tcnicas utilizadas
habitualmente en el diagnstico de patologas humanas o de animales domsticos
terrestres. En su mayora se trata de pruebas ya completamente estandarizadas y
contrastadas en condiciones de campo, de las que se conocen muy bien sus
cualidades como sensibilidad, especificidad, etc.
Todas estas tcnicas estn tambin tericamente disponibles para poderlas utilizar en
el diagnstico en peces. Sin embargo, en las tcnicas aparentemente ms especficas
como las tcnicas inmunolgicas o las tcnicas moleculares nos encontramos muy
frecuentemente con el problema que muchas de estas tcnicas estn nicamente
disponibles como herramientas de investigacin y aplicadas slo a estudios
56
Manual de Tcnicas Bsicas de Diagnstico Patolgico en Peces - 2005
experimentales concretos. El problema surge cuando pretendemos utilizar estas
tcnicas sobre muestras de campo o en muestras distintas a las testadas
experimentalmente. En ese momento nos encontramos con grandes problemas para
conseguir una fiabilidad de los resultados y por lo tanto se nos reduce mucho la
confianza que podamos tener en esos resultados.
3.8.- DIAGNSTICO E INTERPRETACIN DE LOS RESULTADOS
Una vez hemos realizado todo los anlisis correspondientes de forma ordenada y
completa y con todos los resultados de las pruebas complementarias, ya podemos
emitir nuestro diagnstico. A la hora de interpretar los resultados de una analtica,
hemos de recordar que nunca una sola prueba es definitiva, y siempre, como ltimos
responsables de la salud de los animales, podemos dudar de estos resultados.
Ejemplo: En un chequeo rutinario de mis alevines de lubina me han detectado un
positivo por PCR a Nodavirus, pero en mi granja los peces estn sanos y no hay
mortalidad, debo creerme este diagnstico? Quizs debera esperar al cultivo celular.
O tambin puedo enviar nuevas muestras a otro laboratorio.
57
Manual de Tcnicas Bsicas de Diagnstico Patolgico en Peces - 2005
4.- EL DIAGNSTICO EN LA GRANJA DE CULTIVO
En el apartado anterior hemos revisado de forma detallada los protocolos de diagnstico
patolgico en peces. Para la realizacin de muchos de ellos en ocasiones se requiere un
equipo especializado que no siempre se dispone en los centros de produccin.
Es importante recalcar que nosotros siempre recomendamos que haya un responsable
de salud en cada granja, que sea capaz de emitir un primer diagnstico preliminar que
le permita iniciar un tratamiento. De este modo, uno debe adaptarse a cada situacin e
intentar realizar en diagnstico con los medios que tenga a su alcance: Nadie cometi
un mayor error que aqul que no hizo nada porque slo poda hacer un poco
De todas formas, siempre enviaremos una muestra al laboratorio especializado para
confirmar el diagnstico.
4.1.- NIVELES DE DIAGNSTICO EN PLANTA
0.- Examen externo y necropsia con navaja
Disponemos de lo ms bsico y slo podemos intuir la causa del problema por
nuestros conocimientos tericos y las
lesiones observadas externa e
internamente. Puede parecer justito, pero muchas veces suele ser suficiente.
1.- Material de necropsia, pruebas rpidas, tinciones y microscopio
Tenemos la enorme suerte de disponer de un microscopio, material de diseccin
y tinciones. Ya no se nos puede escapar casi nada, pues podemos realizar las
pruebas ms importantes del diagnstico, las pruebas rpidas directas,
preparaciones en fresco e improntas.
Nosotros consideramos que hasta aqu es lo imprescindible que debe poder
realizar en una granja.
2..- Siembras en medios de cultivo y antibiogramas
Disponemos adems de placas variadas y discos de antibiograma. Puedo
realizar siembras y confirmar la sensibilidad de las cepas bacterianas que asle
en mi granja. Tambin puedo controlar la flora microbiana del agua. Despus
enviar las bacterias al laboratorio de microbiologa para que las identifiquen.
3.- Sistemas de identificacin bioqumica
Tenemos un laboratorio perfectamente equipado para poder diagnosticar la
mayora de enfermedades que sufrirn mis peces. Puedo identificar casi todas
las cepas que asle.
58
Manual de Tcnicas Bsicas de Diagnstico Patolgico en Peces - 2005
4.2.- TELEDIAGNSTICO
El proceso de diagnstico puede y debe aprovecharse de las nuevas tecnologas como
soporte. Muchas veces al tcnico le pueden surgir dudas mientras est realizando el
anlisis, as que puede servirse de estos elementos para recoger la opinin de los
patlogos expertos de una forma rpida y sencilla.
De menor a mayor tecnificacin podemos encontrar diferentes formas de soporte al
diagnstico:
Mvil
Consulta telefnica normal de una duda.
Mvil con cmara incorporada
Enviamos una imagen de las lesiones concretas que queremos consultar.
Mvil con cmara incorporada y microscopio
Podemos enviar imgenes de las lesiones y de lo que encontremos al realizar las
pruebas rpidas de diagnstico, si tenemos habilidad para fotografiar lo que vemos por
el ocular.
Cmara digital y microscopio
Como antes, pero con mayor calidad de imagen
Quizs en un futuro no muy lejano, los procedimientos de diagnstico on-line sern
habituales, aunque deberemos seguir siendo cautos. Sern de ayuda, pero nunca
sustitutivas. Al final siempre ser necesario interpretar lo que encontremos.
59
Manual de Tcnicas Bsicas de Diagnstico Patolgico en Peces - 2005
5.- ANEXO I: EJEMPLO DE HISTORIA CLNICA
CLIENTE
CODIGO
DIRECCION
TELEFONO / FAX
DIRECCION ELECTRONICA
CENTRO DE ORIGEN DE LOS PECES
CODIGO DE CENTRO
ESPECIES
TIPO DE AGUA
TEMPERATURAS DEL AGUA REGISTRADAS
APETITO
EVOLUCION DE LAS MORTALIDADES DIARIAS
EVOLUCION
OBSERVACION CLNICA:
NATACIN:
RESPIRACION:
ASPECTO EXTERNO (PIEL, ALETAS, OJOS):
ASPECTO BRANQUIAL:
60
Manual de Tcnicas Bsicas de Diagnstico Patolgico en Peces - 2005
NECROPSIA:
MUESTRAS TOMADAS:
(Preparaciones en fresco,
histopatologa, toxicologa)
improntas,
DIAGNOSTICO PRELIMINAR
DIAGNOSTICO DEFINITIVO
TRATAMIENTO RECOMENDADO
61
sangre,
microbiologa,
virologa,
Manual de Tcnicas Bsicas de Diagnstico Patolgico en Peces - 2005
6.- ANEXO II: EJEMPLO DE FICHA DE LESIONES
FICHA DE IDENTIFICACIN DE LESIONES EXTERNAS E INTERNAS
N de caso:
N de ejemplar:
Especie:
Lesiones en piel:
Fornculos...
lceras...
Prdida de escamas...
Despigmentacin...
Perdida de piel...
Presencia de masas algodonosas ......
Parsitos...
Nodulaciones...
Hiperpigmentacin...
Hemorragias ...
Petequias...
Cuerpos extraos...
Dilataciones....
Melanosis...
Equimosis ...
Erosiones ...
Vesculas...
Otros..
Lesiones en branquias:
Anemia...
Necrosis...
Hemorragias ...
Masas amarillentas....
Inflamacin ..
Mucosidad...
Oscuras...
Parsitos......
Deshilachamiento ...
Otros..
Lesiones en aletas:
Erosiones...
Deshilachamiento...
Masas extraas...
Parsitos...
Atrofia ....
Prdida parcial ...
Hemorragias...
Total ....
Otros
Lesiones en ojos:
Exoftalmia...
Exoftalmia...
Hemorragias...
Microftalmia ....
Prdida de globo ocular...
Panoftalmitis...
Opacidad corneal...
Presencia de masas extraas...
Otros.............
Lesiones en la boca:
Hemorragias...
Masas extraas...
Material necrtico....
Parsitos.... Otros
Lesiones en el ano:
Ano prolapsado...
Hipermico...
Hemorrgico...
Otros.
Lesiones internas:
Ascitis ....
Inflamacin....
Parsitos...
Granulomas...
Congestin...
Abscesos....
Hemorragias...
Nodulaciones ....
62
Parsitos.......
Otros..................
También podría gustarte
- Presentacion Introduccion A La AcuaponiaDocumento21 páginasPresentacion Introduccion A La Acuaponiaedson100% (1)
- ACTIVIDADES DE INGLES DE REPASO PARA 3º y 4º Año 2020Documento16 páginasACTIVIDADES DE INGLES DE REPASO PARA 3º y 4º Año 2020Vanesa AbadiaAún no hay calificaciones
- Principios de Nutricion Aplicada Al Cultivo de PecesDocumento71 páginasPrincipios de Nutricion Aplicada Al Cultivo de Pecesjaime_andres100% (1)
- Enfermedades de Los PecesDocumento6 páginasEnfermedades de Los PecesAlberth SejasAún no hay calificaciones
- Biologia Pesquera Digital PDFDocumento154 páginasBiologia Pesquera Digital PDFkilldestroyerAún no hay calificaciones
- Poster IDocumento1 páginaPoster ICarlos OlivaresAún no hay calificaciones
- AcuaculturaDocumento71 páginasAcuaculturaJuan Ramirez100% (1)
- Preguntas de AcuiculturaDocumento37 páginasPreguntas de AcuiculturaKarlucha344Aún no hay calificaciones
- JGomez - Distribuciones de Frecuencias y Sus GráficasDocumento18 páginasJGomez - Distribuciones de Frecuencias y Sus GráficasLaboratorio ProAún no hay calificaciones
- Etas PDFDocumento43 páginasEtas PDFGJAUFHAún no hay calificaciones
- Algas en Tu AcuarioDocumento22 páginasAlgas en Tu AcuarioMoisés Raín MontecinosAún no hay calificaciones
- ICH Punto Blanco en PecesDocumento8 páginasICH Punto Blanco en PecesJeAn PieRcito OsiToAún no hay calificaciones
- Actividad 2 - CyanoprokaryotaDocumento2 páginasActividad 2 - CyanoprokaryotaErick Diaz100% (1)
- Clase 11 Sintesis y Degradacion de GlucogenoDocumento25 páginasClase 11 Sintesis y Degradacion de GlucogenoNicole Bravo FAún no hay calificaciones
- Informe Practicas Jimmy Polo CorregidoDocumento31 páginasInforme Practicas Jimmy Polo CorregidoFlores JairAún no hay calificaciones
- PRÁCTICA 6 - Taxonomía de Bacillariophyceae SAMANTADocumento9 páginasPRÁCTICA 6 - Taxonomía de Bacillariophyceae SAMANTAErick DiazAún no hay calificaciones
- Algario PDFDocumento50 páginasAlgario PDFBrenda PalaciosAún no hay calificaciones
- Reproducciòn Inducida de PecesDocumento3 páginasReproducciòn Inducida de PecesbrianAún no hay calificaciones
- Hoja de Guayabo en El Acuario PDFDocumento1 páginaHoja de Guayabo en El Acuario PDFFelixAún no hay calificaciones
- Proceso de Curtido PielesDocumento16 páginasProceso de Curtido PielesPublio Castro SantanderAún no hay calificaciones
- La Produccion de Alimento Vivo y Su Importancia en AcuaculturaDocumento19 páginasLa Produccion de Alimento Vivo y Su Importancia en AcuaculturaJose David CastroAún no hay calificaciones
- Estructura de Un Proyecto de Inversión en Acuicultura 1Documento4 páginasEstructura de Un Proyecto de Inversión en Acuicultura 1MichelCahuasAún no hay calificaciones
- Ficha Técnica KampachiDocumento5 páginasFicha Técnica Kampachijesus lopezAún no hay calificaciones
- Dialnet EvaluacionMicrobiologicaDePescadosYMariscosExpendi 7099902 PDFDocumento8 páginasDialnet EvaluacionMicrobiologicaDePescadosYMariscosExpendi 7099902 PDFNatalia GonzalezAún no hay calificaciones
- Diseño Laboratorio de Moluscos PDFDocumento8 páginasDiseño Laboratorio de Moluscos PDFSocorroSanchezFajardoAún no hay calificaciones
- Flujograma Peces NativosDocumento1 páginaFlujograma Peces NativosRosa Isabel Flores TurpoAún no hay calificaciones
- Cuadro Informativosobre Tiempo de Congelamiento y Temperaturas Adecuadas para El Pescado CongeladoDocumento3 páginasCuadro Informativosobre Tiempo de Congelamiento y Temperaturas Adecuadas para El Pescado CongeladoFrankLeeAún no hay calificaciones
- Ensayo de Ecologia de PecesDocumento5 páginasEnsayo de Ecologia de PecesmichaelAún no hay calificaciones
- Enfermedades Comunes en PisciculturaDocumento16 páginasEnfermedades Comunes en PisciculturaJose Andres MoralesAún no hay calificaciones
- Introduccion A La BromatologiaDocumento31 páginasIntroduccion A La BromatologiaYasmin CortezAún no hay calificaciones
- Proyecto PisciculturaDocumento46 páginasProyecto PisciculturaAlsuab BaAún no hay calificaciones
- Productos Listos para Consumir-ItpDocumento115 páginasProductos Listos para Consumir-ItpNestor Velazco100% (1)
- Acuicultura de Poliquetos: Avances y Perspectivas Taller de Acuicultura y AmbienteDocumento39 páginasAcuicultura de Poliquetos: Avances y Perspectivas Taller de Acuicultura y AmbienteCristhian Diaz0% (1)
- David SaldarriagaDocumento91 páginasDavid Saldarriagatomasinoperu100% (2)
- Captacion de Agua para Piscinas de TruchasDocumento3 páginasCaptacion de Agua para Piscinas de TruchasLaly ReyesAún no hay calificaciones
- GENBANK +bioeditDocumento11 páginasGENBANK +bioeditDaniel Costas ImbernónAún no hay calificaciones
- Silabo de Acuicultura IiDocumento6 páginasSilabo de Acuicultura IiAntony VasquezAún no hay calificaciones
- Aspectos NutricionalesDocumento16 páginasAspectos NutricionalesKaren cuellarAún no hay calificaciones
- Manual ArawanaDocumento11 páginasManual ArawanaFroilan Salazar GonzalesAún no hay calificaciones
- Camarón de MalasiaDocumento6 páginasCamarón de MalasiaROY EDSON ARPASI BARTOLOAún no hay calificaciones
- Tarea 1 - Mimbela - Topicos Selectos de La AcuiculturaDocumento30 páginasTarea 1 - Mimbela - Topicos Selectos de La AcuiculturaMaria Mercedes Mimbela GonzalesAún no hay calificaciones
- Reproduccion Inducida Tesis PDFDocumento52 páginasReproduccion Inducida Tesis PDFAntonio Mariluz100% (2)
- Boyd Sales Disueltas en Agua de Cultivo de CamaronDocumento14 páginasBoyd Sales Disueltas en Agua de Cultivo de CamaronAngeloAún no hay calificaciones
- Factores Antinutricionales en Los AlimentosDocumento12 páginasFactores Antinutricionales en Los Alimentosdalcro0% (1)
- Métodos de Conservación Del Pescado Conserva de PescadoDocumento25 páginasMétodos de Conservación Del Pescado Conserva de PescadoAdrian Quio RuizAún no hay calificaciones
- Separata I FicologíaDocumento7 páginasSeparata I FicologíaLuiggi Ronaldo Rios DiazAún no hay calificaciones
- Ostra PerleraDocumento14 páginasOstra PerleraCRISTHIAN LEONARDO OLIVOS SALDARRIAGAAún no hay calificaciones
- TrabajoDocumento16 páginasTrabajoEdinson Padilla PajaroAún no hay calificaciones
- El Proyecto GAMA PDFDocumento19 páginasEl Proyecto GAMA PDFcristian003Aún no hay calificaciones
- Práctica Hidratación de ArtemiaDocumento2 páginasPráctica Hidratación de ArtemiaJorge LNHAún no hay calificaciones
- Libro PisciculturaDocumento80 páginasLibro PisciculturahombreraAún no hay calificaciones
- 208-Acuicultura para VeterinariosDocumento2 páginas208-Acuicultura para VeterinariosBeto Aravena0% (1)
- Proyecto Carachama Dietas Alimenticias 01-05-14Documento36 páginasProyecto Carachama Dietas Alimenticias 01-05-14José Condori MuñizAún no hay calificaciones
- Uso de Probiotico en La Rpoduccion de Truchas Arcoiris en Etapa de Alevianje Bajo Un Sistema de Recirculacion CerradaDocumento153 páginasUso de Probiotico en La Rpoduccion de Truchas Arcoiris en Etapa de Alevianje Bajo Un Sistema de Recirculacion CerradaAlejandro Echeverre HuamanAún no hay calificaciones
- Prevencion y Tratamiento de Enfermedades de Los Peces PDFDocumento27 páginasPrevencion y Tratamiento de Enfermedades de Los Peces PDFovejacaracolAún no hay calificaciones
- Cultivo de Peces en JaulasDocumento30 páginasCultivo de Peces en JaulasVictor H Bejarano100% (1)
- Cultivo Artemia SalinaDocumento7 páginasCultivo Artemia SalinaHugo Felipe Suárez MaldonadoAún no hay calificaciones
- FAO DOC TEC PESCA 306-1 Rev 2 - Sparre #1 PDFDocumento459 páginasFAO DOC TEC PESCA 306-1 Rev 2 - Sparre #1 PDFMaria Laura Naranjo OrdonioAún no hay calificaciones
- Enfermedades BacterianasDocumento18 páginasEnfermedades BacterianasNorma Liseth DiazAún no hay calificaciones
- Cadena Productiva ZapatosaDocumento75 páginasCadena Productiva Zapatosaomar sierraAún no hay calificaciones
- Leguminosas espontaneas de posible valor forrajero en ColombiaDe EverandLeguminosas espontaneas de posible valor forrajero en ColombiaAún no hay calificaciones
- Clinica Bovinos-20Documento9 páginasClinica Bovinos-20Ricardo Ponce Rodríguez100% (1)
- Tema 4 Vibraciones PDFDocumento23 páginasTema 4 Vibraciones PDFERICK OMAR ARIAS RUIZAún no hay calificaciones
- El Poder de La Palabra TransformadoraDocumento17 páginasEl Poder de La Palabra TransformadoraAbraham AbsalonAún no hay calificaciones
- Tarea 3 (Investigacion Caso) MICROECONOMIA III - Curso 5-2 - IIC-2023-2024Documento2 páginasTarea 3 (Investigacion Caso) MICROECONOMIA III - Curso 5-2 - IIC-2023-2024Rosita AndradeAún no hay calificaciones
- Instrumentos de LaboratorioDocumento15 páginasInstrumentos de LaboratorioLuis Enrique De Los Santos IzquierdoAún no hay calificaciones
- Generador de Señal SPWM Con ArduinoDocumento3 páginasGenerador de Señal SPWM Con ArduinoGustavo Rodriguez0% (1)
- Enfermeria Nacional y InternacionalDocumento6 páginasEnfermeria Nacional y InternacionalEdgard HernandezAún no hay calificaciones
- Libro de Resúmenes VII Jornada Internacional Aprendizaje, Educación y NeurocienciasDocumento22 páginasLibro de Resúmenes VII Jornada Internacional Aprendizaje, Educación y NeurocienciasSergio MoraAún no hay calificaciones
- Clima Organizacional en Las Instituciones Prestadoras de Salud-Entrega-Sefi - 22 (1) (1) (Autoguardado)Documento7 páginasClima Organizacional en Las Instituciones Prestadoras de Salud-Entrega-Sefi - 22 (1) (1) (Autoguardado)GERENCIA KSV ADVISORSAún no hay calificaciones
- Problemas Inferencia EstadisticaDocumento6 páginasProblemas Inferencia EstadisticaRodolfo Sabala VeilesAún no hay calificaciones
- Guia Mapa de La EmpatiaDocumento6 páginasGuia Mapa de La EmpatiaVista HermosaAún no hay calificaciones
- Las 7 Herramientas de La CalidadDocumento19 páginasLas 7 Herramientas de La CalidadJosé Van StrahlenAún no hay calificaciones
- Estado Del Arte - 2017-2Documento30 páginasEstado Del Arte - 2017-2Yudith Delgado GavidiaAún no hay calificaciones
- 8 Medidas de Tendencia CentralDocumento4 páginas8 Medidas de Tendencia Centraljose hernandezAún no hay calificaciones
- Anaximandro PDFDocumento1 páginaAnaximandro PDFKAREN ORDOÑEZAún no hay calificaciones
- Calculadora de Colores para ResistenciasDocumento3 páginasCalculadora de Colores para ResistenciasEdgar Jose Aranguibel MorilloAún no hay calificaciones
- COWAN ROS EstatalidadesDocumento43 páginasCOWAN ROS EstatalidadesGuido DiblasiAún no hay calificaciones
- Shipibo - ConiboDocumento25 páginasShipibo - ConiboALVAROAún no hay calificaciones
- Decreto Municipal Ord. TerritorialDocumento35 páginasDecreto Municipal Ord. TerritorialMiguel Alfonso AvilaAún no hay calificaciones
- Formato Control de DocumentosDocumento6 páginasFormato Control de DocumentosBrendaChiquinquiraAún no hay calificaciones
- LiderazgoDocumento2 páginasLiderazgoGloria Mendez GuzmanAún no hay calificaciones
- Contrato de Licencia de Uso de Programas Informatico1Documento2 páginasContrato de Licencia de Uso de Programas Informatico1disferchAún no hay calificaciones
- 4prim Com ActDocumento21 páginas4prim Com ActBrayan GalindoAún no hay calificaciones
- Ejercicios 3er Grado de PrimariaDocumento7 páginasEjercicios 3er Grado de PrimariaArmando Fuentes HernandezAún no hay calificaciones
- Tarea 4 Contabilidad II .14-4463Documento10 páginasTarea 4 Contabilidad II .14-4463PedroLuisAndersonAún no hay calificaciones
- Monitoreo Primer Grado Sem. Del 1 Al 5 de JunioDocumento10 páginasMonitoreo Primer Grado Sem. Del 1 Al 5 de JunioFacu GalvanAún no hay calificaciones
- Tesina de Cementación de Pozoz PetrolerosDocumento23 páginasTesina de Cementación de Pozoz Petrolerosveronica soledadAún no hay calificaciones
- Geologia Leon DormidoDocumento13 páginasGeologia Leon DormidoKevin Cornejo MartînezAún no hay calificaciones