Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Ecuaciones y Cálculos para El Tratamiento de Aguas: Capítulo 50: Desinfección
Cargado por
JULIO JUAN MUÑOZ FARFANTítulo original
Derechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
Ecuaciones y Cálculos para El Tratamiento de Aguas: Capítulo 50: Desinfección
Cargado por
JULIO JUAN MUÑOZ FARFANCopyright:
Formatos disponibles
Ecuaciones y cálculos para
el tratamiento de aguas
Capítulo 50: Desinfección
Roberto Rosal
Mario Díaz (Coord.), Editorial Paraninfo, ISBN 13: 9788428341523,
ISBN 10: 8428341524. Fecha de publicación: 02.01.2019
Ecuaciones y cálculos para el tratamiento de aguas
50. DESINFECCIÓN
i. Consideraciones teóricas
50. 1. Introducción y objetivos
La desinfección del agua es la operación por la cual se desactivan o eliminan los posibles
patógenos que pueda contener. La desactivación de los microorganismos supone la
supresión de su capacidad de reproducción y crecimiento en la extensión suficiente para
cumplir con los criterios sanitarios de calidad establecidos por la legislación vigente (En
España y en agua potable el R.D. 140/2003, de 7 de febrero, por el que se establecen los
criterios sanitarios de la calidad del agua de consumo humano). La eliminación de bacterias
se puede llevar a cabo mediante membranas de microfiltración, mientras que para los virus
se requiere el uso de membranas de ultrafiltración. Aparte de los procesos de separación
física, se pueden emplear agentes de desinfección, que pueden ser físicos o químicos. Entre
los primeros se encuentran los tratamientos térmicos, la radiación ultravioleta y los
ultrasonidos. Los agentes químicos son el cloro y sus derivados y el ozono, además de otros
menos empleados como el permanganato o determinadas sales metálicas.
El cloro, particularmente en forma de cloro gas, Cl2, es el más frecuentemente utilizado en
las plantas de potabilización de agua. Otras formas de dosificación de cloro son las
disoluciones de hipoclorito sódico, NaOCl; el hipoclorito cálcico en forma sólida, Ca(OCl)2; el
dióxido de cloro, ClO2, que se produce in situ por reacción entre cloro gas o ácido clorhídrico,
HCl(aq), con clorito de sodio, y las cloraminas, producidas por la combinación de cloro libre y
amonio. El ozono, O3, es un gas con una gran capacidad de desinfección cuyo poder oxidante
permite la eliminación simultánea de sustancias orgánicas e inorgánicas tales como sales de
hierro y manganeso y compuestos de azufre. El uso del ozono se tratará en detalle en el
capítulo 51.
50. 2. Exposición al desinfectante: parámetro c · t
La velocidad de desactivación de un determinado microrganismo depende de la
concentración de desinfectante y del tiempo en el que este actúe. La relación matemática
más usual es la cinética de Chick-Watson:
= − [50.1]
Siendo N el número de microorganismos de un tipo determinado, kCW, su constante de
inactivación o de letalidad, c la concentración de desinfectante, t el tiempo de contacto y n
un orden de reacción, usualmente comprendido entre 0.8 y 1.2 por lo que se suele
Roberto Rosal Página 1
Ecuaciones y cálculos para el tratamiento de aguas
aproximar a la unidad. En forma integrada la cinética de Chick-Watson se corresponde con la
siguiente expresión:
= − [50.2]
La exposición del microorganismo al agente desinfectante se calcula como el área bajo la
curva C(t) desde t = 0 hasta un tiempo genérico, t:
· = [50.3]
Las unidades de c · t son mg min L-1 o análogas. En caso de que la concentración sea
constante o se pueda extraer un valor medio, c · t es simplemente el producto de la
concentración por el tiempo de actuación del desinfectante. En caso de que la concentración
sea constante a partir de 50.2 y para n = 1 se obtiene:
· = − [50.4]
Por tanto, conociendo la constante de letalidad de Chick-Watson para unas condiciones
dadas y el grado de desinfección deseado se puede estimar el valor de c · t objetivo. La
Figura 50.1 muestra algunos ejemplos de combinaciones c · t en desinfección de agua
potable. En la práctica se producen ciertas desviaciones de la cinética de Chick-Watson,
siendo éstas habituales a concentraciones de desinfectante bajas debido a la reacción del
desinfectante con compuestos presentes en el agua y a concentraciones elevadas debido a
cambios fisiológicos en los microorganismos o a la aparición de subpoblaciones resistentes.
Figura 50.1. Relación c · t (exposición) para diversos sistemas de desinfección (La flecha se
refiere al ejemplo 50.1)
Roberto Rosal Página 2
Ecuaciones y cálculos para el tratamiento de aguas
Habitualmente la eficacia de inactivación de microorganismos se expresa en forma
logarítmica como “x-log”, siendo x-log:
− = − [50.5]
Es decir, una eficacia 1-log supone una inactivación del 90% de los microorganismos en la
población inicial, 2-log un 90%, 3-log un 99.9% y así sucesivamente. Los patógenos
usualmente más resistentes a la desinfección son los virus entéricos (rotavirus, hepatovirus)
y los protozoos parásitos (Giardia lamblia). También son particularmente resistentes las
esporas bacterianas como las de la bacteria anaerobia Clostridium perfringens, de origen
esencialmente fecal y que se asocian a contaminación por aguas residuales, por lo que es
uno de los organismos indicadores cuyo control establece la legislación. Los desinfectantes
se dosifican para los microrganismos más resistentes y así, la exposición necesaria para una
inactivación 3-log de G. lamblia es suficiente para asegurar una desinfección 4-log de todos
los virus importantes, por lo que la práctica habitual es fijar la dosis para el organismo
indicador e ignorar el resto.
Un aspecto relevante para el cálculo de la exposición al desinfectante es la estimación
correcta del tiempo de contacto. Si el desinfectante se introduce en una conducción en flujo
turbulento, el tiempo de contacto será el volumen interior del conducto dividido entre el
caudal de agua; pero en el caso de tanques u otros dispositivos con retromezcla es necesario
introducir un parámetro de mezcla. Es habitual tomar el tiempo de contacto como t10, que
es el tiempo que corresponde al 10% de elementos de fluido con menor tiempo de
residencia:
= ! " [50.6]
Fm es el factor de mezcla y τ el tiempo espacial o cociente entre el volumen de líquido y el
caudal de alimentación. El factor de mezcla varía entre 0.1 para tanque agitado sin divisiones
y 1.0 para conducciones con flujo turbulento. Si, por ejemplo, en una balsa de contacto se
introducen dos divisiones para crear tres tanques en serie entre la entrada y la salida Fm =
0.3. Para otras posibilidades los factores se encuentran tabulados en la bibliografía.
50. 3. Química de los desinfectantes basados en cloro
La cloración es el método usual de desinfección de agua potable y el más usado desde su
implantación hace casi un siglo por su facilidad de uso y su bajo coste. Tanto si se utiliza
como gas como si la forma de dosificación es un hipoclorito, la química es la misma ya que
las reacciones de disociación son instantáneas y el equilibrio de la primera está desplazado
hacia la derecha:
# $ + &$ ' → &# ' + & ) + # *
[50.7]
Roberto Rosal Página 3
Ecuaciones y cálculos para el tratamiento de aguas
&'# ⇋ # '* + & ) [50.8]
La constante de equilibrio de la segunda reacción es:
0 123 4 05 6 4
, 20 °# = 052 14
= 2,0 10*9 : /< [50.9]
El valor del pH determina las concentraciones relativas de ambas especies. A partir de 50.9
se obtiene un valor de [ClO-] = [HOCl] para pH = 8,3 por lo que a pH < 8.3 predomina el ácido
hipocloroso, que es un biocida más eficaz que el hipoclorito en el rango de pH usual en los
tratamientos de potabilización. A la suma de ácido hipocloroso e hipoclorito se le denomina
“cloro residual libre”.
El cloro reacciona con especies reductoras presentes en el agua tales como manganeso,
hierro, nitritos, sulfuros, con la materia orgánica y, significativamente, con el amoníaco
dando lugar a las reacciones siguientes:
&= + &'# → &$ # + &$ ' [50.10]
&$ # + &'# → &# $ + &$ ' [50.11]
&# $ + &'# → # = + &$ ' [50.12]
Estas reacciones generan una demanda inmediata de cloro y las tres indicadas
anteriormente producen cloraminas. Las cloraminas son también agentes desinfectantes
que si bien tienen una eficacia menor que el sistema HOCl/ClO- se mantienen activas por
más tiempo en la conducción de agua, motivo por el cual se utilizan como desinfectantes
secundarios. Como resultado de estas reacciones la curva de cloro residual frente al cloro
dosificado (Figura 50.2) presenta un mínimo que corresponde al momento en el cual las
reacciones con el amonio dejan de consumir cloro y este puede acumularse en el agua en
forma de cloro residual libre. A la técnica de cloración que consiste en añadir cloro más allá
del mínimo de la curva, se la denomina cloración residual libre (breakpoint chlorination) y es
la más usada en la práctica. Otra posibilidad es la cloración residual combinada en la cual se
dosifica el cloro para que reaccione con el amoníaco sin llegar a la destrucción total de éste,
de manera que sea este cloro residual combinado el encargado de mantener la actividad
antimicrobiana en la red. La suma del cloro residual libre y el combinado constituye el cloro
residual total.
En las conducciones de distribución de agua potable es necesario mantener un cierto nivel
de desinfectante residual. En muchas ocasiones, en lugar de incrementar los niveles de cloro
residual libre, se adicionan cloraminas que, además de actuar como desinfectante
secundario durante un tiempo prolongado, permiten reducir la exposición al cloro y con ello
la formación de subproductos halogenados de desinfección, principalmente trihalometanos.
Roberto Rosal Página 4
Ecuaciones y cálculos para el tratamiento de aguas
Figura 50.2. Ejemplo de curva de cloración mostrando las cantidades de cloro residual libre y
combinado. (Los datos y las flechas se refieren al ejemplo 50.4)
50. 4. Radiación ultravioleta
A diferencia de los tratamientos basados en la utilización de productos químicos, la
desinfección de agua mediante el uso de radiación ultravioleta (UV) es un proceso físico por
el cual los microorganismos expuestos a longitudes de onda germicidas, se vuelven inviables
o incapaces de reproducirse e infectar. La luz UV se subdivide, de menor a mayor energía en
UV-A (400 nm - 315 nm), UV-B (315 nm - 280 nm) y UV-C (280 nm - 200 nm), siendo esta
última la que tiene eficacia germicida. Esto es así porque la máxima absorción de la radiación
por parte del ADN tiene lugar a 200 nm y 265 nm. A 200 nm la absorción se produce en el
esqueleto ribosa-fosfato y a 265 nm la absorción tiene lugar en las bases nitrogenadas. El
daño principal consiste en la creación de enlaces entre dos grupos tiamina adyacentes con lo
que los microorganismos pierden su posibilidad de reproducirse o de sintetizar proteínas
esenciales. En la práctica se utilizan lámparas de vapor de mercurio de baja presión, que
tienen un espectro de emisión muy estrecho (254 nm + una línea menor a 185 nm en
lámparas con envoltura de cuarzo), o lámparas de media presión, que presentan un espectro
con múltiples picos entre 250 y 600 nm y son de mayor intensidad, aunque su eficacia en la
conversión de energía eléctrica en UV-C es menor (15% frente a 40% de las de baja presión).
La energía requerida para una desinfección dada se denomina dosis, que es el producto de la
tasa de fluencia por el tiempo de aplicación:
?
> !@
= A′
!@
C [50.13]
Roberto Rosal Página 5
Ecuaciones y cálculos para el tratamiento de aguas
E' o tasa de fluencia es la energía que atraviesa en todas direcciones una esfera de área
diferencial dividida entre su superficie. (La tasa de fluencia a veces se denomina
erróneamente “intensidad de radiación”, que es otro concepto.) Las dosis objetivo para
distintos microorganismos y grados de eficacia se recogen en tablas ampliamente
difundidas. Por ejemplo, una reducción 2-log de un cultivo de E. coli requiere una dosis de 9
mJ/cm2, mientras que microorganismos más resistentes como Bacillus subtilis o C.
perfringens requieren 46 y 95 mJ/cm2 respectivamente para un mismo grado de
desinfección.
En todo caso, las dosis deben de incrementarse debido a factores operativos que limitan la
eficacia de la desinfección tales como agregación de microorganismos, asociación de estos
con partículas, efecto sombra de material particulado en suspensión o la capacidad que
poseen los microrganismos para autorreparar los daños producidos por la radiación. La
reparación puede producirse en oscuridad, en el período subsiguiente a la irradiación o
activada por luz visible (que emiten las propias lámparas de mercurio de media presión, por
ejemplo). Los mecanismos de reparación permiten reactivar hasta el 1% del total de
microorganismos originales.
La desactivación de microorganismos por radiación UV puede modelizarse mediante la
expresión cinética de Hom, similar a la indicada en 50.1/2; pero sustituyendo la
concentración de desinfectante por la tasa de fluencia de la radiación:
= −: DE AF !*
[50.14]
Que en forma integrada da lugar a la siguiente expresión:
= − DE AF !
[50.15]
El modelo 50.14/15 se reduce a Chick-Watson de orden “n” para m = 1 y predice
menores eficacias de desinfección a dosis bajas y altas para m > 1 y m < 1 respectivamente,
que son fenómenos asociados a la autoreparación, la formación de agregados de
microrganismos y el efecto de las partículas en suspensión.
Para calcular la tasa de fluencia efectiva se suele aplicar un factor de corrección de 0,85 que
tiene en cuenta las variaciones de intensidad de emisión de un punto a otro de las lámparas,
ya que esta tiende a disminuir en los extremos con el uso. La transmitancia del fluido a la
radiación UV depende de las características del agua y a falta de medidas precisas se puede
aproximar por un coeficiente corrector del 0,75 para unidades de pequeño tamaño en las
que no se dispone de mejores datos.
Roberto Rosal Página 6
Ecuaciones y cálculos para el tratamiento de aguas
ii. Cálculos
50.1. Cálculo de exposición al desinfectante.
En una conducción se inyecta cloro 50 m antes de la primera toma de agua. El diámetro
nominal de la acometida es de 40 mm con un espesor de tubo de 4,0 mm. El máximo
caudal de agua es 2.5 L/s y la mínima concentración de cloro residual es de 1,2 mg/L. El pH
del agua es 7,5 y su temperatura es de 10 °C. ¿Cuál es la exposición al desinfectante?
Solución:
El volumen de agua en la conducción es:
40 − 2 ∙ 4 $
G ∙ 50 ∙ J L = 0,161 :=
1000
El tiempo mínimo que transcurre hasta el primer punto de toma de agua es:
0,161 :=
= 643 C = 1,07 :P
2,5
1000 : = /C
: :P
· = 1,2 : /< 1,07 :P = 1,29
<
La exposición corresponde al punto señalado con una flecha en la Figura 50.1.
50.2. Cálculo del tiempo de contacto para una eficacia de desinfección dada.
En una cloración de un agua potable, se observa que con una concentración de 0,1 mg/L de
cloro libre se produce una reducción de un 99 % de la población de bacterias en 5 min.
¿Qué tiempo de contacto sería necesario para aumentar la eficacia de la desinfección a 3-
log si la concentración de cloro libre se reduce a 0,06 mg/L? Se puede suponer que se
cumple la cinética de Chick-Watson de primer orden.
Solución:
A partir de la expresión 50.2:
1
− J L = − 0,1 : /< 5 :P
100
De donde se obtiene la constante de letalidad, kCW = 9,2 L mg-1 min-1. Para una eficacia del
99,9% y C = 0,02 mg/L, el tiempo necesario es:
1
= 1000 = 12,5 :P
9,2 < : * :P * 0,06 : /<
50.3. Tiempo de contacto en un sistema con mezcla.
Un sistema de desinfección está constituido por un tanque de 20 m3 de capacidad al que se
añade el cloro suficiente para una reducción 3-log de G. lamblia. El volumen ocupado del
Roberto Rosal Página 7
Ecuaciones y cálculos para el tratamiento de aguas
tanque es como mínimo 10 m3. El máximo caudal de alimentación es de 0,05 m3/mim, el
pH es 7,0 y la temperatura es de 10 °C. La concentración mínima de cloro residual libre es
de 2,0 mg/L. Determinar si es posible llevar a cabo la desinfección y qué posibles
actuaciones se podrían llevar a cabo en caso negativo.
Solución:
En primer lugar, se debe de obtener el valor de c · t objetivo. En la Figura 50.1 se puede leer
que el tiempo necesario es de 60 min (aproximadamente).
: :P
· RSTU VWR = 2 : /< 60 :P = 120
<
El valor real de c · t, en cambio, es (Fm = 0.1):
10 := : :P
· XUY1 = 2 : /< 0,1 Z [ = 40
0,05 : /:P
= <
Obviamente, la desinfección es insuficiente para el propósito indicado, pero si se introducen
dos divisiones verticales en el tanque de forma que se convierta en un sistema de tres
tanques en serie, Fm sería ahora 0,3 y la desinfección deseada resultaría factible:
10 := : :P
· XUY1 = 2 : /< 0,3 Z [ = 120
0,05 := /:P <
50.4. Demanda de desinfectante para un cloro residual libre dado.
Determinar la cantidad diaria de hipoclorito sódico que se necesita para clorar el agua al
que se refiere la Figura 50.2 produciendo una concentración de cloro residual libre de 0,4
mg/L para un caudal tratado de 4500 m3/día de agua. ¿Qué dosis sería necesaria para
obtener una concentración de cloro residual combinado de 0,35 mg/L?
Solución:
La cantidad de cloro residual combinada se obtiene del mínimo de la curva de la Figura 50.2
(punto 1), que es 0,3 mg/L para una dosis de 1,7 mg/L en el breakpoint. La dosis requerida
para obtener un cloro residual total de 0,3 + 0,4 = 0,7 mg/L es aproximadamente 2,3 mg/L.
Para obtener una concentración de cloro residual combinado de 0,35 mg/L es preciso no
superar el breakpoint. De la Figura 50.2 (punto 2) se obtiene una dosis de 0,5 mg/L. Para
obtener dosis de 2.3 y 0.5 mg/L de cloro (Cl2) se necesita, aplicando la estequiometría de la
reacción 50.7 (1:1) y los pesos moleculares de hipoclorito (74,5 g/mol) y cloro (71 g/mol), se
obtienen las cantidades solicitadas:
Roberto Rosal Página 8
Ecuaciones y cálculos para el tratamiento de aguas
74,5 : ]# ' 1000 < 1 ]'#
4500 := / í] 2,3 : # $ /< J LJ L J L = 10,9
71 : # $ 1 := 10^ : í]
Análogamente, para una dosis de 0,5 mg/L se necesitan 2,36 kg NaOCl/día.
50.5. Dosis de radiación ultravioleta necesaria para una desinfección.
Una lámpara de mercurio de baja presión emite una tasa de fluencia en su punto central
de 5,5 mW/cm2. La cámara de irradiación tiene un volumen libre de 6,3 L y el flujo máximo
que se desea es de 15 L/min. ¿Sería suficiente para una inactivación 2-log de C.
perfringens?
Solución:
La corrección correspondiente a la lámpara da una tasa de fluencia promedio de (5,5) (0,85)
= 4,68 mW/cm2 y un valor efectivo, considerando la corrección por la transmitancia del
agua, de (4,68) (0,75) = 3,51 mW/cm2. El tiempo de retención (tiempo espacial) es:
6,3 <
= 0,42 min = 25,2 C
15 </:P
La dosis sería, por tanto:
:b :b
> = J3,51 L 25,2 C = 88,5 $
C : $ :
Para reducir 2-log C. perfringens se requieren 95 mJ/cm2 respectivamente, algo más de lo
que da el sistema propuesto. Se podría reducir ligeramente el flujo para conseguirlo: con 14
L/min ya se alcanzaría la dosis de 95 mJ/cm2. Sin embargo, el coeficiente corrector de la
transmitancia (75%) es bastante conservador y salvo aguas superficiales con gran cantidad
de sólidos en suspensión, es improbable que la transmitancia baje del 80%. En caso de un
exceso de sólidos se podrían eliminar con un tratamiento previo.
50.6. Cinética de desinfección mediante radiación ultravioleta.
Los datos indicados corresponden a una desinfección mediante radiación UV de cultivos de
E. coli K-12 (ATCC 25253). Determinar si se sigue la cinética de la inactivación de Hom y
calcular la constante kUV suponiendo que n = 1.
t(min) 0 3 5 7 10 13 17 20
Dosis (mJ/cm2) 0 3,96 6,61 9,25 13,2 17,2 22,5 26,4
x-log 0 0,270 0,372 0,448 0,522 0,541 0,739 0,896
* Int. J. Food Microbiol. 142, 341, 2010
Solución:
La cinética de Hom integrada (50.16) permite relacionar la reducción de la concentración de
microorganismos con el tiempo:
Roberto Rosal Página 9
Ecuaciones y cálculos para el tratamiento de aguas
= 2,303 = − DE AF !
La tasa de fluencia se puede obtener fácilmente como constante de proporcionalidad entre
la dosis y el tiempo:
!
A F = 0,022 d!@
Tomando logaritmos en la primera expresión:
e− f= 0 DE A F 4 + :
Representando el primer miembro frente a ln(t) se obtiene una línea recta de pendiente m:
0.8
0.6
0.4
ln[-ln(N/No)]
0.2
0.0
-0.2
m = 0,603
-0.4
-0.6
0.5 1.0 1.5 2.0 2.5 3.0 3.5
ln(t)
La ordenada en el origen es ln[kUV (E’)n] y si n = 1, DE A′ = −1,15 y kUV = 14,4 cm2 mW-
1 s-0,603. Lógicamente las unidades dependen de m.
Bibliografía:
Bolton, J.R., Cotton, C.A., The Ultraviolet Disinfection Handbook, American Water Works Association,
2008.
Howe, K.J., Hand, D.W., Crittenden, J.C., Trussell, R.R., Tchobanoglous. G., Principles of Water
Treatment, John Wiley & Sons, New Jersey, 2012, pp. 525-584.
Metcalf & Eddy Inc. Tchobanoglous, G., Burton, F.L., Stensel, H.D., Wastewater Engineering:
Treatment and Reuse, McGraw-Hill, 2003, pp. 1217-1343.
Roberto Rosal P á g i n a 10
También podría gustarte
- Manual práctico de ensayos de toxicidad en medio acuático con organismos del género DaphniaDe EverandManual práctico de ensayos de toxicidad en medio acuático con organismos del género DaphniaCalificación: 1 de 5 estrellas1/5 (1)
- Programación y control del riego y la fertilización de los cultivos. AGAU0208De EverandProgramación y control del riego y la fertilización de los cultivos. AGAU0208Aún no hay calificaciones
- Camara de ContactoDocumento6 páginasCamara de Contactoadonis100% (3)
- Camara de ContactoDocumento6 páginasCamara de ContactoMaru BaidaAún no hay calificaciones
- Control de La Desinfeccion CL O3 PDFDocumento69 páginasControl de La Desinfeccion CL O3 PDFCarlos MendozaAún no hay calificaciones
- Determinación de La Demanda de Cloro para La Desinfección de Una Muestra de Agua FINDocumento11 páginasDeterminación de La Demanda de Cloro para La Desinfección de Una Muestra de Agua FINJulián Tobón González100% (1)
- DesinfeccionDocumento6 páginasDesinfeccionSantiago RolleroAún no hay calificaciones
- DesinfeccionDocumento61 páginasDesinfeccionJuan Carlos CorderoAún no hay calificaciones
- DesinfecciónDocumento8 páginasDesinfecciónAndrés SalazarAún no hay calificaciones
- Desinfección del agua con cloro y cloraminas: alternativas para mantener un residualDocumento10 páginasDesinfección del agua con cloro y cloraminas: alternativas para mantener un residualJohao Girón AzañeroAún no hay calificaciones
- Desinfección-Cloración y UVDocumento50 páginasDesinfección-Cloración y UVLuis Adolfo Morello100% (1)
- DESINFECCIONDocumento8 páginasDESINFECCIONYurley LopezAún no hay calificaciones
- Carpeta de Cloracion de Agua Grupo 3Documento17 páginasCarpeta de Cloracion de Agua Grupo 3David RobalinoAún no hay calificaciones
- Ubicación Óptima de Estaciones de Reinyección de Cloro en Redes de Abastecimiento de Agua PotableDocumento7 páginasUbicación Óptima de Estaciones de Reinyección de Cloro en Redes de Abastecimiento de Agua PotableDanielCervantesAún no hay calificaciones
- 7 Desinfección CT Capitulo7Documento21 páginas7 Desinfección CT Capitulo7erikAún no hay calificaciones
- Ecuaciones y Cálculos para El Tratamiento de Aguas: Capítulo 51: OzonizaciónDocumento11 páginasEcuaciones y Cálculos para El Tratamiento de Aguas: Capítulo 51: OzonizaciónMayerly Giraldo AvilaAún no hay calificaciones
- Introduccion TratamientoDocumento12 páginasIntroduccion TratamientoIsa BelitaAún no hay calificaciones
- DESINFECCIONDocumento17 páginasDESINFECCIONÁngel DavidAún no hay calificaciones
- Propiedades y uso del cloro como desinfectanteDocumento3 páginasPropiedades y uso del cloro como desinfectanteVictor Jm BpmAún no hay calificaciones
- Desinfección del agua con cloro y cloraminasDocumento13 páginasDesinfección del agua con cloro y cloraminasYDO AYME MAYRA ALEJANDRAAún no hay calificaciones
- Reactor de Clorinacion - Tratamiento de Aire, Agua y SueloDocumento10 páginasReactor de Clorinacion - Tratamiento de Aire, Agua y SueloYesenia Sullca RomeroAún no hay calificaciones
- Desinfección del aguaDocumento61 páginasDesinfección del agualoliaguirre55Aún no hay calificaciones
- DESINFECCIÓNDocumento9 páginasDESINFECCIÓNChristian Dominguez VillafanaAún no hay calificaciones
- Preinforme de Laboratorio Sección Iii PDFDocumento42 páginasPreinforme de Laboratorio Sección Iii PDFManuel RamosAún no hay calificaciones
- Ecuaciones Diferenciales ProyectoDocumento10 páginasEcuaciones Diferenciales ProyectoLaura PachecoAún no hay calificaciones
- Métodos de Desinfección Del AguaDocumento4 páginasMétodos de Desinfección Del Agualury sibelit100% (1)
- Procesos de desinfección del aguaDocumento26 páginasProcesos de desinfección del aguaDavid Eduardo E. CrespoAún no hay calificaciones
- Demanda de CloroDocumento48 páginasDemanda de CloroMiguel AceroAún no hay calificaciones
- Clase 8 CloraciónDocumento27 páginasClase 8 CloraciónKatherine BedoyaAún no hay calificaciones
- DesinfecciónDocumento38 páginasDesinfecciónHernan D. RuidiazAún no hay calificaciones
- Medicion de Cloro y Demanda de CloroDocumento3 páginasMedicion de Cloro y Demanda de CloroDANNA GABRIELA VALENCIA CAICEDOAún no hay calificaciones
- Curva de CloroDocumento12 páginasCurva de ClororubyyamileAún no hay calificaciones
- Cloracion de AguaDocumento6 páginasCloracion de AguaIvanovich SalasAún no hay calificaciones
- El Factor CTDocumento3 páginasEl Factor CTMhax ̺̿a̺̿n̺̿t̺̿h̺̿o̺̿n̺̿y̺̿ ThumyAún no hay calificaciones
- 368 Parte 111Documento48 páginas368 Parte 111Ricardo Gamero ClaaveriasAún no hay calificaciones
- Cloración Del Agua ResidualDocumento8 páginasCloración Del Agua ResidualcesarAún no hay calificaciones
- T3. Desinfección de AguasDocumento89 páginasT3. Desinfección de AguasCris100% (1)
- Determinación de CloroDocumento14 páginasDeterminación de CloroAlexis Puente BurgaAún no hay calificaciones
- Soluciones Integrales para La Medición y Control de Cloro Residual en Agua de Proceso Ing Mauricio Pinzón JiménezDocumento42 páginasSoluciones Integrales para La Medición y Control de Cloro Residual en Agua de Proceso Ing Mauricio Pinzón JiménezCésar Torrejón PrietoAún no hay calificaciones
- (SABA) Cloración y DesinfeccionDocumento123 páginas(SABA) Cloración y Desinfecciongrelyop0% (1)
- Desinfección RilesDocumento30 páginasDesinfección RilesLili Jara CastilloAún no hay calificaciones
- VelasquezMedinaDanielFelipe2013 PDFDocumento9 páginasVelasquezMedinaDanielFelipe2013 PDFJuan Jimenez JiménezAún no hay calificaciones
- TP Desinfecccion Presentacion 2013Documento20 páginasTP Desinfecccion Presentacion 2013Nay Esperanza Jauregui MixanAún no hay calificaciones
- CLORACIONDocumento12 páginasCLORACIONSilviaLimenAún no hay calificaciones
- Ejercicios Reactores 2019-2020Documento11 páginasEjercicios Reactores 2019-2020Luisa BolañosAún no hay calificaciones
- Cómo Se Potabilizan Las Aguas para El Consumo HumanoDocumento3 páginasCómo Se Potabilizan Las Aguas para El Consumo HumanoArnold MijailAún no hay calificaciones
- Cuestionario de Prevención y Control de La Contaminación Del AguaDocumento12 páginasCuestionario de Prevención y Control de La Contaminación Del Aguajackieline93Aún no hay calificaciones
- Practica 03 - Cloro Residual en AguasDocumento12 páginasPractica 03 - Cloro Residual en AguasDiana VentAún no hay calificaciones
- Camara de Contacto de CloroDocumento11 páginasCamara de Contacto de CloroHarold Klinton Surichaqui Gomes100% (5)
- 02 Cloración y DesinfecciónDocumento62 páginas02 Cloración y DesinfecciónChanita Melchor AlmonacidAún no hay calificaciones
- Taller 2 Reacciones CineticasDocumento4 páginasTaller 2 Reacciones CineticasDiana S. VásquezAún no hay calificaciones
- Determinación de la demanda de cloroDocumento11 páginasDeterminación de la demanda de cloroNatalie Muñoz GutierrezAún no hay calificaciones
- Break PointDocumento11 páginasBreak PointfernandovillotaAún no hay calificaciones
- Informe de Cloro ResidualDocumento27 páginasInforme de Cloro ResidualAlex Escobedo FloresAún no hay calificaciones
- Plantas piloto de tratamiento de agua potable y agua residualDe EverandPlantas piloto de tratamiento de agua potable y agua residualCalificación: 5 de 5 estrellas5/5 (1)
- Aguas residuales: una visión integralDe EverandAguas residuales: una visión integralCalificación: 5 de 5 estrellas5/5 (1)
- UF1667 - Tratamiento de agua potableDe EverandUF1667 - Tratamiento de agua potableCalificación: 4.5 de 5 estrellas4.5/5 (2)
- UF1671 - Mantenimiento del entorno de plantas de tratamiento de agua y plantas depuradorasDe EverandUF1671 - Mantenimiento del entorno de plantas de tratamiento de agua y plantas depuradorasCalificación: 5 de 5 estrellas5/5 (1)
- Técnicas analíticas básicas: En el control de la calidad del agua según normatividadDe EverandTécnicas analíticas básicas: En el control de la calidad del agua según normatividadAún no hay calificaciones
- Calidad de Aguas: Usos y AprovechamientoDe EverandCalidad de Aguas: Usos y AprovechamientoCalificación: 5 de 5 estrellas5/5 (1)
- Archivodiapositiva 202362693639Documento56 páginasArchivodiapositiva 202362693639JULIO JUAN MUÑOZ FARFANAún no hay calificaciones
- Tarea Estadistica R1Documento16 páginasTarea Estadistica R1JULIO JUAN MUÑOZ FARFANAún no hay calificaciones
- Alabanza EzequiasDocumento1 páginaAlabanza EzequiasJULIO JUAN MUÑOZ FARFANAún no hay calificaciones
- Tesis Prototipo PDFDocumento89 páginasTesis Prototipo PDFOswaldo GuerraAún no hay calificaciones
- S11-Tarea - 2 - Grupo DDocumento22 páginasS11-Tarea - 2 - Grupo DJULIO JUAN MUÑOZ FARFANAún no hay calificaciones
- Archivodiapositiva 202362693639Documento56 páginasArchivodiapositiva 202362693639JULIO JUAN MUÑOZ FARFANAún no hay calificaciones
- Test 4 Lodos Activos AlcazxarDocumento2 páginasTest 4 Lodos Activos AlcazxarJULIO JUAN MUÑOZ FARFANAún no hay calificaciones
- Curso Contaminacion 2 A Parte 2008Documento88 páginasCurso Contaminacion 2 A Parte 2008JULIO JUAN MUÑOZ FARFANAún no hay calificaciones
- La Gestion de Residuos Solidos en Milagro - Tema - 1P - 2023Documento24 páginasLa Gestion de Residuos Solidos en Milagro - Tema - 1P - 2023JULIO JUAN MUÑOZ FARFANAún no hay calificaciones
- Análisis FODA Empresa Editora QueyámDocumento5 páginasAnálisis FODA Empresa Editora QueyámJULIO JUAN MUÑOZ FARFAN100% (1)
- Semana 5Documento22 páginasSemana 5JULIO JUAN MUÑOZ FARFANAún no hay calificaciones
- 5 - Estudio Armónico de Marea LebuDocumento4 páginas5 - Estudio Armónico de Marea LebuOscar Burgos OrtizAún no hay calificaciones
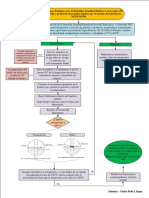
- Diagrama de Flujo - ASTM D1298 - Cintia Felix PDFDocumento1 páginaDiagrama de Flujo - ASTM D1298 - Cintia Felix PDFCintia FelixAún no hay calificaciones
- Primer Examen Parcial HDPDocumento4 páginasPrimer Examen Parcial HDPJose David Escobar Muñoz0% (1)
- Colgii05 Algebra Matematica Discreta Trabajo EditadoDocumento5 páginasColgii05 Algebra Matematica Discreta Trabajo EditadoMiguel AngelAún no hay calificaciones
- Una Señal PWMDocumento5 páginasUna Señal PWMonepiece24Aún no hay calificaciones
- LAB 05 Simulación e Implementación de Un Circuito de Control de Velocidad de Un Motor CCDocumento3 páginasLAB 05 Simulación e Implementación de Un Circuito de Control de Velocidad de Un Motor CCVICENTE ALEXANDER CONDORI HUILLCAAún no hay calificaciones
- Biomecanica de La Cadera - FinalDocumento29 páginasBiomecanica de La Cadera - FinalCrisAme TPAún no hay calificaciones
- Modulo de Administracion de RedesDocumento33 páginasModulo de Administracion de RedesOriental EstereoAún no hay calificaciones
- Mquina Tipo GDocumento37 páginasMquina Tipo GjimmytoroAún no hay calificaciones
- Reacciones Aldehidos CetonasDocumento7 páginasReacciones Aldehidos CetonasPaulina LopezAún no hay calificaciones
- Fuente Auxiliar o StandbyDocumento8 páginasFuente Auxiliar o StandbyMechín Rodriguez EjvrAún no hay calificaciones
- Docsity Apuntes Sobre La Fisica en La Anestesiologia PDFDocumento64 páginasDocsity Apuntes Sobre La Fisica en La Anestesiologia PDFMarco CamposAún no hay calificaciones
- Almacenamiento LPG TQDocumento8 páginasAlmacenamiento LPG TQguillermo_f_4Aún no hay calificaciones
- ACL ExtendidaDocumento3 páginasACL ExtendidauraharadonoAún no hay calificaciones
- Transporte, Asignaci-N y TransbordoDocumento34 páginasTransporte, Asignaci-N y TransbordoJaneth BedoyaAún no hay calificaciones
- ADEL35LZ EspañolDocumento1 páginaADEL35LZ EspañolJhon GarciaAún no hay calificaciones
- AjaxDocumento123 páginasAjaxhipolito100% (1)
- Imfluencia de La Luna y Del Sol en La AgriculturaDocumento6 páginasImfluencia de La Luna y Del Sol en La AgriculturaDannyEstrada100% (1)
- Autoprueba EEC IV - Inyección de Combustible Ford y Control Electrónico Del Motor EEC IV - EEC 4 - TroubleCodes - Net (Español)Documento10 páginasAutoprueba EEC IV - Inyección de Combustible Ford y Control Electrónico Del Motor EEC IV - EEC 4 - TroubleCodes - Net (Español)Juan Pablo Rey BravoAún no hay calificaciones
- CT Geometría5°Documento92 páginasCT Geometría5°Lazaro Berrocal Muje45% (11)
- Utilizar Símbolos en Los Formatos de ExcelDocumento3 páginasUtilizar Símbolos en Los Formatos de Excelsecretariadoies5Aún no hay calificaciones
- Practica 2 Mecanica de FluidosDocumento23 páginasPractica 2 Mecanica de FluidosAdolfo AlmonteAún no hay calificaciones
- Ati 5005Documento2 páginasAti 5005José Roberto Esquivel RuisecoAún no hay calificaciones
- Tarea 2 - Dibujo de piezas con spectraCAD Engraver y funciones CNCDocumento6 páginasTarea 2 - Dibujo de piezas con spectraCAD Engraver y funciones CNCJose Daniel Ochoa MoyaAún no hay calificaciones
- Factorizacion ColoquioDocumento18 páginasFactorizacion ColoquioIsabel NolascoAún no hay calificaciones
- Los Cuentos 1.1Documento8 páginasLos Cuentos 1.1PRIMOAún no hay calificaciones
- Instalacion de Linux Mint Manual PDFDocumento21 páginasInstalacion de Linux Mint Manual PDFぱちん けんかAún no hay calificaciones
- Proceso de Compresión IsotérmicoDocumento5 páginasProceso de Compresión IsotérmicoCristian Diaz33% (3)
- Asignatura: Actividad de Aprendizaje NO. Tema DesarrolladoDocumento20 páginasAsignatura: Actividad de Aprendizaje NO. Tema DesarrolladoKARLA HAYDEE MARTINEZ SALASAún no hay calificaciones
- Normas y Prácticas Recomendadas API en Fluidos de PerforaciónDocumento1 páginaNormas y Prácticas Recomendadas API en Fluidos de PerforaciónAngélicaArdilaAún no hay calificaciones