Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Analítica
Analítica
Cargado por
Diana Téllez0 calificaciones0% encontró este documento útil (0 votos)
7 vistas1 páginaSe mezclaron 50 ml de una solución de níquel 0.03 M y 50 ml de una solución de EDTA 0.05 M a pH 3 para calcular la concentración de níquel resultante. Usando las concentraciones iniciales, el equilibrio de formación del complejo NiY2- y la constante de formación del complejo, se calculó que la concentración final de níquel era de 1.4x10-8 M.
Descripción original:
Derechos de autor
© © All Rights Reserved
Formatos disponibles
DOCX, PDF, TXT o lea en línea desde Scribd
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoSe mezclaron 50 ml de una solución de níquel 0.03 M y 50 ml de una solución de EDTA 0.05 M a pH 3 para calcular la concentración de níquel resultante. Usando las concentraciones iniciales, el equilibrio de formación del complejo NiY2- y la constante de formación del complejo, se calculó que la concentración final de níquel era de 1.4x10-8 M.
Copyright:
© All Rights Reserved
Formatos disponibles
Descargue como DOCX, PDF, TXT o lea en línea desde Scribd
0 calificaciones0% encontró este documento útil (0 votos)
7 vistas1 páginaAnalítica
Analítica
Cargado por
Diana TéllezSe mezclaron 50 ml de una solución de níquel 0.03 M y 50 ml de una solución de EDTA 0.05 M a pH 3 para calcular la concentración de níquel resultante. Usando las concentraciones iniciales, el equilibrio de formación del complejo NiY2- y la constante de formación del complejo, se calculó que la concentración final de níquel era de 1.4x10-8 M.
Copyright:
© All Rights Reserved
Formatos disponibles
Descargue como DOCX, PDF, TXT o lea en línea desde Scribd
Está en la página 1de 1
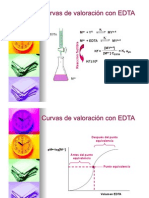
Se desea calcular la concentración de níquel en una solución que se preparó
mezclando 50 ml de Ni2+ 0.03 M con 50 ml de EDTA 0.05 M a pH = 3.
Ni= 1.4*10-8M
CNiY2-= 50*(0.03/100) = 0.015
50∗0.05−50∗0.03
CEDTA=
100
= 0.01M
0.015
KMY= = 4KMY
¿¿
= (2.5*10-11) (4.2*1018) =1.05*108
0.015
[Ni2+]= 8 = 1.4*10 M
-8
(0.01)(1.05∗10 )
También podría gustarte
- Boh + H O B+OhDocumento20 páginasBoh + H O B+OhMichelle Yánez75% (8)
- Ejercicios Resuelto Quimica AnaliticaDocumento9 páginasEjercicios Resuelto Quimica AnaliticaGeovanny Alcivar80% (10)
- ProblemaDocumento2 páginasProblemawrammar50% (4)
- Tarea Equlibrio Acido-BaseDocumento2 páginasTarea Equlibrio Acido-BaseKatia LealAún no hay calificaciones
- Se Preparó Una Disolución de EDTA Disolviendo 3Documento4 páginasSe Preparó Una Disolución de EDTA Disolviendo 3JEAN CAMILO PORRAS RICO100% (1)
- Cinética de Reacciones Redox Azul Met-Acido AscorbicoDocumento3 páginasCinética de Reacciones Redox Azul Met-Acido AscorbicoGRECIAAún no hay calificaciones
- Vol Complejometría EjjerciciDocumento6 páginasVol Complejometría EjjerciciPiter Ortega MuñozAún no hay calificaciones
- EjercicioFinal CuantiDocumento7 páginasEjercicioFinal CuantijotaAún no hay calificaciones
- QA 02 Complejos Problemas01Documento6 páginasQA 02 Complejos Problemas012112mariaAún no hay calificaciones
- Primera Lista de Ejercicios Antes Del ParcialDocumento12 páginasPrimera Lista de Ejercicios Antes Del ParcialDiego PeláezAún no hay calificaciones
- Problemario U4-Ago-DicDocumento7 páginasProblemario U4-Ago-DicJUAN GERARDO CIGARROA RENDONAún no hay calificaciones
- Examen Analisis QuimicoDocumento4 páginasExamen Analisis Quimicopisignatus123Aún no hay calificaciones
- Informe Analitica 4 Gravimetría y VolumetríaDocumento10 páginasInforme Analitica 4 Gravimetría y VolumetríaValeria Berrio AlvarezAún no hay calificaciones
- Calculo de PH de Ácidos y Bases Débiles y Soluciones AmortiguadorasDocumento8 páginasCalculo de PH de Ácidos y Bases Débiles y Soluciones AmortiguadorasSalvador Zúñiga IbarraAún no hay calificaciones
- INFORME 2 Lab Quimica AnaliticaDocumento8 páginasINFORME 2 Lab Quimica AnaliticaAnder FrancoAún no hay calificaciones
- Meta 3.5.GarciaAndreaDocumento2 páginasMeta 3.5.GarciaAndreaandrea munguiaAún no hay calificaciones
- Ejercicios de Quim. General IiDocumento3 páginasEjercicios de Quim. General IiJheferson Bailón ArellanAún no hay calificaciones
- Resolucion Turno1Documento3 páginasResolucion Turno1Cami TurdoAún no hay calificaciones
- Durbin Chacon QuimicaDocumento3 páginasDurbin Chacon QuimicaKley CorreaAún no hay calificaciones
- Disoluciones AcuosasDocumento11 páginasDisoluciones AcuosasAnnie CabreraAún no hay calificaciones
- Informe Lab 4Documento12 páginasInforme Lab 4Daniel Hernandez PeñaAún no hay calificaciones
- Trabajo Quimica AplicadaDocumento3 páginasTrabajo Quimica Aplicadaeltor nadoAún no hay calificaciones
- ÁCIDO Base ProblemasDocumento45 páginasÁCIDO Base ProblemasMercedes LOPEZ CARBAJALESAún no hay calificaciones
- Titulacion Acido Fuerte, Base FuerteDocumento17 páginasTitulacion Acido Fuerte, Base FuerteRodrigo DalenceAún no hay calificaciones
- Equilibrio Ionico en Soluciones Acuosas Jose David Lozano BeltranDocumento12 páginasEquilibrio Ionico en Soluciones Acuosas Jose David Lozano BeltranValentina DuqueAún no hay calificaciones
- Reporte 3 Analitica LLDocumento4 páginasReporte 3 Analitica LLanaivonne1912agAún no hay calificaciones
- Valoraciones ComplejaciónDocumento27 páginasValoraciones ComplejaciónAntonioGonzalezAún no hay calificaciones
- Informe 1 de Laboratorio Química AgroindustrialDocumento7 páginasInforme 1 de Laboratorio Química AgroindustrialMaria Alejandra Villamil JaramilloAún no hay calificaciones
- Guia Disoluciones Acuosas-Angie Castro 11TDDocumento11 páginasGuia Disoluciones Acuosas-Angie Castro 11TDAngie CastroAún no hay calificaciones
- Anexo KPSDocumento3 páginasAnexo KPSDiana MoraAún no hay calificaciones
- Act Practica 4 Quimica Analitica 2Documento3 páginasAct Practica 4 Quimica Analitica 2Jesus Cardona GomezAún no hay calificaciones
- Unidadvi Calculos Valoraciones ComplejometricasDocumento4 páginasUnidadvi Calculos Valoraciones ComplejometricasarielAún no hay calificaciones
- Ácidos y Bases CuestionarioDocumento47 páginasÁcidos y Bases CuestionarioCristina Aguayo0% (1)
- Ejercicios Resueltos - Reactores QuímicosDocumento5 páginasEjercicios Resueltos - Reactores QuímicosMABAún no hay calificaciones
- Estudiante Numero 3, Ejercicio Numero 1 y 2Documento5 páginasEstudiante Numero 3, Ejercicio Numero 1 y 2cedu126Aún no hay calificaciones
- Valoraciones Acido - Base DébilDocumento8 páginasValoraciones Acido - Base DébilJoyce Jeannine Demera TelloAún no hay calificaciones
- Calculos y ResultadosDocumento6 páginasCalculos y ResultadosMaría NavasAún no hay calificaciones
- Ejercicios Aplicacion Sem 4Documento5 páginasEjercicios Aplicacion Sem 4marcoAún no hay calificaciones
- 30 Ejercicios de Redox Nernst, Equilibrio Quimico y Constante de EquilibrioDocumento11 páginas30 Ejercicios de Redox Nernst, Equilibrio Quimico y Constante de EquilibrioBraan Brandon Brandi100% (1)
- Preparación de Soluciones A Emplear en Prácticas de Espectrofotometría.Documento3 páginasPreparación de Soluciones A Emplear en Prácticas de Espectrofotometría.Eduardo GomezAún no hay calificaciones
- Ejercicios Practico Unidad 5Documento5 páginasEjercicios Practico Unidad 5Osmel Elias Suero Terrero0% (1)
- Problema 1Documento2 páginasProblema 1Nestor SanchezAún no hay calificaciones
- Trabajo Domiciliario 02Documento13 páginasTrabajo Domiciliario 02Irania AguilarAún no hay calificaciones
- Ejercicios Pre Parcial CoronavirusDocumento18 páginasEjercicios Pre Parcial Coronaviruscristian pulidoAún no hay calificaciones
- Práctica 1. Equilibrio Ácido-BaseDocumento21 páginasPráctica 1. Equilibrio Ácido-BaseAlexandra LópezAún no hay calificaciones
- Eqan U2 A3 JommDocumento8 páginasEqan U2 A3 JommArmando Muñoz MorenoAún no hay calificaciones
- Quimica AnalíticaDocumento8 páginasQuimica Analíticaalegoria2013Aún no hay calificaciones
- Una Alicuota de 50 ML de NaCNDocumento3 páginasUna Alicuota de 50 ML de NaCNDaniela Michel Flores CotaAún no hay calificaciones
- Taller 5 Valoraciones de Neutralización.Documento26 páginasTaller 5 Valoraciones de Neutralización.Mayra CarvajalAún no hay calificaciones
- Problemas de QuimicaDocumento2 páginasProblemas de QuimicaAna Lucia Alcantara CernaAún no hay calificaciones
- SolAB PAU UnizarDocumento11 páginasSolAB PAU UnizarOctavioAún no hay calificaciones
- Primer Taller de Quimica Analitica I Sem 2020.Documento8 páginasPrimer Taller de Quimica Analitica I Sem 2020.Daniiela Tiria100% (2)
- tp11 Resuelto - Equilibrio IonicoDocumento18 páginastp11 Resuelto - Equilibrio IonicoIaraAún no hay calificaciones
- Bioenergetica Ejercicios 1Documento45 páginasBioenergetica Ejercicios 1Minchola Ipanaque BryamAún no hay calificaciones
- Cálculo de ViscosidadesDocumento26 páginasCálculo de ViscosidadesAbner LugoAún no hay calificaciones
- Cálculos de Curva de TitulaciónDocumento7 páginasCálculos de Curva de TitulaciónKevinAún no hay calificaciones
- Practica 1Documento2 páginasPractica 1Yenly Alexandra Zamoraaquino100% (3)
- Resolución Hoja de Trabajo 3Documento3 páginasResolución Hoja de Trabajo 3Priscila De LeónAún no hay calificaciones
- Quimica Ejercicios de Acidos y Bases EspeDocumento11 páginasQuimica Ejercicios de Acidos y Bases EspeJOHNNY KEVIN BECERRA GUTIERREZAún no hay calificaciones
- Parte 1aDocumento57 páginasParte 1aDiana TéllezAún no hay calificaciones
- Práctica de ChorizosDocumento8 páginasPráctica de ChorizosDiana TéllezAún no hay calificaciones
- Práctica 1 LácteosDocumento12 páginasPráctica 1 LácteosDiana TéllezAún no hay calificaciones
- Parte 2Documento34 páginasParte 2Diana TéllezAún no hay calificaciones
- 1er Examen Calidad Diana TéllezDocumento4 páginas1er Examen Calidad Diana TéllezDiana TéllezAún no hay calificaciones
- Alimentación en MéxicoDocumento3 páginasAlimentación en MéxicoDiana TéllezAún no hay calificaciones
- Trabajo - 1 - Análisis de DatosDocumento2 páginasTrabajo - 1 - Análisis de DatosDiana Téllez0% (1)