Documentos de Académico
Documentos de Profesional
Documentos de Cultura
FLUJOGRAMAS
Cargado por
Helen Tomalá LainezDerechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
FLUJOGRAMAS
Cargado por
Helen Tomalá LainezCopyright:
Formatos disponibles
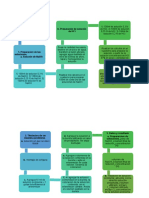
Preparación de Pesar 2g de NaOH y disolver en 200
solución NaOH mL de agua destilada y el volumen
0,1 N se completará hasta 500 mL
Llenar la bureta con la solución de
NaOH necesaria para la titulación.
Para evitar la
exposición de
Llenar la bureta con la solución de NaOH a la
NaOH necesaria para la titulación. atmosfera y CO2
Pesar 0,59g de ácido succínico y
Preparación de disolver en un matraz aforado de
solución de ácido 100 mL y completar el volumen a
succínico 0,1N 100 ml con agua destilada recién
preparada
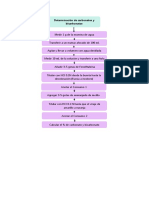
Estandarización Usando una pipeta, transferir 10 ml
de 0,1 N NaOH de ácido succínico en el matraz
solución cónico limpio
No soplar la última
gota de la pipeta
Añadir 2-3 gotas del indicador
fenolftaleína. Tenga en cuenta el
color de la solución
Agitar
Agregue la solución de NaOH de la constantemente el
bureta con agitación constante hasta matraz para
que el color de la solución cambie asegurar la mezcla
de incoloro a rosa pálido. completa de los
reactivos
Anote la lectura de la bureta y calcule
cuánta base se usó
La lectura
Esta es solo una titulación de prueba aproximada
y da el valor aproximado del punto permitirá
final titulaciones
posteriores
rápidas
Repita la titulación hasta que dos
lecturas coincidan con 0,1 ml.
Tome el promedio de las lecturas
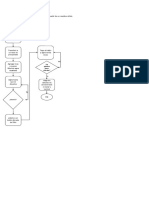
Preparación de Medir 4,2 ml de HCl y disolver en 200 mL
solución HCl de agua destilada y el volumen se
0,1 N completará hasta 500 mL
Llene la bureta con solución de Retire el embudo,
ácido clorhídrico hasta la marca cero
para que las gotas
usando un embudo. de solución del
embudo no
caigan en la
Preparación de Pesar 0,53 g de carbonato de sodio bureta y registre
solución 0,1N de en un matraz aforado (100 ml) y la lectura
Na2CO3 enrasar a 100 ml
Usando una pipeta, transferir 10 ml
Estandarización
de solución de carbonato sódico en
de 0,1 N HCl
un matraz limpio
solución
No soplar la última
gota de la pipeta
Añadir 2-3 gotas del indicador
anaranjado de metilo. Tenga en
cuenta el color de la solución
Agitar
Agregue la solución de HCl de la
constantemente el
bureta con agitación constante
matraz para
hasta que el color de la solución
asegurar la mezcla
cambie de incoloro a tonos
completa de los
amarillos o amarillos rojizos
reactivos
Anote la lectura de la bureta y calcule
cuánto de acido se usó
Esta es solo una titulación de prueba
y da el valor aproximado del punto
final La lectura
aproximada
permitirá
Repita la titulación hasta que dos titulaciones
lecturas coincidan con 0,1 ml. posteriores
rápidas
Tome el promedio de las lecturas
Recomendaciones:
Bajo ningún concepto se debe tomar un volumen del frasco de reactivo de HCl con una
pipeta mediante aspiración con la boca puesto que sus vapores tóxicos llegarían a las vías
respiratorias; así, el volumen debe medirse con una probeta o bien con una pipeta y con
ayuda de una pera.
Cualquier manipulación del frasco de reactivo debe realizarse bajo una campana extractora
de vapores, con el fin de evitar que los vapores del ácido, los cuales comienzan a aparecer
inmediatamente después de destapado el frasco, contaminen el local de laboratorio.
También podría gustarte
- Curso de Pendulo Hebreo. Nelibeat 4shared - Com 56 JM20352 ColDocumento56 páginasCurso de Pendulo Hebreo. Nelibeat 4shared - Com 56 JM20352 ColDiana ceglia67% (3)
- ISO - 14001 - 2015 RequisitosDocumento48 páginasISO - 14001 - 2015 RequisitosHelen Tomalá Lainez100% (1)
- Importancia de La Ética en La SaludDocumento3 páginasImportancia de La Ética en La SaludHelen Tomalá LainezAún no hay calificaciones
- Ya Nadie Incendia & El MarDocumento49 páginasYa Nadie Incendia & El MarInés HazbunAún no hay calificaciones
- Patrón de Pantaleta N°1 para ImprimirDocumento7 páginasPatrón de Pantaleta N°1 para ImprimirNathaly Marcano100% (1)
- Evaluaciones Investigación de MercadosDocumento25 páginasEvaluaciones Investigación de MercadosA1100% (9)
- Lab 4Documento8 páginasLab 4LarissaVegaAún no hay calificaciones
- Previo, Práctica 1Documento9 páginasPrevio, Práctica 1Mike ContrerasAún no hay calificaciones
- Volumetria de NeutralizacionDocumento12 páginasVolumetria de Neutralizacionjuan carlosAún no hay calificaciones
- Diagrama de Flujo - Practica 4 - Componente PracticoDocumento4 páginasDiagrama de Flujo - Practica 4 - Componente PracticoEl BichónAún no hay calificaciones
- Silvio 2Documento3 páginasSilvio 2Natalia CanoAún no hay calificaciones
- Preinforme N°10 Jean Sebastián Sarmiento Agudelo 1202318Documento7 páginasPreinforme N°10 Jean Sebastián Sarmiento Agudelo 1202318SevenCash 11Aún no hay calificaciones
- Informe de Lab. 15 Q.a.ii - Grupo 3Documento6 páginasInforme de Lab. 15 Q.a.ii - Grupo 3kevin saraguroAún no hay calificaciones
- Si La Concentración de La Solución TitulanteDocumento1 páginaSi La Concentración de La Solución TitulanteAndre CadavidAún no hay calificaciones
- Informe de Laboratorio 4 1Documento5 páginasInforme de Laboratorio 4 1Jeison Estiven Lopez OrtegaAún no hay calificaciones
- So2 CaDocumento10 páginasSo2 Casupervisorlab ihaAún no hay calificaciones
- Laboratorio 7 Diagrama de FlujoDocumento6 páginasLaboratorio 7 Diagrama de FlujoAreAún no hay calificaciones
- Informe Lab Qmc. DisolucionesDocumento13 páginasInforme Lab Qmc. DisolucioneseddyAún no hay calificaciones
- LABORATORIO BUFFER (TAREA) (1) UuuDocumento4 páginasLABORATORIO BUFFER (TAREA) (1) UuuAngel Chury loayzaAún no hay calificaciones
- Diagrama de Flujo 10Documento5 páginasDiagrama de Flujo 10Valeria lozano ramirezAún no hay calificaciones
- Pre-Informe 1 Titulación Ácido BaseDocumento5 páginasPre-Informe 1 Titulación Ácido BaseYefrei SierraAún no hay calificaciones
- Análisis de La Acidez VinagreDocumento2 páginasAnálisis de La Acidez VinagreMaria Celina Moyano CarreteroAún no hay calificaciones
- Diagrama de Flujo CloruroDocumento1 páginaDiagrama de Flujo CloruroLina Alejandra Reyes ÁvilaAún no hay calificaciones
- DISOLUCIONESDocumento15 páginasDISOLUCIONESFernando OrtizAún no hay calificaciones
- Determinacion de Acido Acetico en VinagreDocumento1 páginaDeterminacion de Acido Acetico en VinagreCAROLINA ANDREA ARCOS SOTOAún no hay calificaciones
- p2. Cinetica - Desarrollo ExperimentalDocumento1 páginap2. Cinetica - Desarrollo ExperimentalvanneloveraAún no hay calificaciones
- Titulacion de HCL y NaohDocumento8 páginasTitulacion de HCL y Naohjosecueva1618Aún no hay calificaciones
- Laboratorio 5Documento9 páginasLaboratorio 5Edgar EspinozaAún no hay calificaciones
- Informe 1 - Titulaciones AlcalimetricasDocumento34 páginasInforme 1 - Titulaciones AlcalimetricasAntony Corso100% (1)
- Informe Sobre Determinacio de Acido Citrico de Jugo de Frutas ComercialDocumento7 páginasInforme Sobre Determinacio de Acido Citrico de Jugo de Frutas ComercialRocioAún no hay calificaciones
- Laboratorio Semana 6 - Maria de Los Angeles Vasquez AvalosDocumento3 páginasLaboratorio Semana 6 - Maria de Los Angeles Vasquez AvalosMARY PCAún no hay calificaciones
- Diagrama p10Documento1 páginaDiagrama p10Fany DiazAún no hay calificaciones
- Flujograma 6Documento1 páginaFlujograma 6Neiver UltimateAún no hay calificaciones
- Uni2 Act3 Ane 2 Pra Lab 2 Sol TitDocumento6 páginasUni2 Act3 Ane 2 Pra Lab 2 Sol TitAstrid Yuleimy JAIMES VILLAMIZARAún no hay calificaciones
- Practica Titulacion Acido - Base - 3Documento4 páginasPractica Titulacion Acido - Base - 3laura araujoAún no hay calificaciones
- Practica de VolumetriaDocumento5 páginasPractica de VolumetriaAlexander Guarenas-ManzanoAún no hay calificaciones
- Lp-Ac-I-01.02 Determinacion de Dureza Parcial Del AguaDocumento1 páginaLp-Ac-I-01.02 Determinacion de Dureza Parcial Del AguayolandaAún no hay calificaciones
- 35 30spanisheditionsamplemonograph PDFDocumento2 páginas35 30spanisheditionsamplemonograph PDFKARLA CRISTIANA ALFARO GARCIAAún no hay calificaciones
- Práctica 3. Valoración Ácido-Base: Tabla 1. Medida Del PHDocumento2 páginasPráctica 3. Valoración Ácido-Base: Tabla 1. Medida Del PHmarcos lngAún no hay calificaciones
- Procedimiento JHONDocumento2 páginasProcedimiento JHONjhon yepesAún no hay calificaciones
- Basica Lab8Documento16 páginasBasica Lab8Brandon Calef Alain Estrada MartinezAún no hay calificaciones
- Pre-Informe 5Documento3 páginasPre-Informe 5estephaniaAún no hay calificaciones
- Diagrama de Bloques P2 EPAU Lab. CyRH 3IM56Documento7 páginasDiagrama de Bloques P2 EPAU Lab. CyRH 3IM56Alfredo EscamillaAún no hay calificaciones
- Diagrama Práctica 3 LqgiiDocumento2 páginasDiagrama Práctica 3 LqgiiEsteban Davila CeronAún no hay calificaciones
- Valoracion de VinagreDocumento2 páginasValoracion de VinagrenickAún no hay calificaciones
- Diagramas de Flujo Lab 10Documento3 páginasDiagramas de Flujo Lab 10Andres GomezAún no hay calificaciones
- Estequimetría de Las Reacciones Químicas (Autoguardado)Documento5 páginasEstequimetría de Las Reacciones Químicas (Autoguardado)Maria Jose Pérez GonzalezAún no hay calificaciones
- DiagramaDocumento1 páginaDiagramaLucero :vAún no hay calificaciones
- Informe 2 Quimica AnaliticaDocumento5 páginasInforme 2 Quimica AnaliticaSara Lizbeth Martinez MorochoAún no hay calificaciones
- Preparación de Una Solución NaOH 0Documento2 páginasPreparación de Una Solución NaOH 0Julian RuizAún no hay calificaciones
- Practica 1 Diagramas de FlujoDocumento3 páginasPractica 1 Diagramas de Flujo4ndrickkAún no hay calificaciones
- Documento de - ° - D NI L ? - °Documento6 páginasDocumento de - ° - D NI L ? - °Arley PazAún no hay calificaciones
- DETERMINACION DE ACIDO CITRICO Y ACIDO ASCORBICO EN MUESTRAS DE POLVO PARA HACER JUGOS Volumetria de Neutralizacion y Oxidacion ReduccionDocumento11 páginasDETERMINACION DE ACIDO CITRICO Y ACIDO ASCORBICO EN MUESTRAS DE POLVO PARA HACER JUGOS Volumetria de Neutralizacion y Oxidacion ReduccionrafelemirAún no hay calificaciones
- Gelatine en EsDocumento2 páginasGelatine en EsAnaly Pocón HernándezAún no hay calificaciones
- Preparacion NAOHDocumento8 páginasPreparacion NAOHOsmin RiveraAún no hay calificaciones
- Preparaion de Reactivos y Valoracion de Soluciones AcidoDocumento7 páginasPreparaion de Reactivos y Valoracion de Soluciones AcidoMissael ArellanoAún no hay calificaciones
- DisolucionesDocumento2 páginasDisolucionesLebrónAún no hay calificaciones
- CompetenciaDocumento4 páginasCompetenciaEnrike ValladaresAún no hay calificaciones
- Preparación de Soluciones y Valoracion de Soluciones: Universidad Peruana Cayetano HerediaDocumento17 páginasPreparación de Soluciones y Valoracion de Soluciones: Universidad Peruana Cayetano Herediakapitu mendozaAún no hay calificaciones
- Experimento de LaboratorioDocumento5 páginasExperimento de LaboratoriocamiloAún no hay calificaciones
- Antes de La Practica 10 PQADocumento4 páginasAntes de La Practica 10 PQACesia CastilloAún no hay calificaciones
- Jarabe Simple 2Documento5 páginasJarabe Simple 2Victoria Michiel ChinoAún no hay calificaciones
- Diagrama de Flujo Práctica 5Documento1 páginaDiagrama de Flujo Práctica 5Fer ZamAún no hay calificaciones
- Soluciones StandarDocumento2 páginasSoluciones StandarAle JaimeAún no hay calificaciones
- 5 Riesgos y Preparación de ReactivosDocumento1 página5 Riesgos y Preparación de ReactivosHelen Tomalá LainezAún no hay calificaciones
- Flujogramas Determinación de Carbonatos y BicarbonatosDocumento1 páginaFlujogramas Determinación de Carbonatos y BicarbonatosHelen Tomalá LainezAún no hay calificaciones
- 5 Charla ATM Calidad Del Aire PRIMARIOS Y SECUNDARIOSDocumento71 páginas5 Charla ATM Calidad Del Aire PRIMARIOS Y SECUNDARIOSHelen Tomalá LainezAún no hay calificaciones
- IntroducciónDocumento1 páginaIntroducciónHelen Tomalá LainezAún no hay calificaciones
- 3 Charla CONTA CLASIF COV COP AQ OKIDocumento88 páginas3 Charla CONTA CLASIF COV COP AQ OKIHelen Tomalá LainezAún no hay calificaciones
- Codigo de Etica FarmaceuticoDocumento5 páginasCodigo de Etica FarmaceuticoHelen Tomalá LainezAún no hay calificaciones
- TAREADocumento3 páginasTAREAHelen Tomalá LainezAún no hay calificaciones
- Comités de EticaDocumento7 páginasComités de EticaHelen Tomalá LainezAún no hay calificaciones
- Comités de EticaDocumento7 páginasComités de EticaHelen Tomalá LainezAún no hay calificaciones
- Codigo de Etica FarmaceuticoDocumento6 páginasCodigo de Etica FarmaceuticoHelen Tomalá LainezAún no hay calificaciones
- Instructivo Paz y SalvoDocumento7 páginasInstructivo Paz y SalvoPao RAún no hay calificaciones
- Consulta PreviaDocumento14 páginasConsulta PreviaJoséLuisPinaresAún no hay calificaciones
- Centros de Mesa MontecarloDocumento34 páginasCentros de Mesa MontecarloKarla RodriguezAún no hay calificaciones
- Sesión 2 - Derecho Constitucional TributarioDocumento29 páginasSesión 2 - Derecho Constitucional TributarioSarahi CurillaAún no hay calificaciones
- Analis - Dimens. y VectoresDocumento6 páginasAnalis - Dimens. y Vectoresjoshcordova884Aún no hay calificaciones
- INFORME TÉCNICO Localización y Diseño de VíasDocumento87 páginasINFORME TÉCNICO Localización y Diseño de VíasMARIA CAMILA VILLAMIL FOREROAún no hay calificaciones
- Tema 2Documento16 páginasTema 2Antoni Martinez ColomerAún no hay calificaciones
- Guia de Actividades y Rúbrica de Evaluación - Fase 5 - Implementación y Evaluación de La Política Pública de DeporteDocumento5 páginasGuia de Actividades y Rúbrica de Evaluación - Fase 5 - Implementación y Evaluación de La Política Pública de Deporteeducacion superiorAún no hay calificaciones
- Plan 20 de Julio 2023 BirorDocumento5 páginasPlan 20 de Julio 2023 BirorRubén David Ruiz MontañezAún no hay calificaciones
- Taller 20 SSTDocumento3 páginasTaller 20 SSTLaura Cano100% (1)
- Verif EPI Poulies Bloqueurs Procedure ESDocumento4 páginasVerif EPI Poulies Bloqueurs Procedure ESJose Leonel Zarate FrancoAún no hay calificaciones
- Guia Aprendizaje Sena Desarrollo GraficoDocumento59 páginasGuia Aprendizaje Sena Desarrollo Graficomauricionieto867% (3)
- Presentación 4Documento16 páginasPresentación 4Mylene BanegasAún no hay calificaciones
- Mina Media LunaDocumento26 páginasMina Media Lunalemofo9898Aún no hay calificaciones
- El Día Del Tsunami de Agosto de 1868Documento15 páginasEl Día Del Tsunami de Agosto de 1868jorge_rivera1002Aún no hay calificaciones
- Benavides Flor Tarea5Documento7 páginasBenavides Flor Tarea5Flor Benavides HuamanAún no hay calificaciones
- Guía Relación Hispano-Indígenas IIDocumento20 páginasGuía Relación Hispano-Indígenas IIMoisés SaavedraAún no hay calificaciones
- Proyecto Morral SolarDocumento58 páginasProyecto Morral Solarcarlos rojasAún no hay calificaciones
- Pau ProgramacionDocumento14 páginasPau ProgramacioncapsantinoAún no hay calificaciones
- INFORME 2 BioquimmicaDocumento5 páginasINFORME 2 BioquimmicaEduardo Jose Lopez EspañolAún no hay calificaciones
- Mediana SPDocumento3 páginasMediana SPYanqui IvanAún no hay calificaciones
- Las Playas A Lo Largo Del TiempoDocumento21 páginasLas Playas A Lo Largo Del TiempoBriana Angélica BombanaAún no hay calificaciones
- Ficha - Eca Proyecto-6 Act - Semana 32 Bte-Bgu 2doDocumento3 páginasFicha - Eca Proyecto-6 Act - Semana 32 Bte-Bgu 2doDarlyn Betbony ToyBetAún no hay calificaciones
- Deformacion de Materiales No FerrososDocumento25 páginasDeformacion de Materiales No FerrososPepe AlAún no hay calificaciones
- Modelo de Gestion MiaffDocumento39 páginasModelo de Gestion Miaffjose saavedraAún no hay calificaciones
- Datos e Interpretación de ResultadosDocumento7 páginasDatos e Interpretación de ResultadosBryan Santiago PallascoAún no hay calificaciones