Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Termo
Cargado por
Natali ValdesDescripción original:
Derechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
Termo
Cargado por
Natali ValdesCopyright:
Formatos disponibles
m: masa V 1
^v = v^ =
m ρ
V: volumen
m 1
^v : volumen especifico ρ= ρ=
V v^
T: temperatura
F
P=
ρ : densidad A
P: presión m
PV = RT
Mm
n: número de moles
gas real P=ρ∗R sustancia∗T
g: gravedad
h: altura iteracion Pn =Z n∗Pn−1 → Z n=Z n−1
F: fuerza F1 F 2
Principio de pascal =
A1 A2
A: área
Pmanometrica =Pabsoluta −Patmosferica
Z: desviación
Pmanometrica=ρ∗g∗h
Mm: masa molecular
P A =PB + ρ sustancia∗g∗h
PV
Z=
RT
T ( ° K )=T (° C )+ 273,15 P
Preducida=
T ( ° R )=1,8∗T ( ° K ) Pcrítica
T ( ° F ) =T ( ° R )−459,67 T 1 +T 2
principiocero T eq =
2
2 Ley de Boyle P1 V 1=P2 V 2
Acirculo =π r
2 V1 V2
πd Ley de charles =
A= T1 T2
4
P 1 P2
Ley Gay-Lussac =
T1 T 2
V1 V2
Ley de Avogadro =
n1 n 2
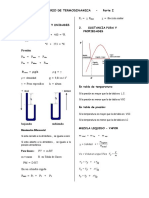
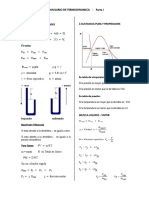
Calidad o título:
v^ , ^μ , h^ , ^stotal −v^ , μ^ , h^ , ^sfluido
X ( ^v , ^μ , h^ , s^ )=
v^ , ^μ , h^ , ^s gas −^v , μ^ , h^ , ^sfluido
^ =V^
V ^
total fluido + X V f g
Balance de masa: mentra + minicial =msale +mfinal
También podría gustarte
- Fórmulas de geometría, física y álgebra con valores numéricosDocumento3 páginasFórmulas de geometría, física y álgebra con valores numéricosvictor soteldoAún no hay calificaciones
- Despejar Formulas.1511120088Documento1 páginaDespejar Formulas.1511120088GSebastianPico80% (5)
- Formulario TermodinamicaDocumento26 páginasFormulario TermodinamicaSaul Alex Mendoza67% (3)
- Formulario Modulos 1 y 2Documento1 páginaFormulario Modulos 1 y 2Jenni SanchezAún no hay calificaciones
- Propiedades residuales y equilibrio de fases en sistemas purosDocumento3 páginasPropiedades residuales y equilibrio de fases en sistemas purosPili BezanillaAún no hay calificaciones
- Formulario de estáticaDocumento2 páginasFormulario de estáticave425264Aún no hay calificaciones
- Despejar - Formulas 1001 IEMDSDocumento1 páginaDespejar - Formulas 1001 IEMDSNanas NanisAún no hay calificaciones
- Formulario TermodinámicaDocumento4 páginasFormulario TermodinámicaConstanza BravoAún no hay calificaciones
- Fórmulas Química ExamenDocumento2 páginasFórmulas Química ExamenEmily TumamaentangasAún no hay calificaciones
- ACTIVIDADES DE PORTAFOLIO 3Documento2 páginasACTIVIDADES DE PORTAFOLIO 3Tadeo CampaAún no hay calificaciones
- Formulario (Quimica Aplicada)Documento20 páginasFormulario (Quimica Aplicada)luisAún no hay calificaciones
- Ecuación de estado gas ideal PV=nRTDocumento12 páginasEcuación de estado gas ideal PV=nRTJose Alonzo VivancosAún no hay calificaciones
- 2 Resumen FormulasDocumento2 páginas2 Resumen FormulasPatricio PautassiAún no hay calificaciones
- Formulario Fisica IIDocumento2 páginasFormulario Fisica IIJose Carlos Vidal GhermanAún no hay calificaciones
- Tablas de Fórmulas - TermodinámicaDocumento2 páginasTablas de Fórmulas - TermodinámicaAlberto JoseAún no hay calificaciones
- Gases ideales y ecuaciones de estadoDocumento13 páginasGases ideales y ecuaciones de estadoLuis CONDORI SOTOAún no hay calificaciones
- Fisica2 Termodinamica1Documento40 páginasFisica2 Termodinamica1solanoAún no hay calificaciones
- Despejar Formulas.1511120088Documento1 páginaDespejar Formulas.1511120088tomas.telles.vazques2003Aún no hay calificaciones
- FormularioDocumento1 páginaFormularioAlejandro CastañedaAún no hay calificaciones
- Formulario Termodinamica I PDFDocumento14 páginasFormulario Termodinamica I PDFPaúl Alexander Mora VireriAún no hay calificaciones
- Formulario de física de la escuela preparatoria Benjamín FranklinDocumento3 páginasFormulario de física de la escuela preparatoria Benjamín FranklinYesenia GAAún no hay calificaciones
- Formulario de TermodinamicaDocumento2 páginasFormulario de TermodinamicaDiego FrancoAún no hay calificaciones
- Formulario de TermodinamicaDocumento5 páginasFormulario de TermodinamicaAylin PérezAún no hay calificaciones
- Autoevaluacion 2º Parcial PDFDocumento50 páginasAutoevaluacion 2º Parcial PDFKANDERMORADOAún no hay calificaciones
- Formulario Termo3Documento2 páginasFormulario Termo3lupasa.14Aún no hay calificaciones
- Formulario de Termodinamica 1Documento2 páginasFormulario de Termodinamica 1Jaime muñoz portugalAún no hay calificaciones
- Hoja de Formulas PDFDocumento3 páginasHoja de Formulas PDFsonlopusAún no hay calificaciones
- Formulario TermodinamicaDocumento25 páginasFormulario TermodinamicaPenélope ManzurAún no hay calificaciones
- Tarea3 FQDocumento1 páginaTarea3 FQLIZETH ANGELES AVALOSAún no hay calificaciones
- TT Problemas Resueltos 2019Documento211 páginasTT Problemas Resueltos 2019ainhoa murAún no hay calificaciones
- Clase Integradora GasesDocumento35 páginasClase Integradora Gasessofia gomezAún no hay calificaciones
- Formulario de FisicoquímicaDocumento1 páginaFormulario de Fisicoquímica김문니Aún no hay calificaciones
- Ficha Tecnica FisicaDocumento2 páginasFicha Tecnica FisicaLuz Mirian Montoya MorantesAún no hay calificaciones
- Termodinámica FORMULARIODocumento3 páginasTermodinámica FORMULARIOAbril HerreraAún no hay calificaciones
- Formulario Quimica Aplicada CDocumento4 páginasFormulario Quimica Aplicada Ccervantesmmelaniemv3Aún no hay calificaciones
- Formulas Mecanica de FluidosDocumento1 páginaFormulas Mecanica de FluidosLaptop YoselinAún no hay calificaciones
- Formulas Fisico Quimica C2Documento7 páginasFormulas Fisico Quimica C2The_buzzcutAún no hay calificaciones
- Unidad 1Documento11 páginasUnidad 1Alberto Bailon QuijijeAún no hay calificaciones
- Práctica 10Documento2 páginasPráctica 10Anais Briggit Jacinto Chavez0% (1)
- Termodinámica FundamentalDocumento25 páginasTermodinámica FundamentalfanfanfanAún no hay calificaciones
- Anexo 1 Ecuaciones Generales en Ingeniería QuímicaDocumento3 páginasAnexo 1 Ecuaciones Generales en Ingeniería QuímicaValeria VillalobosAún no hay calificaciones
- Formulario Quimica GasesDocumento9 páginasFormulario Quimica GasesFrancisco Bueno CalixtoAún no hay calificaciones
- Formulario FisicaDocumento2 páginasFormulario FisicaFernando Montes de Oca Zona 1Aún no hay calificaciones
- Principios de Termodinamica FinalDocumento4 páginasPrincipios de Termodinamica FinalAndrei Jared Beteta VilledaAún no hay calificaciones
- Formulario TermodinamicaDocumento25 páginasFormulario TermodinamicaMiguel AcostaAún no hay calificaciones
- ACTIVIDAD #1 FORMULAS Y DESPEJES FÍSICA DEL II MOMENTO... Alfredo Martirnez 3er Año ADocumento5 páginasACTIVIDAD #1 FORMULAS Y DESPEJES FÍSICA DEL II MOMENTO... Alfredo Martirnez 3er Año AAlfredo Martinez50% (2)
- 90-Aire HumedoDocumento17 páginas90-Aire HumedoJuliana ZabertAún no hay calificaciones
- Formulario de Quimica AplicadaDocumento5 páginasFormulario de Quimica AplicadaDiego Fer15Aún no hay calificaciones
- 26 de Marzo de 2020Documento2 páginas26 de Marzo de 2020luis enrique priego moralesAún no hay calificaciones
- Cbarajas - 06 - GasVaporDocumento69 páginasCbarajas - 06 - GasVaporJuan Felipe PeraltaAún no hay calificaciones
- Transformaciones cuasiestáticas y no cuasiestáticas de gases idealesDocumento2 páginasTransformaciones cuasiestáticas y no cuasiestáticas de gases idealesJUSTFORGEEKSAún no hay calificaciones
- Formulario TERMODocumento8 páginasFormulario TERMOJuanMi TorresAún no hay calificaciones
- Formulario FisicoquímicaDocumento6 páginasFormulario Fisicoquímicavaam0507Aún no hay calificaciones
- Ejemplos GasesDocumento9 páginasEjemplos GasesŘôjâš ĞřôvĕřAún no hay calificaciones
- EstadogaseosoDocumento9 páginasEstadogaseosoVania RomeroAún no hay calificaciones
- Energias Libres Problemas ResueltosDocumento10 páginasEnergias Libres Problemas ResueltosAlexander sancho nietoAún no hay calificaciones
- UNM Fisica - Formulas - 2022-10-05Documento2 páginasUNM Fisica - Formulas - 2022-10-05Sofia MacielAún no hay calificaciones