Documentos de Académico
Documentos de Profesional
Documentos de Cultura
661 Modifica Lineamientos Técnicos y Operativos para La Vacunación Contra El COVID-19
Cargado por
MALLAMAS EPSITítulo original
Derechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
661 Modifica Lineamientos Técnicos y Operativos para La Vacunación Contra El COVID-19
Cargado por
MALLAMAS EPSICopyright:
Formatos disponibles
República de Colombia
MINISTERIO DE SALUD Y PROTECCIÓN SOCIAL
RESOLUCIÓN NÚMERO 661 DE 2022
( 2 7 ABR 2022 )
Por la cual se modifican los lineamientos técnicos y operativos para la vacunación contra
el COVID-19, contenidos en el Anexo Técnico 1 de la Resolución 1151 de 2021, en
relación con la aplicación de refuerzos a la población de 12 a 17 años
EL MINISTRO DE SALUD Y PROTECCIÓN SOCIAL
En ejercicio de sus facultades, especialmente de las conferidas por el literal b del
artículo 488 de la Ley 9 de 1979, los numerales 3 del artículo 173 de la Ley 100 de
1993, 42.1 del artículo 42 de la Ley 715 de 2001, 3,4 y 9 del artículo 2 del Decreto Ley
4107 de 2011, 19.1 del artículo 19 del Decreto 109 de 2021, en desarrollo del inciso
segundo del artículo 592 de la Ley 9 de 1979 y
CONSIDERANDO
Que el Gobierno nacional mediante el Decreto 109 de 2021 modificado por los Decretos
404, 466, 630, 744 y 1671 todos de 2021 y 416 de 2022 estableció como objetivos del
Plan Nacional de Vacunación contra el COVID-19 la reducción de la morbilidad grave y
la mortalidad específica por COVID-19, disminuir la incidencia de casos graves, proteger
a la población con alta exposición al virus y aportar a la reducción de la transmisión del
SARS-CoV-2 en la población general con el propósito de contribuir al control de la
epidemia en el país.
Que, en sesión del 10 de marzo de 2022, el Consenso Colombiano COVID-19 discutió
la evidencia disponible sobre una dosis de refuerzo en vacunas contra COVID-19 en
niños y adolescentes, recomendando aplicar una dosis de refuerzo con la vacuna de
Pfizer en la población de 12 a 17 años sin comorbilidades a partir de los 4 meses de la
segunda dosis.
Que en sesión del 23 de marzo de 2022 el Comité Asesor para el Proceso Estratégico
de Inmunización de la Población Colombiana frente a la COVID-19, analizó y recomendó
la aplicación de un refuerzo de la vacuna la población de 12 a 17 años con el biológico
Pfizer.
Que, teniendo en cuenta lo anterior, se hace necesario modificar el numeral 8.7 del
Anexo Técnico 1 de la Resolución 1151 de 2021, modificado por las Resoluciones 1866,
1877 de 2021, 092 y 419 de 2022 en el sentido de incluir una dosis de refuerzo con el
biológico Pfizer, para la población de 12 a 17 años.
En mérito de lo expuesto,
RESUELVE
Artículo 1. Modificar el numeral 8.7 "Consideraciones relacionadas con la aplicación de
refuerzos" del Anexo Técnico 1 "Lineamientos técnicos y operativos para la vacunación
DEL2 7 ABR 2a2 2022
RESOLUCIÓN NÚNI.ERCr U661 Hoja No.2
Continuación de la resolución "Por la cual se modifican los lineamientos técnicos y operativos para la
vacunación contra el COVID-19, contenidos en el Anexo Técnico 1 de la Resolución 1151 de 2021, en relación
con la aplicación de refuerzos a la población de 12 a 17 años"
contra el COVID-19" de la Resolución 1151 de 2021 y sus modificatorias, en los
siguientes términos:
"8.7 Aplicación de refuerzos
Las poblaciones que se enuncian en el presente numeral podrán acceder a las dosis de
refuerzo, de acuerdo con la siguiente tabla:
Esquema primario Dosis de refuerzo Plataforma
ARNm (Pfizer) Homóloga
ARNm (Pfizer) ARNm Moderna
Heteróloga
Vector viral (AstraZeneca y Janssen)
ARNm Moderna Homóloga
ARNm (Moderna) ARNm (Pfizer)
Heteróloga
Vector viral (AstraZeneca y Janssen)
Vector Viral (AstraZeneca) Homóloga
Vector Viral (AstraZeneca) ARNm (Pfizer— Moderna)
Heteróloga
Vector virar (Janssen)
Vector Virar (Janssen) Homóloga
Vector Viral (Janssen) ARNm (Pfizer— Moderna)
Heteróloga
Vector Vira! (AstraZeneca)
ARNm (Pfizer— Moderna)
Heteróloga
Virus Inactivado (Sinovac) Vector Viral (AstraZeneca - Janssen)
Virus Inactivado (Sinovac) Homóloga
a. Población de 12 años en adelante con la siguiente condicbn clínica:
Trasplante de corazón
Trasplante de riñón
Trasplante de páncreas
Trasplante de pulmón
Trasplante de intestino
Trasplante de hígado
Trasplante de médula ósea en los 2 años anteriores o que reciben tratamiento
de inmunosupresión
Leucemia en quimioterapia
Mieloma en quimioterapia
Linfoma en quimioterapia
Síndrome mielodisplásico en quimioterapia
Pacientes con enfermedades autoinmunes como artritis reumatoide, lupus
eritematoso sistémico o esclerosis múltiple que reciben tratamiento
inmunosupresor y otras enfermedades que usen: alemtuzumab, abatacept,
belatacept, obinutuzumab, rituximab, fin golimod, ocrelizumab, antimetabolicos
e inhibidores de la calcineurina en último año
lnmunodeficiencias primarias
b. Población de trasplante de órgano sólido, población de trasplante de progenitores
de hematopoyéticos (durante los primeros 2 años o que reciban tratamiento
inmunosupresor), pacientes con neoplasia hematológica en quimioterapia activa y
pacientes con inmunosupresión severa, como anti-CD 20.
27 ABR 2022
RESOLUCIÓN NÚMERO-i .‘d 661DEL DE 2022 Hoja No. 3
Continuación de la resolución "Por la cual se modifican los lineamientos técnicos y operativos para la
vacunación contra el COVID-19, contenidos en el Anexo Técnico 1 de la Resolución 1151 de 2021, en relación
con la aplicación de refuerzos a la población de 12 a 17 años"
c. Personas de 12 años o más, a partir de los 4 meses de haber completado el
esquema primario.
Las poblaciones señaladas en los literales a y b podrán recibir una segunda dosis de
refuerzo con el biológico de la plataforma de ARNm después de su esquema primario y de
su primer refuerzo a partir de los 30 días de aplicación de su última dosis bajo
recomendación del médico tratante.
La población del literal c sólo recibirá una dosis de refuerzo después de completar el
esquema primario.
Las personas de 12 a 17 años del literal c solamente podrán recibir dosis de refuerzo con
el biológico Pfizer Inc BioNTech.
Se podrán aplicar la dosis de un determinado biológico por recomendación médica,
siempre y cuando esté disponible y autorizado en el país.
Personas mayores de 12 años, que han presentado CO VID - 19 deben completar el
esquema primario y colocar la dosis de refuerzo, ninguna dosis debe ser retrasada.
Adicionalmente, tener en cuenta que para su aplicación deben pasar treinta (30) días
contados desde la fecha de inicio de síntomas en personas sintomáticas o treinta (30) días
contados desde la toma de muestra en personas asintomáticas.
No se considera necesaria la medición de anticuerpos para determinar la administración
de la dosis de refuerzo adicional"
Artículo 2. La presente resolución rige a partir de la fecha de su publicación, modifica el
Anexo Técnico 1 de la Resolución 1151 de 2021, modificada por la Resoluciones 1866 y
1887 de 2021, 092 y419 de 2022.
PUBLÍ E Y CÚMPLASE
Dada en Bogotá, D.C.,
27A
FERNANDO RU G MEZ
inistro de Salud y Protección Social
Viceministerio de Salud Pública y Prestación
Dirección de Promoción y Prevención
Dirección de Epidemiología y Demografia
Dirección de Medicamgntos y Tecnologia en Salud CP
Dirección Juridica lkat
También podría gustarte
- 762 Modifica Lineamientos Técnicos y Operativos para La Vacunación Contra El COVID-19 - Anexo Técnico 1 de La Resolución 1151 de 2021Documento3 páginas762 Modifica Lineamientos Técnicos y Operativos para La Vacunación Contra El COVID-19 - Anexo Técnico 1 de La Resolución 1151 de 2021MALLAMAS EPSIAún no hay calificaciones
- Protocolo de Dosis de Refuerzo Vacuna Contra Covid-19 para Personas de 18 Anos A MasDocumento5 páginasProtocolo de Dosis de Refuerzo Vacuna Contra Covid-19 para Personas de 18 Anos A MasMel IsSaAún no hay calificaciones
- 1738 Modifican Los Anexos Técnicos 1,2 y 7 de La Resolución 1151 de 2021 en Relacion Vacinacion Población PediatricaDocumento13 páginas1738 Modifican Los Anexos Técnicos 1,2 y 7 de La Resolución 1151 de 2021 en Relacion Vacinacion Población PediatricaTacio Lorran SilvaAún no hay calificaciones
- Resoluciión No. 092 de 2022Documento6 páginasResoluciión No. 092 de 2022DIANA LORENA HERNANDEZAún no hay calificaciones
- Lineamientos Dosis Refuerzo Vacunación COVID19Documento4 páginasLineamientos Dosis Refuerzo Vacunación COVID19Cristian LopezAún no hay calificaciones
- Ivermectina y DR - CarvalloDocumento15 páginasIvermectina y DR - CarvalloJosé SarmientoAún no hay calificaciones
- Efectividad y Seguridad de Las Vacunas Par - 2021 - FMC - Formaci N M Dica ContiDocumento10 páginasEfectividad y Seguridad de Las Vacunas Par - 2021 - FMC - Formaci N M Dica Contileonardo.dm793Aún no hay calificaciones
- Lineamiento para Vacunación Segundas Dosis Vacuna No Disponible Ecuador Versión 2 - 27 - 10 - 2021-Signed-Signed-Signed-SignedDocumento10 páginasLineamiento para Vacunación Segundas Dosis Vacuna No Disponible Ecuador Versión 2 - 27 - 10 - 2021-Signed-Signed-Signed-SignedJOHANNA ROJASAún no hay calificaciones
- Resolución 2021-1671Documento4 páginasResolución 2021-1671TélamAún no hay calificaciones
- Reglamento InfectoDocumento14 páginasReglamento InfectoJose Luis Alvarado CabralAún no hay calificaciones
- Guía para La Administración de La Tercera Dosis de La Vacuna Contra El COVID-19Documento4 páginasGuía para La Administración de La Tercera Dosis de La Vacuna Contra El COVID-19El Nuevo Día100% (2)
- Resolución No. 2046 de 2021Documento10 páginasResolución No. 2046 de 2021Adrián Quiroga RodríguezAún no hay calificaciones
- Memorándum Recomendación Sobre El Intervalo de Dosis de Refuerzo de Vacunación Contra Covid-19Documento3 páginasMemorándum Recomendación Sobre El Intervalo de Dosis de Refuerzo de Vacunación Contra Covid-19Sitio AndinoAún no hay calificaciones
- 1140 Adopta Nuevos Lineamientos para La Aplicación de Las Vacunas Contra El COVID-19Documento75 páginas1140 Adopta Nuevos Lineamientos para La Aplicación de Las Vacunas Contra El COVID-19diana gonzalezAún no hay calificaciones
- Hexaxim Prospecto MCdicosDocumento15 páginasHexaxim Prospecto MCdicosCintia IralaAún no hay calificaciones
- Protocolo 3era y 4ta Dosis PDFDocumento6 páginasProtocolo 3era y 4ta Dosis PDFWallpaper TigerAún no hay calificaciones
- UntitledDocumento6 páginasUntitledLilia J. MendozaAún no hay calificaciones
- INSTRUCCION VACUNACION COVID ANDALUCIA Actualizacion 24112021 Resumen EjecutivoDocumento12 páginasINSTRUCCION VACUNACION COVID ANDALUCIA Actualizacion 24112021 Resumen EjecutivoCarmen Lambea De JesúsAún no hay calificaciones
- Resolucion No 2021025659 - 24 Junio 2021Documento9 páginasResolucion No 2021025659 - 24 Junio 2021DIANAAún no hay calificaciones
- Vacunación Segundas DosisDocumento7 páginasVacunación Segundas DosisCarolina ZuletaAún no hay calificaciones
- Resolución No.1379 de 2021Documento29 páginasResolución No.1379 de 2021NoticiasBQ Atl.Aún no hay calificaciones
- Protocolo para La Adminitración de Tercera Dosis, Cuarta Dosis Y Dosis de Refuerzo de La Vacuna Contra La Covid-19 - 2023Documento18 páginasProtocolo para La Adminitración de Tercera Dosis, Cuarta Dosis Y Dosis de Refuerzo de La Vacuna Contra La Covid-19 - 2023Lizbeth CordovaAún no hay calificaciones
- Guía Rápida de Prescripción Nirmatrelvir - Ritonavir - 160123Documento11 páginasGuía Rápida de Prescripción Nirmatrelvir - Ritonavir - 160123chuyramosmtzAún no hay calificaciones
- Modificatoria de Directiva .EsaviDocumento29 páginasModificatoria de Directiva .Esavimaria horna lopezAún no hay calificaciones
- Resolucion Exenta 1558 Lineamientos Tecnicos Vacunacion Contra SARS CoV Con Vacuna Actualizada 2023 2024Documento61 páginasResolucion Exenta 1558 Lineamientos Tecnicos Vacunacion Contra SARS CoV Con Vacuna Actualizada 2023 2024mabelvargas019Aún no hay calificaciones
- Actualización de Vacunación Contra SARS CoV 2 Desde Los 6 Meses en AdelanteDocumento22 páginasActualización de Vacunación Contra SARS CoV 2 Desde Los 6 Meses en AdelanteAnita Sepúlveda RojasAún no hay calificaciones
- Resolución 1866 de 2021 MinSaludDocumento61 páginasResolución 1866 de 2021 MinSaludingri carolina caceres martinezAún no hay calificaciones
- Consentimiento Informado 12 16 CastellanoDocumento4 páginasConsentimiento Informado 12 16 CastellanoAlfAún no hay calificaciones
- Analisis y Distribucion de Vacuna Astrazeneca para Dosis de RefuerzoDocumento11 páginasAnalisis y Distribucion de Vacuna Astrazeneca para Dosis de RefuerzoDancy Sonia Labra HuamanvilcaAún no hay calificaciones
- Lineam Vac COVID Con Dosis de Refuerzo y Adicional - Final 25 de Noviembre ZDDocumento12 páginasLineam Vac COVID Con Dosis de Refuerzo y Adicional - Final 25 de Noviembre ZDmillermikeAún no hay calificaciones
- Info Segunda DosisDocumento1 páginaInfo Segunda DosisGermán Dorantes Ch67% (3)
- Info Segunda DosisDocumento1 páginaInfo Segunda Dosisesteban reneAún no hay calificaciones
- Covid GustavoDocumento1 páginaCovid GustavoAlex TecAún no hay calificaciones
- Bivalente Moderna 04-6-23Documento16 páginasBivalente Moderna 04-6-23jhonAún no hay calificaciones
- Consentimiento PARA PFIZER informado-adolescente-12-a-17-anos-REFUERZO-COVID-19Documento2 páginasConsentimiento PARA PFIZER informado-adolescente-12-a-17-anos-REFUERZO-COVID-19Brayan CruzAún no hay calificaciones
- Covid PerlaDocumento1 páginaCovid PerlaAlex TecAún no hay calificaciones
- Informe de Los ESAVI Vacunas COVID 19 Al 31.12.21Documento17 páginasInforme de Los ESAVI Vacunas COVID 19 Al 31.12.21Bandejas 2017Aún no hay calificaciones
- Ley Chile - Decreto 15 29-ABR-2021 MINISTERIO DE SALUD, SUBSECRETARÍA DE SALUD PÚBLICA - Biblioteca Del Congreso NacionalDocumento1 páginaLey Chile - Decreto 15 29-ABR-2021 MINISTERIO DE SALUD, SUBSECRETARÍA DE SALUD PÚBLICA - Biblioteca Del Congreso NacionalKinesiologo A DomicilioAún no hay calificaciones
- CCDUE 00212397 Vacunacion 03012022122044Documento1 páginaCCDUE 00212397 Vacunacion 03012022122044FRANCISCO CANDEL BOQUERAAún no hay calificaciones
- Norma InmunizacionesDocumento22 páginasNorma InmunizacionesYango la RosaAún no hay calificaciones
- CCDUE 07324857 Vacunacion 22012022074917Documento1 páginaCCDUE 07324857 Vacunacion 22012022074917Chris CambeilhAún no hay calificaciones
- NORMA Oficial Mexicana 036Documento4 páginasNORMA Oficial Mexicana 036Martin GarzaAún no hay calificaciones
- Lineamientos PaxlovidDocumento34 páginasLineamientos PaxlovidDiana LopezAún no hay calificaciones
- Balotario Sin ResaltarDocumento15 páginasBalotario Sin ResaltarDelia Roxana Millones VelasquezAún no hay calificaciones
- Tramiento Plasma Convalecientes COVID Rev Sist y MetaDocumento8 páginasTramiento Plasma Convalecientes COVID Rev Sist y Metarodolfo gorveñaAún no hay calificaciones
- Ficha Vacuna Pfizer BioNTech BivalenteDocumento8 páginasFicha Vacuna Pfizer BioNTech BivalenteNidia AguileraAún no hay calificaciones
- PlasmaDocumento5 páginasPlasmaGabriel ConteAún no hay calificaciones
- CCDUE 00212397 Vacunacion 03012022122000Documento1 páginaCCDUE 00212397 Vacunacion 03012022122000FRANCISCO CANDEL BOQUERAAún no hay calificaciones
- Reporte Cuatrimestral 2-JmpgDocumento4 páginasReporte Cuatrimestral 2-JmpgJuan M Peralta GarciaAún no hay calificaciones
- Esquema Primario Heterólogo COVID-19 Población de 12 Años en AdelanteDocumento17 páginasEsquema Primario Heterólogo COVID-19 Población de 12 Años en Adelantemexonac4Aún no hay calificaciones
- Gripe 2021-2022. DefinitivaDocumento5 páginasGripe 2021-2022. DefinitivaMonica COROAMAAún no hay calificaciones
- Bivalente Moderna 09-8-2023Documento18 páginasBivalente Moderna 09-8-2023Vasty Moreno ChengAún no hay calificaciones
- Consentimiento Informado Adolescente 12 A 17 Anos REFUERZO COVID 19Documento2 páginasConsentimiento Informado Adolescente 12 A 17 Anos REFUERZO COVID 19Cecibel AnchundiaAún no hay calificaciones
- 2º Refuerzo Pba Campaña FDocumento13 páginas2º Refuerzo Pba Campaña FJonatan GarciaAún no hay calificaciones
- COVIDDocumento6 páginasCOVIDisette.landerosAún no hay calificaciones
- Pasaporte Covid AdrianDocumento1 páginaPasaporte Covid Adriangema morenoAún no hay calificaciones
- Ruta Atencion Covid Clinica Castellana Version 2 Corregico Calidad y SubgerenciaDocumento6 páginasRuta Atencion Covid Clinica Castellana Version 2 Corregico Calidad y SubgerenciaYolanda Pinto CastroAún no hay calificaciones
- Información Técnica Vacuna Spikevax ModernaDocumento18 páginasInformación Técnica Vacuna Spikevax Modernamaria horna lopezAún no hay calificaciones
- PLASMA HIPERINMUNE1905 - Opt PDFDocumento34 páginasPLASMA HIPERINMUNE1905 - Opt PDFLiz PMAún no hay calificaciones
- Presentación Primera JNV Enero 2023Documento23 páginasPresentación Primera JNV Enero 2023MALLAMAS EPSIAún no hay calificaciones
- Lineamientos Gestion y Administracion PAI 2023 FINALDocumento33 páginasLineamientos Gestion y Administracion PAI 2023 FINALMALLAMAS EPSI100% (1)
- Lineamientos Enero 2023Documento25 páginasLineamientos Enero 2023MALLAMAS EPSIAún no hay calificaciones
- Actualizacion Esquema 23-1-2023Documento9 páginasActualizacion Esquema 23-1-2023MALLAMAS EPSIAún no hay calificaciones
- 20-Texto Del Artículo-62-3-10-20200620Documento5 páginas20-Texto Del Artículo-62-3-10-20200620MALLAMAS EPSIAún no hay calificaciones
- Admin, V66n2a01Documento4 páginasAdmin, V66n2a01MALLAMAS EPSIAún no hay calificaciones
- Plan de Accion Jornada de Vacunacion FirmadoDocumento3 páginasPlan de Accion Jornada de Vacunacion FirmadoMALLAMAS EPSIAún no hay calificaciones
- Circular Externa No. 028 de 2022 Aplicacioìn de La Vacuna Contra El COVID-19 en Los Puntos Establecidos Por El PAIDocumento3 páginasCircular Externa No. 028 de 2022 Aplicacioìn de La Vacuna Contra El COVID-19 en Los Puntos Establecidos Por El PAIMALLAMAS EPSIAún no hay calificaciones
- PNutricion AnimalDocumento42 páginasPNutricion Animaldiegopimentel55Aún no hay calificaciones
- Guia HNP Revista PDFDocumento57 páginasGuia HNP Revista PDFValeria Gohurdett100% (1)
- Tratamiento Estenosis EsofágicaDocumento9 páginasTratamiento Estenosis EsofágicaJhos Madahi QCAún no hay calificaciones
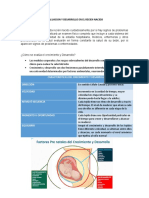
- Evaluacion y Desarrollo en El Recien NacidoDocumento3 páginasEvaluacion y Desarrollo en El Recien NacidoJulieth TorresAún no hay calificaciones
- Paciente OncologicoDocumento10 páginasPaciente OncologicoGary MendozaAún no hay calificaciones
- Lista de Cotejo - FluidoterapiaDocumento2 páginasLista de Cotejo - Fluidoterapiaalejandro miss mendezAún no hay calificaciones
- Niveles de Prevención para El DengueDocumento4 páginasNiveles de Prevención para El DengueAriana Cerquin RiosAún no hay calificaciones
- Epidemiologia Cancer Cuello UterinoDocumento51 páginasEpidemiologia Cancer Cuello UterinoEdinson Aquino LópezAún no hay calificaciones
- Plan A2Documento2 páginasPlan A2esperanzaelias94Aún no hay calificaciones
- Pro Hepatitis B C y DeltaDocumento48 páginasPro Hepatitis B C y DeltajulioAún no hay calificaciones
- HidrodinamicaDocumento5 páginasHidrodinamicaNayleth Peyton Escobar CabezasAún no hay calificaciones
- Anaya Quispe Melany - EnFERMERÍA TÉCNICA (Enfermedades Venéreas)Documento17 páginasAnaya Quispe Melany - EnFERMERÍA TÉCNICA (Enfermedades Venéreas)Melany Anaya QuispeAún no hay calificaciones
- Caracteres Sexuales y La VozDocumento52 páginasCaracteres Sexuales y La VozpaolaAún no hay calificaciones
- Paciente PolitraumatizadoDocumento22 páginasPaciente PolitraumatizadoYosbi GollesAún no hay calificaciones
- Lesiones Músculo EsqueléticasDocumento1 páginaLesiones Músculo EsqueléticasJaider PalmaAún no hay calificaciones
- Sindrome de Berardinelli SeipDocumento4 páginasSindrome de Berardinelli Seipapi-3697492Aún no hay calificaciones
- Lavado de Manos UpanaDocumento9 páginasLavado de Manos UpanaAbner LopezAún no hay calificaciones
- Vaginosis Bacteriana - ActualizaciónDocumento9 páginasVaginosis Bacteriana - ActualizaciónMicaela CalvopiñaAún no hay calificaciones
- Consulta: Sistema de Registro Clinico AvicenaDocumento2 páginasConsulta: Sistema de Registro Clinico AvicenaLU VELASQUEZAún no hay calificaciones
- Aspectos Historicos de La NeurologiaDocumento5 páginasAspectos Historicos de La NeurologiaYorisbel De La CruzAún no hay calificaciones
- Qué Es La ATMDocumento4 páginasQué Es La ATMDaly OrtizAún no hay calificaciones
- ABORTO Dr. CocaDocumento46 páginasABORTO Dr. CocaAndré Luiz QueirozAún no hay calificaciones
- RESUMEN CIRUG+ìA COMPLETO (Se Usa Este)Documento312 páginasRESUMEN CIRUG+ìA COMPLETO (Se Usa Este)capricornioAún no hay calificaciones
- Triptico Educacion AlimentariaDocumento2 páginasTriptico Educacion AlimentariaSaraCortes'50% (2)
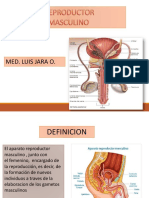
- Aparato Reproductor MasculinoDocumento23 páginasAparato Reproductor Masculinonilk andromeda100% (1)
- Área de Urgencias - Ginger RomanDocumento3 páginasÁrea de Urgencias - Ginger RomanAndrea RodríguezAún no hay calificaciones
- CASO ParafilicoDocumento3 páginasCASO Parafilicoanon_228178749Aún no hay calificaciones
- CLINICAL NEWS NUTRITION DAY COLOMBIA WebDocumento8 páginasCLINICAL NEWS NUTRITION DAY COLOMBIA WebAstrid Lozano ElorzaAún no hay calificaciones
- Tarea 8 AifcDocumento11 páginasTarea 8 AifcAlicia TorresAún no hay calificaciones
- Tecnica Quirurgica Del Ligamento Cruzado AnteriorDocumento7 páginasTecnica Quirurgica Del Ligamento Cruzado AnteriorLaura OrozcoAún no hay calificaciones