Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Cinetica Ejercicio 1
Cargado por
RT Espe0 calificaciones0% encontró este documento útil (0 votos)
70 vistas1 páginaLa reacción de descomposición del cloruro de sulfurilo sigue una cinética de primer orden, con la concentración de SO2Cl2 disminuyendo constantemente a medida que avanza la reacción. La constante de velocidad de la reacción de primer orden se calcula a partir de los datos de concentración en función del tiempo.
Descripción original:
Título original
CineticaEjercicio1
Derechos de autor
© © All Rights Reserved
Formatos disponibles
PDF, TXT o lea en línea desde Scribd
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoLa reacción de descomposición del cloruro de sulfurilo sigue una cinética de primer orden, con la concentración de SO2Cl2 disminuyendo constantemente a medida que avanza la reacción. La constante de velocidad de la reacción de primer orden se calcula a partir de los datos de concentración en función del tiempo.
Copyright:
© All Rights Reserved
Formatos disponibles
Descargue como PDF, TXT o lea en línea desde Scribd
0 calificaciones0% encontró este documento útil (0 votos)
70 vistas1 páginaCinetica Ejercicio 1
Cargado por
RT EspeLa reacción de descomposición del cloruro de sulfurilo sigue una cinética de primer orden, con la concentración de SO2Cl2 disminuyendo constantemente a medida que avanza la reacción. La constante de velocidad de la reacción de primer orden se calcula a partir de los datos de concentración en función del tiempo.
Copyright:
© All Rights Reserved
Formatos disponibles
Descargue como PDF, TXT o lea en línea desde Scribd
Está en la página 1de 1
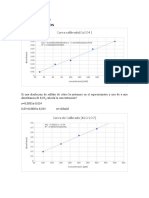
Considere la reacción de descomposición del cloruro de sulfurilo.
SO2Cl2(g) → SO2 (g) +Cl2(g)
La concentración del SO2Cl2(g) se determinó a temperatura constante en función del tiempo durante
la reacción de descomposición, con los siguientes resultados:
Tiempo (s) [SO2Cl2] (M) Tiempo (s) [SO2Cl2] (M)
0 0.1 800 0.0793
100 0.0971 900 0.077
200 0.0944 1000 0.0748
300 0.0917 1100 0.0727
400 0.089 1200 0.0706
500 0.0865 1300 0.0686
600 0.084 1400 0.0666
700 0.0816 1500 0.0647
Indique la molecularidad de la reacción, confirme si es una reacción de primer orden y calcule la
constante de la reacción.
También podría gustarte
- Previo 1. Oxidación de Los Metales y Propiedades PeriódicasDocumento4 páginasPrevio 1. Oxidación de Los Metales y Propiedades PeriódicasRT EspeAún no hay calificaciones
- Preguntas UnamDocumento15 páginasPreguntas UnamRT EspeAún no hay calificaciones
- Aplicaciones de Titulaciones Conductimétricas AcidoDocumento5 páginasAplicaciones de Titulaciones Conductimétricas Acidowilder condori choqueAún no hay calificaciones
- Reporte No 1 - Constante Cinética y Orden de Reacción en Un Reactor BatchDocumento23 páginasReporte No 1 - Constante Cinética y Orden de Reacción en Un Reactor BatchJimena AlvaradoAún no hay calificaciones
- Calculadora Regulación Blindobarras 3M MathewDocumento6 páginasCalculadora Regulación Blindobarras 3M MathewjuanAún no hay calificaciones
- Problema 2Documento2 páginasProblema 2Victor Cen100% (1)
- Minimos Cuadrados Multivariable Ejercicios ResueltosDocumento7 páginasMinimos Cuadrados Multivariable Ejercicios ResueltosJosue Carmona100% (1)
- ILAQ CICySBDocumento11 páginasILAQ CICySBMarinoChavarroCordobaAún no hay calificaciones
- Informe 2Documento10 páginasInforme 2Monica BravoAún no hay calificaciones
- Discusion 10Documento4 páginasDiscusion 10Elmer CardonaAún no hay calificaciones
- Práctica 1-Equipo 1Documento16 páginasPráctica 1-Equipo 1Alexis JesusAún no hay calificaciones
- Reporte Practica 8Documento17 páginasReporte Practica 8Verónica ChávezAún no hay calificaciones
- Práctica de Análisis 1Documento10 páginasPráctica de Análisis 1Felipe IdárragaAún no hay calificaciones
- Informe 1 - Freites y Gamboa - Lab. FisicoquimicaDocumento15 páginasInforme 1 - Freites y Gamboa - Lab. FisicoquimicaGabriel FreitesAún no hay calificaciones
- Verificacion Del Funcionamiento de Un EspectroDocumento3 páginasVerificacion Del Funcionamiento de Un EspectroReymundo SeguraAún no hay calificaciones
- Soldadura Tarea 2 (Autoguardado)Documento6 páginasSoldadura Tarea 2 (Autoguardado)Chärly ZumbäAún no hay calificaciones
- Ejercicios de Correlacion y Regresión Lineal 1Documento6 páginasEjercicios de Correlacion y Regresión Lineal 1CarlosR GonzalesAún no hay calificaciones
- Diseño de Una Destilación Binaria Acetona-AguaDocumento4 páginasDiseño de Una Destilación Binaria Acetona-AguaJuliana CastellanosAún no hay calificaciones
- 03 Balance de Materia Con Reaccion Quimica Hidratacion de Anhidrido AceticoDocumento9 páginas03 Balance de Materia Con Reaccion Quimica Hidratacion de Anhidrido AceticoAlexisEstradaAún no hay calificaciones
- Conductividad Molar de Los ElectrolitosDocumento6 páginasConductividad Molar de Los ElectrolitosAldahir FrankAún no hay calificaciones
- Practica 4 CineticaDocumento13 páginasPractica 4 Cineticacasandra alvaradoAún no hay calificaciones
- Tarea p4Documento1 páginaTarea p4AXEL URIEL VILLEDA CORONAAún no hay calificaciones
- Lab 5 de FisDocumento11 páginasLab 5 de Fiserik gomez67% (3)
- Conservacion de La EnergiaDocumento5 páginasConservacion de La EnergiaGuillermo Yucra Santa CruzAún no hay calificaciones
- Informe 9, Determinacion de La Actividad Enzimatica y Parametros de La Ecuacion de M-MDocumento11 páginasInforme 9, Determinacion de La Actividad Enzimatica y Parametros de La Ecuacion de M-MWendy AltamirandaAún no hay calificaciones
- 3.1. Ejercicios Módulo 3Documento6 páginas3.1. Ejercicios Módulo 3Octavio LunaAún no hay calificaciones
- Resistividad y ResistenciaDocumento6 páginasResistividad y ResistenciaAndrés CaicedoAún no hay calificaciones
- FugacidadDocumento3 páginasFugacidadWilhelm José Poclín RojasAún no hay calificaciones
- Sistema MúltipleDocumento10 páginasSistema MúltipleBertario Ríos GarcíaAún no hay calificaciones
- Tecnica DQODocumento4 páginasTecnica DQOZaira DelgadoAún no hay calificaciones
- Tecnica DQODocumento4 páginasTecnica DQOZaira DelgadoAún no hay calificaciones
- Practica 2 - FisicoquimicaDocumento9 páginasPractica 2 - FisicoquimicaCecilia Liliana Chavez FloresAún no hay calificaciones
- Tarea de CineticaDocumento1 páginaTarea de CineticaSnikeAún no hay calificaciones
- Acero 1045Documento6 páginasAcero 1045CaM0fLaG03Aún no hay calificaciones
- Espectroscopía 1Documento1 páginaEspectroscopía 1Jhonny Tituaña0% (1)
- RESULTADOS Práctica 8Documento3 páginasRESULTADOS Práctica 8Carlos BonifazAún no hay calificaciones
- Ejercicio AplicativoDocumento3 páginasEjercicio Aplicativomartin lopezAún no hay calificaciones
- Evaluacion EstadisticaDocumento3 páginasEvaluacion EstadisticaJesus VazquezAún no hay calificaciones
- Informe Dinamica #4Documento8 páginasInforme Dinamica #4JuanSebas GTRAún no hay calificaciones
- Memoria DescriptivaDocumento7 páginasMemoria DescriptivaJury Antony QA.Aún no hay calificaciones
- Problema 4 - 3 - 15 GeankopolisDocumento5 páginasProblema 4 - 3 - 15 GeankopolisMario JosafatAún no hay calificaciones
- Actividad Cinética EnzimáticaDocumento2 páginasActividad Cinética Enzimáticacristian lopezAún no hay calificaciones
- Informe 2Documento10 páginasInforme 2Encinas Montecinos Angie MishelAún no hay calificaciones
- Práctica 4. Ensayo de Tensión de Un PolimeroDocumento5 páginasPráctica 4. Ensayo de Tensión de Un PolimeroRene SolanoAún no hay calificaciones
- Resolucion de Ejercicio de SO3Documento6 páginasResolucion de Ejercicio de SO3Leydy Peña ChavarriaAún no hay calificaciones
- Practica 2 FPEDocumento7 páginasPractica 2 FPEJuanQueteImportaAún no hay calificaciones
- Parametros de EspesaminetosssDocumento57 páginasParametros de EspesaminetosssLisbethAyquiPaAún no hay calificaciones
- R6 Equipo 02Documento12 páginasR6 Equipo 02David Ramirez TorresAún no hay calificaciones
- Informe de La Verificación Del Espectrofotómetro de GISAM UTNDocumento10 páginasInforme de La Verificación Del Espectrofotómetro de GISAM UTNCa Res Mza S3Aún no hay calificaciones
- Espectro de Diseno Covenin 1756 2018Documento8 páginasEspectro de Diseno Covenin 1756 2018JuanAún no hay calificaciones
- TablaDocumento1 páginaTablaCamila MilAún no hay calificaciones
- Análisis de Una Muestra de Carbonato de CalcioDocumento8 páginasAnálisis de Una Muestra de Carbonato de CalcioNickole VillabonaAún no hay calificaciones
- G4-Termodinámica de Soluciones de Electrolitos PDFDocumento4 páginasG4-Termodinámica de Soluciones de Electrolitos PDFmariasolruiz1984Aún no hay calificaciones
- Lab 6 Fis 3Documento4 páginasLab 6 Fis 3Daniel MartinezAún no hay calificaciones
- Espectro Gonzalo ClementeDocumento9 páginasEspectro Gonzalo ClementeGONZALO CLEMENTE TRUJILLANOAún no hay calificaciones
- Producto Final de Mecanica de FluidosDocumento41 páginasProducto Final de Mecanica de FluidosPepeAún no hay calificaciones
- Copia de TTTTTTTTTTTDocumento5 páginasCopia de TTTTTTTTTTTRicardo ObandoAún no hay calificaciones
- Cinetica 9Documento9 páginasCinetica 9jonathan H.Aún no hay calificaciones
- AbsorbanciaDocumento3 páginasAbsorbanciaJulioAún no hay calificaciones
- Práctica 4Documento9 páginasPráctica 4Juan TamayoAún no hay calificaciones
- Plan 1142 8151 EDDocumento9 páginasPlan 1142 8151 EDRT EspeAún no hay calificaciones
- Plan 1143 8151 EDDocumento8 páginasPlan 1143 8151 EDRT EspeAún no hay calificaciones
- Plan 1151 8152 EDDocumento5 páginasPlan 1151 8152 EDRT EspeAún no hay calificaciones
- Plan 1344 8352 EDDocumento10 páginasPlan 1344 8352 EDRT EspeAún no hay calificaciones
- Plan 1156 8151 EDDocumento8 páginasPlan 1156 8151 EDRT EspeAún no hay calificaciones
- Plan 1141 8153 EDDocumento7 páginasPlan 1141 8153 EDRT EspeAún no hay calificaciones
- Museo Interactivo de EconomíaDocumento5 páginasMuseo Interactivo de EconomíaRT EspeAún no hay calificaciones
- Graficas AnaliticaDocumento2 páginasGraficas AnaliticaRT EspeAún no hay calificaciones
- AcordeonDocumento7 páginasAcordeonRT EspeAún no hay calificaciones
- Reacciones Oxido - ReducciónDocumento4 páginasReacciones Oxido - ReducciónRT EspeAún no hay calificaciones
- 1410 Microbiologiagen QADocumento3 páginas1410 Microbiologiagen QART EspeAún no hay calificaciones
- 0167 Confiteria QADocumento3 páginas0167 Confiteria QART EspeAún no hay calificaciones
- 1620 Nutri QADocumento3 páginas1620 Nutri QART EspeAún no hay calificaciones
- Serie. QO. Núñez Esparza Perla FabiolaDocumento15 páginasSerie. QO. Núñez Esparza Perla FabiolaRT EspeAún no hay calificaciones
- 1809 Labtec QaDocumento3 páginas1809 Labtec QaRT EspeAún no hay calificaciones
- Terc-Butoxido de PotasioDocumento2 páginasTerc-Butoxido de PotasioRT EspeAún no hay calificaciones
- Tarea EycDocumento2 páginasTarea EycRT EspeAún no hay calificaciones