Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Semana #01 Materia Y Energía Coordinador: Ing. Elmer Arenas Rios
Cargado por
Julio Sangay MantillaTítulo original
Derechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
Semana #01 Materia Y Energía Coordinador: Ing. Elmer Arenas Rios
Cargado por
Julio Sangay MantillaCopyright:
Formatos disponibles
IDEPUNP/ CICLO ENERO-MARZO 2007 1 QUIMICA
SEMANA Nº 01
MATERIA Y ENERGÍA
COORDINADOR: ING. ELMER ARENAS RIOS
1. Sobre la materia es una proposición falsa: 7. De los siguientes cambios ¿Cuántos son fenómenos
químicos?
a) Es toda realidad objetiva
b) Una de sus propiedades más importantes es el - Emisión de una partícula alfa
movimiento e incesante transformación. - Transformación de leche en yogurt
c) Existe en el espacio y en el tiempo independiente - Formación de una molécula de Oxígeno a partir de
de nuestros sentidos. oxigeno elemental
d) Otra forma de existencia es como un campo - Extracción de oro de un mineral diseminado
eléctrico. - Explosión de una bomba atómica.
e) Nada es absoluto, todo es relativo.
a) 1
b) 2
2. Un compuesto químico, es la sustancia: c) 3
d) 4
I. Formada por átomos con igual número atómico e) 5
II. Constituida por moléculas heterogéneas
III. Que se pueda dividir en otras sustancias mas 8. Si se tiene lo siguiente:
simples El material Q es un polvo gris que se puede separar por
IV.Eléctricamente neutra un magneto en un polvo negro y en otro amarillo; y
V. Formada por átomos de elementos diferentes. cuando se calienta se obtiene un material sólido R, que
no es atraído por el magneto y funde completamente
Son ciertas: para formar un liquido que es homogéneo,
a) III, IV y V b) I y IV c) II y V ¿Cuántas afirmaciones son correctas?
d) I,II,II e) II,III,IV y V
I. Q es una sustancia pura
II. R es un elemento
3. En un laboratorio se presenta: un frasco y un vaso de III. Q es una mezcla homogénea
polietileno llenos de agua, una probeta de polietileno con IV. R puede ser un compuesto
solución de cloruro de sodio; al clasificarlos
encontramos: a) Ninguna b) 1 c) 2
d) 3 e) 4
I. Todas son sustancias
II. Solo hay dos sustancias 9. Para solidificar un líquido se debe
III. Todos son cuerpos
IV. Solo hay tres cuerpos a) Aumentar la temperatura y la presión
V. Solo hay tres sustancias b) Bajar la presión y aumentar la temperatura
c) Bajar la temperatura y aumentar la presión
De las afirmaciones son ciertas: d) Aumentar la presión y el volumen
a) I y IV b) IIl y V c) II y V e) Bajar la presión y aumentar la temperatura.
d) II y IV e) IV y V
10. De las siguientes propiedades no es intensiva:
4. ¿Cuál de los siguientes conceptos contiene menor
cantidad de materia? a) El punto de ebullición
b) La densidad de los líquidos
a) Atomo b) Partícula c) Molécula c) El numero de átomos contenidos en un mol de
d) Elemento e) Electrón cualquier elemento
d) La constante de equilibrio de una reacción química a
temperatura dada
5. Se mezclan en cualquier proporción: e) El tiempo en llegar al punto fusión de una
a) Sólido con sólido determinada sustancia.
b) Liquido con solido
c) Gas con gas
d) Gas con líquido 11. ¿Cuántas aseveraciones son correctas?
e) Líquido con líquido
I. CO2: Se emplea en la fabricación de hielo seco,
bebidas gaseosas, etc.
6. Una mezcla es una conjunto de dos o mas sustancias II. NH3: Toxico muy soluble en agua, se usa para
que se caracteriza porque: preparar fertilizantes, etc.,. Refrigerante.
I. Sus propiedades son fijas y constantes. III. H2O2: Oxidante, antiséptico, bactericida,
II. Sus componentes no se pueden distinguir blanqueador, etc.
fácilmente IV. Mg(OH)2 y Al(OH)3 . Medicamentos antiácidos y
III. Sus componentes se pueden separar por medios laxantes
físicos y mecánicos V. NaClO: Lejía comercial, se usa en lavado y
IV. Cada uno de sus componentes conserva sus blanqueo de ropa.
propiedades y características físicas y
químicas a) 1
V. Está constituida por una sola fase. b) 2
c) 3
Son ciertas: d) 4
e) 5
a) I y II b) II y III c)III y IV
d) IV y V e) Todas
IDEPUNP/ CICLO ENERO-MARZO 2007 2 QUIMICA
12. Una sustancia que al disolverse en agua se disocia I. Según EINSTEIN a mayor velocidad, mayor será la
totalmente en iones (% de ionización prácticamente masa de un cuerpo
100%) Se denomina: II. Según EINSTEIN la mayor velocidad que se puede
desarrollar es la de la luz
a) Electrolito Fuerte III. En el estado plasmático hay una ionización de las
b) Electrolito Débil moléculas y se encuentra a temperaturas muy
c) No electrolito elevadas,
d) Soluto
e) Solvente a) I b)II c) NInguna
d)III e) Todas
13. Calcular la energía cinética, en ergios de una partícula 20. Determinar la cantidad de calorías que se irradian al
alfa, cuya velocidad es 1,6 x 10 7 m/s. Se sabe que una explosionar una bomba atómica de medio kilogramo de
partícula alfa tiene una masa de 4 umas masa inicial, recogiéndose 400 g de material de
productos
a) 3,50 x 10-6
b) 2,88 x 10-6 a) 2,15 x 1015 b) 4,41x 1014 c) 1,42 x 1010
c)5,88 x 10-6 d) 9,1 x 107 e) 1,14 x 1016
d) 6,25 x 10-6
e) 8,55 x 10-6 21. Un protón y un antiprotón al chocar mutuamente, sus
14. Cuando se quema un galón de gasolina, se desprende masas se transforman totalmente en energía, Calcular la
126 MJ/gal de calor. La reacción se puede simbolizar cantidad de Joules desprendidos,
por la combustión del octano. Masa p+ = 1,67 x 10-24 g
25 a) 4,3 x 10-14 b) 5x 10-11 c) 4,4 x 1012
C8 H18 + O 2 8CO 2 + 9H 2O d) 6 x 10-14 e) 3 x 10-10
2
H=126MJ/gal 22. En una explosión nuclear se observa que la masa de los
productos es un centésimo menor que la masa de los
Calcular la masa por mol asociada con esta energía. En reactantes, que inicialmente fueron 2 kg, Determinar
el supuesto que el galón contiene 28 moles de octano. cuantos ergios de energía se desprenderá en la
explosión
a) 5x10-18 kg
b) 5x10-14kg a) 4,1 x 1019 b) 1,41 x 1019 c) 4,2 x 1022
c) 5x10-11kg d) 8,1 x 1018 e) 1,8 x 1022
d) 5x10-8 kg
e) 5x103kg 23. Determinar la masa en gramos que se desintegra en la
explosión de una bomba de hidrogeno de 10 megatones,
15. ¿Qué cantidad de energía en joules se necesita o se donde un megaton es igual a 4,186 x 1022 ergios ,
desprende en la siguiente reacción?
a) 341 b) 465 c) 181,4
d) 0,418 e) 148
1
1 H Li 2 He
7
3
4
2
24. ¿ Cual será la relación entre la masa final y la masa
Además: inicial de un cuerpo, cuya masa en reposo es llevada
7
Li = 7,016g ; 11 H = 1,0078g ; 4
He = 4,0026g 12
3 2 hasta una velocidad de de la velocidad de la luz
13
a) 9,0702 x 1027
b) 9,0702 x 1013
c) 14,0702 x 1015
12 13 8 4 1
a) b) c) d) e)
d) 4,0702 x 1013 13 5 12 9 2
e) 1,674 x 1012
16. Un cuerpo cuya masa en la tierra es de 173 g al ser 25. Si en la siguiente transmutación:
lanzado al espacio adquiere una velocidad equivalente
al mitad de la velocidad de la luz. La masa del cuerpo en
ese instante en gramos será: 3
He 01n11H 13H
2
a) 50 b) 100 c) 200
d) 400 e) 500 Se desprendieron 7,38 x 1017 ergios de energía, Hallar la
3
masa del 2 He si se tiene:
17. Calcular la velocidad que deberá adquirir un cuerpo si se
desea que su masa se triplique ( Expresar velocidad en 1 1 3
km/s) 0 n = 1,00867 g 1 H = 1,00783g 1 H =3,0161 g
a) 0,28 b) 2,8 c) 2,8 x 102 a) 5,018 g b) 3,016 g c) 3,821g
d) 2,8 x 105 e) 2,8 x 108 d) 5,964 g e) 4,021g
18. Determinar cuantas lámparas de mil watts podrán
alimentarse durante un año con la energía de un gramo
de plutonio sabiendo que la conversión nuclear es total.
a) 2 b) 28 c) 285
d) 2857 e) 28570
19. ¿Qué afirmación es incorrecta?
IDEPUNP/ CICLO ENERO-MARZO 2007 3 QUIMICA
HOJA DE CLAVES
CICLO: ENERO MARZO 2007
CURSO: QUÍMICA
SEMANA: 01 – MATERIA Y ENERGÍA
Pregunta Clave Tiempo Dificultad
(Min.)
01 d 1 F
02 e 2 F
03 d 2 F
04 e 1 F
05 c 1 F
06 c 2 F
07 c 2 F
08 b 2 F
09 c 2 F
10 e 3 M
11 e 2 F
12 a 1 F
13 e 3 M
14 c 3 M
15 e 3 M
16 c 3 M
17 d 3 M
18 d 3 M
19 c 2 F
20 a 3 M
21 e 3 M
22 e 4 D
23 b 3 M
24 b 3 M
25 b 3 M
También podría gustarte
- Motor Autoexcitado y Conexión ShutDocumento2 páginasMotor Autoexcitado y Conexión ShutFernando Coronc50% (2)
- Quimica Elmer Ronald ArenaDocumento4 páginasQuimica Elmer Ronald ArenaPERCY TORRES AVALOSAún no hay calificaciones
- Sol Semana 1 2015-I JunioDocumento9 páginasSol Semana 1 2015-I JunioVÍCTOR ATÍLIO BARREDA DEL ARROYOAún no hay calificaciones
- Repaso CepreDocumento9 páginasRepaso Cepreflordmvasquez87Aún no hay calificaciones
- PROBLEMAS DE QUÍMICA FÍSICA Y QUÍMICADocumento3 páginasPROBLEMAS DE QUÍMICA FÍSICA Y QUÍMICAMATEO TAIPE TANIAAún no hay calificaciones
- Materia IiDocumento4 páginasMateria IiJorge Luis Valdez CondeñaAún no hay calificaciones
- M G01 QuimDocumento2 páginasM G01 QuimDrakenAún no hay calificaciones
- Conceptos básicos de química: materia, energía y fenómenos químicosDocumento2 páginasConceptos básicos de química: materia, energía y fenómenos químicosDrakenAún no hay calificaciones
- N° 01 - Ciclo 2018 - C - MateriaDocumento5 páginasN° 01 - Ciclo 2018 - C - MateriaRaul Leon EspinozaAún no hay calificaciones
- Semana 1 2015-I JUNIODocumento5 páginasSemana 1 2015-I JUNIOVÍCTOR ATÍLIO BARREDA DEL ARROYOAún no hay calificaciones
- Practica QuimicaDocumento2 páginasPractica Quimicacarlosvt94Aún no hay calificaciones
- Adicional 1 Química CepreDocumento2 páginasAdicional 1 Química CeprejanelAún no hay calificaciones
- Quimica 1 PDFDocumento5 páginasQuimica 1 PDFBruce Mirko Apaza BejarAún no hay calificaciones
- U1 Química I PRUEBA F1Documento6 páginasU1 Química I PRUEBA F1Leslie Parra100% (1)
- Centro de estudios preuniversitarios UNA-PUNO: Química primera semanaDocumento3 páginasCentro de estudios preuniversitarios UNA-PUNO: Química primera semanaToribio Washington Mamani Quispe100% (1)
- MATERIA PRACTICA I ColegioDocumento4 páginasMATERIA PRACTICA I ColegioRebeca I-jAún no hay calificaciones
- Ing. Uni Materia PucallpaDocumento3 páginasIng. Uni Materia Pucallpamark steven cuyubamba nuñezAún no hay calificaciones
- Quimica Bco 169761 Downloable 2384608Documento3 páginasQuimica Bco 169761 Downloable 2384608Jhasmani Vir100% (1)
- Problemas - MateriaDocumento3 páginasProblemas - MateriaMATEO TAIPE TANIAAún no hay calificaciones
- Semana 01 - CD - Cepunt-2021-Ii-LetrasDocumento2 páginasSemana 01 - CD - Cepunt-2021-Ii-LetrasJuanita Lucia Gastelo AjipAún no hay calificaciones
- 1tema 1. Ejercicios de MateriaDocumento2 páginas1tema 1. Ejercicios de MateriaBicho BichitoAún no hay calificaciones
- Fenómenos químicos y físicosDocumento2 páginasFenómenos químicos y físicosalvaroAún no hay calificaciones
- CUESTIONARIO DE CLASE Sesión 5Documento3 páginasCUESTIONARIO DE CLASE Sesión 5fernandito1803Aún no hay calificaciones
- EXAMEN #1 Ordinario Enero-MarzoDocumento2 páginasEXAMEN #1 Ordinario Enero-MarzoSmith SacAún no hay calificaciones
- QUIMICA TAREA 01 35ñpoDocumento2 páginasQUIMICA TAREA 01 35ñpoSebastian Soto ArevaloAún no hay calificaciones
- Quimica Royveli CarhuachinDocumento3 páginasQuimica Royveli Carhuachinjose humberto gomez jimenez100% (1)
- UCLDocumento4 páginasUCLjuan nelsonAún no hay calificaciones
- Balota 1Documento1 páginaBalota 1LINDA CORNEJO TORRESAún no hay calificaciones
- Química de la materiaDocumento2 páginasQuímica de la materiaisis gonzalesAún no hay calificaciones
- Introducción A La Quimica-Materia-Energia: I. II. IiiDocumento2 páginasIntroducción A La Quimica-Materia-Energia: I. II. IiiMarcelo MontoyaAún no hay calificaciones
- Quimica Sem 1Documento3 páginasQuimica Sem 1Alexis Esmith Castañeda RequejoAún no hay calificaciones
- Quimica Tema 1 SabadoDocumento3 páginasQuimica Tema 1 SabadoEdson Luis Egusquiza CordovaAún no hay calificaciones
- CENTRO PRE UNIVERSITARIO: CICLO VIRTUAL 2022-IADocumento3 páginasCENTRO PRE UNIVERSITARIO: CICLO VIRTUAL 2022-IAMELANY ヅAún no hay calificaciones
- Química en el colegio San AgustínDocumento4 páginasQuímica en el colegio San AgustínCN Kram100% (1)
- 1 MateriaDocumento3 páginas1 MateriaRosa Rodas CastilloAún no hay calificaciones
- Química básica: materia, energía y cambios físicos y químicosDocumento4 páginasQuímica básica: materia, energía y cambios físicos y químicosPercy Torres Avalos KeplerAún no hay calificaciones
- La Química como ciencia naturalDocumento8 páginasLa Química como ciencia naturalKeneth Denner Chagua NamucheAún no hay calificaciones
- Repaso de Química GeneralDocumento7 páginasRepaso de Química GeneralJeelmy Zapata ChávezAún no hay calificaciones
- Química SEM1: Estados de la materia, cambios físicos y químicosDocumento5 páginasQuímica SEM1: Estados de la materia, cambios físicos y químicosKaren Yuly Hilares SuelAún no hay calificaciones
- Primer Material de Quìmica Pre-2023-1Documento54 páginasPrimer Material de Quìmica Pre-2023-1Nicolle Campos chamorroAún no hay calificaciones
- Quimica - PRACTICA #01 CEPU VERANO 2016 PDFDocumento3 páginasQuimica - PRACTICA #01 CEPU VERANO 2016 PDFsalcedomaniaAún no hay calificaciones
- Ev 1 Medio Reacciones QuimicasDocumento5 páginasEv 1 Medio Reacciones QuimicasLeslie ParraAún no hay calificaciones
- (Repaso y Tarea)Documento4 páginas(Repaso y Tarea)Carlos Antonio Mendoza ArteagaAún no hay calificaciones
- Miscelánea 2Documento3 páginasMiscelánea 2DAYANA ANGELA CASTILLA VARGASAún no hay calificaciones
- Quimica 1 ChaucaDocumento2 páginasQuimica 1 ChaucaMiguel Angel Chauca AguilarAún no hay calificaciones
- Problemas Química Gral - BIOmedDocumento13 páginasProblemas Química Gral - BIOmedJavier Eduardo Corzo LequericaAún no hay calificaciones
- 1-Estudiante (18) Pag2Documento4 páginas1-Estudiante (18) Pag2Yesenia Mamani100% (1)
- Actividades de Evaluación para Practicar Unidad 4Documento6 páginasActividades de Evaluación para Practicar Unidad 4danieldeagredagonzalezAún no hay calificaciones
- SEMANA 01-MATERIA Y ENERGIA-INTERMEDIO. DesarrolloDocumento2 páginasSEMANA 01-MATERIA Y ENERGIA-INTERMEDIO. Desarrollojhon riscoAún no hay calificaciones
- Materia y EnergiaDocumento2 páginasMateria y EnergiajuanAún no hay calificaciones
- Modulo Ciencias Fase IDocumento16 páginasModulo Ciencias Fase INicole MVAún no hay calificaciones
- QUPA1009Documento1 páginaQUPA1009Nekano Bandera Duran Jr.Aún no hay calificaciones
- CEPRE UNJBG 2020 II Semana 01Documento2 páginasCEPRE UNJBG 2020 II Semana 01Nelson GonzalesAún no hay calificaciones
- Quimic ADocumento30 páginasQuimic AJOEL WILLIAM MTAún no hay calificaciones
- Q Tarea UNP Niv1Documento2 páginasQ Tarea UNP Niv1nicol anabela sanchez espinozaAún no hay calificaciones
- Ejercicios de Verano para El ExamenDocumento2 páginasEjercicios de Verano para El ExamenCN KramAún no hay calificaciones
- Problemas Propuestos-La MateriaDocumento3 páginasProblemas Propuestos-La MateriaMATEO TAIPE TANIAAún no hay calificaciones
- 7A - SEM 01 - QU+ìMICA - PRDocumento2 páginas7A - SEM 01 - QU+ìMICA - PRJosé Tandaipa'nAún no hay calificaciones
- Termodinámica y diagramas de equilibrioDe EverandTermodinámica y diagramas de equilibrioAún no hay calificaciones
- Semana 1 - QuímicaDocumento2 páginasSemana 1 - QuímicaJulio Sangay MantillaAún no hay calificaciones
- Semana 05 - QuímicaDocumento4 páginasSemana 05 - QuímicaJulio Sangay MantillaAún no hay calificaciones
- QI-08M-101 (P - Unidades Químicas de Masa I) C4Documento1 páginaQI-08M-101 (P - Unidades Químicas de Masa I) C4Julio Sangay MantillaAún no hay calificaciones
- HCANALESDocumento4 páginasHCANALESJulio Sangay MantillaAún no hay calificaciones
- Análisis de ConsistenciaDocumento41 páginasAnálisis de ConsistenciaJulio Sangay MantillaAún no hay calificaciones
- Peso Equivalente para Primer Grado de SecundariaDocumento5 páginasPeso Equivalente para Primer Grado de SecundariaeddAún no hay calificaciones
- ELECTRODINÁMICADocumento3 páginasELECTRODINÁMICAJulio Sangay MantillaAún no hay calificaciones
- Caratula QuimicaDocumento2 páginasCaratula QuimicaJulio Sangay MantillaAún no hay calificaciones
- Desarrollo de EjerciciosDocumento5 páginasDesarrollo de EjerciciosJulio Sangay MantillaAún no hay calificaciones
- Ejercicio 567Documento4 páginasEjercicio 567Julio Sangay MantillaAún no hay calificaciones
- Sal - PLAGIADocumento4 páginasSal - PLAGIAJulio Sangay MantillaAún no hay calificaciones
- Acido y SalesDocumento4 páginasAcido y SalesJulio Sangay MantillaAún no hay calificaciones
- Reactivo LimDocumento4 páginasReactivo LimJulio Sangay MantillaAún no hay calificaciones
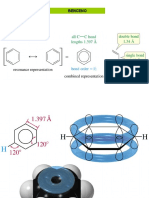
- Hidrocarburos AromaticosDocumento43 páginasHidrocarburos AromaticosAngela Chui cruzAún no hay calificaciones
- Semana 08 Ejerciccios Desarrollados de Impulso y Cantidad de MovimientoDocumento9 páginasSemana 08 Ejerciccios Desarrollados de Impulso y Cantidad de MovimientoJulio Sangay MantillaAún no hay calificaciones
- Tarea - Practica de Cinetica de Sistemas de PartículasDocumento2 páginasTarea - Practica de Cinetica de Sistemas de PartículasJulio Sangay MantillaAún no hay calificaciones
- Semana 09 Flujos de MasaDocumento27 páginasSemana 09 Flujos de MasaJulio Sangay MantillaAún no hay calificaciones
- SilabusDocumento6 páginasSilabusJulio Sangay MantillaAún no hay calificaciones
- Estudio de Caso Aplicado A Obras HidraulicasDocumento40 páginasEstudio de Caso Aplicado A Obras HidraulicasJulio Sangay MantillaAún no hay calificaciones
- 02 Densidad, PE, GEDocumento19 páginas02 Densidad, PE, GEJulio Sangay MantillaAún no hay calificaciones
- DENSIDAD Y GRAVEDAD ESPECÍFICA Grupo 2Documento8 páginasDENSIDAD Y GRAVEDAD ESPECÍFICA Grupo 2JHONATAN JEYSON MANTILLA CARRASCOAún no hay calificaciones
- Syllabus Suelos 3Documento7 páginasSyllabus Suelos 3Julio Sangay MantillaAún no hay calificaciones
- Ejercicios Densidad (MDF)Documento8 páginasEjercicios Densidad (MDF)Anaís HuamánAún no hay calificaciones
- 01 Relacion Fuerza MasaDocumento12 páginas01 Relacion Fuerza MasaJulio Sangay MantillaAún no hay calificaciones
- 05.APUSDocumento218 páginas05.APUSHenry Maguiña AllendeAún no hay calificaciones
- Revision Del Expediente TecnicoDocumento84 páginasRevision Del Expediente TecnicoJulio Sangay MantillaAún no hay calificaciones
- Viscocidad - PotterDocumento11 páginasViscocidad - PotterMitzyAún no hay calificaciones
- Estudio de Caso Aplicado A Obras HidraulicasDocumento40 páginasEstudio de Caso Aplicado A Obras HidraulicasJulio Sangay MantillaAún no hay calificaciones
- Control de calidad del concretoDocumento37 páginasControl de calidad del concretoJulio Sangay MantillaAún no hay calificaciones
- Componentes Del Expediente TecnicoDocumento3 páginasComponentes Del Expediente TecnicoJulio Sangay MantillaAún no hay calificaciones
- Informe de 2 Turbina de GasDocumento75 páginasInforme de 2 Turbina de GasJavier RodriguezAún no hay calificaciones
- Guia de Trabajo Grado SeptimoDocumento3 páginasGuia de Trabajo Grado SeptimoArturo Jose Beltran MendozaAún no hay calificaciones
- Tuberías en Serie y ParaleloDocumento32 páginasTuberías en Serie y ParalelobrayanfimuniAún no hay calificaciones
- Guia TP Parte 1-2-3Documento8 páginasGuia TP Parte 1-2-3Rodrigo Dos SantosAún no hay calificaciones
- Glosario de AgitacionDocumento2 páginasGlosario de AgitacionarantzaAún no hay calificaciones
- Determinación de propiedades de cemento asfálticoDocumento10 páginasDeterminación de propiedades de cemento asfálticoMaritza Ramirez FernandezAún no hay calificaciones
- Compendio de Fisica Walter PerezDocumento144 páginasCompendio de Fisica Walter PerezAngyBelAún no hay calificaciones
- PRÁCTICA DE LABORATORIO N0 3: BALANCEO ESTÁTICO Y DINÁMICODocumento4 páginasPRÁCTICA DE LABORATORIO N0 3: BALANCEO ESTÁTICO Y DINÁMICOIvan GarzonAún no hay calificaciones
- de Potencial EléctricoDocumento16 páginasde Potencial EléctricoFrank HuingoAún no hay calificaciones
- 2344Documento6 páginas2344metanoia88Aún no hay calificaciones
- Practica2 InerciaDocumento14 páginasPractica2 InerciajavimonleongomisAún no hay calificaciones
- Sensores y Actuadores 2023Documento17 páginasSensores y Actuadores 2023Kevin MirandaAún no hay calificaciones
- 1 Resonancia Magnética NuclearDocumento18 páginas1 Resonancia Magnética NuclearMarta RodriguezAún no hay calificaciones
- Wa0031.Documento23 páginasWa0031.Ricardo ZambranoAún no hay calificaciones
- Camara FrigorificaDocumento12 páginasCamara FrigorificaJorge Wilis Julca TapiaAún no hay calificaciones
- Laboratorio HidraulicaDocumento14 páginasLaboratorio HidraulicaYESICA ORDOÑEZ SOLAEZAún no hay calificaciones
- Tema 4 MEdicion Angular (Brújula)Documento29 páginasTema 4 MEdicion Angular (Brújula)Lucia PaitaAún no hay calificaciones
- Informe N°13Documento9 páginasInforme N°13JHONATAN JOSSUE FARRO ROJASAún no hay calificaciones
- Especificaciones Tecnicas de IieeDocumento14 páginasEspecificaciones Tecnicas de IieejesusAún no hay calificaciones
- 05 Variacion Presion Informe FinalDocumento26 páginas05 Variacion Presion Informe FinalCARLOS ALEXANDER CAMPOS MELCONAún no hay calificaciones
- Discusión 1 Cii-19Documento5 páginasDiscusión 1 Cii-19francisco polancoAún no hay calificaciones
- 03 Ejercicios de Entropía y Segunda Ley de La TermodinámicaDocumento5 páginas03 Ejercicios de Entropía y Segunda Ley de La TermodinámicaLuisAún no hay calificaciones
- Cátedra de Geofísica AplicadaDocumento29 páginasCátedra de Geofísica Aplicadawendyk28Aún no hay calificaciones
- Propiedades Fisicas de Los Gases, Expo 1Documento83 páginasPropiedades Fisicas de Los Gases, Expo 1carlos sanchezAún no hay calificaciones
- Hidráulica 2 Capitulo 3Documento43 páginasHidráulica 2 Capitulo 3Stiven CasañasAún no hay calificaciones
- Informe Laboratorio 1Documento7 páginasInforme Laboratorio 1juan camilo gutierrez buitrago100% (1)
- 02 Problemas de Maquinas SimplesDocumento8 páginas02 Problemas de Maquinas SimplesPaulo H.Aún no hay calificaciones
- Cuaderno Trabajo Cálculo IntegralDocumento47 páginasCuaderno Trabajo Cálculo IntegralCisne SalasAún no hay calificaciones
- Nivelación y sus tipos enDocumento27 páginasNivelación y sus tipos enIrbin SarmientoAún no hay calificaciones