Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Práctica 9. Fisicoquímica
Práctica 9. Fisicoquímica
Cargado por
Sangriento MartinezDescripción original:
Título original
Derechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
Práctica 9. Fisicoquímica
Práctica 9. Fisicoquímica
Cargado por
Sangriento MartinezCopyright:
Formatos disponibles
INSTITUTO POLITÉCNICO NACIONAL
ESCUELA NACIONAL DE CIENCIAS BIOLÓGICAS
PRÁCTICA No. 9
“Conductividad eléctrica en soluciones”
FISICOQUÍMICA
GRUPO: 2QM3
ELABORÓ:
- MARTINEZ SEGOVIANO MIGUEL ANGEL
- MENDOZA SALAS LESLIE CITLALI
- MORENO CASTILLO RODOLFO
Fecha: 09 / 05 / 2021 GRUPO: 2QM3
INSTITUTO POLITÉCNICO NACIONAL
ESCUELA NACIONAL DE CIENCIAS BIOLÓGICAS
PRÁCTICA No. 9
“Conductividad eléctrica en soluciones”
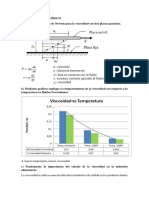
⮚ INTRODUCCIÓN:
Un electrolito es cualquier sustancia que contiene en su composición iones libres, que hacen
que se comporte como un conductor eléctrico. La conductividad eléctrica es una característica
de los electrolitos y se puede determinar mediante la ley de Ohm, que determina la resistencia
al paso de corriente de un conductor electrolítico.
Existen varias formas de calcular la conductividad eléctrica. El método más adecuado consiste
en calcular la constante indirectamente midiendo su resistencia cuando contiene una solución
de conductividad conocida.
En una solución electrolítica, Kolhrausch descubrió que la conductividad depende de la
concentración del electrolito y que en soluciones diluidas de electrolitos fuertes está dada por
la ecuación:
Una parte importante de la conductividad en una disolución es el grado de ionización, donde
Arrhenius decía que el grado de concentración interviene en la conductividad eléctrica del
electrolito por la siguiente ecuación:
⮚ PARTE EXPERIMENTAL:
Utilizando un conductímetro, determinar las lecturas de conductividad (eléctrica y equivalente)
de cada una de las soluciones de electrolito proporcionadas (fuertes y débiles), posteriormente,
realizar gráficas con los datos pertenecientes.
Las determinaciones se harán en orden ascendente de concentración.
Fecha: 09 / 05 / 2021 GRUPO: 2QM3
INSTITUTO POLITÉCNICO NACIONAL
ESCUELA NACIONAL DE CIENCIAS BIOLÓGICAS
⮚ RESULTADOS:
1. Se determinó la Conductividad eléctrica (k) en mS/cm para el NaCl a diferentes
concentraciones.
[NaCl] √[𝑵𝒂𝑪𝒍] K ⋀m=K/[NaCl]
moles/L mS/cm Scm2/N
4.97x10-3 .070 .649 130.58
9.901x10-3 .099 1.252 126.45
19.60x10-3 .14 2.231 113.82
29.13x10-3 .170 3.214 110.33
47.62x10-3 .218 5.157 108.29
65.42x10-3 .255 6.974 106.60
82.56x10-3 .287 8.961 108.53
107.14x10-3 .327 11.200 104.53
Figura 1.- Conductividad eléctrica equivalente de NaCl en solución, en función de
la raíz cuadrada de su concentración.
Realizando los cálculos, se obtuvo el valor de la ordenad, pendiente y el coeficiente de correlación
lineal.
a= 132.018 b= -93.883 r= -.89114 r2= .79413
Ec. Empírica ⋀m= 132.018 - 93.883 x
Fecha: 09 / 05 / 2021 GRUPO: 2QM3
INSTITUTO POLITÉCNICO NACIONAL
ESCUELA NACIONAL DE CIENCIAS BIOLÓGICAS
2. Se determinó la Conductividad eléctrica (k) en mS/cm para el KCl a diferentes concentraciones.
[KCl] √[𝑲𝑪𝒍] K ⋀m=K/[KCl]
moles/L mS/cm Scm2/N
4.97x10-3 .070 .7004 140.78
9.901x10-3 .099 1.296 130.89
19.60x10-3 .14 2.431 124.03
29.13x10-3 .170 3.523 120.94
47.62x10-3 .218 5.595 117.49
65.42x10-3 .255 7.640 116.78
82.56x10-3 .287 9.537 115.51
107.14x10-3 .327 13.110 114.74
Figura 2.- Conductividad eléctrica equivalente de KCl en solución, en función de
la raíz cuadrada de su concentración.
Realizando los cálculos, se obtuvo el valor de la ordenad, pendiente y el coeficiente de correlación
lineal.
a= 140.252 b= -89.948 r= -.90647 r2= .82168
Ec. Empírica ⋀m= 140.252 – 89.948 x
Fecha: 09 / 05 / 2021 GRUPO: 2QM3
INSTITUTO POLITÉCNICO NACIONAL
ESCUELA NACIONAL DE CIENCIAS BIOLÓGICAS
3. Se determinó la Conductividad eléctrica (k) en mS/cm para el HCl a diferentes concentraciones.
[HCl] √[𝑯𝑪𝒍] K ⋀m=K/[HCl]
moles/L mS/cm Scm2/N
4.97x10-3 .070 1.907 383.32
9.901x10-3 .099 3.911 395.01
19.60x10-3 .14 7.513 383.31
29.13x10-3 .170 10.96 376.24
47.62x10-3 .218 17.88 375.47
65.42x10-3 .255 24.17 369.45
82.56x10-3 .287 30.40 368.21
107.14x10-3 .327 39.13 365.21
Figura 3.- Conductividad eléctrica equivalente de HCl en solución, en función de
la raíz cuadrada de su concentración.
Realizando los cálculos, se obtuvo el valor de la ordenad, pendiente y el coeficiente de correlación
lineal.
a= 396.100 b= -97.435 r= -.90356 r2= .81642
Ec. Empírica ⋀m= 396.100 – 97.435 x
Fecha: 09 / 05 / 2021 GRUPO: 2QM3
INSTITUTO POLITÉCNICO NACIONAL
ESCUELA NACIONAL DE CIENCIAS BIOLÓGICAS
4. Se determinó la Conductividad eléctrica (k) en mS/cm para el CH3COOH a diferentes
concentraciones.
[CH3COOH] √[𝑪𝑯𝟑𝑪𝑶𝑶𝑯] K ⋀m=K/[CH3COOH]
moles/L mS/cm Scm2/N
4.97x10-3 .070 .1015 20.40
9.901x10-3 .099 .1450 14.64
19.60x10-3 .14 .2020 10.30
29.13x10-3 .170 .2479 8.51
47.62x10-3 .218 .3200 6.71
65.42x10-3 .255 .3827 5.84
82.56x10-3 .287 .4260 5.15
107.14x10-3 .327 .4833 4.51
Figura 4.- Conductividad eléctrica equivalente de CH3COOH en solución, en
función de la raíz cuadrada de su concentración.
Realizando los cálculos, se obtuvo el valor de la ordenad, pendiente y el coeficiente de correlación
lineal.
a= 20.274 b= -55.003 r= -.91404 r2= .83546
Ec. Empírica ⋀m= 20.274 – 55.003 x
Fecha: 09 / 05 / 2021 GRUPO: 2QM3
INSTITUTO POLITÉCNICO NACIONAL
ESCUELA NACIONAL DE CIENCIAS BIOLÓGICAS
⮚ DISCUSIÓN:
Una vez obtenida la conductividad molar junto la gráfica de raíz cuadrada de la concentración
y la conductividad molar se pueden sacar algunos datos interesantes respecto a las
disoluciones analizadas. Cuando la concentración disminuye ó la dilución aumenta, la Λ
aumenta y tiende hacia un valor límite el cual se conoce como conductividad molar límite Λ∞.
La conductividad molar depende de la concentración del electrolito. Sería independiente de la
misma si la conductividad fuese directamente proporcional a la concentración, pero esto no es
así debido a que la interacción entre los iones es disociativa a concentraciones bajas y
asociativa a concentraciones altas.
Por un lado, los electrolitos fuertes, como el KCl, el HCl, muestran una disminución lineal de la
conductividad molar con la raíz cuadrada de la concentración. Disminuye lentamente cuando
aumenta la concentración, debido a que aumentan las atracciones entre iones de signo
contrario disminuyendo su movilidad
⮚ CONCLUSIONES:
La conductividad eléctrica nos ayudará a saber que el equivalente de una solución
electrolítica no va a variar linealmente con la concentración, también identificará que el
equivalente de una solución electrolítica aumentará en función de su disociación.
La conductividad eléctrica es usada en varios sectores como parámetro y que existen
gran variedad de aparatos para su medición, algunos de los sectores que usan a la
conductividad son: industrias químicas, alimenticias, textiles,papeleras, etc.
⮚ CUESTIONARIO:
1. Escriba qué factores afectan la conductividad de una solución de electrolitos.
Puede ser por: la concentración del soluto,cambios térmicos, constante dieléctrica del
medio solvente,la atracción interiónica, las velocidades absolutas de los iones y el grado
de ionización en dichas soluciones.
2. Escriba aplicaciones de las mediciones de conductividad en:
a) Control de calidad del agua (en la industria alimentaria, en agricultura).
Conservas vegetales, lixiviación, salmueras, centrales azucareras y elaboración de
queso.
Sistemas de regadío, hidroponía etc.
Fecha: 09 / 05 / 2021 GRUPO: 2QM3
INSTITUTO POLITÉCNICO NACIONAL
ESCUELA NACIONAL DE CIENCIAS BIOLÓGICAS
b) Medición de sólidos disueltos en una solución (salinidad del agua).
La identificación de conductividad en las concentraciones de sólidos disueltos, pueden
ayudar a saber si tienen contaminantes, ya que un alto nivel de ellos sabran si el agua
tiene contaminantes humanos pero si tiene bajas concentraciones significará que puede
limitar el crecimiento de vida acuático.
3. Enuncie algunas características de medidores de conductividad comerciales, como el
tipo de sensores para uso directo en matriz sólida, etc.
● Conductímetros de mesa:
Combina parámetros de pH, conductividad, resistencia, TDS y salinidad.
● Conductímetro portátil:
Tiene un electrodo de titanio el cual evitará al máximo las roturas y posee 5 puntos de
calibración.
● Conductímetro en campo educativo.
Realiza medidas de 3 rangos diferentes, utiliza el método de 4 anillos lo cual ayudará aa
mayor precisión y fiabilidad.
⮚ BIBLIOGRAFÍA:
1.- Chang. Raymond (1987). “Fisicoquímica con aplicaciones a sistemas biológicos” 3era
edición, ediciones CECSA. pp 158, 159.
2.- Zumdahl, Steven (2009). Principios químicos (6ª ed.). Bostón. Nueva York: Houghton
Mifflin. págs. 384–387. ISBN 978-0-547-19626-8.
Fecha: 09 / 05 / 2021 GRUPO: 2QM3
También podría gustarte
- Ingeniería química. Soluciones a los problemas del tomo IDe EverandIngeniería química. Soluciones a los problemas del tomo IAún no hay calificaciones
- 16 ProblemarioDocumento8 páginas16 ProblemarioLEONEL CRUZ ORTIZAún no hay calificaciones
- Guia Uam Azc QuimicaDocumento18 páginasGuia Uam Azc Quimicadorian hernandez100% (2)
- Practica 1 Solubilidad Del AzucarDocumento8 páginasPractica 1 Solubilidad Del AzucarAlex Tapara Mantilla100% (1)
- 01 - Ejercicios PropuestosDocumento17 páginas01 - Ejercicios PropuestosGeorge Albert Ruiz Arce100% (1)
- Informe de Titulacion Acido-BaseDocumento7 páginasInforme de Titulacion Acido-Baseandres guerrero100% (2)
- Problemario de EspectrofotometríaDocumento12 páginasProblemario de Espectrofotometríarene123456789eduardo40% (5)
- Universidad de Las Fuerzas Armadas Cuestionario 3Documento4 páginasUniversidad de Las Fuerzas Armadas Cuestionario 3Josue Pazmino100% (1)
- Práctica 2 Densidad. FISICOQUÍMICADocumento7 páginasPráctica 2 Densidad. FISICOQUÍMICASangriento MartinezAún no hay calificaciones
- Trabajo Tema 8Documento10 páginasTrabajo Tema 8Cärlos Månuel Seguil SolânoAún no hay calificaciones
- Ptap QuicapataDocumento86 páginasPtap Quicapatakevin100% (1)
- Eym 3Documento10 páginasEym 3Keyla Areli Ruiz GarciaAún no hay calificaciones
- ResistividadDocumento8 páginasResistividadJose Angel Palomeque SanchezAún no hay calificaciones
- Unidad 1 2 3 Tarea 4 Componente PracticoDocumento28 páginasUnidad 1 2 3 Tarea 4 Componente PracticoJorge Fabian GualteroAún no hay calificaciones
- Tarea 4 Componente PracticoDocumento23 páginasTarea 4 Componente Practicoyulitza muñozAún no hay calificaciones
- Laboratorio #3 - Fisica IiiDocumento15 páginasLaboratorio #3 - Fisica IiiDipaola Zuniga MarmanilloAún no hay calificaciones
- Ejercicios PolidispersidadDocumento32 páginasEjercicios PolidispersidadUriel Pamplona VidrioAún no hay calificaciones
- Reporte Atomo de HidrogenoDocumento5 páginasReporte Atomo de HidrogenoLeo MartinezAún no hay calificaciones
- Avila Carlos Examen Final de Análisis Instrumental Módulo Uv - g2Documento3 páginasAvila Carlos Examen Final de Análisis Instrumental Módulo Uv - g2Ivn CorderoAún no hay calificaciones
- Practica 2 Electricidad y MagnetismoDocumento9 páginasPractica 2 Electricidad y Magnetismobusytrejoe100% (1)
- Practica de Fisica Basica 0Documento3 páginasPractica de Fisica Basica 0Daniela MendezAún no hay calificaciones
- Informe de Lab 4Documento14 páginasInforme de Lab 4Renzo HuamanAún no hay calificaciones
- Practica Estructura MolecularDocumento18 páginasPractica Estructura MolecularLucas Felipe Torres RojasAún no hay calificaciones
- Mecanic ADocumento6 páginasMecanic AAlvaro Calderon0% (1)
- P1GEOHIDROLOGIADocumento8 páginasP1GEOHIDROLOGIADaff AcostaAún no hay calificaciones
- Ejer Cici Quimica AmbientalDocumento14 páginasEjer Cici Quimica AmbientalHenry GarciaAún no hay calificaciones
- Labo. de Fisica2 .Practica2.para - ArreglarDocumento14 páginasLabo. de Fisica2 .Practica2.para - ArreglarJHOSELIN MISHEL BENAVIDEZ TAPIAAún no hay calificaciones
- Bfi06m p4Documento1 páginaBfi06m p4MARIA CRISTINA LIMACHI PAUCARAún no hay calificaciones
- Campo y Potencial ElectricoDocumento7 páginasCampo y Potencial ElectricoDaniel Vargas TrujilloAún no hay calificaciones
- 2.1. Ejercicios Módulo 2Documento6 páginas2.1. Ejercicios Módulo 2Octavio LunaAún no hay calificaciones
- Laboratorio de Extructura FinalDocumento27 páginasLaboratorio de Extructura FinalCristian RicaurteAún no hay calificaciones
- Preparación Ex - Parcial!Documento29 páginasPreparación Ex - Parcial!Jean Pierre Torres MedinaAún no hay calificaciones
- Fase 4 Transporte de Sólidos y FluidosDocumento11 páginasFase 4 Transporte de Sólidos y FluidosJovany rojano100% (1)
- Practica 4 - Constante Dielectrica PDFDocumento9 páginasPractica 4 - Constante Dielectrica PDFtasty cherryAún no hay calificaciones
- Examen de Electricidad 1Documento4 páginasExamen de Electricidad 1David MontorAún no hay calificaciones
- CapacitanciaDocumento9 páginasCapacitanciaGabriela BojorquezAún no hay calificaciones
- Cuestionario EXAMEN FINAL 20211Documento3 páginasCuestionario EXAMEN FINAL 20211JORGE JOSSUE OLIVARES PARDOAún no hay calificaciones
- 3er Trabajo Grupal BFI04 - B - Grupo - 6Documento17 páginas3er Trabajo Grupal BFI04 - B - Grupo - 6Stephanie QuispeAún no hay calificaciones
- Tarea 4 - Componente PracticoDocumento23 páginasTarea 4 - Componente Practicoanon_6871011320% (1)
- Caso1. Ingeniería de MaterialesDocumento6 páginasCaso1. Ingeniería de MaterialesDarling MedinaAún no hay calificaciones
- Velocidad y Rapidez InstantaneaDocumento4 páginasVelocidad y Rapidez InstantaneaalonsoAún no hay calificaciones
- Resolución de Los Ejercicios Del Capítulo 39 Impare1Documento56 páginasResolución de Los Ejercicios Del Capítulo 39 Impare1Diego Andrade100% (2)
- Tarea4 ComponentePrácticoDocumento18 páginasTarea4 ComponentePrácticojohnAún no hay calificaciones
- Informe Práctica 2 Version 2Documento7 páginasInforme Práctica 2 Version 2Emmanuel BonillaAún no hay calificaciones
- Factor de Inercia para Moléculas PolaresDocumento8 páginasFactor de Inercia para Moléculas Polaresghella MendozaAún no hay calificaciones
- Producto Académico N1 QUIMICADocumento6 páginasProducto Académico N1 QUIMICAGIANELLE KEZIAH CATALAN ESTRADAAún no hay calificaciones
- Ejercicios QuimicaDocumento7 páginasEjercicios QuimicaAngel Bailey BaezaAún no hay calificaciones
- Informe de Laboratorio I3Documento12 páginasInforme de Laboratorio I3lineyAún no hay calificaciones
- Fenomenos (REYNOLDS)Documento13 páginasFenomenos (REYNOLDS)Alecc AbregoAún no hay calificaciones
- 3 Carga Eléctrica Elemental - Actualizada 2021Documento8 páginas3 Carga Eléctrica Elemental - Actualizada 2021GONZALO RAUL TICONA GRANADOSAún no hay calificaciones
- UntitledDocumento6 páginasUntitledFernando AcostaAún no hay calificaciones
- Termodinamica - Enrique 5 CicloDocumento4 páginasTermodinamica - Enrique 5 CicloEnrique Rojas BermudoAún no hay calificaciones
- Semana 3Documento17 páginasSemana 3Kevin Perez RiquelmeAún no hay calificaciones
- Examen Sustitutorio de Suelos I - 2021 - II.Documento2 páginasExamen Sustitutorio de Suelos I - 2021 - II.Luis GuerreroAún no hay calificaciones
- Practica 4 Equipo 1Documento7 páginasPractica 4 Equipo 1Byron Saúl CMAún no hay calificaciones
- Ejercicio 1Documento5 páginasEjercicio 1Jesus Fabian ArenasAún no hay calificaciones
- Tarea Semana EstadísticaDocumento4 páginasTarea Semana EstadísticaJAQUELINE SUCET FLORES MUYAún no hay calificaciones
- Informe5Documento7 páginasInforme5Samantha Navarro100% (1)
- Tercer ParcialDocumento9 páginasTercer ParcialEdwin AmayaAún no hay calificaciones
- Practica Analisis InstrumentalDocumento28 páginasPractica Analisis InstrumentalAlejandra Franco Vasquez100% (1)
- Informe 3Documento3 páginasInforme 3Fritz Rodriguez OchoaAún no hay calificaciones
- Verificacion EspectrofotometroDocumento6 páginasVerificacion EspectrofotometroSangriento MartinezAún no hay calificaciones
- Práctica 4 - Eq 2 Sec BDocumento8 páginasPráctica 4 - Eq 2 Sec BSangriento MartinezAún no hay calificaciones
- LOWRYDocumento2 páginasLOWRYSangriento MartinezAún no hay calificaciones
- Verificación Del Funcionamiento de Un EspectrofotómetroDocumento8 páginasVerificación Del Funcionamiento de Un EspectrofotómetroSangriento MartinezAún no hay calificaciones
- P1 Determinación AireDocumento9 páginasP1 Determinación AireSangriento MartinezAún no hay calificaciones
- Práctica 3 - Martinez Segoviano Miguel AngelDocumento5 páginasPráctica 3 - Martinez Segoviano Miguel AngelSangriento MartinezAún no hay calificaciones
- EXAMEN EXTRAORDINARIO - Martinez Segoviano Miguel AngelDocumento5 páginasEXAMEN EXTRAORDINARIO - Martinez Segoviano Miguel AngelSangriento MartinezAún no hay calificaciones
- Tercer Problemario - Martinez Segoviano Miguel AngelDocumento5 páginasTercer Problemario - Martinez Segoviano Miguel AngelSangriento MartinezAún no hay calificaciones
- Práctica 8. FisicoquímicaDocumento10 páginasPráctica 8. FisicoquímicaSangriento MartinezAún no hay calificaciones
- Práctica 3 y 4 - Leyes de Los Gases. FISICOQUÍMICADocumento14 páginasPráctica 3 y 4 - Leyes de Los Gases. FISICOQUÍMICASangriento MartinezAún no hay calificaciones
- Práctica 1 Refractometría. FISICOQUÍMICADocumento6 páginasPráctica 1 Refractometría. FISICOQUÍMICASangriento MartinezAún no hay calificaciones
- Práctica 5. FisicoquímicaDocumento10 páginasPráctica 5. FisicoquímicaSangriento MartinezAún no hay calificaciones
- Información Técnica Alta RBM®-QDocumento11 páginasInformación Técnica Alta RBM®-QXavi PerezAún no hay calificaciones
- Proyecto 2 RESUMENDocumento3 páginasProyecto 2 RESUMENjuan sebastian aristizabalAún no hay calificaciones
- Diseño ExperimentalDocumento4 páginasDiseño ExperimentalKata Rapers Fuentes Martinez LdsAún no hay calificaciones
- Taller N AboniaDocumento8 páginasTaller N AboniaDAMIAN CAMILO NARVAEZ SANTACRUZAún no hay calificaciones
- Taller de Teoría de Membranas 2020Documento7 páginasTaller de Teoría de Membranas 2020Miguel Leon GuzmanAún no hay calificaciones
- Carta Gantt Segundo Medio (Lista)Documento4 páginasCarta Gantt Segundo Medio (Lista)Nicol Wachtendorff ChandíaAún no hay calificaciones
- Universidad Tecnológica de Panamá Facultad de Ingeniería Eléctrica Técnico en Electrónica Biomédica Guia de Laboratorios de Ciencias Básicas 2023Documento72 páginasUniversidad Tecnológica de Panamá Facultad de Ingeniería Eléctrica Técnico en Electrónica Biomédica Guia de Laboratorios de Ciencias Básicas 2023Thais Michell BatistaAún no hay calificaciones
- Taller de Disoluciones AcuosasDocumento3 páginasTaller de Disoluciones AcuosasJEYSON ADRIAN GONZALEZ GONZALEZAún no hay calificaciones
- Grupo 7 LIXIVIACION-exposicion - pptx111111111111111111Documento46 páginasGrupo 7 LIXIVIACION-exposicion - pptx111111111111111111erika jimenaAún no hay calificaciones
- DETERMINACIÓN DEL Volumen Específico y Viscosidad Del GlicerolDocumento4 páginasDETERMINACIÓN DEL Volumen Específico y Viscosidad Del GlicerolSebastian ViverosAún no hay calificaciones
- Laboratorio #01 Tecnologia IndustrialDocumento24 páginasLaboratorio #01 Tecnologia IndustrialEDITH NAARA CAMPOS SILVAAún no hay calificaciones
- Contaminación Atmosférica. Técnicas de Muestreo en Emisión.: Master en Ingeniería y Gestión MedioambientalDocumento40 páginasContaminación Atmosférica. Técnicas de Muestreo en Emisión.: Master en Ingeniería y Gestión MedioambientalmarcoaqmAún no hay calificaciones
- Manual Química Inorgánica 2022Documento38 páginasManual Química Inorgánica 2022Alexandra Isabella Lopez ValdezAún no hay calificaciones
- 5.2.2. Conceptos y Caiculos de Molaridad, Molalidad, Norm. y Form.Documento8 páginas5.2.2. Conceptos y Caiculos de Molaridad, Molalidad, Norm. y Form.Claudia de la RosaAún no hay calificaciones
- Cuestiones y Problemas de Las Olimpiadas de Quimica Parte 4Documento285 páginasCuestiones y Problemas de Las Olimpiadas de Quimica Parte 4Yeimi VanessaAún no hay calificaciones
- Taller Metodos Numericos InterpolacionDocumento7 páginasTaller Metodos Numericos InterpolacionMariel Bazán100% (1)
- Informe de Confitado - Tecnologia de AlimDocumento14 páginasInforme de Confitado - Tecnologia de AlimGabriela ArciniegaAún no hay calificaciones
- MEDICIÓN DE LA CONCENTRACIÓN DE LOS CONTAMINANTES Y IIDocumento11 páginasMEDICIÓN DE LA CONCENTRACIÓN DE LOS CONTAMINANTES Y IIFiorella AliagaAún no hay calificaciones
- Informe Metalurgia ExtractivaDocumento20 páginasInforme Metalurgia ExtractivaLoreto Petersen ceaAún no hay calificaciones
- Proc Ind Sem3 - Balance de Materia en Proc QuimicosDocumento24 páginasProc Ind Sem3 - Balance de Materia en Proc QuimicosMarcialCabreraRuizAún no hay calificaciones
- Diseño de Un Sistema de Evaporacion para Concentrar Liquido de Prensado Del Proceso de Harina de PescadoDocumento116 páginasDiseño de Un Sistema de Evaporacion para Concentrar Liquido de Prensado Del Proceso de Harina de PescadoAlex Ostos AlvaAún no hay calificaciones
- Taz PFC 2011 504 - AneDocumento93 páginasTaz PFC 2011 504 - AneNikol Lopez ValdezAún no hay calificaciones
- Resolucion de Problemas-Quispe Herna Sergio LuisDocumento9 páginasResolucion de Problemas-Quispe Herna Sergio LuisSergio Quispe HernaAún no hay calificaciones
- Tipos de Mezcladores PDFDocumento177 páginasTipos de Mezcladores PDFGissela Venlasaga100% (1)
- Extracción de ADNDocumento4 páginasExtracción de ADNLaura VargasAún no hay calificaciones
- Inf.5 Preparación y Conductividad de DisolucionesDocumento8 páginasInf.5 Preparación y Conductividad de Disoluciones雪花Aún no hay calificaciones