Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Se Disuelven 90 Gramos de NaOH en 200 Gramos de Agua
Se Disuelven 90 Gramos de NaOH en 200 Gramos de Agua
Cargado por
CESAR GAMBOA ANAYA0 calificaciones0% encontró este documento útil (0 votos)
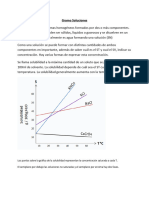
51 vistas1 páginaSe disuelve 90 gramos de NaOH en 200 gramos de agua, resultando en una solución acuosa de hidróxido de sodio con una densidad de 1.340 g/ml, una concentración de 415.858 g/L de NaOH, y una concentración molar de 10.396 M.
Descripción original:
Título original
Se disuelven 90 gramos de NaOH en 200 gramos de agua (1).docx
Derechos de autor
© © All Rights Reserved
Formatos disponibles
DOCX, PDF, TXT o lea en línea desde Scribd
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoSe disuelve 90 gramos de NaOH en 200 gramos de agua, resultando en una solución acuosa de hidróxido de sodio con una densidad de 1.340 g/ml, una concentración de 415.858 g/L de NaOH, y una concentración molar de 10.396 M.
Copyright:
© All Rights Reserved
Formatos disponibles
Descargue como DOCX, PDF, TXT o lea en línea desde Scribd
0 calificaciones0% encontró este documento útil (0 votos)
51 vistas1 páginaSe Disuelven 90 Gramos de NaOH en 200 Gramos de Agua
Se Disuelven 90 Gramos de NaOH en 200 Gramos de Agua
Cargado por
CESAR GAMBOA ANAYASe disuelve 90 gramos de NaOH en 200 gramos de agua, resultando en una solución acuosa de hidróxido de sodio con una densidad de 1.340 g/ml, una concentración de 415.858 g/L de NaOH, y una concentración molar de 10.396 M.
Copyright:
© All Rights Reserved
Formatos disponibles
Descargue como DOCX, PDF, TXT o lea en línea desde Scribd
Está en la página 1de 1
Se disuelven 90 gramos de NaOH en 200 gramos de agua, resultando un volumen de 216.
42
ml. Determinar:
Soluto: m=90 g NaOH; masa molar: 40; n= 2.25
Solvente: m=200 g H2O; masa molar: 18; n=11.1
Solución: m=290 g; volumen: 216.42 ml
1. La densidad de la solución
D=m/v : (90+200) g/216.42ml
D=1.340 g/ml
2. La concentración de NaOH en gramos por litro
nNaOH=90/40=2.25 mol
x= (90 g NaOH * 1 L)/0.21642 L
X=415.858 g
3. La concentración molar de NaOH
MNaOH=n/v= (2.25 mol)/0.21642L = 10.396 M
4. La concentración normal de NaOH
O=1
N=M*O
N=10.396*1=10.396 N
5. La concentración de NaOH en % en peso
%p/p=(msto)/(mste)*100=90/290*100=31.03
6. La concentración molal de NaOH
Molalidad = (nsto)/(mste)= 2.25 mol/0.2 kg = 11.25 m
7. Las fracciones molares del soluto y disolvente
%gfmsto= 2.25/(2.25+11.1) = 2.25/13.35 =0.169
%gfmste= 11.1/(2.25+11.1) = 11.1/13.35 =0.831
También podría gustarte
- Practica de Concentracion (Informe)Documento5 páginasPractica de Concentracion (Informe)Jossue MorenoAún no hay calificaciones
- QuimicaDocumento7 páginasQuimicaKely Ticona Chiara50% (4)
- Términos de Concentración y Especifique Sus UnidadesDocumento2 páginasTérminos de Concentración y Especifique Sus UnidadesPercy Waldemar Ticona Queque0% (2)
- Taller de SolucionesDocumento16 páginasTaller de SolucionesJavier Hoyos100% (1)
- Volumen Molal ParcialDocumento23 páginasVolumen Molal Parcialwilmer100% (2)
- Soluciones 5to. de SecundariaDocumento23 páginasSoluciones 5to. de SecundariaFernando MercadoAún no hay calificaciones
- Propiedades-Coligativas-Ejercicios TerminadoDocumento19 páginasPropiedades-Coligativas-Ejercicios TerminadonayelisAún no hay calificaciones
- 1 Ejercicios PropuestosDocumento7 páginas1 Ejercicios PropuestosArnaldo ArizaAún no hay calificaciones
- DISOLUCIONESDocumento15 páginasDISOLUCIONESSergio Lazarte Mercado80% (5)
- 5 Disoluciones - OcepbDocumento20 páginas5 Disoluciones - Ocepbwilly chaveAún no hay calificaciones
- EJERCICIOSDocumento13 páginasEJERCICIOSDELMY ISABEL ÁLVAREZ VILLAFRANCOAún no hay calificaciones
- Aporte FisicoquimicaDocumento8 páginasAporte FisicoquimicaNohoralia MuñozAún no hay calificaciones
- Previo Al Laboratorio 55Documento3 páginasPrevio Al Laboratorio 55Carlos Enrique Gutierrez Pachas100% (1)
- Ejercicio 1Documento3 páginasEjercicio 1dairyAún no hay calificaciones
- TALLER DISOLUCIONES EN QUIMICA Fase 3Documento8 páginasTALLER DISOLUCIONES EN QUIMICA Fase 3Carlos Uriel Cortes CamposAún no hay calificaciones
- Taller 10 Ejercicios-SolucionesDocumento7 páginasTaller 10 Ejercicios-SolucionesKris ArizaAún no hay calificaciones
- Sesión 1. Introduccion A La Química AnaliticaDocumento18 páginasSesión 1. Introduccion A La Química AnaliticaANDERSON JHORDY CARRION PELAEZAún no hay calificaciones
- Soluciones Ingreso 26-8-2021Documento13 páginasSoluciones Ingreso 26-8-2021verocatebielAún no hay calificaciones
- Problemas de MolaridadDocumento4 páginasProblemas de MolaridaddavidhAún no hay calificaciones
- Soluciones y Propiedades ColigativasDocumento6 páginasSoluciones y Propiedades ColigativasKamer JouediehAún no hay calificaciones
- Quimica Ambiental. TALLER N°3Documento9 páginasQuimica Ambiental. TALLER N°3JANIER PALACIOS MARMOLEJOAún no hay calificaciones
- QuimicaDocumento7 páginasQuimicaIngrid Catalina CuaranAún no hay calificaciones
- Ejercicios Clase 07 de OctubreDocumento3 páginasEjercicios Clase 07 de OctubreSergio Rozo PerdomoAún no hay calificaciones
- Taller de Quimica 2Documento17 páginasTaller de Quimica 2Jeisson AlvarezAún no hay calificaciones
- Química Analítica I-2do Examen Parte ADocumento52 páginasQuímica Analítica I-2do Examen Parte AsaruausAún no hay calificaciones
- Desarrollo de EjerciciosDocumento15 páginasDesarrollo de EjerciciosGISELLA MANCHAY TOCTOAún no hay calificaciones
- Hoja de Reporte #8 Lab QmaDocumento4 páginasHoja de Reporte #8 Lab QmaFrandaly CabreraAún no hay calificaciones
- Las Soluciones-CsjDocumento57 páginasLas Soluciones-CsjQuenguan FranklinAún no hay calificaciones
- Taller Soluciones QuimicasDocumento14 páginasTaller Soluciones QuimicasMafe MorenoAún no hay calificaciones
- PREVIO DE LABORATORIO 6.docx ImprimirDocumento4 páginasPREVIO DE LABORATORIO 6.docx Imprimirmishellaguilar667Aún no hay calificaciones
- Concentración de Las DisolucionesDocumento9 páginasConcentración de Las Disolucionesĸathy Maradiaga LagosAún no hay calificaciones
- Ejercicios de Soluciones DesarrolladosDocumento8 páginasEjercicios de Soluciones DesarrolladosMarianoo Montalvo FonsecaAún no hay calificaciones
- Taller 1 Química Sanitaria (Molaridad, Molalidad, Normalidad)Documento10 páginasTaller 1 Química Sanitaria (Molaridad, Molalidad, Normalidad)MARIA CAMILA BUITRAGO OLIVEROSAún no hay calificaciones
- Practica Quimica 2 BDocumento4 páginasPractica Quimica 2 BJulio LiranzoAún no hay calificaciones
- Ejercicios QuimicaDocumento26 páginasEjercicios QuimicaMauro Fernando Hoyos Moya0% (1)
- DisolucionesDocumento39 páginasDisolucionesJimenaAún no hay calificaciones
- Parte 1 SolucionesDocumento90 páginasParte 1 SolucionesBryan GuamanAún no hay calificaciones
- 3era Guia de Actividades 4to Año QuímicaDocumento13 páginas3era Guia de Actividades 4to Año QuímicaJohan ParraAún no hay calificaciones
- Problemas de Análisis VolumétricoDocumento4 páginasProblemas de Análisis VolumétricoQuique Báez García100% (1)
- Volumen Molar (Co) 1Documento14 páginasVolumen Molar (Co) 1Yuri CarolinaAún no hay calificaciones
- Taller N0.1 de Quimica Sanitaria - ArregladoDocumento15 páginasTaller N0.1 de Quimica Sanitaria - ArregladoCapricornioGamerAún no hay calificaciones
- QuimicaDocumento6 páginasQuimicaluis eduardoAún no hay calificaciones
- Expresiones de Concentración QuímicasDocumento20 páginasExpresiones de Concentración Químicasomarjesus03Aún no hay calificaciones
- Respuestas de Guia de Unidades de ConcentracionDocumento7 páginasRespuestas de Guia de Unidades de Concentracionenzo tolozaAún no hay calificaciones
- PREPARACIO Y VALORIZACIO DE NaOH Y H2SO4Documento4 páginasPREPARACIO Y VALORIZACIO DE NaOH Y H2SO4Joseph GmrAún no hay calificaciones
- Soluciones 1 2023Documento21 páginasSoluciones 1 2023souliergeralAún no hay calificaciones
- Ejercicios Resueltos. Unidad 5 - QuímicaDocumento4 páginasEjercicios Resueltos. Unidad 5 - QuímicaRamiro ReinaldoAún no hay calificaciones
- Una Muestra de 135 Gramos de Agua de Mar Se Evapora A Sequedad y Queda Un Residuo de 4Documento11 páginasUna Muestra de 135 Gramos de Agua de Mar Se Evapora A Sequedad y Queda Un Residuo de 4deybi encarnacion beltreAún no hay calificaciones
- Practica 4 QuimicaDocumento3 páginasPractica 4 QuimicaEric VillanuevaAún no hay calificaciones
- Soluciones QuimicasDocumento58 páginasSoluciones QuimicasrdiazbetetaAún no hay calificaciones
- Unidad 7Documento42 páginasUnidad 7Alvaro GuerreroAún no hay calificaciones
- Ejercicios Resueltos. Unidad 5 - QuímicaDocumento4 páginasEjercicios Resueltos. Unidad 5 - Químicacamii.y.yonakaAún no hay calificaciones
- CN-5 Seminario - MergedDocumento17 páginasCN-5 Seminario - MergedJULISSA YASMIN CONDOR MAMANIAún no hay calificaciones
- FIcha de Actividad Repaso 2 UD4 CorregidaDocumento4 páginasFIcha de Actividad Repaso 2 UD4 CorregidaMalena Silvia MassaAún no hay calificaciones
- Informes 11 - 14Documento25 páginasInformes 11 - 14MARIA ALEJANDRA ORELLANO VELASQUEZAún no hay calificaciones
- Matias Weiler, Semana 5Documento7 páginasMatias Weiler, Semana 5Matias WeilerAún no hay calificaciones
- Disoluciones Ejercicios (Autoguardado)Documento9 páginasDisoluciones Ejercicios (Autoguardado)Keissy Brenda Valles DreyfusAún no hay calificaciones
- Tema 6 Soluciones - CompletoDocumento11 páginasTema 6 Soluciones - CompletoDavid DeelavillaAún no hay calificaciones
- 3ro Medio Disoluciones QuimicasDocumento40 páginas3ro Medio Disoluciones Quimicaseioa3Aún no hay calificaciones
- PC 4 de Operaciones y Procesos MetalurgicosDocumento4 páginasPC 4 de Operaciones y Procesos MetalurgicosCESAR GAMBOA ANAYAAún no hay calificaciones
- Resolucion de Problemas Ope 4Documento4 páginasResolucion de Problemas Ope 4CESAR GAMBOA ANAYAAún no hay calificaciones
- Informe 05 OpeDocumento11 páginasInforme 05 OpeCESAR GAMBOA ANAYAAún no hay calificaciones
- Lectura N°4Documento2 páginasLectura N°4CESAR GAMBOA ANAYAAún no hay calificaciones
- PC Semana 9Documento6 páginasPC Semana 9CESAR GAMBOA ANAYAAún no hay calificaciones
- PC Semana 9Documento4 páginasPC Semana 9CESAR GAMBOA ANAYAAún no hay calificaciones
- Labo 12Documento2 páginasLabo 12CESAR GAMBOA ANAYAAún no hay calificaciones
- Informe de La Práctica 5Documento20 páginasInforme de La Práctica 5CESAR GAMBOA ANAYAAún no hay calificaciones
- Normas y Especificaciones Del Fierro Fundido NodularDocumento9 páginasNormas y Especificaciones Del Fierro Fundido NodularCESAR GAMBOA ANAYAAún no hay calificaciones
- Segundo Reporte de Laboratorio de Fisica (Cesar Adrian Gamboa Anaya 18160262)Documento8 páginasSegundo Reporte de Laboratorio de Fisica (Cesar Adrian Gamboa Anaya 18160262)CESAR GAMBOA ANAYAAún no hay calificaciones
- HP - 3º - I Bal-Men - 19Documento5 páginasHP - 3º - I Bal-Men - 19CESAR GAMBOA ANAYAAún no hay calificaciones
- U-3-Estructura CristalinaDocumento34 páginasU-3-Estructura CristalinaCESAR GAMBOA ANAYAAún no hay calificaciones
- F3 2 PDFDocumento1 páginaF3 2 PDFCESAR GAMBOA ANAYAAún no hay calificaciones
- GEOGRAFÍA - 3°-I Bal-Men - 19Documento3 páginasGEOGRAFÍA - 3°-I Bal-Men - 19CESAR GAMBOA ANAYAAún no hay calificaciones