Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Afinidad Electronica1
Cargado por
Diego HernandezTítulo original
Derechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
Afinidad Electronica1
Cargado por
Diego HernandezCopyright:
Formatos disponibles
AFINIDAD ELECTRONICA
¿Qué es la afinidad eléctrica?
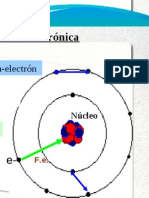
La afinidad eléctrica, afinidad electrónica o
AE es la energía intercambiada cuando un
átomo neutro, gaseoso, y en su estado
fundamental, capta un electrón y se
convierte en un ión mononegativo.
La afinidad electrónica es la cantidad de
energía absorbida por un átomo aislado en
fase gaseosa para formar un ión con una
carga eléctrica de −1. Si la energía no es
absorbida, sino liberada en el proceso, la
afinidad electrónica tendrá, en
consecuencia, valor negativo tal y como sucede para la mayoría de los elementos
químicos; en la medida en que la tendencia a adquirir electrones adicionales sea mayor,
tanto más negativa será la afinidad electrónica. De este modo, el flúor es el elemento que
con mayor facilidad adquiere un electrón adicional, mientras que el mercurio es el que
menos.
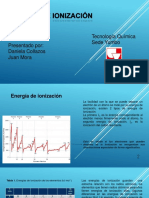
Aunque la afinidad electrica parece variar de forma caótica y desordenada a lo largo de la
tabla periódica, se pueden apreciar patrones. Los no metales tienen afinidades
electrónicas más bajas que los metales, exceptuando los gases nobles que presentan
valores positivos por su estabilidad química, ya que la afinidad electrónica está
influenciada por la regla del octeto.
Los elementos del grupo 1, tienden a ganar un electrón y formar aniones −1, completando
el subnivel s, mientras que los elementos del grupo 2, que ya lo tienen completo, no
presentan esa tendencia. Análogamente sucede en el bloque p, donde las afinidades
electrónicas se van haciendo más negativas a medida que nos acercamos a los gases
nobles.
Existen átomos que presentan capas de valencia con lugares vacantes o "huecos", que
pueden ser ocupados por electrones.
Entonces cuando a un átomo neutro se le añaden uno o más electrones se presenta un
desprendimiento de energía, conocida como afinidad eléctrica, obteniéndose como
resultado la formación de aniones.
Aunque la magnitud de dicha energía liberada sólo puede determinarse indirectamente y
muy rara vez con gran exactitud, en la tabla periódica la podemos predecir en orden
ascendente en un mismo período, de izquierda a derecha, y en un mismo grupo, de abajo
hacia arriba.
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18
Periodo
H He
1
-73 21
Li Be B C N O F Ne
2
-60 19 -27 -122 7 -141 -328 29
Na Mg Al Si P S Cl Ar
3
-53 19 -43 -134 -72 -200 -349 35
K Ca Sc Ti V Cr Mn Fe Co Ni Cu Zn Ga Ge As Se Br Kr
4
-48 10 -18 -8 -51 -64 -16 -64 -112 -118 47 -29 -116 -78 -195 -325 39
Rb Sr Y Zr Nb Mo Tc Ru Rh Pd Ag Cd In Sn Sb Te I Xe
5
-47 -30 -41 -86 -72 -53 -101 -110 -54 -126 32 -29 -116 -103 -190 -295 41
Cs Ba Lu Hf Ta W Re Os Ir Pt Au Hg Tl Pb Bi Po At Rn
6
-45 -31 -79 -14 -106 -151 -205 -223 61 -20 -35 -91 -183 -270 41
Fr Ra Lr Rf Db Sg Bh Hs Mt Ds Rg Cn Uut Uuq Uup Uuh Uus Uuo
7
-44
tabla periódica de afinidades electrónicas, en kJ/mol
También podría gustarte
- Estructura atómica y enlace químicoDe EverandEstructura atómica y enlace químicoCalificación: 3 de 5 estrellas3/5 (2)
- AREA CIENCIA Y TECNOLOGÍA-competencias y CapacidadesDocumento19 páginasAREA CIENCIA Y TECNOLOGÍA-competencias y CapacidadesFroilán Gómez100% (7)
- Bauer Problems Bohr 20201Documento8 páginasBauer Problems Bohr 20201Jorge MatarAún no hay calificaciones
- Afinidad Electronica1 PDFDocumento3 páginasAfinidad Electronica1 PDFAnonymous vd5JxNCAún no hay calificaciones
- Afinidad Electronica QuimicaDocumento4 páginasAfinidad Electronica QuimicaJorge Quintero100% (1)
- Afinidad ElectrónicaDocumento4 páginasAfinidad ElectrónicaGabino Garcia SorianoAún no hay calificaciones
- AFINIDAD ELECTRÓNICA Segunda Unidad QuimicaDocumento10 páginasAFINIDAD ELECTRÓNICA Segunda Unidad QuimicaAbel Nohpal BrionesAún no hay calificaciones
- Afinidad ElectrónicaDocumento1 páginaAfinidad ElectrónicaHugo Alonso Rodriguez CasasAún no hay calificaciones
- Potencial de IonizacionDocumento10 páginasPotencial de IonizacionLuisa SierraAún no hay calificaciones
- Serie 2 2022Documento25 páginasSerie 2 2022Fidel GonzalezAún no hay calificaciones
- ElectronegatividadDocumento3 páginasElectronegatividadjovmac2uAún no hay calificaciones
- Cuestionario Propiedades PeriodicasDocumento4 páginasCuestionario Propiedades PeriodicasErnesto ZavalaAún no hay calificaciones
- Afinidad ElectrónicaDocumento9 páginasAfinidad ElectrónicaWill Morales de la Cuba0% (1)
- Afinidad ElectronicaDocumento4 páginasAfinidad ElectronicaHilda Araceli Flores CabralAún no hay calificaciones
- 4 - Propiedades PeriodicasDocumento12 páginas4 - Propiedades PeriodicasKatherin AiteAún no hay calificaciones
- Clase 4Documento46 páginasClase 4Matias AcostaAún no hay calificaciones
- Configuracion Electronica PDFDocumento9 páginasConfiguracion Electronica PDFun usuario más0% (1)
- Orbitales SDocumento8 páginasOrbitales SDianita LozaAún no hay calificaciones
- ElectronegatividadDocumento7 páginasElectronegatividadNicol VázquezAún no hay calificaciones
- ElectronegatividadDocumento4 páginasElectronegatividadOliver Martínez BermúdezAún no hay calificaciones
- Capitulo Nº6Documento18 páginasCapitulo Nº6EDDY0% (1)
- Garritz, (2005), PP. 108-110Documento3 páginasGarritz, (2005), PP. 108-110Esmeralda Belén DomínguezAún no hay calificaciones
- Enlace IonicoDocumento68 páginasEnlace IonicoKevin VilcamangoAún no hay calificaciones
- Unidad 2-Configuración Electrónica, Tabla Periódica y NomenclaturaDocumento33 páginasUnidad 2-Configuración Electrónica, Tabla Periódica y NomenclaturaDaniel BedriñanaAún no hay calificaciones
- Química 5to Secundaria 6Documento18 páginasQuímica 5to Secundaria 6Metade Marvel A ChAún no hay calificaciones
- Configuraciones Electrónicas (2023)Documento9 páginasConfiguraciones Electrónicas (2023)Daniel Sánchez PovedaAún no hay calificaciones
- Taller2operaciones MatematicasDocumento5 páginasTaller2operaciones MatematicasFranquy Carmona GomezAún no hay calificaciones
- Resolucion Problemes Tema 1 - Generalidades - 2022 - 23Documento21 páginasResolucion Problemes Tema 1 - Generalidades - 2022 - 23nacho cervantesAún no hay calificaciones
- Afinidad Electrónica Es La Cantidad de Energía Absorbida Por Un Átomo Aislado en Fase Gaseosa para Formar Un Ión Con Una Carga Eléctrica deDocumento8 páginasAfinidad Electrónica Es La Cantidad de Energía Absorbida Por Un Átomo Aislado en Fase Gaseosa para Formar Un Ión Con Una Carga Eléctrica deJorge AndresAún no hay calificaciones
- Enlace IonicoDocumento21 páginasEnlace IonicopatriciaAún no hay calificaciones
- Energía de Ionización PDFDocumento8 páginasEnergía de Ionización PDFSofii melendez100% (1)
- Tabla Períodica 2013 SalaDocumento112 páginasTabla Períodica 2013 SalaAndrés De la GranaAún no hay calificaciones
- Tema 1. Introducción SemiconductoresDocumento29 páginasTema 1. Introducción SemiconductoresJuanfran Martínez LópezAún no hay calificaciones
- Propiedades Atómicas y Su Variación PeriódicaDocumento7 páginasPropiedades Atómicas y Su Variación PeriódicaMauricio MauAún no hay calificaciones
- Estructura Atomica: 2.1) Generalidades. 2.1.1) Tamaño de Los ÁtomosDocumento12 páginasEstructura Atomica: 2.1) Generalidades. 2.1.1) Tamaño de Los Átomosgd6s2bpj25Aún no hay calificaciones
- 01 - Propiedades PeriódicasDocumento40 páginas01 - Propiedades PeriódicasLuciaAngrigianiAún no hay calificaciones
- PT Química Sem-03 Sesión-05 2022-2Documento60 páginasPT Química Sem-03 Sesión-05 2022-2Javier Rime SalvatierraAún no hay calificaciones
- Ejercicios Resueltos Del LibroDocumento7 páginasEjercicios Resueltos Del LibroDaniel Sopla CubasAún no hay calificaciones
- Tema 2. Hibridación y EnlacesDocumento78 páginasTema 2. Hibridación y EnlacesAriana HerreraAún no hay calificaciones
- Fisica Del Estado SolidoDocumento22 páginasFisica Del Estado SolidoGerardo Parra GutierrezAún no hay calificaciones
- Asm-Semana 07 (Propiedades Periódicas)Documento20 páginasAsm-Semana 07 (Propiedades Periódicas)Jazmin Parí quispeAún no hay calificaciones
- Qui MicaDocumento13 páginasQui MicaRobochipAún no hay calificaciones
- Estructura Basica Del Atomo y Sus InteraccionesDocumento32 páginasEstructura Basica Del Atomo y Sus InteraccionesJUAN CAMILO RUIZ LINARESAún no hay calificaciones
- S09.s1 - MaterialllDocumento35 páginasS09.s1 - MaterialllKaterine HuamanAún no hay calificaciones
- 1 - Configuración ElectrónicaDocumento5 páginas1 - Configuración ElectrónicaDennisAlexanderPérezRobinsonAún no hay calificaciones
- Dispositivos Electrónicos - Carlos Novillo MonteroDocumento51 páginasDispositivos Electrónicos - Carlos Novillo MonteroEdison Patricio Crucerira100% (1)
- Clase 2 ElectronegatividadDocumento25 páginasClase 2 ElectronegatividadIreneAún no hay calificaciones
- Química - Propiedades Periódicas de Los Elementos.Documento23 páginasQuímica - Propiedades Periódicas de Los Elementos.Noel MatíasAún no hay calificaciones
- Power Point Clase Del 25-8-21Documento38 páginasPower Point Clase Del 25-8-21Maria Julia GomezAún no hay calificaciones
- Radio AtómicoDocumento13 páginasRadio AtómicoGabriela AvilesAún no hay calificaciones
- Estructura Molecular Unidad 4 Física ModernaDocumento50 páginasEstructura Molecular Unidad 4 Física ModernaNico FernandezAún no hay calificaciones
- Clase 5A Estructura ElectrónicaDocumento16 páginasClase 5A Estructura ElectrónicaDan Levi ArratiaAún no hay calificaciones
- Acordeón InorganicaDocumento5 páginasAcordeón InorganicamarkoagustinAún no hay calificaciones
- Radio Atomico Energia de Ionizacion Electronegatividad Carácter MetalicoDocumento21 páginasRadio Atomico Energia de Ionizacion Electronegatividad Carácter MetalicoRoberto CastañoAún no hay calificaciones
- Transp Tema 2 RDocumento6 páginasTransp Tema 2 RMEUBROAún no hay calificaciones
- ElectronegatividadDocumento6 páginasElectronegatividadAbby AvendañoAún no hay calificaciones
- Seminario 1 Con AudioDocumento22 páginasSeminario 1 Con AudioViole BoschettiAún no hay calificaciones
- Presentación - Métodos ElectroquímicosDocumento33 páginasPresentación - Métodos Electroquímicosreinaldo rodriguezAún no hay calificaciones
- 1 Conocimientos Básicos de ElectricidadDocumento25 páginas1 Conocimientos Básicos de Electricidadalejandro sanchez manteroAún no hay calificaciones
- Texto 9Documento28 páginasTexto 9Pedro MartinezAún no hay calificaciones
- Experiencias sobre circuitos eléctricos en serie operados por corriente directaDe EverandExperiencias sobre circuitos eléctricos en serie operados por corriente directaAún no hay calificaciones
- Visor Nocturno PVS14 - EspañolDocumento31 páginasVisor Nocturno PVS14 - Españoljuly romeroAún no hay calificaciones
- T32104 PDFDocumento239 páginasT32104 PDFRoberto De La OlivaAún no hay calificaciones
- Efecto FotoeléctricoDocumento2 páginasEfecto Fotoeléctricocivil.engineer.miranda.autocatAún no hay calificaciones
- Fuego en Las EntrañasDocumento3 páginasFuego en Las EntrañasFranklin Miranda RoblesAún no hay calificaciones
- Separata 2Documento19 páginasSeparata 2Roberto Cespedes100% (6)
- Recurso - 1648675756731 - SEMANA 3 - QUÍMICADocumento5 páginasRecurso - 1648675756731 - SEMANA 3 - QUÍMICAKefaztAún no hay calificaciones
- Unión de Todo Tema 6Documento33 páginasUnión de Todo Tema 6Sarita RoseroAún no hay calificaciones
- Elementoterapia Magnetica Entrega 4Documento22 páginasElementoterapia Magnetica Entrega 4guidoaguilarbarqueroAún no hay calificaciones
- Informe de SimulacionDocumento5 páginasInforme de SimulacionNicolas GuzmanAún no hay calificaciones
- Semana 6Documento5 páginasSemana 6Andres MonroyAún no hay calificaciones
- Evaluacion Sobre La Materia AlbertoDocumento6 páginasEvaluacion Sobre La Materia Albertooctavio paz secundaria0% (1)
- Ciencias - Ii, Iii - Bloque Iv PDFDocumento70 páginasCiencias - Ii, Iii - Bloque Iv PDFelizabel jesus alavezAún no hay calificaciones
- Análisis Morfológico Por SEM y TEMDocumento5 páginasAnálisis Morfológico Por SEM y TEMPaulina ArangoAún no hay calificaciones
- Enlace QuimicoDocumento18 páginasEnlace QuimicoSamir NasibAún no hay calificaciones
- Control Semana 2Documento6 páginasControl Semana 2maria100% (10)
- Metodo GeoelectricoDocumento111 páginasMetodo GeoelectricoA Renzo Torres Potosino100% (1)
- Caracteristicas Del DisplayDocumento9 páginasCaracteristicas Del DisplayPatrik Ramos100% (1)
- Unidad I Quimica OrganicaDocumento21 páginasUnidad I Quimica OrganicaArturo Perez GuzmanAún no hay calificaciones
- Hidrostática - Hidrodinámica - BioelectricidadDocumento115 páginasHidrostática - Hidrodinámica - BioelectricidadjordychemicalAún no hay calificaciones
- Practicas GabineteDocumento10 páginasPracticas GabineteRaynielci Javier100% (1)
- Efectos Dirigidos y No Dirigidos de La Radiación IonizanteDocumento12 páginasEfectos Dirigidos y No Dirigidos de La Radiación IonizantePaola12Aún no hay calificaciones
- Instrumental b3Documento30 páginasInstrumental b3hinchoAún no hay calificaciones
- Espectroscopia de MasasDocumento21 páginasEspectroscopia de MasasMartin ParedesAún no hay calificaciones
- Problemas para La ClaseDocumento1 páginaProblemas para La Clasebabilon2012Aún no hay calificaciones
- Práctica 9 EyMDocumento7 páginasPráctica 9 EyMcarlos aAún no hay calificaciones
- Activiad Virtual 2 - Periodo 2 - Grado 8 - TI - (Energia) 09 - 05 - 21Documento16 páginasActiviad Virtual 2 - Periodo 2 - Grado 8 - TI - (Energia) 09 - 05 - 21EVERTH EFREN MARTINEZ RUALESAún no hay calificaciones
- Tabla PeriodicaDocumento4 páginasTabla PeriodicanatachaAún no hay calificaciones
- El Efecto FotoelectricoDocumento23 páginasEl Efecto FotoelectricoDavidSuarezAún no hay calificaciones